Похідні тіазолу як модулятори рецепторів канабіноїдів
Номер патенту: 83862
Опубліковано: 26.08.2008
Автори: Слідрегт Леонардус А.Й.М., Крузе Корнеліс Г., ван Стьойвенберг Герман Г., Ланге Йозефус Г.М.
Формула / Реферат
1. Застосування сполуки формули (I)
 , (I)
, (I)
де
- R та R1 однакові або різні та представляють феніл або піридиніл, який може бути заміщений 1-3 замісниками Y, де Y представляє замісник з групи метил, етил, пропіл, метокси, етокси, гідрокси, гідроксиметил, гідроксіетил, хлор, йод, бром, фтор, трифторметил, трифторметокси, метилсульфоніл, метилсульфаніл, трифторметилсульфоніл, феніл або ціан, за умови, що Х не представляє підгрупу (іі),
або одна з частин R та R1 представляє фенільну або піридинільну групу, яка може бути заміщена 1-3 замісниками Y, де Y має вищенаведені значення, а інша частина представляє атом водню або С1-8 розгалужену або лінійну алкільну групу, С3-8 розгалужену або лінійну гетероалкільну групу, що містить один гетероатом з групи (N, О, S), С3-7 циклоалкільну групу, С3-7-циклоалкіл-С1-3-алкільну групу, С3-7-гетероциклоалкіл-С1-3-алкільну групу, які можуть бути заміщені гідрокси, метокси, метильною, трифторметилсульфонільною або трифторметильною групою, або атомом фтору, причому С3-7-гетероциклоалкіл-С1-3-алкільна група містить один або два гетероатоми з групи (О, N, S), або зазначена інша частина містить бензильну групу, яка може бути заміщена у фенільному кільці 1-3 замісниками Y, де Y має вищенаведене значення, Х представляє одну з підгруп (і) або (іі),
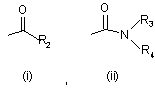 ,
,
де
- R2 представляє C1-8 розгалужену або лінійну алкільну групу, С3-7циклоалкільну групу, С3-7-циклоалкіл-С1-2-алкільну групу, С3-7-гетероциклоалкіл-С1-2-алкільну групу, причому ці групи можуть бути заміщені гідрокси, метильною або трифторметильною групою, або атомом фтору, а С3-7-гетероциклоалкіл-С1-2-алкільна група містить один або два гетероатоми з групи (О, N, S), або R2 представляє фенільну, бензильну, фенетильну або фенілпропільну групу, яка може бути заміщена у фенільному кільці 1-3 замісниками Y, де Y має вищенаведене значення, або R2 представляє піридильну, тієнільну або нафтильну групу, причому нафтильна група може бути заміщена атомом галогену, метильною групою або метокси або трифторметильною групою,
- R3 представляє атом водню або розгалужену або лінійну С1-3 алкільну групу,
- R4 представляє водень, розгалужену або лінійну С1-10 алкільну або С3-8-циклоалкіл-С1-2-алкільну групу, розгалужену або лінійну С1-10алкокси, С3-8циклоалкільну, С5-10 біциклоалкільну, С5-10-біциклоалкіл-С1-2-алкільну, С6-10трициклоалкільну, С6-10 трициклоалкілметильну, розгалужену або лінійну С3-10 алкенільну, C5-8 циклоалкенільну групу, причому ці групи можуть містити один або більше гетероатомів з групи (О, N, S) і можуть бути заміщені гідроксигрупою, 1-3 метильними групами, етильною групою або 1-3 атомами фтору, або R4 представляє фенільну, феніламінову, фенокси, бензильну, фенетильну або фенілпропільну групу, які можуть бути заміщені у фенільному кільці 1-3 замісниками Y, де Y має вищенаведене значення, або R4 представляє піридильну або тієнільну групу, або R4 представляє групу NR5R6, де
R5 та R6 разом з атомом азоту, до якого вони приєднані, утворюють насичену або ненасичену, моноциклічну або біциклічну, гетероциклічну групу з 4-10 атомами у кільці, яка містить один або більше гетероатомів з групи (О, N, S) і може бути заміщена розгалуженою або лінійною С1-3 алкільною, фенільною, гідрокси або трифторметильною групою або атомом фтору, або R3 та R4 разом з атомом азоту, до якого вони приєднані, утворюють насичену або ненасичену, моноциклічну або біциклічну, гетероциклічну групу з 4-10 атомами у кільці, яка містить один або більше гетероатомів з групи (О, N, S) і може бути заміщена розгалуженою або лінійною С1-3 алкільною, фенільною, аміно, гідрокси, метокси, ціано або трифторметильною групою або атомом фтору або хлору,
та їх фармакологічно прийнятні солі, а також пролікарські речовини, що є похідними сполук формули (І), де присутня група, яка легко видаляється після потрапляння до організму, вибрані з-поміж амідину, енаміну, основи Манніха, похідного гідроксилметилену, похідного О-(ацилоксиметиленкарбамату), карбамату або енаміну,
для виготовлення фармацевтичної композиції для лікування психозу, бентежності, депресії, дефіциту уваги, розладів пам'яті, гіперсексуальності, алкоголізму, наркозалежності, дистонії, м'язових спазмів, дрижавки, хвороби Паркінсона, епілепсії, хвороби Гантінгтона, синдрому Туретта, травми хребта, вірусного енцефаліту, больових синдромів, септичного шоку, глаукоми, раку, блювання, нудоти, сексуальних розладів та діареї.
2. Сполука формули (І)
 , (I)
, (I)
де
- R та R1 однакові або різні та представляють феніл, 3-піридиніл або 4-піридиніл, який може бути заміщений 1-3 замісниками Y, де Y представляє замісник з групи метил, етил, пропіл, метокси, етокси, гідрокси, гідроксиметил, гідроксіетил, хлор, йод, бром, фтор, трифторметил, трифторметокси, метилсульфоніл, метилсульфаніл, трифторметилсульфоніл, феніл або ціан, за умови, що Х не представляє підгрупу (іі),
або одна з частин R та R1 представляє фенільну, 3-піридинільну або 4-піридинільну групу, яка може бути заміщена 1-3 замісниками Y, де Y має вищенаведені значення, а друга частина представляє C2-8 розгалужену або лінійну алкільну групу, С3-8 розгалужену або лінійну гетероалкільну групу, що містить один гетероатом з групи (N, О, S), С3-7 циклоалкільну групу, С3-7-циклоалкіл-С1-3-алкільну групу, С3-7-гетероциклоалкіл-С1-3-алкільну групу, причому ці групи можуть бути заміщені гідрокси, метокси, метильною, трифторметилсульфонільною або трифторметильною групою або атомом фтору, а С3-7-гетероциклоалкіл-С1-3-алкільна група містить один або два гетероатоми з групи (О, N, S), або зазначена друга частина представляє бензильну групу, яка може бути заміщена у фенільному кільці 1-3 замісниками Y, де Y має вищенаведені значення, Х представляє одну з підгруп (і) або (іі),
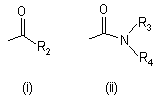 ,
,
де
- R2 представляє С3-8 розгалужену або лінійну алкільну групу, С3-7 циклоалкільну групу, С3-7-циклоалкіл-С1-2-алкільну групу, С3-7-гетероциклоалкіл-С1-2-алкільну групу, які можуть бути заміщені гідрокси, метильною або трифторметильною групою або атомом фтору, а С3-7-гетероциклоалкіл-С1-2-алкільна група містить один або два гетероатоми з групи (О, N, S), або R2 представляє фенільну, бензильну, фенетильну або фенілпропільну групу, яка може бути заміщена у фенільному кільці 1-3 замісниками Y, де Y має вищенаведені значення, або R2 представляє піридильну, тієнільну або нафтильну групу, причому нафтильна група може бути заміщена атомом галогену, метильною групою або метокси або трифторметильною групою за умови, що, коли R2 представляє феніл, R не є фенільна, 4-хлорфенільна, 4-метилфенільна або 4-метоксифенільна група,
- R3 представляє атом водню або розгалужену або лінійну С1-3 алкільну групу,
- R4 представляє розгалужену або лінійну С1-10 алкільну або С3-8-циклоалкіл-С1-2-алкільну групу, розгалужену або лінійну С1-10алкокси, С3-8циклоалкільну, С5-10 біциклоалкільну, С5-10-біциклоалкіл-С1-2-алкільну С6-10 трициклоалкільну, С6-10 трициклоалкілметильну, розгалужену або лінійну С3-10 алкенільну, C5-8 циклоалкенільну групу, причому ці групи можуть містити один або більше гетероатомів з групи (О, N, S) і можуть бути заміщені гідроксигрупою, 1-3 метильними групами, етильною групою або 1-3 атомами фтору, або R4 представляє фенільну, феніламінову, фенокси, бензильну, фенетильну або фенілпропільну групу, які можуть бути заміщені у фенільному кільці 1-3 замісниками Y, де
- Y має вищенаведені значення, або R4 представляє піридильну або тієнільну групу, або R4 представляє групу NR5R6, де R5 та R6 разом з атомом водню, до якого вони приєднані утворюють насичену або ненасичену, моноциклічну або біциклічну, гетероциклічну групу з 4-10 атомами у кільці, причому ця гетероциклічна група містить один або більше гетероатомів з групи (О, N, S) і може бути заміщена розгалуженою або лінійною С1-3 алкільною, фенільною, гідрокси або трифторметильною групою або атомом фтору, або R4 представляє групу NR5R6, де R5 та R6 разом з атомом водню, до якого вони приєднані, утворюють насичену або ненасичену, моноциклічну або біциклічну, гетероциклічну групу з 4-10 атомами у кільці, причому ця гетероциклічна група містить один або більше гетероатомів з групи (О, N, S) і може бути заміщена розгалуженою або лінійною С1-3 алкільною, фенільною, аміновою, гідрокси, метокси, ціано або трифторметильною групою або атомом фтору або хлору,
та їх фармакологічно прийнятні солі, а також пролікарські речовини, що є похідними сполук формули (І), де присутня група, яка легко видаляється після потрапляння до організму, вибрані з-поміж амідину, енаміну, основи Манніха, похідного гідроксилметилену, похідного О-(ацилоксиметиленкарбамату), карбаматуабо енаміну,
3. Сполука за п. 2 або її сіль для застосування як лікарського засобу.
4. Фармацевтична композиція, яка містить принаймні одну сполуку за п. 2 як діючу речовину.
5. Застосування сполуки за п. 2 для виготовлення фармацевтичної композиції для лікування таких хвороб, як психоз, бентежність, депресія, дефіцит уваги, розлади пам'яті, розлади сприйняття, відсутність апетиту, опасистість, алкоголізм, гіперсексуальність, наркозалежність, нейродегенеративні розлади, недоумство, дистонія, м'язові спазми, дрижавка, епілепсія, множинний склероз, травматичні пошкодження мозку, інсульт, хвороба Паркінсона, хвороба Альцгеймера, хвороба Гантінгтона, синдром Туретта, мозкова ішемія, церебральна апоплексія, черепно-мозкова травма, травми хребта, бляшковий склероз, вірусний енцефаліт, розлади демієлінізації, лікування септичного шоку, глаукоми, раку, діабету, блювання, нудоти, астми, респіраторних захворювань, шлунково-кишкових захворювань, виразки шлунку, діареї та серцево-судинних захворювань.
6. Сполука загальної формули (IV)
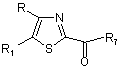 , (IV)
, (IV)
де один з R та R1 представляє фенільну, або 3-піридинільну, або 4-піридинільну групу, яка може бути заміщена 1-3 замісниками Y, де Y має значення, наведені вище, а друга частина представляє C2-8 розгалужену або лінійну алкільну групу, С3-8 розгалужену або лінійну гетероалкільну групу, що містить один гетероатом з групи (N, О, S) або групу SO2, С3-7 циклоалкільну групу, С3-7-циклоалкіл-С1-3-алкільну групу, С3-7-гетероциклоалкіл-С1-3-алкільну групу, причому ці групи можуть бути заміщені гідрокси, метокси, метильною, трифторметилсульфонільною або трифторметильною групою або атомом фтору, а С3-7-гетероциклоалкіл-С1-3-алкільна група містить один або два гетероатоми з групи (О, N, S), або зазначена друга частина представляє бензильну групу, яка може бути заміщена у фенільному кільці 1-3 замісниками Y, де Y має вищенаведене значення, a R7 представляє гідрокси, С1-4 розгалужену або лінійну алкоксигрупу, або бензилоксигрупу, або атом хлору, або N-метокси-N-метиламінову групу, причому ці сполуки можуть застосовуватися при синтезі сполук загальної формули (І).
Текст
1. Застосування сполуки формули (I) 2 (11) 1 , де - R2 представляє C1-8 розгалужену або лінійну алкільну групу, С3-7циклоалкільну групу, С3-7циклоалкіл-С 1-2-алкільну групу, С3-7гетероциклоалкіл-С1-2-алкільну гр упу, причому ці групи можуть бути заміщені гідрокси, метильною або трифторметильною групою, або атомом фто 3 83862 ру, а С3-7-ге тероциклоалкіл-С1-2-алкільна група містить один або два гетероатоми з групи (О, N, S), або R2 представляє фенільну, бензильну, фенетильну або фенілпропільну групу, яка може бути заміщена у фенільному кільці 1-3 замісниками Y, де Y має вищенаведене значення, або R2 представляє піридильну, тієнільну або нафтильну групу, причому нафтильна група може бути заміщена атомом галогену, метильною групою або метокси або трифторметильною групою, - R3 представляє атом водню або розгалужену або лінійну С1-3 алкільну груп у, - R4 представляє водень, розгалужену або лінійну С1-10 алкільну або С3-8-циклоалкіл-С 1-2-алкільну груп у, розгалужену або лінійну С 1-10алкокси, С3С5-10 біциклоалкільну, С5-108циклоалкільну, біциклоалкіл-С 1-2-алкільну, С6-10 трициклоалкільну, С6-10 трициклоалкілметильну, розгалужену або лінійну С3-10 алкенільну, C5-8 циклоалкенільну групу, причому ці групи можуть містити один або більше гетероатомів з групи (О, N, S) і можуть бути заміщені гідроксигрупою, 1-3 метильними групами, етильною групою або 1-3 атомами фтору, або R 4 представляє фенільну, феніламінову, фенокси, бензильну, фенетильну або фенілпропільну гр упу, які можуть бути заміщені у фенільному кільці 1-3 замісниками Y, де Y має вищенаведене значення, або R4 представляє піридильну або тієнільну групу, або R4 представляє гр упу NR5R6 , де R5 та R6 разом з атомом азоту, до якого вони приєднані, утворюють насичену або ненасичену, моноциклічну або біциклічну, гетероциклічну гр упу з 4-10 атомами у кільці, яка містить один або більше гетероатомів з групи (О, N, S) і може бути заміщена розгалуженою або лінійною С 1-3 алкільною, фенільною, гідрокси або трифторметильною групою або атомом фтору, або R3 та R4 разом з атомом азоту, до якого вони приєднані, утворюють насичену або ненасичену, моноциклічну або біциклічну, гетероциклічну груп у з 4-10 атомами у кільці, яка містить один або більше гетероатомів з групи (О, N, S) і може бути заміщена розгалуженою або лінійною С1-3 алкільною, фенільною, аміно, гідрокси, метокси, ціано або трифторметильною групою або атомом фтору або хлору, та їх фармакологічно прийнятні солі, а також пролікарські речовини, що є похідними сполук формули (І), де присутня група, яка легко видаляється після потрапляння до організму, вибрані з-поміж амідину, енаміну, основи Манніха, похідного гідроксилметилену, похідного О(ацилоксиметиленкарбамату), карбамату або енаміну, для виготовлення фармацевтичної композиції для лікування психозу, бентежності, депресії, дефіциту уваги, розладів пам'яті, гіперсексуальності, алкоголізму, наркозалежності, дистонії, м'язових спазмів, дрижавки, хвороби Паркінсона, епілепсії, хвороби Гантінгтона, синдрому Туретта, травми хребта, вір усного енцефаліту, больових синдромів, септичного шоку, глаукоми, раку, блювання, нудоти, сексуальних розладів та діареї. 2. Сполука формули (І) 4 X N S R R1 , (I) де - R та R1 однакові або різні та представляють феніл, 3-піридиніл або 4-піридиніл, який може бути заміщений 1-3 замісниками Y, де Y представляє замісник з групи метил, етил, пропіл, метокси, етокси, гідрокси, гідроксиметил, гідроксіетил, хлор, йод, бром, фтор, трифторметил, трифторметокси, метилсульфоніл, метилсульфаніл, трифторметилсульфоніл, феніл або ціан, за умови, що Х не представляє підгрупу (іі), або одна з частин R та R1 представляє фенільну, 3-піридинільну або 4-піридинільну гр упу, яка може бути заміщена 1-3 замісниками Y, де Y має ви щенаведені значення, а друга частина представляє C2-8 розгалужену або лінійну алкільну групу, С3-8 розгалужену або лінійну гетероалкільну групу, що містить один гетероатом з групи (N, О, S), С3- 7 циклоалкільну гр упу, С3-7-циклоалкіл-С 1-3-алкільну груп у, С3-7-ге тероциклоалкіл-С1-3-алкільну групу, причому ці групи можуть бути заміщені гідрокси, метокси, метильною, трифторметилсульфонільною або трифторметильною групою або атомом фтор у, а С3-7-гетероциклоалкіл-С1-3-алкільна група містить один або два гетероатоми з групи (О, N, S), або зазначена друга частина представляє бензильну груп у, яка може бути заміщена у фенільному кільці 1-3 замісниками Y, де Y має вищенаведені значення, Х представляє одну з підгруп (і) або (іі), O O N R2 (i) R3 R4 (ii) , де - R2 представляє С 3-8 розгалужену або лінійну алкільну групу, С3-7 циклоалкільну групу, С3-7циклоалкіл-С 1-2-алкільну групу, С3-7гетероциклоалкіл-С1-2-алкільну груп у, які можуть бути заміщені гідрокси, метильною або трифторметильною групою або атомом фтору, а С3-7гетероциклоалкіл-С1-2-алкільна група містить один або два гетероатоми з групи (О, N, S), або R 2 представляє фенільну, бензильну, фенетильну або фенілпропільну гр упу, яка може бути заміщена у фенільному кільці 1-3 замісниками Y, де Y має вищенаведені значення, або R2 представляє піридильну, тієнільну або нафтильну групу, причому нафтильна група може бути заміщена атомом галогену, метильною групою або метокси або трифторметильною групою за умови, що, коли R2 представляє феніл, R не є фенільна, 4хлорфенільна, 4-метилфенільна або 4метоксифенільна група, - R3 представляє атом водню або розгалужену або лінійну С1-3 алкільну груп у, - R4 представляє розгалужену або лінійну С 1-10 алкільну або С 3-8-циклоалкіл-С 1-2-алкільну групу, 5 83862 6 розгалужену або лінійну С 1-10алкокси, С3С5-10 біциклоалкільну, С5-108циклоалкільну, біциклоалкіл-С 1-2-алкільну С 6-10 трициклоалкільну, С6-10 трициклоалкілметильну, розгалужену або лінійну С3-10 алкенільну, C5-8 циклоалкенільну групу, причому ці групи можуть містити один або більше гетероатомів з групи (О, N, S) і можуть бути заміщені гідроксигрупою, 1-3 метильними групами, етильною групою або 1-3 атомами фтору, або R 4 представляє фенільну, феніламінову, фенокси, бензильну, фенетильну або фенілпропільну гр упу, які можуть бути заміщені у фенільному кільці 1-3 замісниками Y, де - Y має вищенаведені значення, або R 4 представляє піридильну або тієнільну групу, або R4 представляє групу NR5R6, де R5 та R6 разом з атомом водню, до якого вони приєднані утворюють насичену або ненасичену, моноциклічну або біциклічну, гетероциклічну групу з 4-10 атомами у кільці, причому ця гетероциклічна група містить один або більше гетероатомів з групи (О, N, S) і може бути заміщена розгалуженою або лінійною С 1-3 алкільною, фенільною, гідрокси або трифторметильною групою або атомом фтору, або R4 представляє груп у NR5R6, де R5 та R 6 разом з атомом водню, до якого вони приєднані, утворюють насичену або ненасичену, моноциклічну або біциклічну, гетероциклічну груп у з 4-10 атомами у кільці, причому ця гетероциклічна група містить один або більше гетероатомів з групи (О, N, S) і може бути заміщена розгалуженою або лінійною С 1-3 алкільною, фенільною, аміновою, гідрокси, метокси, ціано або трифторметильною групою або атомом фтору або хлору, та їх фармакологічно прийнятні солі, а також пролікарські речовини, що є похідними сполук формули (І), де присутня група, яка легко видаляється після потрапляння до організму, вибрані з-поміж амідину, енаміну, основи Манніха, похідного гідроксилметилену, похідного О(ацилоксиметиленкарбамату), карбамату або енаміну, 3. Сполука за п.2 або її сіль для застосування як лікарського засобу. 4. Фармацевтична композиція, яка містить принаймні одну сполуку за п.2 як діючу речовину. 5. Застосування сполуки за п.2 для виготовлення фармацевтичної композиції для лікування таких хвороб, як психоз, бентежність, депресія, дефіцит уваги, розлади пам'яті, розлади сприйняття, відсутність апетиту, опасистість, алкоголізм, гіперсексуальність, наркозалежність, нейродегенеративні розлади, недоумство, дистонія, м'язові спазми, дрижавка, епілепсія, множинний склероз, травматичні пошкодження мозку, інсульт, хвороба Паркінсона, хвороба Альцгеймера, хвороба Гантінгтона, синдром Туретта, мозкова ішемія, церебральна апоплексія, черепно-мозкова травма, травми хребта, бляшковий склероз, вірусний енцефаліт, розлади демієлінізації, лікування септичного шоку, глаукоми, раку, діабету, блювання, нудоти, астми, респіраторних захворювань, шлунково-кишкових захворювань, виразки шлунку, діареї та серцевосудинних захворювань. 6. Сполука загальної формули (IV) Цей винахід стосується групи похідних тіазолу, способів одержання цих сполук, фармаційних композицій, які містять принаймні одну з цих сполук у якості діючої речовини, а також застосування таких композицій для лікування психічних та нервових розладів й інших хвороб, пов'язаних з нейротрансмісією канабіноїдів CB. Похідні тіазолу за винаходом можуть бути антагоністами рецепторів канабіноїдів (CB), агоністами рецепторів CB, зворотними або частковими агоністами рецепторів CB. Похідні тіазолу за винаходом прив'язуються або до рецептора CB1, або до рецептора СВ2 , або до обох рецепторів CB1 та СВ2. Винахід стосується застосування сполуки, яка описується далі, при виготовленні лікарського засобу, що дає сприятливий ефект. Цей сприятливий ефект, описаний далі, стане очевидним для фа хівця при вивченні опису винаходу з ура хуванням рівня техніки. Винахід також стосується застосування сполуки згідно з винаходом у виробництві засобу для лікування або профілактики хвороби чи хворобливого стану. Зокрема, винахід стосується нового застосування для лікування хвороби чи хворобливого стану, як описано тут і як стане ясно фа хівцю при вивченні опису винаходу з урахуванням рівня техніки. У варіантах здійснення винахо R R1 N S R7 O , (IV) де один з R та R1 представляє фенільну, або 3піридинільну, або 4-піридинільну групу, яка може бути заміщена 1-3 замісниками Y, де Y має значення, наведені вище, а друга частина представляє C2-8 розгалужену або лінійну алкільну гр упу, С3-8 розгалужену або лінійну гетероалкільну гр упу, що містить один гетероатом з групи (N, О, S) або груп у SO2 , С3-7 циклоалкільну груп у, С3-7циклоалкіл-С 1-3-алкільну групу, С3-7гетероциклоалкіл-С1-3-алкільну гр упу, причому ці групи можуть бути заміщені гідрокси, метокси, метильною, трифторметилсульфонільною або трифторметильною групою або атомом фтору, а С3-7гетероциклоалкіл-С1-3-алкільна група містить один або два гетероатоми з групи (О, N, S), або зазначена друга частина представляє бензильну групу, яка може бути заміщена у фенільному кільці 1-3 замісниками Y, де Y має вищенаведене значення, a R7 представляє гідрокси, С1-4 розгалужену або лінійну алкоксигрупу, або бензилоксигрупу, або атом хлору, або N-метокси-N-метиламінову гр упу, причому ці сполуки можуть застосовуватися при синтезі сполук загальної формули (І). 7 83862 ду для виробництва ліків застосовують ті чи інші сполуки, що описуються тут. Тіазоли описані у [заявці WOO127094] як інгібітори тригліцериду. У [WO0426863] похідні тіазолу виступають як інгібітори трансформаційного фактору зростання (TrF). Похідні 4,5-діарилтіазолу за [EP 388909 та EP 377457] слугують інгібіторами 5-ліпоксігенази для лікування тромбозу, гіпертензії, алергії та запалень. Структури, що наведені там, усі містять два фенільних кільця, які рзаміщуються метокси, фторною, метилтіо або метилсульфінільною групою. У [WO 9603392] описані сульфоніларил-арилтіазоли для лікування запалень та болю, артриту або лихоманки як запалювальних розладів. Згідно з [JP 05345772] 4,5діарилтіазоли є інгібіторами ацетилхолинестерази, а у [JP 04154773] 4,5-діарилтіазоли мають анальгетичну, протизапалювальну та антипіретичну дію. Нами несподівано встановлено, що похідні тіазолу формули (І), їх пролікарські форми та солі де - R та R1 однакові або різні та представляють феніл або піридиніл, який може бути заміщений 13 замісниками Y, де Y представляє замісник з групи метил, етил, пропил, метокси, етоксі, гідрокси, гідроксиметил, гідроксиетил, хлор, йод, бром, фтор, трифторметил, трифторметокси, метилсульфоніл, метилсульфанил, трифторметилсульфоніл, феніл або ціан, за умови, що X не представляє підгрупу (іі), або одна з частин R та R1 представляє фенільну або піридинільну груп у, яка може бути заміщена 1-3 замісниками Y, де Y має вищенаведене значення, а інша частина представляє атом водню або С1-8 розгалужену або лінійну алкільну гр упу, С3-8 розгалужену або лінійну гетероалкільну гр упу, що містить один гетероатом з групи (N, O, S), С3-7 циклоалкільну групу, С3-7-циклоалкіл-С 1-3-алкільну груп у, С3-7-ге тероциклоалкіл-С1-3-алкільну групу, які можуть бути заміщені гідрокси, метокси, метильною, трифторметилсульфонільною або трифторметильною групою, або атомом фтору, причому С3-7-гетероциклоалкіл-С1-3-алкільна група містить один або два гетероатоми з групи (O, N, S), або зазначена інші частина містить бензильну гр упу, яка може бути заміщена у фенільному кільці 1-3 замісниками Y, де Y має вищенаведене значення, X представляє одну з підгруп (і) або (іі), де - R2 представляє C1-8 розгалужену або лінійну алкільну гр упу, С3-7-циклоалкільну гр упу, С3-7циклоалкіл-С 1-2-алкільну групу, С3-7гетероциклоалкіл-С1-2-алкільну гр упу, причому ці 8 групи можуть бути заміщені гідрокси, метильною або трифторметильною групою, або атомом фтору, а С3-7-ге тероциклоалкіл-С1-2-алкільна група містить один або два гетероатоми з групи (O, N, S), або R2 представляє фенільну, бензильну, фенетильну або фенілпропильну групу, яка може бути заміщена у фенільному кільці 1-3 замісниками Y, де Y має вищенаведене значення, або R2 представляє піридільну, тієнильну або нафтильну груп у, причому зазначена нафтильна група може бути заміщена атомом галогену, метильною групою або метокси або трифторметильною групою, - R3 представляє атом водню або розгалужену або лінійну C1-3-алкільну груп у, - R4 представляє водень, розгалужену або лінійну C1-10-алкільну або С 3-8-циклоалкіл-С 1-2алкільну гр упу, розгалужену або лінійну C1-10 алкокси, С3-8 циклоалкільну, C5-10-біциклоалкільну, С510-біциклоалкіл-С 1-2-алкільну, С 6-10 трициклоалкільну, С6-10-трициклоалкіл-метильну, розгалужену або лінійну С3-10 алкенільну, С5-8 циклоалкенільну групу, причому ці групи можуть містити один або більше гетероатомів з групи (O, N, S) і можуть бути заміщені гідроксигрупою, 1-3 метильними групами, етильною групою або 1-3 атомами фтору, або R4 представляє фенільну, феніламінову, фенокси, бензильну, фенетильну або фенілпропильну групу, які можуть бути заміщені у фенільному кільці 13 замісниками Y, де Y має вищенаведене значення, або R4 представляє піридільну або тієнильну груп у, або R4 представляє гр упу NR5R6, де R5 та R6 разом з атомом азоту, до якого вони приєднані, утворюють насичену або ненасичену, моноциклічну або біциклічну, гетероциклічну гр упу з 4-10 атомами у кільці, яка містить один або кілька гетероатомів з групи (O, N, S) і може бути заміщена розгалуженою або лінійною C1-3-алкільною, фенільною, гідрокси або трифторметильною групою або атомом фтору, або R3 та R4 разом з атомом азоту, до якого вони приєднані, утворюють насичену або ненасичену, моноциклічну або біциклічну, гетероциклічну групу з 4-10 атомами у кільці, яка містить один або кілька гетероатомів з групи (O, N, S) і може бути заміщена розгалуженою або лінійною C1-3 алкільною, фенільною, аміно, гідрокси, метокси, ціано або трифторметильною групою або атомом фтору або хлор у, є модуляторами рецептора канабіноїду CB. Винахід охоплює всі сполуки формули (І), рацемати, суміші діастереометрів та окремі стереоізомери. Отже, сполуки, у яких замісники потенційно асиметричних атомів вуглецю знаходяться у Rконфігурації або у S-конфігурації, належать до обсягу винаходу. Також до обсягу винаходу належать пролікарські речовини, тобто сполуки, які, потрапляючи до людського організму будь-яким відомим чином, метаболізуються у сполуки формули (І). Пролікарські речовини - то біооборотні похідні молекул лікарських речовин, які використовуються для подолання якихось перешкод на користь молекули вихідної лікарської речовини. До цих перешкод належать, зокрема, розчинність, проникність, стабільність, пресистемний метаболізм та обмеження прицільності [J. Stella, "Prodrms as therapeutics", 9 83862 Expert Opin. Ther. Patents, 14(3), 277-280, 2004]. Зокрема, це стосується сполук з первинними чи вторинними аміновими або гідроксигрупами. Такі сполуки здатні реагувати з органічними кислотами, даючи сполуки формули (І), де присутня додаткова група, яка легко відщеплюється після введення до організму, наприклад, такі, як енамін, основа Манніха, похідне гідроксил-метилену, похідне О(ацілоксіметиленкарбамату), карбамату, е фіру, аміду або енаміну. Пролікарська речовина є неактивною сполукою, яка при засвоєнні набуває активної форми [Медісіпаї Chemistry: Principles та Practice, 1994, ISBN 0-85186-494-5, Ed.: F. D. Kіnr, p.216]. Завдяки активності щодо рецепторів CB сполуки за винаходом можуть застосовуватися при лікуванні таких хвороб, як психоз, бентежність, депресія, дефіцит уваги, розлади пам'яті, розлади сприйняття, відсутність апетиту, опасистість, алкоголізм, гіперсексуальність, наркозалежність, неврологічних розладів, як от нейродегенеративні роздали, недоумство, дистонія, м'язові спазми, дрижавка, епілепсія, множинний склероз, травматичні пошкодження мозку, інсульт, хвороба Паркінсона, хвороба Альцгеймера, хвороба Гантінгтона, синдром Туретта, мозкова ішемія, церебральна апоплексія, черепно-мозкова травма, травми хребта, нейрозапалювальні розлади, бляшковий склероз, вірусний енцефалит, м'язові розлади, а також больових синдромів, включаючи невропатичні болі, та інших хвороб центральної нервової системи, пов'язаних з нейротрансмісією канабіноїдів, лікування септичного шоку, глаукоми, раку, діабету, блювання, нудоти, астми, респіраторних захворювань, шлунково-кишкових захворювань, сексуальних розладів, виразки шлунку, діареї та серцево-судинних захворювань. Фармакологічні методи Спорідненість до людських рецепторів канабіноїдів CB1 in vitro Спорідненість сполук за винаходом до рецепторів канабіноїдів CB1 можна визначити за допомогою препаратів з мембран клітин яєчників китайського хом'яка (ЯКХ), у яких людський рецептор канабіноїдів CB1 стабільно трансфектується у зв'язку з [3Н]СР-55,940 як радіоліганд. Після інкубування свіжоприготованих препаратів клітинних мембран з [3H]-лігандом, з доданням сполук за винаходом або без них, розділяють фільтрацією крізь фільтри зі скловолокна зв'язані та вільні ліганди. Радіоактивність фільтра вимірюють лічильником сцинтиляцій у рідині. Спорідненість до людських рецепторів канабіноїдів СВ2 in vitro Спорідненість сполук за винаходом до рецепторів канабіноїдів СВ2 можна визначити за допомогою препаратів з мембран клітин яєчників китайського хом'яка (ЯКХ), у яких людський рецептор канабіноїдів СВ2 стабільно трансфектується у зв'язку з [3Н]СР-55,940 як радіоліганд. Після інкубування свіжоприготованих препаратів клітинних мембран з [3H]-лігандом, з доданням сполук за винаходом або без них, розділяють фільтрацією крізь фільтри зі скловолокна зв'язані та 10 вільні ліганди. Радіоактивність фільтра вимірюють лічильником сцинтиляцій у рідині. Антагонізм до людських рецепторів канабіноїдів CB1 in vitro Антагонізм до рецепторів CB1 in vitro CB1 визначають на людському рецепторі CBi, клонованому в клітинах яєчника китайського хом'яка (ЯКХ). Клітини ЯКХ вирощують у модифікованому за Дульбекко середовищі Ігла (DMEM) з доданнім 10% інактивованої нагріванням сироватки телячого зародку. Середовище відсмоктують і замінюють DMEM, до якої замість сироватки телячого зародку додана [3H]-арахідонова кислота, та інкубують усю ніч у пічці з культурою клітин (5% СО2/95% повітря; 370C; атмосфера насичена водою). Протягом цього часу [3H]-арахідонова кислота вкорінюється до фосфоліпідів мембран. У день випробування середовище відсмоктують і тричі промивають клітини 0.5мл DMEM з вмістом 0.2% альбуміну бичачої сироватки (BSA). Стимуляція рецепторів CB1 WIN 55,212-2 призводить до активації PLА2 з наступним виділенням [3H]-арахідонової кислоти до середовища. Цьому спричиненому WIN 55,212-2 виділенню протидіють у залежності від концентрації антагоністи рецептора CB1. Антагоністична потужність дослідних сполук відносно CB1 виражається у величинах рА2 . Антагонізм до людських рецепторів CB1 in vivo І Антагонізм до CB1 in vivo визначається за допомогою спричиненої СР-55,940 гіпотензії у щурів. Самців щурів з нормальним тиском (225-300г; Harlan, Горст, Нідерланди) анестезують пентобарбіталом (80мг/кг підшкірно). Вимірюють кров'яний тиск через канюлю, вставлену до лівої сонної артерії, апаратом Spectramed DTX-plus (Spectramed B.V., Білтховен, Нідерланди). Після підсилення у підсилювачі Nihon Kohden (тип АР-621Г; Nihon Kohden B.V., Амстердам, Нідерланди), сигнал про кров'яний тиск реєструється на персональному комп'ютері (Compaq Deskpro 386s), за допомогою програми збору даних Po-Ne-Mah (Po-Ne-Mah Inc., Сторрс, США). П ульс вираховують з пульсуючого сигналу про тиск. Усі сполуки вводять орально у вигляді мікросуспензії у 1% метилцелюлозі за 30 хвилин до анестезії, тобто за 60 хвилин до введення агоніста рецептора CB1 СР-55,940. Обсяг ін'єкції 10мл кг-1. Після гемодинамічної стабілізації вводять агоніст рецептора CB1 СР-55,940 (0.1мг кг1 внутрішньовенно) та визначають гіпотензивну дію. [Warner, J.A. et аl., Hemodynamic effects of cannabinoids: coronary and cerebral vasodilation mediated by cannabinoid CB1 receptors. Eur. J. Pharmacol. 2001, 423, 203-210]. За допомогою цього гіпотензивного випробування можна також визначити агоністичну дію сполук щодо рецептора CB1. Такій агоністичній дії CB1 на кров'яний тиск можна протидіяти за допомогою селективного антагоніста рецептора CB1, наприклад, рімонабанту. Агоністичну або частково агоністичну активність сполук за винаходом щодо рецепторів канабіноїдів можна визначати за опублікованими методиками, наприклад, дослідженням канабіміметичних ефектів in vi vo [Wiley, J. L. et al., J. Pharmacol. Exp. Ther. 2001, 296, 1013]. 11 83862 Сполукам за винаходом можна надавати форм, придатних для введення до організму, відомими способами із застосуванням допоміжних речовин та/або рідких чи твердих носіїв. Сполуки за винахдом звичайно вводять у вигляді фармаційних композицій, що являють собою нові та важливі аспекти здійснення винаходу завдяки вмісту сполук, зокрема, сполук згідно з винаходом. Серед видів фармаційних композицій можна зазначити таблетки, жувальні таблетки, капсули, розчини, парентеральні розчини, супозиторії, суспензії та інші, зазначені у цьому описі або очевидні для фахівця після вивчення опису на підставі його загальних знань з рівня техніки. У варіантах здійснення винаходу передбачений фармаційний набір, утворений однією або кількома вмістинами, заповненими одним або кількома компонентами фармаційної композиції згідно з винаходом. До такої вмістини (вмістин) можуть додаватися друковані матеріали, наприклад, інструкція із вживання або нотатка за формою, передбаченою державним органом, який контролює виробництво, застосування або продаж фармаційних продуктів, причому ця нотатка означає затвердження таким органом виробництва, застосування або продажу композиції для людей або тварин. Загальний опис синтезу Похідні тіазолу можна одержувати відомими способами, наприклад: [a) Orranic Reactions, Vol. VI, (1951), p.367-409, Ed. R. Adams, John Wiley and Sons Inc., New York b) J. S. Carter et al., Bioorg. Med. Chem. Lett. (1999), 9, 1167-1170 c) T. T. Sakai et al., Bioorg. Med. Chem. (1999), 7, 1559-1566 d) A. Tanaka et al., J. Med. Chem. (1994), 37, 1189-1199 e) J. J. Talley et al., WO 9603392: Chem. Abstr. 125, 33628 f) V. Cecchetti et al., Bioorg. Med. Chem. (1994), 2, 799-806 r) T. Eicher et al., The Chemistry of Heterocycles, (1995) p.149-155, Feorg Thieme Verlar, Stuttgart, 1995, ISBN 313-100511-4, та наведені посилки уній h) Gilchrist, T.L., Heterocyclic Chemistry, 3th Ed. 1997, p.319-327, Longman, UK, ISBN 0-582-278430]. Альфагалокетони можна одержувати галогенуванням відповідного кетону. Реакція альфагалокарбонільних сполук з тіоамідом дає широкий спектр похідних тіазолу. Зокрема, конденсація альфа-бромкетонів з етилтіоксаматом дає (2етоксікарбоніл)тіазоли загальної формули (II). Сполуки формули (II) можна перетворювати на відповідний N-метокси-N-метиламід (III), а потім обробляти алкіллітієвим або ариллітієвим реагентом з одержанням сполуки загальної формули (І), де X представляє підгрупу (і). 12 Сполуки загальної формули (II) можна амідувати аміном загальної формули R3R4NH у сполуку загальної формули (І), де X представляє підгрупу (іі). Таке амідування можна каталізувати (СН3)3 АІ. (Більш детально про конверсію ефірів у аміди за допомогою алюмінію [див.: J. І. Levin, E. Turos, S. M. Weinreb, Synth. Соmmun. (1982), 12, 989-993].) Або ж сполуку формули (II) перетворюють на відповідну карбонову кислоту, а далі обробляють так званим галогенуючим агентом, наприклад, тіонилхлоридом (SOCl2). Ця реакція дає відповідний карбонілхлорид, який далі вступає до реакції зі сполукою формули R3R4NH, де R3 та R4 мають вищенаведені значення. Також можна ефірну груп у в (II) перетворити на відповідну карбонову кислоту. Вона вступає до реакції зі сполукою формули R3R4NH, де R3 та R4 мають вищенаведені значення, за допомогою способів активації та сполучення, наприклад, утворення активного ефіру або у присутності так званого сполучувального реагента, наприклад, DCC, HBTU, HOAT (N-гідрокси-7-азабензотриазолу), BOP, CIP (2-хлор-1,3-діметилімідазоліній гексафторфосфату), PyAOP (7-азабензотриазол-1ілоксітрис(піролідин)фосфоній гексафторфосфату) та подібних. (Більш детально про методи активації та сполучення [див. a) M. Bodanszky, A. Bodanszky: The Practice of Peptide Synthesis, Sprinrer-Verlar, New York, 1994; ISBN: 0-387-57505-7; b) K. Akaji et al, Tetrahedron Lett. (1994), 35, 3315-3318; c) F. Albericio et al., Tetrahedron Lett. (1997), 38,48534856]). Згідно з цими методиками можна одержувати наступні сполуки. Приклади лише докладніше ілюструють винахід і ніяким чином не обмежують його обсяг. Приклади синтезу 1 H ЯМР спектри визначають на приладі Varian UN400 (400МГц) з тетраметилсиланом у якості внутрішнього еталона. Хімічні зсуви наведені у ч. на млн. (шкала δ) у бік слабкого поля від тетраметилсилану. Константи взаємодії (J) виражені у Гц. Тонкошарову хроматографію виконують на пластинах Merck з покриттям 60 F254, а плями висвічують УФ світлом. Випарювальну хроматографію виконують з силікагелем 60 (0.040-0.063мм, Merck). Колонкову хроматографію виконують з силікагелем 60 (0.063-0.200мм, Merck). Точки топлення фіксують на пристрої для визначення точок топлення Büchi B-545 без наступного коригування. Приклад 1 Частина А: До розчину 1-(2,4-діхлорфеніл)-2фенілетанону (54.35г, 0.205молів) у бензолі (220мл) повільно додають бром (10.6мл, 0.205молів) і одержаний розчин перемішують при кімнатній температурі 1 годину. Повільно додають водний розчин (5%) NaHCO3. Органічну фаз у відокремлюють, сушать над MgSО 4, фільтрують та випарюють у вакуумі, одержуючи сирий 2-бром-1(2,4-діхлорфеніл)-2-фенілетанон (69.4г, 98% вихід) у вигляді олії. 1Н-ЯМР (400МГц, CDCl3): δ 6.20 (s, 1H), 7.26 (dd, J=8 та 2Гц, 1H), 7.31-7.50 (m, 7H). Частина В; 2-бром-1-(2,4-діхлорфеніл)-2фенілетанон (25.83г, 0.075молів) та етилтіооксамат (15.0г, 0.112молів) розчиняють в абсолютному 13 83862 спирті (200мл). Одержану суміш нагрівають зі зворотним холодильником 16 годин. Після випарювання у вакуумі сирий матеріал розчиняють у суміші води з діхлорметаном. Діхлорметанову фазу відокремлюють, а водну тричі екстрагують діхлорметаном. Змішані органічні фази сушать (MgSO4), фільтрують та концентрують. Одержаний матеріал очищують колонковою хроматографією (силікагель/діхлорметан) одержуючи етил-4-(2,4діхлорфеніл)-5-фенілтіазол-2-карбоксилат (10.5г, 37% вихід). 1Н-Я МР (400МГц, CDCl3): δ 1.46 (t, J=7Гц, 3Н), 4.53 (q, J=7Гц, 2H), 7.24-7.38 (m, 7H), 7.43 (d, J=2Гц, 1H). Частина С: До розчину етил-4-(2,4діхлорфеніл)-5-фенілтіазол-2-карбоксилату (10.5г, 0.028молів) у метанолі (170мл) повільно додають розчин KOH (8.9г, 0.0896молів) у воді (170мл). Одержаний розчин нагрівають при 90°C 2 години та охолоджують до кімнатної температури. Додають суміш концентрованої HCl з кригою. Утворений осад збирають, промивають водою та діетилетером і сушать, одержуючи 4-(2,4-діхлорфеніл)-5фенілтіазол-2-карбонову кислоту (8.99г, 92% вихід). Точка топлення: 105°C. Частина D: До суспензії 4-(2,4-діхлорфеніл)-5фенілтіазол-2-карбонової кислоти (4.2г, 0.012молів) у безводному діхлорметані (170мл) послідовно додають при магнітному перемішуванні 7-аза-1-гідроксибензотриазол (HOAT) (4.083г, 0.030молів), 7-азабензотриазол-1ілоксітрис(піролідин)фосфоній гексафторфорсфат (PyAOP) (15.64г, 0.03молів), діізопропилетиламін (6.26мл, 0.036молів) та N-метокси-N-метиламін. НСІ (2.925г, 0.030молів), одержаний розчин перемішують протягом 16 годин при кімнатній температурі. Повільно додають 5% водний розчин NaHCO3, одержану суміш тричі екстрагують ді хлорметаном. Зібрані органічні фази сушать (MgSO4), фільтрують та концентрують, одержуючи сиру олію (18.9г). Очистка випарювальною хроматографією (силікагель/етилацетат/петролейний етер =1/1) дає N-метил-N-метокси-4-(2,4-діхлорфеніл)5-фенілтіазол-2-карбоксамід (4.0г, 85% вихід). 1HЯMP (400МГц, CDCl3): δ 3.60 (br s, 3H), 3.90 (s, 3H), 7.21-7.33 (m, 7H), 7.45 (d, J=2Гц, 1H). Подібним чином одержують: N-метил-Nметокси-4-(2-хлорфеніл)-5-фенілтіазол-2карбоксамід. 1Н-ЯМР (400МГц, CDCl3): δ 3.62 (br s, 3H), 3.90 (s, 3H), 7.22-7.45 (m, 9H). Частина E: До охолодженого (-70°C) та перемішаного розчину N-метил-N-метокси-4-(2,4діхлорфеніл)-5-фенілтіазол-2-карбоксаміду (2.0г, 0.005молів) у ТГФ (20мл) в атмосфері N2 додають n-BuLi (3.13мл, розчин 1.6M у гексані, 0.005молів). Після 30 хвилин перемішування розчину дають нагрітися до кімнатої температури та перемішують протягом 16 годин. Додають водний розчин HCl (20мл, 1N), одержану суміш екстрагують діетилетером. Діетилетерні фази двічі промивають водою, сушать (MgSO4), фільтрують та концентрують, одержуючи сиру олію (2.03г). Очистка випарювальною хроматографією (силікагель/діхлорметан) дає 1-[4-(2,4-діхлорфеніл)-5-фенілтіазол-2іл]пентан-1-он (0.6г, 31% вихід). 1Н-ЯМР (400МГц, CDCl3): δ 0.95 (t, J=7Гц, 3H), 1.38-1.48 (m, 2H), 14 1.72-1.80 (m, 2H), 3.16 (t, J~7Гц, 2Н), 7.20-7.35 (m, 7H), 7.46 (d, J=2Гц, 1H). Подібним чином одержують: Приклад 2:1H-ЯMP (400МГц, CDCl3): δ 0.93 (t, J=7Гц, 3Н), 1.26-1.44 (m, 6H), 1.73-1.82 (m, 2H), 3.15 (t, J~7Гц, 2H), 7.21-7.34 (m, 7H), 7.47 (d, J=2Гц, 1H). Приклад 3: Точка топлення: 78-80°C. Приклад 4: 1Н-ЯМР (400МГц, CDCl3): δ 0.93 (t, J=7Гц, 3Н), 1.25-1.44 (m, 6H), 1.73-1.82 (m, 2H), 3.17 (t, J~7Гц, 2H), 7.22-7.40 (m, 8H), 7.47 (dd, J=8 та 2Гц, 1H). Приклад 5: Точка топлення: 131-132°C. Приклад 6 Частина А: До розчину of 1-фенілгептан-1-ону (23.7г, 0.125молів) у бензолі (160мл) повільно до 15 83862 дають при магнітному перемішуванні бром (7.0мл, 0.125молів) і одержаний розчин витримують при кімнатній температурі 1 годину. Повільно додають водний розчин (5%) NaHCO3 і потім діхлорметан. Органічну фазу відокремлюють, сушать над MgSO4 , фільтрують та випарюють у вакуумі, одержуючи сирий 2-бром-1-фенілгептан-1-он (41.8г, 100% вихід) у вигляді олії. 1Н-ЯМР (400МГц, CDCl3): δ 0.90 (t, J=7Гц, 3Н), 1.28-1.78 (m, 6H), 2.04-2.25 (m, 2H), 5.11-5.16 (m, 1H), 7.42-7.62 (m, 3H), 8.00-8.04 (m, 2H). Частина В; 2-бром-1-фенілгептан-1-он (20.17г, 0.075молів) та етилтіооксамат (15.0г, 0.112молів) розчиняють в абсолютному етанолі (200мл). Одержану суміш нагрівають зі зворотним холодильником 16 годин. Після випарювання у вакуумі сирий матеріал розчиняють у суміші води з діхлорметаном. Діхлорметанову фаз у відокремлюють, а водну фазу тричі екстрагують діхлорметаном. Зібрані органічні фази сушать (MgSC4), фільтрують та концентрують. Одержаний матеріал очищують колонковою хроматографією (силікагель/діхлорметан/петролейний етер =1/1), одержуючи етил-5-(n-пентил)-4-фенілтіазол-2карбоксилат (12.09г, 53% вихід) у вигляді олії, яка повільно твердне. Точка топлення: 51-52°C. Частина C: До розчину етил-5-(n-пентил-4фенілтіазол-2-карбоксилату (12.09г, 0.039молів) у метанолі (240мл) повільно додають при магнітному перемішуванні розчин KOH (8.9 г) у воді (240мл). Одержаний розчин нагрівають зі зворотним холодильником 2 години, після чого охолоджують до кімнатної температури. Додають суміш концентрованої HCl з кригою. Утворений осад збирають, послідовно промивають водою та холодним діетилетером і сушать, одержуючи 5-(nпентил)-4-фенілтіазол-2-карбонову кислоту (3.54г, 32% вихід). 1Н-Я МР (400МГц, CDCl3): δ 0.87 (t, J=7Гц, 3Н), 1.28-1.40 (m, 4H), 1.66-1.76 (m, 2H), 2.93-3.00 (m, 2H), 4.00 (br s, 1H), 7.35-7.46 (m, 3H), 7.58-7.64 (m, 2H). Частина D: До суспензії 5-(n-пентил)-4фенілтіазол-2-карбонової кислоти (1.18г, 0.0043молів) у безводному діхлорметані (35мл) послідовно додають при магнітному перемішуванні 7-аза-1-гідроксибензотриазол (HOAT) (1.46г, 0.0107молів), 7-азабензотриазол-1ілоксітрис(піролідин)фосфоній гексафторфосфат (PyAOP) (5.59г, 0.0107молів), діізопропилетиламін (2.24мл, 0.0129молів) та анілін (0.98мл, 0.0107молів); одержаний розчин перемішують протягом 16 годин при кімнатній температурі. Одержану суміш концентрують та очищують випарювальною хроматографією (силікагель/діхлорметан), одержуючи N-феніл-5-(nпентил)-4-фенілтіазол-2-карбоксамід (0.89г, 59% вихід). 1Н-ЯМР (400МГц, CDCl3): δ 0.98 (t, J=7Гц, 3Н), 1.26-1.41 (m, 4H), 1.68-1.78 (m, 2H), 2.97 (t, J=7Гц, 2Н), 7.12-7.18 (m, 1H), 7.34-7.52 (m, 5H), 7.60-7.64 (m, 2H), 7.69-7.74 (m, 2H), 9.10 (br s 1H). 16 Подібним чином одержують: із 5-(n-пентил)-4-фенілтіазол-2-карбонової кислоти та 1-амінадамантану. Приклад 7: Точка топлення: 90-92°C. із 5-(n-пентил)-4-фенілтіазол-2-карбонової кислоти та цис-міртаниламіну (CAS 38235-68-6) Приклад 8: 1Н-ЯМР (400МГц, CDCl3): δ 0.89 (t, J=7Гц, 3Н), 1.08 (s, 3H), 1.20 (s, 3Н), 1.26-1.38 (m, 4H), 1.50-1.62 (m, 1H), 1.66-1.74 (m, 2H), 1.82-2.04 (m, 5H), 2.28-2.40 (m, 2H), 2.94 (t, J=7Гц, 2Н), 3.393.50 (m, 2H), 7.29 (br t, J=7Гц, 1H), 7.37-7.60 (m, 5H). Приклад 9 Частина А: 1-Бром-1-фенілгептан-2-он (19.98г, 0.074молів) та етилтіооксамат (15.0г, 0.112молів) розчиняють в абсолютному етанолі (200мл). Одержану суміш нагрівають зі зворотним холодильником 2 години. Після випарювання у вакуумі сирий матеріал розчиняють у суміші води з діхлорметаном. Діхлорметанову фаз у відокремлюють, а водну фазу тричі екстрагують діхлорметаном. Зібрані органічні фази сушать (MgSO4), фільтрують та концентрують. Одержаний матеріал очищують колонковою хроматографією (силікагель/діхлорметан/петролейний етер =1/1), одержуючи етил-4-(n-пентил)-5-фенілтіазол-2карбоксилат (5.24г, 23% вихід) у вигляді олії. 1НЯМР (400МГц, CDCl3): δ 0.89 (t, J=7Гц, 3Н), 1.241.32 (m, 4H), 1.44 (t, J=7Гц, 3Н), 1.70-1.78 (m, 2H), 2.81-2.87 (m, 2H), 4.48 (q, J=7Гц, 2Н), 7.40-7.48 (m, 5H). Подібним чином одержують: Етил-4-бензил-5-фенілтіазол-2-карбоксилат у вигляді олії. Етил-5-(n-пентил)-4-(2,4-діхлорфеніл)тіазол-2карбоксилат. Точка топлення: 92-93°C. Частина В: До розчину 1-амінадамантану (1.607г, 0.0086молів) у безводному діхлорметані (10мл) додають при магнітному перемішуванні 17 83862 розчин Аl(СН3)3 (4.3мл, 2М у гексані, 0.0086молів), одержаний розчин витримують при кімнатній температурі 10 хвилин. Повільно додають водний розчин (5%) NaHCO3. Екстрагують діхлорметаном, сушать над MgSO4, фільтрують та концентрують у вакуумі, після чого колонковою хроматографією (силікагель/діхлорметан) одержують N-(адамант-1ил)-4-(n-пентил)-5-фенілтіазол-2-карбоксамід (1.17г, 72% вихід). 1Н-ЯМР (400МГц, CDCl3): δ 0.88 (t, J=7Гц, 3H), 1.26-1.34 (m, 4H), 1.68-1.78 (m, 8H), 2.08-2.18 (m, 9H), 2.71-2.76 (m, 2H), 7.02 (br s, 1H), 7.36-7.45 (m, 5H). Подібним чином одержують: з етил-4-(n-пентил-5-фенілтіазол-2карбоксилату та цис-міртаниламіну (CAS 3823568-6) Приклад 10:1H-ЯMP (400МГц, CDCl3): δ 0.89 (t, J=7Гц, 3H), 1.10 (s, 3H), 1.22 (s, 3H), 1.25-1.34 (m, 4H), 1.54-1.78 (m, 3H), 1.84-2.06 (m, 5H), 2.31-2.42 (m, 2H), 2.72-2.78 (m, 2H), 3.44-3.50 (m, 2H), 7.247.28 (m, 1H), 7.37-7.46 (m, 5H). з етил-4-(n-пентил)-5-фенілтіазол-2карбоксилату та циклогексиламіну Приклад 11: Точка топлення: 84-85°C. з етил-5-(n-пентил)-4-фенілтіазол-2карбоксилату та екзо-2-амін-біцикло[2.2.1]гептану Приклад 12: Точка топлення: 64-65°C. 18 з етил-5-(n-пентил-4-фенілтіазол-2карбоксилату та ендо-2-амін-біцикло[2.2.1]гептану Приклад 13: Точка топлення: 80-82°C. з етил 5-(n-пентил)-4-фенілтіазол-2карбоксилату та 4-ізопропилпіперазину Приклад 14: Точка топлення: 84-85°C. з етил-5-(n-пентил)-4-фенілтіазол-2карбоксилату та індан-2-іламіну Приклад 15: 1Н-ЯМР (400МГц, CDCl3): δ 0.85 (t, J=7Гц, 3Н), 1.26-1.38 (m, 4H), 1.65-1.75 (m, 2H), 2.90-3.01 (m, 4H), 3.36-3.44 (m, 2H), 4.86-4.96 (m, 1H), 7.15-7.27 (m, 4H), 7.35-7.47 (m, 4H), 7.52-7.56 (m, 2H). з етил-5-(n-пентил)-4-фенілтіазол-2карбоксилату та 3-амін-3-аза-біцикло[3.3.0]октану Приклад 16: Точка топлення: 86-87°C. з етил-5-(n-пентил)-4-фенілтіазол-2карбоксилату та 1,2,3,4-те трагідроізохіноліну. Приклад 17: Точка топлення: 50-51°C. 19 83862 з етил-5-(n-пентил)-4-фенілтіазол-2карбоксилату та R-(+)-борніламіну (CAS 32511-345). Приклад 18: 1Н-ЯМР (400МГц, CDCl3): δ 0.901.02 (m, 13Н), 1.22-1.47 (m, 6H), 1.60-1.84 (m, 5Н), 2.36-2.45 (m, 1H), 2.94 (t, J=7Гц, 2Н), 4.36-4.44 (m, 1H), 7.32 (br d, J=7Гц, 1H), 7.38-7.50 (m, 3H), 7.587.63 (m, 2Н). з етил-4-бензил-5-фенілтіазол-2-карбоксилату та циклогексиламіну Приклад 19: Точка топлення: 104-106°C. з етил-5-(n-пентил)-4-(2,4-діхлорфеніл)тіазол2-карбоксилату та циклогексиламіну Приклад 20: 1Н-ЯМР (400МГц, CDCl3): δ 0.85 (t, J=7Гц, 3Н), 1.13-1.46 (m, 8H), 1.55-1.68 (m, 4H), 1.71-1.80 (m, 2H), 1.96-2.06 (m, 2H), 2.67 (t, J=7Гц, 2Н), 3.86-3.98 (m, 1H), 7.05 (br d, J=7Гц, 1H), 7.267.37 (m, 2H), 7.53 (d, J=2Гц, 1H). з етил-5-(n-пентил)-4-(2,4-діхлорфеніл)тіазол2-карбоксилату та циклопентил аміну Приклад 21: 1Н-ЯМР (400МГц, CDCl3): δ 0.85 (t, J=7Гц, 3Н), 1.20-1.30 (m, 4H), 1.48-1.77 (m, 8H), 2.01-2.10 (m, 2H), 2.67 (t, J=7Гц, 2H), 4.31-4.41 (m, 1H), 7.09 (br d, J=7Гц, 1H), 7.25-7.37 (m, 2H), 7.53 (d, J=2Гц, 1H). 20 з етил-4-бензил-5-фенілтіазол-2-карбоксилату та n-пентиламіну Приклад 22: 1H-ЯMP (400МГц, CDCl3): δ 0.89 (t, J=7Гц, 3Н), 1.33-1.40 (m, 4H), 1.59-1.67 (m, 2H), 3.40-3.47 (m, 2H), 4.16 (s, 2H), 7.15-7.32 (m, 6H), 7.39-7.42 (m, 5Н). з етил-5-(n-пентил)-4-(2,4-діхлорфеніл)тіазол2-карбоксилату та 1-амінпіперидину Приклад 23:1H-Я-MP (400МГц, CDCl3): δ 0.85 (t, J=7Гц, 3Н), 1.20-1.28 (m, 4H), 1.39-1.46 (m, 2H), 1.56-1.64 (m, 2H), 1.71-1.79 (m, 4H), 2.66 (t, J=7Гц, 2Н), 2.82-2.88 (m, 4H), 7.29 (d, J=8Гц, 1H), 7.35 (dd, J=8 та 2Гц, 1H), 7.53 (d, J=2Гц, 1H), 7.88 (br s, 1H). з етил-5-(n-пентил)-4-(2,4-діхлорфеніл)тіазол2-карбоксилату та 4-амінморфоліну Приклад 24: 1Н-ЯМР (400МГц, CDCl3): δ 0.85 (t, J=7Гц, 3Н), 1.21-1.29 (m, 4H), і 1.57-1.66 (m, 2H), 2.67 (t, J=7Гц, 2Н), 2.93-2.98 (m, 4H), 3.82-3.88 (m, 4H), 7.29 (d, J=8Гц, 1H), 7.35 (dd, J=8 та 2Гц, 1H), 7.54 (d, J=2Гц, 1H), 7.95 (br s, 1H). з етил-5-(n-пентил)-4-(2,4-діхлорфеніл)тіазол2-карбоксилату та N-метиланіліну Приклад 25: 1Н-ЯМР (400МГц, CDCl3): δ 0.80 (br t, J=7Гц, 3Н), 1.14-1.28 (m, 4Н), 1.50-1.62 (m, 2H), 2.56-2.66 (m, 2Н), 3.56 (br s, 3H), 6.80-7.45 (m, 8Н). 21 83862 22 Результати фармакологічних досліджень Дані щодо спорідненості до рецепторів канабіноїдів одержують за вищенаведеними методиками, результати яких представлені нижче у таблиці. Таблиця Сполука Приклад 1 Приклад 4 Приклад 7 Приклад 8 Приклад 9 Приклад 10 Приклад 11 Комп’ютерна в ерстка Т. Чепелев а Спорідненість до рецептора Людського СВ1 Людського СВ2 Значення рКі Значення рКі 6.6 6.8 7.3 6.8 7.8 8.1 6.9 8.1 6.6 7.7 Підписне Тираж 28 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюThiazole derivatives as cannabinoid receptor modulators
Автори англійськоюLange Josephus H. M., Kruse Cornelis G., van Stuivenberg Herman H., Sliedregt Leonardus A. J. M.
Назва патенту російськоюПроизводные тиазола как модуляторы рецепторов канабиноидов
Автори російськоюЛанге Йозефус Г.М., Крузе Корнелис Г., ван Стёйвенберг Герман Г., Слідрегт Леонардус А.Й.М..
МПК / Мітки
МПК: A61K 31/4439, C07D 417/04, C07D 277/56, A61K 31/426, C07D 417/14, C07D 417/12, A61P 25/00, C07D 277/24
Мітки: тіазолу, модулятори, канабіноїдів, рецепторів, похідні
Код посилання
<a href="https://ua.patents.su/11-83862-pokhidni-tiazolu-yak-modulyatori-receptoriv-kanabinodiv.html" target="_blank" rel="follow" title="База патентів України">Похідні тіазолу як модулятори рецепторів канабіноїдів</a>
Попередній патент: Спосіб регулювання параметрів кутового руху ракети-носія космічного апарата
Наступний патент: Спосіб відображення інформації на холестеричному рідкокристалічному дисплеї та рідкокристалічний дисплей
Випадковий патент: Двох'ярусний радіальний підшипник












