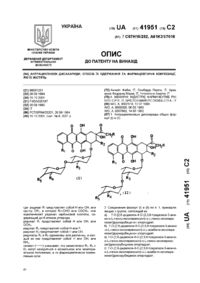
Фармацевтичні композиції, що містять похідні 3-аміноазетидину, похідні і спосіб їхнього одержання
Номер патенту: 72319
Опубліковано: 15.02.2005
Автори: Грізоні Серж, Міерс Мішель, Філош Бруно, Боушард Херве, Ашард Даніель, Букерель Жан, Хіттінгер Огюстін
Формула / Реферат
1. Фармацевтична композиція, що містить як активний інгредієнт сполуку формули:
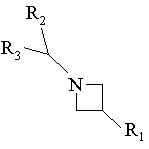 , (І)
, (І)
у якій
R1 означає радикал –NНСОR4 або -N(R5)-Y-R6,
Υ означає CO або SO2,
R2 і R3, однакові або різні, означають або ароматичний радикал, вибраний з фенілу, нафтилу і інденілу, що можуть бути незаміщеними або заміщеними одним або декількома замісниками: галоген, алкіл, алкокси, форміл, гідрокси, трифторметил, трифторметокси, -CO-alk, ціано, -СООН, -COOalk, -CONR7R8, -CO-NH-NR9R10, алкілсульфаніл, алкілсульфініл, алкілсульфоніл, алкілсульфанілалкіл, алкілсульфінілалкіл, алкілсульфонілалкіл, гідроксіалкіл або -alk-NR7R8; або гетероароматичний радикал, вибраний з циклів: бензофурил, бензотіазоліл, бензотієніл, бензоксазоліл, хроманіл, 2,3-дигідробензофурил, 2,3-дигідробензотієніл, піримідиніл, фурил, імідазоліл, ізохроманіл, ізохіноліл, піроліл, піридил, хіноліл, 1,2,3,4-тетрагідроізохіноліл, тіазоліл і тієніл, що можуть бути незаміщеними або заміщеними галогеном, алкілом, алкоксилом, гідроксилом, трифторметилом, трифторметоксилом, ціано, -СООН, -COOalk, -CO-NH-NR9R10, -CONR7R8, -alk-NR9R10, алкілсульфанілом, алкілсульфінілом, алкілсульфонілом, алкілсульфанілалкілом, алкілсульфінілалкілом, алкілсульфонілалкілом або гідроксіалкілом;
R4 означає радикал alk-SO2-R11, alk-SO2-CH=CH-R11, Het, заміщений групою –SO2-R11, або феніл, заміщений групою –SO2-R11 або -alk-SO2-R11;
R5 означає атом водню або радикал алкіл;
R6 означає радикал фенілалкіл, Het або Аr;
R7 i R8, однакові або різні, означають атом водню або радикал алкіл, або R7 і R8, разом з атомом азоту, з яким вони з'єднані, утворюють насичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що може містити другий гетероатом, вибраний з кисню, сірки й азоту, і бути заміщеним одним або декількома алкілами;
R9 і R10, однакові або різні, означають атом водню або радикал алкіл, -COOalk, циклоалкіл, алкілциклоалкіл, -alk-O-alk або гідроксіалкіл, або R9 і R10, разом з атомом азоту, з яким вони з'єднані, утворюють насичений або ненасичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що може містити другий гетероатом, вибраний з кисню, сірки й азоту, і бути заміщеним одним або декількома радикалами: алкіл, -COalk, -COOalk, -CO-NHalk, -CS-NHalk, оксо, гідроксіалкіл, -alk-O-alk або -CO-NH2;
R11 означає радикал алкіл, Аr або Het;
Аr означає радикал феніл, нафтил або інденіл, що можуть бути заміщені одним або декількома замісниками: галоген, алкіл, алкокси, ціано, -CO-alk, -COOH, -COOalk, -CONR12R13, -CO-NH-NR14R15, алкілсульфаніл, алкілсульфініл, алкілсульфоніл, alk-NR14R15, -NR14R15 алкілтіоалкіл, форміл, гідрокси, гідроксіалкіл, Неt, -O-alk-NH-циклоалкіл, OCF3, CF3, -NH-CO-alk, -SO2NH2, -NH-СОСН3, -NH-COOalk, Het, або по двох суміжних атомах вуглецю, зв'язаних діоксиметиленом;
Het означає ненасичений або насичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що містять один або декілька гетероатомів, вибраних з кисню, сірки й азоту, і який може бути заміщений одним або декількома радикалами: алкіл, алкокси, вініл, галоген, алкоксикарбоніл, оксо, гідрокси, OCF3 або СF3, причому азотвмісні гетероцикли можуть бути у формі N-оксидів;
R12 і R13 однакові або різні, означають атом водню або радикал алкіл, або R12 і R13, разом з атомом азоту, з яким вони з'єднані, утворюють насичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що може містити другий гетероатом, вибраний з кисню, сірки й азоту, і бути заміщеним одним або декількома алкільними радикалами;
R14 і R15, однакові або різні, означають атом водню або радикал алкіл, -COOalk, циклоалкіл, алкілциклоалкіл, -alk-O-alk або гідроксіалкіл, або R14 і R15, разом з атомом азоту, з яким вони з'єднані, утворюють насичений або ненасичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що може містити другий гетероатом, вибраний з кисню, сірки й азоту, і бути заміщеним одним або декількома радикалами: алкіл, -COalk, -COOalk, -CO-NHalk, -CS-NHalk, оксо, гідроксіалкіл, -alk-O-alk або -CO-NH2;
alk означає радикал алкіл або алкілен,
причому алкільні або алкіленові радикали і частини молекул або алкоксильні радикали і частини молекул знаходяться в прямому або розгалуженому ланцюзі і містять від 1 до 6 атомів вуглецю, а циклоалкільні радикали містять від 3 до 10 атомів вуглецю,
оптичний ізомер такої сполуки або одну з її фармацевтично прийнятних солей.
2. Фармацевтична композиція за п.1, у якій в сполуці формули І:
Het вибрано із бензімідазолу, бензоксазолу, бензотіазолу, бензотіофену, циноліну, тіофену, хіназоліну, хіноксаліну, хіноліну, піразолу, піролу, піридину, імідазолу, індолу, ізохіноліну, піримідину, тіазолу, тіадіазолу, піперидину, піперазину, піролідину, триазолу, фурану, тетрагідроізохіноліну і тетрагідрохіноліну, що можуть бути заміщені одним або декількома замісниками: алкіл, алкокси, вініл, галоген, алкоксикарбоніл, оксо, гідрокси, ОСF3 або СF3.
3. Фармацевтична композиція, за п.1, що містить як активний початок щонайменше одну сполуку формули І, у якій:
R1 означає радикал -N(R5)-Y-R6,
Υ означає SO2,
R2 означає або феніл, незаміщений або заміщений одним або декількома замісниками: галоген, алкіл, алкокси, трифторметил, трифторметокси, ціано, -CONR7R8, гідроксіалкіл або -alk-NR7R8, або гетероароматичний радикал, вибраний з циклів: піридил, піримідиніл, тіазоліл і тієніл, що можуть бути незаміщеними або заміщеними галогеном, алкілом, алкокси, гідрокси, трифторметилом, трифторметокси, -CONR7R8, -alk-NR9R10, алкілсульфанілом, алкілсульфінілом, алкілсульфонілом або гідроксіалкілом;
R3 означає або феніл, незаміщений або заміщений одним або декількома замісниками: галоген, алкіл, алкокси, трифторметил, трифторметокси, ціано, -CONR7R8, гідроксіалкіл, -alk-NR7R8, або гетероароматичний радикал, вибраний з циклів: піридил, піримідиніл, тіазоліл і тієніл, що можуть бути незаміщеними або заміщеними галогеном, алкілом, алкокси, гідрокси, трифторметилом, трифторметокси, -CONR7R8, -alk-NR9R10, алкілсульфанілом, алкілсульфінілом, алкілсульфонілом або гідроксіалкілом;
R5 означає атом водню або алкіл;
R6 означає радикал нафтил, фенілалкіл, Het або феніл, що може бути заміщений одним або декількома замісниками: галоген, алкіл, алкокси, ціано, -CO-alk, -COOalk, -CONR12R13 -alk-NR14R15, -NR14R15, гідрокси, гідроксіалкіл, Het, ОСF3, СF3, -NH-CO-alk, -SO2NH2, -NH-COOalk, або по двох атомах вуглецю, зв'язаних діоксиметиленом;
R7 і R8, однакові або різні, означають атом водню або радикал алкіл, або R7 і R8, разом з атомом азоту, з яким вони з'єднані, утворюють насичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що може містити другий гетероатом, вибраний з кисню, сірки й азоту, і бути заміщеним одним або декількома алкілами;
R9 і R10, однакові або різні, означають атом водню або радикал алкіл, циклоалкіл, алкілциклоалкіл або гідроксіалкіл, або R9 і R10, разом з атомом азоту, з яким вони з'єднані, утворюють насичений або ненасичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що може містити другий гетероатом, вибраний з кисню, сірки й азоту, і бути заміщеним одним або декількома радикалами: алкіл, оксо або -CO-NH2;
R12 і R13, однакові або різні, означають атом водню або радикал алкіл, або R12 і R13, разом з атомом азоту, з яким вони з'єднані, утворюють насичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що може містити другий гетероатом, вибраний з кисню, сірки й азоту, і бути заміщеним одним або декількома алкільними радикалами;
R14 і R15, однакові або різні, означають атом водню або радикал алкіл, циклоалкіл, алкілциклоалкіл або гідроксіалкіл, або R14 і R15, разом з атомом азоту, з яким вони з'єднані, утворюють насичений або ненасичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що може містити другий гетероатом, вибраний з кисню, сірки й азоту, і бути заміщеним одним або декількома радикалами алкіл, оксо, гідроксіалкіл або -CO-NH2;
Het означає ненасичений або насичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що містить один або декілька гетероатомів, вибраних з кисню, сірки й азоту, і який може бути заміщений одним або декількома радикалами: алкіл, алкокси, вініл, галоген, алкоксикарбоніл, оксо, гідрокси, причому азотвмісні гетероцикли можуть бути у формі N-оксидів, і, переважно, Het означає гетероцикл, вибраний з наступних гетероциклів: бензімідазол, бензоксазол, бензотіазол, бензотіофен, тіофен, хіназолін, хіноксалін, хінолін, пірол, піридин, імідазол, індол, ізохінолін, піримідин, тіазол, тіадіазол, фуран, тетрагідроізохінолін і тетрагідрохінолін, що можуть бути заміщені одним або декількома замісниками: алкіл, алкокси, вініл, галоген, оксо, гідрокси, ОСF3 або СF3,
оптичний ізомер такої сполуки або одну з її фармацевтично прийнятних солей.
4. Фармацевтична композиція, за п.1, що містить як активний початок щонайменше одну сполуку формули І, у якій:
R1 означає радикал -N(R5)-Y-R6,
Υ означає SO2,
R2 означає або феніл, незаміщений або заміщений одним або декількома замісниками: галоген, алкіл, алкокси, трифторметил, трифторметокси або гідроксіалкіл, або гетероароматичний радикал, вибраний з циклів: піридил і піриміділ, що можуть бути незаміщеними або заміщеними галогеном, алкілом, алкокси, гідрокси, трифторметилом або трифторметокси;
R3 означає або феніл, незаміщений або заміщений одним або декількома замісниками: галоген, алкіл, алкокси, трифторметил, трифторметокси, гідроксіалкіл, або гетероароматичний радикал, вибраний з циклів: піридил і піриміділ, що можуть бути незаміщеними або заміщеними галогеном, алкілом, алкокси, гідрокси, трифторметилом, трифторметокси;
R5 означає атом водню або алкіл;
R6 означає радикал нафтил, фенілалкіл, Het або феніл, що може бути заміщений одним або декількома замісниками: галоген, алкіл, алкокси, -NR14R15, гідрокси, гідроксіалкіл, OCF3, CF3 або –SO2NH2, або ж по двох атомах вуглецю, зв'язаних діоксиметиленом;
R14 і R15, однакові або різні, означають атом водню або радикал алкіл, циклоалкіл, алкілциклоалкіл або гідроксіалкіл, або R14 і R15, разом з атомом азоту, з яким вони з'єднані, утворюють насичений або ненасичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що може містити другий гетероатом, вибраний з кисню, сірки й азоту, і бути заміщеним одним або декількома радикалами алкіл, оксо, гідроксіалкіл або -CO-NH2;
Het означає ненасичений або насичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що містить один або декілька гетероатомів, вибраних з кисню, сірки й азоту, і який може бути заміщений одним або декількома радикалами: алкіл, алкокси, вініл, галоген, алкоксикарбоніл, оксо, гідрокси, причому азотвмісні гетероцикли можуть бути у формі N-оксидів, і, переважно, Het означає гетероцикл, вибраний з наступних гетероциклів: бензімідазол, бензоксазол, бензотіазол, бензотіофен, тіофен, хінолін, пірол, піридин, піримідин, тіазол, тіадіазол, фуран, тетрагідроізохінолін і тетрагідрохінолін, що можуть бути заміщені одним або декількома замісниками: алкіл, алкокси, вініл, галоген, оксо, гідрокси, ОСF3 або СF3,
оптичний ізомер такої сполуки або одну з її фармацевтично прийнятних солей.
5. Похідні 3-аміноазетидину формули І:
 , (І)
, (І)
у якій
R1 означає радикал –NHCOR4 або -N(R5)-Y-R6,
Υ означає CO або SO2,
R2 і R3, однакові або різні, означають або ароматичний радикал, вибраний з фенілу, нафтилу і інденілу, що можуть бути незаміщеними або заміщеними одним або декількома замісниками: галоген, алкіл, алкокси, форміл, гідрокси, трифторметил, трифторметокси, -CO-alk, ціано, -СООН, -COOalk, -CONR7R8, -CO-NH-NR9R10, алкілсульфаніл, алкілсульфініл, алкілсульфоніл, алкілсульфанілалкіл, алкілсульфінілалкіл, алкілсульфонілалкіл, гідроксіалкіл або -alk-NR7R8; або гетероароматичний радикал, вибраний з циклів: бензофурил, бензотіазоліл, бензотієніл, бензоксазоліл, хроманіл, 2,3-дигідробензофурил, 2,3-дигідробензотієніл, піримідиніл, фурил, імідазоліл, ізохроманіл, ізохіноліл, піроліл, піридил, хіноліл, 1,2,3,4-тетрагідроізохіноліл, тіазоліл і тієніл, які можуть бути незаміщеними або заміщеними одним або декількома замісниками: галоген, алкіл, алкокси, гідрокси, трифторметил, трифторметокси, ціано, -СООН, -COOalk, -CO-NH-NR9R10, -CONR7R8, -alk-NR9R10, алкілсульфаніл, алкілсульфініл, алкілсульфоніл, алкілсульфанілалкіл, алкілсульфінілалкіл, алкілсульфонілалкіл або гідроксіалкіл;
R4 означає радикал alk-SO2-R11, alk-SO2-CH=CH-R11, Het, заміщений групою –SO2-R11, або феніл, заміщений групою -SО2-R11 або -alk-SO2-R11;
R5 означає атом водню або радикал алкіл;
R6 означає радикал фенілалкіл, Het або Аr;
R7 і R8, однакові або різні, означають атом водню або радикал алкіл, або R7 і R8, разом з атомом азоту, з яким вони з'єднані, утворюють насичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що може містити другий гетероатом, вибраний з кисню, сірки й азоту, і бути заміщеним одним або декількома алкілами;
R9 і R10, однакові або різні, означають атом водню або радикал алкіл, -COOalk, циклоалкіл, алкілциклоалкіл, -alk-O-alk або гідроксіалкіл, або R9 і R10, разом з атомом азоту, з яким вони з'єднані, утворюють насичений або ненасичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що може містити другий гетероатом, вибраний з кисню, сірки й азоту, і бути
заміщеним одним або декількома радикалами: алкіл, -COalk, -COOalk, -CO-NHalk, -CS-NHalk, оксо, гідроксіалкіл, -alk-O-alk або -CO-NH2;
R11 означає радикал алкіл, Аr або Het;
Аr означає радикал феніл, нафтил або інденіл, що можуть бути заміщені одним або декількома замісниками: галоген, алкіл, алкокси, ціано, -CO-alk, -СООН, -COOalk, -CONR12R13, -CO-NH-NR14R15 алкілсульфаніл, алкілсульфініл, алкілсульфоніл, alk-NR14R15, -NR14R15 алкілтіоалкіл, форміл, гідрокси, гідроксіалкіл, Het, -O-alk-NH-циклоалкіл, ОСF3, СF3, -NH-CO-alk, -SO2NH2, -NH-СОСН3, -NH-COOalk, Het, або двома атомами вуглецю, зв'язаними між собою через діоксиметилен;
Het означає ненасичений або насичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що містить один або декілька гетероатомів, вибраних з кисню, сірки й азоту, і який може бути заміщений одним або декількома радикалами: алкіл, алкокси, вініл, галоген, алкоксикарбоніл, оксо, гідрокси, OCF3 або СF3, причому азотвмісні гетероцикли можуть бути у формі N-оксидів;
R12 і R13, однакові або різні, означають атом водню або радикал алкіл, або R12 i Р13, разом з атомом азоту, з яким вони з'єднані, утворюють насичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що може містити другий гетероатом, вибраний з кисню, сірки й азоту, і бути заміщеним одним або декількома алкільними радикалами;
R14 і R15 однакові або різні, означають атом водню або радикал алкіл, -COOalk, циклоалкіл, алкілциклоалкіл, -alk-O-alk або гідроксіалкіл, або R14 і R15, разом з атомом азоту, з яким вони з'єднані, утворюють насичений або ненасичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що може містити другий гетероатом, вибраний з кисню, сірки й азоту, і бути заміщеним одним або декількома радикалами: алкіл, -COalk, -COOalk, -СО-NHalk, -CS-NHalk, оксо, гідроксіалкіл, -alk-O-alk або -CO-NH2;
alk означає радикал алкіл або алкілен,
причому алкільні або алкіленові радикали і частини молекул або алкоксильні радикали і частини молекул знаходяться в прямому або розгалуженому ланцюзі і містять від 1 до 6 атомів вуглецю, а циклоалкільні радикали містять від 3 до 10 атомів вуглецю,
їхні оптичні ізомери і їх фармацевтичнo прийнятні солі,
за винятком сполуки, у якій R2 і R3 є фенільними радикалами, R1 є радикалом -N(R5)-Y-R6, Y є SO2, R5 є метильним радикалом і R6 - фенільним радикалом.
6. Сполуки формули І за п. 5, у яких Het вибирають з бензімідазолу, бензоксазолу, бензотіазолу, бензотіофену, циноліну, тіофену, хіназоліну, хіноксаліну, хіноліну, піразолу, піролу, піридину, імідазолу, індолу, ізохіноліну, піримідину, тіазолу, тіадіазолу, піперидину, піперазину, піролідину, тіазолу, фурану, тетрагідроізохіноліну і тетрагідрохіноліну, що можуть бути заміщені одним або декількома замісниками: алкіл, алкокси, вініл, галоген, алкоксикарбоніл, оксо, гідрокси, ОСF3 або CF3, R2 і R3 означають фенільні радикали, R1 означає радикал -N(R5)-Y-R6, Y означає SO2, R5 означає метильний радикал і R6 означає фенільний радикал.
7. Сполуки формули І за п. 5, у якій
R1 означає радикал -N(R5)-Y-R6,
Υ означає SO2,
R2 означає або феніл, незаміщений або заміщений одним або декількома замісниками: галоген, алкіл, алкокси, трифторметил, трифторметокси, ціано, -CONR7R8, гідроксіалкіл або -alk-NR7R8, або гетероароматичний радикал, вибраний з циклів: піридил, піримідиніл, тіазоліл і тієніл, що можуть бути незаміщеними або заміщеними галогеном, алкілом, алкокси, гідрокси, трифторметилом, трифторметокси, -CONR7R8, -alk-NR7R10, алкілсульфанілом, алкілсульфінілом, алкілсульфонілом або гідроксіалкілом;
R3 означає або феніл, незаміщений або заміщений одним або декількома замісниками: галоген, алкіл, алкокси, трифторметил, трифторметокси, ціано, -CONR7R8, гідроксіалкіл, -alk-NR7R8, або гетероароматичний радикал, вибраний з циклів: піридил, піримідиніл, тіазоліл і тієніл, що можуть бути незаміщеними або заміщеними галогеном, алкілом, алкокси, гідрокси, трифторметилом, трифторметокси, -CONR7R8, -alk-NR9R10, алкілсульфанілом, алкілсульфінілом, алкілсульфонілом або гідроксіалкілом;
R5 означає атом водню або алкіл;
R6 означає радикал нафтил, фенілалкіл, Het або феніл, що може бути заміщений одним або декількома замісниками: галоген, алкіл, алкокси, ціано, -CO-alk, -COOalk, -CONR12R13, -alk-NR14R15, -NR14R15, гідрокси, гідроксіалкіл, Het, OCF3, CF3, -NH-CO-alk, -SO2NH2, -NH-COOalk, або ж двома атомами вуглецю, зв'язаними між собою через діоксиметилен;
R7 і R8, однакові або різні, означають атом водню або радикал алкіл, або R7 і R8, разом з атомом азоту, з яким вони з'єднані, утворюють насичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що може містити другий гетероатом, вибраний з кисню, сірки й азоту, і бути заміщеним одним або декількома алкілами;
R9 і R10, однакові або різні, означають атом водню або радикал алкіл, циклоалкіл, алкілциклоалкіл або гідроксіалкіл, або R9 і R10, разом з атомом азоту, з яким вони з'єднані, утворюють насичений або ненасичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що може містити другий гетероатом, вибраний з кисню, сірки й азоту, і бути заміщеним одним або декількома радикалами: алкіл, оксо або -CO-NH2;
R12 і R13, однакові або різні, означають атом водню або радикал алкіл, або R12 і R13, разом з атомом азоту, з яким вони з'єднані, утворюють насичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що може містити другий гетероатом, вибраний з кисню, сірки й азоту, і бути заміщеним одним або декількома алкільними радикалами;
R14 і R15, однакові або різні, означають атом водню або радикал алкіл, циклоалкіл, алкілциклоалкіл або гідроксіалкіл, або R14 і R15, разом з атомом азоту, з яким вони з'єднані, утворюють насичений або ненасичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що може містити другий гетероатом, вибраний з кисню, сірки й азоту, і бути заміщеним одним або декількома радикалами алкіл, оксо, гідроксіалкіл або -CO-NH2;
Het означає ненасичений або насичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що містить один або декілька гетероатомів, вибраних з кисню, сірки й азоту, і який може бути заміщений одним або декількома радикалами: алкіл, алкокси, вініл, галоген, алкоксикарбоніл, оксо, гідрокси, причому азотвмісні гетероцикли можуть бути у формі N-оксидів, і, переважно, Het означає гетероцикл, вибраний з наступних гетероциклів: бензімідазол, бензоксазол, бензотіазол, бензотіофен, тіофен, хіназолін, хіноксалін, хінолін, пірол, піридин, імідазол, індол, ізохінолін, піримідин, тіазол, тіадіазол, фуран, тетрагідроізохінолін і тетрагідрохінолін, що можуть бути заміщені одним або декількома замісниками: алкіл, алкокси, вініл, галоген, оксо, гідрокси, OCF3 або СF3,
їхні оптичні ізомери і їх фармацевтично прийнятні солі,
за винятком сполуки, у якій R2 і R3 є фенільними радикалами, R1 є радикалом -N(R5)-Y-R6, Υ є SO2, R5 є метильним радикалом і R6 - фенільним радикалом.
8. Сполуки формули І за п. 5, у якій
R1 означає радикал -N(R5)-Y-R6,
Υ означає SO2,
R2 означає або феніл, незаміщений або заміщений одним або декількома замісниками: галоген, алкіл, алкокси, трифторметил, трифторметокси або гідроксіалкіл, або гетероароматичний радикал, вибраний з циклів: піридил і піримідил, що можуть бути незаміщеними або заміщеними галогеном, алкілом, алкокси, гідрокси, трифторметилом або трифторметокси;
R3 означає або феніл, незаміщений або заміщений одним або декількома замісниками: галоген, алкіл, алкокси, трифторметил, трифторметокси, гідроксіалкіл, або гетероароматичний радикал, вибраний з циклів: піридил і піриміділ, що можуть бути незаміщеними або заміщеними галогеном, алкілом, алкокси, гідрокси, трифторметилом, трифторметокси;
R5 означає атом водню або алкіл;
R6 означає радикал нафтил, фенілалкіл, Het або феніл, що може бути заміщений одним або декількома замісниками: галоген, алкіл, алкокси, -NR14R15, гідрокси, гідроксіалкіл, OCF3, СF3 або –SO2NH2, або ж двома атомами вуглецю, зв'язаними між собою через діоксиметилен;
R14 і R15, однакові або різні, означають атом водню або радикал алкіл, циклоалкіл, алкілциклоалкіл або гідроксіалкіл, або R14 і R15, разом з атомом азоту, з яким вони з'єднані, утворюють насичений або ненасичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що може містити другий гетероатом, вибраний з кисню, сірки й азоту, і бути заміщеним одним або декількома радикалами алкіл, оксо, гідроксіалкіл або -CO-NH2;
Het означає ненасичений або насичений моно- або біциклічний гетероцикл, що має від 3 до 10 ланок, що містить один або декілька гетероатомів, вибраних з кисню, сірки й азоту, і який може бути заміщений одним або декількома радикалами: алкіл, алкокси, вініл, галоген, алкоксикарбоніл, оксо, гідрокси, причому азотвмісні гетероцикли можуть бути у формі N-оксидів, і, переважно, Нet означає гетероцикл, вибраний з наступних гетероциклів: бензімідазол, бензоксазол, бензотіазол, бензотіофен, тіофен, хінолін, пірол, піридин, піримідин, тіазол, тіадіазол, фуран, тетрагідроізохінолін і тетрагідрохінолін, що можуть бути заміщені одним або декількома замісниками: алкіл, алкокси, вініл, галоген, оксо, гідрокси, ОСF3 або СF3,
їхні оптичні ізомери і їх фармацевтичнo прийнятні солі,
за винятком сполуки, у якій R2 і R3 є фенільними радикалами, R1 є радикалом -N(R5)-Y-R6, Y є SO2, R5 є метильним радикалом і R6 фенільним радикалом.
9. Спосіб одержання сполук формули І за п. 5, у яких R1 є радикалом -NHCOR4, який відрізняється тим, що кислоту R4COOH, у якій R4 має ті ж значення, як у п. 5, вводять у взаємодію з похідним формули:
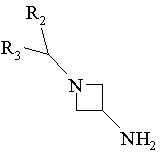 ,
,
у якій R2 і R3 мають ті ж значення, як у п. 5, виділяють продукт і перетворюють його при необхідності у фармацевтично прийнятну сіль.
10. Спосіб одержання сполук формули І за п. 5, у яких R1 є радикалом -Ν(R5)-Υ-R6, який відрізняється тим, що похідне формули:
 ,
,
у якій R2 і R3 мають ті ж значення, як у п. 5, вводять у взаємодію з похідним Hal-Y-R6, у якому Υ і R6 мають ті ж значення, як у п. 5, a Hal означає атом галогену, і потім, при необхідності, з похідним Hal-alk, де Hal означає атом галогену, a alk означає алкільний радикал (1-6 С в прямому або розгалуженому ланцюгові), одержуючи сполуки, у яких R5 є алкілом, виділяють продукт і перетворюють його при необхідності у фармацевтично прийнятну сіль.
11. Спосіб одержання сполук формули І за п. 5, який відрізняється тим, що похідне R2-CHBr-R3, у якому R2 і R3 мають ті ж значення, як у п. 5, вводять у взаємодію з сполукою формули:
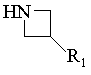 ,
,
у якій R1 має ті ж значення, як у п. 5, виділяють продукт і перетворюють його при необхідності у фармацевтично прийнятну сіль.
12. Спосіб одержання сполук формули І за п. 5, у яких R1 є радикалом -N(R5)-Y-R6, де R6 означає гідроксизаміщений фенільний радикал, який відрізняється тим, що здійснюють гідроліз відповідної сполуки формули І, у якій R1 є радикалом -N(R5)-Y-R6, де R6 означає алкоксизаміщений фенільний радикал, виділяють продукт і перетворюють його при необхідності у фармацевтично прийнятну сіль.
13. Спосіб одержання сполук формули І за п. 5, у яких R1 є радикалом -N(R5)-Y-R6, де R6 означає гідроксіалкіл(1С)-заміщений фенільний радикал, який відрізняється тим, що гідрид діізобутилалюмінію вводять у взаємодію з відповідною сполукою формули І, у якій R1 є радикалом -N(R5)-Y-R6, де R6 означає алкоксикарбонілзаміщений фенільний радикал, виділяють продукт і перетворюють його при необхідності у фармацевтично прийнятну сіль.
14. Спосіб одержання сполук формули І за п. 5, у яких R1 є радикалом -N(R5)-Y-R6, де R6 означає піролідиніл-1-заміщений фенільний радикал, який відрізняється тим, що піролідин вводять у взаємодію з відповідною сполукою формули І, у якій R1 є радикалом -N(R5)-Y-R6, де R6 означає фторзаміщений фенільний радикал, виділяють продукт і перетворюють його при необхідності у фармацевтично прийнятну сіль.
Текст
Даний винахід стосується фармацевтичних композицій, що містять як активний інгредієнт сполуки формули: або одну з його фармацевтично прийнятних солей, до нових похідних формули І, їх фармацевтично прийнятних солей і їх одержання. Сполуки формули І, у якій R2 і R3 є фенільними радикалами, R1 означає радикал -N(R5)-Y-R6, Υ означає груп у SO2 , R5 означає метильний радикал і R6 означає фенільний радикал, описані в патенті WO 99/01451. Інші сполуки і їх фармацевтично прийнятні солі є новими сполуками і складають частину винаходу. У формулі І R1 означає радикал -NHCOR4 або -N(R 5)-Y-R6, Υ означає CO або SO2, R2 і R3, однакові або різні, означають або ароматичний радикал, обраний з фенілу, нафтилу і інденілу, які можуть бути незаміщеними або заміщеними одним або декількома замісниками: галоген, алкіл, алкокси, форміл, гідрокси, трифторметил, трифторметокси, -CO-alk, ціано, -СООН, -COOalk, -CONR 7R8, -CO-NHNR9R10, алкілсульфаніл, алкілсульфініл, алкілсульфоніл, алкілсульфанілалкіл, алкілсульфінілалкіл, алкілсульфонілалкіл, гідроксіалкіл або -alk-NR 7R8; або гетероароматичний радикал, обраний з циклів: бензофурил, бензотіазоліл, бензотієніл, бензоксазоліл, хроманіл, 2,3-дигідробензофурил, 2,3дигідробензотієніл, піримідиніл, фурил, імідазоліл, ізохроманіл, ізохіноліл, піроліл, піридил, хіноліл, 1,2,3,4тетрагідроізохіноліл, тіазоліл і тієніл, що можуть бути незаміщеними або заміщеними одним або декількома замісниками: галоген, алкіл, алкокси, гідрокси, трифторметил, трифторметокси, ціано, -СООН, -COOalk, -CONH-NR9R10, -CONR7R8, -alk-NR 9R10, алкілсульфаніл, алкілсульфініл, алкілсульфоніл, алкілсульфанілалкіл, алкілсульфінілалкіл, алкілсульфонілалкіл або гідроксіалкіл; R4 означає радикал alk-SO2-Rn, alk-SCVCHkCH-Rn, Het, заміщений групою -SO2-Rn, або феніл, заміщений групою -SO2-R11 або -alk-SO2-R11; R5 означає атом водню або радикал алкіл; R6 означає радикал фенілалкіл, Het або Аг; R7 і R8, однакові або різні, означають атом водню або радикал алкіл, або ж R 7 і R8, разом з атомом азоту, з яким вони з'єднані, утворюють насичений моно- або біциклічний гетероцикл, який має від 3 до 10 ланок, що може містити другий гетероатом, обраний з кисню, сірки й азоту, і бути заміщеним одним або декількома алкілами; R9 і R10, однакові або різні, означають атом водню або радикал алкіл, -COOalk, циклоалкіл, алкілциклоалкіл, -alk-0-alk або гідроксіалкіл, або ж R 9 і R10, разом з атомом азоту, з яким вони з'єднані, утворюють насичений або ненасичений моно- або біциклічний гетероцикл, який має від 3 до 10 ланок, що може містити другий гетероатом, обраний з кисню, сірки й азоту, і бути заміщеним одним або декількома радикалами: алкіл, -COalk, -COOalk, -СО-NHalk, -CS-NHalk, оксо, гідроксіалкіл, -alk-O-alk або -CO-NH2; R11 означає радикал алкіл, Аг або Het; Аг означає радикал феніл, нафтил або інденіл, що можуть бути заміщені одним або декількома замісниками: галоген, алкіл, алкокси, ціано, -CO-alk, -СООН, -COOalk, -CONR 12R13, -CO-NH-NR 14R15, алкілсульфаніл, алкілсульфініл, алкілсульфоніл, alk-NR 14R15, -NR14R15 , алкілтіоалкіл, форміл, гідрокси, гідроксіалкіл, Het, -O-alk-NH-циклоалкіл, OCF3, CF 3, -NH-CO-alk, -SO2NH2, -NH-СОСН3, -NH-COOalk, Het, або по двох суміжних атомах вуглецю, зв'язаним діоксиметиленом; Het означає ненасичений або насичений моно- або біциклічний гетероцикл, який має від 3 до 10 ланок, що містить один або декілька гетероатомів, обраних з кисню, сірки й азоту, і який може бути заміщений одним або декількома радикалами: алкіл, алкокси, вініл, галоген, алкоксикарбоніл, оксо, гідрокси, OCF3 або CF3, причому азотвмісні гетероцикли можуть бути у формі N-оксидів. R12 і R13, однакові або різні, означають атом водню або радикал алкіл, або ж R 12 і R13, разом з атомом азоту, з яким вони з'єднані, утворюють насичений моно- або біциклічний гетероцикл, який має від 3 до 10 ланок, що може містити другий гетероатом, обраний з кисню, сірки й азоту, і бути заміщеним одним або декількома алкільними радикалами; R14 і R15, однакові або різні, означають атом водню або радикал алкіл, -COOalk, циклоалкіл, алкілциклоалкіл, -alk-0-alk або гідроксіалкіл, або R14 і R15, разом з атомом азоту, з яким вони з'єднані, утворюють насичений або ненасичений моно- або біциклічний гетероцикл, який має від 3 до 10 ланок, що може містити другий гетероатом, обраний з кисню, сірки й азоту, і бути заміщеним одним або декількома радикалами: алкіл, -CO-alk, -COOalk, -СО-NHalk, -CS-NHaik, оксо, гідроксіалкіл, -alk-O-alk або -CO-NH2; alk означає радикал алкіл або алкілен. В наведених і наступних визначеннях, якщо не обговорено особливо, алкільні або алкіленові радикали і частини молекул або алкоксильні радикали і частини молекул є прямими або розгалуженими ланцюгами і містять від 1 до 6 атомів вуглецю, а циклоалкільні радикали містять від 3 до 10 атомів вуглецю. З алкільних радикалів можна назвати метил, етил, н-пропіл, ізопропіл, н-бутил, втор-бутил, ізобутил, третбутил, пентил, гексил. З радикалів алкокси можна назвати радикали метокси, етокси, н-пропокси, ізопропокси, н-бутокси, втор-бутокси, ізобутокси, трет-бутокси, пентилокси. З циклоалкільних радикалів можна назвати радикали циклопропіл, циклобутил, циклопентил, циклогексил. Термін галоген це хлор, фтор, бром і йод. З гетероциклічних радикалів, які позначаються Het, можна назвати наступні гетероцикли: бензімідазол, бензоксазол, бензотіазол, бензотіофен, циннолін, тіофен, хіназолін, хіноксалін, хінолін, піразол, пірол, піридин, імідазол, індол, ізохінолін, піримідин, тіазол, тіадіазол, піперидин, піперазин, піролідин, триазол, фуран, тетрагідроізохінолін і тетрагідрохінолін, що можуть бути заміщені одним або декількома замісниками: алкіл, алкокси, вініл, галоген, алкоксикарбоніл, оксо, гідрокси, OCF3 або CF3. Сполуки формули І можуть бути у формі енантіомерів або діастереоізомерів. Ці оптичні ізомери і їхні суміші також складають частину винаходу. Сполуки формули І являють собою переважно такі сполуки, для яких: R1 означає радикал -N(R5)-Y-R6, Υ означає SO2, R2 означає або феніл, незаміщений або заміщений одним або декількома замісниками: галоген, алкіл, алкокси, трифторметил, трифторметокси, ціано, -CONR7R8, гідроксіалкіл або -alk-NR7R9, або гетероароматичний радикал, обраний з циклів: піридил, піримідиніл, тіазоліл і тієніл, що можуть бути незаміщеними або заміщеними галогеном, алкілом, алкокси, гідрокси, трифторметилом, трифторметокси, CONR7R8, -alk-NR 9R10, алкілсульфанілом, алкілсульфінілом, алкілсульфонілом або гідроксіалкілом; R3 означає або феніл, незаміщений або заміщений одним або декількома замісниками: галоген, алкіл, алкокси, трифторметил, трифторметокси, ціано, -CONR7R8, гідроксіалкіл, -alk-NR9R10, або гетероароматичний радикал, обраний з циклів: піридил, піримідиніл, тіазоліл і тієніл, що можуть бути незаміщеними або заміщеними галогеном, алкілом, алкокси, гідрокси, трифторметилом, трифторметокси, -CONR7R8, -alk-NR 7R9, алкілсульфанілом, алкілсульфінілом, алкілсульфонілом або гідроксіалкілом; R5 означає атом водню або алкіл; R6 означає радикал нафтил, фенілалкіл, Het або феніл, що може бути заміщений одним або декількома замісниками: галоген, алкіл, алкокси, ціано, -CO-alk, -COOalk, -CONR 12R13, -alk-NR 14R15, -NR14R15, гідрокси, гідроксіалкіл, Het, OCF3) CF3, -NH-COOalk, -SO2NH2) -NH-COOalk, або ж по двох суміжних атомах вуглецю, зв'язаним діоксиметиленом; R7 і R8, однакові або різні, означають атом водню або радикал алкіл, або R7 і Rs. разом з атомом азоту, з яким вони з'єднані, утворюють насичений моно- або біциклічний гетероцикл, який має від 3 до 10 ланок, що може містити другий гетероатом, обраний з кисню, сірки й азоту, і бути заміщеним одним або декількома алкілами; R9 і R10, однакові або різні, означають атом водню або радикал алкіл, циклоалкіл, алкілциклоалкіл або гідроксіалкіл, або R9 і R10, разом з атомом азоту, з яким вони з'єднані, утворюють насичений або ненасичений моно- або біциклічний гетероцикл, який має від 3 до 10 ланок, що може містити другий гетероатом, обраний з кисню, сірки й азоту, і бути заміщеним одним або декількома радикалами: алкіл, оксо або -CO-NH 2; R12 і Ri3, однакові або різні, означають атом водню або радикал алкіл, або R12 і R13, разом з атомом азоту, з яким вони з'єднані, утворюють насичений моно- або біциклічний гетероцикл, який має від 3 до 10 ланок, що може містити другий гетероатом, обраний з кисню, сірки й азоту, і бути заміщеним одним або декількома алкільними радикалами; R14 і R15, однакові або різні, означають атом водню або радикал алкіл, циклоалкіл, алкілциклоалкіл або гідроксіалкіл, або R14 і R15 разом з атомом азоту, з яким вони з'єднані, утворюють насичений або ненасичений моно- або біциклічний гетероцикл, який має від 3 до 10 ланок, що може містити другий гетероатом, обраний з кисню, сірки й азоту, і бути заміщеним одним або декількома радикалами алкіл, оксо, гідроксіалкіл або -CONH2; Het означає ненасичений або насичений моно- або біциклічний гетероцикл, який має від 3 до 10 ланок, що містить один або декілька гетероатомів, обраних з кисню, сірки й азоту, і який може бути заміщений одним або декількома радикалами: алкіл, алкокси, вініл, галоген, алкоксикарбоніл, оксо, гідрокси, причому азотвмісні гетероцикли можуть бути у формі N-оксидів, і, переважно, Het означає гетероцикл, обраний з наступних гетероциклів: бензімідазол, бензоксазол, бензотіазол, бензотіофен, тіофен, хіназолін, хіноксалін, хінолін, пірол, піридин, імідазол, індол, ізохінолін, піримідин, тіазол, тіадіазол, фуран, тетрагідроізохінолін і тетрагідрохінолін, що можуть бути заміщені одним або декількома замісниками: алкіл, алкокси, вініл, галоген, оксо, гідрокси, OCF3 або CF3. Ще більш переважні сполуки формули І, обирані з наступних сполук: R1 означає радикал -N(R5)-Y-R6, Υ означає SO2, R2 означає або феніл, незаміщений або заміщений одним або декількома замісниками: галоген, алкіл, алкокси, трифторметил, трифторметокси або гідроксіалкіл, або гетероароматичний радикал, обраний з циклів: піридил і піриміділ, що можуть бути незаміщеними або заміщеними галогеном, алкілом, алкокси, гідрокси, трифторметилом або трифторметокси; R3 означає або феніл, незаміщений або заміщений одним або декількома замісниками: галоген, алкіл, алкокси, трифторметил, трифторметокси, гідроксіалкіл, або гетероароматичний радикал, обраний з циклів: піридил і піриміділ, що можуть бути незаміщеними або заміщеними галогеном, алкілом, алкокси, гідрокси, трифторметилом, трифторметокси; R5 означає атом водню або алкіл; R6 означає радикал нафтил, фенілалкіл, Het або феніл, що може бути заміщений одним або декількома замісниками: галоген, алкіл, алкокси, -NR14R15, гідрокси, гідроксіалкіл, OCF3, CF3 або -SO2NH2, або ж по двох суміжних атомах вуглецю, зв'язаним діоксиметиленом; R14 і R15, однакові або різні, означають атом водню або радикал алкіл, циклоалкіл, алкілциклоалкіл або гідроксіалкіл, або R14 і R15 разом з атомом азоту, з яким вони з'єднані, утворюють насичений або ненасичений моно- або біциклічний гетероцикл, який має від 3 до 10 ланок, що може містити другий гетероатом, обраний з кисню, сірки й азоту, і бути заміщеним одним або декількома радикалами алкіл, оксо, гідроксіалкіл або -CONH2; Het означає ненасичений або насичений моно- або біциклічний гетероцикл, який має від 3 до 10 ланок, що містить один або декілька гетероатомів, обраних з кисню, сірки й азоту, і який може бути заміщений одним або декількома радикалами: алкіл, алкокси, вініл, галоген, алкоксикарбоніл, оксо, гідрокси, причому азотвмісні гетероцикли можуть бути у формі N-оксидів, і, переважно, Het означає гетероцикл, обраний з наступних гетероцикпів: бензімідазол, бензоксазол, бензотіазол, бензотіофен, тіофен, хінолін, пірол, піридин, піримідин, тіазол, тіадіазол, фуран, тетрагідроізохінолін і тетрагідрохінолін, що можуть бути заміщені одним або декількома замісниками: алкіл, алкокси, вініл, галоген, оксо, гідрокси, OCF3 або CF3. Сполуки формули І, у яких R1 є радикалом -NHCOR 4, можуть бути отримані по наступній реакційній схемі: У наведених формулах R2 , R3 і R 4 мають ті ж значення, що й у формулі І. Стадію а звичайно проводять в інертному розчиннику такому як тетрагідрофуран, діоксан, хлоровмісний розчинник (наприклад дихлорметан, хлороформ) при температурі в межах від 15 до 30°С в присутності основи такої як триалкіламін (наприклад триетіламін, дипропілетіламін) або в піридині при температурі в межах від 0 до 30°С. Стадію b проводять переважно в метанолі в автоклаві при температурі в межах від 50 до 70°С. Стадію с звичайно проводять у присутності агента конденсації, який використовують в хімії пептидів, такого як карбодіімід (наприклад 1-(3-диметіламінопропіл)-3-етилкарбодіімід, Ν,Ν'-дициклогексилкарбодіімід) або Ν,Ν'-діімідазолкарбоніл в інертному розчиннику такому як простий ефір (наприклад тетрагідрофуран, діоксан), амід (диметилформамід) або хлоровмісний розчинник (наприклад дихлорметан, 1,2-дихлоретан, хлороформ) при температурі в межах від 0°С до температури кипіння реакційної суміші. Можна також використовува ти реакційноздатне похідне кислоти, таке як хлорангідрид, можливо в присутності акцептора кислоти, такого як азотвмісна органічна основа (наприклад триалкіламін, піридин, діаза-1,8біцикло[5.4.0]ундецен-7 або діаза-1,5-біцикло[4.3.0]нонен-5), у розчиннику такому, як зазначено вище, або в суміші цих розчинників при температурі в межах від 0°С до температури кипіння реакційної суміші. Похідні R4COOH є комерційними або можуть бути отримані по методах, описаних R.C.LAROCK, Comprehensive Organic Transformations, VCH editor. Азетидиноли формули І можуть бути отримані, використовуючи або адаптуючи методи, описані KATRITZKY A.R. із співроб., J. Heterocycl. Chem., 271 (1994) або DAVE P.R., J. Org. Chem., 61, 5453 (1996), і в прикладах. Роботу звичайно ведуть за наступною схемою реакції: у формула х якої R2 і R3 мають ті ж значення, що й у формулі І, a Hal означає атом хлору або брому. На стадії А працюють переважно в інертному розчиннику такому як аліфатичний С 1-С4-спирт (наприклад метанол, етанол), можливо в присутності гідроксиду лужного металу, при температурі кипіння реакційного середовища. На стадії В відновлення звичайно проводять з використанням гідриду літіюй алюмінію в тетрагідрофурані при температурі кипіння реакційного середовища. На стадії С працюють переважно в інертному розчиннику такому як аліфатичний С 1-С4-спирт (наприклад етанол, метанол) у присутності гідрокарбонату натрію при температурі в межах від 20°С до температури кипіння реакційного середовища. На стадії D працюють по методу, описаному GRISAR Μ. із співроб., у J. Med. Chem., 885 (1973). Готують магнієву сполуку з бром-похідного і потім у реакцію вводять нітрил в ефірі, такому як діетиловий ефір, при температурі від 0°С до температури кипіння реакційного середовища. Після гідролізу спиртом проміжний імін відновлюють in situ борогідридом натрію при температурі від 0°С до температури кипіння реакційного середовища. Похідні R2-CO-R3 можуть бути придбані на ринку або можуть бути отримані з застосуванням або адаптуванням методів, описаних KUNDER N.G. із співавтор., J. Chem. Soc. Perktn Trans 1, 2815 (1997); MORENO - MARRAS M., Eur. J. Med. Chem., 23 (5) 477 (1988); SKINNER із співавтор., J. Med. Chem., 14 (6) 546 (1971); HURN N.K., Tetr. Lett., 36 (52) 9453 (1995); MEDICI A. із співавтор., Tetr. Lett., 24 (28) 2901 (1983); RIECKE R.D. із співавтор., J. Org. Chem., 62 (20) 6921 (1997); KNABE J. із співавтор., Arch, Pharm., 306 (9) 648 (1973); CONSONNI R. із співавтор., J. Chem. Soc. Perkin Trans 1, 1989 (1996); FR-96-2481 і JP-94-261393. Похідні R3Br купують на ринку або можуть бути отримані з застосуванням або адаптуванням методів, описаних BRANDSMA L. Synth. Comm., 20 (11) 1967 із співавтор., 3153 (1990); LEMAIRE Μ. із співавтор., Synth. Comm., 24 (1) 95 (1994); GODA Η. із співавтор., Synthesis, 9, 849 (1992) ;BAUERLE P. із співавтор., J. Chem. Soc. Perkin Trans 2, 489 (1993). Похідні R3CN купують на ринку або можуть бути о тримані з застосуванням або адаптуванням методів, описаних BOUYSSOU Р. із співавтор., J. Het. Chem., 29 (4) 895 (1992); SUZUKIN. із співавтор., J. Chem. Soc. Chem. Comm., 1523 (1984); MARBURG S. із співавтор., J. Het. Chem., 17, 1333 (1980); PERCEC V. із співавтор., J. Org. Chem., 60 (21) 6895 (1995). Сполуки формули І, у яких R1 є радикалом -N(R5)-Y-R6, можуть бути отримані за наступною схемою реакції: у формулах якої Υ, R2, R3 і R6 мають ті ж значення, що й у формулі І, а Hal означає атом галогену, переважно атом йоду, хлору або брому. Стадію а звичайно проводять в інертному розчиннику такому як тетрагідрофуран, діоксан, хлоровмісний розчинник (наприклад дихлорметан, хлороформ) у присутності аміну такого як триалкіламін (наприклад триетіламін) при температурі від 5 до 20°С. Стадію b звичайно проводять в інертному розчиннику такому як тетрагідрофуран у присутності гідриду натрію при температурі в межах від 0°С до температури кипіння реакційної суміші. Похідні Hal-SO2R6 купують на ринку або можуть бути отримані галогенуванням відповідних сульфонових кислот, зокрема in situ у присутності хлорсульфонілізоціанату і спирту в галогеновмісному розчиннику (наприклад дихлорметані, хлороформі). Похідні Hal-CO-R6 купують на ринку або можуть бути отримані по методах, описаним у R.C. LAROCK, Comprehensive Organic Transformations, VCH editor. Сполуки формули І можуть бути також отримані за наступною схемою реакції: у формула х якої R1, R2 і R3 мають ті ж значення, що й у формулі І, a Ph означає феніл. Стадію а звичайно проводять у спирті такому як метанол у присутності борогідриду натрію при температурі близької до 20°С. На стадії b готують із бром-похідного магнієву сполуку і вводять її в реакцію в інертному розчиннику такому як діетиловий ефір або тетрагідрофуран при температурі в межах від 0°С до температури кипіння реакційного середовища. Стадію с проводять використовуючи галогенуючий агента такий як бромистоводнева кислота, тіонілбромід, тіонілхлорид, суміш трифенілфосфіну і чотирибромистого або чотирихлористого вуглецю в оцтовій кислоті або в інертному розчиннику такому як дихлорметан, хлороформ, чотирихлористий вуглець або толуол при температурі від 0°С до температури кипіння реакційного середовища. Стадію d проводять з використанням водню в присутності палладія на вуглеці в спирті такому як метанол при температурі близькій до 20°С. Стадію є проводять в інертному розчиннику такому як ацетонітрил у присутності карбонату лужного металу (наприклад карбонату калію) і йодиду калію при температурі від 20°С до температури кипіння реакційного середовища. Похідні R3Br і R2-CHO купують на ринку або можуть бути отримані по методах, описаних, наприклад, R.C. LAROCK, Comprehensive Organic Transformations, VCH editor. Сполуки формули І, у яких R1 є радикалом -N(R5)-Y-R6, де R6 означає гідроксизаміщений фенільний радикал, можуть бути також отримані гідролізом відповідної сполуки формули І, у якій R1 є радикалом -N(R5)Y-R6, де R6 означає алкоксизаміщений фенільний радикал. Цей гідроліз звичайно проводять в інертному розчиннику такому як хлоровмісний розчинник (наприклад дихлорметан, хлороформ) з використанням триброміду бору при температурі близької до 20°С. Сполуки формули І, у яких R1 є радикалом -N(R5)-Y-R6, де R6 означає гідроксіалкіл(1С)-заміщений фенільний радикал, можуть бути також отримані дією гідриду диізобутилалюмінію на відповідну сполуку формули І, у якій R^ є радикалом -N(R 5)-Y-R6, де R6 означає алкоксикарбонілзаміщений фенільний радикал. Цю реакцію звичайно проводять в інертному розчиннику такому як толуол з використанням гідриду диізопропілалюмінію при температурі в межах від -50°С до 25°С. Сполуки формули І, у яких R1 є радикалом -N(R5)-Y-R6, де R6 означає піролідин-1-іл-заміщений фенільний радикал, можуть бути також отримані дією піролідину на відповідну сполуку формули І, у якій R 1 є радикалом N(R5)-Y-R6, де R6 означає фторзаміщений фенільний радикал. Цю реакцію переважно проводять в інертному розчиннику такому як диметилсульфоксид при температурі 90°С. Для фа хівця є очевидним, що при здійсненні описаних вище способів згідно винаходу може виявитися необхідним щоб уникнути побічних реакцій вводити захисні групи для амінних, гідроксильних і карбоксильних реакційних груп. Такими групами є групи, що можуть бути вилучені без порушення іншої частини молекули. Як приклади захисних груп для амінної функції можна назвати трет-бутил- або метилкарбамати, що можуть бути регенеровані за допомогою йодтриметилсилану, або алілкарбамат, що може бути вилучений за допомогою паладієвих каталізаторів. Як приклади захисних груп для гідроксильної реакційної групи можна назвати триетилсиліл, трет-бутилдиметилсиліл, що можуть бути регенеровані за допомогою фториду тетрабутиламонію, або ж несиметричні ацеталі (наприклад метоксиметил, тетрагідропіраніл), які регенеруються за допомогою хлористоводневої кислоти. Як захисні групи для карбоксильних реакційних гр уп можна назвати складні ефіри (наприклад аліловий, бензиловий), оксазоли і 2-алкіл-1,3-оксазоліни. Інші придатні для використання захисні групи описані GREENE T.W. с співавтор., Protecting groups in Organic Synthesis, second edition, 1991, John Wiley & Sons. Сполуки формули І можуть бути очищені звичайними відомими методами, наприклад кристалізацією, хроматографією або екстракцією. Енантіомери сполук формули І можуть бути отримані розщепленням рацемічних сумішей, наприклад за допомогою хроматографії на хіральній колонці по PICKLE W.H. с співавтор., Asymmetric Synthesis, vol.1, Academic Press (1983) або шляхом утворення солей або синтезом з хіральних попередників. Діастереоізомери можуть бути о тримані за допомогою відомих класичних методів (кристалізації, хроматографії або з хіральних попередників). Сполуки формули І можуть бути при необхідності перетворені в сольові аддукти з мінеральними або органічними кислотами дією кислоти в органічному розчиннику такому як спирт, кетон, простий ефір або хлоровмісний розчинник. Ці солі також складають частину винаходу. Як приклади фармацевтично прийнятних солей можуть бути названі такі солі: бензолсульфонат, гідробромід, гідрохлорид, цитарат, етансульфонат, фумарат, глюконат, йодат, ізотіонат, малеат, метансульфонат, метилен-біс-b-оксинафтоат, нітрат, оксалат, памоат, фосфат, саліцилат, сукцинат, сульфат, тартрат, тео філінацетат і п-толуолсульфонат. Сполуки формули І мають цікаві фармакологічні властивості. Ці сполуки характеризуються великою спорідненістю до канабінодних рецепторів і, зокрема, до рецепторів типу СВ1. Вони є антагоністами рецептора СВ1 і, отже, можуть бути використані при лікуванні і профілактиці розладів, що стосуються центральної нервової системи, імунної системи, серцево-судинної або ендокринної системи, респіраторної системи, шлунково-кишкового апарату і розладів репродуктивної системи (Hollister, Pharm. Rev., 38, 1986, 120; Reny i Sinha, Prog. Drug. Res., 36, 71-114 (1991); Consroe і Sandyk, у Marijuana/Cannabinoids, Neurobiology and Neurophysiology, 459; Murphy L. and Barthe A. Eds, CRC Press, 1992). Таким чином, ці сполуки можуть бути використані для лікування і попередження психозів, включаючи шизофренію, відчуття тривоги, депресії, епілепсії, нейродегенерації, мозкових і спинномозкових розладів, порушення функції пізнання, черепної травми, панічних приступів, периферичних нейропатій, глауком, мігрені, хвороби Паркінсона, хвороби Альцгеймера, хореї Хантінгтона, синдрому Рейно, тремтіння, симптомів примусової нав'язливості, старечого слабоумства, порушень тимуса, синдрому Туретта, уповільненої дискінезії, двополюсних розладів, раків, порушень рухового апарату під впливом ліків, дистоній, ендотоксимічних шоків, геморагічних шоків, гіпотензії, безсоння, імунологічних захворювань, бляшаного склерозу, рвот, астми, порушень апетиту (булімія, анорексія), ожиріння, порушень пам'яті, при відбиранні від грудей у процесі хронічного лікування, і зловживання алкоголем або ліками (наприклад опіоідами, барбітуратами, коноплею, кокаїном, амфетамінуми, фенциклідом, галюциногенами, бензодіазепінами), такими як анальгетики або підсилювачі анальгетичної активності наркотичних і ненаркотичних лік. Вони можуть бути також використані для лікування або профілактики проходу по кишечнику. Спорідненість сполук формули І до рецепторів коноплі було визначено по методу, описаному KUSTER J.E., STEVENSON J.I., WARD S.J., D'AMBR A Т.Е., H AYCOCK DA у J. Pharmacol. Exp. Ther., 264, 1352-1363 (1993). У проведеному тесті значення СІ50 для сполук формули І нижче або дорівнює 1000нМ. Їхня антагоністична активність була продемонстрована за допомогою моделі гіпотермії, яка викликана агоністом рецепторів коноплі (СР-55940) у миші по методу, описаному Pertwee у R.G. у Marijuana, Harvey D.J. eds, 84 Oxford IRL Press, 263-277 (1985). У цьому тесті значення DE50 для сполук формули І нижче або дорівнює 50мг/кг. Сполуки формули І мають низьку токсичність. їх DL50 вище 40мг/кг при підшкірному введенні у миші. Винахід ілюструють такі приклади. Приклад 1 До розчину 61,4мг 1-[біс(4-хлорфеніл)метил]азетидин-3-іламіну в 3см 3 дихлорметану послідовно додають при кімнатній температурі в атмосфері аргону 69,3мм 3 триетіламіну і 110мг тієн-2-іл-сульфонілхлориду. Після 68 годин перемішування при кімнатній температурі реакційну суміш вводять у патрон Bond ElutÒ SC{(3см 3/500мг), послідовно елююючи два рази 2см 3 дихлорметану і потім два рази 2см 3 1Μ розчином аміаку в метанолі. Аміачні фракції поєднують і випарюють до суха при зниженому тиску (2,7кПа). Отриманий залишок розчиняють у 5см 3 дихлорметану, тричі промивають 3см 3 дистильованої води, висушують над сульфатом магнію, фільтрують і випарюють досуха при зниженому тиску (2,7кПа). Одержують таким способом 60мг N-{1[біс(4-хлорфеніл)метил]азетидин-3-іл}тієн-2-іл-сульфонаміду у вигляді пінистої маси кремового кольору [Спектр ЯМР 1Н (300мгц, CDCl3, d у м.ч.): 2,77 (т розщепл., J=7 і 2Гц:2Н); 3,40 (т розщепл., J=7 і 2Гц:2Н); 4,06 (м:1Н); 4,21 (с:1Н); від 4,85 до 5,25 (м розтягнутий: 1Н); 7,06 (т, J=4,5Гц:1Н); від 7,15 до 7,35 (м:8Н); 7,58 (м:2Н)]. 1-[Біс(4-хлорфеніл)метил]азетидин-3-іламін може бути отриманий таким способом: до 27г 1-[біс(4хлорфеніл)метил]азетидин-3-ілового ефіру метансульфонової кислоти, поміщеного в попередньо охолоджений до -60°С автоклав, додають 400см 3 суміші метанолу і рідкого аміаку (50/50 за об'ємом). Реакційну суміш перемішують 24 години при 60°С, залишають на повітрі для випарювання аміаку і потім випарюють при зниженому тиску (2,7кПа). Залишок поглинають 500см 3 0,37н. водного розчину гідроксиду натрію і чотири рази екстрагують 500см 3 діетилового ефіру. Об'єднані органічні фази послідовно промивають двічі 100см 3 дистильованої води і 100см 3 насиченого розчину хлориду натрію, висушують над сульфатом магнію, фільтрують і випарюють при зниженому тиску (2,7кПа). Отриманий залишок очищають флешхроматографією на силікагелі [елюент: дихлорметан/метанол (95/5 за об'ємом)]. Одержують 14,2г 1-[біс(4хлорфеніл)метил]азетидин-3-іламіну у вигляді масла, що застигає з утворенням твердої речовини кремового кольору. 1-[Біс(4-хлорфеніл)метил]азетидин-3-ілового ефіру метансульфонової кислоти може бути отриманий таким способом: до розчину 12г 1-[біс(4-хлорфеніл)метил]азетидин-3-олу в 200см 3 дихлорметану додають протягом 10хв під аргоном 3,5см 3 метилсульфонілхлориду, о холоджують до +5°С і протягом 10хв доливають 3,8см 3 піридину. Після 30хв перемішування при +5°С і потім 20 годин при 20°С реакційну суміш розбавляють 100см 3 води і 100см 3 дихлорметану, після чого суміш фільтрують і розділяють фази. Органічну фазу промивають водою, висушують над сульфатом магнію, фільтрують і випарюють до суха при зниженому тиску (2,7кПа). Отримане масло піддають хроматографії на колонці із силікагелем (гранулометрія: 0,063-0,200мм, висота 40см, діаметр 3,0см), елююючи під тиском аргону 0,5бар сумішшю циклогексану з етилацетатом (70/30 за об'ємом) і збирають фракції об'ємом 100см 3. Фракції 4-15 поєднують і випарюють до суха при зниженому тиску (2,7кПа), одержуючи 6,8г 1-[біс(4-хлорфеніл)метил]азетидин-3-ілового ефіру метансульфонової кислоти у вигляді жовтого масла. 1-[Біс(4-хлорфеніл)метил]азетидин-3-ол може бути отриманий відповідно до послідовності операцій, описаної KATRITZKY A.R. с співавтор. J. Heterocycl. Chem., 271 (1994), виходячи з 35,5г гідрохлориду [біс(4хлорфеніл)метил]аміну і 11,0см 3 епіхлоргідрину. Виділяють 9,0г 1-[біс(4-хлорфеніл)метил]азетидин-3-олу. Гідрохлорид [біс(4-хлорфеніл)метил]аміну може бути отриманий методом, описаним GRISAR М. із співавтор. J. Med. Chem., 885 (1973). Приклад 2 Повторюючи послідовність операцій прикладу 1, але виходячи з 124мг 4метоксибензолсульфонілхлориду, одержують 12мг N-{1-[бic(4-хлорфеніл)метил]азетидин-3-іл}-4метоксибензолсульфонаміду у вигляді лаку кремового кольору [Спектр ЯМР 1Н (300мгц, CDCl3, d у м.ч.): 2,7 (т розщепл., J=7 і 2Гц:2Н); 3,35 (т розщепл., J=7 і 2Гц:2Н); 3,85 (с:ЗН); 3,94 (м:1Н); 4,18 (с:1Н); 4,83 (д, J=9Гц:1Н); 6,94 (д ушир., J=9Гц:2Н); 7,22 (с:8Н); 7,75 (д ушир., J=9Гц:2Н)]. Приклад 3 Повторюючи послідовність операцій прикладу 1, але виходячи з 140мг 4ацетамідофенолсульфонілхлориду, одержують 13мг N-[4-(N-{1-[бic(4-хлорфеніл)метил]азетидин-3іл}сульфамоїл)феніл]ацетаміду у вигляді лаку кремового кольору [Спектр ЯМР 1Н (300мгц, CDCl3, d у м.ч.): 2,26 (с:3Н); 2,74 (т розщепл., 0=7 і 2Гц:2Н); 3,39 (т розщепл., J=7 і 2Гц:2Н); 4,01 (м:1Н); 4.22 (с:1Н); 4,92 (д, J=9Гц:1Н); 7,32 (м:8Н); 7,49 (с ушир.:1Н); 7,68 (д ушир., J=9Гц:2Н); 7,81 (д ушир., J=9Гц:2Н)]. Приклад 4 Повторюючи послідовність операцій прикладу 1, але виходячи з 114мг 4-метилфенілсульфонілхлориду, одержують 19мг N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}-4-метилфенілсульфонаміду у вигляді безбарвного лаку [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,42 (с:3Н); 2,71 (т розщепл., J=7 та 2Гц:2Н); 3,36 (т розщепл., J=7 та 2Гц:2Н); 3,97 (м:1Н); 4,19 (с:1Н); 4,81 (д, J=9,5Гц:1Н); від 7,15 до 7,40 (м:10Н); 7,71 (с ушир., J=8,5Гц:2Н)]. Приклад 5 Повторюючи послідовність операцій прикладу 1, але виходячи з 142 мг 3,4диметоксифенілсульфонілхлориду, одержують 10мг N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}-3,4диметоксифенілсульфонаміду у вигляді лаку кремового кольору [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,72 (т розщепл., J=7,5Гц:2Н); 3,37 (т ушир., J=7,5Гц:2Н); від 3,85 до 4,00 (м:1Н); 3,91 (с:3Н); 3,93 (с:3Н); 4,19 (с:1Н); 4,84 (д, J=9Гц:1Н); 6,90 (д, J=8,5Гц:1Н); 7.23 (м:8Н); 7,29 (д, J=2Гц:1Н); 7,43 (дд, J=8,5 та 2Гц:1Н)]. Приклад 6 Повторюючи послідовність операцій прикладу 1, але виходячи з 117мг 3-фторфенілсульфонілхлориду, одержують 13,5мг N-{1-[бic(4-хлорфеніл)метил]азетидин-3-іл}-3-фторфенілсульфонаміду у вигляді лаку кремового кольору [Спектр ЯМР 1Н (400мгц, CDCl3, d у м.ч.): 2,79 (т розщепл., J=7 та 2Гц:2Н); 3,43 (т розщепл., J=7 та 2Гц:2Н); 4,05 (м:1Н); 4,24 (с:1Н); 4,91 (м:1Н); від 7,20 до 7,40 (м:9Н); від 7,50 до 7,65 (м:2Н); 7,67 (д ушир., J=8Гц:1Н)]. Приклад 7 Повторюючи послідовність операцій прикладу 1, але ви ходячи з 147мг 3,4-дихлорфенілсульфонілхлориду, одержують 20мг N-{1-[бic(4-хлорфеніл)метил]азетидин-3-іл}-3,4-дихлорфенілсульфонаміду у вигляді лаку кремового кольору [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,77 (т розщепл., J=7 та 2Гц:2Н); 3,40 (т розщепл., J=7 та 2Гц:2Н); 3,98 (м:1Н); 4,21 (с:1Н); від 4,85 до 5,15 (м:1Н); від 7,20 до 7,35 (м:8Н); 7,57 (д, J=8,5Гц:1Н); 7,65 (дд, J=8,5 та 2Гц:1Н); 7,93 (д, J=2Гц:1Н)]. Приклад 8 Повторюючи послідовність операцій прикладу 1, але виходячи з 121мг 3-ціанофенілсульфонілхлориду, одержують 21мг N-{1-[бic(4-хлорфеніл)метил]азетидин-3-іл}-3-ціанофенілсульфонаміду у вигляді лаку кремового кольору [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,76 (т розщепл., J=7 та 2Гц:2Н); 3,39 (т розщепл., J=7 та 2Гц:2Н); 3,99 (м:1Н); 4,21 (с:1Н); від 4,80 до 5,60 (м дуже розтягнутий:1Н); від 7,15 до 7,35 (м:8Н); 7,65 (т, J=8Гц:1Н); 7,86 (д ушир., J=8Гц:1Н); 8,05 (д ушир., J=8Гц:1Н); 8,13 (с ушир.:1Н)]. Приклад 9 Повторюючи послідовність операцій прикладу 1, але ви ходячи з 142мг 2,5диметоксифенілсульфонілхлориду, одержують 31мг N-{1-[бic(4-хлорфеніл)метил]азетидин-3-іл}-2,5диметоксифенілсульфонаміду у вигляді лаку кремового кольору [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,73 (т розщепл., J=7 та 2Гц:2Н); 3,27 (т розщепл., J=7 та 2Гц:2Н); 3,80 (с:3Н); від 3,85 до 4,00 (м:1Н); 3,94 (с:3Н); 4,19 (с:1Н); 5,32 (д, J=8Гц:1Н); 6,94 (д, J=9Гц:1Н); від 7,05 (дд, J=9 та 3Гц:1Н); 7,23 (м:8Н); 7,40 (д, J=3Гц:1Н)]. Приклад 10 Повторюючи послідовність операцій прикладу 1, але виходячи з 147мг 3трифторметилфенілсульфонілхлориду, одержують 8мг N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}-3трифторметилфенілсульфонаміду у вигляді лаку кремового кольору [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,79 (т розщепл., J=7 та 2Гц:2Н); 3,41 (т розщепл., J=7 та 2Гц:2Н); 4,03 (м:1Н); 4,23 (с:1Н); від 4,80 до 5,10 (м розтягнутий: 1Н); від 7,20 до 7,35 (м:8Н); 7,68 (т, J=8Гц:1Н); 7,87 (д ушир., J=8Гц:1Н); 8,05 (д ушир., J=8Гц:1Н); 8,15 (с ушир.:1Н)]. Приклад 11 Повторюючи послідовність операцій прикладу 1, але ви ходячи з 136мг нафт-2-илсульфонілхлориду, одержують 20мг N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}нафт-2-илсульфонаміду у ви гляді лаку кремового кольору [Спектр ЯМР 1Н (400мгц, CDCI3, d у м.ч.): 2,74 (м:2Н); 3,35 (м:2Н); 4,02 (м:1Н); 4,17 (с:1Н); 4,96 (м:1Н); від 7,10 до 7,30 (м:8Н); 7,64 (м:2Н); 7,78 (дд, J=7 та 1,5Гц:1Н); від 7,90 до 8,05 (м:3Н); 8,41 (с ушир.:1Н)]. Приклад 12 Повторюючи послідовність операцій прикладу 1, але ви ходячи з 136мг нафт-1-илсульфонілхлориду, одержують 52мг N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}нафт-1-илсульфонаміду у ви гляді лаку кремового кольору [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,63 (т розщепл., J=7 та 2Гц:2Н); 3,20 (т розщепл., J=7 та 2Гц:2Н); 3,90 (м:1Н); 4,12 (с:1Н); 5,26 (м:1Н); 7,16 (м:8Н); 7,52 (т, J=8Гц:1Н); від 7,55 до 7,75 (м:2Н); 7,95 (д, J=8,5Гц:1Н); 8,06 (д, J=8,5Гц:1Н); 8,23 (дд, J=7,5 та 1Гц:1Н); 8,64 (д, J=8,5Γ4:1Η)]. Приклад 13 Повторюючи послідовність операцій прикладу 1, але ви ходячи з 128мг 3,4дифторфенілсульфонілхлориду, одержують 7мг N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}-3,4дифторфенілсульфонаміду у вигляді лаку кремового кольору [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,76 (т ушир., J=7,5Гц:2Н); 3,39 (т ушир., J=7,5Гц:2Н); 3,98 (м:1Н); 4,20 (с ушир.:1Н); від 4,85 до 5,25 (м розтягнутий: 1Н); від 7,15 до 7,35 (м:9Н); від 7,55 до 7,75 (м:2Н)]. Приклад 14 Повторюючи послідовність операцій прикладу 1, але виходячи з 108мг 1-метилімідазол-4сульфонілхлориду, одержують 22мг N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}-1-метил-1-Н-імідазол-4-ілсульфонаміду у вигляді пінистої маси кремового кольору [Спектр ЯМР 1Н (300мгц, CDCI3 з добавкою декількох крапель CD3COOD d4, d в м.ч.): 3,22 (м:2Н); 3,67 (м:2Н); 3,74 (с:3Н); 4,10 (м:1Н); 4,65 (с ушир.:1Н); 7,27 (м:8Н); 7,47 (д ушир., J=1Гц:1Н);7,53(душир., J=1Гц:1Н)]. Приклад 15 Повторюючи послідовність операцій прикладу 1, але виходячи з 152мг 4-ацетамідо-3хлорфенілсульфонілхлориду, одержують 69мг N-[4-(N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}сульфамоїл)-2хлорфеніл]ацетаміду у вигляді пінистої маси кремового кольору [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,30 (с:3Н); 2,73 (м:2Н); 3,38 (м:2Н); 3,97 (м:1Н); 4,19 (с:1Н); 7,24 (с:8Н); 7,70 (дд, J=7 та 1,5Гц:1Н); 7,78 (с ушир.:1Н); 7,86 (д, J=1,5Гц:1Н); 8,61 (д, J=7Гц:1Н)]. Приклад 16 До розчину 0,7г 1-[біс(4-хлорфеніл)метил]азетидин-3-іламіну в 25см 3 дихлорметану додають при кімнатній температурі в атмосфері аргону 0,79см 3 триетиламіну. Суміш охолоджують до 0°С, після чого додають розчин 1,2г пірид-3-илсульфонілхлориду в 25см 3 дихлорметану та перемішують 16 годин при кімнатній температурі. Реакційну суміш розбавляють 50см 3 дихлорметану та двічі промивають 25см 3 дистильованої води. Органічну фазу висушують над суль фатом магнію, фільтрують та насухо випарюють при зниженому тиску (2,7кПа). Отриманий залишок очищають флеш-хроматографією на силікагелі [елюент: дихлорметан/метанол (97,5/2,5 по об'єму)], одержуючи 0,7г N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}пірид-3-илсульфонаміду у вигляді пінистої маси кремового кольору, що затвердіває у присутності ізопропілового спирту з утворенням порошку кремового кольору з т.пл.164°С. Пірид-3-илсульфонілхлорид може бути отриманий по методу, описаному Breant P. у співав. Synthesis, 10, 833-4 (1983). Приклад 17 До розчину 0,307г 1-[біс(4-хлорфеніл)метил]азетидин-3-іламіну в 10см 3 дихлорметану додають при кімнатній температурі в атмосфері аргону 0,214г 4-фторфенілсульфонілхлориду та 0,28см 3 триетиламіну. Після 16 годин перемішування при кімнатній температурі реакційну суміш промивають 10см 3 дистильованої води, висушують над сульфатом магнію, фільтрують та насухо випарюють при зниженому тиску (2,7кПа). Отриманий залишок очищають флеш-хроматографією на силікагелі [елюент: градієнт дихлорметан/етилацетат (100/0 до 95/5 по об'єму)]. Одержують 0,18г N-{1-[біс(4-хлорфеніл)метил]азетидин-3іл}-4-фторфенілсульфонаміду у вигляді білої пінистої маси [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,74 (т ушир., J=7,5Гц:2Н); 2,39 (т ушир., J=7,5Гц:2Н); 3,98 (м:1Н); 4,20 (с:1Н); 4,79 (д, J=9Гц:1Н); від 7,10 до 7,35 (м:10Н); 7,86 (м:2Н)]. Приклад 18 Повторюючи послідовність операцій прикладу 17, але виходячи з 0,25г хінол-8-ілсульфонілхлориду, одержують 0,36г N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}хінол-8-ілсульфонаміду у вигляді білого порошку [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,63 (т розщепл., J=7 та 2Гц:2Н); 3,16 (т розщепл., J=7 та 2Гц:2Н); 3,98 (м:1Н); 4,11 (с:1Н); 6,77 (д, J=8Гц:1Н); 7,15 (м:8Н); 7,61 (дд, J=8 та 4Гц:1Н); 7,64 (дд, J=8 та 7,5Гц:1Н); 8,06 (дд, J=8 та 1,5Гц:1Н); 8,30 (дд, J=8 та 1,5Гц:1Н); 8,40 (дд, J=7,5 та 1,5Гц:1Н); 9,09 (дд, J=4 та 1,5Гц:1Н)]. Приклад 19 Повторюючи послідовність операцій прикладу 17, але виходячи з 0,14см 3 фенілсульфонілхлориду, одержують 0,35г N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}фенілсульфонаміду у вигляді білого порошку [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,75 (т ушир., J=7,5Гц:2Н); 3,40 (т ушир., J=7,5Гц:2Н); 4,03 (м:1Н); 4,22 (с:1Н); 4,79 (д, J=10Гц:1Н); 7,31 (с:8Н); від 7,45 до 7,65 (м:3Н); 7,87 (д ушир., J=7,5Гц:2Н)]. Приклад 20 Повторюючи послідовність операцій прикладу 17, але виходячи з 0,21г фенілметилсульфонілхлориду, одержують 0,27г N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}фенілметилсульфонаміду у вигляді білого порошку [Спектр ЯМР 1Н (400мгц, CDCI3, d у м.ч.): 2,76 (т розщепл., J=7 та 2Гц:2Н); 3,41 (т розщепл., J=7 та 2Гц:2Н); 3,85 (м:1Н); 4,20 (с:1Н); 4,23 (с:2Н); 4,46 (д, J=9Гц:1Н); від 7,25 до 7,45 (м:13Н)]. Приклад 21 Повторюючи послідовність операцій прикладу 17, але ви ходять з 0,42г 3,5-дифторфенілсульфонілхлориду в 30см 3 дихлорметану, та двічі промивають органічну фазу 20см 3 дистильованої води. Після очищення флешхроматографією на силікагелі [елюент: градієнт дихлорметан/метанол (100/0 до 95/5 по об'єму)] одержують 0,1г N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}-3,5-дифторфенілсульфонаміду у ви гляді жовтого порошку [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,77 (т розщепл., J=7 та 2Гц:2Н); 3,41 (т розщепл., J=7 та 2Гц:2Н); 4,01 (м:1Н); 4,21 (с:1Н); 4,90 (д, J=9Гц:1Н); 7,02 (тт, J=8,5 та 2,5Гц:1Н); від 7,20 до 7,35 (м:8Н); 7,38 (м:2Н)]. 3,5-дифторфенілсульфонілхлорид може бути отриманий по методу, описаному в патенті FR 9615887. Приклад 22 Повторюючи послідовність операцій прикладу 21, але виходячи з 0,21г пірид-2-илсульфонілхлориду та 0,17см 3 триетиламіну, та двічі промиваючи органічну фазу 30см 3 дистильованої води, після очищення флешхроматографією на силікагелі [елюент: градієнт дихлорметан/метанол (100/0 до 98/2 по об'єму)] одержують 0,3г N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}пірид-2-илсульфонаміду у ви гляді білого порошку [Спектр ЯМР 1 Н (300мгц, CDCI3, d у м.ч.): 2,78 (т розщепл., J=7 та 2Гц:2Н); 3,35 (τ розщепл., J=7 та 2Гц:2Н); 4,12 (м:1Н); 4,20 (с:1Н); 5,30 (д, J=9Гц:1Н); від 7,15 до 7,35 (м:8Н); 7,47 (ддд, J=7,5 та 5 та 1Гц:1Н); 7,90 (т розщепл., J=7,5 та 2Гц:1Н); 7,98 (д ушир., J=7 ,5Гц:1Н); 8,65 (д ушир., J=5Гц:1Н)]. Пірид-2-илсульфонілхлорид може бути отриманий по методу, описаному Corey E.J., J. Org. Chem. (1989) 54(2), 389-93. Приклад 23 До розчину 0,24г 1-[біс(4-хлорфеніл)метил]азетидин-3-іл)-(3,5-дифторбензол)сульфонаміду в 6см 3 диметилсульфоксиду додають при кімнатній температурі 0,104см 3 піролідину та нагрівають суміш 18 годин при 90°С. Після цього реакційну суміш розбавляють 30см 3 дихлорметану та тричі промивають 30см 3 дистильованої води. Органічну фазу висушують над сульфатом магнію, фільтрують насухо випарюють при зниженому тиску (2,7кПа). Залишок очищають флеш-хроматографією з дихлорметаном як з елюентом. Одержують 50мг N-{1-[бic(4-хлорфент)метил]азетидин-3-т}-3-фтор-5-піролідин-1-ілфенілсульфонаміду у вигляді білого порошку [Спектр ЯМР 1Н (600мгц, CDCI3 з добавкою декількох крапель CD3COOD d4, d у м.ч.): 2,04 (м:4Н); від 3,20 до 3,35 (м:6Н); 3,60 (т, J=8,5Гц:2Н); 4,14 (м:1Н); 4,57 (с:1Н); 6,31 (д ушир., J=11,5Гц:1Н); 6,70 (д ушир., J=8,5Гц:1Н); 6,72 (с ушир.:1Н); від 7,20 до 7,35 (м:8Н)]. Приклад 24 До 80%-ний суспензії 20,5мг гідриду натрію в 10см 3 тетрагідрофурану додають при кімнатній температурі в атмосфері аргону розчин 0,26г N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}-4-фторфенілсульфонаміду в 5см 3 тетрагідрофурану. Після 1 години перемішування при 20°С додають 60мм 3 йодметану, перемішують суспензію ще 16 годин та додають 30см 3 етилацетату та 20см 3 дистильованої води. Органічну фазу висушують над сульфатом магнію, фільтрують та насухо випарюють при зниженому тиску (2,7кПа). Залишок очищають флешхроматографією на силікагелі [елюент: циклогексан/етилацетат (90/10 по об'єму)], одержуючи в такий спосіб 19мг N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}-N-метил-4-фторфенілсульфонаміду у вигляді білого порошку [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,69 (с:3Н); 3,02 (т розщепл., J=7 та 2Гц:2Н); 3,35 (т розщепл., J=7 та 2Гц:2Н); 3,91 (м:1Н); 4,27 (с:1Н); від 7,15 до 7,35 (м:10Н); 7,75 (дд, J=9 та 5Гц:2Н)]. Приклад 25 Повторюючи послідовність операцій прикладу 24, але виходячи з 0,25г N-{1-[біс(4хлорфеніл)метил]азетидин-3-іл}хінол-8-ілсульфонаміду та 18мг 80%-ного гідриду натрію, після очищення флеш-хроматографією на силікагелі [елюент: циклогексан/етилацетат (80/20 по об'єму)] одержують 70мг N-{1[біс(4-хлорфеніл)метил]азетидин-3-іл}хінол-8-ілсульфонаміду у вигляді білого порошку [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): від 3,00 до 3 ,10 (м:2Н); 3,05 (с:3Н); 3,35 (м:2Н); 4,27 (с:1Н); 4,93 (м:1Н); від 7,15 до 7,35 (м:8Н); 7,50 (дд, J=8,5 та 4Гц:1Н); 7,62 (дд, J=8 та 8,5Гц:1Н); 8,03 (дд, J=8,5 та 1,5Гц:1Н); 8,22 (дд, J=8,5 та 1,5Гц:1Н); 8,48 (дд, J=8 та 1,5Гц:1Н); 8,98 (дд, J=4 та 1,5Гц:1Н)]. Приклад 26 Повторюючи послідовність операцій прикладу 24, але виходячи з 0,21г N-{1-[біс(4хлорфеніл)метил]азетидин-3-іл}фенілсульфонаміду, 17мг 80%-ного гідриду натрію та двічі вводячи йодметан з інтервалом 3 години. Одержують у такий спосіб 80мг N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}-Nметилфенілсульфонаміду в виді білого лаку [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,70 (с:3Н); 3,03 (т ушир., J=7,5Гц:2Н); 3,37 (т ушир., J=7,5Гц:2Н); 3,94 (м:1Н); 4,28 (с.іН); від 7,20 до 7,35 (м:8Н); від 7,45 до 7,65 (м:ЗН); 7,74 (д ушир., J=8Гц:2Н)]. Приклад 27 Повторюючи послідовність операцій прикладу 26, але виходячи з 0,17г N-{1-[біс(4хлорфеніл)метил]азетидин-3-іл}фенілметилсульфонаміду, 14мг 80%-ного гідриду натрію та перемішуючи потім суміш при 20°С протягом 48 годин, після очищення флеш-хроматографією на силікагелі [елюент: дихлорметан/етилацетат (95/5 по об'єму)] одержують 120мг N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}-Nметил(фенілметан)сульфонаміду у вигляді білої пінистої маси [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,81 (с:3Н); 2,88 (т розщепл., J=7 та 2Гц:2Н); 3,16 (т розщепл., J=7 та 2Гц:2Н); від 4,10 до 4,25 (м:4Н); від 7,20 до 7,40 (м.:13Н)]. Приклад 28 До розчину 0,412г бензол-1,3-дисульфодихлориду та 0,165см 3 триетиламіну в 20см 3 ацетонітрилу додають по краплях при кімнатній температурі розчин 0,0307г 1-[біс(4-хлорфеніл)метил]азетидин-3-іламіну в 10см 3 ацетонітрилу. Після 3 годин перемішування при кімнатній температурі додають 0,28см 3 20%-ного розчину аміаку та залишають суміш при кімнатній температурі. Через 18 годин суміш фільтрують та насухо випарюють при зниженому тиску (2 ,7кПа). Після хроматографії на колонці із силікагелем (гранулометрія: 0,06-0,200мм, висота 35см, діаметр 2см), елююя під тиском аргону 0,9бар дихлорметаном, потім сумішшю дихлорметан+1об% метанолу та потім сумішшю дихлорметан+2об% метанолу та збираючи фракції об'ємом 30см 3, фракції 23-34 поєднують, насухо випарюють при зниженому тиску (2,7кПа), одержуючи 90мг N-{1-[біс(4хлорфеніл)метил]азетидин-3-іл}-3-сульфамоїлфенілсульфонаміду у вигляді білої твердої речовини [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,78 (т ушир., J=7Гц:2Н); 3,35 (т ушир., J=7Гц:2Н); 4,01 (м:1Н); 4,24 (с:1Н); 5,27 (м:2Н); 5,61 (м:1Н); від 7,15 до 7,35 (м:8Н); 7,67 (т, J=8Гц:1Н); 8,04 (д ушир., J=8Гц:1Н); 8,12 (д ушир., J=8Гц:1Н); 8,49 (с ушир.:1Н)]. Приклад 29 До розчину 80,1мг бензолсульфонілоцтової кислоти та 27мг гідроксибензотриазолу в 0,5см 3 диметилформаміду додають в інертній атмосфері аргону при температурі близької до 23°С 0,031см 3 діізопропілкарбодііміду, розчин 30мг 1-[біс(4-хлорфеніл)метил]азетидин-3-іламіну в 0,5см 3 безводного дихлорметану та 3см 3 безводного дихлорметану. Реакційну суміш залишають на 17 годин при температурі близької до 23°С завантажують у патрон SPE об'ємом 3см 3, що містить 1г фази SCX, попередньо кондиціонованої метанолом. Після дворазового промивання 5см 3 метанолу та потім 4см 3 0,1н. аміачного метанолу цільовий продукт елююють 4см 3 1н. аміачного метанолу. Фракцію, що містить цільовий продукт, випарюють у струмі повітря при температурі близької до 45°С та потім сушать при зниженому тиску (1мбар) при температурі близької до 40°С. У такий спосіб одержують 2-бензолсульфоніл-N-{1-[біс(4хлорфеніл)метил]азетидин-3-іл}ацетаміду у вигляді білої твердої речовини [Спектр ЯМР 1Н (500мгц, CDCI3, d у м.ч.): 2,96 (м:2Н); 3,51 (м:2Н); 4,00 (с:2Н); 4,34 (м:1Н); 4,48 (м:1Н); 7,10 (м:1Н); від 7,20 до 7,45 (м:8Н); 7,57 (т, J=8Гц:2Н); 7,70 (т, J=8Гц:1Н); 7,90 (д, J=8Гц:2Н)]. Приклад 30 До розчину 85,7мг толуолсуль фонілоцтової кислоти та 27мг гідроксибензотриазолу в 0,5см 3 диметилформаміду додають в інертній атмосфері аргону при температурі близької до 23°С 0,031см 3 діізопропілкарбодііміду, розчин 30мг 1-[біс(4-хлорфеніл)метил]азетидин-3-іламіну в 0,5см 3 безводного дихлорметану та 3см 3 безводного дихлорметану. Реакційну суміш залишають на 17 годин при температурі близької до 23°С завантажують у патрон SPE об'ємом 3см 3, що містить 1г фази SCX, попередньо кондиціонованої метанолом. Після дворазового промивання 5см 3 метанолу та потім 4см 3 0,1н. аміачного метанолу цільовий продукт елююють 4см 3 1н. аміачного метанолу. Фракцію, що містить цільовий продукт, випарюють у струмі повітря при температурі близької до 45°С та потім сушать при зниженому тиску (1мбар) при температурі близької до 40°С. Одержують N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}-2-(толуол-4сульфоніл)ацетамід у вигляді жовтого лаку [Спектр ЯМР 1Н (500мгц, CDCI3, d у м.ч.): 2,85 (т, J=7Гц:2Н); 3,07 (c:3H); 3,48 (т, J=7Гц:2Н); 4,24 (c:1H); 4,49 (м:1Н); 7,19 (д ушир., J=6Гц:1Н); від 7,20 до 7,40 (м:8Н); 8,40 (с:1Н)]. Приклад 31 Повторюючи послідовність операцій прикладу 30, ви ходячи з розчину 85,7мг 3-хлор-4метилсульфонілтіофен-2-карбонової кислоти, 27мг гідроксибензотриазола в 0,5см 3 диметилформаміду, 0,031см 3 діізопропілкарбодііміду, розчину 30мг 1-[біс(4-хлорфеніл)метил]азетидин-3-іламіну в 0,5см 3 безводного дихлорметану та 3см 3 безводного дихлорметану, одержують (3-хлор-4-метилсульфонілтіофен-2карбокси)-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}амід у вигляді жовтого лаку [Спектр ЯМР 1Н (500мгц, CDCI3, d у м.ч.): 2,44 (с:3Н); 2,96 (м:2Н); 3,52 (м:2Н); 3,98 (с:2Н); 4,35 (м:1Н); 4,49 (м:1Н); від 7,00 до 7,30 (м розтягнутий:2Н); від 7,20 до 7,45 (м:10Н); 7,76 (д, J=8Гц:2Н)]. Приклад 32 Повторюючи послідовність операцій прикладу 30, виходячи з 96,1мг 3-(2фенілетиленсульфоніл)пропіонової кислоти, 27мг гідроксибензотриазолу, розчинених у 0,5см 3 диметилформаміду, 0,031см 3 діізопропілкарбодііміду, розчину 30мг 1-[біс(4-хлорфеніл)метил]азетидин-3іламіну в 0,5см 3 безводного дихлорметану та 3см 3 безводного дихлорметану, одержують N-{1-[біс(4хлорфеніл)метил]азетидин-3-іл}-3-(2-фенілетиленсульфоніл)пропіонамід у вигляді білої пінистої маси [Спектр ЯМР 1Н (500мгц, CDCI3, d у м.ч.): 2,64 (т, J=7Гц:2Н); 2,88 (м:2Н); 3,33 (т, J=7Гц:2Н); 3,49 (м:2Н); 4,29 (м:1Н); 4,48 (м:1Н); від 5,90 до 6,15 (м розтягнутий: 1Н); 6,41 (д, J=12Гц:1Н); 7,17 (д, J=12Гц:1Н); від 7,20 до 7,35 (м:8Н); 7,41 (м:3Н); 7,64 (м:2Н)]. Приклад 33 Повторюючи послідовність операцій прикладу 31, ви ходячи з 58,5мг 4-метилсульфонілбензойної кислоти та 26,4мг гідроксибензотриазолу, розчинених у 0,5см 3 диметилформаміду, 0,0302см 3 діізопропілкарбодііміду, розчину 30мг 1-[біс(4-хлорфеніл)метил]азетидин-3-іламіну в 0,5см 3 безводного дихлорметану та 3см 3 безводного дихлорметану, одержують N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}-4-метилсульфонілбензамід у вигляді білих кристалів [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 3,03 (м:2Н); 3,09 (с:3Н); 3,61 (т ушир., J=7,5Гц:2Н); 4,35 (с:1Н); 4,73 (м:1Н); 6,55 (д ушир., J=7,5Гц:1Н); від 7,20 до 7,35 (м:8Н); 7,96 (д, J=8Гц:2Н); 8,03 (д, J=8Гц:2Н)]. Приклад 34 Повторюючи послідовність операцій прикладу 31,виходячи з 58,5мг 4-фенілсульфонілбензойної кислоти та 26,4мг гідроксибензотриазолу, розчинених у 0,5см 3 диметилформаміду, 0,0302см 3 діізопропілкарбодііміду, розчину 30мг 1-[біс(4-хлорфеніл)метил]азетидин-3-іламіну в 0,5см 3 безводного дихлорметану та 3см 3 безводного дихлорметану, одержують N-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}4-метансульфонілбензамід у вигляді лаку [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,71 (т, J=7,5Гц:2Н); 2,86 (м:2Н); від 3,40 до 3,55 (м:4Н); 4,26 (с:1Н); 4,45 (м:1Н); 6,22 (д ушир., J=7,5Гц:1Н); від 7,20 до 7,35 (м:8Н); 7,59 (т ушир., J=7,5Гц:2Н); 7,69 (тт, J=7,5 та 1,5Гц:1Н); 7,93 (д ушир., J=7,5Гц:2Н)]. Приклад 35 Повторюючи послідовність операцій прикладу 31, виходячи з 60,2мг 5-метилсульфонілтіофен-2карбонової кислоти та 26,4мг гідроксибензотриазолу, розчинених у 0,5см 3 диметилформаміду, 0,0302см 3 діізопропілкарбодііміду, розчину 30мг 1-[біс(4-хлорфеніл)метил]азетидин-3-іламіну в 0,5см 3 безводного дихлорметану та 3см 3 безводного дихлорметану, одержують (5-метилсул ьфонілтіофен-2-карбокси)-{1-[біс(4хлорфеніл)метил]азетидин-3-іл}амід у вигляді білих кристалів [Спектр ЯМР Η (300мгц, CDCI3, d у м.ч.): 3,03 (м:2Н); 3,21 (с:3Н); 3,57 (дд, J=8 та 7,5Гц:2Н); 4,34 (с:1Н); 4,67 (м:1Н); 6,40 (д ушир., J=7,5Гц:1Н); від 7,20 до 7,35 (м:8Н); 7,48 (д, J=4Гц:1Н); 7,67 (д, J=4Гц:1Н)]. Приклад 36 Повторюючи послідовність операцій прикладу 31, ви ходячи з 71,9мг 5-метилсульфоніл-3-метил-4вінілтіофен-2-карбонової кислоти, розчину 26,4мг гідроксибензотриазолу в 0,5см 3 диметилформаміду, 0,0302см 3 діізопропілкарбодііміду, розчину 30мг 1-[біс(4-хлорфеніл)метил]азетидин-3-іламіну в 0,5см 3 безводного дихлорметану та 3см 3 безводного дихлорметану, одержують (5-метилсульфоніл-3-метил-4вінілтіофен-2-карбокси)-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}амід у вигляді білого порошку [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,47 (с:3Н); 2,97 (м:2Н); 3,14 (с:3Н); 3,57 (дд, J=8 та 7,5Гц:2Н); 4,32 (с:1Н); 4,65 (м:1Н); 5,69 (дд, J=18 та 1Гц:1Н); 5,77 (дд, J=12 та 1Гц:1Н); 6,30 (д ушир., J=7,5Гц:1Н); 6,96 (дд, J=18 та 12:1Н); від 7,20 до 7,35 (м:8Н)]. Приклад 37 Повторюючи послідовність операцій прикладу 31, виходячи з 62,6мг 3-метилсульфонілметилбензойної кислоти, розчину 26,4мг гідроксибензотриазолу в 0,5см 3 диметилформаміду, 0,0302см 3 3 діізопропілкарбодііміду, розчину 30мг 1-[біс(4-хлорфеніл)метил]азетидин-3-іламіну в 0,5см безводного дихлорметану та 3см 3 безводного дихлорметану, одержують (5-метилсульфоніл-3-метил-4-вінілтіофен-2карбокси)-{1-[біс(4-хлорфеніл)метил]азетидин-3-іл}амід у виді білих голок [Спектр ЯМР 1Н (300мгц, (CD3)2SO d6 з добавкою CDCI3, d у м.ч.): 2,84 (с:3Н); 3,02 (т ушир., J=7Гц:2Н); 3,48 (т, J=7Гц:2Н); 4,38 (с:3Н); 4,53 (м:1Н); 7,21 (д, J=8Гц:4Н); 7,34 (д, J=8Гц:4Н); 7,40 (т, J=7,5Гц:1Н); 7,53 (д ушир., J=7,5Гц:1Н); 7,84 (д ушир., J=7,5Гц:1Н); 7,89 (с ушир.:1Н); 8,54 (д, J=7Гц:1Н)]. Приклад 38 (RS)-N-{1-[(4-Хлорфеніл)пірид-3-илметил]азетидин-3-іл}-3,5-дифторбензолсульфонамід може бути отриманий у такий спосіб: до суміші 0,3г гідроброміду (RS)-3-[бром(4-хлорфеніл)метилпіридину та 0,28г гідрохлориду N-азетидин-3-іл-3,5-дифторбензолсульфонаміду в 20см ацетонітрилу додають 0,46г карбонату калію та 41мг йодиду калію, після чого суміш кип'ятять протягом 4 годин. Після охолодження до температури близької до 20°С видаляють фільтрацією нерозчинні матеріали та насухо випарюють суміш при зниженому тиску. Отриманий залишок поглинають 100см 3 етилацетату. Органічну фазу 2 рази промивають 50см 3 води, висушують над сульфатом магнію в присутності тваринного вугілля, фільтрують на целіте та насухо випарюють при зниженому тиску. Одержують 230мг жовтогарячої твердої речовини, що розчиняють у суміші циклогексан/етилацетат (50/50 по об'єму) та очищають хроматографією під тиском на патроні з 10г силікагелю з тієї ж елююючою сумішшю при витраті 6см 3/хв. Фракції 22-56 поєднують та насухо випарюють при зниженому тиску, одержуючи 100мг (RS)-N-{1-[(4-хлорфеніл)піридин-3-ілметил]азетидин-3-іл}-3,5дифторбензолсульфонаміду у вигляді блідо-жовтої пінистої маси, що плавиться при 70°С [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,81 (м:2Н); 3,42 (м:2Н); 4,03 (м:1Н); 4,29 (с:1Н); 5,43 (д, J=9Гц:1Н); 7,01 (тт, J=9 та 2,5Гц:1Н); 7,22 (дд, J=8 та 5Гц:1Н); 7,28 (м:4Н); 7,36 (м:2Н); 7,62 (д ушир., J=8Гц:1Н); 8,48 (дд, J=5 та 1Гц:1Н); 8,59 (д, J=1Гц:1Н)]. (RS)-3-[Бром(4-хлорфеніл)метилпіридин одержують у такий спосіб: до 1,5г (4-хлорфеніл)пірид-3илметанолу додають 3,5см 3 48%-ного розчину бромистоводневої кислоти в оцтовій кислоті та 1см 3 ацетилброміду. Отриману в такий спосіб суміш бурштинового кольору кип'ятять протягом 4 годин, після чого охолоджують до 20°С, насухо випарюють при 40°С та тиску 2,7кПа, що дає 1,53г (RS)-3-[бром(4хлорфеніл)метилпіридину (Rf=75/90, 254нм, пластини із силікагелем, посилання 1.05719, Merck KgaA, 64271 Darmstadt, Німеччина). Гідрохлорид N-азетидин-3-іл-3,5-дифторбензолсульфоніламіду може бути отриманий у такий спосіб: у гідрогенізаторі об'ємом 2000см 3 протягом приблизно 20 годин піддають гідруванню розчин 7,5г N-(1бензгідрилазетидин-3-іл)-3,5-дифторбензолсульфоніламіду в суміші 10см 3 концентрованої (36% мас) соляної кислоти, 1,7см 3 оцтової кислоти та 500см 3 метанолу в присутності 4,21г гідроксиду паладію на вуглі (20% мас каталізатора) під тиском 1,7 бар водню. Каталізатор видаляють фільтрацією через шар целіту, після чого фільтрат насухо випарюють при зниженому тиску. Отриманий залишок приблизно 16 годин розтирають з 100см діізопропілового ефіру при температурі близької до 20°С. Суспензію фільтрують та твердий залишок знову розтирають з 100см 3 діетилового ефіру при температурі близької до 20°С. Відфільтровану після цього пасту сушать при зниженому тиску при температурі близької до 40°С, одержуючи 5,52г гідрохлориду Nазетидин-3-іл-3,5-дифторбензолсульфоніламіду, у формі білого порошку. N-(1-бензгідрилазетидин-3-іл)-3,5-дифторбензолсульфоніламід може бути отриманий у такий спосіб: до суспензії 5г 1-бензгідрилазетидин-3-іламіну в 80см 3 дихлорметану при температурі близької до 20°С послідовно додають 5,1г 3,5-дифторбензолсульфонілхлориду та потім 4,2см 3 триетиламіну. Після 20 годин перемішування при температурі близької до 20°С додають 50см 3 води, органічну фазу відокремлюють, двічі промивають 50см 3 води, висушують над сульфатом магнію та випарюють при зниженому тиску. Одержують у такий спосіб 8,99г жовтого масла, що поступово кристалізується. 4,5г цього продукту очи щають хроматографією під тиском на 500г силікагелю Аmісоn (діаметр часток 0,020-0,045мм), елююя сумішшю метанол/дихлорметан (1/99 по об'єму). Фракції, що містять цільовий продукт, поєднують та насухо випарюють при зниженому тиску, одержуючи 3,58г N-(1-бензгідрилазетидин-3-іл)-3,5-дифторбензолсульфоніламіду у вигляді порошку бежевого кольору. Кількість, що залишилася, отриманої вище жовтого масла очищають у тих же умовах, одержуючи 3,92г N-(і-бензгідрилазетидин-3-іл)-3,5-дифторбензолсульфоніламіду у вигляді порошку бежевого кольору. 1-бензгідрилазетидин-3-іламін може бути отриманий як описано в J. Antibiot., 39(9), 1243-1256, 1986. 3,5-дифторбензолсульфонілхлорид може бути отриманий як описано в патенті FR 2757509. Приклад 39 (RS)-N-{1-[(4-хлорфеніл)піримід-3-илметил]азетидин-3-іл}-3,5-дифторбензолсульфонамід може бути отриманий, повторюючи послідовність операцій для одержання (RS)-N-{1-[(4-хлорфеніл)пірид-3илметил]азетидин-3-іл}-3,5-дифторбензолсульфонаміду: виходячи з 0,64г гідроброміду (RS)-5-[бром(4хлорфеніл)метилпіримідину, 0,5г гідрохлориду N-азетидин-3-іл-3,5-дифторбензолсульфонаміду в 20см 3 ацетонітрилу, 1,213г карбонату калію та 379мг йодиду калію, одержуючи при цьому 71мг (RS)-N-{1-[(4хлорфеніл)піримідин-5-ілметил]азетидин-3-іл}-3,5-дифторбензолсульфонаміду у виді жовтої пінистої маси [Спектр ЯМР 1Н (300мгц, CDCI3, d у м.ч.): 2,83 (м:2Н); 3,46 (м:2Н); 4,03 (м:1Н); 4,30 (с:1Н); 5,00 (д, J=9Гц:1Н); 7,04 (тт, J=9 та 2,5Гц:1Н); від 7,20 до 7,35 (м:4Н); 7,37 (м:2Н); 8,69 (с:2Н);9,09(с:1Н)]. (RS)-5-[Бром(4-хлорфеніл)метилпіримідин може бути отриманий, повторюючи послідовність операцій для одержання (RS)-3-[бром-(4-хлорфеніл)метил]піридин, виходячи з (4-хлорфеніл)піридин-5-илметанолу. (4-хлорфеніл)піридин-5-ілметанол може бути отриманий як при одержанні (4-хлорфеніл)піридин-3ілметанолу, ви ходячи з піримідин-5-карбоксальдегиду та 4-хлор фенілмагнійброміду. Лікарські засоби за винаходом являють собою сполуку формули І або ізомер, або сіль цієї сполуки в чистому стані, або у вигляді композиції, у якій ця сполука асоційована з будь яким іншим фармацевтично прийнятним продуктом, що може бути інертним або фізіологічно активним. Лікарські засоби за винаходом можуть застосовуватися перорально, парентерально, ректально або місцево. Як тверді композиції для перорального застосування можуть використовува тися таблетки, пігулки, порошки (желатинові капсули, крохмальні облатки) або гранули. Активний початок згідно винаходу змішують в цих композиціях у струмі аргону з одним або декількома інертними розріджувачами такими як крохмаль, целюлоза, сахароза, лактоза або кремнезем. Ці композиції можуть також містити інші речовини, що відрізняються від розріджувачів, наприклад один або кілька мастильних агентів таких як стеарат магнію або тальк, барвник, оболонку (драже) або лак. Як рідкі композиції для перорального застосування можуть використовуватися фармацевтично прийнятні розчини, суспензії, емульсії, сиропи й еліксири, що містять інертні розріджувачі такі як вода, етанол, гліцерин, рослинні олії або парафінова олія. Ці композиції можуть містити й відмінні від розріджувачів речовини, наприклад які змочують, підсолоджують, загущають, ароматизують або стабілізуючі продукти. Стерильні композиції для парентерального застосування можуть бути переважно водними або неводними розчинами, суспензіями або емульсіями. Як розчинник або носій може бути використана вода, пропіленгліколь, поліетиленгліколь, рослинні олії (зокрема маслинова олія), прийнятні для ін'єкції органічні складні ефіри, наприклад етилолеат, або інші придатні органічні розчинники. Ці композиції можуть також містити допоміжні засоби, зокрема агенти, що змочують, ізотонізатори, емульгатори, дисперсанти та стабілізатори. Стерилізація може бути здійснена безліччю способів, наприклад асептичною фільтрацією, введенням у композицію агентів, що стерилізують, опроміненням або нагріванням. Вони можуть бути також отримані у виді твердих стерильних композицій, що можуть бути розчинені безпосередньо перед застосуванням у стерильній воді або будь-якому іншому придатному для ін'єкцій стерильному середовищі. Композиції для ректального застосування являють собою свічі або ректальні капсули, що крім активного продукту містять наповнювачі, такі як олія какао, напівсинтетичні гліцериди або поліетиленгліколі. Композиції для місцевого застосування можуть, наприклад, являти собою креми, лосьйони, очні примочки, рідини для полоскання порожнини рота, краплі для носа або аерозолі. В області терапії людини сполуки за винаходом можуть бути, зокрема, використані для лікування та/або попередження психозів, включаючи шизофренію, відчуття тривоги, депресію, епілепсію, нейродегенерацію, мозкові та спинномозкові розлади, порушення функції пізнання, черепні травми, панічні приступи, периферичні нейропатії, глаукоми, мігрень, хворобу Паркінсона, хворобу Альцгеймера, хорею Хантингтона, синдром Рейно, тремтіння, симптоми примусової нав'язливості, старече слабоумство, порушення тимусу, синдром Туретта, уповільненої дискінезії, двополюсних розладів, раку, порушення рухового апарата під впливом лік, дистонії, ендотоксемічних шоків, геморагічних шоків, гіпотензії, безсоння, імунологічних захворювань, бляшаного склерозу, блювоти, астми, порушення апетиту (булімія, анорексія), ожиріння, порушення пам'яті, порушення проходу по кишечнику, при відібранні від грудей у процесі хронічного лікування, та зловживання алкоголем або ліками (наприклад опіоідами, барбітуратами, коноплею, кокаїном, амфетамінами, фенциклідом, галюциногенами, бензодіазепінами), такі як анальгетики або підсилювачі анальгетичної активності наркотичних та ненаркотичних лік. Дози залежать від бажаного ефекту, від тривалості лікування та від використовуваного способу введення. Звичайно вони лежать у межах від 5 до 1000мг у добу при пероральному застосуванні у дорослого, у той час як разові дози варіюють від 1 до 250мг активної речовини. У загальному випадку лікарю варто визначати придатне дозування в залежності від віку, ваги й інших факторів, що відносяться до лікування індивідууму, що піддається такому лікування. Композиції винаходу ілюстр ують наступні приклади: ПРИКЛАД А Використовуючи звичайні методи, готують желатинові капсули з дозою 50мг активного продукту, що мають наступний склад: Сполука формули І 50мг Целюлоза 18мг Лактоза 55мг Колоїдальний кремнезем 1мг Карбоксиметилкрохмаль натрієвий 10мг Тальк 10мг Стеарат магнію 1мг ПРИКЛАД В Використовуючи звичайні методи, готують таблетки з дозою 50мг активного продукту, що мають наступний склад: Сполука формули І 50мг Лактоза 104мг Целюлоза 40мг Полівідон 10мг Карбоксиметилкрохмаль натрієвий 22мг Тальк 10мг Стеарат магнію 2мг Колоїдальний кремнезем 2мг Суміш гідроксиметилцелюлози, 245мг у гліцерину й оксиду титана кінцевій (72/3,5/24,5) у достатній кількості таблетці з до оболонкою ПРИКЛАД С Готують розчин для ін'єкцій, який містить 10мг активного продукту, що має наступний склад: Сполука формули І 10мг Бензойна кислота 80мг Бензиловий спирт 0,06мл Бензоат натрію 80мг 95%-ний етанол 0,4мл Гідроксид натрію 24мг Пропіленгліколь 1,6мл Вода в достатній кількості до 4мл
ДивитисяДодаткова інформація
Назва патенту англійськоюPharmaceutical compositions containing 3-aminoazetidine derivatives, derivatives and a method for obtaining thereof
Назва патенту російськоюФармацевтические композиции, которые содержат производные 3-аминоазетидина, производные и способ их получения
МПК / Мітки
МПК: A61P 25/28, A61P 25/24, A61P 25/00, A61P 29/00, A61P 9/02, A61K 31/4427, A61P 37/00, C07D 403/08, A61P 5/00, A61K 31/4709, A61K 31/4025, A61K 47/00, A61P 25/02, A61P 27/02, A61P 11/00, A61K 31/4178, A61P 25/20, C07D 205/00, C07D 401/12, A61P 9/08, A61P 25/14, A61K 31/506, A61P 25/08, A61P 1/08, A61P 35/00, A61K 31/397, A61P 25/16, C07D 409/12, A61P 1/00, A61P 11/06, C07D 401/06, A61P 1/14, A61P 9/00, A61P 25/18, A61P 3/04, C07D 403/12, A61P 25/22, A61P 23/00
Мітки: спосіб, 3-аміноазетидину, одержання, похідні, містять, композиції, фармацевтичні, їхнього
Код посилання
<a href="https://ua.patents.su/13-72319-farmacevtichni-kompozici-shho-mistyat-pokhidni-3-aminoazetidinu-pokhidni-i-sposib-khnogo-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">Фармацевтичні композиції, що містять похідні 3-аміноазетидину, похідні і спосіб їхнього одержання</a>
Попередній патент: Печиво вівсяне з кунжутом
Наступний патент: Фармацевтична композиція, що містить водну суспензію субмікронних ефірів 9-гідроксирисперидон жирних кислот
Випадковий патент: Багатопульсова несиметрична випрямна система