Антихолінергічні засоби, які застосовуються як медикаменти, спосіб їх одержання та фармацевтична композиція
Номер патенту: 73804
Опубліковано: 15.09.2005
Автори: Райхль Річард, Спек Георг, Майсснер Гельмут, Піпер Міхаель Пауль, Моршойзер Герд, БАНХОЛЬЦЕР Рольф, Поль Геральд
Формула / Реферат
1. Сполуки загальної формули 1
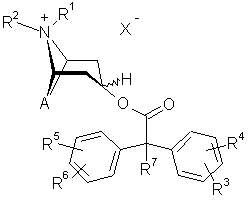 , 1
, 1
у якій
A означає залишок із двома зв'язками, вибраний із групи, яка включає
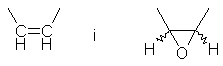 ,
,
X- означає однозарядний аніон,
R1 і R2 мають ідентичні або різні значення і являють собою залишок, вибраний із групи, яка включає метил, етил, н-пропіл і ізопропіл, при цьому такий залишок необов'язково може бути заміщений гідроксигрупою або фтором,
R3, R4, R5 і R6 мають ідентичні або різні значення і являють собою водень, метил, етил, метилоксигрупу, етилоксигрупу, гідроксигрупу, фтор, хлор, бром, CN, CF3 або NO2, і
R7 означає метил, етил, метилоксигрупу, етилоксигрупу, -CH2-F, -CH2-CH2-F, -O-CH2-F, -O-CH2-CH2-F, -CH2-OH, -CH2-CH2-OH, CF3, -CH2-OMe, -CH2-CH2-OMe, -CH2-OEt, -CH2-CH2-OEt, -O-COMe, -O-COEt, -O-COCF3, фтор, хлор або бром,
необов'язково у вигляді окремих оптичних ізомерів, сумішей окремих енантіомерів або рацематів.
2. Сполуки загальної формули 1 за п. 1, у якій
X- переважно вибирають із групи, яка включає хлорид, бромід, метилсульфат, 4-толуолсульфонат і метансульфонат.
3. Сполуки загальної формули 1 за п. 1 або п. 2, у якій
A означає залишок із двома зв'язками, вибраний із групи, яка включає
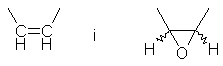 ,
,
X - означає однозарядний аніон, вибраний із групи, яка включає хлорид, бромід і метансульфонат,
R1 і R2 мають ідентичні або різні значення і являють собою залишок, вибраний із групи, яка включає метил і етил, при цьому такий залишок необов'язково може бути заміщений гідроксигрупою або фтором,
R3, R4, R5 і R6 мають ідентичні або різні значення і являють собою водень, метил, етил, метилоксигрупу, етилоксигрупу, гідроксигрупу, фтор, хлор або бром, і
R7 означає метил, етил, метилоксигрупу, етилоксигрупу, CF3 або фтор,
необов'язково у вигляді окремих оптичних ізомерів, сумішей окремих енантіомерів або рацематів.
4. Сполуки загальної формули 1 за будь-яким з пп. 1 - 3, у якій
A означає залишок із двома зв'язками, вибраний із групи, яка включає
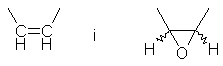 ,
,
X - означає бромід,
R1 і R2 мають ідентичні або різні значення і являють собою залишок, вибраний із групи, яка включає метил і етил,
R3, R4, R5 і R6 мають ідентичні або різні значення і являють собою водень, метил, метилоксигрупу, хлор або фтор, і
R7 означає метил або фтор,
необов'язково у вигляді окремих оптичних ізомерів, сумішей окремих енантіомерів або рацематів.
5. Сполуки загальної формули 1 за будь-яким з пп. 1-4, у якій
A означає залишок із двома зв'язками, вибраний із групи, яка включає
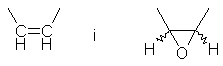 ,
,
X- означає бромід,
R1 і R2 мають ідентичні або різні значення і являють собою метил або етил,
R3, R4, R5 і R6 мають ідентичні або різні значення і являють собою водень або фтор, і
R7 означає метил або фтор,
необов'язково у вигляді окремих оптичних ізомерів, сумішей окремих енантіомерів або рацематів.
6. Застосування сполуки загальної формули 1 за будь-яким з пп.1-5 як лікарського засобу.
7. Застосування сполуки загальної формули 1 за будь-яким з пп. 1-5 для одержання лікарського засобу, призначеного для лікування астми, хронічного обструктивного захворювання легень (ХОЗЛ), вагальних синусових брадикардій, порушень серцевого ритму, спазмів у шлунково-кишковому тракті, спазмів у сечовивідних шляхах і при больових відчуттях при менструації.
8. Застосування сполуки загальної формули 1 за п. 7 для одержання лікарського засобу, призначеного для лікування астми або ХОЗЛ.
9. Фармацевтична композиція, яка містить як діючу речовину одну або декілька сполук загальної формули 1 за будь-яким з пп.1-5 або їх фізіологічно прийнятні солі, необов'язково в сполученні із звичайними допоміжними речовинами і/або носіями.
10. Фармацевтична композиція за п. 8, яка відрізняється тим, що вона разом з однією або декількома сполуками формули 1 містить також принаймні ще одну діючу речовину, вибрану з групи, яка включає бетаміметики, протиалергічні засоби, антагоністи фактора активації тромбоцитів, антагоністи лейкотриєну і стероїди.
11. Спосіб одержання сполуки загальної формули 1
 , 1
, 1
у якій A, X- і залишки R1, R2, R3, R4, R5, R6 і R7 можуть мати вказані в пп. 1-5 значення, який відрізняється тим, що на першій стадії сполуку загальної формули 3
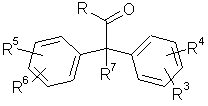 , 3
, 3
у якій залишки R3, R4, R5, R6 і R7 можуть мати вказані в пп. 1-5 значення, а R означає хлор або C1-C4алкілоксигрупу, піддають взаємодії зі сполукою формули 2
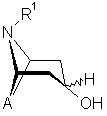 , 2
, 2
у якій A і R1 можуть мати вказані в пп. 1-5 значення, з одержанням сполуки формули 4
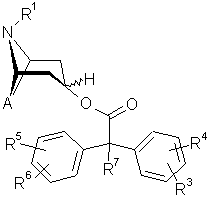 , 4
, 4
у якій A і залишки R1, R3, R4, R5, R6 і R7 можуть мати вказані в пп. 1-5 значення, і потім цю сполуку взаємодією зі сполукою формули
R2-X,
у якій R2 і X можуть мати вказані в пп. 1-5 значення, піддають кватернізації до сполуки формули 1.
Текст
Даний винахід стосується нових анти холінергічних засобів загальної формули І у якій А, X- і залишки R1, R2, R3, R4, R5, R6 і R7 можуть мати вказані у формулі винаходу й у подальшому описі значення, способу їх одержання, а також їх застосування як лікарських засобів. Застосування антихолінергічних засобів доцільно з терапевтичної точки зору при багатьох захворюваннях. При цьому особливо слід зазначити, наприклад, терапію астми або ХОЗЛ (хронічне обструктивне захворювання легень). Для лікування подібних захворювань у WO 92/16528 були запропоновані антихолінергічні засоби, основу молекули яких утворює скопіновий, тропеноловий або ж тропіновий скелет. Покладена в основу заявленого в WO 92/16528 винаходу задача полягала у тому, щоб запропонувати сполуки, які мають антихолінергічну активність, що характеризуються дією, яка зберігається впродовж тривалого періоду часу. Для вирішення цієї задачі в WO 92/16528 минулого запропоновані серед інших бензилові ефіри скопіну, тропенолу або ж тропіну. Для медикаментозної терапії хронічних захворювань часто бажано мати у своєму розпорядженні лікарські засоби, які мають тривалу дію. За рахунок цього, як правило, вдається протягом тривалого проміжку часу забезпечити підтримання в організмі необхідної для досягнення терапевтичного ефекту концентрації діючої речовини без необхідності надмірно частого повторного введення лікарського засобу. В іншому ж введення діючої речовини з меншою періодичністю в значній мірі сприяє хорошому самопочуттю пацієнта. Найбільш бажано при цьому мати у своєму розпорядженні лікарський засіб, який дозволяв б досягати потрібного терапевтичного ефекту при його однократному введенні в день (тобто лікарський засіб, розрахований на однократний прийом на день). Перевага, пов'язана із застосуванням лікарського препарату тільки один раз на день, полягає в зручності подібної схеми лікування для пацієнта завдяки порівняно швидкому його звиканню до регулярного прийому медикаменту у певний період доби. До призначеної для введення в організм діючої речовини, щоб її можна було використовувати як медикамент, розрахований на однократне застосування на день, пред'являються особливі вимоги. З одного боку, необхідна дія повинна наставати порівняно швидко після введення лікарського засобу, ефективність якої в ідеальному випадку повинна зберігатися по можливості на постійному рівні протягом наступного досить тривалого проміжку часу. З іншого боку, тривалість дії лікарського засобу не повинна істотно перевищувати одну добу. В ідеальному випадку діюча речовина повинна мати такий профіль дії, щоб можна було цілеспрямовано керувати процесом одержання розрахованого на однократне введення в день лікарського засобу, що містить діючу речовину в терапевтично оптимальних дозах. Було встановлено, що описані в WO 92/16528 бензилові ефіри скопіну, тропенолу або ж тропіну не задовольняють подібним підвищеним вимогам. Ці сполуки, оскільки їх дія зберігається протягом винятково тривалого періоду часу, що значно перевищує вказаний вище проміжок часу, який становить приблизно одну добу, не придатні для їх терапевтичного застосування як медикаменти, розрахованих на один прийом на день. Виходячи з вищевикладеного, в основу даного винаходу була покладена задача запропонувати нові антихолінергічні засоби, які завдяки їх профілю дії дозволяли б одержувати на їх основі лікарські препарати, розраховані на однократне введення на день. Ще одна задача винаходу полягала в тому, щоб запропонувати сполуки з дією, яка порівняно швидко наступає. Задача винаходу полягала також у тому, щоб запропонувати сполуки, ефективність яких зберігалася б після швидкого настання їх дії по можливості на постійному рівні протягом наступного досить тривалого проміжку часу. Інша задача винаходу полягала в тому, щоб запропонувати сполуки, тривалість дії яких при їх застосуванні в терапевтично оптимальних дозах не перевищувала б істотно період часу, що дорівнює приблизно одній добі. Крім цього задача винаходу полягала також у тому, щоб запропонувати сполуки з таким профілем дії, який дозволяв би ефективно регулювати їх терапевтичну дію (тобто їх терапевтичний ефект повинен виявлятися повною мірою без побічної дії, яка полягає в накопиченні сполуки в організмі пацієнта). При створенні винаходу несподівано було встановлено, що вказані вище задачі вдається вирішити за допомогою сполук загальної формули 1, у яких залишок R7 не означає гідроксигрупу. Відповідно до цього в даному винаході пропонуються сполуки загальної формули 1. у якій А означає залишок із двома зв'язками, вибраний із групи, яка включає X- означає однозарядний аніон, R1 і R2 означають С1-С4-алкіл, який необов'язково може бути заміщений гідроксигрупою або галогеном, R3, R4, R5 і R6 мають ідентичні або різні значення і являють собою водень, С1-С4алкіл, С1С4алкілоксигрупу, гідроксигрупу, CF 3, CN, NO 2 або галоген, R7 означає водень, С1-С4алкіл, С1-С4алкілоксигрупу, С1-С4алкіленгалоген, галоген-С1-С4алкілоксигрупу, С1-С4алкілен-ОН, CF3, - С1-С4алкілен-С1-С4алкілоксигрупу, -О-СОС 1-С4алкіл, -О-СОС1-С4алкілгалоген, -OCOCF3 або галоген, при цьому в тому випадку, якщо А представляє собою залишок то R1 і R2 означають метил, R3, R4, R* і R6 означають водень, а R7 не може означати водень. Переважні сполуки загальної формули 1, у яких А означає залишок із двома зв'язками, вибраний із групи, яка включає X- означає однозарядний аніон, вибраний із групи, яка включає хлорид, бромід, метилсульфат, 4толуолсульфонат і метансульфонат, переважно бромід, R1 і R2 мають ідентичні або різні значення і являють собою залишок, вибраний із групи, яка включає метил, етил, н-пропіл і ізопропіл, при цьому такий залишок необов'язково може бути заміщений гідроксигрупою або фтором, переважно незаміщений метил, R3, R4, R5 і R6 мають ідентичні або різні значення і являють собою, водень, метил, етил, метилоксигрупу, етилоксигрупу, гідроксигрупу, фтор, хлор, бром, CN, CF3 або NO2 і R7 означає водень, метил, етил, метилоксигрупу, етилоксигрупу, -CH2-F, -CH2-CH2-F, -O-CH2-F, -O-CH2CH2-F, -CH2-OH, -CH 2-CH2-OH, CF3, -СН3-ОМе, -СН2-СН2-ОМе, -CH2-OEt, -CH2-CH2-OEt, -О-СОМе, -O-COEt, O-COCF3, -O-COCF3 , фтор, хлор або бром. Більш переважні сполуки загальної формули 1, у яких А означає залишок із двома зв'язками, вибраний із групи, яка включає X- означає однозарядний аніон, вибраний із групи, яка включає хлорид, бромід і метансульфонат, переважно бромід, R1 і R2 мають ідентичні або різні значення і являють собою залишок, вибраний із групи, яка включає метил і етил, при цьому такий залишок необов'язково може бути заміщений гідроксигрупою або фтором, переважно незаміщений метил, R3, R4, R5 і R6 мають ідентичні або різні значення і являють собою, водень, метил, етил, метилоксигрупу, етилоксигрупу, гідроксигрупу, фтор, хлор або бром і R7 означає водень, метил, етил, метилоксигрупу, етилоксигрупу, CF3 , або фтор. Відповідно до винаходу переважними є також сполуки загальної формули 1, у яких А означає залишок із двома зв'язками, вибраний із групи, яка включає X- означає бромід, R1 і R2 мають ідентичні або різні значення і являють собою залишок, вибраний із групи, яка включає метил і етил, переважно метил, R3, R4, R5 і R6 мають ідентичні або різні значення і являють собою, водень, метил, метилоксигрупу, хлор або фтор і R7 означає водень, метил або фтор. Особливо переважними є відповідно до винаходу сполуки загальної формули 1, у яких А означає залишок із двома зв'язками, вибраний із групи, яка включає X- означає бромід, R1 і R2 мають ідентичні або різні значення і являють собою метил або етил, переважно метил, R3, R4, R5 і R6 мають ідентичні або різні значення і являють собою водень або фтор, переважно водень, і R7 означає водень, метил або фтор, переважно метил або фтор, найбільш переважно метил. Об'єктом винаходу є відповідні сполуки формули X, представлені за певних умов у вигляді окремих оптичних ізомерів, сумішей окремих енантіомерів або рацематів. У сполуках загальної формули 1 кожний із залишків R3, R4, R5 і R6, якщо вони не означають водень, може знаходитися в орто-, мета- або пара-положенні відносно місця приєднання до групи "-C-R7". Якщо ні один із залишків R3, R4, R5 і R6 не означає водень, то R3 і R5 переважно приєднані в пара-положенні, a R4 і R6 переважно приєднані в орто- або мета-положенні, найбільш переважно в .мета-положенні. Якщо ж один із залишків R3 і R4 і один із залишків R і R6 означає водень, то відповідний інший залишок переважно приєднаний у мета- або пара-положенні, найбільш переважно в пара-положенні. Якщо ні один із залишків R3, R4, R5 і R6 не означає водень, то особливо переважні відповідно до винаходу сполуки загальної формули 1, у котрих залишки R3, R4, R5 і R6 мають ідентичне значення. Особливо переважними є відповідно до винаходу сполуки загальної формули 1, у яких складноефірний замісник в біциклічному атомі азоту має а-конфігурацію. Такі сполуки відповідають загальній формулі 1-a Особливе значення мають відповідно до винаходу наступні сполуки: - метобромід тропенолового ефіру 2,2-дифенілпропіонової кислоти, - метобромід скопінового ефіру 2,2-дифенілпропіонової кислоти, - метобромід скопінового ефіру 2-фтор-2,2-дифенілоцтової кислоти, - метобромід тропенолового ефіру 2-фтор-2,2-дифенілоцтової кислоти. У контексті даного опису під алкільними групами маються на увазі, якщо не вказано інше, розгалужені і нерозгалужені алкільні групи з 1-4 атомами вуглецю. Як приклад можна назвати метил, етил, пропіл або бутил. Для позначення подібних груп, тобто метилу, етилу, пропілу або ж бутилу, у деяких випадках використовуються також відповідні для них скорочені назви Me, Et, Prop або Вu. Якщо не вказане інше, то в поняття "пропіл" і "бутил" включені також усі можливі ізомерні форми кожного з таких залишків. Так, наприклад, у поняття "пропіл" включений н-пропіл і ізопропіл, а в поняття "бутил" включений ізобутил, вторбутил, mpem-бутил і т.д. Під алкіленовими групами маються на увазі, якщо не вказано інше, розгалужені і нерозгалужені алкільні містки з двома зв'язками і з 1-4 атомами вуглецю. Як приклад при цьому можна назвати метилен, етилен, пропілен або бутилен. Алкіленгалогеновими групами позначаються, якщо не вказано інше, розгалужені і нерозгалужені алкільні містки з двома зв'язками і з 1-4 атомами вуглецю, одно-, дво- або тризаміщені, переважно однозаміщені, галогеном. Аналогічним способом алкілен-ОН-групи являють собою, якщо не вказано інше, розгалужені і нерозгалужені алкільні містки з двома зв'язками і з 1-4 атомами вуглецю, одно-, дво- або тризаміщені, переважно однозаміщені, гідроксигрупою. Під алкілоксигрупами маються на увазі, якщо не вказано інше, розгалужені і нерозгалужені алкільні групи з 1-4 атомами вуглецю, приєднані через атом кисню. Як приклад при цьому можна назвати метилокси-, етилокси-, пропілокси- або бутилоксигрупу. У деяких випадках для позначення таких гр уп, тобто метилокси-, етилокси-, пропілокси- або ж бутилоксигрупи, використовуються також відповідні для них скорочення MeO-, EtO-, PropO- або Вu-. Якщо не вказано інше, то в поняття "пропілоксигрупа" і "бутилоксигрупа" включені також усі можливі ізомерні форми кожного з таких залишків. Так, наприклад, у поняття "пропілоксигрупа" включені н-пропілоксигрупа і ізопропілоксигрупа, у поняття "бутилоксигрупа" включені ізобутилоксигрупа, вmор-бутилоксигрупа, mpem-бутилоксигрупа і т.д. У деяких випадках у даному описі замість позначення "алкілоксигрупа" використовується також еквівалентне до нього поняття "алкоксигрупа". Відповідно до цього для позначення таких груп, як метилокси-, етилокси-, пропілокси- або ж бутилоксигрупа, у деяких випадках використовуються еквівалентні для них поняття метокси-, етокси-, пропокси- або бутоксигрупа. Алкіленалкілоксигрупи являють собою, якщо не вказано інше, розгалужені і нерозгалужені алкільні містки з двома зв'язками і з 1-4 атомами вуглецю, одно-, дво- або тризаміщені, переважно однозаміщені, алкілоксигрупою. Під -О-СО-алкільними групами маються на увазі, якщо не вказано інше, розгалужені і нерозгалужені алкільні групи з 1-4 атомами вуглецю, приєднані через складноефірну груп у. При цьому алкільні групи безпосередньо приєднані до вуглецю карбонілу складноефірної групи. Аналогічним способом трактується і поняття "-О-СО-алкілгалогенова група". Група -О-СО-CF 3 являє собою трифторацетат. Галоген у контексті даного винаходу являє собою фтор, хлор, бром або йод. Якщо не вказано інше, то фтор і бром є переважними галогенами. Група CO являє собою карбонільну гр упу. Запропоновані у винаході сполуки частково можна одержувати, як це більш докладно описано нижче, аналогічно до уже відомих з рівня техніки методів (схема 1). Похідні карбонової кислоти формули 3 відомі з рівня техніки або їх можна одержувати за відомими з рівня техніки методами синтезу. Якщо з рівня техніки відомі тільки відповідним чином заміщені карбонові кислоти, то сполуки формули 3 можна також безпосередньо одержувати з них шляхом каталізованою кислотою або основою етерифікації відповідними спиртами або шляхом галогенування відповідними галогенувальними агентами. Складні ефіри загальної формули 4 одержують виходячи зі сполук формули 2 їх взаємодією з похідними карбонової кислоти формули 3, у яких R означає, наприклад, хлор або С 1-С4алкілоксигрупу. Якщо R являє собою С1-С4алкілоксигрупу, то таку взаємодію можна проводити, наприклад, у розплаві натрію при підвищеній температурі, переважно при приблизно 50-150°С, найбільш переважно при приблизно 90-100°С, і при зниженому тиску, переважно при тиску менше 500мбар, найбільш переважно менше 75мбар. В іншому варіанті замість похідних формули 3, у яких R являє собою С1-С4алкілоксигрупу, можна також використовува ти відповідні хлорангідриди кислот (R означає СІ). Отримані таким шляхом сполуки формули 4 взаємодією зі сполуками формули R2-X, у яких R2 і X можуть мати вказані вище значення, можна перевести в необхідні сполуки формули 1. Цю стадію синтезу також можна проводити аналогічно до розглянутих у WO 92/16528 прикладів синтезу. Альтернативно до представленого на схемі 1 методу синтезу сполук формули 4 похідні формули 4, у яких азотвмісний біцикл являє собою похідне скопіну, можна одержувати окисленням (епоксидуванням) сполук формули 4, у яких азотвмісний біцикл являє собою залишок тропенілу. З цією метою відповідно до винаходу можна використовувати наступний підхід. Сполуку формули 4, у якій А являє собою -СН=СН -, суспендують у полярному органічному розчиннику, переважно в розчиннику, вибраному з групи, яка включає N-метил-2-піролідон (Ν-ΜΠ), диметилацетамід і диметилформамід, переважно диметилформамід, і потім отриману суспензію нагрівають до температури порядку 30-90°С, переважно 40-70°С. Після цього додають прийнятний окисник і перемішують при постійній температурі протягом 2-8год, переважно 3-6год. Як окисник переважно використовувати пентоксид ванадію в суміші з Н 2О 2, найбільш переважно комплекс Н2О2-сечовина в сполученні з пентоксидом ванадію. Наступну переробку реакційної суміші проводять звичайним способом. Продукт залежно від його тенденції до кристалізації можна очищати кристалізацією або хроматографією. В іншому варіанті сполуки формули 4, у яких R7 означає галоген, можна також одержувати за методом, проілюстрованим нижче на схемі 2. Відповідно до цього методу бензилові ефіри формули 5 переводять із застосуванням прийнятних галогенувальних агентів у сполуки формули 4, у яких R7 означає галоген. Реакція галогенування, проведена відповідно до схеми 2, досить добре відома з рівня техніки. Бензилові ефіри формули 5 одержують за відомими або аналогічно до відомих з рівня техніки методів (див., наприклад, WO 92/16528). Очевидно, що в реакції, проілюстрованій на схемі 1, важливе значення мають проміжні продукти загальної формули 4. Відповідно до цього ще одним об'єктом даного винаходу є проміжні сполуки формули 4 у якій А означає залишок із двома зв'язками, вибраний із групи, яка включає R1 означає С1-С4алкіл, який необов'язково може бути заміщений гідроксигрупою або галогеном, R3, R4, R5 і R6 мають ідентичні або різні значення і являють собою, водень, С1-С4алкіл, Сі С4алкілоксигрупу, гідроксигрупу, CF 3, CN, NO 2 або галоген і R7 означає водень, С1-С4алкіл, С1-С4алкілоксигрупу, С1-С4алкіленгалоген, галоген-С1-С4алкілоксигрупу, С1-С4-алкілен-ОН, CF3, -С1-С4алкілен-С 1-С4алкілоксигрупу, -О-СОС1-С4алкіл, -О-СОС1-С4алкілгалоген, -OCOCF3 або галоген, при цьому в тому випадку, якщо А являє собою залишок , то R1 означає метил, 3 4 5 6 R , R , R і R означають водень, а R7 не може означати н-пропіл. Переважні при цьому ті сполуки загальної формули 4, у яких А означає залишок із двома зв'язками, вибраний із групи, яка включає R1 являє собою залишок, вибраний із групи, яка включає метил, етил, н-пропіл і ізопропіл, при цьому такий залишок необов'язково може бути заміщений гідроксигрупою або фтором, переважно являє собою незаміщений метил, R3, R4, R5 і R6 мають ідентичні або різні значення і являють собою, водень, метил, етил, метилоксигрупу, етилоксигрупу, гідроксигрупу, фтор, хлор, бром, CN, CF3 або NO2 і R7 означає водень, метил, етил, метилоксигрупу, етилоксигрупу, -CH2-F, -CH2-CH2-F, -O-CH2-F, -O-CH2CH2-F, -CH2-OH, -CH 2-CH2-OH, CF3, -СН2-ОМе, -СН2-СН2-ОМе, -CH2-OEt, -CH2-CH2-OEt, -О-СОМе, -O-COEt, O-COCF3, -O-COCF3, фтор, хлор або бром. Більш переважні ті сполуки загальної формули 4, у яких А означає залишок із двома зв'язками, вибраний із групи, яка включає R1 являє собою залишок, вибраний із групи, яка включає метил і етил, при цьому такий залишок необов'язково може бути заміщений гідроксигрупою або фтором, переважно являє собою незаміщений метил, R3, R4, R5 і R6 мають ідентичні або різні значення і являють собою, водень, метил, етил, метилоксигрупу, етилоксигрупу, гідроксигрупу, фтор, хлор або бром і R7 означає водень, метил, етил, метилоксигрупу, етилоксигрупу, CF3 , або фтор. Відповідно до винаходу особливо переважними є сполуки загальної формули 4, у яких А означає залишок із двома зв'язками, вибраний із групи, яка включає R1 являє собою залишок, вибраний із групи, яка включає метил і етил, переважно метил, R3, R4, R5 і R6 мають ідентичні або різні значення і являють собою, водень, метил, метилоксигрупу, хлор або фтор і R7 означає водень, метил або фтор. Найбільш переважними є відповідно до винаходу сполуки загальної формули 4, у яких А означає залишок із двома зв'язками, вибраний із групи, яка включає R1 являє собою метил або етил, переважно метил, R3, R4, R5 і R6 мають ідентичні або різні значення і являють собою, водень або фтор, переважно водень, і R7 означає водень, метил або фтор, переважно метил або фтор, найбільш переважно метил. У проміжних сполуках формули 4 аналогічно до сполук загальної формули 1 кожний із залишків R3, R4, 5 R і R6, якщо вони не означають водень, також може знаходитися в орто-, мета- або пара-положенні відносно місця приєднання до групи "-С-ОН". Якщо ні один із залишків R3, R4, R5 і R6 не означає водень, то R3 і R5 переважно приєднані в пара-положенні, a R4 і R6 переважно приєднані в орто- або мета-положенні, найбільш переважно в мета-положенні. Якщо ж один із залишків R і R 4 і один із залишків R5 і R6 означає водень, то відповідний інший залишок переважно приєднаний у мета- або пара-положенні, найбільш переважно в пара-положенні. Якщо ні один із залишків R3, R4, R5 і R6 не означає водень, то особливо переважні відповідно до винаходу проміжні сполуки загальної формули 4, у яких залишки R3, R4, R5 і R6 мають ідентичні значення. Нижче даний винахід пояснюється на прикладах синтезу. Очевидно, що такі приклади мають винятково ілюстративний характер і служать лише для пояснення принципів, які покладені в основі винаходу, не обмежуючи його обсяг розглянутими в наступному описі як приклади конкретними варіантами його здійснення. Приклад 1: Метобромід скопінового ефіру 2,2-дифенілпропіонової кислоти 1.1: Хлорангідрид 2,2-дифенілпропіонової кислоти 3а До суспензії з 25,0г (0,11 моля) 2,2-дифенілпропіонової кислоти, 100мл дихлорметану і 4 крапель диметилформаміду при 20°С по краплях повільно додають 52,08г (0,33 моля) оксалілхлориду. Далі суміш перемішують протягом 1год при 20°С і протягом 0,5год при 50°С. Після цього розчинник відганяють і отриманий залишок без додаткового очищення використовують на наступній стадії. 1.2: Скопіновий ефір 2,2-дифенілпропіонової кислоти 4а Отриманий на стадії 1.1 залишок розчиняють у 100мл дихлорметану і при 40°С по краплях змішують з розчином 51,45г (0,33 моля) скопіну в 200мл дихлорметану. Отриману суспензію перемішують протягом 24год при 40°С, після чого утворений осад відокремлюють вакуум-фільтрацією і фільтрат піддають кислотній екстракції спочатку водою, а потім водною соляною кислотою. Значення рН об'єднаних водних фаз встановлюють на лужне за допомогою водного розчину карбонату натрію, екстрагують ди хлорметаном, органічну фазу суша ть над Na2SO4, упарюють досуха і з залишку осаджують гідрохлорид. Продукт очищають перекристалізацією з ацетонітрилу. Вихід: 20,85г (47% від теорії). ТШХ: Rf-значення: 0,24 (система розчинників: вmор-бутанол/мурашина кислота/вода в співвідношенні 75:15:10). tпл 203-204°С. 1.3: Ме тобромід скопінового ефіру 2,2-дифенілпропіонової кислоти 11,98г (0,033 моля) сполуки 4а об'єднують при 20°С з 210мл ацетонітрилу, 70мл дихлорметану і 20,16г (0,1 моля) 46,92%-ного бромметану в ацетонітрилі і залишають стояти протягом 3 днів. Після цього розчин упарюють досуха і залишок перекристалізовують з ізопропанолу. Вихід: 11,34г (75% від теорії). tпл 208-209°С. C24H28NО 3 xBr (458,4). Елементний аналіз: розраховано: С (62,89) Η (6,16) N(3,06) виявлено: С (62,85) Η (6,12) Ν (3,07) Приклад 2: Метобромід скопінового ефіру 2-фтор-2,2-дифенілоцтової кислоти 2.1: Скопіновий ефір бензилової кислоти 5а Одержання скопінового ефіру бензилової кислоти відоме з рівня техніки й описане в WO 92/16528. 2.2: Скопіновий ефір 2-фтор-2.2-дифенілоцтової кислоти 4b 2,66г (0,02 моля) трифториду диметиламіносірки охолоджують у 10мл дихлорметану до 0°С і по краплях додають розчин 5,48г (0,015 моля) скопінового ефіру бензилової кислоти 5а у 100мл дихлорметану. Далі перемішують протягом 30хв при 0°С і протягом 30хв при 20°С. Після цього розчин при охолодженні змішують з водою, додають NaHCO3 (до рН 7-8) і органічну фазу відокремлюють. Водну фазу екстрагують дихлорметаном, об'єднані органічні фази промивають водою, сушать над Na2SO4 і упарюють досуха. З залишку осаджують гідрохлорид і перекристалізовують з ацетонітрилу. Вихід: 6,90г (85% від теорії). tпл 227-230°С. 2.3: Ме тобромід скопінового ефіру 2-фтор-2,2-дифенілоцтової кислоти 2,88г (0,0078 моля) вільної основи скопінового ефіру бензилової кислоти піддають хімічному перетворенню аналогічно до стадії 1.3. Продукт очищають перекристалізацією з ізопропанолу. Вихід: 2,62г (73% від теорії). ТШХ: Rf-значення: 0,31 (система розчинників аналогічна до стадії 1.2). tпл 130-134°С. Приклад 3: Метобромід тропенолового ефіру 2,2-дифенілпропіонової кислоти 3.1.: Метиловий ефір 2.2-дифенілпропіонової кислоти 3b До суспензії 50,8г (0,225 моля) 2,2-дифенілпропіонової кислоти і 200мл ацетонітрилу при 20°С по краплях додають 37,60г (0,247 моля) ДБУ. До отриманого розчину далі по краплях протягом 30хв додають 70,10г (0,494 моля) метилйодиду. Після цього перемішують протягом ночі при 20°С. На завершення розчинник випарюють, залишок екстрагують діетиловим ефіром/водою, органічну фазу промивають водою, сушать над Na2SO4 сушать і упарюють досуха. Вихід: 48,29г в'язкого залишку 3b (89% від теорії). 3.2: Тропеноловий ефір 2.2-дифенілпропіонової кислоти 4с 4,80г (0,02 моля) метилового ефіру 2,2дифенілпропіонової кислоти 3b, 2,78г (0,02 моля) тропенолу і 0,046г натрію нагрівають у вигляді розплаву протягом 4год при тиску 75мбар на киплячій водяній бані при помірному струшуванні. Після охолодження натрієві залишки розчиняють ацетонітрилом, розчин упарюють досуха і залишок екстрагують дихлорметаном/водою. Органічну фазу промивають водою, сушать над MgSO4 і упарюють досуха. З залишку сполуку 4с осаджують у вигляді гідрохлориду, який перекристалізовують з ацетону. Вихід: 5,13г (67% від теорії). ТШХ: Rf-значення: 0,28 (система розчинників: вmор-бутанол/мурашина кислота/вода в співвідношенні 75:15:10). tпл 134-135°С. 3.3: Ме тобромід тропенолового ефіру 2,2-дифенілпропіонової кислоти 2,20г (0,006 моля) сполуки 4с піддають хімічному перетворенню аналогічно до прикладу 1, стадія 1.3. Утворені кристали відокремлюють вакуум-фільтрацією, промивають дихлорметаном, сушать і на завершення перекристалізовують з метанолу/діетилового ефіру. Вихід: 1,84г (66% від теорії). ТШХ: Rf-значення: 0,11 (система розчинників аналогічно до стадії 1.2). tпл 222-223°С. C24H28NO 2 xBr (442,4). Елементний аналіз: розраховано: С (65,16) Η (6,38) N(3,17) виявлено: С (65,45) Η (6,29) N(3,16) Приклад 4: Метобромід тропенолового ефіру 2-фтор-2.2-біс(3.4-дифторфеніл)оптової кислоти 4.1.: Етиловий ефір 3.3'.4.4'-тетрафторбензилової кислоти 3с Реактив Грин'яра одержують з 2,24г (0,092 моля) магнієвої стружки, декількох дрібок йоду і 17,80г (0,092 моля) 1-бром-3,4-дифторбензолу в 100мл ТГФ при 50°С. Після завершення додавання галогеніду суміш перемішують ще протягом години. Отриманий таким шляхом реактив Грин'яра при 10-15°С по краплях додають до 18,81г (0,088 моля) етилового ефіру 3,4-дифторфенілгліоксилової кислоти в 80мл ТГФ і отриману суміш перемішують протягом 2год при 5°С. Після цього білу суспензію для переробки зливають на суміш льоду із сірчаною кислотою, екстрагують етилацетатом, органічну фазу промивають водою, сушать над MgSO4 і упарюють досуха. Сирий продукт очищають колонковою хроматографією (розчинник: толуол). Вихід: 10,80г масла (38% від теорії). 4.2: Тропеноловий ефір 3.3'.4.4'-тетрафторбензилової кислоти 5b 4,27г (0,013 моля) етилового ефіру 3,3',4,4'-тетрафторбензилової кислоти 3с, 1,81г (0,013 моля) тропенолу і 0,03г натрію нагрівають у вигляді розплаву протягом 4год при тиску 75мбар на киплячій водяній бані при помірному струшуванні. Після охолодження натрієві залишки розчиняють ацетонітрилом, розчин упарюють досуха і залишок екстрагують дихлорметаном/водою. Органічну фазу промивають водою, сушать над MgSO4 і упарюють досуха. Отриманий залишок змішують з діетиловим ефіром/петролейним ефіром (у співвідношенні 1:9), відокремлюють вакуум-фільтрацією і промивають. Вихід: 2,50г (46% від теорії). ТШХ: Rf-значення: 0,29 (система розчинників: вmор-бутанол/мурашина кислота/вода в співвідношенні 75:15:10). tпл 147-148°С. 4.3: Тропеноловий ефір 2-фтор-2,2-біс(3.4-дифторфеніл)оцтової кислоти 4d 2,66г (0,012 моля) трифториду біс(2-метоксіетил)аміносірки додають до 10мл дихлорметану і протягом 20хв при 15-20°С по краплях змішують з розчином 0,01 моля сполуки 5b у 65мл дихлорметану. Після цього протягом 20год перемішують при кімнатній температурі, охолоджують до 0°С і при інтенсивному перемішуванні обережно змішують з 80мл води. Потім значення рН встановлюють на 8, обережно додаючи водний розчин NaHCO3, органічну фазу відокремлюють, водну фазу повторно екстрагують дихлорметаном, об'єднані органічні фази промивають водою, сушать над MgSO4 і упарюють досуха. На завершення осаджують гідрохлорид і перекристалізовують з ацетонітрилу/діетилового ефіру. Вихід: 2,60г білих кристалів (57% від теорії). tпл:·233°С. 4.4: Ме тобромід тропенолового ефіру 2-фтор-2,2-біс(3,4-дифторфеніл)оцтової кислоти 2,20г (0,0052 моля) 4d піддають хімічному перетворенню аналогічно до прикладу 1, стадія 1.3. Утворені кристали відокремлюють вакуум-фільтрацією, промивають дихлорметаном, сушать і на завершення перекристалізовують з метанолу/діетилового ефіру. Вихід: 1,95г (72% від теорії). ТШХ: Rf-значення: 0,17 (система розчинників: н-бутанол/вoда/мурашина кислота (конц.)/ацетон/дихлорметан у співвідношенні 36:15:15:15:5). tпл 247°С. C23H21F 5NO2 xBr (518,3). Елементний аналіз: розраховано: С (53,30) Η (4,08) Ν (2,70) виявлено: С (53,22) Η (4,19) N(2,69) Приклад 5: Етилбромід скопінового ефіру 2,2-дифенілпропіонової кислоти 1,81г (0,005 моля) сполуки 4а об'єднують при 20°С з 35мл ацетонітрилу і 1,64г (0,015 моля) етилброміду і залишають стояти протягом 3 днів. Після цього розчин упарюють досуха і залишок перекристалізовують з етанолу. Вихід: 1,38г (58% від теорії). tпл: 208-209°С. ТШХ: Rf-значення: 0,33 (система розчинників аналогічно до стадії 1.2). tпл: 210-211°C. C25H30NO 3 xBr (472,42); Елементний аналіз: розраховано: С (63,56) Η (6,40) Ν (2,96) виявлено: С (63,49) Η (6,24) N(2,88) Приклад 6: Метобромід скопінового ефіру 2-фтор-2,2-біс(3.4-дифторфеніл)оцтової кислоти 6.1: Скопіновий ефір 3,3',4,4'-тетрафторбензилової кислоти 5с 3,61г (0,011 моля) етилового ефіру 3,3',4,4'-тетрафторбензилової кислоти 3с, 1,71г (0,011 моля) скопіну і 0,03г натрію нагрівають у ви гляді розплаву протягом 4год при тиску 75мбар на киплячій водяній бані при помірному стр ушуванні. Після охолодження натрієві залишки розчиняють ацетонітрилом, розчин упарюють досуха і залишок екстрагують дихлорметаном/водою. Органічну фазу промивають водою, сушать над MgSO4 і упарюють досуха. Отриманий залишок змішують з діетиловим ефіром/петролейним ефіром (у співвідношенні 1:9), відокремлюють вакуум-фільтрацією і промивають. Вихід: 1,75г (36% від теорії). tпл: 178-179°С. 6.2: Скопіновий ефір 2-фтор-2.2-біс(3.4-дифторфеніл)оцтової кислоти 4е 0,6мл (0,0033 моля) трифториду біс(2-метоксіетил)аміносірки піддають взаємодії з 1,2г (0,0028 моля) сполуки 5с аналогічно до прикладу 4, стадія 4.3. Вихід: 1,15г безбарвного масла 01 (95% від теорії). 6.3: Ме тобромід скопінового ефіру 2-фтор-2,2-біс(3,4-дифторфеніл)оцтової кислоти 1,15г (0,0026 моля) сполуки 4е і 1,5г (0,0079 моля) 50%-ного розчину метилброміду піддають хімічному перетворенню аналогічно до прикладу 1, стадія 1.3. Утворені кристали відокремлюють вакуум-фільтрацією, промивають дихлорметаном, сушать і на завершення перекристалізовують з ацетону. Вихід: 0,88г (63% від теорії). ТШХ: Rf-значення: 0,27 (система розчинників: н-бутанол/вода/мурашина кислота (конц.)/ацетон/дихлорметан у співвідношенні 36:15:15:15:5). tпл: 212°С. C23H21F 5NO3 xBr (535,33). Приклад 7: Метобромід тропенолового ефіру 2-фтор-2,2-біс(4-фторфеніл)оптової кислоти 7.1: Ме тиловий ефір 4.4'-дифторбензилової кислоти 3d 7.1.1:4,4'-дифторбензилова кислота До розчину 49,99г (1,25 моля) NaOH-таблеток у 300мл води при температурі приблизно 100°С по краплях додають розчин 24,62г (0,1 моля) 4,4'-дифторбензилу в 250мл діоксану і перемішують протягом 2год. Після цього більшу частину діоксану відганяють і водний розчин, що залишився, екстрагують дихлорметаном. При підкисленні цього водного розчину сірчаною кислотою випадає осад, який відокремлюють вакуум-фільтрацією, промивають і сушать. Фільтрат екстрагують дихлорметаном, органічну фазу сушать над Na2SO4 і упарюють досуха. Вихід: 25,01г (95% від теорії). tпл: 133-136°C. 7.1.2: Ме тиловий ефір 4,4'-дифторбензилової їсислоти До свіжоприготовленого з 2,17г (0,095 моля) натрію і 200мл етанолу розчину етаноляту натрію при 20°С додають 25,0г (0,095 моля) 4,4'-дифторбензилової кислоти і перемішують протягом 3 год. Після цього розчин упарюють досуха, залишок розчиняють у ДМФ, при 20°С по краплях змішують з 22,57г (0,16 моля) метилйодиду і перемішують протягом 24 год. Переробку й очищення проводять аналогічно до сполуки 3b. Вихід: 21,06г (80% від теорії). 7.2: Тропеноловий ефір 4,4'-дифторбензилової кислоти 5d 11,13г (0,04 моля) метилового ефіру 4,4'-дифторбензилової кислоти 3d і 5,57г (0,04 моля) тропенолу піддають взаємодії з 0,09г натрію аналогічно до прикладу 3, стадія 3.2. Продукт перекристалізовують з ацетонітрилу. Вихід: 10,43г (62% від теорії). tпл: 233-235°С. 7.3: Тропеноловий ефір 2-фтор-2.2-біс(4-фторфеніл)оцтової кислоти 4f 2,94г (0,013 моля) трифториду біс(2-метоксіетил)аміносірки аналогічно до прикладу 4, стадія 4.3, піддають взаємодії з 3,85г (0,01 моля) сполуки 5d у 100мл дихлорметану. Продукт перекристалізовують у вигляді його гідрохлориду з ацетонітрилу. Вихід: 2,93г (69% від теорії). 7.4: Ме тобромід тропенолового ефіру 2-фтор-2,2-біс(4-фторфеніл)оцтової кислоти 2,6г (0,0067 моля) сполуки 4f і 1,9г (0,0079 моля) 50%-ного розчину метилброміду піддають хімічному перетворенню аналогічно до прикладу 1, стадія 1.3. Утворені кристали відокремлюють вакуум-фільтрацією, промивають дихлорметаном, сушать і на завершення перекристалізовують з метанолу/діетилового ефіру. Вихід: 2,82г білих кристалів (87% від теорії). ТШХ: Rf-значення: 0,55 (система розчинників: відповідно до прикладу 1, стадія 1.2). tпл: 230-231 °С. C23H23F 3NO2 xBr (482,34). Елементний аналіз: розраховано: С (57,27) Η (4,81) N(2,90) виявлено: С (57,15) Η (4,84) N(2,96) Приклад 8: Метобромід скопінового ефіру 2-фтор-2.2-біс(4-фторфеніл)оцтової кислоти 8.1: Скопіновий ефір 4,4'-дифторбензилової кислоти 5е 4,22г (0,01 моля) тропенолового ефіру 4,4'-дифторбензилової кислоти 5d суспендують у 80мл ДМФ. Далі при внутрішній температурі порядку 40°С додають розчин 2,57г (0,0273 моля) Н2О2-сечовини в 20мл води, а також 0,2г (0,0011 моля) оксиду ванадію(V) і перемішують протягом 4,5год при 60°С. Після охолодження до 20°С утворений осад відокремлюють вакуум-фільтрацією, значення рН фільтрату встановлюють на 3 за допомогою 4. соляної кислоти і змішують з Na2S2O5, розчиненим у воді. Отриманий у результаті зелений розчин упарюють досуха і залишок екстрагують дихлорметаном/водою. Значення рН кислої водної фази встановлюють на лужне за допомогою Na2CO3, після чого екстрагують дихлорметаном, органічну фазу сушать над Na2SO4 і концентрують. Після цього при температурі близько 15°С додають 0,5мл ацетилхлориду і перемішують протягом 1,5 год. Після екстракції 0,1н. соляною кислотою значення рН водної фази встановлюють на лужне, екстрагують дихлорметаном, органічну фазу суша ть над Na2SO4 і упарюють досуха. З залишку осаджують гідрохлорид і потім перекристалізовують з метанолу/діетилового ефіру. Вихід: 3,61г білих кристалів (78% від теорії). tпл: 243-244°С. 8.2: Скопіновий ефір 2-фтор-2.2-біс(4-фторФеніл)оцтової кислоти 4g 1,48г (0,0067 моля) трифториду біс(2-метоксіетил)аміносірки піддають взаємодії аналогічно до прикладу 4, стадія 4.3, з 2,0г (0,005 моля) сполуки 5е у 80мл дихлорметану. Продукт перекристалізовують у вигляді його гідрохлориду з етанолу. Вихід: 2,07г (94% від теорії). tпл: 238-239°С. 8.3: Ме тобромід скопінового ефіру 2-фтор-2.2-біс(4-фторфеніл)оцтової кислоти 1,6г (0,004 моля) сполуки 4g і 1,14г (0,0079 моля) 50%-ного розчину метилброміду піддають хімічному перетворенню аналогічно до прикладу 1, стадія 1.3. Утворені кристали відокремлюють вакуум-фільтрацією, промивають дихлорметаном, сушать і на завершення перекристалізовують з ацетонітрилу. Вихід: 1,65г білих кристалів (61% від теорії). ТШХ: Rf-значення: 0,25 (система розчинників: відповідно до прикладу 1, стадія 1.2). tпл: 213-214°С. C23H23F 3NO3 xBr (498,34). Елементний аналіз: розраховано: С (55,43) Η (4,65) N(2,81) виявлено: С (54,46) Η (4,67) N(2,80) Приклад 9: Метобромід тропенолового ефіру 2-фтор-2,2-дифенілоцтової кислоти 9.1.: Тропеноловий ефір бензилової кислоти 5f Тропеноловий ефір бензилової кислоти, а також спосіб його одержання відомі з WO 92/16528. 9.2: Тропеноловий ефір 2-фтор-2,2-дифенілоцтової кислоти 4h 15,86мл (0,086 моля) трифториду біс(2-метоксіетил)аміносірки піддають взаємодії аналогічно до прикладу 4, стадія 4.3, з 25г (0,072 моля) сполуки 5f у 480мл хлороформу. Продукт перекристалізовують у вигляді його гідрохлориду з ацетону. Вихід: 18,6г білих кристалів (67% від теорії). tпл: 181-182°С. 9.3: Ме тобромід тропенолового ефіру 2-фтор-2,2-дифенілоцтової кислоти 11,12г (0,032 моля) сполуки 4h і 18,23г (0,096 моля) 50%-ного розчину метилброміду піддають хімічному перетворенню аналогічно до прикладу 1, стадія 1.3. Утворені кристали перекристалізовують з ацетонітрилу. Вихід: 11,91г білих кристалів (83% від теорії). ТШХ: Rf-значення: 0,4 (система розчинників: відповідно до прикладу 4, стадія 4.4). tпл: 238-239°С. C23H25FNO 2 xBr (446,36). Елементний аналіз: розраховано: С (61,89) Η (5,65) N(3,14) виявлено: С (62,04) Η (5,62) N(3,17) Приклад 10: Метобромід тропенолового ефіру 2-фтор-2,2-(3-хлорфеніл)оцтової кислоти 10.1: Метиловий ефір 3.3'-ди хлорбензилової кислоти 3е 10.1.1:3,3'-дихлорбензил У реакційну посудину при кімнатній температурі завантажують 100мл етанолу і додають 50,0г (0,356 моля) 3-хлорбензальдегіду і 4,54г (0,018 моля) броміду 3-етил-5-(2-гідроксіетил)-4-метилтіазолію. Після цього по краплях додають 10,7г (0,11 моля) триетиламіну. Потім протягом 3год кип'ятять зі зворотним холодильником і упарюють досуха. Залишок розчиняють у етилацетаті й екстрагують водою, піросульфітом натрію у воді і розчином Na2CO3. Після сушіння над MgSO4 упарюють досуха. Отриманий продукт перекристалізовують з ізопропанолу і петролейного ефіру. Вихід: 13,2г білих кристалів (13% від теорії). tпл: 69-70°С. 13,0г отриманого таким шляхом ацилоїну при кімнатній температурі розчиняють у 460мл ацетонітрилу, додають 0,0867г окситрихлориду ванадію(У) і вводять кисень. Після закінчення 1,5год розчин упарюють досуха, екстрагують етилацетатом і водою, а також розчином Na2CO3, сушать над MgSO 4 і упарюють досуха. Отриманий залишок виділяють перемішуванням з петролейним ефіром/етилацетатом (у співвідношенні 95:5). Вихід: 12,59г жовтих кристалів (97% від теорії). tпл: 116-117°С. 10.1.2:3,3'-дихлорбензилова кислота У реакційну посудину при інтенсивному перемішуванні в киплячій водяній бані завантажують 51,45г (1,286 моля) гідроксиду натрію в 1000мл води, після чого по краплях додають розчин 28,5г (0,102 моля) 3,3'дихлорбензилу в 700мл діоксану і потім перемішують протягом 1 год. Після охолодження діоксан випарюють, залишок розбавляють водою й екстрагують діетиловим ефіром. Значення рН органічної фази встановлюють на кисле, після чого її екстрагують ди хлорметаном, сушать над MgSO 4 і упарюють досуха. Вихід: 32,7г ( 71% від теорії). 10.1.3: Метиловий ефір 3.3'-ди хлорбензилової кислоти З 100мл етанолу і 1,97г (0,0855 моля) натрію готують розчин етаноляту натрію, до якого потім по краплях додають 26,6г (0,0855 моля) 3,3'-дихлорбензилової кислоти в 50мл етанолу. Після цього перемішують протягом 4год при кімнатній температурі. Після відгону розчинника залишок розчиняють у 150мл ДМФ, по краплях додають 24,27г (0,171 моля) метилйодиду і потім перемішують протягом наступних 24 год. Далі при охолодженні льодом по краплях додають 300мл води і 200мл діетилового ефіру, фази розділяють, водну фазу екстрагують діетиловим ефіром, після чого органічні фази промивають розчином ЫагСОз і струшують з водою до нейтральної реакції. Після сушіння над Na2SO4 упарюють досуха. Ви хід: 22,91г жовтого масла (82% від теорії). Ю.2.: Тропеноловий ефір 3,3'-дихлорбензилової кислоти 5g 22,9г (0,074 моля) метилового ефіру 3,3'-ди хлорбензилової кислоти 3е, 15,37г (0,11 моля) тропенолу і 0,17г натрію нагрівають у вигляді розплаву протягом 4год при тиску 75мбар на киплячій водяній бані при помірному стр ушуванні. Після охолодження натрієві залишки розчиняють ацетонітрилом, розчин упарюють досуха і залишок екстрагують дихлорметаном/водою. Органічну фазу промивають водою, сушать над MgSO4 і упарюють досуха. Продукт перекристалізовують у вигляді його гідрохлориду з ацетонітрилу. Вихід: 16,83г білих кристалів (50% від теорії). tпл: 184-185°С. 10.3: Тропеноловий ефір 2-фтор-2.2-біс(3-хлорфеніл)оцтової кислоти 4і 1,48г (0,0067 моля) трифториду біс(2-метоксіетил)аміносірки додають до 10мл дихлорметану і протягом 20хв при 15-20°С по краплях змішують з розчином 2,09г сполуки 5g у 65мл дихлорметану. Далі протягом 20год перемішують при кімнатній температурі, охолоджують до 0°С і при інтенсивному перемішуванні обережно змішують з 80мл води. Після цього значення рН установлюють на 8, обережно додаючи водний розчин NаНСО3, органічну фазу відокремлюють, водну фазу повторно екстрагують дихлорметаном, об'єднані органічні фази промивають водою, сушать над MgSO4 і упарюють досуха. На завершення осаджують гідрохлорид і потім перекристалізовують з ацетонітрилу/діетилового ефіру. Вихід: 1,20г білих кристалів (53% від теорії). tпл: 136-137°С. 10.4: Метобромід тропенолового ефіру 2-фтор-2,2-біс(3-хлорфеніл)оцтової кислоти 1,0г (0,002 моля) сполуки 4h піддають хімічному перетворенню аналогічно до прикладу 1, стадія 1.3. Утворені кристали відокремлюють вакуум-фільтрацією, промивають дихлорметаном, сушать і на завершення перекристалізовують з метанолу/діетилового ефіру. Вихід: 0,82г білих кристалів (80% від теорії). ТШХ: Rf-значення: 0,14 (система розчинників: н-бутанол/вода/мурашина кислота (конц.)/ацетон/дихлорметан у співвідношенні 36:15:15:15:5). tпл: 180-181°С. C23H23Cl2FNO 2 xBr (515,25). Сполуки загальної формули 1, мають, як було встановлено, широкі можливості для застосування з терапевтичною метою, відповідно мають високий терапевтичний потенціал. Особливо при цьому слід відзначити переважну можливість застосування запропонованих у винаході сполук формули 1, завдяки їх фармацевтичній дії як антихолінергічних засобів. Як приклад застосування сполук за винаходом в цих цілях можна назвати терапію астми або ХОЗЛ (хронічне обструктивне захворювання легень). Сполуки загальної формули 1 можуть також застосовуватися для лікування пов'язаних із блукаючим нервом (вагальних) синусових брадикардій і для лікування порушень серцевого ритму. У цілому запропоновані у винаході сполуки придатні також для лікування спазмів, наприклад, у шлунково-кишковому тракті з досягненням відповідного терапевтичного ефекту. Запропоновані у винаході сполуки можуть використовуватися також для лікування спазмів у сечовивідних шляха х, а також, наприклад, больових відчуттів при менструації. Серед представлених вище як прикладу показань особливе значення надається застосуванню запропонованих у винаході сполук формули 1 у терапії астми і ХОЗЛ. Сполуки загальної формули 1 можна застосовувати індивідуально або в сполученні з іншими запропонованими у винаході діючими речовинами формули 1. За певних умов сполуки загальної формули 1 можна також застосовувати в сполученні з іншими фармакологічно активними діючими речовинами. При цьому мова насамперед йде про бетаміметики, протиалергічні засоби, антагоністи фактора активації тромбоцитів (PAF), антагоністи лейкотриєну і кортикостероїди, а також про різні сполучення таких діючих речовин. Як приклад бетаміметиків, які відповідно до винаходу можна використовувати в сполученні зі сполуками формули 1_, можна назвати сполуки, вибрані з групи, яка включає бамбутерол, бітолтерол, карбутерол, кленбутерол, фенотерол, формотерол, гексопреналін, ібутерол, пірбутерол, прокатерол, репротерол, салметерол, сульфонтерол, тербуталін, толубутерол, 4-гідрокси-7-[2-{[2-{[3-(2фенілетокси)пропіл]сульфоніл}етил]аміно}етил]-2(3Н)-бензотіазолон, 1-(2-фтор-4-гідроксифеніл)-2-[4-(1бензимідазоліл)-2-метил-2-бутиламіно]етанол, 1-[3-(4-метоксибензиламіно)-4-гідроксифеніл]-2-[4-(1бензимідазоліл)-2-метил-2-бутиламіно]етанол, 1-[2Н-5-гідрокси-3-оксо-4Н-1,4-бензоксазин-8-іл]-2-[3-(4-N,Nдиметиламінофеніл)-2-метил-2-пропіламіно]етанол, 1-[2Н-5-гідрокси-3-оксо-4Н-1,4-бензоксазин-8-іл]-2-[3-(4метоксифеніл)-2-метил-2-пропіламіно]етанол, 1-[2Н-5-гідрокси-3-оксо-4Н-1,4-бензоксазин-8-іл]-2-[3-(4-нбутилоксифеніл)-2-метил-2-пропіламіно]етанол, 1-[2Н-5-гідрокси-3-оксо-4Н-1,4-бензоксазин-8-іл]-2-{4-[3-(4метоксифеніл)-1,2,4-триазол-3-іл]-2-метил-2-бутиламіно}етанол, 5-гідрокси-8-(1-гідрокси-2ізопропіламінобутил)-2Н-1,4-бензоксазин-3-(4Н)-он, 1-(4-аміно-3-хлор-5-трифторметилфеніл)-2-mpеmбутиламіно)етанол і 1-(4-етоксикарбониламіно-3-ціано-5-фторофеніл)-2-(mреm-бутиламіно)етанол, за певних умов у вигляді їх рацематів, їх енантіомерів, їх діастереомерів, а також за певних умов їх фармакологічно прийнятних кислотно-адитивних солей і гідратів. Як бетаміметики більш переважно застосовувати в сполученні з запропонованими у винаході сполуками формули 1 діючі речовини, вибрані з групи, яка включає фенотерол, формотерол, салметерол, 1-[3-(4-метоксибензиламіно)-4-гідроксифеніл]-2[4-(1-бензимідазоліл)-2-метил-2-бутиламіно]етанол, 1-[2Н-5-гідрокси-3-оксо-4Н-1,4-бензоксазин-8-іл]-2-[3-(4ЇЧ,]Ч-диметиламінофеніл)-2-метил-2-пропіламіно]етанол, 1-[2Н-5-гідрокси-3-оксо-4Н-1,4-бензоксазин-8-іл]2-[3-(4-метоксифеніл)-2-метил-2- -пропіламіно] етанол, 1-[2Н-5-гідрокси-3-оксо-4Н-1,4-бензоксазин-8-іл]-2[3-(4-н-бутилоксифеніл)-2-метил-2-пропіламіно]етанол, 1-[2Н-5-гідрокси-3-оксо-4Н-1,4-бензоксазин-8-іл]-2{4-[3-(4-метоксифеніл)-1,2,4-триазол-3-іл]-2-метил-2-бутиламіно}етанол, за певних умов у вигляді їх рацематів, їх енантіомерів, їх діастереомерів, а також за певних умов їх фармакологічно прийнятних кислотно-адитивних солей і гідратів. Серед вказаних вище бетаміметиків особливо переважними є сполуки формотерол і салметерол, за певних умов у ви гляді їх рацематів, їх енантіомерів, їх діастереомерів, а також за певних умов їх фармакологічно прийнятних кислотно-адитивних солей і гідратів. Відповідно до винаходу переважними кислотно-адитивними солями бетаміметиків є солі, вибрані з групи, яка включає гідрохлорид, гідробромід, сульфат, фосфат, фумарат, метансульфонат і ксинафоат. У випадку салметеролу переважними його солями є гідрохлорид, сульфат і ксинафоат, з яких найбільш переважні сульфати і ксинафоати. Відповідно до винаходу особливо переважні салметеролx½H2SO4 і ксинафоат салметеролу. У випадку формотеролу переважними його солями є гідрохлорид, сульфат і фумарат, з яких найбільш переважні гідрохлорид і фумарат. Відповідно до винаходу особливо переважний фумарат формотеролу. У контексті даного винаходу під кортикостероїдами, які за певних умов можна застосовувати в сполученні зі сполуками формули 1, маються на увазі сполуки, вибрані з групи, яка включає флунісолід, беклометазон, триамцинолон, будесонід, флутиказон, мометазон, циклесонід, рофлепонід, GW 215864, KSR 592, ST-126 і дексаметазон. Переважні згідно із даним винаходом кортикостероїди вибрані з групи, яка включає флунісолід, беклометазон, триамцинолон, будесонід, флутиказон, мометазон, циклесонід і дексаметазон, серед яких найбільш переважні будесонід, флутиказон, мометазон і циклесонід, насамперед будесонід і флутиказон. У деяких випадках у даному описі замість поняття "кортикостероїди" використовується також лише поняття "стероїди". При згадуванні в даному описі стероїдів маються на увазі також солі або похідні, які можуть бути утворені зі стероїдів. Як приклад подібних можливих солей або похідних можна назвати натрієві солі, сульфобензоати, фосфати, ізонікотинати, ацетати, пропіонати, дигідрофосфати, пальмітати, півалати або фуроати. За певних умов кортикостероїди можуть бути також представлені у ви гляді їх гідратів. У контексті даного винаходу під агоністами допаміну, які за певних умов можна застосовувати в сполученні зі сполуками формули 1, маються на увазі сполуки, вибрані з групи, яка включає бромокриптин, каберголін, альфа-дигідроергокриптин, лісурід, перголід, праміпексол, роксіндол, ропінірол, таліпексол, тергурід і віозан. Переважними згідно із даним винаходом агоністами допаміну, придатними для застосування в сполученні зі сполуками формули 1, є праміпексол, таліпексол і віозан, з яких найбільш переважним є праміпексол. Під вказаними вище агоністами допаміну в контексті даного винаходу маються на увазі також їх можливі фармакологічно прийнятні кислотно-адитивні солі і за певних умов їх гідрати. Під фізіологічно сумісними кислотно-адитивними солями, які можуть бути утворені з вищеописаних агоністов допаміну, маються на увазі, наприклад, фармацевтично прийнятні солі, вибрані із солей соляної кислоти, бромистоводневої кислоти, сірчаної кислоти, фосфорної кислоти, метансульфонової кислоти, оцтової кислоти, фумарової кислоти, янтарної кислоти, молочної кислоти, лимонної кислоти, винної кислоти і малеїнової кислоти. Як приклад протиалергічних засобів, які відповідно до винаходу можуть використовуватися в сполученні зі сполуками формули 1, можна назвати епінастин, цетиризин, азеластин, фексофенадін, левокабастин, лоратадин, мізоластин, кетотифен, емедастин, диметинден, клемастин, баміпін, цексхлорфенірамін, фенірамін, доксиламін, хлорфеноксамін, дименгідринат, дифенгидрамін, прометазин, ебастин, деслоратидин і меклозин. Переважні протиалергічні засоби, які згідно із даним винаходом можна використовува ти в сполученні із запропонованими в ньому сполуками формули 1, вибрані з групи, яка включає епінастин, цетиризин, азеластин, фексофенадін, левокабастин, лоратадин, ебастин, деслоратидин і мізоластин, з яких особливо переважні епінастин і деслоратидин. Під вказаними вище протиалергічними засобами в контексті даного винаходу маються на увазі також їх можливі фармакологічно прийнятні кислотно-адитивні солі. Як приклад PAF-антагоністів, які відповідно до винаходу можна використовувати в сполученні зі сполуками формули 1, можна назвати 4-(2-хлорфеніл)-9-метил-2-[3-(4-морфолініл)-3-пропанон-1-іл]-6Нтієно[3,2-f][1,2,4]триазоло[4,3-а][1,4]діазепін, 6-(2-хлорфеніл)-8,9-дигідро-1-метил-8-[(4морфолініл)карбоніл]-4Н,7Н-циклопента-[4,5]тієно[3,2-f][1,2,4]триазоло[4,3-а][1,4] діазепін. Якщо сполуки формули І передбачається застосовувати в сполученні з іншими діючими речовинами, то найбільш переважними для використання в подібних комбінаціях сполуками серед їх вказаних вище класів є стероїди або бетаміметики. При цьому особливе значення надається застосуванню запропонованих у винаході сполук у сполученні з бетаміметиками, насамперед з бетаміметиками пролонгованої дії. До особливо переважного слід віднести комбінації запропонованих у винаході сполук формули 1 із салметеролом або формотеролом, при цьому комбінація з формотеролом є найбільш переважною. Як приклад придатних для введення сполук формули і лікарських форм можна назвати таблетки, капсули, супозиторії, розчини і т.д. Особливе значення має введення запропонованих у винаході сполук шляхом інгаляції (насамперед при лікуванні астми або ХОЗЛ). На частку фармацевтично активної(-их) сполуки(-к) у таких лікарських формах повинно припадати в кожному випадку від 0,05 до 90мас. %, переважно від 0,1 до 50мас. %, від загальної маси препарату. Відповідні таблетки можна виготовляти, наприклад, змішуванням діючої речовини або діючих речовин з відомими допоміжними речовинами, наприклад інертними розріджувачами, такими як карбонат кальцію, фосфат кальцію або лактоза, розпушувачами, такими як кукурудзяний крохмаль або альгінова кислота, зв'язуючими, такими як крохмаль або желатин, змащувальними речовинами, такими як стеарат магнію або тальк, і/або засобами для забезпечення депо-ефекту, такими як карбоксиметилцелюлоза, ацетатфталат целюлози або полівінілацетат. Таблетки можуть також складатися з декількох шарів. Відповідним чином можна виготовляти драже, наносячи на отримані аналогічно до таблеток ядра покриття зі звичайно застосовуваних у цих цілях матеріалів, наприклад колідону або шелаку, гуміарабіку, тальку, діоксиду титану або цукру. Для забезпечення ефекту або для уникнення несумісності ядра драже можна також виготовляти багатошаровими. Так само й оболонка драже також може складатися для забезпечення депо-ефекту з декількох шарів, при цьому можна використовувати допоміжні речовини, вказані вище для таблеток. До складу мікстур на основі запропонованих у винаході діючих речовин, відповідно комбінацій діючих речовин додатково можуть входити також підсолоджувальна речовина, така як сахарин, цикламат, гліцерин або цукор, а також поліпшувач смаку, наприклад ароматизатор, такий як ванілін або апельсиновий екстракт. Крім цього мікстури можуть містити суспендувальні допоміжні речовини або загусники, такі як натрійкарбоксиметилцелюлоза, змочувачі, наприклад продукти конденсації жирних спиртів з етиленоксидом, або захисні речовини, такі як n-гідроксибензоати. Розчини одержують за відомою технологією, наприклад з додаванням агентів, які надають ізотонічність, консервантів, таких як и-гідроксибензоати, або стабілізаторів, таких як лужнометалеві солі етилендіамінтетроцтової кислоти, і при необхідності з застосуванням емульгаторів і/або диспергаторів, при цьому, наприклад, при застосуванні води як розріджувача при необхідності можна використовувати органічні розчинники як гідротропні солюбілізатори, відповідно допоміжний розчинник, і розливають по пляшках для ін'єкцій, ампулах або пляшках для інфузії. Капсули, які містять одну або декілька діючих речовин, відповідно комбінації діючих речовин, можна виготовляти, наприклад, змішуванням діючих речовин з інертними носіями, такими як лактоза або сорбіт, і включенням отриманої суміші в желатинові капсули. Відповідні супозиторії можна виготовляти, наприклад, змішуванням з передбаченими для цієї мети носіями, такими як нейтральні жири або поліетиленгліколь, відповідно їх похідні. Як приклад допоміжних речовин, що використовують при приготуванні лікарських форм, можна назвати воду, фармацевтично прийнятні, (нешкідливі) органічні розчинники, такі як парафіни (наприклад фракції мінерального масла), олії рослинного походження (наприклад арахісова або кунжутна олія), моно- або поліфункціональні спирти (наприклад етанол або гліцерин), носії, такі як природне борошно гірських порід (наприклад каолін, глиноземи, тальк, крейда), синтетичне борошно гірських порід (наприклад високодисперсна кремнієва кислота і силікати), цукри (наприклад тростинний, молочний і виноградний цукор), емульгатори (наприклад лігнін, сульфітний щолок, метилцелюлоза, крохмаль і полівінілпіролідон) і змащувальні речовини (наприклад стеарат магнію, тальк, стеаринова кислота і лаурилсульфат натрію). Введення здійснюють за звичайною методикою, при цьому при терапії астми або ХОЗЛ переважне інгаляційне введення. У випадку перорального введення відповідні таблетки можуть, як очевидно, крім вищевказаних носіїв містити також добавки, такі, наприклад, як цитрат натрію, карбонат кальцію і дикальційфосфат, разом з різноманітними наповнювачами, такими як крохмаль, переважно картопляний крохмаль, желатин і т.п. Крім цього при виробництві таблеток можуть використовуватися також змащувальні речовини, такі як стеарат магнію, лаурилсульфат натрію і тальк. У випадку водних суспензій діючі речовини крім вищеописаних допоміжних речовин можна також змішува ти з різного роду поліпшувачами смаку або барвниками. Призначувана доза запропонованих у винаході сполук істотно залежить, як очевидно, від шляху введення і захворювання, яке підлягає лікуванню. При інгаляції виражений ефект від застосування сполук формули 1 виявляється вже при їх введенні в дозах, що знаходяться у мікрограмовому діапазоні. Однак сполуки формули 1 доцільно застосовувати й у дозах, які перевищують мікрограмовий діапазон. При цьому відповідна доза може, наприклад, знаходитися в грамовому діапазоні. Запропоновані у винаході сполуки можна застосовувати в більш високих дозах насамперед при їх введенні відмінним від інгаляції шляхом (наприклад у дозах, що становлять від 1 до 1000мг, але не обмежених лише вказаними межами). Нижче винахід проілюстрований на прикладах, у яких представлені склади деяких лікарських форм і які не обмежують його обсяг. Приклади фармацевтичних композицій А) Таблетки Компонент діюча речовина лактоза кукурудзяний крохмаль полівінілпіролідон стеарат магнію Вміст із розрахунку на одну таблетку 100мг 140мг 240мг 15мг 5мг 500мг Тонкоподрібнену діючу речовину змішують з лактозою і частиною від усієї передбаченої кількості кукурудзяного крохмалю. Отриману суміш просіюють, після чого її зволожують розчином полівінілпіролідону у воді, місять, гранулюють у вологому стані і сушать. Отриманий гранулят разом з іншою кількістю кукурудзяного крохмалю і стеаратом магнію просіюють і змішують між собою. З отриманої суміші пресують таблетки потрібних форми і розмірів. Б) Таблетки Вміст із розрахунку на одну таблетку діюча речовина 80мг лактоза 55мг кукурудзяний крохмаль 190мг мікрокристалічна целюлоза 35мг полівінілпіролідон 15мг натрійкарбоксиметилкрохмаль 23мг стеарат магнію 2мг 400мг Компонент Тонкоподрібнену діючу речовину змішують з частиною від усієї передбаченої кількості кукурудзяного крохмалю, лактозою, мікрокристалічною целюлозою і полівінілпіролідоном, отриману суміш просіюють і разом з іншою кількістю кукурудзяного крохмалю іводи переробляють у гранулят, який сушать і просіюють. Далі додають натрійкарбоксиметилкрохмаль і стеарат магнію, перемішують і з отриманої суміші пресують таблетки потрібних розмірів. В) Розчин в ампулах діюча речовина хлорид натрію вода з розрахунку на одну ін'єкцію 50мг 50мг 5мл Діючу речовину при власному значенні рН або при необхідності при рН від 5,5 до 6,5 розчиняють у воді і змішують із хлоридом натрію як агентом, який надає ізотонічність. Отриманий розчин фільтрують у непірогенних умовах і фільтрат в асептичних умовах розфасовують в ампули, які потім стерилізують і запаюють. Такі ампули можуть містити 5мг, 25мг і 50мг діючої речовини. Г) Дозований аерозоль діюча речовина сорбітантриолеат монофтортрихлорметан і дифтордихлорметан у співвідношенні 2:3 0,005мас.% 0,1мас.% до 100мас.% Суспензію заливають у звичайний аерозольний балончик, обладнаний дозувальним клапаном. Порція суспензії, яка видається за однократне натискання на такий клапан, переважно становить 50мкл. При необхідності діючу речовину можна вводити й у більш високих дозах (наприклад 0,02мас. %). Д) Розчини (νмг/100мл) діюча речовина фумарат формотеролу бензалконію хлорид ЕДТК НСl (1н.) 333,3мг 333,3мг 10,0мг 50,0мг до рН 3,4 Розчин такої сполуки можна готувати за звичайною технологією. Е) Порошок для інгаляції діюча речовина фумарат формотеролу моногідрат лактози 6мкг 6мкг до 25мг Порошок для інгаляції вказаного складу одержують за звичайною технологією змішуванням окремих компонентів. Ж) Порошок для інгаляції діюча речовина моногідрат лактози 10мкг до 5мг Порошок для інгаляції вказаного складу одержують за звичайною технологією змішуванням окремих компонентів.
ДивитисяДодаткова інформація
Назва патенту англійськоюAnticholinergic agents being used as medicaments, a method for the preparation thereof and a pharmaceutical composition
Автори англійськоюBANHOLZER ROLF
Назва патенту російськоюАнтихолинергические средства, которые применяются в качестве медикаментов, способ их получения и фармацевтическая композиция
Автори російськоюБанхольцер Рольф
МПК / Мітки
МПК: A61P 13/02, A61P 43/00, A61P 15/08, A61K 31/439, A61K 45/00, A61P 9/06, C07B 55/00, A61P 1/06, A61P 11/06, C07D 451/10
Мітки: композиція, фармацевтична, антихолінергічні, одержання, застосовуються, спосіб, засоби, медикаменти
Код посилання
<a href="https://ua.patents.su/14-73804-antikholinergichni-zasobi-yaki-zastosovuyutsya-yak-medikamenti-sposib-kh-oderzhannya-ta-farmacevtichna-kompoziciya.html" target="_blank" rel="follow" title="База патентів України">Антихолінергічні засоби, які застосовуються як медикаменти, спосіб їх одержання та фармацевтична композиція</a>
Попередній патент: Спосіб моделювання цукрового предіабету
Наступний патент: Повітророзподільник (варіанти)
Випадковий патент: Спосіб комбінованого лікування раку яєчників


















