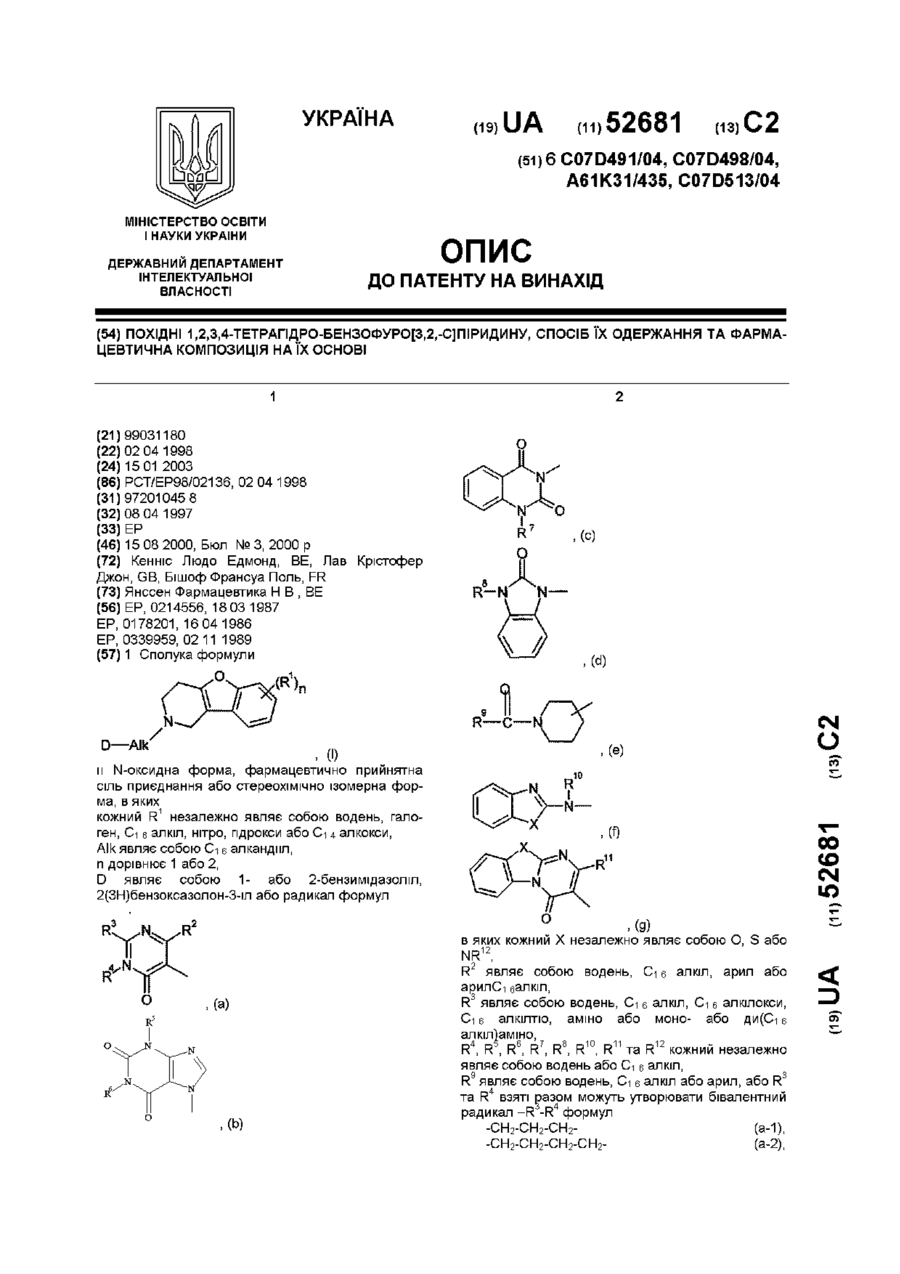
Похідні 1,2,3,4-тетрагідро-бензофуро[3,2,-c]піридину, спосіб їх одержання та фармацевтична композиція на їх основі
Номер патенту: 52681
Опубліковано: 15.01.2003
Автори: Кенніс Людо Едмонд Жозефін, Бішоф Франсуа Поль, Лав Крістофер Джон
Формула / Реферат
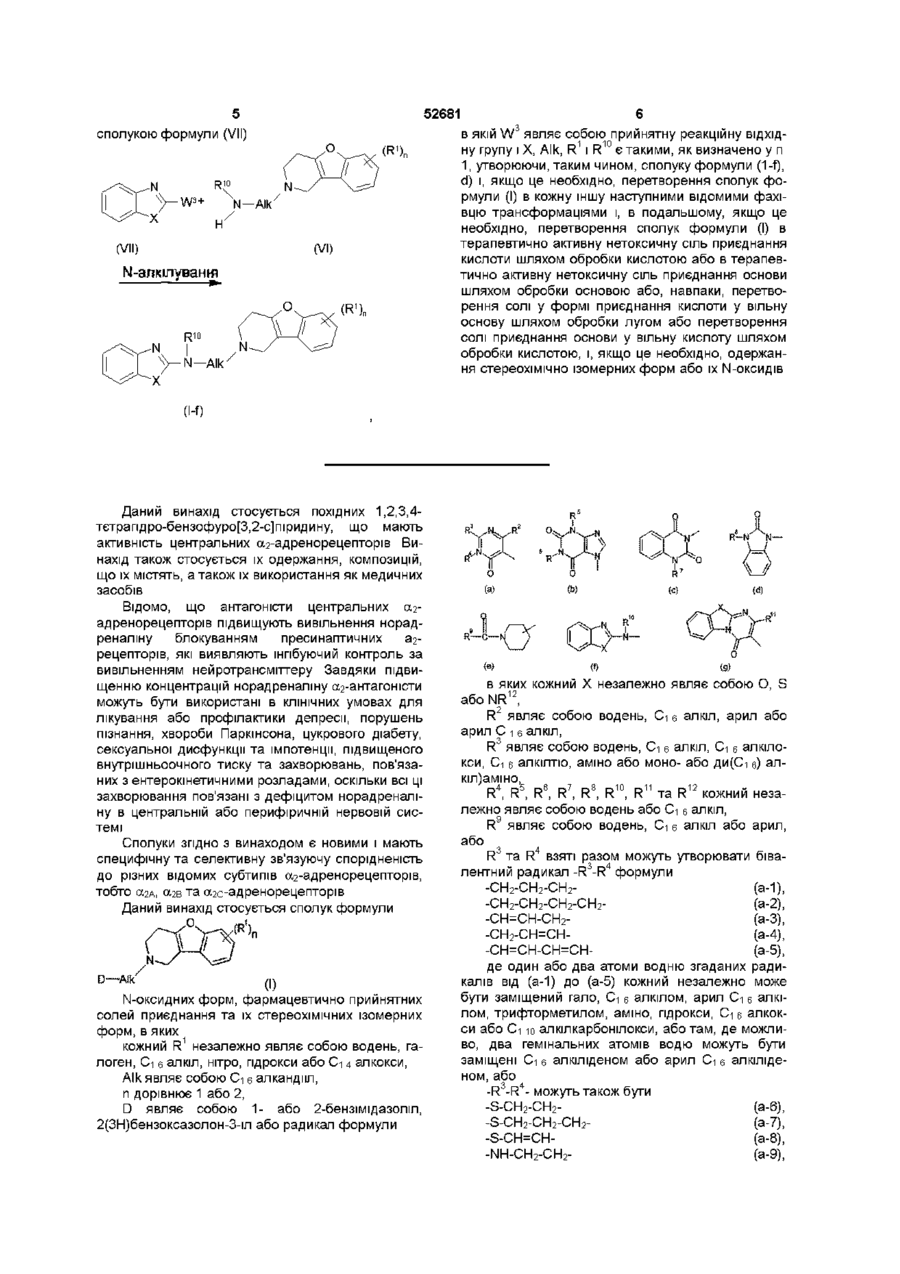
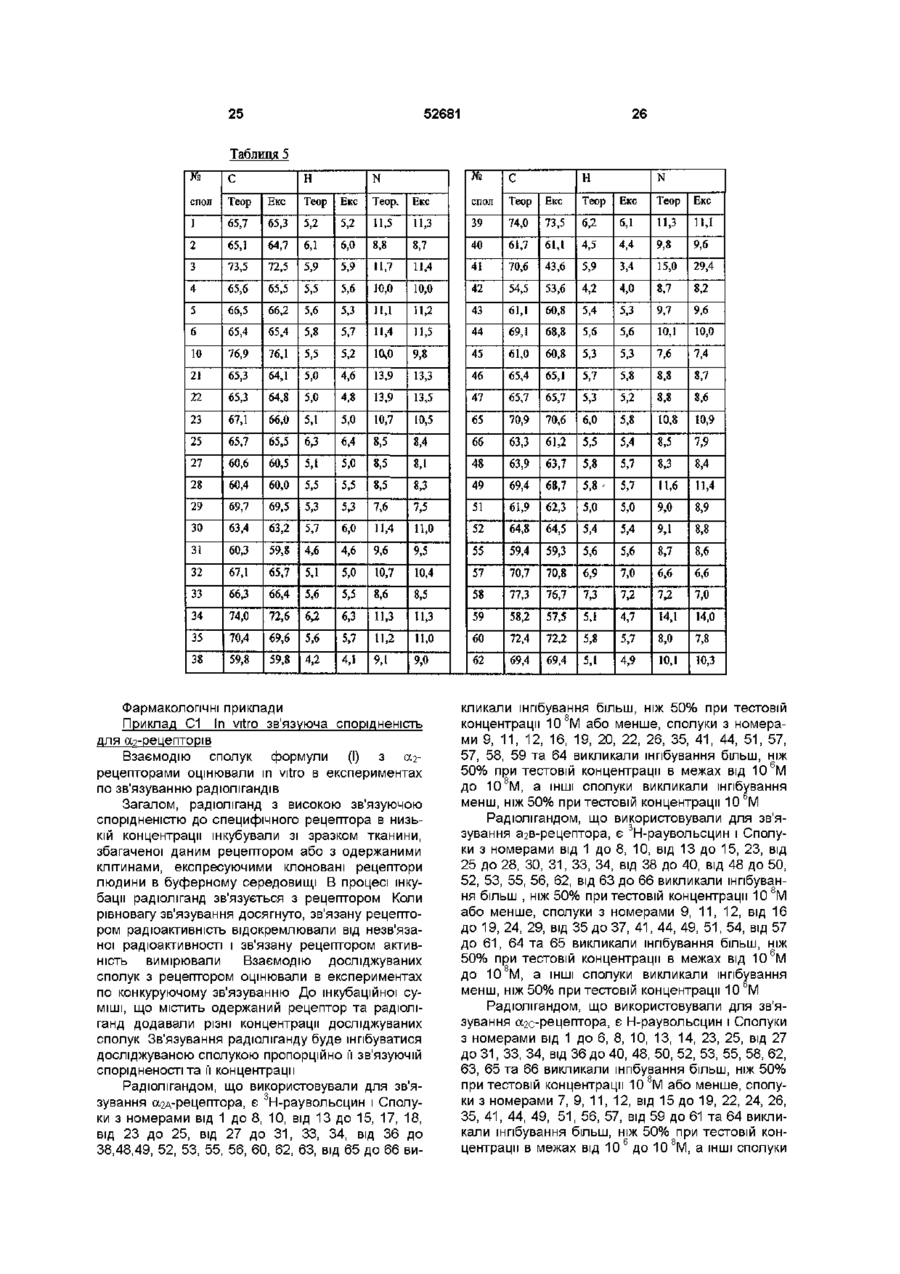
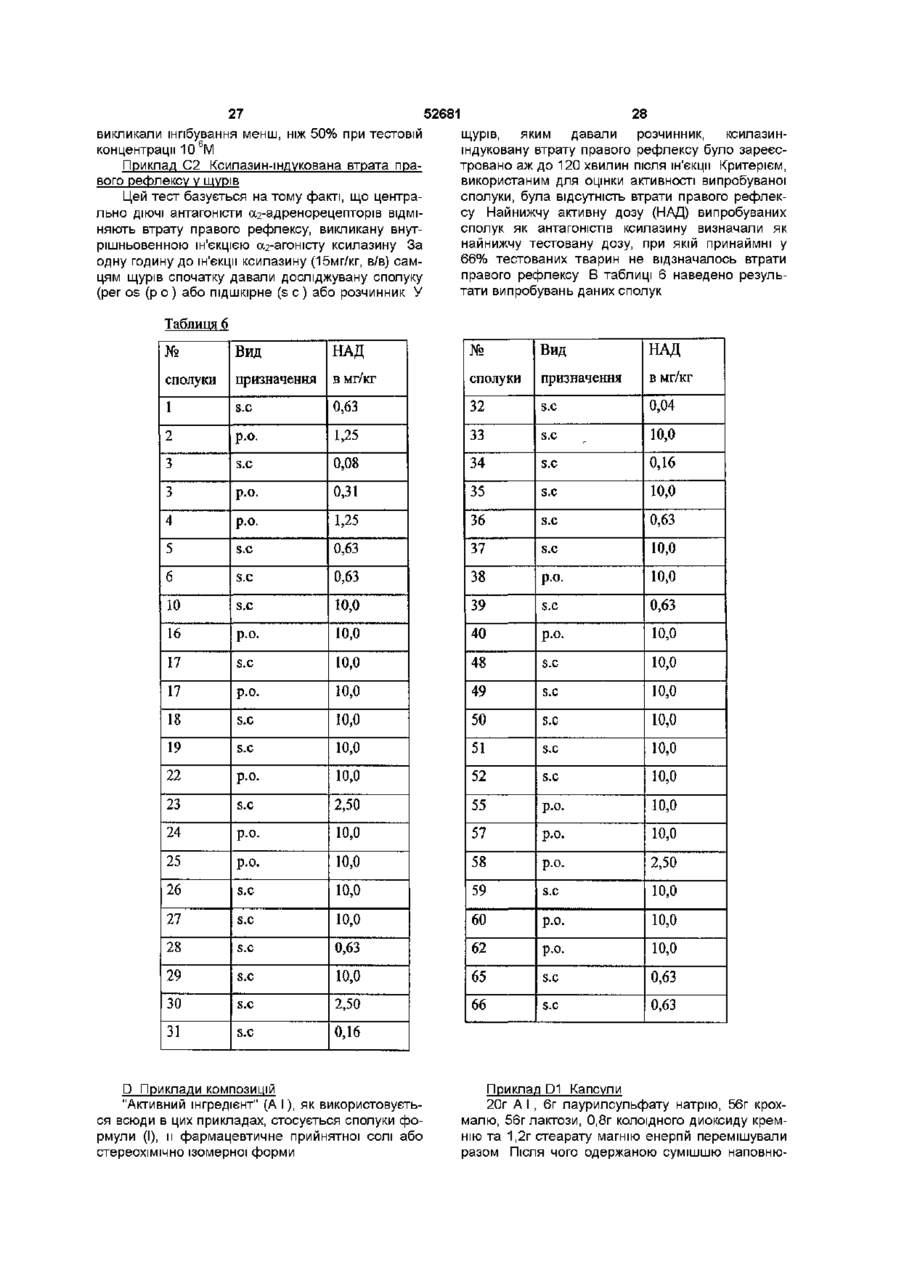
1. Сполука формули
, (I)
її N-оксидна форма, фармацевтично прийнятна сіль приєднання або стереохімічно ізомерна форма, в яких:
кожний R1 незалежно являє собою водень, галоген, С1-6 алкіл, нітро, гідрокси або С1-4 алкокси;
Alk являє собою С1-6 алкандіїл;
n дорівнює 1 або 2;
D являє собою 1- або 2-бензимідазоліл, 2(3Н)бензоксазолон-3-іл або радикал формул
, (a)
, (b)
, (c)
, (d)
, (e)
, (f)
, (g)
в яких кожний Χ незалежно являє собою О, S або NR12;
R2 являє собою водень, С1-6 алкіл, арил або арилС1-6алкіл;
R3 являє собою водень, С1-6 алкіл, С1-6 алкілокси, С1-6 алкілтіо, аміно або моно- або ди(С1-6 алкіл)аміно;
R4, R5, R6, R7, R8, R10, R11 та R12 кожний незалежно являє собою водень або С1-6 алкіл;
R9 являє собою водень, С1-6 алкіл або арил; або R3 та R4 взяті разом можуть утворювати бівалентний радикал –R3-R4 формул
-СН2-СН2-СН2-
(а-1),
-СН2-СН2-СН2-СН2-
(а-2),
-СН=СН-СН2-
(а-3),
-СН2-СН=СН-
(а-4),
-CH=CH-CH=CH
(а-5),
де один або два атоми водню згаданих радикалів від (а-1) до (а-5) кожний незалежно може бути заміщений гало, С1-6 алкілом, арилС1-6алкілом, трифторметилом, аміно, гідрокси, С1-6 алкокси або С1-10 алкілкарбонілокси; або там де можливо, два гемінальних атоми водню можуть бути заміщені С1-6 алкіліденом або арилС1-6алкіліденом; або –R3-R4- можуть також бути
-S-CH2-CH2-
(a-6),
-S-CH2-CH2-CH2-
(a-7),
-S-CH=CH-
(a-8),
-NH-CH2-CH2-
(a-9),
-NH-CH2-CH2-CH2-
(a-10),
-NH-CH=CH-
(a-11),
-NH-CH=N-
(a-12),
-S-CH=N-
(a-13),
-CH=CH-O-
(a-14),
в яких один або, там де можливо, два або три атоми водню згаданих радикалів від (a-6) до (a-14) кожний незалежно може бути заміщений С1-6 алкілом або арилом, і
арил являє собою феніл або феніл, заміщений гало або С1-6 алкілом.
2. Сполука згідно з п. 1, в якій D являє собою 1-бензимідазоліл;
2(3H)бензоксазолон-3іл або D являє собою радикал формули (а), в якій R3 є С1-6алкілтіо і R4 є С1-6алкіл; або R3 і R4 , взяті разом утворюють бівалентний радикал формули (а-2) або (а-5), в яких один або два атоми водню згаданих радикалів, кожний незалежно, можуть являти собою гало, С1-6алкіл, С1-6алкілокси, арилС1-6алкіл, трифторметил, аміно, гідрокси, С1-6алкілокси або С1-10алкілкарбонілокси; або, де це можливо, два гемінальних атоми водню можуть бути заміщені С1-6алкіліденом або арилС1-6алкіліденом; або бівалентний радикал формул (а-6), (а-7), (а-8), (а-11) або (а-14), в яких один або, де це можливо, два або три атоми водню в згаданих радикалах кожний незалежно може бути заміщений С1-6алкілом або арилом; або D являє собою радикал формули (b), в якій R5 і R6 являють собою С1-6алкіл; або D являє собою радикал формули (b), в якій R5 і R6 являють собою С1-6алкіл; або D являє собою радикал формули (с), в якій R7 є воднем; або D являє собою радикал формули (d), в якій R8 є воднем або С1-6алкілом; або D являє собою радикал формули (е), в якій R9 є арилом; або D являє собою радикал формули (f), в якій Χ є S і R10 є воднем; або D являє собою радикал формули (g), в якій Χ є S і R11 є С1-6алкілом.
3. Сполука згідно з п. 1 або 2, в якій n дорівнює 1 і R1 являє собою водень, хлор, фтор, метил або нітро, або в якій n дорівнює 2 і R1 є метокси.
4. Спокука згідно з будь-яким пунктом з 1 по 3, в якій R1 є воднем і D являє собою радикал формули (а), в якій R3 і R4, взяті разом, утворюють бівалентний радикал формули (а-2) або (а-5), в яких один або два атоми водню, кожний незалежно, може бути заміщений гало, метилом, метокси, арилметилом, трифторметилом, аміно або гідрокси, або в яких два гемінальних атоми водню заміщені арилметиленом; або R3 і R4, взяті разом, утворюють бівалентний радикал формули (а-6), (а-7), (а-8), (а-11) або (а-14), в яких один або, де це можливо, два або три атоми водню заміщені метилом.
5. Сполука згідно з п. 1, де ця сполука являє собою 3-[2-[3,4-дигідробензофуро[3,2-с]піридин-2(1H)-іл]етил]-2-метил-4H-піридо-[1,2-а]-піримідин-4-он;
6-[[3,4-дигідробензофуро[3,2-с]піридин-2(1H)-іл]етил]-7-метил-5H-тіазоло-[3,2-а]-піримідин-5-он;
6-[[3,4-дигідробензофуро[3,2-с]піридин-2(1H)-іл]етил]-3,7-диметил-5H-тіазоло-[3,2-а]-піримідин-5-он;
3-[2-[3,4-дигідробензофуро[3,2-с]піридин-2(1H)-іл]етил]-2,7-диметил-4H-піридо-[1,2-а]піримідин-4-он; N-оксид, фармацевтично прийнятна сіль приєднання або їх стереохімічно ізомерна форма.
6. Сполука згідно з будь-яким пунктом з 1 по 5 для використання як лікарського препарату.
7. Композиція, що містить фармацевтично прийнятний носій і, як активний інгредієнт, терапевтично ефективну кількість сполуки згідно з будь-яким пунктом з 1 по 5.
8. Спосіб одержання сполуки згідно з п. 1, який відрізняється тим, що проводять
а) N-алкілування похідних 1, 2, 3, 4-тетрагідробензофурано-[3,2-с]-піридину формули (II) алкілуючим реагентом формули (III)
(I),
в якому W1 являє собою прийнятну реакційну відхідну групу і D, Alk і R1 є такими, як це визначено у п. 1;
b) зняття захисту з N-захищеної проміжної сполуки формули (IV) з наступним N-ацилюванням одержаної проміжної сполуки ацилпохідним формули (V)
,
в якій Р являє собою захисну групу, W являє собою прийнятну реакційну відхідну групу і R1, R9 і Alk є такими, як визначено у п. 1; утворюючи, таким чином, сполуку формули (1-е);
с) N-алкілування аміну формули (VI) проміжною сполукою формули (VII)
,
в якій W3 являє собою прийнятну реакційну відхідну групу і X, Alk, R1 і R10 є такими, як визначено у п. 1; утворюючи, таким чином, сполуку формули (1-f);
d) і, якщо це необхідно, перетворення сполук формули (І) в кожну іншу наступними відомими фахівцю трансформаціями і, в подальшому, якщо це необхідно, перетворення сполук формули (І) в терапевтично активну нетоксичну сіль приєднання кислоти шляхом обробки кислотою або в терапевтично активну нетоксичну сіль приєднання основи шляхом обробки основою або, навпаки, перетворення солі у формі приєднання кислоти у вільну основу шляхом обробки лугом або перетворення солі приєднання основи у вільну кислоту шляхом обробки кислотою; і, якщо це необхідно, одержання стереохімічно ізомерних форм або їх N-оксидів.
Текст
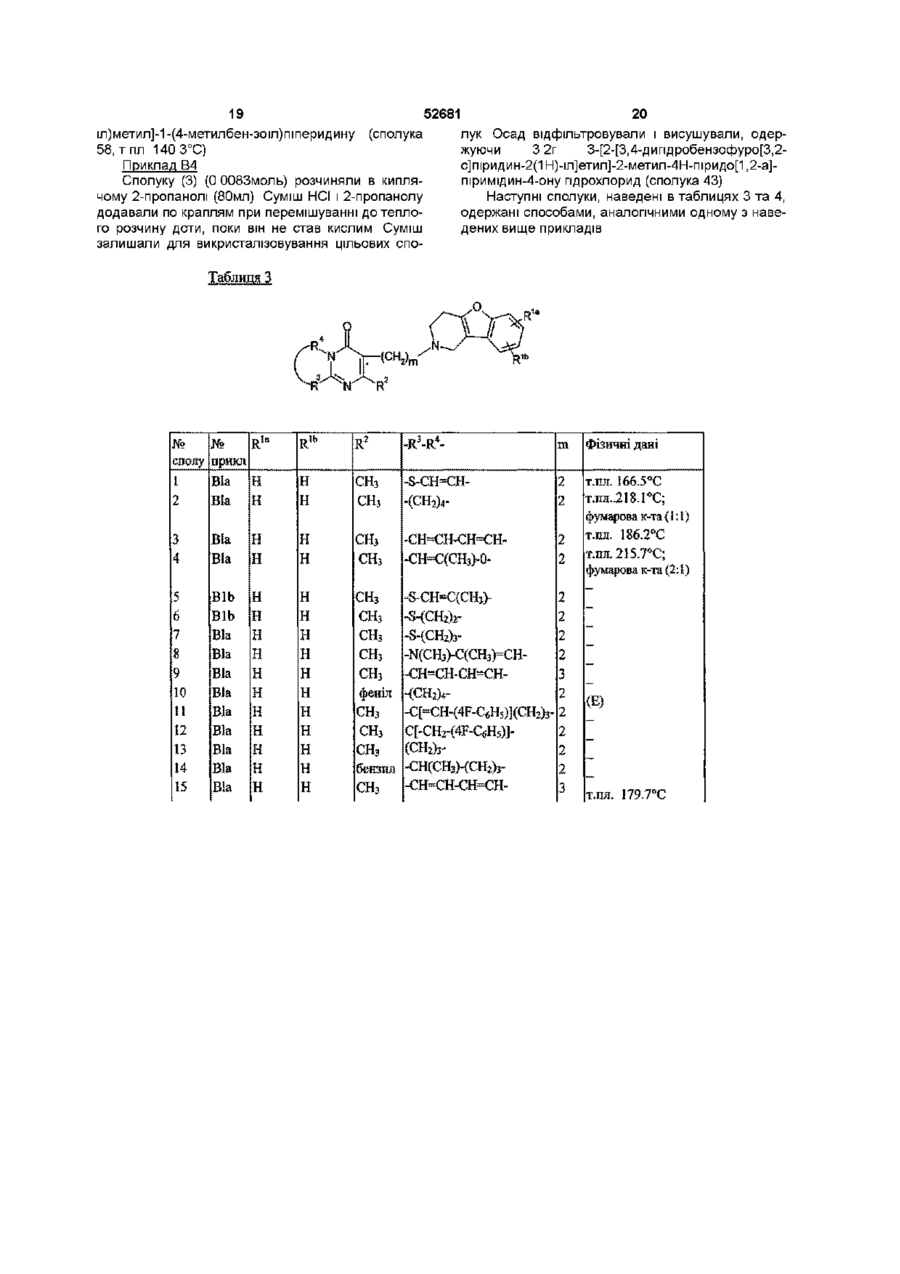
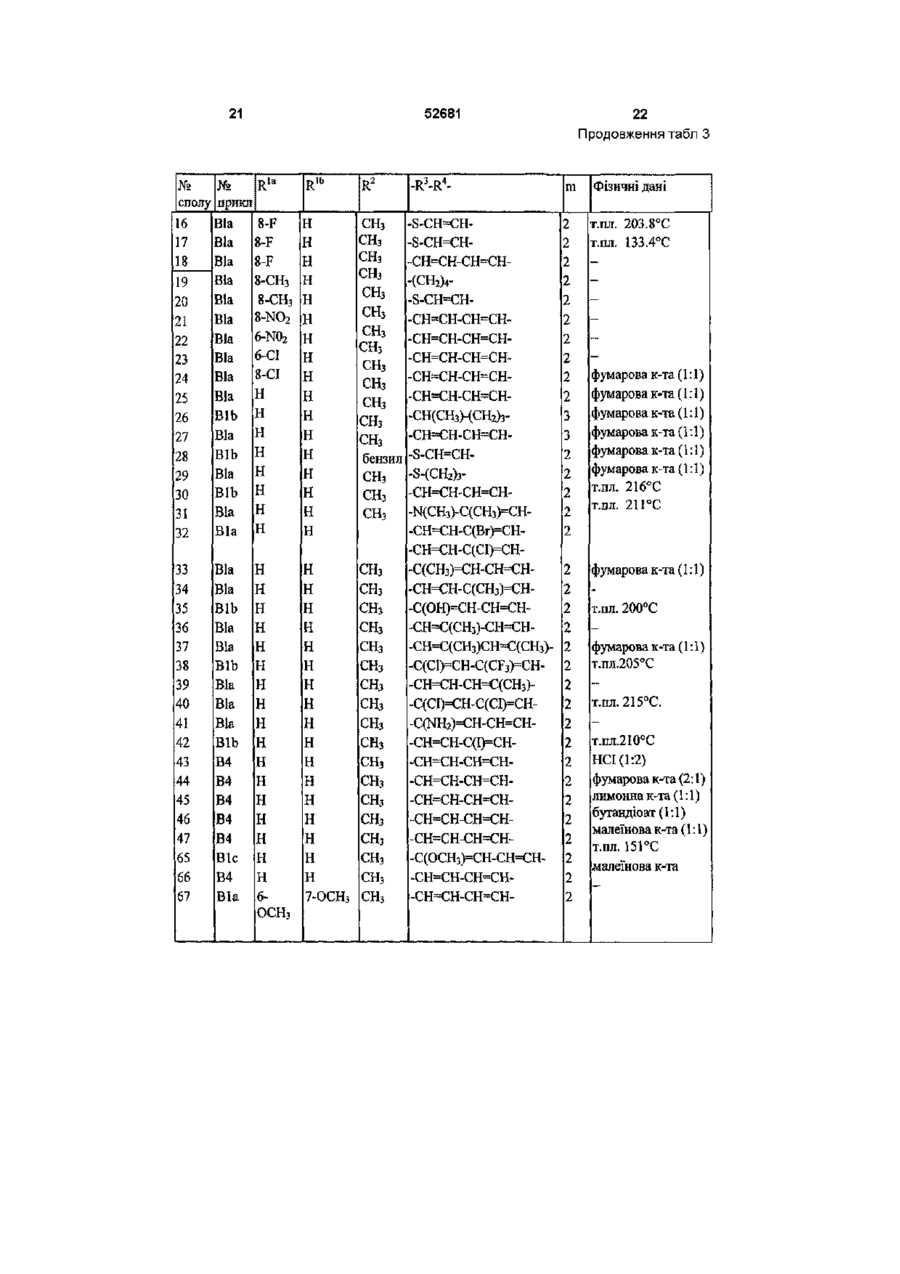
1 Сполука формули R D—Alk (І) и N-оксидна форма, фармацевтично прийнятна сіль приєднання або стереохімічно ізомерна форма, в яких кожний R1 незалежно являє собою водень, галоген, Сі є алкіл, нітро, гідрокси або Сі 4 алкокси, Alk являє собою Сі є алкандмл, п дорівнює 1 або 2, D являє собою 1 - або 2-бензимідазоліл, 2(ЗН)бензоксазолон-3-іл або радикал формул О 00 (О ю в яких кожний X незалежно являє собою О, S або NR 1 2 , R2 являє собою водень, Сі є алкіл, арил або арилСі єалкіл, R3 являє собою водень, Сі f алкіл, Сі є алкілокси, Сі є алкілтю, аміно або моно- або ди(Сі є алкіл)аміно, R4, RS, R6, R7, R8, R10, R 11 та R 12 кожний незалежно являє собою водень або Сі % алкіл, R9 являє собою водень, Сі є алкіл або арил, або R3 та R4 взяті разом можуть утворювати бівалентний радикал -R -R4 формул -СН2-СН2-СН2(а-1), -СН2-СН2-СН2-СН2(а-2), 52681 утворюють бівалентнии радикал формули (а-6), (а-СН=СН-СН2(а-3), 7), (а-8), (а-11) або (а-14), в яких один або, де це -СН2-СН=СН(а-4), можливо, два або три атоми водню заміщені ме-СН=СН-СН=СН (а-5), тилом де один або два атоми водню згаданих радикалів від (а-1) до (а-5) кожний незалежно може бути 5 Сполука згідно з п 1, де ця сполука являє собою заміщений гало, Сі є алкілом, арилСі єалкілом, 3-[2-[3,4-дипдробензофуро[3,2-с]піридин-2(1Н)трифторметилом, аміно, гідрокси, Сі є алкокси або іл]етил]-2-метил-4Н-піридо-[1,2-а]-піримідин-4-он, Сі ю алкілкарбонілокси, або там де можливо, два 6-[[3,4-дипдробензофуро[3,2-с]піридин-2(1Н)гемшальних атоми водню можуть бути заміщені іл]етил]-7-метил-5Н-тіазоло-[3,2-а]-піримідин-5-он, 3 Сі є алкіліденом або арилСі єалкіліденом, або -R 6-[[3,4-дипдробензофуро[3,2-с]піридин-2(1Н)4 R - можуть також бути іл]етил]-3,7-диметил-5Н-тіазоло-[3,2-а]-піримідин5-он, -S-CH2-CH2(а-6), 3-[2-[3,4-дипдробензофуро[3,2-с]піридин-2(1Н)-S-CH2-CH2-CH2(а-7), іл]етил]-2,7-диметил-4Н-піридо-[1,2-а]піримідин-4-S-CH=CH(а-8), он, N-оксид, фармацевтично прийнятна сіль при-NH-CH2-CH2(а-9), єднання або їх стереохімічно ізомерна форма -NH-CH2-CH2-CH2(а-10), -NH-CH=CH(а-11), 6 Сполука згідно з будь-яким пунктом з 1 по 5 для використання як лікарського препарату -NH-CH=N(а-12), -S-CH=N(а-13), 7 Композиція, ЩО МІСТИТЬ фармацевтично прийня-СН^СН-О(а-14), тний носій і, як активний інгредієнт, терапевтично ефективну КІЛЬКІСТЬ сполуки згідно з будь-яким в яких один або, там де можливо, два або три пунктом з 1 по 5 атоми водню згаданих радикалів від (а-6) до (а-14) кожний незалежно може бути заміщений Сі є 8 Спосіб одержання сполуки згідно з п 1, який алкілом або арилом, і відрізняється тим, що проводять арил являє собою феніл або феніл, заміщений а) N-алкілування похідних 1, 2, 3, 4гало або Сі є алкілом тетрапдробензофурано-[3,2-с]-піридину формули (II) алкілуючим реагентом формули 2 Сполука згідно з п 1, в якій D являє собою 1бензимідазоліл, 2(ЗН)бензоксазолон-Зіл або D являє собою радиD—Alk—W1 + кал формули (а), в якій R3 є Сі єалкілтю і R4 є Сі бал кіл, або R3 і R4 , взяті разом утворюють бівалентнии радикал формули (а-2) або (а-5), в яких один або два атоми водню згаданих ради(III) калів, кожний незалежно, можуть являти собою гало, Сі єалкіл, Сі єалкілокси, арилСі єалкіл, трифN-алкілувант торметил, аміно, гідрокси, Сі єалкілокси або Сі (І), юалкілкарбонілокси, або, де це можливо, два 1 гемшальних атоми водню можуть бути заміщені в якому W являє собою прийнятну реакційну відСі єалкіліденом або арилСі єалкіліденом, або хідну групу і D, Alk і R1 є такими, як це визначено у бівалентнии радикал формул (а-6), (а-7), (а-8), faп 1, l l ) або (а-14), в яких один або, де це можливо, Ь) зняття захисту з N-захищеноі проміжної сполуки два або три атоми водню в згаданих радикалах формули (IV) з наступним N-ацилюванням одеркожний незалежно може бути заміщений Сі жаної проміжної сполуки ацилпохідним формули єалкілом або арилом, або D являє собою радикал (V) 5 6 формули (Ь), в якій R і R являють собою Сі •О(R') єалкіл, або D являє собою радикал формули (Ь), в 5 6 якій R і R являють собою Сі єалкіл, або D являє собою радикал формули (с), в якій R7 є воднем або D являє собою радикал формули (d), в якій R є воднем або Сі єалкілом, або D являє собою ра(IV) (V) дикал формули (є), в якій R9 є арилом, або D яв10 ляє собою радикал формули (f), в якій X є S і R є воднем, або D являє собою радикал формули (д), в якій X є S і R11 є Сі єалкілом n 3 Сполука ЗГІДНО з п 1 або 2, в якій п дорівнює 1 і R1 являє собою водень, хлор, фтор, метил або нітро, або в якій п дорівнює 2 і R1 є метокси 4 Спокука згідно з будь-яким пунктом з 1 по 3, в якій R1 є воднем і D являє собою радикал формули (а), в якій R3 і R4, взяті разом, утворюють бівалентнии радикал формули (а-2) або (а-5), в яких один або два атоми водню, кожний незалежно, може бути заміщений гало, метилом, метокси, арил метилом, трифторметилом, аміно або гідрокси, або в яких два гемшальних атоми водню заміщені арилметиленом, або R3 і R4, взяті разом, (1-е) в якій Р являє собою захисну групу, W являє собою прийнятну реакційну відхідну групу і R1, R9 і Alk є такими, як визначено у п 1, утворюючи, таким чином, сполуку формули (1-е), с) N-алкілування аміну формули (VI) проміжною 52681 сполукою формули (VII) 1 0 R. 3 W+ N—Alk (VI) (VII) N-алкілувант в якій W являє собою прийнятну реакційну відхід1 10 ну групу і X, Alk, R і R є такими, як визначено у п 1, утворюючи, таким чином, сполуку формули (1-f), d) і, якщо це необхідно, перетворення сполук формули (І) в кожну іншу наступними відомими фахівцю трансформаціями і, в подальшому, якщо це необхідно, перетворення сполук формули (І) в терапевтично активну нетоксичну сіль приєднання кислоти шляхом обробки кислотою або в терапевтично активну нетоксичну сіль приєднання основи шляхом обробки основою або, навпаки, перетворення солі у формі приєднання кислоти у вільну основу шляхом обробки лугом або перетворення солі приєднання основи у вільну кислоту шляхом обробки кислотою, і, якщо це необхідно, одержання стереохімічно ізомерних форм або їх N-оксидів (l-f) Даний винахід стосується похідних 1,2,3,4тєтрапдро-бензофуро[3,2-с]піридину, що мають активність центральних аг-адренорецепторів Винахід також стосується їх одержання, композицій, що їх містять, а також їх використання як медичних засобів Відомо, ЩО антагоністи центральних a-zадренорецепторів підвищують вивільнення норадреналіну блокуванням пресинаптичних агрецепторів, які виявляють інгібуючий контроль за вивільненням нейротрансміттеру Завдяки підвищенню концентрацій норадреналіну аг-антагоністи можуть бути використані в КЛІНІЧНИХ умовах для лікування або профілактики депресії, порушень пізнання, хвороби Паркінсона, цукрового діабету, сексуальної дисфункції та імпотенції, підвищеного внутрішньоочного тиску та захворювань, пов'язаних з ентерокшетичними розладами, оскільки всі ці захворювання пов'язані з дефіцитом норадреналіну в центральній або перифіричній нервовій системі Сполуки згідно з винаходом є новими і мають специфічну та селективну зв'язуючу спорідненість до різних відомих субтипів а2-адренорецепторів, тобто (Х2А, ( 2 та агс-адренорецепторів ХВ Даний винахід стосується сполук формули 1 Dсад — k A l N-оксидних форм, фармацевтично прийнятних солей приєднання та їх стереохімічних ізомерних форм, в яких кожний R1 незалежно являє собою водень, галоген, Сі є алкіл, нітро, гідрокси або Сі 4 алкокси, Alk являє собою Сі є алкандмл, п дорівнює 1 або 2, D являє собою 1 - або 2-бензімідазоліл, 2(ЗН)бензоксазолон-3-іл або радикал формули Y о "С R О (а) 7 (Ь) N 0 • № (3) в яких кожний X незалежно являє собою О, S або NR12, R2 являє собою водень, Сі є алкіл, арил або арил С і є алкіл, R3 являє собою водень, Сі є алкіл, Сі є алкілокси, Сі є алкілтю, аміно або моно- або ди(Сі є) алкіл)амшо, R4, R5, R6, R7, R8, R10, R11 та R12 кожний незалежно являє собою водень або Сі алкіл, R9 являє собою водень, Сі алкіл або арил, або R3 та R4 взяті разом можуть утворювати бівалентний радикал -R3-R4 формули -СН2-СН2-СН2(а-1), -СН2-СН2-СН2-СН2(а-2), -СН=СН-СН2(а-3), -СН2-СН=СН(а-4), -СН=СН-СН=СН(а-5), де один або два атоми водню згаданих радикалів від (а-1) до (а-5) кожний незалежно може бути заміщений гало, Сі є алкілом, арил Сі є алкілом, трифторметилом, аміно, гідрокси, Сі є алкокси або Сі ю алкілкарбонілокси, або там, де можливо, два гемшальних атомів водю можуть бути заміщені Сі є алкіліденом або арил Сі є алкіліденом, або -R3-R4- можуть також бути -S-CH2-CH2(а-6), -S-CH2-CH2-CH2(а-7), -S-CH=CH(а-8), -NH-CH2-CH2(а-9), 52681 -NH-CH2-CH2-CH2-NH-CH=CH-NH-CH=N-S-CH-N-CH^CH-O (a-10), (a-11), (a-12), (a-13), (a-14), в яких один або, там де можливо, два або три атоми водню згаданих радикалів від (а-6) до (а-14) кожний незалежно може бути заміщений Сі є алкілом або арило, і арил являє собою феніл або феніл, заміщений гало або Сі є алкілом Як використовувалось у попередніх визначеннях термін галоген являє собою тривіальну назву по відношенню до фтору, хлору, брому та йоду Термін Сі є алкіл означає насичені вуглеводневі радикали з ЛІНІЙНИМ або розгалуженим ланцюгом, що мають від 1 до 6 атомів вуглецю, такі як, наприклад, метил, етил, пропіл, бутил, 1-метилетил, 1,1-диметил-етил, 2-метилпропіл, пентил, гексил і т ін Термін Сі ю алкіл включає Сі є алкільні радикали та вищі гомологи, що мають від 7 до 10 атомів вуглецю, такі як, наприклад, гептил, октил, ноніл, децил і т ш Термін Сі є алкандмл означає бівалентні алкіліденові радикали з ЛІНІЙНИМ або розгалуженим ланцюгом, що мають від 1 до 6 атомів вуглецю, такі як, наприклад, метилен, 1,2етандмл, 1,3-пропандмл, 1,4-бутандмл, 1,5пентандил, 1,6-гександмл і т ш , термін Сі є алкіліден означає бівалентні алкіліденові радикализ ЛІНІЙНИМ або розгалуженим ланцюгом, що мають від 1 до 6 атомів вуглецю, такі як, наприклад, метилен,етил іден, 1-пропіліден, 1-бутил іден, 1пентиліден, 1-гексиліден іт ін Згадані тут солі приєднання включають форми терапевтичне активних солей приєднання, які сполуки формули (І) здатні утворювати з прийнятними кислотами, такими як, наприклад, неорганічні кислоти, такі як галоводневі кислоти, наприклад, хлороводнева або бромоводнева кислоти, сірчана, азотна, фосфорна та подібні кислоти, або органічні кислоти, такі як, наприклад, оцтова, пропанова, пдроксиоцтова, молочна, піровиноградна, щавелева, малонова, бурштинова, малеїнова, фумарова, винна, лимонна, метансульфонова, етансульфонова, бензолсульфонова, р-толуолсульфонова, цикламшова, саліцилова, р-амшосаліцилова, ратоїс та подібні кислоти Фармацевтичне прийнятні солі приєднання, як згадувалося тут вище, також включають терапевтичне активні нетоксичні основи, зокрема, форми солей приєднання металу або аміну, які сполуки формули (І) здатні утворювати Згадані солі можуть бути зручно одержані обробкою сполук формули (І), що мають кислотні атоми водню, прийнятними органічними та неорганічними основами, такими як, наприклад, солі аммонію, солі лужних або лужно-земельних металів, наприклад, солі ЛІТІЮ, натрію, калію, магнію та подібні, солі з органічними основами, наприклад, бензатин, N-метилD-глюкамш, солі пдрабамшу та солі з амінокислотами, таким як, наприклад, арпнінова, лізинова і т п Навпаки, форми згаданих солей можуть бути перетворені обробкою прийнятними основами або кислотами у форму вільних кислот або основ Термін солі приєднання, що використовується тут вище, також охоплює сольвати, які сполуки 8 формули (І) здатні утворювати, це означає, що згадані сольвати також входять до об'єму даного винаходу Прикладами таких сольватів є, наприклад, гідрати, алкоголяти і т П Форма N-оксидів сполук формули (І) означає сполуки формули (І), в яких один або декілька атомів азоту оксидовані до так званих N-оксидів Термін стереохімічні ізомерні форми, використаний тут, визначає всі можливі ізомерні форми, в яких можуть існувати сполуки формули (І) Якщо не згадано або не вказано інакше, хімічне позначення сполук означає суміш всіх можливих стереохімічних ізомерних форм, причому згадані суміші містять всі діастереомери та енантюмери базової молекулярної структури Деякі сполуки формули (І) можуть також існувати в їх таутомерних формах Такі форми, хоча й точно не вказані в вище наведеній формулі, знаходяться в межах даного винаходу Кожного разу використаний тут в подальшому термін сполуки формули (І) означає, що він також охоплює N-оксидні форми, фармацевтичне прийнятні солі приєднання і всі стереоізомерні форми Спеціальною групою сполук є такі сполуки формули (І), в яких п дорівнює 1 і R являє собою водень, галоген, Сі-Сб-алкіл або нітро Цікавою групою сполук є такі сполуки формули (І), в яких п дорівнює 1 і R1 являє собою водень хлор, фтор, метил або нітро, особливо коли R являє собою водень або коли п дорівнює 2 і R1 являє собою метокси Іншою цікавою групою сполук є такі сполуки формули (І), в яких Alk являє собою метилен, 1,2етандмл, 1,3-пропандил, 1,4-бутандмл або 1,5пентандил Ще однією цікавою групою сполук є такі сполуки формули (І), в яких D являє собою 1бензімідазоліл, 2(ЗН)-бензоксазолон-3-іл, або D являє собою радикал формули (а) в якій R3 являє собою Сі-Сб-алкілтю і R4 являє собою Сі-Сє-алкіл, або в якій R3 та R4, взяті разом, утворюють бівалентний радикал формули (а-2) або (а-5), в яких один або два атоми водню згаданих радикалів кожний незалежно може бути заміщений гало, С г Сє-алкілом, арил Сі-Сє-алкілом, трифторметилом, аміно, гідрокси, Сі-Сє-алкілокси або С-і-С-юалкілкар-бонілокси, або, де це можливо, два гемінальні атоми водню можуть бути заміщені С-і-Сєалкіліденом або арил Сі-Сє-алкіліденом, або бівалентами радикал формули (а-6), (а-7), (а-8), (а-11) або (а-14), в яких один або, де це можливо, два або три атоми водню в згаданих радикалах, кожний незалежно, може бути заміщений С-і-Сєалкілом або арилом, або D являє собою радикал формули (Ь), в якій R5 і R6 являють собою С-і-Сєалкіл, або D являє собою радикал формули (с), в якій R7 є воднем, або D являє собою радикал формули (d), в якій R8 являє собою водень або С-і-Сєалкіл, або D являє собою радикал формули (є), в якій R9 є арилом, або D являє собою радикал формули (f), в якій X являє собою S і R ° є воднем, або D являє собою радикал формули (д), в якій X являє собою S і R11 є Сі-Сб-алкіл Особливими сполуками є такі сполуки формули (І), в яких D являє собою 2(ЗЯ)бензоксазолон-3іл, або D є радикал формули (а), вякій R3 є метил 52681 тю і R є метил, або в яких R і R , взяті разом, утворюють бівалентний радикал формули (а-2) або (а-5), в яких один або два атоми водню, кожний незалежно, можуть бути заміщені гало, С-і-Сєалкілом, Сі-Сб-алкілокси, арил Сі-Сє-алкілом, трифторметилом, аміно або гідрокси, або в яких два гемшальні атоми водню заміщені арил С-і-Сє3 алкіліденом, або R і R , взяті разом, утворюють бівалентний радикал формули (а-6), (а-7), (а-8), (а11) або (а-14), в яких один або, де це можливо, два або три атоми водню заміщені СгСє-алкілом або D являє собою радикал формули (Ь), в якій R 6 і R являють собою метил, або D являє собою ра7 дикал формули (с), в якій R є водень, або D являє 8 собою радикал формули (d), в якій R є водень або D являє собою радикал формули (є), в якій R є арил, пов'язаний з Alk в 4 положенні піперидинового залишку, або D являє собою радикал формули (f), в якій X являє собою S і R10 є водень, або D являє собою радикал формули (д), в якій X являє собою S і R11 є метил Переважними сполуками є такі сполуки формули (І), в яких п дорівнює 1, R1 є водень і D являє собою радикал формули (а), в якій R3 і R4, взяті разом, утворюють бівалентний радикал формули (а-2) або (а-5), в яких один або два атоми водню, кожний незалежно, можуть бути заміщені гало, метилом, метокси, арил метилом, трифторметилом, аміно або гідрокси, або в яких два гемшальні атоми водню заміщені арилметиленом, або R31 R4, взяті разом, утворюють бівалентний радикал формули (а-6), (а-7), (а-8), (а-11) або (а-14), в яких один або, де це можливо, два або три атоми водню заміщені метилом Найбільш переважними сполуками є 3-[2-[3,4-дипдробензофуро[3,2-с]піридин2(1 Н)-іл]етил]-2-метил-4Н-піридо-[1,2-а]піримідин4-он, 6-[[3,4-дипдробензофуро[3,2-с]піридин-2(1Н)іл]етил]-7-метил-5Н-тіазоло-[3,2-а]-шримідин-5-он, 6-[[3,4-дипдробензофуро[3,2-с]піридин-2(1Н)іл]етил]-3,7-диметил-5Н-тіазоло-[3,2-а]-піримідин5-он, 3-[2-[3,4-дипдробензофуро[3,2-с]піридин2(1 Н)-іл]етил]-2,7-диметил-4Н-пІридо-[1,2а]піримідин-4-он, N-оксиди, фармацевтично прийнятні солі приєднання та їх стереохімічно,ізомерні форми Загалом сполуки формули (І) можуть бути одержані N-алкілуванням похідних 1,2,3,4тетрапдробензофурано[3,2-с]піридину формули (II) алкілуючим реагентом формули (III) за наступною методикою, описаною в ЕР-А-0 037 265, ЕР-А0 070 053, ЕР-А-0 196 132 і ЕР-А-0 378 255 N-зпкщувзни • Alk (Iff) H " (II .N (И) Проміжні сполуки формули (III), в яких W 1 являє собою придатну реакційну відхідну групу, таку як, наприклад, гало, наприклад, хлор, бром або і йод, сульфонілокси, наприклад, метансульфонілокси, 4-метилбензолсульфо-нілокси В цих та наступних реакціях, продукти реакції можуть бути виділені з реакційного середо 10 вища і, якщо це необхідно, в подальшому очищені загальновідомими методами, такими як екстракція, кристалізація, порошкування та хроматографія Сполуки формули (І), в яких D являє собою радикал формули (є), будучи представлені формулою (1-е), можуть бути одержані знаттям захисту з N-захищеноі проміжної сполуки формули (IV), в якій Р є захисна група, така як, наприклад, d 4алкілоксикарбонільна група, з подальшим Nацилюванням одержаної проміжної сполуки аци2 льними похідними формули (V), в якій W є придатна реакційна відхідна, така як, наприклад, галоген Сполуки формули (І), в яких D є радикал формули (І), будучи представлені формулою (l-f), можуть бути одержані N-алкілуваиням аміну формули (VI) з проміжною сполукою формули (VII), в якій W 3 являє собою придатну відхідну групу, таку, як, наприклад, галоген ^ t Сполуки формули (І) можуть бути перетворені одна в іншу відомими реакціями перетворення функціональних груп Сполуки формули (І) можуть також бути перетворені у ВІДПОВІДНІ N-оксидні форми наступними відомими способами перетворення тривалентного азоту в його N-оксидну форму Згадана реакція Nоксидування загалом може бути проведена шляхом реагування вихідного матеріалу формули (І) з придатним органічним або неорганічним пероксидом До придатних неорганічних пероксидів належать, наприклад, пероксид водню, пероксиди лужних або лужно-земельних металів, наприклад, пероксид натрію, пероксид калію, придатні органічні переоксиди можуть включати пероксикислоти, такі як, наприклад, пероксибензойна кислота або гало-заміщена пероксибензойна кислота, наприклад, 3-хлорпероксибензойна кислота, пероксиалканові кислоти, наприклад, пероксиоцтова кислота алкіл гід ропероксиди, наприклад, третбутилпдропероксид Придатними розчинниками є, наприклад, вода, нижчі алканоли, наприклад, етанол і т п , вуглеводні, наприклад, толуол, кетони, наприклад, 2-бутанон, галогеновані вуглеводні, наприклад, дихлорметан, та суміш таких розчинників Багато проміжних сполук та вихідних матеріалів є комерційне доступними або відомими сполуками, які можуть бути одержані згідно з відомими методиками Наприклад, деякі проміжні сполуки формули (III) та їх одержання описані в ЕР-А0 037 265, ЕР-А-0 070 053, ЕР-А-0 196 132 та в ЕРА-0 378 255 Проміжні сполуки формули (II) можуть бути одержані наступними способами, описаними в Cattanach Et al , (J Chem Soc (С), 1971, р 53-6 0), Kartashova T (Khim Geterotsicl Soedm , 1979 (9), p 1178 - 1180) і Zakusov V Et al , (Izobretemya, 1992(15), p247) 52681 12 11 Особливий шлях синтезу для одержання проформули (І) можуть також бути отримані з стереохімічно чистих ізомерних форм придатних проміжміжних сполук формули (II) подано на схемі 1 них сполук та вихідних матеріалів при умові, що реакції проходять стереоспецифічно Чисті та змішані стереохімічно ізомерні форми сполук формуC , H стадія ь К л? O j C ли (І) також охоплюються рамками даного винахоДУ Сполуки формули (І), N-оксиди, фармацевтично прийнятні солі приєднання та їх стереохімічно ІЗОМерНІ су. Стадія а може бути проведена аналогічно процесу, описаному в Tetrahedron (1981, 37, р 979 - 982) Бензофурани, отримані на стадії с, використовували як проміжні сполуки в US 4 210 655 Подальші стадії реакції є аналогічними реакціям, описаним в US 3 752 820 Альтернативно, проміжні сполуки формули (II) можуть бути, одержані з використанням стадій реакції, поданих на схемі 2 Сішж2 о—ш.—с=сн СН^-СН, NK, Стадія а може бути проведена аналогічно процесу, описаному в Heterocycles (1994, 39(1), р 371 - 380) Стадія b може бути проведена аналогічно процесу, описаному в J Med Chem (1986), 29(9), р1643 - 1650 Подальші стадії реакції можуть бути проведені аналогічно реакціям, описаним в J Heterocycl Chem (1979), 16, р 1321 Деякі сполуки формули (І) та деякі проміжні сполуки згідно з даним винаходом мають принаймні один асиметричний атом вуглецю Чисті стереохімічне ізомерні форми згаданих сполук та згадані проміжні сполуки можуть бути одержані з використанням відомих методик Наприклад, діастереоізомери можуть бути розділені фізичними методами, таким як селективна кристалізація або хроматографія, наприклад, протитечійне розділення, рідинна хроматографія та подібні методи Енантюмери можуть бути одержані з рацемічних сумішей спочатку перетворенням згаданих рацемічних сумішей з придатними розділяючими агентами, такими як, наприклад, хіральні кислоти, в суміші діастереомерних солей або сполук, а потім фізичним розділенням згаданих сумішей суміші діастереомерних солей або сполук, наприклад, методами селективної кристалізації або хроматографії, наприклад, рідинною хроматографією і подібними методами, і в КІНЦІ перетворенням згаданих розділених діастереомерних солей або сполук у ВІДПОВІДНІ енантюмери Чисті стереохімічне ізомерні форми сполук форМИ, бЛОКуЮТЬ ПреСИНаПТИЧНІ (Х2 рецептори на центральних норадренерпчних нейронах, підвищуючи, таким чином, вивільнення норадреналіну Блокування згаданих рецепторів буде пригнічувати або полегшувати багато симптомів, пов'язаних з дефіцитом норадреналіну в центральній та периферичній нервовій системі Терапевтичними показаннями для використання даних сполук є депресія, хвороба Паркінсона, сексуальна дисфункція та імпотенція та підвищений внутрішньоочний тиск Було показано, що блокування аг-рецепторів в центральній нервовій системі підвищує вивільнення серотоніну, який може підвищувати терапевтичну дію при лікуванні депресії (Maura et al , 1992, Naunyn-Schmiedeberg's Arch Pharmacol, 345 410 416) Також було показано, що блокування агрецепторів даними сполуками викликає збільшення КІЛЬКОСТІ позаклітинної DOPAC (3,4дипдрофенілоцтової кислоти), яка являє собою метаболіт допамшута норадреналіну С точки зору корисності даних сполук в лікуванні захворювань, пов'язаних з дефіцитом норадреналіну в центральній нервовій системі, зокрема, депресії та хвороби Паркінсона, даний винахід охоплює спосіб лікування теплокровних тварин, що страждають від таких захворювань, особливо депресії та хвороби Паркінсона, згаданий спосіб полягає в систематичному призначенні терапевтичне ефективної КІЛЬКОСТІ сполуки формули (І) або и фармацевтично прийнятної солі приєднання Дані сполуки є також потенційно корисними для лікування хвороби Альцгеймера та деменції, оскільки відомо, що а2-антагоністи сприяють вивільненню ацетилхоліну (Tellez et al 1977, J Neurochem, 68 778 - 785) Загалом прийнято, що терапевтичне ефективна щоденна КІЛЬКІСТЬ повинна бути від приблизно 0 01 мг/кг до приблизно 4 мг/кг ваги тіла Таким чином, даний винахід також стосується сполук формули (І), які визначено тут вище, для використання у медицині Крім того, даний винахід також стосується використання сполук формули (І) для виробництва медикаменту для лікування депресії та хвороби Паркінсона Ex vivo так як і in vitro дослідження рецептора трансдукції сигналу та рецептора зв'язування та здатності ВІДМІНЯТИ клонідин-індуковане відновлення електричко стимульованого вивільнення норадреналіну з кори головного мозку кролика може бути використано для оцінки антагонізму агадренорецептора даних сполук Як показники блокади центрального аг-адренорецептора in vivo можуть бути використані відміна втрати правого рефлексу, що спостерігається у щурів після внутрішньовенної ін'єкції ксилазину, та інгібування 13 тремору, викликаного у щурів резерпином В тесті на соціальну перевагу, в якому щури повинні змагатися за пиття цукрового розчину, сполуки згідно з винаходом здатні підвищувати конкуруючу поведінку покірних щурів Дані сполуки також проявляють вплив на кишечник, вони пригнічують антидіарейний ефект клонідину і стимулюють фекальну екскрецію у нагодованих щурів У собак вони здатні прискорювати напад діареї, індукованої MgSO4, і в тесті по спорожненню кишечнику у собак вони мають здатність пригнічувати уповільнення спорожнення кишечника, викликане сі2-агоністами лідамідину Таким чином, дані сполуки також корисні для лікування захворювань, пов'язаних з порушенням ентерокінезм Сполуки згідно з винаходом також мають здатність до швидкого проникнення в центральну нервову систему Для лікувальних цілей дані сполуки можуть бути уведені до складу різних фармацевтичних композицій, що містять фармацевтичне прийнятний носій і, як активний інгредієнт, терапевтично ефективну КІЛЬКІСТЬ сполуки формули (І) Для приготування фармацевтичних композицій згідно з винаходом, комбінують, як активний інгредієнт, ефективну КІЛЬКІСТЬ конкретної сполуки у вигляді солі приєднання або у формі вільної кислоти або основи при ретельному перемішуванні з фармацевтичне прийнятним носієм, який може приймати величезну КІЛЬКІСТЬ форм в залежності від форми приготування, необхідної для призначення Такі фармацевтичні композиції, бажано у формі одиничної дози, підходять, переважно, для орального призначення, трансдермального або парентеральних ІН'ЄКЦІЙ Наприклад, при приготуванні композицій у формі оральної дози, можуть використовуватися будь-які звичайні фармацевтичні середовища, такі як, наприклад, вода, ГЛІКОЛІ, масла, спирти і т ш у випадку оральних рідких рецептур, таких як суспензії, сиропи, еліксири та розчини, або тверді носи, такі як крохмалі, цукри, каолін, змащуючі речовини, зв'язуючі, агенти дезінтеграції і т ш у випадку порошків, драже, капсул і таблеток В зв'язку з легкістю призначення таблетки та капсули являють собою найбільш переважні оральні форми одиничної дози, у випадку яких звичайно використовують тверді фармацевтичні носи Для парентеральних композицій носи зазвичай будуть складатися з води, принаймні, велика їх частина, хоча можуть бути уведені і ІНШІ ІНГЄДІЄНТИ, наприклад, з метою розчинності Наприклад, можуть бути приготовані розчини для ІН'ЄКЦІЙ, В ЯКИХ НОСИ складаються з розчину солі, розчину глюкози або суміші розчинів солі і глюкози Розчини для ІН'ЄКЦІЙ, що містять сполуки формули (І) можуть бути зроблені у маслі для пролонгованої дії Придатними маслами для цих цілей є, наприклад, арахісове масло, кунжутне масло, масло насіння бавовни, кукурудзяне масло, масло сої, синтетичні гліцеринові ефіри довголанцюгових жирних кислот і суміш їх та ІНШІ масла Можуть також бути приготовані суспензії для ІН'ЄКЦІЙ, у випадку яких можуть застосовуватися придатні рідкі носи, суспендуючі агенти та ш В композиціях, придатних для трансдермального призначення, носи необов'язково 52681 14 містять агент, що підвищує проникність і/або придатний змочувальний агент, необов'язково у сполученні з придатними добавками будь-якої природи в незначній КІЛЬКОСТІ, які не викликають будьякого значного подразнюючого впливу на шкіру Згадані добавки можуть сприяти призначенню на шкіру і/ або можуть бути корисними для приготування бажаних композицій Такі композиції можуть бути призначені різними шляхами, наприклад, як трансдермальний пластир або як мазь Солі приєднання (І) завдяки їх підвищеній розчинності у воді через ВІДПОВІДНІ форми вільної основи або вільної кислоти, очевидно більш придатні для приготування ВОДНИХ КОМПОЗИЦІЙ Це особливо вигідно для приготування рецептур вищезгаданих фармацевтичних композицій у формі одиничної дози для полегшення призначення та одноманітності доз Форма одиничної дози, як вона використовується у описі та формулі винаходу, відноситься до фізично дискретних одиниць, придатних як єдині дози, кожна одиниця яких містить зумовлену КІЛЬКІСТЬ активного інгредієнту, розраховану для забезпечення бажаного терапевтичного ефекту, у поєднанні з необхідним фармацевтичним носієм, Прикладами таких форм одиничної дози є таблетки (у тому числі шершаві (без оболонки) та вкриті оболонкою таблетки), капсули, драже, пакети порошку Наступні приклади призначені для ілюстрації даного винаходу Експериментальна частина Тут в подальшому "КГГ" означає кімнатну температуру, "ТГФ" означає тетрапдрофуран, "ДМФ" означає N.N-диметилформамід і "ДІПЕ" означає дмзопропіловий ефір А Одержання проміжних сполук Приклад А1 Суміш О-фенілпдроксиламіну пдрохлориду (1 1) (0 625моль) і 4,4-піперидиндюл пдрохлориду (1 1) (0 682моль) в 2-пропанолі (615мл) перемішували при 20°С По краплям додавали НСІ (353мл) при 20°С Реакційну суміш обережно нагрівали температури кипіння Реакційну суміш перемішували і кип'ятили зі зворотнім холодильником протягом 3 годин, потім охолоджували до кімнатної температури Осад відфільтровували, промивали ДІПЕ і висушували Цю фракцію кристалізували з води (1600мл) Цільова сполука кристалізувалася під час перемішування Осад відфільтровували, промивали 2-пропанолом та ДІПЕ, потім висушували, одержуючи 84г (64%) 1,2,3,4тетрапдробензофуро[3,2-с]піридин пдрохлориду (1 1) (проміжна сполука 1) Приклад А2 1,4-дюкса-8-азаспіро[4,5]декану (012моль) додавали по краплям до суміші О-(4фторфеніл)пдроксиламшу пдрохлориду (1 1) (0 1моль) в суміші НСІ і 1,1-оксибісетану (150мл) Реакційну суміш перемішували і кип'ятили зі зворотнім холодильником протягом 4 годин, а потім охолоджували Осад відфільтровували і висушували, потім перекристалізовували з води, отримуючи 10г (43,9%) 1,2,3,4-тетрапдро-8фторбензофуро[3,2-е]піридин пдрохлориду (проміжна сполука 2, т пл > 300°С) Приклад З 52681 16 15 a) 1,2,3,4-тетрапдро-2-метил-6Приклад А5 нітробензофуро[3,2-с]піридин (0 0224моль), одерa) Суміш проміжної сполуки (1) (0 ОЗмоль), жаний згідно з методикою, описаною в J Chem етил(5-хлорпентил)карба-мату (0 04моль), йодиду Soc (С), 1971, р53 - 60, розчинювали в 1,2калію (0 1г) і ІЧа2СОз (5 7г) в толуолі (250мл) передихлоретані (40мл) і охолоджували до 0°С При цій мішували і кип'ятили зі зворотнім холодильником температурі по краплям додавали (1протягом ночі Реакційну суміш охолоджували, хлоретил)ацети л хлорид (0 0291 моль) Суспензію перемішували з водою (200мл), і шари відокремперемішували і кип'ятили зі зворотнім холодильлювали Органічну фазу випаровували Залишок ником протягом 2 годин, 1,2-дихлоретан випароочищали колонковою хроматографією на силікагевували Суміш розчиняли у метанолі, перемішувалі (елюент СН2СІ2/СНз0Н 95/5) Очищені фракції ли і кип'ятили зі зворотнім холодильником збирали і розчинник випаровували, одержуючи 7 г протягом 2 годин, потім фільтрували Як фільтрат, етил[5-(3,4-дипдро-бензофуро[3,2-с]піридшІ-2(1Н)так і кристали обробляли 2 N ІЧа2СОз і цю суміш іл)пентил]карбамату (проміжна сполука 15) екстрагували СН2СІ2 Відокремлений органічний b) Суміш проміжної сполуки (15) (0 021 моль) і шар висушували, фільтрували і розчинник випарогідроксиду калію (12г) в 2-пропанолі (120мл) перевували Залишок очищали за допомогою колонкомішували і кип'ятили зі зворотнім холодильником вої хроматографії на сілікагелі (елюент протягом 6 годин Розчинник випаровували ЗалиСН2СІ2/СН3ОН 90/10) ЦІЛЬОВІ фракції збирали і шок розподіляли між СН2СІ2 і водою Органічний розчинник випаровували, одержуючи 1 5г 1,2,3,4шар відокремлювали, висушували, фільтрували і тетрапдро-6-нітробензофуро[3,2-с]піридину (пророзчинник випаровували, одержуючи 4г 3,4міжна сполука 4) дипдробензофуро[3,2-с]піридин-2(1Н)-пентанамшу b) Суміш 1,2,3,4-тетрапдро-2-метил-6нітробензофуро[3,2-с]піридину (0 0215моль) і триетиламшу (2г) в ТГФ (200мл) гідрували у присутності каталізатора - палладія на вуглі 10% (2г) в присутності тюфену 4 % ( мл) Після поглинання Н2 (3 еквіваленти) каталізатор відфільтровували і фільтрат випаровували, одержуючи 4 2г 1,2,3,4тетрапдро-6-амшо-2-метилбензофуро-[3,2с]піридину (проміжна сполука 7) c) Суміш проміжної сполуки (7) (0 01000 моль) і НСІ (2мл) діазотували при -5°С з використанням NaNO2 (0 0105моль) у воді (1 2мл) протягом ЗО хвилин Розчин перемішували протягом ЗО хвилин при -5°С Додавали суміш СиСІ (0 010 моль) в НСІ (10 6 мл) протягом 10 ХВИЛИН Одержану реакційну суміш перемішували протягом 15 хвилин при 80°С, потім охолоджували до 20°С Після розбавлення водою додавали в надлишку 40% К2СОз і одержану суміш екстрагували СН 2 СІ 2 Відокремлений органічний шар висушували, фільтрували і розчинник випарювали, одержуючи 17г (78%) 1,2,3,4тетрапдро-6-хлор-2-метилбензофуро-[3,2с]піридину (проміжна сполука 8) Приклад А4 a) Суміш проміжної сполуки (1) (0 ОЗмоль), хлорацетонітрилу (0 04моль), йодиду калію (0 1г) і ІЧа2СОз (5г) в 4-метил-2-пентпноні (180мл) перемішували і кип'ятили зі зворотнім холодильником протягом 3 годин Суміш фільтрували теплою і фільтрат випаровували Залишок очищали через силікагель на скляному фільтрі (елюент СН2СІ2/(СНз0Н/МНз) 95/5) ЦІЛЬОВІ фракції збирали і розчинник випаровували Залишок кристалізували з ДІПЕ/петролейний ефір 1/1 Осад відфільтровували і висушували, одержуючи 5 74г (90%) 3,4дипдрбензофуро[3,2-с]піридин-2(1Н)-ацетонітрилу (проміжна сполука 10, т пл 78°С) b) Суміш проміжної сполуки (10) (0 027моль) в CH3OH/NH3 (200мл) гідрували за допомогою нікелю Ренею (2г) як каталізатора в присутності тюфену 4% (1мл) Після поглинання Н2 (2 еквіваленти) каталізатор відфільтровували через дикаліт і фільтрат випаровували, одержуючи 5г (85 6%) 1,2,3,4-тетрапдро-2-(амшоетил)бензофуро-[3,2с]піридину (проміжна сполука 12) (проміжна сполука 16) Приклад А6 a) Суміш 3-пдроксиметилпіперидину (0 бмоль) і Na2CO3 (130г) в СНСІз (600мл) і води (600мл) перемішували при 10°С Додавали по краплям етилхлорформіат (115г) (при цьому підтримували температуру 10°С) Суміш перемішували до тих пір, поки температура не досягала кімнатної, і потім реакційну суміш перемішували протягом ночі Додавали воду (500мл) Органічний шар відокремлювали, промивали водою, висушували, фільтрували і розчинник випаровували, одержуючи 110г (98%) (±)-етил-3-(пдроксиметил)-1піперидинкарбоксилату (проміжна сполука 17) b) Розчин метилфенілсульфонілхлориду (0 79моль) в піридині (200мл) додавали по краплям до розчину проміжної сполуки (17) (0 4моль) в піридині (150мл) і перемішували при 10°С Реакційну суміш перемішували до тих пір, поки температура не досягала кімнатної, і потім реакційну суміш перемішували протягом ночі Продовжуючи перемішування, суміш виливали у воду (ЮООмл) і екстрагували метилізобутилкетоном Відокремлений органічний шар промивали водою, висушували, фільтрували і розчинник випаровували Залишок кристалізували із суміші дмзопропілового ефіру та петролейного ефіру Осад відфільтровували і висушували, одержуючи 96г (70 3%) (±)етил-3-[[[(4-метилфеніл)сульфоніл]окси]метил]-1піперидинкарбоксилату (проміжна сполука 18) c) Суміш проміжної сполуки (18) (0 0088моль), вільної основи проміжної сполуки (1) (0 0080моль) і ІЧа2СОз (0 01 бмоль) в ДМФ (25мл) перемішували і кип'ятили зі зворотнім холодильником протягом ночі Реакційну суміш охолоджували і розчинник випаровували Залишок розподіляли мід СН2СІ2 і 50% водним розчином NaCI Шари розділяли Водний шар тричі екстрагували СН2СІ2 Об'єднані органічні шари висушували, фільтрували і розчинник випаровували Залишок очищали HPLC на силікагелі (елюент СН2СІ2/СНз0Н 95/5) Очищені фракції збирали і розчинник випаровували, одержуючи 1 5г (55%) етил-4-[[3,4дипдробензофуро[3,2-с]піридин-2(1 Н)-іл]метил]-1 піперидинкарбокси-лату (проміжна сполука 19) 52681 18 17 Наступні проміжні сполуки, вказані в табл 1 та реакційної суміші не додавали йодид калію 2, одержані аналогічно до однієї з вище наведених с) Суміш проміжної сполуки (1) (0 015моль) і триетиламшу (4г) в 4-метил-2-пентаноні (150мл) прикладів перемішували протягом 5 хвилин Додавали 9Таблиця 1 метокси-2-метил-3-[2[(метилсульфоніл)окси]етил]-4Н-піри-до[1,2а]піримідин-4-он (0 015моль), одержаний як це описано в WO95/14691, і одержану реакційну суміш перемішували і кип'ятили зі зворотнім холодильником протягом 6 годин Суміш фільтрували теплою і фільтрат перемішували у воді (ЮОмл) Ха R' Фізичні дані Органічний шар відокремлювали, висушували, прошжн. приклада фільтрували і розчинник випаровували Залишок 1 А1 Н НСІ (1:1) кристалізували з ДІПЕ і невеликої КІЛЬКОСТІ CH3CN Продукт відфільтровували і висушували Одержа2 А2 8-F Тлш.>300°С;НСІ(і:1) ну фракцію очищали колонковою хроматографією 3 А2 8-СН3 НСЇ (1:1) на силікагелі (елюент СН2СІ2/С2Н5ОН 92/8) Очи4 АЗа 6-N02 щені фракції об'єднували і розчинник випаровува5 АЗа 6-С1 ли Залишок кристалізували з ДІПЕ Осад відфільтровували і висушували, одержуючи 0 6г 3-[2-[3,4б АЗа 8-а дипдробензофуро[3,2-с]піридин-2(1Н)-іл]етил]-9метокси-2-метил-4Н-піридо[1,2-а]-піримідин-4-он (сполука 65, т пл 151 °С) R промшн. 7 8 9 10 11 12 13 14 15 16 прикяа АЗЪ АЗс АЗс А4а А4а А4Ъ А4Ь А4Ь А5а А5Ь m D 6NH2 6-CI 8-Cl Н Н Н Н Н Н 1 1 1 I 3 2 4 3 5 5 Н Н Н CN CN NH2 NH3 NH ; C2HsG-C(=0)-NHNH2 В Одержання кінцевих сполук Приклад В1 а) Суміш 3-(2-хлоретил)-2-метил-4Нпіридо[1,2-а]піримідин-4-ону (0 0050моль), одержаного згідно з методиками, описаними в ЕР 0 070 053, вільної основи проміжної сполуки (1) (0 0040моль), ЫагСОз (О 008моль) та йодиду калію (0 0040моль) в 4-метил-2-пентаноні (8мл) перемішували і кип'ятили зі зворотнім холодильником протягом ночі Реакційну суміш охолоджували Додавали 50% водний розчин NaCI і СН2СІ2 Об'єднані органічні шари висушували, фільтрували і розчинник випаровували Залишок очищали флеш колонковою хроматографією на силікагелі (елюент С2Н5ОН/СН2СІ2 5/95) ЦІЛЬОВІ фракції об'єднували і розчинник випаровували Залишок розтирали в порошок і sonicated під ДШЕ, потім відфільтровували і висушували, одержуючи 0 9г (63%) 3-[2-[3,4-дипдробензофуро[3,2-с]піридин2(1 Н)-іл]етил]-2-метил-4Н-піридо-[1,2-а]-піримідин4-ону (сполука 3, т пл 186,2°С) Ь)6-[[3,4-дипдробензофуро[3,2-с]піридин2(1Н)-іл]етил]-3,7-диме-тил-5Н-тіазоло-[3,2-а]піримідин-5-он (сполука 5) був одержаний аналогічно способу, описаному в прикладі В1а, але до Приклад В2 Суміш проміжної сполуки (12) (0 0116моль), 2хлорбензотіазолу (0 0118моль) і NaHCO3 (2г) в 2етоксиетанолі (45мл) перемішували і кип'ятили протягом 2 годин Реакційну суміш охолоджували і додавали під час перемішування воду (45мл) Тверду речовину відфільтровували відсмоктуванням, промивали водою перемішували в ДІПЕ, відфільтровували і висушували Одержану фракцію розчиняли в невеликій КІЛЬКОСТІ метанолу і перетворювали в сіль (Е)-2-бутендикислоти (1 1) в процесі перемішування і нагрівання Суміш залишали охолоджуватися при перемішуванні до кімнатної температури і одержаний осад відфільтровували і висушували, одержуючи 3 4г (63%) N-2бензотіазол-3,4-дипдробензофуро[3,2-с]піридин2(1Н)етанамшу (Е)-2-бутендюат (1 1) (сполука 51, т п л 210°С) Приклад ВЗ Гідроксид калію (0 088моль) додавали до гарячого розчину проміжної сполуки (19) (0 0044моль) в 2-пропанолі (50мл) і одержану реакційну суміш перемішували і кип'ятили протягом 16 годин Розчинник випаровували Залишок розподіляли між водою і СН2СІ2 Шари відокремлювали Водну фазу тричі екстрагували СН2СІ2 Об'єднані органічні фази висушували, фільтрували і розчинник видаляли Залишок очищали флеш-колонковою хроматографією на силікагелі (елюент CH2CI2/CH3OH/NH3 95/5) ЦІЛЬОВІ фракції об'єднували і розчинник випаровували Залишок розчиняли в СНСІз (15мл) Додавали триетиламш (0 726г) Додавали 4-метилбензоілхлорид (0 0075моль) і реакційну суміш перемішували протягом однієї години Додавали 50% водний розчин NaOH Шари відокремлювали Водний ДВІЧІ екстрагували СН2СІ2 Об'єднані органічні шари висушували, фільтрували і розчинник випаровували Залишок очищали флеш-колонковою хроматографією на силікагелі (елюент СН2СІ2/С2Н5ОН 97/3) Очищені фракції збирали і розчинник випаровували Залишок висушували, одержуючи 11г (64%) 4[(3,4-дипдробензофуро[3,2-с]піридин-2(1Н) 19 52681 20 іл)метил]-1-(4-метилбен-зоіл)піперидину (сполука лук Осад відфільтровували і висушували, одер58, т п л 140 3°С) жуючи 3 2г 3-[2-[3,4-дипдробензофуро[3,2с]піридин-2(1 Н)-іл]етил]-2-метил-4Н-піридо[1,2-а]Приклад В4 піримідин-4-ону гідрохлорид (сполука 43) Сполуку (3) (0 0083моль) розчиняли в киплячому 2-пропанолі (80мл) Суміш НСІ і 2-пропанолу Наступні сполуки, наведені в таблицях 3 та 4, додавали по краплям при перемішуванні до теплоодержані способами, аналогічними одному з навего розчину доти, поки він не став кислим Суміш дених вище прикладів залишали для викристалізовування цільових споТаблиця З R -R -R 4 га ФЬмчні дані H H СНз СНз -S-CH=CH 2 2 H H H H СНз СНз -сн-сн-сн=сн~ 2 2 H H H H H H H H H H H H H H H H H H H H H H СНз СНз СНз СНз СН3 феніл СНз СНз СНз бензш СНз -S-CH=C{CHj)~$-
ДивитисяДодаткова інформація
Назва патенту англійськоюDerivatives of 1,2,3,4-tetrahydro-benzofuro [3,2,-c] pyridine
Автори англійськоюLove Christopher John
Назва патенту російськоюПроизводные 1,2,3,4-тетрагидро-бензофуро [3,2,-c] пиридина
Автори російськоюЛав Кристофер Джон, Лав Крістофер Джон
МПК / Мітки
МПК: A61K 31/4375, C07D 491/04, A61K 31/529, A61P 15/00, A61K 31/00, A61P 1/00, A61P 25/00, C07D 519/00, A61K 31/4355, A61P 15/10, A61K 31/505, A61P 3/10, C07D 491/048, A61P 25/16, A61P 3/00, A61K 31/4353, A61P 25/28, A61K 31/435, C07D 513/04, A61K 31/506, A61P 9/00, A61K 31/519, A61P 25/02, A61P 25/24, C07D 498/04, A61K 31/445
Мітки: основі, похідні, фармацевтична, 1,2,3,4-тетрагідро-бензофуро[3,2,-c]піридину, спосіб, одержання, композиція
Код посилання
<a href="https://ua.patents.su/15-52681-pokhidni-1234-tetragidro-benzofuro32-cpiridinu-sposib-kh-oderzhannya-ta-farmacevtichna-kompoziciya-na-kh-osnovi.html" target="_blank" rel="follow" title="База патентів України">Похідні 1,2,3,4-тетрагідро-бензофуро[3,2,-c]піридину, спосіб їх одержання та фармацевтична композиція на їх основі</a>
Попередній патент: Спосіб одержання ( 1,1-діоксотіолан-3-іл)-дитіокарбамату калію
Наступний патент: Таблетка малеату тримебутину в оболонці
Випадковий патент: Надтвердий композиційний матеріал