Кальцилітична сполука, спосіб лікування та спосіб підвищення рівнів паратиреоїдного гормону
Номер патенту: 81642
Опубліковано: 25.01.2008
Автори: Маркус Роберт В., Касіллас Лінда Н., Раманджул Джоші М., Каллахан Джеймс Францис
Формула / Реферат
1. Сполука формули І
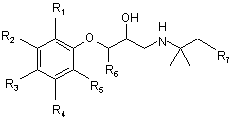 , I
, I
де:
R1 і R5 незалежно вибраний із групи, що включає Н і галоген;
R2, R3 і R4 незалежно вибраний із групи, що включає Н, галоген і J-K, де:
J є ковалентний зв'язок, нижчий алкілен або нижчий алкенілен; і
К є CO2R8, причому R8 означає Н або нижчий алкіл;
R6 є Н або нижчий алкіл;
R7 є індан-2-іл,
або її фармацевтично прийнятна сіль.
2. Сполука за п. 1, вибрана з групи, що включає
гідрохлорид 3-{3,4-дифтор-5-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}акрилової кислоти;
гідрохлорид 3-{3,4-дифтор-5-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонової кислоти;
гідрохлорид етилового ефіру 3-{3,4-дифтор-5-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонової кислоти;
гідрохлорид (Е)-5-{3,4-дифтор-5-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пент-4-енової кислоти;
гідрохлорид 5-{3,4-дифтор-5-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пентанової кислоти;
етиловий ефір 5-{3,4-дифтор-5-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пентанової кислоти;
гідрохлорид етилового ефіру 3-{4-бром-3-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонової кислоти;
гідрохлорид 3-{4-бром-3-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонової кислоти;
гідрохлорид 3-{2,3-дифтор-4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонової кислоти;
гідрохлорид етилового ефіру 3-{2,3-дифтор-4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонової кислоти;
гідрохлорид (Е)-3-{2,3-дихлор-5-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}акрилової кислоти;
гідрохлорид 3-{2,3-хлор-4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонової кислоти;
трифторацетат етилового ефіру 3-{2,3-хлор-4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонової кислоти;
гідрохлорид етилового ефіру 3-{4-фтор-3-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонової кислоти;
гідрохлорид 3-{4-фтор-3-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонової кислоти;
гідрохлорид етилового ефіру 3-{2-хлор-5-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонової кислоти;
гідрохлорид 3-{2-хлор-5-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонової кислоти;
етиловий ефір 3-{2,4-дихлор-5-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонової кислоти;
трифторацетат 5-{2,3-дихлор-4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пентанової кислоти;
трифторацетат етилового ефіру 5-{2,3-дихлор-4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пентанової кислоти;
гідрохлорид етилового ефіру 3-{2,3-дихлор-4-[2-(R)-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)-1(R)-метилпропокси]фенілпропіонової кислоти;
гідрохлорид етилового ефіру 3-{2,3-дихлор-4-[2-(S)-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)-1(S)-метилпропокси]фенілпропіонової кислоти;
гідрохлорид етилового ефіру 3-{2,3-дихлор-4-[2-(R)-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)-1(S)-метилпропокси]фенілпропіонової кислоти;
гідрохлорид етилового ефіру 3-{2,3-дихлор-4-[2-(S)-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)-1(R)-метилпропокси]фенілпропіонової кислоти;
гідрохлорид 3-{2,3-дихлор-4-[2-(R)-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)-1(R)-метилпропокси]фенілпропіонової кислоти;
гідрохлорид 3-{2,3-дихлор-4-[2-(S)-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)-1(S)-метилпропокси]фенілпропіонової кислоти;
гідрохлорид 3-{2,3-дихлор-4-[2-(R)-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)-1(S)-метилпропокси]фенілпропіонової кислоти;
гідрохлорид 3-{2,3-дихлор-4-[2-(S)-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)-1(R)-метилпропокси]фенілпропіонової кислоти;
етиловий ефір 3-{3-хлор-4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонової кислоти;
3-{3-хлор-4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонову кислоту;
етиловий ефір 3-{3-бром-4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонової кислоти;
3-{3-бром-4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонову кислоту;
етиловий ефір 3-{3-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-
диметилетиламіно)пропокси]феніл}пропіонової кислоти;
3-{3-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонову кислоту і
3-{4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)пропокси]феніл}пропіонову кислоту.
3. Спосіб лікування захворювання або порушення, що характеризується аномальним гомеостазом кісток або мінералів, який відрізняється тим, що включає введення суб'єкту, що потребує такого лікування, ефективної кількості сполуки за п. 1.
4. Спосіб за п. 3, який відрізняється тим, що порушення гомеостазу кісток або мінералів вибране з групи, що включає остеосаркому, періодонтальне захворювання, зрощення переломів, остеоартрит, ревматоїдний артрит, хворобу Педжета, злоякісне захворювання, пов'язане з гуморальною гіперкальціємією, і остеопороз.
5. Спосіб за п. 3, який відрізняється тим, що захворювання або порушення гомеостазу кісток або мінералів є остеопорозом.
6. Спосіб підвищення рівнів паратиреоїдного гормону в ссавців, який відрізняється тим, що включає введення суб'єкту, що потребує такого лікування, ефективної кількості сполуки за п. 1.
Текст
1. Сполука формули І R1 OH H R2 O N R6 ТА (19) 1 ЛІКУВАННЯ 3 81642 4 диметилетиламіно)пропокси]феніл}пропіонової гідрохлорид 3-{2,3-дихлор-4-[2-(R)-гідрокси-3-(2кислоти; індан-2-іл-1,1-диметилетиламіно)-1(S)гідрохлорид етилового ефіру 3-{4-фтор-3-[(R)-2метилпропокси]фенілпропіонової кислоти; гідрокси-3-(2-індан-2-іл-1,1гідрохлорид 3-{2,3-дихлор-4-[2-(S)-гідрокси-3-(2диметилетиламіно)пропокси]феніл}пропіонової індан-2-іл-1,1-диметилетиламіно)-1(R)кислоти; метилпропокси]фенілпропіонової кислоти; гідрохлорид 3-{4-фтор-3-[(R)-2-гідрокси-3-(2-інданетиловий ефір 3-{3-хлор-4-[(R)-2-гідрокси-3-(22-іл-1,1індан-2-іл-1,1диметилетиламіно)пропокси]феніл}пропіонової диметилетиламіно)пропокси]феніл}пропіонової кислоти; кислоти; гідрохлорид етилового ефіру 3-{2-хлор-5-[(R)-23-{3-хлор-4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1гідрокси-3-(2-індан-2-іл-1,1диметилетиламіно)пропокси]феніл}пропіонову диметилетиламіно)пропокси]феніл}пропіонової кислоту; кислоти; етиловий ефір 3-{3-бром-4-[(R)-2-гідрокси-3-(2гідрохлорид 3-{2-хлор-5-[(R)-2-гідрокси-3-(2-інданіндан-2-іл-1,12-іл-1,1диметилетиламіно)пропокси]феніл}пропіонової диметилетиламіно)пропокси]феніл}пропіонової кислоти; кислоти; 3-{3-бром-4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1етиловий ефір 3-{2,4-дихлор-5-[(R)-2-гідрокси-3-(2диметилетиламіно)пропокси]феніл}пропіонову індан-2-іл-1,1кислоту; диметилетиламіно)пропокси]феніл}пропіонової етиловий ефір 3-{3-[(R)-2-гідрокси-3-(2-індан-2-ілкислоти; 1,1трифторацетат 5-{2,3-дихлор-4-[(R)-2-гідрокси-3диметилетиламіно)пропокси]феніл}пропіонової (2-індан-2-іл-1,1кислоти; диметилетиламіно)пропокси]феніл}пентанової 3-{3-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1кислоти; диметилетиламіно)пропокси]феніл}пропіонову трифторацетат етилового ефіру 5-{2,3-дихлор-4кислоту і [(R)-2-гідрокси-3-(2-індан-2-іл-1,13-{4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1диметилетиламіно)пропокси]феніл}пентанової диметилетиламіно)пропокси]феніл}пропіонову кислоти; кислоту. гідрохлорид етилового ефіру 3-{2,3-дихлор-4-[23. Спосіб лікування захворювання або порушення, (R)-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)що характеризується аномальним гомеостазом 1(R)-метилпропокси]фенілпропіонової кислоти; кісток або мінералів, який відрізняється тим, що гідрохлорид етилового ефіру 3-{2,3-дихлор-4-[2включає введення суб'єкту, що потребує такого (S)-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)лікування, ефективної кількості сполуки за п. 1. 1(S)-метилпропокси]фенілпропіонової кислоти; 4. Спосіб за п. 3, який відрізняється тим, що гідрохлорид етилового ефіру 3-{2,3-дихлор-4-[2порушення гомеостазу кісток або мінералів (R)-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)вибране з групи, що включає остеосаркому, 1(S)-метилпропокси]фенілпропіонової кислоти; періодонтальне захворювання, зрощення гідрохлорид етилового ефіру 3-{2,3-дихлор-4-[2переломів, остеоартрит, ревматоїдний артрит, (S)-гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)хворобу Педжета, злоякісне захворювання, 1(R)-метилпропокси]фенілпропіонової кислоти; пов'язане з гуморальною гіперкальціємією, і гідрохлорид 3-{2,3-дихлор-4-[2-(R)-гідрокси-3-(2остеопороз. індан-2-іл-1,1-диметилетиламіно)-1(R)5. Спосіб за п. 3, який відрізняється тим, що метилпропокси]фенілпропіонової кислоти; захворювання або порушення гомеостазу кісток гідрохлорид 3-{2,3-дихлор-4-[2-(S)-гідрокси-3-(2або мінералів є остеопорозом. індан-2-іл-1,1-диметилетиламіно)-1(S)6. Спосіб підвищення рівнів паратиреоїдного метилпропокси]фенілпропіонової кислоти; гормону в ссавців, який відрізняється тим, що включає введення суб'єкту, що потребує такого лікування, ефективної кількості сполуки за п. 1. Даний винахід стосується нових сполук, здатних інгібувати активність кальцієвих рецепторів, і застосування таких сполук. Переважно вводити описані тут сполуки для забезпечення терапевтичного ефекту. Даний винахід стосується нових каталітичних сполук, фармацевтичних композицій, що містять дані сполуки, і їхнього застосування як антагоністів кальцієвих рецепторів. У ссавців позаклітинний Са 2+ знаходиться під твердим гомеостатичним контролем і регулює різні процеси, такі як згортання крові, нервову і м'язову збудливість і правильне формування кісток. Позаклітинний Са2+ інгібує секрецію паратиреоїдного гормону (ПТГ) з паратиреоїдних клітин, інгібує резорбцію кісток за допомогою остеокластів і стимулює секрецію кальцитоніну з С-клітин. Кальцій-рецепторні білки дають можливість визначеним спеціалізованим клітинам реагувати на зміни концентрації позаклітинного Са2+. ПТГ являє собою основний, ендокринний фактор, що регулює гомеостаз Са 2+ у крові і позаклітинних рідинах. ПТГ при дії на клітини 5 81642 6 кісток і нирок підвищує рівень Са 2+ у крові. Це періодонтальне захворювання, зрощення збільшує позаклітинний Са 2+, діючи як негативний переломів, остеоартрит, ревматоїдний артрит, сигнал зворотного зв'язку і придушуючи секрецію хвороба Педжета, гуморальна гіперкальціємія, ПТГ. Взаємозв'язок між позаклітинним Са 2+ і зв'язана зі злоякісним захворюванням і зрощенням секрецією ПТГ утворює важливий механізм, переломів, і остеопороз. підтримуючи існуючий гомеостаз Са2+. Даний винахід представляє кальцилітичні Позаклітинний Са2+ діє безпосередньо на сполуки. Термін "кальцилітичні сполуки" паратиреоїдні клітини, регулюючи секрецію ПТГ. відноситься до сполук, здатних інгібувати кальційПідтверджено наявність поверхневого білка рецепторну активність. Здатність сполуки паратиреоїдних клітин, що детектує зміни "інгібувати кальцій-рецепторну активність" позаклітинного Са2+. Дивись [роботу Brown і ін., означає, що дана сполука дає зниження однієї або Nature 366:574, 1993]. У паратиреоїдних клітинах більш кальцій-рецепторних активностей, даний білок, кальцієвий рецептор, діє як рецептор викликаних позаклітинним Са2+. для позаклітинного Са 2+, детектує зміни Нижче описано застосування кальцилітичних концентрації позаклітинного Са 2+ і ініціює сполук для інгібування кальцій-рецепторної функціональну клітинну реакцію, секрецію ПТГ. активності і/або для забезпечення доброчинної дії Позаклітинний Са2+ впливає на різні клітинні на пацієнта. Крім того, нижче описані методики, які функції, розглянуті в [роботі Nemeth і ін., Cell можна застосовувати для одержання додаткових Calcium 11:319, 1990]. Наприклад, позаклітинний кальцилітичних сполук. Са2+ відіграє певну роль у парафолікулярних (СПрикладом характерних кальцилітичних клітинах) і паратиреоїдних клітинах. Дивись сполук є сполуки структури І, що мають хімічну [роботу Nemeth, Cell Calcium 11:323, 1990. Також формулу: досліджена роль позаклітинного Са 2+ в остеокластах кісток. Дивись [роботу Zaidi, Bioscience Reports 10:493,1990]. Відомо, що різні сполуки копіюють ефекти позаклітинного Са2+ на кальцій-рецепторну молекулу. Кальциліти являють собою сполуки, здатні інгібувати кальцій-рецепторну активність, викликаючи тим самим зниження однієї або більше кальцій-рецепторних активностей, де: обумовлених позаклітинним Са 2+. Кальциліти R1 і R5 незалежно обрані з групи, що включає корисні як ключові молекули при відкритті, Н і галоген; розробці, проектуванні, модифікації і/або R2, R3 і R4 незалежно обрані з групи, що конструюванні корисних кальцієвих модуляторів, включає Н, галоген і J-K, де: що активні на Са 2+-рецепторах. Такі кальциліти J означає ковалентний зв'язок, алкілен або корисні при лікуванні різних хворобливих станів, алкеніл; і що характеризуються аномальними рівнями К обраний із групи CO2R8 таким чином, що R8 одного або більш компонентів, наприклад, являє собою Н або алкіл; поліпептидів, таких як гормони, ферменти або R6 обраний із групи, що включає Н або алкіл; фактори росту, експресія і/або секреція яких R7 обраний із групи, що включає арил або регулюється або зачіпається активністю на одному конденсований арил, дигідро-, тетрагідроабо декількох рецепторах Са 2+. Цільові конденсований арил, гетероарил, незаміщений захворювання або порушення для кальцилітичних або заміщений будь-яким замісником, обраним із сполук включають захворювання, що торкаються групи, що включає ОН, галоген, С1-4 алкіл, С1-4 аномального гомеостазу кісток і мінералів. алкокси, С3-6 циклоалкіл, CF3, OCF3, CN і NO2, і їх Аномальний кальцієвий гомеостаз фармацевтично прийнятні солі і комплекси. характеризується однією або декількома з "Alk" означає або алкіл, або алкеніл. "Нижчий наступних активностей: аномальне підвищення alk" означає або нижчий алкіл, або нижчий алкеніл, або зниження кальцію в сироватці; аномальне переважно нижчий алкіл. підвищення або зниження сечовиділення кальцію; Термін "алкеніл" означає необов'язково аномальне підвищення або зниження рівнів заміщену вуглеводневу гр уп у, що містить, кальцію в кістках (наприклад, по оцінці за щонайменше, один подвійний зв'язок вуглецьдопомогою визначень мінеральної щільності вуглець і 2-6 з'єднаних разом атомів вуглецю. кісток); аномальна абсорбція харчового кальцію; Алкенільна вуглеводнева група може бути аномальне підвищення або зниження виробництва лінійною. Лінійний алкеніл переважно має від 2 до і/або вивільнення мессенджерів, що впливають на 4 атомів вуглецю. рівні кальцію в сироватці, таких як ПТГ і Термін "алкіл" означає необов'язково кальцитонін; і аномальна зміна реакції, викликана заміщену вуглеводневу гр упу, з'єднану простими мессенджерами, що впливають на рівні кальцію в зв'язками вуглець-вуглець і має від 1 до 6 сироватці. з'єднаних разом атомів вуглецю. Алкільна Таким чином, антагоністи кальцієвих вуглеводнева група може бути лінійною або рецепторів пропонують унікальний підхід стосовно містити одне або більш розгалужень. фармакотерапії захворювань, зв'язаних з Розгалужений і лінійний алкіл переважно має від 1 аномальним гомеостазом кісток або мінералів, до 4 атомів вуглецю, кожний з яких необов'язково таких як гіпопаратиреоз, остеосаркома, може бути заміщеним. Кожний з алкільних 7 81642 8 замісників незалежно обраний із групи, що диметилетиламіно)пропокси]феніл}акрилової включає: нижчий алкіл, незаміщений арил, ОН, кислоти; NH2, NH-нижчий алкіл і М(нижчий алкіл)2. гідрохлорид 3-{2,3-хлор-4-[(R)-2-гідрокси-3-(2Переважно присутні не більше двох замісників. Ще індан-2-іл-1,1більш переважно, якщо алкіл являє собою нижчий диметилетиламіно)пропокси]феніл}пропіонової алкіл, що є незаміщеним розгалуженим або кислоти; лінійним алкілом, що має від 2 до 4 атомів трифторацетат етилового ефіру 3-{2,3-хлор-4вуглецю. [(R)-2-гідрокси-3-(2-індан-2-іл-1,1Термін "арил" означає необов'язково заміщену диметилетиламіно)пропокси]феніл}пропіонової ароматичну групу, щонайменше, з одним кільцем, кислоти; що має сполучену або конденсовану циклічну гідрохлорид етилового ефіру 3-{4-фтор-3-[(R)систему. Арил включає карбоциклічні арильні, 2-гідрокси-3-(2-індан-2-іл-1,1гетероциклічні арильні і діарильні групи, кожна з диметилетиламіно)пропокси]феніл}пропіонової яких необов'язково може бути заміщеною. кислоти; Переважний арил являє собою необов'язково гідрохлорид 3-{4-фтор-3-[(R)-2-гідрокси-3-(2заміщений феніл або необов'язково заміщений індан-2-іл-1,1піридил. диметилетиламіно)пропокси]феніл}пропіонової Термін "алкокси" означає атом кисню, кислоти; з'єднаний з незаміщеним алкілом довжиною від 1 гідрохлорид етилового ефіру 3-{2-хлор-5-[(R)до 4 атомів вуглецю, переважно довжиною від 1 до 2-гідрокси-3-(2-індан-2-іл-1,12 атомів вуглецю. Більш переважним алкокси є диметилетиламіно)пропокси]феніл}пропіонової метокси. кислоти; Переважні сполуки, корисні в даному винаході, гідрохлорид 3-{2-хлор-5-[(R)-2-гідрокси-3-(2обрані з групи, що включає: індан-2-іл-1,1Гідрохлорид 3-{3,4-дифтор-5-[(R)-2-гідрокси-3диметилетиламіно)пропокси]феніл}пропіонової (2-індан-2-іл-1,1кислоти; диметилетиламіно)пропокси]феніл}акрилової етиловий ефір 3-{2,4-дихлор-5-[(R)-2-гідроксикислоти; 3-(2-індан-2-іл-1,1гідрохлорид 3-{3,4-дифтор-5-[(R)-2-гідрокси-3диметилетиламіно)пропокси]феніл}пропіонової (2-індан-2-іл-1,1кислоти; диметилетиламіно)пропокси]феніл}пропіонової трифторацетат 5-{2,3-дихлор-4-[(R)-2-гідроксикислоти; 3-(2-індан-2-іл-1,1гідрохлорид етилового ефіру 3-{3,4-дифтор-5диметилетиламіно)пропокси]феніл}пентанової [(R)-2-гідрокси-3-(2-індан-2-іл-1,1кислоти; диметилетиламіно)пропокси]феніл}пропіонової трифторацетат етилового ефіру 5-{2,3-дихлоркислоти; 4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1гідрохлорид (Е)-3-{3,4-дифтор-5-[(R)-2диметилетиламіно)пропокси]феніл}пентанової гідрокси-3-(2-індан-2-іл-1,1кислоти; диметилетиламіно)пропокси]феніл}пент-4-енової гідрохлорид етилового ефіру 3-{2,3-дихлор-4кислоти; [2-(R)-гідрокси-3-(2-індан-2-іл-1,1гідрохлорид 5-{3,4-дифтор-5-[(R)-2-гідрокси-3диметилетиламіно)-1(R)(2-індан-2-іл-1,1метилпропокси]фенілпропіонової кислоти; диметилетиламіно)пропокси]феніл}пентанової гідрохлорид етилового ефіру 3-{2,3-дихлор-4кислоти; [2-(S)-гідрокси-3-(2-індан-2-іл-1,1етиловий ефір 5-{3,4-дифтор-5-[(R)-2-гідроксидиметилетиламіно)-1(S)3-(2-індан-2-іл-1,1метилпропокси]фенілпропіонової кислоти; диметилетиламіно)пропокси]феніл}пентанової гідрохлорид етилового ефіру 3-{2,3-дихлор-4кислоти; [2-(R)-гідрокси-3-(2-індан-2-іл-1,1гідрохлорид етилового ефіру 3-{4-бром-3-[(R)диметилетиламіно)-1(S)2-гідрокси-3-(2-індан-2-іл-1,1метилпропокси]фенілпропіонової кислоти; диметилетиламіно)пропокси]феніл}пропіонової гідрохлорид етилового ефіру 3-{2,3-дихлор-4кислоти; [2-(S)-гідрокси-3-(2-індан-2-іл-1,1гідрохлорид 3-{4-бром-3-[(R)-2-гідрокси-3-(2диметилетиламіно)-1(R)індан-2-іл-1,1метилпропокси]фенілпропіонової кислоти; диметилетиламіно)пропокси]феніл}пропіонової гідрохлорид 3-{2,3-дихлор-4-[2-(R)-гідрокси-3кислоти; (2-індан-2-іл-1,1-диметилетиламіно)-1(R)гідрохлорид 3-{2,3-дифтор-4-[(R)-2-гідрокси-3метилпропокси]фенілпропіонової кислоти; (2-індан-2-іл-1,1гідрохлорид 3-{2,3-дихлор-4-[2-(S)-гідрокси-3диметилетиламіно)пропокси]феніл}пропіонової (2-індан-2-іл-1,1-диметилетиламіно)-1(S)кислоти; метилпропокси]фенілпропіонової кислоти; гідрохлорид етилового ефіру 3-{2,3-дифтор-4гідрохлорид 3-{2,3-дихлор-4-[2-(R)-гідрокси-3[(R)-2-гідрокси-3-(2-індан-2-іл-1,1(2-індан-2-іл-1,1-диметилетиламіно)-1(S)диметилетиламіно)пропокси]феніл}пропіонової метилпропокси]фенілпропіонової кислоти; кислоти; гідрохлорид 3-{2,3-дихлор-4-[2-(S)-гідрокси-3гідрохлорид (Е)-3-{2,3-дихлор-5-[(R)-2(2-індан-2-іл-1,1-диметилетиламіно)-1(R)гідрокси-3-(2-індан-2-іл-1,1метилпропокси]фенілпропіонової кислоти; 9 81642 10 етиловий ефір 3-{3-хлор-4-[(R)-2-гідрокси-3-(2основою, такою як гідроксид натрію, у етанолі і індан-2-іл-1,1воді, забезпечуючи похідне акрилової кислоти 7. диметилетиламіно)пропокси]феніл}пропіонової Акрилову кислоту 7 відновлюють у звичайних кислоти; умовах, таких як водень у присутності 3-{3-хлор-4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1каталізатора, наприклад, паладію на вуглеці, диметилетиламіно)пропокси]феніл}пропіонову одержуючи кислоту 8, що етерифікують у кислоту; звичайних умовах, одержуючи складний ефір 9. етиловий ефір 3-{3-бром-4-[(R)-2-гідрокси-3-(2Як показано на схемі 2, сполуки загальної індан-2-іл-1,1формули (І) можна одержати галогенуванням диметилетиламіно)пропокси]феніл}пропіонової фенолу, такого як етиловий ефір 3-(3кислоти; гідроксифеніл)пропіонової кислоти 10, одержуючи 3-{3-бром-4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1етиловий ефір 3-(4-бром-3диметилетиламіно)пропокси]феніл}пропіонову гідроксифеніл)пропіонової кислоти 11. Складний кислоту; ефір 11 можна перетворити в епоксид 12, як етиловий ефір 3-{3-[(R)-2-гідрокси-3-(2-індан-2описано вище. Епоксид 12 можна перетворити в іл-1,1пари кислота/складний ефір 13 і 14, як описано диметилетиламіно)пропокси]феніл}пропіонової вище для синтезу 8 і 9. кислоти; 3-(3-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1диметилетиламіно)пропокси]феніл}пропіонову кислоту і 3-{4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1диметилетиламіно)пропокси]феніл}пропіонову кислоту. Дана заявка демонструє здатність кальцилітичних сполук робити фізіологічно важливий вплив на клітину, ілюструючи здатність таких сполук підвищувати секрецію ПТГ, і також установлює цільове місце для кальцилітичних сполук. де: R1 і R5 незалежно обрані з групи, що включає Н і галоген; R2, R3 і R4 незалежно обрані з групи що включає Н, галоген і J-K, де: J означає ковалентний зв'язок, алкілен або алкеніл; і К обраний із групи CO2R8 таким чином, щоб R8 являв собою Н або алкіл; R6 обраний із групи, що включає Н або алкіл; R7 обраний із групи, що включає арил або конденсований арил, дигідро-, тетрагідроконденсований арил, гетероарил, незаміщений або заміщений будь-яким замісником, обраним із групи, що включає ОН, галоген, С1-4 алкіл, С1-4 алкокси, С3-6 циклоалкіл, CF3, OCF 3, CN і NO2 , і їх фармацевтично прийнятні солі і комплекси. Схеми синтезу Синтез сполук загальної формули (І) можна провести, як описано нижче на схемах 1 і 2. Обробка фенолу 1 основою, такою як карбонат калію, у присутності нозилепоксиду 2 дає епоксидний проміжний продукт 3. Обробка 3 аміном, таким як 4, у розчиннику, такому як етанол, при підвищеній температурі дає аміноспирт 5. Взаємодія 5 по Хеку (Heck) з олефіном, таким як етилакрилат, дає a,bненасичений складний ефір 6, який омилюють Експериментальні методики Наступні приклади приведені тільки з метою ілюстрації і ні яким чином не є обмежувальними. Приклад 1 Одержання гідро хлориду (Е)-3-{3,4-дифтор-5 11 81642 12 [(R)-2-гідрокси-3-(2-індан-2-іл-1,1кімнатній температурі протягом 12 годин. Етанол диметилетиламіно)пропокси]феніл}акрилової видаляють і водну частину (рН14) розбавляють до кислоти 200мл і тричі екстрагують порціями діетилового (а) (R)-2-(5-бром-2,3ефіру по 30мл. Додають при перемішуванні водну дифторфеноксиметил)оксиран НСІ, доводячи рН до 5, що викликає виділення До ацетонового розчину (0,1М, 240мл) продукту з розчину у вигляді смоли. Додають комерційно доступного 5-бром-2,3-дифторфенолу СН2СІ2 і двофазну суміш добре перемішують (5,0г, 23,93ммоль) додають К2СО3 (9,92г, протягом 5-30хв. Даним способом продукт 71,77ммоль) і дану суміш нагрівають при кип'ятінні переводять у білу тверду речовину і виділяють зі зворотним холодильником протягом 30хв. Після фільтруванням у вигляді цвітеріона (3,3г, 70% для охолодження даної суміші до кімнатної 2 стадій). температури додають (2R)-(-)-гліцидил 3До ацетонітрильної суспензії цвітеріонного нітробензолсульфонат (6,20г, 23,93ммоль) і продукту додають 2М НСІ у діетиловому е фірі. отриману суміш нагрівають при кип'ятінні зі Даний матеріал швидко переходить у розчин і зворотним холодильником протягом ночі. Після потім осаджується у вигляді білої кристалічної охолодження до кімнатної температури тверді твердої речовини, даючи (Е)-3-{3,4-дифтор-5-[(R)речовини видаляють фільтруванням і добре 2-гідрокси-3-(2-індан-2-іл-1,1промивають етилацетатом. Фільтрат диметилетиламіно)пропокси]феніл}акрилову концентрують і розподіляють між етилацетатом і кислоту у вигляді чистої солі з НСІ. 1 1N НСІ. Органічну частину промивають послідовно Н ЯМР (ДМСО-d6) d:12,53 (с, 1Н); 8,91 (м, 1Н); 5% NaHCO3 і насиченим розчином солі, сушать 8,58 (м, 1Н); 7,54 (д, J=16,0Гц, 1Н); 7,49 (м, 2Н); (MgSO4), фільтр ують і концентрують до твердого 7,18 (м, 2Н); 7,11 (м, 2Н); 6,67 (д, J=16,0Гц, 1Н); 6,0 стану. (д, J=4,4Гц, 1Н); 4,27 (м, 1Н); 4,23 (м, 2Н); 3,17 (м, Очищення методом РКХ (15% 1Н);3,09 (дд, J=13,4, 7,05Гц, 2Н); 2,96 (м, 1Н); 2,56 етилацетат/гексан) дає продукт у вигляді білої (м, 3Н); 1,96 (д, J=5,4Гц, 2Н); 1,39 (с, 6Н). твердої речовини з виходом 97% (6,19г). Приклад 2 (b) (R)-1 -(5-бром-2,3-дифторфенокси)-3-(2Одержання гідрохлориду 3-{3,4-дифтор-5-{(R)індан-2-іл-1,1-диметилетиламіно)пропан-2-ол 2-гідрокси-3-(2-індан-2-іл-1,1Етанольний розчин (0,2М, 93мл) оксирану диметилетиламіно)пропокси]феніл}пропіонової приклади 1а (5г, 18,67ммоль) і 2-індан-2-іл-1,1кислоти диметилетиламіну (вільна основа, 3,57г, До розчину акрилової кислоти прикладу 1 18,67ммоль) нагрівають при кип'ятінні зі зворотним (2,5г, 5,62ммоль) в оцтовій кислоті (30мл) і холодильником протягом 12 годин. Після етилацетаті (20мл) додають 5% Pd/СаО3 (0,50г). видалення розчинника сиру реакційну суміш Реакційну колбу продувають Н 2 і ізолюють у Н2очищають методом РКХ (5% СН3ОН/СН2СІ2), камері на 15 годин. Дану суміш фільтрують через одержуючи чистий продукт у вигляді жовтого целіт і фільтрат концентрують до об'єму масла (твердне при стоянні) з виходом 84% (7,1г). приблизно 5мл. Додають толуол (100мл) і 2М НСІ 1 у діетиловому ефірі (10мл) і розчин концентрують Н ЯМР (ДМСО-d6) d:9,05 (т, J=9,0Гц, 1Н); 8,65 (т, J=9,0Гц, 1Н); 7,40 (дд, J=9,75, 6,4, 2,2Гц, 1Н); до білої твердої речовини. 7,34 (дд, J=6,7, 2,0, 2,0Гц, 1Н); 7,1,8 (м, 2Н); 7,10 Дану тверду речовину суспендують в (м, 2Н); 6,0 (д, J=4,8Гц, 1Н); 4,25 (м, 1Н); 4,20 (м, ацетонітрилі і обробляють 2М НСІ у діетиловому 2Н); 3,17 (м, 1Н); 3,08 (м, 2Н); 2,95 (м, 1Н); 2,58 (м, ефірі. Даний розчин концентрують досуха, 3Н); 1,97 (д, J=5,43Гц, 2Н); 1,39 (с, 6Н). РХМС одержуючи зазначену в заголовку сполук у, як сіль (m/z) M+H=454/456. НСІ у вигляді білої твердої речовини: 1 (c) Гідрохлорид (Е)-3-{3,4-дифтор-5-[(R)-2Н ЯМР (ДМСО-D6) d:9,0 (м, 1Н); 8,6 (м, 1Н); гідрокси-3-(2-індан-2-іл-1,17,19 (м, 2Н); 7,11 (м, 2Н); 6,98 (удаваний д, диметилетиламіно)пропокси]феніл}акрилової J=7,1Гц, 1Н); 6,91 (м, 1Н); 6,0 (широкий с, 1Н); 4,27 кислоти (м, 1Н); 4,14 (д, J=5,1Гц, 2Н); 3,20 (м, 1Н); 3,10 (м, До розчину броміду прикладу 1b (21,0г, 2Н); 2,98 (м, 1Н); 2,79 (т, J=7,7Гц, 2Н); 2,58 (м, 5Н); 46,26ммоль) у дегазованому пропіонітрилі (0,2М, 1,97 (д, J=5,4Гц, 2Н); 1,39 (с, 6Н). РХМС (m/z) 230мл) додають Pd(OAc)2 (0,52г, 2,31ммоль), P(oM+H=448. tol)3 (2,11г, 6,94ммоль), DIPEA (17,7мл, Приклад 3 101,76ммоль) і етилакрилат (6,51мл, 60,13ммоль). Одержання гідрохлориду етилового ефіру 3Реакційну колбу оснащують холодильником, для {3,4-дифтор-5-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1пропускання Аr і поміщають на попередньо нагріту иметилетиламіно)пропокси]феніл}пропіонової баню (115°С) на 3,5 годин. Після охолодження до кислоти кімнатної температури реакційну суміш До суспензії пропіонової кислоти прикладу 2 фільтрують через целіт і фільтрат концентрують, (2г) у е танолі (20мл) додають 2М НСІ у розподіляють між етилацетатом і 1N НСІ. Шари діетиловому ефірі (2мл). Дану суміш нагрівають розділяють і органічну частину промивають при кип'ятінні зі зворотним холодильником послідовно 5% NаНСО3 і насиченим розчином протягом 3 годин. Після охолодження до кімнатної солі, сушать, фільтрують і концентрують до температури отриманий розчин концентрують до коричневого масла. жовтого масла і сушать у вакуумі. Частину сирого залишку (6,2г) переносять у Вміст колби затвердіває, даючи зазначену в етанол і воду (0,2 М, 50мл, 13мл) і обробляють 2N заголовку сполуку у вигляді солі НСІ (2г): 1 NaOH (13мл). Реакційну суміш перемішують при Н ЯМР (ДМСО-d6) d:9,05 (м,1 Н); 8,62 (м, 1Н); 13 81642 14 7,18 (м, 2Н); 7,11 (м, 2Н); 6,98 (удаваний d, кислоти J=7,1Гц, 1Н); 6,91 (м, 1Н); 6,0 (широкий з, 1Н); 4,27 (а) Етиловий ефір 3-(3(м, 1Н); 4,14 (д, J=5,2Гц, 2Н); 4,06 (квартет, гідроксифеніл)пропіонової кислоти J=7,1Гц, 2Н); 3,18 (м, 1Н); 3,09 (м, 2Н); 2,98 (м, До розчину комерційно доступної 3-(31Н); 2,82 (т, J=7,5Гц, 2Н); 2,61 (м, 5Н); 1,97 (д, гідроксифеніл)пропіонової кислоти (25г, J=5,4Гц, 2Н); 1,39 (с, 6Н); 1,17 (т, J=7,1Гц, 3Н). 150,4ммоль) у етанолі (250мл) додають РХМС (m/z) M+H=476. концентровану сірчану кислоту (3,0мл). Розчин Приклад 4 нагрівають при кип'ятінні зі зворотним Одержання гідрохлориду 5-{3,4-дифтор-5-[(R)холодильником протягом ночі. Розчинник 2-гідрокси-3-(2-індан-2-іл-1,1видаляють у вакуумі і отримане масло диметилетиламіно)пропокси]феніл}пентанової розбавляють етилацетатом і поміщають у кислоти ділильну лійку. Органічну частину екстрагують Зазначену в заголовку сполуку одержують в двічі 5% NaHCO3 і один раз насиченим розчином дві стадії способами, описаними вище для солі. Даний розчин сушать (МgО4), фільтрують і одержання сполуки прикладу 1, за винятком того, концентрують до темного червоно-коричневого що використовують етил-4-пентеноат замість масла (30г). Даний матеріал переносять на етилакрилату в реакції сполучення Хека, наступну стадію без додаткового очищення. одержуючи етиловий ефір 5-{3,4-дифтор-5-[(R)-2(b) Етиловий ефір 3-(4-бром-3гідрокси-3-(2-індан-2-іл-1,1гідроксифеніл)пропіонової кислоти диметилетиламіно)пропокси]феніл}пент-4-еновоЇ До розчину етилового ефіру 3-(3кислоти. Продукт реакції Хека, етиловий ефір гідроксифеніл)пропіонової кислоти (2,0г, гідролізують до карбонової кислоти способом, 10,31ммоль) у хлороформі (0,2М, 51мл) при -10°С аналогічним описаному вище. Одержання солі НСІ додають N-бромсукцинімід (1,93г, 10,83ммоль). проводять описаним вище способом: Після перемішування при кімнатній температурі 1 протягом ночі розчин концентрують у вакуумі й Н ЯМР (ДМСО-d6) d:8,9 (широкий, 1Н); 8,55 очищають методом колоночної флеш(широкий, 1Н); 7,18 (м, 2Н); 7,07 (м, 5Н); 6,38 (с, хроматографії (SiO2, від 5 до 15% 1Н); 5,99 (широкий з, 1Н); 4,25 (м, 1Н); 4,15 (м, 2Н); 3,36 (м, 2Н); 3,19 (м, 1Н); 3,08 (дд, J=13,3, 7,05Гц, етилацетат/гексан), одержуючи продукт у вигляді безбарвного масла (0,45г, 16%). 2Н); 2,95 (м, 1Н); 2,55 (м, 3Н); 2,40 (с, 2Н); 1,95 (д, (c) (R)-2-(5-бром-2,3J=5,3Гц, 2Н); 1,39 (с, 6Н). РХМС (m/z) M+H=474,6. дифторфеноксиметил)оксиран Приклад 5 Суспензію етилового ефіру 3-(4-бром-3Одержання 5-{3,4-дифтор-5-[(R)-2-гідрокси-3(2-індан-2-іл-1,1гідроксифеніл)пропіонової кислоти (0,6г, 2,20ммоль) і К2СО3 (0,91г, 6,59ммоль) в ацетоні диметилетиламіно)пропокси]феніл}пентанової (0,1М, 22мл) нагрівають при кип'ятінні зі зворотним кислоти холодильником протягом 30хв. Після охолодження Зазначену в заголовку кислоту одержують даної суміші до кімнатної температури додають гідруванням у присутності каталітичного Pd/СаО3 в оцтовій кислоті і етилацетаті способом, (2R)-(-)-гліцидил 3-нітробензолсульфонат (0,57г, 2,20ммоль) і отриману суміш нагрівають при аналогічним описаному вище в прикладі 2: 1 кип'ятінні зі зворотним холодильником протягом Н ЯМР (ДМСО-d6) d: 8,75 (м, 1Н); 8,50 (м, 1Н); ночі. Тверді речовини видаляють фільтруванням і 7,19 (м, 2Н); 7,10 (м, 2Н); 6,90 (м, 2Н); 5,95 (д, промивають етилацетатом. Фільтрат J=4,3Гц, 1Н); 4,22 (м, 1Н); 4,15 (м, 2Н); 3,4 (м, 2Н); концентрують і розподіляють між етилацетатом і 3,20 (м, 1Н); 3,10 (дд, J=13,8, 7,2Гц, 2Н); 2,98 (м, 1N НСІ. Органічну частину промивають послідовно 1Н); 2,60 (м, 3Н); 2,24 (т, J=7,2Гц, 2Н); 1,95 (д, 5% NaHCO3 і насиченим розчином солі, сушать J=5,7Гц, 2Н); 1,56 (м, 2Н); 1,51 (м, 2Н), 1,38 (с, 6Н). (МgО4), фільтрують і концентрують до жовтого РХМС (m/z) M+H=476. масла. Приклад 6 (d) Гідрохлорид етилового ефіру 3-{4-бром-3Одержання етилового ефіру 5-{3,4-дифтор-5[(R)-2-гідрокси-3-(2-індан-2-іл-1,1[(R)-2-гідрокси-3-(2-індан-2-іл-1,1диметилетиламіно)пропокси]феніл}пропіонової диметилетиламіно)пропокси]феніл}пентанової кислоти кислоти Розчин сирого оксирану (0,7г) і 2-індан-2-ілДо розчину етилового ефіру 5-{3,4-дифтор-51,1-диметилетиламіну (0,42г, 2,2ммоль) у етанолі [(R)-2-гідрокси-3-(2-індан-2-іл-1,1(0,2М, 11мл) нагрівають при кип'ятінні зі зворотним диметилетиламіно)пропокси]феніл}пент-4-енової холодильником протягом ночі. Після видалення кислоти прикладу 4 (12,0г, 23,95ммоль) у етанолі розчинника сиру реакційну суміш очищають (250мл) додають 5% Pd/СаСО3 (2,4г). Реакційну методом РКХ (5% СН3ОН/СН2СІ2), одержуючи колбу продувають Н 2 і ізолюють у Н 2-камері на 15 чистий продукт у вигляді жовтого масла. Даний годин. Дану суміш фільтрують через целіт і матеріал розчиняють в ацетонітрилі і СН 2СІ2 і фільтрат концентрують. Колоночна хроматографія обробляють 2М НСІ у діетиловому ефірі. залишку (SiO2, 5% СН3ОН/СН2СІ2) забезпечує Видалення розчинників і сушіння у вакуумі дають чистий продукт - ефір, що перетворюють у сіль зазначену в заголовку сполуку як сіль НСІ у НСІ, застосовуючи описаний вище спосіб. вигляді не зовсім білої твердої речовини (0,5г, 44% Приклад 7 для 2 стадій). Одержання гідрохлориду етилового ефіру 31 Н ЯМР (ДМСО-d6) d:8,70 (м, 1Н); 8,52 (м, 1Н); {4-бром-3-[(R)-2-гідрокси-3-(2-індан-2-іл-1,17,47 (д, J=8,1Гц, 1Н); 7,18 (м, 2Н); 7,11 (м, 2Н); 7,05 диметилетиламіно)пропокси]феніл}пропіонової 15 81642 16 (д, J=1,7Гц, 1Н); 6,79 (дд, J=8,1, 1,6Гц, 1Н); 5,92 (д, концентрують і піддають флеш-хроматографії J=4,7Гц, 1Н); 4,15 (м, 1Н); 4,05 (квартет, J=7,1Гц, (10% метанол/дихлорметан), одержуючи 3Н); 3,25 (м, 1Н); 3,09 (м, 3Н); 2,83 (т, J=7,4Гц, 2Н); необхідний продукт (3,06г, 84%). МС (ЕР) m/z 454 2,64 (т, J=7,4Гц, 2Н); 2,56 (м, 3Н); 1,96 (д, J=5,5Гц, (М+Н)+. 2Н); 1,39 (с, 6Н); 1,17 (т, J=7,1Гц, 3Н). РХМС (m/z) (c) Етиловий ефір (Е)-3-{2,3-дифтор-4-[(R)-2M+H=518/520. гідрокси-3-(2-індан-2-іл-1,1Приклад 8 диметилетиламіно)пропокси]феніл}акрилової Одержання гідрохлориду 3-{4-бром-3-[(R)-2кислоти гідрокси-3-(2-індан-2-іл-1,1У герметичну пробірку на 150мл завантажують диметилетиламіно)пропокси]феніл}пропіонової за допомогою стрижня, що перемішує, (R)-1-(4кислоти бром-2,3-дифторфенокси)-3-(2-індан-2-іл-1,1До розчину етилового ефіру 3-{4-бром-3-[(R)-2диметилетиламіно)пропан-2-ол (3,06г) 1 і гідрокси-3-(2-індан-2-іл-1,1пропіонітрил (70мл). До суміші додають диметилетиламіно)пропокси]феніл}пропіонової послідовно Pd(OAc)2 (0,151г), P(O-tol)3 (0,82г), кислоти прикладу 7 (0,25г, 0,48ммоль) у етанолі етилакрилат (1,35г), триетиламін (2,73г) і (4мл) і воді (0,8мл) додають 2N NaOH (0,36мл, обезкиснюють реакційну суміш, барботуючи азот 0,72ммоль). Розчин перемішують при кімнатній протягом 15хв. Герметичну пробірку щільно температурі протягом ночі. Етанол видаляють і закривають і занурюють у попередньо нагріту залишок розбавляють водою, доводять рН до 6 і (120°С) масляну баню. Реакційну суміш нагрівають екстрагують тричі СН 2СІ2. Органічну частину при даній температурі протягом 12 годин. сушать (Na2SO4), фільтрують і концентрують у Охолоджують до температури навколишнього вакуумі, одержуючи чистий цвітеріон у вигляді середовища і концентрують при зниженому тиску. білої твердої речовини. Сирий залишок очищають методом колоночної До ацетонітрильної суспензії цвітеріонного флеш-хроматографії, елюючи спочатку 50% ЕtOАс продукту додають 2М НСІ у діетиловому е фірі. у гексані і 100% ЕtOАс. У цей час суміші елюючих Даний матеріал швидко переходить у розчин і розчинників переключають на 100% дихлорметан, потім осаджується у вигляді білої кристалічної 5% МеОН у дихлорметані, а потім 8% МеОН у речовини, даючи чисту сіль НСІ, що виділяють дихлорметані. Продукт збирають і концентрують, 1 фільтруванням і сушать у вакуумі (0,18г, 76%): Н одержуючи необхідний продукт (2,40г, 75%) у вигляді ясно-жовтої піни. МС (ЕР) m/z 474 [М+Н]+. ЯМР (ДМСО-d6) d: 8,80 (м, 1Н); 8,55 (м, 1Н); 7,47 (d) Етиловий ефір 3-{2,3-дифтор-4-[(R)-2(д, J=8,1Гц, 1Н); 7,19 (м, 2Н); 7,11 (м, 2Н); 7,05 (д, гідрокси-3-(2-індан-2-іл-1,1J=1,7Гц, 1Н); 6.79 (дд, J=8,1, 1,7Гц, 1Н); 5,93 (широкий с, 1Н); 4,25 (м, 1Н); 4,16 (м, 1Н); 4,05 (м, диметилетиламіно)пропокси]феніл}пропіонової кислоти 1Н); 3,26 (м, 1Н); 3,09 (м, 3Н); 2.80 (т, J=7,6Гц, 2Н); У круглодонну колбу на 250мл, постачену 2,62-2,52 (м, 5Н); 1,96 (д, J=5,4Гц, 2Н); 1,39 (с, 6Н). магнітною мішалкою, вносять сполуку прикладу 8 РХМС (m/z) M+H=490/492. (2,40г) і 100мл абсолютного етанолу. До суміші Приклад 9 Одержання гідрохлориду 3-{2,3-дифтор-4-[(R)додають 0,24г (10% мас/мас.) каталізатора (Pd/СаСО3) і поміщають в атмосферу водню. 2-гідрокси-3-(2-індан-2-іл-1,1Через 16год. перемішування усі вихідні матеріали диметилетиламіно)пропокси]феніл}пропіонової витрачаються. Реакційну суміш фільтрують через кислоти набивання з целіту, промивають додатковою (a) 4-бром-2,3-дифтороксиранілметоксибензол Розчин сирого 4-бром-2,3-дифторфенолу кількістю етанолу і концентрують, одержуючи сирий продукт (2,35г, 98%). МС (ЕР) m/z 476 (0,40г) [отриманий із застосуванням опублікованої [М+Н]+. методики WOO121606] і (2R)-гліцидил 3(e) Гідрохлорид 3-{2,3-дифтор-4-[(R)-2нітробензолсульфонату (0,49г) у сухому ацетоні гідрокси-3-(2-індан-2-іл-1,1(19мл) обробляють карбонатом калію (0,79г) і кип'ятять зі зворотним холодильником під азотом диметилетиламіно)пропокси]феніл}пропіонової кислоти протягом 12 годин. Реакційну суміш о холоджують, Розчин складного ефіру (1,6г) у е танолі (30мл) фільтрують, фільтрат концентрують у вакуумі і обробляють 2,5N NaOH (6мл) і перемішують при залишок піддають флеш-хроматографії (20% кімнатній температурі під аргоном протягом ночі. етилацетат/гексан), одержуючи необхідний продукт (0,33г) з виходом 71%. Етанол видаляють у вакуумі і водному шарі 1 розбавляють водою (10мл) і потім екстрагують Н ЯМР (400Мгц, CDCI3) d: 7,23-7,19 (м, 1Н), ефіром (3´20мл). Водний шар збирають і доводять 6,74-6,71 (м, 1Н), 4,35-4,32 (м, 1Н), 4,03-3,99 (м, рН до 5 за допомогою концентрованої НСІ при 1Н), 3,38-3,35 (м, 1Н), 2,93-2,92 (м, 1Н), 2,77-2,76 перемішуванні. Висаджену білу тверду речовину (м,1Н). збирають фільтруванням і сушать на повітрі, (b) (R)-1-(4-бром-2,3-дифторфенокси)-3-(2одержуючи 1,3г (86%) білої твердої речовини: МС індан-2-іл-1,1-диметилетиламіно)пропан-2-ол (ЕР) m/z 448 [М+Н]+. Суміш 2-(5-бром-2,3Дану кислоту (0,65г) суспендують у сухому дифторфеноксиметил)оксирану прикладу 8а ацетонітрилі (15мл) і обробляють 2,0М НСІ (4мл) в (2,12г, 8ммоль) і 2-індан-2-іл-1,1ефірі. Через кілька хвилин реакційна суміш стає диметилетиламіну (1,51г, 8ммоль) поміщають в гомогенною, коли руйнується біла тверда абсолютний етанол (32мл) і кип'ятять зі зворотним речовина. Реакційну суміш перемішують ще 10хв., холодильником протягом ночі. Після витрати після чого її фільтрують і сушать, одержуючи усього епоксиду реакційну суміш охолоджують, 17 81642 18 зазначену в заголовку сполуку (0,52г, 15 74%). МС CDCI3) d: 7,48 і 6,82 (д, 2Н), 4,37 і 4,34 (дд, 1Н), (ЕР) m/z 448 [М+Н]+. 1Н ЯМР (400Мгц, ДМСО-d6) d: 4,06 і 4,03 (дд, 1Н), 3,42-3,39 (м, 1Н), 2,96-2,94 (м, 8,63 (с, 1Н), 8,39 (с, 1Н), 7,13-6,90 (м, 6Н), 5,86 (д, 1Н), 2,85-2,83 (м, 1Н). 1Н), 4,14 (широкий, 1Н), 4,05 (д, 2Н), 3,13-3,09 (м, (c) (R)-1-(4-бром-2,3-дихлорфенокси)-3-(21Н), 3,04 і 3,00 (дд, 2Н), 2,93-2,89 (м, 1Н), 2,75 (т, індан-2-іл-1,1-диметилетиламіно)пропан-2-ол 2Н), 2,55-2,44 (м, 5Н), 1,89 (д,2Н), 1,31 (с, 6Н). Суміш епоксиду (0,5г) і інданіламіну (0,32г) Приклад 10 вносять в абсолютний етанол (16мл) і кип'ятять зі Одержання гідрохлориду 3-{2,3-дифтор-4-[(R)зворотним холодильником протягом ночі. Після 2-гідрокси-3-(2-індан-2-іл-1,1витрати усього епоксиду реакційну суміш диметилетиламіно)пропокси]феніл}пропіонової охолоджують, концентрують і очищають методом кислоти флеш-хроматографії (10% метанол/дихлорметан), Кислоту прикладу 9 (0,65г) розчиняють в одержуючи 86% необхідного продукту (0,71г). МС абсолютному етанолі (10мл) і додають каталітичну (ЕР) m/e 488 [М+Н]+. кількість концентрованої сірчаної кислоти. (d) Етиловий ефір (Е)-3-{2,3-дихлор-4-[(R)-2Реакційну суміш перемішують і нагрівають при гідрокси-3-(2-індан-2-іл-1,1кип'ятінні зі зворотним холодильником протягом диметилетиламіно)пропокси]феніл}акрилової ночі. Реакційну суміш концентрують, потім кислоти розбавляють етилацетатом і промивають 2,5N У герметичну пробірку на 75мл завантажують за допомогою стрижня, що перемішує, бромід NaOH (2´10мл), насиченим розчином солі (10мл), (0,9г) і пропіонітрил (10мл). До даної суміші сушать над сульфатом натрію. додають послідовно Pd(OAc)2 (0,042г), P(O-tol)3 Фільтрат концентрують, очищають методом (0,23г) і етилакрилат (0,40мл) і обезкиснюють ВЕРХ і перетворюють у сіль НСІ, застосовуючи реакційну суміш, барботуючи азот протягом 15хв. стандартний протокол. МС (ЕР) m/z 476 [М+Н]+. 1Н Герметичну тр убку щільно закривають і занурюють ЯМР (400Мгц, ДМСО-d6) d: 8,72 (с, 1Н), 8,48 (с, у попередньо нагріту (120°С) масляну баню. 1Н), 7,20-6,99 (м, 6Н), 5,93 (д, 1Н), 4,20 (широкий, Реакційну суміш нагрівають при даній температурі 1Н), 4,12 (д, 2Н), 4,04 (квартет, 2Н), 3,20-3,16 (м, протягом 12 годин. Охолоджують до температури 1Н), 3,11 і 3,07 (дд, 2Н), 3,00-2,96 (м, 1Н), 2,85 (т, навколишнього середовища і концентрують при 2Н), 2,62-2,51 (м, 5Н), 1,95 (д, 2Н), 1,37 (с, 6Н), зниженому тиску. Сирий залишок очищають 1,15 (т, 3Н). методом колоночної флеш-хроматографії, елюючи Приклад 11 спочатку 50% EtOAc у гексані і 100% ЕtOАс. У цей Одержання гідрохлориду (Е)-3-{2,3-дихлор-5час суміші елюючих розчинників переключають на [(R)-2-гідрокси-3-(2-індан-2-іл-1,1100% ДХМ, 5% Меон у дихлорметані, а потім 8% диметилетиламіно)пропокси]феніл}акрилової МеОН у ДХМ. Продукт збирають і концентрують, кислоти одержуючи необхідний продукт (0,95г) з виходом (а) 4-бром-2,3-дихлорфенол 98% у вигляді ясно-жовтої піни. МС (ЕР) m/е 506 У круглодонній колбі на 250мл розчиняють 10г [М+Н]+. 2,3-дихлорфенолу в суміші розчинників (крижана (є) (Е)-3-{2,3-дихлор-4-[(R)-2-гідрокси-3-(2оцтова кислота (16мл) і хлороформ (4мл)) і індан-2-іл-1,1охолоджують до 10°С. До даної суміші додають по диметилетиламіно)пропокси]феніл}акрилової краплі бром (3,45мл) у 15мл крижаної оцтової кислоти гідрохлорид кислоти, підтримуючи температур у. Реакційну Розчин складного ефіру (5,0г) у е танолі (49мл) суміш енергійно перемішують при додаванні обробляють 2,5N NaOH (4,5мл) і перемішують під брому і продовжують енергійне перемішування аргоном протягом ночі. Етанол видаляють у протягом 0,5 години, після закінчення додавання. вакуумі і водний шар розбавляють водою (10мл) і У даний момент реакційну суміш виливають у потім екстрагують ефіром (3´100мл). Водний шар колбу, що містить 60мл води і 30мл дихлорметану. Органічний шар відокремлюють і водний шар збирають і доводять рН до 4 за допомогою концентрованої НСІ при перемішуванні. екстрагують дихлорметаном (3´50мл). Органічні Висаджену білу тверду речовину збирають шари поєднують, промивають насиченим фільтруванням і сушать на повітрі, одержуючи бікарбонатом натрію (3´100мл) і насиченим зазначену в заголовку сполуку (3,92г, 83%). МС розчином солі (100мл) і сушать над сульфатом (ЕР) m/е 478 [М+Н]+. 1Н ЯМР (400Мгц, ДМСО-d6) d: натрію. Сирий продукт (9,65г) переносять на 1 7,76 і 7,15 (АВ квартет, 2Н), 7,66 (д, 1Н), 7,06-6,97 наступну стадію без якого-небудь очищення. Н (м, 4Н), 6,41 (д,1Н), 4,12-3,92 (м, 3Н), 3,20 ЯМР (400Мгц, CDCI3) d: 7,47 і 6,89 (АВ квартет, (широкий, 1Н), 2,95 і 2,92 (дд, 2Н), 2,84 і 2,81 (дд, 2Н), 5,69 (широкий, 1Н). 2Н), 2,70 і 2,67 (дд, 2Н), 2,50-2,43 (м, 2Н), 1,67 (д, (b) 4-бром-2,3-дихлороксиранілметокси бензол 2Н), 1,10 (с, 6Н). Розчин сирого 4-бром-2,3-дихлорфенолу Приклад 12 (7,96г) і (2R)-гліцидил 3-нітробензолсульфонату Одержання гідрохлориду 3-{2,3-хлор-4-[(R)-2(8,52г) у сухому ацетоні (250мл) обробляють гідрокси-3-(2-індан-2-іл-1,1карбонатом калію (13,61г) і кип'ятять зі зворотним диметилетиламіно)пропокси]феніл}пропіонової холодильником під азотом протягом 12 годин. кислоти Реакційну суміш о холоджують, фільтрують і У круглодонну колбу на 250мл, постачену фільтрат концентрують у вакуумі, залишок магнітною мішалкою, поміщають акрилову кислоту піддають флеш-хроматографії (20% прикладу 11 (2,0г), 100мл абсолютного етанолу і етилацетат/гексан), одержуючи необхідний 50мл метанолу. До даної суміші додають 0,2г (10% продукт (6,94г) з виходом 71%. 1Н ЯМР (400Мгц, 19 81642 20 мас/мас.) каталізатора (5% родій/АІ2О 3) і іл-1,1-диметилетиламіно)пропан-2-ол поміщають в атмосферу водню. Через 16год. Суміш епоксиду (3,0г) і інданіламіну (2,24г) перемішування усі вихідні матеріали поміщають в абсолютний етанол (60мл) і кип'ятять витрачаються. Реакційну суміш фільтрують через зі зворотним холодильником протягом ночі. Після набивання з целіту, промивають додатковою витрати усього епоксиду реакційну суміш кількістю метанолу і концентрують, одержуючи охолоджують, концентрують і очищають методом необхідний продукт (1,96г) з виходом 98%. МС флеш-хроматографії (10% метанол/дихлорметан), (ЕР) m/е 480,2 [М+Н]+. одержуючи 87% необхідний продукт (4,55г). МС Кислоту (0,5г) суспендують у сухому (ЕР) m/е 437 [М+Н]+. ацетонітрилі (10мл) і обробляють 1,0М НСІ (5,2мл) (c) Етиловий ефір (Е)-3-{4-фтор-3-[(R)-2в ефірі. Реакційну суміш перемішують протягом гідрокси-3-(2-індан-2-іл-1,115хв., потім концентрують, одержуючи ясно-жовту диметилетиламіно)пропокси]феніл}акрилової піну з кількісним виходом. МС (ЕР) m/е 480,2 кислоти У герметичну пробірку завантажують за [М+Н]+. 1Н Я МР (400Мгц, ДМСО-d 6) d: 8,64 (т, 1Н), допомогою стрижня, що перемішує, бромід (5,20г) і 8,45 (т, 1Н), 7,27 (д, 1Н), 7,15-7,04 (м, 4Н), 5,86 (д, пропіонітрил (60мл). До даної суміші додають 1Н), 4,20-4,03 (м, 3Н), 3,37-2,82 (м, 10Н), 2,55-2,45 послідовно Pd(OAc)2 (0,54г), P(O-tol)3 (2,91г) і (м, 2Н), 1,93 (д, 2Н), 1,35 (с,6Н). Приклад 13 етилакрилат (1,95мл) і обезкиснюють реакційну суміш барботуючи азот протягом 15хв. Герметичну Одержання трифрторацетата етилового ефіру пробірку щільно закривають і занурюють у 3-{2,3-хлор-4-[(R)-2-гідрокси-3-(2-індан-2-ил-1,1попередньо нагріту (120°С) масляну баню. диметилетиламіно)пропокси]феніл}пропіонової Реакційну суміш нагрівають при даній температурі кислоти Кислоту прикладу 12 (2,0г) розчиняють в протягом 12 годин. Охолоджують до температури навколишнього середовища і концентрують при абсолютному етанолі (50мл) і додають каталітичну зниженому тиску. Сирий залишок очищають кількість концентрованої сірчаної кислоти. методом колоночної флеш-хроматографії, елюючи Реакційну суміш перемішують і нагрівають при спочатку 50% ЕtOАс у гексані і 100% ЕtOАс. У цей кип'ятінні зі зворотним холодильником протягом ночі. Наступного дня реакційну суміш час суміші елюючих розчинників переключають на 100% ДХМ, 5% МеОН у дихлорметані, а потім 8% концентрують, розбавляють етилацетатом і МеОН у ДХМ. Продукт збирають і концентрують, промивають 2,5N NaOH (2´20мл), насиченим одержуючи необхідний продукт (4,81г) з виходом розчином солі (20мл) і сушать над сульфатом 88% у вигляді ясно-жовтої піни. МС (ЕР) m/е 556 натрію. МС (ЕР) m/е 508 [М+Н]+. [М+Н]+. Етиловий ефір (33,7г) розчиняють у сухому (d) Гідрохлорид етилового ефіру 3-{4-фтор-3ацетонітрилі і поміщають в інертну атмосферу. До [(R)-2-гідрокси-3-(2-індан-2-іл-1,1даної суміші додають 6мл трифтороцтової диметилетиламіно)пропокси]фенілпент-4-енової кислоти, перемішують протягом 15хв. і кислоти концентрують, одержуючи густий ясно-жовтий У круглодонну колбу на 250мл, постачену сироп з кількісним виходом (41,2г). МС (ЕР) m/е магнітною мішалкою, завантажують етилакрилат 508 [М+Н]+. 1Н ЯМР (400Мгц, ДМСО-d6) d:8,35 (3,2г, 7ммоль), 100мл абсолютного етанолу. До (широкий, 2Н), 7,31 30 (д, 1Н), 7,20-7,08 (м, 5Н), даної суміші додають 0,32г (10% мас/мас.) 5,91 (широкий, 1Н), 4,20-4,02 (м, 5Н), 3,27-3,20 (м, каталізатора (Pd/CaCO3) і поміщають в атмосферу 1Н), 3,09, 3,05 (дд, 1Н), 2,95 (т, 1Н), 2,61-2,47 (м, водню. Через 16год. перемішування усі вихідні 5Н), 1,93 (д, 2Н), 1,35 (с, 6Н), 1,28 (д, 3Н), 1,16 (т. матеріали витрачаються. Реакційну суміш 3Н). фільтрують через набивання з целіту, промивають Приклад 14 додатковою кількістю етанолу і концентрують, Одержання гідрохлориду етилового ефіру 3одержуючи необхідний продукт 7 (3,12г, 97%). МС {4-фтор-3-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1(ЕР) m/z 458 [М+Н]+. диметилетиламіно)пропокси]феніл}пропіонової Складний ефір 7 (0,5г, 1ммоль) суспендують у кислоти сухому ацетонітрилі (10мл) і обробляють 2,0М НСІ (a) (R)-2-(5-бром-2(3мл, 5екв.) в ефірі. Через кілька хвилин реакційна фтор феноксиметил)оксиран суміш стає гомогенною, коли руйнується біла Розчин сирого 5-бром-2-фторфенолу (4,0г), тверда речовина. Реакційну суміш перемішують отриманого з застосуванням літературної ще 10хв., після чого фільтр ують і сушать, методики [ЕР0238272], і (2R)-гліцидил 3одержуючи необхідну сіль (0,43г, 80%). МС (ЕР) нітробензолсульфонату (5,37г) у сухому ацетоні m/z 458 [М+Н]+. 1Н Я МР (400 Мгц, DMCO-d6) d:8,56 (175мл) обробляють карбонатом калію (8,58г) і (с, 1Н), 8,45 (с, 1Н), 7,28-7,15 (м, 6Н) 6,91-6,88 (м, кип'ятять зі зворотним холодильником під азотом 1Н), 5,98 (д, 1Н), 4,26 (широкий, 1Н), 4,19-4,14 (м, протягом 12 годин. Реакційну суміш о холоджують, 2Н), 4,13 (квартет, 2Н), 3,30-3,24 (м, 1Н), 3,18 і 3,14 фільтрують і фільтрат концентрують у вакуумі, (дд, 2Н), 3,09-3,02 (м, 1Н), 2,90 (т, 2Н), 2,71-2,57 залишок піддають флеш-хроматографії (20% (м, 5Н), 2,02 (д, 2Н), 1,45 (с, 6Н), 1,28 (т, 3Н). етилацетат/гексан), одержуючи необхідний Приклад 15 продукт (4,25г) з виходом 82%. 1Н ЯМР (400Мгц, Одержання гідрохлориду 3-{4-фтор-3-[(R)-2CDCI3) d: 7,15-6,96 (м, 3Н), 4,33 і 4,30 (дд, 1Н), 4,02 гідрокси-3-(2-індан-2-ил-1,1і 4,00 (дд, 1Н), 3,41-3,37 (м, 1Н), 2,97(м, 1Н), 2,78 диметилетиламіно)пропокси]феніл}пропіонової (м, 1Н). кислоти (b) (R)-1-(5-бром-2-фторфенокси)-3-(2-індан-2 21 81642 22 Розчин складного ефіру прикладу 14 (2,58г, 3,36-3,32 (м, 2Н); 3,12-3,04 (м, 2Н); 2,90-2,84 (м, 5,6ммоль) у етанолі (250мл) обробляють 2,5N 2Н); 2,62-2,44 (м, 6Н); 1,38 (с, 6Н). РХМС (m/z) NaOH (10мл, 4,5екв.) і перемішують при кімнатній M+H=446/448. температурі під аргоном протягом ночі. Етанол Приклад 18 видаляють у вакуумі і водному шарі розбавляють Одержання етилового ефіру 3-{2,4-дихлор-5водою (30мл) і потім екстрагують ефіром [(R)-2-гідрокси-3-(2-індан-2-іл-1,1диметилетиламіно)пропокси]феніл}пропіонової (3´100мл). Водний шар збирають і доводять рН до 5 концентрованої НСІ при перемішуванні. кислоти До розчину етилового ефіру 3-{3-[(R)-2Висаджену білу тверду речовину збирають гідрокси-3-(2-індан-2-іл-1,1фільтруванням і сушать на повітрі, одержуючи диметилетиламіно)пропокси]феніл}пропіонової зазначену в заголовку сполуку 8 (1,98г, 81%). МС кислоти (0,35г, 0,683ммоль, отриманої з етилового (ЕР) m/z 430 [М+Н]+. Кислоту 8 (0,10г, 0,23ммоль) суспендують у ефіру 3-(3-гідроксифеніл)пропіонової кислоти описаними тут способами) у хлороформі (6,8мл) сухому ацетонітрилі (5мл) і обробляють 2,0М НСІ додають N-хлорсукцинімід (0,27г, 2,05ммоль) при (1мл, 5екв.) в ефірі. Через кілька хвилин реакційна кімнатній температурі. Реакційну суміш нагрівають суміш стає гомогенною, коли біла тверда речовина при кип'ятінні зі зворотним холодильником руйнується. Реакційну суміш перемішують ще 10хв., після чого її фільтрують і сушать, протягом ночі. Розчинник видаляють у вакуумі і сирий продукт очищають методом ВЕРХ з одержуючи необхідну сіль (96мг, 89%). МС (ЕР) оберненою фазою (65% CH3CN/H2O з 0,1% TFA). m/z 430 [М+Н]+. 1Н ЯМР (400Мгц, ДМСО-d6) d: 8,61 Чистий продукт одержують у вигляді білої твердої (т, 1Н), 8,43 (т, 1Н), 7,20-7,07 (м, 6Н), 6,84-6,81 (м, речовини (0,12г, вихід 30%): 1Н ЯМР (CDCI3) d:7,2 1Н), 5,91 (с, 1Н), 4,20 (широкий, 1Н), 4,12-4,07 (м, (с, 1Н); 7,26 (с, 1Н); 7,18-7,12 (м, 4Н); 6,86 (с, 1Н); 2Н), 3,22-3,17 (м, 1Н), 3,11 і 3,07 (дд, 2Н), 3,01-2,97 4,51 (с, 1Н); 4,28-4,18 (м, 2Н); 4,16-4,12 (м, 2Н); (м, 1Н), 2,79 (т, 2Н), 2,62-2,49 (м, 5Н), 1,95 (д, 2Н), 3,40 (м, 1Н); 3,22-3,18 (м, 2Н); 3,14 (дд, J=15, 1,38 (с, 6Н). 7,6Гц, 2Н); 3,00 (т, J=7,5Гц, 2Н); 2,26-2,22 (м, 2Н); Приклад 16 2,60 (т, J=7,5 Гц, 2Н); 2,54 (м, 1Н); 2,08 (м, 2Н); Одержання гідрохлориду етилового ефіру 31,52 (с, 6Н); 1,26 (т, J=7,1Гц, 3Н). РХМС (m/z) {2-хлор-5-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1M+H=508/510/512. диметилетиламіно)пропокси]феніл}пропіонової Приклад 19 кислоти Одержання 5-{2,3-дихлор-4-[(R)-2-гідрокси-3(a) Етиловий ефір 3-(2-хлор-5(2-індан-2-іл-1,1гідроксифеніл)пропіонової кислоти диметилетиламіно)пропокси]феніл}пентанової До розчину етилового ефіру 3-(3кислоти гідроксифеніл)пропіонової кислоти (1,0г, (а) Етиловий ефір (Е)-3-{2,3-дихлор-4-[(R)-25,15ммоль) у діетиловому ефірі (50мл) при 0°С гідрокси-3-(2-індан-2-іл-1,1додають сульфурилхлорид (0,493мл, 6,18ммоль). диметилетиламіно)пропокси]феніл}пент-4-енової Через 2,5 години при 0°С реакцію гасять кислоти насиченим карбонатом натрію (50мл). Водний шар У герметичну пробірку на 75мл завантажують екстрагують етилацетатом. Органічні частини за допомогою стрижня, що перемішує, (R)-1-(4поєднують і сушать сульфатом магнію. Розчинник бром-2,3-дихлорфенокси)-3-(2-індан-2-іл-1,1видаляють у вакуумі, одержуючи сирий продукт, диметилетиламіно)пропан-2-ол прикладу 11 (2,0г) і що очищають методом колоночної хроматографії пропіонітрил (50мл). До даної суміші додають (10% етилацетат/гексан). Зазначену в заголовку послідовно Pd(OAc)2 (0,09г), Р(О-toІ) 3 (0,5г), е тилсполуку одержують у вигляді безбарвної олії 4-пентеноат (1,05г) і діізопропіламін (2,08мл) і (0,73г, вихід 62%). 1Н ЯМР (CDCI3) d: 6,96 (д, обезкиснюють реакційну суміш, барботуючи J=10,1Гц, 1Н); 6,54(д, J=2,97Гц, 1Н); 6,46 (дд, азотом протягом 15хв. Герметичну пробірку J=8,6, 3,0Гц, 1Н); 3,96 (дд, J=12,5 5,3Гц, 2Н); 2,82щільно закривають і занурюють у попередньо 2,78 (м, 2Н); 1,08-1,00 (м, 3Н). нагріту (120°С) масляну баню. Реакційну суміш (b) Гідрохлорид етилового ефіру 3-{2-хлор-5нагрівають при даній температурі протягом 12 [(R)-2-гідрокси-3-(2-індан-2-іл-1,1годин. Охолоджують до температури диметилетиламіно)пропокси]феніл}пропіонової навколишнього середовища і концентрують при кислоти зниженому тиску. Сирий залишок очищають Застосовуючи описані вище в прикладах 1а-b методом колоночної флеш-хроматографії, елюючи методики, перетворюють етиловий ефір 3-(2-хлорспочатку 50% EtOAc у гексані і 100% EtOAc. У цей 5-гідроксифеніл)пропіонової кислоти в зазначену в час суміші елюючих розчинників переключають на заголовку сполуку: РХМС (m/z) M+H=474,4. 100% дихлорметан, 5% МеОН у дихлорметані, а Приклад 17 потім 8% МеОН у дихлорметані. Продукт збирають Одержання гідрохлориду 3-{2-хлор-5-[(R)-2і концентрують,одержуючи зазначену в заголовку гідрокси-3-(2-індан-2-іл-1,1сполуку (2,0г) з виходом 92% у вигляді ясно-жовтої диметилетиламіно)пропокси]феніл}пропіонової піни. МС (ЕР) m/е 534 [М+Н]+. кислоти (b) (Е)-3-{2,3-дихлор-4-[(R)-2-гідрокси-3-(2Етиловий ефір прикладу 16 омилюють, індан-2-іл-1,1одержуючи зазначену в заголовку сполуку. 1Н ЯМР диметилетиламіно)пропокси]феніл}пент-4-енова (ДМСО-d6) d: 8,78 (с, 1Н); 8,46 (с, 1Н); 7,36 (д, кислота 7=8,7Гц, 2Н); 7,20-7,18 (м, 2Н); 7,12-7,16 (м, 2Н); Розчин складного ефіру прикладу 19а (2,0г) у 6,90 (с, 1Н); 6,86 (д, J=3,0Гц, 1Н); 4,02-3,98 (м, 2Н); 23 81642 24 етанолі (2 мл) обробляють 2,5N NaOH (6мл) і метилпропокси]фенілпропіонової кислоти перемішують під азотом протягом ночі. Етанол гідрохлориду етилового ефіру 3-{2,3-дихлор-4випарюють, водний шар розбавляють водою [2-(S)-гідрокси-3-(2-індан-2-іл-1,1диметилетиламіно)-1(R)(10мл) і потім екстрагують ефіром (3´100мл). метилпропокси]фенілпропіонової кислоти Доводять рН водного шару до 5 концентрованою (a) 1-бром-2,3-дихлор-4-(1НСІ, екстрагують дихлорметаном, сушать і метилалілокси)бензол концентрують, одержуючи ясно-жовту піну з виходом 81% (1,53г). МС (ЕР) m/е 506 [М+Н]+. До холодної суміші бут-3-ен-1-олу (1,29г) і 4бром-2,3-дихлорфенолу (4,35г) додають (c) Трифторацетат 3-{2,3-дихлор-4-[(R)-2послідовно трифенілфосфін (5,65г) і DEAD (3,69г). гідрокси-3-(2-індан-2-іл-1,1Реакційну суміш повільно нагрівають до кімнатної диметилетиламіно)пропокси]фенілпент-4-енової температури при перемішуванні. Через 12 годин кислоти У круглодонну колбу на 250мл, постачену реакційну суміш концентрують і сирий залишок очищають методом колоночної флешмагнітною мішалкою, завантажують кислоту хроматографії, елююючи ЕtOАс у гексані і прикладу 19b (1,0г), 100мл абсолютного етанолу і одержуючи необхідний продукт (3,83г) з виходом 50мл метанолу. До даної суміші додають 0,2г (10% 72% у вигляді ясно-жовтої піни. 1Н ЯМР (400Мгц, мас/мас.) каталізатора (5% родій/АІ2О 3) і поміщають в атмосферу водню. Через 16 годин CDCI3) d: 7,44 і 6,77 (АВ квартет, 2Н), 5,95-5,87 (м, перемішування усі вихідні матеріали 1Н), 5,31-5,20 (м, 2Н), 4,81-4,78 (м, 1Н), 1,52 (д, витрачаються. Реакційну суміш фільтрують через 3Н). набивання з целіту, промивають додатковою (b) 2-[1-(4-бром-2,3кількістю метанолу і концентрують. Отриманий дихлорфенокси)етил]оксиран ясно-жовтий сироп очищають методом ВЕРХ 1-бром-2,3-дихлор-4-(1-метилалілокси)бензол (елюють сумішшю CH3CN/H2O, що містить 0,1% (2,5г), 1,1,1-трифторацетон (6,05мл) і бікарбонат TFA), одержуючи необхідний продукт із виходом натрію (2,12г) поміщають у суміш розчинників 72% (0,88г). МС (ЕР) m/е 508 [М+Н]+. 1Н ЯМР ацетонітрилу і води (2:1, 45мл) і охолоджують до 0°С. Додають трьома порціями оксон (5,19г) і (400Мгц, DMCO-d6) d:8,19 (широкий, 2Н), 7,14 (д, реакційну суміш повільно нагрівають до кімнатної 1Н), 7,03-6,92 (м, 5Н), 5,77 (широкий, 1Н), 4,05температури. По закінченню реакційну суміш 3,91 (м, 2Н), 3,13-3,05 (м, 2Н), 2,97-2,88 (м, 4Н), фільтрують, концентрують і повторно розчиняють 2,55-2,35 (м, 4Н), 2,08 (т, 2Н), 1,77 (д, 2Н), 1,63у е тилацетаті. Даний розчин промивають 1,58 (м, 2Н), 1,37-1,35 (м, 2Н), 1,20 (д, 6Н). насиченим NH 4CI, насиченим розчином солі і Приклад 20 сушать над сульфатом натрію. Після Одержання трифторацетату етилового ефіру фільтрування його концентрують і очищають 3-{2,3-дихлор-4-[(R)-2-гідрокси-3-(2-індан-2-іл-1,1методом колоночної флеш-хроматографії диметилетиламіно)пропокси]фенілпент-4-енової елююючи EtOAc у гексані й одержуючи необхідний кислоти продукт (2,39г) з виходом 91% у вигляді білої Кислоту прикладу 19 (0,5г) розчиняють в абсолютному етанолі (10мл) і додають каталітичну твердої речовини. 1Н ЯМР (400Мгц, CDCI3) d: 7,48 кількість концентрованої сірчаної кислоти. (д, 2Н), 6,97 (д, 1Н), 6,83 (д, 1Н), 4,40-4,38 (м, 1Н), Реакційну суміш перемішують і нагрівають при 4,15-4,08 (м, 1Н), 3,25-3,21 (м, 1Н), 3,18-3,16 (м, кип'ятінні зі зворотним холодильником протягом 1Н), 2,89 (т, 1Н), 2,85-2,68 (м, 3Н), 1,49-1,44 (м, ночі. Наступного дня реакційну суміш 6Н). концентрують і розбавляють етилацетатом, (c) 3-(4-бром-2,3-дихлорфенокси)-1-(2-індан-2іл-1,1-диметилетиламіно)бутан-2-ол промивають 2,5N NaOH (2´20мл), насиченим Суміш епоксиду (4,44г) і інданіламіну (2,69г) розчином солі (20мл) і сушать над сульфатом поміщають в абсолютний етанол (16мл) і кип'ятять натрію. Сиру суміш очищають методом ВЕРХ (елюють сумішшю CH3CN/H2O, що містить 0,1% зі зворотним холодильником протягом ночі. Після витрати усього епоксиду реакційну суміш TFA), одержуючи необхідний продукт із виходом охолоджують, концентрують і піддають флеш81% (0,43г). МС (ЕР) m/е 536 [М+Н]+. 1Н ЯМР хроматографії (10% метанол/дихлорметан), (400Мгц, ДМСО-d6) d:8,35-8,48 (широкий, 2Н), 7,31одержуючи 93% необхідного продукту (6,61г). МС 7,10 (м, 6Н), 4,17-4,01 (м, 5Н), 3,26-3,05 (м, 4Н), (ЕР) m/е 502,4 [М+Н]+. 2,69-2,50 (м, 7Н), 2,32 (т, 2Н), 1,94 (д, 2Н), 1,58(d) Етиловий ефір (Е)-3-{2,3-дихлор-4-[21,54 (т, 2Н), 1,33 (с, 3Н), 1,35 (с, 3Н), 1,18 (т, 3Н). гідрокси-3-(2-індан-2-іл-1,1-диметилетиламіно)-1Приклад 21 метилпропокси]феніл}акрилової кислоти Одержання У герметичну пробірку на 75мл завантажують гідрохлориду етилового ефіру 3-{2,3-дихлор-4за допомогою стрижня, що перемішує, бромід [2-(R)-гідрокси-3-(2-індан-2-іл-1,1прикладу 21 (5,0г) і пропіонітрил (100мл). До даної диметилетиламіно)-1(R)суміші додають послідовно Pd(OAc)2 (0,22г), P(Oметилпропокси]фенілпропіонової кислоти tol)3 (1,22г), етилакрилат (2,17мл) і N,Nгідрохлориду етилового ефіру 3-{2,3-дихлор-4діізопропілетиламін (7,10мл) і обезкиснюють [2-(S)-гідрокси-3-(2-індан-2-іл-1,1реакційну суміш, барботуючи азотом протягом диметилетиламіно)-1(S)15хв. Герметичну трубку щільно закривають і метилпропокси]фенілпропіонової кислоти занурюють у попередньо нагріту (120°С) масляну гідрохлориду етилового ефіру 3-{2,3-дихлор-4баню. Реакційну суміш нагрівають при даній [2-(R)-гідрокси-3-(2-індан-2-іл-1,1температурі протягом 12 годин. Охолоджують до диметилетиламіно)-1(S) 25 81642 26 температури навколишнього середовища і елююючи спочатку 50% ЕtOАс у гексані і 100% концентрують при зниженому тиску. Сирий ЕtOАс. У цей час суміші елююючих розчинників залишок очищають методом колоночної флешпереключають на 100% дихлорметан, 5% МеОН у хроматографії, елююючи спочатку 50% EtOAc у дихлорметані, а потім 8% МеОН у ДХМ. Продукт гексані і 100% ЕtOАс. У цей час суміші елююючих збирають і концентрують, одержуючи необхідний розчинників переключають на 100% дихлорметан, продукт: 0,8г чистого продукту (продуктів) і ще 0,7г 5% МеОН у дихлорметані, а потім 8% МеОН у продукту з 10% домішок. Чистий продукт, що ДХМ. Продукт збирають і концентрують, містить усі чотири діастереомери, розділяють одержуючи необхідний продукт (5,10г) з виходом методом ВЕРХ, одержуючи 100-250мг кожного 98% у вигляді ясно-жовтої піни. МС (ЕР) m/е 520 індивідуального діастереомеру зі ступенем [М+Н]+. чистоти більш 99%. МС (ЕР) m/е 522 [М+Н]+. (e) (Е)-3-{2,3-дихлор-4-[2-гідрокси-3-(2-індан-2Кожен чистий стереомер суспендують у іл-1,1-диметилетиламіно)-1сухому ацетонітрилі й обробляють 1,0М НСІ в метилпропокси]феніл}акрилова кислота ефірі. Через 15хв. реакційну суміш концентрують, Розчин складного ефіру прикладу 21d (5,0г) у одержуючи зазначені в заголовку сполуки у етанолі (100мл) обробляють 2,5N NaOH (16мл) і вигляді чистих діастереомерів: кожен перемішують при кімнатній температурі під індивідуальний діастереомер має молекулярну аргоном протягом ночі. Етанол видаляють при масу (за даними мас-спектрального аналізу), що зниженому тиску, водний шар розбавляють водою узгоджується з молекулярною формулою: МС (ЕР) m/е 522 [М+Н]+. (10мл) і потім екстрагують ефіром (3´100мл). Приклад 22 Водний шар збирають і доводять рН до 4 Одержання концентрованою НСІ. Осаджену білу тверду речовину збирають фільтруванням і сушать на гідрохлориду 3-{2,3-дихлор-4-[2-(R)-гідрокси-3(2-індан-2-іл-1,1-диметилетиламіно-1(R)повітрі, одержуючи діастереомерні суміші з метилпропокси]фенілпропіонової кислоти виходом 77% (3,64г). МС (ЕР) m/е 492 [М+Н]+. гідрохлориду 3-{2,3-дихлор-4-[2-(S)-гідрокси-3(f) 3-{2,3-дихлор-4-[2-гідрокси-3-(2-індан-2-іл(2-індан-2-іл-1,1-диметилетиламіно)-1(S)1,1-диметилетиламіно)-1метилпропокси]фенілпропіонова кислота метилпропокси]фенілпропіонової кислоти гідрохлориду 3-{2,3-дихлор-4-[2-(R)-гідрокси-3У круглодонну колбу на 250мл, постачену (2-індан-2-іл-1,1-диметилетиламіно-1(S)магнітною мішалкою, завантажують акрилову метилпропокси]фенілпропіонової кислоти кислоту прикладу 21e (0,58г) і 20мл абсолютного гідрохлориду 3-{2,3-дихлор-4-[2-(S)-гідрокси-3етанолу. До даної суміші додають 0,2г (10% мас/мас.) каталізатора (5% родій/АІ2О 3) і (2-індан-2-іл-1,1-диметилетиламіно)-1(R)метилпропокси]фенілпропіонової кислоти поміщають в атмосферу водню. Через 48 години Кожний з індивідуальних діастереомерних перемішування усі вихідні матеріали складних ефірів прикладу 21 омилюють водним витрачаються. Реакційну суміш фільтрують через NaOH і потім перетворюють у сіль соляної набивання з целіту, промивають додатковою кількістю метанолу і концентрують, одержуючи кислоти, обробляючи соляною кислотою в сухому ацетонітрилі й одержуючи зазначену в заголовку необхідний продукт у вигляді суміші сполуку. діастереомерів (0,58г). МС (ЕР) m/е 494 [М+Н]+. Кожна індивідуальна діастереомерна кислота (g) Гідрохлорид етилового ефіру 3-{2,3має молекулярну масу (за даними масдихлор-4-[2-(R)-гідрокси-3-(2-індан-2-іл-1,1диметилетиламіно)-1(R)спектрального аналізу), що узгоджується з молекулярною формулою: МС (ЕР) m/е 494 метилпропокси]фенілпропіонової кислоти [М+Н]+. Гідрохлорид етилового ефіру 3-{2,3-дихлор-4Приклад 23 [2-(S)-гідрокси-3-(2-індан-2-іл-1,1Одержання етилового ефіру 3-{3-хлор-4-[(R)-2диметилетиламіно)-1(S)метилпропокси]фенілпропіонової кислоти гідрокси-3-(2-індан-2-іл-1,1диметилетиламіно)пропокси]феніл}пропіонової Гідрохлорид етилового ефіру 3-{2,3-дихлор-4кислоти [2-(R)-гідрокси-3-(2-індан-2-іл-1,1Зазначену в заголовку сполуку одержують, диметилетиламіно)-1(S)дотримуючись загальної методики прикладу 1а-b метилпропокси]фенілпропіонової кислоти Гідрохлорид етилового ефіру 3-{2,3-дихлор-4за винятком того, що заміняють бром-2,3дифторфенол на етиловий ефір 3-(3-хлор-4[2-(S)-гідрокси-3-(2-індан-2-іл-1,1гідроксифеніл)пропіонової кислоти. диметилетиламіно)-1(R)Приклад 24 метилпропокси]фенілпропіонової кислоти Одержання 3-{3-хлор-4-[(R)-2-гідрокси-3-(2Кислоту прикладу 20f (2,50г) розчиняють в абсолютному етанолі і додають каталітичну індан-2-іл-1,1диметилетиламіно)пропокси]феніл}пропіонової кількість концентрованої сірчаної кислоти. кислоти Реакційну суміш перемішують і нагрівають при Зазначену в заголовку сполуку одержують, кип'ятінні зі зворотним холодильником протягом дотримуючись загальної методики прикладу 1 за ночі. Наступного дня реакційну суміш концентрують, розбавляють етилацетатом і винятком того, що заміняють бром-2,3дифторфенол на складний ефір прикладу 23. промивають 2,5N NaOH, насиченим розчином Приклад 25 соли і сушать (Na2SO4). Сирий залишок очищають Одержання етилового ефіру 3-{3-бром-4-[(R)методом колоночної флеш-хроматографії, 27 81642 28 2-гідрокси-3-(2-індан-2-іл-1,120,0ммоль) нагрівають при кип'ятінні зі зворотним диметилетиламіно)пропокси]феніл}пропіонової холодильником протягом 15 годин. Після кислоти видалення розчинника сиру реакційну суміш Зазначену в заголовку сполуку одержують, очищають методом РКХ (від 2 до 5% дотримуючись загальної методики прикладу 1 за СН3ОН/СН2СІ2), одержуючи зазначену в заголовку винятком того, що заміняють бром-2,3сполуку у вигляді жовтого масла з виходом 85% дифторфенол на етиловий ефір 3-(3-бром-4(7,5г). РХМС (m/z) M+H: 440. гідроксифеніл)пропіонової кислоти. Приклад 28 Приклад 26 Одержання 3-(3-[(R)-2-гідрокси-3-(2-індан-2-ілОдержання 3-{3-хлор-4-[(R)-2-гідрокси-3-[21,1-диметилетиламіно)пропокси]феніл}пропіонової індан-2-іл-1,1кислоти диметилетиламіно)пропокси]феніл}пропіонової До розчину етилового ефіру 3-{3-[(R)-2кислоти гідрокси-3-(2-індан-2-іл-1,1Зазначену в заголовку сполуку одержують, диметилетиламіно)пропокси]феніл}пропіонової дотримуючись загальної методики прикладу 1 за кислоти (1,3г, 3,0ммоль) прикладу 27 у етанолі винятком того, що заміняють бром-2,3(12мл) і воді (3мл) додають 2N NaOH (3мл, дифторфенол на складний ефір прикладу 25. 6,0ммоль). Розчин перемішують при кімнатній Приклад 27 температурі протягом ночі. Етанол видаляють і Одержання етилового ефіру 3-{3-[(R)-2залишок розподіляють між діетиловим ефіром і гідрокси-3-(2-індан-2-іл-1,1водою. Водну частину промивають 3 рази диметилетиламіно)пропокси]феніл}пропіонової діетиловим ефіром і потім доводять рН до 5. кислоти Тверда речовина, що осаджується з водного (a) Етиловий ефір 3-(3шару, виділяють фільтруванням, одержуючи гідроксифеніл)пропіонової кислоти чистий цвітеріон у вигляді білої твердої речовини. Етанольний розчин (250мл) 3-(3До ацетонітрильної суспензії цвітеріонного гідроксифеніл)пропіонової кислоти (25г, продукту додають 2М НСІ у діетиловому е фірі. 100,4моль) і концентрованої сірчаної кислоти Речовина швидко переходить у розчин і потім (3,0мл) нагрівають при кип'ятінні зі зворотним осаджується у вигляді білої твердої речовини, холодильником протягом 2 годин і потім при таким чином одержується зазначена в заголовку кімнатній температурі протягом ночі. Розчинник сполука у вигляді солі НСІ, що виділяють видаляють, випарюючи на роторі, і залишок фільтруванням і сушать у вакуумі (0,85г, 63%). переносять у етилацетат. Органічну частину РХМС (m/z) M+H: 412. промивають послідовно 5% NaНСО3 (2х) і Приклад 29 насиченим розчином солі, сушать над MgSO4, Одержання 3-{4-[(R)-гідрокси-3-(2-індан-2-ілфільтрують і концентрують до коричневого масла 1,1-диметилетиламіно)пропокси]феніл}пропіонової (30г, кількісно), даний матеріал використовують кислоти без додаткового очищення. У круглодонну колбу на 25мл, постачену (b) Етиловий ефір 3-[3-((R)-1магнітною мішалкою, завантажують оксиранилметокси)феніл]пропіонової кислоти дихлорпропіонову кислоту (0,12г, 0,25ммоль) і 3мл До ацетонового розчину (0,15М, 170мл) абсолютного етанолу. До даної суміші додають етилового ефіру 3-(3-гідроксифеніл)пропіонової 0,012г (10% мас/мас.) каталізатору (Pd/C) і кислоти (5,0г, 25,77ммоль) додають К2СО3 (10,69г, поміщають в атмосферу водню. Перемішують при 77,32ммоль) і дану суміш нагрівають при кип'ятінні кімнатній температурі до завершення зі зворотним холодильником протягом 30хв. Після дихлорування. Реакційну суміш фільтрують через охолодження суміші до кімнатної температури набивання з целіту, промивають додатковою додають (2R)-(-)-гліцидил 3-нітробензолсульфонат кількістю етанолу, концентрують і очищають (6,68г, 25,77ммоль) і отриману суміш нагрівають методом ВЕРХ, одержуючи сіль TFA (36мг). МС при кип'ятінні зі зворотним холодильником (ЕР) m/z 412 [М+Н]+. протягом ночі. Після охолодження до кімнатної Усі приведені в даному описі публікації, температури видаляють тверді речовини включаючи (але не обмежуючись) патенти і фільтруванням і добре промивають етилацетатом. патентні заявки, включені тут у вигляді посилань, Фільтрат концентрують і розподіляють між начебто для кожної індивідуальної публікації етилацетатом і 1N НСІ. Органічну частину конкретно й індивідуально зазначено, що вона промивають послідовно 5% NaHCO3 і насиченим включена тут у вигляді посилання, хоча вони розчином солі, сушать (MgSO4), фільтрують і досить повно викладені. концентрують до твердого стану. Очи щення Наведений вище опис цілком розкриває даний методом РКХ (30% етилацетат/гексан) дає продукт винахід, включаючи його кращі варіанти. у вигляді білої твердої речовини з виходом 93% Модифікації і виправлення варіантів, докладно тут (6,0г). РХМС (m/z) M+H: 187. розкритих, включені до обсягу наведеної далі (с) Етиловий ефір 3-{3-[(R)-2-гідрокси-3-(2формули винаходу. Не уточнюючи додатково, індан-2-іл-1,1вважають, що фахівець у даній галузі може, диметилетиламіно)пропокси]феніл}пропіонової використовуючи наведений опис, застосовувати кислоти даний винахід повною мірою. Таким чином, Етанольний розчин (0,2М, 100мл) зазначеного приведені тут приклади складені тільки як вище оксирану (5г, 20,0ммоль) і 2-індан-2-іл-1,1ілюстративні і ніяким чином не обмежують обсяг диметилетиламіну (вільна основа, 3,78г, даного винаходу. Варіанти даного винаходу, у яких 29 заявлені особливі властивості визначені таким чином. або 81642 переваги, 30
ДивитисяДодаткова інформація
Назва патенту англійськоюCalcilytic compound, method fo treatment and method for increase of a parathyroid hormone level
Автори англійськоюMarquis Robert W, Casillas Linda N, Ramanjulu Joshi M, Callahan James Francis
Назва патенту російськоюКальцилитическое соединение, способ лечения и способ повышения уровней паратиреоидного гормона
Автори російськоюМаркус Роберт В., Касиллас Линда Н., Раманджул Джоши М., Каллахан Джеймс Францис
МПК / Мітки
МПК: C07C 229/00, C07C 217/36, C07C 217/34, C07C 217/00
Мітки: підвищення, кальцилітична, паратиреоїдного, гормону, рівнів, спосіб, лікування, сполука
Код посилання
<a href="https://ua.patents.su/15-81642-kalcilitichna-spoluka-sposib-likuvannya-ta-sposib-pidvishhennya-rivniv-paratireodnogo-gormonu.html" target="_blank" rel="follow" title="База патентів України">Кальцилітична сполука, спосіб лікування та спосіб підвищення рівнів паратиреоїдного гормону</a>
Попередній патент: Спосіб одержання залеплону
Наступний патент: З’єднання між задньою стінкою камери згоряння і соплом ракетного двигуна
Випадковий патент: Високочастотна кмон інтегральна схема для генераторів з кварцовою стабілізацією частоти












