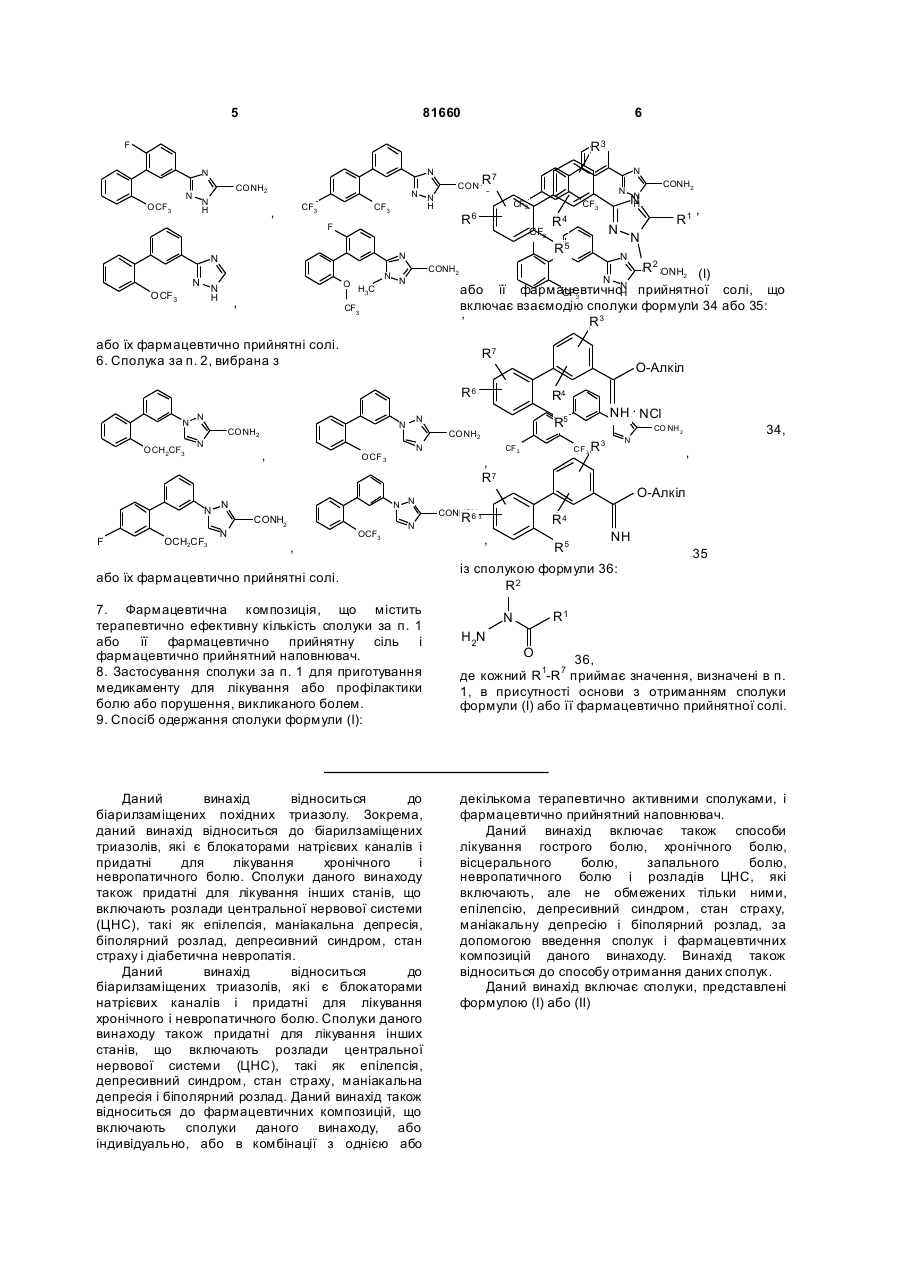
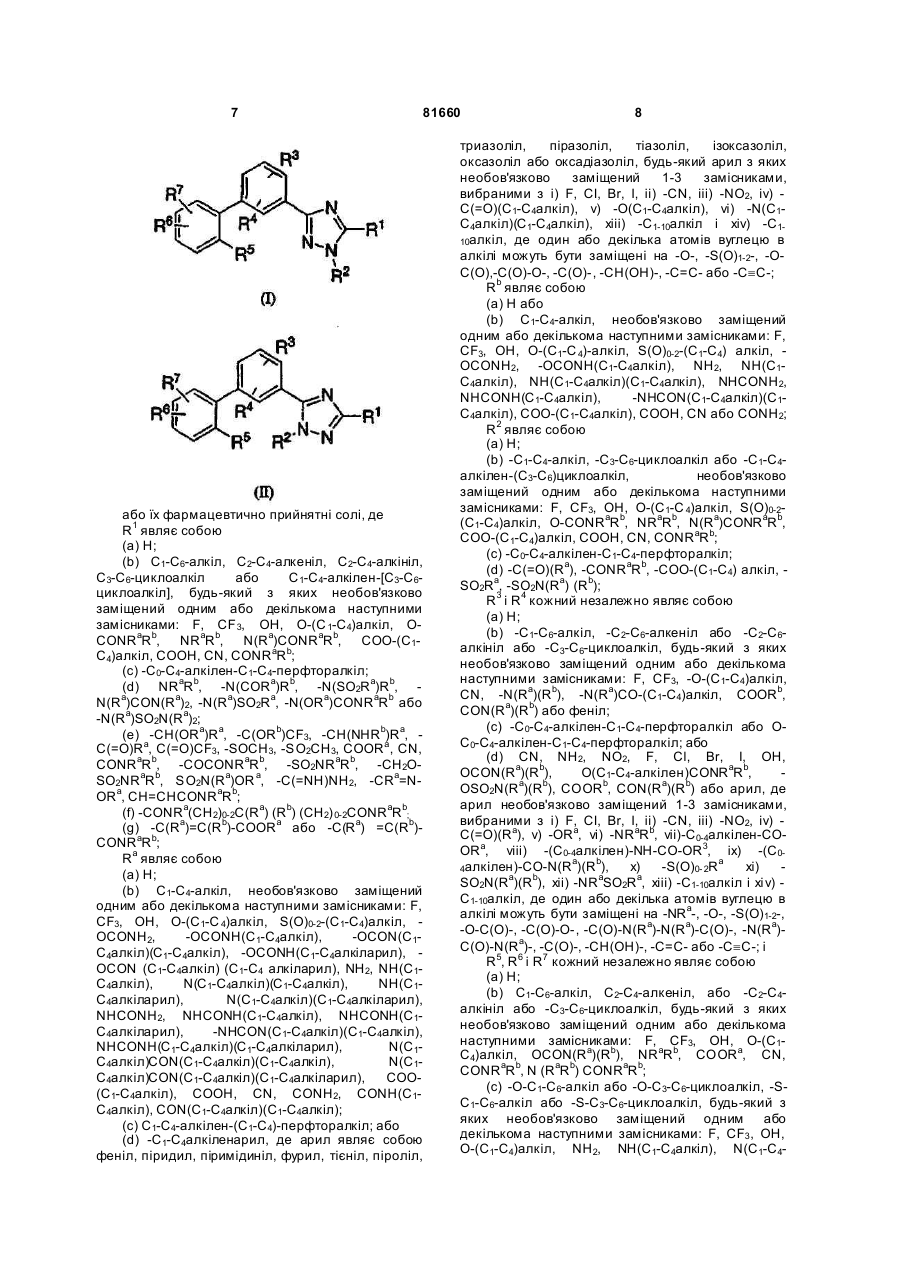
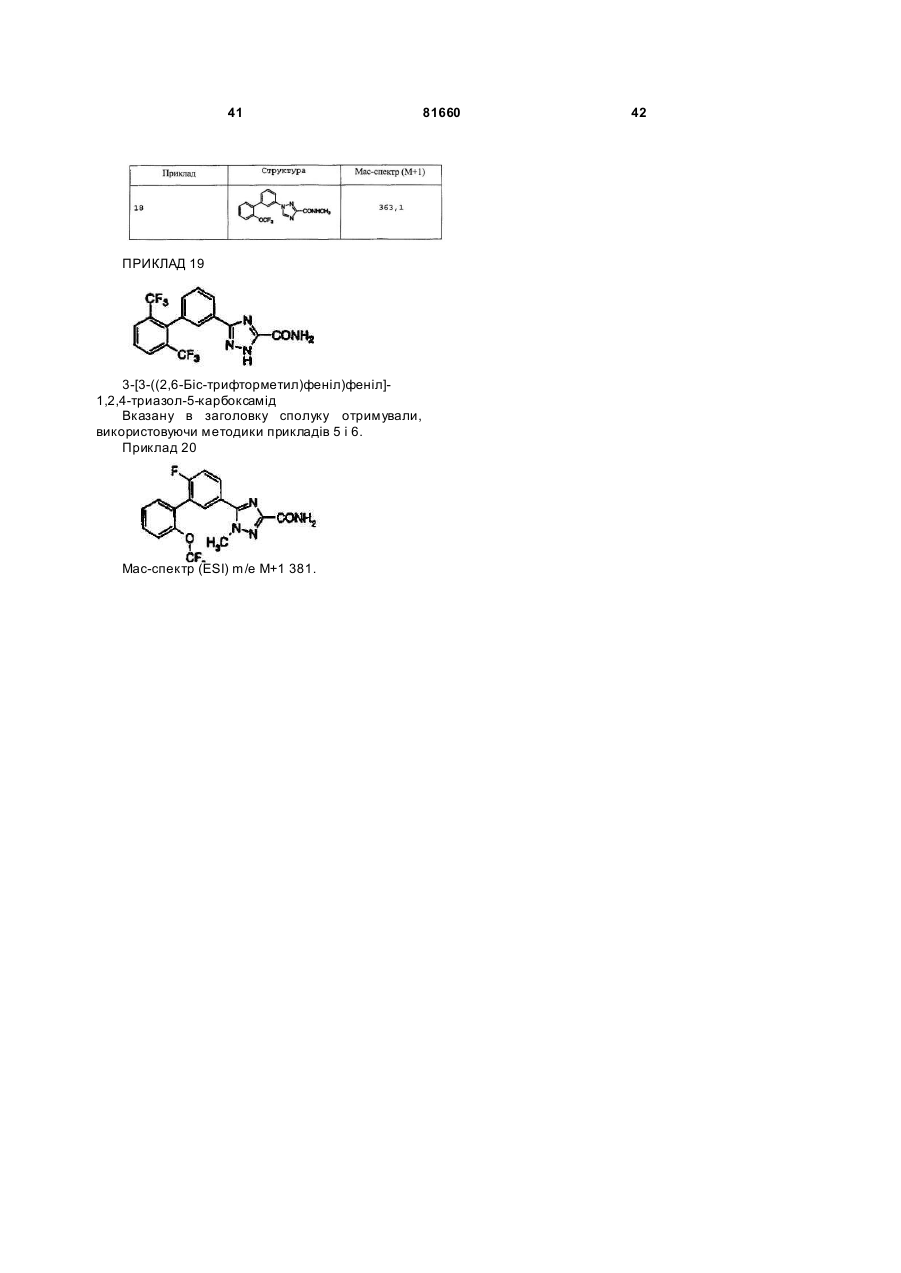
Біарилзаміщені триазоли як блокатори натрієвих каналів
Номер патенту: 81660
Опубліковано: 25.01.2008
Автори: Франц Дуглас Е., Фішер Майкл Х., Чжоу Бішань, Парк Мін К., Уівер Дейміан, Кері Джеймс П., Палукі Бренда, Парсонз Уільям Х., Чакраварті Прасун К., Кресс Майкл Х.
Формула / Реферат
1. Сполука, представлена формулою (І) або (II)
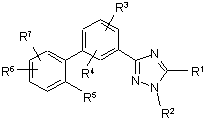 , (I)
, (I)
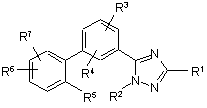 , (II)
, (II)
або її фармацевтичнo прийнятна сіль, де
R1 являє собою
Н;
С1-С6-алкіл, С2-С4-алкеніл, С2-С4-алкініл, С3-С6-циклоалкіл або С1-С4-алкілен-[С3-С6-циклоалкіл], будь-який з яких необов'язково заміщений одним або декількома наступними замісниками: F, СF3, ОН, O-(С1-С4)алкіл, O-CONRaRb, NRaRb, N(Ra)CONRaRb, СОО-(С1-С4)алкіл, СООН, CN, CONRaRb;
(a) -С0-С4-алкілен-С1-С4-перфторалкіл;
(b) NRaRb, -N(CORa)Rb, -N(SO2Ra)Rb, -N(Ra)CON(Ra)2, -N(Ra)SO2Ra, -N(ОRa)СОNRaRb або -N(Ra)SO2N(Ra)2;
(c) –CH(ORa)Ra, -С(ОRb)СF3, -CH(NHRb)Ra, -C(=O)Ra, С(=O)СF3, -SOСН3, -SO2СН3, COORa, CN, CONRaRb, -COCONRaRb, -SO2NRaRb, -CH2O-SO2NRaRb, SO2N(Ra)ORa, -C(=NH)NH2, -CRa=N-ORa, CH=CHCONRaRb;
(d) -CONRa(CH2)0-2C(Ra)(Rb)(CH2)0-2CONRaRb;
(e) -C(Ra)=C(Rb)-COORa або -C(Ra)=C(Rb)-CONRaRb;
Ra являє собою
(a) H;
(b) С1-С4-алкіл, необов'язково заміщений одним або декількома наступними замісниками: F, СF3, ОН, O-(С1-С4)алкіл, S(O)0-2-(С1-С4)алкіл, -OCONH2, -ОСОNН(С1-С4алкіл), -ОСОN(С1-С4алкіл)(С1-С4алкіл), -ОСОNН(С1-С4алкіларил), -ОСОN(С1-С4алкіл)(С1-С4алкіларил), NH2, NН(С1-С4алкіл), N(С1-С4алкіл) (С1-С4алкіл), NН(С1-С4алкіларил), N(С1-С4алкіл)(С1-С4алкіларил), NHCONH2, NHCONH(С1-С4aлкіл), NHСОNH(С1-С4алкіларил), -NHСОN(С1-С4алкіл)( С1-С4алкіл), NНСОN(С1-С4алкіл)(С1-С4алкіларил), N(С1-С4алкіл)СОN(С1-С4алкіл)(С1-С4алкіл), N(С1-С4алкіл)СОN(С1-С4алкіл)(С1-С4алкіларил), СОО-(С1-С4алкіл), СООН, CN, CONH2, СОNН(С1-С4алкіл), СОN(С1-С4алкіл)(С1-С4алкіл);
(c) С0-С4-алкілен-(С1-С4)-перфторалкіл; або
(d) -С1-С4алкіленарил, де арил являє собою феніл, піридил, піримідиніл, фурил, тієніл, піроліл, триазоліл, піразоліл, тіазоліл, ізоксазоліл, оксазоліл або оксадіазоліл, будь-який арил з яких необов'язково заміщений 1-3 замісниками, вибраними з і) F, Сl, Вr, І, іі) -CN, ііі) -NO2, iv) -С(=O)(С1-С4алкіл), v) -O(С1-С4алкіл), vi) -N(С1-С4алкіл)(С1-С4алкіл), vii) –С1-10алкіл і viii) –С1-10алкіл, де один або декілька атомів вуглецю в алкілі можуть бути заміщені на -O-, -S(O)1-2-, -О-С(О)-, -С(O)-O-, -С(O)-, -СН(ОН)-, -С=С- або -С![]() C-;
C-;
Rb являє собою
(a) Н; або
(b) С1-С6-алкіл, необов'язково заміщений одним або декількома наступними замісниками: F, СF3, ОН, O-(С1-С4)-алкіл, S(O)0-2-(С1-С4)алкіл, -OCONH2, -OCONH(С1-С4алкіл), NH2, NН(С1-С4алкіл), N(С1-С4алкіл)(С1-С4алкіл), NHCONH2, NНСОNН(С1-С4алкіл), -NНСОН(С1-С4алкіл)(С1-С4алкіл), СОО-(С1-С4алкіл), СООН, CN або CONH2;
R2 являє собою
(a) Н;
(b) -С1-С4-алкіл, -С3-С6-циклоалкіл або -С1-С4-алкілен-(С3-С6)циклоалкіл, необов'язково заміщений одним або декількома наступними замісниками: F, СF3, ОН, O-(С1-С4) алкіл, S(O)0-2-(С1-С4)алкіл, O-CONRaRb, NRaRb, N(Ra)CONRaRb, СОО-(С1-С4)алкіл, СООН, CN, CONRaRb;
(c) -С0-С4-алкілен-С1-С4-перфторалкіл;
(d) -С(=O)(Ra), -CONRaRb, -СОО-(С1-С4)алкіл, -SO2Ra, -SO2N(Ra)(Rb);
R3 і R4 кожний незалежно являє собою (а) Н;
(b) -С1-С6-алкіл, -С2-С6-алкеніл або -С2-С6-алкініл або -С3-С6-циклоалкіл, будь-який з яких необов'язково заміщений одним або декількома наступними замісниками: F, СF3, -O-(С1-С4)алкіл, CN, -N(Ra)(Rb), -N(Ra)CO-(С1-С4)aлкiл, COORb, CON(Ra)(Rb) або феніл;
(c) -С0-С4-алкілен-С1-С4-перфторалкіл або O-С0-С4-алкілен-С1-С4-перфторалкіл; або
(d) CN, NH2, NO2, F, Cl, Br, I, ОН, OCON(Ra)(Rb), O(С1-С4-aлкiлeн)CONRaRb, -OSO2N(Ra)(Rb), COORb, CON(Ra)(Rb) або арил, де арил необов'язково заміщений 1-3 замісниками, вибраними з і) F, Сl, Br, І, іі) -CN, ііі) –NO2, iv) –C(=O)(Ra), v) –ORa, vi) –NRaRb, vii) -С0-4алкілен-СО-ОRa, viii) -(C0-4aлкілен)-NH-CO-ORа, ix) -(C0-4aлкiлeн)CO-N(Ra)(Rb), x) -S(O)0-2Ra, xi) -SO2N(Ra)(Rb), xii) –NRaSO2Ra, xiii) –C1-10алкіл і xiv) –С1-10алкіл, де один або декілька атомів вуглецю в алкілі можуть бути заміщені на –NRa-, -O-, -S(O)1-2-, -О-С(О)-, -С(O)-O-, -C(O)-N(Ra)-, -N(Ra)-C(O)-, -N(Ra)-C(O)-N(Ra)-, -С(O)-, -СН(ОН)-, -С=С- або -С![]() C-; і
C-; і
R5, R6 і R7 кожний незалежно являє собою
(a) Н;
(b) С1-С6-алкіл, С2-С4-алкеніл, -С2-С4-алкініл або -С3-С6-циклоалкіл, будь-який з яких необов'язково заміщений одним або декількома наступними замісниками: F, СF3, ОН, O-(С1-С4)алкіл, OCON(Ra)(Rb), NRaRb, COORa, CN, CONRaRb, N(RaRb)CONRaRb;
(c) -O-С1-С6-алкіл, -O-С3-С6-циклоалкіл, -S-С1-С6-алкіл або -S-С3-С6-циклоалкіл, будь-який з яких необов'язково заміщений одним або декількома наступними замісниками: F, СF3, ОН, O-(С1-С4)алкіл, NH2, NH(С1-С4aлкіл), N(С1-С4-алкіл)2, COOH, CN, CONH2, CONH(С1-С4aлкіл), СОN(С1-С4алкіл)2, SO2NH2, SO2NH(С1-С4-алкіл), тетразоліл, триазоліл, імідазоліл, оксазоліл, оксадіазоліл, ізоксазоліл, тіазоліл, фурил, тієніл, піразоліл, піроліл, піридил, піримідиніл, піразиніл, феніл, піперидиніл, морфолініл, піролідиніл або піперазиніл;
(d) -С0-С4-алкілен-С1-С4-перфторалкіл або O-С0-С4-алкілен-С1-С4-перфторалкіл;
(e) CN, N(Ra)(Rb), NO2, F, Cl, Br, I, -ORa, -SRa, -ОСON(Ra)(Rb), -ОSО2N(Ra)(Rb), COORb, CON(Ra)(Rb), -N(Ra)CON(Ra)(Rb), -N(Ra)SO2N(Ra)(Rb), -C(ORb)Ra, -С(ОRa)СF3, -С(NНRa)СF3, -C(=O)Ra, -С(=O)СF3, -SOСН3, -SО2СН3, -NHSO2(С1-С6-алкіл), NHSO2-арил, SO2N(Ra)(Rb), -CH2OSO2N(Ra)(Rb), SO2N(Rb)-ORa, -C(=NH)NH2, -CRa=NORa, CH=CH2 або арил, де арил необов'язково заміщений 1-3 замісниками, вибраними з і) F, Сl, Br, I, ii) -CN, iii) –NO2, iv) -C(=O)(Ra), v) -ORa, vi) –NRaRb, vii) –С0-4алкілен-СО-ОRa, viii) -(C0-4aлкілен)-NH-CO-ORa, ix) -(C0-4aлкiлeн)CO-N(Ra)(Rb), x) -S(O)0-2Ra, xi) –SO2N(Ra)(Rb), xii) –NRaSO2Ra, xiii) –C1-10алкіл і xiv) –С1-10алкіл, де один або декілька атомів вуглецю в алкілі можуть бути заміщені на –NRa-, -O-, -S(O)1-2-, -O-C(O)-, -C(O)-O-, -C(O)-N(Ra)-, -N(Ra)-C(O)-, -N(Ra)-C(O)-N(Ra)-, -С(O)-, -СН(ОН)-, -С=С- або -С![]() С-.
С-.
2. Сполука, представлена формулою (III)
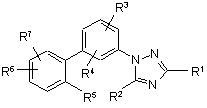 , (III)
, (III)
або її фармацевтично прийнятна сіль, де R5 приймає значення, відмінні від Н, і всі інші змінні приймають значення, визначені вище.
3. Сполука за п. 1, представлена хімічною формулою (І), або її фармацевтично прийнятна сіль, де
R5 приймає значення, відмінні від Н, і всі інші змінні приймають значення, визначені вище.
4. Сполука за п. 1, представлена хімічною формулою (II), або її фармацевтично прийнятна сіль, де
R5 приймає значення, відмінні від Н, і всі інші змінні приймають значення, визначені вище.
5. Сполука за п. 1, вибрана з
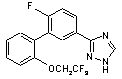 ,
,
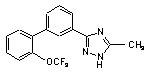 ,
,
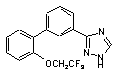 ,
,
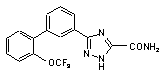 ,
,
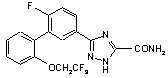 ,
,
 ,
,
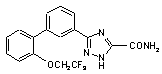 ,
,
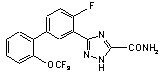 ,
,
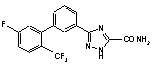 ,
,
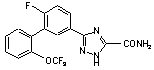 ,
,
 ,
,
 ,
,
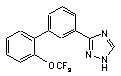 ,
,
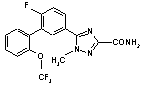 ,
,
 ,
,
або їх фармацевтично прийнятні солі.
6. Сполука за п. 2, вибрана з
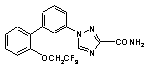 ,
,
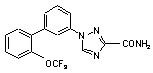 ,
,
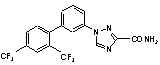 ,
,
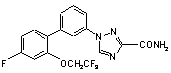 ,
,
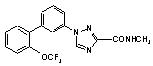 ,
,
або їх фармацевтично прийнятні солі.
7. Фармацевтична композиція, що містить терапевтично ефективну кількість сполуки за п. 1 або її фармацевтично прийнятну сіль і фармацевтично прийнятний наповнювач.
8. Застосування сполуки за п. 1 для приготування медикаменту для лікування або профілактики болю або порушення, викликаного болем.
9. Спосіб одержання сполуки формули (І):
 (І)
(І)
або її фармацевтично прийнятної солі, що включає взаємодію сполуки формули 34 або 35:
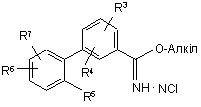 34,
34, 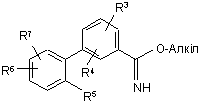 35
35
із сполукою формули 36:
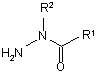 36,
36,
де кожний R1-R7 приймає значення, визначені в п. 1, в присутності основи з отриманням сполуки формули (І) або її фармацевтично прийнятної солі.
Текст
1. Сполука, представлена формулою (І) або (II) R3 C2 2 (19) 1 3 81660 алкілі можуть бути заміщені на -O-, -S(O)1-2-, -ОС(О)-, -С(O)-O-, -С(O)-, -СН(ОН)-, -С=С- або -С º C; Rb являє собою (a) Н; або (b) С1-С6-алкіл, необов'язково заміщений одним або декількома наступними замісниками: F, СF3, ОН, O-(С1-С4)-алкіл, S(O)0-2-(С1-С4)алкіл, -OCONH2, -OCONH(С1-С4алкіл), NH2, NН(С1-С4алкіл), N(С1С4алкіл)(С1-С4алкіл), NHCONH2, NНСОNН(С1С4алкіл), -NНСОН(С1-С4алкіл)(С1-С4алкіл), СОО(С1-С4алкіл), СООН, CN або CONH2; R2 являє собою (a) Н; (b) -С1-С4-алкіл, -С3-С6-циклоалкіл або -С1-С4алкілен-(С3-С6)циклоалкіл, необов'язково заміщений одним або декількома наступними замісниками: F, СF3, ОН, O-(С1-С4) алкіл, S(O)0-2(С1-С4)алкіл, O-CONRaRb, NRaRb, N(Ra)CONR aRb, СОО-(С1-С4)алкіл, СООН, CN, CONR aRb; (c) -С0-С4-алкілен-С 1-С4-перфторалкіл; (d) -С(=O)(Ra), -CONRaRb, -СОО-(С1-С4)алкіл, SO2Ra, -SO2N(Ra)(Rb); R3 і R4 кожний незалежно являє собою (а) Н; (b) -С1-С6-алкіл, -С2-С6-алкеніл або -С2-С6-алкініл або -С3-С6-циклоалкіл, будь-який з яких необов'язково заміщений одним або декількома наступними замісниками: F, СF3, -O-(С1-С4)алкіл, CN, -N(Ra)(Rb), -N(Ra)CO-(С1-С4)aлкiл, COORb, CON(Ra)(Rb) або феніл; (c) -С0-С4-алкілен-С 1-С4-перфторалкіл або O-С0С4-алкілен-С 1-С4-перфторалкіл; або (d) CN, NH2, NO2, F, Cl, Br, I, ОН, OCON(R a)(Rb), O(С1-С4-aлкiлeн)CONRaRb, -OSO2N(Ra)(Rb), b a b COOR , CON(R )(R ) або арил, де арил необов'язково заміщений 1-3 замісниками, вибраними з і) F, Сl, Br, І, іі) -CN, ііі) –NO2, iv) – C(=O)(Ra), v) –OR a, vi) –NRaRb, vii) -С0-4алкілен-СООRa, viii) -(C 0-4aлкілен)-NH-CO-ORа, ix) -(C0a b x) -S(O) 0-2Ra, xi) 4aлкiлeн)CO-N(R )(R ), a b a a SO2N(R )(R ), xii) –NR SO2R , xiii) –C1-10алкіл і xiv) –С1-10алкіл, де один або декілька атомів вуглецю в алкілі можуть бути заміщені на –NRa-, -O-, -S(O)1-2, -О-С(О)-, -С(O)-O-, -C(O)-N(Ra)-, -N(Ra)-C(O)-, N(Ra)-C(O)-N(Ra)-, -С(O)-, -СН(ОН)-, -С=С - або С º C-; і R5, R6 і R7 кожний незалежно являє собою (a) Н; (b) С1-С6-алкіл, С2-С4-алкеніл, -С2-С4-алкініл або С3-С6-циклоалкіл, будь-який з яких необов'язково заміщений одним або декількома наступними замісниками: F, СF3, ОН, O-(С1-С4)алкіл, OCON(Ra)(Rb), NRaRb, COORa, CN, CONRaRb, N(RaRb)CONRaRb; (c) -O-С1-С6-алкіл, -O-С3-С6-циклоалкіл, -S-С1-С6алкіл або -S-С3-С6-циклоалкіл, будь-який з яких необов'язково заміщений одним або декількома наступними замісниками: F, СF3, ОН, O-(С1С4)алкіл, NH2, NH(С1-С4aлкіл), N(С1-С4-алкіл)2, COOH, CN, CONH2, CONH(С1-С4aлкіл), СОN(С1С4алкіл)2, SO2NH2, SO2NH(С1-С4-алкіл), тетразоліл, триазоліл, імідазоліл, оксазоліл, оксадіазоліл, ізоксазоліл, тіазоліл, фурил, тієніл, піразоліл, піроліл, піридил, піримідиніл, піразиніл, феніл, 4 піперидиніл, морфолініл, піролідиніл або піперазиніл; (d) -С0-С4-алкілен-С 1-С4-перфторалкіл або O-С0С4-алкілен-С 1-С4-перфторалкіл; (e) CN, N(R a)(Rb), NO2, F, Cl, Br, I, -OR a, -SRa, ОСON(Ra)(Rb), -ОSО2N(Ra)(Rb), COORb, a b a a b CON(R )(R ), -N(R )CON(R )(R ), N(Ra)SO2N(Ra)(Rb), -C(ORb)Ra, -С(ОR a)СF3, С(NНRa)СF3, -C(=O)Ra, -С(=O)СF3, -SOСН3, SО2СН3, -NHSO2(С1-С6-алкіл), NHSO2-арил, SO2N(Ra)(Rb), -CH2OSO 2N(Ra)(Rb), SO 2N(Rb)-ORa, C(=NH)NH 2, -CRa=NOR a, CH=CH2 або арил, де арил необов'язково заміщений 1-3 замісниками, вибраними з і) F, Сl, Br, I, ii) -CN, iii) –NO2, iv) C(=O)(Ra), v) -ORa , vi) –NRaRb, vii) –С0-4алкілен-СООRa, viii) -(C 0-4aлкілен)-NH-CO-ORa, ix) -(C0a b x) -S(O)0-2Ra, xi) – 4aлкiлeн)CO-N(R )(R ), a b a a SO2N(R )(R ), xii) –NR SO2R , xiii) –C1-10алкіл і xiv) –С1-10алкіл, де один або декілька атомів вуглецю в алкілі можуть бути заміщені на –NRa-, -O-, -S(O)1-2, -O-C(O)-, -C(O)-O-, -C(O)-N(R a)-, -N(Ra)-C(O)-, N(Ra)-C(O)-N(Ra)-, -С(O)-, -СН(ОН)-, -С=С - або С º С-. 2. Сполука, представлена формулою (III) R3 R7 N N R6 R4 R2 R5 R1 N , (III) або її фармацевтично прийнятна сіль, де R 5 приймає значення, відмінні від Н, і всі інші змінні приймають значення, визначені вище. 3. Сполука за п. 1, представлена хімічною формулою (І), або її фармацевтично прийнятна сіль, де R5 приймає значення, відмінні від Н, і всі інші змінні приймають значення, визначені вище. 4. Сполука за п. 1, представлена хімічною формулою (II), або її фармацевтично прийнятна сіль, де R5 приймає значення, відмінні від Н, і всі інші змінні приймають значення, визначені вище. 5. Сполука за п. 1, вибрана з F N N N OCH2CF3 N H OCF3 , CH3 N N H , F N OCF3 N N CONH 2 N H N , OCH2CF3 CONH2 N H , F F N N N OCH2 CF 3 H N CONH 2 , O CF 3 N N H CONH2 , 5 81660 6 R3 F N N CONH2 N N H OCF3 CF3 , N N H CF3 R CONH2 N N H OCF3 O HC 3 , CF3 CF3 CONH2 N N OCH2CF3 CF3 N O-Алкіл F OCH2CF3 , OCF3 NH . NCl N R5 N N CF3 R CF3 , R7 N CONH2 R4 CONH2 OCF 3 N N N R2 CONH2 (І) або її прийнятної солі, що , включає взаємодію сполуки формули 34 або 35: , 3 R N N CONH2 , N R7 N , R1 N N фармацевтично CF 3 H R6 N R4 N або їх фармацевтично прийнятні солі. 6. Сполука за п. 2, вибрана з N CONH2 N N N H R5 N N CF3 , R6 F N 7 N 3 , O-Алкіл N N або їх фармацевтично прийнятні солі. 7. Фармацевтична композиція, що містить терапевтично ефективну кількість сполуки за п. 1 або її фармацевтично прийнятну сіль і фармацевтично прийнятний наповнювач. 8. Застосування сполуки за п. 1 для приготування медикаменту для лікування або профілактики болю або порушення, викликаного болем. 9. Спосіб одержання сполуки формули (І): Даний винахід відноситься до біарилзаміщених похідних триазолу. Зокрема, даний винахід відноситься до біарилзаміщених триазолів, які є блокаторами натрієвих каналів і придатні для лікування хронічного і невропатичного болю. Сполуки даного винаходу також придатні для лікування інших станів, що включають розлади центральної нервової системи (ЦНС), такі як епілепсія, маніакальна депресія, біполярний розлад, депресивний синдром, стан страху і діабетична невропатія. Даний винахід відноситься до біарилзаміщених триазолів, які є блокаторами натрієвих каналів і придатні для лікування хронічного і невропатичного болю. Сполуки даного винаходу також придатні для лікування інших станів, що включають розлади центральної нервової системи (ЦНС), такі як епілепсія, депресивний синдром, стан страху, маніакальна депресія і біполярний розлад. Даний винахід також відноситься до фармацевтичних композицій, що включають сполуки даного винаходу, або індивідуально, або в комбінації з однією або 34, CO NH 2 CONHCH 3 R6 R4 , R5 NH із сполукою формули 36: R2 R1 N H2N 35 O 36, де кожний R1-R7 приймає значення, визначені в п. 1, в присутності основи з отриманням сполуки формули (І) або її фармацевтично прийнятної солі. декількома терапевтично активними сполуками, і фармацевтично прийнятний наповнювач. Даний винахід включає також способи лікування гострого болю, хронічного болю, вісцерального болю, запального болю, невропатичного болю і розладів ЦНС, які включають, але не обмежених тільки ними, епілепсію, депресивний синдром, стан страху, маніакальну депресію і біполярний розлад, за допомогою введення сполук і фармацевтичних композицій даного винаходу. Винахід також відноситься до способу отримання даних сполук. Даний винахід включає сполуки, представлені формулою (І) або (II) 7 81660 або їх фармацевтично прийнятні солі, де R1 являє собою (а) Н; (b) С1-С6-алкіл, С2-С4-алкеніл, С2-С4-алкініл, С3-С6-циклоалкіл або С 1-С4-алкілен-[С3-С6циклоалкіл], будь-який з яких необов'язково заміщений одним або декількома наступними замісниками: F, CF 3, OH, О-(С 1-С4)алкіл, OCONRaRb, NRaRb, N(Ra)CONRaRb, СОО-(С1С4)алкіл, COOH, CN, CONR aRb; (c) -С0-С4-алкілен-С 1-С4-перфторалкіл; (d) NRaRb, -N(COR a)Rb, -N(SO2Ra)Rb, a N(R )CON(Ra)2, -N(Ra)SO2Ra, -N(OR a)CONRaRb або -N(Ra)SO2N(Ra)2; (e) -CH(OR a)Ra, -C(OR b)CF3, -CH(NHRb)Ra, C(=O)Ra, C(=O)CF3, -SOCH 3, -SO2CH3, COORa , CN, CONRaRb, -COCONRaRb, -SO2NRaRb, -CH2OSO2NRaRb, SO2N(Ra)OR a, -C(=NH)NH2, -CRa=NORa, CH=CHCONRaRb; (f) -CONR a(CH2)0-2C(Ra) (Rb) (CH2) 0-2CONRaRb; (g) -C(Ra)=C(Rb)-COOR a або -C(Ra) =C(Rb)CONRaRb; Ra являє собою (a) H; (b) С1-С4-алкіл, необов'язково заміщений одним або декількома наступними замісниками: F, CF3, ОН, О-(С1-С 4)алкіл, S(О)0-2-(С1-С4)алкіл, OCONH2, -OCONH(С1-С4алкіл), -OCON(С1С4алкіл)(С1-С4алкіл), -OCONH(C1-C4aлкiлaрил), OCON (С1-С4алкіл) (С1-С4 алкіларил), NH2, NH(С1С4алкіл), N(C1-C4aлкiл)(C1-C4aлкiл), NH(C1С4алкіларил), N(С1-С4алкіл)(С1-С4алкіларил), NHCONH2, NHCONH(C1-C4aлкiл), NHCONH(С1С4алкіларил), -NHCON(С1-С4алкіл)(С1-С4алкіл), NHCONH(C1-С4алкіл)(С1-С4алкіларил), N(С1С4алкіл)СОN(С1-С4алкіл)(С1-С4алкіл), N(C1С4алкіл)СОN(С1-С4алкіл)(С1-С4алкіларил), СОО(С1-С4алкіл), СООН, CN, CONH2, CONH(C1С4алкіл), CON(C1-С4алкіл)(С1-С4алкіл); (c) С1-С4-алкілен-(С1-С4)-перфторалкіл; або (d) -С1-С4алкіленарил, де арил являє собою феніл, піридил, піримідиніл, фурил, тієніл, піроліл, 8 триазоліл, піразоліл, тіазоліл, ізоксазоліл, оксазоліл або оксадіазоліл, будь-який арил з яких необов'язково заміщений 1-3 замісниками, вибраними з і) F, СІ, Br, I, ii) -CN, iii) -NO2, iv) С(=О)(С1-С4алкіл), v) -О(С1-С4алкіл), vi) -N(С1С4алкіл)(С1-С4алкіл), хііі) -С1-10алкіл і xiv) -С110алкіл, де один або декілька атомів вуглецю в алкілі можуть бути заміщені на -О-, -S(O)1-2-, -ОС(О),-С(О)-О-, -С(О)-, -СН(ОН)-, -С=С- або -СºC-; Rb являє собою (a) Н або (b) С1-С4-алкіл, необов'язково заміщений одним або декількома наступними замісниками: F, CF3, ОН, О-(С1-С 4)-алкіл, S(O)0-2-(C1-C4) алкіл, OCONH2, -OCONH(C1-С4алкіл), NH2, NH(C1C4aлкiл), NH(C1-C4aлкiл)(C1-C4aлкiл), NHCONH2, NHCONH(C1-С4алкіл), -NНСОN(С1-С4алкіл)(С1С4алкіл), СОО-(С1-С4алкіл), СООН, CN або CONH2; R2 являє собою (а) Н; (b) -С1-С4-алкіл, -С3-С6-циклоалкіл або -С1-С4алкілен-(С3-С6)циклоалкіл, необов'язково заміщений одним або декількома наступними замісниками: F, CF3, OH, О-(С1-С 4)алкіл, S(O)0-2(С1-С4)алкіл, O-CONRaRb, NRaRb, N(Ra)CONR aRb, СОО-(С1-С4)алкіл, СООН, CN, CONR aRb; (c) -С0-С4-алкілен-С 1-С4-перфторалкіл; (d) -C(=O)(R a), -CONRaRb, -COO-(C1-C4) алкіл, SO2Ra, -SO2N(Ra) (Rb); R3 і R4 кожний незалежно являє собою (a) Н; (b) -С1-С6-алкіл, -С2-С6-алкеніл або -С2-С6алкініл або -С3-С6-циклоалкіл, будь-який з яких необов'язково заміщений одним або декількома наступними замісниками: F, CF3, -О-(С1-С4)алкіл, CN, -N(Ra)(Rb), -N(Ra)CO-(C1-C4)алкіл, COORb, CON(Ra)(Rb) або феніл; (c) -С0-С4-алкілен-С 1-С4-перфторалкіл або ОС0-С4-алкілен-С 1-С4-перфторалкіл; або (d) CN, NH2, NO2, F, Cl, Br, I, OH, OCON(Ra)(Rb), O(C1-C4-aлкiлeн)CONRaRb, a b OSO2N(R )(R ), COOR b, CON(Ra)(Rb) або арил, де арил необов'язково заміщений 1-3 замісниками, вибраними з і) F, СІ, Br, I, ii) -CN, iii) -NO2, iv) C(=O)(Ra), v) -ORa, vi) -NRaRb, vii)-C0-4алкілен-COORa, viii) -(С0-4алкілен)-NH-СО-OR3, іх) -(С0a b x) -S(O)0- 2Ra xi) 4алкілен)-СО-N(R )(R ), SO2N(Ra)(Rb), xii) -NRaSO2Ra, xiii) -С1-10алкіл і xi v) С1-10алкіл, де один або декілька атомів вуглецю в алкілі можуть бути заміщені на -NRa-, -О-, -S(O)1-2-, -О-С(О)-, -С(О)-О-, -C(O)-N(R a)-N(Ra)-C(O)-, -N(R a)C(O)-N(Ra)-, -C(O)-, -СН(ОН)-, -С=С- або -СºС-; і R5, R6 і R7 кожний незалежно являє собою (а) Н; (b) С1-С6-алкіл, С2-С4-алкеніл, або -С2-С4алкініл або -С3-С6-циклоалкіл, будь-який з яких необов'язково заміщений одним або декількома наступними замісниками: F, CF3, ОН, О-(С1С4)алкіл, OCON(Ra)(Rb), NRaRb, COOR a, CN, CONRaRb, N (R aRb) CONRaRb; (c) -О-С1-С6-алкіл або -О-С3-С6-циклоалкіл, -SС1-С6-алкіл або -S-C3-C6-циклоалкіл, будь-який з яких необов'язково заміщений одним або декількома наступними замісниками: F, CF3 , ОН, О-(С1-С4)алкіл, NH2, NH(C1-C4aлкiл), N(C1-C4 9 81660 алкіл)2, СООН, CN, CONH 2, CONH(C1-C4 алкіл), CON(C1-C4-алкіл)2, SO2NH2, SO2NH(C1-C4-алкіл), тетразоліл, триазоліл, імідазоліл, оксазоліл, оксадіазоліл, ізоксазоліл, тіазоліл, фурил, тієніл, піразоліл, піроліл, піридил, піримідиніл, піразиніл, феніл, піперидиніл, морфолініл, піролідиніл або піперазиніл; (d) -С0-С4-алкілен-С 1-С4-перфторалкіл або ОС0-С4-алкілен-С 1-С4-перфторалкіл; (е) CN, N(Ra)(Rb), NO2, F, СІ, Br, I, -OR a, -SRa , OCON(Ra)(Rb), -OSO2N(Ra)(Rb), COORb, a b a a b CON(R )(R ), -N(R )CON(R )(R ), N(Ra)SO2N(Ra)(Rb), -C(ORb)Ra, -C(OR a)CF3, C(NHRa)CF3, -C(-O)Ra, -C(=O)CF3, -SOCH 3, SO2CH3, -NHSO2(C1-6-алкіл), NHSO2-алкіл, SO2N(Ra)(Rb), -CH2OSO 2N(Ra)(Rb), SO 2N(Rb)-ORa, C(=NH)NH 2, -CR a=NOR a, CH=CH або арил, де арил необов'язково заміщений 1-3 замісниками, вибраними з і) F, СІ, Вr, І, іі) -CN, iii) -NO2, iv) a a a b C(=O)(R ), v) -OR , vi) - NR R , vii) -С0-4алкілен-COOR3, viii) -(C0-4алкілен) -NH-CO-OR3, іх) -(С0-CO-N(Ra)(Rb), x) -S(O)0-2Ra , xi) 4алкілен) SO2N(Ra)(Rb), xii) -NRaSO2Ra, xiii) -С1-10алкіл і xi v) С1-10алкіл, де один або декілька атомів вуглецю в алкілі можуть бути заміщені на -NRa-, -О-, -S(O)1-2-, -OC(O)-, -C(O)-O-, -C(O)-N(Ra)-, -N(Ra)-C(O)-, N(Ra)-C(O)-N(Ra)-, -С(О)-, -СН(ОН)-, -С=С - або СºC-. Даний винахід, крім того, включає сполуки формули III або їх фармацевтичні солі, де кожний R 1-R7 приймає значення, визначені вище. Наступні сполуки виключені з даного винаходу: 1-метил-3-(2-хлорфеніл)-5-[3-(4трифторметилфеніл)феніл]-1,2,4-триазол, 1 -метил-3-(2-хлор-6-фторфеніл )-5-[3-(4трифторметил феніл)-феніл]-1,2,4-триазол, 1-метил-3-(2,6-дифторфеніл)-5-[3-(4трифторметилфеніл)-феніл]-1,2,4-триазол, 1-метил-3-(2,6-дифторфеніл)-5-[3-(4трифторметоксифеніл)-феніл]-1,2,4-триазол, 1-(3-феніл)феніл-1,2,4-триазол. У першому аспекті даний винахід відноситься до сполуки, представленої хімічною формулою (І), або до її фармацевтично прийнятної солі, де R 5 приймає значення, відмінні від Н, і всі інші змінні приймають значення, визначені вище. У варіанті здійснення вказаного першого аспекту даний винахід відноситься до сполуки, представленої хімічною формулою (І), або до її фармацевтично прийнятної солі, де R5 являє собою -ORa, і всі інші змінні приймають значення, визначені вище. В іншому варіанті здійснення вказаного першого аспекту даний винахід відноситься до 10 сполуки, представленої хімічною формулою (І), або до її фармацевтично прийнятної солі, де R 1 являє собою необов'язково заміщений C1-С6-алкіл, необов'язково заміщений С 3-С6-циклоалкіл, C(=O)Ra або CONRaRb, і всі інші змінні приймають значення, визначені вище. У другому аспекті даний винахід відноситься до сполуки, представленої хімічною формулою (II), або до її фармацевтично прийнятної солі, де R 5 приймає значення, відмінні від Н, і всі інші змінні приймають значення, визначені вище. У варіанті здійснення вказаного другого аспекту даний винахід відноситься до сполуки, представленої хімічною формулою (II), або до її фармацевтично прийнятної солі, де R5 являє собою -ORa, і всі інші змінні приймають значення, визначені вище. В іншому варіанті здійснення вказаного другого аспекту даний винахід відноситься до сполуки, представленої хімічною формулою (II), або до її фармацевтично прийнятної солі, де R 1 являє собою необов'язково заміщений C1-C6-алкіл, C1-C6 необов'язково заміщений С 3-С6-циклоалкіл, C(=O)Ra або CONRaRb, і всі інші змінні приймають значення, визначені вище. У третьому аспекті даний винахід відноситься до сполуки, представленої хімічною формулою (III), або до її фармацевтично прийнятної солі, де R5 приймає значення, відмінні від Н, і всі інші змінні приймають значення, визначені вище. У варіанті здійснення вказаного третього аспекту даний винахід відноситься до сполуки, представленої хімічною формулою (III), або до її фармацевтично прийнятної солі, де R5 являє собою -ORa, і всі інші змінні приймають значення, визначені вище. В іншому варіанті здійснення вказаного третього аспекту даний винахід відноситься до сполуки, представленої хімічною формулою (III), або до її фармацевтично прийнятної солі, де R 1 являє собою необов'язково заміщений С 1-С6-алкіл, необов'язково заміщений С 3-С6-циклоалкіл, C(=O)Ra або CONRaRb, і всі інші змінні приймають значення, визначені вище. Даний винахід також відноситься до способу отримання сполуки формули (І) або її фармацевтично прийнятної солі, що включає взаємодію сполуки формули 34 або 35: із сполукою формули 36: де кожний R1-R7 приймає значення, визначені вище, в присутності основи для отримання 11 81660 сполуки формули (І) або її фармацевтично прийнятної солі. У першому аспекті способу, що пропонується, даний винахід відноситься до способу отримання сполуки формули (І) або її фармацевтично прийнятної солі, де R1 являє собою H, -C(=O)R a, COORa, CONRaRb, С1-С6алкіл або С3-С6циклоалкіл, де вказаний алкіл або циклоалкіл необов'язково заміщений одним або декількома F, ОН або NRaRb, R2 являє собою Н, R5, R6 і R7 кожний незалежно являє собою Н, F, -ORa , С1-С6-алкіл або -О-С1-С6-алкіл, де вказаний алкіл необов'язково заміщений одним або декількома F, CF3 або -O-(C1-C4)алкіл, і всі інші змінні приймають значення, визначені вище. У другому аспекті способу, що пропонується, даний винахід відноситься до способу отримання сполуки формули (І) або її фармацевтично прийнятної солі, де основа являє собою ацетат металу, карбонат металу або третинний амін. У третьому аспекті способу, що пропонується, даний винахід відноситься до способу отримання сполуки формули (І) або її фармацевтично прийнятної солі, де основа являє собою ацетат калію. Даний винахід також відноситься до способу отримання сполуки формули (І) або її фармацевтично прийнятної солі, що включає взаємодію сполуки формули 34 або 35: із сполукою формули 36: де кожний R1-R7 приймає значення, визначені вище, в присутності основи і необов'язково в спиртовому розчиннику, і необов'язково при нагріванні, для отримання сполуки формули (І) або її фармацевтично прийнятної солі. Термін "алкіл", що використовується в даному описі, так само, як і інші групи, що містять префікс "алк", такі як, наприклад, алкокси, алканоїл, алкеніл і алкініл, означають вуглецеві ланцюги, які можуть бути лінійними або розгалуженими або їх комбінацією. Приклади алкільних груп включають метил, етил, пропіл, ізопропіл, бутил, втор- і третбутил, пентил, гексил і гептил. Терміни "алкеніл", "алкініл" і інші подібні терміни включають вуглецеві ланцюги, що містять, щонайменше, один ненасичений С-С зв'язок. Термін "циклоалкіл" означає вуглецеві цикли, що не містять гетероатомів, і включає моно-, бі- і трициклічні насичені вуглецеві цикли, також як і 12 конденсовані циклічні системи. Такі конденсовані циклічні системи можуть включати одне кільце, яке є частково або повністю ненасиченим, таке як бензольне кільце, для утворення конденсованих циклічних систем, таких як бензоконденсовані вуглецеві цикли. Циклоалкіл включає такі конденсовані циклічні системи як спіроконденсовані циклічні системи. Приклади циклоалкілу включають циклопропіл, циклобутил, циклопентил, циклогексил, декагідронафталін, адамантан, інданіл, інденіл, флуореніл і 1,2,3,4тетрагідронафталін. Термін "арил" включає без обмеження ароматичний замісник, який являє собою єдине кільце або декілька кілець, конденсованих разом. При наявності множини кілець, щонайменше, одне з складаючих кілець є ароматичним. Термін "арил", якщо не обумовлено особливо, також включає гетероарили і, таким чином, включає стабільні 5-7-членні моноциклічні і стабільні 9-10членні конденсовані біциклічні гетероциклічні кільцеві системи, які містять атоми вуглецю і від одного до чотирьох гетероатомів, вибраних з групи, що містить N, O і S, де гетероатоми азоту і сірки необов'язково можуть бути окислені і гетероатоми азоту необов'язково можуть бути кватернізовані. Відповідні арильні групи включають феніл, нафтил, піридил, піримідиніл, фурил, тієніл, піроліл, триазоліл, піразоліл, тіазоліл, ізоксазоліл, оксазоліл і оксадіазоліл. Термін "циклоалкілокси", якщо не обумовлено особливо, включає циклоалкільну групу, приєднану через короткий С 1-2алкіл до зв'язуючого атома кисню. Термін "С0-6алкіл" включає алкіли, які містять 6, 5, 4, 3, 2, 1 атомів вуглецю або не містять їх. Алкіл з відсутністю атомів вуглецю являє собою замісник у вигляді атома водню, коли алкіл є термінальною групою, або направлений зв'язок, коли алкіл є зв'язуючою групою. Термін "амін", якщо не обумовлено особливо, включає первинні, вторинні і третинні аміни. Термін "карбоніл", якщо не обумовлено особливо, включає С0-6алкільний замісник, коли карбоніл є термінальним. Термін "галоген" включає атоми фтору, хлору, брому і йоду. Термін "необов'язково заміщений" призначений для включення як заміщених, так і незаміщених фрагментів. Так, наприклад, необов'язково заміщений арил може являти собою пентафторфеніл або феніл. Крім того, необов'язково заміщені складові структурні фрагменти, такі як, наприклад, алкіларил, означають, що алкільні і арильні групи необов'язково заміщені. Якщо тільки один з складових фрагментів є необов'язково заміщеним, то він буде спеціально відмічений таким чином як "алкіларил, причому арил, необов'язково заміщений галогеном або гідроксилом". Сполуки, описані в описі, можуть містити один або декілька подвійних зв'язків і, отже, можуть утворювати цис/транс-ізомер так само, як і інші конформаційні ізомери. Даний винахід включає всі 13 81660 такі можливі ізомери, так само, як і суміші подібних ізомерів, якщо не обумовлено особливо. Сполуки, описані в описі, можуть містити один або декілька асиметричних центрів і, отже, можуть утворювати діастереоізомери і оптичні ізомери. Даний винахід включає все можливі діастереоізомери так само, як і їх рацемічні суміші, їх по суті чисті розділені енантіомери, всі можливі геометричні ізомери і їх фармацевтично прийнятні солі. Вищенаведені хімічні формули показані без вказівки стереохімії в деяких положеннях. Даний винахід включає все стереоізомери хімічних формул і їх фармацевтично прийнятні солі. Крім того, включені суміші стереоізомерів, так само як і виділені специфічні стереоізомери. При проведенні синтетичних процедур, застосованих для приготування таких сполук, або використанні процедур рацемізації або епімеризації, відомих фа хівцям в даній галузі, продукти подібних процедур можуть бути сумішшю стереоізомерів. Термін "фармацевтично прийнятні солі" відноситься до солей, приготованих з фармацевтично прийнятних нетоксичних основ або кислот. Якщо сполуки даного винаходу є кислотними, то їх відповідні солі зручно можуть бути приготовані з фармацевтично прийнятних нетоксичних основ, що включають неорганічні основи і органічні основи. Солі таких неорганічних основ включають солі алюмінію, амонію, кальцію, міді (двох- і одновалентної), заліза (трьох- і двовалентного), літію, магнію, марганцю (чотирьох-, трьох- і двовалентного), калію, натрію, цинку і подібні солі. Солі фармацевтично прийнятних органічних нетоксичных основ включають солі первинних, вторинних і третинних амінів, так само як і циклічних амінів і заміщених амінів, таких як аміни природного походження і синтезовані заміщені аміни. Інші фармацевтично прийнятні органічні нетоксичні основи, з яких можуть бути утворені солі, включають іоніти, такі як, наприклад, аргінін, бетаїн, кофеїн, холін, N,N’дибензилетилендіамін, діетиламін, 2діетиламіноетанол, 2-диметиламіноетанол, етаноламін, етилендіамін, N-етилморфолін, Nетилпіперидин, глюкамін, глюкозамін, гістидін, гідрабамін, ізопропіламін, лізин, метилглюкамін, морфолін, піперазин, піперидин, поліамінні полімери, прокаїн, пурини, теобромін, триетиламін, триметиламін, трипропіламін і трометамін. Якщо сполуки даного винаходу є основними, то їх відповідні солі зручно можуть бути приготовані з фармацевтично прийнятних нетоксичних кислот, що включають неорганічні і органічні кислоти. Такі кислоти включають, наприклад, оцтову, бензолсульфонову, бензойну, камфорсульфонову, лимонну, етансульфонову, фумарову, глюконову, глутамінову, бромистоводневу, хлористоводневу, ізетіонову, молочну, малеїнову, яблучн у, мигдалеву, метансульфонову, слизеву, азотну, памову, пантотенову, фосфорну, янтарну, сірчану, винну, п-толуолсуль фонову кислоту і т.п. Фармацевтичні композиції даного винаходу містять сполуку, представлену формулою І, II або 14 III (або її фармацевтично прийнятну сіль), як активний інгредієнт, фармацевтично прийнятний наповнювач і необов'язково один або декілька додаткових терапевтичних засобів або ад'ювантів. Такі додаткові терапевтичні засоби можуть включати, наприклад, і) опіатні агоністи або антагоністи, іі) антагоністи кальцієвих каналів, ііі) агоністи 5НТ рецептору або антагоністи, iv) антагоністи натрієвих каналів, v) агоністи NMDA рецептору або антагоністи, vi) селективні інгібітори СОХ-2, vii) антагоністи NK1, viii) нестероїдні протизапальні засоби (НПЗЗ, "NSAID"), іх) селективні інгібітори зворотного захоплення серотоніну ("SSRI") і/або селективні інгібітори зворотного захоплення серотоніну і норепінефрину ("SSNRI"), х) трициклічні антидепресантні лікарські засоби, хі) модулятори норепінефрину, хіі) літій, хііі) вальпроат і xiv) нейронтин (габапентин). Відповідні композиції включають композиції, придатні для перорального, ректального, місцевого і парентерального (включаючи підшкірне, внутрішньом'язове і внутрішньовенне) введення, хоча найбільш придатний шлях в будь-якому конкретному випадку буде залежати від конкретного реципієнта, природи і тяжкості станів, при яких вводиться активний інгредієнт. Фармацевтичні композиції можуть бути зручно представлені у вигляді стандартної лікарської форми і приготовані будь-яким способом, добре відомим в галузі фармації. Дані сполуки і композиції придатні для лікування хронічних, вісцеральних, запальних і невропатичних больових синдромів. Вони придатні для лікування болю, отриманого внаслідок травматичного пошкодження нерва, компресії або ущемлення нерва, постгерпетичної невралгії, тригемінальної невралгії і діабетичної невропатії. Дані сполуки і композиції придатні також для лікування хронічного поперекового болю, фантомного болю, хронічного тазового болю, невромного болю, комплексного регіонального больового синдрому, хронічного артритного болю і родинних невралгій і болю, пов'язаного з раком, хіміотерапією, ВІЛ і невропатією, викликаною лікуванням ВІЛ. Сполуки даного винаходу можуть бути також використані як місцеві анестетики. Сполуки даного винаходу придатні для лікування синдрому подразненої товстої кишки і родинних розладів, а також хвороби Крона. Дані сполуки мають клінічні застосування для лікування епілепсії і часткових і генералізованих тонічних припадків. Вони також придатні для нейрозахисту при ішемічних станах, викликаних ударом або травмою нервів, і для лікування множинного склерозу. Сполуки даного винаходу придатні для лікування депресії, стану страху, біполярного розладу і та хіаритмій. Крім того, мається на увазі, що сполуки даного винаходу можуть бути введені в профілактично ефективних дозованих кількостях для запобігання вищезгаданим станам і порушенням, а також для запобігання іншим станам і порушенням, пов'язаним з активністю натрієвих каналів. 15 81660 Пасти, мазі, желеподібні форми, розчини або суспензії, що містять дані сполуки, можуть бути застосовані для місцевого використання. Розчини і рідини для полоскання ротової порожнини включені в рамках локального застосування для цілей даного винаходу. Дозовані кількості приблизно від 0,01мг/кг до приблизно 140мг/кг маси тіла на добу придатні для лікування запального і невропатичного болю, або альтернативно приблизно від 0,5мг до приблизно 7г на пацієнта на добу. Наприклад, запальний біль може бути ефективно пролікований введенням приблизно від 0,01мг до приблизно 75мг сполуки на кілограм маси тіла на добу, або альтернативно приблизно від 0,5мг до приблизно 3,5г на пацієнта на добу. Невропатичний біль може бути ефективно пролікований введенням приблизно від 0,01мг до приблизно 125мг сполуки на кілограм маси тіла на добу, або альтернативно приблизно від 0,5мг до приблизно 5,5г на пацієнта на добу. Кількість активного інгредієнта, який може бути об'єднаний з матеріалами-наповнювачами для створення однократної лікарської форми, буде мінятися в залежності від реципієнта, що піддається лікуванню, і конкретного способу введення. Наприклад, препарат, призначений для перорального введення людям, може просто містити приблизно від 0,5мг до приблизно 5г активного інгредієнта, змішаного з відповідною і придатною кількістю матеріалу-наповнювача, яка може змінюватися приблизно від 5 до приблизно 95 процентів від загальної композиції. Стандартні лікарські форми переважно будуть містити приблизно від 1мг до приблизно 1000мг активного інгредієнта, звичайно 25мг, 50мг, 100мг, 200мг, 300мг, 400мг, 500мг, 600мг, 800мг або 1000мг. Мається на увазі, однак, що специфічний рівень доз для будь-якого конкретного пацієнта буде залежати від множини факторів. Такі фактори, пов'язані з пацієнтом, включають вік, масу тіла, загальний стан здоров'я, стать і дієту пацієнта. Інші фактори включають час і шлях введення, швидкість виділення, комбінацію лікарських засобів і тяжкість конкретного захворювання, що піддається терапії. Практично сполуки, представлені формулою І, II і III, або їх фармацевтично прийнятні солі можуть бути сполучені як активні інгредієнти в однорідній суміші з фармацевтичним наповнювачем за традиційними фармацевтичними методиками змішування. Наповнювач може бути в різних формах в залежності від форми препарату, призначеного для введення, наприклад, перорального або парентерального (включаючи внутрішньовенне). Таким чином, фармацевтичні композиції даного винаходу можуть бути представлені у вигляді дискретних одиниць, придатних для перорального введення, таких як капсули, крохмальні облатки або таблетки, кожна з яких містить заздалегідь визначену кількість активного інгредієнта. Крім того, композиції можуть бути представлені у вигляді порошку, гранул, розчину, суспензії у водній рідині, неводній рідині, емульсії масло-в-воді або емульсії вода-в-маслі. У доповнення до вищенаведеного звичайного 16 набору лікарських форм, сполуки, представлені формулою І, II і III, або їх фармацевтично прийнятні солі можуть бути також введені контрольованими засобами вивільнення діючої речовини, і/або пристроями для її вивільнення. Композиції можуть бути приготовані будь-яким з способів фармації. По суті, такі способи включають стадію внесення активного інгредієнта в асоціацію з наповнювачем, який містить один або декілька необхідних інгредієнтів. По суті, композиції готують при постійному і однорідному перемішуванні активного інгредієнта з рідкими наповнювачами або тонко розмеленими твердими наповнювачами або з тими і іншими разом. Продукту потім може бути додана зручна бажана форма. Таким чином, фармацевтичні композиції даного винаходу можуть включати фармацевтично прийнятний наповнювач і сполуку або фармацевтично прийнятну сіль формули І, II або III. Сполуки формули І, II і III або їх фармацевтично прийнятні солі також можуть бути включені в фармацевтичні композиції в комбінації з однією або декількома терапевтично активними сполуками. Застосований фармацевтичний наповнювач може являти собою, наприклад, тверду речовину, рідину або газ. Приклади твердих наповнювачів включають лактозу, гіпс, сахарозу, тальк, желатин, агар, пектин, аравійську камедь, магнію стеарат і стеаринову кислоту. Приклади рідких наповнювачів являють собою цукровий сироп, арахісову олію, оливкову олію і воду. Приклади газоподібних наповнювачів включають діоксид вуглецю і азот. При приготуванні композицій для перорального введення лікарської форми може бути застосована будь-яке зручне фармацевтичне середовище. Наприклад, вода, гліколі, масла, спирти, коригенти, консерванти, барвники і т.п. можуть бути застосовані для утворення рідких препаратів для перорального введення, таких як суспензії, еліксири і розчини; в той час як наповнювачі, такі як крохмалі, цукри, мікрокристалічна целюлоза; розріджувачі, гранулюючі агенти, змащувальні речовини, зв'язуючі речовини і дезінтегруючі агенти можуть бути застосовані для утворення пероральних твердих препаратів, таких як порошки, капсули і таблетки. Внаслідок легкості їх введення, таблетки і капсули є переважним стандартним дозуванням для перорального введення тому використовують тверді фармацевтичні наповнювачі. Необов'язково, але таблетки можуть бути з покриттям, виконаним по стандартних водних і неводних методиках. Таблетка, що містить композицію даного винаходу, може бути приготована компресією або формуванням, необов'язково з одним або декількома додатковими інгредієнтами або ад'ювантами. Пресовані таблетки можуть бути приготовані у відповідній машині пресуванням активного інгредієнта у вільно-текучій формі, такій як порошок або гранули, необов'язково змішаного зі зв'язуючою речовиною, змащувальною 17 81660 речовиною, інертним розріджувачем, поверхневоактивним або диспергуючим засобом. Формовані таблетки можуть бути приготовані у відповідній машині формуванням суміші порошкоподібної сполуки, зволоженої інертним рідким розріджувачем. Кожна таблетка переважно містить приблизно від 0,1мг до приблизно 500мг активного інгредієнта і кожна крохмальна облатка або капсула переважно містить приблизно від 0,1мг до приблизно 500мг активного інгредієнта. Таким чином, таблетка, крохмальна облатка або капсула звичайно містить 0,1мг, 1мг, 5мг, 25мг, 50мг, 100мг, 200мг, 300мг, 400мг або 500мг активного інгредієнта, що приймається у вигляді однієї або двох таблеток, крохмальних облаток або капсул один, два або три рази на добу. Фармацевтичні композиції даного винаходу, придатні для парентерального введення, можуть бути приготовані у вигляді розчинів або суспензій активного інгредієнта у воді. Відповідний сур фактант може бути, наприклад, гідроксипропілцелюлозою. Можуть бути також приготовані дисперсії в гліцерині, рідких поліетиленгліколях і їх сумішах в маслах. Додатково може бути включений консервант для запобігання шкідливому росту мікроорганізмів. Фармацевтичні композиції даного винаходу, придатні для ін'єкцій, включають стерильні водні розчини або дисперсії. Крім того, композиції можуть бути в формі стерильних порошків, приготованих для негайного прийому таких стерильних ін'єктованих розчинів або дисперсій. У всіх випадках кінцева ін'єктована форма повинна бути стерильною і повинна бути ефективно рідкою для легкого введення за допомогою шприца. Фармацевтичні композиції повинні бути стійкими в умовах виробництва і зберігання і, отже, повинні бути законсервовані від заражаючої дії мікроорганізмів, таких як бактерії і грибки. Наповнювач може являти собою розчинник або дисперсійне середовище, що містить, наприклад, воду, етанол, поліол (наприклад, гліцерин, пропіленгліколь і рідкий поліетиленгліколь), рослинні олії і відповідні суміші на їх основі. Фармацевтичні композиції даного винаходу можуть мати форму, придатну для місцевого застосування, таку як, наприклад,, аерозоль, крем, мазь, лосьйон і порошок для розпилення. Крім того, композиції можуть мати форму, придатну для застосування трансдермальними способами. Дані препарати можуть бути приготовані при використанні сполук формули І, II або III або їх фармацевтично прийнятних солей за допомогою звичайних методик. Наприклад, крем або мазь готують змішуванням гідрофільного матеріалу і води разом з приблизно від 5 мас.% до приблизно 10 мас.% сполуки для отримання крему або мазі бажаної консистенції. Фармацевтичні композиції даного винаходу можуть мати форму, придатну для ректального введення, де наповнювач являє собою тверду речовину, наприклад, коли суміш утворює стандартну дозу у вигляді супозиторіїв. Відповідні наповнювачі включають масло какао і інші матеріали, що звичайно застосовуються в даній 18 галузі. Супозиторії можуть бути приготовані спочатку змішуванням композиції з розм'якшеним(и) або розплавленим(и) наповнювачем(ами), потім охолоджуванням і формуванням. У доповнення до вищезазначених інгредієнтівнаповнювачів фармацевтичні препарати, описані вище, можуть включати, якщо доцільно, один або декілька додаткових інгредієнтів-наповнювачів, такі як розріджувачі, буфери, коригенти, зв'язуючі речовини, поверхнево-активні речовини, загусники, змащувальні речовини і консерванти (включаючи антиоксиданти). Крім того, можуть бути включені інші ад'юванти для придания препарату ізотонічності з кров'ю передбачуваного реципієнта. Композиції, що містять сполуку, описану формулою І, II або III, або їх фармацевтично прийнятні солі, також можуть бути приготовані в порошкоподібній або рідкій концентрованій формі. Фармацевтичні композиції даного винаходу призначені для блокування натрієвих каналів. Відповідно, даний винахід відноситься до лікування захворювань у ссавців, інтенсивність яких може знижуватися через блокування нейронних натрієвих каналів, що включають, наприклад, гострий біль, хронічний біль, вісцеральний біль, запальний біль і невропатичний біль, введенням ефективної кількості сполуки даного винаходу. Термін "ссавці" включає людей, а також тварин, таких як, наприклад, собаки, кішки, коні, свині і велика рогата худоба. Відповідно, мається на увазі, що лікування ссавців, відмінних від людей, відноситься до лікування клінічних станів у теплокровних, відмінних від людини, але, які корелюють з вищезгаданими станами. Як використовується в описі для цілей способу згідно з даним винаходом, термін "основа" включає ацетати металів, карбонати металів і третинні аміни. Приклади ацетатів металів включають ацетат калію і ацетат натрію. Приклади карбонатів металів включають карбонат калію і карбонат натрію. Основи третинних амінів включають триалкіламіни, такі як триетиламін. Як указано в описі для цілей способу згідно з даним винаходом, термін "спиртовий розчинник" включає, наприклад, метанол, етанол, ізопропанол і 1-бутанол. Коли в способі згідно з даним винаходом використовується нагрівання, то спосіб може бути здійснений в температурному інтервалі приблизно від 40°С до приблизно 150°С, що включає інтервали приблизно від 50°С до приблизно 140°С, приблизно від 50°С до приблизно 130°С, приблизно від 60°С до приблизно 120°С, приблизно від 65°С до приблизно 100°С, або приблизно від 65°С до приблизно 85°С. Як використовується в описі, термін "розчинник/співрозчинник" включає суміші розчинників, такі як толуол/тетрагідрофуран, тетрагідрофуран/діетиловий ефір, толуол/діетиловий ефір, тетрагідрофуран/метилтрет-бутиловий ефір, толуол/метил-третбутиловий ефір, толуол/діоксан і тетрагідрофуран/діоксан. 19 81660 Скорочення, що використовуються в описі, мають наступні значення (скорочення, не приведені тут, мають загальноприйняті значення, якщо не обумовлено особливо): Ас (ацетил), AIBN (2,2'-азобіс(ізобутиронітрил)), BINAP (1,1’-бі-2нафтол), Вn (бензил), CAMP (циклічний аденозин3',5'-монофосфат), DAST ((діетиламіно)трифторид сірки), DEAD (діетилазодикарбоксилат), DBU (1,8діазабіцикло[5.4.0]ундец-7-ен), DIBAL (діізобутилалюмінійгідрид), DMAP (4(диметиламіно)піридин), DMF (N,Nдиметилформамід), Dppf (1,1’біс(дифенілфосфіно)фероцен), EDCI (1-(3диметиамінопропіл)-З-етилкарбодіімід гідрохлорид), Et3N (триетиламін), GST (глутатіонтрансфераза), HMDS (гексаметилдисилазид), LDA (літійдіізопропіламід), m-CPBA (метахлорпербензойна кислота), ММРР (монопероксифталева кислота), Ms (метансульфоніл; мезил або SO2Me), MsO (метансульфонат або мезилат), NBS (Nбромсукцинімід), NSAID (нестероїдні протизапальні лікарські засоби), о-Тоl (орто-толіл), OXONEo (2KHSO5×KHSO4×K2SO4), PCC (піридиній хлорхромат), Pd2(dba)3 (біс(дибензиліденацетон)паладій(0)), PDC (піридиній дихромат), PDE (фосфодіестераза), Ph (феніл), Phe (бензолдіїл), РМВ (параметоксибензил), Руе (піридиндіїл), r.t. або RT (кімнатна температура), Rac (рацемічний), SAM (аміносульфоніл; сульфонамід або SO2NH2), SEM (2-(триметилсиліл)етоксиметокси), SPA (сцинтиляційний приблизний аналіз), TBAF (тетран-бутиламоній фторид), Th (2- або 3-тієніл), TFA (трифтороцтова кислота), TFAA (ангідрид трифтороцтової кислоти), THF (тетрагідрофуран), Тhi (тіофендіїл), TLC (тонкошарова хроматографія), TMC-CN (триметилсилілціанід), TMSI (триметилсилілйодид), Tz (1H(або 2Н)тетразол-5-іл), XAN TPHOS (4,5-бісдифенілфосфаніл-9,9-диметил-9Н-ксантен), С3Н5 (аліл), Me (метил), Et (етил), n-Рr (нормальний пропіл), і-Pr (ізопропіл), n-Bu (нормальний бутил), i-Butyl (ізобутил), s-Bu (вторинний бутил), t-Bu (третинний бутил), с-Рг (циклопропіл), с-Вu (циклобутил), с-Pen (циклопентил), с-Нех (циклогексил). Наступні аналізи in vitro і in vivo були проведені для оцінки біологічної активності даних сполук. Оцінка сполуки (аналіз in vitro) Ідентифікація інгібіторів натрієвого каналу основана на здатності натрієвих каналів викликати деполяризацію клітини, коли іони натрію проникають через канали, модифіковані агоністом. За відсутності інгібіторів вплив на канал, модифікований агоністом, іонами натрію буде викликати деполяризацію клітини. Інгібітори натрієвих каналів будуть перешкоджати деполяризація клітини, що викликається рухом іонів натрію через натрієві канали, модифіковані агоністом. Зміни в мембранному потенціалі можуть бути визначені за допомогою чутливого до напруження флуоресцентного резонансного перенесення енергії (FRET) красильною парою із 20 застосуванням двох компонентів, де донором служить кумарин (CC 2DMPE) і акцептор оксанол (DiSBAC2(3) ). Оксанол являє собою ліпофільний аніон і розподіляється вздовж мембрани відповідно до мембранного потенціалу. В присутності агоністу натрієвого каналу, але за відсутності натрію, внутрішня частина клітини є негативною по відношенню до зовнішньої частини, оксанол акумулюється на зовнішній частині мембрани і збудження кумарину буде причиною здійснення FRET. Додання натрію викличе деполяризацію мембрани, що приводить до перерозподілу оксанолу на внутрішню частину клітини і, як наслідок, до зменшення FRET. Таким чином, відношення зміни (донор/акцептор) збільшується після мембранної деполяризації. У присутності інгібітору натрієвого каналу деполяризація клітини не буде відбуватися і тому розподіл оксанолу і FRET буде залишатися незмінним. Клітини, стабільно трансфіковані натрієвим каналом підтипу PN1 (HEK-PN1), вирощували в 96-ямкових планшетах, покритих полілізином, при щільності приблизно 140000 клітин/ямка. Середовище аспірували, клітини промивали PBS буфером і інкубували зі 100мкл, що складаються з 10мкМ CC2-DMPE в 0,02% плуронієвій кислоті. Після інкубації при 25°С протягом 45хв. середовище видаляли і клітини промивали 2 рази буфером. Клітини інкубували зі 100мкл DiSBAC 2(3) в ТМА буфері, що містить 20мкМ вератридину, 20нМ бреветоксину-3 і випробуваний зразок. Після інкубації при 25°С протягом 45хв. в темряві планшети вміщували в VIPR апарат і реєстрували флуоресцентну емісію обох компонентів, CC2DMPE і DiSBAC2(3), протягом 10 сек. У цей момент в ямки додавали 100мкл сольового (фізіологічного) буферу для визначення міри залежної від натрію деполяризації клітин і реєстрували флуоресцентну емісію обох фарб додатково протягом 20 сек. Відношення CC2DMPE/DiSBAC 2(3) перед доданням сольового буфера дорівнює 1. За відсутності інгібіторів дане відношення після додання сольового буфера становить >1,5. Коли натрієвий канал повністю інгібований або відомим стандартом, або випробуваною сполукою, то дане відношення залишається таким, що дорівнює 1. Тому можна титрувати активність інгібітору натрієвого каналу моніторингом змін, залежних від концентрації, у флуоресцентному відношенні. Електрофізіологічні аналізи (аналізи in vitro) Приготування клітин: використали власну клітинну лінію НЕК-293, стабільно експресуючу натрієві канали підтипу PN1. Клітини культивували в середовищі для росту MEM (Gibco) з 0,5мг/мл G418, 50 одиниць/мл Pen/Strep і 1мл інактивованої нагріванням фетальної бичачої сироватки при 37°С і в 10% СО2. Для електрофізіологічної реєстрації клітини вміщували на 35мм чашки, покриті полі-D-лізином. Загальна реєстрація клітин: клітини НЕК-293, стабільно експресуючі підтип PN1 натрієвих каналів, досліджували за допомогою повного закріплення клітинного напруження [Hamill, et al. 21 81660 Pfluegers Archives 391:85-100 (1981)] із застосуванням підсилювача ЕРС-9 і імпульсного програмного засобу [Pulse software, HEKA Electronics, Lamprecht, Germany]. Експерименти проводили при кімнатній температурі. Електроди були оплавлені до опору 2-4МW. Помилки напруження були мінімізовані серією компенсаційного опору, і помилковий сигнал електричної ємності був виключений за допомогою ЕРС-9 компонента в електричному ланцюгу. Дані отримували при 50кГц і фільтрували при 7-10кГц. Розчин для промивання складався з 40мм NaCl, 120мм NMDG СІ, 1мм КСl, 2,7мм СаСl2, 0,5мм MgCl2, 10мм NMDG HEPES, рН 7,4, і внутрішній (піпетковий) розчин містив 110мм Csметансульфонату, 5мм NaCl, 20мм CsCl, 10мм CsF, 10мм ВАРТА (тетра Cs сіль), 10мм Cs HEPES, pH 7,4. Наступні протоколи використали для оцінки стійкої спорідненості сполук в спокої і інактивованому стані каналу (Кr і Кi відповідно): 1. 8мс (мілісек.) дослідні імпульси застосовували до деполяризуючих напруг від 60мВ до +50мВ від початкового потенціалу -90мВ для побудови залежності ампераж напруги (IVкриві). Напругу, близьку до піка IV-кривої (звичайно -10 або 0мВ), застосовували як дослдну імпульсну напругу протягом всього залишку експерименту. 2. Криві рівноважної інактивації (здатності) будували вимірюванням амперажу, активованого за рахунок 8мс долідного імпульсу з подальшими 10 сек. імпульсами до потенціалів в інтервалі від 120мВ до -10мВ. 3. Сполуки застосовували при вихідному потенціалі, при якому 20-50% каналів було інактивовано і блокада натрієвих каналів контролювалася протягом 8мс дослідних імпульсів з інтервалом в 2 сек. 4. Після того як встановлювалося рівновага для сполук, визначали залежну від напруги рівноважну інактивацію в присутності сполуки по вищенаведеному протоколу 2. Сполуки, які блокують стан спокою каналу, знижують ампераж, виявлений протягом дослідних імпульсів від всіх вихідних потенціалів, в той час як сполуки, які по суті блокують інактивований стан, переміщують серединну точку кривої рівноважної інактивації. Максимум амперажу при негативних вихідних потенціалах (Іmах) і різницю в серединних точках на кривих рівноважної інактивації (AV) в контролі і в присутності сполуки використали для розрахунку Кr і Ki за наступними рівняннями: [Лікар.зас.] × ІМах ,Лікар .зас. Kr = , ІМах,контроль - ІМах, Лікар. зас . Ki = [Лікар.зас.] -DV . æ [Лікарзас.] ö 1+ ×e k -1 ç ÷ Kr è ø Якщо сполука не впливала на стан спокою, Ki обчислювали за наступним рівнянням: [Лікар.зас.] Ki = -D V e k -1 22 Формаліновий тест на лапі щура (аналіз in vi vo) Сполуки оцінювали по їх здатності інгібувати поведінкову відповідь, викликану 50мкл ін'єкцією формаліну (5%). Металеву смужку фіксували на лівій задній лапі самців щурів Sprague-Dawley (Charles River, 200-250г) і кожного щура утримували з смужкою протягом 60хв. всередині пластмасового циліндра (діаметр 15см). Щурам давали дозу або наповнювача, або випробуваної сполуки перед (локальним) або після (системного) введення формаліну. Для локального введення сполуки приготовляли в етанолі як наповнювачі, PEG400 і фізіологічного розчину (EPEGS) при їх співвідношенні 1:4:5 і вводили шляхом ін'єкції підшкірно в дорсальну поверхню лівої задньої лапи за 5хв. перед формаліном. Для системного введення сполуку приготовляли або в наповнювачі EPEGS, або в наповнювачі Tween 80 (10%)/стерильна вода (90%) і вводили шляхом ін'єкції внутрішньовенно (через латеральну хвостову вену через 15хв. після введення формаліну) або перорально (за 60хв. перед введенням формаліну). Число посмикувань від болю рахували безперервно протягом 60 хв. за допомогою автоматичного аналізатора больової рецепції (UCSD Anesthesiology Research, San Diego, CA). Статистичну значущість визначали шляхом порівняння загального числа посмикувань в ранній (0-10хв.) і пізній (11-60хв.) фазах з непарним t-тестом. Аналіз in vivo з використанням моделі CFA на щурі Одностороннє запалення викликали ін'єкцією 0,2мл повного ад'юванта Фройнда (CFA: Mycobacterium tuberculosis, Sigma; суспендований в емульсії масло/фізіологічний розчин (1:1); 0,5мг Mycobacterium/мл) в плантарну поверхню лівої задньої лапи. Дана доза CFA спричиняла значне розпухання задньої лапи, але тварини виявляли нормальну поведінку з чищенням тіла і приростом у вазі протягом всього експерименту. Механічну гіпералгезію оцінювали через 3 дні після пошкодження тканини за допомогою тесту RandallSelitto. Повторно робили аналіз варіантів (ANOVA), що супроводжувався Dunnet's Post Hoc тестом. SNL: Ме ханічна алодинія (аналіз in vivo) Дотикову алодинію оцінювали з допомогою каліброваних філаментів Фрея, використовуючи ефект підйом-падіння перед і після двох тижнів услід за нервовим пошкодженням. Тварин вміщували в пластмасові клітки з дном з дротяних отворів і дозволяли акліматизуватися протягом 15хв. перед проведенням кожного досліду. Для визначення 50% порога реакції у відповідь застосовували філаменти Фрея (інтервал інтенсивності від 0,4 до 28,8г) до середньоплантарної поверхні протягом 8 сек. або доти, поки не відбувалася реакція абстиненції. Після позитивної відповіді оцінювали значно більш слабий подразник. Якщо не виникала відповідь на подразник, то брали набагато більш сильний подразник. Після початкового порогового переходу процедуру повторювали для представлення чотирьох подразників на одну тварина на 23 81660 проведення досліду. Механічну чутливість оцінювали 1 і 2 години після перорального введення випробуваної сполуки. Сполуки, описані в даному винаході, виявляють активність по блокуванню натрієвих каналів в концентраціях від приблизно менших, ніж 0,05мкМ, до приблизно менших, ніж 50мкМ в дослідах in vitro, приведених вище. Перевага полягає в тому, що дані сполуки виявляють активність по блокуванню натрієвих каналів в концентраціях, менших, ніж приблизно 5мкМ, в аналізах in vitro. Більша перевага полягає в тому, що дані сполуки виявляють активність по блокуванню натрієвих каналів в концентраціях, менших, ніж приблизно 1мкМ, в аналізах in vitro. Ще більша перевага полягає в тому, що дані сполуки виявляють активність по блокуванню натрієвих каналів в концентраціях, менших, ніж приблизно 0,1мкМ, в аналізах in vitro. Найбльша перевага полягає в тому, що дані сполуки виявляють активність по блокуванню натрієвих каналів в концентраціях, менших, ніж приблизно 0,05мкМ, в аналізах in vitro. Дані сполуки можуть бути приготовані відповідно до загальних схем, представленим нижче, а також відповідно до методик, приведених в прикладах. Наступні схеми і приклади додатково розкривають, але не обмежують об'єм винаходу. Якщо не обумовлено особливо, то експериментальні процедури виконували при наступних умовах. Всі операції проводили при кімнатній температурі або при температурі навколишнього середовища; тобто в інтервалі температур 18-25°С. Випаровування розчинника проводили за допомогою роторного випарника при зниженому тиску (600-4000 паскалів; 4,5-30мм Hg) з температурою бані аж до 60°С. Хід реакції супроводжували тонкошаровою хроматографією (TLC, ТШХ) і часи протікання реакції дані тільки для ілюстрації. Температури плавлення є некоректованими і "d" означає розкладання. Дані температури плавлення являють собою температури плавлення, отримані для матеріалів, приготованих, як описано. Поліморфізм в деяких приготуваннях може бути результатом виділення матеріалів з різними температурами плавлення. Структуру і чистоту всі х цільових продуктів підтверджували, щонайменше, одним з наступних методів: ТШХ (TLC), мас-спектрометрією, спектрометрією ядерного магнітного резонансу (ЯМР (N MR)) або мікроаналітичними даними. Якщо приведені виходи, то вони являють собою тільки ілюстрацію. Дані ЯМР, якщо вони приведені, представлені у вигляді (d) величин для більшості протонів, що діагностуються з розмірністю в частинах на мільйон (ррт) відносно тетраметилсилану (TMS), як внутрішнього стандарту, визначених при 300МГц, 400МГц або 500МГц із застосуванням вказаного розчинника. Звичайні скорочення, застосовані для конфігурації сигналів, являють собою: s. синглет; d. дуплет; t. триплет; т. мультиплет; br. уширення; і т.д. Додатково, "Аr" означає ароматичний сигнал. Хімічні символи мають їх звичайні значення; застосовані наступні скорочення: v (об'єм), w 24 (маса), b.р. (температура кипіння), m.р. (температура плавлення), 1 (літр(и)), ml (мілілітри), g (грам(и)), mg (міліграм(и)), mol (молі), mmol (мілімолі), eq (еквівалент(и)). Способи синтезу Сполуки даного винаходу можуть бути приготовані відповідно до загальних схем, представлених нижче, а також відповідно до методик, приведених в прикладах. Замісники є тими ж самими, що і у вищенаведених формулах, за винятком випадків, де вони визначені інакше або в іншому відношенні очевидні для звичайних фа хівців-препараторів. Нові сполуки даного винаходу можуть бути легко синтезовані за допомогою методик, відомих фа хівцям в даній галузі, таких як, наприклад, описані в Advanced Organic Chemistry, March, 4th Ed., John Wiley and Sons, New York, NY, 1992; Ad vanced Organic Chemistry, Carey and Sundberg, Vol. A and B, 3rd Ed., Plenum Press, Inc., New York, NY, 1990; Protective groups in Organic Synthesis, Green and Wuts, 2nd Ed., John Wiley and Sons, New York, NY, 1991; Comprehensive Organic Transformations, Larock, VCH Publishers, Inc., New York, NY, 1988; Handbook of Heterocyclic Chemistry, Katritzky and Pozharskii, 2 nd Ed., Pergamon, New York, N Y, 2000, і у виносках, цитованих в них. Вихідні матеріали для даних сполук можуть бути приготовані при застосуванні стандартних синтетичних перетворень хімічних попередників, які є легко доступними від комерційних джерел, що включають Aldrich Chemical Co. (Milwaukee, WI); Sigma Chemical Co. (St. Louis, MO); Lancaster Synthesis (Windham, N.H.); Ryan Scientific (Columbia, S.C.; Ma ybridge (Cornwall, UK); Matrix Scientific (Columbia, S.C.; Arcos, (Pittsburgh, PA) and Trans World Chemicals (Rockville, MD). Методики, описані в описі для синтезу сполук, можуть включати одну або декілька стадій по маніпуляціях із захисною групою або по очищенню, такі як перекристалізація, перегонка, колонкова хроматографія, флеш-хроматографія, тонкошарова хроматографія (ТШХ, TLC) і високоефективна рідинна хроматографія (ВЕРХ, HPLC). Продукти можуть бути охарактеризовані із застосуванням різних методів, добре відомих в галузі хімії, що включають протонний і вуглець-13 ядерний магнітний резонанс (1Н і 13С ЯМР), інфрачервону і ультрафіолетову спектроскопію (ІЧ і УФ), рентгенівську кристалографію, елементний аналіз і ВЕРХ і мас-спектрометрію (РХ-МС). Способи зняття захисної групи, очищення, ідентифікації структури і визначення кількості добре відомі кожному фахівцеві в галузі хімічного синтезу. Мається на увазі, що функціональні групи, присутні в сполуках, представлених на схемах нижче, можуть бути далі перетворені, коли доцільно, за допомогою стандартних методик перетворення функціональних груп, доступних для фа хівців в даній галузі, для отримання цільових сполук, описаних в даному винаході. Інші зміни або модифікації, які будуть очевидними для фахівців в даній галузі, охоплюються об'ємом і прописами даного 25 81660 26 винаходу. Даний винахід не треба обмежувати, крім тих випадків, які викладаються в наступній формулі винаходу. В одному з протоколів 3-бромбензойну кислоту 1 вводять у взаємодію з третбутилкарбазатом активуванням за допомогою HOBt (гідроксибензотриазол) в присутності відповідного карбодііміду, такого як EDC [1-(3диметиламінопропіл)-3-етилкарбодіімід], і діізопропілетиламіну (DIEA)) в дихлорметані або ТГФ для отримання захищеного гідразиду 2. Існує ряд інших придатних способів активування карбонових кислот для взаємодії [див. March J. "Ad vanced Organic Chemistry", 5 th ed., John Wiley & Sons, New York, pp. 506-512 (2001)]. Сполука 2 може бути перетворена в цілий ряд несиметричних біфенільних проміжних продуктів 3 за допомогою різних зв'язуючи х взаємодій. Одна з них являє собою реакцію Сузуки, де бром, йод або трифлат похідне 2 піддають взаємодії з арилбороновою кислотою в присутності паладієвого каталізатора, такого як ацетат паладію, з трифенілфосфіном і водним карбонатом натрію в розчиннику, такому як толуол, і співрозчиннику, такому як н-пропанол [див. Suzuki, et al. Chem. Rev., 95, 2457, 1995]. Різні арилборонові кислоти комерційно доступні або можуть бути приготовані зручно з відповідного арилброміду або йодиду перетворенням його в органолітіеве похідне [Baldwin, J.E., et al. Tetrahedron Lett. 39, 707-710 (1998)] або реактиву Гріньяра з подальшою обробкою триалкілборатом [Li, J.J. et al. J. Med. Chem., 38: 4570-4578 (1995) and Piettre, S.R., et al. J. Med. Chem., 40: 4208-4221 (1997)]. Арилборонати можуть бути також застосовані як альтернатива арилбороновим кислотам в цих зв'язуючих взаємодіях, каталізованих Pd [Giroux, A., et al., Tetrahedron Lett., 38, 3841 (1997)]. Боронати можуть бути легко приготовані з арилбромідів, йодидів і трифторметансульфонатів за способом, описаним Murata, М., et al. [J. Org. Chem. 65: 164-168 (2000)]. Вос-захисну гр упу сполуки 3 видаляють в стандартних умовах - трифтороцтова кислота в дихлорметані - що приводить до TFA солі гідразиду 4, який може бути знесолювати водним розчином NaOH. На схемі 2 представлений спосіб приготування похідних 5-біфеніл-3-заміщеного-1,2,4-триазолу, де заміщення може являти собою залишки ефірів, кислот, амідів і т.д. [Catarzi, et al. J. Med. Chem., 38, 2196-2201, 1995]. Взаємодія гідразиду 4 з тетрафторборатом карбетокси-Sметилтіоформімідію і триетиламіном в дихлорметані дає оксамідразонат 7, який циклізується в триазоловий ефір 8. Реагент карбетокси-3-метилтиоформімідій тетрафторборату отримували взаємодією етил-2тіооксамату з триметилоксоній тетрафторборатом [див. Catarzi, et al., вище] в дихлорметані. Ефір 8 може бути перетворений в амід нагріванням його з відповідним аміном, в цьому випадку з аміаком, в розчиннику, такому як метанол. Ефір 8 може бути підданий гідролізу до відповідної кислоти в стандартних умовах, і кислота, що утворилася, може бути перетворена в амід в різних умовах, таких, як описано на схемі 1. Крім того, ефір 8 може бути відновлений до первинного спирту, наприклад, борогідридом натрію (NaBH4) для отримання сполук формули (І), де R1 являє собою гідроксиметил. Альтернативно, ефір 8 може бути перетворений у вторинний спирт взаємодією із сумішшю борогідриду літію і реактиву Грін'яра в апротонному розчиннику, такому як ТГФ. Такий первинний або вторинний спирт, отриманий з ефіру 8, може бути потім перетворений в похідне за допомогою ряду способів, що включають окислення до кетону окислювальним реагентом, таким як хромвмісний реагент. Такий спирт може бути також перетворений у фторпохідне, наприклад, взаємодією діетиламінотрифториду сірки (DAST) в дихлорметані при знижених температурах. 27 81660 28 допомогою способів, представлених на схемах 13. У варіанті протоколів, описаних вище на схемах 1, 3 і 4, анілін 26, який захищений Восгрупою і містить групу боронової кислоти або боронатного ефіру, і арилбромід, йодид або трифлат перетворювали в ряд несиметричних біфенільних проміжних продуктів 23, як представлено на схемі 1. На схемі 3 описаний спосіб приготування незаміщеної 3-триазолової циклічної системи [Lin, et al., J. Org. Chem., 44(23), 4160-4165, 1979]. Етил-3-бромбензоат 10 піддають взаємодії з арилбороновою кислотою, як описано на схемі 1, для отримання біфенільного ефіру 11. Ефір 11 забезпечує попереднє утворення біфенільного проміжного продукту, який потім може бути перетворений в сполуку 4 або родинні похідні, як описано на більш ранніх схемах 1-2. По схемі З ефір 11 перетворюють в амід 12 в стандартних умовах. Зокрема, ефір 11 гідролізують у відповідну кислоту, яку потім активують карбонілдіімідазолом (CDI) в ДМФА (D MF) з подальшим доданням аміаку у ви гляді ацетату амонію, отримуючи амід 12. Амід 12 нагрівають в диметилацеталі диметилформаміду, отримуючи проміжний продукт 13, який при нагріванні з гідразином в оцтовій кислоті дає триазол 14. У протоколі для приготування похідних 1біфеніл-3-заміщеного-1,2,4-триазолу, вихідний броманілін 22, де аміногрупа захищена за допомогою Вос-групи, і арилборонову кислоту перетворюють в ряд несиметричних біфенільних проміжних продуктів 23, як представлено на схемі 1. Вос-захисну групу сполуки 23 видаляють, як описано раніше, і перетворюють в її діазонієву сіль 24 стандартною взаємодією з нітритом натрію і НСl у воді. Додавання сполуки 24 до суміші метилізоціаноацетату і ацетату натрію в метанолі і воді приводить до триазолового ефіру 25. Ключова проміжна сполука 25 потім може бути перетворена в ряд корисних похідних за Відповідно до схеми 6, 31 і 32 можуть бути перетворені в біфенільний проміжний продукт 33, наприклад, по реакції Suzuki-Miyaura із застосуванням каталітичної системи ацетат паладію/трифенілфосфін. Біфенільний проміжний продукт 33 може бути перетворений в НСl сіль імідату 34 в стандартних умовах Пінера, наприклад, за допомогою концентрованого розчину хлористоводневої кислоти в етанолі. Імідат 34 може бути перетворений в триазол 37 підлуговуванням із застосуванням біфазної суміші, такої як ЕtOАс і NaOH, через отримання етилімідату 35 з подальшою обробкою гідразидом оксамінової кислоти 36, спиртовим розчинником, таким як етанол, і будь-якою відповідною основою, однією з багатьох, включаючи ацетат металу, таких як ацетат калію, третинний амін або карбонат металу, при нагріванні. У варіанті до схеми 6, проміжний продукт 34 перетворюють в триазол 37 прямим додаванням гідразиду оксамінової кислоти 36, спиртового розчинника, такого як етанол, і будь-якої відповідної основи, однієї з багатьох, включаючи ацетат металу, таких як ацетат калію, третинний амін або карбонат металу, при нагріванні. Відповідно до схеми 8, сполуки формул (І) або (II), де R2 являє собою Н, 38, можуть бути 29 81660 перетворені депротонізацією за допомогою основи алкоксиду металу, такого як трет-бутоксид калію або трет-бутоксид натрію, у відповідній суміші розчинник/співрозчинник в сіль 39. ПРИКЛАД 1 3-[3-(2-Трифторметоксифеніл)феніл]-1,2,4триазол Стадія А: 2-Трифторметоксифенілбороновая кислота До розчину 2г (9,5 ммоль) і-бром-2трифторметоксибензолу, що перемішується в 28мл тетрагідрофурану (THF, ТГФ), при -78°С обережно додавали 5,9мл 1,7М розчину третбутиллітію в гексані (9,5 ммоль). Реакційну суміш перемішували 45хв. при -78°С. До реакційної суміші при -78°С додавали 2,58мл (11,1 ммоль) триізопропілборату і дану суміш повільно нагрівали при кімнатній температурі (RT) протягом 16 годин. Реакційну суміш розбавляли водою і обробляли 2N NaOH до лужної реакції. Реакційну суміш промивали ЕtOАс. Водну фракцію підкисляли розчином 2N НСl і перемішували 1 годину при RT. Реакційну суміш екстрагували EtOAc і органічні фракції промивали водою, насиченим розчином NaCl (розсолом), сушили над Na2SO4 і фільтр ували. Фільтрат концентрували, отримуючи вказану в заголовку сполуку у виглядібілої твердої речовини. 1Н ЯМР(СDСl3) (d, м.д.): 7,96 (дд, J=7,2, 1,6Гц, 1H), 7,53 (ддд, J=9,1, 7,3, 1,8Гц, 1H), 7,38 (тд, J=7,3, 0,7Гц, 1Н), 7,28 (д, J=8,2Гц, 1Н), 5,25 (уш.с, 2Н), МС (М+Н): 206,9. Стадія В: Етил-3-(2трифторметоксифеніл)бензоат До розчину 0,94г (4,58 ммоль) етил-3бромбензоату в 14,5мл толуолу при RT додавали 0,25г (0,218 ммоль) тетракіс(трифенілфосфін)паладію(0), 0,94г (4,58 ммоль) 2-трифторметоксифенілборонової кислоти, 2,22мл (4,45 ммоль) водного 2М розчину карбонату натрію і 7мл етанолу. Реакційну суміш нагрівали із зворотним холодильником протягом 18 годин. Реакційну суміш охолоджували і розбавляли етилацетатом і водою. Органічну фракцію відділяли і промивали насиченим розчином NaCl (розсолом), сушили над MgSO4, фільтрували і фільтрат концентрували до отримання масла, яке очищали хроматографією (двоокис кремнію, 1%, 5%, 30% послідовно етилацетат:гексани), отримуючи вказану в заголовку сполуку. 1H ЯМР (CD3OD) (d, м.д.): 8,02 (с, 1H), 7,97 (дд, J=7,8, 1,2Гц, 1Н), 7,60 (дд, J=7,7, 1,3Гц, 1Н), 7,50-7,33 (м, 5Н), 4,31 (кв, 2Н), 1,31 (т, 3Н). Мас-спектр (ESI) m/e (M+1): 311,2. Стадія С: 3-(2Трифторметоксифеніл)бензойна кислота Розчин 0,3г (4,19 ммоль) етил-3-(2трифторметоксифеніл)бензоату і 8,3мл (8,3 30 ммоль) 1N розчину NaOH в 12,5мл метанолу перемішували 18 годин при RT. Реакційну суміш концентрували і доводили до рН=2 за допомогою 1N розчину НСl. Суміш екстрагували етилацетатом (EtOAc) і органічну фракцію сушили над MgSO4 , фільтрували і фільтрат концентрували, отримуючи вказану в заголовку сполуку у вигляді білої твердої речовини, яку використали без додаткового очищення. Стадія D: 3-(2-Трифторметоксифеніл)бензамід До розчину 0,94г (3,36 ммоль) 3-(2трифторметоксифеніл)бензойної кислоти в 17мл ДМФА (D MF) додавали 0,55г (3,36 ммоль) карбонілдіімідазолу (CDI) і реакційну суміш перемішували при RT 4 години. До реакційної суміші додавали 2,6г (33,6 ммоль) ацетату амонію і суміш перемішували протягом ночі при RT. Реакційну суміш розподіляли між етилацетом і водою і органічну фракцію промивали насиченим сольовим розчином, сушили над MgSO4, фільтрували і фільтрат концентрували. Залишок очищали хроматографією (двоокис кремнію, 30%, 50% послідовно ЕtOАс:гексани), отримуючи вказану в заголовку сполуку. Мас-спектр (ESI) m/e (M+1): 282,2. Стадія Е: 3-[3-(2Трифторметоксифеніл)феніл]-1,2,4-триазол Розчин 0,137г (0,48 ммоль) 3-(2трифторметоксифеніл)бензаміду в 1мл диметилацеталю N,N-диметилформаміду нагрівали 2 години при 120°С, одночасно реакційну суміш концентрували у вакуумі. До даного продукту в 2,3мл оцтової кислоти додавали 0,028г (0,55 ммоль) гідразингідрату і реакційну суміш нагрівали 2 години при 90°С. Потім реакційну суміш концентрували і розподіляли між EtOAc і насиченим розчином NaHCO3. Органічну фракцію промивали насиченим сольовим розчином, сушили над MgSO4, фільтрували і фільтрат концентрували. Залишок очищали хроматографією (двоокис кремнію, 30:1, 9:1, 3:1 послідовно СН2Сl2:ацетон), отримуючи вказану в заголовку сполуку. 1Н ЯМР (CD3OD) (d, м.д.): 8,32 (с, 1Н), 8,06 (с, 1H), 7,98 (м, 1Н), 7,50 (м, 3Н), 7,39 (м, 3Н). Мас-спектр (ESI) m/e (M+1): 306,1. ПРИКЛАД 2 3-[3-(2-(2,2,2-Трифторетоксифеніл)феніл]1,2,4-триазол Стадія А: 2-(2,2,2-Трифторетокси)фенілбромід Розчин 0,35г (2 ммоль) 2-бромфенолу, 0,63г (3 ммоль) 2,2,2-трифторетилйодиду, 0,55г (4 ммоль) карбонату калію в 2мл ДМФА піддавали взаємодії при 150°С в мікрохвильовій системі (Personal Chemistry, Smithcreator) 30хв. Після охолоджування до RT реакційну суміш розбавляли водою і екстрагували етилацетатом. Органічну фракцію сушили над MgSO4, фільтрували і фільтрат концентрували. Залишок очищали хроматографією (5%, 10% послідовно 31 81660 ЕtOАс:гексани), отримуючи вказану в заголовку сполуку. Стадія В: Етил 3-(2-(2,2.2трифторетоксифеніл)бензоат До розчину 2,5г (9,8 ммоль) 2трифторетоксифенілброміду в 33мл толуолу при RT додавали 0,57г (0,49 ммоль) тетракіс(трифенілфосфін)паладії(0), 0,2г (10,3 ммоль) 3-етоксикарбонілфенілборонової кислоти, 5,9мл (11,8 ммоль) 2М водного розчину карбонату натрію і 17мл етанолу. Реакційну суміш нагрівали із зворотним холодильником протягом 18 годин. Реакційну суміш о холоджували і розбавляли етилацетатом і водою. Органічну фракцію відділяли і промивали насиченим розчином NaCl (розсолом), сушили над MgSO 4, фільтрували і фільтрат концентрували до отримання масла, яке очищували хроматографією (двоокис кремнію, 1%, 5%, 30% послідовно етилацетат:гексани), отримуючи вказану в заголовку сполуку. Масспектр (ESI) m/e (M+1): 325,1. Стадія С: 3[3-(2-(2,2,2Трифторетоксифеніл)феніл]-1,2,4-триазол Вказана в заголовку сполука може бути приготована за допомогою процедур, аналогічних процедурам, описаним в прикладі 1, стадії С-Е. ПРИКЛАД 3 3-[3-((2-(2,2,2-Трифторетокси)феніл)-(4фтор)феніл]-1,2,4-триазол Мас-спектр (ESI) m/e (M+1): 338,0. Стадія А: Метил 3-((2-гідрокси)феніл)-4фторбензоат До розчину 2г (8,45 ммоль) метил-3-бром-4фторбензоату в 28мл толуолу при RT додавали 0,49г (0,42 ммоль) тетракіс(трифенілфосфін)паладій(0), 1,95г (8,9 ммоль) 2-(4,4,5,5-тетраметил-1,3,2-діоксаборолан2-іл)фенолу, 5,1мл (10,15 ммоль) 2М водного розчину карбонату натрію і 14 мл н-пропанолу. Реакційну суміш нагрівали із зворотним холодильником протягом 18 годин. Реакційну суміш охолоджували і розбавляли етилацетатом і водою. Органічну фракцію відділяли і промивали насиченим розчином NaCl (розсолом), сушили над MgSO4 , фільтрували і фільтрат концентрували до масла, яке очищали хроматографією (двоокис кремнію, 90:1, 30:1 послідовно СН 2СІ2:ацетон), отримуючи вказану в заголовку сполуку. Масспектр (ESI) m/e (M+1): 247,0. Стадія В: Метил 3-((2-(2.2.2трифторетокси)феніл)-4-фторбензоат Суміш 1,7г (7,1 ммоль) метил 3-((2гідрокси)феніл)-4-фторбензоату, 2,46г (10,6 ммоль) 2,2,2-трифторетил трифторметансульфонату і 3,45г (10,6 ммоль) карбонату цезію в 35мл ДМФА перемішували 18 годин при 60°С. Охолоджену реакційну суміш 32 розподіляли між ЕtOАс і водою. Водний шар екстрагували EtOAc і об'єднані органічні фракції промивали водою, насиченим розчином NaCl, сушили над MgSO4 і фільтрували. Фільтрат концентрували і очищали хроматографією (двоокис кремнію, 5%, 30% послідовно ЕtOАс:гексани), отримуючи вказану в заголовку сполуку. Мас-спектр (ESI) m/e (M+1): 329,0. Стадія С: 3-[3-((2-(2,2,2Трифторетокси)феніл)-(4-фтор)феніл 3-1,2,4триазол Вказана в заголовку сполука може бути приготована за допомогою процедур, аналогічних процедурам, описаним в прикладі 1, стадії С-Е. ПРИКЛАД 4 5-Метил-3-[3-((2трифторметокси)феніл)феніл]-1,2,4-триазол Стадія А: 3-Бромфенілкарбоніл-(N-третбутоксикарбонил)гідразид Розчин 1г (4,97 ммоль) 3-бромбензойної кислоти, 0,59г (4,52 ммоль) трет-бутилкарбазату, 0,95г (4,97 ммоль) EDC [1-(3диметиламінопропіл)3-етилкарбодіімід), 0,67г (4,97 ммоль) гідроксибензотриазолу (НОВt) і 3,15мл (18,1 ммоль) діізопропілетиламіну в 23мл СН2СІ2 перемішували 18 год. при RT. Реакційну суміш розбавляли СН2Сl2 і промивали 1N розчином НСl, насиченим розчином NaHCO3 і насиченим розчином NaCl. Розчин сушили над MgSO4, фільтрували і фільтрат концентрували. Залишок очищали хроматографією (двоокис кремнію, 30:1, 9:1, 3:1 послідовно СН2Сl2:ацетон), отримуючи вказану в заголовку сполуку. Мас-спектр (ESI) m/e CM): 314,0 (М+2): 316,0. Стадія В: 3-((2Трифторметокси)феніл)фенілгідразид Розчин 0,22г (1,07 ммоль) 2трифторметоксифенілборонової кислоти і 0,32г (1,02 ммоль) 3-бромфенілкарбоніл-N-третбутоксикарбонілгідразиду в 5мл толуолу і 2,5мл нпропанолу перемішували 30хв. До реакційної суміші додавали 0,0007г (0,003 ммоль) ацетату паладію, 0,0024г (0,009 ммоль) трифенілфосфіну і 0,61мл (1,2 ммоль) 2М водного розчину карбонату натрію і суміш нагрівали із зворотним холодильником протягом 18 годин. Реакційну суміш охолоджували і розбавляли EtOAc і водою. Органічну фракцію сушили над Mg2SO4, фільтрували і фільтрат концентрували. Залишок очищали хроматографією (двоокис кремнію, 30:1, 9:1 послідовно, СН2Сl2:ацетон), отримуючи захищений гідразид, який потім розчиняли в суміші 2,1мл TFA і 2,1мл СН2Сl2. Реакційну суміш перемішували 2 год., після чого її концентрували, розчиняли в СН2Сl2 і промивали 1N розчином NaOH. Органічну фракцію сушили над Mg2SO4, фільтрували і фільтрат концентрували, отримуючи вказану в заголовку сполуку у вигляді білої твердої речовини. Мас-спектр (ESI) m/e (M+1): 297,1. 33 81660 Стадія С: 5-3-[3-((2трифторметокси)феніл)феніл]-1,2,4-триазол До розчину 0,093г (0,98 ммоль) гідрохлориду ацетамідину в 1,1мл етанолу додавали 0,22мл (0,98 ммоль) 25% розчину метилату натрію в метанолі і реакційну суміш перемішували 30хв., після чого її фільтрували. До фільтрату додавали 0,19г (0,66 ммоль) 3-((2трифторметокси)феніл)фенілгідразиду і реакційну суміш перемішували протягом ночі. Реакційну суміш концентрували і очищали хроматографією (двоокис кремнію, 3%, 10%, 30% послідовно, метанол:СН 2Сl2), отримуючи білу тверду речовину. Білу тверду речовину нагрівали (обережно) при його температурі плавлення 30хв. Реакційну суміш охолоджували до RT, розчиняли в СН 2Сl2 і концентрували. Залишок очищали хроматографією (двоокис кремнію, 3%, 10%, послідовно, метанол:СН2Сl2), отримуючи вказану в заголовку сполуку у вигляді білої твердої речовини. 1H ЯМР (CD3OD) (d, м.д.): 8,00 (с, 1Н), 7,93 (м, 1H), 7,49-7,34 (м, 6H), 2,41 (с, 3Н). Масспектр (ESI) m/e (M+1): 320,5. ПРИКЛАД 5 3-[3-((2-Трифторметокси)феніл)феніл]-1,2,4триазол-5-карбоксамід Стадія А: Етил N1-3-(22 трифторметокси)бензоїл-N -оксамідразонат До розчину 0,45г (1,54 ммоль) 3-(2трифторметоксифеніл)фенілгідразиду (приклад 4, стадія В) в 20мл СН 2Сl2 додавали 0,54г (2,3 ммоль) тетрафторборату карбетокси-Sметилтіоформімідію і 0,43мл (3,08 ммоль) триетиламіну і реакційну суміш нагрівали із зворотним холодильником при перемішуванні 4 години. Реакційну суміш охолоджували до RT, промивали водою, сушили над Na2SO4, фільтрували і фільтрат концентрували до затвердіння. Додавали два мл СН 2Сl2 і твердий продукт, що утворився, виділяли фільтруванням. Мас-спектр (ESI) m/e (М+1): 396,1. Стадія В: Етил 3-[3-((2трифторметокси)феніл)феніл]-1,2,4-триазол-5карбоксилат Твердий етил N1-3-(2трифторметокси)бензоїл-N2-оксамідразонат зі стадії А (0,25г, 0,616 ммоль) нагрівали на масляній бані при температурі вище його температури плавлення 20хв. Після охолоджування до RT залишок розчиняли в СН2Сl2 і концентрували, отримуючи жовту тверду речовину. Її очищали хроматографією (двоокис кремнію, 10%, 30%, 50% послідовно ЕtOАс: гексани), отримуючи білу тверду речовину. Мас-спектр (ESI) m/e (M+1): 378,1. Стадія С: 3-[3-((2трифторметокси)феніл)феніл]-1,2,4триазол-5карбоксамід 34 Розчин 0,13г (0,34 ммоль) етил 3-[3-((2трифторметокси)феніл)феніл]-1,2,4-триазол-5карбоксилату (зі стадії В) в 2мл метанолу в пробірці насичували аміаком. Пробірку герметизували і реакційну суміш нагрівали при 60°С протягом ночі. Реакційну суміш потім концентрували і залишок очищали хроматографією (двоокис кремнію, 3%, 10%, 20% послідовно, метанол:СН2Сl2), отримуючи вказану в заголовку сполуку. 1Н ЯМР (CD3OD) (d, м.д.): 8,10 (с, 1Н), 8,02 (м, 1H), 7,54-7,36 (м, 6Н). Мас-спектр (ESI) m/e (M+1): 349,2. ПРИКЛАД 6 3-[3-((2-(2,2,2-Трифторетокси)феніл)-4фтор феніл]-1,2,4-триазол-5-карбоксамід Стадія А: 3-((2-(2,2,2-Трифторетокси)феніл)-4фторбензойна кислота До розчину 0,75г (2,29 ммоль) метил 3-(2(2,2,2-трифторетокси)феніл)-4-фторбензоату (приклад 3, стадія В) в 11,5мл суміші ТГФ:вода 3:1 додавали 0,164г (6,86 ммоль) LiOH і реакційну суміш перемішували 18 годин при RT. Реакційну суміш концентрували і доводили до рН=2 за допомогою 1N розчину НСl. Суміш екстрагували EtOAc і об'єднані органічні фракції промивали насиченим розчином NaCl, сушили над MgSO4, фільтрували і фільтрат концентрували, отримуючи вказану в заголовку сполуку, яку використали без додаткового очищення. Стадія В: 3-[3-((2-(2,2,2-Трифторетокси)феніл)4-фторфеніл]-1,2,4-триазол-5-карбоксамід Вказану в заголовку сполук у отримували з 3((2-трифторетокси)феніл)-4-фторбензойної кислоти відповідно до методик, описаних в прикладі 4, стадії А і В, і прикладі 4. 1H ЯМР (CD3OD) (d, м.д.): 8,02 (м, 2Н), 7,99 (м, 1H), 7,39 (м, 1Н), 7,30 (м, 1Н), 7,16 (м, 2Н), 4,45 (kb, J=8,5Гц, 2Н). Мас-спектр (ESI) m/e (M+1): 381,0. Наступні приклади 7-10 виконували відповідно до методик, описаних в прикладах 5 і 6. ПРИКЛАД 11 35 81660 3[3-((2-Трифторметокси)феніл)-(4фтор)феніл]-1,2,4-триазол-5-карбоксамід Мас-спектр (ESI) m/e (M+1): 367,0. Стадія А: Приготування 4-фтор-3-(2трифторметоксифеніл)бензонітрилу З-Бром-4-фторбензонітрил (1,0 еквівалент), 2(трифторметокси) бензолборонову кислоту (1,25 еквіваленти), ацетат паладію (0,005 еквіваленти) і трифенілфосфін (0,01 еквіваленти) послідовно завантажували в колбу з декількома отворами. Після продуття колби азотом, додавали толуол (5мл/г 3-бром-4-фторбензонітрилу) і суспензію, що утворилася, перемішували, барботуючи азот углиб реакційної суміші приблизно 20 хвилин. В окремій колбі готували водний розчин фосфату калію розчиненням твердого фосфату калію (2,0 еквівалент) у воді (2мл/г фосфату калію). Отриманий розчин дезоксигенували барботуванням азоту углиб реакційної суміші при перемішуванні приблизно 30 хвилин. Водний розчин фосфату калію додавали до толуольної суспензії і реакційну суміш нагрівали при 60-65°С з паровим обігрівом. Хід реакції контролювали ВЕРХ і температуру реакційної суміші підтримували в інтервалі 63-69°С. Коли 3-бром-4-фторбензонітрил був витрачений, нагрівання припиняли і реакційну суміш охолоджували до RT на крижаній бані. Водний шар сифонували з посудини і додавали в реакційну посудину Ecosorb С-941 (0,5г/г 3-бром-4фторбензонітрилу, комерційно доступний від Graver Technologies, Глазго, Делавер). Чорну суспензію, що утворилася, перемішували при RT 15 годин. Вугілля видаляли фільтруванням суспензії через рихлий шар солкафлок на фільтрувальному тиглі. Осад на фільтрі промивали толуолом (4мл/г 3-бром-4фторбензонітрилу). Об'єднані фільтрати дозовано концентрували (40-50°С) до отримання біарилнітрильного продукту у вигляді густого яснооранжевого масла (вихід 94%). Стадія В: Приготування: Абсолютний етанол (1,8мл/г біарилнітрилу) вміщували в круглодонну колбу. Етанол, що перемішується, охолоджували на бані лід/ацетон і барботували углиб розчину газоподібний хлористий водень, при цьому внутрішню температуру підтримували менше 20°С. Додавання НСl контролювали титруванням протону за допомогою Metrohm 808 Titrando (комерційно доступний від Metrohm Ltd.) для визначення концентрації НСl в розчині етанолу. Додавання припиняли після того, як концентрація НСl досягала 38% (7,5 еквівалентів). Біарилнітрил 36 зі стадії А (1,0 еквівалент) додавали у вигляді нерозбавленого масла до охолодженого етанольного розчину НСl і реакційному розчину дозволяли нагріватися до RT при перемішуванні протягом ночі (>15 годин). Реакцію вважали завершеною, коли аналіз ВЕРХ не показував присутності початкового біарилнітрилу. Отриману реакційну суміш потім розбавляли толуолом (8мл/г біарилнітрилу). Для того, щоб викликати кристалізацію, завантаження розчинників перемикали на толуол спільною перегонкою з етанолом (
ДивитисяДодаткова інформація
Назва патенту англійськоюBiaryl substituted triazoles as sodium channel blockers
Автори англійськоюChakravarty Prasun K., Fisher Michael H., Palucki Brenda, Park Min K., Parsons William H., Zhou Bishan, Carey James P., Frantz Douglas E., Kress Michael H., Weaver Damian
Назва патенту російськоюБиарилзамещённые триазолы как блокираторы натриевых каналов
Автори російськоюЧакраварти Прасун К., Фишер Майкл Х., Палуки Бренда, Парк Мин К., Парсонз Уильям Х., Чжоу Бишань, Кери Джеймс П., Франц Дуглас Э., Кресс Майкл Х., Уивер Деймиан
МПК / Мітки
МПК: A61P 25/00, C07D 249/10, C07D 249/08
Мітки: триазоли, каналів, натрієвих, біарилзаміщені, блокатори
Код посилання
<a href="https://ua.patents.su/21-81660-biarilzamishheni-triazoli-yak-blokatori-natriehvikh-kanaliv.html" target="_blank" rel="follow" title="База патентів України">Біарилзаміщені триазоли як блокатори натрієвих каналів</a>
Попередній патент: Моноклінний 2-хлор-n-(4′ -хлорбіфеніл-2-іл)нікотинамід, спосіб його одержання, фунгіцидний засіб та спосіб боротьби з шкідливими грибами
Наступний патент: Спосіб виробництва ароматичного напою
Випадковий патент: Горілка особлива