Заміщені конденсовані гетероциклічні с-глікозиди
Формула / Реферат
1. Сполука формули IV:
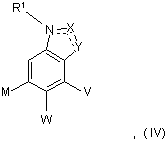
в якій:
присутня одна з пунктирних ліній між NR1 та X або між X та Y, або обидві пунктирні лінії відсутні;
два з V, М та W являють собою Н та третій являє собою
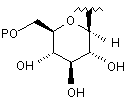 ,
,
R1 являє собою Н або С1-4алкіл; або R1 відсутній, коли присутня пунктирна лінія між NR1 та X;
X являє собою N, С=О, СН або C-Q-Z;
Y являє собою N-Q-Z або C-Q-Z, коли X являє собою N, С=О або СН;
Y являє собою СН, коли X являє собою C-Q-Z;
Q = -(СН2)n-, де n = 1 або 2;
Р = Н, С1-7ацил або (С1-6алкокси)карбоніл;
Z є заміщеним або незаміщеним та вибраний з С3-7циклоалкілу, фенілу, 5- або 6-членного гетероарилу, який містить 1 або 2 гетероатоми, незалежно вибрані з N, О та S, біарилу, 9- або 10-членного конденсованого біциклілу та конденсованого гетеробіциклілу, де зазначений конденсований гетеробіцикліл містить 1-4 гетероатоми, незалежно вибрані з N, О та S;
або її фармацевтично прийнятна сіль.
2. Сполука за пунктом 1, де R1 являє собою Н або відсутній.
3. Сполука за пунктом 1, де Z незалежно заміщений 1-3 замісниками, незалежно вибраними з С1-4алкокси, фенокси, С1-4алкілу, С3-6циклоалкілу, гало, гідрокси, ціано, аміно, С1-4алкілтіо, С1-4алкілсульфонілу, С1-4алкілсульфінілу, С1-4аміноалкілу, моно- та ді-С1-4алкіламіно, фенілу, С1-4алкіламіносульфонілу (SO2NHR), аміно(С1-4алкілсульфонілу) (NHSO2R), ді-С1-4алкіламіносульфінілу (SONHRR), С1-4алкіламідо (NHCOR), С1-4алкілкарбамідо (CONHR), 5-6-членного гетероциклілу, що містить 1-3 гетероатоми, незалежно вибрані з N, S та О; та де замісник(и) на Z може бути додатково незалежно заміщений 1-3 замісниками, незалежно вибраними з С1-4алкокси, С1-4алкілу, гало, гідрокси, ціано, аміно, моно- або ді-С1-4алкіламіно та С1-4алкілтіо.
4. Сполука за пунктом 1, де Z являє собою 4-заміщений феніл, 3,4-дизаміщений феніл, бензгідрил, заміщений або незаміщений тіофеніл, біарил, бензофураніл, гідробензофураніл, дигідробензофураніл, 4-заміщений піридил, бензо[b]тієніл, хроманіл, бензотіофеніл, інданіл, нафтил та 2,3-дигідробензо[1,4]діоксан.
5. Сполука за пунктом 3, де Z незаміщений або заміщений 1-2 замісниками, незалежно вибраними з метокси, етокси, фтору, хлору, метилу, етилу, пропілу, бутилу та ізопропілу.
6. Сполука за пунктом 1, де Z являє собою біфеніл, 4-(3-піридил)феніл, 4-(2-тієніл)феніл, 4-(1Н-піразол-1-іл)-феніл, (4-етил)феніл, (4-пропіл)феніл, (4-метокси)феніл, дигідробензофуран-5-іл або дигідробензофуран-6-іл.
7. Сполука за пунктом 1, де R1 являє собою Н.
8. Сполука за пунктом 1, де n означає 1.
9. Сполука за пунктом 8, де R1 являє собою Н або відсутній.
10. Сполука за пунктом 1, де Z являє собою біфеніл, 4-(3-піридил)феніл, 4-(2-тієніл)феніл, 4-(1Н-піразол-1-іл)-феніл, (4-етил)феніл, (4-пропіл)феніл, (4-метокси)феніл, дигідробензофуран-5-іл або дигідробензофуран-6-іл; та Z незаміщений або заміщений 1-2 замісниками, незалежно вибраними з метокси, етокси, фтору, хлору, метилу, етилу, пропілу, бутилу та ізопропілу.
11. Сполука за пунктом 10, де n означає 1.
12. Сполука за пунктом 10, де R1 являє собою Н.
13. Сполука за пунктом 1, де М та V являють собою Н.
14. Сполука за пунктом 1, де М та W являють собою Н.
15. Сполука за пунктом 1, де X являє собою СН та Y являє собою C-Q-Z.
16. Сполука за пунктом 1, де X являє собою C-Q-Z та Y являє собою СН.
17. Сполука за пунктом 15, де R1 являє собою Н або відсутній, та n = 1.
18. Сполука за пунктом 1, вибрана з: 3-(4-етилбензил)-5-(![]() -D-глюкопіранозил)-1Н-індолу; 5-(
-D-глюкопіранозил)-1Н-індолу; 5-(![]() -D-глюкопіранозил)-3-(4-метоксибензил)-1Н-індолу; 5-(
-D-глюкопіранозил)-3-(4-метоксибензил)-1Н-індолу; 5-(![]() -D-глюкопіранозил)-3-[2-(4-метоксифеніл)-етил]-1Н-індолу та 3-(4-етилбензил)-4-(β-D-глюкопіранозил)-1Н-індолу.
-D-глюкопіранозил)-3-[2-(4-метоксифеніл)-етил]-1Н-індолу та 3-(4-етилбензил)-4-(β-D-глюкопіранозил)-1Н-індолу.
19. Сполука за пунктом 1, вибрана з 2-(4-етилбензил)-4-(![]() -D-глюкопіранозил)-1Н-індолу; 3-[2-(2,3-дигідробензофуран-5-іл)-етил]-5-(
-D-глюкопіранозил)-1Н-індолу; 3-[2-(2,3-дигідробензофуран-5-іл)-етил]-5-(![]() -D-глюкопіранозил)-1Н-індолу; 5-(
-D-глюкопіранозил)-1Н-індолу; 5-(![]() -D-глюкопіранозил)-3-(5-метил-2-тієніл)-1Н-індолу; 3-(4-етилбензил)-4-(
-D-глюкопіранозил)-3-(5-метил-2-тієніл)-1Н-індолу; 3-(4-етилбензил)-4-(![]() -D-глюкопіранозил)-3Н-бензимідазолу; 3-(4-етилбензил)-4-(
-D-глюкопіранозил)-3Н-бензимідазолу; 3-(4-етилбензил)-4-(![]() -D-глюкопіранозил)-1,3-дигідробензоімідазол-2-ону та 3-(4-етилбензил)-4-(
-D-глюкопіранозил)-1,3-дигідробензоімідазол-2-ону та 3-(4-етилбензил)-4-(![]() -D-глюкопіранозил)-3Н-бензотриазолу.
-D-глюкопіранозил)-3Н-бензотриазолу.
20. Сполука за пунктом 1, вибрана з 3-(4-етилбензил)-5-(![]() -D-глюкопіранозил)-1Н-індолу; 2-(4-етилбензил)-4-(
-D-глюкопіранозил)-1Н-індолу; 2-(4-етилбензил)-4-(![]() -D-глюкопіранозил)-1Н-індолу; 5-(
-D-глюкопіранозил)-1Н-індолу; 5-(![]() -D-глюкопіранозил)-3-(5-метил-2-тієніл)-1Н-індолу; 3-(4-етилбензил)-4-(
-D-глюкопіранозил)-3-(5-метил-2-тієніл)-1Н-індолу; 3-(4-етилбензил)-4-(![]() -D-глюкопіранозил)-3Н-бензимідазолу та 3-(4-етилбензил)-4-(
-D-глюкопіранозил)-3Н-бензимідазолу та 3-(4-етилбензил)-4-(![]() -D-глюкопіранозил)-3Н-бензотриазолу.
-D-глюкопіранозил)-3Н-бензотриазолу.
21. Фармацевтична композиція, що містить сполуку за будь-яким з пунктів 1, 5, 6, 11, 12, 13, 14, 15, 16, 17, 18, 19 або 20.
22. Фармацевтична композиція за пунктом 21, що містить сполуку за пунктом 14 та фармацевтично прийнятний носій.
23. Спосіб лікування діабету у ссавця, який включає введення ссавцю, що потребує лікування, ефективної кількості фармацевтичної композиції за пунктом 21.
24. Спосіб за пунктом 23, де зазначений діабет є діабетом II типу.
25. Спосіб зниження рівня глюкози в сироватці у ссавця, який включає введення ссавцю, що потребує лікування, ефективної кількості фармацевтичної композиції за пунктом 21.
26. Спосіб лікування порушеної толерантності до глюкози у ссавця, який включає введення ссавцю, що потребує лікування, ефективної кількості фармацевтичної композиції за пунктом 21.
27. Спосіб лікування або інгібування порушеної толерантності до глюкози у ссавця, який включає введення ссавцю, що потребує лікування, ефективної кількості фармацевтичної композиції за пунктом 21.
28. Спосіб зниження індексу маси тіла, маси тіла або відсотка жиру в тілі у ссавця, який включає введення ссавцю, що потребує лікування, ефективної кількості фармацевтичної композиції за пунктом 21.
29. Спосіб за пунктом 28, де зазначене зниження індексу маси тіла є способом лікування ожиріння або стану надлишкової ваги.
30. Спосіб інгібування транспортеру натрій/глюкози в клітині, який включає піддавання зазначеної клітини дії сполуки за пунктом 1 або її метаболіту.
31. Спосіб лікування діабету або cиндрому X, або симптомів, пов'язаних з ними, або їх ускладнень у суб'єкта, який включає:
(a) введення зазначеному суб'єкту спільно ефективної кількості інгібітора реабсорбції глюкози формули (IV); та
(b) введення зазначеному суб'єкту спільно ефективної кількості другого антидіабетичного агента,
зазначене спільне введення проводять в будь-якому порядку.
32. Спосіб за пунктом 31, де другим антидіабетичним агентом є агоніст RXR.
33. Спосіб за пунктом 31, де діабет або cиндром X, або симптоми, пов'язані з ними, або їх ускладнення вибрані з IDDM NIDDM, IGT, IFG, ожиріння, нефропатії, невропатії, ретинопатії, атеросклерозу, синдрому полікістозного яєчника, гіпертензії, ішемії, інсульту, серцевої хвороби, синдрому подразненого кишечнику, запалення та катаракт.
34. Спосіб за пунктом 31, де діабет або синдром X, або симптоми, пов'язані з ними, або їх ускладнення являють собою IDDM.
35. Спосіб за пунктом 31, де діабет або синдром X, або симптоми, пов'язані з ними, або їх ускладнення являють собою NIDDM.
36. Спосіб за пунктом 31, де діабет або синдром X, або симптоми, пов'язані з ними, або їх ускладнення являють собою 1GT або IFG.
37. Спосіб за пунктом 31, який, крім того, включає введення зазначеному суб'єкту спільно ефективної кількості третього антидіабетичного агента.
38. Спосіб за пунктом 37, де третій антидіабетичний агент вибраний з:
(аа) інсулінів,
(bb) аналогів інсуліну;
(сс) модуляторів секреції інсуліну, та
(dd) стимуляторів секреції інсуліну.
39. Спосіб за пунктом 31, де інгібітор реабсорбції глюкози являє собою інгібітор SGLT.
40. Спосіб за пунктом 31, де інгібітор реабсорбції глюкози являє собою інгібітор SGLT1.
41. Спосіб за пунктом 31, де інгібітор реабсорбції глюкози являє собою інгібітор SGLT2.
42. Спосіб за пунктом 31, де інгібітор реабсорбції глюкози являє собою сполуку формули (IV) або її оптичний ізомер, енантіомер, діастереомер, рацемат або рацемічну суміш, ефір, пролікарську форму або її фармацевтично прийнятну сіль.
43. Спосіб за пунктом 31, де спільно ефективна кількість інгібітора SGLT складає від приблизно 10 до 1000 мг.
44. Спосіб за пунктом 31, де спільно ефективна кількість інгібітора SGLT являє собою кількість, достатню для зменшення коливань рівня глюкози в плазмі після їжі.
45. Спосіб інгібування початку діабету або синдрому X, або симптомів, пов'язаних з ними, або їх ускладнень у суб'єкта, який включає:
(a) введення зазначеному суб'єкту спільно ефективної кількості інгібітора реабсорбції глюкози формули (IV); та
(b) введення зазначеному суб'єкту спільно ефективної кількості другого антидіабетичного агента,
зазначене спільне введення проводять в будь-якому порядку.
46. Спосіб за пунктом 45, де зазначеним початком є стан від переддіабетичного стану до NIDDM.
47. Фармацевтична композиція, яка містить інгібітор реабсорбції глюкози формули (IV), другий антидіабетичний агент та фармацевтично прийнятний носій.
48. Фармацевтична композиція за пунктом 45, 46 або 47, де інгібітор реабсорбції глюкози являє собою інгібітор SGLT.
49. Фармацевтична композиція за пунктом 45, де інгібітор реабсорбції глюкози являє собою інгібітор SGLT1.
50. Фармацевтична композиція за пунктом 45, де інгібітор реабсорбції глюкози являє собою інгібітор SGLT2.
51. Спосіб одержання фармацевтичної композиції, який включає поєднання разом інгібітора реабсорбції глюкози, другого антидіабетичного агента та фармацевтично прийнятного носія.
52. Спосіб виготовлення фармацевтичної композиції, який включає змішування одного або більше інгібіторів реабсорбції глюкози в комбінації з другим антидіабетичним агентом для лікування стану, вибраного з IDDM NIDDM, IGT, IFG, ожиріння, нефропатії, невропатії, ретинопатії, атеросклерозу, синдрому полікістозного яєчника, гіпертензії, ішемії, інсульту, серцевої хвороби, синдрому подразненого кишечнику, запалення та катаракт.
53. Спосіб інгібування розвитку переддіабетичного стану у суб'єкта в діабетичний стан, який включає:
(a) введення зазначеному суб'єкту спільно ефективної кількості інгібітора реабсорбції глюкози формули (IV); та
(b) введення зазначеному суб'єкту спільно ефективної кількості другого антидіабетичного агента,
зазначене спільне введення проводять в будь-якому порядку.
54. Спосіб за пунктом 53, де зазначеним станом є IGT або IFG.
55. Спосіб за пунктом 53, де зазначеним інгібуванням розвитку переддіабетичного стану є попередження розвитку переддіабетичного стану в діабетичний стан.
56. Спосіб за пунктом 53, де інгібітор реабсорбції глюкози являє собою сполуку формули (IV), яка необов'язково містить одну або більше гідроксил- або діолзахисних груп, або її оптичний ізомер, енантіомер, діастереомер, рацемат або рацемічну суміш, ефір, пролікарську форму або фармацевтично прийнятну сіль.
Текст
1. Сполука формули IV: 2 3 85569 рил, заміщений або незаміщений тіофеніл, біарил, бензофураніл, гідробензофураніл, дигідробензофураніл, 4-заміщений піридил, бензо[b]тієніл, хроманіл, бензотіофеніл, інданіл, нафтил та 2,3дигідробензо[1,4]діоксан. 5. Сполука за пунктом 3, де Z незаміщений або заміщений 1-2 замісниками, незалежно вибраними з метокси, етокси, фтору, хлор у, метилу, етилу, пропілу, бутилу та ізопропілу. 6. Сполука за пунктом 1, де Z являє собою біфеніл, 4-(3-піридил)феніл, 4-(2-тієніл)феніл, 4-(1Нпіразол-1-іл)-феніл, (4-етил)феніл, (4пропіл)феніл, (4-метокси)феніл, дигідробензофуран-5-іл або дигідробензофуран-6-іл. 7. Сполука за пунктом 1, де R 1 являє собою Н. 8. Сполука за пунктом 1, де n означає 1. 9. Сполука за пунктом 8, де R1 являє собою Н або відсутній. 10. Сполука за пунктом 1, де Z являє собою біфеніл, 4-(3-піридил)феніл, 4-(2-тієніл)феніл, 4-(1Нпіразол-1-іл)-феніл, (4-етил)феніл, (4пропіл)феніл, (4-метокси)феніл, дигідробензофуран-5-іл або дигідробензофуран-6-іл; та Z незаміщений або заміщений 1-2 замісниками, незалежно вибраними з метокси, етокси, фтору, хлору, метилу, етилу, пропілу, бутилу та ізопропілу. 11. Сполука за пунктом 10, де n означає 1. 12. Сполука за пунктом 10, де R1 являє собою Н. 13. Сполука за пунктом 1, де М та V являють собою Н. 14. Сполука за пунктом 1, де М та W являють собою Н. 15. Сполука за пунктом 1, де X являє собою СН та Y являє собою C-Q-Z. 16. Сполука за пунктом 1, де X являє собою C-Q-Z та Y являє собою СН. 17. Сполука за пунктом 15, де R 1 являє собою Н або відсутній, та n = 1. 18. Сполука за пунктом 1, вибрана з: 3-(4етилбензил)-5-( b -D-глюкопіранозил)-1Н-індолу; 5( b -D-глюкопіранозил)-3-(4-метоксибензил)-1Ніндолу; 5-( b -D-глюкопіранозил)-3-[2-(4метоксифеніл)-етил]-1Н-індолу та 3-(4етилбензил)-4-(β-D-глюкопіранозил)-1Н-індолу. 19. Сполука за пунктом 1, вибрана з 2-(4етилбензил)-4-( b -D-глюкопіранозил)-1Н-індолу; 3[2-(2,3-дигідробензофуран-5-іл)-етил]-5-( b -Dглюкопіранозил)-1Н-індолу; 5-( b -Dглюкопіранозил)-3-(5-метил-2-тієніл)-1Н-індолу; 3(4-етилбензил)-4-( b -D-глюкопіранозил)-3Нбензимідазолу; 3-(4-етилбензил)-4-( b -Dглюкопіранозил)-1,3-дигідробензоімідазол-2-ону та 3-(4-етилбензил)-4-( b -D-глюкопіранозил)-3Нбензотриазолу. 20. Сполука за пунктом 1, вибрана з 3-(4етилбензил)-5-( b -D-глюкопіранозил)-1Н-індолу; 2(4-етилбензил)-4-( b -D-глюкопіранозил)-1Н-індолу; 5-( b -D-глюкопіранозил)-3-(5-метил-2-тієніл)-1Ніндолу; 3-(4-етилбензил)-4-( b -D-глюкопіранозил)3Н-бензимідазолу та 3-(4-етилбензил)-4-( b -Dглюкопіранозил)-3Н-бензотриазолу. 4 21. Фармацевтична композиція, що містить сполуку за будь-яким з пунктів 1, 5, 6, 11, 12, 13, 14, 15, 16, 17, 18, 19 або 20. 22. Фармацевтична композиція за пунктом 21, що містить сполуку за пунктом 14 та фармацевтично прийнятний носій. 23. Спосіб лікування діабету у ссавця, який включає введення ссавцю, що потребує лікування, ефективної кількості фармацевтичної композиції за пунктом 21. 24. Спосіб за пунктом 23, де зазначений діабет є діабетом II типу. 25. Спосіб зниження рівня глюкози в сироватці у ссавця, який включає введення ссавцю, що потребує лікування, ефективної кількості фармацевтичної композиції за пунктом 21. 26. Спосіб лікування порушеної толерантності до глюкози у ссавця, який включає введення ссавцю, що потребує лікування, ефективної кількості фармацевтичної композиції за пунктом 21. 27. Спосіб лікування або інгібування порушеної толерантності до глюкози у ссавця, який включає введення ссавцю, що потребує лікування, ефективної кількості фармацевтичної композиції за пунктом 21. 28. Спосіб зниження індексу маси тіла, маси тіла або відсотка жиру в тілі у ссавця, який включає введення ссавцю, що потребує лікування, ефективної кількості фармацевтичної композиції за пунктом 21. 29. Спосіб за пунктом 28, де зазначене зниження індексу маси тіла є способом лікування ожиріння або стану надлишкової ваги. 30. Спосіб інгібування транспортеру натрій/глюкози в клітині, який включає піддавання зазначеної клітини дії сполуки за пунктом 1 або її метаболіту. 31. Спосіб лікування діабету або cиндрому X, або симптомів, пов'язаних з ними, або їх ускладнень у суб'єкта, який включає: (a) введення зазначеному суб'єкту спільно ефективної кількості інгібітора реабсорбції глюкози формули (IV); та (b) введення зазначеному суб'єкту спільно ефективної кількості другого антидіабетичного агента, зазначене спільне введення проводять в будьякому порядку. 32. Спосіб за пунктом 31, де другим антидіабетичним агентом є агоніст RXR. 33. Спосіб за пунктом 31, де діабет або cиндром X, або симптоми, пов'язані з ними, або їх ускладнення вибрані з IDDM NIDDM, IGT, IFG, ожиріння, нефропатії, невропатії, ретинопатії, атеросклерозу, синдрому полікістозного яєчника, гіпертензії, ішемії, інсульту, серцевої хвороби, синдрому подразненого кишечнику, запалення та катаракт. 34. Спосіб за пунктом 31, де діабет або синдром X, або симптоми, пов'язані з ними, або їх ускладнення являють собою IDDM. 35. Спосіб за пунктом 31, де діабет або синдром X, або симптоми, пов'язані з ними, або їх ускладнення являють собою NIDDM. 36. Спосіб за пунктом 31, де діабет або синдром X, або симптоми, пов'язані з ними, або їх ускладнення являють собою 1GT або IFG. 5 85569 6 37. Спосіб за пунктом 31, який, крім того, включає введення зазначеному суб'єкту спільно ефективної кількості третього антидіабетичного агента. 38. Спосіб за пунктом 37, де третій антидіабетичний агент вибраний з: (аа) інсулінів, (bb) аналогів інсуліну; (сс) модуляторів секреції інсуліну, та (dd) стимуляторів секреції інсуліну. 39. Спосіб за пунктом 31, де інгібітор реабсорбції глюкози являє собою інгібітор SGLT. 40. Спосіб за пунктом 31, де інгібітор реабсорбції глюкози являє собою інгібітор SGLT1. 41. Спосіб за пунктом 31, де інгібітор реабсорбції глюкози являє собою інгібітор SGLT2. 42. Спосіб за пунктом 31, де інгібітор реабсорбції глюкози являє собою сполуку формули (IV) або її оптичний ізомер, енантіомер, діастереомер, рацемат або рацемічну суміш, ефір, пролікарську форму або її фармацевтично прийнятну сіль. 43. Спосіб за пунктом 31, де спільно ефективна кількість інгібітора SGLT складає від приблизно 10 до 1000 мг. 44. Спосіб за пунктом 31, де спільно ефективна кількість інгібітора SGLT являє собою кількість, достатню для зменшення коливань рівня глюкози в плазмі після їжі. 45. Спосіб інгібування початку діабету або синдрому X, або симптомів, пов'язаних з ними, або їх ускладнень у суб'єкта, який включає: (a) введення зазначеному суб'єкту спільно ефективної кількості інгібітора реабсорбції глюкози формули (IV); та (b) введення зазначеному суб'єкту спільно ефективної кількості другого антидіабетичного агента, зазначене спільне введення проводять в будьякому порядку. 46. Спосіб за пунктом 45, де зазначеним початком є стан від переддіабетичного стану до NIDDM. 47. Фармацевтична композиція, яка містить інгібітор реабсорбції глюкози формули (IV), другий антидіабетичний агент та фармацевтично прийнятний носій. 48. Фармацевтична композиція за пунктом 45, 46 або 47, де інгібітор реабсорбції глюкози являє собою інгібітор SGLT. 49. Фармацевтична композиція за пунктом 45, де інгібітор реабсорбції глюкози являє собою інгібітор SGLT1. 50. Фармацевтична композиція за пунктом 45, де інгібітор реабсорбції глюкози являє собою інгібітор SGLT2. 51. Спосіб одержання фармацевтичної композиції, який включає поєднання разом інгібітора реабсорбції глюкози, другого антидіабетичного агента та фармацевтично прийнятного носія. 52. Спосіб виготовлення фармацевтичної композиції, який включає змішування одного або більше інгібіторів реабсорбції глюкози в комбінації з другим антидіабетичним агентом для лікування стану, вибраного з IDDM NIDDM, IGT, IFG, ожиріння, нефропатії, невропатії, ретинопатії, атеросклерозу, синдрому полікістозного яєчника, гіпертензії, ішемії, інсульту, серцевої хвороби, синдрому подразненого кишечнику, запалення та катаракт. 53. Спосіб інгібування розвитку переддіабетичного стану у суб'єкта в діабетичний стан, який включає: (a) введення зазначеному суб'єкту спільно ефективної кількості інгібітора реабсорбції глюкози формули (IV); та (b) введення зазначеному суб'єкту спільно ефективної кількості другого антидіабетичного агента, зазначене спільне введення проводять в будьякому порядку. 54. Спосіб за пунктом 53, де зазначеним станом є IGT або IFG. 55. Спосіб за пунктом 53, де зазначеним інгібуванням розвитку переддіабетичного стану є попередження розвитку переддіабетичного стану в діабетичний стан. 56. Спосіб за пунктом 53, де інгібітор реабсорбції глюкози являє собою сполуку формули (IV), яка необов'язково містить одну або більше гідроксилабо діолзахисних груп, або її оптичний ізомер, енантіомер, діастереомер, рацемат або рацемічну суміш, е фір, пролікарську форму або фармацевтично прийнятну сіль. Даний винахід відноситься до заміщених конденсованих гетероциклічних С-глікозидів, композицій, що їх містять, та способів їх використання, наприклад, для лікування або профілактики діабету та Синдрому X. Діабет - хронічний розлад, що впливає на метаболізм вуглеводів, жирів та протеїнів у тварин. Цукровий діабет І типу, що включає приблизно 10% від усіх випадків діабету, раніше відносили до інсулін-залежного цукрового діабету ("IDDM") або до діабету, що починається у ранньому віці. Ця хвороба характеризується поступовою втратою бета-клітинами підшлункової залози функції секреції інсуліну. Ця характеристика також розповсюджується на не-ідіопатичний або "вторинний" діабет, що виникає внаслідок хвороби підшлункової залози. Цукровий діабет І типу пов'язаний із на ступними клінічними ознаками або симптомами: постійно підвищена концентрація глюкози у плазмі або гіперглікемія; поліурія; полідипсія та/або гіперфагія; хронічні мікросудинні ускладнення, такі, як ретинопатія, нефропатія та нейропатія; та макросудинні ускладнення, такі, як гіперліпідемія та гіпертензія, що можуть призвести до сліпоти, хвороби нирок останньої стадії, ампутації кінцівок та інфаркту міокарду. Цукровий діабет II типу (не-інсуліно-залежний цукровий діабет або NIDDM) - метаболічний розлад, що включає недостатню регуляцію метаболізму глюкози та погіршену чутливість до інсуліну. Цукровий діабет II типу зазвичай розвивається у зрілих осіб та пов'язаний із неспроможністю тіла вживати або виробляти достатню кількість інсуліну. Додатково до резистентності до інсуліну, що 7 85569 спостерігалась у тканинах, що вивчались, пацієнти, хворі на цукровий діабет II типу, мали відносну інсулінову недостатність - тобто, пацієнти мали рівень інсуліну менший, ніж розрахований для даної концентрації глюкози у плазмі. Цукровий діабет II тип у характеризується наступними клінічними ознаками або симптомами: постійно підвищена концентрація глюкози у плазмі або гіперглікемія; поліурія; полідипсія та/або гіперфагія; хронічні мікросудинні ускладнення, такі, як ретинопатія, нефропатія та нейропатія; та макросудинні ускладнення, такі як гіперліпідемія та гіпертензія, що можуть призвести до сліпоти, хвороби нирок останньої стадії, ампутації кінцівок та інфаркту міокарду. Синдром X, що також має назву синдрому резистентності до інсуліну (IRS), метаболічного синдрому, або метаболічного синдрому X, з устрічається у 2% діагностичних коронарних характеристик. Часто призводячи до інвалідності, він є симптомом або фактором ризику для розвитку цукрового діабету II типу та серцево-судинного захворювання, включаючи порушену толерантність до глюкози (IGT), знижений рівень глюкози крові натщесерце, гіперінсулінемію, резистентність до інсуліну, дисліпідемію (наприклад, високий рівень тригліцеридів, низький вміст HDL), гіпертензію та ожиріння. Терапія пацієнтів з IDDM завжди концентрувалась на прийманні зовнішнього інсуліну, що може бути о триманий з різних джерел (наприклад, людський, коров'ячий, свинячий інсулін). Використання матеріалу гетерологічних видів призводить до утворення анти-інсулінових антитіл, що мають дію, яка обмежує активність, та призводить до прогресуючої потреби у більших дозах для досягнення бажаного гіпоглікемічного ефекту. Типове лікування цукрового діабету II тип у концентрується на підтримці якомога близького до нормального рівня глюкози у крові за допомогою зміни способу життя в тому, що стосується дієти та фізичного навантаження, та, у разі необхідності, лікування антидіабетичними агентами, інсуліном або їх комбінацією. NIDDM, що не можна контролювати за допомогою дієт, лікують за допомогою перорального приймання антидіабетичних агентів. Хоча резистентність до інсуліну не завжди лікується в усіх пацієнтів із синдромом X, тих, хто проявляє переддіабетичний стан (наприклад, IGT, IFG), коли рівень глюкози у крові натщесерце може перевищувати нормальний, але не відповідає критерію діагностики діабету, у деяких країнах (наприклад, у Німеччині) лікують метформіном для запобігання діабету. Антідіабетичні агенти можуть бути поєднані з фармакологічними агентами для лікування супутніх захворювань (наприклад, антигіпертензивними засобами для лікування гіпертензії, гіполіпідемічними агентами для лікування ліпідемії). Пріоритетна терапія зазвичай включає метформін та сульфонілсечовини, а також тіазолідиндіони. Монотерапія метформіном є пріоритетним вибором, особливо для лікування пацієнтів, хворих на діабет II типу, які також страждають на ожиріння та/або дисліпідемію. Відсутність належної реакції на метформін часто призводить до наступного 8 лікування метформіном у поєднанні з сульфонілсечовинами, тіазолідиндіонами або інсуліном. Монотерапія сульфонілсечовинами (включаючи усі покоління ліків) є також розповсюдженим пріоритетним терапевтичним вибором. Іншим пріоритетним терапевтичним вибором можуть бути тіазолідіндіони. Інгібітори альфа-глюкозидази також використовують як пріоритетну та вторинну терапії. Пацієнтам, в яких була відсутня адекватна реакція на пероральну антидіабетичну терапію, дають комбінації вищевказаних агентів. Коли глікемічний контроль не може бути підтриманий лише за допомогою перорального приймання антидіабетичних агентів, застосовують терапію інсуліном, або як монотерапію, або у комбінації з пероральними антидіабетичними агентами. Одна остання розробка у терапії гіперліпідемії сконцентрована на виведенні надлишкової глюкози безпосередньо із сечею. Було показано, що специфічні інгібітори SGLT підвищують виведення глюкози із сечею та знижують рівень глюкози у крові у зразків гризунів з IDDM або NIDDM. Один аспект даного винаходу направлений на способи та композиції для лікування або профілактики діабету, Синдрому X або симптомів, пов'язаних з ними, чи їх ускладнень. Більш особливо, даний винахід направлений на новий спосіб лікування діабету або Синдрому X, або симптомів, пов'язаних з ними, чи їх ускладнень у суб'єкта, що страждає від такого стану, зазначений спосіб включає введення одного або більше інгібіторів реабсорбції глюкози та введення одного або більше антидіабетичного агенту(ів) для лікування діабету або Синдрому X, або симптомів, пов'язаних з ними, чи їх ускладнень. Інший аспект винаходу розкриває сполуки формули (IV): (IV) в якій: присутня одна з пунктирних ліній між NR1 та X або між X та Y, або обидві пунктирні лінії відсутні; двоє з V, Μ та W являють собою Η та третій являє собою R1 являє собою Η або С1-4алкіл; або R1 відсутній, коли присутня пунктирна лінія між NR1 та X; X являє собою N, С=О, СН або C-Q-Z; Υ являє собою N-Q-Z або C-Q-Z, коли X являє собою Ν, С=О або СН; Υ являє собою СН, коли X являє собою C-Q-Z; Q=-(CH2)n-, де n=1 або 2; Ζ є заміщеним або незаміщеним, та вибраний з С3-7циклоалкілу, фенілу, 5- або 6-членного гетероарилу, який містить 1 або 2 гетероатоми, незалежно вибрані з Ν, О та S, біарилу, 9- або 10 9 85569 членного конденсованого біциклілу (такого як нафтил) та конденсованого гетеробіциклілу, де зазначений конденсований гетеробіцикліл містить 1-4 гетероатоми (та переважно 1-3 або 1-2 гетероатоми), незалежно вибрані з Ν, Ο та S; Ρ=Н, С1-7ацил або (С1-6алкокси)карбоніл; або їх фармацевтично прийнятну сіль. Один аспект винаходу розкриває фармацевтичну композицію, що містить інгібітор реабсорбції глюкози, принаймні, один додатковий антидіабетичний агент та фармацевтично прийнятний носій. Винахід також забезпечує спосіб одержання фармацевтичної композиції, який включає поєднання разом інгібітора реабсорбції глюкози, одного або більше антидіабетичного агента(ів) та фармацевтично прийнятного носія. Втіленням винаходу є спосіб лікування діабету або Синдрому X, або симптомів, пов'язаних з ними, або їх ускладнень у суб'єкта, зазначений спосіб включає введення зазначеному суб'єкту спільно ефективної кількості інгібітора реабсорбції глюкози та введення зазначеному суб'єкту спільно ефективної кількості, принаймні, одного антидіабетичного агента, зазначене об'єднане введення забезпечує бажаний терапевтичний ефект. Іншим втіленням винаходу є спосіб інгібування початку діабету або Синдрому X, або симптомів, пов'язаних з ними, або їх ускладнень у суб'єкта, зазначений спосіб включає введення зазначеному суб'єкту спільно ефективної дози інгібітора реабсорбції глюкози та введення зазначеному суб'єкту спільно ефективної кількості одного або більше антидіабетичного агенту(ів), зазначене об'єднане введення забезпечує бажаний профілактичний ефект. У розкритих способах діабет або Синдром X або симптоми, пов'язані з ними, або їх ускладнення вибрані з IDDM, NIDDM, IGT, IFG, ожиріння, нефропатії, невропатії, ретинопатії, атеросклерозу, синдрому полікістозного яєчника, гіпертензії, ішемії, інсульту, серцевої хвороби, синдрому подразненого кишечнику, запалення та катаракт. Також винахід включає використання одного або більше інгібіторів реабсорбції глюкози в комбінації з одним або більше антидіабетичними агентами для одержання лікарських засобів для лікування стану, вибраного з IDDM, NIDDM, IGT, IFG, ожиріння, нефропатії, невропатії, ретинопатії, атеросклерозу, синдрому полікістозного яєчника, гіпертензії, ішемії, інсульту, серцевої хвороби, синдрому подразненого кишечнику, запалення та катаракт. Всі діабетики, незалежно від їх генетичного та екологічного середовища, сукупно мають виражену нестачу інсуліну або неадекватну функцію інсуліну. Оскільки перенесення глюкози з крові в м'яз та жирову тканину залежить від інсуліну, діабетики відчувають нестачу здатності використовувати глюкозу відповідно, що призводить до небажаного накопичення глюкози в крові (гіперглікемія). Хронічна гіперглікемія призводить до зниження секреції інсуліну та сприяє збільшеній резистентності до інсуліну, та в результаті концентрація глюкози в крові збільшується, так що діабет самозагострюється [Diabetologia, 1985, "Hyperglycaemia as an 10 inducer as well as a consequence of impaired isle cell function and insulin resistance: implications for the management of diabetes", Vol.28, p.119; Diabetes Cares, 1990, Vol.13, No.6, "Glucose Toxicity", pp.610-630]. Таким чином, за допомогою лікування гіперглікемії вищезазначений самозагострений цикл переривається, так що стає можливим профілактика або лікування діабету. Патент [US 6,153,632 R. Rieveley] розкриває спосіб та композицію, заявлені для лікування цукрового діабету (І тип, Порушена толерантність до глюкози ["IGT"] та II тип), що включають терапевтичну кількість одного або більше сенсибілізаторов інсуліну разом з одним або більше інсуліном, який приймають всередину перорально, інсуліном, який вводять за допомогою ін'єкції, сульфонілсечовиною, бігуанідом або інгібітором альфаглюкозидази для лікування цукрового діабету. Відповідно до одного аспекту, винахід розкриває комбінацію модулятора PPAR, переважно агоніста PPAR δ, та інгібітора SGLT, переважно інгібітора SGLT 2 або селективного інгібітора SGLT 2. Терміни Деякі терміни визначено нижче та при їх використанні в цьому описі. Якщо не зазначено інше, як використовується в даній заявці, терміни "алкіл" та "алкокси", які використовуються самі по собі або як частина замішуючої групи, включають алкіл з прямим, циклічним та розгалуженим ланцюгом, що містить від 1 до 8 атомів вуглецю або будь-яку їх кількість в межах цього діапазону. Наприклад, алкільні радикали включають метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, втор-бутил, трет-бутил, 2бутеніл, 2-бутиніл, н-пентил, 3-(2-метил)бутил, 2пентил, 2-метилбутил, неопентил, н-гексил, 2гексил та 2-метилпентил. Алкокси радикали являють собою кисневі ефіри, утворені з попередньо описаних алкільних груп з прямим або розгалужених ланцюгом. Алкільна та алкокси група може бути незалежно заміщена від однієї до п'яти, переважно від однієї до трьох, групами, вибраними з галогену (F, СІ, Вr, І), оксо, ОН, аміно, карбоксилу та алкокси. Алкільна та алкокси група також може бути незалежно зв'язана з одним або більше PEG радикалами (поліетилен гліколь). Як використовується в даній заявці, термін "ацил", який використовується сам по собі або як частина заміщуючої гр упи, означає органічний радикал, що містить карбонільну групу, зв'язану з гідрокарбільною групою, що містить від 1 до 7 атомів вуглецю (прямий чи розгалужений ланцюг або циклічний), отриманий з органічної кислоти видаленням гідроксильної групи. Наприклад, С4ацил може включати (СО)СН2СН2СН2СН3 та (СО)(СН2(СН)(СН3)2; так само, С6ацил включає як (СО)(С6Н13), так і (СО)(С6Н5). Термін "Ас", як використовується в даній заявці, який використовується сам по собі або як частина заміщуючої гр упи, означає ацетил. Термін "арил" являє собою карбоциклічний ароматичний радикал, включаючи, але не обмежуючись, феніл, 1- або 2-нафтил та подібні. Карбоциклічний ароматичний радикал може бути заміщений шляхом незалежної заміни 1-3 атомів 11 85569 водню на ньому на галоген, ОН, CN, меркапто, нітро, аміно, ціано, необов'язково заміщений С1С8-алкіл, необов'язково заміщений алкокси, алкілтіо, алкілсульфініл, алкілсульфоніл, алкіл-аміно, ді(С1-С8-алкіл)аміно, форміл, карбоксил, алкоксикарбоніл, алкоксикарбонілокси, алканоїлокси, феніл, карбамоїл, карбоксамід, ди-нижчий алкілкарбамоїлокси, феноксикарбонілокси групу, нижчий алкілендіокси, бензоїлокси, алкіл-СО-О-, алкіл-ОСО-, -CONH2, алкіл-О-СО-О- або алкіл-CO-NH-. Приклади арильних радикалів включають, наприклад, феніл, нафтил, біфеніл, інде ( ( ), індан ), фторфеніл, ди фторфеніл, бензил, бен зоїлоксифеніл, карбоетоксифеніл, ацетилфеніл, етоксифеніл, феноксифеніл, гідроксифеніл, карбоксифеніл, трифторметилфеніл, метоксіетилфеніл, ацетамідофеніл, толіл, ксиліл, диметилкарбамілфеніл та подібні. "Ph" або "РН" означає феніл. Термін "гетероарил", як використовується в даній заявці, представляє стійку п'яти або шестичленну моноциклічну або біциклічну ароматичну кільцеву систему, яка містить атоми вуглецю та від одного до трьох гетероатомів, вибраних з Ν, Ο та S. Гетероарильна група може бути приєднана при будь-якому гетероатомі або атомі вуглецю, що приводить до утворення стійкої структури. Приклади гетероарильних груп включають, але не обмежуються, бензофураніл, бензотіофеніл, піридиніл, піразиніл, піридазиніл, піримідиніл, тіофеніл, фураніл, імідазоліл, ізоксазоліл, оксазоліл, піразоліл, піроліл, тіазоліл, тіадіазоліл, триазоліл, бензимідазоліл, бензофураніл, бензотієніл, бензизоксазоліл, бензоксазоліл, бензопіразоліл, індоліл, бензотіазоліл, бензотіадіазоліл, бензотриазоліл або хінолініл. Переважні гетероарильні групи включають піридиніл, тіофеніл, фураніл та хінолініл. Коли гетероарильна група є заміщеною, гетероарильна група може мати від одного до трьох замісників, які незалежно вибрані з галогену, ОН, CN, меркапто, нітро, аміно, ціано, необов'язково заміщеного С 1-С8-алкілу, необов'язково заміщеного алкокси, алкілтіо, алкілсульфінілу, алкілсульфонілу, алкіл-аміно, ді(С1-С8-алкіл)аміно, формілу, карбоксилу, алкоксикарбонілу, алкоксикарбонілокси, алканоїлокси, фенілу, карбамоїлу, карбоксаміду, ди-нижчий алкілкарбамоїлокси, феноксикарбонілокси групи, нижчого алкілендіокси, бензоїлокси, алкіл-СО-О-, алкіл-О-СО-, -CONH2, алкіл-ОСО-Oабо алкіл-СО-NH-. Терміни "гетероцикл", "гетероциклічний" та "гетероцикліл" відносяться до необов'язково замі Під терміном "композиція" мається на увазі продукт, що містить вказані інгредієнти у вказаних 12 щеної, повністю або частково насиченої, ароматичної або неароматичної, циклічної групи, яка являє собою, наприклад, 4 - 7-членну моноциклічну, 711-членну (або 9-10-членну) біциклічну (або гетеробіцикліл) або 10 -15-членну трициклічну кільцеву систему, яка містить, принаймні, один гетероатом в, принаймні, одному кільці, що містить атоми вуглецю. Кожне кільце гетероциклічної групи, що містить гетероатом, може мати 1, 2 або 3 гетероатоми, вибрані з атомів азоту, кисню та сірки, де гетероатоми азоту та сірки також можуть бути необов'язково окиснені. Атоми азоту необов'язково можуть бути кватернізовані. Гетероциклічна група може бути приєднана при будь-якому гетероатомі або атомі вуглецю. Приклади моноциклічних гетероциклічних груп включають піролідиніл; оксетаніл; піразолініл; імідазолініл; імідазолідиніл; оксазоліл; оксазолідиніл; ізоксазолініл; тіазолідиніл; ізотіазолідиніл; тетрагідрофурил; піперидиніл; піперазиніл; 2оксопіперазиніл; 2-оксопіперидиніл; 2оксопіролідиніл; 4-піперидоніл; тетрагідропіраніл; тетрагідротіопіраніл; тетрагідротіопіраніл сульфон; морфолініл; тіоморфолініл; тіоморфолініл сульфоксид; тіоморфолініл сульфон; 1,3-діоксолан; діоксаніл; тієтаніл; тіїраніл; та подібні. Приклади біциклічних гетероциклічних груп (або гетеробіциклілів) включають хінуклідиніл; тетрагідроізохінолініл; дигідроізоіндоліл; дигідрохіназолініл (як наприклад 3,4-дигідро-4-оксо-хіназолініл); дигідробензофурил; дигідробензотієніл; дигідробензотіопіраніл; дигідробензотіопіраніл сульфон; дигідробензопіраніл; індолініл; ізохроманіл; ізоіндолініл; бензимідазоліл, бензтіазоліл; піпероніл; тетрагідрохінолініл; та подібні. Коли гетероарильна група є заміщеною, гетероцикліл незалежно може бути заміщений від однієї до п'яти, переважно від однієї до трьох, гр упами, вибраними з галогену, ОН, CN, меркапто, нітро, аміно, ціано, необов'язково заміщеного С1-С8-алкілу, необов'язково заміщеного алкокси, алкілтіо, алкілсульфінілу, алкілсульфонілу, алкіл-аміно, ді(С1-С8-алкіл)аміно, формілу, карбоксилу, алкоксикарбонілу, алкоксикарбонілокси, алканоїлокси, фенілу, карбамоїлу, карбоксаміду, ди-нижчий алкілкарбамоїлокси, феноксикарбонілокси групи, нижчого алкілендіокси, бензоїлокси, алкіл-СО-О-, алкіл-О-СО-, -CONH2, алкіл-О-СО-Оабо алкіл-CO-NH-. Термін "біарил" включає гетероарил, зв'язаний з фенілом, феніл, зв'язаний з гетероарилом (таким як тіофен, піридин та піразол) та феніл, зв'язаний з фенілом. Приклади феніл-фенілу, гетероарилфенілу та феніл-гетероарилу включають: кількостях, а також будь-який продукт, який вини 13 85569 кає, безпосередньо або побічно, з комбінації вказаних інгредієнтів у вказаних кількостях. Термін "об'єднане введення" включає спільне введення, де: 1) два або більше агентів вводять суб'єкту в, по суті, один і той же час; та 2) два або більше агентів вводять суб'єкту в різний час, з незалежними проміжками, які можуть або не можуть частково перекриватися або співпадати. Термін "суб'єкт", як використовується в даній заявці, відноситься до тварини, переважно ссавця, найбільш переважно людини, яка є об'єктом лікування, нагляду або експерименту. Термін "модулятор RXR", як використовується в даній заявці, відноситься до агоністів, часткових агоністів або антагоністів рецептора ретиноїда X. Переважно модулятор збільшує чутливість до інсуліну. Відповідно до одного аспекту, модулятор є агоністом RXR. Діабет, Синдром X та симптоми, пов'язані з ними, або їх ускладнення включають такі стани, як IDDM, NIDD M, IGT, IFG, ожиріння, нефропатія, невропатія, ретинопатія, атеросклероз, синдром полікістозного яєчника, гіпертензія, ішемія, інсульт, серцева хвороба, синдром подразненого кишечнику, запалення та катаракти. Приклади переддіабетичного стану включають IGT та IFG. З рівня техніки відомі способи визначення ефективних доз для терапевтичних та профілактичних цілей для описаних фармацевтичних композицій або описаних лікарських комбінацій, так чи інакше виготовлених в ти х же самих композиціях. Для терапевтичних цілей, термін "спільно ефективна кількість", як використовується в даній заявці, означає ту кількість кожної активної сполуки або фармацевтичного агента, самого по собі або в комбінації, яка викликає біологічну або лікарську реакцію в тканинній системі, тварині або людині, що шукає дослідник, ветеринар, медичний лікар або інший клінічній лікар, яка включає полегшення симптомів хвороби або розладу, що лікують. Для профілактичних цілей (тобто, інгібування початку або розвитку розладу) термін "спільно ефективна кількість" відноситься до тієї кількості кожної активної сполуки або фармацевтичного агента, самого по собі або в комбінації, яка інгібує у суб'єкта початок або розвиток розладу, яку шукає дослідник, ветеринар, медичний лікар або інший клінічній лікар, затримка цього розладу опосередкована модуляцією активності реабсорбції глюкози або іншої активності антидіабетичного агента або обох. Таким чином, даний винахід забезпечує комбінації двох або більше лікарських засобів, де, наприклад, (а) кожний лікарський засіб вводять в незалежно терапевтично або профілактично ефективній кількості; (b) принаймні, один лікарський засіб в комбінації вводять в кількості, яка є субтерапевтичною або суб-профілактичною, якщо вводять лише його, але є терапевтичною або профілактичною, коли його вводять в комбінації з другим або додатковим лікарським засобом відповідно до винаходу; або (с) обидва лікарські засоби вводять в кількості, яка є суб-терапевтичною або суб-профілактичною, якщо їх вводять по-одному, але є терапевтичною або профілактичною, коли їх вводять разом. 14 Термін "захисні групи" відноситься до тих компонентів, відомих з рівня техніки, які використовують для маскування функціональних груп; захисні групи можуть бути видалені протягом подальших синтетичних перетворень або за допомогою метаболічних або інших in vivo умов введення. Протягом будь-якого з процесів одержання сполук за даним винаходом, може бути необхідним та/або бажаним захистити чутливі або хімічно активні групи на будь-якій з молекул, яких це стосується. Це може бути досягнуто за допомогою традиційних захисних груп, таких як описано в [Protective Groups in Organic Chemistry, ed. J.F.W. McOmie, Plenum Press, 1973; та T.W. Greene & P.G.M. Wuts, Protective Groups in Organic Synthesis, Third Edition, John Wiley & Sons, 1999]. Захисні групи можуть бути видалені на придатній подальшій стадії, використовуючи способи, відомі з рівня техніки. Приклади гідроксил та діол захисних груп наведено нижче. Захист для гідроксильних груп включає метилові ефіри, заміщені метилові ефіри, заміщені етилові ефіри, заміщені бензилові ефіри та силілові ефіри. Заміщені метилові ефіри Приклади заміщених метилових ефірів включають метилоксиметил, метилтіометил, третбутилтіометил, (фенілдиметилсиліл)метоксиметил, бензилоксиметил, рметоксибензилоксиметил, (4метоксифенокси)метил, трет-бутоксиметил, 4пентенілоксиметил, силоксиметил, 2метоксіетоксиметил, 2,2,2-трихлоретоксиметил, біс(2-хлоретокси)метил, 2(триметилсиліл)етоксиметил, тетрагідропіраніл, 3бромтетрагідропіраніл, тетрагідротіопіраніл, 1метоксициклогексил, 4-метокситетрагідропіраніл, 4-метокситетрагідротіопіраніл, 4метокситетрагідротіопіраніл 8,8-діоксидо, 1-[(2хлор-4-метил)феніл]-4-метоксипіперидин-4-іл, 1,4діоксан-2-іл, тетрагідрофураніл, тетрагідротіофураніл та 2,3,3а,4,5,6,7,7а-октагідро-7,8,8-триметил4,7-метанобензофуран-2-іл. Заміщені етилові ефіри Приклади заміщених етилових ефірів включають 1-етоксіетил, 1-(2-хлоретоксі)етил, 1-метил-1метоксіетил, 1-метил-1-бензилоксіетил, 1-метил-1бензилокси-2-фторетил, 2,2,2-трихлоретил, 2триметилсилілетил, 2-(фенілселеніл)етил, третбутил, аліл, р-хлор феніл, р-метоксифеніл, 2,4динітрофеніл, бензил та ефіри поліетиленгліколю. Заміщені бензилові ефіри Приклади заміщених бензилових ефірів включають р-метоксибензил, 3,4-диметоксибензил, онітробензил, р-нітробензил, р-галобензил, 2,6дихлорбензил, р-ціанобензил, р-фенілбензил, 2та 4-піколіл, 3-метил-2-піколіл N-оксид, дифенілметил, p,p'-динітробензгідрил, 5-дибензосуберіл, трифенілметил, α-нафтилдифенілметил, рметоксифенілдифенілметил, ди(рметоксифеніл)фенілметил, три(рметоксифеніл)метил, 4-(4'бромфенацилокси)фенілдифенілметил, 4,4',4"трис(4,5-дихлорфталімідофеніл)метил, 4,4',4"трис(левуліноїлоксифеніл)метил, 4,4',4" 15 85569 трис(бензоїлоксифеніл)метил, 3-(імідазол-1ілметил)біс(4',4"-диметоксифеніл)метил, 1,1-біс(4метоксифеніл)-1'-піренілметил, 9-антрил, 9-(9феніл)ксантеніл, 9-(9-феніл-10-оксо)антрил, 1,3бензодитіолан-2-іл та бензизотіазоліл 8,8діоксидо. Силілові ефіри Приклади силілових ефірів включають триметилсиліл, триетилсиліл, триізопропілсиліл, диметилізопропілсиліл, діетилізопропілсиліл, диметилтексилсиліл, трет-бутилдиметилсиліл, третбутилди фенілсиліл, трибензилсиліл, три-рксилілсиліл, трифенілсиліл, дифенілметилсиліл та трет-бутилметоксифенілсиліл. Складні ефіри На додаток до простих ефірів, гідроксильна група може бути захищена як складний ефір. Приклади складних ефірів включають форміат, бензоїлформіат, ацетат, хлорацетат, ди хлорацетат, трихлорацетат, трифторацетат, метоксіацетат, трифенілметоксіацетат, феноксіацетат, рхлорфеноксіацетат, р-P-фенілацетат, 3фенілпропіонат, 4-оксопентаноат(левулінат), 4,4(етилендитіо)пентаноат, півалоат, адамантоат, кротонат, 4-метоксикротонат, бензоат, рфенілбензоат, 2,4,6-триметилбензоат(мезитоат) та ефіри поліетиленгліколю. Карбонати Приклади карбонатів включають метил, 9флуоренілметил, етил, 2,2,2-трихлоретил, 2(триметилсиліл)етил, 2-(фенілсульфоніл)етил, 2(трифенілфосфоніо)етил, ізобутил, вініл, аліл, рнітрофеніл, бензил, р-метоксибензил, 3,4диметоксибензил, о-нітробензил, р-нітробензил, Sбензил тіокарбонат, 4-етокси-1-нафтил, метил дитіокарбонат та карбонати поліетиленгліколю. Допоміжне розщеплення Приклади допоміжного розщеплення включають 2-йодобензоат, 4-азідобутират, 4-нітро-4метилпентаноат, о-(дибромметил)бензоат, 2формілбензолсульфонат, 2-(метилтіометоксі)етил карбонат, 4-(метилтіометокси)бутират та 2(метилтіометоксиметил)бензоат. Змішані ефіри Приклади змішаних ефірів включають 2,6дихлор-4-метилфеноксіацетат, 2,6-дихлор-4(1,1,3,3-тетраметилбутил)феноксіацетат, 2,4біс(1,1-диметилпропіл)феноксіацетат, хлордифенілацетат, ізобутират, моносукциноат, (Е)-2-метил2-бутеноат(тиглоат), о-(метоксикарбоніл)бензоат, р-Р-бензоат, α-нафтоат, нітрат, алкіл Ν,Ν,Ν',Ν' 16 тетраметилфосфородіамідат, N-фенілкарбамат, борат, диметилфосфінотіоїл та 2,4динітрофенілсульфенат. Сульфонати Приклади сульфонатів включають сульфат, метансульфонат(мезилат), бензилсульфонат та тозилат. Захист для 1,2- та 1,2-діолів Циклічні ацеталі та кеталі Приклади циклічних ацеталів та кеталів включають метилен, етиліден, 1-трет-бутилетиліден, 1фенілетиліден, (4-метоксифеніл)етилiден, 2,2,2трихлоретиліден, ацетонід (ізопропіліден), циклопентиліден, циклогексиліден, циклогептиліден, бензиліден, р-метоксибензиліден, 2,4диметоксибензиліден, 3,4-диметоксибензиліден та 2-нітробензиліден. Циклічні орто ефіри Приклади циклічних орто ефірів включають метоксиметилен, етоксиметилен, диметоксиметилен, 1-метоксіетиліден, 1-етоксіетиліден, 1,2диметоксіетиліден, α-метоксибензиліден, 1-(N,Nдиметиламіно)етиліден похідне, α-(N,Nдиметиламіно)бензиліден похідне та 2оксациклопентиліден. Похідні силілу Приклади похідних силілу включають групу дитрет-бутилсилілен та 1,3-(1,1,3,3тетраізопропілдисилоксаніліден) похідне. Інгібітори реабсорбції глюкози Одним з методів лікування гіперглікемії є виведення надлишкової глюкози безпосередньо із сечею, нормалізуючи таким чином концентрацію глюкози у крові. Наприклад, ко-транспортери натрію/глюкози (SGLT), що, в основному, знаходяться у хоріонічній мембрані кишечнику та нирок, є родиною протеїнів, що приймають активну участь у нормальному процесі абсорбції глюкози. Серед них, SGLT1 присутній в клітинах епітелію кишечнику та нирок [Lee at al., 1994], тоді як SGLT2 знайдено в епітелію нирок [You et al., 1995, MacKenzie et al., 1994]. Абсорбція глюкози у кишечнику відбувається, головним чином, через SGLT1, транспортер з високою афінністю та низькою здатністю до перенесення, із співвідношенням переносу Nа+:глюкоза - 2:1. SGLT2, відомий також як SAAT1, переносить Na+ та глюкозу у співвідношенні 1:1 та діє як транспортер із низькою афінністю та високою здатністю до перенесення. Ці SGLT охарактеризовані у Таблиці 1: Таблиця 1 Ізоформ SGLT1 SGLT2 SAAT1 Тканина Стехіометрія Тонкий ки2:1 шечник Нирки (SI, 2:1 S3) Нирки (S3) 1:1 Переважний субстрат D-глюкоза D-галактоза D-глюкоза D-галактоза Km*, in vitro TmG** in vitro Km*, in vivo од Дані відсутні Дані відсутні 0,39 7,9 0,3 D-глюкоза 1,64 83 6 *(мМ) для D-глюкози ** Максимальна швидкість перенесення пмоль/хв/мм 17 85569 1. Ниркова реабсорбція глюкози відбувається через SGLT1 та SGLT2 [Silverman et al., 1992; Deetjen et al., 1995]. Глюкоза у плазмі фільтрується у гломерулах та трансепітеліально реабсорбується у проксимальних тр убочках. SGLT1 та SGLT2 розташовані в апікальних плазматичних мембранах епітелію та отримують енергію із внутрішнього градієнту концентрацій натрію, що створюється АТР-насосами Na+/K+, розташованими у базолатеральній мембрані. Після реабсорбції підвищена цитозольна глюкоза переноситься до міжвузловини полегшеними транспортерами глюкози (GLUT1 та GLUT2). Тому інгібування SGLT зменшує рівень глюкози у плазмі шляхом пригнічення реабсорбції глюкози у нирках. Терапевтично або профілактично ефективну кількість інгібітору SGLT, наприклад, достатню для підвищення виведення глюкози із сечею, або для зниження вмісту глюкози у плазмі, у суб'єкта по відношенню до бажаної кількості на день, може бути легко визначена за допомогою способів, відомих з рівня техніки. Нещодавно було знайдено, що флоризин, природний глюкозид, що знаходиться у корі та стеблі Rosaceae (наприклад, яблук, груш та інш.), інгібує ко-транспортери Nа+-глюкози, розташовані у хоріонічній мембрані кишечнику та нирок. Шляхом інгібування активності ко-транспортеру Na+-глюкози, флоризин інгібує реабсорбцію глюкози у ниркових канальцях та сприяє виведенню глюкози таким чином, що рівень глюкози у плазмі зберігається на нормальному рівні протягом тривалого часу за допомогою підшкірного щоденного введення [Journal of Clinical Investigation, 1987, Vol.79, p.1510]. Інші інгібітори SGLT включають алкіл- та феніл-глюкозиди, 1-5-ізохінолінсульфоніл)-2метилпіперазин-НС1 (опосередковано через протеїн кіназу С), р-хлорртутьбензоат (РСМВ), Ν,Ν'дициклогексилкарбодіімід (DCCD), іони міді та кадмію та тривалентні лантаніди. В. Сполуки Винахід розкриває сполуки Формули (IV): (IV) в якій: присутня одна з пунктирних ліній між NR1 та X або між X та Y, або обидві пунктирні лінії відсутні; двоє з V, Μ та W являють собою Η та третій являє собою R1 являє собою Η або С1-4 алкіл; або R1 відсутній, коли присутня пунктирна лінія між NR1 та X; X являє собою N, С=О, СН або C-Q-Z; 18 Υ являє собою N-Q-Z або C-Q-Z, коли X являє собою Ν, С=О або СН; Υ являє собою СН, коли X являє собою C-Q-Z; Q=-(CH2)n-, де n=1 або 2; Ζ є заміщеним або незаміщеним, та вибраний з С3-7циклоалкілу, фенілу, 5- або 6-членного гетероарилу, який містить 1 або 2 гетероатоми, незалежно вибрані з Ν, Ο та S, біарилу, 9- або 10членного конденсованого біциклілу (такого як нафтил) та конденсованого гетеробіциклілу, де зазначений конденсований гетеробіцикліл містить 1-4 гетероатоми (та переважно 1-3 або 1-2 гетероатоми), незалежно вибрані з Ν, Ο та S; Ρ=Η, Сладил або (С1-6алкокси)карбоніл; або їх фармацевтично прийнятну сіль. Приклади переважних сполук Формули (IV) включають: (a) R1 являє собою Η або відсутній; (b) Z незалежно заміщений 1-3 замісниками, незалежно вибраними з С1-4алкокси, фенокси, С1-4алкілу, С3-6циклоалкілу, гало, гідрокси, ціано, аміно, С14алкілтіо, С 1-4алкілсульфонілу, С 1-4алкілсульфінілу, С1-4аміноалкілу, моно та діС 1-4алкіламіно, фенілу, С1-4алкіламіносульфонілу (SO2NHRX аміно(С1(NHSO2R), діС14алкілсульфоніл) 4алкіламіносульфінілу (SONHRR), С 1-4алкіламідо (NHCOR), С1-4алкілкарбамідо (CONHR), 5-6членного гетероциклілу, що містить 1-3 гетероатоми, незалежно вибрані з N, S та О; та де замісник(и) на Ζ може бути додатково незалежно заміщений 1-3 замісниками, незалежно вибраними з С1-4алкокси, С1-4алкілу, гало, гідрокси, ціано, аміно, моно або діС 1-4алкіламіно та С1-4алкілтіо; (с) Ζ являє собою 4-заміщений феніл, 3,4-дизаміщений феніл, бензгідрил, заміщений або незаміщений тієніл, біарил, бензофураніл, дигідробензофураніл, 4-заміщений піридил, бензо[b]тієніл, хроманіл, бензотіофеніл, інданіл, нафтил та 2,3-дигідробензо[1,4]діоксан; (d) обмеження (с), де Ζ незаміщений або заміщений 1-2 замісниками, незалежно вибраними з метокси, етокси, фтору, хлору, метилу, е тилу, пропілу, бутилу та ізопропілу; (e) Ζ являє собою біфеніл, 4-(3-піридил)феніл, 4-(2тієніл)феніл, 4-(1Н-піразол-1-іл)-феніл, (4етил)феніл, (4-пропіл)феніл, (4-метокси)феніл, дигідробензофуран-5-іл або дигідробензофуран-6іл; (f) R1 являє собою Н; (g) n означає 1; (h) R1 являє собою Η або відсутній, та n означає 1; (і) Ζ являє собою біфеніл, 4-(3-піридил)феніл, 4-(2тієніл)феніл, 4-(1Н-імідазол-1-іл)-феніл, 4-(1Нпіразол-1-іл)-феніл, (4-етил)феніл, (4пропіл)феніл, (4-метокси)феніл, дигідробензофуран-5-іл або дигідробензофуран-6-іл; та Ζ незаміщений або заміщений 1-2 замісниками, незалежно вибраними з метокси, етокси, фтору, хлору, метилу, етилу, пропілу, бутилу та ізопропілу; (j) обмеження (і) та R1 являє собою Н; (k) обмеження (і) та n означає 1; (1) W та Μ являють собою Н; (m) V та Μ являють собою Η; (n) Χ являє собою СН та Υ являє собою C-Q-Z; (о) X являє собою С-Q-Z та Υ являє собою СН; (р) та комбінації зазначеного вище. Переважні приклади сполук за винаходом включають: 3-(4-Етилбензил)-5-(β-Dглюкопіранозил)-1Η-індол; 5-(β-D-Глюкопіранозил) 19 85569 20 3-(4-метоксибензил)-1H-індол; 5-(β-DГлюкопіранозил)-3-[2-(4-метоксифеніл)-етил]-1Ніндол; та 3-(4-Етилбензил)-4-(β-D-глюкопіранозил)1Н-індол. Додаткові переважні сполуки включають сполуки, вибрані з 2-(4-Етилбензил)-4-(β-Dглюкопіранозил)-1Η-індолу; 3-[2-(2,3-Дигідро бензофуран-5-іл)-етил]-5-(β-D-глюкопіранозил)-1Ніндолу; 5-(β-D-Глюкопіранозил)-3-(5-етил-2-тієніл)1Η-індолу; 3-(4-Етилбензил)-4-(β-Dглюкопіранозил)-3Η-бензимідазолу; 3-(4Етилбензил)-4-(β-D-глюкопіранозил)-1,3-дигідробензоімідазол-2-ону та 3-(4-Етилбензил)-4-(β-Dглюкопіранозил)-3Η-бензотриазолу. Найбільш переважні сполуки вибрані з: 3-(4Етилбензил)-5-(β-D-глюкопіранозил)-1Η-індолу; 2(4-Етилбензил)-4-(β-D-глюкопіранозил)-1Н-індолу; 5-(β-D-Глюкопіранозил)-3-(5-метил-2-тієніл)-1Ηіндолу; 3-(4-Етилбензил)-4-(β-D-глюкопіранозил)3Η-бензимідазолу та 3-(4-Етилбензил)-4-(β-Dглюкопіранозил)-3Η-бензотриазолу. С. Способи синтезу. Один аспект винаходу описує сполуки формули (IV). Ці сполуки можуть бути одержані за допомогою традиційних способів органічного синтезу або матриці чи способів комбінаторного синтезу. Наступні схеми та хімічні Приклади 1-4 забезпечують загальну інструкцію. Схема 1 21 85569 Сполуки за даним винаходом, в яких X являє собою С-Н, Υ являє собою C-Q-Z (наприклад 3алкіл індол), можуть бути одержані, як наведено на Схемі 1. Сполуки формули 1, в яких R3 являє собою Η та Р1 являє собою Ν,Ν-діетилкарбаміл, можуть бути одержані обробкою натрієвої солі комерційно доступного 5-бром-1Н-індол-3карбоксальдегіду Ν,Ν-діетилкарбаміл хлоридом в безводному THF. Захищений індол може бути оброблений ілідами в стандартних умовах реакції Вітига з одержанням Ε/Ζ суміші сполук. Гідрогенізація алкену над оксидом платини (IV) (каталізатор Адама) в хлорованому розчиннику при 1 атмосфері забезпечує сполуки формули 2, в яких n означає 2. Сполука формули 1 також може бути оброблена арил бромідом магнію в THF з одержанням індолкарбінолу. Неочищений індолкарбінол може бути відновлений триетилсиланом та хлоридом олова в дихлорметані при -78°С з одержанням сполуки формули 2, в якій n означає 1. Захист з азоту індолу в сполуках формули 2, в яких n означає 1 або 2, може бути знятий обробкою основою, такою як гідроксид натрію, в етанолі, що кип'ятили зі зворотним холодильником, щоб видалити Ν,Νдіетилкарбамільну групу, з наступним повторним захистом трет-бутилдиметилсилільною (TBDMS) групою (Р2) за допомогою обробки третбутилдиметилсиліл хлоридом, використовуючи відомі методики, з одержанням похідного 5-бром індолу 5. Альтернативно, сполука формули 5, в якій n означає 1 (або похідні 4-броміндолу або похідні 5броміндолу чи 6-броміндолу), може бути одержана в три стадії з комерційно доступних вихідних сполук формули 3. Ацилювання Фріделя-Крафтса сполук формули 3 заміщеними бензоїл хлорида 22 ми, використовуючи кислоту Льюїса, таку як трихлодид алюмінію, в хлорованому розчиннику, такому як дихлорметан, з наступним відновленням карбонільної групи боргідридом натрію забезпечує сполуки формули 4. Азот індолу формули 4 може бути захи щений TBDMS групою, як викладено вище, з одержанням сполук формули 5, в яких n означає 1. Сполуки формули 5 активують для сполучення обробкою t-BuLi при -78°С в розчиннику, такому як THF, перед додаванням 2,3,4,6-тетра-О-бензил-pD-глюколактону, як описано Czemecki та Ville [J. Org. Chem. 1989, 53, 610-612]. Одержаний лактол може бути оброблений силанами, такими як триетилсилан, в розчиннику, такому як дихлорметан, при -30°С з одержанням сполук формули 6. TBDMS гр упа може бути видалена водною основою, такою як гідроксид натрію, в THF, що кип'ятили зі зворотним холодильником з одержанням сполук формули 7. Гідрогеноліз глюкопіранози 7 над гідроксидом паладію (каталізатор Пірлмана) при одній атмосфері може забезпечити сполуки формули 8, в яких Ρ являє собою Н. Натрієва сіль 7 може бути оброблена алкіл галогенідом з одержанням N-алкілованого (R1) продукту 9, який піддавали гідрогенолізу, як описано вище, щоб одержати сполуку формули 10, в якій Ρ являє собою Н. Подальша обробка сполук формули 8 або 10, в яких Ρ являє собою Н, одним еквівалентом алкіл хлорформіату або алканоїл хлориду в колідині, щоб селективно ацилювати 6-ОН групу глюкопіранози, може забезпечити сполуки формули 8 або 10, в яких Ρ являє собою ацил або алкоксикарбоніл. Схема 2 23 85569 Сполуки за даним винаходом, в яких Υ являє собою N-Q-Z, X являє собою Ν, С =О або С-Н, та R1 є таким, як визначено вище, можуть бути одержані, як наведено на Схемі 2, використовуючи методики, відомі з рівня техніки для описаних перетворень в процесі синтезу. Комерційно доступний N-(2-Бром-6-нітро-феніл)-ацетамід може бути нагрітий в кислих умовах для видалення ацетильної групи, потім алкілований заміщеними бензил, арил або гетероарил алкіл галогенідами, ацильований бензоїл або фенілацетил хлоридами, з наступним LAH або борановим відновленням, або відновно амінований заміщеними бензальдегідами в присутності ціаноборгідриду натрію з одержанням сполук формули 9. Нітрогрупа потім може бути відновлена, використовуючи реагенти, такі як хлорид олова (II) або залізо, в оцтовій кислоті, з одержанням сполук формули 11, де бром приєднаний в положенні V у пункті 1 формули винаходу. Альтернативно, спосіб може починатися з комерційно доступного 4-Бром-2-нітроаніліну, вводячи бічний ланцюг, що містить Z, як описано вище, з одержанням сполук формули 10, в яких R' являє собою -(CH2)nZ, потім відновлюючи нітрогрупу з одержанням сполук формули 11, де бром приєднаний в положення Μ у пункті 1 формули винаходу. З іншого боку, азот аніліну комерційно доступного 4-Бром-2-нітроаніліну може бути ацетильований або альтернативно захищений відповідною захисною групою, такою як толуолсульфоніл або бензолсульфоніл, з одержанням сполук формули 24 10, в яких R' є захисною групою. Нітрогрупа потім може бути відновлена до первинного аміну хлоридом олова (II) та потім алкілована обробкою заміщеними бензил, арил або гетероарил алкіл галогенідами, в основних умовах або відновно амінована заміщеними бензальдегідами в присутності ціаноборгідриду натрію. Альтернативно, первинний амін може бути ацильований бензоїл або фенілацетил хлоридами, з наступним LAH або борановим відновленням. Кінцеве видалення захисної гр упи з азоту, використовуючи методики, відомі з рівня техніки, може забезпечити сполуки формули 11, в яких бром приєднаний в положенні W у п ункті 1 формули винаходу. Сполуки формули 11 можуть, крім того, бути піддані реакції з утворенням сполук формули 12, 13 та 14. Ці перетворення можуть бути здійснені обробкою діаміну 1,1'-тіокарбонілдіімідазолом або дисульфідом вуглецю з одержанням сполуки формули 12 або трифосгеном, сечовиною або карбонілдіімідазолом з одержанням сполук формули 13. Альтернативно, діамін 11 може бути оброблений нітратом натрію в кислих умовах при температурах охолодження з одержанням сполук Формули 14. Метилування сполук формули 12 йодометаном в присутності основи може надати сполуки формули 16. Сполуки формули 13 можуть бути оброблені основою, такою як гідрид натрію, та алкіловані алкіл галогенідами з одержанням сполук формули 17, в яких R1 являє собою алкіл. Незаміщений азот сполуки формули 13 також може 25 85569 бути захи щений алкокси карбонільною групою, як описано Meanwell et. al. [J. Org. Chem. 1995, 60, 1565-1582], з одержанням сполук формули 17, в яких R1 є або етокси карбонільним компонентом , або t-бутоксикарбонільною групою. Утворення С-глікозидів може досягатися обробкою сполук формули 14, 16 або 17 (сполука 15 не включена) бутиллітієм при -78°С перед додаванням 2,3,4,6-тетра-О-бензил-β-D-глюколактону, з наступним відновленням одержаного напівацеталю в присутності надлишку триетилсилану та трифторид бору діетил етерату у відповідному розчиннику, такому як дихлорметан, як описано Czemecki та Ville [J. Org. Chem. 1989, 54, 610-612]. Сполуки формули 18, в яких R1 являє собою Н, можуть бути одержані видаленням захисних груп в основних умовах (для етокси карбонільної групи) або в кислих умовах (для третбутоксикарбонільної групи), з наступним дебензи 26 луванням гідроксильних гр уп, використовуючи каталізатори паладію в умовах гідрогенізації. Сполуки формули 18, в яких R1 являє собою алкільну груп у, або формули 19 можуть бути одержані дебензилуванням гідроксильних груп, використовуючи каталізатори паладію в умовах гідрогенізації. Сполуки формули 20, в яких R3 являє собою Н, можуть бути одержані за допомогою розщеплення 2-метилтіо групи, опосередкованого нікелем Ренея, як описано Townsend, et. al. [J. Med. Chem. 1994, 37, 2942-2949], з наступним дебензилуванням гідроксильних гр уп, використовуючи каталізатори паладію в умовах гідрогенізації. Подальша обробка одним еквівалентом алкіл хлорформіату або алканоїл хлориду в колідині, щоб селективно ацилювати 6-ОН групу глюкопіранози, може забезпечити сполуки формули 21, в яких Ρ являє собою ацил або алкоксикарбоніл. Схема 3 Сполуки за даним винаходом, в яких X являє собою C-Q-Z та Υ являє собою СН (наприклад 2алкіл індол), як визначено у визначеннях вище, можуть бути одержані, як наведено на Схемі 3. Сполуки формули 22 можуть бути одержані обробкою натрієвої солі комерційно доступних броміндолів (або 4-броміндолу, або 5-броміндолу, чи 6броміндолу) алкіл галогенідами в безводному THF. Одержаний 1-алкіл індол може бути перегрупований в 2-алкіл індол при 180°С в поліфосфорній кислоті в мікрохвильових умовах, з наступним захистом азоту індолу TBDMS групою (Р2) з одержанням сполуки формули 23. Утворення С-глікозидів може досягатися обробкою сполук формули 23 бутиллітієм при -78°С перед додаванням 2,3,4,6-тетра-О-бензил-β-Dглюколактону, як описано на Схемі 1. Одержаний лактол може бути оброблений силанами, такими як триетилсилан, в розчиннику, такому як дихлорметан, при -30°С з наступним депротектуванням TBDMS гр упи водною основою, такою як гідроксид натрію, в THF, що кип'ятили зі зворотним холодильником з одержанням сполук формули 24. Гідрогеноліз глюкопіранози 24 над гідроксидом паладію (каталізатор Пірлмана) при одній атмосфері може забезпечити сполуки формули 25, в яких Ρ являє собою Н. Натрієва сіль 24 може бути оброблена алкіл галогенідом з одержанням Nалкілованого (R1) продукту 26, з наступним гідрогенолізом, описано вище, щоб одержати сполуку формули 27, в якій Ρ являє собою Н. D. Додаткові антидіабетичні агенти Антидіабетичні агенти, які можуть бути використані відповідно до винаходу, як другий, третій або подальший антидіабетичний агент, в композиції, препараті або комбінаційному способі лікування (режим дозування) включають, але не обмежуються, класи та сполуки, що наведені, як приклад в Таблиці 2. 27 85569 Таблиця 2 Комбінаційні терапії з інгібіторами SGLT Механізм або Клас Бігуанід (клас) Лікарський засіб/Сполука метформін Фортамет (метформін XT) метформін GR метформін XL NN-414 фенофібрат/метформін комбо Стимулятор секреції глімепарид інсуліну (мех), Сульфонілсечов ини (клас) глібурид/глібенкламід комбо глібурид/метформін комбо гліпізид гліпізид/метформін комбо гліклазид хлорпропамід толбутамід толазамід Стимулятор секреції репаглінід інсуліну (мех), Меглітиніди (клас) натеглінід мітиглінід Інгібітори альфа- акарбоза глюкозидази (мех) міглітол в оглібоза еміглітат Інсулін та аналоги інсулін ліспро інсуліну (клас) інсулін гларгін інсулін детемір інсулін глулізин інсулін аспарт людський інсулін (Humulin R) людський інсулін (Novolin R) людський інсулін (Novolin BR) інсулін, цинков а суспензія (Humulin L) інсулін NHP (Humulin N) інсулін, цинков а суспензія (Novolin L) інсулін NHP (Novolin N) інсулін, цинков а суспензія (Humulin U) людський інсулін, суміш регулярного та NHP (Humulin 50/50) людський інсулін, суміш регулярного та NHP (Humulin 70/30) людський інсулін, суміш регулярного та NHP (Novolin 70/30) Інсулін для інгаляцій- Бксубера ного застосування (клас) AERx Insulin Diabetes Management System AIR inhaled insulin Інсулін для перора- Оралін льного застосування (клас) PPAR гамма (мех) розиглітазон розиглітазон/метформін комбо піоглітазон 28 Ізаглітазон (нетоглітазон, МСС-555) розиглітазон/сульфонілсечов ина рагаглітазар балаглітазон (NN-2344) R-483 рів огліт азон (CS-011) FK-614 SCD-DKY тезагліт азар Т131 CLX0921 LY-293111(VML-295) МВХ102 АА10090 CDDO(TP-155C) DRF-2189 РНТ-46 фарглітазар GW-7845 L-764406 NC-2100 PN 2022 (PN 2034) PPAR аль фа/гамма МK767/МK0767 (KRP 297) подв ійні агоністи (мех) мураглітазар (BMS-298585) тезагліт азар LY-818 оксегліт азар (EML-4156) LY-929 BVT-142 DRF-2655 DRF-4832 DRF-4158 LY-465608 КТ6-207 LSN-862 PPAR альфа агоніст Фенофібрат (мех) Гемфіброзил Клофібрат Ципрофібрат Бензафібрат K-111 LY518674 (LY674) KRP-101 NS-220 GW-9578 GW-7647 GW-9820 LF-200337 ST-1929 Wy-14643 PPAR дельта агоніст GW501516 (мех) GW-1514 L-165041 GW 8547 PPAR альфа/дельта GW-2433 подв ійний агоніст (мех) PPAR гамма/дельта жоден з останніх PPAR CEA подв ійний агоніст (мех) PPAR аль- CLX-0940 фа/гамма/дельта модулятор (мех) RXR агоніст (мех) 29 Стимулятор секреції Ексанатид для ін'єкцій інсуліну (мех), GLP-1 аналог (клас) Ексанатид LAR для ін'єкцій Ексанатид пероральний Ліраглутид GLP-1 агоніст (мех) ексенатид (АС2993) ліраглутид (NN2211) LY-307161 CJC-113 ZP10 GLP-1 ВІМ-51077 DPPIV інгібітор (мех) LAP-237 Р32/98 Р93/01 NVP-728 Інгібітор ліпази (мех) Орлістат ATL962 Активатор глюкокіна- Ro 28-1675 зи (мех) Ro 27-4375 бета-3 агоніст (мех) LY-337604 L-796568 CP-331684 CP-331679 CP-114271 Рафабегрон (ТАК-677) YM-178 N5984 GW427353 ШАТ інгібітор (мех) AZD-7806 SC-990 SC-017 GW-264 НМ74а/НМ74 агоніст Аципімокс (мех) Глюкокортикоїдний A348441 антагоніст (мех) A362947 CP394531 CP409069 СР472555 Інгібітор глікоген фо- NN4201 сфорилази (мех) Інгліфориб (СР368296) FXR антагоніст (мех) GW-4064 LXR агоніст (мех) GW-3965 Т-0901317 Т-0314407 FXR антагоніст (мех) GLP-1 аналог (клас) Альбугон GSK-Збета інгібітор (мех) PTP-lb інгібітор (мех) ISIS-113715 КР102 Агоніст рецепторів Прамлінтид (симлін/амілін) аміліну NO Очисник (мех) NOX-700 Інгібітор 11бета- BVT-3498 гідроксистероїд дегідрогенази Гормон пептиду YY АС162325 Глюкагон антагоніст NN-2501 (мех) РЕРСК інгібітор (мех) R1438 СоматотропінSOM230 рилізинг інгібуючий фактор (мех) СРТ-1 інгібітор (мех) ST1326 85569 30 Інгібітор карбоксипе- MLN-4760 птидази (мех) Аналог лептину Метрилептин (клас) Ε. Комбінації Винахід розкриває комбінаційну терапію, що включає введення інгібітора реабсорбції глюкози, такого як інгібітор SGLT, та одного або більше антидіабетичного агенту(ів) для лікування діабету або Синдрому X, або симптомів, пов'язаних з ними, або їх ускладнень. Продемонстрована ефективність інгібіторів SGLT в численних моделях NIDDM підтверджує корисність цих лікарських засобів тільки для лікування NIDDM в людях. Оскільки інгібітори реабсорбції глюкози мають механізм дії, відмінний від механізму дії інших антидіабетичних агентів, таких як модулятори RXR, описана комбінація може мати перевагу щодо зниження кількості кожного лікарського засобу, необхідної для досягнення спільної терапевтичної або фармацевтичної ефективності, пов'язаної з використанням кожного лікарського засобу самого по собі, таким чином знижуючи один або більше несприятливих побічних ефектів, які часто включають приріст маси, набряк, гіпертрофію серця, гепатогіпертрофію, гіпоглікемію або гепатотоксичність, або будь-яку їх комбінацію. Винахід забезпечує спосіб лікування діабету або Синдрому X, або їх ускладнень у суб'єкта, який включає введення зазначеному суб'єкту спільно ефективної кількості інгібітора реабсорбції глюкози в комбінації із спільно ефективною кількістю антидіабетичного агента, такого як модулятор RXR. В одному аспекті винаходу, антидіабетичним агентом є агоніст RXR або антагоніст RXR, що збільшує чутливість до інсуліну у суб'єкта. Наприклад, сенсибілізатор інсуліну може збільшува ти толерантність до глюкози у суб'єкта в пероральному випробуванні на толерантність до глюкози. Переважно, діабет або Синдром X, або симптоми, пов'язані з ними, або їх ускладнення вибрані з IDDM, NIDD M, IGT та IFG. Даний винахід також забезпечує фармацевтичну композицію, що містить один або більше інгібіторів реабсорбції глюкози (самих по собі або в комбінації з одним або більше антидіабетичними агентами) та фармацевтично прийнятний носій. В одному аспекті винаходу, антидіабетичним агентом є агоніст RXR або антагоніст RXR, що збільшує чутливість до інсуліну у суб'єкта. Зокрема, інгібітором реабсорбції глюкози є інгібітор SGLT1 та/або SGLT2. Для використання в медицині, сіль або солі сполук Формули (IV) відносяться до нетоксичної "фармацевтично прийнятної солі або солей". Проте, інші солі можуть бути корисні при одержанні сполук відповідно до даного винаходу або їх фармацевтично прийнятних солей. Характерні органічні або неорганічні кислоти включають, але не обмежуються, соляну кислоту, бромистоводневу кислоту, йодистоводневу кислоту, перхлорну кислоту, сірчану кислоту, азотну кислоту, фосфорну кислоту, оцтову кислоту, пропіонову кислоту, гліколеву кислоту, молочну кислоту, бурштинову кислоту, малеїнову кислоту, фу 31 85569 марову кислоту, яблучну кислоту, винну кислоту, лимонну кислоту, бензойну кислоту, мигдальну кислоту, метансульфонову кислоту, гідроксіетансульфонову кислоту, бензолсульфонову кислоту, щавлеву кислоту, памову кислоту, 2нафталенсульфонову кислоту, ртолуолсульфонову кислоту, циклогексансульфамінову кислоту, саліцилова кислоту, цукрову кислоту або трифтороцтову кислоту. Характерні основні/кислотні солі включають, але не обмежуються, солі бензатину, хлорпрокаїну, холіну, діетаноламіну, етилендіаміну, меглуміну, прокаїну, алюмінію, кальцію, літію, магнію, калію, натрію або цинку. Сполуки Формули (IV) або їх фармацевтично прийнятна сіль можуть включати їх внутрішньомолекулярну сіль або їх сольват, або гідрат. F. Введення, препарати та дозування Корисність розкритих сполук, композицій та комбінацій для лікування розладів в метаболізмі глюкози та ліпідів може бути визначена відповідно до методик, добре відомих з рівня техніки (див. посилання, наведені нижче), а також і всіх методик, описаних в патентах [US 5424406, 5731292, 5767094, 5830873, 6048842, WO01/16122 та WO01/16123], які включені в дану заявку за допомогою посилання. Сполука може бути введена пацієнту будь-яким традиційним шляхом введення, включаючи, але не обмежуючись, внутрішньовенне, пероральне, підшкірне, внутрішньом'язове, інтрадермальне та парентеральне введення. Переважно, препарати призначені для перорального введення. Даний винахід також забезпечує фармацевтичні композиції, що містять один або більше інгібіторів реабсорбції глюкози та один або більше модуляторів RXR в сполученні з фармацевтично прийнятним носієм. Щоденне дозування продуктів може змінюватися в широкому діапазоні від 1 до 1000мг для дорослої людини на день. Для перорального введення композиції переважно забезпечені у формі таблеток, що містять 0,01, 0,05, 0,1, 0,5, 1,0, 2,5, 5,0, 10,0, 15,0, 25,0, 50,0, 100, 150, 200, 250 або 500 міліграм активного інгредієнта для симптоматичного регулювання дозування для пацієнта, якого лікують. Сполуки можуть бутивведені в режимі 1-2 рази на день. Проте, дозування може змінюватися, в залежності від потреб пацієнтів, тяжкості стану, що лікують, та сполуки, що застосовують. Може використовува тися або щоденне введення, або постперіодичне дозування. Переважно ці композиції знаходяться у формах одиничного дозування, таких як таблетки, пілюлі, капсули, порошки, гранули, стерильні парентеральні розчини або суспензії, дозований аерозоль або рідкі спреї, краплі, ампули, автоінжекторні пристрої або супозиторії; для перорального, парентерального, інтраназального, під'язикового або ректального введення, або для введення шляхом інгаляції або вдування. Альтернативно, композиція може бути представлена у формі, прийнятній для введення один раз на тиждень або один раз на місяць; наприклад, нерозчинна сіль активної сполуки, така як сіль деканової кислоти, може бути пристосована, щоб забезпечити запасну підготовку для внутрі 32 шньом'язової ін'єкції. Для одержання твердих композицій, таких як таблетки, основний активний інгредієнт або інгредієнти змішують з фармацевтичним носієм, наприклад традиційними таблетковими інгредієнтами, такими як кукурудзяний крохмаль, лактоза, сахароза, сорбіт, тальк, стеаринова кислота, стеарат магнію, фосфат дикальцію або смоли, та іншими фармацевтичними розріджувачами, наприклад водою, щоб отримати тверду попередню композицію, яка містить однорідну суміш одного або більше інгібіторів реабсорбції глюкози та одного або більше антидіабетичних агентів або їх фармацевтично прийнятної солі. Посилання на ці попередні композиції, як на однорідні, означає, що активний інгредієнт або інгредієнти рівномірно розподілені в усій композиції, так що композиція легко може бути розділена на однаково ефективні форми дозування, такі як таблетки, пілюлі та капсули. Потім цю тверду попередню композицію розділяють на види форм одиничної дози, які описані вище, що містять від 0,1 до приблизно 500мг активного інгредієнта або інгредієнтів за даним винаходом. Таблетки або пілюлі нових композицій можуть бути покриті або комбіновані іншим шляхом, щоб забезпечити форму дозування, віддаючи перевагу пролонгованій дії. Наприклад, таблетка або пілюля може містити внутрішнє дозування та зовнішній компонент дозування, останній буде у формі оболонки над першим. Два компоненти можуть бути відділені за допомогою кишкового прошарку, що підходить, щоб не піддаватися дезінтеграції в шлунку та дозволити вн утрішньому компоненту пройти непошкодженим в дванадцятипалу кишку або бути затриманим при вивільненні. Для таких кишкових прошарків або покриттів можуть бути використані різноманітні речовини, такі речовини включають ряд полімерних кислот з такими речовинами як шелак, ацетиловий спирт та ацетат целюлози. Рідкі форми, в яких нові композиції за даним винаходом можуть бути поєднані для введення перорально або за допомогою ін'єкції, включають водні розчини, прийнятні ароматизовані сиропи, водні або маслянисті суспензії та ароматизовані емульсії з харчовими маслами, такими як бавовняне масло, масло сезаму, кокосове масло або арахісове масло, а також еліксири та подібні фармацевтичні наповнювачі. Прийнятні диспергуючі або суспендуючі агенти для водних суспензій включають синтетичні та природні смоли, такі як трагакант, гуміарабік, альгінат, декстран, натрієва карбоксиметилцелюлоза, метилцелюлоза, полівінілпіролідон або желатин. Рідкі форми в прийнятно ароматизованих суспендуючи х або диспергуючих агентах також можуть включати синтетичні та природні смоли, наприклад, трагакант, гуміарабік, метилцелюлозу та подібні. Для парентерального введення бажані стерильні суспензії та розчини. Коли бажаним є внутрішньовенне введення, використовують ізотонічні препарати, які звичайно містять прийнятні консерванти. Переважно, комбінації одного або більше інгібіторів реабсорбції глюкози за даним винаходом, самі по собі або в комбінації з одним або більше додатковим антидіабетичним агентом, можуть 33 85569 бути введені в одиничній денній дозі, або кількість денного дозування може бути введена розділеними дозами два, три або чотири рази на день. Крім того, один або більше інгібіторів реабсорбції глюкози та/або один або більше антидіабетичних агентів відповідно до даного винаходу можуть бути введені в інтраназальній формі за допомогою місцевого використання прийнятних інтраназальних засобів або за допомогою трансдермальних пластирів, які добре відомі кваліфікованому фа хівцю в даній галузі техніки. При введенні у формі трансдермальної системи доставки дозоване введення, звичайно, буде переважно безперервним, ніж переривчастим, протягом усього режиму дозування. Наприклад, для перорального введення у формі таблетки або капсули активний лікарський компонент може бути поєднаний з пероральним, нетоксичним фармацевтично прийнятним інертним носієм, таким як етанол, гліцерин, вода та їм подібні. Крім того, коли бажано або необхідно, прийнятні зв'язуючі речовини; змащуючі речовини, агенти дезинтеграції та барвники також можуть бути поєднані в суміш. Прийнятні зв'язуючі речовини включають, без обмеження, крохмаль, желатин, природні цукри, такі як глюкоза або беталактоза, кукурудзяні підсолоджувачі, природні та синтетичні смоли, такі як гуміарабік, трагакант або олеат натрію, стеарат натрію, стеарат магнію, бензоат натрію, ацетат натрію, хлорид натрію та їм подібні. Дезинтеграторы включають, без обмеження, крохмаль, метилцелюлозу, агар, бентоніт, ксантанову смолу та їм подібні. Коли даний винахід направлений на введення комбінації, сполуки можуть бути спільно введені одночасно, послідовно або в одній фармацевтичній композиції. Коли сполуки вводять окремо, кількість дозувань кожної сполуки, надана на день, не обов'язково може бути такою ж, наприклад, коли одна сполука може мати більшу тривалість активності, та, таким чином, буде введена менш часто. Оптимальні дозування для введення можуть бути легко визначені кваліфікованими фахівцями в даній галузі техніки та будуть змінюватися в залежності від конкретної сполуки, що використовують, концентрації препарату, способу введення та розвитку хворобливого стану. Крім того, чинники, пов'язані з індивідуальним пацієнтом, якого лікують, включаючи вік пацієнта, вагу, режим харчування та час введення, призведуть до необхідності пристосувати дозування. Нові композиції за даним винаходом також можуть бути введені у формі ліпосомних систем доставки, таких як малі одношарові везикули, великі одношарові везикули та багатошарові везикули. Ліпосоми можуть бути утворені з різноманітності ліпідів, включаючи, але не обмежуючись, амфіпатичні ліпіди, такі як фосфатидилхоліни, сфінгомієліни, фосфатидилетаноламіни, фосфатидилхоліни, кардіоліпіни, фосфатидилсеріни, фосфатидилгліцерини, фосфатидні кислоти, фосфатидилінозитоли, пропани діацил триметиламонію, пропани діацил диметиламонію та стеариламін, нейтральні ліпіди, як наприклад тригліцериди, та їх комбінації. Вони можуть або містити холестерин або можуть бути вільними від холестерину. 34 З Формули (IV) та інших наведених формул очевидно, що деякі сполуки в композиціях за винаходом можуть мати один або більше асиметричних атоми вуглецю в їх стр уктурі. Мається на увазі, що стереохімічно чисті ізомерні форми сполук, а також їх рацемати, включені в межі даного винаходу. Стереохімічно чисті ізомерні форми можуть бути одержані, використовуючи методики, відомі з рівня техніки. Діастереоізомери можуть бути розділені за допомогою фізичних способів розділення, таких як фракційна кристалізація, та хроматографічних способів, та енантіомери можуть бути відділені один від одного за допомогою селективної кристалізації діастереомерних солей з оптично активними кислотами або основами, або хіральною хроматографією. Чисті стереоізомери також можуть бути синтетично одержані з відповідних стереохімічно чистих ви хідних речовин, або використовуючи стереоспецифічні реакції. Деякі сполуки в композиціях за даним винаходом можуть мати різні індивідуальні ізомери, як наприклад транс та цис, та різні альфа та бета приєднання (нижче та вище намальованої площини). Крім того, якщо способи одержання сполук за даним винаходом дають суміш стереоізомерів, ці ізомери можуть бути розділені традиційними способами, такими як препаративна хроматографія. Сполуки можуть бути одержані у формі індивідуального стереоізомеру або в рацемічній формі, як суміш декількох можливих стереоізомерів. Нерацемічні форми можуть бути одержані або синтезом, або розділенням. Сполуки можуть, наприклад, бути розділені на їх складові енантіомери стандартними способами, такими як утворення діастереомерних пар шляхом утворення солі. Сполуки також можуть бути розділені за допомогою ковалентного сполучення з хіральною допоміжною речовиною, з наступним хроматографічним розділенням та/або кристалографічним розділенням та видаленням хіральної допоміжної речовини. Альтернативно, сполуки можуть бути розділені, використовуючи хіральну хроматографію. Якщо не зазначено інше, мається на увазі, що в межі даного винаходу включені всі такі ізомери або стереоізомери per se, а також суміші цис та транс ізомерів, суміші діастереомерів та рацемічні суміші енантіомерів (оптичні ізомери). Терапевтичний ефект інгібітора реабсорбції глюкози, введеного в комбінації з одним або більше антидіабетичним агентом(ами) при лікуванні діабету, Синдрому X, або симптомів, пов'язаних з ними, або їх ускладнень, може бути показаний за допомогою способів, відомих з рівня техніки. Мається на увазі, що подальші приклади комбінаційного лікування з інгібіторами SGLT та іншими антидіабетичними агентами, такими як модулятори RXR, наведено для ілюстрації винаходу, не обмежуючи його. G. Хімічні приклади синтезу. Один аспект винаходу розкриває сполуки формули (IV), як описано вище в Короткому описі суті винаходу, описі та доданій формулі винаходу. Ці описані сполуки можуть бути одержані відповідно до традиційних способів синтезу органічної хімії або матриці чи способів комбінаторного хімії. Схе 35 85569 ми та Приклади 1-4, наведені нижче, забезпечують загальну інструкцію та детальні приклади того, як описані сполуки можуть бути одержані. Спектри 1Н ЯМР були виміряні на спектрометрі Brucker AC-300 (300МГц), використовуючи тетраметилсилан (TMS), як внутрішній стандарт. Приклад 1 3-(4-Етилбензил)-5-(β-D-глюкопіранозил)-1Ηіндол A. 5-Бром-3-форміл-індол-1-карбонової кислоти діетиламід: До суспензії гідриду натрію (0,93г, 37ммоль) в безводному THF (75мл) по краплям додавали розчин 5-бром-1Н-індол-3-карбальдегіду (7,5г, 34ммоль) в безводному THF (60мл) при 0°С. Після перемішування при 0°С протягом 15хв. в реакційну суміш по краплям додавали Ν,Νдіетилкарбаміл хлорид (5,0г, 37ммоль). Суміш нагрівали до кімнатної температури та перемішували протягом ночі. Реакцію потім гасили водою та екстрагували етил ацетатом. Органічні екстракти промивали сольовим розчином, сушили над безводним сульфатом натрію та концентрували у вакуумі. Залишок кристалізували з ефір/гексан, одержуючи зазначену у заголовку сполуку (8,75г, 80%) у вигляді білої твердої речовини. B. 5-Бром-3-(4-етил-бензил)-індол-1карбонової кислоти діетиламід: До розчину зі Стадії А (3,3г, 10ммоль) в 20мл безводного THF по краплям додавали 0,5Μ розчин броміду 4етилфенілмагнію в безводному THF (22мл, 11ммоль) при 0°С. Реакційну суміш продовжували перемішува ти при 0°С протягом 30хв., гасили насиченим розчином хлориду амонію та екстрагували етил ацетатом. Органічні екстракти сушили над сульфатом натрію та концентрували у вакуумі. Неочищений продукт безпосередньо використовували на наступній стадії. До розчину неочищеного індолкарбінолу в 20мл дихлорметану додавали триетилсилан (1,16г, 10,0ммоль) при -78°С, з наступним додаванням 1,0Μ розчину хлориду олова в ди хлорметані (20мл, 20ммоль). Реакційну суміш продовжували перемішувати при -78°С протягом 20хв., гасили водою та нагрівали до кімнатної температури. Після екстракції дихлорметаном органічні екстракти сушили над сульфатом натрію, концентрували у вакуумі та хроматографували на силікагелі, елююючи етил ацетат/гексан (10:100), одержуючи зазначену у заголовку сполуку (3,4г, вихід: 82%) у вигляді білої твердої речовини. C. 5-Бром-3-(4-етил-бензил)-1Н-індол: Сполуку, одержану на Стадії В (3,4г, 8,2ммоль), розчиняли в етанолі (60мл) та 25% водному гідроксиді натрію (20мл) та одержаний розчин кип'ятили зі зворотним холодильником протягом 3 годин. Після охолодження до кімнатної температури суміш розбавляли водою (60мл), концентрували у вакуумі, 36 щоб видалити більшу частину етанолу, та екстрагували етил ацетатом. Органічні екстракти промивали водою та сольовим розчином, сушили над безводним сульфатом натрію та концентрували у вакуумі. Неочищений продукт очищали за допомогою хроматографії на силікагелі, елююючи етил ацетат/гексан (1:4), одержуючи зазначену у заголовку сполуку (2,0г, 79%) у вигляді білих голкоподібних кристалів. D. 5-Бром-1-(трет-бутил-диметил-силаніл)-3(4-етил-бензил)-1Η-індол: До суспензія гідриду натрію (0,12г, 4,8ммоль) в безводному THF (2мл) по краплям додавали розчин сполуки, одержаної на Стадії С (1,28г, 4,0ммоль), в безводному THF (6мл) при 0°С. Після перемішування при 0°С протягом 30хв. в реакційну суміш по краплям додавали 1,0Μ розчин трет-бутил-хлор-диметилсилану в безводному THF (4,5мл 4,5ммоль). Суміш нагрівали до кімнатної температури та перемішували протягом ночі. Потім реакцію гасили з водою та екстрагували етил ацетатом. Органічні екстракти промивали сольовим розчином, сушили над безводним сульфатом натрію та концентрували у вакуумі. Неочищений продукт очищали за допомогою хроматографії на силікагелі, елююючи етил ацетат/гексан (0,5:100), одержуючи зазначену у заголовку сполуку (1,75г 100%) у вигляді світложовтого масла. Е. 3-(4-Етилбензил)-5-(2,3,4,6-тетра-O-бензилβ-D-глюкопіранозил)-1-(трет-бутил-диметилсиланіл)-1Н-індол: До перемішаного розчину сполуки, одержаної на Стадії D (1,75г, 4,0ммоль), в сухому THF (2мл) при -78°С додавали 1,7Μ розчин трет-бутил літію в гептані (4,7мл, 8,0ммоль) протягом 15хв. Після перемішування протягом 30хв. додавали розчин 2,3,4,6-тетра-О-бензил-β-Dглюколактону (4,3г, 8,0ммоль; одержаний, як описано [Benhaddou, R.; Carbohydrate Research 1994, 260, 243-250]) в сухому THF (10мл) при -78°С протягом 15хв. Реакційну суміш перемішували при 78°С протягом 1 години (розвиток реакції контролювали за допомогою ТШХ). Після завершення реакції реакційну суміш гасили насиченим водним NH4CI (5мл), нагрівали до кімнатної температури та реакційну суміш розбавляли етил ацетатом. Органічні екстракти промивали водою та сольовим розчином, сушили над безводним сульфатом натрію та концентрували у вакуумі. Неочищений продукт очищали за допомогою хроматографії на силікагелі, елююючи етил ацетат/гексан (1:4), одержуючи суміш бажаного лактолу та непрореагувавшого 2,3,4,6-те тра-О-бензил-β-D-глюколактону (2,8г, ~50% бажаного лактолу) у вигляді світлокоричневого масла. Цю суміш безпосередньо використовували на наступній стадії без подальшого очищення. До розчину одержаної вище суміші (2,8г) в дихлорметані (20мл) додавали триетилсилан (0,5мл, 3,2ммоль) при -30°С, з наступним додаванням трифторборанового діетилового ефіру (0,2мл, 1,6ммоль). Після перемішування при від -30 до 20°С протягом 1 години, коли аналіз ТШХ показав, що реакція завершена, реакцію гасили додаванням насиченого водного NаНСО3 (3мл). Суміш нагрівали до кімнатної температури та перемішу 37 85569 вали протягом 1 години. Реакційну суміш екстрагували етил ацетатом. Органічні екстракти промивали водою та сольовим розчином, сушили над безводним сульфатом натрію та концентрували у вакуумі. Неочищений продукт очищали за допомогою хроматографії на силікагелі, елююючи етил ацетат/гексан (1:4), одержуючи зазначену у заголовку сполуку (0,68г, 19% для двох стадій) у вигляді жовтого масла. F. 3-(4-Етилбензил)-5-(2,3,4,6-тетра-O-бензилβ-D-глюкопіранозил)-1Н-індол: Сполуку зі Стадії Ε (0,68г, 0,78ммоль) розчиняли в THF (15мл) та 25% водному гідроксиді натрію (5мл) та одержаний розчин кип'ятили зі зворотним холодильником протягом 3 годин. Після охолодження до кімнатної температури суміш розбавляли водою (30мл) та екстрагували етил ацетатом. Органічні екстракти промивали водою та сольовим розчином, сушили над безводним сульфатом натрію та концентрували у вакуумі. Неочищений продукт очищали за допомогою хроматографії на силікагелі, елююючи етил ацетат/гексан (1:3), одержуючи зазначену у заголовку сполуку (0,5г, 85%) у вигляді білої твердої речовини. G. 3-(4-Етилбензил)-5-(β-D-глюкопіранозил)1H-індол: Розчин зі Стадії F (0,30г, 0,4ммоль) в етанолі (10мл) та етил ацетаті (20мл) гідрогенізували над 10% каталізатора Пірлмана (0,30г) при 14 фунт/дюйм 2 Н2 протягом 40 годин. Каталізатор видаляли фільтруванням та фільтрат концентрували у вакуумі. Неочищений продукт очищали за допомогою хроматографії на силікагелі, елююючи метанол/хлороформ (10:100), одержуючи зазначену у заголовку сполук у (0,04г, 25%) у вигляді білої твердої речовини. 1H ЯМР (300МГц, CD3OD) δ 7,51 (s, 1H), 7,32 (d, J=8,52Гц, 1H), 7,19-7,15 (m, 3H), 7,06 (d, J=7,87Гц, 2H), 6,95 (s, 1H), 4,18-4,15 (m, 1H), 4,04 (s, 2H), 3,87 (d, J=12,2Гц, 1Н), 3,71-3,65 (m, 1H), 3,53-3,48 (m, 2H), 3,45-3,41 (m, 2H), 2,58 (q, J=7,58Гц, 2Н), 1,19 (t, J=7,65Гц, 3Н). MS: m/z (M+Na) 420. Приклад 2 5-(β-D-Глюкопіранозил)-3-(4-метоксибензил)1Н-індол Зазначену у заголовку сполуку одержували у вигляді білої твердої речовини з 5-бром-3-форміліндол-1-карбонової кислоти діетиламіду (Приклад 1, Стадія А) та броміду 4-метоксифеніл-магнію за допомогою такої ж методики, як описано в Прикладі 1, Стадії В-G). 1H ЯМР (300МГц, CD3OD) δ 7,49 (s, 1H), 7,32 (d, J=8,20Гц, 1H), 7,19-7,15 (m, 3H), 6,95 (s, 1H), 6,79 (d, J=8,55Гц, 2Н), 4,18-4,15 (m, 1H), 4,02 (s, 2H), 3,88-3,85 (m, 1H), 3,74 (s, 3H), 3,70-3,66 (m, 1H), 3,50-3,48 (m, 2H), 3,42-3,35 (m, 2H). MS: m/z (M+Na) 422. Приклад 3 38 5-(β-D-Глюкопіранозил)-3-[2-(4-метоксифеніл)етил]-1Η-індол Α. 5-Бром-3-[2-(4-метокси-феніл)-етил]-індол1-карбонової кислоти діетиламід: До розчину 4метоксибензил трифенілфосфонію хлориду (7,5г, 18ммоль) в безводному THF (75мл) при -78°С додавали LDA (9,0мл, 18ммоль) та одержану реакційну суміш залишали перемішуватися при -78°С протягом 1 години. Після цього додавали 5-бром3-форміл-індол-1-карбонової кислоти діетиламід (1,9г, 6ммоль, Приклад 1, Стадія А) та одержану реакційну суміш залишали перемішуватися при 78°С протягом 1 години та потім нагрівали до кімнатної температури, перемішуючи протягом ночі. Реакційну суміш виливали в 1N розчин НСl та екстрагували етил ацетатом. Об'єднані етил ацетатні екстракти промивали сольовим розчином, сушили над безводним сульфатом натрію та концентрували у вакуумі. Неочищений продукт очищали за допомогою хроматографії на силікагелі, елююючи етил ацетат/гексан (1:4), одержуючи суміш алкенів (2,3г, 90%, E:Z~1:1) у вигляді коричневого масла. Розчин одержаних вище алкенів (2,3г, 5,4ммоль) в дихлорметані (100мл) гідрогенізували над каталізатором Адама (300мг) під Н2 (15фунт/дюйм) протягом 2 годин. Каталізатор видаляли фільтруванням та фільтрат концентрували у вакуумі. Неочищений продукт очищали за допомогою хроматографії на силікагелі, елююючи етил ацетат/гексан (1:4), одержуючи зазначену у заголовку сполуку (1,43г, 62%) у вигляді безбарвного масла. B. 5-Бром-3-[2-(4-метокси-феніл)-етил]-1Ніндол: Сполуку зі Стадії В (1,43г, 3,3ммоль) розчиняли в етанолі (30мл) та 25% водному гідроксиді натрію (10мл) та одержаний розчин кип'ятили зі зворотним холодильником протягом 3 годин. Після охолодження до кімнатної температури суміш розбавляли водою (30мл), концентрували у вакуумі, щоб видалити більшу частину етанолу, та екстрагували етил ацетатом. Органічні екстракти промивали водою та сольовим розчином, сушили над безводним сульфатом натрію та концентрували у вакуумі. Неочищений продукт очищали за допомогою хроматографії на силікагелі, елююючи етил ацетат/гексан (1:4), одержуючи зазначену у заголовку сполуку (1,0г, 91%) у вигляді світлокоричневого масла. C. 5 -Бром-1-(трет-бутил-диметил-силаніл)-3[2-(4-метокси-феніл)-етил]-1Н-індол: До суспензії гідриду натрію (0,081г, 4,0ммоль) в безводному THF (2мл) по краплям додавали розчин зі Стадії С (0,85г, 2,7ммоль) в безводному THF (3мл) при 0°С. Після перемішування при 0°С протягом 30хв. в реакційну суміш по краплям додавали 1,0Μ розчин трет-бутил-хлор-диметил-силану в безводному THF (3,2мл, 3,2ммоль). Суміш нагрівали до кімнатної температури та перемішували протягом ночі. Потім реакцію гасили водою та екстрагували етил 39 85569 ацетатом. Органічні екстракти промивали сольовим розчином, сушили над безводним сульфатом натрію та концентрували у вакуумі. Неочищений продукт очищали за допомогою хроматографії на силікагелі, елююючи етил ацетат/гексан (0,5:100), одержуючи зазначену у заголовку сполуку (0,92г, 79%) у вигляді світло-жовтого масла. D. 5-(β-D-Глюкопіранозил)-3-[2-(4метоксифеніл)-етил]-1H-індол: Зазначену у заголовку сполуку одержували у вигляді білої твердої речовини із сполуки зі Стадії С за допомогою такої ж методики, як описано в Прикладі 1, Стадії Е, F та G. 1Н ЯМР (300МГц, CD3OD) δ 7,58 (s, Ш), 7,31 (d, J=8,06Гц, 1H), 7,18 (dd, J=8,39, 1,59Гц, 1H), 7,10 (dd, J=6,63, 2,16Гц, 2H), 6,92 (s, 1H), 6,81 - 6,78 (m, 2H), 4,21 (d, J=8,99Гц, 1H), 3,91 - 3,87 (m, 1H), 3,75 (s, 3H), 3,73 -3,69 (m, 1H), 3,54 - 3,51 (m, 2H), 3,49 - 3,45 (m, 2H), 3,00 - 2,98 (m, 2H), 2,94 - 2,90 (m, 2H). MS: m/z (M+Na) 436. Приклад 4 3-(4-Етилбензил)-4-(β-D-глюкопіранозил)-1Ηіндол A. (4-Бром-1Н-індол-3-іл)-(4-етил-феніл)метанон: До суспензії АІСl3 (3,0г, 22,5ммоль) в дихлорметані (50мл) додавали розчин 4броміндолу (2,21г, 11,3ммоль) в дихлорметані (25мл) при кімнатній температурі протягом 20хв., з наступним додаванням розчину 4-етил-бензоїл хлориду (2,5мл, 17ммоль) в дихлорметані (25мл) протягом 20хв. Одержаний розчин перемішували при кімнатній температурі протягом ночі та додавали насичений розчин бікарбонату натрію в льодяній бані, щоб погасити реакцію. Водний шар екстрагували дихлорметаном. Органічні екстракти промивали сольовим розчином, сушили над безводним сульфатом натрію та концентрували у вакуумі. Неочищений продукт розтирали в порошок в діетиловому ефірі, отримуючи зазначену у заголовку сполуку (1,8г, 48%) у вигляді білої твердої речовини. B. (1-Бензолсульфоніл-4-бром-1Η-індол-3-іл)(4-етил-феніл)-метанон: Суміш сполуки, одержаної на Стадії А (1,6г, 5ммоль), бромід тетрабутиламонію (0,16г, 0,5ммоль) та бензолсульфоніл хлорид (1,3г, 7,5ммоль) в 25% водному гідроксиді натрію (10мл) та бензолі (50мл) перемішували при кімнатній температурі протягом ночі. Реакційну суміш гасили додаванням води та екстрагували етил ацетатом. Органічний шар промивали водою та сольовим розчином, сушили над безводним сульфатом натрію та концентрували у вакуумі та хроматографували на силікагелі, елююючи етил ацетат/гексан (30:100), одержуючи зазначену у заголовку сполуку (1,80г, 76%). C. 1-Бензолсульфоніл-4-бром-3-(4-етилбензил)-1Η-індол: До суспендованого АІСl3 (0,8г, 40 6ммоль) в дихлорметані (10мл) додавали комплекс боран-трет-бутиламін (0,52г, 6ммоль) при 0°С. Одержану суміш перемішували при 0°С протягом 10хв., потім додавали розчин сполуки зі Стадії В (0,94г, 2ммоль) в дихлорметані (15мл). Реакційну суміш перемішували при кімнатній температурі протягом ночі, та додавали NaOH (3М, 20мл) з подрібненим льодом, щоб погасити реакцію. Основний водний шар екстрагували дихлорметаном. Органічні екстракти промивали сольовим розчином, сушили над безводним сульфатом натрію та концентрували у вакуумі. Неочищений продукт (0,90г, 99%) був достатньо чистим для використання на наступній стадії без подальшого очищення. D. 4-Бром-3-(4-етил-бензил)-1Η-індол: Сполуку зі Стадії С (0,90г, 2ммоль) розчиняли в 1:1 суміші етанолу та THF (20мл) з 50% водним гідроксидом натрію (2мл). Одержаний розчин кип'ятили зі зворотним холодильником протягом 3 годин. Після охолодження до кімнатної температури суміш розбавляли водою (20мл), концентрували у вакуумі, щоб видалити більшу частину етанолу, та екстрагували етил ацетатом. Органічні екстракти промивали водою та сольовим розчином, сушили над безводним сульфатом натрію та концентрували у вакуумі. Неочищений продукт очищали за допомогою хроматографії на силікагелі, елююючи етил ацетат/гексан (30:100), одержуючи зазначену у заголовку сполуку (0,53г, 84%) у вигляді безбарвного масла. E. 3-(4-Етилбензил)-4-(β-D-глюкопіранозил)1Η-індол: Зазначену у заголовку сполуку одержували у вигляді білої твердої речовини із сполуки зі Стадії D за допомогою такої ж методики, як описано в Прикладі 1, Стадії D, Е, F та G. 1Н ЯМР (300МГц, CD3OD) δ 7,33 (dd, J=7,42, 1,64Гц, 1H), 7,18 (d, J=1,79Гц, 1H), 7,16 - 7,07 (m, 5H), 6,90 (s, 1H), 4,72 (d, J=9,64Гц, 1H), 4,35 (d, J=16,5Гц, 1H), 4,26 (d, J=16,4, 1H), 3,69-3,52 (m, 3H), 3,44-3,39 (m, 2H), 2,95 (s, 1H), 2,58 (q, J=7,58Гц, 2Н), 1,19 (t, J=7,65Гц, 3Н). MS: m/z (M+Na) 420. Η. Біологічні приклади Приклад 1 Матеріали та способи Клонування сДНК SGLT1 людини та SGLT2 людини та складання вектору експресії ссавців: сДНК SGLT1 людини (банк генів М24847) була клонована з тонкої кишки людини. сДНК SGLT1 людини (банк генів М95549) була клонована з нирки людини. Обидві повні сДНК були субклоновані до псДНК та складені у послідовність для перевірки єдності конструкції. Генерація клітин СНО-K1, що стабільно експресують SGLT1 людини або SGLT2 людини: трансфекція клітин СНО-K1 була виконана із застосуванням реагенту D MRIE-C (Life Technologies, Gaithersburg, MD). Потім трансфектанти були відібрані у присутності антибіотику G418 (Gibco-BRL, Grand Island, NY) при 400мкг/мл. Потім індивідуальні клони були о характеризовані із використанням функціонального аналізу, описаного нижче. Аналіз переносу натрій-залежної глюкози, заснований на клітинах: колонії клітин, що стабільно експресують SGLT1 та SGLT2 людини, потім вико 41 85569 ристовували для функціонального аналізу поглинання Na+-залежної глюкози. Коротко кажучи, клітини були поміщені на планшету з 96 лунками (густина становила 65000 клітин на лунку), де вони зростали протягом 48 годин. Потім клітини промили один раз буфером аналізу (50мМ HEPES рН7,4; 20мМ Тріс, 5мМ KСl, 1мМ MgCl2, 1мМ СаСl2 та 137мМ NaCl) та обробляли сполукою у відсутності або у присутності NaCl протягом 15 хвилин. Потім клітини помітили 14С-α-метилглюкопіранозидом (AMG, Sigma, St. Louis, МО), аналогом неметаболізуючої глюкози, специфічним для транспортерів натрій-залежної глюкози, як було описано вище [Peng, Η. та Lever J.E. Post-transcriptional regulation of Na+/glucose cotransporter (SGTL1) gene expression in LLC-PK1 cells. J. Biol. Chem 1995; 270: 20536-20542]. Через 2 години помічені клітини тричі промили льодяним PBS. Після аспірації клітини солюбілізовали за допомогою Microscint 20 (Packard, Meriden, СТ) та поглинання Na-залежної 14C-AMG визначали шляхом вимірювання радіоактивності. Планшети підраховували на TopCount (Packard, Meriden, CT). Результати були повідомлені у ви гляді % інгібування або значення ІС50, отриманого у типовому експерименті. Варіабельність функціонального аналізу зазвичай знаходилась в межах 20%. Таблиця 3 № прикладу 4 3 2 1 CHOK-SGLT2 ІС50 (uМ) 12% Інг. при 10uM 60% Інг. при 10uM 1,395±0,067 0,132±0,024 CHOK-SGLT1 ІС50 (uМ) неактив ний неактивний неактивний неактивний Приклад 2 Аналіз ефективності in vivo Хворі на цукровий діабет та ожиріння (ZDF) щури чоловічої статі (7-8 тижнів) були отримані від Charles River. Тварин утримували у кімнаті з регулюванням температури з циклом освітлення: 12 годин освітлення/темряви. Тваринам надавався вільний доступ до їжі (стандартна дієта для гризунів Purina 5008) та води. За 12 годин до початку експерименту тваринам протягом 12 годин їжі не давали. У ранок експерименту тваринам ввели наповнювач (0,5% метилцелюлозу) або сполуку перорально (1мл/кг). Через одну годину тварини отримали глюкозу перорально (4мл/кг 50% розчину) та були негайно поміщені до метаболічних кліток. Тваринам був наданий вільний доступ до води, та сечу збирали протягом 4 годин. Вміст глюкози у сечі визначали за допомогою Trinder Reagent (Sigma). Приклад 3 Вплив на вміст глюкози у плазмі, інсуліну у плазмі, тригліцеридів у плазмі, вільних жирних кислот у плазмі, масу печінки та масу тіла Для дослідження впливу інгібітору SGLT у комбінації з агоністом RXR, мишам db/db жіночої статі (віком 67 тижнів/Jackson Labs, ME) щоденно протягом 11 днів давали наповнювач (0,5% метилцелюлоза), агоніст RXR (0,1-10мпк (мг/кг)), інгібітор SGLT 42 (100мпк), або агоніст RXR плюс інгібітор SGLT. Миші (n=8 тварин на групу) отримували тестові сполуки або наповнювач перорально в об'ємі 10мл/кг маси тіла. Масу тіла записували у перший день, до приймання ліків, та на 4, 8, та 11 день. Через вісімнадцять годин після останнього приймання, мишей зважили та піддали анестезії СС2/О2 (70:30). Потім у мишей взяли кров шляхом пункції ретро-орбітальних синусних пазух та налили її до 2мл гепарінізованих поліпропіленових трубочок, що охолоджувались льодом. Зразки плазми були потім проаналізовані на вміст глюкози, інсуліну, тригліцеридів та вільних жирних кислот. Печінку вирізали, зважили та заморозили. Інгібітори SGLT та агоністи RXR мають чіткі механізми дії. Покращений глікемічний контроль, виміряний як зменшення вмісту глюкози у плазмі, інсуліну у плазмі, вільних жирних кислот у плазмі або тригліцеридів у плазмі, або їх комбінації, може спостерігатись при більш низьких концентраціях агоністу RXR при його прийманні у комбінації з інгібітором SGLT. Тому, зсув вліво кривої дозареакція, викликаний впливом агоністу R XR на вказані вище параметри, може стати очевидним. Додатково, приріст маси, що спостерігався після лікування агоністами RXR, є менш вираженим при прийманні з інгібітором SGLT, так що сприяння інгібіторів SGLT виведенню глюкози з сечею та втраті тілом калорій було продемонстровано шляхом зменшення маси або приросту маси. Також, так як інгібітори SGLT сприяють помірному діурезу, то набряк (та приріст ваги, викликаний набряком), який, як правило, спостерігається після лікування агоністами RXR, може бути менш вираженим або відсутнім. Зменшення кількості агоністу RXR, такого як МХ-6054, необхідної для досягнення ефекту, в свою чергу, покращує профіль побічних ефектів. Зменшені побічні ефекти можуть включати такі стани, як ожиріння печінки, збільшення маси печінки, приріст маси тіла, приріст маси серця, набряк, гіпертрофію серця, гіпертрофію печінки, гіпоглікемію та гепатотоксичність, або будь-яку їх комбінацію. Приклад 4 Вплив на вміст глюкози у плазмі, НbА1с, гематокрит, вміст інсуліну у плазмі, вміст тригліцеридів у плазмі, вміст вільних жирних кислот у плазмі, загальний холестерин, HDL, концентрацію ліків у плазмі, масу печінки, масу серця, вміст жиру та масу тіла Для дослідження впливу інгібітору SGLT у комбінації з агоністом RXR, щури чоловічої породи із ZDF (віком 6 тижнів/GMI) щодня лікувались протягом 28 днів наповнювачем (0,5% метилцелюлоза), агоністом RXR (0,1-10мпк), інгібітором SGLT (3-100мпк) або агоністом RXR плюс інгібітор SGLT. Щури (n=8 тварин на групу) отримували тестові сполуки або наповнювач перорально в об'ємі 2мл/кг маси тіла. Масу тіла записували у перший день, до приймання ліків, та двічі на тиждень протягом дослідження. За день до приймання останньої дози тваринам не давали їжу всю ніч. Через годину після приймання останньої дози щурів зважили та піддали анестезії СО2/О2 (70:30). Потім у щурів взяли кров шляхом пункції ретро 43 85569 орбітальних синусних пазух та налили її до 2мл гепарінізованих поліпропіленових трубочок, що охолоджувались льодом. Потім щурам ввели глюкозу (2г/кг перорально) та помістили до метаболічних кліток для збирання сечі (4 години). Потім тварин вбили, а жирові тільця статевих залоз, печінки та серця вирізали, зважили та заморозили для гістологічних досліджень. Потім зразки плазми були проаналізовані на вміст глюкози, НbА1с, інсуліну, гематокрит, концентрацію ліків у крові, загальний холестерин, HDL, вільні жирні кислоти та тригліцериди. Виміряли об'єм сечі та вміст глюкози у сечі, протеїни, осмотичний тиск, електроліти (Na, K, СІ), BUN та креатинін. Інгібітори SGLT та агоністи RXR мають чіткі механізми дії. Покращений глікемічний контроль, виміряний як зменшення вмісту глюкози у плазмі, НbА1с, інсуліну у плазмі або тригліцеридів у плазмі, або їх комбінації, може спостерігатись при більш низьких концентраціях агоністів RXR при їх прийманні у комбінації з інгібітором SGLT. Тому, зсув вліво кривої доза-реакція, викликаний впливом агоністів RXR на вказані вище параметри може стати очевидним. Додатково, приріст маси, що спостерігався після лікування агоністами RXR, є менш вираженим при прийманні з інгібітором SGLT, так що сприяння інгібіторів SGLT виведенню глюкози з сечею та втраті тілом калорій було продемонстровано шляхом зменшення маси або приросту маси. Також, так як інгібітори SGLT сприяють помірному діурезу, то набряк (та приріст ваги, викликаний набряком), який, як правило, спостерігається після лікування агоністами RXR, може бути менш вираженим або відсутнім. Це може бути продемонстровано зниженням прирісту ваги серця, викликаного агоністами RXR. Зменшення кількості агоністів RXR, необхідної для досягнення ефекту, в свою чергу, покращує профіль побічних ефектів. Зменшені побічні ефекти можуть включати такі стани, як ожиріння печінки, збільшення маси печінки, приріст маси тіла, приріст маси серця, набряк, гіпертрофію серця, гіпертрофію печінки, гіпоглікемію та гепатотоксичність, або будь-яку їх комбінацію. Приклади, наведені вище, можуть також вказувати на те, що пероральне введення інгібітору SGLT у комбінації із антидіабетичними агентами, такими, як модулятор RXR, покращує стан інших маркерів цукрового діабету, включаючи концентрацію глікозованого гемоглобіну (Hgb A1С). Зокрема, пероральне введення інгібітору SGLT у комбінації з одним чи більше модуляторами RXR може зменшува ти масу тіла або знижувати приріст маси тіла, а також зменшувати масу печінки або знижувати приріст маси печінки, порівняно із введенням одного чи більше модуляторів RXR самих по собі. Комп’ютерна в ерстка Т. Чепелев а 44 Таким чином, для лікування діабету, особливо цукрового діабету II тип у, або Синдрому X, може застосовуватись сполука Формули (IV) в комбінації з одним або більше антидіабетичними агентами, такими як агоніст RXR, що збільшує чутливість до інсуліну, включаючи введення повторних пероральних доз сполуки Формули (IV) в діапазоні від приблизно 25 до 1000мг один раз або двічі на день та повторних доз антидіабетичного агента або агентів в спільно ефективних дозуваннях. Спільно ефективне дозування для антидіабетичних агентів, описаних в даній заявці, може бути легко визначене кваліфікованим фахівцем в даній галузі техніки, базуючись на стандартних методиках визначення дозування. Зокрема, таке об'єднане введення може бути е фективним для досягнення зниження маси тіла, приросту маси тіла, маси печінки або приросту маси печінки у суб'єкта. Додатково, спосіб, що включає (а) введення суб'єкту спільно ефективної кількості інгібітора реабсорбції глюкози; та (b) введення суб'єкту спільно ефективної кількості антидіабетичного агента, такого як модулятор RXR, може використовуватись для зниження маси тіла, приросту маси тіла або маси печінки у суб'єкта, що цього потребує, де об'єднане введення може проводитись в будь-якому порядку та об'єднані спільно ефективні кількості забезпечують бажаний терапевтичний ефект. Також, спосіб, що включає (а) введення суб'єкту спільно ефективної кількості інгібітора реабсорбції глюкози; та (b) введення суб'єкту спільно ефективної кількості антидіабетичного агента, може використовува тись для контролю над масою тіла, приростом маси тіла, масою печінки або приростом маси печінки у суб'єкта, що страждає на діабет, Синдром X, або симптоми, пов'язані з ними, або їх ускладнення, де об'єднане введення може проводитись в будь-якому порядку та об'єднані спільно ефективні кількості забезпечують бажаний терапевтичний ефект. Оптимальні дозування для введення, можуть бути легко визначені кваліфікованим фахівцем в даній галузі техніки та будуть змінюватися в залежності від конкретної сполуки, що використовують, способу введення, концентрації препарату та розвитку хворобливого стану. Крім того, чинники, пов'язані з індивідуальним пацієнтом, якого лікують, включаючи стать пацієнта, вік, вагу, режим харчування, час введення та супутні захворювання призведуть до необхідності пристосувати дозування. Тоді як вищенаведений опис викладає принципи даного винаходу, з прикладами, наведеними з метою ілюстрації, слід розуміти, що застосування винаходу включає всі звичайні варіації, адаптації та/або модифікації, які входять в межі наступної формули винаходу, та їх еквіваленти. Підписне Тираж 28 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstituted fused heterocyclic c-glycosides
Автори англійськоюRybczynski Philip, Urbanski Maud, Zhang Xiaoyan
Назва патенту російськоюЗамещенные конденсированные гетероциклические с-гликозиды
Автори російськоюРибчински Филип, Урбански Мод, Жанг Сяоян
МПК / Мітки
МПК: A61K 31/70, A01N 43/04, C07H 5/00, C07H 1/00, C07H 7/00
Мітки: с-глікозиди, конденсовані, заміщені, гетероциклічні
Код посилання
<a href="https://ua.patents.su/22-85569-zamishheni-kondensovani-geterociklichni-s-glikozidi.html" target="_blank" rel="follow" title="База патентів України">Заміщені конденсовані гетероциклічні с-глікозиди</a>
Попередній патент: Пристрій для виконання арифметичних операцій
Наступний патент: Заміщені хіноліни та їх застосування як мікобактеріальних інгібіторів
Випадковий патент: Придатний для лазерного спікання порошок із поліоксиметилену, спосіб його виготовлення і формовані вироби, виготовлені з цього порошку












