Похідні n-(гетероарил)-1-гетероарилалкіл-1н-індол-2-карбоксамідів, їх одержання і їх застосування у терапії
Формула / Реферат
1. Сполука, що відповідає формулі (І):
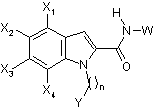 , (I)
, (I)
в якій
Х1, Х2, Х3, Х4 означають, незалежно один від одного, атом водню або галогену або (С1-С6)-алкіл, (С3-С7)-циклоалкіл, (С3-С7)-циклоалкіл-(С1-С3)-алкілен, (С1-С6)-фторалкіл, (С1-С6)-алкоксил, (С1-С6)-фторалкоксил, ціаногрупу, C(O)NR1R2, нітрогрупу, NR1R2, (С1-С6)-тіоалкіл, -S(О)-(С1-С6)-алкіл, -S(O)2-(С1-С6)-алкіл, SO2NR1R2, NR3COR4, NR3SO2R5 або арил, причому арил можливо заміщений одним або декількома замісниками, вибраними з галогену, (С1-С6)-алкілу, (С3-С7)-циклоалкілу, (С3-С7)-циклоалкіл-(С1-С3)-алкілену, (С1-С6)-фторалкілу, (С1-С6)-алкоксилу, (С1-С6)-фторалкоксилу, нітрогрупи або ціаногрупи;
W означає конденсовану біциклічну групу формули:
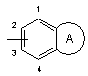 ,
,
зв'язану з атомом азоту у положеннях 1, 2, 3 або 4;
А означає 5-7-членний гетероцикл, що включає від одного до трьох гетероатомів, вибраних з О, S або N; причому
атом або атоми вуглеців А можливо заміщені однією або декількома групами, вибраними з атома водню або (С1-С6)-алкілу, (С3-С7)-циклоалкілу, (С3-С7)-циклоалкіл-(С1-С3)-алкілену, (С1-С6)-фторалкілу, арилу, арил-(С1-С6)-алкілену, оксогрупи або тіогрупи;
атом або атоми азоту А можливо заміщені радикалом R6, коли азот є суміжним з атомом вуглецю, заміщеним оксогрупою, або радикалом R7 в інших випадках;
n дорівнює 1, 2 або 3;
Y означає гетероарил, можливо заміщений однією або декількома групами, вибраними з атома галогену або (С1-С6)-алкілу, (С3-С7)-циклоалкілу, (С3-С7)-циклоалкіл-(С1-С3)-алкілену, (С1-С6)-фторалкілу, гідроксилу, (С1-С6)-алкоксилу, (С1-С6)-фторалкоксилу, ціаногрупи, C(O)NR1R2, нітрогрупи, NR1R2, (С1-С6)-тіоалкілу, SH, -S(О)-(С1-С6)-алкілу, -S(О)2-(С1-С6)-алкілу, SO2NR1R2, NR3COR4, NR3SO2R5, арил-(С1-С6)-алкілену або арилу, причому арил і арил-(С1-С6)-алкілен можливо заміщені одним або декількома замісниками, вибраними з галогену, (С1-С6)-алкілу, (С3-С7)-циклоалкілу, (С3-С7)-циклоалкіл-(С1-С3)-алкілену, (С1-С6)-фторалкілу, (С1-С6)-алкоксилу, (С1-С6)-фторалкоксилу, нітрогрупи або ціаногрупи;
R1 і R2 означають, незалежно один від одного, атом водню або (С1-С6)-алкіл, (С3-С7)-циклоалкіл, (С3-С7)-циклоалкіл-(С1-С3)-алкілен, арил-(С1-С6)-алкілен або арил; або R1 і R2 разом з атомом азоту, що їх несе, утворюють групу азетидиніл, піролідиніл, піперидиніл, азепініл, морфолініл, тіоморфолініл, піперазиніл, гомопіперазиніл, причому ця група можливо заміщена (С1-С6)-алкілом, (С3-С7)-циклоалкілом, (С3-С7)-циклоалкіл-(С1-С3)-алкіленом, арил-(С1-С6)-алкіленом або арилом;
R3 і R4 означають, незалежно один від одного, атом водню або (С1-С6)-алкіл, арил-(С1-С6)-алкілен або арил;
R5 означає (С1-С6)-алкіл, арил-(С1-С6)-алкілен або арил;
R6 означає атом водню або (С1-С6)-алкіл, (С3-С7)-циклоалкіл, (С3-С7)-циклоалкіл-(С1-С3)-алкілен, (С1-С6)-фторалкіл, арил-(С1-С6)-алкілен або арил;
R7 означає атом водню або (С1-С6)-алкіл, (С3-С7)-циклоалкіл, (С3-С7)-циклоалкіл-(С1-С3)-алкілен, (С1-С6)-фторалкіл, арил-(С1-С6)-алкілен, (С1-С6)-алкіл-С(О)-, (С3-С7)-циклоалкіл-(С1-С3)-алкілен-С(О)-, (С1-С6)-фторалкіл-С(О)-, (С3-С7)-циклоалкіл-С(О)-, арил-С(О)-, арил-(С1-С6)-алкілен-С(О)-, (С1-С6)-алкіл-S(O)2-, (С1-С6)-фторалкіл-S(О)2-, (С3-С7)-циклоалкіл-S(О)2-, (С3-С7)-циклоалкіл-(С1-С3)-алкілен-S(О)2-, арил-S(О)2-, арил-(С1-С6)-алкілен-S(О)2- або арил;
причому
атом або атоми сірки гетероциклу А або гетероарилу Y можуть бути в окисненій формі;
атом або атоми азоту гетероциклу А або гетероарилу Y можуть бути в окисненій формі;
у формі основи або адитивної солі з кислотою, а також у формі гідрату або сольвату.
2. Сполука формули (І) за п. 1, яка відрізняється тим, що
Х1, Х2, Х3, Х4 означають, незалежно один від одного, атом водню, атом галогену або (С1-С6)-алкіл, або (С1-С6)-фторалкіл, або групу NR1R2, причому R1 і R2 мають значення, як зазначені у випадку загальної формули (І) за п. 1;
у формі основи або адитивної солі з кислотою, а також у формі гідрату або сольвату.
3. Сполука формули (І) за будь-яким з пп. 1, 2, яка відрізняється тим, що W означає конденсовану біциклічну групу формули:
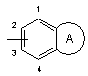 ,
,
зв'язану з атомом азоту у положеннях 1, 2, 3 або 4;
і W вибирають з наведених нижче груп: індолініл, ізоіндоліл, ізоіндолініл, бензофураніл, дигідробензофураніл, бензотіофеніл, дигідробензотіофеніл, бензоксазоліл, дигідробензоксазолініл, ізобензофураніл, дигідроізобензофураніл, бензімідазоліл, дигідробензімідазоліл, індоліл, індазоліл, бензотіазоліл, ізобензотіазоліл, дигідроізобензотіазоліл, бензотриазоліл, хінолініл, дигідрохінолініл, тетрагідрохінолініл, ізохінолініл, дигідроізохінолініл, тетрагідроізохінолініл, бензоксазиніл, дигідробензоксазиніл, бензотіазиніл, дигідробензотіазиніл, цинолініл, хіназолініл, дигідрохіназолініл, тетрагідрохіназолініл, хіноксалініл, дигідрохіноксалініл, тетрагідрохіноксалініл, фталазиніл, дигідрофталазиніл, тетрагідрофталазиніл, тетрагідробенз[b]азепініл, тетрагідробенз[с]азепініл, тетрагідробенз[d]азепініл, тетрагідробензо[b][1,4]діазепініл, тетрагідробензо[е][1,4]діазепініл, тетрагідробензо[b][1,4]оксазепініл або тетрагідробензо[b][1,4]тіазепініл;
причому атом або атоми вуглецю і/або азоту вказаної вище групи W можливо заміщені, як зазначено у випадку загальної формули (І) за п. 1;
у формі основи або адитивної солі з кислотою, а також у формі гідрату або сольвату.
4. Сполука формули (І) за пп. 1-3, яка відрізняється тим, що W означає конденсовану біциклічну групу формули:
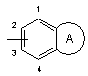 ,
,
зв'язану з атомом азоту у положеннях 2 або 3;
і W вибирають з бензімідазолілу, індолілу, бензотіазолілу, хінолінілу, тетрагідрохінолінілу і бензоксазинілу; і/або
атом або атоми вуглеців А можливо заміщені одним або декількома (С1-С6)-алкілами, (С1-С6)-фторалкілами, (С3-С7)-циклоалкілами або оксогрупами; і/або
атом або атоми азоту А можливо заміщені радикалом R6, коли азот є суміжним з атомом вуглецю, заміщеним оксогрупою, причому R6 означає атом водню або (С1-С6)-алкіл; або радикалом R7 в інших випадках, причому R7 означає (С1-С6)-алкіл або (С3-С7)-циклоалкіл-(С1-С3)-алкілен;
у формі основи або адитивної солі з кислотою, а також у формі гідрату або сольвату.
5. Сполука формули (І) за будь-яким з пп. 1-4, яка відрізняється тим, що n дорівнює 1 або 2;
у формі основи або адитивної солі з кислотою, а також у формі гідрату або сольвату.
6. Сполука формули (І) за будь-яким з пп. 1-5, яка відрізняється тим, що
Y означає гетероарил, вибраний з наведених нижче груп: піридиніл, піримідиніл, піразиніл, піридазиніл, імідазоліл, бензімідазоліл, бензотіазоліл, тіазоліл, фураніл, хінолініл, ізохінолініл, хіноксалініл, причому гетероарил можливо заміщений однією або декількома групами, вибраними з (С1-С6)-алкілу, (С1-С6)-фторалкілу, арил-(С1-С6)-алкілену або NR1R2; причому R1 і R2 разом з атомом азоту, що їх несе, утворюють морфолініл;
у формі основи або адитивної солі з кислотою, а також у формі гідрату або сольвату.
7. Сполука формули (І) за п. 1, яка відрізняється тим, що
Х1, Х2, Х3, Х4 означають, незалежно один від одного, атом водню або галогену або (С1-С6)-алкіл, (С1-С6)-фторалкіл або NR1R2, причому R1 і R2 мають значення, як зазначені у випадку загальної формули (І) за п. 1;
W означає конденсовану біциклічну групу формули:
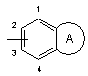 ,
,
зв'язану з атомом азоту у положеннях 2 або 3; і W вибирають з бензімідазолілу, індолілу, бензотіазолілу, хінолінілу, тетрагідрохінолінілу і бензоксазинілу; причому
атом або атоми вуглеців А можливо заміщені одним або декількома (С1-С6)-алкілами, (С1-С6)-фторалкілами, (С3-С7)-циклоалкілами або оксогрупами; і/або
атом або атоми азоту А можливо заміщені радикалом R6, коли азот є суміжним з атомом вуглецю, заміщеним оксогрупою, причому R6 означає атом водню або (С1-С6)-алкіл; або радикалом R7 в інших випадках, причому R7 означає (С1-С6)-алкіл або (С3-С7)-циклоалкіл-(С1-С3)-алкілен; і/або
n дорівнює 1 або 2; і/або
Y означає гетероарил, вибраний з наведених нижче груп: піридиніл, піримідиніл, піразиніл, піридазиніл, імідазоліл, бензімідазоліл, бензотіазоліл, тіазоліл, фураніл, хінолініл, ізохінолініл, хіноксалініл, причому гетероарил можливо заміщений однією або декількома групами, вибраними з (С1-С6)-алкілу, (С1-С6)-фторалкілу, арил-(С1-С6)-алкілену або NR1R2; причому R1 і R2 разом з атомом азоту, що їх несе, утворюють морфолініл;
у формі основи або адитивної солі з кислотою, а також у формі гідрату або сольвату.
8. Спосіб одержання сполуки формули (І) за п. 1, який відрізняється тим, що сполуку загальної формули (IV):
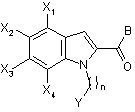 , (IV)
, (IV)
в якій X1, X2, X3, X4, Y і n мають значення, як зазначені у випадку загальної формули (І) за п. 1, і В означає (С1-С6)-алкоксил,
вводять у взаємодію з амідом сполуки загальної формули (V):
![]() , (V)
, (V)
в якій W має значення, як зазначене у випадку загальної формули (І) за п. 1, при температурі кипіння зі зворотним холодильником розчинника, причому амід сполуки загальної формули (V) одержують шляхом попереднього впливу триметилалюмінію на аміни загальної формули (V).
9. Сполука формули (IV), вибрана з наведених нижче сполук:
етил-5-фтор-1-[(тіазол-2-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(піридин-3-іл)етил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(піридин-3-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(піридин-4-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(піридин-2-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(2-метилпіридин-3-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(1-N-бензилімідазол-2-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(2-піролідинопіридин-3-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(бензотіазол-2-іл)метил]-1H-індол-2-карбоксилат;
етил-5-фтор-1-[(1-метилбензімідазол-2-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(4-метилтіазол-5-іл)етил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(хінолін-2-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(хіноксалін-2-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(піразин-2-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(3-метилпіридин-2-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(ізохінолін-1-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(4-метилпіридин-2-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(2-метилпіридин-4-іл)етил]-1H-індол-2-карбоксилат;
етил-5-фтор-1-[(2-метилпіридин-4-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(5-метилпіридин-2-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(диметилпіразин-2-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(6-метилпіразин-2-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(6-метилпіридазин-3-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(6-метилпіридин-2-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-фтор-1-[(2-фенілпіридин-4-іл)метил]-1Н-індол-2-карбоксилат;
метил-6-трет-бутил-1-[(піридин-4-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-трифторметил-1-[(піридин-4-іл)метил]-1Н-індол-2-карбоксилат;
етил-6-N-диметиламіно-1-[(піридин-4-іл)метил]-1Н-індол-2-карбоксилат;
метил-6-трифторметил-1-[(піридин-4-іл)метил]-1H-індол-2-карбоксилат;
етил-5-трет-бутил-1-[(піридин-4-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-трет-бутил-1-[(піридин-2-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-трет-бутил-1-[(піридин-3-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-трет-бутил-1-[(2-метилпіридин-3-іл)метил]-1Н-індол-2-карбоксилат;
етил-5-трет-бутил-1-[(6-метилпіридин-2-іл)метил]-1H-індол-2-карбоксилат;
етил-5-фтор-1-[(піримідин-4-іл)метил]-1Н-індол-2-карбоксилат;
у формі основи або адитивної солі з кислотою, а також у формі гідрату або сольвату.
10. Сполука формули (V), вибрана з наведених нижче сполук:
5-аміно-1-(циклопропіл)метил-2-метил-1Н-бензімідазол;
5-аміно-2-циклопропіл-1-метил-1Н-бензімідазол;
5-аміно-2-ізопропіл-1-метил-1Н-бензімідазол;
6-аміно-1-(циклопропіл)метил-2-метил-1Н-бензімідазол;
6-аміно-2-циклопропіл-1-метил-1Н-бензімідазол;
6-аміно-2-ізопропіл-1-метил-1Н-бензімідазол;
у формі основи або адитивної солі з кислотою, а також у формі гідрату або сольвату.
11. Лікарський засіб, який відрізняється тим, що він містить сполуку формули (І) за будь-яким з пп. 1-7 або фармацевтично прийнятну сіль, гідрат або сольват сполуки формули (І).
12. Фармацевтична композиція, яка відрізняється тим, що вона містить сполуку формули (І) за будь-яким з пп. 1-7 або фармацевтично прийнятну сіль, гідрат або сольват цієї сполуки, а також щонайменше один фармацевтично прийнятний ексципієнт.
13. Застосування сполуки формули (І) за будь-яким з пп. 1-7 для одержання лікарського засобу, призначеного для профілактики або лікування патологій, в яких беруть участь рецептори типу TRPV1.
14. Застосування сполуки формули (І) за п. 13 для одержання лікарського засобу, призначеного для профілактики або лікування болю, запалення, урологічних порушень, гінекологічних порушень, шлунково-кишкових порушень, респіраторних порушень, псоріазу, свербежу, дермальних іритацій, іритацій очей або слизових оболонок, герпесу, оперізувального лишаю або лікування депресії або діабету.
Текст
1. Сполука, що відповідає формулі (І): X1 H C2 2 (13) 1 3 пи, NR1R2, (С1-С6)-тіоалкілу, SH, -S(О)-(С1-С6)алкілу, -S(О)2-(С1-С6)-алкілу, SO2NR1R2, NR3COR4, NR3SO2R5, арил-(С1-С6)-алкілену або арилу, причому арил і арил-(С1-С6)-алкілен можливо заміщені одним або декількома замісниками, вибраними з галогену, (С1-С6)-алкілу, (С3-С7)-циклоалкілу, (С3С7)-циклоалкіл-(С1-С3)-алкілену, (С1-С6)фторалкілу, (С1-С6)-алкоксилу, (С1-С6)фторалкоксилу, нітрогрупи або ціаногрупи; R1 і R2 означають, незалежно один від одного, атом водню або (С1-С6)-алкіл, (С3-С7)-циклоалкіл, (С3-С7)-циклоалкіл-(С1-С3)-алкілен, арил-(С1-С6)алкілен або арил; або R1 і R2 разом з атомом азоту, що їх несе, утворюють групу азетидиніл, піролідиніл, піперидиніл, азепініл, морфолініл, тіоморфолініл, піперазиніл, гомопіперазиніл, причому ця група можливо заміщена (С1-С6)-алкілом, (С3-С7)циклоалкілом, (С3-С7)-циклоалкіл-(С1-С3)алкіленом, арил-(С1-С6)-алкіленом або арилом; R3 і R4 означають, незалежно один від одного, атом водню або (С1-С6)-алкіл, арил-(С1-С6)-алкілен або арил; R5 означає (С1-С6)-алкіл, арил-(С1-С6)-алкілен або арил; R6 означає атом водню або (С1-С6)-алкіл, (С3-С7)циклоалкіл, (С3-С7)-циклоалкіл-(С1-С3)-алкілен, (С1С6)-фторалкіл, арил-(С1-С6)-алкілен або арил; R7 означає атом водню або (С1-С6)-алкіл, (С3-С7)циклоалкіл, (С3-С7)-циклоалкіл-(С1-С3)-алкілен, (С1С6)-фторалкіл, арил-(С1-С6)-алкілен, (С1-С6)-алкілС(О)-, (С3-С7)-циклоалкіл-(С1-С3)-алкілен-С(О)-, (С1-С6)-фторалкіл-С(О)-, (С3-С7)-циклоалкіл-С(О)-, арил-С(О)-, арил-(С1-С6)-алкілен-С(О)-, (С1-С6)алкіл-S(O)2-, (С1-С6)-фторалкіл-S(О)2-, (С3-С7)циклоалкіл-S(О)2-, (С3-С7)-циклоалкіл-(С1-С3)алкілен-S(О)2-, арил-S(О)2-, арил-(С1-С6)-алкіленS(О)2- або арил; причому атом або атоми сірки гетероциклу А або гетероарилу Y можуть бути в окисненій формі; атом або атоми азоту гетероциклу А або гетероарилу Y можуть бути в окисненій формі; у формі основи або адитивної солі з кислотою, а також у формі гідрату або сольвату. 2. Сполука формули (І) за п. 1, яка відрізняється тим, що Х1, Х2, Х3, Х4 означають, незалежно один від одного, атом водню, атом галогену або (С1-С6)-алкіл, або (С1-С6)-фторалкіл, або групу NR1R2, причому R1 і R2 мають значення, як зазначені у випадку загальної формули (І) за п. 1; у формі основи або адитивної солі з кислотою, а також у формі гідрату або сольвату. 3. Сполука формули (І) за будь-яким з пп. 1, 2, яка відрізняється тим, що W означає конденсовану біциклічну групу формули: 1 2 A 3 4 , зв'язану з атомом азоту у положеннях 1, 2, 3 або 4; і W вибирають з наведених нижче груп: індолініл, ізоіндоліл, ізоіндолініл, бензофураніл, дигідробен 93687 4 зофураніл, бензотіофеніл, дигідробензотіофеніл, бензоксазоліл, дигідробензоксазолініл, ізобензофураніл, дигідроізобензофураніл, бензімідазоліл, дигідробензімідазоліл, індоліл, індазоліл, бензотіазоліл, ізобензотіазоліл, дигідроізобензотіазоліл, бензотриазоліл, хінолініл, дигідрохінолініл, тетрагідрохінолініл, ізохінолініл, дигідроізохінолініл, тетрагідроізохінолініл, бензоксазиніл, дигідробензоксазиніл, бензотіазиніл, дигідробензотіазиніл, цинолініл, хіназолініл, дигідрохіназолініл, тетрагідрохіназолініл, хіноксалініл, дигідрохіноксалініл, тетрагідрохіноксалініл, фталазиніл, дигідрофталазиніл, тетрагідрофталазиніл, тетрагідробенз[b]азепініл, тетрагідробенз[с]азепініл, тетрагідробенз[d]азепініл, тетрагідробензо[b][1,4]діазепініл, тетрагідробензо[е][1,4]діазепініл, тетрагідробензо[b][1,4]оксазепініл або тетрагідробензо[b][1,4]тіазепініл; причому атом або атоми вуглецю і/або азоту вказаної вище групи W можливо заміщені, як зазначено у випадку загальної формули (І) за п. 1; у формі основи або адитивної солі з кислотою, а також у формі гідрату або сольвату. 4. Сполука формули (І) за пп. 1-3, яка відрізняється тим, що W означає конденсовану біциклічну групу формули: 1 2 A 3 4 , зв'язану з атомом азоту у положеннях 2 або 3; і W вибирають з бензімідазолілу, індолілу, бензотіазолілу, хінолінілу, тетрагідрохінолінілу і бензоксазинілу; і/або атом або атоми вуглеців А можливо заміщені одним або декількома (С1-С6)-алкілами, (С1-С6)фторалкілами, (С3-С7)-циклоалкілами або оксогрупами; і/або атом або атоми азоту А можливо заміщені радикалом R6, коли азот є суміжним з атомом вуглецю, заміщеним оксогрупою, причому R6 означає атом водню або (С1-С6)-алкіл; або радикалом R7 в інших випадках, причому R7 означає (С1-С6)-алкіл або (С3-С7)-циклоалкіл-(С1-С3)-алкілен; у формі основи або адитивної солі з кислотою, а також у формі гідрату або сольвату. 5. Сполука формули (І) за будь-яким з пп. 1-4, яка відрізняється тим, що n дорівнює 1 або 2; у формі основи або адитивної солі з кислотою, а також у формі гідрату або сольвату. 6. Сполука формули (І) за будь-яким з пп. 1-5, яка відрізняється тим, що Y означає гетероарил, вибраний з наведених нижче груп: піридиніл, піримідиніл, піразиніл, піридазиніл, імідазоліл, бензімідазоліл, бензотіазоліл, тіазоліл, фураніл, хінолініл, ізохінолініл, хіноксалініл, причому гетероарил можливо заміщений однією або декількома групами, вибраними з (С1-С6)алкілу, (С1-С6)-фторалкілу, арил-(С1-С6)-алкілену або NR1R2; причому R1 і R2 разом з атомом азоту, що їх несе, утворюють морфолініл; 5 93687 у формі основи або адитивної солі з кислотою, а також у формі гідрату або сольвату. 7. Сполука формули (І) за п. 1, яка відрізняється тим, що Х1, Х2, Х3, Х4 означають, незалежно один від одного, атом водню або галогену або (С1-С6)-алкіл, (С1С6)-фторалкіл або NR1R2, причому R1 і R2 мають значення, як зазначені у випадку загальної формули (І) за п. 1; W означає конденсовану біциклічну групу формули: 1 2 A 3 4 , зв'язану з атомом азоту у положеннях 2 або 3; і W вибирають з бензімідазолілу, індолілу, бензотіазолілу, хінолінілу, тетрагідрохінолінілу і бензоксазинілу; причому атом або атоми вуглеців А можливо заміщені одним або декількома (С1-С6)-алкілами, (С1-С6)фторалкілами, (С3-С7)-циклоалкілами або оксогрупами; і/або атом або атоми азоту А можливо заміщені радикалом R6, коли азот є суміжним з атомом вуглецю, заміщеним оксогрупою, причому R6 означає атом водню або (С1-С6)-алкіл; або радикалом R7 в інших випадках, причому R7 означає (С1-С6)-алкіл або (С3-С7)-циклоалкіл-(С1-С3)-алкілен; і/або n дорівнює 1 або 2; і/або Y означає гетероарил, вибраний з наведених нижче груп: піридиніл, піримідиніл, піразиніл, піридазиніл, імідазоліл, бензімідазоліл, бензотіазоліл, тіазоліл, фураніл, хінолініл, ізохінолініл, хіноксалініл, причому гетероарил можливо заміщений однією або декількома групами, вибраними з (С1-С6)алкілу, (С1-С6)-фторалкілу, арил-(С1-С6)-алкілену або NR1R2; причому R1 і R2 разом з атомом азоту, що їх несе, утворюють морфолініл; у формі основи або адитивної солі з кислотою, а також у формі гідрату або сольвату. 8. Спосіб одержання сполуки формули (І) за п. 1, який відрізняється тим, що сполуку загальної формули (IV): X1 X2 B N X3 X4 O (IV) n Y , в якій X1, X2, X3, X4, Y і n мають значення, як зазначені у випадку загальної формули (І) за п. 1, і В означає (С1-С6)-алкоксил, вводять у взаємодію з амідом сполуки загальної формули (V): H N (V) H , B в якій W має значення, як зазначене у випадку загальної формули (І) за п. 1, при температурі кипіння зі зворотним холодильником розчинника, 6 причому амід сполуки загальної формули (V) одержують шляхом попереднього впливу триметилалюмінію на аміни загальної формули (V). 9. Сполука формули (IV), вибрана з наведених нижче сполук: етил-5-фтор-1-[(тіазол-2-іл)метил]-1Н-індол-2карбоксилат; етил-5-фтор-1-[(піридин-3-іл)етил]-1Н-індол-2карбоксилат; етил-5-фтор-1-[(піридин-3-іл)метил]-1Н-індол-2карбоксилат; етил-5-фтор-1-[(піридин-4-іл)метил]-1Н-індол-2карбоксилат; етил-5-фтор-1-[(піридин-2-іл)метил]-1Н-індол-2карбоксилат; етил-5-фтор-1-[(2-метилпіридин-3-іл)метил]-1Ніндол-2-карбоксилат; етил-5-фтор-1-[(1-N-бензилімідазол-2-іл)метил]1Н-індол-2-карбоксилат; етил-5-фтор-1-[(2-піролідинопіридин-3-іл)метил]1Н-індол-2-карбоксилат; етил-5-фтор-1-[(бензотіазол-2-іл)метил]-1H-індол2-карбоксилат; етил-5-фтор-1-[(1-метилбензімідазол-2-іл)метил]1Н-індол-2-карбоксилат; етил-5-фтор-1-[(4-метилтіазол-5-іл)етил]-1Н-індол2-карбоксилат; етил-5-фтор-1-[(хінолін-2-іл)метил]-1Н-індол-2карбоксилат; етил-5-фтор-1-[(хіноксалін-2-іл)метил]-1Н-індол-2карбоксилат; етил-5-фтор-1-[(піразин-2-іл)метил]-1Н-індол-2карбоксилат; етил-5-фтор-1-[(3-метилпіридин-2-іл)метил]-1Ніндол-2-карбоксилат; етил-5-фтор-1-[(ізохінолін-1-іл)метил]-1Н-індол-2карбоксилат; етил-5-фтор-1-[(4-метилпіридин-2-іл)метил]-1Ніндол-2-карбоксилат; етил-5-фтор-1-[(2-метилпіридин-4-іл)етил]-1Hіндол-2-карбоксилат; етил-5-фтор-1-[(2-метилпіридин-4-іл)метил]-1Ніндол-2-карбоксилат; етил-5-фтор-1-[(5-метилпіридин-2-іл)метил]-1Ніндол-2-карбоксилат; етил-5-фтор-1-[(диметилпіразин-2-іл)метил]-1Ніндол-2-карбоксилат; етил-5-фтор-1-[(6-метилпіразин-2-іл)метил]-1Ніндол-2-карбоксилат; етил-5-фтор-1-[(6-метилпіридазин-3-іл)метил]-1Ніндол-2-карбоксилат; етил-5-фтор-1-[(6-метилпіридин-2-іл)метил]-1Ніндол-2-карбоксилат; етил-5-фтор-1-[(2-фенілпіридин-4-іл)метил]-1Ніндол-2-карбоксилат; метил-6-трет-бутил-1-[(піридин-4-іл)метил]-1Ніндол-2-карбоксилат; етил-5-трифторметил-1-[(піридин-4-іл)метил]-1Ніндол-2-карбоксилат; етил-6-N-диметиламіно-1-[(піридин-4-іл)метил]-1Ніндол-2-карбоксилат; метил-6-трифторметил-1-[(піридин-4-іл)метил]-1Hіндол-2-карбоксилат; етил-5-трет-бутил-1-[(піридин-4-іл)метил]-1Ніндол-2-карбоксилат; 7 93687 8 етил-5-трет-бутил-1-[(піридин-2-іл)метил]-1Ніндол-2-карбоксилат; етил-5-трет-бутил-1-[(піридин-3-іл)метил]-1Ніндол-2-карбоксилат; етил-5-трет-бутил-1-[(2-метилпіридин-3-іл)метил]1Н-індол-2-карбоксилат; етил-5-трет-бутил-1-[(6-метилпіридин-2-іл)метил]1H-індол-2-карбоксилат; етил-5-фтор-1-[(піримідин-4-іл)метил]-1Н-індол-2карбоксилат; у формі основи або адитивної солі з кислотою, а також у формі гідрату або сольвату. 10. Сполука формули (V), вибрана з наведених нижче сполук: 5-аміно-1-(циклопропіл)метил-2-метил-1Нбензімідазол; 5-аміно-2-циклопропіл-1-метил-1Н-бензімідазол; 5-аміно-2-ізопропіл-1-метил-1Н-бензімідазол; 6-аміно-1-(циклопропіл)метил-2-метил-1Нбензімідазол; 6-аміно-2-циклопропіл-1-метил-1Н-бензімідазол; 6-аміно-2-ізопропіл-1-метил-1Н-бензімідазол; у формі основи або адитивної солі з кислотою, а також у формі гідрату або сольвату. 11. Лікарський засіб, який відрізняється тим, що він містить сполуку формули (І) за будь-яким з пп. 1-7 або фармацевтично прийнятну сіль, гідрат або сольват сполуки формули (І). 12. Фармацевтична композиція, яка відрізняється тим, що вона містить сполуку формули (І) за будьяким з пп. 1-7 або фармацевтично прийнятну сіль, гідрат або сольват цієї сполуки, а також щонайменше один фармацевтично прийнятний ексципієнт. 13. Застосування сполуки формули (І) за будьяким з пп. 1-7 для одержання лікарського засобу, призначеного для профілактики або лікування патологій, в яких беруть участь рецептори типу TRPV1. 14. Застосування сполуки формули (І) за п. 13 для одержання лікарського засобу, призначеного для профілактики або лікування болю, запалення, урологічних порушень, гінекологічних порушень, шлунково-кишкових порушень, респіраторних порушень, псоріазу, свербежу, дермальних іритацій, іритацій очей або слизових оболонок, герпесу, оперізувального лишаю або лікування депресії або діабету. Об'єктом винаходу є сполуки, похідні N(гетероарил)-1-гетероарилалкіл-1Н-індол-2карбоксамідів, які мають антагоністичну активність in vitro та in vivo відносно рецепторів типу TRPV1 (або VR1). Перший об'єкт винаходу стосується сполук, що відповідають наведеній нижче загальній формулі (І). Інший об'єкт винаходу стосується способів одержання сполук загальної формули (І). Наступний об'єкт винаходу стосується застосування сполук загальної формули (І), зокрема, у лікарських засобах або у фармацевтичних композиціях. Сполуки відповідно до винаходу відповідають загальній формулі (І): циклоалкілу, (С3-С7)-циклоалкіл-(С1-С3)-алкілену, (С1-С6)-фторалкілу, (С1-С6)-алкоксилу, (С1-С6)фторалкоксилу, нітрогрупи або ціаногрупи; W означає конденсовану біциклічну групу формули: в якій Х1, Х2, Х3, Х4 означають, незалежно один від одного, атом водню або галогену, або (С1-С6)алкіл, (С3-С7)-циклоалкіл, (С3-С7)-циклоалкіл-(С1С3)-алкілен, (С1-С6)-фторалкіл, (С1-С6)-алкоксил, (С1-С6)-фторалкоксил, ціаногрупу, C(O)NR1R2, нітрогрупу, NR1R2, (С1-С6)-тіоалкіл, -S(О)-( С1-С6)алкіл, -S(O)2-(C1-С6)-алкіл, SO2NR1R2, NR3COR4, NR3SO2R5 або арил, причому арил можливо заміщений одним або декількома замісниками, вибраними з галогену, (С1-С6)-алкілу, (С3-С7) , зв'язану з атомом азоту у положеннях 1, 2, 3 або 4; А означає 5-7-членний гетероцикл, що включає від одного до трьох гетероатомів, вибраних з О, S або N; причому атом або атоми вуглеців А можливо заміщені однією або декількома групами, вибраними з атома водню або (С1-С6)-алкілу, (С3-С7)циклоалкілу, (С3-С7)-циклоалкіл-(С1-С3)-алкілену, (С1-С6)-фторалкілу, арилу, арил-(С1-С6)-алкілену, оксогрупи або тіогрупи; причому атом або атоми азоту А можливо заміщені радикалом R6, коли азот є суміжним з атомом вуглецю, заміщеним оксогрупою, або радикалом R7 в інших випадках; n дорівнює 1, 2 або 3; Υ означає гетероарил, можливо заміщений однією або декількома групами, вибраними з атома галогену або (С1-С6)-алкілу, (С3-С7)циклоалкілу, (С3-С7)-циклоалкіл-(С1-С3)-алкілену, (С1-С6)-фторалкілу, гідроксилу, (С1-С6)-алкоксилу, (С1-С6)-фторалкоксилу, ціаногрупи, C(O)NR1R2, нітрогрупи, NR1R2, (С1-С6)-тіоалкілу, SH, -S(О)-(С1С6)-алкілу, -S(О)2-(С1-С6)-алкілу, SO2NR1R2, NR3COR4, NR3SO2R5, арил-(С1-С6)-алкілену або 9 арилу, причому арил і арил-(С1-С6)-алкілен можливо заміщений одним або декількома замісниками, вибраними з галогену, (С1-С6)-алкілу, (С3-С7)циклоалкілу, (С3-С7)-циклоалкіл-(С1-С3)-алкілену, (С1-С6)-фторалкілу, (С1-С6)-алкоксилу, (С1-С6)фторалкоксилу, нітрогрупи або ціаногрупи; R1 і R2 означають, незалежно один від одного, атом водню або (С1-С6)-алкіл, (С3-С7)-циклоалкіл, (С3-С7)-циклоалкіл-(С1-С3)-алкілен, арил-(С1-С6)алкілен або арил; або R1 і R2 разом з атомом азоту, що їх несе, утворюють групу азетидиніл, піролідиніл, піперидиніл, азепініл, морфолініл, тіоморфолініл, піперазиніл, гомопіперазиніл, причому ця група можливо заміщена (С1-С6)-алкілом, (С3-С7)циклоалкілом, (С3-С7)-циклоалкіл-(С1-С3)алкіленом, арил-(С1-С6)-алкіленом або арилом; R3 і R4 означають, незалежно один від одного, атом водню або (С1-С6)-алкіл, арил-(С1-С6)-алкілен або арил; R5 означає (С1-С6)-алкіл, арил-(С1-С6)-алкілен або арил; R6 означає атом водню або (С1-С6)-алкіл, (С3С7)-циклоалкіл, (С3-С7)-циклоалкіл-(С1-С3)-алкілен, (С1-С6)-фторалкіл, арил-(С1-С6)-алкілен або арил; R7 означає атом водню або (С1-С6)-алкіл, (С3С7)-циклоалкіл, (С3-С7)-циклоалкіл-(С1-С3)-алкілен, (С1-С6)-фторалкіл, арил-(С1-С6)-алкілен, (С1-С6)С(О)-, (С3-С7)-циклоалкіл-(С1-С3)-алкілен-С(О)-, (С1-С6)-фторалкіл-С(О)-, (С3-С7)-циклоалкіл-С(О)-, арил-С(О)-, арил-(С1-С6)-алкілен-С(О)-, (С1-С6)алкіл-S(O)2-, (С1-С6)-фторалкіл-S(О)2-, (С3-С7)циклоалкіл-S(О)2-, (С3-С7)-циклоалкіл-(С1-С3)алкілен-S(О)2-, арил-S(О)2-, арил-(С1-С6)-алкіленS(О)2- або арил. У сполуках загальної формули (І): - атом або атоми сірки гетероциклу А або гетероарилу Υ можуть бути в окисненій формі (S(O) або S(O)2); - атом або атоми азоту гетероциклу А або гетероарилу Υ можуть бути в окисненій формі (Nоксид). У межах винаходу як приклади групи W можна назвати наступні групи: індоліл, ізоіндоліл, індолініл, ізоіндолініл, бензофураніл, дигідробензофураніл, бензотіофеніл, дигідробензотіофеніл, бензоксазоліл, дигідробензоксазолініл, ізобензофураніл, дигідроізобензофураніл, бензімідазоліл, дигідробензімідазоліл, індазоліл, бензотіазоліл, ізобензотіазоліл, дигідроізобензотіазоліл, бензотриазоліл, хінолініл, дигідрохінолініл, тетрагідрохінолініл, ізохінолініл, дигідроізохінолініл, тетрагідроізохінолініл, бензоксазиніл, дигідробензоксазиніл, бензотіазиніл, дигідробензотіазиніл, цинолініл, хіназолініл, дигідрохіназолініл, тетрагідрохіназолініл, хіноксалініл, дигідрохіноксалініл, тетрагідрохіноксалініл, фталазиніл, дигідрофталазиніл, тетрагідрофталазиніл, тетрагідробенз[b]азепініл, тетрагідробенз[с]азепініл, тетрагідробенз[d]азепініл, тетрагідробензо[b][1,4]діазепініл, тетрагідробензо[е][1,4]-діазепініл, тетрагідробензо[b][1,4]оксазепініл або тетрагідробензо[b][1,4]тіазепініл. 93687 10 Зі сполук загальної формули (І), які є об'єктами даного винаходу, перша підгрупа сполук утворена сполуками, в яких: Х1, Х2, Х3, Х4 означають, незалежно один від одного, атом водню або галогену, наприклад, атом фтору, або (С1-С6)-алкіл, наприклад, трет-бутил, або (С1-С6)-фторалкіл, наприклад, трифторметил. Зі сполук загальної формули (І), які є об'єктами даного винаходу, друга підгрупа сполук утворена сполуками, в яких: Х1, Х2, Х3, Х4 означають, незалежно один від одного, атом водню або галогену, наприклад, атом фтору, або (С1-С6)-алкіл, наприклад, трет-бутил, або (С1-С6)-фторалкіл, наприклад, трифторметил, або групу NR1R2, причому R1 і R2 мають значення, як зазначені у загальній формулі (І), наприклад, диметиламіногрупа. Зі сполук загальної формули (І), які є об'єктами даного винаходу, третя підгрупа сполук утворена сполуками, в яких Х2 відрізняється від атома водню. Зі сполук загальної формули (І), які є об'єктами даного винаходу, четверта підгрупа сполук утворена сполуками, в яких: W означає конденсовану біциклічну групу формули: , зв'язану з атомом азоту у положеннях 1, 2, 3 або 4; і W вибирають з груп: індолініл, ізоіндоліл, ізоіндолініл, бензофураніл, дигідробензофураніл, бензотіофеніл, дигідробензотіофеніл, бензоксазоліл, дигідробензоксазолініл, ізобензофураніл, дигідроізобензофураніл, бензімідазоліл, дигідробензімідазоліл, індоліл, індазоліл, бензотіазоліл, ізобензотіазоліл, дигідроізобензотіазоліл, бензотриазоліл, хінолініл, дигідрохінолініл, тетрагідрохінолініл, ізохінолініл, дигідроізохінолініл, тетрагідроізохінолініл, бензоксазиніл, дигідробензоксазиніл, бензотіазиніл, дигідробензотіазиніл, цинолініл, хіназолініл, дигідрохіназолініл, тетрагідрохіназолініл, хіноксалініл, дигідрохіноксалініл, тетрагідрохіноксалініл, фталазиніл, дигідрофталазиніл, тетрагідрофталазиніл, тетрагідробенз[b]азепініл, тетрагідробенз[с]азепініл, тетрагідробенз[d]азепініл, тетрагідробензо[b][1,4]діазепініл, тетрагідробензо[е][1,4]діазепініл, тетрагідробензо[b][1,4]оксазепініл або тетрагідробензо[b][1,4]тіазепініл; причому атом або атоми вуглецю і/або азоту вказаної вище групи W можливо заміщені, як зазначено у випадку загальної формули (І). Зі сполук четвертої підгрупи, п'ята підгрупа сполук утворена сполуками, в яких: W означає конденсовану біциклічну групу формули: 11 , зв'язану з атомом азоту у положеннях 1, 2, 3 або 4; і W вибирають з бензімідазолілу та індолілу; і/або атом або атоми вуглеців А можливо заміщені одним або декількома (С1-С6)-алкілами, наприклад, метилом; і/або атом або атоми азоту А можливо заміщені радикалом R7, причому R7 означає (С1-С6)-алкіл, наприклад, метил. Зі сполук п'ятої підгрупи, шоста підгрупа сполук утворена сполуками, в яких: W вибирають з бензімідазол-5-ілу та індол-5ілу; і/або атом або атоми вуглеців А можливо заміщені одним або декількома (С1-С6)-алкілами, наприклад, метилом; і/або атом або атоми азоту А можливо заміщені радикалом R7, причому R7 означає (С1-С6)-алкіл, наприклад, метил. Зі сполук четвертої підгрупи, сьома підгрупа сполук утворена сполуками, в яких: W означає конденсовану біциклічну групу формули: , зв'язану з атомом азоту у положеннях 2 або 3; і W вибирають з бензімідазолілу, індолілу, бензотіазолілу, хінолінілу, тетрагідрохінолінілу і бензоксазинілу; і/або атом або атоми вуглеців А можливо заміщені одним або декількома (Cj-C6)-алкілами, наприклад, метилом або ізопропілом, (С1-С6)-фторалкілами, наприклад, трифторметилом, (С3-С7)циклоалкілами, наприклад, циклопропілом, або оксогрупою; і/або атом або атоми азоту А можливо заміщені радикалом R6, коли азот є суміжним з атомом вуглецю, заміщеним оксогрупою, причому R6 означає атом водню або (С1-С6)-алкіл, наприклад, метил; або радикалом R7 в інших випадках, причому R7 означає (С1-С6)-алкіл, наприклад, метил, або (С3С7)-циклоалкіл-(С1-С3)-алкілен, наприклад, циклопропілметил. Зі сполук загальної формули (І), які є об'єктами даного винаходу, восьма підгрупа сполук утворена сполуками, в яких n дорівнює 1 або 2. Зі сполук загальної формули (І), які є об'єктами даного винаходу, дев'ята підгрупа сполук утворена сполуками, в яких: Υ означає гетероарил, наприклад, піридиніл, імідазоліл, бензімідазоліл, тіазоліл, хінолініл, причому гетероарил можливо заміщений однією або декількома групами, вибраними з (С1-С6)-алкілу, 93687 12 наприклад, метил, NR1R2 або арил-(С1-С6)алкілену, наприклад, бензил; причому R1 і R2 разом з атомом азоту, що їх несе, утворюють морфолініл. Зі сполук загальної формули (І), які є об'єктами даного винаходу, десята підгрупа сполук утворена сполуками, в яких: Υ означає гетероарил, вибраний з наступних груп: піридиніл, піримідиніл, піразиніл, піридазиніл, імідазоліл, бензімідазоліл, бензотіазоліл, тіазоліл, фураніл, хінолініл, ізохінолініл, хіноксалініл, причому гетероарил можливо заміщений однією або декількома групами, вибраними з (С1-С6)-алкілу, наприклад, метил, (С1-С6)-фторалкілу, наприклад, трифторметил, арил-(С1-С6)-алкілену, наприклад, бензил, або NR1R2; причому R1 і R2 разом з атомом азоту, що їх несе, утворюють морфолініл. Зі сполук загальної формули (І), які є об'єктами даного винаходу, одинадцята підгрупа сполук утворена сполуками, в яких: W означає бензімідазоліл, причому атом або атоми вуглецю і/або азоту вказаної вище групи W можливо заміщені, як зазначено у випадку загальної формули (І); Υ означає піридиніл, можливо заміщений, як зазначено у випадку загальної формули (І). Зі сполук загальної формули (І), які є об'єктами даного винаходу, дванадцята підгрупа сполук утворена сполуками, в яких: Х1, Х2, Х3, Х4 означають, незалежно один від одного, атом водню або галогену, наприклад, атом фтору, або (С1-С6)-алкіл, наприклад, трет-бутил, або (С1-С6)-фторалкіл, наприклад, трифторметил, або групу NR1R2, причому R1 і R2 мають значення, як зазначені у випадку загальної формули (І), наприклад, диметиламіногрупу; W означає конденсовану біциклічну групу формули: , зв'язану з атомом азоту у положеннях 2 або 3; і W вибирають з бензімідазолілу, індолілу, бензотіазолілу, хінолінілу, тетрагідрохінолінілу і бензоксазинілу; причому атом або атоми вуглеців А можливо заміщені одним або декількома (С1-С6)-алкілами, наприклад, метилом або ізопропілом, (С1-С6)фторалкілами, наприклад, трифторметилом, (С3С7)-циклоалкілами, наприклад, циклопропілом, або оксогрупою; і/або атом або атоми азоту А можливо заміщені радикалом R6, коли азот є суміжним з атомом вуглецю, заміщеним оксогрупою, причому R6 означає атом водню або (С1-С6)-алкіл, наприклад, метил; або радикалом R7 в інших випадках, причому R7 означає (С1-С6)-алкіл, наприклад, метил, або (С3С7)-циклоалкіл-(С1-С3)-алкілен, наприклад, циклопропілметил; і/або n дорівнює 1 або 2; і/або 13 Υ означає гетероарил, вибраний з наступних груп: піридиніл, піримідиніл, піразиніл, піридазиніл, імідазоліл, бензімідазоліл, бензотіазоліл, тіазоліл, фураніл, хінолініл, ізохінолініл, хіноксалініл, причому гетероарил можливо заміщений однією або декількома групами, вибраними з (С1-С6)-алкілу, наприклад, метил, (С1-С6)-фторалкілу, наприклад, трифторметил, арил-(С1-С6)-алкілену, наприклад, бензил, або NR1R2; причому R1 і R2 разом з атомом азоту, що їх несе, утворюють морфолініл. Зі сполук загальної формули (І), які є об'єктами даного винаходу, тринадцята підгрупа сполук утворена сполуками, в яких: Х1 і Х4 означають, кожний, атом водню; Х2 і Х3 є такими, що один з двох означає атом водню, тоді як інший означає групу, вибрану з атома галогену, наприклад, атом фтору, або (С1С6)-алкілу, наприклад, трет-бутил, або (С1-С6)фторалкілу, наприклад, трифторметил, або NR1R2, причому R1 і R2 мають значення, як зазначені у випадку загальної формули (І), наприклад, диметиламіногрупа; W означає конденсовану біциклічну групу формули: , зв'язану з атомом азоту у положеннях 2 або 3; і W вибирають з бензімідазолілу, бензотіазолілу, хінолінілу, тетрагідрохінолінілу; причому атоми вуглеців А можливо заміщені одним або декількома (С1-С6)-алкілами, наприклад, метилом; і/або атом або атоми азоту А можливо заміщені радикалом R7, причому R7 означає (С1-С6)-алкіл, наприклад, метил; n дорівнює 1; Υ означає гетероарил, наприклад, піридиніл, піразиніл, бензотіазоліл, хінолініл, ізохінолініл, хіноксалініл; причому гетероарил можливо заміщений одним або декількома (С1-С6)-алкілами, наприклад, метилом, або NR1R2; причому R1 і R2 разом з атомом азоту, що їх несе, утворюють морфолініл. Сполуки, в яких одночасно Х1, Х2, Х3, Х4, W, n і Υ є такими, як визначені у вказаних вище підгрупах сполук, утворюють чотирнадцяту підгрупу. У межах даного винаходу: - під (Ct-Cz), де t і z мають значення 1-7, розуміють вуглецевий ланцюг, що може включати від t до z атомів вуглецю, наприклад, (С1-С3)вуглецевий ланцюг, що може включати 1-3 атоми вуглецю; - під терміном «алкіл» розуміють лінійну або розгалужену насичену аліфатичну групу. Як приклади можна назвати метил, етил, пропіл, ізопропіл, бутил, ізобутил, трет-бутил, пентил, і т.д.; - під терміном «алкілен» розуміють лінійну або розгалужену, насичену двовалентну групу, наприклад, (С1-С3)-алкілен означає лінійний або розгалужений двовалентний вуглецевий ланцюг з 1-3 93687 14 атомами вуглецю, наприклад, метилен, етилен, 1метилетилен, пропілен; - під терміном «циклоалкіл» розуміють циклічну вуглецеву групу. Як приклади можна назвати циклопропіл, циклобутил, циклопентил, циклогексил, і т.д.; - під терміном «фторалкіл» розуміють алкільну групу, один або декілька атомів водню якої заміщені атомом фтору; - під терміном «алкоксил» розуміють -Оалкільний радикал, де алкільна група має вказане вище значення; - під терміном «фторалкоксил» розуміють алкоксильну групу, один або декілька атомів водню якої заміщені атомом фтору; - під терміном «тіоалкіл» розуміють радикал S-алкіл, де алкіл має вказане вище значення; - під терміном «арил» розуміють циклічну ароматичну групу, що включає 6-10 атомів вуглецю. Як приклади арильних груп можна назвати феніл або нафтил; - під терміном «гетероарил» розуміють 5-10членну циклічну ароматичну групу, що містить 1-4 гетероатоми, вибраних з О, S або N. Як приклад можна назвати імідазоліл, тіазоліл, оксазоліл, фураніл, тіофеніл, оксадіазоліл, тетразоліл, піридиніл, піразиніл, піримідиніл, піридазиніл, індоліл, бензофураніл, бензотіофеніл, бензоксазоліл, бензімідазоліл, індазоліл, бензотіазоліл, ізобензотіазоліл, бензотриазоліл, хінолініл, ізохінолініл, хіноксалініл; - під терміном «гетероцикл» розуміють 5-7членну насичену, частково ненасичену або ароматичну циклічну групу, що включає від одного до трьох гетероатомів, вибраних з О, S або Ν; - під атомом галогену розуміють фтор, хлор, бром або йод; - «оксо» означає «=О»; - «тіо» означає «=S». Сполуки формули (І) можуть включати один або декілька асиметричних атомів вуглецю. Отже, вони можуть існувати у формі енантіомерів або діастереоізомерів. Ці енантіомери, діастереоізомери, а також їх суміші, включаючи рацемічні суміші, складають частину винаходу. Сполуки формули (І) можуть існувати у формі основи або адитивних солей з кислотами. Такі адитивні солі складають частину винаходу. Ці солі переважно одержують з фармацевтично прийнятними кислотами, однак, солі з іншими кислотами, придатні, наприклад, для очищення або виділення сполук формули (І), також складають частину винаходу. Сполуки загальної формули (І) можуть знаходитися у формі гідратів або сольватів, а саме, у формі асоціацій або комбінацій з однією або декількома молекулами води або з розчинником. Такі гідрати і сольвати також складають частину винаходу. У наведеному нижче контексті під терміном «група, що видаляється» розуміють групу, що може бути легко відщеплена від молекули за рахунок розриву гетеролітичного зв'язку, з видаленням електронної пари. Ця група також може бути легко замінена іншою групою, наприклад, під час реакції 15 заміщення. Такими групами, що видаляються, є. наприклад, галогени або активована гідроксильна група, така, як метансульфонат, бензолсульфонат, п-толуолсульфонат, трифлат, ацетат, і т.д. Приклади груп, що видаляються, а також посилання на їх одержання представлені у книзі J. March «Advances in Organic Chemistry», 5-е видання, Wiley Interscience, 2001. Відповідно до винаходу, сполуки загальної формули (І) можна одержувати відповідно до способу, проілюстрованого на наведеній нижче схемі 1. Схема 1 Відповідно до схеми 1, сполуки загальної формули (IV) можуть бути одержані шляхом введення у взаємодію сполуки загальної формули (II), в якій Х1, Х2, Х3, Х4 мають значення, як зазначені у випадку загальної формули (І), і В означає (С1-С6)алкоксил, зі сполукою загальної формули (III), в якій Υ і n мають зазначені у випадку загальної формули (І) значення і GP означає групу, що видаляється, або GP означає гідроксильну групу. Сполуки загальної формули (II) комерційно доступні або їх одержують відповідно до численних способів, описаних у літературі (наприклад, D. Knittel, Synthesis, 2, 186 (1985); T.M. Williams, J. 93687 16 Med. Chem, 36(9), 1291 (1993); заявка на патент Японії JP 2001151771 A2). Коли сполука загальної формули (III) є такою, що n дорівнює 1, 2 або 3 і GP означає групу, що видаляється, таку, як атом хлору, брому або йоду, реакція може бути здійснена у присутності основи, такої, як гідрид натрію або карбонат калію, у полярному розчиннику, такому, як диметилформамід, диметилсульфоксид або ацетон (n=1: Kolasa Т., Bioorg. Med. Chem., 5(3), 507 (1997); n=2: Abramovitch R., Synth, Commun, 25(1), 1 (1995)). Коли сполука загальної формули (III) є такою, що n дорівнює 1, 2 або 3 і GP означає гідроксильну групу, сполуки загальної формули (IV) можуть бути одержані шляхом введення у взаємодію сполуки загальної формули (II) зі сполукою загальної формули (III) у присутності фосфіну, такого, як, наприклад, трифенілфосфін, і реагенту, такого, як, наприклад, діетилазодикарбоксилат, у вигляді розчину у розчиннику, такому, як дихлорметан або тетрагідрофуран (О. Mitsonobu, Synthesis, 1-28 (1981)). Сполуку загальної формули (І) потім одержують шляхом введення у взаємодію сполуки загальної формули (IV), такої, як одержана вище, з амідом сполуки загальної формули (V), в якій W має зазначене у випадку загальної формули (І) значення, при температурі кипіння зі зворотним холодильником розчинника, такого, як толуол. Амід сполуки загальної формули (V) одержують шляхом попереднього впливу триметилалюмінію на аміни загальної формули (V). Сполуки загальних формул (І), (II) і (IV), в яких Х1, Х2, Х3 і/або Х4 означають ціаногрупу або арил, можуть бути одержані шляхом реакції зв'язування, що каталізується металом, таким, як паладій, здійснюваної при використанні сполук відповідних загальних формул (І), (II) і (IV), в яких Х1, Х2, Х3 і/або Х4 означають групу, що видаляється, наприклад, бром, відповідно до способів, які описані у літературі або які відомі фахівцеві у даній галузі. Сполуки загальних формул (І), (II) і (IV), в яких Х1, Х2, Х3 і/або Х4 означають групу C(O)NR1R2, можуть бути одержані зі сполук відповідних загальних формул (І), (II) і (IV), в яких Х1, Х2, Х3 і/або Х4 означають ціаногрупу, відповідно до способів, які описані у літературі або які відомі фахівцеві у даній галузі. Сполуки загальних формул (І), (II) і (IV), в яких Х1, Х2, Х3 і/або Х4 означають групу -S(О)-алкіл або S(О)2-алкіл, можуть бути одержані шляхом окиснення сполук відповідних загальних формул (І), (II) і (IV), в яких Х1, Х2, Х3 і/або Х4 означають (С1-С6)тіоалкільну групу, відповідно до способів, які описані у літературі або які відомі фахівцеві у даній галузі. Сполуки загальних формул (І), (II) і (IV), в яких Х1, Х2, Х3 і/або Х4 означають групу NR1R2, NR3COR4 або NR3SO2R5, можуть бути одержані зі сполук відповідних загальних формул (І), (II) і (IV), в яких Х1, Х2, Х3 і/або Х4 означають нітрогрупу, наприклад, шляхом відновлення, потім ацилювання або сульфонілування, відповідно до способів, які описані у літературі або які відомі фахівцеві у даній галузі. 17 93687 18 Сполуки загальних формул (І), (II) і (IV), в яких Х1, Х2, Х3 і/або Х4 означають групу NR1R2, NR3COR4 або NR3SO2R5, можуть бути одержані зі сполук відповідних загальних формул (І), (II) і (IV), в яких Х1, Х2, Х3 і/або Х4 означають, наприклад, атом брому, шляхом реакції зв'язування, відповідно, з аміном, амідом або сульфонамідом, у присутності основи, фосфіну і каталізатора на основі паладію, відповідно до способів, які описані у літературі або які відомі фахівцеві у даній галузі. Сполуки загальних формул (І), (II) і (IV), в яких Х1, Х2, Х3 і/або Х4 означають групу SO2NR1R2, можуть бути одержані способом, аналогічним такому, описаному у Pharmazie, 45, 346 (1990), або відповідно до способів, які описані у літературі або які відомі фахівцеві у даній галузі. Сполуки загальної формули (І), в якій R7 означає атом водню, можуть бути одержані зі сполук загальної формули (І), в якій, наприклад, R7 означає фенілметил, шляхом гідрування, що каталізу ється, наприклад, паладієм, або будь-якими способами, які описані у літературі або які відомі фахівцеві у даній галузі. У наведеному вище контексті,сполуки формули (III) є комерційно доступними, описуваними у літературі (Carling R.W. та ін., J. Med. Chem., (47), 1807-1822 (2004), або Russel M.G.N. та ін, J. Med. Chem, (48), 1367-1383 (2005)), або доступними шляхом одержання при використанні способів, відомих фахівцеві у даній галузі. Сполуки (V) та інші реагенти, коли спосіб їх одержання не описаний, є комерційно доступними або описуваними у літературі (наприклад, WO 03049702, WO 03068749). Об'єктом винаходу, відповідно до іншого з його аспектів, є також сполуки формули (IV1-35) або (V16). Ці сполуки придатні як проміжні продукти синтезу сполук формули (І) і, загалом, при одержанні призначених для терапії сполук. Індоли (IV1-35), перераховані у таблиці 1, всі були одержані відповідно до одного зі способів, представлених на схемі 1. Наведена нижче таблиця 1 ілюструє хімічні структури і фізичні властивості деяких сполук загальної формули (IV1-35) відповідно до винаходу. У цій таблиці: - у колонці «Т.пл.» вказуються температури плавлення продуктів у градусах Цельсію (°С); - коли продукти виділені у вигляді аморфної твердої речовини або масла, вони характеризуються у цій колонці їх масою ([МН]+) або наведеними нижче докладними даними їх ЯМР; - t-Bu означає трет-бутил, Me означає метил і Et означає етил. 19 Нижче представлені дані ЯМР деяких сполук таблиці 1: Сполука № ІV1: 1Н-ЯМР (CDCl3), (м. ч.): 1,3 (т, 3H); 4,2 (кв, 2Н); 5,79 (с, 2Н); 6,82 (д, 2Н); 7,07 (м, 2Н); 7,27 (м, 2Н); 8,41 (д, 2Н). Сполука № ІV24: 1Н-ЯМР (CDCl3), (м. ч.): 1,38 (т, 3H); 2,6 (с, 3H); 4,32 (кв, 2Н); 5,91 (с, 2Н); 6,39 (д, 1Н); 7,05 (м, 2Н); 7,35 (м, 4Н). Сполука № ІV25: 1Н-ЯМР (CDCl3), (м. ч.): 1,54 (т, 3H); 4,51 (кв, 2Н); 6,1 (с, 2Н); 6,97 (м, 1Н); 7,29 (тхд, 1Н); 7,41 (м, 1Н); 7,6 (м, 6Н); 8,06 (м, 2Н); 7,5 (д, 1Н). Сполука № ІV26: 1Н-ЯМР (ДМСО-d6), (м. ч.): 1,25 (с, 9Н); 3,79 (с, 3H); 5,90 (с, 2Н); 6,96 (дхд, 2Н); 7,27 (дхд, 1Н); 7,35 (с, 1Н); 7,46 (с, 1Н); 7,66 (д, 1Н); 8,45 (дхд, 2Н). Сполука № ІV27: 1Н-ЯМР (ДМСО-d6), (м. ч.): 1,27 (т, 3H); 4,29 (кв, 2Н); 5,95 (с, 2Н); 6,93 (д, 2Н); 7,58 (с, 1Н); 7,61 (дхд, 1Н); 7,80 (д, 1Н); 8,22 (с, 1Н); 8,45 (дхд, 2Н). Сполука № ІV28: 1Н-ЯМР (ДМСО-d6), (м. ч.): 1,23 (т, 3H); 2,91 (с, 6Н); 4,2 (кв, 2Н); 5,79 (с, 2Н); 93687 20 6,56 (с, 1Н); 6,8 (дхд, 1Н); 6,94 (дхд, 2Н); 7,26 (с, 1Н); 7.52 (д, 1Н); 8,45 (дхд, 2Н). Сполука № ІV29: 1Н-ЯМР (ДМСО-d6), (м. ч.): 3,82 (с, 3H); 6 (с, 2Н); 6,9 (д, 2Н); 7,46 (д, 1Н); 7,54 (с, 1Н); 7,99 (д, 1Н); 8,08 (с, 1Н); 8,45 (дхд, 2Н). Сполука № ІV30: 1Н-ЯМР (CDCl3), (м. ч.): 1,41 (м, 12Н); 4,35 (кв, 2Н); 5,81 (с, 2Н); 6,97 (д, 2Н); 7,21 (д, 1Н); 7,45 (м, 2Н); 7,74 (м, 1Н); 8,54 (д, 2Н). Сполука № ІV31: 1Н-ЯМР (ДМСО-d6), (м. ч.): 1,25 (т, 3H); 1,32 (с, 9Н); 4,25 (кв, 2Н); 5,88 (с, 2Н); 6,79 (д, 1Н); 7,22 (м, 1Н); 7,32 (с, 1Н); 7,4 (м, 2Н); 7,65 (м, 2Н); 8,46 (м, 1Н). Сполука № ІV32: 1Н-ЯМР (ДМСО-d6), (м. ч.): 1,28 (т, 3H); 1,32 (с, 9Н); 4,29 (кв, 2Н); 5,85 (с, 2Н); 7,27 (м, 1Н); 7,35 (м, 2Н); 7,48 (м, 2Н); 7,65 (д, 1Н); 8,36 (д, 1Н);8,41(д, 1Н). Аміни (V1-6) можуть бути одержані відповідно до шляху синтезу, представленого на схемі 2. На цій схемі, Ζ1 і Ζ2 означають, кожний, незалежно один від одного, (С1-С6)-алкіл, (С3-С7)циклоалкіл або (С3-С7)-циклоалкіл-(С1-С3)-алкілен. 21 93687 22 Циклізація з використанням 4-нітро-1,2фенілендіаміну (VI) і реагенту, такого, як карбонова кислота формули Z2-CO2H, в якій Ζ2 означає (С1-С6)-алкіл, (С3-С7)-циклоалкіл або (С3-С7)циклоалкіл-(С1-С3)-алкілен, дозволяє одержувати бензімідазол (VII). Він потім може бути заміщений групою Z1 шляхом введення у взаємодію зі сполукою формули Z1-GP, де GP має зазначене у випадку схеми 1 значення і Z1 означає (С1-С6)-алкіл, (С3-С7)-циклоалкіл або (С3-С7)-циклоалкіл-(С1-С3)алкілен, наприклад, у присутності основи, такої як гідрид натрію, у розчиннику, такому як тетрагідрофуран. Одержувану суміш бензімідазолів (VIII) потім перетворюють в аміни (V1-6) шляхом відновлення, наприклад, шляхом каталітичного гідрування у присутності каталізатора, такого, як паладійна-вуглеці, або відповідно до будь-якого іншого способу відновлення нітрогрупи до аміногрупи, відомого фахівцеві у даній галузі. Схема 2 Аміни (V1-6) перераховані у таблицях 2а і 2b. Опис способу одержання одного з цих амінів докладно викладений в експериментальній частині. У наведених нижче прикладах описується одержання деяких сполук відповідно до винаходу. Ці приклади не обмежують об'єм охорони винаходу і служать тільки для ілюстрації даного винаходу. Номери сполук, що наводяться у прикладах, відповідають таким, зазначеним у таблиці 3. Елементні мікроаналізи, аналізи LC-MS (рідинна хроматографія у поєднанні з мас-спектрометрією), ІЧспектри або ЯМР-спектри підтверджують структури одержаних сполук. 23 Приклад 1 (сполука № 3) Гідрохлорид (1:1) N-(1-метил-1Н-індол-5-іл)-5фтор-1-[(піридин-4-іл)метил]-1Н-індол-2карбоксаміду 1.1. Етил-5-фтор-1-[(піридин-4-іл)метил]-1Ніндол-2-карбоксилат Додають, по краплях, розчин 1 г (4,73 ммоль) етил-5-фтор-1Н-індол-2-карбоксилату до перемішуваної при температурі 0°С і в атмосфері аргону суспензії 0,38 г (9,45 ммоль) 60%-ного гідриду натрію у 10 мл диметилформаміду. Суміш перемішують протягом 30 хвилин при температурі 0°С, потім протягом 30 хвилин при температурі 20°С. Реакційну суміш охолоджують і декількома порціями додають 1,24 г (4,2 ммоль) 4бромметилпіридингідроброміду. Суміш перемішують протягом 30 хвилин при температурі 0°С, потім протягом 30 хвилин при температурі 20°С. Реакційну суміш знову охолоджують до температури 0°С і додають додаткові 0,38 г (9,45 ммоль) 60%ного гідриду натрію у 10 мл диметилформаміду. Після витримування протягом 30 хвилин при температурі 0°С, декількома порціями додають 1,24 г (4,2 ммоль) 4-бромметилпіридингідроброміду. Реакційну суміш потім перемішують протягом 20 годин при температурі 20°С. Після цього суміш виливають у розчин зі 100 мл води з льодом і 100 мл діетилового ефіру. Органічну фазу відділяють, а водну фазу знову екстрагують за допомогою 100 мл діетилового ефіру. Органічні фази об'єднують, промивають за допомогою 50 мл води, потім сушать над сульфатом натрію, відфільтровують, потім концентрують при зниженому тиску. Залишок очищають препаративною хроматографією (елюент: дихлорметан-ацетон). Одержують 0,65 г очікуваного продукту у вигляді масла, використовуваного таким, яке є, при продовженні синтезу. 1.2. Гідрохлорид (1:1) N-(1-метил-1Н-індол-5іл)-5-фтор-1-[(піридин-4-іл)метил]-1Н-індол-2карбоксаміду (сполука № 3) В атмосфері аргону, до розчину 0,18 г (1,21 ммоль) 5-аміно-1-метил-1Н-індолу (І.Т. Forbes, J. Med. Chem., 36(8), 1104 (1993)) у 10 мл безводного толуолу додають 1,26 мл триметилалюмінію (2 Μ розчин у толуолі). Через 15 хвилин додають 0,3 г (1,01 ммоль) етил-5-фтор-1-[(піридин-4-іл)метил]1Н-індол-2-карбоксилату, одержаного на стадії 1.1. Кип'ятять зі зворотним холодильником протягом 4 годин, потім реакційне середовище перемішують при кімнатній температурі протягом ночі. Виливають його на лід і екстрагують два рази по 30 мл дихлорметану. Органічні фази об'єднують, промивають за допомогою 50 мл води, потім сушать над сульфатом натрію, відфільтровують, потім концентрують при зниженому тиску. Залишок очищають препаративною хроматографією (елюент: дихлорметан-ацетон). Одержують 0,35 г твердої речовини, яку висушують при зниженому тиску. Температура плавлення (основа): 204-205°С. Одержану тверду речовину обробляють за допомогою 30 мл дихлорметану і додають 0,26 мл 4н розчину хлороводню у діоксані. Розчин концентрують при зниженому тиску і одержаний залишок перекристалізовують з суміші ізопропанолу і мета 93687 24 нолу. Таким чином одержують 0,33 г очікуваного продукту у вигляді гідрохлориду. Температура плавлення (1 HCl): 258-260°С. 1 Н-ЯМР (ДМСО-d6), (м. ч.): 3,76 (с, 3H); 6,1 (с, 2Н); 6,33 (д, 1Н); 7,11 (дхд, 1Н); 7,25 (д, 2Н); 7,37 (м, 2Н); 7,52 (м, 5Н); 7,9 (с, 1Н); 8,7 (д, 2Н). Приклад 2 (сполука № 4) Πдрохлорид (2:1) N-(1-метил-1Н-бензімідазол5-іл)-5-фтор-1-[(піридин-3-іл)метил]-1Н-індол-2карбоксаміду 2.1. Етил-5-фтор-1-[(піридин-3-іл)метил]-1Ніндол-2-карбоксилат Додають, по краплях, розчин 1 г (4,73 ммоль) етил-5-фтор-1Н-індол-2-карбоксилату до перемішуваної при температурі 0°С і в атмосфері аргону суспензії 0,38 г (9,45 ммоль) 60%-ного гідриду натрію у 10 мл диметилформаміду. Суміш перемішують протягом 30 хвилин при температурі 0°С, потім протягом 30 хвилин при температурі 20°С. Реакційну суміш охолоджують і декількома порціями додають 1,24 г (4,8 ммоль) 3бромметилпіридингідроброміду. Суміш перемішують протягом 30 хвилин при температурі 0°С, потім протягом 30 хвилин при температурі 20°С. Реакційну суміш знову охолоджують до температури 0°С і додають додаткові 0,38 г (9,45 ммоль) 60%ного гідриду натрію у 10 мл диметилформаміду. Після витримування протягом 30 хвилин при температурі 0°С, декількома порціями додають 1,24 г (4,8 ммоль) 3-бромметилпіридингідроброміду. Реакційну суміш потім перемішують протягом 58 годин при температурі 20°С. Суміш потім виливають у розчин зі 100 мл води з льодом і 100 мл діетилового ефіру. Органічну фазу відділяють, а водну фазу знову екстрагують за допомогою 100 мл діетилового ефіру. Органічні фази об'єднують, промивають за допомогою 50 мл води, потім сушать над сульфатом натрію, відфільтровують, потім концентрують при зниженому тиску. Залишок очищають препаративною хроматографією (елюент: дихлорметан-ацетон). Одержують 0,5 г очікуваного продукту у вигляді твердої речовини, використовуваної такою, яка є, при продовженні синтезу. Т.пл.=104-105°С. 2.2. Гідрохлорид (2:1) N-(1-метил-1Нбензімідазол-5-іл)-5-фтор-1-[(піридин-3-іл)метил]1Н-індол-2-карбоксаміду (сполука № 4) В атмосфері аргону, до розчину 0,414 г (2,82 ммоль) 5-аміно-1-метил-1Н-бензімідазолу у 10 мл безводного толуолу додають 4,1 мл триметилалюмінію (2 Μ розчин у толуолі). Через 15 хвилин додають 0,7 г (2,35 ммоль) етил-5-фтор-1[(піридин-3-іл)метил]-1Н-індол-2-карбоксилату, одержаного на стадії 2.1. Кип'ятять зі зворотним холодильником протягом 4 годин, потім реакційне середовище перемішують при кімнатній температурі протягом ночі. Виливають його на 100 г льоду і 50 мл дихлорметану. Одержують суспензію, яку відфільтровують і промивають водою і діетиловим ефіром. Залишок очищають препаративною хроматографією на глиноземі (елюент: дихлорметанметанол). Одержують 0,36 г твердої речовини, яку висушують при зниженому тиску. Одержану тверду речовину обробляють за допомогою 30 мл дихлорметану і додають 0,55 мл 4н 25 розчину хлороводню у діоксані. Розчин концентрують при зниженому тиску і одержаний залишок перекристалізовують з суміші ізопропанолу і метанолу. Таким чином одержують 0,36 г очікуваного продукту у вигляді гідрохлориду. Температура плавлення (2 HCl): 268-270°С. 1 Н-ЯМР (ДМСО-d6), (м. ч.): 4,03 (с, 3H); 6 (с, 2Н); 7,18 (дхд, 1Н); 7,56 (дхд, 1Н); 7,68 (м, 2Н); 7,9 (м, 4Н); 8,41 (с, 1Н); 8,69 (м, 2Н); 9,59 (с, 1Н). Приклад 3 (сполука № 6) Гідрохлорид (2:1) Ν-(1,2-диметил-1Нбензімідазол-5-іл)-5-трет-бутил-1-[(піридин-4іл)метил]-1Н-індол-2-карбоксаміду 3.1. Етил-5-трет-бутил-1-[(піридин-4-іл)метил]1Н-індол-2-карбоксилат Додають, по краплях, розчин 1 г (4,08 ммоль) етил-5-трет-бутил-1Н-індол-2-карбоксилату до перемішуваної при температурі 0°С і в атмосфері аргону суспензії 0,33 г (8,15 ммоль) 60%-ного гідриду натрію у 10 мл диметилформаміду. Суміш перемішують протягом 30 хвилин при температурі 0°С, потім протягом 30 хвилин при температурі 20°С. Реакційну суміш охолоджують і декількома порціями додають 1,06 г (4,08 ммоль) 4бромметилпіридингідроброміду. Суміш перемішують протягом 30 хвилин при температурі 0°С, потім протягом 30 хвилин при температурі 20°С. Реакційну суміш знову охолоджують до температури 0°С і додають додаткові 0,33 г (8,15 ммоль) 60%ного гідриду натрію у 10 мл диметилформаміду. Після витримування протягом 30 хвилин при температурі 0°С, декількома порціями додають 1,06 г (4,08 ммоль) 4-бромметилпіридингідроброміду. Реакційну суміш потім перемішують протягом 20 годин при температурі 20°С. Після цього суміш виливають у розчин зі 100 мл води з льодом і 70 мл діетилового ефіру. Органічну фазу відділяють, а водну фазу знову екстрагують за допомогою 50 мл діетилового ефіру. Органічні фази об'єднують, промивають за допомогою 50 мл води, потім сушать над сульфатом натрію, відфільтровують, потім концентрують при зниженому тиску. Залишок очищають препаративною хроматографією (елюент: дихлорметан-ацетон). Одержують 0,7 г очікуваного продукту у вигляді масла, використовуваного таким, яке є, при продовженні синтезу. 3.2. Гідрохлорид (2:1) N-(1,2-диметил-1Нбензімідазол-5-іл)-5-трет-бутил-1-[(піридин-4іл)метил]-1Н-індол-2-карбоксаміду (сполука № 6) В атмосфері аргону, до розчину 0,24 г (1,43 ммоль) 5-аміно-1,2-диметил-1Н-бензімідазолу (WO 2002059110) у 20 мл безводного толуолу додають 0,9 мл триметилалюмінію (2 Μ розчин у толуолі). Через 15 хвилин додають 0,4 г (1,19 ммоль) етил-5-трет-бутил-1-[(піридин-4-іл)метил]-1Hіндол-2-карбоксилату, одержаного на стадії 3.1. Кип'ятять зі зворотним холодильником протягом 4 годин, потім реакційне середовище перемішують при кімнатній температурі протягом ночі. Виливають його на 150 г льоду і 70 мл дихлорметану. Відділяють водну фазу, яку екстрагують два рази по 30 мл дихлорметану. Органічні фази об'єднують, промивають за допомогою 50 мл води, потім сушать над сульфатом натрію, відфільтровують, потім концентрують при зниженому тиску. Залишок 93687 26 очищають препаративною хроматографією (елюент: дихлорметан-метанол). Одержують 0,4 г твердої речовини, яку висушують при зниженому тиску. Температура плавлення (основа): 270-272°С. Одержану тверду речовину обробляють за допомогою 30 мл суміші 9:1 дихлорметану і метанолу і додають 0,5 мл 4н розчину хлороводню у діоксані. Розчин концентрують при зниженому тиску і одержаний залишок перекристалізовують з суміші етанолу і води. Таким чином одержують 0,22 г очікуваного продукту у вигляді гідрохлориду. Температура плавлення (2 HCl): 295-300°С. 1 Н-ЯМР (ДМСО-d6), (м. ч.): 1,31 (с, 9Н), 2,79 (с, 3H), 3,89 (с, 3H); 6,08 (с, 2Н); 7,42 (м, 4Н); 7,8 (м, 4Н); 8,3 (с, 1Н); 8,7 (д, 2Н); 10,9 (с, 1Н обмінюваний). Приклад 4 (сполука № 7) Гідрохлорид (2:1) N-(1,2-диметил-1Нбензімідазол-5-іл)-5-фтор-1-[(піридин-4-іл)метил]1Н-індол-2-карбоксаміду (сполука № 7) В атмосфері аргону, до розчину 0,27 г (1,61 ммоль) 5-аміно-1,2-диметил-1Н-бензімідазолу (WO 02059110) у 20 мл безводного толуолу додають 1 мл триметилалюмінію (2 Μ розчин у толуолі). Через 15 хвилин додають 0,4 г (1,34 ммоль) етил-5-фтор-1-[(піридин-4-іл)метил]-1Н-індол-2карбоксилату, одержаного на першій стадії прикладу 1. Кип'ятять зі зворотним холодильником протягом 3 годин, потім реакційне середовище перемішують при кімнатній температурі протягом ночі. Виливають його на лід і екстрагують два рази по 30 мл дихлорметану. Органічні фази об'єднують, промивають за допомогою 50 мл води, потім сушать над сульфатом натрію, відфільтровують, потім концентрують при зниженому тиску. Залишок очищають препаративною хроматографією (елюент: дихлорметан-ацетон). Одержують 0,46 г твердої речовини, яку висушують при зниженому тиску. Температура плавлення (основа): 249-250°С. Одержану тверду речовину обробляють за допомогою 30 мл дихлорметану і додають 0,26 мл 4н розчину хлороводню у діоксані. Розчин концентрують при зниженому тиску і одержану тверду речовину перекристалізовують з суміші ізопропанолу і метанолу. Таким чином одержують 0,33 г очікуваного продукту у вигляді гідрохлориду. Температура плавлення (2 HCl): 285-287°С. 1 Н-ЯМР (ДМСО-d6), (м. ч.): 2,8 (с, 3H), 3,87 (с, 3H); 6,1 (с, 2Н); 7,16 (дхд, 1Н); 7,51 (м, 4Н); 7,75 (с, 1Н); 7,85 (д, 2Н); 8,3 (с, 1Н); 8,75 (д, 2Н). Приклад 5 (сполука № 11) N-(1-метил-1Н-індол-5-іл)-5-фтор-1-[(піридин3-іл)етил]-1Н-індол-2-карбоксамід 5.1. Етил-5-фтор-1-[(піридин-3-іл)етил]-1Ніндол-2-карбоксилат Додають, по краплях, розчин 0,365 г (1,44 ммоль) 1,1'-(азодикарбоніл)дипіперидину у 10 мл тетрагідрофурану до розчину 0,2 г (0,97 ммоль) етил-5-фтор-1Н-індол-2-карбоксилату, 0,178 г (1,45 ммоль) 2-(піридин-3-іл)етанолу і 0,36 мл (1,44 ммоль) трибутилфосфіну у 30 мл тетрагідрофурану. Реакційну суміш перемішують протягом ночі при кімнатній температурі, потім концентру 27 ють при зниженому тиску і обробляють за допомогою 50 мл циклогексану. Суспензію після цього відфільтровують і фільтрат хроматографують на колонці з діоксидом кремнію (елюент: дихлорметан-метанол). Одержують 0,125 г очікуваного продукту. 5.2. N-(1-метил-1Н-індол-5-іл)-5-фтор-1[(піридин-3-іл)етил]-1Н-індол-2-карбоксамід (сполука № 11) В атмосфері аргону і при температурі 0°С, до розчину 0,7 г (0,478 ммоль) 5-аміно-1-метил-1Ніндолу (І.Т. Forbes, J. Med. Chem., 36(8), 1104 (1993)) у 5 мл безводного толуолу додають 0,54 мл триметилалюмінію (2 Μ розчин у толуолі). Через 15 хвилин додають 0,125 г (0,4 ммоль) етил-5фтор-1-[(піридин-3-іл)етил]-1Н-індол-2карбоксилату, одержаного на стадії 5.1. Кип'ятять зі зворотним холодильником протягом 5 годин, потім реакційне середовище перемішують при кімнатній температурі протягом ночі. Виливають його на 50 г льоду, 10 мл 1н соляної кислоти і 30 мл етилацетату. Органічну фазу відділяють і додають 15 мл 1н розчину гідроксиду натрію до водної фази, яку екстрагують за допомогою додаткових 30 мл етилацетату. Органічні фази об'єднують, промивають насиченим розчином хлориду натрію, сушать над сульфатом натрію і концентрують при зниженому тиску. Одержаний залишок обробляють за допомогою 15 мл діізопропілового ефіру і нерозчинну частину відфільтровують, потім висушують при зниженому тиску. Таким чином виділяють 50 мг очікуваного продукту у вигляді твердої речовини. Температура плавлення (основа): 188-189°С. 1 Н-ЯМР (ДМСО-d6), (м. ч.): 3,19 (т, 2Н); 3,85 (с, 3H); 4,85 (т, 2Н); 6,49 (д, 1Н); 6,92 (с, 1Н); 7,1 (м, 3H); 7,29 (м, 4Н); 7,49 (дхт, 1Н); 7,75 (м, 1Н); 7,9 (с, 1Н); 8,21 (д, 1Н); 8,4 (д, 1Н). Приклад 6 (сполука № 94, 95 і 96) N-(1,2-диметил-1Н-бензімідазол-5-іл)-5-фтор1-[(3,6-диметилпіразин-2-іл)метил]-1Н-індол-2карбоксамід (сполука № 94) N-(1,2-диметил-1Н-бензімідазол-5-іл)-5-фтор1-[(5,6-диметилпіразин-2-іл)метил]-1Н-індол-2карбоксамід (сполука № 95) N-(1,2-диметил-1Н-бензімідазол-5-іл)-5-фтор1-[(3,5-диметилпіразин-2-іл)метил]-1Н-індол-2карбоксамід (сполука № 96) 6.1. (Хлорметил)диметилпіразин (суміш 3 ізомерів) Додають, протягом 1 години, 7,6 г (32,74 ммоль) трихлорізоціанурової кислоти до доведеного до температури кипіння зі зворотним холодильником розчину 10 г триметилпіразину (81,85 ммоль) у 820 мл дихлоретану. Реакційну суміш кип'ятять зі зворотним холодильником протягом 6 годин, потім охолоджують до температури 20°С, перемішують протягом додаткових 12 годин і фільтрують. Фільтрат концентрують при зниженому тиску, обробляють за допомогою 200 мл діетилового ефіру, знову відфільтровують, потім концентрують при зниженому тиску. Одержують 9,6 г метилдиметилпіразинхлориду у вигляді суміші, яку використовують такою, яка є, на наступній стадії. 93687 28 6.2. Етил-5-фтор-1-[(диметилпіразин-2іл)метил]-1Н-індол-2-карбоксилат (суміш сполук ІV21) Додають, по краплях, розчин 5 г (24,13 ммоль) етил-5-фтор-1Н-індол-2-карбоксилату до перемішуваної при температурі 0°С і в атмосфері аргону суспензії 1,45 г (36,2 ммоль) 60%-ного гідриду натрію у 200 мл диметилформаміду. Суміш перемішують протягом 30 хвилин при температурі 0°С, потім протягом 1 години при температурі 20°С. Після цього декількома порціями додають 9,45 г (60,33 ммоль) суміші метилдиметилпіразинхлоридів, одержаної на попередній стадії. Суміш перемішують протягом 2 годин при температурі 20°С, потім додають 200 мл води і 200 мл етилацетату. Органічну фазу відділяють, а водну фазу повторно екстрагують за допомогою 100 мл етилацетату. Органічні фази об'єднують, промивають 2 рази по 50 мл води, 50 мл водного насиченого розчину хлориду натрію, потім сушать над сульфатом магнію, відфільтровують і концентрують при зниженому тиску. Залишок очищають препаративною хроматографією (елюент: дихлорметанетилацетат). Одержують 1,1 г суміші трьох очікуваних ізомерів (IV21), використовуваної такою, яка є, при продовженні синтезу. 6.3. N-(1,2-Диметил-1Н-бензімідазол-5-іл)-5фтор-1-[(3,6-диметилпіразин-2-іл)метил]-1Н-індол2-карбоксамід (сполука № 94) N-(1,2-Диметил-1Н-бензімідазол-5-іл)-5-фтор1-[(5,6-диметилтразин-2-іл)метил]-1Н-індол-2карбоксамід (сполука № 95) N-(1,2-Диметил-1Н-бензімідазол-5-іл)-5-фтор1-[(3,5-диметилпiразин-2-іл)метил]-1Н-індол-2карбоксамід (сполука № 96) В атмосфері аргону, до розчину 0,568 г (3,53 ммоль) 5-аміно-1,2-диметил-1Н-бензімідазолу (WO 02059110) у 20 мл безводного толуолу додають 2,57 мл триметилалюмінію (2 Μ розчин у толуолі). Через 15 хвилин додають 1,05 г (3,21 ммоль) етил-5-фтор-1-[(диметилпіразин-2іл)метил]-1Н-індол-2-карбоксилату, одержаного на попередній стадії. Кип'ятять зі зворотним холодильником протягом 4 годин, потім реакційне середовище перемішують при кімнатній температурі протягом ночі. Виливають його на лід і екстрагують два рази по 100 мл етилацетату. Органічні фази об'єднують, промивають послідовно за допомогою 50 мл води і 50 мл водного насиченого розчину хлориду натрію, після чого сушать над сульфатом магнію, відфільтровують і концентрують при зниженому тиску. Залишок очищають препаративною хроматографією ВЕРХ (елюенти: етанол-гептантриетиламін). Виділяють: - 0,59 г ізомеру № 94 у вигляді твердої речовини; температура плавлення: 269-275°С; 1 Н-ЯМР (ДМСО-d6, (м. ч.): 2,31 (с, 3H); 2,46 (с, 3H); 2,6 (с, 3H); 3,69 (с, 3H); 5,95 (с, 2Н); 7,02 (тхд, 1); 7,4 (м, 5Н); 7,86 (с, 1Н); 8 (с, 1Н) - 0,139 г ізомеру № 95 у вигляді твердої речовини; температура плавлення: 226-228°С; 1 Н-ЯМР (ДМСО-d6), (м. ч.): 2,36 (с, 6Н); 2,49 (с, 3H); 3,9 (с, 3H); 6,41 (с, 2Н); 7,8 (тхд, 1Н); 8,06 29 (с, 1Н); 8,2 (м, 1Н); 8,29 (м, 2Н); 8,4 (м, 1Н); 8,71 (с, 2Н); 11,6 (с, 1Н) - 0,51 г ізомеру № 96 у вигляді твердої речовини; температура плавлення: 266-269°С; 1 Н-ЯМР (ДМСО-d6), (м. ч.): 2,18 (с, 3H); 2,49 (с, 3H); 2,6 (с, 3H); 3,71 (с, 3H); 6,41 (с, 2Н); 7,1 (тхд, 1Н); 7,4 (м, 5Н); 7,85 (с, 1Н); 8,2 (с, 1Н); 10,3 (с, 1Н). Приклад 7 (сполука № 32) N-(1,2-диметил-1Н-бензімідазол-5-іл)-5-фтор1-[(піразин-2-іл)метил]-1Н-індол-2-карбоксамід (сполука № 32) 7.1. Етил-5-фтор-1-[(піразин-2-іл)метил]-1Ніндол-2-карбоксилат (сполука № IV14) За методикою, аналогічною тій, що описана у прикладі 6.2, виходячи з 2 г (9,65 ммоль) етил-5фтор-1Н-індол-2-карбоксилату, одержують 1,55 г етил-5-фтор-1-[(піразин-2-іл)метил]-1Н-індол-2карбоксилату (сполука № IV14) [МН]+=300 7.2. N-(1,2-Диметил-1Н-бензімідазол-5-іл)-5фтор-1-[(піразин-2-іл)метил]-1Н-індол-2карбоксамід (сполука № 32) За методикою, аналогічною тій, що описана у прикладі 6.3, виходячи з 0,5 г етил-5-фтор-1[(піразин-2-іл)метил]-1Н-індол-2-карбоксилату (сполука № IV14), одержують 0,2 г N-(1,2-диметил1Н-бензімідазол-5-іл)-5-фтор-1-[(піразин-2іл)метил]-1Н-індол-2-карбоксаміду (сполука № 32). Температура плавлення: 239-240°С; 1 Н-ЯМР (ДМСО-d6), (м. ч.): 2,5 (с, 3H); 3,7 (с, 3H); 5,98 (с, 2Н); 7,11 (тхд, 1Н); 7,49 (м, 5Н); 7,9 (д, 1Н); 8,4 (с, 1Н); 8,5 (с, 2Н); 10,39 (с, 1Н). Приклад 8 (сполука № 37) N-(1,2-Диметил-1Н-бензімідазол-5-іл)-5-фтор1-[(4-метилпіридин-2-іл)метил]-1Н-індол-2карбоксамід (сполука № 37) 8.1. Етил-5-фтор-1-[(4-метилпіридин-2іл)метил]-1Н-індол-2-карбоксилат (сполука № ІV17) За методикою, аналогічною тій, що описана у прикладі 6.2, виходячи з 2 г (9,65 ммоль) етил-5фтор-1Н-індол-2-карбоксилату, одержують 1,2 г етил-5-фтор-1-[(4-метилпіридин-2-іл)метил]-1Ніндол-2-карбоксилату (сполука № IV17). [МН]+=313. 8.2. N-(1,2-Диметил-1Н-бензімідазол-5-іл)-5фтор-1-[(4-метилпіридин-2-іл)метил]-1Н-індол-2карбоксамід (сполука № 37) За методикою, аналогічною тій, що описана у прикладі 6.3, виходячи з 0,51 г етил-5-фтор-1-[(4метилпіридин-2-іл)метил]-1Н-індол-2-карбоксилату (сполука № IV17), одержують 0,48 г N-(1,2диметил-1Н-бензімідазол-5-іл)-5-фтор-1-[(4метилпіридин-2-іл)метил]-1Н-індол-2-карбоксаміду (сполука № 37). Температура плавлення: 213-215°С; 1 Н-ЯМР (ДМСО-d6), (м. ч.): 2,18 (с, 3H); 2,49 (с, 3H); 3,67 (с, 3H); 5,88 (с, 2Н); 6,82 (с, 1Н); 7,08 (м, 2Н); 7,4 (м, 5Н); 7,9 (с, 1Н); 8,39 (с, 1Н); 10,4 (с, 1Н). Приклад 9 (сполука № 67) N-(1-Метил-1Н-індол-5-іл)-5-фтор-1[(піримідин-4-іл)метил]-1Н-індол-2-карбоксамід (сполука № 67) 93687 30 9.1. Етил-5-фтор-1-[(піримідин-4-іл)метил]-1Ніндол-2-карбоксилат (сполука № IV35) За методикою, аналогічною тій, що описана у прикладі 6.2, виходячи з 3,3 г (15,93 ммоль) етил5-фтор-1Н-індол-2-карбоксилату, одержують 2,6 г етил-5-фтор-1-[(піримідин-4-іл)метил]-1Н-індол-2карбоксилату (сполука № IV35). [МН]+=300. 9.2. N-(1-Метил-1Н-індол-5-іл)-5-фтор-1[(піримідин-4-іл)метил]-1Н-індол-2-карбоксамід (сполука № 67) За методикою, аналогічною тій, що описана у прикладі 6.3, виходячи з 0,5 г етил-5-фтор-1[(піримідин-4-іл)метил]-1Н-індол-2-карбоксилату (сполука № IV35), одержують0,41 г N-(1-метил-1Ніндол-5-іл)-5-фтор-1-[(піримідин-4-іл)метил]-1Ніндол-2-карбоксаміду (сполука № 67). Температура плавлення: 199-200°С; 1 Н-ЯМР (ДМСО-d6), (м. ч.): 2,5 (с, 3H); 3,69 (с, 3H); 5,93 (с, 2Н); 6,91 (д, 1Н); 7,08 (тхд, 1Н); 7,42 (м, 5Н); 7,85 (с, 1Н); 8,62 (д, 1Н); 9,03 (с, 1Н); 10,31 (с, 1Н). Приклад 10 (сполука № 68) N-(1,2-Диметил-1Н-бензімідазол-5-іл)-5-фтор1-[(6-метилпіразин-2-іл)метил]-1Н-індол-2карбоксамід (сполука № 68) 10.1. Етил-5-фтор-1-[(6-метилпіразин-2іл)метил]-1Н-індол-2-карбоксилат (сполука № IV22) За методикою, аналогічною тій, що описана у прикладі 6.2, виходячи з 3,3 г (15,93 ммоль) етил5-фтор-1Н-індол-2-карбоксилату, одержують 0,32 г етил-5-фтор-1-[(6-метилпіразин-2-іл)метил]-1Ніндол-2-карбоксилату (сполука № IV22). [МН]+=314. 10.2. Ν-(1,2-Диметил-1H-бензімідазол-5-іл)-5фтор-1-[(6-метилпіразин-2-іл)метил]-1Н-індол-2карбоксамід (сполука № 68) За методикою, аналогічною тій, що описана у прикладі 6.3, виходячи з 0,38 г етил-5-фтор-1-[(6метилпіразин-2-іл)метил]-1Н-індол-2-карбоксилату (сполука № IV22), одержують 0,28 г N-(1,2диметил-1Н-бензімідазол-5-іл)-5-фтор-1-[(6метилпіразин-2-іл)метил]-1Н-індол-2-карбоксаміду (сполука № 68). Температура плавлення: 244-249°С; 1 Н-ЯМР (ДМСО-d6), (м. ч.): 2,39 (с, 3H); 2,49 (с, 3H); 3,69 (с, 3H); 5,91 (с, 2Н); 7,08 (м, 1Н); 7,42 (м, 5Н); 7,9 (с, 1Н); 7,99 (с, 1Н); 8,36 (с, 1Н). Приклад 11 (сполука № 24) N-(1,2-Диметил-1Н-бензімідазол-5-іл)-5трифторметил-1-[(піридин-4-іл)метил]-1Н-індол-2карбоксамід (сполука № 24) 11.1. Етил-5-трифторметил-1-[(піридин-4іл)метил]-1Н-індол-2-карбоксилат (сполука № ІV27) Додають, по краплях, розчин 1,47 г (5,83 ммоль) 1,1'-(азодикарбоніл)дипіперидину у 50 мл толуолу до розчину 1 г (3,89 ммоль) етил-5трифторметил-1Н-індол-2-карбоксилату, 0,63 г (5,83 ммоль) 4-піридилкарбінолу і 1,46 мл (5,83 ммоль) трибутилфосфіну у 50 мл толуолу. Реакційну суміш перемішують протягом ночі при кімнатній температурі, потім концентрують при зниженому тиску і хроматографують на колонці з діоксидом кремнію (елюент: дихлорметанметанол). Одержують 1,05 г очікуваного продукту. 31 1 Н-ЯМР (ДМСО-d6, (м. ч.): 1,27 (т, 3H); 4,29 (кв, 2Н); 5,95 (с, 2Н); 6,93 (д, 2Н); 7,58 (с, 1Н); 7,61 (дхд, 1Н); 7,80 (д, 1Н); 8,22 (с, 1Н); 8,45 (дхд, 2Н). 11.2. Ν-(1,2-Диметил-1Н-бензімідазол-5-іл)-5трифторметил-1-[(піридин-4-іл)метил]-1Н-індол-2карбоксамід (сполука № 24) За методикою, аналогічною тій, що описана у прикладі 6.3, виходячи з 0,5 г етил-5трифторметил-1-[(піридин-4-іл)метил]-1Н-індол-2карбоксилату (сполука № IV27), одержують 0,65 г N-(1,2-диметил-1Н-бензімідазол-5-іл)-5трифторметил-1-[(піридин-4-іл)метил]-1Н-індол-2карбоксаміду (сполука № 24). Температура плавлення: 250-251 °С; 1 Н-ЯМР (ДМСО-d6, (м. ч.): 2,49 (с, 3H); 3,69 (с, 3H); 5,95 (с, 2Н); 6,98 (д, 1Н); 7,49 (м, 4Н); 7,69 (д, 1Н); 7,9 (с, 1Н); 7,99 (с, 1Н); 8,19 (с, 1Н); 8,42 (д, 2Н). Приклад 12 (сполука № 91) N-(2-Циклопропіл-1-метил-1Н-бензімідазол-5іл)-5-фтор-1-[(піридин-4-іл)метил]-1Н-індол-2карбоксамід (сполука № 91) 12.1. 2-Циклопропіл-5-нітро-1Н-бензімідазол Аналогічно до описаного способу (WO 96/04270), розчин 5 г (32,65 ммоль) 4-нітро-1,2фенілендіаміну у 77 мл (0,979 моль) циклопропанкарбонової кислоти перемішують при температурі кипіння зі зворотним холодильником протягом 14 годин. Реакційну суміш потім концентрують при зниженому тиску, потім обробляють за допомогою 150 мл етилацетату і 100 мл розчину гідрокарбонату натрію. Органічну фазу промивають за допомогою 100 мл води, потім 50 мл насиченого розчину хлориду натрію, сушать над сульфатом магнію, потім концентрують при зниженому тиску. Одержують 6,5 г масла каштанового кольору, яке використовують таким, яке є, на наступній стадії. 12.2. 2-Циклопропіл-1-метил-5-нітро-1Нбензімідазол і 2-циклопропіл-1-метил-6-нітро- 1Нбензімідазол До перемішуваної в атмосфері аргону і при кімнатній температурі суспензії 2,6 г гідриду натрію (63,98 ммоль) у 150 мл тетрагідрофурану додають, по краплях, розчин 6,5 г (32 ммоль) 2циклопропіл-5-нітро-1Н-бензімідазолу, одержаного на попередній стадії, у 20 мл тетрагідрофурану. Реакційну суміш перемішують протягом 3 годин при температурі 20°С, потім додають 2,2 мл (35,2 ммоль) метилйодиду. Перемішування продовжують протягом додаткових 48 годин. Реакційну суміш потім концентрують при зниженому тиску, після чого прямо хроматографують при використанні колонки з діоксидом кремнію (елюент: дихлорметан-метанол). Одержують, таким чином, 4,5 г очікуваної суміші ізомерів у вигляді твердої речовини, яку використовують такою, яка є, на наступній стадії. 12.3. 2-Циклопропіл-1-метил-5-аміно-1Нбензімідазол (сполука № V2) і 2-циклопропіл-1метил-6-аміно-1Н-бензімідазол (сполука № V5) До перемішуваної при температурі 20°С суспензії 0,3 г 10%-ного паладію-на-вугіллі у 50 мл етанолу додають 15 г форміату амонію (0,236 моль). З цим першим реактором з'єднують другий, де при температурі 20°С інтенсивно перемішують 93687 32 суспензію 4,5 г (20,7 ммоль) суміші 2-циклопропіл1-метил-5-нітро-1H-бензімідазолу і 2-циклопропіл1-метил-6-нітро-1Н-бензімідазолу, одержаної на попередній стадії, і 0,4 г 10%-ного паладію-навугіллі у 130 мл етанолу. Після перемішування протягом 48 годин при температурі 20°С, 15 г (0,236 моль) форміату амонію, 0,3 г 10%-ного паладію-на-вугіллі і 50 мл етанолу додають до суміші, яку перемішують протягом додаткових 24 годин, після чого фільтрують через шар целіту і концентрують при зниженому тиску, одержуючи 4 г масла, яке очищають за допомогою ВЕРХ. Виділяють: - 1,1 г продукту V2, [МН]+=188; 1 Н-ЯМР (ДМСО-d6), (м. ч.): 1,05 (м, 4Н); 2,25 (м, 1Н); 3,81 (с, 3H); 6,61 (дхд, 1Н); 6,72 (с, 1Н); 7,26 (д, 1Н). - 0,92 г продукту V5, [МН]+=188; 1 Н-ЯМР (ДМСО-d6), (м. ч.): 1,02 (м, 4Н); 2,2 (м, 1Н); 3,71 (с, 3H); 6,5 (дхд, 1Н); 6,61 (с,1Н); 7,19 (д,1Н). 12.4. N-(2-Циклопроліл-1-метил-1Нбензімідазол-5-іл)-5-фтор-1-[(піридин-4-іл)метил]1Н-індол-2-карбоксамід (сполука № 91) 1,26 мл 2н розчину триметилалюмінію у толуолі додають, по краплях, до перемішуваного при температурі 0°С і в атмосфері аргону, розчину 0,376 г (2,01 ммоль) 2-циклопропіл-1-метил-5аміно-1Н-бензімідазолу (V2) у 70 мл толуолу. Суміш потім протягом 15 хвилин витримують при температурі 50°С, після чого охолоджують і декількома порціями додають 0,5 г (1,68 ммоль) етил5-фтор-1-[(піридин-4-іл)метил]-1Н-індол-2карбоксилату, одержаного на стадії 1.1. Суміш перемішують протягом 14 годин при кип'ятінні зі зворотним холодильником, потім охолоджують. Додають 15 мл води, потім 25 мл 1н розчину соляної кислоти. Значення рН одержаного розчину доводять до величини >8 шляхом додавання концентрованого розчину гідроксиду натрію. Відфільтровують тверду речовину, яку обробляють за допомогою 200 мл етилацетату і 100 мл води. Органічну фазу відділяють, сушать над сульфатом магнію, концентрують при зниженому тиску, потім хроматографують (елюенти: дихлорметан-метанол), одержуючи 0,3 г очікуваного продукту № 91. Температура плавлення=260-261°С 1 Н-ЯМР (ДМСО-d6), (м. ч.): 1 (м, 4Н); 2,19 (м, 1Н); 3,82 (с, 3H); 5,9 (с, 2Н); 7,02 (д, 2Н); 7,12 (тхд, 1Н); 7,47 (м, 5Н); 7,82 (д, 1Н); 8,42 (д, 2Н). У наведеній нижче таблиці 3 представлені хімічні структури і фізичні властивості деяких сполук загальної формули (І) відповідно до винаходу. У цій таблиці: - у колонці «Т.пл.» вказуються температури плавлення продуктів у градусах Цельсію (°С); - у колонці «сіль/основа» знак «-» означає сполуку у формі вільної основи, тоді як «HCl» означає сполуку у вигляді гідрохлориду і зазначене у дужках співвідношення означає співвідношення (кислота:основа); 33 - t-Bu означає трет-бутил і Me означає метил. 93687 34 35 93687 36 37 93687 38 39 Сполуки відповідно до винаходу піддавали фармакологічним випробуванням in vitro та in vivo, які виявили, що вони становлять інтерес як речовини з терапевтичними активностями. Сполуки відповідно до винаходу також мають характеристики розчинності у воді, що сприяє хорошій активності in vivo. Тест відносно інгібування струму, що індукується капсаїцином у DRG щура - Первинна культура гангліонарних клітин заднього корінця (DRG) щура: Нейрони DRG природно продукують рецептор TRPV1. Первинні культури DRG новонароджених щурів готували з щурят у віці 1 день. Коротко, після препарування, ганглії трипсинували і клітини механічно роздробляли шляхом обережного розтирання у порошок. Клітини ресуспендували у база 93687 40 льному культуральному середовищі Ігла, що містить 10% фетальної телячої сироватки, 25 мМ KСl, 2 мМ глутаміну, 100 мкг/мл гентаміцину і 50 нг/мл фактора росту нервової тканини, потім поміщали на тонкі скляні пластинки, покриті ламініном (0,25106 клітин на пластинку), які потім поміщали у 12-ямкові планшети Корнінга. Клітини інкубували при температурі 37°С у вологій атмосфері, що містить 5% СО2 і 95% повітря. Через 48 годин після культивування додавали цитозин--D-арабінозид (1 мкМ) для запобігання розвитку не нейронних клітин. Пластинки переносили в експериментальні камери для досліджень фіксації потенціалу після культивування протягом 7-10 діб. - Електрофізіологія: Вимірювальні камери (об'єм 800 мкл), що містять клітинний препарат, поміщали на предметний 41 93687 столик інвертованого мікроскопа (Olympus IMT2), обладнаний оптикою Hoffman (Modulation Contrast, Нью-Йорк), і проводили спостереження при 400кратному збільшенні. Камери безперервно перфузіювали під силою тяжіння (2,5 мл/хв.) за допомогою дозатора розчинів, що має 8 вхідних отворів, і єдиний вихід якого, утворений поліетиленовою трубкою (отвір 500 мкм), поміщали менш, ніж за 3 мм від досліджуваної клітини. Використовували конфігурацію «ціла клітина» за методом фіксації потенціалу. Піпетки з боросилікатного скла (опір 510 МОм) наближали до клітини завдяки п'єзоелектричному мікроманіпулятору 3D (Burleigh, PC 1000). Загальні струми (мембранний потенціал, фіксований при -60 мВ) реєстрували за допомогою підсилювача Axopatch ID (Axon Instruments, Foster city, Каліфорнія), з'єднаного з персональним комп'ютером (ПК), керованим програмним забезпеченням Pclamp8 (Axon Instrument). Сліди струму реєстрували на папері і одночасно переводили у цифрову форму (частота вибірки 15-25 Гц) і переносили на жорсткий диск ПК. Введення 300 нМ розчину капсаїцину викликає у клітинах DRG (фіксовану при -70 мВ напругу) вхідний катіонний струм. З метою мінімізації десенсибілізації рецепторів, додержувалися інтервалу мінімум одна хвилина між двома введеннями капсаїцину. Після контрольного періоду (стабілізація відповіді на один капсаїцин), сполуки, що тестуються, вводили індивідуально у заданій концентрації (концентрація 10 нМ або 0,1 нМ) протягом 4-5 хвилин, під час яких здійснювали декілька тестів капсаїцин-сполука (досягнення максимального інгібування). Результати виражали у % інгібування контрольної відповіді на капсаїцин. Відсотки інгібування відповіді на капсаїцин (300 нМ) становили від 20% до 100% для найбільш активних сполук відповідно до винаходу, що тестуються у концентрації від 10 нМ до 0,1 нМ (див. приклад таблиці 4). Сполуки відповідно до винаходу, отже, є ефективними антагоністами in vitro відносно рецепторів типу TRPV1. Таблиця 4 № сполуки 6 % інгібування у петч DRG 80% (3 нМ) Тест відносно рогівкового подразнення миші Подразнюючий характер капсаїцину легко помітний на рівні рогівки, тому що цей орган являє собою один з найбільш пронизаних волокнами С. У даному контексті, відповідно до попередніх експериментів, нанесення дуже незначної кількості капсаїцину (2 мкл при концентрації 160 мкМ) на поверхню рогівки тварини викликає деяку кількість стереотипних поведінок, пов'язаних з подразненням, і які легко реєструвати. З них слід назвати: моргання ока, тертя ока, здійснюване передньою гомолатеральною лапою, тертя морди двома передніми лапами, чесання морди задньою гомолатеральною лапою. Тривалість цих поведінок не перевищує 2 хвилини спостереження, і тварина тоді знову здобуває свою нормальну активність. Її 42 зовнішній вигляд, крім того, також нормальний. Миша не забивається у кут зі скуйовдженими волосками і не проявляє яких-небудь помітних симптомів страждання. Можна зробити висновок, що тривалість впливу капсаїцину у цих дозах менше 2 хвилин. Короткий виклад методології: Принципом серії експериментів є визначення, чи можуть сполуки відповідно до винаходу впливати на поведінкову відповідь, що викликається даною кількістю капсаїцину. Капсаїцин спочатку розводили до концентрації 25 мМ у ДМСО і, для його кінцевого використання, розводили у 10%-ному Твін 80 у фізіологічній сироватці. З контрольних досліджень випливає, що у цих умовах розчинник не здійснює ніякого ефекту. На практиці, продукт, що тестується, вводили перорально і у строк (час попередньої обробки: t), що залежить від фармакокінетичних даних, тварині закапують в око 2 мкл 160 мкМ розчину капсаїцину, приготованого як зазначено вище. Під час спостереження протягом 2 хвилин після закапування, зареєстроване деяке число тертя інстальованого ока гомолатеральною задньою лапою. У випадку даної тварини, відсоток захисту розраховували наступним чином: Р=100-((число спостережуваних чесань/середнє число чесань обробленої розчинником групи)100) Цей відсоток захисту усереднювали для кожної групи тварин (n=число тварин, які тестуються за допомогою сполуки відповідно до винаходу). Оцінені відсотки захисту, у випадку цієї моделі, для найбільш активних сполук відповідно до винаходу, використовуваних у дозі 1 мг/кг (перорально), становили від 20% до 100% (див. деякі приклади у таблиці 5): Таблиця 5 № сполуки 6 3 % P-(t) при 1 мг/кг (перорально) 24%-(1 година) 44%-(1 година) Результати цих випробувань показують, що найбільш активні сполуки відповідно до винаходу блокують ефекти, що індукуються стимуляцією рецепторів TRPV1. Отже, сполуки відповідно до винаходу можуть бути використані для одержання лікарських засобів, зокрема, для одержання лікарського засобу, призначеного для запобігання або лікування патологій, в яких беруть активну участь рецептори типу TRPV1. Таким чином, відповідно до іншого з його аспектів, об'єктом винаходу є лікарські засоби, які включають сполуку формули (І) або її фармацевтично прийнятну сіль, або гідрат або сольват вказаної вище сполуки. Ці лікарські засоби знаходять своє застосування у терапії, зокрема, у профілактиці і/або лікуванні болю і запалення; хронічного, невропатичного (травматичного, діабетичного, метаболічного, інфекційного, токсичного, індукованого протирако 43 93687 вим лікуванням або гіатрогенного), (остео)артритного, ревматичного болю; фіброміалгій, болю у спині, болю, пов'язаного з раковим захворюванням, невралгії лицьового нерва, головного болю, мігрені, зубного болю, опіку, сонячного удару, укусу або уколу, постгерпетичної невралгії, м'язового болю, нервової (центральної і/або периферичної) компресії, травм спинного мозку і/або головного мозку, ішемії (спинного мозку і/або головного мозку), нейродегенерації, геморагічних васкулярних порушень (спинного мозку і/або головного мозку), болю після інсульту. Сполуки відповідно до винаходу можуть бути використані для одержання лікарського засобу, призначеного для профілактики і/або лікування урологічних порушень, таких, як гіперактивність сечового міхура, нестабільність сечового міхура, нетримання, невідкладне сечовипускання, нетримання сечі, цистит, ниркова коліка, тазова гіперчутливість і тазовий біль. Сполуки відповідно до винаходу можуть бути використані для одержання лікарського засобу, призначеного для профілактики і/або лікування гінекологічних порушень, таких як вульводинія, болі, пов'язані з сальпінгітами, дисменореями. Ці продукти також можна використовувати для одержання лікарського засобу, призначеного для профілактики і/або лікування шлунково-кишкових порушень, таких, як порушення гастроезофагічного рефлексу, виразка шлунку, виразка дванадцятипалої кишки, функціональна диспепсія, коліт, IBS, хвороба Крона, панкреатит, езофагіт, печінкова коліка. Продукти відповідно до даного винаходу також можуть бути придатні для профілактики і/або лікування респіраторних порушень, таких, як астма, кашель, хронічне обструктивне захворювання легенів, бронхоконстрикція і запальні порушення. Ці продукти також можуть бути використані для профілактики і/або лікування псоріазу, свербежу, дермальних іритацій, іритацій очей або слизових оболонок, герпесу, оперізувального лишаю. Сполуки відповідно до винаходу також можуть бути використані для одержання лікарського засобу, призначеного для лікування депресії. Сполуки відповідно до винаходу також можуть бути використані для одержання лікарського засобу, призначеного для лікування діабету. Відповідно до іншого з його аспектів, даний винахід стосується фармацевтичних композицій, що включають, як діючий початок, сполуку відповідно до винаходу. Ці фармацевтичні композиції містять ефективну дозу щонайменше однієї сполуки відповідно до винаходу або фармацевтично прийнятної солі, гідрату або сольвату вказаної вище сполуки, а також щонайменше один фарма Комп’ютерна верстка О. Гапоненко 44 цевтично прийнятний ексципієнт. Вказані вище ексципієнти вибирають, в залежності від фармацевтичної форми і бажаного способу введення, зі звичайних ексципієнтів, які відомі фахівцеві у даній галузі. У фармацевтичних композиціях відповідно до даного винаходу для перорального, під'язикового, підшкірного, внутрішньом'язового, внутрішньовенного, місцевого, локального, інтратрахеального, інтраназального, трансдермального або ректального введення, діючий початок наведеної вище формули (І), або її можлива(ий) сіль, сольват або гідрат, можуть бути введені у стандартній лікарській формі, у суміші з класичними фармацевтичними ексципієнтами, тваринам і людям для профілактики або лікування порушень або захворювань, зазначених вище. Відповідні стандартні лікарські форми включають форми для перорального шляху введення, такі як таблетки, м'які і тверді желатинові капсули, порошки, гранули і пероральні розчини або суспензії, форми для під'язикового, букального, інтратрахеального, внутрішньоочного, інтраназального введення, шляхом інгаляції, форми для топічного, черезшкірного, підшкірного, внутрішньом'язового або внутрішньовенного введення, форми для ректального введення та імплантати. Для топічного нанесення сполуки відповідно до винаходу можна використовувати у кремах, гелях, мазях або лосьйонах. Як приклад, стандартна лікарська форма сполуки відповідно до винаходу у вигляді таблетки може включати наступні інгредієнти: сполука відповідно до винаходу 50,0 мг маніт 223,75 мг натрієва кроскармелоза 6,0 мг кукурудзяний крохмаль 15,0 мг гідроксипропілметилцелюлоза 2,25 мг стеарат магнію 3,0 мг. Вище вказані стандартні лікарські форми для можливості щоденного введення 0,001-30 мг діючого початку на кг маси тіла, в залежності від галенової форми. Можуть зустрічатися особливі випадки, де застосовні більш високі або більш незначні дози; такі дози не виходять за межі винаходу. Відповідно до звичайної практики, дозу, що відповідає кожному пацієнту, визначає лікар в залежності від способу введення, маси тіла і відповідної реакції вказаного вище пацієнта. Даний винахід, відповідно до іншого з його аспектів, також стосується способу лікування вказаних вище патологій, що включає введення пацієнту ефективної дози сполуки відповідно до винаходу або однієї(го) з її фармацевтично прийнятних солей або гідратів або сольватів. Підписне Тираж 23 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюN-(heteroaryl)-1-heteroarylalkyl-1h-indole-2-carboxamide derivatives, preparation and therapeutic use thereof
Автори англійськоюDubois Laurent, Evanno Yannick, Malanda, Andre
Назва патенту російськоюПроизводные n-(гетероарил)-гетероарилалкил-1н-индол-2-карбоксамидов, их получение и их применение b терапии
Автори російськоюДюбуа Лоран, Эванно Янник, Маланда Андрэ
МПК / Мітки
МПК: A61K 31/4709, C07D 417/14, A61K 31/427, A61K 31/444, C07D 403/14, C07D 401/14, A61K 31/4178, A61K 31/4439, A61P 17/00, C07D 413/14, A61K 31/5355, A61K 31/4184
Мітки: похідні, одержання, терапії, n-(гетероарил)-1-гетероарилалкіл-1н-індол-2-карбоксамідів, застосування
Код посилання
<a href="https://ua.patents.su/22-93687-pokhidni-n-geteroaril-1-geteroarilalkil-1n-indol-2-karboksamidiv-kh-oderzhannya-i-kh-zastosuvannya-u-terapi.html" target="_blank" rel="follow" title="База патентів України">Похідні n-(гетероарил)-1-гетероарилалкіл-1н-індол-2-карбоксамідів, їх одержання і їх застосування у терапії</a>
Попередній патент: Спосіб дегідратації і дегазифікації розчинів сирої нафти або емульсій з водою та пристрій для його здійснення (варіанти)
Наступний патент: Лита сталева стрічка (варіанти)
Випадковий патент: Застосування s-етил-4-амінобензентіосульфонату як біоциду для захисту нафтопродуктів, матеріалів та обладнання












