Композиція, яка містить епотилон (варіанти), і спосіб її одержання (варіанти)
Номер патенту: 88182
Опубліковано: 25.09.2009
Автори: Шпренгер Клаудіа, Томсен Йенс, Захсе Андреас, Реер Олаф, Уффрехт Анка, Ренц Маттіас
Формула / Реферат
1. Композиція, яка містить епотилон, циклодекстрин і принаймні один фармацевтично прийнятний наповнювач, вибраний із групи, яка включає маніт; сорбіт; ксиліт; 2-аміно-2-гідроксиметил-1,3-пропандіол; кислотну форму або солі лимонної кислоти, оцтової кислоти, гістидину, яблучної кислоти, фосфорної кислоти, винної кислоти, янтарної кислоти, MES, HEPES, імідазолу, молочної кислоти, глутарової кислоти й гліцилгліцину.
2. Композиція, яка містить похідне епотилону формули І і циклодекстрин, де формула І являє собою:
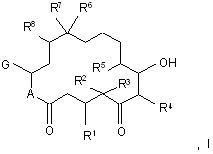
у якій:
R1 означає водень, OR1a або галоген, де R1a означає водень, SО2-алкіл, SO2-арил або SО2-аралкіл,
R2, R3 означають незалежно С1-С10-алкіл, R4 означає -(CH2)r-C≡C-(CH2)p-R4a, -(CH2)r-CH=CH-(CH2)p-R4a,
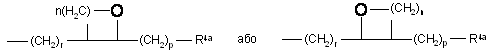 ,
,
n означає 0-5,
r означає 0-4,
p означає 0-3,
R4a означає водень, С1-С10-алкіл, С6-С12-арил або С7-С20-аралкіл; С1-С10-ацил, або, якщо р > 0, додатково групу OR4b,
R4b означає водень або захисну групу PG;
R5 означає С1-С10-алкіл,
R6 означає водень або необов'язково заміщений С1-С10-алкіл,
R7, R8 кожний означає атом водню або разом являють собою додатковий зв'язок, або разом являють собою атом кисню,
G означає групу X=CR9- або бі- або трициклічний арильний радикал,
R9 означає водень, галоген, CN або С1-С20-алкіл,
X означає угруповання CR10R11, причому
R10, R11 є однаковими або різними й означають водень, С1-С20-алкіл, С6-С12-арил або С7-С20-аралкільний радикал, кожний необов'язково заміщений;
або R10 і R11 утворюють разом з метиленовим вуглецем 5-7-членне карбоциклічне кільце;
А означає групу -О- або -NR12-,
R12 означає водень або С1-С10-алкіл.
3. Композиція за пунктом 1, у якій епотилон вибирають із епотилону А, епотилону В, епотилону С, епотилону D і його похідного.
4. Композиція за пунктом 3, у якій епотилон являє собою похідне епотилону В.
5. Композиція за пунктом 3, у якій епотилон являє собою похідне епотилону формули І, як визначено в пункті 2, і де R1, R2, R3, R4, n, r, p, R4a, R4b, R5, R6, R7, R8, G, R9, X, R10, R11, A, R12 мають значення, вказані в пункті 2.
6. Композиція за пунктом 1, у якій епотилон являє собою похідне епотилону, як визначено в пункті 2, у якому R4 означає -(CH2)r-C=C-(CH2)p-R4a, -(СН2)r-СН≡СН-(СН2)p-R4a.
7. Композиція за пунктом 1, у якій епотилон являє собою похідне епотилону, вибране із групи, яка включає:
(1S,3S(Е),7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(проп-2-iн-1-іл)-3-(1-метил-2-(2-метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(2-метилбензоксазол-5-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S(E),7S,10R,11R,12S,16R)-7,11-дигідрокси-10-(проп-2-ін-1-іл)-3-(1-фтор-2-(2-метилоксазол-4-іл)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16-(1-хлор-2-(2-метилтіазол-4-іл)етеніл)-1-окса-5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон;
(4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2-метилбензотіазол-5-іл)-1-окса-5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон;
(4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16-(1-метил-2-(2-піридил)етеніл)-1-окса-5,5,9,13-тетраметил-7-(бут-3-ин-1-іл)-циклогексадец-13-ен-2,6-діон;
(4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16-(1-метил-2-(2-піридил)етеніл)-1-окса-5,5,9,13-тетраметил-7-(бут-3-ен-1-іл)-циклогексадец-13-ен-2,6-діон;
(1S,3S(E),7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(проп-2-eн-1-іл)-3-(1-метил-2-(2-метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16-(1-метил-2-(2-піридил)етеніл)-1-окса-5,5,9,13-тетраметил-7-(проп-2-ін-1-іл)-циклогексадец-13-ен-2,6-діон;
(4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16-(1-фтор-2-(2-метилтіазол-4-іл)етеніл)-1-окса-5,5,9,13-тетраметил-7-(проп-2-ін-1-іл)-циклогексадец-13-ен-2,6-діон;
(1S,3S(E),7S,10R,11S,12S,16R)7,11-дигідрокси-10-(проп-2-ін-1-іл)-3-(1-фтор-2-(2-метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2-метилбензоксазол-5-іл)-1-окса-5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон;
(1R,3S,7S,10R,11S,12S,16S)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(4S,7R,8S,9S,13E/Z,16R)-4,8-дигідрокси-16-(2-метилбензотіазол-5-іл)-1-аза-5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон;
(1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(2-оксациклопропіл-1-метил)-3-(2-метилбензотіазол-5-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1R,3S(Е),7S,10R,11S,12S,16S)-7,11-дигідрокси-10-(бут-3-ин-1-іл)-3-(1-метил-2-(2-піридил)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16-(1-метил-2-(2-метилтіазол-4-іл)етеніл)-1-окса-5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон;
(1R,3S(Е),7S,10R,11S,12S,16S)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(1-метил-2-(2-метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16-(1-метил-2-(-(2-піридил)етеніл)-1-окса-5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон;
(4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16-(1-фтор-2-(2-метилоксазол-4-іл)етеніл)-1-окса-5,5,9,13-тетраметил-7-(проп-2-ін-1-іл)-циклогексадец-13-ен-2,6-діон;
(4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2-метилбензотіазол-5-іл)-1-окса-5,5,9,13-тетраметил-7-(3-метилбут-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон;
(1S,3R,7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(проп-2-eн-1-іл)-3-(2-метилбензотіазол-5-іл)-8,8,12,16-тетраметил-4-аза-17-оксабіцикло[14.1.0]гептадекан-5,9-діон;
(1R,3S,7S,10R,11S,12S,16S)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(хінолін-7-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1R,3S,7S,10R,11S,12S,16S)-7,11-дигідрокси-10-(проп-2-ін-1-іл)-3-(2-метилбензотіазол-5-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S(E),7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(бут-3-ин-1-іл)-3-(1-метил-2-(2-піридил)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1R,3S(E),7S,10R,11S,12S,16S)-7,11-дигідрокси-10-(бут-3-ин-1-іл)-3-(1-метил-2-(2-піридил)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S(E),7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(бут-3-ен-1-іл)-3-(1-метил-2-(2-піридил)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1R,3S(E),7S,10R,11S,12S,16S)-7,11-дигідрокси-10-(бут-3-ен-1-іл)-3-(1-метил-2-(2-піридил)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(4S,7S,8R,9S,13E/Z,16S(Е))-4,8-дигідрокси-16-(1-метил-2-(2-піридил)етеніл)-1-окса-5,5,9,13-тетраметил-7-(бут-3-ин-1-іл)-циклогексадец-13-ен-2,6-діон;
(1'S,4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-7-(проп-2-ен-1-іл)-16-(1'-метил-2'-(піридин-2-іл)етил)-5,5,9,13-тетраметил-1-оксагексадец-13-ен-2,6-діон;
(1'S,4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-7-(проп-2-ен-1-іл)-16-(1'-метил-2'-(піридин-2-іл)етил)-5,5,9,13-тетраметил-1-оксагексадец-13-ен-2,6-діон;
(1S/R,3S(Е),7S,10R,11S,12S,16R/S)-7,11-дигідрокси-10-(2-оксациклопропіл-1-метил)-3-(1-метил-2-(2-піридил)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S/R,3S(E),7S,10R,11S,12S,16R/S)-7,11-дигідрокси-10-(2-оксациклопропіл-1-метил)-3-(1-метил-2-(2-піридил)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S(Е),7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(2-оксациклопропіл-1-метил)-3-(1-метил-2-(2-піридил)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1R,3S(E),7S,10R,11S,12S,16S)-7,11-дигідрокси-10-(проп-2-ін-1-іл)-3-(1-фтор-2-(2-метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1R,3S(E),7S,10R,11S,12S,16S)-7,11-дигідрокси-10-(проп-2-ін-1-іл)-3-(1-фтор-2-(2-метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1R,3S,7S,10R,11S,12S,16S)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(2-метилбензоксазол-5-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1R,3S(Е),7S,10R,11S,12S,16S)-7,11-дигідрокси-10-(проп-2-ін-1-іл)-3-(1-фтор-2-(2-метилоксазол-4-іл)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2-метилбензотіазол-5-іл)-1-окса-5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон;
(1R,3S,7S,10R,11S,12S,16S)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2-метилбензотіазол-5-іл)-1-аза-5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон;
(4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2-метилбензотіазол-5-іл)-1-аза-5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон;
(4S,7R,8S,9S,13E/Z,16R)-4,8-дигідрокси-16-(2-метилбензотіазол-5-іл)-1-aзa-5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон;
(1R,3S,7S,10R,11S,12S,16S)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)-8,8,12,16-тетраметил-4-аза-17-оксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-3-(2-метилбензотіазол-5-іл)-10-(проп-2-ен-1-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(хінолін-7-іл)-1-окса-5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон;
(1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)-8,8,12,16-тетраметил-4-аза-17-оксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)-8,8,12,16-тетраметил-4-аза-17-оксабіцикло[14.1.0]гептадекан-5,9-діон;
(4S,7R,8S,9S,13E/Z,16R)-4,8-дигідрокси-16-(2-метилбензоксазол-5-іл)-1-аза-5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон;
(4S,7R,8S,9S,13E/Z,16R)-4,8-дигідрокси-16-(2-метилбензоксазол-5-іл)-1-аза)-5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон;
(4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2-метилбензоксазол-5-іл)-1-аза-5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон;
(1R,3R,7S,10R,11S,12S,16S)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(2-метилбензоксазол-5-іл)-8,8,12,16-тетраметил-4-аза-17-оксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3R,7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(2-метилбензоксазол-5-іл)-8,8,12,16-тетраметил-4-аза-17-оксабіцикло[14.1.0]гептадекан-5,9-діон;
(1R,3R,7S,10R,11S,12S,16S)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(2-метилбензоксазол-5-іл)-8,8,12,16-тетраметил-4-аза-17-оксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S(Е),7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(1-хлор-2-(2-метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1R,3S(Е),7S,10R,11S,12S,16S)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(1-хлор-2-(2-метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S(E),7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(2-оксациклопропіл-1-метил-3-(1-хлор-2-(2-метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1R,3S(E),7S,10R,11S,12S,16S)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(1-фтор-2-(2-метилтіазол-4-іл)етеніл)-16-гідроксиметил-8,8,12-триметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(2-оксациклопропіл-1-метил)-3-(2-метилбензотіазол-5-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-7-(проп-2-ен-1-іл)-16-(1-фтор-2-(2-метилтіазол-4-іл)етеніл)-13-гідроксиметил-5,5,9-триметил-1-оксагексадец-13-ен-2,6-діон;
(1S,3S(Е),7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(1-фтор-2-(2-метилтіазол-4-іл)етеніл)-16-гідроксиметил-8,8,12-триметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(4S,7S,8R,9S,13E/Z,16S)-4,8-дигідрокси-16-(2-метилбензотіазол-5-іл)-1-окса-5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон;
(1S,3S,7S,10S,11R,12S,16R)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1R,3S,7S,10S,11R,12S,16S)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(4R,7S,8R,9R,13E/Z,16R)-4,8-дигідрокси-16-(2-метилбензотіазол-5-іл)-1-окса-5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон;
(1R,3R,7R,10S,11R,12R,16S)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3R,7R,10S,11R,12R,16R)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S(E),7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(бут-3-ин-1-іл)-3-(1-метил-2-(2-піридил)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S(Е),7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(бут-3-ен-1-іл)-3-(1-метил-2-(2-піридил)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S(Е),7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(1-метил-2-(2-метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(2-метилбензоксазол-5-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S(E),7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(1-хлор-2-(2-метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(проп-2-eн-1-іл)-3-(2-метилбензотіазол-5-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(проп-2-eн-1-іл)-3-(xiнолін-7-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(проп-2-ен-1-іл)-3-(хінолін-7-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(1R,3S(E),7S,10R,11S,12S,16S)-7,11-дигідрокси-10-(проп-2-ін-1-іл)-3-(1-хлор-2-(2-метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон;
(4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2-метилбензотіазол-5-іл)-1-окса-5,5,9,13-тетраметил-7-(проп-2-ін-1-іл)-циклогексадец-13-ен-2,6-діон;
(1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(проп-2-ін-1-іл)-3-(2-метилбензотіазол-5-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон та/або
(4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(хінолін-7-іл)-1-окса-5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон.
8. Композиція за будь-яким з попередніх пунктів 1-7, у якій епотилон являє собою (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-3-(2-метилбензотіазол-5-іл)-10-(проп-2-ен-1-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон.
9. Композиція за будь-яким з попередніх пунктів 1-8, у якій циклодекстрин вибирають із групи, яка включає ![]() -циклодекстрин,
-циклодекстрин, ![]() -циклодекстрин,
-циклодекстрин, ![]() -циклодекстрин і їх похідні.
-циклодекстрин і їх похідні.
10. Композиція за пунктом 9, у якій циклодекстрин являє собою ![]() -циклодекстрин або його похідне.
-циклодекстрин або його похідне.
11. Композиція за пунктом 10, у якій циклодекстрин являє собою простий алкіловий ефір ![]() -циклодекстрину.
-циклодекстрину.
12. Композиція за пунктом 11, у якій циклодекстрин являє собою гідроксіалкілований ![]() -циклодекстрин.
-циклодекстрин.
13. Композиція за пунктом 12, у якій циклодекстрин являє собою 2-гідроксипропіл-![]() -циклодекстрин.
-циклодекстрин.
14. Композиція за будь-яким з пунктів 1-10, у якій циклодекстрин являє собою сульфоалкілований циклодекстрин.
15. Композиція за пунктом 14, у якій сульфоалкілований циклодекстрин являє собою простий сульфобутиловий ефір ![]() -циклодекстрину або простий сульфопропіловий ефір
-циклодекстрину або простий сульфопропіловий ефір ![]() -циклодекстрину.
-циклодекстрину.
16. Композиція за пунктом 2, яка додатково містить тонізуючий засіб, вибраний з маніту, сорбіту й ксиліту.
17. Композиція за будь-яким з пунктів 2-16, яка додатково містить регулятор рН, вибраний з 2-аміно-2-гідроксиметил-1,3-пропандіолу, кислотної форми або солей лимонної кислоти, оцтової кислоти, гістидину, яблучної кислоти, фосфорної кислоти, винної кислоти, янтарної кислоти, MES, HEPES, імідазолу, молочної кислоти, глутарової кислоти й гліцилгліцину.
18. Композиція за пунктом 17, у якій регулятор рН являє собою 2-аміно-2-гідроксиметил-1,3-пропандіол.
19. Композиція за будь-яким з попередніх пунктів 1-18, у якій композиція знаходиться у вигляді ліофілізату.
20. Композиція за будь-яким з пунктів 1-18, одержана після відновлення ліофілізату.
21. Композиція за пунктом 20, яка додатково містить розчинник, вибраний з водних розчинів, що містять 75-100 об. % води, переважно 85%-100 об. %, більш переважно 90-100 об. %, найбільш переважно 95-100 об. %.
22. Композиція, яка містить циклодекстрин і похідне епотилону формули І, як визначено в пункті 2, і в якій R1, R2, R3, R4, n, r, p, R4a, R4b, R5, R6, R7, R8, G, R9, X, R10, R11, A, R12 мають значення, вказані в пункті 2.
23. Композиція за пунктом 22, у якій циклодекстрин являє собою ![]() -циклодекстрин або його похідне.
-циклодекстрин або його похідне.
24. Композиція за пунктом 23, у якій ![]() -циклодекстрин являє собою простий алкіловий ефір
-циклодекстрин являє собою простий алкіловий ефір ![]() -циклодекстрину, переважно гідроксипропіл-
-циклодекстрину, переважно гідроксипропіл-![]() -циклодекстрин та/або простий сульфоалкіловий ефір циклодекстрину.
-циклодекстрин та/або простий сульфоалкіловий ефір циклодекстрину.
25. Композиція за пунктом 24, у якій сульфоалкілциклодекстрин являє собою простий сульфобутиловий ефір ![]() -циклодекстрину й епотилон являє собою (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-3-(2-метилбензотіазол-5-іл)-10-(проп-2-eн-1-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон.
-циклодекстрину й епотилон являє собою (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-3-(2-метилбензотіазол-5-іл)-10-(проп-2-eн-1-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон.
26. Композиція за пунктом 24, у якій гідроксіалкілциклодекстрин являє собою простий гідроксипропіловий ефір ![]() -циклодекстрину й епотилон являє собою (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-3-(2-метилбензотіазол-5-іл)-10-(проп-2-ен-1-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон.
-циклодекстрину й епотилон являє собою (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-3-(2-метилбензотіазол-5-іл)-10-(проп-2-ен-1-іл)-8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон.
27. Спосіб лікування злоякісного новоутворення в пацієнта, який включає введення вказаному пацієнтові терапевтично ефективної однієї або декількох сполук формули І за допомогою композицій згідно із даним винаходом, у якому вказані композиції вводять шляхом внутрішньовенної інфузії протягом періоду близько 30 хвилин у дозі в діапазоні від 10 мг/м2 до 35 мг/м2.
28. Спосіб за пунктом 27, у якому дозу вводять в діапазоні від 16 мг/м2 до 29 мг/м2.
29. Спосіб за пунктом 28, у якому доза становить 22 мг/м2.
30. Спосіб за будь-яким з пунктів 27-29, у якому композицію вводять пацієнтові кожні 3 тижні або щотижня протягом 3 тижнів з наступним семиденним періодом відновлення.
31. Спосіб за будь-яким з пунктів 27-29, у якому композицію вводять пацієнтові кожні 3 тижні.
32. Спосіб за будь-яким з пунктів 27-29, у якому композицію вводять пацієнтові щотижня протягом 3 тижнів з наступним семиденним періодом відновлення.
33. Фармацевтична композиція у вигляді розчину для парентерального введення, яка містить епотилон і воду.
34. Фармацевтична композиція за пунктом 33, яка додатково містить маніт.
35. Фармацевтична композиція за пунктом 33 і 34, яка додатково містить трометамол.
36. Спосіб одержання композиції, в якому здійснюють стадії
(а) розчинення епотилону, як визначено в пункті 2, в органічному розчиннику, такому як спирт, і
б) розчинення циклодекстрину, як визначено в даному винаході, у водному розчині, необов'язково разом із принаймні одним додатковим фармацевтично прийнятним компонентом, як визначено в даному винаході, таким як маніт і /або трометамол; необов'язково
в) доведення значення рН отриманої суміші на стадії б) до рН в інтервалі від 5 до 9, переважно від 6 до 8, таке як приблизно 7,4, за допомогою неорганічної кислоти, такої як соляна кислота; і
г) змішування отриманих розчинників а) і б) або а) і в); і необов'язково
д) здійснення стерильної фільтрації продукту зі стадії г) з одержанням так званого "вихідного розчину";
е) висушування розчину для видалення розчинника з одержанням твердої композиції.
37. Спосіб одержання композиції, в якому здійснюють стадії
а) розчинення епотилону, як визначено в пункті 2, в органічному розчиннику, такому як спирт, і
б) упарювання вказаного органічного розчинника; і
в) розчинення циклодекстрину, як визначено в даному винаході, у водному розчині, необов'язково разом із принаймні одним додатковим фармацевтично прийнятним компонентом, як визначено в даному винаході, таким як маніт і /або трометамол; необов'язково
г) доведення значення рН отриманої суміші на стадії б) до рН в інтервалі від 5 до 9, переважно від 6 до 8, таке як приблизно 7,4, за допомогою неорганічної кислоти, такої як соляна кислота; і
д) розчинення порошку, отриманого на стадії б), у розчинниках, отриманих на стадіях в) або г); і необов'язково
е) здійснення стерильної фільтрації продукту зі стадії д) з одержанням так званого "вихідного розчину";
є) видалення розчинника з "вихідного розчину" з одержанням твердої композиції.
38. Спосіб за пунктом 36 або 37, у якому органічний розчинник, використовуваний на стадії (а), являє собою спирт.
39. Спосіб за будь-яким з попередніх пунктів 36-38, у якому використовуваний епотилон знаходиться в аморфній формі.
40. Спосіб за пунктом 36 або 37, у якому спирт, використовуваний на стадії (а), являє собою етанол.
41. Фармацевтична композиція, отримана способом за пунктом 36.
42. Фармацевтична композиція, отримана способом за пунктом 37.
Текст
1. Композиція, яка містить епотилон, циклодекстрин і принаймні один фармацевтично прийнятний наповнювач, вибраний із групи, яка включає маніт; сорбіт; ксиліт; 2-аміно-2-гідроксиметил-1,3пропандіол; кислотну форму або солі лимонної кислоти, оцтової кислоти, гістидину, яблучної кислоти, фосфорної кислоти, винної кислоти, янтарної кислоти, MES, HEPES, імідазолу, молочної кислоти, глутарової кислоти й гліцилгліцину. 2. Композиція, яка містить похідне епотилону формули І і циклодекстрин, де формула І являє собою: 2 3 або R10 і R11 утворюють разом з метиленовим вуглецем 5-7-членне карбоциклічне кільце; А означає групу -О- або -NR12-, R12 означає водень або С1-С10-алкіл. 3. Композиція за пунктом 1, у якій епотилон вибирають із епотилону А, епотилону В, епотилону С, епотилону D і його похідного. 4. Композиція за пунктом 3, у якій епотилон являє собою похідне епотилону В. 5. Композиція за пунктом 3, у якій епотилон являє собою похідне епотилону формули І, як визначено в пункті 2, і де R1, R2, R3, R4, n, r, p, R4a, R4b, R5, R6, R7, R8, G, R9, X, R10, R11, A, R12 мають значення, вказані в пункті 2. 6. Композиція за пунктом 1, у якій епотилон являє собою похідне епотилону, як визначено в пункті 2, у якому R4 означає -(CH2)r-C=C-(CH2)p-R4a, -(СН2)rСН≡СН-(СН2)p-R4a. 7. Композиція за пунктом 1, у якій епотилон являє собою похідне епотилону, вибране із групи, яка включає: (1S,3S(Е),7S,10R,11S,12S,16R)-7,11-дигідрокси-10(проп-2-iн-1-іл)-3-(1-метил-2-(2-метилтіазол-4іл)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(2-метилбензоксазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S(E),7S,10R,11R,12S,16R)-7,11-дигідрокси-10(проп-2-ін-1-іл)-3-(1-фтор-2-(2-метилоксазол-4іл)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16-(1хлор-2-(2-метилтіазол-4-іл)етеніл)-1-окса-5,5,9,13тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13ен-2,6-діон; (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2метилбензотіазол-5-іл)-1-окса-5,5,9,13тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13ен-2,6-діон; (4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16-(1метил-2-(2-піридил)етеніл)-1-окса-5,5,9,13тетраметил-7-(бут-3-ин-1-іл)-циклогексадец-13-ен2,6-діон; (4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16-(1метил-2-(2-піридил)етеніл)-1-окса-5,5,9,13тетраметил-7-(бут-3-ен-1-іл)-циклогексадец-13-ен2,6-діон; (1S,3S(E),7S,10R,11S,12S,16R)-7,11-дигідрокси-10(проп-2-eн-1-іл)-3-(1-метил-2-(2-метилтіазол-4іл)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16-(1метил-2-(2-піридил)етеніл)-1-окса-5,5,9,13тетраметил-7-(проп-2-ін-1-іл)-циклогексадец-13-ен2,6-діон; (4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16-(1фтор-2-(2-метилтіазол-4-іл)етеніл)-1-окса-5,5,9,13тетраметил-7-(проп-2-ін-1-іл)-циклогексадец-13-ен2,6-діон; (1S,3S(E),7S,10R,11S,12S,16R)7,11-дигідрокси-10(проп-2-ін-1-іл)-3-(1-фтор-2-(2-метилтіазол-4іл)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; 88182 4 (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2метилбензоксазол-5-іл)-1-окса-5,5,9,13тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13ен-2,6-діон; (1R,3S,7S,10R,11S,12S,16S)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16R)-4,8-дигідрокси-16-(2метилбензотіазол-5-іл)-1-аза-5,5,9,13-тетраметил7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(2оксациклопропіл-1-метил)-3-(2-метилбензотіазол5-іл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S(Е),7S,10R,11S,12S,16S)-7,11-дигідрокси-10(бут-3-ин-1-іл)-3-(1-метил-2-(2-піридил)етеніл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16-(1метил-2-(2-метилтіазол-4-іл)етеніл)-1-окса5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)циклогексадец-13-ен-2,6-діон; (1R,3S(Е),7S,10R,11S,12S,16S)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(1-метил-2-(2-метилтіазол-4іл)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16-(1метил-2-(-(2-піридил)етеніл)-1-окса-5,5,9,13тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13ен-2,6-діон; (4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16-(1фтор-2-(2-метилоксазол-4-іл)етеніл)-1-окса5,5,9,13-тетраметил-7-(проп-2-ін-1-іл)циклогексадец-13-ен-2,6-діон; (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2метилбензотіазол-5-іл)-1-окса-5,5,9,13тетраметил-7-(3-метилбут-2-ен-1-іл)циклогексадец-13-ен-2,6-діон; (1S,3R,7S,10R,11S,12S,16R)-7,11-дигідрокси-10(проп-2-eн-1-іл)-3-(2-метилбензотіазол-5-іл)8,8,12,16-тетраметил-4-аза-17оксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S,7S,10R,11S,12S,16S)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(хінолін-7-іл)-8,8,12,16тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан5,9-діон; (1R,3S,7S,10R,11S,12S,16S)-7,11-дигідрокси-10(проп-2-ін-1-іл)-3-(2-метилбензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S(E),7S,10R,11S,12S,16R)-7,11-дигідрокси-10(бут-3-ин-1-іл)-3-(1-метил-2-(2-піридил)етеніл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S(E),7S,10R,11S,12S,16S)-7,11-дигідрокси-10(бут-3-ин-1-іл)-3-(1-метил-2-(2-піридил)етеніл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S(E),7S,10R,11S,12S,16R)-7,11-дигідрокси-10(бут-3-ен-1-іл)-3-(1-метил-2-(2-піридил)етеніл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S(E),7S,10R,11S,12S,16S)-7,11-дигідрокси-10(бут-3-ен-1-іл)-3-(1-метил-2-(2-піридил)етеніл) 5 8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7S,8R,9S,13E/Z,16S(Е))-4,8-дигідрокси-16-(1метил-2-(2-піридил)етеніл)-1-окса-5,5,9,13тетраметил-7-(бут-3-ин-1-іл)-циклогексадец-13-ен2,6-діон; (1'S,4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-7(проп-2-ен-1-іл)-16-(1'-метил-2'-(піридин-2-іл)етил)5,5,9,13-тетраметил-1-оксагексадец-13-ен-2,6-діон; (1'S,4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-7(проп-2-ен-1-іл)-16-(1'-метил-2'-(піридин-2-іл)етил)5,5,9,13-тетраметил-1-оксагексадец-13-ен-2,6-діон; (1S/R,3S(Е),7S,10R,11S,12S,16R/S)-7,11дигідрокси-10-(2-оксациклопропіл-1-метил)-3-(1метил-2-(2-піридил)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S/R,3S(E),7S,10R,11S,12S,16R/S)-7,11дигідрокси-10-(2-оксациклопропіл-1-метил)-3-(1метил-2-(2-піридил)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S(Е),7S,10R,11S,12S,16R)-7,11-дигідрокси-10(2-оксациклопропіл-1-метил)-3-(1-метил-2-(2піридил)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S(E),7S,10R,11S,12S,16S)-7,11-дигідрокси-10(проп-2-ін-1-іл)-3-(1-фтор-2-(2-метилтіазол-4іл)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S(E),7S,10R,11S,12S,16S)-7,11-дигідрокси-10(проп-2-ін-1-іл)-3-(1-фтор-2-(2-метилтіазол-4іл)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S,7S,10R,11S,12S,16S)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(2-метилбензоксазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S(Е),7S,10R,11S,12S,16S)-7,11-дигідрокси-10(проп-2-ін-1-іл)-3-(1-фтор-2-(2-метилоксазол-4іл)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2метилбензотіазол-5-іл)-1-окса-5,5,9,13тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13ен-2,6-діон; (1R,3S,7S,10R,11S,12S,16S)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2метилбензотіазол-5-іл)-1-аза-5,5,9,13-тетраметил7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон; (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2метилбензотіазол-5-іл)-1-аза-5,5,9,13-тетраметил7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон; (4S,7R,8S,9S,13E/Z,16R)-4,8-дигідрокси-16-(2метилбензотіазол-5-іл)-1-aзa-5,5,9,13-тетраметил7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон; (1R,3S,7S,10R,11S,12S,16S)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)8,8,12,16-тетраметил-4-аза-17оксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-3-(2метилбензотіазол-5-іл)-10-(проп-2-ен-1-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; 88182 6 (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16(хінолін-7-іл)-1-окса-5,5,9,13-тетраметил-7-(проп-2ен-1-іл)-циклогексадец-13-ен-2,6-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)8,8,12,16-тетраметил-4-аза-17оксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)8,8,12,16-тетраметил-4-аза-17оксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16R)-4,8-дигідрокси-16-(2метилбензоксазол-5-іл)-1-аза-5,5,9,13-тетраметил7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон; (4S,7R,8S,9S,13E/Z,16R)-4,8-дигідрокси-16-(2метилбензоксазол-5-іл)-1-аза)-5,5,9,13тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13ен-2,6-діон; (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2метилбензоксазол-5-іл)-1-аза-5,5,9,13-тетраметил7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон; (1R,3R,7S,10R,11S,12S,16S)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(2-метилбензоксазол-5-іл)8,8,12,16-тетраметил-4-аза-17оксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3R,7S,10R,11S,12S,16R)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(2-метилбензоксазол-5-іл)8,8,12,16-тетраметил-4-аза-17оксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3R,7S,10R,11S,12S,16S)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(2-метилбензоксазол-5-іл)8,8,12,16-тетраметил-4-аза-17оксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S(Е),7S,10R,11S,12S,16R)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(1-хлор-2-(2-метилтіазол-4іл)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S(Е),7S,10R,11S,12S,16S)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(1-хлор-2-(2-метилтіазол-4іл)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S(E),7S,10R,11S,12S,16R)-7,11-дигідрокси-10(2-оксациклопропіл-1-метил-3-(1-хлор-2-(2метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S(E),7S,10R,11S,12S,16S)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(1-фтор-2-(2-метилтіазол-4іл)етеніл)-16-гідроксиметил-8,8,12-триметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10-(2оксациклопропіл-1-метил)-3-(2-метилбензотіазол5-іл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-7-(проп2-ен-1-іл)-16-(1-фтор-2-(2-метилтіазол-4-іл)етеніл)13-гідроксиметил-5,5,9-триметил-1-оксагексадец13-ен-2,6-діон; (1S,3S(Е),7S,10R,11S,12S,16R)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(1-фтор-2-(2-метилтіазол-4іл)етеніл)-16-гідроксиметил-8,8,12-триметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7S,8R,9S,13E/Z,16S)-4,8-дигідрокси-16-(2метилбензотіазол-5-іл)-1-окса-5,5,9,13тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13ен-2,6-діон; 7 (1S,3S,7S,10S,11R,12S,16R)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S,7S,10S,11R,12S,16S)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4R,7S,8R,9R,13E/Z,16R)-4,8-дигідрокси-16-(2метилбензотіазол-5-іл)-1-окса-5,5,9,13тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13ен-2,6-діон; (1R,3R,7R,10S,11R,12R,16S)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3R,7R,10S,11R,12R,16R)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S(E),7S,10R,11S,12S,16R)-7,11-дигідрокси-10(бут-3-ин-1-іл)-3-(1-метил-2-(2-піридил)етеніл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S(Е),7S,10R,11S,12S,16R)-7,11-дигідрокси-10(бут-3-ен-1-іл)-3-(1-метил-2-(2-піридил)етеніл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S(Е),7S,10R,11S,12S,16R)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(1-метил-2-(2-метилтіазол-4іл)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(2-метилбензоксазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S(E),7S,10R,11S,12S,16R)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(1-хлор-2-(2-метилтіазол-4іл)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10(проп-2-eн-1-іл)-3-(2-метилбензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(2-метилбензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10(проп-2-eн-1-іл)-3-(xiнолін-7-іл)-8,8,12,16тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан5,9-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10(проп-2-ен-1-іл)-3-(хінолін-7-іл)-8,8,12,16тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан5,9-діон; (1R,3S(E),7S,10R,11S,12S,16S)-7,11-дигідрокси-10(проп-2-ін-1-іл)-3-(1-хлор-2-(2-метилтіазол-4іл)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2метилбензотіазол-5-іл)-1-окса-5,5,9,13тетраметил-7-(проп-2-ін-1-іл)-циклогексадец-13-ен2,6-діон; 88182 8 (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-10(проп-2-ін-1-іл)-3-(2-метилбензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон та/або (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16(хінолін-7-іл)-1-окса-5,5,9,13-тетраметил-7-(проп-2ен-1-іл)-циклогексадец-13-ен-2,6-діон. 8. Композиція за будь-яким з попередніх пунктів 17, у якій епотилон являє собою (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-3-(2метилбензотіазол-5-іл)-10-(проп-2-ен-1-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон. 9. Композиція за будь-яким з попередніх пунктів 18, у якій циклодекстрин вибирають із групи, яка включає a -циклодекстрин, b -циклодекстрин, g циклодекстрин і їх похідні. 10. Композиція за пунктом 9, у якій циклодекстрин являє собою b -циклодекстрин або його похідне. 11. Композиція за пунктом 10, у якій циклодекстрин являє собою простий алкіловий ефір b циклодекстрину. 12. Композиція за пунктом 11, у якій циклодекстрин являє собою гідроксіалкілований bциклодекстрин. 13. Композиція за пунктом 12, у якій циклодекстрин являє собою 2-гідроксипропіл- b -циклодекстрин. 14. Композиція за будь-яким з пунктів 1-10, у якій циклодекстрин являє собою сульфоалкілований циклодекстрин. 15. Композиція за пунктом 14, у якій сульфоалкілований циклодекстрин являє собою простий сульфобутиловий ефір b -циклодекстрину або простий сульфопропіловий ефір b -циклодекстрину. 16. Композиція за пунктом 2, яка додатково містить тонізуючий засіб, вибраний з маніту, сорбіту й ксиліту. 17. Композиція за будь-яким з пунктів 2-16, яка додатково містить регулятор рН, вибраний з 2аміно-2-гідроксиметил-1,3-пропандіолу, кислотної форми або солей лимонної кислоти, оцтової кислоти, гістидину, яблучної кислоти, фосфорної кислоти, винної кислоти, янтарної кислоти, MES, HEPES, імідазолу, молочної кислоти, глутарової кислоти й гліцилгліцину. 18. Композиція за пунктом 17, у якій регулятор рН являє собою 2-аміно-2-гідроксиметил-1,3пропандіол. 19. Композиція за будь-яким з попередніх пунктів 1-18, у якій композиція знаходиться у вигляді ліофілізату. 20. Композиція за будь-яким з пунктів 1-18, одержана після відновлення ліофілізату. 21. Композиція за пунктом 20, яка додатково містить розчинник, вибраний з водних розчинів, що містять 75-100 об. % води, переважно 85%-100 об. %, більш переважно 90-100 об. %, найбільш переважно 95-100 об. %. 22. Композиція, яка містить циклодекстрин і похідне епотилону формули І, як визначено в пункті 2, і в якій R1, R2, R3, R4, n, r, p, R4a, R4b, R5, R6, R7, R8, G, R9, X, R10, R11, A, R12 мають значення, вказані в пункті 2. 9 88182 10 23. Композиція за пунктом 22, у якій циклодекстрин являє собою b -циклодекстрин або його похідне. 24. Композиція за пунктом 23, у якій b циклодекстрин являє собою простий алкіловий ефір b -циклодекстрину, переважно гідроксипропіл- b -циклодекстрин та/або простий сульфоалкіловий ефір циклодекстрину. 25. Композиція за пунктом 24, у якій сульфоалкілциклодекстрин являє собою простий сульфобутиловий ефір b -циклодекстрину й епотилон являє собою (1S,3S,7S,10R,11S,12S,16R)-7,11дигідрокси-3-(2-метилбензотіазол-5-іл)-10-(проп-2eн-1-іл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон. 26. Композиція за пунктом 24, у якій гідроксіалкілциклодекстрин являє собою простий гідроксипропіловий ефір b -циклодекстрину й епотилон являє собою (1S,3S,7S,10R,11S,12S,16R)-7,11дигідрокси-3-(2-метилбензотіазол-5-іл)-10-(проп-2ен-1-іл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон. 27. Спосіб лікування злоякісного новоутворення в пацієнта, який включає введення вказаному пацієнтові терапевтично ефективної однієї або декількох сполук формули І за допомогою композицій згідно із даним винаходом, у якому вказані композиції вводять шляхом внутрішньовенної інфузії протягом періоду близько 30 хвилин у дозі в діапазоні від 10 мг/м2 до 35 мг/м2. 28. Спосіб за пунктом 27, у якому дозу вводять в діапазоні від 16 мг/м2 до 29 мг/м2. 29. Спосіб за пунктом 28, у якому доза становить 22 мг/м2. 30. Спосіб за будь-яким з пунктів 27-29, у якому композицію вводять пацієнтові кожні 3 тижні або щотижня протягом 3 тижнів з наступним семиденним періодом відновлення. 31. Спосіб за будь-яким з пунктів 27-29, у якому композицію вводять пацієнтові кожні 3 тижні. 32. Спосіб за будь-яким з пунктів 27-29, у якому композицію вводять пацієнтові щотижня протягом 3 тижнів з наступним семиденним періодом відновлення. 33. Фармацевтична композиція у вигляді розчину для парентерального введення, яка містить епотилон і воду. 34. Фармацевтична композиція за пунктом 33, яка додатково містить маніт. 35. Фармацевтична композиція за пунктом 33 і 34, яка додатково містить трометамол. 36. Спосіб одержання композиції, в якому здійснюють стадії (а) розчинення епотилону, як визначено в пункті 2, в органічному розчиннику, такому як спирт, і б) розчинення циклодекстрину, як визначено в даному винаході, у водному розчині, необов'язково разом із принаймні одним додатковим фармацевтично прийнятним компонентом, як визначено в даному винаході, таким як маніт і /або трометамол; необов'язково в) доведення значення рН отриманої суміші на стадії б) до рН в інтервалі від 5 до 9, переважно від 6 до 8, таке як приблизно 7,4, за допомогою неорганічної кислоти, такої як соляна кислота; і г) змішування отриманих розчинників а) і б) або а) і в); і необов'язково д) здійснення стерильної фільтрації продукту зі стадії г) з одержанням так званого "вихідного розчину"; е) висушування розчину для видалення розчинника з одержанням твердої композиції. 37. Спосіб одержання композиції, в якому здійснюють стадії а) розчинення епотилону, як визначено в пункті 2, в органічному розчиннику, такому як спирт, і б) упарювання вказаного органічного розчинника; і в) розчинення циклодекстрину, як визначено в даному винаході, у водному розчині, необов'язково разом із принаймні одним додатковим фармацевтично прийнятним компонентом, як визначено в даному винаході, таким як маніт і /або трометамол; необов'язково г) доведення значення рН отриманої суміші на стадії б) до рН в інтервалі від 5 до 9, переважно від 6 до 8, таке як приблизно 7,4, за допомогою неорганічної кислоти, такої як соляна кислота; і д) розчинення порошку, отриманого на стадії б), у розчинниках, отриманих на стадіях в) або г); і необов'язково е) здійснення стерильної фільтрації продукту зі стадії д) з одержанням так званого "вихідного розчину"; є) видалення розчинника з "вихідного розчину" з одержанням твердої композиції. 38. Спосіб за пунктом 36 або 37, у якому органічний розчинник, використовуваний на стадії (а), являє собою спирт. 39. Спосіб за будь-яким з попередніх пунктів 36-38, у якому використовуваний епотилон знаходиться в аморфній формі. 40. Спосіб за пунктом 36 або 37, у якому спирт, використовуваний на стадії (а), являє собою етанол. 41. Фармацевтична композиція, отримана способом за пунктом 36. 42. Фармацевтична композиція, отримана способом за пунктом 37. Даний винахід стосується способів одержання лікарських препаратів епотилонів і композицій, придатних для парентерального введення, такого як внутрішньовенне введення. Епотилони належать до класу речовин, які зустрічаються в природі, із цитотоксичною дією, які слід вводити парентерально. На жаль, речовини, які зустрічаються в природі, не є достатньо стабільними, хімічно або метаболічно, для надання 11 можливості використання у вигляді лікарських засобів. Лактонова структура в епотилоновому скелеті спричиняється чутливість молекули до розкладання, особливо при підвищених значеннях рН, таких як значення рН, вище нейтрального. Крім того, епотилони є високо ліпофільними речовинами й практично нерозчинні у воді, тому внутрішньовенне введення сполук цього класу надзвичайно утруднено. Для парентерального введення лікарських препаратів необхідно, щоб епотилони були повністю розчинені в розчиннику, сумісному з фізіологічними рідинами, такими як кров. Деякі успіхи були досягнуті в одержанні нових похідних епотилонів, які мають як хімічну, так і метаболічну стабільністю, достатню для розвитку лікарських засобів. Крім того, похідні епотилонів повинні перевищувати властивості природних похідних щодо їх терапевтичного інтервалу, селективності їх дії та/або небажаних побічних токсичних дій та/або їх терапевтичної ефективності. В WO 00/66589 описані такі поліпшені епотилони, у яких шостий атом вуглецю епотилону, наведеного на сторінці 1 заявки WO 00/66589, має алкенільний, алкінільний або епокси радикал. Однак, такі додаткові бокові ланцюги роблять такі епотилони навіть ще більш ліпофільними й такими, що погано змочуються в розчинниках, що робить їх приготування у вигляді лікарських засобів ще більш складним для фахівця в даній галузі техніки. Були описані деякі способи підвищення розчинності важко розчинних у воді лікарських засобів для одержання лікарських препаратів, придатних для парентерального введення. В US 6,407,079 (Janssen Pharma) описані ін'єковані лікарські препарати, у яких до лікарського засобу, який нестабільний або тільки важкорозчинний у воді, додають частково етерифікований β-циклодекстрин (гідроксіетиловий, гідроксипропіловий, дигідроксипропіловий, метиловий або етиловий прості ефіри). Отримана інкпюзована сполука є краще розчинною у воді, ніж сам лікарський засіб. Прості сульфоалкілові ефіри циклодекстринів і їх похідні для застосування як солюбілізуючі засоби для нерозчинних у воді лікарських засобів раніше були описані в US 5,376,645 і US 5,134,127. В WO 99/396945 описані препарати епотилонів типу А і В, приготовлені у вигляді інфузійного концентрату або у вигляді ліофілізованої композиції. Перед введенням епотилон слід розчинити в кращих розчинниках, таких як суміші ПЕГ/вода, пропіленгліколь/вода або етанол/вода. Розчинність епотилону істотно підвищується при застосувань таких сумішей розчинників. Як наповнювач додають β-циклодекстрин або маніт. В WO 2004/032866 описані ліофілізовані композиції, які містять епотилони, переважно епотилон D разом з β-циклодекстринами, включаючи прості сульфоалкілові ефіри циклодекстринів. Одержання епотилонів ι їх похідних здійснюють відповідно до способів, які відомі фахівцеві в даній галузі, оскільки вони описані, наприклад, в DE 19907588, WO 98/25929, WO 99/58534, WO 99/2514, WO 99/67252, WO 99/67253, WO 99/7692, ЕР 99/4915, WO 00/1333, WO 00/66589, WO 00/49019, WO 00/49020, WO 00/49021, WO 88182 12 00/71521, WO 00/37473, WO 00/57874, WO 01/92255, WO 01/81342, WO 01/73103, WO 01/64650, WO 01/70716, US 6204388, US 6387927, US 6380394, US 02/52028, US 02/58286, US 02/62030, WO 02/32844, WO 02/30356, WO 02/32844, WO 02/14323 ι WO 02/8440. Епотилони, які представляють особливий інтерес згідно із даним винаходом, можуть бути отримані згідно із WO 00/66589. Задачею даного винаходу є забезпечення композиції, яка містить похідне епотилону і яка призначена для парентерального введення, переважно внутрішньовенного введення. Композиція повинна бути стабільною, принаймні стосовно епотилону, при зберіганні й відновленні, якщо це є необхідним, шляхом додавання розчинника, сумісного із кров'ю й придатного для парентерального введення без необхідності додавання поверхневоактивних речовин і органічних розчинників. Даний винахід стосується дозованих форм для парентерального введення, які містять епотилони, і їх приготування, при якому кінцева дозована форма або спосіб приготування відповідає наступним характеристикам: - Швидке розчинення епотилону в рідині, яка може бути вилучена в умовах ліофілізації, в такий спосіб вдається зменшити втрату інтактного епотилону при процесі розчинення. - Ліофілізація рідкої композиції епотилону без втрати інтактного епотилону - Ліофілізат є досить важким. - Повне й швидке розчинення ліофілізованого осаду у фізіологічно прийнятному розчиннику з утворенням при цьому відновленій композиції, яка легко може бути введена або додатково розведена підходящим фізіологічно прийнятним розчинником. - Хімічно стабільні ліофілізовані композиції, принаймні щодо стабільності епотилону. - Фізично стабільні ліофілізовані композиції. - Хімічно стабільний відновлений розчин, принаймні щодо стабільності епотилону. - Фізично стабільний відновлений розчин. - Висока концентрація епотилону в ліофілізованому осаді та/або відновленому розчині. - Висока максимальна переносима доза наступного парентерального введення. Згідно із даним винаходом, забезпечуються ліофілізовані композиції, а також їх відновлені композиції, які як загальну ознаку містять епотилон або його похідне або їх суміші в комбінації із циклодекстрином. На відміну від раніше описаних композицій епотилонів, які вводили парентерально, композиції згідно із даним винаходом забезпечують композиції, які одержують при відновленні ліофілізату в простих розчинниках, таких як вода або мінералізована вода й необов'язково додатково розведені розчином глюкози або декстрози. Для забезпечення достатнього розчинення епотилону не потрібне додавання органічного розчинника й гліколю. Як описано в WO 2004/032866, для відновлення ліофілізату потрібні суміші води, етанолу й гліколю. У ліофілізатах згідно із WO 99/39694 також необхідним є органічний розчинник. Очевидно, що ліофі 13 лізати згідно із даним винаходом мають переваги в порівнянні з раніше описаними, оскільки для приготування кінцевої відновленої композиції необхідна тільки вода для ін'єкцій або сольовий розчин. В одному варіанті здійснення, винахід стосується композицій, які містять епотилон або суміші епотилонів, у яких епотилон має більш ліпофільний боковий ланцюг у порівнянні з епотилонами, які зустрічаються в природі. Відповідно до формули І, наведеної в даному винаході, ліпофільний боковий ланцюг стосується R4 і розташований біля атома вуглецю під номером 10 таким чином, що епотилон конденсований з епокси кільцем, або розташований біля атома вуглецю під номером 7 таким чином, що R7 і R8 являють собою атом водню або разом являють собою додатковий зв'язок. В WO 00/66589 цей атом вуглецю позначений номером 6. Композиції за винаходом додатково містять циклодекстрин, переважно похідне βциклодекстрину, яке етерифіковано гідроксіалкільними групами та/або сульфоалкільними групами, що приводить до одержання гідроксіалкілованих циклодекстринів або сульфоалкілованих циклодекстринів. Було виявлено, що загальний принцип приготування лікарських препаратів епотилонів, придатних для парентерального введення, забезпечується підходящим вибором наповнювачів, які забезпечують необхідну тонічність, рН, стабілізацію композиції, яка містить циклодекстрин і епотилон, хімічну й фізичну стабільність при ліофілізації, хімічну й фізичну стабільність ліофілізованої композиції. Цей принцип надзвичайно придатний для епотилонів з дуже поганими змочуваними властивостями та/або низькою розчинністю у воді, такі як кращі похідні, які охоплюються формулою І, наведеною в даній заявці. Типовими прикладами додаткових наповнювачів є тонізуючий засіб, наповнювач, кріозахисна речовина, ліозахисна речовина й речовина, яка регулює рН. У кращих варіантах здійснення винаходу, додатковий фармацевтично прийнятний наповнювач вибирають із маніту; сорбіту; ксиліту; 2-аміно-2гідроксиметил-1,3-пропандіолу; кислотної форми або солей лимонної кислоти, оцтової кислоти, гістидину, яблучної кислоти, фосфорної кислоти, винної кислоти, янтарної кислоти, MES, HEPES, імідазолу, молочної кислоти, глутарової кислоти та/або гліцилгліцину, переважно маніту та/або трометамолу (TRIS). Винахідники також виявили, що особливо придатними циклодекстринами є простий сульфоалкіловий ефір циклодекстринів, який забезпечує одержання композицій, які мають бажану тонічність без необхідності додавання додаткових наповнювачів або засобів, які модифікують тонічність. Таким чином, в іншому варіанті здійснення, винаходу стосується композицій, які містять епотилон і сульфоалкілований циклодекстрин (наприклад, сульфопропілований і сульфобутилований циклодекстрин). В подальшому варіанті здійснення, винахід стосується композиції, яка містить епотилон відповідно до формули І, описаної в даному винаході, і β-циклодекстрин. Циклодекстрин являє собою пе 88182 14 реважно гідроксіалкілований β-циклодекстрин або сульфоалкілований β-циклодекстрин, як описано вище. В іншому кращому варіанті здійснення, винахід стосується композиції, яка містить епотилон відповідно до формули І, описаної в даному винаході, і сульфоалкілований β-циклодекстрин, переважно простий сульфобутиловий ефір β-циклодекстрину. У кращому варіанті здійснення, винахід стосується композиції, яка містить епотилон відповідно до формули І, описаної в даному винаході, і гідроксилирований, найбільш переважно частково етерифікований гідроксипропіл-β-циклодекстрин. Крім того, винахідники забезпечили спосіб одержання ліофілізованої композиції за винаходом, яка долає початкову критичну стадію розчинення дуже гідрофобних епотилонів, а саме початкове змочування епотилону в підходящій рідині перед наступним здійсненням процесу солюбілізації. Цей спосіб надає можливість швидкого й повного розчинення епотилону й надалі забезпечує підтримку стабільності епотилону в розчині, протягом достатнього періоду часу, перед видаленням розчинника. Наприклад, спосіб розчинення епотилону здійснюється набагато швидше, ніж спосіб, описаний в WO 99/39694, приклад 10. Фактично, для епотилонів, розкритих у даному винаході, не є можливим використовувати спосіб, описаний у прикладі 10 заявки WO 99/39694. Для переведення в розчин епотилонів, розкритих у даному винаході, можуть знадобитися дні, протягом цього періоду часу може відбутися гідроліз. Отже, це приведе до значної втрати епотилону й описаний процес не є підходящим для здійснення в промисловому масштабі. Отже, у ще іншому варіанті здійснення, винахід стосується приготування твердої композиції, такої як ліофілізат, яка може бути отримана з розчинів (надалі в даному винаході називаються "вихідними розчинами"), що містять епотилон, як описано в даному винаході, циклодекстрин, як описано в даному винаході, і необов'язково принаймні один додатковий фармацевтично прийнятний наповнювач, як визначено в даному винаході. Специфічною характеристикою способу є забезпечення можливості розчинення епотилону в розчиннику, який підходить для процесу ліофілізації, протягом більш короткого проміжку часу, ніж відомий з рівня техніки, що є коротким, але достатнім для забезпечення підтримання стабільності епотилону й відсутності розкладання. Розглянутий проміжок часу становить від 0,5 до 5 годин, переважно від 0,5 до 3 годин, більш переважно від 1 до 2,5 годин. В одному варіанті здійснення, метод одержання композиції за винаходом (спосіб) передбачає стадії: а) розчинення епотилону - незалежно від того, чи є він кристалічним або аморфним - як визначено в даному винаході, в органічному розчиннику, такому як спирт, (переважно етанол); і б) розчинення циклодекстрину, як визначено в даному винаході, у водному розчині, необов'язково разом із принаймні одним додатковим фармацев 15 тично прийнятним компонентом, як визначено в даному винаході, таким як маніт і /або трометамол; необов'язково в) доведення значення рН отриманої суміші на стадії б) до рН в інтервалі від 5 до 9, переважно від 6 до 8, таке як приблизно 7,4, за допомогою неорганічної кислоти, такої як соляна кислота; і г) змішування розчинів, отриманих на стадіях а) і б) або а) і в); і необов'язково д) здійснення стерильної фільтрації продукту зі стадії г) для одержання так званого "вихідного розчину" е) видалення розчинників з "вихідного розчину" з одержанням твердої композиції. В одному варіанті здійснення, метод одержання композиції за винаходом (спосіб) передбачає стадії а) розчинення епотилону - незалежно від того, чи є він кристалічним або аморфним - як визначено в даному винаході, в органічному розчиннику, такому як спирт, (переважно етанол); і б) упарювання вказаного органічного розчинника; і в) розчинення циклодекстрину, як визначено в даному винаході, у водному розчині, необов'язково разом із принаймні одним додатковим фармацевтично прийнятним компонентом, як визначено в даному винаході, таким як маніт і /або трометамол; необов'язково г) доведення значення рН отриманої суміші на стадії б) до рН в інтервалі від 5 до 9, переважно від 6 до 8, таке як приблизно 7,4, за допомогою неорганічної кислоти, такої як соляна кислота; і д) розчинення порошку, отриманого на стадії б), у розчині, отриманому на стадії в) або г); і необов'язково е) здійснення стерильної фільтрації продукту зі стадії д) для одержання так званого "вихідного розчину" є) видалення розчинника з "вихідного розчину" з одержанням твердої композиції. Органічні розчинники, придатні для стадії а), якщо друга стадія б) являє собою упарювання розчинника, можуть бути вибрані з полярних апротонних або протонних розчинників, наприклад, можуть бути вибрані з галогенованих вуглеводнів, таких як монохлорметан, дихлорметан; спиртів, таких як метанол, етанол, пропанол; ацетон. Кращими розчинниками є метиленхлорид і етанол. Видалення розчинника в контексті даного винаходу охоплює всі методики для видалення розчинника або розчинників, які відомі фахівцеві в даній галузі техніки, такі як, але не обмежуючись тільки ними, сушіння виморожуванням, ліофілізація, вакуумне сушіння або упарювання. У кращому варіанті здійснення, винахід стосується методів одержання композиції, яка містить епотилон (способів), описаних вище, у яких епотилон використовують в аморфній формі, і композицій, одержуваних цими способами. Аморфний являє собою тверду фазу без кристалічної ґратки. Це може бути підтверджене за допомогою порошкової дифракції рентгенівських променів. 88182 16 Епотилон може бути отриманий в аморфній формі, наприклад, шляхом розчинення кристалічного епотилону в органічному розчиннику й наступному видаленні його розчинника. У кращому варіанті здійснення, винахід стосується методів одержання композиції, яка містить епотилон (способів), описаних вище, у яких епотилон використовують в аморфній формі або його переводять в аморфну форму й циклодекстрин являє собою гідроксипропіл-β-циклодекстрин, і композицій, одержуваних цими способами. У кращому варіанті здійснення, винахід стосується методів одержання композиції, яка містить епотилон (способів), описаних вище, у яких епотилон використовують в аморфній формі або його переводять в аморфну форму й циклодекстрин являє собою простий сульфобутиловий ефір βциклодекстрину, ι композицій, одержуваних цими способами. У кращому варіанті здійснення, винахід стосується методів одержання композиції, яка містить епотилон (способів), описаних вище, у яких використовуваний епотилон являє собою похідне епотилону (1S,3S,7S,10R,11S,12S,16R)-7,11дигідрокси-3-(2-метил-бензотіазол-5-іл)-10-(проп2-ен-1-іл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон, додатково, епотилон знаходиться в аморфній формі або його переводять в аморфну форму, і циклодекстрин являє собою гідроксипропіл-β-циклодекстрин і композицій, одержуваних цими способами. У кращому варіанті здійснення, винахід стосується методів одержання композиції, яка містить епотилон (способів), описаних вище, у яких використовуваний епотилон являє собою похідне епотилону (1S,3S,7S,10R,11S,12S,16R)-7,11дигідрокси-3-(2-метил-бензотіазол-5-іл)-10-(проп2-ен-1-іл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон, додатково, епотилон знаходиться в аморфній формі або його переводять в аморфну форму, і циклодекстрин являє собою простий сульфобутиловий ефір β-циклодекстрину й композицій, одержуваних цими способами. В іншому кращому варіанті здійснення, винахід стосується композицій, одержуваних методами одержання композиції, яка містить епотилон (способами), описаними вище. У ще іншому варіанті здійснення, винахід стосується композицій, які містять епотилон і гідроксилалкілований циклодекстрин у специфічному молярному відношенні від 1:8 до 1:100, переважно від 1:11 до 1:80, що еквівалентно масовому відношенню від 1:21 до 1:300, переважно від 1:29 до 1:200. Особливо кращими є відношення, одержувані в прикладах, наведених у даній заявці. У ще іншому варіанті здійснення, винахід стосується композицій, які містять епотилон і простий сульфобутиловий ефір циклодекстрину в специфічному молярному відношенні від 1:9 до 1:100, переважно від 1:9 до 1:50 яке еквівалентно масовому відношенню від 1:38 до 1:300, переважно від 138 до 1:200. Особливо кращими є відношення, одержувані в прикладах, наведених у даній заявці. 17 Композиції, забезпечувані даним винаходом, являють собою композиції з достатньою й високою розчинністю епотилону шляхом комбінування епотилону, переважно використовуваного в аморфній формі, і циклодекстрину в комбінації з додатковими адаптованими наповнювачами та/або шляхом ретельного вибору циклодекстрину. Після цього композиції переважно готують у вигляді лікарського препарату, що дозволяє здійснити парентеральне введення композиції, такого як у вигляді твердого розчину, такого як ліофілізована композиція, яку потім перетворюють у композицію, одержувану внаслідок відновлення ліофілізату підходящим розчинником. Термін "приготовлені у вигляді лікарського препарату у формі для парентерального використання" у цілому стосується композицій для ін'єкцій. Композиції для ін'єкцій можуть вводитися внутрішньовенно, підшкірно або шляхом інфузії У кращих варіантах здійснення винаходу, композиції для ін'єкцій призначені для внутрішньовенного введення. Терміни "ліофілізована композиція", "ліофілізований осад" і "ліофілізат" є взаємозамінними термінами й використовуються в даному винаході для опису твердої композиції, яку одержують в результаті обробки рідкої композиції, такої як розчин, що містить епотилон, який розчинений або принаймні частково розчинений, в умовах, що включають принаймні одну стадію заморожування розчину, з наступною сублімацією розчинника (iв) у вакуумі (основне сушіння) і необов'язково й додатково упарювання/видалення розчинника (ів) при здійсненні вторинного сушіння й необов'язково післясушіння, наприклад, у наступних умовах: Заморожування при -45°С під тиском 1013ммбар протягом аж до 24 годин, переважно протягом 5 годин, Перша стадія основного сушіння до 15°С під тиском 8,9´10-2ммбар протягом 60 годин, переважно протягом 48 годин, - Друга стадія основного сушіння при 25°С під тиском 8,9´10-2ммбар протягом 2 годин, переважно протягом 1 години й - Стадія післясушіння при 25°С при 6,5´10-3ммбар протягом 10 годин, переважно протягом 6 годин, використовуючи, наприклад, установку для сушіння Fa. Hof, тип СОМ 0590. Терміни "ліофілізація" і "сушіння виморожуванням" стосуються процесу, при якому з розчиненої або принаймні частково розчиненої композиції видаляють рідину в умовах, що включають принаймні одну стадію заморожування розчину, з наступною сублімацією розчинника (ів) у вакуумі (основне сушіння) і необов'язково додаткове упарювання розчинника (ів) при здійсненні вторинного сушіння, і необов'язково післясушіння, наприклад, в умовах, описаних у попередньому абзаці. Термін "відновлений розчин" стосується рідкої композиції, отриманої при повному розчиненні ліофілізату, який може являти собою твердий розчин, у розчиннику, такому як вода (вода для ін'єкцій), сольовий розчин або стерильний розчин Рінгера. Розчинник може містити додаткові наповнювачі, таким чином, щоб забезпечити сумі 88182 18 сність відновленої композиції з фізіологічно релевантними рідинами, такими як кров. Відновлені композиції призначені для того, що самі представляють форму, готову для парентерального введення, або їх додатково розводять перед застосуванням. Під терміном "простий сульфоалкіловий ефір циклодекстрину" мають на увазі похідне, одержуване шляхом введення замісника аніонного типу, такого як (С2-балкілен)-SО3- аніонний замісник у циклодекстрин. Сульфоалкільне похідне циклодекстрину може являти собою єдине похідне або суміш похідних. Оскільки похідні циклодекстрину функціоналізують з (С2-6алкілен)-SО3- групами, то похідні мають заряд. Прості сульфоалкілові ефіри циклодекстрину або заміщені принаймні в одному з положень первинних гідроксильних груп або вони заміщені в обох положеннях первинних гідроксильних групи й в 3-ому положенні гідроксильної групи. Заміщення в 2-ому положенні теоретично можливо. Термін гідроксіалкілований β-циклодекстрин, особливо гідроксипропіл-β-циклодекстрин означає похідне циклодекстрину, у якому в певних умовах (відкрито опубліковано постачальником, наприклад Roquette GmbH, циклодекстрину) вільні гідроксильні групи β-циклодекстрину частково або повністю етерифіковані в результаті контрольованої реакції алкіленоксиду, особливо пропіленоксиду, і бета-циклодекстрину, який зустрічається в природі, при основному каталізі з утворенням гідроксиметильних, гідроксіетильних або гідроксипропільних груп відповідно У випадку часткової етерифікації гідроксильних груп отриманий βциклодекстрин характеризується середнім молярним ступенем заміщення (MS), що являє собою середню кількість молів гідроксипропільних груп на ангідроглюкопіранозну одиницю. Це, відповідно до інформації виробника, не слід плутати зі ступенем заміщення (DS) або загальним ступенем заміщення (TDS), що характеризує середню кількість заміщених гідроксилів на ангідроглюкопіранозну одиницю. Звичайно розчинник для відновлення являє собою водний розчин, що містить 75-100об.% води, переважно 85%-100об.%, більш переважно 90100об.%, найбільш переважно 95-100об.%. Розчинник може містити додаткові наповнювачі, такі як неорганічні солі, наприклад, хлорид натрію, для забезпечення сумісності з фізіологічно релевантними рідинами. Термін "розчинність" стосується розчинності епотилону в розчиннику. Відповідно до винаходу, епотилон слід об'єднувати з одним або декількома засобами, які підвищують розчинність епотилону у воді. Як перший солюбілізуючий засіб, було виявлено, що циклодекстрин поліпшує розчинність епотилону. Проте, у деяких випадках можна додавати інші наповнювачі для подальшого підвищення розчинності епотилону або для обмеження розкладання епотилону при приготуванні парентеральної композиції. Наприклад, додаткові наповнювачі можна додавати для стабілізації епотилону при змішуванні наповнюва 19 чів, при видаленні рідини, або при зберіганні або після відновлення. Отже, в одному варіанті здійснення винаходу, забезпечується композиція, яка містить епотилон, циклодекстрин і принаймні один фармацевтично прийнятний наповнювач, вибраний з тонізуючого засобу, наповнювача, кріозахисної речовини, ліозахисної речовини й регулятора рН. В іншому варіанті здійснення винаходу, забезпечується композиція, яка містить епотилон, такий як похідне епотилону, визначене формулою І, і циклодекстрин, епотилон представлений формулою І, n означає 0 - 5, r означає 0-4, p означає 0 - 3, R4a означає водень, С1-С10алкіл, С6-С12 арил або С7-С20 аралкіл, кожний необов'язково заміщений; С1-С10ацил, або, якщо ρ > 0, додатково групу OR4b, R4b означає водень або захисну групу PG; R5 означає С1-С10алкіл, R6 означає водень або необов'язково заміщений С1-С10алкіл, R7, R8 кожний означає атом водню, або разом являють собою додатковий зв'язок або разом являють собою атом кисню, G означає групу X=CR9- або бі- або трициклічний ароматичний гетероциклічний радикал, R9 означає водень, галоген, CN, або С1-С10гС20 алкіл, X означає угруповання CR10R11, причому R10, R11 є однаковими або різними й означають водень, С1-С20алкіл, С6-С12 арил, або С7-20 аралкільний радикал, кожний необов'язково заміщений; або R10 і R11 утворюють разом з метиленовим вуглецем 5 - 7-членне карбоциклічне кільце; А означає групу -О- або -NR12-, R12 означає водень або С1-С10алкіл Епотилон відповідно до формули І може бути конденсований з епоксидним кільцем, у випадку, коли R7, R8 разом являють собою атом кисню або може існувати у вигляді однієї кільцевої системи, у випадку, коли R7, R8 кожний означає атом водню або разом являють собою додатковий зв'язок. Нумерація атомів вуглецю в епотилоновому скелеті буде залежати від того, чи є епотилон конденсованим з додатковим кільцем, таким як епоксидне кільце. На формулі II, наведеній нижче, показана нумерація атомів вуглецю в обох випадках. 88182 20 I у якій R1 означає водень, OR1a, або галоген, де R1a означає водень, SО2-алкіл, SO2-арил, або SО2аралкіл, R2, R3 означають незалежно С1-С10алкіл, R4 означає -(CH2)r-Cº=C-(CH2)p-R4a, -(CH2)rCH=CH-(CH2)p-R4a, Позначення 1-16 стосуються нумерації епотилонового скелету, коли R7, R8 разом утворюють епоксидне кільце. Позначення (1) - (16) стосуються нумерації епотилонового скелету, коли R7, R8 кожний означає атом водню або разом являють собою додатковий зв'язок. II Термін "галоген" означає фтор, хлор, бром і йод. Термін SО2-алкіл стосується "С1-С10алкілу", який однозаміщений -SO2 групою. Термін SО2-арил стосується "С6-С12арилу", який однозаміщений -SO2 групою. Термін SО2-аралкіл стосується "С6-С12арилу", заміщеного однією групою -SO2 і одним або двома "С1-С10алкілами". Термін "С1-С10алкіл" стосується лінійного або розгалуженого насиченого вуглеводневого ланцюга, де найбільш довгі ланцюги містять від одного до десяти атомів вуглецю, такі як метил, етил, нпропіл, ізопропіл, н-бутил, ізобутил, втоp-бутил, трет-бутил, пентил, изопентил, неопентил, гексил, гептил, октил, ундекацил, додецил, і т.д. С1С10алкільний ланцюг згідно із даним винаходом може бути необов'язково заміщеним. Аналогічно, термін "С1-С20алкіл" стосується лінійного або розгалуженого насиченого вуглевод 21 невого ланцюга, де найбільш довгі ланцюги містять від одного до двадцяти атомів вуглецю. Термін "С6-С12 арил" стосується заміщеного або незаміщеного карбоциклічного ароматичного радикала або гетероциклічного радикала, що містить від 6 до 12 атомів вуглецю. Крім того, термін "арил" охоплює конденсовані кільцеві системи, у яких принаймні два арильні кільця мають принаймні один загальний хімічний зв'язок. Ілюстративними прикладами "арильних" кілець є феніл, нафталеніл. Кращою арильною групою є феніл і заміщені фенільні групи, які несуть один або два, однакові або різні замісники, перераховані вище. Переважно замісники знаходяться у пара-та/або мета-положенні. Характерними прикладами арильних груп є, але не обмежуючись тільки ними, феніл, 3-галофеніл, 4-галофеніл, 3-гідроксифеніл, 4-гідроксифеніл, 3-амінофеніл, 4-амінофеніл, 3метилфеніл, 4-метилфеніл, 3-метоксифеніл, 4метоксифеніл, 3-ціанофеніл, 4-ціанофеніл, диметилфеніл, нафтил, гідроксинафтил, гідроксиметилфеніл, трифторметилфеніл, алкоксифеніл. Термін "ароматичний гетероциклічний радикал" стосується заміщеного або незаміщеного ароматичного гетероциклічного радикала, що містить від 6 до 12 атомів вуглецю, який включає один або декілька гетероатомів. Типовими прикладами ароматичних гетероциклічних радикалів є фурил, тієніл, піридил, піразоліл, піримідиніл, оксазоліл, піридазиніл, піразиніл, хіноліл, тіазоліл, бензотіазоліл, бензоксазоліл, хінолін, що може бути однократно або багаторазово заміщений галогеном, ОН, О-алкілом, СО2Н, СО2-алкілом, NO2, N3, CN, С1-С10алкілом, С1-С10ацилом, С1С10ацилокси групами. Гетероатоми в гетероарильних кільцях можуть бути окислені, таким чином, наприклад, бензотіазольне кільце може знаходитися у вигляді N-оксиду. Кращими ароматичними гетероциклічними радикалами є бензотіазоліл, бензоксазол і хінолін; більш переважно бензотіазоліл, заміщений С1-С10алкілом. Термін "С7-С20аралкіл" стосується карбоциклічного ароматичного кільця або кільцевої системи, що містить від 6 до 12 атомів вуглецю, переважно від 6 до 10, і в алкільному ланцюзі від 1 до 8, переважно від 1 до 4 атомів, у якому принаймні одне арильне кільце має принаймні один загальний хімічний зв'язок з С1-С8алкілом. Як аралкільні радикалів, підходящими є, наприклад, бензил, фенілетил, нафтилметил, нафтилетил, фурилметил, тієнілетил і піридилпропіл. Кільця можуть бути однократно або багаторазово заміщені галогеном, ОН, О-алкілом, СО2Н, СО2-алкілом, NO2, N3, CN, С1-С10алкілом, С1-С10ацилом, С1-С10ацилокси групами. Термін "С1-С10ацил" стосується лінійного або розгалуженого насиченого вуглеводневого ланцюга, у якому найбільш довгі ланцюги містять від одного до десяти атомів вуглецю й у якому один з атомів вуглецю являє собою С(=О)О радикал. Алкокси групи, які містяться в X у загальній формулі І, у кожному випадку містять від 1 до 20 атомів вуглецю, з них кращими є метокси, етокси, пропокси, ізопропокси й -трет-бутилокси групи. 88182 22 Термін "епотилон" і "епотилон*" у цілому розуміють як такі, які охоплюють всі види речовин, які належать до класу епотилонів, які зустрічаються в природі або отримані синтетичним шляхом, або у вигляді окремого епотилону або суміші епотилонів. Це означає, що термін "епотилон" стосується будь-якого епотилону, такого як епотилон А, епотилон В, епотилон С, епотилон D, епотилон Е, епотилон F, їх аналогів, похідних, солей і сумішей. Переважно, епотилон являє собою епотилон А, епотилон В, епотилон С, епотилон D або їх похідні або їх солі або їх суміші. У деяких кращих варіантах здійснення винаходу, епотилон являє собою похідне епотилону В відповідно до формули І, наведеної вище. У деяких варіантах здійснення винаходу, що представляють інтерес, епотилон являє собою похідне епотилону, у якому атом вуглецю 10(7) в 16-ти членній макролідній системі має алкенільну, алкінільну або епоксидну групу, як визначено вище (R4 у формулі І) замість метильної групи в епотилонах, які зустрічаються в природі. Таким чином, епотилон згідно із даним винаходом стосується в цілому похідного будь-якого епотилону, такого як епотилони А, В, С, D, Ε або F, у яких атом вуглецю 10(7) 16-ти членної макролідної системи має алкенільну, алкінільну або епоксидну групу, як визначено за допомогою R4 у формулі І. Оскільки вказані епотилони В становлять особливий інтерес згідно із даним винаходом, то це означає, що вищеописані похідні переважно являють собою похідні епотилону В. В інших варіантах здійснення винаходу, що представляють інтерес, епотилон являє собою похідне епотилону, вибране із групи, яка включає: (1S,3S(Е),7S,10R,11S,12S,16R)-7,11дигідрокси-10-(проп-2-ін-1-іл)-3-(1-метил-2-(2метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(2-метил-бензоксазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S(Ε),7S,10R,11R,12S,16R)-7,11дигідрокси-10-(проп-2-ін-1-іл)-3-(1-фтор-2-(2метилоксазол-4-іл)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16(1-хлор-2-(2-метилтіазол-4-іл)етеніл)-1-окса5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)циклогексадец-13-ен-2,6-діон; (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2метил-бензотіазол-5-іл)-1-окса-5,5,9,13тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13ен-2,6-діон; (4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16(1-метил-2-(2-піридил)етеніл)-1-окса-5,5,9,13тетраметил-7-(бут-3-ин-1-іл)-циклогексадец-13-ен2,6-діон; (4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16(1-метил-2-(2-піридил)етеніл)-1-окса-5,5,9,13тетраметил-7-(бут-3-ен-1-іл)-циклогексадец-13-ен2,6-діон; (1S,3S(E),7S,10R,11S,12S,16R)-7,11дигідрокси-10-(проп-2-ен-1-iл)-3-(1-метил-2-(2 23 метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16(1-метил-2-(2-піридил)етеніл)-1-окса-5,5,9,13тетраметил-7-(проп-2-ін-1-іл)-циклогексадец-13-ен2,6-діон; (4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16(1-фтор-2-(2-метилтіазол-4-іл)етеніл)-1-окса5,5,9,13-тетраметил-7-(проп-2-ін-1-іл)циклогексадец-13-ен-2,6-діон; (1S,3S(Е),7S,10R,11S,12S,16R)-7,11дигідрокси-10-(проп-2-ін-1-іл)-3-(1-фтор-2-(2метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2метил-бензоксазол-5-іл)-1-окса-5,5,9,13тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13ен-2,6-діон; (1R,3S,7S,10R,11S,12S,16S)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(2-метил-бензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16R)-4,8-дигідрокси-16-(2метил-бензотіазол-5-іл)-1-аза-5,5,9,13-тетраметил7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси10-(2-оксациклопропіл-1-метил)-3-(2-метилбензотіазол-5-іл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S(E),7S,10R,11S,12S,16R)-7,11дигідрокси-10-(бут-3-ин-1-іл-3-(1-метил-2-(2піридил)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16(1-метил-2-(2-метилтіазол-4-іл)етеніл)-1-окса5,5,9,13-тетраметил-7-(проп-2-ен-1-іл)циклогексадец-13-ен-2,6-діон; (1R,3S(E),7S,10R,11S,12S,16S)-7,11дигідрокси-10-(проп-2-ен-1-іл)-3-(1-метил-2-(2метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон, (4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16(1-метил-2-(-(2-піридил)етеніл)-1-окса-5,5,9,13тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13ен-2,6-діон; (4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-16(1-фтор-2-(2-метилоксазол-4-іл)етеніл)-1-окса5,5,9,13-тетраметил-7-(проп-2-ін-1-іл)циклогексадец-13-ен-2,6-діон; (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2метил-бензотіазол-5-іл)-1-окса-5,5,9,13тетраметил-7-(3-метил-бут-2-ен-1-іл)циклогексадец-13-ен-2,6-діон; (1S,3R,7S,10R,11S,12S,16R)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(2-метил-бензотіазол-5-іл)8,8,12,16-тетраметил-4-аза-17-оксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S,7S,10R,11S,12S,16S)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(хінолін-7-іл)-8,8,12,16тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан5,9-діон; (1R,3S,7S,10R,11S,12S,16S)-7,11-дигідрокси10-(проп-2-ін-1-іл)-3-(2-метил-бензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; 88182 24 (1S,3S(Ε),7S,10R,11S,12S,16R)-7,11дигідрокси-10-(бут-3-ин-1-іл)-3-(1-метил-2-(2піридил)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S(Е),7S,10R,11S,12S,16S)-7,11дигідрокси-10-(бут-3-ин-1-іл)-3-(1-метил-2-(2піридил)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло [14 1.0]гептадекан-5,9-діон; (1S,3S(Е),7S,10R,11S,12S,16R)-7,11дигідрокси-10-(бут-3-ен-1-іл)-3-(1-метил-2-(2піридил)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло [14 1.0] гептадекан-5,9-діон: (1R,3S(Е),7S,10R,11S,12S,16S)-7,11дигідрокси-10-(бут-3-ен-1-іл)-3-(1-метил-2-(2піридил)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло [14 1.0] гептадекан-5,9-діон; (4S,7S,8R,9S,13E/Z,16S(Е))-4,8-дигідрокси-16(1-метил-2-(2-піридил)етеніл)-1-окса-5,5,9,13тетраметил-7-(бут-3-ин-1-іл)-циклогексадец-13-ен2,6-діон; (1'S,4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси7-(проп-2-ен-1-іл)-16-(1'-метил-2'-(піридин-2ил)етил)-5,5,9,13-тетраметил-1-окса-гексадец-13ен-2,6-діон; (1'S,4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси7-(проп-2-ен-1-іл)-16-(1'-метил-2'-(піридин-2ил)етил)-5,5,9,13-тетраметил-1-окса-гексадец-13ен-2,6-діон; (1S/R,3S(Е),7S,10R,11S,12S,16R/S)-7,11дигідрокси-10-(2-оксациклопропіл-1-метил)-3-(1метил-2-(2-піридил)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S/R,3S(Е),7S,10R,11S,12S,16R/S)-7,11дигідрокси-10-(2-оксациклопропіл-1-метил)-3-(1метил-2-(2-піридил)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0] гептадекан-5,9-діон; (1S,3S(Е),7S,10R,11S,12S,16R)-7,11дигідрокси-10-(2-оксациклопропіл-1-метил)-3-(1метил-2-(2-піридил)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S(E),7S,10R,11S,12S,16S)-7,11дигідрокси-10-(проп-2-ін-1-іл)-3-(1-фтор-2-(2метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S(Ε),7S,10R,11S,12S,16S)-7,11дигідрокси-10-(проп-2-ін-1-іл)-3-(1-фтор-2-(2метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S,7S,10R,11S,12S,16S)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(2-метил-бензоксазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S(Е),7S,10R,11S,12S,16S)-7,11дигідрокси-10-(проп-2-ін-1-іл)-3-(1-фтор-2-(2метилоксазол-4-іл)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2метил-бензотіазол-5-іл)-1-окса-5,5,9,13тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13ен-2,6-діон; (1R,3S,7S,10R,11S,12S,16S)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(2-метил-бензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; 25 (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2метил-бензотіазол-5-іл)-1-аза-5,5,9,13-тетраметил7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон; (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2метил-бензотіазол-5-іл)-1-аза-5,5,9,13-тетраметил7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон; (4S,7R,8S,9S,13E/Z,16R)-4,8-дигідрокси-16-(2метил-бензотіазол-5-іл)-1-аза-5,5,9,13-тетраметил7-(проп-2-ен-1-іл)-циклогексадец-13-ен-2,6-діон; (1R,3S,7S,10R,11S,12S,16S)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(2-метил-бензотіазол-5-іл)8,8,12,16-тетраметил-4-аза-17-оксабщикло[14.1.0]гептадекан-5,9-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-3(2-метил-бензотіазол-5-іл)-10-(проп-2-ен-1-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16(хінолін-7-іл)-1-окса-5,5,9,13-тетраметил-7-(проп-2ен-1-іл)-циклогексадец-13-ен-2,6-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(2-метил-бензотіазол-5-іл)8,8,12,16-тетраметил-4-аза-17-оксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(2-метил-бензотіазол-5-іл)8,8,12,16-тетраметил-4-аза-17-оксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16R)-4,8-дигідрокси-16-(2метил-бензоксазол-5-іл)-1-аза-5,5,9,13тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13ен-2,6-діон; (4S,7R,8S,9S,13E/Z,16R)-4,8-дигідрокси-16-(2метил-бензоксазол-5-іл)-1-аза-5,5,9,13тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13ен-2,6-діон; (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2метил-бензоксазол-5-іл)-1-аза-5,5,9,13тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13ен-2,6-діон; (1R,3R,7S,10R,11S,12S,16S)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(2-метил-бензоксазол-5-іл)8,8,12,16тетраметил-4-аза-17-оксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3R,7S,10R,11S,12S,16R)-7,11-дигідрокси10-проп-2-ен-1-іл)-3-(2-метил-бензоксазол-5-іл)8,8,12,16тетраметил-4-аза-17-оксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3R,7S,10R,11S,12S,16S)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(2-метил-бензоксазол-5-іл)8,8,12,16тетраметил-4-аза-17-оксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S(Е),7S,10R,11S,12S,16R)-7,11дигідрокси-10-(проп-2-ен-1-іл)-3-(1-хлор-2-(2метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S(Е),7S,10R,11S,12S,16S)-7,11дигідрокси-10-(проп-2-ен-1-іл)-3-(1-хлор-2-(2метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S(Ε),7S,10R,11S,12S,16R)-7,11дигідрокси-10-(2-оксациклопропіл-1-метил)-3-(1хлор-2-(2-метил-тіазол-4-іл)етеніл)-8,8,12,16тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан5,9-діон, 88182 26 (1R,3S(Е),7S,10R,11S,12S,16S)-7,11дигідрокси-10-(проп-2-ен-1-іл)-3-(1-фтор-2-(2метил-тіазол-4-іл)етеніл)-16-гідроксиметил-8,8,12триметил-4,17-діоксабіцикло[14.1.0]гептадекан5,9-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси10-(2-оксациклопропіл-1-метил)-3-(2-метилбензотіазол-5-іл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16S(Е))-4,8-дигідрокси-7(проп-2-ен-1-іл)-16-(1-фтор-2-(2-метил-тіазол-4іл)етеніл)-13-гідроксиметил-5,5,9-триметил-1-оксагексадец-13-ен-2,6-діон; (1S,3S(Е),7S,10R,11S,12S,16R)-7,11дигідрокси-10-(проп-2-eн-1-іл)-3-(1-фтор-2-(2метил-тіазол-4-іл)етеніл)-16-гідроксиметил-8,8,12триметил-4,17-діоксабіцикло[14.1.0]гептадекан5,9-діон, (4S,7S,8R,9S,13E/Z,163)-4,8-дигідрокси-16-(2метил-бензотіазол-5-іл)-1-окса-5,5,9,13тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13ен-2,6-діон; (1S,3S,7S,10S,11R,12S,16R)-7,11-дигідрокси10-(проп-2-eн-1-іл)-3-(2-метил-бензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1R,3S,7S,10S,11R,12S,16S)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(2-метил-бензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4R,7S,8R,9R,13E/Z,16R)-4,8-дигідрокси-16-(2метил-бензотіазол-5-іл)-1-окса-5,5,9,13тетраметил-7-(проп-2-ен-1-іл)-циклогексадец-13ен-2,6-діон; (1R,3R,7R,10S,11R,12R,16S)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(2-метил-бензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3R,7R,10S,11R,12R,16R)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(2-метил-бензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S(Ε),7S,10R,11S,12S,16R)-7,11дигідрокси-10-(бут-3-ин-1-іл)-3-(1-метил-2-(2піридил)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S(Е),7S,10R,11S,12S,16R)-7,11дигідрокси-10-(бут-3-ен-1-іл)-3-(1-метил-2-(2піридил)етеніл)-8,8,12,16-тетраметил-4,17діоксабіцикло [14 1.0] гептадекан-5,9-діон; (1S,3S(Е),7S,10R,11S,12S,16R)-7,11дигідрокси-10-(проп-2-ен-1-іл)-3-(1-метил-2-(2метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(2-метил-бензоксазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S(Е),7S,10R,11S,12S,16R)-7,11дигідрокси-10-(проп-2-ен-1-іл)-3-(1-xлop-2-(2метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(2-метил-бензотіазол-5-іл) 27 8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(2-метил-бензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(хінолін-7-іл)-8,8,12,16тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан5,9-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси10-(проп-2-ен-1-іл)-3-(хінолін-7-іл)-8,8,12,16тетраметил-4,17-діоксабіцикло[14.1.0]гептадекан5,9-діон; (1R,3S(Е),7S,10R,11S,12S,16S)-7,11дигідрокси-10-(проп-2-ін-1-іл)-3-(1-хлор-2-(2метилтіазол-4-іл)етеніл)-8,8,12,16-тетраметил4,17-діоксабіцикло[14.1.0]гептадекан-5,9-діон; (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16-(2метил-бензотіазол-5-іл)-1-окса-5,5,9,13тетраметил-7-(проп-2-ін-1-іл)-циклогексадец-13-ен2,6-діон; (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси10-(проп-2-ін-1-іл)-3-(2-метил-бензотіазол-5-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон; та/або (4S,7R,8S,9S,13E/Z,16S)-4,8-дигідрокси-16(хінолін-7-іл)-1-окса-5,5,9,13-тетраметил-7-(проп-2ен-1-іл)-циклогексадец-13-ен-2,6-діон. У варіанті здійснення винаходу, що представляє інтерес, похідне епотилону являє собою (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-3-(2метил-бензотіазол-5-іл)-10-(проп-2-ен-1-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон. Епотилон може використовуватися в композиції в будь-якій кількості. Очевидно, що бажано застосовувати високі концентрації, якщо це є можливим, такі як епотилон у кількості принаймні 0,05мас.% у твердих композиціях, таких як ліофілізат. Слід взяти до уваги, що максимальний вміст епотилону може становити порядку 2, 3, 4, 5 або 10мас.% залежно від кількості й типу відновленої рідини. Звичайно, кількість епотилону знаходиться в інтервалі від 0,05% до 10%, переважно від 0,1% до 4мас.%, більш переважно близько 0,2-2мас.% у ліофілізаті. Щодо відновленого розчину, концентрація знаходиться в інтервалі від 0,2мг/мл до 10мг/мл, переважно від 0,5мг/мл до 5мг/мл, така як приблизно 1мг/мл. Слід зазначити, що великий розмір епотилону за винаходом узгоджується з утворенням комплексу включення, у якому епотилон повністю відповідає порожнині циклодекстрину. Термін "циклодекстрин" використовується для визначення сполук, що містять глюкозні одиниці, об'єднані в кругову структуру, а саме сполук, що містять 7 ангідро глюкозних одиниць (βциклодекстрин); 8 ангідро глюкозних одиниць (gциклодекстрин) або 6 ангідро глюкозних одиниць (α-циклодекстрин), а також їх похідні. Кожна із глюкозних одиниць містить в 2-ому, 3-ому і 6-ому положеннях три гідрокси групи, які можуть бути етерифіковані або естерифіковані, переважно етерифіковані. Отже, термін "похідне циклодекст 88182 28 рину" згідно із даним винаходом охоплює етерифіковані й естерифіковані циклодекстрини. Мається на увазі, що циклодекстрин може бути повністю або частково етерифікований або естерифікований, що означає, що всі або тільки частина гідрокси груп дериватизовані з утворенням простого або складного ефіру. Таким чином, принаймні 10%, такі як принаймні 20, 30, 40, 50, 60, 70, 80 або 90% спиртових груп можуть бути алкілованими або ацилованими. Слід взяти до уваги, що не більш, ніж 40%, 30%, 20%, 10% або 5% з 5% спиртових груп можуть бути алкілованими або ацилованими. У кращих варіантах здійснення винаходу, циклодекстрин являє собою β-циклодекстрин або його похідне, таке як алкілований циклодекстрин, тобто простий алкіловий ефір циклодекстрину. Алкіл може мати ланцюг будь-якої довжини, однак переважно менше, ніж 10 атомів вуглецю, переважно менш, ніж 5 атомів вуглецю, такий як алкіл, вибраний з метилу, етилу, пропілу, бутилу або пентилу, включаючи їх розгалужені ланцюги (ізо-пропіл). У ще більш кращих варіантах здійснення винаходу, алкіл алкілованого циклодекстрину містить функціональну групу, таку як гідрокси група та/або група сірки. Таким чином, у кращих варіантах здійснення винаходу, похідне циклодекстрину, таке як похідне β-циклодекстрину етерифікують гідроксіалкільними групами та/або сульфоалкільними групами, одержуючи гідроксіалкіловані циклодекстрини (наприклад, гідроксиметиловані, гідроксіетиловані, гідроксипропіловані, гідроксибутиловані, гідроксипентиловані циклодекстрини), або сульфоалкіловані циклодекстрини (наприклад, сульфометиловані, сульфоетиловані, сульфопропіловані, сульфобутиловані, сульфопентиловані циклодекстрини). Етерифікація циклодекстрину алкільними групами може вказуватися безпосередньо у вигляді ступеня заміщення (DS) на глюкозну одиницю, що, як вказано вище, відповідає 3 для повного заміщення. Частково етерифіковані циклодекстрини використовуються згідно із даним винаходом, які містять алкільні групи, такі як гідроксіалкільні групи й сульфоалкільні групи, як описано вище, аж до ступеня заміщення від 0,05 до 2,0, переважно від 0,2 до 1,5. Найбільш переважно ступінь заміщення алкільними групами становить від приблизно 0,5 до приблизно 1,2 на глюкозну одиницю. Деякі варіанти здійснення винаходу стосуються композицій, які містять епотилон і циклодекстрин у специфічному молярному відношенні епотилону до циклодекстрину від 1:8 до 1:100, переважно від 1:11 до 1:80, що еквівалентно масовому відношенню від 1:21 до 1:300, переважно від 1 29 до 1:200. Особливо кращими є відношення, отримані в прикладах, наведених у даній заявці. Циклодекстрин у композиціях може використовуватися в будь-якій кількості залежно від типу циклодекстрину. Переважно, кількість знаходиться в інтервалі від 10 до 99,8мас.% у твердих композиціях, таких як у ліофілізаті. Більш переважно, кількість знаходиться в інтервалі від 30 до 98%, найбільш переважно в інтервалі від 50 до 98%, 29 такому як 69-96мас.%. Щодо відновленого розчину, концентрація знаходиться в інтервалі від 10мг/мл до 1000мг/мл, переважно від 50мг/мл до 500мг/мл, така як приблизно 200мг/мл. У кращому варіанті здійснення винаходу, епотилон являє собою похідне епотилону відповідно до формули І, наведеної вище, і циклодекстрин являє собою сульфоалкілований β-циклодекстрин, такий як сульфометилований, сульфопентилований, сульфопропілований, сульфобутилований, сульфопентилований β-циклодекстрин, переважно сульфобутилований β-циклодекстрин. Інакше кажучи, циклодекстрин являє собою простий сульфометиловий ефір β-циклодекстрину, простий сульфоетиловий ефір β-циклодекстрину, простий сульфопропіловий ефір β-циклодекстрину, простий сульфобутиловий ефір β-циклодекстрину, простий сульфопентиловий ефір βциклодекстрину, переважно простий сульфобутиловий ефір β-циклодекстрину. В іншому кращому варіанті здійснення винаходу, епотилон являє собою похідне епотилону відповідно до формули І, наведеної вище, і циклодекстрин являє собою гідроксіалкілований βциклодекстрин, такий як гідроксиметилований, гідроксіетилований, гідроксипропілований, гідроксибутилований, гідроксипентилований βциклодекстрин, переважно гідроксипропілований β-циклодекстрин, за умови, що вказаний епотилон і циклодекстрин надалі комбінують із принаймні одним фармацевтично прийнятним засобом, вибраним з тонізуючого засобу, наповнювача й буферної речовини. Інакше кажучи, циклодекстрин може являти собою простий гідроксиметиловий ефір β-циклодекстрину, простий гідроксіетиловий ефір β-циклодекстрину, простий гідроксипропіловий ефір β-циклодекстрину, простий гідроксибутиловий ефір β-циклодекстрину, простий гідроксипентиловий ефір β-циклодекстрину, переважно простий гідроксипропіловий ефір β-циклодекстрину. У ще іншому варіанті здійснення, винахід стосується композиції, яка містить епотилон відповідно до формули І, наведеної вище, і βциклодекстрин, переважно гідроксіалкілований βциклодекстрин або сульфоалкілований βциклодекстрин, описаний вище, композиція може знаходитися у вигляді комплексу включення або яким-небудь іншим способом ці два компоненти можуть бути зібрані. Комерційно доступні циклодекстрини, які становлять інтерес, включають алкільні й алільні похідні, гідроксіалкільні похідні, такі як гаммациклодекстрин, гідроксипропіл-гаммациклодекстрин, гідроксипропіл-бетациклодекстрин, простий сульфобутиловий ефір бета-циклодекстрину, метил-бета-циклодекстрин, метилтіоуреїдо-бета-циклодекстрин, пропандіамінбета-циклодекстрин, етандіамін-бетациклодекстрин, гідроксіетиламіно-бетациклодекстрин. Як було вказано, композиції можуть додатково містити принаймні один фармацевтично прийнятний засіб, вибраний з тонізуючого засобу, наповнювача або буферної речовини. 88182 30 Терміни "тонізуючий засіб" і "модифікатор тонічності" є взаємозамінними термінами й стосуються сполуки, яка при розчиненні в композиції під час використання забезпечує тонічність у межах фізіологічного інтервалу крові, рідини черевної порожнини або інших релевантних рідин організму людини. Очевидно, додавання "тонізуючого засобу також може залежати від того, чи містить розчинник для відновлення засоби, що модифікують тонічність. Отриманий розчин, наприклад, відновлений розчин, може мати осмолярність в інтервалі від приблизно 100 до 900мОсм/кг Н2О. Переважно, осмолярність знаходиться в інтервалі від приблизно 150 до 900мОсм/кг Н2О, більш переважно в інтервалі від приблизно 200 до 500мОсм/кг Н2О, ще більш переважно в інтервалі від приблизно 250 до 350мОсм/кг Н2О. Найбільш переважно, осмолярність знаходиться в інтервалі від приблизно 280 до 320мОсм/кг Н2О. Як використовується в даному винаході, тонізуючий засіб може являти собою поліол, такий як маніт, сорбіт і ксиліт, переважно маніт або хлорид натрію. У деяких варіантах здійснення, додавання засобу, що модифікує тонічність, не є необхідним, оскільки композиція має бажану осмолярність. Винахідниками було виявлено, що підходяща тонічність досягається при використанні як циклодекстрину простого сульфоалкілового ефіру βциклодекстрину. Таким чином, у варіантах здійснення винаходу, які передбачають використання простого сульфоалкілового ефіру βциклодекстрину як циклодекстрину, відсутня необхідність у використанні будь-якого засобу, що модифікує тонічність, або простий сульфоалкіловий ефір β-циклодекстрину може використовуватися в кількості, що не впливає на тонічність композиції. У кращому варіанті здійснення винаходу, принаймні один додатковий фармацевтично прийнятний наповнювач, який необхідно додавати в комбінації епотилону й циклодекстрину, являє собою маніт, сорбіт та/або ксиліт. Додавання маніту, сорбіту та/або ксиліту може забезпечувати додаткові дії. У цілому, відомо, що маніт являє собою наповнювач (заповнювач), який підходить для ліофілізованих композицій, і, як було вказано, маніт також має модифікуючу тонічність дію в рідкій композиції, такій як композиція, одержувана після відновлення ліофілізату за допомогою підходящого розчинника. Термін "кріозахисні речовини", як використовується в даному винаході, стосується речовин, які забезпечують стабільність епотилону до стресу, що викликається заморожуванням. Прикладами кріозахисних речовин є циклодекстрини, такі як βциклодекстрини і їх похідні, і охоплюють поліоли, такі як, наприклад, маніт, а також регулятори рН. Регулятори рН включають аміни, такі як трометамол, мінеральні кислоти, органічні кислоти, такі як соляна кислота. Додатково як кріозахисні речовини можна використовувати поверхнево-активні речовини. Прикладами поверхнево-активних речовин є аміни, такі як трометамол. Кріозахисні речовини також впливають на тонічність лікарських 31 препаратів. Кріозахисні речовини також можу мати ліозахисні дії. Термін "ліозахисна речовина", як використовується в даному винаході, стосується речовин, які забезпечують стабільність епотилону при видаленні води в процесі сушіння, такого як процес ліофілізації. Прикладами ліозахисних речовин є сахариди, зокрема сахароспирти, особливо маніт. Сахариди, які становлять інтерес, є ди- і трисахаридами, такими як сахароза, декстроза, лактоза, мальтоза та/або трегалоза. Термін "наповнювач" або "заповнювач" є взаємозамінними термінами й означають засіб, що забезпечує гарні властивості ліофілізованому осаду, який утворює фармацевтично гарний продукт, що допомагає епотилону або його похідному подолати різні стреси, наприклад, сколювання/заморожування, зв'язані із процесом ліофілізації. Крім того, наповнювач допомагає підтримати рівні терапевтичної активності при здійсненні процесу сушіння виморожуванням і наступним зберіганням. Типовими прикладами заповнювачів є циклодекстрини, сахароспирти, такі як маніт. Ці засоби також можуть впливати на тонічність лікарських препаратів. Слід взяти до уваги, що необхідна кількість засобу, який модифікує тонічність, наповнювача, ліозахисної речовини або кріозахисної речовини може залежати від деяких факторів, таких як необхідна осмолярність, стабільність, характеристики процесу ліофілізації й відновлення. Стосовно маніту, було виявлено, що необхідна кількість знаходиться в інтервалі від 0,5 до 50мас.% у твердих композиціях, таких як ліофілізат. Більш переважно, кількість знаходиться в інтервалі від 2 до 20%. Стосовно відновленого розчину, концентрація знаходиться в інтервалі від 1мг/мл до 200мг/мл, переважно від 2мг/мл до 100мг/мл, більш переважно від 5мг/мл до 50мг/мл, така як приблизно 20мг/мл. Як було вказано, композиції за винаходом додатково можуть містити регулятор рН, такий як буферна сполука. Слід взяти до уваги, що регулятор рН може використовуватися для подальшої стабілізації епотилонів, які легко піддаються гідролізу у водному розчині, що має значення рН, близьке до нейтрального. Термін "регулятор рН" стосується сполук, які є підходящими для забезпечення/підтримки значення рН у діапазоні від 4 до 9 у відновленому розчині Як використовується в даному винаході, регулятор рН переважно підтримує значення рН у діапазоні від 5 до 8, більш переважно в діапазоні від 6 до 7,5. Отже, в подальшому варіанті здійснення винаходу, що становить інтерес, рН композицій підтримується в інтервалі рН від 5 до 8, більш переважно в інтервалі від 6 до 7,5. Слід зазначити, що рН у розчині епотилону в період часу перед видаленням вологи, яка міститься, наприклад, перед сушінням виморожуванням, необхідно підтримувати в інтервалі рН від 5 до 8. Сприятливо, цей інтервал рН також знаходиться в межах бажаного фізіологічного інтервалу, таким чином, не роблячи небажаного впливу на користувача при парентеральному введенні композиції. Переважно рН при 88182 32 близно дорівнює нейтральному, таке як біля рН 7,4. Типовими прикладами регуляторів рН є TRIS,кислотна форма або солі лимонної кислоти, оцтової кислоти, гістидину, яблучної кислоти, фосфорної кислоти, винної кислоти, янтарної кислоти, MES, HEPES, імідазолу, молочної кислоти, глутарової кислоти й гліцилгліцину. В одному варіанті здійснення винаходу TRIS використовується окремо, а в іншому варіанті здійснення TRIS використовується разом із соляною кислотою. Під терміном "TRIS" мають на увазі 2-аміно-2гідроксиметил-1,3-пропандіол, який також відомий під назвами трометамол; триметилол амінометан; трис(гідроксиметил)амінометан; трисманин; трисбуфер; трометан; ТНАМ; Таластрол; Трис Аміно й Трометамін. Регулятор рН може використовуватися в будьякій кількості. Однак, було виявлено, що необхідна кількість знаходиться в інтервалі від 0,05 до 4,2% у твердих композиціях, таких як у ліофілізаті. Більш переважно, кількість знаходиться в інтервалі від 0,2 до 1,5мас.%. Стосовно відновленого розчину, концентрації знаходиться в інтервалі від 0,1мг/мл до 10мг/мл, переважно в інтервалі від 0,2мг/мл до 5мг/мл, більш переважно в інтервалі від 0,5мг/мл до 3мг/мл, така як приблизно 1,2мг/мл. Крім того, регулятор рН може використовуватися разом з кислотою або основою, такою як соляна кислота. Кислота може використовуватися в будь-якій кількості. Однак, було виявлено, що необхідна кількість знаходиться в інтервалі від 0,01 до 0,9% у твердих композиціях, таких як у ліофілізаті. Більш переважно, кількість знаходиться в інтервалі від 0,05 до 0,3%. Стосовно відновленого розчину, концентрації знаходиться в інтервалі від 0,03мг/мл до 2мг/мл, переважно в інтервалі від 0,05мг/мл до 1мг/мл, більш переважно в інтервалі від 0,1мг/мл до 0,6мг/мл, така як приблизно 0,3мг/мл. Слід взяти до уваги, що композиції відповідно до винаходу готують без додавання поверхневоактивної речовини. Отже, у варіантах здійснення винаходу, які становлять інтерес, композиція не містить поверхнево-активної речовини або принаймні практично не містить поверхнево-активної речовини. Термін "поверхнево-активна речовина" звичайно стосується засобу, який захищає епотилон або його похідне від стресу, викликаного поверхнею розділу повітря/розчин, і стресу, викликаного розчином/поверхнею. Наприклад, поверхнево-активна речовина може захищати епотилон або його похідне від агрегації. Підходящими поверхнево-активними речовинами можуть бути певні аміни, полісорбат або полоксамер, такий як Твін 20, Твін 80 або полоксамер 188. Слід взяти до уваги, що варіанти здійснення винаходу, описані в даній заявці, можна комбінувати будь-яким підходящим чином. Кращий варіант здійснення стосується композиції, яка містить епотилон, як визначено в даному винаході, циклодекстрин, як визначено в даному винаході, і принаймні один фармацевтично прийнятний наповнювач, вибраний із групи, яка включає маніт; сорбіт; ксиліт; 2-аміно-2-гідроксиметил-1,3пропандіол; кислотну форму або солі лимонної 33 кислоти, оцтової кислоти, гістидину, яблучної кислоти, фосфорної кислоти, винної кислоти, янтарної кислоти, MES, HEPES, імідазолу, молочної кислоти, глутарової кислоти й гліцилгліцину, переважно маніт та/або TRIS. У ще більш кращих варіантах здійснення винаходу забезпечуються композиції, які містять: і) похідне епотилону в кількості 0,1-2мас.%, переважно 0,2-1мас.%, іі) гідроксіалкіл-3-циклодекстрин, переважно 2гідроксипропіл-р-циклодекстрин у кількості 5099мас.%, переважно 70-95мас.%, ііі) маніт, ксиліт або сорбіт, переважно маніт у кількості 0-50мас.%, переважно 1-20мас.%, більш переважно 2-15мас.%, iv) регулятор рН, переважно Трометамол у кількості 0-2мас.%, переважно 0,1-1мас.%, ν) соляну кислоту в кількості 0-1мас%, переважно 0,05-0,5мас.%. У ще більш кращих варіантах здійснення винаходу забезпечуються композиції, які містять: і) похідне епотилону в кількості 0,01-2мас%, переважно 0,02-1мас.%, іі) сульфоалкіл-β-циклодекстрин, переважно сульфобутил-3-циклодекстрин у кількості 5099,9мас.%, переважно 85-99,5мас.%, ііі) регулятор рН, переважно Трометамол у кількості 0-2мас.%, переважно 0,1-1мас.%, і iv) соляну кислоту в кількості 0-1мас.%, переважно 0,05-0,5мас.%. Композиції, які забезпечуються даним винаходом, характеризуються гарною хімічною стабільністю стосовно епотилону, незважаючи на той факт, що епотилони легко піддаються гідролізу. Термін "гарна хімічна стабільність" використовується для опису того, що гідроліз або інше хімічне розкладання епотилону мінімізується при зберіганні або приготуванні композиції таким чином, що забезпечується істотне збереження епотилону. Подібним чином, хімічна стабільність твердої композиції, такої як ліофілізат, є високою. Стабільність звичайно визначали шляхом зберігання ліофілізату в скляному флаконі, запечатаному гумовими пробками, і кількості продукту розкладання, утвореного протягом періоду аж до 1, 3, 6, або 9 місяців досліджували шляхом визначення продуктів розкладання в кожному з відновлених розчинів залежно від часу й температури. Концентрацію епотилону й продуктів його розкладання визначали за допомогою кількісних аналізів, таких як ВЕРХ. Епотилон звичайно не є дуже стабільним у розчині. Таким чином, сполукуслід захищати від гідролізу. Додатково, стабільність залежить від рН розчину. Розчинність у насичених умовах у воді дорівнює близько 12мг/л. Низька стабільність епотилону показана в прикладі 4. Розкладання пропорційне до [K´концентрацію]. Приклад 6 стосується стабільності ліофілізату й на Фіг.1 і 2 відповідно до винаходу наведені результати дослідження Фіг.1 Дослідження ліофілізату епотилону при різних умовах зберігання 88182 34 Ліофілізат відповідно до прикладу 1 зберігали при 6°С і 25°С відповідно. Показано, що ліофілізат є стабільним протягом 18 місяців і має постійний вміст епотилону. Фіг.2 Сума домішок при різних умовах зберігання Сума домішок, оскільки вони можуть підвищуватися, якщо сполука є нестабільною, показана для умов зберігання 6°С і 25°С. При обох температурах кількість домішок залишалася нижче 1% і була постійною протягом усього періоду часу. Наприклад, стабільність ліофілізату була такою, що менше ніж 15% вихідної кількості епотилону в композиції розкладалося протягом періоду часу аж до 3 місяців, якщо композицію зберігали запечатаною в темряві при температурі від 2°С до 8°С. Переважно, менше ніж 10%, наприклад, така як менше ніж 5% вихідної кількості епотилону в композиції розкладається при вказаних умовах. Термін "вихідний вміст" стосується кількості епотилону, доданого до композиції під час приготування. Концентрація, наведена в даному винаході (мг/мл), стосується або концентрації в розчині епотилону перед видаленням вологи (наприклад, перед сушінням виморожуванням) або позначається як мас.%, яка потім стосується концентрації у твердій композиції, наприклад у ліофілізованому осаді. Подальший варіант здійснення винаходу стосується приготування твердої композиції, такої як ліофілізат, відповідно до винаходу, що може бути приготовлена з розчинів (надалі в даному винаході описуються як "вихідні розчини"), що містять епотилон, описаний у даному винаході, циклодекстрин, описаний у даному винаході, і необов'язково принаймні один додатковий фармацевтично прийнятний наповнювач, як визначено в даному винаході вище. В одному варіанті здійснення, спосіб одержання композиції за винаходом включає стадії: а) розчинення епотилону, як визначено в даному винаході, в органічному розчиннику, такому як спирт, (переважно етанол); і б) розчинення циклодекстрину, як визначено в даному винаході, у водному розчині, необов'язково разом із принаймні одним додатковим фармацевтично прийнятним компонентом, як визначено в даному винаході, таким як маніт і /або трометамол; необов'язково в) доведення значення рН отриманої суміші на стадії б) до рН в інтервалі від 5 до 9, переважно від 6 до 8, таке як приблизно 7,4, за допомогою неорганічної кислоти, такої як соляна кислота; і г) змішування отриманих розчинників а) і б) або а) і в); і необов'язково д) здійснення стерильної фільтрації продукту зі стадії г) для одержання так званого "вихідного розчину" є) висушування розчину для видалення розчинника з одержанням твердої композиції. В іншому варіанті здійснення, спосіб одержання композиції за винаходом включає стадії: а) розчинення епотилону, як визначено в даному винаході, в органічному розчиннику, такому як спирт, (переважно етанол); і 35 88182 б) упарювання вказаного органічного розчинника; і в) розчинення циклодекстрину, як визначено в даному винаході, у водному розчині, необов'язково разом із принаймні одним додатковим фармацевтично прийнятним компонентом, як визначено в даному винаході, таким як маніт і /або трометамол; необов'язково г) доведення значення рН отриманої суміші на стадії б) до рН в інтервалі від 5 до 9, переважно від 6 до 8, таке як приблизно 7,4, за допомогою неорганічної кислоти, такої як соляна кислота; і д) розчинення порошку, отриманого на стадії б), у розчинниках, отриманих на стадіях в) або г); і необов'язково е) здійснення стерильної фільтрації продукту зі стадії д) для одержання так званого "вихідного розчину" є) видалення розчинника з "вихідного розчину" з одержанням твердої композиції. Підходяще, процес сушіння здійснюють за допомогою ліофілізації або роторного випарника. В одному варіанті здійснення винаходу для вищеописаних способів використовують гідроксипропіл-β-циклодекстрин. В іншому варіанті здійснення винаходу для вищеописаних способів використовують простий сульфобутиловий ефір β-циклодекстрину. Ліофілізат відповідно до другого способу, описаного вище, містить підвищену кількість епотилону в композиції, якщо аморфний епотилон використовується принаймні для стадії д). У цьому випадку не є значимим, за допомогою якої методики одержують аморфний епотилон. Ступінь, до якого кількість епотилону може бути підвищений в порівнянні зі способами, відомими з рівня техніки, є несподіваним і непередбачуваним. Інший аспект винаходу стосується того факту, що кількість циклодекстрину для композиції, яка використовується для внутрішньовенного введення, може бути значно зменшена в порівнянні з композиціями, відомими з рівня техніки, наприклад, як показано в прикладі 1. Композиції за винаходом можуть використовуватися для лікування захворювання або стану, зв'язаного з ростом, поділом та/або проліферацією клітин, наприклад, для лікування злоякісних пухлин в особини, яка цього потребує Як показання до застосування, можуть бути згадані, наприклад, лікування раку яєчника, шлунка, ободової кишки, передміхурової залози, молочної залози, легені, Компоненти Похідне епотилону* 2-Гідроксипропіл-3-циклодекстрин Маніт Трометамол Соляна кислота Усього Ліофілізат (мг) 10,500 2100,000 210,000 12,705 3,267 2336,472 Для способу дивися, будь ласка, приклад 3. Продукт, висушений виморожуванням (ліофілізат), відновлювали шляхом додавання 8,8мл води для ін'єкцій. 36 голови й шиї, злоякісної меланоми, гострого лімфоцитарного, мієлоцитного лейкозу, метастаз у кістках і пухлин головного мозку. Композиції за винаходом також придатні для лікування хронічних запальних захворювань, таких як, наприклад, псоріаз або артрит. Отже, композиції можуть застосовуватися для приготування лікарського засобу для лікування вищеописаних захворювань. В іншому варіанті здійснення, винахід стосується способу лікування захворювання або стану, зв'язаного з ростом, поділом та/або проліферацією клітин у пацієнтів, який передбачає введення пацієнтові терапевтично ефективної однієї або декількох сполук формули І із застосуванням композицій згідно із даним винаходом, де вказані композиції вводять шляхом внутрішньовенної інфузії протягом періоду часу близько 30 хвилин у дозі в діапазоні від 10мг/м2 до 35мг/м2, переважно від 16мг/м2 до 29мг/м2, найбільш переважно 22мг/м2. Способи згідно із даним винаходом також охоплюють схеми дозування, такі як введення композицій пацієнтові один раз кожні З тижні або щотижня протягом 3 тижнів з наступним семиденним періодом відновлення або відпочинку. Композиції вводять до настання прогресування захворювання або до прояву неприйнятних токсичностей (тобто що дозообмежувальних токсичностей). В подальшому варіанті здійснення винаходу, забезпечуються композиції, які при парентеральному введенні, такому як внутрішньовенна інфузія, забезпечують максимально переносиму дозу (MTD), таку як близько 10мг/м2, переважно приблизно 16мг/м2, більш переважно приблизно 22мг/м2. MTD епотилону, що вводиться у вигляді відновленої композиції згідно із даним винаходом, можна спостерігати в стандартних тестах на тваринах і в клінічних дослідженнях. Приклади Незважаючи на те, що в наведених прикладах використовували конкретне похідне епотилону, позначене як епотилон*, винахід не слід розглядати як обмежений тільки цим похідним епотилону, і він може охоплювати багато інших похідних епотилону, як визначено вище. Приклад 1 Композиція, яка містить гідроксипропіл-βциклодекстрин і похідне епотилону*: (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-3-(2метил-бензотіазол-5-іл)-10-(проп-2-ен-1-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон. Ліофілізат (%) 0,449 89,879 8,988 0,544 0,140 Відновлена композиція (мг/мл) 1,000 200,000 20,000 1,210 0,311 37 88182 Приклад 2 Композиція, яка містить простий сульфобутиловий ефір β-циклодекстрину й похідне епотилону*: (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідроксиКомпоненти Епотилон* Простий сульфобутиловий ефір β-циклодекстрину Трометамол Соляна кислота 38 3-(2-метил-бензотіазол-5-іл)-10-(проп-2-ен-1-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон. Кількість у ліофілізованій масі мг 5,500 Концентрація після відновлення мг/мл 1,000 1,100,000 200,000 6,655 до рН7,4 (у розчині) 1,210 до рН7,4 На першій стадії одержання епотилон* розчиняли в 96% етанолі. На другій стадії одержання простий сульфобутиловий ефір β-циклодекстрину розчиняли у воді для ін'єкцій. Після цього до розчину циклодекстрину додавали трометамол. Значення рН отриманого розчину простого сульфобутилового ефіру β-циклодекстрину доводили до рН7,4 шляхом додавання розведеної соляної кислоти. Потім розчин епотилону й розчин циклодекстрину об'єднували й сушили виморожуванням при наступних умовах: заморожування до -45°С під тиском 1013ммбар аж до 24 годин, переважно протягом 5 годин, первинна стадія сушіння до 15°С під тиском 8,9´10-2ммбар протягом 60 годин, переважно протягом 48 годин, первинна стадія Компоненти Розчин мг/мл Епотилон* Простий сульфобутиловий ефір β-циклодекстрину Вода для ін'єкцій 3,0 сушіння при 25°С під тиском 8,9´10-2ммбар протягом 2 годин, переважно в плин 1 години й вторинна стадія сушіння при 25°С під тиском 6,5´103 ммбар протягом 10 годин, переважно протягом 6 годин, використовуючи установку для сушіння Fa. Hof, тип СОМО590. Приклад 2А Композиція, яка містить простий сульфобутиловий ефір β-циклодекстрину й похідне епотилону*: (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси3-(2-метил-бензотіазол-5-іл)-10-(проп-2-ен-1-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон. Молярне відношення DS/CD Масове відношення DS/CD (моль) (мг) 1 1 100,000 8,39 100 до 1мл На першій стадії одержання похідне епотилону* розчиняли в органічному розчиннику й після цього розчинник упарювали. На другій стадії одержання простий сульфобутиловий ефір βциклодекстрину розчиняли у воді для ін'єкцій. На третій стадії одержання порошок епотилону*, отриманий на першій стадії одержання, розчиняли у водному розчині, отриманому на другій стадії одержання. Загальний час перемішування для цього процесу становив 2 дні. Приклад 2В Композиція, яка містить простий сульфобутиловий ефір β-циклодекстрину й похідне епотилону*: (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси3-(2-метил-бензотіазол-6-іл)-10-(проп-2-ен-1-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон 2,6 Молярне відношення DS/CD (моль) 1 Масове відношення DS/CD (мг) 1 100,000 9,68 38,46 Компоненти Розчин мг/мл Епотилон* Простий сульфобутиловий ефір β-циклодекстрину Вода для ін'єкцій до 1мл На першій стадії одержання похідне епотилону* розчиняли в органічному розчиннику й після цього розчинник упарювали. На другій стадії одержання простий сульфобутиловий ефір βциклодекстрину розчиняли у воді для ін'єкцій. На третій стадії одержання порошок епотилону*, отриманий на першій стадії одержання, розчиняли у водному розчині, отриманому на другій стадії одержання. Загальний час перемішування для цього процесу становив 3 години. Приклад 2С Композиція, яка містить простий сульфобутиловий ефір β-циклодекстрину й похідне епотилону*: (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси3-(2-метил-бензотіазол-5-іл)-10-(проп-2-ен-1-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон. 39 88182 40 1,000 Молярне відношення DS/CD (моль) 1 Масове відношення DS/CD (мг) 1 100,000 25,17 100,00 Компоненти Розчин (мг/мл) Похідне епотилону* Простий сульфобутиловий ефір β-циклодекстрину Трометамол Соляна кислота Етанол 96% Вода для ін'єкцій 1,210 до рН7,4 12,15 до 1мл На першій стадії одержання епотилон* розчиняли в 96% етанолі На другій стадії одержання простий сульфобутиловий ефір β-циклодекстрину розчиняли у воді для ін'єкцій. Після цього до розчину циклодекстрину додавали трометамол. Значення рН отриманого розчину простого сульфобутилового ефіру β-циклодекстрину й трометамолу встановлювали рівним 7,4 шляхом додавання розведеної соляної кислоти. Після цього розчин епотилону й розчин циклодекстрину об'єднували. Загальний час перемішування для цього процесу приготування становило 2 години. Органічний розчинник, що переважно використовується для розчинення похідного епотилону в 2А і 2В, являє собою метиленхлорид або 96% етанол. Приклад 3 Процес приготування для "вихідного розчину", з якого одержували ліофілізат. Компоненти Епотилон* Гідроксипропіл-3-циклодекстрин Маніт Трометамол Соляна кислота Етанол 96% - технологічна добавка Вода для ін'єкцій - технологічна добавка Кількість у г 14,250 2850,000 285,000 17,243 44,336 173,850 11862,822 *(1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси3-(2-метил-бензотіазол-5-іл)-10-(проп-2-ен-1-іл)8,8,12,16-тетраметил-4,17-діоксабіцикло[14 1.0]гептадекан-5,9-діон. На першій стадії одержання епотилон* розчиняли в 96% етанолі. На другій стадії одержання гідроксипропіл-β-циклодекстрин розчиняли у воді для ін'єкцій. Після цього до розчину циклодекстрину додавали трометамол, і потім маніт. Значення рН отриманого розчину гідроксипропіл-βциклодекстрину, трометамолу й маніту встановлювали рівним рН7,4 шляхом додавання розведеної соляної кислоти. Після цього розчин епотилону й розчин циклодекстрину об'єднували й сушили виморожуванням у наступних умовах: Заморожування до -45°С під тиском 1013ммбар аж до годин, переважно протягом 5 годин, перша стадія основного сушіння до 15°С під тиском 8,9´10-2ммбар протягом 60 годин, переважно протягом 48 годин, друга стадія основного сушіння при 25°С під тиском 8,9´10-2ммбар протягом 2 годин, переважно протягом 1 години й стадія після сушіння при 25°С під тиском 6,5´10-3ммбар протягом 10 годин, переважно протягом 6 годин, використовуючи установку для сушіння Fa. Hof, тип СОМ 0590. Для одержання твердої композиції, як показано в прикладі 1. Приклад 4 Дані стабільності епотилону* (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-3-(2метил-бензотіазол-5-іл)-10-(проп-2-ен-1-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон) у водних розчинах, що містять гідроксипропіл-бетациклодекстрин. Препарати після сушіння виморожуванням, як показано в прикладі 1, відновлювали за допомогою води для ін'єкцій і після цього значення рН установлювали в інтервалі від 6,1 до 13,6 за допомогою НСІ або NaOH. Розчини залишали при кімнатній температурі або 40°С і здійснювали дослідження й визначали чистоту в вказаних інтервалах за допомогою ВЕРХ. Коефіцієнт швидкості розкладання (K) епотилону* знижувався при наближенні значень рН до нейтрального рН. Швидкість розкладання була мінімальною при рН7. РН 9 8,0 7,5 6,9 6,3 6,1 К при кімнатній температурі 4,5 10-3год-1 1,1 10-3год-1 0,7 10-3год-1 0,1 10-3год-1 0,5 10-3год-1 0,8 10-3год-1 К (40) 4,9 10-3год-1 1,2 10-3год-1 1,7 10-3год-1 Приклад 5 Визначення уявної рівноваги константи стабільності комплексу між епотилоном* (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-3-(2метилбензотіазол-5-іл)-10-(проп-2-ен-1-іл)8,8,12,16-тетраметил-4,17-діоксабіцикло[14.1 0]гептадекан-5,9-діон) і гідроксипропіл-бетациклодекстрином у водному розчині. Діаграмну методику фази розчинності (PSD) застосовували при 25°С і константа стабільності передбачуваного комплексу 1:1 дорівнювала K'=484,5М-1. Розчинність епотилону* дорівнювала So=4,3 10-5моль/л (0,023г/л). Значення K' дозволяло припустити, що якщо все-таки комплекс і утворювався, то він не був достатньо стабільним. 41 88182 Приклад 6 Стабільність ліофілізату й відновленого ліофілізату, що містить епотилон*, при різних умовах зберігання: Стабільність ліофілізату Див. Фіг.1 і 2 Фіг.1 Дослідження ліофілізату епотилону при різних умовах зберігання Ліофілізат відповідно до прикладу 1 зберігали при 6°С і 25°С відповідно. Встановлено, що ліофіпочаток фільтрований 6год. фільтрований 24год. фільтрований Вміст епотилону* [мг/мл] 0,99 1,02 1,01 1,01 1,01 1,00 рН 7,41 42 лізат є стабільним протягом 18 місяців при постійному вмісті епотилону. Фіг.2 Сума домішок при різних умовах зберігання Сума домішок, оскільки вони можуть підвищуватися, якщо сполука є нестабільною, показана для умов зберігання 6°С і 25°С. При обох температурах кількість домішок залишалася нижче 1% і була постійною протягом усього періоду часу. Стабільність відновленого ліофілізату Осмолярність [ммоль/кг] 355 350 7,42 Стабільність відновленого ліофілізату гарантується принаймні протягом одного дня. Цей період часу є максимально необхідним для лікарів для приготування й введення композиції пацієнтові. Приклад 7 Введення епотилону* з використанням композиції із прикладу 1 відповідно до винаходу Пацієнти й методи: Пацієнти з гістологічно підтвердженими прогресуючими солідними пухлинами, які були резистентними або несприйнятливими до загальноприйнятого протипухлинного лікування, є придатними для дослідження. Вони одержували лікування епотилоном* у вигляді 30 хвилинних внутрішньовенних інфузій з 3-х тижневими інтервалами. Лікування продовжували до настання прогресування захворювання або до прояву неприйнятних токсичностей. Початкова доза становила 0,6мг/м2. Дози підвищували відповідно до модифікованої схеми Фібоначчі. Результати: 47 пацієнтів одержували 12 різних дозових рівнів аж до 29мг/м2. Спостережувана дозолімітуюча токсичність (DLT) характеризувалась СТС ступінь З пеКомпоненти Розчин мг/мл Похідне епотилону* 2-Гідроксипропіл-β-циклодекстрин Вода для ін'єкцій 1 200,000 до 1мл На першій стадії одержання гідроксипропіл-βциклодекстрин розчиняли у воді для ін'єкцій. На другій стадії одержання до вказаного розчину додавали кристалічний епотилон* при перемішуванні. Епотилон повністю не розчинявся після перемішування протягом 5 годин, і навіть після перемішування протягом 10 годин. Цільова концентрація >1мг/мл досягалася тільки після перемішування протягом 20 годин. Значення рН отриманого розчину епотилону* і гідроксипропіл-3 351 Колір ³Y7 1,0746 7,41 Густина [г/мл] 1,0745 ³Υ7 1,0750 ³Υ7 риферична невропатія при 16мг/м2 і СТС ступінь 4 атаксія при 29мг/м2. Інших проявів DLT не спостерігали. Гематологічна токсичність максимальної СТС ступінь 2 була рідкою. Найбільш загальною побічною дією була периферична сенсорна невропатія, головним чином 1-2 ступеня. Випадків негематологічної токсичності 3-4 ступеня не було виявлено, за винятком вищезгаданих DLT. Отримані результати свідчать про протипухлинну активність (включаючи об'єктивну реакцію-відповідь) у пацієнтів з раком молочної залози, NSCLC, холангіокарциномою, увеальною меланомою й раком голови й шиї, і яким епотилон* може вводитися кожні 3 тижні в дозах аж до 29мг/м2 без прояву важкої токсичності. Приклад 8 Композиція, яка містить гідроксипропіл-βциклодекстрин і похідне епотилону*: (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-3-(2метил-бензотіазол-5-іл)-10-(проп-2-ен-1-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон. Молярне відношення DS/CD 1 77,3 Масове відношення DS/CD 1 200 циклодекстрину встановлювали рівним 7,4 шляхом додавання розведеної соляної кислоти. Приклад 9 Композиція, яка містить гідроксипропіл-βциклодекстрин і похідне епотилону*: (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-3-(2метил-бензотіазол-5-іл)-10-(проп-2-ен-1-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон. 43 Компоненти Похідне епотилону* 2-Гідроксипропіл-β-циклодекстрин Маніт Трометамол Соляна кислота Етанол 96% Вода для ін'єкцій Усього 88182 Розчин (мг/мл) Розчин (%) 1,000 200,000 20,000 1,210 0,311 12,200 835,279 1070,000 На першій стадії одержання кристалічний епотилон* розчиняли в 96% етанолі. На другій стадії одержання гідроксипропіл-β-циклодекстрин розчиняли у воді для ін'єкцій. Після цього до розчину циклодекстрину додавали трометамол, і потім маніт. Значення рН отриманого розчину гідроксипропіл-β-циклодекстрину, трометамолу й маніту встановлювали рівним рН7,4 шляхом додавання розведеної соляної кислоти. Після цього розчин епотилону й розчин циклодекстрину об'єднували. Загальний час перемішування для цього процесу Компоненти Похідне епотилону* 2-Гідроксипропіл-β-циклодекстрин Маніт Трометамол Соляна кислота Вода для ін'єкцій Розчин (мг/мл) 7,000 200,000 20,000 1,210 до рН7,4 до 1мл 0,093% 18,691% 1,869% 0,113% 0,029% 1,140% 78,063% 44 Молярне відношення Масове відношення DS/CD (моль) DS/CD (мг) 1 77,73 1 200 приготування становив 2 години. На завершення розчин сушили виморожуванням для одержання твердої композиції, як показано в прикладі 1. Приклад 10 Композиція, яка містить гідроксипропіл-βциклодекстрин і похідне епотилону*: (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-3-(2метил-бензотіазол-5-іл)-10-(проп-2-ен-1-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон. Розчин* (%) 0,654% 18,672% 1,867% 0,113% Молярне відношення Масове відношення DS/CD (моль) DS/CD (мг) 1 1 11,10 28,57 * Густина=1,0711г/мл На першій стадії одержання похідне епотилону* розчиняли в органічному розчиннику, такому як метиленхлорид, і після цього розчинник упарювали На другій стадії одержання гідроксипропіл-рциклодекстрин розчиняли у воді для ін'єкцій. Після цього до розчину циклодекстрину додавали трометамол, і потім маніт. На третій стадії одержання порошок епотилону*, отриманий на першій стадії одержання, розчиняли у водному розчині, отриманому на другій стадії одержання. Значення рН отриманого розчину епотилону*, гідроксипропіл-рКомпоненти Похідне епотилону* 2-Гідроксипропіл-β-циклодекстрин Маніт Трометамол Соляна кислота Вода для ін'єкцій циклодекстрину, трометамолу й маніту встановлювали рівним рН 7,4 шляхом додавання розведеної соляної кислоти. Загальний час перемішування для цього процесу становив 2 години. Приклад 11 Композиція, яка містить гідроксипропіл-3циклодекстрин і похідне епотилону*: (1S,3S,7S,10R,11S,12S,16R)-7,11-дигідрокси-3-(2метил-бензотіазол-5-іл)-10-(проп-2-ен-1-іл)8,8,12,16-тетраметил-4,17діоксабіцикло[14.1.0]гептадекан-5,9-діон. Розчин (мг/мл) Розчин* (%) 1,000 50,00 43,000 1,210 до рН7,4 до 1мл 0,097% 4,854% 4,175% 0,117% Молярне відношення Масове відношення DS/CD (моль) DS/CD (мг) 1 1 19,43 50 * Густина: 1,030г/мл На першій стадії одержання похідне епотилону* розчиняли в органічному розчиннику й після цього розчинник упарювали. На другій стадії оде ржання гідроксипропіл-β-циклодекстрин розчиняли у воді для ін'єкцій. Після цього до розчину циклодекстрину додавали трометамол, і потім маніт. На 45 88182 третій стадії одержання порошок епотилону*, отриманий на першій стадії одержання, розчиняли у водному розчині. Значення рН отриманого розчину епотилону*, гідроксипропіл-р-циклодекстрину, Комп’ютерна верстка Т. Чепелева 46 трометамолу й маніту встановлювали рівним 7,4 шляхом додавання розведеної соляної кислоти. Загальний час перемішування для цього процесу становив 2 години. Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюCompositions comprising an epothilone and production methods
Автори англійськоюReer Olaf, Renz Matthias, Sachse Andreas, Sprenger Claudia, Thomsen Jens, Uffrecht Anka
Назва патенту російськоюКомпозиция, которая содержит эпотилон (варианты), и способ ее получения (варианты)
Автори російськоюРеер Олаф, Ренц Маттиас, Захсе Андреас, Шпренгер Клаудиа, Томсен Йенс, Уффрехт Анка
МПК / Мітки
МПК: A61K 47/40, A61P 43/00, A61P 35/00, A61K 31/429, A61K 9/00
Мітки: одержання, варіанти, епотилон, спосіб, яка, містить, композиція
Код посилання
<a href="https://ua.patents.su/23-88182-kompoziciya-yaka-mistit-epotilon-varianti-i-sposib-oderzhannya-varianti.html" target="_blank" rel="follow" title="База патентів України">Композиція, яка містить епотилон (варіанти), і спосіб її одержання (варіанти)</a>
Попередній патент: Спосіб та пристрій для одержання 1,2-дихлоретану
Наступний патент: Спосіб визначення теплотехнічних показників і фактичних характеристик відцентрових нагнітачів газотранспортної системи
Випадковий патент: Протимікробна композиція












