6-заміщені 2-хінолінони та 2-хіноксалінони як інгібітори полі(адф-рибоза)полімерази
Номер патенту: 89618
Опубліковано: 25.02.2010
Автори: Мабір Домінік Жан-Пьер, Воутерс Валтер Боудевіджн Леопольд, Сомерс Марія Вікторіна Франціска, ван Дун Якобу Алфонсус Джосепхус, Жільмон Жером Еміль Жорж
Формула / Реферат
1. Сполуки формули (І)
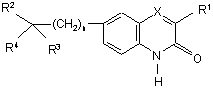 (I)
(I)
та їх N-оксидні форми, фармацевтично прийнятні адитивні солі та стереохімічно ізомерні форми, у яких
n дорівнює 0, 1 або 2;
X означає N або CR5, де R5 означає водень або, узятий разом з R1, може утворювати двовалентний радикал формули -СН=СН-СН=СН-;
R1 означає С1-4-алкіл або тієніл;
R2 означає водень чи гідроксигрупу або, узятий разом з R3 чи R4, може утворювати =O;
R3 означає радикал, вибраний з
-(CH2)s-NR6R7, (а-1)
-O-Н, (а-2)
-O-R8, (а-3)
-S-R9 (а-4) або
-C![]() N, (а-5)
N, (а-5)
де
s дорівнює 0, 1, 2 або 3;
R6 означає -СНO, С1-6-алкіл, гідроксі-С1-6-алкіл, С1-6-алкілкарбоніл, ді(С1-6-алкіл)аміно-С1-6-алкіл, С1-6-алкілоксі-С1-6-алкіл, С1-6-алкілкарбоніламіно-С1-6-алкіл, піперидиніл-С1-6-алкіламінокарбоніл, піперидиніл, піперидиніл-С1-6-алкіл, піперидиніл-С1-6-алкіламінокарбоніл, С1-6-алкілоксигрупу, тієніл-С1-6-алкіл, піроліл-С1-6алкіл, арил-С1-6-алкілпіперидиніл, арилкарбоніл-С1-6-алкіл, арилкарбонілпіперидиніл-С1-6-алкіл, галогеноіндазолілпіперидиніл-С1-6-алкіл або арил-С1-6-алкіл(С1-6-алкіл)аміно-С1-6-алкіл;
R7 означає водень або С1-6-алкіл;
R8 означає С1-6-алкіл, С1-6-алкілкарбоніл або ді(С1-6-алкіл)аміно-С1-6-алкіл; і
R9 означає ді(С1-6-алкіл)аміно-С1-6-алкіл;
або R3 означає групу формули
-Z-, (b-1)
у якій
Z означає гетероциклічну кільцеву систему, вибрану з
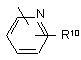 , (c-1)
, (c-1)
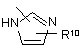 , (c-2)
, (c-2)
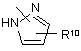 , (c-3)
, (c-3)
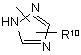 , (c-4)
, (c-4)
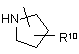 , (c-6)
, (c-6)
де кожен R10 незалежно один від одного означає водень, С1-6-алкіл, амінокарбоніл, гідроксигрупу, групи формули
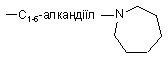 ,
,
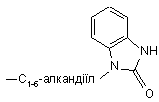 ,
,
С1-6-алкілоксі-С1-6-алкіл, С1-6-алкілоксі-С1-6-алкіламіногрупу, арил-С1-6-алкіл, ді(С2-6-алкеніл), піперидиніл-С1-6-алкіл, С3-10-циклоалкіл, С3-10-циклоалкіл-С1-6-алкіл, арилокси(гідроксі)-С1-6-алкіл, галогеноіндазоліл, арил-С1-6-алкіл, арил-С2-6-алкеніл, морфоліногрупу, С1-6-алкілімідазоліл або піридиніл-С1-6-алкіламіногрупу;
R4 означає водень, С1-6-алкіл, фураніл, піридиніл, арил-С1-6-алкіл або групу формули ![]() ;
;
арил означає феніл або феніл, заміщений галогеном, С1-6-алкілом чи С1-6-алкілоксигрупою;
за умови, якщо
n дорівнює 0, X означає N, R2 означає водень, R3 означає групу формули (b-1), Z означає гетероциклічну кільцеву систему (с-2) або (с-4), і зазначена гетероциклічна кільцева система Z приєднана до залишку молекули атомом нітрогену і R10 означає водень, то R4 не є водень, С1-6-алкіл або піридиніл,
за виключенням сполук, які мають наступні структурні формули:
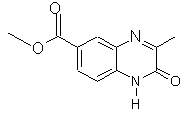 ,
,
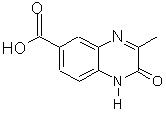 ,
,
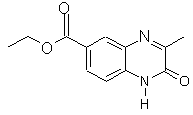 ,
,
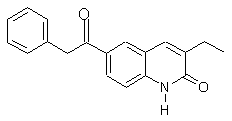 ,
,
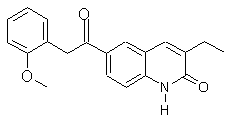 ,
,
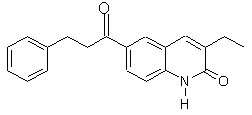 .
.
2. Сполука за п. 1, у якій
n дорівнює 0 чи 1;
X означає N або CR5, де R5 означає водень;
R3 означає радикал, вибраний з (а-1), (а-2) чи (а-3) або групу формули (b-1), тобто -Z-;
s дорівнює 0, 1 чи 2;
R6 означає -СНО, С1-6-алкіл, піперидиніл-С1-6-алкіл, арилкарбонілпіперидиніл-С1-6-алкіл або арил-С1-6-алкіл-(С1-6-алкіл)аміно-С1-6-алкіл;
R8 означає С1-6-алкіл;
якщо R3 означає групу формули (b-1), то Z означає гетероциклічну кільцеву систему, вибрану з (с-2) або (с-4); і
кожен R10 незалежно один від одного означає водень, С1-6-алкіл або С1-6-алкілоксі-С1-6-алкіламіногрупу.
3. Сполука за будь-яким з пп. 1 або 2, у якій
n дорівнює 0; X означає N або CR5, де R5 означає водень; R1 означає С1-6-алкіл; R2 означає водень чи гідроксигрупу або, узятий разом з R4, може утворювати =O; R3 означає радикал, вибраний з (а-1) або (а-2); s дорівнює 0 чи 1; R6 означає -СНО або С1-6-алкіл; і R4 означає водень, С1-6-алкіл або групу формули ![]() .
.
4. Сполука за будь-яким з пп. 1, 2 або 3, у якій сполуку вибрано зі сполуки № 1, сполуки № 5, сполуки № 7, сполуки № 3 та сполуки № 17
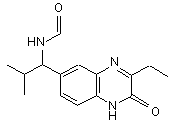 сполука 1
сполука 1
 сполука 5
сполука 5
 сполука 7
сполука 7
 сполука 3
сполука 3
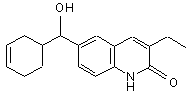 сполука 17
сполука 17
5. Сполука, вказана в будь-якому з пп. 1-4, призначена як лікарський препарат.
6. Фармацевтична композиція, що містить фармацевтично прийнятні носії та, як активний інгредієнт, терапевтично ефективну кількість сполуки за будь-яким з пп. 1-4.
7. Спосіб одержання фармацевтичної композиції за п. 6, при якому ретельно змішують фармацевтично прийнятні носії та сполуки за будь-яким з пп. 1-4.
8. Застосування сполуки для одержання лікарського препарату для хіміосенсибілізації або радіосенсибілізації, в якому зазначена сполука є сполукою формули (І)
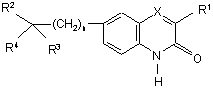 , (I)
, (I)
її N-оксидними формами, фармацевтично прийнятними адитивними солями та стереохімічно ізомерними формами, де
n дорівнює 0, 1 або 2;
X означає N або CR5, де R5 означає водень або, узятий разом з R1, може утворювати двовалентний радикал формули -СН=СН-СН=СН-;
R1 означає С1-6-алкіл або тієніл;
R2 означає водень чи гідроксигрупу або, узятий разом з R3 або R4, може утворювати =O;
R3 означає радикал, вибраний з
-(CH2)s-NR6R7, (a-1)
-O-H, (a-2)
-O-R8, (a-3)
-S-R9 (a-4) або
-CºN, (a-5)
де
s дорівнює 0, 1, 2 або 3;
R6 означає -СНО, С1-6-алкіл, гідроксі-С1-6-алкіл, С1-6-алкілкарбоніл, ді(С1-6-алкіл)аміно-С1-6-алкіл, С1-6-алкілоксі-С1-6-алкіл, С1-6-алкілкарбоніламіно-С1-6-алкіл, піперидиніл-С1-6-алкіламінокарбоніл, піперидиніл, піперидиніл-С1-6-алкіл, піперидиніл-С1-6-алкіламінокарбоніл, С1-6-алкілоксигрупу, тієніл-С1-6-алкіл, піроліл-С1-6-алкіл, арил-С1-6-алкілпіперидиніл, арилкарбоніл-С1-6-алкіл, арилкарбонілпіперидиніл-С1-6-алкіл, галогеноіндазолілпіперидиніл-С1-6-алкіл або арил-С1-6-алкіл(С1-6-алкіл)аміно-С1-6-алкіл;
R7 означає водень або С1-6-алкіл;
R8 означає С1-6-алкіл, С1-6-алкілкарбоніл або ді(С1-6-алкіл)аміно-С1-6-алкіл; і
R9 означає ді(С1-6-алкіл)аміно-С1-6-алкіл;
або R3 означає групу формули
-Z-, (b-1)
у якій
Z означає гетероциклічну кільцеву систему, вибрану з
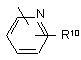 , (c-1)
, (c-1)
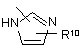 , (c-2)
, (c-2)
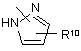 , (c-3)
, (c-3)
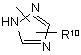 , (c-4)
, (c-4)
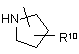 , (c-6)
, (c-6)
де кожен R10 незалежно один від одного означає водень, С1-6-алкіл, амінокарбоніл, гідроксигрупу, групи формули
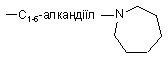 ,
,
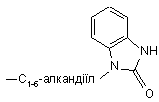 ,
,
С1-6-алкілоксі-С1-6-алкіл, С1-6-алкілоксі-С1-6-алкіламіногрупу, арил-С1-6-алкіл, ді(С2-6-алкеніл), піперидиніл-С1-6-алкіл, С3-10-циклоалкіл, С3-10-циклоалкіл-С1-6-алкіл, арилокси(гідроксі)-С1-6-алкіл, галогеноіндазоліл, арил-С1-6-алкіл, арил-С2-6-алкеніл, морфоліногрупу, С1-6-алкілімідазоліл або піридиніл-С1-6-алкіламіногрупу;
R4 означає водень, С1-6-алкіл, фураніл, піридиніл, арил-С1-6-алкіл або групу формули ![]() ;
;
арил означає феніл або феніл, заміщений галогеном, С1-6-алкілом чи С1-6-алкілоксигрупою.
9. Застосування за п. 8, в якому лікарський препарат є лікарським препаратом для хіміосенсибілізації.
10. Застосування за п. 8, в якому лікарський препарат є лікарським препаратом для радіосенсибілізації.
11. Комбінація сполуки з хіміотерапевтичним агентом, де зазначена сполука є сполукою формули (І)
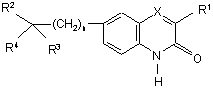 , (I)
, (I)
її N-оксидними формами, фармацевтично прийнятними адитивними солями та стереохімічно ізомерними формами, де
n дорівнює 0, 1 або 2;
X означає N або CR5, де R5 означає водень або, узятий разом з R1, може утворювати двовалентний радикал -СН=СН-СН=СН-;
R1 означає С1-6-алкіл або тієніл;
R2 означає водень чи гідроксигрупу або, узятий разом з R3 або R4, може утворювати =O;
R3 означає радикал, вибраний з
-(CH2)s-NR6R7, (а-1)
-О-Н, (а-2)
-O-R8, (а-3)
-S-R9 (а-4) або
-C=N, (а-5)
де
s дорівнює 0, 1, 2 або 3;
R6 означає -СНО, С1-6-алкіл, гідроксі-С1-6-алкіл, С1-6-алкілкарбоніл, ді(С1-6-алкіл)аміно-С1-6-алкіл, С1-6-алкілоксі-С1-6-алкіл, С1-6-алкілкарбоніламіно-С1-6-алкіл, піперидиніл-С1-6-алкіламінокарбоніл, піперидиніл, піперидиніл-С1-6-алкіл, піперидиніл-С1-6-алкіламінокарбоніл, С1-6-алкілоксигрупу, тієніл-С1-6-алкіл, піроліл-С1-6-алкіл, арил-С1-6-аліалпіперидиніл, арилкарбоніл-С1-6-алкіл, арилкарбонілпіперидиніл-С1-6-алкіл, галогеноіндазолілпіперидиніл-С1-6-алкіл або арил-С1-6-алкіл(С1-6-алкіл)аміно-С1-6-алкіл;
R7 означає водень або С1-6-алкіл;
R8 означає С1-6-алкіл, С1-6-алкілкарбоніл або ді(С1-6-алкіл)аміно-С1-6-алкіл; і
R9 означає ді(С1-6-алкіл)аміно-С1-6-алкіл;
або R3 означає групу формули
-Z-, (b-1)
у якій
Z означає гетероциклічну кільцеву систему, вибрану з
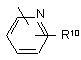 , (c-1)
, (c-1)
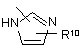 , (c-2)
, (c-2)
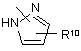 , (c-3)
, (c-3)
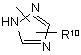 , (c-4)
, (c-4)
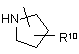 , (c-6)
, (c-6)
де кожен R10 незалежно один від одного означає водень, С1-6-алкіл, амінокарбоніл, гідроксигрупу, групи формули
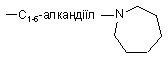 ,
,
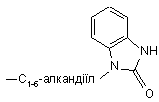 ,
,
С1-6-алкілоксі-С1-6-алкіл, С1-6-алкілоксі-С1-6-алкіламіногрупу, арил-С1-6-алкіл, ді(С2-6-алкеніл), піперидиніл-С1-6-алкіл, С3-10-циклоалкіл, С3-10-циклоалкіл-С1-6-алкіл, арилокси(гідроксі)-С1-6-алкіл, галогеноіндазоліл, арил-С1-6-алкіл, арил-С2-6-алкеніл, морфоліногрупу, С1-6-алкілімідазоліл або піридиніл-С1-6-алкіламіногрупу;
R4 означає водень, С1-6-алкіл, фураніл, піридиніл, арил-С1-6-алкіл або групу формули ![]() ;
;
арил означає феніл або феніл, заміщений галогеном, С1-6-алкілом чи С1-6-алкілоксигрупою, і
де зазначений хіміотерапевтичний засіб вибраний з групи, що включає 5-фторурацил, лейковорин, 5'-аміно-5'-дезокситимідин, кисень, карбоген, перфторкарбон (наприклад, Fluosol 10 DA), 2,3-DPG, BW12C, блокатор кальцієвих каналів, пентоксифілін, сполуку, що пригнічує ріст судин, гідралазин, LBSO, адріаміцин, камтотецин, карбоплатин, цисплатин, даунорубіцин, доцетаксел, доксорубіцин, інтерферон (альфа, бета, гамма), інтерлейкін-2, іринотекан, паклітаксел, топотекан та їхні похідні, метилувальний засіб, інгібітор топоізомерази І, блеоміцин.
12. Спосіб одержання сполуки за п. 1, при якому здійснюють гідроліз проміжних продуктів формули (VIII) відомими способами шляхом обробки проміжних продуктів формули (VIII) відповідними реагентами, такими як хлорид олова, оцтова кислота та соляна кислота, в присутності інертного розчинника, наприклад, тетрагідрофурану;
 ,
,
де R1, R2, R3, R4, X, n є такими, як визначено в п. 1.
13. Спосіб одержання сполуки за п. 1, при якому здійснюють конденсацію відповідного орто-бензолдіаміну формули (XI) зі складним ефіром формули (XII), в якому Rh означає С1-6-алкіл, з утворенням сполук формули (І), у яких X означає N, позначених як сполуки формули (I-і), в присутності карбонової кислоти, наприклад, оцтової кислоти та подібної, мінеральної кислоти, такої як, наприклад, соляна кислота, сірчана кислота, або сульфокислоти, такої як, наприклад, метансульфокислота, бензолсульфокислота, 4-метилбензолсульфокислота та подібні,
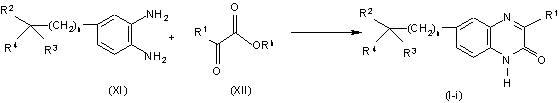 ,
,
де R1, R2, R3, R4, n є такими, як визначено в п. 1.
Текст
1. Сполуки формули (І) R2 R1 X (CH2)n R4 ІНГІБІТОРИ 3 89618 4 O HN R10 N O , (c-6) 10 де кожен R незалежно один від одного означає водень, С1-6-алкіл, амінокарбоніл, гідроксигрупу, групи формули N , O N C1-6-алкандіїл O H , N O H NH N C1-6-алкандіїл O , С1-6-алкілоксі-С1-6-алкіл, С1-6-алкілоксі-С1-6алкіламіногрупу, арил-С1-6-алкіл, ді(С2-6-алкеніл), піперидиніл-С1-6-алкіл, С3-10-циклоалкіл, С3-10циклоалкіл-С1-6-алкіл, арилокси(гідроксі)-С1-6-алкіл, галогеноіндазоліл, арил-С1-6-алкіл, арил-С2-6алкеніл, морфоліногрупу, С1-6-алкілімідазоліл або піридиніл-С1-6-алкіламіногрупу; R4 означає водень, С1-6-алкіл, фураніл, піридиніл, арил-С1-6-алкіл або групу формули ; арил означає феніл або феніл, заміщений галогеном, С1-6-алкілом чи С1-6-алкілоксигрупою; за умови, якщо n дорівнює 0, X означає N, R2 означає водень, R3 означає групу формули (b-1), Z означає гетероциклічну кільцеву систему (с-2) або (с-4), і зазначена гетероциклічна кільцева система Z приєднана до залишку молекули атомом нітрогену і R10 означає 4 водень, то R не є водень, С1-6-алкіл або піридиніл, за виключенням сполук, які мають наступні структурні формули: O O N N O H , O HO , O O N O H , O N O H . 2. Сполука за п. 1, у якій n дорівнює 0 чи 1; X означає N або CR5, де R5 означає водень; 3 R означає радикал, вибраний з (а-1), (а-2) чи (а-3) або групу формули (b-1), тобто -Z-; s дорівнює 0, 1 чи 2; R6 означає -СНО, С1-6-алкіл, піперидиніл-С1-6-алкіл, арилкарбонілпіперидиніл-С1-6-алкіл або арил-С1-6алкіл-(С1-6-алкіл)аміно-С1-6-алкіл; R8 означає С1-6-алкіл; якщо R3 означає групу формули (b-1), то Z означає гетероциклічну кільцеву систему, вибрану з (с-2) або (с-4); і кожен R10 незалежно один від одного означає водень, С1-6-алкіл або С1-6-алкілоксі-С1-6алкіламіногрупу. 3. Сполука за будь-яким з пп. 1 або 2, у якій n дорівнює 0; X означає N або CR5, де R5 означає 1 2 водень; R означає С1-6-алкіл; R означає водень 4 чи гідроксигрупу або, узятий разом з R , може 3 утворювати =O; R означає радикал, вибраний з (а-1) або (а-2); s дорівнює 0 чи 1; R6 означає -СНО або С1-6-алкіл; і R4 означає водень, С1-6-алкіл або N групу формули N H . O , 4. Сполука за будь-яким з пп. 1, 2 або 3, у якій сполуку вибрано зі сполуки № 1, сполуки № 5, сполуки № 7, сполуки № 3 та сполуки № 17 5 89618 6 O HN OH N N H O N H N N N H O сполука 7 OH N H 5. Сполука, вказана в будь-якому з пп. 1-4, призначена як лікарський препарат. 6. Фармацевтична композиція, що містить фармацевтично прийнятні носії та, як активний інгредієнт, терапевтично ефективну кількість сполуки за будь-яким з пп. 1-4. 7. Спосіб одержання фармацевтичної композиції за п. 6, при якому ретельно змішують фармацевтично прийнятні носії та сполуки за будь-яким з пп. 1-4. 8. Застосування сполуки для одержання лікарського препарату для хіміосенсибілізації або радіосенсибілізації, в якому зазначена сполука є сполукою формули (І) R2 R1 X (CH2)n R3 O сполука 5 O OH R4 O N H сполука 1 N O H , (I) її N-оксидними формами, фармацевтично прийнятними адитивними солями та стереохімічно ізомерними формами, де n дорівнює 0, 1 або 2; X означає N або CR5, де R5 означає водень або, узятий разом з R1, може утворювати двовалентний радикал формули -СН=СН-СН=СН-; 1 R означає С1-6-алкіл або тієніл; R2 означає водень чи гідроксигрупу або, узятий 3 4 разом з R або R , може утворювати =O; 3 R означає радикал, вибраний з -(CH2)s-NR6R7, (a-1) -O-H, (a-2) 8 -O-R , (a-3) 9 -S-R (a-4) або -C N, (a-5) де s дорівнює 0, 1, 2 або 3; O сполука 3 сполука 17 R6 означає -СНО, С1-6-алкіл, гідроксі-С1-6-алкіл, С16-алкілкарбоніл, ді(С1-6-алкіл)аміно-С1-6-алкіл, С1-6алкілоксі-С1-6-алкіл, С1-6-алкілкарбоніламіно-С1-6алкіл, піперидиніл-С1-6-алкіламінокарбоніл, піперидиніл, піперидиніл-С1-6-алкіл, піперидиніл-С1-6алкіламінокарбоніл, С1-6-алкілоксигрупу, тієніл-С1-6алкіл, піроліл-С1-6-алкіл, арил-С1-6алкілпіперидиніл, арилкарбоніл-С1-6-алкіл, арилкарбонілпіперидиніл-С1-6-алкіл, галогеноіндазолілпіперидиніл-С1-6-алкіл або арил-С1-6-алкіл(С1-6алкіл)аміно-С1-6-алкіл; R7 означає водень або С1-6-алкіл; R8 означає С1-6-алкіл, С1-6-алкілкарбоніл або ді(С16-алкіл)аміно-С1-6-алкіл; і R9 означає ді(С1-6-алкіл)аміно-С1-6-алкіл; 3 або R означає групу формули -Z-, (b-1) у якій Z означає гетероциклічну кільцеву систему, вибрану з N R10 , (c-1) N HN R10 , (c-2) N HN R10 , (c-3) N HN N R10 , (c-4) HN R10 , (c-6) 7 89618 8 10 де кожен R незалежно один від одного означає диніл, піперидиніл-С1-6-алкіл, піперидиніл-С1-6водень, С1-6-алкіл, амінокарбоніл, гідроксигрупу, алкіламінокарбоніл, С1-6-алкілоксигрупу, тієніл-С1-6групи формули алкіл, піроліл-С1-6-алкіл, арил-С1-6аліалпіперидиніл, арилкарбоніл-С1-6-алкіл, арилкаN C1-6-алкандіїл рбонілпіперидиніл-С1-6-алкіл, галогеноіндазолілпіперидиніл-С1-6-алкіл або арил-С1-6-алкіл(С1-6алкіл)аміно-С1-6-алкіл; , 7 R означає водень або С1-6-алкіл; 8 R означає С1-6-алкіл, С1-6-алкілкарбоніл або ді(С16-алкіл)аміно-С1-6-алкіл; і R9 означає ді(С1-6-алкіл)аміно-С1-6-алкіл; NH або R3 означає групу формули N -Z-, (b-1) C1-6-алкандіїл у якій O , Z означає гетероциклічну кільцеву систему, вибС1-6-алкілоксі-С1-6-алкіл, С1-6-алкілоксі-С1-6рану з алкіламіногрупу, арил-С1-6-алкіл, ді(С2-6-алкеніл), піперидиніл-С1-6-алкіл, С3-10-циклоалкіл, С3-10N циклоалкіл-С1-6-алкіл, арилокси(гідроксі)-С1-6-алкіл, R10 галогеноіндазоліл, арил-С1-6-алкіл, арил-С2-6, (c-1) алкеніл, морфоліногрупу, С1-6-алкілімідазоліл або піридиніл-С1-6-алкіламіногрупу; 4 N HN R означає водень, С1-6-алкіл, фураніл, піридиніл, R10 , (c-2) N арил-С1-6-алкіл або групу формули ; HN R10 арил означає феніл або феніл, заміщений галоге, (c-3) ном, С1-6-алкілом чи С1-6-алкілоксигрупою. N 9. Застосування за п. 8, в якому лікарський препаHN рат є лікарським препаратом для хіміосенсибілізаR10 N ції. , (c-4) 10. Застосування за п. 8, в якому лікарський препарат є лікарським препаратом для радіосенсибіHN лізації. R10 11. Комбінація сполуки з хіміотерапевтичним аген, (c-6) том, де зазначена сполука є сполукою формули (І) де кожен R10 незалежно один від одного означає R2 R1 X водень, С1-6-алкіл, амінокарбоніл, гідроксигрупу, (CH2)n групи формули R4 R3 N O H , (I) її N-оксидними формами, фармацевтично прийнятними адитивними солями та стереохімічно ізомерними формами, де n дорівнює 0, 1 або 2; 5 5 X означає N або CR , де R означає водень або, 1 узятий разом з R , може утворювати двовалентний радикал -СН=СН-СН=СН-; R1 означає С1-6-алкіл або тієніл; 2 R означає водень чи гідроксигрупу або, узятий 3 4 разом з R або R , може утворювати =O; 3 R означає радикал, вибраний з -(CH2)s-NR6R7, (а-1) -О-Н, (а-2) 8 -O-R , (а-3) -S-R9 (а-4) або -C=N, (а-5) де s дорівнює 0, 1, 2 або 3; R6 означає -СНО, С1-6-алкіл, гідроксі-С1-6-алкіл, С16-алкілкарбоніл, ді(С1-6-алкіл)аміно-С1-6-алкіл, С1-6алкілоксі-С1-6-алкіл, С1-6-алкілкарбоніламіно-С1-6алкіл, піперидиніл-С1-6-алкіламінокарбоніл, піпери N C1-6-алкандіїл , NH C1-6-алкандіїл N O , С1-6-алкілоксі-С1-6-алкіл, С1-6-алкілоксі-С1-6алкіламіногрупу, арил-С1-6-алкіл, ді(С2-6-алкеніл), піперидиніл-С1-6-алкіл, С3-10-циклоалкіл, С3-10циклоалкіл-С1-6-алкіл, арилокси(гідроксі)-С1-6-алкіл, галогеноіндазоліл, арил-С1-6-алкіл, арил-С2-6алкеніл, морфоліногрупу, С1-6-алкілімідазоліл або піридиніл-С1-6-алкіламіногрупу; R4 означає водень, С1-6-алкіл, фураніл, піридиніл, арил-С1-6-алкіл або групу формули ; арил означає феніл або феніл, заміщений галогеном, С1-6-алкілом чи С1-6-алкілоксигрупою, і 9 89618 10 де зазначений хіміотерапевтичний засіб вибраний метилувальний засіб, інгібітор топоізомерази І, з групи, що включає 5-фторурацил, лейковорин, 5'блеоміцин. аміно-5'-дезокситимідин, кисень, карбоген, перф12. Спосіб одержання сполуки за п. 1, при якому торкарбон (наприклад, Fluosol 10 DA), 2,3-DPG, здійснюють гідроліз проміжних продуктів формули BW12C, блокатор кальцієвих каналів, пентоксифі(VIII) відомими способами шляхом обробки промілін, сполуку, що пригнічує ріст судин, гідралазин, жних продуктів формули (VIII) відповідними реагеLBSO, адріаміцин, камтотецин, карбоплатин, циснтами, такими як хлорид олова, оцтова кислота та платин, даунорубіцин, доцетаксел, доксорубіцин, соляна кислота, в присутності інертного розчинниінтерферон (альфа, бета, гамма), інтерлейкін-2, ка, наприклад, тетрагідрофурану; іринотекан, паклітаксел, топотекан та їхні похідні, R2 R4 R3 N R2 R1 X (CH2)n R4 O R1 X (CH2)n R3 O N (VIII) H (I) де R1, R2, R3, R4, X, n є такими, як визначено в п. 1. 13. Спосіб одержання сполуки за п. 1, при якому здійснюють конденсацію відповідного ортобензолдіаміну формули (XI) зі складним ефіром формули (XII), в якому Rh означає С1-6-алкіл, з утворенням сполук формули (І), у яких X означає R2 R4 O NH2 (CH2)n + R3 , N, позначених як сполуки формули (I-і), в присутності карбонової кислоти, наприклад, оцтової кислоти та подібної, мінеральної кислоти, такої як, наприклад, соляна кислота, сірчана кислота, або сульфокислоти, такої як, наприклад, метансульфокислота, бензолсульфокислота, 4метилбензолсульфокислота та подібні, R2 N (CH2)n R1 ORh NH2 R4 R3 N O (XI) (XII) (I-i) R1 O H , де R1, R2, R3, R4, n є такими, як визначено в п. 1. Даний винахід стосується інгібіторів PARP і передбачає сполуки та композиції, що містять запропоновані сполуки. Більш того, даний винахід передбачає способи застосування запропонованих інгібіторів PARP, наприклад, як лікарських препаратів. Нуклеарний фермент полі(АДФрибоза)полімераза-1 (PARP-1) є членом групи PARP-ферментів, що складається з PARP-1 та деяких недавно ідентифікованих нових полі(АДФрибозилюючих) ферментів. PARP належить також до полі(аденозин-5'-дифосфорибоза)полімерази або PARS (полі(АДФ-рибоза)синтетази). PARP-1 є головним нуклеарним білком 116кДа, який складається із трьох доменів: домену, що зв'язує N-термінальну ДНК, який містить два «цинкових пальці», домену аутомодифікації та С-термінального каталітичного домену. Він присутній майже у всіх еукаріотів. Фермент синтезує полі(АДФ-рибозу), розгалужений полімер, що складається з більш ніж 200 структурних елементів АДФ-рибози. Акцептори білка полі(АДФ-рибози) безпосередньо або опосередковано залучені до підтримання працездатності ДНК. Вони включають гістони, топоізомерази, ДНК- і РНК-полімерази, ДНК-лігази та залежні від Са2+ - і Mg2+ендонуклеази. Білок PARP експресується на висо кому рівні в багатьох тканинах, найбільш помітно в імунній системі, серці, мозку та статевих клітинах. У нормальних фізіологічних умовах існує мінімальна активність PARP. Однак ушкодження ДНК викликають негайну активацію PARP до 500кратної. Серед багатьох функцій, властивих PARP, і особливо PARP-1, головна роль полягає в полегшенні відновлення ДНК АДФ-рибозилюванням і, отже, в координації числа відновлених білків ДНК. В результаті PARP-активації помітно зменшуються рівні NAD+. Екстенсивна активація PARP спричи+ нює певне виснаження NAD у клітинах, що страждають від масованого ушкодження ДНК. Короткий напівперіод існування полі(АДФ-рибози) приводить до високої швидкості обороту. Одразу після утворення полі(АДФ-рибози) вона швидко розкладається суттєво активною полі(АДФрибоза)глікогідролазою (PARG) разом з фосфодіестеразою та (АДФ-рибоза)протеїнліазою. PARP та PARG утворюють цикл, що перетворює велику + кількість NAD на АДФ-рибозу. Менш ніж за годину надстимуляція PARP здатна викликати падіння + NAD та АТФ до менш ніж 20% від нормального рівня. Такий сценарій особливо шкідливий при ішемії, коли недостатність кисню вже різко ставить під загрозу вихід клітинної енергії. Подальше про 11 89618 12 дукування вільних радикалів під час реперфузії гічних станах, таких як «удар», хвороба Альцгейвважають головною причиною ушкодження тканин. мера та хвороба Паркінсона. Інші дослідження Частково падіння АТФ, що є типовим в багатьох продовжують вивчення ролі активації PARP в цеорганах під час ішемії та реперфузії, може бути ребральних гладких клітинах in vitro та в нейротокпов'язане з виснаженням NAD+, викликаним обосичності МРТР. Надлишкова невральна експозиція ротом полі(АДФ-рибози). Таким чином, очікують, глутамату, який служить переважним нейротрансщо інгібування PARP або PARG зберігає рівень мітером центральної нервової системи та діє на клітинної енергії, тим самим посилюючи виживанрецептори N-метил-D-аспаргінату (NMDA) і рецепня ішемічних тканин після інсульту. тори інших підтипів, часто може наступити в реСинтез полі(АДФ-рибози) залучений також в зультаті «удару» або інших нейродегенеративних індуковану експресію ряду генів, важливих для процесів. Позбавлені кисню нейрони вивільняють запальної реакції. Інгібітори PARP пригнічують глутамат у великих кількостях під час ішемічного продукування індукованої синтази оксиду азоту інсульту мозку, такого як «удар», або серцевого (iNOS) в макрофагах, селектину Р-типу та міжклінападу. Зазначене надлишкове вивільнення глутинних адгезійних молекул-1 (ІСАМ-1) в ендотелітамату, в свою чергу, викликає надстимуляцію альних клітинах. Зазначена активність лежить в (ексайтотоксичність) рецепторів N-метил-Dоснові сильної протизапальної дії, яку виявляють аспартату (NMDA), AMPA, каїнату та MGR, які відінгібітори PARP. Інгібітори PARP здатні зменшувакривають іонні канали та дозволяють (відбуватися) ти некроз шляхом попередження транслокації та неконтрольованій течії іонів (наприклад, Са2+ та + + інфільтрації нейтрофілів в ушкоджені тканини. Na до клітин і K з клітин), приводячи до надстиPARP активують фрагментами ушкодженої муляції нейронів. Надстимульовані нейрони видіДНК і після активування каталізують приєднання ляють більше глутамату, створюючи відповідну до 100 структурних елементів АДФ-рибози до різпетлю або ефект доміно, що негайно приведе до них нуклеарних білків, включаючи гістони та самі ушкодження або загибелі клітини через продукуPARP. Під час сильних клітинних напруг екстенсивання протеаз, ліпаз та вільних радикалів. Надливна активація PARP може швидко привести до шкова активація рецепторів глутамату залучена в ушкодження або загибелі клітин в результаті вирізні неврологічні захворювання та стани, включаснаження запасів енергії. Оскільки кожна молекула ючи епілепсію, «удар», хворобу Альцгеймера, хворегенерованої NAD+ поглинає чотири молекули робу Паркінсона, аміотропний латеральний склеАТФ, при масованій активації PARP NAD+ виснароз (ALS), хворобу Хантінгтона, шизофренію, + жується і при спробах повторного синтезу NAD хронічні болі, ішемію та втрату нейронів внаслідок АТФ може також виявитися виснаженою. гіпоксії, гіпоглікемії, ішемії, травми та ураження Повідомляють, що активація PARP відіграє нервів. Вплив і стимулювання глутамату залучені ключову роль у нейротоксичності, індукованій як також як основа для компульсивних розладів, зокNMDA, так і N0. Це продемонстровано на кортикарема, лікарської залежності. Доказом служать спольних культурах і на гіпокампальних зрізах, при стереження на багатьох видах тварин, а також у яких попередження токсичності прямо корелювацеребральних кортикальних культурах, оброблелося із силою інгібування PARP. Потенційна роль них глутаматом або NMDA, які показують, що анінгібіторів PARP при лікуванні нейродегенеративтагоністи глутаматних рецепторів (тобто, сполуки, них захворювань і травм голови в такий спосіб які блокують глутамат від зв'язування або від акустановлена, навіть якщо механізм дії поки не ястивації його рецептора) блокують невральні ушконий. дження після судинного нападу. Спроби попереАналогічно, показано, що прості ін'єкції інгібідити ексайтотоксичність шляхом блокування торів PARP зменшують розмір інфаркту, викликарецепторів NMDA, AMPA, каїнату та MGR виявиного ішемією та реперфузією серцевого або кістялися невдалими, тому що кожен рецептор має кового м'яза у кроликів. В зазначених множину місць, з якими може зв'язуватися глутадослідженнях проста ін'єкція 3-амінобензаміду мат, і тому важко знайти ефективну суміш антаго(10мг/кг), зроблена або за одну хвилину до оклюзії, ністів або універсальний антагоніст для попереабо за одну хвилину до реперфузії, викликала дження зв'язування глутамату з усіма аналогічні зменшення величини інфаркту на серце рецепторами та перевірки зазначеної теорії. Більш (32-42%), тоді як 1,5-дигідроізохінолін (1мг/кг), інтого, багато композицій, ефективних при блокуший інгібітор PARP, у порівнянних розмірах (38ванні рецепторів, є також токсичними для тварин. 48%) зменшував величину інфаркту. Зазначені Зараз не існує відомого ефективного способу лікурезультати роблять розумним припущення, що вання глутаматних розладів як такого. Стимуляція інгібітори PARP можуть запобігати ішемії серця рецепторів NMDA глутаматом, наприклад, активаабо реперфузійним ушкодженням тканини кістякоція ферменту нейрональної синтази оксиду азоту вих м'язів. (nNOS), приводить до утворення оксиду азоту Активація PARP може також бути використана (NO), що також опосредковує нейротоксичність. для вимірювання ушкоджень в результаті нейроНейротоксичність NMDA може бути попереджена токсичних інсультів, викликаних дією будь-чого з обробкою інгібіторами синтази оксиду азоту (NOS) глутамат-подібних індукторів (через стимуляцію або прицільним генетичним руйнуванням nNOS in NMDA-рецепторів), проміжних продуктів з реакційvitro. Іншим застосуванням інгібіторів PARP є лікуноздатним киснем, амілоїдних -протеїнів, Nвання ушкоджень периферичних нервів і наступнометил-4-феніл-1,2,3,6-тетрагідропіридину (МРТР) го патологічного больового синдрому, відомого як або його активного метаболіту N-метил-4+ невропатичний біль, такий як індукований хронічфенілпіридину (МРР ), які беруть участь у патоло 13 89618 14 ним стискаючим ушкодженням (ССІ) усього сідниінгібітора полі(АДФ-рибоза)полімерази на культичного нерва, при якому наступає транссинаптична вовані пухлинні клітини», Oncol. Res., 6:9, 399-403 зміна дорсального відростка спинного мозку, що (1994), обговорюють інгібуючу дію PARP, що змехарактеризується гіперхроматозом цитоплазми та ншує проліферацію пухлинних клітин, і відзначануклеоплазми (так звані «темні» нейрони). ють синергічний ефект, якщо пухлинні клітини одІснують також докази, що інгібітори PARP є заночасно обробляють алкілувальним лікарським стосовними для лікування запальних захворювань засобом. кишечнику, таких як коліт. Зокрема, коліт викликаСучасний вичерпний огляд стану техніки опубли у пацюків внутрішньопросвітним введенням лікований Li та Zhang в IDrugs 2001, 4(7): 804-812. гаптентринітробензолсульфокислоти в 50%-му Залишається потреба в ефективних та сильетанолі. Оброблені пацюки одержували 3них інгібіторах PARP і, більш конкретно, в інгібітоамінобензамід, специфічний інгібітор активності рах PARP-1, які дають мінімальні побічні ефекти. PARP. Інгібування активності PARP зменшувало Даний винахід стосується сполук, композицій та запальну реакцію і відновлювало морфологію та способів, інгібуючих активність PARP, для лікуваненергетичний статус дистальної товстої кишки. ня раку та/або попередження ушкоджень клітин, Додаткові дані підтверджують, що інгібітори тканин та/або органів, викликаних ушкодженнями PARP є застосовними для лікування артриту. Далі, чи загибеллю клітин, наприклад, некрозу або апоінгібітори PARP, очевидно, застосовні для лікуванптозу. Сполуки та композиції за даним винаходом ня діабету. Показано, що інгібітори PARP застосоособливо застосовні при підвищенні ефективності вні для лікування ендотоксинового бактеріальнохіміотерапії та радіотерапії, при яких первинним токсичного шоку або септичного шоку. результатом лікування є ушкодження ДНК в клітиІнгібітори PARP також можуть бути використанах-мішенях. ні для збільшення тривалості життя та проліфераВ патенті ЕР 371564, опублікованому 6 червня тивної здатності клітин, включаючи лікування та1990p., запропоновані (1H-азол-1ких захворювань, як старіння шкіри, хвороба ілметил)заміщені похідні хіноліну, хіназоліну або Альцгеймера, атеросклероз, остеоартрит, остеохіноксаліну. Описані сполуки пригнічують секрецію пороз, м'язова дистрофія, дегенеративні захворюретиноєвих кислот у плазмі. Більш конкретно, завання кістякових м'язів з реплікаційним фізіологічпропоновані 3-етил-6-[2-метил-1-(1H-1,2,4ним старінням, стареча дегенерація м'язів, імунне триазол-1-іл)пропіл]-2-(1Н)-хіноксалінон (сполука старіння, СНІД та інші старечі імунні захворюван№20 в даній заявці), 3-етил-6-[1-(1H-імідазол-1-іл)ня; і для експресії в мінливі гени старіючих клітин. 2-метилпропіл]-2(1H)-хіноксалінон (сполука №21 в Відомо також, що інгібітори PARP, такі як 3даній заявці), 6-[2-метил-1-(1H-1,2,4-триазол-1амінобензамід, впливають на загальне відновленіл)пропіл]-3-(2-тієніл)-2(1H)-хіноксалінон (сполука ня ДНК при відповідних реакціях, наприклад, на №22 в даній заявці), 6-[2-метил-1-(1H-1,2,4пероксид водню або іонізуючу радіацію. триазол-1-іл)пропіл]-3-(тієніл-2-(1H)-хіноксалінон Основна роль PARP у відновленні розривів (сполука №23 в даній заявці), 6-[1-(1H-імідазол-1тяжей ДНК добре встановлена, особливо якщо іл)-2-метилпропіл]-3-(3-тієніл)-2(1H)-хіноксалінон вони викликані безпосередньо іонізуючою радіаці(сполука №24 в даній заявці) і 6-[1-(1H-імідазол-1єю або опосередковано після ферментативного іл)пентил]-3-метил-2(1H)-хіноксалінон (сполука відновлення ушкоджень ДНК, викликаних метилю№25 в даній заявці). вальними агентами, інгібіторами топоізомерази І Даний винахід стосується сполук формули (І) та іншими хіміотерапевтичними агентами, такими як цисплатин та блеоміцин. Ряд досліджень з використанням «нокаутованих» мишей, трансдомінантних моделей інгібування (надекспресія домену зв'язування ДНК), антисмислових і низькомолекулярних інгібіторів продемонстрували роль PARP у відновленні та виживанні клітин після нанесення ушкодження ДНК. Інгібування ферментата їхніх N-оксидних форм, адитивних солей і тивної активності PARP повинне привести до підстереохімічно ізомерних форм, де вищеної чутливості пухлинних клітин до терапії, n дорівнює 0, 1 або 2; що ушкоджує ДНК. X позначає N або CR5, де R5 позначає водень Повідомляють, що інгібітори PARP ефективні в 1 або, узятий разом з R , може утворювати двоварадіочутливих (гіпоксичних) пухлинних клітинах та лентний радикал формули -СН=СН-СН=СН-; ефективні при попередженні пухлинних клітин від R1 позначає С1-6-алкіл або тієніл; регенерації летального або сублетального ушко2 R позначає водень чи гідроксигрупу або, узядження ДНК після радіаційної терапії, гадано, за3 4 тий разом з R чи R , може утворювати =О; вдяки здатності попереджати повторне з'єднання 3 R позначає радикал, вибраний з -(CH2)Sрозривів тяжей ДНК і шляхом впливу на деякі проNR6R7 (а-1), відні шляхи сигнальної системи ушкодженої ДНК. -О-Н (а-2), Інгібітори PARP можуть бути використані для -O-R8 (а-3), лікування раку. Додатково, у патенті США 9 -S-R (а-4), або №5177075 обговорені деякі ізохіноліни, викорис-C N (а-5), тані для підвищення летальної дії іонізуючої радіде ації або хіміотерапевтичних агентів на пухлинні s дорівнює 0, 1, 2 або 3; клітини. Weltin та ін., «Вплив 6(5-фенантридинону, 15 89618 16 6 R позначає -СНО, С1-6-алкіл, гідроксі-С1-6циклічну кільцеву систему (с-2) або (с-4), де зазнаалкіл, С1-6-алкілкарбоніл, ді-(С1-6-алкіл)аміно-С1-6чена гетероциклічна кільцева система Ζ приєдна10 алкіл, С1-6-алкілоксі-С1-6-алкіл, С1-6на до решти молекули атомом нітрогену, і R поз4 алкілкарбоніламіно-С1-6-алкіл, піперидиніл-С1-6начає водень; то R відрізняється від С1-6-алкілу алкіламінокарбоніл, піперидиніл, піперидиніл-С1-6або піридинілу. алкіл, піперидиніл-С1-6-алкіламінокарбоніл, С1-6Щоразу, коли гетероциклічна кільцева система алкілоксигрупу, тієніл-С1-6-алкіл, піроліл-С1-6-алкіл, Ζ містить фрагмент -СН2-, -СН= або ΝΗ-, замісник 10 арил-С1-6-алкілпіперидиніл, арилкарбоніл-С1-6R або залишок молекули може бути приєднаний алкіл, арилкарбонілпіперидиніл-С1-6-алкіл, галогедо атома карбону або нітрогену, у якого один або ноіндазолілпіперидиніл-С1-6-алкіл або арил-С1-6обидва атоми водню заміщені. алкіл-(С1-6-алкіл)аміно-С1-6-алкіл; Сполуки формули (І) можуть також існувати в R7 позначає водень або С1-6-алкіл; їхніх таутомерних формах. Хоча зазначені форми 8 R позначає С1-6-алкіл, С1-6-алкілкарбоніл або точно не позначені вищевказаною формулою, воді-(С1-6-алкіл)аміно-С1-6-алкіл; і ни також включені до обсягу даного винаходу. 9 R позначає ді-(С1-6-алкіл)аміно-С1-6-алкіл; Далі в описі пояснюється ряд термінів, викори3 або R позначає групу формули станих у попередніх визначеннях і нижче. Зазна-Z- (b-1), чені терміни іноді вжиті як такі або в складних терде мінах. Ζ позначає гетероциклічну кільцеву систему, Як вжито в попередніх визначеннях і нижче, вибрану з галоген позначає фтор, хлор, бром та йод; С1-6алкіл позначає насичений вуглеводневий радикал з лінійним або розгалуженим ланцюгом, що містить від 1 до 6 атомів карбону, такий як, наприклад, метил, етил, пропіл, бутил, пентил, гексил, 1метилетил, 2-метилпропіл, 2-метилбутил, 2метилпентил і подібні; С1-6-алкандіїл позначає двовалентний насичений вуглеводневий радикал з лінійним і розгалуженим ланцюгом, що містить від 1 до 6 атомів карбону, такий як, наприклад, метилен, 1,2-етандіїл, 1,3-пропандіїл, 1,4-бутандіїл, 1,5пентандіїл, 1,6-гександіїл та їхні розгалужені ізомери, такі як 2-метилпентандіїл, 3метилпентандіїл, 2,2-диметилбутандіїл, 2,3диметилбутандіїл і подібні; С2-6-алкеніл позначає вуглеводневий радикал з лінійним або розгалужеде кожен R10 незалежно один від одного позним ланцюгом, що включає один подвійний зв'язок начає водень, С1-6-алкіл, амінокарбоніл, гідроксигі містить від 2 до 6 атомів карбону, такий як, нарупу, групу формули приклад, етеніл, 2-пропеніл, 3-бутеніл, 2-пентеніл, 3-пентеніл, 3-метил-2-бутеніл і подібні; С3-10циклоалкіл включає циклічні вуглеводневі групи, що містять від 3 до 10 атомів карбону, такі як циклопропіл, циклобутил, циклопентил, циклопентеніл, циклогексил, циклогексеніл, циклогептил, циклооктил і подібні. Термін «адитивна сіль» включає солі, які сполуки формули (І) здатні утворювати з органічними чи неорганічними основами, такими як аміни, основи лужних металів і основи лужноземельних металів чи четвертинні амонієві основи, або з органічними чи неорганічними кислотами, такими як С1-6-алкілоксі-С1-6-алкіл, С1-6-алкілоксі-С1-6мінеральні кислоти, сульфокислоти, карбонові алкіламіногрупу, арил-С1-6-алкіл, ді-(С1-6-алкеніл), кислоти або фосфорвмісні кислоти. піперидиніл-С1-6-алкіл, С3-10-циклоалкіл, С3-10Термін «адитивна сіль» додатково включає циклоалкіл-С1-6-алкіл, арилокси(гідроксі)-С1-6-алкіл, фармацевтично прийнятні солі, комплекси металів галогеноіндазоліл, арил-С1-6-алкіл, арил-С2-6і сольвати та їхні солі, які здатні утворювати споалкеніл, морфоліногрупу, С1-6-алкілімідазоліл або луки формули (І). піридиніл-С1-6-алкіламіногрупу; Термін «фармацевтично прийнятні солі» поз4 R позначає водень, С1-6-алкіл, фураніл, піриначає адитивні солі фармацевтично прийнятних кислот чи основ. Адитивні солі фармацевтично диніл, арил-С1-6-алкіл або групу формули прийнятних кислот чи основ, як згадано вище, включають терапевтично активні адитивні сольові форми нетоксичних кислот і нетоксичних основ, які арил позначає феніл або феніл, заміщений здатні утворювати сполуки формули (І). Сполуки галогеном, С1-6-алкілом чи С1-6-алкілоксигрупою; за формули (І), що мають основні властивості, моумови, якщо жуть бути перетворені на їхні фармацевтично приn дорівнює 0, X позначає N, R2 позначає во3 йнятні адитивні солі обробкою зазначених основдень, R позначає групу (b-1), Z позначає гетеро 17 89618 18 них форм відповідною кислотою. Відповідні кислоЩоразу, коли використовується термін «споти включають, наприклад, неорганічні кислоти, такі луки формули (І)», це позначає також включення як галогенводневі кислоти, наприклад, соляну або N-оксидних форм, фармацевтично прийнятних бромистоводневу кислоту; сірчану, азотну, фосадитивних солей з кислотами або основами та всіх форну та подібні кислоти; або органічні кислоти, стереоізомерних форм. такі як, наприклад, оцтову, пропіонову, оксиоцтову, Сполуки, описані в ЕР 371564, пригнічують молочну, піровиноградну, щавлеву, малонову, елімінацію ретиноєвої кислоти в плазмі. В ЕР бурштинову (тобто, бутандіову кислоту), малеїно371564 запропоновані сполуки: 3-етил-6-[2-метилву, фумарову, яблучну, винну, лимонну, метансу1-(1H-1,2,4-триазол-1-іл)пропіл]-2-(1H)льфонову, етансульфонову, бензолсульфонову, хіноксалінон (сполука №20 в даній заявці), 3-етилпара-толуолсульфонову, цикламенову, саліцило6-[1-(1H-імідазол-1-іл)-2-метилпропіл]-2(1H)ву, пара-аміносаліцилову, памову та подібні кисхіноксалінон (сполука №21 в даній заявці), 6-[2лоти. Сполуки формули (І), які мають кислотні метил-1-(1Н-1,2,4-триазол-1-іл)пропіл]-3-(2-тієніл)властивості, можуть бути перетворені на їхні фар2(1H)-хіноксалінон (сполука №22 в даній заявці), 6мацевтично прийнятні адитивні солі з основами [2-метил-1-(1H-1,2,4-триазол-1-іл)пропіл]-3-(тієніл)обробкою зазначеної кислотної форми придатною 2(1H)-хіноксалінон (сполука №23 в даній заявці), 6органічною або неорганічною основою. Відповідні [1-(1H-імідазол-1-іл)-2-метилпропіл]-3-(3-тієніл)форми солей з основами включають, наприклад, 2(1H)-хіноксалінон (№24 в даній заявці) і 6-[1-(1Hсолі амонію, солі лужних та лужноземельних меімідазол-1-іл)пентил]-3-метил-2-(1H)-хіноксалінон талів, наприклад, солі літію, натрію, калію, магнію, (сполука №25 в даній заявці). Несподівано було кальцію та подібні, солі з органічними основами, виявлено, що сполуки за даним винаходом виявнаприклад, солі бензатину, N-метил-D-глюкаміну, ляють PARP-інгібуючу дію. гідрабаміну, і солі з амінокислотами, такими як, Перша група сполук, що представляють інтенаприклад, аргінін, лізин та подібні. рес, складається зі сполук формули (І), до яких Терміни «кислотні» або «основні адитивні созастосовні одне або більше з таких обмежень: лі» включають гідрати та адитивні форми з розa) n дорівнює 0 чи 1; чинником, які здатні утворювати сполуки формули b) X позначає N або CR5, де R5 позначає во(І). Прикладами зазначених форм є, наприклад, день; гідрати, алкоголяти та подібні. c) R3 позначає радикал, вибраний з (а-1), (а-2) Термін «комплекси металів» позначає комчи (а-3), або позначає групу формули (b-1), тобто, плекс, утворений сполукою формули (І) та однією -Ζ-; або більше органічною чи неорганічною сіллю чи d) s дорівнює 0, 1 або 2; солями металу. Прикладами зазначених органічe) R6 позначає -СНО, С1-6-алкіл, піперидинілних чи неорганічних солей є галогеніди, нітрати, С1-6-алкіл, арилкарбонілпіперидиніл-С1-6-алкіл або сульфати, фосфати, ацетати, трифторацетати, арил-С1-6-алкіл-(С1-6-алкіл)аміно-С1-6-алкіл; трихлорацетати, пропіонати, тартрати, сульфонаf) R8 позначає С1-6-алкіл; ти, наприклад, метилсульфонати, 4g) якщо R3 позначає групу формули (b-1), то Ζ метилфенілсульфонати, саліцилати, бензоати та позначає гетероциклічну кільцеву систему, вибраподібні, металів другої основної групи періодичної ну з (с-2) або (с-4); і системи, наприклад, солі магнію або кальцію, треh) кожен R10 незалежно один від одного позтьої або четвертої основних груп, наприклад, начає водень, С1-6-алкіл або С1-6-алкілоксі-С1-6алюмінію, олова, свинцю, а також від першої до алкіламіногрупу. восьмої побічних груп періодичної системи, такі як, Друга група сполук, що представляють інтенаприклад, солі хрому, марганцю, заліза, кобальрес, складається з таких сполук формули (І), до ту, нікелю, міді, цинку та подібні. яких застосовні одне або більше з таких обмеТермін «стереохімічно ізомерні форми сполук жень: формули (І)», ужитий вище, позначає всі можливі a) n дорівнює 0; сполуки, що складаються з тих же атомів, з'єднаb) X позначає N або CR5, де R5 позначає воних у тій же послідовності, але мають різні, не взадень; 1 ємозамінні, тривимірні структури, які можуть утвоc) R позначає С1-6-алкіл; рювати сполуки формули (І). Якщо не зазначено d) R2 позначає водень чи гідроксигрупу або, або визначено інше, хімічна назва сполуки охопузятий разом з R4, може утворювати =O; лює суміш всіх можливих стереохімічно ізомерних e) R3 позначає радикал, вибраний з (а-1) або форм, які здатна утворити зазначена сполука. За(а-2); значені суміші можуть містити всі діастереомери f) s дорівнює 0 чи 1; 6 та/або енантіомери основної молекулярної струкg) R позначає -СНО або С1-6-алкіл; і 4 тури зазначеної сполуки. Всі стереохімічно ізомерh) R позначає водень, С1-6-алкіл або групу ні форми сполук формули (І), як у чистому виді, так і в суміші одна з одною, вважаються такими, формули що входять до обсягу даного винаходу. N-оксидні форми сполук формули (І) означаТретя група сполук, що представляють інтеють включення таких сполук формули (І), в яких рес, складається з таких зазначених сполук фородин або кілька атомів нітрогену окиснені до так мули (І) першої групи сполук, що представляють званого N-оксиду, зокрема, такі N-оксиди, в яких Nінтерес, або другої групи сполук, що представляокиснені один або більше атомів нітрогену піпериють інтерес, у яких Ζ позначає гетероциклічну кідину, піперазину або піридазинілу. 19 89618 20 1 2 льцеву систему, що відрізняється від гетероцикліR позначає С1-6-алкіл; R позначає водень чи гід4 чної кільцевої системи формули (с-2) або (с-4). роксигрупу або, узятий разом з R , може утворю3 Група кращих сполук складається зі сполук вати =О; R позначає радикал, вибраний з (а-1) формули (І), у яких n дорівнює 0 чи 1; X позначає або (а-2); s дорівнює 0 чи 1; R6 позначає -СНО або 5 5 3 N або CR , де R позначає водень; R позначає С1-6-алкіл; і R4 позначає водень, С1-6-алкіл або грурадикал, вибраний з (а-1), (а-2) чи (а-3) або позначає групу формули (b-1), тобто, -Ζ-; s дорівнює 0, 1 пу формули . 6 або 2; R позначає -СНО, С1-6-алкіл, піперидинілС1-6-алкіл, арилкарбонілпіперидиніл-С1-6-алкіл або Так само, додаткова група кращих сполук 8 арил-С1-6-алкіл-(С1-6-алкіл)аміно-С1-6-алкіл; R позскладається з таких сполук формули (І), групи 3 начає С1-6-алкіл; якщо R позначає групу формули кращих сполук або додаткової групи кращих спо(b-1), то Ζ позначає гетероциклічну кільцеву сислук, у яких Ζ позначає гетероциклічну кільцеву 10 тему, вибрану з (с-2) або (с-4); і кожен R незалесистему, що відрізняється від гетероциклічної кіжно один від одного позначає водень, С1-6-алкіл льцевої системи формули (с-2) або (с-4). або С1-6-алкілоксі-С1-6-алкіламіногрупу. Найкращими сполуками є сполука №1, сполуДодаткова група кращих сполук складається із ка №5, сполука №7, сполука №3 і сполука №17. зазначених сполук формули (І), у яких n дорівнює 0; X позначає N або CR5, де R5 позначає водень; Сполуки формули (І) можуть бути одержані відповідно до загальних способів, описаних в ЕР 371564. Ряд зазначених способів одержання буде описаний далі більш докладно. Інші способи одержання кінцевих сполук формули (І) описані в прикладах. Сполуки формули (І), у яких R2 позначає во3 7 7 день, a R позначає -NR -CHO, де R позначає 3 Сполуки формули (І), у яких R позначає гідроксигрупу, позначені в описі як сполуки формули (I-c), можуть бути одержані перетворенням кетогрупи сполук формули (I-а) на гідроксигрупу дією водень або метил, позначені в описі як сполуки формули (І-b), можуть бути одержані, виходячи зі сполук формули (І), у яких R2, узятий разом з R3, утворює =O, позначених в описі як сполуки формули (I-а), в присутності формаміду або метилформаміду, позначених в описі як проміжні сполуки формули (II), та мурашиної кислоти. відповідних відновників, наприклад, боргідриду натрію, в придатному розчиннику, наприклад, метанолі або тетрагідрофурані. 21 89618 22 Сполуки формули (I-а) можуть бути одержані 2 перетворенням сполук формули (I-c), у яких R позначає водень, позначених в описі як сполуки формули (І-с-1), в присутності придатного окис ника, такого як триоксид хрому, і кислоти, такої як сірчана кислота, в придатному розчиннику, такому як 2-пропанон. Проміжні сполуки формули (IV), у яких W позначає відхідну групу, наприклад, хлор, бром, метансульфонілоксигрупу або бензолсульфонілоксигрупу, можуть бути одержані зі сполук формули (І-с-1) обробкою зазначених сполук придат ним реагентом, наприклад, метансульфонілоксихлоридом або бензолсульфонілоксихлоридом, або галогенуючим реагентом, таким як, наприклад, РОСl3 або SOCl2. Сполуки формули (І), визначені як сполуки формули (І), у яких Rb має значення, визначені 6 c 7 b c для R , і R - визначені для R , або R та R , узяті разом з нітрогеном, до якого вони приєднані, утворюють відповідну гетероциклічну кільцеву систему, як визначено для Z, позначені в описі як сполуки формули (I-h), можуть бути одержані взаємодією проміжного продукту формули (IV) із проміжним продуктом формули (V). Реакція може бути проведена в інертному для реакції розчиннику, такому як диметилформамід або ацетонітрил, і, можливо, в присутності придатної основи, такої як, наприклад, карбонат натрію, карбонат калію або триетиламін. Сполуки формули (І) можуть також бути перетворені одна на одну відомими реакціями або перетвореннями функціональних груп. Ряд зазначених перетворень вже описаний вище. Іншими прикладами є гідроліз ефірів карбонових кислот до відповідних карбонових кислот або спиртів; гідроліз амідів до відповідних карбонових кислот або амінів; гідроліз нітрилів до відповідних амідів; аміногрупи в імідазолі або фенілі можуть бути замінені на водень відомими на сучасному рівні техніки реакціями діазотування та заміщення діазогрупи гідрогеном; спирти можуть бути перетворені на складні ефіри та прості ефіри; первинні аміни можуть бути перетворені на вторинні або третинні аміни; подвійні зв'язки можуть бути гідровані до відповідних простих зв'язків; залишок йоду у фенільній групі може бути перетворений на складноефірну групу включенням монооксиду вуглецю в присутності придатного паладієвого каталізатора. Виходячи із цього, сполуки формул (І), (I-а), (І-b), (I-c), (І-с-1), (I-h), (I-і), (I-j) і (I-k) можуть бути піддані наступним перетворенням у будь-якому бажаному порядку: (і) перетворення сполуки формули (І) на іншу сполуку формули (І); (іі) перетворення сполуки формули (І) на її відповідну адитивну сіль або N-оксид; (ііі) перетворення фармацевтично прийнятної адитивної солі або N-оксиду сполуки формули (І) на вихідну сполуку формули (І); (iv) одержання стереохімічно ізомерної форми сполуки формули (І) або її фармацевтично прийнятної адитивної солі або N-оксиду. Проміжні продукти формули (VII), у яких Rd та e R є відповідними радикалами або, узяті разом з атомом карбону, до якого вони приєднані, утворюють відповідну гетероциклічну кільцеву систему, як визначено для Z, можуть бути одержані гідролізом проміжних продуктів формули (VI), у якій R3 позначає групу формули (b-1) або радикал формули (а-1), де s відрізняється від 0, позначені 8 в описі як R , згідно з відомими на сучасному рівні техніки способами, такими як перемішування проміжного продукту (VI) у водному розчині кис 23 89618 24 лоти в присутності інертного розчинника, напринаприклад, соляна кислота. клад, тетрагідрофурану. Придатною кислотою є, 2 Сполуки формули (І), у якій R позначає воg день, a R визначений вище, позначені в описі як сполуки формули (Θ-k), можуть бути одержані, виходячи з проміжних продуктів формули (VII), селективним гідруванням зазначеного проміжного продукту відповідним відновником, таким як, наприклад, каталізатор на основі благородного металу, такий як платина-на-вугіллі, палладій-навугіллі та подібні, і відповідним відновником, таким як водень, в придатному розчиннику, такому як метанол. Сполуки формули (І) можуть бути одержані гідролізом проміжних продуктів формули (VIII) згідно з відомими на сучасному рівні техніки способами, піддаючи проміжні продукти формули (VIII) дії відповідних реагентів, таких як хлорид олова, оцтова кислота та соляна кислота, в присутності інертного розчинника, наприклад, тетрагідрофурану. Сполуки формули (І) можуть бути одержані, виходячи з N-оксидів формули (IX), перетворенням проміжних продуктів формули (IX) в присут ності придатного реагенту, такого як карбонат натрію або оцтовий ангідрид, і, якщо доцільно, в розчиннику, такому як дихлорметан. Сполуки формули (І), у яких X позначає СН, позначені як сполуки формули (I-j), можуть бути одержані циклізацією проміжного продукту формули (X). Реакція циклізації проміжного продукту (X) може бути проведена відповідно до відомих на сучасному рівні техніки методик циклізації. Краще реакцію ведуть в присутності придатної кислоти Льюїса, наприклад, хлориду алюмінію, без розчинника або в придатному розчиннику, такому як, наприклад, ароматичний вуглеводень, наприклад, бензол, хлорбензол, метилбензол і подібні; галогеновані вуглеводні, наприклад, трихлорметан, тетрахлорметан і подібні; простий ефір, наприклад, тетрагідрофуран, 1,4-діоксан і подібні; або суміші зазначених розчинників. У деяких випадках швидкість реакції можуть збільшити підвищені температури, краще, від 70 до 100°С, і перемішування. 25 89618 26 Сполуки формули (І), у яких X позначає N, позначені в описі як сполуки формули (I-і), можуть бути одержані конденсацією відповідного орто-діамінобензолу формули (XI) зі складним h ефіром формули (XII), в якому R позначає С1-6алкіл. Конденсація заміщеного орто-діаміну формули (XI) і складного ефіру формули (XII) може бути проведена в присутності карбонової кислоти, наприклад, оцтової кислоти або подібної, мінеральної кислоти, такої як, наприклад, соляна кислота, сірчана кислота, або сульфокислоти, такої як, наприклад, метансульфокислота, бензолсульфокислота, 4-метилбензолсульфокислота та подібні. Іноді для збільшення швидкості реакції можуть бути доцільні підвищені температури, а в деяких випадках реакція може бути проведена навіть при температурі кипіння реакційної суміші. Вода, що вивільняється в процесі конденсації, може бути видалена із суміші азеотропною перегонкою, перегонкою та подібними способами. Проміжні продукти формули (XI) можуть бути одержані реакцією відновлення нітросполуки до аміну, виходячи із проміжного продукту формули (XIII), в присутності металевого каталізатора, такого як нікель Ренея, і відповідного відновника, такого як водень, в придатному розчиннику, такому як метанол. Проміжні продукти формули (XIII) можуть бути одержані гідролізом проміжних продуктів формули (XIV) згідно з відомими на сучасному рівні техніки способами, такими як перемішування проміжного продукту (XIV) у водному розчині кислоти в присутності інертного розчинника, наприклад, тетрагідрофурану. Придатною кислотою є, наприклад, соляна кислота. Проміжні продукти формули (X) можуть бути зручно одержані взаємодією аніліну формули (XV) з галогенідом формули (XVI) в присутності основи, такої як піридин, в придатному розчиннику, такому як дихлорметан. Проміжні продукти формули (VIII), у яких n 2 дорівнює 0, R позначає водень або гідроксигрупу і, якщо R2 позначає водень, то R3 позначає гідроксигрупу, позначені в описі як проміжні продукти 27 89618 28 формули (VIII-а), можуть бути одержані обробкою ступною взаємодією зазначеного проміжного проміжного продукту формули (XVII), у якій W продукту із проміжним продуктом формули 1 позначає галоген, літійорганічним реагентом, (XVIII), у якому R позначає водень або радикал, таким як, наприклад, н-бутиллітій, в інертному як визначено для R3. розчиннику, наприклад, тетрагідрофурані, і на Даний винахід стосується також сполуки формули (І), як визначено вище, для застосування в медицині. Сполуки за даним винаходом мають PARPінгібуючі властивості, як можна побачити далі з експериментальної частини. В даному винаході розглянуте також застосування сполук при виготовленні лікарських препаратів для лікування будь-якого захворювання та розладу у тварини, описаного в описі, де зазначені сполуки є сполуками формули (І) у якій Ζ позначає гетероциклічну кільцеву систему, вибрану з 10 їхніми N-оксидними формами, фармацевтично прийнятними адитивними солями та стереохімічно ізомерними формами, у яких n дорівнює 0, 1 або 2; X позначає N або CR5, де R5 позначає водень або, узятий разом з R1, може утворювати двовалентний радикал формули -СН=СН-СН=СН-; R1 позначає С1-6-алкіл або тієніл; 2 R позначає водень чи гідроксигрупу або, узятий разом з R3 чи R4, може утворювати =O; R3 позначає радикал, вибраний з 6 7 -(CH2)S-NR R (а-1), -O-Н (а-2), -O-R8 (а-3), -S-R9 (а-4) або (а-5), -C N де s дорівнює 0, 1, 2 або 3; 6 R позначає -СНО, С1-6-алкіл, гідроксі-С1-6алкіл, С1-6-алкілкарбоніл, ді-(С1-6-алкіл)аміно-С1-6алкіл, С1-6-алкілоксі-С1-6-алкіл, С1-6алкілкарбоніламіно-С1-6-алкіл, піперидиніл-С1-6алкіламінокарбоніл, піперидиніл, піперидиніл-С1-6алкіл, піперидиніл-С1-6-алкіламінокарбоніл, С1-6алкілоксигрупу, тієніл-С1-6-алкіл, піроліл-С1-6-алкіл, арил-С1-6-алкілпіперидиніл, арилкарбоніл-С1-6алкіл, арилкарбонілпиперидиніл-С1-6-алкіл, галогеноіндазолілпиперидиніл-С1-6-алкіл або арил-С1-6алкіл-(С1-6-алкіл)аміно-С1-6-алкіл; 7 R позначає водень або С1-6-алкіл; 8 R позначає С1-6-алкіл, С1-6-алкілкарбоніл або ді-(С1-6-алкіл)аміно-С1-6-алкіл; і 9 R позначає ді-(С1-6-алкіл)аміно-С1-6-алкіл; або 3 R позначає групу формули -Ζ- (b-1), де кожен R незалежно один від одного позначає водень, С1-6-алкіл, амінокарбоніл, гідроксигрупу, групи формул С1-6-алкілоксі-С1-6-алкіл, С1-6-алкілоксі-С1-6алкіламіногрупу, арил-С1-6-алкіл, ді-(С2-6-алкеніл), піперидиніл-С1-6-алкіл, С3-10-циклоалкіл, С3-10циклоалкіл-С1-6-алкіл, арилокси(гідроксі)-С1-6-алкіл, галогеноіндазоліл, арил-С1-6-алкіл, арил-С2-6алкеніл, морфоліногрупу, С1-6-алкілімідазоліл або піридиніл-С1-6-алкіламіногрупу; R4 позначає водень, С1-6-алкіл, фураніл, піридиніл, С1-6-алкіларил або групу формули ; арил позначає феніл або феніл, заміщений галогеном, С1-6-алкілом або С1-6-алкілоксигрупою. Завдяки своїй здатності зв'язувати PARP сполуки за даним винаходом можуть бути використані як контрольні препарати або ізотопні індикатори; у цьому випадку один з атомів молекули може бути замінений, наприклад, радіоактивним ізотопом. Для виготовлення фармацевтичних композицій за даним винаходом ефективну кількість конкретної сполуки у формі адитивної солі з основою або кислотою як активний інгредієнт поєднують із фармацевтично прийнятним носієм з утворенням ретельно перемішаної суміші; причому носій може набувати широкого ряду форм залежно від бажа 29 89618 30 ної для введення форми готового препарату. Зажиття або проліферативну здатність клітин; здатні значені фармацевтичні композиції бажано готовизмінювати експресію генів старіючих клітин; здатні ти в стандартній лікарській формі, придатній, крадо радіосенсибілізації та/або хіміосенсибілізації ще, для введення перорально, ректально, клітин. Звичайно інгібування активності PARP обечерезшкірно або шляхом парентеральної ін'єкції. рігає клітини від втрати енергії, попереджаючи, у Наприклад, при виготовленні композицій в оральвипадку нервових клітин, необоротну деполяризаній лікарській формі може бути використане будьцію нейронів, і в такий спосіб забезпечуючи нейрояке застосовне фармацевтичне середовище, таке захист. як, наприклад, вода, гліколі, масла, спирти та поІз зазначених причин даний винахід додатково дібні, у випадку пероральних рідких препаратів, стосується способу введення терапевтично ефектаких як суспензії, сиропи, еліксири та розчини; тивної кількості ідентифікованих вище сполук в або тверді носії, такі як крохмаль, цукри, каолін, кількості, достатній для інгібування активності ковзні речовини, зв'язуючі, дезинтегруючі агенти PARP, для лікування або попередження ураження та подібні, у випадку порошків, пігулок, капсул і тканини в результаті ушкодження чи загибелі клітаблеток. Внаслідок легкості введення таблетки та тин, викликаних некрозом або апоптозом, для капсули є найкращими пероральними лікарськими впливу на нервову активність, не опосередковану стандартними формами, у випадку яких, очевидно, токсичністю NMDA, для впливу на нервову активвикористовують тверді фармацевтичні носії. Для ність, опосередковану токсичністю NMDA, для ліпарентеральних композицій носій звичайно є стекування уражень нервової тканини, викликаних рильною водою, щонайменше, більшою частиною, ішемічними та реперфузійними ушкодженнями, хоча можуть бути включені інші інгредієнти, наприневрологічних захворювань і нейродегенеративклад, для підвищення розчинності. Як розчини для них захворювань; для попередження або лікуванін'єкцій, наприклад, можуть бути приготовлені такі ня судинного нападу; для лікування або поперерозчини, у яких носієм є фізіологічний розчин, роздження серцево-судинних захворювань; для чин глюкози або суміш фізіологічного розчину та лікування інших станів та/або розладів, таких як розчину глюкози. Також можуть бути приготовлені стареча м'язова дегенерація, інші старечі імунні суспензії для ін'єкцій, можуть бути використані захворювання та СНІД, запалення, подагра, артвідповідні рідкі носії, суспендувальні агенти та порит, атеросклероз, кахексія, рак, дегенеративні дібні. В композиціях, придатних для черезшкірного захворювання кістякових м'язів внаслідок реплікавведення, носій може містити агент, що поліпшує ційного старіння, діабет, травми голови, запальні пенетрацію та/або придатний змочувальний агент, захворювання кишечнику (такі як коліт і хвороба можливо, об'єднані з придатними добавками будьКрона), м'язова дистрофія, остеоартрит, остеопоякої природи в незначних пропорціях; причому роз, хронічні та/або гострі болі (такі як невропатидобавки не повинні чинити помітної шкідливої дії чні болі), ниркова недостатність, ішемія сітківки, на шкіру. Зазначені добавки можуть полегшити септичний шок (такий як ендотоксиновий бактеріавведення в шкіру та/або можуть бути корисними льно-токсичний шок) і старіння шкіри, для подовдля виготовлення бажаних композицій. Зазначені ження життя та проліферативної здатності клітин; композиції можуть бути введені різними шляхами, для зміни експресії генів старіючих клітин; для хінаприклад, як трансдермальні бляшки, точково міосенсибілізації та/або радіосенсибілізації (гіпокабо у вигляді мазі. Особливо краще готовити висичних) пухлинних клітин. Даний винахід стосуєтьщезгадані фармацевтичні композиції в стандартся також лікування захворювань і станів у тварин, них лікарських формах для легкості введення та яке включає введення зазначеній тварині терапеводнаковості дозування. Стандартна лікарська фотично ефективної кількості ідентифікованих вище рма, як використовується в описі та формулі винасполук. ходу, позначає фізично дискретні одиниці, придатЗокрема, даний винахід стосується способу ліні для однакового дозування, причому кожна кування, попередження або інгібування неврологіодиниця містить попередньо визначену кількість чних розладів у тварини, який передбачає введенактивного інгредієнта, розраховану на одержання ня зазначеній тварині терапевтично ефективної бажаного терапевтичного ефекту, у поєднанні з кількості ідентифікованих вище сполук. Неврологінеобхідним фармацевтичним носієм. Прикладами чні розлади вибирають з групи, що складається з зазначених стандартних лікарських форм є таблепериферичної невропатії, викликаної психічним тки (включаючи таблетки з надрізами або з покпорушенням або хворобливим станом, травматичриттям), капсули, пігулки, пакетики з порошками, ного ушкодження мозку, фізичного ураження спиноблатки, розчини або суспензії для ін'єкцій, пакеного мозку, нападу, пов'язаного з ушкодженням тики з 5 чи 15мл суспензії і подібні та їхні кратні мозку, обмеженої ішемії, глобальної ішемії, репечастки. рфузійного ураження, демієлінізуючого захворюСполуки за даним винаходом є придатними вання та неврологічного розладу, пов'язаного з для лікування або запобігання ушкоджень, виклинейродегенерацією. каних ушкодженням або загибеллю клітин в реДаний винахід також включає застосування зультаті некрозу або апоптозу; можуть полегшувасполук формули (І) для інгібування активності ти ушкодження нейрональних або серцевоPARP для лікування, попередження або інгібувансудинних тканин, включаючи наслідки обмеженої ня уражень тканин, викликаних ушкодженням або ішемії, інфаркту міокарда та реперфузійних змін; загибеллю клітин в результаті некрозу або апоптопридатні для лікування різних захворювань та стазу, для лікування, попередження або інгібування нів, викликаних або загострених активністю PARP; неврологічних захворювань тварин. можуть продовжувати або збільшувати тривалість 31 89618 32 Термін «попередження нейродегенерації» льний випіт, меланома, мезотеліома, множинна включає здатність попереджати нейродегенерацію мієлома, нейробластома, неходжкінська лімфома, у пацієнтів з діагнозом нейродегенеративного заостеосаркома, яєчковий рак, рак яєчника (зародхворювання або при ризику розвитку нового дегекової клітини), рак простати, рак підшлункової занеративного захворювання та для попередження лози, рак полового члена, ретинобластома, рак додаткової нейродегенерації у пацієнтів, які вже шкіри, саркома м'яких тканин, карцинома клітин страждають від або мають симптоми нейродегепростого плоского епітелію, рак шлунка, тестикунеративного захворювання. лярний рак, рак щитовидної залози, трофобластиТермін «лікування», використаний в описі, чні неоплазми, рак матки, вагінальний рак, рак охоплює будь-яке лікування захворювання та/або вульви та пухлина Вілмса. стану тварини, зокрема, людини, і передбачає: (і) Тому сполуки за даним винаходом можуть бупопередження початку захворювання та/або стану ти використані як «радіосенсибілізатори» та/або у суб'єкта, що може бути схильний до захворю«хіміосенсибілізатори». вання та/або стану, але ще не має діагнозу; (іі) Відомо, що радіосенсибілізатори підвищують інгібування захворювання та/або стану, тобто, зачутливість ракових клітин до токсичної дії іонізуютримання його розвитку; (ііі) ослаблення захворючої радіації. В літературі запропоновано кілька вання та/або стану, тобто, сприяння зворотному механізмів дії радіосенсибілізаторів: радіосенсибірозвитку захворювання та/або стану. лізатори гіпоксичної клітини (наприклад, 2Термін «радіосенсибілізатор», використаний в нітроімідазоли та діоксиди бензотриазину) імітуописі, визначає молекулу, краще, молекулу з низьють кисень або, як альтернатива, ведуть себе як кою молекулярною масою, введену тварині в тебіовідновники при гіпоксії; радіосенсибілізатори рапевтично ефективних кількостях для підвищеннегіпоксичної клітини (наприклад, галогеновані ня чутливості клітин до іонізуючої радіації та/або піримідини) можуть бути аналогами основ ДНК і, для сприяння лікуванню захворювання, що лікукраще, вбудовуються в ДНК пухлинних клітин і при ється іонізуючою радіацією. Захворюваннями, які цьому сприяють індукованому радіацією розщеплікуються іонізуючою радіацією, є пухлинні захволенню молекул ДНК та/або запобігають нормальрювання, доброякісні та злоякісні пухлини і ракові ному механізму відновлення ДНК; висунуті також клітини. Лікування іонізуючою радіацією інших загіпотези інших різних потенційних механізмів дії хворювань, не перелічених в описі, також охоплюрадіосенсибілізаторів при лікуванні захворювань. ється даним винаходом. Багато протоколів лікування ракових захворюТермін «хіміосенсибілізатор», використаний в вань зараз використовують радіосенсибілізатори у описі, визначає молекулу, краще, молекулу з низьзв'язку з опроміненням рентгенівськими променякою молекулярною масою, введену тварині в теми. Приклади радіосенсибілізаторів, активованих рапевтично ефективних кількостях, для підвищенрентгенівськими променями, включають, без обня чутливості клітин до хіміотерапії та/або меження, такі: метронідазол, мізонідазол, дезмесприяння лікуванню захворювання, що лікується тилмізонідазол, пімонідазол, етанідазол, німорахіміотерапією. Захворюваннями, які виліковуються зол, мітоміцин 3, RSU 1069, SR 4233, ЕО9, RB хіміотерапією, є пухлинні захворювання, доброякі6145, нікотинамід, 5-бромдезоксиуридин (BUd), 5сні та злоякісні пухлини і ракові клітини. Хіміотерайоддезоксиуридин (ІUd), бромдезоксицитидин, певтичне лікування інших захворювань, не переліфтордезоксиуридин (FUd), гідроксисечовина, цисчених в описі, також охоплюється даним платин та їхні терапевтично ефективні аналоги і винаходом. похідні. Сполуки, композиції та способи за даним виФотодинамічна терапія (PDT) раку використонаходом є, зокрема, застосовними для лікування вує видиме світло як радіаційний активатор чутлиабо попередження уражень тканин, викликаних вого агента. Приклади фотодинамічних радіосензагибеллю або ушкодженням клітин в результаті сибілізаторів включають, без обмеження, такі: некрозу або апоптозу. похідні гематопорфірину, фотофрин, похідні бенСполуки за даним винаходом можуть бути зопорфірину, етіопорфірин олова, феоборбід-а, «протираковими засобами», назва яких охоплює бактеріохлорофіл-а, нафталоціаніни, фталоціанітакож «засоби проти росту пухлинних клітин» та ни, фталоціанін цинку та їхні терапевтично ефек«антинеопластичні засоби». Наприклад, способи тивні аналоги і похідні. відповідно до винаходу є застосовними для лікуРадіосенсибілізатори можуть бути введені равання раку та хіміочутливих та/або радіочутливих зом з терапевтично ефективною кількістю однієї чи пухлинних клітин при раку, такому як пухлини, що більше інших сполук, включаючи, без обмеження: продукують АСТН, гострий лімфоцитарний лейкоз, сполуки, які сприяють включенню радіосенсибілігострий нелімфоцитарний лейкоз, рак кори наднизатора до клітини-мішені; сполуки, які регулюють ркової залози, рак сечового міхура, рак головного потік лікарських засобів, живильних речовин мозку, рак молочної залози, цервікальний рак, та/або кисню до клітини-мішені; хіміотерапевтичні хронічний лімфоцитарний лейкоз, хронічний мієагенти, які діють на пухлину з або без додаткового лоцитарний лейкоз, рак прямої кишки, лімфома Топромінення; або терапевтично ефективні сполуки клітин шкіри, внутрішньоматковий рак, рак страводля лікування раку чи іншого захворювання. Прикходу, саркома Юїнга, рак жовчного міхура, лейкоз лади додаткових терапевтичних агентів, які моворсинчастих клітин, рак голови та шиї, лімфома жуть бути використані разом з радіосенсибілізатоХоджкіна, саркома Капоші, рак нирки, рак легенів рами, включають, без обмеження: 5-фторурацил, (дрібноклітинний та/або недрібноклітинний), злоялейковорин, 5'-аміно-5'-дезокситимідин, кисень, кісний перитонеальний випіт, злоякісний плевракарбоген, переливання червоних клітин, перфтор 33 89618 34 вуглеці (наприклад, флуозоль 10DA), 2,3-DPG, BW12C, блокатори кальцієвих каналів, пентоксифілін, антиангіогенні сполуки, гідралазин та LBSO. Приклади хіміотерапевтичних агентів, які можуть бути використані разом з радіосенсибілізаторами, включають, без обмеження: адріаміцин, камптотецин, карбоплатин, цисплатин, даунорубіцин, доцетаксел, доксорубіцин, інтерферон (альфа, бета, Суміш 1-(4-аміно-3-нітрофеніл)-2-метил-1гамма), інтерлейкін 2, іринотекан, паклітаксел, пропанону (0,0144моль) у мурашиній кислоті топотекан та їхні терапевтично ефективні аналоги (4,93мл) та формаміді (18,2мл) перемішували при і похідні. 160°С протягом 15 годин, потім охолоджували до Хіміосенсибілізатори можуть бути введені ракімнатної температури, виливали в льодяну воду, зом з терапевтично ефективною кількістю однієї підлуговували концентрованим розчином гідрокабо більше інших сполук, включаючи, без обмесиду амонію та екстрагували EtOAc. Органічний ження: сполуки, які сприяють включенню хіміосеншар відокремлювали, осушали (MgSO4), фільтрусибілізаторів до клітини-мішені; сполуки, які регували та розчинник упарювали досуха, одержуючи люють потік лікарських засобів, живильних 4,8г проміжного продукту 1. речовин та/або кисню в клітину-мішень; хіміотераb) Одержання проміжного продукту 2 певтичні агенти, які діють на пухлину, або інші терапевтично активні сполуки для лікування раку чи іншого захворювання. Приклади додаткових терапевтичних засобів, які можуть бути використані разом з хіміосенсибілізаторами, включають, без обмеження: метилювальні агенти, інгібітори топоізомерази І та інші хіміотерапевтичні агенти, такі як цисплатин та блеоміцин. Сполуки формули (І) можуть також бути використані для визначення або ідентифікації рецепСуміш проміжного продукту 1 (0,0144моль) у торів PARP і, більш конкретно, рецепторів PARP-1. МеОН (50мл) гідрували під тиском 3бар протягом Для зазначеної мети сполуки формули (І) можуть 1 години з нікелем Ренея (3,4г) як каталізатором. бути міченими. Зазначена мітка може бути вибраПісля поглинання Н2 (3екв.) каталізатор відфільтна з групи, що складається з радіоізотопу, спінової ровували через це літ, промивали МеОН і фільтмітки, антигенної мітки, флуоресцентної групи або рат упарювали досуха. Продукт використовували хемілюмінесцентної групи ферменту. без додаткового очищення, одержуючи 4,7г проміНа сучасному рівні техніки буде легко визнажного продукту 2. чити ефективну кількість зарезультатами проб, Приклад А2 представлених нижче. Звичайно вважають, що Одержання проміжних продуктів 3 та 4 ефективна кількість становить від 0,01мг/кг до 100мг/кг маси тіла і, зокрема, від 0,05мг/кг до 10мг/кг маси тіла. Може бути доцільно вводити необхідну дозу у вигляді двох, трьох, чотирьох чи більше піддоз з відповідними інтервалами протягом дня. Зазначені піддози можуть бути виготовлені як стандартні лікарські форми, що містять, наприклад, від 0,5 до 500мг і, зокрема, від 1мг до 200мг активного інгредієнта на стандартну лікарХлорид алюмінію (0,6928моль) додавали порську форму. ціями до розчину хлорацетилхлориду (0,5196моль) Наступні приклади ілюструють даний винахід. в DCM (50,2мл), підтримуючи температуру нижче Експериментальна частина 30 С. Потім додавали 3-етил-2(1H)-хінолінон Далі "BuLi" позначає бутиллітій, "DC" позначає (0,1732моль), підтримуючи температуру нижче дихлорметан, "DIPE" позначає простий діізопропі30°С. Суміш перемішували та кип'ятили зі зворотловий ефір, «ДМФА» позначає Ν,Νним холодильником протягом 15 годин, охолоджудиметилформамід, "EtOAc" позначає етилацетат, вали та виливали в льодяну воду. Осад відфільт"EtOH" позначає етанол, "МЕК" позначає метилеровували, промивали водою та видаляли DCM. тилкетон, «МеОН» позначає метанол і ТГФ познаОрганічний розчин перемішували та фільтрували. чає тетрагідрофуран. Осад сушили, одержуючи 33,5г проміжного продуА. Одержання проміжних сполук кту 3. Фільтрат екстрагували. Органічний шар відоПриклад А1 кремлювали, осушали (MgSO4), фільтрували та а) Одержання проміжного продукту 1 розчинник упарювали досуха, одержуючи 20,46г проміжного продукту 4. Приклад A3 а) Одержання проміжного продукту 5 35 Суміш 6-бром-2-хлор-3-метилхіноліну (0,04483моль) і СН3ОNa (0,224моль) в МеОН (200мл) перемішували при 70°С протягом 36 годин. Суміш охолоджували, виливали на лід, додавали EtOAc та екстрагували EtOAc. Органічний шар промивали водою, осушали (MgSO4), відфільтровували та упарювали, одержуючи 11г (97%) проміжного продукту 5. b) Одержання проміжного продукту 6 1,6М BuLi у гексані (0,0619моль) додавали по краплях при -60°С в потоці N2 до суміші проміжного продукту 5 (0,0476моль) в ТГФ (200мл). Суміш перемішували при -60°С протягом 1 години. По краплях при -60°С додавали суміш 3(диметиламіно)-1-(2-фураніл)-1-пропанону (0,0571моль) у ТГФ (100мл). Суміш перемішували при -60°С протягом 2 годин і потім при -40°С протягом 1 години. Суміш виливали в насичений розчин хлориду амонію та екстрагували EtOAc. Органічний шар відокремлювали, осушали (MgSO4), фільтрували і розчинник упарювали. Продукт використовували без додаткового очищення, одержуючи 16,2г проміжного продукту 6. c) Одержання проміжного продукту 7 Суміш проміжного продукту 6 (0,0476моль) в ЗН соляній кислоті (254мл) і ТГФ (128мл) перемішували та кип'ятили зі зворотним холодильником протягом 6 годин. Суміш виливали на лід, підлуговували концентрованим розчином гідроксиду амонію та екстрагували EtOAc. Органічний шар відокремлювали, осушали (MgSO4), фільтрували та розчинник упарювали. Залишок очищали хроматографією на колонці із силікагелем (15-40мкм) (елюент: DCM/MeOH/NH4OH 95/5/0,2). Чисті фракції збирали та розчинник упарювали, одержуючи 4г (27%) проміжного продукту 7. Приклад А4 Одержання проміжного продукту 8 89618 36 1,6М н-BuLi у гексані (0,129моль) додавали по краплях при -60°С в потоці N2 до суміші 6-бром-3етил-2-метоксихіноліну (0,0996моль) у ТГФ (265мл). Суміш перемішували при -60°С протягом 1 години. Додавали по краплях при -60°С суміш 2етилбутаналю (0,119моль) у ТГФ (100мл). Суміш перемішували при -60°С протягом 2 годин, потім при -40°С протягом 1 години, виливали в насичений розчин хлориду амонію та екстрагували EtOAc. Органічний шар відокремлювали, осушали (MgSO4), фільтрували та розчинник упарювали. Продукт використовували без додаткового очищення, одержуючи 28,62г проміжного продукту 8. Приклад А5 a) Одержання проміжного продукту 9 Розчин (2-брометил)бензолу (0,174моль) в простому діетиловому ефірі (125мл) додавали по краплях при 0°С до суспензії Mg-стружки (0,21моль) в простому діетиловому ефірі (125мл) і суміш перемішували при 0°С протягом 1 години. Додавали по краплях при 0°С розчин 3-метил-6хінолінкарбоксальдегіду (0,116моль) у ТГФ (200мл) і суміш перемішували при кімнатній температурі протягом 2год. Суміш виливали в льодяну воду, фільтрували через целіт і продукт екстрагували EtOAc. Органічний шар промивали водою, осушали (MgSO4), фільтрували та упарювали. Залишок кристалізували із суміші EtOAc/простий діетиловий ефір, одержуючи 19г (59%) проміжного продукту 9. b) Одержання проміжного продукту 10 Перманганат калію (19г) додавали по краплях при 5°С в атмосфері N2 до розчину проміжного продукту 9 (0,069моль) в DCM (300мл) та трис[2(2-метоксіетоксі)етил]аміні (2мл) і суміш перемішували при кімнатній температурі протягом ночі. Суміш фільтрували через целіт і фільтрат упарювали, одержуючи 17г (90%) проміжного продукту 10. c) Одержання проміжного продукту 11 Розчин 3-хлорбензолкарбопероксокислоти (0,123моль) в DCM (200мл) додавали при 5°С в атмосфері N2 до розчину проміжного продукту 10 (0,062моль) в DCM (200мл), суміш перемішували при 5°С протягом 1 години, а потім при кімнатній температурі протягом 3 годин. Додавали водний 10%-ний карбонат калію та продукт екстрагували 37 89618 38 DCM. Органічний шар промивали водою, осушали суміш перемішували при 100°С протягом 3 годин. (MgSO4), відфільтровували та упарювали. Продукт Суміш виливали в льодяну воду, підлуговували використовували без додаткового очищення, одеNH4OH та екстрагували DCM. Суміш фільтрували ржуючи 18г (100%) проміжного продукту 11. через целіт і фільтрат декантували. Органічний d) Одержання проміжного продукту 12 шар осушали (MgSO4), відфільтровували та упарювали досуха. Залишок очищали хроматографією на колонці із силікагелем (35-70мкм) (елюент: DCM/MeOH/NH4OH 95/5/0,1). Чисті фракції збирали та упарювали. Залишок (4г) кристалізували з МЕК, одержуючи 2,12г (29%) сполуки 2, температура плавлення 211,4°С. Приклад В3 Одержання кінцевої сполуки 3 10%-ний карбонат калію (250мл) додавали при кімнатній температурі до розчину проміжного продукту 11 (0,062моль) в DCM (250мл) і суміш перемішували протягом 10хв. Порціями додавали тозилхлорид (0,093моль) і суміш перемішували при кімнатній температурі протягом 2 годин. Осад відфільтровували, промивали водою та сушили. Залишок (10,1г) перекристалізовували з 2-пропанону, одержуючи 2,8г (72%) проміжного продукту 12. В. Одержання кінцевих сполук Приклад В1 Одержання кінцевої сполуки 1 Суміш проміжного продукту 2 (0,011моль) та етилового ефіру 2-оксобутанової кислоти (0,022моль) в EtOH (40мл) перемішували при 60°С протягом 6 годин і потім охолоджували до кімнатної температури. Розчинник упарювали. Залишок видобували насиченим розчином NaHCO3. Суміш екстрагували DCM. Органічний шар відокремлювали, осушали (MgSO4), фільтрували та розчинник упарювали досуха. Залишок очищали хроматографією на колонці із силікагелем (15-40мкм) (елюент: DCM/MeOH/NH4OH 99/1/0,1 та 85/15/0,1). Чисті фракції збирали та розчинник упарювали. Залишок (1,9г) очищали хроматографією на колонці із силікагелем (15-40мкм) (елюент: циклогексан/2-пропанол/NН4ОН 88/12/1). Чисті фракції збирали та розчинник упарювали. Залишок кристалізували з DIPE. Осад відфільтровували та сушили, одержуючи 0,33г (11%) сполуки 1, температура плавлення 204°С. Приклад В2 Одержання кінцевої сполуки 2 Хлорид алюмінію (0,234моль) порціями додавали до розчину N-[4-[1-(1H-імідазол-1-іл)-2метилпропіл]феніл]-2-метил-3-феніл-2пропенаміду (0,026моль) у хлорбензолі (60мл) і Гідрохлорид диметиламіну (0,3моль) порціями додавали при кімнатній температурі в потоці N2 до суспензії карбонату калію (0,3603моль) у ДМФА (300мл). Суміш перемішували протягом 30хв. Обережно додавали суміш проміжного продукту 3 (0,06моль) і проміжного продукту 4 (0,06моль). Суміш перемішували при кімнатній температурі протягом 30хв. Додавали льодяну воду. Осад відфільтровували, промивали водою та фільтрат екстрагували DCM. Органічний шар відокремлювали, осушали (MgSO4), фільтрували та розчинник упарювали досуха. Залишок (16,6г) очищали хроматографією на колонці із силікагелем (20-45мкм) (елюент: DCM/MeOH/NH4OH 95/5/0,2). Чисті фракції збирали та розчинник упарювали. Залишок (4,9г) кристалізували з 2-пропанолу та МеОН. Осад відфільтровували та сушили, одержуючи 1,2г сполуки 3, температура плавлення 180°С. Приклад В4 Одержання кінцевої сполуки 4 Суміш проміжного продукту 7 (0,0113моль) у МеОН (60мл) гідрували при 40°С під тиском 4,8бар протягом 6год. з 10%-ним Pd/C (0,35г) як каталізатором. Після поглинання Н2 (1екв.) каталізатор відфільтровували через целіт і фільтрат упарювали. Залишок видобували водою і концентрованим розчином гідроксиду амонію та екстрагували DCM. Органічний шар відокремлювали, осушали (MgSO4), фільтрували і розчинник упарювали. Залишок очищали хроматографією на колонці із силікагелем (15-40мкм) (елюент: DCM/MeOH/NH4OH 95/5/0,5 та 93/7/0,5). Чисті фракції збирали та розчинник упарювали. Залишок кристалізували з 2пропанону та простого діетилового ефіру. Осад відфільтровували та сушили, одержуючи 0,69г (20%) сполуки 4. Приклад В5 39 Одержання кінцевої сполуки 5 Суміш проміжного продукту 8 (0,0996моль) в ЗН соляній кислоті (426мл) і ТГФ (274мл) перемішували при 70°С протягом ночі, потім виливали на лід, підлуговували концентрованим розчином NH4OH та екстрагували EtOAc. Органічний шар відокремлювали, осушали (MgSO4), фільтрували та розчинник упарювали. Залишок кристалізували з DCM. Осад відфільтровували та сушили, одержуючи 15,21г (56%) сполуки .5. Приклад В6 Одержання кінцевої сполуки 6 Суміш проміжного продукту 12 (0,013моль) у формаміді (61,8мл) та мурашиній кислоті (30мл) перемішували та кип'ятили зі зворотним холодильником протягом 36год. Суміш охолоджували до 89618 40 кімнатної температури, виливали в льодяну воду та відфільтровували. Осад промивали водою, 2пропаноном і простим діетиловим ефіром. Осад сушили та перекристалізовували із суміші МеОН/ТГФ, одержуючи 1,74г (40%) сполуки 6, температура плавлення 221,3°С. Приклад В7 Одержання кінцевої сполуки 7 Боргідрид натрію (0,051моль) додавали при 0°С в потоці N2 до розчину сполуки 3 (0,0116моль) у МеОН (50мл). Суміш перемішували протягом 1 години та виливали у воду. Органічний розчинник упарювали. Водний концентрат витягали DCM і водою та суміш екстрагували. Органічний шар відокремлювали, осушали (MgSO4), фільтрували та розчинник упарювали досуха. Залишок кристалізували з 2-пропанону та МеОН. Осад відфільтровували, промивали простим діетиловим ефіром і сушили, одержуючи 1,2г сполуки 7, температура плавлення 131°С. В таблиці F-1 наведені сполуки, які були одержані відповідно до одного з наведених прикладів. У таблицях використані такі скорочення. 41 89618 42 43 Фармакологічні приклади Аналіз інгібуючої активності PARP-1 in vitro з використанням близькості сцинтилляції Сполуки за даним винаходом були випробувані in vitro за методикою SPA (фірми Amersham Pharmacia Biotech). В принципі, аналіз стосується добре встановленої технології SPA для визначення полі(АDРрибозил)ювання біотинільованих білків-мішеней, тобто, гістонів. Зазначене рибозилювання індукують, використовуючи фермент PARP-1, активова3 ний «нік»-ДНК, і [ Н]-нікотинамідаденіновий динук3 + леотид ([ H]-NAD ) як ADP-рибозильний донор. Як стимулятор активності ферменту PARP-1 готовили «нік»-ДНК. Для цього 25мг ДНК (постачальник: Sigma) розчиняли в 25мл буферного розчину ДНКази (10мМ трис-НСІ, рН 7,4; 0,5мг/мл бичачого сироваткового альбуміну (BSA); 5мМ MgCl2·6H2O та 1мМ KСI), до якого додавали 50мкл розчину ДНКази (1мг/мл в 0,15М NaCl). Після інкубування протягом 90хв. при 37°С реакцію переривали додаванням 1,45г NaCl з наступним додатковим інкубуванням при 58°С протягом 15хв. Реакційну суміш охолоджували на льоді та діалізували при 4°С, відповідно, протягом 1,5 та 2 годин, 1,5л 0,2М KCl і двічі 1,5л 0,01М KCl протягом 1,5 та 2ч, відповідно. Аліквоти суміші зберігали при -20°С. Гістони (1мг/мл, тип ІІ-А, постачальник: Sigma) біотинілювали, використовуючи набір для біотинілювання Amersham і зберігали аліквоти при -20°С. Основний розчин гранул 100мг/мл SPA полі(вінілтолуол) (PVT) (постачальник: Amersham) готували в PBS. Основний розчин [3H]-NAD+ готували додаванням 120мкл [3H]-NAD+ (0,1мКі/мл, постачальник: NEN) до 6мл інкубаційного буферного розчину (50мМ трис/НСІ, рН 8; 0,2мМ DTT; 4 М MgCl2). Розчин 4мМ NAD+ (постачальник: Roche) готували в інкубаційному буферному розчині (з 100мМ основного розчину у воді, що зберігався при -20°С). Фермент PARP-1 одержували, використовуючи відому технологію, тобто, клонування та експресію білка, виходячи із кДНК печінки людини. Інформація, що стосується використання послідовності білка ферменту PARP-1l, включаючи літературні посилання, може бути знайдена в базі даних Swiss-Prot під первинним номером доступу Р09874. Біотині л ьовані гістони та гранули PVTSPA змішували та попередньо інкубували протягом 30хв. при кімнатній температурі. Фермент PARP-1 (часто залежно від концентрації) змішували з «нік»-ДНК і суміш попередньо інку бували протягом 30хв. при 4°С. Рівні частини зазначеного розчину гістонів/гранул PVT-SPA і розчину ферменту PARP-1/ДНК змішували та 75мкл зазначеної суміші разом з 1мкл сполуки в ДМСО та 25мкл 3 + [ H]-NAD вносили в лунки 96-лункового мікропланшета для титрування. Кінцеві концентрації інкубаційної суміші становили 2мкг/мл біотинільованих гістонів, 2мг/мл гранул PVT-SPA, 2мкг/мл «нік»ДНК та від 5 до 10мкг/мл ферменту PARP-1. Після інкубування суміші протягом 15хв. при кімнатній температурі реакцію переривали додаванням + 100мкл 4мМ NAD в інкубаційному буферному розчині (кінцева концентрація 2мМ) і планшети перемішували. 89618 44 Гранулам давали осаджуватися протягом щонайменше 15хв. і планшети переносили в TopCountNXT (Packard) для підрахунку сцинтиляції, значення виражали як число імпульсів за хвилину (срm). Для кожного експерименту паралельно проводили контрольні досліди (що містили фермент PARP-1 і ДМСО без сполуки), сліпе інкубування (що містить ДМСО, але без ферменту PARP-1 чи сполуки) та аналізи (що містять фермент PARP-1 і сполуку, розчинені в ДМСО). Всі випробувані сполуки розчиняли, а потім додатково розбавляли ДМСО. Спочатку сполуки випробову-6 вали в концентрації 10 Μ. Якщо сполука виявляла -6 активність при 10 М, будували криву залежності доза-відповідь, для якої сполуки випробовували при концентраціях від 10-5 Μ до 10-8Μ. В кожній пробі сліпе значення віднімали з контрольного та пробного значень. Контрольна проба представляла максимальну активність ферменту PARP-1. Для будь-якого зразка значення cpm виражали у відсотках від середнього значення cpm контролю. Якщо доцільно, обчислювали значення ІС50 (концентрацію лікарського засобу, необхідну для ослаблення активності ферменту PARP-1 на 50% від контрольної), використовуючи лінійну інтерполяцію між експериментальними точками вище та нижче рівня 50%. При цьому дію випробуваних сполук виражають як рІС50 (значення негативного логарифма величини ІС50). Для підтвердження правильності проби SPA включали еталонну сполуку, 4-аміно1,8-нафталімід. Випробувані сполуки виявили інгібуючу дію при початковій тестовій концентрації 106 Μ (див. таблицю 2). Аналіз інгібування активності ΡARP-1 in vitro фільтрацією Сполуки за даним винаходом були випробувані пробою фільтрації in vitro на активність PARP-1 (викликаною в присутності «нік»-ДНК) шляхом визначення активності полі(АDР-рибозил)ювання гістону із застосуванням [32P]-NAD як ADPрибозильного донора. Радіоактивні рибозильовані гістони осаджували трихлороцтовою кислотою (ТСА) в 96-лункові фільтраційні планшети і впроваджували сцинтиляційний лічильник, що викорис32 товує вимірювання [ Р]. Готували суміш гістонів (основний розчин: 5мг/мл в Н2О), NAD+ (основний розчин: 100мМ в 32 Н2О) і [ P]-NAD в інкубаційному буферному розчині (50мМ трис/НСІ, рН 8; 0,2мМ DTT; 4мМ MgCl2). Готували також суміш ферменту PARP-1 (5-10мкг/мл) і «нік»-ДНК. «Нік»-ДНК одержували, як описано в аналізі in vitro інгібуючої активності PARP-1 з використанням SPA. 75мкл суміші ферменту PARP-1/ДНК з 1мкл сполуки в ДМСО та 25мкл суміші гістон-NAD+/[32P]-NAD+ додавали в лунки 96-лункового фільтраційного планшета (0,45мкм, постачальник: Millipore). Кінцеві концентрації в інкубаційній суміші становили 2мкг/мл гіс+ 32 + тонів, 0,1мМ NAD , 200мкМ (0,5мкС) [ P]-NAD та 2мкг/мл «нік»-ДНК. Планшети інкубували протягом 15хв. при кімнатній температурі та реакцію переривали додаванням 10мкл охолодженої льодом 100%-ної ТСА з наступним додаванням 10мкл охолодженого льодом розчину BSA (1% у Н2О). Білкову фракцію залишали осаджуватися на 10хв. 45 89618 46 при 4°С та планшети відфільтровували у вакуумі. Потім кожну лунку планшета промивали 1мл 10%Таблиця 2 ної охолодженої льодом ТСА, 1мл 5%-ної та охолодженої льодом ТСА та 1мл 5%-ної ТСА при кімIn vitro SPA In vitro проба фільтСполука № натній температурі. Нарешті, до кожної лунки дорІС50 рування pIC50 давали 100мкл сцинтиляційного розчину 1 6,656 (Microscint 40, Packard) і планшети переносили в 2 6,282 5,272 TopCountNXT (постачальник: Packard) для під3 6,587 5,586 рахунку сцинтиляції та значення виражали як чис4 5,983 5,121 ло імпульсів за хвилину (cpm). Для кожного експе5 6,807 6,195 рименту паралельно проводили контрольні 6 6,114 5 досліди (що містять фермент PARP-1 і ДМСО без 7 6,674 6,112 сполуки), сліпе інкубування (що містить ДМСО, 8 6,011 але без ферменту PARP-1 або сполуки) і аналізи 9 6,129 (що містять фермент PARP-1 і сполуку, розчинену 10 6,131 в ДМСО). Всі сполуки розчиняли, а потім додатко11 6,485 во розбавляли ДМСО. Спочатку сполуки випробо-5 12 6,163 вували в концентрації 10 М. Якщо сполуки вияв-5 13 6,434 ляли активність при 10 М, будували криву залежності доза-відповідь, де сполуки випробову14 6,302 -5 -8 вали при концентраціях від 10 Μ до 10 М. В кож15 5,901 5,441 ній пробі сліпе значення віднімали з контрольного 16 6,328 5,665 та тестового значень. Контрольний зразок пред17 6,704 5,834 ставляв максимальну активність ферменту PARP18 5,99 5,196 1. Для кожного прикладу величину cpm виражали у 19 6,127 відсотках від середнього значення cpm контролю. 20 6,359 5,642 Якщо доцільно, обчислювали значення ІС50 (кон21 6,644 5,958 центрацію лікарського засобу, необхідну для 22 6,077 5,364 ослаблення активності ферменту PARP-1 на 50% 23 5,844 5,147 від контрольної), використовуючи лінійну інтерпо24 6,251 5,313 ляцію між експериментальними точками вище та 25 6 5,334 нижче 50%-го рівня. При цьому дію випробуваних сполук виражали як pIC50 (значення негативного Сполуки можуть бути додатково оцінені в прологарифма величини ІС50). Для підтвердження бі клітинної хіміо- та/або радіочутливости, в пробі, вірогідності фільтраційної проби як еталонну спощо вимірює інгібування активності ендогенної луку використовували 4-аміно-1,8-нафталімід. ВиPARP-1 у лініях ракових клітин і, зрештою, in vivo в пробувані сполуки виявили інгібуючу дію при почапробі на радіочутливість. тковій тестовій концентрації 10-5М (див. таблицю 2). Комп’ютерна верстка О. Гапоненко Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійською6-substituted 2-quinolinones and 2-quinoxalinones as poly(adp-ribose)polymerase inhibitors
Автори англійськоюMabire Dominique Jean-Pierre, Guillemont Jerome Emile Georges, Vandun Jacobus Alphonsus Josep, Somers Maria Victorina Francis, Wouters Walter Boudewijn Leopold
Назва патенту російською6-замещенные 2-хинолиноны и 2-хиноксалиноны как ингибиторы поли(адф-рибоза)полимеразы
Автори російськоюМабир Доминик Жан-Пьер, Жильмон Жером Эмиль Жорж, ван Дун Якобу Алфонсус Джосепхус, Сомерс Мария Викторина Франциска, Воутерс Валтер Боудевиджн Леопольд
МПК / Мітки
МПК: A61K 31/498, C07D 409/14, A61P 43/00, C07D 241/44, C07D 407/06, C07D 401/12
Мітки: інгібітори, 2-хінолінони, 6-заміщені, полі(адф-рибоза)полімерази, 2-хіноксалінони
Код посилання
<a href="https://ua.patents.su/23-89618-6-zamishheni-2-khinolinoni-ta-2-khinoksalinoni-yak-ingibitori-poliadf-ribozapolimerazi.html" target="_blank" rel="follow" title="База патентів України">6-заміщені 2-хінолінони та 2-хіноксалінони як інгібітори полі(адф-рибоза)полімерази</a>












