Заміщені біциклічні похідні для лікування аномального росту клітин
Номер патенту: 73990
Опубліковано: 17.10.2005
Автори: Морріс Джоел, Бхаттачаріа Саміт Кумар, Кат Джон Чарльз
Формула / Реферат
1. Сполука формули 1
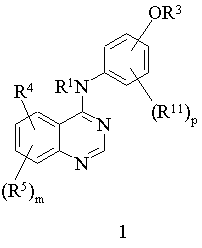
або її фармацевтично прийнятна сіль, сольват або проліки, де:
m дорівнює цілому числу від 0 до 3;
p дорівнює цілому числу від 0 до 4;
кожний з R1 і R2 незалежно вибраний з H і С1-С6-алкілу;
R3 - (CR1R2)t(4-10-членний гетероцикл), де t дорівнює цілому числу від 0 до 5, вказана гетероциклічна група необов'язково конденсована з бензольним кільцем або С5-С8-циклоалкільною групою, -(CR1R2)t-гpyпa вказаної вище R3-групи необов'язково включає подвійний або потрійний вуглець-вуглецевий зв'язок, a t дорівнює цілому числу в інтервалі між 2 і 5, і згадані вище R3 групи, що включають будь-які необов'язково конденсовані кільця, згадані вище, необов'язково заміщені 1-5 R8-групами;
R4 - -(CR16R17)m-C![]() C-(CR16R17)tR9, -(CR16R17)t-C=C-(CR16R17)t-R9, -(CR16R17)m-C
C-(CR16R17)tR9, -(CR16R17)t-C=C-(CR16R17)t-R9, -(CR16R17)m-C![]() C-(CR16R17)k-R13, -(CR16R17)m-C=C-(CR16R17)k-R13 або -(CR16R17)tR9, де приєднання до R9 відбувається через атом вуглецю R9-групи, кожне з k дорівнює цілому числу від 1 до 3, кожне з t дорівнює цілому числу від 0 до 5, і кожне з m дорівнює цілому числу від 0 до 3;
C-(CR16R17)k-R13, -(CR16R17)m-C=C-(CR16R17)k-R13 або -(CR16R17)tR9, де приєднання до R9 відбувається через атом вуглецю R9-групи, кожне з k дорівнює цілому числу від 1 до 3, кожне з t дорівнює цілому числу від 0 до 5, і кожне з m дорівнює цілому числу від 0 до 3;
кожний з R5 незалежно вибраний з галогену, гідрокси, NR1R2, С1-С6-алкілу, трифторметилу, С1-С6-алкокси, трифторметокси, -NR6C(O)R1, -C(O)NR6R7, -SO2NR6R7, -NR6C(O)NR7R1 i -NR6C(O)OR7;
кожний з R6, R6a i R7 незалежно вибраний з H, C1-С6-алкілу, групи -(CR1R2)t(С6-С10арил) і групи (CR1R2)t(4-10-членний гетероцикл), де t дорівнює цілому числу від 0 до 5, 1 або 2 кільцевих атомів вуглецю гетероцикличної групи необов'язково заміщені оксо(=O)-групою, алкільні, арильні і гетероциклічні групи згаданих вище R6 i R7-гpyп необов'язково заміщені 1-3-ма замісниками, незалежно вибраними з галогену, ціано, нітро, -NR1R2, трифторметилу, трифторметокси, С1-С6-алкілу, С2-С6-алкенілу, С2-С6-алкінілу, гідрокси і С1-С6-алкокси;
R6 і R7 або R6а і R7, коли вони приєднані до одного і того ж атома азоту, взяті разом, можуть утворювати 4-10-членне гетероциклічне кільце, яке може включати 1-3 додаткових гетерофрагментів, крім атома азоту, до якого вказані R6, R6а i R7 приєднані, вибраних з N, N(R1), О і S, при умові, що два атоми О, два атоми S або атоми О і S не сполучені безпосередньо один з одним;
кожний з R8 незалежно вибраний з груп: оксо(=О), галоген, ціано, нітро, трифторметокси, трифторметил, азидо, гідрокси, С1-С6-алкокси, С1-С10-алкілу, С2-С6-алкенілу, С2-С6-алкінілу, -C(О)R6, -C(О)OR6, -OC(О)R6, -NR6C(O)R7, -NR6SO2NR7R1, -NR6C(O)NR1R7, -NR6C(O)OR7, -C(O)NR6R7, -NR6R7, -NR6OR7, -SO2NR6R7, -S(O)j(C1-С6-алкіл) де j дорівнює цілому числу від 0 до 2,
-(CR1R2)t(С6-С10-арил), -(CR1R2)t(4-10-членний гетероцикл),
-(CR1R2)qC(O)(CR1R2)t(С6-С10-арил), -(CR1R2)qС(O)(CR1R2)t(4-10-членний гетероцикл), -(CR1R2)tО(CR1R2)q(С6-С10-арил), -(CR1R2)tO(CR1R2)q(4-10-членний гетероцикл), -(CR1R2)qS(O)j(CR1R2)t(С6-С10-арил) і -(CR1R2)qS(O)j(CR1R2)t(4-10-членний гетероцикл), де j дорівнює 0, 1 або 2; кожне з q і t незалежне дорівнює цілому числу від 0 до 5; 1 або 2 кільцевих атоми вуглецю гетероциклічних груп згаданих вище R8-гpyп необов'язково заміщені оксо(=O)-фрагментом, і алкільні, алкенільні, алкінільні, арильні і гетероциклічні групи згаданих вище R8 груп необов'язково заміщені 1-3 замісниками, незалежно вибраними з галогену, ціано, нітро, трифторметилу, трифторметокси, азидо, -OR6, -C(O)R6, -C(O)OR6, -OC(O)R6, -NR6C(O)R7, -С(O)NR6R7, -NR6R7, -NR6OR7, C1-С6-алкілу, С2-С6 алкенілу, С2-С6 алкінілу, груп -(CR1R2)t(С6-С10-арил) і -(CR1R2)t(4-10-членний гетероцикл), де t дорівнює цілому числу від 0 до 5;
R9 - неароматичне моноциклічне кільце, конденсоване або пов'язане містком біциклічне кільце або спіроциклічне кільце, де вказане кільце містить від 3 до 12 атомів вуглецю, в яких від 0 до 3 атомів вуглецю необов'язково заміщені гетерофрагментом, незалежно вибраними з N, О, S(O)j-, де j дорівнює цілому числу від 0 до 2, і -NR1-, при умові, що два атоми О, два S(О)j-фрагменти, атом О і S(O)j-фрагмент, атом N і атом S або атом N і атом О не сполучені безпосередньо один з одним в межах вказаного кільця, і де атоми вуглецю вказаного кільця необов'язково заміщені 1 або 2-ма R8-групами;
кожний R11 незалежно вибраний із замісників, вказаних при визначенні R8, при умові, що R11 не є оксо(=O)-групою;
R12 являє собою R6, -OR6, -OC(O)R6, -ОС(O)NR6R7, -OCO2R6, -S(O)jR6, -S(O)jNR6R7, -NR6R7, -NR6C(O)R7, -NR6SO2R7, -NR6C(O)NR6aR7, -NR6SO2NR6aR7, -NR6CO2R7, CN, -C(O)R6 або галоген, де j дорівнює цілому числу від 0 до 2;
R13 є NR1R14 або -OR14;
R14 є H, R15, -C(O)R15, -SO2R15, -C(O)NR15R7, -SO2NR15R7 або -CO2R15;
R15 - R18, -(CR1R2)t(С6-С10-арил), -(CR1R2)t(4-10-членний гетероцикл), де t дорівнює цілому числу від 0 до 5, 1 або 2 кільцевих атоми вуглецю гетероциклічної групи необов'язково заміщені оксо(=O)-фрагментом, і арильна і гетероциклічна група вказаних вище R15-гpyп необов'язково заміщені 1-3 R8-замісниками;
кожний з R16 і R17 незалежно вибраний з Н, С1-С6-алкілу і -СН2ОН, або R16 і R17, взяті разом, являють собою -СН2СН2- або -СН2СН2СН2-групу;
R18 являє собою С1-С6-алкіл, де кожний вуглець, не пов'язаний з атомом N або О або з S(O)j, де j дорівнює цілому числу від 0 до 2, необов'язково заміщений R12;
і де будь-який з вищезазначених замісників, що містить групи СН3(метил), СН2(метилен) або СН(метин), який не пов'язаний з галогеном, SO або SО2-групою або з атомами N, О або S, необов'язково заміщений групою, вибраною з гідрокси, галогену, С1-С4-алкілу, С1-С4-алкокси і -NR1R2.
2. Сполука за п. 1, де R3 являє собою (CR1R2)t(4-10-членний гетероцикл), де t дорівнює цілому числу від 0 до 5; вказана гетероциклічна група необов'язково конденсована з бензольним кільцем або С5-С8-циклоалкільною групою, і згадані вище R3-групи, включаючи будь-які необов'язково конденсовані кільця, згадані вище, необов'язково заміщені 1-3 R8-групами.
3. Сполука за п. 1, де R3 - -(CR1R2)t(4-10-членний гетероцикл), де t дорівнює цілому числу від 0 до 5, і згадані вище R3-групи необов'язково заміщені 1-3 R8-групами.
4. Сполука за п. 1, де R3 вибраний з
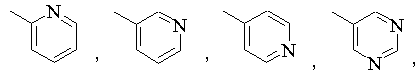
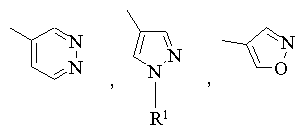
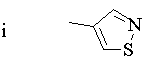 ,
,
де згадані вище R3-групи необов'язково заміщені 1-3-ма R8-групами.
5. Сполука за п. 1, де R3 - піридин-3-іл, необов'язково заміщений 1-3 групами R8.
6. Сполука за п. 1, де наступний структурний фрагмент сполуки формули 1
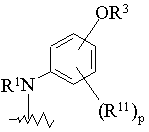
вибраний з групи, що складається з
3-метил-4-(піридин-2-ілокси)феніламіно,
3-хлор-4-(піридин-2-ілокси)феніламіно,
3-метокси-4-(піридин-2-ілокси)феніламіно,
4-(піридин-2-ілокси)феніламіно,
2-метил-4-(піридин-2-ілокси)феніламіно,
2-метокси-4-(піридин-2-ілокси)феніламіно,
3-хлор-4-(6-метилпіридин-2-ілокси)феніламіно,
3-метокси-4-(6-метилпіридин-2-ілокси)феніламіно,
3-метил-4-(6-метилпіридин-2-ілокси)феніламіно,
2-метокси-4-(6-метилпіридин-2-ілокси)феніламіно,
2-метил-4-(6-метилпіридин-2-ілокси)феніламіно,
4-(6-метилпіридин-2-ілокси)феніламіно,
3-метокси-4-(2-метилпіридин-3-ілокси)феніламіно,
3-метил-4-(2-метилпіридин-3-ілокси)феніламіно,
3-хлор-4-(2-метилпіридин-3-ілокси)феніламіно,
2-метокси-4-(2-метилпіридин-3-ілокси)феніламіно,
2-метил-4-(2-метилпіридин-3-ілокси)феніламіно,
4-(2-метилпіридин-3-ілокси)феніламіно,
3-метил-4-(6-метилпіридин-3-ілокси)феніламіно,
3-хлор-4-(6-метилпіридин-3-ілокси)феніламіно,
3-метокси-4-(6-метилпіридин-3-ілокси)феніламіно,
2-метил-4-(6-метилпіридин-3-ілокси)феніламіно,
2-метокси-4-(6-метилпіридин-3-ілокси)феніламіно,
4-(6-метилпіридин-3-ілокси)феніламіно,
3-метил-4-(піридин-3-ілокси)феніламіно,
3-хлор-4-(піридин-3-ілокси)феніламіно,
3-метокси-4-(піридин-3-ілокси)феніламіно,
2-метил-4-(піридин-3-ілокси)феніламіно,
2-метокси-4-(піридин-3-ілокси)феніламіно,
4-(піридин-3-ілокси)феніламіно,
3-метил-4-(2-метилпіримідин-5-ілокси)феніламіно,
3-хлор-4-(2-метилпіримідин-5-ілокси)феніламіно,
3-метокси-4-(2-метилпіримідин-5-ілокси)феніламіно,
2-метил-4-(2-метилпіримідин-5-ілокси)феніламіно,
2-метокси-4-(2-метилпіримідин-5-ілокси)феніламіно,
4-(2-метилпіримідин-5-ілокси)феніламіно,
3-метил-4-(4-метилпіримідин-5-ілокси)феніламіно,
3-хлор-4-(4-метилпіримідин-5-ілокси)феніламіно,
3-метокси-4-(4-метилпіримідин-5-ілокси)феніламіно,
2-метил-4-(4-метилпіримідин-5-ілокси)феніламіно,
2-метокси-4-(4-метилпіримідин-5-ілокси)феніламіно,
4-(4-метилпіримідин-5-ілокси)феніламіно,
3-метил-4-(2-метилпіридин-4-ілокси)феніламіно,
3-хлор-4-(2-метилпіридин-4-ілокси)феніламіно,
3-метокси-4-(2-метилпіридин-4-ілокси)феніламіно,
2-метил-4-(2-метилпіридин-4-ілокси)феніламіно,
2-метокси-4-(2-метилпіридин-4-ілокси)феніламіно,
4-(2-метилпіридин-4-ілокси)феніламіно,
3-метил-4-(піридин-4-ілокси)феніламіно,
3-хлор-4-(піридин-4-ілокси)феніламіно,
3-метокси-4-(піридин-4-ілокси)феніламіно,
2-метил-4-(піридин-4-ілокси)феніламіно,
2-метокси-4-(піридин-4-ілокси)феніламіно,
4-(піридин-4-ілокси)феніламіно,
3-метил-4-(2-метилпіримідин-4-ілокси)феніламіно,
3-метокси-4-(2-метилпіримідин-4-ілокси)феніламіно,
3-хлор-4-(2-метилпіримідин-4-ілокси)феніламіно,
2-метил-4-(2-метилпіримідин-4-ілокси)феніламіно,
2-метокси-4-(2-метилпіримідин-4-ілокси)феніламіно,
4-(2-метилпіримідин-4-ілокси)феніламіно,
3-метил-4-(6-метилпіримідин-4-ілокси)феніламіно,
3-метокси-4-(6-метилпіримідин-4-ілокси)феніламіно,
3-хлор-4-(6-метилпіримідин-4-ілокси)феніламіно,
2-метил-4-(6-метилпіримідин-4-ілокси)феніламіно,
2-метокси-4-(6-метилпіримідин-4-ілокси)феніламіно,
4-(6-метилпіримідин-4-ілокси)феніламіно,
3-метил-4-(піразин-2-ілокси)феніламіно,
3-метокси-4-(піразин-2-ілокси)феніламіно,
3-хлор-4-(піразин-2-ілокси)феніламіно,
2-метил-4-(піразин-2-ілокси)феніламіно,
2-метокси-4-(піразин-2-ілокси)феніламіно,
4-(піразин-2-ілокси)феніламіно,
3-хлор-4-(3-метилпіразин-2-ілокси)феніламіно,
3-метокси-4-(3-метилпіразин-2-ілокси)феніламіно,
3-метил-4-(3-метилпіразин-2-ілокси)феніламіно,
2-метокси-4-(3-метилпіразин-2-ілокси)феніламіно,
2-метил-4-(3-метилпіразин-2-ілокси)феніламіно,
4-(3-метилпіразин-2-ілокси)феніламіно,
3-хлор-4-(5-метилпіразин-2-ілокси)феніламіно,
3-метокси-4-(5-метилпіразин-2-ілокси)феніламіно,
3-метил-4-(5-метилпіразин-2-ілокси)феніламіно,
2-метокси-4-(5-метилпіразин-2-ілокси)феніламіно,
2-метил-4-(5-метилпіразин-2-ілокси)феніламіно,
4-(5-метилпіразин-2-ілокси)феніламіно,
3-хлор-4-(6-метилпіразин-2-ілокси)феніламіно,
3-метокси-4-(6-метилпіразин-2-ілокси)феніламіно,
3-метил-4-(6-метилпіразин-2-ілокси)феніламіно,
2-метокси-4-(6-метилпіразин-2-ілокси)феніламіно,
2-метил-4-(6-метилпіразин-2-ілокси)феніламіно,
4-(6-метилпіразин-2-ілокси)феніламіно,
3-метил-4-(піридазин-3-ілокси)феніламіно,
3-хлор-4-(піридазин-3-ілокси)феніламіно,
3-метокси-4-(піридазин-3-ілокси)феніламіно,
2-метил-4-(піридазин-3-ілокси)феніламіно,
2-метокси-4-(піридазин-3-ілокси)феніламіно,
4-(піридазин-3-ілокси)феніламіно,
3-метил-4-(6-метилпіридазин-3-ілокси)феніламіно,
3-хлор-4-(6-метилпіридазин-3-ілокси)феніламіно,
3-метокси-4-(6-метилпіридазин-3-ілокси)феніламіно,
2-метил-4-(6-метилпіридазин-3-ілокси)феніламіно,
2-метокси-4-(6-метилпіридазин-3-ілокси)феніламіно,
4-(6-метилпіридазин-3-ілокси)феніламіно,
3-метил-4-(6-метилпіридазин-4-ілокси)феніламіно,
3-хлор-4-(6-метилпіридазин-4-ілокси)феніламіно,
3-метокси-4-(6-метилпіридазин-4-ілокси)феніламіно,
2-метил-4-(6-метилпіридазин-4-ілокси)феніламіно,
2-метокси-4-(6-метилпіридазин-4-ілокси)феніламіно,
4-(6-метилпіридазин-4-ілокси)феніламіно,
3-метил-4-(3-метилпіридазин-4-ілокси)феніламіно,
3-хлор-4-(3-метилпіридазин-4-ілокси)феніламіно,
3-метокси-4-(3-метилпіридазин-4-ілокси)феніламіно,
2-метил-4-(3-метилпіридазин-4-ілокси)феніламіно,
2-метокси-4-(3-метилпіридазин-4-ілокси)феніламіно,
4-(3-метилпіридазин-4-ілокси)феніламіно,
3-метил-4-(піридазин-4-ілокси)феніламіно,
3-хлор-4-(піридазин-4-ілокси)феніламіно,
3-метокси-4-(піридазин-4-ілокси)феніламіно,
2-метил-4-(піридазин-4-ілокси)феніламіно,
2-метокси-4-(піридазин-4-ілокси)феніламіно,
4-(піридазин-4-ілокси)феніламіно,
3-хлор-4-(1-метил-1Н-піразол-4-ілокси)феніламіно,
3-метокси-4-(1-метил-1Н -піразол-4-ілокси)феніламіно,
З -метил-4-(1-метил-1Н-піразол-4-ілокси)феніламіно,
2-метокси-4-(1-метил-1Н-піразол-4-ілокси)феніламіно,
2-метил-4-(1-метил-1Н-піразол-4-ілокси)феніламіно і
4-(1-метил-1Н-піразол-4-ілокси)феніламіно.
7. Сполука за п. 1, де R4 - -(CR16R17)m-C![]() С(CR16R17)tR9, де m дорівнює цілому числу від 0 до 3, a t дорівнює цілому числу від 0 до 5.
С(CR16R17)tR9, де m дорівнює цілому числу від 0 до 3, a t дорівнює цілому числу від 0 до 5.
8. Сполука за п. 1, де R4 - -(CR16R17)m-C![]() С(CR16R17)tR9, де m дорівнює цілому числу від 0 до 3, a t дорівнює цілому числу від 0 до 5, і де R9 вибраний з 3-піперидинілу і 4-піперидинілу, кожний з яких необов'язково заміщений 1 або 2 групами R8.
С(CR16R17)tR9, де m дорівнює цілому числу від 0 до 3, a t дорівнює цілому числу від 0 до 5, і де R9 вибраний з 3-піперидинілу і 4-піперидинілу, кожний з яких необов'язково заміщений 1 або 2 групами R8.
9. Сполука за п. 1, де R4 - -(CR16R17)m-C=С-(CR16R17)t-R9, де m дорівнює цілому числу від 0 до 3, a t дорівнює цілому числу від 0 до 5.
10. Сполука за п. 1, де R4 - -(CR16R17)m-C=С-(CR16R17)t-R9, де m дорівнює цілому числу від 0 до 3, a t дорівнює цілому числу від 0 до 5, і де R9 вибраний з 3-піперидинілу і 4-піперидинілу (необов'язково заміщених 1 або 2 групами R8).
11. Сполука за п. 1, де R4 - -(CR16R17)m-C![]() С-(CR16R17)kR13, де k дорівнює цілому числу від 1 до 3, a m дорівнює цілому числу від 0 до 3.
С-(CR16R17)kR13, де k дорівнює цілому числу від 1 до 3, a m дорівнює цілому числу від 0 до 3.
12. Сполука за п. 1, де R4 - -(CR16R17)m-C![]() С-(CR16R17)kR13, де k дорівнює цілому числу від 1 до 3, і m дорівнює цілому числу від 0 до 3, де R13 - -NR1R14, де R14 вибраний з груп -C(O)R15, -SO2R15 i -C(O)NR15R7.
С-(CR16R17)kR13, де k дорівнює цілому числу від 1 до 3, і m дорівнює цілому числу від 0 до 3, де R13 - -NR1R14, де R14 вибраний з груп -C(O)R15, -SO2R15 i -C(O)NR15R7.
13. Сполука за п. 1, де R4 - -(CR16R17)m-C=С-(CR16R17)kR13, де k дорівнює цілому числу від 1 до 3, і m дорівнює цілому числу від 0 до 3.
14. Сполука за п. 1, де R4 - -(CR16R17)m-C=С-(CR16R17)kR13, де k дорівнює цілому числу від 1 до 3, і m дорівнює цілому числу від 0 до 3, де R13 - -NR1R14, де R14 вибраний з груп -C(O)R15, -SO2R15 i -C(O)NR15R7.
15. Сполука за п. 1, де R4 - -(CR16R17)m-C![]() С-(CR16R17)kR13 або -(CR16R17)m-C=С-(CR16R17)kR13, де k дорівнює цілому числу від 1 до 3, і m дорівнює цілому числу від 0 до 3, R13 - -NR1R14 або -OR14, R14 - R15, R15 - R18, і R18 - C1-С6-алкіл, необов'язково заміщений -OR6, -S(O)jR6, -NR6R7, -NR6C(O)R7, -NR6SO2R7, -NR6CO2R7, CN, -C(O)R6 або галогеном.
С-(CR16R17)kR13 або -(CR16R17)m-C=С-(CR16R17)kR13, де k дорівнює цілому числу від 1 до 3, і m дорівнює цілому числу від 0 до 3, R13 - -NR1R14 або -OR14, R14 - R15, R15 - R18, і R18 - C1-С6-алкіл, необов'язково заміщений -OR6, -S(O)jR6, -NR6R7, -NR6C(O)R7, -NR6SO2R7, -NR6CO2R7, CN, -C(O)R6 або галогеном.
16. Сполука за п. 1, вибрана з групи, що складається із сполук:
(±)-[3-метил-4-(піридин-3-ілокси)феніл]-(6-піперидин-3-ілетинілхіназолін-4-іл)амін;
2-метокси-N-(3-{4-[3-метил-4-(піридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-ініл)ацетамід;
(±)-[3-метил-4-(6-метилпіридин-3-ілокси)феніл]-(6-піперидин-3-ілетинілхіназолін-4-іл)амін;
2-метокси-N-(3-{4-[3-метил-4-(2-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-ініл)ацетамід;
[3-метил-4-(2-метилпіридин-3-ілокси)феніл]-(6-піперидин-4-ілетинілхіназолін-4-іл)амін;
[3-метил-4-(6-метилпіридин-3-ілокси)феніл]-(6-піперидин-4-ілетинілхіназолін-4-іл)амін;
2-метокси-N-(3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-ініл)ацетамід;
2-фтор-N-(3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-ініл)ацетамід;
Е-2-метокси-N-(3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}аліл)ацетамід;
[3-метил-4-(піридин-3-ілокси)феніл]-(6-піперидин-4-ілетинілхіназолін-4-іл)амін;
2-метокси-N-(1-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-ілетиніл}циклопропіл)ацетамід;
Е-N-(3-{4-[3-хлор-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}аліл)-2-метоксіацетамід;
N-(3-{4-[3-хлор-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-ініл)ацетамід;
N-(3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл)проп-2-ініл)ацетамід;
Е-N-(3-{4-[3-хлор-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}аліл)ацетамід;
Е-2-етокси-N-(3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}аліл)ацетамід;
1-етил-3-(3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-ініл)сечовина;
(3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-ініл)амідпіперазин-1-карбонової кислоти;
(±)-(3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-ініл)амід-2-гідроксиметилпіролідин-1-карбонової кислоти;
2-диметиламіно-N-(3-{4-[3-метил-4-(піридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-ініл)ацетамід;
Е-N-(3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}аліл)метансульфонамід;
(3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-ініл)амідізоксазол-5-карбонової кислоти;
1-(1,1-диметил-3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-ініл)-3-етилсечовина;
і фармацевтично прийнятні солі, проліки і сольвати згаданих вище сполук.
17. Спосіб лікування аномального росту клітин у ссавців, що включає введення вказаному ссавцеві сполуки за п. 1 в ефективній для лікування аномального росту клітин кількості.
18. Спосіб за п. 17, де вказаний аномальний ріст клітин представляє злоякісне новоутворення.
19. Спосіб за п. 18, де вказане злоякісне новоутворення вибрано з раку легенів, раку кістки, раку підшлункової залози, раку шкіри, пухлини голови або шиї, шкіряної або внутрішньоочної меланоми, раку матки, раку яєчника, раку прямої кишки, раку анальної області, раку шлунка, раку товстої кишки, раку молочної залози, раку матки, карциноми фаллопієвих труб, карциноми ендометрію, карциноми шийки матки, карциноми піхви, карциноми вульви, хвороби Ходжкіна, раку стравоходу, раку тонкої кишки, раку ендокринної системи, раку щитовидної залози, раку паращитовидної залози, раку надниркової залози, саркоми м'яких тканин, раку уретри, раку статевого члена, раку простати, хронічної або гострої лейкемії, лімфолімфом, раку сечового міхура, раку нирки або сечоводу, карциноми клітин ниркового епітелію, карциноми ниркової миски, неоплазм центральної нервової системи (ЦНС), первинної лімфоми ЦНС, пухлин хребта, гліоми стовбура мозку, аденоми гіпофіза або поєднання одного або більше з вищеперелічених злоякісних новоутворень.
20. Спосіб лікування аномального росту клітин у ссавців, який включає введення вказаному ссавцеві сполуки за п. 1 в ефективній для лікування аномального росту клітин кількості в поєднанні з антипухлинним агентом, вибраним з групи, що складається з мітотичних інгібіторів, алкілуючих агентів, антиметаболітів, інтеркалуючих антибіотиків, інгібіторів фактора росту, радіації, інгібіторів клітинного циклу, ферментів, інгібіторів топоізомерази, модифікаторів біологічної відповіді, антитіл, цитотоксинів, антигормонів і антиандрогенів.
21. Фармацевтична композиція для лікування аномального росту клітин у ссавців, що включає сполуку за п. 1 в ефективній для лікування аномального росту клітин кількості і фармацевтично прийнятний носій.
Текст
Даний винахід відноситься до нових біциклічних похідних, які застосовуються для лікування аномального росту клітин, яким є рак у ссавців. Даний винахід також відноситься до способу застосування таких сполук для лікування аномального росту клітин у ссавців, головним чином, у людини і до фармацевтичних композицій, що містять такі сполуки. Відомо, що клітина може стати злоякісною внаслідок трансформації частині її ДНК в онкоген (тобто в ген, активація якого веде до утворення клітин злоякісної пухлини). Багато які онкогени кодують білки, що є аберантними тирозинкіназами, здатними викликати трансформацію клітини. З іншого боку, експресія в підвищених кількостях нормальної протоонкогенної тирозинкінази може також привести до проліферативних порушень, що іноді закінчуються злоякісним фенотипом. Рецепторні тирозинкінази являють собою ферменти, які пронизують клітинну мембрану і володіють позаклітинним доменом, зв'язуючим фактори росту, такі як епідермальний фактор росту, трансмембранним доменом і внутрішньоклітинною частиною, яка функціонує як кіназа для фосфорилювання специфічних залишків тирозину в білках і, отже, впливає на проліферацію клітин. Інші рецепторні тирозинкінази включають c-erbB-2, c-met, tie-2, PDGFr, FGFr i VEGFR. Відомо, що такі кінази часто аберантно експресуються, як правило, при ракових новоутвореннях людини, таких як рак молочної залози, злоякісні новоутворення шлунково-кишкового тракту, такі як рак товстої кишки, прямої кишки або рак шлунка, при лейкозі і ракові яєчників, бронхів або підшлункової залози. Також було показано, що при багатьох злоякісних утвореннях людини, таких як пухлини мозку, легенів, плоскоклітинний рак, рак сечового міхура, шлунка, молочної залози, голови і шиї, стравоходу, при гінекологічних пухлинах і пухлинах щитовидної залози рецептор епідермального фактора росту (EGFR), який володіє тирозинкіназною активністю, мутований і/або експресований в підвищених кількостях. Відповідно було визнано, що інгібітори рецепторних тирозинкіназ застосовні як селективні інгібітори росту ракових клітин у ссавців. Наприклад, ербстатин, інгібітор тирозинкінази, селективно зменшує у бестимусних «голих» мишей ріст трансплантованої карциноми молочної залози людини, яка експресує рецепторні тирозинкінази епідермального фактора росту (EGFR), але не діє на ріст іншої карциноми, яка не експресує EGF-рецептор. Таким чином, сполуки даного винаходу, що є селективними інгібіторами деяких рецепторних тирозинкіназ, застосовні для лікування аномального росту клітин, зокрема, раку у ссавців. Крім рецепторних тирозинкіназ, сполуки даного винаходу можуть також виявляти інгібіторну активність проти ряду інших нерецепторних тирозинкіназ (наприклад: lck, src, abl) або серин/треонінкіназ (наприклад: циклінзалежних кіназ). Багато які інші сполуки, такі як похідні стиролу, також, мабуть, володіють властивостями інгібувати тирозинкіназу. У п'яти раніше опублікованих Європейських патентах, а саме, [в ЕР 0566226 А1 (опублікованому 20 жовтня 1993), ЕР 0602851 А1 (опублікованому 22 червня 1994), ЕР 0635507 А1 (опублікованому 25 січня 1995), ЕР 0635498 А1 (опублікованому 25 січня 1995) і ЕР 0520722 А1 (опублікованому 30 грудня 1992)] повідомляється про деякі біциклічні похідні, зокрема, про похідні хіназоліну, що володіють антиканцерогенними властивостями внаслідок їх здатності інгібувати тирозинкіназу. У міжнародній заявці [на патент WO 92/20642 (опублікованій 26 листопада 1992)] також повідомляється про деякі сполуки біс-моно- і біциклічних арилів і гетероарилів як інгібітори тирозинкінази, які застосовуються для інгібування аномальної проліферації клітин. У міжнародних заявках [на патент WO 96/16960 (опублікованій 6 червня 1996), WO 96/09294 (опублікованій 6 березня 1996), WO 97/30034 (опублікованій 21 серпня 1997), WO 98/02434 (опублікованій 22 січня 1998), WO 98/02437 (опублікованій 22 січня 1998) і WO 98/02438 (опублікованій 22 січня 1998)] також повідомляється про заміщені біциклічні гетероароматичні похідні як інгібітори тирозинкінази, які застосовуються для тієї ж самої мети. В інших заявках [на патент США №09/488350 (зареєстрованої 20 січня 2000) і 09/488378 (зареєстрованої 20 січня 2000)], обидві з яких включені тут в повному об'ємі шляхом посилання, також повідомляється про антиканцерогенні сполуки. Короткий зміст винаходу Даний винахід відноситься до сполук формули 1 і до їх фармацевтично прийнятних солей, сольватів і проліків, де: m дорівнює цілому числу від 0 до 3; p дорівнює цілому числу від 0 до 4; кожний з R1 і R2 незалежно вибраний з Η і С 1-С6-алкілу; R3 представляє (СR1R2)t(4-10-членний гетероцикл), де t дорівнює цілому числу від 0 до 5; вказана гетероциклічна група необов'язково конденсована з бензольним кільцем або С 5-С8-циклоалкільною групою; (CR1R2)t-група згаданої вище R 3-гр упи необов'язково містить подвійний або потрійний вуглець-вуглецевий зв'язок, t дорівнює цілому числу між 2 і 5, і вищезазначені R3-групи, що включають будь-які, необов'язкові конденсовані кільця, згадані вище, необов'язково заміщені 1-5 R 8-групами; R4 представляє -(CR16R17)m-CºС-(CR16R17)tR9; -(CR16R 17) m-C=C-(CR 16R17)t-R9 ; -(CR16R17) m-C C-(CR16R17) kR13; -(CR16R17)m-C=C-(CR 16R17) kR13 або -(CR16R17),R9 , де приєднання до R9 відбувається через атом вуглецю R9групи; кожне з k дорівнює цілому числу від 1 до 3; кожне з t дорівнює цілому числу від 0 до 5; і кожне з m дорівнює цілому числу від 0 до 3; кожний з R5 незалежно вибраний з галогену, гідрокси, -NR1R2, С1-С6-алкілу, трифторметилу, С1-С6алкокси, трифторметокси, -NR6C(O)R1, -C(O)NR6R7, -SO 2NR6R7, -NR 6C (O)NR7R1 і -NR6C(O)OR 7; кожний з R6, R6a і R7 незалежно вибраний з Н, С1-С6-алкілу, групи -(CR1R2)t(С6-С10-арил) і групи (CR1R2)t(4-10-членний гетероцикл), де t дорівнює цілому числу від 0 до 5; 1 або 2 кільцевих вуглецевих атомів гетероциклічної групи необов'язково заміщені оксо(=О)-фрагментом, алкільні, арильні і гетероциклічні групи згаданих вище R6 і R7-груп необов'язково заміщені 1-3 замісниками, незалежно вибраними з галогену, ціано- і нітро-груп, -NR1R2, трифторметилу, три фторметокси, С1-С6-алкілу, С2-С6-алкенілу, С2-С6-алкінілу, гідрокси і С 1С6-алкокси; R6 і R7 або R6a і R7, коли приєднані до атома азоту (до одного і того ж атому азоту, або двох окремих атомів азоту поблизу один одного через проміжний зв'язок, наприклад, -С(О) або -SO2-), взяті разом, можуть утворити 4-10-членне гетероциклічне кільце, яке може включати крім азоту, до якого приєднані вказані R6, R6a і R7, 1-3 додаткових гетероатоми (фрагменти), вибраних з N, N(R1), О і S, при умові, що два атоми О, два атоми S або атоми О і S не сполучені безпосередньо один з одним; кожний R8 незалежно вибраний з оксо(=О), галогену, ціано, нітро, трифторметокси, трифторметилу, азидо, гідрокси, С1-С6-алкокси, С1-С10-алкілу, С2-С6-алкенілу, С2-С6-алкінілу, -C(O)R6, -C(O)OR 6, -OC(O)R 6, NR6C(O)R7, -NR6SO2NR7R1, -NR6C(O)NR1R7, -NR6C(O)OR 7, -C(O)NR6R7, -NR6R7, -NR6OR7 , -SO2NR6R7 , гр упи S(О)j(С1-С6-алкіл), де j дорівнює цілому числу від 0 до 2, з гр уп -(CR1R2)t(С6-С10-арил), -(CR1R2)t(4-10-членний гетероцикл), -(CR1R2)q C(O)(CR1R2)t(С6-С10-арил), -(CR1R2)q C(О)(CR1R2)t(4-10-членний гетероцикл), 1 2 1 2 1 2 1 2 (CR R )tO(CR R )q (С6-С10-арил); (CR R )tO(CR R )q (4-10 членний гетероцикл), -(CR1R2)q S(O)j(CR1R2)t(С6-С10арил) і групи -(CR1R2)q S(O)j(CR1R2)t(4-10-членний гетероцикл), де j дорівнює 0, 1 або 2; кожне з q і t незалежне дорівнює цілому числу від 0 до 5; 1 або 2 кільцевих атомів вуглецю гетероциклічних груп згаданих вище R8груп необов'язково заміщені оксо(=О)-фрагментом і алкільні, алкенільні, алкінільні, арильні і гетероциклічні групи ви щезазначених R8-гр уп необов'язково заміщені 1-3 замісниками, незалежно вибраними з галогену, ціано, нітро, трифторметилу, трифторметокси, азидо, -OR6, -C(O)R6, -C(O)OR 6,-OC(O)R6, -NR6C(O)R7, C(O)NR6R7, -NR6R7, -NR6OR7, С1-С6-алкілу, С2-С6-алкенілу, C2-C6-алкінілу, груп - (CR1R2), (С6-С10-арил) і (CR1R2)t(4-10-членний гетероцикл), де t дорівнює цілому числу від 0 до 5; R9 представляє неароматичне моноциклічне кільце, конденсоване або пов'язане містком біциклічне кільце, або спіроциклічне кільце, де вказане кільце містить від 3 до 12 атомів вуглецю, в яких від 0 до 3 атомів вуглецю необов'язково заміщені гетерофрагментом, незалежно вибраним з N, О, S(O)j, де j дорівнює цілому числу від 0 до 2, і групою NR1, при умові, що два атоми О, два фрагменти S(O)j, атом 0 і фрагмент S(O)j, атом N і атом S або атом N і атом О не сполучені безпосередньо один з одним в межах вказаного кільця, і де атоми вуглецю вказаного кільця необов'язково заміщені 1 або 2R8-групами; кожний R11 незалежно вибраний із замісників, описаних при визначенні R 8, за винятком того, що R11 не представляє оксо(=О); R12 представляє R6, -OR 6, -OC(O)R 6, -OC(O)NR 6R7, -OCO2R6 , -S(O)jR6, -S(O)jNR 6R7, -NR6R7 , -NR6C(O)R7, 6 NR SO2R7, -NR 6C (O) NR 6aR7 , -NR 6SO 2NR6aR7 , -NR 6CO2R7 , CN, -C(O)R 6 або галоген, де j дорівнює цілому числу від 0 до 2; R13 представляє –NR1R14 або -OR14; R14 представляє Н, R15 , -C(O)R15 , -SO 2R15 , -C(O)NR15R 7, -SO2NR15R7 або -CO2R15 ; R15 представляє R18, -(CR1R2)t(С6-С10-арил), -(CR'R2) t (4-10-членний гетероцикл), де t дорівнює цілому числу від 0 до 5, 1 або 2 кільцевих атомів вуглецю гетероциклічної групи необов'язково заміщені оксо(=О)фрагментом, і арильні і гетероциклічні групи згаданих вище R15-rp yn необов'язково заміщені 1-3 замісниками R8; кожний з R16 і R17 незалежно вибраний з Н, С1-С6-алкілу і -СН2ОН або R16 і R17 взяті разом у вигляді груп СН2СН2- або -CH2CH2CH2-; R18 представляє С 1-С6-алкіл, де кожний з атомів вуглецю, непов'язаний з атомом N або О, або з S(O)j, де j дорівнює цілому числу від 0 до 2, необов'язково заміщений R 12; і де будь-який з вищезазначених замісників, утримуючий СН 3 (метил), СН2 (метилен) або СН(метин)-групу, який не пов'язаний з галогеном, SO або SO2-групою або з атомами Ν, Ο або S, необов'язково заміщений групою, вибраною з гідрокси, галогену, С1-С4-алкілу, С1-С 4-алкокси і – NR 1R2. При конкретному втіленні даного винаходу R3 представляє -(CR1R2)t(4-10-членний гетероцикл), де t дорівнює цілому числу від 0 до 5; вказана гетероциклічна група необов'язково конденсована з бензольним кільцем або С 5-С8-циклоалкільною групою, і згадані вище R3-гр упи, що включають будь-які, необов'язкові конденсовані кільця, згадані вище, необов'язково заміщені 1-3 R 6-групами. Інші конкретні приклади сполук формули 1 включають ті сполуки, в яких R3 представляє -(CR1R2)t(4-10членний гетероцикл), де t дорівнює цілому числу від 0 до 5, і згадані вище R3 гр упи необов'язково заміщені 1-3 R8-групами. Ще один конкретний приклад сполук формули 1 включає, ті сполуки, де R3 вибраний з де згадані вище R3-групи необов'язково заміщені 1-3 R-групами. Ще один конкретний приклад сполук формули 1 включає, ті сполуки, де R представляє піридин-3-іл, необов'язково заміщений 1-3 R-групами. Ще один конкретний приклад сполук формули 1 включає ті сполуки, в яких наступна частина структурної формули сполуки формули 1 вибрана з групи, що складається з: 3-метил-4-(піридин-2-ілокси)феніламіно 3-хлор-4-(піридин-2-ілокси)феніламіно 3-метокси-4-(піридин-2-ілокси)феніламіно 4-(піридин-2-ілокси)феніламіно 2-метил-4-(піридин-2-ілокси)феніламіно 2-метокси-4-(піридин-2-ілокси)феніламіно 3-хлор-4-(6-метилпіридин-2-ілокси)феніламіно 3-метокси-4-(6-метилпіридин-2-ілокси)феніламіно 3-метил-4-(6-метилпіридин-2-ілокси)феніламіно 2-метокси-4-(6-метилпіридин-2-ілокси)феніламіно 2-метил-4-(6-метилпіридин-2-ілокси)феніламіно 4-(6-метилпіридин-2-ілокси)феніламіно 3-метокси-4-(2-метилпіридин-3-ілокси)феніламіно 3-метил-4-(2-метилпіридин-3-ілокси)феніламіно 3-хлор-4-(2-метилпіридин-3-ілокси)феніламіно 2-метокси-4-(2-метилпіридин-3-ілокси)феніламіно 2-метил-4-(2-метилпіридин-3-ілокси)феніламіно 4-(2-метилпіридин-3-ілокси)феніламіно 3-метил-4-(6-метилпіридин-3-ілокси)феніламіно 3-хлор-4-(6-метилпіридин-3-ілокси)феніламіно 3-метокси-4-(6-метилпіридин-3-ілокси)феніламіно 2-метил-4-(6-метилпіридин-3-ілокси)феніламіно 2-метокси-4-(6-метилпіридин-3-ілокси)феніламіно 4-(6-метилпіридин-3-ілокси)феніламіно 3-хлор-4-(піридин-3-ілокси)феніламіно 3-метокси-4-(піридин-3-ілокси)феніламіно 2-метил-4-(піридин-3-ілокси)феніламіно 2-метокси-4-(піридин-3-ілокси)феніламіно 4-(піридин-3-ілокси)феніламіно 3-метил-4-(2-метилпіримідин-5-ілокси)феніламіно 3-хлор-4-(2-метилпіримідин-5-ілокси)феніламіно 3-метокси-4-(2-метилпіримідин-5-ілокси)феніламіно 2-метил-4-(2-метилпіримідин-5-ілокси)феніламіно 2-метокси-4-(2-метилпіримідин-5-ілокси)феніламіно 4-(2-метилпіримідин-5-ілокси)феніламіно 3-метил-4-(4-метилпіримідин-5-ілокси)феніламіно 3-хлор-4-(4-метилпіримідин-5-ілокси)феніламіно 3-метокси-4-(4-метилпіримідин-5-ілокси)феніламіно 2-метил-4-(4-метилпіримідин-5-ілокси)феніламіно 2-метокси-4-(4-метилпіримідин-5-ілокси)феніламіно 4-(4-метилпіримідин-5-ілокси)феніламіно 3-метил-4-(2-метилпіридин-4-ілокси)феніламіно 3-хлор-4-(2-метилпіридин-4-ілокси)феніламіно 3-метокси-4-(2-метилпіридин-4-ілокси)феніламіно 2-метил-4-(2-метилпіридин-4-ілокси)феніламіно 2-метокси-4-(2-метилпіридин-4-ілокси)феніламіно 4-(2-метилпіридин-4-ілокси)феніламіно 3-метил-4-(піридин-4-ілокси)феніламіно 3-хлор-4-(піридин-4-ілокси)феніламіно 3-метокси-4-(піридин-4-ілокси)феніламіно 2-метил-4-(піридин-4-ілокси)феніламіно 2-метокси-4-(піридин-4-ілокси)феніламіно 4-(піридин-4-ілокси)феніламіно 3-метил-4-(2-метилпіримідин-4-ілокси)феніламіно 3-метокси-4-(2-метилпіримідин-4-ілокси)феніламіно 3-хлор-4-(2-метилпіримідин-4-ілокси)феніламіно 2-метил-4-(2-метилпіримідин-4-ілокси)феніламіно 2-метокси-4-(2-метилпіримідин-4-ілокси)феніламіно 4-(2-метилпіримідин-4-ілокси)феніламіно 3-метил-4-(6-метилпіримідин-4-ілокси)феніламіно 3-метокси-4-(6-метилпіримідин-4-ілокси)феніламіно 3-хлор-4-(6-метилпіримідин-4-ілокси)феніламіно 2-метил-4-(6-метилпіримідин-4-ілокси)феніламіно 2-метокси-4-(6-метилпіримідин-4-ілокси)феніламіно 4-(6-метилпіримідин-4-ілокси)феніламіно 3-метил-4-(піразин-2-ілокси)феніламіно 3-метокси-4-(піразин-2-ілокси)феніламіно 3-хлор-4-(піразин-2-ілокси)феніламіно 2-метил-4-(піразин-2-ілокси)феніламіно 2-метокси-4-(піразин-2-ілокси)феніламіно 4-(піра3ин-2-ілокси)феніламіно 3-хлор-4-(3-метилпіразин-2-ілокси)феніламіно 3-метокси-4-(3-метилпіразин-2-ілокси)феніламіно 3-метил-4-(3-метилпіразин-2-ілокси)феніламіно 2-метокси-4-(3-метилпіразин-2-ілокси)феніламіно 2-метил-4-(3-метилпіразин-2-ілокси)феніламіно 4-(3-метилпіразин-2-ілокси)феніламіно 3-хлор-4-(5-метилпіразин-2-ілокси)феніламіно 3-метокси-4-(5-метилпіразин-2-ілокси)феніламіно 3-метил-4-(5-метилпіразин-2-ілокси)феніламіно 2-метокси-4-(5-метилпіразин-2-ілокси)феніламіно 2-метил-4-(5-метилпіразин-2-ілокси)феніламіно 4-(5-метилпіра3ин-2-ілокси)феніламіно 3-хлор-4-(6-метилпіразин-2-ілокси)феніламіно 3-метокси-4-(6-метилпіра3ин-2-ілокси)феніламіно 3-метил-4-(6-метилпіразин-2-ілокси)феніламіно 2-метокси-4-(6-метилпіразин-2-ілокси)феніламіно 2-метил-4-(6-метилпіразин-2-ілокси)феніламіно 4-(6-метилпіразин-2-ілокси)феніламіно 3-метил-4-(піридазин-3-ілокси)феніламіно 3-хлор-4-(піридазин-3-ілокси)феніламіно 3-метокси-4-(піридазин-3-ілокси)феніламіно 2-метил-4-(піридазин-3-ілокси)феніламіно 2-метокси-4-(піридазин-3-ілокси)феніламіно 4-(піридазин-3-ілокси)феніламіно 3-метил-4-(6-метилпіридазин-3-ілокси)феніламіно 3-хлор-4-(6-метилпіридазин-3-ілокси)феніламіно 3-метокси-4-(6-метилпіридазин-3-ілокси)феніламіно 2-метил-4-(6-метилпіридазин-3-ілокси)феніламіно 2-метокси-4-(6-метилпіридазин-3-ілокси)феніламіно 4-(6-метилпіридазин-3-ілокси)феніламіно 3-метил-4-(6-метилпіридазин-4-ілокси)феніламіно 3-хлор-4-(6-метилпіридазин-4-ілокси)феніламіно 3-метокси-4-(6-метилпіридазин-4-ілокси)феніламіно 2-метил-4-(6-метилпіридазин-4-ілокси)феніламіно 2-метокси-4-(6-метилпіридазин-4-ілокси)феніламіно 4-(6-метилпіридазин-4-ілокси)феніламіно 3-метил-4-(3-метилпіридазин-4-ілокси)феніламіно 3-хлор-4-(3-метилпіридазин-4-ілокси)феніламіно 3-метокси-4-(3-метилпіридазин-4-ілокси)феніламіно 2-метил-4-(3-метилпіридазин-4-ілокси)феніламіно 2-метокси-4-(3-метилпіридазин-4-ілокси)феніламіно 4-(3-метилпіридазин-4-ілокси)феніламіно 3-метил-4-(піридазин-4-ілокси)феніламіно 3-хлор-4-(піридазин-4-ілокси)феніламіно 3-метокси-4-(піридазин-4-ілокси)феніламіно 2-метил-4-(піридазин-4-ілокси)феніламіно 2-метокси-4-(піридазин-4-ілокси)феніламіно 4-(піридазин-4-ілокси)феніламіно 3-хлор-4-(1-метил-1Н-піразол-4-ілокси)феніламіно 3-метокси-4-(1-метил-1Н-піразол-4-ілокси)феніламіно 3-метил-4-(1-метил-1Н-піразол-4-ілокси)феніламіно 2-метокси-4-(1-метил-1Н-піразол-4-ілокси)феніламіно 2-метил-4-(1-метил-1Н-піразол-4-ілокси)феніламіноі 4-(1-метил-1Н-піразол-4-ілокси)феніламіно. Ще один конкретний приклад сполук формули 1 включає сполуки, в яких R 4 представляє - (CR16R17)m-C C16 17 CR R )tR9, де m дорівнює цілому числу від 0 до 3; t дорівнює цілому числу від 0 до 5. Ще один конкретний приклад сполук формули 1 включає сполуки, в яких R4 представляє - (CR16R17) m-C=C16 17 (CR R )tR9, де m дорівнює цілому числу від 0 до 3; t дорівнює цілому числу від 0 до 5; і де R9 вибраний з 3 піперидинілу і 4-піперидинілу, кожний з яких необов'язково заміщений 1 або 2 R8-групами. Ще один конкретний приклад сполук формули 1 включає сполуки, в яких R4 представляє -(CR16R17)m-C=O 16 17 (CR R )t-R9, де m дорівнює цілому числу від 0 до 3; t дорівнює цілому числу від 0 до 5. Ще один конкретний приклад сполук формули 1 включає сполуки, в яких R4 представляє - (CR16R17) m-C=C16 17 (CR R )t-R9, де m дорівнює цілому числу від 0 до 3; t дорівнює цілому числу від 0 до 5; і де R9 вибраний з 3піперидинілу і 4-піперидинілу (необов'язково заміщених 1 або 2-ма R-групами). Ще один конкретний приклад сполук формули 1 включає сполуки, в яких R 4 представляє - (CR16R17)m-OC16 17 (CR R ) kR13 , де k дорівнює цілому числу від 1 до 3; m дорівнює цілому числу від 0 до 3. Ще один конкретний приклад сполук формули 1 включає сполуки, в яких R 4 представляє - (CR16R17)m-OC16 17 (CR R ) kR13 , де k дорівнює цілому числу від 1 до 3; m дорівнює цілому числу від 0 до 3; R13 представляє – NR1R14, де R14 вибраний з -C(O)R 15, -SO 2R15 і C(O)NR15R7. Ще один конкретний приклад сполук формули 1 включає сполуки, в яких R4 представляє - (CR16R17) m-C=C16 17 (CR R ) kR13 , де k дорівнює цілому числу від 1 до 3; m дорівнює цілому числу від 0 до 3. Ще один конкретний приклад сполук формули 1 включає сполуки, в яких R4 представляє - (CR16R17) m-C=C16 17 (CR R ) kR13 , де k дорівнює цілому числу від 1 до 3; m дорівнює цілому числу від 0 до 3; R13 представляє NR1R14, де R14 вибраний з -C(O)R 15, -SO 2R15 і -C(O)NR15R7. Ще один конкретний приклад сполук формули 1 включає сполуки, в яких R 4 представляє - (CR16R17)m-C C16 17 (CR R ) kR13 або -(CR16R17) m-C=C-(CR 16R17) kR13 , де k дорівнює цілому числу від 1 до 3; m дорівнює цілому числу від 0 до 3; R13 представляє –NR1R14 або -OR14; R14 представляє R15, R15 представляє R18, і R18 представляє С гС6-алкіл, необов'язково заміщений групами -OR6, -S(O)jR6, -NR6R7, -NR6C(O)R7, -NR6SO 2R7, NR6CO2R7, CN, -C(O)R 6 або галогеном. Конкретні переважні сполуки згідно з даним винаходом включають сполуки, вибрані з групи, що містить: (±)-[3-метил-4-(піридин-3-ілокси)феніл]-(6-піперидин-3-ілетинілхіназолін-4-іл)амін; 2-метокси-N-(3-{4-[3-метил-4-(піридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-иніл)ацетамід; (±)-[3-метил-4-(6-метилпіридин-3-ілокси)феніл]-(6-піперидин-3-ілетинілхіназолін-4-іл)амін; 2-метокси-N-(3-{4-[3-метил-4-(2-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-иніл)ацетамід; [3-метил-4-(2-метилпіридин-3-ілокси)феніл]-(6-піперидин-4-ілетинілхіназолін-4-іл)амін; [3-метил-4-(6-метилпіридин-3-ілокси)феніл]-(6-піперидин-4-ілетинілхіназолін-4-іл)амін; 2-метокси-N-(3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-иніл)ацетамід; 2-Н-(3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-иніл)ацетамід; E-2-метокси-N-(3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}аліл)ацетамід; [3-метил-4-(піридин-3-ілокси)феніл]-(6-піперидин-4-ілетинілхіназолін-4-іл) амін; 2-метокси-N-[1-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6ілетиніл}циклопропіл)ацетамід; Е-N-(3-{4-[3-хлор-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}аліл)-2-метоксіацетамід; N-(3-{4-[3-хлор-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-иніл)ацетамід; N-(3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-иніл)ацетамід; Е-N-(3-{4-[3-хлор-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}аліл)ацетамід; Е-2-етокси-М-(3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно] хіназолін-6-іл}аліл)ацетамід; 1-етил-3-(3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-иніл)сечовина; (3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-иніл)амідпіперазин-1карбонової кислоти; (±)-(3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-иніл)амід 2-гідроксиметилпіролідин-1-карбонової кислоти; 2-диметиламіно-N-(3-{4-[3-метил-4-(піридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-иніл)ацетамід; Е-N-(3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}аліл)метансульфонамід; (3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-иніл)амід ізоксазол-5карбонової кислоти; 1-(1,1-диметил-3-{4-[3-метил-4-(6-метилпіридин-3-ілокси)феніламіно]хіназолін-6-іл}проп-2-иніл)-3етилсечовина; і фармацевтично прийнятні солі, проліки і сольвати згаданих вище сполук. Даний винахід також відноситься до способу лікування аномального росту клітин у ссавців, включаючи людину шля хом введення вказаному ссавцеві сполуки формули 1, описаної вище, або її фармацевтично прийнятної солі, сольвату або проліків в кількості, яка ефективна для лікування аномального росту клітин. В одному з втілень вказаного способу аномальний ріст клітин являє собою рак, включаючи, але не обмежуючись перерахованим, рак легенів, рак кістки, рак підшлункової залози, рак шкіри, пухлини голови або шиї, шкіряну або внутрішньоочну меланому, рак матки, рак яєчника, рак прямої кишки, рак анальної області, рак шлунка, рак товстої кишки, рак молочної залози, карциному фаллопієвих (маточних) тр уб, карциному ендометрію, карциному шийки матки, карциному піхви, карциному вульви, хворобу Ходжкіна, рак стравоходу, рак тонкої кишки, рак ендокринної системи, рак щитовидної залози, рак паращитовидної залози, рак надниркової залози, саркому м'яких тканин, рак уретри, рак статевого члена, рак простати, хронічну або гостру лейкемію, лімфолімфоми, рак сечового міхура, рак нирки або сечоводу, карциному клітин ниркового епітелію, карциному ниркової миски, неоплазми (пухлини) центральної нервової системи (ЦНС), первинну лімфому ЦНС, пухлини хребта, гліому стовбура мозку, аденому гіпофіза або поєднання одного або більше вищеперелічених новоутворень. В іншому втіленні даного способу вказаний аномальний ріст клітин представляє доброякісне проліферативне захворювання, включаючи, але не обмежуючись перерахованим, псоріаз, доброякісну гіпертрофію простати або рестеноз. Даний винахід також відноситься до способу лікування аномального росту клітин у ссавців, який включає введення вказаним ссавцям сполуки формули 1 або її фармацевтично прийнятної солі, сольвату або проліків в кількості, ефективній для лікування аномального росту клітин, в поєднанні з протипухлинним агентом, вибраним з групи, що складається з мітотичних інгібіторів, алкілуючих агентів, антиметаболітів, інтеркалуючих антибіотиків, інгібіторів фактора росту, інгібіторів клітинного циклу, ферментів, інгібіторів топоізомерази, модифікаторів біологічної відповіді, антитіл, цитотоксинів, антигормонів і антиандрогенів. Даний винахід також відноситься до фармацевтичної композиції для лікування аномального росту клітин у ссавців, включаючи людину, яка містить сполуку формули 1, описану ви ще, або її фармацевтично прийнятну сіль, сольват або проліки в кількості, ефективній для лікування аномального росту клітин, і фармацевтично прийнятний носій. В одному з втілень вказаної композиції, вказаний аномальний ріст клітин представляє рак, включаючи, але не обмежуючись перерахованим, рак легенів, рак кістки, рак підшлункової залози, рак шкіри, пухлини голови або шиї, шкіряну або внутрішньоочну меланому, рак матки, рак яєчника, рак прямої кишки, рак анальної області, рак шлунка, рак товстої кишки, рак молочної залози, рак матки, карциному фаллопієвих труб, карциному ендометрію, карциному шийки матки, карциному піхви, карциному вульви, хворобу Ходжкіна, рак стравоходу, рак тонкої кишки, рак ендокринної системи, рак щитовидної залози, рак паращитовидної залози, рак надниркової залози, саркому м'яких тканин, рак уретри, рак статевого члена, рак простати, хронічну або гостру лейкемію, лімфолімфоми, рак сечового міхура, рак нирки або сечоводу, карциному клітин ниркового епітелію, карциному ниркової миски, неоплазми (пухлини) центральної нервової системи (ЦНС), первинну лімфому ЦНС, пухлини хребта, гліому стовбура мозку, аденому гіпофіза або поєднання одного або більше вищеперелічених новоутворень. При іншому втіленні вказаної фармацевтичної композиції вказаний аномальний ріст клітин представляє доброякісне проліферативне захворювання, включаючи, але не обмежуючись перерахованим, псоріаз, доброякісну гіпертрофію простати або рестеноз. Винахід також відноситься до фармацевтичної композиції для лікування аномального росту клітин у ссавців, включаючи людину, яка містить сполуку формули 1, описану ви ще, або її фармацевтично прийнятну сіль, сольват або проліки в кількості, ефективній для лікування аномального росту клітин, в поєднанні з фармацевтично прийнятним носієм і протипухлинним агентом, вибраним з групи, що складається з мітотичних інгібіторів, алкілуючих агентів, антиметаболітів, інтеркалуючих антибіотиків, інгібіторів фактора росту, інгібіторів клітинного циклу, ферментів, інгібіторів топоізомерази, модифікаторів біологічної відповіді, антигормонів і антиандрогенів. Даний винахід також відноситься до способу лікування захворювання, пов'язаного з ангіогенезом у ссавців, включаючи людину, що включає введення вказаним ссавцям сполуки формули 1, описаної вище, або її фармацевтично прийнятної солі, сольвату або проліків в кількості, ефективній для лікування вказаного захворювання. Такі захворювання включають злоякісні пухлини, такі як меланома; очні захворювання, такі як вікова дегенерація жовтої плями, синдром передбачуваного очного гістоплазмозу і васкуляризація сітчатки при проліферативній діабетичній ретинопатії; ревматоїдний артрит; порушення, пов'язані з втратою кісткової маси, такі як остеопороз, хвороба Педжета, гуморальна гіперкальціємія при злоякісному розвитку хвороби, гіперкальціємія при пухлинах, що метастазують в кістці, і остеопороз, індукований лікуванням глюкокортикоїдами; коронарний рестеноз; деякі мікробні інфекції, включаючи інфекції пов'язані з патогенними мікробами, вибраними з аденовірусів, hantaviruses, Borrelia burgdorferi, Yersinia spp., Bordetella pertussis і групи стрептококів. Даний винахід також відноситься до способу лікування (і до фармацевтичної композиції для лікування) аномального росту клітин у ссавців, що включає деяку кількість сполуки формули 1 або її фармацевтично прийнятної солі, сольвату або проліків, і деяку кількість однієї або більше речовин, вибраних з антиангіогенних агентів, інгібіторів передачі сигналу і протипроліферативних засобів, загальна кількість яких ефективна для лікування вказаного аномального росту клітин. У способах і фармацевтичних композиціях, описаних тут, разом із сполукою формули 1 можна застосовувати антиангіогенні засоби, такі як інгібітори ММР-2 (матриксної металопротеїнази-2), інгібітори ММР-9 (матриксної металопротеїнази-9) і інгібітори СОХ-ІІ (циклооксигенази II). Приклади інгібіторів СОХ-II, що застосовуються включають CELEBREX™ (alecoxib), вальдекоксиб (valdecoxib) і рофекоксиб (rofecoxib). Приклади застосування інгібіторів матриксної металопротеїнази описані в заявках [WO 96/33172, (опублікованій 24 жовтня 1996), WO 96/27583 (опублікованій 7 березня 1996), в заявці на європейський патент №97304971.1 (зареєстрованій 8 липня 1997), в заявці на європейський патент №99308617.2 (зареєстрованої 29 жовтня, 1999), в заявках WO 98/07697 (опублікованій 26 лютого 1998), WO 98/03516 (опублікованій 29 січня 1998), WO 98/34918 (опублікованій 13 серпня 1998), WO 98/34915 (опублікованій 13 серпня 1998), WO 98/33768 (опублікованій 6 серпня 1998), WO 98/30566 (опублікованій 16 липня 1998), в публікації європейського патенту 606046 (опублікованій 13 липня 1994), в публікації європейського патенту 931788 (опублікованій 28 липня 1999), в заявках WO 90/05719 (опублікованій 31 травня 1990), WO 99/52910 (опублікованій 21 жовтня 1999), WO 99/52889 (опублікованій 21 жовтня 1999), WO 99/29667 (опублікованій 17 червня 1999), в міжнародній заявці РСТ №РСТ/IВ98/01113 (зареєстрованій 21 липня 1998), в заявці на європейський патент №99302232.1 (зареєстрованій 25 березня 1999), в заявці на патент Великобританії номер 9912961.1 (зареєстрованій 3 червня 1999), в попередній заявці на патент США №60/148464 (зареєстрованій 12 серпня 1999), в патенті США 5863949 (виданому 26 січня 1999), в патенті США 5861510 (виданому 19 січня 1999) і в публікації європейського патенту 780386 (опублікованій 25 червня 1997)], кожний з яких включений тут в повному об'ємі шляхом посилання. Переважними інгібіторами ММР-2 і ММР-9 є інгібітори, що володіють слабою інгібуючою активністю до ММР-1 або зовсім їй не володіють. Більш переважними є інгібітори, селективно інгібуючі ММР-2 і/або МНР-9, в порівнянні з іншими матриксними металопротеїназами (тобто, ММР-1, ММР-3, ММР-4, ММР-5, ММР-6, ММР-7, ММР-8, ММР-10, ММР-11, ММР12 і ММР-13). Деякими конкретними прикладами ММР-інгібіторів, що застосовуються в поєднанні із сполуками згідно з даним винаходом, є AG-3340, RO 32-3555, RS 13-0830 і сполуки, вказані в наступному списку: 3-[[4-(4-фторфенокси)бензолсульфоніл]-(1-гідроксикарбамоїлциклопентил)аміно]пропіонова кислота; гідроксіамід 3-екзо-3-[4-(4-фторфенокси)бензолсульфоніламіно]-8-оксабіцикло[3.2.1 ]октан-3-карбонової кислоти; гідроксіамід (2R,3R)-1-[4-(2-хлор-4-фторбензілокси)бензолсульфоніл]-3-гідрокси-3-метилпіперидин-2карбонової кислоти; гідроксіамід 4-[4-(4-фторфенокси)бензолсульфоніламіно]тетрагідропіран-4-карбонової кислоти; 3-[[4-(4-фторфенокси)бензолсульфоніл]-(1-гідроксикарбамоїл-циклобутил)аміно]пропїонова кислота; гідроксіамід 4-[4-(4-хлорфенокси)бензолсульфоніламіно]тетрагідропіран-4-карбонової кислоти; гідроксіамід 3-[4-(4-хлорфенокси)бензолсульфоніламіно]тетрагідропіран-3-карбонової кислоти; гідроксіамід (2R,3R)-1-[4-(4-фтор-2-метилбензилокси)бензолсульфоніл]-3-гідрокси-3-метилпіперидин-2карбонової кислоти; 3-[[4-(4-фторфенокси)бензолсульфоніл]-(1-гідроксикарбамоїл-1-метилетил)аміно]пропіонова кислота; 3-[[4-(4-фторфенокси)бензолсульфоніл]-(4-гідроксикарбамоїлтетра-гідропіран-4-іл)аміно]пропіонова кислота; гідроксіамід 3-екзо-3-[4-(4-хлорфенокси)бензолсульфоніламіно]-8-оксабицикло[3.2.1]октан-3-карбонової кислоти; гідроксіамід 3-ендо-3-[4-(4-фторфенокси)бензолсульфоніламіно]-8-оксабіцикло[3.2.1]октан-3-карбонової кислоти; і гідроксіамід 3-[4-(4-фторфенокси)бензолсульфоніламіно]тетрагідрофуран-3-карбонової кислоти; і фармацевтично прийнятні солі, сольвати і проліки вказаних сполук. Сполуки формули 1 і їх фармацевтично прийнятні солі, сольвати і проліки також можуть застосовува тися в поєднанні з інгібіторами передачі сигналу, такими як засоби, що інгібують EGFR-відповіді (рецептора епідермального фактора росту), такими як EGFR-антитіла, EGF-антитіла і молекули, що є інгібіторами EGFR; з інгібіторами VEGF (васкулярно-ендотеліального фактора росту); і з інгібіторами еrbВ2-рецепторів, такими як органічні молекули або антитіла, які зв'язуються з еrbВ2-рецептором, наприклад, HERCEPTIN™ (Genentech, Inc. South San Francisco, Каліфорнія, США). Інгібітори EGFR описані, наприклад в заявці [WO 95/19970 (опублікованій 27 липня 1995), WO 98/14451 (опублікованій 9 квітня 1998), WO 98/02434 (опублікованій 22 січня 1998) і в патенті США 5747498 (виданому 5 травня 1998)]. EGFR-інгібуючі агенти включають, але не обмежуються перерахованим, моноклональні антитіла С225 і анти-EGFR 22Mab (ImClone Systems Incorporated of New York, Нью-Йорк, США), сполуки ZD1839 (AstraZeneca), BIBX-1382 (Boehringer Ingelheim), MDX-447 (Medarex Inc. Annandale, Нью-Джерсі, СІЛА) і OLX-103 (Merck & Co. of Whitehouse Station, Нью-Джерсі, США), VRCTC-310 (Ventech Research) і пов'язаний з EGF токсин (Seragen Inc. of Hopkinton, Масачусетс). З сполукою формули 1 також можна об'єднувати інгібітори VEGF, наприклад, SU-5416 і SU-6668 (Sugen Inc. of South San Francisco, Каліфорнія, США). Інгібітори VEGF описані, наприклад, в заявці [WO 99/24440 (опублікованій 20 травня 1999), міжнародній заявці РСТ/IВ99/00797 (зареєстрованій 3 травня 1999), в заявці WO 95/21613 (опублікованій 17 серпня 1995), WO 99/61422 (опублікованій 2 грудня 1999), в патенті США 5834504 (виданому 10 листопада 1998), в заявці WO 98/50356 (опублікованій 12 листопада 1998), патенті США 5883113 (виданому 16 березня 1999), патенті США 5886020 (виданому 23 березня 1999), патенті США 5792783 (виданому 11 серпня 1998), в заявці WO 99/10349 (опублікованій 4 березня 1999), WO 97/32856 (опублікованій 12 вересня 1997), WO 97/22596 (опублікованій 26 червня 1997), WO 98/54093 (опублікованій 3 грудня 1998), WO 98/02438 (опублікованій 22 січня 1998), WO 99/16755 (опублікованій 8 квітня 1999) і в заявці WO 98/02437 (опублікованій 22 січня 1998)], кожна з яких включена тут в повному об'ємі шляхом посилання. Іншими прикладами деяких специфічних VEGF-інгібіторів є ІМ862 (Cytran Inc. of Kirkland, Вашингтон, США); анти-VEGF моноклональне антитіло Genentech Inc. of South San Francisco, Каліфорнія; і ангіозим, синтетичний рибозим від Ribozyme (Boulder, Колорадо) і Chiron (Emeryville, Каліфорнія). У поєднанні із сполукою формули 1 можна вводити інгібітори ЕrbВ2-рецепторів, такі як GW-282974 (Glaxo Wellcome ріс), і моноклональні антитіла AR-209 (Aronex Pharmaceuticals Inc. Woodlands, Техас, США) і 2В-1 (Chiron). Такі еrbВ2-інгібітори включають інгібітори, описані в заявках [WO 98/02434 (опублікованій 22 січня 1998), WO 99/35146 (опублікованій 15 липня 1999), WO 99/35132 (опублікованій 15 липня 1999), WO 98/02437 (опублікованій 22 січня 1998), WO 97/13760 (опублікованій 17 квітня 1997), WO 95/19970 (опублікованій 27 липня 1995), в патенті США 5587458 (виданому 24 грудня 1996) і в патенті США 5877305 (виданому 2 березня 1999), кожний з яких включений тут в повному об'ємі шляхом посилання. Інгібітори ЕrbB2-рецепторов, що застосовуються в даному винаході, також описані в попередній заявці на патент [№60/117341, зареєстрованій 27 січня 1999, і в попередній заявці на патент №60/117346, зареєстрованій 27 січня 1999], кожна з яких включена тут в повному об'ємі шляхом посилання. Інші протипроліферативні засоби, які можна застосовувати спільно із сполуками даного винаходу, включають інгібітори ферменту фарнезилпротеїнтрансферази і інгібітори рецепторної тирозинкінази PDGFr, включаючи сполуки, описані і заявлені в наступних заявках [на патент США: 09/221946 (зареєстрованій 28 грудня 1998); 09/454058 (зареєстрованій 2 грудня 1999); 09/501163 (зареєстрованій 9 лютого 2000); 09/539930 (зареєстрованій 31 березня 2000); 09/202796 (зареєстрованій 22 травня 1997); 09/384339 (зареєстрованій 26 серпня 1999) і 09/383755 (зареєстрованій 26 серпня 1999)]; і сполуки, описані і заявлені в наступних попередніх заявках [на патент США: 60/168207 (зареєстрованій 30 листопада 1999); 60/170119 (зареєстрованій 10 грудня 1999); 60/177718 (зареєстрованій 21 січня 2000); 60/168217 (зареєстрованій 30 листопада 1999) і 60/200834 (зареєстрованій 1 травня 2000)]. Кожна із згаданих вище заявок на патент і попередніх заявок на патент включена тут в повному об'ємі шляхом посилання. Сполуки формули 1 також можна застосовувати з іншими засобами, що застосовуються для лікування аномального росту клітин або рака, включаючи, але не обмежуючись перерахованим, агенти, здатні посилювати протипухлинні імунні відповіді, такі як СТLА4(цитотоксичний лімфоцитарний антиген-4)-антитіла, і інші засоби, здатні блокувати CTLA4; протипроліферативні засоби, такі як інші інгібітори фарнезилпротеїнтрансферази, наприклад інгібітори фарнезилпротеїнтрансферази, описані в посиланнях, що цитуються раніше в розділі «попередній рівень техніки». Специфічні СТLА4-антитіла, які можна застосовувати в даному винаході, включають антитіла, описані в попередній заявці [на патент США 60/113647 (зареєстрованій 23 грудня 1998)], яка включена тут в повному об'ємі шляхом посилання. Термін «аномальний ріст клітин» в значенні, що застосовується тут, якщо не обумовлено інакше, відноситься до росту клітин, який не залежить від нормальних регуляторних механізмів (наприклад, втрати контактного гальмування). Він включає аномальний ріст: (1) клітин пухлини (пухлин), яких проліферують шляхом експресії мутованої тирозинкінази або експресії рецепторної тирозинкінази в підвищених кількостях; (2) доброякісних і злоякісних клітин при інших проліферативних захворюваннях, при яких відбувається активація аберантної тирозинкінази; (4) будь-яких пухлин, в проліферації яких беруть участь рецепторні тирозинкінази; (5) будь-яких пухлин, проліферація яких пов'язана з активацією аберантної серин/треонінкінази; і (6) доброякісних і злоякісних клітин при інших проліферативних захворюваннях, в яких відбувається активація аберантної серин/треонінкінази. Термін «лікування» в значенні, що застосовується тут, якщо не обумовлюється інакше, означає реверсію, полегшення, гальмування розвитку (хвороби), або запобігання захворюванню або стану, до якого такий термін застосовується, або одного або більше симптомів такого захворювання або стану. Термін «курс лікування», в значенні, що застосовується тут, якщо не обумовлюється інакше, відноситься до проведення лікування, в тому значенні як безпосередньо «лікування» визначається вище. Термін «галоген» в значенні, що застосовується тут, якщо не обумовлюється інакше, включає фтор, хлор, бром або йод. Переважно галогени представляють фтор і хлор. Термін «алкіл» в значенні, що застосовується тут, якщо не обумовлюється інакше, включає насичені одновалентні вуглеводневі радикали, що містять фрагменти з прямим ланцюгом, циклічні (включаючи моноабо багатоядерні фрагменти) або фрагменти з розгалуженим ланцюгом. Мається на увазі, що вказана алкільна група для включення циклічних фрагментів повинна містити, щонайменше, три атоми вуглецю. Термін «циклоалкіл» в значенні, що застосовується тут, якщо не обумовлюється інакше, включає насичені одновалентні вуглеводневі радикали, що містять циклічні (включаючи моно-або багатоядерні) фрагменти. Термін «алкеніл» в значенні, що застосовується тут, якщо не обумовлюється інакше, включає алкільні групи, вказані вище, що мають, щонайменше, один подвійний зв'язок вуглець-вуглець. Термін «алкініл» в значенні, що застосовується тут, якщо не обумовлюється інакше, включає алкільні групи, вказані вище, що мають, щонайменше, один потрійний зв'язок вуглець-вуглець. Термін «арил» в значенні, що застосовується тут, якщо не обумовлюється інакше, включає органічний радикал, такий як феніл або нафтил, одержаний з ароматичного вуглеводню при видаленні одного атома водню. Термін «алкокси» в значенні, що застосовується тут, якщо не обумовлюється інакше, включає групи -Оалкіл, де алкіл має таке ж значення, як вказане вище. Термін «4-10-членний гетероцикл» в значенні, що застосовується тут, якщо не обумовлюється інакше, включає ароматичні і неароматичні гетероциклічні групи, що містять один або більше гетероатомів, кожний з яких вибраний з О, S і N, де кожна гетероциклічна група має в кільцевій системі від 4 до 10 атомів. Неароматичні гетероциклічні групи включають групи, що містять тільки 4 атоми в кільцевій системі, однак ароматичні гетероциклічні групи повинні містити, щонайменше, 5 атомів в кільцевій системі. Гетероциклічні групи включають конденсовані з бензолом кільцеві системи і кільцеві системи, заміщені одним або більше оксо-фрагментами. Прикладом 4-членної гетероциклічної групи є азетидініл (похідне азетидину). Прикладом 5-членної гетероциклічної групи є тіазоліл, і прикладом 10-членної гетероциклічної групи є хінолініл. Прикладами неароматичних гетероциклічних гр уп є піролідініл, тетрагідрофураніл, тетрагідротієніл, тетрагідропіраніл, тетрагідротіопіраніл, піперидино, морфоліно, тіоморфоліно, тіоксаніл, піперазиніл, азетидініл, оксетаніл, тієтаніл, гомопіперидиніл, оксепаніл, тієпаніл, оксазепініл, діазепініл, тіазепініл, 1,2,3,6тетрагідропіридініл, 2-піролініл, 3-піролініл, індолініл, 2Н-піраніл, 4Н-піраніл, діоксаніл, 1,3-діоксоланіл, піразолініл, дитіаніл, дитіоланіл, дигідропіраніл, дигідротієніл, дигідрофураніл, піразолидініл, імідазолініл, імідазолідиніл, 3-азабицикло[3.1.0]гексаніл, 3-азабицикло[4.1.0]гептаніл, 3Н-індоліл і хінолізиніл. Прикладами ароматичних гетероциклічних груп є піридініл, імідазоліл, піримідиніл, піразоліл, триазоліл, піразиніл, тетразоліл, фурил, тієніл, ізоксазоліл, тіазоліл, оксазоліл, ізотіазоліл, піроліл, хінолініл, ізохінолініл, індоліл, бензімідазоліл, бензофураніл, циннолініл, індазоліл, індолизиніл, фталазиніл, піридазиніл, триазиніл, ізоіндоліл, птеридиніл, пуриніл, оксадіазоліл, тіадіазоліл, фуразаніл, бензофуразаніл, бензотіофеніл, бензотіазоліл, бензоксазоліл, хіназолініл, хіноксалініл, нафтиридініл і фуропіридиніл. Згадані вище групи, похідні від перерахованих вище сполук, можуть приєднуватися до атома С або приєднуватися до атома N, де це можливе. Наприклад, група, похідна від піролу, може бути гр упою пірол-1-іл (приєднаною по N) або пірол-3іл (приєднаною по С). Термін «Me» означає метил, «Et» означає етил, і «Ас» означає ацетил. При даному вище визначенні X1, фрагменти -(CR1R2)m і (CR16R17) K і інші подібні фрагменти, вказані вище, можуть варіюватися при визначенні R1, R2, R16 і R17 для кожної ітерації нижнього індексу (тобто, m, k і т.д) більш ніж на 1. Таким чином, -(CR 1R2)m-, коли m дорівнює 2, може включати -СН2С(Ме) (Et). Фраза «фармацевтично прийнятна сіль(солі)» в значенні, що застосовується тут, якщо не вказане інше значення, включає кислі або основні солі, які можуть бути присутнім в сполуках згідно з даним винаходом. Сполуки даного винаходу, що мають основний характер, здатні до утворення широкого ряду солей з різними неорганічними і органічними кислотами. Кислоти, які можна застосовувати для одержання фармацевтично прийнятних кислотно-адитивних солей таких основних сполук представляють кислоти, які утворюють нетоксичні кислотно-адитивні солі, тобто солі, що містять фармакологічно прийнятні аніони, такі як. хлористоводневі, бромистоводневі, йодистоводневі солі, нітрати, сульфати, бісуль фати, фосфати, кислі фосфа ти, ізонікотинати, ацетати, лактати, саліцилати, цитрати, кислі цитрати, тартрати, пантотенати, бітартрати, аскорбати, сукцинати, малеати, гентизинати, фумарати, глюконати, глюкуронати, сахарати, форміати, бензоати, глютамати, метансульфонати, етансульфонати, бензолсульфонати, п-толуолсульфонати і памоати [тобто 1,1'-метилен-біс-(2-гідрокси-3-нафтоати)]. Сполуки даного винаходу, які містять основну груп у, таку як аміногрупа, крім кислот, згаданих вище, можуть утворювати фармацевтично прийнятні солі з різними амінокислотами. Ті сполуки даного винаходу, які мають кислий характер, здатні утворювати основні солі з різними фармакологічно прийнятними катіонами. Приклади таких солей включають солі лужних металів або лужноземельних металів і зокрема, кальцієві, магнієві, натрієві і калієві солі сполук даного винаходу. Деякі функціональні групи, що містяться в сполуках даного винаходу, можуть бути заміщені на біоізостеричні групи, тобто групи, які мають схожі просторові або електронні умови по відношенню до початкової групи, але відрізняються або поліпшеними фізико-хімічними, або іншими властивостями. Відповідні приклади добре відомі фахівцям в даній області і включають, але не обмежені фрагментами, описаними в публікації [Patini і інш., Chem. Rev., 1996, 96, 3147-3176] і в посиланнях, що цитуються там. Сполуки даного винаходу мають центри асиметрії і тому існують в формі різних енантіомерів і діастереомерів. Даний винахід відноситься до застосування всіх оптичних ізомерів і стереоізомерів сполук даного винаходу і їх сумішей, і до всіх фармацевтичних композицій і способів лікування, які можуть їх застосовувати або містити. Сполуки формули 1 можуть також існувати у вигляді та утомерів. Даний винахід відноситься до застосування всіх таких таутомерів і їх сумішей. Предмет винаходу також включає мічені ізотопами сполуки і їх фармацевтично прийнятні солі, сольвати і проліки, які ідентичні сполукам, вказаним в формулі 1, однак фактично один або більше атомів в них заміщені атомом, що має атомну масу або масове число, відмінне від атомної маси або масового числа, що звичайно знаходиться в природі. Приклади ізотопів, які можуть входити в сполуки згідно з винаходом, включають ізотопи водню, вуглецю, азоту, кисню, фосфору, фтору і хлору, такі як 2Н, 3Н, 13С, 14С, 15N, 16 O, 17 О, 35S, 18F і 36 Сl, відповідно. Сполуки даного винаходу, їх проліки і фармацевтично прийнятні солі вказаних сполук або вказаних проліків, які містять вищезазначені ізотопи і/або інші ізотопи інших атомів знаходяться в об'ємі даного винаходу. Деякі мічені ізотопами сполуки даного винаходу, наприклад, ті, які включають радіоактивні ізотопи, такі як 3Н і 14С застосовуються в лікарському засобі і/або випробуваннях по розподілу його в тканинному субстраті. Ізотопи тритію, тобто 3Н, і вуглецю-14, тобто 14С, особливо переважні завдяки легкості їх одержання і здатності до виявлення. Крім того, заміщення більш важкими ізотопами, такими як дейтерій, тобто 2Н, може дати деякі терапевтичні переваги внаслідок більшої метаболічної стабільності, наприклад внаслідок підвищення часу напівжиття in vivo або внаслідок можливості знизити дозування і, отже, може бути переважним в деяких випадках. Мічені ізотопами сполуки формули 1 даного винаходу і їх проліки в загальному випадку можуть бути одержані при виконанні процедур, описаних нижче на схемах і/або в прикладах і методиках при заміні неміченого ізотопами реагенту на легко доступний мічений ізотопами реагент. Даний винахід також відноситься до фармацевтичних композицій, що містять проліки сполук формули 1, і способи лікування бактерійних інфекцій введенням проліків сполук формули 1. Сполуки формули 1, що мають вільні аміно-, амідо-, гідрокси- або карбоксильні групи, можуть бути перетворені в проліки. Проліки включають сполуки, в яких амінокислотний залишок або поліпептидний ланцюг з двох або більш (наприклад, з двох, трьох або чотирьох) амінокислотних залишків ковалентно приєднані через амідну або складноефірну зв'язку до вільної аміно-, гідрокси- або карбоксильної групи сполук формули 1. Амінокислотні залишки включають, але цим не обмежується, 20 амінокислот, що зустрічаються в природі, що звичайно позначаються символами з трьох букв, і також включають 4-гідроксипролін, гідроксилізин, демозин, ізодемозин, 3-метилгістидин, норвалін, бета-аланін, гамма-аміномасляну кислоту, цитрулінгомоцистеїн, гомосерин, орнітин і метіонінсульфон. Інші види проліків також включені. Наприклад, вільні карбоксильні групи, можуть бути дериватизовані як аміди або складні алкілові ефіри. Вільні гідроксигрупи можуть бути дериватизовані за допомогою груп, що включають, але ними не обмежується, гемісукцинати, складні фосфатні ефіри, диметиламіноацетати і фосфорилоксиметілоксикарбоніли, як намічено в загальних рисах в Ad vanced Drug Delivery Reviews, 1996, 19, 115. Карбаматні проліки, що забезпечують гідрокси- і аміногрупи, також включені як карбонатні проліки, сульфонатні складні ефіри і сульфатні складні ефіри, що забезпечують гідроксигрупи. Також в об'єм винаходу включені похідні сполуки І по гідрокси-групі, утворюючи прості (ацілокси)метилові і (ацілокси)етилові ефіри, де ацильна група може бути групою складного алкілового ефіру, необов'язково заміщеного групами, що включають, але не обмежуючись ними, групи простого ефіру, аміну і карбонової кислоти, або ацильна група представляє складний ефір амінокислоти, як описана вище. Проліки даного типу описані в публікації [J. Med. Chem., 1996,39,10]. Вільні аміни також можуть бути дериватизовані з одержанням амідів, сульфонамідів або фосфонамідів. Всі вказані фрагменти проліків можуть включати групи, що включають, але не обмежуючись ними, групи простого ефіру, аміну і карбонової кислоти. Загальні способи синтезу, які можуть стосуватися одержання сполук даного винаходу, описані [в патенті США 5747498 (виданому 5 травня 1998), в заявці на патент США з порядковим номером 08/953078 (зареєстрованій 17 жовтня 1997), в заявках WO 98/02434 (опублікованій 22 січня 1998), WO 98/02438 (опублікованій 22 січня 1998), WO 96/40142 (опублікованій 19 грудня 1996), WO 96/09294 (опублікованій 6 березня 1996), WO 97/03069 (опублікованій 30 січня 1997), WO 95/19774 (опублікованій 27 липня 1995) і WO 97/13771 (опублікованій 17 квітня 1997)]. Додаткові методики згадуються в заявках [на патент США №09/488350 (зареєстрованій 20 січня 2000) і №09/488378 (зареєстрованій 20 січня 2000)]. Згадані вище патенти і заявки на патенти включені тут в повному об'ємі як посилання. Відповідно до відомих способів можна одержати деякі початкові матеріали і здійснити деякі модифікації синтезу у відповідності до способів, відомих фа хівцям в даній області. Стандартна методика одержання 6-йодхіназолінону описана в публікації [Stevenson T.M., Ka zmierczak F., Leonard N.J., J. Org. Chem. 1986, 51, 5, p.616. Поєднання боронової кислоти, що каталізуються паладієм, описані в публікації Miyaura Ν., Yanagi Т., Suzuki Α., Syn. Comm. 1981, 11, 1, p.513.] Поєднання по Хеку (Heck), що каталізуються паладієм, описані в публікації [Heck і інш., Organic Reactions, 1982, 27, 345 або в публікації Cabri і інш. в Асові. Chem. Res., 1995, 28, 2]. Приклади поєднань алкінів з кінцевими групами з арилгалогенідами, що каталізуються паладієм, приведені в публікаціях: [Castro і інш., J.Org.Chem. 1963, 28, 3136 або Sonogashira і інш. Synthesis, 1977, 777]. Синтез алкінів з кінцевими групами можна провести, застосовуючи відповідно заміщені/захищені альдегіди, як описано в публікаціях: [Colvin E.W.J. і інш., Chem.Soc.Perkin Trans.I, 1977, 869; Gilbert J.C. і інш., J.Org.Chem., 47, 10, 1982; Hauske J.R. і інш., Tet.Lett., 33, 26, 1992, 3715; Ohira S. і інш., J.Chem.Soc.Chem.Commun., 9, 1992, 721; Trost B.M., J.Amer.Chem.Soc, 119, 4, 1997, 698; або Marshall J.A. і інш., J.Org.Chem., 62, 13, 1997, 4313.] Альтернативно алкіни з кінцевими групами можна одержати по двостадійній методиці. Спочатку додають TMS (триметилсиліл) ацетиленід літію до відповідно заміщеного/захищеного альдегіду, як описано в публікації: [Nakatani K. і інш., Tetrahedron, 49, 9, 1993, 1901]. Потім для виділення проміжного алкіну з кінцевою групою можна застосувати подальше зняття захисту основою, як описано в [публікації Malacria M.; Tetrahedron, 33, 1977, 2813; або в публікації White J.D. і інш., Tet. Lett., 31, 1, 1990, 59]. Початкові матеріали, синтез яких спеціально не описується вище, або є в продажу або можуть бути одержані відомими фахівцям в даній області способами. У кожній з реакцій, що обговорюються вище або проілюстрованих на схемах, якщо не обумовлено інакше, тиск не є критичним. У загальному випадку прийнятний тиск близько 0,5-5 атмосфер, а переважним є тиск навколишнього середовища, тобто близько 1 атмосфери, як найбільш зручний. З посиланням на приведену вище схему 1, сполуку формули 1 можна одержати взаємодією сполуки формули D, де R4 і R15 мають такі ж значення, як указано вище, з аміном формули Е, де R1, R3 і R11 мають такі ж значення, як указано вище, в безводному розчиннику, зокрема, в розчиннику, вибраному з DMF (Ν ,Νдиметилформаміду), DME (етиленглікольдиметилового простого ефіру), DCE (дихлоретану), трет-бутанолу і фенолу, або в суміші згаданих розчинників при температурі в межах приблизно 50-150°С протягом періоду часу 1-48 годин. Гетероарилоксіаніліни формули Ε можна одержати за допомогою відомих фахівцям в даній області способів, таких як відновлення відповідних проміжних нітросполук. Відновлення нітрогруп ароматичного кільця можна провести згідно з способами, описаними в загальних рисах в п ублікаціях: [Brown R.K., Nelson N.A., J.Org.Chem., 1954, р.5149; Yuste R., Saldana Μ., Walls F., Tet.Lett, 1982, 23, 2, p.147; або в WO 96/09294], згаданій вище. Відповідні похідні гетероарилоксинітробензолу можна одержати з галогеннітробензольних попередників при нуклеофільному заміщенні галогену відповідним спиртом, як описано в публікаціях: [Dinsmore C.J. і інш., Bioorg.Med.Chem. Lett., 7, 10, 1997, 1345; Loupy А. і інш., Synth. Commun., 20, 18, 1990, 2855; або Brunelle D.J., Tet.Lett., 25, 32, 1984, 3383]. Сполуки формули Ε, в яких R 1 представляє С 1-С6-алкільну групу, можна одержати при відновному амінуванні початкового аніліну з участю R1CH(O). Сполуку формули D можна одержати обробкою сполуки формули С, де Z1 представляє активну груп у, таку як бром, йод, -N2, або -OTf (який представляє групу -OSO2CF3), або попередників активної групи, таких як NO2, NH; або ОН, агентом поєднання, таким як кінцеві алкінові або алкенові групи, вінілгалоген, вінілстанан, вінілборан, алкілборан, алкіл- або алкенілцинковий реагент. Сполуку формули С можна одержати обробкою сполуки формули В хлоруючим агентом, таким як РОСl3, SOCl2 або C1C(O)C(O)Cl/ДМФ(DMF) в галогенованому розчиннику при температурі близько 60-150°С протягом приблизно 2-24 годин. Сполуки формули В можна одержати із сполуки формули А, де Z1 має таке ж значення, як описане вище, a Z2 представляє NH2, С1-С6-алкокси або ОН у відповідності до однієї з методик, описаних в публікації WO 95/19774, згаданій вище. Будь-яка сполука формули 1 може бути перетворена в іншу сполуку формули 1 за допомогою стандартних маніпуляцій з R4-групою. Такі способи відомі фахівцям в даній області і включають: а) видалення захисної групи за допомогою способів, описаних в загальних рисах в публікації [T.W. Greene і P.G.M. Wuts, «Protective Groups in Organic Synthesis» Second Edition, John Wiley and Sons, New York, 1991]; b) заміщення групи (галогену, мезилату, тозилату і т.д), що видаляється первинним або вторинним аміном, тіолом або спиртом з утворенням вторинного або третинного аміну, простого тіоефіру або простого ефіру, відповідно; с) обробка фенілкарбаматів або (заміщених феніл)карбаматів первинними або вторинними амінами з утворенням відповідної сечовини, як описано в публікації [Thavonekham В. і інш., Synthesis (1997), 10, р.1189]; d) відновлення пропаргілового або гомопропаргілового спиртів, або N-BOC-захищених первинних амінів до похідних Е-алілу або Е-гомоалілу при обробці біс-(2-метоксіетокси) алюмогідридом натрію (червоним А1), як описано в публікаціях [Denmark S.E.; Jones T.K J.Org.Chem. (1982) 47, 4595-4597 або van Benthem R.A.T.M.; Michels J.J.; Speckamp W.N., Synlett (1994), 368-370]; е)відновлення алкінів до відповідних похідних Z-алкенів при обробці газоподібним воднем в присутності Pd-каталізатора, як описано в публікації [Tomassy В. і інш., Synth.Coiramm. (1998), 28, p.1201]; f) обробка первинних і вторинних амінів ізоціанатом, хлоридом карбонової кислоти (або іншим активованим похідним карбонової кислоти), алкіл/арилхлорформіатом або сульфонілхлоридом до одержання відповідних сечовини, аміду, карбамату або сульфонаміду; g) відновне амінування первинного або вторинного аміну із застосуванням R1CH(O); і h) обробка спиртів ізоціанатом, хлоридом карбонової кислоти (або іншим активованим похідним карбонової кислоти), алкіл/арилхлорформіатом або сульфонілхлоридом до одержання відповідних карбамату, складного ефіру, карбонату або складного ефіру сульфонової кислоти. Сполуки даного винаходу можуть містити асиметричні атоми вуглецю. Діастереомеричні суміші можна розділити на індивідуальні діастереомери на основі їх фізико-хімічних відмінностей відомими фахівцям в даній області способами, наприклад, хроматографічно або фракційною кристалізацією. Енантіомери можна розділити, перетворюючи суміші енантіомерів в діастереомеричну суміш при взаємодії з відповідною оптично активною сполукою (наприклад, спиртом), відділяючи діастереомери і перетворюючи (наприклад, гідролізом) окремі діастереомери до відповідних чистих енантіомерів. Всі такі ізомери, включаючи суміші діастереомерів і чисті енантіомери, є частиною винаходу. Сполуки формул і, що мають основний характер, здатні до утворення широкого ряду солей з різними неорганічними і органічними кислотами. Хоч такі солі повинні бути фармацевтично прийнятними для введення тваринам, часто на практиці бажано спочатку виділити сполуки формули 1 з реакційної суміші у вигляді фармацевтично неприйнятної солі і потім останню просто перетворити зворотно до вільної основної сполуки, обробляючи лужним реагентом і потім перетворюючи одержану вільну основу до фармацевтично прийнятної кислотно-адитивної солі. Кислотно-адитивні солі основних сполук даного винаходу легко одержати, обробляючи основну сполуку по суті еквівалентною кількістю вибраної мінеральної або органічної кислоти в середовищі водного розчинника або у відповідному органічному розчиннику, такому як метанол або етанол. Після обережного випаровування розчинника легко виходить необхідна тверда сіль. Необхідну кислу сіль можна також осадити з розчину вільної основи в органічному розчиннику при доданні до розчину відповідної мінеральної або органічної кислоти. Ті сполуки формули 1, які є кислими по характеру, здатні утворювати основні солі з різними фармакологічно прийнятними катіонами. Приклади таких солей включають солі лужних металів або лужноземельних металів і зокрема, солі натрію і калію. Всі такі солі одержують звичайними способами. Хімічні основи, що застосовуються як реагенти для одержання фармацевтично прийнятних основних солей даного винаходу, представляють основи, які утворюють нетоксичні основні солі з кислими сполуками формули 1. Такі нетоксичні основні солі включають фармакологічно прийнятні солі таких катіонів як натрій, калій, кальцій, магній і т.д. Такі солі можна легко одержати, обробляючи відповідні кислі сполуки водним розчином, що містить необхідну фармакологічно прийнятні катіони, і потім упарюючи одержаний розчин досуху, переважно при зниженому тиску. Альтернативно їх також можна одержати при спільному перемішуванні розчинів кислих сполук в нижчих спиртах і алкоксиду (алкоголята) необхідного лужного металу, і потім упарюючи одержаний розчин досуху також як раніше. У будь-якому випадку переважно використати стехіометричні кількості реагентів, щоб гарантувати повноту реакції і максимальний вихід необхідного кінцевого продукту. Оскільки окрема сполука даного винаходу може включати більш ніж один кислий або основний фрагмент(частина), сполуки даного винаходу одночасно можуть бути моно-, ди- або три-солями. Сполуки даного винаходу є сильними інгібіторами ЕrbB-сімейства онкогенних і протоонкогенних тирозинпротеїнкіназ, зокрема, ЕrbB2, і тому всі вони підходять для терапевтичного застосування як протипроліферативні засоби (наприклад, протиракові) для ссавців, особливо для людини. Зокрема, сполуки даного винаходу застосовні для запобігання і лікування ряду гіперпроліферативних захворювань у людини, таких як злоякісні і доброякісні пухлини печінки, нирки, сечового міхура, молочної залози, шлунка, яєчника, товстої і прямої кишки, простати, підшлункової залози, легенів, вульви, щитовидної залози, карцином печінки, сарком, гліобластом, пухлин голови і шиї і інших гіперпластичних станів, таких як доброякісна гіперплазія шкіри (наприклад, псоріаз) і доброякісна гіперплазія простати (наприклад, ВРН). Крім того, очікується, що сполука даного винаходу може володіти активністю проти ряду лейкемії і лімфоїдних злоякісних новоутворень. Сполуки даного винаходу також можна застосовувати для лікування адитивних захворювань, в які залучені аберантна експресія ліганд/рецепторних взаємодій або активація, або явища передачі сигналу, пов'язані з різними тирозинпротеїнкіназами. Такі захворювання можуть включати захворювання нейронної, гліальної, астроцитальної природи, розлади гіпоталамуса і інші гландулярні розлади, захворювання макрофагальної, епітеліальної, стромальної і бластоцельної природи, в які залучені аберантна функція, експресія, активація або передача сигналу erbB-тирозинкіназ. Крім того, сполуки даного винаходу можуть мати терапевтичне застосування при запальних, ангіогенних і імунологічних розладах, в які залучені не тільки ідентифіковані, але і поки ще неідентифіковані тирозинкінази, які інгібуються сполуками даного винаходу. Активність in vitro сполук формули І можна визначити по наступній методиці. Аналіз с-ЕrbB2-кінази проводили у відповідності до методики, описаної раніше в публікації [Schrang і інш., Anal. Biochem, 211, 1993, р.233-239]. 96-ямкові планшети Nunc MaxiSorp заповнювалися з розрахунку 100мл на ямку розчином 0,25мг/мл Poly(Glu, Туr) : (PGT) (Sigma Chemical Co., St.Louis, МО), в співвідношенні 4:1 в PBS (фосфатному буферному сольовому розчині) і інкубувалися протягом ночі при 37°С. Надлишок PGT видаляли шляхом аспірації і тричі промивали планшет буферним розчином (0,1% Tween-20 в PBS). Кіназну реакцію проводили в 50мл 50мМ розчині HEPES (рН 7,5), що містить 125мМ хлориду натрію, 10мМ хлориду магнію, 0,1мМ ортованадату натрію, 1мМ АТФ, 0,48мг/мл (24нг/ямка) с-ЕrbB2-внутрішньоклітинного домену. Внутрішньоклітинний домен ЕrbB2-тирозинкінази (амінокислоти 674-1255) експресується як пов'язаний з білком GST в бакуловірусі і очищається шляхом скріплення з намистинками, покритими глутатіоном, і подальшим елююванням. Додавали сполуки в ДМСО (диметилсульфоксиді) до досягнення кінцевої концентрації ДМСО приблизно 2,5%. Фосфорилювання ініціювали доданням АТФ (аденозинтрифосфату) і проводили протягом 6 хвилин при кімнатній температурі з постійним перемішуванням. Кіназну реакцію переривали шляхом аспірації реакційної суміші і подальшим промиванням буферним розчином для промивки (див. ви ще). Фосфорильований PGT визначали після 25-хвилинної інкубації з 50мл на ямку HRP-кон'югованого з PY54 (Oncogene Science Inc. Uniondale, NY)-антифосфо тирозиновим антитілом, розбавленим до 0,2мг/мл в блокуючому буфері (3% BSA і 0,05% Tween-20 в PBS). Антитіло видаляли шляхом аспірації і 4 рази промивали планшет буферним розчином для промивки. Колориметричний сигнал розвивався при доданні 50мл/на ямку ТМВ Microwell Peroxidase Substrate (субстрат пероксидази для мікроямок) (Kirkegaard and Perry, Gaithersburg, MD) і зупинявся при доданні 50мл/на ямку 0,09 Μ сірчаної кислоти. Концентрацію фосфо тирозину встановлювали, вимірюючи поглинання при 450нм. Контрольний сигнал становить звичайно 0,6-1,2 одиниць поглинання в порівнянні з незначним фоном для ямок без PGT-субстрату і пропорційний часу інкубації протягом 10 хвилин. Інгібітори ідентифікують по зменшенню сигналу в порівнянні з ямкою без інгібітору і визначають значення ІС 50, відповідні концентрації сполуки, необхідної для 50%-ного інгібування. Сполуки, що ілюструються тут і відповідні формулі І, мають значення ІС 50
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstituted bicyclic derivatives for the treatment of abnormal cells growth
Автори англійськоюKath John Charles, Bhattacharya Samit Kumar
Назва патенту російськоюЗамещенные бициклические производные для лечения аномального роста клеток
Автори російськоюКат Джон Чарльз, Бхаттачариа Самит Кумар
МПК / Мітки
МПК: A61P 5/28, A61K 31/517, A61K 45/00, A61K 31/55, C07D 403/12, C07D 405/14, C07D 401/14, A61P 35/00, A61P 43/00, C07D 239/94, C07D 401/12, C07D 413/14, C07D 413/12, A61K 39/395, A61P 5/00, A61K 31/5377, C07D 417/12
Мітки: заміщені, аномального, росту, похідні, лікування, клітин, біциклічні
Код посилання
<a href="https://ua.patents.su/26-73990-zamishheni-biciklichni-pokhidni-dlya-likuvannya-anomalnogo-rostu-klitin.html" target="_blank" rel="follow" title="База патентів України">Заміщені біциклічні похідні для лікування аномального росту клітин</a>
Попередній патент: Високоміцний, корозійностійкий суперсплав на основі нікелю та спрямовано скристалізована деталь
Наступний патент: Пристрій для контролю заряджання акумуляторних батарей
Випадковий патент: Автомобіль для перевезення затриманих осіб