Ліганди 5-нт рецептора та їх використання
Номер патенту: 74443
Опубліковано: 15.12.2005
Автори: Новомісле Уільям Альберт, Чіанг Юан-Чінг Фебе, Уелч Уіллард МакКован
Формула / Реферат
1. Сполука формули (IA)
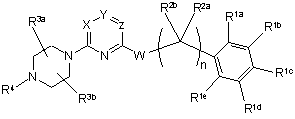 , (ІА)
, (ІА)
в якій
X і Y означають CR і Z означає N, або X означає N, а Y і Z означають CR, де R в кожному випадку означає водень;
W означає окси;
принаймні один з R1a, R1b, R1d та R1e незалежно вибраний з групи, яка складається з галогену, нітро, аміно, ціано, -C(O)NH2 та (C1-C4)алкілу, або R1a та R1b, взяті разом, утворюють п‘яти- або шестичленне ароматичне, або частково або повністю насичене конденсоване кільце, або R1a, взятий разом з R2a або R2b утворює п‘яти- або шестичленне повністю насичене конденсоване кільце;
R1c означає водень;
R2a та R2b кожний незалежно означає водень, (C1-C4)алкіл, частково або повністю насичений (C3-C6)циклоалкіл або один з них, взятий разом з R1a, утворює п‘яти- або шестичленне, повністю насичене конденсоване кільце;
n означає 0, 1 або 2;
R3a та R3b кожний незалежно означає водень, (C1-C4)алкіл або (C1-C4)алкіл, заміщений гідрокси, фтором або (C1-C4)алкокси;
R4 означає водень, гідрокси, (C1-C4)алкіл, (C1-C4)алкіл, заміщений гідрокси або ціано, (C1-C4)алкілкарбоніл, (C1-C4)алкокси, (C1-C4)алкоксикарбоніл або (C3-C4)алкеніл;
її азотний оксид, пролікарська форма згаданої сполуки або згаданого азотного оксиду; фармацевтично прийнятна сіль згаданої сполуки, згаданого азотного оксиду або згаданої пролікарської форми, або сольват, або гідрат згаданої сполуки, згаданого азотного оксиду, згаданої пролікарської форми або згаданої солі.
2. Сполука за п. 1, в якій
X і Y означають CR, а Z означає N, або X означає N, а Y і Z означають CR, де R для кожного випадку означає водень;
(i) R1a означає галоген, (C1-C4)алкіл або ціано, і R1b, R1d та R1е кожний означає водень,
(іi) R1b означає галоген, метил або ціано, і R1a, R1d та R1e кожний означає водень,
(iii) R1a і R1b кожний незалежно означає галоген або метил, і R1d та R1e кожний означає водень,
(іv) R1b і R1d кожний незалежно означає галоген або метил, і R1a та R1e кожний означає водень,
(v) R1a і R1d кожний незалежно означає галоген або метил, і R1b та R1e кожний означає водень,
(vi) R1a і R1e кожний незалежно означає галоген або метил, і R1b та R1d кожний означає водень, або
(vii) R1a, R1b і R1d кожний незалежно означає галоген або метил, і R1e означає водень;
W означає окси;
n означає 1 або 2;
R2a та R2b кожний незалежно означає (C1-C4)алкіл або водень;
R3a та R3b кожний незалежно означає водень або (C1-C2)алкіл; і
R4 означає водень або (C1-C4)алкіл;
її азотний оксид, пролікарська форма згаданої сполуки або згаданого азотного оксиду; фармацевтично прийнятна сіль згаданої сполуки, згаданого азотного оксиду або згаданої пролікарської форми, або сольват або гідрат згаданої сполуки, згаданого азотного оксиду, згаданої пролікарської форми або згаданої солі.
3. Сполука за п. 1, в якій
Z означає N;
X означає CH;
Y означає CR, де R означає водень;
(i) R1a означає галоген, (C1-C4)алкіл або ціано, і R1b, R1d та R1e кожний означає водень,
(ii) R1b означає галоген, метил або ціано, і R1a, R1d та R1e кожний означає водень,
(iii) R1a та R1b кожний незалежно означає галоген або метил, і R1d та R1e кожний означає водень,
(iv) R1b та R1d кожний незалежно означає галоген або метил, і R1a та R1e кожний означає водень,
(v) R1a та R1d кожний незалежно означає галоген або метил, і R1b та R1e кожний означає водень,
(vi) R1a та R1e кожний незалежно означає галоген або метил, і R1b та R1d кожний означає водень, або
(vii) R1a, R1b та R1d кожний незалежно означає галоген або метил, і R1e означає водень;
W означає окси;
n означає 1;
R2a та R2b кожний незалежно означають (C1-C4)алкіл або водень; і
R3a означає водень, (2R)-метил або (2R)-етил; і
R3b означає водень; і
R4 означає водень або (C1-C4)алкіл;
її азотний оксид, пролікарська форма згаданої сполуки або згаданого азотного оксиду; фармацевтично прийнятна сіль згаданої сполуки, згаданого азотного оксиду або згаданої пролікарської форми, або сольват, або гідрат згаданої сполуки, згаданого азотного оксиду, згаданої пролікарської форми або згаданої солі.
4. Сполука за п. 1, вибрана з групи, яка включає
2-(2-хлорбензилокси)-4-піперазин-1-ілпіримідин,
2-(3-фторбензилокси)-4-піперазин-1-ілпіримідин,
2-(3-хлорбензилокси)-4-піперазин-1-ілпіримідин,
2-(3-хлорбензилокси)-4-(2(R)-метилпіперазин-1-іл)піримідин,
2-[1-(3-фторфеніл)етокси]-4-піперазин-1-ілпіримідин,
2-[1-(2-хлорфеніл)етокси]-4-піперазин-1-ілпіримідин,
2-[1-(3-хлорфеніл)етокси]-4-піперазин-1-ілпіримідин,
2-(2,3-дифторбензилокси)-4-піперазин-1-ілпіримідин,
2-(2,5-дифторбензилокси)-4-піперазин-1-ілпіримідин,
2-(2,5-дифторбензилокси)-4-(2(R)-метилпіперазин-1-іл)піримідин,
2-(2,5-дихлорбензилокси)-4-піперазин-1-ілпіримідин,
2-(2,5-дихлорбензилокси)-4-(2(R)-метилпіперазин-1-іл)піримідин,
2-(3,5-дихлорбензилокси)-4-піперазин-1-ілпіримідин,
2-(3,5-дифторбензилокси)-4-піперазин-1-ілпіримідин і
4-піперазин-1-іл-2-(2,3,5-трифторбензилокси)піримідин;
її азотний оксид, пролікарська форма згаданої сполуки або згаданого азотного оксиду; фармацевтично прийнятна сіль згаданої сполуки, згаданого азотного оксиду або згаданої пролікарської форми, або сольват, або гідрат згаданої сполуки, згаданого азотного оксиду, згаданої пролікарської форми або згаданої солі.
5. Сполука за п. 1, вибрана з групи, яка включає
2-(3-хлорбензилокси)-4-піперазин-1-ілпіримідин,
2-(3-хлорбензилокси)-4-(2(R)-метилпіперазин-1-іл)піримідин,
2-(2,3-дифторбензилокси)-4-піперазин-1-ілпіримідин,
2-(2,5-дифторбензилокси)-4-піперазин-1-ілпіримідин,
2-(2,5-дифторбензилокси)-4-(2(R)-метилпіперазин-1-іл)піримідин,
2-(2,5-дихлорбензилокси)-4-(2(R)-метилпіперазин-1-іл)піримідин,
2-(3,5-дихлорбензилокси)-4-піперазин-1-ілпіримідин та
4-піперазин-1-іл-2-(2,3,5-трифторбензилокси)піримідин;
її азотний оксид, пролікарська форма згаданої сполуки або згаданого азотного оксиду; фармацевтично прийнятна сіль згаданої сполуки, згаданого азотного оксиду або згаданої пролікарської форми, або сольват, або гідрат згаданої сполуки, згаданого азотного оксиду, згаданої пролікарської форми або згаданої солі.
6. Сполука за п. 1, вибрана з групи, яка включає
гідрохлорид 2-(2-хлорбензилокси)-4-піперазин-1-ілпіримідину,
гідрохлорид 2-(3-фторбензилокси)-4-піперазин-1-ілпіримідину,
гідрохлорид 2-(3-хлорбензилокси)-4-піперазин-1-ілпіримідину,
гідрохлорид 2-(3-хлорбензилокси)-4-(2(R)-метилпіперазин-1-іл)піримідину,
гідрохлорид 2-(2,3-дифторбензилокси)-4-піперазин-1-ілпіримідину,
гідрохлорид 2-(2,5-дифторбензилокси)-4-піперазин-1-ілпіримідину,
гідрохлорид 2-(2,5-дихлорбензилокси)-4-піперазин-1-ілпіримідину,
гідрохлорид 2-(3,5-дихлорбензилокси)-4-піперазин-1-ілпіримідину та
гідрохлорид 2-(3,5-дифторбензилокси)-4-піперазин-1-ілпіримідину.
7. Сполука формули (IA)
 , (ІА)
, (ІА)
в якій
X і Y означають CR і Z означає N, або X означає N, а Y і Z означають CR, або
коли Z означає N, тоді X означає СН і Y означає СR або X означає СR і Y означає СН; або
коли Х означає N, тоді Y означає СН і Z означає СR або Y означає СR і Z означає СН;
де R в кожному випадку означає галоген, (C1-C4)алкіл, аміно або (C1-C4)алкіламіно;
W означає окси;
принаймні один з R1a, R1b, R1d та R1e незалежно вибраний з групи, яка складається з галогену, нітро, аміно, ціано, -C(O)NH2, (C1-C4)алкілу, (C1-C4)алкілу заміщеного галогеном, (C1-C4)алкокси і (C1-C4)алкокси заміщеного галогеном, або R1a та R1b, взяті разом, утворюють п‘яти- або шестичленне ароматичне або частково, або повністю насичене конденсоване кільце, або R1a, взятий разом з R2a або R2b, утворює п‘яти- або шестичленне, повністю насичене конденсоване кільце;
R1c означає водень;
R2a та R2b кожний незалежно означає водень, (C1-C4)алкіл, частково або повністю насичений (C3-C6)циклоалкіл або один з них, взятий разом з R1a, утворює п‘яти- або шестичленне, повністю насичене конденсоване кільце;
n означає 0, 1 або 2;
R3a та R3b кожний незалежно означає водень, (C1-C4)алкіл або (C1-C4)алкіл, заміщений гідрокси, фтором або (C1-C4)алкокси;
R4 означає водень, гідрокси, (C1-C4)алкіл, (C1-C4)алкіл, заміщений гідрокси або ціано, (C1-C4)алкілкарбоніл, (C1-C4)алкокси, (C1-C4)алкоксикарбоніл або (C3-C4)алкеніл;
її азотний оксид, пролікарська форма згаданої сполуки або згаданого азотного оксиду; фармацевтично прийнятна сіль згаданої сполуки, згаданого азотного оксиду або згаданої пролікарської форми, або сольват, або гідрат згаданої сполуки, згаданого азотного оксиду, згаданої пролікарської форми або згаданої солі.
8. Сполука формули (IA)
 , (ІА)
, (ІА)
в якій
X і Y означають CR і Z означає N, або X означає N, а Y і Z означають CR,
де R в кожному випадку означає водень, галоген, (C1-C4)алкіл, аміно або (C1-C4)алкіламіно;
W означає тіо, аміно, (C1-C4)алкіламіно або ацетиламіно;
принаймні один з R1a, R1b, R1d та R1e незалежно вибраний з групи, яка складається з галогену, нітро, аміно, ціано, -C(O)NH2, (C1-C4)алкілу, (C1-C4)алкілу заміщеного галогеном, (C1-C4)алкокси і (C1-C4)алкокси заміщеного галогеном, або R1a та R1b, взяті разом, утворюють п‘яти- або шестичленне ароматичне або частково, або повністю насичене конденсоване кільце, або R1a, взятий разом з R2a або R2b, утворює п‘яти- або шестичленне, повністю насичене конденсоване кільце;
R1c означає водень;
R2a та R2b кожний незалежно означає водень, (C1-C4)алкіл, частково або повністю насичений (C3-C6)циклоалкіл або один з них, взятий разом з R1a, утворює п‘яти- або шестичленне, повністю насичене конденсоване кільце;
n означає 0, 1 або 2;
R3a та R3b кожний незалежно означає водень, (C1-C4)алкіл або (C1-C4)алкіл, заміщений гідрокси, фтором або (C1-C4)алкокси;
R4 означає водень, гідрокси, (C1-C4)алкіл, (C1-C4)алкіл, заміщений гідрокси або ціано, (C1-C4)алкілкарбоніл, (C1-C4)алкокси, (C1-C4)алкоксикарбоніл або (C3-C4)алкеніл;
її азотний оксид, пролікарська форма згаданої сполуки або згаданого азотного оксиду; фармацевтично прийнятна сіль згаданої сполуки, згаданого азотного оксиду або згаданої пролікарської форми, або сольват, або гідрат згаданої сполуки, згаданого азотного оксиду, згаданої пролікарської форми або згаданої солі.
9. Сполука за п. 8, в якій
X і Y означають CR, а Z означає N, або X означає N, а Y і Z означають CR, де R для кожного випадку означає водень, галоген або (С1-С4)алкіл;
(і) R1a означає галоген, (C1-C4)алкіл, трифторметил, метокси, ціано або трифторметокси і R1b, R1d та R1е кожний означає водень,
(іі) R1b означає галоген, метил, ціано або метокси і R1a, R1d та R1e кожний означає водень,
(ііі) R1a і R1b кожний незалежно означає галоген, ціано або метил, і R1d та R1e кожний означає водень,
(iv) R1b і R1d кожний незалежно означає галоген, ціано або метил, і R1a та R1e кожний означає водень,
(v) R1a і R1d кожний незалежно означає галоген, ціано або метил, і R1b та R1e кожний означає водень,
(vi) R1a і R1e кожний незалежно означає галоген, ціано або метил, і R1b та R1d кожний означає водень, або
(vii) R1a, R1b і R1d кожний незалежно означає галоген, ціано або метил, і R1e означає водень;
W означає аміно;
n означає 1 або 2;
R2a та R2b кожний незалежно означає (C1-C4)алкіл або водень;
R3a та R3b кожний незалежно означає водень або (C1-C2)алкіл; і
R4 означає водень або (C1-C4)алкіл;
її азотний оксид, пролікарська форма згаданої сполуки або згаданого азотного оксиду; фармацевтично прийнятна сіль згаданої сполуки, згаданого азотного оксиду або згаданої пролікарської форми, або сольват, або гідрат згаданої сполуки, згаданого азотного оксиду, згаданої пролікарської форми або згаданої солі.
10. Сполука за п. 8, в якій
Z означає N;
X означає CH;
Y означає CR, де R означає водень або метил;
(i) R1a означає галоген, (C1-C4)алкіл, трифторметил, метокси, ціано або трифторметокси і R1b, R1d та R1е кожний означає водень,
(ii) R1b означає галоген, метил, ціано або метокси і R1a, R1d та R1e кожний означає водень,
(iii) R1a та R1b кожний незалежно означає галоген, ціано або метил, і R1d та R1e кожний означає водень,
(iv) R1b та R1d кожний незалежно означає галоген, ціано або метил, і R1a та R1e кожний означає водень,
(v) R1a та R1d кожний незалежно означає галоген, ціано або метил, і R1b та R1e кожний означає водень,
(vi) R1a та R1e кожний незалежно означає галоген, ціано або метил, і R1b та R1d кожний означає водень, або
(vii) R1a, R1b та R1d кожний незалежно означає галоген, ціано або метил, і R1e означає водень;
W означає аміно;
n означає 1;
R2a та R2b кожний незалежно означають (C1-C4)алкіл або водень; і
R3a означає водень, (2R)-метил або (2R)-етил;
R3b означає водень; і
R4 означає водень або (C1-C4)алкіл;
її азотний оксид, пролікарська форма згаданої сполуки або згаданого азотного оксиду; фармацевтично прийнятна сіль згаданої сполуки, згаданого азотного оксиду або згаданої пролікарської форми, або сольват, або гідрат згаданої сполуки, згаданого азотного оксиду, згаданої пролікарської форми або згаданої солі.
11. Сполука за п. 8, в якій
X означає N;
Y означає CR, де R означає водень або метил;
Z означає CH;
(i) R1a означає галоген, (C1-C4)алкіл, трифторметил, метокси, ціано або трифторметокси і R1b, R1d та R1е кожний означає водень,
(ii) R1b означає галоген, ціано або метокси і R1a, R1d та R1e кожний означає водень,
(iii) R1b та R1d кожний незалежно означає галоген, ціано або метил, і R1a та R1e кожний означає водень,
(iv) R1a та R1d кожний незалежно означає галоген, ціано або метил, і R1b та R1e кожний означає водень,
W означає аміно;
n означає 1;
R2a та R2b кожний незалежно означають (C1-C4)алкіл або водень;
R3a означає водень, (2R)-метил або (2R)-етил;
R3b означає водень; і
R4 означає водень або (C1-C4)алкіл;
її азотний оксид, пролікарська форма згаданої сполуки або згаданого азотного оксиду; фармацевтично прийнятна сіль згаданої сполуки, згаданого азотного оксиду або згаданої пролікарської форми, або сольват, або гідрат згаданої сполуки, згаданого азотного оксиду, згаданої пролікарської форми або згаданої солі.
12. Сполука за п. 8, вибрана з групи, яка включає
(3-хлорбензил)-(4-піперазин-1-ілпіримідин-2-іл)амін,
(3-хлорбензил)-(2-піперазин-1-ілпіримідин-4-іл)амін,
(3-фторбензил)-(4-піперазин-1-ілпіримідин-2-іл)амін і
(3-фторбензил)-(2-піперазин-1-ілпіримідин-4-іл)амін,
її азотний оксид, пролікарська форма згаданої сполуки або згаданого азотного оксиду; фармацевтично прийнятна сіль згаданої сполуки, згаданого азотного оксиду або згаданої пролікарської форми, або сольват або гідрат згаданої сполуки, згаданого азотного оксиду, згаданої пролікарської форми або згаданої солі.
13. Сполука за п. 8, вибрана з групи, яка включає
гідрохлорид (3-хлорбензил)-(4-піперазин-1-ілпіримідин-2-іл)аміну,
гідрохлорид (3-хлорбензил)-(2-піперазин-1-ілпіримідин-4-іл)аміну,
гідрохлорид (3-фторбензил)-(4-піперазин-1-ілпіримідин-2-іл)аміну і
фумарат (3-фторбензил)-(2-піперазин-1-ілпіримідин-4-іл)аміну.
14. Фармацевтична композиція, яка містить
(1) сполуку за будь-яким з пп. 1, 7 або 8 та
(2) фармацевтично прийнятний екципієнт, розріджувач або носій.
15. Фармацевтична композиція за п. 14, де згадана сполука вибрана з групи, яка включає
2-(2-хлорбензилокси)-4-піперазин-1-ілпіримідин,
2-(3-фторбензилокси)-4-піперазин-1-ілпіримідин,
2-(3-хлорбензилокси)-4-піперазин-1-ілпіримідин,
2-(3-хлорбензилокси)-4-(2(R)-метилпіперазин-1-іл)піримідин,
(3-хлорбензил)-(2-піперазин-1-ілпіримідин-4-іл)амін,
(3-хлорбензил)-(4-піперазин-1-ілпіримідин-2-іл)амін,
(3-фторбензил)-(4-піперазин-1-ілпіримідин-2-іл)амін,
(3-фторбензил)-(2-піперазин-1-ілпіримідин-4-іл)амін,
2-[1-(3-фторфеніл)етокси]-4-метил-6-піперазин-1-ілпіримідин,
2-[1-(3-фторфеніл)етокси]-4-піперазин-1-ілпіримідин,
2-[1-(2-хлорфеніл)етокси]-4-піперазин-1-ілпіримідин,
2-[1-(3-хлорфеніл)етокси]-4-піперазин-1-ілпіримідин,
2-[1-(3-хлорфеніл)етокси]-4-метил-6-піперазин-1-ілпіримідин,
2-(2,3-дифторбензилокси)-4-піперазин-1-ілпіримідин,
2-(2,5-дифторбензилокси)-4-піперазин-1-ілпіримідин,
2-(2,5-дифторбензилокси)-4-(2(R)-метилпіперазин-1-іл)піримідин,
2-(2,5-дихлорбензилокси)-4-піперазин-1-ілпіримідин,
2-(2,5-дихлорбензилокси)-4-(2(R)-метилпіперазин-1-іл)піримідин,
2-(3,5-дихлорбензилокси)-4-піперазин-1-ілпіримідин,
2-(3,5-дифторбензилокси)-4-піперазин-1-ілпіримідин і
4-піперазин-1-іл-2-(2,3,5-трифторбензилокси)піримідин;
її азотний оксид, пролікарська форма згаданої сполуки або згаданого азотного оксиду; фармацевтично прийнятна сіль згаданої сполуки, згаданого азотного оксиду або згаданої пролікарської форми, або сольват, або гідрат згаданої сполуки, згаданого азотного оксиду, згаданої пролікарської форми або згаданої солі.
16. Фармацевтична композиція за п. 14, де згадана сполука вибрана з групи, яка включає
2-(3-хлорбензилокси)-4-піперазин-1-ілпіримідин,
2-(3-хлорбензилокси)-4-(2(R)-метилпіперазин-1-іл)піримідин,
(3-хлорбензил)-(4-піперазин-1-ілпіримідин-2-іл)амін,
(3-хлорбензил)-(2-піперазин-1-ілпіримідин-4-іл)амін,
(3-фторбензил)-(4-піперазин-1-ілпіримідин-2-іл)амін,
(3-фторбензил)-(2-піперазин-1-ілпіримідин-4-іл)амін,
2-(2,3-дифторбензилокси)-4-піперазин-1-ілпіримідин,
2-(2,5-дифторбензилокси)-4-піперазин-1-ілпіримідин,
2-(2,5-дифторбензилокси)-4-(2(R)-метилпіперазин-1-іл)піримідин,
2-(2,5-дихлорбензилокси)-4-(2(R)-метилпіперазин-1-іл)піримідин,
2-(3,5-дихлорбензилокси)-4-піперазин-1-ілпіримідин та
4-піперазин-1-іл-2-(2,3,5-трифторбензилокси)піримідин;
її азотний оксид, пролікарська форма згаданої сполуки або згаданого азотного оксиду; фармацевтично прийнятна сіль згаданої сполуки, згаданого азотного оксиду або згаданої пролікарської форми, або сольват, або гідрат згаданої сполуки, згаданого азотного оксиду, згаданої пролікарської форми або згаданої солі.
17. Фармацевтична композиція за п. 14, де згадана сполука вибрана з групи, яка включає
гідрохлорид 2-(2-хлорбензилокси)-4-піперазин-1-ілпіримідину;
гідрохлорид 2-(3-фторбензилокси)-4-піперазин-1-ілпіримідину;
гідрохлорид 2-(3-хлорбензилокси)-4-піперазин-1-ілпіримідин;
гідрохлорид 2-(3-хлорбензилокси)-4-(2(R)-метилпіперазин-1-іл)піримідину;
гідрохлорид (3-хлорбензил)-(2-піперазин-1-ілпіримідин-4-іл)аміну;
гідрохлорид (3-хлорбензил)-(4-піперазин-1-ілпіримідин-2-іл)аміну;
гідрохлорид (3-фторбензил)-(4-піперазин-1-ілпіримідин-2-іл)аміну;
фумарат (3-фторбензил)-(2-піперазин-1-ілпіримідин-4-іл)аміну;
гідрохлорид 2-(2,3-дифторбензилокси)-4-піперазин-1-ілпіримідину;
гідрохлорид 2-(2,5-дифторбензилокси)-4-піперазин-1-ілпіримідину;
гідрохлорид 2-(2,5-дихлорбензилокси)-4-піперазин-1-ілпіримідину;
гідрохлорид 2-(3,5-дихлорбензилокси)-4-піперазин-1-ілпіримідину та
гідрохлорид 2-(3,5-дифторбензилокси)-4-піперазин-1-ілпіримідину.
18. Фармацевтична композиція за п. 14, в якій згаданий агент проти ожиріння вибраний з групи, до складу якої входять апо-B/MTP інгібітор, MCR-4 агоніст, CCK-A агоніст, інгібітор зворотного захоплення моноаміну, симпатоміметичний агент, агоніст ![]() 3 адренергічного рецептора, агоніст дoпаміну, аналог меланоцитстимулюючого гормону, антагоніст канабіноїдного 1 рецептора, антагоніст акумуляції гормону меланіну, лептин, аналог лептину, агоніст лептинового рецептору, антагоніст галаніну, інгібітор ліпази, агоніст бомбезину, антагоніст нейропептиду-Y, тироміметик, дегідроепіандростерон або його аналог, агоніст або антагоніст глюкокортикоїдного рецептора, антагоніст орексинового рецептора, антагоніст урокортинзв‘язувального протеїну, агоніст рецептора глюкагонподібного пептиду-1, циліарний нейротрофічний фактор, асоційований з агуті білок людини, антагоніст gh-relin рецептора, антагоніст або зворотний агоніст гістамінового 3 рецептора, агоніст нейромедин U рецептора.
3 адренергічного рецептора, агоніст дoпаміну, аналог меланоцитстимулюючого гормону, антагоніст канабіноїдного 1 рецептора, антагоніст акумуляції гормону меланіну, лептин, аналог лептину, агоніст лептинового рецептору, антагоніст галаніну, інгібітор ліпази, агоніст бомбезину, антагоніст нейропептиду-Y, тироміметик, дегідроепіандростерон або його аналог, агоніст або антагоніст глюкокортикоїдного рецептора, антагоніст орексинового рецептора, антагоніст урокортинзв‘язувального протеїну, агоніст рецептора глюкагонподібного пептиду-1, циліарний нейротрофічний фактор, асоційований з агуті білок людини, антагоніст gh-relin рецептора, антагоніст або зворотний агоніст гістамінового 3 рецептора, агоніст нейромедин U рецептора.
19. Фармацевтична композиція за п. 14, де згаданий агент проти ожиріння вибраний з групи, до складу якої входять орлистат, сибутрамін, бромокриптин, ефедрин, лептин і псевдоефедрин.
Текст
Даний винахід стосується сполук піримідину, які діють як ліганди 5-НТ рецепторів, зокрема, як ліганди 5НТ2с рецепторів, та їх використання в профілактиці або лікуванні захворювань, пов'язаних з активацією 5-НТ2с рецепторів у тварин. Рецептори серотоніну (5-гідрокситриптамін, 5-НТ) є важливим класом G протеїнозв'язувальних рецепторів. Вважається, що серотонін відіграє важливу роль в процесах, пов'язаних з навчанням та пам'яттю, сном, терморегуляцією, настроєм, рухливістю, болем, сексуальною та агресивною поведінками, апетитом, нейродегенеративною регуляцією та біологічними ритмами. Вважається, що серотонін пов'язаний з такими патофізіологічними станами, як неспокій, депресія, обесивно-компульсивні розлади, шизофренія, суїцид, аутизм, мігрень, блювота, алкоголізм та нейродегенеративні розлади. Рецептори серотоніну на даний час підрозділяються на сім підродин (5-НТ1 до 5-НТ7). Див., Hoyer, D. та ін./'VII International Union of Pharmacology classification of receptors for 5-hydroxytryptaMiHe", Pharmacol. Rev., 56, 157-203 (1994). Підродини в подальшому були розділені на підтипи. Наприклад, 5-НТ2 рецептор на даний час підрозділяється на три підтипи: 5-НТ2а, 5-НТ2b та 5-НТ2с. Три підтипи 5-НТ2 рецепторів зв'язуються з фосфоліпазою С з утворенням двох вторинних месенджерів, діацилгліцерину (який активує протеїнкіназу С) та інозиттрифосфату (який вивільняє інтрацелюлярне депо Са2+). 5-НТ2с рецептори мають дуже високу щільність в хоріоїдному сплетінні, епітеліальній тканині, яка є первинним місцем утворення спинно-мозкової рідини. Див., Sanders-Bush, Ε. та S. Ε. Mayer, "5-HydroxytryptaMiHe (Serotonin) Receptor агоністи and Антагоністи", Goodman & Gilman's The Pharmacological Basis of Therapeutics. Глава 11, 9те вид., McGraw-Hill, New York, NY (1996). Julius та ін. виділили і описали 5-НТ2с рецептор і пізніше доповіли, що трансгенні миші, у яких відсутні 5НТгс рецептори, демонструють розлади прийому їжі, що приводять до збільшеного споживання їжі (див., патенти США №. 4,985,352 та 5,698,766, відповідно). Відповідно, сполуки, селективні для 5-НТ2с рецептора, можуть забезпечувати сприятливе терапевтичне лікування розладів прийому їжі без побічних ефектів, що зазвичай асоціюються з неселективністю лігандів. Були запропоновані декілька сполук як агоністи або антагоністи 5-НТ2с рецепторів для використання в лікуванні ожиріння та інших споріднених захворювань, пов'язаних зі зменшення нейротрансмісії серотоніну у ссавців. Див., наприклад, ЕР 863136 (похідні азетидину та піролідину); ЕР 657426 (трициклічні похідні піролу); ЕР 655440 (заміщені 1-аміноетиліндоли); ЕР 572863 (похідні піразиноіндолу); W0 98/030548 (аміноалкіліндазольні сполуки); WO 98/56768 (трициклічні похідні піролу та піразолу); WO 99/43647 (похідні азетидину та піролідину); WO 99/58490 (похідні арилгідронафталіналканаміну); WO 00/12475 (похідні індоліну); WO 00/12482 (похідні індазолу); WO 00/12502 (похідні піролохіноліну); WO 00/12510 (похідні піролоіндолу, піридоіндолу та азепіноіндолу); WO 00/28993 (похідні нафтилацетилпіперазину); WO 00/44737 (похідні аміноалкілбензофурану); та WO 00/76984 (2,3-заміицені піразини). Неселективність лігандів різних 5-НТ рецепторів залишається складною проблемою. Вважається, що неселетивність деяких лігандів призводить до різних шкідливих побічних ефектів, таких як галюцинації та серцево-судинні ускладнення. Тому залишається необхідність в селективних лігандах 5-НТ2с рецепторів. Даний винахід стосується сполук формули (ІА), які є корисними як ліганди 5-НТ2 рецепторів (зокрема, ліганди 5-НТ2а та 5-НТ2с рецепторів), в якій X і Υ означають CR і Ζ означає Ν, або X означає Ν, а Υ і Ζ означають CR, де R в кожному випадку означає водень, галоген, (С1-С4)алкіл, аміно або (С1-С4)алкіламіно; W означає окси, тіо, аміно, (Ст-С^алкіламіно або ацетиламіно; принаймні один з R1a, R1b, R1d та R1e незалежно вибраний з групи, яка складається з галогену, нітро, аміно, ціано, -C(O)NH2, (С1-С4)алкілу, (С1-С4)алкілу, заміщеного галогеном, (С1-С4)алкокси та (С1-С4)алкокси, заміщеного галогеном, або R1a та R1b взяті разом утворюють п'яти- або шестичленне, ароматичне або частково або повністю насичене конденсоване кільце, або R1a взятий разом з R2a або R2b утворює п'яти-або шестичленне, повністю насичене конденсоване кільце; R1c означає водень; R2a та R2b кожний незалежно означає водень, (СгС^алкіл, частково або повністю насичений (СзСе)циклоалкіл або один з них, взятий разом з R1a, утворює п'яти- або шестичленне, повністю насичене конденсоване кільце; η означає 0, 1 або 2; R3a та R3b кожний незалежно означає водень, (С1-С4)алкіл або (С1-С4)апкіл, заміщений гідрокси, фтором або (С1-С4)алкокси; R4 означає водень, гідрокси, (С1-С4)алкіл, (С1-С4)алкіл, заміщений гідрокси або ціано, (С1-С4)алкілкарбоніл, (С1-С4)алкокси, (С1-С4)алкоксикарбоніл, (С3-С4)алкеніл або амінозахисну групу; їх азотного оксиду, проліків сполуки або азотного оксиду; фармацевтично прийнятної солі сполуки, азотного оксиду або проліків, або сольвату або гідрату сполуки, азотного оксиду, проліків або солі. Переважними сполуками формули (ІА) є сполуки, в яких X і Υ означають CR, a Z означає Ν, або X означає Ν, а Υ і Ζ означають CR, де R означає водень, хлор, фтор або метил; (і) R1a означає галоген, (С1-С4)алкіл, трифторметил, метокси або трифторметокси, і R1b, R1d та R1e кожний означає водень, (іі) R1b означає галоген, метил або метокси, і R1a, R1d та R1e кожний означає водень, (ііі) R1a і R1b кожний незалежно означає галоген або метил, і R1d та R1e кожний означає водень, (iv) R1b і R1d кожний незалежно означає галоген або метил, і R1a та R1e кожний означає водень, (v) R1a і R1d кожний незалежно означає галоген або метил, і R1b та R1e кожний означає водень, (vi) R1a і R1e кожний незалежно означає галоген або метил, і R1b та R1d кожний означає водень, або (vii) R1a, R1b і R1d кожний незалежно означає галоген або метил, і R1e означає водень; W означає окси або аміно; π означає 1; R2a та R2b кожний незалежно означає метил або водень; R3a та R3b кожний незалежно означає водень або (С1-С2)алкіл (переважно (2Р)-метил або (2Н)-етілп); і R4 означає водень або (С1-С4)алкіл; їх азотний оксид, проліки сполуки або азотного оксиду; фармацевтично прийнятна сіль сполуки, азотного оксиду або проліків, або сольват або гідрат сполуки, азотного оксиду, проліків або солі. Коли Ζ означає Ν, то X переважно означає СН; Υ означає CR, де R в кожному випадку означає водень або метил; (і) R1a означає галоген, (С1-С4)алкіл, трифторметил, метокси або трифторметокси, і R1b, R1d та R1e кожний означає водень, (іі) R1b означає галоген, метил або метокси і R1a, R1d та R1e кожний означає водень, (ііі) R1a та R1b кожний незалежно означає галоген або метил, і R1d та R1e кожний означає водень, (iv) R1b та R1d кожний незалежно означає галоген або метил, і R1a та R1e кожний означає водень, (v) R1a та R1d кожний незалежно означає галоген або метил, і R1b та R1e кожний означає водень, (vi) R1a та R1e кожний незалежно означає галоген або метил, і R1b та R1d кожний означає водень, або (vii) R1a, R1b та R1d кожний незалежно означає галоген або метил, і R1e означає водень; W означає окси або аміно; n означає 1; R2a та R2" кожний незалежно означають метил або водень; і R3a означає водень, (2R)-мeтил або (2R)-eтил; і R3b означає водень; і R4 означає водень або (С1-С4)алкіл; їх азотний оксид, проліки сполуки або азотного оксиду; фармацевтично прийнятна сіль сполуки, азотного оксиду або проліків, або сольват або гідрат сполуки, азотного оксиду, проліків або солі. Коли X означає N, та Υ переважно означає CR, де R означає водень або метил; Ζ означає СН; (і) R1a означає галоген, (С1-С4)алкіл, трифторметил, метокси або трифторметокси, і R1b, R1d та R1e кожний означає водень; (іі) R1b означає галоген, метил або метокси, і R1a, R1d та R1e кожний означає водень, (ііі) R1b та R1d кожний незалежно означає галоген або метил, і R1a та R1e кожний означає водень, або (iv) R1a та R1d кожний незалежно означає галоген або метил, і R1b та R1e кожний означає водень; W означає аміно; n означає 1; R 2a та R2b кожний незалежно означає метил або водень; R3a означає водень, (2R)-метил або (2R)етил; і R3b означає водень; і R4 означає водень або (С1-С4)алкіл; їх азотний оксид, проліки сполуки або азотного оксиду; фармацевтично прийнятна сіль сполуки, азотного оксиду або проліків, або сольват або гідрат сполуки, азотного оксиду, проліків або солі. Необмежувальні приклади переважних сполук формули (ІА) включають: 2-(2-хлорбензилокси)-4-піперазин-1-ілпіримідин, 2-(3-фторбензилокси)-4-піперазин-1-ілпіримідин, 2-(3-хлорбензилокси)-4-піперазин-1 -ілпіримідин, 2-(3-хлорбензилокси)-4-(2(R)-метилпіперазин-1-іл)піримідин, 2-(3-метоксибензилокси)-4-піперазин-1 -ілпіримідин, (3-хлорбензил)-(2-піперазин-1-ілпіримідин-4-іл)амін, (3-хлорбензил)-(4-піперазин-1-ілпіримідин-2-іл)амін, (3-фторбензил)-(4-піперазин-1-ілпіримідин-2-іл)амін, (3-фторбензил)-(2-піперазин-1-ілпіримідин-4-іл)амін, 2-[1-(3-фторфеніл)етокси]-4-метил-6-піперазин-1-ілпіримідин, 2-[1 -(3-фторфеніл)етокси]-4-піперазин-1 -ілпіримідин, 2-[1-(2-хлорфеніл)етокси]-4-піперазин-1 -ілпіримідин, 2-[1 -(3-хлорфеніл)етокси]-4-піперазин-1 -ілпіримідин, 2-[1 -(3-хлорфеніл)етокси]-4-метил-6-піперазин-1 -ілпіримідин, 2-(2,3-дифторбензилокси)-4-піперазин-1-ілпіримідин, 2-(2,5-дифторбензилокси)-4-піперазин-1-ілпіримідин, 2-(2,5-дифторбензилокси)-4-(2(Р)-метилпіперазин-1-іл)-піримідин, 2-(2,5-дихлорбензилокси)-4-піперазин-1-ілпіримідин, 2-(2,5-дихлорбензилокси)-4-(2(Н)-метилпіперазин-1-іл)-піримідин, 2-(3,5-дихлорбензилокси)-4-піперазин-1 -ілпіримідин, 2-(3,5-дифторбензилокси)-4-піперазин-1 -ілпіримідин, і 4-піперазин-1-іл-2-(2,3,5-трифторбензилокси)піримідин, їх азотний оксид, проліки сполуки або азотного оксиду; фармацевтично прийнятну сіль сполуки, азотного оксиду або проліків, або сольват або гідрат сполуки, азотного оксиду, проліків або солі. Переважні солі включають гідрохлорид 2-(2-хлорбензилокси)-4-піперазин-1-ілпіримідину; гідрохлорид 2-(3фторбензилокси)-4-піперазин-1-ілпіримідину; гідрохлорид 2-(3-хлорбензилокси)-4-піперазин-1 -ілпіримідин; гідрохлорид 2-(3-хлорбензилокси)-4-(2(Р)-метилпіперазин-1 -іл)піримідину; гідрохлорид (3-хлорбензил)-(2піперазин-1-ілпіримідин-4-іл)-аміну; гідрохлорид (3-хлорбензил)-(4-піперазин-1-ілпіримідин-2-іл)-аміну; гідрохлорид (3-фторбензил)-(4-піперазин-1 -ілпіримідин-2-іл)аміну; фумарат (3-фторбензил)-(2-- піперазин-1ілпіримідин-4-іл)аміну; гідрохлорид 2-(2,3-дифторбензилокси)-4-піперазин-1-ілпіримідину; гідрохлорид 2-(2,5дифторбензилокси)-4-піперазин-1-ілпіримідину; гідрохлорид 2-(2,5-дихлорбензилокси)-4-піперазин-1ілпіримідину; гідрохлорид 2-(3,5-дихлорбензилокси)-4-піперазин-1-ілпіримідину; та гідрохлорид 2-(3,5дифторбензилокси)-4-піперазин-1 -ілпіримідину. Необмежувальні приклади більш переважних сполук формули (1 А) включають: 2-(3-хлорбензилокси)-4-піперазин-1-ілпіримідин, 2-(3-хлорбензилокси)-4-(2(Р)-метилпіперазин-1-іл)піримідин, (3-хлорбензил)-(4-піперазин-1-ілпіримідин-2-іл)амін, (3-хлорбензил)-(2-піперазин-1-ілпіримідин-4-іл)амін, (3-фторбензил)-(4-піперазин-1-ілпіримідин-2-іл)амін, (3-фторбензил)-(2-піперазин-1-ілпіримідин-4-іл)амін, 2-(2,3-дифторбензилокси)-4-піперазин-1-ілпіримідин, 2-(2,5-дифторбензилокси)-4-піперазин-1-ілпіримідин, 2-(2,5-дифторбензилокси)-4-(2R)-метилпіперазин-1-іл)піримідин, 2-(2,5-дихлорбензилокси)-4-(2R)-метилпіперазин-1-іл)піримідин, 2-(3,5-дихлорбензилокси)-4-піперазин-1-ілпіримідин та 4-піперазин-1-іл-2-(2,3,5-трифторбензилокси)піримідин; їх азотний оксид, проліки сполуки або азотного оксиду; фармацевтично прийнятну сіль сполуки, азотного оксиду або проліків, або сольват або гідрат сполуки, азотного оксиду, проліків або солі. Ще в одному іншому втіленні даного винаходу описуються сполуки формули (1С). в якій X і Υ означають CR і Ζ означає Ν, або X означає Ν, а Υ і Ζ означають CR, де R в кожному випадку означає водень, галоген, (С1-С4)алкіл, аміно або (С1-С4)алкіламіно; W означає окси, тіо, аміно, (С1-С4)ал кіл аміно або ацетиламіно; Q означає гетероарильну групу, вибрану з групи, до складу якої входять піридин-2-іл, піридин-3-іл, фуран3-іл, фуран-2-іл, тіофен-2-іл, тіофен-3-іл, тіазол-2-іл, пірол-2-іл, пірол-3-іл, піразол-3-іл, хінолін-2-іл, хінолін-3іл, ізохінолін-3-іл, бензофуран-2-іл, бензофуран-3-іл, ізобензофуран-3-іл, бензотіофен-2-іл, бензотіофен-3-іл, індол-2-іл, індол-3-іл, 2Н-імідазол-2-іл, оксазол-2-іл, ізоксазол-3-іл, 1,2,4-оксадіазол-З-іл, 1,2,4-- триазол-3-іл та 1,2,4-оксатіазол-З-іл, де згадана гетероарильна група необов'язково заміщена одним - трьома замісниками, незалежно вибраними з галогену, (С1-С4)алкілу або (С1-С4)алкілокси; R2a та R2b кожний незалежно означає водень, (С1-С4)алкіл або частково або повністю насичений (С3С6)циклоалкіл; R3a i R3b кожний незалежно означає водень, (С1-С4)алкіл або (С1-С4)алкіл, заміщений гідрокси, фтором або (С1-С4)алкокси; R4 означає водень, гідрокси, (С1-С4)алкіл, (С1-С4)алкіл, заміщений гідрокси або ціано, (С1-С4)алкілкарбоніл, (С1-С4)алкокси, (С1-С4)алкоксикарбоніл, (С3-С4)алкеніл або амінозахисну групу; їх азотний оксид, проліки сполуки або азотного оксиду; фармацевтично прийнятна сіль сполуки, азотного оксиду або проліків, або сольват або гідрат сполуки, азотного оксиду, проліків або солі. Необмежувальні приклади переважних сполук формули (1С) включають: 4-піперазин-1-іл-2-(піридин-2ілметокси)піримідин, 2-(6-метил-піридин-2-ілметокси)-4-піперазин-1-ілпіримідин та 2-(б-хлорпіридин-2ілметокси)-4-піперазин-1-ілпіримідин; їх азотний оксид, проліки сполуки або азотного оксиду; фармацевтично прийнятну сіль сполуки, азотного оксиду або проліків, або сольват або гідрат сполуки, азотного оксиду, проліків або солі. Необмежувальні приклади більш переважних сполук формули (1С) включають 2-(6-метилпіридин-2ілметокси)-4-піперазин-1 -ілпіримідин та 2-(6-хлорпіридин-2-ілметокси)-4-піперазин-1-ілпіримідин; їх азотний оксид, проліки сполуки або азотного оксиду; фармацевтично прийнятну сіль сполуки, азотного оксиду або проліків, або сольват або гідрат сполуки, азотного оксиду, проліків або солі. Деякі сполуки, описані тут, містять принаймні один хіральний центр; відповідно, фахівцю буде зрозумілим, що в об'єм даного винаходу входять усі стереоізомери (наприклад, енантіомери та діастереоізомери) наведених та описаних тут сполук. Крім того, в об'єм даного винаходу входять таутомерні форми сполук. В іншому втіленні даного винаходу описується фармацевтична композиція, яка містить (1) сполуку формули (ІА) або (1С), їх азотний оксид, проліки сполуки або азотного оксиду; фармацевтично прийнятну сіль сполуки, азотного оксиду або проліків, або сольват або гідрат сполуки, азотного оксиду, проліків або солі, та (2) фармацевтично прийнятний екціпієнт, розбавник або носій. Ще в одному іншому втіленні даного винаходу описується спосіб лікування у тварин захворювань, станів або розладів, опосередкованих 5-НТ2 (переважно, 5-НТ2с) рецепторами, який включає введення тварині терапевтично ефективної кількості сполуки формули (IB) в якій X і Υ означають CR і Ζ означає Ν, або X означає Ν, а Υ і Ζ означають CR, де R в кожному випадку означає водень, галоген, (С1-С4)алкіл, аміно або (С1-С4)алкіламіно; W означає окси, тіо, аміно, (С1-С4)алкіламіно або ацетиламіно; R1a, R1b, R1C, R1d та R1e кожний незалежно означає водень, галоген, нітро, ціано, аміно, (С1-С4)алкіл, заміщений галогеном (С1-С4)алкіл, (С1-С4)алкокси, заміщений галогеном (С1-С4)алкокси, -C(O)NH2, R1a та R1b, взяті разом, утворюють п'яти- або шестичленне ароматичне або частково або повністю насичене конденсоване кільце, або R1a, взятий разом з R2a або R2b, утворює п'яти- або шестичленне, повністю насичене конденсоване кільце; R2a та R2b кожний незалежно означає водень, (С1-С4)алкіл, частково або повністю насичений (С3С6)циклоалкіл, або один з яких, взятий разом з R1a, утворює п'яти- або шестичленне, повністю насичене конденсоване кільце; n означає 0, 1 або 2; R3a та R3b кожний незалежно означає водень, (С1-С4)алкіл, (С1-С4)алкіл, заміщений гідрокси, фтором або (С1-С4)алкокси; R4 означає водень, гідрокси, (С1-С4)алкіл, (С1-С4)алкіл, заміщений гідрокси або ціано, (С1-С4)алкілкарбоніл, (С1-С4)алкокси, (С1-С4)алкоксикарбоніл або (С3-С4)алкеніл; її азотного оксиду, проліків сполуки або азотного оксиду; фармацевтично прийнятної солі сполуки, азотного оксиду або проліків, або сольвату або гідрату сполуки, азотного оксиду, проліків або солі. Альтернативно, як терапевтичні агенти можуть використовуватися сполуки, що мають формулу (1С), наведену вище. Необмежувальні приклади переважних сполук формули (IB) включають 2-бензилокси-4-метил-6-піперазин-1-ілпіримідин, 2-бензилокси-4-піперазин-1-ілпіримідин, 4-бензилокси-2-піперазин-1-ілпіримідин, бензил-(4-піперазин-1-ілпіримідин-2-іл)амін, бензил-(2-піперазин-1-ілпіримідин-4-іл)амін, 2-(3-фторбензилокси)-4-піперазин-1-ілпіримідин, 2-(3-хлорбензилокси)-4-піперазин-1-ілпіримідин, 2-(3-хлорбензилокси)-4-(2(Р)-метилпіперазин-1-іл)-піримідин, 2-(3-метокси-бензилокси)-4-піперазин-1-ілпіримідин, 2-(2-хлорбензилокси)-4-піперазин-1 -ілпіримідин, (3-хлорбензил)-(2-піперазин-1-ілпіримідин-4-іл)амін, (3-хлорбензил)-(4-піперазин-1-ілпіримідин-2-іл)амін, (3-фторбензил)-(4-піперазин-1-ілпіримідин-2-іл)амін, (3-фторбензил)-(2-піперазин-1-ілпіримідин-4-іл)амін, 2-[1 -(3-фторфеніл)етокси]-4-метил-6-піперазин-1 -ілпіримідин, 2-[1 -(3-фторфеніл)етокси]-4-піперазин-1 -ілпіримідин, 2-[1 -(2-хлорфеніл)етокси]-4-піперазин-1 -ілпіримідин, 2-[1-(3-хлорфеніл)етокси]-4-піперазин-1 -ілпіримідин, 2-[1 -(3-хлорфеніл)етокси]-4-метил-6-піперазин-1 -ілпіримідин, 2-(2,3-дифторбензилокси)-4-піперазин-1 -ілпіримідин, 2-(2,5-дифторбензилокси)-4-піперазин-1-ілпіримідин, 2-(2,5-дифторбензилокси)-4-(2(Р)-метилпіперазин-1-іл)-піримідин, 9 2-(2,5-дихлорбензилокси)-4-піперазин-1-ілпіримідин, 2-(2,5-дихлорбензилокси)-4-(2(І=І)-метилпіперазин-1-іл)-піримідин, 2-(3,5-дихлорбензилокси)-4-піперазин-1-ілпіримідин, 2-(3,5-дифторбензилокси)-4-піперазин-1 -ілпіримідин та 4-піперазин-1-іл-2-(2,3,5-трифторбензилокси)-піримідин; їх азотний оксид, проліки сполуки або азотного оксиду; фармацевтично прийнятну сіль сполуки, азотного оксиду або проліків, або сольват або гідрат сполуки, азотного оксиду, проліків або солі. Необмежувальні приклади більш переважних сполук включають 2-бензилокси-4-метил-6-піперазин-1-ілпіримідин, бензил-(2-піперазин-1-ілпіримідин-4-іл)амін, бензил-(4-піперазин-1-ілпіримідин-2-іл)амін, 4-бензилокси-2-піперазин-1-ілпіримідин, 2-бензилокси-4-піперазин-1-ілпіримідин, 2-(3-хлорбензилокси)-4-піперазин-1 -ілпіримідин, 2-(3-хлорбензилокси)-4-(2(R)-метилпіперазин-1-іл)-піримідин, (3-хлорбензил)-(4-піперазин-1-ілпіримідин-2-іл)амін, (3-хлорбензил)-(2-піперазин-1-ілпіримідин-4-іл)амін, (3-фторбензил)-(4-піперазин-1-ілпіримідин-2-іл)амін, (3-фторбензил)-(2-піперазин-1-ілпіримідин-4-іл)амін, 2-(2,3-дифторбензилокси)-4-піперазин-1-ілпіримідин, 2-(2,5-дифторбензилокси)-4-піперазин-1-ілпіримідин, 2-(2,5-дифторбензилокси)-4-(2(Р)-метилпіперазин-1-іл)-піримідин, 2-(2,5-дихлорбензилокси)-4-(2(Р)-метилпіперазин-1-іл)-піримідин, 2-(3,5-дихлорбензилокси)-4-піперазин-1 -ілпіримідин та 4-піперазин-1 -іл-2-(2,3,5-трифторбензилокси)піримідин; їх азотний оксид, проліки сполуки або азотного оксиду; фармацевтично прийнятну сіль сполуки, азотного оксиду або проліків, або сольват або гідрат сполуки, азотного оксиду, проліків або солі. Сполуки даного винаходу можуть уводитися в комбінації з іншими фармацевтичними агентами, такими як, апо-В/МТР інгібітори, MCR-4 агоністи, ССК-А агоністи, інгібітори зворотного захвату моноаміну, симпатоміметичні агенти, агоністи Рз адренергічних рецепторів, агоністи допаміну, аналоги меланоцитстимулюючих гормонів, антагоністи канабіноїдних 1 рецепторів, антагоністи акумуляції гормону меланіну, лептини, аналоги лептину, агоністи лептинових рецептор, антагоністи галаніну, інгібітори ліпази, агоністи бомбезину, антагоністи нейропептиду-Y, тіроміметики, дегідроепіандростерон або його аналоги, агоністи або антагоністи глюкокортикоїдних рецепторів, антагоністи орексинових рецепторів, антагоністи урокортинзв'язувального протеїну, агоністи рецепторів глюкагонподібного пептиду-1, циліарні нейротрофічні фактори, AGRPs (людські асоційовані з агуті білки), антагоністи gh-relin рецепторів, антагоністи Н3 рецепторів або зворотні агоністи, агоністи нейромедин U рецепторів і т.п. Комбінована терапія може проводитися у вигляді (а) одиничної фармацевтичної композиції, яка містить сполуку даного винаходу, принаймні один додатковий фармацевтичний агент, описаний вище, та фармацевтично прийнятний екціпієнт, розбавник, або носій; або (b) двох окремих фармацевтичних композицій, які складаються з (і) першої композиції, яка містить сполуку формули (1А), (1С) або (1B) та фармацевтично прийнятний екціпієнт, розбавник або носій, та (іі) другої композиції, яка містить принаймні один додатковий фармацевтичний агент, описаний вище, та фармацевтично прийнятний екціпієнт, розбавник або носій. Фармацевтичні композиції можуть уводитися одночасно або послідовно та в будь-якому порядку. Ще в одному аспекті даного винаходу описується фармацевтичний набір для використання споживачем для лікування або попередження у тварини захворювань, станів або розладів, опосередкованих 5-НТ2 рецепторами (переважно, захворювань, станів або розладів, опосередкованих 5-НТ2с рецепторами). Набір складається з а) придатної дозованої форми, яка містить сполуку даного винаходу; та Ь) інструкції, яка описує спосіб використання дозованої форми для лікування або попередження захворювання, стану або розладу, опосередкованих 5-НТ2 рецепторами. Ще в одному іншому втіленні даного винаходу описується фармацевтичний набір, який містить: а) першу дозовану форму, яка містить (і) сполуку даного винаходу та (іі) фармацевтично прийнятний носій, екціпієнт або розбавник; b) другу дозовану форму, яка містить (і) додатковий фармацевтичний агент, описаний вище, та (іі) фармацевтично прийнятний носій, екціпієнт або розбавник; та с) засіб зберігання (контейнер). Іншим аспектом даного винаходу є спосіб лікування жіночої сексуальної дисфункції (FSD), який полягає в уведенні жінці, яка має в цьому потребу, терапевтично ефективної кількості сполуки даного винаходу. Спосіб може в подальшому включати уведення одного або декількох додаткових активних агентів для лікування FSD. Додаткові активні агенти можуть бути вибрані з групи, до складу якої входять (1) модулятори рецепторів естрогену, агоністи естрогену, антагоністи естрогену або їх комбінації; (2) тестостерон-замінювальний агент, тестостернон (Tostrelle), дигідротестостерон, дегідроепіандростерон (DHEA), імплантат тестостерону або їх комбінації; (3) естроген, комбінація естрогену та медроксипрогестерону або ацетату медроксипрогестерону (МРА), або естроген та агент метилтестостерон-гормонзаміщувальної терапії; (4) один або декілька допамінергічних агентів; (5) один або декілька інгібіторів NPY (нейропептиду Y); (6) один або декілька агоністів меланокортинових рецепторів або модулятор або підсилювач меланокортину; (7) один або декілька інгібіторів NEP; (8) один або декілька інгібіторів PDE; та (9) один або декілька антагоністів або модуляторів рецепторів бомбезину. Лікування FSD охоплює розлади сексуального збудження у жінок (FSAD), оргастичні розлади у жінок (FOD), зниження сексуального бажання (HSDD) або сексуальний біль. В іншому втіленні даного винаходу описується спосіб лікування чоловічої еректильної дисфункції (MED), який полягає в уведенні чоловікові, який має в цьому потребу, терапевтично ефективної кількості сполуки даного винаходу. Іншим аспектом даного винаходу є спосіб підвищення вмісту нежирного м'яса придатних в їжу тварин, який полягає в уведенні придатній в їжу тварині сполуки даного винаходу або композиції, яка містить сполуку даного винаходу, в кількості, яка підвищує вміст нежирного м'яса. Сполуки даного винаходу можуть також уводитися придатній в їжу тварині в комбінації з будь-яким додатковим фармацевтичним агентом, описаним вище. В даному контексті термін «алкіл» стосується вуглеводневого радикалу загальної формули СпНгп+і· Алкановий радикал може бути лінійним або розгалуженим. Наприклад, термін «(СгС4)алкіл» стосується моновалентної, лінійної або розгалуженої аліфатичної групи, яка містить від 1 до 4 атомів вуглецю (наприклад, метил, етил, н-пропіл, Апропіл, н-бутил, i-бутил, emop-бутил, трет-бутил, та інші ізомери, які містять від 1 до 4 атомів вуглецю (включаючи стереоізомери). Алкановий радикал може бути незаміщеним або заміщеним одним або декількома замісниками. Наприклад, термін «гало-заміщений алкіл» стосується алкільної групи, заміщеної одним або декількома атомами галогену (наприклад, фторметил, дифторметил, трифторметил, перфторетил, хлорметил, бромметил та ін.). Аналогічно, алкільна частина алкокси-, алкіламіно-, діалкіламіноабо алкілтіогрупи має теж саме значення, як і алкіл, визначений вище, і гало-заміщена алкільна частина галозаміщеної алкокси-, алкіламіно-, діалкіламіно- або алкілтіогрупи має теж саме значення, як і галозаміщений алкіл, визначений вище. Термін «частково або повністю насичений циклоалкіл» стосується неароматичних кілець, які є або частково, або повністю гідрованими. Наприклад, частково або повністю насичений (С3-С6)циклоалкіл включає групи, такі як, циклопропіл, циклопропеніл, циклобутил, циклобутеніл, циклопентил, циклопентеніл, циклопентадієніл, циклогексил, циклогексеніл, циклогексадієніл та ін. Якщо не зазначено інакше, термін "конденсоване кільце" стосується частково або повністю насичених, а також ароматичних карбоциклічних або гетероциклічних кільцевих системі. Переважно, гетероциклічне кільце містить 1 або 2 гетероатоми, незалежно вибрані з азоту, кисню та сірки (необов'язково окисленої до відповідного сульфону або сульфоксиду). Необмежувальні приклади конденсованих кільцевих систем включають нафталін, індан, інден, ізоінден, бензофуран, ізобензофуран, бензо[b]тіофен, бензо[с]тіофен, індол, 3H-індол, 1H-ізоіндол, індазол, індоксазин, бензоксазол, антраніл, тетралін, 2H-1-бензопіран, хінолін, ізохінолін, цинолін, хіназолін, 2H-1,3-бензоксазин, 2H-1,4-бензоксазин, 1H-2,3-бензоксазин, 4Н-2, Ібензоксазин, 2Н-1.2-бензоксазин, 4H-1,4-бензоксазин та ін. Термін "гетероарил" стосується ароматичних моноциклічних або біциклічних кільцевих систем, які містять 1, 2 або 3 гетероатоми, незалежно вибрані з азоту, кисню та сірки. Гетероарильна група може бути незаміщеною або мати від 1 до 3 замісників. Серед замісників перевага надається галогенам (Вr, СІ, І або F), (С1-С4)алкілу та (С1-С4)алкокси. Придатні гетероарильні групи включають піридин-2-іл, піридин-3-іл, фуран-3іл, фуран-2-іл, тіофен-2-іл, тіофен-3-іл, тіазол-2-іл, пірол-2-іл, пірол-3-іл, піразол-3-іл, хінолін-2-іл, хінолін-3-іл, ізохінолін-3-іл, бензофуран-2-іл, бензофуран-3-іл, ізобензофуран-3-іл, бензотіофен-2-іл, бензотіофен-3-іл, індол-2-іл, індол-3-іл, 2Н-імідазол-2-іл, оксазол-2-іл, ізоксазол-3-іл, 1,2,4-оксадіазол-З-іл, 1,2,4-триазол-З-іл, 1,2,4-оксатіазол-З-іл та ін. Термін «заміщений» означає, що атом водню на молекулі замінений різними атомами або молекулами. Атом або молекула, що замінюють атом водню, визначаються як «замісник». Термін заміщений особливо призначений для заміщення, що є загальноприйнятим в даній галузи техніки. Однак, фахівцю загалом зрозуміло, що замісники повинні вибиратись так, щоб не впливати несприятливим чином на фармакологічні характеристики сполуки або несприятливим чином заважати використанню медикаменту. Термін "азотний оксид" або "N-оксид" стосується оксидування принаймні одного з азотів в піримідиновому або піразиновому кільці сполук формули (1Α), (1Β) або (1С) (наприклад, моно- або діоксид). Азотні монооксиди можуть існувати у вигляді одного позиційного ізомеру або суміші позиційних ізомерів (наприклад, суміш 1 -N-оксиду та 3-N-оксиду піримідину або суміші 1-N-оксиду та 4-Ы-оксиду піразину). Термін "захисна група" або "Рg" стосується замісника, який зазвичай використовується для блокування або захисту конкретної функціональної групи під час реагування інших функціональних груп сполуки. Наприклад, «амінозахисна група» є замісником, приєднаним до аміногрупи, який блокує або захищає функціональну аміногрупу в сполуці. Придатними амінозахисними групами є ацетил, трифторацетил, третбутоксикарбоніл (ВОС), бензилоксикарбоніл (CBz) та 9-флуоренілметиленоксикарбоніл (Fmoc). Подібним чином термін «гідроксизахисна група» стосується замісника гідроксигрупи, який блокує або захищає гідроксильну функціональну групу. Придатні захисні групи включають ацетил та силіл. Термін «карбоксизахисна група» стосується замісника карбоксигрупи, який блокує або захищає карбоксильну функціональну групу. Звичайні карбоксизахисні групи включають -CH2CH2SO2Ph, ціаноетил, 2(триметилсиліл)етил, 2-(триметилсиліл)етоксиметил, 2-(п-толуолсульфоніл)етил, 2(нітрофенілсульфеніл)етил, 2-(дифенілфосфіно)етил, нітроетил та подібні. Загальний опис захисних груп та їх використання, див. Т. W. Greene, Protective Groups in Organic Synthesis, John Wiley & Sons, New York, 1991. Термін "ліганд" стосується сполуки, що приєднується до рецептора. В даному контексті ліганд може проявляти часткову або повну агоністичну або антагоністичну 13 активність. Фраза "терапевтично ефективна кількість" стосується кількості сполуки даного винаходу, яка (і) лікує або попереджує конкретні хвороби, стани або розлади, (іі) пом'якшує перебіг, покращує стан, або знімає один або декілька симптомів конкретної хвороби, стану або розладу, або (ііі) попереджує або затримує прояву одного або декількох симптомів конкретної хвороби, стану або розладу, описаних тут. Термін "тварина" стосується людей, домашніх тварин (наприклад, собак, котів та коней), тварин, м'ясо яких використовується в їжу, зоотварин, морських тварин, птахів та інших подібних видів тварин. Термін "придатні в їжу тварини" стосується тварин, м'ясо яких використовується в їжу, таких як, корови, свині, вівці та домашня птиця. Фраза "фармацевтично прийнятний" вказує на те, що речовина або композиція повинні бути сумісні хімічно та/або токсикологічно з іншими інгредієнтами, що містяться в рецептурі, та/або з ссавцями, яких піддають лікуванню за її допомогою. Терміни "процес лікування", "лікувати" або "лікування" означає як превентивне, тобто, профілактичне, так і паліативне лікування. Термін "сполуки даного винаходу" (якщо спеціально не вказано інакше) стосується сполук формули (ІА), (1С) та (IB), їх азотних оксидів, проліків сполук або азотних оксидів, фармацевтично прийнятних солей сполук, азотних оксидів та/або проліків, та гідратів або сольватів сполук, азотних оксидів, солей та/або проліків, а також усіх стереоізомерів (у тому числі діастереоізомерів та енантіомерів), таутомерів та сполук, мічених ізотопами. Даний винахід стосується способу лікування або попередження захворювань, станів або розладів, опосередкованих 5-НТ2 рецепторами, шляхом уведення сполук формули (IB), які діють як ліганди 5-НТ2 рецепторів (переважно, ліганди 5-НТ2с та/або 5-НТга рецепторів) де X і Υ означають CR і Ζ означає Ν, або X означає Ν, а Υ і Ζ означають CR, де R в кожному випадку означає водень, галоген, (С1-С4)алкіл, аміно або (С1-С4)алкіламін; W означає окси, тіо, аміно, (С1-С4)алкіламіно або ацетиламіно; R1a, R1b, R1c, R1d та R1e кожний незалежно означає водень, галоген, нітро, ціано, аміно, -C(O)NH2, (С1С4)алкіл, гало-заміщений (С1-С4)алкіл, (С1-С4)алкокси, гало-заміщений (С1-С4)алкокси, R1a та R1b, взяті разом, утворюють п'яти- або шестичленне, ароматичне або частково або повністю насичене конденсоване кільце, або R1a, взятий разом з R2* або R2b, утворює п'яти- або шестичленне, повністю насичене конденсоване кільце; R2a та R2b кожний незалежно означає водень, (С1-С4)алкіл, частково або повністю насичений (С3С6)циклоалкіл, або один з яких, взятий разом з R1a, утворює п'яти- або шестичленне, повністю насичене конденсоване кільце; η означає 0, 1 або 2 (переважно 1 або 2); R3a та R3" кожний незалежно означає водень, (С1-С4)алкіл або (С1-С4)алкіл, заміщений гідрокси, фтором або (С1-С4)алкокси; R4 означає водень, гідрокси, (С1-С4)алкіл, (С1-С4)алкіл, заміщений гідрокси або ціано, (С1-С4)алкілкарбоніл, (С1-С4)алкокси, (С1-С6)алкоксикарбоніл або (С3-С4)алкеніл; їх азотний оксид, проліки сполуки або азотного оксиду; фармацевтично прийнятна сіль сполуки, азотного оксиду або проліків, або сольват або гідрат сполуки, азотного оксиду, проліків або солі. Сполуки даного винаходу можуть бути синтезовані шляхами, що включають процеси, аналогічні тим, які відомі в хімічній галузі, особливо з точки зору опису, що міститься тут. Вихідними речовинами загалом є реагенти, доступні від таких комерційних виробників, як Aldrich Chemicals (Milwaukee, WI), або вони можуть бути легко одержані з використанням методик, добре відомих фахівцям (наприклад, одержані за методиками, описаними в книзі Louis F. Fieser та Магу Fieser, Reagents for Organic Synthesis, том. 1-19, Wiley, New York (1967-1999 ed.), або Beilstein Handbuch der orqanischen Chemie, 4, Aufl. Ed. Springer-Verlag, Berlin, включаючи додатки (також доступні через базу даних Beilstein. що працює в оперативному режимі)). Для ілюстрації схеми реакції, наведені нижче, показують потенційні шляхи синтезу сполук даного винаходу, а також ключові проміжні сполуки. Для більш детального опису конкретних стадій реакції дивись розділ Приклади. Фахівцю буде зрозумілим, що можуть бути використані інші шляхи синтезу для одержання сполук винаходу. Хоча на схемах, зображених нижче, наводяться та описуються конкретні вихідні речовини та реагенти, можуть бути використані інші вихідні речовини та реагенти для забезпечення різноманітності похідних та/або умов реакції. Крім того, багато сполук, одержаних за методиками, описаними нижче, можуть бути в подальшому модифіковані з огляду на даний опис, з використанням стандартних хімічних способів, добре відомих фахівцям. Наприклад, сульфідний зв'язок (тобто, W = S) може бути легко оксидований до відповідної сульфінільної або сульфонільної групи (тобто, W = SO або SO2), використовуючи загальні методики оксидування (наприклад, оксидування за допомогою м-хлорпербензойної кислоти). При одержанні сполук даного винаходу, може бути необхідним захист віддаленої функціональної групи (наприклад, первинної або вторинної аміногрупи) проміжних сполук. Необхідність такого захисту буде змінюватись в залежності від природи віддаленої функціональної групи та умов способу одержання. Придатними амінозахисними групами (NH-Pg) ацетильна, трифторацетильна, трет-бутоксикарбонільна (ВОС), бензилоксикарбонільна (CBz) та 9-флуоренілметиленоксикарбонільна (Fmoc) групи. Необхідність такого захисту легко визначається фахівцем. Загальний опис захисних груп та їх використання, див. Т. W. Greene, Protective Groups in Organic Synthesis. John Wiley & Sons, New York, 1991. На схемі І показано одержання сполук даного винаходу, в яких W означає О, S, аміно або (С1С4)алкіламіно. Взаємодією дигалогензаміщеної гетероарильної сполуки Формули II зі сполукою формули III (R4 необов'язково може бути амінозахисною групою) в придатному розчиннику (наприклад, етанолі, трет-бутанолі, w-бутанолі, толуолі, діоксані, THF, DMF або ацетонітрилі) в присутності придатної основи (наприклад, карбонату натрію, карбонат калію, карбонат цезію, гідроксиду натрію (NaOH), гідроксиду калію, 1,8діазабіцикло[5.4.0]ундец-7-ену (DBU), триетиламіну (TEA) або піридину) при температурі від приблизно 25°С до приблизно 200°С протягом від приблизно 1 до приблизно 168 годин одержують проміжну сполуку IV. Обробка проміжної сполуки IV надлишком придатного аміну в розчиннику (наприклад, ЕЮН, трет-ВиОН, діоксані, THF або DMF) в присутності придатної основи (наприклад, карбонату натрію, карбонат калію, карбонат цезію, NaOH, гідриду натрію, DBU, TEA або піридину) при температурі від приблизно 25°C до приблизно 200°С протягом від приблизно 1 до приблизно 7 днів приводить до утворення проміжної сполуки V, в якій W означає амінозв'язувальну групу або амінозв'язувальну групу, заміщену (С1-С4)алкілом. Придатні аміни включають бензиламін, 3-хлорбензил мін, 3-фторбензиламін та ін. Альтернативно, проміжна сполука IV може взаємодіяти з аніоном придатного спирту або тіолу в розчиннику (наприклад, THF, толуолі, діоксані, DMF, бензолі або суміші бензолу та води) в присутності або без каталізатора, такого як, 18-краун-6 при температурі від приблизно 25°C до приблизно 200°C протягом від приблизно 1 до приблизно 48 годин з утворенням сполуки формули V, в якій W означає О або S. Аніон може бути одержаний обробкою відповідного спирту або тіолу основою (наприклад, карбонатом калію, гідридом натрію, гідроксид натрію, гідроксидом калію, трет-бутоксидом калію або металевим натрієм) в інертному розчинник (наприклад, толуолі, діоксані, DMF, THF або бензолі при температурі від приблизно 25°C до приблизно 200°C протягом від приблизно 1 до приблизно 24 годин. Придатними спиртами є бензиловий спирт, сс-фенетиловий спирт, β-фенетиловий спирт, 3 фторбензиловий спирт, 3-хлорбензиловий спирт, 3-метоксибензиловий спирт, 2-хлорбензиловий спирт, 3фтор-а-фенетиловий спирт, 2-хлор-а-фенетиловий спирт, 3-хлор-а-фенетиловий спирт, 2,5дифторбензиловий спирт, 2,5-дихлорбензиловий спирт, 3,5-дифторбензиловий спирт, 3,5-дихлорбензиловий спирт, 2-гідроксиметилпіридин, 2-гідроксиметил-6-хлорпіридин, 2-гідроксиметил-6-метилпіридин та ін. Придатними тіолами є α-толуолтіол, (2-метилфеніл)метантіол, 3-(трифторметил)-ос-толуолтіол, 2-хлор-aтолуолтіол, (3-метилфеніл)метантіол, 2-хлор-6-фторбензилмеркаптан, офторбензилмеркаптан, мхлорбензилмеркаптан, 2,4,6-триметилбензилмеркаптан та ін. Сульфідний зв'язок може бути оксидований до відповідної сульфінільної або сульфонільної групи з використанням стандартних оксидувальних методик, добре відомих фахівцям. Коли R4 означає амінозахисну групу, проміжну сполуку V депротекгують з одержанням аміну VI. Наприклад, амін, захищений ВОС, може бути депротектований шляхом обробки трифтороцтовою кислотою (TFA) в СН2СІ 2. Вторинний амін VI може бути алкілований до аміну VII за методиками, добре відомими фахівцям. Серед методик перевага надається відновному алкілуванню. Загалом, реакції відновного алкілування перетворюють проміжну сполуку VI в основу Schiff шляхом взаємодії з відповідним альдегідом або кетом в полярному розчиннику при температурі від приблизно 10°С до г протягом 140°С протягом від приблизно 2 до приблизно 24 годин в присутності 3А молекулярних сит. Зазвичай до аміну додають еквівалентну кількість або невеликий надлишок альдегіду або кетону. Придатними полярними розчинниками є метиленхлорид, 1,2-дихлоретан, диметилсульфоксид, диметилформамід, спирти (наприклад, метанол або етанол), або їх суміші. Серед розчинників перевага надається метанолу. В тому ж самому реакційному посуді імін потім відновлюють до третинного аміну в присутності відновлювального агента при температурі від приблизно 0°C до приблизно 10°C і потім нагрівають до температури від приблизно 20°C до приблизно 40°C протягом від приблизно ЗО хвилин до приблизно 2 годин. Придатними відновними агентами є піридин, борановий комплекс та борогідриди металів, такі як, борогідрид натрію, триацетоксиборогідрид натрію та ціаноборогідрид натрію. Придатні альдегіди або кетони включають параформальдегід, ацетальдегід, ацетон та ін. Альтернативно, амін VI може бути ацильований або перетворений у карбамат згідно з методиками, добре відомими фахівцям в даній галузі. Сполуки даного винаходу, в яких W означає амінозв'язувальну групу (ΝΗ) або алкіламінозв'язувальну групу, також можуть бути одержані відновним алкілуванням аміногрупи, приєднаної до піримідинового або піразинового кільця, як це показано на Схемі II нижче. Шляхи синтезу є аналогічними тим, що описані вище, для відновного - алкілування проміжної сполуки VI на Схемі І. Сполука формули VIII може бути перетворена в бензиламін XI способами, добре відомими в галузі. Серед цих способів перевага надається відновному алкілуванню, як це описано раніше на Схемі І, де з проміжною сполукою IX утворюють основу Schiff і потім відновлюють відповідним відновлювальним агентом. Придатними альдегідами та кетонами є (тобто, сполукою формули IX) є 3-хлорбензальдегід, 3-фторбензальдегід, мхлорацетофенон, м-хлорпропіофенон, о-хлорацетофенон, 2-фторбензальдегід, 2-хлорбензальдегід, 2,6дихлорбензальдегід, 2,5-дихлорацетофенон, 2-хлор-5-метилацетофенон, 2,5-дифторацетофенон, 2,5дифторпропіофенон, 2,3-дихлорбензальдегід, 2,3-дифторбензальдегід, 2,5-дифторбензальдегід, 2-хлор-5фторацетофенон, 5-хлор-2-метоксибензальдегід, 2-фтор-5-метоксибензальдегід, 2,5-дихлорбензальдегід, 3,5дихлорбензальдегід, 3,5-дихлорацетофенон, 3,5-дифторбензальдегід, 2,3,5-трифторбензальдегід, 2,3,5трифторацетофенон, 2,3,5-трифторпропіофенон, 2,3,5-трихлорбензальдегід, 2,3,6-трифторбензальдегід та ін. Обробкою одержаної сполуки Формули X піперазином III в придатному розчиннику (наприклад, етанолі, mpemбутанолі, н-бутанолі, толуолі, діоксані, THF, DMF або ацетонітрилі) в присутності відповідної основи (наприклад, карбонату натрію, карбонату калію, гідроксиду натрію, TEA, DBU або піридину) при температурі від приблизно 25 до приблизно 200°C протягом від приблизно 1 дня до приблизно семи днів одержують сполуки Формули XI. Для виділення сполук даного винаходу, а також різних проміжних сполук для їх одержання, можуть бути використані стандартні способи та/або методики розділення та очистки, відомі фахівцям. Такі методики будуть добре відомі фахівцю в даній галузі і можуть включати, наприклад, усі типи хроматографії (рідинна хроматографія високого тиску (HPLC), колонкова хроматографія з використанням звичайних адсорбентів, таких як, силікагель, та тонкошарова хроматографія), перекристалізацію та диференційну (тобто, рідина рідина) екстракцію. Сполуки даного винаходу можуть бути виділені та використані самі по собі або у формі їх фармацевтично прийнятної солі, сольвату та/або гідрату. Термін "солі" стосується неорганічних та органічних солей сполуки даного винаходу. Ці солі можуть бути одержані in situ в процесі кінцевого виділення та очистки сполуки, або окремою взаємодією сполуки, N-оксиду або проліків з придатною органічною або неорганічною кислотою та виділенням солі, утвореної таким чином. Типові солі включають гідробромідні, гідрохлоридні, гідройодидні, сульфатні, бісульфатні, нітратні, ацетатні, трифторацетатні, оксалатні, бесилатні, пальмітатні, памоатні, малонатні, стеаратні, лауратні, малатні, боратні, бензоатні, лактатні, фосфатні, гексафторфосфатні, бензолсульфонатні, тозилатні, форміатні, цитратні, малеатні, фумаратні, сукцинатні, тартратні, нафтилатні, мезилатні, глюкогептонатні, лактобіонатні та лаурилсульфонатні солі та ін. Вони можуть містити катіони, що походять від лужних та лужноземельних металів, таких як, натрій, літій, калій, кальцій, магній та ін., а також нетоксичні катіони амонію, четвертинного амонію та аміну, включаючи, але не обмежуючись ними, амоній, тетраметиламоній, тетраетиламоній, метиламін, диметиламін, триметиламін, триетиламін, етиламін та ін. Див., наприклад, Berge, та ін., J. Pharm. Sci., 66,1-19 (1977). Термін "азотний оксид" або "N-оксид" стосується оксидування принаймні одного з атомів азоту в піримідиновому або піразиновому кільці. Оксидування ароматичного азоту добре відоме. Звичайні оксидувальні агенти включають такі реагенти, як пероксид водню, трифторпероцтова кислота, /nхлорпербензойна кислота та ін. Загалом оксидування здійснюють в інертному розчиннику (наприклад, метиленхлориді або хлороформі). Положення N-оксидування може змінюватися в залежності від стеричних перешкод, що спричиняються замісниками, що знаходяться на сусідньому атомі вуглецю. N-Оксид або суміш N-оксидів може бути виділена або розділена з використанням стандартних методик, таких як, рідинна хроматографія та/або селективна кристалізація. Термін "проліки" означає сполуку, яка трансформується in vivo з утворенням сполуки Формули (ІА, IB або 1С) або фармацевтично прийнятної солі, гідрату або сольвату сполуки. Трансформація може відбуватися за різними механізмами, такими як, гідроліз в крові. Детальне обговорення використання проліків подано Т. Higuchi та W. Stella в «Pro-drugs as Novel Delivery Systems», том. 14, A. C. S. Symposium Series, та в Bioreversible Carriers in Drug Design, вид. Edward B. Roche, American Pharmaceutical Association and Pergamon Press, 1987. Наприклад, якщо сполука даного винаходу містить функціональну групу карбонової кислоти, проліки можуть містити естер, утворений заміною атому водню кислотної фупи групою, такою як, (С1-С8)алкіл, (С2С12)алканоїлоксиметил, 1-(алканоїлокси)етил, що має від 4 до 9 атомів вуглецю, 1-метил-1(алканоїлокси)етил, що має від 5 до 10 атомів вуглецю, алкоксикарбонілоксиметил, що має від 3 до 6 атомів вуглецю, 1-(алкоксикарбонілокси)етил, що має від 4 до 7 атомів вуглецю, 1-метил-1(алкоксикарбонілокси)етил, що має від 5 до 8 атомів вуглецю, N-(алкоксикарбоніл)амінометил, що має від 3 до 9 атомів вуглецю, 1-(N-(алкоксикарбоніл)аміно)етил, що має від 4 до 10 атомів вуглецю, 3-фталиділ, 4кротонолактоніл, гамма-бутиролактон-4-іл, ді-N,N-(С1-С2)алкіламіно(С2-С3)алкіл (такий як, βдиметиламіноетил), карбамоїл-(С1-С2)алкіл, N,N-ді(С1-С2)алкілкарбамоїл(С1-С2)алкіл та піперидино-, піролідино- або морфоліно(С2-С3)алкіл. Подібним чином, якщо сполука даного винаходу містить спиртову функціональну групу, проліки можуть бути утворені заміною атому водню спиртової групи групою, такою як, (С1-С6)алканоїлоксиметил, 1-((С1С6)алканоїлокси)етил, 1-метил-1-((С2С6)алканоїлокси)етил, (С1-С6)алкоксикарбонілоксиметил, N-(C1Сб)алкоксикарбоніламінометил, сукциноїл, (Сі-Сб)алканоїл, ос-аміно(С1-С4)алканоїл, арилацил та αаміноацил, або α-аміноацил-а-аміноацил, де кожна сс-аміноацильна група незалежно вибрана з природних Lамінокислот, Р(О)(ОН)2, -Р(О)(О(Сі-Сб)алкіл)2 або глікозил (радикал, отриманий після видалення гідроксильної групи геміацетальної форми карбогідрату). Якщо сполука даного винаходу містить амінову функціональну групу, проліки можуть бути утворені заміною атому водню в аміновій групі на групу, таку як, R-карбоніл, RO-карбоніл, NRR'-карбоніл, де R та R' кожний незалежно означає (С1-С10)алкіл, (С3-С7)циклоалкіл, бензил, або R-карбоніл є природний α-аміноацил або природний а-аміноацил-природний α-аміноацил, -C(OH)C(O)OY', де Y’ означає Н, (С1-С6)іалкіл або бензил, -C(OY0)Y1, де Yo означає(С1-С4)алкіл, a Y1 означає (С1-С6)алкіл, карбокси(С1-С6)алкіл, аміно(С1-С4)алкіл або моно-N- або дi-N,N-(C1-C6)aлкiлaмiнoaлкiл, -C(Y2)Y3 , де Y2 означає Η або метил, a Y3 означає моно-N- або діІЧ,ІЧ-(Сі-С6)алкіламіно, морфоліно, піперидин-1-іл або піролідин-1-іл. Сполуки даного винаходу можуть мати асиметричні або хіральні центри і, таким чином, існувати в різних стереоізомерних формах. Це означає, що всі стереоізомерні форми сполук даного винаходу, також як їх суміші, включаючи рацемічні суміші, утворюють частину даного винаходу. Крім того, даний винахід охоплює усі геометричні та позиційні ізомери. Наприклад, якщо сполука даного винаходу має подвійний зв'язок або конденсоване кільце, в об'єм винаходу входять як цис-, так і транс-форми, а також їх суміші. В об'єм даного винаходу також входять як окремі позиційні ізомери, так і суміші позиційних ізомерів, які отримуються внаслідок N-оксидування піримідинового та піразинового кілець. Діастереомерні суміші можуть бути розділені на їх індивідуальні діастереоізомери на основі відмінностей в їх фізико-хімічних властивостях методами, добре відомими фахівцям, такими як, хроматографія та/або фракційна кристалізація. Енантіомери можуть бути розділені перетворенням енантіомерної суміші в діастереомерну суміш шляхом взаємодії з придатною оптично-активною сполукою (наприклад, хіральною допоміжною речовиною, такою як, хіральний спирт або хлорангідрид Mosher), розділенням діастереоізомерів та перетворенням (наприклад, гідролізом) індивідуальних діастереоізомерів у відповідні чисті енантіомери. Також деякі сполуки даного винаходу можуть бути атропізомерами (наприклад, заміщеними біарилами), і вони також розглядаються як частина цього винаходу. Енантіомери також можуть бути розділені з використанням хіральної HPLC колонки. Сполуки даного винаходу можуть існувати як в несольватованій, так і в сольватованій формі з фармацевтично прийнятними розчинниками, такими як, вода, етанол і т.п., і мається на увазі, що винахід охоплює як сольватовані, так і несольватовані форми. Можливо також, що сполуки даного винаходу можуть існувати в різних таутомерних формах, і усі такі форми входять в об'єм даного винаходу. Наприклад, винаходом охоплюються усі таутомерні форми імідазольного залишку. Також, наприклад, в об'єм даного винаходу входять усі кето-енольні та імін-енамінні форми сполук. Даний винахід також охоплює сполуки винаходу, мічені ізотопами, які є ідентичні сполукам, наведеним тут, лише за винятком того, що один або декілька атомів замінені - атомом, що має атомну масу або масовий номер, які відрізняється від атомної маси або масового номера, що зазвичай зустрічається у природі. Прикладами ізотопів, що можуть бути включені в сполуки винаходу, є ізотопи водню, вуглецю, азоту, кисню, фосфору, фтору та хлору, такі як, 2 Н, 3 Н, 13С, 14С, 15N, 180,170,31P, 32P, "S, 18F та 36СІ, відповідно. Певні сполуки даного винаходу, мічені ізотопами (наприклад, сполуки, мічені 3Н та 14С), є придатними для досліджень сполуки та/або аналізів тканинного розподілу субстрату. Особлива перевага надається ізотопам тритію (тобто, 3Н) та вуглецю-14 (тобто, 14С) в зв'язку з легкістю їх одержання та визначення. Крім того, заміщення більш важкими ізотопами, такими як, дейтерій (тобто, 2Н) може надавати певні терапевтичні переваги, що є результатом більшої метаболічної стабільності (наприклад, збільшений час напівжиття in vivo або зменшене необхідне дозування) і, таким чином, за певних обставин йому може надаватись перевага. Сполуки даного винаходу, мічені ізотопами, загалом можуть бути одержані з використанням методик, аналогічних тим, що описані на Схемах та/або в Прикладах нижче, заміною реагенту, не міченого ізотопом, на реагент, що мічений ізотопом. Сполуки даного винаходу є придатними як 5-НТ2 часткові агоністи або антагоністи (переважно 5-НТ2а або 5-НТ2с часткові агоністи або антагоністи); таким чином, іншим втіленням даного винаходу є фармацевтична композиція, яка містить терапевтично ефективну кількість сполуки даного винаходу та фармацевтично прийнятний екціпіент, розбавник або носій. Звичайні рецептури одержують змішуванням сполуки даного винаходу та носія, розбавника або екціпієнта. Придатні носії, розбавники та екціпієнти є добре відомими в даній галузі і включають такі речовини, як карбогідрати, воски, водорозчинні та/або здатні до набухання полімери, гідрофільні або гідрофобні речовини, желатин, масла, розчинники, воду та ін. Конкретний використовуваний носій, розбавник або екціпієнт буде залежати від методик та призначень, в яких використовують сполуку даного винаходу. Розчинники зазвичай вибирають, виходячи з розчинників, загальновизнаних фахівцями як безпечні (GRAS) для уведення ссавцю. Загалом, безпечними розчинниками є нетоксичні водні розчинники, такі як, вода та інші нетоксичні розчинники, що є розчинними у воді або змішуються з нею. Придатними розчинниками є вода, етанол, пропіленгліколь, поліетиленгліколі (наприклад, PEG400, PEG300) і т.д. та їх суміші. Рецептури також можуть містити один або більше буферів, стабілізаторів, поверхнево-активних речовин, змочувальних агентів, мастильних агентів, емульгаторів, суспендувальних агентів, консервантів, антиоксидантів, матувальних агентів, глідантів, технологічних добавок, барвників,смакових агентів, агентів, що надають запаху, та інших відомих добавок, що забезпечують відмінний вигляд лікарського засобу (тобто, сполуки даного винаходу або її фармацевтичної композиції) або допоміжні речовини для виробництва фармацевтичного продукту (тобто, медикаменту). Рецептури можуть бути одержані з використанням загальноприйнятих процесів розчинення або змішування. Наприклад, основну масу лікарської речовини (тобто, сполуки даного винаходу або стабілізованої форми сполуки (наприклад, комплексу з похідною циклодекстрину або іншими відомими агентами комплексоутворення)) розчиняють у придатному розчиннику в присутності одного або декількох екціпієнтів, описаних вище. Сполуку даного винаходу зазвичай уводять в фармацевтичні дозовані форми, щоб забезпечити легко контрольовану дозу лікарської речовини та запропонувати пацієнтові продукт відмінного вигляду та зручний у використанні. Фармацевтична композиція (або рецептура) може бути упакована для застосування різноманітними засобами в залежності від способу, що використовується для уведення лікарського засобу. Загалом виріб для розповсюдження включає контейнер, в якому розміщена фармацевтична композиція у відповідній формі. Придатні контейнери є добре відомими фахівцям і включають матеріали, такі як, пляшечки (пластикові та скляні), маленькі пакетики, ампули, пластикові пакети, металеві циліндри і т.ін. Контейнер може також включати засіб захисту від невмілого використання вмісту упаковки. Крім того, контейнер має розташовану в ньому бірку, яка описує вміст контейнеру. Бірка може також містити відповідні застереження. Даний винахід в подальшому стосується способів лікування захворювань, станів або розладів, опосередкованих 5-НТ2 рецепторами, у тварини, яка потребує такого лікування, які полягають в уведенні тварини терапевтично ефективної кількості сполуки даного винаходу або фармацевтичної композиції, яка містить ефективну кількість сполуки даного винаходу та фармацевтично прийнятний екціпієнт, розбавник або носій. Спосіб особливо є корисним для лікування захворювань, станів або розладів, опосередкованих 5-НТ2с рецепторами. Переважно сполуки даного винаходу діють як частковий агоніст на сайті 5-НТ2с рецептора. Більш переважно сполуки даного винаходу діють як частковий агоніст на сайті 5-НТ2с рецептора та як антагоніст на сайті 5-НТ2а рецептора. Переважно захворювання, стани або розлади, опосередковані 5-НТ2 рецепторами, вибрані з такої групи: втрата ваги (наприклад, зменшення споживання калорій), ожиріння, булімія, передменструальний синдром або синдром пізньої лютеальної фази, депресія, атипова депресія, біполярні розлади, психози, шизофренія, мігрень, алкоголізм, зловживання тютюнопалінням, панічні розлади, неспокій, пост-травматичний синдром, втрата пам'яті, вікова деменція, соціальна фобія, гіперактивний розлад дефіциту уваги, розлади поведінки, розлади контролювання потягу, граничні розлади особистості, обесивно-компульсивні розлади, синдром хронічної втомлюваності, сексуальна дисфункція у чоловіків (наприклад, передчасна еякуляція та недостатність ерекції"), сексуальна дисфункція у жінок, анорексія на нервовій основі, розлади сну (наприклад, зупинка дихання під час сну), аутизм, конвульсії, епілепсія, мутизм, травма спинного мозку, пошкодження центральної нервової системи (наприклад, травма, інсульт, нейродегенеративні хворобі або токсичні або інфекційні захворювання ЦНС (наприклад, енцефаліт або менінгіт)), серцево-судинні розлади (наприклад, тромбоз), шлунково-кишкові розлади (наприклад, дисфункція моторики шлунково-кишкового тракту), нецукровий діабет та діабет II типу. Таким чином, сполуки даного винаходу, описані тут, є придатними для лікування захворювань, станів або розладів, опосередкованих 5-НТ2 рецепторами. Відповідно, сполуки даного винаходу (у тому числі композиції та способи їх використання) можуть бути придатними для виробництва лікарського засобу для терапевтичного застосування , описаного тут. Сполуки даного винаходу можуть призначатися пацієнтові при рівнях дозувань в межах від приблизно 0.7мг до приблизно 7,000мг на день. Для нормальної дорослої людини, що має вагу тіла близько 70 кг, зазвичай достатнім є рівень дозувань від приблизно 0.01мг до приблизно 100мг на кілограм ваги тіла. Однак, може бути необхідною деяка варіабельність в загальному інтервалі дозувань в залежності від віку та ваги пацієнта, що підлягає лікуванню, призначеного шляху уведення, конкретної сполуки, яка повинна уводитися і т. ін. Визначення інтервалів та оптимальних дозувань для конкретного пацієнта знаходяться в межах компетенції фахівця. Також необхідно відзначити, що сполуки даного винаходу можуть використовуватися в рецептурах уповільненого вивільнення, контрольованого вивільнення та відстроченого вивільнення, форми яких добре відомі фахівцям даної галузі. Сполуки даного винаходу можуть також використовуватися у поєднанні з іншими фармацевтичними агентами для лікування захворювань/станів, що описані тут. Тому способи лікування, що включають уведення сполуки даного винаходу в комбінації з іншими фармацевтичними агентами також входять в об'єм винаходу. Придатні фармацевтичні агенти, що можуть використовуватися в комбінації зі сполуки даного винаходу, включають агенти проти ожиріння, такі як, інгібітори секреції аполіпопротеїну-В/протеїна мікросомального переносу тригліцериду (аро-В/МТР), MCR-4 агоністи, агоністи холецистокініну-А (ССК-А), інгібітори зворотного захвату моноаміну (такі, як сибутрамін), симпатоміметичні агенти, агоністи рз адренергічних рецепторів, агоністи допаміну (такі, як бромкриптин), аналоги меланоцит-стимулюючих гормонів, антагоністи канабіноїдних 1 рецепторів, антагоністи акумуляції гормону меланіну, лептини (ОВ протеїн), аналоги лептину, агоністи рецепторів лептину, антагоністи галаніну, інгібітори ліпази (такі, як тетрагідроліпстатин, тобто орлістат), аноректичні агенти (такі, як агоністи бомбезину), антагоністи Нейропептиду-Y, тіроміметичні агенти, дегідроепіандростерон або його аналог, агоністи або антагоністи глюкокортикоїдних рецепторів, антагоністи орексинових рецепторів, антагоністи урокортин-зв'язувального протеїну, агоністи рецепторів глюкагонподібного пептиду-1, циліарні нейротрофічні фактори (такі, як Axokine від Regeneron Pharmaceuticals, Inc., Tarrytown, NY та Procter & Gamble Company, Cincinnati, OH), людські асоційовані з агуті білки (AGRP), антагоністи gh-relin рецепторіві, антагоністи Н3 рецепторів або зворотні агоністи, агоністи нейромедин U рецепторів. Інші агенти проти ожиріння, у тому числі переважні агенти, що наводяться тут нижче, є добре відомими або будуть абсолютно очевидними для фахівця з огляду на даний опис. Особливо переважні агенти проти ожиріння вибрані з групи, яка складається з, сибутраміну, бромкриптину, ефедрину, лептину та псевдоефедрину. Сполуки даного винаходу та комбіноване лікування призначаються у поєднанні з фізичними вправами та розумною дієтою. Типові агенти проти ожиріння для використання в комбінаціях, фармацевтичних композиціях та способах винаходу можуть бути одержані з використанням методик, відомих фахівцям, наприклад, сибутрамін можна одержати, як описано в патенті US № 4,929,629; бромкриптин може бути одержаний так, як описано в патентах US № 3,752,814 та 3,752,888; а орлістат можна одержати, як описано в патентах US №№. 5,274,143; 5,420,305; 5,540,917; та 5,643,874. Усі вищезгадані патенти US наводяться тут як посилання. Доза додаткового фармацевтичного агенту (наприклад, агенту проти ожиріння) загалом буде також залежати від ряду факторів, у тому числі стану здоров'я суб'єкта, якого піддають лікуванню, степеню необхідного лікування, природи та виду супутньої терапії, якщо така проводиться, частоти лікування та характеру бажаного ефекту. Загалом інтервал дозувань агенту проти ожиріння лежить в межах від приблизно 0.001мг до приблизно 100мг на кілограм ваги тіла індивідуума на день, переважно від приблизно 0.1мг до приблизно 10мг на кілограм ваги тіла індивідуума на день. Однак, може також бути необхідною деяка варіабельність в загальному інтервалі дозувань в залежності від віку та ваги суб'єкта, якого піддають лікуванню, призначеного шляху уведення, конкретного агенту проти ожиріння, що призначається, і т. ін. Визначення інтервалу та оптимальних дозувань для конкретного пацієнта також знаходяться в межах компетенції фахівця. В іншому втіленні даного винаходу сполуки винаходу є придатними для лікування сексуальної дисфункції. Сексуальна дисфункція (SD) є значною клінічною проблемою, яка може впливати як на чоловіків, так і на жінок. В обох випадках причини SD можуть бути органічними, а також психологічними. Органічні аспекти SD зазвичай викликаються судинними захворюваннями, такими як захворювання, що пов'язані з гіпертензією або цукровим діабетом, призначеним медикаментозним лікуванням та/або психічними захворюваннями, такими як, депресія. Фізіологічні фактори включають страх, неспокій та міжособистий конфлікт. SD послаблює сексуальну поведінку, знижує самоповагу та руйнує особисті взаємовідносини, викликаючи, такимчином, особисті душевні страждання. В клінічному прояві SD розлади поділяються на сексуальні дисфункціональні розлади у жінок (FSD) та сексуальні дисфункціональні розлади у чоловіків (MSD) (Melman та ін,1999). FSD найкраще визначається як складність або нездатність жінки отримати задоволення при сексуальному контакті. Чоловіча сексуальна дисфункція (MSD) загалом пов'язана з еректильною дисфункцією, також відомою як чоловіча еректильна дисфункція (MED) (Benet та ін, 1994 - Male Erectile dysfunction assessment and treatment options. Сотр. Ther. 20: 669-673.). Сполуки винаходу є особливо корисними для профілактик та/або лікування сексуальної дисфункції у чоловіків (наприклад, чоловічої еректильної дисфункції - MED) та у жінок - жіночої сексуальної дисфункції (FSD), наприклад, розлад жіночого сексуального збудження (FSAD). Відомо, що деякі індивідууми можуть страждати від чоловічої еректильної дисфункції (MED). MED визначається як: "нездатність досягти та/або підтримувати ерекцію пенісу для одержання сексуального задоволення" (NIH Consensus Development Panel on Impotence, 1993)". Оцінюється, що еректильна дисфункція (ED) усіх ступенів (мінімальна, середня або повна імпотенція) складає 52% у чоловіків у віці від 40 до 70 років, із збільшенням цього показника у чоловіків, старших 70 (Melman, А. & Gingell, J. С. (1999). The epidemiology and pathophysiology of erectile dysfunction. J. Urology 161: 511). Стан має значний негативний вплив на якість життя пацієнта та його партнера, що часто проявляється у підвищеному неспокої та напруженні, що призводить до депресії та низької самоповаги. В той час як два десятиріччя тому вважалось, що MED, головним чином, є психологічним розладом (Benet, A. E. та ін, (1994), Male erectile dysfunction assessment and treatment options. Сотр. Ther. 20: 669-673), зараз відомо, що у більшості пацієнтів в основі лежить органічний фактор. Як результат, було досягнуто значного прогресу в ідентифікації механізму нормальної ерекції пенісу та патофізіології MED. Ерекція пенісу є гемодинамічним процесом, який залежить від контракції та релаксації гладкої мускулатури печеристих тіл та судинної системи пенісу (Lerner, S. Ε. та ін. (1993). A review of erectile dysfunction: new insights and more questions. J. Urology, 149: 1246-1255). Гладка мускулатура печеристих тіл також згадується тут як гладка мускулатура тіл або в широкому розумінні печеристе тіло. Релаксація гладкої мускулатури печеристих тіл призводить до посилення току крові до трабекулярних ділянок печеристих тіл, викликаючи збільшення їх розмірів по відношенню до навколишньої оболонки та стискання дренажних вен. Це викликає значне підвищення тиску крові, яке проявляється в ерекції (Naylor, A. M. (1998). Endogenous neurotransmitters mediating penile erection. Br. J. Urology. 81: 424-431). Зміни, що відбуваються в процесі ерекції, є складними і потребують високого ступеню координованої регуляції, включаючи периферичну та центральну нервову системи, та ендокринну систему (Naylor, 1998). Контракція гладкої мускулатури печеристих тіл регулюється симпатичною норадренергічною інервацією через активацію постсинаптичнихмкл адреноцепторів. MED може бути пов'язана з підвищенням тонусу ендогенної гладкої мускулатури печеристих тіл. Однак, процес релаксації гладкої • мускулатури тіл опосередкований частково неадренергічною, нехолінергічною (NANC) нейротрансмісією. Існують деякі інші NANC нейротрансмітери, виявлені в пенісі, відмінні від N0, такі як пептид, зв'язаний з геном кальцитоніну (CGRP) та вазоактивний інтестинальний пептид (VIP). Головним фактором релаксації, відповідальним за процес цієї релаксації, є оксид азоту (NO), який синтезується з L-аргініну NO-синтазою (NOS) (Taub, Η. С. та ін. (1993). Relationship between contraction and relaxation in human and rabbit corpus cavernosum. Urology 42: 698-704). Вважається, що зменшення тонусу гладкої мускулатури печеристих тіл може допомагати N0 викликати релаксацію печеристих тіл. В процесі сексуального збудження у чоловіка N0 вивільняється з нейронів та ендотелію та зв'язується та активує розчинну гуанілатциклазу (sGC), локалізовану в клітинах гладкої мускулатури та ендотелію, що призводить до підвищення рівнів інтрацелюлярного циклічного гуанозин 3',5'монофосфату (cGMP). Таке підвищення cGMP веде до релаксації печеристих тіл завдяки зменшенню міжклітинної концентрації кальцію ([Са2+]і), який, як вважається, за невідомим механізмом викликає активацію протеїнкінази G (можливо, внаслідок активації Са2+ помп та Са2+-активованих К+ каналів). На відміну від цього, категорії жіночої сексуальної дисфункції (FSD) найкраще визначаються за фазами нормальної сексуальної відповіді жінки: бажання, збудження та оргазм (див. S R Leiblum, (1998), Definition and Classification of Female Sexual Disorders, Int. J. Impotence Res., 10, S104-S106). Бажання або лібідо є пусковим механізмом для сексуального вираження. Його прояви часто включають сексуальні думки або в компанії партнера, яким жінка зацікавлена, або коли вона піддається впливу інших еротичних стимулів. Збудження включає судинну відповідь на сексуальну стимуляцію, важливим компонентом якої є прилив крові до геніталіїв та підвищення вагінального змащування, подовження вагіни та підвищення геніальних відчуттів/чуттєвості та суб'єктивна збуджувальна відповідь. Оргазм є зняття сексуального напруження, яке досягає своєї кульмінації в процесі збудження. Відповідно, FSD виникає, коли у жінки відсутня, неадекватна або незадовільна реакція в будь-якій одній або в декількох з цих фаз, зазвичай, в бажанні, збудженні або в оргазмі. Американська Асоціація Психіатрів класифікує жіночу сексуальну дисфункцію (FSD) на чотири класи: FSAD, гіпоактивне сексуальне бажання (HSDD), жіночі оргастичні розлади (FOD), та сексуальні болі (наприклад, диспареунія та вагінізм) [див. American Psychiatric Association's Diagnostic and Statistical Manual of Mental Disorders, 4Te видання (DSM-IV)]. DSM-IV визначає чотири наступних класи : HSDD - Персистентно або рекурентно недостатні (або відсутні) для сексуальної активності сексуальні фантазії та бажання. Оцінка дефіциту або відсутності проводиться лікарем, приймаючи до уваги фактори, що впливають на функціонування, такі як вік та обставини життя суб'єкту. FSAD - Персистентна або рекурентна нездатність досягати або підтримувати до завершення сексуальної активності адекватну відповідь на сексуальне збудження, яка проявляється у вагінальному змащуванні та набуханні. FOD - Персистентна або рекурентна затримка або відсутність оргазму, що йде за звичайною фазою сексуального збудження. Жінки проявляють велику різноманітність типів та інтесивності стимуляції, яка ініціює оргазм. Діагностування FOD повинно базуватись на клінічних висновках, що оргастична здатність жінки є меншою, ніж та, що повинна відповідати її віку, сексуальному досвіду та адекватності сексуальної стимуляції, яку вона отримує. Розлади, пов'язані з сексуальним болем, такі як, диспареунія та вагінізм. Диспареунія - рекурентний або персистентний вагінальний біль, пов'язаний із статевими відносинами. Вагінізм - рекурентний або персистентний мимовільний спазм мускулатури зовнішньої третини вагіни, що заважає статевим відносинам. HSDD спостерігається, якщо жінка не має або має незначне бажання бути сексуальною і не має або має недостатньо сексуальних думок та фантазій. Цей тип FSD може викликатися низькими рівнями тестостерону внаслідок або природної менопаузи або хірургічної менопаузи. Іншими причинами як у жінок у стані передменопаузи (тобто жінок, які знаходяться у фазі передменопаузи і які не піддавалися гістеректомії), так і у жінок у стані постменопаузи є захворювання, медикаментозне лікування, втома, депресія та/або неспокій. З наявністю/розвитком HSDD у жінок можуть бути пов'язані фактори, що мають потенційний (свідомий або підсвідомий) психологічний вплив, такі як, складності у взаємовідносинах або релігійні фактори. Діагностичний та статистичний довідник (DSM) IV Американської психіатричної асоціації визначає розлади жіночого сексуального збудження (FSAD) як:"... персистентну або рекурентну нездатність досягати або підтримувати до завершення сексуальної активності адекватну відповідь на сексуальне збудження, яка проявляється у вагінальному змащуванні та набуханні. Така патологія може викликати значні страждання або міжособисті складності....". Відповідь на збудження полягає в наповненні судин тазу, змащенні вагіни та збільшенні та набуханні зовнішніх геніталій. Неспокій викликає помітні страждання та/або міжособисті складності. FSAD є широко розповсюдженим сексуальним розладом, що вражає жінок у перед-, пері- та постменопаузі (гормон-заміщувальна терапія (HRT)). Вона супроводжується розладами, такими як депресія, серцево-судинні захворювання, діабети та урогенітальні (UG) розлади. Первинними наслідками FSAD є недостатність приливу крові/набухання, недостатність змащування та недостатність приємних генітальних відчуттів. Вторинними наслідками FSAD є зменшене сексуальне бажання, біль в процесі статевих відносин та складність в досягненні оргазму. Нещодавно було сформульовано гіпотезу про те, що принаймні для частини пацієнтів з симптомами FSAD • в основі лежить судинний фактор (Goldstein та ін.., Int. J. I moot. Res., 10, S84S90, 1998), з даними, що отримані на тваринах, які підтверджують цю точку зору (Park та ін.., Int. J. Impel. Res.. 9, 27-37,1997). Лікарські засоби для лікування FSAD, які досліджують на їх ефективність, є, головним чином, засобами лікування еректильної дисфункції, які підвищують циркуляцію в чоловічих геніталіях. Вони складаються з двох типів композицій, оральних та сублінгвальних лікарських засобів (апоморфіну, фентоламіну, інгібіторів фосфодіестерази типу 5 (PDE5), наприклад, сілденафілу), та простагладину (PGEi), яки вводяться ін'єкційно або трансуретально чоловікам та місцево в геніталії жінкам. Сполуки даного винаходу є корисними для одержання засобу для відновлення нормальної реакції на сексуальне збудження, головним чином, шляхом збільшення генітального кровотоку, що призводить до наповнення кров'ю вагіни, клітора та губ. Це буде проявлятися в посиленому змащуванні вагіни через транссудацію плазми, підвищеній піддатливості вагіни та підвищеній генітальній чуттєвості. Таким чином, даний винахід стосується засобів для відновлення або підсилення нормальної реакції на сексуальне збудження. Під жіночими геніталіями ми розуміємо: "Генітальні органи, які складаються із внутрішніх та зовнішніх груп. Внутрішні органи розташовані в тазу та складаються з яєчників, маткових труб, матки та вагіни. Зовнішні органи є поверхневими по відношенню до урогенітальної діафрагми і розташовані нижче тазового склепіння. Вони складаються з mons pubis, labia majora та minora pudendi, клітора, присінка, цибулина присінка і великі залози присінка" (Gray's Anatomy, С. D. Clemente, 13е американське видання). R. J. Levin вчить нас, що оскільки"... чоловічі та жіночі геніталії розвиваються ембріологічно із загальної тканини зародка, [це] свідчить про те, що чоловічі та жіночі генітальні структури повинні бути гомологами одна іншої. Таким чином, клітор є гомологом пенісу, а губи є гомологом мошонки. ..." (Levin, R. J. (1991), Exp. Clin. Endocrinol., 98,61-69). В короткому викладі, FSAD характеризується неадекватною генітальною реакцією на сексуальну стимуляцію. Геніталії не піддаються приливу крові, яким характеризується нормальне сексуальне збудження. Стінки вагіни недостатньо змащуються для того, щоб статеві відносини були безболісними. Оргазм може бути утрудненим. Розлади збудження можуть викликатися зменшенням кількості естрогену в менопаузі або після народження дитини та в процесі лактації, а також захворюваннями з судинними компонентами, такими як діабети та атеросклероз. Інші причини є наслідками лікування діуретинами, антигістамінами, антидепресантами, наприклад, селективними інгібіторами зворотного захоплення серотоніну (SSRI), або антигіпертензивними агентами. FOD є персистентною або рекурентною затрудненностью, затримкою в досягненні або відсутністю оргазму після достатньої сексуальної стимуляції та збудження, що викликає страждання. Розлади, пов'язані з сексуальним болем (включаючи диспареунію та вагінізм), характеризуються болем, який є результатом пенетрацї та сексуальної активності, і можуть викликатися лікуванням лікарськими засобами, яке зменшує змащування, ендометріозом, запальними захворюваннями внутрішніх тазових органів, запальними захворюваннями кишечника або проблемами сечового тракту. Згідно з подальшим аспектом даний винахід додатково охоплює спосіб лікування та/або профілактики чоловічої сексуальної дисфункції (MSD), зокрема, чоловічої еректильної дисфункції (MED), шлязом лікування з використанням сполук даного винаходу, що детально описані вище. Відповідно до подальшого аспекту даний винахід додатково охоплює спосіб лікування та/або профілактики чоловічої сексуальної дисфункції шляхом лікування комбінацією сполуки даного винаходу, що визначена вище, та однієї або декілької сполук, що інгібують активність PDE, зокрема, сполуки, яка інгібує активність cGMP PDE5, та/або однієї або декілької сполук, що інгібують активність NEP. Чоловіки, які проявляють недостатню реакцію або відсутність реакції на лікування за допомогою Viagra, можуть мати користь або з лікування за допомогою сполук даного винаходу самих по собі або з комбінаційної терапії, за снованій на застосуванні сполук(и) даного винаходу та cGMP PDE5i, таких як, наприклад, сілденафіл. Пацієнти, у яких спостерігається MED незначного та середнього ступеню повинні мати користь з комбінованого лікування з використанням сполук(и) даного винаходу самих по собі або в комбінації з NEPi, і пацієнти з важким ступенем MED можуть також піддаватися такому лікуванню. Незначний, середній та важкий ступінь MED є термінами, відомими фахівцям, але вказівки можуть бути знайдені в: The Journal of Urology, т. 151, 54-61 (Січень 1994). Групами MED, які більш детально описані в Clinical Andrology, т. 23, № 4, с. 773-782, та в главі 3 книги I. Eardley та К. Sethia "Erectile Dysfunction - Current Investigation and Management", опубл. Mosby-Wolfe, є наступні: психогенні, ендокринні, нейрогенні, артеріогенні, викликані ліками сексуальні дисфункції (лактогенні) та сексуальна дисфункція, пов'язана з кавернозними факторами, зокрема, в основі яких лежить патологія вен. Придатними cGMP PDE5 інгібіторами для використання в комбінації із сполукою даного винаходу для лікування MED згідно з даним винаходом є: піразоло[4,3-с!]піримідин-7-они, розкриті в ЕР-А-0463756; піразоло[4,3-с!]піримідин-7-они, описані в опублікованій міжнародній заявці WO 01/27112; піразоло[4,3 сІ]піримідин-7-они, розкриті в опублікованій міжнародній заявці WO 01/27113; індол-1,4-діони, розкриті в W095/19978 та триазин-4-они, описані в опублікованій міжнародній заявці W099/24433. Більша перевага надається сполукам, таким як, 5-[2-етокси-5-(4-метил-1-піперазинілсульфоніл)феніл]-1метил-3-н-пропіл-1,6-дигідро-7Н-піразоло[4,3-сІ]піримідин- 7-он (сілденафіл), також відомий як 1-[[3-(6,7дигідро1-метил-7-оксо-3-пропіл-1Н· піразоло[4,3-с!] піримідин-5-іл)-4етоксифеніл]сульфоніл]-4-метилпіперазин (див. ЕР-А-0463756); 5-[2-етокси-5-(4-етилпіперазин-1-ілсульфоніл)піридин-3-іл]-3-етил-2-[2-метоксиетил]-2,6-дигідро-7Нпіразоло[4,3-сі]піримідин-7-он, також відомий як 1-{6-етокси-5-[3-етил-6,7-дигідро-2-(2-метоксиетил)-7-оксо-2/7піразол[4,3-сІ]піримідин-5-іл]-3-піридилсульфоніл}-4-етилпіперазин (див. WO 01/27113, Приклад 8); 5-(5-ацетил-2-бутокси-3-піридиніл)-3-етил-2-(1-етил-3-азетидиніл)-2,6дигідро-7Н-піразоло[4,3-сІ]піримідин7-он (див. WO 01/27112, Приклад 132); (6R,12aR)-2,3,6,7,12,12а-гексагідро-2-метил-6-(3,4-метилендіоксифеніл)піразино[2',1',6,1]піридо[3,4d]індол1,4-діон (ІС-351, тадалафіл), тобто сполука прикладів 78 та 95 опублікованої міжнародної заявки WO95/19973, а також сполука прикладів 1, 3, 7 і 8; та 2-[2-етокси-5-(4-етилпіперазин-1-іл-1-сульфоніл)феніл]-5-метил-7-пропіл-ЗН-імідазо[5,1-Щ1,2,4]триазин-4он (варденафіл), також відомий як 1-[[3-(3,4-дигідро-5-метил-4-оксо-7-пропілімідазо[5,1-Ї]-аз-триазин-2-іл)4етоксифеніл]сульфоніл-4-етилпіперазин (тобто сполука прикладів 20, 19, 337 та 336 опублікованої міжнародної заявки W099/24433); та їх фармацевтично прийнятні солі. Згідно з подальшим аспектом даний винахід стосується композиції для лікування MED, яка містить сполуку даного винаходу та сілденафіл. Придатність будь-якого конкретного cGMP PDE5 інгібітора для використання в комбінації із сполукою даного винаходу може бути легко визначена шляхом оцінки його ефективності та селективності з використанням літературних методів та наступної оцінки його токсичності, абсорбції, метаболізму, фармакокінетики і т. ін. у відповідності із стандартною фармацевтичною практикою. Переважні cGMP PDE5 інгібітори для використання в рамках винаходу мають IC50 менше, ніж 100нМоль, більш переважно, менше, ніж 50нМоль, ще більш переважно менше, ніж 10нМоль. Переважні cGMP PDE5 інгібітори для використання у фармацевтичних композиціях згідно з даним винаходом діють селективно по відношенню до ферменту PDE5. Переважно вони мають селективність до PDE5 у порівнянні з PDE3 більшу, ніж 100, більш переважно, більшу ніж 300. Більш переважно PDE5 має селективність по відношенню як до PDE3, так і до PDE4 більшу, ніж 100, більш переважно, більшу ніж 300. Співвідношення селективності легко може бути визначено фахівцем. Значення ICso для ферментів PDE3 та PDE4 можуть бути визначені з використанням загальновизнаної в літературі методології, див. S A Ballard та ін., Journal of Urology. 1998, т. 159, с. 2164-2171. В рамках винаходу перевага надається NEP інгібіторам, де згаданим NEP є EC 3.4.24.11, і більш переважно де згаданий NEP інгібітор є селективним інгібітором EC 3.4.24.11, більш переважно селективний NEP інгібітор є селективним інгібітором EC 3.4.24.11, який має ICso меншу, ніж 100нМ (наприклад, омпатрилат, кандоксантрил, кандоксатрилат, сампатрилат). Придатні NEP інгібіторні сполуки описані в ЕР-А-1097719. Зокрема, переважними NEP інгібіторними сполуками, що є допоміжними агентами, для використання при лікуванні MED зідно з даним винаходом є сполуки, описані в міжнародній патентній заявці РСТ/ІВ02/00807, поданій 18 березня 2002, що знаходіться на одночасному розгляді. Особлива перевага надається (8)-2-[(1-{[3-(4-хлорфеніл)пропіл]карбамоїл}-циклопентил)метил]-4метоксибутановій кислоті або її фармацевтично прийнятній солі, що детально описана в Прикладі 22 в РСТ/ІВ02/00807. Деталі синтезу цієї сполуки та її натрієвої солі описані в експериментальній частині нижче. Згідно з подальшим аспектом даний винахід стосується композиції для лікування MED, яка містить сполуку даного винаходу та (8)-2-[(1-{[3-(4-хлорфеніл)пропіл]карбамоїл}циклопентил)метил]-4-метоксибутанову кислоту. Згідно ще з одним подальшим аспектом даного винаходу забезпечується використання сполуки даного винаходу для лікування жіночої сексуальної дисфункції (FSD). Відповідно до іншого аспекту даного винаходу забезпечується використання сполуки даного винаходу та одного або декількох додаткових активних агентів для лікування жіночої сексуальної дисфункції (FSD). Переважно один або декілька додаткових активних агентів вибрані з групи, до складу якої входять: 1) модулятори рецепторів естрогену та/або агоністи естрогену та/або антагоністи естрогену; 2) тестостерон-заміщувальний агент та/або тестостернон (Tostrelle) та/або дигідротестостерон та/або дегідроепіандростерон (DHEA) та/або тестостероновий імплантант; 3) естроген, естроген та медроксипрогестерон або медроксипрогестерону ацетат (МРА) (у вигляді комбінації), або естроген та метилтестостероновий агент гормонзаміщувальної терапії; 4) один або декілька допамінергічних агентів; 5) один або декілька інгібіторів NPY (нейропептиду Y); 6) один або декілька агоністів меланокортинових рецепторів або модуляторів або підсилювачів меланокортину; 7) один або декілька інгібіторів NEP (нейтральної ендопептидази); 8) один або декілька інгібіторів PDE (фосфодіестерази); та 9) один або декілька антагоністів або модуляторів рецепторів бомбезину. Переважно згаданим FSD є розлад жіночого сексуального збудження (FSAD). Альтернативно, згаданим FSD є жіночий оргазмічний розлад (FOD). В подальшій альтернативі, згаданим FSD є гіпоактивне сексуальне бажання (HSDD). Ще в одній подальшій альтернативі згаданим FSD є сексуальний біль, переважно диспареунія або вагінізм. Приклади модуляторів рецепторів естрогену та/або агоністів естроген та/або антагоністів естрогену, включають ралоксифен або лазофоксифен, (-)-цис-6-феніл-5-[4-(2-піролідин-1-ілетокси)феніл]-5,6,7,8тетрагідронафталін-2-ол та його фармацевтично прийнятні солі (сполука (а), наведена нижче), одержання яких детально описано в WO 96/21656. Прикладом тестостерон-заміщувального агенту є дегідроандростендіон. Приклади агентів гормон-заміщувальної терапії включають премарин, ценестин, естрофемінал, еквін, естрасе, естрофем, еллесте соло, естрінг, естрадерм ТТС, естрадерм матрикс, дерместрил, премфазе, прімпро, премпак, премік, естратест, естратест НС та тіболон. Приклади допамінергічних агентів включають апоморфін або селективний D2, D3 або D2/D3 агоніст, такий як, праміпексол та ропіринол (як заявлено у WO-0023056), L-Допа або карбідопа, PNU95666 (як описано в WO0040226). Прикладами інгібіторів NPY (нейропептиду Y) є інгібітори NPY1 або NPY5, переважно інгібітор NPY1. Переважно, згадані інгібітори NPY (включаючи NPY Y1 та NPY Y5) мають ІС50 менше, ніж 100нМ, більш переважно, менше, ніж 50нМ. Придатні сполукі, що є інгібіторами NPY, і зокрема NPY1, описані в ЕР-А1097718. Приклади агоністів або модуляторів або підсилювачів меланокортинових рецепторів включають меланотан II, РТ-14, РТ-141 або сполуки, описані в WO-09964002, WO-00074679, WO-09955679, WO00105401, WO-00058361, WO-00114879, WO-00113112 або WO-09954358. Придатними NEP інгібіторами є речовини, описані тут, вище. Згідно з подальшим аспектом, даний винахід стосується композиції для лікування FSD, яка містить сполуку даного винаходу та (8)-2-[(1-{[3-(4-хлорфеніл)пропіл]карбамоїл}-циклопентил)метил]-4метоксибутанову кислоту. Переважні інгібітори PDE включають інгібітори PDE 2, 3, 4, 5, 7 або 8, переважно інгібітори PDE2 або PDE5 і, більш переважно, інгібітор PDE5 (як описано тут, вище), найбільш перевага надається сілденафілу. Згідно з подальшим аспектом, даний винахід стосується композиції для лікування FSD, яка містить сполуку даного винаходу та сілденафіл. Переважними прикладами антагоністів або модуляторів одного або декількох бомбезинових рецепторів повинні бути антагоністи або модулятори ВВ1, включаючи ті, що описані в заявці PCT/GB01/05018 (поданій 14 листопада 2001) та заявці PCT/GBOO/04380 (поданій 17 листопада 2000). Також переважними є антагоністи бомбезинових ВВ2, ВВЗ або ВВ4 рецепторів. Переважні антагоністи бомбезинових рецепторів також згадуються як "допоміжні агенти" в заявці РСТ/ІВ01/02399 (поданій 10 грудня 2001). Необхідно відзначити, що повний перелік можливих "додаткових активних агентів" можна знайти в заявці РСТ/ІВ01/02399 (поданій 10 грудня 2001) і вони описані там, як "допоміжні агенти". У відповідності ще з одним аспектом даного винаходу, на додаток до сполуки даного винаходу можуть використовуватися інші агоністи 5-НТ2с рецепторів. Такі агоністи 5-НТ2с рецепторів включають, але не обмежуються ними, речовини, що описані в Chaki та Nakazato - Expert Орт. Ther. Patents (2001), 11(11): 16771692 (див. особливо розділ 3.9 -5НТ2с на стор.1687 та фіг.7 на стор.1686), або Isaac - Drugs of the Future (2001), 26(4): 383-393 (див. особливо фіг.2 на стор.385). Для уникнення сумнівів вищезгадані публікації включені тут як посилання. Переважно, згаданими агоністами 5-НТ2с рецепторів є селективні агоністи 5-НТ2с рецепторів. Дані по зв'язуванню рецепторів або дані по селективності зв'язування можуть не завжди корелювати або відображати функціональні дані або дані з функціональної селективності. Наприклад, сполука може бути агоністом 5-НТ2с рецептора, коли аналізується проба на зв'язування, але функціонально сполука може мати однакову ефективність по відношенню до інших 5-НТ рецепторів. Таким чином, термін "селективний" в контексті цього винаходу відносно способів лікування сексуальної дисфункції означає "функціонально селективний". Таким чином, відповідно до іншого аспекту, даний винахід додатково передбачує використання агоністів 5НТ2с рецепторів, переважно, селективних агоністів 5-НТ2с рецепторів, для лікування FSD, переважно, FSAD, FOD, HSDD або розладу сексуального - болю (таких як диспареунія або вагінізм). Відповідно до способів винаходу, сполуку даного винаходу або комбінацію сполуки даного винаходу та принаймні одного додаткового фармацевтичного агенту уводять суб'єкту, який потребує такого лікування, переважно у формі фармацевтичної композиції. В одному з варіантних аспектів винаходу, сполука даного винаходу та принаймні один інший фармацевтичний агент (наприклад, агент проти ожиріння, описаний вище) можуть уводитися або окремо, або у вигляді фармацевтичної композиції, яка містить обидві речовини. Загалом перевага надається оральному уведенню. Однак, якщо суб'єкт, якого лікують, не здатний ковтати, або оральне уведення в іншому відношенні є послабленим або небажаним, прийнятним може бути парентеральне або трансдермальне уведення. Відповідно до способів винаходу, коли комбінація сполуки даного винаходу та принаймні одного іншого фармацевтичного агенту уводиться разом, таке уведення може бути послідовним у часі або одночасним, загалом перевага надається одночасному способу уведення. При послідовному уведенні сполука даного винаходу та додатковий фармацевтичний агент можуть уводитися в будь-якій послідовності. Загалом перевага надається оральному уведенню. Особливо переважним є, коли таке уведення є оральним та одночасним. Коли сполука даного винаходу та додатковий фармацевтичний агент уводяться послідовно, уведення кожного може проводитися однаковим або різними способами. Відповідно до способів винаходу, сполука даного винаходу або комбінація сполуки даного винаходу та принаймні одного додаткового фармацевтичнийого агенту (згадуваної тут як "комбінація") переважно уводяться у формі фармацевтичної композиції. Відповідно, сполуку даного винаходу або комбінацію можна уводити пацієнту окремо або разом в будь-якій загальноприйнятій оральній, ректальній, трансдермальній, парентеральній (наприклад, внутрішньовенній, внутрішньом'язовій або підшкірній), інтрацистенальній, інтравагінальній, інтраперитоніальній, інтравезикулярній, локальній (наприклад, у вигляді порошку, мазі або крапель), або буккальній, або назальній дозованих формах. Композиції, придатні для парентеральних ін'єкцій, загалом включають фармацевтично прийнятні стерильні водні або неводні розчини, дисперсії, суспензії або емульсії та стерильні порошки для перетворення в стерильні розчини або дисперсії, придатні для ін'єкції. Приклади придатних водних та неводних носіїв, розбавників, розчинників або зв'язувальних речовин включають воду, етанол, поліоли (пропіленгліколь, поліетиленгліколь, гліцерин і т.ін.), придатні суміші їх, рослинні олії (такі як оливова олія) та придатні до ін'єкцій естери, такі як, етилолеат. Відповідний рідкий стан можна підтримувати, наприклад, шляхом використання покрить, таких як, лецитин, шляхом підтримання необхідного розміру частинок у випадку дисперсій та шляхом використання поверхнево-активних речовині. Ці композиції можуть також містити адьюванти, такі як, консерванти, змочувальні агенти, емульгатори та диспергатори. Попередження інфікування композицій мікроорганізмами може здійснюватися за допомогою різних антибактеріальних та антигрибкових агентів, наприклад, парабенів, хлорбутанолу, фенолу, сорбінової кислоти і т.ін. Також може бути бажаним уведення до складу композицій ізотонічних агентів, наприклад, цукрів, хлориду натрію і т.ін. Пролонгована абсорбція фармацевтичних композицій, призначених для ін'єкцій, може бути забезпечена шляхом використання агентів, здатних затримувати абсорбцію, наприклад, моностеарату алюмінію та желатину. Тверді дозовані форми для орального уведення включають капсули, таблетки, порошки та гранули. В таких твердих дозованих формах сполуку даного винаходу або комбінацію змішують принаймні з одним інертним звичайним фармацевтичним екціпієнтом (або носієм), таким як, цитрат натрію або гідрофосфат кальцію або (а) наповнювачами або розбавниками (наприклад, крохмалем, лактозою, сахарозою, маннітом, кремнієвою кислотою і т. ін.); (Ь) зв'язувальними речовинами (наприклад, карбоксиметилцелюлозою, альгінатами, желатином, полівінілпіролідоном, сахарозою, гуміарабіком і т. ін.); (с) зволожувачами (наприклад, гліцерином і т. ін.); (d) дезінтегрантами (наприклад, агар-агаром, карбонатом кальцію, картопляним або тапіоковим крохмалем, альгіновою кислотою, певними комплексними силікатами, карбонат натрію і т. ін.); (є) уповільнювачами розчинення (наприклад, парафіном і т. ін.); (f) прискорювачами абсорбції (наприклад, сполуками четвертинного амонію і т. ін.); (д) змочувальними агентами (наприклад, цетиловим спиртом, моностеаратом гліцерину і т. ін.); (h) адсорбентами (наприклад, каоліном, бентонітом і т. ін.); та/або (і) лубрикантами (наприклад, тальком, стеаратом кальцію, стеаратом магнію, твердими поліетиленгліколями, лаурилсульфатом натрію і т. ін.). У випадку капсул і таблеток дозовані форми можуть також містити буферні агенти. Тверді композиції подібного типу можуть також використовуватися як наповнювачі в м'яких та твердих желатинових капсулах, з використанням таких екціпієнтів, як лактоза або молочний цукор, а також високомолекулярні поліетиленгліколі і т. ін. Тверді дозовані форми, такі як, таблетки, драже, капсули та гранули можуть бути одержані з покриттями та оболонками, такими як, кишкові покриття та інші, добре відомі в галузі. Вони можуть також містити матувальні агенти, а також можуть бути такими композиціями, що вивільняють сполуку даного винаходу та/або додатковий фармацевтичний агент в уповільнений спосіб. Прикладами речовин, що можуть використовуватися для одержання лікарських форму уповільненого вивільнення, є полімерні речовини та воски. Лікарська речовина, якщо це доцільно, також може бути в мікроінкапсульованій формі з одним або декількома вищезгаданими екціпієнтами. Рідкі дозовані форми для орального уведення включають фармацевтично прийнятні емульсії, розчини, суспензії, сиропи та еліксири. Крім сполуки даного винаходу або комбінації рідка дозована форма може містити інертні розбавники, зазвичай використовувані в даній галузі, такі як, вода або інші розчинники, солюбілізувальні агенти та емульгатори, такі як, наприклад, етиловий спирт, ізопропіловий спирт, етилкарбонат, етилацетат, бензиловий спирт, бензилбензоат, пропіленгліколь, 1,3-бутиленгліколь, диметилформамід, масла (наприклад, бавовняне масло, арахісове масло, масло зародків зернових, оливове масло, касторове масло, масло з насіння кунжута і т. ін.), гліцерин, фурфуриловий спирт, поліетиленгліколі та сорбітанові естери жирних кислот або суміші цих речовин і т. ін. Крім таких інертних розбавників композиція може також містити ад'юванти, такі як, змочувальні агенти, емульгатори та суспендувальні агенти, підсоложувальні речовини,смакові агенти та агенти для надання запаху. Суспензії, крім сполуки даного винаходу або комбінації, можуть в подальшому містити суспендувальні агенти, наприклад, етоксильовані ізостеарилові спирти, поліоксиетиленові естери сорбіту та сорбітанумікрокристалічна целюлоза, метагідроксид алюмінію, бентоніт, агар-агар та трагакант, або суміші цих речовин і т. ін. Композиції для ректального або вагінального уведення переважно містять супозиторії, які можуть бути одержані змішуванням сполуки даного винаходу або комбінації з придатними екціпієнтами або носіями, що не викликають подразнення, такими як, масло какао, поліетиленгліколь або супозиторійний віск, які є твердими при звичайній кімнатній температурі, але рідкими при температурі тіла і, таким чином, розплавляються в ректальній або вагінальній порожнині, вивільняючи тим самим активний(і) компоненти). Дозовані форми для місцевого уведення сполук даного винаходу та комбінацій сполук даного винаходу з агентами проти ожиріння можуть являти собою мазі, порошки, спреї та засоби для інгаляції. Лікарські речовини змішують в стерильних умовах з фармацевтично прийнятним носієм та будь-якими консервантами, буферами або пропелентами, що можуть бути необхідними. Офтальмічні композиції, очні мазі, порошки та розчини призначені також для включення в об'єм даного винаходу. Наступні абзаци описують приклади композицій, дозованих форм і т.д., що є придатними для тварин, відмінних від людини. Уведення сполук даного винаходу та комбінацій сполук даного винаходу з агентами проти ожиріння може здійснюватися орально та неорально (наприклад, шляхом ін'єкцій). Сполука даного винаходу або комбінація сполуки даного винаходу з агентом проти ожиріння уводиться в такій кількості, що досягається ефективна доза. Загалом, денна доза, що уводиться орально тваринам, складає між приблизно 0.01 та приблизно 1,000мг/кг ваги тіла, переважно між приблизно 0.01 та приблизно 300мг/кг ваги тіла. Зручним є, коли сполука даного винаходу (або комбінація) може бути уведена з питною водою, таким чином, що терапевтична доза сполуки уводиться з денним запасом води. Сполука може бути безпосередньо відміряна у питну воду, переважно у формі • рідкого, водорозчинного концентрату (такого як, водний розчин водорозчинної солі). Зручним є, коли сполука даного винаходу (або комбінація) може бути додана безпосередньо до їжі, як такої, або у формі добавки до їжі тварин, також згадуваної як премікс або концентрат. Премікс або концентрат сполуки в носії у більшості випадків застосовують для включення агенту в їжу. Придатними носіями є рідини і тверді речовини, при необхідності, такі як, вода, різні види муки, такі як, мука люцерни, соєва мука, харчова олія насіння бавовника, харчова олія насіння льону, кукурудзяна мука та мука із зернових, меласа, сечовина, кісткова мука та мінеральні суміші, такі як, зазвичай застосовують для годівлі домашньої птиці. Особливо ефективним носієм є відповідна їжа тварин сама по собі; тобто, невелика порція такої їжі. Носій сприяє однорідному розподіленню сполуки в готовій до вживання їжі, з якою змішують премікс. Переважно сполуку ретельно змішують з преміксом, а потім з їжею. Для цього сполука може бути диспергована або розчинена в придатному масляному носієві, такому як соєве масло, кукурудзяне масло, бавовняне масло і т. ін., або в леткому органічному розчиннику і потім змішана з носієм. Цілком зрозуміло, що допускається значне коливання співвідношення сполуки в концентраті, оскільки кількість сполуки в кінцевій їжі може регулюватись змішуванням відповідної кількості преміксу з їжею до одержання необхідного рівня сполуки. Концентрати з високою ефективністю можуть бути змішані виробниками їжі з білковими носіями, такими як, соєва харчова олія, та іншими видами муки, які описані вище, з одержанням концентрованих добавок, які є придатними для безпосереднього згодовування тваринам. В такому випадку тваринам надається можливість дотримуватися звичайного режиму харчування. Альтернативно, такі концентровані добавки можуть додаватись безпосередньо до їжі з одержанням збалансованої кінцевої їжі, яка містить терапевтично ефективний рівень сполуки даного винаходу. Суміші ретельно змішують з використанням стандартних процедур, таких як, змішування в двошнековому блендері для забезпечення гомогенності. Якщо добавка використовується як домішка для їжі, вона також допомагає забезпечити однорідність розподілу сполуки у всьому об'ємі харчового продукту. Питну воду та їжу, що є ефективними для підвищення утворення пісного м'яса та покращення співвідношення пісного м'яса до жиру, загалом готують змішуванням сполуки даного винаходу з достатньою кількістю тваринної їжі, щоб забезпечити вміст сполуки в їжі або воді від 10-3 до приблизно 500ррт . Переважно лікарська їжа для свиней, великої рогатої худоби, овець та кіз загалом містить від приблизно 1 до приблизно 400 грамів сполуки даного винаходу (або комбінації) на тону їжі, оптимальні кількість для цих тварин зазвичай складає від приблизно 50 до приблизно 300 грамів на тону їжі. Переважно їжа для птиці та домашніх тварин зазвичай містить від приблизно 1 до приблизно 400 грамів, переважно від приблизно 10 до приблизно 400 грамів сполуки даного винаходу (або комбінації) на тону їжі. Для парентерального уведення тваринам сполуки даного винаходу (або їх комбінація) можуть бути одержані у формі мазі або пілюль і можуть бути уведені у вигляді імплантату, зазвичай під шкіру голови або вуха тварини, в якої намагаються досягти підвищення утворення пісного м'яса та покращення співвідношення пісного м'яса до жиру. Загалом, парентеральне уведення полягає в ін'єкції достатньої кількості сполуки даного винаходу (або комбінації) для забезпечення тварині від приблизно 0.01 до приблизно 20мг/кг/день лікарського засобу на вагу тіла. Переважна доза для домашньої птиці, свиней, великої рогатої худоби, овець, кіз та домашніх тварин лежить в інтервалі від приблизно 0.05 до приблизно 10мг/кг/день лікарського засобу на вагу тіла. Композиції мазей можуть бути одержані диспергуванням лікарської речовини у фармацевтично прийнятному маслі, такому як, арахісове масло, кунжутне масло, кукурудзяне масло і т. ін. Пілюлі, що містять ефективну кількість сполуки даного винаходу, фармацевтична композиція або комбінація можуть бути одержані змішуванням сполуки даного винаходу або комбінації з розбавником, таким як, вуглеводневий віск, карнаубський віск і т. п., для покращення процесу виробництва пілюль може додаватися лубрикант, такий як, стеарат магію або кальцію. Цілком зрозуміло, що для досягнення необхідного рівня дозування, що забезпечує підвищення утворення пісного м'яса та покращення бажаного співвідношення пісного м'яса до жиру, тварині може уводитися більше, ніж одна пілюля. Крім того, імплантування також може здійснюватися періодично в процесі лікування тварини для того, щоб підтримувати необхідний рівень лікарської речовини у тілі тварини Даний винахід має декілька корисних можливостей для ветеринарії. Для власників домашніх тварин або ветеринарів, які бажають покращити стрункість та/або прибрати небажаний жир у домашніх тварин, даний винахід забезпечує засоби, за допомогою яких це може бути здійснено. Для власників домашньої птиці та свиней використання способу даного винаходу дозволяє вирощувати тварин, що дають пісне м'ясо, висока продажна ціна на яке диктується м'ясною промисловістю. Реалізація даного винаходу ілюструється наступними Прикладами. Однак, зрозуміло, що втілення винаходу не обмежується конкретними деталями цих Прикладів, оскільки фахівцю будуть відомі або зрозумілі інші їх варіанти з огляду на цей опис. ПРИКЛАДИ Якщо не зазначено інакше, вихідні речовини загалом є наявними у продажу від таких виробників, як Aldrich Chemicals Co. (Milwaukee, Wl), Lancaster Synthesis, Inc. (Windham, NH), Acros Organics (Fairlawn, NJ), Maybridge Chemical Company, Ltd. (Cornwall, England), Tyger Scientific (Princeton, NJ), та AstraZeneca Pharmaceuticals (London, England). Загальні експериментальні методики Спектри ЯМР реєстрували за допомогою Varian Unity™ 400 (від Varian Inc., Palo Alto, CA) при кімнатній температурі з частотою 400мгц для протона. Хімічні зсуви виражали в частинах на мільйон (δ) відносно залишкового розчинника як внутрішнього стандарту. Форми піків зазначали як наступні: с, синглет; д, дублет; т, триплет; к, квартет; м, мультиплет; шс, широкий синглет; 2с, два синглети. Мас-спектри хімічної іонізації при атмосферному тиску (АРСІ) одержували на спектрометрі Fisons™ Platform II (газ-носій : ацетонітрил : від Micromass Ltd, Мапспестер, UK). Мас-спектри хімічної іонізації (СІ) одержували на приладі Hewlett-Packard 5989 (іонізація аміаку, PBMS: від Hewlett-Packard Company, Palo Alto, CA). Мас-спектри іонізації електророзпилюванням (ES) одержували на приладі Waters™ ZMD (газ-носій : ацетонітрил : від Waters Corp., Milord, ΜΑ). Β тих випадках, коли описується інтенсивність хлор- або бром-містких іонів, спостерігали очікуване співвідношення інтенсивності (приблизно 3: 1 для 35СІ/37СІ-містких іонів та 1: 1 для 79Вг/81Вг-містких іонів) і наводиться інтенсивність лише іонів нижчої маси. В деяких випадках наводяться лише характерні 1Н ЯМР піки. Піки МС наводяться для всіх прикладів. Оптичні обертання визначали на поляриметрі PerkinElmerTM 241 (від PerkinElmer Inc., Wellesley, MA), використовуючи натрієву D лінію (λ = 589нМ) при вказаній температурі та розчиннику і наводяться як наступні [a]Dtemp, концентрація (с = гі/100мл). Колонкову хроматографію здійснювали, використовуючи або силікагель Baker™ (400мкм; J. Т. Baker, Phillipsburg, NJ) або силікагель 50 (EM Sciences, Gibbstown, NJ), в скляних колонках або у Flash 40 Biotage колонках (ISC, Inc., Shelton, CT) в атмосфері азоту при зниженому тиску. Приклад 1 Одержання проміжної сполуки тоет-бутилового естеру 4-(2-хлорпіримідин-4-іл)піперазин-1 -карбонової кислоти {1 -1а): До розчину 2,4-дихлорпіримідину (3.00 г, 20.1ммоль) в 100мл етанолу додавали порошкоподібний карбонат натрію (2.1 г, 20.1ммоль) та тре/л-бутиловий естер піперазин-1-карбонової кислоти (3.75 г, 20.1ммоль). Реакційну суміш нагрівали до кипіння протягом 5 годин, потім охолоджували до кімнатної температури і концентрували у вакуумі. Залишок переносили в 400мл етилацетату та екстрагували водою (100мл) та насиченим розчином солі (100мл). Потім органічну фазу висушували над сульфатом натрію, фільтрували та концентрували у вакуумі до одержання прозорого масла. Флеш-колонковою хроматографією (силікагель, градієнтне елюювання від 10% етилацетат-гексан до 50% етилацетат-гексан) одержували 4.63 г вказаної у заголовку сполуки (1-1 а). 1 Н ЯМР (400мгц, CDCI 3) δ 8.06 (д, 1 Η); 6.39 (д, 1 Η); 3.65-3. 50 (м, 8Н); 1.46 (с, 9Н). МС (ES+) Розраховано : 298, Отримано: 299.1 (М+1). Одержання проміжної сполуки тоет-бутилового естеру 4-[2-{3.5-дифторбензилокси)-піримідин-4іл]піперазин-1-карбонової кислоти (1-1 b): 3,5-Дифторбензиловий спирт (227.5мкл, 2.01ммоль) розчиняли в 15мл безводного тетрагідрофурану і обробляли гідридом натрію (80.3мг, 60% дисперсія в мінеральному маслі, 2.01ммоль). Суміш перемішували в атмосфері азоту протягом 15 хвилин при температурі навколишнього середовища, потім реакційну суміш обробляли mpe/77-бутиловим естером 4-(2-хлорпіримідин-4-іл)піперазин-1-карбонової кислоти (1-1 а) (500мг, 1.67ммоль) в одній порції. Одержану суміш кип'ятили в атмосфері азот протягом 4 годин. Після охолодження до кімнатної температури реакційну суміш виливали у воду (50мл) та екстрагували етилацетатом (2x 50мл). Об'єднані органічні екстракти : промивали насиченим розчином солі (20мл), потім висушували над сульфатом натрію, фільтрували та концентрували. Залишок очищали колонковою хроматографією (силікагель, 1 :1 етилацетат : гексан) з одержанням 605.2мг вказаного у заголовку продукту (1-1b). 1 Н ЯМР (400мгц, CDCI 3) δ 8.04 (д, 1 Η); 6.96 (д, 2Н); 6.72 (τ, 1 Η); 6.20 (д, 1 Η); 5.33 (с, 2Н); 3.63 (шс, 4Н); 3.50 (м, 4Н); 1.47 (с, 9Н). МС (ES+) Розраховано : 406.4, Отримано: 407.3 (М+1). Одержання 2-(3.5-диФторбензилокси)-4-піперазин-1-ілпіримідину (1 -А): До розчину трет-бутилового естеру 4-[2-(3,5-дифторбензилокси)піримідин-4-іл]піперазин-1 -карбонової кислоті (1-1 b) (605.2мг, 1.49ммоль) в 5мл дихлорметану додавали трифтороцтову кислоту (1.72мл, 22.33ммоль) і суміш перемішували протягом З годин при температурі навколишнього середовища. Реакційну суміш концентрували у вакуумі, і залишок розчиняли в 1М НСІ (водн.) (70мл). Продукт екстрагували етилацетатом (40мл), шари відокремлювали, і рН водного шару доводили до приблизно 12, використовуючи 5М КОН (водн.). Цю водну суміш екстрагували дихлорметаном (2 x 100мл) і об'єднані органічні екстракти висушували над сульфатом натрію та концентрували з одержанням 414.3мг прозорого безбарвного масла, яке, як було визначено, було сполукою, вказаною у заголовку (1-А). 1 Н ЯМР (400мгц, CD3OD) δ 7.94 (д, 1 Η); 7.02 (дд, 2Н); 6.84 (дт, 1 Н); 6.37 (д, 1 Н); 5.34 (с, 2Н); 3.62 (шс, 4Н); 2.81 (м, 4Н). МС (АРСҐ) Розраховано : 306.3, Отримано : 307.3 (М+1). Одержання гідоохлооиду 2-(3,5-диФторбензилокси)-4-піперазин-1-ілпіримідину (1-В): 2-(3,5-Дифторбензилокси)-4-піперазин-1-ілпіримідин (1-А) (27.5мг, 0.09ммоль) розчиняли в 1мл дихлорметану та обробляли 1М розчином гідрохлориду в етері (89.8мкл, 0.09ммоль) і струшували протягом однієї хвилини. Реакційну суміш потім концентрували у потоці азоту з одержанням 30.8мг вказаної у заголовку сполуки у вигляді твердої речовини жовтого кольору (1-В). 1 Н ЯМР (400мгц, CD3OD) δ 8.09 (д, 1 Η); 7.05 (дд, 2Н); 6.88 (дт, 1 Н); 6.54 (д, 1 Н); 5.39 (с, 2Н); 3.93 (м, 4Н); 3.28 (м, 4Н). МС (АРСГ) Розраховано : 306.3, Отримано : 307.1 (М+1). Одержання фумарату (3,5-диФторбензилокси)-4-піперазин-1-ілпіримідину (1-С): 2-(3,5-Дифторбензилокси)-4-піперазин-1-ілпіримідин (1-А) (414.3мг, 1.35ммоль) розчиняли в 10мл суміші 10 : 1 метанол : ізопропіловий етер і обробляли 0.5 Μ розчином фумарової кислоти в метанолі (2.70мл, 1.35ммоль) та перемішували протягом 1 години. Одержану суспензію розбавляли 35мл ізопропілового етеру та перемішували протягом 10 хвилин. Фільтрацією та наступним висушуванням на повітрі одержували 549.4мг вказаної у заголовку сполуки (1-С). 1 Н ЯМР (400мгц, CD3OD) δ 8.06 (д, 1 Η); 7.03 (дд, 2Н); 6.86 (дт, 1Н); 6.67 (с, 2Н); 6.49 (д, 1Н); 5.37 (с, 2Н); 3.87 (м, 4Н); 3.19 (м, 4Н). МС (АРСГ) Розраховано : 306.3, Отримано: 307.1 (М+1). З використанням придатних вихідних речовин, аналогічно послідовностям реакцій, описаним вище для одержання сполуки (1-А) і відповідних гідрохлоридних та фумаратних солей (І^В) і (1-С), відповідно, були одержані сполуки, наведені в Таблиці 1 . Одержання проміжної сполуки трет-бутилового естеру 4-f4-f1'-(2-хлорФеніл)етокси]-піримідин-2іл)піперазин-1-карбонової кислоти (1-2a): 1-(2-Хлорфеніл)етанол (31.4мг, 0.20ммоль) розчиняли у 1.7мл безводного тетрагідрофурану та обробляли гідридом натрію (8.0мг, 60% дисперсія у мінеральному маслі, 0.20ммоль). Суміш перемішували у атмосфері азоту протягом 1 години при температурі навколишнього середовища, потім реакційну суміш обробляли третбутиловим естером 4-(4-хлорпіримідин-2-іл)піперазин-1-карбонової кислоти П-2а) (50мг, 0.17ммоль) в одній порції. Одержану суміш кип'ятили під азот протягом 4 годин. Після охолодження до кімнатної температури реакційну суміш виливали у воду (20мл) та екстрагували етилацетатом (2 χ 25мл). Об'єднані органічні екстракти промивали насиченим розчином солі (20мл), потім сушили над сульфатом натрію, фільтрували і концентрували. Залишок очищали тонкошаровою TLC (7 : 13 етилацетат : гексан) з одержанням 64.3мг вказаного у заголовку продукту П-2Ь). 1 Н ЯМР (400мгц, CDCI 3) δ 8.00 (д, 1 Η); 7.38-7.13 (м, 4Н); 6.35 (к, 1 Η); 6.02 (д, 1 Η); 3.62 (м, 4Η); 3.30 (м, 4Н); 1.57 (д, 3Н); 1.45 (с, 9Н). МС (АРСҐ) Розраховано : 418, Отримано: 419.1 (М+1). Одержання 4-[1-(2-хлорсЬеніл)етокси1-2-піперазин-1-ілпіримідину (2-А): До розчину mpem-бутилового естеру 4-{4-[1-(2-хлорфеніл)етокси]піримідин-2-іл}піперазин-1 -карбонової кислоти (1-2Ь) (64.3мг, 0.15ммоль) в 2.0мл дихлорметану додавали трифтороцтову кислоту (177.4мкл, 2.30ммоль) і суміш перемішували протягом 1.5 годин при температурі навколишнього середовища. Реакційну суміш потім концентрували і залишок розчиняли в 1М НСІ (водн.) (10мл). Проводили екстрагування етилацетатом (10мл), шари розділяли і доводили рН водного шару до 12, використовуючи 5М КОН (водн.). Цю водну суміш екстрагували етилацетатом (2 x 15мл) і об'єднані органічні екстракти сушили над сульфатом натрію та концентрували з одержанням 58.2мг вказаного у заголовку продукту (2-А). 1 Н ЯМР (400мгц, CDCI 3) δ 8.01 (д, 1 Η); 7.38 (дд, 1 Η); 7.28 (д, 1 Η); 7.18-7.11 (м, 2Н); 6.36 (к, 1Н); 6.00 (д, 1Н); 3.68 (шс, 4Н); 2.82 (шс, 4Н); 1.56 (д, ЗН). МС (АРСҐ) Розраховано : 318, Отримано : 319.1 (М+1). Одержання mpucbmopauemamv 4-[1-(2-хлорФеніл)етокси1-2-піперазин-1-ілпіримідину (2До розчину mpem-бутилового естеру 4-{4-[1-(2-хлорфеніл)етокси]піримідин-2-іл}-піперазин-1-карбонової кислоти (І-2Ь) (64.3мг, 0.15ммоль) в 2.0мл дихлорметану додавали трифтороцтову кислоту (177.4мкл, 2.30ммоль) і суміш перемішували протягом 1.5 годин при температурі навколишнього середовища. Реакційну суміш концентрували і залишок розчинника замінювали 6 x 4мл гексану. В залишку отримували 62.1мг вказаної у заголовку сполуки (2-В). 1 Н ЯМР (400мгц, CDCI 3) δ 8.01 (д, 1Н); 7.38 (дд, 1Н); 7.28 (д, 1Н); 7.18-7.11 (м, 2Н); 6.36 (к, 1Н); 6.00 (д, 1Н); 3.68 (шс, 4Н); 2.82 (шс, 4Н); 1.56 (д, ЗН). МС (АРСГ) Розраховано : 318, Отримано : 319.1 (М+1). З використанням придатних вихідних речовин, аналогічно послідовностям реакцій, описаним вище для одержання сполуки (2-А) і відповідної трифторацетатної солі (2-В). були одержані сполуки, наведені в Таблиці 2. Гідрохлоридну сіль одержували за методикою, аналогічною тій, за якою одержували (1-В) в Прикладі 1. ТАБЛИЦЯ 2 Приклад № Назва сполуки МС Розраховано 2-С 2-D 2-Е 2-F 2-G 2-Н 2-І 2-J 2-К 2-L 4-[1 -(3-Хлорфеніл)етокси]-2-піперазин-1 -ілпіримідин 4-[1 -(4-Хлорфеніл)етокси]-2-піперазин-1 -ілпіримідин 4-(4-Фторбензилокси)-2-піперазин-1-ілпіримідин 4-(3,4-Дихлорбензилокси)-2-піперазин-1 -ілпіримідин 4-(3,4-Дифторбензилокси)-2-піперазин-1-ілпіримідин 4-(3,4-Диметилбензилокси)-2-піперазин-1-ілпіримідину гідрохлорид 4-(2,3-Дифторбензилокси)-2-піперазин-1-ілпіримідину трифторацетат 4-[1 -(3-Хлорфеніл)етокси]-6-метил-2-піперазин-1 -ілпіримідину трифторацетат 4-(2-Етоксибензилокси)-6-метил-2-піперазин-1-ілпіримідину трифторацетат 4-Бензилокси-2-піперазин-1-ілпіримідину гідрохлорид 318.0 318.0 288.3 338.0 306.3 298.2 306. 1 Отримано (М+1) 319.2 319.2 289.2 339.0 307.1 299.2 307.1 332. 1 333.3 328.4 329.3 343.3 344.3 Приклад 3 Одержання проміжної сполуки трет-бутилового естеру 4-{2-(3-хлорбензиламіно)піримідин-4-іл!піперазин-1 -карбонової кислоти (1 -За): Суміш mpem-бутилового естеру 4-(2-хлорпіримідин-4-іл)піперазин-1 -карбонової кислоти (1-1 а) (100мг, 0.33ммоль), 3-хлорбензиламіну (0.65мл, 5.3ммоль) та карбонату калыю (71мг, 0.67ммоль) в етанолі (5мл) нагрівання при кипінні протягом 7 днів. Реакційну суміш охолоджували до кімнатної температури, виливали в Н2О (15мл) та екстрагували за допомогою ЕtOАс (2 x 20мл). Об'єднані органічні екстракти промивали Н2О (3 χ 15мл), насиченим розчином солі, висушували (Na2SO4) та концентрували у вакуумі. Залишок очищали препаративною TLC (10% МеОН в СН2СІ 2) з одержанням твердої речовини жовтого кольору. Тверду жовту речовину розтирали з МеОН (1мл) і тверду речовину збирали фільтрацією з одержанням проміжної сполуки (ІЗа) у вигляді твердої речовини білого кольору (48.5мг). 1 Н ЯМР (400мгц, CD3OD) δ 7. 74 (шс, 1Н); 7.35-7.17 (м, 4Н); 6.01 (шс, 1 Н); 4.45 (с, 2Н); 3.54 (шс, 4Н); 3.37 (шс, 4Н); 1.44 (с, 9Н). МС (ES+) Розраховано : 403.2, Отримано : 404.1 (М+1). Одержання гідрохлориду (3-хлорбензил)-(4-піперазин-1-ілпіримідин-2-іл)аміну (3-А):. До розчину mpem-бутилового естеру 4-[2-(3-хлорбензиламіно)піримідин-4-іл]піперазин-1-карбонової кислоти (N3a) (48.5мг, 0.12ммоль) в СН2СІ 2 (1мл) додавали трифтороцтову кислоту (139 мкд, 1.8ммоль). Після перемішування при кімнатній температурі протягом 3 годин суміш виливали в 1N NaOH (10мл) та екстрагували СН2СІ 2 (1 x 35мл). Органічний шар промивали насиченим розчином солі, висушували та концентрували з одержанням вказаної у заголовку сполуки у вигляді вільного аміну. Вільний амін в СН2СІ 2 (1мл) додавали до 1М НСІ в етері (0.10мл, 0.10ммоль). Після перемішування протягом 10 хвилин при кімнатній температурі, розчин концентрували у вакуумі з одержанням гідрохлоридної солі (3-А) (32.4мг) у вигляді твердої речовини жовтого кольору. 1 Н ЯМР (400мгц, CD3OD) δ 7.82 (д, 1 Η); 7.38 (с, 1 Η); 7.35-7.26 (м, ЗН); 6.51 (д, 1 Н); 4.60 (с, 2Н); 4.04 (шс, 4Н); 3.29 (шс, 4Н). МС (АРСl+) Розраховано : 303.2, Отримано : 304.1 (М+1). Одержання фумарату (3-хлообензил)-4-піперазин-1-ілпіримідин-2-іл)аміну (3-В): До розчину проміжної сполуки (I-3а) (274.2мг, 0.90ммоль) в 10мл суміші 10 : 1 метанол : ізопропіловий етер додавали розчин 0.5 Μ фумарової кислоти в метанолі (1.80мл, 0.90ммоль) і перемішували протягом 1 години. Одержану суспензію розбавляли 35мл ізопропілового етеру і перемішували протягом 10 хвилин. Фільтрацією та наступним висушуванням на повітрі одержували 356.8мг вказаної у заголовку сполуки (3-B). 1 Н ЯМР (400мгц, CD3OD) 8 7. 81 (д, 1Н); 7.32-7.18 (м, 4Н); 6.67 (с, 2Н); 6.16 (д, 1Н) ; 4.50 (с, 2Н); 3.80 (шс, 4Н); 3.11 (шс, 4Н). МС (АРСГ) Розраховано : 303.2, Отримано : 304.3 (М+1). З використанням придатних вихідних речовин, аналогічно послідовностям реакцій, описаним вище для одержання сполуки (3-А) були одержані наступні сполуки. Гідрохлорид (3-фторбензил)-(4-піперазин-1-ілпіримідин-2-іл)аміну (3-С): 1 Н ЯМР (400мгц, CD3OD) δ 7. 82 (д, 1Н); 7.30-7.26 (м, 1Н) ; 7.12 (д, 1 Н); 7.05-7.02 (дд, 1 Н); 6.92-6.91 (тд, 1 Н); 6.16 (д, 1 Н); 4.52 (с, 2Н); 3.81-3.78 (м, 4Н); 3.12-3.11 (м, 4Н). МС (АРСl+) Розраховано : 287.2, Отримано : 288.1 (М+1). Гідрохлорид бензил-(4-піперазин- 1-ілпіримідин-2-іл)аміну (3-D): МС (АРСl+) Розраховано : 305.3, Отримано : 306.2 (М+1). Приклад 4 Одержання проміжної сполуки трет-бутилового естеру 4-[4-(3-хлообензиламіно)-піримідин-2-іл!піперазин1-карбонової кислоти (1-4а): Суміш mpem-бутилового естеру 4-(4-хлорпіримідин-2-іл)піперазин-1-карбонової кислоти (1-2а) (100мг, 0.33ммоль), 3-хлорбензиламіну (0.65мл, 5.3ммоль) та карбонату калыю (71мг, 0.67ммоль) в етанолы (5мл) нагрівали при кипінні протягом 24 годин. Реакційну суміш охолоджували до кімнатної температури, виливали в НгО (15мл) та екстрагували ЕtOАс (2х18мл). Об'єднані органічні екстракти промивали НгО (2 χ 10мл), насиченим розчином солі, висушували (Na2SO4) і концентрували у вакуумі. Залишок очищали хроматографією, використовуючи 40% ЕЮАс в гексані як розчинник для елюювання, з одержанням вказаної у заголовку сполуки (1-4а) (93мг) у вигляді безбарвного масла. 1 Н ЯМР (400мгц, CD3OD) δ 7.69 (д, 1 Η); 7.32 (с, 1 Η); 7.28-7.19 (м, 3Н); 5.88 (д, 1 Н); 4.49 (с, 2Н); 3.64-3.61 (м, 4Н); 3.37-3.29 (м, 4Н); 1.45 (с, 9Н). МС (ES+) Розраховано : 403.2, Отримано : 404.0 (М+1). Одержання гідоохлориду (3-хлорбензил)-(2-піперазин-1-ілпіримідин-4-іл)аміну (4-А): Вказану у заголовку сполуку (4-А) одержували з mpem-бутилового естеру 4-[4-(3хлорбензиламіно)піримідин-2-іл]піперазин-1-карбонової кислоти (І-4а) та TFA відповідно до методики, аналогічної тій, що описана в Прикладі 3. 1 Н ЯМР (400мгц, CD3OD) δ 7. 74 (д, 1 Η); 7.35-7.25 (м, 4Н); 6.15 (д, 1 Н); 4.60 (с, 2Н); 3.97-3.94 (м, 4Н); 3.273.23 (м, 4Н). МС (АРСГ) Розраховано : 303.2, Отримано : 304.1 (М+1). З використанням придатних вихідних речовин, аналогічно послідовностям реакцій, описаним вище для одержання сполуки (^А) була одержана сполука (4-В) і з використанням методики, аналогічної способу одержання фумаратної солі, описаної в Прикладі 3 (сполука (3-В)) була отримана відповідна фумаратна сіль (4-С). Пдрохлорид (3-фторбензил)-(2-піперазин-1-ілпіримідин-4-іл)аміну (4-В): 1 Н ЯМР (400мгц, CD3OD) δ 7.76 (д, 1Н); 7.32-7.28 (м, 1Н); 7.11 (д, 1Н), 7.05-7.01 (дд, 1Н), 6.93 (тд, 1Н); 5.94 (д, 1Н); 4.53 (с, 2Н); 3.903.87 (м, 4Н); 3.13-3.11 (м, 4Н). МС (АРСl+) Розраховано : 287.2, Отримано : 288.1 (М+1). Фумарат (3-Фторбензил)-(2-піперазин-1-ілпіримідин-4-іл)аміну (4-С): 1 Н ЯМР (400мгц, CD3OD) δ 7. 75 (д, 1 Η); 7.30 (дд, 1 Η); 7.11 (д, 1 Η), 7.02 (д, 1 Η), 6.93 (тд, 1 Η); 6.69 (с, ЗН) 5.94 (д, 1 Н); 4.53 (с, 2Н); 3.87 (м, 4Н); 3.13-3. 11 (м, 4Н). МС (АРСl+) Розраховано : 287.2, Отримано : 288. 1 (М+1). Пдрохлорид бензил-(2-піперазин-1-ілпіримідин-4-іл)аміну (4-D): МС (АРСl+) Розраховано : 305.3, Отримано : 306.2 (М+1). Приклад 5 Одержання проміжної сполуки (6-хлорпіридин-2-іл)метанолу (І-5а): В суху колбу завантажували 25мл безводного тетрагідрофурану та 6-хлорпіридин-2-карбонової кислоти (2.00 г, 12.69ммоль) і потім охолоджували до 10°C. Суміш обробляли по краплинам сумішшю тетрагідрофуран-боран (1.0М розчин в THF, 38.1мл) близько 10 хвилин під азотом. Цю суміш перемішували при охолодженні протягом 15 хвилин, потім при температурі навколишнього середовища протягом 4 годин. Потім реакційну суміш охолоджували до 0°C і додавали повільно 10мл води. Одержану суміш виливали в 50мл 1М водного розчину гідроксиду натрію та екстрагували 2 χ 75мл етилацетату. Органічні екстракти об'єднували і промивали насиченим розчином солі, потім висушували над сульфатом натрію і фільтрували. Концентруванням у вакуумі одержували 589.1мг вказаної у заголовку сполуки у вигляді твердої речовини білого кольору (1-5а). 1 Н ЯМР (400мгц, CDCI 3) δ 7.67 (τ, 1 Η); 7.25 (м, 2Η); 4.74 (с, 2Н). МС (ES+) Розраховано : 143, Отримано : 144.3 (М+1). Одержання проміжної сполуки трет-бутилового естеру 4-[2-(6-хлорліридин-2-ілметокси)-піримідин-4 іліпіпеоазин-1-карбонової кислоти (І-5Ь): Вказану у заголовку сполуку (І-5Ь) одержували з (6-хлорпіридин-2-іл)метанолу (І-5а) та mpem-бутилового естеру 4-(2-хлорпіримідин-4-іл)піперазин-1-карбонової кислоти (І-1а) відповідно до методики, аналогічної тій, що описана в Прикладі 1. 1 Н ЯМР (400мгц, CDCI 3) δ 8.03 (д, 1 Η); 7.63 (τ, 1 Η); 7.43 (д, 1 Η); 7.21 (д, 1Н); 6.16 (д, 1Н); 5.42 (с, 2Н); 3.59 (м, 4Н); 3.45 (м, 4Н); 1.46 (с, 9Н). МС (ES+) Розраховано : 405, Отримано: 406.1 (М+1). Одержання гідоохлориду 2-(6-хлорпіридин-2-ілметокси)-4-піперазин-1-ілпіримідину (5-А): Вказану у заголовку сполуку (5-А) одержували з трет-бутилового естеру 4-[2-(6-хлорпіридин-2-ілметокси)піримідин-4іл]піперазин-1-карбонової кислоти (І-5b) та TFA згідно з методикою, аналогічною тій, що описана в Прикладі 3. 1 Н ЯМР (400мгц, CD3OD) δ 8.08 (д, 1Н); 7.80 (τ, 1Н); 7.46 (д, 1Н); 7.36 (д, 1 Н); 6.53 (д, 1Н); 5.41 (с, 2Н); 3.91 (м, 4Н); 3.27 (м, 4Н). МС (ES1) Розраховано : 305, Отримано : 306.0 (М+1). З використанням придатних вихідних речовин, аналогічно послідовностям реакцій, описаним вище для одержання сполуки (5-А) були одержані сполуки, наведені в Таблиці 4. ТАБЛИЦЯ 4 Приклад № 5-В 5-С Назва сполуки МС Розраховано Отримано (М+1) 4-Піперазин-1-іл-2-(піридин-2271.1 272.0 ілметокси)піримідину гідрохлорид 2-(6-Метилпіридин-2285.1 286.0 ілметокси)-4-піперазин-1ілпіримідину гідрохлорид Приклад 6 Приклад 6 ілюструє синтез NEPi Сполуки (3)-2-[(1-{[3-(4-хлорфеніл)пропіл]карбамоїл}циклопентил)метил]-4-метоксибутанової кислоти, згадуваної тут нижче, для використання в комбінації зі сполуками даного винаходу для лікування жіночої сексуальної дисфункції. Одержання проміжної сполуки 1-[2-(трет-бутоксикарбоніл)-4-метоксибутил1-ииклопентанкарбонової кислоти (І-6а): Розчин mpem-бутил 3-(1-карбоксициклопентил)пропаноату (12 г, 49.5ммоль) (див. ЕР274234В1, Приклад 35) в сухому тетрагідрофурані (100мл) додавали при перемішуванні до розчину діізопропіламіду літію (130мл) в суміші гексану (52мл) та тетрагідрофурану (200мл) при -78°C під азотом. Через 1 годину додавали розчин 2брометилметилового етеру в тетрагідрофурані (100мл), підтримуючи температуру при -78°C. Реакційну суміш залишали нагріватися до кімнатної температури протягом ночі. Суміш заливали водою (100мл) і підкисляли до рН 1 за допомогою 2М соляної кислоти та екстрагували етилацетатом (2х 150мл). Об'єднані органічні екстракти висушували на сульфатом магнію і концентрували у вакуумі з одержанням неочищеної кислоти, яку піддавали хроматографічному очищенню на силікагелі. Елюювання із співвідношенням метанолу в дихлорметані, яке збільшувалось (чистий дихлорметан до 1: 50) приводило до одержання масла (7.7 г, 25.6ммоль, 2%); Rf 0.3 метанол, дихлорметан 1: 20; 1 Н ЯМР (CDCI 3 400МГц) δ : 1.4 (с, 9Н), 1.4-1.7 (м, 7Н), 1.75-1.95 (м, 2Н), 2.0-2.15 (м, ЗН), 2.3-2.4 (м, 1Н), 3.3 (с, 3Н), 3.3-3.4 (м, 2Н); НРМС: m/z 299 (М-Н+). Одержання проміжної сполуки 1-[(28)-2-(трет-бутоксикарбоніл)-4-метоксибутил1-циклопентанкарбонової кислоті (І-6a): Проміжну сполуку (1-6а) та (+)-псевдоефедрин перекристалізовували дев'ять разів з гексану з одержанням твердої речовини білого кольору. Сіль розчиняли в етилацетаті, промивали 0.5М розчином соляної кислоти, висушували над сульфатом магнію і концентрували у вакуумі з одержанням (S)-кислоти з 31 % виходом у вигляді масла блідо-жовтого кольору в > 90% єн (енантіомерному надлишку) за результатами ЯМР аналізу δ 3.3 пік (+)-псевдоефедринової солі; 1 Н ЯМР (CDCI 3 400МГц) δ : 1.4 (с, 9Н), 1.4-1.7 (м, 7Н), 1.75-1.9 (м, 2Н), 2.0-2.15 (м, 3Н), 2.35-2.45 (м, 1Н), 3.3 (с, ЗН), 3.3-3.4 (м, 2Н); [a]D- 5.2 (ЕtOН, с 1. 2). Одержання проміжної сполуки трет-бутил (28)-2-{[1-({(3-(4-хлорфеніл)пропіл]аміно}карбоніл)циклопентилiметил}-4-метоксибутаноату (1-6с): До розчину 1,1'-карбонілдіімідазолу (73.9 г, 0.45 моль) в азеотропно висушеному ізопропілацетаті (339мл) при перемішуванні при 60°C в атмосфері N2 додавали ізопропілацетатний розчин проміжної сполуки (N6b) протягом періоду близько 1.5 годин. Автоматичні лінії потім промивали сухим ізопропілацетатом (50мл). Потім одержаний розчин перемішували при 60°C протягом додаткових 4.5 годин, після чого реакційну суміш залишали охолоджуватися до кімнатної температури і перемішували протягом 15 годин. Потім до одержаного розчину додавали триетиламін (46.1 г, 0.46 моль), з наступним додаванням гідрохлориду 3-(4хлорфеніл)пропіламіну (J. Med. Chem., 1996, 39, 4942-51) (94.3 г, 0.46 моль). Потім одержану суміш знову нагрівали до 60°C протягом 7 годин перед охолодженням до кімнатної температури. Після чого до реакційної суміші при перемішуванні додавали деіонізовану воду (100мл) і потім водну соляну кислоту (190мл 5М розчин), поки рН водного шару не досягав значення рН між 2 та 3. Потім водний шар відокремлювали, а органічний шар екстрагували водним розчином карбонату калію (50мл 0.5М розчину). Водну фазу відділяли, а органічну фазу промивали насиченим розчином солі (100мл). Потім водний шар відокремлювали, а органічну фазу концентрували дистиляцією під вакуумом з одержанням вказаної у заголовку сполуки у вигляді масла жовтого кольору (200.3 г, 443ммоль, 98% вихід);. 1 Н ЯМР (CDCI 3 300МГц) δ : 1.45 (с, 9 Η), 1.45-1.56 (м, 1 Η), 1.561.74 (м, 6 Η), 1.74-2.11 (м, 7 Η), 2.32-2.43 (м, 1 Η), 2.64 (τ, 2 Η), 3.22-3.30 (μ, 2 Η), 3.27 (с, 3Η), 3.30-3.38 (μ, 2 Η), 5.75-5.85 (Μ, ш, 1 Η), 7.13 (д, 2 Η), 7.26 (д, 2 Η); НРМС (ES позитиви,): m/z 452 [M+Hf (35CI). Одержання (28)-2-{[1-({[3-(4-хлорфеніл)пропіл]аміно)карбоніл)ииклопентил1метил-4-метоксибутанова кислота та її натрієва сіль (6-А): До розчину проміжної сполуки (1-6с) (9.6 г, 21.2ммоль) в дихлорметані (52мл) додавали трифтороцтову кислоту (16.3мл, 212ммоль) і одержаний розчин перемішували при кімнатній температурі протягом 3.75 годин у атмосфері N2. Потім до реакційної суміші при перемішуванні додавали водний розчин карбонату натрію (95мл 10% ваг./об. розчину) поки рН водного шару не був між рН 2 та 3. Шари потім розділяли і органічний шар екстрагували водним розчином карбонату натрію (2 x 20мл 10% ваг./об. розчину). Водні шари об'єднували і потім додавали насичений розчин солі (80мл), з наступним додаванням 2-бутанону (40мл). Шари розділяли і водний шар екстрагували знову 2-бутаноном (2 x 50мл). Потім об'єднані органічні шари висушували азеотропною перегонкою при атмосферному тиску до об'єму 70мл, після чого відбувалася кристалізація, і суміш розбавляли 2-бутаноном (70мл). Потім продукт збирали фільтрацією і висушували при 50°C протягом 65 годин у вакуумі з одержанням неочищеної натрієвої солі вказаної у заголовку сполуки у вигляді твердої речовини білого кольору (5.76 г), яку потім очищали перекристалізацією наступним чином. До неочищеного продукту додавали етилацетат (87мл) та етанол (13мл) і залишки нерозчиненого продукту видаляли фільтрацією. Потім азеотропною перегонкою при атмосферному тиску видаляли етанол (щоб видалити 110мл розчинника) і заміняли етилацетатом (145мл), після чого відбувалася кристалізація. Потім одержаний кристалічний продукт збирали фільтрацією під вакуумом з одержанням чистої натрієвої солі казаного у заголовку продукту у вигляді твердої речовини білого кольору (4.51 г, 10.8ммоль, 51 %); т.пл. (етилацетат) 214-216°C ; 1 Н ЯМР (DMSO-de 300МГц) δ : 1.26-1.58 (м, 8 Н), 1.62-1.74 (м, З Н), 1.74-1.86 (м, 1 Н), 1.91-2.07 (м, З Н), 2.57 (т, 2 Н), 3.03 (к, 2 Н), 3.10 (с, З Н), 3.13-3.27 (м, 2 Н), 7.22 (д, 2 Н), 7.29 (д, 2 Н), 9.16 (т, ш, 1 Н); НРМС (ES негатив.); 789 [2М-Н]· (3SCI), 394 [М-Н]+ (35СІ). Для аналітичних цілей вказаний у заголовку продукт (тобто, вільну кислоту) отримували шляхом розчинення натрієвої солі у воді, підкисленій за допомогою 5М соляної кислоти, та екстрагували дихлорметаном. Видалення розчинника шляхом продування потоку азоту над зразком приводило до утворення вказаного у заголовку продукту; 1 Н ЯМР (DMSO-d6 300МГц) δ : 1.22-1.80 (м, 11 Н), 1.81-1.96 (м, 2 Н), 1.96-2.08 (м, 1 Н), 2.93-2.27 (м, 1 Н), 2.53 (т, 2 Н), 3.03 (к, 2 Н), 3.11 (с, З Н), 3.16-3.25 (м, 2 Н), 7.20 (д, 2 Н), 7.30 (д, 2 Н), 7.51 (т, 1 Н); НРМС (ES негатив.); 789 [2М-Н]" (35СІ), 394 [М-Н]+ (35СІ); ВЕРХ (колонка : ChiralPak AS (25 x 0.46см); мобільна фаза: гексан/ІПС/оцтова кислота (95/5/0.5 об./об./об.); швидкість протікання: 1.0мл/хвил.; температура: навколишнього середовища; впорскуваний об'єм: 20мкл; визначення: UV220нМ; концентрація зразка: 1.0мг/мл одержана в мобільній фазі), час утримування: неосновний енантіомер 11.4 хвил. (5.7%), основний енантіомер 14.3 хвил. (94.3%). Одержання моногідрату натрієвої солі 6-А : До натрієвої солі (6-А) (200мг) додавали до 1мл 3.9% розчину води в ізопропанолі. Одержану суспензію перемішували протягом 12 днів, після чого її розділяли фільтрацією. Продукт дав наступні дані ДРПП зразка, наведені в Таблиці 5 нижче. ТАБЛИЦЯ 5 Кут 2Тета ° 3.552 7.154 9.526 10.359 10.608 11.03 12.369 12.939 13.233 13.835 14.345 14.887 15.16 16.372 16.813 17.203 17.408 Інтенсивність% % 30.8 8 3.1 15.7 14.3 5 3.7 13.2 12.3 14.2 37.9 16 16.8 24.9 6.9 22.1 32.7 Кут 2Тета ° 17.708 17.93 18.313 18.545 18.811 19.7 19.978 20.273 20. 627 20.829 20.926 21.443 21.611 21.881 22.174 22.472 Інтенсивність% % 13.5 29 12 23.9 14 34.2 100 90.6 51.9 29.4 28.4 52.7 41.6 21.2 24.3 47.1 Кут 2Тета ° 22.881 23.141 23.478 24.088 24.313 24.588 25.013 25.514 25.987 27.107 27.395 27.869 28.716 28.788 28.989 30.232 Інтенсивність% % 35 23.2 15.1 13.9 12.6 22.7 25.8 29.9 25.5 18.2 30.6 19.2 21 19 27.2 13.4 Кут 2Тета ° 30.672 30.952 31.437 31.788 32.114 32.998 33.375 33.815 34.266 35.705 35.989 36.514 38.151 38.925 39.091 39.961 Інтенсивність% % 15 17.5 15.7 13.9 24.6 13.3 18.8 14 14.4 15.7 14.1 16.7 14.6 17 19 13 Диференціальну сканувальну калориметрію (DSC) здійснювали з використанням приладу Perkin Elmer DSC-7, змонтованого з автоматичним замінювачем зразка. Приблизно 3мг зразка акуратно відважували в алюмінієву кювету об'ємом 50мкл і закривали з обжиманням перфорованою кришкою. Зразки нагрівали зі швідкістю 20°C/хвил. в інтервалі від 40°C до 300°C з продувкою газоподібним азотом. Явище дегідратації відбувалось між приблизно 50 та 150°C і основна частина речовини плавилась між 212 та 225°C. Фахівцю буде зрозумілим, що точка плавлення може виходити за межі цього інтервалу як результат наявності домішок. Безводна сіль: Натрієва сіль сполуки (6-Α) дала наступні PXRD зразка, наведені в Таблиці 6 нижче. ТАБЛИЦЯ 6 Кут 2-Тета Інтенсивність% Кут 2-Тета Інтенсивність% Кут 2-Тета Інтенсивність% Кут 2-Тета Інтенсивність% ° % ° % ° % ° % 5.463 12.2 17.714 95.6 22.735 ЗО 28. 926 23.8 6.654 100 18.083 31.7 23.36 56.5 29.802 23.5 7.546 66 18.64 28.8 24.126 31.9 30.454 30.7 9.336 31.3 18.902 82.4 24.388 45.2 30.885 29.2 10.953 9.7 19.696 40.1 24.72 25.8 31.48 21 11.571 55.9 20.406 33.9 25.298 26.7 32.66 16.8 12.56 10.9 20.502 31.8 25.579 20.4 34.027 23.1 13.287 22.9 20.683 45.4 26.718 17.6 34.494 17.6 15.125 33.6 20.942 31.5 27.151 24.2 36.011 19 15.667 60.3 21.559 92.6 27.46 22.7 36.997 17.4 16.403 17.2 21.898 66.2 27.737 20.2 38.704 21.2 17.024 62.2 22.274 36.6 28.56 27.1 39.961 18.7 БІОЛОГІЧНІ ДОСЛІДЖЕННЯ Можливість практичного використання сполук відповідно до даного винаходу може бути підтверджена активністю, принаймні, в одному з аналізів, представлених нижче. Методика 5НТ2C зв 'язування Афінність сполук у зв'язувальному сайті 5НТ2с визначали шляхом конкурентного зв'язування на мишачих клітинах Swiss ЗТЗ (отриманих з Американської колекції типових культур (АТСС), Manassas, VA), трансфікованих людським рецептором на 3Н-5НТ2C. Вказаний спосіб був адаптований Roth та інм J. of Pharm. and Exp. Therap., 260 (3), 1362- 1365 (1992). Клітини вирощували на середовищі DMEM з високим вмістом глюкози, збирали їх, гомогенізували, центрифугували та ресуспендували в 50мм Трис-НСІ. Клітини інкубували при температурі 37°С протягом 15 хвилин, центрифугували, а потім ресуспендували в буфері для аналізу (50мм Трис-НСІ, 4мм СаСІ 2, 0,1% аскорбінової кислоти та 100мкМ паргіліну при рН 7,7) в 100 об'ємах на грам. Пробірки для аналізу містили 25мкл ЮнМ ЗН-5НТ (заключна концентрація 1нМ), 25мкл розчинника (буфер для аналізу), досліджувана речовина (10 X заключного об'єму) або інертна речовина (10мкМ міансерину). 200мкл тканинного гомогената додавали до кожної пробірки та інкубували протягом 30 хвилин при температурі 37°С. Потім швидко фільтрували зразки під вакуумом за допомогою пристрою для збору клітин Skatron™ (наданого Molecular Devices Corporation, Sunnyvale, CA) при використанні фільтрів GF/B, попередньо просочених 0,5% поліетиленіміном (РЕІ), та промитих за допомогою 2 X 5мл холодного 50мМ Трис-НСІ. Фільтри вилучали та проводили підрахунок на лічильнику Wallac Betaplate (наданого Perkin Elmer Life Science, Gaithersburg, MD). Процент інгібування специфічного зв'язування досліджуваними сполуками використовували для підрахунку Кі, або проводили екстраполяцію концентрації досліджуваної сполуки, необхідної для інгібування половини загального специфічного зв'язування для кожної сполуки. Наступні сполуки, описані в приведених вище Прикладах, продемонстрували значення Кі для 5НТ2с зв'язування в межах від 0,2нМ до 238нМ. Приклади № 1-В, 1-D, 1-Е, 1-F, 1-G, 1-Н, 1-І, 1-J, 1-К, 1-L, 1-М, 1-О, 1-Р, 1-Q, 1-R, 1-S, 1-Т, 1-U, 1-V, 1-W, 1Х, 1-Y, 1-Z, 1-АА, 1-ВВ, 1-DD, 1-ЕЕ, 1-FF, 1-GG, 1-НН, 1-11, 1-JJ, 1-КК, 1-LL, 1-ММ, 1-СС, 1-ОО, 1-РР, 1-QQ, 1RR, 1-SS, 1-ТТ, 1-UU, 1-VV, 1-WW, 1-ХХ, 1-YY, 1-ZZ, 1-АВ, 1-АС, 1-AD, 1-АЕ, 1-AJ, 1-АК, 1-AL, 2-А, 2-С, 2-D, 2Е, 2-F, 2-G, 2-Н, 2-І, 2-L, 3-А, 3-С, 3-D, 4-А, 4-В, 4-D та 5-А. Приклади № 1-NN, 5-В та 5-С продемонстрували значення Кі більші, ніж 500нМ, при цьому залишкові сполуки не визначалися Процедура зв'язування 5HT5A Афінність сполук у сайті 5НТ2А зв'язування серотоніну визначали шляхом конкурентного зв'язування на мишачих клітинах NIH3T3, трансфікованих щурячим рецептором 5НТгА при використанні 125I-DOL Спосіб був адаптований Leonhardt та ін., Molecular Pharmacology, 42, 328-335 (1992). Заморожені клітини у вигляді пасти гомогенізували в 50мМ Трис-НСІ буфера, що має рН 7,4 та містить 2мМ МgСІ 2, при використанні Polytron та центрифугували при 45000 χ д протягом 10 хвилин. Отриманий осад ресуспендували в охолодженому на льоду свіжому 50мМ Трис-НСІ буфері з рН 7,4, що містить 2мМ МgСІ 2, при використанні Polytron™ та повторно центрифугували при 45000 х д протягом 10 хвилин. Отриманий осад ресуспендували в 50мМ Трис-НСІ буфері з рН 7,4, що містить 2мМ МgСІ 2 у концентрації 5мг/мл. Комірка в планшеті на 96 комірок містила 25мкл 0,7нМ 125I-DOL (заключна концентрація 70 пМ), 25мкл носія (буфер для аналізу), інертну речовину (10мкМ цінансерину) або досліджувану сполуку (10 X заключного об'єму). Додавали 200мкл тканинного гомогенату в кожну комірку та інкубували протягом 15 хвилин при температурі 37°С на качалці. Зразки потім швидко відфільтровували під вакуумом при використанні пристрою для збору клітин (Skatron™), застосовуючи GF/B фільтри, попередньо просочені 0,5%-ним поліетиленіміном (РЕІ) та промивали за допомогою 2 x 5мл холодного 50мМ Трис-НСІ. Фільтри вилучали, висушували та підраховували на лічильнику Wallac Betaplate. Криві залежності процентного інгібування специфічного зв'язування у відповідь на визначені концентрації та log концентрацію досліджуваних сполук використовували для визначення ІС 50 для кожної сполуки, а значення Кі підраховували на основі вирівнювання Cheng-Prusof (Ki=IC50/(1+L/Kd)), де L являє собою концентрацію радіоліганду, використовувану в аналізі зв'язування, а значення Kd ґрунтується на попередніх дослідженнях насичення радіо лігандом. Наступні сполуки Прикладів, описаних вище, демонструють значення Кі для бНТгд зв'язування в межах від 0,5нМ до 625нМ: Приклади № 1-В, 1-D , 1-Е, 1-F, 1-G, 1-Н, 1-І, 1-J, 1-К, 1-L,1-М, 1-О, 1-Р, 1-Q, 1-R, 1-S, 1-Т, 1-U, 1-Z, 1-АА, 1ВВ, 1-СС, 1-ЕЕ, 1-FF, 1-GG, 1-НН, 1-11, 1-JJ, 1-КК, 1-LL, 1-ММ, 1-00, 1-РР, 1-QQ, 1-RR, 1-SS, 1-ТТ, 1-AJ, 1-АК, 1-AL, 2-А, , 2-С, 2-D, 2-Е, 2-F, 2-G, 2-Н, 2-І, 2-L, 3-А, 3-D і 4-D. Приклади №№1-NN та 1-UU не показують ніякої зв'язувальної активності, при цьому залишки сполук не визначалися. Функціональний аналіз Клітини Swiss 3T3, що експресують рецептори г-5НТ2с, г-5НТ2А (пацюка) h-5HT2c або П-5НТ2А (людини), засівали при щільності 12,500 клітин/комірка у планшети на 384 комірки, покриті колагеном. Через сорок вісім (48) годин до клітин додавали чутливий до кальцію барвник, Fluo 4-АМ (4мкМ, розчинені в ДМСО, що містить плюронову кислоту), у середовищі DMEM, що не містить сироватки в присутності пробенициду (2,5мМ), протягом 75 хвилин при температурі 37°С в СО2-інкубаторі. Барвник, що не зв'язався, видаляли шляхом промивання три рази за допомогою забуференого HEPES фізіологічного розчину, що містить пробеницид (2,5мМ), при використанні пристрою для промивання клітин Skatron™ (заключний об'єм 30мкл). Кожний із планшетів окремо приєднували до флуореметричного пристрою для зчитування (FLIPR 384, що отриманий від Molecular Devices Corporation) та вимірювання флуоресценції проводили кожні 2 секунди протягом періоду 85 секунд. Додання тестової сполуки проводили одночасно для всіх 384 комірок через 20 секунд після реєстрації базової лінії. Криві залежності від концентрації одержували, використовуючи Graphpad Prism™ (отриманий від GraphPad Software Inc., San Diego, CA), ефективності агоністів визначали як % відповіді на 10мкМ 5-НТ (що приймали за 100%). Оцінку ефективностей антагоністів (функціональні Кі) одержували шляхом вимірювання інгібування відповіді досліджуваної сполуки на 5-НТ (10нМ для 5НТ2С и 50нМ для 6НТгд) та використання вирівнювання Cheng Prusoff. Функціональні дані для сполук, приведених в описаних вище Прикладах, де використовували клітини NIH ЗТЗ клітини, що експресують 5НТ2С, приведені нижче. Приклади від 1-А до 1-AL, від 2-а до 2-L, від 3-А до 3-D, від 4-а до 4-D і від 5А до 5-С проявляли свою активність як часткові агоністи, що мають значення ECso У межах від 0,016мкМ до 7,0мкМ для клітин, що експресують 5НТ2С, за винятком: (і) Прикладів №1-S, 1-U, 1-Y, 1-FF, 1-GG, 1-НН, 1-11, 1-КК, 1-LL, 1-ММ, 1-РР, 1-SS, 1-UU, 1-VV, 1-WW, 1-ХХ, 1-YY, 1-АС, 1-AL, 2-Е, 2-F, 2-G, 2-Н, 2-І, 3-D, 4-А, 4-В, 4-С, 4-D, 5-А, 5-В та 5-С, які діють як повні антагоністи, (іі) Прикладів № 1-D, 1-F, 1-AG, 1-АК, 1-AL, 1-NN та 1-QQ, що не демонструють ніякої функціональної активності при 10мкМ та (ііі) Прикладу № 1-ZZ, що не визначався. Приклад № 1-NN не демонстрував ніякої функціональної активності з клітинами NIH 3Т3, що експресують або 5НТ2C, або 5НТ2A. Незважаючи на те, що цис-ізомер (сполука 1-NN) не був активним, не можна при цьому беззастережно припускати, що транс-ізомер не буде демонструвати ніякої функціональної активності. Добровільне споживання їжі Пацюкам Wistar вводили досліджувану сполуку або перорально або підшкірно в 30%-ному βциклодекстриновому носії за 30 хвилин перед початком темнового циклу. Споживання їжі досліджували при використанні комп'ютеризованих систем для спостереження за споживанням їжі окремими тваринами. 3а споживанням їжі спостерігали протягом, принаймні, 16 годин після введення досліджуваної сполуки. Статева дисфункція ПРИКЛАД А-Лікування MED Сполуки згідно з даним винаходом піддавали скринінгу на їх вплив на внутрішньокавернозний тиск статевих органів (ІСР) самців пацюків, що знаходяться у свідомості, у відповідності зі способами, описаними в даній заявці. Пропис ІСР: внутрішньо кавернозний тиск (ІСР) можна вимірювати у пацюка, що перебуває у свідомості, шляхом телеметричної реєстрації. Катетер хірургічно імплантували в печеристе тіло. Кінець катетера з'єднували з пристроєм, що сприймає, обробляє та передає інформацію в цифровій формі від тварини. Приймач перетворює радіочастотний сигнал від імплантату в цифровий потік імпульсів, що зчитуються системою для збору даних. Система, що ґрунтується на PC, збирає телеметричні дані від тварини. Хірургія: Індукували та підтримували загальну анестезію при використанні 5% Ізофлурану® у газі-носії при споживанні 0,5 л/хв. кисню та 1 л/хв. оксиду азоту для індукції анестезії, при цьому зменшували концентрацію Ізофлурану до 2% для підтримання анестезії. Підшкірно вводили 5мг/кг Карпрофену (ін'єкція Римадилу® для великих тварин, 50мг/мл, Pfizer Animal Health) при індукції анестезії, наприкінці дня проведення хірургічного втручання та вранці першого дня після хірургічного втручання для мінімізації болю та дискомфорту. Імплантація зонда в печеристі тіла: Виголювали ділянку шкіри в черевній області та поблизу черевної області для включення ділянки навколо статевого члену та мошонки. Очищали та дезінфікували виголенуділянку шкіри. Пацюка укладали на спину. Робили надріз по середній лінії від зовнішнього краю пеніса в напрямку хвоста приблизно на 2см. Досліджували внутрішню структуру пеніса та ідентифікували печеристі тіла. Проводили лапаротомію по середній лінії довжиною приблизно 4см до досягнення абдомінальної порожнини. Проколювали абдомінальну стінку за допомогою каудального надрізу за допомогою прийнятного троакара або канюлі, слідкуючи за тим, щоб не пошкодити внутрішні органи. Поміщали тіло імплантату в абдомінальну порожнину, орієнтували катетер каудально та вводили кінчик катетера через стінку за допомогою попередньо введеної канюлі. Використовуваний імплантат являв собою модель ТА11РА-С40, катетер розміром 8мМ із модифікованим кінчиком розміром 3 mm (Data Sciences International Inc.). Прикріплювали тіло імплантату до абдомінальної стінки, використовуючи нитки, що не розсмоктуються, і частково закриваючи абдомінальний надріз. Направляли кінчик пеніса краніально та відводили каудальний надріз для оптимізації хірургічного поля. Обережно ізолювали приблизно 10мМ внутрішньої структури пеніса від навколишніх тканин. Обережно відводили губчате тіло на одну сторону для забезпечення доступу до печеристого тіла. Досягали печеристого тіла, використовуючи модифікований надголковий катетер для проколювання оболонки. Вводили кінчик катетера за допомогою переміщення катетера та його просування до повного введення. Обережно видаляли катетер, який • забезпечує підхід, та застосовували прийнятний клей для тканин до сайту введення. Спостерігали, щоб не було підтікання. Закривали підшкірний жировий шар у каудальному надрізі перед закриттям за допомогою прийнятних ниток, що розсмоктуються. Поступово вводили приблизно 5мл теплого фізіологічного розчину через абдомінальний надріз та повністю закривали надріз по середній лінії. Зашивали шкірний надріз за допомогою ниток, що розсмоктуються. Післяопераційний догляд: Слідкували за щоденним споживанням їжі та води, а також стежили за вагою тіла протягом приблизно 7 днів після хірургічного втручання, а потім 2-3 рази в тиждень. Уводили Лектад® (Pfizer Animal Health) у воду для питва протягом 3 днів після хірургії. Розміщали пацюків окремо та поміщали їх в умови зміни світла і темряви через 5 днів після хірургічного втручання. Викликали ветеринара (або обслуговуючий персонал) для одержання сертифіката відповідності умов утримання протягом наступних 2 днів після здійснення хірургічного втручання. Експериментальне використання пацюків починали через 7 днів після хірургічного втручання. Експериментальна процедура: Проводили експеримент у кімнаті в умовах зміни світла і темряви. У день проведення експерименту поміщали пацюка в клітку з підстилкою для поглинання виділень (PhisioTei® моделі RPC-1, Data Sciences International Inc.) і залишали для акліматизації протягом приблизно однієї години. Пересвідчувалися, що пацюк має доступ до корму та питва за своїм бажанням. Проводили зчитування базової лінії внутрішньо кавернозного тиску (ІСР) протягом приблизно 5 хвилин. Переносили дані за допомогою дискети в Excel у розгорнуту таблицю. Сполуки вводили підшкірно або через катетер у яремну вену (JVC). Якщо використовували JVC, то пропускали стерильний фізіологічний розчин після дозування, а після цього використовували стопорний розчин, що містить фізіологічний розчин та глюкозу. Інтервал між введенням сполуки та вимірюванням ІСР буде варіювати в залежності від досліджуваної сполуки. Інтервал 30-60 хвилин після підшкірного введення є гарною орієнтиром. Досліджувані сполуки розчиняли в 50%-ному βциклодектрині у фізіологічному розчині. їх вводили в дозі 5-10мг/кг підшкірно (п.ш). Гемігідрат гідрохлориду апоморфіну (Sigma A-4393) у дозі 60мкг/кг п.ш. використовували як позитивний контроль, оскільки він має проеректильні властивості. Реєстрували ІСР протягом 15-хвилинного періоду, починаючи від 30 хвилини після ін'єкції, тобто в період від ЗО до 35 хвилини, і надалі повторювали двічі протягом 15-хвилинних періодів, починаючи на 60 хвилині після ін'єкції та на 120 хвилині після ін'єкції, відповідно. Реєстрували ІСР протягом 15 хвилин. Сигнал від підстилки, що поглинає виділення, подавали через Data Exchange Matrix® далі до системи програмного забезпечення (Dataquest ART® система для збору даних, Data Sciences International Inc.). Передавали дані за допомогою дискети в Excel для складання розгорнутої таблиці для аналізу. ПРИКЛАД В - Сполуки формули (І) у поєднанні з РОЕ5І для лікування MED Вплив введення сполук відповідно до даного винаходу в поєднанні з інгібітором PDE5 на внутрішньокавернозний тиск чоловічого статевого члена (ІСР) на моделі ерекції у анестезованих кроликів може бути виміряний у відповідності з наступним прописом. Експериментальний пропис Самців Ново-зеландських кроликів (вагою приблизно 2,5 кг) піддавали попередній медикації за допомогою комбінації Медетомідину (Домитор®) 0,5мл/кг внутрішньом'язово (в.м.) та Кетаміну (Веталар®) 0,25мл/кг внутрішньом'язово, підтримуючи надходження кисню за допомогою лицьової маски. Кроликів піддавали трахеотомії при використанні Портекс™ ендотрахеальної трубки без манжети 3ID (внутрішній діаметр), з'єднаної з вентилятором та підтримували вентиляцію на рівні 30-40 дихальних рухів за хвилину з приблизним об'ємом вдиху-видиху 18-20мл та максимальним тиском у повітряних шляхах 10см водного стовпа. Анестезію пізніше переключали на Ізофлуран® та продовжували вентиляцію за допомогою О2 при 2л/хв. У праву маргінальну вушну вену вводили канюлю при використанні катетера 23G або 24G, та перфузували лактатний розчин Рінгера при швидкості 0,5мл/хв. Анестезію у кроликів підтримували за допомогою 3% Ізофлурану під час інвазійної хірургії, поступово вводячи до концентрації 2% для підтримання анестезії. Вичленяли ліву яремну вену, ізолювали її, а потім вводили канюлю за допомогою PVC катетера (17 калібру/17 G) для інфузії лікарського засобу та досліджуваних сполук. Виголювали шерсть з лівої сторони пахової області та здійснювали вертикальний надріз довжиною приблизно 5см уздовж стегна. Стегнову вену та артерію вичленяли, ізолювали, а потім вводили канюлю за допомогою PVC катетера (17G) для інфузії лікарського засобу та сполук. Введення канюлі повторювали для стегнової артерії, вводячи катетер на глибину 10см для того, щоб переконатися, що катетер досяг абдомінальної аорти. Цей артеріальний катетер був зв'язаний із системою Gould для реєстрації тиску крові. Зразки для аналізу газів, що наявні у крові, також здійснювали за допомогою узяття крові через артеріальний катетер. Систолічний та діастолічний тиск вимірювали, а значення артеріального тиску підраховували при використанні формули (діастолічний тиск x 2 + систолічний тиск) -т-3. Серцевий ритм вимірювали за допомогою імпульсного оксиметру та системи програмного забезпечення даних збору даних Ро-пе-mah (Ponemah Physiology Platform, Gould Instrument Systems Inc.). Здійснювали надріз по черевній середній лінії у ділянку черевної порожнини. Надріз був довжиною приблизно 5см майже до лобка. Жировий шар та м'язи без гострих кутів розсікали для вивільнення підчеревного нерва, що спускається в черевну порожнину. Було істотним підтримувати закритою ділянку бічної сторони вигину стінки лобка для того, щоб уникнути пошкодження стегнової вени та артерії, що лежать вище лобка. Місце розташування сідничного та тазового нервів, що залягають глибше, визначали після наступного надрізу на спинній ділянці кролика. Коли було ідентифіковано сідничний нерв, легко знайти розміщення тазового нерва. Тазовий нерв вільно закріплювали; анатомічний атлас з цього приводу не дає достатньої інформації для ідентифікації нервів. Проте, стимуляція нерва спричинює збільшення тиску усередині печеристих тіл та потік крові через печеристі тіла, а також інервацію тазової ділянки. Тазовий нерв вичленяли з навколишніх тканин, та біполярний стимулювальний електрод Гарварда розміщували поблизу нерву. Нерв трохи підіймали для створення деякого тиску, а потім електрод був зафіксований у такому положенні. Приблизно 1мл легкого парафінового масла розміщували навколо нерва та електрода. Він діяв як захисний лубрикант для нерву та запобігав забрудненню електроду кров'ю. Електрод з'єднували з стимулятором Grass S88. Тазовий нерв піддавали стимуляції при використанні наступних параметрів: -5 В, тривалість імпульсу 0,5 мілісекунд, тривалість стимулу 20 секунд з частотою 16Гц. Відтворювані відповіді одержували, коли нерв стимулювали кожні 15-20 хвилин. Проводили декілька стимуляцій при використанні описаних вище параметрів для встановлення значення контрольної відповіді. Сполуки, які піддавали дослідженню, вводили шляхом інфузії через яремну вену, використовуючи | інфузійний насос Harvard 22, що дозволяє проводити тривалий 15-хвилинний цикл : стимуляції. Шкіру та тканини, що оточують статевий член, видаляли для вичленення статевого члену. Комплект для проведення катетеризації (Insyte-W, Becton-Dickinson 20 Gauge 1,1 x 48мМ) вводили через світлу оболонку з лівої сторони кавернозного простору та видаляли голку, залишаючи гнучкий катетер. Катетер з'єднували через перетворювач тиску (Ohmeda 5299-04) з системою Gouldдля реєстрації внутрішньо кавернозного тиску (ІСР). Як тільки було встановлено внутрішньокавернозний тиск, катетер закривали, використовуючи Vetbond (тканинний адгезив, ЗМ). Серцевий ритм вимірювали за допомогою імпульсного оксиметра та системи програмного забезпечення збору даних Ро-ne-mah (Ponemah Physiology Platform, Gould Instrument Systems Inc.). Потік крові через печеристі тіла реєстрували або як значення, одержане безпосередньо з пристрою для вимірювання потоку, використовуючи систему програмного забезпечення збору даних Po-ne-mah (Ponemah Physiology Platform, Gould Instrument Systems Inc.), або опосередковано з діаграмного пристрою-самописця. Калібрування проводили на початку експерименту (0-125мл/хв./100г тканини). Усі дані представляли як значення ± s.e.m. (стандартна похибка значення). Значні зміни були ідентифіковані при використанні t-аналізів Ст'юдента. Досліджувані сполуки розчиняли у 50% β-циклодекстрині у фізіологічному розчині. їх вводили у дозі 5-10мг/кг підшкірно (п.ш.). Використовуючи пропис, описаний у даній заявці вище, можна було продемонструвати корисні впливи на ІСР для поєднаного введення сполуки за даним винаходом (5-10г/кг п.ш) та селективного інгібітора PDE5 (3етил-5-{5-[4-етилпіперазино)сульфоніл-2-пропоксифеніл}-2-(2-піридилметил)-6,7-дигідро-2Нпіразоло[4,3]піримідин-7-он (що описаний у WO98/491066) (1мг/кг, в.в. (внутрішньовенно)). Ці дослідження дають змогу передбачити, що існує ряд клінічних переваг поєднаного введення інгібітора PDE5 та сполуки формули (І). Такі переваги включають підвищену ефективність та можливості для лікування MED підгруп, що не піддаються іншим MED-монотерапіям. ПРИКЛАД С -Лікування FSAD Агоністи серотонінового рецептора 5НТ2С потенціюють стимульоване тазовим нервом збільшення потоку крові у статевих органах самок на моделі статевого збудження кроликів, яких піддавали анестезії. Нормальне статеве збудження, що розвивається у відповідь, складається з ряду фізіологічних відповідей, які спостерігаються під час статевого збудження. Такі зміни, як, наприклад, наповнення кров'ю піхви, статевих губ та клітору, випливає зі збільшення потоку крові через статеві органи. Наповнення кров'ю веде до збільшення змащування піхви з причини витікання плазми, збільшення піддатливості (розслаблення гладенької мускулатури піхви) та підвищення чутливості піхви та клітору. Розлад статевого збудження особин жіночої статі (FSAD) є широко поширеним статевим розладом, що зачіпає до 40% жінок у період перед-, пери- та пост-менопаузи (±HRT). Первинним наслідком FSAD є зменшення потоку крові через статеві органи або опухання, що проявляється як відсутність змащування піхви та відсутність чутливості статевих органів, що забезпечує задоволення. Вторинні наслідки включають зменшене статеве бажання, біль під час статевих зносин та складності у досягненні оргазму. Найбільш загальна причина FSAD полягає у зменшеному потоці крові через статеві органи, що приводить до зменшеного наповнення кров'ю піхви, статевих губ та клітору (Berman, J., Goldstein, I., Werbin, Т. та ін. (1999а). Подвійне сліпе плацебо-контрольоване дослідження для оцінки впливу силденафілу на фізіологічні параметри статевої відповіді особи жіночої статі. J. Urol., 161, 805; Goldstein, I. & Berman, J.R. (1998). Васкулогенна статева дисфункція жінок: синдроми недостатності наповнення кров'ю піхви та клітору. Int. J. Impot. Res., 10, S84-S90; Park, К., Goldstein, I., Andry, C, та ін. (1997). Васкулогенні статеві дисфункції жінок: Гемодинамічна основа недостатнього наповнення кров'ю піхви та клітору. Int. J. Impotence Res., 9, 27-37; Werbin, Т., Salimpour, P., Berman, L, та ін. (1999). Вплив статевої стимуляції та віку на потік крові через статеві органи у жінок з статевою стимуляцією. J. Urol., 161, 688). Як пояснюється вище, даний винахід забезпечує засіб для відновлення або потенціювання нормального статевого збудження у жінок, що страждають на FSAD, шляхом підвищення потоку крові через статеві органи. Спосіб Самок Ново-зеландських кроликів (вагою приблизно 2,5кг) піддавали попередній обробці лікарськими засобами за допомогою комбінації Медетомідину (Домітор® 0,5мл/кг - внутрішньом'язово (в.м.), та Кетаміну (Веталар®) 0,25мл/кг, внутрішньом'язово, поки підтримували споживання кисню за допомогою лицьової маски. Кроликів піддавали трахеотомії при використанні Портекс™ ендотрахеальної трубки без манжети З ID (внутрішній діаметр), з'єднаної з вентилятором та підтримували вентиляцію на рівні 30-40 дихальних рухів за хвилину з приблизним об'ємом вдиху-видиху 18-20мл і максимальним тиском у повітряних шляхах 10см водного стовпа. Анестезію пізніше переключали на Ізофлуран® та продовжували вентиляцію за допомогою О2 при 2 л/хв. У праву маргінальну вушну вену вводили канюлю при використанні 23G або 24G катетера, та вводили перфузією лактатний розчин Рінгера при швидкості 0,5мл/хв. Анестезію у кроликів підтримували за допомогою 3% Ізофлурану® під час інвазійної хірургії, додаючи до концентрації 2% для підтримки анестезії. Виголювали шерсть з лівої сторони пахової області та здійснювали вертикальний надріз довжиною приблизно 5см уздовж стегна. Стегнову вену та артерію вивільняли, ізолювали, а потім вводили канюлю за допомогою PVC катетера (17G) для інфузії лікарського засобу та сполук. Введення канюлі повторювали для стегнової артерії, вводячи катетер на глибину 10см для того, щоб переконатися, що катетер досяг абдомінальної аорти. Цей артеріальний катетер був зв'язаний із системою Gould для реєстрації тиску крові. Зразки для аналізу газів, що наявні у крові, також здійснювали за допомогою узяття крові через артеріальний катетер. Систолічний та діастолічний тиск вимірювали, а значення артеріального тиску підраховували при використанні формули (діастолічний тиск χ 2 + систолічний тиск) -=-3. Серцевий ритм вимірювали за допомогою імпульсного оксиметру та системи програмного забезпечення збору даних Po-ne-mah (Ponemah Physiology Platform, Gould Instrument Systems Inc.). Здійснювали надріз по черевній середній лінії у ділянку черевної порожнини. Надріз був довжиною приблизно 5см майже до лобка. Жировий шар та м'язи без гострих кутів розсікали для вивільнення підчеревного нерва, що спускається в черевну порожнину. Було істотним підтримувати закритою область бічної сторони вигину стінки лобка для того, щоб уникнути пошкодження стегнової вени та артерії, що лежать вище лобка. Сідничний і тазовий нерви залягають глибше, їх місце розташування визначали після наступного надрізу на спинній ділянці кролика. Коли було ідентифіковано сідничний нерв, легко знайти розміщення тазового нерва. Тазовий нерв вільно закріплювали. Термін „тазовий нерв" трактується досить широко; анатомічний атлас з цього приводу є недостатнім для ідентифікації нервів. Проте стимуляція нерву спричинює збільшення потоку крові через піхву та клітор, а також підвищує інервацію тазової ділянки. Тазовий нерв вивільняли з навколишніх тканин та біполярний стимулювальний електрод Гарварда розміщували поблизу нерва. Нерв трохи підіймали для створення деякого тиску, потім електрод фіксували у такому положенні. Наносили приблизно 1мл легкого парафінового масла навкруги нерва та електрода. Воно діяло як захисний лубрикант для нерва та запобігало забрудненню електроду кров'ю. Електрод з'єднували з стимулятором Grass S88. Тазовий нерв піддавали стимуляції при використанні наступних параметрів: -5 В, тривалість імпульсу 0,5 мс, тривалість стимулу 20 секунд з частотою 16 Гц. Відтворювані відповіді одержували, коли нерв стимулювали кожні 15-20 хвилин. Криву частоти відповіді визначали на початку кожного експерименту для того, щоб визначити оптимальну частоту для використання як субмаксимальної відповіді, у нормі 4 Гц. Робили надріз по середній лінії черевної ділянки в каудальній області лобка, для вивільнення лобка. Видаляли навколишні тканини для вивільняли оболонки клітору, таким чином, щоб стінка була вільною від невеликих кровоносних судин. Зовнішню стінку піхви також вивільняли для відокремлення від навколишніх тканин. Один лазерний доплеровський датчик потоку вводили на 3см у піхву, так, щоб половина стрижня датчика перебувала у зоні видимості. Другий датчик розміщували так, щоб він знаходився безпосередньо вище зовнішньої стінки клітору. Положення цих датчиків потім коригували до одержання сигналу. Другий датчик розміщували безпосередньо
ДивитисяДодаткова інформація
Назва патенту англійською5-ht receptor ligands and their use
Назва патенту російськоюЛиганды 5-нт рецептора и их применение
МПК / Мітки
МПК: C07D 239/42, C07D 405/12, A61P 3/04, A61P 3/10, C07D 401/12, A61P 25/18, A61P 25/14, A61K 45/00, A61P 25/22, A61P 9/00, C07D 409/12, A61P 25/32, A61K 31/497, A61P 15/00, C07D 239/46, C07D 241/20, A61P 1/04, A61P 25/08, A61K 31/506, A61P 25/28, A61P 1/00, A61P 25/20, A61P 15/10, C07D 417/12, A61P 15/12, A61P 25/06, A61P 25/24, A61P 9/10, C07D 403/04, A61P 1/14, A61P 25/00, A61P 25/34, A61P 13/02, A61P 43/00
Мітки: рецептора, ліганди, 5-нт, використання
Код посилання
<a href="https://ua.patents.su/31-74443-ligandi-5-nt-receptora-ta-kh-vikoristannya.html" target="_blank" rel="follow" title="База патентів України">Ліганди 5-нт рецептора та їх використання</a>
Попередній патент: Емульсол для холодної обробки металів тиском
Наступний патент: Пристрій для сублімаційного нанесення декоративних покрить на металеві вироби
Випадковий патент: Спосіб ківшової обробки сталі