16-заміщені похідні 4-азаандростану, як інгібітори ізоферменту 5-a-редуктази, спосіб інгібування 5-a-редуктази та її ізоферменту, спосіб лікування, спосіб припинення та обернення андрогенної алопеції та стимулю
Номер патенту: 44257
Опубліковано: 15.02.2002
Автори: Толман Річард Л., Ланген Дерек вон, Хагманн Уільям К., Ланца Томас Дж. мол, Расмуссон Гарі Х., Сахоо Соуміа П., Дьюретте Філіппе Л.
Формула / Реферат
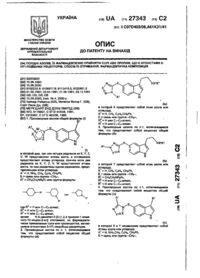
1. 16-Замещенные производные 4-азаандростана формулы 1:
или его фармацевтически приемлемая соль или сложный эфир, где:
С1-С2 углерод-углеродная связь может быть простой связью или двойной связью, обозначенной пунктирной линией,
R1 выбирают из группы, включающей водород и (С1-С10)алкил,
R2 выбирают из группы, включающей водород и (С1-С10)алкил,
один из R3 и R4 выбирают из группы, включающей водород и метил, а другой выбирают из группы, включающей:
(a) амино-группу,
(b) циано-группу,
(c) фтор,
e) гидроксильную группу,
(f) группу -C(О)NRbRc, где Rb и Rс независимо обозначают водород, (С1-С6)алкил, арил или арил(С1-С6)алкил, при этом алкильная часть может быть замещена от 1 до 3 следующими заместителями: галоген, (С1-С4)алкоксигруппа, или трифторметил, и арильная часть может быть замещена от 1 до 3 следующими заместителями: галоген, (С1-С4)алкил, (С1-С4)алкоксигруппа или трифторметил,
(g) (С1-С10)алкил-Х-, при условии, что Х не является -CH(Re)-,
(h) (С2-С10)алкенил-Х-, при условии, что Х не является -CH(Re)-,
где (С1-С10)алкил в
(g) и (С2-С10)алкенил в (h) могут быть не замещены или замещены от 1 до 3 следующими заместителями:
і) галоген, гидроксильная группа, циано-группа, нитро-группа, моно-, ди- или тригалогенметил, оксо-группа, гидрокси-сульфонильная группа, карбоксильная группа,
іі) гидрокси(С1-С6)алкил, (С1-С6)алкилокси-группа, (С1-С6)алкилтио группа, (С1-С6)алкилсульфонильная группа, (С1-С6)алкилоксикарбонильная группа, в которых (С1-С6)алкильная часть может быть дополнительно замещена от 1 до 3 следующими заместителями: галоген, (С1-С4)алкоксигруппа, или трифторметил,
ііі) арилтио-группа, арил, арилокси-группа, арилсульфонильная группа, арилоксикарбонильная группа, в которых арильная часть может быть дополнительно замещена от 1 до 3 следующими заместителями: галоген, (С1-С4)алкил, (С1-С4)алкокси-группа, или трифторметил,
iv) группы -C(О)NRbRc, -N(Rb)-C(О)-Rc, -NRbRc, где значения Rb и Rс указаны
выше,
(і) арил-Х-,
(j) гетероарил-Х-, где гетероарил является 5-, 6- или 7-членным гетероароматическим кольцом, содержащим по крайней мере один член, выбранный из группы, включающей:
один атом кислорода в кольце, один атом серы в кольце, от 1 до 4 атомов азота в кольце или их сочетание, при этом гетероароматическое кольцо может быть также сконденсировано с одним бензольным кольцом или гетероароматическим кольцом, где арил в (і) и гетероарил в (j) могут быть не замещены или замещены от 1 до 3 следующими заместителями:
v) галоген, гидроксильная группа, циано-группа, нитро-группа, моно-, ди- или тригалогенметил, моно-, ди- или тригалогенметокси-группа, (С2-С6)алкенил, (С3-С6)циклоалкил, формильная группа, гидросульфонильная группа, карбоксильная группа, уреидо-группа,
vi) (С1-С6)алкил, гидрокси(С1-С6)алкил, (С1-С6)алкилоксигруппа, (С1-С6)алкилокси(С1-С6)алкил, (С1-С6)алкилкарбонильная группа, (С1-С6)алкилсульфонильная группа, (С1-С6)алкилтиогруппа, (С1-С6)алкилсульфинильная группа, (С1-Сб)алкилсульфонамидогруппа, (С1-С6)алкиларилсульфонамидогруппа, (С1-С6)алкилоксикарбонильная группа, (С1 –С6)алкилоксикарбонил(С1-С6)алкил, RbRcN-C(О)(C1-С6)алкил, (С1-С6)алканоиламино(С1-С6)алкил, ароиламино(С1-С6)алкил, при этом (С1-С6)алкильный фрагмент может быть замещен от 1 до 3 следующими заместителями: галоген, (С1-С4)алкоксигруппа, или трифторметил,
уіі) арил, арилокси-группа, арилкарбонильная группа, арилтиогруппа, арилсульфонильная группа, арилсульфинильная группа, арилсульфонамидо-группа, арилоксикарбонильная группа, при этом арильная часть может быть замещена от 1 до 3 следующими заместителями: галоген, (С1-С4)алкил, (С1-С4)алкоксигруппа, или трифторметил,
viii) группы -C(О)NRbRc-, -О-C(О)-NRbRc, -N(Rb)-C(О)-Rc, -NRbRc, Rb-C(О)N(Rc)-, где значения Rb и Rс указаны выше в (f), и группа -N(Rb)-C(О)-ORg, где Rg обозначает (С1-С6)алкил или арил, где алкильная часть может быть замещена от 1 до 3 следующими заместителями: атом галогена, (С1-С4)алкоксигруппа, или трифторметил, а арильная часть может быть замещена от 1 до 3 следующими заместителями: галоген, (С1-С4)алкил, (С1-С4)алкоксигруппа, или трифторметил, группу -N(Rb)-C(О)NRcRd, где Rd обозначает атом водорода, (С1-С6)алкил и арил, в котором указанный (С1-С6)алкил и арил могут быть замещены, как это указано выше в (f) для Rb и Rс,
(іх) гетероцикл, представляющий собой 5-, 6- или 7-членное кольцо, содержащее по крайней мере один член, выбранный из группы, включающей: один атом кислорода в кольце, один атом серы в кольце, от 1 до 4 атома азота в кольце или их сочетание, где гетероцикл может быть ароматическим, ненасыщенным или насыщенным и гетероцикл может быть сконденсирован с бензольным
кольцом, и где гетероцикл может быть замещен от 1 до 3 заместителями, как указано выше в пп. v), vi), vii), viii), за исключением когда іх) гетероцикл, и
(k) R3 и R4 вместе могут обозначать карбонильный атом кислорода,
(I) R3 и R4 вместе могут обозначать группу =CH-Rg, где значение Rg указано в viii), где:
Х выбирают из группы, включающей:
-О-, -S(О)n-, -C(О)-, -CH(Re)-, -C(О)-О-*, -C(О)-N(Rе,)-*, -N(Re)-C(О)-*, -О-C(О)-N(Re)-
*, -N(Re)C(О)-N(Re)-: -O-CH(Rе)-*, -N(Re)-, где Re обозначает водород, (С1-С3)алкил, арил, арил(С1-С3)алкил или незамещенный или замещенный гетероарил, как указано ранее в (j), при этом звездочка (*) обозначает связь, которая присоединена в положении 16 структуры 1, a n равно 0,1 или 2.
2. Соединение по п. 1, где R1 обозначает водород или метил, и R2 обозначает водород или метил.
3. Соединение по п. 1, где гетероарил выбирают из незамещенного и замещенного:
пиридила, фурила, пиррила, тиенила, изотиазолила, имидазолила, бензимидазолила, тетразолила, пиразинила, пиримидинила, хинолила, изохинолила, хиназолила, бензофурила, изобензофурила, бензотиенила, пиразолила, индолила, изоиндолила, пуринила, карбазолила, изоксазолила, тиазолила, изотиазолила, оксазолила, бензтиазолила и бензоксазолила.
4. Соединение по п. 3, где указанный гетероарил может быть замещен одним или двумя заместителями.
5. Соединение по п. 1, где указанную гетероциклическую группу выбирают из незамещенного или замещенного: пиридила, фурила, пиррила, тиенила, изотиазолила, имидазолила, бензимидазолила, тетразолила, пиразинила, пиримидинила, хинолила, изохинолила, бензофурила, изобензофурила, бензотиенила, пиразолила, индолила, изоиндолила, пуринила, карбазолила, изоксазолила, тиазолила, оксазодила, бензтиазолила и бензоксазолила, и их дигидро-, тетрагидро-, гексагидро- и насыщенных производных.
6. Соединение по п. 5, где указанная гетероциклическая группа может быть замещена одним или двумя заместителями.
7. Соединение по п. 2, где один из заместителей R3 и R4 выбирают из группы, включающей водород или метил, а другой выбирают из группы, включающей:
(b) циано-группу,
(c) атом фтора,
(е) гидроксильную группу,
(g) (С1-С10)алкил-Х-, в котором алкил может быть замещен арилом, а арил, в свою очередь, может быть замещен 1-2 атомами галогена или (С1-С6)алкилом,при условии, что Х не является -ch(rе)-,
(h) (С2-С10)алкенил-Х-, при условии, что Х не является -CH(Re)-,
(і)арил-Х-,
(j) гетероарил-Х-, где гетероарил является 5- или 6-членным гетероароматическим кольцом, содержащим по 1 - 2 атома азота в кольце, где арил в (і) и гетероарил в (j) могут быть незамещенными или замещены от 1 до 2 следующими заместителями:
х) галоген, циано-группа, нитро-группа, тригалогенметил, тригалогенметокси-группа, (С1-С6)алкил, арил, (С1-С6)алкилсульфонил, (С1-С6)алкиларил-сульфонамино-группа,
хі) группы -NRbRc, Rb-C(О)-N(Rc)-, где Rb и Rс независимо обозначают атом водорода, (С1-С6)алкил, арил или арил(С1-С6)алкил, где алкильная часть может быть замещена от 1 до 3 следующими заместителями: галоген, (С1-С4)алкокси-группа, или трифторметил, а арильная часть может может быть замещена от 1 до 3 следующими заместителями: галоген, (С1-С4)алкил, (С1-С4)алкокси-группа, или трифторметил,
(хіі) гетероцикл, представляющий собой 5-членное ароматическое кольцо, содержащее один атом азота в кольце, или один атом кислорода и один атом азота в кольце,
(k) R3 и R4 вместе могут обозначать карбонильный атом кислорода, и где:
Х выбирают из группы, включающей:
-О-, -S(О)n-, -CH(Re)-, -C(О)-N(Re)-*, -О-C(О)-N(Rе)-*, где Rе обозначает атом водорода, (С1-С3)алкил, арил, арил(С1-С3)алкил, при этом звездочка (*) обозначает связь, присоединенную в положении 16 структуры I, a n равно 0 или 2.
8. Соединение по п. 1, выбранное из группы, включающей:
4-аза-4,7- -диметил--андростан-3,1 б-дион,
4-аза-4-метил--андростан-3,16-дион,
3-оксо-4-аза-4-метил-16- -(3-гидрокси--андростан,
3-оксо-4-аза-4-метил-16--(бензиламинокарбонилокси)- 5a-андростан,
3-оксо-4-аза-4-метил-16--бензоиламино--андростан,
3-оксо-4-аза-4-метил-16--метокси--андростан,
3-оксо-4-аза-4-метил-16--аллилокси--андростан,
3-оксо-4-аза-4-метил-16--(н-пропилокси)- -андростан,
3-оксо-4-аза-4-метил-16--гидрокси--андростан,
3-оксо-4-аза-4-метил-16--(фенокси)- -андростан,
3-оксо-4-аза-7--метил-16--(фенокси)- -андрост-1 -ен,
3-оксо-4-аза-4-метил--метокси--андростан,
3-оксо-4-аза-4-метил-16--(4-хлорфенокси)- -андростан,
3-оксо-4-аза-7--метил-16--(4-хлорфенокси)- -андрост-1 -ен,
3-оксо-4-аза-7--метил-16--(4-хлорфенокси)- -андростан,
3-оксо-4-аза-7--метил-16--(3-хлор-4-метилфенокси)- -андростан,
3-оксо-4-аза-7--метил-16--(4-метилфенокси)- -андростан,
3-оксо-4-аза-7--метил-16--(4-метилфенокси)- -андрост-1-ен,
3-оксо-4-аза-7--метил-16--[4-(1-пирролил)фенокси]- -андрост-1 -ен,
3-оксо-4-аза-4,7--диметил-16--гидрокси--андростан,
3-оксо-4-аза-4,7--диметил-16--метокси--андростан,
3-оксо-4-аза-4,7--диметил-16--аллилокси--андростан,
3-оксо-4-аза-4,7--диметил-16--(3,3-диметилалилокси)- -андростан,
3-оксо-4-аза-4,7--диметил-16--(н-пропилокси)- -андростан,
3-оксо-4-аза-4,7--диметил-16--(изопентокси)- -андростан,
3-оксо-4-аза-4,16--диметил-16--гидрокси--андростан,
3-оксо-4-аза-4,7--даметил-16--этилокси--андростан,
3-оксо-4-аза-4,7--диметил-16--бензилокси--андростан,
3-оксо-4-аза-4,7--диметил-16--гидрокси--андростан,
3-оксо-4-аза-4,7--диметил-16--метилтио--андростан,
3-оксо-4-аза-4,7--диметил-16--(н-пропилтио)- -андростан,
3-оксо-4-аза-4,7--диметил-16--фтор--андростан,
3-оксо-4-аза-4,7--диметил-16--циано--андростан,
3-оксо-4-аза-4,7--диметил-16--(1-гексил)- -андростан,
3-оксо-4-аза-4,7--диметил-16--(н-пропил)- -андростан,
3-оксо-4-аза-4,7--диметил-16--бензил--андростан,
3-оксо-4-аза-4,7--диметил-16--(4-хлорбензил)- -андростан,
3-оксо-4-аза-4,16-диметил-16--метокси--андростан,
3-оксо-4-аза-4,7--диметил-16--(4-цианофенокси)--андроетан,
3-оксо-4-аза-4,7--диметил-16--(3-цианофенокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--(4-нитрофенокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--( 1 -нафтилокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--хлор-4-метилфенокси)- -андростан,
3-оксо-4-аза-4,7--диметил-16--(4-метилфенокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--(трет-бутокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--(3-метил-1 -бутилокси)- -андростан,
3-оксо-4-аза-4,7--диметил-16--(н-пропилокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--(4-трифторметилфенокси)- -андростан,
3-оксо-4-аза-4,7--диметил-16--(4-трифторметоксифенокси)- -андростан,
3-оксо-4-аза-4,7--диметил-16--этилтио--андростан,
3-(жсо-4-аза-4,7--диметил-16--этилсульфонил--андростан,
3-оксо-4-аза-4,7--диметил-16--(4-метилсульфонилфенокси)- -андростан,
3-оксо-4-аза-4,7--диметил-16--[4-(4-толилсульфониламино)фенокси]- -андростан,
3-оксо-4-аза-4,7--диметил-16--(3-пиридилокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--[(4-фенил)фенокси]--андростан,
3-оксо-4-аза-4,7-диметил-16--(4-фторфенокси)--андростан,
3-оксо-4-аза-4,7-диметил-16--(2-пиразинилокси)--андростан,
3-оксо-4-аза-4,7-диметил-16--[4-(5-оксазолил)фенокси]- -андростан,
3-оксо-4-аза-4,7-диметил-16--(2-пиримидинилокси)--андростан,
3-оксо-4-аза-4,7-диметил-16--[4-( 1-пиррил)фенокси]--андростан,
3-оксо-4-аза-4,7-диметил-16--(4-аминофенокси)--андростан,
3-оксо-4-аза-4,7-диметил-16--(4-ацетиламинофенокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--(4-бензоиламинофенокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--(4-хлорфенокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--фенокси--андростан,
3-оксо-4-аза-4,7--диметил-16--(2-хлорфенокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--(3-хлорфенокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--(4-хлорфенокси)--андрост-1 -єн,
3-оксо-4-аза-4,7--диметил-16-(4-хлорбензилиден)--андростан,
3-оксо-4-аза-4,7--диметил-16-бензилиден--андростан,
3-оксо-4-аза-4,7--диметил-16-(4-метилбензилиден)--андростан,
3-оксо-4-аза-4,7--диметил-16-(4-хлорбензил)-5a-андростан,
3-оксо-4-аза-4,7--диметил-16-(4-метилбензил)-5a-андростан,
3-оксо-4-аза-4,7--диметил-16-(3-пиридилметил)--андростан,
3-оксо-4-аза-4,7--диметил--метансульфонил--андростан,
3-оксо-4-аза-4,7--диметил-16--тиофенокси--андростан,
3-оксо-4-аза-4,7--диметил-16--(4-хлортиофенокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--(4-фтортиофенокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--(4-метилтиофенокси)- -андростан,
3-оксо-4-аза-4,7--диметил-16--(4-метокситиофенокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--фенилсульфинил--андростан,
3-оксо-4-аза-4,7--диметил-16--фенилсульфонил--андростан,
3-оксо-4-аза-4,7-,-триметил-16--(4-трифторметилфенокси)--андростан,
3-оксо-4-аза-4,7-,-триметил-16--гидрокси--андростан,
3-оксо-4-аза-4,7-,-триметил-16--метокси--андростан,
и их фармацевтически приемлемые соли.
9. Соединение по п. 7, где С1-С2 углерод-углеродная связь является простой связью, R1 обозначает метил, R2 обозначает метил, R3 выбирают из незамещенной или замещенной арилокси-группы, а R4 обозначает водород.
10. Соединение по п. 1, выбранное из группы, включающей:
3-оксо-4-аза-4,7--диметил-16--(4-цианофенокси)- -андростан,
3-оксо-4-аза-4,7--диметил-16--(3-цианофенокси)- -андростан,
3-оксо-4-аза-4,7--диметил-16--(4-нитрофенокси)- -андростан,
3-оксо-4-аза-4,7--диметил-16--(1-нафтилокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--(3-хлор-4-метилфенокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--(4-метилфенокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--(4-трифторметилфенокси)- -андростан,
3-оксо-4-аза-4,7--диметил-16--(4-трифторметоксифенокси)- -андростан,
3-оксо-4-аза-4,7--диметил-16--(4-метилсульфонилфенокси)- -андростан,
3-оксо-4-аза-4,7--диметил-16--[4-(4-толилсульфониламино)фенокси]- -андростан,
3-оксо-4-аза-4,7--диметил-16--[(4-фенил)фенокси]--андростан,
3-оксо-4-аза-4,7--диметил-16--(4-фторфенокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--[4-(5-оксазолил)фенокси]--андростан,
3-оксо-4-аза-4,7--диметил-16--[4-(1-пиррил)фенокси]- -андростан,
3-оксо-4-аза-4,7--диметил-16--(4-аминофенокси)- -андростан,
3-оксо-4-аза-4,7--диметил-16--(4-ацетиламинофенокси)- -андростан,
3-оксо-4-аза-4,7--диметил-16--(4-бензоиламинофенокси)- -андростан,
3-оксо-4-аза-4,7--диметил-16--(4-хлорфенокси)- -андростан,
3-оксо-4-аза-4,7--диметил-16--фенокси--андростан,
3-оксо-4-аза-4,7--диметил-16--(2-хлорфенокси)--андростан,
3-оксо-4-аза-4,7--диметил-16--(3-хлорфенокси)- -андростан,
и их фармацевтически приемлемые соли.
11. Соединение 3-оксо-4-аза-4,7--диметил-16--(4-хлорфенокси)- -андростан или его фармацевтически приемлемая соль.
12. Способ ингибирования -редуктазы или ее изофермента, включающий введение млекопитающему, нуждающемуся в подобном ингибировании, терапевтически эффективного количества соединения по п. 1 или терапевтически эффективного количества соединения по п. 1 в сочетании с ингибитором -редуктазы 2.
13. Способ лечения угрей обыкновенных, андрогенной алопеции, избыточного оволосения у женщин, доброкачественной гиперплазии предстательной железы, простатита и лечения и/или предотвращения рака предстательной железы, включающий введение млекопитающему, нуждающемуся в подобном лечении, терапевтически эффективного количества соединения по п. 1 или терапевтически эффективного количества соединения по п. 1 в сочетании с ингибитором -редуктазы 2.
14. Способ по п. 13, где андрогенной алопецией является островковое облысение у мужчин.
15. Способ по п. 13, где ингибитором 5-a-редуктазы 2 является финастерид, эпристерид или туростерид.
16. Способ по п. 13, где указанным соединением по п. 1 является 3-оксо-4-аза-4,7--диметил-16--(4-хлорфенокси)--андростан или его фармацевтически приемлемая соль.
17. Способ по п. 13 для лечения состояния андрогенной алопеции, включающий введение млекопитающему нуждающемуся в подобном лечении, терапевтически эффективного количества соединения по п. 1 или терапевтически эффективного количества соединения по п. 1 в сочетании с ингибитором -редуктазы 2 и далее в сочетании с веществом, стимулирующим открытие мембранного калиевого канала.
18. Способ по п. 17, где веществом, стимулирующим открытие мембранного калиевого канала, является миноксидил или его фармацевтически приемлемая соль.
19. Способ по п. 13 для лечения угрей обыкновенных, включающий введение млекопитающему, нуждающемуся в подобном лечении, терапевтически эффективного количества соединения по п. 1 или терапевтически эффективного количества соединения по п. 1 в сочетании с ингибитором -редуктазы 2 и далее в сочетании с ретиноидом.
20. Способ по п. 19, где ретиноидом является третиноин, изотретиноин или его фармацевтически приемлемая соль.
21. Способ по п. 13 для лечения и/или предотвращения рака предстательной железы, включающий введение млекопитающему, нуждающемуся в подобном лечении, терапевтически эффективного количества соединения по п.1 или терапевтически эффективного количества соединения по п. 1 в сочетании с ингибитором 5-a-редуктазы 2 и далее в сочетании с антиандрогеном.
22. Способ по п. 21, где антиандроген выбирают из флутамида, спиронолактона, касодекса или их фармацевтически приемлемой соли.
23. Способ по п. 13 для лечения доброкачественной гиперплазии предстательной железы, включающий введение млекопитающему, нуждающемуся в подобном лечении, терапевтически эффективного количества соединения по п. 1 или терапевтически эффективного количества соединения по п. 1 в сочетании с ингибитором 5-a-редуктазы 2.
24. Способ по п. 23, где ингибитором -редуктазы 2 является финастерид, эпристерид, туростерид или их фармацевтически приемлемая соль.
25. Способ по п. 23 для лечения доброкачественной гиперплазии предстательной железы, включающий введение млекопитающему, нуждающемуся в подобном лечении, терапевтически эффективного количества соединения по п. 1 или терапевтически эффективного количества соединения по п. 1 в сочетании с ингибитором 5-а-редуктазы 2 и далее в сочетании с антагонистом а-1-рецептора.
26. Способ по п. 25, где антагонистом альфа-1 рецептора является теразозин.
27. Способ остановки и обращения андрогенной алопеции и стимулирования роста волос у млекопитающего, нуждающегося в подобном лечении, включающий введение указанному млекопитающему терапевтически эффективного количества соединения по п. 1 или терапевтически эффективного количества соединения по п. 1 в сочетании с ингибитором -редуктазы 2.
28. Способ ингибирования биосинтетической конверсии тестостерона в дигидротестостерон у млекопитающего, нуждающегося в подобном лечении, включающий введение указанному млекопитающему терапевтически эффективного количества соединения по п. 1 или терапевтически эффективного количества соединения по п. 1 в сочетании с ингибитором -редуктазы 2.
29. Фармацевтическая композиция, включающая фармацевтически приемлемый носитель и терапевтически эффективное количество соединения по п. 1.
30. Фармацевтическая композиция по п. 29, дополнительно включающая терапевтически эффективное количество ингибитора -редуктазы 2 или его фармацевтически приемлемой соли.
31. Фармацевтическая композиция по п. 30, где ингибитором -редуктазы 2 является финастерид, эпристерид, туростерид.
32. Фармацевтическая композиция по п. 29, где указанным соединением по п. 1 является 3-оксо-4-аза-4,7--диметил-16--(4-хлорфенокси)- -андростан или его фармацевтически приемлемая соль.
33. Фармацевтическая композиция по п. 29, которая дополнительно содержит терапевтически эффективное количество соединения, стимулирующего раскрытие мембранного калиевого канала, или его фармацевтически приемлемой соли.
34. Фармацевтическая композиция по п.33, где указанным соединением, стимулирующим раскрытие мембранного калиевого канала, является миноксидил или его фармацевтически приемлемая соль.
35. Фармацевтическая композиция по п. 33, которая дополнительно содержит фармацевтически приемлемый носитель, пригодный для местного назначения.
36. Фармацевтическая композиция по п.29, которая дополнительно содержит ретиноид или его фармацевтически приемлемую соль.
37. Фармацевтическая композиция по п. 36, указанным ретиноидом в которой является третиноин, изотретиноин или их фармацевтически приемлемая соль.
38. Фармацевтическая композиция по п. 29, которая дополнительно содержит антиандроген или его фармацевтически приемлемую соль.
39. Фармацевтическая композиция по п.38, указанным антиандрогеном в которой является флутамид, спироноланктон, касодекс или их фармацевтически приемлемая соль.
40. Соединение, представляющее собой 3-оксо-4-аза-7-метил-16--(4-метилфенокси--андрост-1-ен.
41. Соединение по п. 40 для получения лекарственного препарата, полезного для ингибирования -редуктазы или ее изозимов.
42. Соединение по п. 40 в сочетании с ингибитором -редуктазы 2 для получения лекарственного препарата, полезного для ингибирования -редуктазы или ее изозимов.
43. Соединение по п.40 в сочетании с финастеридом в качестве ингибитора -редуктазы 2 для получения лекарственного препарата, полезного для ингибирования -редуктазы или ее изозимов.
44. Соединение по п. 40 для получения лекарственного средства полезного для лечения угрей обыкновенных.
45. Соединение по п. 40 в сочетании с ингибитором -редуктазы 2 для лечения угрей обыкновенных.
46. Соединение по п. 40 в сочетании с финастеридом в качестве ингибитора -редуктазы 2 для лечения угрей обыкновенных у мужчин.
Текст
1 16-Замещенные производные 4азаандростана формулы \ Я3 или его фармацевтически приемлемая соль или сложный эфир, где С1-С2 углерод-углеродная связь может быть простой связью или двойной связью, обозначенной пунктирной линией, R1 выбирают из группы, включающей водород и (СгСю)алкил, R2 выбирают из группы, включающей водород и (СгСю)алкил, один из R3 и R4 выбирают из группы, включающей водород и метил, а другой выбирают из группы, включающей (a) амино-группу, (b) циано-группу, (c) фтор, е) гидроксильную группу, (f) группу -C(O)NRbRc, где Rb и Rc независимо обозначают водород, (С-і-Сб)алкил, арил или арил(Сг Сб)алкил, при этом алкильная часть может быть замещена от 1 до 3 следующими заместителями галоген, (СгС4)алкоксигруппа, или трифторметил, и арильная часть может быть замещена от 1 до 3 следующими заместителями галоген, (dС^алкил, (СгС^алкоксигруппа или трифторметил, (д) (СгСю)алкил-Х-, при условии, что X не является -CH(Re)-, (h) (С2-Сю)алкенил-Х-, при условии, что X не является -CH(Re)-, где (С1-С10)алкил в (д) и (С2-Сю)алкенил в (п) могут быть не замещены или замещены от 1 до 3 следующими заместителями і) галоген, гидроксильная группа, циано-группа, нитро-группа, моно-, ди- или тригалогенметил, оксо-группа, гидрокси-сульфонильная группа, карбоксильная группа, м) гидрокси(Сі-Сб)алкил, (Сі-Сє)алкилокси-группа, (Сі-Сє)алкилтио группа, (dСб)алкилсульфонильная группа, (dСб)алкилоксикарбонильная группа, в которых ( d Сб)алкильная часть может быть дополнительно замещена от 1 до 3 следующими заместителями галоген, (СгС4)алкоксигруппа, или трифторметил, їм) арилтио-группа, арил, арилокси-группа, арилсульфонильная группа, арилоксикарбонильная группа, в которых арильная часть может быть дополнительно замещена от 1 до 3 следующими заместителями галоген, (СгС4)алкил, (dС4)алкокси-группа, или трифторметил, iv) группы -C(O)NRbRc, -N(Rb)-C(O)-Rc, -NRbRc, где значения Rb и Rc указаны выше, (і) арил-Х-, {]) гетероарил-Х-, где гетероарил является 5-, 6или 7-членным гетероароматическим кольцом, содержащим по крайней мере один член, выбранный из группы, включающей один атом кислорода в кольце, один атом серы в кольце, от 1 до 4 атомов азота в кольце или их сочетание, при этом гетероа ром этическое кольцо может быть также сконденсировано с одним бензольным кольцом или гетероароматическим коль О 1 ю 44257 цом, где арил в (і) и гетероарил в Q) могут быть не Сз)алкил или незамещенный или замещенный замещены или замещены от 1 до 3 следующими гетероарил, как указано ранее в Q), при этом звеззаместителями дочка (*) обозначает связь, которая присоединена в положении 16 структуры 1, а п равно 0,1 или 2 v) галоген, гидроксильная группа, циано-группа, нитро-группа, моно-, ди- или тригалогенметил, 2 Соединение по п 1, где R1 обозначает водород моно-, ди- или тригалогенметокси-группа, (Сгили метил, и R2 обозначает водород или метил Сб)алкенил, (Сз-Сб)циклоалкил, формильная 3 Соединение по п 1, где гетероарил выбирают группа, гидросульфонильная группа, карбоксильиз незамещенного и замещенного ная группа, уреидо-группа, пиридила, фурила, пиррила, тиенила, изотиазолила, имидазолила, бензимидазолила, тетразолила, vi) (С-і-Сб)алкил, гидрокси(Сі-Сб)алкил, (dпиразинила, пиримидинила, хинолила, изохинолиСб)алкилоксигруппа, (Сі-Сб)алкилокси(Сг ла, хиназолила, бензофурила, изобензофурила, Сє)алкил, (Сі-Сб)ал кил карбонильная группа, ( d бензотиенила, пиразолила, индолила, изоиндолиСб)алкилсульфонильная группа, (dла, пуринила, карбазолила, изоксазолила, тиазоСб)алкилтиогруппа, (С-і-Сє)ал ки л сул ьфин ильная лила, изотиазолила, оксазолила, бензтиазолила и группа, (Сі-Сб)алкилсульфонамидогруппа, (С1бензоксазолила Сб)алкиларилсульфонамидогруппа, (dСб)алкилоксикарбонильная группа, (Сі 4 Соединение по п 3, где указанный гетероарил Сб)алкилокси карбон ил (Сі-Сб)ал кил, RbRcNможет быть замещен одним или двумя заместителями С(О)(Сі-Сє)алкил, (Сі-Сб)алканоиламино(Сг 5 Соединение по п 1, где указанную гетероциклиСє)алкил, ароилами но(Сі-Сє)алкил, при этом ческую группу выбирают из незамещенного или (С-і-Сб)алкильньій фрагмент может быть замещен замещенного пиридила, фурила, пиррила, тиениот 1 до 3 следующими заместителями галоген, ла, изотиазолила, имидазолила, бензимидазоли(СгС4)алкоксигруппа, или трифторметил, ла, тетразолила, пиразинила, пиримидинила, хиум) арил, арилокси-группа, арил карбонильная нолила, изохинолила, бензофурила, группа, арилтиогруппа, арилсульфонильная групизобензофурила, бензотиенила, пиразолила, инпа, арилсульфинильная группа, арилсульфонамидолила, изоиндолила, пуринила, карбазолила, до-группа, арилоксикарбонильная группа, при изоксазолила, тиазолила, оксазодила, бензтиазоэтом арильная часть может быть замещена от 1 лила и бензоксазолила, и их дигидро-, тетрагидродо 3 следующими заместителями галоген, ( d , гексагидро- и насыщенных производных С^алкил, (С-і-С^алкоксигруппа, или трифторме6 Соединение по п 5, где указанная гетероциклитил, ческая группа может быть замещена одним или VIM) группы -C(O)NRbRc-, -O-C(O)-NRbRc, -N(Rb)двумя заместителями C(O)-RC, -NRbRc, Rb-C(O)N(RC)-, где значения Rb и 7 Соединение по п 2, где один из заместителей Rc указаны выше в (f), и группа -N(Rb)-C(O)-ORg, R3 и R выбирают из группы, включающей водород где Rg обозначает (Сі-Сє)алкил или арил, где алили метил, а другой выбирают из группы, вклюкильная часть может быть замещена от 1 до 3 чающей следующими заместителями атом галогена, ( d (b) циано-группу, С4)алкоксигруппа, или трифторметил, а арильная (c) атом фтора, часть может быть замещена от 1 до 3 следующи(е) гидроксильную группу, ми заместителями галоген, (СгС4)алкил, ( d (д) (Сі-Сю)алкил-Х-, в котором алкил может быть С4)алкоксигруппа, или трифторметил, группу замещен арилом, а арил, в свою очередь, может N(Rb)-C(O)NRcRd, где Rd обозначает атом водоробыть замещен 1-2 атомами галогена или ( d да, (Сі-Сє)алкил и арил, в котором указанный ( d Сб)алкилом,при условии, что X не является Сб)алкил и арил могут быть замещены, как это CH(Re)-, указано выше в (f) для Rb и Rc, (h) (С2-Сю)алкенил-Х-, при условии, что X не яв(їх) гетероцикл, представляющий собой 5-, 6- или ляется -CH(Re)-, 7-членное кольцо, содержащее по крайней мере (і)арил-Х-, один член, выбранный из группы, включающей 0) гетероарил-Х-, где гетероарил является 5- или один атом кислорода в кольце, один атом серы в 6-членным гетероароматическим кольцом, содеркольце, от 1 до 4 атома азота в кольце или их сожащим по 1 - 2 атома азота в кольце, где арил в (і) четание, где гетероцикл может быть ароматичеи гетероарил в Q) могут быть незамещенными или ским, ненасыщенным или насыщенным и гетерозамещены от 1 до 2 следующими заместителями цикл может быть сконденсирован с бензольным х) галоген, циано-группа, нитро-группа, тригалокольцом, и где гетероцикл может быть замещен от генметил, тригалогенметокси-группа, (Сі-Сє)алкил, 1 до 3 заместителями, как указано выше в пп v), арил, (Сі-Сє)алкилсульфонил, (Сі-Сє)алкиларилvi), vii), VIM), за исключением когда їх) гетероцикл, и сульфонамино-группа, (k) R3 и R вместе могут обозначать карбонильный хі) группы -NRbRc, Rb-C(O)-N(Rc)-, где Rb и Rc незаатом кислорода, висимо обозначают атом водорода, (Сі-Сє)алкил, (I) R3 и R4 вместе могут обозначать группу =CH-Rg, арил или арил(Сі-Сє)алкил, где алкильная часть где значение Rg указано в VIM), где может быть замещена от 1 до 3 следующими заX выбирают из группы, включающей местителями галоген, (СгС4)алкокси-группа, или -О-, -S(O)n-, -C(O)-, -CH(Re)-, -С(О)-О-*, -С(О)трифторметил, а арильная часть может может N(Re,)-*, -N(Re)-C(O)-*, -O-C(O)-N(Re)быть замещена от 1 до 3 следующими заместите*, -N(Re)C(O)-N(Re)- -O-CH(Re)-*, -N(Re)-, где Re лями галоген, (Сі-С4)алкил, (Сі-С4)алкоксиобозначает водород, (Сі-Сз)алкил, арил, арил(Сг группа, или трифторметил, 5 44257 (хм) гетероцикл, представляющий собой 5-членное 3-оксо-4-аза-7- Р -метил-16- Р -[4-(1ароматическое кольцо, содержащее один атом азота в кольце, или один атом кислорода и один пирролил)фенокси]- J~OC -андрост-1 -ен, атом азота в кольце, (k) R3 и R4 вместе могут обозначать карбонильный 3-оксо-4-аза-4,7- Р -диметил-16- Р атом кислорода, и где J — ОС -андростан, X выбирают из группы, включающей -О-, -S(O)n-, -CH(Re)-, -C(O)-N(Re)-*, -O-C(O)-N(Re)3-оксо-4-аза-4,7- Р -диметил-16- Р *, где Re обозначает атом водорода, (Сі-Сз)алкил, J — ОС -андростан, арил, арил(Сі-Сз)алкил, при этом звездочка (*) обозначает связь, присоединенную в положении 3-оксо-4-аза-4,7- Р -диметил-16- Р 16 структуры I, a n равно 0 или 2 8 Соединение по п 1, выбранное из группы, J — ОС -андростан, включающей 3-оксо-4-аза-4,7- Р -диметил-16- Р -(3,34-аза-4,7- Р -диметил- - ^ -андростан-3,1 б> диметилалилокси)- J~OC -андростан, дион, 3-оксо-4-аза-4,7- Р -диметил-16- Р -(н 4-аза-4-метил- J~OC -андростан-3,16-д ион, 3-оксо-4-аза-4-метил-16- Р андростан, — OC. -(3-гидрокси пропилокси)- J~OC -андростан, 3-оксо-4-аза-4,7- Р -диметил-16-^ -диметил-16- Р -(изопентокси) 3-оксо-4-аза-4-метил-16- Р (бензиламинокарбонилокси)- 5а-андростан, J — ОС -андростан, 3-оксо-4-аза-4-метил-16- Р -бензоиламино- J — OC. андростан, .Р. гидрокси 3-оксо-4-аза-4,16- ^ -диметил-16J — ОС -андростан, -Р, 3-оксо-4-аза-4-метил-16- Р -метокси- J — OC. андростан, 3-оксо-4-аза-4,7- Р -даметил-іб-г 7 -этилокси 3-оксо-4-аза-4-метил-16- Р -аллилокси- J — OC. андростан, 3-оксо-4-аза-4,7- Р -/ диметил-16- Р -бензилокси 3-оксо-4-аза-4-метил-16- Р -(н-пропилокси)— OC. 3-оксо-4-аза-4-метил-16- Р - (фенокси)андростан, J — ОС -андростан, 3-оксо-4-аза-4,7- Р Ъ — ОС. 3-оксо-4-аза-7- Р -метил-16- Р - (фенокси)J — J — ОС -андростан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -гидрокси J — ОС -андростан, 3-оксо-4-аза-4-метил-16- Р - гидроксиандростан, J — ОС -андростан, -андрост-1 -ен, 3-оксо-4-аза-4-метил- 1 " ^ -метокси- — OC. андростан, Ь- г -метилтио J — ОС -андростан, 3-оксо-4-аза-4,7- Р -/ диметил-16- Р -(н-пропилтио)J — ОС -андростан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -фтор- J — OC. андростан, 3-оксо-4-аза-4-метил-16- Р -(4-хлорфенокси) 3-оксо-4-аза-4,7- Р андростан, 5-а -андростан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -(1-гексил) 3-оксо-4-аза-7- Р -метил-16 - Р -(4-хлорфенокси) J — ОС -андростан, J — -диметил-16- Р -(43-оксо-4-аза-4,7- Р 3-оксо-4-аза-7- Р -метил-16- Р -(4-метилфенокси) хлорбензил)- -1 ~& -андростан, J — ОС -андростан, 3-оксо-4-аза-4,16^ -диметил-16- Р -метокси 3-оксо-4-аза-7- Р -метил-16- Р -(4-метилфенокси) 5 — а.т -андростан, : J — ОС -андрост-1 -ен, 3-оксо-4-аза-4,7- Р -диметил-16- Р -(4 Q-P -циано- -' — ОС. Q-P -бензил 7 44257 8 цианофенокси)- J~OC -андроетан, пиримидинилокси)- J~OC -андроетан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -(3 3-оксо-4-аза-4,7 Р -диметил-16- Р -[4-( цианофенокси)- J~OC -андроетан, пиррил)фенокси]- J~OC -андроетан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -(4 3-оксо-4-аза-4,7 Р -диметил-16- Р -(4 нитрофенокси)- J~OC -андроетан, аминофенокси)- J~OC -андроетан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -( 1 3-оксо-4-аза-4,7 Р -диметил-16- Р -(4 1 нафтилокси)- J~OC -андроетан, ацетиламинофенокси)- J~OC -андроетан, 3-оксо-4-аза-4,7- " -диметил-16- Р -хлор-4 3-оксо-4-аза-4,7- Р -диметил-16- Р -(4 метилфенокси)- > — ct: бензоиламинофенокси)- J~OC -андроетан, -андроетан, 3-оксо-4-аза-4,7-" -диметил-16- Р -(4 3-оксо-4-аза-4,7- Р -диметил-16- Р -(4 метилфенокси)- Ь — С -андроетан, С хлорфенокси)- J~OC -андроетан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -(трет 3-оксо-4-аза-4,7- Р -диметил-16- Р -фенокси бутокси)- J~OC -андроетан, J — ОС -андроетан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -(З-метил-1 3-оксо-4-аза-4,7- Р -диметил-16- Р -(2 бутилокси)- - ~& -андроетан, > хлорфенокси)- J~OC -андроетан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -(н 3-оксо-4-аза-4,7- Р -диметил-16- Р -(3 пропилокси)- J~OC -андроетан, хлорфенокси)- J~OC -андроетан, 3-оксо-4-аза-4,7-" -диметил-16- Р -(4 3-оксо-4-аза-4,7- Р -диметил-16- Р -(4 трифторметилфенокси) — СС -андроетан, хлорфенокси)--^— й: -андрост-1 -єн, 3-оксо-4-аза-4,7- Р -диметил-16-(4 3-оксо-4-аза-4,7- Р - -диметил-16- Р -(4- Р -( трифторметоксифенокси) — СС -андроетан, хлорбензилиден)- J~OC -андроетан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -этилтио-Р-Р 3-оксо-4-аза-4,7- Р -диметил-16-бензилиден J — ОС -андроетан, J — ОС -андроетан, 3-(жсо-4-аза-4,7- Р -диметил-16- Р 3-оксо-4-аза-4,7- Р -диметил-16-(4 этилсульфонил- Ь — С -андроетан, С метилбензилиден)- J~OC -андроетан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -(4 3-оксо-4-аза-4,7- Р -диметил-16-(4-хлорбензил)5а-андростан, метилсульфонилфенокси) — СС -андроетан, 3-оксо-4-аза-4,7- Р - -диметил-16- Р -[4-(4- Р -[ толилсульфониламино)фенокси]андроетан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -(3пиридилокси)- Ь — С -андроетан, С 3-оксо-4-аза-4,7- Р -диметил-16- Р -[(4фенил)фенокси]- Ь — С -андроетан, С 3-оксо-4-аза-4,7 Р -диметил-16- Р -(4фторфенокси)- Ь — С -андроетан, С 3-оксо-4-аза-4,7 Р -диметил-16- Р -(2пиразинилокси)- Ь — С -андроетан, С 3-оксо-4-аза-4,7 Р -диметил-16- Р -[4-(5оксазолил)фенокси] — СС -андроетан, 3-оксо-4-аза-4,7 Р -диметил-16- Р -(2- Р -( 5-а. 3-оксо-4-аза-4,7- Р -диметил-16-(4-метилбензил)5а-андростан, 3-оксо-4-аза-4,7- Р -диметил-16-(3пиридилметил)- J~OC -андроетан, 3-оксо-4-аза-4,7- Р -диметил-^"^метансульфонил- J~OC -андроетан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -тиофеноксиJ — ОС -андроетан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -(4хлортиофенокси)- J~OC -андроетан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -(4фтортиофенокси)- J~OC -андроетан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -(4метилтиофенокси)- -1 ~& -андроетан, 44257 10 3-оксо-4-аза-4,7- Р -диметил-16- Р - (4 фторфенокси)- J~OC -андростан, метокситиофенокси)--^ "^-андростан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -[4-(5 3-оксо-4-аза-4,7- Р -диметил-16- Р оксазолил)фенокси]- J~OC -андростан, фенилсульфинил- — СС -андростан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -[4-(1 3-оксо-4-аза-4,7- Р - -диметил-16- Р пиррил)фенокси]- - ~& -андростан, > фенилсульфонил- Ь — С -андростан, С 3-оксо-4-аза-4,7- Р -диметил-16- Р -(4 - Р -(4 3-оксо-4-аза-4,7- Р , іоСС трифторметилфенокси)--^ ~ -андростан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -(4 -андростан, 3-оксо-4-аза-4,7- Р 1 аминофенокси)- - ~^ ацетиламинофенокси)- Ь — С -андростан, С б- Р гидрокси- — СС -андростан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -(4бензоиламинофенокси)- Ь — С -андростан, С -Р 3-оксо-4-аза-4,7 - Р метокси- Ь — ССС -андростан, — Си их фармацевтически приемлемые соли 9 Соединение по п 7, где С1-С2 углеродуглеродная связь является простой связью, R1 обозначает метил, R2 обозначает метил, R3 выбирают из незамещенной или замещенной арилоксигруппы, a R4 обозначает водород 10 Соединение по п 1, выбранное из группы, включающей 3-оксо-4-аза-4,7- Р -диметил-161 — ct: хлорфенокси)- -(4 -андростан, 3-оксо-4-аза-4,7- " -диметил-16- Р диметил-16-^ -феноксиJ — ОС -андростан, 3-оксо-4-аза-4,7- Р -диметил-16хлорфенокси)- J~OC -андростан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -(4 3-оксо-4-аза-4,7- Р -диметил-16 цианофенокси)- - ~& -андростан, > хлорфенокси)-. 5 - ^-андростан, и их фармацевтически приемлемые соли 3-оксо-4-аза-4,7- Р -диметил-16- Р -(3 11 цианофенокси)- - ~& -андростан, > -андростан, 3-оксо-4-аза-4,7- Р -диметил-16- Р -диметил-16- -(1нафтилокси) — СС андростан, 3-оксо-4-аза-4,7 -диметил-16-" -(З-хлор-4 метилфенокси)- Ь ~& -андростан, 3-оксо-4-аза-4,7 -диметил-16- Р -(4 метилфенокси)- Ь ~& -андростан, 3-оксо-4-аза-4,7 -диметил-16- Р -(4 трифторметилфенокси) — СС андростан, 3-оксо-4-аза-4,7-" -диметил-16-" -(4трифторметоксифенокси) — СС андростан, 3-оксо-4-аза-4,7-" -диметил-16-" -(4метилсульфонилфенокси) — СС андростан, 3-оксо-4-аза-4,7- Р -/ .[4.(4 толилсульфониламино)фенокси]андростан, 3-оксо-4-аза-4,7-" -диметил-16-" -[(4фенил)фенокси] — СС андростан, 3-оксо-4-аза-4,7-" -диметил-16-" -(4 Соединение 3-оксо-4-аза-4,7- Р -диметил-16 Р -(4-хлорфенокси)- J — OC -андростан фармацевтически приемлемая соль 3-оксо-4-аза-4,7- Р -диметил-16- Р -(4нитрофенокси)--^ ~& -(3 1 Ъ — а. или его 12 Способ ингибирования -^ ~ ^-редуктазы или ее изофермента, включающий введение млекопитающему, нуждающемуся в подобном ингибировании, терапевтически эффективного количества соединения по п 1 или терапевтически эффективного количества соединения по п 1 в сочетании с ингибитором J~OC -редуктазы 2 13 Способ лечения угрей обыкновенных, андрогенной алопеции, избыточного оволосения у женщин, доброкачественной гиперплазии предстательной железы, простатита и лечения и/или предотвращения рака предстательной железы, включающий введение млекопитающему, нуждающемуся в подобном лечении, терапевтически эффективного количества соединения по п 1 или терапевтически эффективного количества соединения по п 1 в сочетании с ингибитором J~OC. редуктазы 2 14 Способ по п 13, где андрогенной алопецией является островковое облысение у мужчин 15 Способ по п 13, где ингибитором 5-аредуктазы 2 является финастерид, эпристерид или туростерид 16 Способ по п 13, где указанным соединением по п 1 является 3-оксо-4-аза-4,7- Р -/ -диметил-16 Р - (4-хлорфенокси)- — СС -андростан фармацевтически приемлемая соль или его 44257 12 11 17 Способ по п 13 для лечения состояния андротивного количества соединения по п 1 в сочетагенной алопеции, включающий введение млекопинии с ингибитором Ь — С -редуктазы 2 С тающему нуждающемуся в подобном лечении, 28 Способ ингибирования биосинтетической контерапевтически эффективного количества соедиверсии тестостерона в дигидротестостерон у мленения по п 1 или терапевтически эффективного копитающего, нуждающегося в подобном лечении, количества соединения по п 1 в сочетании с ингибитором J~OC -редуктазы 2 и далее в сочетании с включающий введение указанному млекопитаювеществом, стимулирующим открытие мембранщему терапевтически эффективного количества ного калиевого канала соединения по п 1 или терапевтически эффективного количества соединения по п 1 в сочета18 Способ по п 17, где веществом, стимулируюнии с ингибитором Ь — С -редуктазы 2 С щим открытие мембранного калиевого канала, 29 Фармацевтическая композиция, включающая является миноксидил или его фармацевтически фармацевтически приемлемый носитель и тераприемлемая соль певтически эффективное количество соединения 19 Способ по п 13 для лечения угрей обыкновенпо п 1 ных, включающий введение млекопитающему, 30 Фармацевтическая композиция по п 29, донуждающемуся в подобном лечении, терапевтически эффективного количества соединения по п полнительно включающая терапевтически эффек1 или терапевтически эффективного количества тивное количество ингибитора - ~ ^-редуктазы 2 > соединения по п 1 в сочетании с ингибитором или его фармацевтически приемлемой соли J — ОС -редуктазы 2 и далее в сочетании с рети31 Фармацевтическая композиция по п 30, где ноидом ингибитором - ~ ^-редуктазы 2 является фина> 20 Способ по п 19, где ретиноидом является трестерид, эпристерид,туростерид тиноин, изотретиноин или его фармацевтически 32 Фармацевтическая композиция по п 29, где приемлемая соль указанным соединением по п 1 является З-оксо-421 Способ по п 13 для лечения и/или предотврааза-4,7- Р -диметил-16- Р -(4-хлорфенокси)щения рака предстательной железы, включающий введение млекопитающему, нуждающемуся в поJ — С£-андростан или его фармацевтически придобном лечении, терапевтически эффективного емлемая соль количества соединения по п 1 или терапевтически 33 Фармацевтическая композиция по п 29, котоэффективного количества соединения по п 1 в рая дополнительно содержит терапевтически эфсочетании с ингибитором 5-а-редуктазы 2 и далее фективное количество соединения, стимулируюв сочетании с антиандрогеном щего раскрытие мембранного калиевого канала, 22 Способ по п 21, где антиандроген выбирают или его фармацевтически приемлемой соли из флутамида, спиронолактона, касодекса или их 34 Фармацевтическая композиция по п 33, где фармацевтически приемлемой соли указанным соединением, стимулирующим раскры23 Способ по п 13 для лечения доброкачествентие мембранного калиевого канала, является миной гиперплазии предстательной железы, вклюноксидил или его фармацевтически приемлемая чающий введение млекопитающему, нуждающесоль муся в подобном лечении, терапевтически 35 Фармацевтическая композиция по п 33, котоэффективного количества соединения по п 1 или рая дополнительно содержит фармацевтически терапевтически эффективного количества соедиприемлемый носитель, пригодный для местного нения по п 1 в сочетании с ингибитором 5-аназначения редуктазы 2 36 Фармацевтическая композиция по п 29, которая дополнительно содержит ретиноид или его 24 Способ по п 23, где ингибитором J — OC. фармацевтически приемлемую соль редуктазы 2 является финастерид, эпристерид, 37 Фармацевтическая композиция по п 36, укатуростерид или их фармацевтически приемлемая занным ретиноидом в которой является третиносоль ин, изотретиноин или их фармацевтически прием25 Способ по п 23 для лечения доброкачественлемая соль ной гиперплазии предстательной железы, вклю38 Фармацевтическая композиция по п 29, коточающий введение млекопитающему, нуждающерая дополнительно содержит антиандроген или муся в подобном лечении, терапевтически его фармацевтически приемлемую соль эффективного количества соединения по п 1 или 39 Фармацевтическая композиция по п 38, укатерапевтически эффективного количества соедизанным антиандрогеном в которой является флунения по п 1 в сочетании с ингибитором 5-атамид, спироноланктон, касодекс или их фармаредуктазы 2 и далее в сочетании с антагонистом цевтически приемлемая соль а-1 -рецептора 40 Соединение, представляющее собой З-оксо-426 Способ по п 25, где антагонистом альфа-1 рецептора является теразозин аза-7 Р -метил-16- Р -(4-метилфенокси- J~Oi 27 Способ остановки и обращения андрогенной андрост-1-ен алопеции и стимулирования роста волос у млеко41 Соединение по п 40 для получения лекарстпитающего, нуждающегося в подобном лечении, венного препарата, полезного для ингибирования включающий введение указанному млекопитающему терапевтически эффективного количества Ъ — СС -редуктазы или ее изозимов соединения по п 1 или терапевтически эффек42 Соединение по п 40 в сочетании с ингибито 13 44257 14 венного средства полезного для лечения угрей ром - ~ ^ -редуктазы 2 для получения лекарст> ~ обыкновенных венного препарата, полезного для ингибирования 45 Соединение по п 40 в сочетании с ингибитоЪ — СС -редуктазы или ее изозимов ром - ~ ^-редуктазы 2 для лечения угрей обык> 43 Соединение по п 40 в сочетании с финастериновенных дом в качестве ингибитора - — С -редуктазы 2 > £ 46 Соединение по п 40 в сочетании с финастедля получения лекарственного препарата, полезридом в качестве ингибитора - ~ ^-редуктазы 2 > ного для ингибирования - ~ ^-редуктазы или ее > для лечения угрей обыкновенных у мужчин изозимов 44 Соединение по п 40 для получения лекарст Настоящее изобретение относится к новым соединениям, новым композициям, методам их использования и способам получения, причем данные соединения в общем случае фармакологически полезны в качестве терапевтических средств, механизм действия которых основан на селективном ингибировании изофермента 5-аредуктазы 1 Определенные нежелательные проявления, такие как угри обыкновенные, себорея, избыточное оволосение у женщин, андрогенетическая алопеция, которая включает островковое облысение у женщин и мужчин, и доброкачественная гиперплазия предстательной железы, являются результатом гиперандрогеновой стимуляции, вызванной избыточным накоплением в метаболической системе тестостерона или аналогичного андрогенового гормона Ранние попытки получить химиотерапевтическое средство против нежелательных последствий гиперандрогенности привели к открытию нескольких стероидных антиандрогенов, обладающих нежелательной собственной гормональной активностью Например, эстрогены не только противодействуют влиянию андрогенов, но оказывают также феминизирующее воздействие Были также разработаны нестероидные антиандрогены, например, 4'-нитро-3'трифторметил-изобутиранилид См Nen at al , Endocrmol 19722, 91 (2) Однако эти вещества, хотя они и не обладают гормональным воздействием, конкурируют с природными андрогенами за рецепторные места, а потому имеют тенденцию вызывать появление вторичных женских половых признаков у мужчин или эмбрионов мужского пола в женской утробе и/или вызывают обратную реакцию, которая приводит к гиперстимуляции тестов Основным медиатором активности андрогенов в некоторых поражаемых органах, в частности, предстательной железы, является 5-а-дигидротестостерон, который локально образуется в поражаемом органе под действием тестостерон-5-аредуктазы (или просто 5-а-редуктазы) Ингибиторы 5-а-редуктазы служат для предотвращения или ослабления симптомов гиперандрогеновой стимуляции в указанных органах См , в частности Патенты США 4377584 (опубликован 22 марта 1983) и 4760071 (опубликован 26 июля 1988), полученные фирмой "Merck & Со , Inc " Известно, что существует второй изофермент 5-а-редуктазы, который взаимодействует с тканями кожи, в частности, волосистой частью кожи головы См , в частности, G Harris et al , Proc Natl Acad Sci USA, Vol 89, pp 10787-10791 (Nov 1992) Изофермент, который взаимодействует с тканями кожи, для удобства обозначают как 5-а-редуктаза 1 (или 5-аредуктаза типа 1), а изофермент, который взаимодействует главным образом с тканями предстательной железы, обозначают как 5-а-редуктаза 2 (или 5-а-редуктаза типа 2) При лечении чувствительных к андрогенам болезненных состояний, в частности, доброкачественной гиперплазии предстательной железы и/или предотвращения и лечения рака предстательной железы желательно использовать одну лекарственную единицу, которая активна по отношению к обоим изоферментам в предстательной железе, с тем чтобы значительно подавить воспроизводство дигидротестостерона Желательно также иметь еще одну лекарственную единицу, которая обладает высокой селективностью при ингибировании изофермента 5-аредуктазы 1, связанного с волосистой частью кожи головы, и использовать ее при лечении заболеваний кожи и волосистой части кожи головы, в частности, угрей обыкновенных, островкового облысения у мужчин и избыточного оволосения у женщин, кроме того, селективный ингибитор 5-аредуктазы 1 мог бы использоваться в сочетании с ингибитором 5-а-редуктазы 2, например, финастеридом (торговое название PROCAR) для терапевтического лечения гиперандрогеновых состояний, таких как доброкачественная гиперплазия предстательной железы, и/или предотвращения или лечения рака предстательной железы и при лечении заболеваний кожи и волосистой части кожи головы, таких как угри обыкновенные, себорея, избыточное оволосение у женщин и андрогеновая алопеция Далее, ингибиторы 5-а-редуктазы 1 по настоящему изобретению могли бы использоваться в сочетании со средствами, вызывающими раскрытие мембранных калиевых каналов, таких как миноксидил, при лечении указанных состояний кожи и волосистой части кожи головы Таким образом, предметом изобретения являются соединения, которые обладают достаточной активностью при ингибировании изофермента 5-аредуктазы 1 Новые соединения настоящего изобретения 15 имеют формулу и являются селективными ингибиторами 5-аредуктазы 1 Целью настоящего изобретения являются соединения, которые самостоятельна или в сочетании с ингибиторами 5-а-редуктазы 2 полезны для лечения доброкачественной гиперплазии предстательной железы, простатита, и/или для предотвращения ига лечения рака предстательной железы Еще одной целью настоящего изобретения являются соединения, кото рые самостоятельно или в сочетании с ингибиторами 5а-редуктазы 1 полезны для лечения угрей обыкновенных, избыточного оволосение , женщин, андрогеновой алопеции (известной также как андрогенетическая алопеция или островковое облысение у мужчин) и недостаточное содержания в плазме крови липопротеинов высокой плотности, соединения по настоящему изобретению находят применение для достижение одной или большего количества указанных целей Новые соединения по настоящему изобретению имеют структурную формулу 1 или представляют собой фармацевтические приемлемую соль или сложный эфир, где C1Q-C2 углерод-углеродная связь может быть простой связью или двойной связью, обозначенной пунктирной линией, R1 выбирают из группы, включающей атом водорода и (С-і-С-іо) алкил, R выбирают из группы, включающей атом водорода и (C-i-C-io) алкил, один из R1 и R2 выбирают из группы, включающей атом водорода или метил, а другой выбирают из группы, включающей (a) амино-группу, (b) циано-группу, (c) фтор, (d) метил, (e) гидроксильную группу, 44257 16 (f) группу -C(O)NRbRc, где Rb и Rc независимо обозначают атом водорода, (Сі-Сє)алкил, арил или арил((Сі-Сє)алкил, при этом алкильная часть может иметь от 1 до 3 следующих заместителей галоген, (С-і-С^алкокси-группа, или трифторметил, а арильная часть может иметь от 1 до 3 следующих заместителей галоген, (СгС^алкил, ( d С^алкокси-группа, или трифторметил, (д) (Сі-Сю)алкил-Х-, (h) (С2-Сю)алкенил-Х-, где (С-і-Сю)алкил в (g) и (С2-Сю)алкенил в (h) могут быть замещены или незамещены от 1 до 3 следующими заместителями і) галоген, гидроксильная группа, цианогруппа, нитро-группа , моно-, ди- или тригалогенметил, оксо-группа, гид рокси-сульфон ильная группа, карбоксильная группа, м) гидрокси(Сі-Сб)алкил, (СгСб)алкилоксигруппа, (С-і-Сб)алкилтио группа, (dСб)алкилсульфон ильная группа, (dСб)алкокси карбон ильная группа, в которых ( d Сб)алкильный фрагмент может быть дополнительно замещен от 1 до 3 следующими заместителями галоген, (СгС4)алкоксигруппа, или трифторметил, їм) арилтио-группа, арил, арилокси-группа, арилсульфониль-ная группа, арилоксикарбонильная группа, в которых арильный фрагмент может быть дополнительно замещен от 1 до 3 следующими заместителями галоген, (СгС4)алкил, ( d С4)алкокси-группа, или трифторметил, iv) группы -C(O)NRbRc, -N(Rb)-C(O)- Rc, -NRbRc, где значения Rb и Rc указаны ранее, (і) арил-Х-, (j) гетероарил-Х-, где гетероарил является 5-, 6- или 7-членным гетероароматическим кольцом, содержащим по крайней мере один член, выбранный из группы, включающей один атом кислорода в кольце, один атом серы в кольце, 1-4 атома азота в кольце или их сочетание, при этом гетероароматическое кольцо может быть также сконденсировано с одним бензольным кольцом или гетероароматическим кольцом, где арил в (і) и гетероарил в Q) могут быть не замещены или замещены от 1 до 3 следующими заместителями v) галоген, гидроксильная группа, цианогруппа, нитро-группа, моно-, ди- или тригалогенметил, моно-, ди- или тригалогенметокси-группа, (С2-Сб)алкенил, (Сз-Сб)циклоалкил, формильная группа, гидросульфонильная группа, карбоксильная группа, уреидо-группа, vi) (С-і-Сб)алкил, гидрокси(Сі-Сє)алкил, ( d Сб)алкилокси-группа, (Сі-Сб))алкилокси(Сг Сє)алкил, (С-і-Сб)ал кил карбонильная группа, ( d Сб)алкилсульфонильная группа , (Сі-Сє)алкилтиогруппа, (С-і-Сб)алкилсульфинильная группа, ( d Сб)алкилсульфонамидо-группа, (dСб)алкиларилсульфонамидо-группа, (dСб)алкилоксикарбонильная группа, (dСб)алкилокси карбон ил (Сі-Сб)ал кил, RbRcNС(О)(Сі-Сє)алкил, (Сі-Сб)алканоиламино(Сг Сє)алкил, ароиламино(Сі-Сб)алкил, при этом ( d Сб)алкильный фрагмент может быть замещен от 1 до 3 следующими заместителями галоген, ( d С4)алкокси-группа, или трифторметил, VII) арил, арилокси-группа, арилкарбонильная 44257 18 17 группа, арил-тио-группа, ари лсульфон ильная (h) (С2-Сю)алкенил-Х-, группа, арилсульфинильная группа, арилсульфо(і) арил-Х-, намидо-группа, арилоксикарбонильная группа, при j) гетероарил-Х-, где гетероарил является 5этом арильная часть может быть замещена от 1 или 6-членным гетероароматическим кольцом, до 3 следующими заместителями галоген, ( d содержащим по 1-2 атома азота в кольце, где С^алкил, (СгС^алкокси-группа, или трифтормеарил в (і) и гетероарил в Q) могут быть незаметил, щенными или замещены от 1 до 2 следующими заместителями VIM) группы -C(O)NRbRc, -O-C(O)-NRbRc, -N(Rb)х) галоген, циано-группа, нитро-группа, тригаC(O)-RC, -NRbRc, Rb-C(O)N(RC)-, где значения Rb и логенметил, тригалогенметокси-группа, или тригаRc указаны ранее в (f), и группа -N(Rt,)-C(O)-ORg, логенметокси-группа, (Сі-Сє)алкил, арил, ( d где Rg обозначает (Сі-Сє)алкил или арил, при этом Сб)алкилсульфонил, (Сі-Сє)алкиларилалкильная часть может быть замещена от 1 до 3 следующими заместителями атом галогена, ( d сульфонамино-группа, С4))алкокси-группа, или трифторметил, а арильXI) группы -NRbRc, Rb-C(O)-N(Rc)-, где Rb и Rc ная часть может быть замещена от 1 до 3 сленезависимо обозначают атом водорода, ( d дующими заместителями галоген, (СгС^алкил, Сб)алкил, арил или арил(Сі-Сє)алкил, при этом (Сі-С4)алкокси-группа, или трифторметил, группу алкильная группа может быть замещена от 1 до 3 -N(Rb)-C(O)NRcRd, где Rd обозначает атом водоследующими заместителями галоген, (dрода, (С-і-Сб)алкил и арил, в котором указанный С4)алкокси-группа, или трифторметил, а арильная (Сі-Сє)алкил и арил могут быть замещены, как это группа может может быть замещена от 1 до 3 слеуказывалось выше в (f) для Rb и Rc, дующими заместителями галоген, (СгС4)алкил, (Сі-С4)алкокси-группа, или трифторметил, (їх) гетороцикл, представляющий собой 5-, 6или 7-членное кольцо, содержащее по крайней (хм) гетероцикл, представляющий собой 5мере один член, выбранный из группы, включаючленное ароматическое кольцо, содержащее один щей один атом кислорода в кольце, один атом атом азота в кольце, или один атом кислорода и серы в кольце, 1 - 4 атома азота в кольце или их один атом азота в кольце, сочетание, при этом гетероцикл может быть аро(k) R3 и R4 вместе могут обозначать карбоматическим, ненасыщенным или насыщенным и нильный атом кислорода, и где X выбирают из гетероцикл может быть сконденсирован с бенгруппы, включающей -О-, -S(O)n-, CH(Re)-, C(O)зольным кольцом, при этом гетероцикл может N(Re)-*,rfle Re обозначает атом водорода ( d быть замещен от 1 до 3 заместителями, как указаСз)алкил, арил, арил(Сі-Сз)алкил, при атом звезно выше в пп v), vi), VII), VIM), за исключением кодочка (*) обозначает связь в приложении 16 струкгда їх) обозначает гетероцикл, и туры 1, а п равно 0 или 2 (k) R3 и R4 вместе могут обозначать карбоПримерами новых соединений в этом способе нильный атом кислорода, осуществления настоящего изобретения являются, однако ими не ограничиваются (I) R3 и R4 вместе могут обозначать группу =CH-Rg, где значение Rg указано в VIM), где 4-аза-4,7-р-диметил-5-а-андростан-3,16-дион, X выбирают из группы, включающей -О-, 4-аза-4-метил-5-а-андростан-3,16-дион, S(O)n-, -C(O)-, -CH(Re)-, -C(O)-O-*, -C(O)-N(Re)-*, 3-оксо-4-аза-4-метил-16-р-гидрокси-5-аN(Re)-C(O)-O*, -O-C(O)-N(Re)-*, -N(Re)C(O)-N(Re)- андростан, O-CH(Re)-*, -N(Re)-, где Re обозначает водород, 3-оксо-4-аза-4-метил-16-р(Сі-Сз)алкил, арил, арил(Сі-Сз)алкил или незаме(бензиламинокарбонилокси)-5-а-андростан, щенный или замещенный гетероарил, как указано 3-оксо-4-аза-4-метил-16-р-бензоиламино-5-аранее в (j), при этом звездочка (*) обозначает андростан, связь в положении 16 структуры 1, a n равно 0, 1 3-оксо-4-аза-4-метил-16-р-метокси-5-аили 2 андростан, Допустимы лишь такие комбинации замести3-оксо-4-аза-4-метил-16-р-аллилокси-5-ателей и/или вариантов которые приводят к полуандростан, чению стабильных соединений 3-оксо-4-аза-4-метил-16-р-(н-пропилокси)-5-аОдним из вариантов осуществления настояандростан, щего изобретения являются соединения формулы 3-оксо-4-аза-4-метил-16-а-гидрокси-5-а1, в которых R1 обозначает водород или метил, и андростан, R2 обозначает водород или метил 3-оксо-4-аза-4-метил-16-р-(фенокси)-5-аСледующим вариантом осуществления наандростан, стоящего изобретения являются соединения 3-оксо-4-аза-7-р -метил-16-р-(фенокси)-5-аформулы І, в которых один из заместителей R3 и R4 выбирают из группы, включающей водород или андрост-1-ен, метил, а другой выбирают из группы, включаю3-оксо-4-аза-4-метил-16-а-метокси-5-ащей андростан, (b) циано-группу, 3-оксо-4-аза-4-метил-16-р-(4-хлорфенокси)-5(c) атом фтора, а-андростан, (е) гидроксильную группу, 3-оксо-4-аза-7-р -метил-16-р-(4-хлорфенокси)(д) (Сі-Сю)алкил-Х-, в котором алкил может 5-а-андрост-1-ен, быть замещен арилом, а арил, в свою очередь, 3-оксо-4-аза-7-р -метил-16-р-(4-хлорфенокси)может быть замещен 1-2 атомами галогена или 5-а-андростан, (С-і-Сб)алкила, 3-оксо-4-аза-7-р -метил-16-р-(3-хлор-4 44257 20 19 метилфенокси)-5-а-андростан, 3-оксо4-аза4,7-р-диметил-16-р-(4трифторметилфенокси)-5-а-андростан, 3-оксо-4-аза-7-р -метил-16-р-(4метилфенокси)-5-а-андростан, 3-оксо4-аза4,7-р-диметил-16-р-(43-оксо-4-аза-7-р -метил-16-р-(4трифторметоксифенокси)-5-а-андростан, метилфенокси)-5-а-андростан-1-ен, 3-оксо4-аза4,7-р-диметил-16-р-этилтио-5а3-оксо-4-аза-7-р -метил-16-р-[4-(1 андростан, 3-оксо4-аза4,7-р-диметил-16-рпиррол ил)фенокси]-5-а-андростан-1-ен, этилсульфонил-5-а-андростан, 3-оксо-4-аза-4,7-р -диметил-16-р-гидрокси-5-а3-оксо4-аза4,7-р-диметил-16-р-(4андростан, метилсульфонилфенокси)-5-а-андростан, 3-оксо-4-аза-4,7-р -диметил-16-р-метокси-5-аандростан, 3-оксо-4-аза-4,7-р-диметил-16-р-[4-(43-оксо-4-аза-4,7-р -диметил-16-р-аллилокси-5толилсульфониламино)фенокси]-5-а-андростан, а-андростан, 3-оксо-4-аза-4,7-р-диметил-16-р-(33-оксо-4-аза-4,7-р -диметил-16-р-(3,3пиридилокси)-5-а-андростан, диметилаллилокси)-5-а-андростан, 3-оксо-4-аза-4,7-р-диметил-16-р-[(43-оксо-4-аза-4,7-р -диметил-16-р-(нфенил)фенокси]-5-а-андростан, пропилокси)-5-а-андростан, 3-оксо-4-аза-4,7-р-диметил-16-р-(43-оксо-4-аза-4,7-р -диметил-16-р-(изофторфенокси)-5-а-андростан, пентокси)-5-а-андростан, 3-оксо-4-аза-4,7-р-диметил-16-р-(23-оксо-4-аза-4,16-а-диметил-16-р-гидрокси-5пиразинилокси)-5-а-андростан, а-андростан, 3-оксо4-аза-4,7-р-диметил-16-р-[4-(53-оксо-4-аза-4,7-р-диметил-16-р-этокси-5-аоксазолил)фенокси]-5-а-андростан, андростан, 3-оксо4-аза-4,7-р-диметил-16-р-(23-оксо-4-аза-4,7-р-диметил-16-р-бензилокси-5пиримидинилокси)-5-а-андростан, а-андростан, 3-оксо-4-аза-4,7-р-диметил-16-р-[4-(1 3-оксо-4-аза-4,7-р-диметил-16-а-гидрокси-5-апиррил)фенокси]-5-а-андростан, авдростан, 3-оксо-4-аза-4,7-р-диметил-16-р-(43-оксо-4-аза-4,7-р-диметил-16-р-метилтио-5-ааминофенокси)-5-а-андростан, андростан, 3-оксо-4-аза-4,7-р-диметил-16-р-(43-оксо-4-аза-4,7-р-диметил-16-р-(нацетиламинофенокси)-5-а-андростан, пропилтио)-5-а-андростан, 3-оксо-4-аза-4,7-р-диметил-16-р-(43-оксо-4-аза-4,7-р-диметил-16-р-фтор-5-абензоиламинофенокси)-5-а-андростан, андростан, 3-оксо-4-аза-4,7-р-диметил-16-р-(43-оксо-4-аза-4,7-р-диметил-16-р-циано-5-ахлорфенокси)-5-а-андростан, андростан, 3-оксо-4-аза-4,7-р-диметил-16-р-фенокси-5-а3-оксо-4-аза-4-метил-16-р-(1 -гексил)-5-аандростан, андростан 3-оксо-4-аза-4,7-р-диметил-16-р-(23-оксо-4-аза-4,7-р-диметил-16-р-(н-пропил)-5хлорфенокси)-5-а-андростан, а-андростан, 3-оксо-4-аза-4,7-р-диметил-16-р-(33-оксо-4-аза-4,7-р-диметил-16-р-бензил-5-ахлорфенокси)-5-а-андростан, андростан, 3-оксо-4-аза-4,7-р-диметил-16-р-(43-оксо-4-аза-4,7-р-диметил-16-р-(4хлорфенокси)-5-а-андрост-1 -ен, хлорбензил)-5-а-андростан, 3-оксо-4-аза-4,7-р-диметил-16-р-(43-оксо-4-аза-4,16-а-диметил-16-р-метокси-5-ахлорбензилиден)-5-а-андростан, андростан, 3-оксо-4-аза-4,7-р-диметил-16-бензилиден-53-оксо4-аза4,7-р-диметил-16-р-(4а-андростан, цианофенокси)-5-а-андростан, 3-оксо-4-аза-4,7-р-диметил-16-(43-оксо4-аза4,7-р-диметил-16-р-(3метилбензилиден)-5-а-андростан, цианофенокси)-5-а-андростан, 3-оксо-4-аза-4,7-р-диметил-16-(4-хлорбензил)3-оксо4-аза4,7-р-диметил-16-р-(45-а-андростан, нитрофенокси)-5-а-андростан, 3-оксо-4-аза-4,7-р -диметил-16-(43-оксо4-аза4,7-р-диметил-16-р-(1 метилбензил)-5-а-андростан, нафтилокси)-5-а-андростан, 3-оксо-4-аза-4,7-р -диметил-16-(33-оксо4-аза4,7-р-диметил-16-р-(3-хлор4пиридилметил)-5-а-андростан, метилфенокси)-5-а-андростан, 3-оксо-4-аза-4,7-р -диметил-16-а3-оксо4-аза4,7-р-диметил-16-р-(4метансульфонил-5-а-андростан, метилфенокси)-5-а-андростан, 3-оксо-4-аза-4,7-р -диметил-16-р-тиофенокси3-оксо4-аза4,7-р-диметил-16-р-(трет-бутокси)5-а-андростан, 5-а-андростан, 3-оксо-4-аза-4,7-р -диметил-16-р-(43-оксо4-аза4,7-р-диметил-16-р-(3-метил-1 хлортиофенокси)-5-а-андростан, бутилокси)-5-а-андростан, 3-оксо-4-аза-4,7-р-диметил-16-р-(43-оксо4-аза4,7-р-диметил-16-а-(н-пропилокси)фтортиофенокси)-5-а-андростан, 5-а-андростан, 44257 22 21 3-оксо-4-аза-4,7-р-диметил-16-р-(4хлорфенокси)-5-а-андростан, метилтиофенокси)-5-а-андростан, 3-оксо-4-аза-4,7-р-диметил-16-р-(фенокси)-5а-андростан, 3-оксо-4-аза-4,7-р-диметил-16-р-(4метокситиофенокси)-5-а -андростан, 3-оксо-4-аза-4'?7-р-диметил-16-р-(2хлорфенокси)-5-а-андростан, 3-оксо-4-аза-4,7-р-диметил-16-рфенилсульфонил-5-а-андростан, 3-оксо-4-аза-4,7-р-диметил-16-р-(3хлорфенокси)-5-а-андростан, 3-оксо-4-аза-4,7-р,16-а -триметил-16-р-(4и их фармацевтически приемлимые соли трифторметилфенокси)-5-а-андростан, Полезным соединением по настоящему изо3-оксо-4-аза-4,7-р , 1 6-а-триметил- 16-р бретению является 3-оксо-4-аза-4,7-р-диметил-16гидрокси-5-а-андростан, Р-(4-хлорфенокси)-5-а-андростан, или его фа3-оксо-4-аза-4,7-р,16-а-триметил-16-ррмацевтически приемлемая соль метокси-5-а-андростан, В контексте настоящего изобретения "алкил" их фармацевтически приемлемые соли и анапредставляет собой алифатические углеводородлоги вышеуказанных соединений, в которых С1-С2 ные группы как с разветвленной, так и прямой цеуглерод-углеродная связь является двойной свя1 2 пью, содержащей определенной количество атозью и/или R обозначает атом водорода и/или R мов углерода, в частности метил (Me), этил (Et), обозначает в подходящих случаях атом водорода пропил, бутил, пентил, гексил, гептил, октил, ноили метил нил, децил, изо-пропил (i-Pr), изо-бутил (i-Bu), В другом варианте осуществления настоящего трет-бутил (t-Bu), втор-бутил (s-Bu), изо-пентил и изобретения формула I далее ограничена соедит п "Алкилокси-группа" (или "алкокси-группа") обонениями, в которых С1-С2 углерод-углеродная значает алкильную группу, содержащую указанное связь является простой связью, R обозначает количество атомов углерода, присоединенную 2 3 метил, R обозначает метил, R выбирают из нечерез кислородный мостик, в частности, метоксизамещенной или замещенной арилокси-группы, а группу, этокси-группу, пропилокси-группу и т д "Алкенил" включает углеводородные группы с R4 обозначает атом водорода прямой или разветвленной цепью, содержащей Некоторыми примерами соединений в этом одну или большее количество углерод-углеродных способе осуществления настоящего изобретения двойных связей, которые могут располагаться в являются, но не ограничиваются любом устойчивом положении в углеродной цепи, 3-оксо-4-аза-4,7-р-диметил-16-р-(4такие как этенил, пропенил или аллил, бутенил, цианофенокси)-5-а-андростан, пентенил и т п Настоящее изобретение охваты3-оксо-4-аза-4,7-р-диметил-16-р-(3вает все Е, Z диастереомеры цианофенокси)-5-а-андростан, Алкильные или алкенильные группы могут 3-оксо-4-аза-4,7-р-диметил-16-р-(4быть незамещены или замещены одним или нитрофенокси)-5-а-андростан, большим количеством заместителей, предпочти3-оксо-4-аза-4,7-рр-диметил-16-р-(1 тельно от 1 до 3 следующими заместителями нафтилокси)-5-а-андростан, і) галоген, гидроксильная группа, циано3-оксо-4-аза-4,7-р-диметил-16-р-(3-хлор-4группа, нитро-группа, моно-, ди- или тригалогенметилфенокси)-5-а-андростан, метил, оксо-группа, гидроксисульфонильная груп3-оксо-4-аза-4,7-р-диметил-16-р-(4па, карбоксильная группа, метилфенокси)-5-а-андростан, м) гидрокси(Сі-Сб)алкил, (С і-Сє) ал кил алкокси3-оксо-4-аза-4,7-р-диметил-16-р-(4группа, (Сі-Сє)алкилтио-группа, (dтрифторметилфенокси)-5-а-андростан, Сб)алкилсульфонильная группа, (d3-оксо-4-аза-4,7-р-диметил-16-р-(4Сб)алкокси карбон ильная группа, в которых ( d трифторметоксифенокси)-5-а-андростан, Сб)алкильная часть может быть дополнительно 3-оксо-4-аза4,7-р-диметил-16-р-(4замещена от 1 до 3 следующими заместителями метилсульфонилфенокси)-5-а-андростан, галоген, (СгСб4)алкокси-группа, или трифторме3-оксо-4-аза-4,7-р-диметил-16-р-[4-(4тил, толилсульфониламино)фенокси]-5-а-андростан, їм) арилтио-группа, арил, арилокси-группа, 3-оксо-4-аза-4,7-р-диметил-16-р-[(4арилсульфонильная группа, арилоксикарбонильфенил)фенокси]-5-а-андростан, ная группа, в которых арильная часть может быть 3-оксо-4-аза-4,7-р-диметил-16-р-(4дополнительно замещена от 1 до 3 следующими фторфенокси)-5-а-андростан, заместителями галоген, (СгС^алкил, (dС^алкоксигруппа, или трифторметил, 3-оксо-4-аза-4,7-р-диметил-16-р-[4-(5оксазолил)фенокси]-5-а-андростан, iv) группы -C(O)NRbRc, -N(Rb)-C(O)-RcA, NRbRc, где значения Rb и Rc указаны ранее, а га3-оксо-4-аза-4,7-р-диметил-16-р-[4-(1 логен обозначает фтор, хлор, бром или йод пиррил)фенокси]-5-а-андростан, Термин "оксо-группа" в контексте настоящего 3-оксо-4-аза-4,7-р-диметил-16-р-(4изобретения обозначает оксо-радикал, который аминофенокси)-5-а-андростан, может располагаться в любом устойчивом поло3-оксо-4-аза-4,7-р-диметил-16-р-(4жении в углеродной цепи, что приводит к образоацетиламинофенокси)-5-а-андростан, ванию формильной группы, если он располагается 3-оксо-4-аза-4,7-р-диметил-16-р-(4на конце цепи, или образованию ацильной или бензоиламинофенокси)-5-а-андростан, ароильной группы в других положениях в углерод3-оксо-4-аза-4,7-р-диметил-16-р-(4 23 44257 ной цепи В контексте настоящего изобретения термин "арил", т е (Сб-Сю)арил обозначает фенил или нафтил, в том числе 1-нафтил или 2-нафтил, как замещенный, так и не замещенный, что указано далее В контексте настоящего изобретения "гетероарил" включает 5-, 6-илй 7-членный гетероароматический радикал, содержащий по крайней мере один член, выбранный из группы, включающей один атом кислорода в кольце, атом серы в кольце, 1-4 атомов азота в кольце или их сочетание, при этом гетероарильное кольцо может быть сконденсировано с бензольным или гетероароматическим кольцом Указанный класс включает как незамещенные, так и замещенные следующим гетероаро-мати чес кие кольца пиридил, фурил, пиррил, тиенил, изотиазолил, имидазолил, бензимидазолил, тетразолил, пиразинил, пиримидил, хинолил, хиназолинил, изохинолинил, бензофурил, изобензофурил, бензотиенил, пиразол ил, индолил, изоиндолил, пуринил, карбазолил, изоксазолил, тиазолил, изотиазолил, оксазолил, бензтиазолил и бензоксазолил Гетероарильное кольцо может быть присоединено в структурной формуле 1 через гетероатом, в частности, атом азота, или атом углерода в кольце, что приводит к получению устойчивой структуры Гетероарильное кольцо может быть сконденсировано с бензольным кольцом Указанные выше(Сб-Сю)арильные или гетероарильные группы, могут быть замещены от одного до трех, предпочтительно одним или двумя заместителями, которые независимо выбирают из v) атом галогена, гидроксильной группы, циано-группы, нитро-группа, моно-, ди- или тригалогенметила, моно-, ди- или тригалогенме-токсигруппы, (С2-Сб)алкенила, (Сз-Сб)циклоалкила, формильной группы, гидросульфонильной группы, карбоксильной группы, уреидо-группы, vi) (С-і-Сб)алкила, гидрокси(Сі-Сє)алкила, ( d Сб)алкилокси-группы, (Сі-Сб)алкилокси(Сг Сє)алкила, (Сі-Сє)алкилкарбонильной группы, ( d Сб)алкилсульфонильной группы, (Сі-Сє)алкилтиогруппы, (Сі-Сб)алкилсульфинильной группы, ( d Сб)алкилсульфонамидо-группы, (dСб)алкилоксикарбонильной группы, (dСб)алкилоксикарбонил(Сі-Сб)алкила, RbRcNС(О)(Сі-Сє)алкила, (Сі-Сб)алканоиламино(Сг Сє)алкила, ароиламино(Сі-Сб)алкила, при этом (Сі-Сє)алкильная часть может быть замещена от 1 до 3 следующими заместителями галоген, ( d С4)алкокси-группа, или трифторметил, VII) арила, арилокси-группы, арил карбонильной группы, арилтио-группы, арилсульфонильной группы, арилсульфинильной группы, арилсульфонамидо-группы, арилоксикарбонильной группы, при этом арильный фрагмент может быть замещен от 1 до 3 следующими заместителями галоген, (Сі-С4)алкил, (С1-С4) алкокси-группа,-или трифторметил, VIM) группы -C(O)NRbRc, -O-C(O)-NRbRc, -N(Rb)C(O)-RC, -NRbRc, Rb-C(O)-N(Rc)-, где значения Rb и Rc указаны ранее в (е), и группы -N(R)-C(O)-OR, где в данном случае Rc обозначает (Сі-Сє)алкил или арил, -N(Rb)-C(O)-ORcRd, где в данном случае 24 F Rd обозначает атом водорода, (Сі-Сє)алкил и арил, в которых указанный (Сі-Сє)алкил и арил могут быть замещены заместителями, указанными выше в (е) для Rb и Rc, (їх) гетероцикл, представляющий собой 5-, 6или 7-членное кольцо, содержащее по крайней мере один член, выбранный из группы, включающей один атом кислорода в кольце, один атом серы в кольце, 1 - 4 атома азота в кольце или их сочетание, при этом гетероцикл может быть ароматическим, ненасыщенным или насыщенным и гетероцикл может быть сконденсирован с бензольным кольцом, при этом гетероцикл может быть замещен от одного до трех заместителями, как указано выше в пп v), vi), vn) и VIM), за исключением случая, когда їх) обозначает гетероциклическую группу Сконденсированные гетероциклические системы включают пурин, имидазоимидазол, имидазотиазол, пиридопиримидин, пиридопиридазин, пиримидопиримидин, имидазопиридазин, пирроллопиридин, имидазопи-ридин и т п "Гетероциклические" группы включают полностью ненасыщенные вышеуказанные гетероарильные кольца, а также их соответствующие дигидро-, тетрагидро- и гексагидропроизводные, получаемые из частично ненасыщенных и полностью насыщенных вариантов циклических систем Примеры включают дигидроимидазолил, дигидрооксазолил, дигид-ропиридил, тетрагидрофурил, дигидропиррил, тетрагидротиенил, дигидроизотиазолил, 1,2-дигидробензимидазолил , 1,2дигидротетразолил , 1,2-дигидропиразинил, 1,2дигидропиримидил, 1,2-дигидрохинолил, 1,2,3,4тетрагидроизохинолил , 1,2,3,4тетрагидробензофурил, 1,2,3,4тетрагидроизобензофурил, 1,2,3,4тетрагидробензотиенил, 1,2,3,4тетрагидропиразолил, 1,2,3,4-тетрагидроиндолил, 1,2,3,4-тетрагидроизоиндолил, 1,2,3,4тетрагидропуринил, 1,2,3,4-тетрагидрокарбазолил, 1,2,3,4-тетрагидроизоксазолил, 1,2,3,4тетрагидротиазолил, 1,2,3,4-тетрагидрооксозолил, 1,2,3,4-тетрагидробензтиазолил и 1,2,3,4тетрагидробензоксазолил и т д Гетероциклическая группа может содержать такие же заместители, как приведенные выше для гетероарильной группы Если термины "алкил", "алкенил", "алкилокси" (или "алкокси"), "арил" или "гетероарил" появляются в названии заместителя в формуле I (в частности, аралкоксиарилокси), то они имеют те же значения, что и указанные выше для "алкила", "алкенила", "алкилокси" (или "алкокси"), "арила" или "гетероарила", соответственно Обозначенные количества атомов углерода ( в частности (Сі-Сю) относятся независимо к количеству атомов углерода в алкильном или алкенильном фрагменте или к алкильной или алкенильной части большего по размеру заместителя, в который алкил или алкенил входит как составная часть В объем притязаний по настоящему изобретению входит также фармацевтически приемлемые соли соединений формулы І, в структуре которых присутствуют основные или кислотные группы Если имеется кислый заместитель, в ча 25 44257 26 стности -СООН, то для использования в дозиостровкового облысения у мужчин, угрей обыкноровочных формах может быть получена аммонийвенных, себореи, избыточного оволосения у женная, натриевая, калиевая, кальциевая соль и т п щин, путем перорального, системного, парентеЕсли присутствует основная группа, т е аминорального или местного введения новых группа или обладающий свойствами основания соединений формулы I как самостоятельно, так и гетероарильный радикал, такой как, в частности, в сочетании с ингибиторами 5-а-редуктазы 2 и/или 4-пиридил, то для использования в дозировочных далее в сочетании со средствами, способными формах может быть получена кислая соль, наоткрывать мембранные калиевые каналы, в частпример, гидрохлорид, гидробромид, ацетат, пальности, миноксидилом, антиандрогенами, в частномоат и т п сти, флутамидом, ретиноидами, в частности, третиноином или изотретиноином, антагонистами а-1 Кроме того, если имеется группа -СООН, то рецептора, в частности, тера-зоцином могут использоваться фармацевтически приемлемые сложные зфиры, в частности, ( d Термин "лечение андрогеновой алопеции" Сб)алкиловый, пивалоилоксиметиловый и т п , а подразумевает остановку и обращение андрогетакже сложные зфиры, известные из области техновой алопеции и стимулирование роста волос ники для модифицирования растворимости или Следующей целью настоящего изобретения явизменения параметров при гидролизе, для исляются способы лечения доброкачественная гипользования в препаративных формах, медленно перплазия предстательной железы, простатита и выделяющих лекарственное средство, или в прелечения и/или предотвращения рака предстапаративных формах, содержащих предшественнительной железы путем орального, системного или ки лекарственных средств парентерального назначения новых соединений формулы I как самостоятельно, так и в сочетании Вышеуказанные соли включают следующие с ингибиторами 5-а-редуктазы 2 ацетат, лактобионат, бензолсульфонат, лаурат, бензоат, малат, бикарбонат, малеат, бисульфат, Целью настоящего изобретения являются соль миндальной кислоты, битартрат, мезилат, также фармацевтические композиции, пригодные борат, метилбромид, бромид, метилнитрат, кальдля местного, перорального, системного и паренциевая соль этилендиаминтетрауксусной кислоты, терального введения для использовании в новых метилсульфат, камзилат, соль слизевой кислоты, способах лечения, предложенных в настоящем карбонат, напзилат, хлорид, нитрат, клавуланат, изобретении Композиции, содержащие соединесоль N-метилглюкамина, цитрат, соль аммония, ния настоящего изобретения в качестве активных дигидрохлорид, олеат, соль этилендиаминтетраингредиентов для использования при лечении уксусной кислоты, оксалат, эдизилат, памоат (эмвышеуказанных гиперандрогеновых состояний бонат), эстолат, пальмитат, эзилат, пантотенат, могут вводиться в виде самых разнообразных тефумарат, фосфат/дифосфат, глюцептат, полигарапевтических дозировочных форм вместе с лактуронат, глюконат, салицилат, глютамат, стеаобычными носителями, применяемыми при сисрат, гликоллиларсанилат, сульфат, гексил резортемном введении Например, соединения могут цинат, субадетат, соль гидрабамина, сукцинат, вводиться в виде таких пероральных дозировочгидробромид, соль тан- нина, гидрохлорид, тарных форм, как таблетки, капсулы (каждая из кототрат, гидроксинафталат, теоклат, иодид, тозилат, рых включает составы с отсроченным моментом изотионат, триэтиодид, лактат и валерат выделения лекарственного средства или составы для продолжительного выделения лекарственного Кроме того, некоторые из соединений по насредства), пилюли, порошки, гранулы, эликсиры, стоящему изобретению могут образовывать сольнастойки, растворы, суспензии, сиропы и эмульваты с водой или обычными органическими рассии, или вводиться в виде инъекций Кроме того творителями Подобные сольваты входят в объем они могут вводиться в виде внутривенных (как в притязаний по настоящему изобретению виде болюсов, так и в виде вливаний), внутриТермин "терапевтически эффективное колибрюшинных, подкожных, местных без окклюзии и с чество" означает количество лекарства или фарокклюзией или внутримышечных форм, использомацевтического средства, которое вызывает биование всех этих форм хорошо известно специалилогическую или медицинскую ответную реакцию стам в области фармации ткани, системы, животного или человека, которых осматривает исследователь, ветеринар, врач или Предлагаемые в настоящем изобретении другой специалист в области медицины фармацевтические композиции включают фармаСоединения по настоящему изобретению соцевтические композиции, содержащие фармацевдержат хиральные центры и могут существовать в тически приемлемый носитель и терапевтически виде рацематов, рацемических смесей и в виде аффективное количество соединения формулы I индивидуальных энантиомеров или диастереоменастоящего изобретения, эти фармацевтические ров, при этом все указанные изомерные формы, а композиции дополнительно содержат также их смеси входят в объем притязаний по натерапевтически эффективное количество инстоящему изобретению Более того, некоторые из гибитора 5-а-редуктазы 2 или его фармацевтичекристаллических форм соединений по настоящески приемлемой соли, в частности, финастерида, му изобретению могут существовать в виде полиэпристерида или туростерида, морфных форм и все они входят в объем притявещество, стимулирующее раскрытие мемзаний по настоящему изобретению бранного калиевого канала, или его фармацевтиКроме того целью настоящего изобретения чески приемлемую соль, в частности, миноявляются способы лечения гиперандрогеновых ксидил, состояний андрогеновой алопеции, в том числе терапевтически эффективное количество ре 27 44257 28 тиноида или его фармацевтически приемлемой ных с угрями обыкновенными, андрогеновой соли, в частности, третиноина, изотрети-ноина, алопецией, включая островковое облысение у мужчин, себорею, избыточное оволосение у жентерапевтически эффективное количество анщин, соединения по настоящему изобретению и тиандрогена или его фармацевтически приемлеингибитор 5-а-редуктазы 2 могут готовиться в вимой соли, в частности, флутамида, спироде композиции, пригодной для местного введения нолактона или касодекса Кроме того может применяться комбинированная Дневная доза соединений для взрослого четерапия, при которой соединения формулы I и ловека может варьировать в интервале от ОД до ингибитор 5-а-редуктазы 2 назначаются раздель1000мг в день Для перорального введения компоно в виде пероральных, системных, парентеральзиции предпочтительно готовят в форме имеющих ных или местных дозировочных форм Например, или не имеющих насечки таблеток, содержащих соединение формулы I и, в частности, финастерид 0,1, 0,5, 1,0, 2,5, 5,0, 10,0, 15,0, 25,0 и 55,0мг акмогут вводиться в виде единичной пероральной тивного ингредиента, с целью подбора для пациили местной дозировочной формы или же каждое ента соответствующей симптомам дозировки средство может вводиться в виде раздельных доЭффективное количество лекарства обычно позировочных форм, в частности, раздельных пероступает при дозировке приблизительно от 0,002мг ральных дозировочных форм, или же финастерид на кг веса тела до приблизительно 50мг на кг веса может вводиться в виде пероральной композиции тела в день Более предпочтительный интервал в сочетании с дозировочной формой соединения I, составляет от 0,01 мг/кг до 7 мг/кгв день пригодной для местного назначения См , Патенты Соединения по настоящему изобретению преСША 4377584 и 4760071, в которых описываются имущественно вводят в виде однократной дневдозировки и составы для ингибиторов 5-аной дозы или же общая дневная доза может вворедуктазы Втом случае, если активные вещества диться порционными дозами два, три или четыре применяются в виде раздельных дозировочных раза в день Более того, соединения по настояформ, их можно вводить одновременно или же щему изобретению могут водиться через нос покаждое из них может вводиться в разные периоды средством местного применения пригодных для времени введения через нос носителей или через кожу с помощью дозировочных форм или пластырей, В объем притязаний по настоящему изобрехорошо известных специалистам Для введения в тению включаются и другие ингибиторы 5-аформе, пригодной для введения через кожу, доза, редуктазы типа 2, полезные в указанных выше конечно, готовится таким образом, чтобы дозирометодах Не ограничивающие настоящее изобревочные режимы предусматривали выделение летение примеры включают 17-р-(1Ч-треткарственного средства в течение длительного бутилкарбамоил)андроста-3,5-диен-3-карбоновую) времени, а не в виде отдельных порций кислоту (эпистерид, Smith & Beecham, SKF При лечении андрогенной алопеции, включая островковое облысение у мужчин, угри обыкновенные, себорею и избыточное оволосения у женщин соединения по настоящему изобретению могут вводиться в виде фармацевтических композиций, содержащих активное соединение в сочетании с фармацевтически приемлемым носителем, пригодным для местного использования Фармацевтические композиции для местного введения могут готовиться в форме раствора, крема, мази, геля, лосьона, шампуня или аэрозоля, пригодного для нанесения на кожу Указанные фармацевтические композиции для местного введения, содержащие соединения по настоящему изобретению, обычно' содержат приблизительно от 0,001% до 15% вес активного соединения в смеси с фармацевтически приемлемым носителем При лечении угрей обыкновенных, андрогеновой алопеции, включая островковое облысение у мужчин, себорею, избыточное оволосение у женщин, доброкачественной гиперплазии предстательной железы, простатита и предотвращения и/или лечения рака предстательной железы соединения по настоящему изобретению могут использоваться сами по себе или в сочетании с терапевтически эффективным количеством ингибитора 5-а-редуктазы 2, такого как финастеридин, в виде единичной пероральной, системной или парентеральной фармацевтической дозировочной формы Кроме того при лечении заболеваний кожи и волосистой части кожи головы, связан 105657), описанную 93/19758, и в WO 91/13550 и WO 17-р-[І\І-изопропил-І\І (изопропилкарбамоил)карбамоил]-4-метил-4-аза5-а-андростан-З-он (туростерид, Farmitaha, FCE 26073), который описан в Патенте США 5155107, и их производные Далее, введение соединения по настоящему изобретению в сочетании с терапевтически эффективным количеством вещества, стимулирующего раскрытие мембранных калиевых каналов, такого как миноксидил, хромакалин, пинацидил, соединения, выбранного из класса Sтриазина, тиан-І-оксида, производных бензопирана и пиридинопирана или их фармацевтически приемлемых солей, может использоваться при лечении андрогеновой алопеции, включая островковое облысение у мужчин Активные ингредиенты могут вводиться в виде единичной дозы для местного применения, при этом каждое активное вещество может вводиться в виде отдельных дозировочных форм, в частности, в виде отдельных составов для местного назначения, или в виде пероральных дозировочных форм, содержащих соединение формулы І, в сочетании с дозировочными формами, содержащими, в частности, миноксидил, для местного назначения См , например, Патенты США 4596812, 4139619 и патентную заявку WO 92/02225, опубликованную 20 февраля 1992, в которых приводятся дозировки и составы, содержащие стимуляторы раскрытия мембранных кальциевых каналов Втом случае, если активные вещества применяются в виде раздельных дози 29 44257 30 ровочных форы, их можно вовдить одновременно может легко определить и прописать эффективили же каждое из них может вводиться в разные ное количество лекарства, необходимое для препериоды времени дотвращения, противодействия или остановки развития заболевания Оптимальная оценка досБолее того, при лечении угрей обыкновенных тижения концентраций лекарства для интервала и/или андрогеновой алопеции может применяться значений, который приводит к достижению рекомбинированная терапия, включающая введение зультата, не вызывая токсического воздействия, терапевтически эффективного количества соедитребует применения режимов дозировки, оснонения формулы I, как самостоятельно, так и в сованных на кинетике доставки лекарства в нужные четании с ингибитором 5-а-редуктазы 2, или кроме органы Это требует рассмотрения вопросов растого в сочетании с терапевтически эффективным пределения, равновесного состояния и выведения количеством ретиноида, в частности, ретеновой лекарства кислоты или ее сложного эфира или ее амида, такого как третиноин (RETIN А) или изотретиноин В способах по настоящему изобретению при(ACCUTANE, Roche, см Патенты США 3006939, веденные в настоящем описании соединения яв3746730 и 4556518) ляются активными ингредиентами и обычно их вводят в смеси с фармацевтически пригодными Кроме того при лечении угрей обыкновенных, разбавителями, наполнителями и носителями (их андрогеновой алопеции, себореи, избыточного обозначают общим термином "носители"), котооволосения у женщин, доброкачественной гиперрые преимущественна выбирают в соответствии с плазии предстательной железы, простатита и требуемой формой введения, т е таблеток для предотвращения и/или лечения рака предстаперорального введения, капсул, эликсиров, сиротельной железы может применяться компов и т п , как это обычно практикуется в фармабинированная терапия, включающая введение ции эффективного количества соединения формулы I вместе с терапевтически эффективным количестТак, для перорального введения в форме табвом антиандрогена, такого как флутамид, спиролеток или капсул активные компоненты лекарства нолактон или касодекс смешивают с фармацевтически приемлемым инертным носителем, пригодным для пероральноВ объем притязаний по настоящему изобрего назначения, таким как этанол, глицерин, вода и тению входит также способ лечения доброкачестт п Кроме того, если необходимо, в смесь могут венной гиперплазии предстательной железы, ковходить подходящие связующие, смазывающие торый включает стадию введения средства, разрыхляющие средства и красители млекопитающему, нуждающемуся в подобном Подходящими связующими являются, однако ими лечении, терапевтически эффективного количестне ограничиваются, крахмал, желатин, природные ва соединения формулы І в сочетании с ингибитосахара, такие как глюкоза или р-лактоза, выдером 5-а-редуктазы 2 Указанный способ включает ляемые из кукурузы подсластители, природные также использование антагониста а-1-рецептора в или синтетические смолы, такие как камедь, трачастности, теразозина (Abbott, см Патенты США гакант или альгинат натрия, карбоксиметилцел4026894, 4251532) люлоза, полиэтиленгликоль, воски и т п смазыВ объем притязаний по настоящему изобревающими веществами, которые используются в тению входит также способ ингибирования биоуказанных дозировочных формах, являются, одсинтетической конверсии тестостерона в динако ими не ограничиваются, олеат натрия, стеагидротестостерон у нуждающихся в лечении млерат натрия, стеарат магния, бензоат натрия, ацекопитающих, включающая стадию введения укатат натрия, хлорид натрия и т п Разрыхляющие занному млекопитающему терапевтически эффексредства включают, однако ими не ограничиваюттивного количества соединения формулы I или ся, крахмал, метил целлюлозу, агар, бентонит, терапевтически эффективного количества соедисмолу ксантана и т п нения формулы І в сочетании с ингибитором 5-аредуктазы 2 Жидкие формы содержат отдушку и суспендирующие или диспергирующие средства, такие как В объем притязаний по настоящему изобресинтетические или природные смолы, например, тению входит также способ ингибирования 5-атрагакант, камедь, метилцеллюлозу и т д редуктазы или ее изофермента у млекопитающеДругими используемыми диспергаторами явго, нуждающемуся в подобном лечении, вклюляются глицерин и т п Для парентерального ввечающая стадию введения указанному млекопидения необходимы стерильные суспензии и растающему терапевтически эффективного котворы Изотонические препараты обычно личества соединения формулы I или содержат подходящие консерванты и используюттерапевтически эффективного количества соедися в том случае, когда необходимо внутривенное нения формулы І в сочетании с ингибитором 5-авведение редуктазы 2 Препараты для местного введения, содержаРежимы дозировки при использовании соедищие активные компоненты лекарства, могут сменений по настоящему изобретению выбирают в шиваться с самыми разными носителями, хорошо соответствии с различными факторами, вклюизвестными из области техники, такими как, начающими тип, вид, возраст, вес, пол и медицинпример, спирты, гель алоэ, аллантоин, глицерин, ское состояние пациента, степень тяжести забомасла с витаминами А и Е, минеральное масло, левания, лечение которого проводят, способ миристилпропионат полипропиленгликоля и т п с введения лекарств, состояние функций почек и образованием, в частности, спиртовых растворов, печени пациента, конкретное используемое соочищающих составов, очищающих кремов, гелей единение Обычный опытный врач или ветеринар 31 32 ванием соединения 1 Восстановление 16-кетона 1 в 16-р-спирт 2 проводят подходящим гидридным восстановителем, таким как боргидрид натрия в метаноле или три-фтор-бутилборгидрид лития в тетрагидрофуране ЛТФ) Спирт 2 превращают в его алкильные производные 3 или 4, генерируя вначале алкоксидный анион с помощью гидрида калия в N.N-диметилформамиде (ДМФА) или с помощью гидро-ксида калия в диметилсульфоксиде (ДМСО) с последующим добавлением подходящего алкилбромида или алкилиодида 16-р-(нпропилокси)производное 5 получают из предшествующего 16-р-(аллилокси)производного 4 каталитическим гидрированием Представленные на схеме 2 ингибиторы могут быть получены следующим образом 16-Оксим превращают в 1-р-амин С каталитическим гидрированием в присутствии гетерогенного катализатора, такого как оксид платины, в водном растворе уксусной кислоты Ацилирование соединения С проводят с помощью соответствующего ангидрида кислоты или хлорангидрида кислоты в присутствии акцептора кислоты, такого как пиридин, триэтиламин и 4-диметаламинопиридин Указанным способом получают соединения 6 и 7 Карбаматы, такие как соединения 8, приведенные на Схеме 3, получают, обрабатывая спирт 2 соответствующим изоцианатом в присутствии органического основания, такого как триэтиламин, пиридин и 4диметиламинопиридин Представленные на схеме 4 ингибиторы могут быть получены следующим образом 16-р-Спирт превращают в 16-а-спирт 9 действием 4-нитробензойной кислоты в присутствии диэтилового эфира дназадикарбоновой кислоты и трифенилфосфина с образованием в качестве промежуточного соединения 16-а-(пнитробензоата) D с последующим гидролизом в водном растворе основания в подходящем спирте Алкилирование соединения 9 проводят аналогично тому, как это описано для спирта 2, с образованием целевого 16-а-алкильного эфира, такого как 16-а-метоксипроизводное (пример 10), приведенное на Схеме 4 Представленные на схеме 5 7-р-метильные ингибиторы получают аналогично тому, как это описано ранее для соединений приведенных на схеме 1, однако в качестве исходного соединения используют 4-аза-4,7-диметил-5-а-андростан-3,17дион (Е) Представленные на Схеме 6 7-р-метальные ингибиторы получают следующим образом Соединение 20 получают, действуя на спирт 12 третбутилтрихлорацетимидатом в присутствии органической сульфоки-слоты, такой как трифторметансульфокислота 16-р-арилокси производные, такие, как 21-24, получают, вырабатывая алкоксидный анион из спирта 12 с помощью гидрида калия или натрия в тетрагидрофуране или N,Nдиметилформамиде или с помощью гидроксида калия в димети-лсульфоксиде с последующим добавлением соответствующего фторбен-зола Представленные на Схеме 7 7-р-метильные ингибиторы получают аналогично тому, как это описано ранее для соединений приведенных на схеме 4, однако в качестве исходного соединения 44257 для кожи, лосьонов для кожи и шампуней в виде кремов или гелей См , в частности Европейскую патентную заявку 0285382 Соединения по настоящему изобретению вводиться также в форме липосомной системы доставки, такой как маленькие униламеллярные везикулы, большие униламеллярные везикулы и мультиламеллярные везикулы Липосомы могут образовываться из различных фосфолипидов, таких как холестерин, стериламин или фосфатиди лхолины Соединения по настоящему изобретению могут также доставляться при использования в качестве индивидуальных носителей моноклональных антител, к которым прикреплены молекулы соединений, соединения по настоящему изобретению могут также присоединяться к растворимым полимерам, которые могут использоваться в качестве носителей Указанные полимеры могут включать поливинилпирролидон, сополимеры пирана, полигидроксипропилметакриламид-фенол, полигидроксиэтиласпартамидфенол или полиэтиленоксидполилизин, замещенный пальмитоильными остатками Кроме того, соединения по настоящему изобретению могут присоединяться к биоразлагаемым полимерам, используемым для осуществления контролируемого выделения лекарства, например, к полимолочной кислоте, полиэпсилон-капролактону, поли-гидроксимасляной кислоте, полиортоэфирам, полиацеталям, полидигид-ропиранам, полицианоакрилатам и поперечно сшитым или амфифатическим блок-сополимерам гидрогелей Соединения настоящего изобретения легко могут быть получены в соответствии со следующими схемами реакций и Примерами или в соответствии с их модификации при использовании легко доступных исходных соединений, реагентов и обычных методик синтеза Можно также использовать модификации указанных реакций, которые хорошо известны специалистам в данной области техники и подробно здесь не рассматриваются Специфические определения для переменных, приведенные на схемах (в частности, R = СНз), даны лишь для иллюстрации и не ограничивают настоящее изобретение Используются следующие сокращения Рп обозначает фенил, Ас обозначает ацильную группу, t-Bu обозначает третбутил, Et обозначает этил, Me обозначает метил, i-Am обозначает изо-амил Представленные на Схеме 1 ингибиторы могут быть получены следующими способами Вначале превращают 4-аза-4-метил-5-а-андростан3,17-дион (А) в изомерный 3,16-дион 1, используя следующую последовательность реакций (1) обработка соединения А изоамилнитритом в третбутаноле в присутствии трет-бутоксида калия с образованием промежуточного 16-оксимо-17кетона, (2) восстановление 17-кето-группы гидразингидратом и гидроксидом калия в этиленгликоле при повышенных температурах с образованием 16-оксима В, и (3) расщепление 16-оксимо-группы в соединении В либо с помощью гидролиза водным раствором уксусной кислоты при нагревании или бисульфитом натрия с последующей обработкой водным раствором соляной кислоты с образо 33 44257 34 вают с помощью DDQ и BSTFA в толуоле, формииспользуют промежуточный продукт 7-р-метил-16руя двойную связь в положении I, и получают соР-ол 12 Инверсию конфигурации в положении 16 единение 59 По аналогичной восстановительной с образованием соединения F осуществляют в схеме из 1,2-дигидроандростана 57 получают псоответствии с трансформацией по Мицунобу, как хлорандрост-1-ен 60 Его далее метилируют попоказано на Схеме 7 О-Алкилирование с образоложение 1, обрабатывая йодистым метилом и ванием 15-а-эфиров, таких как 26, осуществляют, гидридом натрия в диметилформамиде, и полукак уже описано ранее чают соединение 62 Представленные на Схеме 8 ингибиторы поПредставленные на Схеме 12 ингибиторы получают следующим образом Добавление метиллучают аналогично Схеме 11 Защищенный с помагнийбромида в тетрагидрофуране либо к кетону мощью І\І-2,4-диметоксибензильной группы 161 либо к 11 приводит к соответствующему 16-а спирт 55 обрабатывают 4-метил-Зметил- 16-р-спирту 27 или 28 О-Алкилирование хлорфторбензолом и гидридом калия в диметилили О-арилирование проводят, как описано на формамиде с образованием 4-метил-Зранее приведенных схемах, с образованием 16-ахлорфенокси производного 63, которое затем обметил-16-р-эфирных производных, таких как в рабатывают трифторуксусной кислотой в хлорипримерах 29 и 30 стом метилене, с целью удаления защитной N-2,4Представленные на схеме 9 ингибиторы полудиметоксибензильной группы, и получают соедичают следующими способами Превращают 7нение 64 Его обрабатывают газообразным водометил-16-а-спирт 25 в 16-р-тиол Н обработкой родом и палладием на угле в метаноле, с целью тиоуксусной кислотой в присутствии ди-изоудаления атома хлора из фенильного кольца, и пропилового эфира азодикарбоновой кислоты и получают п-метилфеноксипроизводное 65 На это трифенилфосфина с образованием в качестве соединение действуют йодистым метилом и гидпромежуточного соединения 16-р-тиоацетата G, ридом натрия в диметилформамиде, с целью мекоторый затем гидроли-зуют в присутствии оснотилирования атома азота в кольце и получения вания и получают тиол Н Алкилирование провосоединения 67 Иначе, соединения 65 обрабатыдят, получая меркаптидный анион с помощью гидвают раствором DDQ и BSTFA в толуоле, формирида натрия или гидрида натрия в руя двойную связь в положении 1, и получают сотетрагидрофуране или N,N -дим етил форм амиединение 66 де, с последующим добавлением соответствующего ал кил галоген ид а Указанный способ примеПредставленные на схеме 13 ингибиторы поняют в примерах 31 - 33 Соответствующие лучают следующим образом Исходный 16-спирт сульфоны, такие как 34, получают, действуя на 25 обрабатывают метансульфокислотой в пирипромежуточные тиоэфиры 31 - 33 окислителем, дине, содержащем 4-диметиламинопиридин, и таким как органическая надкислота или пероксиполучают мезилат77 Его, в свою очередь, обрамоносульфат натрия (OXONE) в метаноле батывают соответствующим тиофенолом в безводном ТГФ, содержащем гидрид натрия, и полуПредставленные на Схеме 10 ингибиторы почают тиофенокси производное 78, 4лучают следующими синтетическими способами хлортиофенокси производное 79, 4п-Нитрофенокси производное 50 восстанавливают фтортиофенокси производное 80, 4палладием на угле при комнатной температуре в метилтиофенокси производное 81 и 4атмосфере водорода с образованием пметокситиофенокси производное 82 Обрабатыаминофенокси производного 51 Амин далее ацивая тиофенокси производное 78 млируют с помощью хлористого ацетила в хлорихлорнадбензойной кислотой в хлористом метилестом метилене в присутствии пиридина с образоне в течение 1 часа при температуре 0°С, получаванием п-ацетиламикофенокси производного 52 ют фенилсульфинильное производное 83 Обраили аналогичным образом обрабатывают хлориботкой фенилсульфинильного производного 83 в стым бензоилом и получают соответствующий птех же условиях, однако в течение трех часов, бензоиламино аналог 53 Иначе, аминопроизводполучают фенил су льфонильное производное 84 ное 51 обрабатывают хлористым тозилом и полуПредставленные на Схеме 14 ингибиторы почают п-тозиламино аналог 54 лучают следующим образом 16-Кетон (11) обраПредставленные на Схеме 11 ингибиторы побатывают подходящим арилметилдиэтилфосфолучают следующим образом Защищенный с понатом в условиях реакции Виттига, используя мощью І\І-2,4-диметоксибензильной группы 16гидрид натрия в ДМФА, при температуре 80 спирт 55 обрабатывают п-фторхлорбензолом и 100°С, и получают соответствующие 4гидридом калия в диметилформамиде с образохлорбензилиденовые 71, бензилиденовые 72 и 4ванием п-хлорфенокси производного 56, которое метилбензилиденовые 73 аналоги Их восстанавзатем обрабатывают трифторуксусной кислотой в ливают в этаноле в атмосфере водорода, исхлористом метилене, целью удаления защитной пользуя в качестве катализатора 5%-ный радий на Н-2,4-диметоксибензильной группы, и получают угле, и получают соответствующие 4соединение 57 Его обрабатывают газообразным хлорбензольное производное 74 и 4водородом и палладием на угле в метаноле, с метилбензольное производное 75 Так же в две целью удаления атома хлора из фенильного стадии получают 3-пиридилметильный аналог 76 кольца, и получают феноксипроизводное 58 На это соединение действуют йодистым метилом и гидридом натрия в диметилформа-миде для метилирования атома азота в кольце и получения соединения 61 Иначе, соединения 58 обрабаты 44257 35 36 СХЕМА 4 СХЕМА І 1.KOBu,f-BuOH 2. гам, 96% N,H« r^T-^v І І I O )—'ОН ANA^ СИ, д дакстияошй эфнр"а (2) 60%AcQH, кимчение «nHNaHSO,, 50% EiQH. JWBM 0.5 N HCI, СН 2 СІг ЄіОН СНэ (D) 'ОН X^L-ч кон, дмсо. жш СНЭ! I (10} сн. CH 3 "ЮСН, fS^Xs^y^y сн. (3): R7 СХЕМА S (4): R7 в СН г СН-СН г LKOffla, МЗиОН СХЕМА Ї AcOH.MjQ NOH J&о -10Х AcjO У PhCOC!, ___ пиридин, -(-дямеяиашямпийинн ' СНС1 NHCOR9 Д ы А^Л,„ и "СН СН3 илв | КН/ДМФД КОН/ДМСО 9 І м и и R i or R s Br Э (11) (13): Я* « СН Э ; i (7):R -Pft {1S):R 9 «CH 2 CH«CH 2 ; (1B):R9 = CH z Ph; СХЕМА З ^ ' (17): R9 4-шш«чпамйнотрвдин, С Н ^ Ca, (2) Ф) «ОТ: H2,io%Pd(C),ElOAc г с к 38 44257 37 СХЕМА « CXEMA8 сна до хсхн «w»peryp« Р г -НогСНз КН. ДМФА KH, ДМФА m ( 2 1 } R l 0 = CN; СШИА9 (22) R ' ° = . C F 3 D {23)-R' -=C!; -.«он CXEMA7 О" "N" I CH-, 4-МОгСбН4СО2Н. PhgP, С 6 Н 6 А 0.4 N водный NaOK р~ CHa 2 Н 2 ,10%Pd(C}, ЕЮАс (25) gC H3 V ^СИ, 3 CHaCOSH, ТГФ SAc 39 44257 СХЕМА 10 .о 40 OBU.U. Hj,io%Pd;D NH-Tos СН, ОШУІАІЗ 0 M s 41 СХШАІ4 Следующие примеры приведены, чтобы подробнее пояснить способы получения соединений по настоящему изобретению Следует понимать, что примеры ни в коем случае не ограничивают настоящее изобретение Далее, не следует рассматривать приведенные ниже примеры в качестве единственных примеров, которые составляют сущность настоящего изобретение, такчто комбинация соединений или их фрагментов может составлять объект изобретения Для специалистов должно быть понятно, что известные вариации условий и способов осуществления следующих методик могут быть использованы для получения этих соединений Все величины температуры, если специально не оговаривается, приведены в градусах Цельсия Исходный 4-аза-4-метил-5-а-андростан-3,17дион (соединение А на приведенной выше Схеме 1) может быть получено в соответствии с методиками, приведенными в публикации Rasmusson et al, М J Med Chem , Vol 27, p 1690 - 1701 (1984) Исходный 4-аза-4,7-р-диметил-5-аандростан-3,17-дион может быть получен по методике, приведенной ниже в Примере 36 Пример 1 4-Аза-4-метил-5-а-андростан-3,16-дион Стадия 1 4-аза-4-метил-5-а-андростан-3,17дион-16-оксим К 2-метил-2-пропанолу (14мл) в круглодонной колбе при продувке азотом добавляют третбутоксид калия (740мг, 6,59ммол) После того, как образуется прозрачный раствор при перемешивании добавляют 4-аза-4-метил-5-а-андростан-3,17дион (1,0г, З.ЗОммол) и перемешивание продолжают в течение часа, при этом образуется раствор золотистого цвета К реакционной смеси по каплям добавляют изоамил нитрит (0,884мл, 6,58ммол) и оставляют на ночь перемешиваться при комнатной температуре, при этом образуется раствор темно-оранжевого цвета Смесь, разбавляют равным объемом воды и подкисляют приблизительно до рН 2 с помощью 2 N соляной кислоты Добавляют диэтиловый эфир и полученное твердое вещество отфильтровывают, промывают эфиром, сушат в вакууме и получают целевое соединение 44257 42 Стадия 2 4-аза-4-метил-5-а-андростан-3-он16-оксим К смеси 4-аза-4-метил-5-а-андростан3,17-дион-16-оксима (596мг, 1,79ммол) в этиленгликоле (5мл) добавляют 98%-ный гидразин (57мкл, 1,74ммол) и порошкообразный гидроксид калия (568мг, 10,12ммол) Смесь нагревают в течение 16 час до температуры 140°С, охлаждают и нейтрализуют 2 N раствором соляной кислоты Полученное твердое вещество отфильтровывают, промывают водой, сушат в вакууме и получают целевое соединение, масс-спектр m/z 318 (М) Стадия 3 4-аза-4-метил-5-а-андростан-3,16дион Смесь 4-аза-4-метил-5-а-андростан-3-он-16оксима (218мг, 0,684ммол) и бисульфита натрия (249мг,23,9ммол) в 50%-ном водном этаноле (10мл) кипятят с обратным холодильником в течение 3 часов Добавляют разбавленную соляную кислоту (0.5N, 33мл) и хлористый метилен (50мл) и энергично перемешивают смесь в течение нескольких минут Органический слой отделяют и промывают раствором бикарбоната натрия, насыщенным раствором соли, сушат (над сульфатом натрия) и упаривают Целевой продукт очищают методом флэш хроматографии на силикагеле, используя в качестве элюента 15% раствор ацетона в хлористом метилене, и получают целевое соединение FAB масс-спектр m/z 304 (М+1) 400Мгц ПМР (хлороформ-d) 5 0,89 (синглет, ЗН), 0,91 (синглет, ЗН), 2,90 (синглет, ЗН), 3,05 (дублет дублетов, 1Н) Пример 2 3-Оксо-4-аза-4-метил-16-р-гидрокси-5-аандростан Раствор 4-аза-4-метил-5-а-андростан-3,16диона (100мг, О.ЗЗОммол) в метаноле (2мл) охлаждают в бане со льдом и в течение 1 час добавляют боргадрид натрия (38мг, 0,989ммол) Разбавляют реакционную смесь водой и экстрагируют хлористым метиленом (2 • 20мл) Органические вытяжки объединяют, промывают насыщенным раствором соли, сушат (над сульфатом натрия) и упаривают Целевой продукт очищают методом испарительной хроматографии на силикагеле, используя в качестве элюента 10% раствор ацетона в хлористом метилене, и получают целевое соединение Масс-спектр rn/z 391 (М) 400Мгц ПМР (хлороформ-d) 5 0,88 (синглет, 6Н), 2,90 (синглет, ЗН), 3,00 (дублет дублетов, 1Н), 3,21 (синглет, ЗН), 3,83 (мультиплет, 1Н) Пример 4 3-Оксо-4-аза-4-метил-16-р-аллилокси-5-аандростан Указанное соединение получают по методике, аналогичной приведенной в Примере 3, взяв вместо йодистого метила бромистый аллил Массспектр m/z 345 (М) 400Мгц ПМР (хлороформ-d) 5 0,88 (синглет, ЗН), 0,90 (синглет, ЗН), 2,90 (синглет, ЗН), 3,00 (дублет дублетов, 1Н), 3,90 (мультиплет, 2Н), 3,99 (мультиплет, 1Н), 5,11-5,27 (мультиплет, 2Н), 5,83-5,93 (мультиплет, 1Н) Пример 5 3-Оксо-4-аза-4-метил-16-р-(н-пропилокси)-5-аандростан Раствор 3-оксо-4-аза-4-метил-16-р-аллилокси 43 44257 44 5-а-андростана в зтилацетате (0,85мл) гидрируют бензиламинокарбонилокси-5-а-андростан в атмосфере водорода в присутствии оксида плаК раствору 3-оксо-4-аза-4-метил-16-ртины (4мг) в течение 30 минут при комнатной темгидрокси-5-а-андростана (40мг, 0,131ммол) в хлопературе Катализатор удаляют путем фильтраристом метилене (2мл) добавляют триэтиламин ции через фильтрующий элемент Millex-HV с (67мкл, 0,481 ммол), 4-диметиламинопиридин (2мг) размером пор 0,45мкм Очищают методом флэш и бензилизоцианат (50мкл, 0,405ммол) Реакционхроматографии на силикагеле, используя в каченую смесь перемешивают в течение 48 час при стве элюента 10% раствор ацетона в хлористом комнатной температуре, упаривают и очищают метилене, и получают целевое соединение Массметодом флэш хроматографии на силикагеле, спектр m/z 348 (М+1) 400Мгц ПМР (хлороформиспользуя в качестве элюента 15% раствор ацеd) 5 0,88 (синглет, ЗН), 0,89 (синглет, ЗН), 2,90 тона в хлористом метилене, и получают целевое (синглет, ЗН), 3,00 (дублет дублетов, 1Н), 3,28 соединение FAB масс-спектр m/z 439 (М+1) (триплет, 2Н), 3,92 (мультиплет, 1Н) 400Мгц ПМР (хлороформ-d) 5 0,87 (синглет, Пример 6 6Н), 2,90 (синглет, ЗН), 3,00 (дублет дублетов, 1Н), 3-Оксо-4-аза-4-метил-16-р-(ацетамидо)-5-а4,33 (мультиплет, 2Н), 4,90 (мультиплет, 1Н), 5,11 андростан (мультиплет, 1Н) Стадия 1 3-оксо-4-аза-4-метил-16-р-амино-5Пример 9 а-андростан 3-Оксо-4-аза-4-метил-16-а-гидрокси-5-аандростан Раствор 4-аза-4-метил-5-а-андростан-3-он-16оксима (150мг, 0,471 ммол) в смеси этанол (15мл) Стадия 1 3-оксо-4-аза-4-метил-16-а-(4уксусная кислота (7мл) оставляют на ночь гидринитробензоилокси)-5-а-андростан роваться при комнатной температуре и при атмоК раствору 3-оксо-4-аза-4-метил-16-рсферном давлении в присутствии оксида платины гидрокси-5-а-андростана (34мг, 0,0111 ммол) в (50мг) Катализатор удаляют фильтрацией через сухом бензоле (1,5мл) добавляют трифенилфосфильтрующий элемент Millex-HV с размером пор фин (35мг, 0,134ммол), 4-нитробензойную кислоту 0,45мкм Остаток растворяют в хлористом мети(22мг, 0,134ммол) и диэтиловый эфир азодикарлене (50мл) и раствор промывают насыщенным боновой кислоты (2ІМКЛ, 0,134ммол), реакраствором бикарбоната натрия, насыщенным расционную смесь нагревают в атмосфере азота в твором соли, сушат (над сульфатом натрия) и течение 1 часа до температуры 80°С (температуупаривают, получая целевой амин ра масляной бани) Бензол упаривают при поСтадия 2 3-оксо-4-аза-4-метил-16-рниженном давлении и сырой продукт подвергают (ацетамидо)-5-а-андростан очистке хроматографией на силикагеле, испольАмин, полученный на стадии 1 (56мг, зуя в качестве элюента 2%-ный раствор метанола 0,184ммол) растворяют в хлористом метилене в хлористом метилене, и получают целевой про(1,0мл), добавляют пиридин (0,6мл), 4дукт, содержащий небольшое количество трифедиметиламинопиридин (5мг) и уксусный ангидрид нилфосфина (97мг), который омыляют как описа(0,3мл) и перемешивают при комнатной темперано на Стадии 2 туре в течение 2 часов Разбавляют реакционную Стадия 2 3-оксо-4-аза-4-метил-1 ба-гидроксисмесь хлористым метиленом, органический слой 5-а-андростан Сырой продукт со Стадии 1 (97мг) отделяют, промывают водой, 1 N раствором солясуспендируют в этаноле (0,5мл) и обрабатывают ной кислоты, насыщенным раствором бикарбона0,4 N раствором гидроксида натрия (0,36мл, та натрия, насыщенным раствором соли, сушат 0,144ммол) После перемешивания в течение 90 (над сульфатом натрия) и упаривают Целевой минут при комнатной температуре реакционную продукт очищают методом испарительной хромасмесь нейтрализуют, добавив несколько капель тографии на силикагеле, используя в качестве ледяной уксусной кислоты, экстрагируют этилацеэлюента 2% раствор метанола в хлористом метитатом (2 • 20мл), промывают водой (20мл), насылене, и получают целевое соединение Массщенным раствором соли, сушат (над сульфатом спектр m/z 346 (М) натрия) и упаривают Продукт подвергают очистке 400Мгц ПМР (хлороформ-d) 5 0,82 (синглет, хроматографией на силикагеле, используя в качеЗН), 0,87 (синглет, ЗН), 1,93 (синглет, ЗН), 2,90 стве элюента 20%-ный раствор метанола в хлори(синглет, ЗН), 3,00 (дублет дублетов, 1Н), 4,28 стом метилене Масс-спектр m/z 305 (М) (мультиплет, 1Н), 5,54 (дублет, 1Н) 400Мгц ПМР (хлороформ-d) 5 0,70 (синглет, Пример 7 ЗН), 0,85 (синглет, ЗН), 2,90 (синглет, ЗН), 3,02 3-Оксо-4-аза-4-метил-16-р-(бензамидо)-5-а(дублет дублетов, 1Н), 4,47 (мультиплет, 1Н) андростан Пример 10 Указанное соединение получают по методике, 3-Оксо-4-аза-4-метил-16-а-метокси-5-ааналогичной приведенной в Примере 6, взяв вмеандростан сто уксусного ангидрида хлористый бензоил К раствору 3-оксо-4-аза-4-метил-16а-гидроксиМасс-спектр m/z 408 (М) 5-а-андростана (20мг, 0,065ммол) в диметил400Мгц ПМР (хлороформ-d) 5 0,89 (синглет, сульфоксиде (0,6мл) добавляют порошкообразЗН), 0,90 (синглет, ЗН), 2,90 (синглет, ЗН), 3,01 ный гидроксид калия (18мг, 0,325ммол) После (дублет дублетов, 1Н), 4,48 (мультиплет, 1Н), 6,12 перемешивания при комнатной температуре в (дублет, 1Н) атмосфере азота в течение 15 минут добавляют Пример 8 йодистый метил (20мкл, 0,325ммол) и оставляют 3-Оксо-4-аза-4-метил-16-рперемешиваться на ночь Разбавляют реакцион 45 44257 46 ную смесь эфиром (25мл), органический слой отняют и промывают раствором бикарбоната деляют, промывают водой (2 • 10мл), насыщенным натрия, сушат (над сульфатом натрия) и упаривараствором соли, сушат (над сульфатом натрия) и ют Целевой продукт очищают методом испариупаривают Целевой продукт очищают методом тельной хроматографии на силикагеле, используя флэш хроматографии на силикагеле, используя в в качестве элюента 2% раствор метанола в хлокачестве элюента 10% раствор ацетона в хлориристом метилене, и получают целевое соединестом метилене, и получают целевое соединение ние Масс-спектр m/z317(M) Масс-спектр m/z319(M) 400Мгц ПМР (хлороформ-d) 5 0,88 (синглет, ЗН), 0,89 (синглет, ЗН), 1,00 (дублет, ЗН), 2,90 400Мгц ПМР (хлороформ-d) 5 0,70 (синглет, (синглет, ЗН), 3,07 (дублет дублетов, 1Н) ЗН), 0,87 (синглет, ЗН), 2,90 (синглет, ЗН), 3,01 Пример 12 (дублет дублетов, 1Н), 3, 22 (синглет, ЗН), 3,92 3-Оксо-4-аза-4,7-р-диметил-16-р-гидрокси-5-а(мультиплет, 1Н) андростан Пример 11 4-Аза-4,7-р-диметил-5-а-андростан- 3,16-дион Раствор 4-аза-4,7-р-диметил-5-а-андростан3,16-диона (390мг, 1,23ммол) в метаноле (8мл) Стадия 1 4-аза-4,7-р-диметил-5-а-андростанохлаждают в бане со льдом и в течение 30 минут 3,17-дион-16-оксим добавляют боргадрид натрия (140мг, 3,68ммол) К 2-метил-2-пропанолу (28мл) в круглодонной Разбавляют реакционную смесь водой и экстрагиколбе при продувке азотом добавляют третруют хлористым метиленом (3 • 50 мл) Органичебутоксид калия (1,35г, 12,1ммол) После того, как ские вытяжки объединяют, промывают насыщенобразуется прозрачный раствор при перемешиваным раствором соли, сушат (над сульфатом нии добавляют 4-аза-4,7-р-диметил-5-анатрия) и упаривают Целевой продукт очищают андростан-3,17-дион (1,92г, б.Оммол) и перемеметодом флэш хроматографии на силикагеле, шивание продолжают в течение часа, при этом используя в качестве элюента вначале 10% расобразуется раствор золотистого цвета К реакцитвор ацетона в хлористом метилене, а затем 10% онной смеси по каплям добавляют изоамилнитрит раствор ацетона в хлористом метилене, и полу(1,63мл, 12,1ммол) и оставляют на ночь перемечают целевое соединение Масс- спектр m/z шиваться при комнатной температуре, при этом 391 (М) образуется раствор темно-оранжевого цвета 400Мгц ПМР (хлороформ-d) 5 0,83 (синглет, Смесь разбавляют равным объемом воды, подЗН), 0,96 (синглет, ЗН), 1,03 (дублет, ЗН), 2,90 кисляют приблизительно до рН 2 с помощью 2 N (синглет, ЗН), 3,00 (дублет дублетов, 1Н), 4,36 соляной кислоты и экстрагируют диэтиловым (мультиплет, 1Н) эфиром (3 • 50 мл) Эфирные вытяжки объединяПример 13 ют, промывают насыщенным раствором соли, су3-Оксо-4-аза-4,7-р-диметил-16-р-метокси-5-ашат ( над сульфатом натрия) и упаривают Полуандростан ченный твердый продукт подвергают очистке методом хроматографии на силикагеле, используя К раствору 3-оксо-4-аза-4,7-р-диметил-16-рв качестве элюента 5%-ный раствор метанола в гидрокси-5-а-андростана (20мг, 0,063ммол) в дихлористом метилене, и получают целевое соедиметилсульфоксиде (0,5мл) добавляют порошнение кообразный гидроксид калия (18мг, 0,313ммол) Стадия 2 4-аза-4,7-р-диметил-5-а-андростанПосле перемешивания при комнатной температу3-ОН-16-ОКСИМ ре в атмосфере азота в течение 15 минут доК смеси 4-аза-4,7-р-диметил-5-а-андростанбавляют йодистый метил (20мкл, 0,313ммол) и 3,17-дион-16-оксима (2,7г, 7,79ммол) в этиленглиоставляют перемешиваться на ночь Разбавляют коле (30мл) добавляют 98%-ный гидразин (0,27мл, реакционную смесь диэтиловым эфиром (25мл), 8,57ммол) и порошкообразный гидроксид калия органический слой отделяют, промывают водой, (2,62г, 46,8ммол) Смесь нагревают в течение 3 насыщенным раствором соли, сушат (над сульфачаов до температуры 140°С, охлаждают, разбавтом натрия) и упаривают Целевой продукт очиляют водой (100мл), нейтрализуют концентрирощают методом флэш хроматографии на силикагеванной соляной кислотами полученный осадок ле, используя в качестве элюента 1,5% раствор коричневого цвета отфильтровывают и сушат метанола в хлористом метилене, и получают це(1,7г) Полученный твердый продукт подвергают левое соединение Масс-спектр rn/z334(M+1) очистке методом хроматографии на силикагеле, 400Мгц ПМР (хлороформ-d) 5 0,83 (синглет, используя в качестве элюента вначале 2%-ный ЗН), 0,89 (синглет, ЗН), 1,03 (дублет, ЗН), 2,90 раствор метанола в хлористом метилене, а затем (синглет, ЗН), 3,00 (дублет дублетов, 1Н), 3,34 5%-ный раствор метанола в хлористом метилене, (синглет, ЗН), 3,80 (мультиплет, 1Н) и получают целевое соединение Пример 14 Стадия 3 4-аза-4,17-р-диметил-5-а3-Оксо-4-аза-4,7-р-диметил-16-р-этилокси-5-аандростан-3,16-дион андростан Смесь 4-аза-4,7-р-диметил-5-а-андростан-3Указанное соединение получают по методике, он-16-оксима (0,55г, 1,65ммол) и бисульфита нааналогичной приведенной в Примере 13, взяв йотрия (249мг, 23,9ммол) в 60%-ной уксусной кислодистый этил вместо йодистого метила и гидрид те (20мл) кипятят с обратным холодильником в калия в N.N-диметилформамиде вместо гидрокситечение 48 часов Охлажденную смесь разбавляда калия Масс-спектр m/z 347 (М) ют водой (25мл) и экстрагируют хлористым мети400Мгц ПМР (хлороформ-d) 5 0,83 (синглет, леном (3 • 50 мл), органические вытяжки объедиЗН), 0,90 (синглет, ЗН), 1,03 (дублет, ЗН), 1,18 47 44257 48 (триплет, ЗН), 2,30 (синглет, ЗН), 3,00 (дублет давлении в присутствии оксида 10%-ного палладублетов, 1Н), 3,39 (мультиплет, 2Н), 4,40 (мульдия на угле (Змг) в течение 30 минут при комнаттиплет, 1Н) ной температуре Катализатор удаляют фильтраПример 15 цией через фильтрующий элемент Millex-HV с 3-Оксо-4-аза-4,7-р-диметил-16-р-аллилокси-5размером пор 0,45мкм Очищают методом флэш а-андростан хроматографии на силикагеле, используя в качестве элюента 2% раствор метанола в хлористом Указанное соединение получают по методике, метилене, и получают целевое соединение Массаналогичной приведенной в Примере 13, взяв спектр m/z 389 (М) вместо йодистого метила бромистый аллил Масс400Мгц ПМР (хлороформ-d) 5 0,82 (синглет, спектр m/z 359 (М) ЗН), 0,88 (синглет, ЗН), 1,03 (дублет, ЗН), 2,90 400Мгц ПМР (хлороформ-d) 5 0,83 (синглет, (синглет, ЗН), 3,00 (дублет дублетов, 1Н), 3,33 ЗН), 0,91 (синглет, ЗН), 1,04 (дублет, ЗН), 2,90 (мультиплет, 2Н), 3,88 (мультиплет, 1Н) (синглет, ЗН), 3,00 (дублет дублетов, 1Н), 3,90 Пример 20 (мультиплет, 2Н), 3,96 (мультиплет, 1Н), 5,11-5,29 3-Оксо-4-аза-4,7-р-диметил-16-р-(трет(мультиплет, 2Н), 5,85-5,93 (мультиплет, 1Н) бутокси)-5-а-андростан Пример 16 3-Оксо-4-аза-4,7-р-диметил-16-р-бензилоксиК раствору 3-оксо-4-аза-4,7-р-диметил-16-р5-а-андростан гидрокси-5-а-андростана (20мг, 0,063ммол) в хлористом метилене (0,5мл), охлажденному в бане со Указанное соединение получают по методике, льдом, добавляют трет-бутилтрихлорацетамидат аналогичной приведенной в Примере 14, взяв (23мкл, 0,126ммол) и трифторметансульфокисловместо йодистого метила бромистый бензил ту (0,56мкл, 0,0063ммол), дают реакционной смеМасс-спектр m/z 409 (М) си нагреться до комнатной температуры и через 400Мгц ПМР (хлороформ-d) 5 0,85 (снимет, один час вносят дополнительные количества третЗН), 0,95 (синглет, ЗН), 1,04 (дублет, ЗН), 2,90 бутилтрихлорацетамидата (23мкл) и трифторме(синглет, ЗН), 3,00 (дублет дублетов, 1Н), 4,01 тансульфокислоты (0,56мкл) По прошествии од(мультиплет, 1Н), 4,43 (квартет, 2Н), 7,31 (мультиного часа добавляют третью порцию каждого реаплет, 5Н) гента и реакционную смесь перемешивают при Пример 17 комнатной температуре в течение 5 часов Раз3-Оксо-4-аза-4,7-р-диметил-16-р-(3,3бавляют реакционную смесь диэтиловым эфиром диметилаллилокси)-5-а-андростан (50мл), органический слой отделяют, промывают 1 Указанное соединение получают по методике, N водным раствором гидроксида натрия (10мл), 1 аналогичной приведенной в Примере 13, взяв N раствором соляной кислоты (10мл), насыщенвместо йодистого метила бромистый 3,3ным раствором бикарбоната натрия, сушат (над диметилаллил сульфатом натрия) и упаривают Целевой продукт 400Мгц ПМР (хлороформ-d) 5 0,82 (синглет, очищают методом флэш хроматографии на силиЗН), 0,90 (синглет, ЗН), 1,02 (дублет, ЗН), 1,67 кагеле, используя в качестве элюента 10% рас(синглет, ЗН), 1,71 (синглет, ЗН), 2,90 (синглет, твор ацетона в хлористом метилене, и получают ЗН), 3,00 (дублет дублетов, 1Н), 3,93 (мультиплет, целевое соединение Масс-спектр m/z 375 (М) 2Н), 5,31 (мультиплет, 1Н) 400Мщ ПМР (хлороформ-d) 5 0,82 (синглет, Пример 18 ЗН), 0,90 (синглет, ЗН), 1,03 (дублет, ЗН), 1,11 3-Оксо-4-аза-4,7-р-диметил-16-р-(н(синглет, 9Н), 2,90 (синглет, ЗН), 3,00 (дублет дубпропилокси)-5-а-андростан летов, 1Н), 4,00 (мультиплет, 1Н) Раствор 3-оксо-4-аза-4,7-р-диметил-16-рПример 21 аллилокси-5-а-андростана (13,0мг, О.ОЗбммол) в 3-Оксо-4-аза-4,7-р-диметил-16-р -(4етилацетате (0,5мл) гидрируют при атмосферном цианофенокси)-5-а-андростан давлении в присутствии оксида платины (4мг) в К раствору 3-оксо-4-аза-4,7-р-диметил-16-ртечение 30 минут при комнатной температуре, гидрокси-5-а-андростана (20мг, 0,063ммол) в N,Nкатализатор удаляют фильтрацией через фильтдиметилформамиде (0,5мл) добавляют порошкорующий элемент Millex-HV с размером пор образный гидрид калия (35% вес) (15мг, 0,45мкм Очищают методом флэш хроматографии 0,126ммол) Перемешивают при комнатной темна силикагеле, используя в качестве элюента 1% пературе в атмосфере азота в течение 15 минут, раствор метанола в хлористом метилене, и полудобавляют 4-фторбензонитрил (38мг, 0,315ммол) чают целевое соединение Масс-спектр m/z и перемешивают при комнатной температуре еще 361 (М) в течение 2 часов Разбавляют смесь хлористым 400Мгц ПМР (хлороформ-d) 5 0 82 (синглет, метиленом (25мл) и выливают в ледяную воду ЗН), 0,89 (синглет, ЗН), 0,89 (триплет, ЗН), 1,05 Водный слой экстрагируют хлористым метиленом (дублет, ЗН), 2,90 (синглет, ЗН), 3,00 (дублет дуб(3 • 25 мл), органические вытяжки объединяют, летов, 1Н), 3,29 (триплет, 2Н), 3,89 (мультипромывают насыщенным раствором соли, сушат плет, 1Н) (над сульфатом натрия) и упаривают Целевой Пример 19 продует очищают методом флэш хроматографии 3-Оксо-4-аза-4,7-р-диметил-16-р-(3-метил-1 на силикагеле, используя в качестве элюента внабутил-окси)-5-а-андростан чале 1,5% раствор метанола в хлористом метилеРаствор 3-оксо-4-аза-4,7-а-диметил-16-а-(3,3не, а затем 2% раствор метанола в хлористом диметилаллилокси)-5-а-андростана (12,0мг) в метилене, и получают целевое соединение Массэтилацетате (0,5мл) гидрируют при атмосферном 49 44257 50 спектр m/z 420 (М) Стадия 2 3-оксо-4-аза-4,7-р-диметил-16-а400Мгц ПМР (хлороформ-d) 5 0,86 (синглет, гидрокси-5-а-андростан ЗН), 0,92 (синглет, ЗН), 1,04 (дублет, ЗН), 2,90 Сырой продукт со Стадии 1 (404мг) суспенди(синглет, ЗН), 3,02 (дублет дублетов, 1Н), 4,76 руют в этаноле (5мл) и обрабатывают 0,4 N рас(мультиплет, 1Н), 6,87 (мультиплет, 2Н), 7,53 твором гидроксида натрия (1,82мл,0,728ммол) (мультиплет, 2Н) После перемешивания в течение 90 минут при Пример 22 комнатной температуре реакционную смесь ней3-Оксо-4-аза-4,7-р-диметил-16-р-(4трализуют, добавив несколько капель ледяной трифторметил-фенокси)-5-р-андростан уксусной кислоты, экстрагируют этилацетатом Указанное соединение получают по методике, (100мл), промывают водой (2 • 25 мл), насыщенаналогичной приведенной в Примере 21, взяв 4ным раствором соли, сушат (над сульфатом нафторбензотрифторид вместо 4трия) и упаривают Продукт подвергают очистке фторбензонитрила Масс-спектр m/z 463 (М) хроматографией на силикагеле, используя в каче400Мгц ПМР (хлороформ-d) 5 0,85 (синглет, стве элюента 20%-ный раствор ацетона в хлориЗН), 0,93 (синглет, ЗН), 1,04 (дублет, ЗН), 2,90 стом метилене Масс-спектр m/z 319 (М) (синглет, ЗН), 3,02 (дублет дублетов, 1Н), 4,76 400Мгц ПМР (хлороформ-d) 5 0,71 (синглет, (мультиплет, 1Н), 6,88 (мультиплет, 2Н), 7,50 ЗН), 0,82 (синглет, ЗН), 1,02 (дублет, ЗН), 2,90 (дублет, 2Н) (синглет, ЗН), 3,03 (дублет дублетов, 1Н), 4,42 Пример 23 (мультиплет, 1Н) 3-Оксо-4-аза-4,7-р-диметил-16-р-(4Пример 26 хлорфенокси)-5-а-андростан 3-Оксо-4-аза-4,7-р-диметил-16-а-(нпропилокси)-5-а-андростан Указанное соединение получают по методике, аналогичной приведенной в Примере 21, взяв 1К раствору 3-оксо-4-аза-4,7-р-диметил-16-ахлор-4-фторбензол вместо 4-фторбензонитрила гидрокси-5-а-андростана (20мг, 0,063ммоль) в Масс-спектр m/z430(M+1) N.N-диметилформамиде (0,5мг) добавляют гидрид 400Мгц ПМР (хлороформ-d) 5 0,85 (синглет, калия (35% вес) (15мг, 0,126ммол) ПеремешиваЗН), 0,93 (синглет, ЗН), 1,03 (дублет, ЗН), 2,90 ют в атмосфере азота при комнатной температуре (синглет, ЗН), 3,02 (дублет дублетов, 1Н), 5,28 в течение 15 минут, добавляют бромистый аллил (мультиплет, 1Н), 6,74 (дублет, 2Н), 7,19 (дуб(27мкл, 0,315ммол) и перемешивают еще в течелет, 2Н) ние 2 час Добавляют дополнительные количества Пример 24 гидрида калия (15мг) и бромистого аллила (27мкл) Указанное соединение получают по методике, и оставляют перемешиваться на ночь Разаналогичной приведенной в Примере 21, взяв 1,4бавляют реакционную смесь диэтиловым эфиром дифторбензол вместо 4-фторбензонитрила Масс(50мл) и водой (10мл) Органический слой отдеспектр m/z 414 (М+1) ляют, промывают 1 N раствором соляной кислоты 400Мгц ПМР (хлороформ-d) 5 0,85 (синглет, (10мл), водой (1 0мл), насыщенным раствором ЗН), 0,94 (синглет, ЗН), 1,04 (дублет, ЗН), 2,91 бикарбоната натрия, сушат (над сульфатом на(синглет, ЗН), 3,02 (дублет дублетов, 1Н), 4,65 трия) и упаривают Целевой продукт очищают ме(мультиплет, 1Н), 6,75 (мультиплет, 2Н), 6,92 тодом испарительной хроматографии на силика(мультиплет, 2Н) геле, используя в качестве элюента 2% раствор Пример 25 метанола в хлористом метилене Полученный 3-Оксо-4-аза-4,7-р-диметил-16а-гидрокси-5-апродукт гидрируют в этилацетате (0,5мл) в приандростан сутствии 10%-ного палладия на угле в течение 2 Стадия 1 3-оксо-4-аза-4,7-р-диметил-16-а-(4часов Катализатор удаляют путем фильтрации нитробензоилокси)-5-а-андростан через фильтрующий элемент Millex-HV с размером пор 0,45мкм Очищают методом испарительК раствору 3-оксо-4-аза-4,7-р-диметил-16-рной хроматографии на силикагеле, используя в гидрокси-5-а-андростана (178мг, 0,560ммоль), в качестве элюента 10% раствор изопропанола в сухом бензоле (10мл) добавляют трифенилгексане, и получают целевое соединение Массфосфин (294мг, 1,12ммол), 4-нитробензойную спектр m/z 361 (М) кислоту (187мг, 1,12ммол) и диэтиловый эфир 400Мгц ПМР (хлороформ-d) 5 0,76 (синглет, азодикарбоновой кислоты (176мкл, 1,12ммол) ЗН), 0,52 (синглет, ЗН), 0,90 (триплет, ЗН), 1,02 Реакционную смесь нагревают в атмосфере азота (дублет, ЗН), 2,90 (синглет, ЗН), 3,02 (дублет дубв течение 1 часа до температуры 80°С (темпералетов, 1Н), 3,29 (триплет, 2Н), 3,98 (мультиплет, тура масляной бани) Бензол упаривают при по1Н) ниженном давлении и сырой продукт подвергают Пример 27 очистке хроматографией на силикагеле, исполь3-Оксо-4-аза-4,16-а-диметил-16-р-гидрокси-5зуя в качестве элюента 2%-ный раствор метанола а-андростан в хлористом метилене, и получают целевой проК раствору 4-аза-4-метил-5-а-андростан-3,16дукт, содержащий небольшое количество трифедиона (50мг, 0,165ммол), охлажденному до минус нилфосфина (404мг), который омыляют как опи40°С по каплям при перемешивании добавляют сано на Стадии 2 метилмагнийбромид (3,0М раствор в диэтиловом 400Мгц ПМР (хлороформ-d), 5 0,80 (синглет, эфире) (275мкл, 0,825ммол) Дают реакционной ЗН), 0,88 (синглет, ЗН), 1,03 (дублет, ЗН), 2,90 смеси нагреться до комнатной температуры и пе(синглет, ЗН), 3,05 (дублет дублетов, 1Н), 5,48 ремешивают в течение 2 часов в атмосфере азо(мультиплет, 1Н) 52 51 44257 та Прерывают реакцию, добавив насыщенный Стадия 1 3-оксо-4-аза-4,7-р-диметил-16-рраствор хлорида аммония (25мл) и экстрагируют ацетилтио-5-а-андростан хлористым метиленом (2 • 50 мл) Органические В круглодонную колбу емкостью 25мл атмовытяжки объединяют, промывают насыщенным сфере азота помещают сухой тетрагидрофуран раствором соли, сушат (над сульфатом натрия) и (4мл) и трифенилфосфин (177мг, 0,676ммол) упаривают, целевой продукт очищают методом Колбу охлаждают в бане со льдом, добавляют флэш хроматографии на силикагеле, используя в диизопропиловый эфир азодикарбоковой кислоты качестве элюента 2% раствор метанола в хлори(133мкл, 0,676ммол) и смесь перемешивают при стом метилене, и получают целевое соединение 0°С в течение 30 минут В реакционную смесь доМасс-спектр m/z319(M) бавляют раствор 3-оксо-4-аза-4,7-р-диметил-16-а400Мгц ПМР (хлороформ-d) 5 0,88 (синглет, гидрокси-5-а-андростана (108мг, 0,338ммол) и ЗН), 0,98 (синглет, ЗН), 1,31 (синглет, ЗН), 2,90 тиоуксусной кислоты (49мкл, 0,676ммол) в тетра(синглет, ЗН), 3,00 (дублет дублетов, 1Н) гидро-фуране (2,0мл) Реакционную смесь переПример 28 мешивают в течение 1 часа при температуре 0°С, 3-Оксо-4-аза-4,7-р -16-а-триметил-16-ра затем 1 час при комнатной температуре Смесь гидрокси-5-а-андростан упаривают и очищают методом флэш хроматоУказанное соединение получают по методике, графии на силикагеле, используя в качестве элюаналогичной приведенной в Примере 27, взяв 4ента 1 0% раствор ацетона в хлористом метилене аза-4,7-р-диметил-5-а-андростан-3,16-дион вмеи получают целевой продукт (содержащий несто 4-аза-4-метил-5-а-андростан-3,16-диона большое количество трифенилфосфина) Масс-спектр m/z 333 (М) 400Мгц ПМР (хлороформ-d) 5 0,80 (синглет, ЗН), 0,82 (синглет, ЗН), 1,00 (дублет, ЗН), 2,28 400Мгц ПМР (хлороформ-d) 5 0,82 (синглет, (синглет, ЗН), 2,90 (синглет, ЗН), 3,00 (дублет дубЗН), 0,98 (синглет, ЗН), 1,01 (дублет, ЗН), 1,30 летов, 1Н), 3,80 (мультиплет, ЗН) (синглет, ЗН), 2,90 (синглет, ЗН), 3,00 (дублет дубСтадия 2 3-оксо-4-аза-4,7-р-диметил-16-рлетов, 1Н) меркапто-5-а-андростан Пример 29 К раствору продукта, полученного на Стадии 1 3-Оксо-4-аза-4,16-а-диметил-16-р-метокси-5(208мг) в этаноле (4,0мл) в атмосфере азота доа-андростан бавляют 0,4 N раствор гидроксида натрия (1,8мл, К раствору 3-оксо-4-аза-4,16-а-диметил-16-р0,716ммол) После перемешивания в течение 1 гидрокси-5-а-андростана (31мг, 0,097ммол) в N,Nчаса при комнатной температуре реакционную диметилформамиде (0,5мл) добавляют гидрид смесь нейтрализуют, добавив несколько капель калия (35% вес) (23мг, 0,194ммол) Перемешиваледяной уксусной кислоты, экстрагируют этилацеют в атмосфере азота при комнатной температуре татом (100мл), промывают экстракт водой ( 2 - 1 0 в течение 15 минут, добавляют йодистый метил мл), насыщенным раствором соли, сушат (над (32мкл, 0,485ммол) и оставляют перемешиваться сульфатом натрия) и упаривают Чистый 16на ночь при комнатной температуре Разбавляют меркаптан получают после очистки хроматограреакционную смесь диэтиловым эфиром, органифией на силикагеле, используя в качестве элюенческий слой отделяют, промывают 2 N раствором та 20%-ный раствор ацетона в хлористом метисоляной кислоты (10мл), водой (10мл), насыщенлене ным раствором бикарбоната натрия, сушат (над 400Мгц ПМР (хлороформ-d) 5 0,82 (синглет, сульфатом натрия) и упаривают, целевой продукт ЗН), 0,93 (синглет, ЗН), 1,02 (дублет, ЗН), 2,90 очищают методом испарительной хроматографии (синглет, ЗН), 3,00 (дублет дублетов, 1Н), 3,28 на силикагеле, используя в качестве элюента 2% (мультиплет, 1Н) раствор метанола в хлористом метилене МассСтадия 3 3-оксо-4-аза-4,7-р-диметил-16-рспектр m/z 333 (М) метантио-5-а-андростан 400Мгц ПМР (хлороформ-d) 5 0,88 (синглет, К раствору 3-оксо-4-аза-4,7-р-диметил-16-рЗН), 0,90 (синглет, ЗН), 1,22 (дублет, ЗН), 2,90 меркапто-5-а-андростана (18мг, 0,054ммоль) в (синглет, ЗН), 3,00 (дублет дублетов, 1Н), 3,17 сухом тетрагидрофуране (0,5мл) добавляют гид(синглет, ЗН) рид натрия (80%-ная дисперсия в минеральном Пример 30 масле) (3,2мг, 0,108ммол) в атмосфере азота По3-Оксо-4-аза-4,7-р-16-а-триметил-16-рсле перемешивания при комнатной температуре в метокси-5-а-андростан атмосфере азота в течение 15 минут добавляют Указанное соединение получают по методике, йодистый метил (17мкл, 0,270ммол) и перемешианалогичной приведенной в Примере 29, взяв 3вают при комнатной температуре в течение 3 чаоксо-4-аза-4,7-р-16-а-триметил-16-р-гидрокси-5-асов Разбавляют реакционную смесь хлористым андростан вместо 3-оксо-4-аза-4,16-а-диметил-16метиленом (50мл), органический слой отделяют, р-гидрокси-5-а-андростана Масс-спектр m/z 347 промывают водой ( 10мл), насыщенным раство(М) ром соли, сушат (над сульфатом натрия) и упари400Мгц ПМР (хлороформ-d) 5 0,82 (синглет, вают Продукт очищают методом испарительной ЗН), 0,90 (синглет, ЗН), 1,02 (дублет, ЗН), 1,22 хроматографии на силикагеле, используя в каче(синглет, ЗН), 2,90 (синглет, ЗН), 3,00 (дублет дубстве элюента 10% раствор изопропилового спирта летов, 1Н), 3,18 (синглет, ЗН) в гексане, и получают целевое соединение МассПример 31 спектр m/z 349 (М) 3-Оксо-4-аза-4,7-р-диметил-16-р-метантио-5400Мгц ПМР (хлороформ-d) 5 0,82 (синглет, а-андростан 53 44257 54 ЗН), 0,91 (синглет, ЗН), 1,04 (дублет, ЗН), 2,10 на силикагеле, используя в качестве элюента 10% раствор ацетона в хлористом метилене, и полу(синглет, ЗН), 2,90 (синглет, ЗН), 3,01 (дублет дубчают целевое соединение Масс-спектра m/z летов, 1Н), 3,08 (мультиплет, 1Н) 321 (М) Пример 32 3-Оксо-4-аза-4,7-р-диметил-16-р-этантио-5-а400Мгц ПМР (хлороформ-d) 5 0,87 (синглет, ЗН), 0,92 (синглет, ЗН), 1,04 (дублет, ЗН), 2,90 андростан (синглет, ЗН), 3,01 (дублет дублетов, 1Н), 5,12 Указанное соединение получают по методике, (мультиплет, 1Н) аналогичной приведенной в Примере 31, взяв йоПример 36 дистый этил на Стадии 3 вместо йодистого метила Масс-спектр m/z 363 (М) 400Мгц ПМР (хлоПолучение 4-аза-4,7-р-диметил-5-ароформ-d) 5 0,82 (синглет, ЗН), 0,91 (синглет, ЗН), андростан-3,17-диона (Соединение Е на Схеме 5) 1,03 (дублет, ЗН), 1,24 (триплет, ЗН), 2,57 (кварСтадия 1 Синтез 3-ацетокси-андрост-5-ен-17ола тет, ЗН), 2,90 (синглет, ЗН), 3,00 (дублет дублетов, 1Н), 3,18 (мультиплет, 1Н) К раствору 100мг (О.ЗОЗммол) З-ацетоксиандрост-5-ен-17-она в Змл этанола при темпераПример 33 туре минус 10°С добавляют при перемешивании 3-Оксо-4-аза-4,7-р-диметил-16-р-(1 22,9мг (0,606ммол) боргидрида натрия Перемепропантио)-5-а-андростан шивают смесь в течение 1,3 часов, добавляют 10 Указанное соединение получают по методике, ил воды, этанол упаривают в вакууме, а остаток аналогичной приведенной в Примере 31, взяв 1экстрагируют этилацетатом Органический слой иодпропан на Стадии 3 вместо йодистого метила промывают водным раствором карбоната калия, Масс-спектр m/z 377 (М) насыщенным раствором соли, сушат над сульфа400Мгц ПМР (хлороформ-d) 5 0,82 (синглет, том натрия и упаривают, получая остаток сырого ЗН), 0,90 (синглет, ЗН), 0,98 (триплет, ЗН), 1,03 продукта Его структуру подтверждает спектр (дублет, ЗН), 2,51 (триплет, 2Н), 2,90 (синглет, ПМР ЗН), 3,01 (дублет дублетов, 1Н), 3,13 (мультиплет, Стад ия 2 Си нтез 17-трет1Н) бутилдиметилсил ильного эфира 3-ацетоксиПример 34 андрост-5-ен-17-ола 3-Оксо-4-аза-4,7-р-диметил-16-рК раствору 4,5г (13,55ммол) андростан-17-ола этансульфонил-5-а-андростан с предыдущей стадии в 50мл диметилформамида К раствору 3-оксо-4-аза-4,7-р-диметил-16-рпри температуре 23°С добавляют 2,76г (40этантио-5-а-андростан (17мг, 0,0047ммол) в мета65ммол) имидазола, а затем 3,063г (20,32ммол) ноле (1,0мл) добавляют раствор OXONE, монотрет-бутилдиметилсилилхлорида Реакционную персульфатного производного (19мг) в воде (1мл) смесь перемешивают до начала образования Перемешивают при комнатной температуре в тетвердого вещества Дополнительно добавляют чение 2 часов, добавляют дополнительное коли20мл ДМФА и оставляют смесь перемешиваться чество OXONE (19мг) в воде (0,5мл) и перемешина ночь Выливают смесь в 1л воды, твердое вевают еще в течение 10 минут Реакционную смесь щество отфильтровывают и промывают водой разбавляют водой (25мл) и экстрагируют хлориТвердое вещество растворяют в этилацетате, орстым метиленом (3 • 50 мл) Органические вытяжганический слой промывают насыщенным раствоки объединяют, промывают насыщенным раствором соли, сушат над сульфатом натрия и упариваром соли, сушат (над сульфатом натрия) и ют, получая целевой 17-ол, имеющий силильнука упаривают Продукт очищают методом испаризащиту Его структуру подтверждает спектр ПНР тельной хроматографии на силикагеле, используя Стадия 3 17-трет-бутилдиметилсил ильный в качестве элюента 2% раствор метанола в хлоэфир 7-он-17-р-ола ристом метилене, и получают целевое соединеК раствору 5,6г (12,55ммол) 17-ола, содержание Масс-спектр m/z 395 (М) 400Мгц ПМР (хлощего трет-бутилдиметилсилильную защиту, полуроформ-d) 5 0,85 (синглет, ЗН), 0,92 (синглет, ЗН), ченного на предыдущей стадии, в 100мл ацето1,03 (дублет, ЗН), 1,39 (триплет, ЗН), 2,91 (сингнитрила при температуре 23°С добавляют 3,958г лет, ЗН), 2,99 (квартет, 2Н), 3,00 (дублет дублетов, (43,92ммол) 90%-ной гидроперекиси трет-бутила и 1Н), 3,41 (мультиплет, 1Н) 138мг гексакарбонила хрома Кипятят смесь в атПример 35 мосфере азота с обратным холодильником в те3-Оксо-аза-4,7-р-диметил-16-р-фтор-5-ачение 24-часов, выливают в 1л воды, твердое веандростан щество отфильтровывают, остаток промывают К раствору 3-оксо-4-аза-4,7-р-диметил-16-а500мл воды и растворяют в 350мл хлористого гидрокси-5-а-андростана (18мг, 0,056ммол) в хлометилена Органический слой промывают насыристом метилене (0,5мл) при комнатной тещенным раствором соли, сушат над сульфатом мпературе добавляют диэтиламиносератрифтонатрия и упаривают, получая сырой продукт Его очищают колоночной хроматографией на силикарид (19мкл, 0,144ммол) Перемешивают 1 час при геле, элюируя 7% раствором этилацетата в гексакомнатной температуре, реакционную смесь разне, и получают целевое соединение Его структуру бавляют хлористым метиленом (25мл) Органичеподтверждает спектр ПМР ский слой отделяют, промывают водой (25мл), насыщенным раствором бикарбоната натрия Стад ия 4 Си нтез 17-трет(10мл), насыщенным раствором соли (10мл), субутилдиметилсилильного эфира 3,7-дигидрокси-7шат (над сульфатом натрия) и упаривают Продукт метиландрост-5-ен-17-ола очищают методом испарительной хроматографии К раствору 440мг (0,956ммол) продукта, полу 55 ченного на предыдущей стадии, в сухом тетрагидрофуране при температуре 0°С в течение 5 - 1 0 минут добавляют по каплям метилмагнийхлорид Затем реакционную смесь перемешивают при комнатной температуре в течение 24 час и выливают в насыщенный водный раствор хлорида аммония ТГФ упаривают в вакууме, водную фазу экстрагируют этилацетатом Органический слой промывают насыщенным раствором соли, сушат над сульфатом натрия и упаривают, получая остаток сырого продукта Его структуру подтверждают с помощью спектра ПМР и используют на следующей стадии без дальнейшей очистки Стад ия 5 Си нтез 17-третбутилдиметилсилильного эфира 7-метиландрост4,6-диен-3-он-17-р-ола Полученный выше продукт реакции Гриньяра (3,5г, 7,142ммол) растворяют в смеси 50мл толуола и 50мл циклогексанона, а затем 20мл растворителей упаривают в вакууме К остатку добавляют 4,54г изопропоксида алюминия и кипятят реакционную смесь с обратным холодильником в течение 15 часов Смесь охлаждают, разбавляют этилацетатом, промывают раствором тартрата натрия-калия, насыщенным раствором соли, органический слой упаривают в вакууме и перегоняют с водяным паром Остаток экстрагируют этилацетатом, промывают насыщенным раствором соли, сушат, очищают колоночной хроматографией на силикагеле, элюируя 5% раствором этилацетата в гексане, и получают целевое соединение Стад ия 6 Си нтез третбутилдиметилсил ильного эфира 7-рметиландрост-5-ен-3-он-17-р-ола К раствору 370мг продукта, полученного на предыдущей стадии, в 5,5мл жидкого аммиака, 1мл ТГФ, 1мл толуола небольшими порциями добавляют 50мг металлического лития Образовавшийся раствор голубого цвета перемешивают в течение 2 часов и добавляют раствор 1,2дибромметана в 2мл ТГФ Раствор перемешивают при температуре минус 78°С в течение 10 минут, добавляют 25мг хлорида аммония и перемешивают еще в течение 10 минут Избыток аммиака удаляют испарением в токе азота, разбавляют реакционную смесь насыщенным раствором соли и экстрагируют этилацетатом Органический слой промывают насыщенным раствором соли, сушат и упаривают, получая сырой продукт, который используют на следующей стадии без дальнейшей очистки Стад ия 7 Си нтез третбутилдиметилсил ильного эфира 7-рметиландрост-4-ен-3-он-17-р-ола К раствору 432мг продукта, полученного на предыдущей стадии, в 4мл ТГФ добавляют в атмосфере азота при перемешивании 150мкл 1,8диазабицик [5,4,0]ундец-7-ена Полученную смесь кипятят с обратным холодильником в течение 1,5 часа, охлаждают, разбавляют раствором хлорид аммония ТГФ упаривают в вакууме и остаток экстрагируют этилацетатом Органический слой промывают насыщенным раствором соли, сушат над сульфатом натрия и упаривают в вакууме, получая сырой продукт Его очищают хроматографией на силикагеле, элюируя 10% раствором этилаце 44257 56 тата в гексане Стадия 8 синтез 17-р-(третбутилдиметилсилилокси)-7-р-метил-5-оксо-А-нор3,5-секоандроста-З-новой кислоты К раствору 884мг продукта, полученного на предыдущей стадии, в 15мл трет-бутилового спирта при 80°С добавляют 248мг карбоната натрия в 1,5мл воды, а затем по каплям в течение 15-20 минут добавляют смесь 2,273г периодата натрия и 16,8мг перманганата калия в 8мл воды Реакционную смесь нагревают до температурь) 80°С в течение 2 часов, охлаждают, отфильтровывают, остаток промывают водой и упаривают в вакууме, остаток подкисляют водным раствором соляной кислоты, экстрагируют этилацетатом и органический слой промывают водным раствором бисульфита натрия, насыщенным раствором соли, сушат и упаривают, получая соединение 9 Его структуру подтверждает спектр ПМР Стад ия 9 Си нтез третбутилдиметилсилильного эфира 4,7-р-диметил-4аза-андрост-5-ен-3-он-17-р-ола К раствору 840мг продукта, полученного на предыдущей стадии, в 5мл этиленгликоля добавляют 1,5г ацетата натрия и 737мг гидрохлорида метиламина Перемешивают реакционную смесь в течение 4 часов при температуре 180°С, охлаждают, разбавляют водой, экстрагируют этилацетатом, экстракт сушат и упаривают, получая сырой продукт Его структуру подтверждает спектр ПМР Стадия 10 Синтез 4,7-р-диметил-4-азаандрост-5-ен-3-он-17-р-ола К раствору 700мг продукта, полученного на предыдущей стадии, в 20мл ацетонитрила при 0°С добавляют 500мкл плавиковой кислоты Перемешивают реакционную смесь а течение 1 часа, нейтрализуют плавиковую кислоту водным раствором карбоната натрия, разбавляют водой, ацетонитрил упаривают в вакууме и остаток экстрагируют этилацетатом Органический слой сушат и упаривают, получая сырой продукт, который затем очищают препаративной хроматографией на силикагеле, элюируя смесью хлороформ/ацетон (3 1) Стадия 11 синтез 4,7-р-диметил-4-азаандростан-З-он-17-р-ола К раствору 350мг продукта, полученного на предыдущей стадии, в 10мл уксусной кислоты добавляют 100мг диоксида платины и подают водород Реакционную смесь встряхивают в течение ночи при комнатной температуре под давлением водорода 275кПа Раствор отфильтровывают и упаривают Остаток экстрагируют этилацетатом, органический слой упаривают в вакууме, разбавляют этилацетатом, промывают водным раствором бикарбоната натрия, насыщенным раствором соли, сушат, упаривают и получают целевое соединение Масс-спектр m/z320(M+1) Стадия 12 синтез 4-аза4,7-р-диметил-5аандростан-3,17-диона К раствору 1,01 Зг (3,176ммол) продукта, полученного на предыдущей стадии, помещают в сухую колбу вместе с 6мл хлористого метилена, добавляют 1,6г молекулярных сит 4А в виде порошка и 0,558г (4,76ммол) г\І-метилморфолин-І\Іоксида, а затем перрутенат тетрапропиламмония, 57 44257 58 55мг (0,159ммол) Реакционную смесь перемеши400Мгц ПМР (хлороформ-d) 5 0,85 (синглет, вают в течение 2 часов, разбавляют 150мл этилЗН), 0,99 (синглет, ЗН), 1,04 (дублет, ЗН), 2,91 ацетата и отфильтровывают Фильтрат упаривают (синглет, ЗН), 3,03 (дублет дублетов, 1Н), 4,80 досуха и получают сырой продукт, который пере(мультиплет, 1Н), 6,81 (мультиплет, 2Н), 7,24 кристаллизовывают из этилацетата и получают (мультиплет, 2Н), 7,32 (мультиплет, 2Н) чистый продукт с т пл 135-136°С Пример 43 Элементный анализ мол вес = 317,48 Масс-спектр rn/z 398 (M+I) вычислено для C 2 oH 3 iN0 2 С, 75,67, Н, 9,84, N, 400Мгц ПМР (хлороформ-d) 5 0,85 (синглет, 4,41, ЗН), 0,95 (синглет, ЗН), 1,04 (дублет, ЗН), 2,90 найдено С, 75,16, Н, 10,22, N, 4,13 (синглет, ЗН), 3,02 (дублет дублетов, 1Н), 5 34 Масс-спектр m/z 318 (М+1) (мультиплет, 1Н), 8,04 (дублет, 2Н), 8,15 (мультиМетодика следующих примеров (37-49) аналоплет, 1Н) гична методике Примера 21, с заменой 4Пример 44 фторбензонитрила соответствующим 43-Оксо-4-аза-4,7-р-диметил-16-р-(2фторпроизводным пиримидинилокси)-5-а-андростан Пример 37 Масс-спектр m/z 398 (M+I) 3-Оксо-4-аза-4,7-р-диметил-16-р-(4400Мгц ПМР (хлороформ-d) 5 0,85 (синглет, метилсульфонилфенокси)-5-а-андростан ЗН), 0,95 (синглет, ЗН), 1,04 (дублет, ЗН), 2,90 Масс-спектр m/z 474 (М+1) (синглет, ЗН), 3,02 (дублет дублетов, 1Н), 5 35 400Мгц ПМР (хлороформ-d) 5 085 (синглет, (мультиплет, 1Н), 6,89 (мультиплет, 1Н), 8,15 ЗН), 0,93 (синглет, ЗН), 1,04 (дублет, ЗН), 2,90 (дублет, 2Н) (синглет, ЗН), 3,00 (дублет дублетов, 1Н), 4,80 Пример 45 (мультиплет, 1Н), 6,92 (дублет, 2Н), 7,81 (дублет, 3-Оксо-4-аза-4,7-р-диметил-16-р-[4-(1 2Н) пиррил)фенокси1 -5-а-андростан Пример 38 Масс-спектр m/z 461 (M+I) 3-Оксо-4-аза-4,7-р-диметил-16-р-(3400Мгц ПМР (хлороформ-d) 5 0,85 (синглет, пиридилокси)-5-а-андростан ЗН), 0,95 (синглет, ЗН), 1,05 (дублет, ЗН), 2,91 Масс-спектр m/z 397 (M+I) (синглет, ЗН), 4,73 (мультиплет, 1Н), 6,30 (мульти400Мгц ПМР (хлороформ-d) 5 0,85 (синглет, плет, 2Н), 6,96 (мультиплет, 2Н), 7,25 (мультиплет, ЗН), 0,94 (синглет, ЗН), 1,04 (дублет, ЗН), 2,91 2Н) (синглет, ЗН), 3,02 (дублет дублетов, 1Н), 4 75 Пример 46 (мультиплет, 1Н), 7,21 (мультиплет, 2Н), 8,22 3-Оксо-4-аза-4,7-р-диметил-16-р-(3(мультиплет, 2Н) цианофенокси)-5-а-андростан Пример 39 Масс-спектр m/z 420 (М) 3-Оксо-4-аза-4,7-р-диметил-16-р-(4400Мгц ПМР (хлороформ-d) 5 0,85 (синглет, фенилфенокси)-5-а-андростан ЗН), 0,93 (синглет, ЗН), 1,04 (дублет, ЗН), 2,91 Масс-спектр m/z 472 (М+1) (синглет, ЗН), 3,02 (дублет дублетов, 1Н), 4,71 400Мгц ПМР (хлороформ-d) 5 0,85 (синглет, (мультиплет, 1Н), 7,05 (мультиплет, 1Н), 7,32 ЗН), 0,96 (синглет, ЗН), 1,05 (дублет, ЗН), 2,91 (мультиплет, 1Н) (синглет, ЗН), 3,02 (дублет дублетов, 1Н), Пример 47 4 76 (мультиплет, 1Н ), 6,9 (дублет,2Н), 7,26 3-Оксо-4-аза-4,7-р-диметил-16-р-(1 (дублет, 2Н), 7,43 (мультиплет, 2Н), 7,52 (мультинафтилокси)-5-а-андростан плет, 4Н) Масс-спектр m/z 445 (М) Пример 40 400Мгц ПМР (хлороформ-d) 5 0,86 (синглет, 3-Оксо-4-аза-4,7-р-диметил-16-р-(3ЗН), 1,03 (синглет, ЗН), 1,07 (дублет, ЗН), 2,92 хлорфенокси)-5-р-андростан (синглет, ЗН), 3,02 (дублет дублетов, 1Н), 6,70 Масс-спектр m/z 431 (М+1) (дублет, 1Н), 7,32 (мультиплет, 2Н), 7,78 (мульти400Мгц ПМР (хлороформ-d) 5 0,85 (синглет, плет, 1Н), 8,24 (1Н) ЗН), 0,93 (синглет, ЗН), 1,05 (дублет, ЗН), 2,90 Пример 48 (синглет, ЗН), 4,68 (мультиплет, 1Н), 6,71 (мульти3-Оксо-4-аза-4,7-р-диметил-16-р-(3-хлор-4плет, 1Н), 6,80 (мультиплет, 1Н), 6,88 (мультиплет, метилфенокси)-5-а-андростан 1Н), 7,13 (мультиплет, 1Н) Масс-спектр m/z 445 (М+1) Пример 41 400Мгц ПМР (хлороформ-d) 5 0,84 (синглет, 3-Оксо-4-аза-4,7-р-диметил-16-р-(4ЗН), 0,92 (синглет, ЗН), 1,04 (дублет, ЗН), 2,26 трифторметоксифенокси)-5-а-андростан (синглет, ЗН), 2,92 (синглет, ЗН), 4,76 (мультиплет, Масс-спектр m/z 480 (М+1) 1Н), 6,62 (мультиплет, 1Н), 6,81 (мультиплет, 1Н), 400Мгц ПМР (хлороформ-d) 5 0,85 (синглет, 7,12 дублет, 1Н) ЗН), 0,94 (синглет, ЗН), 1,04 (дублет, ЗН), 2,91 Пример 49 (синглет, ЗН), 3,02 (дублет дублетов, 1Н), 4,69 3-Оксо-4-аза-4,7-р-диметил-16-р-[4-(5(мультиплет, 1Н), 6,78 (мультиплет, 1Н), 7,09 оксазолил)фенокси]-5-а-андростан (мультиплет, 2Н) Масс-спектр m/z 463 (М+1) Пример 42 400Мгц ПМР (хлороформ-d) 5 0,85 (синглет, 3-Оксо-4-аза-4,7-р-диметил-16-р-(2ЗН), 0,95 (синглет, ЗН), 1,05 (дублет, ЗН), 2,91 хлорфенокси)-5-а-андростан (синглет, ЗН), 4,76 (мультиплет, 1Н), 6,86 (дублет, Масс-спектр m/z 431 (М-М) 2Н), 7,21 (синглет, 1Н), 7,53 (дублет, 2Н), 7,84 60 59 44257 (синглет, 1Н) Пример 54 Пример 50 3-Оксо-4-аза-4,7-р-диметил-16-р-(43-Оксо-4-аза-4,7-р-диметил-16-р-(4метилсульфонамидофенокси)-5-а-андростан нитрофенокси)-5-а-андростан Указанное соединение получают по методике, Указанное соединение получают по методике, аналогичной приведенной в Примере 52, взяв аналогичной приведенной в Примере 21, взяв 1хлористый тозил вместо уксусного ангидрида и фтор-4-нитробензол вместо 4-фторбензонитрила триэтиламин вместо пиридина и не используя 4400Мгц ПМР (хлороформ-d) 5 0,85 (синглет, диметиламинопиридин Масс-спектр m/z 565 ЗН), 0,94 (синглет, ЗН), 1,05 (дублет, ЗН), 2,92 (M+I) (синглет, ЗН), 3,03 (дублет дублетов, 1Н), 4,81 400Мгц ПМР (хлороформ-d) 5 0,84 (синглет, (квартет, 1Н), 6,87 (дублет, 2Н), 8,17 (дублет, 2Н) ЗН), 0,93 (синглет, ЗН), 1,03 (дублет, ЗН), 2,37 Пример 51 (синглет, ЗН), 2,92 (синглет, ЗН), 3,02 (дублет дублетов, 1Н), 4,63 (квартет, 1Н), 6,34 (синглет, 2Н), 3-Оксо-4-аза-4,7-р-диметил-16-р-(46,67 (дублет, 2Н), 6,91 (дублет, 2Н), 7,19 (дублет, аминофенокси)-5-а-андростан 2Н), 7,56 (дублет, 2Н) К раствору 3-оксо-4-аза-4,7-р-диметил-16-р-(4Пример 55 нитрофенокси)-5-а-андростана (163мг, О.Збммол) 3-Оксо-4-аза-4-(2,4-диметоксибензил)-7-рв этилацетате (8мл) и метаноле (8мл) добавляют метил-16-р-гидрокси-5-а-андростан 10%-ный палладий на угле (25мг,0,23ммол) ПеСоединение 55 получают аналогично методиремешивают в течение 4 часов атмосфере водоке синтеза соединения 12, приведенной на схеме рода при комнатнеой температуре Отфильтровы5, за исключением того, что соответствующий вают через целит и упаривают, получая 148мг бенрильный аналог (Соединение Е на Схеме 5) целевого соединения Очистка не требуется получают по методике, приведенной в Примере Масс-спектр m/z 411 (М+1) 36, в котором вместо метиламина используют 2,4400Мгц ПМР (хлороформ-d) 5 0,84 (синглет, диметоксибензиламин ЗН), 0,94 (синглет, ЗН), 1,37 (дублет, ЗН), 2,90 Пример 56 (синглет, ЗН), 3,03 (дублет дублетов, 1Н), 4,64 3-Оксо-4-аза-4-(2,4-диметоксибензил)-7-р(квартет, 1Н), 6,70 (дублет, 2Н), 6,78 (дублет, 2Н) метил-16-р-(4-хлорфенокси)-5-а-андростан Пример 52 Указанное соединение получают по методике, 3-Оксо-4-аза-4,7-р-диметил-16-р-(4аналогичной приведенной в Примере 23, взяв 3ацетиламинофенокси)-5-а-андростан оксо-4-аза-4-(2,4-диметоксибензил)-7-р-метил-16К раствору 3-оксо-4-аза-4,7-р-диметил-16-р-(4Р-гидрокси-5-а-андростан вместо 3-оксо-4-аза-4,7аминофенокси)-5-а-андростана (48мг, 0,116ммол) Р-диметил-16-р-гидрокси-5-а-андростана Никакой в хлористом метилене (1мл) и пиридине (0,037мл, очистки перед проведением следующей реакции 0,46ммол) добавляют уксусный ангидрид (0,22мл, не проводится 0,23ммол) и 4-диметиламинопиридин (5мг, Пример 57 0,04ммол) Реакционную смесь перемешивают в 3-Оксо-4-аза-7-р-метил-16-р-(4-хлорфенокси)атмосфере азота в течение ночи при комнатной 5-а-андростан температуре, разбавляют хлористым метиленом (50мл), органический слой отделяют, промывают К раствору 3-оксо-4-аза-4-(2,4водой (50мл) и насыщенным раствором соли диметоксибензил)-7-р-метил-16-р-(4(50мл) Сушат органический слой над сульфатом хлорфенокси)-5-а-андростан (130мг, 0,23ммол) в натрия и упаривают Сырой продукт очищают преметиленхлориде (1мл) добавляют трифторуксуспаративной тонкослойной хроматографией (силиную кислоту (1мл) Реакционную смесь оставляют кагель, ЮООмикрон), элюируя 5%-ным раствором перемешиваться на ночь при комнатной темпераметанола в хлористом метилене, и получают 51мг туре Растворитель упаривают и остаток раствоцелевого соединения Масс-спектр m/z 453 (М+1) ряют в хлористом метилене Органический слой 400Мгц ПМР (хлороформ-d) 5 0,84 (синглет, промывают насыщенным раствором бикарбоната ЗН), 0,93 (синглет, ЗН), 1,04 (дублет, ЗН), 2,13 натрия и насыщенным раствором соли Сушат (синглет, ЗН), 2,92 (синглет, ЗН), 3,03 (дублет дуборганический слой над сульфатом натрия и упалетов, 1Н), 4,68 (квартет, 1Н), 6,76 (дублет, 2Н), ривают Сырой продукт очищают препаративной 7,11 (дублет, 2Н), 7,33 (дублет, 2Н) тонкослойной хроматографией (силикагель, Пример 53 ЮООмикрон), элюируя 20%-ным раствором ацето3-Оксо-4-аза-4,7-р-диметил-16-р-(4на в хлористом метилене, и получают целевое бензоиламинофенокси)-5-а-андростан соединение 400Мгц ПМР (хлороформ-d) 5 0,86 (синглет, Указанное соединение получают по методике, ЗН), 0,93 (синглет, ЗН), 1,01 (дублет, ЗН), 3,07 аналогичной приведенной в Примере 52, взяв (дублет дублетов, 1 н), 4,67 (квартет, 1Н), 5,49 хлористый бензоил вместо уксусного ангидрида и (синглет, 1Н), 6,73 (дублет, 2Н), 7,18 (дублет, 2Н) триэтиламин вместо пиридина и не используя 4Пример 58 диметиламинопиридин Масс-спектр m/z 515 3-Оксо-4-аза-7-р-метил-16-р-фенокси-5-р(M+I) андростан 400Мгц ПМР (хлороформ-d) 5 0,84 (синглет, К раствору 3-оксо-4-аза-7-р-метил-16-р-(4ЗН), 0,94 (синглет, ЗН), 1,05 (дублет, ЗН), 2,92 хлорфенокси)-5-р-андростана в метаноле добав(синглет, ЗН), 3,04 (дублет дублетов, 1Н), 4,73 ляют 20%-ный алладий на угле Полученный рас(квартет, 1Н), 6,82 (дублет, 2Н), 7,94 (мультиплет, твор встряхивают в атмосфере водорода под дав5Н), 7,72 (синглет, 1Н), 7,84 (дублет, 2Н)
ДивитисяДодаткова інформація
МПК / Мітки
МПК: A61K 31/58, C07J 73/00, A61P 29/00
Мітки: похідні, алопеції, андрогенної, спосіб, ізоферменту, 5-a-редуктази, інгібітори, 4-азаандростану, інгібування, 16-заміщені, припинення, обернення, лікування, стимулю
Код посилання
<a href="https://ua.patents.su/37-44257-16-zamishheni-pokhidni-4-azaandrostanu-yak-ingibitori-izofermentu-5-a-reduktazi-sposib-ingibuvannya-5-a-reduktazi-ta-izofermentu-sposib-likuvannya-sposib-pripinennya-ta-obernennya.html" target="_blank" rel="follow" title="База патентів України">16-заміщені похідні 4-азаандростану, як інгібітори ізоферменту 5-a-редуктази, спосіб інгібування 5-a-редуктази та її ізоферменту, спосіб лікування, спосіб припинення та обернення андрогенної алопеції та стимулю</a>
Попередній патент: Спосіб немедикаментозного лікування хворих з психологічно-вегетативними розладами
Випадковий патент: Спосіб лікування алкогольної залежності