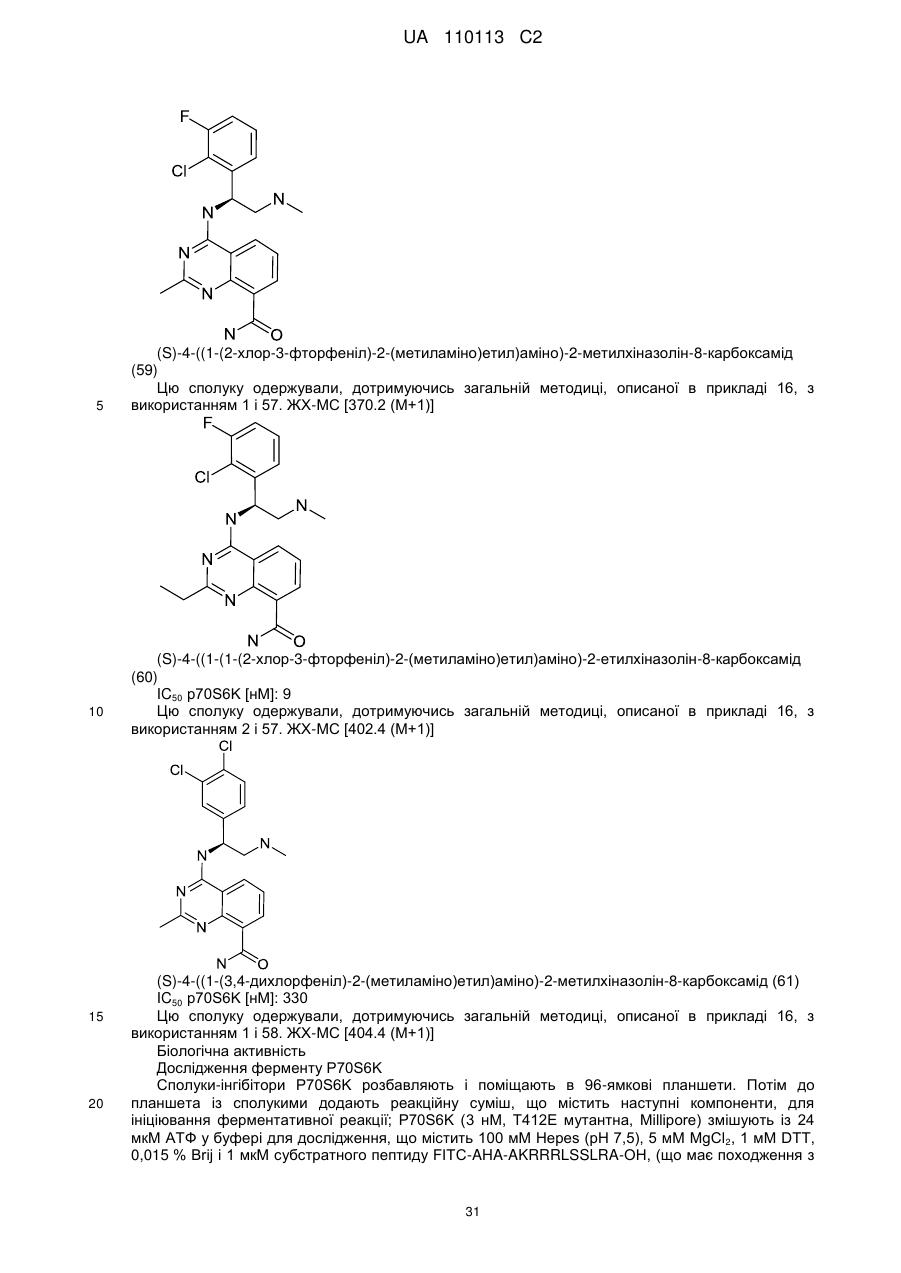
Біциклічні азагетероциклічні карбоксаміди
Номер патенту: 110113
Опубліковано: 25.11.2015
Автори: Ксіао Юфанг, Хак Байярд Р., Дезельм Лізбет Селест, Джонс Рейнальдо С., Саттон Аманда Е., Неагу Константін, Мочалкін Ігор, Лан Руоксі, Річардсон Томас Е., Карра Срініваса Р.
Формула / Реферат
1. Сполука формули (І)
 (I)
(I)
або її фармацевтично прийнятні солі, сольвати або сольвати солей,
де:
X являє собою N або C-R3,
Y являє собою NH, О або відсутній,
R1 являє собою L1-R4-L2-R5 або L1-R4,
R2 являє собою A, LA, Hal, ОН, ОА, SH, CN, NH2, NO2, NHA, NH-L1-Ar, NHCOA, NHCO-L1-Ar, NHSO2A, NHSO2-L1-Ar, NHCONHA, NHCONH-L1-Ar, L1-Ar, O-L1-Ar, L1-R4, або
R2 являє собою метил, етил, ізопропіл або трифторметил,
L1 являє собою одинарний зв'язок, метилен, або метил-заміщений метилен, де метилен, або метильна група метил-заміщеного метилену може бути не заміщена або моно-, або дизаміщена Hal, OH, CN, NH2, NH(LA), N(LA)2, NO2, COOH, N3, етенілом або етинілом, і/або монозаміщена R4, або циклічний А, який може бути моно- або дизаміщений Hal або LA, і де одна або дві СН2-групи можуть бути замінені на О або S атом або на -NH-, -N(LA)-, -CONH-, -N(LA)COO-, -SO2- або -NHCO-групу, або
L1 являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно, диметиламіно або азетидином,
R3 являє собою Н, A, Hal, OH, COOH, SH, NH2, NO2 або CN,
R4, R5 кожний, незалежно один від одного, являють собою Аr або циклічний А, який може бути моно- або дизаміщений Hal або LA, або
R4 являє собою моноциклічний ароматичний гомо- або гетероцикл, який містить 0, 1 або 2 N, О і/або S атомів і 5 або 6 кістякових атомів, і який може бути не заміщений або, незалежно один від одного, моно-, ди- або тризаміщений Hal, A, OH, SH, ОА, NH2, NHA, NA2, NO2, CN, OCN, SCN, COOH, COOA, CONH2, CONHA, CONA2, NHCOA, NHCONHA, NHCONH2, NHSO2A, CHO, COA, SO2NH2, SO2A і/або SO2Hal,
R4 являє собою феніл, який не заміщений або монозаміщений Hal,
L2 являє собою -NHCO-, -NHCOO-, -NHCONH-, -NHCONA-, -NHCOA-, -О-, -S-, -NH- -NHSO2-, -SO2NH- -CONH-, -CONHCONH-, -NHCONHCO-, або -А-,
Аr являє собою моно- або біциклічний ароматичний гомо- або гетеро-цикл, який містить 0, 1, 2, 3 або 4 N, О і/або S атомів й 5, 6, 7, 8, 9 або 10 кістякових атомів, і який може бути не заміщений або, незалежно один від одного, моно-, ди- або тризаміщений Hal, A, OH, SH, ОА, NH2, NHA, NA2, NO2, CN, OCN, SCN, COOH, COOA, CONH2, CONHA, CONA2, NHCOA, NHCONHA, NHCONH2, NHSO2A, CHO, COA, SO2NH2, SO2A і/або SO2Hal, і де кільцевий N-атом може бути заміщений О-атомом з утворенням N-оксидної групи,
і де у випадку біциклічного ароматичного циклу одне із двох кілець може бути частково насиченим,
А являє собою нерозгалужений або розгалужений лінійний або циклічний алкіл, який містить 1, 2, 3, 4, 5, 6, 7 або 8 С атомів, де одна або дві СН2-групи можуть бути замінені на О або S атом і/або на -NH-, -CO-, -NHCOO-, -NHCONH-. -N(LA)-, -CONH-, -NHCO- або -СН=СН-групу, і де 1- 3 Н атомів можуть бути замінені на Hal, і де одна або дві СН3-групи можуть бути замінені на ОН, SH, NH2, NH(LA), N(LA)2, NHCOOH, NHCONH2 або CN,
LA являє собою нерозгалужений або розгалужений лінійний алкіл, який містить 1, 2, 3 або 4 С атоми, де 1, 2 або 3 Н атоми можуть бути замінені на Hal,
Hal являє собою F, Сl, Вr або І.
2. Сполука за п. 1 або її фармацевтично прийнятні солі, сольвати або сольвати солей, де
X являє собою N,
Y являє собою NH,
R1 являє собою L1-R4,
R2 являє собою LA, Hal, OH, O(LA), SH, CN, NH2, NO2, NH(LA), NHCO(LA), NHSO2(LA), NHCONH(LA),
L1 являє собою метил-заміщений метилен, де метильна група метилзаміщеного метилену монозамещіна NH2 або NH(LA), N(LA)2, або циклічним А, який може бути моно- або дизаміщений Hal або LA,
R4 являє собою моноциклічний ароматичний гомо- або гетероцикл, який містить 0, 1 або 2 N, О і/або S атомів і 5 або 6 кістякових атомів, і який може бути не заміщений або, незалежно один від одного, моно-, ди- або тризаміщений Hal, A, OH, SH, ОА, NH2, NHA, NA2, NO2, CN, OCN, SCN, COOH, COOA, CONH2, CONHA, CONA2, NHCOA, NHCONHA, NHCONH2, NHSO2A, CHO, COA, SO2NH2, SO2A і/або SO2Hal,
А являє собою нерозгалужений або розгалужений лінійний або циклічний алкіл, який містить 1, 2, 3, 4, 5, 6, 7 або 8 С атомів, де одна або дві СН2-групи можуть бути замінені на О або S атом і/або на -NH-, -CO-, -NHCOO-, -NHCONH-, -N(LA)-, -CONH-, -NHCO- або -СН=СН-групу, і де 1-3 Н атоми можуть бути замінені на Hal, і де одна або дві СН3-групи можуть бути замінені на ОН, SH, NH2, NH(LA), N(LA)2, NHCOOH, NHCONH2 або CN,
LA являє собою нерозгалужений або розгалужений лінійний алкіл, який містить 1, 2, 3 або 4 С атоми, де 1, 2 або 3 Н атоми можуть бути замінені на Hal,
Hal являє собою F, Сl, Вr або І.
3. Сполука за п. 2, де залишки, які не позначені дуже детально, мають значення, зазначені в п. 2, але де:
у підформулі 1
R2 являє собою LA,
у підформулі 2
L1 являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно, диметиламіно або азетидином,
у підформулі 3
R4 являє собою феніл, який не заміщений або монозаміщений Hal,
у підформулі 4
R2 являє собою метил, етил, ізопропіл або трифторметил,
у підформулі 5
L1 являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно,
у підформулі 6
L1 являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна азетидин-1-ілом,
у підформулі 7
R4 являє собою феніл, який є незаміщеним,
у підформулі 8
R4 являє собою феніл, який мета- або пара-заміщений F або Сl,
у підформулі 9
R2 являє собою LA,
L1 являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно або азетидином,
у підформулі 10
R2 являє собою LA,
R4 являє собою феніл, який не заміщений або монозаміщений Hal,
у підформулі 11
L1 являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно або азетидином,
R4 являє собою феніл, який не заміщений або монозаміщений Hal,
у підформулі 12
R2 являє собою LA,
L1 являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно або азетидином,
R4 являє собою феніл, який не заміщений або монозаміщений Hal,
у підформулі 13
R2 являє собою метил, етил, ізопропіл або трифторметил,
L1 являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно або азетидином,
R4 являє собою феніл, який не заміщений або монозаміщений Hal,
у підформулі 14
R2 являє собою LA,
L1 являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно або азетидином,
R4 являє собою феніл, який мета- або пара-заміщений F або Сl,
у підформулі 15
R2 являє собою метил, етил, ізопропіл або трифторметил,
L1 являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозаміщена метиламіно або азетидином,
R4 являє собою феніл, який мета- або пара-заміщений F або Сl,
у підформулі 16
R2 являє собою метил, етил, ізопропіл або трифторметил,
L1 являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно,
R4 являє собою феніл, який мета- або пара-заміщений F або Сl,
у підформулі 17
R2 являє собою метил, етил, ізопропіл або трифторметил,
L1 являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна азетидин-1-ілом,
R4 являє собою феніл, який мета- або пара-заміщений F або Сl,
у підформулі 18
R2 являє собою метил, етил, ізопропіл або трифторметил,
L1 являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно або азетидином,
R4 являє собою феніл, який мета-заміщений F або Сl,
у підформулі 19
R2 являє собою метил, етил, ізопропіл або трифторметил,
L1 являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно або азетидин-1-ілом,
R4 являє собою феніл, який мета-заміщений F або Сl,
або її фармацевтично прийнятні солі, сольвати або сольвати солей.
4. Сполука за п. 1, де сполука вибрана із групи, яка включає:
4-{[(1S)-1-(4-фторфеніл)-2-(метиламіно)етил]аміно}-2-метилхіназолін-8-карбоксамід,
4-{[(1S)-1-(3-фторфеніл)-2-(метиламіно)етил]аміно}-2-метилхіназолін-8-карбоксамід,
4-{[(1S)-1-(4-хлорфеніл)-2-(метиламіно)етил]аміно}-2-ізопропілхіназолін-8-карбоксамід,
4-{[(1S)-1-(4-хлорфеніл)-2-(метиламіно)етил]аміно}-2-метилхіназолін-8-карбоксамід,
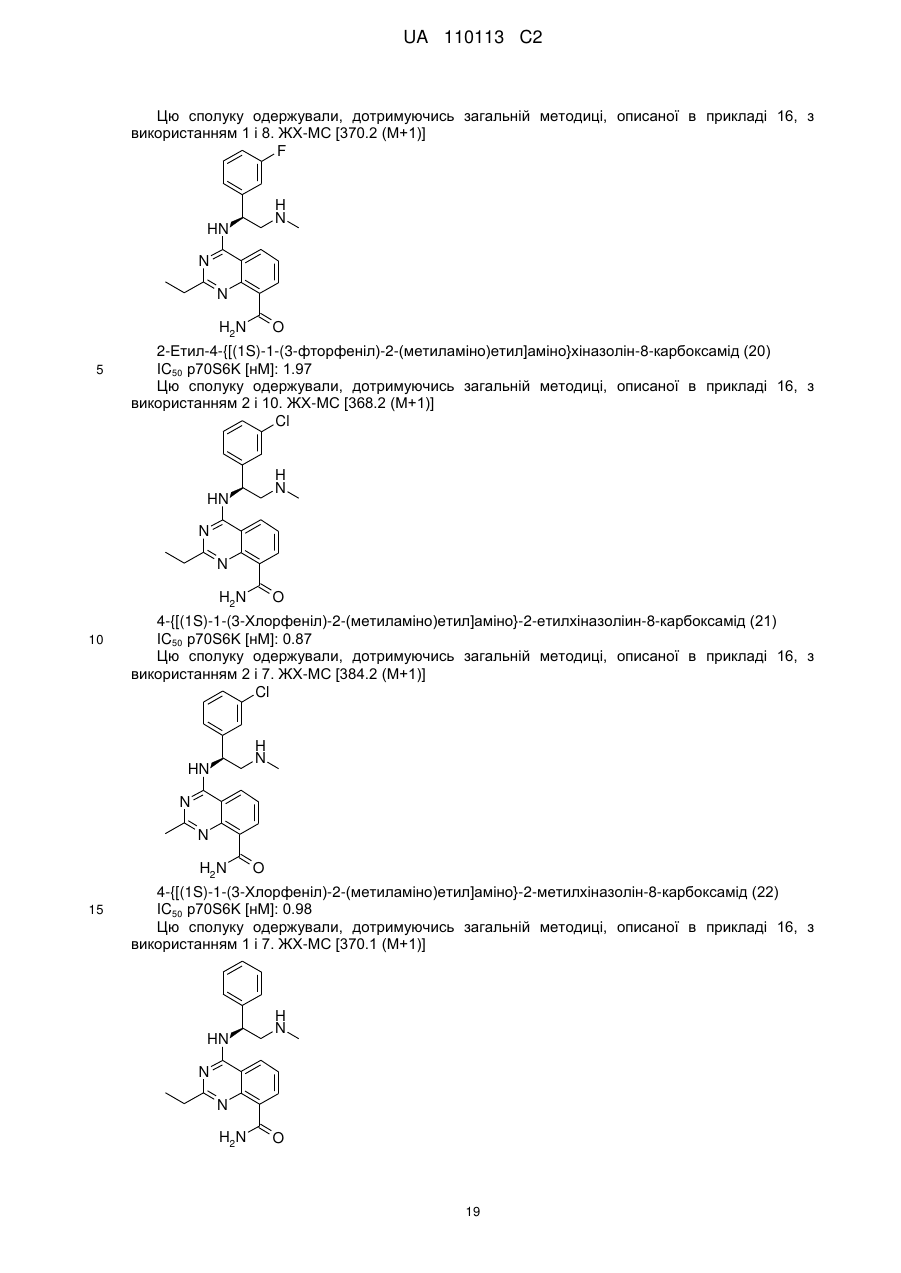
2-етил-4-{[(1S)-1-(3-фторфеніл)-2-(метиламіно)етил]аміно}хіназолін-8-карбоксамід,
4-{[(1S)-1-(3-хлорфеніл)-2-(метиламіно)етил]аміно}-2-етилхіназолін-8-карбоксамід,
4-{[(1S)-1-(3-хлорфеніл)-2-(метиламіно)етил]аміно}-2-метилхіназолін-8-карбоксамід,
2-етил-4-{[(1S)-2-(метиламіно)-1-фенілетил]аміно}хіназолін-8-карбоксамід,
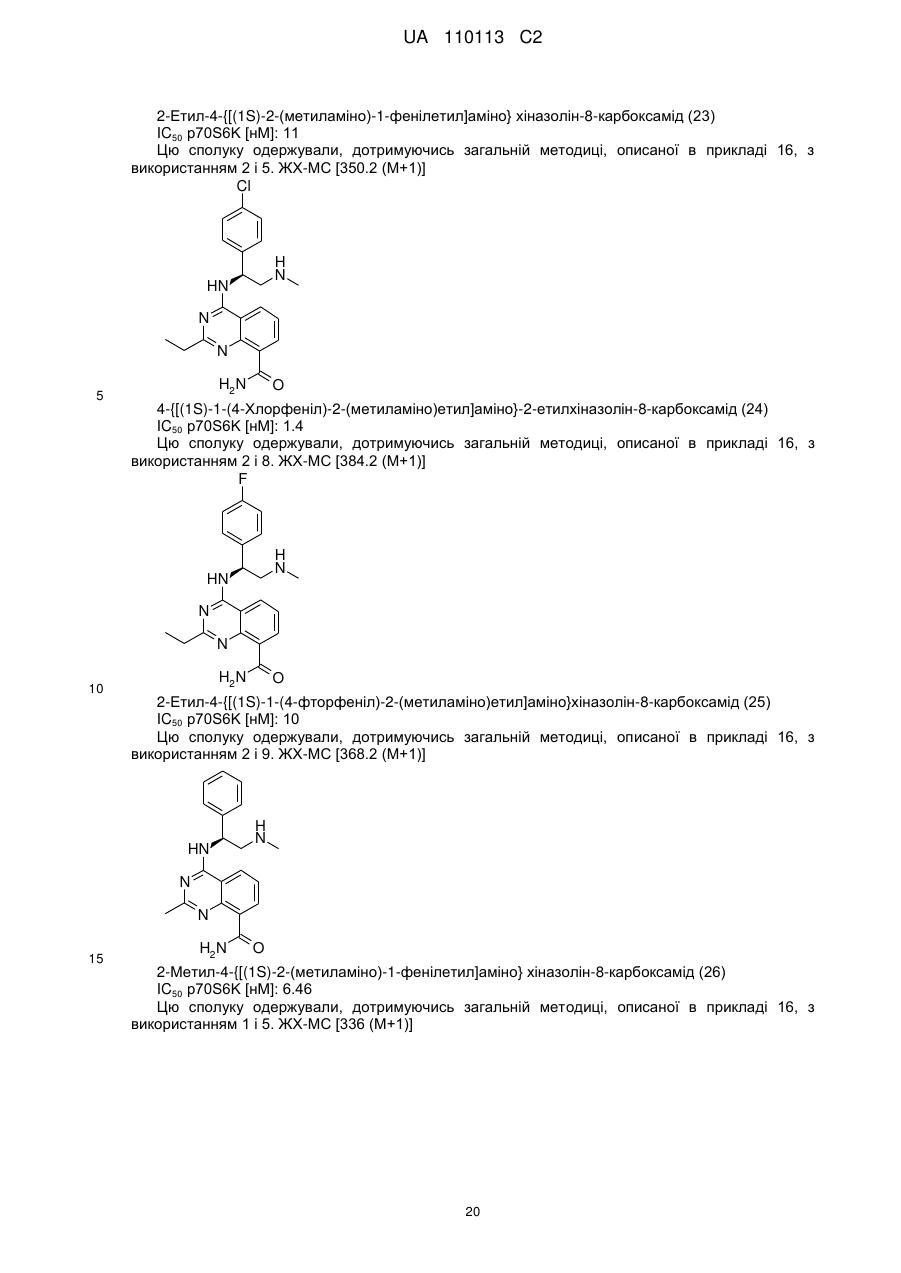
4-{[(1S)-1-(4-хлорфеніл)-2-(метиламіно)етил]аміно}-2-етилхіназолін-8-карбоксамід,
2-етил-4-{[(1S)-1-(4-фторфеніл)-2-(метиламіно)етил]аміно}хіназолін-8-карбоксамід,
2-метил-4-{[(1S)-2-(метиламіно)-1-фенілетил]аміно}хіназолін-8-карбоксамід,
4-{[(1S)-1-(3-фторфеніл)-2-(метиламіно)етил]аміно}-2-(трифторметил)-хіназолін-8-карбоксамід,
амід-4-[(S)-3-азетидин-1-іл-2-(3-фторфеніл)-пропіл]-2-етилхіназолін-8-карбонової кислоти,
амід-4-[(S)-3-азетидин-1-іл-2-фенілпропіл]-2-метилхіназолін-8-карбонової кислоти,
амід-4-[(S)-3-азетидин-1-іл-2-фенілпропіл]-2-етилхіназолін-8-карбонової кислоти,
амід-4-[(S)-3-азетидин-1-іл-2-(4-хлорфеніл)-пропіл]-2-метилхіназолін-8-карбонової кислоти,
амід-4-[(S)-3-азетидин-1-іл-2-(4-хлорфеніл)-пропіл]-2-етилхіназолін-8-карбонової кислоти,
амід-4-[(S)-3-азетидин-1-іл-2-(4-фторфеніл)-пропіл]-2-метилхіназолін-8-карбонової кислоти,
амід-4-[(S)-3-азетидин-1-іл-2-(3-фторфеніл)-пропіл]-2-метилхіназолін-8-карбонової кислоти,
амід-4-[(S)-3-азетидин-1-іл-2-(3-хлорфеніл)-пропіл]-2-метилхіназолін-8-карбонової кислоти,
амід 4-[(S)-3-азетидин-1-іл-2-(4-фторфеніл)-пропіл]-2-етилхіназолін-8-карбонової кислоти,
амід 4-[(S)-3-азетидин-1-іл-2-(3-хлорфеніл)-пропіл]-2-етилхіназолін-8-карбонової кислоти,
і його фармацевтично прийнятні солі, сольвати або сольвати солей.
5. Фармацевтична композиція, яка містить сполуку за будь-яким із пп. 1-4 або її фармацевтично прийнятну сіль, сольват або сольват солі як активний інгредієнт, разом з фармацевтично прийнятним носієм.
6. Сполука за будь-яким із пп. 1-4 або її фармацевтично прийнятна сіль, сольват або сольват солі призначена для застосування як лікарського засобу.
7. Сполука за будь-яким із пп. 1-4 або її фармацевтично прийнятна сіль, сольват або сольват солі призначена для лікування гіперпроліферативних захворювань.
8. Сполука за п. 7 або її фармацевтично прийнятна сіль, сольват або сольват солі, де захворювання вибране із групи, яка включає злоякісне новоутворення, що переважно вибирається з раку молочної залози, колоректального раку, раку легенів, раку простати або раку підшлункової залози або гліобластоми.
9. Набір (комплект), який складається з окремих пакетів:
а) ефективної кількості сполуки по одному або декількох із пп. 1-4 або його фармацевтично прийнятної солі, сольвату або сольвату солі, і
б) ефективної кількості додаткового активного інгредієнта лікарського засобу.
10. Спосіб одержання сполуки формули (І),
де X являє собою N, і Y являє собою NH, і всі інші замісники мають значення, зазначені для Формули (І) у п. 1,
де ефір карбонової кислоти формули (IV)
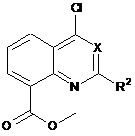 (IV)
(IV)
уводять у реакцію із сполукою формули (III):
H-Y-R1, (III),
з одержанням сполуки формули (II):
 , (II)
, (II)
яку на закінчення перетворюють в амід карбонової кислоти формули (І):
 . (I)
. (I)
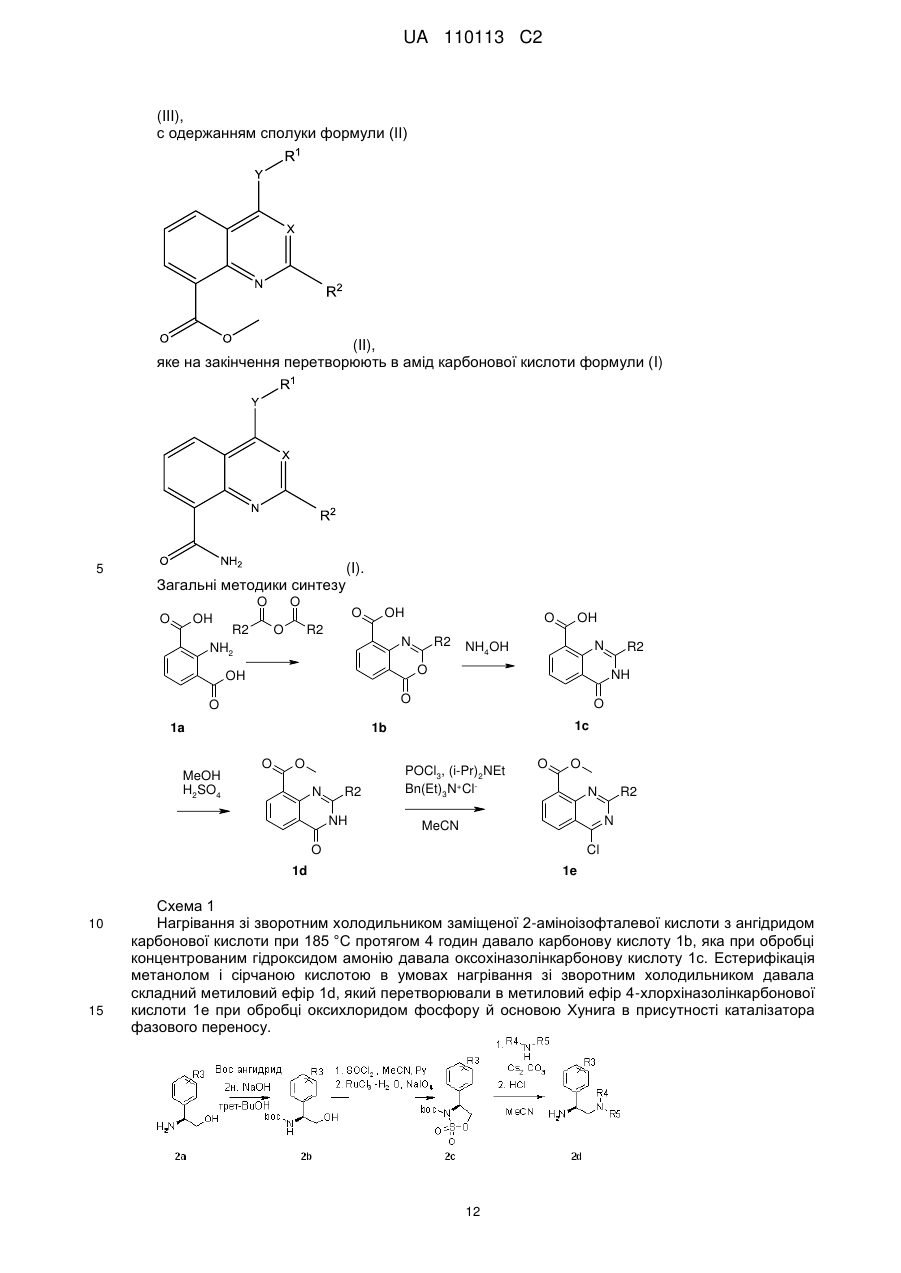
Текст
Реферат: Винахід стосується нових сполук біциклічних азагетероциклічних карбоксамідів відповідно до Формули (І), їх одержання й застосування для лікування гіперпроліферативних захворювань, таких як злоякісне новоутворення. UA 110113 C2 (12) UA 110113 C2 UA 110113 C2 5 10 15 20 25 30 35 40 45 50 55 60 Галузь техніки винаходу Винахід відноситься до ряду сполук біциклічних азагетероциклічних карбоксамідів, придатних для лікування захворювань, таких як злоякісний новотвір, у ссавців. Також даний винахід охоплює застосування таких сполук у лікуванні гіперпроліферативних захворювань у ссавців, особливо людей, і фармацевтичних композицій, які містять такі сполуки. Короткий виклад відомого рівня техніки Протеїнкінази становлять велике сімейство структурно подібних ферментів, які відповідають за регулювання багатьох шляхів передачі сигналів у клітинах (Hardie, G. і Hanks, S. (1995) The Protein Kinase Facts Book. I і II, Academic Press, Сан-Дієго, Каліфорнія). Кінази можуть підрозділятися на сімейства згідно із субстратами, які вони фосфорилюють (наприклад, протеїнтирозин, протеїн-серин/треонин, ліпіди і т.д.). Були ідентифіковані послідовності, які в цілому відповідають кожному із цих сімейств кіназ (наприклад, Hanks, S.K., Hunter, T., FASEB J., 9:576596 (1995); Knighton, і ін., Science, 253:407-414 (1991); Hiles, і ін., Cell, 70:419-429 (1992); Kunz, і ін., Cell, 73:585-596 (1993); Garcia-Bustos, і ін., EMBO J., 13:2352-2361 (1994)). Протеїнкінази можуть бути охарактерізовані за допомогою механізмів, що регулюють їхня активність. Ці механізми включають, наприклад, аутофосфорилювання, трансфосфорилювання за допомогою інших кіназ, білок-білкові взаємодії, білок-ліпідні взаємодії й білок-полінуклеотидні взаємодії. Деякі протеїнкінази можуть регулюватися більш ніж одним механізмом. Кінази регулюють різні процеси в клітинах, включаючи, але не обмежуючись тільки ними, проліферацію, апоптоз, рухливість, транскрипцію, трансляцію й інші сигнальні процеси, шляхом додавання фосфатних груп до білок-мішеням. Таке фосфорилювання діє в якості молекулярних «, що включають»/«, що виключають" "перемикачів", які можуть модулювати або регулювати біологічну функцію білки-мішені. Фосфорилювання білків-мішеней відбувається у відповідь на дію різних позаклітинних сигналів (гормонів, нейромедіаторів, факторів росту й диференціації, і т.д.), подій клітинного циклу, факторів навколишнього середовища або харчових стресів і т.д. Характерною функцією протеїнкіназ у шляхах передачі сигналів є активування або інактивування (безпосередньо або побічно), наприклад, метаболічного ферменту, регуляторного білка, рецептора, білка цитоскелета, іонного каналу або насоса, або фактора транскрипції. Неконтрольована передача сигналів внаслідок порушення контролю фосфорилювання білків залучена в різні захворювання, включаючи, наприклад, запалення, злоякісний новотвір, алергію/астму, захворювання й стану імунної системи, захворювання й станів центральної нервової системи, і ангіогенез. Протеїнкіназа 70S6K, кіназа 70 кДа рибосомного білка p70S6K (також відома як SK6, p70/p85 S6 кіназа, p70/p85 рибосомна S6 кіназа й pp70S6K), є представником AGC субродини протеїнкіназ. p70S6K є серин-треонин кіназою, яка є компонентом фосфатидилінозитол 3 кіназа (PI3K)/AKT шляху. p70S6K розташована нижче PI3K, і активація відбувається шляхом фосфорилювання в різних сайтах у відповідь на дію різних мітогенів, гормонів і факторів росту. Активність p70S6K також перебуває під контролем mTOR-утримуючого комплексу (TORC1), оскільки рапаміцин діє шляхом інгібування p70S6K активності. p70S6K регулюється за допомогою PI3K нижче розташованих мішеней AKT і PKCζ. Діє безпосередньо фосфорилює і інактивує TSC2, у такий спосіб активуючи mTOR. Додатково, дослідження з мутантними алелями p70S6K, яка інгібується вортманіном, але не рапаміцином, свідчить від тому, що Pl3K шлях може проявляти впливи на p70S6K незалежно від регуляції активності mTOR. Фермент p70S6K модулює синтез білка шляхом фосфорилювання S6 рибосомного білка. S6 фосфорилювання корелює з підвищеною трансляцією мРНК, що кодують компоненти трансляційного апарата, включаючи рибосомні білки й фактори елонгації трансляції, підвищена експресія яких є важливою для росту й проліферації кліток. Ці мРНК містять олігопіримідинову ділянку на них 5' транскрипційному початку (позначуваному 5'TOP), який, як було показано, є важливим для їхньої регуляції на трансляційному рівні. Додатково до його залучення в трансляцію, активація p70S6K також задіяна в контролювання клітинного циклу, диференціацію нейронних кліток, регуляцію рухливості кліток і клітинну відповідну реакцію, що є важливим при метастазуванні пухлин, імунній відповіді й відновленні тканини. Антитіла до p70S6K скасовують мітогенну відповідь, що запускає входження фібргалузів пацюків в S фазу, указуючи на те, що p70S6K функція є важливою для проходження з G1 в S фазу в клітинному циклі. Крім того, інгібування проліферації клітинного циклу з G1 в S фазу клітинного циклу за допомогою рапаміцину було ідентифіковано у вигляді наслідку інгібування продукції гіперфосфорилюваної, активованої форми p70S6K. Роль p70S6K у проліферації пухлинних кліток і захисту кліток від апоптоза ґрунтується на його участі в передачі сигналів рецепторів факторів росту, надекспресії й активації в пухлинних тканинах. Наприклад, при нозерн- і вестерн-аналізах було встановлено, що ампліфікація PS6K 1 UA 110113 C2 5 10 15 20 25 30 35 40 45 гена супроводжується відповідними підвищеннями мРНК і експресії білка, відповідно (Cancer Res. (1999) 59: 1408-11-localization of PS6K to Chromosomal Region 17q23 and Determination of Its Amplification in Breast Cancer). Хромосома 17q23 ампліфікована в аж до 20 % первинних пухлин молочної залози, в 87 % пухлин молочної залози, що містить BRCA2 мутації й в 50 % пухлин, що містять BRCA1 мутацій, а також при інших типах злоякісних новотворів, таких як підшлункової залози, сечового міхура й нейробластоми (див. M. Barlund, O. Monni, J. Kononen, R. Cornelison, J. Torhorst, G. Sauter, O.-P. Kallioniemi і Kallioniemi A., Cancer Res., 2000, 60:5340-5346). Було показано, що 17q23 амфліфікації при раку молочної залози залучені PAT1, RAD51C, PS6K, і SIGMA1B гени (Cancer Res. (2000): 60, сс. 5371-5375). Ген p70S6K був ідентифікований у якості мішені ампліфікації й надекспресії в цій ділянці, і спостерігається статистично достовірний зв'язок між ампліфікацією й поганим прогнозом. Клінічне інгібування p70S6K активації спостерігається в пацієнтів з раком бруньки, яких лікували за допомогою CCI-779 (складний ефір рапаміцину), інгібітору више росташованої кінази mTOR. Описана достовірна лінійна асоціація між прогресуванням захворювання й інгібуванням активності p70S6K. У відповідь на енергетичний стрес, пухлинний супресор LKB1 активує AMPK, який фосфорилює TSC1/2 комплекс і надає йому можливість інактивувати mTOR/p70S6K шлях. Мутації в LKB1 викликають синдром Пейтца-Егерса (PJS), де в пацієнтів PJS в 15 раз більше ймовірність розвитку рака, чому в загальної популяції. Додатково, 1/3 аденокарциноми легенів заякоривают інактивувальні LKB1 мутації. p70S6K залучений у метаболічні захворювання й порушення. Було описано, що відсутність p70S6K захищає від вікового й індукованого харчуванням ожиріння, у той час як підсилює чутливість до інсуліну. Роль для p70S6K при метаболічних захворюваннях і порушеннях, таких як ожиріння, діабет, метаболічний синдром, резистентність до інсуліну, гіперглікемія, гіпераміноацидемія, і гіперліпідемія підтверджується цими спостереженнями. Сполуки, описані в якості придатних для інгібування p70S6K, розкриті в WO 03/064397, WO 04/092154, WO 05/054237, WO 05/056014, WO 05/033086, WO 05/117909, WO 05/039506, WO 06/120573, WO 06/136821, WO 06/071819, WO 06/131835, WO 08/140947 і PCT/US10/000313. Опис винаходу Об'єктом даного винаходу є забезпечення нових інгібіторів p70S6K, придатних для лікування гіперпроліферативних захворювань, особливо тих, які пов'язані з гіперактивністю вищевказаних протеїнкіназ, таких як злоякісний новотвір у ссавців, з поліпшеними фармакологічними властивостями як у відношенні їх активності, так і характеристик розчинності, метаболічного кліренсу й біодоступності. У результаті, даний винахід забезпечує нові сполуки біциклічних азагетероциклічних карбоксамідів і їх фармацевтично прийнятних солей, сольватів або проліки, які є інгібіторами кіназ і придатні для лікування вищевказаних захворювань. Сполуки визначаються Формулою (I): (I), і їх фармацевтично прийнятні солі, сольвати солей, або проліки, де: 3 X являє собою N або C-R , Y являє собою NH, O або відсутний, 1 1 4 2 5 1 4 R являє собою L –R –L –R або L –R , 2 1 1 R являє собою A, Hal, OH, OA, SH, CN, NH2, NO2, NHA, NH–L –Ar, NHCOA, NHCO–L –Ar, 1 1 1 1 1 4 NHSO2A, NHSO2–L –Ar, NHCONHA, NHCONH–L –Ar, L –Ar, O-L –Ar, L –R , 1 L являє собою одинарний зв'язок, метилен, або метил-заміщений метилен, де метилен, або метильна група метил-заміщеного метилену може бути незаміщена або моно- або дизаміщена 2 UA 110113 C2 4 5 10 15 20 25 30 35 40 45 50 55 60 Hal, OH, CN, NH2, NH(LA), N(LA)2, NO2, COOH, N3, етенілом або етинілом, і/або монозаміщіна R , і де одна або дві CH2 групи можуть бути замінені на O або S атом або на –NH-, -N(LA)-, -CONH-, -N(LA)COO-, -SO2- або -NHCO- групу, 3 R являє собою H, A, Hal, OH, COOH, SH, NH2, NO2 або CN, 4 5 R , R кожний, незалежно друг від друга, являють собою Ar, або циклічний A, який може бути моно- або дизаміщений Hal або LA, 2 L являє собою –NHCO–, -NHCOO-, –NHCONH–, –NHCONA–, –NHCOA–, –O–, –S–, –NH–, – NHSO2–, –SO2NH–, –CONH–, –CONHCONH–, –NHCONHCO–, або –A-, Ar являє собою моно- або біциклічний ароматичний гомо- або гетероцикл, який містить 0, 1, 2, 3 або 4 N, Oі/або S атома й 5, 6, 7, 8, 9, або 10 кістякових атомів, і який може бути незаміщений або, незалежно друг від друга, моно-, ди- або тризаміщений Hal, A, OH, SH, OA, NH2, NHA, NA2, NO2, CN, OCN, SCN, COOH, COOA, CONH2, CONHA, CONA2, NHCOA, NHCONHA, NHCONH2, NHSO2A, CHO, COA, SO2NH2, SO2A і/або SO2Hal, і де кільцевий N-атом може бути заміщений O-атомом з утвором N-оксидної групи, і де у випадку біциклічного ароматичного циклу одне із двох кілець може бути частково насиченим, A являє собою нерозгалужений або розгалужений лінійний або циклічний алкіл, який містить 1, 2, 3, 4, 5, 6, 7 або 8 C атомів, де одна або дві CH 2 групи можуть бути замінені на O або S атом і/або на –NH-, -CO-, -NHCOO-, -NHCONH-. -N(LA)-, -CONH-, -NHCO- або –CH=CH– групу, і де 13 H атомів можуть бути замінені на Hal, і де одна або дві CH 3 групи можуть бути замінені на OH, SH, NH2, NH(LA), N(LA)2, NHCOOH, NHCONH2 або CN, LA являє собою нерозгалужений або розгалужений, лінійний алкіл, який містить 1, 2, 3 або 4 C атома, де 1, 2 або 3 H атома можуть бути замінені на Hal, Hal являє собою F, Cl, Br або I. Загалом, усі залишки, які зустрічаються більш одного разу можуть бути ідентичними або різними, тобто є незалежними друг від друга. Представлені вище й нижче залишки й параметри мають значення, зазначені для Формули (I), якщо спеціально не зазначене інакше. Відповідно, винахід відноситься, зокрема, до сполук Формули (I), у якій щонайменше один із зазначених залишків має одне із кращих значень, зазначених нижче. Hal означає фтор, хлор, бром або йод, зокрема фтор або хлор. "A" означає, наприклад, метил, крім того, етил, пропіл, ізопропіл, бутил, ізобутил, втор-бутил або тре-бутил, крім того, також пентил, 1-, 2- або 3-метилбутил, 1,1-, 1,2- або 2, 2диметилпропіл, 1- етилпропіл, гексил, 1-, 2-, 3- або 4- метилпентил, 1,1-, 1,2-, 1,3-, 2,2-, 2,3- або 3,3-диметилбутил, 1- або 2-етилбутил, 1-етил-1-метилпропіл, 1 етил-2-метилпропіл, 1,1,2- або 1,2, 2-триметилпропіл. "A" також означає алкіл, як зазначено вище, де одна або дві CH 2 групи можуть бути замінені на O або S атомів і/або на NH, N(LA), CONH, NHCO або -CH=CН-групи й/або на додаток 1- 3 H атомів можуть бути замінені на F і/або Cl, такі як, наприклад, трифторметил, пентафторетил, 1,1-дифторметил, 1,1,1-трифторетил, метокси, етокси, нпропокси, ізопропокси, н-бутокси, ізобутокси, втор-бутокси або трет-бутокси. В інших прикладах "A", одна або дві CH3 групи замінені на OH, SH, NH2, N(LA)H, N(LA)2 або CN, такі як, наприклад, N, N'-диметиламіноалкіл, 2-аміноетил, 3-амінопропіл, 4-амінобутил, 5амінопентил, 3-амінометилциклобутил або ціаноалкіл. Циклічні A переважно означає циклопропіл, циклобутил, циклопентил, циклогексил або циклогептил. "LA" означає нерозгалужений або розгалужений, лінійний алкіл, який містить 1, 2, 3 або 4 C атома, де 1, 2 або 3 H атомів можуть бути замінені на Hal, наприклад, метил, етил, трифторметил, дифторметил, 1,1,1-трифторетил, пропіл, ізопропіл, бутил, ізобутил, втор-бутил або тре-бутил. "Ar" означає, наприклад, незаміщений феніл, нафтил або біфеніл, крім того, переважно, наприклад, феніл, нафтил або біфеніл, кожний з яких моно-, ди- або тризаміщен A, фтором, хлором, бромом, йодом, гідроксилом, метокси, етокси, пропокси, бутокси, пентилокси, гексилокси, нітро, ціано, формилом, ацетилом, пропінилом, трифторметилом, аміно, метиламіно, етиламіно, диметиламіно, діетиламіно, бензилокси, сульфонамідо, метилсульфонамідо, етилсульфонамідо, пропілсульфонамідо, бутилсульфонамідо, диметилсульфонамідо, фенілсульфонамідо, карбоксилом, метоксикарбонілом, етоксикарбонілом, амінокарбонілом. "Ar" додатково означає феніл, o-, м- або п- толил, o-, м- або п- етилфеніл, o-, м- або ппропілфеніл, o-, м- або п-ізопропілфеніл, o-, м- або п-тре-бутилфеніл, o-, м- або пгідроксифеніл, o-, м- або п-нітрофеніл, o-, м- або п-амінофеніл, o-, м- або п-(Nметиламіно)феніл, o-, м- або п-(N-метиламінокарбоніл)феніл, o-, м- або п-ацетамідофеніл, o-, м 3 UA 110113 C2 5 10 15 20 25 30 35 40 45 50 55 60 або п-метоксифеніл, o-, м- або п-етоксифеніл, o-, м- або п-етоксикарбонілфеніл, o-, м- або п-(N, N-диметиламіно)феніл, o-, м- або п-(N, N-диметиламінокарбоніл)феніл, o-, м- або п-(Nетиламіно)феніл, o-, м- або п-(N, N-діетиламіно)феніл, o-, м- або п-фторфеніл, o-, м- або пбромфеніл, o-, м- або п- хлорфеніл, o-, м- або п-(метилсульфонамідо)феніл, o-, м- або п(метилсульфоніл)феніл, также предпочтительно 2,3-, 2,4-, 2,5-, 2,6-, 3,4- або 3,5-дифторфеніл, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- або 3,5-дихлорфеніл, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- або 3,5-дибромфеніл, 2,4або 2,5-динітрофеніл, 2,5- або 3,4-диметоксифеніл, 3-нітро-4-хлорфеніл, 3-аміно-4-хлор-, 2аміно-3-хлор-, 2-аміно-4-хлор-, 2-аміно-5-хлор- або 2-аміно-6-хлорфеніл, 2-нітро-4-N, Nдиметиламіно- або 3-нітро-4-N, N-диметиламінофеніл, 2,3-диамінофеніл, 2,3,4-, 2,3,5-, 2,3,6-, 2,4,6- або 3,4,5-три-хлорфеніл, 2,4,6-триметоксифеніл, 2-гідрокси-3,5-дихлорфеніл, п-йодфеніл, 3,6-дихлор-4-амінофеніл, 4-фтор-3-хлорфеніл, 2-фтор-4-бромфеніл, 2,5-дифтор-4-бромфеніл, 3-бром-6-метоксифеніл, 3-хлор-6-метоксифеніл, 3-хлор-4-ацетамідофеніл, 3-фтор-4метоксифеніл, 3-аміно-6-метилфеніл, 3-хлор-4-ацетамідофеніл або 2,5-диметил-4-хлорфеніл, (4-метоксифеніл)метил, (3-метоксифеніл)метил, (4-метоксифеніл)етил, (3-метоксифеніл)етил. "Ar" додатково переважно означає 2-, 3- або 4-феніл, 2-, 3- або 4-фенілметил, 2-, 3- або 4фенілетил, 2- або 3-фурил, 2- або 3-тієніл, 1-, 2- або 3-піроліл, 1-, 2, 4- або 5-імідазоліл, 1-, 3-, 4або 5-піразоліл, 2-, 4- або 5-оксазоліл, 3-, 4- або 5- ізоксазоліл, 2-, 4- або 5-тіазоліл, 3-, 4- або 5ізотіазоліл, 2-, 3- або 4-піридил, 2-, 3- або 4- піридилметил, 2-, 3- або 4-піридилетил, 2-, 4-, 5або 6-піримідиніл, 2-, 3-, 5-, або 6- піразин-1- або 4-іл, також переважно 1,2,3-триазол-1-, -4- або 5-іл, 1,2,4- триазол-1-, -3- або 5-іл, 1- або 5-тетразоліл, 1,2,3-оксадіазол-4- або 5-іл, 1,2,4оксадіазол-3- або 5-іл, 1,3,4-оксадіазол-2-іл, 1,3,4-тіадіазол-2- або 5-іл, 1,2,4-тіадіазол-3- або 5іл, 1,2,3-тіадіазол-4- або-5-іл, 3- або 4-піридазиніл, 1-, 2-, 3-, 4-, 5-, 6- або 7-індоліл, 2-, 3-, 4- або 5- ізоіндоліл, 2-, 6, або 8-пуриніл, 1-, 2-, 4- або 5-бензімідазоліл, 1-, 3-, 4-, 5-, 6- або 7бензопіразоліл, 2-, 4-, 5-, 6- або 7- бензоксазоліл, 3-, 4-, 5-, 6- або 7- бензізоксазоліл, 2-, 4-, 5-, 6або 7- бензотіазоліл, 2-, 4-, 5-, 6- або 7- бензізотіазоліл, 4-, 5-, 6- або 7- бенз-2,1,3-оксадіазоліл, 1-, 3-, 4-, 5-, 6-, 7- або 8- ізохінолініл, 3-, 4-, 5-, 6-, 7- або 8-хінолініл, 2-, 4-, 5-, 6-, 7- або 8хіназолініл, хіноксалін-2-, 3-, 4- або 5-іл, 4-, 5-, або 6- фталазиніл, 2-, 3-, 5-, 6-, 7- або 8- 2Hбензо-1,4 -оксазиніл, додатково переважно 1,3-бензодіоксол-2-, 4- або 5-іл, тіофен-2- або 3-іл, 1,4- бензодіоксан6-іл, 2,1,3-бензотіадіазол-4- або 5-іл або 2,1,3-бензоксадіазол- 5-іл, фуран-2- або 3-іл, 2, бензофуран-2-, 3-, 4- або 5-іл, кожний з яких незаміщений або може бути моно-, ди- або тризаміщен, наприклад, карбонільним киснем, F, Cl, Br, метилом, етилом, пропілом, фенілом, бензилом, -CH2циклогексилом, гідроксилом, метокси, етокси, аміно, метиламіно, диметиламіно, нітро, ціано, карбоксилом, метоксикарбонілом, амінокарбонілом, метиламінокарбонілом, диметиламінокарбонілом, ацетаміно, уреїдо, метилсульфоніламіно, формилом, ацетилом, аміносульфонілом і/або метилсульфонілом. 1 1 4 2 5 4 У тих випадках, коли R являє собою L –R –L –R , залишок R , мабуть, виконує місткову 1 2 функцію, і заміщений лінкерами L і L , незалежно від будь-яких можливих додаткових заміщень. Термін "заміщений" переважно відноситься до заміщення вищевказаними замісниками, де можлива безліч ступенів заміщення, якщо не зазначене інакше. Усі фізіологічно прийнятні солі, похідні, сольвати, сольвати солей, і стереоізомери цих сполук, включаючи їх суміші у всіх співвідношень, є також відповідно до винаходу. Сполуки Формули (I) можуть мати один або кілька центрів хіральности. Відповідно, вони можуть зустрічатися в різних енантіомерних формах і бути рацемічними або оптично активними формами. Тому винахід також відноситься до оптично активних форм (стереоізомери), енантіомерам, рацематам, діастереомерам і сольватам цих сполук. Оскільки фармацевтична активність рацематів або стереоізомерів сполук відповідно до винаходу може відрізнятися, може бути бажаним застосування енантіомерів. У цих випадках, кінцевий продукт або навіть проміжні сполуки можуть розділятися на енантіомерні сполуки за допомогою хімічних або фізичних методів, відомих фахівцеві в даній галузі техніки, або навіть використовуватися як такі в синтезі. У випадку рацемічних амінів, діастереомери утворюються із суміші шляхом реакції з оптично активним агентом, що розщеплює. Прикладами придатних агентів, що розщеплюють, є оптично активні кислоти, такі як R- і S- форми винної кислоти, діацетилвинної кислоти, дибензоїлвинної кислоти, мигдалевої кислоти, яблучної кислоти, молочної кислоти, відповідно N-захищеної амінокислоти (наприклад, N-бензоїлпролін або N-бензолсульфонілпролін), або різних оптично активних камфорсульфонових кислот. Також сприятливим є хроматографічне розщеплення енантіомерів за допомогою оптично активного агента, що розщеплює (наприклад, 4 UA 110113 C2 5 10 15 20 25 30 35 40 45 50 55 60 динітробензоїлфенілгліцин, триацетат целюлози або інші похідні карбогідратів або хірально похідні метакрилатні полімери імобілізування на силікагелі). Придатними елюентами для цього є водні або спиртові суміші розчинників, такі як, наприклад, гексан/ізопропанол/ ацетонітрил, наприклад, у співвідношенні 82:15:3. Кращим способом розчинення рацематів, що містять складні ефірні групи (наприклад, ацетилові складні ефіри), є застосування ферментів, зокрема естераз. У кращій групі сполук формули (I) змінні й замісники мають наступні значення: X являє собою N, Y являє собою NH, 1 1 4 R являє собою L – R , 2 R являє собою LA, Hal, OH, O(LA), SH, CN, NH 2, NO2, NH(LA), NHCO(LA), NHSO2(LA), NHCONH(LA), 1 L являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна NH2 або NH(LA), N(LA)2, або циклічним A, який може бути моно- або дизаміщений Hal або LA, 4 R являє собою моноциклічний ароматичний гомо- або гетероцикл, який містить 0, 1 або 2 N, O і/або S атома й 5 або 6 кістякових атомів, і який може бути незаміщений або, незалежно друг від друга, моно-, ди- або тризаміщений Hal, A, OH, SH, OA, NH2, NHA, NA2, NO2, CN, OCN, SCN, COOH, COOA, CONH2, CONHA, CONA2, NHCOA, NHCONHA, NHCONH2, NHSO2A, CHO, COA, SO2NH2, SO2A і/або SO2Hal, A являє собою нерозгалужений або розгалужений лінійний або циклічний алкіл, який містить 1, 2, 3, 4, 5, 6, 7 або 8 C атомів, де одна або дві CH2 групи можуть бути замінені на O або S атом і/або на –NH-, -CO-, -NHCOO-, -NHCONH-. -N(LA)-, -CONH-, -NHCO- або –CH=CH– групу, і де 13 H атомів можуть бути замінені на Hal, і де одна або дві CH3 групи можуть бути замінені на OH, SH, NH2, NH(LA), N(LA)2, NHCOOH, NHCONH2 або CN, LA являє собою нерозгалужений або розгалужений, лінійний алкіл, який містить 1, 2, 3 або 4 C атома, де 1, 2 або 3 H атома можуть бути замінені на Hal, Hal являє собою F, Cl, Br або I. Додатково кращими є сполуки підформул 1-19 формули (I), де залишки, які не дуже детально позначені, мають значення, зазначені в кращій групі сполук, зазначеної вище, і їх фармацевтично прийнятні солі, сольвати, сольвати солей, або пролік, де у підформулі 1 2 R являє собою LA, у підформулі 2 1 L являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно, диметиламіно або азетидином, у підформулі 3 4 R являє собою феніл, який незаміщений або монозаміщений Hal, у підформулі 4 2 R являє собою метил, етил, ізопропіл або трифторметил, у підформулі 5 1 L являє собою метил-заміщений метилен, де метильна група метил- заміщеного метилену монозамещіна метиламіно, у підформулі 6 1 L являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна азетидин-1-ілом, у підформулі 7 4 R являє собою феніл, який є незаміщеним, у підформулі 8 4 R являє собою феніл, який мета- або пара- заміщений F або Cl, у підформулі 9 2 R являє собою LA, 1 L являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно або азетидином, у підформулі 10 2 R являє собою LA, 4 R являє собою феніл, який незаміщений або монозаміщений Hal, у підформулі 11 1 L являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно або азетидином, 5 UA 110113 C2 4 5 10 15 20 25 30 35 40 45 50 55 60 R являє собою феніл, який незаміщений або монозаміщенийий Hal, у підформулі 12 2 R являє собою LA, 1 L являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно або азетидином, 4 R являє собою феніл, який незаміщений або монозаміщенийий Hal, у підформулі 13 2 R являє собою метил, етил, ізопропіл або трифторметил, 1 L являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно або азетидином, 4 R являє собою феніл, який незаміщений або монозаміщений Hal, у підформулі 14 2 R являє собою LA, 1 L являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно або азетидином, 4 R являє собою феніл, який мета- або пара- заміщений F або Cl, у підформулі 15 2 R являє собою метил, етил, ізопропіл або трифторметил, 1 L являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно або азетидином, 4 R являє собою феніл, який мета- або пара- заміщений F або Cl, у підформулі 16 2 R являє собою метил, етил, ізопропіл або трифторметил, 1 L являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно, 4 R являє собою феніл, який мета- або пара- заміщений F або Cl, у підформулі 17 2 R являє собою метил, етил, ізопропіл або трифторметил, 1 L являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна азетидин-1-ілом, 4 R являє собою феніл, який мета- або пара- заміщений F або Cl, у підформулі 18 2 R являє собою метил, етил, ізопропіл або трифторметил, 1 L являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно або азетидином, 4 R являє собою феніл, який мета- заміщений F або Cl, у підформулі 19 2 R являє собою метил, етил, ізопропіл або трифторметил, 1 L являє собою метил-заміщений метилен, де метильна група метил-заміщеного метилену монозамещіна метиламіно або азетидин-1-ілом, 4 R являє собою феніл, який мета- заміщений F або Cl, і інші залишки мають значення, зазначені вище для формули (I). Сполуки даного винаходу можуть бути у формі сполук-проліків. " Сполуки-проліки" означає похідне, яке перетворено в біологічно активну сполуку відповідно до даного винаходу у фізіологічних умовах у живому організмі, наприклад, шляхом окиснення, відновлення, гідролізу або т.п., кожне з яких здійснюють ферментативним шляхом, або без участі ферментів. Прикладами проліків є сполуки, де аміногрупа в сполуці даного винаходу ацильована, алкілована або форфорилована, наприклад, ейкозаноїламіно, аланіламіно, пивалоїлоксиметиламіно або де гідроксильна група ацильована, алкілована, форфорилирована або перетворена в борат, наприклад, ацетилокси, палмитоїлокси, пивалоїлокси, сукцинілокси, фумарилокси, аланилокси або де карбоксильна група естерифікована або амідована, або де сульфгідрильна група утворює дисульфидний місток з молекулою-носієм, наприклад, пептид, який доставляє ліки селективно до мети й/або до цитозолю клітки. Ці сполуки можна одержати із сполук даного винаходу відповідно до добре відомих способів. Іншими прикладами проліків є сполуки, де карбоксилат у сполукі даного винаходу перетворений, наприклад в алкіл-, арил-, холін-, аміно, ацилоксиметиловий складний ефір, ліноленоїловий складний ефір. Там, де може мати місце таутомерія, наприклад, кето-енольная таутомерія, сполук даного винаходу або їх проліків, індивідуальні форми, наприклад, кето- або енольна форма, заявляються окремо або разом у вигляді сумішей у будь-якім співвідношенні. Те ж саме стосується стереоізомерів, наприклад, енантіомерів, цис/транс ізомерів, конформерів і т.п. 6 UA 110113 C2 5 10 15 20 25 30 35 40 45 50 55 60 При бажанні, ізомери можна відокремити добре відомими в рівні техніки способами, наприклад, за допомогою рідинної хроматографії. Те ж саме стосується енантіомерів, наприклад, з використанням хіральних нерухливих фаз. Додатково, енантіомери можна виділяти за допомогою їхнього перетворення в діастереомери, тобто, шляхом комбінації з енантіомерно чистим допоміжним сполуким, з наступним відділенням отриманих у результаті діастереомерів і розщепленням допоміжного залишку. Альтернативно, будь-який енантіомер сполуки даного винаходу можна одержати зі стереоселективного синтезу з використанням оптично чистих вихідних речовин. Сполуки даного винаходу можуть бути у формі фармацевтично прийнятної солі або сольвату, або сольвату такої солі. Термін "фармацевтично прийнятні солі" відноситься до солей, отриманих з фармацевтично прийнятних нетоксичних основ або кислот, включаючи неорганічні основи або кислоти й органічні основи або кислоти. У випадках, де сполуки даного винаходу містять одну або кілька кислотних або основних груп, винахід також включає їхні відповідні фармацевтично або токсикологічно прийнятні солі, зокрема їх фармацевтично придатні для використання солі. Таким чином, сполуки даного винаходу, які містять кислотні групи, можуть бути присутнім формі солі, і можуть застосовуватися відповідно до винаходу, наприклад, у вигляді солей лужних металів, солі лужноземельних металів або у вигляді амонієвих солей. Більш точні приклади таких солей включають натрієві солі, калієві солі, кальцієві солі, магнієві солі або солі з аміаком або органічними амінами, такими як, наприклад, етиламін, етаноламін, триетаноламін, або з амінокислотами. Сполуки даного винаходу, які містять одну або кілька основних груп, тобто, груп, які можуть бути протонровани, бути присутнім формі солі, і можуть застосовуватися відповідно до винаходу у вигляді їх адитивних солей з неорганічними або органічними кислотами. Приклади придатних кислот включають хлорид водню, бромід водню, фосфорну кислоту, сірчану кислоту, азотну кислоту, метансульфонову кислоту, п-толуолсульфонову кислоту, нафталіндисульфонові кислоти, щавлеву кислоту, оцтову кислоту, винну кислоту, молочну кислоту, саліцилову кислоту, бензойну кислоту, мурашину кислоту, пропіонову кислоту, пивалеву кислоту, діетилоцтову кислоту, малонову кислоту, бурштинову кислоту, пімелінову кислоту, фумарову кислоту, малеїнову кислоту, яблучну кислоту, сульфамінову кислоту, фенілпропіонову кислоту, глюконову кислоту, аскорбінову кислоту, ізонікотинову кислоту, лимонну кислоту, адипінову кислоту, і інші кислоти, відомі фахівцеві в даній галузі техніки. Якщо сполуки даного винаходу одночасно містять кислотні й основні групи в молекулі, винахід також включає, на додаток до зазначених сольових форм, внутрішні солі або бетаїни (цвиттеріони). Відповідні солі можна одержати звичайними способами, відомими фахівцеві в даній галузі техніки, наприклад, шляхом уведення їх у контакт із органічною або неорганічною кислотою або основою в розчиннику або диспергаторі, або шляхом аніонного або катіонного обміну з іншими солями. Даний винахід також включає всі солі сполук даного винаходу, які, через низьку фізіологічну сумісність, не є придатними для безпосереднього застосування у фармацевтичних засобах, але які можна використовувати, наприклад, у якості проміжних сполук для хімічних реакцій або для одержання фармацевтично прийнятних солей. "Сольвати" означають адитивні форми розчинників, які містять або стехіометричні або нестехіометричні кількості розчинника. Багато сполук мають схильність утримувати фіксоване молярне співвідношення молекул розчинника в кристалічному твердому стані, формуючи в такий спосіб сольват. Наприклад, якщо розчинником є вода, сольват, який утворюється, являє собою гідрат, коли розчинником є спирт, сольват, який утворюється, являє собою алкоголят, если растворителем является ефир, сольват, которий образуется, представляет собой ефират. Специфічні приклади сольватів включають моно- або дигідрати, метанолати, етанолати або діетилефірати. Фахівці в даній галузі визнають, що в багатьох випадках сольвати фармацевтичних активних інгредієнтів, або їх фармацевтично прийнятних солей, використовуються у фармацевтичних композиціях, і їм відомо, як одержувати такі сольвати. Крім того, даний винахід відноситься до фармацевтичних композицій, які містять сполуки даного винаходу, або його сполука-пролік, або його фармацевтично прийнятну сіль або сольват, у якості активного інгредієнта разом з фармацевтично прийнятним носієм. "Фармацевтична композиція" означає один або кілька активних інгредієнтів, і один або кілька інертних інгредієнтів, які утворюють носій, а також будь-який отриманий у результаті продукт, безпосередньо або опосередковано, з комбінацій, комплексних утворювань або агрегації будьяких двох або більш інгредієнтів, або з розкладання одного або декількох інгредієнтів, або з інших типів реакцій або взаємодій одного або декількох інгредієнтів. Відповідно, фармацевтичні композиції даного винаходу охоплюють будь-яку композицію, складену шляхом змішування 7 UA 110113 C2 5 10 15 20 25 30 35 40 45 50 55 60 сполуки даного винаходу й фармацевтично прийнятного носія. Фармацевтична композиція справжнього винаходу може додатково містять одне або трохи інших сполук як активних інгредієнтів, таких як одне або декілька додаткових сполук даного винаходу, або сполуку-проліки або інші інгібітори p70S6K. Фармацевтичні композиції включають композиції, придатні для перорального, ректального, місцевого, парентерального (включаючи підшкірне, внутрішньом'язове, і внутрішньовенне), окулярного (очного), пульмонального (назальна або букальна інгаляція), або назального введення, хоча найбільш підходящий шлях уведення в будь-якому вищевказаному випадку буде залежати від природи й ваги стану, який лікують, і від природи активного інгредієнта. Вони можуть зручним чином бути присутнім у стандартній лікарській формі й бути приготовлені будьяким добре відомим в галузі фармації способом. В одному з варіантів здійснення, зазначені сполуки й фармацевтична композиція призначені для лікування злоякісного новотвору, такого як рак мозку, легені, товстої кишки, епідермоїдний рак, плоскоклітинний рак, рак сечового міхура, рак шлунка, підшлункової залози, молочної залози, голови, шиї, ренальний рак, рак нирки, печінки, яєчника, передміхурової залози, колоректальний рак, рак матки, ректальний рак, рак стравоходу, рак яєчка, гінекологічний рак, рак щитовидної залози, меланома, гематологічних злоякісних пухлин, таких як гостра мієлоцитарна лейкемія, множинна мієлома, хронічний мієлолейкоз, мієлоїдний клітинний лейкоз, гліома, Саркома Капоши, або будь-яких інших видів солідних або так званих "рідких" пухлин. Переважно, злоякісний новотвір, який зазнає лікування, обране з раку молочної залози, колоректального рака, рака легені, передміхурової залози або підшлункової залози або гліобластоми. Винахід також відноситься до застосування сполук відповідно до винаходу для одержання лікарського засобу для лікування гіперпроліферативних захворювань, пов'язані з гіперактивністю p70S6K, а також захворювань, модульованих каскадом p70S6K, у ссавців, або розладів, опосередкованих аберрантной проліферацією, таких як злоякісний новотвір і запалення. Винахід також відноситься до сполуки або фармацевтичної композиції для лікування захворювання, пов'язаного з васкулогенезом або ангіогенезом у ссавця, яка включає терапевтично ефективну кількості сполуки даного винаходу, або його фармацевтично прийнятної солі, проліки або сольвату, і фармацевтично прийнятний носій. В одному з варіантів здійснення, зазначена сполука або фармацевтична композиція призначені для лікування захворювання, обраного із групи, яка включає ангіогенез пухлини, хронічне запальне захворювання, таке як ревматоїдний артрит, запальні захворювання кишечнику, атеросклероз, шкірні захворювання такі як псоріаз, екзема, і склередема, діабет, діабетичну ретинопатію, ретинопатію недоношених і вікову дегенерацію макули. Даний винахід також відноситься до сполуки або фармацевтичної композиції для інгібування атипичного клітинного росту в ссавця, яка включає кількість сполуки даного винаходу, або його фармацевтично прийнятної солі або сольвату або проліки, у комбінації з кількістю іншого протиракового терапевтичного засобу, де кількості сполуки, солі, сольвату, або проліки, і хіміотерапевтичного засобу разом є ефективними для інгібування атипичного клітинного росту. Багато протиракові терапевтичні засоби в цей час відомі в даній галузі техніки. В одному з варіантів здійснення, протиракове терапевтичне є хіміотерапевтичним засобом, обраним із групи, яка включає інгібітори мітозу, алкілуючі агенти, анти-метаболіти, інтеркалирующие антибіотики, інгібітори факторів росту, інгібітори клітинного циклу, ферменту, інгібітори типоізомерази, модифікатори біологічного відгуку, антигормональні засоби, інгібітори ангіогенеза, і антиандрогени. В іншому варіанті здійснення протираковий терапевтичний засіб являє собою антитіло, обране із групи, яка включає бевацизумаб, CD 40-специфічні антитіла, chTNT-1/B, денозумаб, занолимумаб, IGF1R-специфічні антитіла, линтузумаб, едреколомаб, WX G250, ритуксимаб, тицилимумаб, трастузумаб і цетуксимаб. У ще іншому варіанті здійснення протираковий терапевтичний засіб являє собою інгібітор інший протеїнкінази, такий як Akt, Axl, Аурора A, Аурора B, dyrk2, epha2, fgfr3, igf1r, IKK2, JNK3, Vegfr1, Vegfr2, Vegfr3 (також відома як Flt-4), KDR, MEK, MET, Plk1, RSK1, Src, Trka, Zap70, cKit, bRaf, EGFR, Jak2, PI3K, NPM-Alk, c-Abl, BTK, FAK, PDGFR, TAK1, LimK, Flt-3, PDK1 і Erk. Даний винахід також відноситься до способу інгібування атипового клітинного росту в ссавця або лікування гіперпроліферативного порушення, який включає введення ссавцеві кількості сполуки згідно із даним винаходом, або його фармацевтично прийнятної солі або сольвату або проліки, у комбінації із променевою терапією, де кількості сполуки, солі, сольвату, або проліки, представлені в комбінації із променевою терапією, ефективні для інгібування атипичного клітинного росту або лікування гіперпроліферативного порушення в ссавця. Техніки 8 UA 110113 C2 5 10 15 20 25 30 35 40 45 50 55 60 введення променевої терапії відомі з рівня техніки, і ці техніки можна використовувати в комбінованій терапії, описаної в даної заявці. Уведення сполуки згідно з винаходом у цій комбінованій терапії можна визначити, як описано в даної заявці. Уважаються, що сполуки відповідно до даного винаходу можуть надавати атипичним кліткам більшу чутливість до лікування із застосуванням променевої терапії для знищення й/або інгібування росту таких кліток. Отже, даний винахід також відноситься до способу сенсибілізації атипичних кліток у ссавця до лікування із застосуванням променевої терапії, який включає введення ссавцеві кількості сполуки згідно із даним винаходом або його фармацевтично прийнятної солі або сольвату або проліки, де кількість є ефективною для сенсибілізації атипичних кліток до лікування за допомогою променевої терапії. Кількість сполуки, солі, або сольвату в цьому методі можна визначити відповідно до методів для встановлення ефективних кількостей таких сполук, описаних в даної заявці. Винахід також відноситься до способу інгібування атипичного клітинного росту в ссавця, який включає застосування кількості сполуки згідно із даним винаходом, або його фармацевтично прийнятної солі або сольвату, його проліків, або його похідного, міченого радіоактивним ізотопом, і кількості одного або декількох речовин, обраних з антиангіогенних агентів, інгібіторів передачі сигналів, і антипроліферативних агентів. При практичнім використанні, сполуки відповідно до даного винаходу можна комбінувати в якості активного інгредієнта в тісній суміші з фармацевтичним носієм відповідно до загальноприйнятих методик готування лікарських засобів. Носій може мати різні форми залежно від форми препарату, бажаного для введення, наприклад, перорального або парентерального (включаючи внутрішньовенне). Для готування композицій для пероральних дозованих форм, можна використовувати будь-які звичайні фармацевтичні середовища, такі як, наприклад, вода, гліколі, масла, спирти, ароматизатори, консерванти, барвники й інші. У випадку пероральних рідких препаратів, можна використовувати будь-які звичайні фармацевтичні середовища, такі як, наприклад, суспензії, еліксири й розчини; або носії, такі як крохмалі, цукри, мікрокристалічна целюлоза, розріджувачі, що гранулюють агенти, замаслювачи, зв’язуючі, дезінтегратори й інші. У випадку твердих пероральних препаратів, композиція може перебувати в таких формах, як, наприклад, порошки, тверді й м'які капсули й таблетки, при цьому тверді пероральні препарати є кращими щодо рідких препаратів. У зв'язку із простотою їх уведення, таблетки й капсули є найбільш сприятливими пероральними дозуючими одиничними формами, у цих випадках обов'язково використовуються тверді фармацевтичні носії. Якщо це є бажаним, то таблетки можуть бути покриті оболонкою за допомогою стандартних водних або неводних технік. Такі композиції й препарати повинні містити щонайменше 0,1 відсоток активної сполуки. Відсоток активної сполуки в цих композиціях, мабуть, може змінюватися й підходить може становити від приблизно 2 відсотків до приблизно 60 відсотків від маси одиниці. Кількість активної сполуки в таких терапевтично придатних композиціях буде таким, щоб одержати ефективну дозу. Активні сполуки також можна вводити інтраназально, наприклад, у вигляді рідких крапель або спрею. Таблетки, пігулки, капсули, і інші форми також можуть містити зв’язуче, таке як трагакантову камедь, гуміарабік, кукурудзяний крохмаль або желатин; наповнювачі, такі як дикальций фосфат; дезінтегрувальний засіб, таке як кукурудзяний крохмаль, картопляний крохмаль, альгінову кислоту; замаслювач, такий як стеарат магнію; і підсолоджувач, такий як сахароза, лактоза або сахарин. Якщо одинична дозована форма являє собою капсулу, то вона може містити, додатково до речовин вищеописаного типу, рідкий носій, такий як жирне масло. Різні інші речовини можуть бути присутнім у вигляді покриттів або для модифікації фізичної форми дозованої одиниці. Наприклад, таблетки можуть бути покриті за допомогою шелаку, цукру або обох речовин. Сироп або еліксир може містити, додатково до активного компонента, сахарозу в якості підсолоджувача, метил і пропілпарабени в якості консервантів, барвник і ароматизатор, такий як вишневий або апельсиновий ароматизатор. Сполуки згідно із даним винаходом також можуть уводитися парентерально. Розчини або суспензії цих активних сполук можуть бути приготовлені у воді, підходяче змішані з поверхневоактивною речовиною, таким як гідрокси-пропілцелюлоза. Дисперсії також можуть бути приготовлені в гліцерині, рідких поліетиленгліколях і їх сумішах у маслах. При звичайних умовах зберігання й застосування, ці препарати містять консервант для запобігання росту мікроорганізмів. Фармацевтичні форми підхожії для ін'єкцій, включають стерильні водяні розчини або дисперсії й стерильні порошки для екстемпоральних препаратів стерильних ін'єкційних розчинів або дисперсій. У всіх випадках, форма повинна бути стерильної й повинна бути рідкої настільки, щоб її легко можна було вводити за допомогою шприца. Вона повинна бути стабільної в умовах 9 UA 110113 C2 5 10 15 20 25 30 35 виготовлення й зберігання й повинна бути захищена від забруднюючого дії мікроорганізмів, таких як бактерії й гриби. Носій може переставляти собою розчинник або дисперсійне середовище, що містить, наприклад, воду, етанол, поліол (наприклад, гліцерин, пропіленгліколь і рідкий поліетиленгліколь), їхні підходящі суміші, і рослинні олії. Будь-який підходящий шлях уведення може застосовуватися для забезпечення ссавця, особливо людини, ефективною дозою сполуки згідно із даним винаходом. Наприклад, можна застосовувати пероральний, ректальний, місцевий, парентеральний, очний, легеневий, назальний і інші шляхи. Дозовані форми включають таблетки, коржа, дисперсії, суспензії, розчини, капсули, креми, мазі, аерозолі й інші. Переважно сполуки згідно із даним винаходом вводять перорально. Ефективне дозування застосовуваного активного компонента може змінюватися залежно від конкретного застосовуваної сполуки, способу введення, стану, що зазнає лікуванню, і ваги стану, що зазнає лікуванню. Такі дозування легко можуть бути встановлені фахівцем у даній галузі техніки. При лікуванні або запобіганні злоякісного новотвору, запалення або інших проліферативних захворювань, для яких показані сполуки згідно із даним винаходом, звичайно задовільні результати одержують, якщо сполуки відповідно до даного винаходу вводять у добовій дозі від приблизно 0,01 міліграма до приблизно 100 міліграм на кілограм ваги тіла тварини, переважно представлених у вигляді одиничної добової дози. Для найбільш великих ссавців, загальна добова доза становить від приблизно 0,1 міліграма до приблизно 1000 міліграм, переважно від приблизно 0,2 міліграм до приблизно 50 міліграм. Для дорослої людини вагою 70 кг, загальна добова доза звичайно буде становити від приблизно 0,2 міліграм до приблизно 200 міліграм. Ця схема дозування може регулюватися для забезпечення оптимальної терапевтичної відповіді. Винахід також відноситься до набору (комплекту), який складається з окремих пакетів: a) ефективної кількості відповідно до винаходу або його фізіологічно прийнятної солі, сольвату, або проліки, і b) ефективної кількості додаткового активного інгредієнта лікарського засобу. Набір включає підходящі контейнери, такі як коробочки, індивідуальні флакони, пакети або ампули. Набір може, наприклад, включати окремі ампули, кожна з яких містить ефективну кількість сполуки відповідно до винаходу й/або їх фармацевтично придатних похідних, сольватів і стереоізомерів, включаючи їх суміші у всіх співвідношеннях, і ефективна кількість додаткового активного інгредієнта лікарського засобу в розчиненій або ліофілізованной формі. Експериментальний розділ Деякі скорочення, які можна зустріти в даній заявці, зазначені нижче: Скорочення Позначення ACN АТФ b d ДМСО DIEA DTT EDTA еквив. Et г HEPES ВЕРХ РХ/МС m M m/z Me хв МС н. Ацетонітрил Аденозинтрифосфат Широкий пік Дублет Диметилсульфоксид N, N-Діізопропілетиламін Дитіотреїтол Етилендіамінтетраоцтова кислота Еквіваленти Етил Година 4-(2-Гідроксіетил)-1-піперазинетансульфонова кислота Високоефективна рідинна хроматографія Комбінація рідинної хроматографії з мас-спектрометрією Мультиплет Молекулярний іон Відношення маси до заряду Метил Хвилина Мас-спектрометрія Нормальна (одиниця концентрації) 10 UA 110113 C2 NMO ЯМР ЗГ фунт/кв. дюйм q Rf КТ Rt. s Тре TEA ТФО THAB ТГФ УФ ВИД 5 10 15 20 25 30 n-оксид Ядерний магнітний резонанс Захисна група Фунт на квадратний дюйм Квартет Фактор утримання Кімнатна температура Час утримання Синглет Третинний Триетиламін Трифтороцтова кислота Бромід тетрагексиламонію Тетрагідрофуран Ультрафіолетовий Видима частина спектра Сполуки згідно із даним винаходом можна одержати відповідно до методик наступних Схем і Прикладів, з використанням підходящих речовин, і вони додатково проілюстровані за допомогою наступних специфічних прикладів. Крім того, використовуючи методики, описані в даній заявці, у комбінації зі звичайними в рівні техніки, можна легко одержати додаткові сполуки даного винаходу, заявлені в даному документі. Однак, сполуки, проілюстровані в прикладах, не слід тлумачити як формуючі єдиний вид, розглянутий як винахід. Приклади додатково ілюструють деталі для одержання сполук даного винаходу. Фахівці в даній галузі техніки легко зрозуміють, що відомі варіації умов і способів наступних препаративних технологій, можуть бути використані для одержання цих сполук. Справжні сполуки як правило виділяють у формі їх фармацевтично прийнятних солей, таких як описані вище. Аміни у формі вільних основ, відповідні до виділених солей, можна одержати шляхом нейтралізації придатною основою, такою як водяний розчин гідрокарбонату натрію, карбонату натрію, гідроксиду натрію й гідроксиду калію, і екстракції звільненого аміну у формі вільної основи в органічний розчинник, з наступним розпарюванням. Амін у формі вільної основи, виділений таким способом, можна додатково перетворити в іншу фармацевтично прийнятну сіль за допомогою розчинення в органічному розчиннику, з наступним додаванням підходящої кислоти й наступним розпарюванням, осадженням або кристалізацією. Винахід буде проілюстрований, але не обмежене, виходячи зі специфічних варіантів здійснення, описаних у наступних схемах і прикладах. Якщо в схемах не зазначене інакше, змінні мають то ж значення, як описано вище. Якщо не описане інакше, усі вихідні речовини одержують від комерційних постачальників і використовують без додаткового очищення. Якщо не описане інакше, усі температури виражають в (C і всі реакції здійснюють при кімнатній температурі. Сполуки очищали за допомогою або хроматографії на силікагелі, або препаративної ВЕРХ. Даний винахід також відноситься до способів одержання сполук Формули (I) і Підформул 119 відповідно до нижчеописаних схемі демонстраційними прикладами. Зокрема, даний винахід відноситься до способу одержання сполук Формули (I), де X являє собою N і Y являє собою NH, і всі інші замісники мають значення, зазначені для Формули (I) у пункті 1 формули, де ефір карбонової кислоти формули (IV) (IV), уводять у реакцію із сполукою формули (III) 1 H-Y-R 11 UA 110113 C2 (III), с одержанням сполуки формули (II) (II), яке на закінчення перетворюють в амід карбонової кислоти формули (I) (I). 5 Загальні методики синтезу O O OH R2 O O O OH R2 O N NH2 N NH4OH O OH 1a O 1c 1b O O N R2 NH POCl3, (i-Pr)2NEt Bn(Et)3N+Cl O O N O 15 R2 N MeCN Cl 1d 10 R2 NH O O MeOH H2SO4 R2 OH 1e Схема 1 Нагрівання зі зворотним холодильником заміщеної 2-аміноізофталевої кислоти з ангідридом карбонової кислоти при 185 °C протягом 4 годин давало карбонову кислоту 1b, яка при обробці концентрованим гідроксидом амонію давала оксохіназолінкарбонову кислоту 1c. Естерифікація метанолом і сірчаною кислотою в умовах нагрівання зі зворотним холодильником давала складний метиловий ефір 1d, який перетворювали в метиловий ефір 4-хлорхіназолінкарбонової кислоти 1e при обробці оксихлоридом фосфору й основою Хунига в присутності каталізатора фазового переносу. 12 UA 110113 C2 5 Схема 2 Аміноспирт 2a обробляли дитретбутилдикарбонатом у присутності 2н. гідроксиду натрію й тре-бутанолу в якості розчинника з одержанням Boc-захищеного аміноспирту 2b. Після циклізації тіонілхлоридом до сульфоксидної проміжного сполуки випливало окиснення періодатом натрію в присутності рутенієвого каталізатора з одержанням циклічного проміжного сполуки 2c. Нуклеофільна атака 2c вторинним аміном і in-situ зняття захисту Boc хлористоводневої кислотою/метанолом давали бажаний амін 2d. R3 (i-Pr)2NEt, MeCN N R2 15 20 25 30 35 40 45 50 R3 R4 N R5 NH4OH MeOH HN N R1 R1 70°C N O 10 R4 N R5 H2 N Cl R3 3a O R2 N R4 N R5 Cs2CO3 PhSH, MeCN N 70°C O HN R3 R2 O H2N 3b 3c R2 O H N N R1 N HN R5 R1 N H2 N O 3d Схема 3 4-Хлорхіназолінову похідну 3a уводили в реакцію з первинним аміном 2d у присутності основи Хунига з одержанням 4-амінохіназолінової проміжної сполуки 3b. Амонолиз складноефірной групи 7н. розчином аміак/метанол давав карбоксамід 3c. Коли R4 являє собою захисну нозильную групу, у результаті зняття захисту карбонатом цезію в присутності тіофенолу одержують 3d. Аналітичні методики Аналітичну РХ/МС здійснювали, використовуючи три наступні методи: 18 Метод A: Колонкові Discovery C , 5 мкм, 3 × 30 мм, використовували при швидкості потоку 400 мкл/хв, пробовідбірникова петля 5 мкл, рухлива фаза: (A) вода з 0.1 % мурашиної кислоти, рухлива фаза, (B) метанол з 0.1 % мурашиної кислоти; час утримання наведений у хвилинах. Подробиці методу: (I) працювали з використанням насоса G1311A (Agilent) для чотирьохкомпонентних сумішей з УФ/ВИД. детектором на діодної матриці G1315B (Agilent) і МСдетектором Finnigan LCQ Duo в ESI + режим з Уф-детектуванням при 254 і 280 нм із градієнтом 15-95 % (B) за 3.2 хв лінійний градієнт (II) утримували протягом 1.4 хв при 95 % (B) (III) зменшували від 95-15 % (B) за 0.1 хв лінійний градієнт (IV) утримували протягом 2.3 хв при 15 % (B). 18 Метод В: Колонкові Waters Symmetry C , 3.5 мкм, 4.6 × 75 мм, використовували при швидкості потоку 1 мл/хв, пробовідбірникова петля 10 мкл, рухливою фазою (A) є вода з 0.05 % ТФО, рухливою фазою (B) є ACN з 0.05 % ТФО; час утримання наведений у хвилинах. Подробиці методу: (I) працювали з використанням подвійного насоса G1312A (Agilent) з УФ/ВИД детектором на діодной матриці G1315B (Agilent) і МС-детектором Agilent G1956B (SL) в ESI + режим з Уф-детектуванням при 254 і 280 нм із градієнтом 20-85 % (B) за 10 хв лінійний градієнт (II) утримували протягом 1 хв при 85 % (B) (III) зменшували від 20-85 % (B) за 0.2 хв лінійний градієнт (IV) утримували протягом 3.8 хв при 20 % (B). Метод С: Градієнт: 4.2 хв/ потік: 2 мл/хв 99:01-0:100 вода + 0.1 % (про.) ТФО; Ацетонітрил + 0.1 % (про.) ТФО; 0.0-0.2 хв: 99:01; 0.2-3.8 хв: 99:01 0:100; 3.8-4.2 хв: 0:100; Колонка: Chromolith Performance RP18e; довжиною 100 мм, діаметром 3 мм; довжина хвилі: 220 нм. Аналітична хіральна ВЕРХ Аналітичну хіральну ВЕРХ здійснювали з використанням колонки Chiralpak AD-H (250 × 4.6 мм) компанії Daicel Chemical Industries, Ltd. на системі Agilent 1100 Series. Для методу використовували інжекцію 5.0 мкл, зі швидкістю потоку 1 мл/хв 100 % метанолу протягом 15 хв при 25 ºC, і Уф-детектуванням при 254 і 280 нм. Препаративна ВЕРХ Препаративну ВЕРХ здійснювали з використанням колонки Waters Atlantis dC18 OBD ™ 10 мкм (30 × 250 мм) або колонки Waters Sunfire Prep C18 OBD 10 мкм (30 × 250 мм). Колонки використовували при швидкості потоку 60 мл/хв на системі Waters Prep LC 4000, оснащеної пробовідбірниковою петлею (10 мл) і УФ/ВИД-детектором ISCO UA-6. Рухливу фазу добували із двох резервуарів з розчинниками, що містять (A) воду й (B) ацетонітрил кваліфікації "для ВЕРХ". Для типової препаративної роботи використовували лінійний градієнт (наприклад, 0 13 UA 110113 C2 5 60 % розчинник B протягом 60 хв). Приклади Демонстраційні приклади, представлені нижче, призначені для ілюстрації окремих варіантів здійснення винаходу, і не призначені яким-небудь образом обмежувати обсяг опису або формули винаходу. Хімічний синтез У цьому розділі надані експериментальні деталі для ряду сполук відповідно до Формули (I), представлених у якості прикладів, і їх проміжних сполук синтезу. Проміжні сполуки синтезу O O N N 10 15 20 25 30 35 40 45 Cl Метил 4-хлор-2-метилхіназолін-8-карбоксилат (1) 2-метил-4-оксо-4H-3,1-бензоксазин-8-карбонова кислота 2-Аміноізофталеву кислоту (50.0 г; 276.0 ммоль) і Ac 2O (250.0 мл; 5.00 об) поєднували й нагрівали до 140 °C протягом 4 г. Реакційну суміш охолоджували до кімнатної температури й дистилювали у високому вакуумі на ротаційному випарнику. Що залишився AcOH видаляли азеотропною дистиляцією з толуолом. Залишок суспендували в етиловому ефіром, фільтрували, і тверду речовину сушили у вакуумі з одержанням бажаної проміжної сполуки (50.3 г, вихід 89 %). 2-Метил-4-оксо-3,4-дигідрохіназолін-8-карбонова кислота 2-Метил-4-оксо-4H-3,1-бензоксазин-8-карбонову кислоту (51.5 г; 251.26 ммоль) розчиняли в NH4OH (360.0 мл; 6.98 про; 28 % розчин). Додавали ацетат амонію (77.5 г; 1,005 ммоль), і реакційну суміш нагрівали при 80 °C протягом 2 г. Реакційну суміш охолоджували до кімнатної температури й розбавляли за допомогою MeOH (40 мл), після чого нагрівали протягом 72 г. при 80 °C у посудині для реакцій під тиском. Реакційну суміш концентрували на ротаційному випарнику, потім охолоджували на льоді й фільтрували. Тверду речовину сушили у вакуумі з одержанням бажаного продукту (33.5 г, вихід 65 %). Метил 2-метил-4-оксо-3,4-дигідрохіназолін-8-карбоксилат 2-Метил-4-оксо-3,4-дигідрохіназолін-8-карбонову кислоту (28.2 г; 138.11 ммоль) розчиняли в сухому MeOH (1000 мл). Сірчану кислоту (29.4 мл; 552.44 ммоль) по краплях додавали до реакційної суміші під аргоном. Реакційну суміш нагрівали зі зворотним холодильником протягом ночі, охолоджували до кімнатної температури, і потім концентрували. Тверду речовину фільтрували й сушили у вакуумі з одержанням бажаної проміжної сполуки у вигляді сульфатної солі. Сульфатну сіль (40.6 г, 128.36 ммоль) обробляли K2CO3 (8.87 г, 64.18 ммоль) в H2O (100 мл). При розчиненні утворювався білуватий осад. Додатково додавали H2O (100 мл), і значення pН установлювали на 6-7. Білувату тверду речовину фільтрували, промивали H 2O (150 мл), і сушили у вакуумі з одержанням бажаної проміжної сполуки (17.90 г, вихід 64 %). Водний шар екстрагували EtOAc (250 мл) з одержанням ще 1.10 г (вихід 4 %). Метил 4-хлор-2-метилхіназолін-8-карбоксилат Суспензію метил 2-метил-4-оксо-3,4-дигідрохіназолін-8-карбоксилату (2.00 г; 9.17 ммоль; 1.00 екв.) і хлориду бензилтриетиламонію (4.18 г, 18.33 ммоль) у сухому CH 3CN (5 мл) обробляли DIEA (1.75 мл, 10.1 ммоль) і перемішували при повільнім додаванні в колбу POCl 3 (7.3 мл, 80.2 ммоль). Уміст нагрівали до 90 °C протягом 30 хв, охолоджували до ~50 °C, і повільно виливали в 2н. NaОН (80 мл, 160 ммоль) і воду (80 мл), яка охолоджувалася в бані із сумішшю ацетон/сухий лід (у колбі утворювався лід). Обложену червонувату тверду речовину фільтрували, промивали 10 % водним K2CO3 (15 мл), і сушили у вакуумі з одержанням 1 (1.35 г; 62 % вихід). ЖХ-МС [236.8 (M+1)] O O N N Cl Метил 4-хлор-2-етилхіназолін-8-карбоксилат (2) 14 UA 110113 C2 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 1, з використанням ангідриду пропионовой кислоти. ЖХ-МС [251.0(M+1)] O O N N 5 10 Cl Метил 4-хлор-2-ізопропілхіназолін-8-карбоксилат (3) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 1, з використанням ангідриду ізомасляної кислоти. ЖХ-МС [265.0(M+1)] O O F F N F N Cl Метиловий ефір 4-хлор-2-трифторметил-хіназолін-8-карбонової кислоти (4) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 1, з використанням ангідриду трифтороцтової кислоти. ЖХ-МС [291.0(M+1)] H2 N 15 20 25 30 35 40 N Ns N-[(2S)-2-аміно-2-фенілетил]-N-метил-4-нітробензолсульфонамід (5) тре-бутил [(1S)-феніл)- 2-гідроксіетил]карбамат S-аміноспирт (1 г), ди-тре-бутил дикарбонат, і NaОН суспендували в tBuOH, і перемішували протягом 5 год. при 70 C. Реакційну суміш охолоджували до 50 C, додавали до H 2O (50 мл), і енергійно перемішували при КТ протягом 1 год. Отриманий осад білого кольору фільтрували, промивали H2O, і сушили у вакуумі з одержанням бажаної проміжної сполуки. тре-бутил [(1S)-феніл)- 2-гідроксіетил]карбамат Розчин SОСl2 в MeCN (12.0 мл) в атмосфері N2 охолоджували до -40 °C. За допомогою шприца повільно по краплях додавали розчин тре-бутил [(1S)-феніл)- 2-гідроксіетил]карбамату в CH3CN (12.0 мл). По краплях додавали піридин і реакційної суміші дозволяли перемішатися протягом 30 хв. перед видаленням бані із сухим льодом/MeCN. Реакційну суміш перемішували протягом 2 год., і потім концентрували. Залишок розчиняли в EtOAc і фільтрували через набиття силікагелю. Фільтрат концентрували й сушили у вакуумі. Отриману проміжну сполуку, гідрат трихлор-рутенію (0.08 г; 0.35 ммоль), і метаперіодат натрію (0.21 мл; 4.16 ммоль) розчиняли в CH3CN (3 мл) і H2O (3 мл), і перемішували протягом ночі при кімнатній температурі. Реакційну суміш розбавляли H 2O і екстрагували EtOAc (3x). Об'єднані органічні шари промивали соляним розчином, сушили над MgSO4, фільтрували й концентрували. Сирий продукт очищали за допомогою Biotage, елюїруя градієнтом 0-30 % EtOAc у гексанах з одержанням бажаної проміжної сполуки (600 мг, загальний вихід 45 %). тре-бутил ((1S)-2-{метил[(4-нітрофеніл)сульфоніл]аміно}-1-фенілетил)кар-бамат тре-бутил (4S)-4-феніл-1,2,3-оксатіазолідин-3-карбоксилат-2,2-діоксид (1 г; 3.34 ммоль), Nметил-4-нітробензолсульфонамід (722 мг; 3.34 ммоль), і Cs 2CO3 (0.40 мл; 5.01 ммоль) розчиняли в CH3CN (25 мл), і перемішували протягом ночі. Реакційну суміш фільтрували, промивали H2O (50 мл), і сушили у вакуумі з одержанням бажаної проміжної сполуки (1.12 г;77 %). N-[(2S)-2-аміно-2-фенілетил]-N-метил-4-нітробензолсульфонамід 4 M HСl/діоксан (6 мл) додавали до тре-бутил ((1S)-2-{метил[ (4-нітрофеніл) сульфоніл]аміно}-1-фенілетил)карбамату (1.05 г;2.41 ммоль) і перемішували при 50 °C протягом 2 год. Реакційну суміш упарювали у вакуумі з одержанням сполуки 5 (763 мг; 85 % вихід) у вигляді твердої речовини білого кольору (сіль HСl). ЖХ-МС [336 (M+1)] 15 UA 110113 C2 F O N H2 N 5 Ns N-[(2S)-аміно-2-(5-фтор-2-метоксифеніл)етил]-N-метил-4-нітробензолсульфонамід (6) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 5, з використанням N-метил-4-нітробензолсульфонаміду й відповідного аміноспирту. ЖХ-МС [384 (M+1)] Cl H2 N 10 Ns N Ns N-[(2S)-2-аміно-2- (4-фторфеніл)етил]-N-метил-4-нітробензолсульфонамід (9) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 5, з використанням N-метил-4-нітробензолсульфонаміду й відповідного аміноспирту. ЖХ-МС [354 (M+1)] F H2 N 25 N N-[(2S)-2-аміно-2-(4-хлорфеніл)етил]-N-метил-4-нітробензолсульфонамід (8) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 5, з використанням N-метил-4-нітробензолсульфонаміду й відповідного аміноспирту. ЖХ-МС [370 (M+1)] F H2 N 20 Ns N-[(2S)-2- аміно-2- (3-хлорфеніл)етил]-N-метил-4-нітробензолсульфонамід (7) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 5, з використанням N-метил-4-нітробензолсульфонаміду й відповідного аміноспирту. ЖХ-МС [407 (M+1)] Cl H2 N 15 N N Ns N-[(2S)-2-аміно-2-(3-фторфеніл)етил]-N-метил-4-нітробензолсульфонамід (10) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 5, з використанням N-метил-4-нітробензолсульфонаміду й відповідного аміноспирту. ЖХ-МС [354 (M+1)] F H2 N N (1S)-2-азетидин-1-іл-1- (3-фторфеніл)етанамін (11) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 5, з 16 UA 110113 C2 використанням азетидину й відповідного аміноспирту. ЖХ-МС [195 (M+1)] N H2 N 5 (S)-2-азетидин-1-іл-1-феніл-етиламін (12) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 5, з використанням азетидину й відповідного аміноспирту. ЖХ-МС [177 (M+1)] Cl N H2 N (S)-2-азетидин-1-іл-1- (хлор-феніл)-етиламін (13) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 5, з використанням азетидину й відповідного аміноспирту. ЖХ-МС [211 (M+1)] F 10 N H2 N (1S)-2-азетидин-1-іл-1- (4-фторфеніл)етанамін (14) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 5, з використанням азетидину й відповідного аміноспирту. ЖХ-МС [195 (M+1)] Cl N H2 N 15 (S) -2-азетидин-1-іл-1-(3- хлор-феніл)-етиламін (15) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 5, з використанням азетидину й відповідного аміноспирту. ЖХ-МС [211 (M+1)] Приклади сполук відповідно до формули (I) F HN H N N N H2 N 20 25 O 4-{[(1S)-1- (4-фторфеніл)-2-(метиламіно)етил]аміно}-2-метилхіназолін-8-карбоксамід (16) IC50 p70S6K [нМ]: 2.8 Метил 4-[((1S)-1-(4-фторфеніл)-2-{метил[(4-нітрофеніл)сульфоніл]аміно}етил)-аміно]8карбоксилат Сполуки 1 (100 мг; 0.42 ммоль), 9 (123 мг; 0.32 ммоль), і DIEA (0.23 мл) розчиняли в CH 3CN (4 мл), і перемішували при 70 °C протягом 72 год. Реакційну суміш концентрували з одержанням бажаної сирої проміжної сполуки. 4-[((1S)-1(4-фторфеніл)-2-{метил[ (4-нітрофеніл)сульфоніл]аміно}етил)аміно]8 17 UA 110113 C2 5 10 карбоксамід Сирий метил 4-[((1S)-1-(4-фторфеніл)-2-{метил[(4-нітрофеніл)сульфоніл]-аміно}етил)аміно]2-метилхіназолін-8-карбоксилат (177 мг; 0.32 ммоль) обробляли метанольним аміаком (10 мл, 7M), і перемішували при 70 °C протягом ночі. Реакційну суміш концентрували з одержанням бажаної сирої проміжної сполуки. (M+H) 539.1 4-{[(1S)-1- (4-фторфеніл)-2-(метиламіно)етил]аміно}-2-метилхіназолін-8-карбоксамід Сирий 4-[((1S)-1-(4-фторфеніл)-2-{метил[(4-нітрофеніл)сульфоніл]аміно}етил)-аміно]-2метилхиназолин-8-карбоксамід (161 мг; 0.30 ммоль) і Cs2CO3 (488 мг; 1.50 ммоль) суспендували в CH3CN (7 мл), і перемішували протягом 10 хвилин при кімнатній температурі. За допомогою шприца додавали бензолтіол (0.12 мл; 1.20 ммоль) і розчин енергійно перемішували при кімнатній температурі протягом ночі. Реакційну суміш концентрували, розчиняли в ДМСО (3 мл), і очищали за допомогою хроматографії зі зверненою фазою (Yamazen, основний буфер) з одержанням 9 16? (46 мг; вихід 43 %) у вигляді вільної основи. ЖХ-МС [354 (M+1)] F H N HN N N H2 N 15 O 4-{[(1S)-1-(3-фторфеніл)-2-(метиламіно)етил]аміно}-2-метилхіназолі-8-карбоксамід (17) IC50 p70S6K [нМ]: 139 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 16, з використанням 1 і 10. ЖХ-МС [354.2 (M+1)] Cl H N HN N N H2 N 20 O 4-{[(1S)-1-(4-хлорфеніл)-2-(метиламіно)етил]аміно}-2-ізопропілхіназолін-8-карбоксамід (18) IC50 p70S6K [нМ]: 23 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 16, з використанням 3 і 8. ЖХ-МС[398.2 (M+1)] Cl HN H N N N H2 N 25 O 4-{[(1S)-1-(4-хлорфеніл)-2-(метиламіно)етил]аміно}-2-метилхіназолін-8-карбоксамід (19) IC50 p70S6K [нМ]: 0.83 18 UA 110113 C2 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 16, з використанням 1 і 8. ЖХ-МС [370.2 (M+1)] F H N HN N N H2 N 5 O 2-Етил-4-{[(1S)-1-(3-фторфеніл)-2-(метиламіно)етил]аміно}хіназолін-8-карбоксамід (20) IC50 p70S6K [нМ]: 1.97 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 16, з використанням 2 і 10. ЖХ-МС [368.2 (M+1)] Cl H N HN N N H2 N 10 O 4-{[(1S)-1-(3-Хлорфеніл)-2-(метиламіно)етил]аміно}-2-етилхіназоліин-8-карбоксамід (21) IC50 p70S6K [нМ]: 0.87 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 16, з використанням 2 і 7. ЖХ-МС [384.2 (M+1)] Cl H N HN N N H2 N 15 O 4-{[(1S)-1-(3-Хлорфеніл)-2-(метиламіно)етил]аміно}-2-метилхіназолін-8-карбоксамід (22) IC50 p70S6K [нМ]: 0.98 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 16, з використанням 1 і 7. ЖХ-МС [370.1 (M+1)] HN H N N N H2 N O 19 UA 110113 C2 2-Етил-4-{[(1S)-2-(метиламіно)-1-фенілетил]аміно} хіназолін-8-карбоксамід (23) IC50 p70S6K [нМ]: 11 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 16, з використанням 2 і 5. ЖХ-МС [350.2 (M+1)] Cl H N HN N N 5 H2 N O 4-{[(1S)-1-(4-Хлорфеніл)-2-(метиламіно)етил]аміно}-2-етилхіназолін-8-карбоксамід (24) IC50 p70S6K [нМ]: 1.4 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 16, з використанням 2 і 8. ЖХ-МС [384.2 (M+1)] F H N HN N N 10 H2 N O 2-Етил-4-{[(1S)-1-(4-фторфеніл)-2-(метиламіно)етил]аміно}хіназолін-8-карбоксамід (25) IC50 p70S6K [нМ]: 10 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 16, з використанням 2 і 9. ЖХ-МС [368.2 (M+1)] HN H N N N 15 H2 N O 2-Метил-4-{[(1S)-2-(метиламіно)-1-фенілетил]аміно} хіназолін-8-карбоксамід (26) IC50 p70S6K [нМ]: 6.46 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 16, з використанням 1 і 5. ЖХ-МС [336 (M+1)] 20 UA 110113 C2 F H N HN N F F 5 N F H2 N O 4-{[(1S)-1-(3-Фторфеніл)-2-(метиламіно)етил]аміно}-2-(трифторметил)-хіназолін-8карбоксамід (27) IC50 p70S6K [нМ]: 4.3 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 16, з використанням 4 і 10. ЖХ-МС [408 (M+1)] F N HN N N H2 N 10 15 20 O Амід 4-[(S)-3-азетидин-1-ил-2-(3-фторфеніл)-пропіл]-2-етил-хіназолін-8-карбонової кислоти (28) IC50 p70S6K [нМ]: 18.5 Метиловий ефір 4-[(S)-3-азетидин-1-іл-2-(3-фторфеніл)-пропіл]-2-етил-хіназолін-8карбонової кислоти 2 (100 мг; 0.40 ммоль), 11 (69 мг; 0.36 ммоль; 0.90 екв.) і TEA (0.28 мл; 1.99 ммоль) розчиняли в CH3CN (6 мл) і перемішували протягом ночі. Реакційну суміш фільтрували й фільтрат концентрували з одержанням бажаної проміжної сполуки. ЖХ-МС [409 (M+1)]. Амід4-[(S)-3-азетидин-1іл-2-(3-фторфеніл)-пропіл]-2-етилхіназолін-8-карбонової кислоти Метил 4-{[(S)-2-азетидин-1-іл-1-(3-фторфеніл)етил]аміно}-2-етилхіназолін-8-карбоксилат (70.00 мг; 0.17 ммоль) суспендували в метанольном аміаку (0.98 мл; 7.00 M; 6.85 ммоль) і перемішували протягом 24 год. Реакційну суміш концентрували, і сирий продукт очищали за допомогою флеш-хроматографії на силікагелі (MeOH:EtOAc=1:9) з одержанням сполуки 28 (15 мг).ЖХ-МС [394 (M+1)]. 1 H ЯМР (ДМСО-d6, м.д.) 1.21 (3H), 1.91 (2H), 2.50 (2H), 2.74 (3H), 3.00 (1H), 3.13 (2H), 5.50 (1H), 7.22 (1H), 7.30 (2H), 7.44 (2H), 7.54 (1H), 7.78 (1H), 8.56 (3H), 10.69 (1H). HN N N N H2 N 25 O Амід 4-[(S)-3-азетидин-1-іл-2-феніл-пропіл]-2-метил-хіназолін-8-карбонової кислоти (29) IC50 p70S6K [нМ]: 5.84 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 28, з використанням 1 і 12.ЖХ-МС [362 (M+1)]. 1 H ЯМР (ДМСО-d6, м.д.) 1.90 (2H), 2.47 (5H), 2.74 (1H), 2.97 (1H), 3.16 (2H), 5.49 (1H), 7.22 21 UA 110113 C2 (1H), 7.30 (4H), 7.44 (2H), 7.54 (1H), 7.78 (1H), 8.55 (3H), 10.69 (1H). N HN N N H2 N 5 O Амід 4-[(S)-3-азетидин-1-іл-феніл-пропіл]-2-етил-хіназолін-8-карбонової кислоти (30) IC50 p70S6K [нМ]: 33.6 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 28, з використанням 2 і 12. ЖХМС [376 (M+1)]. 1 H ЯМР (ДМСО-d6, м.д.) 1.21 (3H), 1.91 (2H), 2.50 (2H), 2.74 (3H), 3.00 (1H), 3.13 (2H), 5.50 (1H), 7.22 (1H), 7.30 (3H), 7.44 (2H), 7.54 (1H), 7.78 (1H), 8.56 (3H), 10.69 (1H). Cl N HN N N H2 N 10 15 O Амід 4-[(S)-3-азетидин-1-іл-2-(4-хлорфеніл)-пропіл]-2-метил-хіназолін-8-карбонової кислоти (31) IC50 p70S6K [нМ]: 2.6 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 28 з використанням 1 і 13.ЖХ-МС [397 (M+1)]. 1 H ЯМР (ДМСО-d6, м.д.) 1.90 (2H), 2.46 (3H), 2.50 (2H), 2.74 (1H), 2.97 (1H), 3.16 (2H), 5.45 (1H), 7.47 (2H), 7.52 (1H), 7.78 (1H), 8.56 (3H), 10.55 (1H). Cl HN N N N H2 N 20 O Амід4-[(S)-3-азетидин-1-іл-2-(4-хлорфеніл)-пропіл]-2-етил-хіназолін-8-карбонової кислоти (32) IC50 p70S6K [нМ]: 5.5 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 28, з 1 використанням 2 і 13. ЖХМС [411 (M+1)]. H ЯМР (ДМСО-d6, м.д.) 1.21 (3H), 1.91 (2H), 2.5 (1H), 2.73 (3H), 2.98 (1H), 3.13 (3H), 5.43 (1H), 7.37 (3H), 7.47 (2H), 7.78 (1H), 8.56 (3H), 10.66 (1H). 22 UA 110113 C2 F HN N N N H2 N 5 O Амід 4-[(S)-3-азетидин-1-іл-2-(4-фторфеніл)-пропіл]-2-метил-хіназолін-8-карбонової кислоти (33) IC50 p70S6K [нМ]: 44 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 28 з використанням 1 і 14. ЖХМС [380 (M+1)].) ]. 1 H ЯМР (ДМСО-d6, м.д.) 1.90 (2H), 2.47 (5H), 2.7461 (1H), 2.97 (1H), 3.16 (2H), 5.49 (1H), 7.47 (2H), 7.52 (1H), 7.78 (1H), 8.56 (3H), 10.55 (1H). F HN N N N H2 N 10 15 O Амід 4-[(S)-3-азетидин-1-іл-2- (3-фторфеніл)-пропіл]-2-метил-хіназолін-8- карбонової кислоти (34) IC50 p70S6K [нМ]: 7 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 28, з використанням 1 і 11.ЖХ-МС [380 (M+1)]. 1 H ЯМР (ДМСО-d6, м.д.) 1.91 (2H), 2.4821 (5H), 2.75 (1H), 2.98 (1H), 3.16 (2H), 5.49 (1H), 7.47 (2H), 7.52 (1H), 7.78 (1H), 8.56 (3H), 10.55 (1H). Cl HN N N N H2 N 20 O Амід 4-[(S)-3-азетидин-1-іл-2-(3-хлорфеніл)-пропіл-2-метил-хіназолін-8-карбонової кислоти (35) IC50 p70S6K [нМ]: 1.3 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 28, з використанням 1 і 15.ЖХ-МС [396 (M+1)]. 1 H ЯМР (ДМСО-d6, м.д.) 1.91 (2H), 2.48 (5H), 2.74 (1H), 2.98 (1H), 3.16 (2H), 5.49 (1H), 7.47 (2H), 7.52 (1H), 7.78 (1H), 8.56 (3H), 10.55 (1H). 23 UA 110113 C2 F N HN N N H2 N 5 O Амід 4-[(S)-3-азетидин-1-іл-2-(4-фторфеніл)-пропіл]-2-етил-хіназолін-8-карбонової кислоти (36) IC50 p70S6K [нМ]: 30 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 28, з використанням 2 і 14.ЖХ-МС [394 (M+1)]. 1 H ЯМР (ДМСО-d6, м.д.) 1.21 (3H), 1.99 (2H), 2.50 (1H), 2.73 (3H), 2.98 (1H), 3.13 (3H), 5.43 (1H), 7.37 (3H), 7.47 (2H), 7.78 (1H), 8.56 (3H), 10.66 (1H). Cl N HN N N H2 N 10 15 Амід 4-[(S)-3-азетидин-1-іл-2-(3-хлорфеніл)-пропіл]-2-етил-хіназолін-8-карбонової кислоти (37) IC50 p70S6K [нМ]: 1.7 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 28 з використанням 2 і 15.ЖХ-МС [410 (M+1)]. 1 H ЯМР (ДМСО-d6, м.д.) 1.23 (3H), 1.94 (2H), 2.50 (1H), 2.75 (3H), 2.98 (1H), 3.20 (3H), 5.43 (1H), 7.35 (3H), 7.44 (2H), 7.78 (1H), 8.53 (3H), 10.64 (1H). Проміжні сполуки синтезу F F F H2 N 20 25 O N Ns N-[(2S)-аміно-2-(4-трифторметил-феніл)етил]-N-метил-4-нітробензолсульфонамід (38) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 5, з використанням N-метил-4-нітробензолсульфонаміду й відповідного аміноспирту. ЖХ-МС [404 (M+1)] N N 1 1 (S)-N ,N -Диметил-3-фенілпропан-1, 2-діамін (39) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 5 з використанням диметиламіну й відповідного аміноспирту. ЖХ-МС [179 (M+1)] 24 UA 110113 C2 N 5 10 15 20 3 N (S)-2-Азидо-1-феніл-етиламін (40) До розчину тре-бутил [(1S)-феніл)-2-гідроксіетил]карбамату (237 мг, 1.0 ммоль, 1.0 екв.) і TEA (278 мл; 2.0 ммоль; 2.0 екв.) у ДХМ (5 мл) при 0 °C, додавали порцією 4метилбензолсульфонілхлорид (210 мг, 1.1 ммоль, 1.1 екв.). Отриману суміш перемішували при кімнатній температурі протягом ночі. Реакційну суміш розбавляли етилацетатом і промивали насиченим бікарбонатом натрію й соляним розчином. Органічний шар сушили над MgSO4 і концентрували. Сирий продукт очищали за допомогою Biotage з 0-30 % етилацетатом у гексане з одержанням (2S)-2-[(тре-бутоксикарбоніл)аміно]-2-фенілетил 4-метилбензолсульфонату у вигляді твердої речовини білого кольору, вихід 93 %. Суміш (2S)-2-[(тре-бутоксикарбоніл)аміно]-2-фенілетил 4-метилбензол-сульфонату (350 мг, 0.9 ммоль, 1.0 екв.) і азиду натрію (117 мг, 1.8 ммоль, 2.0 екв.) в N, N-диметилформаміде (5 мл) перемішували при 65 °C протягом ночі. Суміш охолоджували до кімнатної температури й розбавляли водою й етилацетатом. Органічний шар відокремлювали й промивали соляним розчином, сушили, і концентрували з одержанням тре-бутил [(1S)-2-азидо-1фенілетил]карбамату, вихід 90 %. До розчину тре-бутил [(1S)-2-азидо-1-фенілетил]карбамату (210 мг, 0.8 ммоль, 1.0 екв.) у ТГФ (2 мл) додавали 4.0M хлороводень у діоксане (2.0 мл, 8.0 ммоль, 10.0 екв.). Реакційну суміш перемішували при кімнатній температурі протягом ночі. Реакційну суміш розбавляли ефіром. Осад фільтрували й промивали ефіром з одержанням (S)-2-Азидо-1-феніл-етиламіну 40 у вигляді твердої речовини білого кольору, вихід 85 %. ЖХ-МС [163 (M+1)] OCF3 Cl N H2 N 25 Ns (S)-N-(2-аміно-2-(3-хлор-4-(трифторметокси)феніл)етил)-N-метил-4-нітробензолсульфонамід (41) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 5, з використанням N-метил-4-нітробензолсульфонаміду й відповідного аміноспирту. ЖХ-МС [454 (M+1)] F F N H2 N 30 Ns (S)-N-(2-аміно-2-(2,4-дифторфеніл)етил)-N-метил-4-нітробензолсульфонамід (42) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 5, з використанням N-метил-4-нітробензолсульфонаміду й відповідного аміноспирту. ЖХ-МС [372 (M+1)] F F H2 N N 35 Ns (S)-N-(2-аміно-2-(2,6-дифторфеніл)етил)-N-метил-4-нітробензолсульфонамід (43) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 5, з використанням N-метил-4-нітробензолсульфонаміду й відповідного аміноспирту. ЖХ-МС [372 (M+1)] 25 UA 110113 C2 F F N H2 N 5 Ns (S)-N-(2-аміно-2-(2,5-дифторфеніл)етил)-N-метил-4-нітробензолсульфонамід (44) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 5, з використанням N-метил-4-нітробензолсульфонаміду й відповідного аміноспирту. ЖХ-МС [372 (M+1)] F F F N H2 N 10 (S)-N-(2-аміно-2-(2,4,5-трифторфеніл)етил)-N-метил-4-нітробензол-сульфонамід (45) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 5, з використанням N-метил-4-нітробензолсульфонаміду й відповідного аміноспирту. ЖХ-МС [390 (M+1)] F F F F H2 N 15 Ns N Ns (S)-1-(4-Фтор-2-трифторметил-феніл)-N*2*,N*2*- диметил-етан-1, 2-діамін (46) Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 5, з використанням N-метил-4-нітробензолсульфонаміду й відповідного аміноспирту. ЖХ-МС [422 (M+1)] Приклади сполук відповідно до формули (I) F O HN H N N N H2N 20 O Амід 4-[(S)-1-(5-фтор-2-метокси-феніл)-2-метиламіно-етиламіно]-2-метил-хіназолін8карбонової кислоти (47) IC50 p70S6K [нМ]: 12 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 16, з використанням 1 і 6. ЖХ-МС [384 (M+1)]. 26 UA 110113 C2 F F F NH HN N N H2N 5 O Амід 2-метил-4-[(S)-2-метиламіно-1-(4-трифторметил-феніл)-етиламіно]-хіназолін-8карбонової кислоти (48) IC50 p70S6K [нМ]: 1 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 16, з використанням 1 і 38. ЖХ-МС [404 (M+1)]. N HN N N H2N 10 O Амід 4-((S)-1-бензил-2- диметиламіно-етиламіно) -2-метил-хіназолін- 8- карбонової кислоти (49) IC50 p70S6K [нМ]: 452 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 16, з використанням 1 і 39. ЖХ-МС [364 (M+1)]. F F F F N NH N N H2N 15 O 4-[(1S)-1-[4-фтор-2-(трифторметил)феніл]-2-(метиламіно)етил]аміно-2-метилхіназолін-8карбоксамід (50) IC50 p70S6K [нМ]: 260 Цю сполуку одержували, дотримуючись загальній методиці, описаної в прикладі 16, з використанням 1 і 46. ЖХ-МС [422 (M+1)]. 27 UA 110113 C2 NH2 HN F N F N F 5 10 15 20 25 H2N O Амід 4-((S)-2-аміно-1-феніл-етиламіно)-2-трифторметил-хіназолін- 8-карбонової кислоти (51) IC50 p70S6K [нМ]: 8 До розчину хлориду 4 (175 мг, 0.60 ммоль) і N, N-діізопропілетиламіну (0.53 мл, 3.0 ммоль) у тетрагідрофуране (8.0 мл) додавали амін 40 (132 мг, 0.66 ммоль) і реакційну суміш нагрівали до 65 °C протягом 16 годин. Реакційну суміш розбавляли насиченим хлоридом натрію й додавали етилацетат. Двофазну суміш тричі екстрагували етилацетатом і об'єднані екстракти сушили над сульфатом натрію. Колоночна хроматографія отриманого залишку (дихлорметан - 10 % метанол у дихлорметане) давала продукт у вигляді блідо-жовтої піни, ЖХМС (ESI) 417 (M+H). Речовина розчиняли в ізопропаноле (5.0 мл) і повільно додавали гідроксид амонію (10.0 мл) і реакційну суміш перемішували протягом 16 годин при кімнатній температурі. Загальний об’єм реакційної суміші зменшували до ¼ у вакуумі й цей розчин розбавляли насиченим бікарбонатом натрію й етилацетатом. Двофазний розчин тричі екстрагували етилацетатом і об'єднані органічні фази сушили над сульфатом натрію. Екстракт концентрували з одержанням сирого аміду 4-((S)-2-азидо-1-феніл-етиламіно)-2-трифторметил-хіназолін-8-карбонової кислоти, головний пік якого показував належне m/z за допомогою аналізу РХ/МС, ЖХМС (ESI) 402 (M+H). Сирий азид розчиняли в етаноле (15 мл) і додавали каталітичну кількість 5 % палладія на вугіллі. Гетерогенний розчин перемішували протягом 2 годин в атмосфері водню й потім суспензію фільтрували через набивання целита й фільтрат концентрували до одержання блідожовтої плівки. Ця речовина повторно розчиняли в тетрагідрофуране (5.0 мл) і обробляли 4н. хлористоводородною кислотою в діоксане (4.0 мл) протягом 15 хвилин. Потім реакційну суміш концентрували досуха, і отриману тверду речовину тричі розтирали в порошок з діетиловим ефіром з одержанням сполуки, зазначеної в заголовку (сіль HСl) у вигляді блідо-жовтого порошку (202 мг) у виході 57 % протягом попередніх чотирьох стадій.ЖХ-МС [376 (M+1)]. 1H ЯМР (400 МГц, ДМСО-d6) δ м.д. 3.19-3.38 (m, 1 H) 3.67-3.89 (m, 1 H) 5.76 (br. s., 1 H) 7.31 (d, J=7.42 Гц, 1 H) 7.38 (t, J=7.52 Гц, 2 H) 7.55 (d, J=7.32 Гц, 2 H) 7.84 (t, J=7.86 Гц, 1 H) 7.898.06 (m, 1 H) 8.63 (dd, J=7.52, 1.37 Гц, 1 H) 9.01 (d, J=8.40 Гц, 2 H) 9.48 (br. s., 1 H) 9.90 (s, 1 H). F F O F Cl HN H N N N H2 N 30 35 O (S)-4-((1-(3-хлор-4-(трифторметокси)феніл)-2-(метиламіно)етил)аміно)-2-метилхіназолін-8карбоксамід (52) IC50 p70S6K [нМ]: 1 (S)-метил 4-((2-(4-аміно-N-метилфенілсульфонамідо)-1-(3-хлор-4(трифторметокси)феніл)етил)аміно)- 8-карбоксилат До розчину метил 2-метил-4-оксо-3,4-дигідрохіназолін-8-карбоксилату (91.65 мг; 0.42 ммоль; 1.20 екв.) в NMP (3мл) додавали 1, 8-діазабіцикло[5.4.0] ундец-7-ен (104.58 мкл; 0.70 ммоль; 2.00 екв.). Розчин перемішували при кімнатній температурі протягом 5 хвилин і потім додавали 28
ДивитисяДодаткова інформація
Назва патенту англійськоюNormal;heading 1;heading 2;heading 3;bicyclic azaheterocyclic carboxamides
Автори англійськоюHuck, Bayard, R., Neagu, Constantin, Jones, Reinaldo C., Deselm, Lizbeth, Celeste, Xiao, Yufang, Karra, Srinivasa, R., Lan, Ruoxi, Mochalkin, Igor, Sutton, Amanda E., Richardson, Thomas, E.
Назва патенту російськоюБициклические азагетероциклические карбоксамиды
Автори російськоюХак Байярд Р., Неагу Константин, Джонс Рейнальдо С., Дезельм Лизбет Селест, Ксиао Юфанг, Карра Сриниваса Р., Лан Руокси, Мочалкин Игор, Саттон Аманда Е., Ричардсон Томас Е.
МПК / Мітки
МПК: A61K 31/517, C07D 403/12, C07D 239/74, A61P 35/00
Мітки: карбоксаміди, азагетероциклічні, біциклічні
Код посилання
<a href="https://ua.patents.su/38-110113-biciklichni-azageterociklichni-karboksamidi.html" target="_blank" rel="follow" title="База патентів України">Біциклічні азагетероциклічні карбоксаміди</a>
Попередній патент: Індоли
Наступний патент: Пристрій, система і спосіб створення магнітоіндукованого візуального ефекту
Випадковий патент: Спосіб визначення показника загасання світла в плівці плоскопаралельної одноплівкової структури