Заміщені бензопірани як селективні агоністи b-рецепторів естрогенів
Номер патенту: 77986
Опубліковано: 15.02.2007
Автори: Додж Джеффрі Алан, Річардсон Тімоті Айво, Нойбауер Блейк Лі, Пфайфер Ланс Аллен, Норман Брайан Херст, Люгар Третій Чарлз Уілліс, Крішнан Венкатеш Гарі
Формула / Реферат
1. Сполука формули І
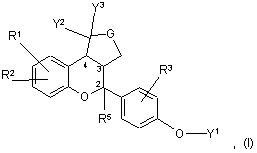
де
кожний з R1, R2 та R3, незалежно від інших, є -Н, С1-С6-алкіл, -ОН, С1-С6-алкоксигрупа, галоген або група –СF3;
R5 є водень або С1-С6-алкіл;
кожний з Y1, Y2 та Y3, незалежно від інших, є -Н або С1-С6-алкіл; і G є -СН2-, -СН2-СН2- або –CH2-CH2-CH2;
або її фармацевтичнo прийнятна сіль.
2. Сполука за п. 1, де G є –СН2-.
3. Сполука за п. 1, де обидві групи Y2 та Y3 є -Н.
4. Сполука за п. 1, де щонайменше одна з груп R1 та R2 є -ОН.
5. Сполука за п. 1, де R3 є -Н.
6. Сполука за п. 1, де Y1 є -Н.
7. Сполука за п. 2, де одна з груп R1 та R2 є -ОН, а друга є -Н.
8. Сполука за п. 1, що має формулу II
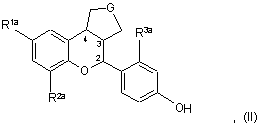
де R1a є -Н, -ОН або F;
R2a є -Н, -СН3 або –ОСН3;
R3a є -Н або –СН3;
G є -СН2-, -СН2-СН2- або -СН2-СН2-СН2-;
або її фармацевтичнo прийнятна сіль.
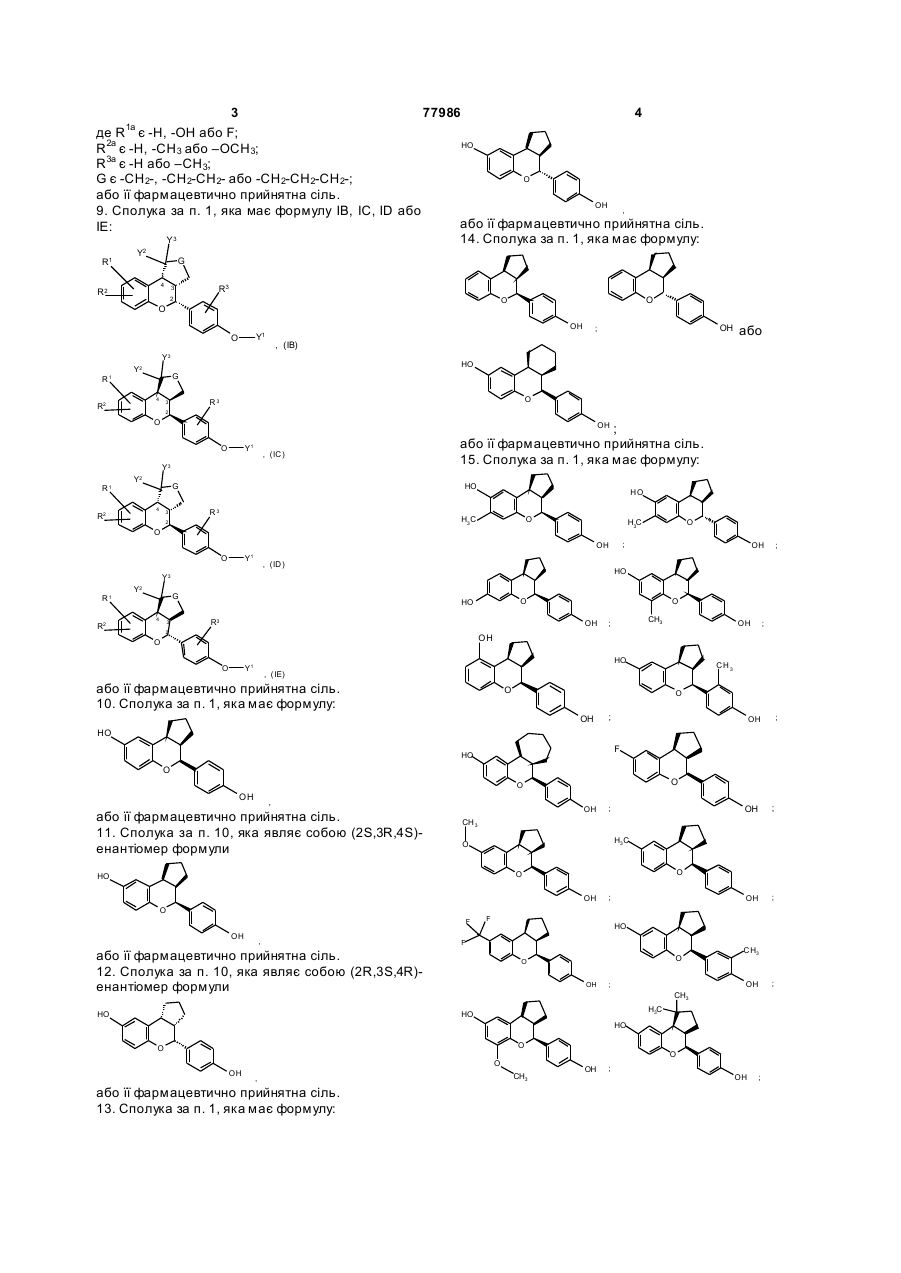
9. Сполука за п. 1, яка має формулу IВ, IC, ID або ІЕ:
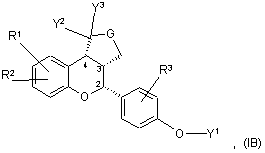
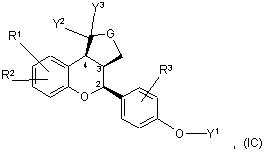
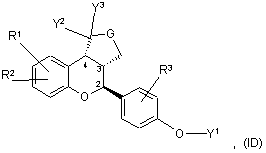
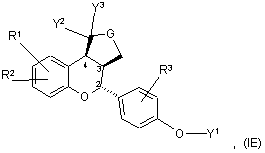
або її фармацевтичнo прийнятна сіль.
10. Сполука за п. 1, яка має формулу:
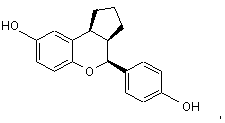
або її фармацевтичнo прийнятна сіль.
11. Сполука за п. 10, яка являє собою (2S,3R,4S)-енантіомер формули
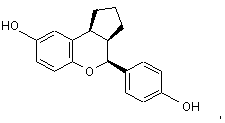
або її фармацевтичнo прийнятна сіль.
12. Сполука за п. 10, яка являє собою (2R,3S,4R)-енантіомер формули
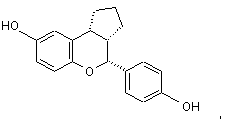
або її фармацевтичнo прийнятна сіль.
13. Сполука за п. 1, яка має формулу:
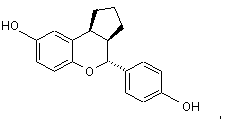
або її фармацевтично прийнятна сіль.
14. Сполука за п. 1, яка має формулу:
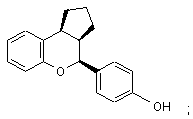
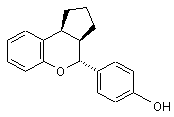 або
або
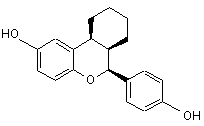 ;
;
або її фармацевтичнo прийнятна сіль.
15. Сполука за п. 1, яка має формулу:
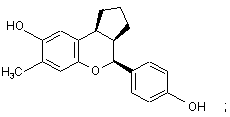
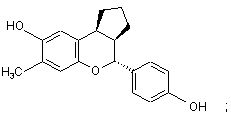
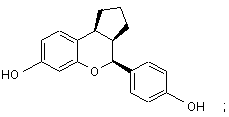
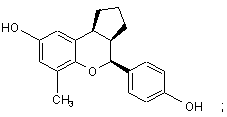
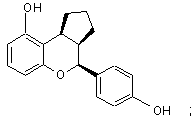
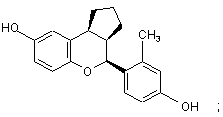
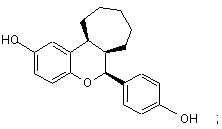
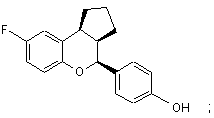
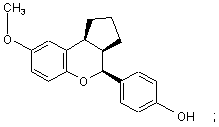
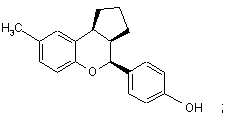
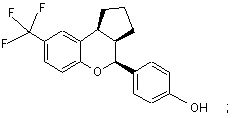
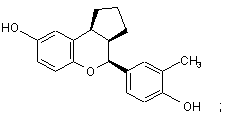
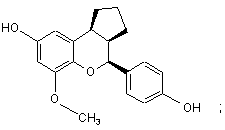
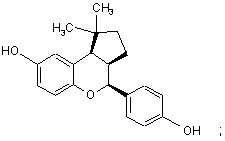
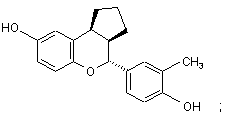
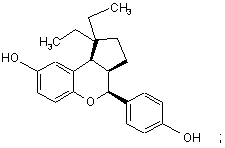
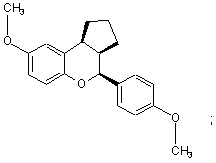
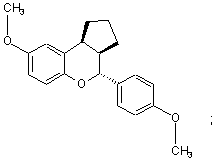
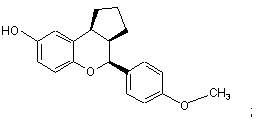
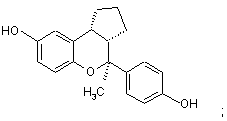
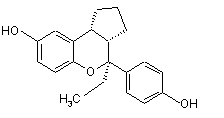 або
або
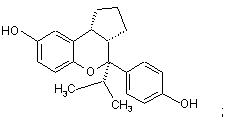
або її фармацевтичнo прийнятна сіль.
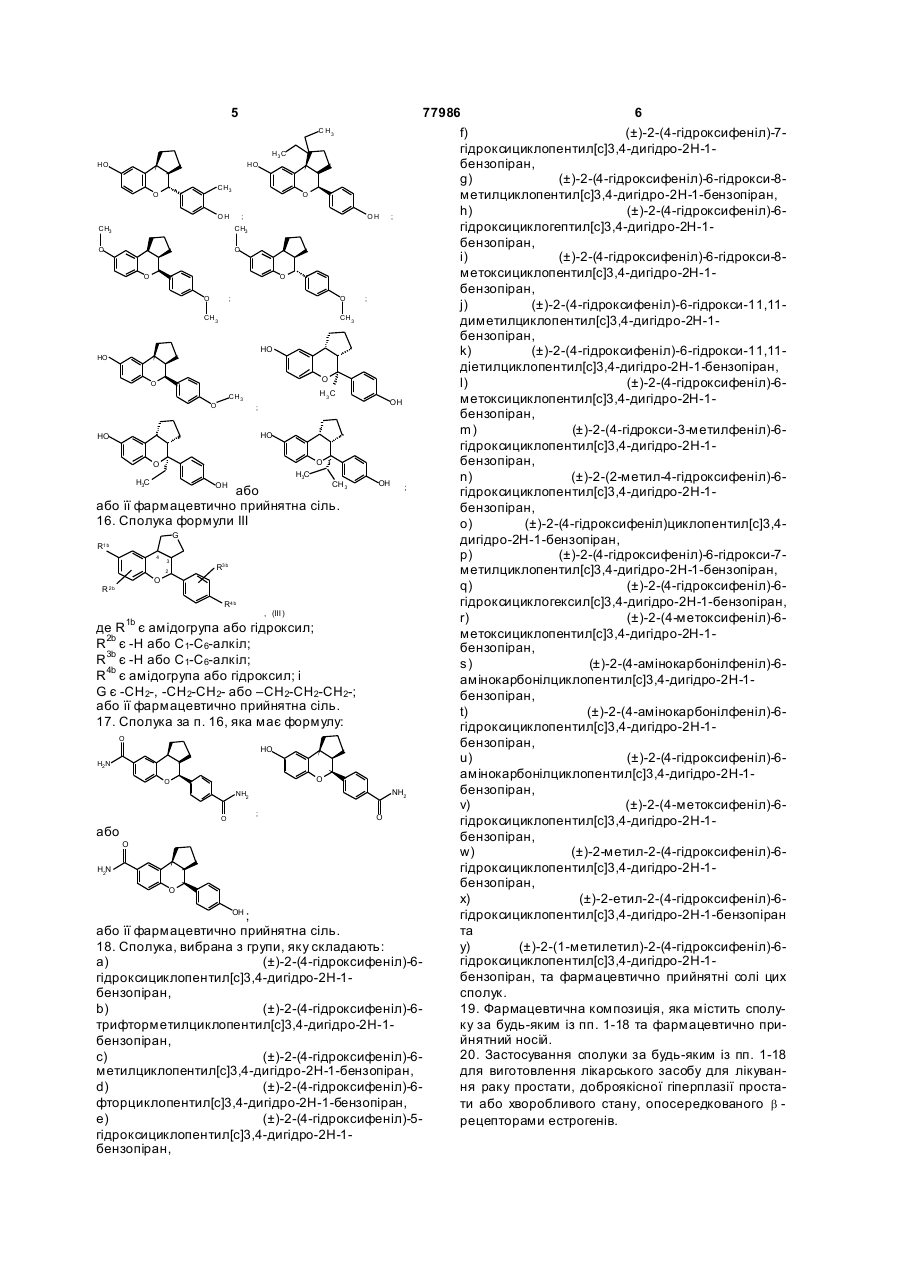
16. Сполука формули III
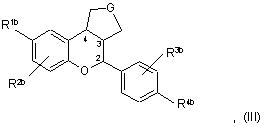
де R1b є амідогрупа або гідроксил;
R2b є -Н або С1-С6-алкіл;
R3b є -Н або С1-С6-алкіл;
R4b є амідогрупа або гідроксил; і
G є -СН2-, -СН2-СН2- або –СН2-СН2-СН2-;
або її фармацевтичнo прийнятна сіль.
17. Сполука за п. 16, яка має формулу:
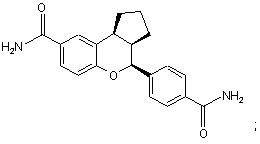
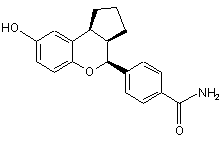 або
або
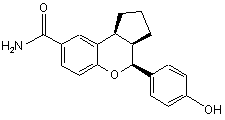 ;
;
або її фармацевтичнo прийнятна сіль.
18. Сполука, вибрана з групи, яку складають:
a) (±)-2-(4-гідроксифеніл)-6-гідроксициклопентил[с]3,4-дигідро-2Н-1-бензопіран,
b) (±)-2-(4-гідроксифеніл)-6-трифторметилциклопентил[с]3,4-дигідро-2Н-1-бензопіран,
c) (±)-2-(4-гідроксифеніл)-6-метилциклопентил[с]3,4-дигідро-2Н-1-бензопіран,
d) (±)-2-(4-гідроксифеніл)-6-фторциклопентил[с]3,4-дигідро-2Н-1-бензопіран,
e) (±)-2-(4-гідроксифеніл)-5-гідроксициклопентил[с]3,4-дигідро-2Н-1-бензопіран,
f) (±)-2-(4-гідроксифеніл)-7-гідроксициклопентил[с]3,4-дигідро-2Н-1-бензопіран,
g) (±)-2-(4-гідроксифеніл)-6-гідрокси-8-метилциклопентил[с]3,4-дигідро-2Н-1-бензопіран,
h) (±)-2-(4-гідроксифеніл)-6-гідроксициклогептил[с]3,4-дигідро-2Н-1-бензопіран,
і) (±)-2-(4-гідроксифеніл)-6-гідрокси-8-метоксициклопентил[с]3,4-дигідро-2Н-1-бензопіран,
j) (±)-2-(4-гідроксифеніл)-6-гідрокси-11,11-диметилциклопентил[с]3,4-дигідро-2Н-1-бензопіран,
k) (±)-2-(4-гідроксифеніл)-6-гідрокси-11,11-діетилциклопентил[с]3,4-дигідро-2Н-1-бензопіран,
l) (±)-2-(4-гідроксифеніл)-6-метоксициклопентил[с]3,4-дигідро-2Н-1-бензопіран,
m) (±)-2-(4-гідрокси-3-метилфеніл)-6-гідроксициклопентил[с]3,4-дигідро-2Н-1-бензопіран,
n) (±)-2-(2-метил-4-гідроксифеніл)-6-гідроксициклопентил[с]3,4-дигідро-2Н-1-бензопіран,
о) (±)-2-(4-гідроксифеніл)циклопентил[с]3,4-дигідро-2Н-1-бензопіран,
р) (±)-2-(4-гідроксифеніл)-6-гідрокси-7-метилциклопентил[с]3,4-дигідро-2Н-1-бензопіран,
q) (±)-2-(4-гідроксифеніл)-6-гідроксициклогексил[с]3,4-дигідро-2Н-1-бензопіран,
r) (±)-2-(4-метоксифеніл)-6-метоксициклопентил[с]3,4-дигідро-2Н-1-бензопіран,
s) (±)-2-(4-амінокарбонілфеніл)-6-амінокарбонілциклопентил[с]3,4-дигідро-2Н-1-бензопіран,
t) (±)-2-(4-амінокарбонілфеніл)-6-гідроксициклопентил[с]3,4-дигідро-2Н-1-бензопіран,
u) (±)-2-(4-гідроксифеніл)-6-амінокарбонілциклопентил[с]3,4-дигідро-2Н-1-бензопіран,
v) (±)-2-(4-метоксифеніл)-6-гідроксициклопентил[с]3,4-дигідро-2Н-1-бензопіран,
w) (±)-2-метил-2-(4-гідроксифеніл)-6-гідроксициклопентил[с]3,4-дигідро-2Н-1-бензопіран,
х) (±)-2-етил-2-(4-гідроксифеніл)-6-гідроксициклопентил[с]3,4-дигідро-2Н-1-бензопіран та
у) (±)-2-(1-метилетил)-2-(4-гідроксифеніл)-6-гідроксициклопентил[с]3,4-дигідро-2Н-1-бензопіран, та фармацевтичнo прийнятні солі цих сполук.
19. Фармацевтична композиція, яка містить сполуку за будь-яким із пп. 1-18 та фармацевтичнo прийнятний носій.
20. Застосування сполуки за будь-яким із пп. 1-18 для виготовлення лікарського засобу для лікування раку простати, доброякісної гіперплазії простати або хворобливого стану, опосередкованого ![]() -рецепторами естрогенів.
-рецепторами естрогенів.
Текст
1. Сполука формули І 2 (19) ДЕРЖАВНИЙ Д ЕПАРТАМЕНТ ІНТЕЛ ЕКТУАЛЬНОЇ ВЛАСНОСТІ 3 77986 4 де R1a є -Н, -ОН або F; HO R2a є -Н, -СН3 або –ОСН3; R3a є -Н або –СН3; O G є -СН2-, -СН2-СН2- або -СН2-СН2-СН2-; або її фармацевтичнo прийнятна сіль. OH , 9. Сполука за п. 1, яка має формулу IВ, IC, ID або або її фармацевтично прийнятна сіль. ІЕ: Y3 14. Сполука за п. 1, яка має формулу: R1 Y2 G 4 R2 3 R3 2 OH Y1 O Y2 HO O R3 3 2 O OH O Y1 , (IC) Y3 R1 Y2 R3 3 ; або її фармацевтичнo прийнятна сіль. 15. Сполука за п. 1, яка має формулу: HO G 4 R2 HO H3C 2 O H3C O O Y1 , (ID) R2 G 4 3 OH ; HO Y3 Y2 O ; OH R1 або G 4 R2 OH ; , (IB) Y3 R1 O O O O HO R3 O OH 2 CH3 ; OH ; OH O O HO Y1 CH 3 , (IE) або її фармацевтичнo прийнятна сіль. 10. Сполука за п. 1, яка має формулу: O O OH ; ; OH HO F HO O O O OH , або її фармацевтичнo прийнятна сіль. 11. Сполука за п. 10, яка являє собою (2S,3R,4S)енантіомер формули OH OH O O OH O F , ; F HO F або її фармацевтичнo прийнятна сіль. 12. Сполука за п. 10, яка являє собою (2R,3S,4R)енантіомер формули HO ; H3C O HO OH ; OH ; CH 3 O O OH CH3 OH ; CH3 H3C HO HO O O O O OH , або її фармацевтичнo прийнятна сіль. 13. Сполука за п. 1, яка має формулу: CH3 OH ; OH ; ; 5 77986 6 f) (±)-2-(4-гідроксифеніл)-7гідроксициклопентил[с]3,4-дигідро-2Н-1H C HO HO бензопіран, g) (±)-2-(4-гідроксифеніл)-6-гідрокси-8CH O O метилциклопентил[с]3,4-дигідро-2Н-1-бензопіран, h) (±)-2-(4-гідроксифеніл)-6OH ; OH ; CH CH гідроксициклогептил[с]3,4-дигідро-2Н-1бензопіран, O O і) (±)-2-(4-гідроксифеніл)-6-гідрокси-8метоксициклопентил[с]3,4-дигідро-2Н-1O O бензопіран, O ; O ; j) (±)-2-(4-гідроксифеніл)-6-гідрокси-11,11CH CH диметилциклопентил[с]3,4-дигідро-2Н-1бензопіран, HO k) (±)-2-(4-гідроксифеніл)-6-гідрокси-11,11HO діетилциклопентил[с]3,4-дигідро-2Н-1-бензопіран, O O l) (±)-2-(4-гідроксифеніл)-6H 3C CH метоксициклопентил[с]3,4-дигідро-2Н-1OH O ; бензопіран, m) (±)-2-(4-гідрокси-3-метилфеніл)-6HO HO гідроксициклопентил[с]3,4-дигідро-2Н-1O бензопіран, O HC n) (±)-2-(2-метил-4-гідроксифеніл)-6HC OH CH OH ; або гідроксициклопентил[с]3,4-дигідро-2Н-1або її фармацевтичнo прийнятна сіль. бензопіран, 16. Сполука формули III о) (±)-2-(4-гідроксифеніл)циклопентил[с]3,4G дигідро-2Н-1-бензопіран, R1b 4 р) (±)-2-(4-гідроксифеніл)-6-гідрокси-73 R3b 2 метилциклопентил[с]3,4-дигідро-2Н-1-бензопіран, O q) (±)-2-(4-гідроксифеніл)-6R 2b гідроксициклогексил[с]3,4-дигідро-2Н-1-бензопіран, R4b , (III ) r) (±)-2-(4-метоксифеніл)-6де R1b є амідогрупа або гідроксил; метоксициклопентил[с]3,4-дигідро-2Н-1R2b є -Н або С 1-С6-алкіл; бензопіран, R3b є -Н або С 1-С6-алкіл; s) (±)-2-(4-амінокарбонілфеніл)-64b R є амідогрупа або гідроксил; і амінокарбонілциклопентил[с]3,4-дигідро-2Н-1G є -СН2-, -СН2-СН2- або –СН2-СН2-СН2-; бензопіран, або її фармацевтичнo прийнятна сіль. t) (±)-2-(4-амінокарбонілфеніл)-617. Сполука за п. 16, яка має формулу: гідроксициклопентил[с]3,4-дигідро-2Н-1O бензопіран, HO u) (±)-2-(4-гідроксифеніл)-6HN амінокарбонілциклопентил[с]3,4-дигідро-2Н-1O O бензопіран, NH NH v) (±)-2-(4-метоксифеніл)-6; O O гідроксициклопентил[с]3,4-дигідро-2Н-1або бензопіран, O w) (±)-2-метил-2-(4-гідроксифеніл)-6HN гідроксициклопентил[с]3,4-дигідро-2Н-1бензопіран, O х) (±)-2-етил-2-(4-гідроксифеніл)-6OH гідроксициклопентил[с]3,4-дигідро-2Н-1-бензопіран ; або її фармацевтичнo прийнятна сіль. та 18. Сполука, вибрана з групи, яку складають: у) (±)-2-(1-метилетил)-2-(4-гідроксифеніл)-6гідроксициклопентил[с]3,4-дигідро-2Н-1a) (±)-2-(4-гідроксифеніл)-6бензопіран, та фармацевтичнo прийнятні солі цих гідроксициклопентил[с]3,4-дигідро-2Н-1бензопіран, сполук. b) (±)-2-(4-гідроксифеніл)-619. Фармацевтична композиція, яка містить сполутрифторметилциклопентил[с]3,4-дигідро-2Н-1ку за будь-яким із пп. 1-18 та фармацевтичнo прийнятний носій. бензопіран, 20. Застосування сполуки за будь-яким із пп. 1-18 c) (±)-2-(4-гідроксифеніл)-6метилциклопентил[с]3,4-дигідро-2Н-1-бензопіран, для виготовлення лікарського засобу для лікуванd) (±)-2-(4-гідроксифеніл)-6ня раку простати, доброякісної гіперплазії простафторциклопентил[с]3,4-дигідро-2Н-1-бензопіран, ти або хворобливого стану, опосередкованого b e) (±)-2-(4-гідроксифеніл)-5рецепторами естрогенів. гідроксициклопентил[с]3,4-дигідро-2Н-1бензопіран, C H3 3 3 3 3 3 3 3 3 3 3 2 2 2 2 7 77986 Цей винахід стосується нових циклоалкілбензопіранів та їхніх похідних, фармацевтичних композицій, що містять ці сполуки, їх застосування як селективних аногістів β-рецепторів естрогенів та їх застосування для лікування захворювань, опосередкованих β-рецепторами естрогенів, наприклад, раку простати, доброякісної гіперплазії простати, раку яєчок, раку яєчників, раку легенів, серцевосудинних захворювань, нейродегенеративних захворювань, нетримання сечі, розладів центральної нервової системи (ЦНС), розладів шлунковокишкового (ШК) тракту та остеопорозу. Естрогени відіграють важливу роль у розвитку та гомеостазі репродуктивної, центральної нервової, скелетної та серцево-судинної систем як у самців, так і в самок.Рецептор естрогенів (ER) на цей час є єдиним членом стероїдного підсімейства ядерних рецепторів, який має кілька різних підтипів. Останнім часом із бібліотеки сДНК простати пацюків була клонована нова ізоформа ER, а саме ER-β (відома також як ER-β1), присутня в простаті пацюка та в простаті людини. Відповідно, відомий раніше ER тепер позначається як ER-α. ER-a та ER-β виявляють високий ступінь гомологічності амінокислот, мають аналогічні показники спорідненості зв'язування з 17-β-естрадіолом (Е2) і здатні гетеро- або гомодимеризуватися з утворенням сигнального комплексу. Дивись роботи Кіпера та інших [G.G.Kuiper et al., Endocrinol. 138: 863-70 (1997); G.G.Kuiper et al., Proc. Natl. Acad. Sci. USA 93: 5925-30 (1996)]. Хоча Е2 активує як ER-α, так і ER-β, проте ER-α стимулює транскрипцію та проліферацію клітин, в той час як ER-β пригнічує активацію ER-α. Цікаво, що як ендогенні ліганди ERβ запропоновано 3-β,17-β-андростандіол та 5-αандростан [З.Вейхуа та інші - Z.Weihua et al., PNAS 98:6330-5 (2001)]. 3-β,17-β-андростандіал є основним метаболітом дигідротестостерону (DHT) - активного внутрішньоклітинного андрогену в придаткових чоловічих статеви х органах, відновленого в положенні 5α. Активація ER-β також стимулює підвищену експресію глутатіон-S-трансферази та хінонредуктази. Показано, що ці два ферменти мають хемопротекторні детоксифікаторні властивості [В.І. Чанг та інші - W.Y. Chang et al., Prostate 40: 115-24 (1999); Монтано та інші - М.М.Montano et al., J.Biol. Chem. 273: 25443-9 (1998)]. З ура хуванням недавньої ідентифікації ER-β та з'ясування того, що ER-α та ER-β відіграють різні біологічні ролі, ER-селективні модулятори також можуть набути великого клінічного значення. Оскільки ER-β сильно експерсований в численних тканинах, в тому числі в простаті, сечовому міхурі, яєчниках, яєчках, легенях, тонкій кишці, судинному ендотелії та різних частинах головного мозку, сполуки, які селективно модулюють ER-β, могли б мати клінічне значення при лікуванні різноманітних хворобливих станів, наприклад, раку простати, раку яєчок, раку яєчників, раку легенів, серцево-судинних захворювань, нейродегенеративних захворювань, нетримання сечі, розладів ЦНС, розладів ШК тракту та остеопорозу. Такі 8 сполуки мали б мінімальний вплив на тканини, що містять ER-α, і, отже, мали б різні профілі побічних ефектів. Таким чином, агоністи ER-β мають терапевтичні профілі, відмінні від профілів антагоністів або агоністів ER-α, і могли б переважно сприятливо впливати на тканини, котрі залежать від сигнального ефекту ER-β. Передміхурова залоза продукує речовини, які виявлено в сімені та в крові. Деякі з них є регуляторними пептидами. Передміхурова залоза містить строму та епітеліальні клітини; остання група складається зі стовпчастих секреторних клітин та базальних несекреторних клітин. Проліферація цих базальних клітин, а також клітин строми, спричиняє доброякісну гіперплазію простати (ВРН), яке являє собою поширене захворювання простати. ВРН - це прогресуючий стан, що характеризується вузловим збільшенням тканини простати, що призводить до обструкції уретри. Це викликає збільшення частоти сечовиділення, нічну поліурію, утруднене відходження сечі та переривання або затримку початку відходження сечі. До можливих наслідків ВРН належать гіпертрофія гладких м'язів сечового міхура, декомпенсація сечового міхура та підвищена схильність до інфекцій сечового тракту. Розвиток ВРН вважається неминучим явищем у чоловіків похилого віку. ВРН спостерігається приблизно у 70% чоловіків у віці понад 70 років. При сучасній фармакотерапії ВРН застосовують αадренергічні антагоністи для симптоматичного підтримання впливу інгібіторів стероїд-5-aредуктази з метою зменшення об'єму тканини, що розрослася. Ці заходи мають обмежений терапевтичний ефект. Смертність внаслідок раку простати у людей, які страждають на локалізовані пухлини, при оцінюванні за принципом обережного очікування, як правило, є низькою (9%-15%). Ці цифри, однак, стосуються пацієнтів із локалізованим захворюванням; вони не обов'язково стосуються більш молодих людей груп підвищеного ризику. Більш молоді чоловіки з пухлинами стадії ТІ а мають довший очікуваний період ризику, ніж літні чоловіки з тою самою стадією захворювання, і тому є кандидатами на потенціально ефективне лікування. При дослідженнях обережного очікування високі показники прогресування захворювання (34%-80%) свідчать, що лише незначна частка клінічно очевидних ракових пухлин простати знаходиться у стані спокою. Цей винахід стосується нових похідних бензопірану формули (І): (І) або похідних формули II 9 77986 10 циклопентил[с]3,4-дигідро-2Н-1-бензопіран, х) (±)-2-етил-2-(4-гідроксифеніл)-6-гідроксициклопентил[с]3,4-дигідро-2Н-1-бензопіран, (ІІ) у) (±)-2-(1-метилетил)-2-(4-гідроксифеніл)-6гідрокси-циклопентил[с]3,4-дигідро-2Н-1бензопіран, їхні фармацевтично прийнятні солі або енантіде омери. кожний з R1, R2, R3 та R4, незалежно від інших, За другим варіантом здійснення, цей винахід є -Н, С1-С6-алкіл, -ОН, С1-С6-алкоксигрупа, галопропонує фармацевтичну композицію, яка містить ген, амідогрупа або група -CF3; терапевтично ефективну кількість сполуки формуR5 є водень або С 1-С6-алкіл; 1 2 3 ли (І) та фармацевтично прийнятний носій. кожний з Υ , Y та Y , незалежно від інших, є За іншим варіантом здійснення, цей винахід Н або С 1-С6-алкіл; і пропонує медичні способи застосування сполук G є -СН2-, -СН2-СН2- або -СН2-СН2-СН2-; формули (І) як агоністів β-рецепторів естрогенів або їхніх фармацевтично прийнятних солей. ("ER"), а також їх подальше застосування для ліДо сполук за цим винаходом належать перелікування захворювань, опосередкованих ER-β, начені нижче сполуки, котрі жодним чином не слід приклад, раку простати, доброякісної гіперплазії розглядати як такі, що обмежують сполуки, вклюпростати, раку яєчок, серцево-судинних захворючені в обсяг винаходу: вань, нейродегенеративних розладів, нетримання a) (±)-2-(4-гідроксифеніл)-6-гідроксисечі, розладів центральної нервової системи циклопентил[с]3,4-дигідро-2Н-1-бензопіран, (ЦНС), розладів шлунково-кишкового (ШК) тракту b) (±)-2-(4-гідроксифеніл)-6-трифторметилта остеопорозу. циклопентил[с]3,4-дигідро-2Н-1-бензопіран, У значенні, вживаному в цьому описі: c) (±)-2-(4-гідроксифеніл)-6-метилa) термін "амідо(група)" означає амінокарбоніл циклопентил[с]3,4-дигідро-2Н-1-бензопіран, (C(O)NH2); d) (±)-2-(4-гідроксифеніл)-6-фторb) термін "галоген" означає атом фтору, хлору, циклопентил[с]3,4-дигідро-2Н-1-бензопіран, брому або йоду; е) (±)-2-(4-гідроксифеніл)-5-гідроксиb) термін "С1-С6-алкіл" означає алкільний рациклопентил[с]3,4-дигідро-2Н-1-бензопіран, дикал розгалуженої або нормальної будови, який f) (±)-2-(4-гідроксифеніл)-7-гідроксимістить від 1 атому до 6 атомів вуглецю, наприциклопентил[с]3,4-дигідро-2Н-1-бензопіран, клад, метил, етил, н-пропіл, ізопропіл, н-бутил, g) (±)-2-(4-гідроксифеніл)-6-гідрокси-8-метилізобутил, втор-бутил, трет-бутил, пентил, гексил циклопентил[с]3,4-дигідро-2Н-1-бензопіран, тощо; h) (±)-2-(4-гідроксифеніл)-6-гідроксиc) термін "С1-С6-алкокси(група)" означає алкоциклогептил[с]3,4-дигідро-2Н-1-бензопіран, ксигрупу нормальної або розгалуженої будови, яка і) (±)-2-(4-гідроксифеніл)-6-гідрокси-8-метоксимістить від 1 атому до 6 атомів вуглецю, наприциклопентил[с]3,4-дигідро-2Н-1-бензопіран, клад, метоксигрупу, етоксигрупу, «-пропоксигрупу, j) (±)-2-(4-гідроксифеніл)-6-гідрокси-11,11ізопропоксигрупу, н-бутоксигруп у, ізобутоксигрупу, диметил-циклопентил[с]3,4-дигідро-2Н-1втор-бутоксигрупу, трет-бутоксигрупу, пентоксигбензопіран, рупу, гексилоксигрупу тощо; k) (±)-2-(4-гідроксифеніл)-6-гідрокси-11,11d) позначення означає зв'язок, стереохідіетил-циюіопентил[с]3,4-дигідро-2Н-1-бензопіран, мічна конфігурація якого не вказана; l) (±)-2-(4-гідроксифеніл)-6-метоксие) позначення означає зв'язок, спрямоциклопентил[с]3,4-дигідро-2Н-1-бензопіран, ваний вперед від площини сторінки (до читача); m) (±)-2-(4-гідрокси-3-метилфеніл)-6-гідроксиf) позначення означає зв'язок, спрямовациклопентил[с]3,4-дигідро-2Н-1-бензопіран, ний назад від площини сторінки (від читача); n) (±)-2-(2-метил-4-гідроксифеніл)-6-гідроксиg) перелічені нижче терміни та абревіатури, циклопентил[с]3,4-дигідро-2Н-1-бензопіран, вжиті в описах підготовчих синтезів та в приклао) (±)-2-(4-гідроксифеніл)-циклопентил[с]3,4дах, мають такі значення: нг - нанограми; мкг - мікдигідро-2Н-1-бензопіран, рограми; мг - міліграми; г - грами; кг - кілограми; р) (±)-2-(4-гідроксифеніл)-6-гідрокси-7-метилнмоль - наномолі;ммоль - мілімолі; моль - молі; циклопентил[с]3,4-дигідро-2Н-1-бензопіран, мкл - мікролітри; мл - мілілітри; л - літри; Rf - коеq) (±)-2-(4-гідроксифеніл)-6-гідроксифіцієнт затримання; °С - градуси за Цельсієм; т.к. циклогексил[с]3,4-дигідро-2Н-1-бензопіран, – температура кипіння; мм рт.ст. - тиск у міліметг) (±)-2-(4-метоксифеніл)-6-метоксирах ртутного стовпа; т.пл. - температура плавленциклопентил[с]3,4-дигідро-2Н-1-бензопіран, ня; розкл. - розклад; [α]20D - питоме обертання лінії s) (±)-2-(4-амінокарбонілфеніл)-6D натрію при 20°С, одержане в комірці довжиною 1 амінокарбоніл-циклопентил[с]3,4-дигідро-2Н-1дециметр; с - концентрація в г/мл; нМ - наномолябензопіран, рний; мкМ - мікромолярний; мМ - мілімолярний; Μ t) (±)-2-(4-амінокарбонілфеніл)-6-гідрокси- молярний; Ki - константа інгібування; Kd - констациклопентил[с]3,4-дигідро-2Н-1-бензопіран, нта дисоціації; psi - фунти на квадратний дюйм; u) (±)-2-(4-гідроксифеніл)-6-амінокарбонілоб/хв - оберти за хвилину; HPLC - рідинна хромациклопентил[с]3,4-дигідро-2Н-1-бензопіран, тографія високої ефективності; HRMS - мас-спектр ν) (±)-2-(4-метоксифеніл)-6-гідроксивисокого розділення; ТГФ - тетрагідрофуран; розциклопентил[с]3,4-дигідро-2Н-1-бензопіран, еол - насичений водний розчин хлориду натрію; w) (±)-2-метил-2-(4-гідроксифеніл)-6-гідрокси 11 77986 12 ВПВ - втрати при висушуванні; мкКі - мікрокюрі; ми, індивідуальні ізомери та їхні комбінації охопв.оч. - вн утрішньоочеревинно; в.в. - внутрішньолюються цим винаходом. Три основні хіральні венно; і р/хв - розпадів за хвилину; центри, позначені 2, 3 та 4, показані в формулі (І). h) позначення У відносній стереохімічній конфігурації сполук формули (І), якій віддається перевага, всі хіральні центри 2, 3 та 4 мають цис-конфігурацію, як показано нижче формулами IB та 1С: означає, що метил приєднаний в положенні 1, а замісник чи замісники, позначені R, можуть бути приєднані в будь-якому з положень 2, 3, 4, 5 або 6; і) позначення означає феніл або заміщений феніл, при цьому мається на увазі, що будь-який замісник може бути приєднаний в будь-якому з положень 1, 2, 3, 4, 5 або 6. Крім того, мається на увазі, що, коли один із замісників приєднаний у положенні 1, то інший замісник, позначений R, може бути приєднаний у будь-якому з положень 2, 3, 4, 5 або 6; коли один із замісників приєднаний у положенні 2, то інший замісник, позначений R, може бути приєднаний у будь-якому з положень 1, 3, 4, 5 або 6; коли один із замісників приєднаний у положенні 3, то інший замісник, позначений R, може бути приєднаний у будь-якому з положень 1, 2, 4, 5 або 6; коли один із замісників приєднаний у положенні 4, то інший замісник, позначений R, може бути приєднаний у будь-якому з положень 1, 2, 3, 5 або 6; коли один із замісників приєднаний у положенні 5, то інший замісник, позначений R, може бути приєднаний у будь-якому з положень 1, 2, 3, 4 або 6; і коли один із замісників приєднаний у положенні 6, то інший замісник, позначений R, може бути приєднаний у будь-якому з положень 1, 2, 3, 4 або 5; j) система нумерації та найменування трициклічної системи формули (І) та формули (II) відповідають поданим нижче прикладам: якщо G є -СН2-: циклопентил[с]3,4-дигідро-2Н-1-бензопіран якщо G є -СН2-СН2-: циклогексил [с] 3,4-дигідро-2Н-1-бензопіран якщо G є -СН2-СН2-СН2-: циклогептил[с]3,4-дигідро-2Н-1-бензопіран k) термін "енантіомерний надлишок" або "ее" означає процент надлишку одного з енантіомерів, Е1, в суміші двох енантіомерів, Е1+Е2, при цьому {(Е1-Е2)/(Е1+Е2)}´100=ее. Сполуки за цим винаходом можуть мати один або кілька асиметричних центрів. Внаслідок наявності цих хіральних центрів сполуки за цим винаходом можуть існувати в формі рацематів та індивідуальних енантіомерів, а також діастереомерів та сумішей діастереомерів. Усі асиметричні фор Для цілей цього винаходу сполука, позначена як "рацемічна IB" або "рацемічна lС", або її структурна формула, означає рацемічну структур у сполук IB та lС. Крім того, для цілей цього винаходу сполука, позначена як "рацемічна ID" або "рацемічна IE", або її стр уктурна формула, показана нижче, означає рацемічну структур у сполук ID та IE. Для виготовлення переважно одного оптичного ізомеру у порівнянні з його енантіомером можна застосувати численні способи. Наприклад, можна виготовити суміш енантіомерів із подальшим розділенням двох енантіомерів. Способом, який звичайно застосовують для розділення рацемічної суміші, є рідинна хроматографія високої ефективності на хіральному сорбенті. Подальші подробиці, що стосуються розділення сумішей енантіомерів, можна знайти в монографії Жака та інших "Енантіомери, рацемати та їх розділення" [J. Jacques et al., Enantiomers, Racemates, and Resolutions, 1991]. Термін "фармацевтично прийнятна сіль" стосується будь-якої солі з кислотою або основою. Вираз "фармацевтично прийнятні солі з кислотами" призначено для використання стосовно до будь-якої нетоксичної солі сполук формули (І) основного характеру з органічними або неорганічними кислотами. До прикладів неорганічних кислот, які утворюють придатні солі, належать хлористоводнева, бромистоводнева, сірчана та фосфорна кислоти, а також солі металів із кислотами, наприклад, моногідроортофосфат натрію та гідросульфат калію. До прикладів органічних кислот, які утворюють придатні солі, належать моно-, ди- та трикарбонові кислоти. Прикладами таких кислот є оцтова, гліколева, молочна, піровиноградна, малонова, бурштинова, глутарова, фумарова, яблучна, винна, лимонна, аскорбінова, малеїнова, гідроксималеїнова, бензойна, гідроксибензойна, фенілоцтова, корична, саліцилова, 2феноксибензойна, n-толуолсуль фонова кислоти та сульфокислоти, наприклад, бензолсульфокислота, метансульфокислота та 2гідроксіетансульфокислота. Такі солі можуть існувати в гідратній або практично безводній формах. Як правило, солі вищезгаданих сполук із кислотами є розчинними у воді та різноманітних гідрофільних органічних розчинниках і мають вищі температури плавлення порівняно з їхніми вільними 13 77986 основами. Вираз "фармацевтично прийнятні солі з основами" призначено для використання стосовно до будь-якої нетоксично! солі сполук формули (І) з органічними або неорганічними основами. До прикладів основ, які утворюють придатні солі, належать гідроксиди лужних або лужноземельних металів, наприклад, гідроксиди натрію, калію, кальцію, магнію або барію; аміак та аліфатичні, аліциклічні або ароматичні органічні аміни, наприклад, метиламін, диметиламін, триметиламін та піколін. Можна одержувати як одно-, так і двоосновні солі з цими сполуками. Нижче перелічено варіанти формули (І), яким віддається перевага: (1) Сполуки, в яких усі хіральні центри, позначені 2, 3 та 4, мають цис-конфігурацію; (2) Сполуки, де G є -СН2-; (3) Сполуки, де обидва Y2 та Y3 є -Н; (4) Сполуки, де один з R1 та R2 є -ОН; (5) Сполуки, де R3 є -Н; (6) Сполуки, де Y1 є -Н; (7) Сполуки, де один із R1 та R2 є -ОН, а др угий є -Н. Мається на увазі, що за вимогами до вищевказаних сполук, яким віддається перевага, можуть бути обрані додаткові варіанти сполук, яким віддається перевага. Наприклад, обмеження (1) можна поєднати з обмеженням (2); обмеження (3) можна поєднати з обмеженням (4); обмеження (1), (2), (3), (5), (6) та (7) можна поєднати між собою; тощо. Іншим варіантом здійснення цього винаходу є сполуки формули III: (lІІ) де R1а є - Н, -ОН або F; R2a є -Н, -СН3 або -ОСН3; R3a є -Н або -СН3; G є -СН2-, -СН2-СН2- або -СН2-СН2-СН2-; або їхні фармацевтично прийнятні солі. Ще одним варіантом здійснення цього винаходу є сполуки формули IV: (ІV) де R1b є амідогрупа або гідроксил; R2b є -Н або С1-С6-алкіл; R3b є -Н або С1-С6-алкіл; R4b є амідогрупа або гідроксил; і G є -СН2-, -СН2-СН2- або СН2-СН2-СН2-; або їхні фармацевтично прийнятні солі. Ілюстративними прикладами сполук, які охоплюються цим винаходом, є рацемічні суміші та конкретні енантіомери таких сполук: 14 15 77986 16 пами захисту з одержанням захищеного фенолу формули (4), застосовуючи способи та процедури, добре відомі фахівцям у цій галузі. Наприклад, фенол формули (2) змішують із суспензією, яка містить придатний безводний розчинник, наприклад, безводний диметилформамід (ДМФ) та придатну сильну основу, наприклад, гідрид металу, найкраще гідрид натрію. До цієї суспензії додають хлорид алкоксиметилового простого ефіру, найкраще MOM-СІ, в кількості, яка відповідає приблизно еквімолярній кількості, залежно від кількості гідроксилів, які підлягають захисту, в фенолі формули (2). Реакцію можна проводити при кімнатній температурі протягом часу в межах від приблизно 30хв. до приблизно 2 діб. Потім до реакційної маси додають воду та придатний ефір, наприклад, діетиловий ефір або EtOAc, і органічний шар промивають придатною основою, наприклад, гідроксиСхеми реакцій дом натрію або NaHCО3, та розсолом. Захи щений Сполуки формули (І) та їхні проміжні продукти фенол формули (4) можна виділити та очистити можна одержати, як ілюстровано нижче Схемами способами, добре відомими в цій галузі, наприреакцій A-D. Усі замісники, якщо не обумовлено клад, екстракцією, випаровуванням, розтиранням, інше, відповідають поданим вище означенням. хроматографією та перекристалізацією. Реагенти та вихідні матеріали легко одержати фаЗа Схемою А, стадія 1b, 2хівцю. оксоциклоалканкарбоксилат формули (3) активують трифлатом (трифтрометансульфонатом) з одержанням активованого циклоалканкарбоксилату формули (5), застосовуючи способи та процедури, добре відомі в цій галузі; див. Крісп та інші [G.T. Crisp et al., J. Org. Chem. 57, 6972-6975, 1992]. Наприклад, метил-2оксоциклоалканкарбоксилат формули (3) розчиняють у безводних умовах в придатному розчиннику, наприклад, в тетрагідрофурані, дихлорметані, ацетоні, етилацетаті, толуолі або діетиловому ефірі, і вводять у контакт із придатним активувальним агентом, наприклад, трифторметансульфоновим ангідридом. Реакцію проводять у присутності основи, наприклад, N-метилморфоліну, карбонату натрію, триетиламіну, Ν,Νдіізопропілетиламіну, карбонату калію, бікарбонату натрію, піридину або 2,6-ди-трет-бутил-4метилпіридину. Реакцію проводять, як правило, при температурах від -78°С до температури навколишнього середовища. Тривалість реакції становить, як правило, від 1год до 24год. Потім реакційну суміш можна погасити. Продукт формули (5) можна виділити та очистити способами, добре відомими в цій галузі, наприклад, екстракцією, випаровуванням, розтиранням, хроматографією та перекристалізацією. За Схемою А, стадія 2, захи щений фенол формули (4) сполучають з активованим циклоалканкарбоксилатом формули (5) з одержанням продукту сполучення формули (6). Наприклад, реакцію 1 У значенні, вживаному в цій схемі, символи R , сполучення проводять у присутності бутиллітію, 2 3 1 1 R , R та Y відповідають замісникам відповідно R , хлориду цинку та сполуки паладію. Реакцію пере2 3 1 R , R та Y , за винятком випадків, коли замісники важно проводять у придатному розчиннику, напри1 2 3 1 R , R та R є гідроксилами, а замісник Y є -Н (таклад, в тетрагідрофурані (ТГФ), і можна проводити 1 ким чином, група -O-Y є гідроксилом). В таких її спочатку у безводних умовах. У варіанті, якому випадках відповідну гідроксильну групу захи щають віддається перевага, захищений фенол формули радикалом алкоксиметилового простого ефіру, (4) розчиняють у придатному розчиннику, напринаприклад, метоксиметилом ("MOM") або метоксіклад, в ТГФ, обробляють бутиллітієм при зниженій етоксиметилом ("MEM"). температурі, потім додають хлорид цинку в розЗа Схемою А, стадія 1а, гідроксильні групи чиннику і дають суміші нагрітися до температури фенолу формули (2) захищають придатними грунавколишнього середовища. Потім додають спо 17 77986 18 луку паладію, наприклад, тетрацію гасять джерелом протонів, наприклад, насичекіс(трифенілфосфін)Рd(0), разом з активованим ним розчином бікарбонату натрію. Кетон формули циклоалканкарбоксилатом формули (5), і темпера(10) можна виділити та очистити способами, добре туру у варіанті, якому віддається перевага, підвивідомими в цій галузі, наприклад, екстракцією, щують до температури кипіння розчинника на певипаровуванням, розтиранням, хроматографією та ріод часу в межах від приблизно 6год. до 24год. перекристалізацією. Продукт сполучення формули (6) можна виділити За Схемою А, стадія 6а або 6b, кетон формули та очистити способами, добре відомими в цій га(10) піддають циклізації у присутності кислотного лузі, наприклад, екстракцією, випаровуванням, каталізатора з подальшим відновленням одержарозтиранням, хроматографією та перекрисного гемікеталю для одержання сполуки формули талізацією. (ІА або ІА'), яка являє собою рацемічну суміш споЗа Схемою А, стадія 3, продукт сполучення луки формули (І). Наприклад, на стадії 6а додають формули (6) відновлюють придатним відновлюваn-толуолсульфонову кислоту у приблизно еквімочем з одержанням відновленого продукту формулярному співвідношенні до кетону формули (10) у ли (7), застосовуючи способи та процедури, добре придатному спиртовому розчиннику, наприклад, у відомі в цій галузі. Наприклад, продукт сполучення безводному метанолі. Потім суміш нагрівають до формули (6) вводять у контакт із придатним віднотемператури в межах від 40°С до 60°С, у варіанті, влювальним агентом, наприклад, сполуки паладію, якому віддається перевага, до 50°С, протягом пеу варіанті, якому віддається перевага, 5% або 10% ріоду часу від 12год. до 24год, у варіанті, якому паладієм на вугіллі, у придатному розчиннику або віддається перевага, 18год. Охолоджують суміш суміші розчинників, наприклад, в метанолі. Реакдо температури навколишнього середовища і доцію у варіанті, якому віддається перевага, проводають до неї придатний відновлювальний агент, дять у присутності придатної основи, наприклад, наприклад, ціанборгідрид натрію, разом із придаттриалкіламіну, у варіанті, якому віддається більша ним індикатором, наприклад, бромкрезоловим перевага, триетиламіну. Потім реакційну суміш зеленим, згідно з методикою, аналогічною описанагрівають до температури в межах від 30°С до ній Срікрішна та іншими [A. Srikrishna et al., Tetraтемператури кипіння на період часу в межах від hedron, vol.51, no.11, pp.3339-3344, 1995]. Потім приблизно 2год. до 24год. Відновлений продукт повільно додають метанол, насичений хлороводформули (7) можна виділити та очистити способанем, до одержання стійкого жовтого кольору суміми, добре відомими в цій галузі, наприклад, екстші. Після досягнення остаточної зміни кольору ракцією, випаровуванням, розтиранням, хроматогсуміш перемішують протягом приблизно 1-2год. рафією та перекристалізацією. Потім реакцію гасять придатним акцептором проЗа Схемою А, стадія 4, відновлений продукт тонів, наприклад, насиченим розчином бікарбонаформули (7) можна перетворити у Вайнреб-амід ту натрію. При такій комбінації умов проведення формули (8). Це перетворення можна здійснити, реакції одержують цис-конфігурацію хіральних застосовуючи реакцію типу, описаного Уїльямсом центрів (тобто, таких центрів у сполуках IB або lС). та іншими [J.M. Williams et al., Tetrahedron Letters Застосовуючи R3SiH/TFA (триалкілсилан та три36, 5461-5464, 1995]. Наприклад, відновлений фтороцтову кислоту) на стадії 6Ь, одержують продукт формули (7) змішують із гідрохлоридом транс-конфігурацію хіральних центрів (тобто таких Ν,Ο-диметилгідроксиламіну у відповідному апроцентрів у сполуках ID або IE). Потім продукт фортонному розчиннику, наприклад, у тетрагідрофумули (ІА) або (ІА') можна виділити та очистити рані, у варіанті, якому віддається перевага, у безспособами, добре відомими в галузі, наприклад, водних умовах, і охолоджують до температури в екстракцією, випаровуванням, розтиранням, хромежах від приблизно 0°С до приблизно -30°С, у матографією та перекристалізацією. варіанті, якому віддається більша перевага, до За альтернативним варіантом, продукт сполуприблизно -10°С. Потім додають придатний реачення формули (6) можна синтезувати, як показагент Гріньяра, у варіанті, якому віддається перевано в схемі реакції В. Усі замісники, якщо не обумога, ізопропілмагнійхлорид, у молярному співвідновлено інше, відповідають поданим вище шенні приблизно 1,5, і перемішують реакційну означенням. Реагенти та вихідні матеріали легко суміш приблизно від 15хв. до 2год. Потім реакцію одержати фахівцю у цій галузі. гасять джерелом протонів, наприклад, насиченим розчином хлориду амонію. Вайнреб-амід формули (8) можна виділити та очистити способами, добре відомими в цій галузі, наприклад, екстракцією, випаровуванням, розтиранням, хроматографією та перекристалізацією. За Схемою А, стадія 5, Вайнреб-амід формули (8) сполучають з ариллітієм формули (9), і одержують кетон формули (10). Наприклад, ариллітій За Схемою В, стадія 1, гідроксильні групи формули (9) додають до розчину Вайнреб-аміду бромфенолу формули (11) захищають придатними формули (8) у придатному апротонному розчиннигрупами захисту з одержанням захищеного бромку, наприклад, у безводному тетрагідрофурані, фенолу формули (12), застосовуючи способи та охолоджують до температури в межах від приблипроцедури, описані в Схемі А, стадія 1а. зно -20°С до приблизно 5°С, краще до приблизно За Схемою В, стадія 2, захищений бромфенол 0°С, і перемішують реакційну суміш протягом періформули (12) сполучають з активованим циклоалоду часу приблизно від 15хв. до 3год. Потім реакканкарбоксилатом формули (5) з одержанням 19 77986 продукту сполучення формули (6), застосовуючи способи та процедури, описані в Схемі А, стадія 2. Альтернативний спосіб одержання конкретних бромзаміщених проміжних продуктів показано на Схемі С Крім того, конкретні сполуки формули (І), де Y' є метил, можна одержати за Схемою D. Крім того, амідовмісні сполуки формули (II), зображені формулами (16) та (17), можна синтезувати, як описано в Схемі Е. Усі замісники, за відсутності інших вказівок, відповідають поданим вище визначенням. Реагенти та вихідні матеріали легко одержати фа хівцю у цій галузі. За Схемою Е, стадія 1, дигідроксисполуку формули (13) можна перетворити в суміш монотрифлату формули (14) та дитрифлату формули (15). Одержану суміш можна розділити, застосовуючи звичайну хроматографію. За Схемою Е, стадія 2, монотрифлат формули (14) та дитрифлат формули (15) спільно сполучають із 1,1,1,3,3,3-гексаметилдисилазаном в умовах карбонілування з паладієвим каталізатором і одержують карбоксаміди формул (16) та (17). Крім того, амідовмісні сполуки формули (19) можна синтезувати, як описано в Схемі F. Усі замісники, якщо не обумовлено інше, відповідають поданим вище визначенням. 20 Реагенти та вихідні матеріали легко одержати фа хівцю у цій галузі. За Схемою F, стадія 1, дигідроксисполуку формули (13) можна селективно перетворити в бензиловий простий ефір формули (18). За Схемою F, стадія 2, фенольну гр упу, що залишилася, обробляють трифлатом, після чого проводять спільне сполучення в умовах, ідентичних вказаним для Схеми Е, стадія 2. Нарешті, відщеплюють бензильну групу, і після очищення HPLC одержують карбоксамід формули (19). Крім того, сполуки, де R5 є C1-С6-алкіл, можна одержати, як описано в Схемі G. За Схемою G, кетон формули (10) вводять у реакцію з алкілвмісним металоорганічним реагентом, наприклад, із метиллітієм або етилмагнійбромідом, і одержують третинні спирти формули (20). У кислотних умовах, описаних у Схемі А, стадія 6а, з цих третинних спиртів одержують бензопірани формули (21). Суспензію гідриду натрію (60% у мінеральному маслі, 3,81г, 95,45ммоль) у безводному ДМФ (50мл) перемішують в атмосфері азоту при 0°С, і крапля за краплею додають розчин гідрохінону (5,00г, 45,45ммоль) в безводному ДМФ (50мл). До цієї суспензії додають крапля за краплею метоксиметилхлорид (7,2мл,95,45ммоль), при цьому спостерігається додаткове виділення газу. Дають реакційній суміші нагрітися до температури навколишнього середовища, і перемішують протягом 1год. Гасять реакцію водою та діетиловим ефіром. Органічний шар промивають 1-н. розчином гідроксиду натрію і розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 20% етилацетату в гексані, одержуючи Проміжний продукт 1 (5,64г, 63%) у вигляді прозорого масла. 1 H ЯМР (CDCI3): 6,97 (s, 4H), 5,11 (s, 4H), 3,47 (s, 6H). 21 77986 22 20% етилацетату в гексані, одержуючи Проміжний продукт 4 (2,45г, 72%) у ви гляді прозорого масла. Суспензію гідриду натрію (60% у мінеральному маслі, 0,67г, 16,67ммоль) у безводному ДМФ (25мл) перемішують в атмосфері азоту при 0°С і крапля за краплею додають розчин α,α,αтрифторметил-п-креозолу (2,50г, 15,15ммоль) в безводному ДМФ (25мл). До цієї суспензії додають крапля за краплею метоксиметилхлорид (1,3мл, 16,67ммоль). Дають реакційній суміші нагрітися до температури навколишнього середовища і перемішують протягом 1год. Гасять реакцію водою та діетиловим ефіром. Органічний шар промивають 1-н. розчином гідроксиду натрію і розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флешхроматографією з елююванням 20% етилацетату в гексані, одержуючи Проміжний продукт 2 (2,50г, 80%) у вигляді прозорого масла. 1Н ЯМР (CDCІ3): 7,25 (d, J=8,6Гц, 2Н), 6,83 (d, J=8,3Гц, 2Н), 4,93 (s, 2Н), 3,19 (s, 3Н). Суспензію гідриду натрію (60% у мінеральному маслі, 0,89г, 22,17ммоль) у безводному ДМФ (25мл) перемішують в атмосфері азоту при 0°С, і крапля за краплею додають розчин гваяколу (2,50г, 20,16ммоль) в безводному ДМФ (25мл). До цієї суспензії додають крапля за краплею метоксиметилхлорид (1,7мл, 22,17ммоль). Дають реакційній суміші нагрітися до температури навколишнього середовища, і перемішують протягом 1год. Гасять реакцію водою та діетиловим ефіром. Органічний шар промивають 1-н. розчином гідроксиду натрію і розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 20% етилацетату в гексані, одержуючи Проміжний продукт 3 (2,22г, 66%) у вигляді прозорого масла. 1H ЯМР (CDCI3): 6,97-6,89 (m, 4Н), 5,01 (s, 2Н), 3,89 (s, 3Н), 3,22 (s, 3Н). Суспензію гідриду натрію (60% у мінеральному маслі, 0,41г, 10,30ммоль) у безводному ДМФ (25мл) перемішують в атмосфері азоту при 0°С, і крапля за краплею додають розчин 2-бром-4метилфенолу (2,50г, 14,71ммоль) в безводному ДМФ (25мл). До цієї суспензії додають крапля за краплею метоксиметилхлорид (0,78мл, 10,30ммоль). Дають реакційній суміші нагрітися до кімнатної температури, і перемішують протягом 1год. Гасять реакцію водою та діетиловим ефіром. Органічний шар промивають 1-н. розчином гідроксиду натрію і розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографкю з елююванням Суспензію гідриду натрію (60% у мінеральному маслі, 0,58г, 14,40ммоль) у безводному ДМФ (25мл) перемішують в атмосфері азоту при 0°С, і крапля за краплею додають розчин 2-бром-4фтор фенолу (2,50г, 13,09ммоль) в безводному ДМФ (25мл). До цієї суспензії додають крапля за краплею метоксиметилхлорид (1,1мл, 14,40ммоль). Дають реакційній суміші нагрітися до кімнатної температури, і перемішують протягом 1год. Гасять реакцію водою та діетиловим ефіром. Органічний шар промивають 1-н. розчином гідроксиду натрію і розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 20% етилацетату в гексані, одержуючи Проміжний продукт 5 (2,71г, 88%) у вигляді прозорого масла. 1 H ЯМР (CDCI3): 7,40-7,35 (m, 1Н), 7,01-6,89 (m, 1H), 6,85-6,79 (m, 1H), 4,99 (s, 2H), 3,87 (s, 3H). Суспензію гідриду натрію (60% у мінеральному маслі, 1,90г, 47,68ммоль) у безводному ДМФ (25мл) перемішують в атмосфері азоту при 0°С, і крапля за краплею додають розчин резорцину (2,50г, 22,70ммоль) в безводному ДМФ (25мл). До цієї суспензії додають крапля за краплею метоксиметилхлорид (3,6мл, 47,68ммоль), при цьому спостерігається додаткове виділення газу. Дають реакційній суміші нагрітися до температури навколишнього середовища, і перемішують протягом 1год. Гасять реакцію водою та діетиловим ефіром. Органічний шар промивають 1-н. розчином гідроксиду натрію і розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 20% етилацетату в гексані, одержуючи Проміжний продукт 6 (2,49г, 55%) у вигляді прозорого масла. 1 Н ЯМР (CDCІ3): 7,20 (t, J=8,2Гц, Ш), 6,74-6,68 (m, ЗН), 5,16 (s, 4H), 3,48 (s, 6H). MS (мас-спектр) обчислено 198,2; MS (M+l) 199,0. Суспензію гідриду натрію (60% у мінеральному маслі, 1,11г, 27,78ммоль) у безводному ДМФ (25мл) перемішують в атмосфері азоту при 0°С, і крапля за краплею додають розчин 4бромрезорцину (2,50г, 13,22ммоль) в безводному ДМФ (25мл). До цієї суспензії додають крапля за краплею метоксиметилхлорид (2,1мл, 27,78ммоль), при цьому спостерігається додаткове виділення газу. Дають реакційній суміші нагрітися до температури навколишнього середовища, і пе 23 77986 24 ремішують протягом 1год. Гасять реакцію водою та діетиловим ефіром. Органічний шар промивають 1-н. розчином гідроксиду натрію і розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флешСуспензію гідриду натрію (60% у мінеральному хроматографією з елююванням 20% етилацетату в маслі, 3,54г, 88,61ммоль) у безводному ДМФ гексані, одержуючи Проміжний продукт 7 (2,46г, (100мл) перемішують в атмосфері азоту при 0°С, і 67%) у вигляді прозорого масла. 1H ЯМР (CDCI3): крапля за краплею додають розчин 47,40 (d, J=7,8Гц, 1Н), 6,87 (d, J=2,7, 1H), 6,63 (dd, метоксифенолу (10,00г, 80,55ммоль) в безводному J=2,7Гц, 7,8Гц, 1Н), 5,22 (s, 2H), 5,14 (s, 2H), 3,51 ДМФ (50мл). До цієї суспензії додають крапля за (s, 3H), 3,46 (s, 3H). MS обчислено 277,12; MS краплею метоксиметилхлорид (6,7мл, (M+1) 277,2, 279,2. 88,61ммоль). Дають реакційній суміші нагрітися до температури навколишнього середовища, і перемішують протягом 1год. Гасять реакцію водою та діетиловим ефіром. Органічний шар промивають 1-н. розчином гідроксиду натрію і розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флешСуспензію гідриду натрію (60% у мінеральному хроматографією з елююванням 20% етилацетату в маслі, 1,58г, 39,21ммоль) у безводному ДМФ гексані, одержуючи Проміжний продукт 10 (11,55г, (50мл) перемішують в атмосфері азоту при 0°С, і 85%) у вигляді прозорого масла. крапля за краплею додають розчин 2,6дибромгідрохінону (5,00г, 18,67ммоль) в безводному ДМФ (50мл). До цієї суспензії додають крапля за краплею метоксиметилхлорид (3,0мл, 39,21ммоль), при цьому спостерігається додаткове До суспензії промитого гексаном гідриду навиділення газу. Дають реакційній суміші нагрітися трію (60% у мінеральному маслі, 1,64г, 68,2ммоль) до температури навколишнього середовища, і пеу безводному ТГФ (70мл) в атмосфері азоту при ремішують протягом 1год. Гасять реакцію водою кімнатній температурі додають крапля за краплею та діетиловим ефіром. Органічний шар промиварозчин 4-бром-2-крезолу (10,6г, 56,8ммоль) та ють 1-н. розчином гідроксиду натрію і розсолом. метоксиметилброміду (5,6мл, 68,2ммоль) у безвоОрганічний шар сушать над сульфатом натрію, дному ТГФ (30мл). Після перемішування протягом концентрують у вакуумі і очищають флеш18год. суміш розподіляють між розбавленим водхроматографією з елююванням 20% етилацетату в ним розчином бікарбонату натрію та діетиловим гексані, одержуючи Проміжний продукт 8 (3,49г, ефіром. Органічний шар промивають водою і роз53%) у вигляді прозорого масла. 1Н ЯМР (CDCІ3): солом, сушать над безводним сульфатом натрію і 7,23 (s, 2H), 5,10 (s, 4H), 3,46 (s, 6H). концентрують у вакуумі, одержуючи Проміжний продукт 11 (12,74г, 97%) у вигляді прозорого масла. Суспензію гідриду натрію (60% у мінеральному маслі, 3,00г, 74,92ммоль) у безводному ДМФ (50мл) перемішують в атмосфері азоту при 0°С, і крапля за краплею додають розчин метоксигідрохінону (5,00г, 35,67ммоль) в безводному ДМФ (50мл). До цієї суспензії додають крапля за краплею метоксиметилхлорид (5,2мл, 74,92ммоль), при цьому спостерігається додаткове виділення газу. Дають реакційній суміші нагрітися до температури навколишнього середовища, і перемішують протягом 1 год. Гасять реакцію водою та діетиловим ефіром. Органічний шар промивають 1-н. розчином гідроксиду натрію і розсолом. Органічний шар суша ть над сульфатом натрію, концентрують у вакуумі і очищають фле ш-хроматографією з елююванням 20% етилацетату в гексані, одержуючи Проміжний продукт 9 (5,84г, 72%) у вигляді прозорого масла. 1H ЯМР (CDCI3): 7,05 (d, J=8,6Гц, 1Н), 6,63 (d, J=2,7Гц, 1Н), 6,55 (dd, J=9,0Гц, 2,7Гц, 1H), 5,14 (s, 2H), 5,12 (s, 2H), 3,86 (s, 3H), 3,51 (s, 3H), 3,47 (s, 3H). Розчин Проміжного продукту 8 (1,00г, 2,81ммоль) охолоджують до -78°С і крапля за краплею додають до нього втор-бутиллітій (1,3Μ розчин у циклогексані, 2,10мл, 2,81ммоль). Перемішують суміш протягом 15хв., після чого додають метилйодид (0,18мл, 2,81ммоль) і перемішують протягом ночі, даючи суміші нагріватися до температури навколишнього середовища. Гасять реакцію насиченим розчином бікарбонату натрію і додають етилацетат. Промивають розсолом, сушать органічний шар над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 10% етилацетату в гексані, одержуючи Проміжний продукт 12 (0,66г, 81%) у вигляді прозорого масла. 1Н ЯМР (CDCІ3): 7,12 (d, 3=2,9Гц, 1Н), 6,83 (d, J=2,9Гц, 1H), 5,10 (s, 2H), 5,04 (s, 2H), 3,63 (s, 3H), 3,48 (s, 3H), 2,30 (s, 3H). MS обчислено 291,1; MS (M+1) 291,2, 293,2. 25 77986 Цей синтез проводять, [як описано в J. Org. Chem. 57, 1992, 6972-6975]. До розчину метил-2оксоциклопентанкарбоксилату (10,0г, 70,42ммоль) у безводному дихлорметані (300мл), охолодженого до -78°С, додають діізопропілетиламін (61,5мл, 352,1ммоль) та трифторметансульфоновий ангідрид (14,2мл, 84,51ммоль). Перемішують реакційну суміш протягом 16год, даючи їй нагріватися до температури навколишнього середовища. Гасять реакцію водою, і промивають суміш 10% лимонною кислотою, а потім розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 15% етилацетату в гексані, одержуючи Проміжний продукт 13 (12,0г, 63%) у вигляді темного масла, яке використовують без додаткового очищення. 1H ЯМР (CDCI3): 3,79 (s, 3Н), 2,75-2,68 (m, 4Н), 2,03-1,98 (m, 2Н). Проводять за методикою, аналогічною описаній для Проміжного синтезу 13, з тим винятком, що застосовують метил-2-оксо-1циклогептанкарбоксилат (5,00г, 29,37ммоль), і одержують Проміжний продукт 14 (4,34г, 49%) у вигляді темного масла. До розчину метил-2-оксо-5,5-диметилциклопентанкарбоксилату [J. Chem. Soc. 1996, 1539-1540] (0,85г, 5,00ммоль) у безводному дихлорметані (15мл), охолодженого до -78°С, додають при перемішуванні діізопропілетиламін (4,4мл, 25,00ммоль) та трифторметансульфоновий ангідрид (1,0мл, 6,00ммоль). Перемішують реакційну суміш протягом 16год., даючи їй нагріватися до температури навколишнього середовища. Гасять реакцію водою, і промивають суміш 10% лимонною кислотою, а потім розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 15% етилацетату1 в гексані, одержуючи Проміжний продукт 15 (1,16г, 77%) у вигляді темного масла, яке використовують без додаткового очищення. 1Н ЯМР (CDCI3): 3,78 (s, 3Н), 2,64 (t, J=7,1Гц, 2Н), 1,83 (t, J=7,1Гц, 2Н), 1,18 (s, 6H). 26 До розчину метил-2-оксо-5,5-діетилциклопентанкарбоксилату [J. Chern. Soc. 1996, 1539-1540] (2,94г, 14,85ммоль) у безводному дихлорметані (100мл), охолодженого до -78°С, додають при перемішуванні діізопропілетиламін (13,0мл, 74,25ммоль) та трифторметансульфоновий ангідрид (3,0мл, 17,82ммоль). Перемішують реакційну суміш протягом 16год., даючи їй нагріватися до температури навколишнього середовища. Гасять реакцію водою, і промивають суміш 10% лимонною кислотою, а потім розсолом. Органічний шар суша ть над сульфатом натрію, концентрують у вакуумі і очищають фле ш-хроматографією з елююванням 15% етилацетату в гексані, одержуючи Проміжний продукт 16 (3,96г, 82%) у вигляді темного масла, яке використовують без додаткового очищення. 1H ЯМР (CDCI3): 3,78 (s, 3Н), 2,60 (t, J=7,4Гц, 7,8Гц, 2Н), 1,83 (t, J=7,8Гц, 7,1Гц, 2Н), 1,46 (q, J=7,4Гц, 7,4Гц, 7,4Гц, 4Н), 0,91 (t, J=7,4Гц, 7,4Гц, 6Н). Розчин Проміжного продукту 1 (0,95г, 4,81ммоль) у безводному ТГФ (25мл) охолоджують до -78°С, і додають до нього трет-бутиллітй (1,7Μ розчин у пентані, 2,8мл, 4,81ммоль). Перемішують суміш протягом 15хв., після чого нагрівають до 0°С. Додають крапля за краплею розчин хлориду цинку (1,0Μ в діетиловому ефірі, 4,8мл, 4,81ммоль), і дають одержаному розчину нагрітися до температури навколишнього середовища. За допомогою канюлі додають цей розчин до розчину Проміжного продукту 13 (0,88г, 3,21ммоль) та тетракіс-(трифенілфосфін)Рd(0) (0,37г, 0,32ммоль) у безводному ТГФ (25мл), і нагрівають одержаний розчин при 50°С протягом 16год. Охолоджують реакційну суміш до температури навколишнього середовища і гасять водою. Додають етилацетат, і промивають одержаний органічний шар насиченим розчином бікарбонату натрію і розсолом. Сушать органічний шар над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 30% етилацетату в гексані, одержуючи Проміжний продукт 17 (0,56г, 55%) у вигляді прозорого масла. 1Н ЯМР (CDCI3): 7,04 (d, J=9,0Гц, 1Н), 6,90 (dd, J=3,lГц, 9,0Гц, 1Н), 6,81 (d, J=3,1Гц, 1H), 5,10 (s, 2H), 5,02 (s, 2H), 3,56 (s, 3H), 3,46 (s, 3H), 3,42 (s, 3H), 2,80 (t, J=8,6Гц, 8,2Гц, 4H), 2,051,95 (m, 2H). MS обчислено 322,2; MS (M+1) 323,1. 27 77986 28 4H), 3,52 (s, 3H), 3,42 (s, 6H), 2,83-2,77 (m, 4H), 2,04-1,99 (m, 2H). MS обчислено 322,1; MS (M+1) 323,1. Розчин Проміжного продукту 2 (2,50г, 12,14ммоль) у безводному ТГФ (40мл) охолоджують до -78°С, і додають до нього трет-бутиллітій (1,7Μ розчин у пентані, 7,9мл, 13,35ммоль). Перемішують суміш протягом 15хв., після чого нагрівають до 0°С. Додають крапля за краплею розчин хлориду цинку (1,0Μ в діетиловому ефірі, 12,1мл, 12,14ммоль), і дають одержаному розчину нагрітися до температури навколишнього середовища. За допомогою канюлі додають цей розчин до розчину Проміжного продукту 13 (3,32г, 12,14ммоль) та тетракіс-(трифенілфосфін)Pd(0) (0,70г, 0,61ммоль) у безводному ТГФ (40мл), і нагрівають одержаний розчин при 50°С протягом 16 год. Охолоджують реакційну суміш до температури навколишнього середовища і гасять водою. Додають етилацетат, і промивають одержаний органічний шар насиченим розчином бікарбонату натрію і розсолом. Сушать органічний шар над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 15% етилацетату в гексані, одержуючи Проміжний продукт 18 (2,87г, 72%) у вигляді прозорого масла. 1Н ЯМР (CDCI3): 7,49 (dd, J=1,9Гц, 8,2Гц, 1Н), 7,37 (d, J=2,3Гц, 1Н), 7,20 (d, J=8,6Гц, 1Н), 5,16 (s, 2H), 3,55 (s, 3H), 3,43 (s, 3H), 2,80 (t, J=7,4Гц, 7,8Гц, 4Н), 2,06-1,98 (m, 2Н). MS обчислено 330,1; MS (M+1) 331,1. Розчин Проміжного продукту 6 (2,49г, 12,57ммоль) у безводному ТГФ (25мл) охолоджують до -78°С, і додають до нього трет-бутиллітій (1,7Μ розчин у пентані, 7,4мл, 12,57ммоль). Перемішують суміш протягом 15хв., після чого нагрівають до 0°С. Додають крапля за краплею розчин хлориду цинку (1,0 Μ в діетиловому ефірі, 12,6мл, 12,57ммоль), і дають одержаному розчину нагрітися до температури навколишнього середовища. За допомогою канюлі додають цей розчин до розчину Проміжного продукту 13 (2,30г, 8,38ммоль) та тетракіс-(трифенілфосфін)Рd(0) (0,48г, 0,41ммоль) у безводному ТГФ (25мл), і нагрівають одержаний розчин при 50°С протягом 16 год. Охолоджують реакційну суміш до температури навколишнього середовища і гасять водою. Додають етилацетат, і промивають одержаний органічний шар насиченим розчином бікарбонату натрію і розсолом. Сушать органічний шар над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 20% етилацетату в гексані, одержуючи Проміжний продукт 19 (1,70г, 41%) у вигляді безбарвного масла. 1Н ЯМР (CDCI3): 7,15 (t, J=8,2Гц, 8,6Гц, 1Н), 6,78 (d, J=8,2Гц, 2Н), 5,09 (bs, Розчин Проміжного продукту 1 (2,00г, 10,13ммоль) у безводному ТГФ (25мл) охолоджують до -78°С, і додають до нього трет-бутиллітій (1,7Μ розчин у пентані, 5,9мл, 10,13ммоль). Перемішують суміш протягом 15хв., після чого нагрівають до 0°С. Додають крапля за краплею розчин хлориду цинку (1,0Μ в діетиловому ефірі, 10,1мл, 10,13ммоль), і дають одержаному розчину нагрітися до температури навколишнього середовища. За допомогою канюлі додають цей розчин до розчину Проміжного продукту 14 (2,04г, 6,75ммоль) та тетракіс-(трифенілфосфін)Рd(0) (0,40г, 0,34ммоль) у безводному ТГФ (25мл), і нагрівають одержаний розчин при 50°С протягом 16год. Охолоджують реакційну суміш до температури навколишнього середовища і гасять водою. Додають етилацетат, і промивають одержаний органічний шар насиченим розчином бікарбонату натрію і розсолом. Сушать органічний шар над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 20% етилацетату в гексані, одержуючи Проміжний продукт 20 (2,13г, 90%) у вигляді безбарвного масла. 1H ЯМР (CDCI3): 6,98 (d, J=9,0Гц, 1H, 6,85 (dd, J=3,1Гц, 9,0Гц, 1Н), 6,65 (d, J=3,1Гц, 1H), 5,10 (s, 4H), 3,45 (s, 3H), 3,44 (s, 3H), 3,38 (s, 3H), 2,56-2,50 (m, 4H), 1,84-1,80 (m, 2H), 1,65-1,60 (m, 4H). MS обчислено 350,1; MS (M+1) 351,1. Розчин Проміжного продукту 9 (2,18г, 9,56ммоль) у безводному ТГФ (40мл) охолоджують до -78°С, і додають до нього трет-бутиллітій (1,7Μ розчин у пентані, 6,2мл, 10,52ммоль). Перемішують суміш протягом 15хв., після чого нагрівають до 0°С. Додають крапля за краплею розчин хлориду цинку (1,0Μ в діетиловому ефірі, 9,6мл, 9,56ммоль), і дають одержаному розчину нагрітися до температури навколишнього середовища. За допомогою канюлі додають цей розчин до розчину Проміжного продукту 13 (2,62г, 9,56ммоль) та тетракіс-(трифенілфосфін)Pd(0) (0,55г, 0,48ммоль) у безводному ТГФ (40мл), і нагрівають одержаний розчин при 50°С протягом 16 год. Охолоджують реакційну суміш до температури навколишнього середовища і гасять водою. Додають етилацетат, і промивають одержаний органічний шар насиченим розчином бікарбонату натрію і розсолом. Сушать органічний шар над сульфатом натрію, концент 29 77986 30 рують у вакуумі і очищають флеш-хроматографією органічний шар над сульфатом натрію, концентз елююванням 20% етилацетату в гексані, одеррують у вакуумі і очищають флеш-хроматографією жуючи Проміжний продукт 21 (0,62г, 18%) у вигляді з елююванням 15% етилацетату в гексані, одербезбарвного масла. 1Н ЯМР (CDCI3): 6,57 (d, жуючи Проміжний продукт 23 (3,30г, 84%) у вигляді J=2,7Гц, 1Н), 6,40 (d, J=2,7Гц, 1H), 5,11 (s, 2H), безбарвного масла. 1H ЯМР (CDCI3): 7,05 (d, 4,89 (s, 2H), 3,81 (s, 3H), 3,58 (s, 3H), 3,47, (s, 3H), J=9,0Гц, 1Н), 6,89 (dd, J=3,1Гц, 9,0Гц, 1Н), 6,62 (d, 3,44 (s, 3H), 2,83-2,77 (m, 4H), 2,03-1,96 (m, 2H). J=2,7Гц, 1H), 5,11 (s, 2H), 5,00 (s, 2H), 3,49 (s, 3H), MS обчислено 352,1; MS (M+1) 353,1. 3,46 (s, 3H), 3,40 (s, 3H), 2,65 (bt, J=7,8Гц, 7,0Гц, 2Н), 1,87 (t, J=7,8Гц, 7,4Гц, 2Н), 1,45-1,38 (m, 4H), 0,90-0,82 (m, 6H). MS обчислено 378,1; MS (M+1) 379,1. Розчин Проміжного продукту 1 (1,13г, 5,71ммоль) у безводному ТГФ (40мл) охолоджують до -78°С, і додають до нього трет-бутиллітій (1,7Μ розчин у пентані, 3,4мл, 5,71ммоль). Перемішують суміш протягом 15хв., після чого нагрівають до 0°С. Додають крапля за краплею розчин хлориду цинку (1,0 Μ в діетиловому е фірі, 5,7мл, 5,71ммоль), і дають одержаному розчину нагрітися до температури навколишнього середовища. За допомогою канюлі додають цей розчин до розчину Проміжного продукту 15 (1,15г, 3,80ммоль) та тетракіс-(трифенілфосфін)Рd(0) (0,55г, 0,48ммоль) у безводному ТГФ (40мл), і нагрівають одержаний розчин при 50°С протягом 16 год. Охолоджують реакційну суміш до температури навколишнього середовища і гасять водою. Додають етилацетат і промивають одержаний органічний шар насиченим розчином бікарбонату натрію і розсолом. Сушать органічний шар над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 15% етилацетату в гексані, одержуючи Проміжний продукт 22 (0,42г, 32%) у вигляді безбарвного масла. 1Н ЯМР (CDCI3): 7,05 (d, J=9,0Гц, 1Н), 6,92 (dd, J=3,1Гц, 9,0Гц, 1Н), 6,62 (d, J=3,1Гц, 1H), 5,11 (s, 2H), 5,01 (s, 2H), 3,49 (s, 3H), 3,46 (s, 3H), 3,40 (s, 3H), 2,70 (t, J=7,0Гц, 7,4Гц, 2Н), 1,86 (t, J=7,4Гц, 7,0Гц, 2Н), 1,59 (bs, 6H). MS обчислено 350,1; MS (M+1) 351,1. Розчин Проміжного продукту 1 (3,64г, 18,38ммоль) у безводному ТГФ (50мл) охолоджують до -78°С, і додають до нього трет-бутиллітій (1,7Μ розчин у пентані, 3,4мл, 5,71ммоль). Перемішують суміш протягом 15хв., після чого нагрівають до 0°С. Додають крапля за краплею розчин хлориду цинку (1,0Μ в діетиловому ефірі, 10,8мл, 18,38ммоль), і дають одержаному розчину нагрітися до температури навколишнього середовища. За допомогою канюлі додають цей розчин до розчину Проміжного продукту 16 (3,96г, 12,25ммоль) та тетракіс-(трифенілфосфін)Рd(0) (0,71г, 0,61ммоль) у безводному ТГФ (50мл), і нагрівають одержаний розчин при 50°С протягом 16год. Охолоджують реакційну суміш до температури навколишнього середовища і гасять водою. Додають етилацетат, і промивають одержаний органічний шар насиченим розчином бікарбонату натрію і розсолом. Сушать Розчин Проміжного продукту 4 (2,43г, 10,51ммоль) у безводному ТГФ (25мл) охолоджують до -78°С, і додають до нього втор-бутиллітій (1,3Μ розчин у циклогексані, 8,9мл, 11,56ммоль). Перемішують суміш протягом 15хв., після чого нагрівають до 0°С. Додають крапля за краплею розчин хлориду цинку (1,0 Μ в діетиловому е фірі, 10,51мл, 10,51ммоль), і дають одержаному розчину нагрітися до температури навколишнього середовища. За допомогою канюлі додають цей розчин до розчину Проміжного продукту 13 (2,88г, 10,51ммоль) та тeтpaкic-(тpифeнiлфocфін)Pd(0) (0,60г, 0,52ммоль) у ТГФ (25мл), і нагрівають одержаний розчин при 50°С протягом 16год. Охолоджують реакційну суміш до температури навколишнього середовища і гасять водою. Додають етилацетат, і промивають одержаний органічний шар насиченим розчином бікарбонату натрію і розсолом. Сушать органічний шар над сульфатом натрію, концентрують у вакуумі і очищають флешхроматографією з елююванням 20% етилацетату в гексані, одержуючи Проміжний продукт 24 (1,07г, 26%) у вигляді масла світло-жовтого кольору. 1 Н ЯМР (CDCI3): 7,05 (bs, 2Н), 6,95 (bs, 1Н), 5,10 (s, 2H), 3,59 (s, 3H), 3,48 (s, 3H), 2,85 (t, J=7,0Гц, 7,0Гц, 4H), 2,32 (s, ЗН), 2,06-1,99 (m, 2H). MS обчислено 276,1; MS (M+1) 277,1. Розчин Проміжного продукту 5 (2,60г, 11,06ммоль) у безводному ТГФ (25мл) охолоджують до -78°С, і додають до нього втор-бутиллітій (1,3Μ розчин у циклогексані, 9,3мл, 12,16ммоль). Перемішують суміш протягом 15хв., після чого нагрівають до 0°С. Додають крапля за краплею розчин хлориду цинку (1,0 Μ в діетиловому е фірі, 11,0мл, 11,06ммоль), і даюгь одержаному розчину нагрітися до температури навколишнього середовища. За допомогою канюлі додають цей розчин до розчину Проміжного продукту 13 (3,03г, 11,06ммоль) та тетракіс-(трифенілфосфін)Рd(0) (0,63г, 0,50ммоль) у ТГФ (25мл), і нагрівають одержаний розчин при 50°С протягом 16год. Охолоджують реакційну суміш до температури навколишнього середовища і гасять водою. Додають 31 77986 32 етилацетат, і промивають одержаний органічний (0,24г, 0,21ммоль) у ТГФ (20мл), і нагрівають одешар насиченим розчином бікарбонату натрію і ржаний розчин при 50°С протягом 16год. Охолорозсолом. Сушать органічний шар над сульфатом джують реакційну суміш до температури навколинатрію, концентрують у вакуумі і очищають флешшнього середовища і гасять водою. Додають хроматографією з елююванням 15% етилацетату в етилацетат, і промивають одержаний органічний гексані, одержуючи Проміжний продукт 25 (1,49г, шар насиченим розчином бікарбонату натрію і 48%) у вигляді масла світло-жовтого кольору. 1H розсолом. Сушать органічний шар над сульфатом ЯМР (CDCI3): 7,07-7,04 (m, 1Н), 6,93-6,90 (m, 1H), натрію, концентрують у вакуумі і очищають флеш6,82 (dd, J=3,1Гц, 9,0Гц, 1H), 5,05 (s, 2H), 3,56 (s, хроматографією з елююванням 20% етилацетату в 3H), 3,42 (s, 3H), 2,82-2,78 (m, 4H), 2,03-1,96 (m, гексані, одержуючи Проміжний продукт 27 (0,54г, 2H). MS обчислено 280,1; MS (M+1) 281,1. 38%) у вигляді безбарвного масла. 1Н ЯМР (CDCI3): 6,80 (d, J=2,4Гц, 1Н), 6,61 (d, J=2,3Гц, 1H), 5,09 (s, 2H), 4,79 (s, 2H), 3,57 (s, 3H), 3,48 (s, 3H), 3,46 (s, 3H), 2,83-2,76 (m, 4H), 2,29 (s, 3H), 2,021,96 (m, 2H). MS обчислено 336,2; MS (M+1) 337,2. Розчин Проміжного продукту 7 (2,46г, 8,88ммоль) у безводному ТГФ (25мл) охолоджують до -78°С, і додають до нього втор-бутиллітій (1,3Μ розчин у циклогексані, 6,8мл, 8,88ммоль). Перемішують суміш протягом 15хв., після чого нагрівають до 0°С. Додають крапля за краплею розчин хлориду цинку (1,0 Μ в діетиловому е фірі, 8,9мл, 8,88ммоль), і дають одержаному розчину нагрітися до температури навколишнього середовища. За допомогою канюлі додають цей розчин до розчину Проміжного продукту 13 (1,60г, 5,86ммоль) та тетракіс-(трифенілфосфін)Рd(0) (0,51г, 0,44ммоль) у ТГФ (25мл), і нагрівають одержаний розчин при 50°С протягом 16год. Охолоджують реакційну суміш до температури навколишнього середовища і гасять водою. Додають етилацетат, і промивають одержаний органічний шар насиченим розчином бікарбонату натрію і розсолом. Сушать органічний шар над сульфатом натрію, концентрують у вакуумі і очищають флешхроматографією з елююванням 20% етилацетату в гексані, одержуючи Проміжний продукт 26 (1,20г, 42%) у вигляді безбарвного масла. 1Н ЯМР (CDCI3): 7,05 (d, J=8,6Гц, 1Н), 6,81 (d, J=2,0Гц, 1Н), 6,69 (dd, J=2,3Гц, 8,6Гц, 1Н), 5,15 (s, 2H), 5,09 (s, 2H), 3,58 (s, 3H), 3,48 (s, 3H), 3,43 (s, 3H), 2,79 (t, J=7,0Гц, 7,4Гц, 4H), 2,04-1,95 (m, 2H). MS обчислено 322,2; MS (M+1) 323,1. Розчин Проміжного продукту 10 (2,00г, 11,90ммоль) у безводному ТГФ (20мл) охолоджують до -78°С, і додають до нього втор-бутиллітій (1,3Μ розчин у циклогексані, 7,7мл, 13,09ммоль). Перемішують суміш протягом 15хв., після чого нагрівають до 0°С. Додають крапля за краплею розчин хлориду цинку (1,0 Μ в діетиловому е фірі, 11,9мл, 11,90ммоль), і дають одержаному розчину нагрітися до температури навколишнього середовища. За допомогою канюлі додають цей розчин до розчину Проміжного продукту 13 (3,26г, 11,90ммоль) та тeтpaкic-(тpифeнiлфocфiн)Pd(0) (0,69г, 0,58ммоль) у ТГФ (20мл) і нагрівають одержаний розчин при 50°С протягом 16год. Охолоджують реакційну суміш до температури навколишнього середовища і гасять водою. Додають етилацетат, і промивають одержаний органічний шар насиченим розчином бікарбонату натрію і розсолом. Сушать органічний шар над сульфатом натрію, концентрують у вакуумі і очищають флекіхроматографією з елююванням 20% етилацетату в гексані, одержуючи вказану в заголовку сполуку (1,28г, 38%) у вигляді безбарвного масла, яке, за даними ЯМР, являє собою суміш регіоізомерів. MS обчислено 292,1; MS (M+1) 293,1. Розчин Проміжного продукту 12 (1,24г, 4,26ммоль) у безводному ТГФ (20мл) охолоджують до -78°С, і додають до нього втор-бутиллітій (1,3М розчин у циклогексані, 3,3мл, 4,26ммоль). Перемішують суміш протягом 15хв., після чого нагрівають до 0°С. Додають крапля за краплею розчин хлориду цинку (1,0 Μ в діетиловому е фірі, 4,3мл, 4,26ммоль), і дають одержаному розчину нагрітися до температури навколишнього середовища. За допомогою канюлі додають цей розчин до розчину Проміжного продукту 13 (1,17г, 4,26ммоль) та тeтpaкic-(тpифeнiлфocф1Н)Pd(0) До суспензії 5% паладію на вугіллі (0,27г) в метанолі (15мл) додають розчин Проміжного продукту 17 (0,27г, 0,84ммоль) у метанолі (10мл). Суміш витримують при струшуванні в апараті Парра під тиском водню (60 фунтів на кв. дюйм, 414кПа) при 40°С протягом 12год. Продувають реакційну суміш азотом, і фільтрують через шар целіту. Фільтрат концентрують у вакуумі і очищають флешхроматографією з елююванням 30% етилацетату в гексані, одержуючи Проміжний продукт 29 (0,20г, 75%) у вигляді прозорого масла. 1Н ЯМР (CDCI3): 6,98 (d, J=8,6Гц, 1Н), 6,86 (d, J=3,lГц, 1Н), 6,81 (dd, J=3,1Гц, 9,0Гц, 1H), 5,1 (s, 2H), 5,08 (s, 2H), 3,64 33 77986 34 3,59 (m, 1H), 3,50 (s, 3H), 3,45 (s, 3H), 3,39-3,30 (m, трують через шар целіту. Фільтрат концентрують у 1H), 3,19 (s, 3H), 2,12-1,98 (m, 4H), 1,93-1,82 (m, вакуумі і очищають флеш-хроматографією з елю1H), 1,72-1,63 (m, 1H). MS обчислено 324,2; MS юванням 30% етилацетату в гексані, одержуючи (M+1) 325,2. Проміжний продукт 32 (1,01г, 77%) у вигляді прозорого масла. MS обчислено 282,1; MS (M+1) 283,1. До суспензії 5% паладію на вугіллі (0,19г) в суміші метанолу (50мл) з триетиламіном (1,0мл) додають розчин Проміжного продукту 18 (1,51г, 4,58ммоль) у метанолі (10мл). Суміш витримують при струшуванні в апараті Парра під тиском водню (60 фунтів на кв. дюйм, 414кПа) при 40°С протягом 12год. Продувають реакційну суміш азотом і фільтрують через шар целігу. Фільтрат концентрують у вакуумі і очищають флеш-хроматографією з елююванням 30% етилацетату в гексані, одержуючи Проміжний продукт 30 (0,95г, 63%) у вигляді прозорого масла. 1Н ЯМР (CDCI3): 7,42 (m, 2H), 7,15 (d, J=9,0Гц, 1Н), 5,26 (s, 2H), 3,65-3,62 (m, 1H), 3,51 (s, 3H), 3,35-3,31 (m, 1Н), 3,15 (s, 3H), 2,16-2,00 (m, 4H), 1,90-1,86 (m, 1H), 1,70-1,68 (m, 1H). MS обчислено 332,1; MS (M+1) 333,1. До суспензії 5% паладію на вугіллі (0,13г) в суміші метанолу (50мл) з триетиламіном (1,0мл) додають розчин Проміжного продукту 24 (1,07г, 3,88ммоль) у метанолі (10мл). Суміш витримують при струшуванні в апараті Парра під тиском водню (60 фунтів на кв. дюйм, 414кПа) при 40°С протягом 12год. Продувають реакційну суміш азотом і фільтрують через шар целіту. Фільтрат концентрують у вакуумі і очищають флеш-хроматографією з елююванням 30% етилацетату в гексані, одержуючи Проміжний продукт 31 (0,72г, 67%) у вигляді прозорого масла. 1Н ЯМР (CDCI3): 6,96-6,93 (m, 3Н), 5,17 (s, 2Н), 3,67-3,60 (m, 1Н), 3,50 (s, 3Н), 3,343,28 (m, 1Н), 3,15 (s, 3Н), 2,25 (s, ЗН), 2,15-1,99 (m, 4Н), 1,90-1,83 (m, 1Н), 1,70-1,63 (m, 1Н). MS обчислено 294,1; MS (M+1) 295,1. До суспензії 5% паладію на вугіллі (0,24г) в суміші метанолу (50мл) із триетиламіном (1,0мл) додають розчин Проміжного продукту 25 (1,31г, 4,68ммоль) у метанолі (10мл). Суміш витримують при струшуванні в апараті Парра під тиском водню (60 фунтів на кв. дюйм, 414кПа) при 40°С протягом 12год. Продувають реакційну суміш азотом і філь До суспензії 5% паладію на вугіллі (0,34г) в метанолі (50мл) додають розчин Проміжного продукту 19 (1,70г, 5,28ммоль) у метанолі (10мл). Суміш витримують при струшуванні в апараті Парра під тиском водню (60 фунтів на кв. дюйм, 414кПа) при 40°С протягом 12год. Продувають реакційну суміш азотом і фільтрують через шар целіту. Фільтрат концентрують у вакуумі і очищають флешхроматографією з елююванням 30% етилацетату в гексані, одержуючи Проміжний продукт 33 (0,99г, 58%) у вигляді прозорого масла. 1Н ЯМР (CDCI3): 7,05 (t, J=8,6Гц, 8,2Гц, 1Н), 6,78 (d, J=8,2Гц, 2Н), 5,11 (dd, J=6,6Гц, 18,4Гц, 4Н), 4Д8-4Д1 (m, 1H), 3,49 (s, 6H), 3,21 (s, 3H), 3,15-3,08 (m, 1Н), 2,282,19 (m, 2Н), 2,03-1,89 (m, ЗН), 1,62-1,50 (m, 1Н). MS обчислено 324,2; MS (M+1) 325,2. До суспензії 5% паладію на вугіллі (0,60г) в метанолі (25мл) додають розчин Проміжного продукту 26 (1,20г, 3,73ммоль) у метанолі (10мл). Суміш витримують при струшуванні в апараті Парра під тиском водню (60 фунтів на кв. дюйм, 414кПа) при 40°С протягом 12год. Продувають реакційну суміш азотом і фільтрують через шар целіту. Фільтрат концентрують у вакуумі і очищають флешхроматографією з елююванням 20% етилацетату в гексані, одержуючи Проміжний продукт 34 (0,82г, 68%) у вигляді прозорого масла. 1Н ЯМР (CDCI3): 7,06 (d, J=8,6Гц, 1Н), 6,77 (d, J=2,3Гц, 1Н), 6,60 (dd, J=2,4Гц, 8,6Гц, 1H), 5,20 (s, 2H), 5,14 (dd, J=6,6Гц, 9,7Гц, 2Н), 3,61-3,54 (m, 1Н), 3,50 (s, 6H), 3,45 (s, 3H), 3,31-3,26 (m, 1H), 2,16-1,94 (m, 4H), 1,86-1,80 (m, 1H), 1,71-1,60 (m, 1H). MS обчислено 324,2; MS (M+1) 325,2. До суспензії 5% паладію на вугіллі (0,25г) в метанолі (25мл) додають розчин Проміжного про 35 77986 36 дукту 27 (0,54г, 1,61ммоль) у метанолі (10мл). СуMS обчислено 354,1; MS (M+1) 355,1. міш витримують при струшуванні в апараті Парра під тиском водню (60 фунтів на кв. дюйм, 414кПа) при 40°С протягом 12год. Продувають реакційну суміш азотом і фільтрують через шар целіту. Фільтрат концентрують у вакуумі і очищають флешхроматографією з елююванням 20% етилацетату в гексані, одержуючи Проміжний продукт 35 (0,49г, 89%) у вигляді прозорого масла. 1Н ЯМР (CDCI3): До суспензії 5% паладію на вугіллі (0,05г) в 6,69 (d, J=2,8Гц, 1Н), 6,65 (d, J=3,lГц, 1H), 5,04 (m, суміші метанолу (50мл) із триетиламіном (1,0мл) додають розчин Проміжного продукту 22 (0,42г, 2H), 4,93 (dd, J=5,9Гц, 16,0Гц, 2H), 3,73-3,67 (m, 1,19ммоль) у метанолі (10мл). Суміш витримують 1H), 3,57 (s, 3H), 3,42 (s, 3H), 3,25-3,19 (m, 4H), при струшуванні в апараті Парра під тиском водню 2,25 (s, 3H), 2,17-2,12 (m, 1H), 2,05-1,85 (m, 4H), 1,70-1,60 (m, 1H). MS обчислено 338,2; MS (M+1) (60 фунтів на кв. дюйм, 414кПа) при 40°С протягом 12год. Продувають реакційну суміш азотом і філь339,2. трують через шар целіту. Фільтрат концентрують у вакуумі і очищають флеш-хроматографією з елююванням 20% етилацетату в гексані, одержуючи Проміжний продукт 38 (0,16г, 38%) у вигляді прозорого масла. 1Н ЯМР (CDCI3): 7,00 (d, J=8,2Гц, 0,5Н), 6,94 (d, J=7,8Гц, 0,5Н), 6,84-6,75 (m, 1,5Н), 6,67 (d, J=3,lГц, 0,5Н), 5,12-5,01 (m, 4H), 3,77 (d, J=9,0Гц, 0,5Н), 3,64 (d, J=11,3Гц, 0,5Н), 3,52 (s, 1,5Н), 3,49 (s, 1,5Н), 3,48-3,43 (s, 4,5Н), 3,35 (s, 1,5Н), 2,55-2,42 (m, 0,5Н), 2,17-2,02 (m, 1Н), 1,95До суспензії 5% паладію на вугіллі (0,38г) в 1,88 (m, 0,5H), 1,81-1,75 (m, 1H), 1,69-1,60 (m, метанолі (35мл) додають розчин Проміжного про0,5H), 1,55-1,50 (m, 0,5H), 1,15 (s, 1,5H), 1,01 (s, дукту 20 (0,75г, 2,14ммоль) у метанолі (10мл). Су1,5H), 0,78 (s, 3H). MS обчислено 352,2; MS (M+1) міш витримують при струшуванні в апараті Парра 353,2. під тиском водню (60 фунтів на кв. дюйм, 414кПа) при 40°С протягом 12год. Продувають реакційну суміш азотом, і фільтрують через шар целіту. Фільтрат концентрують у вакуумі і очищають флешхроматографією з елююванням 20% етилацетату в гексані, одержуючи Проміжний продукт 36 (0,63г, 84%) у вигляді прозорого масла. 1Н ЯМР (CDCI3): 6,95 (d, J=9,0Гц, 1Н), 6,85 (d, J=3,1Гц, 1Н), 6,79 (dd, J=3,1Гц, 9,0Гц, 1H), 5,15 (s, 2H), 5,13-5,05 (m, 2H), 3,56-3,51 (m, 1H), 3,50 (s, 3H), 3,45 (s, 3H), 3,30 (s, 3H), 3,08-3,04 (m, 1H), 2,23-2,17 (m, 1H), 2,04-1,80 (m, 6H), 1,55-1,40 (m, 3H). MS обчислено 352,2; MS (M+1) 353,2. До суспензії 5% паладію на вугіллі (0,08г) в суміші метанолу (50мл) із триетиламіном (1,0мл) додають розчин Проміжного продукту 21 (0,62г, 1,76ммоль) у метанолі (10мл). Суміш витримують при струшуванні в апараті Парра під тиском водню (60 фунтів на кв. дюйм, 414кПа) при 40°С протягом 12год. Продувають реакційну суміш азотом і фільтрують через шар целіту. Фільтрат концентрують у вакуумі і очищають флеш-хроматографією з елююванням 20% етилацетату в гексані, одержуючи Проміжний продукт 37 (0,50г, 81%) у вигляді прозорого масла. 1Н ЯМР (CDCI3): 6,50 (d, J=2,7Гц, 1Н), 6,44 (d, J=2,7Гц, 1H), 5,14-5,05 (m, 4H), 3,80 (m, 4H), 3,58 (s, 3H), 3,46 (s, 3H), 3,25 (m, 4H), 2,152,09 (m, 1H), 2,07-1,90 (m, 4H), 1,72-1,64 (m, 1H). До суспензії 5% паладію на вугіллі (0,58г) в суміші метанолу (50мл) із триетиламіном (1,0мл) додають розчин Проміжного продукту 23 (1,25г, 3,89ммоль) у метанолі (10мл). Суміш витримують при струшуванні в апараті Парра під тиском водню (60 фунтів на кв. дюйм, 414кПа) при 40°С протягом 12год. Продувають реакційну суміш азотом і фільтрують через шар целіту. Фільтрат концентрують у вакуумі і очищають флеш-хроматографією з елююванням 15% етилацетату в гексані, одержуючи Проміжний продукт 39 (0,89г, 72%) у вигляді прозорого масла. MS обчислено 380,2; MS (M+1) 381,2. До суспензії 5% паладію на вугіллі (0,15г) в суміші метанолу (50мл) із триетиламіном (1,0мл) додають розчин Проміжного продукту 28 (0,58г, 1,80ммоль) у метанолі (10мл). Суміш витримують при струшуванні в апараті Парра під тиском водню (60 фунтів на кв. дюйм, 414кПа) при 40°С протягом 12год. Продувають реакційну суміш азотом і фільтрують через шар целіту. Фільтрат концентрують у 37 77986 38 вакуумі і очищають флеш-хроматографією з елюреакційну масу протягом 30хв. Гасять реакцію наюванням 15% етилацетату в гексані, одержуючи сиченим розчином хлориду амонію. Додають етиПроміжний продукт 40 (0,25г, 43%) у вигляді пролацетат, і промивають органічний шар розсолом. зорого масла. MS обчислено 294,1; MS (M+1) Органічний шар сушать над сульфатом натрію, 295,1. концентрують у вакуумі і очищають флешхроматографією з елююванням 50% етилацетату в гексані, одержуючи Проміжний продукт 43 (0,36г, 46%) у вигляді прозорого масла, яке використовують без додаткової ідентифікації. Цей синтез проводять за методикою, [описаною в Tetrahedron Letters 36, 31, 1995, 5461-5464]. Суспензію Проміжного продукту 29 (0,50г, 1,54ммоль) та гідрохлориду Ν,Οдиметилгідроксиламіну (0,23г, 2,31ммоль) у безводному ТГФ (25мл) охолоджують до -10°С в бані (сухий лід з ацетоном), додають ізопропілмагнійхлорид (2,0М, 2,3мл, 4,62ммоль), і перемішують реакційну масу протягом 30хв. Гасять реакцію насиченим розчином хлориду амонію. Додають етилацетат, і промивають органічний шар розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флешхроматографією з елююванням 50% етилацетату в гексані, одержуючи Проміжний продукт 41 (0,49г, 90%) у вигляді прозорого масла, яке використовують без додаткової ідентифікації. Суспензію Проміжного продукту 32 (0,98г, 3,48ммоль) та гідрохлориду Ν,Οдиметилгідроксиламіну (0,51г, 5,22ммоль) у безводному ТГФ (40мл) охолоджують до -10°С в бані (сухий лід з ацетоном), додають ізопропілмагнійхлорид (2,0М, 5,2мл, 10,42ммоль), і перемішують реакційну масу протягом 30хв. Гасять реакцію насиченим розчином хлориду амонію. Додають етилацетат, і промивають органічний шар розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флешхроматографією з елююванням 50% етилацетату в гексані, одержуючи Проміжний продукт 44 (0,61г, 56%) у вигляді прозорого масла, яке використовують без додаткової ідентифікації. Суспензію Проміжного продукту 30 (0,95г, 2,86ммоль) та гідрохлориду Ν,Οдиметилгідроксиламіну (0,42г, 4,29ммоль) у безводному ТГФ (40мл) охолоджують до -10°С в бані (сухий лід з ацетоном), додають ізопропілмагнійхлорид (2,0М, 4,3мл, 8,58ммоль), і перемішують реакційну масу протягом 30хв. Гасять реакцію насиченим розчином хлориду амонію. Додають етилацетат, і промивають органічний шар розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флешхроматографією з елююванням 50% етилацетату в гексані, одержуючи Проміжний продукт 42 (0,86г, 83%) у вигляді прозорого масла, яке використовують без додаткової ідентифікації. Суспензію Проміжного продукту 33 (0,97г, 2,99ммоль) та гідрохлориду Ν,Οдиметилгідроксиламіну (0,44г, 4,49ммоль) у безводному ТГФ (40мл) охолоджують до -10°С в бані (сухий лід з ацетоном), додають ізопропілмагнійхлорид (2,0М, 4,5мл, 9,00ммоль), і перемішують реакційну масу протягом 30хв. Гасять реакцію насиченим розчином хлориду амонію. Додають етилацетат, і промивають органічний шар розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флешхроматографією з елююванням 50% етилацетату в гексані, одержуючи Проміжний продукт 45 (0,71г, 67%) у вигляді прозорого масла, яке використовують без додаткової ідентифікації. Суспензію Проміжного продукту 31 (0,71г, 2,55ммоль) та гідрохлориду Ν,Οдиметилгідроксиламіну (0,37г, 3,83ммоль) у безводному ТГФ (40мл) охолоджують до -10°С в бані (сухий лід з ацетоном), додають ізопропілмагнійхлорид (2,0М, 2,5мл, 5,10ммоль), і перемішують Суспензію Проміжного продукту 34 (0,82г, 2,53ммоль) та гідрохлориду Ν,Οдиметилгідроксиламіну (0,37г, 3,80ммоль) у безводному ТГФ (30мл) охолоджують до -10°С в бані 39 77986 40 (сухий лід з ацетоном), додають ізопропілмагнійСуспензію Проміжного продукту 37 (0,50г, хлорид (2,0М, 3,8мл, 7,60ммоль), і перемішують 1,41ммоль) та гідрохлориду Ν,Οреакційну масу протягом 30хв. Гасять реакцію надиметилгідроксиламіну (0,24г, 2,12ммоль) у безсиченим розчином хлориду амонію. Додають етиводному ТГФ (30мл) охолоджують до -10°С в бані лацетат, і промивають органічний шар розсолом. (сухий лід з ацетоном), додають ізопропілмагнійОрганічний шар сушать над сульфатом натрію, хлорид (2,0М, 2,1мл, 4,20ммоль), і перемішують концентрують у вакуумі і очищають флешреакційну масу протягом 30хв. Гасять реакцію нахроматографією з елююванням 50% етилацетату в сиченим розчином хлориду амонію. Додають етигексані, одержуючи Проміжний продукт 46 (0,80г, лацетат, і промивають органічний шар розсолом. 90%) у вигляді прозорого масла, яке використовуОрганічний шар сушать над сульфатом натрію, ють без додаткової ідентифікації. концентрують у вакуумі і очищають флешхроматографією з елююванням 50% етилацетату в гексані, одержуючи Проміжний продукт 49 (0,31г, 57%) у вигляді прозорого масла, яке використовують без додаткової ідентифікації. Суспензію Проміжного продукту 35 (0,48г, 1,42ммоль) та гідрохлориду Ν,Οдиметилгідроксиламіну (0,21г, 2,13ммоль) у безводному ТГФ (20мл) охолоджують до -10°С в бані (сухий лід з ацетоном), додають ізопропілмагнійхлорид (2,0М, 2,1мл, 4,20ммоль), і перемішують реакційну масу протягом 30 хв. Гасять реакцію насиченим розчином хлориду амонію. Додають етилацетат, і промивають органічний шар розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флешхроматографією з елююванням 50% етилацетату в гексані, одержуючи Проміжний продукт 47 (0,46г, 88%) у вигляді прозорого масла, яке використовують без додаткової ідентифікації. Суспензію Проміжного продукту 36 (0,63г, 2,53ммоль) та гідрохлориду Ν,Οдиметилгідроксиламіну (0,26г, 2,68ммоль) у безводному ТГФ (30мл) охолоджують до -10°С в бані (сухий лід з ацетоном), додають ізопропілмагнійхлорид (2,0М, 2,7мл, 5,40ммоль), і перемішують реакційну масу протягом 30хв. Гасять реакцію насиченим розчином хлориду амонію. Додають етилацетат і промивають органічний шар розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флешхроматографією з елююванням 50% етилацетату в гексані, одержуючи Проміжний продукт 48 (0,54г, 76%) у вигляді прозорого масла, яке використовують без додаткової ідентифікації. Суспензію Проміжного продукту 38 (0,16г, 0,45ммоль) та гідрохлориду Ν,Οдиметилгідроксиламіну (0,07г, 0,68ммоль) у безводному ТГФ (10мл) охолоджують до -10°С в бані (сухий лід з ацетоном), додають ізопропілмагнійхлорид (2,0М, 0,7мл, 1,40ммоль), і перемішують реакційну масу протягом 30 хв. Гасять реакцію насиченим розчином хлориду амонію. Додають етилацетат, і промивають органічний шар розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флешхроматографією з елююванням 50% етилацетату в гексані, одержуючи Проміжний продукт 50 (0,15г, 87%) у вигляді прозорого масла, яке використовують без додаткової ідентифікації. Суспензію Проміжного продукту 39 (0,25г, 0,77ммоль) та гідрохлориду Ν,Οдиметилгідроксиламіну (0,11г, 1,16ммоль) у безводному ТГФ (20мл) охолоджують до -10°С в бані (сухий лід з ацетоном), додають ізопропілмагнійхлорид (2,0М, 1,2мл, 2,40ммоль), і перемішують реакційну масу протягом 30 хв. Гасять реакцію насиченим розчином хлориду амонію. Додають етилацетат, і промивають органічний шар розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флешхроматографією з елююванням 50% етилацетату в гексані, одержуючи Проміжний продукт 51 (0,20г, 74%) у вигляді прозорого масла, яке використовують без додаткової ідентифікації. 41 77986 42 Суспензію Проміжного продукту 40 (0,91г, над сульфатом натрію, концентрують у вакуумі і 3,07ммоль) та гідрохлориду Ν,Οочищають флеш-хроматографією з елююванням диметилгідроксиламіну (0,45г, 4,64ммоль) у без30% етилацетату в гексані, одержуючи Проміжний водному ТГФ (20мл) охолоджують до -10°С в бані продукт 55 (7,11г, 97%) у вигляді безбарвної піни. 1 (сухий лід з ацетоном), додають ізопропілмагнійН ЯМР (CDCI3): 7,61 (d, J=8,6Гц, 2Н), 6,83 (d, хлорид (2,0М, 3,1мл, 6,20ммоль), і перемішують J=8,6Гц, 2Н), 6,76 (d, J=2,7Гц, 1Н), 6,71 (d, J=8,7Гц, реакційну масу протягом 30хв. Гасять реакцію на1Н), 6,60 (dd, J=2,7Гц, 8,6Гц, 1H), 5,18 (s, 2H), 5,08сиченим розчином хлориду амонію. Додають ети4,95 (m, 4H), 4,27-4,23 (m, 1H), 3,83-3,79 (m, 1H), лацетат, і промивають органічний шар розсолом. 3,43 (s, 3H), 3,40 (s, 3H), 3,39 (s, 3H), 2,25-1,93 (m, Органічний шар сушать над сульфатом натрію, 5H), 1,79-1,70 (m, 1H). концентруютьу вакуумі і очищають флешхроматографією з елююванням 50% етилацетату в гексані, одержуючи Проміжний продукт 52 (0,36г, 36%) у вигляді прозорого масла, яке використовують без додаткової ідентифікації. Суспензію гідриду натрію (60% у мінеральному маслі, 2,54г, 63,58ммоль) у безводному ДМФ (50мл) охолоджують в атмосфері азоту до 0°С і крапля за краплею додають до неї розчин 4бромфенолу (10,00г, 57,80ммоль) у безводному ДМФ (50мл). До одержаної суспензії додають крапля за краплею метоксиметилхлорид (4,8мл, 63,58ммоль). Нагрівають реакційну суміш до температури навколишнього середовища і перемішують протягом 1год. Гасять реакцію водою та діетиловим ефіром. Органічний шар промивають 1-н. розчином гідроксиду натрію і розсолом. Органічний шар сушать над суль фатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 10% етилацетату в гексані, одержуючи Проміжний продукт 53 (10,42г, 83%) у вигляді прозорого масла. 1Н ЯМР (CDCI3): 7,38 (d, J=8,8Гц, 2Н), 6,93 (d, J=8,7Гц, 2Н), 5,14 (s, 2Н), 3,43 (s, 3Н). Розчин Проміжного продукту 53 (3,03г, 14,00ммоль) у безводному ТГФ (40мл) охолоджують до -78°С в атмосфері азоту і крапля за краплею додають до нього втор-бутиллітій (1,3Μ в циклогексані, 10,7мл, 14,00ммоль). Перемішують розчин при -78°С протягом 30хв., і одержують розчин з концентрацією 0,40М. Використовують негайно, підтримуючи температуру -78°С. Проміжний продукт 54 (0,40Μ, 42,5мл, 17,00ммоль) додають при 0°С до розчину Проміжного продукту 41 (6,00г, 17,00ммоль) в безводному ТГФ (50мл), і одержаний розчин перемішують протягом 30хв. при 0°С. Гасять реакцію насиченим розчином бікарбонату натрію. Додають етилацетат і промивають розсолом. Органічний шар сушать Проміжний продукт 54 (0,40Μ, 8,9мл, 3,57ммоль) додають при 0°С до розчину Проміжного продукту 42 (0,86г, 2,38ммоль) в безводному ТГФ (50мл), і одержаний розчин перемішують протягом 30хв. при 0°С. Гасять реакцію насиченим розчином бікарбонату натрію. Додають етилацетат і промивають розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 20% етилацетату в гексані, одержуючи Проміжний продукт 56 (1,03г, 99%) у вигляді прозорого масла. Проміжний продукт 54 (0,40Μ, 6,1мл, 2,34ммоль) додають при 0°С до розчину Проміжного продукту 43 (0,36г, 1,17ммоль) в безводному ТГФ (20мл), і одержаний розчин перемішують протягом 30хв. при 0°С. Гасять реакцію насиченим розчином бікарбонату натрію. Додають етилацетат і промивають розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 30% етилацетату в гексані, одержуючи Проміжний продукт 57 (0,41г, 92%) у вигляді прозорого масла. 1 Н ЯМР (CDCI3): 7,61 (d, J=7,4Гц, 2Н), 6,92-6,81 (m, 3Н), 6,76-6,65 (m, 2Н), 5,15 (s, 2Н), 4,93 (m, 2Н), 4,29-4,23 (m, 1Н), 3,82-3,76 (m, 1H), 3,45 (s, 3H), 3,40 (s, 3H), 2,23-1,92 (m, 8H), 1,80-1,69 (m, 1H). 43 77986 44 Проміжний продукт 54 (0,40Μ, 9,8мл, продукт 60 (0,87г, 90%) у вигляді прозорого масла. 1 3,92ммоль) додають при 0°С до розчину ПроміжН ЯМР (CDCI3): 7,61 (d, J=8,6Гц, 2Н), 6,99-6,96 (m, ного продукту 44 (0,61г, 1,96ммоль) в безводному 1Н), 6,86 (d, J=8,7Гц, 2H), 6,50-6,46 (m, 2H), 5,15 (s, ТГФ (20мл), і одержаний розчин перемішують про2H), 5,40-4,97 (m, 2H), 4,92 (s, 2H), 4,26-4,21 (m, тягом 30хв. при 0°С. Гасять реакцію насиченим 1Н), 3,80-3,74 (m, 1H), 3,44 (s, 3H), 3,40 (s, 3H), розчином бікарбонату натрію. Додають етилацетат 3,38 (s, 3H), 2,24-1,90 (m, 5H), 1,79-1,71 (m, 1H). і промивають розсолом. Органічний шар сушать MS обчислено 430,2; MS (M+1) 431,2. над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 30% етилацетату в гексані, одержуючи Проміжний продукт 58 (0,59г, 92%) у вигляді прозорого масла. 1 Н ЯМР (CDCI3): 7,61 (d, J=7,4Гц, 2Н), 6,92-6,80 (m, 3Н), 6,78-6,72 (m, 1Н), 6,63-6,59 (m, 1H), 5,17 (dd, J=6,6Гц, 9,4Гц, 2Н), 4,90 (dd, J=4,5Гц, 6,6Гц, 2H), 4,30-4,26 (m, 1Н), 3,80-3,75 (m, 1H), 3,43 (s, 3H), 3,39 (s, 3H), 2,20-1,91 (m, 5H), 1,80-1,70 (m, 1H). Проміжний продукт 54 (0,40Μ, 7,5мл, 3,03ммоль) додають при 0°С до розчину Проміжного продукту 45 (0,71г, 2,01ммоль) в безводному ТГФ (20мл), і одержаний розчин перемішують протягом 30хв. при 0°С. Гасять реакцію насиченим розчином бікарбонату натрію. Додають етилацетат і промивають розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 30% етилацетату в гексані, одержуючи Проміжний продукт 59 (0,80г, 93%) у вигляді прозорого масла. 1 Н ЯМР (CDCI3): 7,55 (d, J=7,0Гц, 2Н), 6,80-6,75 (m, 3Н), 6,48 (d, J=8,2Гц, 2Н), 5,15-5,06 (m, 2H), 4,96 (s, 4H), 4,39-4,31 (m, 1Н), 3,80-3,76 (m, 1H), 3,46 (s, 6H), 3,40 (s, 3H), 2,55-2,45 (m, 1H), 2,30-2,20 (m, 1H), 2,15-2,05 (m, 1H), 1,96-1,85 (m, 2H), 1,70-1,60 (m, 1H). MS обчислено 430,2; MS (M+1) 431,2. Проміжний продукт 54 (0,40Μ, 8,5мл, 3,40ммоль) додають при 0°С до розчину Проміжного продукту 46 (0,80г, 2,26ммоль) в безводному ТГФ (20мл), і одержаний розчин перемішують протягом 30хв. при 0°С. Гасять реакцію насиченим розчином бікарбонату натрію. Додають етилацетат і промивають розсолом. Органічний шарсушать над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 30% етилацетату в гексані, одержуючи Проміжний Проміжний продукт 54 (0,40Μ, 4,7мл, 1,88ммоль) додають при 0°С до розчину Проміжного продукту 47 (0,46г, 1,25ммоль) в безводному ТГФ (20мл), і одержаний розчин перемішують протягом 30хв. при 0°С. Гасять реакцію насиченим розчином бікарбонату натрію. Додають етилацетат і промивають розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 30% етилацетату в гексані, одержуючи Проміжний продукт 61 (0,43г, 77%) у вигляді прозорого масла. 1 Н ЯМР (CDCI3): 7,61 (d, J=8,6Гц, 2Н), 6,80 (d, J=9,0Гц, 2Н), 6,51 (d, J=2,7Гц, 1Н), 6,41 (d, J=2,7Гц, 1Н), 5,13 (s, 2H), 4,97-4,85 (m, 4H), 4,26-4,21 (m, 1H), 3,85-3,80 (m, 1H), 3,61 (s, 3H), 3,42 (s, 3H), 3,37 (s, 3H), 2,33-2,22 (m, 1H), 2,15-1,89 (m, 7H), 1,80-1,69 (m, 1H). MS обчислено 444,2; MS (M+1) 445,2. Проміжний продукт 54 (0,40Μ, 6,8мл, 2,74ммоль) додають при 0°С до розчину Проміжного продукту 48 (0,54г, 1,37ммоль) в безводному ТГФ (20мл), і одержаний розчин перемішують протягом 30хв. при 0°С. Гасять реакцію насиченим розчином бікарбонату натрію. Додають етилацетат, і промивають розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 30% етилацетату в гексані, одержуючи Проміжний продукт 62 (0,25г, 40%) у вигляді прозорого масла. 1Н ЯМР (CDCI3): 7,55 (d, J=8,6Гц, 2Н), 6,83 (d, J=9,0Гц, 1Н), 6,76-6,72 (m, ЗН), 6,57 (dd, J=3,2Гц, 9,0Гц, 1H), 5,14 (s, 2H), 5,00-4,92 (m, 4H), 4,10-4,03 (m, 1H), 3,70-3,63 (m, 1H), 3,45 (s, 3H), 3,43 (s, 3H), 3,38 (s, 3H), 2,38-2,30 (m, 1H), 2,10-1,82 (m, 8H), 1,55-1,45 (m, 1H). 45 77986 46 тягом 30хв. при 0°С. Гасять реакцію насиченим розчином бікарбонату натрію. Додають етилацетат, і промивають розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 30% етилацетату в гексані, одержуючи Проміжний продукт 65 (0,21г, 86%) у вигляді прозорого масла. Проміжний продукт 54 (0,40Μ, 4,0мл, 1,62ммоль) додають при 0°С до розчину Проміжного продукту 49 (0,31г, 0,81ммоль) в безводному ТГФ (10мл), і одержаний розчин перемішують протягом 30хв. при 0°С. Гасять реакцію насиченим розчином бікарбонату натрію. Додають етилацетат, і промивають розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 30% етилацетату в гексані, одержуючи Проміжний продукт 63 (0,12г, 32%) у вигляді прозорого масла. 1Н ЯМР (CDCI3): 7,65 (d, J=8,0Гц, 2Н), 6,99-6,96 (m, 1H), 6,80 (d, J=8,0Гц, 2Н), 6,29 (d, J=2,7Гц, 1Н), 6,23 (d, J=2,7Гц, 1Н), 5,13 (s, 2H), 5,02-4,89 (m, 4H), 4,24-4,19 (m, 1H), 3,94-3,89 (m, 1H), 3,67 (s, 3H), 3,60 (s, 3H), 3,44 (s, 3H), 3,39 (s, 3H), 2,30-2,27 (m, 1H), 2,13-2,02 (m, 1H), 1,99-1,90 (m, 2H), 1,80-1,74 (m, 1H). Проміжний продукт 54 (0,40Μ, 1,5мл, 0,59ммоль) додають при 0°С до розчину Проміжного продукту 50 (0,15г, 0,39ммоль) в безводному ТГФ (10мл), і одержаний розчин перемішують протягом 30хв. при 0°С. Гасять реакцію насиченим розчином бікарбонату натрію. Додають етилацетат, і промивають розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 30% етилацетату в гексані, одержуючи Проміжний продукт 64 (50мг, 28%) у вигляді прозорого масла. Проміжний продукт 54 (0,40Μ, 2,1мл, 0,85ммоль) додають при 0°С до розчину Проміжного продукту 51 (0,20г, 0,57ммоль) в безводному ТГФ (10мл), і одержаний розчин перемішують про Проміжний продукт 54 (0,40М, 5,5мл, 2,22ммоль додають при 0°С до розчину Проміжного продукту 52 (0,36г, 1,11ммоль) в безводному ТГФ (20мл), і одержаний розчин перемішують протягом 30хв. при 0°С. Гасять реакцію насиченим розчином бікарбонату натрію. Додають етилацетат, і промивають розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією з елююванням 50% етилацетату в гексані, одержуючи Проміжний продукт 66 (0,41г, 92%) у вигляді прозорого масла. До розчину 0,92г (2,8ммоль) Проміжного продукту 11 в 10мл ТГФ додають при -78°С 3,4мл (5,6ммоль) 1,7Μ розчину трет-бутиллітію. Одержану суміш додають за допомогою канюлі при -78°С до розчину 0,7г (2,0ммоль) Проміжного продукту 41 в 10мл безводного ТГФ при перемішуванні магнітною мішалкою, і дають суміші нагрітися до кімнатної температури. Через 5год. суміш розподіляють між діетиловим ефіром і насиченим водним розчином бікарбонату натрію. Органічний шар промивають водою і розсолом, сушать над сульфатом натрію, концентрують у вакуумі і очищають флеш-хроматографією на силікагелі з елююванням 10% етилацетату в гексані, одержуючи Проміжний продукт 67 (0,51г, 57%). Спектр 1Н-ЯМР продукту (в CDCI3) містить сигнал арилметильного синглету при 2,13млн-1, і продукт використовують без додаткової обробки. 47 77986 48 До розчину 0,70г (3,0ммоль) 4-бром-Ометоксиметил-м-крезолу в 10мл ТГФ додають при -78°С 3,6мл (6,1ммоль) 1,7 Μ розчину третбутиллітію. Одержану суміш додають за допомогою канюлі при -78°С до розчину 0,98г (2,77ммоль) Проміжного продукту 41 в 10мл безводного ТГФ Із застосуванням стандартного обладнання при перемішуванні магнітною мішалкою, і дають для HPLC хроматографують продукт за Прикласуміші нагрітися до кімнатної температури. Через 5год. суміш розподіляють між діетиловим ефіром і дом 1 (3,51г, колонка ChiralpakAD 8´32см, елюент насиченим водним розчином бікарбонату натрію. 80% гептану в ізопропіловому спирті, 350мл/хв, Органічний шар промивають водою і розсолом, детектування на довжині хвилі 252нм). Після консушать над сульфатом натрію, концентрують у центрування чистих фракцій одержують ізомери вакуумі і очищають флеш-хроматографією на си(S,S,S) (1,67г, ее 99,9%, час затримання 6,9хв.) та лікагелі з елююванням 10% етилацетату в гексані (R,R,R) (1,71г, ее 98,9%, час затримання 9,3хв.) у з домішкою 0,1% триетиламіну, одержуючи Промівигляді білих пін. жний продукт 68 (0,31г, 25%). 1Н Я МР (CDCI3): 7,39 Приклад 2 (d, J=9,5Гц, 1Н), 6,83 (s, 1H), 6,70 (dd, J=9,5Гц, Одержання (+)-2-(4-гідроксифеніл)-62,5Гц, 1H), 6,68 (s, 1H), 6,61 (d, J=2,5Гц, 1H), 5,15трифторметил-циклопентил[с]3,4-дигідро-2Н-14,98 (m, 4H), 4,76 (d, J=6,3Гц, 1H), 4,65 (d, J=6,4Гц, бензопірану 1H), 4,24 (m, 1H), 3,68 (m, 1H), 3,47 (m, 1H), 3,44 (s, 3H), 3,43 (s, 3H), 3,30 (s, 3H), 2,00 (s, 3H), 2,28-1,88 (m, 4H), 1,74 (m, 1H). Приклад 1 Одержання (+)-2-(4-гідроксифеніл)-6-гідроксициклопентил[с]3,4-дигідро-2Н-1-бензопірану До розчину Проміжного продукту 56 (1,03г, До розчину Проміжного продукту 55 (7,10г, 16,51ммоль) в безводному метанолі (200мл) додають n-толуолсульфокислоту (1,04г, 16,51ммоль), і нагрівають одержаний розчин при 50°С протягом 18год. Охолоджують реакційну суміш до температури навколишнього середовища і додають до неї бромкрезоловий зелений (10мг) та ціанборгідрид натрію (5,18г, 82,55ммоль). Додають крапля за краплею метанол, насичений НСl (газоподібним), до одержання стійкого жовтого кольору суміші. Після досягнення остаточної зміни кольору суміш перемішують ще протягом 1 год. Реакцію гасять насиченим розчином бікарбонату натрію, додають до суміші етилацетат, і промивають органічний шар розчином бікарбонату натрію та розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і піддають флешхроматографії з елююванням 10% діетилового ефіру в ди хлорметані. Одержаний продукт повторно розчиняють у діетиловому ефірі (приблизно 2мл), осаджують дихлорметаном і фільтрують, одержуючи сполуку за Прикладом 1 (2,10г, 45%) у вигляді масла світло-пурпурового кольору. 1Н ЯМР (d6-DMSO): 9,28 (s, 1Н), 8,80 (s, 1Н), 7,20 (d, J=8,6Гц, 2Н), 6,73 (d, J=8,6Гц, 2Н), 6,61 (d, J=8,7Гц, 1Н), 6,53 (d, J=2,7Гц, 1Н), 6,45 (dd, J=2,7Гц, 8,5Гц, 1H), 4,92 (d, J=2,0Гц, 1H), 3,38-3,32 (m, 1H), 2,532,47 (m, 1H), 2,07-2,02 (m, 1H), 1,65-1,59 (m, 1H), 1,45-1,22 (m, 4H). MS обчислено 282.1; MS (M-1) 281,1. Приклад 1А Одержання (2R,3R,4R)-(4гідроксифеніл)-6-гідрокси-циклопентил[с]3,4дигідро-2Н-1-бензопірану та (2S,3S,4S)-(4-гідроксиФеніл)-6-гідроксициклопентил[с]3,4-дигідро-2Н-1-бензопірану 2,35ммоль) в безводному метанолі (40мл) додають n-толуолсульфокислоту (0,11г, 1,76ммоль), і нагрівають одержаний розчин при 50°С протягом 18год. Охолоджують реакційну суміш до температури навколишнього середовища, і додають до неї бромкрезоловий зелений (10мг) та ціанборгідрид натрію (0,74г, 11,75ммоль). Додають крапля за краплею метанол, насичений НСl (газоподібним), до одержання стійкого жовтого кольору суміші. Після досягнення остаточної зміни кольору суміш перемішують ще протягом 1год. Реакцію гасять насиченим розчином бікарбонату натрію, додають до суміші етилацетат і промивають органічний шар розчином бікарбонату натрію та розсолом. Органічний шар сушать над суль фатом натрію, концентрують у вакуумі і піддають флеш-хроматографії з елююванням 20% етилацетату в гексані, одержуючи сполуку за Прикладом 2 (0,38г, 48%) у вигляді масла світло-рожевого кольору. 1H ЯМР (d6DMSO): 9,37 (s, 1Н), 7,54 (d, J=1,9Гц, 1Н), 7,40 (dd, J=1,9Гц, 8,6Гц, 1Н), 7,24 (d, J=8,2Гц, 2Н), 7,00 (d, J=8,6Гц, 1Н), 6,74 (d, J=8,2Гц, 2H), 5,17 (d, J=2,0Гц, 1Н), 3,53 (t, J=7,4Гц, 6,6Гц, 1Н), 2,65-2,62 (m, 1H), 2,18-2,10 (m, 1H), 1,78-1,72 (m, 1H), 1,46-1,29 (m, 4H). MS обчислено 334,1; MS (M-1) 333,1. Приклад 3 Одержання (+)-2-(4-гідроксифеніл)-6-метилциклопентил[с]3,4-дигідро-2Н-1-бензопірану До розчину Проміжного продукту 57 (0,40г, 1,04ммоль) в безводному метанолі (50мл) додають n-толуолсульфокислоту (0,05г, 0,78ммоль), і нагрівають одержаний розчин при 50°С протягом 18год. Охолоджують реакційну суміш до температури навколишнього середовища, і додають до неї бромкрезоловий зелений (10мг) та ціанборгідрид 49 77986 50 натрію (0,33г, 5,20ммоль). Додають крапля за кранагрівають одержаний розчин при 50°С протягом плею метанол, насичений НСl (газоподібним), до 18год. Охолоджують реакційну суміш до темпераодержання стійкого жовтого кольору суміші. Після тури навколишнього середовища, і додають до неї досягнення остаточної зміни кольору суміш перебромкрезоловий зелений (10мг) та ціанборгідрид мішують ще протягом 1год. Реакцію гасять насинатрію (0,58г, 9,30ммоль). Додають крапля за краченим розчином бікарбонату натрію, додають до плею метанол, насичений НСl (газоподібним), до суміші етилацетат, і промивають органічний шар одержання стійкого жовтого кольору суміші. Після розчином бікарбонату натрію та розсолом. Органідосягнення остаточної зміни кольору суміш перечний шар сушать над суль фатом натрію, концентмішують ще протягом 1год. Реакцію гасять насирують у вакуум і піддають флеш-хроматографії з ченим розчином бікарбонату натрію, додають до елююванням 20% етилацетату в гексані, одержусуміші етилацетат, і промивають органічний шар ючи сполуку за Прикладом 3 (0,21г, 72%) у вигляді розчином бікарбонату натрію та розсолом. Органітвердої речовини світло-пурпурового кольору. !Н чний шар сушать над суль фатом натрію, концентЯМР (CDCI3): 7,33 (d, J=9,0Гц, 2Н), 7,00 (d, рують у вакуумі і піддають флеш-хроматографії з J=1,2Гц, 1Н), 6,92 (dd, J=2,0Гц, 8,2Гц, 1H), 6,87елююванням 5% діетилового ефіру в ди хлормета6,81 (m, 3H), 5,44 (s, 1H), 5,09 (d, J=2,0Гц, 1H), ні, одержуючи сполуку за Прикладом 5 (0,41г, 78%) 3,50-3,46 (m, 1H), 2,61-2,54 (m, 1H), 2,30 (s, 3H), у вигляді твердої речовини світло-рожевого кольо2,20-2,10 (m, 1H), 1,90-1,82 (m, 1H), 1,71-1,60 (m, ру. 1H ЯМР (d6-DMSO): 9,31 (s, 1H), 9,30 (s, 1Н), 1H), 1,57-1,36 (m, 3H). MS обчислено 280,1; MS (M7,20 (d, J=8,2Гц, 2Н), 6,83 (t, J=7,4Гц, 10,0Гц, 1Н), 1) 279,1. 6,75 (d, J=8,6Гц, 2Н), 6,39 (d, J=7,9Гц, 1Н), 6,28 (d, Приклад 4 J=7,9Гц, 1Н), 4,87 (d, J=l,0Гц, 1H), 3,46-3,41 (m, Одержання (+)-2-(4-гідроксифеніл)-6-фтор1H), 2,60-2,56 (m, 1H), 2,14-2,09 (m, 1H), 1,62-1,56 циклопентил[с]3,4-дигідро-2Н-1-бензопірану (m, 1H), 1,51-1,29 (m, 4H). MS обчислено 282,1; MS (M-1) 281,1. Приклад 6 Одержання (+)-2-(4-гідроксифеніл)-7-гідроксициклопентил[с]3,4-дигідро-2Н-1-бензопірану До розчину Проміжного продукту 58 (0,59г, 1,52ммоль) в безводному метанолі (30мл) додають n-толуолсульфокислоту (0,07г, 1,14ммоль), і нагрівають одержаний розчин при 50°С протягом 18год. Охолоджують реакційну суміш до температури навколишнього середовища, і додають до неї бромкрезоловий зелений (10мг) та ціанборгідрид натрію (0,48г, 7,60ммоль). Додають крапля за краплею метанол, насичений НСl (газоподібним), до одержання стійкого жовтого кольору суміші. Після досягнення остаточної зміни кольору суміш перемішують ще протягом 1год. Реакцію гасять насиченим розчином бікарбонату натрію, додають до суміші етилацетат, і промивають органічний шар розчином бікарбонату натрію та розсолом. Органічний шар сушать над суль фатом натрію, концентрують у вакуумі і піддають флеш-хроматографії з елююванням 20% етилацетату в гексані, одержуючи сполуку за Прикладом 4 (0,34г, 79%) у вигляді твердої речовини світло-пурпурового кольору. 1H ЯМР (CDCI3): 7,33 (d, J=8,6Гц, 2Н), 6,88-6,76 (m, 5Н), 5,13 (s, 1Н), 5,08 (d, J=2,3Гц, 1Н), 3,49-3,45 (m, 1H), 2,62-2,55 (m, 1H), 2,20-2,11 (m, 1H), 1,83-1,75 (m, 1H), 1,67-1,58 (m, 1H), 1,56-1,39 (m, 3H). MS обчислено 284,1; MS (M-1) 283,1. Приклад 5 Одержання (+)-2-(4-гідроксифеніл)-5-гідроксициклопентил[с]3,4-дигідро-2H-1-бензопірану До розчину Проміжного продукту 59 (0,80г, 1,86ммоль) в безводному метанолі (30мл) додають n-толуолсульфокислоту (0,09г, 1,40ммоль), і До розчину Проміжного продукту 60 (0,86г, 2,00ммоль) в безводному метанолі (50мл) додають n-толуолсульфокислоту (94мг, 1,50ммоль), і нагрівають одержаний розчин при 50°С протягом 18год. Охолоджують реакційну суміш до температури навколишнього середовища, і додають до неї бромкрезоловий зелений (10мг) та ціанборгідрид натрію (0,63г, 10,00ммоль). Додають крапля за краплею метанол, насичений НСl (газоподібним), до одержання стійкого жовтого кольору суміші. Після досягнення остаточної зміни кольору суміш перемішують ще протягом 1год. Реакцію гасять насиченим розчином бікарбонату натрію, додають до суміші етилацетат, і промивають органічний шар розчином бікарбонату натрію та розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і піддають флешхроматографії з елююванням 5% діетилового ефіру в ди хлорметані, одержуючи сполуку за Прикладом 6 (0,32г, 57%) у вигляді твердої речовини світло-жовтого кольору. 1Н Я МР (d6-D MSO): 9,31 (s, 1Н), 9,30 (s, 1H), 7,21 (d, J=8,6Гц, 2H), 6,84-6,80 (m, 1H), 6,73 (d, J=8,6Гц, 2Н), 6,38 (d, J=7,8Гц, 1H), 6,29 (d, J=8,2Гц, 1H), 4,87 (s, 1H), 3,45-3,41 (m, 1H), 2,62-2,58 (m, 1H), 2,18-2,09 (m, 1H), 1,61-1,54 (m, 1H), 1,50-1,22 (m, 4H). MS обчислено 282,1; MS (M1) 281,1. Приклад 7 Одержання (+)-2-(4-гідроксифеніл)-6-гідрокси8-метил-циклопентил[с]3,4-дигідро-2Н-1бензопірану 51 77986 До розчину Проміжного продукту 61 (0,15г, 2,00ммоль) в безводному метанолі (30мл) додають n-толуолсульфокислоту (45мг, 0,73ммоль), і нагрівають одержаний розчин при 50°С протягом 18год. Охолоджують реакційну суміш до температури навколишнього середовища, і додають до неї бромкрезоловий зелений (10мг) та ціанборгідрид натрію (0,29г, 4,65ммоль). Додають крапля за краплею метанол, насичений НСl (газоподібним), до одержання стійкого жовтого кольору суміші. Після досягнення остаточної зміни кольору суміш перемішують ще протягом 1год. Реакцію гасять насиченим розчином бікарбонату натрію, додають до суміші етилацетат, і промивають органічний шар розчином бікарбонату натрію та розсолом. Органічний шар сушать над суль фатом натрію, концентрують у вакуумі і піддають флеш-хроматографії з елююванням 5% діетилового ефіру в ди хлорметані, одержуючи сполуку за Прикладом 7 (0,15г, 54%) у вигляді твердої речовини світло-жовтого кольору. 1Н ЯМР (d6-DMSO): 9,29 (s, 1Н), 8,66 (s, 1H), 7,24 (d, J=8,6Гц, 2H), 6,65 (d, J=8,2Гц, 2H), 6,36 (s, 2H), 4,89 (s, 1H), 2,58-2,47 (m, 1H), 2,08 (s, 3H), 2,07-2,00 (m, 1H), 1,62-1,59 (m, 1H), 1,42-1,21 (m, 5H). MS обчислено 296,1; MS (M-1) 295,1. Приклад 8 Одержання (+)-2-(4-гідроксифеніл)-6-гідроксициклогептил[с]3,4-дигідро-2Н-1-бензопірану До розчину Проміжного продукту 62 (0,25г, 0,54ммоль) в безводному метанолі (20мл) додають n-толуолсульфокислоту (25мг, 0,41ммоль), і нагрівають одержаний розчин при 50°С протягом 18год. Охолоджують реакційну суміш до температури навколишнього середовища, і додають до неї бромкрезоловий зелений (10мг) та ціанборгідрид натрію (0,17г, 2,70ммоль). Додають крапля за краплею метанол, насичений НСl (газоподібним), до одержання стійкого жовтого кольору суміші. Після досягнення остаточної зміни кольору суміш перемішують ще протягом 1год. Реакцію гасять насиченим розчином бікарбонату натрію, додають до суміші етилацетат, і промивають органічний шар розчином бікарбонату натрію та розсолом. Органічний шар сушать над суль фатом натрію, концентрують у вакуумі і піддають флеш-хроматографії з елююванням 5% діетилового ефіру в ди хлорметані та хроматографують HPLC (колонка YMC ODSA, 0,46´5см, градієнт 5-95% 0,1% TFA/вода та 0,1% TFA/ацетонітрил, 3,0мл/хв., детектування на довжині хвилі 214нм), одержуючи сполуку за Прикладом 8 (35мг, 21%) у вигляді твердої речовини світло-рожевого кольору. 1H ЯМР (d6-DMSO): 9,31 (s, 1Н), 8,77 (s, 1H), 7,21 (d, J=8,6Гц, 2Н), 6,75 (d, J=8,6Гц, 2H), 6,49-6,46 (m, 2H), 6,47 (dd, J=2,4Гц, 52 8,7Гц, 1H), 4,93 (s, 1H), 3,40-3 32 (m, 1H), 2,45-2,37 (m, 1H), 2,19-2,14 (m, 1H), 1,78-1,40 (m, 5H), 1,351,26 (in, 1H), 1,20-1-07 (m, 1H), 1,02-0,83 (m, 2H). MS обчислено 310,2; MS (M-1) 309,2. Приклад 9 Одержання (+)-2-(4-гідроксифеніл)-6-гідрокси8-метокси-циклопентил[с]3,4-дигідро-2Н-1бензопірану До розчину Проміжного продукту 63 (0,12г, 0,26ммоль) в безводному метанолі (15мл) додають n-толуолсульфокислоту (12мг, 0,20ммоль), і нагрівають одержаний розчин при 50°С протягом 18год. Охолоджують реакційну суміш до температури навколишнього середовища, і додають до неї бромкрезоловий зелений (10мг) та ціанборгідрид натрію (0,08г, 1,30ммоль). Додають крапля за краплею метанол, насичений НСl (газоподібним), до одержання стійкого жовтого кольору суміші. Після досягнення остаточної зміни кольору суміш перемішують ще протягом 1год. Реакцію гасять насиченим розчином бікарбонату натрію, додають до суміші етилацетат, і промивають органічний шар розчином бікарбонату натрію та розсолом. Органічний шар сушать над суль фатом натрію, концентрують у вакуумі і піддають флеш-хроматографії з елююванням 40% етилацетату в гексані, одержуючи сполуку за Прикладом 9 (37мг, 46%) у вигляді твердої речовини світло-жовтого кольору. 1H ЯМР d6-ацетон): 8,25 (bs, 1Н), 7,90 (bs, 1H), 7,32 (d, J=8,3Гц, 2Н), 6,85 (d, J=2,7Гц, 2Н), 6,30 (d, J=2,7Гц, 1Н), 6,24 (d, J=2,4Гц, 1H), 4,94 (d, J=2,3Гц, 1H), 3,74 (s, 3H), 3,44-3,40 (m, 1H), 2,69-2,62 (m, 1H), 2,18-2,10 (m, 1H), 1,85-1,69 (m, 1H), 1,59-1,55 (m, 1H), 1,49-1,41 (m, 2H), 1,39-1,33 (m, 1H). MS обчислено 312,2; MS (M-1) 311,2. Приклад 10 Одержання (+)-2-(4-гідроксифеніл)-6-гідрокси11,11-диметил-циклопентил[с]3,4-дигідро-2Н-1бензопірану До розчину Проміжного продукту 64 (40мг, 0,09ммоль) в безводному метанолі (10мл) додають n-толуолсульфокислоту (45мг, 0,73ммоль), і нагрівають одержаний розчин при 50°С протягом 18год. Охолоджують реакційну суміш до температури навколишнього середовища, і додають до неї бромкрезоловий зелений (10мг) та ціанборгідрид натрію (27мг, 0,43ммоль). Додають крапля за краплею метанол, насичений НСl (газоподібним), до одержання стійкого жовтого кольору суміші. Після досягнення остаточної зміни кольору суміш перемішують ще протягом 1год. Реакцію гасять насиченим розчином бікарбонату натрію, додають до суміші етилацетат, і промивають органічний шар 53 77986 54 розчином бікарбонату натрію та розсолом. Органібромкрезоловий зелений (10мг) та ціанборгідрид чний шар сушать над суль фатом натрію, концентнатрію (0,31г, 5,00ммоль). Додають крапля за крарують у вакуумі і хроматографують, застосовуючи плею метанол, насичений НСl (газоподібним), до хроматотрон (пластина 1мм) з елююванням 30% одержання стійкого жовтого кольору суміші. Після етилацетату в гексані, одержуючи сполуку за Придосягнення остаточної зміни кольору суміш перекладом 10 (16мг, 59%) у вигляді твердої речовини мішують ще протягом 1год. Реакцію гасять насисвітло-рожевогокольору. 1H ЯМР d6-ацетон): 8,20 ченим розчином бікарбонату натрію, додають до (s, 1Н), 7,80 (s, 1Н), 7,28 (d, J=8,2Гц, 2Н), 6,84 (d, суміші етилацетат, і промивають органічний шар J=8,6Гц, 2Н), 6,72 (d, J=8,6Гц, 1Н), 6,64 (d, J=3,2Гц, розчином бікарбонату натрію та розсолом. Органі1Н), 6,60 (dd, J=3,lГц, 8,6Гц, 1Н), 4,73 (d, J=2,7Гц, чний шар сушать над суль фатом натрію, концент1H), 3,04-2,98 (m, 2H), 1,64-1,59 (m, 1H), 1,43-1,37 рують у вакуумі і піддають флеш-хроматографії з (m, 2H), 1,25-1.20 (m, 1H), 1,19 (s, 3H), 0,53 (s, 3H). елююванням 40% етилацетату в гексані, одержуMS обчислено 310,2; MS (M-1) 309,2. ючи сполуку за Прикладом 12 (0,15г, 51%) у виПриклад 11 гляді твердої речовини світло-пурпурового кольоОдержання (+)-2-(4-гідроксифеніл)-6-гідроксиру. 1H ЯМР (CDCI3): 7,33 (d, J=8,2Гц, 2Н), 6,85-6,82 11.11-діетил-циклопентил[с]3,4-дигідро-2Н-1(m, 3Н), 6,72-6,66 (m, 2Н), 5,27 (s, 1Н), 5,05 (d, бензопірану J=2,0Гц, 1H), 3,79 (s, 3H), 3,50-3,45 (m, 1Н), 2,582,54 (m, 1H), 2,19-2,11 (m, 1H), 1,84-1,79 (m, 2H), 1,67-1,58 (m, 1H), 1,55-1,68 (m, 2H). MS обчислено 296,1; MS (M-1) 295,1. Приклад 13 Одержання (+)-2-(4-гідрокси-3-метилфеніл)-6гідрокси-циклопентил[с]3,4-дигідро-2Н-1бензопірану До розчину Проміжного продукту 65 (0,21г, 0,57ммоль) в безводному метанолі (10мл) додають n-толуолсульфокислоту (31мг, 0,48ммоль), і нагрівають одержаний розчин при 50°С протягом 18год. Охолоджують реакційну суміш до температури навколишнього середовища, і додають до неї До розчину Проміжного продукту 67 (0,51г, бромкрезоловий зелений (10мг) та ціанборгідрид 1,10ммоль) в безводному метанолі (15мл) при натрію (150мг, 2,40ммоль). Додають крапля за барботуванні газоподібним азотом із метою видакраплею метанол, насичений НСl (газоподібним), лення кисню додають «-толуолсульфокислоту до одержання стійкого жовтого кольору суміші. (0,17г, 0,86ммоль). Припиняють барботування, і Після досягнення остаточної зміни кольору суміш нагрівають одержаний розчин при 50°С протягом перемішують ще протягом 1год. Реакцію гасять 18год в атмосфері азоту. До реакційної суміші донасиченим розчином бікарбонату натрію, додають дають при температурі навколишнього середовидо суміші етилацетат, і промивають органічний ща бромкрезоловий зелений (приблизно 1мг) та шар розчином бікарбонату натрію та розсолом. ціанборгідрид натрію (0,35г, 5,50ммоль). Додають Органічний шар сушать над сульфатом натрію, порціями метанол, насичений НСl (газоподібним), концентрують у вакуумі і хроматографують, застопротягом деякого часу так, щоб підтримувати жовсовуючи хроматотрон (пластина 2мм) з елюювантий колір суміші. Після припинення спонтанної ням 30% етилацетату в гексані, одержуючи сполузміни кольору на синій суміш розподіляють між ку за Прикладом 11 (50мг, 26%) у вигляді твердої діетиловим ефіром і насиченим водним розчином речовини світло-рожевого кольору. 1H ЯМР тартрату натрію-калію. Органічний шар сушать над (MeOD): 7,20 (d, J=8,2Гц, 2Н), 6,75 (d, J=8,2Гц, 2Н), сульфатом натрію, концентрують у вакуумі і під6,70 (d, J=8,2Гц, 1Н), 6,56 (d, J=2,8Гц, 1H), 6,52 (dd, дають флеш-хроматографії на силікагелі з елююJ=2,7Гц, 8,2Гц, 1Н), 4,70 (d, J=3,5Гц, 1Н), 3,20 (d, ванням 3% діетилового ефіру в хлористому меJ=10,5Гц, 1H), 2,92-2,83 (m, 1H), 1,61-1,53 (m, 2H), тилені, одержуючи 0,11г (34%) суміші цис- і транс1,49-1,20 (m, 5H), 1,05-0,95 (m, 4H), 0,50 (t, стереоізомерів (3:2). Шляхом хроматографування J=8,8Гц, ЗН). MS обчислено 338,2; MS (M-1) 337,2. з оберненою фазою на колонці С18 із градієнтним Приклад 12 елююванням ацетонітрилом та водою з домішкою Одержання (+)-2-(4-гідроксифеніл)-6-метокси0,1% TFA одержують 10мг (3%) цис-конденсованої циклопентил[с]3,4-дигідро-2Н-1-бензопірану сполуки за Прикладом 13. 1Н ЯМР (DMSO-d6): 9,30 (s, 1Н), 8,81 (s, 1H), 7,10 (s, 1H), 7,03 (d, J=8,2Гц, 1Н), 6,74 (d, J=8,2Гц, 1Н), 6,63 (d, J=8,2Гц, 1Н), 6,55 (d, J=2,8Гц, 1H), 6,47 (dd, J=2,7Гц, 8,2Гц, 1H), 4,95 (s, 1H), 3,37 (m, 1H), 2,55 (m, 1H), 2,12 (s, 3H), 2,02 (m, 1H), 1,65-1,24 (m, 5H). MS обчислено 296,3; MS (M-1) 295,1. До розчину Проміжного продукту 66 (0,40г, Приклад 14 1,00ммоль) в безводному метанолі (20мл) додаОдержання (+)-2-(4-гідрокси-3-метилфеніл)-6ють n-толуолсульфокислоту (47мг, 0,75ммоль), і гідрокси-циклопентил[с]3,4-дигідро-2Н-1нагрівають одержаний розчин при 50°С протягом бензопірану 18год. Охолоджують реакційну суміш до температури навколишнього середовища, і додають до неї 55 77986 Фракцію, що містить транс-конденсований продукт, піддають повторному хроматографуванню з оберненою фазою на колонці С18 з елююванням сумішшю ацетонітрилу з водою (40:60) і одержують 8,2мг (2%) транс-конденсованої сполуки за Прикладом 14. 1Н ЯМР (DMSO-d6): 9,05 (s, 1Н), 7,10 (s, 1H), 7,03 (d, J=8,2Гц, 1H), 6,74 (d, J=8,2Гц, 1H), 6,62-6,55 (m, 2H), 6,47 (dd, J=2,7Гц, 8,2Гц, 1Н), 4,13 (d, J=11,0Гц, 1H), 2,95 (m, 1H), 2,43 (m, 1H), 2,20 (m, 1H), 2,12 (s, 3H), 1,70-1,40 (m, 4H), 1,17 (m, 1H). Приклад 15 Одержання (+)-2-(2-метил-4-гшроксифеніл)-6гідрокси-циклопентил[с]3,4-дигідро-2Н-1бензопірану До розчину Проміжного продукту 68 (0,31г, 0,70ммоль) в безводному метанолі (15мл) при барботуванні газоподібним азотом із метою видалення кисню додають n-толуолсульфокислоту (0,10г, 0,52ммоль). Припиняють барботування, і нагрівають одержаний розчин при 50°С протягом 18год в атмосфері азоту. До реакційної суміші додають при температурі навколишнього середовища бромкрезоловий зелений (приблизно 1мг) та ціанборгідрид натрію (0,22г, 3,5ммоль). Додають порціями метанол, насичений HCI (газоподібним), протягом деякого часу так, щоб підтримувати жовтий колір суміші. Після припинення спонтанної зміни кольору на синій суміш розподіляють між діетиловим ефіром і водою. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і піддають флеш-хроматографії на силікагелі з елююванням 3% діетилового ефіру в хлористому метилені, одержуючи 0,07г неочищеного продукту. Шляхом хроматографування з оберненою фазою на колонці С18 із градієнтним елююванням ацетонітрилом та водою з домішкою 0,1% TFA з подальшою ліофілізацією одержують 17мг (8%) сполуки за Прикладом 15 у вигляді гумоподібної речовини червоного кольору. 1H ЯМР (D MSO-d6): 9,21 (s, 1Н), 8,83 (s, 1H), 7,26 (d, J=8,0Гц, 1Н), 6,60 (d, J=7,6Гц, 2H), 6,56 (s, 2H), 6,47 (dd, J=7,6Гц, 2,8Гц, 2H), 5,04 (s, 1H), 3,42 (m, 1H), 2,50 (m, 1H), 2,19 (s, 3H), 2,07 (m, 1H), 1,64-1,18 (m, 5H). Синтез проводять, [як описано в Tetrahedron, 53, 39, 1997, pp.13329-13338]. Розчин 4метоксифенолу (7,5г, 60,67ммоль) у сірчаній кислоті (12мл, 121,3ммоль) та TFA (9,0мл, 121,3ммоль) охолоджують до 0°С і додають ме 56 тил-2-оксоциклопентан-карбоксилат (17,25г, 121,3ммоль). Перемішують суміш при температурі навколишнього середовища протягом 48год. Виливають суміш в насичений розчин бікарбонату натрію, забезпечуючи кінцеву основну реакцію суміші, потім додають етилацетат, і промивають суміш 1-н. розчином гідроксиду натрію і розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і піддають флешхроматографії з елююванням 100% дихлорметаном. Одержаний неочищений продукт осаджують із суміші дихлорметану з гексаном, і одержують Проміжний продукт 69 (1,84г, 17%) у вигляді твердої сполуки світло-жовтого кольору. 1H ЯМР (CDCI3): 7,25 (d, J=7,3Гц, 1Н), 7,03 (dd, J=2,9Гц, 8,8Гц, 1Н), 6,82 (d, J=2,9Гц, 1H), 3,82 (s, 3H), 3,03 (t, J=5,7Гц, 5,8Гц, 2Н), 2,90 (t, J=7,3Гц, 8,1Гц, 2Н), 2,23-2,15 (m, 2H). MS обчислено 216,1; MS (M+1) 217,1. Розчин фенолу (5,0г, 53,19ммоль) у 80% сірчаній кислоті (60мл) охолоджують до 0°С і додають метил-2-оксоциклопентан-карбоксилат (18,88г, 133,97ммоль). Перемішують суміш при температурі навколишнього середовища протягом 48 год. Виливають суміш в насичений розчин бікарбонату натрію, забезпечуючи кінцеву основну реакцію суміші, потім додають етилацетат, і промивають суміш 1-н. розчином гідроксиду натрію і розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і піддають флешхроматографії з елююванням 100% дихлорметаном. Одержаний неочищений продукт осаджують із суміші дихлорметану з гексаном, і одержують Проміжний продукт 70 (1,32г, 13%) у вигляді твердої сполуки білого кольору. 1H ЯМР (CDCI3): 7,467,40 (m, 2Н), 7,35-7,32 (m, 1Н), 7,26-7,22 (m, 1H), 3,09-3,4 (m, 2H), 2,93-2,88 (m, 2H), 2,24-2,18 (m, 2H). MS обчислено 186,1; MS (M+1) 187,1. Розчин метилгідрохінону (4,09г, 33,00ммоль) у 80% сірчаній кислоті (40мл) охолоджують до 0°С і додають метил-2-оксоциклопентан-карбоксилат (11,70г, 82,50ммоль). Перемішують суміш при температурі навколишнього середовища протягом 48год. Виливають суміш в насичений розчин бікарбонату натрію, забезпечуючи кінцеву основну реакцію суміші, потім додають етилацетат, і промивають суміш 1-н. розчином гідроксиду натрію і розсолом. Органічний шар суша ть над сульфатом натрію і концентрують у вакуумі. Неочищений твердий продукт розчиняють в 1-н. NaOH, промивають діетиловим ефіром і осаджують з водного шару 1-н. HCI. С уміш фільтрують, і одержують Проміжний продукт 71 (3,10г, 43%) у вигляді твердої сполуки жовтувато-коричневого кольору. 1H ЯМР (d6-DMSO): 9,61 (s, 1Н), 7,11 (s, 1H), 6,78 (s, 1H), 2,67 (t, J=6,4Гц, 7,3Гц, 4H), 2,15 (s, 3Н), 2,08 57 77986 2,01 (m, 2H). MS обчислено 216,1; MS (M+1) 217,1. Розчин гідрохінону (3,10г, 28,17ммоль) у 80% сірчаній кислоті (40мл) охолоджують до 0°С, і додають метил-2-оксоциклопентан-карбоксилат (10,00г, 70,42ммоль). Перемішують суміш при температурі навколишнього середовища протягом 9 діб. Виливають суміш у льодяну воду і фільтрують. Твердий продукт розчиняють у метанолі і концентрують у вакуумі. Твердий продукт розчиняють у хлороформі, фільтрують у гарячому вигляді і концентрують у вакуумі. Фільтрат хроматографують з елююванням 4% метанолу в хлороформі, і одержують Проміжний продукт 72 (1,10г, 19%) у вигляді твердої сполуки світло-жовтого кольору. 1Н ЯМР (d6-DMSO): 9,67 (s, 1Н), 7,23 (d, J=8,8Гц, 1Н), 6,95 (dd, J=2,9Гц, 8,8Гц, 1Н), 6,84 (d, J=2,4Гц, 1H), 2,98 (t, J=6,8Гц, 8,3Гц, 2Н), 2,71 (t, J=7,3Гц, 7,3Гц, 2Н), 2,10-2,02 (m, 2Н). MS обчислено 202,2; MS (M+1) 203,2. Розчин 4-бромфенолу (25,00г, 144,5ммоль), трет-бутилдиметилсиліл-хлориду (23,96г, 158,95ммоль) та імідазолу (10,82г, 158,95ммоль) в безводному ДМФ (200мл) перемішують протягом 18 год. Додають діетиловий ефір, промивають водою і розсолом, і сушать органічний шар над сульфатом натрію. Концентрують у вакуумі і піддають флеш-хроматографії з елююванням 10% етилацетату в гексані, одержуючи Проміжний продукт 73 (40,98г, 99%) у вигляді прозорого масла. 1 Н ЯМР (CDCI3): 7,24 (d, J=8,8Гц, 2Н), 6,73 (d, J=8,8Гц, 2Н), 0,99 (s, 9H), 0,20 (s, 6H). Розчин Проміжного продукту 71 (2,20г, 10,19ммоль), трет-бутилдиметилсиліл-хлориду (2,30г, 15,28ммоль) та імідазолу (1,04г, 15,28ммоль) в безводному ДМФ (200мл) перемішують протягом 18год. Додають діетиловий ефір, промивають водою і розсолом, і суша ть органічний шар над сульфатом натрію. Концентрують у вакуумі і піддають флеш-хроматографії з елююванням 20% етилацетату в гексані, одержуючи Проміжний продукт 74 (3,33г, 99%) у вигляді білої твердої речовини. 1Н ЯМР (CDCI3): 7,16 (s, 1Н), 6,75 (s, 1H), 3,04-3,00 (m, 2H), 2,98-2,90 (m, 2H), 2,29 (s, 3H), 2,25-2,20 (m, 2H), 1,04 (s, 9H), 0,24 (s, 6H). 58 Розчин Проміжного продукту 73 (2,04г, 7,11ммоль) у безводному ТГФ (25мл) охолоджують до -78°С, і крапля за краплею додають до нього втор-бутиллітій (1,3Μ в циклогексані, 5,5мл, 7,11ммоль). Перемішують розчин при -78°С протягом 15хв., і використовують його без додаткового очищення. До розчину Проміжного продукту 72 (0,90г, 4,45ммоль) та імідазолу (0,45г, 6,68ммоль) в безводному ДМФ (15мл) додають при перемішуванні трет-бутилдиметилсиліл-хлорид (1,00г, 6,68ммоль). Перемішують одержаний розчин протягом 48год., потім гасять насиченим розчином бікарбонату натрію. Додають діетиловий ефір, промивають розсолом, сушать органічний шар над сульфатом натрію і концентрують у вакуумі. Одержаний неочищений продукт хроматографують з елююванням 10% етилацетату в гексані, і одержують Проміжний продукт 76 (1,01г, 72%) у вигляді білої твердої речовини. 1Н ЯМР (CDCI3): 7,24 (d, J=4,4Гц, 1Н), 6,96 (dd, J=2,9Гц, 9,3Гц, 1Н), 6,82 (d, J=2,5Гц, 1H), 3,03 (m, 2H), 2,93 (m, 2H), 2,20 (m, 2H). MS обчислено 314; MS (M+1) 315. Розчин Проміжного продукту 76 (0,50г, 1,58ммоль) у безводному ди хлорметані (30мл) охолоджують до -78°С, додають діізобутилалюміній-гідрид (1,0Μ в толуолі, 1,8мл, 1,81ммоль) і перемішують протягом 3год. Гасять суміш метанолом (5,0мл), і нагрівають до температури навколишнього середовища. Додають до суміші етилацетат, і промивають розчином бікарбонату і розсолом. Органічний шар суша ть над сульфатом натрію і концентрують у вакуумі. Одержану піну розчиняють в безводному ТГФ (10мл) і охолоджують до -78°С. Додають Проміжний продукт 75 (0,21М, 22,5мл, 4,74ммоль) і перемішують протягом 10хв. Додають 1-н. HCI (50мл), нагрівають до температури навколишнього середовища і перемішують протягом 30хв. Додають до суміші етилацетат, і промивають її розсолом. Органічний шар сушать над сульфатом натрію і концентрують у вакуумі, одержуючи Проміжний продукт 77 (0,81г, 100%) у вигляді масла червоного кольору. Цей продукт використовують на наступній стадії без додаткового очищення. 59 77986 Приклад 16 Одержання (+)-2-(4-гідроксифеніл)-6-гідроксициклопентил[с]3,4-дигідро-2Н-1-бензопірану Розчин Проміжного продукту 77 (0,81г, 1,58ммоль) та тетрабутиламоній-фториду (1,0 Μ в ТГФ, 6,3мл, 6,32ммоль) у ТГФ (20мл) перемішують при температурі навколишнього середовища протягом 30хв., потім додають 1-н. HCI (7мл), і перемішують протягом 5хв. Додають до суміші етилацетат, промивають її насиченим розчином бікарбонату і розсолом, органічний шар сушать над сульфатом натрію і концентрують у вакуумі. Неочищений продукт піддають флешхроматографії з елююванням 5% метанолу в дихлорметані. Одержаний продукт розчиняють в метанолі (10мл), додають 5% паладій на вугіллі (60мг) та розчин аміаку (2,0Μ в метанолі, 0,25ммоль, 0,13мл), встановлюють на реакційній посудині еластичну камеру з воднем, і перемішують суміш при температурі навколишнього середовища протягом ночі. Фільтрують суміш через шар целіту, концентрують у вакуумі і піддають флеш-хроматографії з елююванням 10% діетилового ефіру в дихлорметані, одержуючи сполуку за Прикладом 16 (40мг, 10%) у вигляді твердої речовини світло-рожевого кольору. 1Н Я МР (MeOD): 7,19 (d, J=8,8Гц, 2Н), 6,75 (d, J=8,3Гц, 2Н), 6,62 (m, 2Н), 6,47 (dd, J=2,9Гц, 8,8Гц,1Н), 4,14 (d, J=11,3Гц, 1Н), 3,00 (m, 1H), 2,48 (m, 1H), 2,28 (m, 1H), 1,70 (m, 2H), 1,56 (m, 2H), 1,28 (m, 1H). MS обчислено 282; MS (M+1) 283. Розчин Проміжного продукту 69 (0,76г, 3,52ммоль) у безводному ди хлорметані (60мл) охолоджують до -78°С, додають діізобутилалюміній-гідрид (1,0Μ в толуолі, 3,9мл, 3,87ммоль), і перемішують протягом 2год. Гасять суміш метанолом і нагрівають до температури навколишнього середовища. Додають до суміші етилацетат, і промивають розчином бікарбонату і розсолом. Органічний шар сушать над сульфатом натрію і концентрують у вакуумі. Одержану піну розчиняють в безводному ТГФ (10мл) і охолоджують до 0°С. Додають магнійароматичний реагент (0,51М, 3,6мл, 1,84ммоль) і перемішують протягом 10хв. Додають 1-н. HCI (50мл), нагрівають до температури навколишнього середовища і перемішують протягом ЗО хв. Додають до суміші етилацетат, і промивають її розсолом. Органічний шар сушать над сульфатом натрію, концентрують у вакуумі і піддають флеш-хроматографії з елююванням 50% дихлорметану в гексані, одержуючи Проміжний 60 продукт 78 (0,33г, 30%) у вигляді масла червоного кольору. 1Н ЯМР (CDCI3): 7,33 (d, J=8,3Гц, 2Н), 6,89 (d, J=8,8Гц, 2Н), 6.80 (d, J=8,8Гц, 1Н), 6,686,63 (m, 2H), 5,04 (d, J=2,5Гц, 1H), 3,80 (s, 3H), 3,75 (s, 3H), 3,47-3,43 (m, 1H), 2,60-2,54 (m, 1H), 2,142,09 (m, 1H), 1,82-1,76 (m, 1H), 1,67-1,57 (m, 1H), 1,50-1,30 (m, 3H). Розчин Проміжного продукту 70 (0,44г, 2,37ммоль) у безводному ди хлорметані (40мл) охолоджують до -78°С, додають діізобутилалюміній-гідрид (1,0Μ в толуолі, 2,8мл, 2,84ммоль) і перемішують протягом 2год. Гасять суміш метанолом і нагрівають до температури навколишнього середовища. Додають до суміші етилацетат, і промивають розчином бікарбонату і розсолом. Органічний шар сушать над сульфатом натрію і концентрують у вакуумі. Одержану піну розчиняють в безводному ТГФ (10мл) і охолоджують до 78°С. Додають Проміжний продукт 75 (0,21М, 35,5мл, 7,11ммоль), і перемішують протягом 10хв. Додають 1-н. HCI (50мл), нагрівають до температури навколишнього середовища і перемішують протягом 30хв. Додають до суміші етилацетат, і промивають її розсолом. Органічний шар сушать над сульфатом натрію і концентрують у вакуумі, одержуючи Проміжний продукт 79 (0,40г, 43%). Цей продукт використовують на наступній стадії без додаткового очищення. 1Н ЯМР (MeOD): 7,257,18 (m, 2Н), 7,1-7,08 (m, 2H), 6,91-6,83 (m, 2H), 6,80-6,75 (m, 2H), 4,90 (m, 2H), 3,35-3,31 (m, 1Н), 2,81-2,60 (m, 3Н), 2,28-2,17 (m, 1H), 1,98-1,90 (m, 2H), 1,00 (s, 9H), 0,24 (s, 6H). MS обчислено 396,2; MS (M-1) 395,4. Розчин Проміжного продукту 74 (1,00г, 3,03ммоль) у безводному ди хлорметані (60мл) охолоджують до -78°С, додають діізобутилалюміній-гідрид (1,0Μ в толуолі, 3,6мл, 3,63ммоль), і перемішують протягом 2год. Гасять суміш метанолом і нагрівають до температури навколишнього середовища. Додають до суміші етилацетат, і промивають розчином бікарбонату і розсолом. Органічний шар сушать над сульфатом натрію і концентрують у вакуумі. Одержану піну розчиняють в безводному ТГФ (10мл) і охолоджують до 78°С. Додають Проміжний продукт 75 (0,21М, 45,4мл, 9,09ммоль) і перемішують протягом 10 хв. Додають 1-н. HCI (50мл), нагрівають до температури навколишнього середовища і перемішують протягом 30 хв. Додають до суміші етилацетат, і промивають її розсолом. Органічний шар сушать над сульфатом натрію і концентрують у вакуумі,
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstituted benzopyran derivatives as selective estrogen beta-receptor agonists
Автори англійськоюDodge Jeffrey Alan
Назва патенту російськоюЗамещенные бензопираны в качестве селективных агонистов бета-рецепторов эстрогенов
Автори російськоюДодж Джеффри Алан, Ричардсон Тимоти Айво
МПК / Мітки
МПК: A61K 31/353, A61P 19/10, A61P 35/00, C07D 311/80, A61P 13/02, A61P 9/00, A61P 11/00, A61P 13/08, A61P 25/00, A61P 15/00, C07D 311/94, A61P 25/28, A61P 43/00, A61P 1/04
Мітки: агоністи, естрогенів, селективні, бензопірани, заміщені, b-рецепторів
Код посилання
<a href="https://ua.patents.su/39-77986-zamishheni-benzopirani-yak-selektivni-agonisti-b-receptoriv-estrogeniv.html" target="_blank" rel="follow" title="База патентів України">Заміщені бензопірани як селективні агоністи b-рецепторів естрогенів</a>
Попередній патент: Спосіб лікування пов’язаного з bcl-2 порушення з використанням bcl-2-антисмислових олігомерів (варіанти), фармацевтична композиція (варіанти)
Наступний патент: Поліарилкарбоксаміди, придатні для застосування як ліпідознижуючі агенти
Випадковий патент: Спосіб виробництва пісочного печива