Інгібітори 11-бета-гідроксистероїддегідрогенази 1
Номер патенту: 94741
Опубліковано: 10.06.2011
Автори: Мебрі Томас Едвард, Буш Джулі Кей, Лі Женьхуа, Ю Янпінь, Снайдер Ненсі Джун, Уолліс Оуен Брендан, Хансен Марвін Мартін
Формула / Реферат
1. Сполука, структура якої представлена формулою:
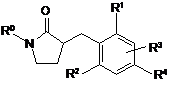 ,
,
де
R0 є:
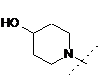 ,
,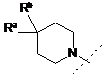 або
або 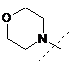 ,
,
де пунктирною лінією позначено точку приєднання у положення R0;
де Ra - -галоген; Rb - -Н або галоген;
R1 - -Н, -галоген, -О-СН3 (факультативно заміщений одним-трьома галогенами) або -СН3 (факультативно заміщений одним-трьома галогенами);
R2 - -Н, -галоген, -О-СН3 (факультативно заміщений одним-трьома галогенами) або -СН3 (факультативно заміщений одним-трьома галогенами);
R3 - -Н або -галоген;
R4 - -ОН, -галоген, -CN, -(С1-С4)-алкіл (факультативно заміщений одним-трьома галогенами), -О-(С1-С6)-алкіл (факультативно заміщений одним-трьома галогенами), -SCF3, -С(О)О(С1-С4)-алкіл, -O-CH2-C(O)NH2, -(С3-С8)-циклоалкіл, -О-феніл-С(О)О-(С1-С4)-алкіл, -СН2-феніл, -NHSO2-(С1-С4)-алкіл, -NHSO2-фeнiл-(R21)(R21), -(С1-С4)-алкіл-C(O)N(R10)(R11),
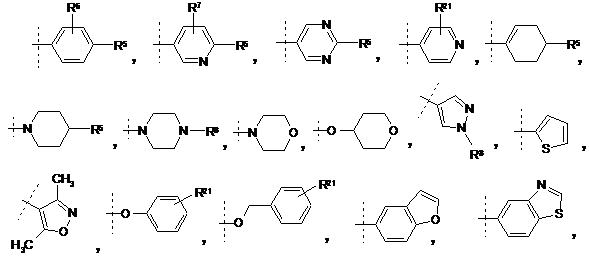
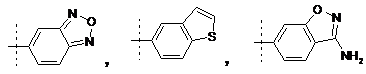 або
або 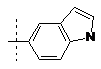 ,
,
де пунктирною лінією позначено точку приєднання у положення R4;
R5 - -Н, -галоген, -ОН, -CN, -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)ОН, -С(О)О-(С1-С4)-алкіл, -С(О)-(С1-С4)-алкіл, -О-(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами), -SO2-(С1-С4)-алкіл, -N(R8)(R8), -фeнiл-(R21)(R21), -С(О)-NН-(С3-С6)-циклоалкіл,
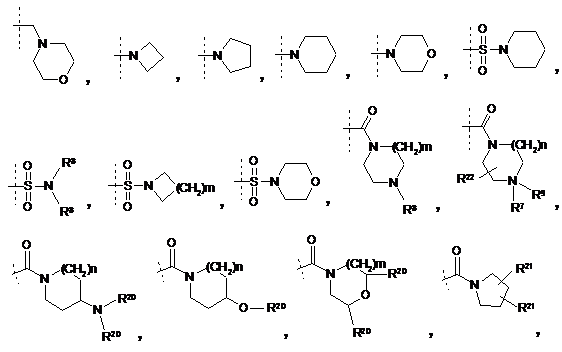
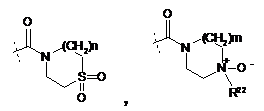 або
або 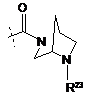 ,
,
де пунктирною лінією позначено точку приєднання у положення, позначене R5;
де m - 1, 2 або 3;
де n - 0, 1 або 2, та де, якщо n - 0, то "(СН2)n" - зв'язок;
R6 - -Н, -галоген, -CN або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами);
R7 - -Н, -галоген або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами);
R8 незалежно у кожному випадку є -Н, -(С1-С6)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)(С1-С6)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)-(С3-С8)-циклоалкіл, -S(О2)-(С3-С8)-циклоалкіл або -S(О2)-(С1-С3)-алкіл (факультативно заміщений 1-3 галогенами);
R9 - -Н або -галоген;
кожен з R10 та R11 незалежно один від одного є -Н або -(С1-С4)-алкіл, або R10 та R11 спільно з атомом азоту, до якого вони приєднані, утворюють піперидиніл, піперазиніл або піролідиніл;
R20 незалежно у кожному випадку є -Н або -(С1-С3)-алкіл (факультативно заміщений 1-3 галогенами);
R21 незалежно у кожному випадку є -Н, -галоген або -(С1-С3)-алкіл (факультативно заміщений 1-3 галогенами), -CN, -C(O)-N(R22)(R22) (де факультативно два наявні R22 спільно з азотом, до якого вони приєднані, утворюють азетидиніл, піролідиніл або піперидиніл);
R22 незалежно у кожному випадку є -Н або -(С1-С6)-алкіл (факультативно заміщений 1-3 галогенами); та
R23 незалежно у кожному випадку є -Н, -(С1-С4)-алкіл або -С(О)О-(С1-С4)-алкіл,
або фармацевтично прийнятна сіль такої сполуки.
2. Сполука за п. 1, де R0 є 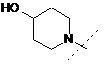 , або фармацевтично прийнятна сіль такої сполуки.
, або фармацевтично прийнятна сіль такої сполуки.
3. Сполука за п. 1 де R0 є 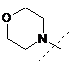 , або фармацевтично прийнятна сіль такої сполуки.
, або фармацевтично прийнятна сіль такої сполуки.
4. Сполука за будь-яким із пп. 1-3, де R1 та R2 - хлор, або фармацевтично прийнятна сіль такої сполуки.
5. Сполука за будь-яким із пп. 1-4, де R3 - водень, або фармацевтично прийнятна сіль такої сполуки.
6. Сполука за будь-яким із пп. 1-5,
де R4 - 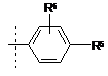 ,
,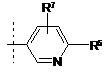 або
або 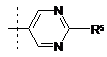 ,
,
або фармацевтично прийнятна сіль такої сполуки.
7. Сполука за будь-яким із пп. 1-5, де R4 - 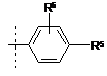 та R6 - -Н, або фармацевтично прийнятна сіль такої сполуки.
та R6 - -Н, або фармацевтично прийнятна сіль такої сполуки.
8. Сполука за будь-яким із пп. 1-7, де
R5 - 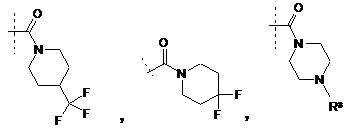 ,
,
де R8 - -(С1-С3)-алкіл (факультативно заміщений 1-3 галогенами) або 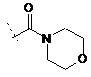 , або фармацевтично прийнятна сіль такої сполуки.
, або фармацевтично прийнятна сіль такої сполуки.
9. Сполука за будь-яким із пп. 1-7, де R5 - 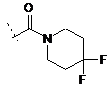 , або фармацевтично прийнятна сіль такої сполуки.
, або фармацевтично прийнятна сіль такої сполуки.
10. Сполука за будь-яким із пп. 1-7, де R5 -  , або фармацевтично прийнятна сіль такої сполуки.
, або фармацевтично прийнятна сіль такої сполуки.
11. Сполука за будь-яким із пп. 1-7, де R5 - хлор або фтор, або фармацевтично прийнятна сіль такої сполуки.
12. Фармацевтична композиція, яка містить сполуку або сіль за будь-яким із пп. 1-11 та фармацевтично прийнятний носій.
13. Сполука або сіль цієї сполуки за будь-яким із пп. 1-11 для застосування у лікуванні діабету типу 2.
14. Застосування сполуки або солі цієї сполуки за будь-яким із пп. 1-11 для виготовлення лікарського засобу для лікування діабету типу 2.
15. Сполука за п. 1, яка являє собою (R)-3-[3,5-дихлор-4'-(4-трифторметилпіперидин-1-карбоніл)біфеніл-4-ілметил]-1-(4-гідроксипіперидин-1-іл)піролідин-2-он, або фармацевтично прийнятна сіль такої сполуки.
16. Сполука за п. 1, яка являє собою (R)-3-[3,5-дихлор-4'-(4,4-дифторпіперидин-1-карбоніл)біфеніл-4-ілметил]-1-(4-гідроксипіперидин-1-іл)піролідин-2-он, або фармацевтично прийнятна сіль такої сполуки.
17. Проміжна сполука для одержання сполуки за п. 15, яка являє собою (R)-3-[3,5-дихлор-4'-(4-трифторметилпіперидин-1-карбоніл)біфеніл-4-ілметил]-5-гідроксидигідрофуран-2-он.
18. Кристалічний (R)-3-[3,5-дихлор-4'-(4-трифторметилпіперидин-1-карбоніл)біфеніл-4-ілметил]-1-(4-гідроксипіперидин-1-іл)піролідин-2-он.
19. Кристалічний (R)-3-[3,5-дихлор-4'-(4-трифторметилпіперидин-1-карбоніл)біфеніл-4-ілметил]-1-(4-гідроксипіперидин-1-іл)піролідин-2-он за п. 18 у практично чистій формі.
20. Кристалічний (R)-3-[3,5-дихлор-4'-(4-трифторметилпіперидин-1-карбоніл)біфеніл-4-ілметил]-1-(4-гідроксипіперидин-1-іл)піролідин-2-он за п. 18 або п. 19, який характеризується піками на рентгенодифрактограмі при кутах дифракції 2q 8,6±0,1° та 15,3±0,1°.
Текст
1. Сполука, структура якої представлена формулою: S , 3 94741 5 O N R - -Н, -галоген, -ОН, -CN, -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)ОН, С(О)О-(С1-С4)-алкіл, -С(О)-(С1-С4)-алкіл, -О-(С1С4)-алкіл (факультативно заміщений 1-3 галогена8 8 ми), -SO2-(С1-С4)-алкіл, -N(R )(R ), -фeнiл21 21 (R )(R ), -С(О)-NН-(С3-С6)-циклоалкіл, N O S N , , 4 NH2 N або , де пунктирною лінією позначено точку приєднання 4 у положення R ; O N O N , ,N ,N N , , O N N N N O , , N O ,S , R8 S O N O , R8 S S R8 O O N S N O , R8 (CH2)m O O S , O N O O R20 N O (CH2)n N (CH2)m N S O + O N O O (CH2)n S O , O , R22 22 N R8 ,R , R20 N (CH2)m + N OR22 або N N , де пунктирною лінією позначено точку приєднання 5 у положення, позначене R ; де m - 1, 2 або 3; де n - 0, 1 або 2, та де, якщо n - 0, то "(СН2)n" зв'язок; 6 R - -Н, -галоген, -CN або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами); 7 R - -Н, -галоген або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами); 8 R незалежно у кожному випадку є -Н, -(С1-С6)алкіл (факультативно заміщений 1-3 галогенами), С(О)(С1-С6)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)-(С3-С8)-циклоалкіл, -S(О2)-(С3С8)-циклоалкіл або -S(О2)-(С1-С3)-алкіл (факультативно заміщений 1-3 галогенами); 9 R - -Н або -галоген; 10 11 кожен з R та R незалежно один від одного є -Н 10 11 або -(С1-С4)-алкіл, або R та R спільно з атомом азоту, до якого вони приєднані, утворюють піперидиніл, піперазиніл або піролідиніл; N (CH2)m (CH2)n N N R8 R9 R7 O R22 (CH2)n N R9 , R7 , , O N O (CH2)m O R21 R20 N R21 R21 N , 20 O R23 ,R O (CH2)n N (CH2)m R20 N O R20 O ,O ,O R20 O , O O (CH2)n N (CH2)n 20 R N N (CH2)n N , , O O O N O R20 N (CH2)m O O N N N O , O N (CH2)m S N O O , N O O S O R20 R21 , , , , 20 R незалежно у кожному випадку є -Н або -(С1С3)-алкіл (факультативно заміщений 1-3 галогенами); 21 R незалежно у кожному випадку є -Н, -галоген або -(С1-С3)-алкіл (факультативно заміщений 1-3 22 22 галогенами), -CN, -C(O)-N(R )(R ) (де факульта22 тивно два наявні R спільно з азотом, до якого вони приєднані, утворюють азетидиніл, піролідиніл або піперидиніл); 22 R незалежно у кожному випадку є -Н або -(С1С6)-алкіл (факультативно заміщений 1-3 галогенами); та 23 R незалежно у кожному випадку є -Н, -(С1-С4)алкіл або -С(О)О-(С1-С4)-алкіл, або фармацевтично прийнятна сіль такої сполуки. HO N 0 2. Сполука за п. 1, де R є , або фармацевтично прийнятна сіль такої сполуки. O N 0 3. Сполука за п. 1 де R є , або фармацевтично прийнятна сіль такої сполуки. 1 2 4. Сполука за будь-яким із пп. 1-3, де R та R хлор, або фармацевтично прийнятна сіль такої сполуки. 3 5. Сполука за будь-яким із пп. 1-4, де R - водень, або фармацевтично прийнятна сіль такої сполуки. 6. Сполука за будь-яким із пп. 1-5, 5 94741 R5R5 R5R5 де R 4 5 R7R7 R6R6 ,, NN , або N R5 N , або фармацевтично прийнятна сіль такої сполуки. 4 7. Сполука за будь-яким із пп. 1-5, де R R6 R5 6 та R - -Н, або фармацевтично прийнятна сіль такої сполуки. 8. Сполука за будь-яким із пп. 1-7, де O O O N N N N F F 5 F , F , 6 R8 F R , 8 де R - -(С1-С3)-алкіл (факультативно заміщений 1O N O 3 галогенами) або , або фармацевтично прийнятна сіль такої сполуки. 5 9. Сполука за будь-яким із пп. 1-7, де R O N F F , або фармацевтично прийнятна сіль такої сполуки. 5 10. Сполука за будь-яким із пп. 1-7, де R O N 11. Сполука за будь-яким із пп. 1-7, де R - хлор або фтор, або фармацевтично прийнятна сіль такої сполуки. 12. Фармацевтична композиція, яка містить сполуку або сіль за будь-яким із пп. 1-11 та фармацевтично прийнятний носій. 13. Сполука або сіль цієї сполуки за будь-яким із пп. 1-11 для застосування у лікуванні діабету типу 2. 14. Застосування сполуки або солі цієї сполуки за будь-яким із пп. 1-11 для виготовлення лікарського засобу для лікування діабету типу 2. 15. Сполука за п. 1, яка являє собою (R)-3-[3,5дихлор-4'-(4-трифторметилпіперидин-1карбоніл)біфеніл-4-ілметил]-1-(4гідроксипіперидин-1-іл)піролідин-2-он, або фармацевтично прийнятна сіль такої сполуки. 16. Сполука за п. 1, яка являє собою (R)-3-[3,5дихлор-4'-(4,4-дифторпіперидин-1карбоніл)біфеніл-4-ілметил]-1-(4гідроксипіперидин-1-іл)піролідин-2-он, або фармацевтично прийнятна сіль такої сполуки. 17. Проміжна сполука для одержання сполуки за п. 15, яка являє собою (R)-3-[3,5-дихлор-4'-(4трифторметилпіперидин-1-карбоніл)біфеніл-4ілметил]-5-гідроксидигідрофуран-2-он. 18. Кристалічний (R)-3-[3,5-дихлор-4'-(4трифторметилпіперидин-1-карбоніл)біфеніл-4ілметил]-1-(4-гідроксипіперидин-1-іл)піролідин-2он. 19. Кристалічний (R)-3-[3,5-дихлор-4'-(4трифторметилпіперидин-1-карбоніл)біфеніл-4ілметил]-1-(4-гідроксипіперидин-1-іл)піролідин-2-он за п. 18 у практично чистій формі. 20. Кристалічний (R)-3-[3,5-дихлор-4'-(4трифторметилпіперидин-1-карбоніл)біфеніл-4ілметил]-1-(4-гідроксипіперидин-1-іл)піролідин-2-он за п. 18 або п. 19, який характеризується піками на рентгенодифрактограмі при кутах дифракції 2 8,6±0,1° та 15,3±0,1°. F F , або фармацевтично прийнятна сіль такої сполуки. F Ця заявка претендує на пріоритет попередньої заявки № 60/745,475 на патент США, поданої 24 квітня 2006 р. Цей винахід стосується сполук, які є інгібіторами ΙΙ--гідроксистероїддегідрогенази типу 1 ("ΙΙ-HSD1"), та фармацевтичних композицій, які містять ці сполуки, застосування цих сполук та композицій для лікування людей або тварин та нових проміжних сполук, корисних при виготовленні цих інгібіторів. Згадані сполуки демонструють ефективне та селективне інгібування ΙΙ-HSD1, а також є корисними для лікування розладів, чутливих до модулювання ΙΙ--HSD1, наприклад, діабету, метаболічного синдрому, розладів пізнавальної здібності тощо. Глкжокортикоїди, які діють на печінку, жирову тканину та м'язи, є важливими регуляторами метаболізму глюкози, ліпідів та білків. Хронічний надлишок глюкокортикоїдів пов'язаний з резистентністю до інсуліну, вісцеральним ожирінням, гіпертензією та дисліпідемією, які також вважаються класичними ознаками метаболічного синдрому. ΙΙ--HSD1 каталізує перетворення неактивного кортизону у активний кортизол та бере участь у розвитку метаболічного синдрому. Інформація, одержана при дослідженнях на гризунах та людях, посвідчує зв'язок ΙΙ--HSD1 з метаболічним синдромом. Ця інформація дозволяє припустити, що лікарські засоби, які специфічно інгібують ΙΙ--HSD1 в організмі хворих на діабет типу 2, 7 мають знижувати рівень глюкози у крові шляхом послаблення глюконеогенезу у печінці, зменшувати помірне ожиріння, покращувати фенотипи атерогенних ліпопротеїнів, знижувати кров'яний тиск та знижувати резистентність до інсуліну. Вплив інсуліну на м'язи має покращуватися, також може посилюватися секреція інсуліну з бетаклітин острівців. Інформація, одержана при дослідженнях на гризунах та людях, вказує також, що надлишок глюкокортикощів погіршує пізнавальну функцію. Результати недавніх досліджень вказують, що інактивація ΙΙ--HSD1 покращує функцію пам'яті як у людей, так і у мишей. Показано, що карбеноксолон, який є інгібітором ΙΙ-HSD, покращує пізнавальну функцію у здорових літніх людей та у хворих на діабет типу 2, та що інактивація гена ΙΙ--HSD1 запобігає віковим розладам у мишей. Останнім часом було показано, що селективне інгібування ΙΙ--HSD1 фармацевтичними засобами покращує здатність до запам'ятовування у мишей. За останні роки з'явилися численні публікації, що сповіщають про засоби, які інгібують ΙΙ-HSD1. Дивись міжнародну заявку WO2004/056744, де описано адамантилацетаміди як інгібітори ΙΙ--HSD; міжнародну заявку WO2005/108360, де описано похідні піролідин-2ону та піперидин-2-ону як інгібітори ΙΙ--HSD; та міжнародну заявку WO2005/108361, де описано похідні адамантилпіролідин-2-ону як інгібітори ΙΙ-HSD. Незважаючи на численні способи лікування захворювань, пов'язаних із впливом ΙΙ-HSD1, сучасні способи терапії мають окремі вади або групи вад, до яких належать низька або неповна ефективність, неприйнятні побічні ефекти та протипоказання до застосування для деяких груп пацієнтів. Отже, залишається потреба в удосконаленні лікування із застосуванням альтернативних або удосконалених фармацевтичних засобів, які інгібують ΙΙ--HSD1, та лікування захворювань, при яких є корисним інгібування ΙΙ-HSD1. Цей винахід пропонує такий внесок у рівень техніки, який грунтується на віднайденні того, що новий клас сполук має сильну та селек 94741 8 тивну інгібувальну дію на ΙΙ--HSD1. Цей винахід відрізняється конкретними структурами та їхніми активностями. Існує постійна потреба у нових способах лікування діабету, метаболічного синдрому та розладів пізнавальної здібності, і метою цього винаходу є задоволення цих та інших потреб. Цей винахід пропонує сполуку, структура якої представлена формулою: або фармацевтично прийнятну сіль такої сполуки, де І 0 R є де пунктирною лінією позначено точку приєднанa b ня групи у положення R°; де R - -галоген; R - -Η або галоген; 1 R - -Н, -галоген, -О-СН3 (факультативно заміщений одним-трьома галогенами), або -СН3 (факультативно заміщений одним-трьома галогенами); 2 R - -Н, -галоген, -О-СН3 (факультативно заміщений одним-трьома галогенами), або -СН3 (факультативно заміщений одним-трьома галогенами); 3 R - -Н або -галоген; 4 R - -ОН, -галоген, -CN, -(С1-С4)-алкіл (факультативно заміщений одним-трьома галогенами), -О-(С1-С6)-алкіл (факультативно заміщений одним-трьома галогенами), -SCF3, -С(О)О(С1-С4)алкіл, -O-CH2-C(O)NH2, -(С3-С8)-циклоалкіл, -Офеніл-С(О)О-(С1-С4)-алкіл, -СН2-феніл, -NHSO221 21 (С1-С4)-алкіл, -NHSO2-фeнiл(R )(R ), -(С1-С4)10 11 алкіл-С(О)N(R )(R ), 9 94741 10 де пунктирною лінією позначено точку приєд4 нання у положення R ; 5 R - -Η, -галоген, -ОН, -CN, -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами), С(О)ОН, -С(О)О-(С1-С4)-алкіл, -С(О)-(С1-С4)-алкіл, -О-(С1-С4)-алкіл (факультативно заміщений 1-3 8 8 галогенами), -SO2-(C1-C4)-алкіл, -N(R )(R ), 21 21 фeнiл-(R )(R ), -С(О)-NН-(С3-С6)-циклоалкіл, де пунктирною лінією позначено точку приєд5 нання у положення, позначене R ; де m - 1, 2 або 3; де n - 0, 1 або 2, та у разі якщо n - 0, то "(СН2)n" - зв'язок; 6 R - -Н, -галоген, -CN або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами); 7 R - -Н, -галоген або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами); 8 R незалежно у кожному випадку є -Н, -(С1С6)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)(С1-С6)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)-(С3-С8)-циклоалкіл, -S(О2)-(С3-С8)-циклоалкіл або -S(О2)-(С1-С3)-алкіл (факультативно заміщений 1-3 галогенами); 9 R - -Н або -галоген; 10 11 кожен з R та R незалежно один від одного 10 11 є -Н або -(С1-С4)-алкіл або R та R спільно з атомом азоту, до якого вони приєднані, утворюють піперидиніл, піперазиніл або піролідиніл; 20 R незалежно у кожному випадку є -Н або (С1-С3)-алкіл (факультативно заміщений 1-3 галогенами); 21 R незалежно у кожному випадку є -Н, галоген, -(С1-С3)-алкіл (факультативно заміщений 22 22 1-3 галогенами), -CN або -C(O)-N(R )(R ) (де 22 факультативно два наявні R спільно з азотом, до якого вони приєднані, утворюють азетидиніл, піролідиніл або піперидиніл); 22 R незалежно у кожному випадку є -Н або (С1-С6)-алкіл (факультативно заміщений 1-3 галогенами); та 23 R незалежно у кожному випадку є -Н, -(С1С4)-алкіл або -С(О)О-(С1-С4)-алкіл. За іншим варіантом здійснення цей винахід пропонує сполуку, структура якої представлена формулою І: або фармацевтично прийнятну сіль такої сполуки, де 0 R є де пунктирною лінією позначено точку приєднання у 0 a b положення R у формулі І; де R - -галоген; R - Η або галоген; 1 R - -Н, -галоген, -О-СН3 (факультативно заміщений одним-трьома галогенами) або -СН3 (факультативно заміщений одним-трьома галогенами); 2 R - -Н, -галоген, -О-СН3 (факультативно заміщений одним-трьома галогенами) або -СН3 (факультативно заміщений одним-трьома галогенами); 3 R - -Н або -галоген; 4 R - -ОН, -галоген, -CN, -(С1-С4)-алкіл (факультативно заміщений одним-трьома галогенами), -О-(С1-С6)-алкіл (факультативно заміщений од 11 94741 12 21 21 ним-трьома галогенами), -SCF3, -С(О)О(С1-С4)алкіл, -O-CH2-C(O)NH2, -(С3-С8)-циклоалкіл, -Oфеніл-С(O)О-(С1-С4)-алкіл, -СН2-феніл, -NHSO2 (С1-С4)-алкіл, -NHSO2-феніл-(R )(R ), -(С1-С4)10 11 алкіл-С(О)N(R )(R ), де пунктирною лінією позначено точку приєд4 нання у положення R у формулі І; 5 R - -Н, -галоген, -ОН, -CN, -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами), С(О)ОН, -С(О)О-(С1-С4)-алкіл, -С(О)-(С1-С4)-алкіл, -О-(С1-С4)-алкіл (факультативно заміщений 1-3 8 8 галогенами), -SO1-(С1-С4)-алкіл, -N(R )(R ), 21 21 фeнiл-(R )(R ), -С(О)-NН-(С3-С6)-циклоалкіл, де пунктирною лінією позначено точку приєд5 нання у положення, позначене R ; де m - 1, 2 або 3; де n - 0, 1 або 2, та у разі якщо n - 0, то "(CH2)n" - зв'язок; 6 R - -Η, -галоген, -CN або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами); 7 R - -Η, -галоген або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами); 8 R незалежно у кожному випадку є -Н, -(С1С6)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)(С1-С6)-алкіл (факультативно замі щений 1-3 галогенами), -С(О)-(С3-С8)-циклоалкіл, -S(О2)-(С3-С8)-циклоалкіл або -S(О2)-(С1-С3)-алкіл (факультативно заміщений 1-3 галогенами); 9 R - -Н або -галоген; 10 11 кожен з R та R незалежно один від одного 10 11 є -Н або -(С1-С4)-алкіл або R та R спільно з атомом азоту, до якого вони приєднані, утворюють піперидиніл, піперазиніл або піролідиніл; 20 R незалежно у кожному випадку є -Н або (С1-С3)-алкіл (факультативно заміщений 1-3 галогенами); 13 21 94741 14 R незалежно у кожному випадку є -Н, галоген або -(С1-С3)-алкіл (факультативно замі22 22 щений 1-3 галогенами), -CN, -C(O)-N(R )(R ) (де 22 факультативно два наявні R спільно з азотом, до якого вони приєднані, утворюють азетидиніл, піролідиніл або піперидиніл); 22 R незалежно у кожному випадку є -Н або (С1-С6)-алкіл (факультативно заміщений 1-3 галогенами); та 23 R незалежно у кожному випадку є -Н, -(С1С4)-алкіл або -С(О)О-(С1-С4)-алкіл. Цей винахід пропонує сполуки формули І, які є корисними як сильнодіючі та селективні інгібітори ΙΙ--HSD1. Цей винахід також пропонує фармацевтичну композицію, яка містить сполуку формули І або фармацевтичну сіль цієї сполуки та фармацевтично прийнятні носій, розріджувач або наповнювач. Крім того, цей винахід пропонує спосіб лікування метаболічного синдрому та захворювань, які мають відношення до нього, який включає введення в організм пацієнта, який цього потребує, ефективної кількості сполуки формули І або фармацевтично прийнятної солі такої сполуки. За одним варіантом здійснення цей винахід пропонує сполуки формули І або фармацевтично прийнятні солі цих сполук, детально описані вище. В той час як всі сполуки за цим винаходом є корисними, певні сполуки становлять особливий інтерес, і їм віддається перевага. Нижче наведені декілька груп сполук, яким віддається перевага. За іншим варіантом здійснення цей винахід пропонує сполуку, структура якої представлена формулою І, або фармацевтично прийнятну сіль такої сполуки, де 0 R є де пунктирною лінією позначено точку приєд4 нання у положення R у формулі І; 5 R - -Н, -галоген, -ОН, -CN, -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами), С(О)ОН, -С(О)О-(С1-С4)-алкіл, -С(О)-(С1-С4)-алкіл, -О-(С1-С4)-алкіл (факультативно заміщений 1-3 8 8 галогенами), -SO2-(C1-C4)-алкіл, -N(R )(R ), 21 21 фeнiл-(R )(R ), -С(О)-NН-(С3-С6)-циклоалкіл, дє пунктирною лінією позначено точку приєднання у 0 a bположення R у формулі І; де R - -галоген; R -Η або галоген; 1 2 3 R - -галоген; R - -галоген; R - -Н або галоген; 4 R - -ОН, -галоген, -CN, -(С1-С4)-алкіл (факультативно заміщений одним-трьома галогенами), -(С1-С6)-алкоксигрупа (факультативно заміщена одним-трьома галогенами), -SCF3, -С(О)О(С1-С4)алкіл, -O-CH2-C(O)NH2, -(С3-С8)-циклоалкіл, -Офеніл-С(О)О-(С1-С4)-алкіл, -СН2-феніл, -NHSO221 21 (С1-С4)-алкіл, -NHSO2-феніл-(R )(R ), -(С1-С4)10 11 алкіл-С(О)N(R )(R ), 15 де пунктирною лінією позначено точку приєд5 нання у положення, позначене R ; де m - 1, 2 або 3; де n - 0, 1 або 2, та у разі якщо n - 0, то "(СН2)n" - зв'язок; 6 R - -Н, -галоген, -CN або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами); 7 R - -Н, -галоген або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами); 8 R незалежно у кожному випадку є -Н, -(С1С6)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)(С1-С6)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)-(С3-С8)-циклоалкіл, -S(О2)-(С3-С8)-циклоалкіл або -S(О2)-(С1-С3)-алкіл (факультативно заміщений 1-3 галогенами); 9 R - -Н або -галоген; 10 11 кожен з R та R незалежно один від одного 10 11 є -Н або -(С1-С4)-алкіл або R та R спільно з атомом азоту, до якого вони приєднані, утворюють піперидиніл, піперазиніл або піролідиніл; 20 R незалежно у кожному випадку є -Н або (С1-С3)-алкіл (факультативно заміщений 1-3 галогенами); 21 R незалежно у кожному випадку є -Н, галоген або -(С1-С3)-алкіл (факультативно замі 94741 16 22 22 щений 1-3 галогенами), -CN, -C(O)-N(R )(R ) (де 22 факультативно два наявні R спільно з азотом, до якого вони приєднані, утворюють азетидиніл, піролідиніл або піперидиніл); 22 R незалежно у кожному випадку є -Н або (С1-С6)-алкіл (факультативно заміщений 1-3 галогенами); та 23 R незалежно у кожному випадку є -Н, -(С1С4)-алкіл або -С(О)О-(С1-С4)-алкіл. За іншим варіантом здійснення цей винахід пропонує сполуку, структура якої представлена формулою І, або фармацевтично прийнятну сіль такої сполуки, де 0 R є де пунктирною лінією позначено точку приєднання у 0 a b положення R у формулі І; де R - -галоген; R - Η або галоген; 1 2 R - -хлор, -фтор або -бром; R - -хлор, -фтор 3 або -бром; R - -Н або -галоген; 17 94741 18 5 де пунктирною лінією позначено точку приєд4 нання у положення R у формулі І; де пунктирною лінією позначено точку приєд5 нання у положення, позначене R ; де m - 1, 2 або 3; 6 R - -Η, -галоген, -CN або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами); 7 R - -Н, -галоген або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами); 8 R незалежно у кожному випадку є -Н, -(С1С6)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)(С1-С6)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)-(С3-С8)-циклоалкіл, -S(О2)-(С3-С8)-циклоалкіл або -S(О2)-(С1-С3)-алкіл (факультативно заміщений 1-3 галогенами); 9 R - -Н або -галоген; 20 R незалежно у кожному випадку є -Н або (С1-С3)-алкіл (факультативно заміщений 1-3 галогенами); 21 R незалежно у кожному випадку є -Н, галоген або -(С1-С3)-алкіл (факультативно замі22 22 щений 1-3 галогенами), -CN, -C(O)-N(R )(R ) (де 22 факультативно два наявні R спільно з азотом, R - -Н, -галоген, -ОН, -CN, -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами), С(О)ОН, -С(О)О-(С1-С4)-алкіл, -С(О)-(С1-С4)-алкіл, -О-(С1-С4)-алкіл (факультативно заміщений 1-3 8 8 галогенами), -SO2-(С1-С4)-алкіл, -N(R )(R ), 21 21 фeніл-(R )(R ), -С(О)-NН-(С3-С6)-циклоалкіл, до якого вони приєднані, утворюють азетидиніл, піролідиніл або піперидиніл); 22 R незалежно у кожному випадку є -Н або (С1-С6)-алкіл (факультативно заміщений 1-3 галогенами); та 23 R незалежно у кожному випадку є -Н, -(С1С4)-алкіл або -С(О)О-(С1-С4)-алкіл. За іншим варіантом здійснення цей винахід пропонує сполуку, структура якої представлена формулою І, або фармацевтично прийнятну сіль такої сполуки, де 0 R є де пунктирною лінією позначено точку приєднанa ня у положення R° у формулі І; де R - -галоген; bR -Η або галоген; 1 2 R - -хлор, -фтор або -бром; R - -хлор, -фтор 3 або -бром; R - -Н або -галоген; 19 94741 20 де пунктирною лінією позначено точку приєд4 нання у положення R у формулі І; 5 R - -Н, -галоген, -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)ОН, -С(О)О (С1-С4)-алкіл, -С(О)-(С1-С4)-алкіл, -О-(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами), -SO28 8 (С1-С4)-алкіл, -N(R )(R ), де пунктирною лінією позначено точку приєд5 нання у положення, позначене R ; де m - 1, 2 або 3; 6 R - -Н, -галоген, -CN або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами); 7 R - -Н, -галоген або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами); 8 R незалежно у кожному випадку є -Н, -(С1С6)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)(С1-С6)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)-(С3-С8)-циклоалкіл, -S(О2)-(С3-С8)-циклоалкіл або -S(О2)-(С1-С3)-алкіл (факультативно заміщений 1-3 галогенами); 9 R - -Н або -галоген; 20 R незалежно у кожному випадку є -Н або (С1-С3)-алкіл (факультативно заміщений 1-3 галогенами); 21 R незалежно у кожному випадку є -Н, галоген або -(С1-С3)-алкіл (факультативно замі22 22 щений 1-3 галогенами), -CN, -C(O)-N(R )(R ) (де 22 факультативно два наявні R спільно з азотом, до якого вони приєднані, утворюють азетидиніл, піролідиніл або піперидиніл); 22 R незалежно у кожному випадку є -Н або (С1-С6)-алкіл (факультативно заміщений 1-3 галогенами); та 23 R незалежно у кожному випадку є -Н, -(С1С4)-алкіл або -С(О)О-(С1-С4)-алкіл. За іншим варіантом здійснення цей винахід пропонує сполуку, структура якої представлена формулою І, або фармацевтично прийнятну сіль такої сполуки, де 0 R є де пунктирною лінією позначено точку приєднан0 a ня у положення R у формулі І; де R - -галоген; b R - -Η або галоген; 1 2 R - -хлор, -фтор або -бром; R - -хлор, -фтор 3 або -бром; R - -Н або -галоген; 4 де пунктирною лінією позначено точку приєднання у положення R у формулі І; 21 94741 22 22 де пунктирною лінією позначено точку приєд5 нання у положення, позначене R ; 6 R - -Н, -галоген, -CN або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами); 7 R - -Н, -галоген або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами); 8 R незалежно у кожному випадку є -Н, -(С1С6)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)(С1-С6)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)-(С3-С8)-циклоалкіл, -S(О2)-(С3-С8)-циклоалкіл або -S(О2)-( 1-С3)-алкіл (факультативно заміщений 1-3 галогенами); 9 R - -Н або -галоген; 20 R незалежно у кожному випадку є -Н або (С1-С3)-алкіл (факультативно заміщений 1-3 галогенами); 21 R незалежно у кожному випадку є -Н, галоген або -(С1-С3)-алкіл (факультативно замі22 22 щений 1-3 галогенами), -CN, -C(O)-N(R )(R ) (де 22 факультативно два наявні R спільно з азотом, до якого вони приєднані, утворюють азетидиніл, піролідиніл або піперидиніл); R незалежно у кожному випадку є -Н або (С1-С6)-алкіл (факультативно заміщений 1-3 галогенами); та 23 R незалежно у кожному випадку є -Н, -(С1С4)-алкіл або -С(О)О-(С1-С4)-алкіл. За іншим варіантом здійснення цей винахід пропонує сполуку, структура якої представлена формулою І, або фармацевтично прийнятну сіль такої сполуки, де 0 R є де пунктирною лінією позначено точку приєд4 нання у положення R у формулі І; 5 R -SО2-(С1-С4)-алкіл, -S(О2)-(С3-С8)-циклоалкіл або -S(О2)-(С1-С3)-алкіл (факультативно заміщений 1-3 галогенами). За іншим варіантом здійснення цей винахід пропонує сполуку, структура якої представлена формулою І, або фармацевтично прийнятну сіль такої сполуки, де 0 R є або , де пунктирною лінією позначено 5 точку приєднання у положення, позначене R ; де m - 1, 2 або 3; 6 R - -Н, -галоген, -CN або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами); 7 R - -Н, -галоген або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами); та 8 R незалежно у кожному випадку є -Н, -(С1С6)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)(С1-С6)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)-(С3-С8)-циклоалкіл, де пунктирною лінією позначено точку приєднання у 0 a bположення R у формулі І; де R - -галоген; R -Η або галоген; 1 2 R - -хлор, -фтор або -бром; R - -хлор, -фтор 3 або -бром; R - -Н або -галоген; де пунктирною лінією позначено точку приєднан0 a ня у положення R у формулі І; де R - -галоген; b R - -Η або галоген; 1 2 R - -хлор, -фтор або -бром; R - -хлор, -фтор 3 або -бром; R - -Н або -галоген; 23 94741 24 1 R є де пунктирною лінією позначено точку приєд4 нання у положення R у формулі І; R5 -N(R8)(R8), 0 вага, R є . У варіанті, якому відда 0 де пунктирною лінією позначено точку приєд5 нання у положення, позначене R ; 6 R - -Н, -галоген, -CN або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами); 7 R - -Н, -галоген або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами); та 8 R незалежно у кожному випадку є -Н, -(С1С6)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)(С1-С6)-алкіл (факультативно заміщений 1-3 галогенами), -С(О)-(С3-С8)-циклоалкіл, -S(О2)-(С3-С8)-циклоалкіл або -S(О2)-(С1-С3)-алкіл (факультативно заміщений 1-3 галогенами). Пропонуються інші варіанти здійснення винаходу, причому кожний з описаних вище варіантів додатково конкретизований згідно з варіантами, яким віддається перевага, описаними нижче. Конкретно, кожний з описаних нижче варіантів,яким віддається перевага, незалежно від інших комбінується з кожним із варіантів, описаних вище, і кожна конкретна комбінація відповідає новому варіанту здійснення винаходу, в якому змінна, вказана як така, що їй віддається перевага, конкретизована згідно зі значенням, якому віддається перевага. 0 У варіанті, якому віддається перевага, R є ється перевага, R є . У варіанті, якому a віддається перевага, R - -хлор, фтор або -бром. b У варіанті, якому віддається перевага, R - -хлор, фтор або -бром. У варіанті, якому віддається пе1 ревага, R - -галоген. У варіанті, якому віддається 1 перевага, R - -СН3. У варіанті, якому віддається 1 перевага, R - -хлор, -фтор або -бром. У варіанті, 1 якому віддається перевага, R - -хлор. У варіанті, 1 якому віддається перевага, R - -фтор. У варіанті, 1 якому віддається перевага, R - -бром. У варіанті, 2 якому віддається перевага, R - -галоген. У варіа2 нті, якому віддається перевага, R - -СН3. У варі2 анті, якому віддається перевага, R - -хлор, -фтор або -бром. У варіанті, якому віддається перевага, 2 R - -хлор. У варіанті, якому віддається перевага, 2 R - -фтор. У варіанті, якому віддається перевага, 2 R - -бром. У варіанті, якому віддається перевага, 1 2 R - -хлор та R - -хлор. У варіанті, якому відда3 ється перевага, R - -Н. У варіанті, якому відда3 ється перевага, R - -галоген. 4 У варіанті, якому віддається перевага, R . У варіанті, якому віддається пере . 4 У варіанті, якому віддається перевага, R є 4 вага, R є У варіанті, якому віддається перевага, R 4 6 та R - водень. У варіанті, . є 4 якому віддається перевага, R є варіанті, якому віддається перевага, 4 R . У є . У варіанті, якому віддається пере. У варіанті, якому віддається перевага, R 4 є 25 94741 26 4 У варіанті, якому віддається перевага, R є якому віддається . У варіанті, 4 перевага, R є абo . 5 У варіанті, якому віддається перевага, R - . У варіанті, 4 R є якому віддається перевага, якому віддається . У перевага, варіанті, 4 R є 8 8 N(R )(R ), , 5 У варіанті, якому віддається перевага, R - SО2-(С1-С4)-алкіл, . 5 абo У варіанті, якому віддається перевага, R . 5 У варіанті, якому віддається перевага, R є 8 , де R - (С1-С3)-алкіл (факультативно заміщений 1-3 гало генами) або . У варіанті, якому відда 5 ється перевага, R є . У варіанті, 5 якому віддається перевага, R; є . У 6 варіанті, якому віддається перевага, R - -Н. У 6 варіанті, якому віддається перевага, R - 6 галоген. У варіанті, якому віддається перевага, R - -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами). У варіанті, якому віддається перева7 га, R - -Н. У варіанті, якому віддається перевага, 7 R - -галоген або -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами). У варіанті, якому від7 дається перевага, R - -галоген. У варіанті, якому 7 віддається перевага, R - -(С1-С4)-алкіл (факультативно заміщений 1-3 галогенами). У варіанті, 8 якому віддається перевага, R незалежно у кожному випадку є -Н. У варіанті, якому віддається 8 перевага, R незалежно у кожному випадку є -(С1С6)-алкіл (факультативно заміщений 1-3 галоге8 нами). У варіанті, якому віддається перевага, R незалежно у кожному випадку є -СН3. У варіанті, 9 якому віддається перевага, R - -Н. У варіанті, 9 якому віддається перевага, R - -галоген. У варіа7 9 нті, якому віддається перевага, R - -фтор та R -фтор. Варіантом здійснення цього винаходу, якому віддається перевага, є сполука, яка має назву (R)-3-[3,5-диxлop-4'-(4-тpифтopмeтилпiпepидин-1карбоніл)біфеніл-4-ілметил]-1-(4гідроксипіперидин-1-іл)піролідин-2-он, або фармацевтично прийнятні солі такої сполуки. Варіантом здійснення цього винаходу, якому віддається перевага, є сполука, яка має назву (R)-3-[3,5дихлор-4'-(4,4-дифторпіперидин-1карбоніл)біфеніл-4-ілметил]-1-(4гідроксипіперидин-1-іл)піролідин-2-он, або фар 27 мацевтично прийнятні солі такої сполуки. Іншим варіантом здійснення цього винаходу є описані у цьому документі нові проміжні сполуки, які є корисними для виготовлення інгібіторів ΙΙ--HSD1 формули І та варіантів здійснення, описаних у цьому документі. Іншим варіантом здійснення цього винаходу є описані у цьому документі нові проміжні сполуки, які є корисними для виготовлення (R)-3-[3,5-дихлор-4'-(4трифторметилпіперидин-1-карбоніл)біфеніл-4ілметил]-1-(4-гідроксипіперидин-1-іл)піролідин-2ону або фармацевтично прийнятної солі цієї сполуки. У пацієнтів, що хворіють на діабет типу 2, часто розвивається "резистентність до інсуліну", наслідком якої є аномальний гомеостаз глюкози та гіперглікемія, яка призводить до посилення захворюваності та передчасної смертності. Аномальний гомеостаз глюкози пов'язаний з ожирінням, гіпертензією та змінами у метаболізмі ліпідів, ліпопротеїдів та аполіпопротеїдів. У хворих на діабет типу 2 підвищується ризик розвитку серцево-судинних ускладнень, наприклад, атеросклерозу, ішемічної хвороби серця, інсульту, хвороби периферичних судин, гіпертензії, нефропатії, невропатії та ретинопатії. Отже, регулювання гомеостазу глюкози, метаболізму ліпідів, ожиріння та гіпертензії за допомогою терапевтичних засобів має важливе значення у профілактиці та лікуванні цукрового діабету. Багато пацієнтів, які мають резистентність до інсуліну, але у яких не розвився діабет типу 2, також знаходяться у групі ризику розвитку "синдрому X" або "метаболічного синдрому". Метаболічний синдром характеризується резистентністю до інсуліну разом із абдомінальним ожирінням, гіперінсулінемією, високим кров'яним тиском, низьким рівнем ліпопротеїдів високої густини (HDL), високим рівнем ліпопротеїдів дуже низької густини (VLDL), гіпертензією, атеросклерозом, ішемічною хворобою серця та хронічною нирковою недостатністю. Ці пацієнти знаходяться у групі підвищеного ризику розвитку серцево-судинних ускладнень, перелічених вище, спільно з розвитком явного цукрового діабету або без нього. Внаслідок здатності до інгібування ΙΙ--HSD1, згадані сполуки є корисними у лікуванні різноманітних хворобливих станів та розладів, при яких інгібування ΙΙ--HSD1 є сприятливим чинником. Ці розлади та хворобливі стани визначено у цьому описі як "діабетичні розлади" та "розлади типу метаболічного синдрому". Фахівець у галузі здатен ідентифікувати "діабетичні розлади" та "розлади типу метаболічного синдрому" за ознакою участі діяльності ΙΙ--HSD1 або у патофізіології розладу, або у гомеостатичній реакції на розлад. Таким чином, ці сполуки можуть знайти застосування, наприклад, для попередження, лікування або полегшення захворювань, патологічних станів або пов'язаних із ними симптомів чи наслідків "діабетичних розладів" та "розладів типу метаболічного синдрому". До "діабетичних розладів" та "розладів типу метаболічного синдрому" належать, проте без обмеження цим переліком, діабет, діабет типу 1, 94741 28 діабет типу 2, гіперглікемія, гіперінсулінемія, аномалія розвитку базофільних клітин, посилене функціонування базофільних клітин внаслідок відновлення першої фази реакції, пов'язана з прийманням їжі гіперглікемія, перешкоджання апоптозу, порушення рівня глюкози натщесерце (IFG), метаболічний синдром, гіпоглікемія, гіперкаліємія/гіпокаліємія, нормалізування рівнів глюкагону, підвищення відношення рівня ліпопротеїдів низької густини до рівня ліпопротеїдів високої густини (LDL/HDL), послаблення схильності до нерегулярного приймання їжі, розлади харчування, втрата маси тіла, синдром полікістозного яєчника (PCOS), ожиріння як наслідок діабету, латентний аутоімунний діабет дорослих (LADA), інсульт, трансплантація острівцевих клітин, дитячий діабет, обумовлений вагітністю діабет, пізні ускладнення діабету, мікроальбумінурія/макроальбумінурія, нефропатія, ретинопатія, невропатія, діабетичне вкривання ніг виразками, послаблена рухливість кишечнику внаслідок застосування глюкагону, синдром скороченої тонкої кишки, застосування антидіаретиків, посилена шлункова секреція, послаблення кровотоку, еректильна дисфункція, глаукома, післяопераційний стрес, загоєння пошкоджень тканин органів, спричинених післяішемічною реперфузією, ішемічне пошкодження серця, серцева недостатність, застійна серцева недостатність, інсульт, інфаркт міокарда, аритмія, передчасна смерть, антиапоптоз, загоєння ран, порушення толерантності до глюкози (IGT), синдром резистентності до інсуліну, метаболічний синдром, синдром X, гіперліпідемія, дисліпідемія, гіпертригліцеридемія, гіперліпопротеїнемія, гіперхолестеринемія, артеріосклероз, в тому числі атеросклероз, глюкагономи, гострий панкреатит, серцево-судинні захворювання, гіпертензія, гіпертрофія серця, шлунково-кишкові розлади, ожиріння, діабет як наслідок ожиріння, діабетична дисліпідемія тощо. Отже, цей винахід також пропонує спосіб лікування "діабетичних розладів" та "розладів типу метаболічного синдрому" при послабленні та/або усуненні одного або декількох небажаних побічних ефектів, пов'язаних із чинними способами лікування. Крім того, цей винахід пропонує сполуку формули І або фармацевтичну сіль цієї сполуки, або фармацевтичну композицію, яка містить сполуку формули І або фармацевтичну сіль цієї сполуки та фармацевтично прийнятні носій, розріджувач або наповнювач: для застосування при інгібуванні активності ΙΙ--HSD1; для застосування при інгібуванні опосередкованої активністю ΙΙ--HSD1 клітинної реакції у ссавців; для застосування при зниженні рівня глюкози в крові у ссавців; для застосування у лікуванні захворювань, які виникають внаслідок надмірної активності ΙΙ--HSD1; для застосування у лікуванні діабетичних та інших розладів типу метаболічного синдрому у ссавців; та для застосування у лікуванні діабету, метаболічного синдрому, ожиріння, гіперглікемії, атеросклерозу, ішемічної хвороби серця, інсульту, невропатії та лікуванні ран. Отже, способи за 29 цим винаходом охоплюють профілактичне та терапевтичне застосування сполуки формули І. Цей винахід також пропонує застосування сполуки формули І або фармацевтичної солі цієї сполуки для виготовлення лікарського засобу для інгібування активності ΙΙ--HSD1; для виготовлення лікарського засобу для інгібування опосередкованої активністю ΙΙ--HSD1 клітинної реакції у ссавців; для виготовлення лікарського засобу для зниження рівня глюкози у крові у ссавців; для виготовлення лікарського засобу для лікування захворювань, спричинених надмірною активністю ΙΙ--HSD1; для виготовлення лікарського засобу для лікування діабетичних та інших розладів типу метаболічного синдрому у ссавців; та для виготовлення лікарського засобу для попередження або лікування діабету, метаболічного синдрому, ожиріння, гіперглікемії, атеросклерозу, ішемічної хвороби серця, інсульту, невропатії та погіршеного загоєння ран. Цей винахід також пропонує спосіб лікування патологічних станів, які виникли внаслідок надмірної активності ΙΙ--HSD1 у ссавців; спосіб інгібування активності ΙΙ--HSD1 у ссавців; спосіб інгібування опосередкованої активністю ΙΙ--HSD1 клітинної реакції у ссавців; спосіб зниження рівня глюкози в крові у ссавців; спосіб лікування діабетичних та інших розладів типу метаболічного синдрому у ссавців; спосіб попередження або лікування діабету, метаболічного синдрому, ожиріння, гіперглікемії, атеросклерозу, ішемічної хвороби серця, інсульту, невропатії та погіршеного загоєння ран; згадані способи включають введення в організм ссавця, який потребує такого лікування, сполуки формули І або фармацевтично прийнятної солі такої сполуки, або фармацевтичної композиції, яка містить сполуку формули І або фармацевтичну сіль цієї сполуки та фармацевтично прийнятні носій, розріджувач або наповнювач, у кількості, що забезпечує інгібування активності ΙΙ--HSD1. Крім того, цей винахід пропонує фармацевтичну композицію, яка містить сполуку формули І або фармацевтичну сіль цієї сполуки та фармацевтично прийнятні носій, розріджувач або наповнювач: адаптовану для застосування при інгібуванні активності ΙΙ--HSD1; адаптовану для застосування при інгібуванні опосередкованої активністю ΙΙ--HSD1 клітинної реакції; адаптовану для застосування при зниженні рівня глюкози в крові у ссавців; адаптовану для застосування у лікуванні діабетичних та інших розладів типу метаболічного синдрому у ссавців; та адаптовану для застосування у попередженні або лікуванні діабету, метаболічного синдрому, ожиріння, гіперглікемії, атеросклерозу, ішемічної хвороби серця, інсульту, невропатії та лікуванні ран. За ще одним аспектом винаходу згадані сполуки застосовують у комбінації з одною або декількома додатковими активними речовинами у будь-якому придатному співвідношенні. Такі додаткові активні речовини можуть, наприклад, бути вибрані з групи, яку складають протидіабетичні засоби, засоби проти ожиріння, засоби для зниження артеріального тиску, засоби для ліку 94741 30 вання ускладнень, спричинених діабетом або пов'язаних із ним, та засоби для лікування ускладнень та розладів, спричинених ожирінням або пов'язаних із ним. У поданих нижче переліках вказано кілька груп таких комбінацій. Мається на увазі, що кожний з названих засобів можна об'єднувати з іншими названими засобами, створюючи додаткові комбінації. Таким чином, за ще одним варіантом здійснення винаходу, згадані сполуки можна застосовувати у комбінації з одним або декількома протидіабетичними засобами. До придатних протидіабетичних засобів належать інсулін, аналоги та похідні інсуліну, наприклад, засоби, розкриті у ЕР 792290 (Novo В29 Nordisk A/S), наприклад, N -тетрадеканоїл-dеs(В30)-людський інсулін, ЕР 214826 та ЕР 705275 В28 (Novo Nordisk A/S), наприклад, Аsр -людський B28 інсулін, US 5,504,188 (Eli Lilly), наприклад, Lys B29 Pro -людський інсулін, ЕР 368187 (Aventis), наприклад, Lantus, похідні GLP-1 та GLP-1, наприклад, розкриті у заявці WO 98/08871 (Novo Nordisk A/S), а також активні при пероральному введенні гіпоглікемічні засоби. До активних при пероральному застосуванні гіпоглікемічних засобів, яким віддається перевага, належать імідазоліни, сульфонілсечовини, бігуаніди, меглітиніди, оксадіазолідиндіони, тіазолідиндіони, сенсибілізатори до інсуліну, посилювачі секреції інсуліну, наприклад, глімепірид, інгібітори -глюкозидази, засоби, які впливають на залежні від АТР калієві канали базофільних клітин, наприклад, активатори калієвих каналів, наприклад, засоби, розкриті у заявках WO 97/26265, WO 99/03861 та WO 00/37474 (Novo Nordisk A/S), або мітиглінід, або блокатори калієвих каналів, наприклад, BTS-67582, натеглінід, антагоністи глюкагону, наприклад, засоби, розкриті у заявках WO 99/01423 та WO 00/39088 (Novo Nordisk A/S та Agouron Pharmaceuticals, Inc.), антагоністи GLP-1, інгібітори DPP-IV (дипептидилпептидазиIV), інгібітори РТР-ази (протеїн-тирозинфосфатази), інгібітори печінкових ферментів, що беруть участь у стимулюванні глюконеогенезу та/або глюкогенолізу, модулятори засвоєння глюкози, активатори глюкокінази (GK), наприклад, засоби, розкриті у заявках WO 00/58293, WO 01/44216, WO 01/83465, WO 01/83478, WO 01/85706, WO 01/85707 та WO 02/08209 (HoffmanLa Roche) або розкриті у заявках WO 03/00262, WO 03/00267 та WO 03/15774 (AstraZeneca), Інгібітори GSK-3 (глюкоген-синтази-кінази-3), сполуки, які модифікують метаболізм ліпідів, наприклад, протиліпідемічні засоби, наприклад, інгібітори HMG СоА (статини), сполуки, які зменшують споживання їжі, ліганди PPAR (рецептора, що активується проліфератами пероксисом), в тому числі підтипів PPAR-альфа, PPAR-гамма та PPAR-дельта та агоністи RXR (рецептора ретиноїду X), наприклад, ALRT-268, LG-1268 або LG1069. За іншим варіантом здійснення згадані сполуки застосовують у комбінації з інсуліном або В29 аналогом чи похідним інсуліну, наприклад, N тетрадеканоїл-dеs-(В30)-людським інсуліном, 31 В28 94741 В28 В29 Аsр -людським інсуліном, Lуs -Рrо людським інсуліном, Lantus, або композицією, яка містить один або декілька із цих засобів. За іншим варіантом здійснення цього винаходу згадані сполуки застосовують у комбінації із сульфонілсечовиною, наприклад, глібенкламідом, гліпізидом, толбутамідом, хлоропамідемом, толазамідом, глімепридом, гліказидом та глібуридом. За іншим варіантом здійснення цього винаходу згадані сполуки застосовують у комбінації з бігуанідом, наприклад, метформіном. За ще одним варіантом здійснення цього винаходу згадані сполуки застосовують у комбінації з меглітинідом, наприклад, репаглінідом або натеглінідом. За ще одним варіантом здійснення цього винаходу згадані сполуки застосовують у комбінації з тіазолідиндіоновим сенсибілізатором до інсуліну, наприклад, троглітазоном, циглітазоном, піоглітазоном, розиглітазоном, ізаглітазоном, дарглітазоном, енглітазоном, CS-011/СІ-1037 або Τ 174, або зі сполуками, розкритими у заявках WO 97/41097, WO 97/41119, WO 97/41120, WO 00/41121 та WO 98/45292 (Dr. Reddy's Research Foundation). За ще одним варіантом здійснення цього винаходу згадані сполуки можуть застосовуватися у комбінації із сенсибілізатором до інсуліну, наприклад, GI 262570, YM-440, МСС-555, JTT-501, ARH039242, KRP-297, GW-409544, CRE-16336, ARH049020, LY510929, МВХ-102, CLX-0940, GW501516, або зі сполуками, розкритими у заявках WO 99/19313, WO 00/50414, WO 00/63191, WO 00/63192, WO 00/63193, наприклад, рагаглітазаром (NN 622 або (-)DRF 2725) (Dr. Reddy's Research Foundation) та у WO 00/23425, WO 00/23415, WO 00/23451, WO 00/23445, WO 00/23417, WO 00/23416, WO 00/63153, WO 63196, WO 00/63209, WO 00/63190 та WO 00/63189 (Novo Nordisk A/S). За іншим варіантом здійснення цього винаходу згадані сполуки застосовують у комбінації з інгібітором -глюкозидази, наприклад, воглібозом, емїглітатом, міглітолом або акарбозою. За іншим варіантом здійснення цього винаходу згадані сполуки застосовують у комбінації із засобом, який впливає на залежні від АТР калієві канали базофільних клітин, наприклад, із толбутамідом, глібенкламідом, гліпізидом, гліказидом, BTS-67582 або репаглінідом. За ще одним варіантом здійснення цього винаходу згадані сполуки можуть застосовуватися у комбінації з натеглінідом. За ще одним варіантом здійснення цього винаходу згадані сполуки застосовують у комбінації з протиліпідемічним засобом або протигіперліпідемічним засобом, наприклад, холестираміном, колестиполом, клофібратом, гемфіброзилом, ловастатином, правастатином, симвастатином, пітавастатином, розувастатином, пробуколом, декстротироксином, фенофібратом або аторвастином. 32 За ще одним варіантом здійснення цього винаходу згадані сполуки застосовують у комбінації зі сполуками, які зменшують споживання їжі. За іншим варіантом здійснення цього винаходу згадані сполуки застосовують у комбінації з декількома вищезгаданими сполуками, наприклад, у комбінації з метформіном та сульфонілсечовиною, наприклад, із глібуридом; сульфонілсечовиною та акарбозою; з натеглінідом та метформіном; із репаглінідом та метформіном, акарбозою та метформіном; із сульфонілсечовиною, метформіном та троглітазоном; з інсуліном та сульфонілсечовиною; з інсуліном та метформіном; з інсуліном, метформіном та сульфонілсечовиною; з інсуліном та троглітазоном; з інсуліном та ловастатином; тощо. Загальні терміни, вжиті при описуванні сполук в цьому документі, мають свої звичайні значення. У значенні, вживаному у цьому описі, терміни "(С1-С3)-алкіл", "(С1-С4)-алкіл" або "(С1-С6)-алкіл" означають нерозгалужені або розгалужені ланцюгові насичені аліфатичні групи, які містять вказану кількість атомів вуглецю, наприклад, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, вторбутил, трет-бутил тощо. Термін "(С1-С6)алкокси(група)" означає групу С1-С6-алкіл, приєднану через атом кисню, та охоплює, наприклад, такі групи, як метокси-, етокси-, н-пропокси-, ізопропоксигрупа тощо. Термін "галоген" означає фтор, хлор, бром та йод. Термін "(С3-С8)циклоалкіл" означає насичену або частково насичену карбоциклічну групу, яка містить 3-8 атомів вуглецю, у типовому варіанті 3-7 атомів вуглецю. Приклади (С3-С8)-циклоалкілів охоплюють, проте без обмеження ними, циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил, тощо. Термін "факультативно заміщений" або "факультативні замісники" у значенні, вживаному у цьому описі, означає, що групи, про які йде мова, або незаміщені, або заміщені одним або декількома з перелічених замісників. Якщо групи, про які йде мова, заміщені декількома замісниками, ці замісники можуть бути однаковими або різними. Крім того, у разі вживання термінів "незалежно (один від одного або від інших)", "незалежно (один від одного або від інших) є" та "незалежно (один від одного або від інших) вибрані" мається на увазі, що групи, про які йде мова, можуть бути однаковими або різними. Деякі з визначених у цьому описі термінів можуть зустрічатися у структурній формулі більше одного разу, і в цьому випадку кожний з термінів буде визначений незалежно від інших. Мається на увазі, що прикладами пацієнтів, які охоплюються терміном "пацієнт", є морські свинки, собаки, кішки, щури, миші, хом'ячки та примати, в тому числі люди. До пацієнтів, яким віддається перевага, належать люди. Термін "пацієнт" охоплює свійських тварин. Свійськими тваринами є тварини, яких вирощують для виробництва продуктів харчування. Прикладами свійських тварин є жуйні тварини, наприклад, корови, бики, телички, бички, вівці, буйволи, бізони, кози та антилопи. Іншими прикладами свійсь 33 ких тварин є свині та птиця (свійська птиця), наприклад, кури, качки, індики та гуси. Серед пацієнтів, які потребують лікування, перевага віддається ссавцям, зокрема, людям. Терміни "лікування" та "лікувати" у значенні, вживаному в цьому описі, охоплюють їхні загальновживані значення, тобто лікування та догляд хворого для цілей профілактики, зменшення ризику наслідків або розвитку даного стану або захворювання, запобігання, обмеження, полегшення, покращання, сповільнення, припинення, затримання або обернення напряму розвитку чи тяжкості, та тримання під контролем та/або лікування наявних характеристик певного захворювання, розладу або патологічного стану, описаного в цьому документі, в тому числі полегшення або зняття симптомів чи ускладнень, або вилікування чи усунення захворювання, розладу або патологічного стану. Цей винахід охоплює відповідно терапевтичне лікування та/або профілактичні заходи. У значенні, вживаному у цьому описі, термін "терапевтично ефективна кількість" означає кількість сполуки за цим винаходом, яка здатна полегшити симптоми різноманітних патологічних станів, описаних у цьому документі. Конкретна доза сполуки, яка вводиться відповідно до цього винаходу, безперечно, визначається конкретними обставинами випадку, в тому числі, наприклад, сполукою, яку вводять, шляхом введення, станом пацієнта та патологічним станом, який підлягає лікуванню. Термін "композиція" означає фармацевтичну композицію та охоплює фармацевтичні препарати, які містять активний інгредієнт (інгредієнти), в тому числі сполуку (сполуки) формули І, та інертний інгредієнт (інгредієнти), які складають носій. Відповідно, фармацевтичні композиції за цим винаходом охоплюють будь-які композиції, виготовлені шляхом змішування сполуки за цим винаходом та фармацевтично прийнятного носія. Термін "практично чистий" означає чисту кристалічну форму сполуки, яка містить більше ніж приблизно 90% бажаної кристалічної форми, перевага віддається вмісту більше ніж приблизно 95% бажаної кристалічної форми. Термін "придатний розчинник" означає будьякий розчинник або суміш розчинників, інертний стосовно до здійснюваної реакції, який достатньою мірою розчиняє реагенти, забезпечуючи середовище, в якому проходить бажана реакція. Термін "одинична дозована форма" означає фізично дискретну одиницю лікарської форми, придатну для введення одиничної дози в організм людей та інших живих істот; кожна така одиниця містить заздалегідь визначену кількість активного інгредієнта, розраховану на досягнення бажаного терапевтичного ефекту, у комбінації з придатним фармацевтичним носієм. Сполуки за цим винаходом можуть мати один або декілька хіральних центрів та можуть існувати у різноманітних стереоізомерних конфігураціях. Внаслідок присутності цих хіральних центрів сполуки за цим винаходом можуть мати форму рацематів, індивідуальних енантіомерів або су 94741 34 мішей енантіомерів, а також у формі діастереомерів та сумішей діастереомерів. Усі такі рацемати, енантіомери, діастереомери та суміші охоплюються обсягом цього винаходу незалежно від того, є вони чистими, частково очищеними або неочищеними сумішами. У прикладах, наведених у цьому описі, якщо представлена молекула, що містить хіральний центр або центри відомої конфігурації, то її стереохімія відображена у назві та у структурній формулі молекули. Якщо ця стереохімія невідома або не визначена, то вона не відображена у назві та у структурній формулі молекули. Варіанти здійснення винаходу включають наведені в цьому описі приклади, і, незважаючи на те, що поданий приклад стосується однієї хіральної форми або певної конформації, або її солі, подальші варіанти здійснення винаходу охоплюють усі інші стереоізомерні форми та/або конформації сполук, описаних у прикладах, а також фармацевтично прийнятні солі таких сполук. Ці варіанти включають будь-які ізольовані енантіомери, діастереомери та/або конформери таких структур, а також будь-які суміші, що містять декілька форм. Крім того, діастереомери можуть утворюватися, якщо молекула включає подвійний зв'язок або частково насичену циклічну систему, або більше одного центра асиметрії, або зв'язок, повертання навколо якого утруднене. Мається на увазі, що обсяг винаходу охоплює будь-які діастереомери, як виділені, чисті або частково очищені діастереомери, так і їх суміші. Крім того, деякі сполуки за цим винаходом можуть існувати у різних таутомерних формах, і мається на увазі, що обсяг винаходу охоплює будь-які таутомерні форми, які можуть утворювати ці сполуки. Термін "енантіомерне збагачення" у значенні, вживаному у цьому описі, означає збільшення кількості одного енантіомера у порівнянні з кількістю іншого. Звичайний спосіб вираження досягнутого енантіомерного збагачення грунтується на понятті енантіомерного надлишку, або "ее", який визначають, використовуючи таке рівняння: 1 2 2 ее=[(Ε -E )/(Ε1+Ε )]100, 1 2 де Ε - кількість першого енантіомера, а Е кількість другого енантіомера. Таким чином, якщо початкове відношення двох енантіомерів становить 50:50, наприклад, якщо вони присутні у рацемічній суміші, та виконано енантіомерне збагачення, достатнє для досягнення кінцевого відношення 70:30, то значення ее стосовно до першого енантіомера становить 40%. Однак якщо кінцеве відношення становить 90:10, то ее стосовно до першого енантіомера становить 80%. Перевага віддається значенням ее понад 90%, більша перевага - ее понад 95% та особлива перевага - ее понад 99%. Пересічному фахівцю у галузі легко визначити енантіомерне збагачення, використовуючи стандартні способи та методики, наприклад, газову або високоефективну рідинну хроматографію на колонці з хіральним сорбентом. Вибір придатного хірального сорбенту, елюенту та умов, необхідних для розділення пари 35 енантіомерів, лежить у межах знань пересічного фахівця у галузі. Крім того, пересічний фахівець у галузі може одержати конкретні стереоізомери та енантіомери сполук формул I-IV, використовуючи добре відомі способи та процеси, наприклад, описані у монографіях Жак та ін. (J. Jacques, et al., "Enantiomers. Racemates. and Resolutions". John Wiley and Sons, Inc., 1981) та Ельєль та Уайлен (E.L. Eliel and S.H. Wilen, "Stereochemistry of Organic Compounds", (Wiley-Interscience 1994), а також у заявці ЕР-А-838448, опублікованій 29 квітня 1998 p. Прикладами способів розділення є перекристалізація та хіральна хроматографія. Сполуки формули І можуть бути одержані фахівцем у галузі із застосуванням різноманітних способів; деякі з них ілюстровано поданими нижче методиками та схемами. Конкретна послідовність стадій, необхідних для одержання сполуки формули І, залежить від конкретної сполуки, яку слід синтезувати, вихідних сполук та відносної міцності зв'язування груп-замісників. Реагенти або вихідні матеріали легко доступні для фахівця у галузі і, в разі відсутності їх на ринку, можуть бути без утруднень синтезовані пересічним фахівцем у галузі за стандартними методиками, загальновживаними у галузі, а також за різноманітними способами та схемами, поданими нижче. Подані нижче схеми, описи підготовчих синтезів, приклади та методики наведено з метою кращого роз'яснення практики здійснення цього винаходу, і їх у жодному разі не слід розглядати як такі, що обмежують обсяг винаходу. Фахівцям у галузі зрозуміло, що можливі численні модифікації згаданих способів без відходу від суті та обсягу цього винаходу. Усі публікації, згадані в цьому описі, є характерними для рівня знань фахівця у галузі, якої стосується цей винахід. Оптимальну тривалість реакцій, вказаних у схемах, описах підготовчих синтезів, прикладах та методиках, можна визначити шляхом спостерігання за ходом реакцій із застосуванням звичайних хроматографічних способів. Крім того, перевага віддається проведенню реакцій за цим винаходом в інертній атмосфері, наприклад, в аргоні чи азоті. Вибір розчинника, як правило, не має вирішального значення, за умови, що застосовуваний розчинник є інертним відносно виконуваної реакції та достатньою мірою розчиняє реагенти для забезпечення здійснення бажаної реакції. Перевага віддається виділенню та очищенню сполук перед їх застосуванням у подальших реакціях. Деякі сполуки можна кристалізувати з реакційного розчину під час їх утворення з подальшим відділенням фільтруванням, або можна видаляти з реакційної суміші розчинник шляхом екстрагування, випарювання або декантування. Проміжні сполуки та кінцеві продукти формули І можна в разі бажання додатково очищати відомими способами, наприклад, перекристалізацією або хроматографією на твердих сорбентах, наприклад, на силікагелі або оксиді алюмінію. Для досвідченого фахівця зрозуміло, що не всі замісники є сумісними з усіма умовами реакцій. Такі сполуки можна захистити або модифіку 94741 36 вати на відповідних стадіях синтезу способами, добре відомими у галузі. Терміни та абревіатури, уживані у поданих схемах, описах підготовчих синтезів, прикладах та методиках, мають їхні звичайні значення, якщо не вказано інше. Наприклад, при вживанні в цьому описі подані нижче терміни мають вказані значення: "psi" означає фунти на кв. дюйм (1 фунт на кв. дюйм=6,9 кПа); "ТШХ (TLC)" означає хроматографію в тонкому шарі; "РХВЕ (HPLC)" означає рідинну хроматографію високої ефективності; "Rf" означає коефіцієнт затримання; "Rt" означає час затримання; "" означає зсув відносно тетраметилсилану у мільйонних частках; "МС (MS)" означає мас-спектрометрію, "спостережувана маса" відповідає [М+Н], якщо не вказано інше. "MS(APCi) означає мас-спектрометрію з хімічною іонізацією при атмосферному тиску, "УФ" означає 1 ультрафіолетову спектрометрію, " H ЯМР" означає спектрометрію ядерного магнітного резонансу на протонах. "РХМС (LCMS)" означає рідинну хроматографію з мас-спектрометрією, "ГХ/МС (GC/MS)" означає газову хроматографію/масспектрометрію. "ІЧ" означає інфрачервону спектрометрію, а переліки максимумів поглинання, вказані для ІЧ спектрів, охоплюють не всі максимуми, а тільки ті, що становлять інтерес. "К.т." означає кімнатну температуру. "THF" означає тетрагідрофуран, "LAH" означає алюмогідрид літію, "LDA" означає діізопропіламід літію, "DMSO" означає диметилсульфоксид, "DMF" означає диметилформамід, "EtOAc" означає етилацетат, "Pd-C" означає паладій на вугіллі, "DCM" означає дихлорметан, "DMAP" означає диметиламінопіридин, "LiHMDS" означає гексаметиддисилазанід літію, "TFA" означає трифтороцтову кислоту, "EDAC" означає гідрохлорид N-етил-N'(3-диметиламінопропіл)карбодііміду, "НОВТ" означає 1-гідроксибензотриазол, "Bn-9-BBN" означає бензил-9-борабіцикло[3,3,1]нонан, "Pd(dppf)Cl2" означає [1,1'-біс(дифенілфосфіно)фероцен)дихлорпаладій(ІІ), "EDCI" означає гідрохлорид N-етил-N'-(3диметиламінопропіл)карбодііміду, "DBU" означає 1,8-діазабіцикло[5,4,0]ундецен-7, "TBSCl" означає трет-бутилдиметилсиланілоксиметилхлорид, "NBS" означає N-бромсукцинімід, "TsOH" означає пара-толуолсульфокислоту, "DCE" означає дихлоретан, "DAST" означає трифторид (діетиламіно)сірки, "ЕА/Н" означає суміш етилацетат/гексан, "Pd2(dba)3" означає біс(дибензиліденацетон)паладій, "BINAP" означає 2,2'-біс(дифенілфосфіно-1,1'-бінафталін, "NMP" означає N-метилпіролідин, "TMSCN" означає триметилсилілціанід, "TBAF" означає фторид тетрабутиламонію, "Tf2O" означає трифторметансульфоновий ангідрид, "TBSO" означає третбутилдиметилсиланілоксигрупу, "ОТГ означає трифторметансульфонат, МеТі(Оі-Рr)3 означає триізопропоксид метилтитану, "ВBr3" означає трибромід бору, "РBr3" означає трибромід фосфору, "Pd(PPh3)4" означає тетракіс(трифенілфосфін)паладій (0), "ОАс" означає ацетат, "DME" означає диметилетан, "Et2O" означає діетиловий простий ефір, "(Ph3P)4Pd" означає 37 94741 38 1 тетракіс(трифенілфосфін)паладій (0), "DMFDMA" означає Ν,Ν-диметилацеталь диметилформаміду, "Et3N" означає триетиламін, "tBu" означає трет-бутил, "DIPEA" означає діізопропілетиламін, "EDC" означає гідрохлорид (3диметиламінопропіл)-3-етилкарбодііміду, "НОАс" означає оцтову кислоту, "bос" означає третбутоксикарбоніл. У структурних формулах "Ph" означає феніл, "Me" означає метил, "Et" означає етил, "Вn" означає бензил, "МеОН" означає метанол, "OTf" означає трифторметансульфонат, "TIPSO" означає триізопропілсиланілоксигрупу, "TBSO" означає третбутилдиметилсиланілоксигрупу, "NaBH(OAc)3" означає триацетоксиборгідрид натрію, "[Ir(cod)Cl]2" означає дихлорбіс((1,2,5,6-ета)-1,5циклооктадієн)дііридій. Приклади, представлені в цьому описі, ілюструють заявлений винахід та жодним чином не призначені для обмеження обсягу цього винаходу. Назви сполук, описаних у методиках підготовчих синтезів та прикладах, утворено із застосуванням пакетів програм AutoNom 2.2 у складі ChemDraw Ultra або AutoNom 2000 у складі MDL ISIS/Draw, версія 2.5 SP1, продуктах фірми MDL Information Systems, Inc., або, у відповідних випадках, згідно з Chemical Abstracts Services. Спектри H-ЯМР реєструвалися на спектрометрі Varian INOVA 400 МГц у вказаному розчиннику. Для одержання даних РХМС застосовано прилад Agilent HP1100, обладнаний масспектрометром (Agilent MSD SL). Як стаціонарна фаза застосовувався сорбент Waters Xterra C18 (колонка 2,150 мм, розмір зерен сорбенту 3,5 мкм), а як стандартна процедура елюювання градієнт 5-100% ацетонітрилу в метанолі (50:50) з домішкою 0,2% форміату амонію протягом 3,5 хв, із подальшим елююванням 100% елюенту В протягом 0,5 хв при температурі колонки 50°С та швидкості потоку 1,0 мл/хв. Інша стандартна процедура - градієнт 5-100% ацетонітрилу в метанолі (50:50) з домішкою 0,2% форміату амонію протягом 7,0 хв із подальшим елююванням 100% елюенту В протягом 1,0 хв при температурі колонки 50°С та швидкості потоку 1,0 мл/хв. Додатковий мас-спектроскопічний (MS) аналіз виконувався на приладі Agilent MSD (для контурного аналізу) за стандартною методикою аналізу з інжекцією потоку (Flow injection Analysis, FIA), без колонки при швидкості потоку 0,5 мл/хв елюенту 80% МеОН із домішкою 6,5 мМ ацетату амонію та тривалості циклу 30 с. Як показано на Схемі А, факультативно заміщений фенол (1) захищають (наприклад, групою TBSCl) для одержання сполуки 2, після чого сполуку 2 перетворюють у альдегід (3). Сполуку 3 вводять у реакцію зі сполукою, яка містить групу захисту (Pg) та відщеплювану групу (Lg), одержуючи простий ефір 4. Група Pg може бути -СН3 або -СН2-фенілом, а група Lg може бути мезилатом або галогеном. У варіанті, якому віддається перевага, сполукою Lg-Pg є І-СН3 або Br-СН2феніл. Одержаний альдегід відновлюють, одер жуючи спирт (5), після чого перетворюють у сполуку 6. У варіанті, якому віддається перевага, сполуку 5 галогенують за допомогою РBr3, одержуючи 2-бром-метильне похідне. Введення та відщеплення груп захисту від сполук з одержанням сполук формули І тощо добре відоме фахівцю у галузі та розкрито у літературі. (Дивись, наприклад: Greene and Wuts, Protective Groups in Organic Synthesis. Third Edition, John Wiley and Sons Inc., 1999). 39 94741 40 На Схемі В показано стереоселективний синтез проміжної сполуки 9. Сполуку 7 одержують шляхом ацилювання наявного на ринку (R)-4бензилоксазолідин-2-ону 4-пентеноїлхлоридом. Після цього її алкілують факультативно заміще ною сполукою 6 (дивись Схему А), та одержують сполуку 8. Сполуку 8 окиснюють для одержання альдегідної проміжної сполуки 9, застосовуючи озон та трифенілфосфін або тетроксид осмію та окиснювач, наприклад, метаперйодат натрію. Як показано на Схемі С, обробляють альдегід 9 аміном, та одержують гідразид 10. Від сполуки 10 відщеплюють групу захисту для одержання фенольної сполуки 11, після чого одержують трифлатну сполуку 12 шляхом обробки трифтор метансульфоновим ангідридом та основою, наприклад, піридином. Сполуку (12) піддають реакції сполучення, застосовуючи як реагент фенілборну кислоту та каталізатор, наприклад, тетракістрифенілфосфінпаладій, для одержання 41 складного ефіру (13), який гідролізують, одержуючи кислоту (14). Кислоту (14) сполучають з аміном, застосовуючи стандартні умови амідного 94741 42 сполучення, наприклад, 1,1'-карбоніддіімідазол, та одержують амід (15). Як показано на Схемі D, сполуку (16) піддають реакції сполучення, застосовуючи як реагент фенілборну кислоту та каталізатор, наприклад, тетракістрифенілфосфінпаладій, для одержання сполуки 17. Як показано на Схемі Е, сполуку (16) піддають реакції сполучення, застосовуючи як реагент фенілборну кислоту та каталізатор, наприклад, тетракістрифенілфосфшпаладій, для одержання сполуки 19. Амід (20), бензоізоксазол (21) та індазол (22) одержують зі сполуки 19, застосовуючи описані реагенти. 43 Як показано на Схемі G, обробляють альдегід 9 аміном, та одержують гідразид 26, який обробляють сульфонатом триізопропілсилілтрифторметану, одержуючи сполуку 27. Від сполуки 27 відщеплюють групу захисту, застосовуючи паладій на вугіллі, та одержують фенол (28), який обробляють трифторметансульфоновим ангідридом, одержуючи сполуку 29. Піддають сполуку (29) реакції сполучення, застосовуючи як реагент 94741 44 фенілборну кислоту та каталізатор, наприклад, тетракістрифенілфосфінпаладій, для одержання складного ефіру (30), який гідролізують, одержуючи кислоту (31). Кислоту (31) сполучають з аміном, застосовуючи стандартні умови амідного сполучення, наприклад, 1,1'-карбоніддіімідазол, та одержують амід (32). Амід (32) після цього обробляють кислотою, наприклад, трифтороцтовою кислотою, одержуючи амін (33). 45 Як показано на Схемі Н, сполуку (34) піддають реакції сполучення, застосовуючи як реагент фенілборну кислоту (R-B(OH)2) та каталізатор, 94741 46 наприклад, тетракістрифенілфосфінпаладій, для одержання сполуки 35, яку обробляють трифтороцтовою кислотою для одержання сполуки 36. Як показано на Схемі І, сполуку (37) піддають реакції сполучення, застосовуючи як реагент фенілборну кислоту (R-B(OH)2) та каталізатор, наприклад, тетракістрифенілфосфінпаладій, для одержання сполуки 38. Як показано на Схемі J, бензоізоксазол (40), індазол (41) та амід (42) одержують зі сполуки 39, застосовуючи описані реагенти. 47 Підготовчий синтез 1 2,6-дихлор-4-гідроксибензальдегід Розчиняють 3,5-дихлорфенол (1 кг, 6,13 моль) у 3 л диметилформаміду (DMF) та охолоджують до 0°С. Додають імідазол (918,74 г, 6,75 моль), після чого трет-бутиддиметилсилілхлорид (1017,13 г, 6,75 моль). Нагрівають суміш до кімнатної температури та перемішують протягом 15 хв. Виливають у воду (6 л), та екстрагують суміш діетиловим ефіром (4 л). Промивають одержаний органічний шар водою двічі, 10% водним розчином хлориду літію та розсолом, а потім сушать над сульфатом натрію. Фільтрують, та концентрують у вакуумі, одержуючи трет-бутил-(3,5дихлорфенокси)диметилсилан (1700 г) у вигляді масла. Розчиняють трет-бутил-(3,5дихлорфенокси)диметилсилан (425 г, 1,5 моль) у 4 л безводного тетрагідрофурану, та охолоджують до -68°С. Повільно додають 1,1 екв. emopбутиллітію (103,1 г, 1,61 моль) при -68°С (приблизно 1,75 год). Після завершення додавання перемішують одержану реакційну суміш при -70°С протягом 30 хв. Додають диметилформамід (168,5 г, 2,3 моль), та перемішують одержану реакційну суміш при -70°С протягом 1 год. Додають 1 Μ розчин хлористоводневої кислоти у воді (3,5 л), та дозволяють реакційній суміші нагрітися до кімнатної температури. Виливають реакційну суміш у діетиловий ефір (5 л), промивають водою та розсолом. Су 94741 48 шать над сульфатом натрію, та концентрують у вакуумі до одержання оранжевої твердої речовини. Розтирають із холодним дихлорметаном, та фільтрують, одержуючи 250 г (80%) блідо-жовтої твердої речовини. Підготовчий синтез 2 2,6-дихлор-4-метоксибензальдегід Змішують 2,6-дихлор-4-гідроксибензальдегід (120 г, 628,24 ммоль) та карбонат калію (173,65 г, 1256,5 ммоль) у 900 мл диметилформаміду, та обробляють йодметаном (107 г, 753,9 ммоль). Перемішують одержану реакційну суміш при кімнатній температурі протягом 3 год. Відфільтровують тверді домішки, та виливають фільтрат у 6 л води. Відділяють фільтруванням тверду речовину, промивають декілька разів водою, сушать на повітрі, та розчиняють у етилацетаті. Промивають водою, після чого розсолом, а потім сушать над сульфатом натрію. Фільтрують, та концентрують у вакуумі до об'єму приблизно 100 мл, при досягненні такого об'єму починається випадання твердої речовини. Фільтрують, потім концентрують фільтрат, одержуючи другу порцію продукту. Промивають гексаном, змішують всі тверді продукти, та сушать у вакуумі, одержуючи 1 112,3 г злегка забарвленої твердої речовини: H ЯМР (400 МГц, CDCl3) 10,41 (s, 1Н), 6,90 (s, 2H), 3,87 (s, 3Н). Підготовчий синтез 3 2,6-дихлор-4-бензилоксибензальдегід 49 Обробляють суміш 2,6-дихлор-4гідроксибензальдегіду (250 г, 1,3 моль) та карбонату калію (361,8 г, 2,62 моль) у 2 л диметилфо1 рмаміду бензилбромідом (268,64 г, 1,57 моль). Перемішують одержану реакційну суміш при кімнатній температурі протягом 1 год. Відфільтровують тверді домішки, та виливають фільтрат у 12 л води. Відділяють тверду речовину фільтруванням, промивають декілька разів водою, сушать на повітрі, та розчиняють у етилацетаті. Сушать над сульфатом магнію, фільтрують, та концентрують у вакуумі до приблизно 1,5 л. Дозволяють відстоятися протягом ночі, після чого фільтрують. Промивають одержану тверду речовину мінімальною кількістю гексану та сушать у вакуумі. Концентрують одержаний фільтрат у вакуумі, та розтирають залишок із гексаном, одержуючи другу порцію продукту, яку потім змішують із першою порцією, одержуючи в сумі 245 г білих кристалів. Повторюють вищевказані операції для одержання третьої порції продукту (80 г) у вигляді світло-жовто-коричневого порошку (зага1 льний вихід 88%): H ЯМР (400 МГц, DMSO-d6) 10,26 (s, 1Н), 7,43 (m, 5H), 7,28 (s, 2H), 5,25 (s, 2H). Підготовчий синтез 4 (2,6-дихлор-4-метоксифеніл)метанол Суспендують 2,6-дихлор-4метоксибензальдегід (112 г, 546 ммоль) у 1500 мл етанолу, та охолоджують у льодяній бані до 7°С. Додають порціями боргідрид натрію (20,67 г, 546 ммоль), одержуючи розчин. Відстороняють льодяну баню, та перемішують протягом 2 год. Обережно додають реакційну суміш до насиченого розчину хлориду амонію (приблизно 4 л), та перемішують до повного гасіння. Екстрагують дихлорметаном (31 л), та сушать змішані органічні екстракти над сульфатом натрію. Фільтрують, та концентрують у вакуумі, одержуючи 113 г 1 світло-жовто-коричневої твердої речовини: H ЯМР (400 МГц, CDCl3) 6,86 (s, 2H), 4,86 (s, 2H), 3,78 (s, 3Н), 2,07 (s, 1Н). Підготовчий синтез 5 (2,6-дихлор-4-бензилоксифеніл)метанол Вказану в заголовку сполуку одержують практично за методикою Підготовчого синтезу 4. 1 H ЯМР (DMSO-d6) 7,38 (m, 4Н), 7,33 (m, 1Н), 7,12 (s, 2H), 5,14 (s, 2H), 5,05 (t, 1H), 4,59 (d, 2H). Підготовчий синтез 6 2-бромметил-1,3-дихлор-5-метоксибензол Розчиняють (2,6-дихлор-4метоксифеніл)метанол (113 г, 545,76 ммоль) у 1200 мл безводного тетрагідрофурану, та охолоджують до 0°С у атмосфері азоту. Додають у атмосфері азоту РBr3 (59,1 г, 218,3 ммоль), та перемішують при 0°С протягом 30 хв. Виливають у насичений водний розчин бікарбонату натрію, та екстрагують етилацетатом. Сушать, та концентрують у вакуумі, одержуючи 129,4 г продукту у 1 вигляді злегка забарвленої твердої речовини. H ЯМР (CDCl3) 6,88 (s, 2Н), 4,73 (s, 2Н), 3,79 (s, 3Н). Підготовчий синтез 7 2-бромметил-1,3-дихлор-5-бензилоксибензол 94741 50 Вказану в заголовку сполуку одержують практично за методикою Підготовчого синтезу 6 із виходом 89%. ES MS (m/z): 347 (M+1). Підготовчий синтез 8 (R)-4-бензил-3-пент-4-еноїлоксазолідин-2-он Продувають азотом протягом 20 хв 3-горлу круглодонну колбу місткістю 12 л, обладнану механічною мішалкою, датчиком внутрішньої температури, патрубком для впуску азоту та завантажувальною лійкою місткістю 1 л, після чого додають (R)-4-бензил-2-оксазолідинон (250 г, 1,41 моль). Розводять тетрагідрофураном (1,8 л), та охолоджують на бані із сухого льоду з ацетоном до досягнення внутрішньої температури 74°С. Переносять 1,6М гексановий розчин нбутиллітію (970 мл, 1,552 моль) у завантажувальну лійку за допомогою канюлі, та додають його до оксазолідинонового розчину з такою швидкістю, щоб внутрішня температура не підвищувалася вище -65°С. Після завершення додавання залишають одержану реакційну суміш при перемішуванні на охолоджувальній бані протягом 30 хв. Переносять 4-пентеноїлхлорид (175 мл, 1,585 моль) у завантажувальну лійку, та додають його краплями до розчину аніону протягом 25 хв. Перемішують одержану реакційну суміш протягом 45 хв на охолоджувальній бані. Відстороняють охолоджувальну баню, та перемішують реакційну суміш 18 год, причому вона повільно досягає кімнатної температури. Розводять суміш 1-н. водним розчином хлористоводневої кислоти (1,5 л) та діетиловим ефіром (1,0 л). Розділяють шари, та промивають органічну фазу водою (21 л) та розсолом (1 л). Екстрагують об'єднані водні змиви діетиловим ефіром (1 л). Сушать об'єднані органічні фази над безводним сульфатом магнію, фільтрують, та концентрують, одержуючи 390 г жовтувато-коричневого масла. Очищають цю речовину хроматографією на силікагелі, елююючи сумішшю гексан:етилацетат, та одержують 345 г (94,5%) прозорого жовтого масла. Підготовчий синтез 9 (R)-4-бензил-3-[(S)-2-(4-бензилокси-2,6дихлорбензил)пент-4-еноїл] оксазолідин-2-он Перемішують у атмосфері азоту суміш (R)-4бензил-3-пент-4-еноїлоксазолідин-2-ону (345 г, 1,33 моль) та THF (1,8 л) у 3-горлій круглодонній колбі місткістю 12 л, обладнаній датчиком внутрішньої температури, патрубком для впуску азоту та завантажувальною лійкою, та охолоджують до -75°С. Переносять 1M розчин LiHMDS (1,6 л) у завантажувальну лійку, та додають його у колбу з такою швидкістю, щоб внутрішня температура не підвищувалася вище -60°С. Після завершення додавання залишають одержану реакційну суміш при перемішуванні при -25°С протягом 30 хв, після чого охолоджують до приблизно -60°С. При цій температурі додають частинами твердий 2бромметил-1,3-дихлор-5-бензилоксибензол протягом 5 хв. Після завершення додавання переносять реакційну посудину у ацетонову баню з температурою -10°С, та підтримують внутрішню температуру нижче 10°С протягом 1 год. Охолоджують суміш до 0°С, після чого гасять 2 л 1-н. водного розчину хлористоводневої кислоти. Пе 51 реносять суміш у ділильну лійку місткістю 22 л, та розводять її 2,5 л води та 2 л діетилового ефіру. Розділяють шари, та екстрагують водний шар діетиловим ефіром. Сушать об'єднані органічні фази над безводним сульфатом магнію, фільтрують, та концентрують, одержуючи 800 г в'язкого масла. Очищають хроматографією на силікагелі, елююючи сумішшю гексан:етилацетат, та одержують 597 г (86%) безбарвного масла. Підготовчий синтез 10 (R)-4-((R)-4-бензил-2-оксооксазолідин-3-іл)-3(4-бензилокси-2,6-дихлорбензил)-4-оксомасляний альдегід Охолоджують суміш (R)-4-бензил-3-[(S)-2-(4бензилокси-2,6-дихлорбензил)пент-4еноїл]оксазолідин-2-ону (100 г, 190,68 ммоль) та дихлорметану (800 мл) до -74°С. Барботують озон, який виробляється генератором озону А113 з концентрацією 75%, через одержану реакційну суміш із застосуванням як газу-носія повітря при швидкості 5 куб. футів за хвилину (0,14 3 м /хв) до одержання розчину блакитного кольору (приблизно 3 год). Додають трифенілфосфін (60 г, 228,8 ммоль) у вигляді розчину у 200 мл дихлорметану, та залишають одержану реакційну суміш при перемішуванні до досягнення кімнатної температури протягом ночі. Концентрують розчин у вакуумі, очищають хроматографією на силікагелі, елююючи градієнтом 20-50% етилацетату у гексані, та одержують 82,1 г (82%) продукту у вигляді білої піни: MS (m/z): 526 (М+). Альтернативна методика одержання (R)-4((R)-4-бензил-2-оксооксазолідин-3-іл)-3-(4бензилокси-2,6-дихлорбензил)-4-оксомасляного альдегіду: Обробляють суміш (R)-4-бензил-3-[(S)-2-(4бензилокси-2,6-дихлорбензил)пент-4еноїл]оксазолідин-2-ону (0,96 г, 1,8 ммоль), THF (21 мл) та води (7 мл) 2,5% розчином тетроксиду осмію у wpem-бутанолі (46 мг, 0,18 ммоль). Додають перйодат натрію (1,17 г, 5,5 ммоль), та перемішують одержану реакційну суміш 4 год при кімнатній температурі. Гасять реакційну суміш водою, та екстрагують етилацетатом. Промивають органічну фазу 1-н. водним розчином тіосульфату натрію та розсолом. Сушать органічний шар над сульфатом магнію, фільтрують, та концентрують у вакуумі. Очищають неочищену речовину хроматографією на силікагелі, елююючи сумішшю гексан:етилацетат, та одержують чистий продукт. Концентрують продукт, який містить фракції, у вакуумі, та одержують 0,46 г (48%) бажаного продукту. MS (m/z): 526 (М+). Підготовчий синтез 11 (R)-4-бензил-3-[(S)-2-(4-метокси-2,6дихлорбензил)пент-4-еноїл]оксазолідин-2-он Перемішують суміш (R)-4-бензил-3-пент-4еноїлоксазолідин-2-ону (5,0 г, 19,3 ммоль) та тетрагідрофурану (75 мл) у круглодонній колбі місткістю 250 мл при -75°С. Переносять 2 Μ розчин LDA (14,5 мл) у колбу за допомогою шприца, та додають його у колбу з такою швидкістю, щоб внутрішня температура не підвищувалася вище 60°С. Після завершення додавання залишають одержану реакційну суміш при перемішуванні при 94741 52 -25°С протягом 30 хв, після чого охолоджують до приблизно -60°С. При цій температурі додають розчин 2-бромметил-1,3-дихлор-5метоксибензолу (7,76 г, 28,96 ммоль) у THF (25 мл). Після завершення додавання реакційній суміші дозволяють повільно нагрітися до 0°С, та підтримують внутрішню температуру реакційної суміші біля 0°С протягом 4 год. Гасять реакційну суміш 30 мл водного 1-н. розчину хлористоводневої кислоти. Переносять суміш у ділильну лійку місткістю 500 мл, та розводять її 100 мл води та 100 мл діетилового ефіру. Розділяють шари, та екстрагують водний шар діетиловим ефіром. Сушать об'єднані органічні фази над безводним сульфатом натрію, фільтрують, та концентрують, одержуючи густе масло. Очищають хроматографією на силікагелі, елююючи сумішшю гексан:етилацетат, та одержують 6,65 г (76%) блідожовтого масла. Підготовчий синтез 12 (R)-4-((R)бензил-2-оксооксазолідин-3-іл)-3-(4метокси-2,6-дихлорбензил)-4-оксомасляний альдегід Обробляють суміш (R)-4-бензил-3-[(S)-2-(4метокси-2,6-дихлорбензил)пент-4еноїл]оксазолідин-2-ону (6,65 г, 14,87 ммоль), тетрагідрофурану (140 мл) та води (45 мл) 2,5% розчином тетроксиду осмію у трет-бутанолі (378 мл, 1,487 ммоль). Додають перйодат натрію (9,55 г, 44,63 ммоль), та перемішують одержану реакційну суміш 4 год при кімнатній температурі. Гасять реакційну суміш водою, та екстрагують етилацетатом. Промивають органічну фазу 1-н. водним розчином тіосульфату натрію та розсолом. Сушать органічний шар над сульфатом магнію, фільтрують, та концентрують у вакуумі. Очищають неочищену речовину хроматографією на силікагелі, елююючи сумішшю гексан: етилацетат, та одержують чистий продукт. Концентрують продукт, який містить фракції, у вакуумі, та одержують 3,35 г (49%) бажаного продукту. MS (m/z): 451 (М+). Підготовчий синтез 13 1-нітрозопіперидин-4-ол Додають розчин нітриту натрію (13,8 г, 200 ммоль) у воді (40 мл) до 4-гідроксипіперидину (10,1 г, 100 ммоль) у воді (20 мл). Охолоджують суміш до 0°С на льодяній бані. Додають краплями оцтову кислоту (8,6 мл, 150 ммоль) протягом 20 хв. Після завершення додавання продовжують перемішування при 0°С протягом 30 хв, повільно нагрівають до кімнатної температури та перемішують при кімнатній температурі протягом 5 год. Додають частинами карбонат натрію (15,9 г, 150 ммоль) для гасіння кислоти. Екстрагують одержану реакційну суміш етилацетатом (360 мл), об'єднують органічні фази, сушать над сульфатом натрію, фільтрують, та концентрують, одержуючи бажаний продукт у вигляді жовтого масла. Вихід: 12,9 г, (98%). Підготовчий синтез 14 1-амінопіперидин-4-ол Додають невеликими частинами розчин LAH (1,0 М, 175 мл) протягом 40 хв до 1нітрозопіперидин-4-олу (12,9 г) у THF (250 мл). 53 Після завершення додавання нагрівають одержану реакційну суміш зі зворотним холодильником протягом 3 год, охолоджують на льодяній бані до кімнатної температури, після чого до 0°С. Додають воду (40 мл), повільно нагрівають реакційну суміш до кімнатної температури протягом 10 хв, після чого нагрівають зі зворотним холодильником протягом 30 хв. Відділяють фільтруванням осад, суспендують у гарячому THF (100 мл), та знову фільтрують. Об'єднують одержані фільтрати, сушать над сульфатом натрію, фільтрують, та концентрують, одержуючи бажаний продукт у вигляді блідо-жовтого масла. Вихід: 10,7 г, 94%. Підготовчий синтез 15 3,5-дихлор-4-[1-(4-гідроксипіперидин-1-іл)-2оксопіролідин-3-ілметил]феніловий складний ефір (R)-трифторметансульфонової кислоти Обробляють суміш (R)-3-(2,6-дихлор-4гідроксибензил)-1-(4-гідроксипіперидин-1іл)піролідин-2-ону (0,2 г, 0,558 ммоль), 4диметиламіно-піперидину (0,204 г, 1,676 ммоль) у дихлорметані при 0°С трифторметансульфоновим ангідридом (0,473 г, 1,676 ммоль). Перемішують одержану реакційну суміш протягом 1 год при 0°С та 2 год при кімнатній температурі. Розводять реакційну суміш дихлорметаном, та промивають водою. Сушать органічний шар (Na2SO4), видаляють розчинник у вакуумі, та очищають неочищений продукт на колонці із силікагелем, елююючи градієнтом від 50% етилацетату у гексані до 100% етилацетату, та одержують 0,17 г (62%) вказаної в заголовку сполуки. MS (m/z): 490 (М+). Підготовчий синтез 16 (R)-3',5'-дихлор-3-фтор-4'-[2-оксо-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин3-ілметил]біфеніл-4-карбонітрил Продувають азотом протягом 10 хв суміш 3,5-дихлор-4-[2-оксо-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин3-ілметил]фенілового складного ефіру (R)трифторметансульфонової кислоти (0,18 г, 0,28 ммоль), 3-фтор-4-ціанофенілборної кислоти (0,055 г, 0,33 ммоль), карбонату натрію (0,089 г, 0,84 ммоль) у THF (10 мл) та воді (3 мл). Додають до суміші Рd(РРh3)4 (0,016 г, 0,01 ммоль). Перемішують одержану реакційну суміш при 80°С протягом 1 год. Охолоджують реакційну суміш, розводять етилацетатом, та промивають водою та розсолом. Сушать органічний шар (Na2SO4), видаляють розчинник у вакуумі, одержуючи неочищений продукт, який очищають на колонці із силікагелем, елююючи градієнтом 0-50% етилацетату у гексані, та одержують 0,151 г вказаного у заголовку продукту. MS (m/z): 617 (М+). Підготовчий синтез 17 (R)-4-{3,5-дихлор-4-[2-оксо-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин3-ілметил]фенокси}бензонітрил Перемішують суміш (R)-4-{3,5-дихлор-4-[1-(4гідроксипіперидин-1-іл)-2-оксопіролідин-3ілметил]фенокси}бензонітрилу (0,238 г, 0,5 ммоль) та 15 мл дихлорметану на льодяній бані. Додають піридин (0,205 г, 2,59 ммоль), після чого 94741 54 триізопропілсилілтрифторметансульфонат (0,19 г, 0,62 ммоль). Відстороняють охолоджувальну баню, та перемішують одержану реакційну суміш 1 год при кімнатній температурі. Розводять реакційну суміш дихлорметаном, та промивають водою. Сушать органічну фазу над сульфатом натрію, фільтрують, та концентрують. Очищають одержаний залишок хроматографією на силікагелі, елююючи градієнтом 0-50% етилацетату у гексані, та одержують 0,295 г вказаної в заголовку сполуки. MS (m/z): 615 (М+). Підготовчий синтез 18 (R)-4-{3,5-дихлор-4-[2-оксо-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин3-ілметил]фенокси}бензамід Охолоджують розчин (R)-4-{3,5-дихлор-4-[2оксо-1-(4-триізопропіл-силанілоксипіперидин-1іл)піролідин-3-ілметил]фенокси}-бензонітрилу (0,295 г, 0,48 ммоль) у DMSO (5 мл) на льодяній бані. Додають до розчину карбонат калію (0,331 г, 2,4 ммоль) та пероксид водню (30% у воді, 1 мл), та перемішують одержану реакційну суміш при 0°С протягом 1,5 год, після чого при кімнатній температурі протягом 12 год. Розводять реакційну суміш етилацетатом, та промивають тричі водою, після чого один раз розсолом. Сушать органічну фазу над сульфатом натрію, фільтрують, та концентрують. Очищають одержаний залишок хроматографією на силікагелі, елююючи градієнтом від 40% етилацетату у гексані до 100% етилацетату, одержуючи 0,210 г (69%) вказаної в заголовку сполуки. MS (m/z): 633 (М+). Підготовчий синтез 19 3,5-дихлор-4-(1-морфолін-4-іл-2оксопіролідин-3-ілметил)феніловий складний ефір (R)-трифторметансульфонової кислоти Обробляють суміш (R)-3-(2,6-дихлор-4гідроксибензил)-1-морфолін-4-іл-піролідин-2-ону (0,4 г, 1,16 ммоль) та піридину (10 мл) при 0°С трифторметансульфоновим ангідридом (1,05 г, 3,72 ммоль). Перемішують одержану реакційну суміш протягом 1 год при 0°С, після чого протягом 1 год при кімнатній температурі. Видаляють надлишок піридину у вакуумі, додають до одержаного залишку дихлорметан, та промивають суміш водою та насиченим розчином хлориду амонію. Сушать органічний шар (Na2SO4), видаляють розчинник у вакуумі, та очищають неочищений продукт на колонці із силікагелем, елююючи градієнтом від 50% етилацетату у гексані до 100% етилацетату, та одержують 0,4 г (72%) вказаної в заголовку сполуки. MS (m/z): 477 (М+). Підготовчий синтез 19А (R)-3-(3,5-дихлор-4'-фторбіфеніл-4-ілметил)1-морфолін-4-іл-піролідин-2-он трифторацетат Нагрівають суміш (R)-3,5-дихлор-4-(1морфолін-4-іл-2-оксопіролідин-3ілметил)фенілового складного ефіру трифторметансульфонової кислоти (0,126 г, 0,26 ммоль), 4фторфенілборної кислоти (0,044 г, 0,31 ммоль), карбонату натрію (0,084 г, 0,79 ммоль) у THF (10 мл) та воді (3 мл) до 60°С. До суміші при 60°С додають Pd(PPh3)4 (0,015 г, 0,011 ммоль), після чого підвищують температуру реакційної суміші до 80°С та перемішують протягом 2 год. Охоло 55 джують реакційну суміш, розводять етилацетатом, та промивають водою та розсолом. Сушать органічний шар (Na2SO4), видаляють розчинник у вакуумі, одержуючи неочищений продукт, та очищають його на колонці із силікагелем, елююючи градієнтом від 50% етилацетату у гексані до 100% етилацетату, та одержують 0,102 г (92%) вказаного у заголовку продукту, який потім перетворюють у сіль трифтороцтової кислоти шляхом обробки трифтороцтовою кислотою. MS (m/z): 423 (М+). Підготовчий синтез 19В Tрет-бутиловий складний ефір (R)-3',5'дихлор-4'-(1-морфолін-4-іл-2-оксопіролідин-3ілметил)біфеніл-4-карбонової кислоти Нагрівають суміш 3,5-дихлор-4-(1-морфолін4-іл-2-оксопіролідин-3-ілметил)фенілового складного ефіру (R)-трифторметансульфонової кислоти (0,19 г, 0,4 ммоль), 4-тpетбутилоксикарбонілфенілборної кислоти (0,106 г, 0,48 ммоль), карбонату натрію (0,127 г, 1,2 ммоль) у THF (10 мл) та воді (3 мл) до 60°С. До суміші при 60°С додають Pd(PPh3)4 (0,023 г, 0,02 ммоль), після чого підвищують температуру реакційної суміші до 80°С та перемішують протягом 3 год. Охолоджують реакційну суміш, розводять етилацетатом, та промивають водою та розсолом. Сушать органічний шар (Na2SO4), видаляють розчинник у вакуумі, одержуючи неочищений продукт, після чого очищають на колонці із силікагелем, елююючи 40% етилацетату у гексані, та одержують 0,15 г (74%) вказаного у заголовку продукту. MS (m/z): 461 (М+). Підготовчий синтез 19С Трифторацетат (R)-3',5'-дихлор-4'-(1морфолін-4-іл-2-оксопіролідин-3-ілметил)біфеніл4-карбонової кислоти Обробляють розчин трет-бутилового складного ефіру (R)-3',5'-дихлор-4'-(1-морфолін-4-іл-2оксопіролідин-3-ілметил)біфеніл-4-карбонової кислоти (0,15 г) у дихлорметані (5 мл) трифтороцтовою кислотою (1 мл), та перемішують одержану реакційну суміш при кімнатній температурі протягом 12 год. Видаляють розчинник та надлишок TFA у вакуумі, одержуючи 0,165 г (98%) вказаної в заголовку сполуки. MS (m/z): 449 (М+). Підготовчий синтез 20 (R)-3-(4-бензилокси-2,6-дихлорбензил)-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин2-он Перемішують суміш (R)-3-(4-бензилокси-2,6дихлорбензил)-1-(4-гідроксипіперидин-1іл)піролідин-2-ону (1,23 г, 2,75 ммоль) та 15 мл дихлорметану на льодяній бані. Додають піридин (0,52 г, 6,6 ммоль), після чого триізопропілсилілтрифторметансульфонат (0,924 г, 3,02 ммоль). Відстороняють охолоджувальну баню, та перемішують одержану реакційну суміш 12 год при кімнатній температурі. Розводять реакційну суміш дихлорметаном, та промивають водою. Сушать органічну фазу над сульфатом натрію, фільтрують, та концентрують. Очищають одержаний залишок хроматографією на силікагелі, елююючи сумішшю 4:1 гексан:етилацетат, та одержують 94741 56 1,2 г (72%) вказаної в заголовку сполуки. MS (m/z): 605 (М+). Підготовчий синтез 21 (R)-3-(2,6-дихлор-4-гідроксибензил)-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин2-он Продувають суміш (R)-3-(4-бензилокси-2,6дихлорбензил)-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин2-ону (1,2 г) та 20% гідроксиду паладію (II) на вугіллі (0,24 г) у етанолі(40 мл) азотом та воднем, після чого перемішують у атмосфері водню під тиском 20 фунтів на кв. дюйм (0,138 МПа) протягом 2 год при кімнатній температурі. Фільтрують суміш через целіт, та концентрують одержаний фільтрат у вакуумі, одержуючи 0,95 г (99%) вказаного у заголовку продукту. MS (m/z): 515 (М+). Підготовчий синтез 22 3,5-дихлор-4-[2-оксо-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин3-ілметил]феніловий складний ефір (R)трифторметансульфонової кислоти Обробляють суміш (R)-3-(2,6-дихлор-4гідроксибензил)-1-(4триізопропілсиланілоксипіперидйн-1-іл)піролідин2-ону (20,2 г, 39,3 ммоль), піридину (31,05 г, 393 ммоль) у дихлорметані (200 мл) при 0°С трифторметансульфоновим ангідридом (13,30 г, 47,16 ммоль). Перемішують одержану реакційну суміш протягом 1 год при 0°С, після чого протягом 1 год при кімнатній температурі. Розводять реакційну суміш дихлорметаном, та промивають водою. Сушать органічний шар (Na2SO4), видаляють розчинник у вакуумі, та очищають неочищений продукт на колонці із силікагелем, елююючи 25% етилацетату у гексані, та одержують 22 г (87%) вказаної в заголовку сполуки. MS (m/z): 647 (М+). Підготовчий синтез 23 Метиловий складний ефір (R)-3',5'-дихлор-4'[2-оксо-1-(4-триізопропілсиланілоксипіперидин-1іл)піролідин-3-ілметил]біфеніл-4-карбонової кислоти Нагрівають суміш 3,5-дихлор-4-[2-оксо-1-(4триізопропілсиланіл-оксипіперидин-1іл)піролідин-3-ілметил] фенілового складного ефіру (R)-трифторметансульфонової кислоти (0,52 г, 0,8 ммоль), 4метоксикарбонілфенілборної кислоти (0,174 г, 0,966 ммоль), карбонату натрію (0,256 г, 2,41 ммоль) у THF (20 мл) та воді (6 мл) до 60°С. До суміші при 60°С додають Pd(PPh3)4 (0,046 г, 0,04 ммоль), підвищують температуру реакційної суміші до 80°С та перемішують протягом 1 год. Охолоджують одержану реакційну суміш, розводять етилацетатом, та промивають водою та розсолом. Сушать органічний шар (Na2SO4), видаляють розчинник у вакуумі, одержуючи неочищений продукт, який очищають на колонці із силікагелем, елююючи градієнтом від 25% до 50% етилацетату у гексані, та одержують 0,49 г (96%) вказаного у заголовку продукту. MS (m/z): 633 (М+). Підготовчий синтез 24 57 (R)-3',5'-дихлор-4'-[2-оксо-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин3-ілметил]біфеніл-4-карбонова кислота Обробляють розчин метилового складного ефіру (R)-3',5'-дихлор-4'-[2-оксо-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин3-ілметил]біфеніл-4-карбонової кислоти (0,36 г) у THF (5 мл) та метанолі (2 мл) 2-н. розчином LiOH (5 мл), та перемішують суміш при кімнатній температурі протягом 3 год. Розділяють суміш між етилацетатом (25 мл) та 1-н. розчином HCl (10 мл). Сушать органічний шар (Na2SO4), та видаляють розчинник у вакуумі, одержуючи 0,34 г (97%) вказаної в заголовку сполуки. MS (m/z): 619 (М+). Підготовчий синтез 25 (R)-3-[3,5-дихлор-4'-(4трифторметилпіперидин-1-карбоніл)біфеніл-4ілметил]-1-(4-триізопропілсиланілоксипіперидин1-іл)піролідин-2-он Обробляють розчин (R)-3',5'-дихлор-4'-[2оксо-1-(4-триізопропіл-силанілоксипіперидин-1іл)піролідин-3-ілметил]біфеніл-4-карбонової кислоти (0,337 г, 0,545 ммоль) у СН2Сl2 (20 мл) 1,1'карбонілдіімідазолом (0,177 г, 1,09 ммоль), та перемішують протягом 45 хв при кімнатній температурі. Обробляють одержану реакційну суміш гідро хлоридом 4-трифторметилпіперидину (0,155 г, 0,818 ммоль) та діізопропілетиламіном (0,106 г, 0,818 ммоль), та перемішують протягом 12 год при кімнатній температурі. Завантажують суміш у колонку із силікагелем, та елююють її градієнтом від 25% до 50% етилацетату у гексані, одержуючи 0,34 г (84%) вказаної в заголовку сполуки. MS (m/z): 754 (М+). Підготовчий синтез 26 (R)-3-[3,5-дихлор-4'-(4,4-дифторпіперидин-1карбоніл)біфеніл-4-ілметил]-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин2-он Обробляють розчин (R)-3',5'-дихлор-4'-[2оксо-1-(4-триізопропіл-силанілоксипіперидин-1іл)піролідин-3-ілметил]біфеніл-4-карбонової кислоти (4,0 г, 6,45 ммоль) у СН2Сl2 (40 мл) 1,1'карбонілдіімідазолом (2,09 г, 12,91 ммоль), та перемішують протягом 1 год при кімнатній температурі. Обробляють одержану реакційну суміш гідрохлоридом 4,4-дифторпіперидину (1,53 г, 9,68 ммоль) та діізопропілетиламіном (1,69 г, 9,68 ммоль), та перемішують протягом 12 год при кімнатній температурі. Завантажують суміш у колонку із силікагелем, та елююють її градієнтом від 25% до 35% етилацетату у гексані, одержуючи 3,8 г (81%) вказаної в заголовку сполуки. MS (m/z): 722 (М+). Підготовчий синтез 27 (R)-3-[3,5-дихлор-4'-(морфолін-4карбоніл)біфеніл-4-ілметил]-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин2-он Обробляють розчин (R)-3',5'-дихлор-4'-[2оксо-1-(4-триізопропіл-силанілоксипіперидин-1іл)піролідин-3-ілметил]біфеніл-4-карбонової кислоти (0,2 г, 0,32 ммоль) у СН2Сl2 (15 мл) 1,1'карбоніддіімідазолом (0,10 г, 0,65 ммоль), та пе 94741 58 ремішують протягом 1 год при кімнатній температурі. Обробляють одержану реакційну суміш морфоліном (0,06 г, 0,65 ммоль), та перемішують протягом 12 год при кімнатній температурі. Завантажують суміш у колонку із силікагелем, та елююють її градієнтом від 25% до 35% етилацетату у гексані, одержуючи 0,20 г (90%) вказаної в заголовку сполуки. MS (m/z): 688 (М+). Підготовчий синтез 28 (R)-3-[4-(3-амінобензо[d]ізоксазол-6-іл)-2,6дихлорбензил]-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин2-он Перемішують суміш ацетогідроксамової кислоти (0,046 г, 0,61 ммоль), карбонату калію (0,169 г, 1,22 ммоль) у DMF (5 мл) та воді (2 мл) при кімнатній температурі протягом 10 хв. До суміші додають розчин (R)-3',5'-дихлор-3-фтор-4'-[2оксо-1-(4-триізопропілсиланілоксипіперидин-1-іл)піролідин-3-ілметил]біфеніл-4-карбонітрилу (0,151 г, 0,244 ммоль), та перемішують одержану реакційну суміш при кімнатній температурі протягом 5 год, після чого при 60°С протягом 1 год. Охолоджують реакційну суміш, розводять етилацетатом (40 мл), та промивають тричі водою (15 мл кожного разу) та розсолом (15 мл). Потім сушать органічний шар над сульфатом натрію, фільтрують, та, концентрують у вакуумі. Очищають одержаний залишок хроматографією на силікагелі, елююючи градієнтом 0-50% етилацетату у гексані, та одержують 0,095 г (62%) вказаної в заголовку сполуки. MS (m/z): 631 (M+). Підготовчий синтез 29 (R)-3-(2-хлор-4-гідроксибензил)-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин-2-он Продувають азотом та воднем суміш (R)-3-(4бензилокси-2,6-'дихлорбензил)-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин2-ону (36,61 г) та 20% гідроксиду паладію (II) на вугіллі (7,2 г) у етанолі (250 мл) та метанолі (250 мл), та перемішують у атмосфері водню протягом 12 год при кімнатній температурі. Фільтрують суміш через целіт. Концентрують одержаний фільтрат у вакуумі, та очищають неочищену суміш на колонці із силікагелем, елююючи градієнтом від 25% до 35% етилацетату у гексані, та одержують 0,75 г вказаного у заголовку продукту. MS (m/z): 481 (М+). Підготовчий синтез 30 3-хлор-4-[(R)-2-оксо-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин3-ілметил]феніловий складний ефір трифторметансульфонової кислоти Обробляють суміш (R)-3-(2-хлор-4гідроксибензил)-1-(4-триізопропілсиланілоксипіперидин-1-іл)піролідин-2-ону (0,75 г, 1,56 ммоль), піридину (1,26 г, 15,6 ммоль) у дихлорметані (200 мл) при 0°С трифторметансульфоновим ангідридом (0,66 г, 2,34 ммоль), та перемішують одержану реакційну суміш протягом с 1 год при 0 С, після чого 1 год при кімнатній температурі. Розводять реакційну суміш дихлорметаном, та промивають водою. Сушать органічний шар за допомогою Na2SO4, видаляють розчинник 59 у вакуумі, та очищають неочищений продукт на колонці із силікагелем, елююючи 25% етилацетату у гексані, та одержують 0,94 г (98%) вказаної в заголовку сполуки. MS (m/z): 613 (М+). Підготовчий синтез 31 Метиловий складний ефір 3'-хлор-4'-[(R)-2оксо-1-(4-триізопропілсиланілоксипіперидин-1іл)піролідин-3-ілметил]біфеніл-4-карбонової кислоти Нагрівають суміш 3-хлор-4-[(R)-2-оксо-1-(4триізопропілсиланіл-оксипіперидин-1іл)піролідин-3-ілметил]фенілового складного ефіру трифторметансульфонової кислоти (0,83 г, 1,35 ммоль), 4-метоксикарбонілфенілборної кислоти (0,29 г, 1,62 ммоль), карбонату натрію (0,43 г, 4,06 ммоль) у THF (20 мл) та воді (6 мл) до 60°С. До суміші при 60°С додають Рd(РРh3)4 (0,08 г, 0,07 ммоль). Підвищують температуру реакційної суміші до 80°С та перемішують протягом 1 год. Охолоджують одержану реакційну суміш, розводять етилацетатом, та промивають водою та розсолом. Сушать органічний шар за допомогою Na2SO4, видаляють розчинник у вакуумі, та очищають на колонці із силікагелем, елююючи градієнтом 0-50% етилацетату у гексані, та одержують 0,76 г (93%) вказаного у заголовку продукту. MS (m/z): 599 (М+). Підготовчий синтез 32 3'-хлор-4'-[(R)-2-оксо-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин3-ілметил]біфеніл-4-карбонова кислота Обробляють розчин метилового складного ефіру 3'-хлор-4'-[(R)-2-оксо-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин3-ілметил]біфеніл-4-карбонової кислоти (0,76 г) у THF (15 мл) 2-н. розчином LiOH (15 мл) при кімнатній температурі протягом 5 год. Розподіляють суміш між етилацетатом (25 мл) та 1-н. розчином HCl (10 мл). Сушать органічний шар за допомогою Na2SO4, та видаляють розчинник у вакуумі, одержуючи 0,73 г (98%) вказаної в заголовку сполуки. MS (m/z): 585 (М+). Підготовчий синтез 33 (R)-3-[3'-хлор-4'-(4-трифторметилпіперидин1-карбоніл)біфеніл-4-ілметил]-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин2-он Обробляють розчин 3'-хлор-4'-[(R)-2-оксо-1(4-триізопропілсиланілоксипіперидин-1іл)піролідин-3-ілметил]біфеніл-4-карбонової кислоти (0,2 г, 0,34 ммоль) у СН2Сl2 (15 мл) 1,1'карбонілдіїмідазолом (0,11г, 0,68 ммоль), та перемішують протягом 60 хв при кімнатній температурі. Обробляють одержану реакційну суміш гідрохлоридом 4-трифторметил-піперидину (0,10 г, 0,51 ммоль) та діізопропілетиламіном (0,07 г, 0,51 ммоль), та перемішують протягом 12 год при кімнатній температурі. Завантажують суміш у колонку із силікагелем, та елююють її градієнтом 0-50% етилацетату у гексані, одержуючи 0,12 г (49%) вказаної в заголовку сполуки. MS (m/z): 720 (М+). Підготовчий синтез 34 (R)-3-[3-хлор-4'-(4,4-дифторпіперидин-1карбоніл)біфеніл-4-ілметил]-1-(4 94741 60 триізопропілсиланілоксипіперидин-1-іл)піролідин2-он Обробляють розчин 3'-хлор-4'-[2-оксо-1-(4триізопропілсиланілоксипіперидин-1-іл)піролідин3-ілметил]біфеніл-4-карбонової кислоти (0,2 г, 0,34 ммоль) у СН2СІ2 (15 мл) 1,1'карбонілдіімідазолом (0,11 г, 0,68 ммоль), та перемішують протягом 1 год при кімнатній температурі. Обробляють одержану , реакційну суміш гідрохлоридом 4,4-дифторпіперидину (0,08 г, 0,51 ммоль) та діізопропілетиламіном (0,07 г, 0,51 ммоль), та перемішують протягом 12 год при кімнатній температурі. Завантажують суміш у колонку із силікагелем, та елююють її градієнтом 0-50% етилацетату у гексані, одержуючи 0,15 г (64%) вказаної в заголовку сполуки. MS (m/z): 688 (М+). Підготовчий синтез 35 (S)-4-бензил-3-[(R)-2-(4-бензилокси-2,6дихлорбензил)пент-4-еноїл]оксазолідин-2-он Розчиняють 4-бензил-3-пент-4еноїлоксазолідин-2-он (2,21 г, 8,52 ммоль) у 25 мл безводного тетрагідрофурану. Охолоджують до -78°С. Додають LiN(TMS)2 (10,23 мл, 10,23 ммоль). Перемішують протягом 30 хв при тій самій температурі. Додають 5-бензилокси-2бромметил-1,3-дихлорбензол (3,10 г, 8,95 ммоль) у 5 мл THF. Одержану реакційну суміш повільно нагрівають до кімнатної температури. Гасять насиченим розчином хлориду амонію. Екстрагують у етилацетаті. Розділяють на колонці, одержуючи 3,09 г (69%) продукту. Підготовчий синтез 36 (S)-4-((S)-4-бензил-2-оксооксазолідин-3-іл)-3(4-бензилокси-2,6-дихлорбензил)-4-оксомасляний альдегід Розчиняють 4-бензил-3-[2-(4-бензилокси-2,6дихлорбензил)пент-4-еноїл]оксазолідин-2-он (3,09 г, 5,89 ммоль) у суміші 3/1 THF/вода (100 мл). Додають OsO4 (5,99 г, 0,59 ммоль) та NaIO4 (3,82 г, 17,86 ммоль). Перемішують одержану суспензію протягом 3 год при кімнатній температурі. Гасять 1M розчином тіосульфату натрію (300 мл). Екстрагують у етилацетаті. Розділяють на колонці, одержуючи 0,885 г (28,5%) 4-(4бензил-2-оксооксазолідин-3-іл)-3-(4-бензилокси2,6-дихлорбензил)-4-оксомасляного альдегіду. Приклад 1 (R)-3-(4-бензилокси-2,6-дихлорбензил)-1морфолін-4-іл-піролідин-2-он Перемішують суміш дихлоретану (25 мл), Nаміноморфоліну (0,204 г, 2 ммоль), (R)-4-((R)-4бензил-2-оксооксазолідин-3-іл)-3-(4-бензилокси2,6-дихлорбензил)-4-оксомасляного альдегіду (1,064 г, 2 ммоль) та триацетоксиборгідриду натрію (1,266 г, 6 ммоль) при кімнатній температурі протягом 12 год. Нагрівають одержану реакційну суміш до 60°С та перемішують протягом 3 год. Охолоджують реакційну суміш, розводять дихло
ДивитисяДодаткова інформація
Назва патенту англійськоюInhibitors of 11-beta-hydroxysteroid dehydrogenase 1
Автори англійськоюBush Julie Kay, Hansen Marvin Martin, Li Renhua, Mabry Thomas Edward, Snyder Nancy June, Wallace Owen Brendan, Xu Yanping
Назва патенту російськоюИнгибиторы 11-бета-гидроксистероиддегидрогеназы 1
Автори російськоюБуш Джули Кей, Хансен Марвин Мартин, Ли Женьхуа, Мебри Томас Эдвард, Снайдер Ненси Джун, Уоллис Оуэн Брендан, Ю Янпинь
МПК / Мітки
МПК: C07D 401/12, C07D 207/26, A61K 31/4015, A61K 31/4025, A61P 3/10
Мітки: 11-бета-гідроксистероїддегідрогенази, інгібітори
Код посилання
<a href="https://ua.patents.su/41-94741-ingibitori-11-beta-gidroksisteroddegidrogenazi-1.html" target="_blank" rel="follow" title="База патентів України">Інгібітори 11-бета-гідроксистероїддегідрогенази 1</a>
Попередній патент: Спосіб збільшення індуктивного зв’язку кабелів тягової мережі з обмоткою енергоприймача безконтактного електровоза та пристрій для його реалізації
Наступний патент: Гербіцидна суміш, гербіцидна композиція, способи їх одержання та способи боротьби з небажаною рослинністю
Випадковий патент: Хемілюмінесцентний газоаналізатор оксидів азоту