Похідні сульфонаміду для лікування захворювань, спосіб їх одержання (варіанти), фармацевтична композиція на їх основі, проміжна сполука
Номер патенту: 82283
Опубліковано: 25.03.2008
Автори: Моузес Йан Брайан, Джеймс Кім, Браун Алан Деніел, Томсон Ніколас Маррей, Лейн Шарлотт Еліс Луіз
Формула / Реферат
1. Сполука загальної формули (1):
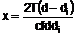
де (CH2)n-C(=O)Q1 група розташована в мета- або пара-положенні, R1 і R2, незалежно, вибирають з Н і С1-С4 алкілу, n є 0, 1 або 2 і Q1 є групою, що вибирають з:
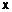
і групи *-NR11-Q2-A, де р є 1 або 2, Q2 є С1-С4 алкілен, R11 є Н або С1-С4 алкіл і А є піридил, С3-С10 циклоалкіл, згаданий циклоалкіл, необов'язково, містить місток з одним або декількома атомами вуглецю, тетрагідропіраніл, піперидиніл, необов'язково, заміщений бензилом, тетрагідротіопіраніл або група
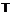 ,
,
де R3, R4, R5, R6 і R7 є однаковими або різними і вибрані з Н, С1-С4 алкілу, OR8, SR9, гало, CN, CF3, OCF3, COOR9, SO2NR9R10, CONR9R10, NR9R10, NHCOR10 і феніл;
де R8 є С1-С4 алкіл і R9 і R10 є однаковими або різними і вибрані з Н або С1-С4 алкілу і * вказує точку приєднання до карбонільної групи;
або, якщо прийнятно, її фармацевтично прийнятні солі і/або ізомери, таутомери, сольвати або їх ізотопні модифікації.
2. Сполука згідно з пунктом 1, де Q1 є NH-Q2-A, де Q2 є СН2 і А є циклогексил, тетрагідротіопіраніл, піперидиніл, необов'язково, заміщений бензилом, або нафтил.
3. Сполука згідно з пунктом 1, де Q1 є
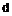 ,
,
де R3, R4, R5 і R6 є Н.
4. Сполука згідно з пунктом 1, де Q1 є групою *-NH-Q2-A, де Q2 є С1-С4 алкілен і А є групою
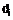 ,
,
де R3, R4, R5, R6 і R7 є однаковими або різними і вибрані з Н, С1-С4 алкілу, OR8, SR9, CN, гало, CF3, OCF3, SO2NR9R10, CONR9R10, NR9R10, NHCOR10 і фенілу, за умови, що принаймні 2 з R3-R7 є еквівалентними Н;
де R8 є С1-С4 алкіл і R9 і R10 є однаковими або різними і вибрані з Н або С1-С4 алкілу.
5. Сполука згідно з пунктом 4, де Q2 є -СН2-, -(СН2)2- або -(СН2)3-.
6. Сполука згідно з пунктом 5, де Q2 є -СН2-.
7. Сполука згідно з будь-яким з пунктів 4-6, де А є групою
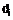 ,
,
де R3, R4, R5, R6 і R7 є однаковими або різними і вибрані з Н, СН3, ОСН2-СН3, SCH3, гало, CF3, OCF3, фенілу, диметиламіно, CN, трет-бутилу, за умови, що принаймні 2 з R3-R7 є еквівалентними Н.
8. Сполука згідно з пунктом 7, де R3, R4, R5, R6 і R7 є однаковими або різними і вибрані з Н, СН3, Сl, F, CF3, за умови, що принаймні 2 з R3-R7 є еквівалентними Н.
9. Сполука згідно з будь-яким з пунктів 1-8, де R1 є Н або С1-С4 алкіл і R2 є С1-С4 алкіл.
10. Сполука згідно з пунктом 9, де R1 є Н або СН3 і R2 є СН3.
11. Сполука згідно з пунктом 10, де n є 1.
12. Сполука згідно з будь-яким з пунктів 1-11 як (R,R)-стереоізомер.
13. Сполука згідно з будь-яким з пунктів 1-11, де (CH2)n-C(=O)Q1 група розташована в мета-положенні.
14. Сполука згідно з пунктом 1, яку вибирають з групи, що містить:
N-бензил-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)-N-(4-метоксибензил)ацетамід,
2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)-N-(2-метоксибензил)ацетамід,
N-(2-етоксибензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)-N-(3-метоксибензил)ацетамід,
2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)-N-(4-метилбензил)ацетамід,
2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)-N-(2-метилбензил)ацетамід,
2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)-N-(3-метилбензил)ацетамід,
N-(3,4-диметоксибензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-(2,4-диметоксибензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-(3,5-диметоксибензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-(4-хлорбензил)-2-(3-{2-[((2R-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-(2-хлорбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-(3-хлорбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-(4-фторбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-(2,4-дихлорбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-(3,4-дихлорбензил)-2-(3-{2-[((2R)-2-пдрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-(4-трет-бутилбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-
[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-(2-хлор-6-фторбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-(2,3-диметилбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-(3,5-дихлорбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-[3,5-біс(трифторметил)бензил]-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-(3,4-диметилбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-(2,5-дихлорбензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)-N-(2-фенілетил)ацетамід,
2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)-N-(3-фенілпропіл)ацетамід,
N-(2,3-дихлорбензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
N-(2,4-дихлор-6-метилбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-(циклогексилметил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-(2-хлор-6-метилбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-(2-етоксибензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
N-(3,4-диметилбензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
N-(3,4-дихлорбензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N-(3-фенілпропіл)ацетамід,
N-(циклогексилметил)-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
N-(2-хлор-6-фторбензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
N-(2-хлор-4-фторбензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-
[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
N-(3,5-дихлорбензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}-етил)амiно]пропіл}фенiл)-N-[4-(трифторметил)бензил]ацетамід,
N-(2,5-дихлорбензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
N-[4-фтор-2-(трифторметил)бензил]-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
N-[4-фтор-3-(трифторметил)бензил]-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
N-[2-фтор-4-(трифторметил)бензил]-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
N-(2,4-дихлор-6-метилбензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
N-[4-хлop-3-(тpифтopмeтил)бeнзил]-2-(3-{(2R)-2-[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
N-[2-хлор-5-(трифторметил)бензил]-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
N-[3,5-біс(трифторметил)бензил]-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
N-[3-фтор-5-(трифторметил)бензил]-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
N-(3,4-дихлорбензил)-2-(4-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-[2-хлор-5-(трифторметил)бензил]-2-(4-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-[4-хлор-3-(трифторметил)бензил]-2-(4-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-[3,5-біс(трифторметил)бензил]-2-(4-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-[3-фтор-5-(трифторметил)бензил]-2-(4-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-[2-фтор-5-(трифторметил)бензил]-2-(4-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-[4-фтор-2-(трифторметил)бензил]-2-(4-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
N-[4-фтор-3-(трифторметил)бензил]-2-(4-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-
[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
2-(4-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N-(2-метоксибензил)ацетамід,
N-(2-етоксибензил)-2-(4-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
N-бeнзил-2-(4-{(2R)-2-[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
2-(4-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N-(3-фенілпропіл)ацетамід,
N-(2,3-дигідро-1H-інден-2-іл)-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N-(2-метоксибензил)ацетамід,
N-бeнзил-2-(3-{(2R)-2-[((2R)-2-гiдpoкcи-2-{4-riдpoкcи-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N-(2-фенілетил)ацетамід,
2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N-(мезитилметил)ацетамід,
2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-
[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N-(2,3,6-трихлорбензил)ацетамід,
2-(3-{2-[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3-[(мeтилcyльфoнiл)aмiнo]фeнiл}eтил)aмiнo]-2-метилпропіл}феніл)-N-[3-(трифторметил)бензил]ацетамід,
N-(2,3-дихлорбензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
N-(3-хлop-4-метилбензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
2-(3-{2-[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3-[(мeтилcyльфoнiл)aмiнo]фeнiл}eтил)aмiнo]-2-метилпропіл}феніл)-N-[2-(метилтіо)бензил]ацетамід,
2-(3-{2-[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3-[(мeтилcyльфoнiл)aмiнo]фeнiл}eтил)aмiнo]-2-метилпропіл}феніл)-N-[4-(метилтіо)бензил]ацетамід,
2-(3-{2-[((2R)-2-гiдpoкcи-2-{4-гідpoкcи-3-[(мeтилcyльфoнiл)аміно]фeнiл}eтил)aмiнo]-2-метилпропіл}феніл)-N-(тетрагідро-2Н-тiопiран-4-іл)ацетамiд,
N-(біфеніл-2-ілметил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід,
2-(3-{(2R)-2-[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3-[(мeтилcyльфoнiл)aмiнo]фeнiл}eтил)-аміно]пропіл}феніл)-N-(1-нафтилметил)ацетамід,
2-(3-{(2R)-2-[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N-(піридин-2-ілметил)ацетамід,
2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)-аміно]пропіл}феніл)-N-[4-(трифторметокси)бензил]ацетамід,
N-(4-ціанобензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
N-(4-диметиламіно)бензил]-2-(3-{(2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід,
2-(3-{(2R)-2-[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N-фенілацетамід,
N-(1-бензилпіперидин-4-іл)-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)ацетамід і
2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)aміно]феніл}етил)aміно]-2-метилпропіл}феніл)-N-(мезитилметил)ацетамід.
15. N-бензил-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]-феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід.
16. 2-(3-{2-[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3-[(мeтилcyльфoнiл)aмiнo]фeнiл}eтил)аміно]-2-метилпропіл}феніл)-N-(4-метоксибензил)ацетамід.
17. 2-(3-{2-[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3-[(мeтилcyльфoнiл)aмiнo]фeнiл}етил)аміно]-2-метилпропіл}феніл)-N-(4-метилбензил)ацетамід.
18. N-(4-хлорбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)-аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід.
19. N-(3,4-дихлорбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід.
20. Фармацевтична композиція, що містить сполуку формули (1), як описано в будь-якому з пунктів 1-19, або її фармацевтично прийнятну сіль або похідне разом із звичайними фармацевтично безпечними екципієнтами і/або добавками.
21. Сполука формули (1), як описано в будь-якому з пунктів 1-19, або її фармацевтично прийнятна сіль, похідне або композиція для використання як медикаменту.
22. Сполука формули (1), як описано в будь-якому з пунктів 1-19, або її фармацевтично прийнятна сіль, похідне або композиція для використання при лікуванні захворювань, розладів і станів, в які втягнутий ![]() 2 рецептор.
2 рецептор.
23. Сполука формули (1), як описано в будь-якому з пунктів 1-19, або її фармацевтично прийнятна сіль, похідне або композиція для використання при лікуванні захворювань, розладів і станів, що вибирають з групи, яка включає:
- астма усіх типів, етіології або патогенезу, зокрема астма, яку вибирають з групи, яка містить атопічну астму, неатопічну астму, алергічну астму, атопічну бронхіальну lgE-опосередковану астму, бронхіальну астму, есенціальну астму, істинну астму, інфекційно-алергійну астму, викликану патофізіологічними розладами, зовнішню астму, викликану факторами оточуючого середовища, есенціальну астму невідомої або неочевидної причини, неатопічну астму, бронхіальну астму, емфізематозну астму, астму, викликану навантаженням, астму, викликану алергеном, астму, викликану холодним повітрям, професійну астму, інфекційну астму, викликану бактеріями, грибками, протозойними або вірусними інфекціями, неалергічну астму, початкову астму, синдром задухи у немовлят і бронхіоліт,
- хронічна або гостра бронхоконстрикція, хронічний бронхіт, обструкція малих дихальних шляхів і емфізема,
- обструктивні або запальні захворювання дихальних шляхів усіх типів, етіології або патогенезу, зокрема обструктивні або запальні захворювання дихальних шляхів, які вибирають з групи, що містить хронічну еозинофільну пневмонію, хронічне обструктивне легеневе захворювання (COPD), COPD, що включає хронічний бронхіт, легеневу емфізему або задуху, пов'язану або непов'язану з COPD, COPD, що характеризується незворотною прогресуючою обструкцією дихальних шляхів, респіраторний дистрессиндром повнолітніх (ARDS), загострення гіперреактивності дихальних шляхів після лікування іншим лікарським засобом і захворювання дихальних шляхів, що пов'язані з легеневою гіпертензією,
- бронхіт усіх типів, етіології або патогенезу, зокрема бронхіт, який вибирають з групи, що містить гострий бронхіт, гострий гортанно-трахіальний бронхіт, арахідоновий бронхіт, катаральний бронхіт, фібринозний бронхіт, сухий бронхіт, інфекційний астматичний бронхіт, продуктивний бронхіт, стафілококовий або стрептококовий бронхіт і везикулярний бронхіт,
- гостре пошкодження легені,
- бронхоектазія усіх типів, етіології або патогенезу, зокрема бронхоектазія, яку вибирають з групи, що містить циліндричну бронхоектазію, осумковану бронхоектазію, веретеноподібну бронхоектазію, капілярну бронхоектазію, циститну бронхоектазію, суху бронхоектазію і фолікулярну бронхоектазію.
24. Застосування сполуки формули (1), як описано в будь-якому з пунктів 1-19, або її фармацевтично прийнятної солі, похідного або композиції для виготовлення лікарського засобу, що має ![]() 2 агоністичну активність.
2 агоністичну активність.
25. Застосування сполуки формули (1), як описано в будь-якому з пунктів 1-19, або її фармацевтично прийнятної солі, похідного або композиції для виготовлення лікарського засобу для лікування захворювань, розладів і станів, що вибирають з групи, як описано в пункті 23.
26. Спосіб лікування ссавця, включаючи людину, в якому вводять згаданому ссавцю ефективну кількість сполуки формули (1), як описано в будь-якому з пунктів 1-19, або її фармацевтично прийнятної солі, похідного або композиції, що має ![]() 2 агоністичну активність.
2 агоністичну активність.
27. Спосіб згідно з пунктом 26, де захворювання, розлад або стан вибирають з групи, як описано в пункті 23.
28. Спосіб одержання сполуки формули (1) згідно з будь-яким з пунктів 1-19, який включає наступні стадії:
(а) конденсування кислоти формули (2):
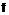
де R1, R2 і n є такими, як визначено в пункті 1, з аміном формули NH2-Q2-A (3)
 ,
,
де R3 - R6, Q2 і А є такими, як визначено в пункті 1,
(б) виділення згаданої сполуки формули (1).
29. Спосіб одержання сполуки формули (1) згідно з пунктом 1, де R1 і R2 є метил і n є 1, який включає наступні стадії:
(а) взаємодію сполуки формули (21)
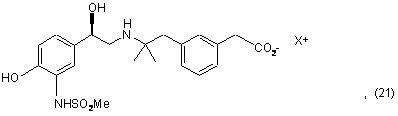
де X є Н, Li, К або Na і, потенційно, органічною аміноосновою або іншою сіллю металу, з придатним аміном формули NHR8-Q2-A (3)
 ,
,
в присутності звичайного конденсувального агента, такого як гідрохлорид 1-(3-диметиламінопропіл)-3-етилкарбодііміду або дициклогексилкарбодіімід, в придатному розчиннику, такому як піридин, диметилформамід і диметилацетамід, необов'язково, в присутності органічної основи і добавки з одержанням згаданої сполуки формули (1),
(б) виділення згаданої сполуки формули (1).
30. Спосіб згідно з пунктом 29, де згадану сполуку формули (21) одержують внаслідок гідрування сполуки формули (22)
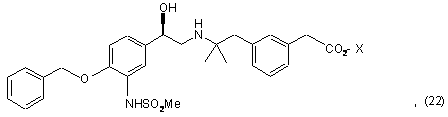
де X є Н, Na, Li або К і, потенційно, органічною аміноосновою або іншою сіллю металу, в присутності придатного розчинника, такого як метанол, ІРА, ТГФ і вода, і в присутності придатного каталізатора, такого як гідроксид паладію на вугіллі або паладій на вугіллі.
31. Спосіб згідно з пунктом 30, де згадану сполуку формули (22) одержують внаслідок взаємодії сполуки формули (23)
 (23)
(23)
з М-ОН, де М вибирають з Na, К або Li, необов'язково, в присутності придатного розчинника, такого як пропіонітрил, тетрагідрофуран або діоксан.
32. Спосіб згідно з пунктом 31, де згадану сполуку формули (23) одержують внаслідок зняття захисту зі сполуки формули (24)
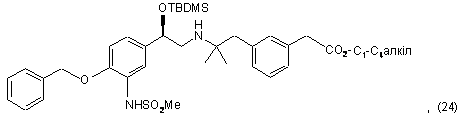
використовуючи агент для зняття захисту, такий як фторид тетрабутиламонію, HF або тригідрофторид триетиламіну в присутності придатного розчинника, такого як пропіонітрил.
33. Спосіб згідно з пунктом 32, де згадану сполуку формули (24) одержують внаслідок взаємодії сполуки формули
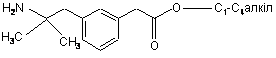
зі сполукою формули
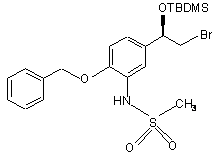
в присутності придатного розчинника, такого як пропіонітрил, ТГФ, толуол, етилацетат, ацетонітрил, пропіонітрил, діоксан, ДМФА, ДМСО, і, необов'язково, в присутності основи, такої як гідрокарбонат натрію, гідрокарбонат калію, основа Хюніга або триетиламін, при температурі від 50 °С до 150 °С протягом 12-36 годин.
34. Комбінація сполуки згідно з будь-яким з пунктів 1-19 з іншим терапевтичним агентом(ами), що вибирають з наступного переліку:
(а) інгібітори 5-ліпоксигенази (5-LO) або антагоністи 5-ліпоксигенази активуючого протеїну (FLAP),
(b) антагоністи лейкотриєну (LTRAs) включаючи антагоністи LTB4, LTC4, LTD4 і LTE4,
(c) антагоністи рецептора гістаміну, включаючи Н1 і Н3 антагоністи,
(d) агоністи ![]() 1- і
1- і ![]() 2-адренорецептора, судинозвужувальні симпатоміметичні агенти для протизастійного застосування,
2-адренорецептора, судинозвужувальні симпатоміметичні агенти для протизастійного застосування,
(e) антагоністи мускаринового М3 рецептора або антихолінергічні агенти,
(f) інгібітори PDE, наприклад, інгібітори PDE3, PDE4 і PDE5,
(g) теофілін,
(h) хромоглікат натрію,
(і) інгібітори СОХ як неселективні, так і селективні інгібітори СОХ-1 або СОХ-2 (NSAID),
(j) пероральні і інгальовані глюкокортикоїди, такі як DAGR (дисоційовані агоністи кортикоїдного рецептора),
(k) моноклональні антитіла активні проти ендогенного запалення,
(i) антагоністи фактора некрозу пухлини (анти-TNF-![]() ),
),
(m) інгібітори адгезії молекули, включаючи VLA-4 антагоністи,
(n) антагоністи рецептора кініну-В1 і -В2,
(о) імуносуспресивні агенти,
(р) інгібітори матриксних металопротеїназ (ММР),
(q) антагоністи рецептора тахікініну NK1, NK2 і NK3,
(r) інгібітори еластази,
(s) агоністи рецептора аденозину А2а,
(t) інгібітори урокінази,
(u) сполуки, що діють як допамінові рецептори, наприклад, D2 агоністи,
(v) модулятори NF![]() шляху, наприклад, ІКК інгібітори,
шляху, наприклад, ІКК інгібітори,
(w) модулятори цитокінових сигнальних шляхів, такі як р38 МАР кіназа або syk кіназа,
(х) агенти, що можуть класифікуватися як муколітики або протикашлеві агенти, і
(у) антибіотики.
35. Сполука формули (2) або її сіль
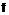
де R1, R2 і n є такими як визначено в пункті 1.
Текст
УКРАЇНА (19) UA (11) 82283 (13) C2 (51) МПК C07C 311/08 (2006.01) МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ ОПИС ДЕРЖАВНИЙ ДЕПАРТАМЕНТ ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ ДО ПАТЕНТУ НА ВИНАХІД (54) ПОХІДНІ СУЛЬФОНАМІДУ ДЛЯ ЛІКУВАННЯ ЗАХВОРЮВАНЬ, СПОСІБ ЇХ ОДЕРЖАННЯ (ВАРІАНТИ), ФАРМАЦЕВТИЧНА КОМПОЗИЦІЯ НА ЇХ ОСНОВІ, ПРОМІЖНА СПОЛУКА 1 2 NHSO 2CH3 R2 R11 * R5 R6 N H R5 R4 R6 , де R3, R4, R5 і R6 є Н. 4. Сполука згідно з пунктом 1, де Q1 є групою *-NHQ2-A, де Q2 є С1-С4 алкілен і А є групою R3 R4 N R5 N 11 , R5 R6 і групи *-NR -Q2-A, де р є 1 або 2, Q2 є С1-С4 алкілен, R11 є Н або С1-С4 алкіл і А є піридил, С3С10 циклоалкіл, згаданий циклоалкіл, необов'язково, містить місток з одним або декількома атомами вуглецю, тетрагідропіраніл, R7 R6 , де R3, R4, R5, R6 і R7 є однаковими або різними і вибрані з Н, С1-С4 алкілу, OR8, SR9, CN, гало, CF3, OCF3, SO2NR9R10, CONR9R10, NR9R10, NHCOR10 і C2 (13) , де R3, R4, R5, R6 і R7 є однаковими або різними і вибрані з Н, С1-С4 алкілу, OR8, SR9, гало, CN, CF3, OCF3, COOR9, SO2NR9R10, CONR9R10, NR9R10, NHCOR10 і феніл; де R8 є С1-С4 алкіл і R9 і R10 є однаковими або різними і вибрані з Н або С1-С4 алкілу і * вказує точку приєднання до карбонільної групи; або, якщо прийнятно, її фармацевтично прийнятні солі і/або ізомери, таутомери, сольвати або їх ізотопні модифікації. 2. Сполука згідно з пунктом 1, де Q1 є NH-Q2-A, де Q2 є СН2 і А є циклогексил, тетрагідротіопіраніл, піперидиніл, необов'язково, заміщений бензилом, або нафтил. 3. Сполука згідно з пунктом 1, де Q1 є R3 * R3 * R6 1 R4 (CH2) p R7 R4 , (1) O R5 або R5 Q1 де (CH2)n-C(=O)Q група розташована в мета- або пара-положенні, R1 і R2, незалежно, вибирають з Н і С1-С4 алкілу, n є 0, 1 або 2 і Q1 є групою, що вибирають з: R3 R4 82283 R1 HO (CH2) n R4 (11) H N R3 R3 UA OH піперидиніл, необов'язково, заміщений бензилом, тетрагідротіопіраніл або група (19) (21) a200608230 (22) 12.01.2005 (24) 25.03.2008 (86) PCT/IB2005/000112, 12.01.2005 (31) 0406388.9 (32) 22.03.2004 (33) GB (31) 04290168.6 (32) 22.01.2004 (33) EP (31) 60/600,259 (32) 09.08.2004 (33) US (46) 30.12.1899, Бюл.№ , 1899 р. (72) БРАУН АЛАН ДЕНІЕЛ, ДЖЕЙМС КІМ, ЛЕЙН ШАРЛОТТ ЕЛІС ЛУІЗ, МОУЗЕС ЙАН БРАЙАН, ТОМСОН НІКОЛАС МАРРЕЙ (73) ПФАЙЗЕР ІНК. (56) WO 03/099764 A, 04.12.2003 EP 0659737 A, 28.06.1995 US 2003/229058 A1, 11.12.2003 US 2002/143034 A1, 03.10.2002 US 5776983 A, 07.07.1998 WO 2004/100950 A, 25.11.2004 (57) 1. Сполука загальної формули (1): 3 фенілу, за умови, що принаймні 2 з R3-R7 є еквівалентними Н; де R8 є С1-С4 алкіл і R9 і R10 є однаковими або різними і вибрані з Н або С1-С4 алкілу. 5. Сполука згідно з пунктом 4, де Q2 є -СН2-, (СН2)2- або -(СН2 )3-. 6. Сполука згідно з пунктом 5, де Q2 є -СН2-. 7. Сполука згідно з будь-яким з пунктів 4-6, де А є групою R3 R4 R5 R7 R6 , де R3, R4, R5, R6 і R7 є однаковими або різними і вибрані з Н, СН3, ОСН2-СН3, SCH3, гало, CF3, OCF3, фенілу, диметиламіно, CN, трет-бутилу, за умови, що принаймні 2 з R3-R7 є еквівалентними Н. 8. Сполука згідно з пунктом 7, де R3, R4, R5, R6 і R7 є однаковими або різними і вибрані з Н, СН3, Сl, F, CF3, за умови, що принаймні 2 з R3-R7 є еквівалентними Н. 9. Сполука згідно з будь-яким з пунктів 1-8, де R1 є Н або С1-С4 алкіл і R2 є С1-С4 алкіл. 10. Сполука згідно з пунктом 9, де R1 є Н або СН3 і R2 є СН3. 11. Сполука згідно з пунктом 10, де n є 1. 12. Сполука згідно з будь-яким з пунктів 1-11 як (R,R)-стереоізомер. 13. Сполука згідно з будь-яким з пунктів 1-11, де (CH2)n-C(=O)Q1 група розташована в метаположенні. 14. Сполука згідно з пунктом 1, яку вибирають з групи, що містить: N-бензил-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, 2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-(4-метоксибензил)ацетамід, 2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-(2-метоксибензил)ацетамід, N-(2-етоксибензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, 2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-(3-метоксибензил)ацетамід, 2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-(4-метилбензил)ацетамід, 2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-(2-метилбензил)ацетамід, 2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-(3-метилбензил)ацетамід, N-(3,4-диметоксибензил)-2-(3-{2-[((2R)-2-гідрокси2-{4-гідрокси-3 82283 4 [(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(2,4-диметоксибензил)-2-(3-{2-[((2R)-2-гідрокси2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(3,5-диметоксибензил)-2-(3-{2-[((2R)-2-гідрокси2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(4-хлорбензил)-2-(3-{2-[((2R-гідрокси-2-{4гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(2-хлорбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(3-хлорбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(4-фторбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(2,4-дихлорбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(3,4-дихлорбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(4-трет-бутилбензил)-2-(3-{2-[((2R)-2-гідрокси-2{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(2-хлор-6-фторбензил)-2-(3-{2-[((2R)-2-гідрокси2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(2,3-диметилбензил)-2-(3-{2-[((2R)-2-гідрокси-2{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(3,5-дихлорбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-[3,5-біс(трифторметил)бензил]-2-(3-{2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(3,4-диметилбензил)-2-(3-{2-[((2R)-2-гідрокси-2{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(2,5-дихлорбензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, 2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-(2-фенілетил)ацетамід, 5 2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-(3-фенілпропіл)ацетамід, N-(2,3-дихлорбензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-(2,4-дихлор-6-метилбензил)-2-(3-{2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(циклогексилметил)-2-(3-{2-[((2R)-2-гідрокси-2{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(2-хлор-6-метилбензил)-2-(3-{2-[((2R)-2-гідрокси2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(2-етоксибензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси-2{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-(3,4-диметилбензил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-(3,4-дихлорбензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, 2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)-N-(3-фенілпропіл)ацетамід, N-(циклогексилметил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-(2-хлор-6-фторбензил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-(2-хлор-4-фторбензил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-(3,5-дихлорбензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, 2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)амiно]пропіл}фенiл)-N-[4(трифторметил)бензил]ацетамід, N-(2,5-дихлорбензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-[4-фтор-2-(трифторметил)бензил]-2-(3-{(2R)-2[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-[4-фтор-3-(трифторметил)бензил]-2-(3-{(2R)-2[((2R)-2-гідрокси-2-{4-гідрокси-3 82283 6 [(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-[2-фтор-4-(трифторметил)бензил]-2-(3-{(2R)-2[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-(2,4-дихлор-6-метилбензил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-[4-хлop-3-(тpифтopмeтил)бeнзил]-2-(3-{(2R)-2[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-[2-хлор-5-(трифторметил)бензил]-2-(3-{(2R)-2[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-[3,5-біс(трифторметил)бензил]-2-(3-{(2R)-2[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-[3-фтор-5-(трифторметил)бензил]-2-(3-{(2R)-2[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-(3,4-дихлорбензил)-2-(4-{2-[((2R)-2-гідрокси-2-{4гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-[2-хлор-5-(трифторметил)бензил]-2-(4-{2-[((2R)2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-[4-хлор-3-(трифторметил)бензил]-2-(4-{2-[((2R)2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-[3,5-біс(трифторметил)бензил]-2-(4-{2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-[3-фтор-5-(трифторметил)бензил]-2-(4-{2-[((2R)2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-[2-фтор-5-(трифторметил)бензил]-2-(4-{2-[((2R)2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-[4-фтор-2-(трифторметил)бензил]-2-(4-{2-[((2R)2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-[4-фтор-3-(трифторметил)бензил]-2-(4-{2-[((2R)2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, 2-(4-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)-N-(2-метоксибензил)ацетамід, N-(2-етоксибензил)-2-(4-{(2R)-2-[((2R)-2-гідрокси-2{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, 7 N-бeнзил-2-(4-{(2R)-2-[((2R)-2-гiдpoкcи-2-{4гiдpoкcи-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, 2-(4-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)-N-(3-фенілпропіл)ацетамід, N-(2,3-дигідро-1H-інден-2-іл)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, 2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)-N-(2-метоксибензил)ацетамід, N-бeнзил-2-(3-{(2R)-2-[((2R)-2-гiдpoкcи-2-{4riдpoкcи-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, 2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)-N-(2-фенілетил)ацетамід, 2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)-N-(мезитилметил)ацетамід, 2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)-N-(2,3,6-трихлорбензил)ацетамід, 2-(3-{2-[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3[(мeтилcyльфoнiл)aмiнo]фeнiл}eтил)aмiнo]-2метилпропіл}феніл)-N-[3(трифторметил)бензил]ацетамід, N-(2,3-дихлорбензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-(3-хлop-4-метилбензил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, 2-(3-{2-[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3[(мeтилcyльфoнiл)aмiнo]фeнiл}eтил)aмiнo]-2метилпропіл}феніл)-N-[2(метилтіо)бензил]ацетамід, 2-(3-{2-[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3[(мeтилcyльфoнiл)aмiнo]фeнiл}eтил)aмiнo]-2метилпропіл}феніл)-N-[4(метилтіо)бензил]ацетамід, 2-(3-{2-[((2R)-2-гiдpoкcи-2-{4-гідpoкcи-3[(мeтилcyльфoнiл)аміно]фeнiл}eтил)aмiнo]-2метилпропіл}феніл)-N-(тетрагідро-2Н-тiопiран-4іл)ацетамiд, N-(біфеніл-2-ілметил)-2-(3-{2-[((2R)-2-гідрокси-2-{4гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, 2-(3-{(2R)-2-[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3[(мeтилcyльфoнiл)aмiнo]фeнiл}eтил)аміно]пропіл}феніл)-N-(1-нафтилметил)ацетамід, 2-(3-{(2R)-2-[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)-N-(піридин-2-ілметил)ацетамід, 2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N-[4(трифторметокси)бензил]ацетамід, 82283 8 N-(4-ціанобензил)-2-(3-{(2R)-2-[((2R)-2-гідрокси-2{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-(4-диметиламіно)бензил]-2-(3-{(2R)-2-гiдpoкcи-2{4-гiдpoкcи-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, 2-(3-{(2R)-2-[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)-N-фенілацетамід, N-(1-бензилпіперидин-4-іл)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід і 2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)aміно]феніл}етил)aміно]-2метилпропіл}феніл)-N-(мезитилметил)ацетамід. 15. N-бензил-2-(3-{2-[((2R)-2-гідрокси-2-{4-гідрокси3-[(метилсульфоніл)аміно]-феніл}етил)аміно]-2метилпропіл}феніл)ацетамід. 16. 2-(3-{2-[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3[(мeтилcyльфoнiл)aмiнo]фeнiл}eтил)аміно]-2метилпропіл}феніл)-N-(4-метоксибензил)ацетамід. 17. 2-(3-{2-[((2R)-2-гiдpoкcи-2-{4-гiдpoкcи-3[(мeтилcyльфoнiл)aмiнo]фeнiл}етил)аміно]-2метилпропіл}феніл)-N-(4-метилбензил)ацетамід. 18. N-(4-хлорбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід. 19. N-(3,4-дихлорбензил)-2-(3-{2-[((2R)-2-гідрокси2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід. 20. Фармацевтична композиція, що містить сполуку формули (1), як описано в будь-якому з пунктів 1-19, або її фармацевтично прийнятну сіль або похідне разом із звичайними фармацевтично безпечними екципієнтами і/або добавками. 21. Сполука формули (1), як описано в будь-якому з пунктів 1-19, або її фармацевтично прийнятна сіль, похідне або композиція для використання як медикаменту. 22. Сполука формули (1), як описано в будь-якому з пунктів 1-19, або її фармацевтично прийнятна сіль, похідне або композиція для використання при лікуванні захворювань, розладів і станів, в які втягнутий β 2 рецептор. 23. Сполука формули (1), як описано в будь-якому з пунктів 1-19, або її фармацевтично прийнятна сіль, похідне або композиція для використання при лікуванні захворювань, розладів і станів, що вибирають з групи, яка включає: - астма усіх типів, етіології або патогенезу, зокрема астма, яку вибирають з групи, яка містить атопічну астму, неатопічну астму, алергічну астму, атопічну бронхіальну lgE-опосередковану астму, бронхіальну астму, есенціальну астму, істинну астму, інфекційно-алергійну астму, викликану патофізіологічними розладами, зовнішню астму, викликану факторами оточуючого середовища, есенціальну астму невідомої або неочевидної причини, неатопічну астму, бронхіальну астму, емфізематозну астму, астму, викликану 9 навантаженням, астму, викликану алергеном, астму, викликану холодним повітрям, професійну астму, інфекційну астму, викликану бактеріями, грибками, протозойними або вірусними інфекціями, неалергічну астму, початкову астму, синдром задухи у немовлят і бронхіоліт, - хронічна або гостра бронхоконстрикція, хронічний бронхіт, обструкція малих дихальних шляхів і емфізема, - обструктивні або запальні захворювання дихальних шляхів усіх типів, етіології або патогенезу, зокрема обструктивні або запальні захворювання дихальних шляхів, які вибирають з групи, що містить хронічну еозинофільну пневмонію, хронічне обструктивне легеневе захворювання (COPD), COPD, що включає хронічний бронхіт, легеневу емфізему або задуху, пов'язану або непов'язану з COPD, COPD, що характеризується незворотною прогресуючою обструкцією дихальних шляхів, респіраторний дистрессиндром повнолітніх (ARDS), загострення гіперреактивності дихальних шляхів після лікування іншим лікарським засобом і захворювання дихальних шляхів, що пов'язані з легеневою гіпертензією, - бронхіт усіх типів, етіології або патогенезу, зокрема бронхіт, який вибирають з групи, що містить гострий бронхіт, гострий гортаннотрахіальний бронхіт, арахідоновий бронхіт, катаральний бронхіт, фібринозний бронхіт, сухий бронхіт, інфекційний астматичний бронхіт, продуктивний бронхіт, стафілококовий або стрептококовий бронхіт і везикулярний бронхіт, - гостре пошкодження легені, - бронхоектазія усіх типів, етіології або патогенезу, зокрема бронхоектазія, яку вибирають з групи, що містить циліндричну бронхоектазію, осумковану бронхоектазію, веретеноподібну бронхоектазію, капілярну бронхоектазію, циститну бронхоектазію, суху бронхоектазію і фолікулярну бронхоектазію. 24. Застосування сполуки формули (1), як описано в будь-якому з пунктів 1-19, або її фармацевтично прийнятної солі, похідного або композиції для виготовлення лікарського засобу, що має β 2 агоністичну активність. 25. Застосування сполуки формули (1), як описано в будь-якому з пунктів 1-19, або її фармацевтично прийнятної солі, похідного або композиції для виготовлення лікарського засобу для лікування захворювань, розладів і станів, що вибирають з групи, як описано в пункті 23. 26. Спосіб лікування ссавця, включаючи людину, в якому вводять згаданому ссавцю ефективну кількість сполуки формули (1), як описано в будьякому з пунктів 1-19, або її фармацевтично прийнятної солі, похідного або композиції, що має β 2 агоністичну активність. 27. Спосіб згідно з пунктом 26, де захворювання, розлад або стан вибирають з групи, як описано в пункті 23. 28. Спосіб одержання сполуки формули (1) згідно з будь-яким з пунктів 1-19, який включає наступні стадії: (а) конденсування кислоти формули (2): 82283 10 OH H N (CH2 ) n R1 R2 HO OH , (2) O NHSO2Me де R1, R2 і n є такими, як визначено в пункті 1, з аміном формули NH2-Q2-A (3) R3 R3 R4 R4 H2N R5 R5 HN R6 (3') , R6 або (3") , де R3 - R6, Q2 і А є такими, як визначено в пункті 1, (б) виділення згаданої сполуки формули (1). 29. Спосіб одержання сполуки формули (1) згідно з пунктом 1, де R1 і R2 є метил і n є 1, який включає наступні стадії: (а) взаємодію сполуки формули (21) OH H N CO 2 X+ HO , (21) NHSO 2Me де X є Н, Li, К або Na і, потенційно, органічною аміноосновою або іншою сіллю металу, з придатним аміном формули NHR8-Q2-A (3) R3 R3 R4 (CH2) p R8 HN R6 R4 N H R5 (3') , або R5 R6 (3") , в присутності звичайного конденсувального агента, такого як гідрохлорид 1-(3диметиламінопропіл)-3-етилкарбодііміду або дициклогексилкарбодіімід, в придатному розчиннику, такому як піридин, диметилформамід і диметилацетамід, необов'язково, в присутності органічної основи і добавки з одержанням згаданої сполуки формули (1), (б) виділення згаданої сполуки формули (1). 30. Спосіб згідно з пунктом 29, де згадану сполуку формули (21) одержують внаслідок гідрування сполуки формули (22) OH H N CO 2- X O NHSO2 Me , (22) де X є Н, Na, Li або К і, потенційно, органічною аміноосновою або іншою сіллю металу, в присутності придатного розчинника, такого як метанол, ІРА, ТГФ і вода, і в присутності придатного каталізатора, такого як гідроксид паладію на вугіллі або паладій на вугіллі. 31. Спосіб згідно з пунктом 30, де згадану сполуку формули (22) одержують внаслідок взаємодії сполуки формули (23) 11 82283 OH H N CO2- C1-C4алкіл O NHSO2Me (23) з М-ОН, де М вибирають з Na, К або Li, необов'язково, в присутності придатного розчинника, такого як пропіонітрил, тетрагідрофуран або діоксан. 32. Спосіб згідно з пунктом 31, де згадану сполуку формули (23) одержують внаслідок зняття захисту зі сполуки формули (24) OTBDMS H N CO2 - C1 -C4алкіл O NHSO2Me , (24) використовуючи агент для зняття захисту, такий як фторид тетрабутиламонію, HF або тригідрофторид триетиламіну в присутності придатного розчинника, такого як пропіонітрил. 33. Спосіб згідно з пунктом 32, де згадану сполуку формули (24) одержують внаслідок взаємодії сполуки формули C1 -C4алкіл H 2N O H 3C CH3 O зі сполукою формули OTBDMS Br O HN CH3 S O O в присутності придатного розчинника, такого як пропіонітрил, ТГФ, толуол, етилацетат, ацетонітрил, пропіонітрил, діоксан, ДМФА, ДМСО, і, необов'язково, в присутності основи, такої як гідрокарбонат натрію, гідрокарбонат калію, основа Хюніга або триетиламін, при температурі від 50 °С до 150 °С протягом 12-36 годин. 34. Комбінація сполуки згідно з будь-яким з пунктів 1-19 з іншим терапевтичним агентом(ами), що вибирають з наступного переліку: Цей винахід стосується β2 агоністів загальної формули: 12 (а) інгібітори 5-ліпоксигенази (5-LO) або антагоністи 5-ліпоксигенази активуючого протеїну (FLAP), (b) антагоністи лейкотриєну (LTRAs) включаючи антагоністи LTB4, LTC4, LTD4 і LTE4, (c) антагоністи рецептора гістаміну, включаючи Н1 і Н3 антагоністи, (d) агоністи α 1- і α 2-адренорецептора, судинозвужувальні симпатоміметичні агенти для протизастійного застосування, (e) антагоністи мускаринового М3 рецептора або антихолінергічні агенти, (f) інгібітори PDE, наприклад, інгібітори PDE3, PDE4 і PDE5, (g) теофілін, (h) хромоглікат натрію, (і) інгібітори СОХ як неселективні, так і селективні інгібітори СОХ-1 або СОХ-2 (NSAID), (j) пероральні і інгальовані глюкокортикоїди, такі як DAGR (дисоційовані агоністи кортикоїдного рецептора), (k) моноклональні антитіла активні проти ендогенного запалення, (i) антагоністи фактора некрозу пухлини (антиTNF- α ), (m) інгібітори адгезії молекули, включаючи VLA-4 антагоністи, (n) антагоністи рецептора кініну-В1 і -В2, (о) імуносуспресивні агенти, (р) інгібітори матриксних металопротеїназ (ММР), (q) антагоністи рецептора тахікініну NK1, NK2 і NK3, (r) інгібітори еластази, (s) агоністи рецептора аденозину А2а, (t) інгібітори урокінази, (u) сполуки, що діють як допамінові рецептори, наприклад, D2 агоністи, (v) модулятори NF κβ шляху, наприклад, ІКК інгібітори, (w) модулятори цитокінових сигнальних шляхів, такі як р38 МАР кіназа або syk кіназа, (х) агенти, що можуть класифікуватися як муколітики або протикашлеві агенти, і (у) антибіотики. 35. Сполука формули (2) або її сіль OH H N R1 R2 HO NHSO2Me 1 (CH2 ) n OH O , (2) 2 де R , R і n є такими як визначено в пункті 1. де R1, R2, n і Q1 мають значення вказані нижче, і способів одержання, проміжних сполук, що викристовуються, композицій, що містять, і застосування таких похідних. Адренорецептори є членами великої суперродини рецептора злитого G-протеїну. Родина адренорецептора само по собі 13 розділяється на α і β підродини, де β підродина складається з принаймні 3 підтипів рецептора: β1, β2 і β3. Ці рецептори проявляють диференціальну експресію форм в тканинах різних систем і органів ссавців. β2 адренергічні (β2) рецептори є найбільш експресуємими в клітинах гладких м'язів (наприклад, васкулярних, бронхіальних, маткових або кишкових гладких м'язів), в той час як β3 адренергічні рецептори найбільше експресуються в жирових тканинах (тому β3 агоністи можуть потенційно бути корисні при лікуванні ожиріння і діабетів) і β1 адренергічні рецептори в основному експресуються в серцевих тканинах (тому β1 агоністи найбільш часто використовуються як кардіологічні стимулятори). Патофізіологія і лікування захворювань дихальних шляхів добре описується в літературі (для ознайомлення дивіться Barnes, P. J. Chest, 1997, 111:2, pp 17S-26S і Bryan, S. A. et al, Expert Opinion on investigational drugs, 2000, 9:1, pp25-42) і тому сюди був включений тільки короткий опис для забезпечення деякої базової інформації. Глюкокортикоїди, антилейкотрієни, теофілін, кромоліни, антихолінергіки і β2 агоністи складають класи лікарських засобів, що на даний час використовуються для лікування алергічних і неалергічних захворювань дихальних шляхів, таких як астма і хронічне обструктивне захворювання дихальних шляхів (COPD). Лікування цих захворювань полягає в інгаляції недовго або довгодіючих β2 агоністів. Недовгодіючі, швидко діючі β2 агоністи використовуються для "зняття" бронходилатації, в той час як довгодіючі форми забезпечують тривале полегшення і використовуються при підтримуючій терапії. Бронходилатація опосередковується через агонізм β2 адренорецептора, що експресується на клітинах гладких м'язів дихальних шляхів, що призводить до розслаблення і відповідно бронходилатації. Таким чином, як функціональні антагоністи, β2 агоністи можуть попереджати і обертати дію всіх бронхозвужуючих речовин, включаючи лейкотрієн D4 (LTD4), ацетилхолін, брадикінін, простагландини, гістамін і ендотелій. Оскільки β2 рецептори так широко розповсюджені в дихальних шляхах, β2 агоністи також можуть діяти на інші типи клітин, що відіграють роль в астмі. Наприклад, повідомлялось, що β2 агоністи можуть стабілізувати тучні клітини. Інгібування вивільнення бронхозвужуючих речовин може бути як блокування β2 агоністів бронхозвуження, що викликано алергенами, навантаженням і холодним повітрям. Крім того, β2 агоністи інгібують холінергічну нейротрансмісію в дихальних шляхах людини, що може призводити до зменшення холінергічно-рефлексного бронхозвуження. На додаток до дихальних шляхів, також повідомлялось, що β2 адренорецептори також експресуються в інших органах і тканинах і таким чином β2 агоністи, так як ті що описані в представленому винаході, можуть застосовуватись при лікуванні інших захворювань, таких як, але не обмежується, захворювання нервової системи, передчасні пологи, застійна 82283 14 серцева недостатність, депресія, запальні і алергічні захворювання шкіри, псоріаз, проліферативні захворювання шкіри, глаукома і при станах, при яких необхідне зменшення шлункової кислотності, особливо при виразці шлунку і дванадцятипалої кишки. Однак, ряд β2 агоністів мають обмежене застосування завдяки їх низькій селективності або шкідливим побічним ефектам обумовленим високою системною дією і головним чином опосередковану через дію β2 адренорецепторів, що експресуються не в дихальних шляхах (м'язовий тремор, тахікардія, серцебиття, неспокій). Тому існує потреба в покращенні агентів цього класу. Відповідно, все ще існує потреба в нових β2 агоністах, що будуть мати прийнятний фармакологічний профіль, наприклад, в одиницях активності, селективності, тривалості дії і/або фармакодинамічних властивостей. В цьому контексті, представлений винахід стосується нових β2 агоністів. Вже були описані різні похідні сульфонаміду. Наприклад, WO02066250 описує сполуки активні як β3 агоніст, більш селективній ніж β2, формули: де m може бути 2, R1 може бути Н, ОН або NR SO2R5 (R5 є Η або С1-С6 алкіл), Ζ може бути зв'язком, R2 може бути Η або С1-С6 алкіл, R4 може бути С1-С6 алкіл, В може бути феніл, Υ є С1-С6 алкіл і А може бути феніл. WO02/000622 описує селективні β3 агоністи формули : 5 де R1 може бути фенілом заміщеним гідрокси і алкілсульфоніламіно, Х1 може бути зв'язком, R2 може бути воднем, R3 є водень або гідроксиалкіл, Х2 може бути СН2, Х3 є зв'язком, О або ΝΗ і R4 є циклічною групою. Інші похідні сульфонаміду також описуються в US5,776,983 як β3 агоністи Вони мають формулу: де R1 може бути СН3, R2 може бути ОН, R6 може бути Н, R3 може бути Η або алкіл, R4 може бути Н, алкіл, R5 може бути Н, R5' може бути C(O)NR6R6' де R6 і R6' може бути Η або нижчий алкіл. Однак, описані вище похідні сульфонаміду не проявляють β2 агоністичної активності і їх фармакологічний профіль не дозволяє їх використання як ефективних лікарських засобів 15 при лікуванні β2-οпосередкованих захворювань і/або станів, зокрема, алергічних і неалергічних захворювань дихальних шляхів або інших хвороб, таких як ті, що згадані раніше. Винахід стосується сполук загальної формули (1): де (CH2)n-C(=O)Q1 група розташована в мета або пара положенні, R1 і R2, незалежно, вибирають з Η і С1-С4 алкілу, n є 0, 1 або 2 і Q1 є групою, що вибирають з, 82283 16 С3-С10 циклоалкілом, де 2 або більше атомів вуглецю, необов'язково, з'єднані містком з одним або декількома атомами вуглецю, є циклопропіл, циклобутил, циклопентил, циклогексил і циклогептил, адамантил, біцикло[3.1.1]гептан, біцикло[2.2.1]гептан, біцикло[2.2.2]октан. Переважними циклоалкільними групами є циклогексил і адамантил. На закінчення, гало означає атом галогену, що вибирають з групи, яка містить фтор, хлор, бром і йод, зокрема, фтор або хлор. Надалі, вільний зв'язок на фенільній групі, такій як структура показана нижче, означає, що феніл може бути заміщений в мета або пара положенні. Сполуки формули (1) і групи *-NR11-Q2-A, де p є 1 або 2, Q2 є С1-С4 алкілен, R11 є Η або С1-С4 алкіл і А є піридил, С3С10 циклоалкіл, згаданий циклоалкіл, необов'язково, містить місток з одним або декількома атомами вуглецю, переважно, з 1, 2, 3 або 4, тетрагідропіраніл, піперидиніл, необов'язково, заміщений бензилом, тетрагідротіопіраніл або група де R3, R4, R5, R6 і R7 є однаковими або різними і вибирають з Н, С1-С4 алкілу, OR8, SR9, гало, CN, CF3, OCF3, COOR9, SO2NR9R10, CONR9R10, NR9R10, NHCOR10 і феніл; де R8 є С1-С4 алкіл і R9 і R10 є однаковими або різними і вибирають з Η або С1-С4 алкілу і * вказує точку приєднання до карбонільної групи; або, якщо прийнятно, їх фармацевтично прийнятні солі і/або ізомери, таутомери, сольвати або їх ізотопні модифікації. Сполуки формули (1) є агоністами β2 рецепторів, що є особливо корисними для лікування β2-опосередкованих захворювань і/або станів, і показують добру активність, зокрема, коли вводяться шляхом інгаляції. В приведеній вище загальній формулі (1), С1С4 алкіл і С1-С4 алкілен означають нерозгалужену або розгалужену групу, що містить 1, 2, 3 або 4 атоми вуглецю. Це також використовується, якщо вона несе замісники або зустрічаються як замісники на інших радикалах, наприклад, в О-(С1С4)алкільних радикалах, S-(С1-С4)алкільних радикалах і т.і..... Прикладами придатних (С1С4)алкільних радикалів є метил, етил, н-пропіл, ізо-пропіл, н-бутил, ізо-бутил, втор-бутил, третбутил .... Прикладами придатних О-(С1С4)алкільних радикалів є метокси, етокси, нпропілокси, ізо-пропілокси, н-бутилокси, ізобутилокси, втор-бутилокси і трет-бутилокси .... можна одержати використовуючи звичайні методики, такі як наступні ілюстративні методики, в яких R1, R2, Q1, і n є таким як визначено раніше для сполук формули (1), якщо не вказано інше. Амідні похідні формули (1) можна одержати шляхом конденсування кислоти формули (2) або її солі: з аміном формули NHR11-Q2-A (3), Конденсування зазвичай проводять у надлишку згаданого аміну як акцептора кислоти, із звичайним конденсувальним агентом (наприклад, гідрохлорид 1-(3-диметиламінопропіл)-3етилкарбодііміду або Ν,Ν'дициклогексилкарбодіімід), необов'язково, в присутності каталізатора (наприклад, гідрат 1гідроксибензотриазолу або 1-пдрокси-7азабензотриазол), і, необов'язково, в присутності основи - третинного аміну (наприклад Nметилморфолін, триетиламін або діізопропілетиламін). Реакцію можна проводити в придатному розчиннику, такому як піридин, диметилформамід, тетрагідрофуран, диметилсульфоксид, дихлорметан або етилацетат, і при температурі від 10°С до 40°С (кімнатна температура) протягом часу 1-24 години. Згаданий амін (3), (3’) або (3") є або комерційно доступним, або можна одержати за допомогою загальновідомих методик добре відомих спеціалісту в цій галузі (наприклад 17 відновлення, окислення, алкілування, конденсування опосередковане перехідним металом, захист, зняття захисту і т.і....) з комерційно доступних матеріалів. Кислоту формули (2) можна одержати з відповідного естеру формули (4): в якій Ra є придатною кислото-захисною групою, переважно (С1-С4)алкільною групою, яка включає, але не обмежується, метил і етил, згідно з будь-якою методикою добре відомою спеціалісту в цій галузі для одержання кислоти з естеру, без модифікування залишку молекули. Наприклад, естер можна гідролізувати шляхом обробки водною кислотою або основою (наприклад, хлоридом водню, гідроксидом калію, гідроксидом натрію або гідроксидом літію), необов'язково в присутності розчинника або суміші розчинників (наприклад, вода, 1,4-діоксан, тетрагідрофуран/вода), при температурі від 20°С до 100°С, протягом часу 1 - 40 годин. Естер формули (4) можна одержати за допомогою реакції аміну формули (5): де Ra і n є такими як визначено раніше, з бромідом формули (6): В типовій методиці, амін формули (5) взаємодіє з бромідом формули (6), необов'язково, в присутності розчинника або суміші розчинників (наприклад, диметилсульфоксид, толуол, Ν,Νдиметилформамід, ацетонітрил), необов'язково, в присутності придатної основи (наприклад, триетиламін, діізопропілетиламін, карбонат калію, гідрокарбонат калію) при температурі від 80°С до 120°С, протягом 12-48 годин.. Бромід формули (6) можна одержати згідно з способом WO 02/06258 (стор. 36, приклад 14а). Амін формули (5), де R1 є Me і R2 є Н, можна одержати як або (R), або (S) енатіомер з відповідного захищеного аміну формули (7): в якій Ra і n є такими як визначено вище і Rb і Re представляють будь-який придатний замісник так що HNRbRc є хіральним аміном (наприклад, Rb може бути воднем і Rc може бути αметилбензилом), за умови, що зв'язки між N і Rb і 82283 18 N і Rc можуть бути легко розщеплені даючи вільний амін формули (5) використовуючи стандартні методики для відщеплення азотзахисних груп, такі як ті що описані в книзі Т. W. GREENE, Protective Groups in Organic Synthesis, A. Wiley-lnterscience Publication, 1981. Амін формули (7) можна одержати як окремий діастереомер за допомогою реакції аміну формули HNRbRc з кетоном формули (8): де Ra, Rb, Rc і n є такими як визначено раніше. В типовій методиці, реакцію кетону формули (8) з аміном формули HNRbRc призводить до хіральної проміжної сполуки, яка в свою чергу відновлюється придатним відновлюючим агентом (наприклад, ціаноборгідридом натрію формули NaCNBH3 або триацетоксиборгідридом натрію формули Na(OAc)3BH), необов'язково, в присутності осушника (наприклад, молекулярні сита, сульфат магнію) і, необов'язково, в присутності кислотного каталізатору (наприклад, оцтової кислоти) з одержанням аміну формули (7) як суміш діастереомерів. Реакцію зазвичай проводять в розчиннику, такому як тетрагідрофуран або дихлорметан при температурі від 20°С до 80°С протягом 3-72 годин. Одержаний продукт потім перетворюють у гідрохлоридну сіль і селективно кристалізують з придатного розчинника або суміші розчинників (наприклад, ізопропанол, етанол, метанол, діізопропіловий етер або діізопропіловий етер/метанол) одержуючи (7) як окремий діастереомер. Кетон формули (8), в якому n=1, можна одержати шляхом конденсування, медійованого паладієм, з арилгалідом формули (9): в якій Ra є таким як визначено вище і Hal представляє атом галогену, яким є, але не обмежується, бром і йод, з енолатом або еквівалентом енолату. В типовій методиці, арилгалід формули (9) взаємодіє з енолатом олова одержаним in situ шляхом обробки ізопропенілацетату метоксидом три-н-бутилолова формули Bu3SnOMe в присутності придатного паладієвого каталізатора (ацетат паладію/три-орто-толілфосфін формули Pd(OAc)2/P(o-Tol)3) в неполярному розчиннику (наприклад, толуол, бензол, гексан). Переважно, реакцію проводять при температурі від 80°С до 110°С протягом 6-16 годин. Арилгалід формули (9) можна одержати шляхом естерифікації відповідної кислоти формули (10). 19 в якій Hal є таким як визначено вище, згідно з будь-яким методом добре відомим спеціалісту в цій галузі для одержання естерів з кислоти, без модифікування залишку молекули. В типовій методиці, кислота формули (10) взаємодіє із спиртовим розчинником формули RaOH, в якій Ra є таким як визначено вище, в присутності кислоти, такої як хлорид кислоти при температурі від 10°С до 40°С (кімнатна температура) протягом 8-16 годин. Кислота формули (10) є комерційно доступним продуктом. Амін формули (5), де R1 = R2 = алкіл, можна одержати згідно з приведеною далі схемою: де R1, R2 і Ra є такими як визначено раніше. В типовій методиці, естер формули (11) реагує з "активованим" алкілом (органометалічний алкіл, такий як R2MgBr, R2MgCI або R2Li) з утворенням відповідного третинного спирту формули (12) використовуючи спосіб описаний вище. Згаданий третинний спирт формули (12) надалі взаємодіє з алкілнітрилом (наприклад, ацетонітрил, хлорацетонітрил) в присутності кислоти (наприклад, сірчана кислота, оцтова кислота) з утворенням захищеної проміжної сполуки, яку в свою чергу розщеплюють використовуючи стандартні методики для відщеплення азот-захисної групи, такої як ті що згадані в книгах. Одержану амінокислоту естерифікують використовуючи способи описані тут з одержанням аміну формули (5). Альтернативно, амін формули (5), де R1 = R2 = С1-С4 алкіл і n=0, можна одержати згідно з наступною схемою: де R1, R2 і Ra є такими як визначено раніше. В типовій методиці, естер формули (13) реагує з "активованим" алкілом (органометалічний алкіл, такий як R2MgBr, R2MgCI або R2Li) з утворенням відповідного третинного спирту формули (14) використовуючи спосіб описаний вище. Згаданий третинний спирт формули (14) надалі взаємодіє з алкілнітрилом (наприклад, ацетонітрил, хлорацетонітрил) в присутності кислоти Наприклад, сірчана кислота, оцтова 82283 20 кислота) з утворенням захищеної проміжної сполуки, яку в свою чергу розщеплюють використовуючи стандартні методики для відщеплення азот-захисної групи, такої як ті що згадані в книгах з одержанням бромаміну формули (15). Одержаний бромамін (15) обробляють придатним паладієвим каталізатором (наприклад, [1,1'-біс(дифенілфосфіно)фероцен]дихлорпаладій (II)) в атмосфері монооксиду вуглецю використовуючи RaOH як розчинник (наприклад МеОН, EtOH) при підвищеній температурі (100°С) i тиску (до 100 псі) одержуючи естер формули (5). Кетон формули (8), де n=2, можна одержати шляхом відновлення алкену формули (16): В типовій методиці, розчин олефіну формули (16) в придатному розчиннику (наприклад, метанол, етанол, етилацетат) обробляють паладієвим каталізатором (наприклад, 10% паладій на вугіллі) і перемішують в атмосфері водню, необов'язково, при підвищеному тиску (наприклад, 60 псі), при температурі від кімнатної до 60°С протягом 8-24 годин. Алкен формули (16) можна одержати використовуючи медійоване паладієвим каталізатором конденсування активованого олефіну з арилгалідом формули (17): В типовій методиці, арилгалід (17) конденсують з вініловим естером (наприклад, метилакрилат) в присутності придатного паладієвого каталізатору (наприклад тетракіс(трифенілфосфіно)паладій (0) формули Pd(PPh3)4, ацетат паладію/три-орто-толілфосфін формули Pd(OAc)2/P(o-tol)3 або хлорид (дифенілфосфіно)фероценілпаладію формули dppfPdCI 2) в придатному розчиннику (наприклад, ацетонітрил, Ν,Ν-диметилформамід, толуол), необов'язково, в присутності основи, такої як триетиламін при температурі від 40°С до 110°С протягом від 8 до 24 годин. Кетон формули (17) є комерційним продуктом. Амін формули (5), де R1 і R2 обидва є Н, можна одержати згідно з наступною схемою: де R1, R2 і Ra є такими як визначено раніше. В типовій методиці, кислоту формули (18), переважно, відновлюють у відповідний спирт (19) в присутності естеру. Це можна здійснити шляхом 21 формування ацилімідазолу або змішаного ангідриду і подальшого відновлення боргідридом натрію або іншим придатним відновлювальним агентом. Згаданий первинний спирт формули (19) надалі перетворюють у групу, що відходить, таку як мезилат, тозилат, бромід або йодид і замінюють прийнятним нуклеофільним аміном. Переважним нуклеофілом є іон азиду, який можна відновити до первинного аміну шляхом гідрування або трифенілфосфін. Альтернативними нуклеофілами можуть бути аміак або алкіламіни, такі як бензиламін або аліламін і надалі відщеплюють алкільну группу для одержання аміну. В типовій методиці, сполуки формули (І), де R1 і R2 обидва є метил і n є 1, можна одержати за допомогою реакції сполуки формули (21) де X є Н, К, Na, Li i, потенційно, органічною аміноосновою або іншою сіллю металу, з придатним аміном формули NHR8-Q2-A (3) 82283 22 з М-ОН, де Μ вибирають з Li, Na або К, необов'язково, в присутності придатного розчинника, такого як пропіонітрил, тетрагідрофуран або діоксан, переважно пропіонітрил. Згадану сполуку формули (23) можна одержати шляхом зняття захисту з сполуки формули (24) використовуючи агент, що видаляє захист, такий як фторид тетрабутиламонію, HF або тригідрофторид триетиламіну в присутності придатного розчинника, такого як пропіонітрил. Згадану сполуку формули (24) можна одержати за допомогою реакції сполуки формули з сполукою формули в присутності звичайного конденсувального агенту, такого як пдрохлорид 1-(3диметиламінопропіл)-3-етилкарбодііміду або дициклогексилкарбодіїмід, в придатному розчиннику, такому як піридин, диметилформамід і диметилацетамід, необов'язково в присутності органічної основи (такої як основа Хюніга) і добавки (такої як 1-гідроксибензотриазол) з одержанням сполуки формули (1): де R1 і R2 є метил і n є 1. Згадану сполуку формули (21) можна одержати шляхом гідрування сполуки формули (22) де X є Н, Na, Li або К і, потенційно, органічний амін або інші солі металу, в присутності придатного розчинника, такого як метанол, ІРА, ТГФ і вода і в присутності придатного каталізатору, такого як гідроксид паладію на вугіллі або паладій на вугіллі. Згадану сполуку формули (22) можна одержати шляхом взаємодії сполуки формули (23) в присутності придатного розчинника, такого як пропіонітрил, ТГФ, толуол, етилацетат, ацетонітрил, пропіонітрил, діоксан, ДМФА, ДМСО, і, необов'язково, в присутності основи, такої як гідрокарбонат натрію, гідрокарбонат калію, основа Хюніга або триетиламін, при температурі від 50°С до 150°С протягом 12-36 годин. Для деяких стадій описаного тут вище способу одержання сполук формули (1), може бути необхідний захист потенційно реакційноздатних груп, що не повинні вступати в реакцію, і відщеплення згаданих захисних груп в подальшому. В такому випадку, можуть бути використані будь-які сумісні захисні радикали. Окремі способи захисту і зняття захисту описуються Т. W. GREENE (Protective Groups in Organic Synthesis, A. Wiley-Interscience Publication, 1981) або P. J. Kocienski (Protecting groups, Georg Thieme Verlag, 1994), і можуть бути використані. Всі згадані вище реакції і способи одержання нових вихідних матеріалів, що використовуються в попередніх методах є звичайними і прийнятними реагентами і умови реакцій для їх здійснення або проведення, також як і методики виділення бажаних продуктів будуть добре відомі спеціалісту в цій галузі з посиланням на попередню літературу і приклади і рецептури приведені тут. 23 Також, сполуки формули (1), також як і проміжні сполуки для їх одержання можуть бути очищені за допомогою різних добре відомих методів, таких як, наприклад, кристалізація або хроматографія. Переважно Q1 є групою *-NH-Q2-A, де Q2 є СН2 і А є циклогексил, тетрагідротіопіраніл, піперидиніл, необов'язково, заміщений бензил, або нафтил. Переважно, Q1 є де R3, R4, R5 і R6 є Н. Переважно, Q1 є групою *-NH-Q2-A, де Q2 є С1С4 алкілен і А є групою де R3, R4, R5, R6 і R7 є однаковими або різними і вибирають з Н, С1-С4 алкілу, OR8, SR9, CN, гало, CF3, OCF3, SO2NR9R10, CONR9R10, NR9R10, NHCOR10 і фенілу, за умови, що принаймні 2 з R3R7 є еквівалентними Н; де R8 є С1-С4 алкіл і R9 і R10 є однаковими або різними і вибирають з Η або С1-С4 алкілу. Більш переважно, Q1 є групою *-NH-Q2-A, де Q2 є -СН2-, -(СН2)2-, -(СН2)3-, переважно -СН2-, і А є групою де R3, R4, R5, R6 і R7 є однаковими або різними і вибирають з Н, СН3, ОСН2-СН3, SCH3, гало, CF3, OCF3, фенілу, диметиламіне CN, трет-бутилу, за умови, що принаймні 2 з R3-R7 є еквівалентними Н. Більш переважно, Q1 є групою *-NH-Q2-A, де 2 Q є а -СН2-, -(СН2 )2-, -(СН2)3-, переважно, -СН2-, і А є групою де R3, R4, R5, R6 і R7 є однаковими або різними і вибирають з Н, СН3, СІ, F, CF3 за умови, що принаймні 2 з R3-R7 є еквівалентними Н. В згаданих вище групах сполук, наступні замісники є особливо переважними: R1 є Η або С1-С4 алкіл і R2 є С1-С4 алкіл. Більш переважно, R1 є Η або СН3 і R2 є СН3. n є 1, 2 або 3. Більш переважно n є 1. R1 є H i R2 є CH3 i n є1. 82283 24 R1є CH3, R2 є CH3 i n є1. Особливо переважними є сполуки формули (1) описані в розділі Приклади, тобто: N-Бензил-2-(3-{2-[((2R)-2-гідрокси-2-{4гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід, 2-(3-{2-[((2Р)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-(4-метоксибензил)ацетамід 2-(3-{2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-(2-метоксибензил)ацетамід, N-(2-Етоксибензил)-2-(3-{2-[((2R)-2-гідрокси-2{4-гідрокси-3-[(метилсульфоніл)аміно]феніл}етил)аміно]-2-метилпропіл}феніл)ацетамід, 2-(3-{2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-(3-метоксибензил)ацетамід, 2-(3-{2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-(4-метилбензил)ацетамід, 2-(3-{2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-(2-метилбензил)ацетамід, 2-(3-{2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-(3-метилбензил)ацетамід, N-(3,4-Диметоксибензил)-2-(3-{2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(2,4-Диметоксибензил)-2-(3-{2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(3,5-Диметоксибензил)-2-(3-{2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(4-Хлорбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(-(2-Хлорбензил)-2-(3-{2-[((2R)-2-гідрокси-2{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(3-Хлорбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(4-Фторбензил)-2-(3-{2-[((2R)-2-гідрокси-2-{4гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(2,4-Дихлорбензил)-2-(3-{2-[((2R)-2-гідрокси2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(3,4-Дихлорбензил)-2-(3-{2-[((2R)-2-пдрокси2-{4-пдрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(4-трет-Бутилбензил)-2-(3-{2-[((2R)-2гідрокси-2-{4-гідрокси-3 25 [(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(2-Хлор-6-фторбензил)-2-(3-{2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(2,3-Диметилбензил)-2-(3-{2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(3,5-Дихлорбензил)-2-(3-{2-[((2R)-2-гідрокси2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-[3,5-бiс(Трифторметил)бензил]-2-(3-{2[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(3,4-Диметилбензил)-2-(3-{2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(2,5-Дихлорбензил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, 2-(3-{2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-(2-фенілетил)ацетамід, 2-(3-{2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-(3-фенілпропіл)ацетамід, N-(2,3-Дихлорбензил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-(2,4-Дихлор-6-метилбензил)-2-(3-{2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(Циклогексилметил)-2-(3-{2-[((2R)-2-гідрокси2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(2-Хлор-6-метилбензил)-2-(3-{2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-(2-Етоксибензил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-(3,4-Диметилбензил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-(3,4-Дихлорбензил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, 2-(3-{(2R)-2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N-(3-фенілпропіл)ацетамід, N-(Циклогексилметил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3 82283 26 [(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-(2-Хлор-6-фторбензил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-(2-Хлор-4-фторбензил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-(3,5-Дихлорбензил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, 2-(3-{(2R)-2-[((2Я)-2-Пдрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N-[4(трифторметил)бензил]ацетамід, N-(2,5-Дихлорбензил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-[4-Фтор-2-(трифторметил)бензил]-2-(3-{(2R)2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-[4-Фтор-3-(трифторметил)бензил]-2-(3-{(2R)2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-[2-Фтор-4-(трифторметил)бензил]-2-(3-{(2R)2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-(2,4-Дихлор-6-метилбензил)-2-(3-{(2R)-2[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-[4-Хлор-3-(трифторметил)бензил]-2-(3-{(2R)2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-[2-Хлор-5-(трифторметил)бензил]-2-(3-{(2R)2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-[3,5-бiс(Tрифторметил)бензил]-2-(3-{(2R)-2[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-[3-Фтор-5-(трифторметил)бензил]-2-(3-{(2R)2-[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-(3,4-Дихлорбензил)-2-(4-{2-[((2R)-2-гідрокси2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2і\летилпропіл}феніл)ацетамід, N-[2-Хлор-5-(трифторметил)бензил]-2-(4-{2[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-[4-Хлор-3-(трифторметил)бензил]-2-(4-{2[((2R)-2-гідрокси-2-{4-гідрокси-3 27 [(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-[3,5-бiс(Трифторметил)бензил]-2-(4-{2[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-[3-Фтор-5-(трифторметил)бензил]-2-(4-{2[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-[2-Фтор-5-(трифторметил)бензил]-2-(4-{2[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-[4-Фтор-2-(трифторметил)бензил]-2-(4-{2[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, N-[4-Фтор-3-(трифторметил)бензил]-2-(4-{2[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, 2-(4-{(2R)-2-[((2R)-2-Пдрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N-(2-метоксибензил)ацетамід, N-(2-Етоксибензил)-2-(4-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-Бензил-2-(4-{(2R-2-[((2R)-2-гідрокси-2-{4гідрокси-3-[(метилсульфоніл)аміно] феніл}етил)аміно]пропіл}феніл)ацетамід, 2-(4-{(2R)-2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)-N-(3-фенілпропіл)ацетамід, N-(2,3-Дигідро-1Н-інден-2-іл)-2-(3-{(2R)-2[((2R)-2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, 2-(3-{(2R)-2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N(2-метоксибензил)ацетамід, N-Бензил-2-(3-{(2R)-2-[((2R)-2-гідрокси-2-{4гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, 2-(3-{(2R)-2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)-N-(2-фенілетил)ацетамід, 2-(3-{(2R)-2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N(мезитилметил)ацетамід, 2-(3-{(2R)-2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N-(2,3,6трихлорбензил)ацетамід, 2-(3-{2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-[3(трифторметил)бензил]ацетамід, N-(2,3-Дихлорбензил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, 82283 28 N-(3-Хлор-4-метилбензил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, 2-(3-{2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-[2(метилтіо)бензил]ацетамід, 2-(3-{2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-[4(метилтіо)бензил]ацетамід, 2-(3-{2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-(тетрагідро-2Н-тіопіран-4іл)ацетамід, N-(Біфеніл-2-ілметил)-2-(3-{2-[((2R)-2-гідрокси2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетамід, 2-(3-{(2R)-2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N-(1нафтилметил)ацетамід, 2-(3-{(2R)-2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N-(піридин-2ілметил)ацетамід, 2-(3-{(2R)-2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аіиіно]феніл}етил)аміно]пропіл}феніл)-N-[4(трифторметокси)бензил]ацетамід, N-(4-Ціанобензил)-2-(3-{(2R)-2-[((2R)-2гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, N-[4-(Диметиламіно)бензил]-2-(3-{(R)-2-[((2R)2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, 2-(3-{(2R)-2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл}феніл)-N-фенілацетамід, N-(1-Бензилпіперидин-4-іл)-2-(3-{(2R)-2-[((2R)2-гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетамід, і 2-(3-{2-[((2R)-2-Гідрокси-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)-N-(мезитилметил)ацетамід. Згідно з одним з аспектів представленого винаходу, сполуки формули (І), де (СН2)n-C(=O)Q1 група розташована в мета положенні, є особливо переважними. Фармацевтично прийнятними солями сполук формули (1) є кислотно-адитивні і основноадитивні солі. Придатні кислотно-адитивні солі утворюються з кислот, які утворюють нетоксичні солі. Прикладами солей є ацетат, аспартат, бензоат, безилат, бікарбонат/карбонат, бісульфат/сульфат, борат, камсилат, цитрат, едисилат, езилат, форміат, фумарат, глуцептат, глюконат, глюкуронат, гексафторфосфат, гібензат, гідрохлорид/хлорид, гідробромід/бромід, 29 гідройодид/йодид, ізетіонат, лактат, малат, малеат, малонат, мезилат, метилсульфат, нафтилат, 2-напсилат, нікотинат, нітрат, оротат, оксалат, пальмітат, памоат, фосфат/гідрофосфат/дигідрофосфат, сахарат, стеарат, сукцинат, тартрат, тозилат і трифторацетат і ксинафоат. Придатні основні солі одержують з основ, які утворюють нетоксичні солі. Прикладами є солі алюмінію, аргініну, бензатину, кальцію, холіну, діетиламіну, діоламіну, гліцину, лізину, магнію, меглуміну, оламіну, калію, натрію, трометаміну і цинку. Також можуть бути одержані гемісолі кислот і основ, наприклад, гемісульфатні і гемікальцієві солі. Для ознайомлення з придатними солями, дивіться, Stahl and Wermuth, Handbook of Pharmaceutical Salts: Properties, Selection, and Use, Wiley-VCH, Weinheim, Germany (2002). Фармацевтично прийнятні солі сполук формули (1) можна одержати за допомогою одного або декількох з трьох методів: (і) за допомогою взаємодії сполуки формули (1) з бажаною кислотою або основою; (іі) шляхом видалення кислото- або основонестійкої захисної групи в придатному попереднику сполуки формули (1) або шляхом розмикання циклу придатного циклічного попередника, наприклад, лактону або лактаму, використовуючи бажану кислоту або основу; або (ііі) шляхом перетворення однієї солі сполуки формули (1) у іншу за допомогою реакції з прийнятною кислотою або основою або використовуючи придатну іонообмінну колонку. Всі три реакції типово проводять в розчині. Одержана сіль може випасти в осад і може бути зібрана фільтруванням або може бути відновлена шляхом випаровування розчинника. Ступінь іонізації одержаної солі може змінюватись з повністю іонізованої до майже неіонізованої. Сполуки винаходу можуть існувати у несольватованій і сольватованій формах. Термін 'сольват' використовується тут для опису молекулярних комплексів, що містять сполуку винаходу і стехіометричну кількість однієї або декількох фармацевтично прийнятних молекул розчинника, наприклад, етанол. Термін 'гідрат' використовується, коли згаданий розчинник є водою. Включеними в межі винаходу є комплекси, такі як клатрати, комплекси включення лікарський засіб-хазяїн, в яких, на противагу згаданим вище сольватам, лікарський засіб і хазяїн присутні в стехіометричній або нестехіометричній кількості. Також включеними є комплекси лікарського засобу, що містять два або більше органічних і/або неорганічних компонентів, які можуть бути в стехіометричній або нестехіометричній кількостях. Одержані комплекси можуть бути іонізованими, частково іонізованими або неіонізованими. Огляд таких комплексів приводиться в J Pharm Sci, 64 (8), 1269-1288 by Haleblian (August 1975). 82283 30 Тут і далі всі посилання на сполуки формули (1) включають посилання на їх солі, сольвати і комплекси і сольвати і комплекси їх солей. Сполуки винаходу включають сполуки формули (1), як тут визначено вище, включаючи всі їх поліморфи і кристали, їх пролікарські форми і ізомери (включаючи оптичні, геометричні і таутомерні ізомери), як тут визначено, і мічені ізотопами сполуки формули (1). Як вказується, так звані 'проліки' сполук формули (1) також включаються в рамки винаходу. Таким чином, деякі похідні сполук формули (1), які можуть мати малу або немати зовсім фармакологічної активності можуть, коли вводяться в або на тіло, перетворюватись у сполуки формули (1), що мають бажану активність, наприклад, шляхом гідролітичного розщеплення. Такі похідні відносяться до 'проліків'. Додаткову інформацію по використанню проліків можна знайти в 'Pro-drugs as Novel Delivery Systems, Vol. 14, ACS Symposium Series (T. Higuchi and W. Stella) і 'Bioreversible Carriers in Drug Design', Pergamon Press, 1987 (ed. Ε. Β Roche, American Pharmaceutical Association). Проліки у відповідності з винаходом можуть, наприклад, бути одержані шляхом заміни прийнятної групи присутньої в сполуці формули (1) деякими замісниками відомими спеціалістам в цій галузі як 'прο-замісники', як описується, наприклад, в "Design of Prodrugs" by H. Bundgaard (Elsevier, 1985). Деякими прикладами проліків у відповідності з винаходом є: (і) коли сполуки формули (1) містять карбоксильну групу (-СООН), її естер, наприклад, сполука, в якій водень карбонової кислоти сполуки формули (1) замінений (С1-С8)алкілом; (іі) коли сполуки формули (1) містять спиртову групу (-ОН), її етер, наприклад, сполука, в якій водень спиртової групи сполуки формули (1) замінений (С1-С6)алканоїлоксиметилом; і (ііі) коли сполуки формули (1) містять первинну або вторинну аміногрупу (-NH2 або -NHR, де R¹Н), її амід, наприклад, сполука, в якій, в залежності від обставин, один або обидва водні аміногрупи сполуки формули (1) є заміненим(и) (С1С10)алканоїлом. Інші приклади заміщувальних груп у відповідності із згаданими вище прикладами і прикладами інших типів проліків можна знайти в приведених вище посиланнях. Однак, деякі сполуки формули (1) можуть самі по собі виступати як проліки інших сполук формули (1). Також включені в рамки винаходу метаболіти сполук формули (1), що є сполуками, які утворюються in vivo після введення лікарського засобу. Деякими прикладами метаболітів згідно з винаходом є (і) коли сполука формули (1) містить метильну групу, її гідроксиметильне похідне (-СН3 ® СН2ОН): (іі) коли сполука формули (1) містить алкоксигрупу, її гідроксипохідне (-OR ® -ОН); 31 (ііі) коли сполука формули (1) містить третинну аміногрупу, її вторинний амін (-NR1R2 ® -NHR1 або -NHR2); (iv) коли сполука формули (1) містить вторинну аміногрупу, її первинне похідне (-NHR1 ® -NH2); (ν) коли сполука формули (1) містить фенільний замісник, її фенольне похідне (-Рh ® PhOH); і (vi) коли сполука формули (1) містить амідну групу, похідне карбонової кислоти (-CONH2 ® СООН). Сполуки формули (1), що містять один або декілька асиметричних атомів вуглецю можуть існувати як два або більше стереоізомерів. Коли сполука формули (1) містить алкенільну або алкеніленову групу, можлива геометрична цис/транс (або Z/E) ізомерія. Коли структурний ізомеризм є взаємозмінюваним завдяки низькій енергії бар'єру, може мати місце таутомерний ізомеризм („таутомеризм"). Це може мати місце у формі прогонової таутомерії в сполуках формули (1), що містять, наприклад, іміно, кето або оксимні групи, або так званий валентний таутомеризм в сполуках, які містять ароматичний замісник. Звідси випливає, що одна сполука може проявляти більше ніж один тип ізомеризму. Включеними в межі представленого винаходу є всі стереоізомери, геометричні ізомери і таутомерні форми сполук формули (1), включаючи сполуки, що проявляють більше ніж один тип ізомеризму і суміші одного або декількох. Також включеними є кислотноадитивні солі або основні солі, в яких протиіон є оптично-активним, наприклад, d-лактат або І-лізин, або рацемічний, наприклад, dl-тартрат або dl-аргінін. Цис/транс ізомери можуть бути розділені за допомогою загальновідомих методик добре відомих спеціалісту в цій галузі, наприклад, хроматографія і фракційна кристалізація. Загальновідомі методики для одержання/виділення окремих енантіомерів включають хіральний синтез з придатного оптично чистого попередника або розділення рацемату (або рацемату солі або похідного) використовуючи, наприклад, хіральну високоефективну рідинну хроматографію (ВЕРХ). Альтернативно, рацемат (або рацемічний попередник) може реагувати з придатною оптичноактивною сполукою, наприклад, спиртом, або, у випадку, коли сполука формули (1) містить кислотний або основний замісник, кислотою або основою, такою як винна кислота або 1фенілетиламін. Одержану діастереомерну суміш можна розділити використовуючи хроматографію і/або фракційну кристалізацію і один або обидва діастереоізомери перетворюють у відповідний чистий енантіомер(и) за способами добре відомими спеціалісту в цій галузі. Хіральні сполуки винаходу (і їх хіральні попередники) можна одержати в енантіомернозбагаченій формі використовуючи хроматографію, типово ВЕРХ, на асиметричній смолі χ рухомою фазою, що містить вуглеводень, типово гептан або гексан, що містить від 0 до 50% об'ємних ізопропанолу, типово від 2% до 20%, і від 82283 32 0 до 5% об'ємних алкіламіну, типово 0,1% діетиламіну. Концентрування елюенту дає збагачену суміш. Стереізомерні конгломерати можна розділити за допомогою звичайних методик відомих спеціалісту в цій галузі, дивіться, наприклад, "Stereochemistry of Organic Compounds" by Ε. L Eliel (Wiley, New York, 1994). Згідно з аспектом представленого винаходу, (R,R)-стереоізомер формули приведеної нижче, де R1 є водень і R2 є С1-С4алкіл, переважно феніл, і n і Q1 є такими як визначено вище, є особливо переважним: Представлений винахід включає всі фармацевтично прийнятні ізотопічно-мічені сполуки формули (1), в яких один або декілька атомів замінена атомами, що мають теж саме атомне число, але атомну масу або масове число, що відрізняється від атомної маси або масового числа, яке домінує в природі. Прикладами ізотопів для включення в сполуки винаходу є ізотопи водню, такі як 2 Н і 3 Н, вуглецю, такі як 11С, 13С і 14С, хлору, такі як 36СІ, фтору, такі як 18F, йоду, такі як 123І і 125І, азоту, такі як 13N і 15 N, кисню, такі як 15О, 17О і 18О, фосфору, такі як 32Р і сірки, такі як 35S. Деякі ізотопічно-мічені сполуки формули (1), наприклад, ті що включають радіоактивний ізотоп, є корисними в дослідженнях лікарського засобу і/або розподілення субстрату в тканині. Радіоактивні ізотопи тритію, тобто 3Н, і вуглецю14, тобто 14С, є особливо корисними для цих цілей з огляду на легкість їх включення і легкість детектування. Заміщення тяжчими ізотопами, такими як дейтерій, тобто 2Н, може давати деякі терапевтичні переваги внаслідок збільшення метаболітичної стабільності, наприклад, збільшення in vivo часу напіврозкладу або зменшення необхідної дози, і звідси може бути переважним в деяких випадках. Заміщення позитрон емітуючими ізотопами, такими як 11С, 18F, 15O і 13N, може бути корисним в дослідженнях позитронноемісійної топографії (PET) для визначення блокування рецептора субстратом. Ізотопічно-мічені сполуки формули (1) загалом можна одержати за допомогою звичайних методик відомих спеціалісту в цій галузі або за допомогою процесів аналогічних тим, що описуються в супровідних Прикладах і Приготуваннях використовуючи прийнятні мічені ізотопами реагенти замість не мічених реагентів використовуваних раніше. Фармацевтично прийнятними сольватами у відповідності з винаходом є такі, в яких кристалізаційний розчинник може бути ізотопічно заміщеним, наприклад, D2O, d6-ацетон, d6-ДМСО. 33 Сполуки формули (1), їх фармацевтично прийнятні солі і/або похідні є цінними фармацевтично активними сполуками, які є придатними для лікування і профілактики ряду розладів, в які втягнутий β2 рецептор або в яких агонізм цього рецептора може давати користь, зокрема, алергічні і неалергічні захворювання дихальних шляхів, але також для лікування інших захворювань, таких як, але не обмежується, захворювання нервової системи, передчасні пологи, застійна серцева недостатність, депресія, запалення і алергічні захворювання шкіри, псоріаз, проліферативні захворювання шкіри, глаукома і при станах, при яких необхідне зменшення шлункової кислотності, особливо при виразці шлунку і дванадцятипалої кишки. Сполуки винаходу призначені для фармацевтичного застосування можуть бути введені як кристалічні або аморфні продукти. Вони можуть бути одержані, наприклад, як тверді речовини, порошки або плівки за методами, такими як осадження, кристалізація, сублімація, висушуванням розпиленням або упарюванням. Для цих цілей може бути використано висушування із використанням мікрохвильового або радіовипромінування. Вони можуть бути введені окремо або в комбінації з іншими сполуками винаходу або в комбінації з одним або декількома іншими лікарськими засобами (або будь-яка їх комбінація). Загалом, вони будуть вводитись як рецептури у поєднанні з одним або більшою кількістю фармацевтично прийнятних екціпієнтів. Термін "екціпієнт" використовується тут для опису будьякого інгредієнту іншого ніж сполука(и) винаходу. Вибір екціпієнту буде у великій мірі залежати від ряду факторів, таких як вибраний шлях введення, вплив екціпієнту на розчинність і стабільність і природа дозованої форми. Фармацевтичні композиції придатні для вивільнення сполук представленого винаходу і способи їх одержання очевидні спеціалісту в цій галузі. Такі композиції і способи їх одержання можна знайти, наприклад, в 'Remington's Pharmaceutical Sciences', 19th Edition (Mack Publishing Company, 1995). Сполуки винаходу також можна вводити безпосередньо в потік крові, в м'яз або у внутрішній орган. Придатними шляхами для парентерального введення є внутрішньовенне, внутрішньоартеріальне, внутрішньоочеревинне, інтратекальне, інтравентрикулярне, інтрауретральне, інтрастернальне, інтракраніальне, внутрішньом'язове і підшкірне. Придатними пристроями для парентерального введення є голкові (включаючи мікроголки) ін'єктори, безголкові ін'єктори і засоби вливання. Парентеральні рецептури типово є водними розчинами, які можуть містити екціпієнти, такі як солі, карбогідрати і буфереючі агенти (переважно до рН від 3 до 9), але, для деяких застосувань, вони можуть бути більш придатносформовані як стерильний неводний розчин або як суха форма, що використовується у поєднанні з придатним 82283 34 розчинником, таким як стерильна пірогенвільна вода. Одержання парентеральних рецептур в стерильних умовах, наприклад, шляхом ліофілізації, можна легко здійснити використовуючи стандартні фармацевтичні методики добре відомі спеціалісту в цій галузі. Розчинність сполук формули (1), що використовується при одержанні парентеральних розчинів, може бути збільшена шляхом використання прийнятних методик формування рецептур, таких як включення агентів, що збільшують розчинність. Рецептури для парентерального введення можуть бути сформовані для негайного і/або модифікованого вивільнення. Рецептури модифікованого вивільнення мають відстрочене-, тривале-, пульсуюче-, контрольоване-, цільове і програмоване вивільнення. Таким чином, сполуки винаходу можуть бути сформовані як тверда, напівтверда або тиксотропна рідина для введення як імплантуємого депо, для забезпечення модифікованого вивільнення активної сполуки. Прикладами таких рецептур є покриті лікарським засобом стенти і мікросфери з полі(dІ-молочнаспівгліколева)кислоти (PGLA). Сполуки винаходу також можуть бути нанесені на шкіру або слизову оболонку, тобто дермально або трансдермально. Типовими рецептурами для цих цілей є гелі, гідрогелі, лосьйони, розчини, креми, мазі, порошки для обтрушування, пов'язки, піни, плівки, пластири, пластинки, імплантати, губки, волокна, бандажі і мікроемульсії. Також можуть бути використані ліпосоми. Типовими носіями є спирт, вода, мінерально масло, рідкий вазелін, білий вазелін, гліцерин, поліетиленгліколь і пропіленгліколь. Можуть бути включені покращувачи проникнення - дивіться, наприклад, J Pharm Sci, 88 (10), 955-958 by Finnin and Morgan (October 1999). Iншими засобами місцевого введення є доставка за допомогою електропорації, фонтофорез, фонофорез, сонофорез і мікроголкова або безголкова методика (наприклад Powderject™, Bioject™, etc.) ін'єктування. Рецептури для місцевого введення можуть бути сформовані для негайного і/або модифікованого вивільнення. Рецептури модифікованого вивільнення мають відстрочене-, тривале-, пульсуюче-, контрольоване-, цільове і програмоване вивільнення. Сполуки винаходу також можуть бути введені інтраназально або за допомогою інгаляції, типово у формі сухого порошку (або окремо, або як суміш, наприклад, суха суміш з лактозою, або як змішані часточки компонентів, наприклад, суміші з фосфоліпідами, такими як фосфатидилхолін) з інгалятору сухого порошку або як аерозоль з контейнеру під тиском, насосу, спрею, пульверизатор (переважно використовують електродинамічний пульверизатор для одержання тонкого туману) або розпилювач, з або без використання придатного пропеланту, такого як 1,1,1,2-тетрафторетан або 1,1,1,2,3,3,3гептафторпропан. Для інтраназального 35 використання, порошок може містити біоадгезивні агенти, наприклад, цитозан або циклодекстрин. Контейнер під тиском, насос, спрей, пульверизатор або розпилювач містить розчин або суспензію сполук(и) винаходу, що включає, наприклад, етанол, водний етанол, або придатний альтернативний агент для диспергування, солюблізування або розтягування вивільнення активної речовини, пропелан(и) як розчинник і, необов'язково, поверхнево-активну речовину, таку як триолеат сорбіту, олеїнова кислота або олігомолочна кислота. Перед використанням сухого порошку або суспензії, лікарський продукт мікронізують до розміру придатного для вивільнення за допомогою інгалювання (типово менше ніж 5 мікрон). Це можна досягти будь-яким прийнятним методом подрібнення, таким як спіральний струминний млин, струминний млин з псевдо-зрідженим шаром, суперкритична рідинна обробка для одержання наночасточок, гомогенізація при високому тиску або висушування розпиленням. Капсули (виготовлені, наприклад, з желатину або гідроксипропілметилцелюлози), блістери і картриджі для використання в інгаляторі або інсуфлаторі можуть бути сформовані таким чином, що містять порошкову суміш сполуки винаходу, придатної порошкової основи, такі як лактоза або крохмаль і модифікатор експлуатаційних якостей, таки як І-лейцин, маніт або стеарат магнію. Лактоза може бути безводною або у формі моногідрату, переважно остання. Іншими придатними екціпієнтами є декстран, глюкоза, мальтоза, сорбіт, ксиліт, фруктоза, цукроза і трехалоза. Придатний розчин для використання в пульверизаторі, що використовує електродинамічну силу для одержання тонкого туману, може містити від 1 мкг до 20 мг сполуки винаходу і випускний об'єм може змінюватись від 1 мкл до 100 мкл. Типово рецептура може містити сполуку формули (1), пропіленгліколь, стерильну воду, етанол і хлорид натрію. Альтернативними розчинниками, які можуть бути використані замість пропіленгліколю є гліцерин гліцерин і поліетиленгліколь. В такі рецептури винаходу, що призначені для інгалювання/інтраназальнного введення, можуть бути додані придатні ароматизатори, такі як ментол і левоментол, або підсолоджувачи, такі як сахарин або сахарин натрію. Рецептури для інгалювання/інтраназальнного введення можуть бути сформовані для негайного і/або модифікованого вивільнення використовуючи, наприклад, PGLA. Рецептури модифікованого вивільнення мають відстрочене-, тривале-, пульсуюче-, контрольоване-, цільове і програмоване вивільнення. У випадку інгалятору сухого порошку і аерозолю, одиниця дозування визначається за допомогою клапану, який вивільнює виміряну кількість. Одиниці у відповідності з винаходом типово готовляться для введення виміряної дози або "пшику", що містить від 0,001 мг до 10 мг сполуки формули (1). Загальна добова доза 82283 36 зазвичай знаходиться в інтервалі від 0,001 мг до 40 мг, яка може вводитись однією дозою або, що типовіше, як розподілені дози протягом дня. Сполуки формули (1) є особливо придатними для введення за допомогою інгаляції. Сполуки винаходу можуть бути введені ректально або вагінально, наприклад, у формі супозиторію, песарію або клізми. Масло какао є традиційною супозиторійною основою, але можуть бути використані різні альтернативи, якщо це можливо. Рецептури для ректального/вагінального введення можуть бути сформовані для негайного і/або модифікованого вивільнення. Рецептури модифікованого вивільнення мають відстрочене-, тривале-, пульсуюче-, контрольоване-, цільове і програмоване вивільнення. Сполуки винаходу також можуть бути введені безпосередньо у око або вухо, типово у формі крапель мікронізованої суспензії або розчину в ізотонічному, рН-коригованому, стерильному саліні. Іншими рецептурами придатними для окулярного або вушного введення є мазі, біодеградуємі (наприклад, абсорбуємі гелеві губки, колаген) і небіодеградуємі (наприклад, силікон) імплантати, пластинки, лінзи і часточкові або везикулярні системи, такі як ніосоми або ліпосоми. Можуть бути включені полімери, такі як поперечнозшиті поліакрилові кислоти, полівініловий спирт, гіалуронова кислота, полімери целюлози, наприклад, гідроксипропілметилцелюлоза, гідроксиетилцелюлоза, або метилцелюлоза, або гетерополісахаридні полімери, наприклад, геланова смола, разом з консервантом, таким як бензалконійхлорид. Такі рецептури можуть бути вивільнені за допомогою іонтофорезу. Рецептури для окулярного/вушного введення можуть бути сформовані для негайного і/або модифікованого вивільнення. Рецептури модифікованого вивільнення мають відстрочене-, тривале-, пульсуюче-, контрольоване-, цільове і програмоване вивільнення. Сполуки винаходу можуть бути об'єднані з розчинними макромолекулярними сполуками, такими як циклодекстрин і їх придатні похідні або поліетиленгліколь-вмісні полімери, для того щоб покращити їх розчинність, швидкість розчинення, замаскувати смак, біодоступність і/або стабільність для використання в будь-якому з вищезгаданих шляхів введення. Комплекси лікарський засіб-циклодекстрин, наприклад, знайшли застосування в більшості видів дозованих форм і шляхів введення. Можуть бути використані комплекси включення і невключения. Як альтернатива безпосередньому комплексуванню з лікарським засобом, циклодекстрин може бути використаний як допоміжна добавка, тобто, як носій, розріджувач або солюбілізатор. Найбільш часто для цих цілей використовується альфа-, бетаі гамациклодекстрини, приклади яких можна знайти в міжнародних заявках WO 91/11172, WO 94/02518 і WO 98/55148. 37 Оскільки може бути бажано ввести комбінацію активних сполук, наприклад, з ціллю лікування окремої хвороби або стану, в межах представленого винаходу, що дві або більше фармацевтичних композицій, принаймні, одна з яких містить сполуку у відповідності з винаходом, можуть легко бути об'єднані у формі набору придатного для спільного введення композицій. Таким чином, набір винаходу містить дві або більше окремих фармацевтичних композиції, принаймні, одна з яких містить сполуку формули (1) у відповідності з винаходом, і пристрої для окремого утримання згаданих композицій, такі як контейнер, окремі пляшечки або окремі пакетики з фольги. Прикладом такого набору є звичайна блістерна упаковка, що використовується для пакування таблеток, капсул і їм подібних. Набір винаходу є особливо придатним для введення різних дозованих форм, наприклад, парентерально, для введення окремих композицій з різними інтервалами дозування, або для титрування окремих композицій одна до одної. Для сприяння відповідності, набір типово містить вказівки по введенню і може бути забезпечений так званою пам'яткою. Для введення людям, загальна добова доза сполуки винаходу типово знаходиться в інтервалі від 0,001 мг до 5000 мг, що звичайно залежить від шляху введення. Наприклад, внутрішньовенна добова доза може потребувати тільки від 0,001 мг до 40 мг. Загальна добова доза може бути введена за один раз або розподілена на декілька доз і може, на розсуд лікаря, випадати з типового інтервалу приведеного тут. Ці дози формуються виходячи з середньої людини, що має вагу приблизно 65 - 70 кг. Лікар легко визначить дози для суб'єкта вага якого випадає з цього інтервалу, такого як дитина і людина похилого віку. Для уникнення сумнівів, посилання тут на "лікування" включає посилання на зцілююче, паліативне і профілактичне лікування. Згідно з іншим втіленням представленого винаходу, сполуки формули (1) або їх фармацевтично прийнятні солі, похідні або композиції, також можуть бути використані як комбінації з одним або декількома додатковими терапевтичними агентами для спільного введення пацієнтові для одержання деякого окремого терапевтичного кінцевого результату, такого як лікування патофізіологічно-релевантного захворювання, що включає, але не обмежується (і) бронхоконстрикція, (іі) запалення, (ііі) алергія, (ίν) руйнування тканини, (ν) ознаки і симптоми, такі як задуха, кашель. Другим і більше додатковим терапевтичним агентом також може бути сполука формули (1), або їх фармацевтично прийнятна сіль, похідна або композиція, або один або більше β2 агоністів відомих в цій галузі. Більш типово, другий і більше терапевтичний агент будуть вибирати з різних класів терапевтичних агентів. Як тут використовується, терміни "спільне введення", "спільно введенні" і "в комбінації з", стосовно сполук формули (1) і одного або більше 82283 38 інших терапевтичних агентів, призначені для означення, і віднесення, і включення наступного: • одночасне введення такої комбінації сполук(и) формули (1) і терапевтичного агенту(ів) пацієнтові, що потребує лікування, коли такі компоненти сформовані разом в одну дозовану форму, яка вивільнює згадані компоненти, по суті, в той же самий час у згаданому пацієнті, • по суті, одночасне введення такої комбінації сполук(и) формули (1) і терапевтичного агенту(ів) пацієнтові, що потребує лікування, коли такі компоненти сформовані окремо один від одного в різні дозовані форми, які приймаються, по суті, одночасно згаданим пацієнтом, де згадані компоненти вивільнюються, по суті, в той же самий час у згаданому пацієнті, • послідовне введення такої комбінації сполук(и) формули (1) і терапевтичного агенту(ів) пацієнтові, що потребує лікування, коли такі компоненти сформовані окремо один від одного в різні дозовані форми, які приймаються, по суті, послідовно згаданим пацієнтом із значним інтервалом часу між кожним прийомом, де згадані компоненти вивільнюються, по суті, в різний час у згаданому пацієнті; і • послідовне введення такої комбінації сполук(и) формули (1) і терапевтичного агенту(ів) пацієнтові, що потребує лікування, коли такі компоненти сформовані разом в одну дозовану форму, яка вивільнює згадані компоненти контрольовано, де вони одночасно, безперервно і/або з накладенням вивільнюються в той же самий час і/або в різний час у згаданому пацієнті, де кожна частина може бути введення одним або різними шляхами. Придатними прикладами інших терапевтичних агентів, які можуть бути використані в комбінації з сполукою(ами) формули (1) або їх фармацевтично прийнятними солями, похідними або композиціями, є, але не обмежується: (a) інгібітори 5-ліпоксигенази (5-LO) або антагоністи 5-ліпоксигенази активуючого протеїну (FLAP), (b) антагоністи лейкотріену (LTRAs) включаючи антагоністи LTB4, LTC4, LTD4 і LTE4, (c) антагоністи рецептора гістаміну, включаючи Н1 і НЗ антагоністи, (d) агоністи a 1- і a 2-адренорецептора, судинозвужувальні симпатоміметичні агенти для протизастійного застосування, (є) антагоністи мускаринового МЗ рецептора або антихолінергічні агенти, (f) інгібітори PDE, наприклад, інгібітори PDE3, PDE4 і PDE5, (g) теофілін, (h) хромоглікат натрію, (і) інгібітори СОХ як неселективні, так і селективні інгібітори СОХ-1 або СОХ-2 (NSAID), (j) пероральні і інгалюємі глюкокортикоїди, такі як DAGR (дисоційовані агоністи кортикоїдного рецептору), (к) моноклональні антитіла активні проти ендогенного запалення, (І) антагоністи фактору некрозу пухлини (антиTNF-a), 39 (т) інгібітори адгезії молекули, включаючи VLA4 антагоністи, (n) антагоністи рецептора кініну-В1 і -В2, (о) імуносуспресивні агенти, (р) інгібітори матриксних металопротеїназ (ММР), (q) антагоністи рецептора тахікініну NK1, NK2 і NK3, (г) інгібітори еластази, (s) агоністи рецептора аденозину А2а, (t) інгібітори урокінази, (u) сполуки, що діють як допамінові рецептори, наприклад, D2 агоністи, (v) модулятори NFkb шляху, наприклад, ІКК інгібітори, (w) модулятори цитокінових сигнальних шляхів, такі як р38 МАР кіназа або syk кіназа, (х) агенти, що можуть класифікуватись як муколітики або протикашлеві агенти, і (у) антибіотики. Згідно з представленим винаходом, комбінація сполук формули (1) з: - НЗ антагоністами, - антагоністами мускаринового МЗ рецептора, - інгібіторами PDE4, - глюкортикоідами, - агоністами аденозинового А2а рецептору, модуляторами цитокінових сигнальних шляхів, таких як р38 МАР кіназа або syk кіназа, або, антагоністами лейкотрієну (LTRAs) включаючи антагоністи LTB4, LTC4, LTD4 і LTE4, є переважними. Згідно з представленим винаходом, комбінація сполуки формули (1) з: глюкортикостероїдами, зокрема, глюкортикостероїдами, що інгалюються, із зменшеними системними побічними ефектами, включаючи преднізон, преднізолон, флунізолід, тріамцинолон ацетонід, беклометазону дипропіонат, будезонід, флутіказону пропіонат, циклезонід і мометазону фуроат, або - антагоністи мускаринового МЗ рецептора або антихолінергічні агенти, включаючи, зокрема, солі іпратропію, а саме бромід, солі тіотропію, а саме бромід, солі окситропію, а саме бромід, перензепін і телензепін, є переважними. Зрозуміло, що всі посилання тут на лікування включають зцілююче, пом'якшуюче і профілактичне лікування. Опис, приведений далі, стосується терапевтичного застосування при якому сполуки формули (1) можуть бути застосовані. Сполуки формули (1) мають здатність взаємодіяти з β2 рецептором і тому мають широкий спектр терапевтичного застосування, як описується далі, оскільки рецептор β2 відіграє суттєву роль в фізіології всіх ссавців. Тому, наступний аспект представленого винаходу стосується сполук формули (1), або їх фармацевтично прийнятних солей, похідних або композицій, для використання при лікуванні захворювань, розладів і станів, в які включений β2 рецептор. Більш особливо, представлений винахід 82283 40 також стосується сполук формули (1) або їх фармацевтично прийнятних солей, похідних або композицій, для використання при лікуванні захворювань, розладів і станів, що вибирають з групи, яка містить: • астма усіх типів, етіології або патогенезу, зокрема, астма, яку вибирають з групи, яка включає атопічну астму, неатопічну астму, алергічну астму, атопічну бронхіальну ІgЕопосередковану астму, бронхіальну астму, ессенціальну астму, істинну астму, інфекційноалергійну астму викликану патофізіологічними розладами, зовнішню астму викликану факторами оточуючого середовища, ессенціальну астму невідомої або неочевидної причини, неатопічну астму, бронхіальну астму, емфізематозну астму, астму викликану навантаженням, астму викликану алергеном, астму викликану холодним повітрям, професійну астму, інфекційну астму викликану бактеріями, грибками, протозойними або вірусними інфекціями, неалергічну астму, початкову астму, синдром задухи у немовлят і бронхіоліт, • хронічна або гостра бронхоконстрикція, хронічний бронхіт, обструкція малих дихальних шляхів і емфізема, • обструктивні або запальні захворювання дихальних шляхів усіх типів, етіології або патогенезу, зокрема, обструктивні або запальні захворювання дихальних шляхів, які вибирають з групи, що включає хронічну еозинофільну пневмонію, хронічне обструктивне легеневе захворювання (COPD), COPD, що включає хронічний бронхіт, легеневу емфізему або задуху пов'язану або непов'язану з COPD, COPD, що характеризується незворотною прогресуючою обструкцією дихальних шляхів, респіраторний дистрессиндром повнолітніх (ARDS), загострення гіперреактивності дихальних шляхів після лікування іншим лікарським засобом і захворювання дихальних шляхів, що пов'язані з легеневою гіпертензією, • бронхіт усіх типів, етіології або патогенезу, зокрема, бронхіт, який вибирають з групи, що включає гострий бронхіт, гострий гортаннотрахіальний бронхіт, арахідоновий бронхіт, катаральний бронхіт, фібринозний бронхіт, сухий бронхіт, інфекційний астматичний бронхіт, продуктивний бронхіт, стафілококовий або стрептококовий бронхіт і везикулярний бронхіт, • гостре пошкодження легені, • бронхоектазія усіх типів, етіології або патогенезу, зокрема, бронхоектазія, яку вибирають з групи, що включає циліндричну бронхоектазію, осумковану бронхоектазію, веретеноподібну бронхоектазію, капілярну бронхоектазію, циститну бронхоектазію, суху бронхоектазію і фолікулярну бронхоектазію. Ще один наступний аспект представленого винаходу стосується застосування сполук формули (1), або їх фармацевтично прийнятних солей, похідних або композицій, для виготовлення лікарського засобу, що має β2 агоністичну активність. Зокрема, представлений винахід стосується застосування сполук формули (1) або 41 їх фармацевтично прийнятних солей, похідних або композицій, для виготовлення лікарського засобу для лікування β2-опосередкованих захворювань і/або станів, зокрема, захворювань і/або станів приведених вище. Як результат, представлений винахід забезпечує особливо цікавий метод лікування ссавця, включаючи людину, що включає лікування згаданого ссавця ефективною кількістю сполуки формули (1) або її фармацевтично прийнятною сіллю, похідним або композицією. Більш особливо, представлений винахід забезпечує особливо цікавий спосіб лікування ссавця, включаючи людину, для лікування β2-опосередкованого захворювань і/або станів, зокрема, захворювань і/або станів приведених вище, що включає лікування згаданого ссавця ефективною кількістю сполуки формули (1) або її фармацевтично прийнятними солями або похідними. Наступні приклади ілюструє одержання сполук формули (1): Приготування 1 : Метил [3-(2оксопропіл)феніл]ацетат Трибутилолова метоксид (28,3мл, 98ммоль), метил (3-бромфеніл)ацетат (WO 95/27692, стор. 16, наприклад 5а) (15,0г, 65,0ммоль), ізопропенілацетат (10,8мл, 98,0ммоль), ацетат паладію (II) (750мг, 3,30ммоль) і три-ортотолілфосфін (2,0г, 6,5ммоль) перемішували в толуолі (75мл) при 100°С в атмосфері азоту протягом 5 годин. Після охолодження реакцію розводили етилацетатом (150мл) і 4М водним розчином фториду калію (90мл) і перемішували протягом 15 хвилин. Суміш фільтрували через Арбоцель® і органічну фазу відокремлювали і концентрували у вакуумі. Залишок очищали за допомогою колонкової хроматографії на силікагелі, елюювали діетиловий етер:пентан (0:100 - 25:75 і потім змінювали до дихлорметану), одержуючи вказану в заголовку сполуку як блідожовте масло, 12,6г. 1 Н ЯМР(СОСІ 3, 400МГц) δ: 2,15 (с, 3Н), 3,61 (с, 2Н), 3,69 (с, 5Н), 7,10-7,13 (м, 2Н), 7,19 (д, 1Н), 7,30 (т, 1Н)м.ч. МС (електророзпилення): m/z 229 [MNa]+ Приготування 2 : Метил [3-((2R)-2-{[(1R)-1феніл етил]аміно}пропіл)феніл]-ацетату гідрохлорид Розчин кетону приготування 1 (8,5г, 41,2ммоль), (R)-a-метилбензиламіну (4,8мл, 37,2ммоль), триацетоксиборгідриду натрію (11,6г, ббммоль) і оцтової кислоти (2,2мл, 38ммоль) в дихлорметані (400мл) перемішували при кімнатній температурі 48 годин. Реакційну суміш гасили 82283 42 додаючи насичений водний бікарбонат натрію (200мл) і залишали перемішуватись до завершення виділення газу. Органічну фазу відокремлювали і водну фазу екстрагували дихлорметаном (100мл). Об'єднані органічні екстракти сушили (сульфат магнію) і концентрували у вакуумі. Очищали за допомогою колонкової хроматографії на силікагелі елюювали дихлорметан:метанол:0,880 аміак (99:1:0,1 змінювали до 95:5:0,5) одержуючи 4:1 суміш діастереомерів (R,R основний) як блідо-жовте масло (8,71г). Обробка 1М розчином хлориду водню в метанолі (40мл, 40ммоль), з наступною трикратною кристалізацією з суміші діізопропіловий етер:метанол давала вказану в заголовку сполуку як безбарвну кристалічну речовину, 5,68г. Приготування 3 : Метил {3-[(2R)-2амінопропіл]феніл}ацетат Розчин аміну приготування 2 (7,69г, 22ммоль) і форміату амонію (6,94г, 110ммоль) в метанолі (50мл) нагрівали при 75°С в присутності 20% гідроксиду паладію-на-вугіллі (2,00г). Через 90 хвилин реакційну суміш охолоджували до кімнатної температури, фільтрували через Арбоцель® і фільтрат концентрували у вакуумі. Залишок розділяли між дихлорметаном (100мл) і 0,880 аміаком (100мл) і органічну фазу відокремлювали. Водну фазу екстрагували дихлорметаном (100мл) і об'єднані органічні екстракти сушили (сульфат магнію) і концентрували у вакуумі одержуючи вказану в заголовку сполуку як безбарвне масло, 4,78г. 1 Н ЯМР (CD3OD, 400МГц) δ: 1,06 (д, 3Н), 2,572,67 (м, 2Н), 3,05-3,12 (м, 1Н), 3,63 (с, 2Н), 3,67 (с, 3H), 7,09-7,13 (м, 3H), 7,23-7,27 (т, 1Н) м.ч. МС (електророзпилення): m/z 208 [М+Н]+ Приготування 4 : N-{2-(бензилокси)-5-[(1R)-2бром-1-гідроксиетил]фенш}-метансульфонамід Розчин (1R)-1-[3-аміно-4-(бензилокси)феніл]-2брометаноле (Org. Process Research and Development, 1998, 2, 96) (30,8г, 95,6ммоль) в дихлорметані (300мл) обробляли піридином (9,3мл, 115ммоль). Одержаний розчин охолоджували до 5°С і по краплям додавали розчин метансульфонілхлориду (7,8мл, 100,7ммоль) в дихлорметані (10мл). Суміш перемішували при 5°С протягом ще 30 хвилин і залишали поступово нагріватись до кімнатної температури протягом 16 годин. Реакційну суміш промивали 2N хлорводневою кислотою (110мл) і органічну фазу відокремлювали, сушили (сульфат магнію) і розчинник видаляли у вакуумі одержуючи 43 оранжеве масло. Залишок кристалізували з гарячого толуолу (100мл) одержуючи вказану в заголовку сполуку як блідо-рожеву тверду речовину (33,7г). 1 Н ЯМР (ДМСOd6, 400МГц) δ: 2,93 (с, 3Н), 3,52-3,66 (м, 2Н), 4,74 (м, 1Н), 5,19 (с, 2Н), 7,11 (д, 1Н), 7,19-7,22 (м, 1Н), 7,33-7,36 (м, 2Н), 7,40-7,43 (м, 2Н), 7,56 (д, 2Н), 8,95 (с, 1Н)м.ч. МС (електророзпилення): m/z 398/400 [М-Н]Приготування 5: N-[2-(бензилокси)-5-((1R)-2бром-1-{[трет-бутил(диметил)силіл]окси}етил)феніл]метансульфонамід Розчин броміду приготування 4 (21,5г, 53,7ммоль) в Ν,Ν-диметилформаміді (125мл) обробляли імідазолом (4,16г, 75,2ммоль) і третбутил(диметил)силілхлоридом (9,73г, 64,5ммоль) і одержаний розчин залишали перемішуватись протягом 16 годин. Реакційну суміш розводили етилацетатом (200мл) і промивали водою (2x100мл). Водні фази об'єднували і екстрагували етилацетатом (100мл). Об'єднані органічні екстракти промивали 2Ν хлорводневою кислотою (100мл), сушили (сульфат магнію) і упарювали у вакуумі. Залишок суспендували в пентан:етилацетат (200мл, 1:1 об'ємних) і розчинник упарювали. Залишок розтирали з пентан:етилацетат (200мл, 1:1 об'ємних) і одержану тверду речовину відфільтровували і сушили у вакуумі одержуючи вказану в заголовку сполуку як безбарвну тверду речовину (23,7г). 1 Н ЯМР (CDCI 3, 400МГц) δ: -0,07 (с, 3H), 0,11 (с, 3H), 0,89 (с, 9Н), 2,91 (с, ЗНО, 4,80-4,83 (м, 1Н), 6,80 (шс, 1Н), 6,98 (д, 1Н), 7,12 (д, 1Н), 7,36-7,44 (м, 5Н), 7,52-7,54 (м, 1Н) м.ч. Альтернативний спосіб одержання сполуки приготування 5: Розчин броміду приготування 4 (10г, 24,98ммоль) розчиняли в DCM (20мл, 2мл/г) і потім додавали імідазол (4,58г, 37,47ммоль, 1,5ек) після чого TBDMSiCI (5,27г, 34,97ммоль, 1,4ек). Реакційну суміш нагрівали із зворотнім холодильником протягом 1 години і залишали охолоджуватись до 30°С. Суміш розводили ізопропілацетатом (80мл, 8мл/г) і гасили 2М НСІ (50, 5мл/г) і інтенсивно перемішували протягом 10 хвилин. Фази розділяли і органічну фазу промивали водою (50мл, 5мл/г). Органічну фазу упарювали до об'єму 25-30мл при пониженому тиску при 45°С. Розчин охолоджували до кімнатної температури і швидко утворювалась суспензія і перемішували при кімнатній температурі ЗО хвилин. Протягом 10 хвилин додавали гептан (20мл, 2мл/г) і суспензію охолоджували до 5-10°С і перемішували протягом 1 години. Суспензію фільтрували і промивали на фільтрувальному папері гептаном (2x10мл). Одержаний на фільтрі залишок сушили у вакуумній печі при 50°С протягом 12 годин одержуючи вказану в заголовку 82283 44 сполуку як білу тверду речовину (11,05г, вихід 86%). 1 Н ЯМР (CDCI 3, 400МГц) δ: -0,07 (с, 3H), 0,11 (с, 3H), 0,89 (с, 9Н), 2,91 (с, 3Н0, 4,80-4,83 (м, 1Н), 6,80 (шс, 1Н), 6,98 (д, 1Н), 7,12 (д, 1Н), 7,36-7,44 (м, 5Н), 7,52-7,54 (м, 1Н) м.ч. Приготування 6: Метил (3-{(2R)-2-[((2R)-2-{4(бензилокси)-3-[(метилсульфоніл)аміно]феніл}-2{[трет-бутил(диметил)силіл]окси}етил)аміно]пропіл}феніл)ацетат Амін приготування 3 (4,2г, 20,2ммоль) розчиняли в дихлорметані (20мл), обробляли бромідом приготування 5 (8,0г, 15,6ммоль) і реакційну суміш нагрівали при 90°С протягом 16 годин (розчиннику дозволяли упаритись). Реакційну суміш розводили етилацетатом (200мл), промивали 1М водним гідроксидом натрію (30мл), сушили (сульфат магнію) і концентрували у вакуумі. Залишок очищали за допомогою колонкової хроматографії на силікагелі елюювали етилацетат:пентан (1:1 змінювали до 3:2) одержуючи вказаний в заголовку продукт (5,8г). 1 Н ЯМР (CD3OD, 400МГц) δ: -0,18 (с, 3Н), -0,01 (с, 3Н), 0,82 (с, 9Н), 1,05 (д, 3Н), 2,54-2,66 (м, 3Н), 2,83 (с, 3Н), 2,85-2,93 (м, 2Н), 3,59 (с, 2Н), 3,66 (с, 3H), 7,69-4,72 (м, 1Н), 5,18 (с, 2Н), 6,97-7,07 (м, 5Н), 7,14-7,18 (м, 1Н), 7,30-7,40 (м, 4Н), 7,48 (д, 2Н) м.ч. МС (електророзпилення): m/z 641 [М+Н]+ Приготування 7: Метил [4-((2R)-2-{[(1R)-1фенілетил]аміно}пропіл)-феніл]ацетату гідрохлорид Вказану в заголовку сполуку одержували за методикою подібною описаній для приготування 2 використовуючи метил 4-(оксопропіл)-фенілацетат (WO 97/24331, стор. 68, наприклад 24D). 1 Н ЯМР (CD3OD, 400МГц) δ: 1,18 (д, 3Н), 1,70 (д, 3Н), 2,62 (дд, 1Н), 3,18 (м, 1Н), 3,30 (м, 1Н), 3,62 (с, 2Н), 3,66 (с, 3H), 4,61 (к, 1Н), 7,06 (д, 2Н), 7,21 (д, 2Н), 7,53 (м, 5Н) м.ч. МС (електророзпилення): m/z 312 [М+Н]+ Приготування 8 : Метил {4-[(2R)-2амінопропіл]феніл}ацетат Вказану в заголовку сполуку одержували за методикою подібною описаній для приготування 3 використовуючи амін приготування 7. 1 Н ЯМР (CDCIs, 400МГц) δ: 1,14 (д, 3Н), 2,79 (м, 2Н), 3,39 (к, 1Н), 3,60 (с, 2Н), 3,68 (с, 3Н), 7,17 (д,2Н), 7,22 (д,2Н)м.ч. 45 МС (елекгророзпилення): m/z 208 [М+Н]+ Приготування 9: Метил (4-{(2R)-2-[((2R)-2-{4(бензилокси)-3-[(метилсульфоніл)аміно]феніл}-2{[трет-бутил(диметил)силіл]окси}етил)аміно]пропіл}феніл)ацетат Бромід приготування 5 (2,0г, 4,11ммоль), амін приготування 6 (852мг, 4,11ммоль) і Nетилдіізопропіламін (531 мг, 4,11ммоль) розчиняли в диметилсульфоксиді (бмл) і реакційну суміш нагрівали при 90°С протягом 16 годин. Реакційну суміш розводили етилацетатом (100мл) і промивали нас. вод. хлоридом натрію (4х50мл), сушили (сульфат магнію) і концентрували у вакуумі. Залишок очищали за допомогою колонкової хроматографії на силікагелі елюювали дихлорметан:метанол (100:0 змінювали до 95:5) одержуючи вказаний в заголовку продукт, 520мг. 1 Н ЯМР (CDCI 3, 400МГц) δ: -0,16 (с, 3Н), -0,04 (с, 3Н), 0,83 (с, 9Н), 1,07 (с, 3Н), 2,51 (м, 1Н), 2,75 (м, 2Н), 2,88 (с, 3Н), 2,96 (м, 2Н), 3,18 (с, 2Н), 3,67 (с, 3Н), 4,73 (м, 1Н), 5,09 (с, 2Н), 6,77 (м, 1Н), 6,93 (д, 1Н), 7,04 (дд, 2Н), 7,10 (м, 2Н), 7,16 (м, 2Н), 7,35-7,43 (м, 5Н), 7,50 (д, 1Н)м.ч. МС (електророзпилення): m/z 641 [М+Н]+ Приготування 10 : Діетил 2,2'-(1,4фенілен)діацетат 2,2'-(1,4-фенілен)діоцтова кислота (10,0г, 51ммоль) розчиняли в етанолі (100мл) і розчин обробляли по краплям каталітичною кількістю ацетилхлориду (2,5мл). Реакційну суміш перемішували при нагріванні із зворотнім холодильником протягом 18 годин і потім залишали охолоджуватись і концентрували у вакуумі. Залишок переносили в етилацетат (100мл) і екстрагували розчином бікарбонату натрію (3х50мл) і розсолом (3х50мл). Органічну фазу сушили (сульфат магнію) і концентрували у вакуумі. Залишок розтирали з пентаном одержуючи вказаний в заголовку продукт, 11,8г. 1 Н ЯМР (CDCI 3, 400МГц) δ: 1,26 (τ, 6Н), 3,57 (с, 4Н), 4,12 (к, 4Н), 7,21 (м, 4Н) МС (електророзпилення): m/z 273 [М+Н]+ Приготування 11 : [4-(2-етокси-2оксоетил)феніл]оцтова кислота Розчин діестеру з приготування 9 (11,8г, 47,0ммоль) і 2,2'-(1,4-фенілен)діоцтової кислоти (15,73г, 81,0ммоль) в етанолі (6,14мл) і діоксані (75мл) обробляли по краплям 12М хлорводневою кислотою (1,57мл, 18,8ммоль). Реакційну суміш перемішували при нагріванні із зворотнім холодильником протягом 18 годин і потім залишали охолоджуватись і концентрували до 82283 46 меншого об'єму. Реакційну суміш розводили толуолом (125мл) і одержану суспензію фільтрували. Фільтрат концентрували у вакуумі і залишок переносили у воду і підлуговували бікарбонатом натрію до рН нейтрального. Суміш розводили етилацетатом (200мл) і органічний шар відокремлювали і промивали розчином бікарбонату натрію (5х30мл) і нас. вод. хлоридом натрію (50мл). Об'єднані водні екстракти підкислювали до рН 3 використовуючи 6М хлорводневу кислоту і екстрагували етером (3х30мл). Органічні розчини об'єднували, сушили (сульфат магнію) і концентрували у вакуумі. Залишок розтирали з пентаном одержуючи вказану в заголовку сполуку як безбарвну тверду речовину 10,8г. 1 Н ЯМР (CD3OD, 400МГц) δ: 1,23 (τ, 3Н), 3,56 (м, 2Н), 3,60 (м, 2Н), 4,10 (κ, 2Η), 7,22 (м, 4Н) м.ч. МС (електророзпилення): m/z 245 [MNa]+ Приготування 12 : [4-(2-Гідрокси-2метилпропіл)феніл]оцтова кислота Карбонову кислоту приготування 11 (18,26г, 82,0ммоль) розчиняли в тетрагідрофурані (450мл) і розчин охолоджували до 0°С і обробляли по краплям розчином метилмагнійхлориду в тетрагідрофурані (82мл, 246ммоль). Реакційну суміш залишали нагріватись до кімнатної температури і залишали стояти протягом 18 годин. Реакційну суміш повільно розводили водою (80мл) і потім 2М хлорводневою кислотою (120мл, 240ммоль). Суміш екстрагували етилацетатом (3x100мл) і органічні екстракти об'єднували і промивали розсолом (3х50мл). Етилацетатну фазу сушили (сульфат магнію) і концентрували у вакуумі. Залишок очищали за допомогою колонкової хроматографії на силікагелі елюювали дихлорметан:метанол:оцтова кислота (99,6:0:0,4 змінювали до 94,6:5:0,4) одержуючи вказаний в заголовку продукт як безбарвну тверду речовину. 1 Н ЯМР (CDCI 3, 400МГц) δ: 1,15 (с, 6Н), 2,70 (с, 2Н), 3,55 (с, 2Н), 7,18 (с, 4Н) МС (електророзпилення): m/z 207 [М-Н]Приготування 13: (4-{2-[(Хлорацетил)аміно]-2метилпропіл}феніл)оцтова кислота Вказаний в заголовку продукт одержували за методикою подібною описаній для приготування 19 використовуючи спирт приготування 12. 1 Н ЯМР (CD3OD, 400МГц) δ: 1,30 (с, 6Н), 3,02 (с, 2Н), 3,55 (с, 2Н), 3,90 (с, 2Н), 7,10 (д, 2Н), 7,20 (д, 2Н), 7,55 (м, 1Н)м.ч. МС (електророзпилення): m/z 282 [М-Н]Приготування 14 : [4-(2-Аміно-2-метил-пропіл)феніл]-оцтової кислоти метиловий естер 47 Амід приготування 13 (500мг, 1,77ммоль) розчиняли в оцтовій кислоті (10мл) і розчин обробляли тіосечовиною (160мг, 2,10ммоль) і перемішували при 95°С протягом 2 годин. Реакційну суміш залишали охолоджуватись до кімнатної температури і концентрували у вакуумі. Залишок переносили в метанол (40мл), обробляли метанольною хлорводневою кислотою (10мл) і нагрівали із зворотнім холодильником протягом 18 годин. Реакційну суміш залишали охолоджуватись до кімнатної температури і потім концентрували у вакуумі. Залишок переносили у воду і екстрагували етером (3х20мл). Водну фазу підлуговували до рН 11 розчином карбонату натрію і екстрагували етилацетатом (3х30мл). Об'єднані етилацетатні екстракти сушили (сульфат магнію) і концентрували у вакуумі. Одержане масло одержували після упарювання ефіру (х5) одержуючи вказаний в заголовку продукт, 280мг. 1 Н ЯМР (CDCI 3, 400МГц) δ: 1,10 (с, 6Н), 2,60 (с, 2Н), 3,60 (с, 2Н), 3,70 (с, 3Н), 7,12 (д, 2Н), 7,20 (д, 2Н) м.ч. МС (електророзпилення): m/z 222 [М+Н]+ Приготування 15: Метил (4-{2-[((2R)-2-{4(бензилокси)-3-[(метилсульфоніл)-аміно]феніл}-2{[трет-бутил(диметил)силіл]окси}етил)аміно]-2метилпропіл}феніл)ацетат Бромід приготування 5 (2,00г, 3,90ммоль) і амін приготування 12 нагрівали разом в розплаві при 95°С в атмосфері азоту протягом 44 годин і потім охолоджували до кімнатної температури. Реакційну суміш суспендували в дихлорметан:0,880 аміак 99,8:0,2 і очищали за допомогою колонкової хроматографії на силікагелі, елюювали дихлорметан:метанол:0,880 аміак 99,8:0:0,2 до 97,8:2:0,2 до 80:20:5. Неочищений продукт упарювали з ефіру (х3) одержуючи вказаний в заголовку продукт, 1,76г. 1 Н ЯМР (CDCI 3, 400МГц) δ: -0,09 (с, 3Н), 0,00 (с, 3Н), 0,90 (с, 9Н), 1,00 (с, 3H), 1,05 (с, 3H), 2,552,70 (м, 3Н), 2,80-2,85 (м, 1Н), 2,85 (с, 3Н), 3,60 (с, 2Н), 3,70 (с, 3H), 4,71 (м, 1Н), 5,10 (с, 2Н), 6,70-6,90 (м, 1Н), 6,90-7,15 (м, 6Н), 7,35-7,45 (м, 5Н), 7,55 (д, 1Н) м.ч. МС (ХІАТ): т/2 655 [М+Н]+ Приготування 16: Діетил 2,2'-(1,3фенілен)діацетат 2,2'-(1,3-фенілен)діоцтову кислоту (10,0г, 51ммоль) розчиняли в етанолі (100мл) і розчин 82283 48 обробляли по краплям каталітичною кількістю ацетилхлориду (2,5мл). Реакційну суміш перемішували при нагріванні із зворотнім холодильником протягом 18 годин і потім залишали охолоджуватись і концентрували у вакуумі. Залишок переносили в етилацетат (100мл) і екстрагували розчином бікарбонату натрію (3х50мл) і розсолом (3х50мл). Органічну фазу сушили (сульфат магнію) і концентрували у вакуумі. Залишок розтирали з пентаном одержуючи вказаний в заголовку продукт, 11,8г. 1 Н ЯМР (CDCI 3, 400МГц) δ: 1,31 (τ, 6Н), 3,65 (с, 4Н), 4,20 (к, 4Н), 7,24-7,36 (м, 4Н) м.ч. МС (електророзпилення): m/z 251 [М+Н]+ Приготування 17 : [3-(2-етокси-2оксоетил)феніл]оцтова кислота Розчин діестеру з приготування 16 (44,3г, 177ммоль) і 2,2'-(1,3-фенілен)діоцтову кислоту (59,2, 308ммоль) в етанолі (24мл) і діоксані (290мл) обробляли по краплям 12М хлорводневою кислотою (4,9мл, 58,8ммоль). Реакційну суміш перемішували при нагріванні із зворотнім холодильником протягом 18 годин і потім залишали охолоджуватись і концентрували до меншого об'єму. Реакційну суміш розводили толуолом (125мл) і одержану суспензію фільтрували. Фільтрат концентрували у вакуумі і залишок переносили у воду і підлуговували бікарбонатом натрію до рН нейтрального. Суміш розводили етилацетатом (200мл) і органічний шар відокремлювали і промивали розчином бікарбонату натрію (5х30мл) і розсолом (50мл). Об'єднані водні екстракти підкислювали до рН 3 використовуючи 6М хлорводневу кислоту і екстрагували етером (3х30мл). Органічні розчини об'єднували, сушили (сульфат магнію) і концентрували у вакуумі. Залишок розтирали з пентаном одержуючи вказану в заголовку сполуку як безбарвну тверду речовину 10,8г. 1 Н ЯМР (CD3OD, 400МГц) δ: 1,25 (τ, 3H), 3,60 (м, 2Н), 3,63 (м, 2Н), 4,15 (κ, 2Η), 7,18-7,32 (м, 4Н) м.ч. МС (електророзпилення): m/z 245 [MNa]+ Приготування 18 : [3-(2-Гідрокси-2метилпропіл)феніл]оцтова кислота Метилмагнійхлорид (51 мл 3М розчину в тетрагідрофурані, 153ммоль) додавали по краплям до перемішуваного розчину приготування 17 (11,6г, 51ммоль) (International Journal of Peptide and Protein Research, 1987, 29(3), 331) в тетрагідрофурані (300мл) при 0°С в атмосфері азоту. Реакцію залишали нагріватись до кімнатної температури протягом ночі з утворенням тонкого білого осаду і потім обережно додавали воду (50мл) і 2N хлорводневу кислоту (80мл). Водну фазу екстрагували етилацетатом (2х300мл) і 49 об'єднані органічні розчини промивали розсолом (50мл), сушили (сульфат натрію) і розчинник видаляли у вакуумі одержуючи вказану в заголовку сполуку як золотисте масло (11,2г). 1 Н ЯМР (CDCI 3, 400 МГц) δ: 1,22 (6Н, с), 2,75 (2Н, с), 3,63 (2Н, с), 7,12-7,30 (4Н, м). МС (ЕСІ): m/z 209 [М+Н]+ Приготування 19 : (3-{2-[(Хлорацетил)аміно]-2метилпропіл}феніл)оцтова кислота 2-Хлорацетонітрил (8,8мл, 140ммоль) додавали до розчин спирту з приготування 18 (16,0г, 70ммоль) в оцтовій кислоті (33мл). Одержаний розчин охолоджували до 0°С, обробляли концентрованою сірчаною кислотою (33мл) і реакційну суміш залишали поступово нагріватись до кімнатної температури. Через 4 години реакційну суміш виливали на лід і підлуговували твердим карбонатом натрію. Розчин екстрагували етилацетатом (2х500мл) і об'єднані органічні екстракти сушили (сульфат магнію) і концентрували у вакуумі одержуючи вказаний в заголовку продукт як безбарвну тверду речовину, 19,0г. 1 Н ЯМР (CDCI 3, 400МГц) δ: 1,36 (с, 6Н), 3,02 (с, 2Н), 3,62 (с, 2Н), 3,95 (с, 2Н), 6,19 (м, 1Н), 7,06-7,31 (м, 4Н)м.ч. МС (електророзпилення): m/z 282 [М-Н]Приготування 20: [3-(2-Аміно-2-метил-пропіл)феніл]-оцтової кислоти метиловий естер Розчин аміду з приготування 19 (5,1г, 18ммоль), тіосечовину (1,6г, 21ммоль) і оцтову кислоту (18мл) в етанолі (80мл) нагрівали із зворотнім холодильником в атмосфері азоту протягом 16 годин. Реакційну суміш залишали охолоджуватись до кімнатної температури і фільтрували. Фільтрат концентрували у вакуумі, залишок розчиняли в етанолі (150мл), насичували хлороводнем і одержаний розчин нагрівали із зворотнім холодильником протягом 16 годин. Суміш концентрували у вакуумі і залишок розділяли між етилацетатом (200мл) і 5% водним розчином карбонату натрію (200мл). Органічну фазу промивали розсолом (100мл), сушили (сульфат магнію) і концентрували у вакуумі. Залишок очищали за допомогою сильної катіонобмінної смоли, елюювали метанолом і потім 2М розчином аміаку в метанол, до елюювання продукту. Елюент концентрували у вакуумі одержуючи вказану в заголовку сполуку як жовте масло, 2,68г. 1 Н ЯМР (CDCI 3, 400МГц) δ: 1,14 (с, 6Н), 2,68 (с, 2Н), 3,62 (с, 2Н), 3,69 (с, 2Н), 7,08-7,16 (м, 3H), 7,23-7,27 (м, 1Н) м.ч. МС (електророзпилення): m/z 222 [М+Н]+ Приготування 21 : (3-{2-[(2Р)-2-(4-Бензилокси3-метансульфоніламіно-феніл)-2-(трет-бутил 82283 50 диметил-силанілокси)-етиламіно]-2-метил-пропіл}феніл)-оцтової кислоти метиловий естер Бромід приготування 5 (36,0г, 70,8ммоль) і амін приготування 20 (36,0г, 153ммоль) нагрівали при 85°С протягом 72 годин. Реакційну суміш охолоджували до кімнатної температури і очищали за допомогою колонкової хроматографії на силікагелі, елюювали пентан:етилацетат (50:50 об'ємних), одержуючи вказаний в заголовку продукт як блідо-жовте масло (37,2г). 1 Н ЯМР (CDCI 3, 400МГц) δ: -0,15 (с, 3Н), 0,00 (с, 3Н), 0,83 (с, 9Н), 1,01 (с, 3Н), 1,04 (с, 3Н), 2,572,97 (м, 7Н), 3,59 (с, 2Н), 3,68 (с, 3H), 4,68472 (м, 1Н), 5,09 (с, 2Н), 6,79 (шс,1Н), 6,95 (д, 1Н), 7,047,21 (м, 7Н), 7,37-7,44 (м, 5Н), 7,56 (д, 1Н) м.ч. МС (ХІАТ): m/z 655 [М+Н]+ Приготування 22 : Метил (4-{(2R)-2-[((2R)-2{[трет-бутип(диметил)силіл]окси}-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)ацетат Бензилзахищений продукт приготування 9 (520мг, 0,813ммоль) додавали до розчину 10% Pd/C (100мг) в метанолі (25мл) і реакційну суміш перемішували при кімнатній температурі при тиску водню 60псі протягом 8 годин. Реакційну суміш фільтрували через Арбоцель® і фільтрат концентрували у вакуумі одержуючи вказаний в заголовку продукт. 1 Н ЯМР(СОСІ 3, 400МГц) δ: -0,16 (с, 3Н), -0,01 (с, 3Н), 0,80 (с, 9Н), 1,25 (д, 3H), 2,77-2,87 (м, 3H), 2,91 (с, 3H), 3,08-3,19 (м, 2Н), 3,61 (с, 2Н), 3,74 (с, 3H), 4,84 (м, 1Н), 6,65 (д, 1Н), 6,80 (д, 1Н), 7,08 (д, 2Н), 7,16 (д, 2Н), 7,18 (м, 1Н) МС (електророзпилення) m/z 551 [М+Н]+ Приготування 23 : (4-{(2R)-2-[((2R)-2-{[третБутил(диметил)силіл]окси}-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)оцтова кислота Естер приготування 22 (844мг, 1,53ммоль) додавали до розчину гідроксиду літію (71 мг, 1,69ммоль) втетрагідрофуран:вода 10:1 (11мл) і реакційну суміш перемішували при кімнатній температурі 4 годин. Додавали ще гідроксид літію (142мг, 3,38ммоль) і реакційну суміш 51 перемішували при кімнатній температурі протягом ще 18 годин. Реакційну суміш розводили 4М розчином хлорводневої кислоти в діоксані (1,27мл, 5,0ммоль) і концентрували у вакуумі. Залишок переносили у воду (20мл) і етилацетат (20мл), органічний шар відокремлювали, сушили (сульфат магнію) і концентрували у вакуумі одержуючи вказаний в заголовку продукт, 748мг. 1 Н ЯМР(СО3OD, 400МГц) δ: -0,19 (с, 3H), -0,01 (с, 3H), 0,79 (с, 9Н), 1,13 (д, 3H), 2,66 (м, 1Н), 2,82 (м, 1Н), 2,84 (с, 3H), 3,00 (м, 1Н), 3,17 (м, 1Н), 3,32 (м, 1Н), 3,42 (с, 2Н), 4,86 (м, 1Н), 6,80 (д, 1Н), 6,95 (д, 1Н), 7,00 (д, 2Н), 7,17 (д, 2Н), 7,31 (д, 1Н) м.ч. МС (електророзпилення): m/z 537 [М+Н]+ Приготування 24: Метил (4-{2-[((2R)-2-{[третбутил(диметил)силіл]окси}-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетат Бензилзахищений спирт приготування 15 (1,72г, 2,60ммоль) розчиняли в метанолі (40мл) і розчин обробляли 10% Pd/C (200мг) і при тиску водню 60псі при кімнатній температурі 18 годин. Реакційну суміш фільтрували через Арбоцель® і фільтрат концентрували до меншого об'єму у вакуумі. Розчин обробляли 10%Pd/C (250мг) і поміщали в атмосферу водню з тиском бОпсі при кімнатній температурі на 72 години. Реакційну суміш фільтрували через Арбоцель® і фільтрат концентрували у вакуумі. Одержували масло після упарювання ефіру (х3) одержуючи вказаний в заголовку продукт, 1,43г. 1 Н ЯМР (CD3OD, 400МГц) δ: -0,08 (с, 3H), 0,00 (с, 3H), 0,80 (с, 9Н), 1,12 (д, 6Н), 2,65-3,00 (м, 7Н), 3,60 (с, 2Н), 3,70 (с, 3H), 4,70 (м, 1Н), 6,85 (д, 1Н), 7,00-7,20 (м, 5Н), 7,35 (д, 1Н)м.ч. МС (ХІАТ): m/z 565 [М+Н]+ Приготування 25: (4-{2-[((2R)-2{[третБутил(диметил)силіл]окси}-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)оцтова кислота Естер приготування 24 (1,41г, 2,50ммоль) розчиняли в діоксані (16мл) і воді (2мл) і розчин обробляли по краплям 5М розчином гідроксиду натрію (3,49мл, 17,5ммоль). Реакційну суміш перемішували при кімнатній температурі 18 годин і потім концентрували у вакуумі. Залишок переносили у воду і охолоджували і потім обробляли 2М хлорводневою кислотою (8,78мл, 17,6ммоль). Розчин розводили етилацетатом і концентрували у вакуумі внаслідок поганого 82283 52 розділення. Залишок упарювали з етилацетату (хЗ) одержуючи вказаний в заголовку продукт, 1,67г. 1 Н ЯМР (ДMCO-D6, 400МГц) δ: -0,08 (с, 3H), 0,00 (с, 3H), 0,85 (с, 9Н), 0,90 (с, 3H), 0,95 (с, 3H), 2,50-2,80 (м, 4Н), 2,85 (с, 3H), 2,90 (с, 2Н), 4,60 (м, 1Н), 6,75-7,30 (м, ЮН) м.ч. МС (XIAT): m/z 551 [М+Н]+ Приготування 26: (3-{(2R)-2-[((2R)-2-{4(Бензилокси)-3-[(метилсульфоніл)аміно]феніл}-2{[третбутил(диметил)силіл]окси}етил)аміно]пропіл}феніл )оцтова кислота Естер приготування 6 (2,90г, 4,5ммоль) розчиняли в розчині гідроксиду літію (216мг, 9,0ммоль) у воді (30мл) і тетрагідрофурані (60мл) і реакційну суміш перемішували при кімнатній температурі 48 годин. Реакційну суміш підкислювали до рН 6 використовуючи 2М хлорводневу кислоту і концентрували до меншого об'єму у вакуумі. Суміш екстрагували етилацетатом (х2) і органічні розчини об'єднували і промивали розсолом, сушили (сульфат магнію) і концентрували у вакуумі одержуючи вказаний в заголовку продукт. 1 Н ЯМР (CDCI 3, 400МГц) δ: -0,21 (с, 3H), 0,01 (с, 3H), 0,80 (с, 9Н), 1,09 (д, 3H), 2,54-2,61 (м, 1Н), 2,84-2,98 (м, 2Н), 3,15-3,20 (м, 1Н), 3,52 (с, 2Н), 4,91-4,94 (м, 1Н), 5,08 (с, 2Н), 6,59 (шс, 3H), 6,906,93 (м, 2Н), 7,04-7,17 (м, 4Н), 7,35-7,42 (м, 5Н), 7,49 (с, 1Н) м.ч. МС (електророзпилення): m/z 627 [М+Н]+ Приготування 27: (3-{(2К)-2-[((2Н)-2-{[третБутил(диметил)силіл]окси}-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]пропіл} феніл)оцтова кислота Бензилзахищений продукт приготування 26 (250мг, 0,40ммоль) додавали до суміші 20% Pd/C (30мг) і форміату амонію (126мг, 2,0ммоль) в етанолі (15мл) і реакційну суміш нагрівали із зворотнім холодильником протягом 3 годин. Реакційну суміш залишали стояти при кімнатній температурі 18 годин і потім концентрували у вакуумі. Залишок, що містить каталізатор, очищали за допомогою колонкової хроматографії на силікагелі елюювали дихлорметан:метанол:0,880аміак 95:5:0,5 до 90:10:1 до 80:20:5 одержуючи вказаний в заголовку продукт. 1 Н ЯМР(СО3OD, 400МГц) δ: -0,07 (с, 3H), 0,12 (с, 3H), 0,90 (с, 9Н), 1,25 (д, 3H), 2,73-2,79 (м, 1Н), 53 2,95-3,05 (м, 4Н), 3,14-3,49 (м, 3H), 3,53 (с, 2Н0, 5,00-5,03 (м, 1Н), 6,96 (д, 1Н), 7,06-7,17 (м, 3H), 7,23-7,30 (м, 2Н), 7,45 (м, 1Н) м.ч. МС (елекгророзпилення): m/z 537 [М+Н]+, 559 [M+Na]+ Приготування 28: Метил (3-{2-[((2R)-2-{4(бензилокси)-3-[(метилсульфоніл)-аміно]феніл}-2{[трет-бутил(диметил)силіл]окси}етил)аміно]-2метилпропіл}-феніл)ацетат Розчин бензилзахищеного спирту приготування 21 (36,8г, 56ммоль) в етанолі (550мл) обробляли форміатом амонію (16,0г, 254ммоль) і 20% гідроксидом паладію на вугіллі (1,5г). Одержану суспензію нагрівали при 85°С протягом 2 годин. Через 2 години додавали ще 20% гідроксид паладію на вугіллі (1,0г) і нагрівання продовжували протягом 1 години. Реакційну суміш охолоджували до кімнатної температури, фільтрували і розчинник видаляли у вакуумі. Залишок розділяли між етилацетатом (500мл) і 2N водним аміаком (100мл). Органічну фазу відокремлювали, сушили (сульфат магнію) і розчинник видаляли у вакуумі. Залишок очищали за допомогою колонкової хроматографії на силікагелі елюювали дихлорметан : метанол : 0,88 аміак (95:5:0,5 об'ємних) одержуючи вказаний в заголовку продукт як блідо-жовте масло (20,6г). 1 Н ЯМР (400МГц, CDCI 3): -0,17 (с, 3H), -0,05 (с, 3H), 0,80 (с, 9Н), 1,07 (с, 3H), 1,09 (с, 3H), 2,662,91 (м, 7Н), 3,62 (д, 2Н), 3,69 (с, 3H), 4,71-4,74 (м, 1Н), 6,58 (д, 1Н), 6,88 (дд, 1Н), 7,05-7,14 (м, 3H), 7,21-7,25 (м, 1Н), 7,30 (с, 1Н) м.ч. МС (електророзпилення): m/z 565 [М+Н]+ Приготування 29: (3-{2-[((2R)-2-{[третБутил(диметил)силіл]окси}-2-{4-гідрокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)оцтова кислота Естер приготування 28 (20,6, 36ммоль) розчиняли в тетрагідрофурані (150мл) і розчин обробляли по краплям 1М водним розчином гідроксиду літію (72мл, 72ммоль). Реакційну суміш перемішували при кімнатній температурі 72 годин. Реакційну суміш нейтралізували додаючи 1М хлорводневу кислоту (72мл, 72ммоль) і концентрували до меншого об'єму. Водну фазу декантували і залишок промивали водою (2х50мл). Залишок розчиняли в тетрагідрофурані (50мл) і толуолі (50мл) і розчинник видаляли у вакуумі 82283 54 одержуючи вказану в заголовку сполуку як блідокоричневу піну (20,17г). 1 Н ЯМР (400МГц, CD3OD): -0,14 (с, 3H), 0,07 (с, 3H), 0,83 (с, 9Н), 0,91 (м, 1Н), 1,32 (м, 6Н), 2,93 (м, 5Н), 3,23 (м, 2Н), 3,54 (м, 2Н), 4,94 (м, 1Н), 6,91 (д, 1Н), 7,03-7,16 (м, 3H), 7,26 (м, 2Н), 7,60 (м, 1Н). МС (ХІАТ): m/z 551 [М+Н]+ Приготування 20а : [3-(2-аміно-2-метилпропіл)-феніл]-оцтової кислоти етиловий естер Суміш аміду з приготування 19 (151,4г, 534ммоль), тіосечовини (48,7г, 640ммоль) і оцтової кислоти (303мл) в етанолі (1,5л) нагрівали із зворотнім холодильником в атмосфері азоту протягом 5 годин. Реакційну суміш залишали охолоджуватись до кімнатної температури і суспензію концентрували у вакуумі. Залишок азеотропували з толуолом (2x900мл), обробляли етанолом (1,5л) і перемішували протягом 1 години. Твердий осад видаляли фільтруванням і фільтрат охолоджували на бані з льодом, обробляли 98% сірчаною кислотою (227мл) і перемішували протягом 1 години при кімнатній температурі. Розчин концентрували у вакуумі видаляючи більшу частину етанолу і доводили до рН9 використовуючи водний бікарбонат натрію. Твердий осад видаляли фільтруванням і промивали водою (ЗООмл), потім етилацетатом (1,0л). Шари об'єднаного біфазного фільтрату і промивних розчинів розділяли і водний шар екстрагували етилацетатом (1,0л + 500мл). Об'єднані етилацетатні екстракти сушили над сульфатом магнію, фільтрували і концентрували у вакуумі одержуючи вказану в заголовку сполуку як коричневе масло (89,5г). 1 Н ЯМР (d6-ДМСО, 400МГц) δ : 0,99 (с, 6Н), 1,16 (τ, 3H), 2,59 (с, 2Н), 3,61 (с, 2Н), 4,06 (к, 2Н), 7,06 (м, 3H), 7,21 (м, 1Н) Приготування 20b : [3-(2-аміно-2-метилпропіл)-феніл]-оцтової кислоти етиловий естер, ди-п-толуоїл-L-тартрат Розчин амін з приготування 20а (124,9г, 531ммоль) в ацетонітрилі (1,0л) обробляли розчином ди-п-толуоїл-L-винної кислоти (194,8г, 504ммоль) в ацетонітрилі (750мл). Oдержану суспензію перемішували протягом 3 годин і твердий осад виділяли фільтруванням і промивали ацетонітрилом (2x250мл) одержуючи вказану в заголовку сполуку як майже-білу тверду речовину (210г). 1 Н ЯМР (d6-ДМСО, 400МГц) δ : 1,13 (с, 6Н), 1,17 (τ, 3H), 2,34 (с, 6Н), 2,78 (с, 2Н), 3,63 (с, 2Н), 4,06 (к, 2Н), 5,61 (с, 2Н), 7,02 (д, 2Н), 7,15 (д, 1Н), 7,25 (м, 5Н), 7,80 (д, 4Н) Приготування 20с: [3-(2-Аміно-2-метил-пропіл)феніл]-оцтової кислоти етиловий естер 55 Розчин карбонату калію (37,90г, 274,22ммоль) у воді (213мл) додавали до суспензії приготування 20b (42,62г, 68,56ммоль) в пропіонітрилі (213мл) і перемішували до розчинення всіх твердих речовин. Фази розділяли і пропіонітрильну фазу промивали водою (107мл). Об'єм розчину зменшували до об'єму приблизно 30 мл при пониженому тиску одержуючи вказану в заголовку сполуку як пропіонітрильний розчин. Зразок видаляли і концентрували до суха одержуючи зразок для вагового аналізу і вихід становив 81%. 1 Н ЯМР (d6-ДМСО, 400МГц) δ : 0,99 (с, 6Н), 1,16 (τ, 3H), 2,59 (с, 2Н), 3,61 (с, 2Н), 4,06 (к, 2Н), 7,06 (м, 3H), 7,21 (м, 1Н) Приготування 21а: Етил (3-{2-[((2R)-2-{[третбутил(диметил)силіл]окси}-2-{4-бензилокси-3[(метилсульфоніл)аміно]феніл}етил)аміно]-2метилпропіл}феніл)ацетат N-[2-(бензилокси)-5-((1R)-2-бром-1-{[третбутил(диметил)силіл]окси}етил)феніл] метансульфонамід (14,34г, 27,88ммоль) додавали до розчину приготування 20с (13,12г, 55,75ммоль) в пропіонітрилі (15мл). Суміш нагрівали із зворотнім холодильником протягом 3 днів. Розчин розводили пропіонітрилом (55мл) і охолоджували до 20-25°С. Розчин промивали 1М HCI (вод) (70мл), потім водою (35мл) і розчин безпосередньо використовували на наступній стадії, при умові 100% виходу. Приготування 28а : Етил (R)-2-(3-{2-[2гідрокси-2-(4-бензилокси-3метансульфонамідофеніл)етиламіно]-2метилпропіл}феніл)ацетат Триетиламіну тригідрофторид (9,1мл, 8,99г, 55,76ммоль) додавали до розчину приготування 21а (18,64г, 27,88ммоль) в пропіонітрилі (72мл). Розчин перемішували при 20-25°С протягом 3 годин. Розчин гасили 5М NH3(вод) (72мл) перемішували протягом 10 хвилин і фази розділяли. Пропіонітрильний розчин промивали водою (72мл) і розчин безпосередньо використовували на наступній стадії, при умові 100% виходу. Приготування 29а: (R)-2-(3-{2-[2-гідрокси-2-(4бензилокси-3метансульфонамідофеніл)етиламіно]-2метилпропіл}феніл)оцтова кислота 82283 56 Розчин гідроксиду натрію (6,69г, 167,28ммоль) у воді (72мл) додавали до розчину приготування 28а (15,47г, 27,88ммоль) в пропіонітрилі (72мл). Двофазну суміш інтенсивно перемішували протягом 3 годин. Фази залишали розділятись і водну фазу промивали свіжим пропіонітрилом (72мл), потім розводили 1,4-діоксаном (72мл). рН розчину доводили до рН 6-7 додаючи 37% м/м НСІ (вод) і одержану суспензію перемішували протягом однієї години. Суспензію фільтрували і промивали на фільтрувальному папері водою, сушили одержуючи вказану в заголовку сполуку як майже білу тверду речовину (13,55г, 92% після 3 стадій). 1 Н ЯМР (400МГц, CD3OD) δ : 1,33 (с, 3H), 1,35 (с, 3H), 2,89 (с, 3H), 2,96 (с, 2Н), 3,06-3,19 (м, 2Н), 3,50 (с, 2Н), 4,50 (м, 1Н), 5,22 (с, 2Н), 7,08 (д, 1Н), 7,13 (д, 1Н), 7,19 (с, 1Н), 7,24 (т, 2Н), 7,27 (д, 1Н), 7,31 (д, 1Н), 7,38 (т, 2Н), 7,48 (д, 2Н), 7,49 (с, 1Н) м.ч. Приготування 29b: (R)-2-(3-{2-[2-гідрокси-2-(4гідрокси-3-метансульфонамідофеніл)етиламіно]-2метилпропіл}феніл)оцтової кислоти натрієва сіль Розчин гідроксиду натрію (1,40г, 35,05ммоль) у воді (100мл) додавали до суспензії приготування 29а (18,46г, 35,05ммоль) в метанолі (600мл). Суміш гідрували над 20ваг.% гідроксидом паладію на вугіллі при 150псі і 60°С протягом 5 годин. Суміш фільтрували видаляючи залишок каталізатору і потім об'єм зменшували до 100мл при пониженому тиску. Суміш переганяли і заміняли при пониженому тиску ацетонітрилом при постійному об'ємі. Одержану суспензію фільтрували і промивали на папері ацетонітрилом, сушили одержуючи вказану в заголовку сполуку як майже-білу тверду речовину (15,34г, 95%). 1 Н ЯМР (400МГц, CD3OD) δ : 1,07 (с, 3H), 1,09 (с, 3H), 2,70 (с, 2Н), 2,73-2,81 (м, 2Н), 2,87 (с, 3H), 3,44 (с, 2Н), 4,60-4,63 (м, 1Н), 6,84 (д, 1Н), 6,92 (д, 1Н), 7,04 (д, 1Н), 7,11 (с, 1Н), 7,14 (д, 1Н), 7,15 (т, 1Н), 7,34 (с, 1Н) м.ч. Згадані сполуки формули 29Ь потім можуть реагувати з придатним аміном формули NHR8-Q2A (3) в присутності звичайного конденсувального агенту, такого як гідрохлорид 1-(3диметиламінопропіл)-3-етилкарбодііміду або дициклогексилкарбодіімід в придатному 57 розчиннику, такому як піридин, диметилформамід або диметилацетамід. з одержанням сполуки формули (1): де R1 і R2 є метил і η є 1. Приготування 30-106 Прийнятну карбонову кислоту з приготування 23, 25, 27 або 29 (0,15ммоль) розчиняли в розчині гідрату 1-гідроксибензотриазолу (22мг, 0,16ммоль), гідрохлориду 1-(3диметиламінопропіл)-3-етилкарбодііміду (34мг, 0,18ммоль) і N-етилдіізопропіламіну (ІЗОмкл, 0,73ммоль) в Ν,Ν-диметилформаміді (2мл). Розчин обробляли прийнятним аміном (0,23ммоль) і реакційну суміш збовтували при кімнатній температурі 18 годин. Реакційну суміш концентрували у вакуумі і залишок розділяли між дихлорметаном (3мл) і водою (1мл). Фази розділяли і органічний шар промивали розсолом (1мл), сушили (сульфат натрію) і концентрували у вакуумі. Залишок очищали за допомогою колонкової хроматографії на силікагелі, елюювали дихлорметан:метанол:0,88 аміак 98:2:0 до 94:6:0,5одержуючи бажаний продукт. Альтернативно, наступний спосіб може бути використаний для синтезу сполук приготувань 30106: Розчин прийнятної карбонової кислоти з приготування 23, 25, 27 або 29 (36ммоль) в Ν,Νдиметилформаміді (200мл) обробляють гідратом 1-гідроксибензотриазолу (5,26г, 39ммоль), прийнятним аміном (43ммоль), гідрохлоридом 1(3-диметиламінопропіл)-3-етилкарбодііміду (7,5г, 39ммоль). Одержану суспензію залишають перемішуватись протягом 18 годин. Розчинник видаляють у вакуумі і залишок розділяють між дихлорметаном (400мл) і нас. вод. бікарбонатом натрію (100мл). Органічну фазу відокремлюють і промивають насиченим водним хлоридом натрію (100мл), сушать (сульфат натрію) і розчинник видаляють у вакуумі. Залишок очищають за допомогою колонкової хроматографії на силікагелі, елююють дихлорметан : метанол : етилацетат : 0,88 аміак (95:5:0:0,5 змінюють до 0:5:95:0), одержуючи бажаний продукт. 82283 58 59 82283 60
ДивитисяДодаткова інформація
Назва патенту англійськоюSulfonamide derivatives for the treatment of deseases , process for preparation thereof (variants), pharmaceutical composition based on them, and transient compound
Автори англійськоюBrown Alan Daniel, James Kim, Lane, Charlotte Alice Louise, MOSES IAN BRIAN, THOMSON NICHOLAS MURRAY
Назва патенту російськоюПроизводные сульфонамида для лечения заболеваний, способ их получения (варианты), фармацевтическая композиция на их основе, промежуточное соединение
Автори російськоюБраун Алан Дениэл, Джеймс Ким, Лейн Шарлотт Элис Луиз, Моузес Йан Брайан, Томсон Николас Маррей
МПК / Мітки
МПК: C07C 311/08
Мітки: варіанти, проміжна, захворювань, спосіб, сульфонаміду, лікування, одержання, фармацевтична, сполука, композиція, основі, похідні
Код посилання
<a href="https://ua.patents.su/42-82283-pokhidni-sulfonamidu-dlya-likuvannya-zakhvoryuvan-sposib-kh-oderzhannya-varianti-farmacevtichna-kompoziciya-na-kh-osnovi-promizhna-spoluka.html" target="_blank" rel="follow" title="База патентів України">Похідні сульфонаміду для лікування захворювань, спосіб їх одержання (варіанти), фармацевтична композиція на їх основі, проміжна сполука</a>
Попередній патент: Засіб для лікування і профілактики інфекційних захворювань людини, що передаються статевим шляхом, і спосіб його одержання
Наступний патент: Клей термопластичний
Випадковий патент: Спосіб регулювання реактивної потужності компенсуючого пристрою












