Заміщені похідні 2,3-дигідроімідазо[1,2-с]хіназоліну, корисні для лікування гіперпроліферативних порушень та хвороб, пов’язаних з ангіогенезом
Номер патенту: 96965
Опубліковано: 26.12.2011
Автори: Вуд Джілл, Міхельс Мартін, Скотт Вілльям, Хентеманн Мартін, Кемпбелл Анн-марі, Роулі Р. Брюс, Редман Аніко, Булліон Анн-Марі
Формула / Реферат
1. Сполука, що має формулу:
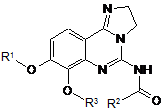 ,
,
або її фізіологічно прийнятна сіль, сольват, гідрат або стереоізомер, причому:
R1 являє собою (CH2)n-(CHR4)-(CH2)m-N(R5)(R5');
R2 являє собою гетероарил, необов'язково заміщений 1, 2 або 3 групами R6;
R3 являє собою алкіл або циклоалкіл;
R4 являє собою водень, гідроксигрупу або алкоксигрупу, та R5 та R5' можуть бути однаковими або різними та являють собою, незалежно один від іншого, водень, алкіл, циклоалкілалкіл, або алкоксіалкіл, або R5 та R5' можуть бути взяті разом з атомом азоту, з яким вони зв'язані, для утворення 3-7-членного азотовмісного гетероциклічного кільця, що необов'язково містить принаймні один додатковий гетероатом, вибраний з кисню, азоту або сірки, та який може бути необов'язково замінений на 1 або кілька R6'-груп, або R4 та R5 можуть бути взяті разом з атомами, з якими вони зв'язані, для утворення 5-6-членного азотовмісного гетероциклічного кільця, що необов'язково містить 1 або кілька атомів азоту, кисню або сірки, та які можна необов'язково замінити на 1 або кілька R6'-груп;
при кожній появі R6 може бути таким же або різним та являє собою незалежно галоген, алкіл, алкеніл, алкініл, циклоалкіл, циклоалкілалкіл, арил, арилалкіл, гетероарил, гетероарилалкіл, гетероциклічне кільце, гетероциклілалкіл, алкіл-OR7, алкіл-SR7, алкіл-N(R7)(R7'), алкіл-COR7, -CN, -COOR7, -CON(R7)(R7'), -OR7, -SR7, -N(R7)(R7') або -NR7COR7, кожен з яких можна необов'язково замінити на 1 або кілька груп R8;
при кожній появі R6' може бути таким же або різним та являє собою незалежно алкіл, циклоалкілалкіл або алкіл-OR7;
при кожній появі R7 та R7' можуть бути такими ж або різними та являють собою незалежно водень, алкіл, алкеніл, алкініл, циклоалкіл, циклоалкілалкіл, циклоалкеніл, арил, арилалкіл, гетероарил, гетероциклічне кільце, гетероциклілалкіл або гетероарилалкіл;
при кожній появі R8 являє собою незалежно нітрогрупу, гідроксигрупу, ціаногрупу, форміл, ацетил, галоген, аміногрупу, алкіл, алкоксигрупу, алкеніл, алкініл, циклоалкіл, циклоалкілалкіл, циклоалкеніл, арил, арилалкіл, гетероарил, гетероциклічне кільце, гетероциклілалкіл або гетероарилалкіл;
n являє собою ціле число від 1-4, та m являє собою ціле число від 0-4, за умови, що, коли R4 та R5 беруть разом з атомами, з якими вони зв'язані, для утворення 3-7-членного азотовмісного кільця, n+m£4.
2. Сполука за п. 1, у якій R2 являє собою азотовмісний гетероарил, необов'язково заміщений 1, 2 або 3 групами R6.
3. Сполука за п. 1, у якій R5 та R5' являють собою незалежно алкіл.
4. Сполука за п. 1, у якій R5 та R5' взяті разом з атомом азоту, з яким вони зв'язані, для утворення 5-6-членного азотовмісного гетероциклічного кільця, що містить принаймні один додатковий гетероатом, вибраний з кисню, азоту або сірки, та який можна необов'язково замінити на 1 або кілька R6'-груп.
5. Сполука за п. 1, у якій R4 являє собою гідроксигрупу.
6. Сполука за п. 1, у якій R4 та R5 взяті разом з атомами, з якими вони зв'язані, для утворення 5-6-членного азотовмісного гетероциклічного кільця, що необов'язково містить 1 або кілька атомів азоту, кисню або сірки, та які можна необов'язково замінити на 1 або кілька груп R6'.
7. Сполука за п. 1, у якій R3 являє собою метил.
8. Сполука за п. 1, у якій R2 являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол, тіазол, фуран або тіофен, необов'язково заміщений 1, 2 або 3 групами R6.
9. Сполука за п. 2, у якій R2 являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол або тіазол, необов'язково заміщений 1, 2 або 3 групами R6.
10. Сполука за п. 1, що має формулу:
 ,
,
11. Сполука за п. 10, у якій R2 являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол, тіазол, фуран або тіофен, необов'язково заміщений 1, 2 або 3 групами R6.
12. Сполука за п. 11, у якій R2 являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол або тіазол, необов'язково заміщений 1, 2 або 3 групами R6.
13. Сполука за п. 1, що має формулу:
 .
.
14. Сполука за п. 13, у якій R2 являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол, тіазол, фуран або тіофен, необов'язково заміщений 1, 2 або 3 групами R6.
15. Сполука за п. 14, у якій R2 являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол або тіазол, необов'язково заміщений 1, 2 або 3 групами R6.
16. Сполука за п. 1, що має формулу:
 .
.
17. Сполука за п. 16, у якій R2 являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол, тіазол, фуран або тіофен, необов'язково заміщений 1, 2 або 3 групами R6.
18. Сполука за п. 17, у якій R2 являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол або тіазол, необов'язково заміщений 1, 2 або 3 групами R6.
19. Сполука за п. 1, що має формулу:
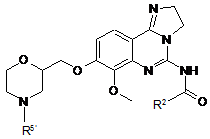 .
.
20. Сполука за п. 19, у якій R2 являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол, тіазол, фуран або тіофен, необов'язково заміщений 1, 2 або 3 групами R6.
21. Сполука за п. 20, у якій R2 являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол або тіазол, необов'язково заміщений 1, 2 або 3 групами R6.
22. Сполука за п. 19, у якій R5' являє собою алкіл.
23. Сполука за п. 1, що має формулу:
 .
.
24. Сполука за п. 23, у якій R2 являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол, тіазол, фуран або тіофен, необов'язково заміщений 1, 2 або 3 групами R6.
25. Сполука за п. 24, у якій R2 являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол або тіазол, необов'язково заміщений 1, 2 або 3 групами R6.
26. Сполука за п. 23, у якій R5' являє собою алкіл.
27. Сполука за будь-яким з попередніх пунктів, вибрана з групи:
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-піримідин-5-карбоксамід;
N-(8-{3-[(2R,6S)-2,6-димeтилмopфoлiн-4-iл]пpoпoкcи}-7-мeтoкcи-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл)нікотинамід;
N-(8-{3-[(2R,6S)-2,6-димeтилмopфoлiн-4-iл]пpoпoкcи}-7-мeтoкcи-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл)-2,4-диметил-1,3-тіазол-5-карбоксамід;
2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-1,3-тіазол-5-карбоксамід;
2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]ізонікотинамід;
2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-4-метил-1,3-тіазол-5-карбоксамід;
2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-4-пропілпіримідин-5-карбоксамід;
N-{8-[2-(4-етилморфолін-2-іл)етокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід;
N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}піримідин-5-карбоксамід;
N-(8-{3-[2-(гідроксиметил)морфолін-4-іл]пропокси}-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл)нікотинамід;
N-(8-{3-[2-(гідроксиметил)морфолін-4-іл]пропокси}-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл)нікотинамід;
N-{8-[3-(диметиламіно)пропокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід 1-оксид;
2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]піримідин-5-карбоксамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-6-(2-піролідин-1-ілетил)нікотинамід;
6-(циклопентиламіно)-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
N-[8-(2-гідрокси-3-морфолін-4-ілпропокси)-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
N-{7-метокси-8-[3-(3-метилморфолін-4-іл)пропокси]-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}нікотинамід;
N-(8-{3-[2-(гідроксиметил)морфолін-4-іл]пропокси}-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл)нікотинамід;
N-(8-{2-[4-(циклобутилметил)морфолін-2-іл]етокси}-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл)нікотинамід;
N-(7-метокси-8-{2-[4-(2-метоксіетил)морфолiн-2-іл]етокси}-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл)нікотинамід;
N-{8-[(4-етилморфолін-2-іл)метокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід;
N-(7-метокси-8-{[4-(2-метоксіетил)морфолін-2-іл]метокси}-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл)нікотинамід;
N-{7-метокси-8-[(4-метилморфолін-2-іл)метокси]-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-піримідин-4-карбоксамід;
2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]піримідин-4-карбоксамід;
N-[7-мeтoкcи-8-(3-мopфoлiн-4-iлпpoпoкcи)-2,3-дигiдpoiмiдaзo[1,2-c]xiнaзoлiн-5-iл]-1-метил-1Н-імідазол-4-карбоксамід;
рел-(8-{3-[(2R,6S)-2,6-диметилморфолін-4-іл]пропокси}-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл)піримідин-5-карбоксамід;
рел-(8-{3-[(2R,6S)-2,6-диметилморфолін-4-іл]пропокси}-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл)-6-метилнікотинамід;
рел-6-ацетамідо-N-(8-{3-[(2R,6S)-2,6-диметилморфолін-4-іл]пропокси}-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл)нікотинамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-1-метил-1Н-імідазол-5-карбоксамід;
6-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-2-метилнікотинамід;
2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-4-метилпіримідин-5-карбоксамід;
6-аміно-5-бром-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-1,3-оксазол-5-карбоксамід;
N-[7-метокси-8-(морфолін-2-ілметокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
2-{[2-(диметиламіно)етил]аміно}-N-{8-[3-(диметиламіно)пропокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}піримідин-5-карбоксамід;
2-аміно-N-{8-[3-(диметиламіно)пропокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-1,3-тіазол-5-карбоксамід;
рел-2-аміно-N-(8-{3-[(2R,6S)-2,6-диметилморфолін-4-іл]пропокси}-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл)піримідин-5-карбоксамід;
рел-6-аміно-N-(8-{3-[(2R,6S)-2,6-диметилморфолін-4-іл]пропокси}-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл) нікотинамід;
2-[(2-гідроксіетил)аміно]-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]піримідин-5-карбоксамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-2-[(3-метоксипропіл)аміно]піримідин-5-карбоксамід;
2-аміно-N-{8-[3-(диметиламіно)пропокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}піримідин-5-карбоксамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-2-[(3-морфолін-4-ілпропіл)аміно]піримідин-5-карбоксамід;
2-[(2-метоксіетил)аміно]-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]піримідин-5-карбоксамід;
2-{[2-(диметиламіно)етил]аміно}-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]піримідин-5-карбоксамід;
6-аміно-N-{8-[3-(диметиламіно)пропокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}нікотинамід;
N-[7-метокси-8-(3-морфолiн-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-2-піролідин-1-ілпіримідин-5-карбоксамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-2-(4-метилпіперазин-1-іл)піримідин-5-карбоксамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-2-морфолін-4-ілпіримідин-5-карбоксамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-6-піперазин-1-ілнікотинаміду гідрохлорид;
6-[(3S)-3-амінопіролідин-1-іл]-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинаміду гідрохлориду гідрат;
6-[(3R)-3-амінопіролідин-1-іл]-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинаміду гідрохлорид;
6-[(4-фторобензил)аміно]-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
6-[(2-фурилметил)аміно]-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
6-[(2-метоксіетил)аміно]-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-6-(1Н-пірол-1-іл)нікотинамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-6-морфолін-4-ілнікотинамід;
N-{7-метокси-8-[3-(метиламіно)пропокси]-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}нікотинамід;
6-[(2,2-диметилпропаноїл)аміно]-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
6-[(циклопропілкарбоніл)аміно]-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-6-(2,2,2-трифторетокси)нікотинамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-6-(трифторометил)нікотинамід;
6-(ізобутириламіно)-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
N-{7-метокси-8-[3-(4-метилпіперазин-1-іл)пропокси]-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}нікотинамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-2-{[(метиламіно)карбоніл]аміно}-1,3-тіазол-4-карбоксамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-6-{[(метиламіно)карбоніл]аміно}нікотинамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-2-(метиламіно)-1,3-тіазол-4-карбоксамід;
N-[7-метокси-8-(2-морфолін-4-ілетокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-2,4-диметил-1,3-тіазол-5-карбоксамід;
N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-6-метилнікотинамід;
6-{[(ізопропіламіно)карбоніл]аміно}-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-6-піролідин-1-ілнікотинамід;
6-(диметиламіно)-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
N-[7-метокси-8-(3-піперидин-1-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
N-[7-метокси-8-(2-піролідин-1-ілетокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
N-[7-мeтoкcи-8-(2-пiпepидин-l-iлeтoкcи)-2,3-дигiдpoiмiдaзo[1,2-c]xiнaзoлін-5-іл]нікотинамід;
6-{[(етиламіно)карбоніл]аміно}-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
6-фтор-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-1,3-оксазол-4-карбоксамід;
2-(етиламіно)-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-1,3-тіазол-4-карбоксамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]піразин-2-карбоксамід;
N-[8-(2-аміноетокси)-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
6-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]ізонікотинамід;
N-{8-[3-(діетиламіно)пропокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід;
N-{8-[2-(діізопропіламіно)етокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}нікотинамід;
N-{8-[2-(діетиламіно)етокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід;
N-{8-[3-(диметиламіно)пропокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід;
N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід;
N-[7-мeтoкcи-8-(3-мopфoлiн-4-iлпpoпoкcи)-2,3-дигiдpoiмiдaзo[1,2-c]xiнaзoлін-5-iл]-2-(метиламіно)піримідин-5-карбоксамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-2-(метилтіо)піримідин-5-карбоксамід;
N-[8-(3-амінопропокси)-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинаміду трифторацетат;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-тіофен-2-карбоксамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-2,4-диметил-1,3-тіазол-5-карбоксамід;
2-метокси-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]піримідин-5-карбоксамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-3-фурамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-тіофен-3-карбоксамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-2-метил-1,3-тіазол-4-карбоксамід;
6-метокси-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
5-метокси-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-6-метилнікотинамід;
6-(ацетиламіно)-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
або її фізіологічно прийнятна сіль, сольват, гідрат або стереоізомер.
28. Сполука за будь-яким з пп. 1-26, вибрана з групи:
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-6-метилнікотинамід;
5-метокси-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-2,4-диметил-1,3-тіазол-5-карбоксамід;
N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід;
N-{8-[3-(диметиламіно)пропокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}нікотинамід;
6-{[(ізопропіламіно)карбоніл]аміно}-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-2,4-диметил-1,3-тіазол-5-карбоксамід;
N-[7-метокси-8-(2-морфолін-4-ілетокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід;
рел-6-аміно-N-(8-{3-[(2R,6S)-2,6-диметилморфолін-4-іл]пропокси}-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл)нікотинамід;
рел-2-аміно-N-(8-{3-[(2R,6S)-2,6-диметилморфолін-4-іл]пропокси}-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл)піримідин-5-карбоксамід;
2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]піримідин-5-карбоксамід;
N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-піримідин-5-карбоксамід;
N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-піримідин-5-карбоксамід;
або її фізіологічно прийнятна сіль, сольват, гідрат або стереоізомер.
29. Фармацевтична композиція, що містить сполуку за п. 1 або її фізіологічно прийнятну сіль, сольват, гідрат або стереоізомер та фармацевтично прийнятний розріджувач або носій.
30. Фармацевтична композиція за п. 29, у якій сполука присутня в терапевтично ефективній кількості.
31. Фармацевтична композиція за п. 29, що додатково містить принаймні одну додаткову активну сполуку.
32. Фармацевтична композиція за п. 29, у якій додаткова активна сполука являє собою антигіперпроліферативний, протизапальний, болезаспокійливий, імунорегуляторний, діуретичний, антиаритмічний, антигіперхолестеринемічний, антидисліпідемічний, протидіабетичний або противірусний засіб.
33. Фармацевтична композиція за п. 32, у якій додаткова активна сполука являє собою гемцитабін, паклітаксель, цисплатин, карбоплатин, бутират натрію, 5-FU, доксирубіцин, тамоксифен, етопозид, трастумазаб, гефітиніб, інтрон А, рапаміцин, 17-AAG, U0126, інсулін або похідну інсуліну, ліганд PPAR, препарат сульфонілсечовини, інгібітор a-глікозидази, бігуанід, інгібітор РТР-1В, інгібітор DPP-IV, інгібітор 11-бета-HSD, GLP-1, похідну GLP-1, GIP, похідну GIP, РАСАР, похідну РАСАР, секретин або похідну секретину, алдеслейкін, алендронову кислоту, альфаферон, алітретіноїн, алопуринол, алоприм, алокси, альтретамін, аміноглутетимід, аміфостин, амрубіцин, амсакрин, анастрозол, анзмет, аранесп, арглабін, триоксид миш'яку, аромасин, 5-азацитидин, імуран, БЦЖ або tice БЦЖ, бестатин, бетаметазон ацетат, бетаметазон фосфат натрію, бексаротен, блеоміцину сульфат, броксуридин, бортезоміб, бусульфан, кальцитонін, кампат, капецитабін, карбоплатин, казодекс, цефезон, целмолейкін, церубідин, хлорамбуцил, цисплатин, кладрибін, кладрибін, клодронову кислоту, циклофосфамід, цитарабін, дакарбазин, дактиноміцин, ДауноКсом, декадрон, декадрону фосфат, делестроген, денілейкін дифтитокс, депо-медрол, деслорелін, дексразоксан, діетилстилбестрол, дифлюкан, доцетаксель, доксифлуридин, доксорубіцин, дронабінол, DW-166HC, елігард, елітек, еленце, еменд, епірубіцин, епоетин альфа, епоген, ептаплатин, ергамізол, естраке, естрадіол, естрамустин фосфат натрію, етинілестрадіол, етіол, етидронову кислоту, етопофос, етопозид, фадрозол, фарстон, філграстим, фінастерид, фліграстим, флоксуридин, флуконазол, флударабін, 5-фтордеоксіуридину монофосфат, 5-фтороурацил (5-FU), флуоксиместерон, флутамід, форместан, фостеабін, фотемустин, фульвестрант, гаммагард, гемцитабін, гемтузумаб, глеевек, гліадел, госерелін, гранісетрон НСl, гістрелін, гікамтин, гідрокортон, еритрогідроксиноніладенін, гідроксисечовину, ібритумомаб тіуксетан, ідарубіцин, іфостамід, інтерферон альфа, інтерферон альфа 2, інтерферон альфа-2А, інтерферон альфа-2В, інтерферон альфа-n1, інтерферон альфа-n3, інтерферон бета, інтерферон гамма-1а, інтерлейкін-2, інтрон А, іресу, іринотекан, кітрил, лентинану сульфат, летрозол, лейковорин, лейпролід, лейпроліду ацетат, левамізол, кальцієву сіль левофолієвої кислоти, левотроїд, левоксил, ломустин, лонідамін, маринол, мехлоретамін, мекобаламін, медроксипрогістерону ацетат, мегестролу ацетат, мелфалан, менест, 6-меркаптопурин, Месну, метотрексат, метвікс, мілтефосин, міноциклін, мітоміцин С, мітотан, мітоксантрон, модренал, міоцет, недаплатин, нойласту, ноймегу, нойпоген, нілутамід, нолвадекс, NSC-631570, ОСТ-43, остреотид, ондансетрон НСl, орапред, оксаліплатин, паклітаксел, педіапред, пегаспаргаз, пегасис, пентостатин, піцибаніл, пілокарпін НСl, пірарубіцин, плікаміцин, натрію порфімер, преднімустин, преднізолон, преднізон, премарин, прокарбазин, прокрит, ралтитрексед, ребіф, ренію-186 етидронат, ритуксимаб, роферон-А, ромуртид, салаген, сандостатин, сарграмостим, семустин, сизофіран, собузоксан, солу-медрол, спарфозову кислоту, терапію стовбуровими клітинами, стрептозоцин, стронцію-89 хлорид, синтроїд, тамоксифен, тамсулозин, тасонермін, тастолактон, таксотеру, тецелейкін, темозоломід, теніпозид, тестостерону пропіонат, тестред, тіогуанін, тіотепу, тиротропін, тилудронову кислоту, топотекан, тореміфен, тоситумомаб, трастузумаб, треосульфан, третиноїн, трексал, триметилмеламін, триметрексат, триптореліну ацетат, триптореліну памоат, UFT, уридин, валрубіцин, веснаринон, вінбластин, вінкристин, віндезин, вінорелбін, вірулізин, зинекард, зиностатин, стималамер, зофран, АВІ-007, аколбіфен, актимун, афінітак, аміноптерин, арзоксифен, азоприсніл, атаместан, атрасентан, BAY 43-9006 (сорафеніб), авастин, ССІ-779, CDC-501, целебрекс, цетуксимаб, криснатол, ципротерону ацетат, децитабін, DN-101, доксорубіцин-МТС, dSLIM, дутастерид, едотекарин, ефлорнітин, ексатекан, фенретинід, гістаміну дигідрохлорид, гістреліновий гідрогель, гольмій-166 DOTMP, ібадронову кислоту, інтерферон гамма, інтрон-PEG, іксабепілон, гемоціанін фісурели, L-651582, ланреотид, лазофоксифен, лібру, лонафарніб, міпроксифен, мінодронат, MS-209, ліпосомал МТР-РЕ, МХ-6, нафарелін, неморубіцин, неовастат, нолатрексед, облімерсен, онко-TCS, осидем, паклітакселю поліглутамат, памідронат динатрію, PN-401, QS-21, квазепам, R-1549, ралоксифен, ранпірнас, 13-цис-ретиноєву кислоту, сатраплатин, сеокальцитол, Т-138067, тарцеву, таксопрексин, тимосин альфа 1, тіазофурин, типіфарніб, тирапазамін, TLK-286, тореміфен, TransMID-107R, валсподар, вапреотид, ваталаніб, вертепорфін, вінфлунін, Z-100, золедронову кислоту або їх комбінації.
34. Упакована фармацевтична композиція, що включає контейнер, фармацевтичну композицію за п. 29 та інструкцію для застосування фармацевтичної композиції для лікування хвороби або стану у ссавця.
35. Спосіб інгібування фосфотидилінозитол-3-кінази в клітинах, в якому здійснюють контакт клітини з однією або декількома сполуками за п. 1.
36. Спосіб лікування порушення, опосередковуваного інгібуванням фосфотидилінозитол-3-кінази, у ссавця, що включає введення ссавцеві, який цього потребує, терапевтично ефективної кількості однієї або декількох сполук за п. 1.
37. Спосіб за п. 36, у якому порушення, опосередковуване фосфотидилінозитол-3-кіназою, являє собою ангіогенне порушення, запальне порушення, аутоімунне порушення, серцево-судинне порушення, нейродегенеративне порушення, метаболічне порушення, ноцицептивне порушення, очне порушення, легеневе порушення або ниркове порушення.
38. Спосіб за п. 37, у якому серцево-судинне порушення являє собою тромбоз, легеневу гіпертензію, серцеву гіпертрофію, атеросклероз або серцеву недостатність.
39. Спосіб за п. 37, у якому запальне порушення являє собою COPD.
40. Спосіб за п. 37, у якому ангіогенне порушення являє собою діабетичну ретинопатію, ішемічну оклюзію вен сітківки, ювенільну ретинопатію, неоваскулярну глаукому, псоріаз, ретролентальні фіброплазії, ангіофіброму, запалення, ревматоїдний артрит, рестеноз, рестеноз у стенті або рестеноз судинного трансплантата.
41. Спосіб лікування гіперпроліферативного порушення у ссавця, що включає введення ссавцеві, який цього потребує, терапевтично ефективної кількості однієї або декількох сполук за п. 1.
42. Спосіб за п. 41, у якому гіперпроліферативне порушення являє собою рак.
43. Спосіб за п. 42, у якому рак являє собою рак молочної залози, дихальних шляхів, головного мозку, репродуктивних органів, травного тракту, сечових шляхів, ока, печінки, шкіри, голови та шиї, щитовидної залози, паращитовидної залози та віддалені метастази солідної пухлини.
44. Спосіб за п. 42, у якому рак являє собою лімфому, саркому або лейкемію.
Текст
1. Сполука, що має формулу: 2 (19) 1 3 96965 атом, вибраний з кисню, азоту або сірки, та який 6' можна необов'язково замінити на 1 або кілька R груп. 4 5. Сполука за п. 1, у якій R являє собою гідроксигрупу. 4 5 6. Сполука за п. 1, у якій R та R взяті разом з атомами, з якими вони зв'язані, для утворення 5-6членного азотовмісного гетероциклічного кільця, що необов'язково містить 1 або кілька атомів азоту, кисню або сірки, та які можна необов'язково 6' замінити на 1 або кілька груп R . 3 7. Сполука за п. 1, у якій R являє собою метил. 2 8. Сполука за п. 1, у якій R являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол, тіазол, фуран або тіофен, необов'язково заміщений 6 1, 2 або 3 групами R . 2 9. Сполука за п. 2, у якій R являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол або тіазол, необов'язково заміщений 1, 2 або 3 група6 ми R . 10. Сполука за п. 1, що має формулу: N N O N NH N N O N O NH O R2 . 14. Сполука за п. 13, у якій R являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол, тіазол, фуран або тіофен, необов'язково заміще6 ний 1, 2 або 3 групами R . 2 15. Сполука за п. 14, у якій R являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол або тіазол, необов'язково заміщений 1, 2 або 3 6 групами R . 16. Сполука за п. 1, що має формулу: 2 N O N N O N O N O O N O N NH O R2 R5' . 2 20. Сполука за п. 19, у якій R являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол, тіазол, фуран або тіофен, необов'язково заміще6 ний 1, 2 або 3 групами R . 2 21. Сполука за п. 20, у якій R являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол або тіазол, необов'язково заміщений 1, 2 або 3 6 групами R . 5' 22. Сполука за п. 19, у якій R являє собою алкіл. 23. Сполука за п. 1, що має формулу: N N O O O R2 . 2 11. Сполука за п. 10, у якій R являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол, тіазол, фуран або тіофен, необов'язково заміще6 ний 1, 2 або 3 групами R . 2 12. Сполука за п. 11, у якій R являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол або тіазол, необов'язково заміщений 1, 2 або 3 6 групами R . 13. Сполука за п. 1, що має формулу: N N R5' O O або тіазол, необов'язково заміщений 1, 2 або 3 6 групами R . 19. Сполука за п. 1, що має формулу: N N O 4 NH O R2 . 17. Сполука за п. 16, у якій R являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол, тіазол, фуран або тіофен, необов'язково заміще6 ний 1, 2 або 3 групами R . 2 18. Сполука за п. 17, у якій R являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол 2 N O NH O R2 . 24. Сполука за п. 23, у якій R являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол, тіазол, фуран або тіофен, необов'язково заміще6 ний 1, 2 або 3 групами R . 2 25. Сполука за п. 24, у якій R являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол або тіазол, необов'язково заміщений 1, 2 або 3 6 групами R . 5' 26. Сполука за п. 23, у якій R являє собою алкіл. 27. Сполука за будь-яким з попередніх пунктів, вибрана з групи: N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-піримідин-5карбоксамід; N-(8-{3-[(2R,6S)-2,6-димeтилмopфoлiн-4iл]пpoпoкcи}-7-мeтoкcи-2,3-дигідроімідазо[1,2с]хіназолін-5-іл)нікотинамід; N-(8-{3-[(2R,6S)-2,6-димeтилмopфoлiн-4iл]пpoпoкcи}-7-мeтoкcи-2,3-дигідроімідазо[1,2с]хіназолін-5-іл)-2,4-диметил-1,3-тіазол-5карбоксамід; 2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-1,3-тіазол-5карбоксамід; 2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)2,3-дигідроімідазо[1,2-с]хіназолін-5іл]ізонікотинамід; 2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-4-метил-1,3тіазол-5-карбоксамід; 2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-4пропілпіримідин-5-карбоксамід; N-{8-[2-(4-етилморфолін-2-іл)етокси]-7-метокси2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід; 2 5 N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}піримідин-5карбоксамід; N-(8-{3-[2-(гідроксиметил)морфолін-4-іл]пропокси}7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5іл)нікотинамід; N-(8-{3-[2-(гідроксиметил)морфолін-4-іл]пропокси}7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5іл)нікотинамід; N-{8-[3-(диметиламіно)пропокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід 1оксид; 2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]піримідин-5карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6-(2-піролідин1-ілетил)нікотинамід; 6-(циклопентиламіно)-N-[7-метокси-8-(3-морфолін4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]нікотинамід; N-[8-(2-гідрокси-3-морфолін-4-ілпропокси)-7метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]нікотинамід; N-{7-метокси-8-[3-(3-метилморфолін-4іл)пропокси]-2,3-дигідроімідазо[1,2-с]хіназолін-5іл}нікотинамід; N-(8-{3-[2-(гідроксиметил)морфолін-4-іл]пропокси}7-метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5іл)нікотинамід; N-(8-{2-[4-(циклобутилметил)морфолін-2іл]етокси}-7-метокси-2,3-дигідроімідазо[1,2с]хіназолін-5-іл)нікотинамід; N-(7-метокси-8-{2-[4-(2-метоксіетил)морфолiн-2іл]етокси}-2,3-дигідроімідазо[1,2-с]хіназолін-5іл)нікотинамід; N-{8-[(4-етилморфолін-2-іл)метокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід; N-(7-метокси-8-{[4-(2-метоксіетил)морфолін-2іл]метокси}-2,3-дигідроімідазо[1,2-с]хіназолін-5іл)нікотинамід; N-{7-метокси-8-[(4-метилморфолін-2-іл)метокси]2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-піримідин-4карбоксамід; 2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]піримідин-4карбоксамід; N-[7-мeтoкcи-8-(3-мopфoлiн-4-iлпpoпoкcи)-2,3дигiдpoiмiдaзo[1,2-c]xiнaзoлiн-5-iл]-1-метил-1Німідазол-4-карбоксамід; рел-(8-{3-[(2R,6S)-2,6-диметилморфолін-4іл]пропокси}-7-метокси-2,3-дигідроімідазо[1,2с]хіназолін-5-іл)піримідин-5-карбоксамід; рел-(8-{3-[(2R,6S)-2,6-диметилморфолін-4іл]пропокси}-7-метокси-2,3-дигідроімідазо[1,2с]хіназолін-5-іл)-6-метилнікотинамід; рел-6-ацетамідо-N-(8-{3-[(2R,6S)-2,6диметилморфолін-4-іл]пропокси}-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл)нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-1-метил-1Німідазол-5-карбоксамід; 96965 6 6-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-2метилнікотинамід; 2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-4метилпіримідин-5-карбоксамід; 6-аміно-5-бром-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]нікотинамід; 2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-1,3-оксазол5-карбоксамід; N-[7-метокси-8-(морфолін-2-ілметокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; 2-{[2-(диметиламіно)етил]аміно}-N-{8-[3(диметиламіно)пропокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}піримідин-5карбоксамід; 2-аміно-N-{8-[3-(диметиламіно)пропокси]-7метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-1,3тіазол-5-карбоксамід; рел-2-аміно-N-(8-{3-[(2R,6S)-2,6диметилморфолін-4-іл]пропокси}-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл)піримідин-5карбоксамід; рел-6-аміно-N-(8-{3-[(2R,6S)-2,6диметилморфолін-4-іл]пропокси}-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл) нікотинамід; 2-[(2-гідроксіетил)аміно]-N-[7-метокси-8-(3морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]піримідин-5-карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2-[(3метоксипропіл)аміно]піримідин-5-карбоксамід; 2-аміно-N-{8-[3-(диметиламіно)пропокси]-7метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5іл}піримідин-5-карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2-[(3-морфолін4-ілпропіл)аміно]піримідин-5-карбоксамід; 2-[(2-метоксіетил)аміно]-N-[7-метокси-8-(3морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]піримідин-5-карбоксамід; 2-{[2-(диметиламіно)етил]аміно}-N-[7-метокси-8-(3морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]піримідин-5-карбоксамід; 6-аміно-N-{8-[3-(диметиламіно)пропокси]-7метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5іл}нікотинамід; N-[7-метокси-8-(3-морфолiн-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2-піролідин-1ілпіримідин-5-карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2-(4метилпіперазин-1-іл)піримідин-5-карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2-морфолін-4ілпіримідин-5-карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6-піперазин-1ілнікотинаміду гідрохлорид; 6-[(3S)-3-амінопіролідин-1-іл]-N-[7-метокси-8-(3морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинаміду гідрохлориду гідрат; 7 6-[(3R)-3-амінопіролідин-1-іл]-N-[7-метокси-8-(3морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинаміду гідрохлорид; 6-[(4-фторобензил)аміно]-N-[7-метокси-8-(3морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинамід; 6-[(2-фурилметил)аміно]-N-[7-метокси-8-(3морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинамід; 6-[(2-метоксіетил)аміно]-N-[7-метокси-8-(3морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6-(1Н-пірол-1іл)нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6-морфолін-4ілнікотинамід; N-{7-метокси-8-[3-(метиламіно)пропокси]-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}нікотинамід; 6-[(2,2-диметилпропаноїл)аміно]-N-[7-метокси-8-(3морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинамід; 6-[(циклопропілкарбоніл)аміно]-N-[7-метокси-8-(3морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6-(2,2,2трифторетокси)нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6(трифторометил)нікотинамід; 6-(ізобутириламіно)-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]нікотинамід; N-{7-метокси-8-[3-(4-метилпіперазин-1іл)пропокси]-2,3-дигідроімідазо[1,2-с]хіназолін-5іл}нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2{[(метиламіно)карбоніл]аміно}-1,3-тіазол-4карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6{[(метиламіно)карбоніл]аміно}нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2-(метиламіно)1,3-тіазол-4-карбоксамід; N-[7-метокси-8-(2-морфолін-4-ілетокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}-2,4-диметил1,3-тіазол-5-карбоксамід; N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}-6метилнікотинамід; 6-{[(ізопропіламіно)карбоніл]аміно}-N-[7-метокси-8(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6-піролідин-1ілнікотинамід; 6-(диметиламіно)-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]нікотинамід; 96965 8 N-[7-метокси-8-(3-піперидин-1-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; N-[7-метокси-8-(2-піролідин-1-ілетокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; N-[7-мeтoкcи-8-(2-пiпepидин-l-iлeтoкcи)-2,3дигiдpoiмiдaзo[1,2-c]xiнaзoлін-5-іл]нікотинамід; 6-{[(етиламіно)карбоніл]аміно}-N-[7-метокси-8-(3морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинамід; 6-фтор-N-[7-метокси-8-(3-морфолін-4-ілпропокси)2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; 2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]-1,3-оксазол4-карбоксамід; 2-(етиламіно)-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]1,3-тіазол-4-карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]піразин-2карбоксамід; N-[8-(2-аміноетокси)-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; 6-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]ізонікотинамід; N-{8-[3-(діетиламіно)пропокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід; N-{8-[2-(діізопропіламіно)етокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}нікотинамід; N-{8-[2-(діетиламіно)етокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід; N-{8-[3-(диметиламіно)пропокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід; N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід; N-[7-мeтoкcи-8-(3-мopфoлiн-4-iлпpoпoкcи)-2,3дигiдpoiмiдaзo[1,2-c]xiнaзoлін-5-iл]-2(метиламіно)піримідин-5-карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2(метилтіо)піримідин-5-карбоксамід; N-[8-(3-амінопропокси)-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинаміду трифторацетат; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-тіофен-2карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2,4-диметил1,3-тіазол-5-карбоксамід; 2-метокси-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]піримідин-5-карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-3-фурамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-тіофен-3карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2-метил-1,3тіазол-4-карбоксамід; 6-метокси-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]нікотинамід; 9 5-метокси-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6метилнікотинамід; 6-(ацетиламіно)-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; або її фізіологічно прийнятна сіль, сольват, гідрат або стереоізомер. 28. Сполука за будь-яким з пп. 1-26, вибрана з групи: N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6метилнікотинамід; 5-метокси-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2,4-диметил1,3-тіазол-5-карбоксамід; N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід; N-{8-[3-(диметиламіно)пропокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}нікотинамід; 6-{[(ізопропіламіно)карбоніл]аміно}-N-[7-метокси-8(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинамід; N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}-2,4-диметил1,3-тіазол-5-карбоксамід; N-[7-метокси-8-(2-морфолін-4-ілетокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; рел-6-аміно-N-(8-{3-[(2R,6S)-2,6диметилморфолін-4-іл]пропокси}-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл)нікотинамід; рел-2-аміно-N-(8-{3-[(2R,6S)-2,6диметилморфолін-4-іл]пропокси}-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл)піримідин-5карбоксамід; 2-аміно-N-[7-метокси-8-(3-морфолін-4-ілпропокси)2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]піримідин-5карбоксамід; N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}-піримідин-5карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-піримідин-5карбоксамід; або її фізіологічно прийнятна сіль, сольват, гідрат або стереоізомер. 29. Фармацевтична композиція, що містить сполуку за п. 1 або її фізіологічно прийнятну сіль, сольват, гідрат або стереоізомер та фармацевтично прийнятний розріджувач або носій. 30. Фармацевтична композиція за п. 29, у якій сполука присутня в терапевтично ефективній кількості. 96965 10 31. Фармацевтична композиція за п. 29, що додатково містить принаймні одну додаткову активну сполуку. 32. Фармацевтична композиція за п. 29, у якій додаткова активна сполука являє собою антигіперпроліферативний, протизапальний, болезаспокійливий, імунорегуляторний, діуретичний, антиаритмічний, антигіперхолестеринемічний, антидисліпідемічний, протидіабетичний або противірусний засіб. 33. Фармацевтична композиція за п. 32, у якій додаткова активна сполука являє собою гемцитабін, паклітаксель, цисплатин, карбоплатин, бутират натрію, 5-FU, доксирубіцин, тамоксифен, етопозид, трастумазаб, гефітиніб, інтрон А, рапаміцин, 17-AAG, U0126, інсулін або похідну інсуліну, ліганд PPAR, препарат сульфонілсечовини, інгібітор глікозидази, бігуанід, інгібітор РТР-1В, інгібітор DPP-IV, інгібітор 11-бета-HSD, GLP-1, похідну GLP-1, GIP, похідну GIP, РАСАР, похідну РАСАР, секретин або похідну секретину, алдеслейкін, алендронову кислоту, альфаферон, алітретіноїн, алопуринол, алоприм, алокси, альтретамін, аміноглутетимід, аміфостин, амрубіцин, амсакрин, анастрозол, анзмет, аранесп, арглабін, триоксид миш'яку, аромасин, 5-азацитидин, імуран, БЦЖ або tice БЦЖ, бестатин, бетаметазон ацетат, бетаметазон фосфат натрію, бексаротен, блеоміцину сульфат, броксуридин, бортезоміб, бусульфан, кальцитонін, кампат, капецитабін, карбоплатин, казодекс, цефезон, целмолейкін, церубідин, хлорамбуцил, цисплатин, кладрибін, кладрибін, клодронову кислоту, циклофосфамід, цитарабін, дакарбазин, дактиноміцин, ДауноКсом, декадрон, декадрону фосфат, делестроген, денілейкін дифтитокс, депо-медрол, деслорелін, дексразоксан, діетилстилбестрол, дифлюкан, доцетаксель, доксифлуридин, доксорубіцин, дронабінол, DW166HC, елігард, елітек, еленце, еменд, епірубіцин, епоетин альфа, епоген, ептаплатин, ергамізол, естраке, естрадіол, естрамустин фосфат натрію, етинілестрадіол, етіол, етидронову кислоту, етопофос, етопозид, фадрозол, фарстон, філграстим, фінастерид, фліграстим, флоксуридин, флуконазол, флударабін, 5-фтордеоксіуридину монофосфат, 5-фтороурацил (5-FU), флуоксиместерон, флутамід, форместан, фостеабін, фотемустин, фульвестрант, гаммагард, гемцитабін, гемтузумаб, глеевек, гліадел, госерелін, гранісетрон НСl, гістрелін, гікамтин, гідрокортон, еритрогідроксиноніладенін, гідроксисечовину, ібритумомаб тіуксетан, ідарубіцин, іфостамід, інтерферон альфа, інтерферон альфа 2, інтерферон альфа-2А, інтерферон альфа-2В, інтерферон альфа-n1, інтерферон альфа-n3, інтерферон бета, інтерферон гамма-1а, інтерлейкін-2, інтрон А, іресу, іринотекан, кітрил, лентинану сульфат, летрозол, лейковорин, лейпролід, лейпроліду ацетат, левамізол, кальцієву сіль левофолієвої кислоти, левотроїд, левоксил, ломустин, лонідамін, маринол, мехлоретамін, мекобаламін, медроксипрогістерону ацетат, мегестролу ацетат, мелфалан, менест, 6-меркаптопурин, Месну, метотрексат, метвікс, мілтефосин, міноциклін, мітоміцин С, мітотан, мітоксантрон, модренал, міоцет, недаплатин, нойласту, ноймегу, ной 11 96965 12 поген, нілутамід, нолвадекс, NSC-631570, ОСТ-43, остреотид, ондансетрон НСl, орапред, оксаліплатин, паклітаксел, педіапред, пегаспаргаз, пегасис, пентостатин, піцибаніл, пілокарпін НСl, пірарубіцин, плікаміцин, натрію порфімер, преднімустин, преднізолон, преднізон, премарин, прокарбазин, прокрит, ралтитрексед, ребіф, ренію-186 етидронат, ритуксимаб, роферон-А, ромуртид, салаген, сандостатин, сарграмостим, семустин, сизофіран, собузоксан, солу-медрол, спарфозову кислоту, терапію стовбуровими клітинами, стрептозоцин, стронцію-89 хлорид, синтроїд, тамоксифен, тамсулозин, тасонермін, тастолактон, таксотеру, тецелейкін, темозоломід, теніпозид, тестостерону пропіонат, тестред, тіогуанін, тіотепу, тиротропін, тилудронову кислоту, топотекан, тореміфен, тоситумомаб, трастузумаб, треосульфан, третиноїн, трексал, триметилмеламін, триметрексат, триптореліну ацетат, триптореліну памоат, UFT, уридин, валрубіцин, веснаринон, вінбластин, вінкристин, віндезин, вінорелбін, вірулізин, зинекард, зиностатин, стималамер, зофран, АВІ-007, аколбіфен, актимун, афінітак, аміноптерин, арзоксифен, азоприсніл, атаместан, атрасентан, BAY 43-9006 (сорафеніб), авастин, ССІ-779, CDC-501, целебрекс, цетуксимаб, криснатол, ципротерону ацетат, децитабін, DN-101, доксорубіцин-МТС, dSLIM, дутастерид, едотекарин, ефлорнітин, ексатекан, фенретинід, гістаміну дигідрохлорид, гістреліновий гідрогель, гольмій-166 DOTMP, ібадронову кислоту, інтерферон гамма, інтрон-PEG, іксабепілон, гемоціанін фісурели, L-651582, ланреотид, лазофоксифен, лібру, лонафарніб, міпроксифен, мінодронат, MS-209, ліпосомал МТР-РЕ, МХ-6, нафарелін, неморубіцин, неовастат, нолатрексед, облімерсен, онко-TCS, осидем, паклітакселю поліглутамат, памідронат динатрію, PN-401, QS-21, квазепам, R-1549, ралоксифен, ранпірнас, 13-цисретиноєву кислоту, сатраплатин, сеокальцитол, Т138067, тарцеву, таксопрексин, тимосин альфа 1, тіазофурин, типіфарніб, тирапазамін, TLK-286, тореміфен, TransMID-107R, валсподар, вапреотид, ваталаніб, вертепорфін, вінфлунін, Z-100, золедронову кислоту або їх комбінації. 34. Упакована фармацевтична композиція, що включає контейнер, фармацевтичну композицію за п. 29 та інструкцію для застосування фармацевтичної композиції для лікування хвороби або стану у ссавця. 35. Спосіб інгібування фосфотидилінозитол-3кінази в клітинах, в якому здійснюють контакт клітини з однією або декількома сполуками за п. 1. 36. Спосіб лікування порушення, опосередковуваного інгібуванням фосфотидилінозитол-3-кінази, у ссавця, що включає введення ссавцеві, який цього потребує, терапевтично ефективної кількості однієї або декількох сполук за п. 1. 37. Спосіб за п. 36, у якому порушення, опосередковуване фосфотидилінозитол-3-кіназою, являє собою ангіогенне порушення, запальне порушення, аутоімунне порушення, серцево-судинне порушення, нейродегенеративне порушення, метаболічне порушення, ноцицептивне порушення, очне порушення, легеневе порушення або ниркове порушення. 38. Спосіб за п. 37, у якому серцево-судинне порушення являє собою тромбоз, легеневу гіпертензію, серцеву гіпертрофію, атеросклероз або серцеву недостатність. 39. Спосіб за п. 37, у якому запальне порушення являє собою COPD. 40. Спосіб за п. 37, у якому ангіогенне порушення являє собою діабетичну ретинопатію, ішемічну оклюзію вен сітківки, ювенільну ретинопатію, неоваскулярну глаукому, псоріаз, ретролентальні фіброплазії, ангіофіброму, запалення, ревматоїдний артрит, рестеноз, рестеноз у стенті або рестеноз судинного трансплантата. 41. Спосіб лікування гіперпроліферативного порушення у ссавця, що включає введення ссавцеві, який цього потребує, терапевтично ефективної кількості однієї або декількох сполук за п. 1. 42. Спосіб за п. 41, у якому гіперпроліферативне порушення являє собою рак. 43. Спосіб за п. 42, у якому рак являє собою рак молочної залози, дихальних шляхів, головного мозку, репродуктивних органів, травного тракту, сечових шляхів, ока, печінки, шкіри, голови та шиї, щитовидної залози, паращитовидної залози та віддалені метастази солідної пухлини. 44. Спосіб за п. 42, у якому рак являє собою лімфому, саркому або лейкемію. Даний винахід стосується нових сполук 2,3дигідроімідазо[1,2-с]хіназоліну, фармацевтичних композицій, що містять такі сполуки та використання цих сполук або композицій для інгібування фосфотидилінозитол-3-кінази (РІ3K) та лікування хвороб, пов'язаних з активністю фосфотидилінозитол-3-кінази (РІ3K), при певному лікуванні гіперпроліферативних порушень та/або порушень ангіогенезу, як окремий агент або в комбінації з іншими активними компонентами. У минуле десятиліття поняття розробки протиракових лікарських засобів, мішенями яких є патологічно активні протеїнкінази, привело до ряду успіхів. На додаток до дій протеїнкіназ, ліпідкі нази також відіграють важливу роль у генерації критичних регулюючих вторинних месенджерів. Сімейство РІ3K ліпідкіназ робить 3'фосфоінозитиди, які зв'язуються з безліччю клітинних мішеней та активують їх, починаючи широкий діапазон каскадів трансдукції сигналу (Vanhaesebroeck et al., 2001; Toker, 2002; Pendaries et al., 2003; Downes et al., 2005). Ці каскади в остаточному підсумку викликають зміни в багатьох клітинних процесах, включаючи проліферацію клітин, виживання клітин, диференціювання, транспорт у везикулах, міграцію та хемотаксис. РІ3K можуть бути розділені на три різних класи на підставі розходжень і у структурі, і в перевазі 13 до субстрату. У той час як члени сімейства Класу II РІ3K були залучені в регулювання росту пухлини (Brown and Shepard, 2001; Traer et al., 2006), більша частина дослідження зосередилася на ферментах Класу І та їх ролі при раку (Vivanco And Sawyers, 2002; Workman, 2004, Chen et al., 2005; Hennessey et al., 2005; Stauffer et al., 2005; Stephens et al., 2005; Cully et al., 2006). РІ3K Класу І були традиційно розділені на два різних підкласи на підставі розходжень у складі білкової субодиниці. РІ3K Класу ІA складаються з каталітичної р110 каталітичної субодиниці (р110 α, β або δ), гетеродимеризованої зі членом сімейства р85 регулюючих субодиниць. Навпаки, каталітична субодиниця РІ3K Класу lB (р110 γ) гетеродимеризирується з іншою p 101 регулюючою субодиницею (розглянуте Vanhaesebroeck and Waterfield, 1999; Funaki et al., 2000; Katso et al., 2001). Стермінальна ділянка цих білків містить каталітичний домен, що має віддалену гомологію до протеїнкіназ. Структура РІ3Kγ подібна р110 Класу ІA, але не містить N-термінальної р85 зв'язуючої ділянки (Domin й Waterfield, 1997). Хоча вони подібні по загальної структури, гомологія між каталітичними р110 субодиницями є низкою або середньою. Найвища гомологія між РІ3K ізоформами знаходиться в кишені кінази кіназного домену. РІ3K ізоформи Класу ІA зв'язуються з активованими рецепторними тирозинкіназами (RTK) (включаючи PDGFR, EGFR, VEGFR, IGF1-R, с-КІТ, CSF-R та Met), або з тирозин фосфорильованими адаптерними білками (такими як Grb2, Cb1, IRS-1 або Gab1), через їх р85 регулюючі субодиниці, що приводить до стимуляції ліпідкіназної активності. Активація ліпідкіназної активності р110 β та р110 γ ізоформ, як показано, відбувається у відповідь на зв'язування з активованими формами ras Онкогену (Kodaki et al., 1994). Фактично, онкогенна активність цих ізоформ може потребувати зв'язування з ras (Kang et al., 2006). Навпаки, р110 α і р110 δ ізоформи показують онкогенну активність незалежно від зв'язування ras, через конститутивну активацію Akt. РІ3K Класу І каталізують перетворення РІ(4,5) Р2 [РІР2] в РІ(3,4,5) Р3 [РІР3]. Вироблення РІР3 за допомогою РІ3K зачіпає багато сигнальних процесів, які регулюють і координують біологічні кінцеві точки клітинної проліферації, клітинного виживання, диференціювання та клітинної міграції. РІР3 зв'язується білками, що містять домен Pleckstrinгомології (РН), включаючи фосфоінозитидзалежну кіназу, PDK1 та Akt прото-онкогенний продукт, обмежуючи ці білки в ділянках активної трансдукції сигналу і також безпосередньо сприяючи їх активації (Klippel et al., 1997; Fleming et al., 2000; Itoh and Takenawa, 2002; Lemmon, 2003). Ця сумісна локалізація PDK1 з Akt полегшує фосфорилювання та активацію Akt. Карбокси473 термінальне фосфорилювання Akt на Ser спри308 яє фосфорилюванню Thr у петлі активації Akt (Chan and Tsichlis, 2001; Hodgekinson et al., 2002; Scheid et al., 2002; Hresko et al., 2003). При активації Akt фосфорилює та регулює множинні регулюючі кінази шляхів, які безпосередньо впливають на прогресію клітинного циклу та клітинне виживання. 96965 14 Багато з ефектів активації Akt опосередковуються через її негативне регулювання шляхів, які впливають на виживання клітини та які звичайно дисрегульовані при раку. Akt сприяє виживанню пухлинних клітин шляхом регулювання компонентів апоптозних механізмів та механізмів клітинного циклу. Akt - одна з декількох кіназ, що фосфорилює та інактивує про-апоптичні білки BAD (del Paso et al., 1997; Pastorino et al., 1999). Akt може також сприяти клітинному виживанню через блокування цитохром С-залежної каспазної активації 196 шляхом фосфорилювання Каспази 9 на Ser (Cardone et al., 1998). Akt впливає на генну транскрипцію на декількох рівнях. Akt-опосередковане фосфорилювання 166 186 MDM2 Е3 убіквітинлігази на Ser та Ser полегшує ядерний імпорт MDM2 та формування та активацію комплексу убіквітинлігази. Ядерний MDM2 націлюється на р53 пухлинний супресор для деградації, процесу, що може бути заблокований за допомогою LY294002 (Yap et al., 2000; Ogarawa et ah, 2002). Спадне регулювання р53 за допомогою MDM2 негативно впливає на транскрипцію р5 3регульованих про-апоптичних генів (наприклад, Вах, Fas, PUMA та DR5), інгібітор клітинного циклу, Сip1 р21 та PTEN пухлинний супресор (Momand et al., 2000; Hupp et al., 2000; Mayo et al., 2002; Su et al., 2003). Подібним чином, Akt-опосередковане фосфорилювання факторів транскрипції Forkhead FKHR, FKHRL та AFX (Kops et al., 1999; Tang et al., 1999), полегшує їх зв'язування з білками 14-3-3 та експорт із клітинного ядра в цитозоль (Brunet et al., 1999). Ця функціональна інактивація активності Forkhead також впливає на транскрипцію проапоптичних та про-ангіогенних генів, включаючи транскрипцію ліганду Fas (Ciechomska et al., 2003) Віm, члена про-апоптичного Bcl-2 сімейства (Dijkers et al., 2000), та антагоніста Ангіопоетину-1 (Ang-1), Ang-2 (Daly et al., 2004). Фактори транскрипції Forkhead регулюють експресію інгібітору Kip1 циклін-залежної кінази (Cdk) р27 . Дійсно, інгібітори РІ3K, як було продемонстровано, індукують Kір1 експресію р27 , що приводить до інгібування Cdk1, зупинення клітинного циклу та апоптозу (Dijkers et al., 2000). Також повідомляють, що Akt Сір1 145 Kір1 157 фосфорилює р21 на Thr та р27 на Thr , полегшуючи їх асоціацію з білками 14-3-3, що приводить до ядерного експорту та утримання в цитоплазмі, запобігаючи їх інгібуванню Cdks ядра (Zhou et al., 2001; Motti et al., 2004; Sekimoto et al., 2004). На додаток до цих ефектів, Akt фосфорилює IKK (Romashkova and Makarov, 1999), що приводить до фосфорилювання та деградації ІκВ та наступної ядерної транслокації NFκB, що приводить до експресії генів виживання, таких як ІАР та Bcl-XL. Шлях РІ3K/Akt також пов'язаний із супресією МАРK апоптозу через JNK та р38 МАР Кінази, які пов'язані з індукцією апоптозу. Akt, як постулюєтьМАРK ся, пригнічує сигнальний шлях JNK та р38 через фосфорилювання та інгібування двох JNK/p38 регулюючих кіназ, Кінази 1, що регулює сигнал апоптозу (ASK1) (Kim et al., 2001: Liao and Hung, 2003; Yuan et al., 2003), і Кінази Змішаного Походження 3 (MLK3) (Lopez-Ilasaca et al., 1997; 15 Barthwal et al., 2003; Figueroa et al., 2003). Індукція АРК р38 активності спостерігається в пухлинах, що лікують за допомогою цитотоксичних агентів, та потрібна для цих агентів для індукції смерті клітини (розглянуте Olson й Hallahan, 2004). Таким чином, інгібітори шляху РІЗ К можуть сприяти активностям цитотоксичних препаратів, що вводять сумісно. Додаткова роль для передачі сигналів РІ3KΓ Akt залучає регулювання прогресії клітинного циклу через модуляцію активності Глікоген Синтаз Кінази 3 (GSK3). Активність GSK3 підвищена в нерухомих клітинах, де вона фосфорилює циклін Di на Ser , націлюючи білок для убіквітинації та деградації (Diehl et al., 1998) та блокуючи вхід в Sфазу. Akt інгібує активність GSK3 через фосфори9 лювання на Ser (Cross et al., 1995). Це приводить до підвищення рівнів Цикліну D1, що сприяє прогресії клітинного циклу. Інгібування активності GSK3 також впливає на проліферацію клітин через активацію wnt/бета-катенінового сигнального шляху (Abbosh and Nephew, 2005; Naito et al., 2005; Wilker et al., 2005; Kim et al., 2006; Segrelles et al., 2006). Akt-опосередковане фосфорилювання GSK3 приводить до стабілізації та ядерної локалізації бета-катенінового білку, що у свою чергу приводить до збільшення експресії с-mус та цикліну D1, мішеней бета-катенінового /Tcf шляху. Хоча передача сигналів РІ3K використовується багатьма мережами трансдукції сигналу, пов'язаними з онкогенами та пухлинними супресорами, РІ3K та її активність були безпосередньо пов'язані з раком. Надекспресія обох ізоформ р110 α і р110 β спостерігалася в пухлинах сечового міхура та товстої кишки та у клітинних лініях, та надекспресія взагалі корелює зі збільшеною активністю РІ3K (Benistant et al., 2000). Також повідомлялося про над експресію р110а у пухлинах яєчнику та шейки матки та пухлинних клітинних ліній, так само як у лусочкоклітинних карциномах легені. Над експресія р110 α у лініях пухлини шейки матки та яєчника пов'язана зі збільшенням активності РІ3K (Shayesteh et al., 1999; Ma et al., 2000). Підвищена активність РІ3K спостерігалася при колоректальних карциномах (Phillips et al., 1998), та збільшена експресія спостерігалася при карциномах молочної залози (Gershtein et al., 1999). За минулі кілька років соматичні мутації в гені, що кодує р110 α (РІK3СА), були ідентифіковані в багатьох ракових утвореннях. Дані, зібрані дотепер, свідчать, що РІK3СА мутована приблизно в 32 % випадків колоректального раку (Samuels et al., 2004; Ikenoue et al., 2005), 18 - 40 % - раку молочної залози (Bachman et al., 2004; Campbell et al., 2004; Levine et al., 2005; Saal et al., 2005; Wu et al., 2005), 27 % - гліобластом (Samuels et al., 2004; Hartmann et al., 2005, Gallia et al., 2006), 25 % раку шлунку (Byun et al., 2003; Samuels et al., 2004; Li et al., 2005), 36 % - гепатоцелюлярної карциноми (Lee et al., 2005), 4 - 12 % - раку яєчнику (Levine et al., 2005; Wang et al., 2005), 4 % - раку легені (Samuels et al., 2004; Whyte and Holbeck, 2006), та до 40 % - раку ендометрію (Oda et al., 2005). Повідомлялося про мутації РІK3СА при олігодендромі, астроцитомі, медулобластомі й також пухлинах 96965 16 щитовидної залози (Broderick et al., 2004; GarciaRostan et al., 2005). На підставі високої частоти мутації РІK3СА, що спостерігається, є одним із двох найбільш часто мутуємих генів, пов'язаних з раком, іншим є K-ras. Більше ніж 80 % групи мутацій РІK3СА у межах двох ділянок білку, спірального (Е545К) і каталітичного (H1047R) доменів. Біохімічний аналіз і дослідження експресії білку продемонстрували, що обидві мутації приводять до збільшення конститутивноїрі 10 α каталітичної активності та фактично є онкогенними (Bader et al., 2006; Kang et al., 2005; Samuels et al., 2005; Samuels and Ericson, 2006). Нещодавно повідомлялося, що РІK3СА фібробласти ембріона миші «knockout» не мали ни східної передачі сигналів від різних рецепторів фактору росту (IGF-1, Інсулін, PDGF, EGF), та є резистентними до перетворення багатьма онкогенними RTK (IGFR, EGFR дикого типу та соматичні активуючі мутанти EGFR, Her2/Neu ) (Zhao et al., 2006). Функціональні дослідження РІ3K in vivo продемонстрували, що siPHK-опосередкована низхідна регуляція р110 β інгібує і фосфорилювання Akt і ріст пухлини клітин HeLa у голих мишей (Czauderna et al., 2003). У подібних експериментах siPHK-опосередкована низхідна регуляція р110 β, як також показано, інгібувала ріст клітин злоякісної гліоми in vitro та in vivo (Pu et al., 2006). Інгібування функції РІ3K домінант-негативними р85 регулюючими субодиницями може блокувати мітогенез і клітинну трансформацію (Huang et al., 1996; Rahimi et al., 1996). Декілька соматичних мутацій у генах, що кодують р85 α і р85 β регулюючі субодиниці РІ3K, які приводять до підвищеної ліпідкіназної активності, були також ідентифіковані в багатьох ракових клітинах (Janssen et al., 1998; Jimenez et al., 1998; Philp et al., 2001; Jucker et al., 2002; Shekar et al., 2005). Нейтралізація антитіл РІ3K також блокує мітогенез та може викликати апоптоз in vitro (Roche et al., 1994: Roche et al., 1998; Benistant et al., 2000). Дослідження доказу принципу in vivo з використанням інгібіторів РІ3K LY294002 та вортманніна демонструють, що інгібування передачі сигналів РІ3K уповільнює ріст пухлини in vivo (Powis et al., 1994; Shultz et al., 1995; Semba et al., 2002; Ihle et al., 2004). Надекспресія активності РІ3K Класу І або стимуляція їх ліпідкіназних активностей пов'язана з резистентністю як до націленого (таким як іматиніб і тратсузумаб), так і цитотоксичних хіміотерапевтичних підходів, а також променевої терапії (West et al., 2002; Gupta et al., 2003; Osaki et al., 2004; Nagata et al., 2004; Gottschalk et al., 2005; Kim et al., 2005). Активація РІ3K, як також було показано, приводить до експресії білку-1 із множинною медикаментозною резистентністю (MRP-1) у клітинах раку передміхурової залози та наступної індукції резистентності до хіміотерапії (Lee et al., 2004). Важливість передачі сигналів РІ3K при канцерогенезі додатково підкреслена результатами про те, що пухлинний супресор PΤΔΝ, PΗ(3) P фосфатаза належить до звичайно інактивованих генів при людських ракових утвореннях (Li et al., 1997, Steck et al., 1997; Ali et al., 1999; Ishii et al., 1999). PΤΔΝ дефосфорилює РІ(3,4,5)Р3 до РІ(4,5) Р2, у 17 такий спосіб антагонізуючи РІ3K-залежну передачу сигналів. Клітини, що містять функціонально неактивний PΤΔΝ, мають підвищені рівні РІР3, високі рівні активності передачі сигналів РІ3K (HaasKogan et al., 1998; Myers et al., 1998; Taylor et al., 2000), збільшений проліферативний потенціал та зменшену чутливість до про-апоптичних стимулів (Stambolic et al., 1998). Відновлення функціонального PΤΔΝ пригнічує передачу сигналів РІ3K (Taylor et al., 2000), інгібує клітинний ріст та повторно сенсибілізує клітини до про-апоптичних стимулів (Myers et al., 1998; Zhao et al., 2004). Подібним чином, відновлення функції PΤΔΝ у пухлинах, що не мають функціонального PΤΔΝ, інгібує ріст пухлини in vivo (Stahl et al., 2003; Su et al., 2003; Tanaka та Grossman, 2003), та сенсибілізує клітини до цитотоксичних агентів (Tanaka й Grossman, 2003). Сімейство РІЗ К класу І чітко відіграє важливу роль у регулюванні багатьох шляхів трансдукції сигналу, які сприяють клітинному виживанню та клітинній проліферації, та активація їх ліпідкіназної активності значно сприяє розвиненню злоякісних новоутворень людини. Крім того, інгібування РІ3K може потенційно обійти клітинні механізми, які лежать в основі резистентності до хіміотерапевтичних агентів. Тому в потужного інгібітору активностей РІ3K Класу І був би потенціал не тільки для інгібування росту пухлини, але й також для сенсибілізації пухлинних клітин до про-апоптичних стимулів in vivo. Шляхи трансдукції сигналу, що відбуваються з хемоаттрактантних рецепторів, як думають, є важливими мішенями в контролі рухливості лейкоцитів при запальних хворобах. Пересування лейкоцитів контролюється хемоаттрактантними факторами, які активують гетеротримерні GPCR й, таким чином, викликають безліч низхідних внутрішньоклітинних явищ. Трансдукція сигналу уздовж одного із цих шляхів, що приводить до мобілізації вільних 2+ Са , перебудові цитоскелету та спрямованого руху, залежить від ліпідних вторинних месенджерів, які продукуються активністю РІ3K (Wymann et al., 2000; Stein and Waterfield, 2000). РІ3K γ модулює вихідні рівні сАМР та контролює скорочуваність у клітинах. Нещодавнє дослідження вказує на те, що зміни у вихідних рівнях сАМР сприяють збільшенню скорочування в мишей-мутантів. Тому, це дослідження показує, що РІ3K γ інгібітори представляли б потенційні терапії для застійної серцевої недостатності, ішемії, легеневої гіпертензії, ниркової недостатності, серцевої гіпертрофії, атеросклерозу, тромбоемболії та діабету. Інгібітори РІ3K, як очікується, блокували б трансдукцію сигналу від GPCR та блокували б активацію різних імунних клітин, приводячи до широкого протизапального профілю з потенціалом для лікування запальних та імунорегулюючих хвороб, включаючи астму, атопічний дерматит, риніт, алергійні хвороби, хронічну обструктивну легеневу хворобу (COPD), септичний шок, хвороби суглобів, аутоімунні патології, такі як ревматичний артрит і хвороба Грейва, діабет, рак, порушення скорочування міокарда, тромбоемболію та атеросклероз. 96965 18 Композиції та сполуки інгібітору РІ3K, описані авторами, включаючи їх солі, метаболіти, сольвати, сольвати солей, гідрати та стереоізомерні форми, показують антипроліферативну активність й, таким чином, є корисними для профілактики або лікування порушень, пов'язаних з гіперпроліферацією. Один варіант здійснення цього винаходу охоплює сполуку, що має формулу (І): Формула І або її фізіологічно прийнятну сіль, сольват, гідрат або стереоізомер, у якій: 1 4 R являє собою (CH2)n-(CHR )-(CH2)m5 5' N(R )(R ); 2 R являє собою гетероарил, необов'язково за6 міщений 1, 2 або 3 групами R ; 3 R являє собою алкіл або циклоалкіл; 4 R являє собою водень, гідрокси групу або ал5 5' кокси групу, та R і R можуть бути однаковими або різними і являють собою незалежно один від іншого водень, алкіл, циклоалкілалкіл, або алкок5 5' сиалкіл або R та R можуть бути взяті разом з атомом азоту, з яким вони зв'язані для утворення 3 - 7-членного азот-вмісного гетероциклічного кільця, що необов'язково містить принаймні один додатковий гетероатом, вибраний з кисню, азоту або сірки, та який може бути необов'язково замі6' 4 5 нений на 1 або більше R груп, або R та R можуть бути взяті разом з атомами, з якими вони зв'язані, для утворення 5 - 6-членного азотвмісного гетероциклічного кільця, що необов'язково містить 1 або більше атомів азоту, кисню або сірки, та які можна необов'язково замінити на 1 6' або більше R груп; 6 при кожній появі R може бути таким же або різним та являє собою незалежно галоген, алкіл, алкеніл, алкініл, циклоалкіл, циклоалкілалкіл, арил, арилалкіл, гетероарил, гетероарилалкіл, гетероциклічне кільце, гетероциклілалкіл, алкіл7 7 7' 7 OR, алкіл-SR , алкіл-N(R )(R ), алкіл-COR ,-CN,7 7 7' 7 7 7 7' COOR , -CON(R )(R ), -OR , -SR , -N(R )(R ), або 7 7 NR COR , кожний з яких можна необов'язково за8 мінити на 1 або більше груп R ; 6' при кожній появі R може бути таким же або різним та являє собою незалежно алкіл, циклоал7 кілалкіл або алкіл-OR ; 7 7' при кожній появі R та R може бути таким же або різним та являє собою незалежно водень, алкіл, алкеніл, алкініл, циклоалкіл, циклоалкілалкіл, циклоалкеніл, арил, арилалкіл, гетероарил, гетероциклічне кільце, гетероциклілалкіл або гетероарилалкіл; 8 при кожній появі R являє собою незалежно нітро групу, гідрокси групу, ціано групу, форміл, ацетил, галоген, аміно групу, алкіл, алкокси групу, алкеніл, алкініл, циклоалкіл, циклоалкілалкіл, циклоалкеніл, арил, арилалкіл, гетероарил, гетероци 19 клічне кільце, гетероциклілалкіл або гетероарилалкіл; n являє собою ціле число від 1 - 4, і m є цілим 4 5 числом від 0 - 4 з умовою, що, коли R та R беруть разом з атомами, з якими вони зв'язані, для утворення 5 - 6-членного азот-вмісного кільця, n + m ≤ 4. У кращому варіанті здійснення винахід охоп2 лює сполуку Формули (І), у якій R - азот-вмісний гетероарил, необов'язково заміщений 1, 2 або 3 6 групами R . В іншому кращому варіанті здійснення винахід 5 5' охоплює сполуку Формули (І), у якій R та R являють собою незалежно алкіл; У ще одному кращому варіанті здійснення ви5 5' нахід охоплює сполуку Формули (І), у якій R та R взяті разом з атомом азоту, з яким вони зв'язані, для утворення 5 - 6-членного азот-вмісного гетероциклічного кільця, що містить принаймні один додатковий гетероатом, вибраний з кисню, азоту або сірки, та який можна необов'язково замінити 6' на 1 або більше R груп. У ще одному кращому варіанті здійснення ви4 нахід охоплює сполуку Формули (І), у якій R являє собою гідрокси групу. В іншому кращому варіанті здійснення винахід 4 5 охоплює сполуку Формули (І), у якій R та R узяті разом з атомами, з якими вони зв'язані, для утворення 5 - 6-членного азот-вмісного гетероциклічного кільця, що необов'язково містить 1 або більше атомів азоту, кисню або сірки, і які можна необо6 в'язково замінити на 1 або більше груп R . У ще одному кращому варіанті здійснення винахід охоплює сполуку Формули (І), у якій R являє собою метил. У ще одному кращому варіанті здійснення ви2 нахід охоплює сполуку Формули (І), у якій R являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол, тіазол, фуран або тіофен, необов'яз6 ково заміщений 1, 2 або 3 групами R ; більш переважно піридин, піридазин, піримідин, піразин, пірол, оксазол або тіазол, необов'язково заміще6 ний 1, 2 або 3 групами R . У відмінному варіанті здійснення винахід охоплює сполуку формули (Іа) або її фізіологічно прийнятну сіль, сольват, гі2 драт або стереоізомер, у якій R приймає значення, визначені вище. В іншому відмінному варіанті здійснення винахід охоплює сполуку формули (Іb) 96965 20 або її фізіологічно прийнятну сіль, сольват, гі2 драт або стереоізомер, у якій R приймає значення, визначені вище. У ще одному відмінному варіанті здійснення винахід охоплює сполуку формули (Іс) або її фізіологічно прийнятну сіль, сольват, гі2 драт або стереоізомер, у якій R приймає значення, визначені вище. У ще одному відмінному варіанті здійснення винахід охоплює сполуку формули (Id): або її фізіологічно прийнятну сіль, сольват, гі2 4 драт або стереоізомер, у якій R та R приймають значення, визначені вище. У ще одному відмінному варіанті здійснення винахід охоплює сполуку формули (Іе): або її фізіологічно прийнятну сіль, сольват, гі2 4 драт або стереоізомер, у якій R та R приймають значення, визначені вище. У кращому варіанті здійснення винахід охоп2 лює сполуку формули (І) - (V), у якій R являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол, тіазол, фуран або тіофен, необов'язково 6 заміщений 1, 2 або 3 групами R ; більш переваж2 но, у якому R являє собою піридин, піридазин, піримідин, піразин, пірол, оксазол або тіазол, не6 обов'язково заміщений 1, 2 або 3 групами R . У ще одному кращому варіанті здійснення винахід охоплює сполуку, що має формулу: 21 N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]піримідин-5карбоксамід; N-(8-{3-[(2R,6S)-2,6-димeтилмopфoлiн-4iл]пpoпoкcи}-7-мeтoкcи-2,3-дигідроімідазо[1,2с]хіназолін-5-іл)нікотинамід; N-(8-{3-[(2R,6S)-2,6-димeтилмopфoлiн-4iл]пpoпoкcи}-7-мeтoкcи-2,3-дигідроімідазо[1,2с]хіназолін-5-іл)-2,4-диметил-1,3-тіазол-5карбоксамід; 2-аміно-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]1,3-тіазол-5-карбоксамід; 2-аміно-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл] ізонікотинамід; 2-аміно-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]4-метил-1,3-тіазол-5-карбоксамід; 2-аміно-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]4-пропілпіримідин-5-карбоксамід; N-{8-[2-(4-етилморфолін-2-іл)етокси]-7метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5іл}нікотинамід; N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}піримідин-5карбоксамід; N-(8-{3-[2-(гідроксиметил)морфолін-4іл]пропокси}-7-метокси-2,3-дигідроімідазо[1,2с]хіназолін-5-іл)нікотинамід; N-(8-{3-[2-(гідроксиметил) морфолін-4іл]пропокси}-7-метокси-2,3-дигідроімідазо[1,2с]хіназолін-5-іл)нікотинамід; N-{8-[3-(диметиламіно)пропокси]-7-метокси2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}нікотинамід 1-оксид; 2-аміно-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]піримідин-5-карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6-(2-піролідин1-ілетил)нікотинамід; 6-(циклопентиламіно)-N-[7-метокси-8-(3морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинамід; N-[8-(2-гідрокси-3-морфолін-4-ілпропокси)-7метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]нікотинамід; N-{7-метокси-8-[3-(3-метилморфолін-4-іл) пропокси]-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}нікотинамід; N-(8-{3-[2-(гідроксиметил)морфолін-4іл]пропокси}-7-метокси-2,3-дигідроімідазо[1,2с]хіназолін-5-іл)нікотинамід; N-(8-{2-[4-(циклобутилметил) морфолін-2іл]етокси}-7-метокси-2,3-дигідроімідазо[1,2с]хіназолін-5-іл)нікотинамід; N-(7-метокси-8-{2-[4-(2-метоксиетил) морфолін-2-іл]етокси}-2,3-дигідроімідазо[1,2-с]хіназолін5-іл)нікотинамід; N-{8-[(4-етилморфолін-2-іл)метокси]-7метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}нікотинамід; 96965 22 N-(7-метокси-8-{[4-(2-метоксиетил)морфолін-2іл]метокси}-2,3-дигідроімідазо[1,2-с]хіназолін-5іл)нікотинамід; N-{7-метокси-8-[(4-метилморфолін-2іл)метокси]-2,3-дигідроімідазо[1,2-с]хіназолін-5іл}нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]піримідин-4карбоксамід; 2-аміно-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]піримідин-4-карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-1-метил-1Німідазол-4-карбоксамід; рел-(8-{3-[(2R,6S)-2,6-диметилморфолін-4іл]пропокси}-7-метокси-2,3-дигідроімідазо[1,2с]хіназолін-5-іл)піримідин-5-карбоксамід; рел-(8-{3-[(2R,6S)-2,6-диметилморфолін-4іл]пропокси}-7-метокси-2,3-дигідроімідазо[1,2с]хіназолін-5-іл)-6-метилнікотинамід; рел-6-ацетамидо-N-(8-{3-[(2R,6S)-2,6диметилморфолін-4-іл]пропокси}-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл)нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-1-метил-1Німідазол-5-карбоксамід; 6-аміно-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]2-метилнікотинамід; 2-аміно-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]4-метилпіримідин-5-карбоксамід; 6-аміно-5-бромо-N-[7-метокси-8-(3-морфолін4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]нікотинамід; 2-аміно-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]1,3 -оксазол-5-карбоксамід; N-[7-метокси-8-(морфолін-2-ілметокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; 2-{[2-(диметиламіно)етил]аміно}-N-{8-[3(диметиламіно)пропокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}-піримідин-5карбоксамід; 2-аміно-N-{8-[3-(диметиламіно)пропокси]-7метокси-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-1,3тіазол-5-карбоксамід; рел-2-аміно-N-(8-{3-[(2R,6S)-2,6диметилморфолін-4-іл]пропокси}-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл)піримідин-5карбоксамід; рел-6-аміно-N-(8-{3-[(2R,6S)-2,6диметилморфолін-4-іл]пропокси}-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл)-нікотинамід; 2-[(2-гідроксиетил)аміно]-N-[7-метокси-8-(3морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл] піримідин-5-карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2-[(3метоксипропіл)аміно]піримідин-5-карбоксамід; 2-аміно-N-{8-[3-(диметиламіно)пропокси]-7метокси-2,3-дигідроімідазо [1,2-с]хіназолін-5-іл}піримідин-5-карбоксамід; 23 N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2-[(3-морфолін4-ілпропіл)аміно]піримідин-5-карбоксамід; 2-[(2-метоксиетил)аміно]-N-[7-метокси-8-(3морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]піримідин-5-карбоксамід; 2-{[2-(диметиламіно)етил]аміно}-N-[7-метокси8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]піримідин-5карбоксамід; 6-аміно-N-{8-[3-(диметиламіно)пропокси]-7метокси-2,3-дигідроімідазо [1,2-с]хіназолін-5-іл}нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2-піролідин-1ілпіримідин-5-карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2-(4метилпиперазин-1-іл)піримідин-5-карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2-морфолін-4ілпіримідин-5-карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6-пиперазин-1ілнікотинаміду гідрохлорид; 6-[(3S)-3-амінопіролідин-1-іл]-N-[7-метокси-8(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинаміду гідрохлориду гідрат; 6-[(3R)-3-амінопіролідин-1-іл]-N-[7-метокси-8(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинаміду гідрохлорид; 6-[(4-фторобензил)аміно]-N-[7-метокси-8-(3морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинамід; 6-[(2-фурилметил) аміно]-N-[7-метокси-8-(3морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинамід; 6-[(2-метоксиетил) аміно]-N-[7-метокси-8-(3морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6-(1Ζ-пірол-1іл)нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6-морфолін-4ілнікотинамід; N-{7-метокси-8-[3-(метиламіно)пропокси]-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}нікотинамід; 6-[(2,2-диметилпропаноїл)аміно]-N-[7-метокси8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; 6-[(циклопропілкарбоніл)аміно]-N-[7-метокси-8(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6-(2,2,2трифтороетокси)нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6(трифторометил)нікотинамід; 6-(ізобутириламіно)-N-[7-метокси-8-(3морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинамід; 96965 24 N-{7-метокси-8-[3-(4-метилпиперазин-1іл)пропокси]-2,3-дигідроімідазо[1,2-с]хіназолін-5іл}-нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2{[(метиламіно)карбоніл]аміно}-1,3-тіазол-4карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6{[(метиламіно)карбоніл]аміно}нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2-(метиламіно)1,3-тіазол-4-карбоксамід; N-[7-метокси-8-(2-морфолін-4-ілетокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}-2,4-диметил1,3-тіазол-5-карбоксамід; N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}-6метилнікотинамід; 6-{[(ізопропіламіно)карбоніл]аміно}-N-[7метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6-піролідин-1ілнікотинамід; 6-(диметиламіно)-N-[7-метокси-8-(3-морфолін4-ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]нікотинамід; N-[7-метокси-8-(3-піперидин-1-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; N-[7-метокси-8-(2-піролідин-1-ілетокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; N-[7-метокси-8-(2-піперидин-1-ілетокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; 6-{[(етиламіно)карбоніл]аміно}-N-[7-метокси-8(3-морфолін-4-ілпропокси)-2,3-дигідроімідазо[1,2с]хіназолін-5-іл]нікотинамід; 6-фтор-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]нікотинамід; 2-аміно-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]1,3-оксазол-4-карбоксамід; 2-(етиламіно)-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]1,3-тіазол-4-карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]піразин-2карбоксамід; N-[8-(2-аміноетокси)-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; 6-аміно-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-ізонікотинамід; N-{8-[3-(діетиламіно)пропокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}нікотинамід; N-{8-[2-(діізопропіламіно)етокси]-7-метокси2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід; N-{8-[2-(діетиламіно)етокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід; 25 Ν-{8-[3-(диметиламіно)пропокси]-7-метокси2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід; N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл} нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2(метиламіно)піримідин-5-карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2-(метилтіо)піримідин-5-карбоксамід; N-[8-(3-амінопропокси)-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинаміду трифторацетат; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]тіофен-2карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2,4-диметил1,3-тіазол-5-карбоксамід; 2-метокси-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]піримідин-5-карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-3-фурамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]тіофен-3карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2-метил-1,3тіазол-4-карбоксамід; 6-мeтокси-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]нікотинамід; 5-метокси-Н-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3Дигідроімідазо[1,2-с]хіназолін-5-іл]-6метилнікотинамід; 6-(ацетиламіно)-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; або її фізіологічно прийнятну сіль, сольват, гідрат або стереоізомер. В кращому варіанті здійснення винахід охоплює сполуку, що має формулу: N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-6метилнікотинамід; 5-метокси-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]-2,4-диметил1,3-тіазол-5-карбоксамід; N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід; N-{8-[3-(диметиламіно)пропокси]-7-метокси2,3-дигідроімідазо[1,2-с]хіназолін-5-іл}-нікотинамід; 96965 26 6-{[(ізопропіламіно)карбоніл]аміно}-N-[7метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл}-2,4-диметил1,3-тіазол-5-карбоксамід; N-[7-метокси-8-(2-морфолін-4-ілетокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]нікотинамід; рел-6-аміно-N-(8-{3-[(2R,6S)-2,6диметилморфолін-4-іл]пропокси}-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл)нікотинамід; рел-2-аміно-N-(8-{3-[(2R,6S)-2,6диметилморфолін-4-іл]пропокси}-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл)піримідин-5карбоксамід; 2-аміно-N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5іл]піримідин-5-карбоксамід; N-{8-[2-(диметиламіно)етокси]-7-метокси-2,3дигідроімідазо[1,2-с]хіназолін-5-іл} піримідин-5карбоксамід; N-[7-метокси-8-(3-морфолін-4-ілпропокси)-2,3дигідроімідазо[1,2-с]хіназолін-5-іл]піримідин-5карбоксамід; або її фізіологічно прийнятну сіль, сольват, гідрат або стереоізомер. У випадку якщо існує невідповідність між хімічною назвою та зображеною хімічною структурою, зображена хімічна структура має пріоритет перед даною хімічною назвою. Не обмежуючись теорією або механізмом, сполуки існуючого винаходу демонструють несподівану активність для інгібування фосфатидилінозитол-3-кінази та хімічну й структурну стабільність у порівнянню з такими сполуками з попереднього рівня техніки. Вважається, що ця несподівану активність основана на хімічній структурі сполук, особливо основності сполук у результаті того, що 1 5 5' R є аміном, необов'язково заміщеним R та R . 3 2 Далі, відповідний вибір R та R забезпечує необхідну активність проти відповідних ізоформ, щоб надати активність in vivo. Визначення Термін 'алкіл' стосується радикалу нерозгалуженого або розгалуженого вуглеводневого ланцюга, що складається винятково з вуглецевих і водневих атомів, що містить винятково вуглецеві та водневі атоми, що не містить ненасиченості, що має від одного до восьми вуглецевих атомів, і який приєднаний до іншої частини молекули одинарним зв'язком, такого як ілюстративно, метил, етил, нпропіл, 1-метилетил (ізопропіл), н-бутил, н-пентил та 1,1-диметилетил (т-бутил). Термін "алкеніл" стосується аліфатичної вуглеводневої групи, що містить подвійний зв'язок вуглець-вуглець та яка може являти собою нерозгалужений або розгалужений ланцюг, що має приблизно від 2 приблизно до 10 вуглецевих атомів, наприклад, етеніл, 1-пропеніл, 2-пропеніл (аліл), ізопропеніл, 2-метил-1-пропеніл, 1-бутеніл, і 2бутеніл. Термін "алкініл" стосується гідрокарбонільних радикалів з нерозгалуженим або розгалуженим ланцюгом, що мають принаймні один потрійний зв'язок вуглець-вуглець, і, що мають у діапазоні приблизно від 2 до 12 вуглецевих атомів (при цьо 27 му на даний момент кращими є радикали, що мають у діапазоні приблизно від 2 до 10 вуглецевих атомів) наприклад, етиніл. Термін "алкокси" позначає алкільну групу, визначену авторами, приєднану через кисневий зв'язок до іншої частини молекули. Характерні приклади цих груп - метокси та етокси групи. Термін "алкоксиалкіл" позначає алкокси-групу, визначену авторами, приєднану через кисневий зв'язок до алкільної групи, що потім приєднується до головної структури на будь-якому вуглеці з алкільної групи, що приводить до створення стійкої іншої частини структури молекули. Характерні приклади таких груп -СН2ОСН3, -CH2OC2H5. Термін "циклоалкіл" позначає неароматичну моно- або поліциклічну кільцеву систему, що складається приблизно з 3 - 12 вуглецевих атомів, таку як циклопропіл, циклобутил, циклопентил, циклогексил, і приклади поліциклічних циклоалкільних груп включають пергідронафтилову, адамантилову та норборнілову групи, з'єднані містками циклічні групи або спіробіциклічні групи, наприклад, спіро (4,4) нон-2-іл. Термін "циклоалкілалкіл" стосується радикалів, що мають циклічне кільце, що містять у діапазоні приблизно від 3 до 8 вуглецевих атомів, безпосередньо приєднаних до алкільної групи, що потім також приєднується до головної структури на будь-якому вуглеці з алкільної групи, що приводить до створення стійкої структури, такої як циклопропілметил, циклобутилетил, циклопентилетил. Термін "арил" стосується ароматичних радикалів, що мають у діапазоні від 6 до 14 вуглецевих атомів, таких як феніл, нафтил, тетрагідронафтил, інданіл, біфеніл. Термін "арилалкіл" стосується арильної групи, визначеної авторами, безпосередньо зв'язаної з алкільною групою, визначеною авторами, що потім приєднується до головної структури на будь-якому вуглеці з алкільної групи, що приводить до створення стійкої іншої частини структури молекули, наприклад, -СН2С6Н5, -С2Н5С6Н5. Термін "гетероциклічне кільце" стосується радикалу зі стійкого 3 - 15-членного кільця, що складається з вуглецевих атомів і від одного до п'яти гетероатомів, вибраних із групи, що складається з азоту, фосфору, кисню та сірки. Для цілей цього винаходу радикал гетероциклічного кільця може являти собою моноциклічну, біциклічну або трициклічну кільцеву систему, що може включати сконденсовані, з'єднані містками або спіро кільцеві системи, та атоми азоту, фосфору, вуглецю, кисню або сірки в радикалі гетероциклічного кільця можуть бути необов'язково окислені до різних станів окислювання. Крім того, атом азоту може бути необов'язково четвертинним; і кільцевий радикал може бути частково або повністю насиченим (тобто, гетероароматичним або гетероарильним ароматичним). Приклади таких радикалів гетероциклічного кільця включають, крім інших, азетидиніл, акридиніл, бензодіоксоліл, бензодіоксаніл, бензофурніл, карбазоліл циннолініл діоксоланіл, індолізиніл, нафтиридиніл, пергідроазериніл, феназиніл, фенотіазиніл, феноксазиніл, фталазил, піридил, 96965 28 птеридиніл, пуриніл, хіназолініл, хіноксалініл, хінолініл, ізохінолініл, тетразоїл, імідазоліл тетрагідроізоуіноліл, піперидиніл, піперазиніл, 2оксопіперазиніл, 2-оксопіперидиніл, 2оксопіролідиніл, 2-оксоазериніл, азериніл, піроліл, 4-піперидоніл, піролідиніл, піразиніл, піримідиніл піридазиніл, оксазоліл оксазолініл оксазолідиніл, триазоліл, інданіл, ізоксазоліл, ізоксазолідиніл, морфолініл, тіазоліл, тіазолініл, тіазолідиніл, ізотіазоліл, хінуклідиніл, ізотіазолідиніл, індоліл, ізоіндоліл, індолініл, ізоіндолініл, октагідроіндоліл, октагідроізоіндоліл хіноліл, ізохіноліл, декагідроізохіноліл, бензімідазоліл, тіадіазоліл, бензопіраніл, бензотіазоліл, бензооксазоліл, фурил, тетрагідрофуртил, тетрагідропіраніл, тієніл, бензотієніл, тіаморфолініл, тіаморфолініл сульфоксид тіаморфолініл сульфон, діоксафосфоланіл, оксадіазоліл, хроманіл, ізохроманіл. Термін "гетероарил" стосується радикала гетероциклічного кільця, визначеного авторами, що є ароматичним. Радикал гетероарильного кільця може бути приєднаний до головної структури на будь-якому гетероатомі або вуглецевому атомі, що приводить до створення стійкої структури. Радикал гетероциклічного кільця може бути приєднаний до головної структури на будь-якому гетероатомі або вуглецевому атомі, що приводить до створення стійкої структури. Термін "гетероарилалкіл" стосується радикала гетероарильного кільця, визначеного авторами, безпосередньо пов'язаного з алкільною групою. Гетероарилалкільний радикал може бути приєднаний до головної структури на будь-якому вуглецевому атомі з алкільної групи, що приводить до створення стійкої структури. Термін "гетероцикліл" стосується радикала гетероциклічного кільця, визначеного авторами. Радикал гетероциклічного кільця може бути приєднаний до головної структури на будь-якому гетероатомі або вуглецевому атомі, що приводить до створення стійкої структури. Термін "гетероциклілалкіл" стосується радикала гетероциклічного кільця, визначеного авторами, безпосередньо пов'язаного з алкільною групою. Гетероциклілалкільний радикал може бути приєднаний до головної структури на вуглецевому атомі в алкільній групі, що приводить до створення стійкої структури. Термін "карбоніл" стосується кисневого атома пов'язаного з вуглецевим атомом молекули подвійним зв'язком. Термін "галоген" стосується радикалів фтору, хлору, брому та йоду. При використанні авторами форми множини слів сполуки, солі, поліморфи, гідрати, сольвати й т. п.,, це також означає окрему сполуку, сіль, поліморф, ізомер, гідрат, сольват або подібне. Сполуки цього винаходу можуть містити один або кілька асиметричних центрів, залежно від положення та природи різних бажаних замісників. Асиметричні вуглецеві атоми можуть бути присутніми в (R) або (S) конфігурації, що приводить до утворення рацемічних сумішей у випадку єдиного асиметричного центру та діастереомерних сумішей у випадку багатьох асиметричних центрів. У 29 певних випадках асиметрія може також бути присутньою через обмежене обертання навколо даного зв'язку, наприклад, центрального зв'язку, пов'язаного із двома заміщеними ароматичними кільцями зазначених сполук. Замісники на кільці можуть також бути присутніми або в цис- або в транс- формі. Вважається, що всі такі конфігурації (включаючи енантіомери та діастереомери), включені в рамки існуючого винаходу. Кращі сполуки ті, які демонструють більш бажану біологічну активність. Відділені, чисті або частково очищені ізомери та стереоізомери або рацемічні або діастереомерні суміші сполук цього винаходу також включені в рамки існуючого винаходу. Очищення та розділення таких матеріалів можуть бути досягнуті стандартними методами, відомими в даній галузі техніки. Існуючий винахід також стосується корисних форм сполук, розкритих авторами, таких як фармацевтично прийнятні солі, ко-преципітати, метаболіти, гідрати, сольвати та проліки всіх сполук із прикладів. Термін "фармацевтично прийнятна сіль" відноситься до нетоксичної адитивної солі неорганічної або органічної кислоти та сполуки існуючого винаходу. Наприклад, див. S. М. Berge, et al. "Pharmaceutical Salts," J. Pharm. Sci. 1977, 66, 1-19. Фармацевтично прийнятні солі включають отримані шляхом реакції головної сполуки, що функціонує як основа, з неорганічною або органічною кислотою для утворення солі, наприклад, солі соляної кислоти, сірчаної кислоти, фосфорної кислоти, метансульфонової кислоти, камфорсульфонової кислоти, щавлевої кислоти, малеїнової кислоти, бурштинової кислоти та лимонної кислоти. Фармацевтично прийнятні солі також включають ті, у яких головна сполука функціонує як кислота та реагує з відповідною основою для утворення, наприклад, солі натрію, калію, кальцію, магнію, амонію та хлорину. Кваліфіковані фахівці в даній галузі далі визнають, що кислотні адитивні солі зазначених у формулі сполук можуть бути отримані шляхом реакції сполук із відповідною неорганічною або органічною кислотою за допомогою будьякого з багатьох відомих методів. Альтернативно, солі лужних і лужноземельних металів кислотних сполук винаходу одержують шляхом реакції сполук винаходу з відповідною основою за допомогою багатьох відомих методів. Характерні солі сполук цього винаходу включають звичайні нетоксичні солі та солі четвертинного амонію, які утворені, наприклад, з неорганічних або органічних кислот або основ способами, відомими в даній галузі. Наприклад, такі кислотні адитивні солі включають ацетат, адипат, альгінат, аскорбат, аспартат, бензоат, бензолсульфонат, бісульфат, бутират, цитрат, камфорат, камфорсульфонат, цинамат, циклопентанпропіонат, диглюконат, додецилсульфат, етансульфонат, фумарат, глюкогептаноат, гліцерофосфат, гемісульфат, гептаноат, гексаноат, хлорид, бромід, йодид, 2гідроксиетансульфонат, ітаконат, лактат, малеат, манделат, метансульфонат, 2нафталенсульфонат, нікотинат, нітрат, оксалат, памоат, пектинат, персульфат, 3-фенілпропіонат, пікрат, півалат, пропіонат, сукцинат, сульфонат, 96965 30 сульфат, тартрат, тіоціанат, тозилат та ундеканоат. Основні солі включають солі лужних металів, такі як солі калію та натрію, солі лужноземельних металів, такі як солі кальцію та магнію, та солі амонію з органічними основами, такими як дициклогексиламін та N-метил-D-глюкамін. Крім того, основні азот-вмісні групи можуть бути перетворені в четвертинні за допомогою таких агентів як нижчі алкілгаліди, такі як метил-, етил-, пропіл- або бутилхлориди, броміди та йодиди; діалкілсульфати, такі як диметил-, діетил-, дибутилсульфат або діамілсульфати, довголанцюгові галіди, такі як децил-, лаурил-, міристил- і стеарилхлориди, броміди та йодиди, аралкілгаліди, такі як бензил- і фенетилброміди та інші. Сольват для цілей цього винаходу являє собою комплекс розчинника та сполуки винаходу у твердому стані. Характерні сольвати включали б, крім інших, комплекси сполуки винаходу з етанолом або метанолом. Гідрати являють собою специфічну форму сольвату, у якому розчинником є вода. Фармацевтичні композиції сполук винаходу Цей винахід також стосується фармацевтичних композицій, що містять одну або кілька сполук існуючого винаходу. Ці композиції можуть бути використані для досягнення бажаного фармакологічного ефекту шляхом введення пацієнтові, що має потребу в цьому. Пацієнт, для цілей цього винаходу, є ссавцем, включаючи людину, що має потребу в лікуванні специфічного стану або хвороби. Тому, існуючий винахід включає фармацевтичні композиції, які складаються з фармацевтично прийнятного носія та фармацевтично ефективної кількості сполуки або її солі існуючого винаходу. Фармацевтично прийнятний носій - переважно носій, що відносно нетоксичний та нешкідливий для пацієнта при концентраціях, сумісних з ефективною активністю активного компонента таким чином, щоб будь-які побічні ефекти, приписувані носію, не спотворювали сприятливі впливи активного компонента. Фармацевтично ефективна кількість сполуки переважно являє собою ту кількість, що приведе до результату або робить вплив на специфічний стан, що піддається лікуванню. Сполуки існуючого винаходу можна вводити з фармацевтично прийнятними носіями, відомими в даній галузі, використовуючи будь-які ефективні звичайні форми дозування, включаючи препарати з негайним, уповільненим та відстроченим вивільненням, перорально, парентерально, місцево, назально, офтальмічно, оптично, сублінгвально, ректально, вагінально й т. п.. Для перорального введення сполуки можуть бути сформульовані у тверді або рідкі препарати, такі як капсули, пігулки, таблетки, льодяники, пастилки, порошки, розчини, суспензії або емульсії, і можуть бути підготовлені відповідно до методів, відомих у даній галузі для одержання фармацевтичних композицій. Тверді дозовані форми можуть являти собою капсулу, що може бути стандартного желатинового типу із твердою або м'якою оболонкою, що містить, наприклад, сурфактанти, любриканти та інертні наповнювачі, такі як лактоза, са 31 хароза, фосфат кальцію та кукурудзяний крохмаль. В іншому варіанті здійснення сполуки цього винаходу можуть бути таблетовані зі звичайними таблетковими основами, такими як лактоза, сахароза та кукурудзяний крохмаль у комбінації з сполучними речовинами, такими як акація, кукурудзяний крохмаль або желатин, дезінтегруючими агентами, призначеними для того, щоб сприяти розпаду та розчиненню таблетки після введення, такими як картопляний крохмаль, альгінова кислота, кукурудзяний крохмаль і гуарова смола, трагакантова камедь, акація, любрикантами, призначеними для поліпшення текучості при гранулюванні таблеток і для запобігання прилипання таблеткового матеріалу на поверхню таблеткового пресу та пуансонів, наприклад, тальк, стеаринова кислота або магнію, кальцію або цинку стеарат, барвниками, забарвлюючими агентами та ароматизуючими агентами, такими як м'ята, масло гаультерії або ароматизатор «вишня», призначеними для підвищення естетичних якостей таблеток та, щоб зробити їх більш прийнятними для пацієнта. Підходящі допоміжні речовини для використання в пероральних рідких дозованих формах включають дикальцію фосфат і розріджувачі, такі як вода та спирти, наприклад, етанол, бензиловий спирт та поліетиленспирти, або з додаванням фармацевтично прийнятного сурфактанта, суспендуючого агента або емульгуючого агента або без них. Різні інші матеріали можуть бути присутніми як оболонки або для модифікації іншим способом фізичної форми одиниці дозування. Наприклад, таблетки, пігулки або капсули можуть бути покриті шелаком, цукром або і тим, і іншим. Диспергуємі порошки та гранули підходять для підготовки водної суспензії. Вони забезпечують активний компонент у суміші з диспергуючим або змочувальним агентом, суспендуючим агентом та одним або декількома консервантами. Підходящі диспергуючі або змочувальні агенти та суспендуючі агентів ілюструються вже згаданими вище. Можуть також бути присутніми додаткові допоміжні речовини, наприклад, підсолоджуючі, ароматизуючі та забарвлюючі агенти, описані вище. Фармацевтичні композиції цього винаходу можуть також бути у вигляді емульсій масло у воді. Масляна фаза може являти собою рослинне масло, таке як рідкий парафін або суміш рослинних масел. Підходящі емульгуючі агенти можуть являти собою (1) природні смоли, такі як смола акації та трагакантова камедь, (2) природні фосфатиди, такі як соєві боби та лецитин, (3) естери або часткові естери отримані з жирних кислот і гекситол ангідридів, наприклад, сорбітан моноолеат, (4) продукти конденсації зазначених часткових естерів з етиленоксидом, наприклад, поліоксиетиленсорбітан моноолеат. Емульсії можуть також містити підсолоджуючі та ароматизуючі агенти. Масляні суспензії можуть бути сформульовані шляхом суспендування активного компонента в рослинному маслі, такому як, наприклад, арахісове масло, маслинове масло, сезамове масло або кокосове масло, або в мінеральному маслі, такому як рідкий парафін. Масляні суспензії можуть місти 96965 32 ти згущувач, такий як, наприклад, віск, твердий парафін або цетиловий спирт. Суспензії можуть також містити один або кілька консервантів, наприклад, етил або н-пропіл п-гідроксибензоат; один або декілька забарвлюючих агентів; один або кілька ароматичних агентів; та один або кілька підсолоджуючих агентів, таких як сахароза або сахарин. Сиропи та еліксири можуть бути сформульовані за допомогою підсолоджуючих агентів, таких як, наприклад, гліцерин, пропіленгліколь, сорбіт або сахароза. Такі формулювання можуть також містити заспокійливий засіб, та консервант, такий як метил- і пропілпарабени та ароматизуючі та забарвлюючі агенти. Сполуки цього винаходу можна також вводити парентерально, тобто, підшкірно, внутрівенно, інтраокулярно, інтрасиновіально, внутрішньом'язово або інтраперітонеально, у вигляді ін'єкційних дозувань сполуки в переважно фізіологічно прийнятному розріджувачі з фармацевтичним носієм, що може являти собою стерильну рідину або суміш рідин, таких як вода, фізіологічний розчин, водні розчини декстрози та родинних цукрів, спирт, такий як етанол, ізопропіловий спирт або гексадециловий спирт, гліколі, такі як пропіленгліколь або поліетиленгліколь, гліцеринкеталі, такі як 2,2-диметил-1,1-діоксолан-4-метанол, етери, такі як полі(етиленгліколь) 400, масло, жирна кислота, естер жирної кислоти або гліцерид жирної кислоти, або ацетильований гліцерид жирної кислоти з додаванням фармацевтично прийнятного сурфактанта, такого як мило або детергент, суспендуючого агента, такого як пектин, карбомери, метилцелюлоза, гідроксипропілметилцелюлоза, або карбоксиметилцелюлоза, або емульгуючий агент та інші фармацевтичні ад'юванти або без них. Приклади масел, які можуть використовуватися в парентеральних формулюваннях цього винаходу, включають масла з нафти, тваринного, рослинного або синтетичного походження, наприклад, арахісове масло, соєве масло, сезамове масло, бавовняне масло, кукурудзяне масло, маслинове масло, вазелін і мінеральне масло. Підходящі жирні кислоти включають олеїнову кислоту, стеаринову кислоту, ізостеаринову кислоту та міристинову кислоту. Підходящі естери жирної кислоти включають, наприклад, етилолеат та ізопропілміристат. Підходящі мила включають солі жирної кислоти та лужного металу, амонію та триетаноламіну та підходящі детергенти включають катіоноактивні детергенти, наприклад, диметилдіалкіламонію галіди, алкілпіридинію галіди, і алкіламінацетати; аніонні детергенти, наприклад, алкіл-, арил- і олефінсульфонати, алкіл-, олефін-, етер- та моногліцеридсульфати та сульфосукцинати; неіонні детергенти, наприклад, оксиди жирних амінів, алканоламіди жирних кислот, та поли(оксиетилен-оксипропілен)и або кополімери етиленоксиду або пропіленоксиду; та амфотерні детергенти, наприклад, алкіл-бетаамінопропіонати та четвертинні амонієві солі 2алкілімідазоліну, а також суміші. Парентеральні композиції цього винаходу будуть типово містити приблизно від 0,5 % приблиз 33 но до 25 % по масі активного компонента в розчині. Консерванти та буфери можуть також корисно використовуватися. Щоб мінімізувати або усунути подразнення в місці ін'єкції, такі композиції можуть містити неіонний сурфактант, що має гідрофільноліпофильну рівновагу (HLB) переважно від приблизно 12 до приблизно 17. Кількість сурфактанту в такому формулюванні переважно коливається приблизно від 5 % приблизно до 15 % по масі. Сурфактант може бути одним компонентом, що має вищезгадану HLB, або може являти собою суміш двох або більше компонентів, що мають бажану HLB. Приклад сурфактантів, використовуваних у парентеральних формулюваннях, включає клас естерів поліетиленсорбітану та жирної кислоти, наприклад, сорбітанмоноолеат та високомолекулярні адукти етиленооксиду з гідрофобною основою, сформовані конденсацією пропіленоксиду із пропіленгліколем. Фармацевтичні композиції можуть бути у вигляді стерильних ін'єкційних водних суспензій. Такі суспензії можуть бути сформульовані відповідно до відомих методів з використанням підходящих диспергуючих або змочувальних агентів та суспендуючих агентів, таких як, наприклад, натрій карбоксиметилцелюлоза, метилцелюлоза, гідроксипропілметил-целюлоза, натрію альгінат, полівінілпіролідон, трагакантова камедь та акацієва смола; диспергуючих або змочувальних агентів, які можуть являти собою природний фосфатид, такий як лецитин, продукт конденсації алкіленоксиду з жирною кислотою, наприклад, поліоксиетиленстеарат, продукт конденсації етиленоксиду із довголанцюговим аліфатичним спиртом, наприклад, гептадека-етиленоксицетанол, продукт конденсації етиленоксиду із частковим естером, отриманим з жирної кислоти та гекситолу, такий як поліоксиетиленсорбітолмоноолеат, або продукт конденсації етиленоксиду із частковим естером, отриманим з жирної кислоти та гекситолангідриду, наприклад, поліоксиетиленсорбітанмоноолеат. Стерильний ін'єкційний препарат може також являти собою стерильний ін'єкційний розчин або суспензію в нетоксичному парентерально прийнятному розріджувачі або розчиннику. Розріджувачі та розчинники, які можуть використовуватися, включають, наприклад, воду, розчин Рінгера, ізотонічні розчини натрію хлориду та ізотонічні розчини глюкози. Крім того, стерильні фіксовані масла традиційно використовуються як суспендуючі середовища або розчинники. Із цією метою, може використовуватися будь-яке м'яке, жирне масло, включаючи синтетичні моно- або дигліцериди. Крім того, у одержанні ін'єкцій можуть використовуватися жирні кислоти, такі як олеїнова кислота. Композицію винаходу можна також вводити у вигляді супозиторіїв для ректального введення активної речовини. Ці композиції можуть бути підготовлені шляхом змішування активної речовини з підходящою неподразнюючою допоміжною речовиною, що є твердою за звичайних температур, але стає рідкою при ректальній температурі і тому буде танути в прямій кишці для вивільнення акти 96965 34 вної речовини. Такі матеріали включають, наприклад, масло какао та поліетиленгліколь. Інше формулювання, використовуване в методах існуючого винаходу, використовує пристрої трансдермальної доставки ("пластири"). Такі трансдермальні пластири можуть використовуватися для забезпечення безперервної або переривчастої інфузії сполук існуючого винаходу в контрольованій кількості. Конструкція та використання трансдермальних пластирів для доставки фармацевтичних агентів відомі в даній галузі (див., наприклад, патент США № 5 023 252, опублікований 11 червня 1991 p., включений авторами шляхом посилання). Такі пластири можуть бути сконструйовані для безперервної, періодичної доставки або доставки на вимогу фармацевтичних агентів. Формулювання з контрольованим вивільненням для парентерального введення включають ліпосомальну, полімерну мікросферу та полімерні гелеві формулювання, які відомі в даній галузі. Може бути бажано або необхідно вводити фармацевтичну композицію пацієнтові через механічний пристрій доставки. Конструкція та використання механічних пристроїв доставки для доставки фармацевтичних агентів відомі в даній галузі. Прямі методи, наприклад, для введення активної речовини безпосередньо в головний мозок звичайно залучають розміщення катетера для доставки препарату в систему шлуночків пацієнта, щоб обійти гемоенцефалічний бар'єр. Одна така система доставки, яка імплантується, яку використовують для транспорту агентів у певні анатомічні ділянки організму, описана в патенті США № 5 011 472, опублікованому 30 квітня 1991 р. Композиції даного винаходу можуть також містити інші звичайні фармацевтично прийнятні компоненти, у загальному позначувані як носії або розріджувачі, по мірі необхідності або за бажанням. Можуть використовуватися звичайні процедури для підготовки таких композицій у відповідних дозуємих формах. Такі компоненти та процедури включають описані в наступних посиланнях, кожне з яких включене авторами шляхом посилання: Powell, M.F. et al., "Compendium of Excipients for Parenteral Formulations" PDA Journal of Pharmaceutical Science & Technology 1998, 52(5), 238-311; Strickley, R.G "Parenteral Formulations of Small Molecule Therapeutics Marketed in the United States (1999)- Part-1" PDA Journal of Pharmaceutical Science & Technology 1999, 53 (6), 324-349; та Nema, S. et al., "Excipients and Their Use in Injectable Products" PDA Journal of Pharmaceutical Science & Technology 1997, 51 (4), 166-171. Звичайно використовувані фармацевтичні компоненти, які можуть використовуватися як відповідні для формулювання композиції для її наміченого шляху введення, включають: підкислюючі агенти (приклади включають, крім інших, оцтову кислоту, лимонну кислоту, фумарову кислоту, соляну кислоту, азотну кислоту); підлужуючі агенти (приклади включають, крім інших, розчин амонію, карбонат амонію, діетаноламін, моноетаноламін, гідрооксид калію, борат натрію, карбонат натрію, гідроксид натрію, триетаноламін, троламін); 35 адсорбенти (приклади включають, крім інших, порошкоподібну целюлозу та активоване деревне вугілля); аерозольні пропеленти (приклади включають, крім інших, вуглекислий газ, CCI2F2, F2CIC-ССl2 та ССІ3), агенти для витиснення повітря (приклади включають, крім інших, азот та аргон); протигрибкові консерванти (приклади включають, крім інших, бензойну кислоту, бутилпарабен, етилпарабен, метилпарабен, пропілпарабен, бензоат натрію); антибактеріальні консерванти (приклади включають, крім інших, бензалконію хлорид, бензетонію хлорид, спирт бензиловий, цетилпіридинію хлорид, хлоробутанол, фенол, фенілетиловий спирт, фенілмеркурію нітрат та тимерозал); антиоксиданти (приклади включають, крім інших, аскорбінову кислоту, аскорбіл пальмітат, бутильований гідроксианізол, бутильований гідрокситолуол, гіпофосфорну кислоту, монотіогліцерин, пропілгалат, аскорбат натрію, бісульфіт натрію, сульфоксилат формальдегід натрію, метабісульфіт натрію); сполучні матеріали (приклади включають, крім інших, блоккополімери, природний та синтетичний каучук, поліакрилати, поліуретани, силікони, полісилоксани та кополімери бутадієнстиролу); буферні агенти (приклади включають, крім інших, калію метафосфат, дикалію фосфат, натрію ацетат, безводний натрію цитрат і дигідрат натрію цитрату), агенти-носії (приклади включають, крім інших, акацієвий сироп, ароматичний сироп, ароматичний еліксир, вишневий сироп, сироп какао, апельсиновий сироп, сироп, кукурудзяне масло, мінеральне масло, арахісове масло, сезамове масло, бактеріостатичний натрію хлорид для ін'єкцій та бактеріостатичну воду для ін'єкції), хелатуючі агенти (приклади включають, крім інших, динатрію едетат та едетову кислоту), барвники (приклади включають, крім інших, FD&C Червоний № 3, FD&C Червоний № 20, FD&C Жовтий № 6, FD&C Синій № 2, D&C Зелений № 5, D&C Помаранчевий № 5, D&C Червоний № 8, карамель та оксид заліза червоний); агенти, що освітлюють (приклади включають, крім інших, бентоніт); емульгуючі агенти (приклади включають, крім інших, акацію, цетомакрогол, цетиловий спирт, гліцерилмоностеарат, лецитин, сорбітанмоноолеат, поліоксиетилен 50 моностеарат); інкапсулюючі агенти (приклади включають, крім інших, желатин і целюлози ацетат фталат), ароматизатори (приклади включають, крім інших, анісове масло, коричне масло, какао, ментол, апельсинове масло, масло м'яти та ванілін); гігроскопічні речовини (приклади включають, крім інших, гліцерин, пропіленгліколь та сорбіт); відмучуючі агенти (приклади включають, крім інших, мінеральне масло та гліцерин); масла (приклади включають, крім інших, арахісове масло, мінеральне масло, маслинове масло, арахісове масло, сезамове масло та рослинне масло); 96965 36 основи мазей (приклади включають, крім інших, ланолін, гідрофільну мазь, поліетиленгліколеву мазь, ванілін, м'який гідрофільний ванілін, білу мазь, жовту мазь та мазь із трояндовою водою); посилюючі проникність агенти (трансдермальна доставка) (приклади включають, крім інших, моногідрокси- або полігідроксиспирти, моно- або полівалентні спирти, насичені або ненасичені жирні спирти, насичені або ненасичені жирні естери, насичені або ненасичені дикарбонові кислоти, ефірні масла, фосфатидил похідні, цефалін, терпени, аміди, ефіри, кетони та сечовини), пластифікатори (приклади включають, крім інших, діетилфталат та гліцерин); розчинники (приклади включають, крім інших, етанол, кукурудзяне масло, бавовняне масло, гліцерин, ізопропіловий спирт, мінеральне масло, олеїнову кислоту, арахісове масло, очищену воду, воду для ін'єкцій, стерильну воду для ін'єкцій та стерильну воду для іригацій); посилюючі твердість агенти (приклади включають, крім інших, цетиловий спирт, цетилові естери, віск, мікрокристалічний віск, парафін, стеариловий спирт, білий віск та жовтий віск); основи супозиторіїв (приклади включають, крім інших, масло какао та поліетиленгліколі (суміші)); сурфактанти (приклади включають, крім інших, бензалконію хлорид, ноноксинол 10, октоксинол 9, полісорбат 80, натрію лаурилсульфат і сорбітанмонопальмітат); суспендуючі агенти (приклади включають, крім інших, агар, бентоніт, карбомери, натрій карбоксиметилцелюлозу, гідроксиетилцелюлозу, гідроксипропілцелюлозу, гідроксипропілметилцелюлозу, каолін, метилцелюлозу, трагакант та вігум); підсолоджуючі агенти (приклади включають, крім інших, аспартам, декстрозу, гліцерин, маніт, пропіленгліколь, натрій сахарин, сорбіт та сахарозу); таблеткові антиадгезивні речовини (приклади включають, крім інших, стеарат магнію та тальк); таблеткові сполучні речовини (приклади включають, крім інших, акацію, альгінову кислоту, натрій карбоксиметилцелюлозу, пресований цукор, етилцелюлозу, желатин, рідку глюкозу, метилцелюлозу, незшитий полівінілпіролідон та крохмаль переджелатинізований); розріджувачі таблеток і капсул (приклади включають, крім інших, двоосновний кальцію фосфат, каолін, лактозу, маніт, мікрокристалічну целюлозу, порошкоподібну целюлозу, осаджений карбонат кальцію, карбонат натрію, фосфат натрію, сорбіт та крохмаль); агенти для таблеткової оболонки (приклади включають, крім інших, рідку глюкозу, гідроксиетилцелюлозу, гідроксипропілцелюлозу, гідроксипропілметилцелюлозу, метилцелюлозу, етилцелюлозу, ацетат фталат целюлози та шелак); допоміжні речовини для прямого пресування таблеток (приклади включають, крім інших, двоосновний кальцію фосфат); таблеткові дезінтегранти (приклади включають, крім інших, альгінову кислоту, кальцій карбок 37 симетилцелюлозу, мікрокристалічну целюлозу, полакрилін калію, перехресно зшитий полівінілпіролідон, натрію альгінат, натрію крохмальгліколят та крохмаль); таблеткові ковзні речовини (приклади включають, крім інших, колоїдний кремнію діоксид, кукурудзяний крохмаль і тальк); таблеткові любриканти (приклади включають, крім інших, стеарат кальцію, стеарат магнію, мінеральне масло, стеаринову кислоту та стеарат цинку); пігменти таблеток/капсул (приклади включають, крім інших, діоксид титану); таблеткові поліруючі агенти (приклади включають, крім інших, карнаубський віск та білий віск); згущувачі (приклади включають, крім інших, бджолиний віск, цетиловий спирт та парафін); агенти тонічності (приклади включають, крім інших, декстрозу та хлорид натрію); агенти, що збільшують в'язкість, (приклади включають, крім інших, альгінову кислоту, бентоніт, карбомери, натрій карбоксиметилцелюлозу, метилцелюлозу, полівінілпіролідон, альгінат натрію та трагакант); та змочувальні агенти (приклади включають, крім інших, гептадекаетиленоксицетанол, лецитин, сорбітмоноолеат, поліоксиетиленсорбітмоноолеат та поліоксиетиленстеарат). Фармацевтичні композиції відповідно до даного винаходу можуть бути проілюстровані в такий спосіб: Стерильний в/в розчин: 5 мг/мл розчин бажаної сполуки цього винаходу можна приготувати з використанням стерильної ін'єкційної води, і, якщо буде потреба, проводять корекцію рН. Розчин розводять для введення до 1 - 2 мг/мл за допомогою стерильної 5% декстрози та вводять як в/в інфузію приблизно впродовж 60 хвилин. Ліофілізований порошок для в/в введення: може бути приготовлений стерильний препарат з використанням (і) 100 - 1000 мг бажаної сполуки цього винаходу у вигляді ліофілізованого порошку, (іі) 32 - 327 мг/мл цитрату натрію, і (ііі) 300 - 3000 мг Декстрану 40. Формулювання розчиняють за допомогою стерильного, ін'єкційного фізіологічного розчину або 5 % декстрози до концентрації 10 - 20 мг/мл, що додатково розбавляють за допомогою фізіологічного розчину або 5 % декстрози до 0,2 0,4 мг/мл, та вводять або в/в болюсом або в/в інфузіями впродовж 15 - 60 хвилин. Внутрім'язова суспензія: для внутрім'язової ін'єкції можуть бути приготовлені наступний розчин або суспензія: 50 мг/мл бажаної, водонерозчинної сполуки цього винаходу 5 мг/мл натрій карбоксиметилцелюлози 4 мг/мл ТВІН 80 9 мг/мл натрію хлориду 9 мг/мл бензилового спирту Капсули із твердою оболонкою: велику кількість капсул готують шляхом заповнення в стандартні подвійні тверді желатинові капсули по 100 мг порошкоподібного активного компонента, 150 мг лактози, 50 мг целюлози та 6 мг стеарату магнію. 96965 38 М'які желатинові капсули: готують суміш активного компонента в харчовому маслі, такому як соєве масло, бавовняне масло або маслинове масло та вводять за допомогою насоса позитивного витиснення в розм'якшений желатин для утворення м'яких желатинових капсул, що містять 100 мг активного компонента. Капсули промивають і висушують. Активний компонент може бути розчинений у суміші поліетиленгліколя, гліцерину та сорбіту для одержання суміші препарату, що змішується з водою. Таблетки: велику кількість таблеток готують відповідно до звичайних процедур таким чином, щоб одиниця дозування склала 100 мг активного компонента, 0,2 мг колоїдного кремнію діоксиду, 5 мг стеарату магнію, 275 мг мікрокристалічної целюлози, 11 мг крохмалю та 98,8 мг лактози. Можуть наноситися відповідні водні та неводні покриття для збільшення смакової привабливості, поліпшення елегантності та стабільності або затримки всмоктування. Таблетки/капсули з негайним вивільненням: Вони являють собою тверді пероральні дозовані форми, отримані за допомогою стандартних і нових процесів. Ці одиниці приймають перорально без води для негайного вивільнення та доставки препарату. Активний компонент змішують у рідини, що містить компонент, такий як цукор, желатин, пектин та підсолоджувані. Ці рідини стужавіють у тверді таблетки або каплети шляхом висушування виморожувановим та методами екстракції із твердого стану. Сполуки препарату можуть бути стиснені з в'язкопружним та термоеластичним цукром та полімерами або шипучими компонентами для одержання пористих матриць, призначених для негайного вивільнення без необхідності запивати водою. Метод лікування гіперпроліферативних порушень Даний винахід стосується способів для використання сполук даного винаходу та їх композицій для лікування гіперпроліферативних порушень ссавців. Сполуки можуть бути використані для інгібування, блокування, зменшення, зниження і т. д., проліферації клітин та/або розподілу клітин та/або продукування апоптозу. Цей метод включає введення ссавцеві, який цього потребує, включаючи людину, кількості сполуки цього винаходу або її фармацевтично прийнятної солі, ізомеру, поліморфа, метаболіту, гідрату, сольвату або естеру; і т. д., що є ефективною для лікування порушення. Гіперпроліферативні порушення включають, крім інших, наприклад, псоріаз, келоїди та інші гіперплазії, що уражують шкіру, доброякісну гіперплазію простати (ВРН), солідні пухлини, такі як ракові утворення молочної залози, дихальних шляхів, головного мозку, репродуктивних органів, травного тракту, сечових шляхів, ока, печінки, шкіри, голови та шиї, щитовидної залози, паращитовидної залози та їх віддалені метастази. Такі порушення також включають лімфоми, саркоми та лейкемії. Приклади раку молочної залози включають, крім інших, інвазивну дуктальну карциному, інвазивну лобулярну карциному, дуктальну карциному in situ та лобулярну карциному in situ. 39 Приклади ракових утворень дихальних шляхів включають, крім інших, дрібноклітинну й "не дрібноклітинну" карциному легені, а також аденому бронха та плевропульмонарну бластому. Приклади ракових утворень головного мозку включають, крім інших, гліому стовбура головного мозку та гіпофтальмічну гліому, астроцитому мозочка та мозку, медулобластому, епендимому, а також нейроектодермальну та шишкоподібну пухлину. Пухлини чоловічих репродуктивних органів включають, крім інших, рак простати і яєчка. Пухлини жіночих репродуктивних органів включають, крім інших, рак ендометрію, шейки матки, яєчника, піхви й вульви, а також саркому матки. Пухлини травного тракту включають, крім інших, анальний рак, рак товстої кишки, колоректальний рак, рак стравоходу, жовчного міхура, шлунку, підшлункової залози, ректальний рак, рак тонкої кишки та слинної залози. Пухлини сечових шляхів включають, крім інших, рак сечового міхура, рак чоловічого статевого члена, рак нирки, ниркової балії, сечоводу, уретри, та людський папілярний нирковий рак. Очні ракові утворення включають, крім інших, внутріочну меланому та ретинобластому. Приклади ракових утворень печінки включають, крім інших, гепатоцелюлярну карциному (карциному клітин печінки з фіброламелярним варіантом або без нього), холангіокарциному (внутріпечіночна карцинома жовчних проток) та змішану гепатоцелюлярну холангіокарциному. Ракові утворення шкіри включають, крім інших, лусочковоклітинну карциному, саркому Капоши, злоякісну меланому, рак шкіри клітин Меркеля, та немеланомний рак шкіри. Ракові утворення голови та шиї включають, крім інших, гортанний, гіпофаренгіальний, носоглотковий, орофарингеальний рак, рак губ та ротової порожнини та лусочковоклітинний. Лімфоми включають, крім інших, зв'язану зі СНІДом лімфому, неходжкінську лімфому, шкірну Т-клітинну лімфому, лімфому Burkitt, хворобу Ходжкіна та лімфому центральної нервової системи. Саркоми включають, крім інших, саркому м'яких тканин, остеосаркому, злоякісну волокнисту гістіоцитому, лімфосаркому та рабдоміосаркому. Лейкемії включають, крім інших, гостру мієлоїдну лейкемію, гостру лімфообластну лейкемію, хронічну лімфоцитарну лейкемію, хронічну мієлогенну лейкемію та волосяноклітинну лейкемію. Ці порушення були добре охарактеризовані в людей, але також й існують із подібною етіологією в інших ссавців, і можуть лікуватися шляхом введення фармацевтичних композицій існуючого винаходу. Термін "лікування" або "лікувати", заявлений скрізь по цьому документу, використаний традиційно, наприклад, ведення пацієнта або догляд за пацієнтом з метою боротьби зі станом, полегшення, зниження, звільнення, поліпшення стану, і т.д., хвороби або порушення, такого як карцинома. Методи лікування кіназних порушень Даний винахід також пропонує способи для лікування порушень, пов'язаних з аберантною кіназ 96965 40 ною активністю (такою як тирозинкіназна активність), включаючи фосфотидилінозитол-3-кіназу. Ефективна кількість сполук даного винаходу може використовуватися для лікування порушень, включаючи ангіогенні порушення, такі як рак; запальні порушення (включаючи, крім інших, хронічний обструктивний легеневий розлад (COPD)), аутоімунні порушення, серцево-судинні порушення (включаючи, крім інших, тромбоз, легеневу гіпертензію, серцеву гіпертрофію, атеросклероз або серцеву недостатність), нейродегенеративні порушення, метаболічні порушення, ноцицептивні порушення, очні порушення, легеневі порушення або ниркові порушення. Проте, такі ракові утворення та інші хвороби можна лікувати за допомогою сполук даного винаходу, незалежно від механізму дії та/або взаємозв'язку між кіназою і порушенням. Фраза "аберантна кіназна активність " або "аберантна тирозинкіназнаактивність" включає будь-яку патологічну експресію або активність гену, що кодує кіназу, або поліпептиду, що він кодує. Приклади такої аберантної активності, включають, крім інших, надекспресію гену або поліпептиду; генну ампліфікацію; мутації, які роблять конститутивно-активну або гіперактивну кіназну активність; генні мутації, делеції, заміни, доповнення, і т. д. Даний винахід також передбачає способи інгібування активності кінази, особливо фосфотидилінозитол-3-кінази, включаючи введення ефективної кількості сполуки даного винаходу, включаючи її солі, поліморфи, метаболіти, гідрати, сольвати, проліки (наприклад: естери), та її діастереоізомерні форми. Активність кінази може бути інгібована в клітинах (наприклад, in vitro), або в клітинах ссавця суб'єкта, особливо людського пацієнта, що має потребу в лікуванні. Методи лікування ангіогенного порушення Даний винахід також пропонує способи лікування порушень та хвороб, пов'язаних з надмірним та/або патологічним ангіогенезом. Невідповідна та зміщена експресія ангіогенезу може бути шкідливою для організму. Багато патологічних станів пов'язані з ростом сторонніх кровоносних судин. Вони включають, наприклад, діабетичну ретинопатію, ішемічну оклюзію вен сітківки і ювенільну ретинопатію (Aiello et al. New Engl. J. Med. 1994, 331, 1480; Peer et al. Lab. Invest. 1995, 72, 638), вікову макулярну дегенерацію (AMD; див., Lopez et al. Invest. Opththalmol. Vis. Sci. 1996, 37, 855), неоваскулярну глаукому, псоріаз, ретролентальні фіброплазії, ангіофіброму, запалення, ревматоїдний артрит (РА), рестеноз, рестеноз у стенті, рестеноз судинного трансплантата, і т.д. Крім того, збільшене кровопостачання, зв'язане зі злоякісною та неопластичною тканиною, сприяє росту, що приводить до швидкого поширення пухлини та метастазів. Крім того, ріст нових кровоносних і лімфатичних судин у пухлині забезпечує запасний вихід для клітинок-зрадниць, сприяючи метастазам і наступному поширенню раку. Таким чином, сполуки даного винаходу можуть бути використані для лікування та/або профілактики кожного з вищезгаданих порушень ангіогенезу, наприклад, шляхом інгібування та/або зменшення формуван 41 ня кровоносних судин; шляхом інгібування, блокування, зменшення, зниження, і т.д. проліферації ендотеліальних клітин або інших типів, залучених в ангіогенез, також викликаючи смерть клітин або апоптоз таких типів клітин. Доза та введення На підставі стандартних лабораторних методів, відомих для оцінки сполук, корисних для лікування гіперпроліферативних порушень та ангіогенних порушень, за допомогою стандартних тестів на токсичність та стандартні фармакологічні випробування для визначення лікування станів, ідентифікованих вище у ссавців, і шляхом порівняння цих результатів з результатами відомих ліків, які використовуються для лікування цих станів, може бути легко визначене ефективне дозування сполук цього винаходу для лікування кожного бажаного показання. Кількість активного компонента, що буде вводитися при лікуванні одного із цих станів, може широко варіюватися відповідно до таких розглянутих факторів, як конкретна сполука та використовувана одиниця дозування, спосіб введення, період лікування, вік і стать пацієнта, що піддається лікуванню, та природи та ступеня стану, що піддається лікуванню. Загальна кількість активного компонента, що буде вводитися, взагалі коливається приблизно від 0,001 мг/кг до приблизно 200 мг/кг маси тіла на добу, і переважно приблизно від 0,01 мг/кг до приблизно 20 мг/кг маси тіла на добу. Клінічно корисні схеми дозування будуть коливатися від дозування один-три рази на добу до дозування один раз кожні чотири тижні. Крім того, "перерви в прийомі препарату", протягом яких пацієнт не приймає препарат протягом певного проміжку часу, можуть бути вигідними для загальної рівноваги між фармакологічним ефектом і переносимістю. Одиниця дозування може містити приблизно від 0,5 мг приблизно до 1500 мг активного компонента, і може вводитися один або кілька разів у добу або менше одного разу за добу. Середнє добове дозування для введення шляхом ін'єкції, включаючи внутрішньовенні, внутрім'язові, підшкірні та парентеральні ін'єкції, та використання методик інфузії переважно буде становити від 0,01 до 200 мг/кг загальної маси тіла. Режим середнього добового ректального дозування переважно буде становити від 0,01 до 200 мг/кг загальної маси тіла. Режим середнього добового піхвового дозування переважно буде становити від 0,01 до 200 мг/кг загальної маси тіла. Режим середнього добового місцевого дозування переважно буде становити від 0,1 до 200 мг, які застосовують один-чотири рази на добу. Трансдермальна концентрація буде переважно такою, яка необхідна для підтримання добової дози від 0,01 до 200 мг/кг. Режим середнього добового дозування інгаляцією переважно буде становити від 0,01 до 100 мг/кг загальної маси тіла. Звичайно певний початковий і триваючий режим дозування для кожного пацієнта будуть варіювати залежно від природи та важкості стану, визначеного лікуючим діагностом, активності певної використовуваної сполуки, віку та загального стану пацієнта, часу введення, шляху введення, швидкості виведення препарату з організму, комбінацій 96965 42 речовин, і т. п.. Бажаний спосіб лікування та кількість доз сполуки даного винаходу або її фармацевтично прийнятної солі або естеру або їх комбінації можуть бути встановлені кваліфікованими фахівцями в даній галузі, що використовують звичайні тести лікування. Комбіновані терапії Сполуки цього винаходу можна вводити у вигляді окремого фармацевтичного агента або в комбінації з одним або декількома іншими фармацевтичними агентами, якщо комбінація не викликає неприпустимих негативних ефектів. Наприклад, сполуки цього винаходу можуть бути комбіновані з відомими антигіперпроліферативними, протизапальними, болезаспокійливими, імунорегуляторними, діуретичними, антиаритмічними, антигіперхолестеринемічними, антидисліпідемічними, антидіабетичними або противірусними засобами, і т.п., а також з їх сумішами та комбінаціями. Додатковий фармацевтичний агент може являти собою такі як: алдеслейкін, алендронова кислота, альфаферон, алітретіноїн, алопуринол, алоприм, алокси, альтретамін, аміноглутетимід, аміфостин, амрубіцин, амсакрин, анастрозол, анзмет, аранесп, арглабін, триоксид миш'яку, аромасин, 5-азацитидин, імуран, БЦЖ або tice БЦЖ, бестатин, бетаметазон ацетат, бетаметазон фосфат натрію, бексаротен, блеоміцину сульфат, броксуридин, бортезоміб, бусульфан, кальцитонін, кампат, капецитабін, карбоплатин, казодекс, цефезон, целмолейкін, церубідин, хлорамбуцил, цисплатин, кладрибін, кладрибін, клодронова кислота, циклофосфамід, цитарабін, дакарбазин, дактиноміцин, ДауноКсом, декадрон, декадрон фосфат, делестроген, денілейкін дифтитокс, депо-медрол, деслорелін, дексразоксан, діетилстилбестрол, дифлюкан, доцетаксель, доксифлуридин, доксорубіцин, дронабінол, DW-166HC, елігард, елітек, елленце, еменд, епірубіцин, епоетин альфа, епоген, ептаплатин, ергамізол, естраке, естрадіол, естрамустин фосфат натрію, етинілестрадіол, етіол, етидронова кислота, етопофос, етопозид, фадрозол, фарстон, філграстим, фінастерид, фліграстим, флоксуридин, флуконазол, флударабін, 5фтордеоксиуридин монофосфат, 5-фтороурацил (5-FU), флуоксиместерон, флутамід, форместан, фостеабін, фотемустин, фульвестрант, гаммагард, гемцитабін, гемтузумаб, глеевек, гліадел, госерелін, гранісетрон НСl, гістрелін, гікамтин, гідрокортон, еритро-гідроксиноніладенін, гідроксисечовина, ібритумомаб тіуксетан, ідарубіцин, іфостамід, інтерферон альфа, інтерферон-альфа 2, інтерферон-альфа-2А, інтерферон-альфа-2В, інтерферональфа-n1, інтерферон-альфа-n3, інтерферон бета, інтерферон гама-1а, інтерлейкін-2, інтрон А, іресса, іринотекан, кітрил, лентинан сульфат, летрозол, лейковорин, лейпролід, лейпролід ацетат, левамізол, кальцієва сіль левофолієвої кислоти, левотроїд, левоксил, ломустин, лонідамін, маринол, мехлоретамін, мекобаламін, медроксипрогістерону ацетат, мегестрол ацетат, мелфалан, менест, 6-меркаптопурин, Месна, метотрексат, метвікс, мілтефосин, міноциклін, мітоміцин С, мітотан, мітоксантрон, модренал, міоцет, недаплатин, нойласта, ноймега, нойпоген, нілутамід, нол 43 вадекс, NSC-631570, ОСТ-43, остреотид, ондансетрон НСl, орапред, оксаліплатин, паклітаксел, педіапред, пегаспаргаз, пегасис, пентостатин, піцибаніл, пілокарпін НСl, пірарубіцин, плікаміцин, натрію порфімер, преднімустин, преднізолон, преднізон, премарин, прокарбазин, прокрит, ралтітрексед, ребіф, реній-186 етидронат, ритуксимаб, роферон-А, ромуртид, салаген, сандостатин, сарграмостим, семустин, сизофіран, собузоксан, солумедрол, спарфозова кислота, терапія стовбуровими клітинами, стрептозоцин, стронцій-89 хлорид, синтроід, тамоксифен, тамсулозин, тасонермін, тастолактон, таксотера, тецелейкін, темозоломід, теніпозид, тестостерону пропіонат, тестред, тіогуанін, тіотепа, тиротропін, тилудронова кислота, топотекан, тореміфен, тоситумомаб, трастузумаб, треосульфан, третиноїн, трексалл, триметилмеламін, триметрексат, трипторелін ацетат, трипторелін памоат, UFT, уридин, валрубіцин, веснаринон, вінбластин, вінкристин, віндезин, вінорелбін, вірулізин, зинекард, зиностатин, стималамер, зофран, АВІ-007, аколбіфен, актиммун, афінітак, аміноптерин, арзоксифен, азоприсніл, атаместан, атрасентан, BAY43-9006 (сорафеніб), авастин, ССІ-779, CDC-501, целебрекс, цетуксимаб, криснатол, ципротерону ацетат, децитабін, DN-101, доксорубіцин-МТС, dSLIM, дутастерид, едотекарин, ефлорнітин, ексатекан, фенретинід, гістаміну дигідрохлорид, гістреліновий гідрогель, гольмій 166 DOTMP, ібадронова кислота, інтерферон гама, інтрон-PEG, іксабепілон, гемоціанін фісурела, L-651582, ланреотид, лазофоксифен, лібра, лонафарніб, міпроксифен, мінодронат, MS-209, ліпосомал МТР-РЕ, МХ-6, нафарелін, неморубіцин, неовастат, нолатрексед, облімерсен, онко-TCS, осидем, паклітаксель поліглутамат, памідронат динатрію, PN-401, QS-21, квазепам, R-1549, ралоксифен, ранпірнас, 13 цис-ретиноєва кислота, сатраплатин, сеокальцитол, Т-13 8067, тарцева, таксопрексин, тимосин альфа 1, тіазофурин, типіфарніб, тирапазамін, TLK-286, тореміфен, TransMID-107R, валсподар, вапреотид, ваталаніб, вертепорфін, вінфлунін, Z-100, золедронова кислота або їх комбінації. Додатковий фармацевтичний агент може також являти собою такі як: гемцитабін, паклітаксель, цисплатин, карбоплатин, бутират натрію, 5FU, доксирубіцин, тамоксифен, етопозид, трастумазаб, гефітиніб, інтрон А, рапаміцин, 17-AAG, U0126, інсулін, або похідна інсуліну, ліганд PPAR, препарат сульфонілсечовини, інгібітор αглікозидази, бігуанід, інгібітор РТР-1В, інгібітор DPP-IV, інгібітор 11-бета-HSD, GLP-1, похідна GLP-1, GIP, похідна GIP, РАСАР, похідна РАСАР, секретин або похідна секретину. Додаткові антигіперпроліферативні агенти, які можуть бути додані в композицію, включають, крім інших, сполуки, перераховані в режимах протираому кової хіміотерапії в 11 виданні Merck Index, (1996), що включений авторами шляхом посилання, такі як аспарагіназа, блеоміцин, карбоплатин, кармустин, хлорамбуцил, цисплатин, коласпаза, циклофосфамід, цитарабін, дакарбазин, дактиноміцин, даунорубіцин, доксорубіцин (адріаміцин), епірубіцин, етопозид, 5-фтороурацил, гексаметил 96965 44 меламін, гідроксисечовина, іфосфамід, іринотекан, лейковорин, ломустин, мехлоретамін, 6меркаптопурин, месна, метотрексат, мітоміцин С, мітоксантрон, преднізолон, преднізон, прокарбазин, ралоксифен, стрептозоцин, тамоксифен, тіогуанін, топотекан, вінбластин, вінкристин та віндезин. Інші антигіперпроліферативні агенти, що підходять для використання з композицією винаходу, включають, крім інших, такі сполуки, які визнані для використання в лікуванні неопластичних хвороб в Goodman and Gilman's The Pharmacological Basis of Therapeutics (Дев'яте видання), редактор Molinoff et al., опубл. McGraw-Hill, сторінки 12251287, (1996), що включений авторами шляхом посилання, такі як аміноглутетимід, L- аспарагіназа, імуран, 5-азацитидин кладрибін, бусульфан, діетилстилбестрол, 2',2'-дифтордезоксицитидин, доцетаксель, еритрогідроксиноніл аденін, етинілестрадіол, 5-фтордезоксиуридин, 5фтордезоксиуридину монофосфат, флударабіну фосфат, фтороксиместерон, флутамід, гідроксипрогестерону капроат, ідарубіцин, інтерферон, медоксипрогестерону ацетат, мегестролу ацетат, мелфалан, мітотан, паклітаксель, пентостатин, Nфосфонацетил-L-аспартат (РALA), плікаміцин, семустин, теніпозид, пропіонат тестостерону, тіотепа, триметилмеламін, уридин і вінорелбін. Інші антигіперпроліферативні агенти, що підходять для використання з композицією винаходу, включають, крім інших, інші антиракові агенти, такі як епотилон та його похідні, іринотекан, ралоксифен та топотекан. Взагалі, використання цитотоксичних та/або цитостатичних агентів у комбінації із сполуками або комбінацією даного винаходу буде служити для: (1) одержання кращої ефективності в зниженні росту пухлини або навіть усунення пухлини в порівнянні із введенням тільки одного агента, (2) забезпечення введення меншої кількості хіміотерапевтичних агентів, що вводять, (3) забезпечення хіміотерапевтичного лікування, що добре переноситься пацієнтом з меншою кількістю шкідливих фармакологічних ускладнень, ніж спостерігаються при монохіміотерапіях та певних інших комбінованих терапіях, (4) забезпечення лікування більш широкого спектру різних типів раку у ссавців, особливо людей, (5) забезпечення більш високого показника відповіді серед пацієнтів, яких лікували, (6) забезпечення більш тривалого часу виживання серед пацієнтів, яких лікували, у порівнянні зі стандартними хіміотерапевтичними лікуваннями, (7) забезпечення більш тривалого часу до прогресії пухлини, та/або (8) одержання результатів ефективності та переносимості, принаймні настільки ж гарних як результати для агентів, використовуваних окремо, у порівнянні з відомими випадками, коли комбінації інших протиракових агентів роблять антагоністичні ефекти. ЕКСПЕРИМЕНТ Скорочення та акроніми 45 Всебічний список скорочень, використовуваних органічними хіміками зі звичайними навичками в даній галузі, знаходиться в ACS Style Guide (третє видання) або Настанові для Авторів Journal of Organic Chemistry. Скорочення, що містяться в зазначених списках, і всі скорочення, використовувані органічними хіміками зі звичайними навичками в даній галузі, включені авторами шляхом посилання. Для цілей цього винаходу хімічні елементи ідентифіковані відповідно до Періодичної таблиці елементів, версії CAS, Посібника з Хімії та Фізики, 67-ого вид, 1986-87. Більш особливо, при використанні наступних скорочень у цьому розкритті, вони мають наступні значення: асас Ас2О Ас (або ОАс) Безводн. водн. Аr Атм. 9-BBN BINAP Вn bр br s Bz ВОC u-BuOH t-BuOH t-BuOK С розрах. CAN Cbz CDI CD3OD Celite® ацетилацетонат оцтовий ангідрид ацетат безводний водний арил атмосфера 9-борабіцикло[3.3.1]ноніл 2,2'-біс (дифенілфосфіно)-1,1'-бінафтил бензил точка кипіння широкий синглет бензоїл трет-бутоксикарбоніл н-бутанол тpeт-бутанол калію трет-бутоксид Цельсію розрахований церію амонію нітрат карбобензилокси карбонілдіімідазол метанол-d4 фільтруючий засіб з діатомової землі, Celite® Corp.. хімічна іонізаційна мас-спектроскопія вуглець-13 ядерний магнітний резонанс мета-хлорпероксибензойна кислота дуплет дуплет дуплетів 1,4-діазабіцикло[2.2.2]октан 1,8-діазабіцикло[5.4.0]ундец-7-ен Ν,Ν'-дициклогексилкарбодіімід дихлорметан діетилазодикарбоксилат розкладання діізопропіламін діізобутилалюмінію гідрид 4-(Ν,N-диметиламіно)піридин 1,2-диметоксиетан Ν,N-диметилформамід диметилсульфоксид entgegen (конфігурація) 1-(3-диметиламінопропіл)-3етилкарбодіімід гідрохлорид CI-MS 13 C ЯМР m-CPBA d dd DABCO DBU DCC DCM DEAD розкл. DIA DIBAL DMAP DME DMF DMSO Δ EDCl або EDCI · HCl ее енантіомерний надлишок ΔΗ вплив електрона 96965 46 випаровуючий світлорозсіюючий датчик еквівалентний електророзпилювальна масспектроскопія EtOAc етилацетат EtOH етанол (100 %) EtSH етантіол Et2O діетиловий ефір Et3N триетиламін Fmoc 9-фторенілметоксикарбоніл ΓΦ газова хроматографія ГХ-МС газова хроматографія масспектроскопія год. година, години hex гексани або гексан 1 Н ЯМР протонний ядерний магнітний резонанс HMPA гексаметилфосфорамід HMPT гексаметилфосфорний триамід HOBT гідроксибензотриазол ВЕРХ високоефективна рідинна хроматографія нерозч. нерозчинний ΗPΑ ізопропіламін tPrOH ізопропіловий спирт ІЧ інфрачервоний J константа спарювання (спектроскопія ЯМР) л літр LAH літій-алюміній гідрид PX рідинна хроматографія PX-MC рідинна хроматографія масспектрометрія LDA діізопропіламід літію -1 Μ моль л (молярний) m мультиплет м мета MeCN ацетонітрил MeOH метанол МГц мегагерц хвил. хвилина, хвилини мкл мікролітр мл мілілітр мкМ мікромолярний моль моль Τ пл. точка плавлення МС мас-спектр, мас-спектрометрія Ms метансульфоніл m/z відношення маси до заряду -1 Ν екв л (нормальний) NBS N-бромсукцинімід нм наномолярний NMM 4-метилморфолін ЯМР ядерний магнітний резонанс o орто споcт. спостережуваний n пара стор сторінка стор сторінки PdCl2dppf [1,1'біс(дифенілфосфіно)фероцен]дихлорпа ладій (II) Pd(OAc)2 ацетат паладію рН негативний логарифм концентрації іонів водню Ph феніл ELSD еквів. ES-MS 47 рК негативний логарифм константи рівноваги рKа негативний логарифм константи рівноваги для асоціації РРА полі(фосфорна кислота) PS-DIEA полістирол-зв'язаний діізопропілетиламін РуВОР бензотриазол-1-іл-окси-тріс-піролідинофосфонію гексафторфосфат q квартет рац рацемічний R rectus (конфігураційний) Rf коефіцієнт уповільнення (ТШХ) RT час утримання (ВЕРХ) кт кімнатна температура s синглет S sinister (конфігураційний) t триплет TBDMS, трет-бутилдиметилсиліл TBP TBDPS, трет-бутилдифенілсиліл TPS TEA триетиламін THF тетрагідрофуран Tf трифторометансульфоніл (трифліл) TFA трифторооцтова кислота TFFH фтор-N,N,N',N,'тетраметилформамідинію гексафторфосфат ТШХ тонкошарова хроматографія TMAD Ν,Ν,Ν',Ν'-тетраметилетилендіамін TMSCl триметилсиліл хлорид Ts n-толуолсульфоніл об./об. відношення об'єму до об'єму м/об. відношення маси до об'єму м/м відношення маси до маси Ε zusammen (конфігурація) Процентні виходи, про які повідомляють у наступних прикладах, основані на вихідному компоненті, що використовують в найнижчій молярній кількості. Чутливі до повітря та вологості рідини та розчини переносилися через шприц або канюлю, та вводилися в реакційні посудини через гумові перегородки. Реактиви та розчинники комерційного класу використовувалися без подальшого очищення. Термін "сконцентрований під зниженим тиском" стосується використання ротаційного випарника Buchi при приблизно 15 мм Hg. Всі температури реєструються нескоригованими в градусах Цельсію (°С). Тонкошарова хроматографія (ТШХ) проводилася на попередньо покритих скляних силікагелевих 60 F-254 250-мкм пластинах. Структури сполук цього винаходу були підтверджені з використанням однієї або декількох наступних процедур. ЯМР Спектри ЯМР були отримані для кожної сполуки та були сумісні з показаними структурами. Звичайна одномірна ЯМР спектроскопія була виконана на 300 або 400 МГц спектрометрах Varian® Mercury-plus. Зразки розчинили в дейтерованих розчинниках. Хімічні зсуви були зареєстровані на шкалі ррm та були віднесені до відповідних сигналів розчинників, таких як 2,49 ррm для 96965 48 DMSO-d6, 1,93 ррm для CD3CN, 3,30 ррm для CD3OD, 5,32 ррm для CD2Cl2 та 7,26 ррm для 1 CDCl3 для H спектрів. ГХ/МС Мас-спектри електронного впливу (ЕІ-МС) були отримані за допомогою мас-спектрометра Hewlett Packard, 5973, постаченого Газовим Хроматографом Hewlett Packard 6890 зі колонкою J & W НР-5 (0,25 мМ покриття; 30 м × 0,32 мм). Джерело іонів підтримували при 250 °С, та спектри сканували від 50-550 amu при 0,34 сек на сканування. РХ/МС Якщо не зазначено інакше, усі часи утримання отримані із РХ/МС та відповідають молекулярному іону. Спектри рідинної хроматографії високого тиску електророзпилювальні мас-спектри (РХ/МС) були отримані, використовуючи один з наступних: Метод A (LCQ) ВЕРХ Hewlett Packard 1100, обладнана четвертинним насосом, детектором зі змінною довжиною хвилі, встановленим на 254 нм, колонкою Waters Sunfire С18 (2,1 × 30 мм, 3,5 мкм), автосамплером Gilson та мас-спектрометром з уловлювачем іонів з електророзпилювальною іонізацією Finnigan LCQ. Спектри сканували від 120 - 1200 amu, використовуючи змінний іонний час відповідно до числа іонів у джерелі. Елюентами були А: 2% ацетонітрил у воді з 0,02 % TFA, та В: 2% ацетонітрил у воді з 0,018 % TFA. Елюювання градієнта від 10 % В до 95 % В протягом 3,5 хвилин при швидкості потоку 1,0 мл/хвил. використовувалося з початковою затримкою 0,5 хвилин та кінцевою затримкою при 95 % В 0,5 хвилин. Загальний час хроматографування становив 6,5 хвилин. Метод В (LCQ5) Система ВЕРХ Agilent 1100. Система ВЕРХ 1100 Agilent була обладнана автосамплером 1100 Agilent, четвертинним насосом, детектором зі змінною довжиною хвилі, встановленим на 254 нм. Використовувана колонка ВЕРХ - колонка Waters Sunfire С18 (2,1 × 30 мм, 3,5 мкм). ВЕРХ елюент був безпосередньо з'єднаний без розщеплення з мас-спектрометром з уловлювачем іонів з електророзпильною іонізацією Finnigan LCQ DECA. Спектри сканували від 140 - 1200 amu, використовуючи змінний іонний час відповідно до числа іонів у джерелі при застосуванні позитивного режиму іонів. Елюентами були А: 2% ацетонітрил у воді з 0,02 % TFA, та В: 2% ацетонітрил у воді з 0,02 % TFA. Елюювання градієнта від 10 % В до 90 % В протягом 3,0 хвилин при швидкості потоку 1,0 мл/хвил. використовувалося з початковою затримкою 1,0 хвилина та кінцевою затримкою при 95 % В 1,0 хвилина. Загальний час хроматографування становив 7,0 хвилин. Метод С (LTQ) Система ВЕРХ Agilent 1100. Система ВЕРХ 1100 Agilent була обладнана автосамплером 1100 Agilent, четвертинним насосом та діодною матрицею. Використовувана колонка ВЕРХ -колонка Waters Sunfire C18 (2,1 × 30 мм, 3,5 мкм). ВЕРХ елюент був безпосередньо з'єднаний з розщепленням 1:4 з мас-спектрометром з уловлювачем іонів з електророзпилюючою іонізацією Finnigan 49 LTQ. Спектри сканували від 50 - 800 amu, використовуючи змінний іонний час відповідно до числа іонів у джерелі при застосуванні позитивного або негативного іонного режиму. Елюентами були А: вода з 0,1 мурашиною кислотою, та В: ацетонітрил з 0,1 %. мурашиною кислотою. Елюювання градієнту від 10 % В до 90 % В протягом 3,0 хвилин при швидкості потоку 1,0 мл/хвил. використовувалося з початковою затримкою 2,0 хвилини та кінцевою затримкою при 95 % В 1,0 хвилина. Загальний час хроматографування становив 8,0 хвилин. Метод D Система ВЕРХ Gilson, обладнана детектором зі змінною довжиною хвилі, встановленим на 254 нм, колонка YMC pro С-18 (2 × 23 мм, 120А), і масспектрометром з уловлювачем іонів з електророзпилюючою іонізацією Finnigan LCQ. Спектри сканували від 120 - 1200 amu, використовуючи змінний іонний час відповідно до числа іонів у джерелі. Елюентами були А: 2% ацетонітрил у воді з 0,02 % TFA та В: 2% вода в ацетонітрилі з 0,018 % TFA. Елюювання градієнта від 10 % В до 95 % В протягом 3,5 хвилин при швидкості потоку 1,0 мл/хвил. використовувалося з початковою затримкою 0,5 хвилин і кінцевою затримкою при 95 % В 0,5 хвилин. Загальний час хроматографування становив 6,5 хвилин. Метод Δ Система ВЕРХ Agilent 1100. Система ВЕРХ 1100 Agilent була обладнана автосамплером 1100 Agilent, четвертинним насосом і діодною матрицею. Використовуваний колонку ВЕРХ-колонка Waters Sunfire C18 (2,1 × 30 мм, 3,5 мкм). ВЕРХ елюент був безпосередньо з'єднаний з розщепленням 1:4 з мас-спектрометром з уловлювачем іонів з електророзпилювальною іонізацією Finnigan LTQ. Спектри сканували від 50-1000 amu, використовуючи змінний іонний час відповідно до числа іонів у джерелі або в позитивному або в негативному іонному режимі. Елюентами були А: вода з 0,1 мурашиною кислотою, і В: ацетонітрил з 0,1 % мурашиною кислотою. Елюювання градієнта від 10 % В до 90 % В протягом 3,0 хвилин при швидкості потоку 1,0 мл/хвил. використовувалося з початковою затримкою 2,0 хвилини та кінцевою затримкою при 95 % В 1,0 хвилина. Загальний час хроматографування становив 8,0 хвилин. Препаративна ВЕРХ: Препаративна ВЕРХ була виконана у режимі оберненої фази, як правило, використовуючи систему ВЕРХ Gilson, обладнану двома насосами Gilson 322, автосамплером Gilson 215, детектором діодної матриці Gilson та колонкою С-18 (наприклад, YMC Pro 20 × 150 мм, 120 А). Елюювання градієнта використовувалося з розчинником А вода з 0,1 % TFA, та розчинником В - ацетонітрил з 0,1 % TFA. Після інжекції в колонку у вигляді розчину, сполука, як правило, елюювалась із градієнтом змішаних розчинників, таким як 10-90 % Розчинник В у Розчиннику А протягом 15 хвилин при швидкості потоку 25 мл/хвил. Фракція(ії), що містить(ять) бажаний продукт, була зібрана УФ контролем при 254 або 220 нм. Препаративна MPLC: 96965 50 Препаративна рідинна хроматографія середнього тиску (MPLC) була виконана стандартними методами «флеш» хроматографії на силікагелі (наприклад, Still, W. С. et al. J. Org. Chem. 1978, 43, 2923-5), або при застосуванні силікагелевих картриджів та пристроїв, таких як системи Biotage Flash. Використовувалося багато розчинників для елюювання, як описано в експериментальних протоколах. Загальні препаративні методи Певний процес, що буде використаний в одержанні сполук, використовуваних у цьому варіанті здійснення винаходу, залежить від певної бажаної сполуки. Такі фактори як вибір певних замісників відіграє роль у шляху, якому будуть слідувати в одержанні певних сполук цього винаходу. Ці фактори легко розпізнаються фахівцем зі звичайними навичками в даній галузі. Сполуки винаходу можуть бути отримані за допомогою відомих хімічних реакцій і процедур. Однак, представлені наступні загальні препаративні методики, щоб допомогти читачеві в синтезі сполук існуючого винаходу, з більш детальними специфічними прикладами, що представляють нижче в експериментальному розділі, що описує робочі приклади. Сполуки винаходу можуть бути отримані відповідно до звичайних хімічних методів, і/або як розкрито нижче, з вихідних матеріалів, які або комерційно доступні або виробляються відповідно до звичайних, стандартних хімічних методів. Загальні методи для одержання сполук наведені нижче, і одержання характерних сполук чітко ілюструється у прикладах. Синтетичні перетворення, які можуть використовуватися в синтезі сполук цього винаходу та у синтезі проміжних продуктів, залучених у синтез сполук цього винаходу, відомі або доступні для фахівця, кваліфікованого в даній галузі. Колекції синтетичних перетворень можуть бути знайдені в компіляціях, таких як: J. March. Advanced Organic Chemistry, 4th ed.; John Wiley: New York (1992) R.C. Larock. Comprehensive Organic Transformations, 2nd ed.; Wiley-VCH: New York (1999) F.A. Carey; R.J. Sundberg. Advanced Organic Chemistry, 2nd ed.; Plenum Press: New York (1984) T.W. Greene; P.G.M. Wuts. Protective Groups in Organic Synthesis, 3rd ed.; John Wiley: New York (1999) L.S. Hegedus. Transition Metals in the Synthesis of Complex Organic Molecules, 2nd ed.; University Science Books: Mill Valley, CA (1994) L.A. Paquette, Ed. The Encyclopedia of Reagents for Organic Synthesis; John Wiley: New York (1994) A.R. Katritzky; O. Meth-Cohn; C.W. Rees, Eds. Comprehensive Organic Functional Group Transformations; Pergamon Press: Oxford, UK (1995) G. Wilkinson; F.G A. Stone; E.W. Abel, Eds. Comprehensive Organometallic Chemistry; Pergamon Press: Oxford, UK (1982) B.M. Trost; I. Fleming. Comprehensive Organic Synthesis; Pergamon Press: Oxford, UK (1991) 51 A.R. Katritzky; C.W. Rees Eds. Comprehensive Heterocylic Chemistry; Pergamon Press: Oxford, UK (1984) A.R. Katritzky; C.W. Rees; E.F.V. Scriven, Eds. Comprehensive Heterocylic Chemistry II; Pergamon Press: Oxford, UK (1996) С. Hansch; P.G. Sammes; J.B. Taylor, Eds. Comprehensive Medicinal Chemistry: Pergamon Press: Oxford, UK (1990). Крім того, огляди синтетичної методології та зв'язаних питань включають Organic Reactions; John Wiley: New York; Organic Syntheses; John Wiley: New York; Reagents for Organic Synthesis: John Wiley: New York; The Total Synthesis of Natural Products; John Wiley: New York; The Organic Chemistry of Drug Synthesis; John Wiley: New York; Annual Reports in Organic Synthesis; Academic Press: San Diego CA; та Methoden der Organischen Chemie (Houben-Weyl); Thieme: Штутгарт, Німеччина. Крім того, бази даних синтетичних перетворень включають Chemical Abstracts, які можна знайти, використовуючи CAS OnLine or SciFinder, Handbuch der Organischen Chemie (Beilstein), яких можна знайти, використовуючи SpotFire та REACCS. У Схемі Реакції 1, ванілін ацетат може бути перетворений у проміжний продукт (III) через умови нітрування, такі як нерозведена азотна кислота, що димить, або азотна кислота в присутності іншої сильної кислоти, такої як сірчана кислота. Гідроліз ацетату в проміжному продукті (III) очікувався б у 96965 52 присутності основ, таких як гідроксид натрію, гідрооксид літію або гідрооксид калію в протонному розчиннику, такому як метанол. Захисту проміжного продукту (IV) для одержання сполук Формули (V) можна досягти стандартними методами (Greene, T.W.; Wuts, P.G.M.; Protective Groups in Organic Synthesis; Wiley & Sons: New York, 1999). Перетворення сполук формули (V) у сполуки формули (VI) можна досягти, використовуючи аміак у присутності йоду в апротонному розчиннику, такому як THF або діоксан. Відновлення нітрогрупи у формулі (VI) могло бути досягнуте з використанням заліза в оцтовій кислоті або водневому газі в присутності підходящого каталізатора з паладію, платини або нікелю. Перетворення сполук формули (VII) в імідазолін формули (VIII) найкраще досягають із використанням етилендіаміну в присутності каталізатора, такого як елементна сірка при нагріванні. Циклізація сполук формули (VIII) у сполуки формули (IX) досягають, використовуючи бромід ціаногену у присутності амінної основи, такої як триетиламін, діізопропілетиламін або піридин у галогенованому розчиннику, такому як DCM або дихлоретан. Видалення захисної групи у формулі (IX) буде залежати від обраної групи та може бути досягнуто стандартними методами (Greene, T.W.; Wuts, P.G.M.; Protective Groups in Organic Synthesis; Wiley & Sons: New York, 1999). Алкілування фенолу у формулі (X) може бути досягнуте з використанням основи, такої як карбонат цезію, гідрид натрію, або т-бутоксид калію в полярному апротонному розчиннику, такому як DMF або DMSO із введенням бічного ланцюга, що має відповідну відхідну групу, таку як галід або сульфонатна група. Нарешті, аміди формули (І) можуть бути утворені з використанням активованих естерів, таких як кислотні хлориди та ангідриди або альтернативно сформовані з використанням карбонових кислот та відповідних сполучних агентів, таких як PYBOP, DCC або EDCI у полярних апротонних розчинниках. 53 У Схемі реакції 2 сполука формули (IV), підготовлена як описано вище, може бути перетворена в структуру формули (XII), використовуючи аміак у присутності йоду в апротонному розчиннику, такому як THF або діоксан. Алкілування фенолу у формулі (XII) може бути досягнуте з використанням основи, такої як карбонат цезію, гідрид натрію, або т-бутоксид калію в полярному апротонному розчиннику, такому як DMF або DMSO із введенням бічного ланцюга, що має відповідну відхідну групу, таку як галід або сульфонатна група. Відновлення нітрогрупи у формулі (XIII) могло бути досягнуте з використанням заліза в оцтовій кислоті або водневому газі в присутності підходящого каталізатора з паладію, платини або нікелю. Перетворення сполук формули (XIV) в імідазолін формули (XV) найкраще досягають із використанням етилендіаміну в присутності каталізатора, такого як елементна сірка, при нагріванні. Циклізації сполук формули (XV) у сполуки формули (XVI) досягають, використовуючи ціаногену бромід у присутності амінної основи, такої як триетиламін, діізопропілетиламін або піридин у галогенованому розчиннику, такому як DCM або дихлоретан. Нарешті, аміди формули (І) можуть бути утворені, використовуючи активовані естери, такі як кислотні хлориди та ангідриди, або альтернативно сформовані з використанням карбонових кислот та відповідних сполучних агентів, таких як PYBOP, DCC або EDCI у полярних апротонних розчинниках. 96965 54 У Схемі реакції 4 сполука формули (IX), отримана як описано вище, може бути перетворена в амід (XVII) з використанням активованих естерів, таких як кислотні хлориди та ангідриди або альтернативно сформовані з використанням карбонових кислот та відповідних сполучних агентів, таких як PYBOP, DCC або EDCI у полярних апротонних розчинниках. Видалення захисної групи у формулі (XVII) буде залежати від обраної групи та може бути досягнуте стандартними методами (Greene, T.W.; Wuts, P.G.M.; Protective Groups in Organic Synthesis; Wiley & Sons: New York, 1999). Алкілування фенолу у формулі (XVI) може бути досягнуте з використанням основи, такої як карбонат цезію, гідрид натрію, або т-бутоксид калію в полярному апротонному розчиннику, такому як DMF або DMSO із введенням бічного ланцюга, що має відповідну відхідну групу, таку як галід або сульфонатна група. У Схемі реакції 3 сполука формули (X), отримана як описано вище, може бути перетворена в амід (XVI) з використанням активованих естерів, таких як кислотні хлориди та ангідриди або альтернативно сформовані з використанням карбонових кислот та відповідних сполучних агентів, таких як PYBOP, DCC або EDCI у полярних апротонних розчинниках. Вона могла потім бути перетворена в сполуку формули (І) з використанням основи, такої як карбонат цезію, гідрид натрію, або т-бутоксид калію в полярному апротонному розчиннику, такому як DMF або DMSO із введенням бічного ланцюга, що має відповідну відхідну групу, таку як галід або сульфонатна група. У Схемі реакції 5 сполука формули XVIII може бути перетворена біс-хлоридну сполуку формули XIX з використанням агентів, що хлорують, таких як РОСl3 або СОСl2 в апротонних розчинниках. 55 Отриманий у такий спосіб хлорид може бути перетворений в імідазоліни формули XXI через реакцію з відповідними кількостями етаноламіну або відповідно захищеного замісника, що супроводжується активацією за допомогою підходящого активуючого агента, такого як сульфоніл хлорид, РРh3 або галогенізуючого агента, такого як SOCl2. Хлорид XXI може бути перетворений в амін XXII за допомогою будь-якого джерела нуклеофільного аміну, такого як аміак, фталімід або захищені аміни, такі як бензил амін у полярному розчиннику, такому як DMF або DMSO. Утворення фенолу, зображеного у формулі X, може бути досягнуте шляхом зняття захисту метилового ефіру, використовуючи будьяку з умов, зазначених у літературі (Greene, T.W.; Wuts, P.G.M.; Protective Groups in Organic Synthesis; Wiley & Sons: New York, 1999). Для кращого розуміння цього винаходу, зазначені наступні приклади. Ці приклади служать тільки для ілюстративних цілей, і не повинні ніяким чином розглядатися як обмеження галузі застосування винаходу. Всі публікації, згадані авторами, включені шляхом посилання в їх повному обсязі. Проміжні продукти Проміжний продукт А Одержання піримідин 4-карбонової кислоти 4-Метилпіримідин (1,00 г, 10,6 ммоль) розвели у воді (90 мл). Додали перманганат калію (4,20 г, 26,5 ммоль) та гідроксид калію (4,20 г, 74,8 ммоль), та суміш нагрівали при 75 °С впродовж 1,5 год. Етанол додали по краплях, та осад видалили фільтрацією через Celite. Фільтрат сконцентрували під зниженим тиском, розвели у воді та обробили концентрованим розчином НСI до кислого середовища. Сполуку, зазначену в назві, осадили у вигляді тонкого порошку, що зібрали вакуумною фільтрацією та висушили у вакуумній печі (770 мг, 1 58 %): Н ЯМР (DMSO-d6) δ: 13,92 (1H, br s), 9,35 (1H, d), 9,05 (1H, d), 7,99 (1H, dd). Проміжний продукт В Одержання 2-амінопіримідин-5-карбонової кислоти Натрію (1Z)-2-(диметоксиметил)-3-метокси-3оксопроп-1-ен-1-олат був отриманий як описано Zhichkin et al. (Synthesis 2002, 6, стор. 7720). Натрію (1Z)-2-(диметоксиметил)-3-метокси-3окопроп-1-ен-1-олат (1,37 г, 7,8 ммоль) розвели в DMF (12 мл), і додали гуанідину гідрохлорид (640 мг, 6,7 ммоль). Суміш перемішували при 100 °С протягом 1 год., потім остудили до кт та розвели водою. Метил 2-амінопіримідин-5-карбоксилат, осаджений у вигляді твердої речовини світложовтого кольору, виділили вакуумною фільтрацією 1 (510 мг, 50 %): H ЯМР (DMSO-d6) δ: 8,67 (s, 2Н), 7,56 (br s, 2H), 3,79 (s, 3Н). 96965 56 Метил 2-амінопіримідин-5-карбоксилат (300 мг, 2,0 ммоль) розвели в метанолі (5 мл), що містить декілька крапель води. Додали літію гідроксид (122 мг, 5,1 ммоль). та реакційну суміш розмішували при 60 °С протягом ночі. Суміш сконцентрували під зниженим тиском, потім розвели у воді та довели до рН 4 за допомогою 1 Μ НСI. 2Амінопіримідин-5-карбонову кислоту, осаджену у вигляді твердої речовини білого кольору, виділили 1 вакуумною фільтрацією (244 мг, 90 %): Н ЯМР (DMSO-d6) δ: 12,73 (1H, br s), 8,63 (2H, s), 7,44 (2H, br s). Проміжний продукт С Одержання 4-(3-хлорпропіл)морфоліну гідрохлориду До розчину 1-бромо-3-хлорпропану (45 г, 0,29 моль) у толуолі (100 мл) додали морфолін (38 г, 0,44 моль). Розчин перемішували при 84 °С протягом 3 год., протягом цього часу утворився осад. Після охолодження до кт осад виділили шляхом вакуумною фільтрацією, промили ефіром, і осад відкинули. Матковий розчин підкислили за допомогою НСI (4 Μ у діоксані, 72 мл, 0.29 моль), що викликало осадження бажаного продукту у вигляді солі НСI. Розчинник видалили під зниженим тиском, і отриману тверду речовину висушили для одержання зазначеної в назві сполуки (53 г, 90 %): 1 Н ЯМР (DMSO-d6) δ: 11,45 (1H, br s), 3,94 - 3,77 (4H, m), 3,74 (2H, t), 3,39 (2H, m), 3,15 (2H, m), 3,03 (2H, m), 2,21 (2H, m). Проміжний продукт D Одержання 2-аміно-4-пропілпіримідин-5карбонової кислоти До розчину етил 2-аміно-4-пропілпіримідин-5карбоксилату (1,0 г, 4,8 ммоль) в МеОН (20 мл) та THF (30 мл) додали 2 н. розчин NaOH (10 мл). Розчин перемішували при кімнатній температурі протягом ночі та потім нейтралізували за допомогою 1 н. НСI (20 мл). Його потім концентрували під зниженим тиском до 30 мл, фільтрували та висушили для одержання бажаного продукту, що використовувався без подальшого очищення (0,6 г, 69 %). Проміжний продукт Δ Одержання 6-аміно-2-метилнікотинової кислоти Суспензію 6-аміно-2-метилнікотинонітрилу (1,0 г, 7,5 ммоль) у водному розчині КОН (20 %, 12 мл) нагрівали зі зворотним холодильником протягом 3 днів. Після цього часу його остудили до кімнатної температури, нейтралізували концентрованою НСI, відфільтрували та висушили для одержання 57 бажаного продукту, що використовувався без подальшого очищення (1,1 г, 96 %). Проміжний продукт F Одержання трет-бутил 2-(2гідроксиетил)морфолін-4-карбокcилату Метилморфолін-2-іл ацетат (5,0 г, 31,4 ммоль) розвели за допомогою THF (10 мл) та води (10 мл) і обробили карбонатом калію (4,34 г, 31,4 ммоль). Густу суспензію повільно перевели в розчин. Додали ди-трет-бутил дикарбонат (6,85 г, 31,4 ммоль), та реакційну суміш перемішували при кт протягом ночі. Потім реакційну суміш екстрагували за допомогою THF та ЕtOАс. Органічний шар висушили (MgSO4) та сконцентрували під зниженим тиском. В'язке масло розтирали за допомогою ефіру, та отриману тверду речовину зібрали вакуумною фільтрацією (3,7 г, 45 %). Суміш розчинили в THF (20 мл) і обробили розчином гідроксиду натрію (2 н., 5 мл) та перемішували протягом ночі. Реакційну суміш сконцентрували під зниженим тиском і потім розвели водою та ЕtOАс. рН водного шару довели до 5, та відокремили органічний шар, висушили (MgSC4) та сконцентрували під зниженим тиском. Потім тверду речовину (2 г, 8,15 ммоль) розчинили в THF (10 мл) і обробили розчином борану (1 Μ у THF, 16 мл, 16.4 ммоль) і суміш перемішували при кт протягом 12 год.. Реакційну суміш потім розвели метанолом (100 мл) та перемішували при кт протягом ночі. Розчин потім сконцентрували під зниженим тиском і потім розчинили за допомогою DCM. Розчин відфільтрували через шар діоксиду кремнію, щоб видалити солі борану, і фільтрат сконцентрували під зниженим тиском для одержання масла (1,8 г, 96 %): МС + 1 ВЕРХ RT = 2,22 хвилини, МН = 232,2; Н ЯМР (DMSO-d6) δ: 4,46 (1H, t), 3,81 - 3,73 (2H, m), 3,72 3,64 (1H, br d), 3,45 (2H, t), 3,40 - 3,29 (3H, m), 2,93 - 2,73 (1H, br s), 1,55 - 1,48 (2H, m), 1,39 (9H,s). Проміжний продукт G Одержання 2-({[третбутил(диметил)силіл]окcи}метил)-4-(3хлорпропіл)морфоліну 96965 58 dd), 3,76-3,63 (2H, m), 3,47-3,32 (2H, m), 3,22 - 3,09 (3H, m), 3,92 (1H, td), 2,76 (1H, t). Стадія 2: Одержання 2-({[трeтбутил(диметил)силіл]окси}метил)морфоліну Морфолін-2-ілметанолу трифторацетат (0,7 г, 3,03 ммоль) в DCM обробили триетиламіном (1,67 мл, 12,1 ммоль) та трeт-бутилдиметилсиліл хлоридом (0,91 г, 6,06 ммоль). Суміш перемішували при кт протягом 2 год. і потім відфільтрували. Фільтрат потім сконцентрували під зниженим тиском, і залишок суспендували в розведеному розчині гідроксиду натрію (10 %, 5 мл), та суміш перемішували протягом 30 хвил. Суміш потім екстрагували DCM та сконцентрували під зниженим тиском до піни. Продукт взяли для наступної Стадії без по1 дальшого очищення: H ЯМР (DMSO-d6) δ: 5,40 5,14 (1Ζ, br s), 3,69 (1H, m), 3,56 - 3,50 (1H, m), 3,46 - 3,3 (3H, m), 3,27 - 2,97 (1H, br s), 2,78 (1H, dd), 2,68-2,55 (2H, m), 2,35 (1H, m), 0,87-0,82 (9H, m), 0,02 (6H, s). Стадія 3: Одержання 2-({[третбутил(диметил)cиліл]окcи}метил)-4-(3-хлорпропіл)морфоліну Розчин 2-({[третбутил(етан)силіл]окси}метил)морфоліну (2,1 г, 9,07 ммоль) в DCM (20 мл) обробили триетиламіном (3,8 мл, 27,2 ммоль) та 1-хлор-3-йодопропаном (1,95 мл, 18,1 ммоль). Реакційну суміш перемішували при кт протягом ночі. Реакційну суміш сконцентрували під зниженим тиском, потім очистили MPLC (ISCO, 0% МеОН/100% DCM до 25% МеОН/75% DCM). Продукт виділили у вигляді масла + (560 мг, 20 %): МС ВЕРХ RT = 2,66 хвилини, ΜΖ = 1 308,4, 310,4; H ЯМР (DMSO-d6) δ: 3,79 - 3,69 (1Ζ, m), 3,63 (2H, t) 3,59 - 3,52 (1H, m), 3,50 - 3,36 (3H, m), 2,73 (1H, d), 2,61 (1H, d), 2,35 (2H, t), 1,94 (1H, td), 1,83 (2H, qt), 1,73 (1H, t), 0,83 (9H, s), 0,00 (6H, s). Проміжний продукт Ζ Одержання 4-[(2-оксидо-1,3,2-діоксатіолан-4іл)метил]морфоліну гідрохлориду Стадія 1: Одержання морфолін-2-ілметанол трифторацетату Розчин трет-бутилу 2(гідроксимeтил)морфолін-4-карбоксилату (1,1 г, 5,06 ммоль) в DCM (15 мл) обробили трифтороцтовою кислотою (2,5 мл, 10,1 ммоль) та перемішували при кт протягом ночі. Реакційну суміш сконцентрували під зниженим тиском для одержання густого масла (1,1 г, 94 %): ЯМР (OMSO-d6) δ: 9,30 (1H, s), 4,95 (1H, s), 4,19 - 4,06 (1H, br s), 3,93 (1H, 3-Морфолін-4-ілпропан-1,2-діол (2,1 г, 9,07 ммоль) розчинили в DCM (15 мл) і остудили до 0 °С. Охолоджений розчин обробили тіонілхлоридом (1,81 мл, 24,8 ммоль) і потім нагріли зі зворотним холодильником протягом 1 год. Реакційну суміш потім сконцентрували під зниженим 1 тиском до твердої речовини (2,5 г, 97 %): Н ЯМР (DMSO-d6) δ: 11,4 (1Н, br s), 5,64-5,55 (1H, m), 4,82 (1H, dd), 4,50 (1H, dd), 4,02 - 3,71 (4H, m), 3,55 3,33 (4H, m), 3,26 - 3,06 (2H, br s). Проміжний продукт I 59 Одержання кислоти. 96965 60 6-(циклопентиламіно)нікотинової 6-Фторнікотинову кислоту (300 мг, 2,13 ммоль) та циклопентиламін (0,84 мл, 8,50 ммоль) об'єднали в безводному THF (5 мл) та триетиламіні (0,59 мл, 4,25 ммоль). Суміш нагрівали при 60 ° протягом 3 днів. Суміш сконцентрували під зниженим тиском, і залишок суспендували у воді. Водну суміш довели до рН 3 за допомогою фосфорної кислоти. Отриманий осад зібрали вакуумною фільтрацією, промили водою, і висушили у вакуумній печі протягом 1 год. при 50 ° для одержання зазначеної в назві сполуки у вигляді твердої речови+ ни (63 мг, 14 %): МС ВЕРХ RT = 1,14 хвилини, МН 1 = 207.2; Н ЯМР (DMSO-d6) δ: 12,29 (1Н, широкий s), 8,50 (1Н, d), 7,73 (1Н, dd), 7,29 (1H, d), 6,42 (1Н, d), 4,16 (1Н, широкий s,), 1,90 (2Н, m), 1,67 (2Н, m), 1,53 (2Н, m), 1,43 (2Н, m). Приклади Приклад 1 Одержання N-[7-метокси-8-(3-морфолін-4ілпропокси)-2,3-дигідроімідазо[1,2-с]хіназолін-5-іл]піримідин-5-карбоксаміду. Стадія 1: Одержання 4-форміл-2-метокси-3нітрофеніл ацетату Димлячу азотну кислоту (2200 мл) під азотом остудили до 0 °С, після чого порціонно додали ваніліну ацетат (528 г, 2,7 моль), підтримуючи внутрішню температуру нижче 10 °С. Через 2 год. отриману суміш остудили на льоді при перемішуванні. Рідкий розчин відфільтрували, і отримані тверді частки промили водою (3 × 100 мл) та висушили на повітрі. Через 2 дні тверді частки нагрівали в DCM (3000 мл) до повного розчинення. Розчин залишили остудитися до кімнатної температури, у цей час по краплях додавали гексани (3000 мл). Тверду речовину відфільтрували, промили гексаном (500 мл) і висушили на повітрі 1 для одержання бажаного продукту (269 г, 41 %): H ЯМР, (DMSO-d6) δ: 9,90 (s, 1H), 7,94 (d, 1H), 7,75 (d, 1H), 3,87 (s, 3H), 2,40 (s, 3H). Стадія 2: Одержання 4-гідрокси-3-метокси-2нітробензальдегіду Суміш 4-форміл-2-метокси-3-нітрофеніл ацетату (438 г, 1,8 моль) та карбонату калію (506 г, 3,7 моль) в МеОН (4000 мл) перемішували при кімнатній температурі протягом 16 год. Реакційну суміш сконцентрували під зниженим тиском для одержання в'язкого масла. Його розчинили у воді, підкислили за допомогою розчину НСI (2 н.) та екстрагували за допомогою ЕtOАс. Органічний шар промили сольовим розчином, висушили (MgSO4) та відфільтрували. Розчинник сконцентрували під зниженим тиском до 1/3 об'єму, та отриману тверду речовину відфільтрували та висушили на повітрі для одержання зазначеної в назві сполуки (317 1 г, 88 %): Н ЯМР (DMSO-d6) δ: 9,69 (1H, s), 7,68 (1H, d), 7,19 (1H, d), 3,82 (3Н, s). Стадія 3: Одержання 4-(бензилокси)-3метокси-2-нітробензальдегіду 4-Гідрокси-3-метокси-2-нітробензальдегід (155 г, 786 ммоль) розчинили в DMF (1500 мл), і перемішуваний розчин обробили карбонатом калію (217 г, 1,57 моль), а потім бензилбромідом (161 г, 0,94 моль). Після перемішування протягом 16 год. реакційну суміш сконцентрували під зниженим тиском та розділили між водою (2 л) та EtOAc (2 л). Органічний шар промили сольовим розчином (3 × 2 л), висушили (сульфат натрію) та сконцентрували під зниженим тиском. Отриману тверду речовину розтирали з Еt2О (1 л) для одержання зазна1 ченої в назві сполуки (220 г, 97 %): H ЯМР (DMSO-d6) δ: 9,77 (1Н, s), 7,87 (1H, d), 7,58 (1H, d), 7,51 (1H, m), 7,49 (1H, m), 7,39 (3Н, m), 5,36 (2Н, s), 3,05 (3Н, s). Стадія 4: Одержання 4-(бензилокси)-3метокси-2-нітробензонітрилу Йод (272 г, 1,1 ммоль) додали до суміші 4(бензилокси)-3-метокси-2-нітробензальдегіду (220 г, 766 ммоль) та гідроксиду амонію (28% розчин, 3 л), розчиненого в THF (5 л). Через 16 год. реакційну суміш обробили сульфітом натрію (49 г, 383 ммоль) та сконцентрували під зниженим тиском для одержання густої суспензії. Густу суспензію відфільтрували, промили водою (250 мл) та висушили для одержання зазначеної в назві сполуки у 1 вигляді твердої речовини (206 г, 95 %): H ЯМР (DMSO-d6) δ: 7,89 (1H, d), 7,59 (1Н, d), 7,49 (2Н, m), 7,40 (3Н, m), 5,35 (2Н, s), 3,91 (3Н, s). Стадія 5: Одержання 2-аміно-4-(бензилокси)-3метоксибензонітрилу
ДивитисяДодаткова інформація
Назва патенту англійською2,3-dihydroimidazo[1,2-c]quinazoline substituted derivatives useful for treating hyper-proliferative and angiogenesis disorders
Автори англійськоюHentemann, Martin, Wood, Jill, Scott, William, Michels, Martin, Campbell, Ann-Marie, Bullion, Ann-Marie, Rowley, R., Bruce, Redman, Aniko
Назва патенту російськоюЗамещенные производные 2,3-дигидроимидазо[1,2-с]хиназолина, полезные для лечения гиперпролиферативных нарушений и болезней, связанных с ангиогенезом
Автори російськоюХентманн Мартин, Вуд Джилл, Скотт Вилльям, Михельс Мартин, Кемпбелл Анн-Мари, Буллион Анн-Мари, Роули Р. Брюс, Редман Анико
МПК / Мітки
МПК: A61K 31/519, C07D 413/14, A61P 35/00, A01N 43/54, C07D 487/04
Мітки: лікування, хвороб, гіперпроліферативних, пов'язаних, корисні, заміщені, порушень, 2,3-дигідроімідазо[1,2-с]хіназоліну, похідні, ангіогенезом
Код посилання
<a href="https://ua.patents.su/48-96965-zamishheni-pokhidni-23-digidroimidazo12-skhinazolinu-korisni-dlya-likuvannya-giperproliferativnikh-porushen-ta-khvorob-povyazanikh-z-angiogenezom.html" target="_blank" rel="follow" title="База патентів України">Заміщені похідні 2,3-дигідроімідазо[1,2-с]хіназоліну, корисні для лікування гіперпроліферативних порушень та хвороб, пов’язаних з ангіогенезом</a>
Попередній патент: Сполуки поліциклічної сечовини з антибактеріальними властивостями
Наступний патент: Спосіб трансакцій грошових коштів
Випадковий патент: Мийно- диспергуюча присадка до мастил для двигунів внутрішнього згоряння та спосіб її одержання












