Селективні модулятори андрогенного рецептора
Номер патенту: 110766
Опубліковано: 10.02.2016
Автори: Томпсон Дейвід П., Андерсон Джеймс Томас, Рікеттс Ентоні П., Унвалла Рейоманд Джал, Чеклер Юджин Лвовіч П'ятніцкі, Вергест Патрік Роберт, Еллсворт Едмунд Л., Еріксон Брюс Кіпп, ілберт Адам Меттью
Формула / Реферат
1. Сполука формули 1, 2 або 3:
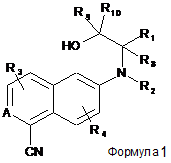 ,
,
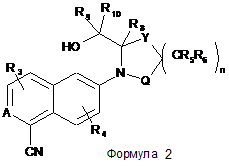 ,
,
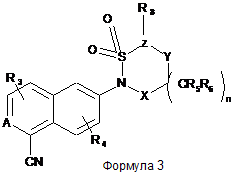 ,
,
в якій А є N або -CR0-, де R0 є гідрогеном, С1-С6-алкілом з лінійним або розгалуженим ланцюгом, С1-С6-перфлуоралкілом з лінійним або розгалуженим ланцюгом, арилом, перфлуорарилом, алкіларилом, гетероарилом або алкілгетероарилом;
X та Y незалежно є -СН2-, -CHRa- або -CRaRb-, де Ra та Rb незалежно є С1-С6-алкілом з лінійним або розгалуженим ланцюгом, арилом, алкіларилом, гетероарилом або алкілгетероарилом; або Ra та Rb разом утворюють ланцюг, що містить -(СН2)j-, -(CHRc)j-, або -(CRcRd)j-, де Rc та Rd незалежно є С1-С6-алкілом з лінійним або розгалуженим ланцюгом, С1-С6-перфлуоралкілом з лінійним або розгалуженим ланцюгом, арилом, алкіларилом, гетероарилом або алкілгетероарилом; де j є 2, 3, 4 або 5;
Z є -CRe- або -N-, де Re є гідрогеномом, С1-С6-алкілом з лінійним або розгалуженим ланцюгом, С1-С6-перфлуоралкілом з лінійним або розгалуженим ланцюгом, арилом, алкіларилом, гетероарилом або алкілгетероарилом;
R1 є гідрогеном, С1-С6-алкілом з лінійним або розгалуженим ланцюгом, арилом, С1-С6-перфлуоралкілом з лінійним або розгалуженим ланцюгом, алкіларилом, гетероарилом, алкілгетероарилом, С1-С6-алкоксикарбонілом з лінійним або розгалуженим ланцюгом, С1-С6-алкіламінокарбоніламіном з лінійним або розгалуженим ланцюгом, С1-С6-алкілоксикарбоніламіно з лінійним або розгалуженим ланцюгом, С1-С6-алкілкарбоніламіно з лінійним або розгалуженим ланцюгом або С1-С6-алкіламінокарбонілом з лінійним або розгалуженим ланцюгом;
R2 незалежно є гідрогеном або С1-С6-алкілом з лінійним або розгалуженим ланцюгом;
R3 та R4 незалежно є гідрогеном, С1-С6-алкілом з лінійним або розгалуженим ланцюгом, С1-С6-перфлуоралкілом з лінійним або розгалуженим ланцюгом, С1-С6перфлуоралкокси з лінійним або розгалуженим ланцюгом, галогеном, ціано, гідроксилом, аміно, карбокси, арилом, гетероарилом, С1-С6-алкоксикарбонілом з лінійним або розгалуженим ланцюгом, С1-С6-алкіламінокарбоніламіном з лінійним або розгалуженим ланцюгом або С1-С6-алкіламінокарбонілом з лінійним або розгалуженим ланцюгом;
R5 та R6 незалежно є гідрогеном або С1-С6-алкілом з лінійним або розгалуженим ланцюгом, С1-С6-перфлуоралкілом з лінійним або розгалуженим ланцюгом, ціано, гідроксилом, аміно, карбокси, арилом, гетероарилом, або R5 та R6 разом утворюють ланцюг, що містить -(СН2)k-, -(CHR7)k- або -(CR7aR7b)k-, де R7, R7a та R7b незалежно є С1-С6-алкілом з лінійним або розгалуженим ланцюгом, С1-С6-перфлуоралкілом з лінійним або розгалуженим ланцюгом, арилом, алкіларилом, гетероарилом або алкілгетероарилом; де k є 2, 3, 4 або 5;
R8 є гідрогеном, С1-С6-алкілом з лінійним або розгалуженим ланцюгом, С1-С6-перфлуоралкілом з лінійним або розгалуженим ланцюгом, арилом, арилом, заміщеним одним, двома або трьома атомами флуору, перфлуорарилом, алкіларилом, гетероарилом або алкілгетероарилом, або R1 та R8 разом утворюють ланцюг, що містить -(CH2)m-, -(CHRf)m-, або -(CRfRg)m-, де Rf та Rg незалежно є С1-С6-алкілом з лінійним або розгалуженим ланцюгом, арилом, алкіларилом, гетероарилом або алкілгетероарилом; де m є 2, 3, 4 або 5;
R9 та R10 незалежно є гідрогеном або С1-С6алкілом з лінійним або розгалуженим ланцюгом, С1-С6-перфлуоралкілом з лінійним або розгалуженим ланцюгом, ціано, гідроксилом, аміно, карбокси, арилом, гетероарилом, або R9 та R10 разом утворюють ланцюг, що містить -(СН2)р-, -(CHRh)p- або -(CRhRi)p-, де Rh та Ri незалежно є С1-С6-алкілом з лінійним або розгалуженим ланцюгом, арилом, алкіларилом, гетероарилом або алкілгетероарилом; де p є 2, 3, 4 або 5;
Q є -СО-, -(СН2)q-, -(CHRs)q- або -(CRsRt)q-, де Rs та Rt незалежно є С1-С6-алкілом з лінійним або розгалуженим ланцюгом, арилом, алкіларилом, гетероарилом або алкілгетероарилом; де q є 0, 1, 2 або 3; та деn є 0, 1, 2, 3, 4 або 5;
або її фармацевтично прийнятна сіль.
2. Сполука за п. 1, яка має формулу 1, в якій R1 та R2 незалежно є С1-С6-алкілом з лінійним або розгалуженим ланцюгом; та R3 та R4 обидва є гідрогеном.
3. Сполука за п. 2, в якій R1 та R2 незалежно є метилом, етилом або пропілом.
4. Сполука за п. 1, яка має формулу 2, в якій Q є -(СН2)q-, -(CHRs)q- або -(CRsRt)q-, де Rs та Rt незалежно є С1-С6алкілом з лінійним або розгалуженим ланцюгом; та q є 1 або 2.
5. Сполука за п. 4, в якій Q є -CO-.
6. Сполука за п. 1, яка має формулу 3, в якій X та Y незалежно є -СН2-, -CHRa- або -CRaRb-, де Ra та Rb незалежно є С1-С6-алкілом з лінійним або розгалуженим ланцюгом, арилом, алкіларилом, гетероарилом або алкілгетероарилом.
7. Сполука за п. 6, в якій X та Y незалежно є -СН2-, -CHRa- або -CRaRb-, де Ra та Rb незалежно є метилом, етилом.
8. Сполука за п. 1, вибрана з групи, що включає:
6-[(3S)-3-метил-1,1-діоксидо-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрил;
6-[(3S)-3-етил-1,1-діоксидо-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрил;
6-[(3R)-1,1-діоксидо-3-(2,2,2-трифлуоретил)-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрил;
6-[(3R)-1,1-діоксидо-3-(2-фенілетил)-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрил;
6-[1-метил-(3S)-3-метил-1,1-діоксидо-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрил;
6-{(3R)-1,1-діоксидо-3-[3-(трифлуорметил)феніл]-1,2,5-тіадіазолідин-2-іл}ізохінолін-1-карбонітрил;
6-[(3S)-3-(4-хлорфеніл)-1,1-діоксидо-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрил;
6-[(3S)-3-метил-1,1-діоксидо-1,2-тіазолідин-2-іл]ізохінолін-1-карбонітрил;
6-[(3S)-3-метил-1,1-діоксидо-1,2,5-тіадіазолідин-2-іл]нафталін-1-карбонітрил;
6-[(4R)-4-метил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил;
6-[(4S)-4-метил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил;
6-{(3R)-1,1-діоксидо-3-(3-феніл)-1,2,5-тіадіазолідин-2-іл}ізохінолін-1-карбонітрил;
6-(4,4-диметил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл)ізохінолін-1-карбонітрил;
6-(6,6-діоксидо-6-тіа-5,7-діазаспіро[2.5]окт-5-ил)ізохінолін-1-карбонітрил;
6-[(4R)-4-(3-метилбензил)-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил;
6-[(4R)-6-етил-4-метил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил;
6-(5-метил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл)ізохінолін-1-карбонітрил;
6-[(4S)-4-(4-метилфеніл)-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил;
6-[(4R)-4-(4-метилфеніл)-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил;
6-[(4S)-4-(3-метилфеніл)-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил;
6-[(4S)-4-етил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил;
6-(1,1-діоксидо-4-пропіл-1,2,6-тіадіазинан-2-іл)ізохінолін-1-карбонітрил,
6-{[(2R,3S)-4,4,4-трифлуор-3-гідроксибутан-2-іл]аміно}ізохінолін-1-карбонітрил;
6-{(2R)-2-[(1R)-2,2,2-трифлуор-1-гідроксіетил]азетидин-1-іл}ізохінолін-1-карбонітрил;
6-{(2S)-2-[(1S)-2,2,2-трифлуор-1-гідроксіетил]азетидин-1-іл}ізохінолін-1-карбонітрил;
6-{метил-[(2R,3R)-4,4,4-трифлуор-3-гідроксибутан-2-іл]аміно}ізохінолін-1-карбонітрил;
6-{метил-[(2R,3S)-4,4,4-трифлуор-3-гідроксибутан-2-іл]аміно}ізохінолін-1-карбонітрил;
6-{(2R)-2-[(1R)-2,2,2-трифлуор-1-гідроксіетил]піперидин-1-іл}ізохінолін-1-карбонітрил;
6-{(2R)-2-[(1S)-2,2,2-трифлуор-1-гідроксіетил]піперидин-1-іл}ізохінолін-1-карбонітрил;
6-{(2R,5R)-2-метил-5-[(1R)-2,2,2-трифлуор-1-гідроксіетил]піролідин-1-іл}ізохінолін-1-карбонітрил;
6-{(2R,5R)-2-[(1R)-1-гідроксіетил]-5-метилпіролідин-1-іл}ізохінолін-1-карбонітрил;
6-{(5R)-2-оксо-5-[(1S)-2,2,2-трифлуор-1-гідроксіетил]піролідин-1-іл}ізохінолін-1-карбонітрил;
6-{(5S)-2-оксо-5-[(1S)-2,2,2-трифлуор-1-гідроксіетил]піролідин-1-іл}ізохінолін-1-карбонітрил;
6-{(2R)-2-[(1R)-2,2,2-трифлуор-1-гідроксіетил]піролідин-1-іл}ізохінолін-1-карбонітрил;
6-{(2R)-2-[(1S)-2,2,2-трифлуор-1-гідроксіетил]піролідин-1-іл}ізохінолін-1-карбонітрил;
6-{(2S)-2-[(1S)-2,2,2-трифлуор-1-гідроксіетил]піролідин-1-іл}ізохінолін-1-карбонітрил;
6-{(2S)-2-[(1R)-2,2,2-трифлуор-1-гідроксіетил]піролідин-1-іл}ізохінолін-1-карбонітрил;
6-{(2S,5S)-2-метил-5-[(1S)-2,2,2-трифлуор-1-гідроксіетил]піролідин-1-іл}ізохінолін-1-карбонітрил;
6-{(2R,5R)-2-[(1S)-1-гідроксіетил]-5-метилпіролідин-1-іл}ізохінолін-1-карбонітрил;
6-((2R,3S)-4,4,4-трифлуор-3-гідроксибутан-2-іламіно)-1-нафтонітрил;
6-((R)-2-((R)-2,2,2-трифлуор-1-гідроксіетил)азетидин-1-іл)-1-нафтонітрил;
6-((S)-2-((S)-2,2,2-трифлуор-1-гідроксіетил)азетидин-1-іл)-1-нафтонітрил;
6-(метил((2R,3R)-4,4,4-трифлуор-3-гідроксибутан-2-іл)аміно)-1-нафтонітрил;
6-(метил((2R,3S)-4,4,4-трифлуор-3-гідроксибутан-2-іл)аміно)-1-нафтонітрил;
6-((R)-2-((R)-2,2,2-трифлуор-1-гідроксіетил)піперидин-1-іл)-1-нафтонітрил;
6-((R)-2-((S)-2,2,2-трифлуор-1-гідроксіетил)піперидин-1-іл)-1-нафтонітрил;
6-((2R,5R)-2-метил-5-((R)-2,2,2-трифлуор-1-гідроксіетил)піролідин-1-іл)-1-нафтонітрил;
6-((2R,5R)-2-((R)-1-гідроксіетил)-5-метилпіролідин-1-іл)-1-нафтонітрил;
6-((R)-2-оксо-5-((S)-2,2,2-трифлуор-1-гідроксіетил)піролідин-1-іл)-1-нафтонітрил;
6-((S)-2-оксо-5-((S)-2,2,2-трифлуор-1-гідроксіетил)піролідин-1-іл)-1-нафтонітрил;
6-((R)-2-((R)-2,2,2-трифлуор-1-гідроксіетил)піролідин-1-іл)-1-нафтонітрил;
6-((R)-2-((S)-2,2,2-трифлуор-1-гідроксіетил)піролідин-1-іл)-1-нафтонітрил;
6-((S)-2-((S)-2,2,2-трифлуор-1-гідроксіетил)піролідин-1-іл)-1-нафтонітрил;
6-((S)-2-((R)-2,2,2-трифлуор-1-гідроксіетил)піролідин-1-іл)-1-нафтонітрил;
6-((2S,5S)-2-метил-5-((S)-2,2,2-трифлуор-1-гідроксіетил)піролідин-1-іл)-1-нафтонітрил та
6-((2R,5R)-2-((S)-1-гідроксіетил)-5-метилпіролідин-1-іл)-1-нафтонітрил,
або її фармацевтично прийнятна сіль.
9. Сполука за п. 1, яка є 6-[(3R)-3-метил-1,1-діоксидо-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрилом, або її фармацевтично прийнятна сіль.
10. Сполука за п. 1, яка є 6-[(3S)-3-метил-1,1-діоксидо-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрилом, або її фармацевтично прийнятна сіль.
11. Сполука за п. 1, яка є 6-[(4R)-4-метил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрилом, або її фармацевтично прийнятна сіль.
12. Сполука за п. 1, яка є 6-[(4S)-4-метил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрилом, або її фармацевтично прийнятна сіль.
13. Сполука за п. 1, яка є 6-(метил-((2R,3R)-4,4,4-трифлуор-3-гідроксибутан-2-іл)аміно)-1-нафтонітрилом, або її фармацевтично прийнятна сіль.
14. Спосіб модулювання активності андрогенного рецептора у суб'єкта, який цього потребує, за яким зазначений андрогенний рецептор піддають контакту з ефективною кількістю сполуки за п. 1, тим самим модулюючи активність зазначеного андрогенного рецептора.
15. Спосіб лікування розладу або стану у суб'єкта, де розлад або стан вибирають з анемії; анорексії; артриту; захворювання кісток; порушення опорно-рухового апарату; кахексії; слабкості; вікового функціонального зниження у літніх людей; дефіциту гормону росту; гематопоетичних розладів; гормонозамісної терапії; втрати сили та/або функції м'язів; м'язової дистрофії; втрати м'язової маси внаслідок хірургічної операції; м'язової атрофії; нейродегенеративних захворювань; нервово-м'язового захворювання; ожиріння; остеопорозу та атрофії м'язів, за яким зазначеному суб'єкту вводять ефективну кількість сполуки за п. 1, тим самим лікуючи зазначене захворювання або стан.
Текст
Реферат: Винахід стосується сполуки формули 1, 2 або 3: R 9 R 10 R 9 R 10 R1 HO R3 N HO R8 CR5 R6 R3 N R2 A R8 Y n Q A R4 R4 Формула 1 CN CN , Формула 2 , R8 O z O S R3 Y N X CR5R6 n A R4 CN Формула 3 , в якій А є N або –CR0-, де R0 є гідрогеном, С1-С6-алкілом з лінійним або розгалуженим ланцюгом тощо, Z є -CRe-, або -N-, де Re є гідрогеном, С1-С6-алкілом з лінійним або розгалуженим ланцюгом тощо; R1 є гідрогеном, С1-С6-алкілом з лінійним або розгалуженим ланцюгом тощо; R2 незалежно є гідрогеном або С1-С6-алкілом з лінійним або розгалуженим ланцюгом; R3 та R4 незалежно є гідрогеном, С1-С6-алкілом з лінійним або розгалуженим ланцюгом тощо; R5 та R6 незалежно є гідрогеном або С1-С6-алкілом з лінійним або розгалуженим ланцюгом тощо; R8 є гідрогеном, С1-С6-алкілом з лінійним або розгалуженим ланцюгом тощо; R9 та R10 незалежно є гідрогеном або С1-С6-алкілом з лінійним або розгалуженим ланцюгом тощо; Q є -CO-, -(CH2)q-, (CHRs)q- або -(CRsRt)q-, де Rs та Rt незалежно є С1-С6-алкілом з лінійним або розгалуженим ланцюгом, арилом, алкіларилом, гетероарилом або алкілгетероарилом; де q є 0, 1, 2 або 3; та де n є 0, 1, 2, 3, 4 або 5; або її фармацевтично прийнятної солі, композицій, що містять такі сполуки; та застосувань таких сполук в лікуванні різних захворювань, зокрема тих, які викликані або опосередковані андрогенним рецептором. UA 110766 C2 5 10 15 20 25 Галузь винаходу Винахід стосується нових гетероциклічних сполук, які є ефективними як селективні модулятори андрогенного рецептору (SARM). Винахід також стосується композицій, що містять селективні модулятори андрогенного рецептору, та способів одержання таких сполук. Крім того, винахід стосується застосування даних сполук в лікуванні захворювань або розладів, що пов’язані з модулюванням андрогенного рецептору. Передумови створення винаходу Андрогенний рецептор ("AR") представляє собою ліганд-активований транскрипційний регуляторний протеїн, який опосередковує індукцію чоловічого статевого розвитку та функцію за рахунок його активності з ендогенними андрогенами. Андрогенні стероїди відіграють важливу роль в багатьох фізіологічних процесах, включаючи розвиток та підтримування чоловічих статевих характеристик, таких як м’язова та кісткова маса, ріст передміхурової залози, сперматогенез, та волосіння за чоловічим типом. Ендогенні стероїдні андрогени включають тестостерон та дигідротестостерон ("DHT"). Стероїдні ліганди, які зв’язують AR та діють як андрогени (наприклад, тестостерону енантат) або як антиандрогени (наприклад, ципротерону ацетат), є відомими протягом багатьох років та застосовуються клінічно. Необхідними є нові сполуки, які є прийнятними для лікування та/або попередження різних гормон-залежних станів, наприклад, станів, пов’язаних зі зниженням рівня андрогену, таких як, зокрема, анемія; анорексія; артрит; захворювання кісток; порушення опорно-рухового апарату ; кахексія; слабкість; вікові функціональні зниження у літніх людей; дефіцит гормону росту; гематопоетичні розлади; гормон-замісна терапія; втрата сили та/або функції м’язів; м’язові дистрофії; втрата м’язової маси внаслідок хірургічної операції; м’язова атрофія; нейродегенеративні захворювання; нервово-м’язові захворювання; ожиріння; остеопороз; та, атрофія м’язів. Суть винаходу Винахід передбачає сполуку формули 1, 2 або 3: Формула 1 Формула 2 Формула 3 1 UA 110766 C2 5 10 15 20 25 30 35 40 45 50 55 60 де A є N або -CR0-, де R0 є гідрогеномом, C1-C6-алкілом з лінійним або розгалуженим ланцюгом, C1-C6-перфлуоралкілом з лінійним або розгалуженим ланцюгом, арилом, перфлуорарилом, алкіларилом, гетероарилом; або, алкілгетероарилом; X та Y незалежно є -CH2-, -CHRa- або CRaRb-, де Ra та Rb незалежно є C1-C6-алкілом з лінійним або розгалуженим ланцюгом, арилом, алкіларилом, гетероарилом або алкілгетероарилом; або, R a та Rb разом утворюють ланцюг, що містить -(CH2)j-, -(CHRc)j-, або -(CRcRd)j-, де Rc та Rd незалежно є C1-C6-алкілом з лінійним або розгалуженим ланцюгом, C1-C6-перфлуоралкілом з лінійним або розгалуженим ланцюгом, арилом, алкіларилом, гетероарилом або алкілгетероарилом; де j є 2; 3, 4 або 5; Z є -CRe- або N-, де Re є гідрогеномом, C1-C6-алкілом з лінійним або розгалуженим ланцюгом, C1-C6перфлуоралкілом з лінійним або розгалуженим ланцюгом, арилом, алкіларилом, гетероарилом або алкілгетероарилом; R1 є гідрогеномом, C1-C6-алкілом з лінійним або розгалуженим ланцюгом, арилом, C1-C6-перфлуоралкілом з лінійним або розгалуженим ланцюгом, алкіларилом, гетероарилом, алкілгетероарилом, C 1-C6-алкоксикарбонілом з лінійним або розгалуженим ланцюгом, C1-C6-алкіламінокарбоніламіном з лінійним або розгалуженим ланцюгом, C1-C6-алкілоксикарбоніламіно з лінійним або розгалуженим ланцюгом, C 1-C6алкілкарбоніламіно з лінійним або розгалуженим ланцюгом, або, C 1-C6-алкіламінокарбонілом з лінійним або розгалуженим ланцюгом; R2 незалежно є гідрогеном або C1-C6-алкілом з лінійним або розгалуженим ланцюгом; R3 та R4 незалежно є гідрогеном, C1-C6-алкілом з лінійним або розгалуженим ланцюгом, C1-C6-перфлуоралкілом з лінійним або розгалуженим ланцюгом, C 1C6-перфлуоралкокси з лінійним або розгалуженим ланцюгом, галогеном, ціано, гідроксилом, аміно, карбокси, гідроксилом, арилом, гетероарилом, C 1-C6-алкоксикарбонілом з лінійним або розгалуженим ланцюгом, C1-C6-алкіламінокарбоніламіном з лінійним або розгалуженим ланцюгом, або, C1-C6-алкіламінокарбонілом з лінійним або розгалуженим ланцюгом; R5 та R6 незалежно є гідрогеном або C1-C6-алкілом з лінійним або розгалуженим ланцюгом, C1-C6перфлуоралкілом з лінійним або розгалуженим ланцюгом, ціано, гідроксилом, аміно, карбокси, гідроксилом, арилом, гетероарилом, або, R5 та R6 разом утворюють ланцюг, що містить -(CH2)k-, -(CHR7)k-, або -(CR7aR7b)k-, де R7, R7a, та R7b незалежно є C1-C6-алкілом з лінійним або розгалуженим ланцюгом, C1-C6-перфлуоралкілом з лінійним або розгалуженим ланцюгом, арилом, алкіларилом, гетероарилом або алкілгетероарилом; де k є 2; 3, 4 або 5; R 8 є гідрогеномом, C1-C6-алкілом з лінійним або розгалуженим ланцюгом, C1-C6-перфлуоралкілом з лінійним або розгалуженим ланцюгом, арилом, арилом, заміщеним одним, двома або трьома атомами флуору, перфлуорарилом, алкіларилом, гетероарилом; або, алкілгетероарилом; або, R1 та R8 разом утворюють ланцюг, що містить -(CH2)m-, -(CHRf)m-, або -(CRfRg)m-, де Rf та Rg незалежно є C1-C6-алкілом з лінійним або розгалуженим ланцюгом, арилом, алкіларилом, гетероарилом або алкілгетероарилом; де m є 2; 3, 4 або 5; R 9 та R10 незалежно є гідрогеном або C1-C6-алкілом з лінійним або розгалуженим ланцюгом, C1-C6-перфлуоралкілом з лінійним або розгалуженим ланцюгом, ціано, гідроксилом, аміно, карбокси, гідроксилом, арилом, гетероарилом, або, R9 та R10 разом утворюють ланцюг, що містить -(CH2)p-, -(CHRh)p-, або (CRhRi)p-, де Rh та Ri незалежно є C1-C6-алкілом з лінійним або розгалуженим ланцюгом, арилом, алкіларилом, гетероарилом або алкілгетероарилом; де p є 2; 3, 4 або 5; Q є -CO-, (CH2)q-, -(CHRs)q-, або -(CRsRt)q-, де Rs та Rt незалежно є C1-C6-алкілом з лінійним або розгалуженим ланцюгом, арилом, алкіларилом, гетероарилом або алкілгетероарилом; де q є 0, 1, 2, або 3; та, де n є 0, 1, 2, 3, 4 або 5; або її фармацевтично прийнятну сіль. Детальний опис винаходу Винахід стосується нових сполук, які є селективними модуляторами андрогенного рецептору, прийнятного для лікування захворювань та станів, пов’язаних з дефіцитом андрогенної та/або анаболічної активності. Винахід, крім того, передбачає фармацевтичні композиції, які містять такі SARM, а також способи лікування та/або попередження таких захворювань та станів. Відповідно, винахід передбачає сполуку, що має формулу 1, в якій R 1 та R2 незалежно є C1-C6-алкілом з лінійним або розгалуженим ланцюгом; та, R3 та R4 обидва є гідрогеном. В конкретному варіанті здійснення в сполуці, що має формулу 1, R 1 та R2 незалежно є метилом, етилом або пропілом. В іншому варіанті здійснення в сполуці, що має формулу 2, Q є -(CH2)q-, -(CHRs)q-, або -(CRsRt)q-, де Rs та Rt незалежно є C1-C6-алкілом з лінійним або розгалуженим ланцюгом; та, q є 1 або 2. В ще іншому варіанті здійснення в сполуці, що має формулу 2, Q є -CO-. В конкретному варіанті здійснення в сполуці, що має формулу 3, X та Y незалежно є -CH2-, CHRa- або -CRaRb-, де Ra та Rb незалежно є C1-C6-алкілом з лінійним або розгалуженим ланцюгом, арилом, алкіларилом, гетероарилом або алкілгетероарилом. В іншому варіанті здійснення в сполуці, що має формулу 3, X та Y незалежно є -CH2-, -CHRa- або -CRaRb-, де Ra та 2 UA 110766 C2 5 10 15 20 25 30 35 40 45 50 55 60 Rb незалежно є метилом або етилом. В певних конкретних варіантах здійснення, сполуку за винаходом вибирають з групи, що включає: 6-[(3S)-3-метил-1,1-діоксидо-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрил; 6-[(3S)-3-етил-1,1-діоксидо-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрил 6-[(3R)-1,1-діоксидо-3-(2,2,2-трифлуоретил)-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрил; 6-[(3R)-1,1-діоксидо-3-(2-фенілетил)-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрил; 6-[1-метил-(3S)-3-метил-1,1-діоксидо-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрил; 6-{(3R)-1,1-діоксидо-3-[3-(трифлуорметил)феніл]-1,2,5-тіадіазолідин-2-іл}ізохінолін-1карбонітрил; 6-[(3S)-3-(4-хлорфеніл)-1,1-діоксидо-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрил; 6-[(3S)-3-метил-1,1-діоксидо-1,2-тіазолідин-2-іл]ізохінолін-1-карбонітрил; 6-[(3S)-3-метил-1,1-діоксидо-1,2,5-тіадіазолідин-2-іл]нафталін-1-карбонітрил; 6-[(4R)-4-метил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил; 6-[(4S)-4-метил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил; 6-{(3R)-1,1-діоксидо-3-(3-феніл)-1,2,5-тіадіазолідин-2-іл}ізохінолін-1-карбонітрил; 6-(4,4-диметил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл)ізохінолін-1-карбонітрил; 6-(6,6-діоксидо-6-тіа-5,7-діазаспіро[2.5]окт-5-іл)ізохінолін-1-карбонітрил; 6-[(4R)-4-(3-метилбензил)-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил; 6-[(4R)-6-етил-4-метил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил; 6-(5-метил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл)ізохінолін-1-карбонітрил; 6-[(4S)-4-(4-метилфеніл)-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил; 6-[(4R)-4-(4-метилфеніл)-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил; 6-[(4S)-4-(3-метилфеніл)-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил; 6-[(4S)-4-етил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил; та 6-(1,1-діоксидо-4-пропіл-1,2,6-тіадіазинан-2-іл)ізохінолін-1-карбонітрил, або її фармацевтично прийнятну сіль. В певних конкретних варіантах здійснення, сполуку за винаходом вибирають з групи, що включає: 6-{[(2R,3S)-4,4,4-трифлуор-3-гідроксибутан-2-іл]аміно}ізохінолін-1-карбонітрил; 6-{(2R)-2-[(1R)-2,2,2-трифлуор-1-гідроксіетил]азетидин-1-іл}ізохінолін-1-карбонітрил; 6-{(2S)-2-[(1S)-2,2,2-трифлуор-1-гідроксіетил]азетидин-1-іл}ізохінолін-1-карбонітрил; 6-{метил[(2R,3R)-4,4,4-трифлуор-3-гідроксибутан-2-іл]аміно}ізохінолін-1-карбонітрил; 6-{метил[(2R,3S)-4,4,4-трифлуор-3-гідроксибутан-2-іл]аміно}ізохінолін-1-карбонітрил; 6-{(2R)-2-[(1R)-2,2,2-трифлуор-1-гідроксіетил]піперидин-1-іл}ізохінолін-1-карбонітрил; 6-{(2R)-2-[(1S)-2,2,2-трифлуор-1-гідроксіетил]піперидин-1-іл}ізохінолін-1-карбонітрил; 6-{(2R,5R)-2-метил-5-[(1R)-2,2,2-трифлуор-1-гідроксіетил]піролідин-1-іл}ізохінолін-1карбонітрил; 6-{(2R,5R)-2-[(1R)-1-гідроксіетил]-5-метилпіролідин-1-іл}ізохінолін-1-карбонітрил; 6-{(5R)-2-оксо-5-[(1S)-2,2,2-трифлуор-1-гідроксіетил]піролідин-1-іл}ізохінолін-1-карбонітрил; 6-{(5S)-2-оксо-5-[(1S)-2,2,2-трифлуор-1-гідроксіетил]піролідин-1-іл}ізохінолін-1-карбонітрил; 6-{(2R)-2-[(1R)-2,2,2-трифлуор-1-гідроксіетил]піролідин-1-іл}ізохінолін-1-карбонітрил; 6-{(2R)-2-[(1S)-2,2,2-трифлуор-1-гідроксіетил]піролідин-1-іл}ізохінолін-1-карбонітрил; 6-{(2S)-2-[(1S)-2,2,2-трифлуор-1-гідроксіетил]піролідин-1-іл}ізохінолін-1-карбонітрил; 6-{(2S)-2-[(1R)-2,2,2-трифлуор-1-гідроксіетил]піролідин-1-іл}ізохінолін-1-карбонітрил; 6-{(2S,5S)-2-метил-5-[(1S)-2,2,2-трифлуор-1-гідроксіетил]піролідин-1-іл}ізохінолін-1карбонітрил; 6-{(2R,5R)-2-[(1S)-1-гідроксіетил]-5-метилпіролідин-1-іл}ізохінолін-1-карбонітрил; 6-((2R,3S)-4,4,4-трифлуор-3-гідроксибутан-2-іламіно)-1-нафтонітрил; 6-((R)-2-((R)-2,2,2-трифлуор-1-гідроксіетил)азетидин-1-іл)-1-нафтонітрил; 6-((S)-2-((S)-2,2,2-трифлуор-1-гідроксіетил)азетидин-1-іл)-1-нафтонітрил 6-(метил((2R,3R)-4,4,4-трифлуор-3-гідроксибутан-2-іл)аміно)-1-нафтонітрил; 6-(метил((2R,3S)-4,4,4-трифлуор-3-гідроксибутан-2-іл)аміно)-1-нафтонітрил; 6-((R)-2-((R)-2,2,2-трифлуор-1-гідроксіетил)піперидин-1-іл)-1-нафтонітрил; 6-((R)-2-((S)-2,2,2-трифлуор-1-гідроксіетил)піперидин-1-іл)-1-нафтонітрил; 6-((2R,5R)-2-метил-5-((R)-2,2,2-трифлуор-1-гідроксіетил)піролідин-1-іл)-1-нафтонітрил; 6-((2R,5R)-2-((R)-1-гідроксіетил)-5-метилпіролідин-1-іл)-1-нафтонітрил; 6-((R)-2-оксо-5-((S)-2,2,2-трифлуор-1-гідроксіетил)піролідин-1-іл)-1-нафтонітрил; 6-((S)-2-оксо-5-((S)-2,2,2-трифлуор-1-гідроксіетил)піролідин-1-іл)-1-нафтонітрил; 6-((R)-2-((R)-2,2,2-трифлуор-1-гідроксіетил)піролідин-1-іл)-1-нафтонітрил; 3 UA 110766 C2 5 10 15 20 25 30 35 40 6-((R)-2-((S)-2,2,2-трифлуор-1-гідроксіетил)піролідин-1-іл)-1-нафтонітрил; 6-((S)-2-((S)-2,2,2-трифлуор-1-гідроксіетил)піролідин-1-іл)-1-нафтонітрил; 6-((S)-2-((R)-2,2,2-трифлуор-1-гідроксіетил)піролідин-1-іл)-1-нафтонітрил; 6-((2S,5S)-2-метил-5-((S)-2,2,2-трифлуор-1-гідроксіетил)піролідин-1-іл)-1-нафтонітрил; та 6-((2R,5R)-2-((S)-1-гідроксіетил)-5-метилпіролідин-1-іл)-1-нафтонітрил або її фармацевтично прийнятну сіль. Особливо переважні варіанти здійснення включають 6-[(3R)-3-метил-1,1-діоксидо-1,2,5тіадіазолідин-2-іл]ізохінолін-1-карбонітрил, 6-[(3S)-3-метил-1,1-діоксидо-1,2,5-тіадіа золідин-2іл]ізохінолін-1-карбонітрил, 6-[(4R)-4-метил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1карбонітрил, 6-[(4S)-4-метил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил та 6(метил-((2R,3R)-4,4,4-трифлуор-3-гідроксибутан-2-іл)аміно)-1-нафто нітрил або їх фармацевтично прийнятна сіль. Винахід, крім того, передбачає фармацевтичну композицію, яка містить: сполуку, що має формулу 1, 2 або 3, або її фармацевтично прийнятну сіль; та фармацевтичні прийнятний носій. Винахід, до того ж, передбачає спосіб модулювання активності андрогенного рецептору у суб’єкта, який цього потребує, який включає контактування зазначеного андрогенного рецептору з ефективною кількістю сполуки, що має формулу 1, 2 або 3, таким чином, модулюючи активність зазначеного андрогенного рецептору. Винахід крім того, передбачає спосіб лікування розладу або стану, пов’язаного з дисрегуляцією андрогенного рецептору у суб’єкта, який включає введення суб’єкту терапевтично ефективної кількості сполуки, що має формулу 1, 2 або 3. В певних варіантах здійснення, розлад або стан, який лікують за цим способом, вибирають серед анемії; анорексії; артриту; захворювання кісток; порушення опорно-рухового апарату ; кахексії; слабкості; вікового функціонального зниження у літніх людей; дефіциту гормону росту; гематопоетичних розладів; гормон-замісної терапії; втрати сили та/або функції м’язів; м’язової дистрофії; втрати м’язової маси внаслідок хірургічної операції; м’язової атрофії; нейродегенеративних захворювань; нервово-м’язових захворювань; ожиріння; остеопорозу; та атрофії м’язів. Сполуки за винаходом можуть одержувати відповідно до способів, описаних в даному документі, з комерційно доступних вихідних речовин, сполук, відомих в літературі, або проміжних сполук, які легко одержати, шляхом застосування стандартних синтетичних способів та методик, відомих кваліфікованому фахівцю в даній галузі з рівня техніки. Стандартні синтетичні способи та методики для одержання органічних молекул та перегрупування та перетворення функціональної групи легко можуть бути отримані з відповідної найкової літератури або із загальноприйнятих підручників в даній галузі. Слід мати на увазі, що, коли надаються типові або переважні умови процесу (тобто, температури реакцій, час, мольне співвідношення компонентів, розчинники, тиски, тощо); то також можуть застосовувати інші умови процесу, якщо не вказано інше. Оптимальні умови реакції можуть варіювати в залежності від конкретних реагентів або розчинника, що використовують. Кваліфікованому фахівцю в даній галузі буде зрозуміло, що характер та порядок представлених стадій синтезу можуть варіювати з метою оптимізації утворення сполук, описаних в даному документі. Відповідно, загальні схеми реакції, представлені в даному документі, ілюструють одержання сполук за винаходом. Якщо не вказано інше, змінні замісники, які використовують в схемах реакції та обговоренні, яке додається, є визначеними такими, як зазначено вище. 4 UA 110766 C2 Pd-каталізатор, ліганд, основа MsCl, основа 1) зняття захисту 2) умови алкілування або ацилювання ClSO 2NHBoc, основа VII 5 10 15 Броміди загальної формули I сполучають з аміноспиртами II в умовах сполучення, таких як умови сполучення, що каталізуються Pd. Гідроксильні групи сполук III активують як групи, що відщеплюються, шляхом утворення мезилата, серед інших способів, в присутності основи, отримуючи сполуки IV. Обробка сполук IV реагентом V дає Boc-захищені проміжні сполуки VI. Зняття захисних Boc-груп, з наступним алкілуванням або ацилюванням проміжних NH сполук завершує синтез хімічного класу сполук загальної формули VII. Одержання продуктів VII з R 3 та R4, що мають незахищені аміно, гідроксильні або карбоксильні групи, повинні потребувати захисту відповідних функціональностей, використовуючи стандартні способи органічної хімії, та зняття захисту у відповідний момент послідовності синтезу. Одержання сполук з A, який є карбоном, ілюструється синтезом 6-[(3S)-3-метил-1,1діоксидо-1,2-тіазолідин-2-іл]ізохінолін-1-карбонітрилу (Приклад 8). Коли Z (Формула 3) не є N, повинна застосовуватись альтернативна методика до тієї, що описана вище. Одержання сполук з A, який є карбоном, ілюструється синтезом 6-[(3S)-3-(4хлорфеніл)-1,1-діоксидо-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрилу. 5 UA 110766 C2 SOCl2 MeOH IX VIII Відновлюючий агент X XI Pd-каталізатор, ліганд, основа Me 3Si-CF3 або M-R10 IBX XII XIII або 5 10 15 Амінокислоти VIII перетворюють в метилові естери IX за стандартними протоколами утворення хлорангідридів кислоти. Естери IX піддають перетворенням у відповідні кетони (або альдегіди) X, застосовуючи нуклеофільні реагенти M-R9, що надають фрагменти R9. Альтернативний підхід щодо одержання кетонів X повинен бути таким, що застосовує функціональні еквіваленти, такі як аміди Вайнреба, які є описаними в літературі з органічної хімії. Кето або альдегідні групи відновлюють, одержуючи аміноспирти XI, які сполучають з бромідом I в умовах, що каталізуються Pd. Гідроксильні групи сполук XII окиснюють, одержуючи кето або альдегідні сполуки XIII, які обробляють або CF 3-групою, яка надається реагентами, або нуклеофільними реагентами M-R10, що містять фрагменти R10. Продукт XIV містить R10 функціональність, де R10 може бути представлений CF3 або іншою групою, описаною в формулі винаходу. Одержання продуктів XIV з R3, R4, R5, R6, R8, R9, та R10, що містять незахищені NH, OH або COOH групи повинні потребувати захисту відповідних функціональностей, використовуючи стандартні способи органічної хімії та зняття захисту у відповідний момент в послідовності синтезу. 6 UA 110766 C2 Pd-каталізатор, ліганд, основа TBDMS-Cl XV XVI R 2-Hal XVII XVIII XIX або IBX Me 3Si-CF3 або M-R10 XXI 5 10 15 20 25 30 Аміноспирти XV сполучають з бромідів I в умовах сполучення, таких як амідні умови сполучення, що каталізується Pd. Гідроксильні групи XVI захищають TBDMS або подібними групами, та NH група XVII може бути модифікована шляхом введення R 2. Захисні групи в XVIII видаляють, одержуючи в результаті аміноспирт XIX. Гідроксильні групи XIX окиснюють, одержуючи кето або альдегідні сполуки XX, які обробляють або CF 3-групою, що містить реагент, або нуклеофільними реагентами M-R10, що містять фрагменти R10. Продукти XXI містять R10 функціональність, де R10 може бути представленим CF3 або іншою групою, описаною в формулі винаходу. Одержання продуктів XXIII з R1, R2, R3, R8, R9, та R10, які містять незахищені NH, OH або COOH групи, повинні потребувати захисту відповідних функціональностей, використовуючи стандартні способи органічної хімії, та зняття захисту у відповідний момент в послідовності синтезу. Процеси, описані в даному документі, можуть контролювати відповідно до будь-якого прийнятного способу, відомого в даній галузі з рівня техніки. Наприклад, утворення продукту можуть контролювати застосовуючи спектроскопічні методи, такі як спектроскопія ядерно1 13 магнітного резонансу (наприклад, H або C), інфрачервона спектроскопія, спектрофотометрія (наприклад, електронна спектроскопія поглинання), мас-спектрометрія, або застосовуючи хроматографію, таку як високо ефективна рідинна хроматографія (ВЕРХ), газова хроматографія (ГХ), гель-проникаюча хроматографія (ГПХ), або тонкошарова хроматографія (ТШХ). Одержання сполук може включати захист та зняття захисту з різних хімічних груп. Хімія захисних груп може бути знайдена, наприклад, в Greene et al., Protective Groups in Organic Synthesis, 4th. Ed. (John Wiley & Sons, 2007), повне розкриття якого є включеним в даний документ шляхом посилання для всіх цілей. Якщо в даному документі не вказано інше, наукові та технічні терміни, які застосовують в представленому винаході, мають значення, які як правило, є зрозумілими кваліфікованому фахівцю в даній галузі. Фраза “терапевтично ефективний” призначена, щоб визначати кількість сполуки або фармацевтичної композиції, або сумарну кількість активних інгредієнтів у випадку комбінованої терапії. Дана кількість або сумарна кількість буде досягати мети лікування відповідного стану. Термін “лікування”, як використовується в даному документі, щоб описати винахід та крім випадків, обумовлених особливо, означає введення сполуки, фармацевтичної композиції або 7 UA 110766 C2 5 10 15 20 25 30 35 40 45 50 55 60 комбінації для здійснення профілактичного, паліативного, підтримуючого, відновлюючого або радикального лікування. Термін лікування охоплює будь-які об’єктивні або суб’єктивні покращення у суб’єкта по відношенню до відповідного стану або захворювання. Термін “профілактичне лікування”, як використовується в даному документі, щоб описати винахід, означає, що сполуку, фармацевтичну композицію або комбінацію вводять суб’єкту, щоб стримати або призупинити відповідний, який проявляється у суб’єкта, зокрема у суб’єкта або представника населення, що є в значній мірі схильним до відповідного стану. Термін “алкіл”, самостійно або в комбінації, означає ациклічну, насичену вуглеводневу групу формули CnH2n+1, яка може бути лінійною або розгалуженою. Приклади таких груп включають метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, втор-бутил, трет-бутил, пентил, ізо-аміл та гексил. Якщо не передбачено інше, алкільна група містить від 1 до 6 атомів карбону. Кількість атомів карбону в алкілі та різних інших фрагментах, що містять вуглеводневу групу, вказують у вигляді префіксу, що вказує меншу та більшу кількість атомів карбону в фрагменті, іншими словами, префікс Ci-Cj позначає фрагмент, що включає від цілого числа "i" до цілого числа "j" атомів карбону. Таким чином, наприклад, C1-C6-алкіл стосується алкілу, що включає від одного до шести атомів карбону. Термін “гідрокси”, як використовується в даному документі, означає OH радикал. Термін “гетероциклічний” стосується насиченого або частково насиченого (тобто, неароматичного) гетероцикла, який може бути приєднаним через атом нітрогену кільця (коли гетероцикл є приєднаним до атому карбону) або атом карбону кільця (в усіх випадках). Аналогічним чином, коли заміщений, замісник може бути розташованим на атомі нітрогену кільця (якщо замісник є приєднаним через атом карбону) або на атомі карбону кільця (в усіх випадках). Конкретні приклади включають оксираніл, азирідиніл, оксетаніл, азетидиніл, тетрагідрофураніл, піролідиніл, тетрагідропіраніл, піперидиніл, 1,4-діоксаніл, морфолінил, піперазиніл, азепаніл, оксепаніл, оксазепаніл та діазепініл. Термін “гетероарил” стосується ароматичного гетероцикла, який може бути приєднаним через атом карбону кільця (в усіх випадках) або атом нітрогену кільця з відповідною валентністю (коли гетероцикл є приєднаним до атому карбону). Аналогічним чином, коли заміщений, замісник може бути розташованим на атомі карбону кільця (в усіх випадках) або атомі нітрогену кільця з відповідною валентністю (якщо замісник є приєднаним через атом карбону). Конкретні приклади включають тієніл, фураніл, піроліл, піразоліл, імідазоліл, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, триазоліл, оксадіазоліл, тіадіазоліл, тетразоліл, піридил, піридазиніл, піримідиніл та піразиніл. Термін "циклоалкіл" означає моноциклічну, насичену вуглеводневу групу формули C nH2n-1. Приклади включають циклопропіл, циклобутил, циклопентил, циклогексил та циклогептил. Якщо не передбачено інше, циклоалкільна група містить від 3 до 8 атомів карбону. Термін “оксо” означає оксиген, приєднаний подвійним зв’язком. Термін “алкокси” означає радикал, що містить алкільний радикал, який є зв’язаним з атомом оксигену, такий як метокси радикал. Приклади таких радикалів включають метокси, етокси, пропокси, ізопропокси, бутокси та трет-бутокси. Термін “галоген” означає флуор, хлор, бром або йод. Як використовується в даному документі, терміни “спів-введення”, “спів-введений” та “в комбінації з”, стосовно комбінації сполуки формули 1, 2 або 3 та одного або більше інших терапевтичних агентів, включає наступне: a. одночасне введення такої комбінації сполуки формули 1, 2 або 3 та додаткового терапевтичного агента пацієнту, який потребує такого лікування, коли такі компоненти формулюють разом в одну дозовану форму, яка вивільняє зазначені компоненти фактично в один і той же час у зазначеному пацієнті, b. фактично одночасне введення такої комбінації сполуки формули 1, 2 або 3 та додаткового терапевтичного агента пацієнту, який потребує такого лікування, коли такі компоненти формулюють окремо один від одного в окремих дозованих формах, які беруться фактично в один і той же час зазначеним пацієнтом, після чого зазначені компоненти вивільняються фактично в один і той же час у зазначеному пацієнті, c. послідовне введення такої комбінації сполуки формули 1, 2 або 3 та додаткового терапевтичного агента пацієнту, який потребує такого лікування, коли такі компоненти формулюють окремо один від одного в окремих дозованих формах, які беруться послідовно один за одним зазначеним пацієнтом зі значним часовим інтервалом між кожним введенням, після чого зазначені компоненти вивільняються фактично в різний час в зазначеному пацієнті; та, d. послідовне введення такої комбінації сполуки формули 1, 2 або 3 та додаткового терапевтичного агента пацієнту, який потребує такого лікування, коли такі компоненти 8 UA 110766 C2 5 10 15 20 25 30 35 40 45 50 55 60 формулюють разом в одну дозовану форму, яка вивільняє зазначені компоненти за контрольованим способом. Термін ’ексципієнт’ використовують в даному документі, щоб описати будь-який інший інгредієнт, ніж сполука формули 1, 2 або 3. Вибір ексципієнта буде в значній мірі залежати від чинників, таких як конкретний спосіб введення, вплив ексципієнта на розчинність та стабільність та природа лікарської форми. Термін “ексципієнт” охоплює розріджувач, носій або ад’ювант. Одним зі способів здійснення винаходу є введення сполуки формули 1, 2 або 3 в формі проліків. Таким чином, деякі похідні сполук формули 1, 2 або 3, які можуть мати невелику або не мають фармакологічної активності самі по собі, можуть, при введенні в організм або на тіло, бути перетвореними в сполуку формули 1, 2 або 3, що має необхідну активність, наприклад, шляхом гідролітичного розщеплення, зокрема, гідролітичним розщепленням, яке стимулюється естеразним або пептідазним ферментом. Такі похідні називаються як "проліки". Додаткова інформація щодо застосування проліків може бути знайдена в ‘Pro-drugs as Novel Delivery Systems’, Vol. 14, ACS Symposium Series (T. Higuchi та W. Stella) та ‘Bioreversible Carriers in Drug Design’, Pergamon Press, 1987 (Ed. E. B. Roche, American Pharmaceutical Association). Крім того, посилання може бути зроблене на Nature Reviews/Drug Discovery, 2008, 7, 355 та Current Opinion in Drug Discovery and Development, 2007, 10, 550. Проліки відповідно до винаходу, наприклад, можуть отримувати шляхом заміщення відповідних функціональностей, присутніх в сполуках формули 1, 2 або 3 на певні фрагменти, відомі кваліфікованому фахівцю в даній галузі з рівня техніки як ‘про-фрагменти’, як описано, наприклад, в ‘Design of Prodrugs’ H. Bundgaard (Elsevier, 1985). Таким чином, проліки відповідно до винаходу є (a) естерною або амідною похідною карбонової кислоти в сполуці формули 1, 2 або I3; (b) естерною, карбонатною, карбаматною, фосфатною або екерною похідною гідроксильної групи в сполуці формули 1, 2 або 3; (c) амідною, імінною, карбаматною або амінною похідною аміно групи в сполуці з формулою 1, 2 або 3; (d) тіоестерною, тіокарбонатною, тіокарбаматною або сульфідною похідними тіольної групи в сполуці формули 1, 2 або 3; або (e) оксимною або імінною похідною карбонільної групи в сполуці формули 1, 2 або 3. Деякі конкретні приклади проліків відповідно до винаходу включають: (i) коли сполука формули 1, 2 або 3 містить карбоксильну функціональність (-COOH), її естер, такий як сполука, в якій гідроген карбоксильної функціональності сполуки формули 1, 2 або 3 заміщується на C1-C8-алкіл (наприклад, етил) або (C1-C8-алкіл)C(=O)OCH2- (наприклад, t BuC(=O)OCH2-); (ii) коли сполука формули 1, 2 або 3 містить спиртову функціональність (-OH), її естер, такий як сполука, в якій гідроген спиртової функціональності сполуки формули 1, 2 або 3 заміщується на -CO(C1-C8-алкіл) (наприклад, метилкарбоніл) або спирт етерефікують амінокислотою; (iii) коли сполука формули 1, 2 або 3 містить спиртову функціональність (-OH), її етер, такий як сполука, в якій гідроген спиртової функціональності сполуки формули 1, 2 або 3 заміщується на (C1-C8-алкіл)C(=O)OCH2- або -CH2OP(=O)(OH)2; (iv) коли сполука формули 1, 2 або 3 містить спиртову функціональність (-OH), її фосфат, такий як сполука, в якій гідроген спиртової функціональності сполуки формули 1, 2 або 3 2+ заміщується на -P(=O)(OH)2, або -P(=O)(ONa)2, або -P(=O)(O )2Ca ; (v) коли сполука формули 1, 2 або 3 містить первинну або вторинну амінну функціональність (-NH2 або -NHR, де R ≠ H), її амід, наприклад, сполука в якій, як можливий випадок, один або обидва гідрогени амінної функціональності сполуки формули 1, 2 або 3 є заміщеними на (C1-C10)алканоїл, -COCH2NH2 або аміно група є одержаною з амінокислоти; або, (vi) коли сполука формули 1, 2 або 3 містить первинну або вторинну амінну функціональність (-NH2 або -NHR, де R ≠ H), її амін, наприклад, сполука в якій, як можливий випадок, один або обидва гідрогени амінної функціональності сполуки формули 1, 2 або 3 є заміщеними на -CH2OP(=O)(OH)2. Певні сполуки формули 1, 2 або 3 самі по собі можуть діяти як проліки інших сполук формули 1, 2 або 3. Крім того, можливим для двох сполук формули 1, 2 або 3 є бути сполученими разом в формі проліків. За певних обставин, проліки сполук формули 1, 2 або 3 можуть бути створені за рахунок внутрішнього зв’язування двох функціональних груп в сполуці формули 1, 2 або 3, наприклад, шляхом утворення лактону. Посилання нижче на сполуки формули 1, 2 або 3 беруть, щоб включити сполуки самі по собі та їх проліки. Винахід включає такі сполуки формули 1, 2 або 3, а також фармацевтично прийнятні солі таких сполук та фармацевтично прийнятні сольвати зазначених сполук та солей. Фармацевтично прийнятні солі сполук формули 1, 2 або 3 включають кислотні адитивні та 9 UA 110766 C2 5 10 15 20 25 30 35 40 45 50 55 60 основні солі. Прийнятні кислотні адитивні солі утворюються з кислот, які утворюють нетоксичні солі. Приклади включають ацетатні, адипатні, аспартатні, бензоатні, безилатні, бікарбонатні/карбонатні, бісульфатні/сульфатні, боратні, камсилатні, цитратні, цикламатні, едизилат, езилатні, форміатні, фумаратні, глюцептатні, глюконатні, глюкуронатні, гексафлуорфосфатні, гібензатні, гідрохлоридні/хлоридні, гідробромідні/бромідні, гідройодидні/йодидні, ізетіонатні, лактатні, малатні, малеатні, малонатні, мезилатні, метилсульфатні, нафтилатні, 2-напсилатні, нікотинатні, нітратні, оротатні, оксалатні, пальмітатні, памоатні, фосфатні/гідрогенфосфатні/дигідрогенфосфатні, піроглутаматні, сахаратні, стеаратні, сукцинатні, танатні, тартратні, тозилатні, трифлуорацетатні солі, солі нафталін-1,5-дисульфонової кислоти та ксинафоатні солі. Прийнятні основні солі утворюються з основ, які утворюють нетоксичні солі. Приклади включають солі алюмінію, аргініну, бензатину, кальцію, холіну, діетиламіну, діоламіну, гліцину, лізину, магнію, меглуміну, оламіну, калію, натрію, трометамину та цинку. Крім того, можуть утворюватися гемісолі кислот та основ, наприклад, гемісульфатні солі та гемі солі кальцію. Для огляду прийнятних солей, дивись Handbook of Pharmaceutical Salts: Properties, Selection, and Use by Stahl and Wermuth (Wiley-VCH, 2002). Фармацевтично прийнятні солі сполук формули 1, 2 або 3 можуть одержувати за одним або більше з трьох способів: (i) шляхом взаємодії сполуки формули 1, 2 або 3 з бажаною кислотою або основою; (ii) шляхом видалення кислотно- або основно-лабільної захисної групи з прийнятного попередника сполуки формули 1, 2 або 3 або шляхом розкриття кільця прийнятного циклічного попередника, наприклад, лактона або лактама, використовуючи бажану кислоту або основу; або, (iii) шляхом перетворення однієї солі сполуки формули 1, 2 або 3 в іншу шляхом реакції з відповідною кислотою або основою, або шляхом застосування прийнятної іонообмінної колонки. Всі три реакції, як правило, здійснюють в розчині. Одержану в результаті сіль можуть осаджувати та збирати фільтруванням, або можуть виділяти шляхом випаровування розчинника. Ступінь іонізації в одержаній в результаті солі може варіювати від повністю іонізованого до майже неіонізованого. Сполуки формули 1, 2 або 3, та їх фармацевтично прийнятні солі, можуть існувати в несольватованій та сольватованих формах. Термін ‘сольват’ використовують в даному документі, щоб описати молекулярний комплекс, який містить сполуку формули 1, 2 або 3, або її фармацевтично прийнятну сіль, та одну або більше молекул фармацевтично прийнятного розчинника, наприклад, етанолу. Термін ‘гідрат’ можуть використовувати, коли зазначеним розчинником є вода. На даний момент прийнятною класифікаційною системою для органічних гідратів є система, яка визначає гідрати з окремим місцем, каналом або з координованим іоном металу - дивись Polymorphism in Pharmaceutical Solids K. R. Morris (Ed. H. G. Brittain, Marcel Dekker, 1995). Гідрати з окремим місцем представляють собою гідрати, в яких молекули води є відокремленими від прямого контакту одна з одною за рахунок вклинених між ними органічних молекул. В канальних гідратах, молекули води знаходяться в канал кристалічної ґратки, де вони знаходяться поруч з іншими молекулами води. В гідратах з координованим іоном металу, молекули води є зв’язаними з іоном металу. Коли розчинник або вода є міцно зв’язаним, комплекс буде мати добре визначену стехіометрію незалежно від вологості. Коли, однак, розчинник або вода є слабо зв’язаним, як в канальних сольватах та гігроскопічних сполуках, вміст води/розчинника буде залежити від умов вологості та сухості. В таких випадках, нестехіометричність буде нормою. Крім того, включеними в межі обсягу винаходу є багатокомпонентні комплекси (інші ніж солі та сольвати), в яких лікарський засіб та, щонайменше, один інший компонент є присутнім в стехіометричних або нестехіометричних кількостях. Комплекси даного типу включають клатрати (комплекси включення лікарський засіб-господар) та співкристали. Останні, як правило, визначають як кристалічні комплекси нейтральні молекулярні компоненти, які є зв’язаними разом через нековалентні взаємодії, але також могли б бути комплексом нейтральної молекули з сіллю. Співкристали можуть одержувати шляхом кристалізації розплаву, шляхом перекристалізації з розчинників, або шляхом фізичного подрібнення компонентів разом - дивись Chem Commun, 17, 1889-1896, O. Almarsson та M. J. Zaworotko (2004). Для загального огляду багатокомпонентних комплексів дивись J Pharm Sci, 64 (8), 1269-1288, Haleblian (August 1975). Далі в даному документі, всі посилання на сполуки формули 1, 2 або 3 включають посилання на фармацевтично прийнятні солі, сольвати, багатокомпонентні комплекси та їх рідкі кристали, та на сольвати, багатокомпонентні комплекси та рідкі кристали їх фармацевтично 10 UA 110766 C2 5 10 15 20 25 30 35 40 45 50 55 60 прийнятних солей. Сполуки формули 1, 2 або 3 можуть демонструвати поліморфізм та/або один або більше видів ізомерії (наприклад, оптичну, геометричну або таутомерну ізомерію). Сполуки формули 1, 2 або 3, крім того, можуть бути ізотопно міченими. Мається на увазі, що варіація сполук формули 1, 2 або 3, визначених як вони є з урахуванням їх структурних особливостей, таким чином, є в межах обсягу винаходу. Сполуки формули 1, 2 або 3, що містять один або більше асиметричних атомів карбону, можуть існувати як два або більше стереоізомерів. Коли сполука формули 1, 2 або 3 містить алкенільну або алкеніленову групу, можливими є геометричні цис/транс (або Z/E) ізомери. Коли структурні ізомери є взаємоперетворюваними через низький енергетичний бар’єр, може відбуватись таутомерна ізомерія (‘таутомерія’). Вона може приймати форму протонної таутомерії в сполуках формули 1, 2 або 3, що містять, наприклад, іміно, кето або оксимну групу, або так званої валентної таутомерії в сполуках, які містять ароматичний фрагмент. Звідси випливає, що одна сполука може демонструвати більше ніж один тип ізомерії. Фармацевтично прийнятні солі сполук формули 1, 2 або 3 також можуть містити протиіон, який є оптично активним (наприклад, d-лактат або l-лізин) або рацемічним (наприклад, dlтартрат або dl-аргінін). Цис/транс ізомери можуть бути розділені, застосовуючи традиційні методики, добре відомі кваліфікованому фахівцю в даній галузі з рівня техніки, наприклад, хроматографію та фракційну кристалізацію. Загальноприйняті способи одержання/виділення індивідуальних енантіомерів включають хіральний синтез з прийнятного оптично чистого попередника або розділення рацемату (або рацемату солі або похідної), застосовуючи, наприклад, хіральну високоефективну рідинну хроматографію (ВЕРХ). Альтернативно, рацемат (або рацемічний попередник) може взаємодіяти з прийнятною оптично активною сполукою, наприклад, спиртом, або, у випадку, коли сполука формули 1, 2 або 3 містить кислотний або основний фрагмент, основою або кислотою, такою як 1-фенілетиламін або винна кислота. Одержану в результаті діастереомерну суміш можуть розділяти, застосовуючи хроматографію та/або фракційну кристалізацію, та один або обидва діастереоізомери перетворюють у відповідний(і) чистий(і) енантіомер(и) за способами, добре відомими кваліфікованому фахівцю. Хіральні сполуки формули 1, 2 або 3 (та їх хіральні попередники) можуть одержувати в енантіомерно-збагаченій формі, застосовуючи хроматографію, як правило, ВЕРХ, на асиметричній смолі з рухомою фазою, що складається з вуглеводню, як правило, гептану або гексану, що містить від 0 до 50% за об’ємом ізопропанолу, як правило, від 2% до 20%, та від 0 до 5% за об’ємом алкіламіну, як правило, 0,1% діетиламіну. Концентрування елюату дає збагачену суміш. Хіральна хроматографія, що використовує суб- та надкритичні рідини, може застосовуватись. Способи для хіральної хроматографії, прийнятні в деяких варіантах здійснення представленого винаходу, є відомими в даній галузі з рівня техніки (дивись, наприклад, Smith, Roger M., Loughborough University, Loughborough, UK; Chromatographic Science Series (1998), 75 (Supercritical Fluid Chromatography with Packed Columns), pp. 223-249 та посилання, цитовані в даному документі). В деяких відповідних прикладах в даному документі, колонки одержували від Chiral Technologies, Inc, West Chестер, ® Pennsylvania, USA, дочірньої компанії Daicel Chemical Industries, Ltd., Tokyo, Japan. Коли будь-який рацемат кристалізується, можливими є кристали двох різних типів. Перший тип є рацемічною сполукою (справжнім рацематом), про який говориться вище, де одержують одну гомогенну форму кристалу, що містить обидва енантіомери в еквімолярних кількостях. Другий тип представляє собою рацемічну суміш або конгломерат, де одержують дві форми кристалу в еквімолярних кількостях, де кожен містить один енантіомер. В той же час, обидві з кристалічних форм, присутніх в рацемічній суміші, мають ідентичні фізичні властивості, вони можуть мати різні фізичні властивості в порівнянні зі справжнім рацематом. Рацемічні суміші можуть розділяти, застосовуючи загальноприйняті способи, відомі кваліфікованому фахівцю в даній галузі з рівня техніки. Stereochemistry of Organic Compounds E. L. Eliel та S. H. Wilen (Wiley, 1994). Представлений винахід включає всі фармацевтично прийнятні ізотопно-мічені сполуки формули 1, 2 або 3, в яких один або більше атомів є заміщеними на атоми, що мають однаковий атомний номер, але атомна маса або масове число відрізняється від атомної маси або масового числа, яке переважає в природі. Ізотопно-мічені сполуки формули 1, 2 або 3, як правило, можуть одержувати, застосовуючи загальноприйняті способи, відомі кваліфікованому фахівцю в даній галузі з рівня техніки, або застосовуючи процеси аналогічні до тих, що описані в супроводжуючих прикладах та одержаннях, використовуючи відповідний ізотопно-мічений реагент замість неміченого реагенту, що раніше застосовували. Зокрема, атоми гідрогену можуть бути заміщені на атоми дейтерію, оскільки такі дейтеровані сполуки іноді є більш 11 UA 110766 C2 5 10 15 20 25 30 35 40 45 50 55 60 резистентними до метаболізму. Крім того, включеними в межах обсягу винаходу є активні метаболіти сполук формули 1, 2 або 3, іншими словами, сполуки утворилися in vivo зразу після введення лікарського засобу, часто шляхом окиснення або деалкілування. Деякі приклади метаболітів відповідно до винаходу включають (i) коли сполука формули 1, 2 або 3 містить метильну групу, її гідроксиметильна похідна (CH3 -> -CH2OH): (ii) коли сполука формули 1, 2 або 3 містить алкокси групу, її гідрокси похідна (-OR -> -OH); (iii) коли сполука формули 1, 2 або 3 містить третинну аміногрупу, її вторинна аміно похідна ’ ’ (-NRR -> -NHR або -NHR ); (iv) коли сполука формули 1 містить вторинну аміногрупа, її первинна похідна (-NHR -> NH2); (v) коли сполука формули 1, 2 або 3 містить фенільний фрагмент, його фенольна похідна (Ph -> -PhOH); та, (vi) коли сполука формули 1, 2 або 3 містить амідну групу, її карбоксильна похідна (-CONH2 > COOH). Для введення пацієнтам людям, загальна добова доза сполуки формули 1, 2 або 3, як правило, знаходиться в діапазоні від 0,01 мг до 500 мг в залежності від, звичайно, способу введення. В іншому варіанті здійснення за представленим винаходом, загальна добова доза сполуки формули 1, 2 або 3, як правило, знаходиться в діапазоні від 0,1 мг до 300 мг. В ще іншому варіанті здійснення за представленим винаходом, загальна добова доза сполуки формули 1, 2 або 3, як правило, знаходиться в діапазоні від 1 мг до 30 мг. Загальну добову дозу можуть вводити однією або розділеними дозами, та може, на розсуд лікаря, виходити за межі типового діапазону, наданого в даному документі. Дані дозування ґрунтуються на середній вазі, яку має суб’єкт-людина, від приблизно 65 кг до 70 кг. Лікар легко зможе визначити дози для суб’єктів, чия вага виходить за межі даного діапазону, наприклад, діти та люди похилого віку. У випадку сухих порошкових інгаляторів та аерозолів, дозовану одиницю визначають за способами наповненої капсули, блістера або пакета, або з допомогою системи, що використовує дозуючу камеру з гравіметричною подаючою. Одиниці відповідно до винаходу, як правило, встановлюють, щоб вводити відміряну дозу або “випускання”, що містить від 1 до 5000 мкг лікарського засобу. Загальна добова доза, як правило, буде знаходитись в діапазоні від 1 мкг до 20 мг, яка може бути введена однією дозою або, більш звичайно, як розділені дози протягом дня. Сполуку формули 1, 2 або 3 можуть вводити в чистому вигляді або в формі фармацевтичної композиції, яка, як активний компонент, містить ефективну дозу, щонайменше, однієї сполуки за винаходом, а також звичайні фармацевтично безпечні ексципієнти та/або добавки. Фармацевтичні композиції прийнятні для доставки сполук за представленим винаходом та способи їх одержання будуть очевидні кваліфікованому фахівцю в даній галузі. Такі композиції та способи їх одержання можуть бути знайдені, наприклад, в Remington’s Pharmaceutical Sciences, 19th Edition (Mack Publishing Company, 1995). Сполуки формули 1, 2 або 3 можуть вводити перорально. Пероральне введення може включати проковтування, так що сполука потрапляє в шлунково-кишковий тракт, або можуть застосовувати букальне або сублінгвальне введення, за яким сполука потрапляє в кровоток безпосередньо з ротової порожнини. Препарати, прийнятні для перорального введення включають тверді препарати, такі як таблетки, капсули, що містять частинки, рідини або порошки, пастилки (включаючи наповнені рідиною), жувальні гумки, мульти- та нано-частинки, гелі, твердий розчин, ліпосома, плівки, супозирорії, спреї та рідкі препарати. Рідкі препарати включають суспензії, розчини, сиропи та еліксири. Такі препарати можуть застосовувати як наповнювачі в м'яких або твердих капсулах та, як правило, містять носій, наприклад, воду, етанол, поліетиленгліколь, пропіленгліколь, метилцелюлозу або прийнятну олію, та один або більше емульгуючих агентів та/або суспендуючих агентів. Рідкі препарати також можуть одержувати шляхом розбавлення твердої речовини, наприклад, із саше. Сполуки формули 1, 2 або 3 також можуть застосовувати в швидкорозчинних дозованих формах, дозованих формах, таких як ті, що описані в Expert Opinion in Therapeutic Patents, 11 (6), 981-986, Liang та Chen (2001). Для таблеткових дозованих форм, в залежності від дози, лікарський засіб може становити від 1 масового % до 80 масових % дозованої форми, більш типово від 5 масових % до 60 масових % дозованої форми. На додаток до лікарського засобу, таблетки зазвичай містять розпушувач. Приклади розпушувачів включають крохмальгліколят натрію, карбоксиметилцелюлозу натрію, карбоксиметилцелюлозу кальцію, кроскармелозу натрію, кросповідон, полівінілпіролідон, метилцелюлозу, мікрокристалічну целюлозу, заміщену 12 UA 110766 C2 5 10 15 20 25 30 35 40 45 50 55 60 нижчим алкілом гідроксипропілцелюлозу, крохмаль, попередньо желатинізований крохмаль та альгінат натрію. Як правило, розпушувач буде становити від 1 масового % до 25 масових %. В одному варіанті здійснення представленого винаходу, розпушувач буде становити від 5 масових % до 20 масових % дозованої форми. Зв’язуючі речовини, як правило, застосовують, щоб надати когезивних властивостей таблетованому препарату. Прийнятні зв’язуючі речовини включають мікрокристалічну целюлозу, желатин, цукри, поліетиленгліколь, природні та синтетичні смоли, полівінілпіролідон, попередньо желатинізований крохмаль, гідроксипропілцелюлозу та гідроксипропілметилцелюлозу. Таблетки також можуть містити розріджувачі, такі як лактоза (моногідрат, висушений розпиленням моногідрат, безводний, тощо), маніт, ксиліт, декстроза, сахароза, сорбіт, мікрокристалічна целюлоза, крохмаль та дигідрат двоосновного кальцію фосфату. Таблетки також можуть необов'язково містити поверхнево-активні речовини, такі як лаурилсульфат натрію та полісорбат 80, та ковзкі речовини, такі як діоксид силіцію та тальк. Якщо вони присутні, поверхнево-активні речовини можуть становити від 0,2 масових % до 5 масових % таблетки, та ковзкі речовини можуть становити від 0,2 масових % до 1 масового % таблетки. Таблетки також зазвичай містять змащувальні речовини, такі як стеарат магнію, стеарат кальцію, стеарат цинку, стеарилфумарат натрію та суміші стеарату магнію з лаурилсульфатом натрію. Змащувальні речовини зазвичай становлять від 0,25 масових % до 10 масових %. В одному варіанті здійснення представленого винаходу, змащувальні речовини становлять від 0,5 масових % до 3 масових % таблетки. Інші можливі інгредієнти включають антиоксиданти, барвники, ароматизуючи агенти, консерванти та агенти, які маскують смак. Ілюстративні таблетки містять аж до приблизно 80% лікарського засобу, від приблизно 10 масових % до приблизно 90 масових % зв’язуючої речовини, від приблизно 0 масових % до приблизно 85 масових % розріджувача, від приблизно 2 масових % до приблизно 10 масових % розпушувача, та від приблизно 0,25 масових % до приблизно 10 масових % змащувальної речовини. Суміші для таблеток можуть пресувати безпосередньо або з допомогою валику, щоб сформувати таблетки. Суміші для таблеток або частини сумішей альтернативно можуть бути волого-, сухо- або розплавлено-гранульованими, застиглими з розплаву, або екструдованими перед таблетуванням. Кінцевий препарат може містити один або більше шарів та може бути покритим або непокритим; ще він може бути інкапсульованим. Склади таблеток обговорюються в Pharmaceutical Дозована формаs: Tablets, Vol. 1, H. Lieberman and L. Lachman (Marcel Dekker, New York, 1980). Придатними до споживання пероральними плівками для людини або ветеринарного застосування є, як правило, пластичні розчинні у воді або такі, що набухають у воді тонкі плівчасті дозовані форми, які можуть бути швидко розчинними або мукоадгезивними, та, як правило, містять сполуку формули 1, 2 або 3, плівкоутворюючий полімер, зв’язуючу речовину, розчинник, зволожувач, пластифікатор, стабілізатор або емульгатор, агент, що модифікує в’язкість та розчинник. Деякі компоненти препарата можуть виконувати більше, ніж одну функцію. Плівкоутворюючий полімер може бути вибраний з природних полісахаридів, протеїнів або синтетичних гідроколоїдів, та, як правило, є присутніми в діапазоні від 0,01 до 99 масових %, більш вірогідно, як правило, в діапазоні від 30 до 80 масових %. Інші можливі інгредієнти включають антиоксиданти, барвники, ароматизатори та підсилювачі смаку, консерванти, стимулюючі слиновиділення агенти, охолоджуючі агенти, співрозчинники (включаючи олії), пом'якшуючі засоби, наповнювачі, протипіноутворюючі агенти, поверхнево-активні речовини та маскуючі смак агенти. Плівки відповідно до винаходу, як правило, одержують шляхом випарювальної сушки тонких водних плівок, нанесених на зйомну каркасну підкладку або папір. Це може бути зроблено в сушильній шафі або тунелі, як правило, в комбінованому апараті для нанесення покриття - сушарці, або шляхом висушування при заморозці, або вакуумуванням. Тверді препарати для перорального введення можуть бути сформульовані як такі, що мають негайне та/або модифіковане вивільнення. Модифіковане вивільнення включає уповільнене, подовжене, переривчасте, контрольоване, цільове та програмоване вивільнення. Прийнятні препарати з модифікованим вивільненням для цілей винаходу описані в патенті США № 6,106,864. Детальна інформація про інші прийнятні способи вивільнення, такі як високо енергетичні дисперсії, та осмотичні та покриті частинки, можуть бути знайдені в Pharmaceutical Technology On-line, 25(2), 1-14, Verma et al (2001). Застосування жувальної гумки для досягнення контрольованого вивільнення описане в WO-A-00/35298. Сполуки формули 1, 2 або 3 також можуть вводити безпосередньо в кровоток, в м'яз або у внутрішній орган. Таке парентеральне введення включає внутрішньовенне, внутрішньоартеріальне, внутрішньочеревне, інтратекальне, внутрішньошлуночкове, 13 UA 110766 C2 5 10 15 20 25 30 35 40 45 50 55 60 інтрауретральне, внутрішньогрудинне, внутрішньочерепне, внутрішньом'язове та підшкірне введення. Прийнятні пристрої для парентерального введення включають голкові (включаючи мікроголкові) шприці, безголкові шприці та інфузійні методики. Сполуки за винаходом також можуть вводити місцево на шкіру або слизову оболонку, тобто дермально або трансдермально. Сполуки формули 1, 2 або 3 також можуть вводити інтраназально або шляхом інгаляції, як правило, у формі сухого порошку (або самостійно, у вигляді суміші, наприклад, в сухій суміші з лактозою, або у вигляді змішаних частинок компонентів, наприклад, змішаний з фосфоліпідами, такими як фосфатидилхолін) з інгалятора сухого порошку, у вигляді аерозольного спрею з контейнера, що знаходиться під тиском, насоса, спрею, розпилювача (переважно аерозольний інгалятор з використанням електрогідродинаміки для отримання дрібнодисперсного туману), або небулайзера, з або без застосування прийнятного пропелента, такого як 1,1,1,2тетрафлуоретан або 1,1,1,2,3,3,3-гептафлуорпропан, або у вигляді назальних крапель. Для інтраназального застосування порошок може містити біоадгезивний агент, наприклад, хітозан або циклодекстрин. Контейнер під тиском, насос, спрей, аерозольний інгалятор або небулайзер містить розчин або суспензію сполуки формули 1, 2 або 3, що містить, наприклад, етанол, водний етанол або прийнятний альтернативний агент для диспергування, солюбілізації або подовження вивільнення сполуки, пропелент як розчинник, та необов’язкову поверхнево-активну речовину, таку як сорбітану триолеат, олеїнова кислота або олігомолочна кислота. Перед використанням в препараті сухого порошку або суспензії, продукт лікарського засобу мікронізують до розміру, прийнятного для доставки шляхом інгаляції (як правило, менше ніж 5 мікрон). Це може бути досягнуто, застосовуючи будь-який відповідний спосіб подрібнення, такий як помол на спіральному струменевому млині, помол на струменевому млині з псевдозрідженим шаром, обробка надкритичною рідиною з утворенням наночасток, гомогенізація високого тиску або сушка з розпиленням. Капсули (виготовлені, наприклад, з желатину або гідроксипропілметилцелюлози), блістери та картриджі для застосування в інгаляторі або інсуфляторі можуть бути сформульовані таки чином, що містять порошкову суміш сполуки за винаходом, прийнятну порошкову основу, таку як лактоза або крохмаль, та високоякісний модифікатор, такий як l-лейцин, маніт або магнію стеарат. Лактоза може бути безводною або у формі моногідрату, переважно, останнього. Інші прийнятні ексципієнти включають декстран, глюкозу, мальтозу, сорбіт, ксиліт, фруктозу, сахарозу та трегалозу. Прийнятний препарат у вигляді розчину для застосування в аерозольному інгаляторі з використанням електрогідродинаміки для отримання дрібнодисперсного туману може містити від 1 мкг до 20 мг сполуки за винаходом на одне спрацьовування, та об’єм одного спрацьовування може варіювати від 1 мкл до 100 мкл. Типовий препарат може містити сполуку формули 1, 2 або 3, пропіленгліколь, стерильну воду, етанол та хлорид натрію. Альтернативні розчинники, які можуть застосовувати замість пропіленгліколю включають гліцерин та поліетиленгліколь. Прийнятні ароматизатори, такі як ментол та левоментол, або підсолоджувачі, такі як сахарин або сахарин натрію, можуть додавати до даних препаратів за винаходом, призначених для інтраназального введення. Препарати для інтраназального введення можуть бути сформульовані так, що вони є негайного та/або модифікованого вивільнення з використанням, наприклад, PGLA. Модифіковане вивільнення включає уповільнене, подовжене, переривчасте, контрольоване, цільове та програмоване вивільнення. Сполуки формули 1, 2 або 3 також можуть вводити безпосередньо в око або у вухо, як правило, у формі крапель мікронізованої суспензії або розчину в ізотонічному, pHрегульованому, стерильному сольовому розчині. Сполуки формули 1, 2 або 3 можуть комбінувати з розчинними макромолекулярними одиницями, такими як циклодекстрин та його прийнятні похідні або полімери, що містять поліетиленгліколь, для того, щоб покращити їх розчинність, швидкість розчинення, смак, біодоступність та/або стабільність при використанні будь-якого з вищезгаданих способів введення. Виявлено, наприклад, що комплекси лікарський засіб-циклодекстрин, як правило, є прийнятними для більшості дозованих форм та способів введення. Застосовуватись можуть як комплекси включення, так і не комплекси включення. В якості альтернативи безпосередньому комплексоутворенню з лікарським засобом, циклодекстрин можуть застосовувати як допоміжну добавку, тобто, як носій, розріджувач або солюбілізатор. Найбільш загально застосованим для даних цілей є альфа-, бета- та гама-циклодекстрини, приклади яких можуть бути знайдені в міжнародних публікаціях патентів WO-A-91/11172, WO-A-94/02518 та WO-A-98/55148. Оскільки бажаним може бути вводити комбінацію активних сполук, наприклад, з метою 14 UA 110766 C2 5 10 15 20 25 30 35 40 45 50 55 60 лікування конкретного захворювання або стану, вона знаходиться в межах обсягу представленого винаходу, таким чином дві або більше фармацевтичних композиції, щонайменше, одна з яких містить сполуку формули 1, 2 або 3, можуть легко комбінувати у формі набору, прийнятного для спільного введення композицій. Таким чином, набір за винаходом містить дві або більше окремих фармацевтичних композицій, щонайменше, одна з яких містить сполуку формули 1, 2 або 3, та засоби для зберігання по окремості зазначених композицій, такі як контейнер, розділений флакон або розділений пакет з фольги. Прикладом такого набору є відома блістерна упаковка, яку використовують для пакування таблеток, капсул, тощо. Такий набір є особливо прийнятним для введення різних дозованих форм, наприклад, пероральних та парентеральних, для введення окремих композицій в різні інтервали дозування, або для титрування окремих композицій один проти іншого. Для того, щоб сприяти дотриманню режима терапії, набір, як правило, включає інструкції щодо введення та може бути забезпечений так званої пам'яткою. Нові сполуки за представленим винаходом також є корисними в галузі ветеринарної медицини. На додаток до використання у відмінних від людини тварин для застосувань, описаних в даному документі вище для суб’єктів людей, сполуки за представленим винаходом також є особливо корисними в лікуванні відмінних від людини тварин, яких вирощують для споживання в їжу людиною. Дозування та дозовані форми, описані в даному документі вище для суб’єктів людей можуть регулюватися, щоб пристосувати для різного розміру тварин, як це добре відомо кваліфікованим фахівцям в галузі ветеринарії. Нові сполуки за представленим винаходом є придатними для збільшення м'язової маси, зниження жирової маси, зниження відсотку жирової маси та збільшення співвідношення пісне м’ясо:жир при введенні в організм тварин. Таким чином, представлений винахід крім того, передбачає спосіб впливу на склад туші, збільшення м'язової маси, зниження жирової маси, зниження відсотку жирової маси, збільшення співвідношення пісне м’ясо:жир, збільшення середньодобового приросту (ADG), або зменшення годування, щоб отримати співвідношення (F:G) у тварини, або збільшення ефективності годування у тварин, де спосіб включає введення тварині ефективної кількості сполуки, що має формулу 1, 2 або 3, або її фармацевтично прийнятної солі. В одному варіанті здійснення даного способу, тварина є твариною, що утримується на кормовому майданчику. В іншому варіанті здійснення даного способу, тварина є кінцевою сільськогосподарською твариною. Термін "тварина, що утримується на кормовому майданчику" стосується тварини, м'ясо, якої вважається їстівним в даній культурі або країні. В деяких варіантах здійснення, такий термін може включати, без обмеження, свиней (домашню свиню, диких кабанів), велику рогату худобу (бізон, корова, яки), оленів (олень, марал, лось), овець (вівця/ягня), та кіз (кози). Твариною, що утримується на кормовому майданчику, крім того, може бути птиця, такі як курки або індички, яких вирощують для споживання м’яса. Термін "кінцева сільськогосподарська тварина" стосується тварини, яка, як правило, є відгодованою протягом останніх декількох днів, тижнів або місяців перед переробкою. В одному варіанті здійснення, кінцева сільськогосподарська тварина є великою рогатою худобою. В іншому варіанті здійснення, кінцева сільськогосподарська тварина є свинею. В іншому варіанті здійснення, кінцева сільськогосподарська тварина є птицею, такою як курка або індичка. В одному варіанті здійснення, кінцева сільськогосподарська тварина є рибою, що штучно вирощується. В переважному варіанті здійснення, тварина є великою рогатою худобою або свинею. Свинею може бути, наприклад, свиня, порося, молода свиня або відгодована свиня. Велика рогата худоба може бути, наприклад, м’ясна худоба, телят після відлучення, телят, яке випасається, або худоба in utero. Фраза “збільшення м’язової маси”, як правило, стосується збільшення м’язів у тварини, що в багатьох випадках вважається більш бажаним в туші для споживання в їжу людиною. “Зниження жирової маси” та “зниження відсотка жирової маси” стосується зменшення продукування жиру у тварини. Фраза “співвідношення пісне м’ясо:жир”, як, наприклад, в фразі “збільшення співвідношення пісне м’ясо:жир”, як правило, стосується м’язової маси у тварини по відношенню до жирової маси у тварини. Вважається, що підвищене співвідношення пісне м’ясо:жир у тварини, яке одержують в туші, в багатьох випадках, є більш бажаним для споживання в їжу людиною. Фраза “F:G” стосується співвідношення корму, що споживається твариною, до приросту маси (на виході) у тварини. Зниження F:G підвищує продуктивність з економічної точки зору. Винахід також передбачає ветеринарні композиції для лікування тварин, зокрема відмінних від людини тварин, щоб досягти довгострокові результати (наприклад, збільшений ADG) за способами, описаними в даному документі, в яких композиції містять ефективну кількість 15 UA 110766 C2 5 10 15 20 25 30 35 40 45 50 55 60 сполуки формули 1, 2, або 3, або фармацевтично прийнятної солі зазначеної сполуки. Такі композиції можуть знаходитись в будь-якій дозована формі, відомій кваліфікованому фахівцю в галузі ветеринарії з рівня техніки. В одному варіанті здійснення, ветеринарна композиція за представленим винаходом знаходиться в формі прийнятній для перорального введення тварині. В іншому варіанті здійснення, ветеринарна композиція за винаходом знаходиться в формі прийнятній для парентерального введення. В іншому варіанті здійснення, ветеринарна композиція за винаходом знаходиться в формі імплантату, наприклад, контрольованого вивільнення або подовженого вивільнення імплантату. Інші дозовані форми, відомі кваліфікованому фахівцю, можуть бути використані для ветеринарної композиції, такі як супозиторії або спреї, креми або мазі для місцевого застосування. Для пероральні введення, ветеринарні композиції можуть бути в формі капсул, таблеток (включаючи, але не обмежуючись, таблетки з покриттям), болюсів, гранул, порошків, харчових добавок або рідких форм, таких як пероральні рідкі суспензії або рідкі концентрати. Такі пероральні форми можуть бути прийнятними для введення безпосередньо тварині, або вони можуть бути сконцентровані та прийнятні для розбавлення, наприклад, шляхом змішування з, або іншим включенням в, їжу тварини або шляхом розчинення у питній воді для тварин. Такі форми є відомими кваліфікованому фахівцю в галузі ветеринарії з рівня техніки. Композиції для відкорму та композиції для змішування, перемішування або іншого комбінування з кормом для тварини будуть варіювати в залежності від виду тварини, але, як правило, містять речовини, такі як, але не обмежуючись цим, зернові, соєве борошно, борошно кукурудзяного качана, кукурудзяне борошно, люцернове борошно, кукурудзяна крупа, цукри, очеретяна патока, злаки та/або подрібнені зернові (наприклад кукурудза, соя), рибне борошно, кісткове борошно та/або подрібнені кістки, та необов’язково також можуть бути включеними до них поживні речовини, наприклад, амінокислоти, мінеральні солі, вітаміни та/або антиоксиданти. Сполуки за винаходом в одному варіанті здійснення є покритими або іншим чином включеними в носій, наприклад, кукурудзяні крупи, прийнятні для годування тварин. Способи формулювання ветеринарних композицій, прийнятних для парентерального введення тварині є відомими в даній галузі з рівня техніки та можуть бути використані для ветеринарних композицій за даним винаходом. Для парентерального введення тваринам для ветеринарного застосування, сполуки за винаходом можуть бути змішані із загальноприйнятими носіями, такими як мінеральна олія, кукурудзяна олія, кунжутна олія, карбовакс, кальцію стеарат, тощо. В одному варіанті здійснення, такі препарати формують в пелети та вводять як ін’єкцію або як повільного вивільнення підшкірний імплант. Частота та/або кількість ін’єкції можуть бути зміненими в залежності від виду, розміру тварини, та ступеню стимуляції росту, покращення пісності в туші, або бажаної ефективності корму. У випадку домашньої птиці, даний винахід, крім того, передбачає спосіб обробки птиці шляхом введення SARM, наприклад, сполуки формули 1, 2, або 3, або її фармацевтично прийнятної солі, in ovo, з метою досягнення у птиці результатів (наприклад, збільшення ADG, збільшення росту м’язів, зниження продукування жиру) за способами, описаними в даному документі. Винахід передбачає спосіб обробки птиці, зазначеним способом, що включає введення in ovo ефективної кількості SARM. Винахід, крім того, передбачає ветеринарну композицію для обробки птиці, де зазначена композиція знаходиться в формі для введення in ovo, та де зазначена композиція містить ефективну кількістьSARM, наприклад, сполуки формули 1, 2, або 3, або її фармацевтично прийнятної солі, та носій прийнятний для введення in ovo. In ovo стосується ін’єкції, розчину або інших сформульованих систем доставки різних речовин в пташині яйця. Ілюстративна in ovo ін’єкційна система, яку можуть застосовувати, щоб ін’єкційно вводити речовину в яйця представляє собою автоматичний ін’єкційний пристрій INOVOJECT® (Embrex, Inc., Durham, North Carolina). Ефективна кількість сполуки формули 1, 2, або 3 для ветеринарних способів та композицій, описаних в даному документі є кількістю, що є ефективною в спричиненні збільшення ADG, м’язової маси, співвідношення пісне м’ясо:жир, ефективності харчування або зниження жирової маси. Ефективна кількість, яку вводять, може дещо варіювати в залежності від конкретних видів тварин, яких вирощують, та конкретного активного інгредієнта, який застосовують, але загалом ефективна кількість становить від приблизно 0,1 мг до приблизно 60 мг, переважно від приблизно 0,1 мг до приблизно 30 мг, сполуки на кг маси тіла тварини, яку обробляють. В іншому варіанті здійснення, ефективна кількість становить від приблизно 0,3 мг до приблизно 30 мг сполуки на кг маси тіла тварини, яку обробляють. Дана кількість (від приблизно 0,1 мг до приблизно 60 мг сполука/кг маси тіла тварини) є, як правило, кількістю, яку вводять тварині приблизно щоденно; однак, інша частота дозування (наприклад, одноразове, кожні два дні, або щотижнево) є включеними в межі винаходу. 16 UA 110766 C2 5 10 15 20 25 30 35 40 45 50 55 60 Як приклад, у випадку введення in ovo, приймаючи до уваги той факт, що вага ембріона становить від приблизно 1 грама до приблизно 20 грам, ефективна кількість сполуки, яку вводять, буде знаходитись в діапазоні від приблизно 0,0001 мг до приблизно 1,2 мг. В іншому варіанті здійснення, ефективна кількість сполуки формули 1, 2 або 3 становить від приблизно 0,1 до приблизно 20 частин на мільйон (м.ч.) від загального споживання корму в день твариною, яку обробляють сполукою. Для введення in ovo SARM, переважно, та в одному варіанті здійснення, SARM вводять в яйце від приблизно E0 дня до приблизно E18 день, в якій E0 представляє собою дату, коли яйце відкладається. Винахід крім того, передбачає спосіб обробки ссавця, переважно великої рогатої худоби або свині, шляхом введення SARM, наприклад, сполуки формули 1, 2, або 3 в даному документі, або її фармацевтично прийнятної солі, ссавцю, коли ссавець знаходиться in utero. Зазначений спосіб обробки має на меті досягнення у ссавців результатів (наприклад, збільшення ADG, збільшення росту м'язів, та/або зменшення продукування жиру) за способами, описаними в даному документі. Вважається, що введення in utero SARM, наприклад, сполуки формули 1, 2, або 3 в даному документі, або її фармацевтично прийнятної солі, збільшує загальну кількість волокон м’язів у ссавця. У ссавця, всі із загальних м'язових клітин протягом життя ссавця генеруються in-utero, тобто, до народження. Після того, як будь-який ссавець народжується, нові м'язові клітини не утворюються. Винахід передбачає спосіб обробки ссавця, переважно свині або великої рогатої худоби, де зазначений спосіб включає in utero введення ссавцю ефективної кількості SARM. Даний спосіб збільшує загальну кількість м'язових клітин та кількість м'язового волокна у ссавців. Винахід також передбачає ветеринарну композицію для обробки ссавця, зазначену композицію в формі для введення in utero, та де зазначена композиція містить ефективну кількість SARM, наприклад, сполуки формули 1, 2, або 3, або її фармацевтично прийнятної солі, та носій прийнятний для введення in utero. Введення іn utero ссавцю, як правило, досягають шляхом введення матері ссавця in utero в будь-якій з форм, описаних в даному документі, наприклад, пероральній, парентеральній, в кормі, у воді, що було б прийнятним для обробки матері. В одному варіанті здійснення, SARM, наприклад, сполуку формули 1, 2, або 3, або її фармацевтично прийнятну сіль, вводять матері ссавця in utero з приблизно 5 дня по приблизно 75 день після запліднення ссавця. В іншому варіанті здійснення, SARM вводять матері ссавця, в той час як ссавець знаходиться in utero, з приблизно 5 дня по приблизно 35 день після запліднення ссавця. В іншому варіанті здійснення, SARM вводять матері ссавця, в той час як ссавець знаходиться in utero, з приблизно 55 дня по приблизно 75 день після запліднення ссавця. Інші стадії розвитку in utero, під час яких SARM можуть вводити матері ссавця in utero, а також тривалість та частота обробки, є включеними в межі винаходу; дані стадії розвитку, тривалість та частота будуть визначатися приймаючи до уваги такі чинники, відомі в даній галузі з рівня техніки як, наприклад, вид ссавця та розмір ссавця. Нові сполуки заявленого винаходу також ефективно можуть комбінувати з іншими активними фармацевтичними інгредієнтами, відомими в ветеринарних галузях. Такі комбінації можуть здійснювати шляхом введення сполуки за представленим винаходом тварині, як описано в даному документі, в одній дозованій формі або одиниці, та введення другого активного фармацевтичного інгредієнта тварині окремо, в окремій дозованій формі або одиниці. Введення тварині двох окремих дозованих форм може відбуватися одночасно або в будь-якому порядку. В іншому варіанті здійснення, сполуку за представленим винаходом та другий фармацевтичний інгредієнт (або додаткові фармацевтичні інгредієнти) комбінують разом в одній тій самій дозованій формі та вводять тварині разом. В одному варіанті здійснення, сполуку за представленим винаходом вводять тварині в комбінації з бета адренергічним агоністом або бета адренергічним модулятором. Така комбінація може продвигати цілі дослідження способів за представленим винаходом, такі як збільшення ADG та збільшення співвідношення пісне м’ясо:жир та ефективність харчування. Приклади бета адренергічних агоністів або модуляторів, які можуть застосовувати в представленому винаході включають, але не обмежуються цим, зілпатерол (дивись, наприклад патент Сполучених Штатів 4 900 735), рактопамін (дивись, наприклад, патент Сполучених Штатів 5 631 298), сальбутамол (дивись, наприклад, патент Сполучених Штатів 3 644 353), та циматерол (дивись, наприклад, патент Сполучених Штатів 5 248 695). Іншими необмежуючими прикладами бета адренергічних агоністів або модуляторів, які можуть застосовувати у винаході є гексопреналін (дивись, наприклад, патент Сполучених Штатів 3 329 709), ізопреналін (дивись, наприклад, патент Сполучених Штатів 2 715 141), рімітерол (дивись, наприклад, патент Сполучених Штатів 3 705 169), ізоетарин (дивись, наприклад, DE 638650 (I.G. Farben, 1936)), 17 UA 110766 C2 5 10 15 20 25 30 35 40 45 50 55 60 метапротеренол (дивись, наприклад, патент Сполучених Штатів 3 341 594), репротерол (дивись, наприклад заявку на патент Сполучених Штатів US 2002132830, прокатерол (дивись, наприклад, патент Сполучених Штатів 4 026 897), карбутерол (дивись, наприклад, патент Сполучених Штатів 3 763 232), тулобутерол (дивись, наприклад, DE 2244737), пірбутерол (дивись, наприклад, патент Сполучених Штатів 3 700 681), мабутерол (дивись, наприклад, патент Сполучених Штатів 4 119 710), бітолтерол (дивись, наприклад, патент Сполучених Штатів 4 138 581), кленбутерол (дивись, наприклад, патент Сполучених Штатів 3 536 712), та бамбутерол (дивись, наприклад, патент Сполучених Штатів 4 419 364). В іншому варіанті здійснення, сполуку за представленим винаходом можуть вводити тварині в комбінації з антибіотиком, з метою досягнення переваг (наприклад, збільшення м’язової маси, збільшення ADG). Приклади антибіотиків, які можуть застосовувати в представленому винаході включають, але не обмежуються цим, тетрациклін (дивись, наприклад, патент Сполучених Штатів 2 482 055), окситетрациклін (дивись, наприклад, патент Сполучених Штатів 2 482 055), тіамулін (дивись, наприклад патент Сполучених Штатів 3 919 290; 3 987 194; та 4 278 674), моненсин (дивись, наприклад, патент Сполучених Штатів 3 839 557 та 3 995 027), та тілозин (дивись наприклад патент Сполучених Штатів 4 048 268 та 4 283 388). В іншому варіанті здійснення, сполуку за представленим винаходом можуть вводити тварині в комбінації зі стероїдом з метою досягнення мети дослідження, такої як збільшення ADG, застосовуючи ветеринарні способи, описані в даному документі. Приклади стероїдів, які можуть застосовувати в представленому винаході включають, але не обмежуються цим, меленгестролу ацетат (дивись, наприклад, патенти Сполучених Штатів №№ 3 332 940; 3 359 287 та 4 154 748), тренболону ацетат (дивись, наприклад, патент Сполучених Штатів 3 939 265), зеранол (дивись, наприклад патент Сполучених Штатів 3 239 345), та естрадіол, наприклад Synovex® або Revalor® (дивись, наприклад, патент Сполучених Штатів 4 192 870). Представлений винахід, крім того, передбачає введення SARM, наприклад, сполуки формули 1, 2, або 3 за представленим винаходом, тварині, яка була кастрованою, застосовуючи фізичні способи, або фармацевтичні способи, або біофармацевтичні способи. Кастрацію застосовують у випадку свиней, а саме кабанів, для того, щоб зменшити, наприклад, агресивну поведінку та, в деяких випадках, неприємний присмак кабана, який є результатом гормональних рівнів, наприклад, рівнів тестостерону, у тварини. Кастрація знижує рівень тестостерону, тим самим знижуючи агресію та присмак кабана. Але, кастрація, в силу подальшого зниження деяких гормонів, також впливає на якість м'яса свиней. В зв’язку з цим, представлений винахід передбачає введення SARM, наприклад, нової сполуки за представленим винаходом, кастрованій тварині, такій як кастрована свиня, для того, щоб вплинути на склад туші тварини, збільшити м’язову масу у тварини, зменшити жирову масу, зменшити відсоток жирової маси, збільшити співвідношення пісне м’ясо:жир, збільшити середньодобовий приріст (ADG), або зменшити співвідношення корму до приросту (F:G) у тварини. В одному варіанті здійснення за винаходом, кастрація тварини представляє собою фізичну кастрацію. В іншому варіанті здійснення за винаходом, кастрація відбувається фармацевтичним або біофармацевтичним способом. Приклади біофармацевтичного способу кастрації включають, але не обмежуються цим, вакцини, що містять антитіла, спрямовані на певні гормони, такі як GnRH (гормон, що вивільняє гонадотропін) або LHRH (гормон, що вивільняє лютеїнізуючий гормон), наприклад, вакцина Improvac® (дивись, наприклад, патент Сполучених Штатів 7 534 441). Інші фармацевтичні або біофармацевтичні способи кастрації включають, але не обмежуються цим, діетилстильбестрол (дивись, наприклад, U.V. Solmssen, Chem. Rev. 37, 481-598 (1945)), медроксипрогестерон (дивись, наприклад, патент Сполучених Штатів 3 377 364) та ципротерон (дивись, наприклад, патент Сполучених Штатів 3 234 093). В повному обсязі положення всіх патентів та опублікованих заявок на патент, що наведені в даному документі вище, є включеними в даний документ як посилання. Всі сполуки формули 1, 2 або 3 можуть бути отримані, застосовуючи спеціальні та загальні експериментальні методики, описані нижче в поєднанні із загальними знаннями кваліфікованого фахівця в даній галузі (дивись, наприклад, Comprehensive Organic Chemistry, Ed. Barton and Ollis, Elsevier; Comprehensive Organic Transformations: A Guide to Functional Group Preparations, Larock, John Wiley and Sons). Далі необмежуючі одержання та приклади ілюструють одержання сполук за винаходом. 1 Спектри H ядерного магнітного резонансу (ЯМР) в усіх випадках відповідали запропонованим структурам. Характеристичні хімічні зсуви () надаються в частинах на мільйон в бік слабкого поля від тетраметилсилану, використовуючи загальноприйняті скорочення щодо позначення основних піків: наприклад, с, синглет; д, дублет; т, триплет; кв, квартет; м, 18 UA 110766 C2 5 мультиплет; ш, широкий. Мас-спектри (m/z) записували, використовуючи або електроспрей іонізацію (ЕСІ) або хімічну іонізацію при атмосферному тиску (APCI). Наступні скорочення застосовували для загальноприйнятих розчинників: CDCl3, дейтерохлороформ; d6-ДМСО, дейтеродиметилсульфоксид; CD3OD, дейтерометанол; ТГФ, тетрагідрофуран; ДХМ, дихлорметан; EtOAc, етилацетат; MeOH, метанол; ДМФ, диметилформамід. 'Аміак' стосується концентрованого розчину аміаку у воді, що має питому вагу 0,88. Коли використовують тонкошарову хроматографію (ТШХ), то вона стосується силкагелевої ТШХ з використанням силікагелевих пластин 60 F254, Rf є відстанню, яку проходить сполука, розділена відстанню, пройденою фронтом розчинника на ТШХ пластині. 10 Толуол, кип'ятіння, 12год ClCO2Et, 30 хв mCPBA, CH2Cl2, 25 oC, 18год P(OMe)3, 12год TiCl4, CH2Cl2, 6 днів #A1 TMSCN, DBU, ТГФ, 25oC, 1год Pd2(dba) 3, BINAP, Cs 2CO3, толуол, 110oC, 3 год #A2 #A3 ClSO2NHBoc, ДІПЕА, ТГФ, 0oC, 2год MsCl, Et 3N, ДХМ, 0-25oC, 3год #A4 #A5 ClSO2NHBoc, ДІПЕА, ТГФ, 0oC, 2год #1 #A6 15 20 25 Стадія 1. Синтез 6-бромізохіноліну (#A1). Суміш 4-бромбензальдегіду (300,0 г, 1620,0 ммоль) та аміноацетальдегіду диметилацеталю (170,4 г, 1620 ммоль) в безводному толуолі (1,5 л) кип’ятили з насадкою Діна-Старка протягом 12 год. Розчин концентрували в вакуумі. Залишок розчиняли в безводному ТГФ та охолоджували до -10 °C. Етилхлорформіат (193,3 мл, 1782 ммоль) додавали та перемішували протягом 10 хв при -10 °C, та потім давали нагрітися до кімнатної температури. Потім до реакційної суміші по краплям додавали триметилфосфіт (249,6 мл, 1782,0 ммоль) та перемішували протягом 10 год при кімнатній температурі. Розчинник випаровували в вакуумі, та залишок розчиняли в безводному ДХМ (1,5 л) та перемішували протягом 30 хвилин. Реакційну суміш охолоджували до 0 °C, та по краплям додавали тетрахлорид титану (1,2 л, 6480 ммоль). Реакційну суміш перемішували при 40 °C протягом 6 днів. Реакційну суміш виливали на кригу, та регулювали pH до 8-9 6N водним розчином NaOH. Суспензію тричі екстрагували EtOAc. Органічний шар екстрагували 3 M HCl. pH кислотного водного розчину регулювали до 7-8 3N розчином NaOH та двічі екстрагували EtOAc. Органічний шар сушили над безводним сульфатом натрію та концентрували при пониженому тиску, одержуючи продукт. Сиру сполуку розчиняли в мінімальній кількості ДХМ та змішували з пентаном, одержуючи сполуку #A1 у вигляді світло-коричневої твердої речовини. Вихід: 90 г (35%). Rf: 0,6 (30% EtOAc в петролейному етері). 19 UA 110766 C2 РХ-МС m/z = 209 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 7,82 (м, 2H), 8,11 (д, J = 8,8 Гц, 2H), 8,30 (ш с, 1H), 8,56 (д, J = 6,0 Гц, 1H), 9,35 (с, 1H). Стадія 2. Синтез 6-бромізохіноліну 2-оксиду (#A2). м-Хлорпероксибензойну кисоту (120,0 г, 720,0 ммоль) додавали до розчину #A1 (90,0 г, 480,0 ммоль) в ДХМ (500 мл) при кімнатній температурі, та реакційну суміш перемішували протягом 16 год. 1N NaOH додавали до реакційної суміші, що перемішувалась, щоб регулювати pH до 7-8. Шари розділяли, та водний шар екстрагували ДХМ. Органічний шар сушили над безводним сульфатом натрію та концентрували при пониженому тиску, одержуючи сирий продукт. Твердий продукт розтирали із сумішшю н-пентана та етанола (8:2), одержуючи #A2 у вигляді білої твердої речовини. Вихід: 65 г (60%). Rf: 0,2 (EtOAc). 1 РХ-МС m/z = 225 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 7,83 (м, 2H), 7,91 (д, J = 6,8 Гц, 1H), 8,21 (дд, J = 8,0, 1,2 Гц, 1H), 8,26 (ш с, 1H), 8,97 (с, 1H). Стадія 3. Синтез 6-бромізохінолін-1-карбонітрилу (#A3). Триметилсилілціанід (52,0 мл, 580,0 ммоль) додавали по краплям до розчину, який перемішували, #A2 (65,0 г, 290,0 ммоль) та DBU (50,0 мл, 348,0 ммоль) в ТГФ (500 мл) при кімнатній температурі протягом періоду часу 15 хвилин. Реакційну суміш перемішували при кімнатній температурі протягом 1 год. До реакційної суміші додавали воду, та розчин екстрагували ДХМ. Органічний шар сушили над безводним Na2SO4 та концентрували при пониженому тиску, одержуючи сирий продукт. Продукт чистили, використовуючи колоночну хроматографію на силікагелі (100-200 меш) з 0-4% EtOAc в петролейному етері як елюєнті, одержуючи #A3 у вигляді білої твердої речовини. Вихід: 41 г (61%). Rf: 0,6 (30% EtOAc в петролейному етері). 1 РХ-МС m/z = 233 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 8,07 (дд, J = 11,2, 2,0 Гц, 1H), 8,21 (м, 2H), 8,55 (ш с, 1H), 8,77 (д, J = 7,6 Гц, 1H). Загальна методика одержання проміжних сполук #A4, #A5, #A6 та #1, #2, #3, #4, #6, #7. Стадія 4. Розчин #A3 (1 екв.) в толуолі (50 мл) дегазували шляхом барботування газоподібним аргоном протягом 15 хв. та потім Pd2dba3 (0,03 екв.), BINAP (0,06 екв.) та Cs2CO3 (3 екв.) додавали до розчину, з наступним додаванням аміноспирту (2 екв.). Суміш нагрівали при 100 °C в атмосфері аргону протягом 3 год. Реакційну суміш охолоджували до кімнатної температури, розбавляли EtOAC та промивали водою та насиченим сольовим розчином. Органічний шар сушили над Na2SO4 та концентрували, одержуючи сирий продукт. Сирі сполуки чистили, використовуючи колоночну хроматографію на силікагелі (100-200 меш) із застосуванням 0-5% MeOH в ДХМ. Виходи: 25-45%. Стадія 5. MsCl (1 екв.) додавали по краплям до розчину #A4 (1 екв.) та Et 3N (2 екв.) в ДХМ (10 мл) при 0 °C та перемішували при кімнатній температурі протягом 3 год. Реакційну суміш розбавляли ДХМ, промивали водою та насиченим сольовим розчином. Органічний шар сушили над Na2SO4 та концентрували. Сирі продукти застосовували на наступній стадії без додаткової очистки. Стадія 6. трет-бутанол (2 екв.) повільно додавали до розчину хлорсульфонілізоціанату (2 екв.) в толуолі (1 мл/1 ммоль) при 0 °C. Реакційну суміш перемішували при кімнатній температурі протягом 45 хв. Даний розчин (трет-бутилхлорсульфонілкарбамату) потім додавали до розчину #A5 (1 екв.) та ДІПЕА (4 екв.) в ТГФ та перемішували при кімнатній температурі протягом 12 год. Реакційну суміш розбавляли водою та екстрагували EtOAc. Органічний шар промивали водою, насиченим сольовим розчином, потім сушили над безводним Na2SO4 та концентрували. Сирі продукти чистили, використовуючи колоночну хроматографію на силікагелі (100-200 меш), застосовуючи 0-40% EtOAc в петролейному етері. Стадія 7. ТФО додавали до розчину #A6 (1 екв.) в ДХМ (8 мл) при 0 °C та перемішували при кімнатній температурі протягом 2 год. Реакційну суміш концентрували, розбавляли водою, нейтралізували насиченим водним розчином NaHCO3, потім екстрагували ДХМ. Органічний шар промивали водою та сушили над Na2SO4, потім концентрували. Сирі продукти чистили розтиранням з ДХМ та пентаном, одержуючи сполуку. У випадку рацемічних речовин, енантіомери розділяли, застосовуючи хіральну препаративну ВЕРХ. Колонка: CHIRALPAK IA, 4,6 мм × 250, 5 мкм; Рухома фаза: н-Гексан: EtOH (65:35) (Для X3: 35:65; Для X2: 70:30); Швидкість потоку: 1 мл/хв; Елюєнт: EtOH. Приклад 1 6-[(3S)-3-метил-1,1-діоксидо-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрил (#1; R = CH3) 1 РХ-МС m/z =289,1 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 1,37 (д, J = 6,3 Гц, 3H), 3,27 (м, 1H), 3,74 (м, 1H), 4,63 (м, 1H), 7,17 (д, J = 5,7 Гц, 1H), 7,72 (м, 1H), 7,89 (дд, J = 10,7, 2,1 Гц, 1H), 8,26 (м, 2H), 8,62 (д, J = 5,7 Гц, 1H). Приклад 2 6-[(3S)-3-етил-1,1-діоксидо-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрил (довільно 1 5 10 15 20 25 30 35 40 45 50 55 60 20 UA 110766 C2 5 10 15 20 25 30 35 40 призначена стереохімія) (#2; R = CH2CH3) 1 РХ-МС m/z = 303,1 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 0,92 (т, J = 7,4 Гц, 3H), 1,61-1,86 (м, 2H), 3,36 (дд, J = 12,6, 4,0 Гц, 1H), 3,67 (дд, J = 12,5, 6,5 Гц, 1H), 4,40-4,54 (м, 1H), 7,73 (д, J = 2,2 Гц, 1H), 7,89 (дд, J = 9,2, 2,3 Гц, 1H), 8,11 (ш с, 1H), 8,17 (д, J = 5,7 Гц, 1H), 8,27 (д, J = 9,3 Гц, 1H) 8,62 (д, J = 5,7 Гц, 1H). Приклад 3 6-[(3R)-1,1-діоксидо-3-(2,2,2-трифлуоретил)-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрил (довільно призначена стереохімія) (#3; R = CH 2CF3) 1 РХ-МС m/z = 357,1 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 2,72-3,02 (м, 2H), 3,72-3,87 (м, 1H), 4,94-5,06 (м, 1H), 7,76 (д, J = 2,2 Гц, 1H), 7,89 (дд, J = 9,2, 2,2 Гц, 1H), 8,19 (д, J = 5,7 Гц, 1H), 8,28-8,36 (м, 2H), 8,65 (д, J = 5,7 Гц, 1H) (додатковий пік знаходиться під піком води). Приклад 4 6-[(3R)-1,1-діоксидо-3-(2-фенілетил)-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрил (довільно призначена стереохімія) (#4; R = CH 2CH2C6H5) РХ-МС m/z = 379,2 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 2,01 (ш с, 2H), 2,63-2,81 (м, 2H), 3,51 (ш с, 1H), 3,71 (д, J = 5,4 Гц, 1H), 4,52 (ш с, 1H), 7,10-7,39 (м, 5H), 7,51 (ш с, 1H), 7,85 (д, J = 9,1 Гц, 1H), 8,05 (д, J = 4,8 Гц, 1H), 8,17-8,33 (м, 2H), 8,62 (д, J = 5,1 Гц, 1H). Приклад 5 6-[1-метил-(3S)-3-метил-1,1-діоксидо-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрил (#5, R = CH3, N-CH3) K2CO3 (2 екв.) та MeI (2 екв.) додавали до розчину #1 (1 екв.) в ДМФ (3 мл) при 0 °C та перемішували при кімнатній температурі протягом 2 год. Реакційну суміш розбавляли водою. Одержану в результаті тверду речовину фільтрували, промивали водою та сушили. Сирі продукти чистили розтиранням з ДХМ та пентаном, одержуючи чисту сполука. 1 РХ-МС m/z = 303,1 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 1,34 (д, J = 6,1 Гц, 3H), 2,78 (с, 3H), 3,20 (дд, J = 10,1, 6,5 Гц, 1H) 3,77 (дд, J = 10,2, 6,44 Гц, 1H) 4,68 (кв, J = 6,3 Гц, 1H) 7,85 (д, J = 2,2 Гц, 1H) 7,90 (дд, J = 9,2, 2,3 Гц, 1H) 8,21 (д, J = 5,6 Гц, 1H) 8,31 (д, J = 9,1 Гц, 1H) 8,66 (д, J = 5,7 Гц, 1H). Приклад 6 6-{(3R)-1,1-діоксидо-3-[3-(трифлуорметил)феніл]-1,2,5-тіадіазолідин-2-іл}ізохінолін-1карбонітрил (довільно призначена стереохімія) (#6; R = м-CF3-C6H5) 1 РХ-МС m/z = 419,1 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 3,41 (дд, J = 12,7, 4,8 Гц, 1H), 4,11 (дд, J = 12,7, 6,9 Гц, 1H), 5,84 (т, J = 5,9 Гц, 1H), 7,61-7,66 (м, 2H), 7,66-7,76 (м, 2H), 7,81 (дд, J = 9,2, 2,4 Гц, 1H), 7,88 (с, 1H), 8,07 (д, J = 5,8 Гц, 1H), 8,22 (д, J = 9,2 Гц, 1H), 8,51 (с, 1H), 8,57 (д, J = 5,8 Гц, 1H). Приклад 7 6-[(3S)-3-(4-хлорфеніл)-1,1-діоксидо-1,2,5-тіадіазолідин-2-іл]ізохінолін-1-карбонітрил (довільно призначена стереохімія) (#7; R = п-Cl-C6H5) 1 РХ-МС m/z = 385,6 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 4,06 (дд, J = 12,5, 6,9 Гц, 1H), 5,70 (т, J = 6,1 Гц, 1H), 7,41-7,52 (м, 4H), 7,57 (д, J = 2,2 Гц, 1H), 7,78 (дд, J = 9,2, 2,3 Гц, 1H), 8,06 (д, J = 5,6 Гц, 1H), 8,20 (д, J = 9,2 Гц, 1H), 8,43 (ш с, 1H), 8,56 (д, J = 5,8 Гц, 1H) (додатковий пік знаходиться під піком води). 1 21 UA 110766 C2 Boc 2O, ДХМ PCC, ДХМ LDA, ТГФ -78 кт, 3 год oC-кт, 16 год кт, 4 год #B1 ТФО, ДХМ Pd2dba3, Cs 2CO3 толуол NaBH4, MeOH кип'ятіння, 48 год кт, 4 год #B4 #B3 #B2 Розділення енантиомерів 110 oC ,мкВт, 20 хв #B5 #B6 #8 5 10 15 20 25 30 35 Стадія 1. Синтез трет-бутилметилсульфонілкарбамату (#B1). Розчин Boc 2O (41,2 г, 189,2 ммоль) в ДХМ (200 мл) додавали по краплям до суспензії, яку перемішували, метансульфонаміду (15,0 г, 157,7 ммоль), Et3N (23,6 мл, 173,5 ммоль) та DMAP (1,9 г, 15,8 ммоль) в ДХМ (200 мл). Одержану в результаті суспензію перемішували протягом 3 год при кімнатній температурі та концентрували в вакуумі. Одержаний в результаті залишок розбавляли EtOAc (300 мл) та підкислювали 1 N HCl (200 мл). Органічний шар промивали водою, потім насиченим сольовим розчином, сушили над Na2SO4 та концентрували при пониженому тиску, одержуючи сиру суміш, яку розтирали з 10% EtOAc в петролейному етері, одержуючи #B1 у вигляді білої твердої речовини (25,0 г, 81%). Rf: 0,6 (50% EtOAc в петролейному етері). 1 РХ-МС m/z = 194,3 (M-H). H ЯМР (400 МГц, CDCl3): 1,44 (с, 9H), 3,19 (с, 3H), 7,19 (с, 1H). Стадія 2. Синтез трет-бутил 3-гідроксибутилсульфонілкарбамату (#B2). Freitag, D., Metz, P. Тетраhedron 2006, 62(8), 1799-1805. н-BuLi (10,2 мл, 1M в гексані, 10,2 ммоль) додавали до розчину діізопропіламіну (1,7 мл, 10,2 ммоль) в ТГФ (20 мл) при -78 °C, та одержану в результаті суміш перемішували протягом 10 хвилин при -78 °C та потім 30 хвилин при -5 °C. Реакційну суміш знову охолоджували до -78 °C, потім розчин #B1 (1,0 г, 5,1 ммоль) в ТГФ (10 мл) додавали по краплям до даної реакційної суміші (підтримуючи температуру реакційної суміші на -78 °C), та перемішування продовжували протягом 20 хвилин. Розчин пропіленоксиду (0,47 мл, 6,7 ммоль) в ТГФ (15 мл) додавали по краплям до даної реакційної суміші при -78 °C та перемішування продовжували протягом 30 хвилин. Реакційну суміш повільно нагрівали до кімнатної температури, та перемішування продовжували протягом 16 год. Суміш виливали в охолоджений кригою насичений водний розчин NH4Cl. Одержаний в результаті осад розчиняли шляхом додавання води, та суміш підкислювали 1N HCl до pH = 3. Водний шар екстрагували ДХМ. Органічний шар промивали насиченим сольовим розчином, сушили над безводним Na 2SO4, концентрували, одержуючи залишок, який хроматографували на силікагелі (230-400 меш), застосовуючи діетиловий етер, як елюєнт, одержуючи #B2 у вигляді безбарвної олії (0,3 г. 25%). R f: 0,3 (Et2O). РХ-МС m/z = 252,1 (M-1) Стадія 3. Синтез Boc-захищеного сульфонамідкетону (#B3). Піридинію хлорхромат (0,53 г, 2,5 ммоль) додавали до розчину #B2 (0,30 г, 1,2 ммоль) в ДХМ (15 мл), та одержаний в результаті темно-коричневий розчин перемішували протягом 4 год при температурі навколишнього середовища. Реакційну суміш розбавляли Et 2O (10 мл), та перемішування продовжували протягом 15 хвилин. Його фільтрували через силікагель (230-400 меш) та промивали Et2O, та фільтрат концентрували при пониженому тиску, одержуючи #B3 у вигляді коричневої олії (0,2 г. 68%). Rf: 0,4 (Et2O). 1 РХ-МС m/z = 250,1 (M-H). H ЯМР (300 МГц, CDCl3): 1,51 (с, 9H), 2,23 (с, 3H), 3,02 (т, J = 7,2 Гц, 2H), 3,68 (т, J = 6,9 Гц, 2H), 7,00 (с, 1H). Стадія 4. Синтез ненасиченого гетероциклу (#B4). ТФО (4,2 мл, 55,7 ммоль) додавали до 22 UA 110766 C2 5 10 15 20 25 30 35 40 розчину #B3 (3,5 г, 13,9 ммоль) в ДХМ (50 мл), та одержаний в результаті розчин нагрівали при кип’ятінні зі зворотним холодильником протягом 48 год. Після охолодження, до даного розчину додавали EtOH (40 мл), та розчин концентрували в вакуумі до однієї треті від початкового об’єму та потім проводили кристалізацію при -20 °C, одержуючи #B4 у вигляді майже білої твердої сполуки (1,1 г, 61%). Rf: 0,3 (1:1 EtOAc/ДХМ). 1 ГХ-МС m/z = 133,0 (M). H ЯМР (400 МГц, CDCl3): 2,34 (с, 3H), 3,18-3,29 (м, 4H). Стадія 5. Синтез насиченого гетероциклу (#B5). NaBH4 (0,46 г, 12,4 ммоль) додавали невеликими порціями до розчину #B4 (1,1 г, 8,3 ммоль) в сухому MeOH (40 мл) при 0 °C, та реакційну суміш перемішували при кімнатній температурі протягом 4 год. Реакційну суміш гасили крижаною водою та екстрагували ДХМ. Органічні шари сушили над Na 2SO4 та концентрували одержуючи чистий #B5 у вигляді безбарвної олії (0,85 г, 77%). R f: 0,4 (1:1 EtOAc/ДХМ). 1 ГХ-МС m/z = 135,1 (M). H ЯМР (400 МГц, CDCl3): 1,30 (д, J = 6 Гц, 3H), 2,00-2,10 (м, 1H), 2,40-2,56 (м, 1H), 3,09-3,17 (м, 1H), 3,20-3,27 (м, 1H), 3,70-3,77 (м, 1H), 4,12 (ш с, 1H). Стадія 6. Синтез продукту сполучення (#B6). Pd2dba3 (0,094 г, 0,10 ммоль), BINAP (0,19 г, 0,31 ммоль) та Cs2CO3 (3,3 г, 10,3 ммоль) додавали до дегазованого розчину 6-бромізохінолін1-карбонітрилу (0,8 г, 3,4 ммоль) в толуолі (10 мл) з наступним додаванням #B5 (0,52 г, 3,8 ммоль) в атмосфері азоту. Одержану в результаті реакційну суміш піддавали дії мікрохвильового випромінення при 110 °C протягом 20 хвилин. Реакційну суміш охолоджували до кімнатної температури, розбавляли EtOAc, фільтрували, та фільтрат промивали водою. Органічний шар відокремлювали, та водний шар екстрагували EtOAc. Органічні шари об’єднували, сушили над Na2SO4 та випаровували при пониженому тиску, одержуючи сиру суміш, яку хроматографували на силікагелі (100-200 меш), використовуючи 25% EtOAc в петролейному етері, одержуючи #B6 як світло-коричневу тверду речовину (0,25 г, 25%). Rf: 0,4 (25% EtOAc/петролейний етер). 1 Рацемічний: РХ-МС m/z = 288,1 (M + H). H ЯМР (300 МГц, CDCl3): 1,41 (д, J = 6,3 Гц, 3H), 2,27-2,38 (м, 1H), 2,71-2,79 (м, 1H), 3,30-3,38 (м, 1H), 3,50-3,58 (м, 1H), 4,38-4,44 (м, 1H), 7,67 (д, J = 2,1 Гц, 1H), 7,71 (дд, J = 2,1, 9,3 Гц, 1H), 7,83 (д, J = 5,7 Гц, 1H), 8,35 (д, J = 9 Гц, 1H), 8,61 (д, J = 5,7 Гц, 1H). Рацемічну сполуку хроматографували для енантіомерного розділення. Умови: Колонка: CHIRAL PAK IA, 4,6 X 250мм, 5 мкм; Колонка ID: ANL_CHIR IA_145; Рухома фаза: A = гексан, B = ізопропіловий спирт; ISOCRATIC: 60:40; FLOW: 0,8 мл/хв; Колонка Temp: 25°C; Елюєнт: EtOH Енантіомер #8: Чистота за хіральною ВЕРХ: 99,38 % (час утримання 12,55 хвилин). 1 РХ-МС m/z = 287,9 (M + H). H ЯМР (300 МГц, d6-ДМСО): 1,30 (д, J = 6,3 Гц, 3H), 2,10-2,17 (м, 1H), 2,65-2,76 (м, 1H), 3,51-3,55 (м, 1H), 3,70-3,79 (м, 1H), 4,50-4,57 (м, 1H), 7,81 (д, J = 2,1 Гц, 1H), 7,87 (дд, J = 2,7, 9,0 Гц, 1H), 8,20 (д, J = 5,4 Гц, 1H), 8,28 (д, J = 9,0 Гц, 1H), 8,64 (д, J = 5,7 Гц, 1H). Приклад 8 6-[(3S)-3-метил-1,1-діоксидо-1,2-тіазолідин-2-іл]ізохінолін-1-карбонітрил 1 РХ-МС m/z = 287,9 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 1,31 (д, J = 5,7 Гц, 3H), 2,08-2,27 (м, 1H), 2,67-2,74 (м, 1H), 3,49-3,59 (м, 1H), 3,71-3,79 (м, 1H), 4,50-4,57 (м, 1H), 7,81 (с, 1H), 7,87 (д, J = 9,3 Гц, 1H), 8,21 (д, J = 5,4 Гц, 1H), 8,29 (д, J = 9,0 Гц, 1H), 8,64 (д, J = 5,7 Гц, 1H). Чистота за хіральною ВЕРХ: 98,9% (час утримання 20,42 хвилин). Pd2dba3, BINAP Cs 2CO3, толуол 30% ДХМ, 00С кт, 2 год 80% #C1 ТФО, CH2Cl2 кт, 15 год 60% #C2 Хіральне 0 oC-кт, 2 год 59% #C3 ДІПЕА, ТГФ MsCl, Et 3N розділення #9 #C4 23 UA 110766 C2 5 10 15 20 25 30 35 40 45 50 Стадія 1. Синтез продукту сполучення (#C1). Розчин #A3 (1,0 г, 4,3 ммоль) в толуолі (100 мл) барботували газоподібним аргоном протягом 15 хвилин. Pd 2dba3 (0,12 г, 0,13 ммоль), BINAP (0,24 г, 0,39 ммоль) та Cs2CO3 (4,7 г, 14,6 ммоль) додавали до розчину з наступним додаванням рацемічного 2-амінопропан-1-олу (0,66 мл, 8,6 ммоль). Суміш нагрівали при 100 °C в атмосфері аргону протягом 3 год. Реакційну суміш охолоджували до кімнатної температури, розбавляли EtOAc та промивали водою. Органічний шар промивали насиченим сольовим розчином, сушили над Na2SO4 та концентрували при пониженому тиску. Сиру сполуку чистили, застосовуючи силікагелеву колонка хроматографію, використовуючи 25% EtOAc в петролейному етері, як елюєнті, одержуючи продукт #C1 у вигляді жовтої твердої речовини (0,3 г, 30%). Rf: 0,3 (40% EtOAc в петролейному етері). РХ-МС m/z = 227,0 (M + H). Стадія 2. Синтез мезилатного продукту (#C2). Мезилхлорид (0,80 мл, 10,6 ммоль) додавали до розчину #C1 (0,60 г, 2,7 ммоль) та Et3N (1,4 мл, 10,6 ммоль) в ДХМ (40 мл) при 0 °C, та суміш перемішували при кімнатній температурі протягом 2 год. Реакційну суміш розбавляли ДХМ та, промивали водою. Органічний шар промивали насиченим сольовим розчином, сушили над Na2SO4 та концентрували при пониженому тиску. Сирий продукт #C2 (0,65 г олієподібної твердої речовини) використовували на наступній стадії без очистки. Rf: 0,4 (40% EtOAc в петролейному етері). РХ-МС m/z = 305,0 (M + H). Стадія 3. Синтез циклізованого Boc-захищеного продукт (#C3). ClSO2NCO (1 мл, 10,6 ммоль) додавали по краплям протягом 5 хвилин до суміші з трет-бутанолу (1 мл) та толуолу (2,5 мл), та реакційну суміш перемішували при кімнатній температурі протягом 45 хвилин. Суміш (третбутилхлорсульфонілкарбамат) додавали до розчину #C2 (0,65 г, 2,1 ммоль) та ДІПЕА (1,8 мл, 10,6 ммоль) в ТГФ (10 мл), та суміш перемішували при кімнатній температурі протягом 15 год. Реакційну суміш розбавляли ДХМ та екстрагували водою. Органічний шар сушили над Na 2SO4 та концентрували в вакуумі. Продукт чистили пропусканням через силікагелеву колонку (100200 меш), використовуючи 25% EtOAc в петролейному етері, одержуючи 0,5 г (60%) #C3 у вигляді майже білої твердої речовини. Rf: 0,5 (50% EtOAc в петролейному етері). 1 H ЯМР (400 МГц, d6-ДМСО): 1,29 (д, J = 6,2 Гц, 3H), 1. 59 (с, 9H), 3,62 (м, 1 H), 4,19 (м, 1H), 4,26 (м, 1H), 7,75 (т, J = 7,8 Гц, 1H), 7,83 (м, 1 H), 8,17 (д, J = 6,6 Гц, 1H), 8,21 (д, J = 6,6 Гц, 1H), 8,24 (д, J = 8,4 Гц, 1H), 8,40 (д, J = 8,9 Гц, 1H). Стадія 4. Синтез рацемічної суміші (#C4) та кінцевого продукту #9. ТФО (10 мл) додавали до розчину #C3 (0,50 г, 0,82 ммоль) в ДХМ (10 мл) при 0 °C, та суміш перемішували при кімнатній температурі протягом 2 год. Реакційну суміш концентрували, розбавляли водою, нейтралізували NaHCO3, екстрагували ДХМ та промивали водою. Органічний шар сушили над Na2SO4 та концентрували. Сиру сполуку чистили, обробляючи ДХМ та н-пентаном, одержуючи 0,22 г (59%) #C4 у вигляді білої твердої речовини. Rf: 0,3 (60% EtOAc в петролейному етері). #C4 (рацемічний, 220 мг) піддавали хіральній препаративній ВЕРХ, одержуючи два енантіомери у вигляді майже білих твердих речовин (65 мг #9 та 35 мг іншого енантіомера). Умови хіральної препаративної ВЕРХ: Колонка: CHIRALPAK IC, 250×30 мм, 5 мкм; Рухома фаза: н-Гексан/EtOH (60%/40%); Швидкість потоку: 30 мл/хв. Енантіомер #9: Чистота за хіральною ВЕРХ: 98,60 % (час утримання 10,93 хвилин) Приклад 9 6-[(3S)-3-метил-1,1-діоксидо-1,2,5-тіадіазолідин-2-іл]нафталін-1-карбонітрил (стереохімія призначається довільно) 1 РХ-МС m/z = 286,0 (M-H). H ЯМР (400 МГц, d6-ДМСО): 1,31 (д, J = 6,2 Гц, 3H), 3,13-3,25 (м, 1H), 3,71 (дт, J = 12,5, 6,8 Гц, 1H), 4,49-4,62 (м, 1H), 7,62-7,70 (м, 1H), 7,75-7,83 (м, 2H), 7,99 (т, J = 7,8 Гц, 1H), 8,07 (д, J = 6,6 Гц, 1H), 8,14 (д, J = 8,9 Гц, 1H), 8,28 (д, J = 8,4 Гц, 1H). Чистота за хіральною ВЕРХ: 99,1% (час утримання 17,12 хвилин) 24 UA 110766 C2 SOCl2/MeO 00С-кт 90% #D1 LAH, ТГФ нагрівання, 2 год 86% #D2 MsCl, Et 3N Pd2dba3, BINAP ДХМ, 00С-кт, 1 год К 3РО4, ДМСО 1050С, 2 год 48,5% #D4 #D3 ДІПЕА/ТГФ ТФО/ДХМ 00С-кт, 12 год 60% за 2 стадії 00С, 1 год 73% #D5 #D6 ДІПЕА/ТГФ Хіральне розділення #D7 5 10 15 20 25 #10 #11 Стадія 1. Синтез аміноестеру (#D1). Тіонілхлорид (8,5 мл, 116,5 ммоль) додавали до розчину амінокислоти (4,0 г, 38,8 ммоль) в MeOH (170 мл) при 0 °C, та реакційну суміш перемішували протягом 6 год при кімнатній температурі. Реакцію контролювали за ТШХ, та після зникнення вихідної речовини охолоджували до кімнатної температури, та додавали твердий NaHCO3. Реакційну суміш фільтрували, концентрували в вакуумі, та одержаний в результаті залишок розтирали з діетиловим етером, одержуючи сирий #D1 (4 г, 90%) у вигляді білої твердої речовини. Rf: 0,4 (t-BuOH: AcOH: H2O (4:0,5:0,5)). 1 ГХ-МС m/z = 117,1 (M). H ЯМР (400 МГц, d6-ДМСО): 1,17 (д, J = 6,8 Гц, 3H), 2,83-2,88 (м, 2H), 3,03-3,05 (м, 1H), 3,65 (с, 3H), 8,02-8,30 (ш с, 3H). Стадія 2. Синтез аміноспирту (#D2). #D1 (2,0 г, 13,0 ммоль) додавали порціями до суспензії LiAlH4 (1,4 г, 39,2 ммоль) в ТГФ (75 мл) в атмосфері азоту при 0 °C. Реакційну суміш перемішували протягом 30 хвилин, та потім давали перемішуватись при кімнатній температурі протягом наступних 30 хвилин. Реакційну суміш кип’ятили протягом 2 год, та потім охолоджували до -10 °C та обережно гасили охолодженою кригою водою (1,4 мл). Додавали 10% NaOH розчин (2,8 мл) та охолоджену кригою воду (4,2 мл), та суміш перемішували протягом 15 хвилин. ЇЇ фільтрували, та фільтрат промивали EtOAc (3 x 100 мл), сушили над безводним Na2SO4 та концентрували в вакуумі, одержуючи #D2 (1,2 г, 86%) у вигляді світложовтої рідини. Rf: 0,2 (20% MeOH в ДХМ). 1 H ЯМР (400 МГц, d6-ДМСО): 0,78 (д, J = 6,8 Гц, 3H), 1,46-1,54 (м, 1H), 2,41-2,45 (м, 2H), 2,50-2,54 (м, 1H), 3,22-3,34 (м, 4H). Стадія 3. Синтез продукту сполучення (#D3). K3PO4 (6,1 г, 28,8 ммоль), BINAP (0,44 г, 0,72 ммоль) та Pd2(dba)3 (0,32,0 г, 0,36 ммоль) додавали до дегазованої суспензії 6-бром-1ціаноізохіноліну #A3 (1,7 г, 7,2 ммоль), #D2 (1,2 г, 14,5 ммоль) в ДМСО при кімнатній температурі. Реакційну суміш нагрівали при 105 °C протягом 2 год. Реакційну суміш охолоджували до кімнатної температури, додавали воду (500 мл), після чого EtOAc (100 мл), та суміш перемішували протягом 10 хвилин. Двофазну суміш фільтрували через шар Celite™ та промивали EtOAc (100 мл). Органічний шар відокремлювали, та водний шар екстрагували 25 UA 110766 C2 5 10 15 20 25 30 35 40 45 50 55 60 EtOAc (3 x 100 мл). Об’єднані органічні шари сушили над безводним Na2SO4, концентрували при пониженому тиску, одержуючи сиру речовину. Її чистили, використовуючи колоночну хроматографію на силікагелі 100-200 меш, використовуючи 50-70% EtOAc в петролейному етері як елюєнт, одержуючи #D3 (0,5 г, 48,5%) у вигляді жовтої твердої речовини. Rf: 0,4 (60% EtOAC в петролейному етері). 1 РХ-МС m/z = 242,0 (M + H). H ЯМР (400 МГц, d6-ДМСО): 0,97 (д, J = 6,4 Гц, 3H), 1,87-1,99 (м, 1H), 2,92-2,99 (м, 1H), 3,20-3,27 (м, 1H), 3,38-3,42 (м, 2H), 4,59 (т, J = 5,2 Гц, 1H), 6,77 (д, J = 2,0, 1H), 7,01 (т, J = 5,6 Гц, 1H), 7,34 (дд, J = 9,2 Гц, J = 2,0 Гц, 1H), 7,73 (д, J = 6,0 Гц, 1H), 7,88 (д, J = 8,8 Гц, 1H), 8,312 (д, J = 6,0 Гц, 1H). Стадія 4. Mетансульфонований продукт сполучення (#D4). Триетиламін (0,44 мл, 3,1 ммоль) додавали до розчину #D3 (0,50 г, 2,0 ммоль) в ДХМ при 0 °C. Mетансульфонілхлорид (0,25 мл, 3,1 ммоль) додавали протягом 10 хвилин, та реакційну суміш перемішували протягом 1 год при кімнатній температурі. Після зникнення вихідної речовини за ТШХ, її розбавляли ДХМ та промивали водою. Органічний шар відокремлювали, сушили над Na 2SO4, концентрували при пониженому тиску, одержуючи сирий #D4 (0,6 г, сирий) у вигляді жовтої твердої речовини. Її використовували на наступній стадії без будь-якої очистки. Rf: 0,6 (50% EtOAc в петролейному етері). 1 РХ-МС m/z = 320,0 (M + H). H ЯМР (400 МГц, CDCl3): 1,17 (д, J = 6,8 Гц, 3H), 2,32-2,37 (м, 1H), 3,06 (с, 3H), 3,26-3,41 (м, 2H), 4,16-4,20 (м, 1H), 4,33-4,37 (м, 1H), 4,75 (ш с, 1H), 6,70 (д, J = 2,4, 1H), 7,09 (дд, J = 9,2 Гц, 2,4 Гц, 1H), 7,57 (д, J = 6,0 Гц, 1H), 8,05 (д, J = 9,2 Гц, 1H), 8,39 (д, J = 5,6 Гц, 1H). Стадія 5. Циклізовані та нециклізовані проміжні сполуки (#D5, #D6). Хлорсульфонілізоціанат (1,2 мл, 13,1 ммоль) додавали по краплям до розчину t-BuOH (1,4 мл, 13,1 ммоль) в толуолі (4,0 мл) при -5 °C. Реакційну суміш перемішували при кімнатній температурі протягом 20 хвилин, та потім до одержаної в результаті суспензії додавали ТГФ (1 мл) одержуючи прозорий розчин. В іншій колбі, ДІПЕА (2,3 мл, 13,1 ммоль) додавали до розчину #D4 (0,6 г, сирий 2,6 ммоль) в сухому ТГФ (3 мл). Одержаний вище реагент (ClSO 2NH-Boc) додавали до даної реакційної суміші по краплям при кімнатній температурі протягом періоду часу 20 хвилин. Одержану в результаті реакційну суміш потім перемішували протягом 16 год при кімнатній температурі. Суміш розбавляли EtOAc (100 мл) та промивали водою (100 мл). Водний шар промивали EtOAc (2 x 100 мл), об’єднували всі органічні шари, сушили над Na 2SO4, концентрували при пониженому тиску, одержуючи сирий продукт (РХ-МС показує потрібний #D6 та нециклізовані #D5). Даний сирий продукт чистили, використовуючи колоночну хроматографію на силікагелі 100-200 меш, використовуючи 10-30% EtOAc в петролейному етері, як елюєнт, одержуючи потрібний #D6 (0,35 г, 47,8%), та нециклізовані #D5 (0,22 г, сирий). Нециклізовані #D5 (0,22 г, сирий) розчиняли в ТГФ (1 мл) та ДІПЕА (0,6 мл), додавали до розчину. Реакційну суміш перемішували протягом наступних 12 год при кімнатній температурі. Після цього, розбавляли EtOAc (100 мл) та промивали водою (100 мл). Водний шар промивали EtOAc (2 x 100 мл), об’єднували всі органічні шари, сушили над Na 2SO4, концентрували при пониженому тиску, одержуючи сирий продукт. Даний сирий продукт чистили, використовуючи колоночну хроматографію на силікагелі 100-200 меш, використовуючи 10-30% EtOAc в петролейному етері, як елюєнт, одержуючи потрібний #D6 (1,1 г, 13,2%). Загальна кількість #D6 (0,5 г, 60% за двома стадіями, 82% РХ-МС чистоти). Rf: 0,8 (60% EtOAc в петролейному етері). 1 РХ-МС m/z = 403,1 (M+H). H ЯМР (400 МГц, CDCl3): 1,04 (д, J = 6,8 Гц, 3H), 1,50 (с, 9H), 2,38-2,48 (м, 1H), 3,65-3,82 (м, 2H), 3,92-4,02 (м, 1H), 4,30-4,38 (м, 1H), 7,79-7,81 (м, 1H), 7,867,88 (м, 2H), 8,34-8,37 (д, J = 9,2 Гц, 1H), 8,67 (д, J = 6,0 Гц, 1H). Стадія 6. Рацемат #D7 та кінцеві продукти (#10, #11). ТФО (5 мл) додавали до розчину #D6 (0,15 г, 0,37 ммоль) в ДХМ (100 мл) при 0 °C. Реакційну суміш перемішували протягом 1 год при 0 °C. Розчин нейтралізували насиченим водний розчином NaHCO 3 при 0 °C. Суміш розбавляли водою, екстрагували ДХМ (3 x 100 мл). Об’єднані органічні шари сушили над безводним Na 2SO4 та концентрували при пониженому тиску, одержуючи рацемічний #D7 (0,10 мг, 73%). РХ-МС m/z = 303,0 (M + H). Rf: 0,3 (60% EtOAc в петролейному етері). Енантіомерне розділення: #D7 піддавали хіральному розділенню, одержуючи кінцеві сполуки #10 (0,015 мг) та #11 (0,016 мг). Колонка: CHIRALPAK IA, 4,6 × 250 мм, 5 мкм; Рухома фаза: н-Гексан/i-PrOH/ДХМ (60%/15%/15%); Швидкість потоку: 0,8 мл/хв. Приклад 10 6-[(4R)-4-метил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил (#10; R = (R)CH3) 1 РХ-МС m/z = 303,0 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 0,98 (д, J = 6,4 Гц, 3H), 2,22-2,26 26 UA 110766 C2 5 10 (м, 1H), 3,16-3,22 (м, 1H), 3,34-3,39 (м, 1H), 3,59-3,65 (м, 1H), 3,77-3,81 (м, 1H), 7,75-7,79 (м, 1H, зникав в D2O обміні), 7,95 (дд, J = 8,8 Гц, J = 2,0 Гц, 1H), 8,06 (д, J = 1,6 Гц, 1H), 8,23-8,27 (м, 2H), 8,703 (д, J = 5,2 Гц, 1H). Rf: 0,3 (60% EtOAc в петролейному етері). Чистота за хіральною ВЕРХ: 98,2% (час утримання 11,43 хвилин). Приклад 11 6-[(4S)-4-метил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил (#11; R = (S)-CH3) 1 РХ-МС m/z = 301,0 (M-1). H ЯМР (400 МГц, d6-ДМСО): 0,98 (д, J = 7,2 Гц, 3H), 2,22-2,27 (м, 1H), 3,13-3,22 (м, 1H), 3,32-3,39 (м, 1H), 3,59-3,65 (м, 1H), 3,77-3,81 (м, 1H), 7,76-7,79 (м, 1H, зникав в D2O обміні), 7,96 (дд, J = 9,2 Гц, J = 2,0 Гц, 1H), 8,06 (д, J = 2,0 Гц, 1H), 8,23-8,27 (м, 2H), 8,70 (д, J = 5,2 Гц, 1H). Rf: 0,3 (60% EtOAc в петролейному етері). Чистота за хіральною ВЕРХ: 97,5% (час утримання 12,81 хвилин). Цільові сполуки #12, #13, #14, #15, #17, #18, #19, #20, #21, #22 загальної формули нижче одержували за аналогічною методикою, описаною вище для цільових сполук #10, #11. O O S N N R' N CN 15 20 25 30 35 40 45 50 Приклад 12 6-{(3R)-1,1-діоксидо-3-(3-феніл)-1,2,5-тіадіазолідин-2-іл}ізохінолін-1-карбонітрил (довільно призначена стереохімія) (#12; R = C6H5) 1 РХ-МС m/z = 365,1 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 3,39-3,57 (м, 2H), 3,67-3,81 (м, 1H), 3,87 (д, J = 11,2 Гц, 1H), 4,14 (т, J = 11,9 Гц, 1H), 7,26-7,48 (м, 5H), 8,02 (д, J = 9,37 Гц, 2H), 8,13 (ш с, 1H), 8,25 (д, J = 7,0 Гц, 2H) 8,69 (д, J = 5,4 Гц, 1H). Приклад 13 6-(4,4-диметил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл)ізохінолін-1-карбонітрил (#13; R’ = (гем(CH3)2) 1 РХ-МС m/z = 317,0 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 1,10 (с, 6H), 3,16 (д, J = 7,3 Гц, 2H), 3,55 (с, 2H), 7,92 (дд, J = 9,1, 2,1 Гц, 1H), 7,97-8,04 (м, 2H), 8,21-8,28 (м, 2H), 8,69 (д, J = 5,6 Гц, 1H). Приклад 14 6-(6,6-діоксидо-6-тіа-5,7-діазаспіро[2.5]окт-5-іл)ізохінолін-1-карбонітрил (#14; R’ = циклопропіл) 1 РХ-МС m/z = 315,2 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 0,66 (д, J = 6,2 Гц, 4H), 3,24 (д, J = 7,1 Гц, 2H), 3,64 (с, 2H), 7,89-8,00 (м, 2H), 8,03 (д, J = 2,1 Гц, 1H), 8,21-8,27 (м, 2H), 8,69 (д, J = 5,6 Гц, 1H). Приклад 15 6-[(4R)-4-(3-метилбензил)-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил (довільно призначена стереохімія) (#15; R’=CH2-[м-CH3-C6H4]) 1 РХ-МС m/z = 393,0 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 2,26 (с, 3H), 2,58-2,69 (м, 1H), 2,69-2,78 (м, 1H), 3,63-3,81 (м, 2H), 6,98-7,11 (м, 3H), 7,18 (т, J = 7,5 Гц, 1H), 7,69-7,78 (м, 1H), 7,93 (дд, J = 9,1, 2,0 Гц, 1H), 8,03 (д, J = 2,1 Гц, 1H), 8,21-8,28 (м, 2H), 8,70 (д, J = 5,6 Гц, 1H) (Додаткові сигнали протонів під сигналом води та не можуть бути інтегрованими). Цільову сполуку #16 одержували за аналогічною методикою, описаною вище для цільової сполуки #5. Приклад 16 6-[(4R)-6-етил-4-метил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил (довільно призначена стереохімія) (#16; R’=CH3, N-C2H5) 1 РХ-МС m/z = 303,0 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 0,95 (д, J = 6,3 Гц, 3H), 1,15 (т, 3H), сигнал одного протона під сигналом ДМСО, 3,09-3,14 (м, 1H), 3,20-3,26 (м, 3H), 3,64-3,69 (м, 2H), 7,96 (дд, J = 8,8 Гц, J = 2,1 Гц, 1H), 8,05 (м, 1H), 8,21-8,25 (м, 2H), 8,703 (м, 1H). Приклад 17 6-(5-метил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл)ізохінолін-1-карбонітрил (рацемічна суміш) 1 РХ-МС m/z = 303,1 (M + 1). H ЯМР (400 МГц, CDCl3): 1,39 (д, J = 6,3 Гц, 3H), 1,79-1,94 (м, 1H), 2,05 (дд, J = 14,1, 2,5 Гц, 1H), 3,66-3,77 (м, 1H), 4,03-4,18 (м, 2H), 7,78-7,91 (м, 3H), 8,34 (д, J = 9,0 Гц, 1H), 8,66 (д, J = 5,7 Гц, 1H) (протон NH в обміні). Приклад 18 6-[(4S)-4-(4-метилфеніл)-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил 27 UA 110766 C2 5 10 15 20 25 30 (довільно призначена стереохімія) (#18; R’ = (S)-п-CH3-C6H4) 1 РХ-МС m/z = 379,1 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 2,29 (с, 3H), 3,36-3,52 (м, 2H), 3,71 (д, J = 12,0 Гц, 1H), 3,83 (д, J = 11,0 Гц, 1H), 4,05-4,16 (м, 1H), 7,19 (м, J = 7,9 Гц, 2H), 7,30 (м, J = 7,9 Гц, 2H), 7,95-8,05 (м, 2 год), 8,09-8,14 (м, 1H), 8,21-8,28 (м, 2H), 8,69 (д, J = 5,6 Гц, 1H). Приклад 19 6-[(4R)-4-(4-метилфеніл)-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил (довільно призначена стереохімія) (#19; R’ = (R)-п-CH3-C6H4]) 1 РХ-МС m/z = 379,1 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 2,29 (с, 3H), 3,36-3,53 (м, 2H), 3,63-3,77 (м, 1H), 3,83 (д, J = 11,0 Гц, 1H), 4,03-4,16 (м, 1H), 7,19 (м, J = 7,9 Гц, 2H), 7,30 (м, J = 8,0 Гц, 2H), 7,94-8,05 (м, 2H), 8,12 (д, J = 1,9 Гц, 1H), 8,21-8,30 (м, 2H), 8,69 (д, J = 5,5 Гц, 1H). Приклад 20 6-[(4S)-4-(3-метилфеніл)-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил (довільно призначена стереохімія) (#20; R’ = (S)-C2H5) 1 РХ-МС m/z = 317,1 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 0,94 (т, J = 7,5 Гц, 3H), 1,31-1,44 (м, 2H), 1,91-2,07 (м, 1H), 3,19 (дд, J = 14,0, 10,4 Гц, 1H), 3,37-3,48 (м, 1H), 3,63 (дд, J = 12,4, 10,3 Гц, 1H), 3,74-3,84 (м, 1H), 7,73 (с, 1H), 7,95 (дд, J = 9,1, 2,2 Гц, 1H), 8,06 (д, J = 2,1 Гц, 1H), 8,208,30 (м, 2H), 8,70 (д, J = 5,6 Гц, 1H). Приклад 21 6-[(4S)-4-етил-1,1-діоксидо-1,2,6-тіадіазинан-2-іл]ізохінолін-1-карбонітрил (довільно призначена стереохімія) (#21; R’ = (S)-м-CH3-C6H4) 1 РХ-МС m/z = 379,1 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 2,32 (с, 3H), 3,35-3,54 (м, 2H), 3,66-3,79 (м, 1H), 3,84 (д, J = 10,7 Гц, 1H), 4,06-4,19 (м, 1H), 7,12 (д, J = 7,3 Гц, 1H), 7,17-7,22 (м, 1H), 7,22-7,31 (м, 2H), 7,96-8,05 (м, 2H), 8,12 (д, J = 2,1 Гц, 1H), 8,21-8,28 (м, 2H), 8,69 (д, J = 5,7 Гц, 1H). Приклад 22 6-(1,1-діоксидо-4-пропіл-1,2,6-тіадіазинан-2-іл)ізохінолін-1-карбонітрил (рацемічна суміш) (#22; R’ = C3H7) 1 РХ-МС m/z = 331,2 (M + 1). H ЯМР (400 МГц, d6-ДМСО): 0,81-0,96 (м, 3H), 1,33 (ш с, 4H), 2,09 (ш с, 1H), 3,12-3,25 (м, 1H), 3,41 (д, J = 13,5 Гц, 1H), 3,56-3,68 (м, 1H), 3,77 (д, J = 10,4 Гц, 1H), 7,73 (дд, J = 9,0, 4,6 Гц, 1H), 7,95 (д, J = 9,1 Гц, 1H), 8,06 (с, 1H), 8,20-8,30 (м, 2H), 8,70 (д, J = 5,6 Гц, 1H). MeOH SOCl2 LAH/ТГФ 700C 50% 00C-кт 100%, (сирий) #E2 #A3 К 3РО4, ДМСО,900C 20% #E1 Me3SiCF3 CsF ТГФ IBX EtOAc / 70 oC 100%, (сирий) #E3 35 40 45 -780C-кт 30% #E4 #23 Стадія 1. Синтез метилаланіну (#E1). Тіонілхлорид (18,4 мл, 252,8 ммоль) додавали до розчину аланіну (15,0 г, 168,5 ммоль) в метанолі при 0 °C. Потім, реакційну суміш перемішували при кімнатній температурі протягом 3 год. Після витрачення вихідної речовини, реакційну суміш охолоджували до 0 °C та обробляли твердим NaHCO3. Глинисту суспензію фільтрували через шар Celite™, та промивали MeOH (100 мл). Фільтрат концентрували при пониженому тиску, одержуючи залишок, який розбавляли ДХМ, промивали водою, насиченим сольовим розчином, сушили та концентрували, одержуючи #E1 (19,0 г, сирий продукт), який використовували на наступній стадії без додаткової очистки. Rf: 0,6 (20% метанол в ДХМ). 1 H ЯМР (400 МГц, d6-ДМСО): 1,36 (д, J = 7,2 Гц, 3H), 3,11 (с, 1H), 3,68 (с, 3H), 3,90 (кв, J = 7,2 Гц, 1H), 6,50 (ш с, 3H). Стадія 2. Синтез аміноспирту (#E2). Розчин #E1 (19,0 г, 184,5 ммоль) в ТГФ (300 мл) охолоджували до 0 °C, та порціями додавали LiAlH4 (21,0 г, 553,4 ммоль) протягом 30 хвилин. Реакційну суміш перемішували при кімнатній температурі доки реакційна суміш стане глинистою суспензією, та потім кип’ятили зі зворотним холодильником протягом 2 год. Реакційну суміш охолоджували до кімнатної температури, гасили 2N розчином NaOH до pH 7. 28
ДивитисяДодаткова інформація
Назва патенту англійськоюNovel selective androgen receptor modulators
Автори англійськоюAnderson, James, Thomas, Chekler, Eugene, Lvovich, Piatnitski, Ellsworth, Edmund, L., Erickson, Bruce, Kipp, Gilbert, Adam, Matthew, Ricketts, Anthony, P., Thompson, David, P., Unwalla, Rayomand, Jal, Verhoest, Patrick, Robert
Автори російськоюАндерсон Джэймс Томас, Чеклер Юджин Лвович Пьятницки, Эллсворт Эдмунд Л., Эриксон Брюс Кипп, Гилберт Адам Меттью, Рикеттс Энтони П., Томпсон Дэйвид П., Унвалла Рэёманд Джал, Вергест Патрик Роберт
МПК / Мітки
МПК: A61K 31/4725, C07D 285/10, C07D 211/22, C07D 217/26, C07D 401/04, C07C 255/58, A61P 25/00, A61P 5/26, A61P 19/00, A61P 5/28, C07D 417/04, C07D 207/08, A61P 3/00, A61P 21/00, C07D 205/04
Мітки: селективні, рецептора, андрогенного, модулятори
Код посилання
<a href="https://ua.patents.su/50-110766-selektivni-modulyatori-androgennogo-receptora.html" target="_blank" rel="follow" title="База патентів України">Селективні модулятори андрогенного рецептора</a>
Попередній патент: Спосіб визначення мікрокількостей фосфору
Наступний патент: Спосіб визначення присутності giardia lamblia у досліджуваному зразку та набір праймерів для його здійснення
Випадковий патент: Установка для культивування мікроорганізмів












