Напівсинтетичний спосіб одержання сполук з конденсованою циклічною системою і проміжні сполуки
Номер патенту: 75333
Опубліковано: 17.04.2006
Автори: Гальєго Пілар, Мансанарес Ігнасіо, Сарсуело Марія, Перес Марта, де ла Кальє Фернандо, Фернандес Кароліна, Чічарро Хосе Луіс, Куевас Кармен, Франсесч Андрес
Формула / Реферат
1. Спосіб одержання сполуки формули (XVIIb):
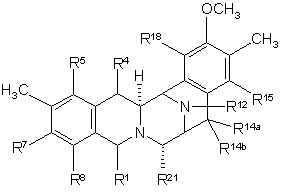 ,
,
де
R1 являє собою необов'язково захищену або модифіковану амінометиленову групу, необов'язково захищену або модифіковану гідроксиметиленову групу; і
R4 являє собою -Н; або
R1 і R4 разом утворюють групу формули (IV), (V), (VI) або (VII):
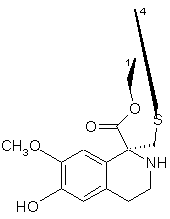 ,
,
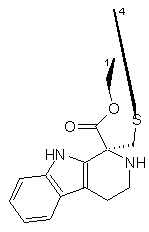 ,
,
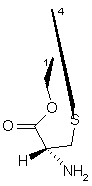 або
або
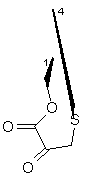 ;
;
R5 являє собою -Н або -ОН;
R7 являє собою –ОСН3 і R8 являє собою -OR, або R7 і R8 разом утворюють групу -О-СН2-О-;
R14a і R14b обидва являють собою –Н, або один являє собою -Н, а інший являє собою -ОН, -ОСН3 або -OCH=CH2, або R14а і R14b разом утворюють кетогрупу; і
R15 являє собою -Н або -ОН;
R18 являє собою -Н або -ОН;
R21 являє собою -Н, -ОН або CN;
і похідних,
з 21-ціаносполуки формули (XVIb):
 ,
,
у якій R1 являє собою амідометиленову групу або ацилоксиметиленову групу;
R5 і R8 незалежно вибирають з -Н, -ОН або –ОСОСН2ОН, або R5 і R8 обидва є кето, і кільце А є п-бензохіноновим кільцем;
R12 являє собою -Н, -СН3 або –СН2СН3;
R14a і R14b обидва являють собою -Н, або один являє собою -Н, а інший являє -ОН, -ОСН3 або –ОСН2СН3, або R14a і R14b разом утворюють кетогрупу; і
R15 і R18 незалежно вибирають з -Н або -ОН, або R15 і R18 обидва є кето, і кільце Е є п-бензохіноновим кільцем;
за умови, що, принаймні, одне з кілець А або Е є п-бензохіноновим кільцем, який відрізняється тим, що здійснюють при необхідності такі реакції:
a) хінонову систему кільця Е перетворюють у фенольну систему;
b) хінонову систему кільця А перетворюють у фенольну систему;
c) фенольну систему кільця А перетворюють в метилендіоксифенольне кільце;
d) здійснюють утворення місточкової спірокільцевої системи формули (IV), (V), (VI) або (VII), що проходить через 1-положення і 4-положення в кільці В; і
e) здійснюють перетворення в похідні;
з одержанням необхідної сполуки формули (XVIIb).
2. Спосіб за пунктом 1, де стадію а) перетворення хінонової системи кільця Е в фенольну систему здійснюють відновленням з використанням водню з каталізатором паладій-вуглець.
3. Спосіб за пунктом 1 або 2, де стадію b) перетворення хінонової системи кільця А в фенольну систему здійснюють відновленням з використанням водню з каталізатором паладій-вуглець.
4. Спосіб за пунктом 3, що включає, принаймні, стадії b), с) і е).
5. Спосіб за будь-яким з пунктів 1-4, де R1 і R4 разом утворюють групу формули (IV), (V), (VI) або (VII), і стадію d) утворення місточкової спірокільцевої системи, що проходить через 1-положення і 4-положення в кільці В, здійснюють заміщенням у 1-положення реагентом, що бере участь в утворенні містка, утворенням екс-ендо хінонметиду в 4-положенні, і взаємодією метиду з 1-замісником з утворенням місточкової спірокільцевої системи.
6. Спосіб за пунктом 5, де реагент, який використовують в утворенні містка, має структуру, представлену формулою (XIX)
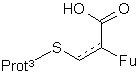 ,
,
де Fu означає захищену функціональну групу, Prot3 являє собою захисну групу, а пунктирна лінія показує необов'язково присутній подвійний зв'язок.
7. Спосіб за пунктом 6, де Fu являє собою групу -NHProt4a або OProt4b, де Prot4a являє собою амінозахисну групу, і Prot4b являє собою гідроксизахисну групу.
8. Спосіб за пунктом 7, де реагент, який використовують в утворенні містка, являє собою Int-29 або Int-37:
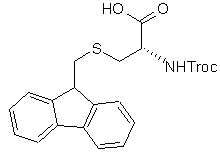 Int-29
Int-29
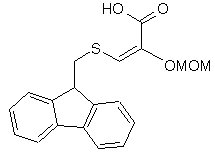 , Int-37.
, Int-37.
9. Спосіб за будь-яким з пунктів 5-8, де утворення метиду здійснюють шляхом введення гідроксигрупи в 10-положення в місці сполучення кілець А і В з утворенням фрагмента структури формули (XX):
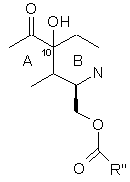 ,
,
де групу R'' вибирають для утворення необхідної групи формули (IV), (V), (VI) або (VII).
10. Спосіб за п. 9, де введення гідроксигрупи в 10-положення в місці з'єднання кілець А і В приводить до фрагмента формули (XXI):
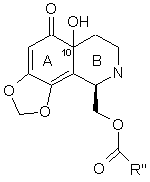 ,
,
де група R'' має вказані значення.
11. Спосіб за пунктом 9 або 10, де група R'' являє собою -CHFu-CH2-Sprot3, де Fu являє собою захищену функціональну групу, і Prot3 представляє тіолзахисну групу.
12. Спосіб за будь-яким з пунктів 1-11, де стадію е) здійснюють шляхом перетворення в похідні, що включає ацилювання.
13. Спосіб за будь-яким з пунктів 1-12, де 21-ціаносполуку формули (XVIb) одержують введенням 21-ціаногрупи в сафраміцин А, сафраміцин В, сафраміцин С, сафраміцин G, сафраміцин Н, сафраміцин S, сафраміцин Y3, сафраміцин Yd1, сафраміцин Ad1, сафраміцин Yd2, сафраміцин АН2, сафраміцин AH2Ac, сафраміцин АН1, сафраміцин АН1Ас, сафраміцин АR3, ренієраміцин А, ренієраміцин В, ренієраміцин С, ренієраміцин D, ренієраміцин Е, ренієраміцин F, ксестоміцин, сафраміцин D, сафраміцин F, сафраміцин Мх-1, сафраміцин Мх-2, сафрацин А або сафрацин В, або являє собою сафраміцин R.
14. Спосіб за пунктом 13, де 21-ціаносполука формули (XVIb) являє собою ціаносафрацин В, сполуку (2):
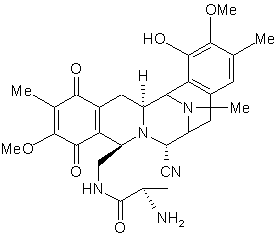 сполука 2.
сполука 2.
15. Спосіб за будь-яким з пунктів 1-14, де R5 у сполуці формули (XVIIb) являє собою алканоїлокси з 1-5 атомами вуглецю.
16. Спосіб за будь-яким з пунктів 1-15, де R5 у сполуці формули (XVIIb) являє собою ацетилокси.
17. Спосіб за будь-яким з пунктів 1-16, де R12 являє собою –СН3.
18. Спосіб за будь-яким з пунктів 1-17, де R14a і R14b у сполуці формули (XVIIb) являють собою водень.
19. Спосіб за будь-яким з пунктів 1-18, де R15 у сполуці формули (XVIIb) являє собою водень.
20. Спосіб за будь-яким з пунктів 1-19, де R18 у сполуці формули (XVIIb) являє собою гідрокси.
21. Спосіб за будь-яким з пунктів 1-20, де R21 у сполуці формули (XVIIb) являє собою -ОН або -CN.
22. Спосіб за будь-яким з пунктів 1-21, де R7 і R8 у сполуці формули (XVIIb) разом утворюють групу -О-СН2-О-.
23. Спосіб за будь-яким з пунктів 1-22, де R1 і R4 y сполуці формули (XVIIb) разом утворюють групу формули (IV), (V), (VI) або (VII):
 ,
,
 ,
,
 або
або
 .
.
24. Спосіб за будь-яким з пунктів 1-23, де R1 у сполуці формули (XVIIb) являє собою необов'язково захищену або модифіковану амінометиленову групу, необов'язково захищену або модифіковану гідроксиметиленову групу, і R4 являє собою -Н.
25. Спосіб за пунктом 24, де R1 у сполуці формули (XVIIb) являє собою групу –СН2NН2 або –CH2NH-aa, де аа являє собою ацильну групу амінокислоти.
26. Спосіб за пунктом 25, де сполука формули (XVIIb) являє собою N-ацилпохідне по групі R1, коли R1 являє собою групу –СH2NН2 або –CH2NH-aa.
27. Спосіб за пунктом 26, де R1 у сполуці формули (XVIIb) являє собою N-ацилпохідне, де ацильна група представлена формулою -CO-Ra, де Ra являє собою алкіл, алкокси, алкілен, арилалкіл, арилалкілен, амінокислотний ацил або гетероцикліл; кожна з яких необов'язково заміщена галогеном, ціано, нітро, карбоксіалкілом, алкокси, арилом, арилокси, гетероциклілом, гетероциклілокси, алкілом, аміно або заміщеною аміногрупою; або ацильна група являє собою аа.
28. Спосіб за пунктом 25, 26 або 27, де присутні одна або більше груп аа, яка являє собою аланіл, аргініл, аспартил, аспарагіл, цистил, глутаміл, глутамініл, гліцил, гістидил, гідроксипропіл, ізолейцил, лейцил, лізил, метіоніл, фенілаланіл, проліл, серил, треоніл, тироніл, триптофіл, тирозил, валіл або іншу ацильну групу амінокислоти.
29. Спосіб за пунктом 26 або залежними від нього пунктом, де аа являє собою аланіл.
30. Спосіб за будь-яким з пунктів 1-29, де в будь-якій реакції одна або більше груп-замісників захищена за допомогою захисної групи.
31. Спосіб за пунктом 29, де аланіл захищений бутоксикарбонільною групою.
32. Спосіб одержання сполуки формули (ХХІІb):
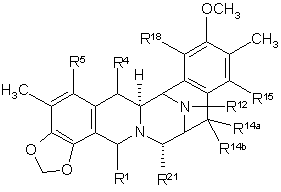 ,
,
де
R1 являє собою –CH2-NH2 або –СН2ОН, або захищений або модифікований варіант такої групи, і R4 являє собою -Н; або
R1 і R4 разом утворюють групу формул (IV), (V), (VI) або (VII):
 ,
,
 ,
,
 або
або
 ;
;
R5 являє собою -ОН або захищений або модифікований варіант такої групи;
R12 являє собою -Н, -СН3 або –СН2СН3;
R14a i R14b обидва являють собою -Н, або один являє собою -Н, а інший являє собою -ОН, або захищений або модифікований варіант такої групи; -ОСН3 або –ОСН2СН3, або R14a і R14b разом утворюють кетогрупу;
R15 являє собою Н, -ОН або захищений або модифікований варіант такої групи;
R18 являє собою -ОН, або захищений або модифікований варіант такої групи;
і
R21 являє собою -Н, -ОН або -CN;
з 21-ціаносполуки формули (XVIb):
 ,
,
де R1 являє собою амідометиленову групу або ацилоксиметиленову групу;
R5 і R8 незалежно вибирають з -Н, -ОН або –ОСОСН2ОН, або R5 і R8 обидва є кето, і кільце А є п-бензохіноновим кільцем;
R12 являє собою -Н, -СН3 або –CH2СН3;
R14a і R14b обидва являють собою -Н, або один являє собою -Н, а інший являє собою -ОН, -ОСН3 або –ОСН2СН3, або R14a і R14b разом утворюють кетогрупу; і
R15 і R18 незалежно вибирають з -Н або -ОН, або R15 і R18 обидва є кето, і кільце Е є п-бензохіноновим кільцем;
за умови, що, принаймні, одне з кілець А або Е є п-бензохіноновим кільцем,
який відрізняється тим, що здійснюють при необхідності такі реакції:
a) хінонову систему кільця Е перетворюють у фенольну систему;
b) хінонову систему кільця А перетворюють у фенольну систему;
c) фенольну систему кільця А перетворюють у метилендіоксифенольне кільце;
d) здійснюють утворення місточкової спірокільцевої системи формули (IV), (V), (VI) або (VII), яка проходить через 1-положення і 4-положення в кільці В; і
е) здійснюють перетворення в похідні;
з одержанням необхідної сполуки формули (ХХІІb).
33. Спосіб за пунктом 32, де в сполуці формули (ХХІІb) R5 являє собою -ОН, R14a і R14b являють собою Н, R15 являє собою Н і R18 являє собою ОН.
34. Спосіб за пунктом 32, де сполука формули (ХХІІb) являє собою ектеїнасцидин 743 або ектеїнасцидин 770:
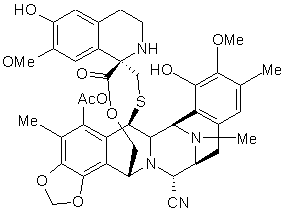 , Et-770
, Et-770
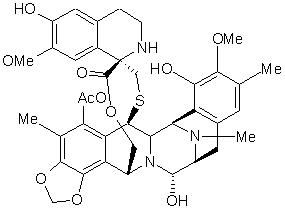 Et-743.
Et-743.
35. Спосіб за пунктом 34, де сполука формули (ХХІІb) являє собою ектеїнасцидин 743:
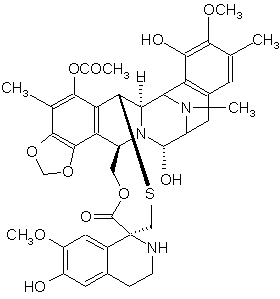 .
.
36. Спосіб за пунктом 32, де продукт являє собою сполуку формули (XXIII):
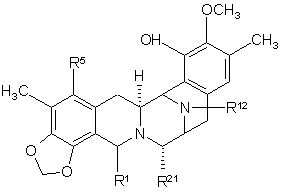 ,
,
де R1 являє собою модифіковану амінометиленову групу формули CH2-NH-CO-Ra, де Ra має лінійний ланцюг довжиною менше ніж 20 атомів;
R5 являє собою ацетильну групу;
R12 являє собою –СН3 і
R21 являє собою гідрокси або ціаногрупу.
37. Спосіб за пунктом 36, де Ra має лінійний ланцюг довжиною менше ніж 15 атомів.
38. Спосіб за пунктом 37, де Ra має лінійний ланцюг довжиною менше ніж 10 атомів.
39. Спосіб за пунктом 36, де сполука формули (XXIII) являє собою фталасцидин формули (III):
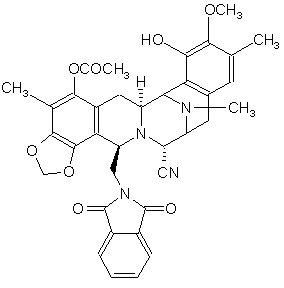 .
.
40. Спосіб за будь-яким з пунктів 1-39, що включає реакцію:
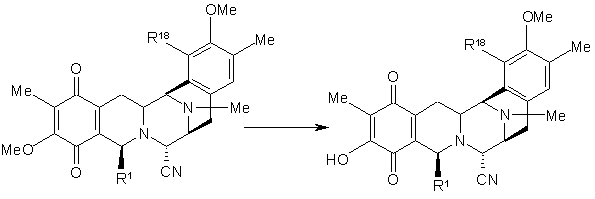 ,
,
де R1 і R18 мають вказані значення.
41. Спосіб за пунктом 40, де R18 являє собою захищену ОН групу.
42. Спосіб за будь-яким з пунктів 1-41, що включає реакцію:
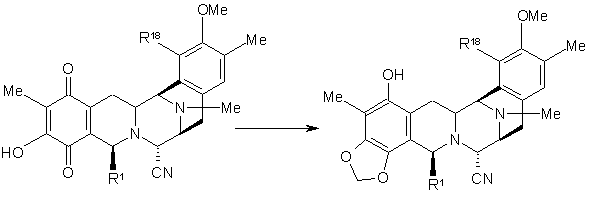 ,
,
де R1 і R18 мають вказані значення.
43. Спосіб за будь-яким з попередніх пунктів, що включає здійснення реакції, у якій сполуку з групою R1, що являє собою амінометилен, перетворюють у сполуку з групою R1, що являє собою гідроксиметиленову групу.
44. Сполука формули
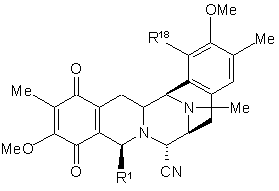 ,
,
де R1 являє собою необов'язково захищену або модифіковану амінометиленову групу; і R18 являє собою захищену ОН групу.
45. Сполука за пунктом 44, яка представлена формулою:
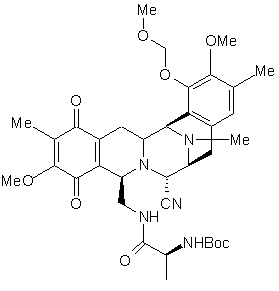 .
.
46. Сполука формули:
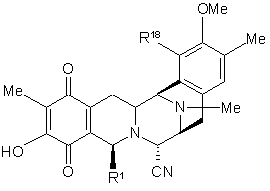 ,
,
де R1 являє собою необов'язково захищену або модифіковану амінометиленову групу; і R18 являє собою захищену ОН групу.
47. Сполука за пунктом 46, яка представлена формулою:
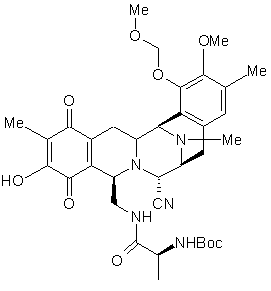 .
.
48. Сполука формули:
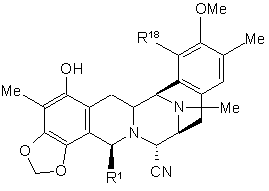 ,
,
де R1 являє собою необов'язково захищену або модифіковану амінометиленову групу; і R18 являє собою захищену ОН групу.
49. Сполука за пунктом 48, представлена формулою:
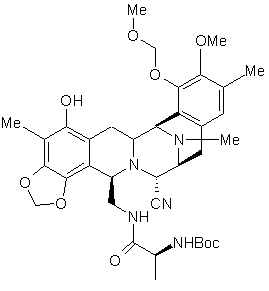 .
.
Текст
1. Спосіб одержання сполуки формули (XVIIb): R15 R12 R14a 14b R , 3 75333 4 HO O у якій R1 являє собою амідометиленову групу або ацилоксиметиленову групу; S R5 і R8 незалежно вибирають з -Н, -ОН або – NHTroc 5 8 ОСОСН2ОН, або R і R обидва є кето, і кільце А є п-бензохіноновим кільцем; 12 R являє собою -Н, -СН3 або –СН2СН3; R14a і R14b обидва являють собою -Н, або один явInt-29 ляє собою -Н, а інший являє -ОН, -ОСН3 або – HO O ОСН2СН3, або R14a і R14b разом утворюють кетогS рупу; і OMOM R15 і R18 незалежно вибирають з -Н або -ОН, або R15 і R18 обидва є кето, і кільце Е є пбензохіноновим кільцем; за умови, що, принаймні, одне з кілець А або Е є п, Int-37. бензохіноновим кільцем, який відрізняється тим, 9. Спосіб за будь-яким з пунктів 5-8, де утворення що здійснюють при необхідності такі реакції: метиду здійснюють шляхом введення гідроксигруa) хінонову систему кільця Е перетворюють у фепи в 10-положення в місці сполучення кілець А і В нольну систему; з утворенням фрагмента структури формули (XX): b) хінонову систему кільця А перетворюють у феO нольну систему; OH c) фенольну систему кільця А перетворюють в метилендіоксифенольне кільце; 10 A B d) здійснюють утворення місточкової спірокільцеN вої системи формули (IV), (V), (VI) або (VII), що проходить через 1-положення і 4-положення в кіO льці В; і e) здійснюють перетворення в похідні; з одержанням необхідної сполуки формули (XVIIb). O R'' , 2. Спосіб за пунктом 1, де стадію а) перетворення де групу R'' вибирають для утворення необхідної хінонової системи кільця Е в фенольну систему групи формули (IV), (V), (VI) або (VII). здійснюють відновленням з використанням водню 10. Спосіб за п. 9, де введення гідроксигрупи в 10з каталізатором паладій-вуглець. положення в місці з'єднання кілець А і В приводить 3. Спосіб за пунктом 1 або 2, де стадію b) перетдо фрагмента формули (XXI): ворення хінонової системи кільця А в фенольну систему здійснюють відновленням з використанням водню з каталізатором паладій-вуглець. 4. Спосіб за пунктом 3, що включає, принаймні, стадії b), с) і е). 5. Спосіб за будь-яким з пунктів 1-4, де R1 і R4 разом утворюють групу формули (IV), (V), (VI) або (VII), і стадію d) утворення місточкової спірокільцевої системи, що проходить через 1-положення і 4положення в кільці В, здійснюють заміщенням у 1положення реагентом, що бере участь в утворенні містка, утворенням екс-ендо хінонметиду в 4положенні, і взаємодією метиду з 1-замісником з утворенням місточкової спірокільцевої системи. 6. Спосіб за пунктом 5, де реагент, який використовують в утворенні містка, має структуру, представлену формулою (XIX) HO O S Prot3 Fu , де Fu означає захищену функціональну групу, Prot3 являє собою захисну групу, а пунктирна лінія показує необов'язково присутній подвійний зв'язок. 7. Спосіб за пунктом 6, де Fu являє собою групу NHProt4a або OProt4b, де Prot4a являє собою амінозахисну групу, і Prot4b являє собою гідроксизахисну групу. 8. Спосіб за пунктом 7, де реагент, який використовують в утворенні містка, являє собою Int-29 або Int-37: O A OH 10 B N O O O O R'' , де група R'' має вказані значення. 11. Спосіб за пунктом 9 або 10, де група R'' являє собою -CHFu-CH2-Sprot3, де Fu являє собою захищену функціональну групу, і Prot3 представляє тіолзахисну групу. 12. Спосіб за будь-яким з пунктів 1-11, де стадію е) здійснюють шляхом перетворення в похідні, що включає ацилювання. 13. Спосіб за будь-яким з пунктів 1-12, де 21ціаносполуку формули (XVIb) одержують введенням 21-ціаногрупи в сафраміцин А, сафраміцин В, сафраміцин С, сафраміцин G, сафраміцин Н, сафраміцин S, сафраміцин Y3, сафраміцин Yd1, сафраміцин Ad1, сафраміцин Yd2, сафраміцин АН2, сафраміцин AH2Ac, сафраміцин АН1, сафраміцин АН1Ас, сафраміцин АR3, ренієраміцин А, ренієраміцин В, ренієраміцин С, ренієраміцин D, ренієраміцин Е, ренієраміцин F, ксестоміцин, сафраміцин D, сафраміцин F, сафраміцин Мх-1, сафраміцин Мх-2, сафрацин А або сафрацин В, або являє собою сафраміцин R. 5 75333 6 14. Спосіб за пунктом 13, де 21-ціаносполука форaa, де аа являє собою ацильну групу амінокисломули (XVIb) являє собою ціаносафрацин В, сполути. ку (2): 26. Спосіб за пунктом 25, де сполука формули OMe (XVIIb) являє собою N-ацилпохідне по групі R1, коли R1 являє собою групу –СH2NН2 або –CH2NHHO Me aa. O 27. Спосіб за пунктом 26, де R1 у сполуці формули H Me (XVIIb) являє собою N-ацилпохідне, де ацильна N Me група представлена формулою -CO-Ra, де Ra явN ляє собою алкіл, алкокси, алкілен, арилалкіл, ариMeO лалкілен, амінокислотний ацил або гетероцикліл; CN O кожна з яких необов'язково заміщена галогеном, HN ціано, нітро, карбоксіалкілом, алкокси, арилом, NH2 арилокси, гетероциклілом, гетероциклілокси, алкіO сполука 2. лом, аміно або заміщеною аміногрупою; або аци15. Спосіб за будь-яким з пунктів 1-14, де R5 у спольна група являє собою аа. луці формули (XVIIb) являє собою алканоїлокси з 28. Спосіб за пунктом 25, 26 або 27, де присутні 1-5 атомами вуглецю. одна або більше груп аа, яка являє собою аланіл, 5 16. Спосіб за будь-яким з пунктів 1-15, де R у споаргініл, аспартил, аспарагіл, цистил, глутаміл, глулуці формули (XVIIb) являє собою ацетилокси. тамініл, гліцил, гістидил, гідроксипропіл, ізолейцил, 17. Спосіб за будь-яким з пунктів 1-16, де R12 явлейцил, лізил, метіоніл, фенілаланіл, проліл, селяє собою –СН3. рил, треоніл, тироніл, триптофіл, тирозил, валіл 18. Спосіб за будь-яким з пунктів 1-17, де R14a і або іншу ацильну групу амінокислоти. 14b R у сполуці формули (XVIIb) являють собою 29. Спосіб за пунктом 26 або залежними від нього водень. пунктом, де аа являє собою аланіл. 19. Спосіб за будь-яким з пунктів 1-18, де R15 у 30. Спосіб за будь-яким з пунктів 1-29, де в будьсполуці формули (XVIIb) являє собою водень. якій реакції одна або більше груп-замісників захи20. Спосіб за будь-яким з пунктів 1-19, де R18 у щена за допомогою захисної групи. сполуці формули (XVIIb) являє собою гідрокси. 31. Спосіб за пунктом 29, де аланіл захищений 21. Спосіб за будь-яким з пунктів 1-20, де R21 у бутоксикарбонільною групою. сполуці формули (XVIIb) являє собою -ОН або 32. Спосіб одержання сполуки формули (ХХІІb): CN. OCH3 7 8 22. Спосіб за будь-яким з пунктів 1-21, де R і R у 18 R CH3 сполуці формули (XVIIb) разом утворюють групу R5 R4 О-СН2-О-. H H3 C 23. Спосіб за будь-яким з пунктів 1-22, де R1 і R4 y R15 N R12 сполуці формули (XVIIb) разом утворюють групу 14a R N формули (IV), (V), (VI) або (VII): 14b R O 4 O 4 1 O CH3O O O S HN S NH NH R21 , де R1 являє собою –CH2-NH2 або –СН2ОН, або захищений або модифікований варіант такої групи, і R4 являє собою -Н; або R1 і R4 разом утворюють групу формул (IV), (V), (VI) або (VII): 1 O R1 4 HO , 4 , 4 1 1 4 O 1 O 1 O O S O O H NH2 O CH3O S O або . 24. Спосіб за будь-яким з пунктів 1-23, де R1 у сполуці формули (XVIIb) являє собою необов'язково захищену або модифіковану амінометиленову групу, необов'язково захищену або модифіковану гідроксиметиленову групу, і R4 являє собою -Н. 25. Спосіб за пунктом 24, де R1 у сполуці формули (XVIIb) являє собою групу –СН2NН2 або –CH2NH HO O S HN NH , S NH , 7 4 4 1 1 O O H O S O NH2 S O або ; R5 являє собою -ОН або захищений або модифікований варіант такої групи; R12 являє собою -Н, -СН3 або –СН2СН3; R14a i R14b обидва являють собою -Н, або один являє собою -Н, а інший являє собою -ОН, або захищений або модифікований варіант такої групи; ОСН3 або –ОСН2СН3, або R14a і R14b разом утворюють кетогрупу; R15 являє собою Н, -ОН або захищений або модифікований варіант такої групи; R18 являє собою -ОН, або захищений або модифікований варіант такої групи; і R21 являє собою -Н, -ОН або -CN; з 21-ціаносполуки формули (XVIb): OCH3 R18 R5 A E B N N H3CO R8 R1 CN HO OMe O AcO O Me OMe NH HO Me S N Me N O O CN , Et-770 HO OMe O AcO O Me OMe NH HO Me S N Me N O O CH3 H H3C 75333 8 33. Спосіб за пунктом 32, де в сполуці формули (ХХІІb) R5 являє собою -ОН, R14a і R14b являють собою Н, R15 являє собою Н і R18 являє собою ОН. 34. Спосіб за пунктом 32, де сполука формули (ХХІІb) являє собою ектеїнасцидин 743 або ектеїнасцидин 770: OH Et-743. 35. Спосіб за пунктом 34, де сполука формули (ХХІІb) являє собою ектеїнасцидин 743: OCH3 R15 R12 R14a R14b , де R1 являє собою амідометиленову групу або ацилоксиметиленову групу; R5 і R8 незалежно вибирають з -Н, -ОН або – ОСОСН2ОН, або R5 і R8 обидва є кето, і кільце А є п-бензохіноновим кільцем; R12 являє собою -Н, -СН3 або –CH2СН3; R14a і R14b обидва являють собою -Н, або один являє собою -Н, а інший являє собою -ОН, -ОСН3 або –ОСН2СН3, або R14a і R14b разом утворюють кетогрупу; і R15 і R18 незалежно вибирають з -Н або -ОН, або R15 і R18 обидва є кето, і кільце Е є пбензохіноновим кільцем; за умови, що, принаймні, одне з кілець А або Е є пбензохіноновим кільцем, який відрізняється тим, що здійснюють при необхідності такі реакції: a) хінонову систему кільця Е перетворюють у фенольну систему; b) хінонову систему кільця А перетворюють у фенольну систему; c) фенольну систему кільця А перетворюють у метилендіоксифенольне кільце; d) здійснюють утворення місточкової спірокільцевої системи формули (IV), (V), (VI) або (VII), яка проходить через 1-положення і 4-положення в кільці В; і е) здійснюють перетворення в похідні; з одержанням необхідної сполуки формули (ХХІІb). HO OCOCH3 CH3 CH3 H N CH3 N O O O S OH O CH3O NH HO . 36. Спосіб за пунктом 32, де продукт являє собою сполуку формули (XXIII): OCH3 OH R5 CH3 H H3C N R12 N O O R1 R21 , де R являє собою модифіковану амінометиленову групу формули CH2-NH-CO-Ra, де Ra має лінійний ланцюг довжиною менше ніж 20 атомів; R5 являє собою ацетильну групу; R12 являє собою –СН3 і R21 являє собою гідрокси або ціаногрупу. 37. Спосіб за пунктом 36, де Ra має лінійний ланцюг довжиною менше ніж 15 атомів. 38. Спосіб за пунктом 37, де Ra має лінійний ланцюг довжиною менше ніж 10 атомів. 39. Спосіб за пунктом 36, де сполука формули(XXIII) являє собою фталасцидин формули (III): 1 9 75333 46. Сполука формули: OCH3 HO OCOCH3 CH3 OMe CH3 R18 H N Me O CH3 Me N N O O N HO O O . 40. Спосіб за будь-яким з пунктів 1-39, що включає реакцію: OMe OMe R18 Me R18 O Me , де R1 являє собою необов'язково захищену або модифіковану амінометиленову групу; і R18 являє собою захищену ОН групу. 47. Сполука за пунктом 46, яка представлена формулою: Me Me O Me Me N N MeO O OMe Me O R , де R1 і R18 мають вказані значення. 41. Спосіб за пунктом 40, де R18 являє собою захищену ОН групу. 42. Спосіб за будь-яким з пунктів 1-41, що включає реакцію: OMe R18 O CN 1 Me O N HO CN R1 CN R1 O N Me N CN O 10 Me N HO O NH CN NHBoc OMe Me R18 O Me N O Me . OH Me N Me Me N N R1 1 OMe N HO O 48. Сполука формули: Me O CN O 18 R1 CN , де R і R мають вказані значення. 43. Спосіб за будь-яким з попередніх пунктів, що включає здійснення реакції, у якій сполуку з групою R1, що являє собою амінометилен, перетворюють у сполуку з групою R1, що являє собою гідроксиметиленову групу. 44. Сполука формули OMe R18 Me O Me N R18 Me N O O O CN R1 , де R являє собою необов'язково захищену або модифіковану амінометиленову групу; і R18 являє собою захищену ОН групу. 49. Сполука за пунктом 48, представлена формулою: 1 Me Me O CN R1 , де R1 являє собою необов'язково захищену або модифіковану амінометиленову групу; і R18 являє собою захищену ОН групу. 45. Сполука за пунктом 44, яка представлена формулою: O Me OH Me N Me N O NH OMe CN NHBoc Me O OMe O O Me Me N N MeO Me OH O . O Me N Me N MeO O NH CN NHBoc O . 11 Даний винахід відноситься до способів синтезу і, зокрема, до напівсинтетичних способів. Європейський патент 309477 має відношення до ектеїнасцидів 729, 743, 745, 759А, 759В і 770. Сполуки ряду ектеїнасцидину, як повідомляється, володіють антибактерійними і іншими корисними властивостями. Ектеїнасцидин 743 в цей час проходить клінічні випробування як протипухлинний засіб. Ектеїнасцидин 743 має складну трис(тетрагідроізохінолінфенольну) структуру, відповідну наступній формулі (І): 75333 12 синтезувати інший, представляючий інтерес протипухлинний засіб, фталасцидин, див. [Proc. Natl. Acad. Sci. USA, 96, 3496-3501, 1999]. Фталасцидин представляє біс(тетрагідроізохінолінфенольне) похідне формули (III): В ектеїнасцидині 743 1,4-містокмає структуру, представлену формулою (IV): Цю сполуку в цей час отримують виділенням з екстракту оболонок морських організмів Ecteinascidin kurbinata. Вихід низький, в зв'язку з чим намагаються знайти альтернативні способи одержання. Синтетичний спосіб одержання сполук ряду ектеїнасцидину представлений в патенті США 5721362. Описаний спосіб є тривалим і складним, причому приведено 38 прикладів, кожний з яких описує одну з послідовних стадій синтезу, необхідних для одержання ектеїнасцидину 743. Пункт 25 формули винаходу, приведеної в патенті США 5721362, відноситься до проміжної фенольної сполуки, відповідної формулі (11), яку автори даного винаходу також позначають як проміжну сполуку 11 або Int-11. Ця сполука має наступну біс(тетрагідроізохінолінфенольну) структуру (II): Інші відомі ектеїнасцидини включають сполуки з різними містковими циклічними кільцевими системами, наприклад, з такою, яка присутня в ектеїнасцидинах 722 і 736, де місток має структуру, представлену формулою (V): а також ектеїнасцидини 583 і 597, в яких місток має структуру, представлену формулою (VI): де MOM представляє метоксиметильний заступник, a TBDPS представляє 3,5-третбутилдифенілсилільний заступник. Виходячи з проміжної сполуки 11, можливо 13 75333 14 і ектеїнасцидини 594 і 596, в яких місток мас структуру, представлену формулою (VII): Повністю структура цих і родинних ним сполук приведена в [J. Am. Chem. Soc. (1996) 118, 90179023]. Ця стаття включена в даний опис за допомогою посилання. Відомі і інші сполуки, в яких відсутня місткова циклічна кільцева система. Такі сполуки включають біс (тетрагідроізохінолінхінонові) протипухлинні-протимікробні антибіотики - сафрацини і сафраміцини, і речовини з природних морепродуктів - реніераміцини і ксестоміцин, виділені з мікроорганізмів або губок, що культивуються. Всі вони володіють загальним димерним тетрагідроізохіноліновим вуглецевим каркасом. Дані сполуки можуть бути систематизовані з виділенням чотирьох типів, типи від І до IV, в залежності від виду окислення ароматичних кілець. Тип І, димерні ізохінолінхінони, представляє систему формули (VIII), що найчастіше зустрічається у сполук цього класу, див. приведену нижче таблицю І. Ароматичні системи типу І спостерігаються у сафраміцинів типу А, В і С; G і Н; і S, виділених з Streptomyces lavendulae у вигляді неосновних компонентів. Ціанопохідне сафраміцину А, яке називають ціанохінонаміном, відомо з патентів Японії Japanese Kokai JP-A.2 59/225189 і 60/084288. Сафраміцини Y3, Yd1, Ad1 і Yd2 продукує S. lavendulae шляхом прямого біосинтезу, при забезпеченні відповідного культурального середовища. Сафраміцини Y2b і димери Y2b-d, що утворюються при скріпленні азоту у С-25 одного з фрагментів з С-14 іншого фрагмента, також продукує S. lavendulae на відповідному культуральному середовищі. Сафраміцини AR1 (=AH2), продукт відновлення сафраміцину А в положенні С-25 під дією мікроорганізмів, що продукується Rhodococcus amidophilus, також отримують шляхом нестереоселективного хімічного відновлення сафраміцину А під дією боргідриду натрію у вигляді суміші епімерів 1:1, з подальшим хроматографічним розділенням [інший ізомер АН і є менш полярним]. Додатковий продукт відновлення сафраміцин AR3, 21-деціано-25дигідро-сафраміцин А, (= 25-дигідросафраміцин В) отримують тим же самим мікробним перетворенням. Інший тип мікробного перетворення сафраміцину А, з використанням виду Nocardia, приводить до продукування сафраміцину В, а подальше відновлення з використанням виду Mucobacterium приводить до продукування сафраміцину AH1Ac. Для біологічних досліджень 25-О-ацетати сафраміцину АН2 і АН1 також отримують хімічним шляхом. Сполуки типу І формули (X) також були виділені з морських губок, див. таблицю II 15 Реніераміцини А-D виділяли з протимікробного екстракту губок виду Reniera, зібраних в Мехіко, нарівні з родинним за біологічним походженням реніероном мономерних ізохінолінів і родинними йому сполуками. Структуру реніераміцину А спочатку зв'язували з інверсною стереохімією в атомів С-3, С-11 і С-13. Однак ретельне вивчення даних 1 Н ЯМР, отриманих для нових, родинних сполук реніераміцинів Ε і F, виділених з тих. же самих губок, зібраних на островах Палау (Тихий океан), показало, що кільцева сполука реніераміцинів ідентична тій, яка властива сафраміцинам. Ці результати дозволили зробити висновок про те, що стереохімія, яку раніше відносили до стереохімії реніераміцинів, від А до D, повинна бути тією ж самою, що і стереохімія сафраміцинів. Ксестоміцин був виявлений в губках виду Xestospongia, зібраних в акваторій Шрі-Ланка. Сполуки типу II формули (XI) з відновленим гідрохіноновим кільцем включають сафраміцини D і F, виділені з S. lavendulae, і сафраміцини Мх-1 і Мх-2, виділені з Myxococcus xanthus. Див. таблицю III. Структура скелету типу III виявлена у антибіотиків сафрацинів А і В, виділених з культури Pseudomonas fluorescens. Ці антибіотики формули (XII) складаються з тетрагідроізохінолінхінонової субодиниці і тетрагідроізохінолінфенольної субодиниці: 75333 16 де R21 представляє Η у випадку сафрацину А і ОН у випадку сафрацину В. Сафраміцин R, єдина сполука, класифікована як сполука, що володіє скелетом типу IV, також була виділена з S. lavendulae. Ця сполука формули (XIII), що складається з гідрохінонового кільця зі складним гліколевим ефіром в бічному ланцюгу у одного з фенольних киснів, представляє, ймовірно, проліки сафраміцину А внаслідок її помірної токсичності. Всі ці сполукимають конденсовану систему з п'яти кілець від (А) до (Е), як показано в наступній структурній формулі (XIV): Дані кільця від (А) до (Е) мають фенольну природу у випадку ектеїнасцидинів і деяких інших сполук, в той час як в інших сполуках, особливо, в сафраміцинах, кільця А і Ε є хіноліновими. У відомих сполуках кільця В і D мають структуру тетрагідро, в той час як кільце С представляє структуру пергідро. Є необхідність в нових активних сполуках, що містять конденсовану систему з п'яти кілець, властиву відомим сполукам, і в альтернативних способах синтезу сполук ряду ектеїнасцидину і родинних ним сполуках. Такі синтетичні підходи могли б забезпечити більш економні шляхи одержання відомих протипухлинних засобів, а також зробити можливим одержання нових активних сполук. 17 75333 18 Один з аспектів даного винаходу відноситься де групи-заступники, що визначаються як R1, до застосування відомої сполуки, сафрацину А, R2, R3, R4, R5, R6, R7, R8, R9, R10 кожну, незалежно, також, який називають хінонаміном, в напівсинтевибирають з ряду, що складається з Н, ОН, ОСН3, тичному способі синтезу. CN, =О, СН3; У більш широкому значенні, даний винахід віде X представляє різні амідні або складноефідноситься до напівсинтетичного способу одержанрні функціональні групи, що містяться у вказаних ня проміжних сполук, похідних і структур, родинних вище продуктах природного походження; ектеїнасцидину або іншим тетрагідроізохінолінфеде кожна з пунктирних кільцевих ліній преднольним сполукам, виходячи з природних ставляє одну, дві або три необов'язково присутні біс(тетра-гідроізохінолінових) алкалоїдів. Відповідподвійні зв'язки. ні початкові речовини для використання в напівсиТаким чином, згідно з даним винаходом, заявнтетичному способі включають сполуки класу саником пропонуються напівсинтетичні способи одефраміцинових і сафрацинових антибіотиків, які ржання проміжних сполук, включаючи проміжну доступні з різних культур, що вирощуються на різсполуку 11, і відповідно, способи одержання споних рідких середовищах, а також сполуки класу лук ряду ектеїнасцидину, а також фталасцидину і реінерамиіцина і класу ксестоміцину, які можуть додаткових сполук. Кожний з напівсинтетичних бути виділені з морських губок. способів, що є предметом даного винаходу, вклюЗагальна структурна формула (XV) початкових чає ряд стадій перетворень, потрібних для того, сполук є наступною: щоб одержати необхідний продукт. Кожна з стадій сама по собі представляє спосіб згідно з даним винаходом. Об'єм винаходу не обмежується способами, які проілюстровані прикладами, і можуть бути здійснені альтернативні варіанти, наприклад, при зміні відповідним образом порядку стадій перетворень. Зокрема, даний винахід включає одержання початкової 21-ціаносполуки загальної формули (XVI): де: R1 представляє амідометиленову групу таку, 25a 25b 25c 25a 25b як - CH2-NH-CO-CR R R , де R і R утворюють кетогрупу або один представляє -ОН, -NH2 або -ОСОСН3, а інший представляє -СН2СОСН3, Н, -ОН або -ОСОСН3, при умові, що в тому випадку, коли R25a представляє -ОН або -NH=, тоді R25b не є -ОН і R25c представляє -Н, -СН3 або -СН2СН3, або R1 представляє ацилоксиметиленову групу, таку як -CH2-O-CO-R, де R представляє С(СН3)=СН-СН3 або -СН3; R5 і R8 незалежно вибирають з -Н, -ОН або ОСОСН2ОН, або R5 і R8 обидва є кето, і кільце А є п-бензохіноновим кільцем; R14a і R14b обидва представляють -Н або один представляє -Н, а інший представляє -ОН, -ОСН3 або -ОСН2СН3, або R14ai R14b разом утворюють кетогрупу; R15 і R18 незалежно вибирають з -Н і -ОН, або 5 R і R8 обидва є кето і кільце А є п-бензохіноновим кільцем; і R21 представляє -ОН або -CN. Більш загальна формула для сполук цього класу приведена нижче: в якій R1, R5, R8, R14a3 R151 R18 є такими, як визначено вище. Інші сполуки формули (XVI) з різними заступниками в 21-положенні можуть також представляти можливі початкові речовини. Загалом, будь-яке похідне, яке може бути отримане при нуклеофільному заміщенні 21-гідроксигрупи сполуки формули (XV), в якій R21 представляє гідроксигрупу, є потенційним варіантом. Приклади відповідних 21заступників включають, але не обмежуються ними, такі групи як: меркаптогрупа; алкілтіогрупа (алкільна група, що містить від 1 до 6 атомів вуглецю); арилтіогрупа (арильна група, що містить від 6 до 10 атомів вуглецю, яка є незаміщеною або заміщеною від 1 до 5 заступниками, вибраними, наприклад, з алкільної групи, що містить від 1 до 6 атомів вуглецю, алкоксигрупи, що містить від 1 до 6 атомів вуглецю., атомів галогену, меркаптогрупи або нітрогрупи); аміногрупа; моно- або діалкіламіногрупа (одна або кожна алкільна група містить від 1 до 6 атомів вуглецю); моно- або діариламіногрупа (одна або кожна арильна група є такою, як визначена вище для арилтіогруп); -карбонілалкільна група формули -С(Ra)(Rb) 19 75333 20 С(=О)Rc, де Ra і Rb вибирають з атомів водню, алраміцин F, сафраміцин Мх-1, сафраміцин Мх-2, кільних груп, що містять від 1 до 20 атомів вуглесафрацин А, сафрацин В і сафраміцин R. Перевацю, арильних груп (таких, як визначено вище для жна початкова речовина містить ціаногрупу в 21арилтіогруп) і аралкільних груп (в яких алкільна положенні, як група R21. група, що містить від 1 до 4 атомів вуглецю, є заУ своєму найбільш переважному аспекті даний міщеною арильною групою, такою як визначено винахід включає напівсинтетичний спосіб, згідно з вище для арилтіогрупХ при умові, що один з радияким стадії перетворення застосовуються до сафкалів Ra і Rb представляє атом водню; рацину В: Rc вибирають з атома водню, агткільної групи, що містить від 1 до 20 атомів вуглецю, арильних груп (таких, як визначено вище для арилтіогруп), аралкільної групи (в якої алкільна група, що містить від 1 до 4 атомів вуглецю, є заміщеною арильною групою, такою як визначено вище для арилтіогруп), алкоксигрупи, що містить від 1 до 6 атомів вуглецю, аміногрупи або моно- або діалкіламіногрупи, як визначено вище. Таким чином, в своєму більш загальному аспекті, даний винахід відноситься до способів, в яких перша стадія представляє одержання 21похідного з використанням нуклеофільиого реагенту. Такі сполуки даного винаходу позначені як 21Nuc сполуки. Сафрацин В Наявність 21-ціаногрупи потрібна для деяких Сафрацин В представляє кільцеву систему, кінцевих продуктів, особливо, ектеїнасцидину 770 і близьку структурі ектеїнасцидинів. Дана сполука фталасцидину, в той час як у випадку інших кінцемає ту ж саму структуру зп'яти циклів і той же хавих продуктів дана група служить як захисна грурактер заміщення в правому ароматичному кільці, па, яка легко може бути перетворена в інші застукільці Е. Крім того, сафрацин В по своїй структурі пники, наприклад, такі як 21-гідроксигрупа дуже близький одній з синтетичних проміжних ектеїнасцидину 743 або 21-гідроксифталасцидину. сполук, що утворюються а повному синтезі ЕТ-743, Вибір 21-ціаносполуки як початкової речовини зокрема, до проміжної сполуки 11. Така проміжна приводить до ефективної стабілізації молекули сполука може бути трансформована в Et-743 з при здійсненні подальших стадій синтезу, доти, використанням добре відпрацьованих методик. поки дана група, необов'язково, не видалена. Інші Таким чином, синтетичне перетворення сафраци21-Nuc сполуки можуть володіти цією і іншими ну В в проміжну сполуку 11 надасть можливість перевагами. здійснити напівсинтетичний спосіб, для того щоб В одному з своїх важливих аспектів даний виодержати ЕТ-743. нахід полягає в застосуванні 21-ціаносполук загаТаким чином, даний винахід надає проміжну льної формули (XVI) для одержання біс- і сполуку 11, отриману з даної сполуки сафрацину трис(тетрагідроізохінолінфенольних) сполук. ПроВ, і сполуки, що є похідними проміжної сполуки 11, дукти, які можуть бути отримані, включають проміособливо, похідних ектеїнасцидину. Додатково жні сполуки, наприклад, такі як проміжна сполука даний винахід пропонує фталасцидин, отриманий 11, ектеїнасцидини і фталасцидин, а також інші з сафрацину В. Винахід також відноситься до занові і відомі сполуки родинної структури. стосування сафрацину В для одержання проміжної Переважні початкові речовини включають такі сполуки 11, фталасцидину, похідних ектеїнасцисполуки формули (XV) або формули (XVI), в яких дину і інших проміжних сполук даного винаходу. обидва R14a і R14 представляють водень. ПереваВинахід також відноситься до сполук, що описужні початкові речовини також включають сполуки ються, які є похідними інших передбачуваних по15 формули (XV) або (XVI), в яких R представляє чаткових речовин, і застосуванню вказаних сполук водень. Крім того, переважні початкові речовини для одержання таких сполук. включають такі сполуки формули (XV) або (XVI), в Найбільш переважна початкова речовина даяких кільце Ε представляє фенольне кільце. Пеного винаходу містить 21-ціаногрупу. У цей час реважні початкові речовини, крім того, включають найбільш переважна сполука, що є предметом такі сполуки формули (XV) або (XVI), в яких, щоданого винаходу, представляє сполуку формули 2. найменше, один, переважно, щонайменше, два Дану сполуку отримують безпосередньо з сафраабо три з R5, R8, R15 і R18 не є воднем. цину В і її розглядають як ключовупроміжну сполуПриклади відповідних початкових речовин для ку при здійсненні напівсинтетичного способу. використання згідно з даним винаходом включають сафраміцин А, сафраміцин В, сафраміцин С, сафраміцин G, сафраміцин Н, сафраміцин S, сафраміцин Y3, сафраміцин Yd1, сафраміцин Ad1, сафраміцин Yd2, сафраміцин АН2, сафраміцин АН2Ас, сафраміцин АН1, сафраміцин АН1Ас, сафраміцин AR3, реніераміцин А, реніераміцин В, реніераміцин С, реніераміцин D, реніераміцин Е, реніераміцин F, ксестоміцин, сафраміцин D, саф 21 Відносно аспекту даного винаходу ціаносафрацин В одержували ферментацією продукуючого сафрацин В штаму Pseudomonas fluorescens і обробкою культуральних рідких середовищ з використанням ціанід-іону. Переважний штам Pseudomonas fluorescens представляє штам А2-2, FERM ВР-14, який використовується відповідно до методики, описаної з ЕР 055299. Відповідне джерело ціанід-іону представляє ціанід калію. При типовій обробці поживне середовище відфільтровують і додають надлишок ціанід-іону. Після відповідного інтервалу перемішування, наприклад, такого як 1 година, значення рН доводять до лужного, наприклад, рН 9,5, і екстракція органічною речовиною дає неочищений екстракт, який далі може бути очищений для одержання ціаносафрацину В. Для усунення сумнівів стереохімія, представлена в даному описі, засновується на розумінні відповідної стереохімії продуктів природного походження. У тій мірі, в якій помилка виявляється у вказаній стереохімії, ця помилка потребує відповідного коректування в формулі, приведеній в даному описі. Крім того, в тій мірі, в якій синтез може бути підданий модифікації, даний винахід розповсюджується на стереоізомери. Продукти, що є предметом даного винаходу, звичайно представлені формулою (XVIIa): або формулою (XVIIb): 75333 22 де R1 представляє необов'язково захищену або модифіковану амінометиленову групу, необов'язково захищену або модифіковану гідроксиметиленову групу, наприклад, таку як група R1, як визначено для формули (XV); R представляє -Н; або R1 і R4 разом утворюють групу формули (IV), (V), (VI) або (VII): R5 представляє -Н або -ОН; R7 представляє -ОСН3 і R8 представляє -ОН, або R7 і R8 разом утворюють групу -О-СН2-О-; R14a і R14b обидва представляють -Η або один представляє -Η, а інший представляє -ОН, -ОСН3 або -ОСН2СН3, або R14a і R14b разом утворюють кетогрупу; і R15 представляє -Н або -ОН; R21 представляє -Н, -ОН або CN; і їх похідні, включаючи ацилпохідні, зокрема, такі похідні, в яких R5 представляє ацетокси або іншу ацилоксигрупу, що містить до 4 атомів вуглецю, а також включаючи похідні, в яких група NCH3- в 12-положенні замінена групами -NH- або NCH3CH3-, і похідні, в яких група-NH2 в сполуці формули (VI) необов'язково модифікована. У формулі (XVIIa) або (XVIIb) R1 звичайно представляє амінометилен, амідометилен, або R1 і R4 разом утворюють групу (IV) або (V). Відповідні амідометиленові групи включають такі групи формули -CH2-NH-CO-CHCH3-NH2, які є похідними аланіну, і схожі групи, які є похідними інших амінокислот, особливо, таких як D, так і L, гліцину, валіну, лейцину, ізолейцину, фенілаланіну, тирозину, триптофану, метіоніну, цистеїну, аспартату, аспарагіну, глутамінової кислоти, глутаміну, лізіну, ар 23 75333 24 гініну, проліну, серину, треоніну, гістидину і гідрокпроміжних продуктів, кільце А модифіковано для сипроліну. Загальна формула групи R1 представтого, щоб включити субструктуру, яка показана ляє, в такому випадку, -CH2-NH-aa, де аа означає формулами (XX) або (XXI), що обговорюється ниацильну групу амінокислоти. жче. Група R може бути ацильованою по NH2-групі, В іншому з варіантів, який відноситься до про1 і, наприклад, N-ацилпохідні можуть бути утворені з міжних сполук, група R може представляти струкгруп -CH2-NH2 і -СН2-NН-аа. Ацилпохідні можуть туру -CH2O-CO-CFu-CH2-S-Prot3, що є похідною від являти собою їх N-ацил або N-тіоацилпохідні, тасполуки формули (XIX), в якій Prot3 і Fu мають вкакож як і циклічні аміди. Ацильні групи, для ілюстзані значення. У такому випадку R7 і R8 утворюють рації, можуть являти собою алканоїл, галоалканооксиметиленоксигрупу. Група R18 звичайно захиїл, арилалканоїл, алкеноїл, гетероциклілацил, щена. Звичайно R21 представляє ціано. ароїл, арилароїл, галоароїл, нітроароїл або інші Переважно, R14a і R14b представляють водень. ацильні групи. Ацильні групи можуть являти собою Переважно, R15 представляє водень. Відповідні Огрупи формули -CO-Ra, де Ra може бути різною ацильні похідні представляють аліфатичні Оацигрупою, наприклад такою, як алкіл, алкокси, алкільні похідні, особливо, ацильні похідні, в яких Олен, арилалкіл, арилалкілен, амінокислотний ацил ацильний фрагмент містить від 1 до 4 атомів вугабо гетероцикліл, кожна з яких може бути необолецю, і звичайно, представляє О-ацетильну групу, в'язково заміщена галогеном, ціано, нітро, карбокособливо, в 5-положенні. сіалкілом, алкокси, арилом, арилокси, гетероцикВідповідні захисні групи для фенольних і гідлілом, гетероциклілокси, алкілом, аміно або роксигруп включають прості і складні ефірні групи, заміщеною аміногрупою. Інші ацилуючі засоби наприклад, такі як алкіл, алкоксіалкіл, арилоксіалвключають ізотіоціанати, такі як арилізотіоціанати, кіл, алкоксіалоксіалкіл, алкілсилілалкоксіалкіл, особливо, фенілізоціанат. Відповідні алкіл, алкокалкілтіоалкіл, арилтіоалкіл, азидоалкіл, ціаноалкіл, си або алкіленові групи радикалу Ra містять від 1 хлоралкіл, гетероциклічні групи, арилацил, галоадо 6 атомів вуглецю, і можуть бути прямими, розрилацил, циклоалкілалкіл, алкеніл, циклоалкіл, галуженими або циклічними. Арильні групи звиалкілариралкіл, алкоксіарилалкіл, нітроарилалкіл, чайно представляють феніл, біфеніл або нафтил. галоарилалкіл, алкіламінокарбоніларилалкіл, алкіГетероциклічні групи можуть бути ароматичними лсульфініларилалкіл, алкілсиліл і інші прості ефірабо частково або повністю ненасиченими і відпоні групи, а також арилацил, арилалкілкарбонатні, відним образом містять в кільці від 4 до 8 атомів, аліфатичні карбонатні, алкілсульфініларилалкільні більш переважно, 5 або 6 атомів, з одним або бікарбонатні групи, алкілкарбонатні, арилгалоалкілльше гетероатомів, вибраних з групи, що включає карбонатні, арилалкенілкарбонатні, арилкарбамаазот, сірку і кисень. тні, алкілфосфінільні, алкілфосфінотіоїльні, арилПерелік типових груп Ra, який не є вичерпним, фосфінотіоїльні, арилалкілсульфонатні і інші включає алкіл, галоалкіл, алкоксіалкіл, галоалкокскладноефірні групи. Такі групи можуть бути несіалкіл, арилалкілен, галоалкіларилалкілен, ацил, обов'язково заміщені групами, вказаними вище галоацил, арилалкіл, алкеніл і залишок амінокиспри описі R1. a лоти. Наприклад, R -CO- може являти собою ацеВідповідні захисні групи для аміногруп вклютил, трифторацетил, 2,2,2-трихлоретоксикарбоніл, чають карбаматні, амідні і інші захисні групи, наізовалерилкарбоніл, транс-3-(трифторметил)приклад, такі як алкіл, арилалкіл, сульфо- або гацинамоїлкарбонил, гептафторбутирилкарбоніл, лоарилалкіл, галоалкіл, алкілсилілалкіл, деканоїлкарбоніл, транс-цинамоїлкарбоніл, бутиарилалкіл, циклоалкілалкіл, алкіларилалкіл, гетерилкарбоніл, 3-хлорпропіоніл-карбоніл, цинамоїлроциклілалкіл, нітроарилалкіл, ациламіноалкіл, карбоніл, 4-метилцииамоїлкарбоніл, гідроцинамоїнітроарилдитіоарилалкіл, дициклоалкілкарбоксалкарбоніл або транс-гексеноїлкарбоніл, або мідоалкіл, циклоалкіл, алкеніл, арилалкеніл, нітроаланіл, аргиніл, аспартил, аспарагіл, цистил, глуарилалкеніл, гетероциклілалкеніл, гетероцикліл, таміл, глутамініл, гліцил, гістиділ, гідроксипропіл, гідроксигетероцикліл, алкілдитіо, алкокси- або гаізолейцил, лейцил, лізіл, метіоніл, фенілаланіл, ло- або алкілсульфініларилалкіл, гетероциклілапроліл, серил, треоніл, тироніл, триптофіл, тироцил і інші карбаматні групи, і алканоїл, галоалканозил, валіл, а також інші ацильні групи менш пошиїл, арилалканоїл, алкеноїл, гетероциклілацил, рених амінокислот, також як фталімідо і інші цикліароїл, арилароїл, галоароїл, нітроароїл і інші амідчні аміди. Інші приклади можуть бути знайдені в ні групи, також як і алкіл, алкеніл, алкілсилілалкопереліку захисних груп. косіалкіл, алкоксіалкіл, ціаноалкіл, гетероцикліл, Сполуки, в яких -CO-Ra є похідним амінокисалкоксіарилалкіл, циклоалкіл, нітроарил, арилаллоти і включають аміногрупу, можуть самі утворюкіл, алкокси- або гідрокси-арилалкіл, і багато які вати ацилпохідні. Відповідні N-ацилсполуки вклюінші групи. Такі групи; може бути необов'язково чають дипептиди, які, в свою чергу, можуть заміщені групами, вказаними вище при описі R1. утворювати N-ацилпохідні. Приклади таких захисних груп приведені в наВ одному з варіантів, який відноситься до ступних таблицях. 25 75333 26 Захист для ОН-груп Прості ефіри метил метоксиметил бензилоксиметил метоксіетоксиметил 2-(триметилсиліл)етоксиметил метилтіометил фенілтіометил азидометил ціанометил 2,2-дихлор-1,1-дифтороетил 2-хлоретил 2-брометил тетрагідропіранил 1-етоксіетил фенацил 4-бромфенацил циклопропілметил аліл пропаргіл ізопропіл циклогексил трет-бутил бензил 2,6-диметилбензил 4-метоксибензил о-нітробензил 2,6-дихлорбензил 3,4-дихлорбензил 4-(диметиламіно)карбонілбензил 4-метилсульфінілбензил 9-антрилметил 4-піколіл гептафтор-п-толіл тетрафтор-4-піридил триметилсиліл трет-бутилдиметилсиліл трет-бутилдифенілсиліл триізопропілсиліл Складніефіри арилформіат арилацетат арилевулінат арилпівалоат арилбензоат арил-9-фторокарбоксилат арилметилкарбонат 1-адамантилкарбонат трет-бутилкарбонат 4-метилсульфінілбензилкарбонат 2,4-диметилпент-3-ілкарбонат арил 2,2,2-трихлороетилкарбонат арилвінілкарбонат арилбензилкарбонат арилкарбамат диметилфосфініл диметилфосфінотіоліл дифенілфосфінотіоліл арилметансульфонат арилтолуолсульфонат Арил 2-формілбензолсульфонат Карбамати Метил Скорочення MOM BOM MEM SEM MTM PTM ΤΗΡ ЕЕ МРМ або РМВ Msib TMS TBDMS TBDPS TIPS ArOPv BOC-OAr Msz-OAr Doc-OAr Dmp-OAr Mpt-OAr Dpt-OAr Захист для NH2-груп Скорочення 27 75333 Етил 9-флуоренілметил 9-(2-сульфо)флуоренілметил 9-(2,7-дибромб)флуоренілметил 17-тетрабензо[а,с,g,-l]флуоренілметил 2-хлор-3-інденілметил бенз[f]інден-3-ілметил 2,7-ди-трет-бутил[9-(10,10-діоксо-10,10,10,10-тетрагідротіоксантил)]метил 2,2,2-трихлороетил 2-триметилсилілетил 2-фенілетил 1-(1-адамантил)-1-метилетил 2-хлоретил 1,1-диметил-2-хлоретил 1,1-диметил-2-брометил 1,1-диметил-2,2-дибромоетил 1,1-диметил-2,2,2-трихлоретил 1-метил-1-(4-біфеніл)етил 1-(3,5-ди-трет-бутилфеніл)-1-1-метилетил 2-(2'- і 4'-піридил)етил 2,2-біс(4'-нітрофеніл)етил М-(2-півалоїламіно)-1,1-диметилетил 2-[(2-нітрофеніл)дитіо]-1-фенілетил 2-(Ν,Ν-діциклогексилкарбоксамідо)етил трет-бутил 1-адамантил 2-адамантил вініл аліл 1-ізопропілаліл цинаміл 4-нітроцинаміл 3-(3'-піридил)проп-2-еніл 8-хіноліл N-гідроксипіперидиніл алкілдитіо бензил п-метоксибензил п-нітробензил п-бромбензил п-хлорбензил 2,4-дихлорбензил 4-метилсульфінілбензил 9-антрилметил дифенілметил фенотіазиніл-(10)-карбоніл N'-п-толуолсульфоніламінокарбоніл N'-феніламінотіокарбоніл Аміди формамід ацетамід хлорацетамід трифторацетамід фенілацетамід 3-фенілпропанамід пент-4-енамід піколінамід 3-піридилкарбоксамід бензамід п-фенілбензамід N-фталімід N-тетрахлорофталімід 4-нітро-N-фталімід N-дитіасукцинімід N-2,3-дифенілмалеїнід N-2,5-диметилпірол 28 Fmoc Tbfrnoc Climoc Bimoc DBD-Tmoc Troc Teoc hZ Adpoc DB-t-BOC TCBOC Врос t-Burmeoc Pyoc Bnpeoc NpSSPeoc BOC 1-Adoc 2-Adoc Voc Aloc або Alloc Іраос Соc Noc Paloc Cbz або Ζ Moz PNZ Msz TFA TCP Dts 29 75333 N-2,5-біс(триізопропілсилоксил)пірол адукт N-1,1,4,4-тетраметилдисиліазациклопентану 1,1,3,3-тетраметил-1,3-дисилаізоіндолін Спеціальні NH-захиснігрупи N-метиламін N-трет-бутиламін N-аліламін N-[2-(триметилсиліл)етокси]метиламін N-3-ацетоксипропіламін N-ціанометиламін N-(1-ізопропіл-4-нітро-2-оксо-3-піролін-3-іл)амін N-2,4-диметоксибензиламін 2-азаноборнен N-2,4-динітрофеніламін N-бензиламін N-4-метоксибензиламін N-2,4-диметоксибензиламін N-2-гідроксибензиламін N-(дифенілметил)аміно N-біс(4-метоксифеніл)метиламін N-5-дибензосубериламін N-трифенілметиламін Тr N-(4-метоксифеніл)[дифенілметил]аміно N-9-фенілфлурениламін N-фероценілметиламін N'-оксидN-2-піколіламіну N-1,1-диметилтіометиленамін N-бензиліденамід N-п-метоксибензиліденамін N-дифеіллметиленамін N-(5,5-диметил-3-оксо-1-циклогексеніл)амін N-нітроамін N-нітрозоамін дифенілфосфінамід диметилтіофосфінамід дифенілтіофосфінамід дибензилфосфорамідат 2-нітробензолсульфенамід N-1-(2,2,2-трифторо-1,1-дифеніл)етилсульфенамід 3-нітро-2-піридинсульфенамід п-толуолсульфонамід бензолсульфонамід 30 BIPSOP STABASE BSB SEM Dmb Bn MPM DMPM Hbn DPM DBS MMTr Pf Fcm Fcm Dpp Mpt Ppt Nps TDE Npys Ts Сафрацин В містить бічний аланільний ланцюг. В одному з варіантів здійснення даного винаходу було виявлено, що захист вільної аміногрупи з використанням Вос-групи може дати більші переваги. Деякі продукти ряду ектеїнасцидину, що є предметом даного винаходу, включають сполуки формули (XVIII): де R1 і R4 разом утворюють групу формули (IV), (V), (VI) або (VII): більш переважно, групу формули (IV) або (V); R21 представляє -Н, -ОН або -CN, більді переважно, -ОН або -CN; і їх ацилпохідні, більш переважно, 5ацилпохідні, що включають 5-ацетилпохідне. Утворення ектеїнасцидину 743 і родинних йому сполук Загалом, перетворення початкової 21ціаносполуки в продукт - ектеїнасцидин, представлене, наприклад, формулою (XVIII), включає: a) перетворення, якщо необхідно, хінонової системи кільця Ε в фенольну систему; b) перетворення, якщо необхідно, хінонової 31 75333 32 системи кільця А в фенольну систему; c) перетворення фенольної системи кільця А в метилендіоксифенольне кільце; d) утворення місткової спірокільцевої системи формули (IV), (VI) або (VII), що проходить через 1положення і 4-положення в кільці В; e) проведення відповідної модифікації, наприклад, ацилювання. Стадія (а), перетворення, якщо це необхідне, хінонової системи кільця Ε в фенольну систему, або, більш переважно, фрагмента формули може бути здійснена з використанням звичайних (XXI): методик відновлення. Відповідна система реагентів представляє водень з каталізатором паладійвуглець, хоча можуть бути використані і інші відновлюючі системи. Стадія (b), перетворення, якщо це необхідно, хінонової системи кільця А в фенольну систему, аналогічна стадії (а), і немає необхідності в додаткових деталях. Стадія (с), перетворення фенольної системи кільця А в метилендіоксифенольне кільце, може бути здійснена декількома шляхами, можливо, разом з стадією (b). Наприклад, хінонове кільце А в якій групу R" вибирають длянеобхідної групи може бути деметильоване біля метоксизаступника формули (IV), (V), (VI) або (VII). Для пертих двох в 7-положенні і відновлено до дигідрохінону і статаких груп група R" звичайно має структуру -CHFuбілізовано за допомогою відповідного електрофіCH2-SProt3. Потім захисні групи можуть бути видального реагенту, наприклад, такого як СН3Вr2, лені, і може бути здійснена необхідна модифікація ВrСН3СІ або подібного біфункціонального реагендля одержанні бажаної сполуки. ту, безпосередньо з утворенням метилендіоксиТипова методика для здійснення стадії (d) кільцевої системи, або з біфункціональним реагеприведена в патенті США 5721362, включеному в нтом, таким як тіокарбонілдіімідазол, який дозводаний опис за допомогою посилання. Особливу ляє одержати заміщену метилендіокси-кільцеву увагу потрібно звернути на колонку 8, стадія (1), і систему, яка може бути перетворена в необхідне приклад 33, приведені у вказаному патенті, і відкільце. повідні частини опису. Стадію (d) звичайно здійснюють за допомогою Одержання похідних на стадії (е) може вклювідповідного заміщення в 1-положенні з викорисчати ацилювання, наприклад, для групи Ra-CO-, а танням містка реагенту, що бере участь в утвотакож перетворення 12-NCH3 групи в 12-NH або іренні, який може сприяти утворенню потрібного NCH2CH3. Таке перетворення може бути здійснене містка, утворюючи екс-ендо хінонметид в 4до або після проведення інших стадій, з викорисположенні з подальшою взаємодією метиду із 1танням доступних методик. заступником з утворенням місткової структури. Як ілюстрація в цей час цілком можливо переРеагенти, що переважно беруть участь в утворенні творити сполуку ціаносафрацин В формули 2 в містка, мають структуру, представлену формулою ЕТ-743, що дає більш короткий і більш прямий (XIX) шлях одержання ЕТ-743, чим описані вище способи. Ціаносафрацин В може бути перетворений в проміжну сполуку 25; в якій Fu означає захищену функціональну групу, таку як група -NHProt4a або OProt4b, Prot3 представляє захисну групу, а пунктирна лінія показує необов'язково присутній подвійний зв'язок. Відповідні метиди утворяться введенням спочатку пдроксигрупи в 10-положення в місці з'єднання кілець А і В з утворенням фрагмента формули (XX): а в це похідне можливо ввести ряд цистеїнових похідних, які далі можуть бути перетворені в Et-743. Переважні цистеїнові похідні представлені наступними двома сполуками: 33 75333 34 схему II): утворення захищеної сполуки формули 14 взаємодією сполуки 2 з трет-бутоксикарбонілангідридом; перетворення сполуки 14 в дизахищену сполуку формули 15 взаємодією з простим бромметилметиловим ефіром і діізопропілетиламіном в ацетонітрилі; селективне видалення метоксигрупи, що знаходиться в хіноновій системі сполуки 15 для того, Ретросинтетичний аналіз одержання ЕТ-743 з щоб одержати сполуку формули 16 шляхом взаєвикористанням сполуки 29 приведений на схемі І. модії з метанольним розчином гідроксиду натрію; перетворення сполуки 16 в метилендіоксисполуку формули 18, використовуючи наступну переважну послідовність реакцій: (1) хінонову групу сполуки 16 відновлюють, використовуючи 10% Pd/C в атмосфері водню; (2) гідрохінонову проміжну сполуку перетворюють в метилендіоксисполуку формули 17 взаємодією з бромхлорметаном і карбонатом цезію в атмосфері водню; (3) сполуку 17 перетворюють в сполуку формули 18 за допомогою захисту вільної гідроксильної групи, у вигляді групи OCH2R. Цю реакцію проводять, використовуючи ВrСН2R і карбонат цезію, де R може представляти арил, СН=СН2, OR' і т.д.; видалення трет-бутоксикарбонільної і метилоксиметильної захисних груп сполуки 18 для того, щоб одержати сполуку формули 19 взаємодією з розчином НСI в діоксані. Дана реакція також протіСлідуючи приведеній вище схемі І, можливо кає при змішуванні сполуки 18 з розчином трифтоодержати ЕТ-743 за 21 послідовну стадію. Цей роцтової кислоти в дихлорметані; метод включає перетворення ціаносафрацину В в утворення тіосечовини формули 20 взаємодіпроміжну сполуку 25 шляхом здійснення послідовєю сполуки 19 з фенілізотіоціанатом; ності реакцій, які включають, по суті: (1) видалення перетворення сполуки формули 20 в амін фометоксигрупи, що знаходиться в кільці А, (2) віднормули 21 взаємодією з розчином хлористого водвлення кільця А і утворення метилендіоксигрупи за ню в діоксані; одну операцію, (3) гідроліз амідної функціональної перетворення сполуки формули 21 в N-Trocгрупи, розташованої біля вуглецю 1, (4) перетвопохідне 22 взаємодією з трихлоретилхлорформіарення отриманої аміногрупи в гідроксильну групу. том і піридином; Крім того, при здійсненні способу виключено ввеутворення захищеної гідроксисполуки формудення і зняття захисту первинної спиртової функли 23 взаємодією сполуки 22 з простим бромметиціональної групи в положенні 1 кільця В сполуки 25 лметиловим ефіром і діізопропілетиламіном; при використанні безпосередньо цистеїнового заперетворення сполуки формули 23 в N-H похілишку 29 для одержання проміжної сполуки 27. дне 24 взаємодією з оцтовою кислотою і цинком; Аміногрупу похідного цистеїну 29 захищають за перетворення сполуки формули 24 в гідроксидопомогою , , -трихлоретоксикарбонільної захисполуку формули 25 взаємодією з нітритом натрію сної групи, для того щоб досягнути сумісності з в оцтовій кислоті. Як альтернатива, може бути алільною і MOM групами, що є. Проміжну сполуку використаний тетраоксид азоту в суміші з оцтовою 27 безпосередньо окисляють і циклізують. Ці обкислотою і ацетонітрилом, з подальшою обробкою ставини, нарівні з різною стратегією введення і гідроксидом натрію. Також може бути використазняття захисту на пізніх стадіях синтезу, дозволяний нітрит натрію в суміші оцтовий ангідрид - оцють вважати спосіб новим і більш придатним для това кислота, з подальшою обробкою гідроксидом промислового застосування, чим спосіб, описаний натрію. в патенті США 5721362. Перетворення 2-ціаносполуки в проміжну сполуку 25 звичайно включає наступні стадії (див. 35 Схема II Перетворення проміжної сполуки 25 в ЕТ-743 з використанням похідного цистеїну 29 звичайно включає наступні стадії (див. схему III): перетворення сполуки формули 24 в похідне 30 шляхом введення захисту первинної гідроксильної функціональної групи з використанням (S)-N2,2,2-трихлоретоксикарбоніл-S-(9Н-флуорен-9ілметил)цистеїну 29; перетворення захищеної сполуки формули 30 в фенольне похідне 31 шляхом відщеплення алільної групи з використанням гідриду трибутилолова і дихлорпаладій-біс(трифенілфосфіну); перетворення фенольної сполуки формули 31 в сполуку формули 32 окисленням ангідридом бензолселенової кислоти при низькій температурі; перетворення гідроксисполуки формули 32 в лактон 33 внаслідок наступної послідовності реакцій: (1) взаємодія сполуки формули 32 з 2екв. ангі 75333 36 дриду трифторметилсірчаної кислоти і 5екв. ДМСО (DMSO), (2) подальша взаємодія з 8екв. діізопропілетиламіну, (3) подальша взаємодія з 4екв. трет-бутилового спирту, (4) подальша взаємодія з 7екв. 2-трет-бутил-1,1,3,3тетраметилгуанідину, (5) подальша взаємодія з 10екв. оцтового ангідриду; перетворення лактону 33 в сполуку 34, що містить гідроксил, шляхом видалення МОМ-захисної групи з використанням TMSI; відщеплення N-трихлоретоксикарбонільної групи сполуки формули 34 з одержанням сполуки 35 реакцією з Zn/AcOH; перетворення аміносполуки 35 у відповідний а-кетолактон 36 взаємодією з хлоридом Nметилпіридиній-карбоксальдегіду і потім з DBU; утворення ЕТ-770 взаємодією сполуки формули 36 з 3-гідрокси-4-метоксифенілетиламіном; перетворення ЕТ-770 в ЕТ-743 взаємодією з нітратом срібла в суміші AcN/H2O. 37 Схема III Описаний вище шлях перетворення проміжної сполуки 25 в сполуку ЕТ-743 може бути легко модифікований з використанням інших похідних цистеїну, наприклад, сполуки 37, яку називають 2метоксиметилокси-3-(9Н-флуорен-9ілметил)тіопропенова кислота. У даній сполуці вже є введена кетогрупа в формі енольного простого ефіру, в той час як в інших аналогах цистеїну присутня аміногрупа, яка повинна бути перетворена далі в кетогрупу шляхом реакції трансамінування, 75333 38 що протікає з помірним виходом - 55-60%. Отже, використання сполуки 37 можливе для того, щоб в значній мірі підвищити вихід постадійного синтезу, оскільки виключається стадія трансамінування. Перетворення проміжної сполуки 25 в сполуку ЕТ-743 з використанням похідного цистеїну 37 може бути здійснене аналогічним образом з використанням тих же самих реагентів, що і у випадку похідного цистеїну 29, з виключенням стадій перетворення (f) і (g). Послідовність реакцій ілюструє наступна схема (схема IV): 39 Схема IV Сполука 38 також може бути отримана взаємодією проміжної сполуки 12, описаної в патенті США 5721362, з проміжною сполукою 37, що є удосконаленням способу, описаного у вказаному патенті. Утворення фталасцидину і родинних йому сполук Згідно з даним винаходом ключовий клас продуктів включає фталасцидин і представлений загальною формулою (XX): в якій R1 представляє амідометиленову групу; R представляє невеликий бічний окси-ланцюг; і 21 R представляє ціаногрупу або гідроксигрупу. У випадку фталасцидину, R1 представляє фталімідометиленову групу; R5 представляє ацетоксигрупу; і R21 представляє ціаногрупу. Інші групи R1 включають моно- і ди-N-заміщені амідометиленові групи, а також і інші циклічні амідометиленові групи, а інші групи у випадку R5 включають, крім того, 5 75333 40 С1-С4 ацильні групи, а також С1-С4 алкільні групи. Перетворення 21-ціаносполуки у фталасцидин або родинні йому продукти формули (XX) включає наступні стадії: a) перетворення, якщо необхідно, хінонової системи кільця Ε в фенольну систему; b) утворення групи -R5 в 5-положенні кільця А; c) утворення групи -R1 в 1-положенні кільця В; d) перетворення, якщо необхідно, хінонової системи кільця А в фенольну систему; e) перетворення, якщо необхідно, фенольної системи кільця А в метилендіоксифенольне кільце. Дані стадії мають багато схожого зі стадіями, вказаними при отриманні ектеїнасцидинів. Стадія (с) звичайно включає утворення групи -CH2-NH2 в 1-положенні і її ацилювання. Фталасцидин може бути отриманий з використанням проміжних сполук, описаних при перетворенні ціаносафрацину В в проміжну сполуку 25. Наприклад, проміжні сполуки 21 і 17 є відповідними початковими речовинами для одержання фталасцидину. Як показано далі на схемі V, спосіб синтезу фталасцидину, виходячи з проміжної сполуки 21, включає наступну послідовність стадій: перетворення сполуки 21 в сполуку формули 27 взаємодією з фталевим ангідридом в дихлорметані і з карбонілдіімідазолом; перетворення сполуки 27 у фталасцидин по реакції з гідридом трибутилолова і дихлорпаладій 41 75333 42 біс(трифенілфосфіном) або лужним середовищем, з подальшою взаємодією з ацетилхлоридом. Схема V Як показано далі на схемі VI, спосіб синтетичного одержання фталасцидину, виходячи з проміжної сполуки 17, включає наступну послідовність стадій: ацетилювання гідроксильної групи сполуки формули 17 ацетилхлоридом з використанням піридину з одержанням ацетильованої проміжної сполуки формули 42; видалення трет-бутоксикарбонільної і метилоксиметильної захисних груп сполуки 42 з одержан Схема VI Утворення проміжної сполуки 11 і родинних їй ням сполуки формули 43 взаємодією з розчином НСl в діоксані. Дана реакція також може протікати при змішуванні сполуки 42 з розчином трифтороцтової кислоти в дихлорметані; утворення похідного тіосечовини формули 44 взаємодією сполуки 43 з фенілізотіоціанатом; перетворення сполуки формули 44 в амін формули 45 взаємодією з розчином хлористого водню в діоксані; перетворення сполуки 45 у фталасцидин взаємодією з фталевим ангідридом в дихлорметані з використанням карбонілдіімідазолу. проміжних сполук Ретросинтетичний аналіз проілюстрований наступною схемою. 43 Згідно з даним винаходом клас ключових проміжних сполук включає проміжну сполуку 11 і характеризується загальною формулою (XXI): в якій Prot1 і Prot2 представляють захисні групи для гідроксигруп, переважно різні. Що стосується самої проміжної сполуки 11, то група Prot1 представляє метоксиметильну групу, a Prot2 представляє трет-бутилдифенілсилільну групу. Перетворення 21-ціаносполуки в проміжну сполуку 11 або родинну їй проміжну сполуку формули (XXI) звичайно включає наступні стадії: a) перетворення, якщо необхідно, хінонової системи кільця Ε в фенольну систему; b) утворення групи -OProt1 в 18-положенні, в кільці Е; c) утворення групи -CH2-OProt2 в 1-положенні, в кільці В; d) перетворення, якщо необхідно, хінонової системи кільця А в фенольну систему; e) перетворення фенольної системи кільця А в метилендіоксифенольне кільце. Стадія (b), утворення захисної групи -OProt1 в 18-положенні, в кільці Е, представляє типову реакцію введення захисту фенольної групи і не потребує спеціальних коментарів. Відповідні умови вибирають в залежності від природи захисної групи. Інші стадії аналогічні стадіям інших реакцій. Стадію (с), утворення групи -CH2-OProt2 в 1положенні кільця В, звичайно здійснюють шляхом утворення групи -CH2-NH2 в 1-положенні, з подальшим перетворенням амінної функціональної групи в функціональну гідроксигрупу і введенням захисту. Таким чином, в тих випадках, коли початкова речовина містить групу R1, яка представляє CH2-NH-CO-CR25aR25bR25c, необхідне видалення Nацильної групи. У тих випадках, коли початкова 1 речовина містить групу R , яка представляє -CH2O-CO-R, при отриманні продукту - ектеїнасцидину, в якому заступник R1 є тим же самим, немає необхідності в змінах. У випадку інших продуктів, виникає задача видалення О-ацильної групи. Для здійснення такого деацетилювання є в розпорядженні різні методики. В одному з варіантів деацетилю 75333 44 вання і модифікація функціональної гідроксигрупи здійснюються в одну стадію. Крім того, гідроксигрупа може бути піддана ацилюванню або бути модифікована іншим образом для одержання відповідної R1-групи. У патенті США 5721362 описані методи синтезу, що використовуються для одержання ЕТ-743 шляхом тривалого багатостадійного синтезу. Однією з проміжних сполук, що одержуються в цьому синтезі, є проміжна сполука 11. Використовуючи як початкову речовину ціаносафрацин В, можна одержати проміжну сполуку 11, використовуючи значно більш короткий шлях одержання такої проміжної сполуки, удосконаливши таким чином спосіб одержання ЕТ-743. Ціаносафрацин В може бути перетворений в проміжну сполуку 25 по методиках, описаних вище. Виходячи з проміжної сполуки 25, можна одержати проміжну сполуку 11, здійснивши наступні стадії, див. схему VII: утворення захищеної гідроксисполуки формули 26 взаємодією сполуки 25 з третбутилдифенілсиліл-хлоридом в присутності основи; заключне відщеплення алільної групи сполуки 26 під дією гідриду трибутилолова і дихлорпаладій-біс(трифенілфосфіну), яке приводить до утворення проміжної сполуки 11. Схема VII Один з варіантів здійснення синтетичного способу згідно з даним винаходом для перетворення сафрацину В в проміжну сполуку 11 представляє 45 75333 46 модифікацію і розширення способу, представлено26 в проміжну сполуку 11 шляхом зняття захисту з го на схемі VIII, і включає наступну послідовність OCH2R захисної групи, взаємодією у відновлювастадій: льних або кислотних умовах. Звичайні методики стереоспецифічне перетворення сполуки фопредставляють використання паладію на вуглеці в рмули 1 (сафрацин В) в сполуку формули 2 шляатмосфері азоту або обробку водним розчином хом селективного заміщення ОН на CN взаємодіTFA, або гідридом трибутилолова і дихлорєю з KCN в кислому середовищі; біс(трифенілфосфінпаладієм). утворення похідного тіосечовини формули 3 Згідно з ще однією переважною модифікацією взаємодією сполуки формули 2 з фенілізотіоціанаціаносполука формули 2 може бути перетворена в том; проміжну сполуку 11 з використанням доповнення перетворення тіосечовини формули 3 в апедо схеми II, що включає наступні стадії: тамід формули 5 шляхом гідролізу в кислому сеутворення захищеної гідроксисполуки формуредовищі з подальшим доданням оцтового ангідли 26 взаємодією сполуки 25 з третриду; проміжний амін формули 4 може бути бутилдифенілсилілхлоридом в присутності основи; виділений шляхом гашення реакції гідролізу в кисзаключного відщеплення алільної групи сполулому середовищі бікарбонатом натрію, однак дане ки 26 гідридом трибутилолова і дихлорпаладійпохідне надто нестабільне і швидко перетворюбіс(трифенілфосфіном), що приводить до утвоється в п'ятичленний циклічний імін, позначений як рення проміжної сполуки 11. сполука 6; Утворення активних сполук утворення захищеної сполуки формули 7 взаМожна перетворити сафрацин В в ряд проміємодією з бромметилметиловим простим ефіром і жних сполук і похідних з потенційною протипухдіізопропілетиламіном в дихлорметані; линною терапевтичною активністю. Такі проміжні селективне деметилювакня метоксигрупи, що сполуки можуть бути отримані з вже описаних належить хіноновій системі сполуки формули 7, з сполук, або з використанням альтернативних підутворенням сполуки формули 8 при взаємодії з ходів. метанольним розчином гідроксиду натрію; Проміжні сполуки, що описуються, включають перетворення сполуки формули 8 в метиленсполуки 47 і ряд амідних похідних, отриманих з діоксисполуку формули 9, переважно при здійсвикористанням сполук 45 і 43. ненні наступної послідовності реакцій: (і) хінонову На схемі VIII показане одержання сполуки 47 з групу сполуки 8 відновлюють, використовуючи використанням наступної послідовності стадій: 10% Pd/C в атмосфері водню; (2) гідрохінонову утворення похідного тіосечовини формули 3 проміжну сполуку перетворюють в метилендіоксивзаємодією сполуки формули 2 з фенідізогіоціанасполуку формули 9 взаємодією з бромхлорметатом: ном і карбонатом цезію в атмосфері водню; (3) перетворення тіосечовини формули 3 в ацесполуку формули 9 переводять в сполуку формули тамід формули 5 шляхом гідролізу в кислому се10 введенням захисту гідроксильної групи у вигляредовищі з подальшим доданням оцтового ангідді групи OCH2R за допомогою взаємодії з ВrСН2R і риду; проміжний амін формули 4 може бути карбонатом цезію, де R може означати арил, виділений гасінням реакції гідролізу в кислому сеСН=СН2, OR' і т.д.; перетворення ацетамідної груредовищі бікарбонатом натрію, однак дане похідне пи сполуки формули 10 у відповідну гідроксильну надто нестабільне і швидко перетворюється в п'ягрупу сполуки формули 11 взаємодією з тетраоктичленний циклічний імін, названий сполукою 6; сидом азоту в суміші оцтової кислоти, і ацетооцтоутворення захищеної сполуки формули 7 взавого ефіру з подальшою обробкою гідроксидом ємодією з бромметилметиловим простим ефіром і натрію; як альтернатива може бути використаний діізопропілетиламівом в дихлорметані; нітрит натрію в суміші оцтового ангідриду i оцтової селективне деметилювання метоксигрупи, що кислоти, з подальшою обробкою гідроксидом наналежить хіноновій системі сполуки формули 7, з трію; утворенням сполуки формули 8 взаємодією з меяк альтернатива ацетамідна група сполуки танольним розчином гідроксиду натрію; формули 10 може бути перетворена в первинну перетворення сполуки формули 8 в метиленаміногрупу взаємодією з гідразином або з ВоС2О, діоксисполуку формули 10, переважно при здійсDMAP після гідразину; така первинна аміногрупа ненні наступної послідовності реакцій: (1) хінонову може бути перетворена у відповідну гідроксильну групу сполуки 8 відновлюють, використовуючи групу (сполуку формули 11) окислювальним пере10% Pd/C в атмосфері водню; (2) гідрохінонову творенням первинного аміну у відповідний альдепроміжну сполуку перетворюють в метилендіоксигід під дією 4-форміл-1сполуку формули 9 взаємодією з бромхлорметаметилпіридинійбензолсульфонату або іншого іону ном і карбонатом цезію в атмосфері водню; (3) піридинію, з подальшою обробкою DBU або іншою сполуку формули 9 переводять в сполуку Формули основою і додатковим гідролізом, і з подальшим 10 введенням захисту гідроксильної групи у виглявідновленням альдегідної групи до відповідної ді алілоксигрупи взаємодією з алілбромідом і каргідроксильної групи алюмогідридом літію або інбонатом цезію; шим відновлюючим засобом; перетворення сполуки формули 9 в ацетилпоутворення захищеної сполуки формули 26 хідне 46 взаємодією з ацетилхлоридом в піридині; взаємодією з трет-бутилдифенілсилілхлоридом і перетворення сполуки формули 46 в захищену диметиламінопіридином в дихлорметані; сполуку 47 взаємодією з хлористоводневою кислоперетворення силілованої сполуки формули тою в діоксані. 47 Схема VIII Інші корисні амідні похідні проміжних сполук можуть бути отримані, виходячи з вже описаної проміжної сполуки 45 по наступній схемі: Друга стадія є необов'язковою. Даний спосіб є важливою частиною даного винаходу, особливо, в тому випадку, коли група R представляє групу Ra, визначену вище. Крім того, схема VIII може бути легко розширена для того, щоб здійснити синтез сполук формули (XXIII), шляхом введення в початкову речовину різних груп в 5-положення або групи, безпосередньо необхідної продукту, або групи, яка може бути видалена або яким-небудь образом модифікована для одержання необхідної групи. Схема IX Виходячи із сполуки 45 може бути отримана група аналогів шляхом здійснення наступної послідовності операцій: 75333 48 ацилювання аміногрупи сполуки формули 45 з використанням широкого діапазону ацилпохідних для одержання відповідних амідів, в яких переважні ацильні групи представляють ацетил, цинамоїлхлорид, п-трифторцинамоїлхлорид, ізовалерилхлорид фенілтіоізоціаната або залишок амінокислоти, або інші групи, вказані вище як приклади груп RaCO-. перетворення CN-групи в ОН-групу взаємодією з нітратом срібла в суміші AcN/Н2О. Інші корисні амідні похідні проміжних сполук можуть бути отримані, виходячи з вже описаної проміжної сполуки 43 по наступній схемі: Схема X З сполуки 43 може бути отримана інша група похідних, що представляють інтерес, з використанням наступної послідовності операцій: (а) ацилювання аміногрупи сполуки формули 49 75333 50 43 з використанням широкого діапазону ацилпохідифікований варіант такої групи; і дних для одержання відповідних амідів, в яких R18 представляє -ОН, або захищений, або мопереважні ацильні групи представляють ацетил, дифікований варіант такої групи. цинамоїлхлорид, п-трифторцинамоїлхлорид, ізоВ одному з втілень, переважно, щонайменше, валерилхлорид або залишок амінокислоти, або одна з груп R1, R5, R14a, R14b, R15 або R18 представa інші групи, вказані вище як приклади груп R CO-. ляє захищений або модифікований варіант такої (b) перетворення CN-групи в ОН-групу взаєгрупи. модією з нітратом срібла в суміші AcN/H2O, В одному з варіантів здійснення винаходу груНові проміжні сполуки па R1 не є 3,5-трет-бутилдифенілсиліл іним застуВ світлі попередніх роз'яснень може бути очепником і/або група R18 не є метоксиметильною видно, що даний винахід забезпечує можливість групою одержання нових проміжних сполук. У залежності Переважно, R1 представляє -CH2-NH2 або від типу кільця А, проміжні сполуки представлені СН2ОН, або захищений або модифікований варіформулою (ХХІІа): ант такої групи, і R4 представляє -Н; або R1а і R4 разом утворюють групу: або формулою (ХХllb): Переважно, R14а і R14b обидва представляють Н. Один з переважних класів проміжних сполук включає сполуку, яка позначена як сполука 25, формули: в яких: R1 представляє -OH2-NH2 або -СН2ОН, або захищений або модифікований варіант такої групи, і R4 представляє -Н; або R1a і R4 разом утворюють групу формул (IV), (VI) або (VII): R5 представляє -ОН, або захищений або модифікований варіант такої групи; 14a 14b R і R обидва представляють -Н, або один представляє -Н, а інший -ОН, або захищений або модифікований варіант такої групи; - ОСН3 або ОСН2СН3, або R14a і R14b разом утворюють кетогрупу; R12 представляє -NH-, -NCH3- або -NCH2CH3-; R15 представляє -ОН, або захищений або мо Переважним класом, є клас сполук вказаної загальної формули, де група MOM замінена будьякою іншою захисною групою. Інші переважні проміжні сполуки включають сполуки, які позначені як сполуки 45 і 47. Інші Nацильні похідні можуть бути легко отримані із сполуки 45 і представляють важливу частину даного винаходу. Відповідні ацильні групи включають такі групи, які були вказані вище. Відповідні 21гідроксисполуки також є корисними і відносяться до числа виявлених активних сполук. Нові активні сполуки У доповненню було виявлено, що деякі із сполук даного винаходу, які спочатку були отримані як проміжні сполуки, володіють винятковою активністю при лікуванні різних різновидів рака, наприклад, таких як лейкемія, рак легенів, рак товстої кишки, рак нирки і меланома. Таким чином, даний винахід надає спосіб лікування якого-небудь ссавця, особливо, людини, схильної до рака, який включає введення суб'єкту, 51 75333 52 що страждає від хвороби, терапевтично ефективаналоги, (такі як пентостатин, метотрексат); ної кількості сполуки даного винаходу або її фарc) алкілуючі засоби, такі як похідні гірчичного мацевтичної композиції. масла, що містять азот (такі як циклофосфамід Даний винахід також відноситься до фармацеабо дифосфамід); втичних композицій, які містять в якості активного d) лікарські засоби, мішенню яких є ДНК, такі інгредієнта сполуку або сполуки даного винаходу, як антрациклінові лікарські засоби адріаміцин, доа також до способів одержання таких композицій. ксорубіцин, фарморубіцин або епірубіцин; Приклади фармацевтичних композицій вклюе) лікарські засоби, мішенню яких є топоізомечають будь-які тверді (таблетки, пілюлі, капсули, рази, такі як етопозид; гранули і або рідкі (розчини, суспензії або емульсії) f) гормони і агсністи гормонів або антагоністи композиції відповідного складу для перорального, гормонів, такі, як естрогени, антиестрогени (тамокмісцевого або парентерального введення, і мосифен і родинні йому сполуки) і андрогени, флужуть містити чисту сполуку даного винаходу або тамід, лейпрорелін, госерелін, ципротрон або октсполуки в поєднанні з будь-яким носієм або іншою реотид; фармакологічно активною сполукою. Такі компоg) лікарські засоби, мішенню яких є система зиції можуть потребувати стерилізації у випадку передачі сигналу в пухлинних клітинах, включаючи парентерального введення. похідні антитіл, такі як герцептин; Введення сполук або композицій даного винаh) алкілуючі лікарські засоби, такі як препарати ходу може здійснюватися будь-яким відповідним платини (цисплатин, карбонплатин, оксалиплатин, способом, наприклад, таким як, внутрішньовенне параплатин) або нітрозосечовини; вливання, використання пероральних препаратів, і) лікарські засоби, що потенційно впливають інтраперитонеальне і внутрішньовенне введення. на метастази пухлин, такі як інгібітори матричних Найбільш переважним є проведення вливання протеїніаз; протягом аж до 24 годин, переважно, 2-12 годин, j) лікарські засоби для генної терапії і засоби, найбільш переважнр, 2-6 годин. Особливо бажані що володіють антисенсивною дією; короткочасні вливання, які дозволяють здійснюваk) лікарські засоби для терапії з участю антити вливання, не залишаючи пацієнта в клініці на тіл; ніч. Однак, якщо потрібно, вливання може продоl) інші біологічно активні сполуки морського вжуватися від 12 до 24 годин і навіть довше. Ввепоходження, особливо, дидемнини, такі як аплидення може продовжуватися, з відповідними інтедин; рвалами, протягом від 2 до 4 тижнів. m) аналоги стероїдів, зокрема, дексаметазон; Фармацевтичні композиції, що містять сполуки n) протизапальні лікарські засоби, зокрема, даного винаходу, можуть бути доставлені за додексаметазон; помогою ліпосом або нанокапсул, з використанням о) протиблювотні лікарські засоби, зокрема, композицій уповільненого вивільнення або з викодексаметазон. ристанням інших звичайних засобів доставки. Даний винахід також розповсюджується на Правильне дотування сполук буде варіюватисполуки даного винаходу для застосування в спося в залежності від конкретної композиції, способу собі лікування, а також на застосування даних застосування, а також конкретного місцезнахосполук для одержання композицій для лікування дження, «господаря» і пухлини, яка підлягає лікурака. ванню. Потрібно брати до уваги і інші чинники, такі Цитотоксична активність як вік, маса тіла, стать, режим харчування, час Культури клітин. Використали клітини в логавведення, швидкість виділення, особливості «госрифмічній фазі зростання, в мінімальному есенціподаря», співвідношення лікарських препаратів, альному середовищі Ігла, що містить добавки підчутливість до препарату і міра вираженості симптримуючих солей Ерла, 2,0мМ L-глутаміну, не томів. Введення може здійснюватися безперервно незамінні амінокислоти, без бікарбонату натрію або періодично в межах максимально допустимої (ΕΜΕΜ/neaa); з доданням 10% фетальної телячої дози. сироватки (FCS), 10-2Μ бікарбонату натрію і 0,1г/л Сполуки і композиції даного винаходу можуть пеніциліну-G + сульфату стрептоміцину. бути використані спільно з іншими препаратами Для оцінки і порівняння протипухлинної активдля проведення комбінованої терапії. Інші лікарсьності цих сполук здійснювали просту методику кі засоби можуть становити частину тієї ж самої скринінгу, використовуючи адаптований варіант композиції або бути представлені у вигляді окреметоду, описаного Bergeron et al. (1984). Лінія клімої композиції для введення в той же самий або тин пухлини, що використовується являла собою інший час. Природа інших лікарських засобів осоР-338 (суспензійна культура лімфоїдної неоплазми бливо не обмежена, відповідні варіанти лікарських миші лінії DBA-2), A-549 (моношарова культура засобів включають: карциноми легеня людини), НТ-29 (моношарова a) лікарські зассби, що володіють антимітотичкультура карциноми товстої кишки людини) і MELною дією, особливо такі, мішенню яких є елементи 28 (моношарова культура меланоми людини). цито скелету, включаючи модулятори мікротрубоКлітини Р-338 висівали а 16мм лунки в кількочок, такі як таксанові лікарські засоби (такі як таксті 1 104 клітин на лунку в 1мл аліквоті MEM 5FCS. сол, паклітаксел, таксотер, доцетаксел), подофіщо містить певну концентрацію лікарського засобу. лотоксини або вінкаалкалоїди (вінкріртин, Окремо висівали набір культур як контроль зросвінбластин); тання, не використовуючи лікарський засіб, для b) лікарські засоби - антиметаболіти, такі як 5того, щоб бути в упевненості в тому, що клітини фторурацил, цитарабін, гемцитабин, пуринові залишаються в експонентній фазі зростання. Всі 53 75333 визначення проводили двічі. Через три дні інкубування при 37°С, 10% СО2 в атмосфері з 98%-ною вологістю визначали приблизне значення ІС50 шляхом порівняння зростання клітин в лунках, що містять лікарський засіб, і в контрольних лунках. A-549, HT-29 і MEL-28 висівали в 16мм лунки в кількості 2 104 клітин на лунку в 1мл аліквоті MEM 10FCS, що містить певну концентрацію лікарського засобу. Окремо висівали набір культур як контроль зростання, не вводячи лікарський засіб, для того, щоб бути в упевненості в тому, що клітини залишаються в експонентній фазі зростання. Всі визначення проводили двічі. Через три дні інкубування при 37°С, 10% СО2 в атмосфері з 98%-ною вологістю лунки забарвлювали 0,1%-ним барвником кристалічним фіолетовим. Приблизне значення ІС50 визначали шляхом порівняння зростання клітин в лунках, що містять лікарський засіб, і в контрольних лунках. [1. Raymond J.Bergeron. Paul F. Cavanaugh, Jr., Steven J. Kline. Robert G. Hughes, Jr., Gary T. Elliot and Carl W. Porter. Antineoplastic and antiherpetic activity of spermidine catecholamide iron сhelators. Biochem. Bioph. Res. Comm. 1984, 121 (3), 848-854. 2. Alan G. Scliroeder, Robert G. Hughes, Jr., and Alexander Bloch. Effects of Acyclic Pyrimidine Nucleoside Analoges. J.Med.Chem. 1981,24 10781083]. 54 55 75333 56 З цих даних, що характеризують активність, і інших аналізів може бути видно, що активні сполуки, що є предметом даного винаходу, включають переважний клас сполук загальної формули (XXIII): в якій R1 є таким, як визначено вище для групи (XVIIb) і переважно представляє похідне амінометиленової групи середнього розміру; R5 є таким, як визначено вище для групи (XVIIb) і переважно представляє похідне гідроксигрупи невеликого розміру; R12 є таким, як визначено вище і переважно представляє -СН3 і R21 представляє гідрокси або ціаногрупу. R1 представляє відповідну гідрофобну групу, в якій, таким чином, відсутні вільні аміно, гідрокси і інші гідрофільні функціональні групи. Звичайно R1 представляє групу -CH2-NH2-CO-Ra, в якій Ra є таким, як визначено, але переважно має лінійний ланцюг довжиною менш, ніж 20 атомів, більш переважно, менш ніж 15 або 10 атомів, де 1,4-феніл визначається як ланцюг довжиною в чотири атоми, і аналогічні міркування застосовуються до інших циклічних груп (наприклад, 1,2-циклогексил представляє ланцюг довжиною в два атоми), і лінійний ланцюг довжиною менш, ніж 10, 15 або 20 атомів сам може бути заміщеним. Зокрема, дані дають можливість передбачити, що повинна бути досягнуте деяка рівновага між відсутністю такої групи, як Ra-CO - і присутністю великої, об'ємної групи. В одному з варіантів є переважним, щоб група R1 не містила циклічних груп, особливо, ароматичних груп. У родинних варіантах даний винахід не відноситься до одержання сполук які описані в статті, опублікованій в: [Proc. Natl. Acad. Sci. USA, 96, 3496-3501, 1999], яка включена за допомогою 57 75333 58 посилання. Інші переважні групи для R1, відповідновить частину способу. Ra в кінцевому продукті є но до даного винаходу, виключають відповідні запереважно такий, як визначено для сполуки форступники CH2R2, приведені в таблиці 1 вказаної мули (XXXIII). статті, особливо групи А, В, С і D для R2. Інший важливий спосіб даного винаходу вклюR5 переважно представляє ацетильну групу. чає реакцію: 1 В особливо переважних сполуках група R ацильована по -NН2-групі, і наприклад, Nацилпохідні можуть бути утворені з груп -CH2-NH2 і -CH2-NH-aa. Ацилпохідні можуть являти собою їх N-ацил або N-тіоацилпохідш. Ацильні групи можуть бути формули -СО-Ra, де Ra є таким, як визначено і вибирається таким чином, щоб задовоІнший важливий спосіб даного винаходу вклюльняти вказаним критеріям. Відповідні ацильні чає реакцію: групи включають аланіл, аргиніл, аспартил, аспарагіл, цистил, глутаміл, глутамініл, гліцил, гістиділ, гідроксипропіл, ізолейцил, лейцил, лізіл, метіоніл, фенілаланіл, проліл, серил, треоніл, тироніл, триптофіл, тирозил, валіл, а також інші ацильні групи амінокислот. Такі ацильні групи амінокислот переважно модифіковані по аміногрупі для досягнення гідрофобності. Інший важливий спосіб даного винаходу вклюВ одному з варіантів група R1 представляє чає реакцію, згідно з якою група R1, що являє сомодифіковану гідроксиметиленову групу. Застособою амінометиленову групу, перетворюється в вні міркування, аналогічні міркуванням відносно гідроксиметиленову групу. модифікації амінометиленової групи. Інший важливий спосіб даного винаходу вклюУ світлі активності даних сполук важливим чає реакцію, згідно з якою сполука, що містить способом згідно з даним винаходом є наступний: групу R1, що являє собою гідроксиметиленову групу, взаємодіє з реагентом формули (XIX) де R5 в кінцевому продукті є таким, як визначено для сполуки (XXXII), і може бути іншим в початковій речовині і утворитися внаслідок перетворення, що становить частину способу, R18 представляє в кінцевому продукті гідроксигрупу, але може бути захищеною гідроксигрупою в початковій речовині і утворитися внаслідок перетворення, що становить частину способу, R12 в кінцевому продукті може бути таким же, як і в початковій речовині, або може утворитися внаслідок перетворення, що становить частину способу, R21 в кінцевому продукті є таким, як визначено, і якщо є гідроксигрупою, то може утворитися з ціаногзупи внаслідок перетворення, що становить частину способу, Ra є таким, ж визначено, і може бути додатково ацильований, що становитиме частину способу вдержання кінцевого продукту з ацильованими групами Ra, як обговорювалося. R5 в початковій речовині переважно представляє ацетильну або іншу невелику ацильну групу і не змінюється при проведенні реакції. R18 в початковій речовині переважно представляє гідроксигрупу і не змінюється при проведенні реакції. R12 переважно представляє -NCH3- в початковій речовині і не змінюється при проведенні реакції. R21 в кіниевому продукті є такою, як визначено, і в тому випадку, якщо є гідроксигрупою, то може утворитися з ціаногрупи внаслідок перетворення, що ста в якій Fu означає захищену функціональну групу, Prot3 представляє захисну групу, а пунктирна лінія показує необов'язковий подвійний зв'язок. Інший важливий спосіб даного винаходу включає реакцію одержання 21-ціаносполуки формули (XVI), яка включає взаємодію сполуки формули (XV): в якій R1, R5, R8, R14a, R15 і R18 є такими, як визначено, і R21 представляє гідроксигрупу, з джерелом ціанід-іону з одержанням при цьому необхідної 21-ціаносполуки. У доповнення також передбачаються способи з використанням інших нуклеофілвмісних сполук, для того, щоб одержати сполуки, аналогічні сполукам формули (XVI), в яких 21-положення захищене іншою нуклеофільною групою, 21-Nuc групою. Наприклад, 21-Nuc сполука формули (XVI) з алкіламінозаступником в 21-положенні може бути отримана взаємодією сполуки формули (XV), в якій R21 представляє гідроксигрупу, з відповідним алкіла 59 75333 60 міном. 21-Nuc сполука формули (XVI) з алкілтіоза0°С діізопропілетиламін (82,96мл, 476,2ммоль), ступниксм в 21-положенні може бути отримана метокси-метиленбромід (25,9мл, 317,5міуоль) і взаємодією сполуки формули (XV), в якій R21 диметиламінопіридин (155мг, 1,27ммоль). Отрипредставляє гідроксигрупу, з відповідним алкантіману суміш перемішують при 23°С протягом 24 олом. Як альтернатива, 21-Nuc сполука формули годин. Реакцію гасять доданням при 0°С водного 0,1N розчину НСІ (750мл) (рН=5), і екстрагують, (XVI) з -карбонілалкілзаступником в 21-положенні використовуючи СН2СІ2 (2 400мл). Органічну фазу може бути отримана взаємодією сполуки формули (XV), в якій R21 представляє гідроксигрупу, з відпосушать (сульфат натрію) і концентрують у вакуумі. відною карбонільною сполукою, як правило, в приЗалишок очищають колонковою флешсутності основи. Для одержання інших 21-Nuc спохроматографією (SіO2, градієнт від геклук доступні інші методики синтезу. сан:етилацетат, 4:1, до гексан:етилацетат, 3:2), Інша важлива реакція даного винаходу вклюодержуючи при цьому сполуку 15 (17,6г, 83%) у чає обробку продукту - 21-ціаносполуки, що є превигляді жовтої твердої речовини. дметом даного винаходу, для утворення 21Rf: 0,38 (гексан: етилацетат, 3:7) 1 гідроксисполуки. Такі сполуки володіють цікавими Н ЯМР (300МГц, СDСІ3): 6,73 (с, 1Н), 5,35 властивостями: in vivo. (шир,с, 1Н), 5,13 (с, 2Н), 4,50 (шир.с, 1Н), 4,25 (д, Приклади J=2,7Гц, 1Н), 4,03 (д, J=2,7Гц, 1Н), 3,97 (с, 3Н) , Приклад 1 3,84 (шир.с, 1Н), 3,82-3,55 (м, 1Н), 3,69 (с, 3Н), 3,56 (с, 3Н), 3,39-3,37 (м, 1Н), 3,23-3,00 (м, 5Н), 2,46 (д, J=18Гц, 1Н), 2,33 (с, 3Н), 2,23 (с, 3Н), 1,85 (с, 3Н), 1,73-1,63 (м, 1Н), 1,29 (с, 9Н), 0,93 (д, J=5,1Гц, 3Н) 13 С ЯМР (75МГц, СDСІ3): 185,4, 180,9, 172,4, 155,9, 154,5, 149,0, 148,4, 141,6, 135,1, 131,0, 129,9, 127,6, 124,4, 123,7, 117,3, 99,1, 79,3, 60,7, 59,7, 58,4, 57,5, 56,2, 55,9, 55,0, 54,2, 50,0, 41,5, 39,9, 28,0, 25,2, 24,0, 18,1, 15,6, 8,5. ESI-мас-спектроскопія m/z: обчислено для C36H47N5O9: 693,8. Знайдено (М+Н)+: 694,3 До розчину сполуки 2 (21,53г, 39,17ммоль) в Приклад 3 етанолі (200ммоль) додають третбутоксикарбонілангідрид (7,7г, 35,25мл) і перемішують суміш протягом 7 годин при 23°С. Потім реакційну суміш концентрують у вакуумі і отриманий залишок очищають колонковою флешхроматографією (SіO2, гексан: етилацетат, 6:4), одержуючи при цьому сполуку 14 (20,6г, 81%) у вигляді жовтої твердої речовини. Rf: 0,52 (етилацетат: СНСІ3, 5:2) 1 Н ЯМР (300МГц, СDСІ3): 6,49 (с, 1Н) , 6,32 (шир.с, 1Н), 5,26 (шир.с, 1Н), 4,60 (шир.с, 1Н), 4,14 (д, J=2,4Гц,·1Н), 4,05 (д, J=2,4Гц, 1Н), 3,94 (с, 3Н), 3,81 (д, J=4,8Гц, 1Н), 3,7 (с, 3Н), 3,34 (шир. д, J=7,2Гц, 1Н), 3,18-3,00 (м, 5Н), 2,44 (д, J=18,3Гц, 1Н), 2,29 (с, 3Н), 2,24 (с, 3Н), 1,82 (с, 3Н), 1,80-1,65 (м, 1Н), 1,48 (с, 9Н), 0,36 (д, J=5,1Гц, 3Н) 13 С ЯМР (75МГц, СDСІ3): 185,5, 180,8, 172,7, 155,9, 154,5, 147,3, 143,3, 141,5, 135,3, 130,4, 129,2, 127,5, 120,2, 117,4, 116,9, 80,2, 60,7, 60,3, 58,5, 55,9, 55,8, 54,9, 54,4, 50,0, 41,6, 40,3, 28,0, 25,3, 24,0, 18,1, 15,6, 8,5. ESI-мас-спектроскопія, m/z: обчислено для C34H43N5O8: 649,7. Знайдено (М+Н)+: 650,3 Приклад 2 До розчину слолуки14, що перемішується (20,6г, 31,75ммоль) в CH3CN (15 мл), додають при У колбу, в якій знаходиться сполука 15 (8г, 11,5ммоль) в метанолі (1,6л), при 0°С додають водний розчин 1Μ гідроксиду натрію (3,2л). Реакційну суміш перемішують протягом 2 годин при цій температурі і потім гасять реакцію доданням 6Μ розчину НСІ до рН=5. Суміш екстрагують етилацетатом (3 1л) і об'єднані органічні шари сушать над сульфатом натрію і концентрують у вакуумі. Отриманий залишок очищають колонковою флешхроматографією (SiO2, градієнт від СНСІ3 до суміші гексан: етилацетат, 2:1), одержуючи при цьому сполуку 16 (5,3мг, 68%). Rf: 0,48 (CН3CN: H2O, 7:3, RP-C18) 1 Н ЯМР (300МГц, СDСІ3): 6,73 (с, 1Н) , 5,43 (шир.с, 1Н), 5,16 (с, 2H), 4,54 (шир.с, 1Н), 4,26 (д, J=1,8Гц, 1H), 4,04 (д, J=2,7Гц 1H), 3,84 (шир.с, 1Н), 3,80-3,64 (м, 1Н), 3,58 (с, 3Н), 3,41-3,39 (м, 1Н), 3,22-3,06 (м, 5Н), 2,49 (д, J=18,6Гц 1Н), 2,35 (с, 3Н), 2,30-2,25 (м, 1Н), 2,24 (с, 3Н), 1,87 (с, 3Н), 1,45-1,33 (м, 1Н), 1,19 (с, 9Н), 1,00 (шир. д, J=6,6Гц, 3Н) 13 С ЯМР (75 МГц, СDСІ3): 184,9, 180,9, 172,6, 154,7, 151,3, 149,1, 148,6, 144,7, 132,9, 131,3, 129,8, 124,5, 123,7, 117,3, 116,8, 99,1, 79,4, 59,8, 58,6, 57,7, 56,2, 55,6, 54,9, 54,5, 50,1, 41,6, 40,1, 28,0, 25,3, 24,4, 18,1, 15,7, 8,0.
ДивитисяДодаткова інформація
Назва патенту англійськоюA semisynthetic method for preparing compounds with condensed cyclic system and intermediary compounds
Назва патенту російськоюПолусинтетический способ получения соединений с конденсированной циклической системой и промежуточные соединения
МПК / Мітки
МПК: C07D 515/00, C07D 471/22, A61P 35/00, A61P 31/04, C07D 471/18, C07D 487/18, C07D 491/22, A61K 31/4995
Мітки: проміжні, сполуки, напівсинтетичний, циклічною, конденсованою, спосіб, системою, одержання, сполук
Код посилання
<a href="https://ua.patents.su/51-75333-napivsintetichnijj-sposib-oderzhannya-spoluk-z-kondensovanoyu-ciklichnoyu-sistemoyu-i-promizhni-spoluki.html" target="_blank" rel="follow" title="База патентів України">Напівсинтетичний спосіб одержання сполук з конденсованою циклічною системою і проміжні сполуки</a>
Попередній патент: Машина і спосіб для монтажу контактного проводу
Наступний патент: Система захисту від перевищення допустимої швидкості у турбомашині
Випадковий патент: П'єзоелектричний перетворювач механічних величин