Похідні 2-азабіцикло[2.2.1]гептану та спосіб їх одержання
Формула / Реферат
1. Похідні 2-азабіцикло[2.2.1]гептану з 1R- або 1S-конфігурацією загальної формули (І) або (І'):
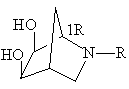 (I)
(I)
або
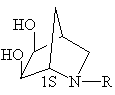 , (I')
, (I')
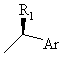
де R означає атом водню або, відповідно, радикал загальної формули (II) або (II'):
 (II)
(II)
або
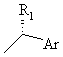 , (II')
, (II')
де R1 означає алкільний радикал з 1-4 атомами вуглецю, а Аr означає феніл або ![]() - або
- або ![]() -нафтил, що може бути заміщеним одним або декількома, однаковими або різними, атомами або радикалами, що вибирають серед атомів галогену та алкільних радикалів з 1-4 атомами вуглецю, алкоксильних радикалів з 1-4 атомами вуглецю або нітрогрупи.
-нафтил, що може бути заміщеним одним або декількома, однаковими або різними, атомами або радикалами, що вибирають серед атомів галогену та алкільних радикалів з 1-4 атомами вуглецю, алкоксильних радикалів з 1-4 атомами вуглецю або нітрогрупи.
2. Похідні 2-азабіцикло[2.2.1]гептану за п. 1, в яких R1 означає метильний або етильний радикал, а Аr означає феніл, можливо заміщений одним або декількома метильними або метоксирадикалами.
3. Похідні 2-азабіцикло[2.2.1]гептану за п. 1, в яких R1 означає метильний радикал та Аr означає фенільний радикал.
4. Спосіб отримання сполук за одним із пп. 1, 2 або 3, де R означає радикал загальної формули (II) або (II'), який відрізняється тим, що здійснюють бісгідроксилювання сполуки загальної формули (III) або (III'):
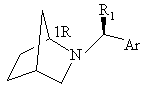 (III)
(III)
або
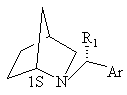 , (III')
, (III')
де R1 та Аr мають значення, вказане у будь-якому з пп. 1, 2 або 3.
5. Спосіб за п. 4, який відрізняється тим, що бісгідроксилювання здійснюють за допомогою перманганату калію або тетроксиду осмію, в присутності N-метилморфоліноксиду або триетиламіноксиду, або фериціаніду калію (К3FеСN6).
6. Спосіб отримання сполуки по п. 1, де R означає атом водню, який відрізняється тим, що сполуку по будь-якому з пп. 1, 2 або 3 обробляють воднем в присутності каталізатора, такого як паладій-на-вугіллі, працюючи в органічому розчиннику, який вибирають серед аліфатичних спиртів з 1-3 атомами вуглецю.
7. Сполука загальної формули (VI):
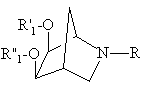 , (VI)
, (VI)
де R означає атом водню або радикал загальної формули (II), такий як вказано в будь-якому з пп. 1, 2 або 3, та R'1, R"1, однакові або різні, означають залишок органічної аліфатичної кислоти з 2-4 атомами вуглецю, такий як ацетил або пропіоніл, або залишок ароматичної кислоти, такий як бензоїльний залишок; або R'1 та R"1 разом утворюють метиленовий радикал, атом вуглецю якого може бути заміщено одним або кількома, однаковими або різними радикалами, що вибирають серед алкільних радикалів з 1-4 атомами вуглецю, які можуть утворювати разом аліциклічний радикал з 5-ма або 6-ма атомами вуглецю; або фенільних радикалів.
8. Сполука загальної формули (VII):
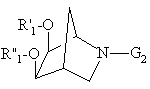 , (VII)
, (VII)
де R'1, R"1, однакові або різні, означають залишок органічної аліфатичної кислоти з 2-4 атомами вуглецю, такий як ацетил або пропіоніл, або залишок ароматичної кислоти, такий як бензоїльний залишок; або R'1 та R"1 разом утворюють метиленовий радикал, атом вуглецю якого може бути заміщено одним або кількома, однаковими або різними радикалами, що вибирають серед алкільних радикалів з 1-4 атомами вуглецю, які можуть утворювати разом аліциклічний радикал з 5-ма або 6-ма атомами вуглецю; або фенільних радикалів, та G2 означає захисну групу для амінофункції.
9. Спосіб отримання сполуки загальної формули (V):
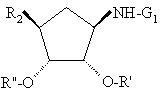 , (V)
, (V)
в якій R2 означає карбоксил; алкоксикарбоніл, алкільна частина якого містить 1-4 атоми вуглецю; N-алкіламінокарбоніл, алкільна частина якого містить 1-4 атоми вуглецю; або гідроксиметил, або алкоксиметил; a R' та R'', однакові або різні, означають атом водню або залишок органічної аліфатичної кислоти з 2-4 атомами вуглецю, такий як ацетил або пропіоніл, або залишок ароматичної кислоти, такий як бензоїльний залишок; або R' та R'' разом утворюють метиленовий радикал, атом вуглецю якого може бути заміщеним одним або кількома, однаковими або різними радикалами, що вибирають серед алкільних радикалів з 1-4 атомами вуглецю, які можуть утворювати разом аліциклічний радикал з 5-ма або 6-ма атомами вуглецю; або фенільних радикалів; та G1 означає атом водню або захисну групу G2 для амінофункції, який відрізняється тим, що захисну групу G2 продукту загальної формули (VIII):
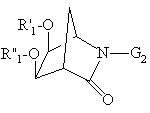 , (VIII)
, (VIII)
де R'1, R''1 та G2 мають вищевказані значення, заміщують на атом водню, потім, залежно від природи радикалу R2, який хочуть отримати, до взаємодії з отриманим продуктом вводять неорганічну основу, алкоголят лужного металу, алкіламін або боргідрид лужного металу; далі, якщо необхідно, заміщують радикали R'1 та R''1 на атом водню.
Текст
Даний винахід стосується нових похідних 2-азабіцикло[2.2.1]гептану з 1R- або 1S-конфігурацією загальної формули (І) або (I’): способу їх отримання та їх застосування. У загальних формулах (І) або (І’) R означає атом водню або, відповідно, радикал загальної формули (II) або (II’): де R2 означає алкільний радикал з 1-4 атомами вуглецю, а Аr означає феніл або a- або b-нафтил, що може бути заміщеним одним або декількома, однаковими або різними, атомами або радикалами, що обирають серед атомів галогену та алкільних радикалів з 1-4 атомами вуглецю, алкоксильних радикалів з 1-4 атомами вуглецю або нітрогрупи. Переважно, R1 означає метильний або етильний радикал, а Аr означає феніл, можливо заміщений одним або декількома метильними або метокси-радикалами. Переважніше, R1 означає метил, а Аr означає феніл. Згідно винаходу, сполуки загальної формули (І) або (I’), де R означає відповідно радикал загальної формули (II) або (II’) можна отримати шляхом біс-гідроксилювання сполуки загальної формули (III) або (III’): де R1 та Аr мають вищевказане значення. Звичайно біс-гідроксилювання здійснюють, працюючи в умовах, що описані V.Van Rheenen et coll., Tetrahedron Letters, 23, 1973-1976 (1976). Зокрема, окислення можна здійснювати за допомогою перманганату калію або тетроксиду осмію в присутності N-метилморфоліноксиду або триетиламіноксиду, або ферицианіду калію(K3FeCN6). Звичайно працюють у водно-органічному середовищі, такому як суміш води з трет-бутанолом або води з ацетоном. Згідно загального правила, окисник потрібно обирати так, щоб він давав лише 5,6-дигідрокси-похідне в екзоформі. Сполуку загальної формули (III) або (III’) можна отримати шляхом реакції Дильс-Альдера між гомохіральним аміном загальної формули (IV) або (IV): де R1 та Аr мають вищевказані значення, у фомі солі, переважно з неорганічною кислотою, такою як соляна кислота, формальдегідом та циклопентадієном, працюючи в умовах, що описані S.D. Larsen та P.A. Grieco, J. Amer. Chem. Soc, 107, 1768-1769 (1985). Виходячи з гомохірального аміну в R- або S-формі, здійснення способу призводить до утворення суміші двох діастереоізомерів, розділення яких не є необхідним, оскільки вони однаково реагують на наступній стадії біс-гідроксилювання. Згідно винаходу, сполуку загальної формули (І) або (I’), де R означає атом водню, можна отримати шляхом гідрогенолізу сполуки загальної формули (І) або (І’), де R означає радикал загальної формули (II) або (II’), за допомогою водню в присутності каталізатора, такого як паладій-на-вугіллі, працюючи в органічному розчиннику, такому як спирт, наприклад, метанол. Ізомер (1R) загальної формули (І), де R означає радикал загальної формули (II), можна виділити із суміші сполук загальної формули (І) та загальної формули (І’) шляхом діастереоселективної кристалізації з оптично активною кислотою у відповідному органічному розчиннику. Найкращим є використання Lдиметоксибурштинової кислоти в аліфатичному спирті, такому як ізопропанол. Нові сполуки загальної формули (І) є особливо цікавими для отримання сполук, що є объектом винаходу патенту US 5364862. Вони також є активними інгредієнтами при лікуванні серцево-судинних захворювань, таких як гіпертонія та міокордиальна ішемія. Найцікавішою є сполука [1-S-[1a,2b,3b,4a(S*)]]-4-[7-[[2-(3-хлор-2-тієніл)-1-етил]аміно]-3Н-імідазо-[4,5b]піридин-3-іл]-N-етил-2,3-дигідроксициклопентанкарбокамід формули: Сполуки загальної формули (І) є особливо корисними для отримання карбоцукру загальної формули (V): де: R2 означає карбоксил; алкоксикарбоніл, алкільна частина якого містить 1-4 атоми вуглецю; Nалкіламінокарбоніл, алкільна частина якого містить 1-4 атоми вуглецю; або гідроксиметил, або алкоксиметил; та R’ та R’’, однакові або різні, означають атом водню або залишок органічної аліфатичної кислоти з 2-4 атомами вуглецю, такий як ацетил або пропіоніл, або залишок ароматичної кислоти, такий як бензоїльний залишок; або R’ та R’’ разом утворюють метиленовий радикал, атом вуглецю якого може бути заміщеним одним або кількома, однаковими або різними радикалами, що обирають серед алкільних радикалів з 1-4 атомами вуглецю, які можуть утворювати разом аліциклічний радикал з 5-ма або 6-ма атомами вуглецю; або фенільних радикалів; та G1 означає атом водню або захисну гр упу G 2 для аміно-функції. Більш конкретно, R2 означає етиламінокарбонільний радикал або гідроксиметильний радикал, a R’ та R’’ разом утворюють ізопропіліденовий радикал. Карбоцукор загальної формули (V) є одним з елементів структури сполук, захищених у патенті US 5634862. Карбоцукор загальної формули (V) можна отримати зі сполуки загальної формули (І) таким чином: Гідроксильні функції сполуки загальної формули (І), де R означає атом водню або радикал загальної формули (II), захи щають з утворенням складного ефіру або ацеталю загальної формули (VI): Де: R означає атом водню або радикал загальної формули (II); та R1’ та R1’’, однакові або різні, означають залишок органічної аліфатичної кислоти з 2-4 атомами вуглецю, такий як ацетил або пропіоніл, або залишок ароматичної кислоти, такий як бензоїльний залишок; або R1’ та R1’’ разом утворюють метиленовий радикал, атом вуглецю якого може бути заміщеним одним або кількома, однаковими або різними радикалами, що обирають серед алкільних радикалів з 1-4 атомами вуглецю, які можуть утворювати разом аліциклічний радикал з 5-ма або 6-ма атомами вуглецю; або фенільних радикалів. Звичайно, захист гідроксильних радикалів здійснюють у звичайних умовах етерифікації або ацеталізації, наприклад, під дією оцтової або пропіонової кислоти в присутності п-толуолсульфокислоти, в органічному розчиннику, такому як ароматичний вуглеводень, наприклад, бензол або толуол, відокремлюючи воду, коли вона утворюється, або під дією альдегіду або кетону, можливо у формі ацеталю, в присутності кислоти такої як трифтороцтова кислота, в органічному розчиннику, такому як ароматичний вуглеводень, наприклад, бензол або толуол, при температурі від 50°С до температури кипіння зі зворотним холодильником реакційної суміші. Сполуку загальної формули (VI), де R означає радикал загальної формули (II), можна перетворювати на сполуки загальної формули (VI), де R означає атом водню, шляхом гідрогенеолізу. Звичайно гідрогеноліз здійснюють за допомогою водню, якщо необхідно під тиском, в присутності каталізатора, такого як паладій-на-вугіллі, в органічному розчиннику, такому як спирт, наприклад, метанол, етанол або ізопропанол, при температурі від 0 до 50°С. Сполуки загальної формули (VI) є новими продуктами та складають інший объект даного винаходу. Сполуку загальної формули (VI), де R означає атом водню, можна перетворити на сполуку загальної формули (VII): де R1’ та R1’’ мають вищевказані значення та G2 означає захисну для аміно-функції груп у, діючи відповідним реагентом, що дозволяє селективно вводити захисну гр упу. Захисні групи обирають з таких груп, що в подальшому можуть бути селективно видалені. З найбільш придатних захисних гр уп можна назвати хлорацетил, метоксиметил, 2,2,2-трихлоретоксикарбоніл, третбутил, бензил, п-нітробензил, п-метоксибензил, дифенілметил, триалкілсиліл, аліоксикарбоніл, бензилоксикарбоніл, в якому фенільне ядро може бути заміщеним атомом галогену або алкільним радикалом з 1-4 атомами вуглецю, або алкокси радикалом з 1-4 атомами вуглецю; або третбутоксикарбоніл. Серед інших захисних груп, які також є придатними, можна назвати такі, що описані Т. W. Greene та P. G. M. Wuts "Protecting Groups in Organic Synthesis", глава 7, друге видання, John Wiley and Sons (1991). Найбільший інтерес представляє трет-бутоксикарбонільна група. Сполуку загальної формули (VII), де G 2 означає трет-бутоксикарбонільний радикал, можна отримати безпосередньо із сполуки загальної формули (VI), де R означає радикал загальної формули (II), шляхом одночасного гідрогенолізу та трет-бутоксикарбонілювання. Звичайно реакцію проводять шляхом одночасної взаємодії водню, в присутності каталізатора, такого як паладій-на-вугіллі, та ди-трет-бутилдикарбонату із сполукою загальної формули (VI), працюючи в органічному розчиннику, такому як спирт, наприклад, метанол, етанол або ізопропанол, при температурі від 0 до 50°С. Сполуки загальної формули (VII) є новими продуктами, що складають наступний объект даного винаходу. Сполуку загальної формули (VII) потім окислюють до сполуки загальної формули (VIII): де R1’, R1’’ та G 2 мають вищезгадане значення. Звичайно окислення здійснюють за допомогою оксиду рутенію(RuO4), який, якщо необхідно, отримують in situ з попередника, такого як RuO2 або RuCl, в присутності окисника, що обирають серед перйодату, такого як перйодат натрію; гіпохлориту, такого як гіпохлорит або гіпобромід натрію; бромату, такого як бромат натрію; або оксиду третинного органічного аміну, такого як N-метилморфоліноксид або триетиламіноксид, працюючи у водному середовищі або гомогенному або гетерогенному водноорганічному середовищі, такому як суміш води з етилацетатом. Окислення також можна здійснювати за допомогою лише гіпохлориту натрію(жавелевая вода) або перманганату калію або вольфрамату натрію, в присутності окисника, такого як гіпохлорит натрію, пероксид водню, або алкілгідропероксиду. Сполуку загальної формули (VIII) можна також отримати шляхом окислення сполуки загальної формули (VI), де R означає атом водню, в умовах, що описані вище, з подальшим захистом атома азоту отриманого лактаму загальної формули (IX): де: R1’ та R1’’ мають вищевказані значення, за допомогою захисної групи, що вказана вище. Сполуки загальної формули (VIII) є новими продуктами становлять інший об'єкт винаходу. Сполуку загальної формули (VIII) можна перетворювати на загальної формули (V) в умовах, відповідних природі замісника R2, що вводять. Сполуку загальної формули (V), де R2 означає карбоксильний радикал, можна отримати шляхом обробки неорганічною основою, такою як гідроксид натрію, сполуки загальної формули (VIII) з подальшою заміною захисної групи G2 на атом водню та, за необхідності, радикалів R1' та R1’’ на атом водню. Сполуку загальної формули (V), де R2 означає карбоксильний радикал, можна отримати шляхом заміни захисної групи G2 сполуки загальної формули (VIII) на атом водню з подальшою обробкою неорганічною основою, такою як гідроксид натрію та, за необхідності, заміною радикалів R1’ та R1’’ на атом водню. Сполуку загальної формули (V), де R2 означає алкоксикарбонільний радикал, алкільна частина якого містить 1-4 атоми вуглецю, можна отримати, діючи алкоголятом лужного металу на сполуку загальної формули (VIII) з подальшою заміною захисної групи G2 на атом водню та, за необхідності, заміною радикалів R1’ та R1’’ на атом водню. Сполуку загальної формули (V), де R2 означає алкоксикарбонільний радикал, алкільна частина якого містить 1-4 атоми вуглецю, можна отримати шляхом заміни захисної групи G2 сполуки загальної формули (VIII) на атом водню, з подальшою обробкою алкоголятом лужного металу та, за необхідності, заміною радикалів R1’ та R1’’ на атом водню. Сполуку загальної формули (V), де R2 означає N-алкіламінокарбонільний радикал, алкільна частина якого містить 1-4 атоми вуглецю, можна отримати, діючи алкіламіном на сполуку загальної формули (VIII) з подальшою заміною захисної групи G2 на атом водню та, за необхідності, заміною радикалів R1’ та R1’’ на атом водню. Сполуку загальної формули (V), де R2 означає N-алкіламінокарбонільний радикал, алкільна частина якого містить 1-4 атоми вуглецю, можна отримати шляхом заміни захисної групи G2 сполуки загальної формули (VIII) на атом водню, з подальшою обробкою алкіламіном та, за необхідності, заміною радикалів R1’ та R1’’ на атом водню. Сполуку загальної формули (V), де R2 означає гідроксиметильний радикал можна отримати, діючи відновником, таким як боргідрид, наприклад, боргідрит натрію або калію, на сполуку загальної формули (VIII) з подальшою заміною захисної групи G2 на атом водню та, за необхідності, заміною радикалів R1’ та R1’’ на атом водню. Сполуку загальної формули (V), де R: означає гідроксиметильний радикал, можна отримати шляхом заміни захисної групи G2 сполуки загальної формули (VIII) на атом водню, з подальшою обробкою відновником, таким як боргідрид, наприклад, боргідрит натрію або калію, та, за необхідності, заміною радикалів R1’ та R1’’ на атом водню. Сполуку загальної формули (V) можна використовувати в умовах, описаних у патенті US 5364862, для отримання терапевтично активних продуктів. Наступні приклади ілюструють даний винахід. Приклад 1 До колби з трьома шийками ємністю 250см 3, що обладнана холодильником та системою перемішування, в атмосфері аргону вводять розчин 20г(165 моль) a-S-метилбензиламіну в 60см 3 води, значення pH якого доводять до 6,10 шляхом додавання 17см 3 36%-ної(маса/об'єм) соляної кислоти. Після охолодження до температури 5°С додають 20см 3 37%-ного(маса/об'єм) водного розчину формальдегіду. Перемішують протягом 5 хвилин при температурі 5°С, після чого додають 21,8г(330моль) циклопентадієну. Перемішують протягом 16 годин при температурі від -5°С до 0°С. Водну фазу відділяють шляхом декантації, потім промивають, використовуючи 50см 3 пентану. Нейтралізують до рН=8,0, додаючи концентрований розчин гідроксиду натрію. Після цього екстрагують двічі по 70см 3 етилацетатом. Водну фазу доводять до значення рН=11, додаючи концентрований розчин гідроксиду натрію, потім екстрагують двічі по 70см 3 етилацетатом. Органічні фази з'єднують, потім промивають двічі по 50см 3 водою, після чого сушать над сульфатом натрію. Після фільтрування та концентрування досуха при зниженому тиску отримують 33,10г 2-(a-S-метилбензил)-2-азабіцикло[2.2.1]гепт-5-єну у вигляді ледь жовтої олії. До колби з трьома шийками ємністю 500см 3, що обладнана холодильником та системою перемішування, в якій міститься розчин 20г(75,34 моль) 2-(a-S-метилбензил)-2-азабіцикло[2.2.1]гепт-5-єну у 220см 3 трет-бутанолу, додають, при темепратурі блізько 25°С, 12г N-метилморфоліоксиду у 32см 3 води, потім повільно додають ще 6,3см 3 2,50-ного(маса/об'єм) розчину тетроксиду осмію () у трет-бутанолі. Перемішують протягом двох годин, при температурі близько 20°С, потім протягом трьох годин при температурі 65°С. Після випарювання трет-бутанолу при зниженому тиску залишок оброблюють за допомогою 350см 3 ізопропанолу. Після концентрування досуха при зниженому тиску отримують 24г цис5,6-дигідрокси-2-(a-S-метилбензил)-2-азабіцикло [2.2.1]гептану у вигляді олії. Шляхом кристалізації з цеклогексану отримують 14г 5R,6S-дигідрокси-2-(a-S-метилбензил)-2-азабіцикло[2.2.1]гептану, ізомерна чистота якого більше 95%. ЯМР-спектр, що знято в дейтерованому хлороформі, виявляє такі хімічні зсуви (δ): 1,21 (3Н, д); 1,38 (д, 1Н); 1,59 (д, 1Н); 2,22 (м, 2Н); 2,45 (дд, 1Н); 2,95 (1Н, с); 3,39 (к, 1Н); 3,78 (д, 1Н); 3,90 (д, 1Н); 7,28 (5Н, м). Приклад 2 До колби з трьома шийками ємністю 500см 3, що обладнана холодильником та системою перемішування, в якій міститься розчин 18,4г(76 моль) 5R,6S-дигідрокси-2-(a-S-метилбензил)-2-азабіцикло [2.2.1]гептану у 130см 3 толуолу, додають 31,7г 2,2-диметоксипролану(304моль), потім повільно додають 13г(114моль) трифтороцтової кислоти. Суміш нагрівають протягом 4 годин 10 хвилин при температурі 65°С. Після охолодження до 30°С та концентрування у роторному випарювачі для видалення толуолу, надлишку 2,2-диметоксипролану та частково трифтороцтової кислоти, реакційну суміш оброблюють дихлорметаном, потім нейтралізують, додаючи 100см 3 2н розчину гідроксиду натрію. Після декантації, висушування органічної фази над сульфатом натрію, фільтрування, обробки знебарвлюючим вугіллям(30г) протягом 30 хвилин при температурі кипіння зі зворотнім холодильником дихлорметану, фільтр ування на "clarcel" з метою просвітлення та концентрування досуха при зниженому тиску отримують 18,8г 5R,6Sізопропілідендиокси-2-(a-S-метилбензил)-2-азабіцикло[2.2.1]гептану, стр уктура якого підтверджується 1Н ЯМР-спектром, що знято в дейтерохлороформі, який виявляє такі хімічні зсуви (δ): 1,22 (д, 3Н); 1,23 (с, 6Н); 1,31 (д, 1Н); 1,57 (д, 1Н); 2,08 (д, 1Н); 2,34 (уш.с, 1Н); 2,45 (дд, 1Н); 3,06 (с, 1Н); 3,40 (к, 1Н); 4,09 (д, 1Н); 4,19 (д, 1Н); 7,26 (м, 5Н). До колби з трьома шийками ємністю 250см 3, що обладнана системою перемішування, вводять 0,5г 5мас.%-ного паладію-на-вугіллі, 5г 5R,6S-ізопропілідендиокси-2-(a-S-метилбензил)-2-азабіцикло[2.2.1] гептану, 3,98г ди-трет-бутилдикарбонату та 36см 3 метанолу. Апарат продувають аргоном, потім воднем, після чого створюють атмосферу водню при температурі 25°С. Реакцію продовжують проводити протягом 5 годин, здійснюючи подування воднем кожні 15 хвилин, для видалення діоксиду вуглецю, що виділяється. Після фільтрування з метою просвітлення(на саrсеl) та концентрування досуха при зниженому тиску отримують 4,84г 5R,6S-ізопропілідендиокси-2-(трет-бутоксикарбоніл)-2-азабіцикло[2.2.1] гептану, структура якого підтверджується 1Н-ЯМР-слектром, що знято в дейтерованому диметилсульфоксиді, який виявляє такі хімічні зсуви (δ): 1,16 (с, 3Н); 1,28 (с, 3Н); 1,32 (с, 1Н); 1,34 (с, 3Н); 1,65 (д, 1Н); 2,38 (м, 1Н); 2,65 (д, 1Н); 2,99 (м, 1Н); 3,84 (м, 1Н); 3,94 (м, 1Н); 4,16 (д, 1Н). До пробірки ємністю 30см 3 вводять 270мг(1 моль) 5R,6S-ізопропілідендиокси-2-(трет-бутоксикарбоніл)2-азабіцикло[2.2.1] гептану та 40мг(0,3 еквівалента) RuO2×H2O. Додають 10см 3 етилацетату та 720мг(40 еквівалентів) води. Потім додають 2,14г(10 еквівалентів) перйодату натрію, та пробірку герметично закривають. Перемішують протягом 16 годин при температурі 50°С. Реакційну суміш відфільтровують для просвітлення(на cracel), потім екстрагують двічі по 20см 3 етилацетатом. Органічні фази висушують над сульфатом натрію. Після фільтрування та концентрування досуха отримують 245мг твердої речовини, що містить 65% 5R,6S-ізопропілідендиокси-2-(трет-бутоксикарбоніл)-2-азабіцикло[2.2.1]гептан-3-ону та 32% вихідної речовини. Структур у отриманого продукту підтверджено 1Н-ЯМР-спектром, який було знято в дейтерованому диметилсульфоксиді. ЯМР-спектр виявляє такі хімічні зсуви (δ): 1,38 (с, 9Н); 1,23 (с, 3Н); 1,33 (с, 3Н); 1,85 (д, 1Н); 1,93 (д, 1Н); 2,69 (с, 1Н); 4,24 (с, 1Н); 4,41 (д, 1Н); 4,51 (д, 1Н). Приклад 3 До автоклаву ємністю 25см 3, який обладнано магнітною мішалкою, вводять 1,47г 5R,6Sізопропілідендиокси-2-(трет-бутоксикарбоніл)-2-азабіцикло[2.2.1]гептан-3-ону у вигляді розчину в 10см 3 безводного толуолу, потім близько 0,7см 3 етиламіну. Автоклав зачиняють, потім нагрівають при температурі в межах від 90° до 100°С протягом 21 години. Після охолодження толуол випарюють та залишок оброблюють, використовуючи 10см 3 дихлорметану та 10см 3 води. Після декантації органічну фазу промивають 10см 3 води. Поєднані водні шари промивають 10см 3 дихлорметану. Поєднані органічні фази промивають 10см 3 насиченого розчину хлориду натрію, потім висушують над сульфатом натрію. Після фільтрування та концентрування досуха при зниженому тиску отримують 1,58г продукту, що містить 95% 2R,3S-ізопропілідендиокси-4R-трет-бутоксикарбоніламіно-1S-етиламінокарбонілциклопентану, стр уктур у якого підтвердженофіг. 1Н-ЯМР-спектром,що знято в дейтерованому диметилсульфоксиді. Спектр виявляє такі хімічні зсуви (δ): 0,95 (т, 3Н); 1,14 (с, 3Н); 1,31 (с, 12Н); 1,55 (м, 1Н); 2,11 (м, 1Н); 2,64 (м, 1Н); 3,00 (квінтет, 2Н); 3,77 (м, 1Н); 4,23 (м, 1Н); 4,54 (м, 1Н); 7,07 (д, 1Н); 8,12 (т, 1Н). До колби ємністю 25см 3 вводять 1,22г 2R,3S-ізопропілідендиокси-4R-трет-бутоксикарбоніламіно-1Sетиламінокарбонілциклопентану та 10см 3 дихлорметану. При температурі близько 25°С, пермішуючи сусміш магнітною мішалкою, додають 0,85г трфтороцтової кислоти. Після перемішування протягом 6 годин та концентрування досуха отримують 1,16г трифторацетату 2R,3S-ізопропілідендиокси-4R-аміно-1Sетиламінокарбонілциклопентану стр уктуру якого підтверджено 1Н-ЯМР-спектром, що знято в дейтерованому диметилсульфоксиді. Спектр виявляє такі хімічні зсуви (δ): 0,79 (т, 3Н); 1,03 (с, 3Н); 1,19 (с, 3Н); 1,42 (м, 1Н); 2,05 (м, 1Н); 2,52 (м, 1Н); 2,89 (квінтет, 2Н); 3,04 (м, 1Н); 4,16 (м, 1Н). Приклад 4 Розчин 0,5ммоль суміші(78:22 в мольному співвідношенні) 5R,6S-дигідрокси-2-(a-S-метилбензил)-2азабіцикло[2.2.1] гептану та 5S,6R-дигідрокси-2-(a-S-метилбензил)-2-азабіцикло[2.2.1] гептану та 0,5ммоль L-диметоксибурштинової кислоти в 1см 3 ізопропанолу перемішують протягом 24 годин при температурі, що змінюється від початкової 25°С до 57°С. Отримані кристали відфільтровують та висушують. Таким чином отримують 110мг 5R,6S-дигідрокси-2-(a-S-метилбензил)-2-азабіцикло[2.2.1] гептану з енантіомерним надлишком 97%. Суміш(78:22 в мольному співвідношенні) 5R,6S-дигідрокси-2-(a-S-метилбензил)-2азабіцикло[2.2.1]гептану 5S,6R-дигідрокси-2-(a-S-метилбензил)-2-азабіцикло[2.2.1] гептану можна отримати таким чином: До колби з трьома шийками ємністю 250см 3, що обладнано холодильником та системою перемішування, в якій міститься 7г(35моль) 2-(-S-метилбензил)-2-азабіцикло[2.2.1]гепт-5-єну в 70см 3 третбутанолу, при температурі близько 25°С додають 4,12г N-метилморфоліоксиду в 11см 3 води, потім повільно додають 360мкл 2,5%-ного(маса/об'єм) розчину тетроксиду осмію в трет-бутанолі. Перемішують протягом 1 години при температурі близько 20°С, потім протягом 4 годин при 65°С. Після випарювання трет-бутанолу при зниженому тиску залишок оброблюють 150см 3 ізопропанолу. Після концентрування досуха при зниженому тиску отримують 8,27г продукту, Н-ЯМР-спектр якого показує, що його утворено сумішшю(78:22 в мольному співвідношенні) 5R,6S-дигідрокси-2-(-S-метилбензил)-2азабіцикло[2.2.1]гептану та 5S,6R-дигідрокси-2-(-S-метилбензил)-2-азабіцикло[2.2.1]гептану. Приклад 5 До пробірки Бергофа вводять 568мг 5R,6S-ізопропіліндендиокси-2-(трет-бутоксикарбоніл)-2азабіцикло[2.2.1]гептан-3-ону та 10см 3 водного 70мас.%-ного розчину етиламіну. Суміш нагрівають протягом 4 годин при температурі 60°С, перемішуючи. Після охолодження видаляють надлишок триетиламіну та води при зниженому тиску. Таким чином, після висушування при зниженому тиску, отримують 650мг 2R,3S-ізопропілідендиокси-4R-трет-бутоксикарбоніламіно-1S етиламінокарбонілциклопентану, вихід якого становить 98%. Структуру продукту підтверджує Н-ЯМРспектр. Обертальна здатність продукту складає [a]D20 = 15,0°(с=1, метанол). До розчину 200мг 2R,3S-iзoпропілідендиокси-4R-трет-бутоксикарбоніламіно-1Sетиламінокарбонілциклопентану в 1,6см 3 безводного дихлорметану додають 275мкл трифтороцтової кислоти. Суміш перемішують протягом однієї ночі при температурі близько -5°С. Реакційну суміш виливають до 4см 3 2,5н розчину гідроксиду натрію. Органічний шар концентрують при зниженому тиску при температурі нижче 25°С. Таким чином отримують 125мг продукту, який розчиняють в 0,5см 3 тетрагідрофурану. Доцього розчину додають 70мг бензойної кислоти. Внаслідок охолодження отриманого розчину до температури близько 0°С утворюються кристали, які відфільтровують та промивають пентаном. Таким чином отримують 138мг 2R,3S-ізопропілідендиокси-4R-аміно-1Sетиламінокарбонілциклопентанбензоату. Приклад 6 До охолодженого до 0°С розчину 167мг 5R,6S-ізопропіліндендиокси-2-(трет-бутоксикарбоніл)-2азабіцикло[2.2.1]гептан-3-ону в 1см 3 дихлорметану, додають 90мкл трифтороцтової кислоти. Дають температурі підвищитися до 23°С протягом 40 хвилин, потім перемішують суміш протягом 22 годин при цій темепратурі. Знову додають 90мкл трифтороцтової кислоти, потім перемішують суміш протягом 1 години при температурі 23С. Після випарювання при зниженому тиску отримують 123мг 5R,6Sізопропіліндендиокси-2-азабіцикло[2.2.1]гептан-3-ону. Чистоту продукту визначають шляхом високоефективної рідинної хроматографії вона бизька до 92%. Структур у продукту підтверджують 1Н-ЯМРспектром. Розчин 10г 5R,6S-ізопропіліндендиокси-2-азабіцикло[2.2.1]гептан-3-ону в 100см 3 водного 70%-ного(за масою) розчину триетиламіну нагрівають протягом 20 годин при температурі 110°С при тиску, що створюється під час цього процесу. Після охолодження надлишок триетиламіну видаляють при зниженому тиску, потім залишок промивають дихлорметаном з метою видалення вихідної речовини, що не прореагувала. Водний шар концентрують та висушують. Таким чином отримують 10,54г 2R,3Sізопропілідендиокси-4R-аміно-1S-етиламіно-карбонілциклопентан-бензоату.
ДивитисяДодаткова інформація
Назва патенту англійською2-azabicyclo[2.2.1]heptane derivatives and a method for preparing the same
Назва патенту російськоюПроизводные 2-азабицикло[2.2.1]гептана и способ их получения
МПК / Мітки
МПК: C07D 471/08
Мітки: похідні, спосіб, одержання, 2-азабіцикло[2.2.1]гептану
Код посилання
<a href="https://ua.patents.su/6-64695-pokhidni-2-azabiciklo221geptanu-ta-sposib-kh-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">Похідні 2-азабіцикло[2.2.1]гептану та спосіб їх одержання</a>
Попередній патент: Еластомерна композиція, суміш для її виготовлення, спосіб її одержання, виріб на її основі
Наступний патент: Ензим, здатний до деградування рамногалактуронану ii та його похідних, способи одержання цього ензиму і рамногалактуронану ii
Випадковий патент: Опорний вузол підйомно-транспортного засобу