Кристалічна основа циталопраму
Номер патенту: 74360
Опубліковано: 15.12.2005
Автори: Бьогесьо Клаус Петер, Петерсен Ханс, Хольм Пер
Формула / Реферат
1. Спосіб одержання солі циталопраму, який відрізняється тим, що основу циталопраму вивільнюють і осаджують у кристалічній формі з розчинника, а після цього відділяють від розчинника та необов'язково перекристалізовують один або більше разів і потім перетворюють у вищевказану сіль.
2. Спосіб за п. 1, який відрізняється тим, що основу циталопраму вивільнюють з неочищеної солі або неочищеної суміші циталопраму.
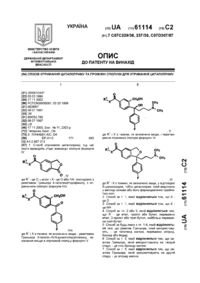
3. Спосіб одержання основи циталопраму або солі циталопраму, який відрізняється тим, що одну або більше домішок формули
,
де Z являє собою галоген, -О-SО2-(СF2)n-СF3, де n дорівнює 0 - 8, -СНО, -NНR1,
-СООR2, -СОNR2R3, де R2 і R3 є вибраними з водню, алкілу, заміщеногоабо незаміщеного арилу або аралкілу, і R1 являє собою водень або алкілкарбоніл, видаляють з неочищеної суміші циталопраму або з неочищеної солі циталопраму осаджуванням основи циталопраму в кристалічній формі, необов'язково перекристалізацією зазначеної основи один або більше разів та/або її перетворенням в вищевказану сіль.
4. Спосіб за п. 3, в якому неочищену суміш циталопраму, яка містить сполуку за формулою II як домішку, одержують шляхом реакції ціанідного обміну сполуки формули II із джерелом ціаніду.
5. Спосіб за п. 3, де Z являє собою галоген, зокрема бром або хлор.
6. Спосіб за будь-яким з пп. 3 - 5, де неочищену суміш циталопраму піддають первісному очищенню перед тим, як основу циталопраму осаджують у кристалічній формі.
7. Спосіб за будь-яким з пп. 3 - 5, де неочищену суміш циталопраму піддають первісному очищенню перед тим, як із зазначеної неочищеної суміші одержують неочищену сіль.
8. Спосіб за будь-яким з пп. 3 - 7, де основу циталопраму вивільнюють з неочищеної солі або неочищеної суміші циталопраму шляхом обробки основою і, необов'язково, піддають додатковому очищенню перед тим, як основу циталопраму осаджують у кристалічній формі.
9. Спосіб за будь-яким з пп. 1 - 8, який відрізняється тим, що основу циталопраму перетворюють у гідробромідну або гідрохлоридну сіль циталопраму.
10. Спосіб за будь-яким з пп. 2, 3, який відрізняється тим, що неочищена сіль являє собою гідробромідну, гідрохлоридну, сульфатну, оксалатну, фосфатну або нітратну сіль.
Текст
Цей винахід відноситься до способів одержання добре відомого антидепресивного лікарського засобу циталопраму, 1-[3-(диметиламіно)пропіл]-1-(4-фторфеніл)-1,3-дигідро-5-ізобензофуранкарбонітрилу, та очищених солей циталопраму, таких як гідробромід. Циталопрам є добре відомим антидепресивним лікарським засобом, що є у продажу вже протягом декількох років і має наступну стр уктуру: Він є селективним, що впливає на центральну нервову систему, інгібітором зворотного захоплення серотоніну (5-гідрокситриптаміну; 5-НТ) і, відповідно, виявляє антидепресивну активність. Про антидепресивну активність даної сполуки повідомлялося в ряді публікацій, наприклад, J. Hyttel, Prog. NeuroPsychopharmacol. & Biol. Psychiat, 1982, 6, 277-295 та A. Gravem, Ada Psychiatr. Scand., 1987, 75, 478-486. Зазначену сполуку додатково розкрито у ЕР-А474580, де описується її дія при лікуванні деменції та цереброваскулярних розладів. Циталопрам був уперше розкритий у DE 2657013, що відповідає US 4 136 193. Зазначена патентна публікація описує одержання циталопраму одним із способів і надає у загальних рисах інший метод, який може використовуватися для одержання циталопраму. Одержаний циталопрам виділяють у виді оксалатної, гідробромідної та гідрохлоридної солі, відповідно. Крім того, основа циталопраму одержана у вигляді олії (В.Р. 175°С/0,03мм рт. ст.). Циталопрам продається у виді гідроброміду та гідро хлориду, відповідно. Був описаний ряд способів одержання циталопраму. У багатьох з них остання стадія є перетворенням групи, відмінної від ціано, у 5 положенні прямого аналога циталопраму на 5-ціаногрупу. Так циталопрам був одержаний: заміною 5-галогену або 5-CF3-(CF2)n-SO 2-O- на ціано (DE 2657013 і WO 00/11926 і WO 00/13648, які знаходяться на одночасному розгляді з цією заявкою), перетворенням 5-амідо- або 5-складноефірної групи в 5-ціаногрупу (WO 98/19513), перетворенням 5-аміногрупи в 5-ціаногрупу (WO 98/19512), перетворенням 5-формільної групи в 5-ціаногрупу (WO 99/00548), перетворенням 5-оксазолінільної або 5-тіазолінільної групи в 5-ціаногрупу (WO 00/23431). Інші способи одержання циталопраму включають заміну 5-бромогрупи 1-(4-фторфеніл)-1,3-дигідро-5ізобензофуранброміду на 5-ціано з наступним алкілуванням 3-(М,М-диметиламіно)пропілгалогенідом (DE 2657013 і WO 98/19511). Багато які зі способів, зазначених вище, мають той недолік, що важко відокремити проміжні сполуки, які утворилися в процесі (проміжні сполуки, зазначені вище, або попередні проміжні сполуки), від кінцевого продукту, і, відповідно, необхідні обширні процедури очищення, зв'язані з втратами циталопраму, для одержання кінцевого продукту необхідної якості. В наш час виявлено, що основа циталопраму може бути одержана у виді дуже тонкого і чистого кристалічного продукту, з яким можна легко мати справу, та з якого можна легко виготовити таблетки та інші фармацевтичні лікарські форми. Крім того, несподівано було виявлено, що дуже гарне й ефективне очищення І циталопраму може бути здійснено в процесі виробництва циталопраму (наприклад, гідробромідної або гідрохлоридної солі) шляхом кристалізації основи і наступного необов'язкового одержання солі даної основи. Спосіб очищення є особливо корисним для видалення проміжних сполук, які структурно близькі до циталопраму, зокрема, сполук, які відрізняються від циталопраму замісником, який знаходиться в положенні 5 ізобензофуранового кільця, і проміжних сполук, що мають фізичні/хімічні властивості, які близькі властивостям циталопраму, наприклад, 1-[3-(диметиламіно)пропіл]-1-(4-фторфеніл)-1,3дигідроізобензофуранів, які містять галоген (наприклад, бром і хлор), амід або складний ефір у положенні 5 ізобензофуранового кільця, або 1-(4-фторфеніл)-1,3-дигідро-5-ізобензофуранброміду або -хлориду. Цей винахід відноситься до способу одержання кристалічної основи сполуки В другому аспекті цей винахід відноситься до способу одержання солі циталопраму, переважно, гідроброміду або гідрохлориду, в якому вільну основу циталопраму осаджують у кристалічній формі, необов'язково перекристалізовують один або більше разів і потім перетворюють у фармацевтично прийнятну сіль циталопраму. Зокрема, цей винахід відноситься до способу одержання солі циталопраму, який характеризується тим, що основу циталопраму вивільнюють й осаджують у кристалічній формі з розчинника, а після цього відділяють від розчинника та необов'язково перекристалізовують один або більше разів і потім перетворюють у вищевказану сіль. Зокрема, цей винахід відноситься до способу одержання солі циталопраму, який характеризується тим, що основу циталопраму вивільнюють з неочищеної солі або неочищеної суміші циталопраму. Більш конкретно, цей винахід відноситься до способу одержання основи циталопраму або солі циталопраму, який характеризується тим, що одну або більше домішок формули де Ζ являє собою галоген, -O-SO2-(CF 2)n-CF3, де n дорівнює 0-8, -СНО, -NHR1, -COOR 2, -CONR2R3, де R і R3 є вибраними з водню, алкілу, необов'язково заміщеного арилу або аралкілу, і R 1 являє собою водень або алкілкарбоніл, видаляють з неочищеної суміші циталопраму або з неочищеної солі циталопраму осаджуванням основи циталопраму в кристалічній формі, необов'язково перекристалізацією зазначеної основи один або більше разів та/або перетворенням зазначеної основи у вище вказану сіль. Неочищена суміш циталопраму, яка містить сполуку за формулою II як домішку, може бути одержана, піддаючи сполуку формули II реакції ціанідного обміну з джерелом ціаніду, або піддаючи 1-(4-фторфеніл)1,3-дигідро-5-ізобензофурангалогенід, зокрема бромід, реакції ціанідного обміну з наступним алкілуванням 3-(N,N-диметиламіно)пропілгалогенідом. В конкретному варіанті здійснення цього винаходу Ζ являє собою галоген, зокрема, бром або хлор. В особливо кращому варіанті здійснення цього винаходу одержана сіль є гідробромідною або гідрохлоридною сіллю циталопраму. Неочищена сіль може бути будь-якою придатною сіллю, такою як гідробромід, гідрохлорид, сульфат, оксалат, фосфат, нітрат або будь-яка інша придатна сіль. Інші солі являють собою солі органічних кислот. В кращому варіанті здійснення цього винаходу неочищена сіль є сульфатною, гідробромідною або гідрохлоридною сіллю. Вільну основу циталопраму або гідробромід або гідрохлорид, одержаний з зазначеної основи, можна застосовувати у фармацевтичних препаратах. Переважно препарат призначений для перорального введення. Препарати за цим винаходом можуть бути одержані безпосереднім пресуванням циталопраму в суміші зі звичайними ад'ювантами або розріджувачами. Альтернативно для пресування таблеток може використовува тися гранулят циталопраму, виготовлений за способом волого гранулювання, або гранулят циталопраму, виготовлений за способом гранулювання з розплавлюванням, необов'язково в суміші зі звичайними ад'ювантами або розріджувачами. Конкретно, фармацевтична композиція за цим винаходом містить рацемічну суміш основи циталопраму, гідрохлориду циталопраму або гідроброміду циталопраму. Чистота кристалічної основи циталопраму складає переважно більш ніж 99,8% мас/мас, найбільш переважно більш ніж 99,9% мас/мас, (площа піка). Температура плавлення переважно знаходиться в межах 90-93°С, найбільш переважно 91-92°С (ДСК початок, відкрита капсула) або вона знаходиться між 92 і 94°С, переважно між 92,5 і 93,5°С (ДСК початок, закрита капсула). Кристалічна основа циталопраму знаходиться переважно у рацемічній формі. Терміни "неочищена сіль" і "неочищена суміш" відносяться до того факту, що дана сіль і дана суміш, відповідно, містять домішки, зокрема домішки за формулою II, які повинні бути видалені або які бажано видалити. Неочищена сіль може бути сіллю, виділеною безпосередньо з реакційної суміші, або неочищену реакційну суміш можна піддати деякому первісному очищенню, наприклад одній перекристалізації, та/або обробці активованим вугіллям або силікагелем, і потім одержати сіль шляхом взаємодії з кислотою, використовуючи методи, відомі фахівцям. Сіль може бути виділена осадженням або вона може існувати в розчині, наприклад у суміші, одержаній безпосередньо при синтезі солі. Подібним же чином неочищену суміш, яка містить циталопрам, можна одержати безпосередньо при синтезі сполуки за будь-яким з вищенаведених способів, або її можна піддати деякому первісному або одночасному очищенню, наприклад, одній перекристалізації, обробці активованим вугіллям або силікагелем. Основу циталопраму можна виділити з неочищеної солі у вільному виді шляхом розчинення неочищеної солі в суміші води й органічного розчинника і наступним додаванням основи. Органічний розчинник може бути толуолом, етилацетатом або будь-яким іншим придатним розчинником, а основа може бути будь-якою придатною основою, переважно NaOH або NH3. Подібним же чином основу циталопраму можна, якщо необхідно, одержати у вільному виді з неочищеної суміші, що містить циталопрам, шляхом обробки основою. Неочищені суміші, які містять основу циталопраму, можна піддати додатковому очищенню й екстрагуванню перед осадженням основи в кристалічній формі. Основа циталопраму може бути виділена відокремленням органічної фази, випарюванням розчинника для одержання основи, найбільш імовірно, у вигляді олії й, потім, кристалізацією основи з апротонного розчинника, такого як алкан, включаючи н-гептан, гексан й ізооктан, і петролейні ефіри з низькою і високою температурою кипіння, і заміщені ароматичні речовини, включаючи толуол і ксилоли. Кристалічна основа циталопраму може бути перекристалізована з тих же розчинників. Фармацевтично прийнятна сіль циталопраму, така як гідробромід або гідрохлорид, може бути одержана за методами, відомими фахівцям. Так, основу піддають реакції або з розрахованою кількістю кислоти в розчиннику, який змішується з водою, такому як ацетон або етанол, з наступним виділенням солі концентруванням і охолодженням, або з надлишком кислоти в розчиннику, який не змішується з водою, такому як етиловий ефір, етилацетат або дихлорометан, при цьому виділення солі здійснюється спонтанно. Гідробромід і гідрохлорид циталопраму, які одержані за способом згідно з цим винаходом, мають дуже високу чистоту, переважно більш ніж 99,8%, найбільш переважно більш ніж 99,9%. Інші солі циталопраму, наприклад оксалат, також можуть бути одержані в дуже чистому виді за цим способом. Реакції ціанідного обміну, зазначені вище, можуть бути проведені так, як описано в заявках на патент, зазначених ви ще. 2 Зокрема, коли Ζ являє собою галоген або CF3-(CF2)n-SO2-O-, де n є цілим числом у межах 0-8, включно, перетворення в ціаногрупу може проводитися шляхом взаємодії з джерелом ціаніду, наприклад, KCN, NaCN, CuCN, Zn(CN)2 або (R4)4NCN, де R4 позначає чотири групи, які можуть бути однаковими або різними й обрані з водню і алкілу з прямим або розгалуженим ланцюгом, у присутності паладієвого каталізатора і каталітичної кількості Сu+ або Zn2+, або з Zn(CN)2 у присутності паладієвого каталізатора. Джерело ціаніду використовується в сте хіометричній кількості або в надлишку, переважно використовуються 1-2 еквіваленти на еквівалент початкового матеріалу. R4N+ може, відповідно, бути (Bu)4N+. Ціанідна сполука, переважно, є NaCN, або KCN, або Zn(CN)2. Паладієвий каталізатор може бути будь-яким придатним каталізатором, який містить Pd(O) або Pd(ll), таким як Pd(PPh3)4, Pd2(dba)3, Pd(PPh)2CI2 тощо. Pd-каталізатор зручно використовувати в кількості 1-10, переважно 2-6, найбільш переважно приблизно 4-5моль%. Каталітичні кількості Сu+ і Zn2+, відповідно, означають субсте хіометричні кількості, такі як 0,1-5, переважно 1-3%. Зручно використовувати приблизно 0,5екв. на екв. Pd. Може використовуватися будь-яке придатне джерело Сu+ і Zn++. Cu+ переважно використовується у виді Cul, і Zn2+ звичайно використовують у виді солі Zn(CN)2. Коли Ζ являє собою Вr або І, тоді перетворення в ціаногрупу може бути також здійснено шляхом взаємодії із Cu(CN) без використання каталізатора. При кращому здійсненні реакцію проводять при підвищеній температурі. В іншому аспекті цього винаходу взаємодію проводять в іонній рідині загальної формули (R5)4N+X-, де 5 R являє собою алкільні групи, або дві з R5 гр уп разом утворюють кільце, і X- являє собою протиіон. В одному з варіантів здійснення цього винаходу (R5)4N+ X- являє собою В іншому конкретному аспекті реакцію проводять у аполярних розчинниках, таких як бензол, ксилол або мезитилен, і під впливом мікрохвильового випромінювання, наприклад застосовуючи прилад Synthewave 1000™, Prolabo. У конкретному аспекті реакцію здійснюють без додавання розчинника. Температурні інтервали залежать від типу реакції. Якщо каталізатор не є присутнім, кращі температури знаходяться в інтервалі 100-200°С. Однак, коли реакцію проводять під впливом мікрохвильового випромінювання, температура в реакційній суміші може підніматися вище 300°С. Більш кращі температурні інтервали знаходяться між 120-170°С. Найбільш кращий інтервал складає 130-150°С. Якщо є присутнім каталізатор, тоді кращий інтервал температур знаходиться між 0 і 100°С. Більш кращими є температури в інтервалі 40-90°С. Найбільш кращими є температури в інтервалі 60-90°С. Інші реакційні умови, розчинники тощо є звичайними умовами для таких реакцій і можуть бути легко встановлені досвідченими фахівцями. Коли Ζ являє собою СІ або Вr, тоді перетворення в ціаногрупу може також проводитися взаємодією з джерелом ціаніду, наприклад, KCN, NaCN, CuCN, Zn(CN)2 або (R4)4NCN, де (R4)4 позначає чотири групи, які можуть бути однаковими або різними і обрані з водню й алкілу з прямим або розгалуженим ланцюгом, у присутності нікелевого каталізатора. Нікелевий каталізатор може бути будь-яким придатним комплексом, який містить Ni(0) або Ni(ll), що діє як каталізатор, таким як Ni(РРh3)3, (s-арил)-Ni(PPh3)2CI тощо. Нікелеві каталізатори та їх одержання описані в WO96/11906, ЕР-А-613720 або ЕР-А-384392. В одному з варіантів здійснення цього винаходу реакцію проводять у присутності каталітичної кількості Сu+ або Zn2+. В особливо кращому варіанті здійснення комплекс нікелю(О) одержують in situ перед реакцією ціанування шляхом відновлення джерела нікелю(ІІ), такого як NiCI2 або NiBr2, металом, таким як Zn, магній або марганець, у присутності надлишку комплексоутворюючи х лігандів, переважно трифенілфосфіну. Ni-каталізатор зручно використовувати в кількості 0,5-10, переважно 2-6, найбільш переважно приблизно 4-5 моль%. Каталітичні кількості Сu+ і Zn2+, відповідно, означають субстехіометричні кількості, такі як 0,1 - 5, переважно 1-3%. Можна використовувати будь-яке придатне джерело Сu+ і Zn2+. Cu+ переважно використовують у виді Cul, a Zn2+ зручно використовувати у виді солі Zn(CN)2, або його утворюють in situ шляхом відновлення сполук нікелю(ІІ), використовуючи цинк. Ni-каталізатори являють собою, наприклад, Ni(0), Pd(0) або Pd(ll) каталізатори, що описані Sakakibara et al. у Bull. Chem. Soc. Jpn., 61, 1985-1990, (1988). Кращими каталізаторами є Ni(PPh3)3 або Pd(PPh3)4 або Pd(PPh)2CI2. Реакції здійснюють у будь-якому придатному розчиннику так, як описано в Sakakibara et al. у Bull. Chem. Soc. Jpn., 61, 1985-1990, (1988). Кращими розчинниками є ацетонітрил, етилацетат, ТГФ, ДМФ або Ν-ΜΠ (Nметилпіролідон). Коли Ζ являє собою СНО, тоді перетворення ціаногрупи може здійснюватися шляхом перетворення формільної групи в оксим або подібну групу шляхом взаємодії з реагентом R 6-V-NH2, де R6 являє собою водень, необов'язково заміщений алкіл, арил або гетероарил, і V являє собою О, N або S, з наступною дегідратацією за допомогою звичайного дегідратуючого агента, наприклад, тіонілхлориду, оцтового ангідриду/піридину, піридину/НСІ або пентахлориду фосфор у. Кра щі реагенти R6-V-NH2 являють собою гідроксиламін і сполуки, де R6 являє собою алкіл або арил, і V являє собою N або О. Коли Ζ являє собою -СООН, тоді перетворення в ціаногрупу може бути здійснено через відповідний хлорангідрид кислоти, складний ефір або амід. Хлорангідрид кислоти зручно одержувати обробкою кислоти РОСІ3, РСІ5 або SOCl2, без розчинника або в придатному розчиннику, такому як толуол або толуол, який містить каталітичну кількість Ν,Νдиметилформаміду. Складний ефір одержують обробкою кислоти спиртом у присутності кислоти, переважно мінеральної кислоти або кислоти Льюїса, такої як НСІ, H2SO4, РОСl3, РСІ5 або SOCl2 Альтернативно, складний ефір може бути одержаний із хлорангідриду кислоти взаємодією зі спиртом. Складний ефір або хлорангідрид кислоти потім перетворюють в амід шляхом амідування аміаком або алкіламіном, переважно трет-бутиламіном. Перетворення в амід також може бути здійснено шляхом взаємодії складного ефіру з аміаком або алкіламіном під тиском і при нагріванні. Амідну гр упу потім перетворюють у ціаногрупу дегідруванням. Дегідратуючим агентом може бути будьякий придатний дегідратуючий агент, і оптимальний агент може бути легко визначений фахівцем у даній галузі. Прикладами придатних дегідратуючи х а гентів є SOCl2, РОСІ 3 і РСІ 5, переважно SOCI2. В особливо кращому варіанті здійснення карбонову кислоту піддають взаємодії зі спиртом, переважно етанолом, у присутності РОСІ3 для одержання відповідного складного ефіру, який потім піддають взаємодії з аміаком з одержанням у такий спосіб відповідного аміду, який, у свою чергу, піддають взаємодії з SOCl2 у толуолі, який містить каталітичну кількість Ν,Ν-диметилформаміду. Альтернативно, сполука, де Ζ являє собою -СООН, може взаємодіяти з хлорсуль фонілізоціанатом з утворенням нітрилу або оброблятися дегідратуючим агентом і сульфонамідом. Коли Ζ являє собою -NHR1, де R1 являє собою водень, тоді перетворення в ціано переважно здійснюють діазотуванням і наступною взаємодією із CN-. Найбільш краще використовувати NaNO2 і CuCN і/або NaCN. Коли R1 являє собою алкілкарбоніл, тоді його спочатку піддають гідролізу з одержанням у такий спосіб відповідної сполуки, де R1 являє собою Н, яку потім перетворюють так, як описано вище. Гідроліз може проводитися або в кислому, або в лужному середовищі. Сполуки формули (II) можуть бути одержані так, як описано в DE 2657013, WO 00/11926 і WO 00/13648, WO 98/19513, WO 98/19512 і WO 99/00548. У цьому описі й формулі винаходу "галоген" означає хлор, бром або йод. В описі та формулі винаходу термін "алкіл" відноситься до розгалуженої або нерозгалуженої алкільної групи, такої як метил, етил, 1-пропіл, 2-пропіл, 1-бутил, 2-бутил, 2-метил-2-пропіл і 2-метил-1-пропіл. Термін "арил" відноситься до карбоциклічної ароматичної групи, зокрема фенілу. Термін "аралкіл" відноситься до аралкільної групи, де арил і алкіл є такими, як визначено вище. Арильні й аралкільні групи можуть бути необов'язково заміщені, наприклад алкільними групами, утворюючи, наприклад, толіл. Фармацевтичні композиції за цим винаходом можна вводити будь-яким придатним шляхом і в будь-якій придатній формі, наприклад, перорально у виді таблеток, капсул, порошків або сиропів, або парентерально у виді звичайних стерильних розчинів для ін'єкцій. Переважно фармацевтичні композиції за цим винаходом вводять перорально. Фармацевтичні форми за винаходом можуть бути приготовлені за звичайними способами відомими в практиці. Наприклад, таблетки можуть бути приготовлені змішанням активних інгредієнтів зі звичайними ад'ювантами та/або розріджувачами і наступним пресуванням суміші в звичайній таблетувальній машині. Приклади ад'ювантів або розріджувачів включають кукурудзяний крохмаль, картопляний крохмаль, тальк, стеарат магнію, желатин, лактозу, смоли тощо. Будь-які інші ад'юванти або добавки, барвники, ароматизатори, консерванти можуть використовуватися за умови їхньої сумісності з активними інгредієнтами. Зокрема, препарати за цим винаходом можуть бути виготовлені безпосереднім пресуванням циталопраму в суміші зі звичайними ад'ювантами або розріджувачами. Альтернативно, для пресування таблеток може використовуватися гранулят циталопраму, виготовлений за способом волого гранулювання, або гранулят циталопраму, виготовлений за способом гранулювання з розплавлюванням, необов'язково в суміші зі звичайними ад'ювантами або розріджувачами. Розчини для ін'єкцій можуть бути приготовлені розчиненням активного інгредієнта і можливих добавок у частині розчинника для ін'єкцій, переважно стерильної води, доведенням розчину до потрібного об'єму, стерилізацією розчину і заповненням їм придатних ампул або пляшечок. Можуть бути додані будь-які придатні добавки, звичайно використовувані в даній галузі, такі як засоби для досягнення ізотонічності, консерванти, антиоксиданти тощо. Відповідно до цього винаходу основа циталопраму, як було виявлено, є кристалічною речовиною зі стабільними і тонкими білими кристалами, і було виявлено, що основа може легко кристалізуватися в дуже чистій формі. Так, наприклад, основа циталопраму з чистотою більш ніж 99,8% мас/мас, була одержана кристалізацією з гідроброміду з чистотою до 95% без додаткового очищення. Відповідно, спосіб одержання солей циталопраму за винаходом, як було виявлено, дає солі у виді дуже чистих продуктів фармацевтично прийнятної якості. Відповідно, може бути істотно поліпшено вихід при виробництві циталопраму. І, нарешті, було виявлено, що з кристалічною основою циталопраму можуть бути одержані дуже гарні стійкі тверді препарати з гарними властивостями вивільнення. Цей винахід додатково ілюструється наступними прикладами. Приклад 1 Кристалізація R,S-циталопраму у виді вільної основи 1-(3-Диметиламінопропіл)-1-(4'-фторфеніл)-1,3-дигідробензофуран-5-карбонітрил Гідробромід 1-(3-диметиламінопропіл)-1-(4'-фторфеніл)-1,3-дигідробензофуран-5-карбонітрилу (101г, 0,25 моль), одержаний з 1-(3-диметиламінопропіл)-1-(4-фторфеніл)-1,3-дигідро-5-ізобензофуранброміду, суспендують у воді (500мл) і толуолі (500мл). Додають NaOH (60мл, 5N (водн.)) і суміш (рН>10) перемішують протягом 15 хвилин, потім фази розділяють. Органічну фазу промивають водою (2x100мл) і фільтрують крізь шар фільтруючого засобу. Леткі речовини видаляють у вакуумі і сполуку, зазначену в заголовку, одержують у вигляді олії. Додають н-гептан (400мл) і суміш нагрівають до 70°С. Після охолодження утворюються кристали. Білі кристали сполуки, зазначеної в заголовку, відфільтровують і сушать при кімнатній температурі протягом ночі у вакуумі. Вихід: 75,4г (93%). ДСК (початок, відкрита капсула): 91,3-91,8°С; ДСК (початок, закрита капсула): 92,8°С. Чистота: (>99,8% (площа піка)). Анал.: обчислено для C20H21N2F 1O1 ; С 74,04; Η 6,54; Ν 8,64. Знайдено С 74,01; Η 6,49; Ν 8,59. 1Н-ЯМР (ДMCO-d6 , 500МГц): 1,21 (1H, м), 1,29 (1Н, м), 2,02 (6Н, с), 2,09-2,23 (4Н, м), 5,15 (1Н, д J=12,5Гц), 5,22 (1Н, д J=12,5Гц), 7,16 (2Н, т J=8,5Гц), 7,60 (2Н, дт J=8,5Гц J=1,2Гц), 7,76 (1Н, д J=8,5Гц), 7,79 (1Н, д J=8,5Гц), 7,80 (1Н, с). 13С-ЯМР (ДMCO-d6, 125МГц): 21,8, 38,3, 45,0, 58,8, 71,0, 90,7, 110,5, 115,1 (д J=22Гц), 118,8, 123,1,125,1, 127,0 (д J=8Гц), 132,0, 140,0 (д J=3Гц), 140,5, 149,5, 161,3 (д J=245Гц). Приклад 2 а) Неочищену суміш циталопраму і сірчаної кислоти підлужують додаванням NaOH і основу циталопраму екстрагують толуолом. Толуол випарюють і одержану основу циталопраму розчиняють у нгептані при підвищеній температурі. Дуже чисту вільну основу циталопраму осаджують шляхом охолодження. b) Неочищену суміш циталопраму і сірчаної кислоти підлужують додаванням NaOH і основу циталопраму екстрагують толуолом. Толуол випарюють і одержану основу циталопраму розчиняють у метанолі. Суміш обробляють активованим вугіллям і фільтрують,, а розчинник випарюють. Очищену вільну основу розчиняють у н-гептані при підвищеній температурі. Потім дуже чисту основу циталопраму осаджують охолодженням. c) Неочищену суміш циталопраму і сірчаної кислоти підлужують додаванням NaOH і основу циталопраму екстрагують толуолом. Толуольну фазу обробляють силікагелем, толуол випарюють і одержану основу циталопраму розчиняють у н-гептані при підвищеній температурі. Дуже чисту вільну основу циталопраму осаджують шляхом охолодження. d) Неочищену суміш циталопраму і сірчаної кислоти підлужують додаванням NaOH і основу циталопраму екстрагують толуолом. Толуольну фазу обробляють силікагелем, толуол випарюють і одержану основу циталопраму розчиняють у метанолі. Суміш обробляють активованим вугіллям і фільтрують, а розчинник випарюють. Очищену вільну основу розчиняють у н-гептані при підвищеній температурі. Потім надзвичайно чисту вільну основу циталопраму осаджують охолодженням. Приклад 3 Вологе гранулювання і виготовлення таблеток Розмір завантаження складав 200г, і гранулювання здійснювали в маломасштабному лабораторному змішувачі з високим зусиллям зсуву (Micromixer). Основу циталопраму просівали крізь сито з отворами 0,3мм. Інгредієнти внутрішньогранульної фази (14 у таблиці 1) змішували при 600об/хв. Додавали 25мл очищеної води (5) протягом 30 секунд і гранулювання припиняли після загального часу обробки у 3 хвилини. Гранулят у вологому стані просівали крізь сито з отворами 0,7мм і сушили при 40°С протягом 30 хвилин до рівноважної відносної вологості у 32%. Висушений гранулят остаточно просівали крізь сито з отворами 0,7мм. Висушений гранулят змішували протягом 3 хвилин з екстрагранульною фазою (6-7) у змішувачі Turbula і наприкінці змішували зі змащувальною речовиною (8) протягом 30сек. Таблиця 1 Композиція для таблеток 1 2 3 4 5 6 7 8 Матеріали Циталопрам (основа) Колідон VA64 Лактоза, 350 меш Кукур удзяний крохмаль Очищена вода Авісел РН 200 (мікрокристалічна целюлоза) Ac-Di-Sol (натрієва сіль кроскармелози) Стеарат магнію % 16,00 2,32 38,98 20,00 25 20,00 2,00 0,7 Таблетки виготовляли на таблетувальній машині з одним пуансоном Korsch ЕКО. Характеристики таблеток показані в таблиці 2. Таблиця 2 Характеристики таблеток Параметр Вміст активної речовини в таблетці, мг Номінальна вага таблетки, мг Діаметр таблетки,мм Форма таблетки Середній час розпаду, хв. Середня міцність до роздавлювання, Η Середня вага таблетки, мг RSD ваги таблетки, % Ламкість, % Значення 20 125 7 з плівковим покриттям (спеціального призначення) 1,77 69,1 125,4 0,42 0,3 Виготовлені таблетки мали задовільні технічні властивості. Приклад 4 Гранулювання з розплавлюванням Розмір завантаження складав 200г. Основу циталопраму просівали крізь сито з отворами 0,3мм. Гранулювання здійснювали в маломасштабному лабораторному змішувачі з високим зусиллям зсуву (Micromixer). Інгредієнти внутрішньогранульної фази (1-3 у таблиці 3) перемішували при 1200об/хв. Температура сорочки складала 80°С. Процес гранулювання припиняли через 3,5 хвилини. Гранулят просівали крізь сито з отворами 1,0мм і перемішували з екстрагранульною фазою (4, 5) протягом 3 хвилин і зі змащувальною речовиною (6) протягом 30сек. Таблиця 3 Композиція таблетки 1 2 3 4 5 6 Матеріали Циталопрам (основа) Поліетиленгліколь 6000 Лактоза, 350меш Авісел РН 200 (мікрокристалічна целюлоза) Колідон CL (структурований повідон) Магнію стеарат % 16,00 9,14 38,98 30,00 4,00 0,7 Таблетки виготовляли на таблетувальній машині Korsch EK0. Характеристики таблеток представлені в таблиці 4. Таблиця 4 Характеристики таблеток Параметр Вміст активної речовини в таблетці, мг Номінальна вага таблетки, мг Діаметр таблетки,мм Форма таблетки Середній час розпаду, хв. Середня міцність до роздавлювання, Η Середня вага таблетки, мг RSD ваги таблетки, % Ламкість, % Значення 20 125 7 з плівковим покриттям, спеціального призначення 1,0 55,5 125,6 0,5 0,4 Виготовлені таблетки мали задовільні технічні властивості.
ДивитисяДодаткова інформація
Назва патенту англійськоюA crystalline base of citalopram
Автори англійськоюPetersen Hans, Bogeso, Klaus, Peter, Holm, Per
Назва патенту російськоюКристаллическая основа циталопрама
Автори російськоюПетерсен Ханс
МПК / Мітки
МПК: C07D 307/87, A61P 25/24
Мітки: циталопраму, основа, кристалічна
Код посилання
<a href="https://ua.patents.su/6-74360-kristalichna-osnova-citalopramu.html" target="_blank" rel="follow" title="База патентів України">Кристалічна основа циталопраму</a>
Попередній патент: Абсорбер із внутрішнім випарним охолодженням
Наступний патент: Фармацевтично активні похідні піролідину
Випадковий патент: Механізм фіксації шнурів підйому горизонтальних світлозахисних жалюзі