Фармацевтично активні похідні піролідину
Номер патенту: 74362
Опубліковано: 15.12.2005
Автори: Томас Рассел, Шеер Александер, Шварц Маттіас, Бакстер Ентоні, Халазі Серж, Куаттропані Анна
Формула / Реферат
1. Похідні піролідину формули І
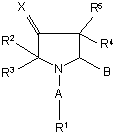 , І
, І
а також їхні геометричні ізомери, їхні оптично активні форми як енантіомери, діастереомери та їхні рацематні форми, а також їхні фармацевтично прийнятні солі, де
Χ вибирають із групи, до складу якої входять CR6R7, NOR6, NNR6R7;
А вибирають із групи, до складу якої входять -(С=O)-, -(С=O)-O-, -C(=NH)-, -(C=O)-NH-, (C=S)-NH, -SO2-, -SO2NH-, -СН2-,
В або є групою -(C=O)-NR8R9, або являє собою гетероциклічний залишок, який має формулу
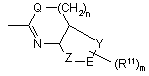 ,
,
де Q - NR10, О або S; n - ціле число, яке вибирають з 0, 1 або 2;
m - ціле число, яке вибирають з 0, 1, 2 або 3;
Y, Z та Е, разом із 2 атомами вуглецю, до яких вони приєднані, утворюють 5-6-членне арильне або гетероарильне кільце,
R1 вибирають із групи, яка складається або до складу якої входять незаміщений або заміщений С1-С6-алкіл, незаміщений або заміщений С2-С6-алкеніл, незаміщений або заміщений С2-С6-алкініл, незаміщений або заміщений арил, незаміщений або заміщений гетероарил, незаміщений або заміщений насичений або ненасичений 3-8-членний циклоалкіл, ацил, незаміщений або заміщений С1-С6-алкіларил, незаміщений або заміщений С1-С6-алкілгетероарил, причому згадані циклоалкільні, арильні або гетероарильні групи можуть бути злитими з 1-2 додатковими циклоалкільними, арильними або гетероарильними групами;
R2, R3, R4 та R5 незалежно один від одного вибирають із групи, до складу якої входять водень, галоген, С1-С6-алкіл, С1-С6-алкоксигрупа;
R6 та R7 незалежно вибирають із групи, яка складається або до складу якої входять водень, незаміщений або заміщений С1-С6 алкіл, незаміщений або заміщений С2-С6 алкеніл, незаміщений або заміщений С2-С6 алкініл, незаміщена або заміщена алкоксигрупа, незаміщена або заміщена тіоалкоксигрупа, галоген, ціаногрупа, нітрогрупа, ацил, алкоксикарбоніл, амінокарбоніл, незаміщений або заміщений насичений або ненасичений 3-8-членний циклоалкіл, до складу якого може входити від 1 гетероатома до 3 гетероатомів, які вибирають з N, О, S, незаміщений або заміщений арил, незаміщений або заміщений гетероарил, незаміщений або заміщений С1-С6-алкіларил, незаміщений або заміщений С1-С6-алкілгетероарил;
R8, R9 та R10 незалежно вибирають із групи, яка складається або до складу якої входять водень, незаміщений або заміщений С1-С6-алкіл, незаміщений або заміщений С2-С6-алкеніл, незаміщений або заміщений С2-С6-алкініл, незаміщений або заміщений насичений або ненасичений 3-8-членний циклоалкіл, до складу якого може входити від 1 гетероатома до 3 гетероатомів, які вибирають з N, О, S, незаміщений або заміщений арил, незаміщений або заміщений гетероарил, або
кожна пара R6, R7 та/або R8, R9 може утворювати разом з атомом N, до якого вони приєднані, 3-8-членне заміщене або незаміщене, насичене або ненасичене гетероциклічне кільце, до складу якого можуть входити 1-2 додаткові гетероатоми, які вибирають з N, S та О, і яке є факультативно злитим з арильним, гетероарильним або 3-8-членним насиченим або ненасиченим циклоалкільним кільцем;
R11 вибирають із групи, яка складається або до складу якої входять водень, незаміщений або заміщений С1-С6-алкіл, незаміщений або заміщений алкеніл, незаміщений або заміщений алкініл, гідроксильна група, меркаптогрупа, алкоксигрупа, тіоалкоксигрупа, арил, гетероарил, галоген, нітрогрупа, ціаногрупа, ацил, ацилоксигрупа, ациламіногрупа, амінокарбоніл, алкоксикарбоніл, сульфоніл, сульфоксигрупа, карбоксильна група, первинна, вторинна або третинна аміногрупи або складові четвертинного амонію, незаміщений або заміщений насичений або ненасичений 3-8-членний циклоалкіл,
за умови, що у разі, коли Χ - (=СН2), А - -(С=O)-O-, R1 - t-бутильна група, В не може бути -(C=O)-NMe2, -(C=O)-NHMe, -(C=O)-NH-CH(Me)-(C=O)-NH-CH(Me)-COOH, -(C=O)-NH-CH(COOCH2-Ph)-CH2-COOPh;
за додаткової умови, що у разі, коли Χ - (=CHR6), де R6 - циклогексилметил, А - -(С=O)-O-, R1 - t-бутильна група, В не може бути -(C=O)-NH-t-бутилом;
за додаткової умови, що у разі, коли Χ - С1-С20 алкіліден, А - -(С=O)-O-, R1 - t-бутил, В не може бути
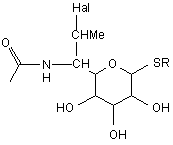 ,
,
де R - С1-С12-алкіл та Hal - Сl, Вr, І;
та за останньої умови, що у разі, коли Χ - С1-С20-алкіліден, A-R1 - захисна група, В не може бути
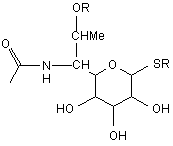 ,
,
де R - Η або С1-С12-алкіл.
2. Похідне піролідину за п. 1, де В - група -(C=O)-NHR9, де R9 вибирають із групи, до складу якої входять незаміщений або заміщений С1-С6-алкіл, незаміщений або заміщений С2-С6-алкеніл, незаміщений або заміщений С2-С6-алкініл, незаміщений або заміщений насичений або ненасичений 3-6-членний циклоалкіл, до складу якого факультативно входить атом N, незаміщений або заміщений арил, незаміщений або заміщений гетероарил, незаміщений або заміщений С1-С2-алкіларил, незаміщений або заміщений С1-С2-алкілгетероарил.
3. Похідне піролідину за п. 1, де В - злитий гетероцикл формули
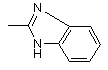 .
.
4. Похідне піролідину за п. 2, де R9 - гетероарил, який вибирають із групи, до якої входять піридил, піроліл, фурил, тієніл, імідазоліл, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, піразоліл, 1,2,3-триазоліл, 1,2,4-триазоліл, 1,2,3-оксадіазоліл, 1,2,4-оксадіазоліл, 1,2,5-оксадіазоліл, 1,3,4-оксадіазоліл, 1,3,4-триазиніл, 1,2,3-триазиніл, бензофурил, [2,3-дигідро]бензофурил, ізобензофурил, бензотієніл, бензотриазоліл, ізобензотієніл, 2,1,3-бензотіадіазоліл, 2,1,3-бензоксадіазоліл, бензодіоксоліл, індоліл, ізоіндоліл, 3Н-індоліл, бензімідазоліл, імідазо[1,2-а]піридил, бензотіазоліл, бензоксазоліл, хінолізиніл, хіназолініл, фталазиніл, хіноксалініл, цинолініл, нафтиридиніл, піридо[3,4-b]піридил, піридо[3,2-b]піридил, піридо[4,3-b]піридил, хіноліл, ізохіноліл, тетразоліл, 5,6,7,8-тетрагідрохіноліл, 5,6,7,8-тетрагідроізохіноліл, пуриніл, птеридиніл, карбазоліл, ксантеніл, акридиніл або бензохіноліл, і де згаданий гетероарил може бути злитим з 3-8-членним циклоалкілом, до складу якого факультативно входять 1-3 гетероатоми, які вибирають з Ν, О, S.
5. Похідне піролідину за будь-яким із попередніх пунктів, де Χ - NOR6, і R6 вибирають із групи, до складу якої входять Н, незаміщений або заміщений С1-С6-алкіл, незаміщений або заміщений С2-С6-алкеніл, незаміщений або заміщений С2-С6-алкініл, незаміщений або заміщений ацил, незаміщений або заміщений арил, незаміщений або заміщений гетероарил, незаміщений або заміщений насичений або ненасичений 3-8-членний циклоалкіл, незаміщений або заміщений С1-С6-алкіларил, незаміщений або заміщений С1-С6-алкілгетероарил, причому згадані циклоалкільна, арильна або гетероарильна групи можуть зливатись з 1-2 додатковими циклоалкільними, арильними або гетероарильними групами.
6. Похідне піролідину за п. 5, де R6 - Н, СН3, незаміщений або заміщений СН2-феніл або аліл, за варіантом, якому віддається перевага, Н або метил.
7. Похідне піролідину за будь-яким із пп. 1-4, де Χ - CHR6 та R6 вибирають із групи, до складу якої входять галоген, ціаногрупа, незаміщений або заміщений С3-С6-алкіл, незаміщений або заміщений С2-С6-алкеніл, незаміщений або заміщений С2-С6-алкініл, незаміщена або заміщена алкоксигрупа, незаміщена або заміщена тіоалкоксигрупа, нітрогрупа, ацил, алкоксикарбоніл, амінокарбоніл, незаміщений або заміщений арил, незаміщений або заміщений гетероарил, незаміщений або заміщений насичений або ненасичений 3-8-членний циклоалкіл, незаміщений або заміщений С1-С6-алкіларил, незаміщений або заміщений С1-С6-алкілгетероарил, причому згадані циклоалкільні, арильні або гетероарильні групи можуть бути злитими з 1-2 додатковими циклоалкільними, арильними або гетероарильними групами.
8. Похідне піролідину за п. 7, де R6 вибирають із групи, до складу якої входять галоген, ціаногрупа, С1-С6-алкіл, незаміщена або заміщена фенільна група.
9. Похідне піролідину за будь-яким із попередніх пунктів, де А - -(С=O)- або -(C=O)-NH-, або -SO2-.
10. Похідне піролідину за п. 9, де А - -(С=O)-.
11. Похідне піролідину за будь-яким із попередніх пунктів, де R1 - С1-С6-алкіл, С2-С6-алкеніл, незаміщений або заміщений С2-С6-алкініл, арил, гетероарил, насичений або ненасичений 3-8-членний циклоалкіл, C1-C6-алкіларил, С1-С6-алкілгетероарил.
12. Похідне піролідину за п. 11, де R1 - С1-С6-алкільна або арильна група.
13. Похідне піролідину за п. 12, де R1 - дифеніл.
14. Похідне піролідину за будь-яким із пп. 1-4, де Χ - =NOR6 або =СНСl, R6 - С1-С6-алкіл або арил, або С1-С6-алкіларильна група, А - -(С=O)- та R1 - С1-С6-алкіл або арил, або С1-С6-алкіларильна група.
15. Похідне піролідину за п. 14, де Χ - =NOR6 або =СНСl, R6 - метил, В - амідна група формули -(C=O)NHR9, де R9 - незаміщена або заміщена С1-С6-алкіларильна група, А - -(С=O)- та R1 - дифенільна або ацетилметильна група.
16. Похідне піролідину за п. 15, де Χ - =NОСН3, В - амідна група формули -(C=O)NHR9, де R9 - заміщена фенілетильна група, А - -(С=O)- та R1 - заміщений дифеніл.
17. Похідне піролідину за будь-яким із попередніх пунктів, вибране з наведеної далі групи:
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-(2-метоксіетил)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-(хлорметилен)-N-(2-гідрокси-2-фенетил)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-(2-гідроксіетил)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-фенетил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(3ЕZ,5S)-5-(1Н-бензімідазол-2-іл)-1-([1,1’-дифеніл]-4-ілкарбоніл)-3-піролідинон O-метилоксим;
(2S,4ЕZ)-N-(2,1,3-бензотіадіазол-4-іл)-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-N-(6-хінолініл)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-ацетоацетил-N-бензил-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-(хлорметилен)-N-(2-фурилметил)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-[(4-хлорфеноксі)ацетил]-4-{[(3,4-дихлорбензил)оксі]іміно}-Ν-[(2RS)-2-гідрокси-2-фенетил]-2-піролідинкарбоксамід;
-10-
(2S,4EZ)-N-аліл-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-N-(2-тієнілметил)-2-піролідинкарбоксамід;
(2S,4ЕZ)-4-(ціанометилен)-N-(2-фурилметил)-1-[(2-оксо-6-пентил-2Н-піран-3-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-Ν-(2-фурилметил)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-ацетил-N-циклопропіл-4-{[(3,4-дихлорбензил)оксі]іміно}-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-(2-фурилметил)-4-(метоксііміно)-1-[(2-оксо-6-пентил-2Н-піран-3-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-бензил-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-N-метил-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-(дифенілацетил)-4-(етоксііміно)-N-(2-тієнілметил)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-(2,1,3-бензотіадіазол-4-іл)-4-(ціанометилен)-1-(дифенілацетил)-2-піролідинкарбоксамід;
(3ЕZ,5S)-5-(1Н-бензімідазол-2-іл)-1-(дифенілацетил)-3-піролідинон O-метилоксим;
-20-
(2S)-2-[1-([1,1’-дифеніл]-4-ілкарбоніл)-4-метилен-2-піролідиніл]-1Н-бензімідазол;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-(хлорметилен)-N-(2-метоксіетил)-2-піролідинкарбоксамід;
(3ЕZ,5S)-5-(1Н-бензімідазол-2-іл)-1-(дифенілацетил)-3-піролідинон O-алілоксим;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-[2-(діетиламіно)етил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-(дифенілацетил)-4-{[(4-метоксибензил)оксі]іміно}-N-(2-тієнілметил)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-Ν-(3,4-диметоксибензил)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-ацетоацетил-4-(метоксііміно)-N-(1-нафтилметил)-2-піролідинкарбоксамід;
(2S,4EZ)-N-aлiл-4-{[(3,4-диxлopбeнзил)oкcі]iмiнo}-1-(дифeнiлaцeтил)-2-піролідинкарбоксамід;
(2S,4EZ)-4-{[(3,4-диxлopбeнзил)oкcі]iмiнo}-Nl-пeнтил-N2-(6-xiнoлiнiл)-1,2-піролідиндикарбоксамід;
(2S,4EZ)-4-(xлopмeтилeн)-1-(дифeнiлaцeтил)-N-[(2RS)-2-гiдpoкcи-2-фенетил]-2-піролідинкарбоксамід;
-30-
(2S)-1-([1,1’-дифeнiл]-4-iлкapбoнiл)-N-[(2RS)-2-гiдpoкcи-2-фeнeтил]-4-метилен-2-піролідинкарбоксамід;
(2S,4ΕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-(хлорметилен)-N-(6-хінолініл)-2-піролідинкарбоксамід;
(2S,4EZ)-4-бeнзилiдeн-N-[2-(дieтилaмiнo)eтил]-1-(дифeнiлaцeтил)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-ацетоацетил-4-(метоксііміно)-N-(2-тієнілметил)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-ацетил-4-{[(3,4-дихлорбензил)оксі]іміно}-N-[(2RS)-2-гідрокси-2-фенетил]-2-піролідинкарбоксамід;
(2S,4EZ)-4-{[(3,4-диxлopбeнзил)oкcі]iмiнo}-Nl-(3,5-диxлopфeнiл)-N2-(6-хінолініл)-1,2-піролідиндикарбоксамід;
(2S,4ЕZ)-4-(метоксііміно)-N-(1-нафтилметил)-1-(феноксіацетил)-2-піролідинкарбоксамід;
(2S,4ЕZ)-4-(хлорметилен)-N-(3,4-диметоксибензил)-1-[(2-оксо-6-пентил-2Н-піран-3-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-(дифенілацетил)-4-(метоксііміно)-N-(2-тієнілметил)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-бензил-1-(дифенілацетил)-4-(метоксііміно)-2-піролідинкарбоксамід;
-40-
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-{[(3,4-дихлорбензил)оксі]іміно}-N-[2-(діетиламіно)етил]-2-піролідинкарбоксамід;
(2S,4ЕZ)-4-{[(3,4-дихлорбензил)оксі]іміно}-1-[4-(диметиламіно)бутаноїл]-N-(6-хінолініл)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифeнiл]-4-iлкapбoнiл)-N-(5-eтил-l,3,4-тiaдiaзoл-2-iл)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-N-бензил-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-N-бензил-1-(дифенілацетил)-4-(етоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-N2-циклoпpoпiл-4-{[(3,4-диxлopбeнзил)oкcі]iмiнo}-Nl-(3-метоксифеніл)-1,2-піролідиндикарбоксамід;
(2S,4ЕZ)-1-(дифенілацетил)-N-[(2RS)-2-гідрокси-2-фенетил]-4-{[(4-метоксибензил)оксі]іміно}-2-піролідинкарбоксамід;
(2S)-N-(2-фурилметил)-4-метилен-1-[(2-оксо-6-пентил-2Н-піран-3-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-(2,1,3-бензотіадіазол-4-іл)-1-(дифенілацетил)-4-(метоксііміно)2-піролідинкарбоксамід;
(2S,4ЕZ)-N-бензил-1-(дифенілацетил)-4-{[(4-метоксибензил)оксі]іміно}-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-бензоїл-4-{[(3,4-дихлорбензил)оксі]іміно}-N-(6-хінолініл)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-ацетоацетил-N-циклопропіл-4-{[(3,4-дихлорбензил)оксі]іміно}-2-піролідинкарбоксамід;
(2S,4EZ)-4-{[(3,4-диxлopбeнзил)oкcі]iмiнo}-N2-[(2RS)-2-гiдpoкcи-2-фенетил]-N1-пентил-1,2-піролідиндикарбоксамід;
(2S,4ЕZ)-1-[(бензилокси)іміно]-N-(1-нафтилметил)-1-(феноксіацетил)-2-піролідинкарбоксамід;
(2S)-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-метилен-N-(6-хінолініл)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-циклопропіл-4-{[(3,4-дихлорбензил)оксі]іміно}-1-(дифенілацетил)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-(4-ціанобензоїл)-4-{[(3,4-дихлорбензил)оксі]іміно}-N-(6-хінолініл)-2-піролідинкарбоксамід;
(2S,4EZ)-N-циклопропіл-4-{[(3,4-дихлорбензил)оксі]іміно}-1-(метоксіацетил)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-(1,3-бензодіоксол-5-ілметил)-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-2-піролідинкарбоксамід;
(3EZ,5S)-5-[(4-ацетил-1-піперазиніл)карбоніл]-1-акрилоїл-3-піролідинон O-(3,4-дихлорбензил)оксим;
(2S)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-(2-фурилметил)-4-метилен-2-піролідинкарбоксамід;
(2S,4EZ)-4-(ціанометилен)-N-(3,4-диметоксибензил)-1-[(2-оксо-6-пентил-2Н-піран-3-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-3-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-(4-бензоїлбензоїл)-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-(3-феноксибензоїл)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-(2-феноксибензоїл)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2R)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-(2-гідроксіетил)-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-(2-гідроксіетил)-4-(метоксііміно)-N-метил-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілсульфоніл)-N-[(1S,2S,3R,4R)-3-(гідроксиметил)біцикло[2.2.1]гепт-2-ил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-Ν-(транс-4-гідроксициклогексил)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-[(1R,2R)-2-(гідроксиметил)циклогексил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-3-феноксипропіл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2RS)-2-гідрокси-3-феноксипропіл]-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілсульфоніл)-N-[(2RS)-2-гідрокси-3-феноксипропіл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-(4-гідроксифеніл)етил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілсульфоніл)-N-[(2RS)-2-гідрокси-2-(4-гідроксифеніл)етил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-[(1-гідроксициклогексил)метил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-N-[(1-гідроксициклогексил)метил]-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілсульфоніл)-N-[(1-гідроксициклогексил)метил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-(3,4-дигідроксифеніл)-2-гідроксіетил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[4-(4-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4EZ)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[4-(2-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2,3-дигідроксипропіл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілсульфоніл)-N-[(2RS)-2,3-дигідроксипропіл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-3-(4-метоксифенокси)пропіл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-(2RS)-2-гідрокси-3-(4-метоксифенокси)пропіл]-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілсульфоніл)-N-[(2RS)-2-гідрокси-3-(4-метоксифенокси)пропіл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідроксипропіл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілсульфоніл)-Ν-[(2RS)-2-гідроксипропіл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілсульфоніл)-N-[(2RS)-2-гідрокси-2-(2-нафтил)етил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-(4-нітрофеніл)етил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-N-[(2RS)-2-гідрокси-2-(4-нітрофеніл)етил]-4-(метоксііміно)-1-[4-(4-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4EZ)-N-[(2RS)-2-гiдpoкcи-2-(4-нiтpoфeнiл)eтил]-4-(мeтoкciiмiнo)-1-[4-(3-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4EZ)-N-[(2RS)-2-гiдpoкcи-2-(4-нiтpoфeнiл)eтил]-4-(мeтoкciiмiнo)-1-[4-(2-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифeнiл]-4-iлcyльфoнiл)-N-[(2RS)-2-гiдpoкcи-2-(4-нітрофеніл)етил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-N-{(2RS)-3-[4-(aцeтилaмiнo)фeнoкcі]-2-гiдpoкcипpoпiл}-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-{(2RS)-3-[4-(ацетиламіно)фенокси]-2-гідроксипропіл}-4-(метоксііміно)-1-[4-(4-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-{(2RS)-3-[4-(ацетиламіно)фенокси]-2-гідроксипропіл}-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-{(2RS)-3-[4-(ацетиламіно)фенокси]-2-гідроксипропіл}-1-([1,1’-дифеніл]-4-ілсульфоніл)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-(2R)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-Ν-[-[(2R)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[4-(4-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2R)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2R)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[4-(2-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілсульфоніл)-N-[(2R)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-(3-гідроксипропіл)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілсульфоніл)-N-(3-гідроксипропіл)-4-(метоксііміно)-2-піролідинкарбоксамід;
(3EZ,5S)-1-([1,1’-дифеніл]-4-ілкарбоніл)-5-[(4-гідрокси-4-феніл-1-піперидиніл)карбоніл]-3-піролідинон O-метилоксим;
(3ЕZ,5S)-5-[(4-гідрокси-4-феніл-1-піперидиніл)карбоніл]-1-[4-(4-піридиніл)бензоїл]-3-піролідинон O-метилоксим;
(3ЕZ,5S)-5-[(4-гідрокси-4-феніл-1-піперидиніл)карбоніл]-1-[4-(3-піридиніл)бензоїл]-3-піролідинон O-метилоксим;
(3EZ,5S)-1-([1,1’-дифеніл]-4-ілсульфоніл)-5-[(4-гідрокси-4-феніл-1-піперидиніл)карбоніл]-3-піролідинон O-метилоксим;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-[(1S,2S)-2-гідроксициклогексил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілсульфоніл)-N-[(1S,2S)-2-гідроксициклогексил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-бензил-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-(2-гідроксіетил)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-бензил-N-(2-гідроксіетил)-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(3ЕZ,5S)-1-([1,1’-дифеніл]-4-ілкарбоніл)-5-{(3RS)-3-гідроксипіперидиніл]карбоніл}-3-піролідинон O-метилоксим;
(3ЕZ,5S)-5-{[(3RS)-3-гідроксипіперидиніл]карбоніл}-1-[4-(4-піридиніл)бензоїл]-3-піролідинон O-метилоксим;
(3ЕZ,5S)-5-{[(3RS)-3-гідроксипіперидиніл]карбоніл}-1-[4-(3-піридиніл)бензоїл]-3-піролідинон O-метилоксим;
(3ЕZ,5S)-1-([1,1’-дифеніл]-4-ілсульфоніл)-5-{[(3RS)-3-гідроксипіперидиніл]карбоніл}-3-піролідинон O-метилоксим;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-[(1S,2S)-2-гідрокси-1-(гідроксиметил)-2-фенілетил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(1S,2S)-2-гідрокси-1-(гідроксиметил)-2-фенілетил]-4-(метоксііміно)-1-[4-(4-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(1S,2S)-2-гідрокси-1-(гідроксиметил)-2-фенілетил]-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілсульфоніл)-N-[(1S,2S)-2-гідрокси-1-(гідроксиметил)-2-фенілетил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-(2-аніліноетил)-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-(2-аніліноетил)-4-(метоксііміно)-1-[4-(4-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-(2-аніліноетил)-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-(2-аніліноетил)-4-(метоксііміно)-1-[4-(2-піридиніл)бензоїл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-(2-аніліноетил)-1-([1,1’-дифеніл]-4-ілсульфоніл)-4-(метоксііміно)-2-піролідинкарбоксамід;
(3ЕZ,5S)-1-([1,1’-дифеніл]-4-ілкарбоніл)-5-[(4-гідрокси-1-піперидиніл)карбоніл]-3-піролідинон O-метилоксим;
(3ЕZ,5S)-1-([1,1’-дифеніл]-4-ілсульфоніл)-5-[(4-гідрокси-1-піперидиніл)карбоніл]-3-піролідинон O-метилоксим;
(2S,4EZ)-N-[(1S,2R,3S,4R)-3-(амінокарбоніл)біцикло[2.2.1]гепт-3-ен-2-іл]-1-([1,1’-дифеніл]-4-ілсульфоніл)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-N-(3-aміно-3-oксопропіл)-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(1S,2S,3R,4R)-3-(амінокарбоніл)біцикло[2.2.1]гепт-5-ен-2-іл]-1-([1,1’-дифеніл]-4-ілсульфоніл)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-(4-гідроксибутил)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілсульфоніл)-N-(4-гідроксибутил)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілсульфоніл)-N-[(1R,2R)-2-(гідроксиметил)циклогексил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілсульфоніл)-N-[(1R,2S,3R,4S)-3-(гідроксиметил)біцикло[2.2.1]гепт-2-ил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілсульфоніл)-N-[(1R,2S)-2-(гідроксиметил)циклогексил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4E та 4Z)-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4E та 4Z)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4E та 4Z)-N-[(2R)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-[(1R,2S)-2-(гідроксиметил)циклогексил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-[2-гідрокси-1-(гідроксиметил)етил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(1S,2R,3S,4R)-3-(амінокарбоніл)біцикло[2.2.1]гепт-5-ен-2-іл]-1-([1,1’-дифеніл]-4-ілкарбоніл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(1S,2S,3R,4R)-3-(амінокарбоніл)біцикло[2.2.1]гепт-5-ен-2-іл]-1-([1,1’-дифеніл]-4-ілкарбоніл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл]-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2RS)-3-({[(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)піролідиніл]карбоніл}аміно)-2-гідроксипропанова кислота;
(2S,4EZ)-N-[(1R,2S)-2-(амінокарбоніл)циклогексил]-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-[(1RS)-2-гідрокси-1-метилетил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-[(1S,2S)-2-гідрокси-1-(гідроксиметил)-2-(4-нітрофеніл)етил]-4-(метоксііміно)-2-піролідинкарбоксамід;
4-({[(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)піролідиніл]карбоніл}аміно)бутанова кислота;
(2S,4ЕZ)-N-[(2S)-2-гідрокси-2-фенілетил]-1-[(2’-метокси[1,1’-дифеніл]-4-іл)карбоніл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(2-нафтил)етил]-1-[(2’-метокси[1,1’-дифеніл]-4-іл)карбоніл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-N-[(1RS)-2-гідрокси-1-метилетил]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(1S,2S)-2-гідрокси-1-(гідроксиметил)-2-(4-нітрофеніл)етил]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(1S,2S)-2-гідрокси-1-(гідроксиметил)-2-(4-нітрофеніл)етил]-4-(метоксііміно)-1-[(2’-метокси[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(3ЕZ,5S)-5-[(4-гідрокси-1-піперидиніл)карбоніл]-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-3-піролідинон O-метилоксим;
(2S,4ЕZ)-N-[(1S,2S,3R,4R)-3-(амінокарбоніл)біцикло[2.2.1]гепт-5-ен-2-іл]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-фенілетил]-1-[(2’-метокси[1,1’-дифеніл]-4-іл)карбоніл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2RS)-2-гідроксипропіл]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2RS)-2,3-дигідроксипропіл]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4EZ)-N-(3-гідроксипропіл)-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4EZ)-Ν-(2-аміно-2-оксоетил)-1-([1,1’-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-(2-аміно-2-оксоетил)-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-(3-гідроксифеніл)етил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-іл)карбоніл]-N-[(1S,2R,3S,4R)-3-(гідроксиметил)біцикло[2.2.1]гепт-2-ил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(1R,2S,3R,4S)-3-(гідроксиметил)біцикло[2.2.1]гепт-2-ил]-1-[(2’-метокси[1,1’-дифеніл]-4-іл)карбоніл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-Ν-(транс-4-гідроксициклогексил)-1-[(2’-метокси[1,1’-дифеніл]-4-іл)карбоніл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-N-[(1R,2R)-2-гідроксиметил)циклогексил)-1-[(2’-метокси[1,1’-дифеніл]-4-іл)карбоніл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-Ν-[(2RS)-2-гідрокси-3-феноксипропіл]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(4-гідроксифеніл)етил]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(4-гідроксифеніл)етил]-4-(метоксііміно)-1-[(2’-метокси[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(4-гідрокси-3-метоксифеніл)етил]-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(4-гідрокси-3-метоксифеніл)етил]-1-[(2’-метокси[1,1’-дифеніл]-4-іл)карбоніл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-Ν-[(2RS)-2-(3,4-дигідроксифеніл)-2-гідроксіетил]-1-[(2’-метокси[1,1’-дифеніл]-4-іл)карбоніл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2R,4EZ)-1-([1,1’-дифеніл]-4-ілкарбоніл]-Ν-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2R,4ЕZ)-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-[(2’-ціано[1,1’-дифеніл]-4-іл)карбоніл]-Ν-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-[(3’,4’-дихлоро[1,1’-дифеніл]-4-іл)карбоніл]-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-[(2’,6’-диметил[1,1’-дифеніл]-4-іл)карбоніл]-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-[(2’,3-диметил[1,1’-дифеніл]-4-іл)карбоніл]-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-Ν-[(2RS)-2-гідрокси-2-(3-гідроксифеніл)етил]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-Ν-[(2RS)-2-гідрокси-2-(3-гідроксифеніл)етил]-4-(метоксііміно)-1-[(2’-ціано[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(3-гідроксифеніл)етил]-4-(метоксііміно)-1-[(3’,4’-дихлоро[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(3-гідроксифеніл)етил]-4-(метоксііміно)-1-[(2’,6’-диметил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(3-гідроксифеніл)етил]-4-(метоксііміно)-1-[(2’,3-диметил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-[(3’,4’-дихлоро[1,1’-дифеніл]-4-іл)карбоніл]-N-[(2RS)-2-гідрокси-2-(4-гідроксифеніл)етил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-[(2’,6’-диметил[1,1’-дифеніл]-4-іл)карбоніл]-N-[(2RS)-2-гідрокси-2-(4-гідроксифеніл)етил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-[(2’,3-диметил[1,1’-дифеніл]-4-іл)карбоніл]-N-[(2RS)-2-гідрокси-2-(4-гідроксифеніл)етил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-[(2’,6-диметил[1,1’-дифеніл]-4-іл)карбоніл]-N-[(2RS)-2-гідрокси-3-(4-метоксифенокси)пропіл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-[(2’,3-диметил[1,1’-дифеніл]-4-іл)карбоніл]-N-[(2RS)-2-гідрокси-3-(4-метоксифенокси)пропіл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-(2-аміно-2-оксоетил)-1-[(2’,6’-диметил[1,1’-дифеніл]-4-іл)карбоніл]-(4-метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-(2-аміно-2-оксоетил)-1-[(2’,3’-диметил[1,1’-дифеніл]-4-іл)карбоніл]-(4-метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-N-(3-aмiнo-3-oкcoпpoпiл)-1-[(2’,6’-димeтил[1,1’-дифeнiл]-4-іл)карбоніл]-(4-метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-(3-аміно-2-оксопропіл)-1-[(2’,3-диметил[1,1’-дифеніл]-4-іл)карбоніл]-(4-метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-[(2’,6’-диметил[1,1’-дифеніл]-4-іл)карбоніл]-N-[2-гідрокси-1-(гідроксиметил)етил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-[(2’,3-диметил[1,1’-дифеніл]-4-іл)карбоніл]-N-[2-гідрокси-1-(гідроксиметил)етил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-[(2’-ціано[1,1’-дифеніл]-4-іл)карбоніл]-N-[(1R,2R)-2-(гідроксиметил)-циклогексил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(3ЕZ,5S)-5-(3,4-дигідро-2(1Н)-ізохінолінілкарбоніл)-1-[(2’,3-диметил[1,1’-дифеніл]-4-іл)карбоніл]-3-піролідинон O-метилоксим;
(2S,4ЕZ)-N-[(1R)-2-гідрокси-1-фенілетил]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-[(2’,6’-диметил[1,1’-дифеніл]-4-іл)карбоніл]-N-[2-(4-гідроксифеніл)етил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-[(2’,3-диметил[1,1’-дифеніл]-4-іл)карбоніл]-N-[2-(4-гідроксифеніл)етил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-[(2’,6’-диметил[1,1’-дифеніл]-4-іл)карбоніл]-N-[2-(3-гідроксифеніл)етил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-[(2’,3-диметил[1,1’-дифеніл]-4-іл)карбоніл]-Ν-[2-(3-гідроксифеніл)етил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-[(2’,3-диметил[1,1’-дифеніл]-4-іл)карбоніл]-N-[(1R,2S)-2-гідрокси-1,2-дифенілетил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2RS)-2-[({(2S,4ЕZ)-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]піролідиніл}карбоніл)аміно]-3-фенілпропанова кислота;
(2S,4ЕZ)-N-[(1R,2S)-2-(амінокарбоніл)циклогексил]-1-[(2’,6’-диметил[1,1’-дифеніл]-4-іл)карбоніл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(1R,2S)-2-(амінокарбоніл)циклогексил]-1-[(2’,3-диметил[1,1’-дифеніл]-4-іл)карбоніл]-4-(метоксііміно)-2-піролідинкарбоксамід;
4’-{[(2S,4ЕZ)-2-{[4-(2-гідроксіетил)-1-піперазиніл]карбоніл}-4-(метоксііміно)піролідиніл]карбоніл}[1,1’-дифеніл]-2-карбонітрил;
(3ЕZ,5S)-1-[(3’,4’-дихлоро[1,1’-дифеніл]-4-іл)карбоніл]-5-{[4-(2-гідроксіетил)-1-піперазиніл]карбоніл}-3-піролідинон O-метилоксим;
(3ЕZ,5S)-1-[(2’,6’-диметил[1,1’-дифеніл]-4-іл)карбоніл]-5-{[4-(2-гідроксіетил)-1-піперазиніл]карбоніл}-3-піролідинон O-метилоксим;
(3ЕZ,5S)-1-[(2’,3-диметил[1,1’-дифеніл]-4-іл)карбоніл]-5-{[4-(2-гідроксіетил)-1-піперазиніл]карбоніл}-3-піролідинон O-метилоксим;
(3ЕZ,5S)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-5-({4-[4-(трифторметил)феніл]-1-піперазиніл}карбоніл)-3-піролідинон O-метилоксим;
(3ЕZ,5S)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-5-({4-[3-(трифторметил)феніл]-1-піперазиніл}карбоніл)-3-піролідинон O-метилоксим;
(2S,4ЕZ)-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-4-(метоксііміно)-N-метил-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-4-(метоксііміно)-N,N-диметил-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(3R)-3-гідрокси-3-фенілпропіл]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(3S)-3-гідрокси-3-фенілпропіл]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-іл)карбоніл]-N-[(3R)-3-гідрокси-3-фенілпропіл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-іл)карбоніл]-N-[(3S)-3-гідрокси-3-фенілпропіл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-{[2’-(трифторметил)[1,1’-дифеніл]-4-іл)карбоніл}-2-піролідинкарбоксамід;
(2S,4EZ)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-{[2’-хлоро[1,1’-дифеніл]-4-іл]карбоніл}-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-(2-гідроксифеніл)-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[2-гідроксиметил)феніл]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4ЕZ)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4E та 4Z)-1-([1,1’-дифеніл]-4-ілкарбоніл]-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-N-(2-фенілетил)-2-піролідинкарбоксамід.
18. Похідне піролідину за будь-яким із попередніх пунктів, яке вибирають з наведеної далі групи:
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілкарбоніл]-4-хлорметилен)-N-[(2RS)-2-гідрокси-2-фенетил]-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл]-N-(2-гідроксіетил)-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4ЕZ)-1-([1,1’-дифеніл]-4-ілкарбоніл]-N-[(2RS)-2-гідрокси-2-фенетил]-4-(метоксііміно)-2-піролідинкарбоксамід;
(3ЕZ,5S)-5-(1Н-бензімідазол-2-іл)-1-([1,1’-дифеніл]-4-ілкарбоніл]-3-піролідинон O-метилоксим;
(2S,4ЕZ)-N-(2,1,3-бензотіадіазол-4-іл)-1-([1,1’-дифеніл]-4-ілкарбоніл]-4-(метоксііміно)-2-піролідинкарбоксамід;
(2S,4EZ)-1-([1,1’-дифеніл]-4-ілкарбоніл]-4-(метоксііміно)-N-(6-хінолініл)-2-піролідинкарбоксамід;
(2S,4Z)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід;
(2S,4Е)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2’-метил[1,1’-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід.
19. Похідне піролідину за будь-яким із пп. 1-18 для застосування як медичний засіб.
20. Застосування похідних піролідину за будь-яким із пп. 1-18 для виготовлення фармацевтичної композиції для лікування та/або запобігання передчасним пологам та дисменореї.
21. Застосування похідних піролідину за будь-яким із пп. 1-18 для виготовлення фармацевтичної композиції для модулювання рецептора окситоцину.
22. Застосування за п. 21, де згадане модулювання полягає у блокуванні рецептора окситоцину або антагонізуванні зв'язування окситоцину зі своїм рецептором.
23. Застосування за п. 22 для лікування або запобігання розладам, які опосередковуються рецептором окситоцину.
24. Фармацевтична композиція, яка містить щонайменше одну похідну піролідину за будь-яким із пп. 1-18 та фармацевтично прийнятний носій, розріджувач або наповнювач.
25. Спосіб одержання похідної піролідину за будь-яким із пп. 1-18, де здійснюють таку реакцію:
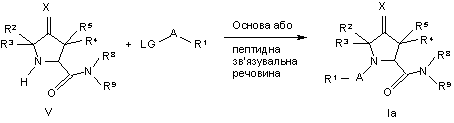 ,
,
де LG - відщеплювана група та замісники R1-R9, А та Х відповідають визначенню, яке було наведено вище.
26. Спосіб одержання похідного піролідину за будь-яким із пп. 1-18, де здійснюють таку реакцію:
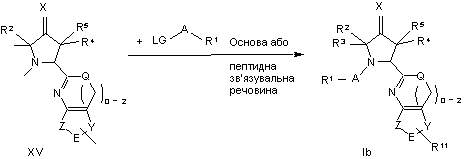 ,
,
де LG - відщеплювана група та замісники R1-R5, R11, A, E, Q, X, Y та Z відповідають визначенню, яке було наведено вище.
27. Спосіб за п. 26, де сполуку XV одержують наведеним далі чином:
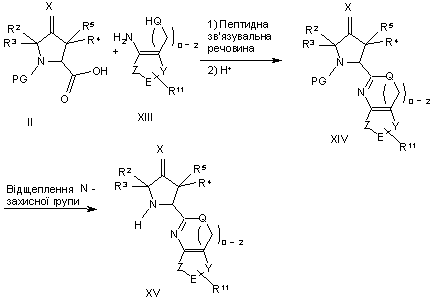 .
.
Текст
Цей винахід має відношення до похідних піролідину. Згадані сполуки призначені, головним чином, для використання у ролі фармацевтично активних сполук. Зокрема, похідні піролідину формули І є придатними для лікування та/або запобігання передчасних пологів та дисменореї. Зокрема, цей винахід має відношення до похідних піролідину, які демонструють значну модуляторну здатність, особливо антагоністичну активність щодо рецептора окситоцину. За варіантом, якому віддається більша перевага, згадані сполуки є придатними для лікування та/або запобігання хворобливих станів, які опосередковуються окситоцином, у тому числі передчасних пологів та дисменореї. Цей винахід, додатково, має відношення до нових похідних піролідину, а також до способів їх одержання. Окситоцин (ОТ) представляє собою пептидний гормон і викликає скорочення матки ссавців під час пологів. Відповідний рецептор окситоцину належить до сімейства рецепторів, сполучених із білком G, і є подібним до рецепторів вазопресину V1a та V2. Кількість рецепторів ОТ різко збільшується під час вагітності. Було показано, що концентрація рецепторів ОТ корелює зі спонтанною активністю матки (Μ. Маггі (Μ. Maggi) та інші, J. Clin. Endocrinol. Metabol; 70; 1142, 1990). Передчасні пологи, однак, є небажаними, оскільки вони є головною причиною перинатальної захворюваності та смертності. Таким чином, контролювання передчасних пологів представляє собою значну проблему у галузі акушерства. Впродовж останніх років було накопичено значні свідчення на користь того, що гормон окситоцин відіграє головну роль у ініціюванні пологів у ссавців, особливо у людей. Гадають, таким чином, що окситоцин здійснює згаданий вплив як безпосереднім, так і опосередкованим шляхом, а саме шляхом скорочення міометрію матки та стимулювання синтезу та виділення скорочувальних простагландинів з ендометрію/відпадної оболонки матки. Ці простагландини можуть додатково відігравати роль у процесі дозрівання шийки матки. "Активація" рецепторів окситоцину та підвищена чутливість матки, як видається, обумовлюються трофічними ефектами підвищення рівнів естрогену у плазмі при наближенні строку пологів. Очікують, що шля хом регуляції окситоцину за типом зворотного зв'язку можуть бути блокованими як прямі (скорочувальні), так і опосередковані (підвищений синтез простагландинів) ефекти окситоцину на матку. Модулятор окситоцину, наприклад, інгібітор або антагоністи, будуть, ймовірно, більш ефективними при лікуванні передчасних пологів, аніж сучасні схеми лікування. Більше того, оскільки окситоцин під час пологів має вплив лише на матку, такий модулятор окситоцину може мати лише незначні, або бути зовсім позбавленим побічного ефекту. Додатковим станом, який пов'язують з окситоцином, є дисменорея, яка характеризується періодичним болем, пов'язаним із менструацією під час овуляторних циклів. Гадають, що згаданий біль є наслідком скорочень та ішемії матки, що, ймовірно, опосередковується впливом простагландинів, які продукуються у секреторному ендометрії. Гадають, що антагоніст окситоцину, принцип дії якого полягає у блокуванні як опосередкованого, так і безпосереднього впливу окситоцину на матку, є більш ефективним для лікування дисменореї, аніж сучасні схеми лікування. Зараз клінічним дослідженням піддають деякі засоби, які протидіють впливу окситоцину (ОТ). До таких токолітичних речовин (тобто речовин, що викликають релаксацію матки) належать бета-2-адренергічні агоністи, сульфат магнію та етанол. Основним бета-2-адренергічним агоністом є ритодрин (ritodrine), який викликає цілий ряд серцево-судинних та метаболічних побічних ефектів, у тому числі та хікардію, підвищену секрецію реніну, гіперглікемію та реактивну гіпоглікемію у немовлят. Додаткові бета-32-адренергічні агоністи, у тому числі тербуталін (terbutaline) та альбутерол (albuterol), мають побічні ефекти, подібні до побічних ефектів ритодрину. Сульфат магнію, у разі рівнів концентрації у плазмі, які перевищують терапевтичний діапазон 48мг/дл, може викликати пригнічення провідності серцевого м'язу та нервово-м'язової передачі, пригнічення дихання та зупинку серця, завдяки чому цей агент виявляється непридатним у разі порушення функції нирок. Ефективність етанолу дорівнює ефективності ритодрину у запобіганні передчасних пологів, однак він не викликає відповідного зменшення кількості випадків респіраторного дистрес-синдрому зародка, що забезпечується введенням ритодрину. Головна вада застосування пептидних антагоністів, у тому числі атозибану (atosiban), полягає у проблемі низької пероральної біодоступності, що є наслідком кишкового розкладення. Унаслідок цього, вони повинні вводитись парентеральним шляхом. Сподіваються, що цю проблему буде подолано розробкою непептидних лігандів для рецепторів пептидних гормонів. Першою про селективні антагоністи окситоцину з невеликою молекулою повідомила компанія Merck. Окрім циклічних гексапептидів, компанія Merck запропонувала інданілпіперидини та толілпіперазини як антагоністи ОТ, придатні для введення пероральним шляхом (Еванс (Evans) та інші, J. Med. Chem., 35, 3919 (1992)). У заявці WO 96/22775 та патенті США №5,756,497 компанія Merck повідомила про бензоксазинілпіперидини або бензоксазинони як антагоністи рецептора ОТ. Ціль цього винаходу полягає у наданні речовин, які з більшою ефективністю регулюють за типом зворотного зв'язку, майже до антагонізування, функцію ОТ при хворобливих станах тварин, за варіантом, якому віддається перевага, ссавців, особливо людей. Інша ціль цього винаходу полягає у наданні способу антагонізування функцій окситоцину при хворобливих станах ссавців. Ціль цього винаходу полягає також у наданні хімічних сполук із невеликою молекулою для модулювання, за варіантом, якому віддається перевага, регуляції за типом зворотного зв'язку, або навіть антагонізування, рецептора окситоцину. Більше того, мета цього винаходу полягає у наданні способів одержання згаданих хімічних сполук із невеликою молекулою. Додаткова мета цього винаходу полягає у наданні фармацевтичних композицій нової категорії для лікування передчасних пологів та дисменореї та/або захворювань, які опосередковуються рецептором окситоцину. І, нарешті, мета цього винаходу полягає у наданні способу лікування або запобігання розладів, які опосередковуються рецептором окситоцину, подібних до передчасних пологів та дисменореї, шляхом антагонізування зв'язування окситоцину з його рецептором. Вищезгадані цілі було досягнуто за незалежними пунктами формули винаходу. Варіанти втілення, яким віддається перевага, наведено у залежних пунктах формули винаходу, які включено до цього опису. У подальших параграфах наведено визначення різних хімічних складових, які утворюють сполуки за цим винаходом, і які призначені для однорідного використання у цьому описі та пунктах формули винаходу, якщо обсяг визначення явно не розширюється іншим чином. Термін "С1-С6-алкіл" означає моновалентні алкільні групи, які мають від 1 атому до 6 атомів вуглецю. Прикладом цього терміну є такі групи, як метил, етил, n-пропіл, ізопропіл, n-бутил, ізобутил, трет-бутил, nгексил тощо. Термін "арил" означає ненасичену ароматичну карбоциклічну групу, до складу якої входять від 6 атомів до 14 атомів вуглецю і яка має одне кільце (наприклад, феніл) або численні конденсовані кільця (наприклад, нафтил). Арилом, якому віддається перевага, є феніл, нафтил, фенантреніл тощо. Термін "С1-С6-алкіларил" означає С1-С6-алкільні групи, які мають замісник арилу, у тому числі бензил, фенетил тощо. Термін "гетероарил" означає моноциклічну гетероароматичну, біциклічну або трициклічну гетероароматичну груп у зі злитим кільцем. Конкретними прикладами гетероароматичних гр уп є факультативно заміщений піридил, піроліл, фурил, тієніл, імідазоліл, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, піразоліл, 1,2,3-триазоліл, 1,2,4-триазоліл, 1,2,3-оксадіазоліл, 1,2,4-оксадіазоліл, 1,2,5-оксадіазоліл, 1,3,4-оксадіазоліл, 1,3,4-триазиніл, 1,2,3-триазиніл, бензофурил, [2,3-дигідро]бензофурил, ізобензофурил, бензотієніл, бензотриазоліл, ізобензотієніл, індоліл, ізоіндоліл, 3Н-індоліл, бензімідазоліл, імідазо[1,2-а]піридил, бензотіазоліл, бензоксазоліл, хінолізиніл, хіназолініл, фталазиніл, хіноксалініл, цинолініл, нафтиридиніл, піридо[3,4-b]піридил, піридо[3,2-b]піридил, піридо[4,3-b]піридил, хіноліл, ізохіноліл, тетразоліл, 5,6,7,8тетрагідрохіноліл, 5,6,7,8-тетрагідроізохіноліл, піриніл, птеридиніл, карбазоліл, ксантеніл або бензохіноліл. Термін "С1-С6-алкілгетероарил" означає С1-С6-алкільні групи, які мають замісник гетероарилу, у тому числі 2-фурилметил, 2-тієнілметил, 2-(1Н-індол-3-іл)етил тощо. Термін "алкеніл" означає алкенільні групи, які за варіантом, якому віддається перевага, мають від 2 атомів до 6 атомів вуглецю і як мінімум 1 центр або 2 центри алкенільної ненасиченості. До алкенільних груп, яким віддається перевага, належить етеніл (-СН=СН2), n-2-пропеніл (аліл, -СН2СН=СН2) тощо. Термін "алкініл" означає алкінільні групи, які за варіантом, якому віддається перевага, мають від 2 атомів до 6 атомів вуглецю і як мінімум 1-2 центри алкінільної ненасиченості. До алкінільних груп, яким віддається перевага, належить етиніл (-СºСН), пропаргіл (-CH2CºCH) тощо. Термін "ацил" означає групу -C(O)R, де R включає "C1-С6-алкіл", "арил", "гетероарил", "С1-С6-алкіларил" або "С1-С6-алкілгетероарил". Термін "ацилокси" означає групу -OC(O)R, де R включає "С1-С6-алкіл", "арил", "гетероарил", "C1-С6-алкіл арил" або "С1-C6-алкілгетероарил". Термін "алкокси" означає групу -O-R, де R включає "С1-С6-алкіл" або "арил", або "гетероарил", або "С1-C6алкіларил", або "С1-С6-алкілгетероарил". До алкоксигруп, яким віддається перевага, належить, наприклад, метоксигрупа, етоксигрупа, феноксигрупа тощо. Термін "алкоксикарбоніл" означає групу -C(O)OR, де R включає "С1-C6-алкіл" або "арил", або "гетероарил", або "C1-С6-алкіларил", або "С1-С6-алкілгетероарил". Термін "амінокарбоніл" означає групу -C(O)NRR', де кожен R, R' незалежно включає водень або С 1-С6алкіл, або арил, або гетероарил, або "С1-С6-алкіларил", або "С1-С6-гетероарил". Термін "ациламіно" означає групу -NR(CO)R', де кожен R, R' незалежно представляє собою водень або "С1-С6-алкіл", або "арил", або "гетероарил", або "С1-С6-алкіларил", або "С1-С6-гетероарил". Термін "галоген" означає атоми фтору, хлор у, брому або йоду. Термін "сульфоніл" означає групу "-SO2-R", де R вибирають із групи, до складу якої входять Н, "арил", "гетероарил", "С1-С6-алкіл", "С1-С6-алкіл", заміщений галогенами, наприклад, -SO2-CF3 групу, "С1-С6-алкіларил" або "С1-С6-алкілгетероарил". Термін "сульфоксигрупа" означає групу "-S(O)-R", де R вибирають із групи, до складу якої входять Н, "С1С6-алкіл", "С1-С6-алкіл", заміщений галогенами, наприклад, -SO2-CF3 групу, "арил", "гетероарил", "С1-C6алкіларил" або "С1-С6-алкілгетероарил". Термін "тіоалкоксигрупа" означає групи -S-R, де R включає "С1-С6-алкіл" або "арил", або "гетероарил", або "С1-C6-алкіларил", або "C1-C6-алкілгетероарил". До тіоалкоксигруп, яким віддається перевага, належить тіометоксигрупа, тіоетоксигрупа тощо. "Заміщена або незаміщена": У разі відсутності обмеження, яке накладається визначенням окремого замісника, вищенаведені групи, наприклад, "алкільна", "алкенільна", "алкінільна", "арильна" та "гетероарильна" і подібні групи можуть факультативно заміщува тись 1-5 замісниками, які вибирають із групи, до складу якої входять "С1-С6-алкіл", "С1-С6-алкіларил", "С1-С6-алкілгетероарил", "С2-С6-алкеніл", "С2-С6алкініл", первинна, вторинна або третинна аміногрупи або складові четвертинного амонію, "ацил", "ацилокси", "ациламіно", "амінокарбоніл", "алкоксикарбоніл", "арил", "гетероарил", карбоксильна група, ціаногрупа, галоген, гідроксильна група, меркаптогрупа, нітрогрупа, сульфоксигрупа, сульфоніл, алкоксигрупа, тіоалкоксигрупа, тригалогенметил тощо. За альтернативним варіантом згадане заміщення може також включати ситуації, коли у сусідніх замісників відбулось замикання кільця, особливо коли залучено суміжні функціональні замісники, з утворенням, таким чином, наприклад, лактамів, лактонів, циклічних ангідридів, а також ацеталів, тіоацеталів, аміналів, які утворюються шляхом циклізації, наприклад, з метою одержання захисної групи. Вираз "фармацевтично прийнятні солі або комплекси" означає солі або комплекси визначених нижче сполук формули І, які зберігають необхідну біологічну активність. Прикладами таких солей є, але ними не обмежуються, солі кислот, які одержують за допомогою неорганічних кислот (наприклад, хлористоводневої кислоти, бромистоводневої кислоти, сірчаної кислоти, фосфорної кислоти, азотної кислоти тощо), та солі, які одержують за допомогою органічних кислот, таких як оцтова кислота, щавлева кислота, винна кислота, бурштинова кислота, яблучна кислота, фумарова кислота, малеїнова кислота, аскорбінова кислота, бензойна кислота, дубильна кислота, памова кислота, альгінова кислота, поліглутамінова кислота, нафталінсульфонова кислота, нафталіндисульфонова кислота та полігалактуронова кислота. Згадані сполуки можуть вводитись також як фармацевтично прийнятні четвертинні солі, відомі фахівцю у цій галузі, які конкретно включають сіль четвертинного амонію формули -NR,R',R"+Z-, де R, R', R" незалежно водень, алкіл або бензил та Ζ - протиіон, у тому числі хлорид, бромід, йодид, -О-алкіл, толуолсульфонат, метилсульфонат, сульфонат, фосфат або карбоксилат (такий як бензоат, сукцинат, ацетат, гліколят, малеат, малат, фумарат, цитрат, тартрат, аскорбат, цинамоат, манделоат та дифенілацетат). Вираз "фармацевтично активна похідна" означає будь-яку сполуку, яка, у разі введення реципієнту, є здатною до забезпечення, безпосередньо або опосередковано, активності, яка розкривається у цьому описі. Вираз "енантіомерний надлишок" (ее) означає продукти, які одержують асиметричним синтезом, наприклад, синтезом, який залучає нерацемічні вихідні матеріали та/або реактиви, або синтезом, який включає як мінімум один енантіоселективний етап, завдяки чому одержують надлишок одного енантіомера порядку як мінімум приблизно 52% ее. У разі відсутності асиметричного синтезу одержують, як правило, рацемічні продукти, які, однак, також мають активність як антагоністи рецептора окситоцину (OT-R) за цим винаходом. Зовсім несподівано було встановлено, що похідні піролідину за формулою І є придатними фармацевтично активними агентами, що активно модулюють, зокрема, ефективно пригнічують функцію OT-R і, більш конкретно, антагонізують рецептор окситоцину. Коли рецептор окситоцину зв'язується сполуками за формулою І, окситоцин антагонізується шляхом блокування його доступу на рецептор, завдяки чому він позбавляється можливості здійснення своїх біологічних або фармакологічних ефектів. Сполуки за цим винаходом є, таким чином, особливо придатними для лікування та/або запобігання пов'язаних з окситоцином розладів у ссавців і, зокрема, у людей. Цими розладами, які опосередковуються рецептором окситоцину, є, головним чином, передчасні пологи та дисменорея. Сполуками за цим винаходом є сполуки формули І. Згадана формула включає також їхні геометричні ізомери, їхні оптично активні форми, як енантіомери, діастереомери та їхні рацематні форми, а також їхні фармацевтично прийнятні солі. Фармацевтично прийнятними солями сполуки І, яким віддається перевага, є солі кислот, наприклад, фармацевтично прийнятних кислот, наприклад, хлористоводнева сіль, бромистоводнева сіль, сульфат або бісульфат, фосфат або кислий фосфат, ацетат, бензоат, сукцинат, фумарат, малеат, лактат, цитрат, тартрат, глюконат, метансульфонат, бензолсульфонат та пара-толуолсульфонат. У згаданій формулі І, X вибирають із групи, до складу якої входять CR6R7, NOR6, NNR6R7. А вибирають із групи, до складу якої входять -(С=О)-, -(С=О)-О-, -C(=NH)-, -(C=O)-NH-, -(C=S)-NH, -SO2-, SO2NH-, -CH2-. В представляє собою амідну групу формули -(C=O)-NR 8R9 або гетероциклічний залишок, який має формулу В1 де Q - NR10, О або S; n - ціле число, яке вибирають з-посеред 0, 1 або 2, за варіантом, якому віддається перевага, 0; m - ціле число, яке вибирають з-посеред 0, 1, 2 або 3, за варіантом, якому віддається перевага, 0 або 1. Υ, Ζ та Е, разом із 2 атомами вуглецю, до яких вони приєднані, утворюють 5-6-членне арильне або гетероарильне кільце. R1 вибирають із групи, яка складається або до складу якої входять незаміщений або заміщений С 1-С6алкіл, незаміщений або заміщений С 2-С6-алкеніл, незаміщений або заміщений С 2-С6-алкініл, незаміщений або заміщений арил, незаміщений або заміщений гетероарил, незаміщений або заміщений насичений або ненасичений 3-8-членний циклоалкіл, ацил, незаміщений або заміщений C1-С6-алкіларил, незаміщений або заміщений С 1-С6-алкілгетероарил, причому згадані циклоалкільні, арильні або гетероарильні групи можуть бути злитими з 1-2 додатковими циклоалкільними, арильними або гетероарильними групами. R2, R3, R4 та R5 незалежно один від одного вибирають із групи, до складу якої входять водень, галоген, С1С6-алкіл, С1-С6-алкоксигрупа; за варіантом, якому віддається перевага, усі вони є воднем. R6 та R7 незалежно вибирають із групи, яка складається або до складу якої входять водень, незаміщений або заміщений С 1-С6 алкіл, незаміщений або заміщений С 2-С6 алкеніл, незаміщений або заміщений С 2-С6 алкініл, незаміщена або заміщена алкоксигрупа, незаміщена або заміщена тіоалкоксигрупа, галоген, ціаногрупа, нітрогрупа, ацил, алкоксикарбоніл, амінокарбоніл, незаміщений або заміщений насичений або ненасичений 3-8-членний циклоалкіл, до складу якого може входити від 1 гетероатому до 3 гетероатомів, які вибирають з-посеред Ν, О, S, незаміщений або заміщений арил, незаміщений або заміщений гетероарил, незаміщений або заміщений С1-С6 алкіларил, незаміщений або заміщений C1-С6 алкілгетероарил. R8, R9 та R10 незалежно вибирають із групи, яка складається або до складу якої входять водень, незаміщений або заміщений C1-C6 алкіл, незаміщений або заміщений С 2-С6 алкеніл, незаміщений або заміщений С2-С6 алкініл, незаміщений або заміщений насичений або ненасичений 3-8-членний циклоалкіл, до складу якого може входити від 1 гетероатому до 3 гетероатомів, які вибирають з-посеред N, О, S, незаміщений або заміщений арил, незаміщений або заміщений гетероарил. За альтернативним варіантом кожна пара R6, R7 та/або R8, R9 може утворювати разом з атомом N, до якого вони приєднані, 3-8-членне заміщене або незаміщене, насичене або ненасичене гетероциклічне кільце, до складу якого можуть входити 1-2 додаткові гетероатоми, які вибирають з-посеред N, S та О, і яке є факультативно злитим з арильним, гетероарильним або 3-8-членним насиченим або ненасиченим циклоалкільним кільцем. R11 вибирають із групи, яка складається або до складу якої входять водень, незаміщений або заміщений С1-С6-алкіл, незаміщений або заміщений алкеніл, незаміщений або заміщений алкініл, гідроксильна група, меркаптогрупа, алкоксигрупа, тіоалкоксигрупа, арил, гетероарил, галоген, нітрогрупа, ціаногрупа, ацил, ацилоксигрупа, ациламіногрупа, амінокарбоніл, алкоксикарбоніл, сульфоніл, сульфоксигрупа, карбоксильна група, первинна, вторинна або третинна аміногрупа або складові четвертинного амонію, незаміщений або заміщений насичений або ненасичений 3-8-членний циклоалкіл. До похідних піролідину, яким віддається перевага, належать ті сполуки за формулою І, де В - гр упа -(C=O)NHR9, де R9 вибирають із групи, до складу якої входять незаміщений або заміщений C1-С6 алкіл, незаміщений або заміщений алкеніл, незаміщений або заміщений алкініл, незаміщений або заміщений насичений або ненасичений 3-6-членний циклоалкіл, до складу якого факультативно входять атом N, незаміщений або заміщений арил, незаміщений або заміщений гетероарил, незаміщений або заміщений С 1-С2-алкіларил, незаміщений або заміщений С1-С2-алкілгетероарил. Гетероарилами, яким віддається перевага, є піридил, піроліл, фурил, тієніл, імідазоліл, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, піразоліл, 1,2,3-триазоліл, 1,2,4-триазоліл, 1,2,3-оксадіазоліл, 1,2,4оксадіазоліл, 1,2,5-оксадіазоліл, 1,3,4-оксадіазоліл, 1,3,4-триазиніл, 1,2,3-триазиніл, бензофурил, [2,3дигідро]бензофурил, ізобензофурил, бензотієніл, бензотриазоліл, ізобензотієніл, 2,1,3-бензотіадіазоліл, 2,1,3бензоксадіазоліл, бензодіоксоліл, індоліл, ізоіндоліл, 3Н-індоліл, бензімідазоліл, імідазо[1,2-а]піридил, бензотіазоліл, бензоксазоліл, хінолізиніл, хіназолініл, фталазиніл, хіноксалініл, цинолініл, нафтиридиніл, піридо[3,4-b]піридил, піридо[3,2-b]піридил, піридо[4,3-b]піридил, хінолін, ізохіноліл, тетразоліл, 5,6,7,8тетрагідрохіноліл, 5,6,7,8-тетрагідроізохіноліл, пуриніл, птеридиніл, карбазоліл, ксантеніл, акридиніл або бензохіноліл, і де згаданий гетероарил може бути злитим із 3-8-членним циклоалкілом, до складу якого факультативно входять 1-3 гетероатоми, які вибирають з-посеред N, О, S. За додатковим варіантом втілення, якому віддається перевага, похідні піролідину за цим винаходом несуть залишок В1, який представляє собою злитий гетероцикл формули Похідними піролідину, яким віддається особлива перевага, є ті сполуки за формулою І, де X - NOR 6, і R6 вибирають із групи, до складу якої входять Н, незаміщений або заміщений C 1-С6 алкіл, незаміщений або заміщений С 2-С6 алкеніл, незаміщений або заміщений С 2-С6 алкініл, незаміщений або заміщений ацил, незаміщений або заміщений арил, незаміщений або заміщений гетероарил, незаміщений або заміщений насичений або ненасичений 3-8-членний циклоалкіл, незаміщений або заміщений C1-С6 алкіларил, незаміщений або заміщений C1-C6 алкілгетероарил, причому згадані циклоалкільна, арильна або гетероарильна групи можуть зливатись з 1-2 додатковими циклоалкільними, арильними або гетероарильними групами. Особлива перевага віддається R6, який є Н, СН3, незаміщений або заміщений СН2-феніл або аліл. За жодних обставин В не може бути групою COOR або групою -(C=O)NR(OR), де R - Η, алкіл або ацил. Такі сполуки, особливо сполуки, які мають групу В=гідроксамову кислоту, описані у заявці WO 99/52868 як активні інгібітори металопротеаз. Додатковими похідними піролідину, яким віддається особлива перевага, є ті сполуки за формулою І, де X CHR6 та R6 вибирають із групи, до складу якої входять галоген, ціаногрупа, незаміщений або заміщений С 3-C6 алкіл, незаміщений або заміщений С 2-С6 алкеніл, незаміщений або заміщений С 2-С6 алкініл, незаміщена або заміщена алкоксигрупа, незаміщена або заміщена тіоалкоксигрупа, нітрогрупа, ацил, алкоксикарбоніл, амінокарбоніл, незаміщений або заміщений арил, незаміщений або заміщений гетероарил, незаміщений або заміщений насичений або ненасичений 3-8-членний циклоалкіл, незаміщений або заміщений C 1-С6-алкіларил, незаміщений або заміщений C1-С6-алкілгетероарил, причому згадані циклоалкільні, арильні або гетероарильні групи можуть бути злитими з 1-2 додатковими циклоалкільними, арильними або гетероарильними групами. R6, якому віддається особлива перевага, є галоген, ціаногрупа, C1-С6 алкіл, незаміщена або заміщена фенільна група. За додатковим варіантом втілення, якому віддається перевага, похідні піролідину мають замісник А, який представляє собою -(С=О)- або -(С=О)-NH-, або -SO2-, за варіантом, якому віддається найбільша перевага, (С=О)-. Групами R1, яким віддається більша перевага, є заміщений або незаміщений C 1-С6-алкіл, С2-С6-алкеніл, незаміщений або заміщений С 2-С6-алкініл, арил, гетероарил, насичений або ненасичений 3-8-членний циклоалкіл і ще більша перевага віддається R1, який є С1-С6-алкіл або арил. Замісником R1, якому віддається особлива перевага, є дифеніл. За варіантом втілення, якому віддається найбільша перевага, похідними піролідину за формулою І є ті сполуки, де X є =NOR6 або =СНСl, R6 є C1-C6-алкіл, наприклад, метильна група, або арил, або С1-С6алкіларильна група, А є -(С=О )- та R1 є C1-С6-алкіл або арил, або C1-С6-алкіларильна група. Ще більша перевага віддається тим похідним піролідину, де X є =NOR6 або =СНСl, R6 є метил, В є амідна група формули -(C=O)NHR 9, де R9 - незаміщена або заміщена С 1-С6-алкіларильна група, наприклад, заміщена фенілетильна група, А - -(С=О)- та R 1 - заміщена або незаміщена дифенільна або ацетилметильна група. Сполуки формули І можуть мати один або декілька асиметричних центрів і, завдяки цьому, існувати у вигляді енантіомерів або діастереоізомерів. Слід розуміти, що цей винахід включає як суміші, так і окремі індивідуальні ізомери або енантіомери сполук формули І. За варіантом втілення, якому віддається особлива перевага, похідні піролідину за формулою І одержують з енантіомерним надлишком, який становить як мінімум 52% ее, за варіантом, якому віддається перевага, як мінімум 92-98% ее. Цей винахід включає також E/Z ізомери, які відносно похідних піролідину мають залишки X, які представляють собою =CR6R7, де обидва R6R7 відрізняються один від одного, та/або відносно похідних піролідину мають залишки X, які представляють собою =NOR6 або =NNR6R7. Конкретними прикладами сполук формули І є наведені далі: (2S,4ЕZ)-1-([1,1¢-дифеніл]-4-ілкарбоніл)-N-(2-метоксіетил)-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(хлорметилен)-N-[(2RS)-2-гідрокси-2-фенетил]-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-(2-гідроксіетил)-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-фенетил]-4-(метоксііміно)-2піролідинкарбоксамід (3ЕZ,5S)-5-(1Н-бензімідазол-2-іл)-1-([1,1'-дифеніл]-4-ілкарбоніл)-3-піролідинон О-метилоксим (2S,4ЕZ)-N-(2,1,3-бензотіадіазол-4-іл)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-N-(6-хінолініл)-2-піролідинкарбоксамід (2S,4ЕZ)-1-ацетоацетил-N-бензил-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(хлорметилен)-N-(2-фурилметил)-2-піролідинкарбоксамід (2S,4ЕZ)-1-[(4-хлорфенокси)ацетил]-4-{[(3,4-дихлорбензил)окси]іміно}-N-[(2RS)-2-гідрокси-2-фенетил]-2піролідинкарбоксамід (2S,4ЕZ)-N-аліл-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-N-(2-тієнілметил)-2-піролідинкарбоксамід (2S,4ЕZ)-4-(ціанометилен)-N-(2-фурилметил)-1-[(2-оксо-6-пентил-2Н-піран-3-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-(2-фурилметил)-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-ацетил-N-циклопропіл-4-{[(3,4-дихлорбензил)окси]іміно}-2-піролідинкарбоксамід (2S,4ЕZ)-N-(2-фурилметил)-4-(метоксііміно)-1-[(2-оксо-6-пентил-2Н-піран-3-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-N-бензил-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-N-метил-2-піролідинкарбоксамід (2S,4ЕZ)-1-(дифенілацетил)-4-(етоксііміно)-N-(2-тієнілметил)-2-піролідинкарбоксамід (2S,4ЕZ)-N-(2,1,3-бензотіадіазол-4-іл)-4-(ціанометилен)-1-(дифенілацетил)-2-піролідинкарбоксамід (3Е2,5S)-5-(1Н-бензімідазол-2-іл)-1-(дифенілацетил)-3-піролідинон О-метилоксим (2S)-2-[1-([1,1'-дифеніл]-4-ілкарбоніл)-4-метилен-2-піролідиніл]-1Н-бензимідазол (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(хлорметилен)-N-(2-метоксіетил)-2-піролідинкарбоксамід (3ЕZ,5S)-5-(1Н-бензимідазол-2-іл)-1-(дифенілацетил)-3-піролідинон О-алілоксим (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[2-(діетиламіно)етил]-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-(дифенілацетил)-4-{[(4-метоксибензил)окси]іміно}-N-(2-тієнілметил)-2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-(3,4-диметоксибензил)-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-ацетоацетил-4-(метоксііміно)-N-(1-нафтилметил)-2-піролідинкарбоксамід (2S,4ЕZ)-N-аліл-4-{[(3,4-дихлорбензил)окси]іміно}-1-(дифенілацетил)-2-піролідинкарбоксамід (2S,4ЕZ)-4-{[(3,4-дихлорбензил)окси]іміно}-N1-пентил-N2-(6-хінолініл)-1,2-піролідиндикарбоксамід (2S,4ЕZ)-4-(хлорметилен)-1-(дифенілацетил)-N-[(2RS)-2-гідрокси-2-фенетил]-2-піролідинкарбоксамід (2S)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-фенетил]-4-метилен-2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(хлорметилен)-N-(6-хінолініл)-2-піролідинкарбоксамід (2S,4ЕZ)-4-бензиліден-N-[2-(діетиламіно)етил]-1-(дифенілацетил)-2-піролідинкарбоксамід (2S,4ЕZ)-1-ацетоацетил-4-(метоксііміно)-N-(2-тієнілметил)-2-піролідинкарбоксамід (2S,4ЕZ)-1-ацетил-4-{[(3,4-дихлорбензил)окси]іміно}-N-[(2RS)-2-гідрокси-2-фенетил]-2піролідинкарбоксамід (2S,4EZ)-4-{[(3,4-диxлopбeнзил)oкcи]iмiнo}-N1-(3,5-диxлopфeнiл)-N2-(6-хінолініл)-1,2піролідиндикарбоксамід (2S,4ЕZ)-4-(метоксііміно)-N-(1-нафтилметил)-1-(феноксіацетил)-2-піролідинкарбоксамід (2S,4ЕZ)-4-(хлорметилен)-N-(3,4-диметоксибензил)-1-[(2-оксо-6-пентил-2Н-піран-3-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-1-(дифенілацетил)-4-(метоксііміно)-N-(2-тієнілметил)-2-піролідинкарбоксамід (2S,4ЕZ)-N-бензил-1-(дифенілацетил)-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-{[(3,4-дихлорбензил)окси]іміно}-N-[2-(діетиламіно)етил]-2піролідинкарбоксамід (2S,4ЕZ)-4-{[(3,4-дихлорбензил)окси]іміно}-1-[4-(диметиламіно)бутаноіл]-N-(6-хінолініл)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-(5-етил-1,3,4-тіадіазол-2-іл)-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-N-бензил-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-N-бензил-1-(дифенілацетил)-4-(етоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-N2-циклопропіл-4-{[(3,4-дихлорбензил)окси]іміно}-N1-(3-метоксифеніл)-1,2піролідиндикарбоксамід (2S,4EZ)-1-(дифeнiлaцeтил)-N-[(2RS)-2-гiдpoкcи-2-фeнeтил]-4-{[(4-метоксибензил)окси]іміно}-2піролідинкарбоксамід (2S)-N-(2-фурилметил)-4-метилен-1-[(2-оксо-6-пентил-2Н-піран-3-іл)карбоніл]-2-піролідинкарбоксамід (2S,4ЕZ)-N-(2,1,3-бензотіадіазол-4-іл)-1-(дифенілацетил)-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-N-бензил-1-(дифенілацетил)-4-{[(4-метоксибензил)окси]іміно}-2-піролідинкарбоксамід (2S,4ЕZ)-1-бензоїл-4-{[(3,4-дихлорбензил)окси]іміно}-N-(6-хінолініл)-2-піролідинкарбоксамід (2S,4ЕZ)-1-ацетоацетил-N-циклопропіл-4-{[(3,4-дихлорбензил)окси]іміно}-2-піролідинкарбоксамід (2S,4ЕZ)-4-{[(3,4-дихлорбензил)окси]іміно}-N2-[(2RS)-2-гідрокси-2-фeнeтил]-N1-пeнтил-1,2пipoлiдиндикapбoкcaмiд (2S,4ЕZ)-1-[(бензилокси)іміно]-N-(1-нафтилметил)-1-(феноксіацетил)-2-піролідинкарбоксамід (2S)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-метилен-N-(6-хінолініл)-2-піролідинкарбоксамід (2S,4ЕZ)-N-циклопропіл-4-{[(3,4-дихлорбензил)окси]іміно}-1-(дифенілацетил)-2-піролідинкарбоксамід (2S,4ЕZ)-1-(4-ціанобензоїл)-4-{[(3,4-дихлорбензил)окси]іміно}-N-(6-хінолініл)-2-піролідинкарбоксамід (2S,4ЕZ)-N-циклопропіл-4-{[(3,4-дихлорбензил)окси]іміно}-1-(метоксіацетил)-2-піролідинкарбоксамід (2S,4ЕZ)-N-(1,3-бензодіоксол-5-ілметил)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-2піролідинкарбоксамід (3ЕZ,5S)-5-[(4-ацетил-1-піперазиніл)карбоніл]-1-акрилоїл-3-піролідинон О-(3,4-дихлорбензил)оксим (2S)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-(2-фурилметил)-4-метилен-2-піролідинкарбоксамід (2S,4ЕZ)-4-(ціанометилен)-N-(3,4-диметоксибензил)-1-[(2-оксо-6-пентил-2Н-піран-3-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-3-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-(4-бензоїлбензоїл)-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-(3-феноксибензоїл)-2-піролідинкарбоксамід (2S,4EZ)-N-[(2RS)-2-гiдpoкcи-2-фeнiлeтил]-4-(мeтoкciiмiнo)-1-(2-феноксибензоїл)-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-N-[(2R)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-N-(2-гідроксіетил)-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-N-(2-гідроксіетил)-4-(метоксііміно)-N-метил-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕN)-1-([1,1'-дифеніл]-4-ілсульфоніл)-N-[(1S,2S,3R,4R)-3-(гідроксиметил)біцикло[2.2.1]гепт-2-іл]-4(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-(транс-4-гідроксициклогексил)-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(1R,2R)-2-(гідроксиметил)циклогексил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-3-феноксипропіл]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-гідрокси-3-феноксипропіл]-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілсульфоніл)-N-[(2RS)-2-гідрокси-3-феноксипропіл]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-(4-гідроксифеніл)етил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілсульфоніл)-N-[(2RS)-2-гідрокси-2-(4-гідроксифеніл)етил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(1-гідроксициклогексил)метил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4EZ)-N-[(1-гідроксициклогексил)метил]-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілсульфоніл)-N-[(1-гідроксициклогексил)метил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-(3,4-дигідроксифеніл)-2-гідроксіетил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[4-(4-піридиніл)бензоїл]-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[4-(2-пірвдиніл)бензоїл]-2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2,3-дигідроксипропіл]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілсульфоніл)-N-[(2RS)-2,3-дигідроксипропіл]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-3-(4-метоксифенокси)пропіл]-4-(метоксііміно)2-піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-гідрокси-3-(4-метоксифенокси)пропіл]-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілсульфоніл)-N-[(2RS)-2-гідрокси-3-(4-метоксифенокси)пропіл]-4-(метоксііміно)2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-Z-[(2RS)-2-гідроксипропіл]-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4EZ)-1-([1,1'-дифеніл]-4-ілсульфоніл)-N-[(2RS)-2-гідроксипропіл]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілсульфоніл)-N-[(2RS)-2-гідрокси-2-(2-нафтил)етил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-(4-нітрофеніл)етил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(4-нітрофеніл)етил]-4-(метоксііміно)-1-[4-(4-піридиніл)бензоїл]-2піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(4-нітрофеніл)етил]-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]-2піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(4-нітрофеніл)етил]-4-(метоксііміно)-1-[4-(2-піридиніл)бензоїл]-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілсульфоніл)-N-[(2RS)-2-гідрокси-2-(4-нітрофеніл)етил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-N-{(2RS)-3-[4-(ацетиламіно)фенокси]-2-гідроксипропіл}-1-([1,1'-дифеніл]-4-ілкарбоніл)-4(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-N-{(2RS)-3-[4-(ацетиламіно)фенокси]-2-гідроксипропіл}-4-(метоксііміно)-1-[4-(4-піридиніл)бензоїл]2-піролідинкарбоксамід (2S,4ЕZ)-N-{(2RS)-3-[4-(ацетиламіно)фенокси]-2-гідроксипропіл}-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]2-піролідинкарбоксамід (2S,4ЕZ)-N-{(2RS)-3-[4-(ацетиламіно)фенокси]-2-гідроксипропіл}-1-([1,1'-дифеніл]-4-ілсульфоніл)-4(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(2R)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-N-[(2R)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[4-(4-піридиніл)бензоїл]-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(2R)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(2R)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[4-(2-піридиніл)бензоїл]-2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілсульфоніл)-N-[(2R)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-(3-гідроксипропіл)-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілсульфоніл)-N-(3-гідроксипропіл)-4-(метоксііміно)-2-піролідинкарбоксамід (3ЕZ,5S)-1-([1,1'-дифеніл]-4-ілкарбоніл)-5-[(4-гідрокси-4-феніл-1-піперидиніл)карбоніл]-3-піролідинон Ометилоксим (3ЕZ,5S)-5-[(4-гідрокси-4-феніл-1-піперидиніл)карбоніл]-1-[4-(4-піридиніл)бензоїл]-3-піролідинон Ометилоксим (3ЕZ,5S)-5-[(4-гідрокси-4-феніл-1-піперидиніл)карбоніл]-1-[4-(3-піридиніл)бензоїл]-3-піролідинон Ометилоксим (3ЕZ,5S)-1-([1,1'-дифеніл]-4-ілсульфоніл)-5-[(4-гідрокси-4-феніл-1-піперидиніл)карбоніл]-3-піролідинон Ометилоксим (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(1S,2S)-2-гідроксициклогексил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілсульфоніл)-N-[(1S,2S)-2-гідроксициклогексил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-N-бензил-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-(2-гідроксіетил)-4-(метоксііміно)-2піролідинкарбоксамід (2S,4EZ)-N-бензил-N-(2-гідроксіетил)-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]-2-піролідинкарбоксамід (3ЕZ,5S)-1-([1,1'-дифеніл]-4-ілкарбоніл)-5-{(3RS)-3-гідроксипіперидиніл]карбоніл}-3-піролідинон Ометилоксим (3ЕZ,5S)-5-{[(3RS)-3-гідроксипіперидиніл]карбоніл}-1-[4-(4-піридиніл)бензоїл]-3-піролідинон О-метилоксим (3ЕZ,5S)-5-{[(3RS)-3-гідроксипіперидиніл]карбоніл}-1-[4-(3-піридиніл)бензоїл]-3-піролідинон О-метилоксим (3ЕZ,5S)-1-([1,1'-дифеніл]-4-ілсульфоніл)-5-{[(3RS)-3-гідроксипіперидиніл]карбоніл}-3-піролідинон Ометилоксим (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(1S,2S)-2-гідрокси-1-(гідроксиметил)-2-фенілетил]-4(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(1S,2S)-2-гідрокси-1-(гідроксиметил)-2-фенілетил]-4-(метоксііміно)-1-[4-(4-піридиніл)бензоїл]-2піролідинкарбоксамід (2S,4ЕZ)-N-[(1S,2S)-2-гідрокси-1-(гідроксиметил)-2-фенілетил]-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілсульфоніл)-N-[(1S,2S)-2-гідрокси-1-(гідроксиметил)-2-фенілетил]-4(метоксііміно)-2-піролідинкарбоксамід (2S,4EZ)-N-(2-аніліноетил)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4EZ)-N-(2-аніліноетил)-4-(метоксііміно)-1-[4-(4-піридиніл)бензоїл]-2-піролідинкарбоксамід (2S,4EZ)-N-(2-аніліноетил)-4-(метоксііміно)-1-[4-(3-піридиніл)бензоїл]-2-піролідинкарбоксамід (2S,4EZ)-N-(2-аніліноетил)-4-(метоксііміно)-1-[4-(2-піридиніл)бензоііл]-2-піролідинкарбоксамід (2S,4EZ)-N-(2-аніліноетил)-1-([1,1'-дифеніл]-4-ілсульфоніл)-4-(метоксііміно)-2-піролідинкарбоксамід (3ЕZ,5S)-1-([1,1'-дифеніл]-4-ілкарбоніл)-5-[(4-гідрокси-1-піперидиніл)карбоніл]-3-піролідинон О-метилоксим (3ЕZ,5S)-1-([1,1'-дифеніл]-4-ілсульфоніл)-5-[(4-гідрокси-1-піперидиніл)карбоніл]-3-піролідинон О метилоксим (2S,4EZ)-N-[(1S,2R,3S,4R)-3-(амінокарбоніл)біцикло[2.2.1]гепт-3-ен-2-іл]-1-([1,1'-дифеніл]-4-ілсульфоніл)-4(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-N-(3-аміно-3-оксопропіл)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4EZ)-N-[(1S,2S,3R,4R)-3-(амінокарбоніл)біцикло[2.2.1]гепт-5-ен-2-іл]-1-([1,1'-дифеніл]-4-ілсульфоніл)-4(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-(4-гідроксибутил)-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілсульфоніл)-N-(4-гідроксибутил)-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілсульфоніл)-N-[(1R,2R)-2-(гідроксиметил)циклогексил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілсульфоніл)-N-[(1R,2S,3R,4S)-3-(гідроксиметил)біцикло[2.2.1]гепт-2-іл]-4(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілсульфоніл)-N-[(1R,2S)-2-(гідроксиметил)циклогексил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4E та 4Z)-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4E та 4Z)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4E та 4Z)-N-[(2R)-2-гiдpoкcи-2-фeнiлeтил]-4-(мeтoкciiмiнo)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(1R,2S)-2-(гідроксиметил)циклогексил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[2-гідрокси-1-(гідроксиметил)етил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4EZ)-N-[(1S,2R,3S,4R)-3-(амінокарбоніл)біцикло[2.2.1]гепт-5-ен-2-іл]-1-([1,1'-дифеніл]-4-ілкарбоніл]-4(метоксііміно)-2-піролідинкарбоксамід (2S,4EZ)-N-[(1S,2S,3R,4R)-3-(амінокарбоніл)біцикло[2.2.1]гепт-5-ен-2-іл]-1-([1,1'-дифеніл]-4-ілкарбоніл]-4(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл]-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2піролідинкарбоксамід (2RS)-3-({[(2S,4EZ)-1-([1,1'-дифeнiл]-4-iлкapбoнiл)-4-(метоксііміно)піролідиніл]карбоніл}аміно)-2гідроксипропанова кислота (2S,4ЕZ)-N-[(1R,2S)-2-(амінокарбоніл)циклогексил]-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(1RS)-2-гідрокси-1-метилетил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(1S,2S)-2-гідрокси-1-(гідроксиметил)-2-(4-нітрофеніл)етил]-4(метоксііміно)-2-піролідинкарбоксамід 4-({[(2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)піролідиніл]карбоніл}аміно)бутанова кислота (2S,4ЕZ)-N-[(2S)-2-гідрокси-2-фенілетил]-1-[(2'-метокси[1,1'-дифеніл]-4-іл)карбоніл]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(2-нафтил)етил]-1-[(2'-метокси[1,1'-дифеніл]-4-іл)карбоніл]-4-(метоксііміно)2-піролідинкарбоксамід (2S,4ЕZ)-N-[(1RS)-2-гідрокси-1-метилетил]-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-N-[(1R,2S)-2-гідрокси-1-(гідроксиметил)-2-(4-нітрофеніл)етил]-4-(метоксііміно)-1-[(2'-метил[1,1'дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(1S,2S)-2-гідрокси-1-(гідроксиметил)-2-(4-нітрофеніл)етил]-4-(метоксііміно)-1-[(2'-метокси[1,1'дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід (3ЕZ,5S)-5-[(4-гідрокси-1-піперидиніл)карбоніл]-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-3-піролідинон Ометилоксим (2S,4EZ)-N-[(1S,2S,3R,4R)-3-(амінокарбоніл)біцикло[2.2.1]гепт-5-ен-2-іл]-4-(метоксііміно)-1-[(2'-метил[1,1'дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-фенілетил]-1-[(2'-метокси[1,1'-дифеніл]-4-іл)карбоніл]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4EZ)-N-[(2RS)-2-гідроксипропіл]-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2,3-дигідроксипропіл]-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-N-(3-гідроксипропіл)-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-N-(2-аміно-2-оксоетил)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)]-2-піролідинкарбоксамід (2S,4ЕZ)-N-(2-аміно-2-оксоетил)-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-(3-гідроксифеніл)етил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-іл)карбоніл]-N-[(1S,2R,3S,4R)-3-(гідроксиметил)біцикло[2.2.1]гепт-2-іл]-4(метоксііміно)-2-піролідинкарбоксамід (2S,4EZ)-N-[(1R,2S,3R,4S)-3-(гідроксиметил)біцикло[2.2.1]гепт-2-іл]-1-[(2'-метокси[1,1'-дифеніл]-4іл)карбоніл]-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-N-(транс-4-гідроксициклогексил)-1-[(2'-метокси[1,1'-дифеніл]-4-іл)карбоніл]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-N-[(1R,2R)-2-(гідроксиметил)циклогексил]-1-[(2'-метокси[1,1'-дифеніл]-4-іл)карбоніл]-4(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-гідрокси-3-феноксипропіл]-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4EZ)-N-[(2RS)-2-гiдpoкcи-2-(4-гiдpoкcифeнiл)eтил]-4-(мeтoкciiмiнo)-1-[(2'-метил[1,1'-дифеніл]-4іл)карбоніл]-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(4-гідроксифеніл)етил]-4-(метоксііміно)-1-[(2'-метокси[1,1'-дифеніл]-4іл)карбоніл]-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(4-гідрокси-3-метоксифеніл)етил]-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-4(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(4-гідрокси-3-метоксифеніл)етил]-1-[(2'-метокси[1,1'-дифеніл]-4-іл)карбоніл]4-(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-(3,4-дигідроксифеніл)-2-гідроксіетил]-1-[(2'-метокси[1,1'-дифеніл]-4-іл)карбоніл]-4(метоксііміно)-2-піролідинкарбоксамід (2R,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл]-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2піролідинкарбоксамід (2R,4EZ)-N-[(2RS)-2-гiдpoкcи-2-фeнiлeтил]-4-(мeтoкciiмiнo)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-1-[(2'-ціано[1,1'-дифеніл]-4-іл)карбоніл]-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-[(3',4'-дихлоро[1,1'-дифеніл]-4-іл)карбоніл]-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-[(2',6'-диметил[1,1'-дифеніл]-4-іл)карбоніл]-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-[(2',3-диметил[1,1-дифеніл]-4-іл)карбоніл]-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(3-гідроксифеніл)етил]-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4іл)карбоніл]-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(3-гідроксифеніл)етил]-4-(метоксііміно)-1-[(2'-ціано[1,1'-дифеніл]-4іл)карбоніл]-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(3-гідроксифеніл)етил]-4-(метоксііміно)-1-[(3',4'-дихлоро[1,1'-дифеніл]-4іл)карбоніл]-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(3-гідроксифеніл)етил]-4-(метоксііміно)-1-[(2',6'-диметил[1,1'-дифеніл]-4іл)карбоніл]-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(2RS)-2-гідрокси-2-(3-гідроксифеніл)етил]-4-(метоксііміно)-1-[(2',3-диметил[1,1'-дифеніл]-4іл)карбоніл]-2-піролідинкарбоксамід (2S,4ЕZ)-1-[(3',4'-дихлоро[1,1'-дифеніл]-4-іл)карбоніл]-N-[(2RS)-2-гідрокси-2-(4-гідроксифеніл)етил]-4(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-[(2',6'-диметил[1,1'-дифеніл]-4-іл)карбоніл]-N-[(2RS)-2-гідрокси-2-(4-гідроксифеніл)етил]-4(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-[(2',3-диметил[1,1'-дифеніл]-4-іл)карбоніл]-N-[(2RS)-2-гідрокси-2-(4-гідроксифеніл)етил]-4(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-[(2',6'-диметил[1,1'-дифеніл]-4-іл)карбоніл]-N-[(2RS)-2-гідрокси-3-(4-метоксифенокси)пропіл]-4(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-[(2',3-диметил[1,1'-дифеніл]-4-іл)карбоніл]-N-[(2RS)-2-гідрокси-3-(4-метоксифенокси)пропіл]-4(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-N-(2-аміно-2-оксоетил)-1-[(2',6'-диметил[1,1'-дифеніл]-4-іл)карбоніл]-(4-метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-N-(2-аміно-2-оксоетил)-1-[(2',3-диметил[1,1'-дифеніл]-4-іл)карбоніл]-(4-метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-N-(3-аміно-3-оксопропіл)-1-[(2',6'-диметил[1,1'-дифеніл]-4-іл)карбоніл]-(4-метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-N-(3-аміно-2-оксопропіл)-1-[(2',3-диметил[1,1'-дифеніл]-4-іл)карбоніл]-(4-метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-[(2',6'-диметил[1,1'-дифеніл]-4-іл)карбоніл]-N-[2-гідрокси-1-(гідроксиметил)етил]-4(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-[(2',3-диметил[1,1'-дифеніл]-4-іл)карбоніл]-N-[2-гідрокси-1-(гідроксиметил)етил]-4-(метоксііміно)2-піролідинкарбоксамід (2S,4ЕZ)-1-[(2'-ціано[1,1'-дифеніл]-4-іл)карбоніл]-N-[(1R,2R)-2-(гідроксиметил)-циклогексил]-4(метоксііміно)-2-піролідинкарбоксамід (3ЕZ,5S)-5-(3,4-дигідро-2(1Н)-ізохінолінілкарбоніл)-1-[(2',3-диметил[1,1'-дифеніл]-4-іл)карбоніл]-3піролідинон О-метилоксим (2S,4ЕZ)-N-[(1R)-2-гідрокси-1-фенілетил]-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-1-[(2',6'-диметил[1,1'-дифеніл]-4-іл)карбоніл]-N-[2-(4-гідроксифеніл)етил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-[(2',3-диметил[1,1'-дифеніл]-4-іл)карбоніл]-N-[2-(4-гідроксифеніл)етил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-[(2',6'-диметил[1,1'-дифеніл]-4-іл)карбоніл]-N-[2-(3-гідроксифеніл)етил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-[(2',3-диметил[1,1'-дифеніл]-4-іл)карбоніл]-N-[2-(3-гідроксифеніл)етил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-[(2',3-диметил[1,1'-дифеніл]-4-іл)карбоніл]-N-[(1R,2S)-2-гідрокси-1,2-дифенілетил]-4(метоксііміно)-2-піролідинкарбоксамід (2RS)-2-[({(2S,4ЕZ)-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]піролідиніл}карбоніл)аміно]-3фенілпропанова кислота (2S,4ЕZ)-N-[(1R,2S)-2-(амінокарбоніл)циклогексил]-1-[(2',6'-диметил[1,1'-дифеніл]-4-іл)карбоніл]-4(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(1R,2S)-2-(амінокарбоніл)циклогексил]-1-[(2',3-диметил[1,1'-дифеніл]-4-іл)карбоніл]-4(метоксііміно)-2-піролідинкарбоксамід 4'-{[(2S,4ЕZ)-2-{[4-(2-гідроксіетил)-1-піперазиніл]карбоніл}-4-(метоксііміно)піролідиніл]карбоніл}[1,1'дифеніл]-2-карбонітрил (3ЕZ,5S)-1-[(3',4'-дихлоро[1,1'-дифеніл]-4-іл)карбоніл]-5-{[4-(2-гідроксіетил)-1-піперазиніл]карбоніл}-3піролідинон О-метилоксим (3ЕZ,5S)-1-[(2',6'-диметил[1,1'-дифеніл]-4-іл)карбоніл]-5-{[4-(2-гідроксіетил)-1-піперазиніл]карбоніл}-3піролідинон О-метилоксим (3ЕZ,5S)-1-[(2',3-диметил[1,1'-дифеніл]-4-іл)карбоніл]-5-{[4-(2-гідроксіетил)-1-піперазиніл]карбоніл}-3піролідинон О-метилоксим (3ЕZ,5S)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-5-({4-[4-(трифторметил)феніл]-1-піперазиніл}карбоніл)-3піролідинон О-метилоксим (3ЕZ,5S)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-5-({4-[3-(трифторметил)феніл]-1-піперазиніл}карбоніл)-3піролідинон О-метилоксим (2S,4ЕZ)-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід (2S,4ЕZ)-4-(метоксііміно)-N-метил-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід (2S,4ЕZ)-4-(метоксііміно)-N,N-диметил-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(3R)-3-гідрокси-3-фенілпропіл]-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-N-[(3S)-3-гідрокси-3-фенілпропіл]-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-іл)карбоніл]-N-[(3R)-3-гідрокси-3-фенілпропіл]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-іл)карбоніл]-N-[(3S)-3-гідрокси-3-фенілпропіл]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-{[2'-(трифторметил)[1,1'-дифеніл]-4іл)карбоніл}-2-піролідинкарбоксамід (2S,4ЕZ)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-{[2'-хлоро[1,1'-дифеніл]-4-іл]карбоніл}-2піролідинкарбоксамід (2S,4ЕZ)-N-(2-гідроксифеніл)-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-N-[2-гідроксиметил)феніл]-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4ЕZ)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4E та 4Z)-1-([1,1'-дифеніл]-4-ілкарбоніл]-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-N-(2-фенілетил)-2-піролідинкарбоксамід Таким чином, сполуками, яким віддається найбільша перевага, є сполуки, вибрані із групи, до складу якої входять: (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл]-4-хлорметилен)-N-[(2RS)-2-гідрокси-2-фенетил]-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл]-N-(2-гідроксіетил)-4-(метоксііміно)-2-піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл]-N-[(2RS)-2-гідрокси-2-фенетил]-4-(метоксііміно)-2піролідинкарбоксамід (3ЕZ,5S)-5-(1Н-бензімідазол-2-іл)-1-([1,1'-дифеніл]-4-ілкарбоніл]-3-піролідинон О-метилоксим (2S,4ЕZ)-N-(2,1,3-бензотіадіазол-4-іл)-1-([1,1'-дифеніл]-4-ілкарбоніл]-4-(метоксііміно)-2піролідинкарбоксамід (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл]-4-(метоксііміно)-N-(6-хінолініл)-2-піролідинкарбоксамід (2S,4Z)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід (2S,4Е)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід Додатковий аспект цього винаходу має відношення до використання похідних піролідину за формулою І для одержання фармацевтичних композицій для лікування та/або запобігання передчасних пологів, для зупинки пологів перед розродженням шляхом кесаревого розтину та дисменореї. За варіантом, якому віддається перевага, сполуки за формулою І є придатними для модулювання функції ОТ, завдяки чому конкретно забезпечують можливість лікування та/або запобігання розладів, які опосередковуються рецептором окситоцину. Згадане лікування залучає модулювання, особливо регуляцію за типом зворотного зв'язку або антагонізування, рецептора окситоцину. Зокрема, сполуки за цим винаходом є придатними для лікування передчасних пологів, лікування дисменореї та зупинки пологів перед виконанням кесаревого розтину. Ще один додатковий аспект цього винаходу має відношення до нових сполук піролідину формули І. Перед поданням цієї заявки фактично була розкрита зовсім незначна кількість сполук, хоча і без будь-якого медичного застосування. Згаданими відомими сполуками формули І є сполуки, де X - (=СН2), А - -С=О)-О-, R1 - t-бутильна група та В - -(C=O)-N Me2 {Tetrahedron 53 (2), 539, 1997); -(C=O)NHMe (WO 95/47718); -(C=O)-NH-CH(Me)-(C=O)-NH-CH(Me)-COOH (WO 95/47718); або -(C=O)-NHCH(COOCH2-Ph)-CH2-COOPh (Tetragedron 48 (31), 6529, 1992). X - (=CHR 6), де R6 - циклогексилметил, А - -(C=O)-O-, R1 -t-бутильна група, тобто -(C=O)-NH-t (Biorg. Chem. Lett. 3 (8), 1485, 1993). X – C1-C 20 алкіліден, А - -(C=O)-O-, R 1 - t-бутил та В є де R - С1-С12 алкіл та Hal - СІ, Вr, І. Згадані сполуки розкриваються у DE-1,932,823 як проміжні продукти. X – С1-С 20 алкіліден, A-R1 - за хисна група та В є де R - Η або С 1-С12 алкіл (GB-1,118,306). Таким чином, новими сполуками є сполуки формули І, із виключенням вищезгаданих відомих сполук. Ще однією додатковою метою цього винаходу є спосіб одержання похідних піролідину за формулою І. Похідні піролідину, приклад яких наведено у цьому винаході, можна одержувати з легкодоступних вихідних матеріалів із використанням наведених далі загальних методів та процедур. Слід розуміти, що у разі, коли наведено типові або переважні експериментальні умови (тобто реакційні температури, час, молі реактивів, розчинників тощо), можуть застосовуватись також інші експериментальні умови, якщо не обумовлюється інше. Оптимальні реакційні умови можуть змінюватись у залежності від конкретних реактивів або розчинників, які використовуються, однак такі умови можуть визначатись фахівцем у цій галузі за допомогою загальноприйнятих процедур оптимізації. Взагалі, похідні піролідину за загальною формулою І можна одержати за допомогою декількох процесів із використанням протоколів як хімії розчинної фази, так і хімії твердої фази. У залежності від природи А, В та X, певним процесам, у деяких випадках, буде надаватись перевага над іншими, і припускається, що вибір найпридатнішого процесу буде відомим фахівцю у цій галузі. За одним зі способів, похідні піролідину за загальною формулою І, де замісник В - C(O)-NR8R9, причому R8 та R9 відповідають визначенню, яке було наведено перед тим, одержують із відповідних N-захищених 4заміщених похідних піролідину II, де замісник X відповідає визначенню, яке було наведено перед тим, за протоколами хімії розчинної фази, такими, наприклад, опис яких наведено у Прикладах та показано на Схемі 1 далі. Відповідні N-захищені 4-заміщені похідні піролідину II спочатку реагують із первинними або вторинними амінами III, де R8 та R9 відповідають визначенню, яке було наведено перед тим, із використанням умов та за допомогою способів, добре відомих фа хівцям у цій галузі, з одержанням аміду з аміну та карбонової кислоти або похідної карбонової кислоти, з використанням стандартних пептидних зв'язувальних речовин, таких як DIC (діізопропілкарбодіімід), EDC (етилендихлорид), TBTU (Ο-Ν,Ν,Ν',Ν'-тетраметилуронію тетрафторборат), DECP (діетилціанофосфоран) або інших з одержанням сполук формули IV. Шляхом видалення N-захисних груп за допомогою відповідних відщеплювальних речовин одержують похідні формули V. Згадані похідні можуть піддаватись обробці ацилювальними агентами загальної формули VI, де замісник R1 відповідає визначенню, яке було наведено перед тим, у той час як LG може бути будь-якою відповідною відщеплюваною групою. Ацилювальними агентами VI, яким віддається перевага, є хлорангідриди (Vla), які застосовують у сполученні із третинною амінною основою, або карбонові кислоти (VIb), які застосовують у сполученні з пептидною зв'язувальною речовиною, наприклад, із вищезгаданої групи, з одержанням продуктів загальної формули І, де В визначається як C(O)N 8R9 (la). Інші похідні формули І одержують за допомогою відомих модифікацій послідовності реакцій Схеми 1. Сполуки формули І, де А відрізняється від карбонільної функціональної групи, одержують шляхом заміни сполук формули VI сполуками, до складу яких входять відповідні функціональні групи, наприклад, сульфонілхлоридами, ізоціанатами, ізотіоціанатами, хлороформіатами, заміщеними алкілгалогенідами або іншими, з одержанням сульфонаміду, сечовини, тіосечовини, карбамату, заміщених алкільних похідних або інших, відповідно. Сполуки формули II, де замісник X - CR6R7 і R6 та R7 відповідають визначенню, яке було наведено перед тим, можна одержати зі сполук загальної формули VII за допомогою реакцій типу реакції Віттіга з аніонами фосфоранів, таких як Vllla та/або фосфонатів, таких як Vlllb, із подальшим омиленням складноефірної функціональної групи за стандартними методами синтезування, опис яких наведено далі у Прикладах та показано на Схемі 2. Сполуки загальної формули VII можна одержати з комерційно доступного придатного N-захищеного 4гідроксипроліну X за допомогою послідовності реакцій, яка включає оксидування та естерифікацію, за допомогою стандартних методів синтезування, опис яких наведено далі у Прикладах та показано на Схемі 3. Сполуки формули II, де замісник X - NOR6 або NNR6R7 і R6 та R7 відповідають визначенню, яке було наведено перед тим, можна одержати зі сполук загальної формули XI за допомогою реакції з заміщеними гідроксиламінами Хllа та/або заміщеними гідразинами та/або гідразидами ХІІb, за допомогою стандартних методів синтезування, опис яких наведено далі у Прикладах та показано на Схемі 4. Сполуки формули ХІІа є комерційно доступними або їх одержують за допомогою стандартних методів синтезування, опис яких наведено далі у Прикладах. Сполуки формули II з X=S є доступними з відповідним чином захищених похідних кетопіролідину VII завдяки стандартним способам взаємоперетворення функціональних груп, добре відомим фахівцю у цій галузі, наприклад, шляхом обробки реактивом Лоуссона або іншими (Педерсен Б.С. (Pedersen B.S.) та інші; Bull Soc. Chim. Belg. 1978, 87, 223), з подальшим омиленням. За іншим способом, похідні піролідину за загальною формулою І, де замісник В представляє собою гетероциклічний залишок В1 за визначенням, яке було наведено перед тим, і замісники відповідають визначенню, яке було наведено перед тим, одержують з відповідних N-захищених 4-заміщених похідних піролідину II, де замісник X відповідає визначенню, яке було наведено перед тим, за протоколами хімії розчинної фази, такими як протоколи, опис яких наведено у Прикладах та показано на Схемі 5 далі. Вихідні відповідно N-захищені 4-заміщені похідні піролідину II спочатку реагують з орто-заміщеними первинними анілінами загальної формули XIII, де замісники Q, Ζ, Ε, Υ та R11 відповідають визначенню, яке було наведено перед тим, із застосуванням стандартних пептидних зв'язувальних речовин, таких як DIC, EDC, TBTU, DECP або інших, з подальшим підданням дії розбавленої слабкої кислоти, такої як оцтова кислота, у придатному органічному розчиннику, такому як DCM (дихлорметан), зі стимулюванням циклізації, наслідком якої є одержання сполук формули XIV. Наслідком видалення N-захисної групи за допомогою відповідних відщеплювальних речовин є одержання циклічних похідних формули XV. Згадані циклічні похідні можуть піддаватись обробці ацилювальними агентами загальної формули VI, де замісник R1 відповідає визначенню, яке було наведено перед тим, у той час як LG може бути будь-якою відповідною відщеплюваною групою. До ацилювальних агентів VI, яким віддається перевага, належать хлорангідриди (Vla), які застосовують у сполученні з третинною амінною основою, або карбонові кислоти (VIb), які застосовують у сполученні з пептидною зв'язувальною речовиною, наприклад, з вищезгаданої групи, з одержанням продуктів загальної формули І, де В визначається як В1 (Іb). Інші похідні формули І одержують за допомогою відомих модифікацій послідовності реакцій Схеми 5. Сполуки формули І, де А відрізняється від карбонільної функціональної групи, одержують шляхом заміни сполук формули VI сполуками, до складу яких входять відповідні функціональні групи, наприклад, сульфонілхлоридами, ізоціанатами, ізотіоціанатами, хлороформіатами, заміщеними алкілгалогенідами або іншими, з одержанням сульфонаміду, сечовини, тіосечовини, карбамату, заміщених алкільних похідних або інших, відповідно. За іншим загальним способом, узагальнення якого наведено на Схемі 6, похідні піролідину за загальною формулою І, де замісники А, В, X та R1 відповідають визначенню, яке було наведено перед тим, одержують зі сполук формули XVI за допомогою способів синтезу, які у загальних рисах наведено на Схемах 2 та 4. Як додатково показано на Схемі 6, сполуки формули XVI є доступними або з XI, за допомогою, наприклад, методологій синтезу, які було введено на Схемах 1 або 5, або з Іс шляхом гідролізу метилоксимової складової, наприклад, за м'яких умов гідролізу, як описується далі у Прикладах. Представленій стратегії синтезу віддається найбільша перевага у разі, коли X - NOH або NNR6R7, де замісники R6 та R7 відповідають визначенню, яке було наведено перед тим. За ще одним способом, похідні піролідину за загальною формулою І, де замісники А, В, X та R 1 відповідають визначенню, яке було наведено перед тим, одержують із придатних N-захищених 4-заміщених похідних піролідину II, де замісник X відповідає визначенню, яке було наведено перед тим, за твердофазним протоколом, який, наприклад, описано у Прикладах та показано на Схемі 7 далі. N-Вос-захищена 4-заміщена похідна піролідину II реагує, наприклад, з оксимовою смолою Кайзера за стандартних карбодіімідопосередкованих умов сполучення, добре відомих фахівцю у цій галузі, з подальшим відщепленням Вос-захисної групи розбавленою TFA (трифтороцтова кислота) у DCM або BF3·OEt 2 у розбавленій НОАс у DC M з одержанням сполуки XIX. Останню згадану сполуку можна піддавати обробці ацилювальними агентами загальної формули VI, де замісник R1 відповідає визначенню, яке було наведено перед тим, у той час як LG може бути будь-якою відповідною відщеплюваною групою. До ацилювальних агентів VI, яким віддається перевага, належать хлорангідриди (Vla), які застосовують у сполученні із третинною амінною основою, або карбонові кислоти (VIb), які застосовують у сполученні з пептидною зв'язувальною речовиною, наприклад, DIC або EDC, з одержанням продуктів загальної формули XX. Сполуки формули І, де А відрізняється від карбонільної функціональної групи, одержують шляхом заміни сполук формули VI сполуками, до складу яких входять відповідні функціональні групи, наприклад, сульфонілхлоридами, ізоціанатами, ізотіоціанатами, хлороформіатами, заміщеними алкілгалогенідами або іншими, з одержанням сульфонаміду, сечовини, тіосечовини, карбамату, заміщених алкільних похідних або інших, відповідно. З метою одержання кінцевих сполук загальної формули І, зв'язок зі смолою розщеплюється шляхом тривалої обробки амінами загальних формул III або XIII та низькими відсотками слабкої кислоти, такої як НОАс. Цикли у межах наведеної далі Схеми 7 ілюструють кульки смоли, з якими відповідні сполуки зв'язуються під час твердофазного синтезу. Інші похідні формули І одержують за допомогою відомих модифікацій або варіантів послідовності реакцій Схеми 7. На додаток до вищезгаданої оксимової смоли Кайзера для твердофазного синтезу сполук загальної формули І можуть використовуватись інші відповідні реактиви, особливо смоли, відомі фахівцю у цій галузі. Послідовності реакцій, надані у загальних рисах на вищенаведених Схемах, забезпечують одержання енантіомерно чистих сполук формули І у разі використання енантіомерно чистих вихідних матеріалів. (R), а також (S) енантіомери можуть одержуватись у залежності від використання (R) або (S) форм комерційно доступних сполук формул II, III, VI та/або X як вихідних матеріалів. Однак реакційні послідовності, наведені у загальних рисах на вищенаведених Схемах, забезпечують, як правило, одержання сумішей (Е) та (Z) ізомерів відповідно до замісників на позакільцевому подвійному місточковому зв'язку піролідинового кільця. В усіх випадках, які піддавались вивченню, ці (E)/(Z)-ізомери можуть відокремлюватись стандартними хроматографічними методами, добре відомими фахівцю у цій галузі, наприклад, за допомогою високоефективного рідинного хроматографування з оберненою фазою (HPLC) або флеш-хроматографування на силікагелі (FC). Визначення абсолютної конфігурації позакільцевого подвійного місточкового зв'язку здійснювали за допомогою методів ЯМР, добре описаних у літературі, а також відомих фа хівцю у цій галузі (для визначення конфігурації, наприклад, оксимових функціональних гр уп, дивись, наприклад, Е. Брайтмайєр (Е. Breitmaier), В. Велтер (W. Voelter), Carbon-13 NMR Spectroscopy, 3 видання, VCH, 1987, стор.240). За додатковим загальним способом, сполуки формули І можна перетворювати на альтернативні сполуки формули І за допомогою придатних методів взаємоперетворення, наприклад, методів, опис яких наведено у подальших Прикладах. У разі, якщо наведені перед тим загальні способи синтезу є непридатними для одержання сполук за формулою І та/або необхідних проміжних сполук для синтезу сполук формули І, слід використовувати придатні способи одержання, відомі фахівцю у цій галузі. Взагалі, шляхи синтезу для одержання будь-якої окремої сполуки формули І будуть залежати від конкретних замісників кожної молекули та від легкодоступності необхідних проміжних продуктів; знову-таки, такі фактори є зрозумілими для пересічних фа хівців у цій галузі. Усі способи захисту та відщеплення захисних груп дивись Філіп Дж. Коцінські (Philip J. Kocienski) у "Protecting Groups", Georg Thieme Verlag Stuttgart, Нью-Йорк, 1994 та Теодора У. Грін (Theodora W. Greene) та Пітер Г.М. Вутс (Peter G.M. Wuts) у "Protecti ve Groups in Organic Synthesis", Wiley-Interscience, 1991. Сполуки за цим винаходом можуть виділятись разом із молекулами розчинника шляхом кристалізації у разі випарювання відповідного розчинника. Фармацевтично прийнятні солі кислот зі сполуками формули І, що включають основний центр, можуть одержуватись традиційним способом. Наприклад, розчин вільної основи може оброблятись придатною кислотою, нерозбавленою або у придатному розчині, і одержана сіль виділятись фільтруванням або випарюванням під вакуумом реакційного розчинника. Фармацевтично прийнятні солі основ можуть одержуватись аналогічним способом шляхом обробки розчину сполуки формули І придатною основою. Солі обох типів можуть одержуватись або взаємно перетворюватись за допомогою способів із використанням іонообмінних смол. У разі, якщо наведені перед тим загальні способи синтезу є непридатними для одержання сполук формули І, слід використовувати придатні способи одержання, відомі фахівцю у цій галузі. Кінцевий аспект цього винаходу має відношення до використання сполук за формулою І для модулювання рецептора окситоцину, використання згаданих сполук для одержання фармацевтичних композицій для модулювання рецептора окситоцину, а також композицій, до складу яких входять активні сполуки за формулою І. Згадане модулювання рецептора окситоцину розглядається як відповідний підхід до запобігання передчасних пологів та лікування дисменореї. Таким чином, сполуки за цим винаходом є придатними для запобігання передчасних пологів та лікування дисменореї. У разі використання як фармацевтичних препаратів, похідні піролідину за цим винаходом, як правило, вводять у формі фармацевтичної композиції. Таким чином, фармацевтичні композиції, до складу яких входять сполука формули І та фармацевтично прийнятний носій, розріджувач або наповнювач, також входять до обсягу цього винаходу. Фахівцю у цій галузі є відомим цілій ряд таких сполук-носіїв, розріджувачів або наповнювачів, придатних для одержання фармацевтичної композиції. Цей винахід надає також сполуки для використання як медичний засіб. Зокрема, цей винахід надає сполуки формули І для використання як антагоністи рецептора окситоцину, для лікування або запобігання розладів, які опосередковуються рецептором окситоцину у ссавців, особливо людей, самостійно або у поєднанні з іншими лікарськими засобами, наприклад, у поєднанні з додатковим антагоністом ОТ. Сполукам за цим винаходом, разом з ад'ювантом, носієм, розріджувачем або наповнювачем, які традиційно використовуються, може надаватись форма фармацевтичних композицій та їх одиничних доз, і у такій формі вони можуть використовуватись як тверді речовини, такі як таблетки або наповнені капсули, або рідини, такі як розчини, суспензії, емульсії, еліксири або капсули, наповнені цими композиціями, усі для перорального використання, або форма стерильних розчинів для парентерального впорскування (з включенням підшкірного використання). Такі фармацевтичні композиції та їх одиничні дози можуть включати інгредієнти у відповідних пропорціях, з або без додання активних сполук або активних елементів, і до складу таких одиничних дозованих лікарських форм може входити будь-яка придатна ефективна кількість активного інгредієнта, пропорційна бажаному діапазону денної дози до застосування. У разі використання як фармацевтичні засоби, похідні піролідину за цим винаходом вводять, як правило, у формі фармацевтичної композиції. Такі композиції можна одержати способом, добре відомим у фармацевтичній галузі, і до їх складу може входити як мінімум одна активна сполука. Взагалі, сполуки за цим винаходом вводяться у фармацевтично ефективній кількості. Кількість сполуки, яка фактично вводиться, буде, як правило, визначатись лікарем із прийняттям до уваги відповідних обставин, у тому числі стан у до лікування, обраного шляху введення, фактичної сполуки, яка вводиться, віку, маси та реакції індивідуального пацієнта, тяжкості симптомів пацієнта тощо. Фармацевтичні композиції за цим винаходом можуть вводитись цілим рядом шляхів, у тому числі пероральним, ректальним, черезшкірним, підшкірним, внутрішньом'язовим та інтраназальним. У залежності від передбачуваного шля ху доставки, сполуки за варіантом, якому віддається перевага, вводяться до складу композицій для впорскування або пероральних композицій. Композиції для перорального введення можуть бути у формі нерозфасованих рідких розчинів або суспензій, або нерозфасованих порошків. Частіше, однак, композиціям надаються одиничні дозовані лікарські форми для полегшення точного дозування. Термін "одиничні дозовані лікарські форми" означає фізично дискретні одиниці, придатні як одиничні дози для людей та інших ссавців, причому кожна одиниця включає попередньо визначену кількість активного матеріалу, розраховану на викликання необхідного терапевтичного ефекту, у поєднанні з придатним фармацевтичним наповнювачем. До типових одиничних дозованих лікарських форм належать ампули або шприци, попередньо заповнені попередньо визначеною кількістю рідких композицій, або пілюлі, таблетки, капсули тощо у разі твердих композицій. У разі таких композицій, піролідинова сполука представляє собою, як правило, меншу складову (від приблизно 0,1% (мас.) до приблизно 50% (мас.) або за варіантом, якому віддається перевага, від приблизно 1% (мас.) до приблизно 40% (мас.)), у той час як залишковою складовою є різні розчинники або носії та технологічні допоміжні речовини, придатні для забезпечення одержання бажаної дозованої лікарської форми. Рідкі лікарські форми, придатні для перорального введення, можуть містити придатний водний або неводний носій з буферами, суспендувальними та диспергувальними агентами, барвниками, ароматизаторами тощо. Тверді лікарські форми можуть містити, наприклад, будь-який з подальших інгредієнтів або сполуки подібної природи: в'яжучу речовину, таку як мікрокристалічна целюлоза, трагакантова камедь або желатина; наповнювач, такий як крохмаль або лактоза, дезінтегратор, такий як альгінова кислота, Прімогель (Primogel) або кукурудзяний крохмаль; змащувальну речовину, таку як стеарат магнію; ковзну речовину, таку як колоїдний діоксид силікону; підсолоджуючу речовину, таку як цукроза або сахарин; або коригент, такий як м'яту перцеву, метилсаліцилат або апельсиновий ароматизатор. Основу композицій для впорскування, як правило, становить стерильний фізіологічний розчин для впорскування, забуферений фосфатом фізіологічний розчин або інші носії для впорскування, відомі у цій галузі. Як згадувалось перед тим, піролідинові похідні формули І у таких композиціях є, як правило, меншою складовою, діапазон якої часто знаходиться у межах від 0,05% (мас.) до 10% (мас), у той час як залишок складається з носія для впорскування тощо. Складові композицій для перорального введення або для впорскування, опис яких було наведено перед тим, є лише репрезентативними. Додаткові матеріали, а також способи обробки тощо наводяться у Частині 8 довідника Remington's Pharmaceutical Sciences, 17 видання, 1985, Marck Publishing Company, Easton, штат Пенсільванія, який включено до цього опису як посилання. Сполуки за цим винаходом можуть також вводитись у вигляді лікарської форми пролонгованого виділення або системами доставки із пролонгованим виділенням лікарського засобу. Опис репрезентативних матеріалів пролонгованого виділення можна також знайти в матеріалах, які включено до Remington's Pharmaceutical Sciences. У подальшому цей винахід буде ілюстровано за допомогою деяких прикладів, які не мають розглядатися як такі, що обмежують обсяг цього винаходу. Дані високоефективної рідинної хроматографії (HPLC), ядерного магнітного резонансу (NMR) та мас-спектрометрії (MS), які наведено у прикладах, опис яких наводиться далі, одержували наведеним далі чином. У подальшому у супроводжувальних прикладах використовують наведені далі скорочення: хв (хвилина), год (година), г (грам), ммол (мілімоль), т.пл. (точка плавлення), екв. (еквіваленти), мл (мілілітр), мкл (мікролітри), ACN (ацетонітрил), CDCl3 (дейтерований хлороформ), сНех (циклогексани), DCM (дихлорметан), DECP (діетилціанофосфонат), DIC (діізопропілкарбодіімід), DMAP (4диметиламінопіридин), DMF (диметиламіноформамід), DMSO (диметилсульфоксид), DMSO-d6 (дейтерований диметилсульфоксид), EDC (1-(3-диметиламінопропіл)-3-етилкарбодіімід), EtOAc (етилацетат), Еt2О (діетиловий ефір), HOBt (1-гідроксибензотриазол), К2СО3 (карбонат калію), NaH (гідрид натрію), NaHCO3 (бікарбонат натрію), nBuLi (n-бутиллітій), TBTU (O-бензотриазол-N,N,N',N'-тетраметилуроніо тетрафторборат), TEA (триетиламін), TFA (трифтороцтова кислота), THF (тетрагідрофуран), MgSO4 (сульфат магнію), PetEther (петролейний ефір), к.т. (кімнатна температура). Приклади Проміжний продукт 1: (2S)-1-(трет-бутоксикарбоніл)-4-оксо-2-піролідинкарбонова кислота Технічну (2S,4R)-1-(трет-бутоксикарбоніл)-4-гідрокси-2-піролідинкарбонову кислоту (30г, 0,13мл) розчиняли у ацетоні (1500мл). До колби вставляли механічну мішалку, і розчин енергійно перемішували. Свіжий розчин 8N хромової кислоти одержували шляхом розчинення триоксиду хрому (66,7г, 0,667ммоль) у воді (40мл) із доданням концентрованої сірчаної кислоти (53,3мл) та кількості води, достатньої для доведення об'єму розчину до 115мл. Після цього 8N розчин хромової кислоти (115мл) додавали крапля за краплею впродовж 30-хвилинного проміжку часу з безперервним енергійним перемішуванням; екзотерму розчину підтримували на рівні оптимальної температури 25°С за допомогою льодяної бані. Після завершення додання хромової кислоти реакційну суміш додатково перемішували впродовж 15хв із підтримуванням оптимальної температури 25°С. Після цього реакційну суміш різко охолоджували шляхом додання метанолу (20мл). Екзотерму регулювали за допомогою льодяної бані і, у разі необхідності, безпосереднім доданням невеликої кількості подрібненого льоду до самої реакційної суміші. Реакційну суміш фільтрували через шар целіту, після чого концентрували in vacuo. Після цього одержаний кислий розчин екстрагували етилацетатом (3x300мл) і змішані органічні шари промивали розсолом (2x200мл). Органіку після цього сушили сульфатом магнію та концентрували in vacuo. Неочищений продукт перекристалізовували з етилацетату з одержанням кристалічного продукту білого кольору, (2S)-1-(трет-бутоксикарбоніл)-4-оксо-2-піролідинкарбонової кислоти (22,55г, 76%). Проміжний продукт-антипод, (2R)-1-(трет-бутоксикарбоніл)-4-оксо-2-піролідинкарбонову кислоту, одержували за таким же самим протоколом, із започаткуванням із технічної (2R,4S)-1-(трет-бутоксикарбоніл)4-гідрокси-2-піролідинкарбонової кислоти. 1 H ЯМР (360 МГц, CDCl3); 1,4 (m, 9H), 2,5-3,0 (m, 2Н), 3,7-3,9 (m, 2H), 4,75 (dd, 1Н). Проміжний продукт 2: 1-трет-бутил-2-метил (2S)-4-оксо-1,2-піролідинкарбоксилат Одержали розчин (2S)-1-(трет-бутоксикарбоніл)-4-оксо-2-піролідинкарбонової кислоти (1г, 4,3ммоль) у суміші (1:1) метанолу та толуолу (60мл). Після цього до перемішуваного розчину при кімнатній температурі у атмосфері азоту додавали крапля за краплею триметилсиліддіазометан (6,5мл 2М розчину у гексанах, 13мл). Після завершення виділення газоподібного азоту, одержаний розчин жовтого кольору випарювали in vacuo і одержаний залишок фільтрували через шар силікагелю з елююванням етилацетатом. Після видалення розчинника з фільтрату одержали масло жовтого кольору (1,05г, майже кількісний вихід). 1 Н ЯМР (400 МГц, CDCl3); 1,4 (m, 9Н), 2,5 (m, 1Н), 2,8-2,9 (m, 1H) 3,7 (s, 3H), 3,9 (m, 2H), 4,6-4,8 (m, 1H). Проміжний продукт 3: 1-трет-бутил-2-метил (2S,4ЕZ)-4-(хлорметилен)-1,2-піролідиндикарбоксилат Хлорметилтрифенілфосфонію йодид (270мг, 0,62ммоль) додавали до розчину трет-бутоксиду калію (67мг, 0,59ммоль) у безводному діетиловому ефірі (5мл) у атмосфері азоту і одержану суміш світло-жовтого кольору перемішували впродовж 30хв при температурі навколишнього середовища. Після цього реакційну суміш охолоджували до температури 0°С і додавали крапля за краплею розчин 1-трет-бутил-2-метил (2S)-4-оксо-1,2піролідиндикарбоксилату (100мг, 0,41ммоль у 2мл безводного діетилового ефіру). Після цього реакційну суміш нагрівали до кімнатної температури та перемішували впродовж 30хв перед доданням насиченого водного розчину амонію хлориду (0,5мл). Органічний шар видаляли in vacuo, водний шар промивали діетиловим ефіром (3x5мл). Змішані органічні шари сушили розсолом та сульфатом магнію перед фільтруванням та видаленням розчинника. Необхідний продукт виділяли шляхом гель-хроматографування з елююванням 15% етиловим ацетатом у гексанах з одержанням 105мг (93% вихід) у ви гляді воску не зовсім білого кольору. 1 Н ЯМР (400 МГц, CDCl3); 1,4 (9Н, m), 2,6-2,75 (m, 1H), 2,8-3,0 (m, 1H), 3,65 (s, 3Н), 4,1 (m, 2Н), 4,4-4,5 (m, 1Н), 5,9-6,0 (m, 1H). Проміжний продукт 4: 1-трет-бутил-2-метил (2S)-4-метилен-1,2-піролідиндикарбоксилат Метилтри фенілфосфонію бромід (22г, 61,6ммоль) додавали до розчину трет-бутоксиду калію (6,5мг, 57,6ммоль) у безводному діетиловому ефірі (450мл) при температурі 0°С у атмосфері азоту і одержану суміш світло-жовтого кольору перемішували впродовж 30хв. Розчин 1-трет-бутил-2-метил (2S)-4-оксо-1,2піролідиндикарбоксилату (10г, 41,1ммоль у 150мл безводного діетилового ефіру) повільно додавали до реакційної суміші, яку після цього нагрівали при температурі 35°С впродовж 3год. Після цього додавали насичений водний розчин амонію хлориду (0,5мл). Органічний шар видаляли, водний шар промивали діетиловим ефіром (3x5мл). Змішані органічні шари сушили розсолом та сульфатом магнію перед фільтруванням та видаленням розчинника. Шляхом гель-хроматографування з елююванням 15% етиловим ацетатом у гексанах одержали 6,9г необхідного продукту (70% вихід) у вигляді воску не зовсім білого кольору. 1 Н ЯМР (400 МГц, CDCl3); 1,4 (9Н, m), 2,5 (m, 1Н), 2,8 (m, 1H), 3,65 (s, 3H), 4,0 (m, 2H), 4,3-4,5 (m, 1H), 4,9 (m, 2H). Проміжний продукт 5: 1-трет-бутил-2-метил (2S,4ЕZ)-4-(ціанометилен)-1,2-піролідиндикарбоксилат Діетилціанометилфосфонат (0,86мл, 4,4ммоль) розчиняли у сухому THF (50мл) і розчин охолоджували до температури 0°С. Після цього обережно додавали гідрид натрію (205мг 60% суспензії у парафіновому маслі, 5,1ммоль) і реакційну суміш перемішували впродовж 30хв. Після цього реакційну суміш охолоджували до температури -78°С і додавали крапля за краплею розчин 1-трет-бутил-2-метил (2S)-4-оксо-1,2піролідиндикарбоксилату (1,0г, 4,1ммоль) у сухому THF (5мл). Після цього реакційну суміш витримували з нагріванням до кімнатної температури. Після цього додавали спочатку насичений водний розчин амонію хлориду (15мл), потім етилацетат (100мл). Органічний шар видаляли, водний шар промивали етилацетатом (3x5мл). Змішані органічні шари сушили розсолом та сульфатом магнію перед фільтруванням та видаленням розчинника. Шляхом гель-хроматографування з елююванням 35% етиловим ацетатом у гексанах одержали необхідний продукт (860мг, 80%) у вигляді воску не зовсім білого кольору. 1 H ЯМР (360 МГц, CDCl3); 1,4 (m, 9Н), 2,7-3,0 (m, 1H), 3,1-3,3 (m, 1H), 3,7 (m, 3H), 4,2-4,4 (m, 2H), 4,5-4,7 (m, 1H), 5,4 (m, 1H). Проміжний продукт 6: 1-трет-бутил-2-метил (2S8,4ЕZ)-4-бензиліден-1,2-піролідиндикарбоксилат Трет-бутоксид калію (6,1г, 54ммоль) порціями додавали до розчину бензилтрифенілфосфонію хлориду (22,45г, 58ммоль) у безводному дихлорметані (400мл) і реакційну суміш перемішували при температурі навколишнього середовища впродовж 1 год. Після цього розчин охолоджували до температури 0°С і додавали крапля за краплею розчин 1-трет-бутил-2-метил (2S)-4-оксо-1,2-піролідиндикарбоксилату (9,36г, 38,5ммоль) у сухому дихлорметані (30мл). Після додаткового перемішування впродовж 1год при температурі 0°С, реакційну суміш додатково перемішували впродовж 3год при температурі навколишнього середовища. Після цього додавали насичений водний розчин амонію хлориду (30мл). Органічний шар видаляли, водний шар промивали дихлорметаном (3x20мл). Змішані органічні шари сушили розсолом та сульфатом магнію перед фільтруванням та видаленням розчинника. Шляхом гель-хроматографування з елююванням 30% ефіру у гексанах одержали 8,65г необхідного продукту (71% вихід) у вигляді воску блідо-жовтого кольору. 1 Н ЯМР (400 МГц, CDCl3); 1,5 (m, 9Н), 2,8-3,0 (m, 1H), 3,2 (m, 1H), 3,7 (m, 3H), 4,2-4,4 (m, 2H), 4,5-4,6 (m, 1H), 6,3-6,4 (m, 1H), 7,1-7,5 (m, 5H). Проміжний продукт 7: (2S,4EZ)-1-(трет-бутиксокарбоніл)-4-(метоксііміно)-2-піролідинкарбонова кислота Одержали розчин, до складу якого входили (2S)-1-(трет-бутоксикарбоніл)-4-оксо-2-піролідинкарбонова кислота (5,0г, 21ммоль) та О-метилгідроксиламіну гідрохлорид (2,7г, 32,8ммоль) у хлороформі (100мл) з триетиламіном (5,5г, 55ммоль). Після цього реакційну суміш перемішували при температурі навколишнього середовища впродовж ночі перед видаленням розчинника. Одержану неочищену реакційну суміш розчиняли у етилацетаті (150мл) та швидко промивали IN HCl (40мл). Після цього кислий шар екстрагували етилацетатом (3x20мл), змішані органічні шари промивали розсолом перед сушінням над сульфатом магнію, фільтруванням та видаленням розчинника in vacuo. Необхідний продукт (5,3г, 94%) виділяли у вигляді масла блідо-жовтого кольору. 1 H ЯМР (400 МГц, CDCl3); 1,45 (m, 9Н), 2,8-3,2 (m, 2Н), 3,9 (s, 3Н), 4,2 (m, 2Н), 4,5-4,7 (m, 1Н). Проміжний продукт 8: (2S,4EZ)-1-(трет-бутиксокарбоніл)-4-(етоксііміно)-2-піролідинкарбонова кислота Одержали розчин, до складу якого входили (2S)-1-(трет-бутоксикарбоніл)-4-оксо-2-піролідинкарбонова кислота (5,0г, 22ммоль) та О-етилгідроксиламіну гідрохлорид (6,4г, 65,5ммоль) у суміші (1:1) піридину та етанолу (100мл). Реакційну суміш нагрівали у колбі зі зворотним холодильником при температурі перегонки впродовж 2,5год перед охолодженням та видаленням розчинника. Залишок розчиняли у етилацетаті та швидко промивали 1,3N HCl (40мл). Після цього кислий шар екстрагували етилацетатом (3x20мл), змішані органічні шари промивали розсолом перед сушінням над сульфатом магнію, фільтруванням та видаленням розчинника in vacuo. Необхідний продукт (5,5г, 93%) виділяли у ви гляді масла блідо-жовтого кольору. 1 H ЯМР (400 МГц, D MSO); 1,3 (t, 3Н), 1,55 (m, 9Н), 2,9-2,7 (m, 1H), 3,4-3,1 (m, 1H), 4,1-4,3 (m, 4H), 4,6 (m, 1H), 12-13,5 (br, 1H). Проміжний продукт 9: (2S,4ЕZ)-4-[(алілокси)іміно]-1-(трет-бутоксикарбоніл)-2-піролідинкарбонова кислота Одержали розчин, до складу якого входили (2S)-1-(трет-бутоксикарбоніл)-4-оксо-2-піролідинкарбонова кислота (5,0г, 22ммоль) та О-алілгідроксиламіну гідрохлориду моногідрат (7,2г, 65,5ммоль) у суміші (1:1) піридину та етанолу (100мл). Реакційну суміш нагрівали у колбі зі зворотним холодильником при температурі перегонки впродовж 2,5год перед охолодженням та видаленням розчинника. Залишок розчиняли у етилацетаті та швидко промивали 1,3N HCl (40мл). Після цього кислий шар екстрагували етилацетатом (3x20мл), змішані органічні шари промивали розсолом перед сушінням над сульфатом магнію, фільтруванням та видаленням розчинника in vacuo. Необхідний продукт (5,9г, 94%) виділяли у вигляді масла блідо-жовтого кольору. 1 H ЯМР (400 МГц, CDCl3); 1,5 (m, 9H), 2,8-3,2 (m, 2H), 4,2 (m, 2H), 4,5-4,7 (m, 3Н), 5,25 (m, 2Н), 5,9 (m, 1 Η), 11,1 (широкий S, 1H). Проміжний продукт 10: 1-[(аміноокси)метил]-4-метоксибензол Одержали розчин Вос ((бутилокси)карбоніл) гідроксиламіну (2,0г, 17,1ммоль) у сухому THF (60мл). Після цього додавали гідрид натрію (1,1г 60% суспензії у парафіновому маслі, 25,7ммоль) і суспензію перемішували. Дореакційної суміші перед обережним доданням 4-метоксибензилхлориду (3,2г, 20,4ммоль) додавали каталітичну кількість КІ. Після цього реакційну суміш перемішували впродовж ночі перед видаленням розчинника in vacuo. Залишок розчиняли у діетиловому ефірі (100мл) і впродовж 20хв барботували газоподібною НСl, що викликало початок осадження продукту. Колбу закривали пробкою і витримували з відстоюванням впродовж ночі. Після цього відфільтровували продукт у вигляді воску не зовсім білого кольору (39-52% вихід у залежності від різних партій). 1 H ЯМР (400 МГц, D2O); 3,8 (s, 3Н), 5 (s, 2H), 7,0 (d, 2H), 7,4 (d, 2H). Проміжний продукт 11: (2S,4EZ)-1-(трет-бутиксокарбоніл)-4-{[(4-метоксибензил)окси]іміно}-2піролідинкарбонова кислота Той же самий спосіб, що і застосований у разі одержання Проміжного продукту 7, однак із започаткуванням із (2S)-1-(трет-бутоксикарбоніл)-4-оксо-2-піролідинкарбонової кислоти (Проміжний продукт 1) та 1-[(аміноокси)метил]-4-метоксибензолу (Проміжний продукт 10), забезпечив одержання цільової сполуки у вигляді смоли з 85% виходом. 1 Н ЯМР (400 МГц, D MSO); 1,5 (m, 9Н), 2,7-2,9 (m, 1Н) 3,9 (s, 3H), 4,2 (m, 3Н), 4,6 (m, 1Н), 5,15 (s, 2H), 7,1 (d, 2H), 7,45 (d, 2H). Проміжний продукт 12: 2-аміноетилацетат, сіль трифтороцтової кислоти Одержали розчин, до складу якого входив етаноламін (36,5мл, 0,6моль) у хлороформі (1000мл). Розчин Вос2О (13,1г, 60ммоль) у хлороформі (600мл) повільно додавали крапля за краплею при температурі 0°С впродовж 6год (температуру підтримували впродовж усього згаданого періоду часу). Реакційну суміш витримували з нагріванням до кімнатної температури і перемішували впродовж ночі. Органічний шар промивали водою (2x500мл), розсолом та сушили над сульфатом магнію перед концентруванням in vacuo. Необхідний продукт (9,5г, >95%) виділяли у ви гляді безбарвного масла і використовували без додаткового очищення. Одержали розчин, до складу якого входив Вос-етаноламін (1,92г, 12ммоль) з карбонатом калію (5г, 36ммоль) у DCM (40мл). Додавали ацетилхлорид (30мл, 0,42моль) і реакційну суміш перемішували впродовж 6год при кімнатній температурі. Надлишок ацетилхлориду видаляли in vacuo і неочищений продукт розчиняли у DC M (100мл). Органічний шар промивали водою (50мл), розсолом та сушили над сульфа том магнію перед концентруванням in vacuo. Необхідний продукт (1,86г, 77%) виділяли у вигляді безбарвного масла і використовували без додаткового очищення. Одержали розчин, до складу якого входили О-ацил, Восетаноламін (1,65г, 8,1ммоль) у DCM (20мл), і додавали TFA (20мл). Після 1год при кімнатній температурі розчинник видаляли in vacuo. Неочищений продукт концентрували з метанолу (2-3 рази) та із DCM (2-3 рази) з одержанням необхідної сполуки (1,75г, кількісний вихід) у вигляді масла, яке використовували без додаткового очищення. 1 Н ЯМР (400 МГц, D2O); 2,0 (m, 9H), 3,1-3,2 (m, 2H), 4,15-4,25 (m, 2H). Проміжний продукт 13: 2'-метил[1.1'-дифеніл]-4-карбонова кислота До суміші 4-бромбензойної кислоти (30г, 0,15моль), 2-метилфенілборонової кислоти (24г, 0,15моль), карбонату натрію (250г) у толуолі (500мл) та воді (500мл) додавали тетракіс-трифенілфосфінпаладій (0) (9г, 0,0074моль) у атмосфері азоту. Реакційну суміш нагрівали у колбі зі зворотним холодильником при температурі перегонки впродовж 10год. Після цього до реакційної суміші додавали 100мл 10% NaOH, водний шар відокремлювали та промивали толуолом (2x200мл). Завдяки підкисленню водного шару 3N розчином НСl одержали твердий продукт, який відфільтровували, промивали водою та сушили. Після цього неочищений продукт кристалізували з толуолу з одержанням 2'-метил[1,1'-дифеніл]-4-карбонової кислоти (20г, 62,5%). Навпаки, згаданий продукт можна також одержати з 1-бром-2-метилбензолу та 4-карбоксибензолборонової кислоти з застосуванням аналогічних умов. 1 H ЯМР (300 МГц, D MSO); 2,2 (s, 3Н), 7,2-7,4 (m, 4Н), 7,43 (d, J=9 Гц, 2Н), 7,99 (d, J=9 Гц, 2Н), 13 (b, 1Н). Подібним же чином, із використанням відповідних технічних боронових кислот та арилбромідів, можна одержати наведені далі споріднені 1,1'-дифенілові проміжні продукти 13: 4'-метил[1,1'-дифеніл]-4-карбонову кислоту; 2',3-диметил[1,1'-дифеніл]-4-карбонову кислоту; 2',6'диметил[1,1'-дифеніл]-4-карбонову кислоту; 2-метил[1,1'-дифеніл]-4-карбонову кислоту; 3-метил[1,1'-дифеніл]4-карбонову кислоту; 2,2'-диметил[1,1'-дифеніл]-4-карбонову кислоту; 2'-метокси[1,1'-дифеніл]-4-карбонову кислоту; 3'-метокси[1,1'-дифеніл]-4-карбонову кислоту; 4'-метокси [1,1'-дифеніл] -4-карбонову кислоту; 2'хлор[1,1'-дифеніл]-4-карбонову кислоту; 3'-хлор[1,1'-ди феніл]-4-карбонову кислоту; 4'-хлор[1,1'-дифеніл]-4карбонову кислоту; 3',4'-ди хлор[1,1'-дифеніл]-4-карбонову кислоту; 2'-(трифторметил)[1,1'-дифеніл]-4карбонову кислоту; 3'-(трифторметил)[1,1'-дифеніл]-4-карбонову кислоту; 2'-ціано[1,1'-дифеніл]-4-карбонову кислоту; 2',4'-дифтор[1,1'-дифеніл]-4-карбонову кислоту; 4-(2-піридиніл)бензойну кислоту; 4-(3піридиніл)бензойну кислоту; 4-(4-піридиніл)бензойну кислоту; 4-(5-піримідиніл)бензойну кислоту. Проміжний продукт 14: 4-(3-метил-2-піридиніл)бензойна кислота Суміш 2-бром-3-метилпіридину (22,5г, 0,1312моль), 4-(гідроксиметил)фенілборонової кислоти (25г, 0,164моль), Pd(PPh3)4 (9,5г, 0,0082моль) та карбонату натрію (200мг у 500мл води) у толуолі (750мл) нагрівали у колбі зі зворотним холодильником при температурі перегонки у атмосфері азоту впродовж 15год. Після відокремлення толуолового шару та дистилювання під зниженим тиском одержали залишок. Після цього залишок піддавали хроматографуванню на колонках з одержанням [4-(3-метил-2-піридиніл)феніл]метанолу (12г, 47%). До розчину [4-(3-метил-2-піридиніл)феніл]метанолу (12г, 0,06моль) у сухому DMF (150мл) додавали піридинійдихромат (91г, 0,24моль) та перемішували при кімнатній температурі впродовж 3 днів. Одержану реакційну суміш виливали до води та екстрагували етилацетатом (250мл). Органічний шар промивали водою, розсолом, сушили та концентрували. Неочищений продукт очищали гель-хроматографуванням на колонках з одержанням 4-(3-метил-2-піридиніл)бензойної кислоти (3г, 25%) у вигляді твердої речовини білого кольору. 1 H ЯМР (300 МГц, DMSO); 2,3 (s, 3Н), 7,33 (dd, J=7,5 Гц, 5 Гц, 1Н), 7,67 (d, J=8 Гц, 2Н), 7,75 (d, J=7,5 Гц, 1Н), 8,01 (d, J=8 Гц, 2Н), 8,50 (d, J=5 Гц, 1Н), 13 (b, 1Н). Проміжний продукт 15: 4-(1-оксидо-3-піридиніл)бензойна кислота До суміші 4-толілборонової кислоти (38г, 0,28моль), 3-бромпіридину (44г, 0,28моль), Na2CO3 (200г) у толуолі (500мл) та воді (500мл) додавали Pd(PPh3)4 (16г, 0,014моль) і нагрівали у колбі зі зворотним холодильником при температурі перегонки впродовж 16год. Реакційну суміш о холоджували, відокремлений органічний шар промивали водою та розсолом і сушили. Розчинник видаляли з одержанням 4-(3піридил)толуолу (42г, 90%). До суміші 4-(3-піридил)толуолу (35г, 0,207моль) у піридині (400мл) та воді (400мл) порціями додавали КМnО4 (163г, 1,03моль) і нагрівали у колбі зі зворотним холодильником при температурі перегонки впродовж 12год. Реакційну суміш фільтрували через целіт та підкислювали концентрованою НСl. Продукт промивали водою та сушили з одержанням 4-(3-піридил)бензойної кислоти (32г, 76%) у вигляді твердої речовини білого кольору. До суміші 4-(3-піридил)бензойної кислоти (22г, 0,11моль) у тетрагідрофурані (2,51) додавали mСРВА (152г, 0,44моль, 50%) і перемішували при кімнатній температурі впродовж 12год. Тверду речовину відфільтровували та промивали тетрагідрофураном з одержанням 4-(1-оксидо-3-піридиніл)бензойної кислоти (20г, 86%). 1 H ЯМР (300 МГц, D MSO); 7,5-7,8 (m, 5Н), 7,9 (d, J=8 Гц, 2Н), 8,33 (d, J=5 Гц, 2Н). Подібним же чином, із започаткуванням із 4-толілборонової кислоти (45г, 0,33моль) та 2-бромпіридину (52г, 0,33моль), одержали споріднений проміжний продукт 4-(1-оксидо-2-піридиніл)бензойну кислоту. Приклад 1: Загальна процедура омилення пролінметилових складних ефірів олефінового типу, таких як Проміжні продукти 3-6. Розчин гідроксиду натрію (4,5г, 112ммоль) у воді (70мл) додавали до відповідного пролінолефінметилового складного ефіру (66ммоль) у суміші (3:1) діоксану:води (500мл) і одержану реакційну суміш перемішували впродовж 3год. Після цього реакційну суміш промивали діетиловим ефіром (2x50мл) і водну фазу підкислювали до pH 2 (0,1N HCl) та екстрагували етилацетатом. Після цього етил ацетатний шар сушили над сульфатом магнію, фільтрували, потім видаляли розчинник in vacuo з одержанням необхідного продукту з майже кількісними виходами у вигляді масла, яке використовували без додаткового очищення. Приклад 2: Загальний протокол синтезу у розчинній фазі похідних оксимового ефіру піролідину загальної формули Іа (С хема 1): Метод А: наприклад, (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-(2-метоксіетил)-4-(метоксііміно)-2піролідинкарбоксамід а) Протокол утворення амідного зв'язку Одержали розчин, до складу якого входили центральний структурний блок, наприклад, (2S,4EZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонова кислота (Проміжний продукт 7) (1,5г, 5,8ммоль), амін або амінова сіль, наприклад, 2-метокси-етиламін (0,51мл, 5,81ммоль) та DMAP (780мг, 5,8ммоль) у DCM (30мл). При температурі 0°С повільно порціями додавали EDC (1,1г, 5,8ммоль). Реакційну суміш витримували з повільним нагріванням до кімнатної температури і перемішували впродовж ночі. DCM випарювали і неочищений продукт очищали хроматографуванням на колонках з використанням EtOAc (100%) для збирання необхідного продукту, наприклад, трет-бутил (2S,4EZ)-2-{[(2-метоксіетил)аміно]карбоніл}-4-(метоксііміно)-1піролідинкарбоксилату (1,5г, 80%) у вигляді безбарвного масла. 1 Н ЯМР (400 МГц, CDCl3); 1,25 (m, 9Н), 2,5-2,9 (m, 2Н), 3,1 (s, 3Н), 3,2-3,3 (m, 4Н), 3,65 (s, 3Н), 3,8-4,4 (m, 3Н), 6,7 (s широкий, 1Н). b) Протокол етапу відщеплення N-захисної групи Одержали розчин, до складу якого входили амідні сполуки попереднього етапу, наприклад, трет-бутил (2S,4ЕZ)-2-{[(2-метоксіетил)аміно]карбоніл}-4-(метоксііміно)-1-піролідинкарбоксилат (1,5г, 0,4ммоль), у безводному ефірі (35мл). Реакційну суміш повільно барботували газоподібною НСl і після відщеплення захисної групи реакційну суміш було піддано тонкошаровому хроматографуванню. Через приблизно 20хв ефір випарювали. Продукт концентрували in vacuo із DCM (2-3 рази) для видалення НСl. Необхідний продукт, наприклад, (2S,4ЕZ)-N-(2-метоксіетил)-4-(метоксііміно)-2-піролідинкарбоксамід (1,2г, кількісний вихід), виділяли у вигляді масла жовтого кольору та використовували без додаткового очищення. c) Протокол етапу N-блокування Одержали розчин, до складу якого входили вільна NH-сполука попереднього етапу, наприклад, (2S,4EZ)N-(2-метоксіетил)-4-(метоксііміно)-2-піролідинкарбоксамід (940мг, 3,7ммоль), карбонова кислота, наприклад, [1,1¢-дифеніл]-4-карбонова кислота (740мг, 3,7ммоль), та DMAP (960мг, 7,8ммоль) у DCM (30мл). При температурі 0°С повільно порціями додавали EDC (715 мг, 3,7ммоль). Реакційну суміш витримували з повільним нагріванням до кімнатної температури і перемішували впродовж ночі. DCM випарювали і неочищений продукт очищали хроматографуванням на колонках із використанням ЕЮАс (100%) для збирання необхідного продукту, наприклад, (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-(2-метоксіетил)-4-(метоксііміно)-2піролідинкарбоксаміду у формі суміші двох ізомерів у вигляді твердої речовини не зовсім білого кольору. 1 H ЯМР (400 МГц, CDCl3); 2,75-2,85 (m, 1H), 3,1-3,3 (m, 4H), 3,4-3,5 (m, 4H), 3,8 (m, 3H), 4,1-4,3 (m, 2H), 5,1 (m, 1H), 6,9 (m, 1H), 7,2-7,7 (m, 10H), Mac-спектрометрія з хімічною іонізацією під атмосферним тиском (М+(АРСІ+)); 396. Метод В: наприклад. (2S,4E та 4Z)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2'-метил[1,1'дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксамід а) Протокол утворення амідного зв'язку До розчину центрального структурного блока, наприклад, (2S,4EZ)-1-(трет-бутоксикарбоніл)-4(метоксііміно)-2-піролідинкарбонової кислоти (Проміжний продукт 7) (24,2ммоль, 6,24г), у сухому тетрагідрофурані (125мл) при температурі -25°С додавали спочатку NMM (2,5екв., 60,4ммоль, 6,64мл), потім ізобутилхлороформіат (1,05екв., 25,4ммоль, 3,3мл). Одержану суміш перемішували при температурі -25°С впродовж 30хв, після чого додавали амін або амінову сіль, наприклад, (S)-2-аміно-1-фенілетанол (1,51екв., 36,5ммоль, 5г). Суміш витримували з поступовим нагріванням до кімнатної температури. Через 16год видаляли розчинники. Залишок розчиняли у AcOEt, двічі промивали насиченим розчином NH4CI, потім двічі 10% розчином NaHCO3. Органічний шар сушили над Na2SO4, фільтр ували та концентрували з одержанням необхідного продукту, наприклад, трет-бутил (2S,4EZ)-2-({[(2S)-2-гiдpoкcи-2-фeнiлeтил]aмiнo}кapбoнiл)-4(мeтoкciiмiнo)-1-піролідинкарбоксилату (8,76г, 96%), у вигляді масла блідо-жовтого кольору 88,5% чистоти за даними високоефективної рідинної хроматографії. 1 Н ЯМР (CDCl3: 300 МГц) δ 1,44 (s, 9H, N-Boc), 3,23-2,85 (m, 4H), 3,72 (m, 1H), 3,85 (s, 3H, O-CH 3), 4,10 (m, 2H), 4,49 (m, 1H), 4,83 (m, 1H), 7,34 (m, 5H, Ar-Η); [M+Na +] електрон-стимульована іонізація (ESI+): 400. b) Протокол етапу відщеплення N-захисної групи Одержали розчин, до складу якого входили амідні сполуки попереднього етапу, наприклад, трет-бутил (2S,4EZ)-2-({[(2S)-2-гідрокси-2-фенілетил]аміно}карбоніл)-4-(метоксііміно)-1-піролідинкарбоксилат (2,64г, 7ммоль), у безводному DCM (35мл). При температурі 0°С реакційну суміш повільно барботували газоподібною НСl і після відщеплення захисної групи реакційну суміш було піддано тонкошаровому хроматографуванню. Через приблизно 20хв DCM випарювали. Продукт концентрували in vacuo із DCM (2-3 рази) для видалення НСl. Необхідний продукт, наприклад, (2S,4EZ)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2піролідинкарбоксамід (1,94г, кількісний вихід), виділяли у вигляді твердої речовини жовтого кольору та використовували без додаткового очищення. c) Протокол етапу N-блокування До суспензії 4-(2-метилфеніл)бензойної кислоти (1,49г, 7ммоль) у 35мл DCM додавали оксалілхлорид та DMF (3мл) з охолодженням за допомогою льоду. Одержану суміш перемішували впродовж 2 год при кімнатній температурі. Розчинник видаляли з одержанням відповідного ацилхлориду у вигляді твердої речовини жовтого кольору. Згадану тверду речовини розчиняли у DCM (30мл) і повільно додавали до розчину, який мав температуру 0°С і до складу якого входили вільна NH-сполука з попереднього етапу, наприклад, (2S,4EZ)-N[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-2-піролідинкарбоксамід (1,94г, 7ммоль), та триетиламін (5екв., 35ммоль, 4,9мл) у сухому DCM (35мл). Реакційну суміш перемішували при кімнатній температурі впродовж ночі. Додавали полтризамін (2,12г, 3,45ммоль/г) з метою видалення надлишку ацилхлориду. С уміш збовтували впродовж 3год, фільтрували і одержаний розчин промивали насиченим розчином NH4CI, розсолом та сушили над Na2SO4 . Після фільтрування та випарювання розчинників одержане масло темного кольору (3,26г) очищали флеш-хроматографуванням (система Biotage, колонка 40М, 90г SiO2, із градієнтами DCM та МеОН як елюент), з одержанням 2S,4EZ)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2'-метил[1,1'дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксаміду. Відокремлення E/Z ізомерів здійснили шляхом кількаразового хроматографування з одержанням (2S,4E)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксаміду (230мг, безбарвний порошок, 98,7% чистота за даними високоефективного рідинного хроматографування) та (2S,4Z)-N-[(2S)-2-гідрокси-2-фенілетил]-4(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2-піролідинкарбоксаміду (266мг, безбарвний порошок, 98,3% чистота за даними високоефективного рідинного хроматографування). (2S,4Е)-N-[(2S)-2-гідрокси-2-фенілетил]-4-(метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід: т.пл. 74°С; ІЧ (нерозбавлений) n 3318, 2932, 1613, 1538, 1416, 1239, 1047, 848 см -1; 1Н ЯМР (300 МГц, CDCl3): 2,27 (s, 3Н, ArCH3), 2,89 (dd, J=6, 12 Гц, 1H), 3,18 (br d, J=12 Гц, 1H), 3,27 (m, 1H), 3,76 (m, 1H), 3,88 (s, 3H, NOCH 3), 4,28 (d, J=10 Гц, 1H), 4,47 (d, J=10 Гц, 1H), 4,59 (широкий s, 1H), 4,88 (m, 1H), 5,20 (m, 1H), 7,03-7,42 (m, 11H, Η ароматичний), 7,45-7,54 (m, 2H, Η ароматичний); М+(АРСІ+): 472; M(APCI): 470. Аналіз обчислено для C28H29N3O 4×0,3 Н2О: С, 70,51; Н, 6,26; N, 8,81. Встановлено: С, 70,53; Н, 6,30; N, 8,87. (2S,4Е)-N-[(2S)-2-гідрокси-2-фенілетил]-4-метоксііміно)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-2піролідинкарбоксамід: т.пл. 78°С; ІЧ (нерозбавлений) n 3318, 2938, 1622, 1538, 1416, 1233, 1045, 852см -1; 1 Н ЯМР (300 МГц, CDCl3): 2,28 (s, 3Н, АrСН3), 2,69 (dd, J=6, 10 Гц, 1Н), 3,02-3,22 (m, 2Н), 3,25 (широкий s, 1Н), 3,60 (m, 1H), 3,86 (s, 3Н, NOCH3), 4,14 (m, 2Н), 4,71 (m, 1Н), 4,96 (m, 1H), 7,03-7,42 (m, 11Н, Η ароматичний), 7,45-7,54 (m, 2Н, Η ароматичний); М+(АРСІ+): 472; M-(APCl·): 470. Аналіз обчислено для C28H29N3 O4×0,9 Н2 О: С, 68,95; Н, 6,36; N, 8,61. Встановлено: С, 68,87; Н, 6,25; N, 8,77. d) E/Z-ізомеризація Чистий Ε-ізомер ізомеризували до суміші E/Z-ізомерів за допомогою наведеної далі процедури: Ε-ізомер розчиняли у суміші діоксану/води (3:1). Додавали NaOH (1,7екв.; 0,52мл 1,6N NaOH) і одержаний розчин перемішували впродовж 2год при кімнатній температурі. Суміш нейтралізували за допомогою 0,1N HCl та ліофілізували. Сполуки одержаної E/Z-суміші відокремлювали та очищали флеш-хроматографуванням за таких же самих умов, що і описані перед тим. Приклад 3: (2S,4ЕZ-([1,1'-дифеніл]-4-іл)карбоніл]-N-[2-(діетиламіно)етил]-4-{[(4-метоксибензил)окси]іміно}2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 2, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-{[(4-метоксибензил)окси]іміно}-2-піролідинкарбонової кислоти, [1,1¢-дифеніл]-4-карбонової кислоти та N1,N1-діетил-1,2-етандіаміну, цільову сполуку одержали після хроматографування на колонках у вигляді твердої речовини не зовсім білого кольору у формі суміші E/Z-ізомерів. 1 H ЯМР (400 МГц, CDCl3); 1,05-1,15 (m, 6Н), 2,7-2,8 (m, 1Н), 2,9-3,2 (m, 6H), 3,4 (m, 1H), 3,6 (s, 3H), 4,0-4,1 (m, 1H), 4,3-4,4 (m, 1H), 3,75 (m, 1H), 3,8 (m, 2H), 6,65 (m, 2H), 7,0-7,1 (m, 2H), 7,2-7,3 (m, 3H), 7,35-7,45 (m, 6H), 8,8 (s широкий, 0,5Н). M+(APCI+); 543. Приклад 4: (2S,4ЕZ)-1-([1,1¢-дифеніл1-4-ілкарбоніл)-4-(хлорметилен)-N-[(2RS)-2-гідрокси-2-фенетил]-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 2, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-(хлорметилен)-2-піролідинкарбонової кислоти, [1,1'-дифеніл]-4-карбонової кислоти та (1RS)-2-аміно-1-фенілетанолу, цільову сполуку одержали після хроматографування на колонках у формі суміші E/Z-ізомерів у вигляді твердої речовини не зовсім білого кольору. Два ізомери можна відокремити за допомогою ще одного етапу очищення шляхом флеш-хроматографування. (2S,4Е)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(хлорметилен)-N-[(2RS)-2-гідрокси-2-фенетил]-2піролідинкарбоксамід: 1Н ЯМР (400 МГц, CDCl3); 2,6-2,7 (m, 1H), 2,8-3,0 (m, 3Н), 3,2 (m, 1H), 3,4-3,6 (m, 1H), 3,9 (m, 1H), 4,15 (t, 1H), 4,6 (m, 1H), 4,85 (m, 1H), 5,75 (s, 1H), 7,0-7,4 (m, 14H). M+(APCI+); 461. (2S,4Z)-1-([1,1¢-дифеніл]-4-ілкарбоніл)-4-(хлорметилен)-N-[(2RS)-2-гідрокси-2-фенетил]-2піролідинкарбоксамід: 1H ЯМР (400 МГц, CDCI3); 2,5-2,6 (m, 1H), 2,7-2,9 (m, 1H), 3,0 (m, 1H), 3,1-3,4 (m, 1H), 3,4-3,6 (m, 1H), 3,9-4,0 (m, 1H), 4,2-4,4 (m, 2H), 4,6 (m, 1H), 4,8-4,9 (m, 1H), 5,75 (s, 1H), 7,0-7,5 (m, 14H). M+(APCI+); 461. Приклад 5: (2S,4ЕZ)-N-[2-(діетиламіно)етил]-1-(дифенілацетил)-4-(метоксііміно)-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 2, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, дифенілоцтової кислоти та N1,N1-діетил-1,2етандіаміну, цільову сполуку одержали після хроматографування на колонках у вигляді твердої речовини не зовсім білого кольору у формі суміші E/Z-ізомерів. 1 H ЯМР (400 МГц, CDCl3); 0,9 (t, 3Н), 1,0 (m, 3Н), 2,6-3,1 (m, 7H), 3,15 (m, 1Н), 3,4 (m, 1H), 3,75 (s, 3H), 3,95 (t, 1H), 4,4-4,7 (m, 4H), 5,1 (m, 1H), 7,0-7,3 (m, 10H), 9,1 (m, 1H). M+(APCI+); 451. Приклад 6: (2S,4ЕZ)-4-(етоксііміно)-N-(9-етил-9Н-карбазол-3-іл)-1-(феноксіацетил)-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 2, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(етоксііміно)-2-піролідинкарбонової кислоти, феноксіоцтової кислоти та 9-етил-9Нкарбазол-3-аміну, цільову сполук у одержали після хроматографування на колонках у вигляді твердої речовини не зовсім білого кольору у формі суміші E/Z-ізомерів. Після цього ізомери були відокремлені шляхом хроматографування на колонках. (2S,4Е)-4-(етоксііміно)-N-(9-етил-9Н-карбазол-3-іл)-1-(феноксіацетил)-2-піролідинкарбоксамід: 1H ЯМР (360 МГц, CDCl3); 1,2 (m, 6Н), 2,7 (m, 1H), 3,35 (d, 1H), 4,1 (m, 4H), 4,3 (d, 1H), 4,45 (d, 1H), 4,7 (m, 2H), 5,15 (d, 1H), 6,9-7,3 (m, 10H), 7,9 (d, 1H), 8,15 (m, 1H), 9,0 (широкий s, 1H). M+(APCI+); 499. (2S,4Z)-4-(етоксііміно)-N-(9-етил-9Н-карбазол-3-іл)-1-(феноксіацетил)-2-піролідинкарбоксамід: 1H ЯМР (360 МГц, CDCl3); 1,2 (m, 6H), 2,7 (m, 1H), 3,2 (m, 1H), 4,1 (m, 4H), 4,35 (m, 2H), 4,7 (m, 2H), 5,1 (m, 1H), 6,9-7,3 (m, 10H), 7,9 (d, 1H), 8,15 (m, 1H), 9,0 (широкий s, 1H). M+(APCI+); 499. Приклад 7: (2S,4ЕZ)-N-(9-етил-9Н-карбазол-3-іл)-4-(метоксііміно)-1-[(2-оксо-6-пентил-2Н-піран-3іл)карбоніл1-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 2, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, 2-оксо-6-пентил-2Н-піран-3-карбонової кислоти та 9-етил-9Н-карбазол-3-аміну, цільову сполуку одержали після хроматографування на колонках у вигляді твердої речовини не зовсім білого кольору у формі суміші E/Z-ізомерів. Ізомери були відокремлені шляхом хроматографування на колонках. (2S,4Е)-N-(9-етил-9Н-карбазол-3-іл)-4-(метоксііміно)-1-[(2-оксо-6-пентил-2Н-піран-3-іл)карбоніл]-2піролідинкарбоксамід: 1H ЯМР (360 МГц, CDCl3); 0,8 (m, 6Н), 1,2 (m, 6Н), 2,5 (m, 2Н), 3,0 (m, 1H), 3,3 (m, 1H), 3,8 (s, 3H), 4,2 (m, 3H), 4,45 (m, 1H), 5,3 (m, 1H), 6,1 (d, 1H), 7,1 (m, 1H), 7,2 (m, 1H), 7,3 (d, 1H), 7,35 (m, 1,H), 7,55 (m, 1H), 7,65 (m, 1H), 8,0 (d, 1H), 8,5 (m, 1H), 9,1 (широкий s, 1H). Mac-спектрометрія із пружним розсіюванням (M+(ES+)); 543. (2S,4Z)-N-(9-етил-9Н-карбазол-3-іл)-4-(метоксііміно)-1-[(2-оксо-6-пентил-2Н-піран-3-іл)карбоніл]-2піролідинкарбоксамід: 1Н ЯМР (360 МГц, CDCl3); 0,8 (m, 6Н), 1,2 (m, 6Н), 2,5 (m, 2Н), 3,05 (m, 1H), 3,25 (m, 1Н), 3,75 (s, 3H), 4,1 (m, 3H), 4,45 (d, 1H), 5,3 (d, 1H), 6,1 (d, 1H), 7,1 (t, 1H), 7,2 (m, 1H), 7,3 (m, 1H), 7,4 (m, 1H), 7,6 (m, 1H), 7,7 (m, 1H), 8,0 (d, 1H), 8,45 (m, 1H), 9,1 (m, 1H). M+(ES+); 543. Приклад 8: (2S,4ЕZ)-4-[(алілокси)іміно]-1-бензоїл-N-(9-етил-9Н-карбазол-3-іл)-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 2, з започаткуванням із (2S,4ЕZ)-4[(алілокси)іміно]-1-(трет-бутоксикарбоніл)-2-піролідинкарбонової кислоти, бензойної кислоти та 9-етил-9Нкарбазол-3-аміну, цільову сполук у одержали після хроматографування на колонках у вигляді твердої речовини не зовсім білого кольору у формі суміші E/Z-ізомерів. 1 H ЯМР (360 МГц, CDCl3); 1,2 (m, 3Н), 2,8 (m, 1H), 3,35 (m, 1H), 4,2 (m, 4H), 4,4 (m, 3H), 5,2 (m, 2H), 5,35 (m, 1H), 5,85 (m, 1H), 7,0-7,5 (m, 5H), 7,9 (m, 3H), 8,1 (m, 2H), 8,3 (m, 1H), 9,2 (широкий s, 1H). M+(APCI+); 481. Приклад 9: Загальний протокол синтезу у розчинній фазі похідних оксимового ефіру піролідину загальної формули І, до складу яких входять додаткові реакційні групи: (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-(2гідроксіетил)-4-(метоксііміно)-2-піролідинкарбоксамід a) Протокол утворення амідного зв'язку Одержали розчин, до складу якого входили центральний структурний блок, наприклад, (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонова кислота (Проміжний продукт 7) (575мг, 2,2ммоль), амін або амінова сіль, до складу якої входить відповідно захищена реакційна група, наприклад, 2-аміноетилацетат (Проміжний продукт 12) (480мг, 2,2ммоль), та DMAP (870мг, 7,1ммоль) у DCM (20мл). При температурі 0°С повільно порціями додавали EDC (427мг, 2,2ммоль). Реакційну суміш витримували з повільним нагріванням до кімнатної температури і перемішували впродовж ночі. DCM випарювали і неочищений продукт очищали хроматографуванням на колонках із використанням суміші EtOAc/гексану: 55/45 для збирання необхідної амідної сполуки, наприклад, трет-бутил (2S,4EZ)-2-({[2-(ацетилокси)етил]аміно}карбоніл)-4-(метоксііміно)-1піролідинкарбоксилату (373мг, 49%) у вигляді масла. 1 Н ЯМР (400 МГц, CDCl3); 1,7 (m, 9Н), 2,1-2,2 (m, 3Н), 2,8-3,3 (m, 2H), 3,7-3,8 (m, 2Н), 4,0-4,1 (m, 3Н), 4,2-4,8 (m, 5Н), 7,3 (s широкий, 1H). b) Протокол етапу відщеплення N-захисної групи Одержали розчин, до складу якого входила Вос-захищена сполука попереднього етапу, наприклад, третбутил (2S,4EZ)-2-({[2-(ацетилокси)етил]аміно}карбоніл)-4-(метоксііміно)-1-піролідинкарбоксилат (373мг, 1,2ммоль) у безводному ефірі (40мл). Реакційну суміш повільно барботували газоподібною НСl і після відщеплення захисної групи реакційну суміш було піддано тонкошаровому хроматографуванню. Через приблизно 20хв ефір випарювали. Продукт концентрували in vacuo із DCM (2-3 рази) для видалення НСl. Необхідний вільний NH продукт, наприклад, 2-({[(2S,4EZ)-4(метоксііміно)піролідиніл]карбоніл}аміно)етилацетат (300мг, кількісний вихід), виділяли у вигляді масла жовтого кольору та використовували бездодаткового очищення. 1 H ЯМР (400 МГц, D2O); 1,75 (s, 3Н), 2,55-2,65 (m, 1Н), 2,8-3,3 (m, 3H), 3,45-3,55 (m, 3H), 3,8-4,0 (m, 4H), 4,25-4,35 (m, 1H). c) Протокол етапу N-блокування Одержали розчин, до складу якого входили аміногідрохлорид попереднього етапу, наприклад, 2({[(2S,4EZ)-4-(метоксііміно)піролідиніл]карбоніл}аміно)етилацетат (560мг, 2ммоль), та хлорангідрид, наприклад, [1,1¢-дифеніл]-4-карбонілхлорид (433мг, 2ммоль) у DCM (20мл). Додавали триетиламін (0,7мл, 5ммоль) і реакційну суміш перемішували впродовж ночі при кімнатній температурі. DCM випарювали і неочищений продукт очищали хроматографуванням на колонках із використанням EtOAc (100%) для збирання необхідної амідної сполуки, наприклад, 2-({[(2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4(метоксііміно)піролідиніл]карбоніл}аміно)етилацетату (457мг, 54%), у вигляді масла. 1 H ЯМР (400 МГц, CDCl3); 1,9 (s, 3Н), 2,7-2,8 (m, 1Н), 3,2-3,6 (m, 3Н), 3,75-3,85 (m, 3Н), 4,0-4,4 (m, 4H), 5,155,25 (m, 1H), 7,2-7,6 (m, 9H). d) Протокол деблокування реакційної групи Одержали розчин, до складу якого входила сполука з захищеним бічним ланцюгом попереднього етапу, наприклад, 2-({[(2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)піролідиніл]карбоніл}аміно)етилацетат (450мг, 10,6ммоль), у тетрагідрофурані (10мл). Додавали водний розчин (10мл) гідроксиду натрію (75мг, 19ммоль) із метанолом (5мл) і реакційну суміш перемішували при кімнатній температурі впродовж 3год. Розчинник видаляли in vacuo і неочищений продукт очищали хроматографуванням на колонках із використанням тетрагідрофурану (100%) з одержанням очікуваного кінцевого продукту, наприклад, (2S,4ЕZ)-1([1,1'-дифеніл]-4-ілкарбоніл)-N-(2-гідроксіетил)-4-(метоксііміно)-2-піролідинкарбоксаміду (300мг, 75%), у вигляді твердої речовини білого кольору. 1 H ЯМР (400 МГц, CDCl3); 2,85-3,0 (m, 1H), 3,3-3,6 (m, 3Н), 3,7-3,8 (2H), 3,85-3,95 (m, 3Н), 4,2-4,5 (m, 2Н), 5,15-5,25 (m, 1H), 7,2-7,9 (m, 9H). M+(APCI+); 382. Приклад 10: (2S,4EZ)-1-([1,1¢-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-фенетил]-4-(метоксііміно)-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 9, із започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, [1,1'-дифеніл]-4-карбонілхлориду та 2-аміно1-фенілетилацетату, цільову сполуку одержали після хроматографування на колонках у формі суміші E/Zізомерів у вигляді твердої речовини не зовсім білого кольору. Два ізомери можна відокремити за допомогою ще одного етапу очищення шляхом флеш-хроматографування. (2S,4Е)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-фенетил]-4-(метоксііміно)-2піролідинкарбоксамід: 1Н ЯМР (400 МГц, CDCl3); 2,75-2,9 (m, 1Н), 3,1-3,25 (m, 2H), 3,35-3,6 (m, 1H), 3,7-3,8 (m, 1H), 3,75 (s, 3H), 4,1-4,3 (m, 2H), 4,8 (m, 1H), 5,1 (dd, 1H), 7,1-7,6 (m, 15H). M+(APCI+); 458. (2S,4Z)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-фенетил]-4-(метоксііміно)-2піролідинкарбоксамід: 1H ЯМР (400 МГц, CDCI3); 2,7-2,85 (m, 1H), 3,05-3,25 (m, 2H), 3,35 (m, 1H), 3,65-3,8 (m, 1H), 3,8 (s, 3H), 4,15-4,25 (d, 1H), 4,25-4,4 (m, 1H), 4,75 (m, 1H), 5,1 (dd, 1H), 7,15-7,6 (m, 15H). M+(APCI+); 458. Приклад 11: Загальний протокол синтезу у розчинній фазі похідних оксимового ефіру піролідину загальної формули Іb (Схема 5); (3EZ,5S)-5-(1H-бензимідазол-2-іл)-1-([1,1'-дифенілі-4-ілкарбоніл)-3-піролідинон Ометилоксим а) Протокол утворення амідного зв'язку Одержали розчин, до складу якого входили центральний структурний блок, наприклад, (2S,4EZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонова кислота (Проміжний продукт 7) (2,1г, 8,1ммоль), ортозаміщений ароматичний амін або амінова сіль, наприклад, 1,2-бензолдіамін (0,88г, 8,1 ммоль) та DMAP (1,59г, 13,0ммоль) у сухому ди хлорметані (30мл). Цей розчин охолоджували до температури 0°С і обробляли EDC (1,56г, 8,2ммоль) перед нагріванням до кімнатної температури та перемішуванням впродовж 2 днів. Розчинник випарювали in vacuo і продукт очищали гель-хроматографуванням з елююванням градієнтом 3080% етилацетату у гексані з одержанням необхідного анілідного продукту, наприклад, трет-бутил (2S,4ЕZ)-2[(2-аміноаніліно)карбоніл]-4-(метоксііміно)-1-піролідинкарбоксилату (2,8г, 97%) у вигляді безбарвної піни. 1 Н ЯМР (360 МГц, CDCl3); 1,7, (m, 9Н), 2,5-3,5 (br, 4Н), 3,4 (m, 1Н), 4,0 (m, 3H), 4,2-4,4 (m, 2H), 4,9 (m, 1H), 6,9-7,5 (m, 4H), 8,5 (br, 1H). b) Протокол утворення злитого гетероциклічного кільця Розчин анілідної сполуки попереднього етапу, наприклад, трет-бутил (2S,4ЕZ)-2-[(2аміноаніліно)карбоніл]-4-(метоксііміно)-1-піролідинкарбоксилату (0,8г, 2,3ммоль), у дихлорметані (30мл) та оцтовій кислоті (3мл) перемішували при кімнатній температурі впродовж 3 днів. До реакційної суміші додавали насичений водний розчин бікарбонату натрію (7мл), органічну фазу збирали та сушили над сульфатом магнію перед фільтруванням та видаленням розчинника in vacuo з одержанням необхідного продукту, наприклад, трет-бутил (2S,4EZ)-2-(1H-бeнзимiдaзoл-2-iл)-4-(метоксііміно)-і-піролідинкарбоксилату (740мг, 97%), у вигляді піни не зовсім білого кольору. 1 Н ЯМР (360 МГц, CDCl3); 1,5 (m, 9Н), 3,1 (m, 1H), 3,8 (m, 3H) 3,9-4,3 (m, 3H), 5,3 (m, 1H), 7,1-7,6 (m, 4H), 10-10,5 (br, 1H). c) Протокол етапу відщеплення N-захисної групи Газоподібним хлористим воднем барботували розчин злитого гетероциклічного продукту попереднього етапу, наприклад, трет-бутил (2S,4ЕZ)-2-(1Н-бензимідазол-2-іл)-4-(метоксііміно)-1-піролідинкарбоксилату (740мг, 2,2ммоль), у сухому DCM (20мл) впродовж 30хв. Розчинник видаляли in vacuo з одержанням необхідного продукту, наприклад, (3EZ,5S)-5-(1Н-бензимідазол-2-іл)-3-піролідинон О-метилоксиму (0,58г, 99%) у вигляді аморфного порошку брунатного кольору, який використовували без додаткового очищення. d) Протокол етапу N-блокування Розчин вільного NH продукту з попереднього етапу, наприклад, (3EZ,5S)-5-(1Н-бензимідазол-2-іл)-3піролідинон О-метилоксиму (0,58г, 2,2ммоль), у сухому ди хлорметані (25мл) обробляли хлорангідридом, наприклад, [1,1'-дифеніл]-4-карбонілхлоридом (0,48г, 2,2ммоль), та триетиламіном (0,9мл, 6,6ммоль). Після цього одержаний розчин перемішували впродовж 3год при кімнатній температурі перед видаленням розчинника in vacuo і необхідні ізомери виділяли флеш-хроматографуванням на силікагелі з елююванням градієнтом етилацетату (10-80%) у гексані з одержанням двох ізомерів (120мг менш полярного та 400мг більш полярного) необхідного продукту, наприклад, (3E,5S)- та (3Z,5S)-5-(1Н-бензімідазол-2-іл)-1-([1,1'-дифеніл]-4ілкарбоніл)-3-піролідинон О-метилоксиму, у вигляді порошків не зовсім білого кольору. (3Е,5S)-5-(1Н-бензімідазол-2-іл)-1-([1,1'-дифеніл]-4-ілкарбоніл)-3-піролідинон О-метилоксим: 1H ЯМР (360 МГц, CDCl3); 3,2, (m, 1Н), 3,8 (s, 3H), 4,0 (m, 1H), 4,3 (m, 2H), 6,0 (m, 1H), 6,0 (m, 1H), 7,2-7,7 (m, 13H), 10-11 (br, 1H). M+(APCI+);411. (3Z,5S)-5-(1Н-бензімідазол-2-іл)-1-([1,1'-дифеніл]-4-ілкарбоніл)-3-піролідинон О-метилоксим: 1H ЯМР (360 МГц, CDCl3); 3,1, (m, 1H), 3,8 (s, 3Н), 3,9 (m, 1H), 4,3 (m, 2H), 6,0 (m, 1H), 6,0 (m, 1H), 7,2-7,7 (m, 13H), 10-11 (br, 1H). M+(APCI+); 411. Приклад 12: (3ЕZ,5S)-5-(1Н-бензімідазол-2-іл)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-3-піролідинон Ометилоксим За загальним методом, опис якого було наведено у Прикладі 11, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, 2'-метил [1,1'-дифеніл]-4-карбонової кислоти та 1,2-бензолдіаміну, цільову сполук у одержали з 91% чистотою за даними високоефективного рідинного хроматографування. Мас-спектроскопія з електрон-стимульованою іонізацією (MS(ESI+)): m/z=425. Приклад 13: (3ЕZ,5S)-5-(1-метил-1Н-бензимідазол-2-іл)-1-[(2'-метил[1,1'-дифеніл]-4-іл)карбоніл]-3піролідинон О-метилоксим За загальним методом, опис якого було наведено у Прикладі 11, із започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, 2'-метил[1,1'-дифеніл]-4-карбонової кислоти та N1-метил-1,2-бензолдіаміну, цільову сполуку одержали з 83% чистотою за даними високоефективного рідинного хроматографування. MS(ESI+): m/z=439. Приклад 14: (3ЕZ,5S)-5-(7-гідрокси-1Н-бензимідазол-2-іл)-1-[(2'-метил[1,1¢-дифеніл]-4-іл)карбоніл]-3піролідинон О-метилоксим За загальним методом, опис якого було наведено у Прикладі 11, із започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, 2'-метил[1,1'-дифеніл]-4-карбонової кислоти та 2,3-діамінофенолу, цільову сполуку одержали з 91% чистотою за даними високоефективного рідинного хроматографування. MS(ESI+): m/z=441. Приклад 15: (3ЕZ,5S)-5-(3,4-дигідро-2-хіназолініл)-1-[(2'-метил[1,1¢-дифеніл1-4-іл)карбоніл1-3-піролідинон О-метилоксим За загальним методом, опис якого було наведено у Прикладі 11, із започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, 2'-метил[1,1'-дифеніл]-4-карбонової кислоти та 2-(амінометил)аніліну, цільову сполук у одержали з 77% чистотою за даними високоефективного рідинного хроматографування. MS(ESI+): m/z=439. Приклад 16: (3ЕZ,5S)-1-([1,1'-дифеніл]-4-ілкарбоніл]-5-(1-метил-1Н-бензімідазол-2-іл)-3-піролідинон Ометилоксим За загальним методом, опис якого було наведено у Прикладі 11, із започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, [1,1'-дифеніл]-4-карбонілхлориду та №метил-1,2-бензолдіаміну, цільову сполуку одержали з 88% чистотою за даними високоефективного рідинного хроматографування. MS(ESI+): m/z=425. Приклад 17: Загальний протокол синтезу у розчинній фазі похідних оксим- або гідразонпіролідину загальної формули І (Схема 6); (2S,4EZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(гідроксііміно)-N-[(2RS)-2-гідрокси-2фенетил]-2-піролідинкарбоксаміду а) Протокол гідролізу оксимефірної групи Вихідні оксимефірні сполуки, наприклад, (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2фенетил]-4-(метоксііміно)-2-піролідинкарбоксамід, одержували за загальними методами, опис яких було наведено, наприклад, у Прикладах 2, 11 або 22. Одержували розчин, до складу якого входили оксимефірна сполука, наприклад, (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-фенетил]-4-(метоксііміно)-2піролідинкарбоксамід (64мг, 0,14ммоль), порошкоподібний параформальдегід (95%, 42мг, 1,41ммоль) та Амберліст 15 (Amberlyst®) (30мг) у ацетоні, який вміщував 10% води (2мл). Реакційну суміш перемішували впродовж 4год при температурі 60°С. Нерозчинні матеріали відфільтровували та промивали невеликою кількістю ацетону. Фільтрат концентрували і залишок розбавляли DCM (15мл). Органічний розчин промивали розсолом (10мл), сушили над Na2SO4 та концентрували. Необхідний кетокарбонільний продукт, наприклад, (2S)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-фенетил]-4-оксо-2-піролідинкарбоксамід (56мг, 92%) виділяли у вигляді масла жовтого кольору та використовували без додаткового очищення. b) Протокол одержання оксимових та/або гідразонових сполук Одержали розчин, до складу якого входили кетопіролідинова похідна попереднього етапу, наприклад, (2S)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-фенетил]-4-оксо-2-піролідинкарбоксамід (46мг, 0,11ммоль), та гідроксиламіну гідрохлорид (12мг, 0,17ммоль) у хлороформі (1мл), який містив триетиламін (29мг, 0,29ммоль). Після цього реакційну суміш перемішували при температурі навколишнього середовища впродовж одного дня перед видаленням розчинника. Одержану неочищену реакційну суміш очищали хроматографуванням на колонках із використанням суміші DCM/MeOH (25:1) для збирання необхідного продукту, наприклад, (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(гідроксііміно)-N-[(2RS)-2-гідрокси-2-фенетил]2-піролідинкарбоксаміду як суміші двох ізомерів у вигляді твердої речовини не зовсім білого кольору (46мг, 96% вихід). 1 H ЯМР (300 МГц, CDCl3); 2,6-3,3 (m, 4Н), 4,0-4,7 (m, 4Н), 4,9 (m, 1Н), 5,5 (m, 1H), 7,1-7,5 (m, 8H), 7,6-7,8 (m, 5H), 8,1 (m, 1H), 10,9 (m, 1H). M+(APCI+); 444. Приклад 18: (2S,4ЕZ)-([1,1'-дифеніл1-4-ілкарбоніл)-4-(диметилгідразоно)-N-[(2RS)-2-гідрокси-2-фенілетил]2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 17, із започаткуванням із (2S)-1-([1,1'дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-фенілетил]-4-оксо-2-піролідинкарбоксаміду та Ν,Νдиметилгідразину, одержану неочищену реакційну суміш очи щали хроматографуванням на колонках із використанням суміші DCM/MeOH (30:1) для збирання необхідного продукту, наприклад, (2S,4ЕZ)-1-([1,1'дифеніл]-4-ілкарбоніл)-4-(диметилгідразоно)-N-[(2RS)-2-гідрокси-2-фенілетил]-2-піролідинкарбоксаміду як суміші двох ізомерів у вигляді масла світло-жовтого кольору з 56% виходом (90,2% чистота за даними високоефективної рідинної хроматографії). 1 H ЯМР (300 МГц, CDCl3); 2,35-2,55 (широкий s, 3Н), 2,40-2,60 (m, 1Н), 2,75-3,55 (m, 5H), 3,55-3,82 (m, 1H), 3,90-4,4 (m, 2H), 4,83 (m, 1H), 4,93-5,35 (m, 1H), 7,18-7,49 (m, 9H), 7,49-7,68 (m, 5H). M+(APCI+); 471. M-(APCI-); 469. Приклад 19: (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-фенілетил]-4-(метилгідразоно)2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 17, із започаткуванням із (2S)-1-([1,1'дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-фенілетил]-4-оксо-2-піролідинкарбоксаміду та N-метилгідразину, одержану неочищену реакційну суміш очищали хроматографуванням на колонках із використанням суміші DCM/MeOH (30:1) для збирання необхідного продукту, наприклад, (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N[(2RS)-2-гідрокси-2-фенілетил]-4-(метилгідразоно)-2-піролідинкарбоксаміду як суміші двох ізомерів у вигляді безбарвної твердої речовини з 57% виходом (95,2% чистота за даними високоефективної рідинної хроматографії). 1 H ЯМР (300 МГц, CDCl3); 2,45-2,70 (m, 1Н), 2,85 (широкий s, 3Н, NNHCH3), 2,85-3,5 (m, 2H), 3,51-4,4 (m, 4H), 4,84 (широкий s, 1H, NNHMe), 4,95-5,35 (m, 1H), 7,18-7,67 (m, 14H). M+(APCI+); 457. M(APCI); 455. Приклад 20: (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-гідразоно-N-[(2RS)-2-гідрокси-2-фенілетил]-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 17, із започаткуванням із (2S)-1-([1,1'дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-фенілетил]-4-оксо-2-піролідинкарбоксаміду та гідразину гідрату (4% у EtOH), одержану неочищену реакційну суміш очищали хроматографуванням на колонках із використанням суміші DCM/MeOH (30:1) для збирання необхідного продукту, наприклад, (2S,4ЕZ)-1-([1,1'дифеніл]-4-ілкарбоніл)-4-гідразоно-N-[(2RS)-2-гідрокси-2-фенілетил]-2-піролідинкарбоксаміду як суміші двох ізомерів у вигляді безбарвної твердої речовини з 63% виходом (95,3% чистота за даними високоефективної рідинної хроматографії). 1 H ЯМР (300 МГц, DMSO-d 6, 80°С); 2,55 (dd, J=9,8; 17,6 Гц, 1H), 2,73 (dd, J=9,8; 18,2 Гц, 1H), 3,28 (m, 2H), 4,12 (m, 2H), 4,61 (m, 1H), 4,85 (m, 1H), 5,15 (m, 1H), 5,70 (широкий s, 2H, NH 2N=C), 7,17-7,43 (m, 6H), 7,44-7,60 (m, 4H), 7,66-7,77 (m, 5H). M+(APCI+); 443. M-(APCI-); 441. Приклад 21: (2S,4ЕZ)-4-(ацетилгідразоно)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-[(2RS)-2-гідрокси-2-фенілетил]2-піролідинкарбоксамід Похідну гідразонопіролідину, яка була одержана за загальним методом, опис якого було наведено у Прикладі 17, наприклад, (2S,4EZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-гідразоно-N-[(2RS)-2-гідрокси-2-фенілетил]2-піролідинкарбоксамід (51мг, 0,11ммоль), розчиняли у піридині (1мл). Додавали оцтовий ангідрид (3екв., 32мкл, 0,35ммоль) і суміш перемішували впродовж ночі. Розчинник випарювали і одержану неочищену реакційну суміш очищали хроматографуванням на колонках з використанням суміші DCM/MeOH (20:1) для збирання необхідного продукту, наприклад, (2S,4ЕZ)-4-(ацетилгідразоно)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N[(2RS)-2-гідрокси-2-фенілетил]-2-піролідинкарбоксаміду як суміші двох ізомерів у вигляді безбарвної твердої речовини з 73% виходом (98,4% чистота за даними високоефективної рідинної хроматографії). 1 Н ЯМР (300 МГц, OMSO-d6 , 80°С); 1,99 (широкий s, 3Н, CH3CON), 2,7-3,4 (m, 5Н), 4,26 (m, 2Н), 4,63 (m, 1H), 4,89 (m, 1H), 5,15 (m, 1H), 7,18-7,44 (m, 6H), 7,45-7,62 (m, 4H), 7,66-7,85 (m, 5H), 9,97 (широкий s, 1H, MeCONHN, головний ізомер), 10,04 (широкий s, 1H, MeCONHN, другорядний ізомер). M+(ESI+); 485. M-(ESI-); 483. Приклад 22: Загальний протокол для твердофазного синтезу похідних піролідину загальної формули І. a) Етап завантаження Оксимову смолу Кайзера (16,5г, завантаження 1,57ммоль/г) додавали до розчину відповідного структурного блока піролідинкарбонової кислоти (51,8ммоль) та діізопропілкарбодііміду (8,1мл, 51,8ммоль) у сухому ди хлорметані (150мл). Одержану суспензію збовтували впродовж ночі перед фільтруванням на насосі та послідовним промиванням DMF, DC M і, нарешті, діетиловим ефіром перед висушуванням при кімнатній температурі in vacuo. b) Етап відщеплення N-захисної групи Смолу, яка була одержана на етапі завантаження, збовтували з 20% розчином трифтороцтової кислоти у дихлорметані (200мл) впродовж 30хв перед фільтруванням на насосі та послідовним промиванням аліквотами DMF, DCM і, нарешті, діетилового ефіру перед висушуванням при кімнатній температурі in vacuo. с) Етап N-блокування Смолу попереднього етапу переносили на 96-лунковий фільтрувальний планшет (приблизно 50мг сухої смоли на лунку) і кожну з лунок обробляли N-реакційним дериватизаційним агентом, наприклад, будь-яким із наведених далі розчинів: a) хлорангідрид (0,165ммоль) та діізопропілетиламін (0,165ммоль) у сухому дихлорметані (1мл), впродовж ночі; b) кислота (0,165ммоль) та DIC (0,165ммоль) у, залежно від розчинності карбонової кислоти, сухому дихлорметані або NPM (1мл), впродовж ночі; c) ізоціанат (0,165ммоль у сухому THF (1мл), впродовж ночі; d) сульфонілхлорид (0,165ммоль) та діізопропілетиламін (0,165ммоль) у N MP (1мл), впродовж ночі; e) бензил (алкіл) бромід (0,165ммоль) та діізопропілетиламін (0,165ммоль) у NMP (1мл), впродовж ночі; f) вінілкетон (0,165ммоль) у THF (1мл), впродовж ночі; g) дикетен (0,165ммоль) у THF (1мл), впродовж ночі. Після цього планшет герметично закривали та збовтували впродовж ночі при температурі навколишнього середовища. Потім смоли відфільтровували, послідовно промивали аліквотами DMF, DCM і, нарешті, діетилового ефіру перед висушуванням при кімнатній температурі in vacuo. d) Етап розщеплення До кожної лунки, яка вміщувала смолу з попереднього етапу, додавали розчин аміну (0,05ммоль) у 2% АсОН у ди хлорметані (1мл). Після цього планшет герметично закривали і збовтували впродовж двох днів при температурі навколишнього середовища. Потім лунки фільтрували до збірного планшету і розчинник видаляли у вакуумній центрифузі з одержанням 2-3мг відповідних продуктів, які, взагалі, одержували у вигляді масел. Характеристики продуктів визначали за допомогою рідинної хроматографії (205нм) та масспектрометрії (ES+). Усі подальші приклади були ідентифіковані на основі спостереження відповідного молекулярного іону у мас-спектрі і за допомогою рідинної хроматографії було показано, що їх чистота дорівнювала як мінімум 40% (як правило, 60-95%). Приклад 23: (2S,4EZ)-N 2-(2-гiдpoкcieтил)-4-(мeтoкciiмiнo)-N1-пeнтил-1,2-піролідиндикарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, 1-ізоціанатопентану та 2-аміноетанолу, цільову сполуку одержали зі 100% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=315,2. Приклад 24: (2S,4ЕZ)-4-бензиліден-1-[1,1¢-дифеніл]-4-ілкарбоніл]-N-[2-(діетиламіно)-етил]-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-4 бензиліден-1-(трет-бутоксикарбоніл)-2-піролідинкарбонової кислоти, [1,1¢-дифеніл ]-4-карбонілхлориду та N1,N1-діетил-1,2-етандіаміну, цільову сполуку одержали з 90% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=482,4. Приклад 25: (2S,4ЕZ)-4-[(алілокси)іміно]-1-(4-ціанобензоїл)-N-[2-(1Н-пірол-1-іл)феніл]-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-4[(алілокси)іміно]-1-(трет-бутоксикарбоніл)-2-піролідинкарбонової кислоти, 4-ціанобензоїлхлориду та 2-(1Нпірол-1-іл)феніламіну, цільову сполуку одержали з 51% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=454,4. Приклад 26: (2S,4ЕZ)-4-{[(3,4-дихлорбензил)окси]іміно}-N-(2-фурилметил)-1-[(2-оксо-6-пентил-2Н-піран-3іл)карбоніл]-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-{[(3,4-дихлорбензил)окси]іміно}-2-піролідинкарбонової кислоти, 2-оксо-6-пентил-2Н-піран-3карбонілхлориду та 2-фурилметиламіну, цільову сполуку одержали з 92% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=574,4. Приклад 27: (2S,4EZ)-4-метоксііміно-N1-(3-метоксифеніл)-N2-(2-тієнілметил)-1,2-піролідиндикарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, 1-ізоціанато-3-метоксибензолу та 2тієнілметиламіну, цільову сполуку одержали з 79% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=403,2. Приклад 28: (2S,4ЕZ)-2-{[4-(1,3-бензодіоксол-5-ілметил)-1-піперазиніл]карбоніл}-4-(метоксііміно)-N-пентил1-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, 1-ізоціанатопентану та 1-(1,3-бензодіоксол-5ілметил)піперазину, цільову сполуку одержали з 72% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=474,4. Приклад 29: (2S,4ЕZ)-4-[(бензилокси)іміно]-1-(4-ціанобензоїл)-N-(2-фурилметил)-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-4[(бензилокси)іміно]-1-(трет-бутоксикарбоніл)-2-піролідинкарбонової кислоти, 4-ціанобензоїлхлориду та 2фурилметиламіну, цільову сполуку одержали з 49% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=443,4. Приклад 30: (2S,4ЕZ)-4-[(бензилокси)іміно]-N-[2-(діетиламіно)eтил]-1-('4-феноксибензоїл)-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-4[(бензилокси)іміно]-1-(трет-бутоксикарбоніл)-2-піролідинкарбонової кислоти, 4-феноксибензоїлхлориду та N1,N2-діетил-1,2-етандіаміну, цільову сполуку одержали з 86% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=529,6. Приклад 31: 4-[((2S,4ЕZ)-4-[(бензилокси)іміно]-2-{[4-(3,4-дихлорфеніл)-1піперазиніл]карбоніл}піролідиніл)карбоніл]бензонітрил За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-4[(бензилокси)іміно]-1-(трет-бутоксикарбоніл)-2-піролідинкарбонової кислоти, 4-ціанобензоїлхлориду та 1-(3,4дихлорфеніл)піперазину, цільову сполуку одержали з 43% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=576,6. Приклад 32: (2S,4ЕZ)-4-(метоксііміно)-N1-пентил-N2-[2-(1Н-пірол-1-іл)]-1,2-піролідиндикарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, 1-ізоціанатопентану та 2-(1Н-пірол-1іл)феніламіну, цільову сполуку одержали з 74% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=412,2. Приклад 33: (28,4ЕZ)-1-акрилоїл-4-{[(3,4-дихлорбензил)окси]іміно}-N-(2-фурилметил)-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-{[(3,4-дихлорбензил)окси]іміно}-2-піролідинкарбонової кислоти, акрилоїлхлориду та 2фурилметиламіну, цільову сполуку одержали з 74% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=436,8. Приклад 34: (2S,4EZ)-4-(трет-бутоксііміно)-N2-циклопропіл-N1-(3,5-дихлорфеніл)-1,2піролідиндикарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(трет-бутоксііміно)-2-піролідинкарбонової кислоти, 1,3-дихлоро-5-ізоціанатобензолу та циклопропіламіну, цільову сполуку одержали з 48% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=427,6. Приклад 35: (2S,4ЕZ)-4-[(алілокси)іміно]-N-[2-(діетиламіно)етил]-1-[(2-оксо-6-пентил-2Н-піран-3іл)карбоніл]2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-4[(алілокси)іміно]-1-(трет-бутоксикарбоніл)-2-піролідинкарбонової кислоти, 2-оксо-6-пентил-2Н-піран-3карбонілхлориду та N1,N1-діетил-1,2-етандіаміну, цільову сполуку одержали з 93% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=475,4. Приклад 36: (2S,4ЕZ)-N2-[(2RS)-2-гідрокси-2-фенетил]-4-(метоксііміно)-N1-(3-метилфеніл)-1,2піролідиндикарбоксамід За загальним методом, опис якогобуло наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, 1-ізоціанато-3-метилбензолу та (1RS)-2 аміно-1-феніл етанолу, цільову сполуку одержали зі 100% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=411,2. Приклад 37: (2S,4ЕZ)-1-[(бензоїламіно)карбоніл]-N-бензил-4-[(бензилокси)іміно]-N-метил-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-4[(бензилокси)іміно]-1-(трет-бутоксикарбоніл)-2-піролідинкарбонової кислоти, бензоїлізоціанату та N-бензил-Nметиламіну, цільову сполуку одержали з 40% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=485,4. Приклад 38: (2S,4ЕZ)-1-(4-ціанобензоїл)-N-(9-етил-9Н-карбазол-3-іл)-4-(метоксііміно)-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, 4-ціанобензоїлхлориду та 9-етил-9Нкарбазол-3-аміну, цільову сполук у одержали з 72% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=480,4. Приклад 39: (2S,4ΕΖ)-4-(метоксііміно)-Ν1-(3-метилфеніл)-Ν2-(2-тієнілметил)-1,2-піролідиндикарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, 1-ізоціанато-3-метилбензолу та 2тієнілметиламіну, цільову сполуку одержали з 98% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=387,2. Приклад 40: (2S,4ЕZ)-4-(трет-бутоксііміно)-N-(2-метоксіетил)-1-[(2-оксо-6-пентил-2Н-піран-3-іл)карбоніл]-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(трет-бутоксііміно)-2-піролідинкарбонової кислоти, 2-оксо-6-пентил-2Н-піран-3карбонілхлориду та 2-метоксіетиламіну, цільову сполуку одержали з 75% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=450,2. Приклад 41: (3ЕZ,5S)-5-{[4-(1,3-бензодіоксол-5-ілметил)-1-піперазиніл]карбоніл}-1-бензоїл-3-піролідинон О-(3,4-дихлорбензил)оксим За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-{[(3,4-дихлорбензил)окси]іміно}-2-піролідинкарбонової кислоти, бензоїлхлориду та 1-(1,3бензодіоксол-5-ілметил)піперазину, цільову сполуку одержали з 71% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=609,8. Приклад 42: трет-бутил 3-[({(2S,4EZ)-4-(етоксііміно)-1-[(2-оксо-6-пентил-2Н-піран-3іл)карбоніл]піролідиніл}карбоніл)аміно]-1-азетидинкарбоксилат За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(етоксііміно)-2-піролідинкарбонової кислоти, 2-оксо-6-пентил-2Н-піран-3-карбонілхлориду та трет-бутил 3-аміно-1-азетидинкарбоксилату, цільову сполуку одержали зі 100% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=519,6. Приклад 43: (2S,4ЕZ)-4-{[(4-метоксибензил)окси]іміно}-N-(3-метилфеніл)-2-(4-морфолінілкарбоніл)-1піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-{[(4-метоксибензил)окси]іміно}-2-піролідинкарбонової кислоти, 1-ізоціанато-3-метилбензолу та морфоліну, цільову сполуку одержали з 41% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=467,4. Приклад 44: (2S,4EZ)-N 2-циклопропіл-4-{[(4-метоксибензил)окси]іміно}-N1-пентил-1,2піролідиндикарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-{[(4-метоксибензил)окси]іміно}-2-піролідинкарбонової кислоти, 1-ізоціанатопентану та циклопропіламіну, цільову сполуку одержали з 75% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=417,2. Приклад 45: (3EZ,5S)-5-{[4-(3,4-диxлopфeнiл)-1-пiпepaзинiл]кapбoнiл}-1-[(2-оксо-6-пентил-2Н-піран-3іл)карбоніл]-3-піролідинон О-бензилоксим За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-4[(бензилокси)іміно]-1-(трет-бутоксикарбоніл)-2-піролідинкарбонової кислоти, 2-оксо-6-пентил-2Н-піран-3карбонілхлориду та 1-(3,4-дихлорфеніл)піперазину, цільову сполуку одержали з 47% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=639,8. Приклад 46: (2S,4ЕZ)-4-(трет-бутоксііміно)-N-[2-(1Н-пірол-1-іл)феніл]-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-(трет-бутоксііміно)-2-піролідинкарбонової кислоти та 2-(1Н-пірол-1-іл)феніламіну, цільову сполуку одержали з 83% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=341,2. Приклад 47: 1-({(2S,4ЕZ)-4-(хлорметилен)-1-[(4-хлорфенокси)ацетил]піролідиніл}карбоніл)-4-(3,4дихлорфеніл)піперазин За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-(хлорметилен)-2-піролідинкарбонової кислоти, (4-хлорфенокси)ацетилхлориду та 1-(3,4дихлорфеніл)піперазину, цільову сполуку одержали з 64% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=543,6. Приклад 48: (2S,4ЕZ)-4-[(бензилокси)іміно]-N-(4,6-диметокси-2-піримідиніл)-1-[(2-оксо-6-пентил-2Н-піран-3іл)карбоніл]-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-4[(бензилокси)іміно]-1-(трет-бутоксикарбоніл)-2-піролідинкарбонової кислоти, 2-оксо-6-пентил-2Н-піран-3карбонілхлориду та 4,6-диметокси-2-піримідинаміну, цільову сполуку одержали з 62% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=564,6. Приклад 49: (2S,4ЕZ)-4-{[(3,4-дихлорбензил)окси]іміно}-1-[4-(диметиламіно)бутаноїл]-N-(1-нафтилметил)2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-{[(3,4-дихлорбензил)окси]іміно}-2-піролідинкарбонової кислоти, 4(диметиламіно)бутаноїлхлориду та 1-нафтилметиламіну, цільову сполуку одержали з 62% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=555,6. Приклад 50: (2S)-N 2-(2,1,3-бензотіадіазол-4-іл)-N1-(3,5-дихлорфеніл)-4-оксо-1,2-піролідиндикарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням з 1-(третбутоксикарбоніл)-4-оксопроліну, 1,3-дихлоро-5-ізоціанатобензолу та 2,1,3-бензотіадіазол-4-аміну, цільову сполуку одержали з 47% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=450,6. Приклад 51: (2S,4EZ)-N-бензил-4-(хлорметилен)-N-метил-1-(4-феноксибензоїл)-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(хлорметилен)-2-піролідинкарбонової кислоти, 4-феноксибензоїлхлориду та N-бензил-Nметиламіну, цільову сполуку одержали з 61% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=461,4. Приклад 52: (2S,4ЕZ)-N2-(9-етил-9Н-карбазол-3-іл)-4-{[(4-метоксибензил)окси]іміно}-N1-(3-метилфеніл)-1,2піролідиндикарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-{[(4-метоксибензил)окси]іміно}-2-піролідинкарбонової кислоти, 1-ізоціанат-3-метилбензолу та 9-етил-9Н-карбазол-3-аміну, цільову сполуку одержали з 72% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=590,8. Приклад 53: (2S)-N-(трет-бутил)-4-метилен-1-[(2-оксо-6-пентил-2Н-піран-3-іл)карбоніл1-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням з 1-(третбутоксикарбоніл)-4-метиленпроліну, 2-оксо-6-пентил-2Н-піран-3-карбонілхлориду та трет-бутиламіну, цільову сполуку одержали зі 100% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=375,4. Приклад 54: (2S,4ЕZ)-4-бензиліден-1-[4-(диметиламіно)бутаноїл]-N-(6-хінолініл)-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-4бензиліден-1-(трет-бутоксикарбоніл)-2-піролідинкарбонової кислоти, 4-(диметиламіно)бутаноїлхлориду та 6хінолінаміну, цільову сполуку одержали з 71% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=443,6. Приклад 55: (2S)-1-[4-(диметиламіно)бутаноїл]-N-(9-етил-9Н-карбазол-3-іл)-4-метилен-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням з 1-(третбутоксикарбоніл)-4-метиленпроліну, 4-(диметиламіно)бутаноїлхлориду та 9-етил-9Н-карбазол-3-аміну, цільову сполуку одержали з 51% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=433,6. Приклад 56: (2S,4ЕZ)-N-(1,3-бензодіоксол-5-ілметил)-4-[(бензилокси)іміно]-1-(4-ціанобензоїл)-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-4[(бензилокси)іміно]-1-(трет-бутоксикарбоніл)-2-піролідинкарбонової кислоти, 4-ціанобензоїлхлориду та 1,3бензодіоксол-5-ілметиламіну, цільову сполуку одержали з 51% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=497,6. Приклад 57: (2S)-1-({[4-(диметиламіно)бутаноїл]-4-метилен-2-піролідиніл}карбоніл)-3-азетидінол За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням з 1-(третбутоксикарбоніл)-4-метиленпроліну, 4-(диметиламіно)бутаноілхлориду та 3-азетидінолу, цільову сполуку одержали зі 100% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=296,4. Приклад 58: (2S,4ЕZ)-1-([1,1¢-дифеніл]-4-ілкарбоніл)-4-{[(3,4-дихлорбензил)окси]іміно}-N-[2-(1Н-пірол-1іл)феніл]-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-{[(3,4-дихлорбензил)окси]іміно}-2-піролідинкарбонової кислоти, [1,1'-дифеніл]-4карбонілхлориду та 2-(1Н-пірол-1-іл)феніламіну, цільову сполуку одержали з 54% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=623,6. Приклад 59: (2S,4ЕZ)-4-бензиліден-1-[(4-хлорфенокси)ацетил]-N-(3,4-диметоксибензил)-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-4бензиліден-1-(трет-бутоксикарбоніл)-2-піролідинкарбонової кислоти, (4-хлорфенокси)ацетилхлориду та 3,4диметоксибензиламіну, цільову сполуку одержали з 49% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=521,6. Приклад 60: (2S,4ЕZ)-4-{[(3,4-дихлорбензил)окси]іміно}-1-(дифенілацетил)-N-(2-тієнілметил)-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-{[(3,4-дихлорбензил)окси]іміно}-2-піролідинкарбонової кислоти, дифенілацетилхлориду та 2-тієнілметиламіну, цільову сполуку одержали з 51% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=592,6. Приклад 61: (2S,4EZ)-N-(3,4-димeтoкcибeнзил)-1-(дифeнiлaцeтил)-4-(метоксііміно)-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, дифенілацетилхлориду та 3,4диметоксибензиламіну, цільову сполуку одержали з 74% чистотою за даними рідинної хроматографії/мас спектроскопії. MS(ESI+): m/z=502,6. Приклад 62: (2S,4ЕZ)-N1-(3,5-дихлорфеніл)-4-(етоксііміно)-N2-[2-(1Н-пірол-1-іл)феніл]-1,2піролідиндикарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-(етоксііміно)-2-піролідинкарбонової кислоти, 1,3-дихлоро-5-ізоціанатобензолу та 2-(1Hпірол-2-іл)феніламіну, цільову сполуку одержали з 54% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=500,6. Приклад 63: (2S,4EZ)-N 2-(1,3-бензодіоксол-5-ілметил)-4-{[(4-метоксибензил)окси]іміно}-N1-пентил-1,2піролідиндикарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-{[(4-метоксибензил)окси]іміно}-2-піролідинкарбоновоїкислоти, 1-ізоціанатопентану та 1,3бензодіоксол-5-ілметиламіну, цільову сполуку одержали з 63% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=511,4. Приклад 64: (2S,4ЕZ)-N-бензил-4-[(бензилокси)іміно]-1-(дифенілацетил)-N-метил-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-4[(бензилокси)іміно]-1-(трет-бутоксикарбоніл)-2-піролідинкарбонової кислоти, дифенілацетилхлориду та Nбензил-N-метиламіну, цільову сполуку одержали з 42% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=532,4. Приклад 65: (2S,4ЕZ)-N-(2,1,3-бензотіадіазол-4-іл)-!-([1,1¢-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, [1,1'-дифеніл]-4-карбонілхлориду та 2,1,3бензотіадіазол-4-аміну, цільову сполуку одержали з 66% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=472,4. Приклад 66: (2S,4EZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-N-(6-хінолініл)-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, [1,1'-дифеніл]-4-карбонілхлориду та 6хінолінаміну, цільову сполуку одержали з 79% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=465,4. Приклад 67: (2S,4ЕZ)-1-ацетоацетил-N-бензил-4-(метоксііміно)-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, 2,4-оксетандіону та бензиламіну, цільову сполуку одержали з 45% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=332,2. Приклад 68: (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(хлорметилен)-N-(2-фурилметил)-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-(хлорметилен)-2-піролідинкарбонової кислоти, [1,1¢-дифеніл]-4-карбонілхлориду та 2фурилметиламіну, цільову сполуку одержали з 70% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=421,4. Приклад 69: (2S,4ЕZ)-1-[(4-хлорфенокси)ацетил]-4-{[(3,4-дихлорбензил)окси]іміно}-N-[(2RS)-2-гідрокси-2фенетил]-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-{[(3,4-дихлорбензил)окси]іміно}-2-піролідинкарбонової кислоти, (4хлорфенокси)ацетилхлориду та (1RS)-2-аміно-1-фенілетанолу, цільову сполуку одержали з 62% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=590,8. Приклад 70: (2S,4ЕZ)-N-аліл-1-(1,1'-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, [1,1'-дифеніл]-4-карбонілхлориду та аліламіну, цільову сполуку одержали з 87% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=378,2. Приклад 71: (2S,4ЕZ)-1-[1,1'-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-N-(2-тієнілметил)-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, [1,1¢-дифеніл]-4-карбонілхлориду та 2тієнілметиламіну, цільову сполуку одержали з 78% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=434,4. Приклад 72: (2S,4ЕZ)-4-(ціанометилен)-N-(2-фурилметил)-1-[(2-оксо-6-пентил-2Н-піран-3-іл)карбоніл)-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(ціанометилен)-2-піролідинкарбонової кислоти, 2-оксо-6-пентил-2Н-піран-3карбонілхлориду та 2-фурилметиламіну, цільову сполуку одержали з 34% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=424,4. Приклад 73: (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-(2-фурилметил)-(4-метоксііміно)-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, [1,1'-дифеніл]-4-карбонілхлориду та 2фурилметиламіну, цільову сполуку одержали з 75% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=418,4. Приклад 74: (2S,4ЕZ)-1-ацетил-N-циклопропіл-4-{[(3,4-дихлорбензил)окси]іміно}-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(трет бутоксикарбоніл)-4-{[(3,4-дихлорбензил)окси]іміно}-2-піролідинкарбонової кислоти, ацетилхлориду та циклопропіламіну, цільову сполуку одержали з 52% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=384,4. Приклад 75: (2S,4ЕZ)-N-(2-фурилметил)-4-(метоксііміно)-1-[(2-оксо-6-пентил-2Н-піран-3-іл)карбоніл]-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, 2-оксо-6-пентил-2Н-піран-3-карбонілхлориду та 2-фурилметиламіну, цільову сполуку одержали з 62% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=430,4. Приклад 76: (2S,4ЕZ)-N-бензил-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(метоксііміно)-N-метил-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, [1,1'-дифеніл]-4-карбонілхлориду та Nбензил-N-метиламіну, цільову сполуку одержали з 67% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=442,4. Приклад 77: (2S,4ЕZ)-1-(дифенілацетил)-4-(етоксііміно)-N-(2-тієнілметил)-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-(етоксііміно)-2-піролідинкарбонової кислоти, дифенілацетилхлориду та 2-тієнілметиламіну, цільову сполуку одержали з 74% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=462,4. Приклад 78: (2S,4EZ)-N-(2,1,3-бензотіадіазол-4-іл)-4-(ціанометилен)-1-(дифенілацетил)-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(ціанометилен)-2-піролідинкарбонової кислоти, дифенілацетилхлориду та 2,1,3бензотіадіазол-4-аміну, цільову сполуку одержали з 42% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=480,4. Приклад 79: (2S)-1-(дифенілацетил)-N-(1-нафтилметил)-4-оксо-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням з 1-(третбутоксикарбоніл)-4-оксопроліну, дифенілацетилхлориду та 1-нафтилметиламіну, цільову сполуку одержали з 60% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=463,4. Приклад 80: (3ЕZ,5S)-5-(1Н-бензімідазол-2-іл)-1-(дифенілацетил)-3-піролідинон О-метилоксим За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, дифенілацетилхлориду та 1,2-бензолдіаміну, цільову сполуку одержали з 72% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=425,4. Приклад 81: (2S)-2-[1-([1,1'-дифеніл]-4-ілкарбоніл)-4-метилен-2-піролідиніл]-1Н-бензимідазол За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням з 1-(третбутоксикарбоніл)-4-метиленпроліну, [1,1'-дифеніл]-4-карбонілхлориду та 1,2-бензолдіаміну, цільову сполуку одержали з 73% чистотою за даними рідинної хроматографії/мас-спектроскопії. MS(ESI+): m/z=380,4. Приклад 82: (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-4-(хлорметилен)-N-(2-метоксіетил)-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(хлорметилен)-2-піролідинкарбонової кислоти, [1,1¢-дифеніл]-4-карбонілхлориду та 2метоксіетиламіну, цільову сполуку одержали з 55% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=399,6. Приклад 83: (3ЕZ,5S)-5-(1Н-бензімідазол-2-іл)-1-(дифенілацетил)-3-піролідинон О-алілоксим За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-4[(алілокси)-іміно]-1-(трет-бутоксикарбоніл)-2-піролідинкарбонової кислоти, дифенілацетилхлориду та 1,2бензолдіаміну, цільову сполуку одержали з 63% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=451,4. Приклад 84: (2S,4EZ)-1-([1,1¢-дифеніл]-4-ілкарбоніл)-N-[2-(діетиламіно)етил]-4-(метоксііміно)-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4ЕZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, [1,1'-дифеніл]-4-карбонілхлориду та N1,N1діетил-1,2-етандіаміну, цільову сполуку одержали з 90% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=437,4. Приклад 85: (2S,4ЕZ)-1-(дифенілацетил)-4-{[(4-метоксибензил)окси]іміно}-N-[2-тієнілметил)-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-{[(4-метоксибензил)окси]іміно}-2-піролідинкарбонової кислоти, дифенілацетилхлориду та 2тієнілметиламіну, цільову сполуку одержали з 63% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=554,4. Приклад 86: (2S,4ЕZ)-1-([1,1'-дифеніл]-4-ілкарбоніл)-N-(3,4-диметоксибензил)-4-(метоксііміно)-2піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(третбутоксикарбоніл)-4-(метоксііміно)-2-піролідинкарбонової кислоти, [1,1¢-дифеніл]-4-карбонілхлориду та 3,4диметоксибензиламіну, цільову сполуку одержали з 58% чистотою за даними рідинної хроматографії/масспектроскопії. MS(ESI+): m/z=488,4. Приклад 87: (2S,4EZ)-1-ацетоацетил-4-(метоксііміно)-N-(1-нафтилметил)-2-піролідинкарбоксамід За загальним методом, опис якого було наведено у Прикладі 22, з започаткуванням із (2S,4EZ)-1-(трет
ДивитисяДодаткова інформація
Назва патенту англійськоюPharnaceutically active derivatives of pyrrolidine
Автори англійськоюSchwarz Matthias, Quattropani Anna
Назва патенту російськоюФармацевтически активные производные пирролидина
Автори російськоюШварц Маттиас, Куаттропани Анна
МПК / Мітки
МПК: A61K 31/403, A61K 31/496, A61P 1/16, C07D 409/12, C07D 403/12, A61K 31/433, C07B 61/00, A61P 31/18, A61P 25/00, A61P 43/00, A61P 25/08, A61P 15/00, C07D 405/06, A61K 31/5377, C07D 401/14, A61K 31/4545, A61K 31/506, A61P 13/12, A61P 15/06, A61K 31/402, C07D 403/06, A61P 9/10, A61K 31/401, C07D 207/22, C07D 401/04, C07D 403/14, C07D 405/14, A61P 37/04, A61K 31/517, A61K 31/4184, A61K 31/454, A61P 7/00, A61K 31/4439, A61K 31/4725, A61K 31/4015, A61K 31/4709, C07D 207/24, A61P 25/28, C07D 401/10, C07D 417/12, C07D 401/12, C07D 405/12, C07D 403/04
Мітки: фармацевтично, активні, похідні, піролідину
Код посилання
<a href="https://ua.patents.su/66-74362-farmacevtichno-aktivni-pokhidni-pirolidinu.html" target="_blank" rel="follow" title="База патентів України">Фармацевтично активні похідні піролідину</a>
Попередній патент: Кристалічна основа циталопраму
Наступний патент: Глиниста суміш, здатна утворювати вологостійкий гель
Випадковий патент: Напівкопчена ковбаса з зародками пшениці












