Спосіб отримання водорозчинних фосфонооксиметильних похідних спирту та фенолу
Номер патенту: 77033
Опубліковано: 16.10.2006
Автори: Делаханті Грег, Уолз Ендрю Дж., Бонневілле Джордж
Формула / Реферат
1. Спосіб отримання водорозчинних фосфонооксиметильних похідних, що включає такі етапи:
перший етап
R-OH піддають реакції з молярним надлишком галогенметану у присутності основи і придатного розчинника, за схемою:
![]() ,
,
другий етап
отриманий продукт піддають реакції з молярним надлишком фосфорної кислоти і основи у придатному розчиннику, за схемою:
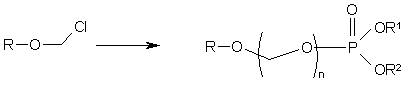 ,
,
при цьому R-OH являє собою лікарський засіб, що містить стерично блокований, слабоводорозчинний спирт або стерично блокований, слабо водорозчинний фенол, n являє собою ціле число 1 або 2, R1 являє собою водень, іон лужного металу або фармацевтично прийнятний катіон, і R2 являє собою водень, іон лужного металу або фармацевтично прийнятний катіон.
2. Спосіб за п. 1, в якому R-OH вибирають з групи, що містить камптотецин, пропофол, етопозид, вітамін Е або циклоспорин А.
3. Спосіб за п. 1, в якому n=1.
4. Спосіб за п. 1, в якому R1 і R2 незалежно один від одного вибирають з групи, що містить водень, натрій, калій, літій, протонований амін і протоновану амінокислоту.
5. Спосіб за п. 1, в якому на першому етапі R-OH піддають реакції з молярним надлишком бромхлорметану у присутності основи і придатного розчинника.
6. Спосіб за п. 1, в якому на першому етапі R-OH піддають реакції з молярним надлишком йодохлорметану у присутності основи і придатного розчинника.
7. Спосіб за п. 5, в якому як основу використовують гідроксид лужного металу або гідрид лужного металу.
8. Спосіб за п. 7, в якому як основу використовують гідроксид натрію або гідрид натрію.
9. Спосіб за п. 5, в якому як розчинник використовують апротонний або непротонний розчинник, що містить кисень.
10. Спосіб за п. 9, в якому як розчинник використовують тетрагідрофуран.
11. Спосіб за п. 5, в якому основу використовують у кількості щонайменше 1,5 моль на 1 моль R-OH.
12. Спосіб за п. 5, в якому бромхлорметан використовують у кількості щонайменше 10 моль на 1 моль R-OH.
13. Спосіб за п. 12, в якому бромхлорметан використовують у кількості від ~10 до ~30 моль на 1 моль 2,6-діізопропілфенолу.
14. Спосіб за п. 1, в якому R-OH являє собою 2,6-діізопропілфенол.
15. Спосіб за п. 1, в якому температуру реакції на першому етапі підтримують в діапазоні від ~25°С до ~65°С.
16. Спосіб за п. 1, в якому на другому етапі R-O-CH2Cl піддають реакції з молярним надлишком фосфорної кислоти і основи у придатному полярному апротонному розчиннику.
17. Спосіб за п. 16, в якому щонайменше близько 3 моль фосфорної кислоти вводять на 1 моль R-O-CH2Cl.
18. Спосіб за п. 17, в якому від ~3 до ~10 моль фосфорної кислоти вводять на 1 моль R-O-CH2Cl.
19. Спосіб за п. 1, в якому температуру реакції на другому етапі підтримують менше 100°С.
20. Спосіб за п. 19, в якому температуру реакції підтримують від ~25°С до ~80°С.
21. Спосіб за п. 16, в якому полярний апротонний розчинник вибирають з групи, що містить ацетонітрил, диметилформамід, диметилсульфоксид або N-метилпіролідон.
22. Спосіб за п. 16, в якому як основу використовують алкіламін або піридин або заміщене похідне піридину.
23. Спосіб за п. 22, в якому як основу використовують триетиламін.
24. Спосіб за п. 1, в якому рН на другому етапі спочатку підтримують від ~1 до ~2, а потім доводять до ~8 - ~11,5.
25. Спосіб отримання водорозчинних фосфонооксиметильних похідних, де 2,6-діізопропілфенол піддають реакції з бромхлорметаном з отриманням O-хлорметилдіізопропілфенолу:
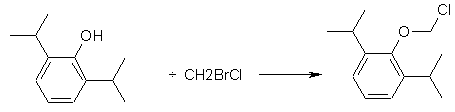 ,
,
а тоді O-хлорметилдіізопропілфенол піддають реакції з фосфорною кислотою з отриманням фосфоно-O-метил-2,6-діізопропілфенолу динатрієвої солі
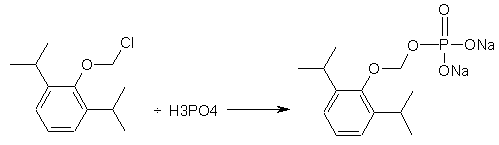 .
.
Текст
1. Спосіб отримання водорозчинних фосфонооксиметильних похідних, що включає такі етапи: перший етап R-OH піддають реакції з молярним надлишком галогенметану у присутності основи і придатного розчинника, за схемою: Cl R O R OH , C2 2 (19) 1 3 77033 4 Cl трил, диметилформамід, диметилсульфоксид або O OH N-метилпіролідон. 22. Спосіб за п. 16, в якому як основу використоCH2BrCl вують алкіламін або піридин або заміщене похідне піридину. , 23. Спосіб за п. 22, в якому як основу використоа тоді O-хлорметилдіізопропілфенол піддають вують триетиламін. реакції з фосфорною кислотою з отриманням фо24. Спосіб за п. 1, в якому рН на другому етапі сфоно-O-метил-2,6-діізопропілфенолу динатрієвої спочатку підтримують від ~1 до ~2, а потім довосолі O дять до ~8 - ~11,5. Cl 25. Спосіб отримання водорозчинних фосфоноокO P ONa O O ONa симетильних похідних, де 2,6-діізопропілфенол піддають реакції з бромхлорметаном з отриманH3PO4 ням O-хлорметилдіізопропілфенолу: . Ця заявка підтверджує пріоритет тимчасової заявки США 60/341,867, зареєстрованої 21.12.2001, опис якої включений в цю заявку у вигляді посилання у всій його повноті. Винахід стосується нового способу отримання водорозчинних проліків фармацевтичних препаратів, що містять блоковану гідроксильну групу ароматичного кільця. Зокрема, винахід стосується способу виготовлення водорозчинних фосфонооксиметильних ефірів фармацевтичних препаратів, що містять блокований спирт або фенол, таких як камптотецин, пропофол, етопозид, вітамін Ε і циклоспорин А. Належна доставка фармацевтичного препарату в організм пацієнта надзвичайно важлива для лікування будь-яких захворювань. Проте застосування багатьох клінічних лікарських засобів із відомими властивостями обмежене дуже низькою їхньою водорозчинністю. Внаслідок низької водорозчинності ці лікарські засоби можуть бути виготовлені тільки у фармацевтичних носіях, що виконують роль допоміжних розчинників, включаючи поверхнево-активні речовини. Було виявлено, що ці поверхнево-активні речовини викликають у людей тяжкі побічні ефекти, які обмежують клінічну безпечність цих лікарських засобів і, таким чином, можливість лікування кількох захворювань. Наприклад, камптотецин є природним продуктом, виділеним з кори китайського дерева камптотека, Camptotheca accuminata. Він показав сильну протипухлинну дію у кількох тваринних моделях, включаючи основні типи пухлин, такі як рак легенів, молочної залози, яєчників, підшлункової залози, товстої кишки і шлунка, а також злоякісна меланома. Серйозний недолік камптотецину - це його дуже обмежена водорозчинність. Для біологічних досліджень необхідно розчиняти цю сполуку у сильному органічному розчиннику (DMSO (диметилсульфоксид)) або готувати суміш у вигляді суспензії у Tween 80/сольовому розчині, що є небажаним фармацевтичним складом для лікування людей. Нещодавно у Сполучених Штатах були схвалені два аналоги камптотецину з помірною водорозчинністю для лікування прогресуючого раку яєчників (Hycamtin) і раку товстої і прямої кишки (Camptosar). Інші лікарські засоби, подібні камптотецину, що мають такі ж недоліки, включають циклоспорин A (CsA), пропофол, етопозид і вітамін Ε (альфатокоферол). Подібно до камптотецину, CsA містить у своїй структурі стерично блокований спирт, зокрема, у цьому випадку вторинний спирт. CsA виготовляють у вигляді суміші у CremophorEL/етанолі. Прикладом стерично блокованого, слабо водорозчинного фенолу є анестезуючий засіб пропофол. Пропофол виготовляють для внутрішньовенного клінічного застосування у вигляді емульсії типу масло/вода. Пропофол не тільки є слабо водорозчинним, але й викликає біль на ділянці ін'єкції. Біль необхідно полегшувати, наприклад, лідокаїном. Крім того, оскільки пропофол виготовляють у вигляді емульсії, важко і небезпечно додавати у цей склад інші засоби і змінювати фізичні параметри препарату, наприклад, збільшення розміру масляної краплі може привести до емболії легенів і т.д. У патенті США 6,204,257 описана водорозчинна форма лікарських засобів, що містять спирт і фенол, таких як камптотецин і пропофол. У випадку камптотецину сполуки являють собою фосфонооксиметильні ефіри камптотецину у формі вільної кислоти та її фармацевтично прийнятних солей. Водорозчинність кислоти і солей полегшує приготування фармацевтичних препаратів. Проте способи отримання водорозчинної форми лікарських засобів, що містять спирт і фенол, описані у патенті США 6,204,257, дуже складні і використовують дорогі і канцерогенні реагенти. Наприклад, синтез Офосфонооксиметилпропофолу включає 6 етапів, як показано нижче на реакційній схемі. 5 77033 6 , при цьому R-OH являє собою лікарський засіб, що містить спирт або фенол, n являє собою ціле число 1 або 2, R1 являє собою водень, іон лужного металу або фармацевтично прийнятний катіон, і R2 являє собою водень, іон лужного металу або фармацевтично прийнятний катіон. У переважному варіанті здійснення 2,6діізопропілфенол піддають реакції з бромхлорметаном з отриманням О-хлорметилдіізопропілфенолу. О-хлорметил-діізопропілфенол піддають реакції з фосфорною кислотою з отриманням фосфоно-О-метил-2,6-діізопропілфенолу динатрієвої солі. Бажано винайти спосіб, що є коротшим і не використовує канцерогенних або дорогих реагентів. Винахід стосується нового способу отримання водорозчинних фосфонооксиметильних похідних лікарських засобів, що містять спирт і фенол, зокрема, фосфоно-О-метил-2,6-діізопропілфенолу динатрієвої солі. Зокрема, винахід стосується способу отримання водорозчинних фосфонооксиметильних похідних, що включає такі етапи: перший етап , другий етап Винахід стосується нового способу отримання водорозчинних фосфонооксиметильних похідних лікарських засобів, що містять спирт і фенол, зокрема, фосфоно-O-метил-2,6-діізопропілфенолу динатрієвої солі. Такі фосфонооксиметильні похідні описані у патенті США 6,204,257, опис якого включений в цю заявку у вигляді посилання у всій його повноті. Спосіб за цим винаходом включає лише два етапи і не потребує канцерогенних і дорогих початкових матеріалів, використовуваних у попередній технології. Крім того, спосіб не потребує хроматографії. Цей спосіб забезпечує високі виходи продукту до 85%, звичайно ~40-85%. Описаний винахід стосується нового способу отримання водорозчинних фосфонооксиметильних похідних фармацевтичних препаратів, що містять спирт і фенол, представлених формулою І: Формула І представляє похідне ROH, при цьому ROH являє собою лікарський засіб, що містить спирт або фенол, наприклад, камптотецин, пропофол, етопозид, вітамін Ε і циклоспорин A. ROH переважно являє собою фармацевтичний препарат, що містить фенол, такий як пропофол. Винахід також стосується деяких лікарських засобів, для яких неможливе виготовлення ін'єкційних 7 77033 8 форм внаслідок властивої їм низької водорозчингідрофурану (THF), з отриманням О-хлорметилності. Ці лікарські засоби включають, але не об2,6-діізопропілфенолу. Температура реакції може межуються ними, даназол, метилтестостерон, йостановити від ~20°С до ~100 °С, переважно від дохінол, атовакуон і флюконат. ~25°С до ~65°С. n являє собою ціле число 1 або 2, переважно Основа переважно являє собою гідроксид лу1 1. R являє собою водень або іон лужного металу, жного металу або гідрид лужного металу. Придатні такого як натрій, калій або літій, або протонований гідроксиди і гідриди лужних металів включають, амін чи протоновану амінокислоту, або будь-який але не обмежуються ними, гідрид натрію і гідрокінший фармацевтично прийнятний катіон. R2 являє сид натрію. собою водень або іон лужного металу, такого як Кількість основи складає щонайменше близько натрій, калій або літій, протонований амін чи про1,5моль основи на 1моль 2,6-діізопропілфенолу. тоновану амінокислоту, або будь-який інший фарКількість бромхлорметану складає щонайменше мацевтично прийнятний катіон. близько 10моль, переважно близько 10-30моль Похідні формули І можуть бути отримані відбромхлорметану на 1моль 2,6-діізопропілфенолу. повідно до наступної реакційної схеми: Припускається, що бромхлорметан може бути замінений йодохлорметаном. перший етап THF може бути замінений іншими відповідними розчинниками, наприклад, непротонними розчинниками, що містять кисень, із сильною розчи, няючою здатністю, такими як глікольні ефіри. другий етап На другому етапі O-хлорметил-2,6діізопропілфенол піддають реакції з молярним надлишком фосфорної кислоти і основи у придатному розчиннику. Щонайменше ~3, переважно від ~3 до ~10, звичайно ~6моль фосфорної кислоти і , основи змішують з 1 моль O-хлорметил-2,6діізопропілфенолу. Температура реакції становить При цьому R-OH являє собою лікарський заменше 100°С, звичайно ~25°С-80°С. сіб, що містить спирт або фенол, n являє собою 1 Придатні розчинники включають полярні апроціле число 1 або 2, R являє собою водень, іон тонні розчинники, такі як ацентонітрил, диметиллужного металу або фармацевтично прийнятний формамід (DMF), диметилсульфоксид (DMSO) або катіон, і R2 являє собою водень, іон лужного метаN-метилпіролідон (NMP). Розчинник повинен бути лу або фармацевтично прийнятний катіон. здатний солюбілізувати триетиламонієву сіль проНа першому етапі R-OH піддають реакції з ведукту. Основа переважно являє собою алкіламін ликим надлишком бромхлорметану у присутності або піридин, або заміщене похідне піридину. основи і тетрагідрофурану (THF). Тоді отриманий Більш переважно, основа являє собою триетилапродукт піддають реакції з надлишком фосфорної мін. кислоти і основи у придатному розчиннику. Потім розчинник видаляють, а залишок розчиНаведена вище схема може бути описана на няють у воді і підкислюють, наприклад, НСI, до рН прикладі використання 2,6-діізопропілфенолу у приблизно від 1 до 2, переважно близько 1,5. Проякості початкового матеріалу. На першому етапі дукт у формі вільної кислоти екстрагують у МТВЕ 2,6-діізопропілфенол піддають реакції з бромхло(трет-бутил-метиловий ефір). рметаном з отриманням О-хлорметилПотім розчинник видаляють, наприклад, під діізопропілфенолу. вакуумом. Залишок розчиняють у воді, рН доводять до ~8-11,5 за допомогою придатного реагенту, наприклад, NAOH, і розчин екстрагують придатним розчинником, наприклад, толуолом. Тоді розчин може бути концентрований. Потім може бути введений ізопропанол або інший придатний розчинник, і тоді продукт осаджують або перекристалізують. Придатні розчинники, що включають На другому етапі О-хлорметилполярні водорозчинні органічні розчинники, такі як діізопропілфенол піддають реакції з фосфорною ацетон, ацетонітрил, спирт, THF або діоксан, закислотою з отриманням фосфоно-O-метил-2,6безпечують отримання фосфоно-О-метил-2,6діізопропілфенолу динатрієвої солі. діізопропілфенолу динатрієвої солі. Приклад 1 Етап 1: 500-мл круглодонну колбу з чотирма шийками обладнали механічною мішалкою, входом для азоту, холодильником і термометром. Загрузили 17,8г (0,10моль) 2,6-діізопропілфенолу, 200мл THF, 8,0г (0,20моль) гранул гідроксиду натрію і 387г (3,0моль, 194мл) бромхлорметану. Реакційну суміш нагріли до 64°С і витримали 2-3 годиБільш детально, на першому етапі 2,6ни до зникнення 2,6-діізопропілфенолу, що діізопропілфенол піддають реакції з великим мовизначали газовою хроматографією. Після охололярним надлишком бромхлорметану у присутності дження до 25°С суспензію профільтрували і залиоснови і придатного розчинника, переважно тетра 9 77033 10 шок на фільтрі промили THF. THF видалили шля(за стандартом USP, фармакопея США). рН суміші хом роторного випарювання і отримане масло доводять до 11 50% водним розчином гідроксиду дистилювали під вакуумом (0-1торр, температура натрію. Водну суміш двічі промивають толуолом. кипіння = 80°С) з отриманням 16,9г (0,074моль, Тоді водну суміш частково концентрують під вакувихід 75%) О-хлорметил-2,6-діізопропілфенолу. умом до ~40-50% початкового об'єму. До концентЕтап 2: 1-л круглодонну колбу з чотирма шийрованого водного розчину додають ізопропіловий ками, обладнану термопарою для контролю темспирт (525кг) при 70°С, тоді охолоджують до 0°С ператури, вмістили у нагрівальний кожух. У колбу для кристалізації продукту. Тверду речовину збизагрузили 300мл ацетонітрилу, а потім триетиларають шляхом фільтрації і висушують під вакуумін (48,7мл, 0,349моль) і 85% фосфорну кислоту мом з отриманням фосфоно-О-метил-2,6(18,7мл, 0,318моль). Тоді додали О-хлорметилдіізопропілфенолу динатрієвої солі (C13H19Na2O5P, 2,6-діізопропілфенол (12г, 0,0529моль) і реакційFW=332). ний розчин нагрівали до 65°С протягом 2 годин. Приклад 3 Завершення реакції визначали за зникненням поЕтап 1: 500-мл круглодонну колбу з чотирма чаткового матеріалу шляхом TLC (тонкошарова шийками обладнали механічною мішалкою, вхохроматографія) і HPLC (рідинна хроматографія дом для азоту, холодильником і термометром. високого тиску). Розчину дали охолодитися і суміш Загрузили 8,9г (0,05моль) 2,6-діізопропілфенолу, концентрували під зниженим тиском. Залишок ро100мл THF і 4,0г (0,10моль) гранул гідроксиду назчинили у 500мл води і підкислили 8N НСI до рН трію. Отриману зелену суспензію нагріли до 601,5. Цей розчин тричі екстрагували 500мл МТВЕ. 65°С і витримали 1 годину. Реакційну суміш охоОб'єднані органічні екстракти промили один раз лодили до 30°С і додали 100мл (199г, 1,54моль) сольовим розчином і органічний шар профільтрубромхлорметану і знову нагріли. Реакційну суміш вали через целіт. До залишку додали 60мл води і витримали при 64°С 2-3 години до зникнення 2,6додали 20% розчин NAOH до рН=8,6. Розчин двічі діізопропілфенолу, що визначали газовою хромапромили 50мл толуолу. Водний розчин концентрутографією. Після охолодження до 25°С суспензію вали під зниженим тиском до половини початковопрофільтрували через целіт і залишок на фільтрі го об'єму і додали 315мл ізопропанолу. Суміш напромили THF. THF видалили роторним випарюгріли до 70°С для розчинення продукту і потім ванням і отримане масло дистилювали під вакууохолодили до 0°С. Білу тверду речовину, що крисмом (0-1торр, температура кипіння = 80°С) з отриталізувалася, виділили шляхом вакуумної фільтманням 9,6г (0,042моль, вихід 85%) О-хлорметилрації, промили один раз 45мл ізопропанолу і ви2,6-діізопропілфенолу. сушили у вакуумній печі (30дюймів (762мм) рт. ст., Етап 2: 500-мл круглодонну колбу з чотирма 45°С) протягом 48 годин з отриманням 13,1г шийками, обладнану термопарою для контролю (0,039моль, вихід 75%) білої твердої речовини. температури, вмістили у нагрівальний кожух. У Приклад 2 колбу загрузили 300мл ацетонітрилу, а потім триеЕтап 1: 2,6-діізопропілфенол (20кг, FW (молетиламін (48,7мл, 0,349моль) і 85% фосфорну кискулярна вага за формулою) = 178, 112моль, 1екв.) лоту (18,7мл, 0,318моль). Тоді додали Опіддають реакції з бромхлорметаном (347кг, хлорметил-2,6-діізопропілфенол (12г, 0,0529моль) FW=129, 2682моль, 24екв.) і гідроксидом натрію і реакційний розчин нагрівали до 65°С протягом 2 (11кг, FW=40, 280моль, 2,5екв) у тетрагідрофурані годин. Завершення реакції визначали за зникнен(108кг, FW=72, 1498моль, 13,3екв.) при зрошуванні ням початкового матеріалу шляхом TLC і HPLC. протягом приблизно 1,5 години. Після охолодженРозчину дали охолодитися і суміш концентрували ня до 20°С реакційну суміш гасять водою (87кг). під зниженим тиском. Залишок розчинили у 500мл Органічний шар збирають і двічі промивають 15% води і підкислили 8N НСI до рН 1,5. Цей розчин водним розчином хлориду натрію (78кг кожного тричі екстрагували 500мл МТВЕ. Об'єднані органіразу). Після відокремлення шарів знову збирають чні екстракти промили один раз сольовим розчиорганічний шар і з органічного шару дистилюють ном і органічний шар профільтрували через целіт. розчинники з отриманням неочищеного масла. Додали 1 еквівалент TEA і розчин концентрували Неочищене масло дистилюють звичайною дистипід зниженим тиском. До залишку додали 60мл ляцією з отриманням очищеного хлорметил(2,6води і додали 20% розчин NAOH до рН 8,6. Цей діізопропілфенілового) ефіру (FW=227) у вигляді розчин двічі промили 50мл толуолу. Водний розсвітло-жовтого масла. чин концентрували під зниженим тиском. Додали Етап 2: Хлорметил(2,6-діізопропілфеніловий) воду (30мл) і розчин охолодили у льодяній бані. ефір (20кг, FW=227, 88,20моль, 1екв.) піддають Додали по краплях ацетон (300мл). Отриману суреакції з фосфорною кислотою (81кг, 85%, FW=98, міш охолоджували у холодильнику протягом ночі. 705моль, 8екв.) і триетиламіном (89кг, FW=101, Тоді суміш охолодили у льодяній бані протягом 1 883моль, 10екв.) в ацетонітрилі (200кг, FW=41, години і відфільтрували тверду речовину. Білу 4872моль, 55екв.) приблизно при 75°С протягом 3 тверду речовину висушили у вакуумній печі (30 годин. Реакційну суміш охолоджують і концентрудюймів (762мм) рт. ст., 45°С) протягом 48 годин з ють під вакуумом. Отриману пастоподібну суміш отриманням 7,50г (0,023моль, вихід 43%) білої розчиняють у воді. рН суміші доводять до 1,5 контвердої речовини. центрованою соляною кислотою. Підкислену суПриклад 4 міш двічі екстрагують толуолом. Обидва органічні 2,6-діізопропілфенол обробили бромхлормеекстракти об'єднують і один раз промивають вотаном у присутності гідроксиду натрію і THF з дою. Органічний розчин концентрують під вакууотриманням 85%-го виходу O-хлорметил-2,6мом. Утворене масло змішують з очищеною водою діізопропілфенолу, який очистили вакуумною дис 11 77033 12 тиляцією. Після обробки О-хлорметил-2,6Хоча винахід був описаний з використанням діізопропілфенолу фосфорною кислотою і триетиокремих прикладів, включаючи переважні на цей ламіном у ацетонітрилі з наступним видаленням час моделі здійснення винаходу, фахівцям у відрозчинника, розчиненням у метанолі, регулюванповідній області науки буде зрозуміло, що існують ням рН і осадженням ацетоном отримали 85%-й численні варіації і видозміни описаних вище сисвихід фосфоно-О-метил-2,6-діізопропілфенолу тем і методик, які входять до області винаходу. динатрієвої солі. Комп’ютерна верстка О. Гапоненко Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for making water-soluble phosphonooxymethyl ethers of hindered alcohol and phenol containing pharmaceuticals
Назва патенту російськоюСпособ получения водорастворимых фосфонооксиметильных производных спирта и фенола
МПК / Мітки
МПК: A61K 31/661, C07F 9/06
Мітки: фосфонооксиметильних, фенолу, похідних, спосіб, отримання, спирту, водорозчинних
Код посилання
<a href="https://ua.patents.su/6-77033-sposib-otrimannya-vodorozchinnikh-fosfonooksimetilnikh-pokhidnikh-spirtu-ta-fenolu.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання водорозчинних фосфонооксиметильних похідних спирту та фенолу</a>
Попередній патент: Металокорд з поліпшеним проникненням гуми
Наступний патент: Спосіб визначення кількості курсів радіойодотерапії при лікуванні хворих на диференційований рак щитовидної залози
Випадковий патент: Експрес-спосіб кількісного визначення основних фракцій вуглеводного комплексу інулінвмісної сировини










