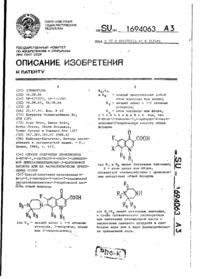
Спосіб одержання похідних пірідазінона або їх водорозчинних солей з фармацевтично прийнятною кислотою
Номер патенту: 6841
Опубліковано: 31.03.1995
Автори: Єсімі Кітада, Макіо Кобаясі, Ісао Сімоода, Рікізо Фуруя, Хіромі Окусіма, Акіхіро Наріматсу
Формула / Реферат
Формула изобретения
Способ получения производных пиридазинона общей формулы
где А - 4-пиридил или 2-пиримидил; R1 и R2 - независимо друг от друга водород или С1-С5-алкил; пунктирная линия - одинарная или двойная связь, или их водорастворимых солей с фармацевтически приемлемой кислотой, отличающийся единение обшей формулы
где R1 и R2 имеют указанные значения, подвергают взаимодействию с соединением формулы
А - X,
где X - галоген;
А имеет указанные значения, в среде полярного растворителя при температуре от 60°С до температуры кипения реакционной среды и выделяют целевой продукт в свободном виде или в виде водорастворимой соли с фармацевтически приемлемой кислотой.
Текст
Изобретение относится к гетероциклическим соединениям, в частности к способу получения производных пиридазинона (ПД) или их водорастворимых солей с фармацевтически приемлемой кислотой, которые обладают кардиотонической активностью и могут найти применение в медицине. Синтез производных ПД общей формулы A-NH-C 6 H 4 - O N - НН-С(О)-С R j-CR,, где А -CR, 4-пиридил или 2-пиримидил; и R2 независимо друг от друга H z или С«-Суалкил, пунктирная линия - одинарная или двойная связь, или их солей ведут их, А-Х и соединения формулы H 2 N - C 6 H 4 -C=N - NH-C(O)-C R 2 -C R,, где R ,, F 2 , А указано выше; X - галоген, в среде полярного растворителя при температуре от 60 С до кипения реакционной среды. Выделяют целевой продукт в свободном виде или в виде водорастворимой соли с фармацевтически приемлемой кислотой. Новые СПД проявляют активность в дозе 0,01-0,03 мг/кг при токсичности LD 5 0 = 97 мг/кг (внутривенно) и 341 мг/кг (через рот). 2 табл. 1 134241 Изобретение относится к способу фураном, сушат и получают 1,2 г получения новых производных пиридази(42,5%) целевого продукта. Полоса понона обшей формулы глощения в ИК-спектре (КВг) при см~* \Ъ ( ) ь 1670 р и м.е р З . 6- [4-(4' -Пиридил) і П аминофенит]-4-метил-4,5-дигидро-З(2Н)"N-N" пиридазинона гидрохлорид. 1,02 г 6-(4-аминофенил)-4-метил10 4,5-дигидро-З(2F)-пиридазинона растгде А - 4-пиридил или 2-пиримидил; воряют в 5 мл N-метиллирролидона, в R, и R 2 - независимо друг от друэтот раствор добавляют 0,35 мл трига - атом водорода или С,- С 5 -алкил; этиламина, нагревают до 90 С, добавпунктирная линия - одинарная или ляют 0,75 г хлористоводородного 4двойная связь, 15 хлорпиридина и продолжают нагревание или их солей с фармацевтически приемв течение 2 ч при 90°С. Реакционную лемой кислотой, которые обладают карсмесь охлаждают на льду и добавляют диотоиической активностью и могут 50 мл ацетона. Осажденное кристаллинайти применение в медицине. ческое вещество отфильтровывают и Целью изобретения является получе- 20 растворяют в 50 мл воды. Водный растние соединений, обладающих более вывор доводят примерно до рН 9 при посокой кардиотонической активностью по мощи 1 н. раствора NaOH. Осажденное сравнению с известными производными кристаллическое вещество собирают по3(2Н)-пиридазинона. средством декантации и промывают П р и м е р I. 6-[4-(4 -Пиридил) 25 смесью ацетона и н-гексана. Полученный кристаллический продукт растворяаминофеншт] -4,5-дигидро-З (2Н) -пиридают в 10 мл ДМФА и хроматографируют на зинон. силикагеле с использованием в качест3,89 г хлористоводородного 4-бромве элюентов хлороформа и метанола. пиридина и 3,78 г 6-(4-аминофенил)4,5-дигидро-З(2Н)-пиридазинона раст- 30 Фракцию продукта концентрируют и сушат, твердый остаток растворяют в воряют в 50 мл ЇТ^-диметилформамида этаноле и смешивают с 1 н. раствором и нагревают 2 ч при 105 С в токе гаНС1 в этаноле и получают хлористовозообразного азота. Реакционную смесь дородную соль, которую осаждают довыливают в 800 мл воды, содержащей 2,12 г карбоната натрия, отфильтровы- 35 бавлением бензола, гексана и этилацетата, отфильтровывают, сушат и полувают осажденные кристаллы, промывают водой и сушат при пониженном давлении, чают 0,98 г С61,8%) гидрохлорида, т.пл. 241-244°С. получают 4,28 г (70,7%) целевого продукта. Полоса поглощения в ИК-спектП р и м е р 4. 6-[4-(4 -Пиридил) ре (КВг) при 1642 см" 1 . Молекулярная 40 аминофенил]-5-метил-4,5-дигидро-З(2Н)масса, определенная с помощью масспиридазинона гидрохлорид. спектроскопии, М 266. 0,81 г 6-(4-аминофенил)-5-метилПолученное основание растворяют в 4,5-дигидро-З(2Н)пиридазинона раствометиловом спирте при нагревании, доряют в 4 мл N-метилпирролидона, смебавляют этанол, насыщенный НС1 и сер- 45 шивают с 0,28 мл триэтиламина, а заным эфиром осаждают хлористоводородтем нагревают до 90 С. Добавляют ную соль полученного основания. 0,60 г хлористоводородного 4-хлорпиП р и м е р 2. 6-[4-(2'-Пиримидиридина и продолжают нагревание в тео нил)аминоАенил]-4,5-дигидро-З(2Н)пичение 2 ч при 90 С. Реакционную смесь ридазинон. 50 охлаждают в ледяной бане и смешивают Смесь, состоящую из 2 г 6-(4-амис 50 мл ацетона для осаждения криснофенил)-4,5-дигидро-З(2Н)-пиридазиталлического вещества. Кристалличеснона и 1,22 г 2-хлорпиримидина нагрекое вещество растворяют в воде и подвают с обратным холодильником в 10 мл диметилформамида в течение 4 ч и ох- 55 щелачивают 1 н. раствором NaOH до выпадения осадка, который хроматографилаждают для осаждения кристаллическоруют на силикагеле с использованием го вещества. Осажденное кристалличессмеси хлороформа и метанола. Нужные кое вещество отфильтровывают, промыфракции концентрируют, сушат и перевают диметилформамидом и тетрагидроводят в хлористоводородную соль, как A З 1342416 описано в примере 1, получают 0,863 г мышцу с целью определения его влия(68,3%) гидрохлорида, т.пл. 249ния на сокращение папиллярной мышцы. 252°С. Степень увеличения сокращения папилП р и м е р 5. 6-[4-(4 -Пиридил) лярной мышцы показана в табл.1. аминофенил]-3(2Н)-пиридаэинона гидроВлияние на сокращение выделенного хлорид. левого предсердия у морской свинки. Смесь, состоящую из 2,33 г хлорисЛевое предсердие выделяли У самца товодородного 4-бромпиридина и 1,87 г морской свинки с весом тела 200 6-С 4-аминофенил)-3(2Н)-пнридазинона, 10 300 г вскоре после нанесения удара в подвергают взаимодействию в 30 мл заднюю часть его головы. Отверстие М,К-диметилформамида в течение 4 ч митрального клапана сердца закрепляпри 110 С в токе газообразного азота. ли у основания ванны для органов, заПосле охлаждения реакционной смеполненной 30 мл раствора Кребса-Хенси в нее добавляют 75 мл воды. Реак- ] селейта с температурой 35 С. Через ционную смесь нейтрализуют при помораствор Кребса-Хенселейта в ванне щи 2 н. раствора гидроокиси натрия с для органов пропускали газовую смесь, последующей фильтрацией осажденного содержащую 95% 0 2 и 5% С0 2 . Изометкристаллического вещества. Сырое крисрическое напряжение измеряли посредталлическое вещество перекристаллизо- 2Q СТВОМ присоединения левого предсердия к датчику с помощью нити. Предвывают из смеси этанола и воды, тщасердию было сообщено напряжение потельно очищают посредством хроматогракоя, равное 0,5 г, после чего его фии на силикагеле с целью удаления возбуждали с помощью прямоугольных следов загрязняющих примесей, нужные фракции концентрируют, сушат и пере- 25 импульсов длительностью 1 мс и напряжения, в 1,5 раза превышающего пороводят в хлористоводородную соль, как говое значение при частоте 2 Гц, с описано в примере 1, получают 0, 23 г использованием биполярных платиновых гидрохлорида. Полоса поглощения в электродов. ИК-спектре (КВг) при 1650 см"' . После стабилизации предсердия в П р и м е р 6. Смесь 2,5 г 4-хлор- 30 течение 30 мин с момента его пригопиридина гидрохлорида и 3,15 г 6-(4товления в ванну для органов добавляаминофенил)-4,5-дигидро-З(2Н)-пирили исследуемое соединение в растворидазинона подвергают взаимодействию теле с целью измерения его действия. в течение 7 ч при 60°С. Затем смесь Степень увеличения сокращения левого охлаждают, добавляют 200 мл ацетона 35 предсердия показана в табл.1. и перемешивают на ледяной бане до выВлияние на сокращение миокарда у падения кристаллов. Выпавшие кристаланестезированных собак. лы фильтруют, сушат, получают 3,49 г Использовали самцов и самок нечис6- [4-(4'-пиридил)аминофенил]-4,5-дигидро-З С2Н)-пиридазинона гидрохлори- 40 токровных собак с весом тела 8-15 кг. Собаку анестезировали посредством да (идентифицировано как соединение внутривенной инъекции пентабарбитала примера 1). натрия в расчете 30 мг/кг веса тела Фармакологические и токсикологии создавали у нее искусственное дыхаческие исследования новых производных пиридазинана 1 на их пригодность 45 ние. У собаки вскрывали грудную клетку между четвертым и пятым ребром, в качестве сердечных средств выполкоторое выпиливали. Перикардий наднены с применением следующих методов. резали с целью обнажения сердца. КроВлияние на сокращение препарата воток через аорту, который измеряли выделенной папиллярной мышцы с перекрестным кровообращением у собаки. 50 с помощью электромагнитного расходомера крови, датчик которого прикрепПрепарат выделенной папиллярной ляли к восходящей части дуги аорты, мышцы с перекрестным кровообращением использовали в качестве приблизительу собаки готовили в соответствии с ного индекса работы сердца (СО). Давметодом Эндо и Хашимото (Американ ление в левом желудочке (LVP) измеряджорнал ов физиолоджи, 1970, 218, 55 ли с помощью катетерного датчика дав1459-1463). Воздействие соединения ления Миллера, а первое производное измеряпи посредством внутриартериальLVP (спад/напсшнение) измеряли при ного впрыскивания соединения, раствопомощи дифференциатора. Сокращение ренного в растворителе, в папиллярную b 1342416 мышцы правого желудочка измеряли с помощью тензодатчика, прикрепленного А-ШЛ стенке. Кровяное давление во всем организме измеряли у левой бедренной артерии. Частоту сердцебиений измеряли с помощью электрокардиограммы (отгде А - 4-пиридил или 2-пирнмидил; ведение II) и кардиотахометра. РастR ( и Rj - независимо друг от друга вор соединения вводили внутривенно водород или С,-С 5 -алкил; через левую бедренную вену. то пунктирная линия - одинарная или двойная с в я з ь , Максимальное значение спада (наполили их водорастворимых солей с фарнение/спад), максимальное наполнение мацевтически приемлемой кислотой, и степень увеличения сокращения мышо т л и ч а ю щ и й с я тем, что соцы правого желудочка и работы сердца показаны в табл.1. 15 единение обшей формулы Острая токсичность. Ri Я Острая токсичность (LD 5 0 ) в случае внутривенного введения н введения через рот у самцов мышей определяли по методу Ричфилда и Билкоксона (Джорнал 2G ов фармаколоджи энд экспериментад тегде R и R z имеют указанные значения, рапетикс, 1949, 96, 99-113). Резульподвергают взаимодействию с соединетат показан в табл.1. нием формулы А - X, В табл.2 приведены данные кардио- 25 где X - галоген; тонической активности для известных А имеет указанные значения, соединений ряда пиридазинона II в в среде полярного растворителя при сравнении с предлагаемым соединени- / температуре от 60°С до температуры ем I. кипения реакционной среды и выделяют Из табл. 2 видно, что предлагаемые 30 целевой продукт в свободном виде или в виде водорастворимой соли с фармасоединения I обладают преимуществами цевтически приемлемой кислотой. по сравнению с известными пиридазиноПриоритет по признакам: нами и могут быть использованы в ме14.12.83 - при А - 4-пиридил и 2дицине. 35 пиримидил; Н, и R 2 - водород;г^^=^ - одинарФ о р м у л а и з о б р е т е н и я ная связь. 16.03.84 - при А - 4-пириднл; Способ получения производных пири- водород; =•=.-- - двойная R, и ; дазинона общей формулы 40 с в я з ь . Т а б л и ц е Соеди- Сокращение папилнение лярной мышцы сопо баки примеру Доза,мкг Увеличевнутри- ние, 7, артеря Сокращение левого предсердия морской свинки Доза г/мл ние, X ально Анестезия собаки Доза, ^величенне спавнутри- да/максивенно мального наполнения, X мкг/кг I LDSD ,нг/кг УвеличеУсиление Внутри- Через рот ние сокработы венно ращения сердца,Z мышиы правого желудочка , X 10 13,2 ю-' 115 10 45 23 13 30 15,4 3 х 1 Соединение 1 • • • ' по примеру 1 2 -! Увеличение,% спада/наполнения макс. 3 0,01 45* 0,03 93* Известное соединение I I где А - СН3С0; R, и R t - Н; 0,01 0,03 26** 54**. двойная связь 0,1 81** 0,3 78** 0,01 46 0,03 94 0,1 130 0,3 120 1,0 89 одинарная связь • *: Известное соединение IT, где 0,01 ANH - 1-имидазолил; R, и R -Н 0,03 9 32*** 2 l 0 1342416 Продолжение табл. 2 57*° 87*** 0,01 3 0,03 15 0,1 АО 0,3 двойная связь 0,1 0,3 одинарная связь 78 *Соль, например, гидрохлорид растворимый в воде, дающий возможность для назначений ** Соединения не образуют водорастворимых солей. Кардиотоническая активность при тех же дозах много ниже, чем у предлагаемый соединений. Хотя соединение растворимо в подкисленной воде, кардиотоническая активность много ниже, чем у предлагаемых соединений Редактор И.Рыбченко Составитель Г.Жукова Техред И.Попович Корректор М.Пожо Заказ 4447/58 Тираж 371 Подписное ВНИИПИ Государственного комитета СССР по делам изобретений и открытий 113035, Москва, Ж-35, Раушская наб., д.4/5 Производственно-полиграфическое предприятие^.Ужгород,ул.Проектная,4
ДивитисяДодаткова інформація
МПК / Мітки
МПК: C07D 403/12, C07D 237/14, C07D 237/00, A61K 31/53, A61P 9/04, A61K 31/50, A61K 31/505, C07D 401/12
Мітки: спосіб, похідних, водорозчинних, солей, прийнятною, кислотою, одержання, пірідазінона, фармацевтично
Код посилання
<a href="https://ua.patents.su/6-6841-sposib-oderzhannya-pokhidnikh-piridazinona-abo-kh-vodorozchinnikh-solejj-z-farmacevtichno-prijjnyatnoyu-kislotoyu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання похідних пірідазінона або їх водорозчинних солей з фармацевтично прийнятною кислотою</a>
Попередній патент: Пристрій керування приводом завантажувального лотка шахтної печи
Наступний патент: Спосіб отримання похідних акрилової кислоти
Випадковий патент: Спосіб гарячої пілігримової прокатки труб