Алкоксіалкілкарбамати імідазо[1,2-а]піридинів, спосіб їх одержання та лікарський засіб на їх основі
Номер патенту: 48122
Опубліковано: 15.08.2002
Автори: Грюндлер Герхард, Постіус Стефан, Сеннбілфінгер Йорг, Рідель Річард, Сімон Вольфганг-Александер
Формула / Реферат
1. Алкоксиалкилкарбаматы имидазо[1,2-а]пиридинов формулы (I)
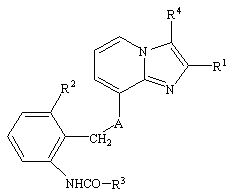 , (І)
, (І)
где R1 обозначает С1-4алкил;
R2 обозначает С1-4алкил;
R3 обозначает С1-4алкокси- С2-4алкокси;
R4 обозначает С1-4алкил или гидроксиметил;
А обозначает О (кислород) или NH,
и их соли.
2. Соединения формулы (I) по п. 1, в которых R обозначает гидроксиметил и А обозначает О (кислород), а R1, R2 и R3 имеют обозначения, указанные в п. 1, и их соли.
3. Замещенный имидазо[1,2-а]пиридин формулы (I) по п. 1, представляющий собой 8-{2-[(2-метоксиэтокси)карбониламино]-6-метилбензилокси}-2-метилимидазо[1,2-а]пиридин-3-метанол и его соли.
4. Замещенный имидазо[1,2-а]пиридин формулы (I) по п. 1, представляющий собой 8-{2-[(2-метоксиэтокси)карбониламино]-6-метилбензиламино}-2-метилимидазо[1,2-а]пиридин-3-метанол и его соли.
5. Замещенный имидазо[1,2-а]пиридин формулы (I) по п. 1, представляющий собой 8-{2-[(2-метоксиэтокси)карбониламино]-6-метилбензиламино}-2,3-диметилимидазо[1,2-а]пиридин и его соли.
6. Замещенные имидазо[1,2-а]пиридины формулы (I) по п.1, обладающие антацидным и противоязвенным действием.
7. Лекарственное антацидное средство, предназначенное для лечения и профилактики желудочно-кишечных заболеваний, в том числе и язвенной болезни, включающее активный ингредиент и фармацевтически приемлемые добавки, отличающееся тем, что в качестве активного ингредиента используют соединение формулы (I) по п. 1.
8. Способ получения соединений формулы (I) по п. 1 и их солей, отличающийся тем, что
а) соединения формулы (II)
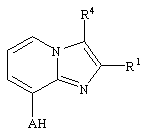 , (ІІ)
, (ІІ)
где R1, R4 и А имеют значения, указанные в п. 1, или их соли подвергают взаимодействию с соединениями формулы (III)
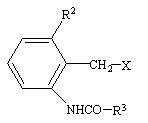 , (ІІІ)
, (ІІІ)
где R2 и R3 имеют значения, указанные в п. 1, а Х представляет собой соответствующую реактивную отщепляемую группу, или с их солями,
или
б) для получения соединений формулы (I), в которых R4 обозначает гидроксиметил, восстанавливают соединения формулы (IV)
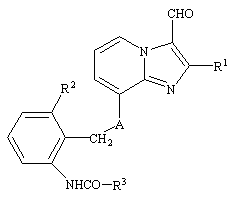 , (IV)
, (IV)
где R1, R2, R3 и А имеют значения, указанные в п. 1, и затем при необходимости соединения формулы (I), полученные согласно а) или б), переводят в их соли, или при необходимости затем из полученных солей соединений I высвобождают соединения формулы (I).
Текст
1 Алкоксиалкилкарбаматы имидазо[1,2а]пиридинов формулы (І) 1 метоксиэтокси)карбониламино]-6метилбензиламино}-2-метилимидазо[1,2а]пиридин-3-метанол и его соли 5 Замещенный имидазо[1,2-а]пиридин формулы (І) по п 1, представляющий собой 8-{2-[(2метоксиэтокси)карбониламино]-6метилбензиламино}-2,3-диметилимидазо[1,2а]пиридин и его соли 6 Замещенные имидазо[1,2-а]пиридины формулы (І) по п 1, обладающие антацидным и противоязвенным действием 7 Лекарственное антацидное средство, предназначенное для лечения и профилактики желудочно-кишечных заболеваний, в том числе и язвенной болезни, включающее активный ингредиент и фармацевтически приемлемые добавки, отличающееся тем, что в качестве активного ингредиента используют соединение формулы (I) по п 1 8 Способ получения соединений формулы (I) по п 1 и их солей, отличающийся тем, что а) соединения формулы (II) ,4 0 0 NHCO-R где R обозначает Сі 4ЭЛКИЛ, R обозначает Сі 4ЭЛКИЛ, R3 обозначает Сі 4алкокси- С-А 4алкокси, R4 обозначает Сі 4алкил или гидроксиметил, А обозначает О (кислород) или NH, и их соли 2 Соединения формулы (I) по п 1, в которых R обозначает гидроксиметил и А обозначает О (кислород), a R1, R2 и R3 имеют обозначения, указанные в п 1, и их соли 3 Замещенный имидазо[1,2-а]пиридин формулы (І) по п 1, представляющий собой 8-{2-[(2метоксиэтокси)карбониламино]-6метилбензилокси}-2-метилимидазо[1,2-а]пиридин3-метанол и его соли 4 Замещенный имидазо[1,2-а]пиридин формулы (І) по п 1, представляющий собой 8-{2-[(2 А Н , (И) где R1, R4 и А имеют значения, указанные в п 1, или их соли подвергают взаимодействию с соединениями формулы (III) ,2 NHCO-R3 2 о 3 где R и R имеют значения, указанные в п 1, а X представляет собой соответствующую реактивную отщепляемую группу, или с их солями, или б) для получения соединений формулы (I), в кото рых R обозначает гидроксиметил, восстанавливают соединения формулы (IV) СНО 48122 4 их соли, или при необходимости затем из полученных солей соединений I высвобождают соединения формулы (I) NHCO-R(IV) где R , R , R и А имеют значения, указанные в п 1, и затем при необходимости соединения формулы (I), полученные согласно а) или б), переводят в Изобретение относится к новым соединениям, предназначенным для применения в фармацевтической промышленности в качестве действующих веществ при изготовлении лекарственных средств В европейской патентной заявке ЕР-А0033094 описываются имидазо[1,2-а]пиридины, содержащие в положении 8 арильный заместитель, представляющий собой фенил, тиснил или пиридил либо фенил, замещенный на хлор, фтор, метил, трет-бутил, трифторметил, метокси или циано В качестве арильных радикалов, представляющих особый интерес, в упомянутой европейской заявке ЕР-А-0033094 названы фенил, о-либо п-фторфенил, п-хлорфенил и 2,4,6триметилфенил, причем наиболее предпочтительными из них являются фенил, о-либо пфторфенил и 2,4,6-триметилфенил В европейских патентных заявках ЕР-А0204285, ЕР-А-0228006, ЕР-А-0268989 и ЕР-А0308917 описываются имидазо[1,2-а]пиридины, содержащие в положении 3 ненасыщенный алифатический радикал, прежде всего (замещенный) алкинильный радикал В европейской патентной заявке ЕР-А0266890 описываются имидазо[1,2-а]пиридины, замещенные в положении 8 на алкенильный, алкильный либо циклоалкильный радикал Задачей настоящего изобретения является разработка новых соединений, обладающих противоязвенными и антисекреторными свойствами, способа их получения и лекарственного средства на их основе Было найдено, что подробно описанные ниже соединения, отличающиеся от известных соединений из уровня техники прежде всего замещением в положении 3 или 8, обладают неожиданными и особенно положительными свойствами Таким образом, объектом настоящего изобретения являются алкоксиалкилкарбаматы имидазо[1,2-а]пиридинов формулы I JHC0-R3 где Ri обозначает Сі-С4алкил, R2 обозначает СгС4алкил, R3 обозначает СгС4алкокси-С2-С4алкокси, R4 обозначает СгС4алкил или гидроксиметил и А обозначает О (кислород) или NH, и их соли Сі-С4алкил представляет собой линейные либо разветвленные алкильные радикалы с числом атомов углерода 1 - 4 В качестве примеров можно назвать бутил, изобутил, втор-бутил, трет-бутил, пропил, изопропил, этил и в первую очередь метил Сі-С4алкокси представляет собой атом кислорода, с которым связан один из вышеназванных СгС4алкильных радикалов Предпочтителен из них метоксильный радикал С2-С4алкокси представляет собой атом кислорода, с которым связан один из С2-С4алкильных радикалов, выбранный из группы указанных выше СгС4алкильных радикалов СгС4алкокси-С2-С4алкокси представляет собой С2-С4алкоксильный радикал, с которым связан СгС4алкоксильный радикал Предпочтителен среди них 2-метоксиэ-токсильный радикал В качестве солей соединений формулы I могут рассматриваться предпочтительно все кислотноаддитивные соли Особо следует назвать фармакологически приемлемые соли неорганических и органических кислот, применяемые обычно при изготовлении средств в галеновой форме Фармакологически неприемлемые соли, которые могут являться первичными продуктами способа, осуществляемого при получении соединений по изобретению в промышленном масштабе, переводятся затем с помощью известных специалисту методов в фармакологически приемлемые соли В 48122 качестве таковых пригодны водорастворимые, равно как и водонерастворимые кислотноаддитивные соли, образованные от таких кислот, как, например, соляная кислота, бромистоводородная кислота, фосфорная кислота, азотная кислота, серная кислота, уксусная кислота, лимонная кислота, D-глюконовая кислота, бензойная кислота, 2-(4-гидроксибензоил)бензойная кислота, масляная кислота, сульфосалициловая кислота, малеиновая кислота, лауриновая кислота, яблочная кислота, фумаровая кислота, янтарная кислота, щавелевая кислота, винная кислота, эмбоновая кислота, стеариновая кислота, толуолсульфоновая кислота, метансульфоновая кислота или З-гидрокси-2-нафтойная кислота, причем для получения соответствующей соли - в зависимости от того, какую кислоту используют одноосновную или многоосновную, и в зависимости оттого, какую соль требуется получить, кислоты применяют в эквимолярном количественном соотношении либо приблизительно в таком соотношении В качестве примеров соединений можно назвать следующие 8-{2-[(2метоксиэтокси)карбониламино]-6метилбензилокси}-2-метилимидазо[1,2-а]пиридин3-метанол, 8-{2-[(2метоксиэтокси)карбониламино]-6метилбензиламино}-2-метилимидазо[1,2а]пиридин-3-метанол и 8-{2-[(2-метоксиэтокси)карбониламино]-6-метилбезиламино}-2,3диметилимидазо[1,2-а]пиридин и их соли Среди соединений формулы I следует выделить такие, в которых R4 обозначает гидроксиметил и А представляет собой О (кислород), a Ri, R2 и R3 имеют указанные выше значения, а также соли этих соединений Другим объектом изобретения является способ получения соединений формулы I и их солей Способ заключается втом, что а) соединения формулы II В4 где R-і, R4 и А имеют указанные выше значения, или их соли подвергают взаимодействию с соединениями формулы III 4C -3 H OR где R2 и R3 имеют указанные выше значения, а X представляет собой соответствующую реакционноспособную отщепляемую группу, либо с их солями, или б) для получения соединений формулы 1, в которых R4 обозначает гидроксиметил, восстанавливают соединения формулы IV JC-3 H OR где R-і, R2, R3 и А имеют указанные выше значения и затем при необходимости соединения I, полученные согласно а) или б), переводят в их соли, или затем при необходимости из полученных солей соединений I высвобождают соединения I Взаимодействие соединений II с соединениями III осуществляют по методике, известной специалистам Соответствующей реакционноспособной отщепляемой группой является, например, атом галогена (предпочтительно хлор либо бром) или метансульфонилоксигруппа Обменную реакцию проводят предпочтительно в присутствии основания (например, неорганического гидроксида, такого, как гидроксид натрия, либо неорганического карбоната, такого, как карбонат калия, либо органического азотистого основания, такого, как триэтиламин, пиридин, коллидин или 4диметиламинопиридин), причем добавками катализаторов, таких, как иодид щелочного металла или бромид тетрабутиламмония, можно эффективно воздействовать на ход реакции Восстановление соединений IV осуществляют по обычной методике, хорошо известной специалистам Реакцию проводят в инертных растворителях, например, в низших алифатических спиртах, например, с использованием соответствующих гидридов, таких, как борогидрид натрия, при необходимости с добавками воды Выбор тех или иных параметров реакции, требуемых для осуществления способа, не доставит квалифицированному специалисту трудностей Выделение и очистку веществ по изобретению осуществляют с помощью известных методов, используя для этой цели, например, отгонку растворителя под вакуумом и перекристаллизацию полученного остатка из соответствующего растворителя или применяя один из обычных методов очистки, как, например, колоночная хроматография на соответствующем носителе Кислотно-аддитивные соли получают путем растворения свободного основания в соответствующем растворителе, например, в хлорированном углеводороде, таком, как метиленхлорид или хлороформ, в низкомолекулярном алифатическом спирте (этаноле, изопропаноле), в кетоне, таком, как ацетон, или в простом эфире, таком, как ТГФ или диизопропиловый эфир, который содержит требуемую кислоту или в который затем вводят требуемую кислоту Выделение солей осуществляют путем фильтрации, переосаждения, высаживания с помощью растворителя, нерастворяющего аддитивную соль, или путем выпаривания растворителя Полученные соли можно переводить подщелачиванием, например, водным раствором аммиака, в свободные основания, которые в свою очередь 48122 могут быть снова переведены в кислотноаддитивные соли Таким путем фармакологически неприемлемые кислотно-аддитивные соли могут быть превращены в фармакологически приемлемые кислотно-аддитивные соли Исходные соединения формулы II известны в частности из европейских патентных заявок ЕР-А0290003 и ЕР-А-0299470 Исходные соединения формулы III являются новыми Их получают аналогично способам, известным из соответствующих публикаций, а именно следующим образом в соединениях III, где X обозначает ОН, гидроксильную группу взаимодействием с галогенирующим средством, таким, как, например, тионилх-лорид, тионилбромид, фосфортрибромид либо оксалилхлорид, переводят в реакционноспо-собную отщепляемую группу, например, в атом галогена, или взаимодействием с метансульфонилхлоридом, при необходимости в присутствии основания, ее превращают в метансульфонилоксигруппу Соединения формулы IV представляют собой новые соединения и также являются объектом настоящего изобретения Как и соединения формулы I, их получают аналогичным взаимодействием соединений II, где R4 обозначает СНО, с соединениями III, описанными выше Нижеследующие примеры поясняют подробнее способ получения соединений формулы I Сокращение КТ обозначает комнатную температуру, ч обозначает час(ы) Примеры Конечные и промежуточные продукты 1 8-{2-[(2-метоксиэтокси) карбониламино]-6метилбензилокси}2-метилимидазо[1,2-а]пиридин3-карбоксальдегид Смесь 2,0г (11,35ммолей) 8-гидрокси-2метилимидазо[1,2-а]пиридин-3-карбоксальдегида, 1,2г безводного карбоната натрия, 0,17г (1,14ммоля) иодида натрия и 3,3г (12,8ммолей) 2мето кс и этил о во го эфира [2-(хлорметил)-3метилфенил]карбаминовой кислоты в 30мл ацетона перемешивают в течение 24ч при КТ и выливают в 200мл ледяной воды Затем осадок отфильтровывают, сушат и перекристаллизовывают из толуола/диизопропилового эфира В результате получают 3,9г (86,5%) соединения, указанного в заголовке, с Т П л 119 - 120°С 2 8-{2-[(2-метоксиэтокси) карбониламино]-6метилбензилокси}2-метилимидазо[1,2-а]пиридин3-метанол Суспензию 3,7г (9,3ммолей) 8-{2-[(2метоксиэтокси) карбониламино]-6метилбензилокси}-2-метилимидазо[1,2-а]пиридин3-карбоксальдегида в 40мл метанола смешивают при КТ с 362мг (9,3ммолей) 97%-ного борогидрида натрия и перемешивают в течение 75мин Затем выливают в ледяную воду, экстрагируют дихлорметаном и концентрируют в ротационновакуумном испарителе Оставшееся масло кристаллизуют с помощью 5мл изопропилового спирта, 5мл толуола и диизопропилового эфира Таким путем получают 2,7г (72,7%) соединения, указанного в заголовке, с Т пл 121 -123°С 3 8-{2-[(2-метоксиэтокси)карбониламино]-6метилбензиламино}-2-метилимидазо[1,2а]пиридин-3-карбоксальдегид Смесь из 2,0г (11,41 ммолей) 8-амино-2 8 метилимидазо[1,2-а]пиридин-3-карбоксальдегида, 1,21г (11,41 ммолей) безводного карбоната натрия, 0,17г (1,14ммоля) иодида натрия и 3,5г (13,6ммолей) 2-мето кс и этил о во го эфира [2(хлорметил)-3-метилфенил]карбаминовой кислоты в 30мл ацетона перемешивают в течение 24ч при КТ и концентрируют в ротационно-вакуумном испарителе Остаток смешивают со 100мл воды, после чего экстрагируют этилацетатом, органическую фазу сушат сульфатом магния и концентрируют в вакууме Остаток перекристаллизовывают из толуола В результате получают 3,31 г (73%) соединения, указанного в заголовке, с Тпл 153 155°С 4 8-{2-[(2-метоксиэтокси)карбониламино]-6метилбензиламино}-2-метилимидазо[1,2а]пиридин-3-метанол 2,8г (7,06молей) 8-{2-[(2метоксиэтокси)карбониламино]-6метилбензиламино}-2-метилимидазо[1,2а]пиридин-3-карбоксальдегида восстанавливают с помощью борогидрида натрия аналогично примеру 2, метанол отгоняют в вакууме, смешивают с водой и этилацетатом и раствором гидрофосфата калия устанавливают рН9 Затем несколько раз экстрагируют этилацетатом, сушат, концентрируют в вакууме и перекристаллизовывают из толуола/д иизопропилового эфира Таким путем получают 2,28г (81%) соединения, указанного в заголовке, с Т П л 138 -140°С 5 8-{2-[(2-метоксиэтокси)карбониламино]-6метилбензиламино}-2,3-диметилимидазо[1,2а]пиридин-изопропиловый спирт (1/1) Смесь 3,0г (18,6ммолей) 8-амино-2,3диметилимидазо[1,2-а]пиридина, 4,9г (46,2ммолей) безводного карбоната натрия, 0,28г (1,86ммоля) иодида натрия и 5,8г (22,5ммоля) 2мето кс и этил о во го эфира [2-(хлор-мети л)-3метилфенил]карбаминовой кислоты в 30мл ацетона перемешивают в течение 20ч при КТ Затем фильтруют, концентрируют в вакууме, смешивают с водой и этилацетатом, разбавленной соляной кислотой устанавливают рН6 и экстрагируют этилацетатом Органический раствор сушат и концентрируют в вакууме Остаток растворяют в 40мл ацетона и смешивают с раствором 1,2г (Ю.Зммолей) фумаровои кислоты в 80мл ацетона Выпадение кристаллов не происходит Тогда повторно концентрированный раствор смешивают с толуолом и изопропиловым спиртом и при температуре 0°С осаждают с помощью диизопропилового эфира 4,9г фумарата Полученный фумарат смешивают с 50мл этилацетата и 10мл воды, едким натром устанавливают рН9 и свободное основание экстрагируют этилацетатом После концентрирования в вакууме растворяют в толуоле/изопропиловом спирте и при температуре 0°С осаждают с помощью петролейного эфира (Ткип 40°С) В результате получают 2,2г (26,7%) соединения, указанного в заголовке, с Тпл 85 86°С 6 8-{2-[(2-мстоксиэтокси)карбониламино]-6метилбензилокси}-2-метилимидазо[1,2-а]пиридин3-метанол Смесь 178мг (1,0ммоль) 8-гидрокси-2метилимидазо[1,2-а]пиридин-3-метанола, 117мг 48122 10 (1,1ммоля) безводного карбоната натрия, 15мг лового эфира) Это соединение аналогично тому, (0,1ммоля) иодида натрия и 283мг (1,1ммоля) 2как это описано у Kammski и др , в Journ Meet мето кс и этил о во го эфира [2-(хлорметил)-3Chem 28, 876 (1985), Methode H , дебензилируют метилфенил]карбаминовой кислоты в 5мл ацетодо соединения, указанного в заголовке, с Т пл 251 на перемешивают в течение 48ч при КГ, затем 252°С Промышленная применимость Соединения перерабатывают аналогично примеру 2 и хромаформулы I и их соли обладают ценными фарматографируют с помощью этилацетакологическими свойствами, обеспечивающими их та/изопропилового спирта (соотношение 9 1) промышленную применимость Прежде всего они Таким путем получают 247мг (62%) соединения, обладают ярко выраженной способностью ингибиуказанного в заголовке ровать секрецию кислоты желудочного сока и отличным защитным действием по отношению к 7 8-{2-[(2-метоксиэтокси)карбониламино]-6желудку и кишечнику у теплокровных При этом метилбензилокси}-2,3-диметилимидазо[1,2наряду с хорошей растворимостью в водной среде а]пиридин соединения по изобретению отличаются высокой Аналогично примеру 5 подвергают взаимоизбирательностью действия, сравнительно продействию 2,0г (12,4ммолей) 8-гидрокси-2,3должительной длительностью действия, хорошей диметилимидазо[1,2-а]пиридина, 3,6г эитеральной эффективностью, отсутствием суще(13,9ммолей) 2-мето кс и этил о во го эфира [2ственных побочных эффектов и широким терапен(хлорметил)-3-метилфенил]карбаминовой кислотическим спектром ты, 0,18г иодида натрия и 1,3г карбоната натрия в 30мл ацетона В результате получают 1,07г Под понятием "защита желудка и кишечника" (22,5%) соединения, указанного в заголовке, с Т п л в контексте изобретения имеются в виду преду107-108°С преждение и лечение заболеваний желудочнокишечного тракта, прежде всего желудочноИсходные продукты кишечных воспалительных заболеваний и пораАа 2-Метоксиэтиловый эфир [2жений (как, например, язвенная болезнь желудка, (гидроксиметил)-3-метилфенил]карбаминовой язва двенадцатиперстной кишки, гастрит, раздракислоты жение желудка, вызванное повышенной кислотноК раствору ЗЗг (0,24моля) 2-амино-6стью или действием определенных лекарств), кометилбензилового спирта и 19,4мл (0,24моля) торые могут быть обусловлены, например, пиридина в 600мл изопропилового спирта при микроорганизмами (например, Hehcobacter pylori), температуре 10°С добавляют по каплям при пебактериальными токсинами, медикаментами (наремешивании и охлаждении 33,2г (0,24моля) 2пример, некоторыми противовоспалительными мето кс и этил о во го эфира хлормураньиной кислосредствами и антиревматическими средствами), ты Перемешивание продолжают еще в течение химикалиями (например, этанолом), кислотой же2ч при 0°С, затем смешивают с водой и изопролудочного сока или стрессовыми ситуациями Сопилацетатом и несколько раз экстрагируют изоединения по изобретению обладают, кроме того, пропилацетатом Органическую фазу сушат сультакже собственным действием против зародыша фатом магния и концентрируют при 50°С в Hehcobacter pylori ротационно-вакуумном испарителе Остаток хроматографируют на силикагельной колонне с поПо своим отличным противоязвенным и антимощью этилацетата После концентрирования в секреционным свойствам, проходившим эксперивакууме получают Збг (68%) соединения, указанментальную проверку на различных моделях, соного в заголовке, в виде масла единения по изобретению неожиданным образом заметно превосходят соединения, известные из Аб 2-Метоксиэтиловый эфир [2-(хлорметил)уровня техники Благодаря этим свойствам соеди3-метилфенил]карбаминовой кислоты К раствору нения формулы I и их фармакологически прием18,0г (0,075моля) указанного выше соединения в лемые соли могут исключительно эффективно 80мл толуола при температуре 17 - 20°С по капприменяться в медицине и ветеринарии, причем лям добавляют при перемешивании и охлаждении свое применение они могут находить в первую 9,4г (0,079моля) тионилхлорида и оставляют на очередь для лечения и/или профилактики заболеночь при КГ Затем охлаждают на ледяной бане, ваний желудка и кишечника, равно как и для лечерастирают и в результате получают 11,2г (57,7%) ния остеопороза соединения, указанного в заголовке, с Т пл 100 102°С После концентрирования маточного расОбъектом изобретения являются поэтому сотвора и кристаллизации из толуола/петролейного единения по изобретению, обладающие способэфира (Ткип 40°С), получают еще 4,8г (24,7%) ностью ингибировать секрецию кислоты желудочосадка с аналогичной температурой плавления ного сока Б 8-гидрокси-2-метилимидазо[1,2-а]пиридинИзобретение включает далее применение со3-карбоксальдегид единений по изобретению для изготовления лекарственных средств, обладающих способностью 4,77г (0,02моля) 8-бензилокси-2-метиингибировать секрецию кислоты желудочного солимидазо[1,2-а]пиридина перемешивают в смеси ка, которые предназначены для лечения и/или Вильсмайера, содержащей 20мл диметилформапрофилактики вышеназванных заболеваний мида и 2,3мл хлорокиси фосфора, в течение 2,5ч при температуре 60°С и смесь разделяют по Изобретение включает далее применение сообычной методике с помощью ледяной воды и единений по изобретению для лечения и/или гидрокарбоната калия Таким путем получают 8профилактики вышеназванных заболеваний бензилокси-2-метилимидазо[1,2-а]пиридин-3Другим объектом настоящего изобретения явкарбоксальдегид с Т пл 105 - 106°С (из диизопропиляются лекарственные средства, содержащие 12 11 48122 одно или несколько соединений формулы I и/или мер, гидроксид алюминия, алюминат магния, их фармакологически приемлемые соли транквилизаторы, такие, как бензодиазепины, наЛекарственные средства изготавливают с попример, диазепам, спазмолитические средства, мощью хорошо известных и доступных специаликак, например, биэтамиверин, камилофин, антисту методов В качестве лекарственных средств холинэргические средства, как, например, оксисоединения по изобретению, обладающие фармафенциклимин, фенкарбамид, местнокологическим действием (те действующие вещеанестезирующие средства, как, на пример, тетраства), применяют либо как таковые, либо предпочкаин, прокаин, при необходимости также ферментительно в комбинации с соответствующими ты, витамины или аминокислоты фармацевтическими вспомогательными вещестВ этой связи следует подчеркнуть особое знавами и/или наполнителями, причем они могут изчение соединений по изобретению при их примеготавливаться в виде таблеток, драже, капсул, нении в сочетании с другими медикаментозными суппозиториев, пластырей (например, в виде чресредствами, ингибирующими секрецию кислоты, к скожно действующей терапевтической системы), каковым относятся, например, ЬЬ-блокаторы (на+ + эмульсий, суспензий или растворов, содержание пример, циметидин, ранитидин), ингибиторы Н /К действующих веществ в которых составляет при - аденозинтрифосфотазы (например, омепразол, этом предпочтительно от 0,1 до 95%, а благодаря пантопразол), или, далее, с так называемыми певыбору вспомогательных веществ и наполнителей риферийными антихолинэргическими средствами можно получать средства в галеновой форме, (как, например, пирензепин, телензепин), а также точно соответствующей действующему веществу с гастриновыми антагонистами с целью дополнии/или желаемому наступлению действия (напрительного и даже сверхдополнительного усиления мер, в форме пролонгированного действия или в основного действия и/или исключения либо сниформе, устойчивой к действию желудочного сока) жения побочных эффектов, или, далее, в сочетании с субстанциями, обладающими антибактериВыбор вспомогательных веществ, соответстальным действием (как, например, венно носителей для изготовления требуемых цефалоспорины, тетрациклины, налидиксиновая препаративных форм для специалиста, обладаюкислота, пенициллины или также висмутовые сощего опытом в данной области, трудностей не ли), для борьбы с Hehcobacter pylori представляет Наряду с растворителями, загустителями, основными веществами для суппозиториФармакология ев, вспомогательными веществами для таблеток и Отличное защитное действие соединений по другими носителями действующих веществ могут изобретению по отношению к желудку и их споприменяться, например, покрытия для таблеток, собность ингибировать секрецию кислоты желуантиоксиданты, диспергаторы, эмульгаторы, антидочного сока подтверждают результаты эксперивспениватели, вкусовые добавки, консерванты, ментальных исследований, проведенных на вещества, способствующие растворимости, красимоделях животных Соединения по изобретению, тели или прежде всего промоторы для проницаепрошедшие экспериментальную проверку на мости и комплексообразователи (например, цикпредставленной ниже модели, получили порядколодекстрины) вые номера, соответствующие нумерации этих соединений в примерах Действующие вещества могут назначаться для орального, парентерального или чрескожного Испытание ингнбирующего секрецию действия введения на перфундированном желудке крыс Было установлено, что для достижения полоВ нижеследующей таблице представлено жительного терапевтического эффекта при лечевлияние соединений по изобретению после внутнии человека суточная доза при оральном введеривенного введения на стимулированную пентагании, при необходимости назначаемая в виде стрином секрецию кислоты перфундированного нескольких, предпочтительно от 1 до 4, разовых желудка крыс in vivo доз, должна содержать действующее вещество, Методика соответственно действующие вещества в количеУ наркотизированных крыс (крыса линии CD, стве от приблизительно 0,01 до приблизительно женская особь, 200 - 250г, 1,5г/кг, і m уретан) по20, предпочтительно 0,05 - 5, прежде всего 0,1 сле трахеотомии разрезом по центральной линии 1,5мг/кг веса тела Для парентерального введения эпистральной области вскрывали живот и введенмогут назначаться препараты примерно с той же ный трансорально один ПХВ-катетер фиксировали дозировкой действующих веществ или (в частнов пищеводе, а другой в привратнике таким обрасти при внутривенном введении), как правило, с зом, что концы мягких трубок входили в просвет более низкой дозировкой Выбор необходимой желудка Катетер, выходящий из привратника, оптимальной дозировки, равно как и формы ввечерез боковое отверстие с правой стороны живота дения действующих веществ и каждом отдельном выходил наружу случае компетентный специалист в данной обласПосле тщательного промывания (приблизити определяет сам тельно 50 - 100мл) желудок при температуре 37°С непрерывно спринцевали теплым физиологичеПри применении соединений по изобретению ским раствором NaCI (0,5мл/мин, рН6,8 - 6,9, прии/или их солей для лечения указанных выше забор типа Braun-Umta І) В собранном (с помощью болеваний фармацевтические композиции могут мерного цилиндра) через каждые 15мин эффлюсодержать в своем составе также один либо неатс определяли значение рН (измеритель кислотсколько фармацевтически активных ингредиентов, ности pH-Meter 632, стеклянный электрод ЕА147, относящихся к другим группам лекарственных 0 = 5мм, прибор Metrohm), а путем титрования средств, такие, как антацидные средства, напри 14 13 48122 свежеприготовленной 0,01Н NaOH до рН7 (прибор вещества Dosimat 655 Metrohm) определяли выделенную ЗООг 8-{2-[(2-метоксиэтокси)карбониламино]-6HCI метилбензилокси}-2-метилимидазо[1,2-а]пиридин3-метанола, 695г микрокристаллической целлюлоСтимулирование желудочной секреции осузы и 5г аморфной кремниевой кислоты подвергаществляли длительным внутривенным вливанием ют тонкому измельчению, тщательному смешива1мкг/кг (= 1,65мл/ч) і v пентагастрина (в левую нию и инкапсулированию с образованием твердых бедренную вену) приблизительно через ЗОмин желатиновых капсул 4 размера после завершения операции (т е после определения двух предварительных фракций) Испытуев) Капсулы с содержанием 10мг действующего мые субстанции вводили внутривенно в объеме вещества жидкости 1 мл/кг через бОмин после начала длиЮОг 8-{2-[(2-мстоксиэтокси)карбониламино]-6тельного внутривенного вливания пентагастрина метилбензиламино}-2-метилимидазо[1,2а]пиридин-3-мстанола, 895г микрокристалличеТемпературу тела подопытных животных с ской целлюлозы и 5г аморфной кремниевой кипомощью инфракрасного облучения и грелки (авслоты подвергают тонкому измельчению, тщатоматическое, бесступенчатое регулирование четельному смешиванию и инкапсулированию с рез ректальный температурный датчик) поддеробразованием твердых желатиновых капсул 4 живали постоянной на уровне 37,8 - 38°С размера Соединения формулы I обладают низкой токсичностью Так, например, для соединения из г) Ампулы с содержанием 10мг действующего примера 2 значения LDso составляют вещества Растворяют 3,16г 8-{2-[(2Мыши р о > 1000мг/кг метоксиэтокси)карбониламино]-6Крысы р о > ЮООмг/кг метилбензилокси}-2,3-диметилимидазо[1,2Мыши в/в около 80мг/кг а]пиридина в растворе 165,5г маннита и 0,5г карКрысы в/в около 20мг/кг боната натрия в 1300мл дистиллированной воды и Получение составов лекарственного средства стерильно фильтруют Полученный раствор разможет быть проиллюстрировано следующими ливают по 5мл в 15мл ампулы и лиофилизуют примерами Лиофилизат может быть вновь переведен в вода) Таблетки с содержанием 40ми действующеный раствор с 10мл воды го вещества 20кг 8-{2-[(2-метоксиэтокси)карбониламино]-6Таблица 1 метилбензилокси}-2-метилимидазо[1,2-а]пиридин3-метанола, 40кг молочного сахара, 26кг маисового крахмала и Зкг поливинилпирролидона смачиМаксимальное ингибирование Доза вают в 20 литрах воды и затем гранулируют провыделения кислоты в течение № (мкмоль/кг) пусканием через сита с размером ячеек 1,25 3,5ч по сравнению с исходным I V Гранулят высушивают в псевдоожиженном слое показателем в % до получения продукта с влажностью 50 - 60% и 2 1 97 затем смешивают с 8кг натрийкарбоксиметилцел4 1 83 люлозы, 2кг талька и Ікгстеарата магния Готовый 5 1 80 гранулят таблетируют в таблетки по 200мг диа1 92 7 метром 8мм б) Капсулы с содержанием 30мг действующего ДП «Український інститут промислової власності» (Укрпатент) вул Сім'ї Хохлових, 15, м Київ, 04119, Україна ( 0 4 4 ) 4 5 6 - 2 0 - 90 ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)216-32-71
ДивитисяДодаткова інформація
Назва патенту англійськоюImidazo[1,2-a]pyridine alkoxyalkyl carbamates, a process of their preparing and a drug on their basis
Назва патенту російськоюАлкоксиалкилкарбаматы имидазо[1,2-а]пиридинов, способ их получения и лекарственное средство на их основе
МПК / Мітки
МПК: A61P 19/10, A61P 1/04, C07D 471/04, A61P 1/00, A61K 31/435
Мітки: засіб, алкоксіалкілкарбамати, основі, спосіб, одержання, лікарський, імідазо[1,2-а]піридинів
Код посилання
<a href="https://ua.patents.su/7-48122-alkoksialkilkarbamati-imidazo12-apiridiniv-sposib-kh-oderzhannya-ta-likarskijj-zasib-na-kh-osnovi.html" target="_blank" rel="follow" title="База патентів України">Алкоксіалкілкарбамати імідазо[1,2-а]піридинів, спосіб їх одержання та лікарський засіб на їх основі</a>
Попередній патент: Інгібітори матричних металопротеаз і фармацетична композиція на їх основі
Наступний патент: Абразивний матеріал (варіанти) та спосіб його виготовлення
Випадковий патент: Спосіб виготовлення макаронних виробів











