Гідроксіетиламіносульфонаміди гетероциклокарбонільних амінокислот, фармацевтична композиція, способи інгібування протеаз ретровірусів та запобігання реплікації ретровірусу, а також способи лікування ретровірусн
Номер патенту: 63879
Опубліковано: 16.02.2004
Автори: Сікорскі Джеймс А., Дікрессенцо Гері А., Браун Дейвід Л., Девадас Балекудру, Фрескос Джон Н., МекДонелд Джозеф Дж., Нагараян Срінівазан, Гетмен Деніел П., Васкес Майкел Л.
Формула / Реферат
1. Сполука формули:
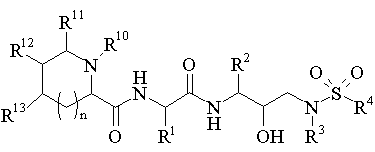
або її фармацевтично прийнятна сіль, похідне лікарського препарату з неї або ефір, де
n означає 0 або 1;
R1 означає алкіл з 1-5 атомами вуглецю, алкеніл з 2-5 атомами вуглецю, алкініл з 2-5 атомами вуглецю, гідроксіалкіл з 1-3 атомами вуглецю, алкоксіалкіл з 1-3 алкіл- і 1-3 алкоксі-атомами вуглецю, ціаноалкіл з 1-3 атомами вуглецю, імідазолілметил, радикали -СН2СОNH2, -CH2CH2CONH2, -CH2S(О)2NH2, -СН2SСН3, -CH2S(О)СН3, -СН2S(О)2СН3, -С(СН3)2SСН3, -С(СН3)2S(О)СН3 або -С(СН3) 2S(О)2СН3;
R2 означає радикали алкілу з 1-5 атомами вуглецю, аралкіл з 1-3 атомами вуглецю, алкілтіоалкіл з 1-3 атомами вуглецю, арилтіоалкіл з 1-3 атомами вуглецю або циклоалкілалкіл з 1-3 атомами вуглецю і з 3-6 членами;
R3 означає радикали алкілу з 1-5 атомами вуглецю, циклоалкіл з 5-8 членами або радикал циклоалкілметилу з 3-6 членами;
R4 означає арил, бензосконденсований гетероарил з 5-6 членами або радикали бензосконденсованого гетероциклу з 5-6 членами, або радикал формули
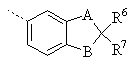 ,
,
де А і В незалежно один від одного означають О, S, SO або SO2;
R6 означає дейтерій, алкіл з 1-5 атомами вуглецю, радикали фтору або хлору;
R7 означає водень, дейтерій, метил, фтор або хлор радикали або радикал формули
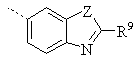 ,
,
де Z означає О, S або NH, і
R9 означає радикал формули
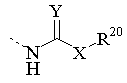 ,
,
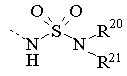
або
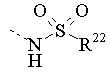 ,
,
де Y означає О, S або NH;
X означає зв'язок, О або NR21;
R20 означає водень, алкіл з 1-5 атомами вуглецю, алкеніл з 2-5 атомами вуглецю, алкініл з 2-5 атомами вуглецю, аралкіл з 1-5 атомами вуглецю, гетероаралкіл з 5-6 членами і 1-5 алкільними атомами вуглецю, гетероциклоалкіл з 5-6 членами і 1-5 алкільними атомами вуглецю, аміноалкіл з 2-5 атомами вуглецю, N-монозаміщений або N,N-двозаміщений аміноалкіл з 2-5 атомами вуглецю, де вказані замісники - радикали алкілу з 1-3 атомами вуглецю, радикали аралкілу з 1-3 атомами вуглецю, карбоксіалкіл з 1-5 атомами вуглецю, алкоксикарбонілалкіл з 1-5 атомами вуглецю, ціаноалкіл з 1-5 атомами вуглецю або гідроксіалкіл з 2-5 атомами вуглецю;
R21 означає водневий радикал або алкільний радикал з 1-3 атомами вуглецю; або радикал формули -NR20R21 означає гетероцикло радикал з 5-6 членами;
R22 означає алкільний радикал з 1-3 атомами вуглецю або радикали R20R21N-алкілу з 1-3 алкільними атомами вуглецю;
R10 означає водень, алкіл з 1-3 атомами вуглецю, бензил, фенілметоксикарбоніл, третбутоксикарбоніл або радикали (4-метоксифенілметокси)карбонілу;
R11 означає водень, гідроксіалкіл або радикали алкоксіалкілу, де алкіл містить 1-3 атома вуглецю;
R12 і R13 кожний незалежно означає водень, гідрокси, алкокси, 2-гідроксіетокси, гідроксіалкіл або радикали алкоксіалкілу, де алкіл містить 1-3 атоми вуглецю;
R11 і R12 або R12 і R13 поряд з атомами вуглецю, до яких вони приєднані, означають бензо-радикал, що довільно заміщений щонайменше одним гідрокси- або алкокси-радикалом з 1-3 атомами вуглецю.
2. Сполука за п. 1, або її фармацевтично прийнятна сіль, похідне лікарського препарату з неї або ефір, де
R1 означає алкіл з 1-4 атомами вуглецю, алкеніл з 2-3 атомами вуглецю, алкініл з 3-4 атомами вуглецю, ціанометил, імідазолілметил, радикали -СН2СОNН2, -CH2CH2CONH2, -СН2S(O)2NH2, -СН2SСН3, -СН2S(О)CH3, -CH2S(О)2СН3, -С(СН3)2SСН3, -С(СН3)2S(О)СН3 або -С(СН3)2S(O)2СН3; і
R2 означає алкільні радикали з 3-5 атомами вуглецю, арилметил, алкілтіоалкіл з 1-3 алкільними атомами вуглецю, арилтіометил або циклоалкілметил радикали з 5-6 членами;
R3 означає алкіл з 1-5 атомами вуглецю, циклоалкілметил з 3-6 членами, циклогексил або циклогептил радикали;
R4 означає радикали: феніл, 2-нафтил, 4-метоксифеніл, 4-гідроксифеніл, 3,4-диметоксифеніл, 3-амінофеніл, 4-амінофеніл, 2-амінобензотіазол-5-іл, 2-амінобензотіазол-6-іл, бензотіазол-5-іл, бензотіазол-6-іл, бензоксазол-5-іл, 2,3-дигідробензофуран-5-іл, бензофуран-5-іл, 1,3-бензодіоксол-5-іл або 1,4-бензодіоксан-6-іл або радикал формули
 ,
,
де А і В кожний означає О;
R6 означає дейтерій, метил, етил, пропіл, ізопропіл або фтор радикали; і R7 означає водень, дейтерій, метил або фтор радикали; або радикал формули
 ,
,
де Z означає О, S або NH; і R9 означає радикал формули
 ,
,

або
 ,
,
де Y означає О, S або NH; Х означає зв'язок, О або NR21;
R20 означає водень, алкіл з 1-5 атомами вуглецю, фенілалкіл з 1-3 атомами вуглецю, гетероциклоалкіл з 5-6 членами і 1-3 алкільними атомами вуглецю або N-монозаміщений або N,N-двозаміщений аміноалкіл з 2-3 атомами вуглецю, де вказані замісники - радикали алкілу з 1-3 атомами вуглецю; і
R21 означає радикали метилу або водню; або радикал формули -NR20R21 означає радикали піролідиніл, піперидиніл, піперазиніл, 4-метилпіперазиніл, 4-бензилпіперазиніл, морфолініл або тіаморфолініл; і
R22 означає алкільний радикал з 1-3 атомами вуглецю.
3. Сполука за п. 2, або її фармацевтично прийнятна сіль, похідне лікарського препарату з неї або ефір, де
n означає 0;
R1 означає радикали: ізопропіл, втор-бутил, трет-бутил, 3-пропініл, імідазолілметил, -CH2CONH2, -CH2SCH3, -CH2S(О)СН3, -СН2S(О)2СН3, -С(СН3)2SСН3, -С(СН3)2S(О)СН3 або -С(СН3)2S(O)2СН3;
R2 означає радикали: ізобутил, н-бутил, СН3SСН2СН2-, фенілтіометил, (2-нафтилтіо)метил, бензил, 4-метоксифенілметил, 4-гідроксифенілметил, 4-фторфенілметил або циклогексилметил;
R3 означає радикали: пропіл, ізоаміл, ізобутил, бутил, циклогексил, циклогептил, циклопентилметил або циклогексилметил;
R4 означає радикали: феніл, 2-нафтил, 4-метоксифеніл, 4-гідроксифеніл, бензотіазол-5-іл, бензотіазол-6-іл, бензоксазол-5-іл, 2,3-дигідробензофуран-5-іл, бензофуран-5-іл, 1,3-бензодіоксол-5-іл, 2-метил-1,3-бензодіоксол-5-іл, 2,2-диметил-1,3-бензодіоксол-5-іл, 2,2-дидейтеро-1,3-бензодіоксол-5-іл, 2,2-дифтор-1,3-бензодіоксол-5-іл або 1,4-бензодіоксан-6-іл,
або радикал формули
 ,
,
де Z означає О, S або NH; і R9 означає радикал формули
 ,
,

або
 ,
,
де Y означає О, S або NH; Х означає зв'язок, О або NR21;
R20 означає радикали: водень, метил, етил, пропіл, ізопропіл, ізобутил, бензил, 2-(1-піролідиніл)етил, 2-(1-піперидиніл)етил, 2-(1-піперазиніл)етил, 2-(4-метилпіперазин-1-іл)етил, 2-(1-морфолініл)етил, 2-(1-тіаморфолініл)етил або 2-(N,N-диметиламіно)етил;
R21 означає водневий радикал; і
R22 означає метильний радикал,
R10 означає радикали: водень, метил або бензил;
R11 означає водневий радикал; і
R12 і R13 кожний незалежно означає водень, гідрокси- або метокси-радикали; або R11 і R12 поряд з атомами вуглецю, до яких вони приєднані, означають бензо-радикал, що довільно заміщений щонайменше одним гідрокси- або метокси-радикалом.
4. Сполука за п. 3 або її фармацевтично прийнятна сіль, похідне лікарського препарату з неї або ефір, де
R1 означає радикали: втор-бутил, трет-бутил, ізопропіл, 3-пропініл або -С(СН3)2S(О)2СН3;
R2 означає радикали: бензил, 4-фторфенілметил або циклогексилметил;
R4 означає радикали: феніл, 4-метоксифеніл, 4-гідроксифеніл, бензотіазол-5-іл, бензотіазол-6-іл, 2,3-дигідробензофуран-5-іл, бензофуран-5-іл, 1,3-бензодіоксол-5-іл, 2-метил-1,3-бензодіоксол-5-іл, 2,2-диметил-1,3-бензодіоксол-5-іл, 2,2-дидейтеро-1,3-бензодіоксол-5-іл, 2,2-дифторо-1,3-бензодіоксол-5-іл, 1,4-бензодіоксан-6-іл, 2-(метоксикарбоніламіно)бензотіазол-6-іл або 2-(метоксикарбоніламіно)бензімідазол-5-іл;
R10 означає водневий або метильний радикали;
R12 означає гідрокси або водневий радикали; і
R13 означає водневий радикал.
5. Сполука за п. 1, де фармацевтично прийнятна сіль є сіллю соляної кислоти, сіллю сірчаної кислоти, сіллю фосфорної кислоти, сіллю щавлевої кислоти, сіллю малеїнової кислоти, сіллю янтарної кислоти, сіллю лимонної кислоти або сіллю метансульфонової кислоти.
6. Сполука за п. 5, де фармацевтично прийнятна сіль є сіллю соляної кислоти, сіллю щавлевої кислоти, сіллю лимонної кислоти або сіллю метансульфонової кислоти.
7. Сполука за п. 1, що є
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(1,3-бензодiоксол-5-іл)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3,3-диметилбутанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(1,3-бензодiоксол-5-іл)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3-метилбутанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(1,3-бензодiоксол-5-іл)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3S-метилпентанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(1,3-бензодiоксол-5-іл)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-4-пентинамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[фенілсульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3,3-диметилбутанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[фенілсульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3-метилбутанамідом;
2S-[[(піролідин-2-іл)карбоніл)аміно]-N-[2R-гідрокси-3-[[фенілсульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3S-метилпентанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[фенілсульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-4-пентинамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(4-метоксифеніл)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3,3-диметилбутанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(4-метоксифеніл)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3-метилбутанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(4-метоксифеніл)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3S-метилпентанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(4-метоксифеніл)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-4-пентинамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(2,3-дигідробензофуран-5-іл)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3,3-диметилбутанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(2,3-дигідробензофуран-5-іл)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3-метилбутанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(2,3-дигідробензофуран-5-іл)сульфоніл](2-метилпропіл)аміно]-1S-фенілметил)пропіл]-3S-метилпентанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(2,3-дигідробензофуран-5-іл)сульфоніл](2-метилпропіл)аміно]-1S-фенілметил)пропіл]-4-пентинамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(бензотiазол-6-іл)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3,3-диметилбутанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(бензотiазол-6-іл)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3-метилбутанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(бензотiазол-6-іл)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3S-метилпентанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(бензотiазол-6-іл)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-4-пентинамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(2-нафтил)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3,3-диметилбутанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-(2R-гідрокси-3-[[(2-нафтил)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3-метилбутанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(2-нафтил)сульфоніл](2-метилпропіл)aміно]-1S-(фенілметил)пропіл]-3S-метилпентанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(2-нафтил)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-4-пентинамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(1,4-бензодiоксан-6-іл)сульфоніл)(2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3,3-диметилбутанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(1,4-бензодіоксан-6-іл)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3-метилбутанамідом;
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(1,4-бензодіоксан-6-іл)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-3S-метилпентанамідом; або
2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(1,4-бензодіоксан-6-іл)сульфоніл](2-метилпропіл)аміно]-1S-(фенілметил)пропіл]-4-пентинамідом.
8. Композиція, що включає сполуку за п. 1 і фармацевтично прийнятний носій.
9. Спосіб інгібування ретровірусної протеази, що включає введення ефективної кількості сполуки за п. 1.
10. Спосіб лікування ретровірусної інфекції, що включає введення ефективної кількості композиції за п. 8.
11. Спосіб відвертання реплікації ретровірусу, що включає введення ефективної кількості сполуки за п. 1.
12. Спосіб відвертання реплікації ретровірусу in vitro, що включає введення ефективної кількості сполуки за п. 1.
13. Спосіб лікування СНІДУ, що включає введення ефективної кількості композиції за п. 8.
Текст
Дана заявка №08/402,419 від 10 березня, 1995 є заявкою, яка частково продовжує заявку того ж заявника, яка, в свою чергу, знаходиться на розгляді та повністю включена до опису винаходу як посилання. Даний винахід стосується ретровірусних інгібіторів протеази і, зокрема, нових сполук, складу і способу інгібування ретровірусних протеаз, таких, як протеаза вірусу імунодефіциту людини (ВІЛ). Цей винахід, зокрема стосується гідроксіетиламіно- сульфонамідних сполук гетероциклокарбонільних амінокислот, що застосовуються як інгибітори протеази, складу та способу інгібування ретровірусних протеаз, профілактичного запобігання ретровірусної інфекції або розповсюдження ретровірусів, а також лікування ретровірусної інфекції, наприклад, ВІЛ інфекції. Предметом винаходу є також засоби отримання таких сполук, а також проміжних сполук, які застосовуються для цих способів. На протязі циклу реплікації ретровірусов продукти транскрипції генів gag і gag - роl транслюються як білки. Ці білки згодом підпадають під обробку вірусно закодованою протеазою (або протеїназою) для отримання вірусних ферментів та структурних білків вірусного ядра. Звичайно попередники gag-білка перетворються до капсидних білків, а попередники роl-білків переробляються до вірусних ферментів, наприклад, у зворотну транскриптазу та ретровірусну протеазу. Виявилось, що правильна обробка попередників білків ретровірусною протеазою необхідна для збирання інфекційних віріонів. Наприклад, доведено, що мутація зі зрушеннями рамки в галузі протеази pol-гену ВІЛ запобігають обробку попередника gag-білку. Встановлено, що сайт-направлений мутагенез залишку аспартанової кислоти в активному сайті протеази ВІЛ запобігає обробку попередника gag-білка. Таким чином, були зроблені спроби інгібувати вірусну реплікацію інгібуванням дії ретровірусних протеаз. Інгібування ретровірусної протеази звичайно включає міметичний перехідний стан, через який ретровірусна протеаза підпадає під вплив міметичної сполуки, яка пов'язується (звичайно реверсивним способом) з ферментом при конкуренції з gag і gag - роl білками, щоб таким чином інгібувати процесинг структурних білків та безпосередньо вивільнення ретровірусної протеази. Цим пособом можна ефективно інгібувати реплікацію ретровірусних протеаз. Було запропоновано декілька класів сполук, зокрема для інгібування протеаз, наприклад для інгібування ВІЛ-протеази. Такі сполуки включають ізостери гідроксіетиламіну та редуковані ізостери аміду. Див, наприклад, патенти ЕР 0 346 847; ЕР 0 342.541; Roberts et al, "Rational Design of Peptide-Based Proteinase Inhibitors," Science 248, 358 (1990); та Erickson et al, Design Activity, and 2.8Å Crystal Structure of a C2 Symmetric Inhibitor Complexed to HIV-1 Protease, "Science, 249, 527 (1990). Патент США 5, 157, 041, міжнародні заявки WO 94/04491, WO 94/04492, WO 94/04493, WO 94/05639, WO 92/08701 та заявка США номер 08/294.468, від 23 серпня, 1994, (кожна з яких повністю включена до опису винаходу як посилання), наприклад, описують ізостери гідроксіетиламіну, гідроксіетилсечевини або гідроксіетил-сульфонаміду, що розміщують інгібітори ретровірусної протеази. Декілька класів сполук, як відомо, використовують як інгибітори протеолітичного ферменту реніну. Див, наприклад, патенти US 4, 599, 198; GB 2, 184, 730; GB 2, 209, 752; ЕР 0 264 795; GB 2, 200, 115 та заявку США SIR H725. У заявках GB 2, 200, 115, GB 2, 209,752, ЕР 0 264 795, заявці США SIR H725 і патенті US 4, 599,198 описані сечевиномісткі інгібітори гідроксіетиламіну реніну. У заявці ЕР 468 641 розкриті інгібітори реніну та проміжні сполуки для отримання інгибіторів, які включають сульфонамідмісткі сполуки гідроксіетиламіну, наприклад 3-(трет-бутоксикарбоніл)-аміно-циклогексил-1-(фенілсульфоніл)-аміно-2 (5)-бутанол. Патент GB 2, 200, 115 також описує сульфамоїлмісткі інгібітори гідроксіетиламіну реніну, а патент ЕР 0264 795 описує певні сульфонамідмісткі інгібітори гідроксіетиламіну реніну. Відомо, що хоча і ренін, і ВІЛ-протеази, також класифікуються як протеази аспартилу, сполуки, які є ефективними інгібіторами реніну, як правило, не прогнозують для ефективного інгібування ВІЛ-протеази. Даний винахід стосується вибіркових сполук для інгібування ретровірусної протеази, їх аналогів та фармацевтично прийнятних солей, ефірів і похідних лікарських препаратів з них (prodrugs). Сполуки, що обговорюються характеризуються як інгібуючі гідроксіетиламін-сульфонамідні сполуки гетероциклокарбоніламінокислот. Сполуки, які заявляються використовують для інгібування ретровірусних протеаз, наприклад протеази віруса імунодефіциту людини (ВІЛ). Тому даний винахід також охоплює фармацевтичні склади, способи інгібування ретровірусних протеаз та способи лікування або профілактики ретровірусної інфекції, наприклад ВІЛ-інфекції. Винахід, що заявляється, також стосується засобів отримання таких сполук, а також проміжних сполук, які застосовуються для таких способів. У відповідності з даним винаходом пропонуються сполуки, які інгібують ретровірусну протеазу за формулою: (І) або його фармацевтично прийнятна сіль, похідна лікарського препарату з нього (prodrug) або ефір, де n означає собою 0 або 1; R1 - алкіл, алкеніл, алкініл, гідроксіалкіл, алкоксіалкіл, ціаноалкіл, імідазолілметил, радикали - -CH2CONH2, -CH2CH2CONH2, -CH2S(O)2NH2, -CH2SCH3, -CH2S(O)CH3, -CH2S(O)2CH3, -С(СН3)2SCH3, -C(CH3)2S(O)CH3 або C(CH3)2S(O)2CH3; перевага надається коли, R1 представляє алкіл з 1-5 атомами вуглецю, алкеніл з 2-5 атомами вуглецю, алкініл з 2-5 атомами вуглецю, гідроксіалкіл з 1-3 атомами вуглецю, алкоксіалкіл з 1-3 атомами алкілу і 1-3 атомами алкокси-вуглецю, ціаноалкіл з 1-3 атомами вуглецю, імідазолілметил, радикали CH2CONH2, -CH2CH2CONH2, -CH2S(O)2NH2, -CH2SCH3, -CH2S(O)CH3, -CH2S(O)2CH3, -С(СН3)2SCH3, C(CH3)2S(O)CH3 або -C(CH3)2S(O)2CH3; найбільш прийняти, R1 - алкіл з 1-4 атомами вуглецю, алкеніл з 2-3 атомами вуглецю, алкініл з 3-4 атомами вуглецю, ціанометил, імідазолілметил, радикали -CH2CONH2, CH2CH2CONH2, -CH2S(O)2NH2, -CH2SCH3, CH2S(O)CH3, -CH2S(O)2CH3, -C(CH3)2SCH3, -C(CH3)2S(O)CH3 або С(СН3)2S(O)2CH3; і ще найбільш прийнятно, R1 - втор бутил, трет-бутил, ізо-пропіл, 3-пропініл або радикали C(CH3)2S(O)2CH3; R2 - алкіл, аралкіл, алкілтіоалкіл, арилтіоалкіл або радикали циклоалкілалкілу; прийнятніше R2 - радикали алкілу з 1-5 атомами вуглецю, аралкіл з 1-3 атомами вуглецю, алкілтіоалкіл з 1-3 атомами вуглецю, арилтіоалкіл з 1-3 атомами вуглецю або циклоалкілалкіл з 1-3 атомами вуглецю і 3-6 атомами вуглецевого кільця; найбільш прийнятно, R2 - радикали алкілу з 3-5 атомами вуглецю, арилметил, алкілтиоалкіл з 1-3 атомами вуглецю, арилтіометил або циклоалкілметил з кільцем 5-6 радикалів з атомів вуглецю; і навіть ще найбільш прийнятне, коли R2 - ізобутил, н-бутил, СН3SCH2СН2-, бензил, фенілтіометил, (2-нафтилтіо) метил, 4-метокси-фенілметил, 4-гідроксифенілметил, радикали 4-фторфенілметилу або циклогексилметилу; найбільша перевага надається, коли R2 - бензил, радикали 4-фторфенілметила або циклогексилметила; найбільш більш прийняти, R2 - бензил; R3 - радикали алкілу, циклоалкілу або циклоалкілалкілу; перевага надоється, коли R3 - радикал алкілу з 1-5 атомами вуглецю, циклоалкіл з 5-8 членами кільця або радикал циклоалкілметилу з 3-6 членами кільця; найбільш прийнятно, коли R3 - пропіл, ізоаміл, ізобутіл, бутил, циклопентилметил, циклогексилметил, циклогексил або радикали циклогептилу; ще найбільш прийнятно R3 радикали ізобутилу або циклопентилметилу; R4- арил, гетероарил або радикали гетероциклу; більш прийнятно, коли R4 - арил, бензо-гетероарил з 5-6 членами або радикали бензогетероциклу з 5-6 членами кільця; або R4 - радикал за формулою де А і В незалежно один від одного означають О, S, SO або SO2; більш прийнятно, коли А і В означають О; R6 означають дейтерій, алкіл або радикали галогену; більш прийнятно, коли R6- дейтерій, алкіл з 1-5 атомами вуглецю, радикали фтору або хлору; найбільш прийнятно, коли R6 - дейтерій, метил, етил, пропіл, ізопропіл або радикали фтору; R7 - водень, дейтерій, алкіл або радикали галогену, більш прийнятно, коли R7 - водень, дейтерій, алкіл з 13 атомами вуглецю, радикали фтору або хлору; найбільш прийнятно, коли R7- водень, дейтерій, метил або радикали фтору, або R6 і R7, кожний незалежно означає радикали фтору або хлору, і ще найбільш прийнятно, коли R6 і R7- радикал фтору; або R4 - радикал за формулою де Ζ - О, S або ΝΗ, і R9 - радикал за формулою де Υ - О, S або ΝΗ; X - зв'язок, О або NR21; R20 - водень, алкіл, алкеніл, алкініл, аралкіл, гетероаралкіл, гетероциклоалкіл, аміноалкіл, Ν-монозаміщений або Ν, N-двозаміщений аміноалкіл, де означені замісники - радикали алкілу або аралкілу, карбоксіалкіл, алкоксикарбонілалкіл, ціаноалкіл або радикали гідроксіалкілу; більш прийнятно, коли R20 означає водень, алкіл з 1-5 атомами вуглецю, алкеніл з 2-5 атомами вуглецю, алкініл з 2-5 атомами вуглецю, аралкіл з 1-5 атомами вуглецю, гетероаралкіл з 5-6 членами кільця і 1-5 атомами вуглецю, гетероциклоалкіл з 5-6 членами кільця і 1-5 атомами вуглецю, аміноалкіл з 2-5 атомами вуглецю, N-моно-заміщений або Ν, Nдвозаміщенний аміноалкіл з 2-5 атомами вуглецю, де означені замісники - радикали алкілу з 1-3 атомами вуглецю, радикали аралкілу з 1-3 атомами вуглецю, карбоксіалкіл з 1-5 атомами вуглецю, алкоксикарбонілалкіл з 1-5 атомами вуглецю, ціаноалкіл з 1-5 атомами вуглецю або гідроксіалкіл з 2-5 атомами вуглецю, найбільш прийнятно, коли R20 - водень, алкіл з 1-5 атомами вуглецю, фенілалкіл з 1-3 атомами вуглецю, гетероциклоалкіл з 5-6 членами кільця та 1-3 атомами вуглецю, або N-моно-заміщений або N, N-двозаміщенний аміноалкіл з 2-3 атомами вуглецю, де визначені замісники - радикали алкілу з 1-3 атомами вуглецю; і ще найбільш прийнятно, коли R20 - водень, метил, етил, пропіл, ізопропіл, ізобутил, бензил, 2-(1-піролідиніл) етил, 2-(1-піперидиніл) етил, 2-(1-піперазиніл) етил, 2-(4-метилпіперазин-1-іл) етил, 2(1-морфолініл) етил, 2-(1-тіаморфолініл) етил або радикали 2-(N, N-диметиламіно) етилу; R21 - радикали алкілу або водню; більш прийнятно, коли R21 - водневий радикал або радикал алкілу з 1-3 атомами вуглецю; більш прийнятно, R21 - радикали метила або водню; і найбільш більш прийнятий, R21 - водневий радикал; або радикал за формулою -NR20R21 - радикал гетероциклу; більш прийнятно, коли радикал за формулою -NR20R21 означає радикал з 5-6 членами кільця гетероциклу; найбільш прийнятно, коли радикал за формулою -NR20R21 -піролідиніл, піперидиніл, піперазиніл, 4-петилпіперазиніл, 4-бензилпіперазиніл, морфолініл або радикали тіаморфолінілу; і R22 - алкіл або радикали R20R21N-алкілу; перевага надається, коли R22 - алкіл або радикали R20R21N-алкілу, де алкіл - 1-3 атоми вуглецю; і найбільш прийнятно, коли R22 - радикал алкілу з 1-3 атомами вуглецю; і превага надається випадку, коли R4 - феніл, 2-нафтил, 4-метоксифеніл, 4-гідроксифеніл, 3,4диметоксифеніл, 3-амінофеніл, 4-амінофеніл, бензотіазол-5-іл, бензотіазол-6-іл, 2-аміно-бензотіазол-5-іл, 2(метоксикарбоніламіно) бензотіазол-5-іл, 2-аміно-бензотіазол-6-іл, 2-(метоксикарбоніламіно) бензотіазол-6-іл, 5-бензоксазоліл, 6-бензоксазоліл, 6-бензопіраніл, 3,4-дигідробензопіран-6-іл, 7-бензопіраніл, 3,4дигідробензопіран-7-іл, 2,3-дигідробензофуран-5-іл, бензофуран-5-іл, 1,3-бензодіоксол-5-іл, 2-метил-1,3 бензодіоксол-5-іл, 2,2-диметил-1,3-бензодіоксол-5-іл, 2,2-дидейтеро-1,3-бензодіоксол-5-іл, 2,2-дифторо-1,3бензодіоксол-5-іл, 1,4-бензодіоксан-6-іл, 5-бензимідазоліл, 2-(метоксикарбоніламіно) бензимідазол-5-іл, 6хінолініл, 7-хінолініл, 6-ізохінолініл або радикали 7-ізохінолініла; найбільш прийнятно, коли R4 - феніл, 2нафтил, 4-метоксифеніл, 4-гідроксифеніл, бензотіазол-5-іл, бензотіазол-6-іл, бензоксазол-5-іл, 2,3дигідробензофуран-5-іл, бензофуран-5-іл, 1,3-бензодіоксол-5-іл, 2-метил-1,3-бензодіоксол-5-іл, 2,2-диметил1,3-бензодіоксол-5-іл, 2,2-дидейтеро-1,3-бензодіоксол-5-іл, 2,2-дифторо-1,3-бензодіоксол-5-іл, 1,4бензодіоксан-6-іл, 2-(метоксикарбоніламіно) бензотіазол-5-іл, (метоксикарбоніламіно) бензотіазол-6-іл або радикали 2-(метоксикарбоніламіно) бензимідазол-5-ілу; і ще найбільш прийнятно, коли R4 - феніл, 4метоксифеніл, 4-гідроксифеніл, бензотіазол-5-іл, бензотіазол-6-іл, 2,3-дигідробензофуран-5-іл, бензофуран-5іл, і,3-бензодіоксол-5-іл, 2-метил-1,3-бензодіоксол-5-іл, 2,2-диметил-1,3-бензодіоксол-5-іл, 2,2-дидейтеро-1, Збензодіоксол-5-іл, 2,2-дифторо-1,3-бензодіоксол-5-іл, 1,4-бензодіоксан-6-іл, 2-(метоксикарбоніламіно) бензотіазол-6-іл або радикали 2-(метоксикарбоніламіно) бензимідазол-5-ілу; R10 - водень, алкіл з 1-3 атомами вуглецю, бензил, фенілметоксикарбоніл, трет-бутоксикарбоніл або радикали 4метоксифенілметоксикарбонілу; більш прийнятно, коли R10 - водень, метил або радикали бензилу; більш прийняти R10 - водневий радикал; R11 - водень, гідроксіалкіл або радикали алкоксіалкілу, де алкіл - 1-3 атоми вуглецю; більш прийнятно, коли R11 - водневий радикал; R12 і R13 незалежно один від одного - водень, гідрокси, алкокси, 2-гідроксіалкокси, гідроксіалкіл або радикали алкоксіалкілу; перевага надається варіанту, коли R12 і R13- водень, гідрокси, алкокси, 2-гідроксіетокси, гідроксіалкіл або радикали алкоксіалкілу, де алкіл 1-3 атоми вуглецю; найбільш прийнятно, коли R12 і R13 - водень, гідрокси, метокси або етокси-радикали; або R11 та R12 або R12 і R13 поряд з атомами вуглецю, до яких вони приєднані, означають бензо-радикал, який довільно заміщений у крайньому разі одним гідрокси-або алкокси-радикалом з 1-3 атомами вуглецю; превага надається варіанту, коли R11 і R12 поряд з атомами вуглецю, до яких вони приєднані, означають бензорадикал, що довільно заміщений у крайньому разі одним гідрокси - або метокси-радикалом. Абсолютна стереохімія атому вуглецю -СН(О)-групи- переважно (R). Абсолютна стереохімія атому вуглецю -CH(Ri)-rpynH - переважно (S). Абсолютна стереохімія атому вуглецю - CH(R2) - групи - переважно (S). Ряд сполук, які особливо цікаві у межах формули, І - це сполуки за формулою (ІІ) або їх фармацевтично прийнятна сіль, похідна лікарського препарату з них (prodrug) або ефір, де п, R1, R2, R3, R4 і R10 як це вказано вище. Ряд сполук, які особливо цікаві у межах формули II - сполуки за формулою (ІІІ) або її фармацевтично прийнятна сіль, похідна лікарського препарату з них (prodrug) або ефір, де n, R1, R2, R3, R4 і R10 як це вказано вище. Найбільш прийнятний ряд сполук у межах формули III складається зі сполук або фармацевтично прийнятної солі, похідної лікарського препарату з них (prodrug) або ефіру, де n- 0; R1 - вторбутил, трет-бутил, ізопропіл, 3-пропініл або радикали - (СH2)2S(O)2CH3; R2 - радикал бензилу; R3 - пропіл, ізоаміл, ізобутіл, бутил, циклогексил, циклогептил, циклопентилметил або радикали циклогексилметилу; R4 має значення як вказано вище; і R10 - водень, метил або радикали бензилу. Сполуками, які становлять певний інтерес, є: 2S-[[піролідин-2-іл)карбоніл]аміноі-N-[2R-гідрокси-3-[[(1,3-бензодіоксол-5-іл)сульфоніл](2метилпропіл)аміно]-1S-(фенілметил)пропіл]-3,3-диметил-бутанамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(1,3-бензодиоксол-5-іл)сульфоніл](2метилпропіл)аміно]-1S-(фенілметил)пропіл]-3-метил-бутанамід; 2S-[[(піролідин-2-іл)карбоніл]аміноі-N-[2R-гідрокси-3-[[(1,3-бензодіоксол-5-іл)сульфоніл](2метилпропіл)аміно]-1S-(фенілметил)пропіл]-3S-метил-пентанамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(1,3-бензодіоксол-5-іл)сульфоніл](2метилпропіл)аміно]-1S-(фенілметил)пропіл]-4-пентинамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[фенілсульфоніл](2-метилпропіл)аміно]-1S(фенілметил)пропіл]-3,3-диметил-бутанамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[фенілсульфоніл](2-метилпропіл)аміно]-1S(фенілметил) пропіл]-3-метил-бутанамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[фенілсульфоніл](2-метилпропіл)аміно]-1S(фенілметил) пропіл]-3S-метил-пентанамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[фенілсульфоніл](2-метилпропіл)аміно]-1S(фенілметил)пропіл]-4-пентинамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(4-метоксифеніл)сульфоніл](2-метилпропіл)аміно]1S-(фенілметил)пропіл]-3,3-диметил-бутанамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(4-метоксифеніл)сульфоніл](2-метилпропіл)аміно] 1S-(фенілметил)пропіл]-3-метил-бутанамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(4-метоксифеніл)сульфоніл](2-метилпропіл)аміно]1S-(фенілметил)пропіл]-3S-метил-пентанамід; 2S-[[(піролідин-2-іл)карбоніламіно]-N-[2R-гідрокси-3-[[(4-метоксифеніл)сульфоніл](2-метилпропіл)аміно]1S-(фенілметил)пропіл]-4-пентинамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(2,3-дигідробензофуран-5-іл)сульфоніл](2метилпропіл)аміно]-1S-(фенілметил)пропіл]-3,3-диметил-бутанамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(2,3-дигідробензофуран-5-іл)сульфоніл](2метилпроліл)аміно]-1S-(фенілметил)пропіл]-3-метил-бутанамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(2,3-дигідробензофуран-5-іл)сульфоніл](2метилпропіл)аміно]-1S-фенілметил)пропіл]-3S-метил-пентанамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(2,3-дигідробензофуран-5-іл)сульфоніл](2метилпропіл)аміно]-1S-фенілметил)пропіл]-4-пентинамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(бензотиазол-6-іл) сульфоніл](2-метилпропіл)аміно]1S-(фенілметил)пропіл]-3,3-диметил-бутанамід; 2S-[[(піролідин-2-іл)карбоніл] аміно]-N-[2R-гідрокси-3-[[(бензотіазол-6-іл)сульфоніл](2-метилпропіл)аміно1S-(фенілметил)пропіл]-3-метил-бутанамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(бензотіазол-6-іл)сульфоніл](2-метилпропіл)аміно]1S-(фенілметил)пропіл]-3S-метил-пентанамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(бензотіазол-6-іл)сульфоніл](2-метилпропіл)аміно]1S-(фенілметил)пропіл]-4-пентинамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(2-нафтил)сульфоніл](2-метилпропіл)аміно]-1S(фенілметил)пропіл]-3,3-диметил-бутанамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(2-нафтил)сульфоніл](2-метилпропіл)аміно]-1S(фенілметил)пропІл]-3-метил-бутанамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(2-нафтил)сульфоніл](2-метилпропіл)аміно]-1S(фенілметил)пропіл]-3S-метил-пентанамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(2-нафтил)сульфоніл](2-метилпропіл)аміно]-1S(фенілметил)пропіл]-4-пентинамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(1,4-бензодіоксан-6-іл)сульфоніл](2метилпропіл)аміно]-1S-(фенілметил)пропіл]-3,3-диметил-бутанамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(1,4-бензодіоксан-6-іл)сульфоніл](2метилпропіл)аміно]-1S-(фенілметил)пропіл]-3-метил-бутанамід; 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(1,4-бензодиоксан-6-іл)сульфоніл](2метилпропіл)аміно]-1S-(фенілметил)пропіл]-3S-метил-пентанамід; та 2S-[[(піролідин-2-іл)карбоніл]аміно]-N-[2R-гідрокси-3-[[(1,4-бензодіоксан-6-іл)сульфоніл](2метилпропіл)аміно]-1S-(фенілметил)пропіл]-4-пентинамід. Термін "алкіл", який використовується в даному описі один або в сполученні, означає прямий або розгалуджений ланцюг радикалу алкілу, що містить більш прийнятно від 1 до 8 атомів вуглецю, найбільш прийнятно від 1 до 5 атомів вуглецю, а ще найбільш прийнятно 1-3 атоми вуглецю. Прикладами таких радикалів є метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, вторбутил, трет-бутил, пентил, ізо-аміл, гексил, октил, тощо. Термін "алкеніл", один або у сполученні, означає радикал вуглеводню з прямим або розгалудженим ланцюгом, який має один або більше подвійних зв'язків та містить переважно від 2 до 10 атомів вуглецю, найпереважніше від 2 до 8 атомів вуглецю, ще найбільш прийнятно від 2 до 5 атомів вуглецю. Приклади більш прийнятних радикалів алкенілу: етеніл, пропеніл, 2-метилпропеніл, 1,4-бутадіеніл, тощо. Термін "алкиніл", один або у сполученні, означає радикал вуглеводню з прямим або розгалуженим ланцюгом, який має один або більше потрійних зв'язків і також містить більш прийнятно від 2 до 10 атомів вуглецю, найбільш прийнятно від 2 до 5 атомів вуглецю. Приклади радикалів алкинілу: етиніл, пропиніл (пропаргіл), бутиніл, тощо. Термін "алкокси", один або у сполученні, означає радикал алкілу ефіру, де термін алкіл має значення, яке визначено вище. Приклади радикалів алкілу ефіру, яким надається перевага: метокси, етокси, н-пропокси, ізопропокси, н-бутокси, ізо-бутокси, втор-бутокси, трет-бутокси, тощо. Термін "циклоалкіл", один або у сполученні, означає насичений або частково насичений моноциклічний, біциклічний або трициклічний радикал алкілу, де кожна циклічна половина містить переважно від 3 до 8 атомів вуглецю елементів кільця, переважніше від 3 до 7 атомів вуглецю елементів кільця, найпереважніше від 5 до 6 атомів вуглецю елементів кільця, і який може бути довільною бензойною сконденсованою кільцевою системою, що може бути довільно заміщена, як вказано при визначенні терміну "арил". Приклади радикалів циклоалкілу: циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил, октагідронафтил, 2,3-дигідро-1H-іденіл, адамантил, тощо. Терміни "біцикличній" і "трицикличній" означає сконденсовані кільцеві системи, наприклад нафтил і βкарболиніл, та заміщені кільцеві системи, наприклад біфеніл, фенілпіридил, нафтил і дифенілпіперазиніл. Термін "циклоалкілалкіл" означає радикал алкілу, означений вище, який заміщений радикалом циклоалкілу, що означено вище. Приклади радикалів циклоалкілалкілу: циклопропілметил, циклобутилметил, циклопентилметил, циклогексилметил, 1-циклопентилетил, 1-циклогексилетил, 2-циклопентилетил, 2циклогексилетил, циклобутилпропіл, циклопентилпропіл, циклогексилбутил, тощо. Термін "бензо", один або у сполученні, означає двовалентний радикал С6Н4=, отриманий з бензолу. Термін "арил", один або у сполученні, означає радикал фенілу або нафтилу, що довільно заміщений однією або більшою кількістю замісників, вибраних з алкілу, алкокси, галогену, гідрокси, аміно, нітро, ціано, галоалкілу, карбокси, алкоксикарбонілу, циклоалкілу, гетероциклу, алканоїламіну, амідо, амідино, алоксикарбоніламіну, N-алкіламідино, алкіламіно, діалкіламіно, N-алкіламідо, N,N-діалкіламідо, аралкоксикарбоніламіно, алкілтіо, алкілсульфінілу, алкілсульфонілу, тощо. Приклади радикалів арилу-феніл, п-толіл, 4-метоксифеніл, 4-(трет-бутокси) феніл, 3метил-4-метоксифеніл, 4-фторфеніл, 4-хлорфеніл, 3-нітрофеніл, 3-амінофеніл, 3-ацетамідофеніл, 4 ацетамідофеніл, 2-метил-3-ацетамідофеніл, 4-СF3-феніл, 2-метил-3-амінофеніл, 3-метил-4-амінофеніл, 2аміно-3-метилфеніл, 2,4-диметил-3-амінофеніл, 4-гідроксифеніл, 3-метил-4-гідроксифеніл, 1-нафтил, 2нафтил, 3-аміно-1-нафтил, 2-метил-3-аміно-1-нафтил, 6-аміно-2-нафтил, 4,6-диметокси-2-нафтил, піперазинілфеніл, тощо. Терміни "аралкіл" і "аралкокси", окремо або у сполученні, означають алкіл або радикал алкокси як вказано вище, в якому у крайньому разі один водневий атом заміщений радикалом арила як вказано вище, наприклад бензил, бензилокси, 2-фенілетил, дибензилметил, гідроксифенілметил, метилфенілметил, дифенілметил, дифенілметокси, 4-метоксифенілметокси, тощо. Термін "аралкоксикарбоніл", один або у сполученні, означає радикал аралкілу за формулою -О-С(О)-, в якій термін "аралкіл" має визначене вище значення. Приклади радикалу аралкоксикарбонілу-бензилоксикарбоніл та метоксифенілметоксикарбоніл. Термін "арилокси" означає радикал арилу за формулою -О-, в якій термін "арил" має значення, яке визначено вище. Термін "алканоїл", один або у сполученні, означає радикал ацилу, отриманий з алканкарбоксильної кислоти, прикладами якого є ацетил, пропіоніл, бутирил, валерил, 4метилвалерил, тощо. Термін "циклоалкілкарбоніл" означає радикал ацилу циклоалкілу за формулою -С(О)-, в якій термін "циклоалкіл" має вище означене значення, таке як циклопропілкарбоніл, циклогексилкарбоніл, адамантилкарбоніл, 1,2, 3,4-тетрагідро-2-нафтоїл, 2-ацетамідо-1,2,3,4-тетрагідро-2-нафтоїл, 1-гідрокси1,2,3,4-тетрагідро-6-нафтоїл, тощо. Термін "аралканоїл" означає радикал ацилу, отриманий з арил-заміщеної алканкарбоксильной кислоти, такий як фенілацетил, 3-фенілпропіоніл (гідроциннамоїл), 4-фенілбутирил, (2нафтил) ацетил, 4-хлоргідроциннамоїл, 4-аміногідроциннамоїл, 4-метоксигідроциннамоїл, тощо. Термін "ароїл" означає радикал ацилу, отриманий з арилкарбоксильної кислоти, термін "арил" має вище вказані значення. Приклади радикалів ароїлу: заміщений і незаміщений бензоїл або нафтоїл, наприклад бензоїл,4хлорбензоїл, 4-карбоксибензоїл, 4-(бензилоксикарбоніл)бензоїл, 1-нафтоїл, 2-нафтоїл, 6-карбокси-2 нафтоїл, 6-(бензилоксикарбоніл)-2-нафтоїл, 3-бензилокси-2-нафтоїл, 3-гідрокси-2-нафтоїл, 3-(бензилоксиформамідо)-2нафтоїл, тощо. Термін "гетероцикло", один або у сполученні, означає насичений або частково ненасичений моноциклічний, бициклічний або трициклічний гетероциклічний радикал, що містить у крайньому разі один, переважно 1-4, переважніше 1-2 гетероатома азоту, кисню або сірки, що містить більш прийнятно 3-8 членів у кожному кільці, найбільш прийнятно 3-7 членів і ще найбільш прийнятніше 5-6 членів у кожному кільці. Термін "гетероцикло" також може включати такі члени, як сульфони, сульфоксиди, N-оксиди третинного азоту і карбоксил та бензо сконденсовані системи. У таких радикалах гетероцикло може бути довільно заміщений у крайньому разі на одному, переважно на 1-4, переважніше на 1-2 атомах вуглецю галогеном, алілом, алкокси, гідрокси, оксо, арилом, аралкілом, гетероарилом, гетероаралкілом, амідино, N-алкіламідино, алоксикарбоніламіно, алкІлсульфоніламіно, тощо, і/або на вторинному атомі азоту (тобто є,-NH-) гідрокси, алкілом, аралкоксикарбонілом, алканоїлом, гетероаралкілом, фенілом або фенілалкілом, і/або на третичном атомі азоту (тобто є, =N-) може бути заміщений оксидо. "Гетероциклоалкіл" значить радикал алкілу як вказано вище, в якому у крайньому разі один водневий атом заміщений радикалом гетероциклу як вказано вище, таким як піролідинілметил, тетрагідротіеншметил, піридилметил, тощо. Термін "гетероарил", один або у сполученні, означає ароматичний радикал гетероциклу як вказано вище, що довільно заміщений як вказано вище при визначенні арилу та гетероциклу. Приклади такого гетероцикло та груп гетероарилів включають піролідиніл, піперидиніл, піперазиніл, морфолініл, тіаморфолиніл, піроліл, імідазоліл (наприклад, імідазол 4-іл, 1-бензилоксикарбонілІмідазол-4-іл, і т. д.), піразоліл, піридил, (наприклад, 2-(1-піперидиніл) піридил та 2-(4-бензилпіперазин-1-іл-І-піридиніл, і т.д.), піразиніл, піримідиніл, фурил, тетрагідрофурил, тіеніл, тетрагідротіеніл і його сульфоксиди і сульфон-похідні, тіазоліл, оксазоліл, тіазоліл, індоліл (наприклад, 2-індоліл, тощо.), хінолиніл, (наприклад, 2-хінолиніл, 3хінолиніл, 1-оксидо-2-хінолініл, тощо), ізохінолініл (наприклад, 1-ізохінолініл, 3-ізохінолініл, тощо), тетрагідрохінолініл (наприклад, 1,2,3,4-тетрагідро-2-хіноліл, і т.д.), 1.2, 3.4-тетрагідроізохінолініл (наприклад, 1,2,3,4-тетрагідро-1-оксо-ізохінолініл, тощо), хіноксалініл, β-карболініл, 2-бензофуранкарбоніл, 1-, 2-, 4- або 5бензімідазоліл, метилендіоксифен-4-іл, метилендіоксифен-5-іл, етилендіоксифеніл, бензотиазолил, бензопираніл, бензофурил, 2,3-дигідробензофурил, бензоксазолил, тиофеніл, тощо. Термін "циклоалкілалкоксикарбоніл" означає групу ацилів, отриману з циклоалкілалкоксикарбонової кислоти циклоалкілалкілу за формулою -О-СООН, де циклоалкілалкіл має визначене вище значення. Термін "арилоксіалканоїл" означає радикал ацилу арила за формулою -О- алканоїл, де арил і алканоїл має вище визначене значення. Термін "гетероциклоалкоксикарбоніл" означає групу ацилів, отриману з гетероциклоалкілу -О-СООН, де гетероциклоалкіл має згадане вище значення. Термін "гетероциклоалканоїл" означає радикал ацилу, отриманий з гетероциклоалкілкарбоксильної кислоти, де гетероцикло має вище означене значення. Термін "гетероциклоалкоксикарбоніл" означає радикал ацилу, отриманий з гетероциклоалкілу -О-СООН, де гетероцикло має вище вказане значення. Термін "гетероарилоксикарбоніл" означає радикал ацилу, отриманий з карбоксильної кислоти, наведеної гетероарилом -О-СООН, де гетероарил має вище означене значення. Термін "амінокарбоніл", один або у сполученні, означає амінозаміщену карбонільну (карбамоїльну) групу, де аміно-група може бути первинною, вторинною, або третиною аміно-групою, що містить замісники, вибрані з алкілу, арилу, аралкілу, циклоалкілу, радикалів циклоалкілалкілу, тощо. Термін "аміноалканоїл" позначає ацильну групу, отриману з аміно-заміщеної алкілкарбонової кислоти, де аміно-група може бути первинною, вторинною, або третинной аміно-групою, що містить замісники, вибрані з алкілу, арилу, аралкілу, циклоалкілу, радикалів циклоалкілалкілу, тощо. Термін "галоген" означає фтор, хлор, бром або йод. Термін "галоалкіл" означає радикал алкілу, що має вище означене значення, де один або більше атомів воденя заміщений галогеном. Приклади радикалів галоалкілу: хлорометил, 1-брометил, фторометил, дифторометил, трифторометил, 1,1,1-трифтороетил, тощо. Термін "остаточна група" (L або W) у цілому стосується груп, які легко заміщуються нуклеофілом, наприклад аміном, тіолом або нуклеофілом спирту. Такі остаточні групи добре відомі у даній галузі техніки. Приклади таких остаточних груп включають, але не обмежені, N-гідроксисукцинімид, N-гідроксибензотріазол, галогеніди, трифлати, тозилати, тощо. Більш прийнятні остаточні групи позначені там, де це необхідно. Методики отримання сполук за формулою І описані нижче. Слід відпозначити, що загальна методика викладається стосовно підготовки сполук, що має визначену стереохімію, наприклад, де абсолютна стереохімія стосовно гідроксильної групи позначена як (R). Однак, такі методики, як правило, застосовують для сполук протилежної конфігурації, наприклад, де стереохімія відносно гідроксильної групи позначена як (S). Крім того, можна використати сполуки, які має (R)-стереохімію, для отримання сполук з (S)-стереохімію. Наприклад, сполуки, що мають (R)-стереохімію, може бути інвертировано до (S8)-стереохімії, застосовуючи добре відомі способи. Отримання сполук за формулою І Сполуки згідно до даного винаходу, подані формулою І, одержують, використовуючи наступні загальні методики, що схематично подані на схемах І і II. N-захищені хлоркетонге похідне амінокислоти за формулою: де Ρ - захисна аміногрупа, і R2 як вказано вище, відновлюють до відповідного спирту, використовуючи відновлення придатного агента. Прийнятні захисні аміно-групи добре відомі у даній галузі техніки і включають карбобензокси, трет-бутоксикарбоніл, тощо. Більш прийнятної захисної аміногрупою є карбобензокси. Більш прийнятним N-захищеним хлоркетоном є N-бензилоксикарбоніл-L-фенілаланін хлорометил кетон. Більш прийнятний відновлюючий агент - боргидрид натрію. Відновлювану реакцію проводять при температурі від 1°С до 25°С, переважно приблизно 0°С, у системі розчинника, що підходить, такій як, наприклад, тетрагідрофуран, тощо. N-захищені хлоркетони, створювані серійно, наприклад, Bachem, Inc, Torrance, California. Як альтернатива хлоркетони можна отримати відповідно до методики, яка сформульована в S.J.Fittkau, J, Prakt. Chem, 315,1037 (1973), а N-захист забезпечують, використовуючи методики, що добре відомі в даній галузі техніки. Галоспирт можна використати безпосередньо, як описано нижче, або, що більше прийнятно, реагуючи при кімнатній температурі з відповідною основою у прийнятній системі розчинника для отримання N-захищеного аміно-епоксиду за формулою: де Ρ і R2 мають вище означені значення. Відповідні системи розчинника для підготовки аміноепоксиду включають етанол, метанол, ізопропанол, тетрагідрофуран, діоксан, тощо. Включаючи їх суміші. Відповідна снова для отримання епоксиду з відновленого хлоркетону включає гідроксид калію, гідрохлорид натрію, третбутилат калію, DBU, тощо. Більш прийнятною основою є гідроксид калію. Як альтернативу можна отримати захищений аміно-епоксид, такий як у заявках РСТ №PCT/US93/04804 (WO 93/23388) і PCT/US94/12201, що належать тому ж заявнику і знаходяться на розгляді, та у заявці США, номер справи патентного повіреного №С-2860, кожна з яких повністю включена у вигляді посилання, в яких описані засоби отримання хірального епоксиду, хірального ціангідрину, хірального аміну та інших хіральних проміжних хімічних сполук, що використовуються при підготовці інгибіторів ретровірусної протеази зі вхідних DL- , D- або L-амінокислот, що реагують з прийнятною захисною аміногрупою у відповідному розчинникові для отримання аміно-захищеної ефіром амінокислоти. Для ілюстрації використовують захищену L-амінокислоту за наступною формулою для отримання інгибіторів згідно до даного винаходу: де Р3 - карбоксильна захисна група, наприклад, метил, етил, бензил, трет-бутил, 4-метоксифенілметил, тощо; R2 як вказано вище, та Р1 і Р2 і/або Ρ незалежно вибрані з захисної аміногрупи, включаючи без обмеження, аралкіл, заміщений аралкіл, циклоалкенілалкіл та заміщений циклоалкенілалкіл, аліл, заміщений аліл, ацил, алкоксикарбоніл, аралкоксикарбоніл та силіл. Приклади аралкілу включають без обмеження бензил, ортометилбензил, тритил і бензгидрил, що може бути довільно заміщений галогеном, алкіл C1-C8, алкокси, гідрокси, нітро, алкілен, аміно, алкіламіно, ациламіно і ацил, або їх солі, такі як солі фосфонію і амонію. Приклади груп арилів: феніл, нафталеніл, інданіл, антраценіл, дуреніл, 9- (9-фенілфтореніл) і фенантреніл, циклоалкенілалкіл або заміщені радикали циклоалкіленілалкілу, що розміщують циклоалкіли С6-С10. Групи ацилів: карбобензокси, трет-бутоксикарбоніл, ізо-бутоксикарбоніл, бензоїл, заміщений бензоїл, бутирил, ацетил, три-фторацетил, три-хлорацетил, фталоїл, тощо. Перевага надоється, коли Р1 і Р2 незалежно вибирають із аралкілу та із заміщеного аралкілу. Найкраще, коли Р1 і Р2 - бензил. На додаток, Р1 і/або Р2 і/або Р' захисні групи можуть формувати гетороциклічне кільце з азотом, до якого вони приєднані, наприклад, 1,2-біс(метилен) бензол, фталімідил, сукцинімідил, імідил малеїнової кислоти, тощо та де ці гетороциклічні групи можуть далі включати суміжний арил і кільця циклоалкілу. Крім того, гетероциклічні групи можуть бути моно-, ди- або три-заміщеними, наприклад, нітрофталімідил. Термін "силіл" відноситься до атому кремнію, довільно заміщеного однією або більше групами алкілу, арилу і аралкілу. Відповідний силіл, який захищає групи, включає, без обмеження, триметилсиліл, триетилсиліл, триізопропілсиліл, трет-бутилдиметилсиліл, диметилфенілсиліл, 1,2-біс (диметилсиліл) бензол, 1,2-біс (диметилсиліл) етан та дифенілметилсиліл. Силілювання функцій аміну для отримання моно- або бісдисиліламіну сприяє отриманню похідного аміноспирту, амінокислоти, амінокислотного ефіру і амінокислотного аміду. У випадку амінокислот, амінокислотних ефірів і амінокислотних амідів, шляхом відновлення функції вуглецю одержують необхідний аміноспирт моно - або біс-силілу. Силілювання аміноспирту дасть похідну Ν, Ν, О-три-силілу. Вилучення функції силілу з функції ефіру силілу виконують при обробці, наприклад, реактивом металевого гідроксиду або фториду амонію, на будь-якій дискретній стадії реакції або in situ на протязі підготовки реактиву аміноальдегіду. Придатні силілуючи агенти, наприклад, хлорид триметилсилілу, хлорид трет-бутил-диметилсилілу, хлорид фенілдиметилсилілу, хлорид дифенілметилсилілу або комбінація їх продуктів з імідазолом або диметилформамідом (ДМФ). Способи силілювання амінів та видалення силілзахисних груп добре відомі фахівцям у даній галузі техніки. Спосіб отримання означених похідних амінів з відповідних амінокислот, амінокислотних амідів або амінокислотних ефирів також добре відомий фахівцям у галузі органічної хімії, що включає хімію амінокислот/амінокислотного ефіру або аміноспирту. Далі аміно-захисний L-амінокислотний ефір відновлюють до відповідного спирту. Наприклад, амінозахисний L-амінокислотний ефір може бути відновлений гідридом діізобутилалюмінію при -78°С у придатному розчинникові, наприклад толуолі. Кращим відновлювуючими агентами є алюмогідрид літію, боргідрид літію, боргідрид натрію, боран, -три-трет-бутоксиалюмогідрид литію, комплекс боран/тетрагідрофуран. Перевага надається випадку, коли відновлюваний агент - гідрид діізобутилалюхвлію (DiBAL-H) у толуолі. Далі отриманий спирт перетворюють, наприклад, шляхом скисання за Сверном, у відповідний альдегід за формулою: де Р1, Р2 і R2 як вказано вище. Таким чином, розчин дихлорметану в спирті додають до охолодженого (-75 до 68°С) розчину оксалілхлориду в дихлорметані та ДМСО у дихлорметані і змішують впродовж 35 хвилин. Придатні окислювальні реактиви, наприклад, комплекс триокису сірки та піридину і ДМСО, оксалілхлорид і ДМСО, ацетилхлорид або ангідрид і ДМСО, трифторацетилхлорид або ангідрид і ДМСО, метансульфонілхлорид і ДМСО або тетрагідротіофен-S-оксид, бромід толуолсульфонілу і ДМСО, трифторметансульфоніл ангідрид (трифторний ангідрид) і ДМСО, пентахлорид фосфору і ДМСО, диметилфосфорилхлорид і ДМСО і хлорформіат ізобутилу і ДМСО. Умови зкисання вказані Reetz et al [Angew Chem, 99, p.1186, (1987)], Angew Chem. Int. Ed. Engl, 26, p.1141, 1987) з використанням оксалілхлориду і ДМСО при -78°С. Кращий спосіб скисання, описаний у цьому винаході, здійснюють за допомогою комплексу триокису сірки і піридину, тріетиламіну і ДМСО при кімнатній температурі. Ця система забезпечує гарний вихід бажаного хірально захищеного аміноальдегіду, придатного до вживання без очищення, тобто усувається необхідність очищення кілограмів проміжних сполук за допомогою хроматографії, а крупномасштабні технологічні дії стають все менш небезпечними. Проведення реакції при кімнатній температурі також усуває необхідність застосування низькотемпературного реактора, що робить спосіб більш придатним для серійного виробництва. Реакцію можна здійснювати в інертній атмосфері, наприклад в азоті або аргоні, або при нормальному або сухому повітрі, при атмосферному тиску або у герметичній реакційній судині при позитивному тиску. Перевага надається атмосфері азоту. Альтернативні амінові основи: три-бутиламін, триізопропіламін, Nметилпіперидин, N-метилморфолін, азабициклононан, диізопропілетиламін, 2,2,6,6-тетраметилпіперидин, N,N-диметиламінопіридин або суміші цих основ. Триетиламін є кращою основою. Альтернативою чистому ДМСО як розчиннику є суміш ДМСО з непротонним або галогенізованним розчинником, наприклад таким, як тетрагідрофуран, етилацетат, толуол, ксилан, дихлорметан, етилендихлорид, тощо. Біполярні апротонні спільні розчинники включають ацетонітрил, диметилформамід, диметилацетамід, ацетамід, сечевину тетраметилу та його циклічний аналог, N-метилпіролідон, сульфолан, тощо. Замість N,Nдибензилфенілаланінолу як попередника альдегіду можна використовувати похідні фенілаланінолу, які описані вище, для отримання відповідного N-монозаміщенного [Р1 або Р2=Н ] або N,N-двозаміщенного альдегіду. Крім того, для отримання альдегідів можна здійснювати гідридне відновлення похідних аміду або ефіру відповідного бензильного (або іншої придатної захисної групи) азотозахисного фенілаланіну, заміщеного фенілаланіну або циклоалкільного аналогу похідної фенілаланіну. Гідрування є додатковим способом синтезу альдегіду за умов, коли уникають конденсації альдегіду, для порівняння, скисання за Оппенауером. Альдегіди згідно до цього способу можна також отримати за допомогою відновлення захищеного фенілаланіну і аналогів фенілаланіну або їх амідів або похідних ефіру, наприклад, натрієвою амальгамою з НСІ в етанолі або літієм, або натрієм, або калієм, або кальцієм - в аміаку. Температура реакції може складати приблизно від -20°С до 45°С, та краще від 5°С до 25°С. Два додаткових способи отримання альдегіду, захищеного азотом, включають скисання відповідного спирту хлорним вапном у присутності каталітичної кількості вільного радикалу 2,2,6,6-тетраметил-1-піридилокси. У другому способі зкисання спирту до альдегіду здійснюють за допомогою каталітичної кількості перутенату тетрапропіламонію у присутності Nметилморфолін-N-оксиду. Крім того, хлорид - похідна захищеного фенілаланіну або похідного фенілаланіну, як описано вище, відновлюють воднем та каталізатором, наприклад паладієм на карбонаті барію або сульфаті барію або за наявністю або відсутності додаткового агента, який пом'якшує каталізатор, наприклад сірки або тіолу (відновлення за Розенмундом). Альдегід, отриманий скисанням за Сверном, після цього реагує з реактивом галометиллітію, реактив якого одержують in situ, при реакції поєднання алкіллітію або ариллітію з дигалометаном, який наведений формулою Х1СН2Х2, де X1 і X2 незалежно означає І, Br або СІ. Наприклад, розчин альдегіду та хлоріодометану в тетрагідрофурані охолоджують до -78°С і додають розчин н-бутиллітію в гексані. Отриманий продукт представляє собою суміш діастереомерів відповідних аміно - захищених епоксидів за формулами: Діастереомери можна розподіляти наприклад, хроматографією, або після однократної реакції діастереомерні продукти розподіляють на наступних стадіях. Для отримання сполук, які мають (S)-стереохімію в атомі вуглецю, пов'язаного з R2, можна використовувати D-амінокислоти замість L-амінокислот. Додавання хлорметиллітію або бромметиллітію до хірального аміноальдегіду є високо діастереоселективним. Перевага надається одержанню хлорметиллітію або бромметиллітію in situ з реакції дигалометана і н-бутиллітію. Прийнятні метиленуючі галометани: хлоріодометан, бромхлорметан, дибромметан, дііодометан, бромфторметан, тощо. Ефір-сульфонат продукту додавання, наприклад, броміду водню до формальдегіду, також є метиленуючим агентом. Тетрагідрофуран є розчинником, якому надається перевага, однак альтернативні розчинники, наприклад толуол, диметоксіетан, етилендихлорид, метиленхлорид використовують як чисті розчинники або у вигляді сумішей. Біполярні апротоні розчинники, наприклад ацетонітрил, диметилформамід (ДМФ), N-метилпіролідон застосовують як розчинники або у вигляді частини суміші розчинників. Реакцію можуть проводити в інертній атмосфері, наприклад в азоті або аргоні. Замість н-бутиллітію можуть бути заміщені інші металоорганічні сполуки, наприклад метиллітій, третбутиллітій, фтор-бутиллітій, феніллітій, феніл натрію, тощо. Реакцію можна проводити при температурі від 80°С до 0°С, більш прийнятно від -80°С до -20°С. Найбільш прийнятна температура реакції складає від -40°С до -15°С. Реактиви додають окремо, але при деяких умовах краще, коли є численні додавання. Більш прийнятним тиском для даної реакції є атмосферний тиск, однак позитивний тиск має важливе значення при певних умовах, наприклад, при високій вологості оточуючого середовища. За іншими способами конверсії до епоксидів згідно до даного винаходу виробляють заміщення протилежно заряджених вхідних продуктів метиленування і наступну їх обробку основою для отримання аналогічного аніону. Приклади таких продуктів включають тозилат триметилсульфоксонію або трифлат, галогенід тетраметиламонію, галогенід метилдифенілсульфоксонію, де галогенід-хлорид, бромід або йодид. Конверсія альдегідів згідно до даного винаходу до похідних їх епоксидів здійснюють також багатократними стадіями. Наприклад, додавання аніону тіоанізолу, отриманого, наприклад, з бутилу або реактиву арила літію, до захищеного аміноальдегиду, скисання отриманого захищеного спирту аміносульфіду такими добре відомими окиснюючими агентами, як пероксид водню, трет-бутилгіпохлорит, хлорне вапно або періодат натрію для отримання сульфоксиду. Алкілювання сульфоксиду, наприклад, здійснюють метил йодидом або бромідом, метил тозилатом, метил метилатом, метил трифлатом, етил бромідом, ізопропіл бромідом, бензил хлоридом, тощо, у присутності органічної або неорганічної основи. Крім того, захищений спирт аміносульфіду алкілюють, наприклад вище означеними агентами алкілювання для отримання солі сульфонію, які згодом конвертують з трет-аміном або мінеральними основами до епоксидів, про які йде мова. Необхідні епоксиди одержують діастереоселективно при використанні найбільш прийнятних умов при кількісному співвідношенні (S:R) у крайньому разі приблизно 85:15. Продукт очищують за допомогою хроматографії для отримання діастереомерно і енантіомерно чистого продукту, однак його зручніше використовувати безпосередньо без очищення для отримання ретровірусних інгибіторів протеази. Описаний вище спосіб застосовують до сумішей оптичних ізомерів, а також до розчинних сполук. Якщо необхідний специфічний оптичний ізомер, то здійснюють вибір вихідного матеріалу, наприклад, L-фенілаланін, Dфенілаланін, L-фенілаланінол, D-фенілаланінол, D-гексагідрофенілаланінол, тощо, або розщеплення може відбуватися на проміжній або на заключній стадії. Хіральні допоміжні речовини, наприклад один або два еквіваленти камфорної сульфокислоти, лимонної кислоти, камфорної кислоти, 2-метоксифенілоцтової кислоти, тощо, використовують для отримання солей, ефірів або амідів сполук згідно до даного винаходу. Ці сполуки або їх похідні кристалізують або поділяють хроматографічно при використанні хіральной або ахіральной колонки, які добре відомі фахівцям у даній галузі техніки. Після цього аміноепоксид реагує у придатній системі розчинника з рівною кількістю або краще з надлишком потрібного аміну за формулою R3NH2, де R3 - водень або так само, як вказано вище. Реакцію проводять у широкому діапазоні температур, наприклад, приблизно від 10С° до 100С°, та перевага надається, але не обов'язково, температурі, коли розчинник починає надходити до зворотного холодильника. Придатні системи розчинника включають протоні, непротоні та біполярні апротоні органічні розчинники як, наприклад, такі, в яких розчинником є спирт, наприклад метанол, етанол, ізопропанол, тощо, ефіри, наприклад тетрагідрофуран, діоксан, тощо, та толуол, N,N-диметилформамід, диметилсульфоксид та їх суміші. Більш прийнятний розчинник - ізопропанол. Одержуваним продуктом є похідна 3-(N-захищений аміно)-3-(R2)-1-(NH3 )пропан-2-ола (далі - аміноспирт), що може бути поданий формулами: де Ρ, Ρ1, Ρ2, R2 і R3 такі, які вказані вище. Як альтернативи використовують галоспирт замість аміноепоксиду. Визначений вище аміноспирт після цього реагує в розчинникові, якому надається перевага, з сульфонілхлоридом R4SO2Cl, сульфонілбромідом R4SO2Br або відповідним сульфонілангидридом, переважно у присутності акцептору кислоти. Відповідні розчинники, в яких проводять реакцію, включають метиленхлорид, тетрагідрофуран, тощо. Відповідні акцептори кислоти включають триетиламін, піридин, тощо. Отримана похідна сульфонаміда в залежності від епоксиду, який використовується, подано формулами: де Р, Р1, Р2, R2, R3 і R4 як це вказано вище. Ці інтермедіати застосовують для підготовки інгібітору сполуки згідно до даного винаходу. Галогениди сульфоніла за формулою R4SO2X одержують шляхом реакції відповідного арила, гетероарила і бензо-сконденсированого гетероцикла за Гриньяром або літієвих реактивів з сульфурилхлоридом, або диоксидом сірки, з наступним зкисанням галогеном, краще хлором. Арил, гетероарил і бензосконденсирований гетероцикл по Грин'яру або літієві реактиви одержують з їх відповідних галогенидів (наприклад хлор або бром) сполук, що виробляються серійно або їх одержують з серійно створюваних вхідних матеріалів згідно відомим засобам в даній галузі техніки. Тиоли також окисляють до сульфонілхлоридів при використанні хлору в присутності води при ретельно контрольованих умовах. Крім того, сульфокислоти, наприклад арилсульфонови кислоти можна конвертувати в сульфоніл-галогениди при використанні реактивів, наприклад, РСl5, SOCl5, СlС(О)С(О)Сl, тощо, і також в ангідриди при використанні підхожих реактивів дегідратирування. Сульфокислоти одержують, в свою чергу, при використанні методики, добре відомої в даній галузі техніки. Деякі сульфокислоти виробляються серійно. Замість сульфоніл-галогенидів використають сульфиніл-галогениди (R4SOX) або сульфеніл-галогениди (R4SX) для отримання сполук, де -SО2 - половина заміщена -SO - або-S-половиною, відповідно. Арилсульфонові кислоти, бензо-сконденсування гетероциклосульфокислоти або гетероарил-сульфокислоти одержують сульфированиям ароматичного кільця з допомогою відомих в даній галузі техніки засобів, наприклад реакцією з сірчаною кислотою, SC3, SО3-комплексами, наприклад, ДМФ (SO3), піридином (SO3), N, N-диметилацетамідом (SO3), тощо. Краще, арилсульфонілгалогеніди одержують з ароматичних сполук шляхом реакції з ДМФ (SO3) і SOCl2 або ClC(О)С(О)СІ. Реакції здійснюють поетапно або в окремому резервуарі. Арилсульфонові кислоти, бензо-сконденсовані гетероцикло-сульфокислоти, гетероарил-сульфокислоти, арилмеркаптани, бензо-сконденсовані гетероцикло меркаптани, гетероарилмеркаптани, арилгалогеніди, бензо-сконденсовани гетероциклогалогеніди, гетероарилгалогеніди, тощо. Вироблюються серійно або їх швидко одержують з серійно створюваних вхідних матеріалів, використовуючи стандартні засоби, добре відомі в даній галузі техніки. Наприклад, ряд сульфокислот (R4SO3H) наведений формулами: де А, В, Z, R6, R7 і R9 як вказано вище, одержують з 1,2-бензолдитіола, 2-меркаптанфенолу, 1,2-бенозолдиола, 2-амінобензотіазола, бензотіазола, 2-амінобензимідазола, бензимідазола, тощо, що виробляються серійно, Carter, патент США 4.595, 407; Ehrenfreund et al, патент США 4.634, 465; Yoder et el, J.Heterocycl. Chem. 4: 166167 (1967); Cole et al, Aust. J. Chem. 33: 675-680 (1980); Cabiddu etal, Synthesis 797-798 (1976); Ncube et al, Tet. Letters 2345-2348 (1978); Neube і ін, Tet. Letters 255-256 (1977); Ansink and Cerfontain, Rec. Trav. Chim. PaysBas 108: 395-403 (1989); and Kajihara and Tsuchiya, EP 638564 Al, кожний з яких включений тут повністю у вигляді заслання. Наприклад, 1.2-бензолдитіол, 2-меркаптанфенол або 1.2-бенозолдіол реагує з R6R7C(L'), де L' як вказане нижче, більш прийняти, Br або І, в присутності основи. Наприклад гідроксиду, або R6R7C=O в присутності кислоти, наприклад як толуолсульфонової кислоти, або Р2О5 для отримання заміщеного бензосконденсированного гетероцикла за формулою: який після цього сульфонілірують до згаданої вище сульфокислоти. Наприклад, CF2Br2 або СО2Br2 реагує з 1.2-бензолдитіолом, 2-меркаптанфенолом або 1.2-бензолдиолом в присутності основи для отримання сполук: відповідно, де А і В позначає О або S, а D-атом дейтерію. Також, коли А і/або В позначає S, то використовуючи нижчеописаний спосіб, сірку окислюють до похідних сульфонів або сульфоксидів. При наступному отриманні похідної сульфонаміда, амінозахисну групу Ρ або амінозахисні групи Р1 і Р2 вилучають за умов, при яких не впливають на частину, що залишалася молекули. Такі засоби добре відомі в даній галузі техніки і включають кислотний гідроліз, гідрогенолиз, тощо. Кращий спосіб включає вилучення захисної групи, наприклад, вилучення карбобензокси-групи гідрогенолізом з використанням палладію на вуглеці в підхожій системі розчинника, наприклад спирті, оцтової кислоті, тощо. Або в їхніх сумішах. Якщо захисною групою є трет-бутоксикарбонільная група, її вилучають при використанні неорганічної або органічної кислоти, наприклад, НСl або трифтороцтової кислоти, в прийнятній системі розчинника, наприклад диоксані або метиленхлориді. Отриманий продукт являє собою похідну солі аміну. Після нейтралізації солі амін приєднують до DL -, D -, або L-амінокислоти, відповідної за формулою PNHCH(R1) СООН, де Ρ і R1 як вказано вище, захист аміну вилучають, як описане вище, приєднують до циклічних амінокислот формул: де n, Ρ, R10, R11 R12 і R13 як вказано вище, і L-остаточна група, наприклад галогенід, ангідрид, активний ефір, тощо. Наприклад, якщо R11, R12 і R13 кожний позначає водневий радикал, то використають активний ефір Nзахищеного або N-заміщеного проліну НОВТ, активний ефір N-захищеного або N-заміщеного Nгідроксисукцинаміда пипеколінової кислоти, тощо. Як альтернативи, захист інтермедіата: вилучають реакцією з R10L, де R10 - алкіл або бензил, або відповідний альдегід або кетон, після цього відновлюють, наприклад цианоборгідридом натрію, тощо. Для отримання де n, R1, R2, R3, R4, R10, R11, R12 і R13 як вказано вище. Циклічні амінокислоти за формулою: виробляються серійно, наприклад пролін, 4-гідроксипролін, N-метилпролін, індолін-2-карбоксильна кислота, тощо.; або їх одержують з серійно створюваних вхідних матеріалів, використовуючи стандартні засоби, добре відомі в даній галузі техніки, наприклад пролін, 4-гідроксипролін, 4-гідроксихінолін-2-карбоксильна кислота, 3гідроксипиколіновая кислота, індолін-2-карбоксильна кислота, 5-метоксиіндол-2-карбоксильна кислотна, каїнова кислота, 4-метокси-2-хінолінкарбоксильна кислота, тощо. Як альтернатива, циклічні амінокислоти одержують шляхом циклізації аміноміст альфа-кетоних карбоксильних кислот або ефірів в циклічний імін, з наступним відновленням, наприклад цианоборгидридом натрію, тощо, в циклічний амін як показано на схемі III, або як альтернативи, шляхом циклізації амінокислот, що має належну остаточну групу L, наприклад хлоро, бромо, тозилат, метилат, тощо, як показано на схемі IV, де п, Р3, R10, R11, R12 і R13 як вказано вище. Альфакетонна карбоксильна кислота або її ефір і амінокислотні вхідні речовини виробляються серійно, або їх одержують з серійно створюваних речовин, використовуючи засоби і методики, добре відомі в даній галузі техніки. Як альтернативи після нейтралізації солі амін приєднують до DL-, D-, або L-амінокислоти, відповідної формулам: де n, Р, R1, R10, R11, R12 i R13 як вказано вище, які одержують аналогічним способом сполуки, описаним вище, з DL-, D-, або L-амінокислоти, відповідній формулі NH2CH(R1)COOP3, де Ρ3 і R1 як вказано вище. DL-, D-, або L-амінокислоти, відповідні формулі PNHCH(R1) СООН або NH2СН(R1) COOP3, де Р, Р3 і R1 як вказано вище, виробляються серійно (Sigma Chemical Co.) або їх одержують, використовуючи стандартні способи, добре відомі в даній галузі техніки з доступних готових вхідних матеріалів. Переважно, Рбензилоксикарбоніл або тре-бутоксикарбонільний радикал і Р 3-бензил - аботрет-бутильний радикали. Для сполуки амінокислот і амінів використають стандартні методики. Після реакції карбоксильної кислотної групи, використовуючи добре відомі методики і умови одержують ангідрид, змішаний ангідрид, кислотний галогенід, наприклад хлорид або бромід, або активний ефір, наприклад ефіри N-гідроксисукцинимида, НОВТ, тощо. Відповідні системи розчинників включають тетрагідрофуран, етиловий ефір, метил-тре-бутиловий ефір, метиленхлорид, Ν,Ν-диметилформамід, тощо, включаючи їхні суміші. Крім того, захищений аміноспирт з відкритого епоксиду захищають далі за допомогою знов введеної аміногрупи з захисною групою Р', що не вилучається при вилученні захисних аміногрупи Ρ або Р1 and Ρ2, та є Ρ' є вибірково вилучаємою групою. Фахівець в даній галузі техніки може вибрати відповідні комбінації Р', Р, Р1 і Р2. Наприклад, відповідними комбінаціями є P=Cbz і Р'=Вос; P'=Cbz і Р =Вос; P'=Cbz, Р2=бензил і Р '=Вос; і Р= Р2=бензил і Р'=Вос. Кінцеві сполуки, наведені формулою: можна обробити залишок синтезу для отримання сполуки за формулою: або де п, Р, Р', R1, R2, R3, R10, R11, R12 і R13 як вказане вище. Згаданий вище залишок синтезу виконують за бажанням або одночасним доданням необхідних залишків або груп або в молекулі, заздалегідь отриманої з більш ніж одного залишку або групи за одну стадію. Колишній підхід являє собою спосіб послідовного синтезу, що представляє собою спосіб конвергентного синтезу. На цій стадії також можливі синтетичні трансформації. Після цього захисну групу Р' вибірково вилучають і реагують отриманий амін з сульфонілхлоридом R4SO2Cl, сульфонілбромідом R4SO2Br або відповідним ангідридом сульфоніла, краще в присутності акцептору кислоти для отримання сполуки згідно нинішньому винаходу: де n, R1, R2, R3, R4, R10, R11, R12 і R13- - як вказано вище. Таке вибіркове вилучення захисних груп і перетворення в сульфонамід можна здійснювати або в кінці синтезу, або бажано на будь-якій відповідній проміжній стадії. Викладені вище хімічні реакції в цілому описані з точки зору найбільш широкого застосування для отримання сполук згідно з даним винаходом. Можливо, що інколи описані реакції не можна використати для кожної сполуки, включеної в обсяг винаходу. Сполуки, яких це стосується, добре відомі фахівцям в даній галузі техніки. В усіх таких випадках реакцію можна успішно здійснити шляхом стандартних модифікацій, відомих фахівцям в даній галузі техніки, наприклад, шляхом відповідного захисту інтерферуючих груп, застосуванням альтернативних стандартних реактивів, шляхом звичайної модифікації умов реакції, тощо, або за допомогою інших реакцій, описаних тут або будь-яких стандартних реакцій, що застосовують при отриманні відповідних сполук згідно з даним винаходом. В усіх засобах отримання всі вхідні матеріали є відомими або їх одержують з відомих вхідних матеріалів. Допускається, що фахівець в даній галузі техніки може повністю використати даний винахід без подальшої розробки. Тому нижченаведені кращі зразки здійснення винаходу слід розглядати тільки як ілюстративні, що ніяким чином не обмежують обсяг винаходу. Всі реактиви використовують в отриманому виді без очистки. Весь спектр ЯМР протона і вуглецю одержують на Varian VXR-300 або ядерномагнітних резонансних спектрометрах VXR-400. Наступні приклади ілюструють отримання інгібуючої сполуки відповідно до нинішнього винаходу і інтермедіатів, при підготовці інгібіруючих сполук, що застосовуються відповідно до нинішнього винаходу. Приклад 1 Отримання 2S-[біс(фенілметил)аміно]бензолпропанолу Спосіб 1: 2S-[біс(фенілметил)аміно]бензолпропанол з відновлення за DIBAL N,N-біс(фенілметил)-Lфенілаланинфенілметилового ефіру Стадія 1: Розчин L-фенілаланину (50.0г, 0.302моль), гідрохлориду натрія (24.2г, 0.605моль) і карбонату калію (83.6г, 0.605моль) в воді (500мл) нагрівають до 97°С. Після цього поволі додають бромід бензилу (108.5мл, 0.605моль) (час додання - 25 хвилин). Суміш змішують при 97°С впродовж 30 хвилин в атмосфері азоту. Розчин охолоджують до кімнатної температури і екстрагують з толуолом (2x250мл). Об'єднані органічні шари промивають водою і соляним розчином, висушують над сульфатом магнію, фільтрують і концентрують до олійної консистенції. Ідентичність продукту підтверджують слідуючим чином. Аналітична тонкошарова хроматографія (10% етилацетата/гексан, силікагель) показує, що головним компонентом для значення Rf=0.32, є бажані трибензилированні сполуки N,N-біс(фенілметил)-L-фенілаланинфенілметиловий ефір. Ці сполуки можна очистити колоночного хроматографією (силікагель, 15% етилацетата/гексан). Як правило, продукт є достатньо чистим для використання безпосередньо в наступній стадії без подальшої очистки. 1H ЯМР спектр відповідає даним літератури. 1H ЯМР (CDCL3)d, 3.00 і 3.14 (АВХ-система, 2Н, JAB=14.1 Гц, JAX=7.3 Гц і JBX=5.9 Гц), 3.54 і 3.92 (АВ-система, 4 Η, JAB=13.9 Гц), 3.71 (t, 1H, J=7.6 Гц), 5.11 і 5.23 (АВ-система, 2Н, JAB=12.3 Hz), і 7.18 (м, 20Н). EIMS: m/z 434 (M-1). Стадія 2: Бензилюючий фенілаланинфенілметиловий ефір (0.302моль) з попередньої реакції розчиняють в толуолі (750мл) і охолоджують до - 55°С. 1.5Μ розчин DIBAL у толуолі (443.9мл, 0.666моль) додають зі швидкістю, необхідної для підтримання температури від - 55 до - 50°С (час додання - 1ч). Суміш змішують впродовж 20 хвилин в атмосфері азоту і після цього охолоджують до - 55°С шляхом повільного додання метанолу (37мл). Після цього холодний розчин наливають в холодний (5°С) 1.5 Η розчин НСl (1.8л). Відстій твердої речовини (приблизно 138г) відфільтровують і промивають толуолом. Твердий матеріал суспендують в суміші толуолу (400мл) і води (100мл). Суміш охолоджують до 5°С і обробляють 2.5Η NaOH (186мл) і після цього змішують при кімнатній температурі до розчинення твердої речовини. Шар толуолу відділяють від водної фази і промивають водою і соляним розчином, висушують над сульфатом магнію, фільтрують і згущують до обсягу 75мл (89г). Етилацетат (25мл) і гексан (25мл) додають до залишку, на якому починає кристалізуватись бажаний спиртовий продукт. Через 30 хвилин додають додаткові 50мл гексану для прискорення подальшого кристалізування. Тверду речовину відфільтровують і промивають 50мл гексану для отримання 34.9г першої партії продукту. Другу партію продукту (5.6г) одержують шляхом перефільтрування маточного розчину. Дві партії об'єднують і вдруге кристалізують з етилацетату (20мл) і гексану (30мл) для отримання 40г b S-2 [біс(феніл-метил) аміно]бензолпропанолу, вихід - 40% з L-фенілаланіна. Додаткові 7г (7%) продукту можна отримати шляхом перекристалізування маточного розчину, що концентрувався. Тонкошарова хроматографія продукту Rf=0.23 (10% етилацетата/гексан, силікагель), - 1H ЯМР (CDCl3)d 2.44 (м, 1Н,), 3.09 (м, 2Н), 3,33 (м, 1H), 3.48 і 3.92 (АВ-система, 4Н, JAB=13. 3 Гц), 3.52 (м, 1Н) і 7.23 (м, 15Н), - [a] D25+42.4 (с 1.45, СН2Сl2), DSC 77.67 С, - Обчислене для C23H25ON: С, 83,34; Н, 7.60; N, 4.23. Знайдене: С, 83.43; Н, 7.59; N, 4.22. Рідинна хроматографія на хиральній постійній фазі: колонка Cyclobond ІSP (250x4.6мм І.D.), рухома фаза: буфер метанол/триетил ацетат амонію рН 4.2 (58: 42, по обсягу), швидкість потоку - 0.5мл/хвл, виявлене вимірювальним приладом при довжині хвилі 230нм і температурі 0°С. Час збереження: 11.25хвл., час збереження бажаного продукту енантіомера: 12.5хвл. Спосіб 2: Отримання b S-2-[біс(фенілметил)аміно]бензол-пропанолу Ν,N-дебензилюванням L-фенілаланінолу L-фенілаланінол (176.6г, 1.168моль) додають до змішаного розчину карбонату калію (484.6г, 3.506моль) в 710мл води. Суміш нагрівають до 65°С в атмосфері азоту. Розчин броміду бензила (400г, 2,339моль) в 3А етанолі (305мл) додають зі швидкістю, що підтримує температуру між 60-68°С. Двофазний розчин змішують при 65°С впродовж 55хвл. і після цього охолоджують до 10°С при енергійному змішуванні. Маслянистий продукт стверджується в маленькі гранули. Продукт розчинюють 2.0л водопровідної води і розмішують впродовж 5 хвилин для розчину неорганічних речовин продуктами. Продукт виділяють фільтруванням при пониженому тиску і промивають водою до отримання рН рівної 7. Отриманий неочищений продукт висушують на повітрі протягом ночі для отримання полусухої твердої речовини (407г), що вдруге кристалізують з 1.1л етилацетата/гептану (1: 10 по обсягу). Продукт виділяють фільтруванням (при 8°С), промивають в 1.6л холодного (-10°С) етилацетата/гептану (1: 10 по обсягу) і - висушують на повітрі для отримання 339г (88% вихід) b S-2-[біс(фенілметил)аміно]бензол-пропанолу, точка плавлення 71.5-73.0°С. При необхідності більшу кількість продукту можна отримати з маточного розчину. Інша аналітична характеристика ідентична сполученню, отриманому згідно способу 1. Приклад 2 Отримання 2S-[біс(фенілметил)аміно]бензолпропанальдегіду Спосіб 1: 2S-[Біс(фенілметил)аміно]бензол-пропанол (200г, 0.604моль) розчиняють в триетиламіні (300мл, 2.15моль). Суміш охолоджують до 1,2°С, і додають розчин сірчаного комплексу трехокиси/піридину (380г, 2,39моль) в диметилсульфоксиді (ДМСО) (1.6л) із швидкістю, достатньої для підтримання температури між 817°С (час додання - 1.0ч). Розчин змішують при температурі довкілля в атмосфері азоту впродовж 1.5 години, за цей час реакцію завершують аналізом тонкошарової хроматографії (33% етилацетата/гексан, силікагель). Реакційну суміш охолоджують крижаною водою і гасять 1.6л холодної води (10-15°С) впродовж 45 хвилин. Результуючий розчин екстрагують етилацетатом (2.0л), миють у 5% лимонної кислоти (2.0л), і соляним розчином (2.2л), висушують над MgSO4 (280г) і фільтрують. Розчинник вилучають на обертальному випарникові при 35-40°С і після цього висушують під вакуумом для отримання 198.8г 2S-[біс(фенілметил)аміно]-бензолпропанальдегіда у вигляді блідо-жовтого мастила (99.9%). Отримана неочищена речовина є достатньо чистою для безпосереднього використання в наступній стадії без очистки. Аналітичні дані сполуки погоджені з виданою літературою, [a] D25=-92.9° (с 1.87, СH2Сl2); 1H ЯМР (400 МГц, CDCl3)d, 2.94 і 3.15 (АВХ-система, 2Н, JAB=13.9 Гц, JAX=7.3 Гц і JBX=6.2 Гц), 3.56 (t, 1H, 7.1 Гц), 3.69 і 3.82 (АВ-система, 4Н, JAB=13.7 Гц), 7.25 (м, 15Н) і 9.72 (s, 1Н); HRMS Обчислене для (М+1) С23Н24NО 330.450, знайдене: 330.1836. Обчислене для C23H23ON: С, 83.86; Н, 7.04; N, 4.25. Знайдене: С, 83.64; Н, 7.42; N, 4.19. Рідинна хроматографія на хиральній постійній фазі: (S, S) колонка Pirkle-Whelk-O 1 (250х4.6мм I.D.), рухома фаза: гексан/ізопропанол (99.5:0.5, в/в), швидкість потоку: 1.5мл/хвл. Виявлене вимірювальним приладом в ультрафіолетовім спектрі при довжині хвилі 210нм. Час збереження бажаного S-ізомеру: 8.75 хвилини, час збереження R-енантиомера 10.62 хвилин. Спосіб 2: Розчин хлориду оксалилу (8.4мл, 0.096моль) в дихлорметані (240мл) охолоджують до -74°С. Після цього поволі додають розчин ДМСО (12.0мл, 0.155моль) в дихлорметані (50мл) зі швидкістю, достатньої для підтримання температури-74°С (час додання »1.25ч). Суміш змішують впродовж 5 хвилин після додання розчину b S-2-[біс(фенілметил)аміно]бензол-пропанолу (0.074моль) в 100мл дихлорметану (час додання - 20 хвилин, температура від - 75°С до - 68°С). Розчин змішують при - 78°С впродовж 35 хвилин в атмосфері азоту. Після цього впродовж 10 хвилин додають триетиламін (41.2мл, 0.295моль) (температура від - 78° до - 68°С), на що осаджується сіль амонію. Охолоджену суміш змішують впродовж 30 хвилин, а після цього додають воду (225мл). Шар дихлорметану відділяють від водної фази і промивають водою, соляним розчином, висушують над сульфатом магнію, фільтрують і концентрують. Залишок розчинюють етилацетатом і гексаном і після цього фільтрують для елімінації солі амонію. Фільтрат концентрують для отримання a S[біс(фенілметил)аміно]бензол-пропанальдегиду. Альдегід використають в наступній стадії без очистки. Спосіб 3: До суміші 1.0г (3.0моль) b S-2-[біс(фенілметил)аміно]бензолпропанолу, 0.531г (4.53моль) Nметилморфоліну, 2.27г молекулярного сита (4А) і 9.1мл ацетонитрилу додають 53мг (0.15моль) перутената тетрапропіламонія (ТРАР). Суміш змішують впродовж 40 хвилин при кімнатній температурі і концентрують при пониженому тиску. Залишок суспендують в 15мл етилацетату, фільтрують через прокладку з силікагелю. Фільтрат концентрують при пониженому тиску для отримання речовини, що містить приблизно 50% a S-2[біс(фенілметил)аміно]бензолпропанальдегида у вигляді блідо-жовтого масла. Спосіб 4: До розчину 1.0г (3.02моль) b S-2-[біс(фенілметил)аміно]бензолпропанолу в 9.0мл толуолу додають 4.69мг (0.03моль) 2.2,6.6-тетраметил-і-пиперидинілокси, вільний радикал (TEMPO), 0.32г (3.11моль) броміду натрію, 9.0мл етилацетату і 1.5мл води. Суміш охолоджують до 0°С, і поволі додають впродовж 25 хвилин водний розчин 2.87мл 5% побутового хлорного вапна, що містить 0.735г (8.75моль) бікарбонату натрію і 8.53мл води. Суміш змішують при 0°С протягом 60 хвилин. Ще дві добавки (по 1.44мл кожна) хлорного вапна вносять при змішуванні впродовж 10 хвилин. Сепарують дві фази суміші. Водний шар екстрагують двічі з 20мл етилацетату. Об'єднаний органічний шар промивають 4.0мл розчину, що містить 25мг йодиду калію і води (4.0мл), 20мл 10%-ного водного розчину тіосульфату натрію і після цього соляним розчином. Органічний розчин висушують над сульфатом магнію, фільтрують і концентрують при пониженому тиску для отримання 1,34г неочищеного масла, що містить невелику кількість бажаного альдегіду, a S-[біс(фенілметил)аміно]бензолпропанальдегиду. Спосіб 5: Додержуючись методик» що описані в способі 1 даного прикладу і використовуючи додатково 3.0 еквівалента комплексу піридину і триокису сірки, одержують порівняний вихід a S[біс(фенілметил)аміно]бензолпропанальдегіду. Приклад 3 Отримання Ν,N-дибензил-3(S)-aміно-1,2-(S)епокси-4-фенілбутану. Спосіб 1: розчин a S-[біс(фенілметил)аміно]бензол-пропанальдегіду (191.7г, 0.58моль) і хлориодометану (56.4мл, 0.77моль) в тетрагідрофурані (1.8л) охолоджують від -30 до -35°С (також використовують більш низьку температуру: - 70°С, а більш високу температуру легше забезпечити при реакціях великого масштабу) в цільном сталевому реакторі в атмосфері азоту. Після цього додають розчин н-бутиллітію в гексані (1.6 М, 365мл, 0.58моль) зі швидкістю, що підтримує температуру нижче -25°С. Після додання суміш змішують при -30 -35°С впродовж 10 хвилин. Більшість добавок реактивів здійснюють таким засобом: додають (1) додатковий хлориодометан (17мл) разом з н-бутиллитием (110мл) при
ДивитисяДодаткова інформація
Назва патенту англійськоюHydroxyethylamino sulfonamides of heterocyclocarbonyl amino acids, a pharmaceutical composition, methods for inhibiting retroviral proteases and preventing retroviral replication, and also methods for treatment of a retroviral infection
Автори англійськоюSikorski James A., Devadas Balekurdu
Назва патенту російськоюГидроксиэтиламиносульфонамиды гетероциклокарбонильных аминокислот, фармацевтическая композиция, способы ингибирования протеаз ретровирусов и предупреждения репликации ретровируса, а также способы лечения ретровирусной инфекции
Автори російськоюСикорски Джеймс А., Девадас Балекудру
МПК / Мітки
МПК: A61P 3/00, C07K 5/078, A61P 31/12, A61K 38/55
Мітки: реплікації, фармацевтична, композиція, способи, протеаз, лікування, запобігання, ретровірусу, також, амінокислот, ретровірусн, ретровірусів, гідроксіетиламіносульфонаміди, гетероциклокарбонільних, інгібування
Код посилання
<a href="https://ua.patents.su/76-63879-gidroksietilaminosulfonamidi-geterociklokarbonilnikh-aminokislot-farmacevtichna-kompoziciya-sposobi-ingibuvannya-proteaz-retrovirusiv-ta-zapobigannya-replikaci-retrovirusu-a-takozh.html" target="_blank" rel="follow" title="База патентів України">Гідроксіетиламіносульфонаміди гетероциклокарбонільних амінокислот, фармацевтична композиція, способи інгібування протеаз ретровірусів та запобігання реплікації ретровірусу, а також способи лікування ретровірусн</a>
Попередній патент: Лікарський засіб на основі мелатоніну для лікування небажаних побічних ефектів, пов’язаних із вживанням бензодіазепінових лікарських засобів
Наступний патент: Міні-тренажер “супутник”
Випадковий патент: Спосіб багатоперехідного листового штампування метастабільних аустенітних сталевих заготовок












