Похідні карбоксаміду як антагоністи мускаринових рецепторів
Номер патенту: 89846
Опубліковано: 10.03.2010
Автори: Ватсон Крістін Анн Луіс, Мантелл Саймон Джон, Стренг Росс Сінклер, Вуд Ентоні, Глоссоп Пол Алан
Формула / Реферат
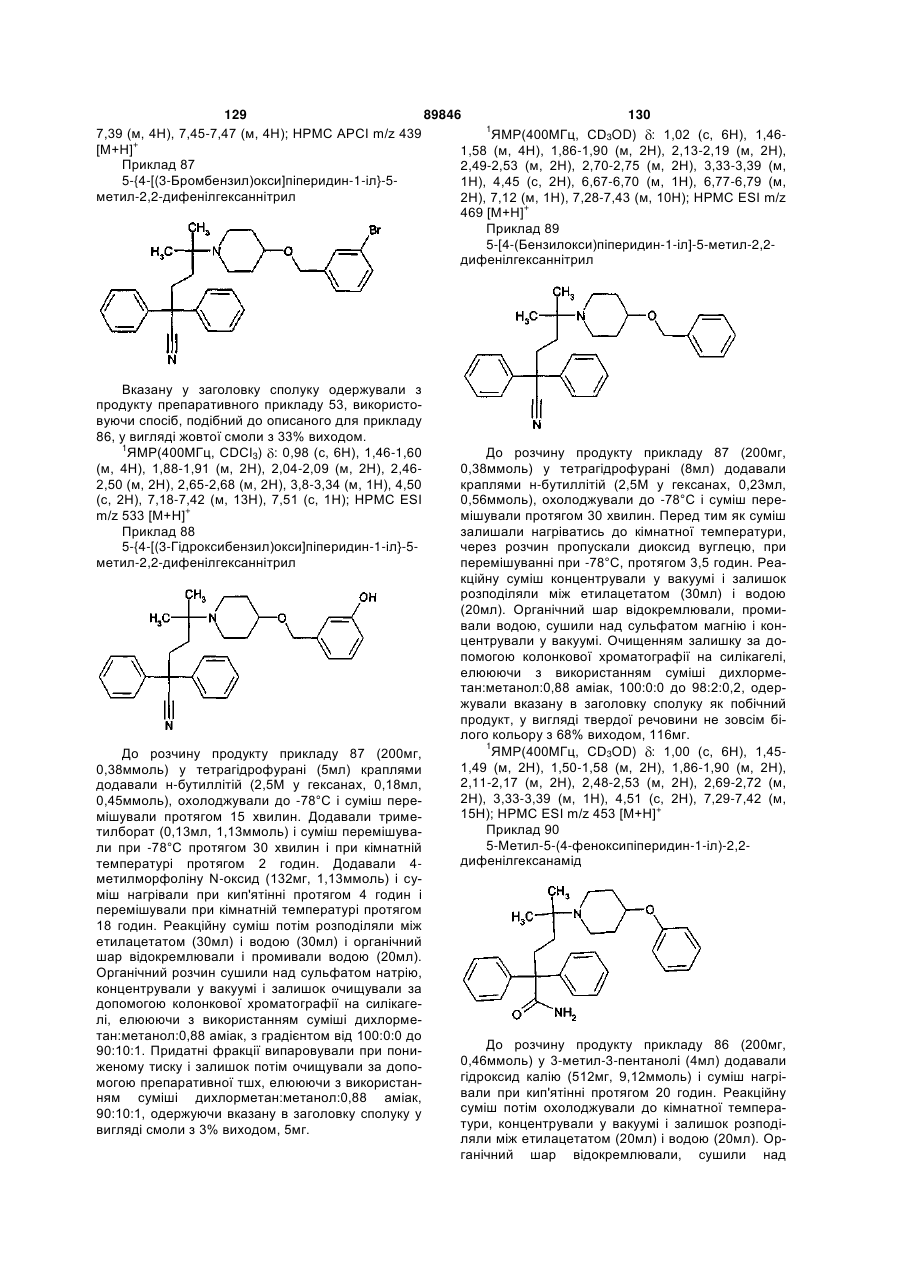
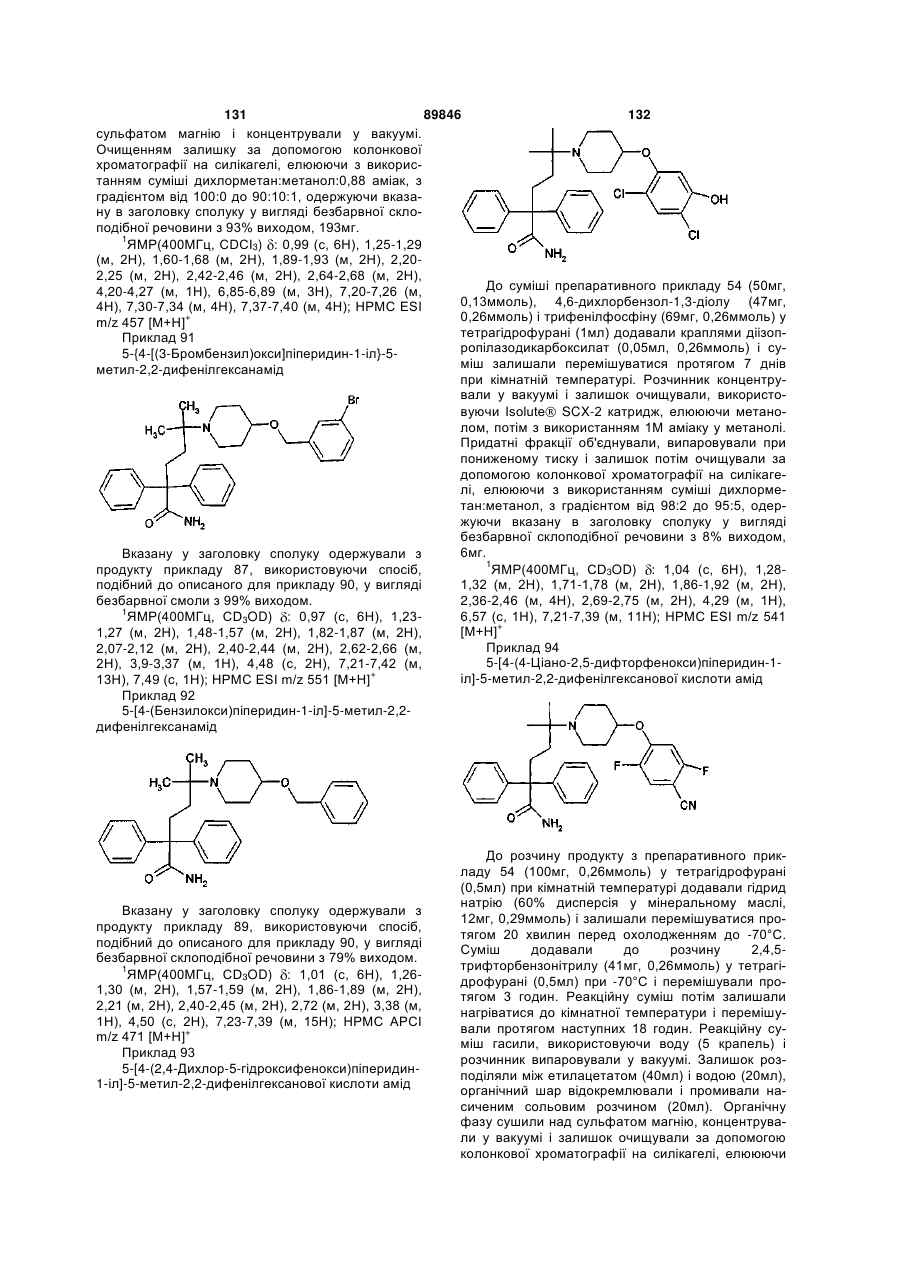
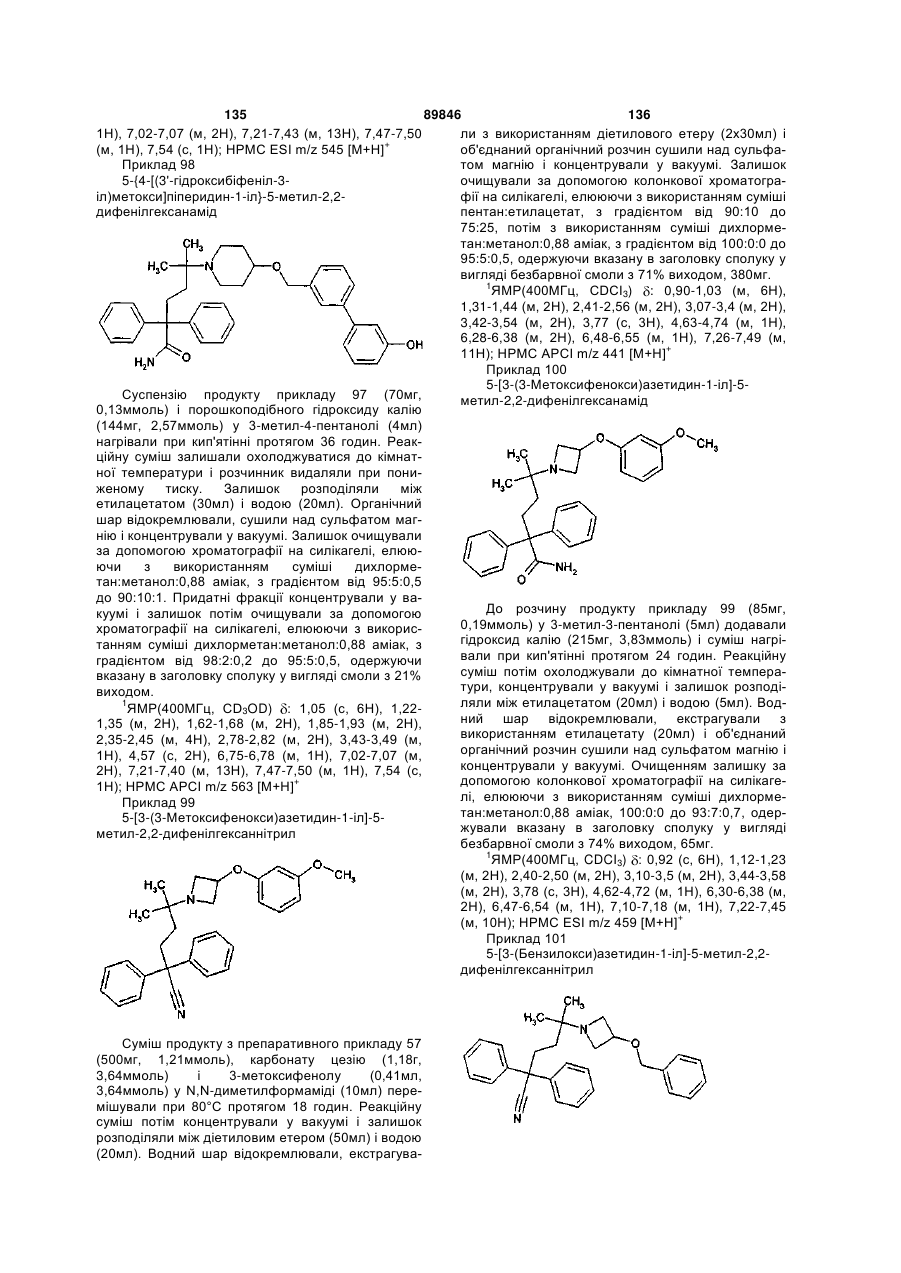
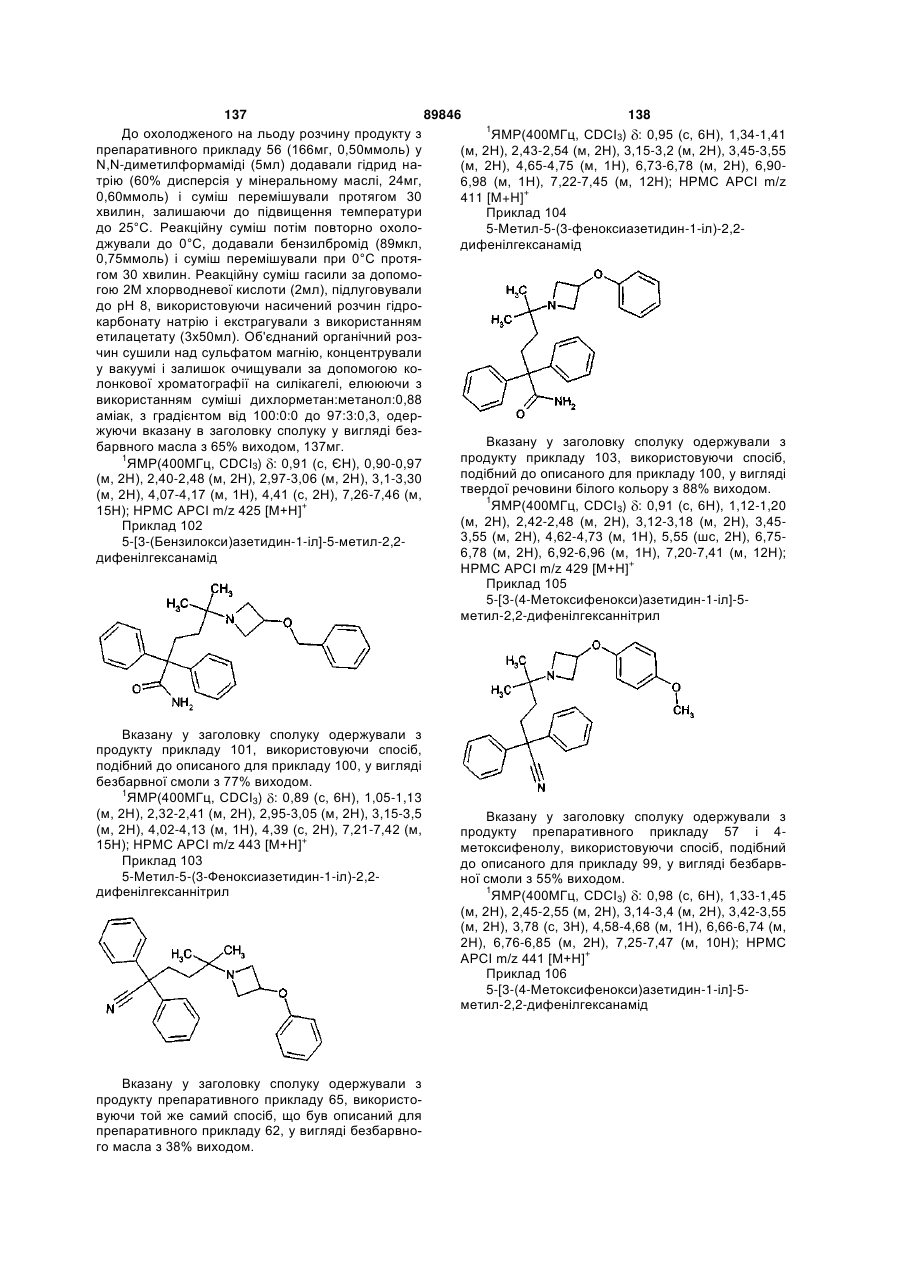
1. Сполука формули (І)
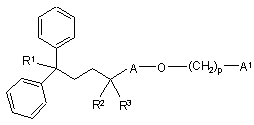 , (I)
, (I)
в якій,
R1 є CN або CONH2;
А вибирають з
![]() ,
, ![]() або
або 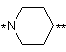 ,
,
де * і ** представляють точки приєднання, ** є місцем приєднання до кисню,
R2 і R3 є метилом, або
А є групою формули
![]() ,
,
R2 і R3 разом з атомом вуглецю, до якого вони приєднані, можуть також утворювати циклопентанове кільце;
р дорівнює 0 або 1;
А1 вибирають з
a) фенілу, необов'язково заміщеного 1, 2 або 3 групами, незалежно вибраними з галогену, CN, CF3, OR4, SR4, OCF3, (С1-С4)алкілу і фенілу, необов'язково заміщеного ОН;
b) нафтилу, необов'язково заміщеного 1 або 2 групами, незалежно вибраними з галогену, CN, CF3, OR4, SR4, OCF3 і (С1-С4)алкілу;
c) 9- або 10-членної біциклічної ароматичної гетероциклічної групи, що включає 1, 2 або 3 гетероатоми, незалежно вибрані з О, S або N, згадана гетероциклічна група є необов'язково заміщеною 1 або 2 замісниками, незалежно вибраними з OR4, (С1-С4)алкілу і галогену;
R4 є Н або (С1-С4)алкілом;
або, при необхідності, фармацевтично прийнятні солі або їх сольвати.
2. Сполука за п. 1, де R1 є CONH2.
3. Сполука за п. 1 або 2, де р дорівнює 0.
4. Сполука за п. 1 або 2, де р дорівнює 1.
5. Сполука згідно з будь-яким з пунктів 1-4, де А1 є фенілом, необов'язково заміщеним 1, 2 або 3 групами, незалежно вибраними з F, Сl, CF3, OH, OCH3, OCF3 i СН3.
6. Сполука за будь-яким з пунктів 1-5, де А1 є фенілом, необов'язково заміщеним 1 або 2 групами, незалежно вибраними з F, Сl, CF3, OH, OCH3, OCF3 i CH3.
7. Сполука за будь-яким з пунктів 1-4, де А1 є нафтилом, необов'язково заміщеним ОН.
8. Сполука за будь-яким з пунктів 1-4, де А1 вибирають з індолілу, ізоіндолілу, хінолілу, ізохінолілу, бензофуранілу, ізобензофуранілу, бензотієнілу, ізобензотієнілу, хіназолілу, хіноксалілу, фталазинілу, бензотіазолілу, бензоксазолілу, бензізотіазолілу, бензізоксазолілу, бензімідазолілу, індазолілу, бензотриазолілу, бензоксадіазолілу, бензізоксадіазолілу, бензотіадіазолілу і бензізотіадіазолілу.
9. Сполука за будь-яким з пунктів 1-4, в якій А1 є бензоксазолілом.
10. Сполука за будь-яким з пунктів 1-9, де R2 і R3 є метилом.
11. Сполука за будь-яким з пунктів 1-10, де А є групою формули
![]() .
.
12. Сполука за будь-яким з пунктів 1-10, де А є групою формули
![]() .
.
13. Сполука за будь-яким з пунктів 1-10, де А є групою формули
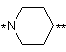 .
.
14. Сполука за п. 1, де згадану сполуку вибирають з наступних:
5-метил-5-[(3S)-3-феноксипіролідин-1-іл]-2,2-дифенілгексанамід;
5-метил-5-[(3R)-3-феноксипіролідин-1-іл]-2,2-дифенілгексанамід;
5-[(3S)-3-(3-гідроксифенокси)піролідин-1-іл]-5-метил-2,2-дифенілгексанамід;
5-[(3R)-3-(3-гідроксифенокси)піролідин-1-іл]-5-метил-2,2-дифенілгексанамід;
5-[(3S)-3-(3-фтор-5-гідроксифенокси)піролідин-1-іл]-5-метил-2,2-дифенілгексанової кислоти амід;
5-[(3S)-3-(2-фтор-3-гідроксифенокси)піролідин-1-іл]-5-метил-2,2-дифенілгексанової кислоти амід;
5-[(3R)-3-(2-фтор-3-гідроксифенокси)піролідин-1-іл]-5-метил-2,2-дифенілгексанамід;
5-[(3R)-3-(2-хлор-3-гідроксифенокси)піролідин-1-іл]-5-метил-2,2-дифенілгексанамід;
5-метил-5-(4-феноксипіперидин-1-іл)-2,2-дифенілгексанамід;
5-[4-(3-гідроксифенокси)піперидин-1-іл]-5-метил-2,2-дифенілгексанамід;
5-метил-5-(3-феноксіазетидин-1-іл)-2,2-дифенілгексанамід;
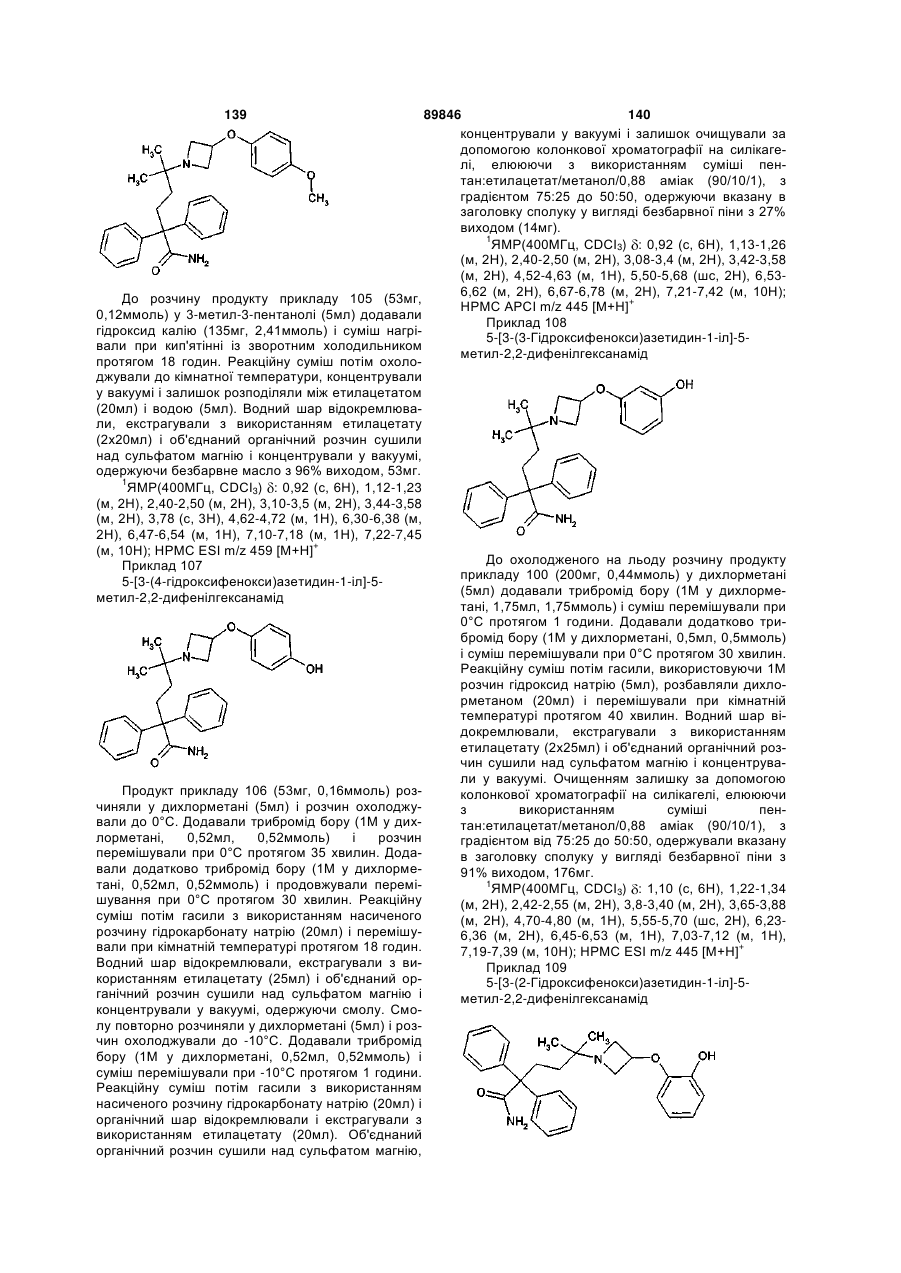
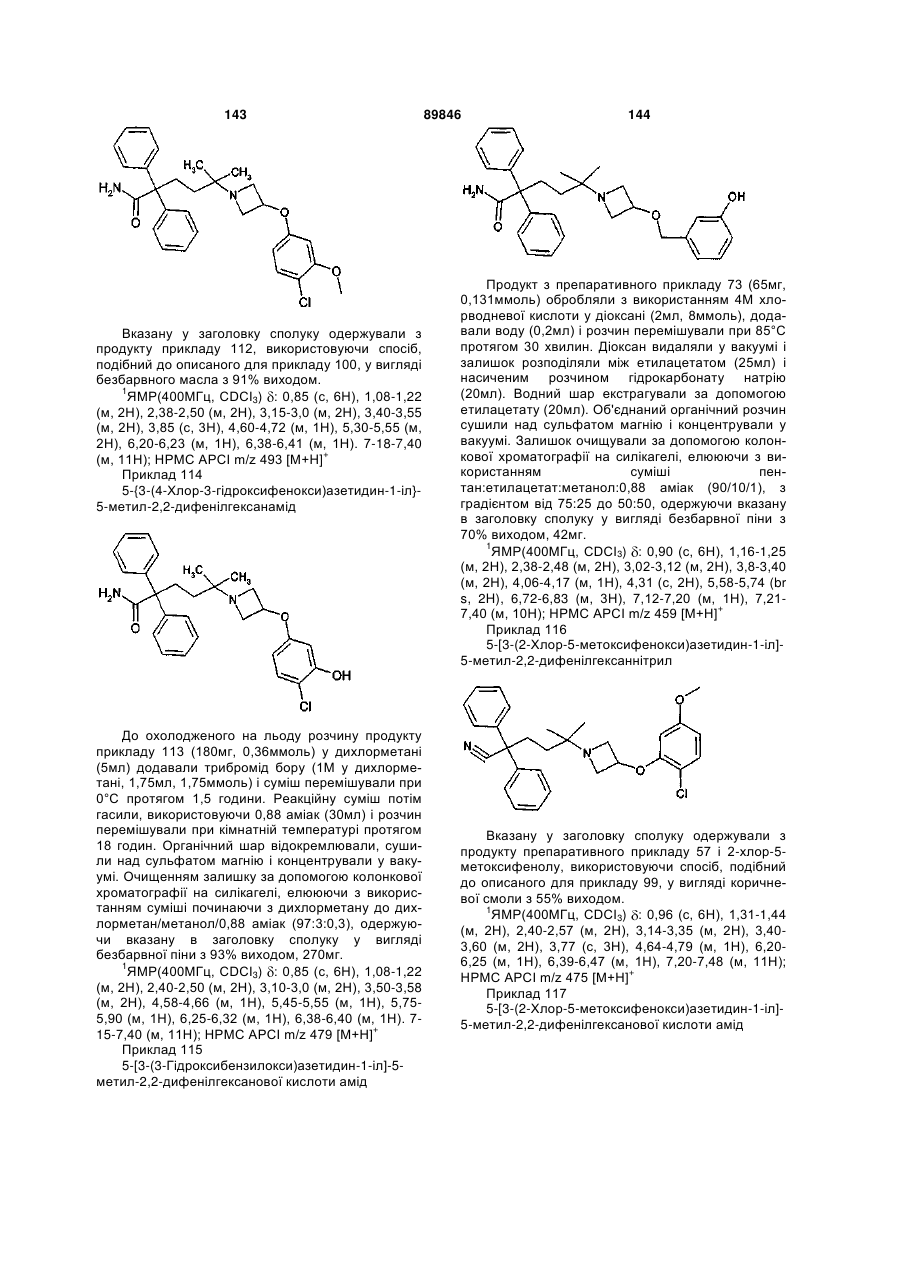
5-[3-(3-гідроксифеноксі)азетидин-1-іл]-5-метил-2,2-дифенілгексанамід;
5-{3-(4-хлор-3-гідроксифеноксі)азетидин-1-іл}-5-метил-2,2-дифенілгексанамід;
5-{3-(3-фтор-5-гідроксифеноксі)азетидин-1-іл}-5-метил-2,2-дифенілгексанамід;
5-{3-(3-хлор-5-гідроксифеноксі)азетидин-1-іл}-5-метил-2,2-дифенілгексанамід;
4-{1-[3-(3-гідроксифеноксі)азетидин-1-іл]циклопентил}-2,2-дифенілбутирамід;
5-[3-(2-фтор-3-гідроксифеноксі)азетидин-1-іл]-5-метил-2,2-дифенілгексанової кислоти амід;
5-[3-(2-фтор-5-гідроксифеноксі)азетидин-1-іл]-5-метил-2,2-дифенілгексанової кислоти амід і
5-[3-(4-хлор-3-гідроксибензилоксі)азетидин-1-іл]-5-метил-2,2-дифенілгексанової кислоти амід
або, при необхідності, їх фармацевтично прийнятні солі або сольвати.
15. Сполука за п. 1, де згаданою сполукою є 5-[3-(3-гідроксифеноксі)азетидин-1-іл]-5-метил-2,2-дифенілгексанамід або його фармацевтично прийнятна сіль або сольват.
16. Фармацевтична композиція, що містить щонайменше ефективну кількість сполуки формули (І), як описано в будь-якому з пунктів 1-15, або її фармацевтично прийнятної солі або сольвату.
17. Сполука формули (І), за будь-яким з пунктів 1-15, або її фармацевтично прийнятні солі або сольвати, для застосування як медикаменту.
18. Застосування сполуки формули (І), як описано в будь-якому з пунктів 1-15, або її фармацевтично прийнятних солей або сольватів, для одержання лікарського засобу, що має антагоністичну активність по відношенню до М3 рецепторів.
19. Застосування сполуки формули (І), як описано в будь-якому з пунктів 1-15, або її фармацевтично прийнятних солей або сольватів, для одержання лікарського засобу для лікування захворювань, розладів і станів, що вибирають з групи, яка включає:
хронічну або гостру бронхоконстрикцію, хронічний бронхіт, обструкцію малих дихальних шляхів та емфізему,
обструктивні або запальні захворювання дихальних шляхів будь-якого типу, етіології або патогенезу, зокрема обструктивне або запальне захворювання дихальних шляхів, що є членом, який вибирають з групи, що включає хронічну еозинофільну пневмонію, хронічне обструктивне легеневе захворювання (COPD), COPD, що включає хронічний бронхіт, легеневу емфізему або диспное, пов'язане або непов'язане з COPD, COPD, що характеризується незворотною прогресуючою обструкцією дихальних шляхів, респіраторний дистрессиндром повнолітніх (ARDS), загострення респіраторної гіперреактивності на фоні іншої фармакотерапії і захворювання дихальних шляхів, що пов'язані з легеневою гіпертензією,
бронхіт будь-якого типу, етіології або патогенезу; зокрема бронхіт, що є членом, який вибирають з групи, яка включає гострий бронхіт, гострий ларинготрахеальний бронхіт, арахідоновий бронхіт, катаральний бронхіт, крупозний бронхіт, сухий бронхіт, інфекційний астматичний бронхіт, продуктивний бронхіт, стафілококовий або стрептококовий бронхіт і везикулярний бронхіт,
астму будь-якого типу, етіології або патогенезу, зокрема астму, що є членом, який вибирають з групи, яка включає атопічну астму, неатопічну астму, алергічну астму, атопічну бронхіальну ІgE-опосередковану астму, бронхіальну астму, есенціальну астму, істинну астму, інфекційно-алергійну астму, викликану патофізіологічними розладами, зовнішню астму, викликану зовнішніми факторами, есенціальну астму невідомого або неочевидного походження, неатопічну астму, бронхітну астму, емфізематозну астму, астму, викликану фізичним навантаженням, астму, індуковану алергеном, астму, індуковану холодним повітрям, професійну астму, інфекційну астму, спричинену бактеріальною, фунгальною, протозойною або вірусною інфекцією, неалергійну астму, початкову астму, синдром ядухи у немовлят і бронхіоліт,
гостре ушкодження легень,
бронхоектазію будь-якого типу, етіології або патогенезу, зокрема бронхоектазію, що є членом, який вибирають з групи, що включає циліндричну бронхоектазію, осумковану бронхоектазію, веретеноподібну бронхоектазію, капілярну бронхоектазію, циститну бронхоектазію, суху бронхоектазію і фолікулярну бронхоектазію.
20. Комбінація сполуки згідно з будь-яким з пунктів 1-15 з іншим терапевтичним агентом(и), що вибирають з наступних:
(a) інгібітори 5-ліпоксигенази (5-LO) або антагоністи 5-ліпоксигенази активуючого протеїну (FLAP),
(b) антагоністи лейкотриєну (LTRAs), включаючи антагоністи LTB4, LTC4, LTD4 і LTE4,
(c) антагоністи рецептора гістаміну, включаючи Н1 і Н3 антагоністи,
(d) агоністи a1- і a2-адренорецептора для протизастійного застосування,
(e) b2 агоністи короткотривалої або довготривалої активності,
(f) інгібітори PDE, наприклад, інгібітори PDE3, PDE4 і PDE5,
(g) теофілін,
(h) хромоглікат натрію,
(і) інгібітори СОХ, як неселективні, так і селективні інгібітори СОХ-1 або СОХ-2 (NSAIDs),
(j) пероральні глюкокортикостероїди і глюкокортикостероїди, що інгалюються,
(k) моноклональні антитіла, активні проти ендогенного запалення,
(l) агенти проти фактора некрозу пухлини (анти-TNF-a),
(m) інгібітори адгезії молекули, включаючи VLA-4 антагоністи,
(n) антагоністи рецептора кініну-В1 і В2,
(о) імуносупресивні агенти,
(р) інгібітори матриксних металопротеаз (MMPs),
(q) антагоністи рецептора тахікініну NK1, NK2 і NK3,
(r) інгібітори еластази,
(s) агоністи рецептора аденозину А2а,
(t) інгібітори урокінази,
(u) сполуки, що діють як допамінові рецептори, наприклад, D2 агоністи,
(v) модулятори NFkB шляху, наприклад, ІКК інгібітори,
(w) модулятори цитокінових сигнальних шляхів, такі як р38 МАР кіназа або syk кіназа,
(х) агенти, що можуть класифікуватись як муколітики або протикашлеві агенти,
(у) антибіотики,
(z) інгібітори HDAC,
(аа) інгібітори РІ3 кінази та
(bb) антагоністи CXCR2.
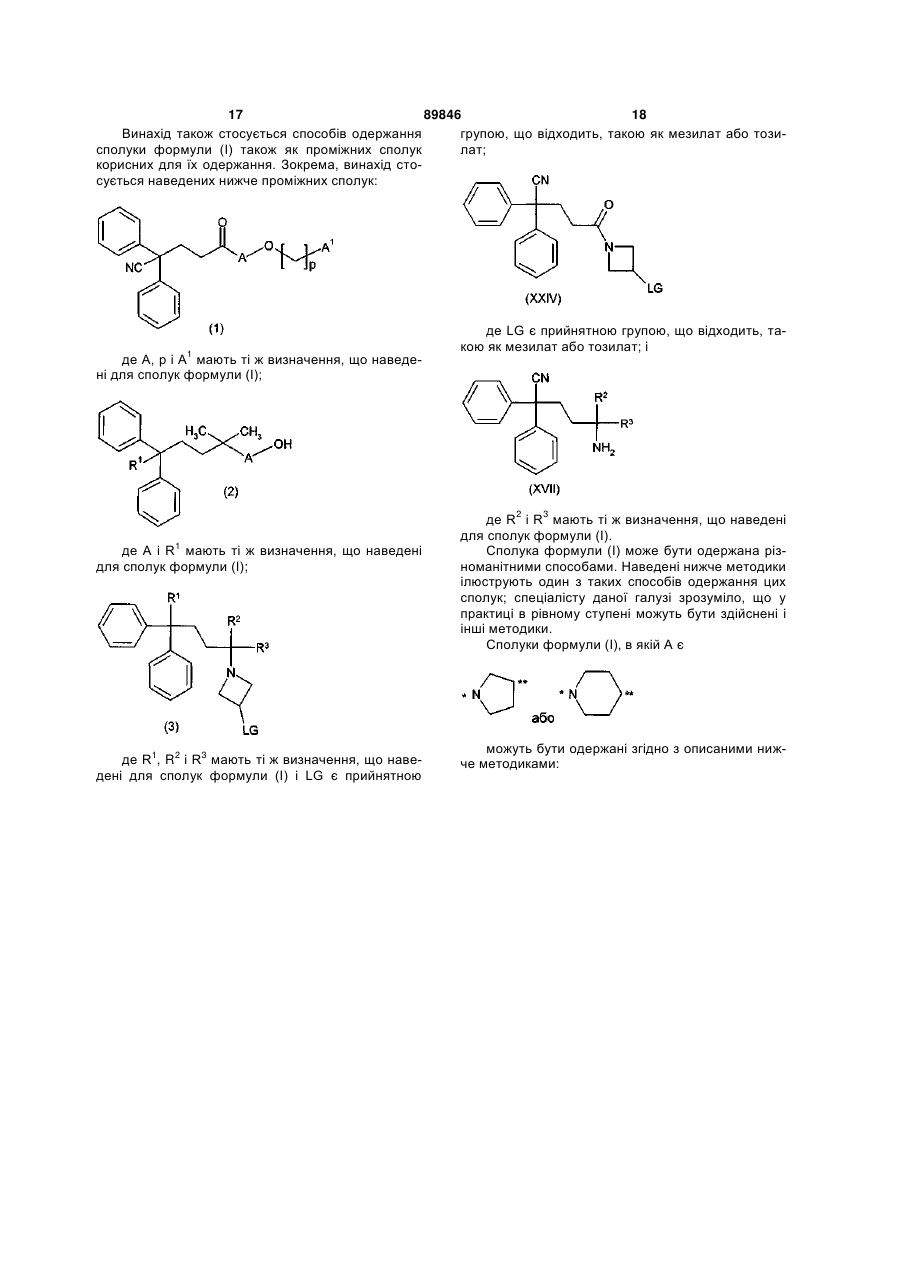
21. Проміжна сполука формули
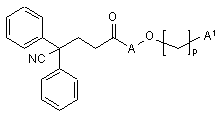 , (1)
, (1)
в якій А, р і А1 мають значення, як визначено в пункті 1.
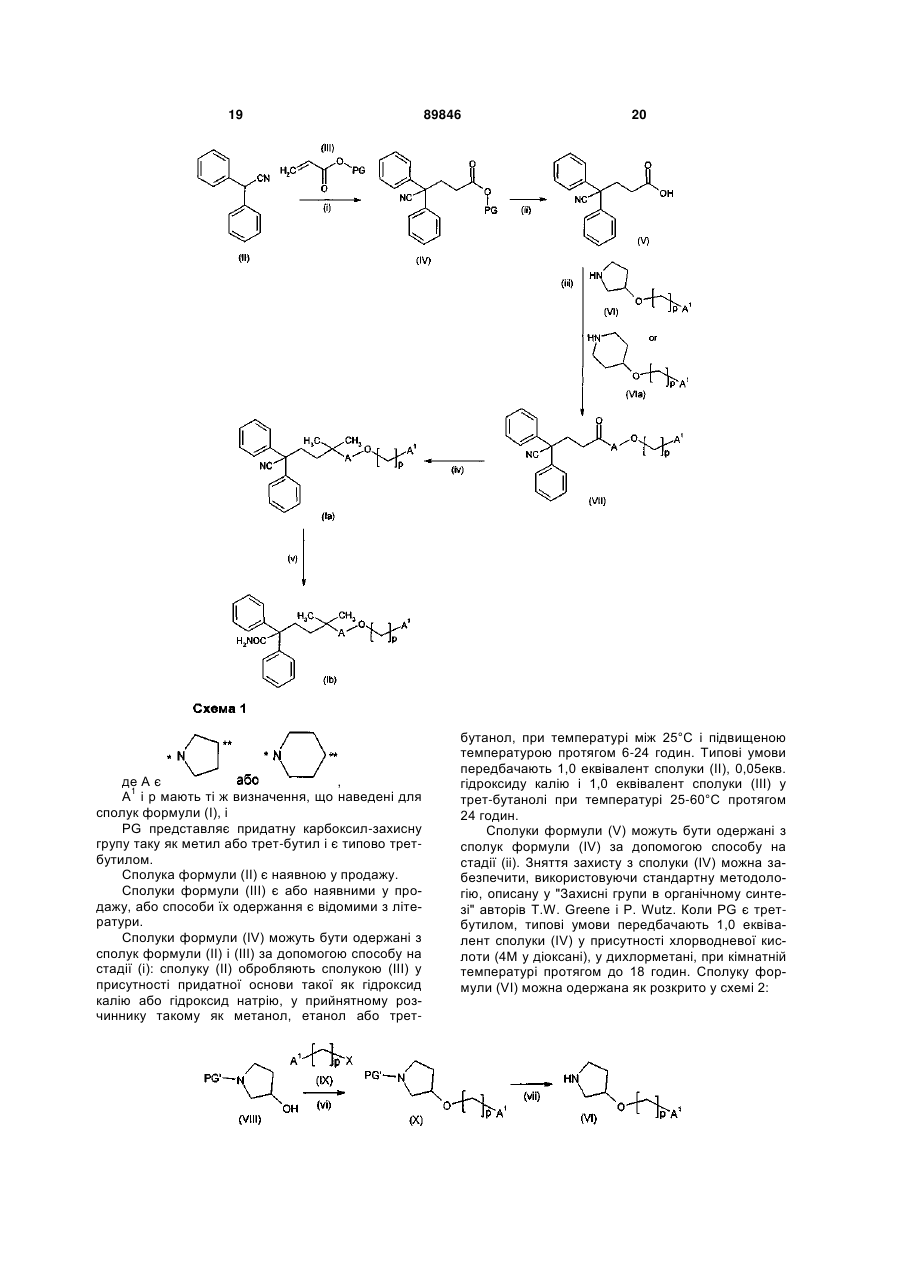
22. Проміжна сполука формули
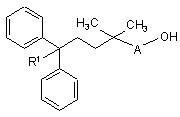 , (2)
, (2)
в якій А і R1 мають значення, як визначено в пункті 1.
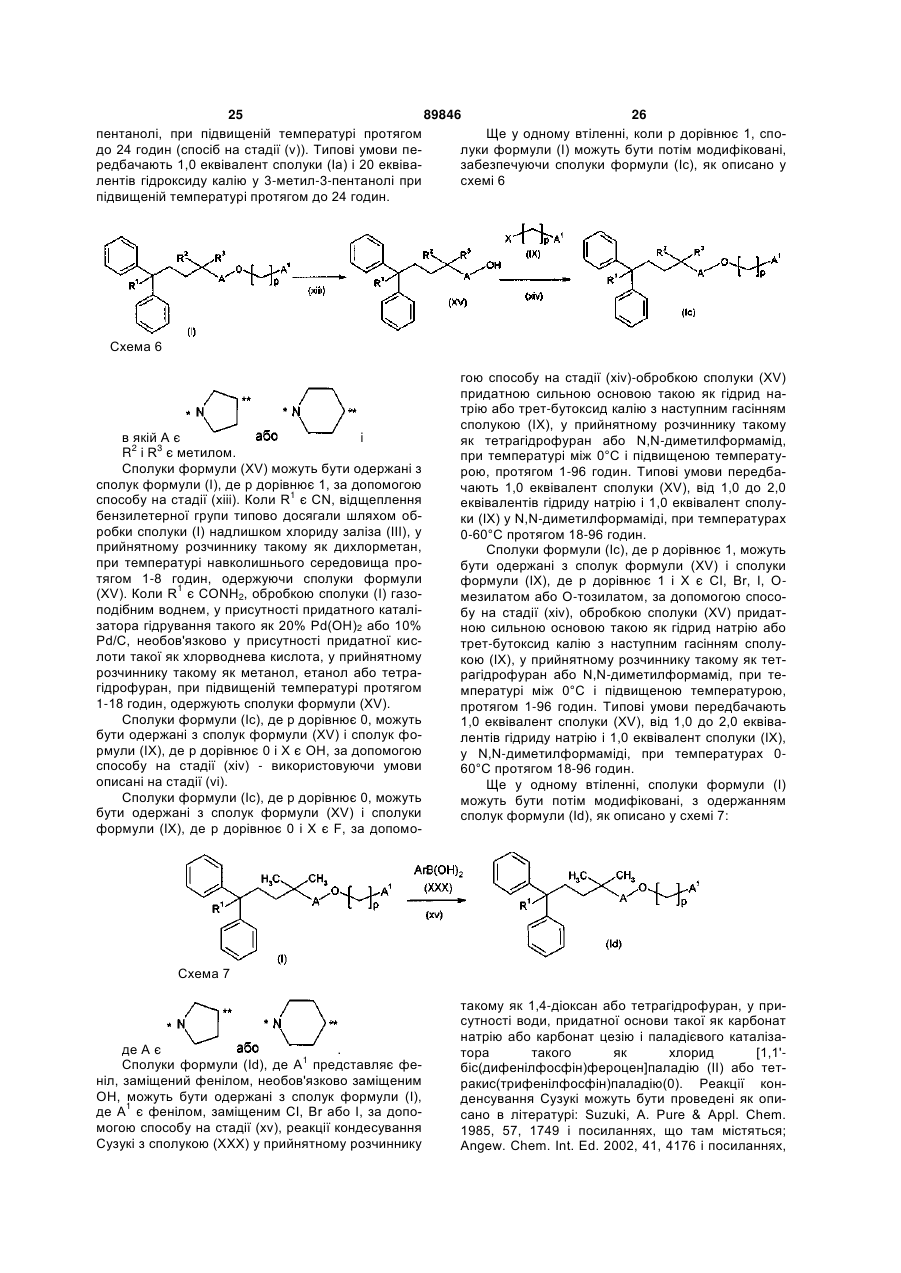
23. Проміжна сполука формули
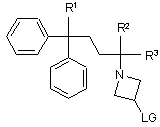 , (3)
, (3)
в якій R1, R2 і R3 мають значення, як визначено в пункті 1, і LG є придатною відхідною групою.
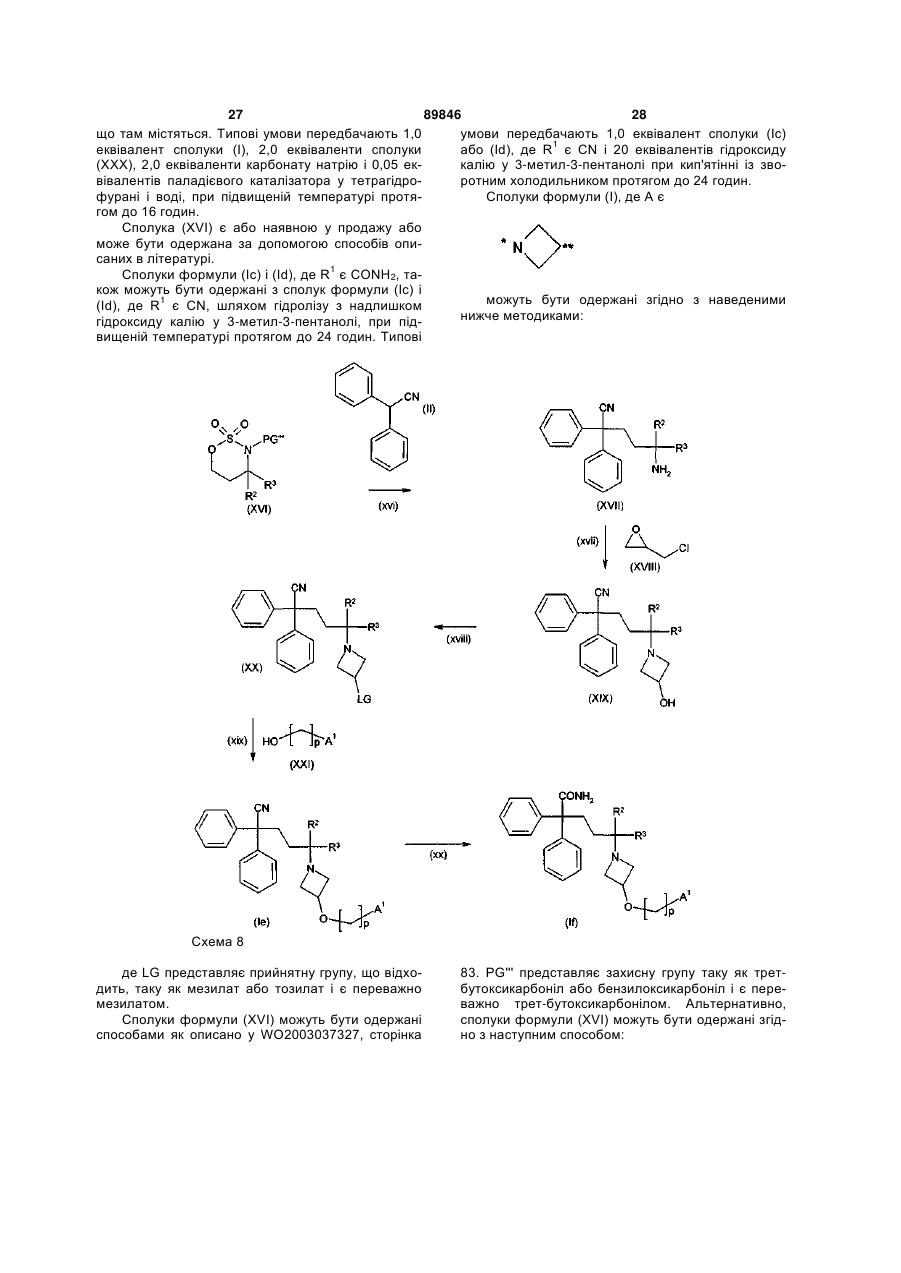
24. Проміжна сполука формули
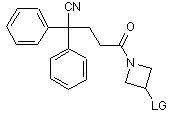 , (XXIV)
, (XXIV)
в якій LG є придатною відхідною групою.
25. Проміжна сполука формули
 , (XVII)
, (XVII)
в якій R2 і R3 мають значення, як визначено в пункті 1.
Текст
УКРАЇНА (19) UA (11) 89846 (13) C2 (51) МПК (2009) C07D 207/12 (2006.01) C07D 413/12 (2006.01) C07D 211/46 (2006.01) C07D 205/00 A61K 31/397 A61K 31/40 A61K 31/4409 A61P 37/00 МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ ДЕРЖАВНИЙ ДЕПАРТАМЕНТ ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ ОПИС ДО ПАТЕНТУ НА ВИНАХІД (54) ПОХІДНІ КАРБОКСАМІДУ ЯК АНТАГОНІСТИ МУСКАРИНОВИХ РЕЦЕПТОРІВ 1 R1 A R2 O (CH2)p (I) A1 R3 , R2 і R3 разом з атомом вуглецю, до якого вони приєднані, можуть також утворювати циклопентанове кільце; р дорівнює 0 або 1; А1 вибирають з a) фенілу, необов'язково заміщеного 1, 2 або 3 групами, незалежно вибраними з галогену, CN, CF3, OR4, SR4, OCF3, (С1-С4)алкілу і фенілу, необов'язково заміщеного ОН; b) нафтилу, необов'язково заміщеного 1 або 2 групами, незалежно вибраними з галогену, CN, CF3, OR4, SR4, OCF3 і (С1-С4)алкілу; c) 9- або 10-членної біциклічної ароматичної гетероциклічної групи, що включає 1, 2 або 3 гетероатоми, незалежно вибрані з О, S або N, згадана гетероциклічна група є необов'язково заміщеною 1 (13) 89846 ** (11) *N UA ** *N або * N ** , ** , де * і ** представляють точки приєднання, ** є місцем приєднання до кисню, R2 і R3 є метилом, або А є групою формули *N C2 , в якій, R1 є CN або CONH2; А вибирають з (19) (21) a200803579 (22) 01.09.2006 (24) 10.03.2010 (86) PCT/IB2006/002727, 01.09.2006 (31) 60/719,467 (32) 21.09.2005 (33) US (31) 60/719,468 (32) 21.09.2005 (33) US (31) 60/719,477 (32) 21.09.2005 (33) US (46) 10.03.2010, Бюл.№ 5, 2010 р. (72) ГЛОССОП ПОЛ АЛАН, GB, МАНТЕЛЛ САЙМОН ДЖОН, GB, СТРЕНГ РОСС СІНКЛЕР, GB, ВАТСОН КРІСТІН АНН ЛУІС, GB, ВУД ЕНТОНІ, GB (73) ПФАЙЗЕР ЛІМІТЕД, GB (56) JP 11100366 A EP 0365093 A1 EP 0948964 A1 DATABASE BEILSTEIN. BEILSTEIN CROSSFIRE INSTITUT ZUR FOERDERUNG DER CHEMISCHEN WISSENSCHAFTEN; BRN 1520424 1976, XP002419977, abstract. &GROCHOWSKY et al: HETEROCYCLES, vol. 5, 1976, pages 101-107. DATABASE CA [Online] CHEMICAL ABSTRACTS SERVICE, COLUMBUS, OHIO, US; RegNo 2310199-7 1968, MAKOSZA, MIECZYSLAW et al: "Reactions of organic anions. XXIII. Reaction of arylacetic nitriles with 1-bromo-3-nitro-3methylbutane" XP002419978 retrieved from STN, Datebase accession no. 1969:421831 abstract & BULLETIN DE L'ACADEMIE POLONAISE DES SCIENCES, SERIE DES SCIENCES CHIMIQUES, 16(11-12), 597-600 CODEN: BARCAQ; ISSN:00014095, 1968 (57) 1. Сполука формули (І) 2 3 89846 4 або 2 замісниками, незалежно вибраними з OR4, 5-метил-5-(4-феноксипіперидин-1-іл)-2,2(С1-С4)алкілу і галогену; дифенілгексанамід; R4 є Н або (С1-С4)алкілом; 5-[4-(3-гідроксифенокси)піперидин-1-іл]-5-метилабо, при необхідності, фармацевтично прийнятні 2,2-дифенілгексанамід; солі або їх сольвати. 5-метил-5-(3-феноксіазетидин-1-іл)-2,21 2. Сполука за п. 1, де R є CONH2. дифенілгексанамід; 3. Сполука за п. 1 або 2, де р дорівнює 0. 5-[3-(3-гідроксифеноксі)азетидин-1-іл]-5-метил-2,24. Сполука за п. 1 або 2, де р дорівнює 1. дифенілгексанамід; 5. Сполука згідно з будь-яким з пунктів 1-4, де А1 є 5-{3-(4-хлор-3-гідроксифеноксі)азетидин-1-іл}-5фенілом, необов'язково заміщеним 1, 2 або 3 груметил-2,2-дифенілгексанамід; пами, незалежно вибраними з F, Сl, CF3, OH, 5-{3-(3-фтор-5-гідроксифеноксі)азетидин-1-іл}-5OCH3, OCF3 i СН3. метил-2,2-дифенілгексанамід; 6. Сполука за будь-яким з пунктів 1-5, де А1 є фе5-{3-(3-хлор-5-гідроксифеноксі)азетидин-1-іл}-5нілом, необов'язково заміщеним 1 або 2 групами, метил-2,2-дифенілгексанамід; незалежно вибраними з F, Сl, CF3, OH, OCH3, 4-{1-[3-(3-гідроксифеноксі)азетидин-1OCF3 i CH3. іл]циклопентил}-2,2-дифенілбутирамід; 7. Сполука за будь-яким з пунктів 1-4, де А1 є наф5-[3-(2-фтор-3-гідроксифеноксі)азетидин-1-іл]-5тилом, необов'язково заміщеним ОН. метил-2,2-дифенілгексанової кислоти амід; 8. Сполука за будь-яким з пунктів 1-4, де А1 виби5-[3-(2-фтор-5-гідроксифеноксі)азетидин-1-іл]-5рають з індолілу, ізоіндолілу, хінолілу, ізохінолілу, метил-2,2-дифенілгексанової кислоти амід і бензофуранілу, ізобензофуранілу, бензотієнілу, 5-[3-(4-хлор-3-гідроксибензилоксі)азетидин-1-іл]-5ізобензотієнілу, хіназолілу, хіноксалілу, фталазиметил-2,2-дифенілгексанової кислоти амід нілу, бензотіазолілу, бензоксазолілу, бензізотіазоабо, при необхідності, їх фармацевтично прийнятні лілу, бензізоксазолілу, бензімідазолілу, індазолілу, солі або сольвати. бензотриазолілу, бензоксадіазолілу, бензізоксаді15. Сполука за п. 1, де згаданою сполукою є 5-[3азолілу, бензотіадіазолілу і бензізотіадіазолілу. (3-гідроксифеноксі)азетидин-1-іл]-5-метил-2,29. Сполука за будь-яким з пунктів 1-4, в якій А1 є дифенілгексанамід або його фармацевтично прибензоксазолілом. йнятна сіль або сольват. 10. Сполука за будь-яким з пунктів 1-9, де R2 і R3 є 16. Фармацевтична композиція, що містить щометилом. найменше ефективну кількість сполуки формули 11. Сполука за будь-яким з пунктів 1-10, де А є (І), як описано в будь-якому з пунктів 1-15, або її групою формули фармацевтично прийнятної солі або сольвату. 17. Сполука формули (І), за будь-яким з пунктів 115, або її фармацевтично прийнятні солі або соль*N ** вати, для застосування як медикаменту. . 18. Застосування сполуки формули (І), як описано 12. Сполука за будь-яким з пунктів 1-10, де А є в будь-якому з пунктів 1-15, або її фармацевтично групою формули прийнятних солей або сольватів, для одержання ** лікарського засобу, що має антагоністичну актив*N ність по відношенню до М3 рецепторів. 19. Застосування сполуки формули (І), як описано . в будь-якому з пунктів 1-15, або її фармацевтично 13. Сполука за будь-яким з пунктів 1-10, де А є прийнятних солей або сольватів, для одержання групою формули лікарського засобу для лікування захворювань, розладів і станів, що вибирають з групи, яка вклюN * ** чає: . хронічну або гостру бронхоконстрикцію, хронічний 14. Сполука за п. 1, де згадану сполуку вибирають бронхіт, обструкцію малих дихальних шляхів та з наступних: емфізему, 5-метил-5-[(3S)-3-феноксипіролідин-1-іл]-2,2обструктивні або запальні захворювання дихальдифенілгексанамід; них шляхів будь-якого типу, етіології або патогене5-метил-5-[(3R)-3-феноксипіролідин-1-іл]-2,2зу, зокрема обструктивне або запальне захворюдифенілгексанамід; вання дихальних шляхів, що є членом, який 5-[(3S)-3-(3-гідроксифенокси)піролідин-1-іл]-5вибирають з групи, що включає хронічну еозинометил-2,2-дифенілгексанамід; фільну пневмонію, хронічне обструктивне легене5-[(3R)-3-(3-гідроксифенокси)піролідин-1-іл]-5ве захворювання (COPD), COPD, що включає хрометил-2,2-дифенілгексанамід; нічний бронхіт, легеневу емфізему або диспное, 5-[(3S)-3-(3-фтор-5-гідроксифенокси)піролідин-1пов'язане або непов'язане з COPD, COPD, що хаіл]-5-метил-2,2-дифенілгексанової кислоти амід; рактеризується незворотною прогресуючою об5-[(3S)-3-(2-фтор-3-гідроксифенокси)піролідин-1струкцією дихальних шляхів, респіраторний дисіл]-5-метил-2,2-дифенілгексанової кислоти амід; трессиндром повнолітніх (ARDS), загострення 5-[(3R)-3-(2-фтор-3-гідроксифенокси)піролідин-1респіраторної гіперреактивності на фоні іншої фаіл]-5-метил-2,2-дифенілгексанамід; рмакотерапії і захворювання дихальних шляхів, 5-[(3R)-3-(2-хлор-3-гідроксифенокси)піролідин-1що пов'язані з легеневою гіпертензією, іл]-5-метил-2,2-дифенілгексанамід; бронхіт будь-якого типу, етіології або патогенезу; зокрема бронхіт, що є членом, який вибирають з 5 89846 6 групи, яка включає гострий бронхіт, гострий ларин(s) агоністи рецептора аденозину А2а, готрахеальний бронхіт, арахідоновий бронхіт, ка(t) інгібітори урокінази, таральний бронхіт, крупозний бронхіт, сухий брон(u) сполуки, що діють як допамінові рецептори, хіт, інфекційний астматичний бронхіт, наприклад, D2 агоністи, продуктивний бронхіт, стафілококовий або стреп(v) модулятори NF B шляху, наприклад, ІКК інгібітококовий бронхіт і везикулярний бронхіт, тори, астму будь-якого типу, етіології або патогенезу, (w) модулятори цитокінових сигнальних шляхів, зокрема астму, що є членом, який вибирають з такі як р38 МАР кіназа або syk кіназа, групи, яка включає атопічну астму, неатопічну ас(х) агенти, що можуть класифікуватись як муколітму, алергічну астму, атопічну бронхіальну ІgEтики або протикашлеві агенти, опосередковану астму, бронхіальну астму, есенці(у) антибіотики, альну астму, істинну астму, інфекційно-алергійну (z) інгібітори HDAC, астму, викликану патофізіологічними розладами, (аа) інгібітори РІ3 кінази та зовнішню астму, викликану зовнішніми факторами, (bb) антагоністи CXCR2. есенціальну астму невідомого або неочевидного 21. Проміжна сполука формули походження, неатопічну астму, бронхітну астму, O емфізематозну астму, астму, викликану фізичним навантаженням, астму, індуковану алергеном, асA1 O тму, індуковану холодним повітрям, професійну A p NC (1) астму, інфекційну астму, спричинену бактеріальною, фунгальною, протозойною або вірусною інфекцією, неалергійну астму, початкову астму, синдром ядухи у немовлят і бронхіоліт, , гостре ушкодження легень, в якій А, р і А1 мають значення, як визначено в бронхоектазію будь-якого типу, етіології або патопункті 1. генезу, зокрема бронхоектазію, що є членом, який 22. Проміжна сполука формули вибирають з групи, що включає циліндричну бронхоектазію, осумковану бронхоектазію, веретеноH3 C подібну бронхоектазію, капілярну бронхоектазію, CH3 OH циститну бронхоектазію, суху бронхоектазію і фоA лікулярну бронхоектазію. (2) R1 20. Комбінація сполуки згідно з будь-яким з пунктів 1-15 з іншим терапевтичним агентом(и), що вибирають з наступних: (a) інгібітори 5-ліпоксигенази (5-LO) або антагоніс, ти 5-ліпоксигенази активуючого протеїну (FLAP), в якій А і R1 мають значення, як визначено в пункті (b) антагоністи лейкотриєну (LTRAs), включаючи 1. антагоністи LTB4, LTC4, LTD4 і LTE4, 23. Проміжна сполука формули (c) антагоністи рецептора гістаміну, включаючи Н1 R1 і Н3 антагоністи, R2 (d) агоністи 1- і 2-адренорецептора для протизастійного застосування, R3 (e) 2 агоністи короткотривалої або довготривалої (3) активності, N (f) інгібітори PDE, наприклад, інгібітори PDE3, PDE4 і PDE5, (g) теофілін, LG , (h) хромоглікат натрію, в якій R1, R2 і R3 мають значення, як визначено в (і) інгібітори СОХ, як неселективні, так і селективні пункті 1, і LG є придатною відхідною групою. інгібітори СОХ-1 або СОХ-2 (NSAIDs), 24. Проміжна сполука формули (j) пероральні глюкокортикостероїди і глюкокортиCN костероїди, що інгалюються, (k) моноклональні антитіла, активні проти ендоO генного запалення, (l) агенти проти фактора некрозу пухлини (анти(XXIV) N TNF- ), (m) інгібітори адгезії молекули, включаючи VLA-4 антагоністи, LG , (n) антагоністи рецептора кініну-В1 і В2, (о) імуносупресивні агенти, в якій LG є придатною відхідною групою. (р) інгібітори матриксних металопротеаз (MMPs), 25. Проміжна сполука формули (q) антагоністи рецептора тахікініну NK1, NK2 і NK3, (r) інгібітори еластази, 7 CN 89846 8 в якій R2 і R3 мають значення, як визначено в пункті 1. R2 R3 (XVII) NH2 , Даний винахід стосується сполук загальної формули (І): в якій R1, R2, R3, А, А1 і p мають значення, наведені нижче та способів їх одержання, композицій, що їх містять, та застосування таких похідних. Холінергічні мускаринові рецептори є членами надродини рецепторів, зв'язаних з G-протеїном і надалі підрозділяються на 5 підтипів, від M1 до М5. Підтипи мускаринових рецепторів експресуються в різних місцях організму і по-різному. Гени були клоновані для всіх 5 підтипів і з них M1, М2 і М3 рецептори були значною мірою фармакологічно охарактеризовані у тканинах тварин і людей. M1 рецептори експресуються у мозку (корі головного мозку і гіпокампі), залозах і у гангліях симпатичних і парасимпатичних нервів. М2 рецептори експресуються в серці, ромбоподібному мозку, гладкій мускулатурі і у синапсі вегетативної нервової системи. М3 рецептори експресуються у мозку, залозах і гладкій мускулатурі. У дихальних шляхах, стимуляція М3 рецепторів викликає скорочення гладкої мускулатури дихальних шляхів, що приводить до бронхоконстрикції, в той же час стимуляція М3 рецепторів у слинній залозі підвищує виділення мокротиння та слизу, що приводить до підвищення слиновиділення. Зрозуміло, що М2 рецептори, експресовані у клітинах гладкої мускулатури відповідають за скорочення, в той час як пресинаптичні М2 рецептори модулюють вивільнення ацетилхоліну з парасимпатичних нервів. Стимуляція М2 рецепторів експресованих у серці викликає брадикардію. Мускаринові антагоністи короткотривалої і довготривалої дії застосовують у перебігу астми і ХОЗЛ; вони включають агенти короткотривалої дії Атровент (іпраторію бромід) і Оксивент (окситропію бромід) і агент довготривалої дії Спіріва (тіотропію бромід). Після введення інгаляційним шляхом ці сполуки викликають ефект бронходилатації. На додаток до покращення у спірометричних оцінках, застосування мускаринових препаратів при лікуванні хронічного обструктивного захворювання дихальних шляхів (ХОЗЛ) пов'язане з пок ращенням стану здоров'я та показники якості життя. Внаслідок широкого розповсюдження мускаринових рецепторів у організмі, значне систематичне застосування мускаринових антагоністів пов'язане з ефектами такими як сухість у роті, запори, мідріаз, затримання сечі (все це переважно викликається через блокаду М3 рецепторів) і тахікардія (викликана через блокаду М2 рецепторів). У більшості випадків побічним ефектом, що спостерігався після введення терапевтичної дози інгаляційним шляхом, при клінічному використанні відомих на сьогодні неселективних мускаринових антагоністів є відчуття сухості у роті і хоча це проявляється тільки у незначному ступені, це дійсно обмежує дозу агента, що інгалюють. Відповідно, все ще існує потреба у покращенні антагоністів М3 рецепторів, які будуть мати прийнятний фармакологічний профіль, наприклад, в одиницях активності, фармакокинетики або тривалості дії. В даному контексті, представлений винахід стосується нових антагоністів М3 рецепторів. Зокрема, існує потреба в антагоністах М3 рецепторів, які будуть мати фармакологічний профіль, що придатний для введення шляхом інгаляції. У науковій літературі описано багато сполук, що мають дію антагоністів мускаринових рецепторів. Фактично, наприклад, ЕР0948964А1 розкриває сполуки формули в якій R означає атом водню, атом галогену або нижчу алкоксигрупу. Винахід стосується сполуки формули (І) в якій, - R1 є CN або CONH2; - А вибирають з 9 де * і ** представляють точки приєднання, ** є місцем приєднання до кисню, - R2 і R3 є метилом або, де А є групою формули R2 і R3 разом з атомом вуглецю, до якого вони приєднані, можуть також утворювати циклопентанове кільце; - p дорівнює 0 або 1; - А1 вибирають з a) фенілу, необов'язково заміщеного 1, 2 або 3 групами незалежно вибраними з галогену, CN, CF3, OR4, SR4, OCF3, (С1-С4)алкілу і фенілу необов'язково заміщеного ОН; b) нафтилу, необов'язково заміщеного 1 або 2 групами незалежно вибраними з галогену, CN, CF3, OR4, SR4, OCF3 і (С1-С4)алкілу; c) 9 або 10-членної біциклічної ароматичної гетероциклічної групи, що включає 1, 2 або 3 гетероатоми незалежно вибрані з О, S або N, згадана гетероциклічна група є необов'язково заміщеною 1 або 2 замісниками незалежно вибраними з OR4, (С1-С4)алкілу і галогену; - R4 є Η або (С1-С4)алкілом; або, при необхідності, фармацевтично прийнятних солей або їх сольватів. В наведеній вище формулі (І), (С1-С4)алкіл означає нерозгалужену або розгалужену групу, що містить 1, 2, 3 або 4 атоми вуглецю. Це стосується також, якщо вони несуть замісники або зустрічаються як замісники на інших радикалах, наприклад, у О-(С1-С4)алкільних радикалах, S-(С1С4)алкільних радикалах і т.і... Прикладами придатних (С1-С4)алкільних радикалів є метил, етил, нпропіл, ізо-пропіл, н-бутил, ізо-бутил, втор-бутил, трет-бутил. Прикладами придатних О-(С1С4)алкільних радикалів є метокси, етокси, нпропілокси, iзопропілокси, н-бутилокси, ізобутилокси, втор-бутилокси і трет-бутилокси... Прикладами 9 або 10-членної біциклічної ароматичної гетероциклічної групи, що включає 1, 2 або 3 гетероатоми незалежно вибрані з О, S або N є індоліл, ізоіндоліл, хіноліл, ізохіноліл, бензофураніл, ізобензофураніл, бензотієніл, ізобензотіеніл, хіназоліл, хіноксаліл, фталазиніл, бензотіазоліл, бензоксазоліл, бензізотіазоліл, бензізоксазоліл, бензімідазоліл, індазоліл, бензотриазоліл, бензоксадіазоліл, бензізоксадіазоліл, бензотіадіазоліл і бензізотіадіазоліл. Переважними 9 або 10-членними біциклічними ароматичними гетероциклічними групами є бензоксазоліл, бензотіазоліл, бензофураніл, бензотієніл, ізохіноліл і хіноліл. Бензоксазоліл є особливо переважним. Гало- означає атом галогену, що вибирають з групи, що включає фтор, хлор, бром і йод. Переважними галогрупами є фтор і хлор. 89846 10 У наведених вище сполуках формули (І) і у проміжних сполуках корисних для їх одержання, переважними є наступні визначення: Переважно, R1 є CONH2. Переважно, R4 є Η або СН3. 1 Переважно, А є фенілом, необов'язково заміщеним 1, 2 або 3 групами незалежно вибраними з F, СІ, CF3, OH, OCH3, OCF3 і СН3. Більш переважно, А1 є фенілом, необов'язково заміщеним 1 або 2 групами незалежно вибраними з F, СІ, CF3, ОН, ОСН3, OCF3 і СН3. Переважно, А1 є нафтилом, необов'язково заміщеним ОН. Переважно, А1 є бензоксазолілом. Переважно, R2 і R3 є метилом. У переважному втіленні, p дорівнює 0. У іншому переважному втіленні, p дорівнює 1. У переважному втіленні, сполука формули (І), в якій А є групою формули має наведену нижче (R) конфігурацію: У переважному втіленні, сполуки формули (І), в якій А є групою формули має наведену нижче (S) конфігурацію: Переважними сполуками згідно з винаходом є наступні: 5-Метил-5-[(3S)-3-феноксипіролідин-1-іл]-2,2дифенілгексаннітрил; 5-Метил-5-[(3S)-3-феноксипіролідин-1-іл]-2,2дифенілгексанамід; 5-Метил-5-[(3R)-3-феноксипіролідин-1-іл]-2,2дифенілгексаннітрил; 5-Метил-5-[(3R)-3-феноксипіролідин-1-іл]-2,2дифенілгексанамід; 5-[(3S)-3-(3-Метоксифенокси)піролідин-1-іл]-5метил-2,2-дифенілгексаннітрил; 11 89846 12 5-[(3S)-3-(3-Метоксифенокси)піролідин-1-іл]-55-[(3S)-3-(4-Хлор-2метил-2,2-дифенілгексанамід; Гідроксифенокси)піролідин-1-іл]-5-метил-2,25-[(3S)-3-(3-Гідроксифенокси)піролідин-1-іл]-5дифенілгексанової кислоти амід; метил-2,2-дифенілгексанамід; 5-[(3S)-3-(2-Хлор-3-Метоксифенокси)піролідин5-[(3R)-3-(Бензилокси)піролідин-1-іл]-5-метил1-іл]-5-метил-2,2-дифенілгексанової кислоти амід; 2,2-дифенілгексаннітрил; 5-[(3S)-3-(2-Хлор-35-[(3R)-3-(Бензилокси)піролідин-1-іл]-5-метилГідроксифенокси)піролідин-1-іл]-5-метил-2,22,2-дифенілгексанамід; дифенілгексанової кислоти амід; 5-[(3S)-3-(Бензилокси)піролідин-1-іл]-5-метил5-[(3S)-3-(4-Хлор-32,2-дифенілгексаннітрил; Гідроксифенокси)піролідин-1-іл]-5-метил-2,25-[(3S)-3-(Бензилокси)піролідин-1-іл]-5-метилдифенілгексанової кислоти амід; 2,2-дифенілгексанамід; 5-[(3S)-3-(2-Хлор-55-[(3R)-3-(3-Метоксифенокси)піролідин-1-іл]-5Гідроксифенокси)піролідин-1-іл]-5-метил-2,2метил-2,2-дифенілгексанамід; дифенілгексанової кислоти амід; 5-[(3R)-3-(3-Гідроксифенокси)піролідин-1-іл]-55-[(3R)-3-(3-Хлор-2метил-2,2-дифенілгексанамід; Метоксифенокси)піролідин-1-іл]-5-метил-2,25-Метил-5-[(3S)-3-(3-метилфенокси)піролідиндифенілгексаннітрил; 1-іл]-2,2-дифенілгексанамід; 5-[(3R)-3-(3-Хлор-25-[(3R)-3-(1,3-Бензоксазол-6-ілокси)піролідинМетоксифенокси)піролідин-1-іл]-5-метил-2,21-іл]-5-метил-2,2-дифенілгексанамід; дифенілгексанової кислоти амід; 5-[(3S)-3-(4-Хлорфенокси)піролідин-1-іл]-55-[(3R)-3-(3-Хлор-2метил-2,2-дифенілгексанамід; Гідроксифенокси)піролідин-1-іл]-5-метил-2,25-[(3S)-3-(3-Бромфенокси)піролідин-1-іл]-5дифенілгексанової кислоти амід; метил-2,2-дифенілгексанамід; 5-[(3S)-3-(3-Гідрокси-2,55-{(3S)-3-[(3'-Гідроксибіфеніл-4диметилфенокси)піролідин-1-іл]-5-метил-2,2іл)окси]піролідин-1-іл}-5-метил-2,2дифенілгексанової кислоти амід; дифенілгексанамід; 5-[(3S)-3-(3-Фтор-5-Метоксифенокси)піролідин5-{(3S)-3-[(3'-Гідроксибіфеніл-31-іл]-5-метил-2,2-дифенілгексанової кислоти амід; іл)окси]піролідин-1-іл}-5-метил-2,25-[(3S)-3-(3-Фтор-5-Гідроксифенокси)піролідиндифенілгексанамід; 1-іл]-5-метил-2,2-дифенілгексанової кислоти амід; 5-{(3S)-3-[(6-Гідрокси-2-нафтил)окси]піролідин5-[(3R)-3-(3-Метокси-51-іл}-5-метил-2,2-дифенілгексанамід; трифторметилфенокси)піролідин-1-іл]-5-метил-2,25-[(3S)-3-(2-Гідроксифенокси)піролідин-1-іл]-5дифенілгексаннітрил; метил-2,2-дифенілгексанамід; 5-[(3R)-3-(3-Метокси-55-[(3S)-3-(4-метоксифенокси)піролідин-1-іл]-5трифторметилфенокси)піролідин-1-іл]-5-метил-2,2метил-2,2-дифенілгексанамід; дифенілгексанової кислоти амід; 5-[(3S)-3-(4-гідроксифенокси)піролідин-1-іл]-55-[(3R)-3-(3-Гідрокси-5метил-2,2-дифенілгексанамід; трифторметилфенокси)піролідин-1-іл]-5-метил-2,25-[(3S)-3-(4-трифторметилфенокси)піролідиндифенілгексанової кислоти амід; 1-іл]-5-метил-2,2-дифенілгексанамід; 5-[(3S)-3-(4-Фтор-3-Метоксифенокси)піролідин5-[(3R)-3-(4-Трифторметилфенокси)піролідин1-іл]-5-метил-2,2-дифенілгексанової кислоти амід; 1-іл]-5-метил-2,2-дифенілгексаннітрил; 5-[(3S)-3-(2-Фтор-3-Метоксифенокси)піролідин5-[(3R)-3-(4-трифторметилфенокси)піролідин1-іл]-5-метил-2,2-дифенілгексанової кислоти амід; 1-іл]-5-метил-2,2-дифенілгексанамід; 5-[(3S)-3-(4-Фтор-3-Гідроксифенокси)піролідин5-[(3R)-3-(3-хлор-4-метоксифенокси)піролідин1-іл]-5-метил-2,2-дифенілгексанової кислоти амід; 1-іл]-5-метил-2,2-дифенілгексаннітрил; 5-[(3S)-3-(2-Фтор-3-Гідроксифенокси)піролідин5-[(3R)-3-(3-хлор-4-метоксифенокси)піролідин1-іл]-5-метил-2,2-дифенілгексанової кислоти амід; 1-іл]-5-метил-2,2-дифенілгексанамід; 5-[(3R)-3-(3-Гідроксибензилокси)піролідин-15-[(3S)-3-(3-Гідрокси-5іл]-5-метил-2,2-дифенілгексанової кислоти амід; метилфенокси)піролідин-1-іл]-5-метил-2,25-{(3S)-3-[(3-Бромбензил)окси]піролідин-1-іл}дифенілгексанової кислоти амід; 5-метил-2,2-дифенілгексаннітрил; 5-[(3S)-3-(3-Гідрокси-25-{(3S)-3-[(3'-Гідроксибіфеніл-3метилфенокси)піролідин-1-іл]-5-метил-2,2іл)метокси]піролідин-1-іл}-5-метил-2,2дифенілгексанової кислоти амід; дифенілгексаннітрил; 5-[(3S)-3-(2,4-Дихлор-55-[(3S)-3-(Біфеніл-3-ілметокси)піролідин-1-іл]Гідроксифенокси)піролідин-1-іл]-5-метил-2,25-метил-2,2-дифенілгексаннітрил; дифенілгексанової кислоти амід; 5-{(3S)-3-[(2'-Гідроксибіфеніл-35-[(3S)-3-(4,5-Дихлор-2іл)метокси]піролідин-1-іл}-5-метил-2,2Гідроксифенокси)піролідин-1-іл]-5-метил-2,2дифенілгексаннітрил; дифенілгексанової кислоти амід; 5-{(3S)-3-[(4-Бромбензил)окси]піролідин-1-іл}5-[(3S)-3-(3-Хлор-5-метоксифенокси)піролідин5-метил-2,2-дифенілгексаннітрил; 1-іл]-5-метил-2,2-дифенілгексанової кислоти амід; 5-{(3S)-3-[(3'-Гідроксибіфеніл-45-[(3S)-3-(3-Хлор-5-гідроксифенокси)піролідиніл)метокси]піролідин-1-іл}-5-метил-2,21-іл]-5-метил-2,2-дифенілгексанової кислоти амід; дифенілгексаннітрил; 5-[(3S)-3-(4-Хлор-2-Метоксифенокси)піролідин1-іл]-5-метил-2,2-дифенілгексанової кислоти амід; 13 89846 14 5-{(3S)-3-[(3'-Гідроксибіфеніл-35-{4-[(3-Бромбензил)окси]піперидин-1-іл}-5іл)метокси]піролідин-1-іл}-5-метил-2,2метил-2,2-дифенілгексаннітрил; дифенілгексанамід; 5-{4-[(3-Гідроксибензил)окси]піперидин-1-іл}-55-{(3S)-3-[(4'-Гідроксибіфеніл-3метил-2,2-дифенілгексаннітрил; іл)метокси]піролідин-1-іл}-5-метил-2,25-[4-(Бензилокси)піперидин-1-іл]-5-метил-2,2дифенілгексаннітрил; дифенілгексаннітрил; 5-{(3S)-3-[(4'-Гідроксибіфеніл-35-Метил-5-(4-феноксипіперидин-1-іл)-2,2іл)метокси]піролідин-1-іл}-5-метил-2,2дифенілгексанамід; дифенілгексанамід; 5-{4-[(3-Бромбензил)окси]піперидин-1-іл}-55-{(3S)-3-[(2'-Гідроксибіфеніл-3метил-2,2-дифенілгексанамід; іл)метокси]піролідин-1-іл}-5-метил-2,25-[4-(Бензилокси)піперидин-1-іл]-5-метил-2,2дифенілгексанамід; дифенілгексанамід; 5-{(3S)-3-[(3'-Гідроксибіфеніл-45-[4-(2,4-Дихлор-5-гідроксифенокси)піперидиніл)метокси]піролідин-1-іл}-5-метил-2,21-іл]-5-метил-2,2-дифенілгексанової кислоти амід; дифенілгексанамід; 5-[4-(4-Ціано-2,5-дифторфенокси)піперидин-15-[(3S)-3-(Біфеніл-3-ілметокси)піролідин-1-іл]іл]-5-метил-2,2-дифенілгексанової кислоти амід; 5-метил-2,2-дифенілгексанамід; 5-[4-(3-гідроксифенокси)піперидин-1-іл]-55-[(3R)-3-(4-Фтор-3метил-2,2-дифенілгексанамід; гідроксибензилокси)піролідин-1-іл]-5-метил-2,25-[4-(3-гідрокси-2-метилфенокси)піперидин-1дифенілгексанамід; іл]-5-метил-2,2-дифенілгексанамід; 5-[(3S)-3-(3-Ціано-55-{4-[(3'-гідроксибіфеніл-3гідроксифенокси)піролідин-1-іл]-5-метил-2,2іл)метокси]піперидин-1-іл}-5-метил-2,2дифенілгексанамід; дифенілгексаннітрил; 5-[(3S)-3-(2-Ціано-55-{4-[(3'-гідроксибіфеніл-3метоксифенокси)піролідин-1-іл]-5-метил-2,2іл)метокси]піперидин-1-іл}-5-метил-2,2дифенілгексанамід; дифенілгексанамід; 5-{(3S)-3-[(7-Гідрокси-2-нафтил)окси]піролідин5-[3-(3-Метоксифенокси)азетидин-1-іл]-51-іл}-5-метил-2,2-дифенілгексанамід; метил-2,2-дифенілгексаннітрил; 5-[(3S)-3-(4-Фенілфенокси)піролідин-1-іл]-55-[3-(3-Метоксифенокси)азетидин-1-іл]-5метил-2,2-дифенілгексанамід; метил-2,2-дифенілгексанамід; 5-[(3R)-3-(3-хлор-4-гідроксифенокси)піролідин5-[3-(Бензилокси)азетидин-1-іл]-5-метил-2,21-іл]-5-метил-2,2-дифенілгексанамід; дифенілгексаннітрил; 5-[(3R)-3-(3-Фтор-5-метоксифенокси)піролідин5-[3-(Бензилокси)азетидин-1-іл]-5-метил-2,21-іл]-5-метил-2,2-дифенілгексанамід; дифенілгексанамід; 5-[(3R)-3-(3-Фтор-5-гідроксифенокси)піролідин5-Метил-5-(3-феноксиазетидин-1-іл)-2,21-іл]-5-метил-2,2-дифенілгексанамід; дифенілгексаннітрил; 5-[(3R)-3-(2-Фтор-3-метоксифенокси)піролідин5-Метил-5-(3-феноксиазетидин-1-іл)-2,21-іл]-5-метил-2,2-дифенілгексанамід; дифенілгексанамід; 5-[(3R)-3-(2-Фтор-3-гідроксифенокси)піролідин5-[3-(4-Метоксифенокси)азетидин-1-іл]-51-іл]-5-метил-2,2-дифенілгексанамід; метил-2,2-дифенілгексаннітрил; 5-[(3R)-3-(2-Хлор-3-метоксифенокси)піролідин5-[3-(4-Метоксифенокси)азетидин-1-іл]-51-іл]-5-метил-2,2-дифенілгексанамід; метил-2,2-дифенілгексанамід; 5-[(3R)-3-(2-Хлор-3-гідроксифенокси)піролідин5-[3-(4-гідроксифенокси)азетидин-1-іл]-51-іл]-5-метил-2,2-дифенілгексанамід; метил-2,2-дифенілгексанамід; 5-[(3R)-3-(4-Хлор-35-[3-(3-Гідроксифенокси)азетидин-1-іл]-5гідроксибензилокси)піролідин-1-іл]-5-метил-2,2метил-2,2-дифенілгексанамід; дифенілгексанамід; 5-[3-(2-Гідроксифенокси)азетидин-1-іл]-55-[(3R)-3-(3-метокси-4-хлорметил-2,2-дифенілгексанамід; фенокси)піролідин-1-іл]-5-метил-2,25-{3-(2,4-Дихлор-5-гідроксифенокси)азетидиндифенілгексаннітрил; 1-іл}-5-метил-2,2-дифенілгексанамід; 5-[(3R)-3-(3-метокси-4-хлор5-{3-(4,5-Дихлор-2-гідроксифенокси)азетидинфенокси)піролідин-1-іл]-5-метил-2,21-іл}-5-метил-2,2-дифенілгексанамід; дифенілгексанамід; 5-[3-(4-Хлор-3-метоксифенокси)азетидин-1-іл]5-[(3R)-3-(3-гідрокси-4-хлор5-метил-2,2-дифенілгексаннітрил; фенокси)піролідин-1-іл]-5-метил-2,25-{3-(4-Хлор-3-метоксифенокси)азетидин-1-іл}дифенілгексанамід; 5-метил-2,2-дифенілгексанамід; 5-[(3R)-3-(3-гідрокси-4-ціано5-{3-(4-Хлор-3-гідроксифенокси)азетидин-1-іл}фенокси)піролідин-1-іл]-5-метил-2,25-метил-2,2-дифенілгексанамід; дифенілгексанамід; 5-[3-(3-Гідроксибензилокси)азетидин-1-іл]-55-[(3S)-3-(3-метоксибензилокси)піролідин-1-іл]метил-2,2-дифенілгексанової кислоти амід; 5-метил-2,2-дифенілгексанамід; 5-[3-(2-Хлор-5-метоксифенокси)азетидин-1-іл]5-[(3R)-3-(2-Хлор-35-метил-2,2-дифенілгексаннітрил; гідроксибензилокси)піролідин-1-іл]-5-метил-2,25-[3-(2-Хлор-5-метоксифенокси)азетидин-1-іл]дифенілгексанамід; 5-метил-2,2-дифенілгексанової кислоти амід; 5-Метил-5-(4-феноксипіперидин-1-іл)-2,25-[3-(2-Хлор-5-гідроксифенокси)азетидин-1-іл]дифенілгексаннітрил; 5-метил-2,2-дифенілгексанової кислоти амід; 15 89846 16 5-[3-(3-Фтор-5-метоксифенокси)азетидин-1-іл]5-{3-[(4-Гідроксибензил)окси]азетидин-1-іл}-55-метил-2,2-дифенілгексаннітрил; метил-2,2-дифенілгексаннітрил; і 5-[3-(3-Фтор-5-метоксифенокси)азетидин-1-іл]5-[3-(4-Гідроксибензилокси)азетидин-1-іл]-55-метил-2,2-дифенілгексанамід; метил-2,2-дифенілгексанової кислоти амід. 5-{3-(3-Фтор-5-гідроксифенокси)азетидин-1-іл}Більш переважними сполуками є наступні: 5-метил-2,2-дифенілгексанамід; 5-Метил-5-[(3S)-3-феноксипіролідин-1-іл]-2,25-[3-(3-Хлор-5-метоксифенокси)азетидин-1-іл]дифенілгексанамід; 5-метил-2,2-дифенілгексаннітрил; 5-Метил-5-[(3R)-3-феноксипіролідин-1-іл]-2,25-[3-(3-Хлор-5-метоксифенокси)азетидин-1-іл]дифенілгексанамід; 5-метил-2,2-дифенілгексанамід; 5-[(3S)-3-(3-Гідроксифенокси)піролідин-1-іл]-55-{3-(3-Хлор-5-гідроксифенокси)азетидин-1-іл}метил-2,2-дифенілгексанамід; 5-метил-2,2-дифенілгексанамід; 5-[(3R)-3-(3-Гідроксифенокси)піролідин-1-іл]-55-[3-(4-Фтор-2-метоксифенокси)азетидин-1-іл]метил-2,2-дифенілгексанамід; 5-метил-2,2-дифенілгексаннітрил; 5-[(3S)-3-(3-Фтор-5-Гідроксифенокси)піролідин5-[3-(4-Фтор-2-метоксифенокси)азетидин-1-іл]1-іл]-5-метил-2,2-дифенілгексанової кислоти амід; 5-метил-2,2-дифенілгексанамід; 5-[(3S)-3-(2-Фтор-3-Гідроксифенокси)піролідин5-{3-(4-Фтор-2-гідроксифенокси)азетидин-1-іл}1-іл]-5-метил-2,2-дифенілгексанової кислоти амід; 5-метил-2,2-дифенілгексанамід; 5-[(3R)-3-(2-Фтор-3-гідроксифенокси)піролідин5-[3-(2,6-Дихлор-31-іл]-5-метил-2,2-дифенілгексанамід; гідроксибензилокси)азетидин-1-іл]-5-метил-2,25-[(3R)-3-(2-Хлор-3-гідроксифенокси)піролідиндифенiлгексанової кислоти амід; 1-іл]-5-метил-2,2-дифенілгексанамід; 4-{1-[3-(3-Метоксифенокси)азетидин-15-Метил-5-(4-феноксипіперидин-1-іл)-2,2іл]циклопентил}-2,2-дифенілбутиронітрил; дифенілгексанамід; 4-{1-[3-(3-Метоксифенокси)азетидин-15-[4-(3-гідроксифенокси)піперидин-1-іл]-5іл]циклопентил}-2,2-дифенілбутирамід; метил-2,2-дифенілгексанамід; 4-{1-[3-(3-Гідроксифенокси)азетидин-15-Метил-5-(3-феноксиазетидин-1-іл)-2,2іл]циклопентил}-2,2-дифенілбутирамід; дифенілгексанамід; 5-[3-(2-Фтор-3-метоксифенокси)азетидин-1-іл]5-[3-(3-Гідроксифенокси)азетидин-1-іл]-55-метил-2,2-дифенілгексаннітрил; метил-2,2-дифенілгексанамід; 5-[3-(2-Фтор-3-метоксифенокси)азетидин-1-іл]5-{3-(4-Хлор-3-гідроксифенокси)азетидин-1-іл}5-метил-2,2-дифенілгексанової кислоти амід; 5-метил-2,2-дифенілгексанамід; 5-[3-(2-Фтор-3-гідроксифенокси)азетидин-1-іл]5-{3-(3-Фтор-5-гідроксифенокси)азетидин-1-іл}5-метил-2,2-дифенілгексанової кислоти амід; 5-метил-2,2-дифенілгексанамід; 5-[3-(2-Фтор-5-метоксифенокси)азетидин-1-іл]5-{3-(3-Хлор-5-гідроксифенокси)азетидин-1-іл}5-метил-2,2-дифенілгексаннітрил; 5-метил-2,2-дифенілгексанамід; 5-[3-(2-Фтор-5-метоксифенокси)азетидин-1-іл]4-{1-[3-(3-Гідроксифенокси)азетидин-15-метил-2,2-дифенілгексанової кислоти амід; іл]циклопентил}-2,2-дифенілбутирамід; 5-[3-(2-Фтор-5-гідроксифенокси)азетидин-1-іл]5-[3-(2-Фтор-3-гідроксифенокси)азетидин-1нл]5-метил-2,2-дифенілгексанової кислоти амід; 5-метил-2,2-дифенілгексанової кислоти амід; 5-[3-(4-Хлор-3-гідроксибензилокси)азетидин-15-[3-(2-Фтор-5-гідроксифенокси)азетидин-1-іл]іл]-5-метил-2,2-дифенілгексанової кислоти амід; 5-метил-2,2-дифенілгексанової кислоти амід; і 4-{1-[3-(4-Хлор-3-гідроксифенокси)азетидин-15-[3-(4-Хлор-3-гідроксибензилокси)азетидин-1іл]циклопентил}-2,2-дифенілбутирамід; іл]-5-метил-2,2-дифенілгексанової кислоти амід. 5-[3-(3-Бром-5-метоксифенокси)азетидин-1-іл]Найбільш переважними сполуками є наступні: 5-метил-2,2-дифенілгексаннітрил; 5-[(3S)-3-(3-Гідроксифенокси)піролідин-1-іл]-55-[3-(3-Бром-5-метоксифенокси)азетидин-1-іл]метил-2,2-дифенілгексанамід; 5-метил-2,2-дифенілгексанової кислоти амід; 5-[(3R)-3-(3-Гідроксифенокси)піролідин-1-іл]-55-[3-(3-Бром-5-гідроксифенокси)азетидин-1-іл]метил-2,2-дифенілгексанамід; 5-метил-2,2-дифенілгексанової кислоти амід; 5-[(3R)-3-(2-Фтор-3-гідроксифенокси)піролідин4-{1-[3-(3-Фтор-4-метоксифенокси)азетидин-11-іл]-5-метил-2,2-дифенілгексанамід; іл]циклопентил}-2,2-дифенілбутиронітрил; 5-[3-(3-Гідроксифенокси)азетидин-1-іл]-54-{1-[3-(3-Фтор-4-метоксифенокси)азетидин-1метил-2,2-дифенілгексанамід; іл]циклопентил}-2,2-дифенілбутирамід; 5-{3-(4-Хлор-3-гідроксифенокси)азетидин-1-іл}4-{1-[3-(3-Фтор-4-гідроксифенокси)азетидин-15-метил-2)2-дифенілгексанамід; іл]циклопентил}-2,2-дифенілбутирамід; 5-{3-(3-Фтор-5-гідроксифенокси)азетидин-1-іл}5-[3-(3-Хлор-4-гідроксибензилокси)азетидин-15-метил-2,2-дифенілгексанамід; іл]-5-метил-2,2-дифенілгексанової кислоти амід; 5-{3-(3-Хлор-5-гідроксифенокси)азетидин-1-іл}5-[3-(4-Хлор-2-гідроксибензилокси)азетидин-15-метил-2,2-дифенілгексанамід; іл]-5-метил-2,2-дифенілгексанової кислоти амід; 4-{1-[3-(3-Гідроксифенокси)азетидин-15-[3-(2-Хлор-3-гідроксибензилокси)азетидин-1іл]циклопентил}-2,2-дифенілбутирамід; іл]-5-метил-2,2-дифенілгексанової кислоти амід; 5-[3-(2-Фтор-3-гідроксифенокси)азетидин-1-іл]5-[3-(3,5-Дигідроксифенокси)азетидин-1-іл]-55-метил-2,2-дифенілгексанової кислоти амід; метил-2,2-дифенілгексанової кислоти амід; 5-[3-(2-Фтор-5-гідроксифенокси)азетидин-1-іл]5-[3-(3-Гідроксифенокси)азетидин-1-іл]-55-метил-2,2-дифенілгексанової кислоти амід; і метил-2,2-дифенілгексаннітрил; 5-[3-(4-Хлор-3-гідроксибензилокси)азетидин-1іл]-5-метил-2,2-дифенілгексанової кислоти амід. 17 89846 18 Винахід також стосується способів одержання групою, що відходить, такою як мезилат або тозисполуки формули (І) також як проміжних сполук лат; корисних для їх одержання. Зокрема, винахід стосується наведених нижче проміжних сполук: де А, р і А1 мають ті ж визначення, що наведені для сполук формули (І); де А і R1 мають ті ж визначення, що наведені для сполук формули (І); де R1, R2 і R3 мають ті ж визначення, що наведені для сполук формули (І) і LG є прийнятною де LG є прийнятною групою, що відходить, такою як мезилат або тозилат; і де R2 і R3 мають ті ж визначення, що наведені для сполук формули (І). Сполука формули (І) може бути одержана різноманітними способами. Наведені нижче методики ілюструють один з таких способів одержання цих сполук; спеціалісту даної галузі зрозуміло, що у практиці в рівному ступені можуть бути здійснені і інші методики. Сполуки формули (І), в якій А є можуть бути одержані згідно з описаними нижче методиками: 19 де А є , А1 і p мають ті ж визначення, що наведені для сполук формули (І), і PG представляє придатну карбоксил-захисну групу таку як метил або трет-бутил і є типово третбутилом. Сполука формули (II) є наявною у продажу. Сполуки формули (III) є або наявними у продажу, або способи їх одержання є відомими з літератури. Сполуки формули (IV) можуть бути одержані з сполук формули (II) і (III) за допомогою способу на стадії (і): сполуку (II) обробляють сполукою (III) у присутності придатної основи такої як гідроксид калію або гідроксид натрію, у прийнятному розчиннику такому як метанол, етанол або трет 89846 20 бутанол, при температурі між 25°С і підвищеною температурою протягом 6-24 годин. Типові умови передбачають 1,0 еквівалент сполуки (II), 0,05екв. гідроксиду калію і 1,0 еквівалент сполуки (III) у трет-бутанолі при температурі 25-60°С протягом 24 годин. Сполуки формули (V) можуть бути одержані з сполук формули (IV) за допомогою способу на стадії (іі). Зняття захисту з сполуки (IV) можна забезпечити, використовуючи стандартну методологію, описану у "Захисні групи в органічному синтезі" авторів T.W. Greene і P. Wutz. Коли PG є третбутилом, типові умови передбачають 1,0 еквівалент сполуки (IV) у присутності хлорводневої кислоти (4М у діоксані), у дихлорметані, при кімнатній температурі протягом до 18 годин. Сполуку формули (VI) можна одержана як розкрито у схемі 2: 21 89846 22 Схема 2 Сполуки формули (VIa) є наявними у продажу або можуть бути одержані як розкрито у схемі 2а Схема 2а де А1 і p мають ті ж визначення, що наведені для сполук формули (І). У деяких випадках, А1 може бути захищена прийнятною захисною групою. Наприклад, коли А1 містить фенол, вона може бути захищена придатною гідроксильною захисною групою. PG' представляє придатну амінозахисну групу таку як третбутоксикарбоніл (ВОС), бензилоксикарбоніл (CBz) і є типово ВОС. X представляє придатну функціональну групу таку як гідрокси, фтор, бром, хлор, йод, О-мезилат або О-тозилат і є типово гідрокси або бром. Коли PG' є ВОС, сполуки формули (VIII) і (VIlla) є наявними у продажу. Сполуки загальної формули (IX) є або наявними у продажу, відомі з літератури або можуть одержуватися як проілюстровано у схемах 3-5. Схема 3 де А1 має ті ж визначення, що наведені вище для сполук формули (І) або може бути необов'язково заміщеною. Сполуки формули (IX), де А1 має ті ж визначення, що наведені для сполук формули (І), p дорівнює 0 і X є ОН, можуть бути одержані з сполук формули (XI) реакцією оксидування БаєраВіллігера і з наступним гідролізом (спосіб на стадії (viii)). Типові умови передбачають взаємодію 1,0 еквіваленту сполуки (XI) з 3,0 еквівалентами 3хлорпероксибензойної кислоти, у прийнятному розчиннику такому як дихлорметан, при кімнатній температурі протягом 18 годин і наступну обробку цього продукту прийнятною основою такою як триетиламін, у прийнятному розчиннику такому як метанол, при кімнатній температурі протягом 18 годин. Схема 4 Сполуки формули (IX), де А1 містить прийнятно захищений фенол, p дорівнює 0 і X є ОН можуть бути одержані з сполук формули (ІХа), де А1 містить фенол, p дорівнює 0 і X є ОН, додаванням придатної фенол-захисної групи такої як бензил, за допомогою способу на стадії (іх). Типові умови передбачають взаємодію 1,0 еквіваленту сполуки (ІХа) з 1,0 еквівалентом бензилброміду і 1,0 еквівалентом придатної основи такої як карбонат цезію, у прийнятному розчиннику такому як диметилформамід, при 80°С протягом 30 хвилин. Альтернативно, сполуки формули (IX), де А1 містить прийнятно захищений фенол, p дорівнює 0 і X є ОН можуть бути одержані з сполук формули (ІХа), де А1 містить прийнятно захищений фенол, p дорівнює 0 і X є ОМе, шляхом точкового зняття захисту, використовуючи умови, описані у "Захисні групи у органічному синтезі" ("Protecting Groups in Organic Synthesis") авторів Т. W. Greene і P. Wutz. Сполуки формули (IX), де А1 містить прийнятно захищений фенол, p дорівнює 0 і X є F, можуть бути одержані з сполук формули (ІХа), де А1 містить фенол, p дорівнює 0 і X є F, шляхом додавання прийнятної фенол-захисної групи такої як метил, за допомогою способу на стадії (іх). Типові умови передбачають взаємодію 1,0 еквіваленту сполуки (ІХа) з 2,0 еквівалентами метилйодиду і 1,0 еквівалентом придатної основи такої як карбонат калію, у прийнятному розчиннику такому як тетрагідрофуран, при кімнатній температурі протягом 3 годин. Схема 5 де А1 має ті ж визначення, що наведені вище для сполук формули (І) або може бути необов'язково захищеною. Сполуки формули (ІХа), де p дорівнює 1 і X є ОН, можуть бути одержані з сполук формули (XI) шляхом відновлення альдегіду прийнятним відновлювальним агентом таким як боргідрид натрію, за допомогою способу на стадії (хі). Типові умови передбачають взаємодію 1,0 еквіваленту сполуки (XI) з 1,0 еквівалентом боргідриду натрію, у прийн 23 89846 24 ятному розчиннику такому як етанол, при кімнатній гасінням сполукою (IX), у прийнятному розчиннику температурі протягом 18 годин. Сполуки формули такому як тетрагідрофуран або диметилформамід, (XIV), де R5 представляє прийнятну кислотопри температурі між 0°С і кімнатною температузахисну групу таку як метил, етил або аліл, можуть рою, протягом 1-18 годин, за допомогою способу бути одержані з сполук формули (XIII) шляхом на стадії (vi). Типові умови передбачають 1,0 еквіприєднання придатної захисної групи такої як аліл, валент сполуки (VIII), 1,0 еквівалент гідриду натрію за допомогою способу на стадії (х). Типові умови і 1,0 еквівалент сполуки (IX), у тетрагідрофурані, передбачають взаємодію 1,0 еквіваленту сполуки при температурах 0-25°С протягом до 18 годин. (XIII) з 2,0 еквівалентами алілброміду і 2,0 еквіваСполуки формули (Ха), де p дорівнює 1, можуть лентами прийнятної основи такої як карбонат кабути одержані з сполук формули (VIIIa) і (IX), з лію, у прийнятному розчиннику такому як диметивикористанням тих ж самих умов. лформамід, при кімнатній температурі протягом 18 Сполуки формули (VI) можуть бути одержані з годин. сполук формули (X) за допомогою способу на стаСполуки формули (ІХа), де p дорівнює 1 і X є дії (vii). Зняття захисту з сполуки (X) можна забезОН, можуть бути одержані з сполук формули (XIV) печити, використовуючи стандартні методики як шляхом відновлення естеру прийнятним відновописано у "Захисні групи в органічному синтезі" люваним агентом таким як алюмінійлітійгідрид, за ("Protecting Groups in Organic Synthesis") авторів допомогою способу на стадії (хі). Типові умови T.W. Greene і P. Wutz. Коли PG' є ВОС, типові передбачають взаємодію 1,0 еквіваленту сполуки умови передбачають 1,0 еквівалент сполуки (X) у (XIV) з 2,0 еквівалентами алюмінійлітійгідриду, у присутності хлорводневої кислоти (4М у діоксані), прийнятному розчиннику такому як тетрагідрофуу дихлорметані, при кімнатній температурі протяран, при температурі від 0°С до кімнатної темпегом до 18 годин. Сполуки формули (VIa) можуть ратури протягом 5 годин. бути одержані з сполук формули (Ха) і з викорисСполуки формули (IX), де p дорівнює 1 і X є танням тих ж самих умов. галогеном, можуть бути одержані з сполук формуСполуки формули (VII) можуть бути одержані з ли (ІХа), де p дорівнює 1 і X є ОН, шляхом галогесполук формул (V) і (VI) або (VIa) за допомогою нування первинного спирту, використовуючи приспособу на стадії (ііі), шляхом конденсування (V) і йнятний реагент такий як тіонілхлорид, (VI) або (VIa) у присутності прийнятного конденсудибромтрифенілфосфоран або йод плюс трифенівального агента такого як гідрохлорид 1-(3лфосфін, переважно тіонілхлорид або дибромтдиметиламінопропіл)-3-етилкарбодііміду, Ν,Ν'рифенілфосфоран, у прийнятному розчиннику карбонілдіімідазол, Ν,Ν'-дициклогексилкарбодіімід, такому як дихлорметан або ацетонітрил, за допонеобов'язково у присутності каталізатора такого як могою способу на стадії (хіі). Коли X є бромом, гідрат 1-гідроксибензотриазолу або 1-гідрокси-7Типові умови передбачають взаємодію 1,0 еквіваазабензотриазолу і необов'язково у присутності ленту сполуки (ІХа) з 1,0 еквівалентом дибромттретинної амінної основи такої як Nрифенілфосфорану, у прийнятному розчиннику метилморфолін, триетиламін або Ν,Νтакому як ацетонітрил, при кімнатній температурі діізопропілетиламін, у прийнятному розчиннику протягом 18 годин. Коли X є хлором, Типові умови такому як Ν,Ν-диметилформамід, тетрагідрофуран передбачають взаємодію 1,0 еквіваленту сполуки або диметилсульфоксид, при температурі навко(ІХа) з 2,5 еквівалентами тіонілхлориду у дихлорлишнього середовища протягом 1-48 годин. Типові метані при кімнатній температурі протягом 10 хвиумови передбачають 1,0 еквівалент сполуки (V), лин. 1,0 еквівалент сполуки (VI) або (VIa) і 1,0-1,2 еквіСполуки формули (X), де p дорівнює 0, можуть валенти гідрохлориду 1-(3-диметиламінопропіл)-3бути одержані з сполук формул (VIII) і (IX), де X є етилкарбодііміду, 1,0-1,2 еквіваленти гідрату 1ОН і p дорівнює 0, за допомогою реакції Міцунобу гідроксибензотриазолу і 1,0-1,2 еквіваленти триеміж сполуками (VIII) і (IX) у присутності прийнятнотиламіну у дихлорметані, при кімнатній темпераго фосфіну такого як три-nбутилфосфін або тритурі протягом 18 годин. фенілфосфін і прийнятної азо сполуки такої як Сполуки формули (Іа) можуть бути одержані з діетилазодикарбоксилат, діізопропілазодикарбоксполук формули (VII) за допомогою способу на силат або ди-трет-бутилазодикарбоксилат, у розстадії (iv). Сполуку (Іа) можна одержати способом чиннику такому як дихлорметан, тетрагідрофуран аналогічним до способів описаних у Denton і Wood або Ν,Ν-диметилформамід, при температурах між (Synlett, 1999, 1, 55); Сполуку (VII) типово попере25-115°С, протягом 1-48 годин, за допомогою сподньо активували за допомогою прийнятної кислоти собу на стадії (νί). Типові умови передбачають 1,0 Льюіса такої як хлорид титану або хлорид циркоеквівалент сполуки (VIII), 1,0 еквівалент сполуки нію, потім обробляли надлишком прийнятного ме(IX) 1,0-1,2 еквіваленти трифенілфосфіну і 1,0-1,2 талоорганічного реагенту такого як МеMgСІ або еквіваленти діізопропілазодикарбоксилату, у тетМеMgBr, у прийнятному розчиннику такому як тетрагідрофурані, при 25°С протягом до 18 годин. рагідрофуран або діетиловий етер, при темпераСполуки формули (Ха), де p дорівнює 0, можуть турі у проміжку від -78°С до 25°С, протягом 1-18 бути одержані з сполук формули (VIIIa) і (IX), з годин. Типові умови передбачають 1,0 еквівалент використанням тих ж самих умов. сполуки (VII), 2 еквіваленти хлориду цирконію і 9,0 Сполуки формули (X), де p дорівнює 1, можуть еквівалентів МеMgСІ у тетрагідрофурані, при бути одержані з сполук формул (VIII) і (IX), де X є 30°С протягом 4-8 годин. галогеном і p дорівнює 1, шляхом обробки сполуки Сполуки формули (Іb) можуть бути одержані з (VIII) прийнятною сильною основою такою як гідсполук формули (Іа) шляхом гідролізу сполуки (Іа) рид натрію або трет-бутоксид калію з наступним надлишком гідроксиду калію у 3-метил-3 25 89846 26 пентанолі, при підвищеній температурі протягом Ще у одному втіленні, коли p дорівнює 1, сподо 24 годин (спосіб на стадії (ν)). Типові умови пелуки формули (І) можуть бути потім модифіковані, редбачають 1,0 еквівалент сполуки (Іа) і 20 еквівазабезпечуючи сполуки формули (Іс), як описано у лентів гідроксиду калію у 3-метил-3-пентанолі при схемі 6 підвищеній температурі протягом до 24 годин. Схема 6 в якій А є i R2 і R3 є метилом. Сполуки формули (XV) можуть бути одержані з сполук формули (І), де p дорівнює 1, за допомогою способу на стадії (хііі). Коли R1 є CN, відщеплення бензилетерної групи типово досягали шляхом обробки сполуки (І) надлишком хлориду заліза (III), у прийнятному розчиннику такому як дихлорметан, при температурі навколишнього середовища протягом 1-8 годин, одержуючи сполуки формули (XV). Коли R1 є CONH2, обробкою сполуки (І) газоподібним воднем, у присутності придатного каталізатора гідрування такого як 20% Pd(OH)2 або 10% Pd/C, необов'язково у присутності придатної кислоти такої як хлорводнева кислота, у прийнятному розчиннику такому як метанол, етанол або тетрагідрофуран, при підвищеній температурі протягом 1-18 годин, одержують сполуки формули (XV). Сполуки формули (Іс), де p дорівнює 0, можуть бути одержані з сполук формули (XV) і сполук формули (IX), де p дорівнює 0 і X є ОН, за допомогою способу на стадії (xiv) - використовуючи умови описані на стадії (vi). Сполуки формули (Іс), де p дорівнює 0, можуть бути одержані з сполук формули (XV) і сполуки формули (IX), де p дорівнює 0 і X є F, за допомо гою способу на стадії (xiv)-обробкою сполуки (XV) придатною сильною основою такою як гідрид натрію або трет-бутоксид калію з наступним гасінням сполукою (IX), у прийнятному розчиннику такому як тетрагідрофуран або Ν,Ν-диметилформамід, при температурі між 0°С і підвищеною температурою, протягом 1-96 годин. Типові умови передбачають 1,0 еквівалент сполуки (XV), від 1,0 до 2,0 еквівалентів гідриду натрію і 1,0 еквівалент сполуки (IX) у Ν,Ν-диметилформаміді, при температурах 0-60°С протягом 18-96 годин. Сполуки формули (Іс), де p дорівнює 1, можуть бути одержані з сполук формули (XV) і сполуки формули (IX), де p дорівнює 1 і X є СІ, Br, І, Омезилатом або О-тозилатом, за допомогою способу на стадії (xiv), обробкою сполуки (XV) придатною сильною основою такою як гідрид натрію або трет-бутоксид калію з наступним гасінням сполукою (IX), у прийнятному розчиннику такому як тетрагідрофуран або Ν,Ν-диметилформамід, при температурі між 0°С і підвищеною температурою, протягом 1-96 годин. Типові умови передбачають 1,0 еквівалент сполуки (XV), від 1,0 до 2,0 еквівалентів гідриду натрію і 1,0 еквівалент сполуки (IX), у Ν,Ν-диметилформаміді, при температурах 060°С протягом 18-96 годин. Ще у одному втіленні, сполуки формули (І) можуть бути потім модифіковані, з одержанням сполук формули (Id), як описано у схемі 7: Схема 7 де А є . Сполуки формули (Id), де А1 представляє феніл, заміщений фенілом, необов'язково заміщеним ОН, можуть бути одержані з сполук формули (І), де А1 є фенілом, заміщеним СІ, Br або І, за допомогою способу на стадії (xv), реакції кондесування Сузукі з сполукою (XXX) у прийнятному розчиннику такому як 1,4-діоксан або тетрагідрофуран, у присутності води, придатної основи такої як карбонат натрію або карбонат цезію і паладієвого каталізатора такого як хлорид [1,1'біс(дифенілфосфін)фероцен]паладію (II) або тетракис(трифенілфосфін)паладію(0). Реакції конденсування Сузукі можуть бути проведені як описано в літературі: Suzuki, A. Pure & Appl. Chem. 1985, 57, 1749 і посиланнях, що там містяться; Angew. Chem. Int. Ed. 2002, 41, 4176 і посиланнях, 27 89846 28 що там містяться. Типові умови передбачають 1,0 умови передбачають 1,0 еквівалент сполуки (Іс) еквівалент сполуки (І), 2,0 еквіваленти сполуки або (Id), де R1 є CN і 20 еквівалентів гідроксиду (XXX), 2,0 еквіваленти карбонату натрію і 0,05 еккалію у 3-метил-3-пентанолі при кип'ятінні із звовівалентів паладієвого каталізатора у тетрагідроротним холодильником протягом до 24 годин. фурані і воді, при підвищеній температурі протяСполуки формули (І), де А є гом до 16 годин. Сполука (XVI) є або наявною у продажу або може бути одержана за допомогою способів описаних в літературі. Сполуки формули (Іс) і (Id), де R1 є CONH2, також можуть бути одержані з сполук формули (Іс) і можуть бути одержані згідно з наведеними (Id), де R1 є CN, шляхом гідролізу з надлишком нижче методиками: гідроксиду калію у 3-метил-3-пентанолі, при підвищеній температурі протягом до 24 годин. Типові Схема 8 де LG представляє прийнятну групу, що відходить, таку як мезилат або тозилат і є переважно мезилатом. Сполуки формули (XVI) можуть бути одержані способами як описано у WO2003037327, сторінка 83. PG''' представляє захисну групу таку як третбутоксикарбоніл або бензилоксикарбоніл і є переважно трет-бутоксикарбонілом. Альтернативно, сполуки формули (XVI) можуть бути одержані згідно з наступним способом: 29 Сполуки формули (XVIc) є наявними у продажу або відомими у літературі. Сполуки формули (XVIb) можуть бути одержані з сполук формули (XVIc) за допомогою реакції сполуки (XVIc) з хлорсульфонілізоціанатом, мурашиною кислотою і піридином, у прийнятному розчиннику такому як дихлорметан, при низькій температурі протягом 2 годин (спосіб на стадій (ххі)). Типові умови передбачають 1,0 еквівалент сполуки (XVIc), 1,5 еквіваленти хлорсульфонілізоціанату, 1,5 еквіваленти мурашиної кислоти і 1,5 еквіваленти піридину у дихлорметані, при низькій температурі протягом 2 годин. Сполуки формули (XVIa) можуть бути одержані з сполук формули (XVIb) за допомогою реакції сполуки (XVIb) з оксидом магнію, йодбензолдіацетатом і димером ацетату родію у прийнятному розчиннику такому як дихлорметан при кімнатній температурі протягом до 24 годин (стадія способу (ххіі)). Типові умови передбачають взаємодію 1,0 еквіваленту сполуки (XVIb), 2,3 еквівалентів діоксиду магнію, 1,1 еквівалентів йодбензолдіацетату і 0,02 еквівалентів димеру ацетату родію у дихлорметані при кімнатній температурі протягом 18 годин. Сполуки формули (XVI) можуть бути одержані з сполук формули (XVIa) шляхом введення придатної захисної групи такої як трет-бутоксикарбоніл або бензилоксикарбоніл, переважно третбутоксикарбоніл, при використанні умов описаних у "Захисні групи в органічному синтезі" ("Protecting Groups in Organic Synthesis") авторів Т. W. Greene і P. Wutz. Типові умови передбачають взаємодію 1,0 еквіваленту сполуки (XVIa), 1,2 еквівалентів ди-трет-бутилдикарбонату, 2,0 еквівалентів триетиламіну і 0,2 еквівалентів 4диметиламінопіридину у дихлорметані, при кімнатній температурі протягом 3 годин. Сполуки формули (XVII) можуть бути одержані з сполук формули (II) і сполук формули (XVI) за допомогою способу на стадії (xvi) 1) Шляхом взаємодії сполуки (II) і (XVI) у присутності сильної основи такої як трет-бутоксид калію або гідрид натрію, у прийнятному розчиннику такому як Ν,Ν-диметилформамід або диметилсульфоксид, при температурі навколишнього середовища або при підвищеній температурі протягом до 18 годин. 2) Шляхом видалення захисної групи (якщо вона використовується), використовуючи прийнятні умови такі як 4Ν хлорводнева кислота у діоксані або трифтороцтова кислота або гідрування у присутності паладієвого каталізатора, як описано у "Захисні групи в органічному синтезі" ("Protecting 89846 30 Groups in Organic Synthesis") авторів T.W. Greene і P. Wutz. Типові умови передбачають 1,2 еквіваленти сполуки (II), 1,0 еквівалент сполуки (XVI) і 1,2 еквівалентів трет-бутоксиду калію у Ν,Νдиметилформаміді, при температурі навколишнього середовища, протягом до 18 годин, з наступною обробкою 4N хлорводневою кислотою у діоксані. Сполуки формули (XVIII) є наявними у продажу. Сполуки формули (XIX) можуть бути одержані з сполук формули (XVII) і (XVIII) за допомогою способу на стадії (xvii) - утворення гетероциклу може бути досягнуте шляхом нуклеофільного приєднання сполуки (XVIII), використовуючи сполуку (XVII) з наступним in situ закриттям циклу, у прийнятному розчиннику такому як метанол або етанол, при підвищеній температурі протягом до 48 годин. Типові умови передбачають 1,0 еквівалент сполуки (XVII) і 1,1 еквіваленти сполука (XVIII) у метанолі, при підвищеній температурі протягом до 48 годин. Сполуки формули (XX) можуть бути одержані з сполук формули (XIX) за допомогою способу на стадії (xviii) - шляхом введення прийнятної групи, що відходить (LG), такої як мезилатні або тозилатні групи за допомогою реакції сполуки (XIX) з мезилхлоридом/ангідридом або тозилхлоридом, у присутності придатної основи такої як основа Хюніга, триетиламін або піридин, необов'язково у прийнятному розчиннику такому як дихлорметан або діетиловий етер, при низькій температурі протягом 1-2 годин. Типові умови передбачають 1,0 еквівалент сполуки (XIX) і 3 еквіваленти мезилхлориду у піридині при низькій температурі протягом до 1-2 годин. Сполуки загальної формули (XXI) є або наявними у продажу або є відомими у літературі. Сполуки формули (XXI), що містять фенольну групу, можуть бути захищені шляхом додавання придатної фенол-захисної групи такої як аліл. Типові умови передбачають взаємодію 1,0 еквіваленту сполуки (XXI), що містить фенол з 1,0 еквівалентом алілброміду і 1,0 еквівалентом придатної основи такої як карбонат калію, у прийнятному розчиннику такому як диметилформамід, при кімнатній температурі протягом 18 годин. Альтернативно, сполуки формули (XXI) можуть бути одержані шляхом точкового зняття захисту біс-захищеного фенолу, при використанні умов описаних у "Захисні групи в органічному синтезі" ("Protecting Groups in Organic Synthesis") авторів Т. W. Greene і P. Wutz. Сполуки формули (Іе) можуть бути одержані з сполук загальної формули (XX) і (XXI) шляхом об 31 89846 32 робки сполуки (XXI) прийняітною основою такою як пературі протягом до 24 годин (стадія (хх) спосокарбонат цезію або карбонат натрію з наступним бу). Типові умови передбачають 1,0 еквівалент гасінням сполукою (XX), у прийнятному розчиннику сполуки (Іе) і 20 еквівалентів гідроксиду калію у 3такому як Ν,Ν-диметилформамід або диметилсуметил-3-пентанолі при підвищеній температурі льфоксид, при підвищеній температурі протягом протягом до 24 годин. до 18 годин (стадія (хіх) способу). Типові умови Альтернативно сполуки формули (І), де А є передбачають 1,0 еквівалент сполуки (XX), 3,0 еквіваленти карбонату цезію і 3,0 еквіваленти сполуки (XXI), у Ν,Ν-диметилформаміді, при підвищеній температурі протягом до 18 годин. Ще у одному втіленні, сполуки формули (If) і R2 і R3 є метилом, можуть бути одержані як можуть бути одержані з сполук формули (Іе) шляописано у схемі 9. хом гідролізу сполуки (Іе) з надлишком гідроксиду калію у 3-метил-3-пентанолі, при підвищеній тем Схема 9 в якій LG представляє прийнятну групу, що відходить таку як мезилат або тозилат і є переважно мезилатом. Сполуки загальної формули (V) можуть бути одержані як описано у WO97/24325. Сполуки формули (XXII) можуть бути одержані з сполук загальної формули (V) за допомогою способу на стадії (xxiv): карбонова кислота (V) може бути оброблена придатним хлорувальним засобом таким як тіонілхлорид або оксалілхлоридом, у прийнятному розчиннику такому як Ν,Ν-диметилформамід, ацетонітрил або дихлорметан, при температурі навколишнього середовища протягом до 8 годин. Типові умови передбачають 1,0 еквівалент сполуки (V) і 2 еквіваленти оксалілхлориду у Ν,Ν диметилформаміді, при кімнатній температурі протягом 2 годин. Сполуки формули (XXIII) можуть бути одержані як описано у J. Org. Chem. 1991, 56, 6729-30. Сполуки загальної формули (XXIV) можуть бути одержані з сполук загальної формули (XXII) і (XXIII) за допомогою способу на стадії (xxv): сполуку (XXII) піддавали нуклеофільному заміщенню сполукою (XXIII), у присутності третинної амінної основи такої як N-метилморфолін, триетиламін або Ν,Ν-діізопропілетиламін, у прийнятному розчиннику такому як Ν,Ν-диметилформамід, тетрагідрофуран або дихлорметан, при низькій температурі протягом 1-8 годин. Типові умови передбачають 1 еквівалент сполуки (XXII), 1 еквівалент сполуки (XXIII) і 3 еквіваленти триетиламі 33 89846 34 ну у дихлорметані, при низькій температурі протягом 1 години. Сполуки загальної формули (XXV) можуть бути одержані з сполук загальної формули (XXIV) і (XXI) за допомогою способу на стадії (xxvi), з використанням умов, описаних для стадії (хіх) у схемі 8. яка є наявною у продажу або відома з літераСполуки формули (Іе) можуть бути одержані з тури. сполук формули (XXV), з використанням умов, Типові умови для стадії (ііі) передбачають 1,0 описаних для стадії (iv) схеми 1. еквівалент сполуки (V), 1,2 еквіваленти сполуки Сполуки формули (If) можуть бути одержані з (Vlb), 1,0-1,2 еквіваленти гідрохлориду 1-(3сполук формули (Іе), з використанням умов, опидиметиламінопропіл)-3-етилкарбодііміду, 1,0-1,2 саних для стадії (хх) схеми 8. еквіваленти гідрату 1-гідроксибензотриазолу і 2,5 Альтернативно, сполуки формули (І) можуть еквіваленти Ν,Ν-діізопропілетиламіну у дихлормебути одержані як описано у схемі 1, використовуютані, при кімнатній температурі протягом 18 годин. чи проміжну сполуку формули (Vlb) Альтернативно, сполука формули (Іе), де p дорівнює 1, може бути одержана як описано у схемі 10: Схема 10 в якій p дорівнює 1 і hаl представляє галоген і є типово хлором або бромом, переважно хлором. Сполука формули (XXVI) може бути одержана як описано у схемі 5. Сполуки загальної формули (Іе) можуть бути одержані з сполук загальних формул (XIX) і (XXVI) шляхом обробки сполуки (XIX) прийнятною сильною основою такою як гідрид натрію або трет-бутоксид калію з наступним гасінням сполукою (XXVI), у прийнятному розчиннику тако му яктетрагідрофуран, при температурі між 0°С і кімнатною температурою, протягом 1-8 годин. Типові умови передбачають 1,0 еквівалент сполуки (XIX), 1,2 еквіваленти гідриду натрію і 1,5 еквіваленти сполуки (XXVI), у тетрагідрофурані, при температурах 0-25°С протягом до 1-2 годин. Альтернативно, сполуки формули (If) можуть бути одержані як описано у схемі 11. Схема 11 в якій Гал представляє гало і є типово хлором або бромом, переважно хлором. Сполуки формули (XXVII) одержували з сполуки формули (If), де А1 представляє феніл і р=1, шляхом видалення бензилової групи, використовуючи стандартні умови гідрування, як описано у "Захисні групи в органічному синтезі" ("Protecting Groups in Organic Synthesis"), авторів Т. W. Greene і P. Wutz. Сполуки формули (If) одержували з сполук формули (XXVII) і сполук формули (XXVI), використовуючи умови описані для стадії (ххіх). Альтернативно, сполуки формули (If) можуть бути одержані як описано у схемі 12. 35 Схема в якій LG представляє прийнятну групу, що відходить таку як мезилат або тозилат і є переважно мезилатом. Сполуки формули (XXVIII) можуть бути одержані з сполук формули (XXVII) за допомогою способу на стадії (xviii), як описано у схемі 8. Сполуки формули (If) можуть бути одержані з сполук формули (XXVIII) і сполук формули (XXI) за допомогою способу на стадії (хіх), як описано у схемі 8. Коли А1 містить прийнятно захищений фенол, сполуки формули (І) піддавали зняттю захисту, одержуючи відповідний фенол. Прийнятні захисні групи (Pg'') включають метил, бензил, аліл і третбутилдиметилсиліл (TBDMS). Зняття захисту можна здійснити, використовуючи стандартну методику як описано у "Захисні групи в органічному синтезі" ("Protecting Groups in Organic Synthesis") авторів T.W. Greene і P. Wutz. Коли Pg'' є метилом, Типові умови цієї процедури передбачають 1,0 еквівалент захищеної сполуки формули (І) і 1-4 еквіваленти 1М трибоміду бору у дихлорметані, у прийнятному розчиннику такому як дихлорметан, при температурі навколишнього середовища, протягом 1-18 годин. Коли Pg'' є алілом, Типові умови цієї процедури передбачають 1,0 еквівалент захищеної сполуки формули (І) і 20 еквівалентів гідроксиду калію у 3-метил-3-пентанолі при кип'ятінні із зворотним холодильником протягом 1-24 годин, з наступним відокремленням залишку і обробкою хлорводневою кислотою (4М у діоксані), у воді, при 60°С, протягом 20 хвилин. Альтернативні умови цієї процедури містять 1,0 еквівалент захищеної сполуки формули (І), 6 еквівалентів боргідриду натрію і 0,1 еквівалентів тетракис(трифенілфосфін)паладію(0) у тетрагідрофурані при підвищеній температурі протягом 30 хвилин. Коли Pg'' є TBDMS, Типові умови цієї процедури передбачають 1,0 еквівалент захищеної сполуки формули (І) і 10 еквівалентів фториду амонію у метанолі і воді при 50°С протягом 18-24 годин. Фармацевтично прийнятні солі сполук формули (І) включають їх кислотно-адитивні і основні солі. Придатні кислотно-адитивні солі утворюються з кислот, які утворюють нетоксичні солі. Приклади солей включають ацетат, адипат, аспартат, бензоат, безилат, бікарбонат/карбонат, бісульфат/сульфат, борат, камсилат, цитрат, цикламат, едизилат, езилат, форміат, фумарат, глуцептат, глюконат, глюкуронат, гексафторфосфат, гібензат, гідрохлорид/хлорид, гідробромід/бромід, гідройодид/йодид, ізетіонат, лактат, малат, малеат, мало 89846 36 12 нат, мезилат, метилсульфат, нафтилат, 2напсилат, нікотинат, нітрат, оротат, оксалат, пальмітат, памоат, фосфат/гідрофосфат/дигідрофосфат, піроглутамат, сахарат, стеарат, сукцинат, танат, тартрат, тозилат, трифторацетат і ксинафоат. Придатні основні солі одержують з основ, які утворюють нетоксичні солі. Приклади включають солі алюмінію, аргініну, бензатину, кальцію, холіну, діетиламіну, діоламіну, гліцину, лізину, магнію, меглуміну, оламіну, калію, натрію, трометаміну і цинку. Також можуть бути одержані гемісолі кислот і основ, наприклад, гемісульфатні і гемікальцієві солі. Для ознайомлення з придатними солями, див. Handbook of Pharmaceutical Salts: Properties, Selection, and Use авторів Stahl і Wermuth (WileyVCH, 2002). Фармацевтично прийнятні солі сполук формули (І) можна одержати за допомогою одного або декількох з трьох способів: (і) за допомогою взаємодії сполуки формули (І) з бажаною кислотою або основою; (іі) шляхом видалення кислото- або основонестійкої захисної групи з придатного попередника сполуки формули (І) або шляхом розмикання циклу придатного циклічного попередника, наприклад, лактону або лактаму, використовуючи бажану кислоту або основу; або (ііі) шляхом перетворення однієї солі сполуки формули (І) в іншу за допомогою реакції з прийнятною кислотою або основою, або використовуючи придатну іонообмінну колонку. Всі три реакції типово проводять у розчині. Одержану сіль можна осаджувати і збирати фільтруванням або отримувати випаровуванням розчиника. Ступінь іонізації одержаної солі може змінюватися від повністю іонізованої до майже не іонізованої. Сполуки винаходу можуть існувати у діапазоні твердих станів, починаючи з повністю аморфного до повністю кристалічного. Термін "аморфний" відповідає стану, в якому у матеріалі на молекулярному рівні відсутній дальній порядок і, залежно від температури, може проявляти фізичні властивості твердого тіла або рідини. Типово такі матеріали не дають характерних рентгенограм і, проявляючи властивості твердого тіла, більш формально можуть бути описані як рідина. При нагріванні відбувається перехід з твердого у рідкий стан з відповідною зміною властивостей, типово другого порядку ("склування"). Термін "кристалічний" відповідає твердому стану, в якому матеріал на молекулярному рівні має регулярну впорядко 37 89846 38 вану структуру і дає характерну картину дифракції ють іонну (такі як - COO Na+, - COO K+, або - SO3 рентгенівських променів (рентгенограму) з визнаNa+) або неіонну (такі як - N N+(CH3)3) групу з поченими дифракційними піками. Такі матеріали при лярною головкою. Більша кількість інформації назначному нагріванні також демонструють властиведена у Crystals and Polarizing Microscope, автовості рідини, зміна твердого стану рідким характерів N. Η. Hartshorne і Α. Stuart, 4th Edition (Edward ризується фазовим переходом, типово першого Arnold, 1970). порядку ("температура плавлення"). В подальшому, всі посилання на сполуки фоСполуки винаходу можуть існувати як у несормули (І) включають також посилання на їх солі, льватованій, так і у сольватованій формах. Термін сольвати, багатокомпонентні комплекси і рідкі кри"сольват" використовується у межах даного винастали їх солей. ходу для опису молекулярного комплексу, що місСполуки винаходу включають сполуки формутить сполуку винаходу і одну або більше молекул ли (І), як це було визначено вище, їх поліморфи і фармацевтично прийнятного розчинника, наприкристалічні форми, проліки, і ізомери (включаючи клад, етанолу. Термін "гідрат" використовується, оптичні і геометричні ізомери і таутомерні форми), коли згаданим розчинником є вода. як це визначено далі і мічені ізотопами сполуки Існуюча система класифікації органічних гідраформули (І). тів визначає наступні: окремо розташовані вузли, Також в межах рамок винаходу знаходяться канальні або координовані навколо іону металу так звані "проліки" сполук формули (І). Таким чигідрати - див. Polymorphism in Pharmaceutical ном, деякі похідні сполук формули (І), які самі по Solids, автора K. R. Morris (Ed. Η. G. Brittain, Marcel собі мають малу або не мають зовсім фармаколоDekker, 1995). В гідратах з окремо розташованими гічної активності, при введенні в або нанесенні на вузлами, молекули води відокремлені одна від тіло можуть перетворюватися у сполуки формули одної розташованими між ними органічними моле(І), що мають бажану активність, наприклад, шлякулами. В канальних гідратах молекули води знахом гідролітичного розщеплення. Такі похідні відходяться в каналах кристалічної ґратки, поруч із носяться до "проліків". Додаткову інформацію по іншими молекулами води. У гідратах координовавикористанню проліків можна знайти в "Pro-drugs них навколо іону металу, молекули води зв'язані з as Novel Delivery Systems. Vol. 14, ACS Symposium іоном металу. Series (T Higuchi і W Stella) і "Bioreversible Carriers Коли розчинник або вода є міцно зв'язаними, in Drug Design". Pergamon Press, 1987 (ed. Ε Β комплекс незалежно від вологості має чітко визнаRoche, American Pharmaceutical Association). чену стехіометричну будову. Однак, коли розчинЯк вказується, так звані "проліки" сполук форник або вода зв'язані слабко, як у канальних сольмули (І) також включаються в межі винаходу. Таватах і гігроскопічних сполуках, вміст ким чином, деякі похідні сполук формули (І), які води/розчинника залежатиме від вологості або можуть мати малу або немати зовсім фармаколоумов висушування. У таких випадках відхилення гічної активності можуть, коли вводяться в оргавід стехіометрії є нормою. нізм або на тіло, перетворюватися в сполуки форТакож включеними у межі винаходу є багатомули (І), що мають бажану активність, наприклад, компонентні комплекси (ті, що не є солями або шляхом гідролітичного розщеплення. Такі похідні сольватами), де лікарська сполука і щонайменше відносяться до "проліків". Додаткову інформацію один додатковий компонент присутні у стехіометпо використанню проліків можна знайти в Proричній або нестехіометричній кількості. Комплекси drugs as Novel Delivery Systems. Vol. 14, ACS цього типу включають клатрати (сполуки включенSymposium Series (T. Higuchi and W. Stella) і ня лікарський засіб-хазяїн) і співкристали. Останні Bioreversible Carriers в Drug Design. Pergamon типово визначають як кристалічні комплекси, Press, 1987 (ed. Ε. Β Roche, American складовими яких є нейтральні молекули, зв'язані Pharmaceutical Association). разом шляхом нековалентних взаємодій, або це Проліки у відповідності з винаходом можуть, також може бути комплекс нейтральної молекули з наприклад, бути одержані шляхом заміни прийнясіллю. Співкристали можуть бути одержані кристатних функціональних груп, присутніх в сполуці фолізацією розплаву, перекристалізацією з розчиннирмули (І), деякими замісниками відомими фахівків або шляхом сумісного розтирання компонентів цям в цій галузі як 'про-замісники' як описується, - див. Chem Commun, 17, 1889-1896, авторів О. наприклад, в Design of Prodrugs. автора Η. Almarsson і М. J. Zaworotko (2004). Загальний Bundgaard (Elsevier, 1985). огляд багатокомпонентних систем дивіться у J Деякими прикладами проліків у відповідності з Pharm Sci, 64 (8), 1269-1288, авторів Haleblian винаходом є: (August 1975). (і) коли сполука формули (І) містить карбоксиУ придатних умовах сполуки винаходу також льну групу (-СООН), її естер, наприклад, сполука, можуть існувати у мезоморфному стані (мезофаза в якій водень карбонової кислоти сполуки формуабо рідкокристалічний стан). Мезоморфний стан є ли (І) замінений (С1-С8)алкілом; проміжним між справжнім кристалічним і справж(іі) коли сполука формули (І) містить спиртову нім рідким станом (розплав або розчин). Мезомогрупу (-ОН), її етер, наприклад, сполука, в якій ворфізм, що виникає в результаті змни температури день спиртової групи сполуки формули (І) заміненазивають "термотропним", а той, що виникає при ний (С1-С6)алканоїлоксиметилом; і додаванні іншого компонента, такого як вода або (ііі) коли сполука формули (І) містить первинну інший розчинник, - "ліотропним". Сполуки, що моабо вторинну аміногрупу (-NH2 або - NHR, де R Н), жуть утворювати ліотропні фази називаються її амід, наприклад, сполука, в якій, в залежності від "амфіфільними" і складаються з молекул, що ма 39 89846 40 обставин, одна або обидві водні аміногрупи сполувипадку, коли сполука формули (І) містить кислотки формули (І) є заміненою(и) (С1-С10)алканоїлом. ний або основний замісник, кислотою або осноІнші приклади заміщувальних груп у відповідвою, такою як 1-фенілетиламін або винна кислота. ності із згаданими вище прикладами і прикладами Одержану діастереомерну суміш можна розділити інших типів проліків можна знайти в наведених використовуючи хроматографію і/або фракційну вище посиланнях. кристалізацію і один або обидва діастереоізомери Однак, деякі сполуки формули (І) можуть самі перетворювали у відповідний чистий енантіопо собі виступати як проліки інших сполук формумер(и) способами, добре відомими фахівцю в цій ли І. галузі. Також в межі винаходу включені метаболіти Хіральні сполуки винаходу (і їх хіральні попесполук формули (І), що є сполуками, які утворюредники) можна одержати в енантіомернозбагачеються in vivo після введення лікарського засобу. ній формі, використовуючи хроматографію, типово Деякими прикладами метаболітів згідно з винахоВЕРХ, на асиметричній смолі з рухомою фазою, дом є: що містить вуглеводень, типово гептан або гексан, (і) коли сполука формули (І) містить метильну що містить від 0 до 50 об'ємних % ізопропанолу, типово від 2% до 20% і від 0 до 5 об'ємних % алкігрупу, її гідроксиметильне похідне (-СН3 -СН2ОН): ламіну, типово 0,1% діетиламіну. Концентрування (іі) коли сполука формули (І) містить алкоксигелюенту надає збагачену суміш. рупу, її гідроксипохідне (-OR -ОН); Коли кристалізується будь-який рацемат, мо(ііі) коли сполука формули (І) містить третинну жливе утворення кристалів двох типів. Перший тип аміногрупу, її вторинний амін (-NR1R2 -NHR1 або представляє собою описану вище рацемічну споNHR2); луку (справжній рацемат), коли утворюються гомо(iv) коли сполука формули (І) містить вторинну генні кристали однієї форми, які містять обидва аміногрупу, її первинне похідне (-NHR1 -NH2); енантіомери в еквімолярних кількостях. Другий тип (ν) коли сполука формули (І) містить фенільпредставляє собою рацемічну суміш або конглоний замісник, її фенольне похідне (-Рh PhOH); і мерат, коли в еквімолярних кількостях утворюють(vi) коли сполука формули (І) містить амідну ся дві форми кристалів, кожен з яких складається групу, похідне карбонової кислоти (з одного енантіомера. CONH2 СООН). Хоча обидві кристалічні форми, присутні у раСполуки формули (І), що містять один або децемічній суміші, мають однакові фізичні властивокілька асиметричних атомів вуглецю можуть існусті, вони можуть відрізнятися від фізичних властивати як два або більше стереоізомерів. Коли сповостей справжнього рацемату. Рацемічні суміші лука формули (І) містить алкенільну або можна розділити за допомогою звичайних методик алкеніленову групу, можлива геометрична відомих фахівцю в цій галузі - дивіться, наприклад, цис/транс (або Z/E) ізомерія. Коли структурний Stereochemistry of Organic Compounds, автора Ε L ізомеризм є взаємозмінюваним завдяки низькій EIiel (Wiley, 1994). енергії бар'єру, може мати місце таутомерний ізоПредставлений винахід включає всі фармацемеризм ("таутомеризм"). Це може мати місце у втично прийнятні мічені ізотопами сполуки формуформі протонової таутомерії в сполуках формули ли (І), в яких один або декілька атомів замінені (І), що містять, наприклад, іміно, кето або оксимну атомами, що мають те ж саме атомне число, але групу, або так званий валентний таутомеризм в атомну масу або масове число, що відрізняється сполуках, які містять ароматичний замісник. Звідси від атомної маси або масового числа, які домінувипливає, що одна сполука може проявляти більють в природі. ше ніж один тип ізомеризму. Прикладами ізотопів для включення в сполуки Включеними в межі представленого винаходу винаходу є ізотопи водню такі як 2Н і 3Н, вуглецю є всі стереоізомери, геометричні ізомери і таутотакі як 11С, 13С і 14С, хлору такі як 36СІ, фтору такі мерні форми сполук формули І, включаючи сполуяк 18F, йоду, такі як 123І і 125І, азоту такі як 13N і 15N, ки, що проявляють більше ніж один тип ізомеризму кисню такі як 15O, 17О і 18О, фосфору такі як 32Р і і суміші одного або декількох. Також включеними є сірки такі як 35S. кислотно-адитивні солі або основні солі, в яких Деякі мічені ізотопами сполуки формули І, напротиіон є оптично-активним, наприклад, d-пакгат приклад, ті що включають радіоактивний ізотоп, є або l-лізин, або рацемічним, наприклад, dl-тартрат корисними в дослідженнях лікарського засобу і/або або dl-аргінін. розподілення субстрату в тканині. Радіоактивні Цис/транс ізомери можуть бути розділені за ізотопи трітію, тобто 3Н, і вуглецю-14, тобто 14С, є допомогою загальновідомих методик, добре відоособливо корисними для цих цілей з огляду на мих фахівцю в цій галузі, наприклад, хроматогралегкість їх включення і легкість виявлення. Заміфії і фракційної кристалізації. щення більш важкими ізотопами, такими як дейтеЗагальновідомі методики для одержанрій, тобто 2Н, може давати деякі терапевтичні пеня/виділення окремих енантіомерів включають реваги внаслідок збільшення метаболітичної хіральний синтез з придатного оптично чистого стабільності, наприклад, збільшення in vivo часу попередника або розділення рацемату (або раценапіврозкладу або зменшення необхідної дози, і мату солі або похідного) використовуючи, напризвідси може бути переважним в деяких випадках. клад, хіральну високоефективну рідинну хроматоЗаміщення позитрон емітуючими ізотопами таграфію (ВЕРХ). кими як 11С, 18F, 15O і 13N, може бути корисним в Альтернативно, рацемат (або рацемічний подослідженнях позитронноемісійної топографії передник) може реагувати з придатною оптичноактивною сполукою, наприклад, спиртом, або, у 41 89846 42 (PET) для визначення блокування рецептора субСполуки, згідно з винаходом, можуть вводитистратом. ся пероральним шляхом. Пероральне введення Мічені ізотопами сполуки формули (І) загалом може включати ковтання, внаслідок чого сполука можна одержати за допомогою звичайних методик потрапляє в шлунково-кишковий тракт, і/або може відомих фахівцю в цій галузі або за допомогою застосовуватися букальне, лінгвальне або сублінпроцесів аналогічних тим, що описуються в супрогвальне введення для того, щоб сполука потрапвідних Прикладах і Препаративних прикладах, ляла в кров безпосередньо з рота. використовуючи прийнятні мічені ізотопами реагеРецептури, придатні для перорального ввенти, замість не мічених реагентів використовувадення, включають тверді, напів-тверді і рідкі комних раніше. позиції, такі як таблетки; м'які або тверді капсули, Фармацевтично прийнятними сольватами у віщо містять мульти- або наночастинки, рідини або дповідності з винаходом є такі, в яких кристалізапорошки; лозенге (включаючи рідинно-наповнені); ційний розчинник може бути ізотопічно заміщеним, гумки; гелі; дозовані форми швидкого вивільнення; наприклад, D2O, d6-ацетон, d6-ДМСО. плівки; овули; спреї; і букальні/мукоадгезивні пласТакож в межі даного винаходу включені сполутирі. ки формули II як визначено раніше у цьому докуРідкі композиції включають суспензії, розчини, менті, всі солі, сольвати і їх комплекси і всі сольсиропи та еліксири. Такі композиції можуть застовати і комплекси їх солей як визначено раніше у совуватися як наповнювачі в м'яких або твердих цьому документі для сполуки формули І. Винахід капсулах (вироблених, наприклад, з желатину або включає всі поліморфи вищезгаданих різновидів і гідроксипропілметилцелюлози) і зазвичай містять їх характерні форми кристалізації. носій, наприклад, воду, етанол, поліетиленгліколь, При одержанні сполуки формули (І) згідно з пропіленгліколь, метилцелюлозу або придатне винаходом, для спеціаліста цієї галузі загальновімасло, та один або декілька емульгаторів та/або домо як вибирати форму сполуки формули II, яка суспенгаторів. Рідкі композиції можуть також одезабезпечує найкращу комбінацію властивостей ржуватися розведенням твердого складу, напридля цієї цілі. Такі властивості включають темпераклад, з пакетику. туру плавлення, розчинність, технологічність і Сполуки винаходу також можуть бути викорисодержання проміжної форми і в результаті полегтані у швидкорозчинних, швидко-дезінтегруючих шення очищення продукту при виділенні. дозованих формах, таких як ті, що описані у Expert Сполуки формули (І) оцінювали щодо їх біоOpinion в Therapeutic Patents, 11 (6), 981-986, авфармацевтичних властивостей, таких як, наприторів Liang та Chen (2001). клад, розчинність, стабільність розчину (в проміжВ таблетованих дозованих формах, в залежку значень рН), проникність і т. п., для того, щоб ності від дози, лікарський засіб може складати від вибрати найбільш прийнятні дозовані форми і 1мас% до 80мас% дозованої форми, більш типово шляхи введення для лікування за бажаним призвід 5мас% до 60мас% дозованої форми. На доданаченням. ток до лікарського засобу, таблетки зазвичай місСполуки винаходу призначені для фармацевтять дезінтегратор. Прикладами дезінтеграторів є тичного застосування можуть бути введені як крикрохмальгліколят натрію, натрій карбоксиметилсталічні або аморфні продукти. Вони можуть бути целюлоза, кальцій карбоксиметилцелюлоза, наодержані, наприклад, як тверді речовини, порошки трій кроскармелоза, кросповідон, полівінілпіроліабо плівки за допомогою способів, таких як осадон, метилцелюлоза, мікрокристалічна целюлоза, дження, кристалізація, сублімація, висушуванням нижча алкіл-заміщена гідроксипропілцелюлоза, розпиленням або випаровуванням. Для цих цілей крохмаль, прежелатинізований крохмаль і алгінат може використовуватися висушування з викориснатрію. Зазвичай, дезінтегратор буде складати від танням мікрохвильового або радіовипромінюван1мас% до 25мас%, переважно від 5мас% до ня. 20мас% дозованої форми. Вони можуть бути введені окремо або в комбіЗв'язувальні агенти зазвичай використовуютьнації з однією або більше сполуками винаходу або ся для склеювання в єдине ціле таблетованої рев комбінації з одним або декількома іншими лікарцептури. Придатними зв'язувальними агентами є ськими засобами (або у вигляді будь-якої їх комбімікрокристалічна целюлоза, желатин, цукри, полінації). Загалом, вони будуть вводитись як рецепетиленгліколь, природні і синтетичні смоли, полівітури у поєднанні з одним або більшою кількістю нілпіролідон, прежелатинізований крохмаль, гідрофармацевтично прийнятних ексціпієнтів. Термін ксипропілцелюлоза і "ексціпієнт" використовується тут для опису будьгідроксипропілметилцелюлоза. Таблетки також якого інгредієнта іншого ніж сполука(и) винаходу. можуть містити розріджувачі, такі як лактоза (моВибір ексціпієнта буде у великій мірі залежати від ногідрат, висушений розпилюванням моногідрат, ряду факторів, таких як вибраний шлях введення, безводна і їм подібні), маніт, ксиліт, декстроза, вплив ексціпієнта на розчинність і стабільність і цукроза, сорбіт, мікрокристалічна целюлоза, крохприрода дозованої форми. маль і дигідрат диосновного фосфату кальцію. Фармацевтичні композиції придатні для достаТаблетки також можуть, необов'язково, містивки сполук представленого винаходу і способи їх ти поверхнево-активні агенти, такі як лаурилсульодержання очевидні фахівцю в цій галузі. Такі фат і полісорбат 80 і агенти, що підвищують ковкомпозиції і способи їх одержання можна знайти, зання, такі як діоксид кремнію і тальк. Коли наприклад, у Remington's Pharmaceutical Sciences, присутні, поверхнево-активні агенти можуть скла19th Edition (Mack Publishing Company, 1995). дати від 0,2мас% до 5мас% таблетки, і агенти, що 43 89846 44 підвищують ковзання, можуть складати від ких водних плівок на носії, з якого вони легко від0,2мас% до 1мас% таблетки. шаровуються, або папері. Це можна здійснити у Таблетки також зазвичай місять змащувальні сушильній шафі або тунелі, типово у комбінованій агенти, такі як стеарат магнію, стеарат кальцію, сушарці для сушки покриттів або шляхом сушіння стеарат цинку, стеаридфумарат натрію і суміші виморожуванням або вакуумуванням. стеарату магнію з лаурилсульфатом натрію. ЗмаТверді рецептури для перорального введення щувальні агенти загалом складають від 0,25мас% можна сформувати для негайного і/або модифікодо 10мас%, переважно від 0,5мас% до 3мас% ваного вивільнення. Рецептури модифікованого таблетки. вивільнення мають відстрочене-, тривале-, пульІншими можливими інгредієнтами є антиоксисуюче-, контрольоване-, цільове і програмоване данти, барвники, ароматизатори, консерванти і вивільнення. агенти, що корегують смак фармацевтичних агенПридатні рецептури з модифікованим вивільтів. ненням для цілей винаходу описані в патенті США Типові таблетки містять приблизно до 80% лі6,106,864. Деталі інших придатних методик вивікарського засобу, від приблизно 10мас% до прибльнення, таких як високоенергійні дисперсії і осмолизно 90мас% зв'язувального агента, від приблизтичні частинки і частинки з покриттям можна знайно 0мас% до приблизно 85мас% розріджувача, від ти в Pharmaceutical Technology On-line, 25 (2), 1приблизно 2мас% до приблизно 10мас% дезінтег14, авторів Verma і інші (2001). Використання журатора і від приблизно 0,25мас% до приблизно вальних гумок для досягнення контрольваного 10мас% змащувального агента. вивільнення описані в WO 00/35298. Таблеткові суміші можна спресувати безпосеСполуки винаходу також можна вводити безредньо або за допомогою валу у формі таблеток. посередньо в потік крові, у м'яз або у внутрішній Таблеткову суміш або частини сумішей можна орган. Придатними шляхами для парентерального альтернативно перед таблетуванням піддати вовведення є внутрішньовенне, внутрішньоартеріалогому-, сухому-гранулюванню або гранулюванню льне, внутрішньочеревинне, інтратекальне, інтрарозплаву, заморожуванню розплаву або екструдувентрикулярне, інтрауретральне, інтрастернальне, ванню. Кінцева рецептура може містити один або інтракраніальне, внутрішньом'язове і підшкірне. декілька шарів і може бути покритою або непокриПридатними пристроями для парентерального тою; вона може бути навіть інкапсульованою. введення є голкові (включаючи мікроголки) ін'єктоРецептури таблеток обговорюються в ри, безголкові ін'єктори і засоби вливання. Pharmaceutical Dosage Forms: Tablets, Vol. 1, by H. Парентеральні рецептури типово є водними Lieberman and L. Lachman (Marcel Dekker, New розчинами, які можуть містити ексціпієнти, такі як York, 1980). солі, карбогідрати і буферуючі агенти (переважно Використовуваними пероральними плівками до рН від 3 до 9), але, для деяких застосувань, для людей або ветеринарії є пластичні водорозвони можуть бути більш придатносформовані як чинні або здатні до набухання від води тонкоплівстерильний неводний розчин або як суха форма, кові дозовані форми, які можуть швидко розчинящо використовується у поєднанні з придатним тися або поглинатися слизовою оболонкою і розчинником, таким як стерильна пірогенвільна типово містять сполуку формули І, плівкоутворюювода. чий полімер, зв'язувальний агент, розчинник, звоОдержання парентеральних рецептур в стеложувач, пластифікатор, стабілізатор або емульрильних умовах, наприклад, шляхом ліофілізації, сифікатор, агент, що модифікує в'язкість і можна легко здійснити, використовуючи стандартні розчинник. Деякі компоненти рецептури можуть фармацевтичні методики, добре відомі фахівцю в виконувати більше ніж одну функцію. цій галузі. Сполука формули (І) може бути водорозчинРозчинність сполук формули (І), що викорисною або нерозчинною. Водорозчинна сполука титовується при одержанні парентеральних розчипово містить від 1мас% до 80мас%, більш типово нів, може бути збільшена шляхом використання від 20мас% до 50мас%, розчиненої речовини. прийнятних методик формування рецептур, таких Менш розчинні сполуки можуть складати більшу як включення агентів, що збільшують розчинність. частину композиції, типово до 88мас% розчиненої Рецептури для парентерального введення речовини. Альтернативно, сполука формули (І) можуть бути сформовані для негайного і/або моможе бути у формі дрібних частинок. дифікованого вивільнення. Рецептури модифікоПлівкоутворюючий полімер може бути вибраваного вивільнення мають відстрочене-, тривале-, ний з природних полісахаридів, протеїнів або синпульсуюче-, контрольоване-, цільове і програмотетичних гідроколоїдів і типово присутній в інтерване вивільнення. Таким чином, сполуки винаходу валі від 0,01 до 99мас%, більш типово в інтервалі можуть бути сформовані як тверда, напівтверда від 30 до 80мас%. або тиксотропна рідина для введення у вигляді Іншими інгредієнтами є антиоксиданти, барвімплантованого депо, для забезпечення модифіники, ароматизатори і підсилювачі аромату, конкованого вивільнення активної сполуки. Прикласерванти, агенти, що стимулюють виділення слидами таких рецептур є покриті лікарським засобом ни, хладогенти, співрозчинники (включаючи олії), стенти і мікросфери з полі(dl-молочнапом'якшувачі, наповнювачі, протиспінювачі, поверспівгліколева)кислоти (PGLA). хнево-активні речовини і агенти, що коригують Сполуки винаходу також можуть бути нанесені смак фармацевтичних агентів. на шкіру або слизову оболонку, тобто дермально Плівки у відповідності з винаходом типово або трансдермально. Типовими рецептурами для одержують шляхом сушіння випаровуванням тонцих цілей є гелі, гідрогелі, лосьйони, розчини, кре 45 89846 46 ми, мазі, порошки для обтрушування, пов'язки, ними ексціпієнтами є декстран, глюкоза, мальтоза, піни, плівки, пластири, пластинки, імплантати, губсорбіт, ксиліт, фруктоза, цукроза і трегалоза. ки, волокна, бандажі і мікроемульсії. Також можуть Придатний розчин для використання в пульбути використані ліпосоми. Типовими носіями є веризаторі, що використовує електродинамічну спирт, вода, мінеральне масло, рідкий вазелин, силу для одержання тонкого туману, може містити білий вазелин, гліцерин, поліетиленгліколь і пропівід 1мкг до 20мг сполуки винаходу і випускний ленгліколь. Можуть бути включені покращувачі об'єм може змінюватись від 1мкл до 100мкл. Типопроникнення - дивіться, наприклад, J Pharm Sci, 88 ва рецептура може містити сполуку формули І, (10), 955-958, авторів Finnin і Morgan (October пропіленгліколь, стерильну воду, етанол і хлорид 1999). натрію. Альтернативними розчинниками, які моІншими засобами місцевого введення є достажуть бути використані замість пропіленгліколю є вка за допомогою електропорації, фонтофорезу, гліцерин і поліетиленгліколь. фонофорезу, сонофорезу і мікроголкової або безВ такі рецептури винаходу, що призначені для інгалювання/інтраназального введення можуть толкової методики (наприклад, Powderject , бути додані придатні ароматизатори, такі як менBioject і т. д.) ін'єктування. тол і левоментол, або підсолоджувані, такі як саРецептури для місцевого введення можуть бухарин або сахарин натрію. ти сформовані для негайного і/або модифікованоРецептури для інгалювання/інтраназального го вивільнення. Рецептури модифікованого вивівведення можуть бути сформовані для негайного льнення мають відстрочене-, тривале-, пульсуючеі/або модифікованого вивільнення використовую, контрольоване-, цільове і програмоване вивільчи, наприклад, PGLA. Рецептури модифікованого нення. вивільнення мають відстрочене-, тривале-, пульСполуки винаходу також можуть бути введені суюче-, контрольоване-, цільове і програмоване інтраназально або за допомогою інгаляції, типово вивільнення. у формі сухого порошку (або окремо, або як суміш, У випадку інгаляторів сухого порошку і аеронаприклад, суха суміш з лактозою, або як змішані золів, одиниця дозування визначається за допомочастинки компонентів, наприклад, суміші з фосфогою клапану, який вивільнює виміряну кількість. ліпідами, такими як фосфатідилхолін) з інгалятору Одиниці у відповідності з винаходом типово вигосухого порошку або як аерозоль з контейнеру під товляються для введення виміряної дози або тиском, насосу, спрею, пульверизатору (переваж"пшику", що містить від 0,001мг до 10мг сполуки но використовують електродинамічний пульвериформули (І). Загальна добова доза зазвичай зназатор для одержання тонкого туману) або розпиходиться в інтервалі від 0,001мг до 40мг, яка може лювача, з або без використанням придатного вводитись однією дозою або, що типовіше, як розпропеланту, такого як 1,1,1,2-тетрафторетан або поділені дози протягом дня. 1,1,1,2,3,3,3-гептафторпропан. Для інтраназальноСполуки формули (І) є особливо придатними го використання, порошок може містити біоадгезидля введення шляхом інгаляції. вний агент, наприклад, цитозан або циклодекстСполуки згідно з винаходом можуть бути вверин. дені ректально або вагінально, наприклад, у формі Контейнер під тиском, насос, спрей, пульверисупозиторію, песарію або клізми. Масло какао є затор або розпилювач містить розчин або суспентрадиційною супозиторійною основою, але можуть зію сполук(и) винаходу, що включає, наприклад, бути використані різні альтернативи, якщо прийняетанол, водний етанол, або придатний альтернатно. тивний агент для диспергування, солюбілізування Рецептури для ректального/інтравагінального або розтягування вивільнення активної речовини, введення можуть бути сформовані для негайного пропелант(и) як розчинник і, необов'язково, повері/або модифікованого вивільнення. Рецептури мохнево-активну речовину, таку як триолеат сорбіту, дифікованого вивільнення мають відстрочене-, олеїнову кислоту або олігомолочну кислоту. тривале-, пульсуюче-, контрольоване-, цільове і Перед використанням сухого порошку або супрограмоване вивільнення. спензії, лікарський продукт мікронізують до розміСполуки згідно з винаходом також можуть бути ру придатного для вивільнення шляхом інгаляції введені безпосередньо в око або у вухо, типово у (типово, менше ніж 5 мікрон). Це можна досягти формі крапель мікронізованої суспензії або розчибудь-яким прийнятним способом подрібнення, ну в ізотонічному, рН-коригованому, стерильному таким як з використанням спірального струминного саліні. Інші рецептури придатні для окулярного або млина, струминного млина з псевдо-зрідженим вушного введення включають мазі, здатні до біошаром, суперкритичною рідинною обробкою для розщеплення (наприклад, здатні до абсорбування одержання наночастинок, гомогенізацією при вигелеві губки, колаген) і нездатні до біорозщепленсокому тиску або висушуванням розпиленням. ня (наприклад, силікон) імплантати, пластинки, Капсули (виготовлені, наприклад, з желатину лінзи і частинкові або везикулярні системи, такі як або гідроксипропілметилцелюлози), блістери і катніосоми або ліпосоми. Можуть бути включені поліриджі для використання в інгаляторі або інсуфламери, такі як поперечнозшита поліакрилова кислоторі можуть бути сформовані таким чином, що та, полівініловий спирт, гіалуронова кислота, полімістять порошкову суміш сполуки винаходу, примери целюлози, наприклад, датної порошкової основи, такої як лактоза або гідроксипропілметилцелюлоза, гідроксиетилцелюкрохмаль і модифікатор експлуатаційних якостей, лоза або метилцелюлоза, або гетерополісахаридтакий як l-лейцин, маніт або стеарат магнію. Лакний полімер, наприклад, геланова смола, разом з тоза може бути безводною або у формі моногідраконсервантом, таким як бензалконійхлорид. Такі ту, останній надається перевага. Іншими придат 47 89846 48 рецептури можуть бути вивільнені за допомогою визначить дози для суб'єкта, вага якого випадає з іонтофорезу. Рецептури для окулярного/вушного цього інтервалу, такого як дитина і людина похивведення можуть бути сформовані для негайного лого віку. і/або модифікованого вивільнення. Рецептури моДля уникнення сумнівів, посилання тут на "лідифікованого вивільнення мають відстрочене-, кування" включає посилання на зцілююче, паліатривале-, пульсуюче-, контрольоване-, цільове і тивне і профілактичне лікування. програмоване вивільнення. Сполуки формули (І) мають здатність взаємоСполуки винаходу можуть бути об'єднані з родіяти з мускариновими рецепторами і таким чином зчинними макромолекулярними сполуками, такими мають широкий діапазон терапевтичних застосуяк циклодекстрин і їх придатні похідні або поліетивань, як описано тут нижче, оскільки мускаринові ленгліколь-вмісні полімери, для того щоб покрарецептори відіграють суттєву роль у фізіології всіх щити їх розчинність, швидкість розчинення, замасссавців. кувати смак, біодоступність і/або стабільність для Тому винахід стосується використання сполук використання в будь-якому з вищезгаданих шляхів формули (І) для одержання лікарських засобів для введення. лікування або попередження захворювань, розлаКомплекси лікарський засіб-циклодекстрин, дів і станів, в які залучений М3 рецептор. Крім тонаприклад, знайшли застосування у більшості виго, винахід стосується способу лікування ссавця, дів дозованих форм і шляхів введення. Можуть включаючи людину, за допомогою антагоністу М3, бути використані комплекси включення і невклювключаючи лікування згаданого ссавця ефективчения. Як альтернатива безпосередньому компленою кількістю сполуки формули (І) або її фармацексуванню з лікарським засобом, циклодекстрин втично прийнятної солі, похідної форми або комможе бути використаний як допоміжна добавка, позиції. тобто, як носій, розріджувач або солюбілізатор. Тому, наступний аспект представленого винаНайбільш часто для цих цілей використовується ходу стосується сполук формули (І), або їх фаральфа-, бета- і гама-циклодекстрини, приклади мацевтично прийнятних солей, похідних форм або яких можна знайти в міжнародних патентних заявкомпозицій, для використання при лікуванні захвоках з номерами публікацій WO 91/11172, WO рювань, розладів і станів, в які залучені мускари94/02518 і WO 98/55148. нові рецептори. Прикладами таких захворювань Оскільки може бути бажано ввести комбінацію розладів і станів є запальне захворювання кишечактивних сполук, наприклад, з ціллю лікування нику, синдром подразненого кишечнику, дивертиокремого захворювання або стану, в межах предкульоз, закачування у транспорті, виразки шлунку, ставленого винаходу забезпечується, що дві або рентгенологічне дослідження кишечнику, симптобільше фармацевтичних композицій, принаймні, матичне лікування ДГП (доброякісної гіперплазії одна з яких містить сполуку у відповідності з винапростати), утворення виразки, індуковане NSAID, ходом, можуть легко бути об'єднані у формі набонетримання сечі (включаючи невідкладний позив ру придатного для спільного введення композицій. до сечовипускання, часте сечовипускання, невідТаким чином, набір згідно з винаходом містить кладне нетримання сечі, гіперактивний сечовий дві або більше окремі фармацевтичні композиції, міхур, нічна поліурія і симптоми з боку нижніх сепринаймні, одна з яких містить сполуку формули чових шляхів), циклоплегія, мідріаз, хвороба Пар(І) у відповідності з винаходом, і пристрої для кінсона. окремого утримання згаданих композицій, такі як Більш особливо, представлений винахід також контейнер, окремі пляшочки або окремі пакетики з стосується сполук формули (І) або їх фармацевтифольги. Прикладом такого набору є звичайна блічно прийнятних солей, похідних форм або компостерна упаковка, що використовується для пакузицій, для використання при лікуванні захворювання таблеток, капсул і їм подібних. вань, розладів і станів, що вибирають з групи, яка Набір згідно з винаходом є особливо придатвключає: ним для введення різних дозованих форм, напри- хронічну або гостру бронхоконстрикцію, хроклад, перорально і парентерально, для введення нічний бронхіт, обструкцію малих дихальних шляокремих композицій з різними інтервалами дозухів та емфізему, вання, або для титрування окремих композицій - обструктивні або запальні захворювання диодна до одної. Для сприяння відповідності, набір хальних шляхів будь-якого типу, етіології або патотипово містить інструкції по введенню і може бути генезу, зокрема, обструктивне або запальне зазабезпечений так званою пам'яткою. хворювання дихальних шляхів, що є членом, який Для введення людям, загальна добова доза вибирають з групи, що включає хронічну еозиносполук згідно з винаходом типово знаходиться в фільну пневмонію, хронічне обструктивне легенеінтервалі від 0,001мг до 5000мг, що звичайно заве захворювання ХОЗЛ (COPD), ХОЗЛ (COPD), що лежить від шляху введення. Наприклад, при перовключає хронічний бронхіт, легеневу емфізему або ральному введенні загальна добова доза може диспное пов'язане або непов'язане з ХОЗЛ потребувати від 0,1мг до 1000мг, в той же час вну(COPD), ХОЗЛ (COPD), що характеризується нетрішньовенна доза може потребувати тільки від зворотною прогресуючою обструкцією дихальних 0,001мг до 100мг. Загальна добова доза може бушляхів, респіраторний дистрессиндром повнолітти введена за один раз або розподілена на декільніх (ARDS), загострення респіраторної гіперреакка доз і може, на розсуд лікаря, не знаходитись у тивності на фоні іншої фармакотерапії і захворюнаведеному тут типовому інтервалі. вання дихальних шляхів, що пов'язані з легеневою Ці дози формуються, виходячі з середньої люгіпертензією, дини, що має вагу приблизно 60-70кг. Лікар легко 49 89846 50 - бронхіт будь-якого типу, етіології, або пато(І) антипухлинні агенти фактору некрозу (антигенезу; зокрема, бронхіт, що є членом, який вибиTNF- ), рають з групи, яка включає гострий бронхіт, гост(m) інгібітори адгезії молекули, включаючи рий ларинготрахеальний бронхіт, арахідоновий VLA-4 антагоністи, бронхіт, катаральний бронхіт, крупозний бронхіт, (n) антагоністи рецептора кініну-В1 і В2, сухий бронхіт, інфекційний астматичний бронхіт, (о) імуносупресивні агенти, продуктивний бронхіт, стафілококовий або стреп(р) інгібітори матриксних металопротеаз тококовий бронхіт і везикулярний бронхіт, (MMPs), - астму будь-якого типу, етіології або патоге(q) антагоністи рецептора тахікініну NK1, NK2 і незу, зокрема, астму, що є членом, який вибираNK3, ють з групи, яка включає атопічну астму, неатопіч(r) інгібітори еластази, ну астму, алергічну астму, атопічну бронхіальну (s) агоністи рецептора аденозину А2а, lgE-опосередковану астму, бронхіальну астму, (t) інгібітори урокінази, есенціальну астму, істинну астму, інфекційно(u) сполуки, що діють як допамінові рецептори, алергійну астму, викликану патофізіологічними наприклад, D2 агоністи, розладами, зовнішню астму, викликану зовнішни(ν) модулятори NF B шляху, наприклад, ІKK ми факторами, есенціальну астму невідомого або інгібітори, неочевидного походження, неатопічну астму, бро(w) модулятори цитокінових сигнальних шлянхітну астму, емфізематозну астму, астму виклихів, такі як р38 МАР кіназа або syk кіназа, кану фізичним навантаженням, астму індуковану (х) агенти, що можуть класифікуватись як муалергеном, астму індуковану холодним повітрям, колітики або протикашлеві агенти професійну астму, інфекційну астму, спричинену (у) антибіотики, бактеріальною, фунгальною, протозойною або (z) інгібітори HDAC та вірусною інфекцією, неалергійну астму, початкову (аа) інгібітори РІ3 кінази астму, синдром задухи у немовлят і бронхіоліт, (bb) антагоністи CXCR2. - гостре ушкодження легень, Згідно з представленим винаходом, комбінація - бронхоектазію будь-якого типу, етіології або сполуки формули (І) з: патогенезу, зокрема, бронхоектазію, що є членом, - Н3 антагоністами, який вибирають з групи, що включає циліндричну - 2 агоністами, бронхоектазію, осумковану бронхоектазію, вере- інгібіторами ФДЕ4, теноподібну бронхоектазію, капілярну бронхоекта- стероїдами, особливо глюкортикостероїдами, зію, циститну бронхоектазію, суху бронхоектазію і - агоністами рецептора аденозину А2а, фолікулярну бронхоектазію. - модуляторами цитокінових сигнальних шляБільш особливо, представлений винахід також хів, такими як р38 МАР кіназа або syk кіназа, або стосується сполук формули (І) або їх фармацевти- антагоністами лейкотрієну (LTRAs), включачно прийнятних солей, похідних форм або компоючи антагоністи LTB4, LTC4, LTD4 і LTE4, є перезицій, для для використання їх при лікуванні ХОЗЛ важними. (COPD) або астми. Згідно з представленим винаходом, комбінація Придатні приклади інших терапевтичних агенсполуки формули (І) з: тів, які можуть бути використані в комбінації з спо- глюкортикостероїдами, зокрема, глюкортиколукою(ами) формули (І) або їх фармацевтично стероїдами, що інгалюються, із зменшеними сисприйнятними солями, похідними формами або темними побічними ефектами, включаючи преднікомпозиціями, включають, але не обмежується зон, преднізолон, флунізолід, триамцинолон ними: ацетонід, беклометазону дипропіонат, будезонід, (a) інгібітори 5-ліпоксигенази (5-LO) або антафлутіказону пропіонат, циклезонід і мометазону гоністи 5-ліпоксигенази активуючого протеїну фуроат, або (FLAP), - 2 агоністами, включаючи, зокрема, сальбу(b) антагоністи лейкотрієну (LTRAs), включаютамол, тербуталін, бамбутерол, фенотерол, сальчи антагоністи LTB4, LTC4, LTD4 і LTE4, метерол, формотерол, тулобутерол і їх солі, є та(c) антагоністи рецептора гістаміну, включаюкож переважними. чи Н1 і Н3 антагоністи, Наступні приклади ілюструють одержання (d) агоністи 1- і 2-адренорецептора, судиносполук формули (І): звужувальні симпатоміметичні агенти для протиПрепаративний приклад 1 застійного застосування, трет-Бутил 4-ціано-4,4-дифенілбутаноат (e) 2 агоністи короткотривалої або довготриСуспензію дифенілацетонітрилу (38,6г, валої активності, 200ммоль) у трет-бутанолі (200мл) нагрівали до (f) інгібітори PDE, наприклад, інгібітори PDE3, 60°С протягом 30 хвилин. Одержаний розчин охоPDE4 і PDE5, лоджували до 50°С і додавали розчин гідроксиду (g) теофілін, калію (0,6г, 10,69ммоль) у метанолі (2мл). Потім (h) хромоглікат натрію, додавали краплями трет-Бутилакрилат (30мл, (і) інгібітори СОХ як неселективні, так і селек200ммоль) і суміш перемішували при 50°С протятивні інгібітори СОХ-1 або СОХ-2 (NSAIDs), гом 2 годин і при кімнатній температурі протягом (j) пероральні глюкокортикостероїди і глюкоко18 годин. Потім, додавали гідроксид калію (0,6г, ртикостероїди, що інгалюються, 10,69ммоль) і суміш повторно нагрівали до 50°С (k) моноклональні антитіла активні проти ендопротягом 3 годин. Реакційну суміш потім концентгенного запалення, рували у вакуумі і залишок розводили діетиловим 51 89846 52 етером (300мл), промивали водою (200мл), суши53,41ммоль) і тетрагідрофуран (50мл) і суміш пели над сульфатом натрію і концентрували у вакуремішували протягом 6 годин, залишаючи нагріваумі, одержуючи вказану в заголовку сполуку у витися до температури 25°С. Реакційну суміш потім гляді твердої речовини білого кольору з 90% повільно розбавляли водою (50мл), концентрувавиходом, 57,95г. ли у вакуумі і водний залишок екстрагували за 1 допомогою етилацетату (3x70мл). Об'єднаний орЯМР(400МГц, CD3OD) : 1,41 (с, 9Н), 2,29 (т, ганічний розчин промивали насиченим сольовим 2Н), 2,72 (т, 2Н), 7,29-7,33 (м, 1Н), 1Н), 7,36-7,42 розчином (30мл), сушили над сульфатом натрію і (м, 9Н); НРМС APCI m/z 322 [М+Н]+ концентрували у вакуумі, одержуючи оранжеве Препаративний приклад 2 масло. Це масло очищували за допомогою колон4-Ціано-4,4-дифенілбутанова кислота кової хроматографії на силікагелі, елююючи з виСуміш продукту препаративного прикладу 1 користанням суміші дихлорметан:метанол:0,88 (57,5г, 179,13ммоль) у хлорводневій кислоті (4N у аміак, з градієнтом від 100:0:0 до 90:10:1. Придатні діоксані, 500мл) перемішували при кімнатній темфракції випаровували при зниженому тиску і запературі протягом 18 годин. Реакційну суміш конлишок потім очищували за допомогою колонкової центрували у вакуумі і залишок обробляли за дохроматографії на силікагелі, елююючи з викориспомогою нагрітого діізопропілового етеру (150мл), танням суміші пентан:етилацетат, 66:33, одержупотім охолоджували до кімнатної температури. ючи вказану в заголовку сполуку у вигляді безбарОдержану тверду речовину відфільтровували, вного масла з 74% виходом, 10,93г. промивали діізопропіловим етером (2x30мл) і су1 шили під вакуумом, одержуючи вказану в заголовЯМР(400МГц, CD3OD) : 1,45 (с, 9Н), 1,91ку сполуку у вигляді кристалічної твердої речовини 2,00 (м, 1Н), 2,02-2,08 (м, 1Н), 3,35-3,44 (м, 4Н), білого кольору з 77% виходом, 36,45г. 4,13-4,17 (м, 1Н), 4,51-4,52 (м, 2Н), 7,24-7,29 (м, 1 1Н), 7,30-7,32 (м, 4Н); НРМС APCI m/z 278 [М+Н]+ ЯМР(400МГц, CD3OD) : 2,35 (т, 2Η), 2,76 (т, + Препаративний приклад 6 2Η), 7,30-7,44 (м, 10H); НРМС APCI m/z 266 [M+H] трет-Бутил (3R)-3-(бензилокси)піролідин-1Препаративний приклад 3 карбоксилат трет-Бутил (3S)-3-Феноксипіролідин-1Вказану у заголовку сполуку одержували з (R)карбоксилат (-)-N-boc-3-піролідинолу і бензилброміду, викорисДо охолодженого на льоду розчину (R)-(-)-Nтовуючи той же самий спосіб, що був описаний bос-3-піролідинолу (5г, 26,71ммоль), фенолу для препаративного прикладу 5. Неочищену спо(2,51г, 26,71ммоль) і трифенілфосфіну (7,71г, луку очищували за допомогою колонкової хрома29,38ммоль) у тетрагідрофурані (70мл) додавали тографії на силікагелі, елююючи з використанням діізопропілазодикарбоксилат (5,7мл, 29,38ммоль) і суміші дихлорметан:метанол:0,88 аміак, 95:5:0,5, суміш перемішували при кімнатній температурі одержуючи цільовий продукт з 97% виходом. протягом 18 годин. Реакційну суміш потім концен1 ЯМР(400МГц, CD3OD) : 1,46 (с, 3H), 1,92трували у вакуумі і залишок два рази розтирали з діетиловим етером і фільтрували. Фільтрат про2,02 (м, 1Н), 2,03-2,10 (м, 1Н), 3,35-3,48 (м, 4Н), мивали 1N розчином гідроксидом натрію (20мл), 4,14-4,19 (м, 1Н), 4,49-4,57 (м, 2Н), 7,24-7,33 (м, сушили над сульфатом натрію і концентрували у 5Н) вакуумі. Очищенням залишку за допомогою колонПрепаративний приклад 7 кової хроматографії на силікагелі, елююючи суміГідрохлорид (3S)-3-Феноксипіролідину шшю пентан:етилацетат, з градієнтом від 90:10 до Суміш продукту з препаративного прикладу 3 83:17, одержували вказану в заголовку сполуку у (5,25г, 19,96ммоль) у хлорводневій кислоті (4N у вигляді безбарвного масла з 75% виходом, 5,27г. діоксані, 50мл) перемішували при кімнатній темпе1 ратурі протягом 2 годин. Реакційну суміш потім ЯМР(400МГц, CD3OD) : 1,45 (м, 9Н), 2,10концентрували у вакуумі, одержуючи вказану в 2,16 (м, 2Н), 3,40-3,59 (м, 4Н), 4,95-4,97 (м, 1Н), заголовку сполуку у вигляді твердої речовини біло6,88-6,95 (м, 3H), 7,24-7,28 (м, 2Н) го кольору з 100% виходом. Препаративний приклад 4 1 трет-Бутил (3S)-3-(3ЯМР(400МГц, CD3OD) : 2,29-2,33 (м, 2Н), метоксифенокси)піролідин-1-карбоксилат 3,42-3,56 (м, 4Н), 5,18-5,21 (м, 1Н), 6,95-7,01 (м, Вказану у заголовку сполуку одержували з (R)3H), 7,29-7,32 (м, 2Н); НРМС АРСІ m/z 164 [М+Н]+ (-)-N-boc-3-піролідинолу і 3-метоксифенолу, викоПрепаративний приклад 8 ристовуючи той же самий спосіб, як описано для (3S)-3-(3-Метоксифенокси)піролідин препаративного прикладу 3, у вигляді смоли з 81% Суміш продукту з препаративного прикладу 4 виходом. (3,19г, 10,8ммоль) у хлорводневій кислоті (4N у 1 діоксані, 27мл) перемішували при кімнатній темпеЯМР(400МГц, CD3OD) : 1,45 (м, 9Н), 2,14 ратурі протягом 3 годин. Реакційну суміш потім (шс, 2Н), 3,40-3,58 (м, 4Н), 3,75 (с, 3H), 4,95 (м, концентрували у вакуумі і залишок очищували за 1Н), 6,45-6,54 (м, 3H), 7,14-7,18 (м, 1Н) допомогою колонкової хроматографії, використоПрепаративний приклад 5 вуючи Isolute SCX-2 катридж, елююючи метанотрет-Бутил (3S)-3-(бензилокси)піролідин-1карбоксилат лом, потім з використанням 1М аміаку в метанолі, До охолодженого на льоду розчину (S)-(-)-Nодержуючи вказану в заголовку сполуку у вигляді boc-3-піролідинолу (10г, 53,41ммоль) у тетрагіджовтого масла з 85% виходом, 1,77г. 1 рофурані (100мл) додавали частинами гідрид наЯМР(400МГц, CD3OD) : 1,91-1,98 (м, 1Н), трію (60% дисперсія у мінеральному маслі, 2,13г, 2,02-2,11 (м, 1Н), 2,85-2,91 (м, 1Н), 3,02-3,08 (м, 53,41ммоль) і суміш перемішували при 0°С протя3H), 3,75 (с, 3H), 4,85-4,89 (м, 1Н), 6,43-6,51 (м, гом 1 години. Додавали бензилбромід (6,4мл, 3H), 7,12-7,16 (м, 1Н); НРМС АРСІ m/z 194 [М+Н]+ 53 89846 54 Препаративний приклад 9 продукт у вигляді безбарвного масла з кількісним Гідрохлорид (3S)-3-(Бензилокси)піролідину виходом. 1 Вказану у заголовку сполуку одержували з ЯМР(400МГц, CD3OD) : 2,03-2,20 (м, 2Н), продукту препаративного прикладу 5, використо2,32-2,37 (м, 1Н), 2,43-2,47 (м, 1Н), 2,66-2,84 (м, вуючи той же самий спосіб, що був описаний для 2Н), 3,44-3,67 (м, 4Н), 3,74 (с, 3H), 4,94-5,00 (м, препаративного прикладу 7, у вигляді твердої ре1Н), 6,44-6,55 (м, 3H), 7,13-7,19 (м, 1Н), 7,28-7,46 човини з 100% виходом. (м, 10H); НРМС АРСІ m/z 412 [М+Н]+ 1 ЯМР(400МГц, CD3OD) : 2,02-2,12 (м, 1Н), Препаративний приклад 14 2,22-2,29 (м, 1Н), 3.26-3,46 (м, 4Н), 4,35-4,37 (м, 5-[(3S)-3-(Бензилокси)піролідин-1-іл]-5-оксо1Н), 4,55 (с, 2Н), 7,25-7,37 (м, 5Н); НРМС АРСІ m/z 2,2-дифенілпентаннітрил 178 [М+Н]+ Вказану у заголовку сполуку одержували з Препаративний приклад 10 продуктів препаративних прикладів 2 і 9, викорисГідрохлорид (3R)-3-(Бензилокси)піролідину товуючи той же самий спосіб, що був описаний Вказану у заголовку сполуку одержували з для препаративного прикладу 11, у вигляді твердої продукту препаративного прикладу 6, використоречовини блідо-оранжевого кольору з 70% виховуючи той же самий спосіб, що був описаний для дом. 1 препаративного прикладу 7, у вигляді твердої реЯМР(400МГц, CD3OD) : 1,86-2,15 (м, 2Н), човини з 100% виходом. 2,32-2,43 (м, 2Н), 2,75-2,82 (м, 2Н), 3,35-3,62 (м, 1 ЯМР(400МГц, CDCI3) : 1,96-2,05 (м, 1Н), 4Н), 4,14-4,21 (м, 1Н), 4,45-4,56 (м, 2Н), 7,22-7,44 2,20-2,15 (м, 1Н), 3,49-3,32 (м, 4Н), 4,23-4,25 (м, (м, 15Н); НРМС APCI m/z 412 [M+H]+ 1Н), 4,44-4,54 (м, 2Н), 7,26-7,36 (м, 5Н), 9,74-9,88 Препаративний приклад 15 (м, 2Н); НРМС АРСІ m/z 178 [М+Н]+ 5-[(3R)-3-(Бензилокси)піролідин-1-іл]-5-оксоПрепаративний приклад 11 2,2-дифенілпентаннітрил 5-Оксо-5-[(3S)-3-феноксипіролідин-1-іл]-2,2До розчину продукту з препаративного прикдифенілпентаннітрил ладу 2 (36г, 135ммоль) у тетрагідрофурані (600мл) Суміш продуктів препаративних прикладів 2 додавали Ν,Ν'-карбонілдіімідазол (27г, 162ммоль) і (2,40г, 9,05ммоль) і 7 (1,99г, 9,96ммоль), гідрохлосуміш перемішували протягом 3 годин при кімнатриду 1-(3-диметиламінопропіл)-3-етилкарбодііміду ній температурі. Додавали розчин продукту з пре(1,55г, 9,96ммоль), гідрату 1паративного прикладу 10 (31г, 141,75ммоль) у тетгідроксибензотриазолу (1,35г, 9,96ммоль) і триерагідрофурані (300мл) і суміш перемішували при тиламіну (1,38мл, 9,96ммоль) у дихлорметані кімнатній температурі протягом 18 годин. Реакцій(40мл) перемішували при кімнатній температурі ну суміш потім фільтрували, промивали тетрагідпротягом 18 годин. Реакційну суміш потім розбаврофураном і фільтрат концентрували у вакуумі. ляли, з використанням дихлорметану (100мл), Залишок розподіляли між водою (200мл) і етилапромивали 1М хлорводневої кислоти (70мл), 1М цетатом (600мл) і органічний шар відокремлюварозчином гідроксиду натрію (30мл) і насиченим ли, промивали водою, 2N хлорводневою кислотою сольовим розчином (30мл), сушили над сульфа(2x100мл) і насиченим сольовим розчином, сушитом натрію і концентрували у вакуумі. Залишок ли над сульфатом магнію і концентрували у вакуперекристалізовували з гарячого етанолу, одерумі. Потім шляхом розтирання залишку з діетиложуючи вказану в заголовку сполуку у вигляді крисвим етером одержували вказану у заголовку талічної твердої речовини з 76% виходом, 2,83г. сполуку з 83% виходом, 48,2г. 1 1 ЯМР(400МГц, CD3OD) : 2,07-2,21 (м, 2Н), ЯМР(400МГц, CD3OD) : 1,87-2,15 (м, 2Н), 2,33-2,38 (м, 1Н), 2,43-2,47 (м, 1Н), 2,69-2,84 (м, 2,32-2,44 (м, 2Н), 2,74-2,82 (м, 2Н), 3,35-3,61 (м, 2Н), 3,44-3,55 (м, 2Н), 3,58-3,67 (м, 2Н), 4,96-5,04 4Н), 4,14-4,22 (м, 1Н), 4,46-4,57 (м, 2Н), 7,23-7,44 (м, 1Н), 6,89 (д, 2Н), 6,93-6,96 (м, 1Н), 7,24-7,46 (м, (м, 15Н); НРМС APCI m/z 425 [М+Н]+ 12Н); НРМС АРСІ m/z 412 [М+Н]+ Препаративний приклад 16 Препаративний приклад 12 5-[(3S)-3-Гідроксипіролідин-1-іл]-5-метил-2,25-Оксо-5-[(3R)-3-феноксипіролідин-1-іл]-2,2дифенілгексанамід дифенілпентаннітрил До розчину продукту прикладу 11 (385мг, Вказану у заголовку сполуку одержували з 0,84ммоль) у дихлорметані (10мл) додавали хло(3R)-3-феноксипіролідину (WO 2005/061457) і прорид заліза (III) (1,57г, 9,70ммоль) і суміш перемідукту з препаративного прикладу 2, використовуюшували при кімнатній температурі протягом 3 гочи той же самий спосіб, що був описаний для предин. Реакційну суміш гасили шляхом додавання паративного прикладу 11, одержуючи вказану в 2М хлорводневої кислоти (6мл), фільтрували чезаголовку сполуку з 41% виходом. рез Arbocel і фільтрат підлуговували, використоПрепаративний приклад 13 вуючи 0,88 розчин аміаку (20мл). Шари фільтрату 5-[(3S)-3-(3-Метоксифенокси)піролідин-1-іл]-5відокремлювали і водний розчин екстрагували за оксо-2,2-дифенілпентаннітрил допомогою дихлорметану (2x25мл). Об'єднаний Вказану у заголовку сполуку одержували з органічний розчин сушили над сульфатом натрію, продуктів препаративних прикладів 2 і 8, викорисконцентрували у вакуумі і очищенням залишку за товуючи той же самий спосіб, що був описаний допомогою колонкової хроматографії на силікагедля препаративного прикладу 11. Неочищену сполі, елююючи з використанням суміші етилацелуку очищували за допомогою колонкової хроматат:метанол:0,88 аміак, з градієнтом від 95:5:0,5 до тографії на силікагелі, елююючи з використанням 85:15:1,5, одержували вказану в заголовку сполуку суміші дихлорметан:метанол:0,88 аміак, з градієну вигляді коричневої смоли з 60% виходом, 415мг. том від 98:2:0,2 до 95:5:0,5, одержуючи цільовий 55 89846 56 0,372ммоль) ЕР625510, р13] і продукту з препараЯМР(400МГц, CD3OD) : 0,99 (с, 6Н), 1,23тивного прикладу 17 (150мг, 0,41ммоль) у тетрагі1,27 (м, 2Н), 1,56-1,64 (м, 1Н), 1,89-1,98 (м, 1Н), дрофурані (5мл) додавали 1,1'-Азобіс(N,N'2,40-2,44 (м, 3H), 2,47-2,52 (м, 1Н), 2,61-2,67 (м, диметилформамід) (95мг, 0,553ммоль) і суміш 1Н), 2,74-2,78 (м, 1Н), 4,17-4,22 (м, 1Н), 7,22-7,26 нагрівали при 60°С протягом 18 годин. Додавали (м, 2Н), 7,29-7,33 (м, 4Н), 7,37 (д, 4Н); НРМС APCI + додатковий трифенілфосфін (145мг, 0,553ммоль) і m/z 367 [М+Н] 1,1'-Азобіс(N,N'-диметилформамід) (95мг, Препаративний приклад 17 0,553ммоль) і продовжували нагрівати протягом 5-[(3R)-3-Гідроксипіролідин-1-іл]-5-метил-2,2наступних 18 годин. Суміш концентрували у вакудифенілгексанамід До розчину продукту прикладу 9 (5г, умі і залишок очищували з використанням Isolute 10,95ммоль) в етанолі (250мл) додавали 1N хлорSCX-2 катриджу, елююючи з використанням метаводневу кислоту (10,95мл, 10,95ммоль) і 20% нолу, потім 0,25М аміаку у метанолі. Основні фраPd(OH)2 (1г) і суміш перемішували при 50°С, при кції концентрували у вакуумі і потім очищували, 50псі газоподібного водню, протягом 4 годин. Реавикористовуючи RediSep силікагелевий катридж, кційну суміш потім фільтрували через Arbocel і елююючи з використанням суміші дихлормефільтрат концентрували у вакуумі, одержуючи білу тан:метанол:0,88 аміак (з градієнтом від 100:0:0 до піну. Піну повторно розчиняли в етанолі (250мл), 92:8:0,8), одержуючи вказану в заголовку сполуку з додавали 20% Pd(OH)2 (1г) і суміш перемішували 20% виходом, 46мг. 1 при 50°С, при 50псі газоподібного водню, протягом ЯМР(400МГц, CD3OD) : 0,24 (с, 6Н), 0,95 (с, 24 годин. Реакційну суміш потім фільтрували че3H), 1,04 (с, 9Н), 1,06 (с, 3H) 1,15-1,29 (м, 2Н), рез Arbocel , промивали етанолом і фільтрат кон1,88-1,99 (м, 1Н), 2,11-2,22 (м, 1Н), 2,30-2,52 (м, центрували у вакуумі. Залишок суспендували у 2Н), 2,54-2,62 (м, 1Н), 2,64-2,69 (м, 1Н), 2,72-2,82 0,88 аміаку, екстрагували з використанням етила(м, 1Н), 2,82-2,90 (м, 1Н), 4,83-4,89 (м, 1Н), 6,96цетату (3x50мл) і об'єднаний органічний розчин 7,06 (м, 2Н), 7,12-7,34 (м, 12Н), 7,53-7,57 (м, 1Н), промивали насиченим сольовим розчином (50мл), 7,60-7,65 (м, 1Н); НРМС APCI m/z 623 [М+Н]+ сушили над сульфатом натрію і концентрували у Препаративний приклад 20 вакуумі, одержуючи вказану в заголовку сполуку у 5-[(3R)-3-Гідроксипіролідин-1-іл]-5-метил-2,2вигляді білої піни з 90% виходом, 3,63г. дифенілгексаннітрил 1 До розчину продукту прикладу 8 (9г, ЯМР(400МГц, CD3OD) : 0,99 (с, 6Н), 1,2320,548ммоль) у дихлорметані (200мл) додавали 1,27 (м, 2Н), 1,56-1,63 (м, 1Н), 1,89-1,96 (м, 1Н), хлорид заліза (III) (13,3г, 82,192ммоль) і суміш пе2,39-2,44 (м, 3H), 2,46-2,52 (м, 1Н), 2,61-2,67 (м, ремішували при кімнатній температурі протягом 1 1Н), 2,74-2,78 (м, 1Н), 4,17-4,22 (м, 1Н), 7,22-7,26 години. Реакційну суміш гасили шляхом додаван(м, 2Н), 7,29-7,33 (м, 4Н), 7,36-7,39 (м, 4Н); НРМС ня 2М хлорводневої кислоти (150мл) і перемішуAPCI m/z 367 [М+Н]+ вали протягом 30 хвилин. Органічний шар відоПрепаративний приклад 18 кремлювали і водні шари повторно екстрагували з 5-P(3S)-3-Гідроксипіролідин-1-іл]-5-метил-2,2використанням додаткових 100мл дихлорметану. дифенілгексаннітрил Об'єднані органічні шари сушили над сульфатом До розчину продукту прикладу 10 (1,2г, натрію і концентрували у вакуумі. Очищенням за 2,74ммоль) у дихлорметані (25мл) додавали хлодопомогою колонкової хроматографії на силікагерид заліза (III) (1,33г, 8,22ммоль) і суміш перемілі, елююючи з використанням суміші дихлормешували при кімнатній температурі протягом 3 готан:метанол:0,88 аміак, з градієнтом від 95:5:0,5 дин. Розчинник видаляли у вакуумі і залишок до 90:1:1,0, одержували вказану в заголовку спорозподіляли між 2М хлорводневою кислотою луку у вигляді блідо-коричневої піни з 89% вихо(водн.) (20мл) і діетиловим етером (30мл). Водний дом, 6,37г. шар відокремлювали і підлуговували до рН14, ви1 користовуючи твердий гідроксид натрію. ОдержаЯМР(400МГц, CD3OD) : 1,18 (с, 6Н), 1,58ний коричневий осад збирали за допомогою філь1,62 (м, 2Н), 1,76-1,84 (м, 1Н), 1,96-2,05 (м, 1Н), трації і очищували за допомогою колонкової 2,55-2,59 (м, 2Н), 2,74-2,81 (м, 1Н), 2,87-2,93 (м, хроматографії на силікагелі, елююючи з викорис1Н), 2,98-3,06 (м, 2Н), 4,32-4,36 (м, 1Н), 7,30-7,34 танням суміші дихлорметан:метанол:0,88 аміак, з (м, 2Н), 7,37-7,46 (м, 8Н); НРМС APCI m/z 349 градієнтом від 95:5:0,5 до 85:15:1,5, одержуючи [М+Н]+ вказану в заголовку сполуку у вигляді безбарвної Препаративний приклад 21 смоли з 50% виходом, 475мг. 2-Хлор-3-Метоксифенол 1 До розчину 2-Хлор-3-Метоксибензальдегіду ЯМР(400МГц, CD3OD) : 1,11 (с, 6Н), 1,52(500мг, 2,931ммоль) у дихлорметані (12мл) дода1,56 (м, 2Н), 1,69-1,76 (м, 1Н), 1,95-2,04 (м, 1Н), вали частинами 3-Хлорпероксибензойну кислоту 2,53-2,57 (м, 2Н), 2,62-2,65 (м, 1Н), 2,69-2,76 (м, (760мг, 4,396ммоль) і суміш перемішували протя1Н), 2,83-2,95 (м, 2Н), 4,27-4,31 (м, 1Н), 7,29-7,33 гом 3 годин при кімнатній температурі. Додатково (м, 2Н), 7,36-7,45 (м, 8Н); НРМС APCI m/z 349 додавали 3-хлорпероксибензойну кислоту (760мг, [М+Н]+ 4,396ммоль) і суміш залишали перемішуватися Препаративний приклад 19 протягом 18 годин. Розчин розводили з викорис5-{(3S)-3-[(6-{[трет-Бутил(диметил)силіл]окси}танням 12мл дихлорметану і промивали насиче2-нафтил)окси]піролідин-1-іл}-5-метил-2,2ним розчином сульфіту натрію (15мл) і насиченим дифенілгексанамід розчином гідрокарбонату натрію (15мл). ОрганічДо охолодженого на льоду розчину трифенілний шар сушили над сульфатом натрію і концентфосфіну (145мг, 0,553ммоль), 6-(третрували у вакуумі, одержуючи жовту смолу. ЗалиБутилдиметилсилілокси)-2-нафтолу [(102мг, 1 57 89846 58 шок розчиняли у метанолі (12мл), додавали триеВказану у заголовку сполуку одержували з 4тиламін (0,05мл) і суміш перемішували протягом фтор-3-метоксибензальдегіду, використовуючи 18 годин при кімнатній температурі. Розчин концетой же самий спосіб, що був описаний для препантрували у вакуумі, розчиняли у діетиловому етері ративного прикладу 21, одержуючи коричневе ма(20мл) і екстрагували з використанням 1N гідроксло з 55% виходом. 1 сиду натрію (20мл). Водний шар підкислювали до ЯМР(400МГц, CD3OD) : 3,79 (с, 3H), 6,23рН1 шляхом додавання краплями 2N хлорводне6,27 (м, 1Н), 6,47-6,50 (дд, 1Н), 6,81-6,86 (м, 1Н) вої кислоти і екстрагували з використанням діетиПрепаративний приклад 26 лового етеру (2x25мл). Ці об'єднані органічні шари 2-Фтор-3-Метоксифенол сушили над сульфатом натрію і концентрували у Вказану у заголовку сполуку одержували з 2вакуумі, одержуючи вказану в заголовку сполуку у фтор-3-метоксибензальдегіду, використовуючи вигляді коричневої смоли з 70% виходом, 325мг. той же самий спосіб, що був описаний для препа1 ЯМР(400МГц, CD3OD) : 3,83 (с, 3H), 6,52ративного прикладу 21, одержуючи коричневе ма6,54 (д, 2Н), 7,01-7,06 (т, 1Η) сло з 33% виходом. 1 Препаративний приклад 22 ЯМР(400МГц, CD3OD) : 3,82 (с, 3H), 6,471-Хлор-3-фтор-2-Метоксибензол 6,55 (м, 2Н), 6,82-6,87 (т, 1Η) До 2-хлор-6-фторфенолу (1,0г, 6,824ммоль) у Препаративний приклад 27 тетрагідрофурані (10мл) додавали метилйодид 1-Алілокси-3-бромметилбензол (850мкл, 13,646ммоль) і карбонат калію (943мг, До розчину (3-алілоксифеніл)метанолу 6,824ммоль) і суміш перемішували при кімнатній (Tetrahedron, 2000, 56 (13), 1873-1882) (1,07г, температурі протягом 3 годин. Реакційну суміш 6,49ммоль) у ТГФ (7мл) при 3°С додавали тетраброзподіляли між діетиловим етером (50мл) і водою ромід вуглецю (2,69г, 8,11ммоль), потім трифені(50мл). Органічну фазу екстрагували і потім пролфосфін (2,13г, 8,11ммоль) у ТГФ (2мл). Реакційну мивали водою (2x20мл), потім сушили над сульсуміш перемішували при 5°С протягом 1 години. фатом натрію і концентрували у вакуумі, одержуРеакційну суміш фільтрували і концентрували у ючи вказану в заголовку сполуку у вигляді вакуумі. Залишок промивали пентаном, одержуюбезбарвної рідини з 94% виходом, 1,03г. чи тверду речовину жовтого кольору, яку очищу1 ЯМР(400МГц, CD3OD) : 3,90-3,91 (с, 3H), вали за допомогою колонкової хроматографії на 7,01-7,12 (м, 2Н), 7,18-7,21 (м, 1Н) силікагелі, елююючи з використанням суміші пенПрепаративний приклад 23 тан:етилацетат, з градієнтом від 100:0 до 95:5, 3-Фтор-5-Метоксифенол одержуючи вказану в заголовку сполуку у вигляді До охолодженого на льоду розчину 3,5блідо-жовтого масла з 24% виходом, 350мг. 1 диметоксифторбензолу (3мл, 22,496ммоль) у дихЯМР(400МГц, CDCI3) : 4,47 (с, 2Н), 4,51-4,60 лорметані (20мл) додавали краплями трибромід (м, 2Н), 5,26-5,35 (м, 1Н), 5,37-5,47 (м, 1Н), 5,99бору (1М у дихлорметані, 9мл, 89,985ммоль) і су6,11 (м, 1Н), 6,82-6,90 (м, 1Н), 6,92-7,01 (м, 2Н), міш перемішували при 0°С до одержання кімнатної 7,21-7,30 (м, 1Н). температури протягом 4 годин. Розчин охолоджуПрепаративний приклад 28 вали до 0°С, потім додавали трибромід бору (4мл, 5-[(3R)-3-(3-Алілоксибензилокси)піролідин-144,992ммоль) і продовжували перемішування, наіл]-5-метил-2,2-дифенілгексаннітрил гріваючи до кімнатної температури протягом додаДо охолодженого на льоду розчину гідриду наткових 18 годин. Реакційну суміш гасили, використрію (60% дисперсія у мінеральному маслі, 31мг, товуючи розчин 0,88 аміаку і перемішували при 0,770ммоль) у диметилформаміді (1мл) додавали кімнатній температурі протягом 90 хвилин. Органікраплями продукт з препаративного прикладу 20 чний шар відокремлювали і екстрагували, викори(179мг, 0,514ммоль) у диметилформаміді (3мл). стовуючи 2Ν гідроксид натрію (30мл), який потім Після перемішування протягом 1 години додавали підкислювали до рН1 шляхом додавання краплями продукт з препаративного прикладу 27 (175мг, концентрованої хлорводневої кислоти. Водний 0,514ммоль) у диметилформаміді (1мл) і суміш шар потім повторно екстрагували з використанням залишали нагріватися до кімнатної температури дихлорметану (3x15мл), об'єднаний органічний протягом 18 годин. Реакційну суміш потім повторрозчин сушили над сульфатом натрію і концентруно охолоджували до 0°С і потім додавали гідрид вали у вакуумі, одержуючи вказану в заголовку натрію (60% дисперсія у мінеральному маслі, сполуку у вигляді твердої речовини білого кольору 31мг, 0,770ммоль), при перемішуванні при кімнатз 54% виходом, 1,72г. ній температурі протягом додаткових 3 годин. Роз1 ЯМР(400МГц, CD3OD) : 3,72 (с, 3H), 6,07чин гасили шляхом додавання краплями води, 6,15 (м, 3H) концентрували у вакуумі і розподіляли між етилаПрепаративний приклад 24 цетатом (10мл) і водою (10мл). Органічний шар 1-Фтор-3-Метокси-5-Трифторметилбензол екстрагували і промивали водою (10мл), потім Вказану у заголовку сполуку одержували з 3сушили над сульфатом натрію і концентрували у фтор-5-трифторметилфенолу, використовуючи вакуумі. Очищенням за допомогою колонкової той же самий спосіб, що був описаний для препахроматографії на силікагелі, елююючи з викорисративного прикладу 22, одержуючи безбарвне танням суміші дихлорметан:метанол:0,88 аміак, масло з 90% виходом. 97:3:0,3, одержували вказану в заголовку сполуку 1 у вигляді блідо-жовтої смоли з 43% виходом, ЯМР(400МГц, CD3OD) : 3,84 (с, 3H), 6,92108мг. 6,97 (м, 2Н), 7,00 (с, 1Н) 1 ЯМР(400МГц, CD3OD) : 1,03 (с, 3H), 1,05 (с, Препаративний приклад 25 4-Фтор-3-Метоксифенол 3H), 1,44-1,51 (м, 2Н), 1,78-1,85 (м, 1Н), 1,93-2,01 59 89846 60 1 (м, 1Н), 2,50-2,55 (м, 3H), 2,64-2,78 (м, 3H), 4,03ЯМР(400МГц, CDCI3) : 4,61-4,63 (м, 4Н), 4,08 (м, 1Н), 4,43 (с, 2Н), 4,50-4,55 (м, 2Н), 5,205,29-5,32 (д, 1Н), 5,41-5,45 (д, 1Н), 6,02-6,11 (м, 5,24 (м, 1Н), 5,34-5,41 (м, 1Н), 5,98-6,09 (м, 1Н), 1Н), 6,85-6,89 (м, 1Н), 7,00-7,07 (м, 2Н); НРМС 6,79-6,84 (м, 1Н), 6,87-6,94 (м, 2Н), 7,18-7,21 (т, АРСІ m/z 165 [М-ОН]+ + 1Η), 7,26-7,43 (м, 10H); НРМС ESI m/z 495 [M+H] Препаративний приклад 32 Препаративний приклад 29 2-Алілокси-4-бромметил-1-фторбензол 5-Метил-2,2-дифеніл-5-[(3R)-3-(3До розчину продукту з препаративного прикпропенілоксибензилокси)піролідин-1-іл]-гексанової ладу 31 (900мг, 4,94ммоль) в ацетонітрилі (40мл) кислоти амід при кімнатній температурі додавали дибромтриВказану у заголовку сполуку одержували з фенілфосфоран (2,3г, 5,43ммоль) і розчин перепродукту препаративного прикладу мішували протягом 18 годин. Розчинник видаляли 28,використовуючи спосіб, подібний до описаного у вакуумі і залишок очищували за допомогою кодля прикладу 2, з додаванням додатково гідроксилонкової хроматографії на силікагелі, елююючи ду калію (2екв.) через 20 годин і продовжували звикористанням суміші пентан:етилацетат (80:20), нагрівання протягом додаткових 4 годин, одержуодержуючи вказану в заголовку сполуку у вигляді ючи продукт у вигляді жовтої смоли з 88% вихобезбарвної рідини з 31% виходом, 380мг. 1 дом. ЯМР(400МГц, CDCI3) : 4,44 (с, 2Н), 4,61-4,63 1 ЯМР(400МГц, CD3OD) : 0,99 (с, 3H), 1,01 (с, (м, 2Н), 5,30-5,34 (м, 1Н), 5,41-5,47 (м, 1Н), 6,023H), 1,23-1,28 (м, 2Н), 1,67-1,69 (д, 3H), 1,74-1,82 6,11 (м, 1Н), 6,91-6,94 (м, 1Н), 6,99-7,05 (м, 2Н); (м, 1Н), 1,88-1,95 (м, 1Н), 2,40-2,44 (м, 2Н), 2,47НРМС APCI m/z 165 [M-Br]+ 2,53 (м, 1Н), 2,55-2,74 (м, 3H), 3,99-4,04 (м, 1Н), Препаративний приклад 33 4,42 (с, 2Н), 4,85-4,87 (м, 1Н), 6,40-6,42 (д, 1Н), 5-[(3R)-3-(3-Алілокси-46,88-6,90 (д, 1Н), 6,96-6,99 (м, 2Н), 7,21-7,38 (м, фторбензилокси)піролідин-1-іл]-5-метил-2,211Н); НРМС ESI m/z 513 [М+Н]+ дифенілгексаннітрил Препаративний приклад 30 До охолодженого на льоду розчину продукту з Аліловий естер 3-Алілокси-4-фторбензойної препаративного прикладу 20 (270мг, 0,775ммоль) кислоти у диметилформаміді (3мл) додавали частинами До суспензії 4-фтор-3-гідроксибензойної кисгідрид натрію (62мг, 1,55ммоль) у атмосфері азолоти (2,5г, 16,0ммоль) і карбонату калію (4,43г, ту. Після перемішування протягом 1,5 годин дода32,03ммоль) у диметилформаміді (50мл) при кімвали розчин продукту з препаративного прикладу натній температурі додавали краплями алілбромід 32 (380мг, 1,55ммоль) у диметилформаміді (2мл) і (3,04мл, 35,2ммоль) і суміш перемішували протясуміш залишали нагріватися до кімнатної темпегом 18 годин. Розчинник видаляли у вакуумі і заратури і перемішували протягом 18 годин. Розчинлишок розподіляли між діетиловим етером (30мл) і ник видаляли у вакуумі і залишок розподіляли між водою (30мл). Водний шар відокремлювали і екстетилацетатом (10мл) і насиченим розчином гідрорагували з використанням додаткового діетиловокарбонату натрію (5мл). Водний шар відокремлюго етеру (2x20мл). Об'єднані органічні шари провали і екстрагували з використанням додаткового мивали водою (3x10мл), сушили над сульфатом етилацетату (10мл). Об'єднані органічні шари натрію і концентрували у вакуумі, одержуючи вкапромивали водою (5мл), насиченим сольовим роззану в заголовку сполуку у вигляді безбарвної річином (5мл), сушили над сульфатом натрію і кондини з 100% виходом, 3,82г. центрували у вакуумі. Залишок очищували за до1 ЯМР(400МГц, CDCI3) : 4,65-4,66 (д, 2Н), 4,80помогою колонкової хроматографії на силікагелі, 4,82 (д, 2Н), 5,28-5,48 (м, 4Н), 5,98-6,12 (м, 2Н), елююючи з використанням суміші дихлорме7,10-7,14 (дд, 1Н), 7,65-7,69 (м, 2Н); НРМС АРСІ тан:метанол:0,88 аміак (з градієнтом від 99:1:0,1 m/z 237 [М+Н]+ до 98:2:0,2 до 95:5:0,5), одержуючи вказану в заПрепаративний приклад 31 головку сполуку у вигляді жовтого масла з 38% (3-Алілокси-4-фторфеніл)метанол виходом, 150мг. 1 До розчину алюмінійлітійгідриду у тетрагідроЯМР(400МГц, CD3OD) : 1,03 (с, 3H), 1,06 (с, фурані (1М, 16,9мл, 16,9ммоль) при 0°С у атмос3H), 1,44-1,53 (м, 2Н), 1,78-1,86 (м, 1Н), 1,93-2,02 фері азоту додавали краплями протягом 20 хви(м, 1Н), 2,50-2,57 (м, 3H), 2,67-2,79 (м, 3H), 4,03лин розчин продукту з препаративного прикладу 4,07 (м, 1Н), 4,41 (с, 2Н), 4,56-4,58 (м, 2Н), 5,2230 (2,0г, 8,47ммоль) у тетрагідрофурані (30мл) і 5,26 (м, 1Н), 5,36-5,41 (м, 1Н), 5,99-6,08 (м, 1Н), розчин залишали нагріватися до кімнатної темпе6,85-6,88 (м, 1Н), 6,98-7,06 (м, 2Н), 7,28-7,43 (м, ратури протягом 5 годин. Суміш охолоджували до 10Н); НРМС ESI m/z 513 [М+Н]+ 0°С і гасили шляхом послідовного додавання краПрепаративний приклад 34 плями води (1мл), водного розчину гідроксиду на5-[(33R)-3-(4-Фтор-3трію (2М, 2мл) і води (3мл) і суміш перемішували пропенілоксибензилокси)піролідин-1-іл]-5-метилпри кімнатній температурі протягом 18 годин. Су2,2-дифенілгексанамід міш фільтрували через Целіт і шар фільтрату Вказану у заголовку сполуку одержували з промивали етилацетатом (3x20мл). Фільтрат відопродукту препаративного прикладу 33, використокремлювали і органічний шар промивалинасичевуючи спосіб, подібний до описаного для прикладу ним сольовим розчином (10мл), сушили над суль2, одержуючи безбарвне масло з 100% виходом. 1 фатом натрію і концентрували у вакуумі, ЯМР(400МГц, CD3OD) : 1,02 (с, 3H), 1,04 (с, одержуючи вказану в заголовку сполуку у вигляді 3H), 1,23-1,32 (м, 2Н), 1,69-1,71 (д, 3H),1,77-1,86 безбарвної рідини з 100% виходом, 1,75г. (м, 1Н), 1,89-1,97 (м, 1Н), 2,40-2,82 (м, 6Н), 4,024,07 (м, 1Н), 4,39 (с, 2Н), 4,88-4,95 (м, 1Н), 6,37
ДивитисяДодаткова інформація
Назва патенту англійськоюCarboxamide derivatives as muscarinic receptor antagonists
Автори англійськоюGlossop Paul Alan, Mantell Simon John, Strang Ross Sinclair, Watson Christine Anne Louise, Wood Anthony
Назва патенту російськоюПроизводные карбоксамида как антагонисты мускариновых рецепторов
Автори російськоюГлоссоп Поль Алан, Мантелл Саймон Джон, Стренг Росс Синклер, Ватсон Кристин Анн Луис, Вуд Энтони
МПК / Мітки
МПК: A61K 31/397, C07D 205/00, C07D 413/12, C07D 211/46, A61P 37/00, C07D 207/12, A61K 31/40, A61K 31/4409
Мітки: карбоксаміду, антагоністи, мускаринових, рецепторів, похідні
Код посилання
<a href="https://ua.patents.su/83-89846-pokhidni-karboksamidu-yak-antagonisti-muskarinovikh-receptoriv.html" target="_blank" rel="follow" title="База патентів України">Похідні карбоксаміду як антагоністи мускаринових рецепторів</a>
Попередній патент: Спосіб керування безконтактним магнітоелектричним двигуном
Наступний патент: Дробарка карпенка
Випадковий патент: Шихта для виготовлення високоглиноземистих вогнетривів