Протиракове лікування комбінацією таксанів та 13-дезоксіантрациклінів
Формула / Реферат
1. Протиракова композиція, що включає:
а) 13-дезоксіантрациклін наступної формули:
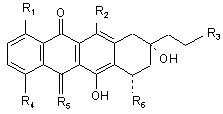 ,
,
де кожний R1, R2 та R3 окремо являє собою Н або ОН;
R4 - це Н, ОН, алкіл або О-алкіл;
R5 - О або NH; і
R6 - це компонент цукру, його фармацевтично прийнятні солі та проліки; і
б) таксан.
2. Композиція за п. 1, в якій 13-дезоксіантрациклін вибрано з групи, що складається з 13-дезоксидоксорубіцину, 13-дезоксидаунорубіцину, 13-дезоксикарміноміцину, 13-дезоксіепірубіцину, 13-дезоксіідарубіцину, 13-дезоксіанаміцину, 13-дезоксіамрубіцину та їх 5-іміноаналогів, а таксаном є паклітаксел або доцетаксел.
3. Фармацевтична композиція, що включає композицію за п. 1 і фармацевтично прийнятний носій або наповнювач.
4. Фармацевтична композиція, що включає композицію за п. 2 і фармацевтично прийнятний носій або наповнювач.
5. Композиція за п. 1, в якій компонентом цукру є даунозамін, епідаунозамін або цукор рамналю.
6. Спосіб лікування раку, який передбачає введення ссавцю, який того потребує, терапевтично ефективної кількості 13-дезоксіантрацикліну наступної формули:
 ,
,
де кожний R1, R2 та R3 окремо являє собою Н або ОН;
R4 - це Н, ОН, алкіл або О-алкіл;
R5 - О або NH; і
R6 - це компонент цукру, його фармацевтично прийнятні солі та проліки; і терапевтично ефективної кількості таксану.
7. Спосіб за п. 6, в якому компонентом цукру є даунозамін, епідаунозамін або цукор рамналю.
8. Спосіб за п. 6, в якому 13-дезоксіантрациклін вибрано з групи, що складається з 13-дезоксидоксорубіцину, 13-дезоксидаунорубіцину, 13-дезоксикарміноміцину, 13-дезоксіепірубіцину, 13-дезоксіідарубіцину, 13-дезоксіанаміцину, 13-дезоксіамрубіцину та їх 5-іміноаналогів, а таксаном є паклітаксел або доцетаксел.
9. Спосіб за п. 6, в якому 13-дезоксіантрациклін і таксан вводять одночасно, окремо у будь-якому порядку або послідовно у будь-якому порядку для забезпечення протиракового ефекту.
Текст
1. Протиракова композиція, що включає: а) 13-дезоксіантрациклін наступної формули: 3 Винахід відноситься до протиракового лікування шляхом уведення в організм таксану, наприклад паклітакселу або доцетакселу, та 13дезоксиантрацикліну. Даний винахід дає можливість досягати поліпшеного протиракового ефекту без незворотної кумулятивної кардіотоксичності. Винахід також відноситься до композицій, що містять таксан і 13-дезоксиантрациклін. Найбільш відомими антрацикліновими протираковими препаратами є доксорубіцин і даунорубіцин, які містять 13-кетогрупу. Доксорубіцин, описаний у пат. США №3590028, має широкий спектр протиракового застосування і використовується при лікуванні лейкозів, лімфом і солідних пухлин. Даунорубіцин, описаний у пат. США №3616242, застосовують при лікуванні гострих лейкозів. Однак використання цих лікарських препаратів обмежується серйозним побічним ефектом кардіотоксичності, так що загальна кількість лікарського препарату, яку можна давати пацієнту, не може перевищувати 550мг/м (E.A.Lefrak et al., Cancer, 32:302, 1973). Навіть при рекомендованій максимальній загальній кумулятивній дозі (430-650мг/м2) або близькій до неї у 60% пацієнтів виникає стійка серцева недостатність і у 14% розвивається гостра серцева недостатність (A.Dresdale et al., Cancer, 52:51, 1983). Отже, хоча ці лікарські препарати є корисними для інгібування росту ракових пухлин, пацієнт може померти від гострої серцевої недостатності через сильний кардіотоксичний побічний ефект цих лікарських препаратів. Було також виявлено, що кардіотоксичність цих антрациклінів викликається метаболічним перетворенням 13-кетогрупи в 13-дигідро-метаболіт спирту (P.S.Mushlin et al., Fed.Proc, 45:809, 1986). В тест-системах, в яких доксорубіцин суттєво не метаболізується в 13-дигідро-метаболіт спирту (доксорубіцинол), значних кардіотоксичних ефектів не спостерігали (P.S.Mushlin et al., Fed. Proc, 44:1274, 198; R.D.Olson et al., Fed. Proc, 45-809, 1986). На відміну від цього, 13-дигідро-метаболіти, доксорубіцинол і даунорубіцинол, викликають кардіотоксичність в тих самих тест-системах при відносно низьких концентраціях (1-2мікрограми/мл, R.D.Olson et al., Proceed. Am. Assoc. Cancer Res., 26:227, 1985; R.D.Olson et al., Proceed. Am. Assoc. Cancer Res., 28:441, 1987). Якщо доксорубіцину дають можливість залишатися в згаданих тест-системах навіть на короткі періоди часу, виникає певне метаболічне перетворення, і 13-дигідро-метаболіт утворюється в значній кількості, так що починає розвиватися кардіотоксичність (L.Rossini et al., Arch. Toxicol. Suppl., 9:474, 1986; M.Del Tocca et al., Pharmacol. Res. Commun., 17:1073, 1985). Отже, накопичена велика кількість даних про те, що кардіотоксичність лікарських препаратів, таких як доксорубіцинол і даунорубіцинол, є результатом сильних кардіотоксичних ефектів, викликаних їхніми 13-дигідрометаболітами (P.Mushlin et al., FASEB Journal, 2:1133, 1988; R.Boucek et al., J. Biol. Chem., 262:15851, 1987; and R.Olson et al., Proc. Natl. 90597 4 Acad. Sci., 85:3585, 1988; Forrest GL, et al., Cancer Res. 60:5158, 2000). Відомо, що доксорубіцин у комбінації з таксанами, наприклад паклітакселом, дає поліпшений протираковий ефект при раку молочної залози порівняно з використанням одного лікарського препарату. Показники протиракової ефективності при застосуванні тільки доксорубіцину при лікуванні раку молочної залози становлять 35-50%. При застосуванні тільки паклітакселу показник ефективності становить 32-62%. Однак в комбінації ці два лікарські препарати можуть дати показники ефективності 83-94% (Gianni L, et al., K Clin Oncol. 13:2688, 1995; Dombernowsk, Ρ et al., Seminars in Oncology 23:23, 1996). На жаль, комбінація паклітакселу та доксорубіцину може викликати клінічну гостру серцеву недостатність у 1820% пацієнтів (Gianni L, et al., K Clin Oncol. 13:2688, 1995; Dombernowsk, Ρ et al., Seminars in Oncology 23:23, 1996). Паклітаксел підсилює кардіотоксичність доксорубіцину, що обмежує або виключає використання антрациклінів у комбінації з таксанами. Кількість випадків гострої серцевої недостатності можна зменшити, зменшуючи дозу доксорубіцину (Giordano SH et al., Clin Cancer Res 8:3360, 2002), але ефективність такої комбінації в результаті цього також зменшиться (Sparano JA et al., J Clin Oncol 17:3828, 1999; Valero V, et al., Semi Oncol 28:15, 2001). Крім того, навіть низькі дози доксорубіцину в комбінації з паклітакселом викликають кардіотоксичність, що проявляється у зменшенні фракції викиду лівого шлуночка (Sparano JA et al., J Clin Oncol 17:3828,1999). Даний винахід вирішує відомі проблеми і пропонує протиракову комбіновану терапію, яка включає використання певних антрациклінів, які у поєднанні з таксанами не викличуть або принаймні значно знизять кардіотоксичність і виключать неприйнятний ризик гострої серцевої недостатності. Це, у свою чергу, забезпечить значний прогрес у лікуванні раку, в тому числі раку молочної залози, порівняно з існуючими методами лікування. Даний винахід стосується способу лікування раку, який передбачає введення ссавцю, в тому числі людині, у разі необхідності, терапевтично ефективної кількості 13-дезоксиантрацикліну наступної формули: де кожний R1, R2 та R3 окремо являє собою Η або ОН; R4 - це Н, ОН, алкіл або О-алкіл; R5 - О або NH; і R6 - це компонент цукру, його фармацевтично прийнятні солі, проліки та суміші, і терапевтично 5 ефективної кількості таксану. Запропонований спосіб можна здійснювати, вводячи 13дезоксиантрациклін і таксан одночасно, окремо у будь-якому порядку або послідовно у будь-якому порядку для забезпечення протиракового ефекту. Інший аспект винаходу стосується композиції, яка забезпечує протираковий, протипухлинний та/або антинеопластичний ефект і є ефективною при лікуванні раку. Запропоновані композиції включають сполуку 13-дезоксиантрацикліну, представлену формулою X: де кожний R1, R2 та R3 окремо являє собою Η або ОН; R4 - це Н, ОН, алкіл або О-алкіл; R5 - О або NH; і R6 - це компонент цукру, його фармацевтично прийнятні солі та проліки, і сполуку таксану, наприклад паклітаксел або доцетаксел. Інші цілі та переваги даного винаходу стануть очевидними з наступного детального опису, в якому описані тільки варіанти, яким віддається перевага і які наведені лише як ілюстрації кращого здійснення винаходу. Зрозуміло, що допустимі інші варіанти, і деякі їх деталі можна модифікувати, не виходячи за межі об'єму винаходу. В зв'язку з цим даний опис слід розглядати тільки як ілюстративний, а не обмежуючий. Фіг.1 і 2 - залежність «доза-ефект» для паклітакселу при інгібуванні росту клітин MCF-7 при застосуванні тільки паклітакселу і в комбінації з ІС30-концентраціями доксорубіцину, даунорубіцину та сполук 13-дезоксиантрацикліну згідно з даним винаходом. Фіг.3 і 4 - залежність «доза-ефект» для паклітакселу при інгібуванні росту лейкозних клітин мишей Р388 при застосуванні тільки паклітакселу і в комбінації з IС10-концентраціями доксорубіцину, даунорубіцину та сполук 13-дезоксиантрацикліну згідно з даним винаходом. Хоча в наступному описі наведені деталі конкретних варіантів даного винаходу, слід розуміти, що винахід не обмежується застосуванням композицій і комбінацій сполук, описаних в наведених прикладах та експериментах, а допускає інші варіанти та способи їх застосування. Застосовані згідно з даним винаходом сполуки 13-дезоксиантрацикліну мають наступну формулу X: 90597 6 де кожний R1, R2 та R3 окремо являє собою Η або ОН; R4 - це Н, ОН, алкіл або О-алкіл; R5 - О або NH; і R6 - це компонент цукру, його фармацевтично прийнятні солі та проліки. Типовими компонентами цукру є даунозамін, епідаунозамін або цукор рамналю. Типовими 13дезокси-сполуками є 13-дезоксидоксорубіцин, 13дезоксидаунорубіцин, 13-дезоксикарміноміцин, 13дезоксиепірубіцин, 13-дезоксиідарубіцин, 13дезоксианаміцин та їх 5-іміно-аналоги. Запропонована комбінована терапія додатково передбачає застосування таксану. Типовими таксанами є паклітаксел і доцетаксел, їхні фармацевтично прийнятні солі та проліки. Запропоновані сполуки можуть утворювати проліки у гідроксильних групах або аміногрупах за допомогою алкокси, амінокислот та інших груп як компонентів, утворюючих проліки. Наприклад, гідроксиметильна група в 4 позиції може утворювати моно-, ди- або трифосфати, і ці фосфати можуть утворювати проліки. Гідроксильну та гідроксиметильну групи можна конвертувати в -ОСН2Р(О)(ОН)2 та проліки фосфонатів. Атом кисню гідроксиметильної групи може конвертуватися в СН2, а потім у СН2Р(О)(ОН)2 та проліки. Пролікарські форми сполук, що містять різні функціональні групи азоту (аміно, гідроксиаміно, амід тощо), можуть включати наступні типи дериватів, в яких кожна група R окремо може бути воднем, заміщеною або незаміщеною алкільною, арильною, алкенільною, алкінільною, гетероциклічною, алкіларильною, аралкільною, аралкенільною, аралкінільною, циклоалкільною або циклоалкенільною групою, як визначалось раніше: (а) карбоксаміди, -NHC(O)R (б) карбамати, -NHC(O)OR (в) (ацилокси)алкілкарбамати, NHC(O)OROC(O)R (г) енаміни, -NHCR(=CHCO2R) або NHCR(=CHCONR2) (д) основи Шиффа, -N=CR2 (e) основи Манніха (з карбоксімідних сполук), RCONHCH2NR2. Препарати таких дериватів проліків описані в різних літературних джерелах (наприклад, Alexander et al., J. med. Chem. 1988, 31, 318; Aligas-Martin et al., PCT WO pp/41531, p. 30). Функціональна група азоту, конвертована при отриманні цих дериватів, являє собою один або більше атомів азоту запропонованої даним винаходом сполуки. Запропоновані пролікарські форми сполук, що містять карбоксильні групи, включають складні ефіри (-CO2R), де група R відповідає будь-якому спирту, вивільнення якого в організмі в результаті ферментних або гідролітичних процесів буде на фармацевтично прийнятних рівнях. Іншою пролікарською формою, отриманою з форми карбонової кислоти, може бути четвертинна сіль типу 7 зі структурою, описаною Bodor et al., J. Med. Chem., 1980, 23, 469. Фармацевтично прийнятні солі запропонованих сполук включають солі, отримані з фармацевтично прийнятних неорганічних або органічних кислот. Приклади відповідних кислот включають соляну, бромистоводневу, сірчану, азотну, хлорну, фумарову, малеїнову, фосфорну, гліколеву, молочну, саліцилову, бурштинову, птолуолсульфонову, винну, оцтову, лимонну, метансульфонову, мурашину, бензойну, малонову, нафталіндисульфонову, трифтороцтову та бензолсульфонову кислоти. Солі, отримані з відповідних основ, включають луги, наприклад натрій та аміак. Нещодавно було відкрито, що 13-дезоксиформи доксорубіцину, даунорубіцину або інших аналогічних антрациклінів метаболічно не конвертуються в кардіотокчисні 13-дигідро-форми і тому не мають незворотної кумулятивної кардіотоксичності. Зокрема, див. міжнародну патентну заявку WO99/08687, патенти США № 5948896 і 5942605 та міжнародну заявку PCT/US99/04704, включені тут як посилання. До цього часу було невідомо, чи матимуть такі антрациклінові протиракові агенти підсилений або навіть синергічний протираковий ефект у комбінації з таксанами. За цим принципом концентрація ІС50 тільки паклітакселу для інгібування росту клітин пухлини молочної залози людини становить 221нМ. За наявності слабких інгібіторних концентрацій запропонованих 13-дезоксиантрациклінів, ІС50 паклітакселу зменшується до 0,55-11нМ. Один паклітаксел не має інгібуючої активності щодо росту лейкозних клітин мишей Р388, але у присутності слабких інгібіторних концентрацій 13-дезоксиантрациклінів ІС50 паклітакселу становить 13-20нМ. У неракових клітинах Н9с2, отриманих від щурів, слабкі інгібіторні концентрації паклітакселу (IC10) зменшують ІС50 13-дезоксидоксорубіцину з 700нМ до 400нМ, зменшують ІС50 13-дезокси-5-імінодоксорубіцину з 1500нМ до 210нМ, але не зменшують ІС50 доксорубіцину, яка залишається такою самою - 210нМ. Запропоновані даним винаходом 13дезоксиантрацикліни у поєднанні з таксанами дають високий протираковий, протипухлинний та/або антинеопластичний ефект. Даний винахід дає можливість підсилити протиракову, протипухлинну та/або антинеопластичну ефективність таксанів низькими дозами 13дезоксиантрациклінів запропонованої формули. Крім того, запропоновані композиції, що включають таксан і 13-дезоксиантрациклін, мають значно меншу кардіотоксичність або не мають її. Запропоноване використання комбінації таксану та 13дезоксиантрацикліну може забезпечити ефективне лікування при низьких дозах порівняно з дозами, необхідними при використанні кожного окремого лікарського препарату. Більш того, використання таксану у поєднанні з 13-дезоксиантрацикліном може забезпечити лі 90597 8 кування, більш безпечне і менш токсичне у порівнянні з використанням кожного окремого лікарського препарату. Важливо зазначити, що 13дезоксиантрациклін і таксан можна застосовувати одночасно, окремо або послідовно. Крім того, запропоноване лікування з використанням комбінації 13-дезоксиантрациклінів і таксанів, виявляє протиракову, протипухлинну та/або антинеопластичну ефективність, яка є корисною для всіх типів терапії при лікуванні злоякісних утворень, неоплазм або пухлин, в тому числі лейкозу, меланоми, пухлин печінки, молочної залози, яєчнику, передміхурової залози, шлунка, підшлункової залози, легенів, нирок, товстої кишки та центральної нервової системи. Запропоноване лікування передбачає спосіб пригнічення росту злоякісних утворень, пухлин та/або неоплазм у ссавців, в тому числі людини. Типова композиція, комбінація, суміш або препарат із запропонованих компонентів являє собою сполуку формули X в комбінації з паклітакселом або доцетакселом. Більш типовою композицією, комбінацією, сумішшю або препаратом є 13дезоксиантрациклін, вибраний з групи, що складається з 13-дезоксидоксорубіцину, 13дезоксидаунорубіцину, 13-дезоксиепірубіцину, 13дезоксиідарубіцину, 13-дезоксианаміцину, 13дезоксикарміноміцину, 13-дезоксиамрубіцину та їх 5-іміно-аналогів, у комбінації з паклітакселом або доцетакселом. Компоненти такої композиції, комбінації, суміші або препарату можна вводити пацієнту одночасно, окремо або послідовно. Ці компоненти можна вводити пацієнту будь-яким способом, прийнятним з медичної точки зору, в тому числі перорально, парентерально, місцево або імплантацією. Пероральне введення включає введення компонентів композицій, комбінацій, сумішей або препаратів у формі таблеток, капсул, таблеток для розсмоктування, суспензій, розчинів, емульсій, порошків, сиропів тощо. Кращим шляхом уведення є парентеральний. Фактичний спосіб і порядок введення компонентів можуть мінятися в залежності від конкретного фармацевтичного складу застосовуваного 13дезоксиантрацикліну формули X, конкретного фармацевтичного складу застосовуваного таксану, конкретного злоякісного утворення, яке лікують, тяжкості хвороби, яку лікують, і конкретного пацієнта, якого лікують. Діапазони доз для введення компонентів можуть мінятися в залежності від віку, стану, статі та ступеня хвороби пацієнта і можуть визначатися фахівцями в цій галузі. Запропонована даним винаходом фармацевтична композиція включає 13-дезоксиантрациклін формули X, змішаний з таксаном у фармацевтично прийнятному носії або наповнювачі. Запропоновані фармацевтичні композиції застосовують у протираковій терапії. Фармацевтично прийнятні носії та наповнювачі добре відомі фахівцям в галузі розробки рецептур сполук у формі фармацевтичних композицій, комбінацій, сумішей та препаратів. Визначення «фармацевтично прийнятний носій» відноситься до одного або більшої кількості сумісних твердого 9 90597 або рідкого наповнювача, розріджувача або інкапсулюючих речовин, придатних для введення ссавцям, в тому числі людині. Фармацевтичні композиції, комбінації, суміші та препарати, придатні для парентерального введення, готують у стерильній формі, якою може бути стерильний розчин або суспензія у прийнятному розріджувачі або розчиннику. Кількість активного інгредієнта, що міститься у фармацевтичній композиції, може значно мінятися в залежності від багатьох факторів, наприклад способу введення та носія. В даному винаході фармацевтична композиція може містити 0,1-1000мг 13-дезоксиантрациклінів формули X і 0,1-1000мг таксану. В запропонованому способі 13дезоксиантрациклін формули X вводять пацієнту, який його потребує, в дозі 0,1-1000мг/м площі поверхні тіла, зазвичай 10-500мг/м площі поверхні тіла, і, як правило, парентерально. Таксан вводять пацієнту, який його потребує, в дозі 0,1-1000мг/м2 площі поверхні тіла, зазвичай 10-500мг/м2 площі поверхні тіла, і, як правило, парентерально. 13дезоксиантрациклін і таксан можна вводити разом (в одній композиції, комбінації, суміші або в одному препараті) або можна вводити окремо у будьякому порядку або послідовно у будь-якому порядку. При окремому введенні другу сполуку, як правило, вводять у межах 72 годин після введення першої сполуки. Завдяки 13-дезоксиантрацикліну формули X протираковий терапевтичний ефект значно збільшується без збільшення токсичності, що частково обумовлено синергізмом між таксаном і 13дезоксиантрацикліном. Дози таксану та 13дезоксиантрациклінів можна вводити так часто, як це необхідно. Фактичний спосіб або порядок уведення будуть мінятися в залежності від конкретної рецептури, композиції, комбінації, суміші або пре 10 парату, конкретного злоякісного утворення, яке лікують, і конкретного пацієнта, якого лікують. Підсилена дія запропонованої комбінації 13дезоксиантрацикліну і таксану описана у вигляді прикладів у наступних тестах, які ілюструють, а не обмежують даний винахід. Протираковий ефект 13-дезоксиантрациклінів In vivo протиракову активність доксорубіцину (сполука І), 13-дезоксидоксорубіцину (сполука II) та 5-іміно-13-дезоксидоксорубіцину (сполука III) тестували на мишиній моделі лейкозу, використовуючи мишей CD2F1, яким увели клітини Р388 (лейкозні клітини від мишей). Групам мишей CD2F1 інтраперитонеально вводили 1 мільйон клітин Р388. В кожній групі було по 10 мишей. В доксорубіциновій групі 0,8мг/кг доксорубіцину вводили інтраперитонеально послідовно упродовж 9 днів всі 1-9 дні дослідження. 13дезоксидоксорубіцин вводили інтраперитонеально в дозі 1,6мг/кг і 5-іміно-13-дезоксидоксорубіцин вводили інтраперитонеально в дозі 3,2мг/кг, по схемі введення доксорубіцину. Контрольній групі вводили носій. Середній час виживання обчислювали для кожної групи. Активність сполуки виражають як тривалість пролонгованого виживання (середнє виживання лікованої групи (Т), поділене на середній час виживання контрольної групи (С) і помножене на 100, Т/С%). Результати наведені в таблиці 1. Як видно, доксорубіцин дає значний протипухлинний ефект - збільшення на 147% середнього часу виживання. 13-дезоксидоксорубіцин і 5-іміно-13-дезоксидоксорубіцин також дають значне збільшення середнього часу виживання, яке несуттєво відрізняється від ефекту доксорубіцину. Результати цих досліджень показують, що 13дезоксиантрацикліни мають протиракову ефективність, аналогічну ефективності доксорубіцину, хоча при різних дозах. Таблиця 1 Протираковий ефект доксорубіцину та 13-дезоксиантрациклінів у мишей, інфікованих мишиним лейкозом Р388 (Т/С=середній час виживання лікованих мишей, поділений на середній час виживання контрольних мишей і помножений на 100; n=10) Група Контрольна Доксорубіцин (І) Сполука II Сполука (III) Доза, мг/кг/день 0 0,8 1,6 3,2 Середній час виживання, дні 19 28 27 27 Т/С, % 100 147* 142* 142* * p
ДивитисяДодаткова інформація
Назва патенту англійськоюAnticancer treatment with a combination of taxanes and 13-deoxyanthracyclines
Автори англійськоюOlson Richard D., Walsh Gerald M.
Назва патенту російськоюПротивораковое лечение комбинацией таксанов и 13-дезоксиантрациклинов
Автори російськоюОлсон Ричард Д., Волш Джеральд М.
МПК / Мітки
МПК: A61K 9/14, A61P 35/00, A61K 31/704, A61K 31/337
Мітки: 13-дезоксіантрациклінів, комбінацією, лікування, протиракове, таксанів
Код посилання
<a href="https://ua.patents.su/10-90597-protirakove-likuvannya-kombinaciehyu-taksaniv-ta-13-dezoksiantracikliniv.html" target="_blank" rel="follow" title="База патентів України">Протиракове лікування комбінацією таксанів та 13-дезоксіантрациклінів</a>
Попередній патент: Конструкція несучого елемента для зубців
Наступний патент: Спосіб виробництва желейного наповнювача для харчових продуктів
Випадковий патент: Торцева фреза












