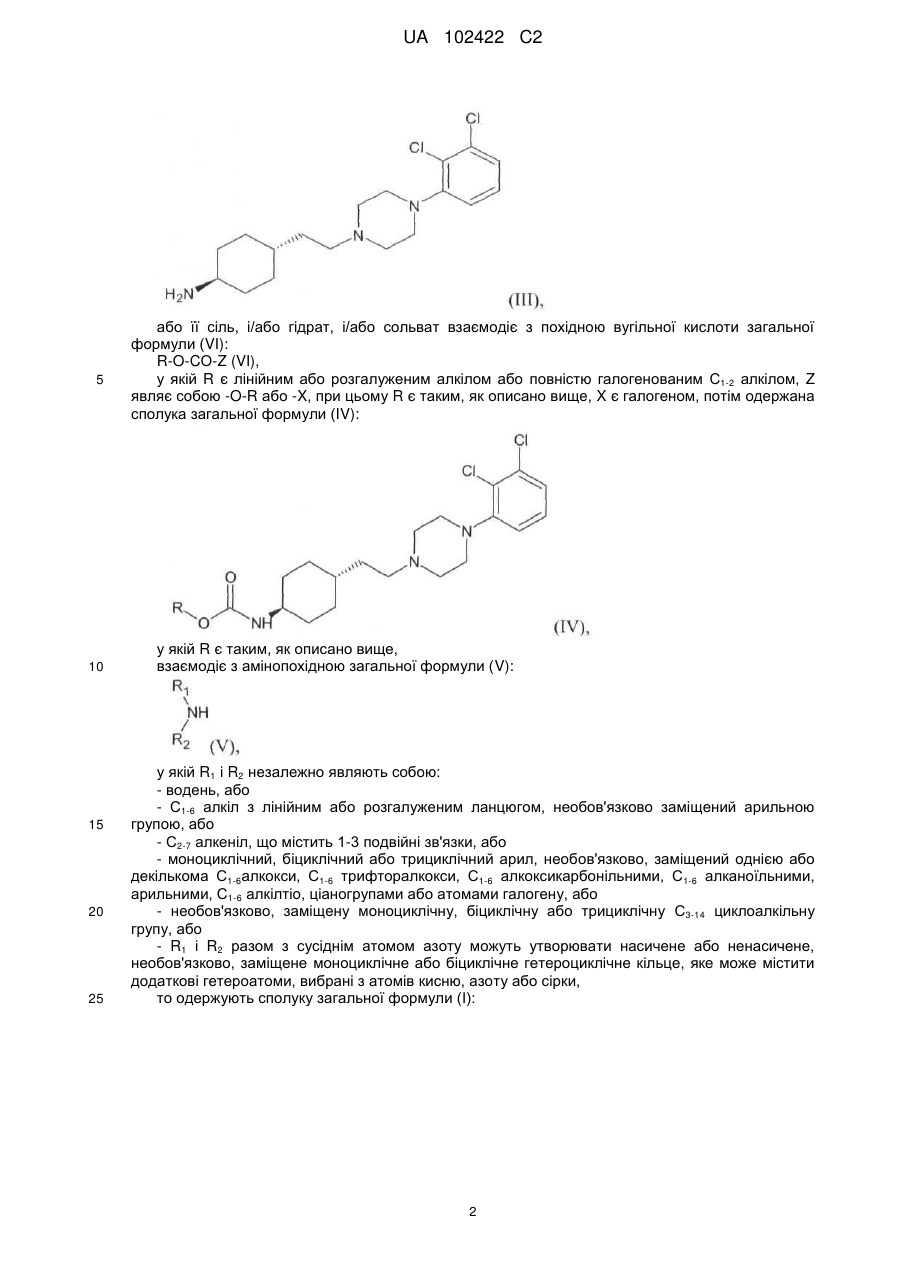
Спосіб одержання сполук ряду піперазину та їх солянокислих солей
Номер патенту: 102422
Опубліковано: 10.07.2013
Автори: Цібула Ласло, Нограді Каталін, Юхас Балінт, Галамбош Янош, Шебок Ференц, Агаїне Чонгор Ева
Формула / Реферат
1. Спосіб одержання сполуки загальної формули (І):
 , (І)
, (І)
у якій R1 і R2 незалежно являють собою:
- водень або
- С1-6 алкіл з лінійним або розгалуженим ланцюгом, необов'язково заміщений арильною групою, або
- С2-7 алкеніл, що містить 1-3 подвійні зв'язки, або
- моноциклічний, біциклічний, або трициклічний арил, необов'язково заміщений однією або декількома С1-6 алкокси, С1-6 трифторалкокси, С1-6 алкоксикарбонільними, С1-6 алканоїльними, арильними, С1-6 алкілтіо, ціаногрупами або атомами галогену, або
- необов'язково заміщену моноциклічну, біциклічну або трициклічну С3-14 циклоалкільну групу, або
- R1 і R2 разом з сусіднім атомом азоту утворюють насичене або ненасичене, необов'язково заміщене моноциклічне або біциклічне гетероциклічне кільце, яке може містити додаткові гетероатоми, вибрані з атомів кисню, азоту або сірки та її солянокислих солей, і/або гідратів, і/або сольватів, який відрізняється тим, що транс-4-{2-[4-(2,3-дихлорфеніл)піперазин-1-іл]етил}циклогексиламін формули (III):
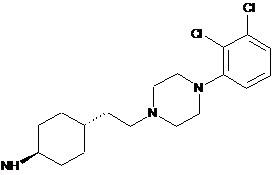 (Ш)
(Ш)
або його сіль, або гідрат, або сольват розчиняють або суспендують в інертному розчиннику в присутності основи, потім додають похідну вугільної кислоти загальної формули (VI):
R-O-CO-Z , (VI)
у якій R є С1-6 алкілом з лінійним або розгалуженим ланцюгом або повністю галогенованим С1-2 алкілом, Ζ являє собою -O-R або -X, при цьому R є таким, як описано вище, X є галогеном, і одержану сполуку загальної формули (IV):
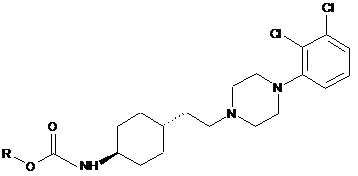 , (IV)
, (IV)
у якій R є таким, як описано вище,
in situ або, необов'язково, у виділеному стані піддають взаємодії з аміном загальної формули (V):
![]() , (V)
, (V)
у якій R1 і R2 є такими, як описано вище, з одержанням сполуки загальної формули (І) і потім, необов'язково, одержують її солянокислі солі і/або гідрати, і/або сольвати.
2. Спосіб за п. 1, який відрізняється тим, що похідна вугільної кислоти загальної формули (VI) являє собою складний ефір хлормурашиної кислоти або біс(трихлорметил)карбонат.
3. Спосіб за п. 1, який відрізняється тим, що взаємодію сполук загальної формули (IV) і (V) здійснюють in situ без виділення сполуки загальної формули (IV).
Текст
Реферат: Винахід належить до нового способу одержання сполуки загальної формули (І): Cl Cl N N O R1 N R2 N H (I), а також її солянокислих солей і/або гідратів, і/або сольватів, розчиненням або суспендуванням транс-4-{2-[4-(2,3-дихлорфеніл)піперазин-1-іл]етил}циклогексиламіну формули (III) або її солі, або гідрату, або сольвату в інертному розчиннику в присутності основи, потім додаванням похідної вугільної кислоти загальної формули (VI), в якій R є С1-6 алкілом з лінійним або розгалуженим ланцюгом або повністю галогенованим С 1-2 алкілом, Ζ являє собою -O-R або -X, UA 102422 C2 (12) UA 102422 C2 при цьому R є таким, як описано вище, X є галогеном, і взаємодією одержаної сполуки загальної формули (IV), в якій R є таким, як описано вище, in situ або, необов'язково, у виділеному стані з аміном загальної формули (V), в якій R1 і R2 є такими, як описано вище, з одержанням сполуки загальної формули (І), а потім, необов'язково, одержанням її солянокислих солей і/або гідратів, і/або сольватів. UA 102422 C2 Галузь техніки, до якої належить винахід Винахід відноситься до нового способу одержання транс-N-{4-{2-[4-(2,3дихлорфеніл)піперазин-1-іл]етил}циклогексил}карбамідів загальної формули (І): 5 10 15 20 25 30 35 у якій R1 і R2 незалежно являють собою: - водень, або - С1-6 алкіл з лінійним або розгалуженим ланцюгом, необов'язково заміщений арильною групою, або - R1 і R2 разом з сусіднім атомом азоту можуть утворювати, необов'язково, заміщене, насичене або ненасичене, моноциклічне або біциклічне гетероциклічне кільце, яке може містити додаткові гетероатоми, вибрані з атомів кисню, азоту або сірки, - С2-7 алкеніл, що містить 1-3 подвійні зв'язки, або - моноциклічну, біциклічну або трициклічну арильну групу, необов'язково заміщену однією або декількома С1-6 алкокси, С1-6 трифторалкокси, С1-6 алкоксикарбонільними, С1-6 алканоїльними, арильними, С1-6 алкілтіо, ціаногрупами або атомами галогену, - необов'язково, заміщену моноциклічну, біциклічну або трициклічну С 3-14 циклоалкільну групу, та - їхніх солянокислих солей, і/або гідратів, і/або сольватів. Попередній рівень техніки Основна форма сполук загальної формули (І) спочатку була розкрита в патенті Угорщини № Р0302451. В описі до даного патенту наведено три шляхи (способи А, В, С) реакцій для одержання основної форми сполук формули (І). У способі "А" відповідний амін піддають взаємодії з (тіо)карбамоїлхлоридом для одержання кінцевого продукту загальної формули (І). У способі "А" за патентом Р0302451 одержують продукт з виходом лише 65 % при дуже довгому часі реакції. За способом В ізо(тіо)ціанат піддають взаємодії з аміносполукою. Недолік способу "В" полягає в тому, що при використанні даного способу можна одержати лише сполуки загальної формули (І), в яких одна з груп R1 і R2 являє собою водень. Згідно із способом "С" за патентом Р0302451, відповідний амін перетворюють на ізо(тіо)ціанатну похідну, потім дану ізо(тіо)ціанатну похідну піддають взаємодії з аміном для одержання бажаних кінцевих продуктів формули (І). Загальний вихід за способом С є дуже низьким, лише 52 %. Недоліками способів "А" і "С" є тривалий час реакції (48 і 20 годин) і низькі виходи (65 % і 52 %). Крім того, в способах "А" і "С" одержаний кінцевий продукт необхідно очищати на додатковій стадії очищення (перекристалізація) для одержання продукту відповідної якості. Суть винаходу Мета авторів полягала в розробці способу, який дозволяє одержувати незаміщені, а також моно- і дизаміщені карбаміди загальної формули (І) з високим виходом. Автори несподівано виявили, що коли транс-4-{2-[4-(2,3-дихлорфеніл)піперазин-1іл]етил}циклогексиламін формули (III): 1 UA 102422 C2 5 10 15 20 25 або її сіль, і/або гідрат, і/або сольват взаємодіє з похідною вугільної кислоти загальної формули (VI): R-O-CО-Z (VI), у якій R є лінійним або розгалуженим алкілом або повністю галогенованим С1-2 алкілом, Z являє собою -O-R або -X, при цьому R є таким, як описано вище, X є галогеном, потім одержана сполука загальної формули (IV): у якій R є таким, як описано вище, взаємодіє з амінопохідною загальної формули (V): у якій R1 і R2 незалежно являють собою: - водень, або - С1-6 алкіл з лінійним або розгалуженим ланцюгом, необов'язково заміщений арильною групою, або - С2-7 алкеніл, що містить 1-3 подвійні зв'язки, або - моноциклічний, біциклічний або трициклічний арил, необов'язково, заміщений однією або декількома С1-6алкокси, С1-6 трифторалкокси, С1-6 алкоксикарбонільними, С1-6 алканоїльними, арильними, С1-6 алкілтіо, ціаногрупами або атомами галогену, або - необов'язково, заміщену моноциклічну, біциклічну або трициклічну С3-14 циклоалкільну групу, або - R1 і R2 разом з сусіднім атомом азоту можуть утворювати насичене або ненасичене, необов'язково, заміщене моноциклічне або біциклічне гетероциклічне кільце, яке може містити додаткові гетероатоми, вибрані з атомів кисню, азоту або сірки, то одержують сполуку загальної формули (І): 2 UA 102422 C2 у якій R1 і R2 є такими, як описано вище, з дуже високим виходом. Здійснення винаходу Винахід відноситься до нового способу одержання сполук загальної формули (І): 5 10 15 20 у якій R1 і R2 незалежно являють собою: - водень, або - С1-6 алкіл з лінійним або розгалуженим ланцюгом, необов'язково заміщеною арильною групою, або - С2-7 алкеніл, що містить 1-3 подвійні зв'язки, або - моноциклічну, біциклічну або трициклічну арильну групу, необов'язково заміщену однією або декількома С1-6 алкокси, С1-6 трифторалкокси, С1-6 алкоксикарбонільними, С1-6 алканоїльними, арильними, С1-6 алкілтіо, ціаногрупами або атомами галогену, або - необов'язково, заміщену моноциклічну, біциклічну або трициклічну С 3-14 циклоалкільну групу, або - R1 і R2 разом з сусіднім атомом азоту можуть утворювати насичене або ненасичене, необов'язково заміщене моноциклічне або біциклічне гетероциклічне кільце, яке може містити додаткові гетероатоми, вибрані з атомів кисню, азоту або сірки, та їхніх солянокислих солей, і/або гідратів, і/або сольватів. Арильна група в значенні R1 і R2 являє собою, наприклад, фенільну, толільну, нафтильну або фенантрильну групи. При здійсненні способу за винаходом транс-4-{2-[4-(2,3-дихлорфеніл)піперазин-1іл]етил}циклогексиламін формули (III): 3 UA 102422 C2 або її сіль, або гідрат, або сольват розчиняють або суспендують в інертному розчиннику у присутності основи й піддають взаємодії з похідною вугільної кислоти загальної формули (VI): 5 у якій R є С1-6 алкілом з лінійним або розгалуженим ланцюгом або повністю галогенованим С1-2 алкілом, Z являє собою -O-R або -X, при цьому R є таким, як описано вище, X є галогеном, з одержанням сполуки загальної формули (IV): у якій R є С1-6 алкільною або повністю галогенованою С1-2 алкільною групою. Потім одержані сполуки загальної формули (IV) піддають взаємодії з аміном загальної формули (V): 10 15 20 25 30 35 40 45 у якій R1 і R2 є такими, як описано вище, з одержанням сполуки загальної формули (І). Вказану вище реакцію можна здійснювати in situ в інертному розчиннику або після виділення сполуки загальної формули (IV). Відповідні розчинники, які можна використовувати в способі за даним винаходом, включають інертні розчинники, що не змішуються з водою, наприклад толуол, дихлорметан, хлорбензол або ксилол. У переважному варіанті здійснення винаходу розчинником є дихлорметан. Відповідні основи, які можна використовувати в способі за даним винаходом, включають органічні основи, переважно третинні аміни, наприклад, триетиламін. Як замісники похідних вугільної кислоти загальної формули (VI), коли R являє собою повністю галогеновану алкільну групу, алкільна група може означати, наприклад, трихлорметильну або пентахлоретильну групу. В переважному варіанті здійснення винаходу похідною вугільної кислоти є складний ефір хлормурашиної кислоти або бістрихлорметилкарбонат. При виконанні способу за даним винаходом взаємодію між сполуками загальної формули (IV) і (V) можна здійснювати таким чином, що після стадії виділення уретанову сполуку загальної формули (IV) піддають взаємодії з аміном загальної формули (V). Проте, внаслідок труднощів виділення сполук загальної формули (IV), вказану вище реакцію переважно можна здійснювати in situ в інертному розчиннику таким чином, що відповідний амін загальної формули (V) додають до реакційної суміші сполук формул (III) і (VI). У даному останньому випадку, виходячи із сполуки формули (III), не виділяючи сполуку загальної формули (IV), одержують сполуку загальної формули (І) з високим виходом вище 90 %. З огляду на відомі публікації переваги способу за даним винаходом є наступними: вихід збільшується від 52-65 % до 95 %, і при використанні способу, окрім N-монозаміщених сполук формули (І), можна також одержати N-дизаміщені сполуки. Винахід відноситься також до способу одержання тpaнс-N-{4-{2-[4-(2,3дихлорфеніл)піперазин-1-іл]етил}циклогексил}карбаміду у формі основи загальної формули (І) і її солянокислих солей. У варіанті здійснення винаходу для одержання транс-N-{4-{2-[4-(2,3-дихлорфеніл)піперазин1-іл]етил}циклогексил} карбаміду у формі основи загальної формули (І) обробку реакційної суміші виконують таким чином, що після розбавлення водою реакційну суміш екстрагують органічним розчинником, і основну сполуку формули (І) можна виділяти відомим способом, переважно видаленням розчинника. У переважному варіанті здійснення винаходу основу не виділяють, але після розбавлення водою реакційну суміш підкисляють соляною кислотою до рівня рН, рівного 2-4, потім реакційну 4 UA 102422 C2 5 10 15 20 25 30 35 40 45 50 55 60 суміш перетворюють на водну суспензію перегонкою і виділяють солянокислу сіль сполуки загальної формули (І) високої міри чистоти й виходом вище 90 %. Приклади Винахід ілюструється наступними необмежуючими прикладами. Приклад 1 Метиловий ефір транс-N-(4-{2-[4-(2,3-дихлорфеніл)піперазин-1іл]етил}циклогексил)карбамінової кислоти 6,45 г (0,015 моль) дигідрохлориду сполуки формули (III) додавали до суміші 125 мл дихлорметану і 12,25 мл триетиламіну й перемішували одержану густу суспензію при температурі 20-25 °C протягом однієї години. Одержану таким чином суспензію додавали до розчину 2,3 мл (0,03 моль) метилхлорформіату в 25 мл дихлорметану при температурі 5-10 °C. Одержану реакційну суміш перемішували при температурі 20-25 °C протягом 3 годин, потім екстрагували 3 × 150 мл (150 г) дистильованої води. Органічну фазу випаровували у вакуумі й залишок перекристалізовували з метанолу. Таким чином одержано 4,5 г сполуки, вказаної в заголовку. Вихід: 72 %. Температура плавлення: 143-147 °C. Приклад 2 Гзопропіловий ефір транс-N-(4-{2-[4-(2,3-дихлорфеніл)піперазин-1іл]етил}циклогексил)карбамінової кислоти 6,45 г (0,015 моль) дигідрохлориду сполуки формули (III) додавали до суміші 125 мл дихлорметану і 12,25 мл триетиламіну й перемішували одержану густу суспензію при температурі 20-25 °C протягом однієї години. Суспензію додавали до розчину 3,7 г (0,03 моль) ізопропілхлорформіату в 30 мл толуолу при температурі 5-10 °C. Реакційну суміш перемішували при температурі 20-25 °C протягом 3 годин, потім екстрагували 3 × 150 мл (150 г) дистильованої води. Органічну фазу випаровували у вакуумі й одержаний залишок перекристалізовували з ізопропанолу. Таким чином одержано 4,4 г сполуки, вказаної в заголовку. Вихід: 67 %. Температура плавлення: 128-131 °C. Приклад 3 Транс-4-{2-[4-(2,3-дихлорфеніл)піперазин-1-іл]етил}-]N,Nдиметилкарбамоїлциклогексиламіну 6,45 г (0,015 моль) дигідрохлориду сполуки формули (III) додавали до суміші 125 мл дихлорметану і 12,25 мл триетиламіну й перемішували одержану густу суспензію при температурі 20-25 °C протягом однієї години. Суспензію додавали до розчину 4,9 г біс(трихлорметил)карбонату в 50 мл дихлорметану при температурі -5-(-10) °С протягом однієї години. Одержану реакційну суміш додавали до розчину 13 г диметиламіну в 100 мл ізопропілового спирту (ІРА) (40 мл; 0,12 моль), охолодженому при температурі 0-(-10) °С, протягом даної операції температуру реакційної суміші підтримували нижче 0 °C. Після перемішування при температурі 0-(-5) °С протягом 30 хвилин до реакційної суміші при перемішуванні додавали 100 мл дистильованої води. Потім рівень рН водної фази встановлювали рівним 7-8 додаванням концентрованої соляної кислоти й реакційну суміш випаровували в вакуумі до об'єму 130 мл. До одержаної реакційної суміші додавали додаткові 70 мл дистильованої води й випаровували суміш у вакуумі до 170 мл. Суспензію перемішували при 20-25 °C протягом однієї години й виділяли одержаний продукт фільтрацією. Таким чином одержано 6,6 г сполуки, вказаної в заголовку. Вихід: 95 %. Температура плавлення: 208-211 °C. Приклад 4 Гідрохлорид транс-4-{2-[4-(2,3-дихлорфеніл)піперазин-1-іл]етил}-N,Nдиметилкарбамоїлциклогексиламіну 6,45 г (0,015 моль) дигідрохлориду сполуки формули (III) додавали до суміші 125 мл дихлорметану і 12,25 мл триетиламіну й перемішували одержану густу суспензію при температурі 20-25 °C протягом однієї години. Суспензію додавали до розчину 4,9 г біс(трихлорметил)карбонату в 50 мл дихлорметану при температурі -5-(-10) °С протягом однієї години. Одержану реакційну суміш додавали до розчину 13 г диметиламіну в 100 мл ізопропілового спирту (IPА) (40 мл; 0,12 моль), охолодженому при температурі 0-(-10) °С, протягом даної операції температуру реакційної суміші підтримували нижче 0 °C. Після перемішування при температурі 0-(-5) °С протягом 30 хвилин до реакційної суміші при 5 UA 102422 C2 5 10 15 20 25 30 35 40 45 50 55 60 перемішуванні додавали 100 мл дистильованої води. Потім рівень рН водної фази встановлювали рівним 2-3 додаванням концентрованої соляної кислоти й реакційну суміш випаровували до об'єму 130 мл, додавали додаткові 70 мл дистильованої води й випаровували суміш до об'єму 170 мл. Суспензію перемішували при 20-25 °C протягом однієї години й виділяли одержаний продукт фільтрацією. Таким чином одержано 6,7 г сполуки, вказаної в заголовку. Вихід: 96 %. Температура плавлення: 221-224 °C. Приклад 5 Гідрохлорид транс-4-{2-[4-(2,3-дихлорфеніл)піперазин-1-іл]етил}-N,Nдиметилкарбамоїлциклогексиламіну 6,72 г (0,015 моль) моногідрату дигідрохлориду сполуки формули (III) додавали до суміші 125 мл дихлорметану і 12,25 мл триетиламіну й перемішували одержану густу суспензію при температурі 20-25 °C протягом однієї години. Суспензію додавали до розчину 4,9 г біс(трихлорметил)карбонату в 50 мл дихлорметану при температурі -5-(-10) °С протягом однієї години. Одержану реакційну суміш додавали до розчину 13 г диметиламіну в 100 мл ізопропілового спирту (ІРА) (40 мл; 0,12 моль), охолодженого при температурі 0-(-10) °С, протягом даної операції температуру реакційної суміші підтримували нижче 0 °C. Після перемішування при температурі 0-(-5) °С протягом 30 хвилин до реакційної суміші додавали 100 мл дистильованої води й рівень рН водної фази встановлювали рівним 2-3 додаванням концентрованої соляної кислоти. Реакційну суміш випаровували у вакуумі до об'єму 130 мл, потім додавали додаткові 70 мл води й випаровували суміш до об'єму 170 мл. Суспензію перемішували при температурі 20-25 °C протягом однієї години й виділяли одержаний продукт фільтрацією. Таким чином одержано 6,7 г сполуки, вказаної в заголовку. Вихід: 96 %. Температура плавлення: 221-224 °C. Приклад 6 1-транс-{4-[2-(4-(2,3-дихлорфеніл)піперазин-1-іл(етил]циклогексил}карбамід 6,45 г (0,015 моль) дигідрохлориду сполуки формули (III) додавали до суміші 160 мл дихлорметану і 12,8 мл триетиламіну й перемішували одержану густу суспензію при температурі 20-25 °C протягом однієї години. Суспензію додавали до розчину 4,9 г біс(трихлорметил)карбонату в 75 мл дихлорметану при температурі -5-(-10) °С протягом однієї години. Одержану реакційну суміш додавали до розчину аміаку в метанолі (110 мл, 17 г/100 мл), охолодженому при температурі 0-(-10) °С, протягом даної операції температуру реакційної суміші підтримували нижче 0 °C. Після перемішування при температурі 0-(-5) °С протягом 30 хвилин реакційну суміш випаровували у вакуумі до об'єму 100 мл, потім додавали 800 мл дистильованої води. Суспензію перемішували при 20-25 °C протягом однієї години й виділяли одержаний продукт фільтрацією. Таким чином одержано 5,6 г сполуки, вказаної в заголовку. Вихід: 94 %. Температура плавлення: 221-224 °C. Приклад 7 Гідрохлорид транс-N-{4-{2-[4-(2,3-дихлорфеніл)піперазин-1-іл]етил}циклогексил}-N'метилкарбаміду 6,45 г (0,015 моль) дигідрохлориду сполуки формули (III) додавали до суміші 125 мл дихлорметану і 12,25 мл триетиламіну й перемішували одержану густу суспензію при температурі 20-25 °C протягом однієї години. Суспензію додавали до розчину 4,9 г біс(трихлорметил)карбонату в 50 мл дихлорметану при температурі -5-(-10) °С протягом однієї години. Одержану реакційну суміш додавали до розчину метиламіну в ізопропіловому спирті (IPА) (60 мл, 12,5 г/100 мл), охолодженому при температурі 0-(-10) °С, протягом даної операції температуру реакційної суміші підтримували нижче 0 °C. Після перемішування при температурі 0-(-5) °С протягом 30 хвилин до реакційної суміші додавали 130 мл дистильованої води, потім рівень рН водної фази встановлювали рівним 2-3 додаванням концентрованої соляної кислоти. Реакційну суміш випаровували у вакуумі до об'єму 120 мл і додавали додаткові 70 мл дистильованої води. Суспензію перемішували при температурі 20-25 °C протягом однієї години і виділяли одержаний продукт фільтрацією. Таким чином одержано 6,6 г сполуки, вказаної в заголовку. Вихід: 95 %. Температура плавлення: 230-255 °C. 6 UA 102422 C2 5 10 15 20 25 30 35 40 45 50 Приклад 8 Гідрохлорид транс-N-{4-{2-[4-(2,3-дихлорфеніл)піперазин-1-іл]етил}циклогексилкарбаміду 6,45 г (0,015 моль) дигідрохлориду сполуки формули (III) додавали до суміші 160 мл дихлорметану і 12,8 мл триетиламін і перемішували одержану густу суспензію при температурі 20-25 °C протягом однієї години. Суспензію додавали до розчину 4,9 г біс(трихлорметил)карбонату в 75 мл дихлорметану при температурі -5-(-10) °С протягом однієї години. Одержану реакційну суміш додавали до розчину аміаку в метанолі (110 мл, 17 г/100 мл), охолодженому при температурі 0-(-10) °С, протягом даної операції температуру реакційної суміші підтримували нижче 0 °C. Після перемішування при 0-10 °C протягом 30 хвилин реакційну суміш випаровували у вакуумі до об'єму 20 мл, потім додавали 140 мл дистильованої води. Рівень рН водної фази встановлювали рівним 2-3 додаванням концентрованої соляної кислоти. Суспензію перемішували при температурі 20-25 °C протягом однієї години й виділяли одержаний продукт фільтрацією. Таким чином одержано 5,86 г сполуки, вказаної в заголовку. Вихід: 90 %. Температура плавлення: 250-253 °C (розкладається). Приклад 9 Амід транс-N-{4-{2-[4-(2,3-дихлорфеніл)піперазин-1-іл]етил}циклогексил}морфолін-4карбонової кислоти 6,45 г (0,015 моль) дигідрохлориду сполуки формули (III) додавали до суміші 125 мл дихлорметану і 12,25 мл триетиламіну й перемішували одержану густу суспензію при температурі 20-25 °C протягом однієї години. Суспензію додавали до розчину 4,9 г біс(трихлорметил)карбонату в 50 мл дихлорметану при температурі -5-(-10) °С протягом однієї години. Одержану таким чином реакційну суміш додавали до розчину 10,44 г (0,12 моль) морфоліну в 70 мл ізопропілового спирту (IPА), охолодженого при температурі 0-(-10) °С, протягом даної операції температуру реакційної суміші підтримували нижче 0 °C. Після перемішування при 0-10 °C протягом 30 хвилин до реакційної суміші при перемішуванні додавали 100 мл дистильованої води й встановлювали рівень рН водної фази рівним 7-8 додаванням концентрованої соляної кислоти. Реакційну суміш випаровували у вакуумі до об'єму 130 мл і додавали додаткові 100 мл дистильованої води. Об'єм реакційної суміші зменшувався у вакуумі до 150 мл. Суспензію перемішували при температурі 20-25 °C протягом однієї години й виділяли одержаний продукт фільтрацією. Таким чином одержано 6,55 г сполуки, вказаної в заголовку. Вихід: 93 %. Температура плавлення: 204-206 °C (розкладається). Приклад 10 Гідрохлорид аміду транс-N-{4-{2-[4-(2,3-дихлорфеніл)піперазин-1іл]етил}циклогексил}морфолін-4-карбонової кислоти 6,45 г (0,015 моль) дигідрохлориду сполуки формули (III) додавали до суміші 125 мл дихлорметану і 12,25 мл триетиламіну й перемішували одержану густу суспензію при температурі 20-25 °C протягом однієї години. Суспензію додавали до розчину 4,9 г біс(трихлорметил)карбонату в 50 мл дихлорметану при температурі -5-(-10) °С протягом однієї години. Одержану таким чином реакційну суміш додавали до розчину 10,44 г (0,12 моль) морфоліну в 70 мл ізопропілового спирту (IPА), охолодженого при температурі 0-(-10) °С, протягом даної операції температуру реакційної суміші підтримували нижче 0 °C. Після перемішування при 0-10 °C протягом 30 хвилин до реакційної суміші при перемішуванні додавали 100 мл дистильованої води, потім встановлювали рівень рН водної фази рівним 2-3. Реакційну суміш випаровували у вакуумі до об'єму 130 мл і додавали додаткові 100 мл дистильованої води. Потім зменшували у вакуумі об'єм реакційної суміші до 150 мл. Суспензію перемішували при температурі 20-25 °C протягом однієї години й виділяли одержаний продукт фільтрацією. Таким чином одержано 7,1 г сполуки, вказаної в заголовку. Вихід: 94 %. Температура плавлення: 197 °C (розкладається). 55 7 UA 102422 C2 ФОРМУЛА ВИНАХОДУ 1. Спосіб одержання сполуки загальної формули (І): Cl Cl N N O R1 5 10 15 20 N N H R2 , (І) у якій R1 і R2 незалежно являють собою: - водень або - С1-6 алкіл з лінійним або розгалуженим ланцюгом, необов'язково заміщений арильною групою, або - С2-7 алкеніл, що містить 1-3 подвійні зв'язки, або - моноциклічний, біциклічний, або трициклічний арил, необов'язково заміщений однією або декількома С1-6 алкокси, С1-6 трифторалкокси, С1-6 алкоксикарбонільними, С1-6 алканоїльними, арильними, С1-6 алкілтіо, ціаногрупами або атомами галогену, або - необов'язково заміщену моноциклічну, біциклічну або трициклічну С 3-14 циклоалкільну групу, або - R1 і R2 разом з сусіднім атомом азоту утворюють насичене або ненасичене, необов'язково заміщене моноциклічне або біциклічне гетероциклічне кільце, яке може містити додаткові гетероатоми, вибрані з атомів кисню, азоту або сірки та її солянокислих солей, і/або гідратів, і/або сольватів, який відрізняється тим, що транс-4-{2-[4-(2,3-дихлорфеніл)піперазин-1іл]етил}циклогексиламін формули (III): Cl Cl N N 25 NH (III) або його сіль, або гідрат, або сольват розчиняють або суспендують в інертному розчиннику в присутності основи, потім додають похідну вугільної кислоти загальної формули (VI): R-O-CO-Z , (VI) у якій R є С1-6 алкілом з лінійним або розгалуженим ланцюгом або повністю галогенованим С 1-2 алкілом, Ζ являє собою -O-R або -X, при цьому R є таким, як описано вище, X є галогеном, і одержану сполуку загальної формули (IV): 8 UA 102422 C2 Cl Cl N N O R O NH , (IV) у якій R є таким, як описано вище, in situ або, необов'язково, у виділеному стані піддають взаємодії з аміном загальної формули (V): R1 NH 5 10 R2 , (V) у якій R1 і R2 є такими, як описано вище, з одержанням сполуки загальної формули (І) і потім, необов'язково, одержують її солянокислі солі і/або гідрати, і/або сольвати. 2. Спосіб за п. 1, який відрізняється тим, що похідна вугільної кислоти загальної формули (VI) являє собою складний ефір хлормурашиної кислоти або біс(трихлорметил)карбонат. 3. Спосіб за п. 1, який відрізняється тим, що взаємодію сполук загальної формули (IV) і (V) здійснюють in situ без виділення сполуки загальної формули (IV). Комп’ютерна верстка Л. Литвиненко Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 9
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of piperazine compounds and hydrochloride salts thereof
Автори англійськоюCzibula, Laszlo, Juhasz, Balint, Againe Csongor, Eva, Sebok, Ferenc, Galambos, Janos, Nogradi, Katalin
Назва патенту російськоюСпособ получения соединений ряда пиперазина и их солянокислых солей
Автори російськоюЦибула Ласло, Юхас Балинт, Агаине Чонгор Эва, Шебек Ференц, Галамбош Янош, Ногради Каталин
МПК / Мітки
МПК: C07D 295/135
Мітки: солянокислих, піперазину, ряду, сполук, одержання, солей, спосіб
Код посилання
<a href="https://ua.patents.su/11-102422-sposib-oderzhannya-spoluk-ryadu-piperazinu-ta-kh-solyanokislikh-solejj.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання сполук ряду піперазину та їх солянокислих солей</a>
Попередній патент: Спосіб оксидування виробів зі сплавів на основі заліза
Наступний патент: Виріб з ідентифікаційною інформацією, призначений для застосування у електронагрівній курильній системі
Випадковий патент: Спосіб формування навчальної вибірки прогнозуючої дрейф пристрою збору даних нейронної мережі