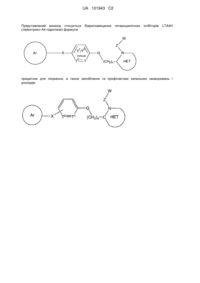
Біарилзаміщені гетероциклічні інгібітори lta4h для лікування запалення
Номер патенту: 101943
Опубліковано: 27.05.2013
Автори: Чжао Лєй, Мамат Б'єрн, Юй Пен, Санданаяка Вінсент, Сінгх Джасбір, Гарні Марк, Беделл Луіс, Мішра Рама К.
Формула / Реферат
1. Сполука формули:
 ,
,
де
Аr вибирають із групи, яка складається з
арилу;
гетероарилу;
арилу, заміщеного від одного до трьох замісниками, незалежно вибраними з групи, яка складається з галогену, нижчого алкілу, нижчого алкокси, нижчого фторалкілу, нижчого фторалкокси, гідрокси, гідроксі(С1-С4)алкілу, формілу, форміл(С1-С4)алкілу, ціано, ціано(С1-С4)алкілу, бензилу, бензилокси, фенілу, гетероарилу, гетероциклілалкілу, заміщеного гетероарилу, нітро;
гетероарилу, заміщеного від одного до трьох замісниками, незалежно вибраними з групи, яка складається з галогену, нижчого алкілу, нижчого алкокси, бензилу;
Х вибирають із групи, яка складається з О, NR1, СН2, СН2СН2, CH2NR1, NR1CH2, С=O, CH2С=О, CR1aR1b, OCR1aR1b і CR1aR1bO;
R1 вибирають окремо в кожному випадку з групи, яка складається з Н і нижчого алкілу;
R1a вибирають із групи, яка складається з Н, ОН і нижчого алкілу;
R1b вибирають із групи, яка складається з Н і нижчого алкілу;
Т1 і Т2 являють собою атоми вуглецю, які утворюють бензольне кільце, або один з Т1 і Т2 може являти собою атом азоту, який утворює піридинове кільце;
Q вибирають з -O-, -NR1- або S(O)p;
р дорівнює нулю;
n дорівнює цілому числу, вибраному з 1-5;
НЕТ вибирають із групи, яка складається з
4-6-членного насиченого азотовмісного гетероциклу;
4-6-членного насиченого азотовмісного гетероциклу, заміщеного одним або двома замісниками, незалежно вибраними з групи, яка складається з галогену, гідроксилу, аміно, карбокси, нижчого алкілу, нижчого ацилу, нижчого алкокси, нижчого фторалкілу, нижчого фторалкокси, формілу, ціано, бензилу, бензилокси, фенілу;
взяті разом, Z-W являють собою Н, або
Z являє собою (CH2)1-10, де одна або дві (СН2) можуть бути необов'язково замінені -NR1-, -С(=O)- або -C=O(NH)-, за умови, що вказані -NR1-, -C(=O)- або -C=O(NH)- не знаходяться в точці приєднання до НЕТ і розділені щонайменше однією -(СН2)-;
W вибирають із групи, яка складається з ацилу, гідроксилу, карбоксилу, аміно, -C(О)NHR4, аміноацилу, -СООалкілу, -СНО, гетероциклілу, заміщеного арилу, заміщеного гетероциклілу, сульфонаміду, -С(O)фторалкілу, -С(O)СН2С(O)Оалкілу, -С(O)СН2С(O)Офторалкілу, -SH, -C(O)NH(OH), -C(O)N(OH)R4, -N(OH)C(O)OH, -N(OH)C(O)R4;
R4 вибирають із групи, яка складається з Н, (С1-С4)алкілу, феніл(С1-С4)алкілу; за умови, що:
(a) якщо Q являє собою -O-, НЕТ являє собою (S)-піролідин, rac-піролідин або піперидин, Аr являє собою феніл або галогензаміщений феніл, Т1/Т2 кільце являє собою п-фенілен, тоді, взяті разом, Z-W відрізняються від Н;
(b) якщо Q являє собою -O-, НЕТ являє собою азетидин, Аr являє собою феніл, n дорівнює 1, Т1/Т2 кільце являє собою 2,5-заміщений піридин, тоді, взяті разом, Z-W відрізняються від Н.
2. Сполука за п. 1, де Т1/Т2 кільце являє собою піридиніл, формули:
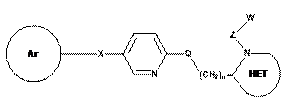 .
.
3. Сполука за п. 1, де Т1/Т2 кільце являє собою піридиніл, формули:
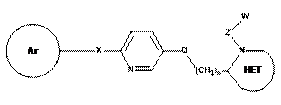 .
.
4. Сполука за п. 1, де Т1/Т2 кільце являє собою парафенілен, формули:
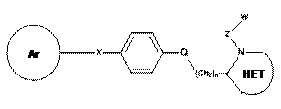 .
.
5. Сполука за п. 4, де Q являє собою -NR1-, формули:
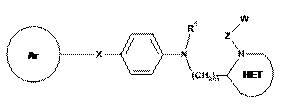 .
.
6. Сполука за п. 4, де Q являє собою -S(O)p-, формули:
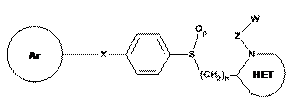 .
.
7. Сполука за п. 4, де Q являє собою -О-, формули:
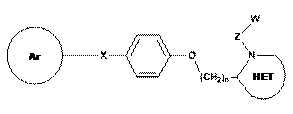 ,
,
де
Аr вибирають із групи, яка складається з
арилу;
гетероарилу;
арилу, заміщеного від одного до трьох замісниками, незалежно вибраними з групи, яка складається з галогену, нижчого алкілу, нижчого алкокси, нижчого фторалкілу, нижчого фторалкокси, формілу, ціано, бензилу, бензилокси, фенілу, гетероарилу, нітро;
гетероарилу, заміщеного від одного до трьох замісниками, незалежно вибраними з групи, яка складається з галогену, нижчого алкілу, нижчого алкокси, бензилу;
Х вибирають із групи, яка складається з О, NR1, СН2, СН2O, С=O, СН2С=O;
R1 вибирають незалежно в кожному випадку з групи, яка складається з Н і нижчого алкілу;
n дорівнює цілому числу, вибраному з 1-5;
НЕТ вибирають із групи, яка складається з
4-6-членного насиченого азотовмісного гетероциклу;
4-6-членного насиченого азотовмісного гетероциклу, заміщеного одним або двома замісниками, незалежно вибраними з групи, яка складається з галогену, нижчого алкілу, нижчого ацилу, нижчого алкокси, нижчого фторалкілу, нижчого фторалкокси, формілу, ціано, бензилу, бензилокси та фенілу;
Z являє собою (СН2)1-10, де одна або дві (СН2) можуть бути необов'язково замінені -NR1-, -С(=O)- або -C=O(NH)-, за умови, що вказані -NR1-, -С(=O)- або -C=O(NH)- не знаходяться в точці приєднання до НЕТ і розділені щонайменше двома -(СH2)-;
W вибирають з ацилу, гідроксилу, карбоксилу, аміно, карбоксамідо, аміноацилу, -СООалкілу, -СНО, гетероциклілу, заміщеного арилу або заміщеного гетероциклілу.
8. Сполука за п. 7, де Х вибирають з СН2, О або NR1.
9. Сполука за п. 7, де НЕТ вибирають із групи, яка складається з піролідину, піперидину, піперазину, а також заміщеного піролідину, заміщеного піперидину, заміщеного піперазину.
10. Сполука за п. 7, де НЕТ являє собою (S)-піролідин, формули
 ,
,
де
R3 вибирають з галогену, СF3, метилу, метокси або СF3О.
11. Сполука за п. 10, де НЕТ являє собою (S)-піролідин, формули
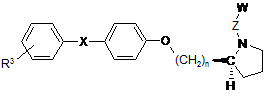 ,
,
де
Х являє собою О або СН2.
12. Сполука за п. 10, де НЕТ являє собою (S)-піролідин, формули
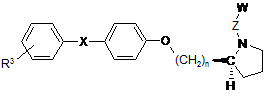 ,
,
де
n дорівнює 1 або 2.
13. Сполука за п. 10, де НЕТ являє собою (S)-піролідин, формули
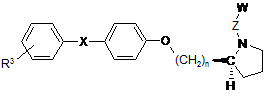 ,
,
де
Z являє собою С1-С4алкілен.
14. Сполука за п. 10, де НЕТ являє собою (S)-піролідин, формули
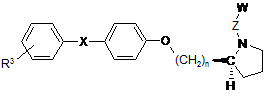 ,
,
де
W являє собою СООН.
15. Сполука за п. 7, де НЕТ являє собою (S)-піролідин, формули
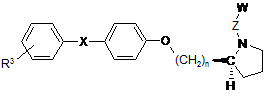 ,
,
де R3 вибирають з галогену, СF3, метилу, метокси, СF3О;
Х являє собою О або СН2;
n дорівнює 1 або 2;
Z являє собою С1-С4алкілен;
W являє собою СООН.
16. Сполука за п. 9, де НЕТ являє собою піролідин і, взяті разом, Z-W відрізняються від Н.
17. Сполука за п. 16, де HET-Z-W вибирають із групи, яка складається з піридинілметилпіролідину, оксадіазолілметилпіролідину, карбоксіалкілпіролідину, алкоксикарбонілалкілпіролідину.
18. Сполука за п. 17, де HET-Z-W являє собою карбоксіалкілпіролідин, формули:
 ,
,
де q дорівнює цілому числу, вибраному з 2-6.
19. Сполука за п. 17, де HET-Z-W являє собою карбоксіалкіл-(S)-піролідин, формули:
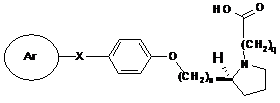 ,
,
де q дорівнює цілому числу, вибраному з 2-6.
20. Сполука за п. 9, де НЕТ вибирають із групи, яка складається з піролідину, піролідинону, піперидину і піперидинону.
21. Сполука за п. 1, де НЕТ являє собою (R)-піролідин, формули:
 ,
,
де
Аr вибирають із групи, яка складається з
арилу;
гетероарилу;
арилу, заміщеного від одного до трьох замісниками, незалежно вибраними з групи, яка складається з галогену, нижчого алкілу, нижчого алкокси, нижчого фторалкілу, нижчого фторалкокси, гідрокси, гідроксі(С1-С4)алкілу, формілу, форміл(С1-С4)алкілу, ціано, ціано(С1-С4)алкілу, бензилу, бензилокси, фенілу, гетероарилу, гетероциклілалкілу, заміщеного гетероарилу, нітро;
гетероарилу, заміщеного від одного до трьох замісниками, незалежно вибраними з групи, яка складається з галогену, (С1-С4)алкілу, (С1-С4)алкокси, бензилу;
Х вибирають із групи, яка складається з О, NR1, CH2, СН2СН2, CH2NH, NHCH2, С=O, СН2С=O;
взяті разом, Z-W являють собою Н, або
Z являє собою (СН2)1-10, де одна або дві (СН2) можуть бути необов'язково замінені -NR1-, -С(=O)- або -C=O(NH)-, за умови, що вказані -NR1-, -С(=O)- або -C=O(NH)- не знаходяться в точці приєднання до НЕТ і розділені щонайменше однією -(СН2)-;
W вибирають із групи, яка складається з ацилу, гідроксилу, карбоксилу, аміно, карбоксамідо, аміноацилу, -СООалкілу, -СНО, гетероциклілу, заміщеного арилу, заміщеного гетероциклілу.
22. Сполука за п. 21, де Z-W являють собою Н, формули:
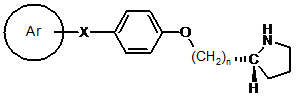 .
.
23. Сполука за п. 22, де Х вибирають з СН2, О або NR1.
24. Сполука за п. 23, де Х являє собою СН2 або О, n дорівнює 1, Аr являє собою паразаміщений феніл.
25. Сполука за п. 24, де Аr являє собою гетероарилфеніл.
26. Сполука за п. 1, де НЕТ являє собою (S)-піролідин, формули
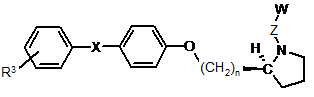 ,
,
де
R3 являє собою один-три залишки, незалежно вибрані з групи, яка складається з бензилу, бензилокси, фенілу, гетероарилу і гетероарилу, заміщеного галогеном, метилом, метокси або трифторметокси.
27. Сполука за будь-яким з пп. 1-9 або 16-25, де Аr являє собою
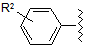 ,
,
де хвиляста лінія вказує на точку приєднання до X, R2 вибирають з водню, галогену, трифторметилу, метилу, метокси, тієнілу або фуранілу.
28. Фармацевтична композиція, що містить фармацевтично прийнятний носій і терапевтично ефективну кількість щонайменше однієї сполуки за будь-яким з пп. 1-26.
29. Фармацевтична композиція, що містить фармацевтично прийнятний носій і терапевтично ефективну кількість щонайменше однієї сполуки за п. 27.
30. Спосіб інгібування лейкотриєн-А4-гідролази, за яким приводять в контакт фермент LTA4H з терапевтично ефективною кількістю сполуки формули:
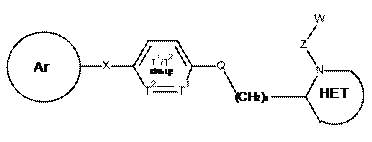 ,
,
де
Аr вибирають із групи, яка складається з
арилу;
гетероарилу;
арилу, заміщеного від одного до трьох замісниками, незалежно вибраними з групи, яка складається з галогену, нижчого алкілу, нижчого алкокси, нижчого фторалкілу, нижчого фторалкокси, гідрокси, гідроксі(С1-С4)алкілу, формілу, форміл(С1-С4)алкілу, ціано, ціано(С1-С4)алкілу, бензилу, бензилокси, фенілу, гетероарилу, гетероциклілалкілу, заміщеного гетероарилу, нітро;
гетероарилу, заміщеного від одного до трьох замісниками, незалежно вибраними з групи, яка складається з галогену, нижчого алкілу, нижчого алкокси, бензилу;
Х вибирають із групи, яка складається з О, NR1, СН2, СН2СН2, CH2NR1, NR1CH2, С=O, CH2С=О, CR1aR1b, OCR1aR1b і CR1aR1bО;
R1 вибирають окремо в кожному випадку з групи, яка складається з Н і нижчого алкілу;
R1a вибирають із групи, яка складається з Н, ОН і нижчого алкілу;
R1b вибирають із групи, яка складається з Н і нижчого алкілу;
Т1 і Т2 являють собою атоми вуглецю, що утворюють бензольне кільце, або один з Т1 і Т2 може являти собою атом азоту, що утворює піридинове кільце;
Q вибирають з -O-, -NR1- або S(O)p;
р дорівнює нулю;
n дорівнює цілому числу, вибраному з 1-5;
НЕТ вибирають із групи, яка складається з
4-6-членного насиченого азотовмісного гетероциклу,
4-6-членного насиченого азотовмісного гетероциклу, заміщеного одним або двома замісниками, незалежно вибраними з групи, яка складається з галогену, гідроксилу, аміно, карбокси, нижчого алкілу, нижчого ацилу, нижчого алкокси, нижчого фторалкілу, нижчого фторалкокси, формілу, ціано, бензилу, бензилокси, фенілу;
взяті разом, Z-W являють собою Н, або
Z являє собою (СН2)1-10, де одна або дві (СН2) можуть бути необов'язково замінені -NR1-, -С(=O)- або -C=O(NH)-, за умови, що вказані -NR1-, -C(=O)- або -C=O(NH)- не знаходяться в точці приєднання до НЕТ і розділені щонайменше однією -(CH2)-;
W вибирають із групи, яка складається з ацилу, гідроксилу, карбоксилу, аміно, -C(O)NHR4, аміноацилу, -СООалкілу, -СНО, гетероциклілу, заміщеного арилу, заміщеного гетероциклілу, сульфонаміду, -С(O)фторалкілу, С(O)СН2С(O)Оалкілу, -С(O)СН2С(O)Офторалкілу, -SH, -C(O)NH(OH), -C(O)N(OH)R4, -N(OH)C(O)OH, -N(OH)C(O)R4;
R4 вибирають із групи, яка складається з Н, (С1-С4)алкілу і феніл(С1-С4)алкілу.
31. Спосіб інгібування лейкотриєн-А4-гідролази, за яким приводять в контакт фермент LTA4H з терапевтично ефективною кількістю сполуки формули:
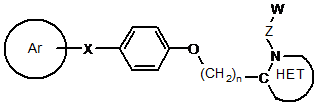 ,
,
де
Аr вибирають із групи, яка складається з
арилу;
гетероарилу;
арилу, заміщеного від одного до трьох замісниками, незалежно вибраними з групи, яка складається з галогену, нижчого алкілу, нижчого алкокси, нижчого фторалкілу, нижчого фторалкокси, формілу, ціано, бензилу, бензилокси, фенілу, гетероарилу, нітро;
гетероарилу, заміщеного від одного до трьох замісниками, незалежно вибраними з групи, яка складається з галогену, нижчого алкілу, нижчого алкокси і бензилу;
Х вибирають із групи, яка складається з О, NR1, СН2, СН2O, С=O, CH2C=O;
R1 вибирають незалежно в кожному випадку з групи, яка складається з Н і нижчого алкілу;
n дорівнює цілому числу, вибраному з 1-5;
НЕТ вибирають із групи, яка складається з
4-6-членного насиченого азотовмісного гетероциклу,
4-6-членного насиченого азотовмісного гетероциклу, заміщеного одним або двома замісниками, незалежно вибраними з групи, яка складається з галогену, нижчого алкілу, нижчого ацилу, нижчого алкокси, нижчого фторалкілу, нижчого фторалкокси, формілу, ціано, бензилу, бензилокси, фенілу;
взяті разом, Z-W являють собою Н, або
Z являє собою (СН2)1-10, де одна або дві (СН2) можуть бути необов'язково замінені -NR1-, -С(=O)- або -C=O(NH)-, за умови, що вказані -NR1-, -С(=O)- або -C=O(NH)- не знаходяться в точці приєднання до НЕТ і розділені щонайменше двома -(СН2)-;
W вибирають з ацилу, гідроксилу, карбоксилу, аміно, карбоксамідо, аміноацилу, -СООалкілу, -СНО, гетероциклілу, заміщеного арилу або заміщеного гетероциклілу.
32. Спосіб лікування захворювання, пов'язаного з лейкотриєн-А4-гідролазою, за яким ссавцю вводять терапевтично ефективну кількість сполуки за будь-яким з пп. 1-26.
33. Спосіб за п. 32, де зазначене захворювання, пов'язане з лейкотриєн-А4-гідролазою, являє собою запалення.
34. Спосіб за п. 32, де вказане захворювання вибирають з алергійного запалення, гострого запалення або хронічного запалення.
35. Спосіб за п. 32, де вказане захворювання вибирають з астми, хронічної стенозної хвороби легень (COPD), ревматоїдного артриту, розсіяного склерозу, запальних захворювань кишечнику (IBD) або псоріазу.
36. Спосіб за п. 32, де вказане захворювання вибирають з атеросклерозу, тромбозу, інсульту, гострого коронарного синдрому, стабільної стенокардії, хвороби периферичних судин, критичної ішемії ніг, переміжної кульгавості, аневризми абдомінальної аорти або інфаркту міокарда.
37. Спосіб лікування захворювання, пов'язаного з лейкотриєн-А4-гідролазою, за яким ссавцю вводять терапевтично ефективну кількості сполуки за п. 27.
38. Спосіб лікування запалення, за яким ссавцю вводять терапевтично ефективну кількість сполуки за будь-яким з пп. 1-26 і інгібітору білка, що активує 5-ліпоксигеназу (FLAP).
39. Спосіб лікування запалення, за яким ссавцю вводять терапевтично ефективну кількість сполуки за будь-яким з пп. 1-26 і антагоніста лейкотриєну-В4 (LTB4).
Текст
Реферат: UA 101943 C2 C07D 207/08 (2006.01) C07D 207/09 (2006.01) C07D 401/06 (2006.01) C07D 413/06 (2006.01) C07D 211/22 (2006.01) C07D 409/12 (2006.01) C07D 207/46 (2006.01) C07D 241/04 (2006.01) C07D 207/26 (2006.01) C07D 207/12 (2006.01) C07D 401/12 (2006.01) C07D 413/12 (2006.01) C07D 405/12 (2006.01) C07D 417/12 (2006.01) C07D 403/12 (2006.01) A61K 31/40 (2006.01) UA 101943 C2 Представлений винахід стосується (лейкотриєн-А4-гідролази) формули Ar біарилзаміщених гетероциклічних інгібіторів LTA4H кільце НЕТ , придатних для лікування, а також запобігання та профілактики запальних захворювань і розладів. UA 101943 C2 5 10 15 20 25 30 35 40 45 50 Галузь техніки винаходу Даний винахід стосується хімічного класу біарилзаміщених гетероциклічних інгібіторів LTA4H (лейкотриєн A4 гідролази), придатних для лікування, а також запобігання і профілактики запальних захворювань і розладів. Рівень техніки Кінцеві продукти лейкотриєнового шляху є сильними ліпідними медіаторами запалення, похідними арахідонової кислоти. Вони потенційно можуть робити внесок у розвиток атеросклерозу і дестабілізацію атеросклеротичних бляшок за рахунок окислювання ліпідів і/або протизапальних ефектів. Як описано в інших джерелах, на хромосомі 13q12 ідентифікували ген, що грає основну роль при інфаркті міокарду (ІМ) (MI), [Helgadottir et al., Nature Genetics doi:10.1038/ng1311, 8 лютого 2004]. Даний ген (ALOX5AP), далі в даному описі називаний геном хвороби ІМ, містить нуклеїнову кислоту, яка кодує білок, що активує 5-ліпоксигеназу (FLAP), далі називаний FLAP. Модифікації ДНК у гені FLAP збільшують ризик інфаркту міокарду в 1,8 разів і інсульту в 1,7 разів. Лейкотриєновий шлях за посередництвом FLAP веде до продукування лейкотриєну B4 за допомогою ферменту лейкотриєн A4 гідролази (LTA4H). Лейкотриєн B4 є одним з найбільш сильних хемокінових медіаторів артеріального запалення. Певні модифікації ДНК у гені, що кодує LTA4H, також збільшують ризик ІМ і інсульту, як описано в інших джерелах [Hakonarsson et al., J. Am. Med. Assoc. 293, 2245-2256 (2005)]. Якщо нейтрофіли, отримані від індивідуумів, що мають в анамнезі ІМ, стимулювати іономіцином, вони продукують більше лейкотриєну B4. Збільшене продукування LTB4 особливо виражене у пацієнтів-чоловіків, що мають в анамнезі ІМ, що мають модифікації ризику в гені FLAP [Helgadottir et al.]. Вплив (профілактичний і/або терапевтичний) на певні захворювання і стани (наприклад, ІМ, гострий коронарний синдром (ГКС) (ACS), інсульт, атеросклероз), пов'язані з FLAP або з LTA4H, можна здійснювати, інгібуючи LTA4H. Інгібування LTA4H дає переваги для способів лікування ІМ або схильності до ІМ; ГКС (наприклад, нестабільна стенокардія, інфаркт міокарду без збільшення ST (NSTEMI) або інфаркт міокарду зі збільшенням ST (STEMI); для зниження ризику другого ІМ; для інсульту (включаючи скороминущий порушення мозкового кровообігу) або схильності до інсульту; для атеросклерозу у таких пацієнтів, що мають потребу в лікуванні (наприклад, ангіопластиці, стентах, аортокоронарному шунтуванні) для відновлення кровотоку в коронарних артеріях, у таких пацієнтів, що мають потребу в лікуванні хвороби периферичних судин, включаючи периферичне оклюзійне ураження артерій, критичну ішемію кінцівок (наприклад, гангрена, виразка) і переміжну кульгавість, для відновлення кровотоку в нижніх кінцівках; для атеросклеротичної нефро-васкулярної хвороби; для аневризми абдомінальної аорти і/або для зниження синтезу лейкотриєнів (наприклад, для лікування ІМ). Публікації патентних заявок США № 20050043378 і 20050043379 відносяться до бензооксазол-2-ільних, бензотіазол-2-ільних і 1H-бензоімідазол-2-ільних сполук і їх похідних, корисних як інгібіторів лейкотриєн A4 гідролази (LTA4H) при лікуванні запалення і захворювань, пов'язаних із запаленням. Дані описи, наскільки вони застосовні, включені в даний опис за допомогою посилань. Суть винаходу Даний винахід стосується сполук, здатних інгібувати фермент LTA4H, що має загальну формулу Ψ Ψ У даних сполуках Ar вибирають із групи, яка складається з арилу; гетероарилу; арилу, заміщеного від одного до трьох замісниками, незалежно вибраними з групи, яка складається з галогену, нижчого алкілу, нижчого ацилу, нижчого алкокси, нижчого фторалкілу, нижчого фторалкокси, гідрокси, гідрокси(C 1-C4)алкілу, формілу, форміл(C 1-C4)алкілу, ціано, ціано(C1-C4)алкілу, бензилу, бензилокси, фенілу, заміщеного фенілу, гетероарилу, гетероциклілалкілу, заміщеного гетероарилу і нітро; і гетероарилу, заміщеного від одного до трьох замісниками, незалежно вибраними з групи, яка складається з галогену, нижчого алкілу, нижчого ацилу, нижчого алкокси, нижчого 1 UA 101943 C2 5 10 15 20 25 30 35 40 45 50 фторалкілу, нижчого фторалкокси, формілу, ціано, бензилу, бензилокси, фенілу, гетероарилу, гетероциклілалкілу і нітро; 1 X вибирають із групи, яка складається з прямого зв'язку, O, SO, S(O 2), NR , CH2, CF2, 1 1 1a 1b 1a 1b 1a 1b 1 CH2CH2, CH2NR , NR CH2, CH=CH, C=O, CH2C=O, CR R , OCR R , CR R О, SО2NR , 1 1 1 NR SO2, C(=O)NR і NR C(=O); 1 R вибирають окремо в кожному випадку з групи, яка складається з H і нижчого алкілу; 1a R вибирають із групи, яка складається з H, OH і нижчого алкілу; 1b 1a 1b R вибирають із групи, яка складається з H і нижчого алкілу, або R і R , узяті разом, можуть утворювати 3-6-членне кільце, що може необов'язково містити гетероатом, вибраний з O, S, і N; HetAr являє собою арильне або гетероарильне кільце, з'єднане через вуглець кільця з Q, що додатково характеризується тим, що Q і X не можуть знаходитися в сусідніх положеннях у вказаному арильному або гетероарильному кільці; 1 Q вибирають з -О-, -NR - і S(О)p; Q і X не можуть знаходитися в сусідніх положеннях у вказаному бензольному або піридиновому кільці; p дорівнює нулю, 1 або 2; n дорівнює цілому числу, вибраному з 1-5; HET вибирають із групи, яка складається з 4-7-членного насиченого азотовмісного гетероциклу і 4-7-членного насиченого азотовмісного гетероциклу, заміщеного одним або двома замісниками, незалежно вибраними з групи, яка складається з галогену, гідроксилу, аміно, карбокси, нижчого алкілу, нижчого ацилу, нижчого алкокси, N-оксиду, нижчого фторалкілу, нижчого фторалкокси, формілу, ціано, бензилу, бензилокси, фенілу, гетероарилу і нітро; і узяті разом, ZW являють собою H або 1 Z являє собою (CH2)1-10, де одна або дві (CH2) можуть бути необов'язково замінені -О-, -NR -, 1 -SO-, -S(O)2-, -C(=O)- або -C=O(NH)-, за умови, що вказані -O-, -NR -, -SO-, -S(O)2-, -C(=O)- або C=O(NH)- не знаходяться в точці приєднання до HET і розділені щонайменше однією -(CH2)-; 4 W вибирають із групи, яка складається з ацилу, гідроксилу, карбоксилу, аміно, -C(O)NHR , аміноацилу, -COOалкілу, -CHO, гетероциклілу, заміщеного арилу, заміщеного гетероциклілу, сульфонаміду, -C(O)фторалкілу, -C(O)CH2C(O)Oалкілу, -C(O)CH2C(O)Oфторалкілу, -SH, 4 4 C(O)NH(OH), -C(O)N(OH)R , -N(OH)C(O)OH, -N(OH)C(O)R ; і 4 R вибирають із групи, яка складається з H, (C1-C4)алкілу і феніл(C1-C4)алкілу. Основний підклас являє собою 1 2 1 2 У даних сполуках T і T являють собою атоми вуглецю, або один з T і T може являти 1 2 собою атом азоту. Якщо T і T являють собою атоми вуглецю, утворюється бензольне кільце. 1 2 Якщо T і T являють собою атоми азоту, утворюється піридинове кільце, і в піридинах X знаходиться в параположенні відносно Q. В другому аспекті винахід стосується способу інгібування лейкотриєн A4 гідролази, що включає приведення в контакт ферменту LTA4H з терапевтично ефективною кількістю сполуки формули Ψ. У третьому аспекті винахід стосується фармацевтичної композиції, що містить фармацевтично прийнятний носій і терапевтично ефективну кількість сполуки формули Ψ. У четвертому аспекті винахід стосується способів лікування, а також запобігання і профілактики захворювання, стани або розлади, пов'язаних з лейкотриєн A4 гідролазою. Способи включають введення ссавцю терапевтично ефективної кількості сполуки, описаного вище. Захворювання або стан може відноситися до алергійного, гострого або хронічного запалення. Захворювання може являти собою, наприклад, контактний або атопічний дерматит, артрит, алергійний риніт, астму або автоімунні захворювання, такі як хвороба Крона, псоріаз, виразковий коліт, запальне захворювання кишечнику, розсіяний склероз, анкілозувальний спондилоартрит тощо. Аналогічно, сполуки, вказані вище, можна застосовувати для запобігання рецидивуючих запальних приступів. Дані сполуки також корисні для лікування і запобігання атеросклерозу, тромбозу, інсульту, гострого коронарного синдрому, стабільної стенокардії, 2 UA 101943 C2 5 10 15 20 25 хвороби периферичних судин, критичної ішемії ніг, переміжної кульгавості, аневризми абдомінальної аорти та інфаркту міокарду. Сполуки за винаходом, що інгібують ріст пухлин і метастазів, знаходять застосування в лікуванні і запобіганні раку, включаючи рак стравоходу, рак головного мозку. Докладний опис винаходу Протягом даного опису замісникам дані визначення при першому згадуванні про їх і ці визначення далі зберігаються. Даний винахід стосується сполук загальної формули Ψ, наведеної нижче. Ψ Усі сполуки, що потрапляють під категорію вказаного вище вихідного класу і його підкласів, корисні як інгібітори лейкотриєн A4 гідролази, однак не всі сполуки є новими. Зокрема, певні відомі види потрапляють під категорію класу Ψ, хоча для даних видів не мається на увазі застосування для інгібування LTA4H. При дослідженні даного опису можна виявити, що сполуки, які виключені з формули винаходу за сполуками, є патентоздатними для авторів даного винаходу; також можна знайти, що додаткові види і класи, у даний час не виключені, не є патентоздатними для авторів даного винаходу. У будь-якому випадку, виключення видів і класів з формули винаходу, що заявляється, варто розглядати як артефакти при процедурі видачі патенту, що не відбиває концепцію авторів винаходу або опис їхнього винаходу. Винаходом, в аспекті композиції, є всі сполуки формули Ψ, за винятком тих, які є загальновідомими. Зокрема, літературний пошук свідчить про те, що наступні три підкласи охоплюють сполуки, що не можуть бути заявлені у формулі винаходу: (1) якщо Q являє собою -O-, HET являє собою (S)-піролідин, rac-піролідин або піперидин, Ar являє собою феніл або галогензаміщений феніл, HetAr являє собою п-фенілен і поєднання Z-W являє собою H; 1 (2) якщо Q являє собою NR , HET являє собою тіазолідин, Ar являє собою феніл або заміщений феніл, HetAr являє собою метафенілен і поєднання ZW являє собою H; і (3) якщо Q являє собою -O-, HET являє собою азетидин, Ar являє собою феніл, n дорівнює 1, HetAr являє собою 2,5-заміщений піридин і поєднання Z-W являє собою H. 1 2 Клас Ψ охоплює чотири підкласи в залежності від Т /Т кільця: 2,5-піридиніл, зворотний 2,5піридиніл, метафенілен і парафенілен: 30 3 UA 101943 C2 В одному варіанті здійснення винахід стосується біарильних гетероциклів, корисних як інгібітори ферменту LTA4H, що має загальну формулу: 5 1 У деяких варіантах здійснення Q вибирають з O, S(O) P і NR : 10 1 У деяких варіантах здійснення X вибирають з CH2, O і NR . 1 2 У деяких варіантах здійснення Т /Т кільце являє собою парафенілен: 15 20 25 У деяких варіантах здійснення HET вибирають із групи, яка складається з піролідинону, піролідину, піперидину, піперидинону, піперазину, морфоліну, тіоморфоліну, тіазолідину, тіазолідинону, оксазолідину й оксазолідинону, а також заміщеного піролідинону, заміщеного піролідину, заміщеного піперидину, заміщеного піперидинону, заміщеного піперазину, заміщеного морфоліну, заміщеного тіоморфоліну, заміщеного тіазолідину, заміщеного тіазолідинону, заміщеного оксазолідину і заміщеного оксазолідинону. У деяких варіантах здійснення HET являє собою піролідин і поєднання Z-W відрізняється від водню. У деяких варіантах здійснення HET-Z-W вибирають з піридинілметилпіролідину, оксадіазолілметилпіролідину, карбоксіалкілпіролідину й алкоксикарбонілалкілпіролідину. У деяких варіантах здійснення HET-Z-W являє собою карбоксіалкілпіролідин, що має хімічну формулу, як представлено нижче: 4 UA 101943 C2 5 10 , де q дорівнює цілому числу, вибраному з 2-6. У деяких варіантах здійснення HET вибирають із групи, яка складається з незаміщеного піролідину, піролідинону, піперидину і піперидинону (тобто, Z-W являє собою H). В інших варіантах здійснення HET-Z-W являє собою карбоксіалкіл(S)піролідин, що має хімічну формулу, як представлено нижче: , де q дорівнює цілому числу, вибраному з 2-6. У визначених варіантах здійснення HET являє собою (R)піролідин, що має хімічну формулу, як представлено нижче: У деяких варіантах здійснення HET являє собою (R)піролідин і ZW являє собою H, що має хімічну формулу, як представлено нижче: 15 У визначених варіантах здійснення HET являє собою (R)піролідин, X вибирають з CH 2, О і 1 NR . У визначених варіантах здійснення HET являє собою (R)піролідин, X являє собою CH2 або 1 O, n дорівнює 1, і Ar вибирають з фенілу і заміщеного фенілу, і X вибирають з CH 2, О і NR . У додаткових варіантах здійснення X являє собою CH2 або O, n дорівнює 1, і Ar являє собою паразаміщений феніл. В інших варіантах здійснення Ar являє собою гетероарилфеніл. В інших 20 варіантах здійснення Ar являє собою , 2 де хвиляста лінія вказує на точку приєднання до X, і R вибирають з водню, галогену, трифторметилу, метилу, метокси, триєнілу, фуранілу, а також триєнілу або фуранілу, заміщених галогеном, трифторметилом, метилом або метокси. У деяких варіантах здійснення HET являє собою (S)піролідин, що має хімічну формулу, як представлено нижче: 25 , 3 де R являє собою галоген, CF3, метил, метокси або CF3O. X являє собою O або CH2, n дорівнює 1 або 2, Z являє собою C1-C4алкілен і W являє собою COOH. 5 UA 101943 C2 У деяких варіантах здійснення HET являє собою (S)піролідин, Q являє собою кисень і Ar являє собою заміщений феніл, що має хімічну формулу, як представлено нижче: 5 10 , де 3 R являє собою один-три залишки, незалежно вибраних із групи, яка складається з бензилу, бензилокси, фенілу і гетероарилу. У деяких варіантах здійснення Ar являє собою феніл, заміщений гетероарилом, або гетероарил, заміщений замісником, вибраним із групи, яка складається з галогену, метилу, метокси і трифторметокси. Триєнил і фураніл є прикладами гетероарилу. 1 2 В інших варіантах здійснення Т /Т кільце являє собою або піридин і Q являє собою кисень, 1 2 1 або Т /Т кільце являє собою парафенілен і Q являє собою -NR - або -S(O)P-. Прикладами загальних формул є: 15 і 20 25 30 У даних сполуках змінні можуть бути такими, як описано вище для класу, в якому Q являє 1 2 собою -O- і Т /Т кільце являє собою п-фенілен. В іншому аспекті даний винахід стосується фармацевтичної композиції, що містить фармацевтично прийнятний носій і терапевтично ефективну кількість щонайменше однієї сполуки, як описано вище. У способах за винаходом проводять паралель між композиціями і препаратами. Способи включають введення пацієнту, потребує лікування, терапевтично ефективної кількості сполуки за даним винаходом. Даний винахід стосується способу інгібування лейкотриєн A4 гідролази, що включає приведення в контакт ферменту LTA4H з терапевтично ефективною кількістю сполуки формули Ψ. Спосіб інгібування лейкотриєн A4 гідролази включає приведення в контакт ферменту LTA4H з терапевтично ефективною кількістю сполуки формули: 6 UA 101943 C2 , і кожним з її підкласів, як описано вище. Наприклад, винахід також стосується способу інгібування лейкотриєн A4 гідролази, що включає приведення в контакт ферменту LTA4H з терапевтично ефективною кількістю сполуки формули: 5 10 15 20 25 30 35 40 45 Крім того, даний винахід стосується способу пригнічення захворювання, пов'язаного з лейкотриєн A4 гідролазою, що включає введення ссавцю терапевтично ефективної кількості або сполуки його солі, або гідрату складного ефіру формули Ψ. У деяких варіантах здійснення захворювання пов'язане з запаленням. У деяких варіантах здійснення захворювання вибирають з алергійного запалення, гострого запалення і хронічного запалення. Даний винахід також стосується способу лікування запалення, що включає введення ссавцю терапевтично ефективної кількості сполуки формули Ψ і інгібітору білка, що активує 5ліпоксигеназу (FLAP) [наприклад, MK-0591 (Merck), BAY-X1005 (Bayer) і R-(-)-2-[4-хінолін-2ілметокси)феніл]-2-циклопентилоцтової кислоти] і/або терапевтично ефективної кількості сполуки формули Ψ і антагоніста лейкотриєну B4 (LTB4) [наприклад, SC 41930 (Searle), SC 53228 (Searle), аколату (зафірлукаст; Zeneca), сингулеру (монтелукаст; Merck), ультаїру (пранлукаст; Ono/Smith-KlineBeecham), етил[[4-[[3-[[4-[1-(4-гідроксифеніл)-1метилетил]фенокси]метил]бензил]окси]феніл](іміно)метил]карбамату (амелубант; Boehringer Ingelheim), 2-[3-[3-[(5-етил-4'-фтор-2-гідроксибіфеніл-4-іл)окси]пропокси]-2пропілфенокси]бензойної кислоти (еталоциб, Lilly) і CP-105696 (+)-1-(3S, 4R)-[3-(4-фенілбензил)4-гідроксихроман-7-іл]циклопентанкарбонової кислоти, J Pharmacol Exp Ther 273: 176-184 (1995)]. Сполуки класу, представленого вище формулою Ψ, є інгібіторами ферменту LTA4H. Внаслідок цього вони є корисними для лікування і запобігання запальних захворювань і розладів, як описано вище, особливо таких станів як астма, хронічна стенозна хвороба легень (COPD), атеросклероз, ревматоїдний артрит, розсіяний склероз, запальне захворювання кишечнику (IBD; включаючи хворобу Крона і виразковий коліт), або псоріаз, кожне з який характеризується надлишковим або тривалим запаленням на деякій стадії захворювання. Недавні дослідження свідчать про те, що дані сполуки також є корисними для лікування і запобігання атеросклерозу, тромбозу, інсульту, гострого коронарного синдрому, стабільної стенокардії, хвороби периферичних судин, критичної ішемії ніг, переміжної кульгавості, аневризми абдомінальної аорти та інфаркту міокарду. Сполуки можуть являти собою солі. Термін "фармацевтично прийнятна сіль" означає солі, протиіон яких походить з фармацевтично прийнятних нетоксичних кислот і основ. Відповідні фармацевтично прийнятні основно-адитивні солі сполук за даним винаходом включають, але не обмежуються ними: солі металів, отримані з алюмінію, кальцію, літію, магнію, калію, натрію і цинку, або органічні солі, отримані з лізину, N,N-діалкільних похідних амінокислот (наприклад, N,N-диметилгліцину, піперидин-1-оцтової кислоти і морфолін-4-оцтової кислоти), N,N'дибензилетилендіаміну, хлорпрокаїну, холіну, діетаноламіну, етилендіаміну, меглуміну (Nметилглюкаміну) і прокаїну. Якщо сполуки містять залишок основи, відповідні фармацевтично прийнятні основно-адитивні солі сполук за даним винаходом включають неорганічні кислоти та органічні кислоти. Приклади включають ацетат, бензолсульфонат (безилат), бензоат, бікарбонат, бісульфат, карбонат, камфорсульфонат, цитрат, етансульфонат, фумарат, глюконат, глутамат, бромід, хлорид, ізетіонат, лактат, малеат, малат, манделат, метансульфонат, мукат, нітрат, памоат, пантотенат, фосфат, сукцинат, сульфат, тартрат, птолуолсульфонат тощо. Для зручності і ясності описані визначені терміни, використовувані в описі, прикладах і формулі винаходу. 7 UA 101943 C2 5 10 15 20 25 30 35 40 45 50 55 60 Під алкілом розуміють, як такий, що включає лінійні, розгалужені або циклічні вуглеводневі структури, а також їхні комбінації. Нижчим алкілом називають алкільні групи, що містять від 1 до 6 атомів вуглецю. Приклади нижчих алкільних груп включають метил, етил, пропіл, ізопропіл, бутил, втор- і тер-бутил, тощо. Переважними алкільними групами є такі, які містять C 20 або менше. Циклоалкіл являє собою підгрупу алкілу і включає циклічні вуглеводневі групи, що містять від 3 до 8 атомів вуглецю. Приклади циклоалкільних груп включають втор-пропіл, вторбутил, втор-пентил, норборніл тощо. Вуглеводні C1-C20 включають алкіл, циклоалкіл, алкеніл, алкініл, арил, арилалкіл і їхні комбінації. Приклади включають фенетил, циклогексилметил, камфорил, адамантил і нафтилетил. Алкокси або алкоксил означає групи, що містять від 1 до 8 атомів вуглецю прямої, розгалуженої, циклічної конфігурації і їхні комбінації, приєднані до вихідної структури через атом кисню. Приклади включають метокси, етокси, пропокси, ізопропокси, циклопропілокси, циклогексилокси тощо. Нижчий алкокси означає групи, що містять від одного до чотирьох атомів вуглецю. Алкоксіалкіл означає ефірні групи, що містять від 3 до 8 атомів прямої, розгалуженої, циклічної конфігурації і їхні комбінації, приєднані до вихідної структури через алкіл. Приклади включають метоксиметил, метоксіетил, етоксипропіл тощо. Алкоксіарил означають алкокси замісники, приєднані до арилу, де арил приєднаний до вихідної структури. Арилалкокси означають арильні замісники, приєднані до атома кисню, де атом кисню приєднаний до вихідної структури. Заміщений арилалкокси означає заміщений арильний замісник, приєднаний до атома кисню, де атом кисню приєднаний до вихідної структури. Ацил означає групи, що містять від 1 до 8 атомів вуглецю прямої, розгалуженої, циклічної конфігурації, насичені, ненасичені й ароматичні, а також їхні комбінації, приєднані до вихідної структури через карбонільні зв'язки. Один або більше атомів вуглецю в ацильному залишку можуть бути заміщені атомом азоту, або кисню сірки, за умови, що точка приєднання до вихідної структури залишається на карбонілі. Приклади включають ацетил, бензоїл, пропіоніл, ізобутирил, трет-бутоксикарбоніл, бензилоксикарбоніл тощо. Нижчий ацил означає групи, що містять від одного до чотирьох атомів вуглецю. Арил і гетероарил означає 5- або 6-членне ароматичне або гетероароматичне кільце, що містить 0-3 гетероатоми, вибрані з O, N або S; біциклічну 9- або 10-членну ароматичну або гетероароматичну кільцеву систему, що містить 0-3 гетероатоми, вибрані з O, N або S; або трициклічну 13- або 14-членну ароматичну або гетероароматичну кільцеву систему, що містить 0-3 гетероатоми, вибрані з O, N або S. Ароматичні 6-14-членні карбоциклічні кільця включають, наприклад, бензол і нафталін, і відповідно до винаходу бензоксалан і залишки, в яких одне або більше кілець, але не обов'язково всі, є ароматичними. 5-10-членні ароматичні гетероциклічні кільця включають, наприклад, імідазол, піридин, індол, тіофен, бензопіранон, тіазол, фуран, бензімідазол, хінолін, ізохінолін, хіноксалін, піримідин, піразин, тетразол і піразол. Арилалкіл означає замісник, в якому арильний залишок приєднаний до вихідної структури через алкіл. Прикладами є бензил, фенетил тощо. Гетероарилалкіл означає замісник, в якому гетероарильний залишок приєднаний до вихідної структури через алкіл. Приклади включають, наприклад, піридинілметил, піримідинілетил тощо. Гетероциклілалкіл означає замісник, в якому гетероциклільний залишок приєднаний до вихідної структури через алкіл. Приклади включають морфолінетил і піролідинілметил. Гетероцикл означає циклоалкільний або арильний залишок, в якому від одного до трьох атомів вуглецю замінені гетероатомом, вибраним із групи, яка складається з N, O і S. Гетероатоми азоту і сірки, за бажанням, можуть бути окислені, і гетероатом азоту, за бажанням, може бути четвертинним. Приклади гетероциклів включають піролідин, піразол, пірол, індол, хінолін, ізохінолін, тетрагідроізохінолін, бензофуран, бензодіоксан, бензодіоксол (зазвичай називаний метилендіоксифенілом, коли виступає як замісник), тетразол, морфолін, тіазол, піридин, піридазин, піримідин, тіофен, фуран, оксазол, оксазолін, ізоксазол, діоксан, тетрагідрофуран тощо. Слід зазначити, що гетероарил являє собою підклас гетероциклів, в якому гетероцикл є ароматичним. Приклади гетероциклільних залишків додатково включають піперазиніл, 2-оксопіперазиніл, 2-оксопіперидиніл, 2-оксопіролідиніл, 2-оксоазепініл, азепініл, 4піперидиніл, піразолідиніл, імідазоліл, імідазолініл, імідазолідиніл, піразиніл, оксазолідиніл, ізоксазолідиніл, тіазолідиніл, ізотіазоліл, хінуклідиніл, ізотіазолідиніл, бензімідазоліл, тіадіазоліл, бензопіраніл, бензотіазоліл, тетрагідрофурил, тетрагідропіраніл, тієніл, бензотієніл, тіаморфолініл, тіаморфолінілсульфоксид, тіаморфолінілсульфон, оксадіазоліл, триазоліл і тетрагідрохінолініл. 8 UA 101943 C2 5 10 15 20 25 30 35 40 45 50 55 60 Кисневмісний гетероцикл являє собою гетероцикл, що містить щонайменше один атом кисню в кільці; він може містити додаткові атоми кисню, а також інші гетероатоми. Сірковмісний гетероцикл являє собою гетероцикл, що містить щонайменше один атом сірки в кільці; він може містити додаткові атоми сірки, а також інші гетероатоми. Азотовмісний гетероцикл являє собою гетероцикл, що містить щонайменше один атом азоту в кільці; він може містити додаткові атоми азоту, а також інші гетероатоми. Кисневмісний гетероарил являє собою підклас кисневмісного гетероциклу; приклади включають фуран і оксазол. Сірковмісний гетероарил являє собою підклас сірковмісного гетероциклу; приклади включають тіофен і тіазин. Азотовмісний гетероарил являє собою підклас азотовмісного гетероциклу; приклади включають пірол, піридин і піразин. Насичений азотовмісний гетероцикл являє собою підклас азотовмісного гетероциклу. Насичений азотовмісний гетероцикл містить щонайменше один атом азоту і може містити додаткові атоми азоту, а також інші гетероатоми. Приклади включають піролідин, піразолідин, піперидин, морфолін і тіоморфолін. Заміщені алкіл, арил, циклоалкіл, гетероцикліл і так далі, означають алкіл, арил, циклоалкіл або гетероцикліл, де аж до трьох атомів H у кожному залишку замінені галогеном, галогеналкілом, гідрокси, нижчим алкокси, карбокси, карбоалкокси (також називаним алкоксикарбонілом), карбоксамідо (також називаним алкіламінокарбонілом), ціано, карбонілом, нітро, аміно, алкіламіно, діалкіламіно, меркапто, алкілтіо, сульфоксидом, сульфоном, ациламіно, амідино, фенілом, бензилом, гетероарилом, фенокси, бензилокси або гетероарилокси. Терміни "галоген" і "гало" означають фтор, хлор, або бром йод. Варто розуміти, що сполуки за даним винаходом можуть існувати в радіоактивно міченій формі, тобто, сполуки можуть містити один або більше атомів, що мають атомну масу або масове число, відмінне від атомної маси або масового числа, що зазвичай зустрічаються в 2 3 13 14 15 природі. Радіоізотопи водню, вуглецю, фосфору, фтору і хлору включають H, H, C, C, N, 35 18 36 S, F і Cl, відповідно. Сполуки, що містять дані радіоізотопи і/або інші радіоізотопи інших 3 14 атомів, входять в обсяг даного винаходу. Радіоізотопи тритію, тобто H, і вуглецю-14, тобто, C, є особливо переважними завдяки легкості їхнього одержання і виявлення. Радіоактивно мічені сполуки формули Ψ за даним винаходом і їх проліки, зазвичай, можуть бути отримані способами, добре відомими фахівцям у даній галузі. Подібні радіоактивно мічені сполуки зручно одержувати за допомогою способів, описаних у розділах прикладів і схем, заміняючи немічені реагенти легко доступними радіоактивно міченими реагентами. Як використано в даному описі і як зрозуміло фахівцю у даній галузі, під використанням терміна "сполука" розуміється включення солей, сольватів, спів-кристалів і комплексів включення даної сполуки. Він також включає всі поліморфи даної сполуки в кристалічній формі. Термін "сольват" означає сполуку формули I у твердому стані, де молекули відповідного розчинника вбудовані в кристалічну ґратку. Відповідний розчинник для терапевтичного введення є таким, що фізіологічно переноситься у дозах введення. Прикладами відповідних розчинників для терапевтичного введення є етанол і вода. Якщо розчинником є вода, сольват називають гідратом. В основному, сольвати одержують розчиненням сполуки у відповідному розчиннику і виділенням сольвату шляхом охолодження, або при використанні антирозчинника. Зазвичай сольват сушать або піддають азеотропній перегонці в умовах навколишнього середовища. Спів-кристали являють собою комбінацію двох або більше різних молекул, розташованих таким чином, що утворюється унікальна кристалічна форма, фізичні властивості якої відрізняються від властивостей її окремих складових. Фармацевтичні спів-кристали з недавнього часу мають значний інтерес з погляду поліпшення розчинності, складання препарату і біодоступності таких лікарських засобів, як ітраконазол [див. Remenar et al. J. Am. Chem. Soc, 125, 8456-8457 (2003)] і флуоксетин. Комплекси включення описані в Remington: The th Science and Practice of Pharmacy 19 Ed. (1995) volume 1, page 176-177. Найбільш широко використовуваними комплексами включення є комплекси з циклодекстринами, і всі циклодекстринові комплекси, природні і синтетичні, з доданими додатковими компонентами і полімером(ами), або без ІМ, як описано в патентах США 5324718 і 5472954, спеціально охоплені формулою винаходу. Опису Remington і патентів '718 і '954 включені в даний опис за допомогою посилань. Сполуки, описані в даному описі, можуть мати асиметричні центри і, таким чином, можуть давати початок енантіомерам, діастереомерам і іншим стереоізомерним формам. Кожен хіральний центр може бути визначений у термінах абсолютної стехіометрії, як (R)- або (S)-. Мається на увазі, що даний винахід охоплює всі можливі ізомери, а також їх рацемічні та оптично чисті форми. Оптично активні (R)- і (S)-ізомери можуть бути отримані, використовуючи 9 UA 101943 C2 5 10 15 20 25 30 35 40 45 50 55 хіральні синтони або хіральні реагенти або зворотне розчинення, з використанням загальноприйнятих методів. Префікс "rac" позначає рацемат. Якщо сполуки, описані в даному описі, містять олефінові подвійні зв'язки або інші центри геометричної асиметрії, і якщо не обговорено особливо, мається на увазі, що сполуки містять як E, так і Z геометричні ізомери. Зображення конфігурації будь-якого вуглець-вуглецевого подвійного зв'язку, представлений у даному описі, вибирають тільки для зручності, і якщо в прямій формі не зазначено, воно не передбачено для позначення конкретної конфігурації. Таким чином, вуглець-вуглецевий подвійний зв'язок, зображений довільно як E, може являти собою Z, E або їхню суміш у будьякій пропорції. Аналогічним чином, мається на увазі, що всі таутомерні форми також включені. Графічні зображення рацемічних, амбіскалемічних і скалемічних або енантіомерно чистих сполук, використовуваних у даному описі, взяті з Maehr J. Chem. Ed. 62, 114-120 (1985): суцільні або переривчасті клини використовують для позначення абсолютної конфігурації хірального елемента; хвилясті лінії й одиночні тонкі лінії вказують на заперечення будь-якої стереохімічної передумови, що мається на увазі, яку зв'язок, що позначається нею, може утворювати; суцільні або переривчасті жирні лінії являють собою геометричні ідентифікатори, що вказують на представлену відносну конфігурацію, але що позначають рацемічний тип; і контури клина, а також пунктирні або переривчасті лінії позначають енантіомерно чисті сполуки невизначеної абсолютної конфігурації. Термінологія, що стосується "захисту", "зняття захисту" і "захищених" зв'язків зустрічається в даному описі скрізь. Дана термінологія добре зрозуміла фахівцям у даній галузі і використовується в контексті способів, що включають послідовну обробку серією реагентів. У даному контексті, захисна група означає групу, яку використовують, щоб замаскувати зв'язок на стадії способу, на якій вона інакше може вступити в реакцію, але на даній стадії реакція є небажаною. Захисна група запобігає реакції на даній стадії, однак згодом її можна видалити, щоб відкрити вихідний зв'язок. Або видалення "зняття захисту" відбувається після завершення або реакції реакцій, при яких даний зв'язок створює перешкоду. Таким чином, коли визначають послідовність реагентів, як це відбувається в способах за винаходом, фахівець у даній галузі зможе легко пророчити такі групи, які можна використовувати як "захисні групи". Придатні групи для даної мети обговорені в стандартних посібниках в галузі хімії, таких як Protective Groups in Organic Synthesis автора T.W. Greene [John Wiley & Sons, New York, 1991], що включено в даний опис за допомогою посилання. Вичерпний список скорочень, використовуваних фахівцями в галузі органічної хімії, є присутнім у першому номері кожного тому Journal of Organic Chemistry. Список, що зазвичай представлений у вигляді таблиці, озаглавленої "Стандартний список скорочень" ("Standard List of Abbreviations"), включений у даний опис за допомогою посилання. Як правило, сполуки за даним винаходом можна одержувати за допомогою способів, проілюстрованих на загальних схемах реакцій, як, наприклад, описано нижче, або їхніх модифікацій, використовуючи легко доступні вихідні речовини, реагенти і загальноприйняті методики синтезу. У даних реакціях також можливо використовувати варіанти, що є відомими самі по собі, але не наведені в даному описі. Вихідні речовини, наприклад, у випадку сполук з відповідним чином заміщеним бензімідазольним кільцем, є або комерційно доступними, синтезованими, як описано в прикладах, або їх можна одержувати способами, добре відомими фахівцям у даній галузі. Як показали доклінічні дослідження, інгібітори LTA4H є ефективними протизапальними засобами. Наприклад, пероральне введення інгібітору LTA4H SC57461 гризунам призводить до інгібування індукованої іонофором продукції LTB4 у крові мишей ex vivo, і в черевній порожнині щурів in vivo (Kachur et al., 2002, J. Pharm. Exp. Ther. 300(2), 583-587). Крім того, лікування протягом восьми тижнів тією ж інгібувальною сполукою істотно зменшило симптоми коліту на моделі приматів (Penning, 2001, Curr. Pharm. Des. 7(3): 163-179). Спонтанний коліт, що розвивається у даних тварин, має сильну подібність з IBD людини. Внаслідок цього, фахівці в даній галузі визнають дані позитивні результати на LTA4H моделях, як такі, що мають прогностичну цінність щодо застосування в терапії даного й інших запальних захворювань людини. Запальна відповідь характеризується болем, підвищеною температурою, почервонінням, припухлістю або зниженням функції, або поєднання двох або декількох таких симптомів. Терміни запалення, запальні захворювання або опосередковані запаленням захворювання або стани включають, але без обмеження, гостре запалення, алергійне запалення і хронічне запалення. 10 UA 101943 C2 5 10 15 20 25 30 Аутоімунні захворювання асоційовані з хронічним запаленням. Відомо приблизно 75 різних аутоімунних захворювань, які можна віднести до двох типів, органоспецифічних (спрямовані в основному на один орган) і не-органоспецифічних (що вражають множинні органи). Прикладами органоспецифічних аутоімунних захворювань є інсулінозалежний діабет (тип I), що вражає підшлункову залозу, тиреоїдит Хашімото і хвороба Грейвса, що уражують щитовидну залозу, перніціозна анемія, що вражає шлунок, хвороба Кушінга і хвороба Аддісона, що уражують надниркові залози, хронічний активний гепатит, що уражує печінку; синдром полікістозу яєчників (PCOS), глютеїнова хвороба, псоріаз, запальне захворювання кишечнику (IBD) і анкілозувальний спондилоартрит. Прикладами не-органоспецифічних аутоімунних захворювань є ревматоїдний артрит, розсіяний склероз, системний червоний вовчак і злоякісна міастенія. Крім того, сполуки, композиції і способи за даним винаходом корисні для лікування раку. Як було показано, є зв'язок між синтезом лейкотриєнів і різними формами раку, включаючи рак стравоходу, рак головного мозку, рак підшлункової залози, рак прямої кишки. Терміни "способи лікування або запобігання" означають зменшення, або запобігання полегшення симптомів і/або ефектів, пов'язаних з ліпідами захворюваннями. Термін "запобігання", як використано в даному описі, означає введення лікарського засобу заздалегідь, щоб попередити або пом'якшити гострий епізод. Фахівцю в галузі медицини (для якого призначений спосіб, що заявляється) буде очевидно, що термін "запобігати" не є абсолютним терміном. В галузі медицини під ним розуміють профілактичне введення лікарського засобу, щоб істотно знизити імовірність або серйозність стану, і саме такий зміст мається на увазі авторами винаходу. Як використано в даному описі, посилання на "лікування" пацієнта передбачають і профілактику, включно. Протягом всього даного опису присутні посилання на різні джерела. Повний зміст описів даних публікацій включено в даний опис за допомогою посилань. "Введення" сполуки за винаходом включає введення пролікарських форм (наприклад, складних ефірів) таким чином, щоб забезпечити ефективні рівні сполуки у суб'єкта. Термін "проліки" означає сполуку, що стає більш активною in vivo. Активація in vivo може відбуватися в результаті хімічного впливу або за посередництвом ферментів. Мікрофлора в GI тракті може також брати участь в активації in vivo. Зазвичай складні ефіри, застосовувані як проліки, являють собою метилові, етилові та оксіалкілові складні ефіри. Наприклад, у відповідних умовах 35 40 45 50 можна вважати проліками . Різноманітні шляхи введення є можливими, включаючи, але, необов'язково обмежуючи ними, парентеральний (наприклад, внутрішньовенна, внутрішньоартеріальна, внутрішньом'язова, підшкірна ін'єкція), пероральний (наприклад, заковтування або інгаляція), місцевий, назальний, ректальний або за допомогою мікроносіїв з уповільненим вивільненням, залежно від захворювання або стану, що піддається лікуванню. Пероральне, парентеральне і внутрішньовенне введення є переважним. Термін "ссавець" використовують у його словниковому змісті. Люди входять до групи ссавців, і люди будуть переважними суб'єктами. Хоча введення сполук формули Ψ у вигляді вихідної хімічної сполуки може бути можливим, переважно представляти їх у вигляді фармацевтичної композиції. У додатковому аспекті даний винахід стосується фармацевтичної композиції, що містить сполуку формули I або її фармацевтично прийнятні сіль або сольват, разом з одним або декількома фармацевтичними носіями і, необов'язково, з одним або декількома іншими терапевтичними інгредієнтами. Носій(ї) повинен бути "прийнятним" у тому сенсі, що повинен бути сумісним з іншими інгредієнтами препарату і не робити шкідливого впливу на реципієнта. Препарати включають композиції, придатні для перорального, парентерального (включаючи підшкірне, внутрішньошкірне, внутрішньом'язове, внутрішньовенне і внутрішньоочне), ректального і місцевого (включаючи шкірне, трансбукальне, під'язичне і внутрішньоочне) введення. Найбільш придатний шлях може залежати від стану і захворювання реципієнта. 11 UA 101943 C2 5 10 15 20 25 30 35 40 45 50 55 60 Препарати можуть бути для зручності надані в одиничній дозованій формі й отримані кожним зі способів, добре відомих у фармацевтичній галузі. Усі способи включають стадію об'єднання сполуки формули Ψ або її фармацевтично прийнятної або солі сольвату ("активний інгредієнт") з носієм, що являє собою один або декілька допоміжних інгредієнтів. Як правило, препарати одержують, рівномірно й однорідно з'єднуючи активний інгредієнт із рідкими носіями або тонкоподрібненими твердими носіями, або тими й іншими, з наступним, при необхідності, додаванням продукту форми бажаного препарату. Препарати за даним винаходом, застосовувані для перорального введення, можна надавати у вигляді дискретних одиниць, таких як капсули, облатки або таблетки, кожна з яких містить заздалегідь визначену кількість активного інгредієнта; у вигляді порошку (включаючи порошки мікронізовані та у вигляді наночастинок) або гранул; у вигляді розчину або суспензії у водній рідині або неводній рідині; або у вигляді рідкої емульсії типу "олія у воді" або "вода в олії". Активний інгредієнт можна також надавати у вигляді болюсу, електуарію або пасти. Таблетка може бути отримана пресуванням або формуванням, за бажанням, з одним або декількома допоміжними інгредієнтами. Спресовані таблетки можна одержувати пресуванням у відповідному апараті активного інгредієнта в сипучому стані, такому як порошок або гранули, за бажанням змішуючи зі зв'язувальною речовиною, лубрикантом, інертним розріджувачем, мастильним, поверхнево-активним або диспергувальним засобом. Формовані таблетки можна одержувати формуванням у відповідному апараті суміші порошкоподібної сполуки, змоченої інертним рідким розчинником. На таблетки можна, за бажанням, наносити покриття або робити шорсткуватими, і їх можна складати таким чином, щоб забезпечити тривале, відстрочене або контрольоване вивільнення з ІМ активного інгредієнта. Фармацевтичні композиції можуть містити "фармацевтично прийнятний інертний носій", і під даним виразом розуміється включення одного або декількох інертних ексципієнтів, що включають крохмалі, високомолекулярні спирти, що гранулюють засоби, мікрокристалічну целюлозу, розріджувачі, лубриканти, зв'язувальні речовини, дезінтегрувальні засоби тощо. При бажанні на таблетовані дози описуваних композицій можна наносити покриття за допомогою стандартних водних і неводних методів. "Фармацевтично прийнятний носій" також охоплює засоби з контрольованим вивільненням. Композиції за даним винаходом можуть також, за бажанням, містити інші терапевтичні інгредієнти, засоби проти спікання, консерванти, підсолоджувачі, пігменти, віддушки, осушувачі, пластифікувальні домішки, барвники тощо. Будь-який такий необов'язковий інгредієнт повинен бути, безумовно, поєднуваний зі сполукою за винаходом, щоб гарантувати стабільність препарату. Діапазон доз для дорослих людей зазвичай складає від 0,1 мкг до 10 г/добу перорально. Таблетки або інші лікарські форми, виконані у вигляді дискретних одиниць, можуть для зручності містити кількість сполуки за винаходом, що є ефективним при даному дозуванні або при багаторазових дозах, наприклад, одиницях, що містять від 0,1 мг до 500 мг, зазвичай приблизно від 5 мг до 200 мг. Точна кількість сполуки, що вводиться пацієнту, повинна залишатися на розсуд лікуючого лікаря. Однак застосовувана доза буде залежати від ряду факторів, включаючи вік і стать пацієнта, конкретне захворювання, що піддається лікуванню, і ступінь його тяжкості. Частота введення буде залежати від фармакодинаміки окремої сполуки і дозованої форми препарату, яку можна оптимізувати способами, добре відомими в даній галузі (наприклад, таблетки з контрольованим або уповільненим вивільненням, ентеросолюбільним покриттям і так далі). Комбіновану терапію можна здійснювати, вводячи два або декілька засобів, кожний з який складають і вводять окремо, або вводячи два або декілька засобів у складі одного препарату. Інші комбінації також охоплюються комбінованою терапією. Наприклад, два засоби можна об'єднати в одному препараті і вводити в комбінації з окремим препаратом, що містить третій засіб. Хоча два або більше засоби при комбінованій терапії можна вводити одночасно, у цьому немає необхідності. Наприклад, введення першого засобу (або комбінації засобів) можна проводити перед введенням другого засобу (або комбінації засобів) за хвилини, години, або дні тижні. Таким чином, два або більше засобів можна вводити протягом декількох хвилин один за іншим або протягом будь-якої кількості годин один за іншим, або протягом будь-якої кількості днів або тижнів один за іншим. У деяких випадках можливими є навіть більш тривалі інтервали. Хоча в багатьох випадках бажано, щоб два або більше засоби, застосовуваних у комбінованій терапії, були присутні в організмі пацієнта в той самий час, у цьому немає необхідності. Комбінована терапія може також включати два або більше введення одного або декількох засобів, використовуваних у комбінації. Наприклад, якщо засіб X і засіб Y використовують у комбінації, їх можна вводити послідовно в будь-якій комбінації один або декілька разів, наприклад, у наступному порядку X-Y-X, X-X-Y, Y-X-Y, Y-Y-X, X-X-Y-Y і так далі. 12 UA 101943 C2 5 10 Як інгібітори LTA4H сполуки формули Ψ можна застосовувати для лікування і запобігання, у числі іншого, запалення. Сполуки і композиції можна застосовувати переважно в комбінації з іншими засобами, придатними для лікування і запобігання запальних станів, а також для лікування і запобігання атеросклерозу, тромбозу, інсульту, гострого коронарного синдрому, стабільної стенокардії, хвороби периферичних судин, критичної ішемії ніг, переміжної кульгавості, аневризми абдомінальної аорти та інфаркту міокарду. Такі засоби включають інгібітори FLAP і антагоністи LTB4. В основному, сполуки за даним винаходом можуть бути отримані за допомогою способів, проілюстрованих на загальних схемах реакцій, як, наприклад, описано нижче, або їхніх модифікацій, використовуючи легкодоступні вихідні речовини, реагенти і загальноприйняті методики синтезу. Схема I 15 20 R1=H, OCF3, Ph, Cl, Me, CF3, F X=CO, CH2NH, CH3CO, CO, NH Y=O, N, S R2=H, Me, Et Ar=піридил, оксадіазол n=0, 1, 2 Схема 1: (i) Na/ДМФА або K2CO3/ДМФА, (ii) HCl, ефір або діоксан, (iii) Br(CH 2)nCO2R2, Et3N, (iv) 2н NaOH або 2M HCl, (v) ArCH2Cl, Et3N, (vi) SОCl2, NH3/MeOH. 13 UA 101943 C2 Схема II 5 X=Br, I; R1=як визначено на схемі I Схема II: (i) (a) Cu, Cs2CO3, N,N-диметилгліцин, (b) BBr3, CH2Cl2. Схема III 10 Схема III: (i) (a) Na(OAc)3, (b) 2M HCl. Схема IV 15 Схема V 14 UA 101943 C2 Схема V: (i) SOCl2, (ii) бензол, AlCl3, (iii) 60 % Na, (iv) NaBH4/EtOH, (v) H2, Pd/C, (vi) 2M HCl ефір. Схема VI 5 10 15 Схема VI: (i) (a) BH3.ТГФ, (b) 4M HCl, діоксан; (ii) SОCl2, CH2Cl2; (iii) SO2Cl2, CH2Cl2; (iv) NaIO4, RuCl3; (v) K2CO3, ДМФА; (vi) ArCH2Cl, Et3N; (vii) Br(CH2)nCO2R2; (viii) 2н NaOH або 2M HCl; (ix) (a) SОCl2, (b) NH3/MeOH. Схема VII Схема VII: (1) 150C, (ii) Na, ДМФА, (iii) HCl, діоксан. Схема VIII 15 UA 101943 C2 5 Схема VIII: (i)Na, SEMCl, ДМФА, (II) CsCO3, ДМФА, (III) TBAF, ТГФ, (IV) HCl, діоксан. Схема IX 10 15 Схема IX: (1) Na, ДМФА, (II) H2, Pd/C, EtOH/ТГФ, (III) HCl, діоксан, (IV) Cs2CO3, ДМФА, (V) Cs2CO3, ацетон. Схема X 16 UA 101943 C2 5 Схема X: (I) AlCl3, нітробензол, (II) Et3Si, ТФОК, (III) BBr3, CH2Cl2, (IV) Na, ДМФА, (V) HCl, діоксан, (VI) Ar Pd(OAc)2/PPh3/CsCO3, DME/EtOH/H2O, (VII) Br(CH2)nCO2R, основа, (VIII) NaOH або HCl. Схема XI 10 Схема XI: (I) Pd2(dba)3/t-Bu3P, NaOtBu/толуол, (II) HCl, діоксан. Схема XII 15 17 UA 101943 C2 5 Схема XII: (I) BBr3, CH2Cl2, (II) Na, ДМФА, (III) Pd(OAc)2/PPh3/CsCO3, DME/EtOH/H2O, (IV) HCl, діоксан, (V) NaBH4, EtOH. Схема XIII 10 15 Схема XIII: (I) Pd(OAc)2/PPh3/K2CO3, DME/EtOH/H2O, (II) Na, ДМФА, (III) CS2CO3/(CH3)2NCHl Cu/діоксан/98C, (IV) HCl, діоксан. Схема XIV Схема XV 18 UA 101943 C2 5 Схема XV: (I) Cs2CO3/(CH3)2NCH2CO2H, Cu/діоксан/98C, (II) HCl, діоксан, (III) K2CO3, ДМФА. Схема XVI 10 15 Схема XVI: (I) TBAB/NaOH(50 %), толуол, (II) CS2CO3/(CH3)2NCH2CO2H, Cu/діоксан/98C, (III) HCl, діоксан, (IV) DIBAL, толуол, (V) NaBH4/EtOH. Схема XVII 20 X=O, S Схема XVII: i) (a) n-BuLi, ТГФ, -78C; (b) ZnCl2,-78-65C (c) ArBr, (Ph3P)4Pd, кт -65C; ii) BBr3, CH2Cl2,-78С-кт, 16 год.; Схема XVIII 19 UA 101943 C2 i) (a) n-BuLi, ТГФ, -78C; (b) ZnCl2,-78-65C; (c) ArBr, (Ph3P)4Pd, кт-65C; ii) HCl, діоксан; iii) складний бромефір, K2CO3, ДМФА; (b) NaOH/H2O/ТГФ; (c) HCl. Схема XIX 5 Схема XIX: (1) 4-MeOBnBr, K2CO3, MEK, (II) BBr3, CH2Cl2, (III) (a)Na, ДМФА/HCl у діоксані, піролідину тозилат (b) HCl у діоксані, (IV) (a) K2CO3, ДМФА, HCl, діоксан. 10 Схема XX 15 Схема XX: (I) (a) (COCl)2, EtOH, Et3N, (II) LiAl4, ТГФ, (III) Na, піролідину тозилат, ДМФА, (IV) K2CO3, бромбутирилова кислота. Схема XXI 20 25 Схема XXI: (I) n-BuLi, -78C, CO2, (II) (COCl)2, EtOH, TEA, (III) Ar(ОH)2, (Ph3)(IV) LiAl4ксан, (V) Na, тозилат піролідину, ДМФА. Схема XXII 20 UA 101943 C2 5 10 15 20 25 30 35 40 45 Схема XXII: (I) Ar(OH)2, Pd/C, i-PrOH/H2O, кип'ятіння зі зворотним холодильником, (II) ArBr, nBuLi, -78C, ТГФ, (III) Et3Si, ТФОК, (IV) BBr3, (V) Na, тозилат піролідину, ДМФА, (VI) галоїдалкіл, K2CO3, ДМФА. Наступні конкретні необмежувальні приклади ілюструють даний винахід. ПРИКЛАД 1 Стадія 1 Трет-бутиловий ефір (R)-2-(толуол-4-сульфонілоксиметил)піролідин-1-карбонової кислоти: До розчину (R)-Boc-пролінолу (500 мг, 2,48 ммоль) у піридині (1,5 мл) додавали тозилхлорид (565 мг, 2,96 ммоль) у піридині (1 мл) при 0 °C і отриману суміш перемішували при 0 °C протягом 20 хв, перед тим, як дати їй нагрітися до кімнатної температури. Суміш перемішували протягом 8 годин при даній температурі. З отриманої суспензії видаляли розчинник і водну 1н HCl додавали до неочищеного продукту й екстрагували EtOAc. Органічний шар промивали насиченим водної NaHCO3 і потім водою і насиченим розчином солі. Органічний шар сушили над безводним Na2SO4 і розчинник видаляли у вакуумі, з одержанням вказаного в заголовку 1 продукту (800 мг, 91 %) у вигляді густої маслянистої речовини: МС (MS); m/z 378 (M+Na); H ЯМР (400 МГц, CDCl3); δ 1,38 (м, 9H), 1,79 (мм, 2H), 1,93 (м, 2H), 2,44 (с, 3H), 3,26-3,32 (м, 3H), 3,88-3,97 (м, 2H), 4,07-4,14 (м, 2H), 7,34 (ушир.с, 2H), 7,77 (д, 2H, J=8,0 Гц); ВЕРХ (ELSD); 99 %. Стадія 2 Трет-бутиловий ефір (R)-2-(4-бензилфеноксиметил)піролідин-1-карбонової кислоти: До розчину 4-бензилфенолу (103 мг, 0,56 ммоль) у ДМФА (1 мл) додавали 95 % Na (19 мг, 0,75 ммоль) при 0 °C і отриману суміш перемішували при 0 °C протягом 10 хв. Розчин тозилату (200 мг, 0,56 ммоль) стадії 1 у ДМФА (2 мл) додавали до реакційної суміші по краплях протягом 5 хв і реакційну суміш нагрівали при 95 °C протягом 10 год. Суміш концентрували, додавали воду й екстрагували EtOAc. Органічний шар промивали насиченим водної NaHCO 3 і потім водою і насиченим розчином солі. Органічний шар сушили над безводним Na 2SO4 і розчинник видаляли у вакуумі, одержуючи неочищений продукт, що очищували флеш-хроматографією на силікагелі, з одержанням вказаного в заголовку продукту (150 мг, 73 %) у вигляді твердої 1 речовини: МС; m/z 368 (M+H); H ЯМР (400 МГц, CDCl3); δ 1,46 (м, 9H), 1,84-2,03 (м, 4H), 3,39 (м, 2H), 3,73-3,93 (м, 3H), 4,10 (м, 2H), 6,84 (м, 2H), 7,08 (м, 2H), 7,17 (м, 2H), 7,26 (м, 3H). ВЕРХ (УФ), 99,8 %. Стадія 3 (R)-2-(4-бензилфеноксиметил)піролідин: До розчину продукту (4,5 г, 2,48 ммоль) стадії 2 у діоксані (2 мл) додавали 4M HCl у діоксані (8 мл) при кімнатній температурі і отриману суміш перемішували протягом 1 год. при даній температурі. Розчинник видаляли у вакуумі, з одержанням густої маслянистої речовини. Маслянисту речовину розтирали з ефіром, з одержанням білої твердої речовини (2,5 г). Тверду речовину перекристалізовували з толуолу (20 мл), з одержанням вказаного в заголовку 1 продукту (1,8 г, 53 %) у вигляді кристалічної твердої речовини: МС; m/z 268 (M+H): H ЯМР (400 МГц, ДМСО-d6); δ 1,73 (м, 1H), 1,89 (м, 1H), 1,98 (м, 1H), 2,09 (м, 1H), 3,18 (м, 2H), 3,87 (м, 1H), 3,88 (с, 2H), 4,13 (дд, 1H, J1=7,2 Гц, J2=6,4 Гц), 4,19 (дд, 1H, J1=8,8, J2=3,2 Гц), 6,91 (д, 2H, J=6,8 Гц), 7,15-7,20 (м, 5H), 7,27 (м, 2H). ВЕРХ (УФ); 97,4 %. ПРИКЛАД 2 Стадія 1 21 UA 101943 C2 5 10 15 20 25 30 35 40 45 50 Трет-бутиловий ефір (S)-2-(толуол-4-сульфонілоксиметил)піролідин-1-карбонової кислоти: До розчину S-(-)-1-Boc-2-піролідинметанолу (22 г, 110 ммоль) у піридині (56 мл) при 0 °C додавали розчин п-толуолсульфонілхлориду (22,9 г, 120 ммоль) у піридині (56 мл) порціями протягом 5 хв. Отриману блідо-жовту реакційну суміш перемішували при 0 °C протягом 2 год. і потім при температурі навколишнього середовища протягом ночі. Піридин видаляли у вакуумі. Неочищену маслянисту речовину екстрагували етилацетатом (400 мл) і послідовно промивали 0,5М HCl (100 мл), насиченим водним NaHCO3 (100 мл) і насиченим розчином солі (100 мл). Об'єднаний органічний шар сушили над безводним Na 2SO4, фільтрували і концентрували у вакуумі, з одержанням вказаного в заголовку продукту (39 г, >100 %) у вигляді жовтої маслянистої речовини. Стадія 2 Трет-бутиловий ефір (S)-2-(4-бензилфеноксиметил)піролідин-1-карбонової кислоти: До розчину 4-гідроксидифенілметану (0,77 г, 4,18 ммоль) у безводному ДМФА (22,5 мл) при 0 °C додавали 60 % дисперсію Na у мінеральному маслі (0,23 г, 5,75 ммоль) порціями протягом 5 хв. Отриману суспензію перемішували при 0 °C протягом 45 хвилин, перед тим, як розчин тозилату стадії 1 (1,50 г, 4,22 ммоль) у ДМФА (11 мл) додавали по краплях протягом 5 хв. Отриману суміш перемішували при 60 °C протягом ночі. Реакційну суміш виливали на лід і потім концентрували при зниженому тиску. Неочищений залишок екстрагували етилацетатом і послідовно промивали водою, насиченим водним NaHCO 3, водою і насиченим розчином солі. Об'єднаний органічний шар сушили безводним Na 2SO4, фільтрували і концентрували у вакуумі, з одержанням вказаного в заголовку продукту (1,8 г, >100 %) у вигляді жовтувато-коричневої маслянистої речовини. Стадія 3 (S)-2-(4-бензилфеноксиметил)піролідин: До розчину продукту стадії 2 (2,9 г, 7,89 ммоль) додавали 4M HCl у діоксані (15 мл) при температурі навколишнього середовища. Отриману суміш перемішували протягом ночі. Розчинник видаляли при зниженому тиску, з одержанням не зовсім білої твердої речовини. Тверду речовину розтирали з ефіром, з одержанням продукту приклада 2 (2,0 г, 74 %) у вигляді 1 білої твердої речовини; МС; m/z 268 (M+H). H ЯМР (400 МГц, ДМСО-d6); δ 1,73 (м, 1H), 1,89 (м, 1H), 1,98 (м, 1H), 2,09 (м, 1H), 3,18 (м, 2H), 3,87 (м, 1H), 3,88 (с, 2H), 4,13 (дд, 1H, J1=7,2 Гц, J2=6,4 Гц), 4,19 (дд, 1H, J1=8,8, J2=3,2 Гц), 6,91 (д, 2H, J=6,8 Гц), 7,15-7,20 (м, 5H), 7,27 (м, 2H). ПРИКЛАД 3 Стадія 1 Метиловий ефір 4-[(S)-2-(4-бензилфеноксиметил)піролідин-1-іл]масляної кислоти: До розчину сполуки приклада 2 (1,5 г, 4,94 ммоль) у ДМФА (23 мл) додавали карбонат калію (1,4 г, 10,1 ммоль) і метил-4-бромбутират (0,72 мл, 6,26 ммоль). Отриману суспензію перемішували при температурі навколишнього середовища протягом ночі. Розчинник концентрували при зниженому тиску і неочищений продукт поглинали етилацетатом. Органічну фракцію промивали водою, промивали насиченим розчином солі, сушили над Na 2SO4, фільтрували і концентрували у вакуумі. Неочищений продукт очищували флеш-хроматографією на силікагелі, використовуючи суміш гексан/EtOAc (градієнтна система), з одержанням вказаної в заголовку сполуки (0,73 г, 40 %) у вигляді жовтої маслянистої речовини. Стадія 2 4-[(S)-2-(4-бензилфеноксиметил)піролідин-1-іл]масляна кислота: До розчину продукту стадії 1 (0,13 г, 0,35 ммоль) додавали 2н NaOH (0,29 мл, 0,58 ммоль) і 80 % MeOH/H2O (4 мл). Отриману суспензію перемішували при 50 °C протягом 67 год. Розчинник видаляли при зниженому тиску і до залишку додавали воду. pН доводили до 4, використовуючи 1н розчин HCl. Неочищений продукт екстрагували етилацетатом. Об'єднані органічні шари промивали водою, промивали насиченим розчином солі, сушили над безводним Na2SO4 і концентрували у вакуумі, з одержанням вказаної в заголовку сполуки (0,09 г, 77 %) у 1 вигляді жовтої напівтвердої речовини. H ЯМР (400 МГц, CDCl3); δ 1,96-2,26 (м, 6H), 2,41 (т, J=6,6 Гц, 2H), 3,02 (м, 2H), 3,47 (м, 1H), 3,67 (м, 2H), 3,89 (с, 2H), 3,85 (дд, J1=4,0 Гц, J2=10,8 Гц, 22 UA 101943 C2 1H), 4,50 (м, 1H), 6,84 (д, J=8,8 Гц, 2H), 7,09-7,19 (м, 5H), 7,25-7,28 (м, 2H); МС (m/z) 352,4 (M-1); РХ (97,6 %); ВЕРХ (96,6 %). ПРИКЛАД 4 5 10 15 20 25 30 35 40 2-[(R)-2-(4-бензилфеноксиметил)піролідин-1-ілетил]піридин: До розчину сполуки приклада 1 (0,20 г, 0,66 ммоль) у ДМФА (5 мл) додавали гідрохлорид 2піколілхлориду (0,10 г, 0,61 ммоль) і триетиламін (0,24 мл, 1,72 ммоль). Отриману суміш перемішували при температурі навколишнього середовища протягом ночі. Реакційну суміш концентрували при зниженому тиску. Неочищений продукт екстрагували етилацетатом (25 мл) і промивали водою (25 мл) і потім насиченим розчином солі (25 мл). Об'єднані органічні шари сушили над безводним Na2SO4, фільтрували і концентрували у вакуумі. Неочищений продукт очищували флеш-хроматографією, використовуючи суміш гексан/EtOAc (градієнтна система), з 1 одержанням вказаної в заголовку сполуки (0,07 г, 36 %); H ЯМР (400 МГц, CDCl3); δ 1,73-1,80 (м, 3H), 2,05 (м, 1H), 2,40 (м, 1H), 3,02-3,08 (м, 2H), 3,71 (д, J=13,6 Гц, 1H), 3,83 (м, 1H), 3,91 (с, 2H), 3,95 (м, 1H), 4,25 (д, J=13,6 Гц, 1H), 6,79 (д, J=8,8 Гц, 2H), 7,07 (д, J=8,8 Гц, 2H), 7,15-7,20 (м, 4H), 7,25-7,27 (м, 2H), 7,41 (м, 1H), 7,61 (м, 1H), 8,53 (м, 1H); МС (m/z) 359,2 (M+1); РХ (100,0 %). ПРИКЛАД 5 3-[(R)-2-(4-бензилфеноксиметил)піролідин-1-ілметил]піридин: Наслідуючи основну методику приклада 4, продукт приклада 1 (0,20 г, 0,66 ммоль) у ДМФА (5 мл) обробляли гідрохлоридом 3-піколілхлориду (0,10 г, 0,61 ммоль) і триетиламіном (0,24 мл, 1 1,72 ммоль), з одержанням вказаної в заголовку сполуки (0,09 г, 46 %); H ЯМР (400 МГц, CDCl3); δ 1,71-1,78 (м, 3H), 2,04 (м, 1H), 2,29 (м, 1H), 2,94-3,03 (м, 2H), 3,51 (д, J=13,6 Гц, 1H), 3,86 (м, 1H), 3,92 (с, 2H), 3,95 (м, 1H), 4,18 (д, J=13,2 Гц, 1H), 6,81 (д, J=8,8 Гц, 2H), 7,09 (д, J=8,4 Гц, 2H), 7,16-7,30 (м, 5H), 7,67 (м, 2H), 8,48 (ушир.с, 1H), 8,56 (ушир.с, 1H); МС (m/z) 359,2 (M+1); РХ (100,0 %). ПРИКЛАД 6 4-[(R)-2-(4-бензилфеноксиметил)піролідин-1-ілметил]піридин: До розчину сполуки приклада 1 (0,25 г, 0,82 ммоль) у дихлорметані (2 мл) додавали гідрохлорид 4-піколілхлориду (0,13 г, 0,79 ммоль) і триетиламін (0,29 мл, 2,08 ммоль). Отриману суміш перемішували при температурі навколишнього середовища протягом ночі. Неочищений продукт екстрагували дихлорметаном, промивали водою і потім насиченим розчином солі. Об'єднані органічні шари сушили над безводним Na2SO4, фільтрували і концентрували у вакуумі. Неочищений продукт очищували флеш-хроматографією, використовуючи суміш 1 гексан/EtOAc (градієнтна система), з одержанням вказаної в заголовку сполуки (0,11 г, 45 %); H ЯМР (400 МГц, CDCl3); δ 1,70-1,81 (м, 3H), 2,03 (м, 1H), 2,27 (м, 1H), 2,94-3,03 (м, 2H), 3,49 (д, J=14,4 Гц, 1H), 3,86 (м, 1H), 3,92 (с, 2H), 3,94 (м, 1H), 4,19 (д, J=14,4 Гц, 1H), 6,79 (д, J=8,8 Гц, 2H), 7,08 (д, J=8,8 Гц, 2H), 7,15-7,20 (м, 3H), 7,26-7,29 (м, 4H), 8,51 (м, 2H); МС (m/z) 359,5 (M+1); РХ (99,7 %); ВЕРХ (91,6 %). ПРИКЛАД 7 23 UA 101943 C2 5 10 15 20 25 30 35 40 Метиловий ефір 3-[(R)-2-(4-бензилфеноксиметил)піролідин-1-іл]пропіонової кислоти: До розчину сполуки приклада 1 (0,2 г, 0,66 ммоль) у ДМФА (5 мл) додавали триетиламін (0,16 мл, 1,14 ммоль) і метил-3-бромпропіонат (0,07 мл, 0,64 ммоль). Отриману суспензію перемішували при температурі навколишнього середовища протягом ночі. Розчинник видаляли при зниженому тиску і неочищений залишок екстрагували етилацетатом. Органічну фракцію промивали водою, потім насиченим розчином солі, сушили над безводним Na 2SO4, фільтрували і концентрували у вакуумі. Неочищений продукт очищували флеш-хроматографією на силікагелі, використовуючи суміш гексан/EtOAc (градієнтна система), з одержанням вказаної в 1 заголовку сполуки (0,03 г, 13 %); H ЯМР (400 МГц, CDCl3); δ 1,68-1,80 (м, 3H), 1,93-2,04 (м, 1H), 2,29 (кв, J=8,4 Гц, 1H), 2,53 (т, J=7,2 Гц, 2H), 2,70 (м, 1H), 2,87 (м, 1H), 3,13 (м, 1H), 3,24 (м, 1H), 3,66 (с, 3H), 3,75 (м, 1H), 3,92 (с, 2H), 3,93 (м, 1H), 6,82 (д, J=8,8 Гц, 2H), 7,08 (д, J=8,4 Гц, 2H), 7,16-7,20 (м, 3H), 7,27 (м, 2H); МС (m/z) 354,2 (M+1); РХ (100,0 %). ПРИКЛАД 8 Метиловий ефір 4-[(R)-2-(4-бензилфеноксиметил)піролідин-1-іл]масляної кислоти: До розчину сполуки приклада 1 (0,5 г, 1,65 ммоль) у дихлорметані (4,8 мл) додавали триетиламін (0,46 мл, 3,30 ммоль) і метил-4-бромбутират (0,24 мл, 1,90 ммоль). Отриманий розчин перемішували при температурі навколишнього середовища протягом 16 годин. У реакційну суміш додавали воду (25 мл) і дихлорметан (25 мл) і неочищений залишок екстрагували дихлорметаном. Органічну фракцію промивали водою (25 мл), промивали насиченим розчином солі (25 мл), сушили над безводним Na2SO4, фільтрували і концентрували у вакуумі. Неочищений продукт очищували флеш-хроматографією на силікагелі, використовуючи суміш гексан/EtOAc (градієнтна система), з одержанням вказаної в заголовку 1 сполуки (0,15 г, 24 %); H ЯМР (400 МГц, CDCl3); δ 1,66-1,86 (м, 5H), 1,96 (м, 1H), 2,20-2,45 (м, 4H), 2,86 (м, 2H), 3,14 (м, 1H), 3,63 (с, 3H), 3,74 (м, 1H), 3,89 (м, 1H), 3,92 (с, 2H), 6,82 (д, J=8,4 Гц, 2H), 7,08 (д, J=8,0 Гц, 2H), 7,16-7,20 (м, 3H), 7,27 (м, 2H); МС (m/z) 368,4 (M+1); РХ (90,6 %). ПРИКЛАД 9 Гідрохлорид 3-[(R)-2-(4-бензилфеноксиметил)піролідин-1-іл]пропіонової кислоти: До розчину сполуки приклада 7 (0,02 г, 0,05 ммоль) додавали 2н NaOH (0,04 мл, 0,08 ммоль) і 80 % MeOH/H2O (0,5 мл). Отриману суспензію перемішували при 50 °C протягом 24 год. Розчинник видаляли при зниженому тиску і до залишку додавали воду. pН доводили до 4, використовуючи 1н розчин HCl. Неочищений продукт екстрагували етилацетатом. Об'єднані органічні шари промивали водою, промивали насиченим розчином солі, сушили над безводним 1 Na2SO4 і концентрували у вакуумі, з одержанням вказаної в заголовку сполуки (12 мг, 67 %); H ЯМР (400 МГц, CDCl3); δ 1,41-1,63 (м, 2H), 1,92-2,22 (м, 2H), 2,75 (м, 3H), 3,02 (м, 1H), 3,50 (м, 3H), 3,90 (с, 2H), 4,09 (дд, J1=4,0 Гц, J2=10,4 Гц, 1H), 4,25 (м, 1H), 6,82 (д, J=8,4 Гц, 2H), 7,087,20 (м, 5H), 7,25-7,29 (м, 2H); МС (m/z) 340,7 (M+1); РХ (100,0 %). ПРИКЛАД 10 24 UA 101943 C2 5 10 15 20 25 30 35 40 45 50 Гідрохлорид 4-[(R)-2-(4-бензилфеноксиметил)піролідин-1-іл]масляної кислоти: Наслідуючи основну методику приклада 9, розчин приклада 8 (11 мг, 0,03 ммоль) у 80 % MeOH/H2O (0,4 мл) обробляли 2н NaOH (0,03 мл, 0,06 ммоль), з одержанням вказаної в 1 заголовку сполуки (9 мг, 86 %) у вигляді жовтої маслянистої речовини; H ЯМР (400 МГц, CDCl3); δ 1,95-2,28 (м, 6H), 2,49 (м, 2H), 2,94 (м, 2H), 3,42-3,65 (м, 3H), 3,91 (с, 2H), 4,14 (дд, J1=3,6 Гц, J2=10,8 Гц, 1H), 4,42 (м, 1H), 6,83 (д, J=8,8 Гц, 2H), 7,10 (д, J=8,4 Гц, 2H), 7,15-7,20 (м, 3H), 7,27 (м, 2H); МС (m/z) 354,7 (M+1); РХ (99,7 %). ПРИКЛАД 11 Стадія 1 До розчину 4-(трифторметокси)йодбензолу (0,54 мл, 3,45 ммоль), 4-метоксифенолу (0,28 г, 2,26 ммоль) і карбонату цезію (1,54 г, 4,73 ммоль) у діоксані (10 мл) додавали гідрохлорид N,Nдиметилгліцину (0,03 г, 0,22 ммоль). Ємність продували азотом перед додаванням йодиду Cu(I) (0,02 г, 0,08 ммоль). Коричнювато-зелену реакційну суміш нагрівали до 90 °C протягом ночі. Реакційну суміш розбавляли водою і етилацетатом. Органічну фракцію промивали насиченим розчином солі, сушили над безводним Na2SO4 і концентрували у вакуумі, з одержанням вказаної в заголовку сполуки (0,8 г, 100 %) у вигляді коричневої маслянистої речовини. Стадія 2 4-(4-трифторметоксифенокси)фенол: До розчину продукту стадії 1 (0,5 г, 1,76 ммоль) у дихлорметані (10 мл) при -78 °C додавали трибромід бору (1,0М розчин у дихлорметані, 5,28 мл, 5,28 ммоль) по краплях протягом 5 хв. Отриману суміш перемішували при -78 °C протягом 30 хв і потім при температурі навколишнього середовища протягом 90 хв. Після охолодження реакційної суміші до 0 °C, її повільно додавали до холодної суміші вода/дихлорметан (50 мл/50 мл). Органічну фракцію промивали водою, насиченим розчином солі, сушили над безводним Na 2SO4 і концентрували у вакуумі. Неочищений продукт очищували флеш-хроматографією на силікагелі, використовуючи суміш гексан/EtOAc (градієнтна система), з одержанням вказаної в заголовку сполуки (0,35 г, 74 %) у вигляді темної маслянистої речовини. Стадія 3 Трет-бутиловий ефір (R)-2-[4-(4-трифторметоксифенокси)феноксиметил]піролідин-1карбонової кислоти: До розчину продукту стадії 2 (0,2 г, 0,74 ммоль) у безводному ДМФА (6 мл) при 0 °C додавали 60 % дисперсію Na у мінеральному маслі (0,04 мг, 0,98 ммоль) порціями протягом 5 хв. Після перемішування отриманої суспензії при 0 °C протягом 45 хвилин, нагрівали до температури навколишнього середовища і потім нагрівали до 35 °C протягом 15 хвилин, розчин проміжної сполуки тозилу (0,33 г, 0,93 ммоль) у ДМФА (4 мл) додавали по краплях протягом 5 хв. Отриману суміш перемішували при 75 °C протягом ночі. Реакційну суміш виливали на лід і потім концентрували при зниженому тиску. Неочищений залишок екстрагували етилацетатом і промивали водою і насиченим розчином солі. Об'єднані органічні фракції сушили над безводним Na2SO4 і концентрували у вакуумі. Неочищений продукт очищували флешхроматографією, використовуючи суміш гексан/EtOAc (градієнтна система), з одержанням вказаної в заголовку сполуки (0,24 г, 70 %) у вигляді жовтої маслянистої речовини. Стадія 4 Гідрохлорид (R)-2-[4-(4-трифторметоксифенокси)феноксиметил]піролідину: До продукту продукту стадії 3 (0,23 г, 0,51 ммоль) додавали 4M HCl у діоксані (5 мл). Отриману суміш перемішували при температурі навколишнього середовища протягом ночі. Розчинник видаляли у вакуумі. Неочищений продукт розтирали з ефіром і сушили при зниженому тиску, з одержанням вказаної в заголовку сполуки (0,12 г, 61 %) у вигляді світло1 зеленої маслянистої речовини; H ЯМР (400 МГц, ДМСО-d6) δ 1,74 (м, 1H), 1,94 (м, 2H), 2,12 (м, 1H), 3,22 (м, 2H), 3,89 (м, 1H), 4,15 (м, 1H), 4,25 (дд, J1=3,8 Гц, J2=10,8 Гц, 1H), 7,00-7,10 (м, 6H), 7,36 (д, J=8,4 Гц, 2H), 9,32 (ушир.с, 1H); МС (m/z) 354,5 (M+1); РХ (98,4 %); ВЕРХ (99,7 %). 25 UA 101943 C2 ПРИКЛАД 12 5 10 15 20 25 30 35 40 45 50 Стадія 1 4-(4-метоксифенокси)біфеніл: До розчину 4-бромбіфенілу (1,00 г, 4,29 ммоль), 4-метоксифенолу (0,35 г, 2,82 ммоль) і карбонату цезію (1,85 г, 5,68 ммоль) у діоксані (10 мл) додавали гідрохлорид N,Nдиметилгліцину (0,04 г, 0,26 ммоль). Ємність продували азотом перед додаванням йодиду Cu(I) (0,02 г, 0,11 ммоль). Реакційну суміш нагрівали до 90 °C протягом ночі. Реакційну суміш розбавляли водою і етилацетатом. Органічну фракцію промивали насиченим розчином солі, сушили над безводним Na2SO4 і концентрували у вакуумі, з одержанням вказаної в заголовку сполуки (1,00 г, 100 %) у вигляді світло-зеленої твердої речовини. Стадія 2 4-(біфеніл-4-ілокси)фенол: До розчину продукту стадії 1 (0,5 г, 1,81 ммоль) у дихлорметані (10 мл) при -78 °C додавали трибромід бору (1,0М розчин у дихлорметані, 5,43 мл, 5,43 ммоль) по краплях протягом 5-10 хв. Отриману суміш перемішували при -78 °C протягом години і потім при температурі навколишнього середовища протягом 1 год. Після охолодження реакційної суміші до 0 °C, її повільно додавали до холодної суміші вода/дихлорметан (50 мл/50 мл). Органічну фракцію промивали водою, насиченим розчином солі, сушили над безводним Na2SO4 і концентрували у вакуумі. Неочищений продукт очищували флеш-хроматографією на силікагелі, використовуючи суміш гексан/EtOAc (градієнтна система), з одержанням вказаної в заголовку сполуки (0,24 г, 47 %) у вигляді не зовсім білої твердої речовини. Стадія 3 Трет-бутиловий ефір (R)-2-[4-(біфеніл-4-ілокси)феноксиметил]піролідин-1-карбонової кислоти: До розчину продукту стадії 2 (0,24 г, 0,91 ммоль) у безводному ДМФА (4 мл) при 0 °C додавали 60 % дисперсію Na у мінеральному маслі (0,05 г, 1,20 ммоль) порціями протягом 5 хв. Після перемішування отриманої суспензії при 0 °C протягом 45 хвилин, нагрівали до температури навколишнього середовища і потім нагрівали до 35 °C протягом 15 хвилин, розчин проміжної сполуки тозилу (0,4 г, 1,13 ммоль) у ДМФА (2 мл) додавали по краплях протягом 5 хв. Отриману суміш перемішували при 75 °C протягом 60 год. Реакційну суміш виливали на лід і потім концентрували при зниженому тиску. Неочищений залишок екстрагували етилацетатом і промивали водою і насиченим розчином солі. Об'єднані органічні фракції сушили над безводним Na2SO4 і концентрували у вакуумі. Неочищений продукт очищували флешхроматографією, використовуючи суміш гексан/EtOAc (градієнтна система), з одержанням необхідної сполуки (0,40 г, 98 %) у вигляді жовтої маслянистої речовини. Стадія 4 Гідрохлорид (R)-2-[4-(біфеніл-4-ілокси)феноксиметил]піролідину: Наслідуючи основну методику приклада 11 (стадія 4), продукт стадії 3 (0,2 г, 0,45 ммоль) обробляли 4M HCl у діоксані (5 мл), з одержанням вказаного в заголовку продукту (0,11 г, 62 %) 1 у вигляді білої твердої речовини; H ЯМР (400 МГц, ДМСО-d6) 1,75 (м, 1H), 1,88-2,02 (м, 2H), 2,12 (м, 1H), 3,23 (м, 2H), 3,91 (м, 1H), 4,14 (м, 1H), 4,26 (дд, J1=3,8 Гц, J2=10,4 Гц, 1H), 7,00 (д, J=8,8 Гц, 2H), 7,04-7,11 (м, 4H), 7,34 (м, 1H), 7,45 (м, 2H), 7,61-7,66 (м, 4H); МС (m/z) 346,7 (M+1); РХ (98,9 %); елементний аналіз (розрахований): C 72,34, H 6,33, N 3,67; (знайдено): C 71,72, H 6,29, N 3,66. ПРИКЛАД 13 Стадія 1 1-метокси-4-(4-хлорфенокси)бензол: Наслідуючи основну методику приклада 12 (стадія 1), гідрохлорид N,N-диметилгліцину (0,04 г, 0,26 ммоль), карбонат цезію (1,85 г, 5,68 ммоль) і йодид Cu(I) (0,02 г, 0,11 ммоль) додавали до розчину 4-бромхлорбензолу (0,82 г, 4,28 ммоль) і 4-метоксифенолу (0,35 г, 2,82 ммоль) у діоксані (10 мл), з одержанням вказаної взаголовку сполуки (0,76 г, 100 %) у вигляді коричневої маслянистої речовини. 26 UA 101943 C2 5 10 15 20 25 30 35 40 45 50 55 Стадія 2 4-(4-хлорфенокси)фенол: Наслідуючи основну методику приклада 12 (стадія 2), трибромід бору (1,0М розчин у дихлорметані, 9,66 мл, 9,66 ммоль) додавали до продукту стадії 1 (0,76 г, 3,22 ммоль) у дихлорметані (15 мл), з одержанням вказаної в заголовку сполуки (0,37 г, 52 %) у вигляді світлозеленої твердої речовини. Стадія 3 Трет-бутиловий ефір (R)-2-[4-(4-хлорфенокси)феноксиметил]піролідин-1-карбонової кислоти: До розчину продукту стадії 2 (0,25 г, 1,13 ммоль) у безводному ДМФА (6 мл) при 0 °C додавали 60 % дисперсію Na у мінеральному маслі (0,06 г, 1,50 ммоль) порціями протягом 5 хв. Після перемішування отриманої суспензії при 0 °C протягом 45 хвилин, нагрівали до температури навколишнього середовища і потім нагрівали до 35 °C протягом 15 хвилин, розчин проміжної сполуки тозилу (0,49 г, 1,38 ммоль) у ДМФА (4 мл) додавали по краплях протягом 5 хв. Отриману суміш перемішували при 75 °C протягом 16 год. Реакційну суміш виливали на лід і потім концентрували при зниженому тиску. Неочищений залишок екстрагували етилацетатом і промивали водою і насиченим розчином солі. Об'єднані органічні фракції сушили над безводним Na2SO4 і концентрували у вакуумі. Неочищений продукт очищували флешхроматографією, використовуючи суміш гексан/EtOAc (градієнтна система), з одержанням вказаної в заголовку сполуки (0,37 г, 81 %) у вигляді жовтої маслянистої речовини. Стадія 4 Гідрохлорид (R)-2-[4-(4-хлорфенокси)феноксиметил]піролідину: До продукту стадії 3 (0,36 г, 0,89 ммоль) додавали 4M HCl у діоксані (5 мл). Отриману суміш перемішували при температурі навколишнього середовища протягом 2 год. Розчинник видаляли у вакуумі. Неочищений продукт розтирали з ефіром і сушили при зниженому тиску, з одержанням вказаної в заголовку сполуки (0,19 г, 70 %) у вигляді світло-жовтої твердої 1 речовини; H ЯМР (400 МГц, ДМСО-d6) 1,75 (м, 1H), 1,87-2,01 (м, 2H), 2,12 (м, 1H), 3,21 (м, 2H), 3,89 (м, 1H), 4,17 (м, 1H), 4,24 (дд, J1=4,0 Гц, J2=10,8 Гц, 1H), 6,94 (д, J=9,2 Гц, 2H), 7,05 (с, 4H), 7,40 (д, J=8,8 Гц, 2H); МС (m/z) 304,2 (M+1); РХ (97,1 %); ВЕРХ (99,1 %); елементний аналіз (розрахований): C 60,01, H 5,63, N 4,12 (знайдено): C 59,81, H 5,63, N 4,11. ПРИКЛАД 14 Стадія 1 1-метокси-4-(4-метилфенокси)бензол: Наслідуючи основну методику приклада 11 (стадія 1), гідрохлорид N,N-диметилгліцину (0,03 г, 0,22 ммоль), карбонат цезію (1,59 г, 4,88 ммоль) і йодид Cu(I) (0,02 г, 0,09 ммоль) додавали до розчину 4-йодтолуолу (0,8 г, 3,67 ммоль) і 4-метоксифенолу (0,3 г, 2,42 ммоль) у діоксані (10 мл), з одержанням вказаної в заголовку сполуки (0,92 г, 100 %) у вигляді коричневої маслянистої речовини. Стадія 2 4-п-толілоксифенол: Наслідуючи основну методику приклада 12 (стадія 2), трибромід бору (1,0М розчин у дихлорметані, 7,75 мл, 7,75 ммоль) додавали до продукту стадії 1 (0,75 г, 3,50 ммоль) у дихлорметані (10 мл), з одержанням вказаної в заголовку сполуки (0,26 г, 36 %) у вигляді жовтої твердої речовини. Стадія 3 Трет-бутиловий ефір (R)-2-(4-п-толілоксифеноксиметил)піролідин-1-карбонової кислоти: До розчину продукту стадії 2 (0,25 г, 1,25 ммоль) у безводному ДМФА (6 мл) при 0 °C додавали 60 % дисперсію Na у мінеральному маслі (0,06 г, 1,43 ммоль) порціями протягом 5 хв. Після перемішування отриманої суспензії при 0 °C протягом 45 хвилин, нагрівали до температури навколишнього середовища і потім нагрівали до 35 °C протягом 15 хвилин, розчин проміжної сполуки тозилу (0,47 г, 1,32 ммоль) у ДМФА (4 мл) додавали по краплях протягом 5 хв. Отриману суміш перемішували при 75 °C протягом 16 год. Реакційну суміш виливали на лід і потім концентрували при зниженому тиску. Неочищений залишок екстрагували етилацетатом і промивали водою і насиченим розчином солі. Об'єднані органічні фракції сушили над безводним Na2SO4 і концентрували у вакуумі. Неочищений продукт очищували флеш 27 UA 101943 C2 5 10 15 20 25 30 35 40 45 50 хроматографією, використовуючи суміш гексан/EtOAc (градієнтна система), з одержанням вказаної в заголовку сполуки (0,42 г, 88 %) у вигляді жовтої твердої речовини. Стадія 4 Гідрохлорид (R)-2-(4-п-толілоксифеноксиметил)піролідину: Наслідуючи основну методику приклада 13 (стадія 4), продукт стадії 3 (0,39 г, 1,02 ммоль) обробляли 4M HCl у діоксані (6 мл), з одержанням вказаної в заголовку сполуки (0,12 г, 67 %) у 1 вигляді не зовсім білої твердої речовини; H ЯМР (400 МГц, ДМСО-d6) 1,74 (м, 1H), 1,94 (м, 2H), 2,11 (м, 1H), 2,27 (с, 3H), 3,21 (м, 2H), 3,88 (м, 1H), 4,13 (м, 1H), 4,22 (дд, J1=3,8 Гц, J2=10,8 Гц, 1H), 6,83 (д, J=8,4 Гц, 2H), 6,98 (м, 4H), 7,16 (д, J=8,4 Гц, 2H), 9,11 (ушир.с, 1H), 9,67 (ушир.с, 1H); МС (m/z) 284,4 (M+1); РХ (98,8 %); ВЕРХ (99,3 %). ПРИКЛАД 15 Стадія 1 4-(4-метоксифенокси)бензонітрил: До розчину 4-йодбензонітрилу (0,458 г, 2 ммоль), 4-метоксифенолу (0,372 г, 3 ммоль) і карбонату цезію (1,30 г, 4 ммоль) у діоксані (4 мл) додавали гідрохлорид N,N-диметилгліцину (0,025 г, 0,18 ммоль). Ємність продували азотом перед додаванням йодиду Cu(I) (0,014 г, 0,07 ммоль). Реакційну суміш нагрівали до 90 °C протягом ночі. Реакційну суміш розбавляли водою і етилацетатом. Органічну фракцію промивали насиченим розчином солі, сушили над безводним 1 Na2SO4 і концентрували у вакуумі, з одержанням вказаної в заголовку сполуки (0,51 г, 100 %); H ЯМР (400 МГц, CDCl3); δ 3,83 (с, 3H), 6,92-7,02 (м, 6H), 7,56-7,58 (м, 2H). Стадія 2 4-(4-гідроксифенокси)бензонітрил: Наслідуючи основну методику приклада 11 (стадія 2), трибромід бору (1,0М розчин у дихлорметані, 5,73 мл, 5,73 ммоль) додавали до продукту стадії 1 (0,43 г, 1,91 ммоль) у дихлорметані (10 мл), з одержанням вказаної в заголовку сполуки (0,30 г, 74 %) у вигляді не зовсім білої твердої речовини. Стадія 3 Трет-бутиловий ефір 2-[4-(4-ціанофенокси)феноксиметил]піролідин-1-карбонової кислоти: Наслідуючи основну методику приклада 12 (стадія 3), 60 % дисперсію Na у мінеральному маслі (0,05 г, 1,25 ммоль) і проміжну сполуку тозилу (0,41 г, 1,15 ммоль) додавали до розчину продукту стадії 2 (0,2 г, 0,95 ммоль) у безводному ДМФА (10 мл), з одержанням вказаної в заголовку сполуки (0,30 г, 81 %) у вигляді жовтої маслянистої речовини. Стадія 4 Гідрохлорид 4-[4-((R)-1-піролідин-2-ілметокси)фенокси]бензонітрилу: Наслідуючи основну методику приклада 11 (стадія 4), продукт стадії 3 (0,3 г, 0,76 ммоль) обробляли 4M HCl у діоксані (5 мл), з одержанням вказаної в заголовку сполуки (0,21 г, 85 %) у 1 вигляді білої твердої речовини; H ЯМР; (400 МГц, ДМСО-d6) 1,75 (м, 1H), 1,88-2,02 (м, 2H), 2,12 (м, 1H), 3,22 (м, 2H), 3,90 (м, 1H), 4,17 (м, 1H), 4,27 (дд, J1=3,8 Гц, J2=10,8 Гц, 1H), 7,03 (д, J=9,2 Гц, 2H), 7,09 (м, 2H), 7,15 (м, 2H), 7,82 (д, J=8,8 Гц, 2H), 9,10 (ушир.с, 1H), 9,65 (ушир.с, 1H); МС (m/z) 295,5 (M+1); РХ (95,1 %). ПРИКЛАД 16 Стадія 1 Трет-бутиловий ефір (R)-2-[4-(4-трифторметилфенокси)феноксиметил]піролідин-1карбонової кислоти: Наслідуючи основну методику приклада 12 (стадія 3), 60 % дисперсію Na у мінеральному маслі (0,06 г, 1,58 ммоль) і проміжну сполуку тозилу (0,51 г, 1,43 ммоль) додавали до розчину 4[(4-трифторметил)фенокси]фенолу (0,3 г, 1,18 ммоль) у безводному ДМФА (10 мл), з одержанням вказаної в заголовку сполуки (0,41 г, 79 %) у вигляді жовтої маслянистої речовини; МС, m/z 437 (M+1). Стадія 2 Гідрохлорид (R)-2-[4-(4-трифторметилфенокси)феноксиметил]піролідину: 28
ДивитисяДодаткова інформація
Назва патенту англійськоюNormal;heading 1;heading 2;heading 3;biaryl substituted heterocycle inhibitors of lta4h for treating inflammation
Автори англійськоюSingh Jasbir, Sandanayaka Vincent, Gurney Mark, Yu Peng, Bedell Louis, Mamat Bjorn, Zhao Lei, Mishra Rama K.
Назва патенту російськоюБиарилзамещенные гетероциклические ингибиторы lta4h для лечения воспаления
Автори російськоюСингх Джасбир, Санданаяка Винсент, Гарни Марк, Юй Пен, Беделл Луис, Мамат Бьерн, Чжао Лей, Мишра Рама К.
МПК / Мітки
МПК: C07D 401/12, C07D 409/12, C07D 241/04, C07D 207/08, C07D 413/06, C07D 207/09, C07D 413/12, C07D 211/22, C07D 417/12, C07D 207/26, C07D 401/06, C07D 403/12, A61K 31/40, C07D 207/46, C07D 405/12, C07D 207/12
Мітки: біарилзаміщені, гетероциклічні, лікування, запалення, інгібітори, lta4h
Код посилання
<a href="https://ua.patents.su/121-101943-biarilzamishheni-geterociklichni-ingibitori-lta4h-dlya-likuvannya-zapalennya.html" target="_blank" rel="follow" title="База патентів України">Біарилзаміщені гетероциклічні інгібітори lta4h для лікування запалення</a>
Попередній патент: Пристрій для роботи з льодом та/або ущільненим снігом, та/або ґрунтом
Наступний патент: Композиції і способи застосування для антитіл dicкkopf-1
Випадковий патент: Спосіб вилучення паладію з матеріалів, які його містять