Спосіб одержання гідрогелю з використанням ферментів ліпаз
Номер патенту: 113188
Опубліковано: 26.12.2016
Автори: Коммісруд Елізабет, Клінкєнбєрг Гєйр, Домаас Йосефсен Хьєлль
Формула / Реферат
1. Застосування ліпази і субстрату, здатного до гідролізу ліпазою, і агента, що вивільняє двовалентний катіон, для одержання альгінатного гідрогелю, де субстрат є сполукою формули І:
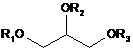 , (І)
, (І)
де R1, R2 і R3 незалежно один від одного є однаковими або різними і позначають лінійний або розгалужений, заміщений або незаміщений С1-С12-алкілкарбонільний ланцюг, і де агент, що вивільняє двовалентний катіон, є карбонатом.
2. Застосування за п. 1, де ліпаза є тригліцеридліпазою.
3. Застосування за будь-яким з пп. 1-2, де гідроліз сполуки формули І ліпазою приводить до утворення Н3О+.
4. Застосування за будь-яким з пп. 1-3, де R1, R2 і R3 вибрані з групи, що складається з метанону, етанону, ацетону, бутанону, пентанону, гексанону, гептанону, октанону, нонанону, деканону, додеканону.
5. Застосування за будь-яким з пп. 1-4, де R1, R2 і R3 незалежно один від одного є однаковими або різними і позначають С1-С4-алкілкарбонільний ланцюг.
6. Застосування за будь-яким з пп. 1-5, де сполука формули І вибрана з групи, що складається з триацетину, трипропіоніну і трибутирину, переважно трипропіоніну і трубутирину.
7. Застосування за будь-яким з пп. 1-6, де ліпаза і сполука формули І використовуються для одержання альгінатного гідрогелю, в який впроваджений біологічний матеріал, переважно сперматозоїди.
8. Спосіб одержання альгінатного гідрогелю, що передбачає змішування розчину, який містить ліпазу, з розчином, який містить субстрат, здатний до гідролізу ліпазою, де розчин, який містить зазначену ліпазу, або розчин, який містить зазначений субстрат, також містить альгінат і сполуку, що вивільняє двовалентний катіон, де субстрат є сполукою формули І:
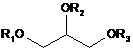 , (І)
, (І)
де R1, R2 і R3 незалежно один від одного є однаковими або різними та позначають лінійний або розгалужений, заміщений або незаміщений С1-С12-алкілкарбонільний ланцюг, і де агент, що вивільняє двовалентний катіон, є карбонатом.
9. Спосіб за п. 8, де розчин, який містить ліпазу, включає карбонат, що вивільняє двовалентний катіон, і альгінат.
10. Спосіб за п. 8, де розчин, який містить сполуку формули І, включає карбонат, що вивільняє двовалентний катіон, і альгінат.
11. Спосіб за будь-яким з пп. 8-10, де R1, R2 і R3 вибрані з групи, що складається з метанону, етанону, ацетону, бутанону, пентанону, гексанону, гептанону, октанону, нонанону, деканону, додеканону.
12. Спосіб за будь-яким з пп. 8-10, де R1, R2 і R3 незалежно один від одного є однаковими або різними і позначають С1-С4-алкілкарбонільний ланцюг.
13. Спосіб за будь-яким з пп. 8-10, де сполука формули І вибрана з групи, що складається з триацетину, трипропіоніну і трибутирину, переважно трипропіоніну і трибутирину.
14. Спосіб за будь-яким з пп. 8-13, де карбонат, що вивільняє двовалентний катіон, є карбонатом кальцію.
15. Спосіб за будь-яким з пп. 8-13, де розчин, який містить ліпазу або розчин, який містить сполуку формули І, також містить об'єкт для впровадження в альгінатний гідрогель.
16. Спосіб за п. 15, де об'єкт для впровадження в альгінатний гель є біологічним матеріалом, таким як сперматозоїди.
17. Альгінатний гідрогель, який містить:
а) альгінат;
б) об'єкт для впровадження в альгінатний гідрогель; і
в) ліпазу, використовувану для одержання альгінатного гідрогелю.
18. Альгінатний гідрогель за п. 17, де об'єкт для впровадження в альгінатний гель є біологічним матеріалом, переважно сперматозоїдами.
19. Набір альгінатного гідрогелю, що включає один контейнер, який містить ліпазу, і другий контейнер, який містить субстрат, здатний до гідролізу ліпазою, де субстрат, здатний до гідролізу ліпазою, є сполукою формули І:
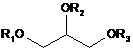 , (І)
, (І)
де R1, R2 і R3, незалежно один від одного, є однаковими або різними і позначають С1-С12-алкілкарбонільний ланцюг і де зазначений набір також включає альгінат і карбонат, що вивільняє двовалентний катіон.
Текст
Реферат: Винахід належить до способу виготовлення гідрогелів, таких як альгінатні гідрогелі, за допомогою використання ліпази, субстрату здатного до гідролізу ліпазою, агента, що вивільняє двовалентні катіони, для іммобілізації і збереження біологічного матеріалу, такого як клітинний матеріал, наприклад сперматозоїди. UA 113188 C2 5 10 15 20 25 30 35 40 45 50 55 60 Область винаходу Даний винахід відноситься до вдосконаленого способу одержання гідрогелів, зокрема альгінатних гідрогелів. Гідрогелі даного винаходу мають широку область застосування і, зокрема, використовуються для іммобілізації біологічного матеріалу, зокрема, для іммобілізації і збереження клітинного матеріалу, такого як, наприклад, сперматозоїди. Рівень техніки Гідрогелі складаються з полімерних ланцюгів, утворюючих гідрофільну мережу, яка містить воду, що має широку область застосування в різних галузях промисловості, зокрема в біотехнологічній і фармацевтичній промисловості. Наприклад, гідрогелі використовуються для іммобілізації біологічного матеріалу, такого як клітини для трансплантації, або як системи доставки, наприклад, для фармацевтично активних інгредієнтів або живильних речовин. Гідрогелі також можуть бути використані як ранові пов'язки. Крім того, гідрогелі, зокрема, альгінатні гідрогелі, широко використовуються як загусники. Широко використовуваним полімером для формування гідрогелів є альгінат. Альгінати - це аніонні полісахариди природного походження, що складаються з 1,4-зв'язаної-β-D-мануронової кислоти (М) і α-L-глюкуронової кислоти (G). (Smidsrød and Skjåk-Bræk, 1990, Trends in biotechnology, vol. 8, no. 3, pp 71-78). Комерційні альгінати витягують з морських водоростей, таких як Ascophyllum nodosum, Macrocystis pyrifera, і Laminaria hyperborea, а також в деякій мірі Laminaria digitata, Laminaria japonica, Eclonia maxima, Lesonia negrescens і Sargassum sp. Альгінати можуть бути виготовлені з деяких бактерій, продукуючих альгінати, наприклад, з деяких видів Pseudomonas і з Azotobacter vinelandii (Smidsrød and Skjåk-Bræk, 1990, див. вище). Альгінати широко використовуються, зокрема, в харчовій промисловості, наприклад, як стабілізатори для контролю в'язкості або як загусники. Альгінати також широко використовуються у фармацевтичній промисловості і косметичній промисловості, а також як стабілізатори, загусники або дезінтегруючі агенти. Для різних цілей доступні альгінати, багаті або гулуроновою кислотою, або мануроновою кислотою, відповідно (Mancini et al. (1999), Journal of Food Engineering 39, 369-378, WO8603781, US 4990601, US 5639467). Завдяки біосумісності та здатності альгінатів утворювати гель в присутності двовалентних катіонів, таких як, наприклад, іони кальцію, альгінати також широко використовуються для інкапсуляції клітин (Nebel, R.l., Balme, J., Saacke, R.g. and Lim. F. (1985), J. Anim. Sci. 60:16311639, Lim, F and Sun, A.m., (1980) Science 210: 908-9100, WO 2006/106400, EP0922451, US6596310, Torre et al. (1998), S.t.p. Pharma Sciences, 8 (4), pp. 233-236, Torre et al., (2000), Biomaterials, 21, pp. 1493-1498, Torre et al. (2002), Journal of Controlled Release, 85, pp. 83-89, Faustini et al, (2004),theriogenology, 61, 173-184, Weber et al. (2006), Journal of Biotechnology, 123, pp. 155-163). Альгінатні гелі також можуть бути використані для іммобілізації різних матеріалів. Наприклад, в WO2008/004890 описані біополімерні частинки, використовувані для збереження сперматозоїдів, де біологічний матеріал впроваджений в полімерну частинку і знаходиться в твердому стані на всьому діаметрі частинки. При впровадженні сперматозоїдів в альгінатні гідрогелі замість інкапсуляції сперматозоїдів, при якій сперматозоїди залишаються в рідкій серцевині капсул, клітини іммобілізовані в альгінатній мережі гелю, що обмежує рухливість клітин під час зберігання. Альгінатні гідрогелі, наприклад альгінатні гелі, використовувані для інкапсуляції або захоплення різних матеріалів, можуть бути одержані шляхом змішування розчину матеріалу, який повинен бути впроваджений, з розчином альгінату натрію, і додавання цього розчину в розчин, що містить багатовалентні катіони, зазвичай двовалентні катіони, такі як іони кальцію (наприклад, розчин CaCl2) (Smidsrød and Skjåk-Bræk, 1990, див. вище). У US 6497902 розкрито інший спосіб одержання біосумісних гідрогелів, таких як альгінатні гідрогелі, що включає змішування клітин, які будуть впроваджені, солі альгінату і агента, що вивільняє кальцій, з подальшим додаванням сполуки, яка вивільняє кальцій, до зазначеної суміші з утворенням поперечно-зшитого гелю. Відповідно до патенту США 6497902 агентом, що вивільняє кальцій, може бути D-глюконо-δ-лактон (GDL). Спосіб, розкритий в патенті США 6497902, може бути використаний для іммобілізації сперматозоїдів, використовуваних для штучного запліднення (наприклад, для виготовлення альгінатних гідрогелів, описаних в WO 2008/004890). Наприклад, розведені та охолоджені (4 °С) сперматозоїди можна додати до розчину, що містить розчинений альгінат натрію і суспендований карбонат кальцію і, можливо, кріопротектор, такий як гліцерин, і після цього ініціювати гелеутворення і одержати потрібний альгінатний гідрогель шляхом додавання розчину, що містить GDL. Додавання GDL приводить до формування глюконової кислоти, яка, у + + свою чергу, вступає в реакцію з водою і формує H3O . Підвищення рівня H3O і присутність 1 UA 113188 C2 2+ 5 10 15 20 25 30 35 40 45 50 55 2+ карбонату кальцію приводить до вивільнення CO 2 і Ca . Введення Ca шляхом додавання GDL приводить до формування альгінатного гідрогелю з впровадженими сперматозоїдами. Після того, як гелеутворення відбулося, контейнери, заповнені сперматозоїдами, впровадженими в альгінат, можна кріоконсервувати в рідкому азоті, забезпечуючи тим самим кріоконсервацію сперматозоїдів з виключно тривалим терміном зберігання. Проте, автори даного винаходу виявили, що застосування GDL у виготовленні альгінатних гідрогелів відповідно до способу, описаному в патенті США 6497902, має декілька недоліків. При виготовленні альгінатного гелю, що містить іммобілізовані сперматозоїди, відповідно до способу, описаного вище, дуже важливо додавати GDL до розчину відразу після приготування розчину GDL, щоб уникнути спонтанного гелеутворення. GDL потрібно додавати в розчиненому вигляді, а не у вигляді порошку, щоб уникнути на початковому етапі локальних областей/зон з високою концентрацією глюконової кислоти, які були б шкідливі для сперматозоїдів. Крім того, після додавання GDL буде проходити період підвищення в'язкості в результаті ініціації реакції гелеутворення. У зв'язку із збільшенням в'язкості контейнер, використовуваний для формування гідрогелю, потрібно заповнювати досить швидко. Тому за час, одержаний для перетворення розчиненого GDL в глюкуронову кислоту, розчин переносять у відповідні контейнери (такі як, наприклад, міні-пробірки, одержані від IMV, L'Aigle, Франція) для подальшого гелеутворення і іммобілізації бажаного біологічного матеріалу. Таким чином, спосіб, описаний в попередньому рівні техніки, приводить до достатньо короткого і негнучкого графіка виготовлення гідрогелів, що містять бажаний біологічний матеріал, та є істотним недоліком з промислової точки зору. Внаслідок недоліків описаного вище способу існує потреба у вдосконаленому способі одержання гідрогелів, зокрема в способі, придатному для виготовлення гідрогелів в промислових масштабах. Різні інші способи одержання гідрогелів описані в попередньому рівні техніки. Різні звіти розкривають застосування ферментів, які, впливаючи на специфічний субстрат, забезпечують різні реакції, які, зрештою, приводять до поперечного зв'язування різних типів полімерів. Наприклад, CN 101439206 розкриває, зокрема, застосування полімерів, що містять фенольну гідроксильну одиницю і діоксигеназу в каталізованому ферментом процесі одержання полімерних гелів. Johnsen et al. (2010), ACS Applied Materials & Interfaces, 2(7), pp. 1963-1972, повідомляють про виготовлення гідрогелю на основі ПЕГ, який полімеризується за допомогою глюкозооксидази. Глюкозооксидаза каталізує окислення β-D-глюкози, і подальше застосування кисню для утворення ферментного кофактора флавінаденіндинуклеотиду приводить до формування H2O2. При об'єднанні іонів заліза з цією ферментативною продукцією H 2O2 утворюються первинні гідроксильні радикали, які далі реагують з акрилатними мономерами. Про застосування H2O2 і пероксидази хріну у виготовленні гідрогелів також повідомлялося, наприклад, в Kurisawa et al., (2010), J. of Materials Chemistry, 20(26), pp. 5371-5375, Sakai et al, (2009), Biomaterials, 30(20), pp. 3371-3377, Sakai and Kawakami (2006), Acta Biomaterialia, 20017, 3, pp. 495-501, Lee et al. (2009), J. of Controlled Release, 134, pp. 186-193, Wang et al.(2010), Biomaterials, 31, pp. 1148-1157. Гідрогелі, виготовлені з використанням оксидази і H 2O2, не підходять для деяких застосувань, оскільки H2O2 є сильним окислювачем. Отже, все ще існує потреба у вдосконаленому і спрощеному процесі одержання альгінатних гідрогелів, зокрема гідрогелів, придатних для іммобілізації біологічного матеріалу. Суть винаходу Завданням даного винаходу є створення вдосконаленого способу одержання альгінатних гідрогелів без недоліків способів попереднього рівня техніки. Іншим завданням даного винаходу є створення спрощеного способу одержання альгінатних гідрогелів, придатних для іммобілізації біологічного матеріалу. Таким чином, винахід відноситься до альгінатного гідрогелю, де гелеутворення ініціюється за допомогою використання гідролази і субстрату, гідролізованого гідролазою, що приводить до + утворення H3O і подальшому вивільненню двовалентного катіона через присутність агента, який вивільняє двовалентні катіони. Відповідно до одного аспекту даного винаходу пропонується спосіб одержання альгінатного гідрогелю, причому зазначений спосіб включає змішування розчину, що містить гідролазу, з розчином, що містить субстрат, гідролізований гідролазою, при цьому розчин, що містить гідролазу, або розчин, що містить субстрат, гідролізований гідролазою, також містить альгінат і агент, що вивільняє двовалентні катіони. При змішуванні двох розчинів зв'язування субстрату з + гідролазою приводить до гідролізу зазначеного субстрату і подальшого утворення H 3O . 2 UA 113188 C2 + 5 10 15 Утворення H3O також приводить до вивільнення двовалентних катіонів, які, таким чином, ініціюють формування гідрогелю. Відповідно до одного втілення сполука, що вивільняє двовалентні катіони, і альгінат присутні в розчині, що містить гідролазу. Відповідно до іншого втілення сполука, що вивільняє двовалентні катіони, і альгінат присутні в розчині, що містить зазначений субстрат. Зазначена гідролаза може бути естеразою, наприклад, ліпазою. Відповідно до одного втілення даного винаходу гідролаза, використовувана в способі відповідно до винаходу, є тригліцеридліпазою. Відповідно до ще одного втілення винаходу сполука, що вивільняє двовалентні катіони, 2+ 2+ 2+ вивільняє двовалентні катіони, вибрані з групи, що складається з Ca , Ba і Sr . Відповідно до іншого втілення даного винаходу сполука, що вивільняє двовалентні катіони, є сполукою, що вивільняє кальцій, такою як, наприклад, карбонат кальцію. Відповідно до ще одного втілення даного винаходу субстратом є складний ефір органічної кислоти. Відповідно до ще одного втілення даного винаходу пропонується спосіб, що включає етапи змішування розчину, який містить триацилгліцеридліпазу, з розчином, який містить субстрат, що гідролізований зазначеною гідролазою, при цьому субстрат є сполукою формули I: OR2 OR3 R1O (I), 20 25 30 35 40 45 де R1, R2 і R3 незалежно один від одного однакові або різні і позначають лінійний або розгалужений, заміщений або незаміщений C1-C12-алкіл карбонільний ланцюг, і де розчин, який містить зазначену ліпазу, або розчин, який містить сполуку формули I, також містить альгінат і сполуку, що вивільняє двовалентні катіони. Відповідно до одного втілення R 1, R2 і R3 незалежно один від одного є однаковими або різними і позначають лінійний або розгалужений, заміщений або незаміщений C1-C12-алкіл карбонільний ланцюг, наприклад, лінійний незаміщений C1-C3алкіл карбонільний ланцюг. Відповідно до ще одного втілення даного винаходу R1, R2 і R3 формули I є однаковими або різними і позначають лінійний або розгалужений, заміщений або незаміщений C 1-C3-алкіл карбонільний ланцюг. Відповідно до одного втілення даного винаходу R1, R2 і R3 формули I вибрані з групи, що складається з метанону, етанону, ацетону, бутанону, пентанону, гексанону, гептанону, октанону, нонанону, деканону або додеканону. Зокрема, наприклад, коли сперматозоїди повинні бути впроваджені в альгінатний гідрогель, субстрат може бути вибраний з групи, що складається з триацетину, трипропіоніну і трибутирину, переважно трипропіоніну і трибутирину. Відповідно до іншого втілення даного винаходу розчин, який містить гідролазу, або розчин, який містить субстрат, гідролізований гідролазою, може також містити об'єкт, який повинен бути впроваджений в альгінатний гідрогель. Об'єкт, який буде впроваджений в альгінатний гель, може відповідно до одного аспекту даного винаходу бути біологічним матеріалом, наприклад, клітинним матеріалом, таким як сперматозоїди. Відповідно до одного втілення даного винаходу пропонується спосіб одержання альгінатних гідрогелів, що містять сперматозоїди, де спосіб включає етапи i) формування першого розчину шляхом розведення сперматозоїдів розчином, що містить триацилгліцеридліпазу; ii) додавання до першого розчину, одержаного на етапі i), другого розчину, який містить альгінат, сполуки, що вивільняє двовалентні катіони, і сполуки формули I: OR2 OR3 R1O (I), 50 де R1, R2 і R3 незалежно один від одного є однаковими або різними і позначають лінійний або розгалужений, заміщений або незаміщений C1-C12-алкіл карбонільний ланцюг, ініціюючи гелеутворення; 3 UA 113188 C2 5 iii) перенесення розчину, одержаного на етапі ii), у контейнер для гелеутворення альгінатного гідрогелю; iv) можливо, кріоконсервації альгінатного гідрогелю iii). Відповідно до ще одного втілення даного винаходу пропонується спосіб одержання альгінатних гідрогелів, що містять сперматозоїди, де спосіб включає етапи i) формування першого розчину шляхом розведення сперматозоїдів розчином, який містить сполуку формули I: OR2 OR3 R1O 10 15 20 25 30 35 40 45 50 55 (I), де R1, R2 і R3 незалежно один від одного є однаковими або різними і позначають лінійний або розгалужений, заміщений або незаміщений C1-C12-алкіл карбонільний ланцюг; ii) додавання до розчину, одержаного на етапі i), другого розчину, який містить альгінат, сполуки, що вивільняє двовалентні катіони, і тригліцеридліпазу, що ініціює гелеутворення; iii) перенесення розчину, одержаного на етапі ii), у контейнер для гелеутворення альгінатного гідрогелю; iv) можливо, кріоконсервації альгінатного гідрогелю iii). Відповідно до одного втілення перший і другий розчини i) та ii) також містять кріопротектор, а розчин, одержаний в iii), також піддають кріоконсервації. Крім того, при виготовленні альгінатних гідрогелів, що містять сперматозоїди, відповідно до даного винаходу, як в цілому описано вище, контейнери, одержані в iii), можуть бути також піддані кріоконсервації, і де розчин етапу i) та/або етапу ii) включає кріопротектор. Кріопротектор, присутній в розчині етапу i) та/або етапу ii) відповідно до цього втілення даного винаходу, може бути вибраний з групи, що складається з гліцерину, етилгліколю, метанолу, DMA, DMSO, пропіленгліколю, трегалози, глюкози. При виготовленні альгінатних гідрогелів, що містять сперматозоїди, відповідно до даного винаходу, сполука, що вивільняє двовалентні катіони, переважно може бути карбонатом кальцію, а субстрат, гідролізований гідролазою, переважно може бути вибраний з групи, що складається з триацетину, трипропіоніну і трибутирину. Відповідно до одного втілення даного винаходу альгінатом є альгінат, багатий гулуроновою кислотою. Відповідно до іншого аспекту даного винаходу запропонований альгінатний гідрогель, одержаний відповідно до даного винаходу. Альгінатний гідрогель відповідно до даного винаходу в одному втіленні даного винаходу може включати: а. альгінат; b. можливо, об'єкт для впровадження в альгінатний гідрогель; с. гідролазу, використовувану у виготовленні альгінатного гідрогелю. Альгінатний гідрогель відповідно до даного винаходу формується шляхом гелеутворення альгінату, де гелеутворення досягається за рахунок вивільнення двовалентних катіонів із сполуки, що вивільняє двовалентні катіони, в результаті гідролізу гидролазного субстрату. Таким чином, утворений гідрогель включає гідролазу, використовувану у формуванні гелю. Присутність гідролази в гідрогелі відповідно до даного винаходу, таким чином, показує, що був застосований спосіб винаходу. Відповідно до іншого втілення альгінатний гідрогель відповідно до винаходу містить впроваджений об'єкт. Відповідно до іншого втілення зазначений об'єкт для впровадження є біологічним матеріалом, таким як клітинний матеріал, наприклад, сперматозоїди. Відповідно до ще одного аспекту даного винаходу запропонований набір альгінатного гідрогелю, що включає один контейнер з гідролазою і другий контейнер з субстратом, гідролізованим гідролазою. Одне втілення відповідно до цього аспекту даного винаходу стосується набору альгінатного гідрогелю, що включає один контейнер з розчином, що містить гідролазу, і другий контейнер з розчином, що містить альгінат, сполуку, що вивільняє двовалентні катіони, і субстрат, гідролізований гідролазою. Ще одне втілення цього аспекту стосується набору альгінатного гідрогелю, що включає один контейнер з розчином, який містить субстрат, гідролізований гідролазою, і другий контейнер з розчином, який містить альгінат, сполуку, що вивільняє двовалентні катіони, і гідролазу. 4 UA 113188 C2 5 10 15 20 25 30 35 40 45 50 55 60 Нарешті, даний винахід відноситься до застосування гідролази і субстрату, гідролізованого гідролазою, у виготовленні альгінатного гідрогелю. Відповідно до одного втілення фермент, використовуваний відповідно до цього аспекту, є естеразою, такою як ліпаза, наприклад, триацилгліцеридліпаза. Відповідно до одного втілення даного аспекту винахід передбачає застосування гідролази і субстрату у виготовленні альгінатного гідрогелю з впровадженням біологічного матеріалу, переважно сперматозоїдів. Докладний опис винаходу Даний винахід передбачає новий спосіб виготовлення альгінатних гідрогелів, використовуваних в різних областях застосування. Зокрема, даний винахід передбачає новий спосіб виготовлення гідрогелів, які, зокрема, використовуються для впровадження та іммобілізації біологічних матеріалів. Різні типи альгінату можуть бути використані для виготовлення гідрогелів відповідно до даного винаходу. Співвідношення гулуронової кислоти і мануронової кислоти не є критичним, тобто тип альгінату і вміст гулуронової кислоти в порівнянні з мануронової кислотою можуть бути вибрані залежно від бажаної міцності, стабільності, здібності до набухання, ерозійних характеристик і так далі. Застосування G-багатих альгінатів буде, наприклад, давати міцніші, стабільніші гідрогелі. Відповідно до одного втілення альгінат, використовуваний для формування гідрогелів, є альгінат, багатий гулуронової кислотою. Термін "альгінат, багатий гулуронової кислотою" або "G-багатий альгінат", використовуваний в даному документі, означає альгінат, що містить більшу кількість гулуронової кислоти в порівнянні з мануроновою кислотою в полісахаридному полімерному ланцюзі використовуваного альгінату. Навпаки, термін "M-багатий альгінат" або "альгінат, багатий мануроновою кислотою", використовуваний в даному документі, означає альгінат, що містить більші кількості мануронової кислоти в порівнянні з гулуронової кислотою. Термін "багатий", використовуваний у зв'язку з альгінатамі, що містять більшу кількість мануронової кислоти або гулуронової кислоти, відповідно, добре відомий і зазвичай використовується фахівцями в даній області, наприклад, в Britt Iren Glaerum Svanem et al Journal of Biological Chemistry Vol 276, No 34, Aug 24 2001 pp31542-31550, Sumita Jain et al Molecular Microbiology (2003) 47(4), pp1123-1133, Marco Mancini et al Journal of Food Engineering 39 (1999) pp369-378, Applied and Environmental Microbiology, Sept 1982, Vol. 44 No.3 pp754-756, патенті США 5639467, публікації патенту США 2006/0159823, Ji Minghou (M. H. Chi) et al Hydrobiologia 116/117 (1984), pp 554-556. Необмежуючі приклади відповідних типів альгінату, які використовуватимуться відповідно до даного винаходу, включають FMC LF 10/40, FMC LF 10/60 і FMC LF 20/60, доступні від FMC Biopolymer AS, Драммен, Норвегія, A2033 від Sigma, Осло, Норвегія, або альгінати Pronova UP MYG, Pronova UP LVG, доступні, наприклад, від Novamatrix, Сандвіка, Норвегія. Функція альгінатного гідрогелю відповідно до даного винаходу не залежить від тривимірної форми освіченого гідрогелю, тобто альгінатний гідрогель може мати різну форму, таку як, наприклад, сферична або циліндрична. Різні форми альгінатного гелю можуть бути одержані залежно від використовуваного контейнера для гелеутворення. Також відповідно до даного винаходу можуть бути використані інші полімери, які після дії ферменту і субстрату, що приводить до вивільнення двовалентних катіонів, формують гідрогелі. Відповідно до даного винаходу фермент, тобто гідролаза, разом з відповідним субстратом до неї використовується для ініціації гелеутворення альгінату. Термін "гідролаза", + використовуваний в даному документі, охоплює гідролази, здатні продукувати H3O при змішуванні розчину, що містить субстрат(и), з іншим розчином, що містить гідролазу. Відповідно до одного втілення даного винаходу гідролаза є ліпазою. Відповідно до ще одного втілення даного винаходу ліпаза є ацилгідролазою, переважніше тригліцеридліпазою, такою як, наприклад, триацилгліцеридліпаза, виділена з дріжджів Candida rugosa. Відповідна ліпаза доступна від Sigma-aldrich Co. LLC (L1754 - тип VII або L3001 тип I, CAS № 9001-62-1). + Слід розуміти, що будь-яка гідролаза, що приводить до чистої продукції H3O при гідролізі її субстрату, може бути використана відповідно до даного винаходу. Гідролаза, яка може бути використана, таким чином, може бути вибрана з групи, що складається з гидролаз ефірів карбонових кислот, глікозидаз і ферментів, що діють на вуглець-вуглецеві зв'язки в кетонових речовинах. Необмежуючі приклади гидролаз ефірів карбонових кислот включають карбоксилестеразу, тригліцеридліпази, ацетилестеразу, стеролестеразу, L-арабінонолактоназу, глюконолактоназу, ацилгліцеролліпазу, γ-ацетилглюкозо-деацетилазу, ліпопротеїнліпазу, синтазу етилових ефірів жирних кислот і діацилгліцерол-ацилгідролазу. 5 UA 113188 C2 5 10 15 Необмежуючі приклади гідролаз, що впливають на вуглець-вуглецеві зв'язки в кетонових речовинах, включають ацилпіруват-гідролазу і ацетилпіруват-гідролазу. Необмежуючим прикладом глікозидази є α -галактуронідаза. При формуванні альгінатного гелю відповідно до даного винаходу гідролаза та її субстрат присутні в різних розчинах, які при перемішуванні ініціюють процес гелеутворення, де один з зазначених двох розчинів на додаток містить альгінат і сполуку, що вивільняє двовалентні катіони. Послідовність змішування, тобто чи додають розчин, що містить фермент, до розчину, що містить субстрат, або навпаки, або ж це розчин, що містить фермент, який на додаток містить альгінат і сполуку, що вивільняє двовалентні катіони, або навпаки, не є критичним. Субстрат, використовуваний у формуванні альгінатного гідрогелю відповідно до даного + винаходу, є субстратом, який після зв'язування з ферментом приводить до продукції H3O . Субстрат, таким чином, може варіювати залежно від типу використовуваної гідролази відповідно до даного винаходу. Відповідними субстратами відповідно до даного винаходу є складні ефіри органічних кислот, таких як карбонові кислоти. Відповідно до одного втілення даного винаходу субстратом є сполука формули I: OR2 OR3 R1O (I), 20 25 30 35 40 де R1, R2 і R3 незалежно один від одного є однаковими або різними і позначають лінійний або розгалужений, заміщений або незаміщений C 1-C12--алкіл карбонільний ланцюг, такий як, наприклад, метанон, етанон, ацетон, бутанон, пентанон, гексанон, гептанон, октанон, нонанон, деканон, додеканон і так далі. Відповідно до одного втілення R 1, R2 і R3 є метанонами. Відповідно до одного втілення R1, R2 і R3 є етанонами. Відповідно до ще одного втілення R1, R2 і R3 є ацетонами. Субстрати формули I, зокрема, використовуються у формуванні альгінатних гідрогелів за допомогою триацилгліцеридліпази в якості гідролази відповідно до даного винаходу. Після зв'язування з ферментом, присутнім в першому розчиннику, зазначений складний ефір формули I розділяється на гліцерин і карбонову кислоту, тобто утворює, таким чином, + H3O . Алкільний карбонільний ланцюг може бути розгалуженим або нерозгалуженим. Алкільний карбонільний ланцюг також може бути заміщеним або незаміщеним. Фахівець в даній області на підставі викладеної тут ідеї зрозуміє, що можуть бути використані різні субстрати, що покриваються формулою I, і зможе на підставі ідей даного документа вибрати правильний субстрат для застосування відповідно до даного винаходу. Таким чином, фахівець в даній області матиме на увазі, що довжина алкільного ланцюга може змінюватися без впливу на здатність ферменту продукувати гліцерин і карбонову кислоту субстрату, що приводить до + вивільнення іонів H3O . Відповідно до переважного втілення даного винаходу субстрат вибирають з групи триацетину, трипропіоніну і трибутирину з формулами: O O O O O O O O 45 50 O O O O O O O O O O Триацетин Трипропіонін Трибутирин Таким чином, відповідно до одного втілення R1, R2 і R3 позначають C1-C4-алкілкарбоніл. Відповідно до ще одного втілення даного винаходу присутній субстрат вибирають з групи, що складається з трипропіоніну і трибутирину. Відповідно до даного винаходу змішування гідролази і субстрату, визначеного вище, + + приводить до продукції H3O . Зазначений H3O , крім того, приводить до вивільнення двовалентних катіонів з агента, що вивільняє двовалентні катіони. Термін "агент, що вивільняє 2+ 2+ двовалентні катіони" охоплює сполуки, що приводять до вивільнення, наприклад, Ca , Br або 2+ Sr . Відповідно до одного втілення даного винаходу агент, що вивільняє двовалентні катіони, є карбонатною сіллю, наприклад CaCO3, BrCO3 або SrCO3. Відповідно до переважного втілення 6 UA 113188 C2 5 10 15 20 25 30 35 40 45 50 55 60 агент, що вивільняє двовалентні катіони, є агентом, що вивільняє кальцій, таким як, наприклад, карбонат кальцію. Відповідно до одного втілення даного винаходу передбачається спосіб за даним винаходом для впровадження різних матеріалів в полімерну матрицю гідрогелю. Термін "впровадження" або "впроваджений", використовуваний в даному документі, слід розуміти як іммобілізацію матеріалу в альгінатних гідрогелях даного винаходу, де альгінатна мережа присутня у всьому діаметрі гідрогелю (на відміну від інкапсуляції, де гідрогель утворює стінку навколо рідкого ядра, що не містить полімерну мережу). Термін "біологічний матеріал" слід розуміти як такий, що охоплює будь-який тип біологічного матеріалу, відповідного для іммобілізації або інкапсульованого в біосумісні гідрогелі. Необмежуючий список біологічних матеріалів включає, наприклад, клітини для трансплантації, такі як, наприклад, інсулін-продукуючі клітини, клітини гібридоми, що продукують моноклональні антитіла, або сперматозоїди для застосування в штучному заплідненні та інших репродуктивних технологіях. У випадку якщо матеріал для впровадження є сперматозоїдами, впровадження приводить до того, що сперматозоїди не мають можливості проявляти свою природну здатність рухатися. Ступінь іммобілізації може змінюватися залежно від характеристик альгінатного гідрогелю, наприклад, від механічної міцності і здібності до дезінтеграції, наприклад, після запліднення тварини-реципієнта. Відповідно до одного переважного втілення біологічний матеріал для іммобілізації відповідно до даного способу, є сперматозоїдами. Сперматозоїди, іммобілізовані в альгінатному гідрогелі, одержаному відповідно до даного винаходу, можливо, можуть бути піддані кріоконсервації для зберігання в рідкому азоті. Альгінатний гідрогель, що містить іммобілізовані сперматозоїди, одержаний відповідно до даного винаходу, може бути виготовлений у вигляді готових до застосування доз запліднення шляхом іммобілізації відповідного числа сперматозоїдів в альгінатном гідрогелі, а також шляхом виконання гелеутворення в контейнері, такому як пробірка, зазвичай використовуваному в процедурах штучного запліднення і такому, що має потрібний розмір, форму і об'єм. Для вбудовування (іммобілізації) сперматозоїдів в гідрогель відповідно до одного втілення даного винаходу сперматозоїди після збору розводять в розчиннику, що містить або фермент, або субстрат. Зазначений розбавлений розчин сперматозоїдів, можливо, охолоджують приблизно до 4 °С. Розчин, використовуваний для розведення сперматозоїдів, в даному документі також називають розчином-наповнювачем (див., наприклад, приклад 1). Відповідно до переважного втілення даного винаходу сперматозоїди спочатку розводять в розчині-наповнювачі, що не містить субстрат або фермент. Потім, на другому етапі розведення, додають субстрат або фермент, при цьому розчин-наповнювач, який потім використовують, на додаток містить або фермент, або субстрат. Відповідно до одного втілення сперматозоїди розводять вдруге в розчині-наповнювачі, що містить фермент гідролазу. Одержаний таким чином розчин потім змішують з другим розчином, який містить альгінат, карбонат кальцію і, можливо, кріопротектор, такий як гліцерин, і субстрат для ферменту, присутнього в першому розчині, який містить розведені сперматозоїди і фермент. Після додавання і змішування двох розчинів фермент зв'язується з субстратом, що + приводить до утворення кислоти і, отже, підвищенню рівня H3O . Карбонат кальцію, що діє як 2+ буфер, запобігатиме підвищенню рН, приводячи до вивільнення Ca і продукції CO2. 2+ Вивільнення Ca приводить до поперечного зшивання полісахаридних ланцюгів альгінату і, таким чином, формування альгінатного гідрогелю. Слід розуміти, що сперматозоїди також можуть бути розведені в розчині-наповнювачі, що містить субстрат, гідролізований ферментом, який використовуватиметься відповідно до даного винаходу, який потім змішують з другим розчином, що містить фермент, карбонат кальцію і, можливо, кріопротектор. Таким чином, сперматозоїди спочатку можуть бути розведені в розчині-наповнювачі і потім піддані другому розведенню шляхом додавання більшої кількості розчину-наповнювача, що також містить субстрат. Одержаний таким чином розчин потім може бути змішаний з розчином, що містить фермент, альгінат, карбонат кальцію і, можливо, кріопротектор, такий як гліцерин. При змішуванні двох розчинів ініціюється гелеутворення. Температура розчинника, використовуваного для розведення сперматозоїдів, і температура подальших етапів формування гелю може змінюватися в залежності, наприклад, від типу і джерела сперматозоїдів. Спосіб даного винаходу, таким чином, може бути здійснений в холодильнику або при кімнатній температурі (наприклад, 20-24 °С) або навіть при більш високій температурі, такої як, наприклад, 30-35 °С. 7 UA 113188 C2 5 10 15 20 25 30 35 40 45 50 55 60 Спосіб за винаходом робить можливим контроль швидкості процесу гелеутворення шляхом варіювання кількості використовуваного ферменту. Крім того, концентрація використовуваного альгінату впливає на механічні характеристики утвореного гідрогелю і, отже, на характеристики розчинення гідрогелю. Концентрація альгінату, таким чином, може варіювати залежно від бажаних характеристик гідрогелю залежно від області застосування гідрогелю. Фахівець в даній області на підставі ідей даного документа зможе вибрати відповідну кількість використовуваного ферменту, субстрату і альгінату для одержання заданої міцності гелю і бажаного часу гелеутворення. Наприклад, застосування 3 г триацилгліцеридліпази на літр і 0,3-1 г субстрату на 100 мл в розчині сперматозоїдів/альгінату, одержаному після змішування двох розчинів відповідно даному винаходу, дає час гелеутворення приблизно 2-3 години, якщо розчин зберігають при температурі приблизно 4 °C. Кількість субстрату може додатково варіювати залежно від типу використовуваного ферменту. + Крім того, кількість кислоти і, таким чином, кількість H 3O , одержаного при змішуванні двох розчинів, можна регулювати за допомогою кількості субстрату, присутнього в другому розчиннику. Таким чином, можна контролювати як швидкість гелеутворення, так і кінцевий рН процесу, що є перевагою з промислової точки зору. Це забезпечує покращуваний і легший процес виробництва, яким можна виконати гелеутворення, коли воно підходить з погляду виробництва, оскільки гелеутворення починається при змішуванні сперматозоїдів, розведеннях в розчині-наповнювачі, що містить або фермент, або субстрат. При впровадженні біологічного матеріалу слід розуміти, що змішуваний розчин на додаток може містити сполуки, використовувані, наприклад, з метою консервації, такі як, наприклад, антибіотики, наповнювачі, антиоксиданти, буфери і так далі, див. WO 2008/ 004890. Концентрація біологічного матеріалу, наприклад живих клітин, впроваджених в альгінатні гідрогелі відповідно даному винаходу, може варіювати залежно від типу/джерела матеріалу. У разі впровадження сперматозоїдів концентрація також може варіювати залежно від породи, тварини-реципієнта, методик запліднення, наявності додаткових сполук (наприклад, з метою консервації) і так далі, див., наприклад, WO 2008/ 004890. Хоча даний винахід особливо корисний для впровадження в альгінатний гель біологічного матеріалу у вигляді клітин або тканин, слід розуміти, що альгінатні гелі, одержані відповідно до даного винаходу, також мають ряд інших застосувань, зокрема впровадження або іммобілізацію інших об'єктів, відмінних від біологічного матеріалу, а також застосувань, що включають гідрогелі самі по собі. Даний винахід, таким чином, не повинен тлумачити як обмежене застосуваннями, конкретно розкритими в прикладах, наведених в описі. Таким чином, інші об'єкти, що представляють інтерес, також можуть бути вбудовані в альгінатний гідрогель, одержаний відповідно до даного винаходу. Термін "об'єкт для впровадження в альгінатний гідрогель", використовуваний в даному описі, охоплює будь-який матеріал, який придатний для іммобілізації в гідрогелі. Наприклад, у разі, коли альгінатний гідрогель відповідно до даного винаходу повинен бути використаний як система з контрольованим вивільненням, об'єкт для впровадження може бути фармацевтично активним інгредієнтом. Наприклад, альгінатні гелі, одержані відповідно до даного винаходу, можуть бути використані як система доставки з контрольованим вивільненням або сповільненим вивільненням для діапазону сполук, таких як фармацевтично активні сполуки, див., наприклад, WO98/46211, US 4695463, US 6656508, які включені в даний документ за допомогою посилання. Необмежуюча група фармацевтично активних інгредієнтів, які будуть впроваджені в альгінатний гідрогель відповідно до даного винаходу, включає, наприклад, рекомбінантні або природні білки або поліпептиди, природні або синтетичні або напівсинтетичні сполуки, такі як фактори росту, гормони, антитіла, інтерферони, інтерлейкіни і так далі. Альгінатні гідрогелі відповідно до даного винаходу також можуть застосовуватися в харчовій промисловості, наприклад, для впровадження живильних речовин. Гідрогелі, одержані відповідно до даного винаходу, також можуть бути використані самі по собі для інших промислових цілей, таких як фармацевтична промисловість або косметична промисловість (наприклад, як загусник, в ранових пов'язках, в стоматологічних продуктах і способах), або в харчовій промисловості для людини і тварин (наприклад, у виготовленні реструктурованої їжі, як загусник і так далі). Даний винахід передбачає переваги в порівнянні з відомим рівнем техніки. Наприклад, при застосуванні методики, описаної в US 6497902, на швидкість реакції, а також на кількість утвореної кислоти можна впливати, змінюючи концентрацію GDL. Зміни в концентрації GDL, проте, будуть одночасно також впливати на кількість утвореної кислоти і, таким чином, на кінцеве значення рН в гелі. Виготовлення альгінатного гідрогелю за допомогою ферменту і 8 UA 113188 C2 5 10 15 20 25 30 35 40 45 50 55 субстрату, гідролізованого зазначеним ферментом, щоб ініціювати гелеутворення, дозволяє значно краще контролювати швидкість реакції і кількість утвореної кислоти (рН в гелі), оскільки швидкість реакції і кінцеве значення рН можуть окремо контролюватися шляхом зміни концентрації ферменту і субстрату, відповідно. Відповідно до ще одного аспекту даний винахід передбачає набір альгінатного гідрогелю, що включає контейнер з гідролазою та інший контейнер з субстратом, гідролізованим гідролазою. Набір відповідно до даного винаходу також може містити інші сполуки, необхідні для заливки альгінатного гідрогелю відповідно до даного винаходу. Таким чином, набір також може включати альгінат і сполуку, що вивільняє двовалентні катіони. Зазначені сполуки можуть міститися в контейнері з гідролазою, в контейнері з субстратом, гідролізованим зазначеною гідролазою, або вони можуть міститися в окремому контейнері(ах). Контейнери також можуть містити інші сполуки, що представляють конкретний інтерес залежно від застосування альгінатного гідрогелю, залитого за допомогою набору даного винаходу. Наприклад, у випадку, якщо набір слід використовувати для заливки гелів, що містять біологічний матеріал, такий як клітинний матеріал, наприклад, сперматозоїди, і якщо одержаний альгінатний гідрогель повинен бути далі підданий кріоконсервації, то набір також може містити кріопротектор, такий як, наприклад, гліцерин, етилгліколь, метанол, DMA, DMSO, пропіленгліколь, трегалозу, глюкозу. Зазначений кріопротектор(и) може міститися в контейнері з гідролазою, в контейнері з субстратом, гідролізованим зазначеною гідролазою, або він може міститися в окремому контейнері(ах). Набір може також містити інші сполуки, використовувані з метою консервації, такі як, наприклад, антибіотики, наповнювачі, антиоксиданти, буфери і так далі, відомі фахівцеві в даній області, див., наприклад, WO 2008/ 004890. Для ілюстративних цілей надані наступні приклади. Слід розуміти, що наведені нижче приклади не повинні тлумачити як такі, що обмежують об'єм даного винаходу. Наведений вище опис різних втілень даного винаходу розкриває загальний характер винаходу, і фахівець в даній області зможе застосувати загальні знання в області гідрогелів, легко модифікувати та/або адаптувати спосіб даного винаходу без зайвого експериментування, не відходячи від загальної концепції даного винаходу та об'єму формули винаходу, що додається. Таким чином, такі адаптації або модифікації включають діапазон еквівалентів розкритих втілень, заснований на ідеях і рекомендаціях, представлених в даному документі. Слід розуміти, що термінологія, використовувана в даному документі, служить для опису, а не для обмеження. Таким чином, термінологія даного опису повинна бути інтерпретована фахівцем в даній області в світлі ідей і рекомендацій, представлених в даному описі, у поєднанні із знаннями в даній області. Приклад 1: Іммобілізація бичачих сперматозоїдів Матеріали і методи Матеріали Використовували наступні хімічні речовини: тризма гідрохлорид і EDTA від Sigma (Сент-Луіс, США), NaHCO3, NaCl, гліцерин (> 99 %), цитрат натрію і піруват натрію від Riedel de Haën (Зельце, Німеччина), моногідрат фруктози і глюкози від Norsk Medisinaldepot (Осло, Норвегія), карбонат кальцію від KSL staubtechnik gmbh (Лауінген, Німеччина) і альгінат натрію (PROTANAL LF 10/60) від FMC Biopolymer A/s (Драммен, Норвегія). Джерело сперматозоїдів Бичачі сперматозоїди збирали з об'єктів Geno Hallsteingård в Тронхейме і Store Ree в Штанге, Норвегія. Буферні розчини Використовували наступні розчини-наповнювачі: Наповнювач для першого розведення сперматозоїдів: 1,45 г/л тризма гідрохлорид глюкози, 0,4 г/л цитрату натрію, 1 г/л фруктози, 0,22 г/л пірувату натрію і 200 мл/л яєчного жовтка. рН розчину доводили до 6,4 додаванням NaOH. Розчин-наповнювач для другого розведення сперматозоїдів: 4 г/л карбонату кальцію (якщо не зазначене інше), 54 г/л фруктози, 170 г/л гліцерину і 24 г/л альгінату натрію LF10/60. Обидва наповнювачі містять стандартний коктейль антибіотиків з кінцевою концентрацією, щонайменше потрібною в директиві ЕС 88/407. Модифікації IVT: 3 г/л глюкози, 20 г/л цитрату натрію, 2,1 г/л NaHCO3, 1,16 г/л NaCl, 3 г/л EDTA, рН 7,35. У розчини-наповнювачі додавали або фермент (Sigma L1754), або субстрат, як зазначено нижче. Розведення, іммобілізація і кріоконсервація бичачих сперматозоїдів 9 UA 113188 C2 5 10 15 20 25 30 35 40 45 50 55 60 Бичачі сперматозоїди збирали з об'єктів Geno і розводили, як описано нижче: відразу ж 6 після збору сперматозоїди розводили до концентрації 219 × 10 клітин/мл в розчині-наповнювачі для першого розведення. Потім цей розчин негайно змішували з рівним об'ємом наповнювача для подальшого розведення, де зазначений наповнювач тепер містив або фермент, або субстрат. Потім одержаний розчин, що містить розведені сперматозоїди, охолоджували до 4 °C. Після охолоджування до 4 °C розчин змішували з рівним об'ємом розчину-наповнювача для третього розведення, де зазначений наповнювач тепер містив або субстрат (триацетин, трипропіонін або трибутирин), якщо розведені сперматозоїди з попереднього етапу містили фермент, або фермент, якщо розведені сперматозоїди з попереднього етапу містили субстрат. Крім того, наповнювач тепер містив карбонат кальцію як сполуку, що вивільняє двовалентні катіони, і альгінат. Потім одержані розчини переносили в пробірки для запліднення і врівноважували при 4 °C протягом приблизно 3 годин. Потім пробірки для запліднення переносили в N2-морозильну камеру і заморожували відповідно до стандартних процедур для сперми биків. Оцінка рухливості Рухливість сперматозоїдів оцінювали в мікроскопічному дослідженні. Заморожені пробірки для запліднення розморожували у водяній бані при температурі 37 °С протягом 30 секунд. Перед вимірюванням альгінатний гель розріджували в модифікованому розчині IVT. Вміст пробірки для запліднення додавали до 0,9 мл розчину IVT і обережно струшували на пристрої для перевертання пробірок протягом зразкового 10 хвилин. Перед оцінкою рухливості пробірки заздалегідь нагрівали в течію мінімум 15 хвилин в нагрівальному блоці при 37 °С. Приблизно 3 мкл розчину вносили на заздалегідь нагріте наочне скло для мікроскопії і відразу ж вивчали його за допомогою світлового мікроскопа. Число рухомих сперматозоїдів в кожній пробі оцінювали з найближчим інтервалом 5 %. Якщо практично це було можливо, оператор в ході оцінки не знав про джерело зразка. Результати а) Іммобілізація бичачих сперматозоїдів з використанням триацетину як субстрату Сперматозоїди збирали і розводили відповідно до процедур, описаних вище. У розчиннаповнювач для другого розведення додавали фермент (Sigma L1754) до концентрації 6 г/л в кінцевому розчині, що містить сперматозоїди. Розчин-наповнювач для третього розведення містив 8 г/л карбонату кальцію, і в нього додавали триацетин до концентрації 0,5 г/100 мл. Приблизно через 4 години після другого розведення формували гель для іммобілізації сперматозоїдів. Приблизно через 24 години зберігання при 4°C гель розріджували і оцінювали рухливість іммобілізованих сперматозоїдів. Приблизно 60 % сперматозоїдів в цей час були рухомими. b) Іммобілізація бичачих сперматозоїдів з використанням трипропіоніну як субстрату Сперматозоїди збирали, розводили, іммобілізували і кріоконсервували відповідно до процедур, описаних вище. У розчин-наповнювач для другого розведення додавали фермент (Sigma L1754) до концентрації 6 г/л в кінцевому розчині, що містить розведені сперматозоїди. Розчин-наповнювач для третього розведення містив 4 г/л карбонату кальцію, і в нього додавали трипропіонін до концентрації 0,30 г на 100 мл. Приблизно через 3 години після другого розведення формували гель і заморожували пробірки, що містять іммобілізовані сперматозоїди. Пробірки для запліднення зберігали в рідкому N2 протягом декількох днів до розморожування і оцінки рухливості. Приблизно 60 % сперматозоїдів були рухомі після розморожування і розрідження гелю. c) Іммобілізація бичачих сперматозоїдів з використанням трипропіоніну як субстрату Сперматозоїди збирали, розводили, іммобілізували і кріоконсервували відповідно до процедур, описаних вище. У розчин-наповнювач для другого розведення додавали трипропіонін до концентрації 0,30 г/100 мл в кінцевому розчині, що містить розведені сперматозоїди. Розчиннаповнювач для третього розведення містив 4 г/л карбонату кальцію, і в нього додавали фермент Sigma L1754 до концентрації 6 г/л. Приблизно через 2 години після другого розведення формували гель. Приблизно через 24 години зберігання при 4°C гель розріджували і оцінювали рухливість іммобілізованих сперматозоїдів. Приблизно 60 % сперматозоїдів в цей час були рухомими. d) Іммобілізація бичачих сперматозоїдів з використанням трибутирину як субстрату Сперматозоїди збирали, розводили, іммобілізували і кріоконсервували відповідно до процедур, описаних вище. У розчин-наповнювач для другого розведення додавали фермент (Sigma L1754) до концентрації 6 г/л в кінцевому розчині, що містить розведені сперматозоїди. Розчин-наповнювач для третього розведення містив 4 г/л карбонату кальцію, і в нього додавали трибутирин до концентрації 0,35 г на 100 мл. Приблизно через 3 години після другого 10 UA 113188 C2 5 10 15 20 розведення формували гель і заморожували пробірки, що містять іммобілізовані сперматозоїди. Пробірки для запліднення зберігали в рідкому N 2 протягом декількох днів до розморожування і оцінки рухливості. Приблизно 60 % сперматозоїдів були рухомі після розморожування і розрідження гелю. Приклад 2 Контрольоване виготовлення кальцій-альгінатного гелю з використанням ферменту ліпази і субстратів триацетину або триоктаноату Матеріали і методи Матеріали Альгінат натрію (PROTANAL LF 10/60) від FMC Biopolymer A/s (Драммен, Норвегія), ферменти L3001 і L1754 від Sigma (Сент-Луіс, США), триацетин і триоктаноат від Sigma (СентЛуіс, США), карбонат кальцію від KSL staubtechnik GMBH (Лауінген, Німеччина). Розчини Використовували наступні розчини. Розчин L1.1: 10 г/л розчин ферменту L3001 у дистильованій воді, розчин L1.2: 0,2 г/л триацетину у дистильованій воді. Розчин L2.1: 4 г/л карбонату кальцію, 24 г/л альгінату натрію LF10/60 і 0,1 г/л триацетину у дистильованій воді. Розчин L2.2: 4 г/л карбонату кальцію, 24 г/л альгінату натрію LF10/60 і 0,2 г/л триацетину у дистильованій воді. Розчин L2.3: 4 г/л карбонату кальцію, 24 г/л альгінату натрію LF10/60 і 0,3 г/л триацетину у дистильованій воді. Розчин L2.4: 4 г/л карбонату кальцію, 24 г/л альгінату натрію LF10/60 і 10 г/л ферменту L3001 у дистильованій воді. Розчин L2.5: 4 г/л карбонату кальцію, 24 г/л альгінату натрію LF10/60 і 0,3 г/л триоктаноату у дистильованій воді. Ініціація гелеутворення Гелеутворення ініціювали шляхом змішування одного з L1-розчинів з рівним об'ємом одного з L2-розчинів. Розчини змішували відповідно таблиці 1. Таблиця 1 Експериментальні дослідження гелеутворення з використанням ферменту L3001 і субстрату триацетину. У таблиці наведені комбінації досліджуваних розчинів, а також використовувані концентрації ферменту і субстрату триацетину. Дослідження 1 2 3 4 5 6 Розчини L1.1+L2.1 L1.1+L2.2 L1.1+L2.3 L1.2+L2.4 L1.2+L2.2 L1.3+L2.5 Концентрації 10 г/л ферменту L3001, 0,1 г/л триацетину 10 г/л ферменту L3001, 0,2 г/л триацетину 10 г/л ферменту L3001, 0,3 г/л триацетину 0,2 г/л триацетину, 10 г/л ферменту L3001 0,2 г/л триацетину, 0,2 г/л триацетину (без додавання ферменту) 10 г/л ферменту L1754, 0,4 г/л триоктаноату 25 30 35 Всі розчини перед змішуванням мали кімнатну температуру, і розчини залишали при кімнатній температурі на час гелеутворення. За тимчасовим ходом реакції гелеутворення стежили шляхом візуального огляду розчинів. Результати Ферменти L3001 (ліпаза із зародків пшениці) і L1754 (ліпаза з Candida rugosa) і субстрати триацетин і триоктаноат використовували для контрольованого гелеутворення натрійальгінатних розчинів. Розчини ферменту і субстрату готували і змішували відповідно таблиці 1. + Реакція між ферментом і субстратом давала H3O -іони, які реагували з суспендованим карбонатом кальцію в розчинах. Ця реакція вивільняла іони кальцію, які взаємодіяли з альгінатними полімерними ланцюгами в розчині, і формувався гель. Час до формування гелю в експериментальних випробуваннях наведений в таблиці 2. Гель не сформувався в експериментальному випробуванні 5, в якому фермент додано не було. Результати показують, що час реакції залежить і від вибраного типу субстрату, і від типу ферменту, а також від використовуваних концентрацій ферменту і субстрату. 40 11 UA 113188 C2 Таблиця 2 Спостережуваний час до гелеутворення, що відбувається після змішування розчинів, що містять ферменти (Sigma L3001 або L1754) та/або субстрат (триацетин або триоктаноат) Дослідження 1 2 3 4 5 6 Розчини L1.1+L2.1 L1.1+L2.2 L1.1+L2.3 L1.2+L2.4 L1.2+L2.2 L1.3+L2.5 Час до гелеутворення (г:х) 2:00 1:50 1:30 1:50 Гель не сформувався 0:30 ФОРМУЛА ВИНАХОДУ 5 1. Застосування ліпази і субстрату, здатного до гідролізу ліпазою, і агента, що вивільняє двовалентний катіон, для одержання альгінатного гідрогелю, де субстрат є сполукою формули І: OR2 OR3 R1O 10 15 20 25 , (І) де R1, R2 і R3 незалежно один від одного є однаковими або різними і позначають лінійний або розгалужений, заміщений або незаміщений С1-С12-алкілкарбонільний ланцюг, і де агент, що вивільняє двовалентний катіон, є карбонатом. 2. Застосування за п. 1, де ліпаза є тригліцеридліпазою. 3. Застосування за будь-яким з пп. 1-2, де гідроліз сполуки формули І ліпазою приводить до + утворення Н3О . 4. Застосування за будь-яким з пп. 1-3, де R1, R2 і R3 вибрані з групи, що складається з метанону, етанону, ацетону, бутанону, пентанону, гексанону, гептанону, октанону, нонанону, деканону, додеканону. 5. Застосування за будь-яким з пп. 1-4, де R1, R2 і R3 незалежно один від одного є однаковими або різними і позначають С1-С4-алкілкарбонільний ланцюг. 6. Застосування за будь-яким з пп. 1-5, де сполука формули І вибрана з групи, що складається з триацетину, трипропіоніну і трибутирину, переважно трипропіоніну і трубутирину. 7. Застосування за будь-яким з пп. 1-6, де ліпаза і сполука формули І використовуються для одержання альгінатного гідрогелю, в який впроваджений біологічний матеріал, переважно сперматозоїди. 8. Спосіб одержання альгінатного гідрогелю, що передбачає змішування розчину, який містить ліпазу, з розчином, який містить субстрат, здатний до гідролізу ліпазою, де розчин, який містить зазначену ліпазу, або розчин, який містить зазначений субстрат, також містить альгінат і сполуку, що вивільняє двовалентний катіон, де субстрат є сполукою формули І: OR2 R1O 30 35 40 OR3 , (І) де R1, R2 і R3 незалежно один від одного є однаковими або різними та позначають лінійний або розгалужений, заміщений або незаміщений С1-С12-алкілкарбонільний ланцюг, і де агент, що вивільняє двовалентний катіон, є карбонатом. 9. Спосіб за п. 8, де розчин, який містить ліпазу, включає карбонат, що вивільняє двовалентний катіон, і альгінат. 10. Спосіб за п. 8, де розчин, який містить сполуку формули І, включає карбонат, що вивільняє двовалентний катіон, і альгінат. 11. Спосіб за будь-яким з пп. 8-10, де R1, R2 і R3 вибрані з групи, що складається з метанону, етанону, ацетону, бутанону, пентанону, гексанону, гептанону, октанону, нонанону, деканону, додеканону. 12. Спосіб за будь-яким з пп. 8-10, де R1, R2 і R3 незалежно один від одного є однаковими або різними і позначають С1-С4-алкілкарбонільний ланцюг. 13. Спосіб за будь-яким з пп. 8-10, де сполука формули І вибрана з групи, що складається з триацетину, трипропіоніну і трибутирину, переважно трипропіоніну і трибутирину. 12 UA 113188 C2 5 10 15 14. Спосіб за будь-яким з пп. 8-13, де карбонат, що вивільняє двовалентний катіон, є карбонатом кальцію. 15. Спосіб за будь-яким з пп. 8-13, де розчин, який містить ліпазу або розчин, який містить сполуку формули І, також містить об'єкт для впровадження в альгінатний гідрогель. 16. Спосіб за п. 15, де об'єкт для впровадження в альгінатний гель є біологічним матеріалом, таким як сперматозоїди. 17. Альгінатний гідрогель, який містить: а) альгінат; б) об'єкт для впровадження в альгінатний гідрогель; і в) ліпазу, використовувану для одержання альгінатного гідрогелю. 18. Альгінатний гідрогель за п. 17, де об'єкт для впровадження в альгінатний гель є біологічним матеріалом, переважно сперматозоїдами. 19. Набір альгінатного гідрогелю, що включає один контейнер, який містить ліпазу, і другий контейнер, який містить субстрат, здатний до гідролізу ліпазою, де субстрат, здатний до гідролізу ліпазою, є сполукою формули І: OR2 R1O OR3 , (І) де R1, R2 і R3, незалежно один від одного, є однаковими або різними і позначають С 1-С12алкілкарбонільний ланцюг і де зазначений набір також включає альгінат і карбонат, що вивільняє двовалентний катіон. 20 Комп’ютерна верстка Л. Ціхановська Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 13
ДивитисяДодаткова інформація
Назва патенту англійськоюMethods for the preparation of hydrogels using lipase enzymes
Автори англійськоюKlinkenberg, Geir, Domaas Josefsen, Kjell, Kommisrud, Elisabeth
Автори російськоюКлинкенберг Гейр, Домаас Йосэфсэн Хьелль, Коммисруд Элизабэт
МПК / Мітки
МПК: C12P 19/04, C12N 5/076, C12N 9/20, A01N 1/02
Мітки: одержання, використанням, ферментів, спосіб, гідрогелю, ліпаз
Код посилання
<a href="https://ua.patents.su/15-113188-sposib-oderzhannya-gidrogelyu-z-vikoristannyam-fermentiv-lipaz.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання гідрогелю з використанням ферментів ліпаз</a>
Попередній патент: Інгібітори кінази
Наступний патент: Застосування 1н-індазол-3-карбоксамідних сполук як інгібіторів глікогенсинтаза-кінази 3-бета
Випадковий патент: Спосіб паркування автомобілів












