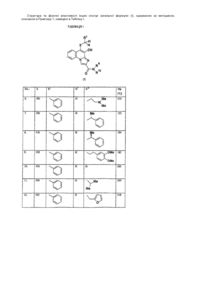
Похідні імідазохіноліну
Номер патенту: 78745
Опубліковано: 25.04.2007
Автори: Баторі Шандор, Тімарі Геза, Боер Кінга, Арані Петер, Урбан-Сабо Каталін, Капуі Зольтан, Балог Марія, Мікуш Ендре, Гербер Каталін, БАЛАЖ Ласло, Варгане Ссереді Юдіт, Т. Надь Лайош
Формула / Реферат
1. Сполуки загальної формули (І)
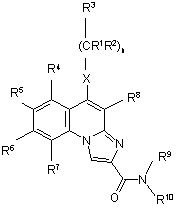 (I)
(I)
в якій
R1 означає атом водню або С1-4 алкільну групу з лінійним або розгалуженим ланцюгом;
R2 означає атом водню або С1-4 алкільну групу з лінійним або розгалуженим ланцюгом;
R3 означає атом водню або С1-4 алкільну групу з лінійним або розгалуженим ланцюгом, або С3-6 циклоалкільну групу, або фенільну групу, тієнільну групу або фурильну групу, що необов'язково заміщені однією або декількома С1-4 алкільними групами з лінійним або розгалуженим ланцюгом, С1-4 алкоксигрупами з лінійним або розгалуженим ланцюгом або атомами галогену, або означає 5- або 6-членне гетероароматичне кільце, що містить один, два або три атоми азоту, або 5-членне гетероароматичне кільце, що містить один атом азоту та один атом кисню або один атом азоту та один атом сірки, які необов'язково заміщені однією або декількома С1-4 алкільними групами з лінійним або розгалуженим ланцюгом, С1-4-алкоксигрупами з лінійним або розгалуженим ланцюгом або атомами галогену;
R4, R5, R6 і R7 означають, незалежно один від іншого, атом водню, С1-4 алкільну групу з лінійним або розгалуженим ланцюгом, С1-4 алкоксигрупу з лінійним або розгалуженим ланцюгом, гідроксильну групу або атом галогену; або R4 і R7 означають атом водню, a R5 і R6 разом утворюють метилендіоксигрупу;
R8 означає атом водню або ціаногрупу, амінокарбонільну групу, С1-4 алкоксикарбонільну групу або карбоксильну групу;
R9 і R10 означають, незалежно один від іншого, атом водню або С1-4 алкільну групу з лінійним або розгалуженим ланцюгом або С3-6 циклоалкільну групу, або фенільну групу, феніл(С1-4)алкільну групу, тієніл(С1-4)алкільну групу або фурил(С1-4)алкільну групу, що необов'язково заміщені метилендіоксигрупою або однією або декількома С1-4 алкільними групами з лінійним або розгалуженим ланцюгом, С1-4алкоксигрупами з лінійним або розгалуженим ланцюгом, гідроксильними групами, трифторметильними групами, ціаногрупами або атомами галогену, або означають 5- або 6-членне гетероароматичне кільце, що містить один, два або три атоми азоту, або 5-членне гетероароматичне кільце, що містить один атом азоту та один атом кисню або один атом азоту та один атом сірки, які необов'язково заміщені однією або декількома С1-4 алкільними групами з лінійним або розгалуженим ланцюгом, С1-4 алкоксигрупами з лінійним або розгалуженим ланцюгом або атомами галогену; або означають -(СН2)m-ОН або -(CH2)o-NR12R13-групу, або
R9 і R10 разом з атомом азоту утворюють 3-7-членну гетероциклічну групу, необов'язково заміщену С1-4 алкільною групою з лінійним або розгалуженим ланцюгом;
R12 і R13 означають, незалежно один від одного, атом водню або С1-4 алкільну групу з лінійним або розгалуженим ланцюгом, або С3-6 циклоалкільну групу, або фенільну групу, феніл(С1-4)алкільну групу, тієніл(С1-4)алкільну групу або фурил(С1-4)алкільну групу, що необов'язково заміщені метилендіоксигрупою або однією або декількома С1-4 алкільними групами з лінійним або розгалуженим ланцюгом, С1-4-алкоксигрупами з лінійним або розгалуженим ланцюгом, гідроксигрупами, трифторметильними групами, ціаногрупами або атомами галогену, або 5- або 6-членне гетероароматичне кільце, що містить, один, два або три атоми азоту, або 5-членне гетероароматичне кільце, що містить, один атом азоту та один атом кисню або один атом азоту та один атом сірки, де згадані кільця необов'язково заміщені однією або декількома С1-4 алкільними групами з лінійним або розгалуженим ланцюгом, С1-4 алкоксигрупами з лінійним або розгалуженим ланцюгом, або атомами галогену, або означають (СН2)m-ОН або -(CH2)o-NR12R13-групу, або
R12 і R13 разом з атом азоту утворюють 3-7-членну гетероциклічну групу, необов'язково заміщену лінійною або розгалуженою С1-4 алкільною групою;
Х означає -СН2-групу, -NН-групу, -NR11-групу або атом сірки або атом кисню, або сульфогрупу або сульфоксигрупу, де R11 означає лінійну або розгалужену С1-4-алкільну групу або С3-6 циклоалкільну групу;
n означає нуль, 1 або 2,
m означає 1, 2, 3 або 4, і
о означає нуль, 1, 2, 3 або 4;
та їх солі, сольвати, та їх оптично активні ізомери, солі та сольвати.
2. Сполуки загальної формули (І) за п. 1, в якій
R1 означає атом водню або лінійну або розгалужену С1-4 алкільну групу;
R2 означає атом водню або лінійну або розгалужену С1-4 алкільну групу;
R3 атом водню або лінійну або розгалужену С1-4 алкільну групу або С3-6 циклоалкільну групу, або фенільну групу, тієнільну групу або фурильну групу, що необов'язково заміщені однією або декількома С1-4 алкільними групами з лінійним або розгалуженим ланцюгом, С1-4 алкоксигрупами з лінійним або розгалуженим ланцюгом або атомами галогену, або означає 5- або 6-членне гетероароматичне кільце, що містить один, два або три атоми азоту, або 5-членне гетероароматичне кільце, що містить один атом азоту та один атом кисню або один атом азоту та один атом сірки, які необов'язково заміщені однією або декількома С1-4 алкільними групами з лінійним або розгалуженим ланцюгом, С1-4 алкоксигрупами з лінійним або розгалуженим ланцюгом або атомами галогену;
R4, R5, R6 і R7 означають, незалежно один від іншого, атом водню, С-1-4 алкільну групу з лінійним або розгалуженим ланцюгом, С1-4 алкоксигрупу з лінійним або розгалуженим ланцюгом, гідроксильну групу або атом галогену; або R4 і R7 означають атом водню, а R5 і R6 разом утворюють метилендіоксигрупу;
R8 означає атом водню або ціаногрупу, амінокарбонільну групу, С1-4 алкоксикарбонільну групу або карбоксильну групу;
R9 і R10 означають, незалежно один від одного, атом водню або С1-4 алкільну групу з лінійним або розгалуженим ланцюгом або С3-6 циклоалкільну групу, або фенільну групу, феніл(С1-4)алкільну групу, тієніл(С1-4)алкільну групу або фурил(С1-4)алкільну групу, що необов'язково заміщені метилендіоксигрупою або однією або декількома С1-4 алкільними групами з лінійним або розгалуженим ланцюгом, С1-4 алкоксигрупами з лінійним або розгалуженим ланцюгом, гідроксильними групами, трифторметильними групами, ціаногрупами або атомами галогену, або означають -(СН2)m-ОН або -(CH2)o-NR12R13-групу, або
R9 i R10 разом з атомом азоту утворюють 3-7-членну гетероциклічну групу, необов'язково заміщену С1-4 алкільною групою з лінійним або розгалуженим ланцюгом;
R12 і R13 означають, незалежно один від одного, атом водню або С1-4 алкільну групу з лінійним або розгалуженим ланцюгом, або С3-6 циклоалкільну групу, або фенільну групу, феніл(С1-4)алкільну групу, тієніл(С1-4)алкільну групу або фурил(С1-4)алкільну групу, що необов'язково заміщені метилендіоксигрупою або однією або декількома С1-4 алкільними групами з лінійним або розгалуженим ланцюгом, С1-4-алкоксигрупами з лінійним або розгалуженим ланцюгом, гідроксигрупами, трифторметильними групами, ціаногрупами або атомами галогену, або означають -(СН2)m-ОН або -(CH2)o-NR12R13-групу, або
R12 і R13 разом з атом азоту утворюють 3-7-членну гетероциклічну групу, необов'язково заміщену лінійною або розгалуженою С1-4 алкільною групою;
Х означає -СН2-групу, -NН-групу, -NR11-групу або атом сірки або атом кисню, або сульфогрупу або сульфоксигрупу, де R11 означає лінійну або розгалужену С1-4-алкільну групу або С3-6 циклоалкільну групу;
n означає нуль, 1 або 2;
m означає 1, 2, 3 або 4, і
о означає нуль, 1, 2, 3 або 4;
та їх солі, сольвати, та їх оптично активні ізомери, солі та сольвати.
3. Сполуки загальної формули (І) за п. 1 або 2, в якій
R1 означає атом водню або метильну групу;
R2 означає атом водню або метильну групу,
R3 означає фенільну або тієнільну, або фурильну групу;
R4, R5, R6 та R7 означають незалежно атом водню або С1-4 алкільну групу з лінійним або розгалуженим ланцюгом, С1-4 алкоксигрупу з лінійним або розгалуженим ланцюгом або гідроксильну групу або атом галогену, або
R4 і R7 означають атом водню, а R5 і R6 разом утворюють метилендіоксигрупу;
R8 означає атом водню або ціаногрупу;
R9 і R10 означають метильну групу, етильну групу або циклопропільну групу, або R9 i R10 разом з атомом азоту утворюють 3-7-членну гетероциклічну групу, необов'язково заміщену лінійну або розгалужену С1-4 алкільну групу,
Х означає -NH-групу або атом кисню, і
n означає 1;
та їх солі, сольвати, та їх оптично активні ізомери, солі та сольвати.
4. Сполуки за будь-яким з пп. 1-3, що наведені нижче:
1-(9-бензиламіно-10-ціаноімідазо[1,2-а]хінолін-2-карбоніл)піролідин;
N,N-диметил-9-бензиламіно-10-ціаноімідазо[1,2-а]хінолін-2-карбоксаміду гемігідрат;
N-етил-9-бензиламіно-10-ціаноімідазо[1,2-а]хінолін-2-карбоксаміду гемігідрат;
1-(9-фурфуриламіно-10-ціаноімідазо[1,2-а]хінолін-2-карбоніл)піролідину гемігідрат;
1-(9-тієніламіно-10-ціаноімідазо[1,2-а]хінолін-2-карбоніл)піролідину гемігідрат;
та їх солі, сольвати, оптично активні ізомери та їх солі і сольвати.
5. Спосіб одержання сполуки загальної формули (І), її солей сольватів, оптично активних ізомерів та їх солей і сольватів, де в формулі R1, R2, R3, R4, R5, R6, R7, R8, X, n, m і о мають такі ж самі значення, які зазначені в п. 1, який полягає в ацилюванні сполуки загальної формули (VIII),
![]() (VIII)
(VIII)
в якій R9 і R10 мають такі ж самі значення, які зазначені в п. 1, кислотою загальної формули (II),
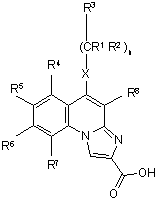 (II)
(II)
в якій R1, R2, R3, R4, R5, R6, R7, R8, Х і n мають такі ж самі значення, які зазначені в п. 1, або її реакційноздатним похідним та, при необхідності, перетворенні замісників сполуки загальної формули (І), одержаної таким чином, одного в інший відомими способами та/або перетворенні сполуки загальної формули (І), одержаної таким чином, в її солі або сольвати, або вивільненні її із її солей або сольватів та/або розділенні її на її оптично активні ізомерні форми або перетворенні оптично активних форм в рацемічну форму.
6. Спосіб за п. 5, який відрізняється тим, що ацилювання проводять в органічному розчиннику в присутності основи.
7. Спосіб за будь-яким з пп. 5-6, який відрізняється тим, що як реакційноздатне похідне кислоти використовують галоїдангідрид або ангідрид.
8. Спосіб за будь-яким з пп. 5-6, який відрізняється тим, що як органічний розчинник використовують галогеновані вуглеводні, переважно хлороформ.
9. Спосіб за будь-яким з пп. 5-8, який відрізняється тим, що як основу використовують органічну основу, переважно триетиламін.
10. Фармацевтична композиція, яка містить як активний інгредієнт одну або декілька сполук загальної формули (І), в якій R1, R2, R3, R4, R5, R6, R7, R8, Х і n мають такі ж самі значення, які зазначені в п. 1, або їх солі, сольвати або оптично активні ізомери та їх солі і сольвати, в суміші з одним або декількома екципієнтами, використовуваними в фармацевтичній промисловості.
11. Фармацевтична композиція за п. 10, яка містить як активний інгредієнт одну або декілька сполук за п. 3.
12. Фармацевтична композиція за п. 10, яка містить як активний інгредієнт одну або декілька сполук за п. 4.
13. Застосування сполук загальної формули (І), в якій R1, R2, R3, R4, R5, R6, R7, R8, Х і n мають такі ж самі значення, які зазначені в п. 1, для лікування захворювань, в перебігу яких відіграють роль А3 рецептори.
14. Застосування сполук загальної формули (І), в якій R1, R2, R3, R4, R5, R6, R7, R8, Х і n мають такі ж самі значення, які зазначені в п. 1, за п. 13 як А3 лігандів у випадку захворювань серця, нирок, органів дихання та центральної нервової системи, для інгібування захисту аденозину в ракових клітинах, які ростуть, запобігання дегрануляції тучних клітин, інгібування утворення цитокінів, зменшення інтраокулярного тиску, інгібування вивільнення ![]() , інгібування міграції еозинофілів, нейтрофілів та інших клітин імунної системи, інгібування бронхоспазму та екстравазації плазми.
, інгібування міграції еозинофілів, нейтрофілів та інших клітин імунної системи, інгібування бронхоспазму та екстравазації плазми.
15. Застосування сполук загальної формули (І), в якій R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, X і n мають такі ж самі значення, які зазначені в п. 1, за п. 13 або 14 як антагоністів А3 рецепторів у антизапальних, антиастматичних, антиішемічних, антидепресантних, антиаритмічних, ниркозахисних, антипухлинних, антипаркінсонічних та покращуючих когнітивні властивості фармацевтичних композиціях та як активного інгредієнта в композиціях для лікування або профілактики міокардіальної реперфузії, хронічних обструктивних захворювань легень (COPD) та респіраторного дистрес-синдрому дорослих (ARDS), включаючи хронічні бронхіти, легеневу емфізему або задишку, алергійних реакцій (наприклад, ринітів, реакцій, викликаних отруєнням плющем, кропивниці, склеродермії, артриту), інших аутоімунних захворювань, запальних захворювань кишечнику, хвороби Едісона, хвороби Крона, псоріазу, ревматизму, гіпертензії, розладів неврологічної функції, глаукоми та діабетів.
16. Застосування сполук загальної формули (І), в якій R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, Х і n мають такі ж самі значення, які зазначені в п. 1, за будь-яким з пп. 13, 14 та 15 як антагоністів А3 рецепторів для лікування астми, COPD і ARDS, глаукоми, пухлин, алергійних та запальних захворювань, ішемії, гіпоксії, аритмії та хвороб нирок та як активного інгредієнта.
17. Сполуки загальної формули (II),
 (II)
(II)
в якій R1, R2, R3, R4, R5, R6, R7, R8, Х та n мають такі ж самі значення, які зазначені в п. 1, за умови, що якщо -X-(CR1R2)n-R3 разом утворює алкокси або алкілтіо, алкілсульфо або алкілсульфоксигрупу, R8 є іншим ніж водень.
18. Сполуки загальної формули (III),
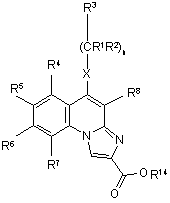 (III)
(III)
в якій R1, R2, R3, R4, R5, R6, R7, R8, Х та n мають такі ж самі значення, які зазначені в п. 1, а R14 означає С1-4 алкільну групу, за умови, що якщо -X-(CR1R2)n-R3 разом утворює алкокси або алкілтіогрупу, R8 є іншим ніж водень.
Текст
Цей винахід стосується лігандів аденозинових А3 рецепторів загальної формули (І), переважно антагоністів, а також їх солей, сольватів та ізомерів, і фармацевтичних композицій, що їх містять; використання сполук загальної формули (І), а також їх солей, сольватів та ізомерів; та одержання сполук загальної формули (І), а також їх солей, сольватів та ізомерів; крім того, нових проміжних сполук загальних формул (II) та (III) та їх одержання. Аденозин є добре відомим компонентом декількох ендогенних молекул (ATP, N AD+, нуклеїнові кислоти). Крім того, він грає важливу регуляторну дію в багатьох фізіологічних процесах. Вплив аденозину на серцеву діяльність був описаний ще в 1929 [Drury та Szentgyorgyi, J Physiol 68: 213,1929]. Визначення збільшуваної кількості фізіологічних функцій, опосередкованих аденозином, та відкриття нових підтипів аденозинових рецепторів надає можливість терапевтичного застосування специфічних лігандів [Poulse, S. А. та Quinn, R. J. Bioorganic and Medicinal Chemistry 6: 619, 1998]. На сьогоднішній день рецептори аденозину підрозділяються на три головні класи: А1 , А2 та А3. Підтип А1 є частково відповідальним за інгібування аденилатциклази шляхом приєднання до G1-мембранного протеїну, деякою мірою впливає на інші системи передачі вторинної інформації. Рецептори А2 підтипу можуть підрозділятися на два додаткових підтипи - А2а та А2b, які стимулюють активність аденилатциклази. Нещодавно було ідентифіковано послідовність аденозинових А3 рецепторів з бібліотеки cDNA яєчок щурів. Пізніше було доведено, що вона відповідає новому функціональному аденозиновому рецептору. Активація А3 рецепторів пов'язана також з декількома системами передачі вторинної інформації: наприклад, інгібуванням аденилатциклази та стимулюванням фосфоліпази С і D. Було виявлено, що аденозинові рецептори знаходяться в певних органах та регулюють їх функції. Як А1 , так і А2а рецептори грають важливу роль в центральній нервовій системі та серцево-судинній системі. В ЦНС аденозин інгібує вивільнення синаптичних трансміттерів, чий вплив опосередковується А1 рецепторами. В серці також А1 рецептори опосередковують негативні інотропний, хронотропний та дромотропний ефекти аденозину. Аденозинові А2а рецептори, розташовані у відносно великій кількості в смугастому тілі, виявляють функціональну взаємодію з рецепторами допаміну в регулюванні синаптичної передачі сигналу. Аденозинові А2а рецептори ендотеліальних клітин та клітин гладкої мускулатури є відповідальними за аденозин-індуковану вазоділатацію. На основі ідентифікації мРНК аденозинові А2b рецептори широко розподіляються в різних тканинах. їх можна ідентифікувати майже в кожному типі клітин, але їх експресія є найбільшою в кишечнику та сечовому міхурі. Цей підтип, можливо, має також важливу регуляторну функцію в регуляції судинного тонусу та відіграє роль у функціонуванні тучних клітин. Всупереч Α1 та А2а рецепторам, розподілення яких в тканинах визначалось за рівнем білка, присутність А2b та А3 рецепторів визначалась на основі їх мДНК рівня. Рівні експресії аденозинових А3 рецепторів є скоріше низькими у порівнянні з іншими підтипами і сильно залежать від виду. Аденозинові А3 рецептори експресуються, головним чином, у центральній нервовій системі, яєчках, імунній системі і вважається, що вони повинні включатися в модуляцію вивільнення медіатора з тучних клітин в безпосередній реакції гіперчуттєвості. Опубліковані на даний час А3 антагоністи належать до груп флавоноїдів, похідних 1,4-дигідропіридину, триазолохіназолінів, тіазолонафтиридинів та тіазолопіримідинів. Даний винахід стосується нового типу ефективних А3 антагоністів, які мають структур у імідазохіноліну. Для терапевтичного використання є важливим забезпечення того, щоб молекула не зв'язувалась або зв'язувалась лише у випадках дуже високих концентрацій з Α1, А2а та А2b підтипами рецепторів аденозину. Даний винахід стосується сполук загальної формули (І), а також їх солей, сольватів та ізомерів, які мають значну селективність до А3 рецепторів аденозину. Нашою задачею було отримати А3 ліганди, перш за все, з імідазохіноліновою структурою і серед них, переважно, антагоністи, які мають сильну антагоністичну дію та проявляють високу селектвність до А3 рецепторів, тобто, вони інгібують А3 рецептори в значно нижчій концентрації, ніж вони інгібують Α1, А2а та А2b рецептори. Подальшими цілями було отримати дані по стабільності, біодоступності, терапевтичному індексу та токсичності, які роблять можливим перетворення нових сполук в лікарські речовини та, завдяки їх сприятливому ентеральному поглинанню, сполуки можуть застосовуватися орально. Нами було виявлено, що сполуки загальної формули (І) в якій R1 означає атом водню або С1-4 алкільну гр упу з лінійним або розгалуженим ланцюгом; R2 означає атом водню або С1-4 алкільну гр упу з лінійним або розгалуженим ланцюгом; R3 означає атом водню або С 1-4 алкільну групу з лінійним або розгалуженим ланцюгом, або С3-6 циклоалкільну груп у, або фенільну групу, тієнільну групу або фурильну гр упу, що необов'язково заміщені однією або декількома С1-4 алкільними групами з лінійним або розгалуженим ланцюгом , С1-4 алкоксигрупами з лінійним або розгалуженим ланцюгом або атомами галогену, або означає 5- або 6-членне гетероароматичне кільце, що містить один, два або три атоми азоту, або 5-членне гетероароматичне кільце, що містить один атом азоту та один атом кисню або один атом азоту та один атом сірки, які необов'язково заміщені однією або декількома С 1-4 алкільними групами з лінійним або розгалуженим ланцюгом, С1-4-алкоксигрупами з лінійним або розгалуженим ланцюгом або атомами галогену; R4, R5, R6 і R7 означають, незалежно один від іншого, атом водню, С1-4 алкільну груп у з лінійним або розгалуженим ланцюгом, С1-4 алкоксигрупу з лінійним або розгалуженим ланцюгом, гідроксильну груп у або атом галогену; або R4 і R7 означають атом водню, a R5 і R6 разом утворюють метилендіоксигрупу; R8 означає атом водню або ціаногрупу, амінокарбонільну груп у, С1-4 алкокси-карбонільну гр упу або карбоксильну груп у; R9 і R10 означають, незалежно один від іншого, атом водню або С 1-4 алкільну груп у з лінійним або розгалуженим ланцюгом або С 3-6 циклоалкільну гр упу, або фенільну гр упу, феніл(С 1-4)алкільну груп у, тіоніл(С 1-4)алкільну груп у або фурил(С 1-4)алкільну гр упу, що необов'язково заміщені метилендіоксигрупою або однією або декількома С 1-4 алкільними групами з лінійним або розгалуженим ланцюгом, С1-4 алкоксигрупами з лінійним або розгалуженим ланцюгом, гідроксильними групами, трифторметильними групами, ціаногрупами або атомами галогену, або означають 5- або 6-членне гетероароматичне кільце, що містить один, два або три атоми азоту, або 5-членне гетероароматичне кільце, що містить один атом азоту та один атом кисню або один атом азоту та один атом сірки, які необов'язково заміщені однією або декількома С1-4 алкільними групами з лінійним або розгалуженим ланцюгом, С1-4 алкоксигрупами з лінійним або розгалуженим ланцюгом або атомами галогену; або означають-(СН2)m-ОН або -(CH2)o-NR12R13 груп у, або R9 i R 10 разом з атомом азоту утворюють 3-7-членну гетероциклічну групу, необов'язково заміщену С 1-4 алкільною групою з лінійним або розгалуженим ланцюгом; R12 і R13 означають, незалежно один від іншого, атом водню або С 1-4 алкільну групу з лінійним або розгалуженим ланцюгом, або С3-6 циклоалкільну груп у, або фенільну груп у, феніл(С 1-4)алкільну груп у, тієніл(С 1-4)алкільну груп у або фурил(С 1-4)алкільну групу, що необов'язково заміщені метилендіоксигрупою, або однією або декількома С1-4 алкільними групами з лінійним або розгалуженим ланцюгом, С1-4-алкоксигрупами з лінійним або розгалуженим ланцюгом, гідроксигрупами, трифторметильними групами, ціаногрупами або атомами галогену, або 5 або 6-членне гетероароматичне кільце, що містить, один, два або три атоми азоту, або 5-членне гетероароматичне кільце, що містить, один атом азоту та один атом кисню або один атом азоту та один атом сірки, де згадані кільця необов'язково заміщені однією або декількома С1-4 алкільними групами з лінійним або розгалуженим ланцюгом, С1-4 алкоксигрупами з лінійним або розгалуженим ланцюгом, або атомами галогену, або означають(СН 2)m-ОН або -(CH2)o-NR12R13 груп у, або R12 і R13 разом з атом азоту утворюють 3-7 членну гетероциклічну групу, необов'язково заміщену лінійною або розгалуженою С1-4 алкільною групою X означає -СН2-групу, -NH-групу, -NR11-rp yny, або атом сірки або атом кисню, або сульфогрупу або сульфоксигрупу, де R11 означає лінійну або розгалужену С1-4-алкільну гр упу або С 3-6 циклоалкільну груп у; n означає нуль, 1 або 2, m означає 1, 2, 3 або 4, і о означає нуль, 1, 2, 3 або 4 та їх солі, сольвати, та їх оптично активні ізомери, солі та сольвати, що задовольняють вищенаведеним критеріям. Конкретними значеннями перерахованих вище замісників є наступні: Під лінійною або розгалуженою С 1-4 алкільною групою ми розуміємо метильну, етильну, пропільну, ізопропільну, бутильну, ізобутильну, втор-бутильну, трет-бутильну, переважно етильну або метильну гр упу. Під лінійною або розгалуженою С 1-4 алкоксигрупою ми розуміємо метокси-, етокси-, пропокси-, ізопропокси-, бутокси-, ізобутокси-, втор-бутокси-, трет-бутокси-, переважно етокси- або метоксигрупу. Під С3-6 циклоалкільною групою ми розуміємо циклопропільну, циклобутильну, циклопентильну або циклогексильну гр упу. Під 3-7-членним гетероциклічним кільцем ми розуміємо диметиленімінову (азиридинову), триметиленімінову, тетраметиленімінову (піролідинову), пентаметиленімінову (піперидинову) або гексаметиленімінову гр упа. Гетероароматичне кільце, що містить один, два або три атоми азоту, означає пірольне, імідазольне, піразольне, 1,2,3-триазольне, 1,2,4-триазольне, піридинове, піримідинове, піридазинове, піразинове та 1,3,4-триазинове кільце. Кільце необов'язково заміщене С 1-4-алкільною або алкоксигрупою або атомом галоген. Гетероароматичне кільце, що містить один атом азоту та один атом кисню або атом сірки, означає оксазольне, ізоксазольне, тіазольне, ізотіазольне кільце. Кільце необов'язково заміщене С1-4-алкільною або алкоксигрупою або атомом галоген. Солі сполук загальної формули (І) означають солі, отримані з неорганічними та органічними кислотами та основами. Перевага надається солям, отриманим з фармацевтично прийнятними кислотами, наприклад, хлороводневою кислотою, сірчаною кислотою, етансульфоновою кислотою, винною кислотою, бурштиновою кислотою, фумаровою кислотою, яблочною кислотою, лимонною кислотою, та основами, такими як, наприклад, гідроксид натрію, гідроксид калію, етаноламін. Під сольватами розуміють сольвати, одержані з різними розчинниками, такими як, наприклад, вода або етанол. Сполуки загальної формули (І) проявляють геометричну та оптичну ізомерію, тому винахід також стосується сумішей геометричних ізомерів, рацемічних або оптично активних геометричних ізомерів, а також їх солей та сольватів. Переважною групою сполук загальної формули (І) є гр упа, утворена сполуками, в яких R1 означає атом водню або лінійну або розгалужену С1-4 алкільну гр упу; R2 означає атом водню або лінійну або розгалужену С1-4 алкільну гр упу; R3 атом водню або лінійну або розгалужену С 1-4 алкільну гр упу, або С3-6 циклоалкільну груп у або фенільну групу, тієнільну групу, або фурильну групу, що необов'язково заміщені однією або декількома С 1-4 алкільними з лінійним або розгалуженим ланцюгом, С1-4 алкоксигрупами з лінійним або розгалуженим ланцюгом або атомами галогену, або означає 5- або 6-членне гетероароматичне кільце, що містить один, два або три атоми азоту, або 5-членне гетероароматичне кільце, що містить один атом азоту та один атом кисню або один атом азоту та один атом сірки, які необов'язково заміщені однією або декількома С 1-4 алкільними групами з лінійним або розгалуженим ланцюгом, С1-4 алкоксигрупами з лінійним або розгалуженим ланцюгом або атомами галогену; R4, R5, R6 і R7 означають, незалежно один від іншого, атом водню, С1-4 алкільну груп у з лінійним або розгалуженим ланцюгом, С1-4 алкоксигрупу з лінійним або розгалуженим ланцюгом, гідроксильну груп у або атом галогену; або R4 і R7 означають атом водню, a R5 і R6 разом утворюють метилендіоксигрупу; R8 означає атом водню або ціаногрупу, амінокарбонільну груп у, С1-4 алкокси-карбонільну гр упу або карбоксильну груп у; R9 і R10 означають, незалежно один від іншого, атом водню або С 1-4 алкільну груп у з лінійним або розгалуженим ланцюгом або С 3-6 циклоалкільну гр упу, або фенільну гр упу, феніл(С 1-4)алкільну груп у, тієніл(С 1-4)алкільну гр упу або фурил(С 1-4)алкільну груп у, що необов'язково заміщені метилендіоксигрупою або однією або декількома С 1-4 алкільними групами з лінійним або розгалуженим ланцюгом, С1-4алкоксигрупами з лінійним або розгалуженим ланцюгом, гідроксильними групами, трифторметильними групами, ціаногрупами або атомами галогену, або означають -(СН2)m-ОН або -(CH2)o-NR12R13 гр упу, або R9 і R10 разом з атомом азоту утворюють 3-7-членну гетероциклічну групу, необов'язково заміщену С 1-4 алкільною групою з лінійним або розгалуженим ланцюгом; R12 і R13 означають, незалежно один від іншого, атом водню або С 1-4 алкільну групу з лінійним або розгалуженим ланцюгом, або С3-6 циклоалкільну груп у, або фенільну груп у, феніл(С 1-4)алкільну груп у, тієнил(С 1-4)алкільну гр упу або фурил(С 1-4)алкільну гр упу, що необов'язково заміщені метилендіоксигрупою, або однією або декількома С1-4 алкільними групами з лінійним або розгалуженим ланцюгом, С1-4-алкоксигрупами з лінійним або розгалуженим ланцюгом, гідроксигрупами, трифторметильними групами, ціаногрупами або атомами галогену, або означають -(СН2)m-ОН або -(CH2)o-NR12R13 гр упу, або R12 і R13 разом з атом азоту утворюють 3-7 членну гетероциклічну групу, необов'язково заміщену лінійною або розгалуженою С1-4 алкільною групою X означає -СН2-групу, -NH-гр упу, -NR11-гр упу, або атом сірки або атом кисню або сульфогрупу або сульфоксигрупу, де R11 означає лінійну або розгалужену С1-4-алкільну гр упу або С 3-6 циклоалкільну груп у; n означає нуль, 1 або 2; m означає 1, 2, 3 або 4, і о означає нуль, 1, 2, 3 або 4 та їх солі, сольвати, та їх оптично активні ізомери, солі та сольвати. Переважною групою сполук загальної формули (І) є гр упа, утворена сполуками, в яких R1 означає атом водню або метильну гр упу; R2 означає атом водню або метильну гр упу, R3 означає фенільну або тієнільну або фурильну гр упу; R4, R5, R6 та R7 означають незалежно атом водню або С 1-4 алкільну групу з лінійним або розгалуженим ланцюгом, С1-4 алкоксигрупу з лінійним або розгалуженим ланцюгом або гідроксильну групу або атом галогену, або R4 і R7 означають атом водню, a R5 і R6 разом утворюють метилендіоксигрупу; R8 означає атом водню або ціаногрупу; R9 і R10 означають метильну груп у, етильну груп у або циклопропільну групу або R9 i R 10 разом з атомом азоту утворюють 3-7-членну гетероциклічну групу, необов'язково заміщену лінійну або розгалужену С 1-4 алкільну гр упу, X означає -NH-групу або атом кисню і n означає 1 та їх солі, сольвати, та їх оптично активні ізомери, солі та сольвати. Особлива перевага надається наступним сполукам, що відповідають вищезазначеним критеріям: 1 -(9-бензиламіно-10-ціаноімідазо[1,2-а]хінолін-2-карбоніл)піролідин; N,N-диметил-9-бензиламіно-10-ціаноімідазо[1,2-а]хінолін-2-карбоксаміду гемігідрат; N-етил-9-бензиламіно-10-ціаноімідазо[1,2-а]хінолін-2-карбоксаміду гемігідрат; 1-(9-фур фуриламіно-10-ціаноімідазо[1,2-а]хінолін-2-карбоніл)піролідину гемігідрат; 1-(9-тієніламіно-10-ціаноімідазо[1,2-а]хінолін-2-карбоніл)піролідину гемігідрат; та їх солі, сольвати, та їх оптично активні ізомери, солі та сольвати. Згідно з іншими аспектами даний винахід також стосується фармацевтичних композицій, що містять як активні компоненти сполуки загальної формули (І) або їх ізомери солі та сольвати, які є переважно оральними композиціями, але інгаляторні, парентеральні та трансдермальні композиції є також об'єктами винаходу. Зазначені вище фармацевтичні композиції можуть бути твердими або рідкими, такими як таблетки, пілюлі, капсули, пластирі, розчини, суспензії або емульсії. Серед фармацевтичних форм перевага надається твердим композиціям, перш за все, таблеткам та капсулам. Зазначені вище фармацевтичні композиції готують з використанням звичайних фармацевтичних екціпієнтів і стандартних методик. Сполуки загальної формули (І) можуть використовуватися для лікування патологій, в перебігу яких відіграють роль А3 рецептори. Сполуки даного винаходу, що мають селективну активність по відношенню до А3 рецепторів, можуть використовува тися в терапевтичному та/або профілактичному лікування порушення діяльності серця, нирок, дихальної системи, центральної нервової системи. Вони інгібують захисний вплив аденозину в пухлинних клітинах, які ростуть, попереджують дегрануляцію тучних клітин, інгібують утворення цитокінів, зменшують інтраокулярний тиск, інгібують вивільнення TNF-a, інгібують міграцію еозинофілів, нейтрофілів та інших імунних клітин, інгібують бронхоспазми та екстравазацію плазми. Засновуючись на цих ефектах, антагоністи аденозинових А3 рецепторів даного винаходу можуть бути терапевтично придатними як антизапальні, антиастматичні, антиішемічні, антидепресантні, антиаритмічні, ниркозахисні, антипухлинні, антипаркінсонічні та покращуючі когнітивні властивості лікарські засоби. Вони також можуть використовуватися в лікуванні або профілактиці порушень міокардіапьної реперфузії, хронічних обструктивних захворювань легень (COPD) та респіраторного дистрес-синдрому дорослих (ARDS), включаючи хронічні бронхіти, легеневу емфізему або задишку, алергійних реакцій (наприклад, ринітів, реакцій, викликаних отруєнням плющем, кропивниці, склеродермії, артриту), інших аутоімунних захворювань, запальних захворювань кишечника, хвороби Едісона, хвороби Крона, псоріазу, ревматизму, гіпертензії, розладів неврологічної функції, глаукоми та діабетів [К. N. Klotz, Naunyn-Schmiedberg's Arch. Pharmacol. 362: 382,2000; P. Г. Baraldi та Р. A. Borea, TiPS 21: 456,2000]. Сполуки даного винаходу можуть переважно використовуватися для лікування захворювань, таких як астма, COPD та ARDS, гла укома, новоутворення, алергійні та запальні захворювання, ішемія, гіпоксія, аритмія та захворювання нирок. Згідно з іншими аспектами даний винахід стосується застосування сполук загальної формули (І) для лікування вищезгаданих патологій. Приблизна денна доза складає 0,1-1000мг активного інгредієнта в залежності від виду захворювання і серйозності стану та статі, ваги пацієнта і т.д. Подальшим об'єктом винаходу є одержання сполук загальної формули (І) та проміжних сполук загальних формул (II) і (III). Проміжні сполуки загальних формул (II) і (III), які використовуються в способі одержання згідно з винаходом, є частково новими. Замісники в загальних формулах (II), (II), (IV) і (V) мають значення, наведені вище. В способі згідно з винаходом сполуку формули (VIII) ацилюють кислотою загальної формули (II) або її реакційно здатним похідним згідно з реакціями ацилювання, відомими в органічній хімії. Як ацилювальні агенти використовують галогенангідриди або змішані ангідриди, і сполуку загальної формули (І), одержану таким чином, при необхідності: перетворюють в її солі, сольвати або виділяють із її солей, сольватів і розділяють на її геометричні або оптичні ізомери. Замісники сполук загальної формули (І) можуть бути перетворені один в інший за відомими методиками. Одержання змішаних ангідридів, використовуваних в реакції ацилювання проводять з півалоїлхлоридом, переважно в присутності органічної основи, переважно триетиламіну в хлороформі, хоча можуть використовуватися також й інші способи, відомі з органічної хімії. Ацилювання може здійснюватися в широкому температурному інтервалі, переважно в межах 0°С-100°С. Сполуки загальної формули (II), в яких значення R 1, R2, R3, R4, R5, R6, R7, R8, X та n є такими, як визначено вище, можуть бути отримані декількома відомими способами, в тому числі способом, що демонструється на Схемі 1, шляхом селективного гідролізу сполук формули (ІІІІ) з використанням процесу селективного гідролізу, відомого в органічній хімії. Як агенти гідролізу переважно можуть застосовуватися гідроксиди лужних металів, але можуть також використовуватися й інші речовини, що сприяють гідролізу. Сполуки загальної формули (III), в яких значення R1, R2, R3, R4, R5, R6, R7, R8, X та n є такими, як визначено вище, a R14 означає С 1-4 алкільну групу, можуть бути одержані із сполуки формули (IV), використовуючи способи, відомі як такі [І. R. Ager та R. Westwood, J. Med. Chem. 31,1098, (1988)]. Сполуки загальної формули (IV), в яких значення R1, R2, R3, R4, R5, R6, R7, R8, X та n є такими, як визначено вище, можуть бути одержані із сполуки формули (V), використовуючи способи, відомі як такі [Nan Zhang, Bioorg. and Med. Chem. Lett., 10,2825, (2000)]. Сполуки загальної формули (V), в яких значення R4, R5, R6, R7 та R8 є такими, як визначено вище, можуть бути одержані із сполуки формули (VI), використовуючи способи, відомі як такі [D. L. Leysen, J. Heterocyclic Chem., 24, 1611, (1987)]. Сполуки загальної формули (VI), в яких значення R4, R5, R6 , R7 та R8 є такими, як визначено вище, можуть бути одержані з використанням способів, відомих як такі [Pfizer (Inc), патент США 4175193]. Сполуки винаходу загальних формул (І), (II), (III), (IV) та (V), їх одержання та біологічна активність демонструються в наступних прикладах, без обмеження об'єму формули винаходу цими прикладами. Фіг.1 зображує сполуки формули (І), Фіг.2 зображує сполуки формули (II), Фіг.3 зображує сполуки формули (III), Фіг.4 зображує сполуки формули (IV), Фіг.5 зображує сполуки формули (V), Фіг.6 зображує сполуки формули (VI), Фіг.7 зображує сполуки формули (VII), Фіг.8 зображує сполуки формули (VIII). Приклади Приклад 1 1-(9-Бензиламіно-10-ціано-імідазо[1,2-a]хінолін-2-карбоніл)піролідин В загальній формулі (І) R1 та R2 означають атом водню, R3 означає фенільну груп у, R4, R 5, R6 та R7 означають атом водню, R9 и R10 утворюють разом 1,3-бутандіільну гр упу, R8 означає ціаногрупу, X означає NH групу, n дорівнює 1. а.) 2-Аміно-3-ціано-4-хлорхінолін: Суміш 10г 2-аміно-3-ціано-4-гідроксихіноліну та 15мл фосфорилхлориду нагрівають при перемішуванні при 110°С. Реакційну суміш охолоджують, виливають в 100мл льодяної води і нейтралізують 60мл 10% розчину гідроксиду натрію. Одержаний жовтий осад відфільтровують, промивають 50мл води. Після висушування одержують 7,5г вказаної в заголовку сполуки. Т.пл.: 210°С. ЯМР, dΗ (400МГц, D MSO-d6): 7,21млн.ч., (с, 2Н, NH2), 7,35-7,40млн.ч., (дд, 1Н, 6-Н), 7,53-7,57млн.ч., (д, 1Н, 5-Н, 7,70-7,75млн.ч., (дд, 1Н, 7-Н), 7,93-7,98млн.ч., (д, 1Н, 8-Н). b.) 2-Аміно-3-ціано-4-бензиламінохінолін 5г 2-Аміно-3-ціано-4-хлорхінолін та 11мл бензиламіну нагрівають при перемішуванні при температурі 130°С. Реакційну суміш виливають в 50мл води, одержаний осад відфільтровують, промивають 50мл води. Осад блідо-жовтого кольору перекристалізовують з диметилформаміду з одержанням 5,2г вказаної у заголовку сполуки. Т.пл.: 206°С. ЯМР, dΗ (400МГц, DMSO-d6): 5,02-5,03млн.ч., (д, 2Н, N-CH 2), 6,22млн.ч., (с, 2Н, NH2), 7,14-7,16млн.ч., (дд, 1Н, 6-Н), 7,24-7,26млн.ч., (дд, 1Н, 5-Н), 7,30млн.ч., (с, 5Н, Ph), 7,50-7,52млн.ч., (дд, 1Н, 7-Н), 8,168,19млн.ч., (д, 1Н, 8-Н), 8,30-8,33млн.ч., (т, 1Н, NH). Використовуючи 2-амінометилпіридин або 3-амінометилпіридин, або 4-амінометилпіридин замість бензиламіну, можуть бути отримані придатні сполуки загальної формули IV. с.) Моногідрат етил 9-бензиламіно-10-ціаноімідазо[1,2-a]хінолін-2-карбоксилату До розчину 2,74г 2-аміно-3-ціано-4-бензиламінохіноліну в 100мл абсолютного етанолу додають при перемішуванні при 70°С 2,14мл етилбромпірувату. Реакційну суміш кип'ятять протягом 2 годин, потім осад відфільтровують. Одержану кристалічну речовину білого кольору перекристалізовують з 150мл ацетонітрилу з одержанням 1,1г вказаної у заголовку сполуки, Т.пл.: 112-114°С. ЯМР, dΗ (400МГц, DMSO-d 6): 1,32млн.ч. (т, 3Н, СООСН 2СН3), 4,30млн.ч. (κ, 2Η, СООСН 2СН3), 5,09млн.ч. (д, 2Н, PhCH2), 7,25-7,38млн.ч. (м, 5Н), 7,64-7, 67млн.ч. (м, 1Н), 7,85-7,88млн.ч. (м, 1Н), 8,43-8,53млн.ч. (м, 3Н), 9,04млн.ч. (с, 1Н, 3-Н). d.) 9-Бензиламіно-10-ціаноімідазо[1,2-a]хінолін-2-карбонова кислота Суміш 2,71г моногідрату етил 9-бензиламіно-10-ціаноімідазо[1,2-a]хінолін-2-карбоксилату, 42мл етанолу та 40мл 10% розчину гідроксиду натрію перемішують протягом 6 годин при 25°С. До густої суспензії додають 100мл води і доводять значення рН суспензії до 3 за допомогою 96% розчину оцтової кислоти. Кристалічну речовину блідо-жовтого кольору відфільтровують, промивають 3´25мл води і висушують. Таким чином отримують 2,3г вказаної у заголовку сполуки. Т.пл.: 178-182°С. ЯМР, dΗ (200МГц, DMSO-d6): 5,09млн.ч. (д, 2Н, РhСН 2), 7,22-7,40млн.ч. (м, 5Н), 7,59-7,67млн.ч. (м, 1Н), 7,81-7,89млн.ч. (м, 1Н), 8,37-8,54млн.ч. (м, 3Н), 8,90млн.ч. (с, 1Н, 3-Н). e.) 1-(9-Бензиламіно-10-ціаноімідазо[1,2-a]хінолін-2-карбоніл)піролі дин До суміші 1,71г 9-бензиламіно-10-ціаноімідазо[1,2-a]хінолін-2-карбонової кислоти, 15мл хлороформу та 0,8г триетиламіну краплями додають розчин 0,6г півалоїлхлориду в 10мл хлороформу при перемішуванні в межах 15 хвилин при 5°С. Реакційну суміш перемішують протягом 1 години при 5°С, після цього до неї додають суміш 0,4г піролідину, 10мл хлороформу та 0,8мл триетиламіну. Суміш перемішують протягом 7 годин при 25°С, розбавляють 100мл хлороформу, екстрагують 50мл води, 50мл 5% розчину гідрокарбонату натрію та 50мл води, сушать над сульфа том натрію і випарюють у вакуумі. Кристалічну речовину блідожовтого кольору перекристалізовують з Ν,Ν-диметилформаміду з одержанням 0,7г вказаної у заголовку сполуки. Т.пл.: 206°С. ЯМР, dΗ (400МГц, DMSO-d6): 1,79-1,92млн.ч. (м, 4Н), 3,47-3, 50млн.ч. (м, 2Н), 3,95-3,98млн.ч. (м, 2Н), 5,08млн.ч. (д, 2Н, РhСН2), 7,23-7,38млн.ч. (м, 5Н), 7,62-7,65млн.ч. (м, 1Н), 7,83-7,87млн.ч. (м, 1Н), 8,368,42млн.ч. (м, 2Н), 8,50-8,52млн.ч. (м, 1Н), 8,80млн.ч. (с, 1Н, 3-Н). Приклад 2 N,N-Диметил-9-бензиламіно-10-ціаноімідазо[1,2-a]хінолін-2-карбоксамідугемігідрат В загальній формулі (І) R1 і R2 означають атом водню, R3 означає фенільну груп у, R4 , R5, R6 і R7 означають водень, R8 означає ціаногрупу, R9 і R10 означають, незалежно один від іншого, метильну групу, X означає -NH-групу, n дорівнює 1. До суміші 1,71г 9-бензиламіно-10-ціаноімідазо[1,2-a]хінолін-2-карбонової кислоти (одержаної згідно прикладу 1), 15мл хлороформу та 0,8г триетиламіну додавали краплями 0,6г півалоїлхлориду в 10мл хлороформу при перемішуванні в межах 15 хвилин при 5°С. Реакційну суміш перемішують протягом 1 години при 9°С, після цього до неї додають суміш 0,45г диметиламонійхлориду, 10мл хлороформу та 1,6мл триетиламіну. Суміш перемішують протягом 3 годин при 25°С, потім одержану кристалічну речовину блідожовтого кольору згідно з методикою, описаною в прикладі 1, перекристалізовують з Ν,Ν-диметилформаміду з одержанням 0,65г вказаної у заголовку сполуки. Т.пл.: 262-264°С. ЯМР, dΗ (400МГц, DMSO-d6): 2,98млн.ч. (с, 3Н), 3,45млн.ч. (с, 3Н), 5,08млн.ч. (д, 2Н, РhСН 2), 7,237,38млн.ч. (м, 5Н), 7,62-7,65млн.ч. (м, 1Н), 7,84-7,87млн.ч. (м, 1Н), 8,37-8,39млн.ч. (м, 2Н), 8,50-8,53млн.ч. (м, 1Н), 8,75млн.ч. (с, 1Н, 3-Н). Приклад 3 N-Етил-9-бензиламіно-10-ціаноімідазо[1,2-a|хінолін-2-карбоксаміду гемігідрат В загальній формулі (І) R1 і R2 означають атом водню, R3 означає фенільну груп у, R4 , R5, R6 і R7 означають водень, R8 означає ціаногрупу, R9 означає водень, R10 означає етильну групу, X означає -NHгруп у, n дорівнює 1. 1,71г 9-Бензиламіно-10-ціаноімідазо[1,2-a]хінолін-2-карбонову кислоту, одержану як описано в Прикладі 1, перетворюють за допомогою 0,45г гідрохлориду етиламіну, аналогічно тому, як це описано в попередньому Прикладі, у вказану в заголовку сполук у. Після перекристалізації блідо-жовтої речовини з 80мл етанолу отримують 0,62г вказаної у заголовку сполуки. Т.пл.: 275-277°С. ЯМР, dΗ (200МГц, DMSO-d6): 1,11млн.ч. (т, 3Н, NHCH2CH3), 3,30млн.ч. (к, 2Н, NHCH2CH3), 5,09млн.ч. (д, 2Н, PhCH2), 7,22-7,40млн.ч. (м, 5Н), 7,60-7,67млн.ч. (м, 1Н), 7,82-7,94млн.ч. (м, 2Н), 8,38-8,42млн.ч. (м, 2Н), 8,50-8,54млн.ч. (м, 1Н), 8,82млн.ч. (с, 1Н, 3-Н). Приклад 4 1-(9-Фурфуриламіно-10-ціаноімідазо[1,2-a]хінолін-2-карбоніл)піролідину гемігідрат В загальній формулі (І) R1 і R2 означають атом водню, R3 означає 2-фурильну груп у, R 4, R5 , R6 і R7 означають водень, R9 і R10 разом означають 1,4-бутандіільну групу, R8 означає ціаногрупу,X означає -NHгруп у, n дорівнює 1. а) 2-Аміно-3-ціано-фур фуриламінохінолін 10г 2-Аміно-3-ціано-4-хлорхіноліну та 19мл фур фуриламіну нагрівають при перемішуванні при 120°С протягом 3 годин. Реакційну суміш охолоджують до 25°С і шість разів послідовно змішують з 50мл води, одержаний осад відфільтровують і висушують. Отриману таким чином речовину перекристалізовують з 60мл диметилформаміду з одержанням 5,8г вказаної у заголовку сполуки. Т.пл.: 206°С. ЯМР, dΗ (200МГц, DMSO-d6): 4,98млн.ч. (д, 2Н, Фурил-СН 2), 6,29млн.ч. (с, 2Н), 6,35-6,42млн.ч. (м, 2Н), 7,10-7,18млн.ч. (м, 1Н), 7,31-7,35млн.ч. (м, 1Н), 7,47-7,60млн.ч. (м, 2Н), 8,13-8,20млн.ч. (м, 2Н). b) Моногідрат етил 9-фур фуриламіно-10-ціаноімідазо[1,2-a]хінолінкарбоксилату До розчину 2,64г 2-аміно-3-ціано-4-фур фуриламінохіноліну в 100мл абсолютного етанолу додають 2,14мл етилбромпірувату при перемішуванні при 70°С. Реакційну суміш кип'ятять протягом 2 годин, потім осад відфільтровують, речовину перекристалізовують і отримують 1,1г вказаної у заголовку сполуки, т.пл.: 242-245°С. ЯМР, dΗ (200МГц, DMSO-d 6): 1,33млн.ч. (т, 3Н, СООСН 2СН3), 4,31млн.ч. (κ, 2Η, СООСН 2СН3), 5,05млн.ч. (д, 2Н, Фурил-СН 2), 6,40-6,43млн.ч. (м, 2Н), 7,58-7,66млн.ч. (м, 2Н); 7,80-7,88млн.ч. (м, 1Н), 8,31млн.ч. (т, 1Н), 8,41-8,45млн.ч. (м, 2Н), 9,04млн.ч. (с, 1Н, 3-Н). c) 9-Фур фуриламіно-10-ціаноімідазо[1,2-a]хінолін-2-карбонова кислота Суміш моногідрату 2,52г етил 9-фур фуриламіно-10-ціаноімідазо[1,2-a]хінолін-2-карбоксилату, 40мл етанолу та 33мл 10% розчину гідроксиду натрію перемішують протягом 3 годин при 25°С. До густої суспензії додають 80мл води і рН суспензії доводять до значення 3 за допомогою 96% розчину оцтової кислоти. Кристалічну речовину блідо-жовтого кольору відфільтровують, промивають 3´25мл води і висушують. Таким чином, отримують 2,32г вказаної у заголовку сполуки. Т.пл.: 180-185°С, (розкладання). ЯМР, dΗ (200МГц, D MSO-d6): 5,05млн.ч. (д, 2Н, Фурил-СН 2), 6,39-6,42млн.ч. (м, 2Н), 7,56-7,64млн.ч. (м, 2Н), 7,79-7,87млн.ч. (м, 1Н), 8,27млн.ч. (т, 1Н), 8,36-8,46млн.ч. (м, 2Н), 8,93млн.ч. (с, 1Н, 3-Н). d) 1-(9-Фурфуриламіно-10-ціаноімідазо[1,2-a]хінолін-2-карбоніл)піролідину гемігідрат До суміші 1,79г 9-фурфуриламіно-10-ціаноімідазо[1,2-a]]хінолін-2-карбонової кислоти, 15мл хлороформу та 0,8г триетиламіну краплями додавали 0,6г півалоїлхлориду в 10мл хлороформу при перемішуванні в межах 15 хвилин при 5°С. Реакційну суміш перемішують протягом 1 години при 5°С, після цього до неї додають суміш 0,36г піролідину, 10мл хлороформу та 0,8мл триетиламіну. Суміш перемішують протягом 3 годин при 25°С, розбавляють 100мл хлороформу, екстрагують 50мл води, 50мл 5% розчину гідрокарбонату натрію та 50мл води, сушать над сульфатом натрію і випарюють у вакуумі. Кристалічну речовину жовтого кольору перекристалізовують з 50мл етанолу з одержанням 0,15г вказаної у заголовку сполуки. Т.пл.: 276-279°С. ЯМР, dΗ (200МГц, D MSO-d 6): 1,79-1,95млн.ч. (м, 4Н), 3,47-3,54млн.ч. (м, 2Н), 3,98-4,04млн.ч. (м, 2Н), 5,05млн.ч. (д, 2Н, Фурил-СН2), 6,40-6,44млн.ч. (м, 2Н), 7,57-7,65млн.ч. (м, 2Н), 7,80-7,88млн.ч. (м, 1Н), 8,23млн.ч. (т, 1Н), 8,39-8,46млн.ч. (м, 2Н), 8,81млн.ч. (с, 1Н, 3-Н). Приклад 5 1-(9-Тієніламіно-10-ціаноімідазо[1,2-a]хінолін-2-карбоніл)піролідину гемі гідрат В загальній формулі (І) R1 і R2 означають атом водню, R3 означає 2-тієнільну групу, R4, R5, R6 і R7 означають водень, R9 і R10 разом означають 1,4-бутандіільну групу, R8 означає ціаногрупу, X означає -NHгруп у, n дорівнює 1. а) 2-Аміно-3-ціано-тіеніламінохінолін 10г 2-Аміно-3-ціано-4-хлорхіноліну та 19мл тієніламіну нагрівають при перемішуванні при 115°С протягом 4 годин. Реакційну суміш охолоджують до 25°С і шість разів послідовно змішують з 50мл води, одержаний осад відфільтровують і висушують. Отриману таким чином речовину перекристалізовують з 60мл Ν,Ν-диметилформаміду з одержанням 6,8г вказаної у заголовку сполуки блідо-жовтого кольору. Т.пл.: 208-209°С. ЯМР, dΗ (200МГц, DMSO-d6): 5,18млн.ч. (д, 2Н, Тієніл-СН 2), 6,28млн.ч. (с, 2Н), 6,96-7,00млн.ч. (м, 1Н), 7,07-7,19млн.ч. (м, 2Н), 7,31-7,42млн.ч. (м, 2Н), 7,48-7,56млн.ч. (м, 1Н), 8,09-8,13млн.ч. (м, 1Н), 8,30млн.ч. (т, 1Η). b.) Етил 9-тіеніламіно-10-ціаноімідазо[1,2-a]хінолін карбоксилат До розчину 5,61г 2-аміно-3-ціано-4-тієніламінохіноліну в 200мл абсолютного етанолу додають 4,29г етилбромпірувату при перемішуванні при 70°С. Реакційну суміш кип'ятять протягом 2 годин, потім осад відфільтровують. Отримують 2,54г вказаної у заголовку сполуки світло-бежевого кольору, т.пл.: 255-256°С. ЯМР, dΗ (200МГц, DMSO-d 6): 1,33млн.ч. (т, 3Н, СООСН 2СН3), 4,31млн.ч. (κ, 2Η, СООСН 2СН3), 5,24млн.ч. (д, 2Н, Тіеніл-СН 2), 6,96-7,00млн.ч. (м, 1Н), 7,14млн.ч. (м, 1Н), 7,40-7,43млн.ч. (м, 1Н), 7,61-7,68млн.ч. (м, 1Н), 7,82-7,90млн.ч. (м, 1Н), 8,42-8,46млн.ч. (м, 3Н), 9,05млн.ч. (с, 1Н, 3-Н). с.) 9-Тієніламіно-10-ціаноімідазо[1,2-а]хінолін-2-карбонова кислота Суміш 2,54г етил 9-тієніламіно-10ціаноімідазо[1,2-a]хінолін-2-карбоксилату, 40мл етанолу та 33мл 10% розчину гідроксиду натрію перемішують протягом 6 годин при 25°С. До густої суспензії додають 80мл води і доводять рН до величини 3 за допомогою 96% розчину оцтової кислоти. Блідо-жовту кристалічну речовину відфільтровують, промивають 5´10мл води і сушать. Таким чином, отримують 2,18г вказаної у заголовку сполуки. Т.пл.: 209217°С (розкладання). ЯМР, dΗ (400МГц, D MSO-d 6): 5,24млн.ч. (д, 2Н, Тієніл-СН 2), 8,88млн.ч. (с, 1Н, 3-Н). d.) 1-(9-Тієніламіно-10-ціаноімідазо[1,2-a]хінолін-2-карбоніл)піролідину гемі гідрат До суміші 1,80г 9-тієніламіно-10-ціаноімідазо[1,2-a]хінолін-2-карбонової кислоти, 10мл хлороформу та 1,1мл триетиламіну краплями додають 0,87г півалоїлхлориду в 10мл хлороформу при перемішуванні протягом 15 хвилин при 5°С. Реакційну суміш перемішують протягом 1 години при температурі 5°С, після чого до неї додають 0,51г піролідину, 10мл хлороформу та 1,1мл триетиламіну. Суміш перемішують протягом 3 годин при температурі 25°С, розбавляють 100мл хлороформу, екстрагують 50мл води, 50мл 5% розчину гідрокарбонату натрію та 50мл води, сушать над сульфатом натрію і випарюють у вакуумі. Кристалічну речовину жовтого кольору перекристалізовують з 200мл етанолу з одержанням 0,29г вказаної у заголовку сполуки. Т.пл.: 267-269°С. ЯМР, dΗ (400МГц, D MSO-d 6): 1,79-1,94млн.ч. (м, 4Н), 3,48-3,51млн.ч. (м, 2Н), 3,98-4,01млн.ч. (м, 2Н), 5,24млн.ч. (д, 2Н, Тієніл-СН 2), 6,97-7,00млн.ч. (м, 1Н), 7,14млн.ч. (м, 1Н), 7,41млн.ч. (м, 1Н), 7,61-7,65млн.ч. (м, 1Н), 7,83-7,87млн.ч. (м, 1Н), 8, 37-8,45млн.ч. (м, 3Н), 8,82млн.ч. (с, 1Н, 3-Н). Структура та фізичні властивості інших сполук загальної формули (І), одержаних за методикою, описаною в Прикладі 1, наведені в Таблиці І. Структура та фізичні властивості проміжних сполук загальної формули (III), одержаних за методикою, описаною в Прикладі 1, наведені в Таблиці (II) Структура та фізичні властивості проміжних сполук загальної формули (IV), одержаних за методикою, описаною в Прикладі 1, наведені в Таблиці (III) Структура та фізичні властивості проміжних сполук загальної формули (V), одержаних за методикою, описаною в Прикладі 1, наведені в Таблиці (IV) Приклад 72 Відомими способами, використовуваними в фармацевтичній промисловості, були зроблені таблетки з наступної композиції Активній інгредієнт 25мг Лактоза 50мг Авісел 21мг Кросповідон 3мг Стеарат магнію 1мг Біологія Методики Зв'язування аденозинових А3 рецепторів людини Одержання мембранної суспензії: збирають СНО клітини, що експресують hА3 рецептори, промиваючи тричі крижаним PBS, центрифугують при 1000´g 10 хвилин, гомогенізують протягом 15сек. В буфері (50мМ Тріс, рН 7,4), центрифугують при 43000´g 10 хвилин (Sigma 3K30), суспендують мембранний препарат в буфері, згаданому ви ще, зберігають аліквоти при -80°С. Протокол зв'язування: інкубують СНО-hА3 мембранний препарат (містить 2мкг білка) в інкубаційному буфері (50мМ Тріс, 10мМ МgСІ2, 1мМ EDTA, 3Од./мл аденозину деамінази, рН 8,0), в присутності 0,5нМ [125І]АВ-МЕС А (п-амінобензилметилкарбоксамідо-аденозин) (100,000імп./хвил.) та 100мкМ R-PIA (N6-[L-2фенілізопропіл]аденозин) для визначення неспецифічного зв'язування або досліджуваної сполуки в загальному об'ємі 50мкл протягом 1 години при кімнатній температурі. Фільтрують через фільтри із скляних волокон Whatman GF/B (попередньо занурені на 3 години в 0,5% поліетиленімін), промивають 4´1мл крижаного 50мМ Тріс, 10мМ МgСІ2, 1мМ EDTA (рН 8,0) на 96-лунковий Brandel Cell планшет. Визначення активності: в гама-лічильнику (1470 Wizard, Wallac). Інгібування [%]=100-((активність в присутності досліджуваної сполуки-неспецифічна активність)/(загальна активність-неспецифічна активність))·100 Зв'язування аденозинових A1 рецепторів людини Одержання мембранної суспензії: збирають СНО клітини, що експресують hА1 рецептори, промиваючи тричі крижаним PBS, центрифугують при 1000´g 10 хвилин, гомогенізують протягом 15сек. В буфері (50мМ Тріс, 10мМ МgСІ2, 1мМ EDTA, рН 8,0), центрифугують при 43000´g 10 хвилин (Sigma 3K30), суспендують мембранний препарат в буфері, згаданому вище, зберігають аліквоти при -80°С. Протокол зв'язування: інкубують CHO-hA1 мембранний препарат (містить 50мкг білка) в інкубаційному буфері (50мМ Тріс, 3Од./мл аденозину деамінази, рН 7,4), 10нМ [3Н]ССРА (2-хлор-N6циклопентиладенозин) (80.000розкл./хвил.) і 10мкМ R-PIA (N6-[L-2-фенілізопропіл]аденозину) для визначення неспецифічного зв'язування або досліджуваної сполуки в загальному об'ємі 100мкL протягом 3 годин при кімнатній температурі. Фільтрують через фільтри із скляних волокон Whatman GF/B (попередньо занурені на 3 години в 0,5% поліетиленімін), промивають 4´1мл крижаного буфера 50мМ Тріс (рН 7,4)) на 96-лунковий Brandel Ceil планшет. Визначення активності: в 96-лунковому планшеті в присутності HiSafe-3 коктейлю в бета-лічильнику (1450 Microbeta, Wallac). Інгібування [%]=100-((активність в присутності досліджуваної сполуки-неспецифічна активність)/(загальна активність-неспецифічна активність))·100 Зв'язування аденозинових А2а рецепторів людини Протокол зв'язування: інкубують 7мкг мембран (аденозинових А2а рецепторів людини, заражених НЕК293 клітинами, джерело: Receptor Biology, Inc.), буфер (50мМ Тріс-НСІ, 10мМ МgСІ2, 1мМ EDTA, 2Од./мл аденозиндіамінази, рН 7,4), 20нМ [3H]CGS-21680 (2-[р-(2-карбонілетил)фенілетиламіно]-5'-Nетилкарбоксамідадоенозин) (200000розкл./хвил) та 50мкМ NECA (5'-N-етилкарбоксамідоаденозин) для визначення неспецифічного зв'язування або досліджуваної сполуки в загальному об'ємі 100мкл протягом 90 хвилин при кімнатній температурі. Фільтрують через фільтри із скляних волокон Whatman GF/B (попередньо занурені в 0,5% поліетиленімін), промивають 4´1мл крижаного 50мМ Тріс, 10мМ МgСl2, 1мМ EDTA, 0,9 % NaCI (pH 7,4) на 96-лунковий Brandel Ceil планшет. Визначення активності: в 96-лунковому планшеті в присутності HiSafe-З коктейлю в бета-лічильнику (1450 Microbeta, Wallac). Інгібування [%]=100((активність в присутності досліджуваної сполуки-неспецифічна активність )/(загальна активністьнеспецифічна активність))·100 Зв'язування аденозинових А2b рецепторів людини Протокол зв'язування: інкубують 20,8мкг мембран (аденозинових А2b рецепторів людини, заражених НЕК-293 клітинами, джерело: Receptor Biology, Inc.), буфер (50мМ Тріс-НСІ, 10мМ МgСІ2, 1мМ EDTA, 0,1мМ бензамідину, 2Од./мл аденозиндіамінази, рН 6,5), 32,4нМ [3H]DPCPX (8-циклопентил-1,3-дипропілксантин) (800.000розкл./хвил.) та 100мкМ NECA (5'-N-етилкарбоксамідоаденозин) для визначення неспецифічного зв'язування або досліджуваної сполуки в загальному об'ємі 100мкл протягом 30 хвилин при кімнатній температурі. Фільтрують через фільтри із скляних волокон Whatman GF/B (попередньо занурені в 0,5% поліетиленімін), промивають 4´1мл крижаного 50мМ Тріс (рН 6,5) на 96-лунковий Brandel Cell планшет. Визначення активності: в 96-лунковому планшеті в присутності HiSafe-3 коктейлю в бета-лічильнику (1450 Microbeta, Wallac). Інгібування [%]=100-((активність в присутності досліджуваної сполуки-неспецифічна активність)/(загальна активність-неспецифічна активність))·100 Результати Ми вважаємо сполуки біологічно активними, якщо вони інгібують зв'язування радіоліганда аденозинових А3 рецепторів людини з активністю вище 80% при 1мкМ в наших експериментальних умовах. Константа дисоціації (Kd) [125 I]AB-MEC A на CHO-hA3 мембранному препараті визначається за дослідженнями ізотопного насичення за допомогою аналіза Scatchard [G. Scatchard, Ann. N. Υ. Acad. Sci. 51: 660, 1949]. ІС50 перетворюють в константу а фінності (Ki), використовуючи рівняння Cheng-Prusoff [Υ. J. Cheng та W. Η. Prusoff, Biochem. Pharmacol. 22: 3099, 1973]. Деякі сполуки загальної формули (І), (II), (III) і (IV) виявляють вражаючі біологічні ефекти. Сполуки загальної формули (І), визначені в п.2, як підгрупа загальної формули (І), визначеної в п.1, виявляють найбільш важливу активність. За винятком 9 сполук, чиї значення Ki не перевищують 150нМ. Сполуки, наведені в прикладах, є особливо переважними. їх значення Ki при дослідженні зв'язування аденозинових А3 рецепторів людини знаходяться в межах між 1,6 і 0,38нМ. Значення Ki найбільш переважних сполук складають 0,52 та 0,38нМ. Сполуки мають необхідну біодоступність і проявляють щонайменше 1,000-кратну селективність по відношенню до Α1, А2а та А2b підтипів рецепторі аденозину людини. Крім того, тривалість їхньої дії при внутрішньовенному та оральному уведенні є достатньо довгою, їх значення ED50 є низькими, їх токсикологічний профіль та вплив побічних ефектів є сприятливими. Дані, наведені вище, роблять сполуки загальної формули (І) придатними для терапевтичного використання.
ДивитисяДодаткова інформація
Назва патенту англійськоюImidazoquinoline derivatives
Автори англійськоюBalog Maria, Batori, Sandor, Boer, Kinga, Kapui, Zoltan, Mikus, Endre, Timari, Geza
Назва патенту російськоюПроизводные имидазохинолина
Автори російськоюБалог Мария
МПК / Мітки
МПК: C07D 215/56, C07D 405/12, A61P 27/16, A61P 11/06, C07D 487/04, C07D 215/54, A61K 31/4545, A61K 31/437, A61P 9/06, C07D 471/04, A61K 31/4709, A61P 3/04, A61P 25/00, A61P 25/24, A61P 13/12, A61P 37/08, A61P 19/02, A61P 9/10, A61P 29/00, A61P 27/02, A61P 17/04, A61P 9/08, A61P 35/00, A61P 37/02, A61P 43/00, A61P 1/04, C07D 409/12, A61P 25/16, A61P 25/28, A61P 7/00, A61P 17/00, A61P 11/00, A61P 3/10, A61P 9/00, A61K 31/4706, A61P 17/06, A61P 9/12, A61P 27/06
Мітки: похідні, імідазохіноліну
Код посилання
<a href="https://ua.patents.su/15-78745-pokhidni-imidazokhinolinu.html" target="_blank" rel="follow" title="База патентів України">Похідні імідазохіноліну</a>
Попередній патент: Спосіб виготовлення підкладки, підкладка, клаптик, листочок, смуга, стрічка або вузенька смужка, виготовлені з підкладки, та папір і банкнота
Наступний патент: Картридж для порошкового фармацевтичного препарату (варіанти) та інгалятор для порошкових фармацевтичних препаратів (варіанти)
Випадковий патент: Пристрій для транспортування і очистки коренебульбоплодів