Похідні тетрагідрохіноліну, фармацевтична композиція на їх основі та їх використання
Номер патенту: 80303
Опубліковано: 10.09.2007
Автори: Карстенс Віллем Фредерік Йоган, Тіммерс Корнеліс Маріус
Формула / Реферат
1. Похідна тетрагідрохіноліну формули І
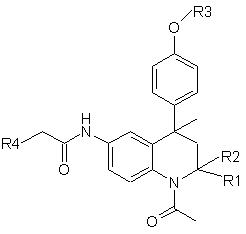 (I)
(I)
або її фармацевтично прийнятна сіль, в якій
R1, R2 є H, Me;
R3 - (2-6С)гетероциклоалкіл(1-4С)алкіл, (2-5С)гетероарил(1-4С)алкіл, (6С)арил(1-4С)-алкіл, (1-4С)(ді)алкіламінокарбоніламіно(2-4С)алкіл, (2-6С)гетероциклоалкілкарбоніламіно(2-4С)алкіл, R5-(2-4C)алкіл або R5-кapбoнiл(1-4C)aлкiл;
R4 - (2-5С)гетероарил, (6С)арил, (3-8С)циклоалкіл, (2-6С)гетероциклоалкіл або (1-6С)алкіл;
R5 - (ді)(1-4С)алкіламіно, (1-4С)алкокси, аміногрупа, гідроксигрупа, (6С)ариламіно, (ді)(3-4С)алкеніламіно, (2-5С)гетероарил(1-4С)алкіламіно, (6С)арил(1-4С)алкіламіно, (ді)[(1-4С)алкоксі(2-4С)алкіл]аміно, (ді)[(1-4С)алкіламіно(2-4С)алкіл]аміно, (ди)[аміно(2-4С)алкіл]аміно або (ди)[гідроксі(2-4С)алкіл]аміно;
2. Похідна за п. 1, яка відрізняється тим, що у ній R3 - (2-6С)гетероциклоалкіл(1-4С)алкіл, (2-5С)гетероарил(1-4С)алкіл, (2-6С)гетероциклоалкілкарбоніламіно(2-4С)алкіл, R5-(2-4C)aлкiл або R5-карбоніл(1-4С)алкіл.
3. Похідна за п. 1 або п. 2, яка відрізняється тим, що у ній R5 - (ді)(1-4С)алкіламіно, аміногрупа, (ді)(3-4С)алкеніламіно, (2-5С)гетероарил(1-4С)алкіламіно або (6С)арил(1-4С)алкіламіно.
4. Похідна за будь-яким з пп. 1-3, яка відрізняється тим, що у ній R5 - (ді)(1-4С)алкіламіно або аміногрупа.
5. Похідна за будь-яким з пп. 1-4, яка відрізняється тим, що у ній R5 - (ді)(1-4С)алкіламіно.
6. Похідна за будь-яким з пп. 1-5, яка відрізняється тим, що у ній R4 - (6С)арил.
7. Похідна за будь-яким з пп. 1-6, яка відрізняється тим, що у ній R3 - (2-6С)-гетероциклоалкіл(1-4С)алкіл, (2-5С)гетероарил(1-4С)алкіл або R5-(2-4C)алкіл.
8. Фармацевтична композиція, яка містить похідну тетрагідрохіноліну за будь-яким з пп. 1-7 і фармацевтично прийнятні допоміжні компоненти.
9. Похідна тетрагідрохіноліну за будь-яким з пп. 1-7, призначена для використання у терапії.
10. Використання похідної тетрагідрохіноліну за будь-яким з пп. 1-7 або її фармацевтично прийнятної солі або сольвату у виготовленні медикаменту, призначеного для регулювання плідності.
Текст
1. Похідна тетрагідрохіноліну формули І C2 2 (19) 1 3 80303 ляцію температури і процес репродукції. Гонадотропіни діють на специфічні гонадні типи клітин для ініціювання оваріальної і тестикулярної диференціації і стероїдо-генезу. Гіпофізний гонадотропін FSH (гормон стимуляції фолікула), наприклад, грає центральну роль у стимуляції розвитку і дозрівання фолікула, a LH (гормон лютенеїзації) індукує овуляцію [Sharp, R.M. Clin Endocrinol. 33:787807, 1990; Dorrington and Armstronr, Recent Prog. Horm. Res. 35: 301-342, 1979]. Сьогодні FSH застосовують клінічно, у комбінації з LH або hСГ, для оваріальної стимуляції, тобто гіперстимуляції для запліднення in vitro (TVF) і індукування овуляції у неплідних ановуляторних жінок [Insler, V., Int. J. Fertility 33:85-97, 1988, Navot and Rosenwaks, J. Vitro Fert. Embryo Transfer 5: 3-13, 1988], а також у випадках недорозвитку статевої системи і неплідності у чоловіків. Гонадотропін FSH вивільняється з переднього гіпофізу під впливом гормону вивільнення гонадотропіну і естрогенів І з плаценти під час вагітності. У жінок FSH діє на яєчники, сприяючи розвитку фолікула, і є головним гормоном, що регулює секрецію естрогенів. У чоловіків FSH відповідає за цілісність сім'яносних канальців і діє на клітини Сертолі для підтримки гаметогенезу. Очи щений FSH використовують клінічно для лікування неплідності жінок і деяких типів відсутності сперматогенезу у чоловіків. Гонадотропіни, призначені для терапії, можуть бути ізольовані з джерел людської сечі, але мають низьку чистоту [Morse et al, Amer. J. Reproduct. Immunol and Microbiology 17:143, 1988]. їх також можна приготувати як рекомбінантні гонадотропіни. Рекомбінантний людський FSH є у продажу і його використовують для допомоги репродукції. [Olijve et al. Моl. Hum. Reprod. 2: 371, 1996; Devroeyetal. Lancet 339:1170, 1992]. Дії гормону FSH опосередковуються специфічним рецептором мембрани плазми, який є членом великої родини зв'язаних G-протеїном рецепторів. Ці рецептори складаються з єдиного поліпептиду з сімома трансмембранними доменами і можуть взаємодіяти з G-протеїном, викликаючи, наприклад, активування циклази аденілату. Рецептор FSH є високоспецифічним об'єктом у процесі росту оваріального фолікула і експресується виключно у яєчнику. Блокування цього рецептора або інгібування сигналізації, яка у нормальних умовах відбувається після опосередкованої активації рецептора FSH, порушує розвиток фолікула і, отже, овуляцію і плідність. Таким чином, низькомолекулярні антагоністи FSH можуть бути основою нових контрацептивів. Такі антагоністи FSH спричиняють розвиток зменшених фолікулів (без овуляції), але забезпечують достатню секрецію естрогену для запобігання шкідливим впливам, наприклад, на кісткову масу. З іншого боку, сполуки, що стимулюють активність рецептора FSH, можуть бути використані для імітації гонадотропічного ефекту природного ліганду. Винахід стосується приготування низькомолекулярнихо аналогів гормону, який селективно виявляє модуляторну активність до рецептора FSH. Сполуки винаходу можуть бути використані як (ча 4 сткові) агоністи або (часткові) антагоністи рецептора FSH. Було виявлено, що описаний далі клас тетрагідрохінолінових сполук формули І або їх фармацевтично прийнятні солі мають FSH-модуляторну активність де R1, R2-H, Me; R3 - (2-6С)гетероциклоалкіл(1-4С)аІІсуІ, (25С)гетероарил(1-4С)алкіл, (6С)арил(1-4С)-алкіл, (1-4С)(ди)алкіламінокарбоніламіно(2-4С)алкіл, (26С)гетероциклоалкіл-карбоніл-аміно(2-4С)алкіл, R5 - (2-4С)алкіл або R5-карбоніл(1-4С)алкіл; R4 (2-5С)гетероарил, (6С)арил, (38С)циклоалкіл, (2-6С)гетероциклоалкіл або (1-6С)алкіл; R5 - (ди)(1-4С)алкіламіно, (1-4С)алкокси, аміно, гідрокси, (6С)ариламіно, (ди)(3-4С)алкеніламіно, (2-5С)гетероарил(1-4С)алкіламіно, (6С)арил(14С)алкіламіно, (ди)[(1-4С)алкокси(24С)алкіл]аміно, (ди)[(1-4С)алкіламіно(24С)алкіл]аміно, (ди)[аміно(2-4С)-алкіл]аміно або (ди)[гідрокси(2-4С)алкіл]аміно. Сполуки згідно з винаходом модулюють функцію рецептора FSH i можуть бути використані клінічно, як і природні FSH, якщо вони поводяться як агоністи, з тією ристані клінічно, як і природні FSH, якщо вони поводяться як агоністи, з тією перевагою, що вони мають змінені якості стабільності і можуть вводитись пацієнту в інший спосіб. Якщо вони блокують рецептор FSH, то можуть бути використані як контрацептивні агенти. Таким чином, модулятори рецептора FSH згідно з винаходом можуть бути використані для лікування неплідності, для контрацепції і для лікування таких гормоно-залежних розладів, як рак грудей, рак простати і ендометріоз. Наведені далі терміни мають визначені для них значення в описі і Формулі винаходу. Термін (1-4С)алкіл у цьому описі означає розгалужену або нерозгалужену алкільну групу, яка містить 1-4 атоми карбону, тобто метил, етил, пропіл, ізопропіл, бутил, втор-бутил і трет-бутил. Термін (2-4С)алкіл у цьому описі означає розгалужену або нерозгалужену алкільну групу, яка містить 2-4 атоми карбону, тобто етил, пропіл, ізопропіл, бутил, втор-бутил і трет-бутил. Термін (1-6С)алкіл у цьому описі означає розгалужену або нерозгалужену алкільну групу, яка містить 1-6 атомів карбону, наприклад, метил, 5 80303 етил, пропіл, ізопропіл, бутил, втор-бутил, третбутил і гексил. Бажаними є (1-5С)алкільні групи, найбільш бажаними -(1-4С)алкільні. Термін (ди)(1-4С)алкіламіно у цьому описі означає аміногрупу, моно- або дизаміщену алкільними групами, кожна з яких містить 1-4 атоми карбону і має визначене вище значення. Термін (ди)(1-4С)алкеніламіно у цьому описі означає аміногрупу, моно- або дизаміщену алкільними групами, кожна з яких містить 2-4 атоми карбону і є, наприклад, алілом і 2-бутенілом, і має визначене вище значення. Термін (3-8С)циклоалкіл у цьому описі означає циклоалкільну груп у з 3-8 атомами карбону, а саме циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил і циклооктил. Бажаними є (36С)циклоалкільні групи. Термін (2-6С)гетероциклоалкіл у цьому описі означає гетероциклоалкільну груп у з 2-6, бажано, 3-5 атомами карбону і з щонайменше одним гетероатомом, вибраним з Ν, Ο і/або S, яка, якщо можливо, може бути приєднана через гетероатом або атом карбону. Бажаними гетероатомами є N або О. Гетероциклоалкільна група може бути заміщена метильною або етильною груп на атомі карбону або гетероатомі, якщо це можливо. Бажаними гетероциклоалкільними групами є піперидиніл, піперазиніл, морфолініл, піролідиніл і 1-метил2-піперидиніл. Термін (1-4С)алкокси у цьому описі означає алкоксигрупу з 1-4 атомами карбону, причому алкільний компонент є таким, що був визначений вище. Бажаними є (1-2С)алкоксифупи. Термін (6С)арил у цьому описі означає фенільну групу, яка, як варіант, може бути заміщеною одним або більше замісниками, вибраними з гідроксигрупи, аміногрупи, йоду, брому, хлору, флуору, нітрогрупи, дифлуорметилу, ціаногрупи, фенілу, (1-4С)алкілу, (1-4С)алкоксигрупи або (14С)(ди)алкіламіногрупи, алкілу, алкоксигрупи і діалкіламінових компонентів, таких, які були визначені вище, наприклад, фенілу, 3,5-дибромфенілу, 4біфенілу, 3,5-ди хлорфенілу, 3-бром-6метиламінофенілу, 3-хлор-2,6-диметоксифенілу і 3,5-диметил фенілу. Термін (2-5С)гетероарил у цьому описі означає заміщену або незаміщену ароматичну груп у з 2-5 атомами карбону і з щонайменше одним гетероатомом, вибраним з Ν, Ο і/або S, наприклад, імідазоліл, піридил, піримідил, тієніл або фурил. Замісники на гетероариль-ній групі можуть бути вибрані з групи замісників, перелічених для (6С)арильної групи. Гетероарильна група може бути приєднана через атом карбону або гетероатом, якщо це можливо. Бажаними гетероарильними групами тієніл, фурил і піридил. Термін (2-6С)гетероциклоалкіл(1-4С)алкіл у цьому описі означає гетероциклоалкільну групу з 2-6 атомами карбону, приєднану до алкільної групи, яка має 1-4 атоми карбону; ці групи є такими, що були визначені вище. Термін (2-6С)гетероциклоалкілкарбоніламіно у цьому описі означає гетероциклоалкільну групу з 2-6 атомами карбону, приєднану до карбонільного компонента карбоніламіногрупи; причому гетеро 6 циклоалкільна група є такою, що була визначена вище. Термін (26С)гетероциклоалкілкарбоніламіно(2-4С)алкіл у цьому описі означає гетероциклоалкілкарбоніламіногрупу, в якій гетероциклоалкільний компонент містить 2-6 атоми карбону, приєднану через аміногруп у до алкільної групи, що має 2-4 атоми карбону; ці групи є такими, що були визначенні вище. Термін (ди)(1-4С)алкіламінокарбоніл у цьому описі означає (ди)алкіламіногрупу, в якій алкільні групи мають 1-4 атоми карбону, приєднані через аміногрупу до карбонільної групи, причому (ди)алкіламіногрупа є такою, що була визначена вище. Термін (3-8С)циклоалкіламінокарбоніл у цьому описі означає циклоалкільну групу з 3-8 атомами карбону, приєднану до амінокомпонента амінокарбонільної групи, причому циклоалкільна група є такою, що була визначена вище. Термін (ди)(1-4С)алкіламінокарбоніламіно у цьому описі означає (ди)алкіламіногрупу, в якій алкільна(і) група(и) мають 1-4 атоми карбону і приєднані через аміногрупу до карбонільного компонента карбоніламіногрупи, створюючи цим мочевин-ну функціональність, причому (ди)алкіламіногрупа є такою, що була визначена вище. Термін (ди)(1-4С)алкіламінокарбоніламіно(24С)алкіл у цьому описі означає (ди)алкіламінокарбоніламіногрупу, в якій алкільна(і) група (і) мають 1-4 атоми карбону, приєднані через аміногрупу до цієї алкільної групи, яка має 24 атоми карбону, а (ди)алкіламінокарбоніламіногрупа і алкільна група є такими, що були визначені вище. Термін (2-5С)гетероарил(1-4С)алкіл у цьому описі означає гетероарильну групу з 2-5 атомами карбону, приєднану до алкільної групи, яка має 1-4 атоми карбону, причому гетероарильна і алкільна групи є такими, що були визначені вище. Термін (6С)арил(1-4С)алкіл у цьому описі означає фенільну групу, як варіант, заміщену одним або більше замісниками, вибраними з групи замісників, перелічених для (6С)арильної групи, і приєднану до алкільної групи з 1-4 атомами карбону, причому арильна і алкільна групи є такими, що були визначені вище. Термін (6С)ариламіно у цьому описі означає фенільну груп у, як варіант, заміщену одним або більше замісниками, вибраними з групи замісників, перелічених для (6С)арильної групи, і приєднану до аміногрупу, причому арильна група є такою, що була визначена вище. Термін (6С)арил(1-4С)алкіламіно у цьому описі означає фенільну групу, як варіант, заміщену одним або більше замісниками, вибраними з групи замісників, перелічених для (6С)арильної групи, і приєднану до алкільного компонента алкіламіногрупи, що має 1-4 атоми карбону, причому арильна і алкіламіногрупа є такими, що були визначені вище. Термін (2-5С)гетероарил(1-4С)алкіламіно у цьому описі означає гетероарильну групу з 2-5 атомами карбону, як варіант, заміщену одним або 7 80303 більше замісниками, вибраними з групи замісників, перелічених для (6С)арильної групи, і приєднану до алкільного компонента алкіламіногрупи, яка має 1-4 атоми карбону, причому гетероарильна група і алкіламіногрупа є такими, що були визначені вище. Термін (1-4С)алкокси(2-4С)алкіл у цьому описі означає алкоксигрупу з 1-4 атомами карбону, приєднану до алкільної групи, яка має 2-4 атоми карбону, причому алкоксигрупа і алкільна групи є такими, що були визначені вище. Термін (ди)[(1-4С)алкокси(2-4С)алкіл]аміно у цьому описі означає аміногрупу, моно-або дизаміщену (1-4С)алкокси(2-4С)алкільними групами. (14С)алкокси(2-4С)алкільна група є алкоксигрупою з 1-4 атомами карбону, приєднаною до алкільної групи, яка має 2-4 атоми карбону і є такою, що була визначена вище. Термін (1-4С)алкіламіно(2-4С)алкіл у цьому описі означає алкіламіногрупу з 1-4 атомами карбону, приєднану через аміногрупу до алкільної групи, яка має 2-4 атоми карбону, причому алкільні компоненти є такими, що були визначені вище. Термін (ди)[(1-4С)алкіламіно(2-4С)алкіл]аміно у цьому описі означає аміногрупу, моно- або дизаміщену (1-4С)алкіламіно(2-4С)алкільними групами. (1-4С)алкіламіно(2-4С)алкіл група є алкіламіногрупою, яка має 1-4 атоми карбону, приєднаною через аміногрупу до алкільної групи з 2-4 атомами карбону, і є такою, що була визначена вище. Термін аміно(2-4С)алкіл у цьому описі означає аміноалкільну груп у з 2-4 атомами карбону, причому алкільний компонент є таким, що був визначений вище. Термін (ди)[аміно(2-4С)алкіл]аміно у цьому описі означає аміногрупу, моно- або дизаміщену аміноалкільними групами з 2-4 атомами карбону і визначеною вище. Термін гідрокси(2-4С)алкіл у цьому описі означає гідроксиалкільну гр упу з 2-4 атомами карбону, причому алкільний компонент є таким, що був визначений вище. Термін (ди)[гідрокси(2-4С)алкіл]аміно у цьому описі означає аміногрупу, моно- або дизаміщену гідроксиалкільними групами з 2-4 атомами карбону, що була визначена вище. Термін R5-(2-4С)алкіл у цьому описі означає груп у R5, приєднану до алкільного компонента з 24 атомами карбону, який є таким, що був визначений вище. Термін R5-карбоніл-(1-4C)алкіл у цьому описі означає групу R5 , приєднану до карбонільного компонента карбонілалкільної групи, який має 1-4 атоми карбону, що був визначений вище. Термін "фармацевтично прийнятна сіль" стосується солей, які згідно з медичними міркуваннями, є придатними для використання у контакті з тканинами людини і нижчих тварин без токсичної дії, без створення подразнення, алергічних реакцій тощо і характеризуються розумним відношенням корисність/ризик. Фармацевтично прийнятні солі є добре відомими. їх можна отримати під час кінцевої ізоляції і очищення сполук винаходу, або реакцією функції вільної основи, якщо вона є, з придатною неорганічною кислотою, наприклад, 8 гідрохлорною, фосфорною або сульфуровою, або з органічною кислотою, наприклад, аскорбіновою, лимонною, винною, молочною, малеїновою, малоновою, фумаровою, гліколевою, бурштиновою, пропіоновою, оцтовою, метансульфоновою, тощо. Кислотну функцію можна ввести в реакцію з органічною або неорганічною основою, наприклад, гідроксидом натрію, калію або літію. Отже, винахід стосується сполуки формули І, визначеної вище. Одним з втілень винаходу є сполуки формули І, в яких R1 і R2 є Me. Винахід також стосується сполук формули І, в яких R3 - (2-6С)гетероциклоалкіл(1-4С)алкіл, (25С)гетероарил(1-4С)алкіл, (2-6С)гетероциклоалкілкарбоніламіно(2-4С)алкіл, R5 - (24С)алкіл, R5 - карбоніл(1-4С)алкіл. В іншому аспекті винахід стосується сполук формули І, в якій R3 - (2-6С)-гетероциклоалкіл(14С)алкіл, (2-5С)гетероарил(1-4С)алкіл, R5 - (24C)алкіл, R5 - карбоніл(1-4С)-алкіл У ще одному аспекті винахід стосується сполук формули І, в яких R3 (2-6С)гетероциклоалкіл(1-4С)алкіл, (2-5С)гетероарил(14С)алкіл або R5 – (2-4С)алкіл. В іншому аспекті винахід стосується сполук формули І, в якій R3 - (2-6С)-гетероциклоалкіл(14С)алкіл. Іншим втіленням винаходу є ге тероциклоалкільна група у гетероцикпоалкіл(1-4С)алкілі у R3 формули І, яка містить 4, 5 або 6 атомів С, і гетероарильна група у гетеро-арилі(1-4С)алкіл у R3, яка містить 3, 4 або 5 атомів С. Інше втілення винаходу стосується сполук формули І, в якій R4 - (6С)арил. Ще одним втіленням винаходу є сполуки формули І, в яких R5 - (ди)(1-4С)алкіламіно, аміногрупа, (ди)(3-4С)алкеніламіногрупа, (25С)гетероарил(1-4С)алкіламіногрупа, (6С)-арил(14С)алкіламіногрупа, (ди)[(1-4С)алкокси(24С)алкіл]аміногрупа, (ди)[(1-4С)алкіламіно-(24С)алкіл]аміногрупа, (ди)[аміно(24С)алкіл]аміногрупа, (ди)[гідрокси-(2-4С)алкіл]аміногрупа. В іншому аспекті винахід стосується сполук формули І, в яких R5 - (ди)(1-4С)алкіламіногрупа, (2-5С)гетероарил(1-4С)алкіламіногрупа, (ди)[(14С)алкокси(2-4С)алкіл]-аміногрупа, (ди)[(14С)алкіламіно(2-4С)алкіл]аміногрупа, (ди)[аміно(24С)алкіл]аміногрупа або (ди)[гідрокси(24С)алкіл]аміногрупа. В іншому аспекті винахід стосується сполук формули І, в яких R5 - (ди)(1-4С)алкіламіногрупа, аміногрупа, (ди)(3-4С)а]алкеніламіногрупа, (25С)гетероарил(1-4С)-алкіламіногрупа, (6С)арил(14С)алкіламіногрупа. Іншим аспектом винаходу є сполуки формули І, в яких R - (ди)(1-4С)алкіламіногрупа або аміногрупа. Ще одним аспектом винаходу є сполуки формули І, в яких R5 - (ди)(1-4С)алкіламіногрупа. Інший аспект винаходу стосується сполук, в яких всі конкретні визначення груп R1 - R5, наведені вище, розповсюджуються на сполуку формули І. 9 80303 10 Далі описано способи приготування сполук винаходу. Сполуки винаходу формули І-а можна приготувати, починаючи з добре документованої реакції Скраупа. Ця реакція на захищеному N-третбутоксикарбонілом (N-Boc) 1,4-фенілендіаміні (II) дає похідну 1,2-дигідрохіноліну (ІІІ-а). Відповідні реакції циклоконденсації Скраупа можна знайти [у літературі: A. Knoeve-nagel, Chem. Ber. 54:1726, 1921; R.L. Atkins and D.E. Bliss, L Org. Chem. 43:1975, 1978; IV. Johnson, B.S. Rauckman, DP. Baccanari and B. Roth., I Med. Chem. 32:1942, 1989; W.C. Lin, S.-T. Huang and S.-T. Lin, J. Chin. Chem. Soc. 43:497, 1996; IP. Edwards, S.I West, ELB, Marschke, D.E. Mais, M.M. Gottardis і Т.K. Jones, J. Med. Chem. 41:303,1998]. Цю реакцію звичайно проводять при підвищеній температурі в ацетоні або мезитило-ксиді у присутності йоду або протоновмісної кислоти, наприклад, гідрохлорної, р-толуолсульфонової кислоти або водного гідройодиду. В іншому варіанті сполуку формули ІІІ-а можна приготувати реакцію сполуки II з ацетоном у присутності MgSO4 , 4-третбутилкатехолу і йоду [L.G. Hamann, R.I. Efiguchi, L. Zhi, I.P.Edwards and X.-N. Wanr, J. Med. Chem, 41: 623, 1998]. Згідно з іншою процедурою, реакцію можна проводити в ацетоні, використовуючи трифлати лантаніду (наприклад, трифлат скандію) як каталізатори. У цьому випадку, реакцію проводять при кімнатній температурі або при підвищеній температурі, застосовуючи звичайне підігрівання або мікрохвильове опромінювання [М. Е. Theoclitou and L. A. Robinson, Tetrahedron Lett. 43: 3907, 2002]. Сполуки формули Ill-b можна приготувати з NBoc-1,4-фенілендіаміну II реакцією з метилвінілкетоном. Належні циклізації [описано у патенті США 2 686 182 (Badische Anilin-& Soda-Fabrik Aktiengesellschaft)]. Подальше Ι-Ν-ацетилування сполук формули Ill-a-b, в якій R1, R2 є такими, що були визначені вище, може бути здійснене в стандартних умовах. У типовому випадку, сполуки формули Ill-a-b гріють під зворотним холодильником в оцтовому ангідриді і вводять у реакцію у розчиннику, наприклад, ДХМ, ТГФ, толуолі або піридині, ацетилхлориді, у присутності основи, наприклад, Ν,Ν-діізопропілетиламіну, триетиламіну або гідриду натрію, і одержують похідні 1-N-ацетил-4метил-1,2-дигідрохіноліну формули IV-a-b. Стандартне відщеплення захисної групи Вое в умовах, добре відомих фахівцям, дає похідні 6аміно-1,2-дигідрохіноліну формули V-a-b. Цю реакцію звичайно проводять у ДХМ у присутності трифлуороцтової кислоти. Подальше 6-N-ацилування сполук формули Va-b можна провести у стандартних умовах і отримати сполуки загальної формули Vl-a-b, в якій R 4 є такою, що була визначена вище. Наприклад, сполуки формули V-a-b вводять у реакцію у розчиннику, наприклад, ДХМ, ТГФ або толуолі, з ацилгалогенідом (R4-C(O)-CI) або кислотним ангідридом (R4-C(O)-O-C(O)-R4) у присутності основи, наприклад, Ν,Ν-діізопропілетиламіну, триети-ламіну, піридину або гідриду натрію, і отримують 6-Nацильовані похідні 4-метил-1 2-дигідрохіноліну формули Vl-a-b. В іншому варіанті ацилування сполук загальної формули V-a-b для отримання сполуки загальної формули Vl-a-b можна також здійснити реакцію з відповідною карбоновою кислотою (R4-CO2H) у присутності сполучаючого реагента, наприклад, тетрафлуорборату О(бензотриазол-1-іл)-N,N,N',N'-тетраметилуронію (ТФТМ), гексафлуорфосфату O-(7азабензотриазол-1-іл)-N,N,N',N'-тетраметилуронію (ГФТМ) або гексафлуорфосфату бромтрипіролідинфосфонію (ГФФБПФ) і третинної основи, наприклад, Ν,Ν-діізопропілетиламіну, у розчиннику, наприклад, Ν,Ν-ДМФ або ДХМ при кімнатній або підвищеній температурі. Введення необхідної заміщеної фенільної групи у позиції 4 каркасу гідрохіноліну можна здійснити алкілуванням Фриделя-Крафта анізолу сполуки загальної структури Vl-a-b Для одержання сполуки загальної формули Vll-a-b. Цю реакцію звичайно проводять при підвищеній температурі в анізолі або у придатному інертному розчиннику, наприклад, гептані або гексані, з анізолом як реагентом і з каталізом кислотою Льюїса (наприклад, АІСІз, АІВrз, FeCI3 або SnCI4). Опис алкілування Фриделя-Крафта 2,2,4-триметил-1,2-дигідрохіноліном можна знайти [у літературі: В.А. Lugovik, L.G. Yudin and A.N. Kost Dokl Akad. Nauk SSSR, 170: 340, 1966; B.A. Lugovik, L.G. Yudin, S.M. Vinogradova and A. N. Kost, Khim. Geterosikl. Soedin, 7: 795, 1971]. В іншому варіанті N-Boc-1,4-фенілендіамін II можна ввести в реакцію з 2-(4метоксифеніл)пропеном і формальдегідом в ацетонітрилі при зовнішній або підвищеній температурі, з подальшим 1-Ν-ацетилуванням, описаним вище, з отриманням сполуки Vll-b, в якій R4=Отрет-Bu. Відповідну циклізацію [описано у літературі: J.M. Mellor and R. D. Merriman, Tetrahedron, 51 :6115, 1995], відщеплення захисної групи Вос і 11 80303 подальше ацилування 6-амінофункціє ацилгалогенідом (R4-C(O)-CI), як описано вище, дає сполуку загальної структури VH-b, де R4 є такою, що описана вище. Відщеплення ароматичного метилового етеру у сполуках загальної формули VH-a-b дає 4-(4гідроксифеніл)-заміщені похідні тетрагідрохіноліну загальної формули VITI-a-b, утворюючи етап для функціоналізації вільної групи ОН. Реакції деметилування ароматичних метилових етерів є добре відомими. У типових випадках деметилування проводять, вводячи в реакцію сполуки формули VH-a-b з ВВr3 в інертному розчиннику, наприклад, ДХМ, при температурах від низької до зовнішньої, і отримують деметиловані сполуки загальної формули VHI-a-b. В іншому варіанті, деметилування здійснюється реакцією сполук формули VH-a-b з комплексом BF3Me2S при зовнішній температурі. Селективне О-алкілування сполук загальної формули VHI-a-b функціалізованими алкілгалогенідами загальної формули ІХ-а, призводить до утворення сполук загальної формули l-a-b. Реакції алкілування ароматичних гідроксигруп є добре відомими. Звичайно розчин сполуки загальної формули VllI-a-b у придатному розчиннику, наприклад, 1,4-діоксані, ТГФ, ДХМ, ацетонітрилі, ацетоні або Ν,Ν-ДМФ, обробляють основою (наприклад, Ν,Ν-діізопропіламіном, триетиламіном, K2СО3, Cs 2CO3 або NaOH) і відповідним алкілувальним реагентом загальної формули ІХ-а, наприклад, бензилбромідом, 3-(диметиламіно)пропілхлоридом, 4-(2-хлоретил)-морфоліном, 2піколілхлоридом або 2-хлорацетамідом. В іншому варіанті алкілування проводять як відоме алкілування Міцуно-бу. У цьому випадку розчин сполуки загальної формули Vlll-a-b у придатному розчиннику, наприклад, 1,4-діоксані, ТГФ або ДХМ, обробляють (зв'язаним смолою) трифенілфосфітом, діетил- або ди-трет-бутилазодикарбоксилатом і функціоналізованим спиртом загальної формули IX-b. У принципі обидва способи алкілування можна застосовувати для всіх груп R3, але може вини 12 кнути необхідність у застосуванні придатних захисних гр уп, якщо R3 містить нуклеофільну гр упу, наприклад, вторинний амін або гідроксигрупу. Вибір захисної групи і зняття захисту є тривіальними для фахівця. Інші процедури отримання сполук винаходу починаються з алкілування сполук загальної формули Vlll-a-b естерами загальної формули X. Реакцію алкілування звичайно проводіть у присутності основи, наприклад, Ν,Νдіізопропілетиламіну або гідриду натрію у придатному розчиннику, наприклад, Ν,Ν-ДМФ або ТГФ при зовнішній або підвищеній температурі. Естерну функцію в отриманій сполуці загальної формули Xl-a-b, де А=Me або Et, можна потім селективно відновити у контрольованих умовах для отримання сполук загальної формули ХІІІ-а-b, використовуючи відповідний відновлювальний агент, наприклад, алюмогідрид літію при низькій температурі або боргідрид натрію в інертному розчиннику, наприклад, ТГФ. Далі вільну гідроксигрупу у сполуках загальної формули Xlll-a-b можна ввести в реакцію з 4-толуолсульфонілхлоридом (Ts-CI) або метансульфонілхлоридом (Ms-CI) в інертному розчиннику, наприклад, 1,4-діоксані, Ν,Ν-ДМФ, ТГФ, у присутності придатної основи, наприклад, триетиламіну або піридину, для формування відповідної відщеплювальної групи (сполуки загальної формули XIV-a-b; LG=Ts або Ms, відповідно). Нуклеофільне заміщення належним нуклеофілом (аміном або алкоксидом) у відомих умовах дає сполуки загальної формули l-a-b, де R3=R3-(2-4C)алкіл і R5 є такою, що була визначена вище. Перетворення сполук загальної формули Xl-ab, в яких А=трет-Bn у карбонові кислоти загальної формули Xll-a-b можна здійснити зняттям захисту з трет-бутил-естерової функції. У звичайних випадках трет-бутиловий естер загальної формули Xla-b (А=трет -Bu) розчиняють у ДХМ і обробляють сильною кислотою, наприклад, трифлуороцтовою. Одержані карбонові кислоти загальної формули Xll-a-b можна потім конденсувати відповідним спиртом або аміном у присутності сполучаючого агента, наприклад, тетрафлуорборату О(бензотриазол-1-іл)-N,N,N',N'-тетраметилуронію (ТФТМ), гексафлуорофосфату О-(7азабензотриазол-1-іл)-N,N,N',N'-тетраметилуронію (ГФТМ) або гексафлуорфосфату бромтрипіролідин-фосфонію (ГФФБПФ) і третинної основи, наприклад, Ν,Ν-діізопропілетиламіну, у розчиннику, наприклад, Ν,Ν-ДМФ або ДХМ при зовнішній або підвищеній температурі з отриманням сполук загальної формули l-a-b, в яких R3=R5-карбоніл(14С)алкіл і R5 є такою, що визначена вище. 13 80303 Деякі сполуки винаходу, які можуть мати форму вільної основи, можна полювати з реакційної суміші у формі фармацевтично прийнятої солі. Такі солі можно також отримати, оброблчючи вільну основу формули І органічною або неорганічною кислотою, наприклад, гідрохлоридною, гідробромідною, гідройодидною, сульфуровою, фосфорною, оцтовою, пропіоновою, гліколевою, малеїновою, малоновою, метансульфоновою, фумаролою, бурштиновою, винною, лимонною, бензойноюі аскорбіновою. Сполуки винаходу містять щонайменше один хоральний атом карбону і тому можуть бути отримані як чисті енантіомери або суміш енантіомерів, або як суміш діастереомерів. Спосіби отримання чистих енантіомерів є добре відомими, наприклад, кристалізація солей, отриманих з оптично чистих кислот і рацемічної суміші або хроматографією з застосуванням хіральних колонок. Для діастереомерів можуть бути використання прямо-фазні або зворотнофазні колонки. Сполуки винаходу можуть утворювати гідрати або сольвати. Відомо, що заряджені сполуки утворюють гідрати, здатні до ліофілізації водою, або утворюють сольватовані форми при концентрації у розчині з належним органічним розчинником. Сполуки згідно з винаходом включають гідрати або сольвати перелічених сполук. Для селекції активних сполук випробування при 10-5М має показати активність, на 20% вищу за максимальну активність FSH як еталона. Іншим критерієм може бути значення IK50, яке має бути менше 10-5М, бажано, менше 10-7М. Фахівцю зрозуміло, що бажані значення IK50 залежать від сполуки, що проходить тестування. Наприклад, сполука з IK50 менше 10-5М взагалі розглядається як кандидат для вибору як ліки. Бажано, щоб це значення було менше 10-7М. Однак, сполука з вищим IK50, але селективна до конкретного рецептора, може бути кращим кандидатом. 14 Методи визначення зв'язування рецептора, а також аналізів in vitro і in vi vo для визначення біологічної активності гонадотропінів є добре відомими. Взагалі експресований рецептор контактує з сполукою, що випробується, і зв'язування або стимуляція або інгібування функціональної реакції виміряється. Для вимірювання функціональної реакції ізольовану ДНК, що кодує ген рецептора FSH, бажано, людського, експресують у придатній хазяйській клітині. Такою клітиною може бути клітина яєчника китайського хом'яка, але придатними є і інші клітини. Бажано, щоб клітини були від ссавця [Jia et al., MoLEndocrin., 5: 759-776, 1991]. Способи конструювання ліній клітин, що експресують рекомбінантний FSH є добре відомими [Sambrook et al., Molecular Cloning: Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, latest edition]. Експресії рецептора досягають експресуванням ДНК, що кодує бажаний протеїн. Техніка спрямованого на сайт мутагенезу, лігування додаткових послідовностей, PCR і конструювання придатної системи експресії є відомими. Частини або ціла ДНК, що кодують бажаний протеїн, можуть бути сконструйовані синтетично, з використанням стандартної твердофазної техніки, бажано, з включенням рестрикційних сайтів для полегшення лігування. До кодуючої ДНК можуть бути додані належні контрольні елементи для транскрипції і трансляції включеної кодової послідовності. Як відомо, існують системи експресії, сумісні з різноманітними хазяями, включаючи прокаріоти, наприклад, бактерії, і еукаріоти, наприклад, дріжджі, клітини рослин, комах, птахів тощо. Клітини, що експресують рецептор, вводять у контакт з сполукою, що випробується, для спостереження зв'язування або стимуляції, або інгібування функціональної реакції. В іншому варіанті для вимірювання зв'язування сполукою можуть бути використані ізольовані мембрани клітин, що містять експресований рецептор. Для вимірювання зв'язування можуть бути використані радіоактивно або флюоресцентно мічені сполуки. Можна також провести конкурентний аналіз зв'язування. Інші аналізи включають скринінг для сполуки агоніста рецептора FSH через визначення стимуляції опосередкованої рецептором акумуляції сАМР. Такий метод включає експресування рецептора на поверхні хазяйської клітини і піддання клітини дії сполуки, що випробується. Після цього виміряють кількість сАМР. Рівень сАМР може бути знижений або підвищений залежно від інгібуючої або стимулюючої дії сполуки на рецептор. Скринінг для антагоністів рецептора FSH включає інкубацію клітин, що експресують рецептор FSH, при належних межах концентрації сполуки, що випробується, і при фіксованій субмаксимально ефективній концентрації FSH (тобто такої, що викликає приблизно 80% від максимальної стимуляції накопичення сАМР за відсутності сполуки, що випробується). З кривих залежності ефективності від концентрації для кожної сполуки, що проходить випробування, можна визначити значення ІК50 і 15 80303 процент інгібування індукованого FSH накопичення сАМР. Як еталон можна використати рекомбінантний FSH людини. Іншим варіантом є конкурентний аналіз. На додаток до прямого вимірювання, наприклад, рівнів сАМР у експонованих клітинах, можна використати лінії клітин, які на додаток до трансфекції ДНК, що кодує рецептор, також трансфековані другою ДНК, що кодує ген рецептора, експресія якого реагує на рівень сАМР. Такі гени можуть бути сАМР-індуцібельними або можуть бути сконструйовані таким чином, що вони стануть новими приєднаними чутливими до сАМР елементами. Взагалі, експресія генів-репортерів можна контролювати будь-яким реактивним елементом, здатним реагувати на зміну рівнів сАМР. Придатними генами-репортерами є, наприклад, гени, що кодують Р-галактозидазу, лужну фосфатазу, сві тлякову люциферазу і протехін зеленої флюоресценції. Принципи такого трансактиваційного аналізу є добре відомими і [описані, наприклад, у Stratowa, С.Η., Himmler, А. і Czemilofsky, A.P., (1995) Curr.Opm-Biotechnol. 6: 574]. Винахід стосується також фармацевтичної композиції, яка включає похідну тетрагідрохіноліну або її фармацевтично прийнятні солі загальної формули І у суміші з фармацевтично прийнятними допоміжними компонентами і, як варіант, з іншими терапевтичними агентами. Допоміжні компоненти мають бути "прийнятними", тобто сумісними з іншими інгредієнтами композиції, і нешкідливими для реципієнтів. Композиції включають такі, що є придатними для орального, під'язичного, підшкірного, внутрішньовенного, внутрішньом'язового, локального або ректального введення пацієнту тощо, всі в одиничних дозованих формах. Для орального введення активний інгредієнт може бути репрезентований дискретними одиницями, наприклад, таблетками, капсулами, порошками, гранулами, розчинами, суспензіями тощо. Для парентерального введення фармацевтична композиція згідно з винаходом може бути презентована в одиничних дозах або у багатодозових контейнерах, наприклад, рідини для ін'єкцій у заздалегідь визначеній кількості, наприклад, у герметичних флаконах і ампулах, і можуть також зберігатись висушеними замороженням (ліофілізованими), потребуючи лише додання стерильного рідкого носія, наприклад, води, перед використанням. У суміші з такими фармацевтично прийнятними допоміжними компонентами, наприклад, як це [описано у стандартному посібнику Gennaro, A.R. et al., Remington: The Science and Practice of Pharmacy (20th Edition., Lippincott Williams & Wilkins, 2000, Part 5: Pharmaceutical Manufacturing)], активний агент може бути спресований у тверді дозовані одиниці, наприклад, пігулки, таблетки, або введений в капсули або супозиторії. З фармацевтично прийнятними рідинами активний агент може бути застосований як рідка композиція, наприклад, як рецептура для ін'єкцій у формі розчин, суспензії, емульсії або уприскування, наприклад, носового. 16 Для виготовлення твердих дозованих одиниць можуть бути використані звичайні добавки, наприклад, наповнювачі, забарвлювачі, полімерні зв'язуючі агенти тощо. Взагалі може бути використана будь-яка фармацевтично прийнятна добавка, яка не порушує функцій активної сполуки. Придатними носіями, з якими активний агент згідно з винаходом може бути введений як тверда композиція лактоза, крохмаль, похідні целюлози тощо, або їх суміші у належних кількостях. Для парентерального введення можуть бути використані водні суспензії, ізотонічні сольові розчини і стерильні розчини для ін'єкцій, які містять фармацевтично прийнятні диспергуючі агенти і/або зволожуючі агенти, наприклад, пропіленгліколь або бутиленгліколь. Винахід також включає описану вище фармацевтичну композицію у комбінації з пакувальним засобом, придатним для цієї композиції, і з інструкцією з використання композиції. Похідні тетрагідрохіноліну згідно з винаходом можна вводити також у формі фармацевтичних засобів, призначених для імплантації, які складаються з серцевини з активних матеріалів у мембрані, здатній регулювати вивільнення. Такі імплантати застосовують підшкірно або локально, і вони вивільняють активний інгредієнт з приблизно постійною швидкістю протягом тривалого часу, наприклад, тижнями і навіть роками. Способи приготування фармацевтичних засобів, призначених для імплантації, є відомими [див., наприклад, Європейський патенті 0 303 306 (AKZO Nobel N.V.)]. Точна доза і режим введення активного інгредієнта або фармацевтичної композиції залежать від бажаної терапевтичної дії (лікування неплідності, контрацепція) і можуть бути різними для різних сполук, способів введення, віку і стану пацієнта, якому вводять медикамент. Взагалі парентеральне введення потребує менших доз, ніж інші способи введення, більш залежні від абсорбції. Бажана доза для людини становить 0,0001-25мг на кг маси тіла. Бажана доза може бути одиничною або розділена на декілька субдоз, які вводять з належними інтервалами протягом дня, або для пацієнтів-жінок - з денними інтервалами протягом менструального циклу. Дозування і режим введення можуть бути різними для чоловіків і жінок. Отже, сполуки згідно з винаходом можуть бути використані у терапії. Ще одним аспектом винаходу є використання похідної тетрагідрохіноліну загальної формули І для виготовлення медикаменту, призначеного для використання у лікуванні розладів, залежних від шляхів опосередкування рецептором FSH. Пацієнту, що потребує лікування, може бути введена належна кількість сполуки згідно з винаходом. Іншим аспектом винаходу є використання похідної тетрагідрохіноліну загальної формули І для виготовлення медикаменту, призначеного для контролю плідності. Ще одним аспектом винаходу є використання похідної тетрагідрохіноліну загальної формули І 17 80303 для виготовлення медикаменту, призначеного для використання у лікуванні неплідності. Іншим аспектом винаходу є використання похідної тетрагідрохіноліну загальної формули І для виготовлення медикаменту, призначеного для запобігання плідності. Сполуки згідно з винаходом можуть бути також використані для лікування гормоно-залежних розладів, наприклад, раку грудей, раку простати і ендометріозу. Винахід ілюструється наведеними далі прикладами. Приклади Загальні зауваження У прикладах використані такі абревіатури: ДМА= Ν,Ν-диметиланілін, ДІПЕА= Ν,Νдіізопропілетиламін; ТФК= трифлуороцтова кислота, ДтБАК - ди-трет-бутил-азодикарбоксилат; ТФТМ= те трафлуорборат О-бензотриазол-1-ілΝ,Ν,Ν',Ν'-тетраметилуронію; ГФТМ= гексафлуорфосфа т О-(7-азабензотриазол-1-іл)-Ν,Ν,Ν',Ν'тетраметилуронію; Fmoc= 9флуоренілоксикарбоніл; Fmoc-CI= 9флуоренілметоксикарбонілхлорид; ДМФ= Ν,Νдиметилформамід; Вос= трет-бутоксикарбоніл; ТГФ= тетрагідрофуран. Найменування кінцевих продуктів у прикладах побудовані з використанням ВеіІ-stein Autonom program (version: 2,02,119). Якщо не визначено інше, всі кінцеві продукти прикладів ліофілізовані з сумішей вода/1,4-діоксан або вода/ацетонітрил. Якщо сполука є сіллю НСІ або ТФК, відповідні кислоти були додані у належній кількості до розчинника перед ліофілізацією. Для визначення часу утримання використано такі аналітичні методи РХВР (рідинна хроматографія високого розрізнення): Метод 1: Колонка: 5мкм Luna C-18(2) 150´4,6мм; потік: 1мл/хвил.; виявлення: 210нм; темп, колонки 40°С: розчинник A: CH3CN/H2O=1/9 (об'єм/об'єм); розчинник В: CH3CN; розчинник С: 0,1Μ водний розчин трифлуороцтової кислот; градієнт: розчинник А/В/С= від 65/30/5 до 10/85/5 (об'єм/об'єм/об'єм) 30,00хвил., потім постійно протягом ще 10,00хвил. при А/В/С=10/85/5 (об'єм/об'єм/об'єм). Метод 2: ідентичний методу 1, за винятком градієнта. Градієнт: розчинник А/В/С= від 75/20/5 до 15/80/5 (об'єм/об'єм/об'єм) 30,00хвил., потім постійно протягом ще 10,00хвил. при А/В/С= 15/80/5 (об'єм/об'єм/об'єм). Метод 3: Колонка: 3мкм Luna C-18(2) 100´2мм; потік: 0,25мл/хвил.; виявлення: 210нм; темп, колонка: 40°С; розчинник А: Н2О; розчинник В: CH3CN; розчинник С: 50мм фосфатний буфер, рН2,1; градієнт: розчинник А/В/С= від 70/20/10 до 10/80/10 (об'єм/об'єм/об'єм) 20,00хвил., потім постійно протягом ще 10,00хвил. при А/В/С= 10/80/10 (об'єм/об'єм/об'єм). Метод 4: ідентичний методу 3, за винятком градієнта; градієнт: розчинник А/В/С= від 65/30/5 до 10/85/5 (об'єм/об'єм/об'єм) 20,00хвил., потім постійно протягом ще 10,00хвил. при А/В/С= 10/85/5 (об'єм/об'єм/об'єм). 18 Метод 5: ідентичний методу 3, за винятком градієнта; градієнт: розчинник А/В= від 75/25 до 0/100 (об'єм/об'єм) 20,00хвил., потім постійно протягом ще 10,00хвил. при А/В/С= 0/100 (об'єм/об'єм). Метод 6: ідентичний методу 1, за винятком градієнта; градієнт: розчинник А/В/С= від 35/60/5 до 10/85/5 (об'єм/об'єм/об'єм) 30,00хвил., потім постійно протягом ще 10,00хвил. при А/В/С= 10/85/5 (об'єм/об'єм/об'єм). Для очищення застосовуються такі методи очищення препаративною РХВР: Метод А: Колонка = Luna C-18. Градієнт: 0,1%на трифлуороцтова кислота у H2 O/CH3CN (9/1, об'єм/об'єм)/CH3CN= від 100/0 до 0/100 (об'єм/об'єм) 30-45хвил., залежно від легкості сепарації. Виявлення: 210нм. Фракції збирають і концентрують (частково) in vacuo. Метод В: Колонка= Luna C-18. Градієнт: H2O/CH3CN (9/1, об'єм/об'єм)/СН3СN= від 80/20 до 0/100 (об'єм/об'єм) 30-45хвил., залежно від легкості сепарації. Виявлення: 210нм. Приклад 1 {1-ацетил-4-[4-(2-диметиламіноетокси)-Феніл]2,2,4-триметил-1,2.3.4-тетрагідрохінолін-6-іл}-амід біфеніл-4-карбонової кислоти (a) Трет-бутиловий естер(2.2.4-триметил-1,2дигідрохінолін-6-іл)-карбамової кислоти Суміш N-Boc-1,4-фенілендіаміну (75г), MgSO 4 (216г), 4-трет-бутилкатехолу (1,8г) і йоду (4,7г) у безводному ацетоні (600мл) гріють під зворотним холодильником 20год. MgSO4 видаляють фільтруванням і фільтрат концентрують in vacuo. Залишок хроматографують на короткій пробці силікагелю з елюентом гептан/етилацетат= 8/2 (об'єм/об'єм) і отримують продукт у вигляді коричневого масла. Вихід: 41г. (b) Трет-бутиловий естер (1-ацетил-2,2,4триметил-1,2-(дигідрохінолін-6-іл)карбамової кислоти Розчин сполуки Прикладу 1а (41г) у піридині (200мл) і СН 2СІ2 (200мл) охолоджують до 0°С. Краплями додають ацетилхлорид (21мл) у СН 2СІ2 (50мл). Після повного додання суміш перемішують 3год. при кімнатній температурі. Додають етилацетат (2л) і Н2О (2л) органічний шар відокремлюють, суша ть і концентрують in vacuo. Бажану сполуку отримують кристалізацією з етилацетату. Вихід: 23г. (c) 1-ацетил-6-аміно-2,2,4-триметил-1,2дигідрохінолін Сполуку Прикладу 1b (15г) перемішують у суміші СН2СІ2 і ТФК (9/1 (об'єм/об'єм), 300мл) 2год. Реакційну суміш охолоджують до 0°С, і рН коригують до 7 водним 2М розчином NaOH. Органічний шар відокремлюють, промивають розсолом, сушать і концентрують in vacuo і отримують сирий продукт, який використовують у наступній операції без очищення. Вихід: 10,4г (d) (1-ацетил-2,2,4-триметил-1,2дигідрохінолін-6-іл)-амідбіфеніл-4-карбонової кислоти До розчину сполуки Прикладу 1с (10г) і ДІПЕА (40мл) у СН 2СІ2 (100мл), додають 4 19 80303 біфенілкарбонілхлорид (9,8г) і отриману суміш перемішують 18год. при кімнатній температурі. Додають воду, органічний шар відокремлюють, сушать і концентрують in vacuo. Продукт кристалізують з етилацетату. Вихід: 15г (е) [1-ацетил-4-(4-метоксифеніл)-2,2,4триметил-1,2,3,4-дигідрохінолін-6-іл]-амід-біфеніл4-карбонової кислоти До суміші сполуки Прикладу 1d (10,0г) і безводного анізолу (50мл) з перемішуванням додають трихлорид алюмінію (9,7г) і суміш перемішують при 35°С 18 год. Потім додають воду при 0°С і суміш екстрагують етилацетатом. Органічний шар відокремлюють, сушать і частково концентрують in vacuo і суміш витримують при 0°С 18год. Осад збирають фільтруванням і сушать in vacuo, отримуючи бажану сполуку. Вихід: 7,9г. (f) [1-ацетил-4-(4-гідроксифеніл)-2,2,4триметил-1,2,3,4-дигідрохінолін-6-іл]-амід біфеніл4-карбонової кислоти До розчину сполуки Прикладу 1е (7,9г) у СН2СІ2 (200мл) при 0°С додають розчин бортриброміду (5мл) у СН2СІ2 (50мл) і витримують 4год. при 0°С. Обережно додають воду (прибл. 500мл) і суміш енергійно перемішують. Органічний шар відокремлюють, сушать і концентрують in vacuo. Кристалізація з етилацетату дає бажану сполуку. Вихід: 6,1г. (r) {1-ацетил-4-[4-(2-диметиламіноетокси)феніл]-2,2,4-триметил-1,2,3,4-тетрагідрохінолін-6іл}-амід біфеніл-4-карбонової кислоти Загальна процедура А: До розчину сполуки Прикладу 1f (70мг) у ДМФ (2мл) додають Cs 2CO3 (200мг) і гідрохлорид 2-диметиламінетилхлориду (17мг). Суміш перемішують протягом ночі, після чого додають воду і етилацетат. Органічний шар відокремлюють, сушать і концентрують in vacuo. Продукт очищають препаративною РХВР (метод А) і ліофілізують з суміші CH3CN і води з ТФК, одержуючи відповідну сіль ТФК. Вихід: 18мг (сіль ТФК); MS-ESI: [М+Н]+=576,6; РХВР: Rt=14,96хвил. (метод 3). Приклад 2 {1-ацетил-4-[4-(2-диметиламінопропокси)феніл]-2,2,4-триметил-1,2,3,4-тетрагідрохінолін-6іл}-амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою А, сполук у Прикладу 1f (70мг) алкілують гідрохлоридом 3диметиламінопропілхлориду (19мг) і Cs 2CO3 (200мг) у ДМФ (2мл). Продукт очищають препаративною РХВР (метод А) і ліофілізують з суміші CH3CN і водовмісної ТФК, отримуючи відповідну сіль ТФК. Вихід: 58мг (сіль ТФК); MS-ESI: [М+Н]+=590,4; РХВР: Rt=15,36хвил. (метод 3). Приклад 3 {1-ацетил-2,2,4-триметил-4-('4-(3-морфолін-4іл-пропокси)-феніл]-1,2,3,4-тетрагідрохінолін-6-іл}амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою А, сполук у Прикладу 1f (70мг) алкілують 3морфолінопропілхлоридом (26мг) і Cs 2CO3 (200мг) у ДМФ (2мл). Продукт очищають препаративною 20 РХВР (метод А) і ліофілізують з суміші CH3CN і водовмісної ТФК, отримуючи відповідну сіль ТФК. Вихід: 56мг (сіль ТФК); MS-ESI: [М+Н]+=631,6; РХВР: Rt=15,40хвил. (метод 3). Приклад 4 {1-ацетил-2,2,4-триметил-4-[4-піридин-2ілметокси)-феніл]-1,2,3,4-тетрагідрохінолін-6-іл}амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою А, сполук у Прикладу 1f (100мг) алкілують 2піколілхлоридгідрохлоридом (33мг) і Cs 2CO3 (325мг) у ДМФ (5мл). Продукт очищають препаративною РХВР (метод А) і ліофілізують з суміші CH3CN і водовмісної ТФК, отримуючи відповідну сіль ТФК Вихід: 60мг (сіль ТФК); MS-ESI: [М+Н]+=596,4; РХВР: Rt=19,75хвил. (метод 2). Приклад 5 {1-ацетил-2,2,4-триметил-4-[4-(1метилпіперидин-3-ілметокси)-феніл]-1,2,3,4тетрагідрохінолін-6-іл}-амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою А, сполук у Прикладу 1f (100мг) алкілують гідрохлоридом 3хлорметилметилпіперидину (33мг) і Cs 2CO3 (325мг) у ДМФ (5мл). Продукт очищають препаративною РХВР (метод А) і ліофілізують з суміші CH3CN і водовмісної ТФК, отримуючи відповідну сіль ТФК. Вихід: 60мг (сіль ТФК); MS-ESI: [М+Н]+=615,4; РХВР: Rt=16,70хвил. (метод 2). Приклад 6 {1-ацетил-4-[4-(2-діетиламіноетокси)-феніл]2,2,4-триметил-1,2,3,4-тетрагідрохінолін-6-іл}-амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою А, сполук у Прикладу 1f (100мг) алкілують 2-гідрохлоридом діетиламіноетилхлоридом (35мг) і Cs 2CO3 (325мг) у ДМФ (5мл). Продукт очищають препаративною РХВР (метод А) і ліофілізують з суміші CH3CN і водовмісної ТФК, отримуючи відповідну сіль ТФК. Вихід: 67мг (сіль ТФК); MS-ESI: [М-Н]+=604,4; РХВР: Rt=16,38хвил. (метод 2). Приклад 7 {1-ацетил-2,2,4-триметил-4-[4-(піридин-4ілметокси)-феніл]-1,2,3,4-тетрагідрохінолін-6-іл}амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою А, сполук у Прикладу 1f (100мг) алкілують 4піколілхлоридгідрохлоридом (33мг) і Cs 2CO3 (325мг) у ДМФ (5мл). Продукт очищають препаративною РХВР (метод А) і ліофілізують з суміші CH3CN і водовмісної ТФК, отримуючи відповідну сіль ТФК. Вихід: 61мг (сіль ТФК); MS-ESI: [М+Н]+=596,4; РХВР: Rt=16,64хвил. (метод 2). Приклад 8 [3-(4-{1-ацетил-6-[(біфеніл-4-карбоніл)-аміно]2,2,4-триметил-1,2,3.4-тетрагідрохінолін-4-іл}фенокси)-пропіл]-амід морфолін-4-карбонової кислоти Згідно з загальною процедурою А, сполук у Прикладу 1f (100мг) алкілують (3хлорпропіл)амідом морфолін-4-карбонової кислоти (53мг) і Cs 2CO3 (325мг) у ДМФ (5мл). Продукт 21 80303 очищають препаративною РХВР (метод А) і ліофілізують з суміші CH3CN і води. Вихід: 95мг; MS-ESI: [М+Н]+=675,6; РХВР: Rt=18,24хвил. (метод 3). Приклад 9 {1-ацетил-4-[4-(2-азепан-1-ілетокси)-феніл2,2,4-триметил-1,2,3,4-тетрагідрохінолін-6-іл}-амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою А, сполук у Прикладу 1f (100мг) алкілують гідрохлоридом 2(гексаметиленіміно)етилхлориду (42мг) Cs 2CO3 (325мг) у ДМФ (5мл). Продукт очищають препаративною РХВР (метод А) і ліофілізують з суміші CH3CN і водовмісної ТФК, отримуючи відповідну сіль ТФК. Вихід: 60мг (сіль ТФК); MS-ESI: [М+Н]+=630,6; РХВР: Rt=17,25хвил. (метод 2). Приклад 10 {1-ацетил-2,2,4-триметил-4-[4-піридин-3ілметокси)-феніл]-1,2,3,4-тетрагідрохінолін-6-іл}амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою А, сполук у Прикладу 1f (1,0г) алкілують гідрохлоридом 3піколоїлхлориду (488мг) і Cs 2CO3 (3,2мг) у ДМФ (10мл). Продукт очищають препаративною РХВР (метод А) і ліофілізують з суміші CH3CN і водовмісної ТФК, отримуючи відповідну сіль ТФК. Вихід: 884мг (сіль ТФК); MS-ESI: [М+Н]+=596,4; РХВР: Rt=16,55хвил. (метод 3). Приклад 11 біфеніл-4-карбонової кислоти [1-ацетил-4-(4карбамоїлметоксифеніл)-2,2,4-триметил-1,2,3,4тетрагідрохінолін-6-іл1-амід Згідно з загальною процедурою А, сполук у Прикладу 1f (100мг) алкілують 2-хлорацетамідом (24мг) і Cs 2CO3 (325мг) у ДМФ (5мл). Продукт очищають препаративною РХВР (метод А) і ліофілізують з суміші CH3CN і водовмісної ТФК, отримуючи відповідну сіль ТФК. Вихід: 40мг; MS-ESI: [M+H]+=562,6; РХВР: Rt=21,63хвил. (метод 2). Приклад 12 [1-ацетил-4-(4-алілкарбамоїлметоксифеніл)2,2,4-триметил-1,2,3,4-тетрагідрохінолін-6-іл}-амід біфеніл-4-карбонової кислоти (а) трет-бутиловий естер (4-{1-ацетил-6[триФеніл-4-карбоніл)аміно]-2,2,4-триметил1,2,3,4-тетрагідрохінолін-4-іл}фенокси)-оцтової кислоти Суміш сполуки Прикладу 1f (2,58г), третбутилбромацетату (826мкл), K2СО3 (2,8г) і ацетону (100мл) перемішують 18год. при 50°С. Тверду речовину видаляють фільтр уванням і фільтрат концентрують in vacuo і отримують продукт, який без очищення використовують у наступній операції. Вихід: 3,2г. (b) [4-{1-ацетил-6-[(Феніл-4-карбоніл)аміно]2,2,4-триметил-1,2,3,4-тетрагідро-хінолін-4іл}фенокси)оцтова кислота Сполуку Прикладу 12а (3,2г) перемішують у суміші СН2СІ2 і ТФК (9/1 (об'єм/об'єм), 100мл) 3год. Додають толуол (100мл) і суміш концентрують in vacuo, отримуючи сирий продукт, який використовують без очищення. Вихід: 3,3г. 22 (c) [1-ацетил-4-(4алілкарбамоїлметоксифеніл)-2,2,4-триметил1,2,3,4-тетрагідрохінолін-6-іл]-амід біфеніл-4карбонової кислоти Загальна процедура В: До розчину сполуки Прикладу 12b (82мг), аліламіну (37мг) і ДІПЕА (226мкл) у СН 2СІ2 (5мл) додають ТФТМ (84мг) при кімнатній температурі. Якщо реакція не завершується через 18 год., додають ще ТФТМ і ДІПЕА. Після завершення реакції додають воду, органічний шар відокремлюють, промивають розсолом, сушать і концентрують in vacuo. Бажану сполуку очищають, препаративною РХВР (метод А). Вихід: 48мг; MS-ESI: [M+H]+=602,4; РХВР: Rt=18,19хвил. (метод 4). Приклад 13 {1-ацетил-4-[4-(ізопропілкарбамоїлметокси)феніл]-2,2,4-триметил-1,2,3,4-тетрагідрохінолін-6іл}-амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою В, сполуку Прикладу 12b (82мг) обробляють ізопропіламіном (38мг), ДІПЕА (226мкл) і ТФТМ (84мг) у СН 2СІ2 (5мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 45мг; MS-ESI: (М+Н]+=604,6; РХВР: Rt=18,63хвил. (метод 4). Приклад 14 1-ацетил-4-(4-діетилкарбамоїлметокси)фенілъ-2,2,4-триметил-1,2,3,4-тетрагідрохінолін-6іл}-амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою В, сполуку Прикладу 12b (82мг) обробляють діетиламінгідрохлоридом (47мг), ДІПЕА (226мкл) і ТФТМ (84мг) у СН2СІ2 (5мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 51мг; MS-ESI: [M+H]+=618,4: РХВР: Rt=19,09хвил. (метод 4). Приклад 15 [1-ацетил-2,2,4-триметил-4-(4{[(піридин-4ілметил)-карбамоїл]-метокси}-феніл)-1,2,3,4тетрагідрохінолін-6-іл]-амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою В, сполуку Прикладу 12b (82мг) обробляють 4-піколіламіном (70мг), ДІПЕА (226мкл) і ТФТМ (84мг) у СН 2СІ2 (5мл). Бажану сполуку очищають препаративною РХВР (метод А) і ліофілізують з суміші CH3CN і водовмісної ТФК, отримуючи відповідну сіль ТФК. Вихід: 52мг (сіль ТФК); MS-ESI: [М+Н]+=653,6; РХВР: Rt=11,31хвил. (метод 4). Приклад 16 [1-ацетил-4-(4-{[(фуран-2-ілметил)-карбамоїл]метекси}-феніл)-2,2,4-триметил-1,2,3,4тетрагідрохінолін-6-іл]-амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою В, сполуку Прикладу 12b (82мг) обробляють 2фурфуриламіном (63мг), ДІПЕА (226мкл) і ТФТМ (84мг) у СН2СІ2 (5мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 50мг; MS-ESI: [М+Н]+=642,6; РХВР: Rt=21,31хвил. (метод 3). Приклад 17 (1-ацетил-4-{4-[(2метоксиетилкарбамоїл)метокси]-феніл}-2,2,4 23 80303 триметил-1,2,3,4-тетрагідрохінолін-6-іл)-амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою В, сполуку Прикладу 12b (82мг) обробляють 2метоксиетиламіном (49мг), ДІПЕА (226мкл) і ТФТМ (84мг) у СН2СІ2 (5мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 34мг; MS-ESI: [М+Н]+=620,4; РХВР: Rt=19,70хвил. (метод 3). Приклад 18 {1-ацетил-4-[4-(бензилкарбамоїлметокси)феніл]-2,2,4-триметил-1,2,3,4-тетрагідрохінолін-6іл}-амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою В, сполуку Прикладу 12b (82мг) обробляють бензиламіном (49мг), ДІПЕА (226мкл) і ТФТМ (84мг) у СН 2СІ2 (5мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 53мг; MS-ESI: [М+Н]+=652,6; РХВР: Rt=22,26хвил. (метод 3). Приклад 19 (1-ацетил-4-{4-[(2диметиламіноетилкарбамоїл)-метокси]феніл}2,2,4-триметил-1,2,3,4-тетрагідрохінолін-6-іл)-амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою В, сполуку Прикладу 12b (82мг) обробляють Ν,Νдиметилетилендіаміном (49мг), ДІПЕА (226мкл) і ТФТМ (84мг) у СН2СІ2 (5мл). Бажану сполуку очищають препаративною РХВР (метод А). Ліофілізація з суміші водної НСІ і 1,4-діоксану дає бажану сполуку як сіль НСІ. Вихід: 11мг (HCI-salt); MS-ESI: [M+H]+=633,4; РХВР: Rt=13,74хвил. (метод 3). Приклад 20 [1-ацетил-2,2,4-триметил-4-(4метилкарбамоїлметоксифеніл)-1,2,3,4тетрагідрохінолін-6-іл]-амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою В, сполуку Прикладу 12b (82мг) обробляють метиламінгідрохлоридом (20мг), ДІПЕА (226мкл) і ТФТМ (84мг) in CH2CI2 (5мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 35мг; MS-ESI: [М+Н]+=576,4; РХВР: Rt=19,25хвил. (метод 3). Приклад 21 {1-ацетил-2,2,4-триметил-4[4-(2-морфолін-4-іл2-оксоетокси)-феніл]-1,2,3,4-тетрагідрохінолін-6іл}-амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою В, сполуку Прикладу 12b (110мг) обробляють морфоліном (74мг), ДІПЕА (296мкл) і ТФТМ (109мг) у СН 2СІ2 (5мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 85мг; MS-ESI: [М+Н]+=632,4; РХВР: Rt=12,48хвил. (метод 3). Приклад 22 N-{1-aцeтил-2,2,4-тpимeтил-4-[4-(3-мopфoлiн4-iл-пpoпoкcи)-фeнiл]-1,2,3,4-тетрагідрохінолін-6іл}-5-бром-2-метиламіно-бензамід (a) 9-Флуоренілметиловий естер (1-ацетил2,2,4-триметил-1,2-дигідрохінолін-6-іл)-карбамової кислоти 24 До розчину сполуки Прикладу 1с (17г) і ДІПЕА (40мл) у СН2СІ2 (100мл), додають FmocCI (25г) і суміш перемішують 18год. при кімнатній температурі. Додають етилацетат (прибл. 200мл) і воду (150мл), органічний шар відокремлюють, сушать і концентрують in vacuo. Бажану сполуку очищають хроматографією на силікагелі з елюентом СН 2СІ2. Вихід: 16,6г (b) 9-флуоренілметиловий естер [1-ацетил-4(4-метоксифеніл)-2,2,4-триметил-1,2,3,4тетрагідрохінолін-6-іл]-карбамової кислоти З перемішуванням трихлорид алюмінію (24,2г) додають до суміші сполуки Прикладу 22а (16,5г) і безводного анізолу (150мл) і суміш перемішують при 35°С 18 год. Після цього додають воду при 0°С і суміш екстрагують етилацетатом. Органічний шар відокремлюють, сушать і частково концентрують in vacuo і суміш витримують при 0°С 18год. Осад збирають фільтруванням і сушать in vacuo, отримуючи бажану сполуку. Вихід: 10,1г. (c) 9-флуоренілетиловий естер [1-ацетил-4-(4гідроксифеніл)-2,2,4-триметил-1,2,3,4тетрагідрохінолін-6-іл]-карбамової кислоти До суміші сполуки Прикладу 22b (10,1г) у безводному СН 2СІ2 (500мл) додають краплями бортрибромід (5,05мл) і суміш перемішують 2,5год. при кімнатній температурі. Реакцію гасять льодяною водою при 0°С і додають СН 2СІ2. Органічний шар відокремлюють, сушать і витримують при 4°С 20год. Утворену тверду речовину збирають фільтруванням і сушать in vacuo, отримуючи сирий продукт, який використовують без очищення. Вихід: 12,5г. (d) 1-ацетил-6-аміно-2,2,4-триметил-4-[4-(3морфолін-4-ілпропокси)-феніл]-1,2,3,4тетрагідрохінолін Суміш сполуки Прикладу 22с (1,0г), Cs 2CO3 (1,8г), 4-(3-хлорпропіл)морфолін (330мг) і ДМФ (5мл) перемішують при 60°С 18год. Додають воду ι суміш екстрагують СН2СІ2. Органічний шар сушать і концентрують in vacuo. Бажану сполуку очи щають хроматографією на силікагелі з елюентом СН2СІ2/2%-й амоній у МеОН=1/0=>9/1 (об'єм/об'єм). Вихід 527мг (e) Ν-{1-метил-2,2,4-триметил-4-[4-(3морфолін-4-ілпропокси)-феніл]-1,2,3,4тетрагідрохінолін-6-іл}-5-бром-2метиламінобензамід Загальна процедура С: До розчину сполуки Прикладу 22d (132мг), 5-бром-2метиламінобензойну кислоту (101мг) і ДІПЕА (255мкл) у СН 2СІ2 (3мл) додають ГФТМ (166мг) при кімнатній температурі. Реакційну суміш перемішують 18 год. при кімнатній температурі. Додають етилацетат (15мл) і 2М водний NaOH (15мл). Органічний шар відокремлюють і промивають 2М водним NaOH (10мл) і водою (15мл), сушать і концентрують in vacuo. Бажану сполуку очи щають препаративною РХВР (метод А). Вихід: 69,8мг; MS-ESI: [M+H]+=663,4; РХВР: Rt=14,65хвил. (метод 3). Приклад 23 25 80303 N-{1-aцeтил-2,2,4-тpимeтил-4-[4-(3-мopфoлiн4-iлпpoпoкcи)-фeнiл]-1,2,3,4-тетрагідрохінолін-6іл}-3,5-дихлор-2,6-диметоксибензамід Згідно з загальною процедурою С, сполуку Прикладу 22d (132мг) ацилують 3,5-дихлор-2,6диметоксибензойною кислотою (110мг), ДІПЕА (255мкл) і ГФТМ (166мг) у СН2СІ2 (3мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 68,3мг; MS-ESI: [М+Н]+=684,3; РХВР: Rt=13,45хвил. (метод 3). Приклад 24 [1-ацетил-4-(4-{2-[(фуран-2-ілметил)-аміно]етокси}-феніл)-2,2,4-триметил-1,2,3,4тетрагідрохінолін-6-іл]-амід біфеніл-4-карбонової кислоти (a) етиловий естер (4-{1-ацетил-6-[(біфеніл-4карбоніл)аміно]-2,2,4-триметил-1,2,3,4тетрагідрохінолін-4-іл}-фенокси)-оцтової кислоти Суміш сполуки Прикладу 1f (1г), етилбромацетату (220мкл), K2СО3 (850мг) і ацетону (25мл) перемішують 6год. при 50°С. Тверду речовину видаляють фільтруванням і фільтрат концентрують in vacua, отримуючи продукт, який використовують без очищення. Вихід: 1,2г (b) {1-ацетил-4-[4-(2-гідроксиетокси)феніл]2,2,4-триметил-1,2,3,4-тетрагідрохінолін-6-іл}-амід біфеніл-4-карбонової кислоти До розчину сполуки Прикладу 24а (1,2г) у ТГФ (10мл) при 0°С обережно додають UALH4 (78мг) і суміш перемішують 3год. при кімнатній температурі. Краплями додають етилацетат (50мл), потім воду (50мл). Водний шар відокремлюють і екстрагують етилацетатом (50мл). Об'єднані органічні фракції промивають розсолом, органічний шар сушать і концентрують in vacuo, одержуючи продукт, який використовують без очищення. Вихід: 1г. (c) 2-(4-{1-ацетил-6-[(біфеніл-4карбоніл)аміно]-2,2,4-триметил-1,2,3,4тетрагідрохінолін-4-іл}фенокси)етиловий естер метансульфонової кислоти До розчину сполуки Прикладу 24b (1г) і ДІПЕА (1,7мл) у СН2СІ2 (15мл), додають краплями розчин метансульфонілхлориду (310мкл) у СН2СІ2 (5мл). Через 2год., додають воду, органічний шар відокремлюють, сушать і концентрують in vacuo. Бажану сполукуочищають хроматографією на силікагелі з елюентом гептан/етилацетат=9/1=>1/1 (об'єм/об'єм). Вихід: 870мг. (d) біфеніл-4-карбонової кислоти [1-ацетил-4{4-(2-[(фуран-2-ілметил)-аміно]-етокси}-феніл)2,2,4-триметил-1,2,3,4-тетрагідрохінолін-6-іл]-амід Загальна процедура D: До розчину сполуки Прикладу 24с (87мг) у CH3CN (5мл) додають 2фурфуриламін (107мг) і суміш перемішують при 70°С 18год. Суміш концентрують in vacuo і продукт очищають препаративною РХВР (метод А) і ліофілізують з суміші CH3CN і водовмісної ТФК, отримуючи відповідну сіль ТФК. Вихід: 47мг (сіль ТФК); MS-ESI: [М+Н]+=628,6; РХВР: Rt=11,53хвил. (метод 4). Приклад 25 26 (1-ацетил-4-{4-[2-(2-гідрокси-1,1-диметилетиламіно)-етокси]-феніл}-2,2,4-триметил-1,2,3,4тетрагідрохінолін-6-іл)-амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою D, сполуку Прикладу 24с (87мг) обробляють 2-аміно-2метилпропан-1-олом (300мг) у CH3CN (5мл). Бажану сполуку очищають препаративною РХВР (метод А) і ліофілізують з суміші CH3CN і водовмісної ТФК, отримуючи відповідну сіль ТФК. Вихід: 21мг (сіль ТФК); MS-ESI:[M+H]+=619,8; РХВР: Rt=10,95хвил. (метод 4). Приклад 26 [1-ацетил-2,2,4-триметил-4-(4-{2-[(піридин-3ілметил)-аміно]-етокси}-феніл)-1,2,3,4тетраугідрохінолін-6-іл]-амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою D, сполуку Прикладу 24с (87мг) обробляють 3амінометилпіридином (119мг) у CH3CN (5мл). Бажану сполуку очищають препаративною РХВР (метод А) і ліофілізують з суміші CH3CN і водовмісної ТФК, отримуючи відповідну сіль ТФК. Вихід: 40мг (сіль ТФК); MS-ESI: [М+Н]+=639,4; РХВР: Rt=10,15хвил. (метод 4). Приклад 27 (1-ацетил-4{4-[2-(2-гідроксиетиламіно)-етокси]феніл}-2,2,4-триметил-1,2,3,4-тетрагідрохінолін-6іл)-амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою D, сполуку Прикладу 24с (100мг) обробляють ета-ноламіном (100мг) у CH3CN (5мл). Бажану сполуку очи щають препаративною РХВР (метод А) і ліофілізують з суміші CH3CN і водовмісної ТФК, отримуючи відповідну сіль ТФК Вихід: 50мг (сіль ТФК); MS-ESI: [М+Н]+=592,6; РХВР: Rt=10,32хвил. (метод 1). Приклад 28 (1-ацетил-4-{4-[2-(2-аміноетиламіно)-етокси]феніл}-2,2,4-триметил-1,2,3,4-тетрагідрохінолін-6іл)-амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою D, сполука Прикладу 24с {100мг) обробляють етилендіаміном (110мг) у CH3CN (5мл). Бажану сполуку очи щають препаративною РХВР (метод А) і ліофілізують з суміші CH3CN і водовмісної ТФК, отримуючи відповідну сіль ТФК Вихід: 45мг (сіль ТФК); MS-ESI: [М+Н]+=591,4; РХВР: Rt=7,04хвил. (метод 1). Приклад 29 {1-ацетил-2,2,4-триметил-4-[4-(2-піперазин-1іл-етокси)-феніл]-1,2,3,4-тетрагідрохінолін-6-іл}амід біфеніл-4-карбонової кислоти Згідно з загальною процедурою D, сполуку Прикладу 24с (100мг) обробляють піперазином (140мг) у CH3CN (5мл). Бажану сполуку очи щають препаративною РХВР (метод А) і ліофілізують з суміші CH3CN і водовмісної ТФК, отримуючи відповідну сіль ТФК Вихід: 95мг (сіль ТФК); MS-ESI: [М+Н]+=617,6; РХВР: Rt=9,54хвил. (метод 1). Приклад 30 (3-{4-[1-ацетил-6-(3,5-дихлор-2,6-диметоксибензоїламіно)-2,2,4-триметил-1,2,3,4 27 80303 тетрагідрохінолін-4-іл]-фенокси}-пропіл)амідморфолін-4-карбонової кислоти (a) (3-{4-[1-ацетил-6-аміно-2,2,4-триметил1,2,3,4-тетрагідрохінолін-4-іл]-фенокси}-пропіл)амід морфолін-4-карбонової кислоти Згідно з процедурою Прикладу 22d, сполуку Прикладу 22с (1,0г), алкілують (з супроводжуючим видаленням захисної групи Fmoc) 3хлорпропіл)амідом морфолін-4-карбонової кислоти (448мг), використовуючи Cs 2CO3 (1,8г) у ДМФ (5мл). Бажану сполуку очищають хроматографією на силікагелі з елюентом СН 2СІ2/2%-й амоній у МеОН=1/0=>9/1 (об'єм/об'єм). Вихід: 894мг. (b) (3-{4[1-ацетил-6-(3,5-дихлор-2,6диметоксибензоїламіно)-2,2,4-триметил-1,2,3,4тетрагідрохінолін-4-іл]-фенокси}-пропіл)-амід морфолін-4-карбонової кислоти Згідно з загальною процедурою С, сполуку Прикладу 30а (228мг) ацилують 3,5-дихлор-2,6диметоксибензойною кислотою (230мг), ДІПЕА (558мкл) і ГФТМ (609мг) у CH2CI2 (5мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 102мг; MS-ESI: [М+Н]+=727,4; РХВР: Rt=22,37хвил. (метод 2). Приклад 31 N-{1-ацетил-2,2,4-триметил-4-[4-(2-морфолін4-ілетокси)-феніл]-1,2,3,4-тетрагідрохінолін-6-іл}3,5-дибромбензамід (a) 1-ацетил-6-аміно-2,2,4-триметил-4-[4-(2морфолін-4-ілетокси)-феніл]-1,2,3,4тетрагідрохінолін Суміш сполуки Прикладу 22с (1,0г), Cs 2CO3 (1,8г), N-(2-хлоретил)-морфолін-гідрохлориду (375мг) і ДМФ (5мл) перемішують при 60°С 18год. Якщо реакція не завершена, додають ще Cs 2CO3 і N-(2-хлоретил)-морфолінгідрохлорид. Після завершення реакції, додають воду і суміш екстрагують СН2СІ2. Органічний шар сушать і концентрують in vacuo. Бажану сполуку очи щають хроматографією на силікагелі з елюентом СН 2СІ2/2% амонію у МеОН=1/0=>9/1 (об'єм/об'єм). Вихід: 905мг. (b) N-{1-ацетил-2,2,4-триметил-4-[4-(2морфолін-4-ілетокси)-феніл]-1,2,3,4тетрагідрохінолін-6-іл}-3,5-дибромбензамід Згідно з загальною процедурою С, сполуку Прикладу 31а (157мг) ацилують 3,5дибромбензойною кислотою (150мг), ДІПЕА (313мкл) і ГФТМ (204мг) у СН2СІ2 (5мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 71мг (сіль ТФК); MS-ESI: [М+Н]+=700,2; РХВР: Rt=16,12мм (метод 2). Приклад 32 N-{1-ацетил-2,2,4-триметил-4-[4-(2-морфолін4-ілетокси)-феніл]-1,2,3,4-тетрагідрохінолін-6-іл}-2хлорбензамід Згідно з загальною процедурою С, сполуку Прикладу 31а (150мг) ацилують 2-хлорбензойною кислотою (81мг), ДІПЕА (299мкл) і ГФТМ (195мг) у СН2СІ2 (6мл). Бажану сполуку очищають препаративною РХВР (метод А). 28 Вихід: 162мг (сіль ТФК); MS-ESI: [М+Н]+=576,4; РХВР: Rt=9,37хвил. (метод 2). Приклад 33 N-{3-ацетил-2,2,4-триметил-4-[4-(2-морфолін4-ілетокси)-феніл]-1,2,3,4-тетрагідрохінолін-6-іл}3,5-диметилбензамід Згідно з загальною процедурою С, сполуку Прикладу 31а (200мг) ацилують 3,5диметилбензойною кислотою (103мг), ДІПЕА (399мкл) і ГФТМ (260мг) у СН 2СІ2 (7,5мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 57,5мг (сіль ТФК); MS-ESI: [M+H]+=570,4; РХВР: Rt=12,62хвил. (метод 2). Приклад 34 N-{1-ацетил-2,2,4-триметил-4-[4-(2-морфолін4-ілетокси)-феніл]-1,2,3,4-тетрагідрохінолін-6-іл}2,5-дихпорбензамід Згідно з загальною процедурою С, сполуку Прикладу 31а (200мг) ацилують 2,5дихлорбензойною кислотою (131мг), ДІПЕА (399мкл) і ГФТМ (260мг) у СН 2СІ2 (7,5мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 130мг (сіль ТФК); MS-ESI: [М+Н]+=610,2; РХВР: Rt=,11,70хвил. (метод 2). Приклад 35 N-{1-ацетил-2,2,4-триметил-4-[4-(2-морфолін4-ілетокси)-феніл]-1,2,3,4-тетрагідрохінолін-6-іл}-5метил-2-нітробензамід Згідно з загальною процедурою С, сполуку Прикладу 31а (157мг) ацилують 5-метил-2нітробензойною кислотою (97,3мг), ДІПЕА (313мкл) і ГФТМ (204мг) у СН2СІ2 (5мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 80мг (сіль ТФК); MS-ESI: [М+Н]+=601,4; РХВР: Rt=9,95хвил. (метод 2). Приклад 36 N-{1-ацетил-2,2,4-триметил-4-[4-(2-морфолін4-ілетокси)-феніл]-1,2,3,4-тетрагідрохінолін-6-іл}бензамід Згідно з загальною процедурою С, сполуку Прикладу 31а (157мг) ацилують бензойною кислотою (65,6мг), ДІПЕА (313мкл) і ГФТМ (204мг) у СН2СІ2 (5мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 59мг (сіль ТФК); MS-ESI: [М+Н]+=542,4; РХВР: Rt=9,99хвил. (метод 2). Приклад 37 N-{1-ацетил-2,2,4-триметил-4-[4-(2-морфолін4-ілетокси)-феніл]-1,2,3,4-тетрагідрохінолін-6-іл}-4трет-бутилбензамід Згідно з загальною процедурою С, сполуку Прикладу 31а (161мг) ацилують 4-третбутилбензойною кислотою (99мг), ДІПЕА (322мкл) і ГФТМ (210мг) у СН2СІ2 (5мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 80мг (сіль ТФК); MS-ESI: [М+Н]+=598,2; РХВР: Rt=15,39хвил. (метод 2). Приклад 38 N-{1-ацетил-2,2,4-триметил-4-[4-(2-морфолін4-ілетокси)-феніл]-1,2,3,4-тетрагідрохінолін-6-іл}2,3-дихлорбензамід 29 80303 Згідно з загальною процедурою С, сполуку Прикладу 31а (161мг) ацилують 2,3дихлорбензойною кислотою (106мг), ДІПЕА (322мкл) і ГФТМ (210мг) у СН2СІ2 (5мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 113мг (сіль ТФК); MS-ESI: [M+H]+=6102; РХВР: Rt=11,42хвил. (метод 2). Приклад 39 N-{1-ацетил-2,2,4-триметил-4-[4-(2-морфолін4-ілетокси)-феніл]-1,2,3,4-тетрагідрохінолін-6-іл}-4бромбензамід Згідно з загальною процедурою С, сполуку Прикладу 31а (260мг) ацилують 4-бромбензойною кислотою (179мг), ДІПЕА (517мкл) і ГФТМ (338мг) у СН2СІ2 (5мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 127мг (сіль ТФК); MS-ESI: [М+Н]+=620,2: РХВР: Rt=12,24мм (метод 2). Приклад 40 N-{1-ацетил-2,2,4-триметил-4-[4-(2-морфолін6-ілетокси)-феніл]-1,2,3,4-тетрагідрохінолін-6-іл}-4метокси-3-метилбензамід Згідно з загальною процедурою С, сполуку Прикладу 31а (260мг) ацилують 4-метокси-3метилбензойною кислотою (148мг), ДІПЕА (517мкл) і ГФТМ (338мг) у СН2СІ2 (5мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 158мг (сіль ТФК); MS-ESI: [М+Н]+=586,2; РХВР: Rt=11,49хвил. (метод 2). Приклад 41 N-{1-ацетил-2,2,4-триметил-4-[4-(2-морфолін4-ілетокси)-феніл]-1,2,3,4-тетрагідрохінолін-6-іл}-4диметиламінобензамід Згідно з загальною процедурою С, сполуку Прикладу 31а (260мг) ацилують 4диметиламінобензойною кислотою (147мг), ДІПЕА (517мкл) і ГФТМ (333мг) у СН2СІ2 (5мл). Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 95мг (сіль ТФК); MS-ESI: [М+Н]+=585,2; РХВР: Rt=9,53хвил. (метод 2). Приклад 42 N-{1-ацетил-2,2,4-триметил-4-[4-(2-морфолін4-ілетокси)-феніл]-1,2,3,4-тетрагідрохінолін-6-іл}-3трифлуорметилбензамід До розчину сполуки Прикладу 31а (260мг) і піридину (500мкл) у толуолі (4,5мл) додають 3 Комп’ютерна в ерстка Т. Чепелев а 30 (трифлуорметил)бензоїлхлорид (185мг) і потім етилацетат (15мл) і воду (15мл). Органічний шар відокремлюють і промивають водою (15мл), сушать і концентрують in vacuo. Бажану сполуку очищають препаративною РХВР (метод А). Вихід 200мг (сіль ТФК); MS-ESI: [М+Н]+=610,2; РХВР: Rt=13,23хвил. (метод 2). Приклад 43 N-{1-ацетил-2,2,4-триметил-4-[4-(2-морфолін4-ілетокси)-феніл]-1,2,3,4-тетрагідрохінолін-6-іл}-3нітробензамід До розчину сполуки Прикладу 31а (260мг) і піридину (500мкл) у толуолі (4,5мл) додають 3нітробензоїлхлорид (165мг) і потім етилацетат (15мл) і воду (15мл). Органічний шар відокремлюють і промивають водою (15мл), сушать і концентрують in vacuo. Бажану сполуку очищають препаративною РХВР (метод А). Вихід: 167мг (сіль ТФК); MS-ESI: [М+Н]+=587,4; РХВР: Rt=10,28хвил. (метод 2). Приклад 44 Біоактивність CHO-FSH in vitro Активність сполук до FSH була випробувана у клітинах яєчника китайського хом'яка (СНО), стабільно трансфекованих рецептором FSH людини і співтрансфекованих чутливим до сАМР елементом (CRE)/промотером, що спрямовує експресію гена-репортера світлякової люциферази. Зв'язування ліганда з з'єднаним Gs рецептором FSH підвищує сАМР, що у свою чергу індукує трансактивацію конструкції репортера люциферази. Для виявлення антагоністичних властивостей додавали (10mU/мл, rec-hFSH) рекомбінантний FSH у концентрації, що забезпечує приблизно 80% максимальної стимуляції акумуляції сАМР за відсутності сполуки, яку випробували. Сигнал люциферази квантували за допомогою люмінесцентного лічильника. Були обчислені значення ІK50 для сполуки, яку випробували (концентрацію сполуки, яка викликала половину максимальної стимуляції або зниження). Для цього була використана комп'ютерна програма GraphPad PRISM, version 3,0 (GraphPad software Inc., San Diego). Сполуки всіх прикладі показали IK50 менше 105 М як у агоністичному, так і антагоністичному аналізі, або в обох. Сполуки прикладів 3, 4, 7, 10-13, 16, 36, 37, 39, 41 і 42 показали ІK50 менше 10-7М у щонайменше одному аналізі. Підписне Тираж 26 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюTetrahydroquinoline derivatives, pharmaceutical composition based thereon and their use
Автори англійськоюTimmers Cornelis Marius, Karstens Willem Frederik Johan
Назва патенту російськоюПроизводные тетрагидрохинолина, фармацевтическая композиция на их основе и их использование
Автори російськоюТиммерс Корнелис Мариус, Карстенс Виллем Фредерик Йоган
МПК / Мітки
МПК: C07D 409/12, A61P 5/08, C07D 401/12, C07D 215/38
Мітки: похідні, фармацевтична, використання, основі, композиція, тетрагідрохіноліну
Код посилання
<a href="https://ua.patents.su/15-80303-pokhidni-tetragidrokhinolinu-farmacevtichna-kompoziciya-na-kh-osnovi-ta-kh-vikoristannya.html" target="_blank" rel="follow" title="База патентів України">Похідні тетрагідрохіноліну, фармацевтична композиція на їх основі та їх використання</a>
Наступний патент: Заміщені 6-(2-галогенфеніл)триазолопіримідини
Випадковий патент: Спосіб виготовлення абразивного інструменту












