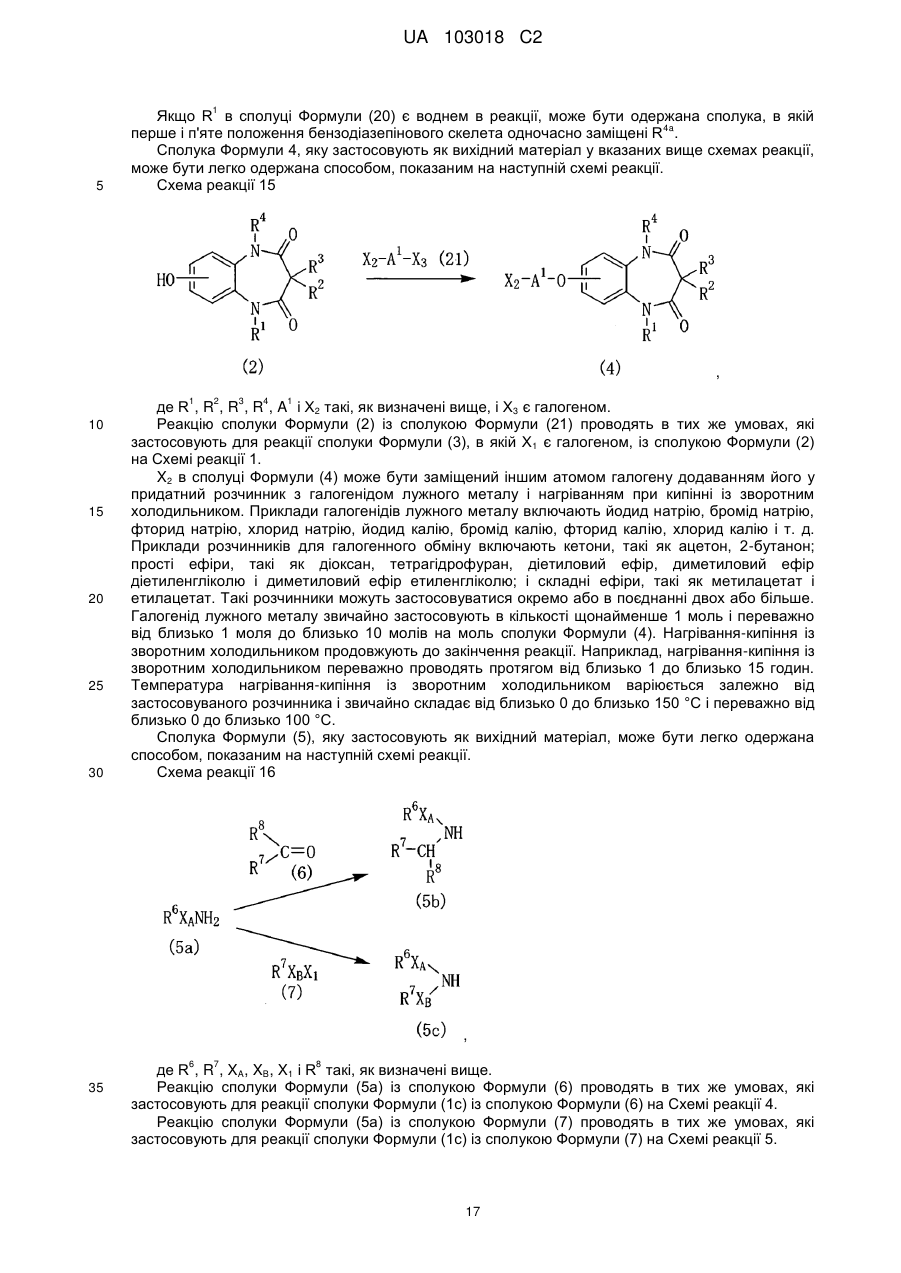
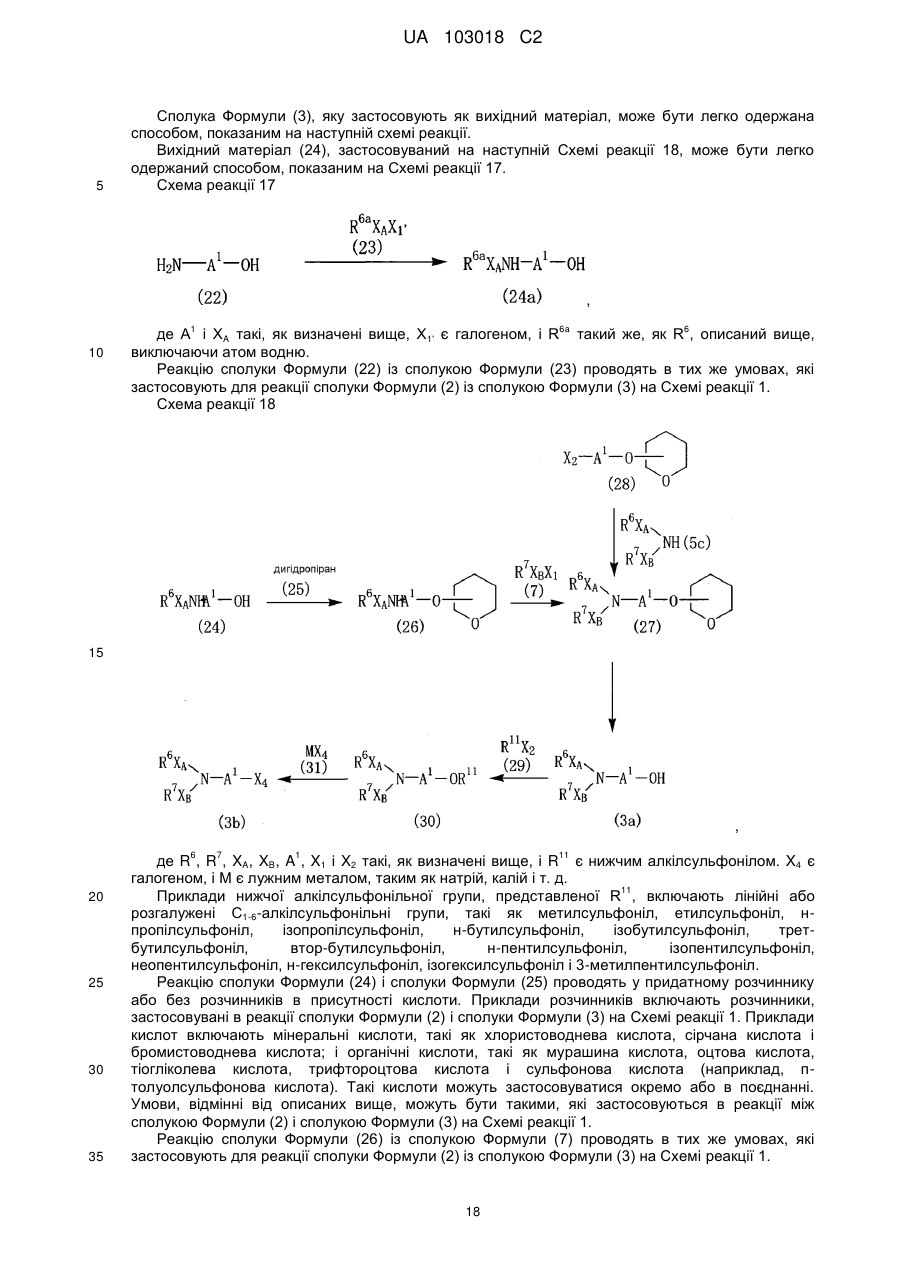
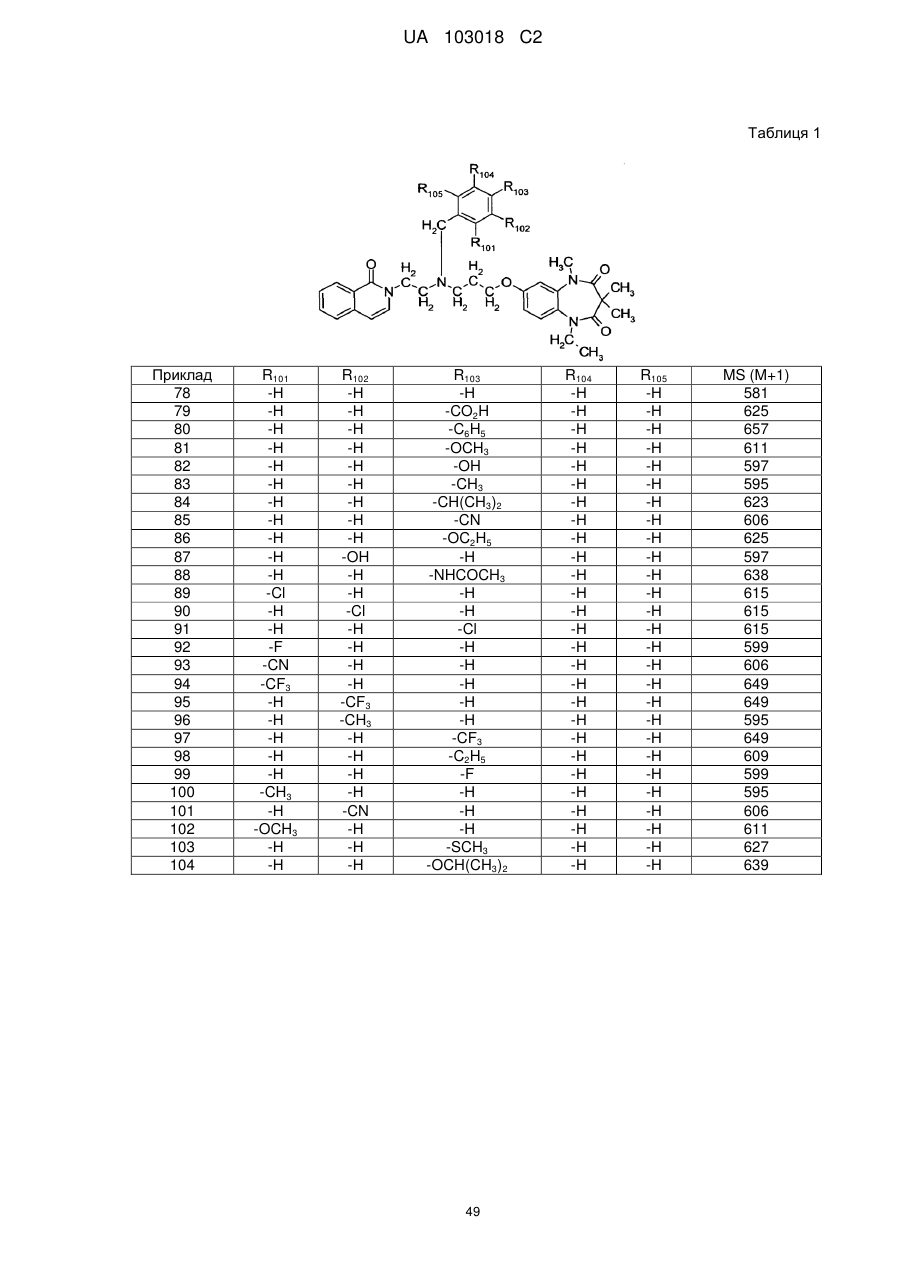
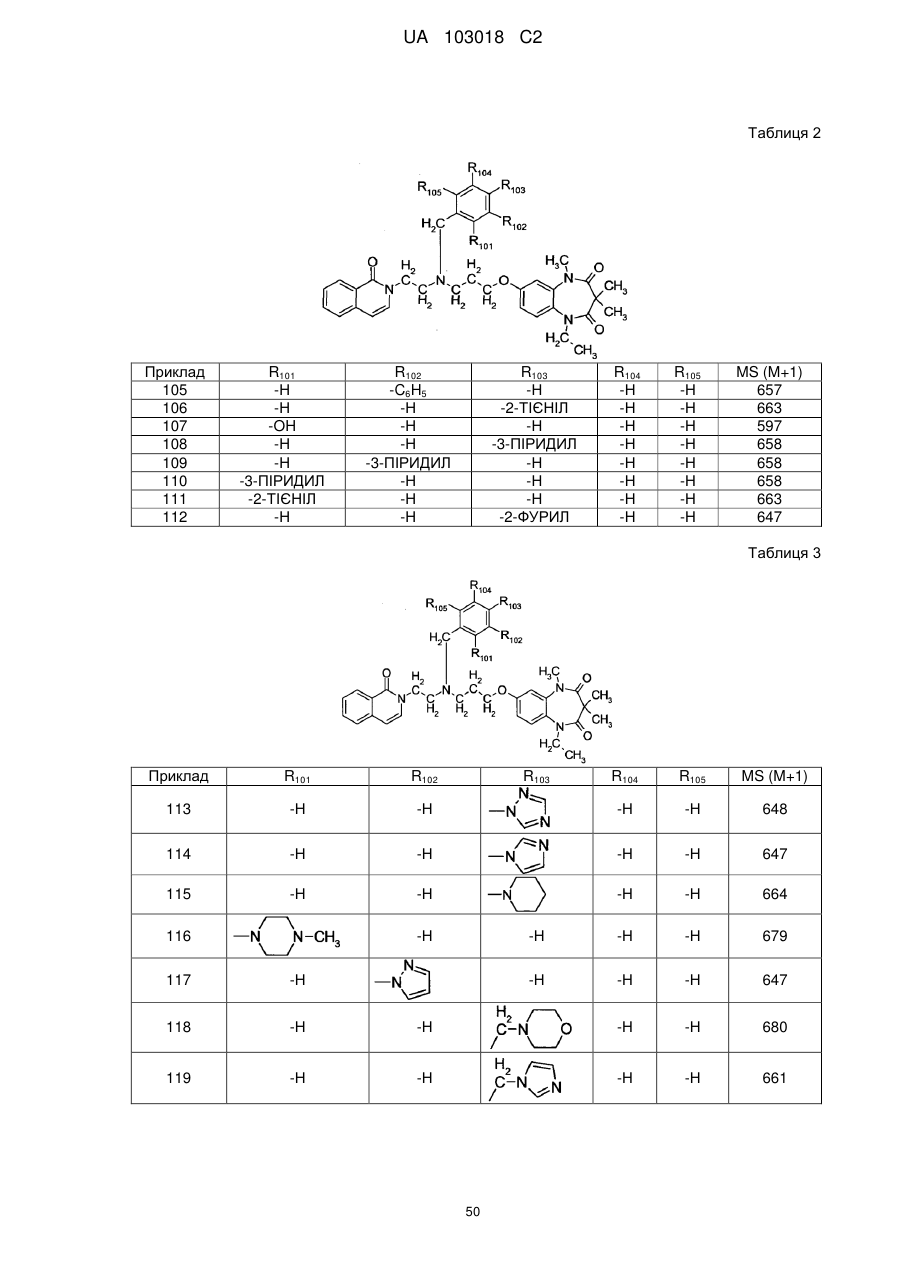
Сполуки бензодіазепіну і фармацевтична композиція
Номер патенту: 103018
Опубліковано: 10.09.2013
Автори: Осіяма Такасі, Мендзо Ясухіро, Ямабе Хокуто, Кога Ясуо, Осіма Куніо, Уеда Масатака, Мацумура Суудзі, Таі Кунінорі, Таіра Сініті, Оногава Тосіюкі, Накаяма Сунао, Цудзімає Кендзі
Формула / Реферат
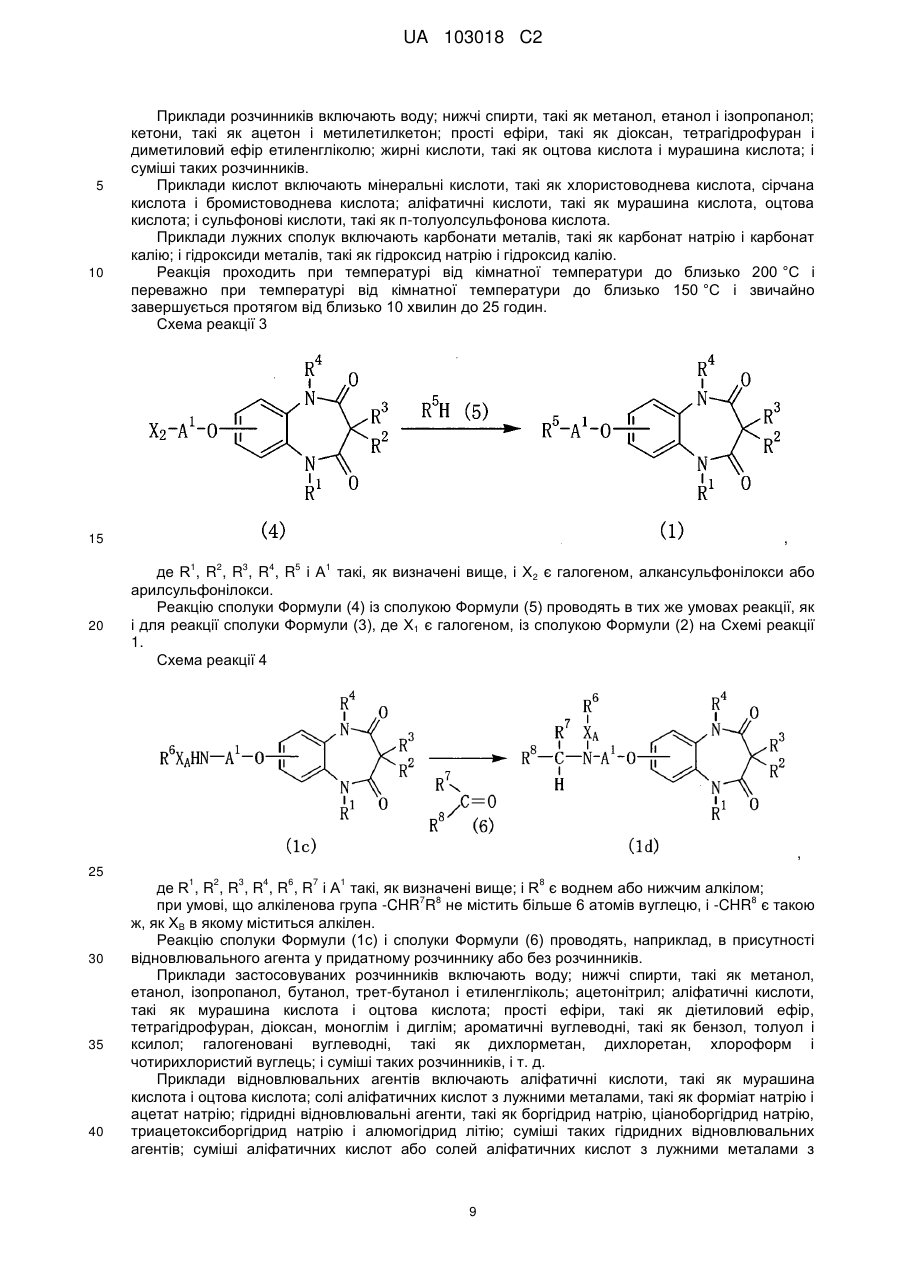
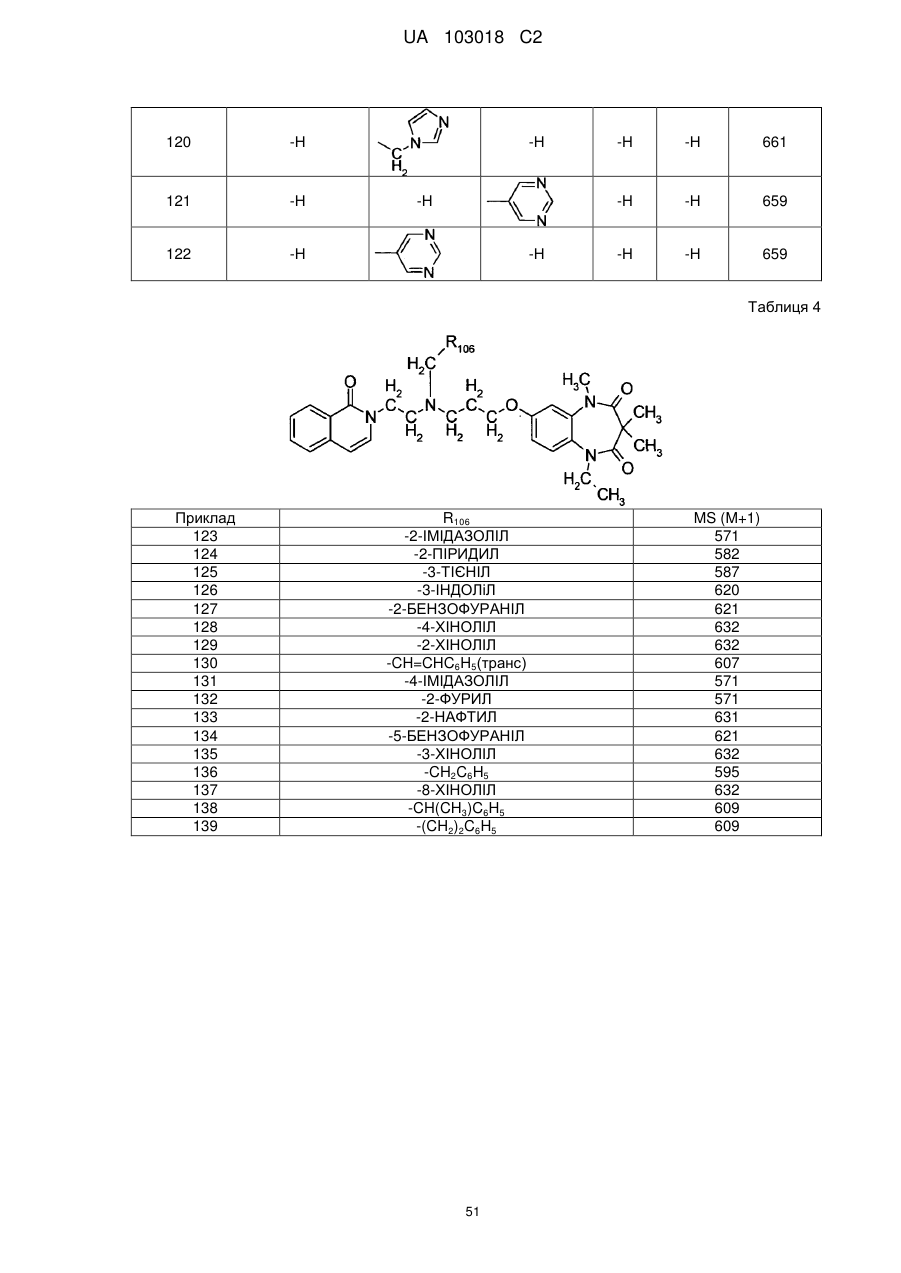
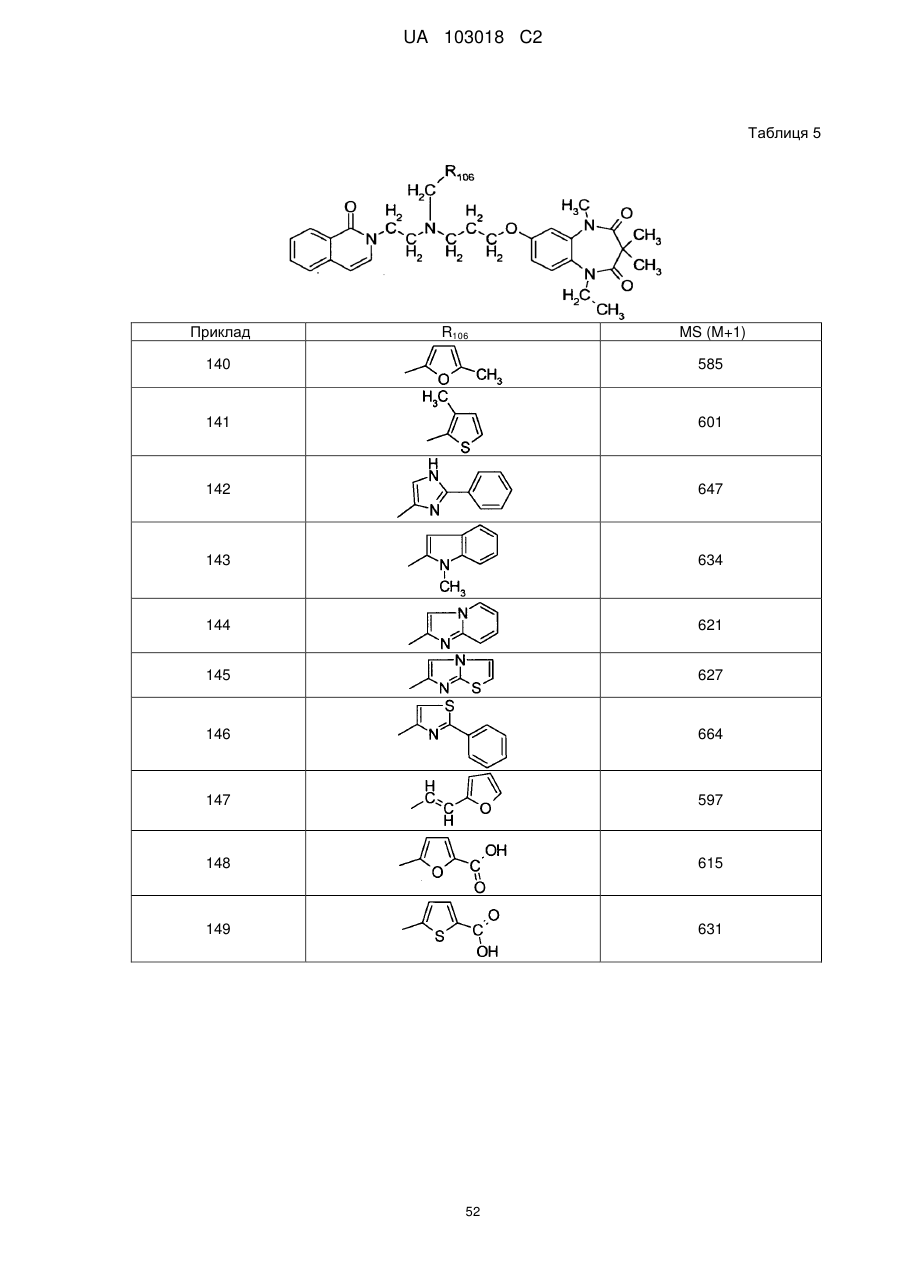
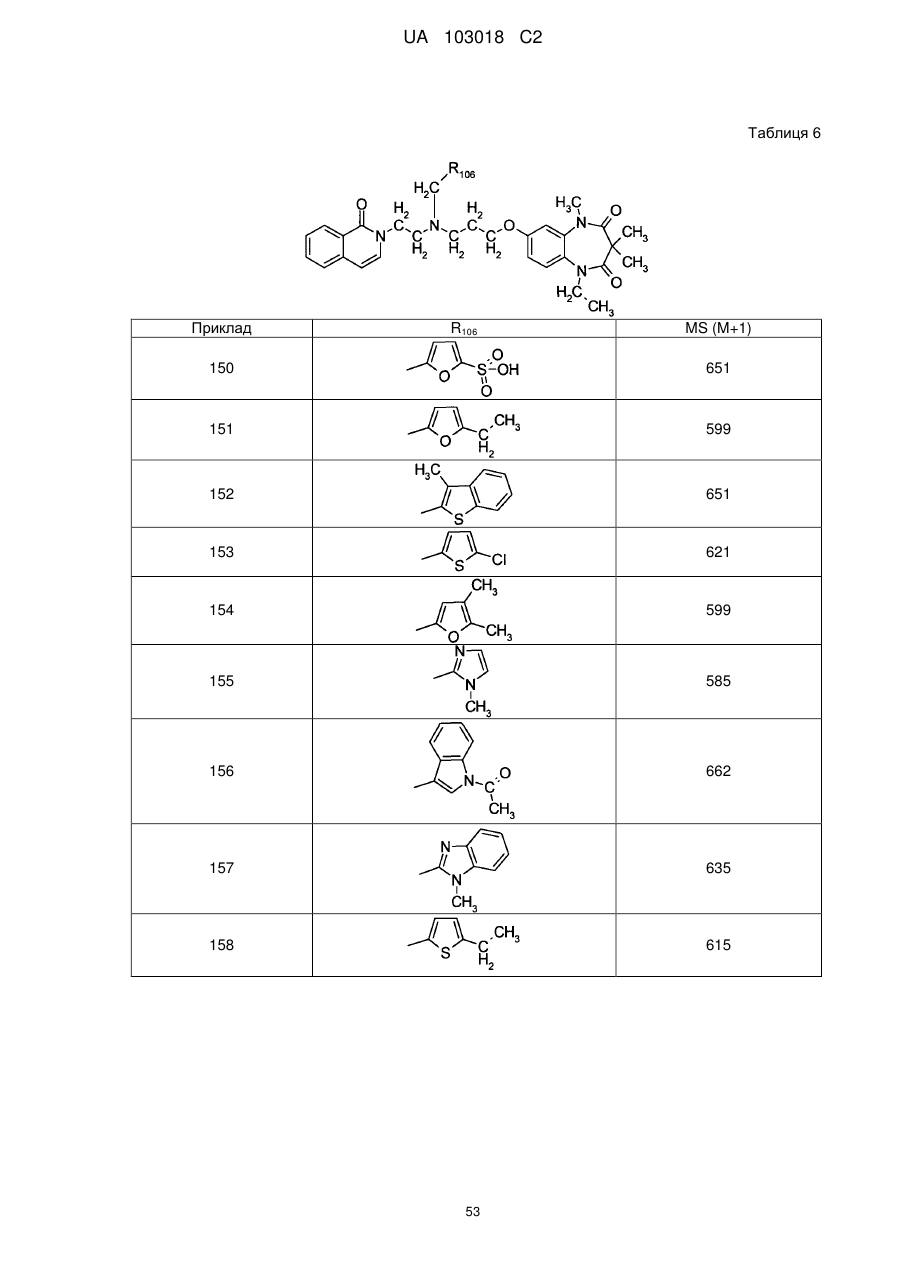
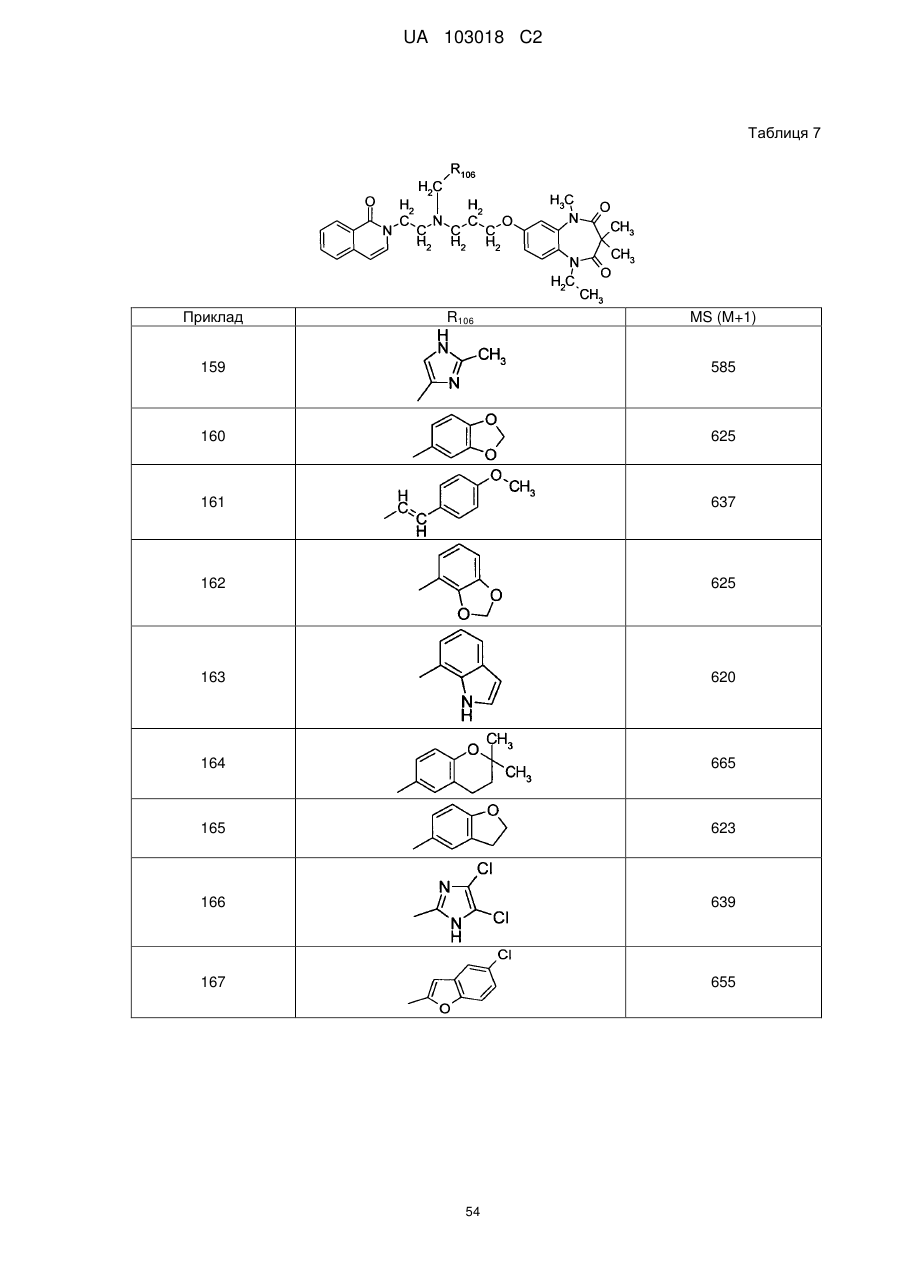
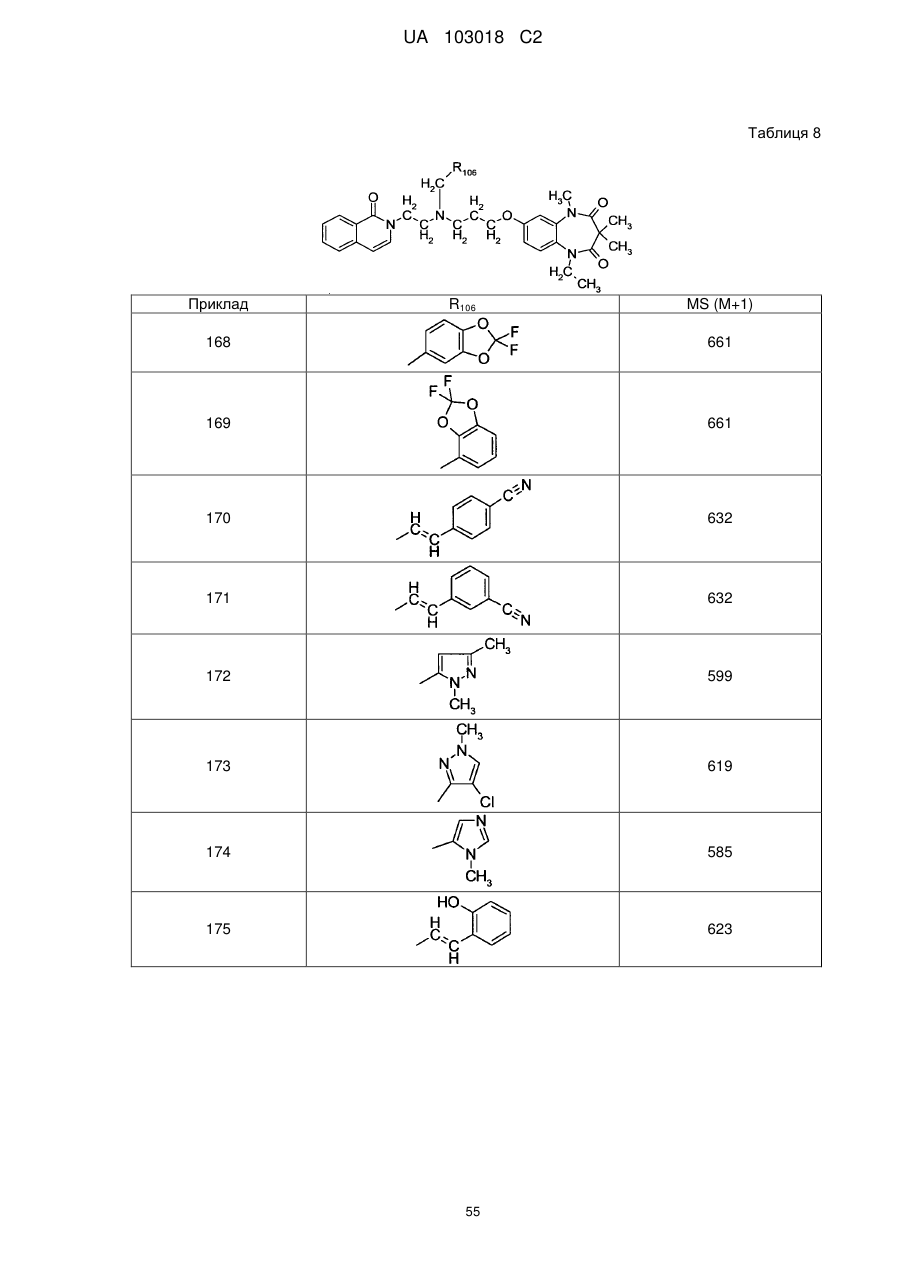
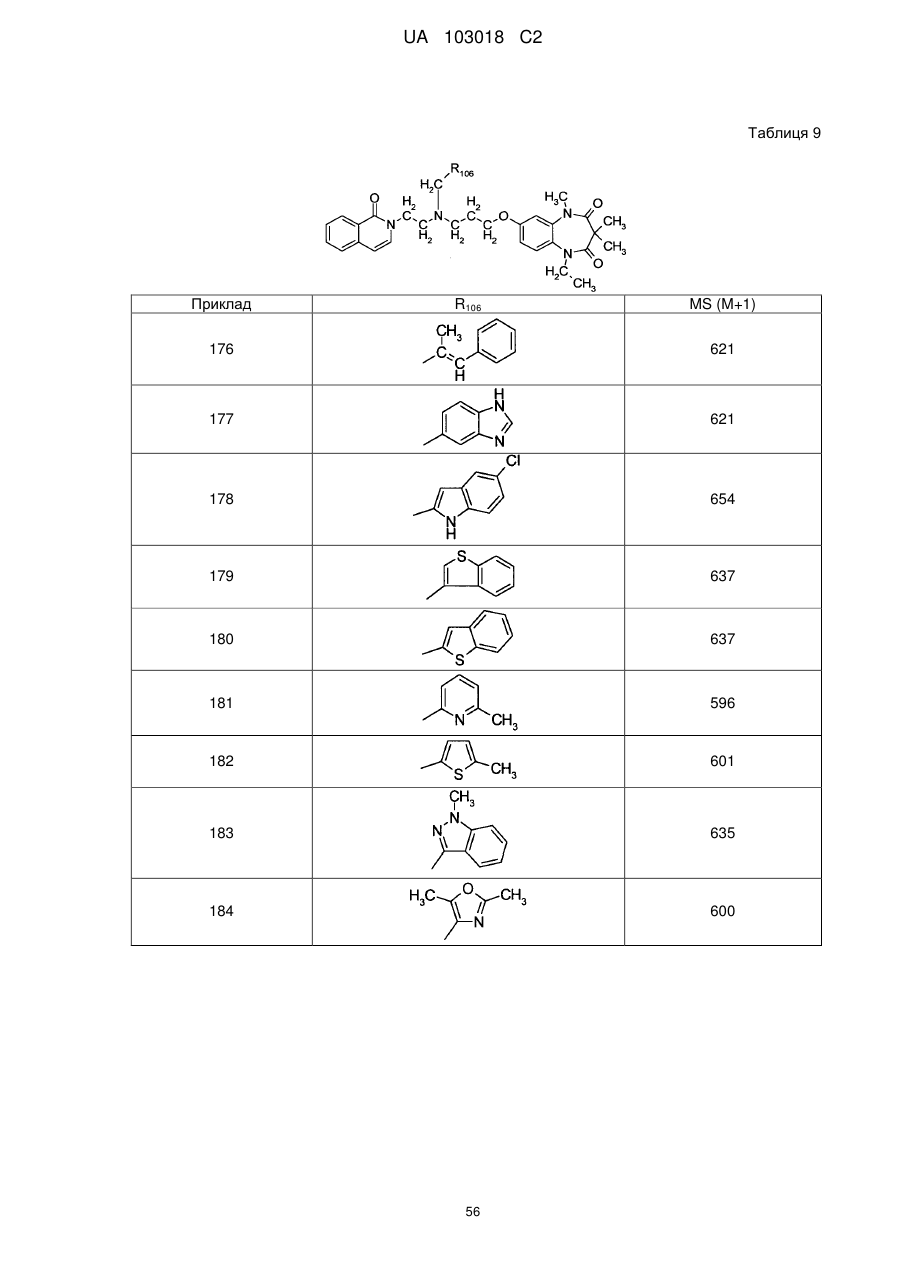
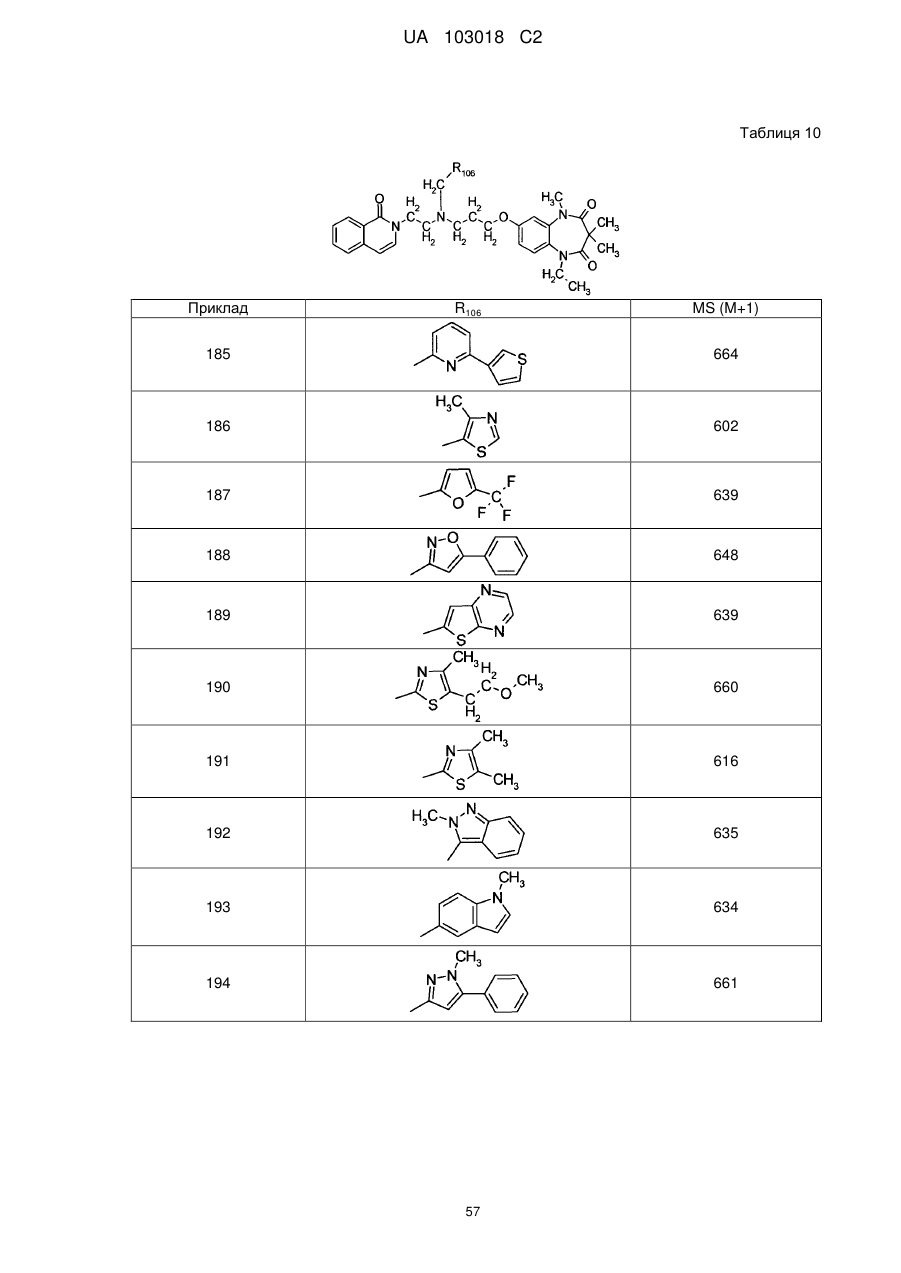
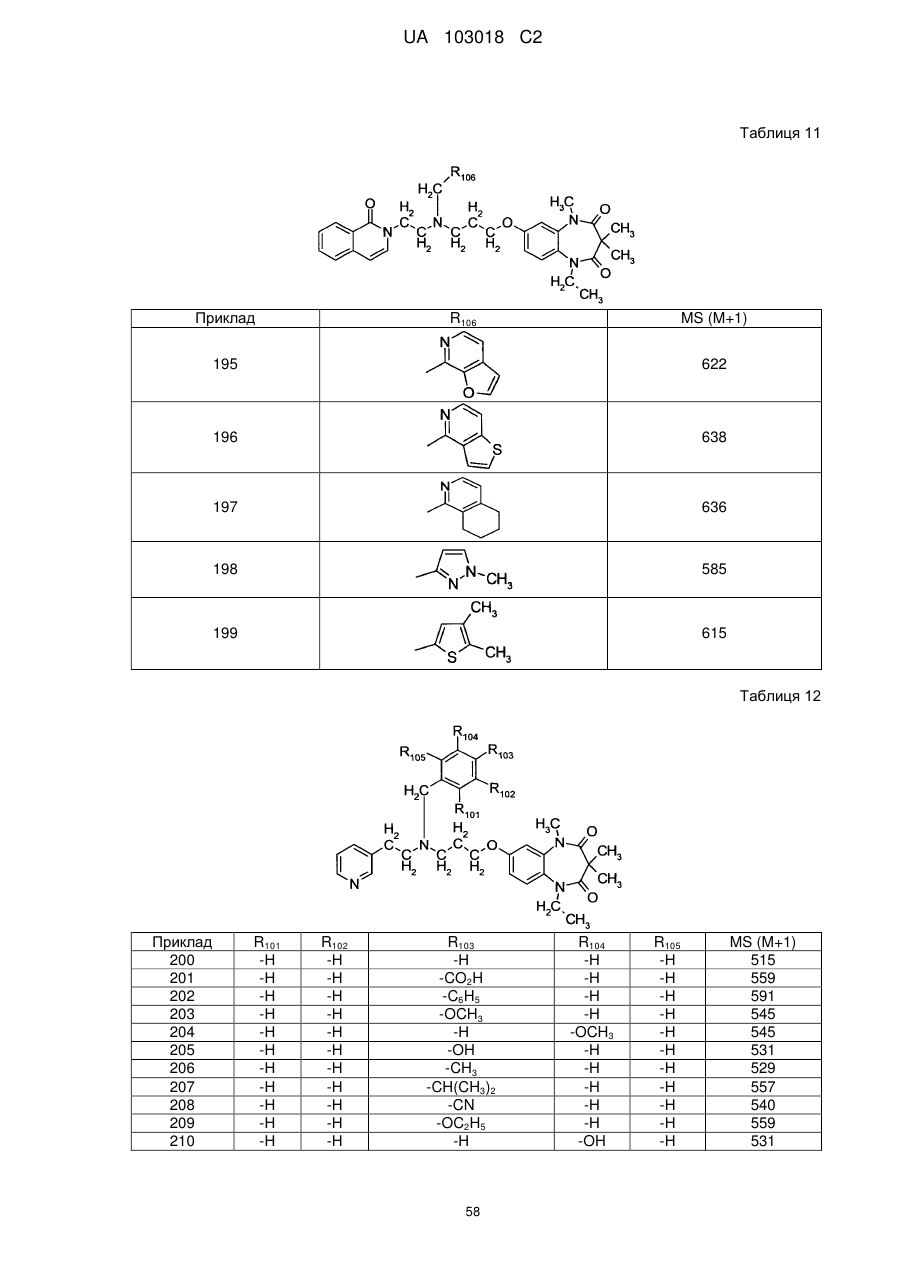
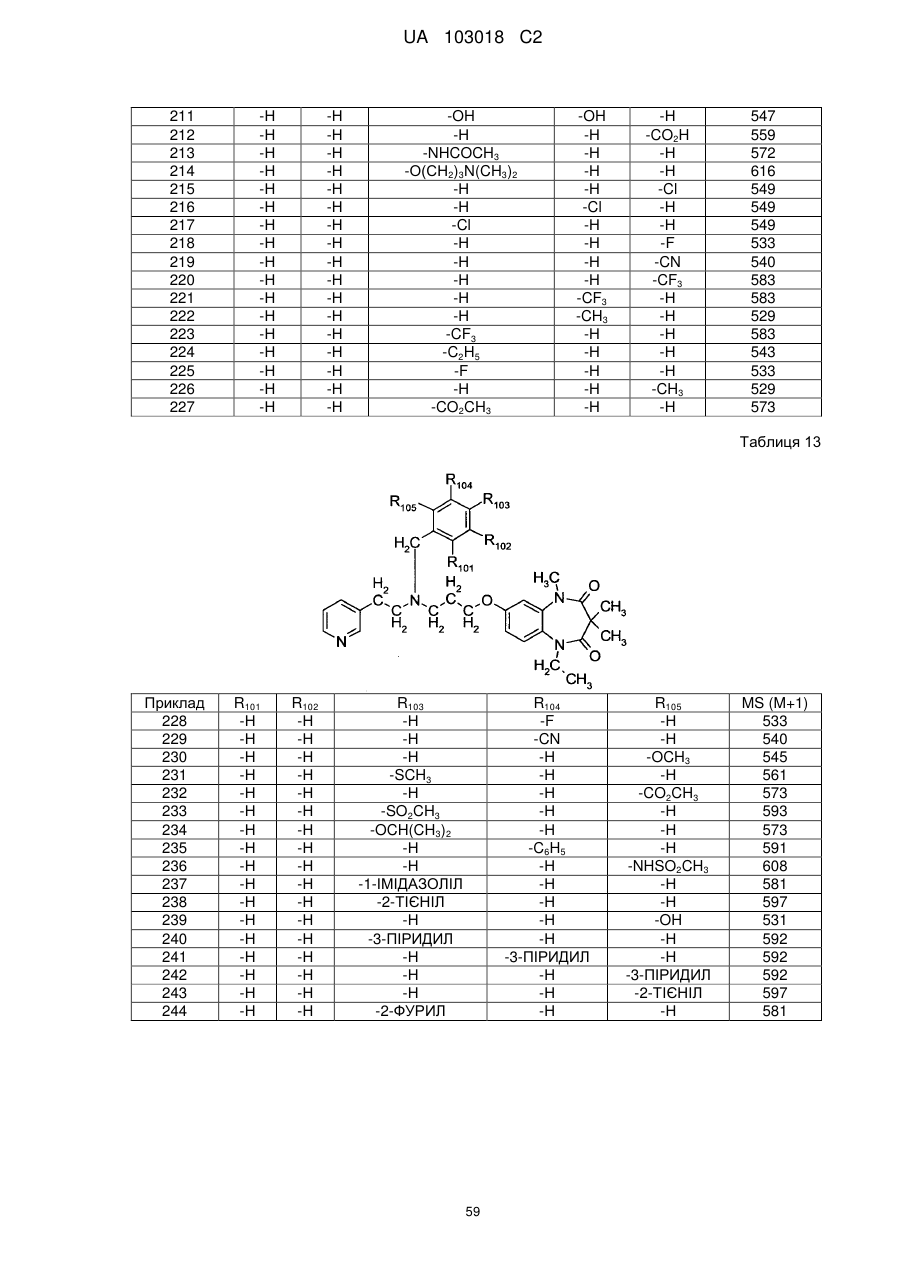
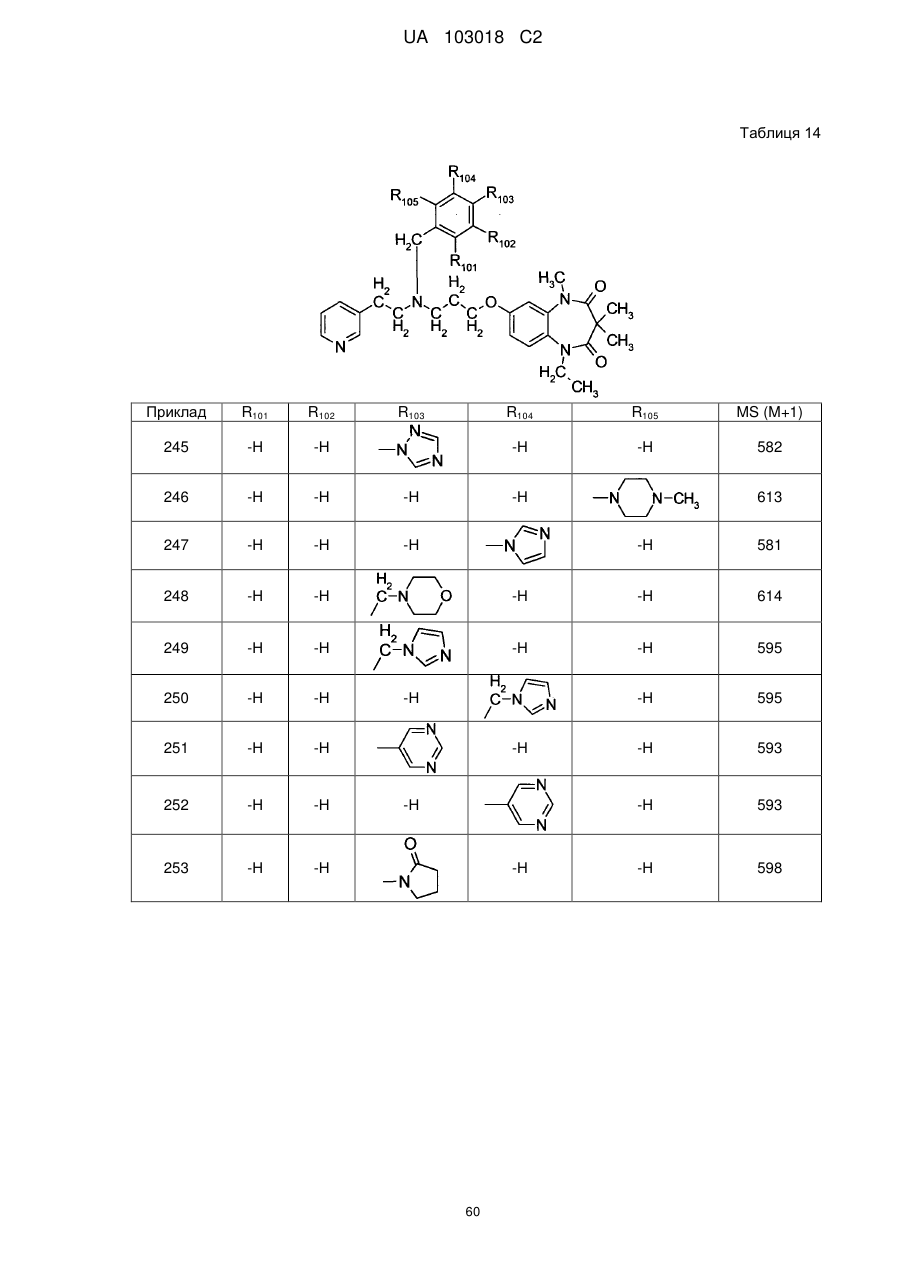
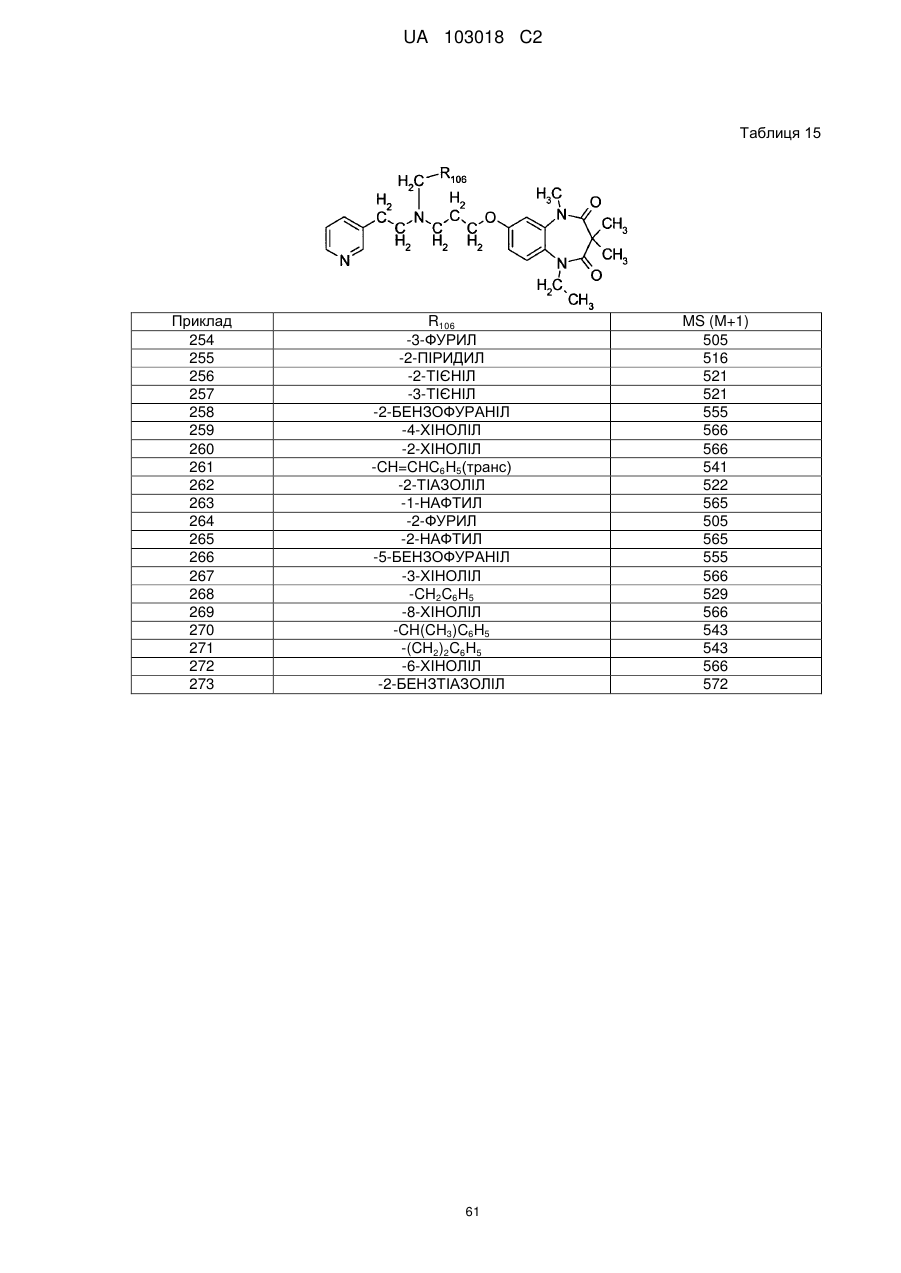
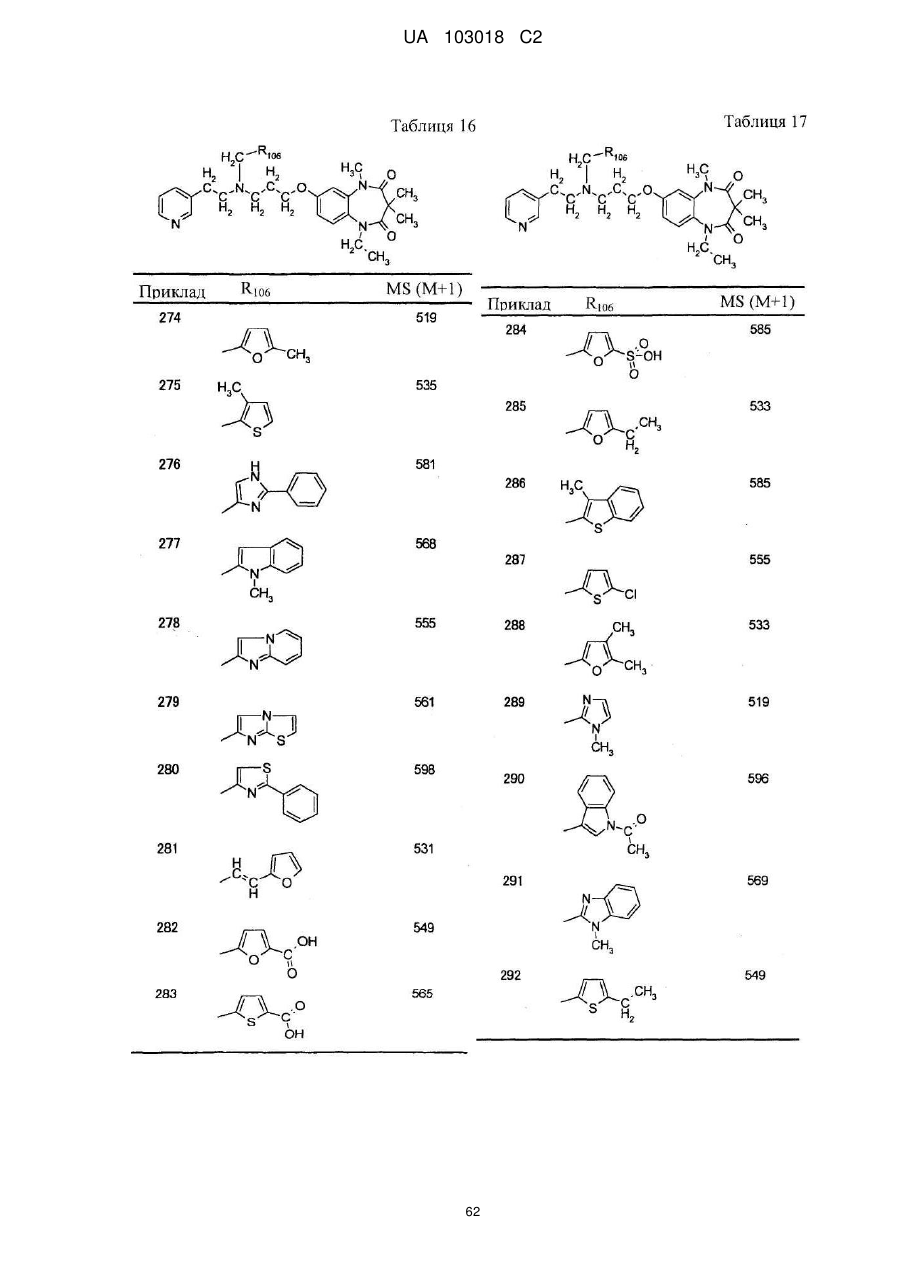
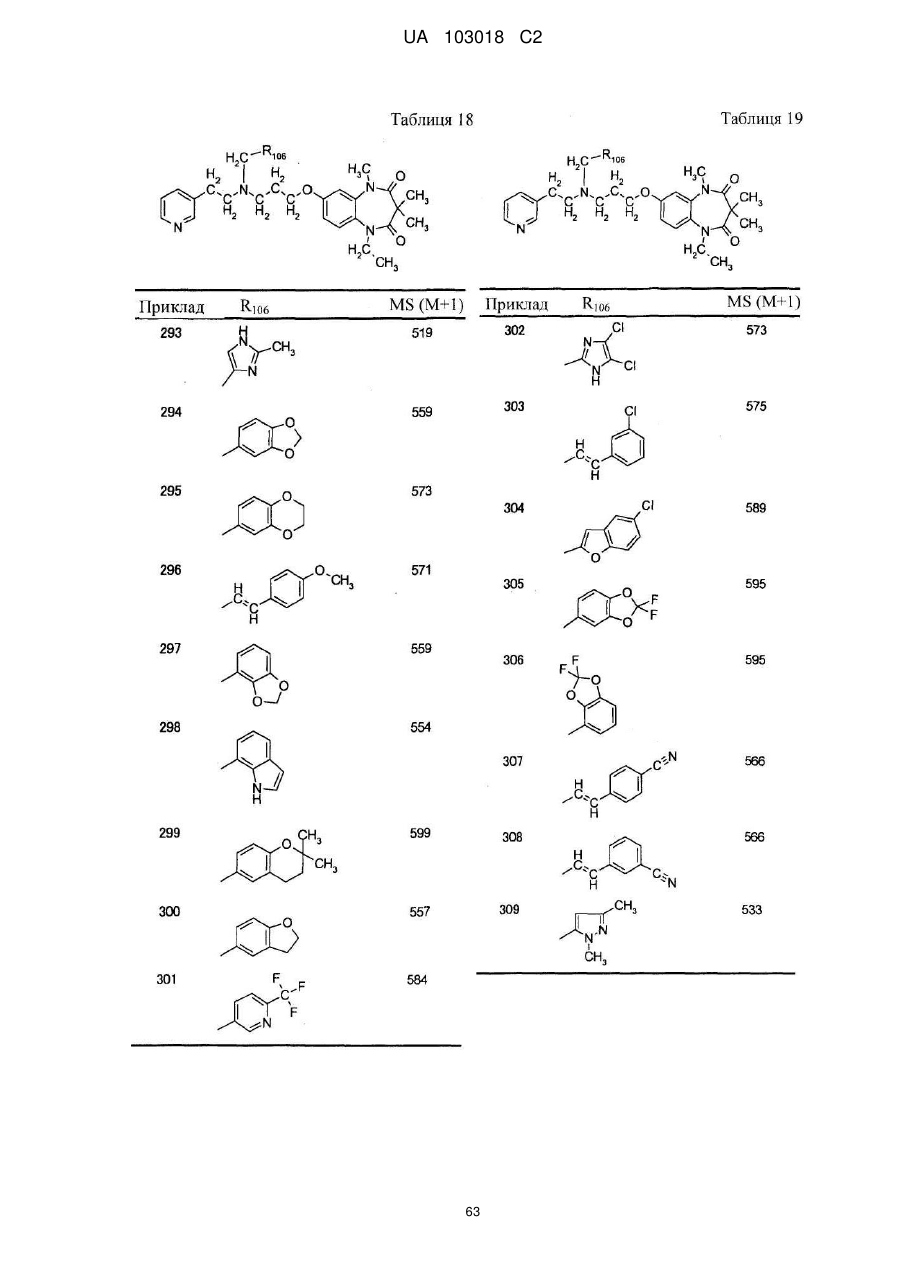
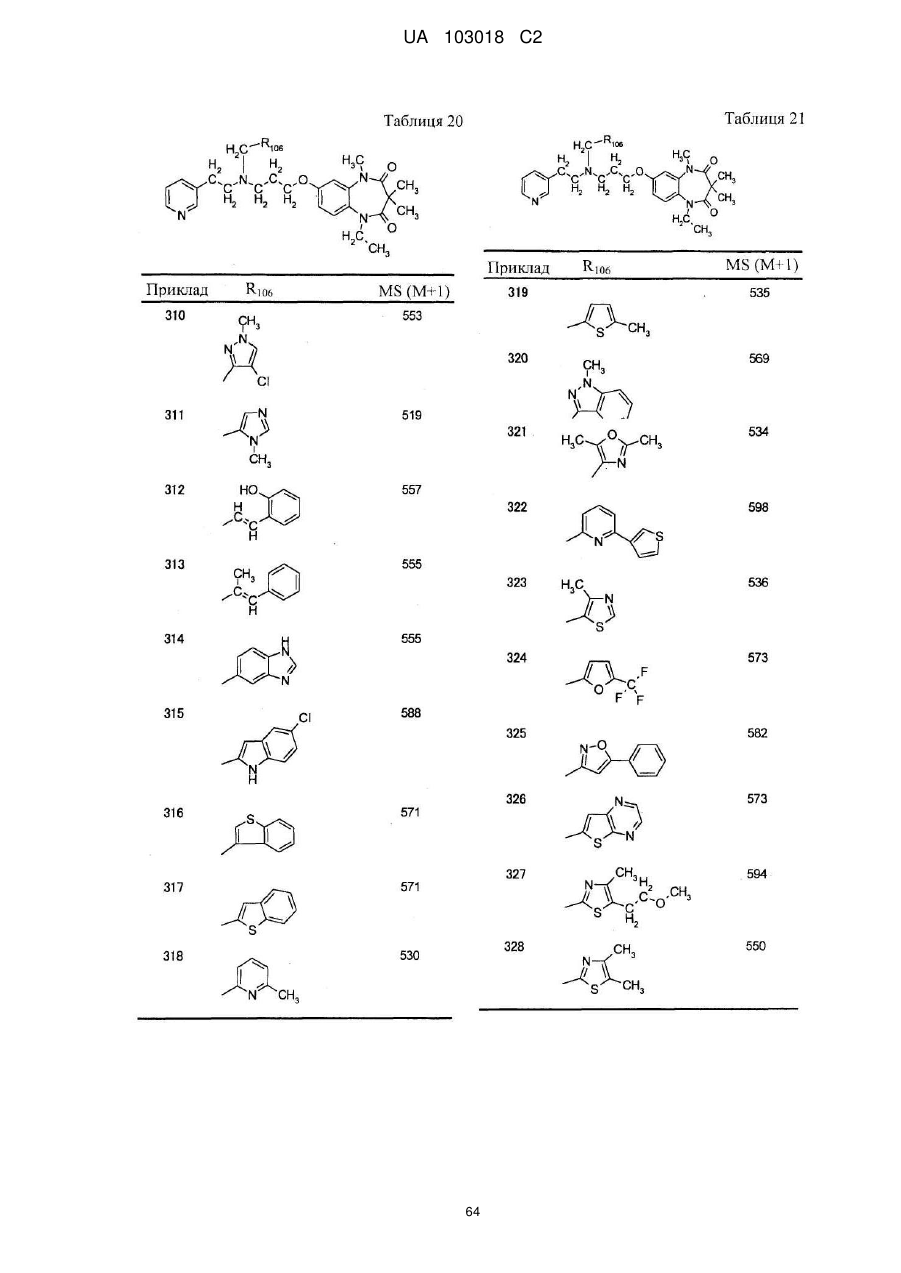
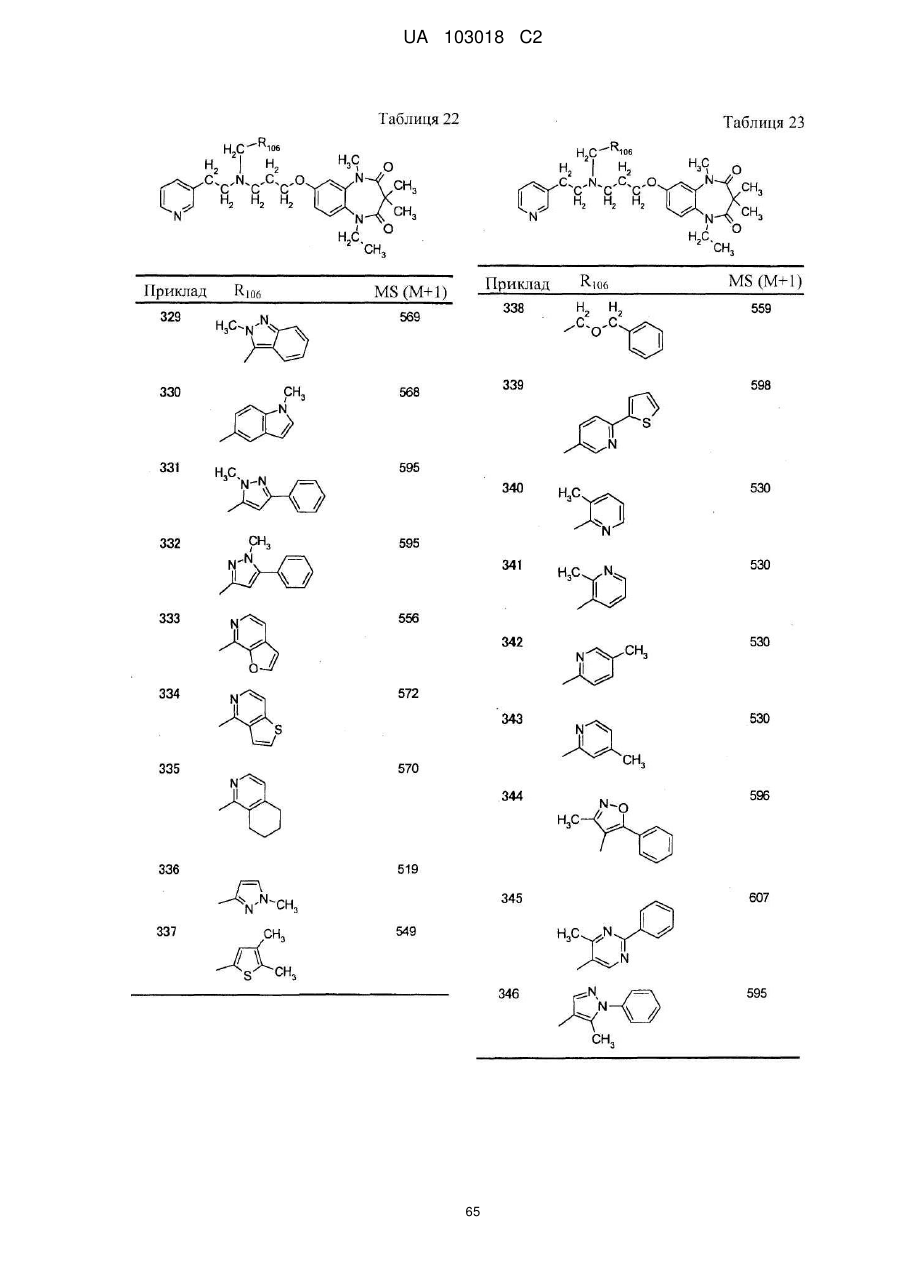
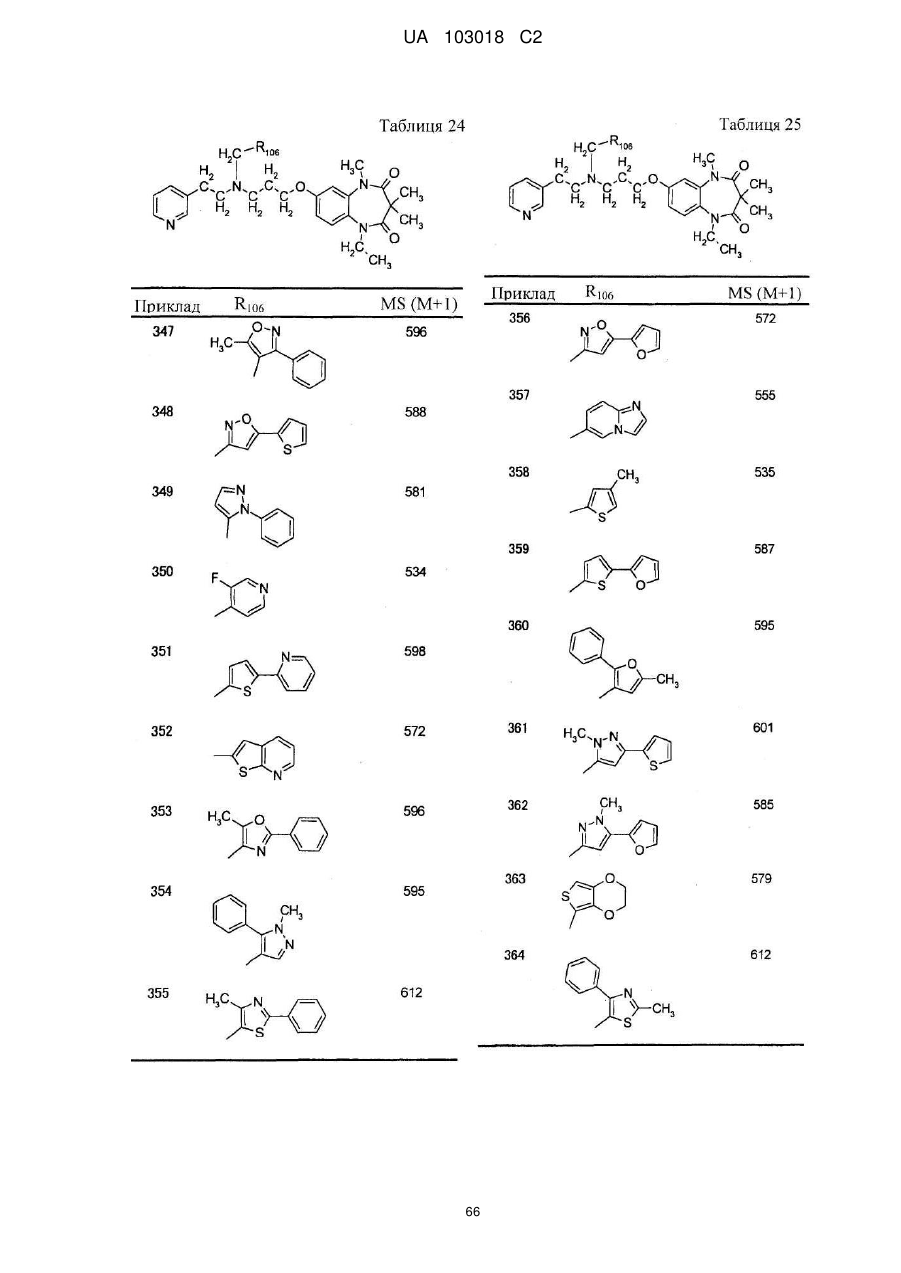
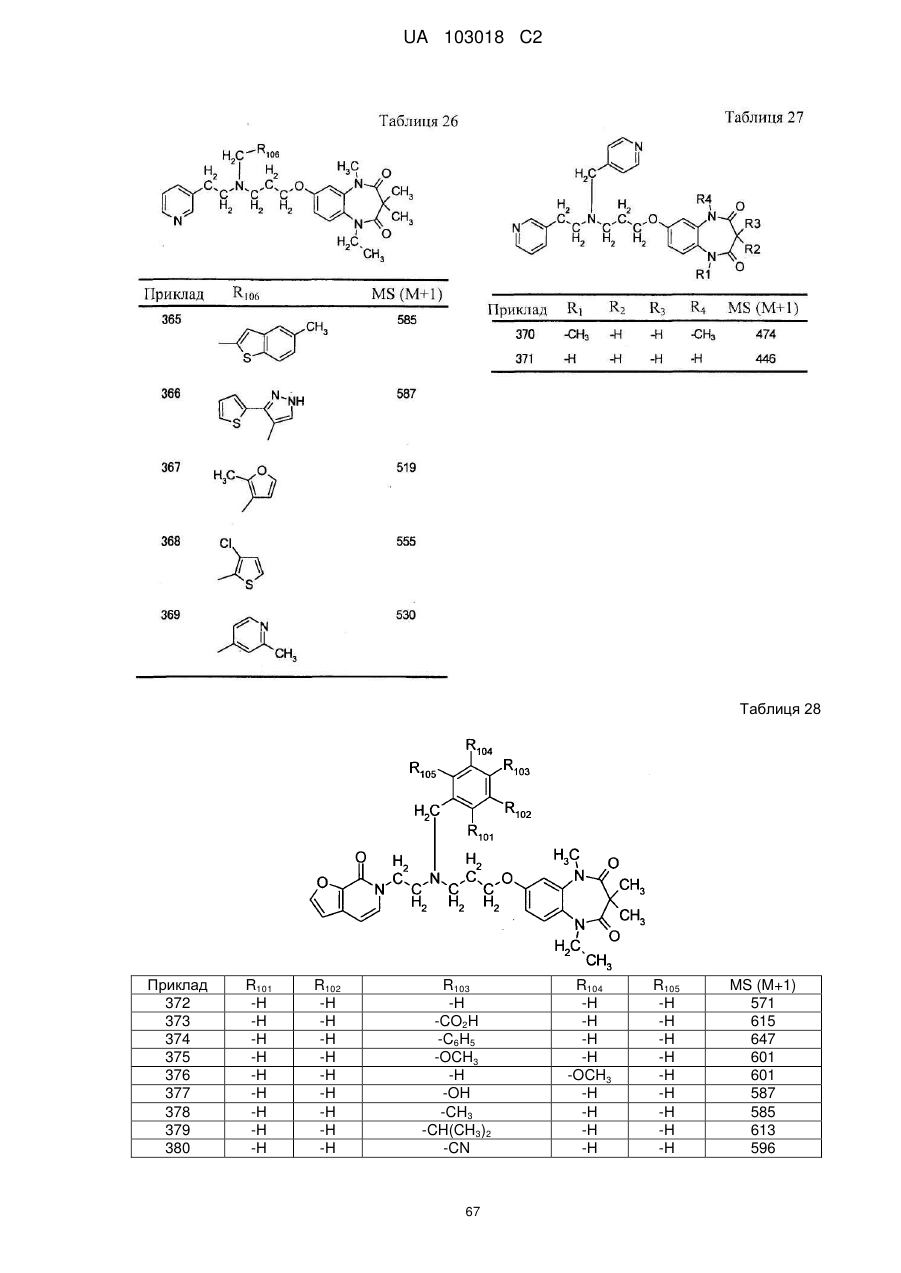
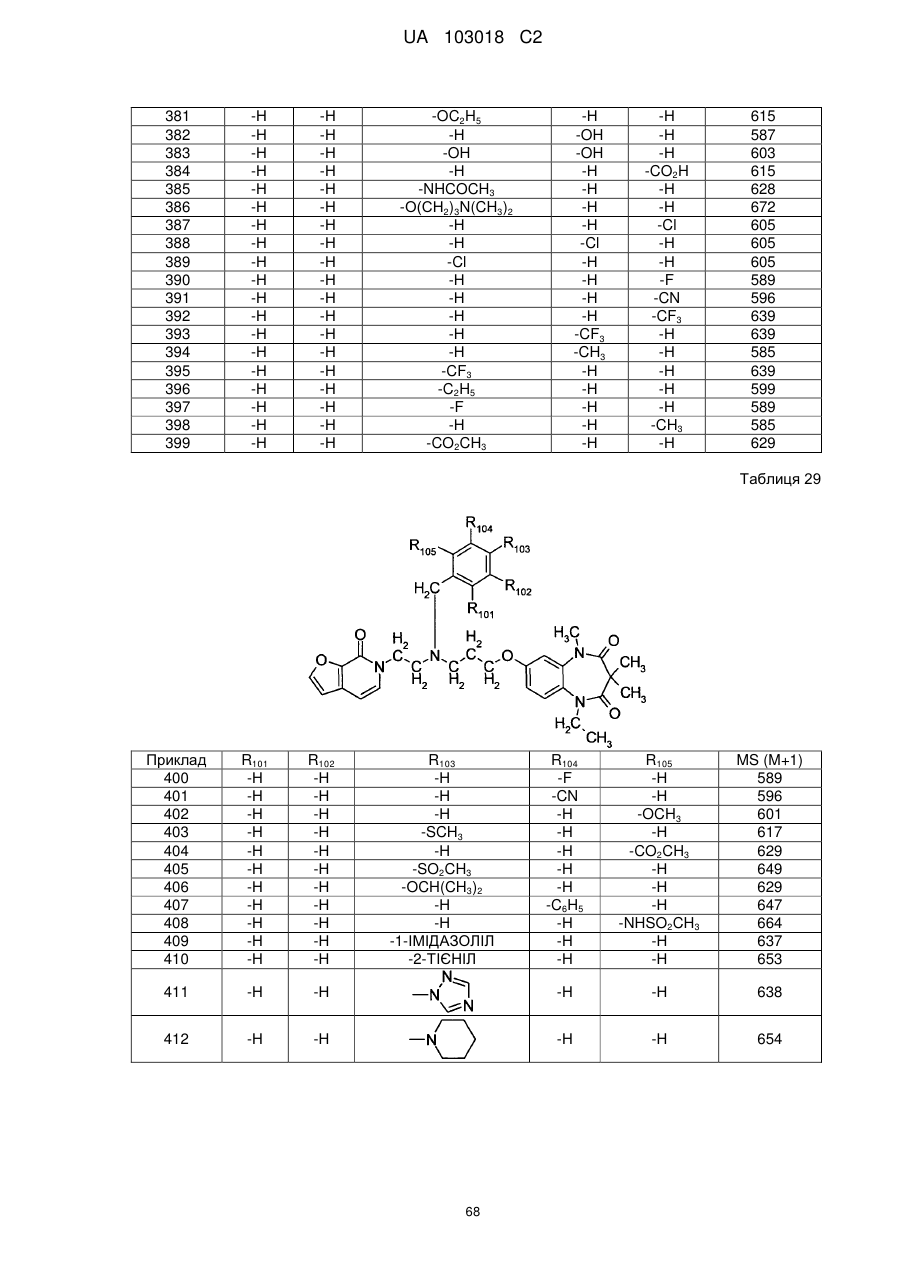
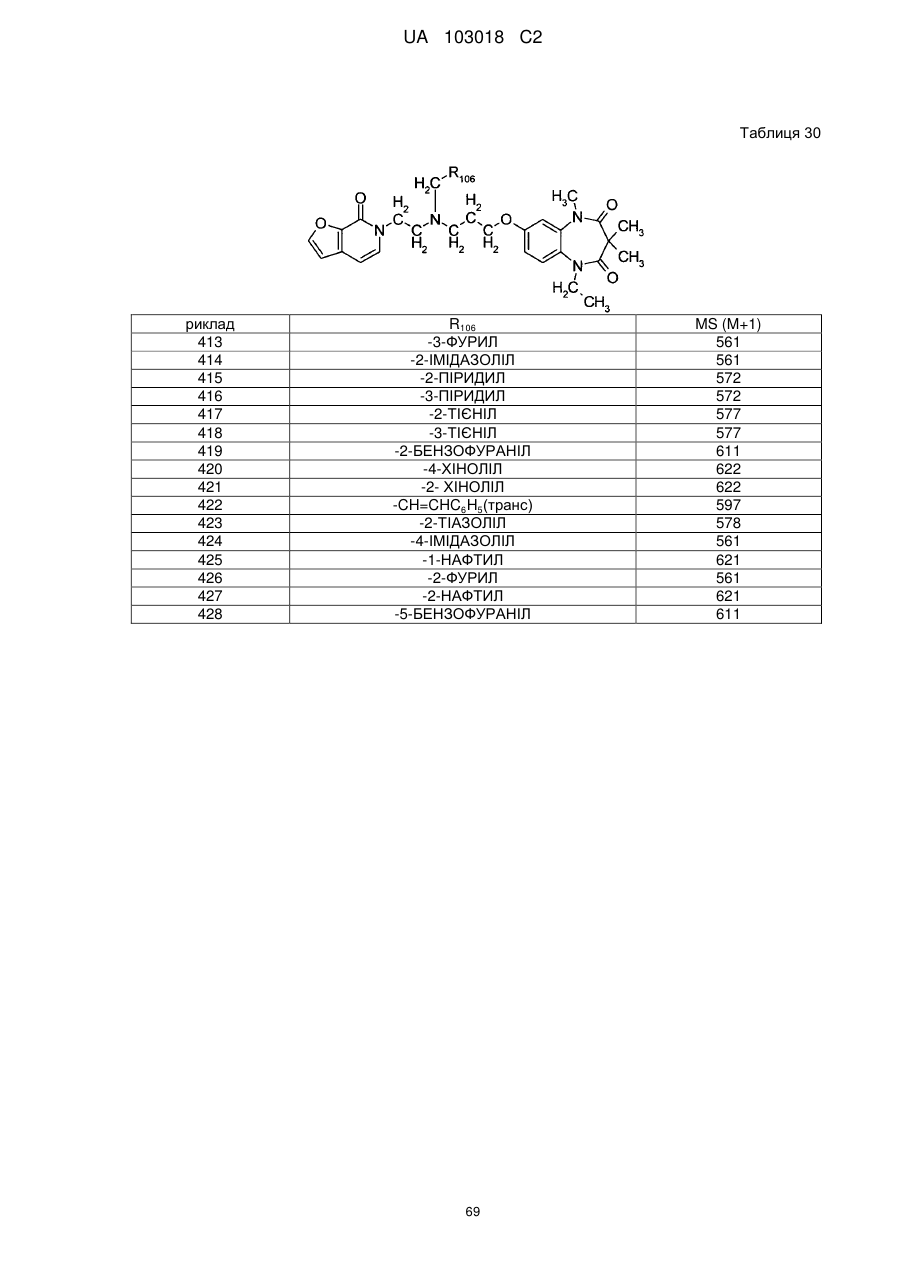
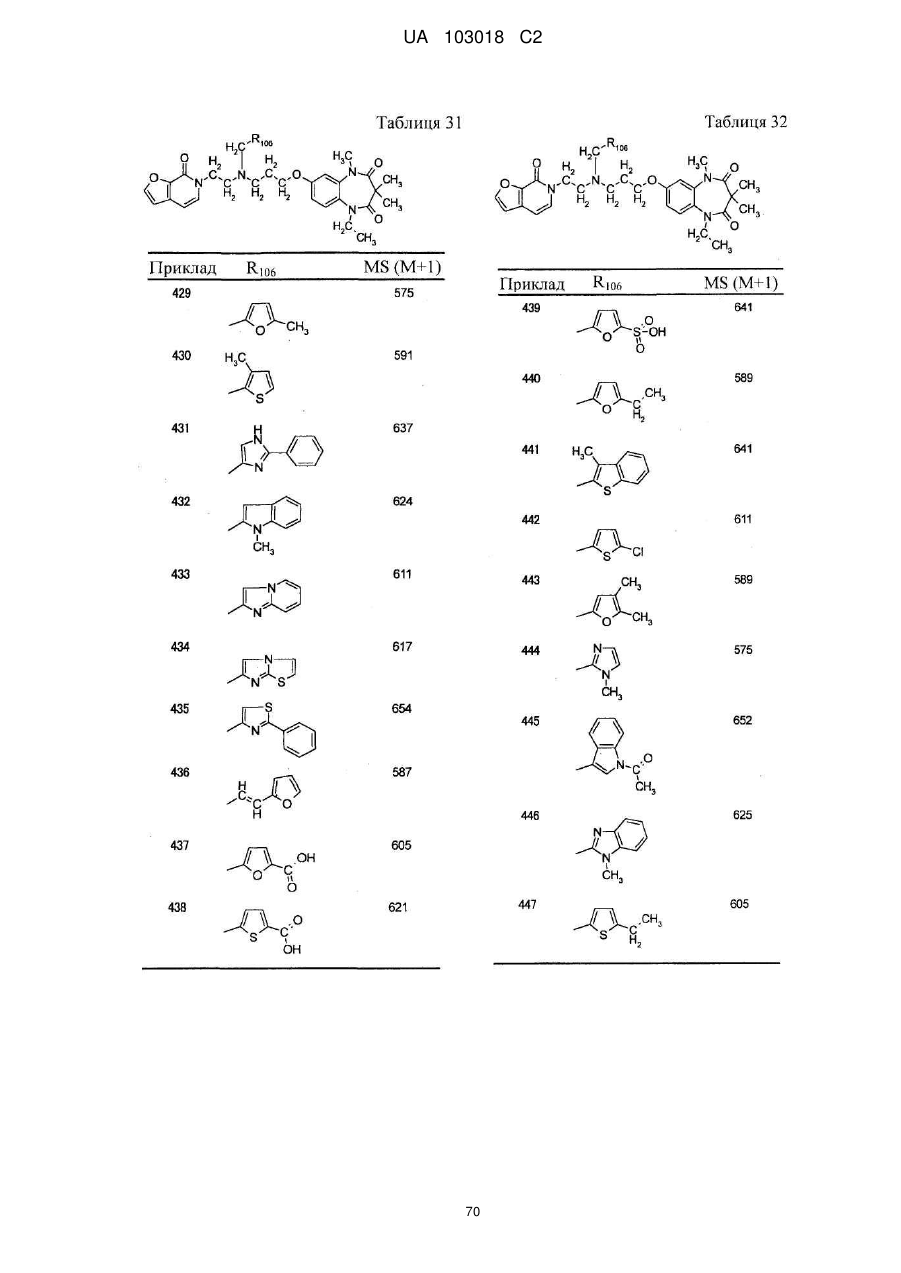
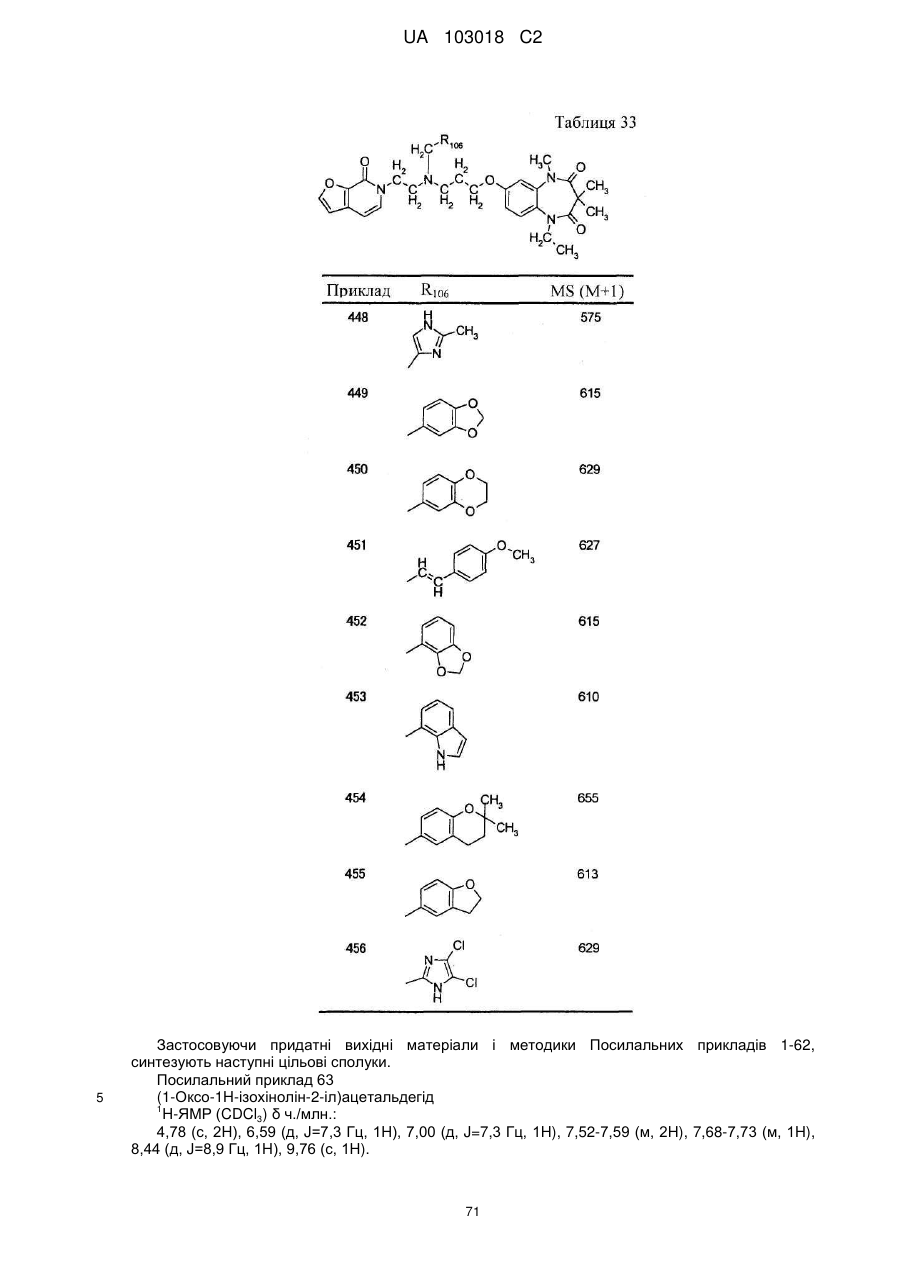
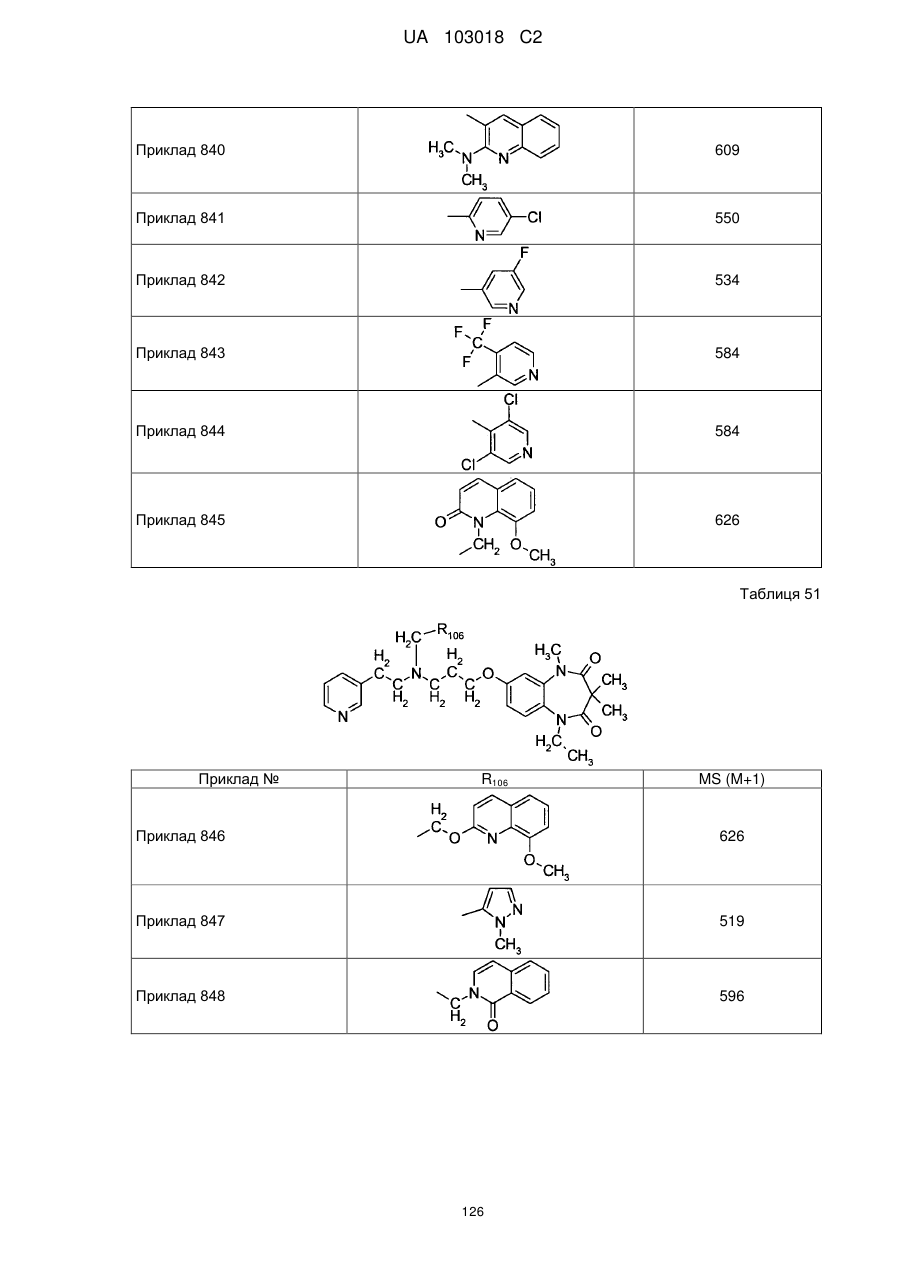
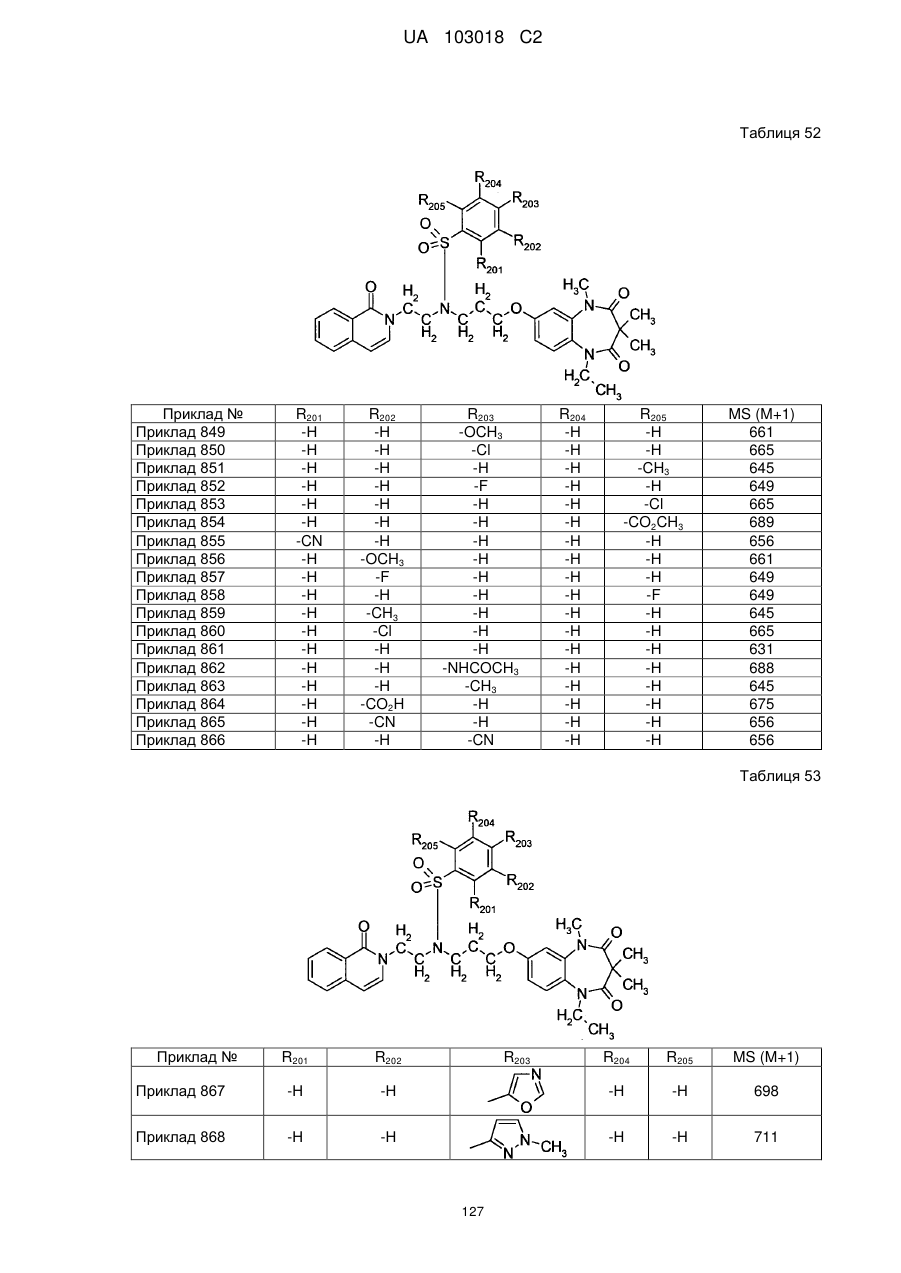
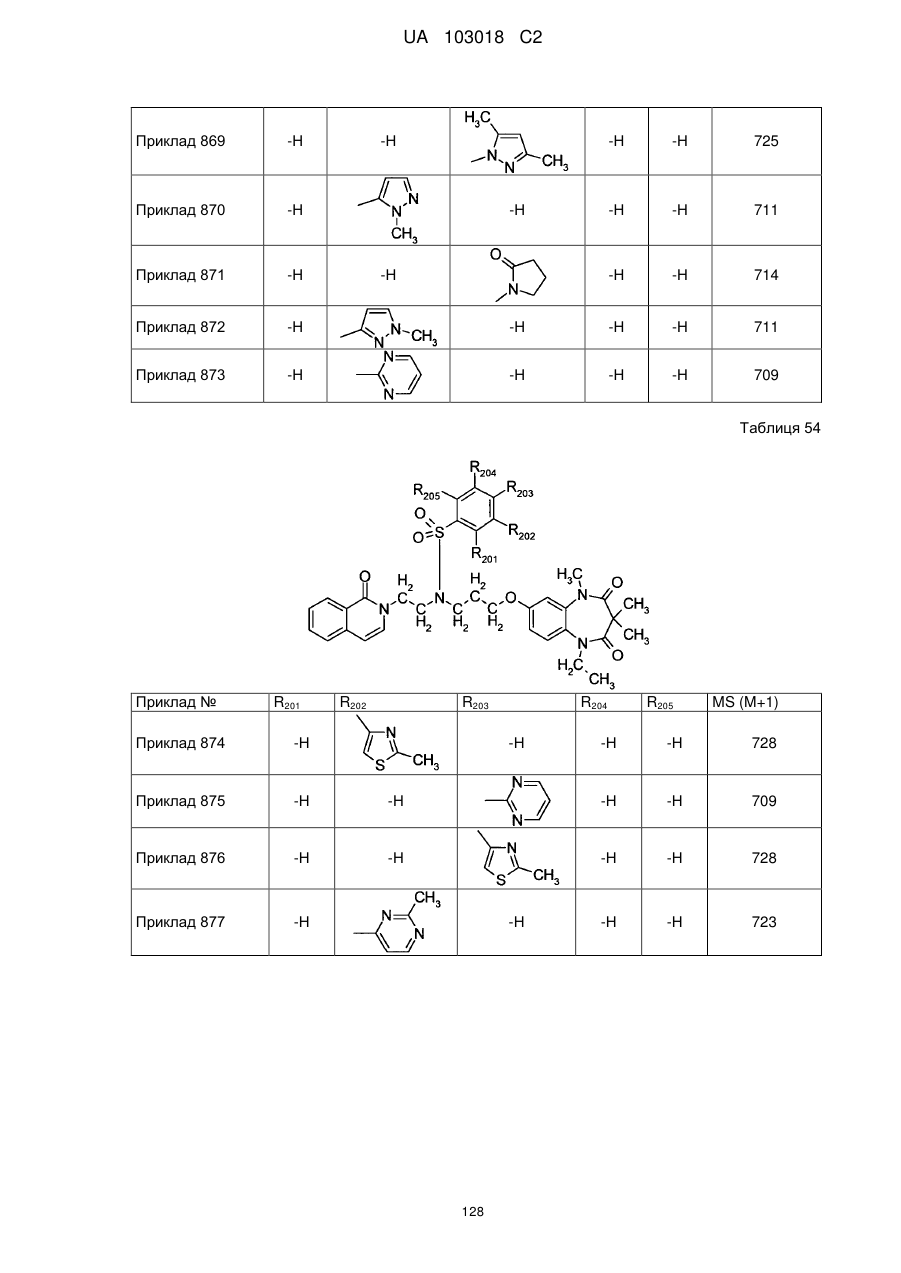
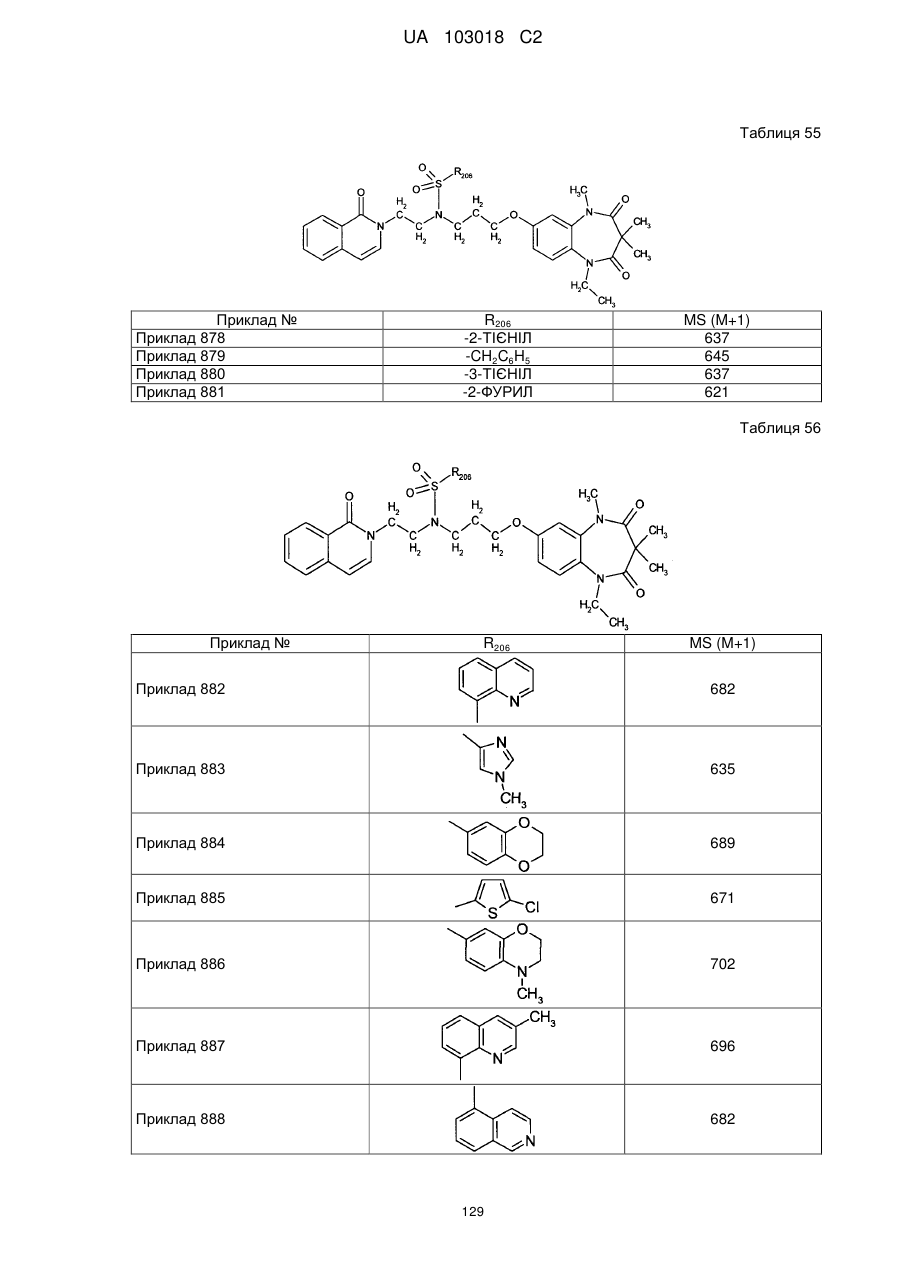
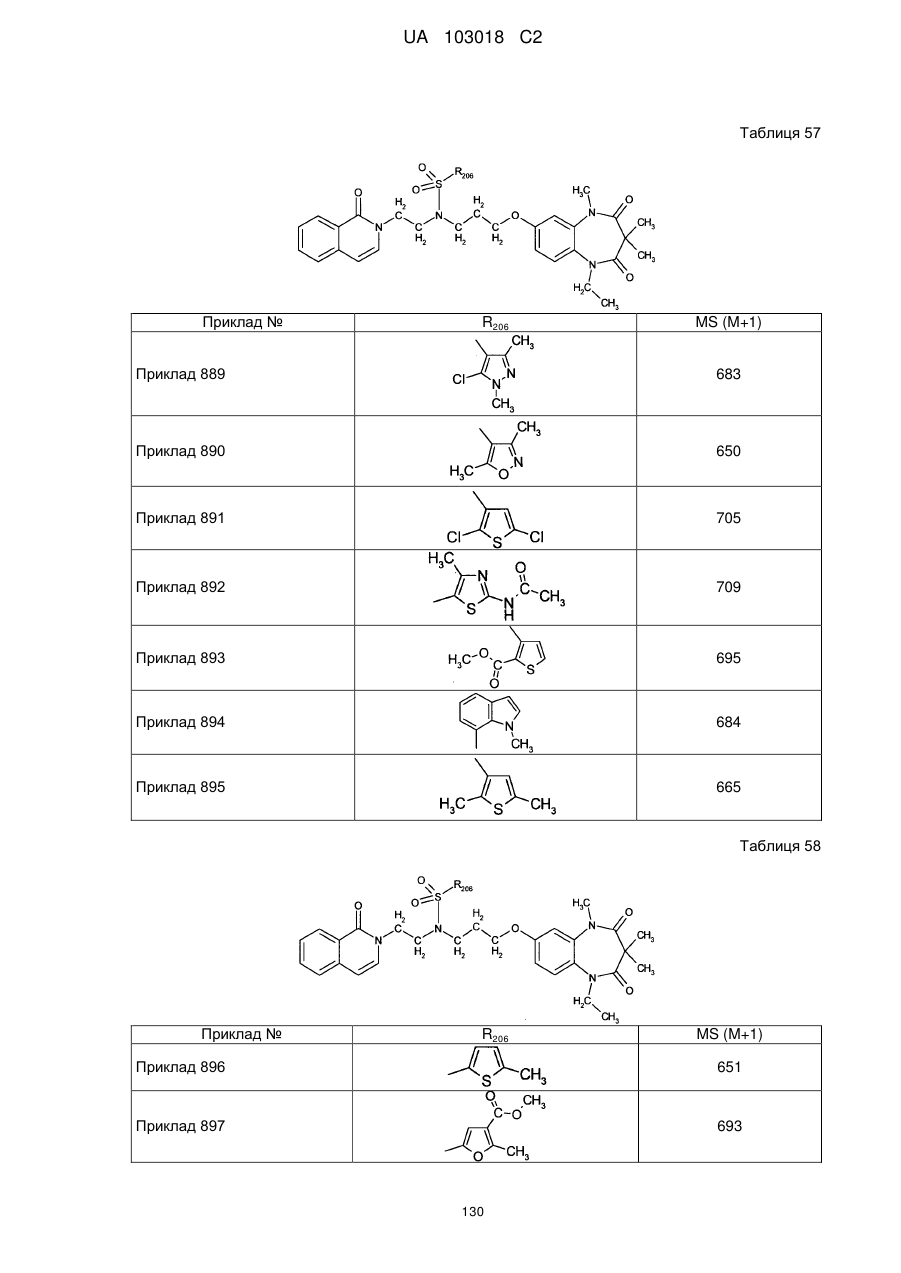
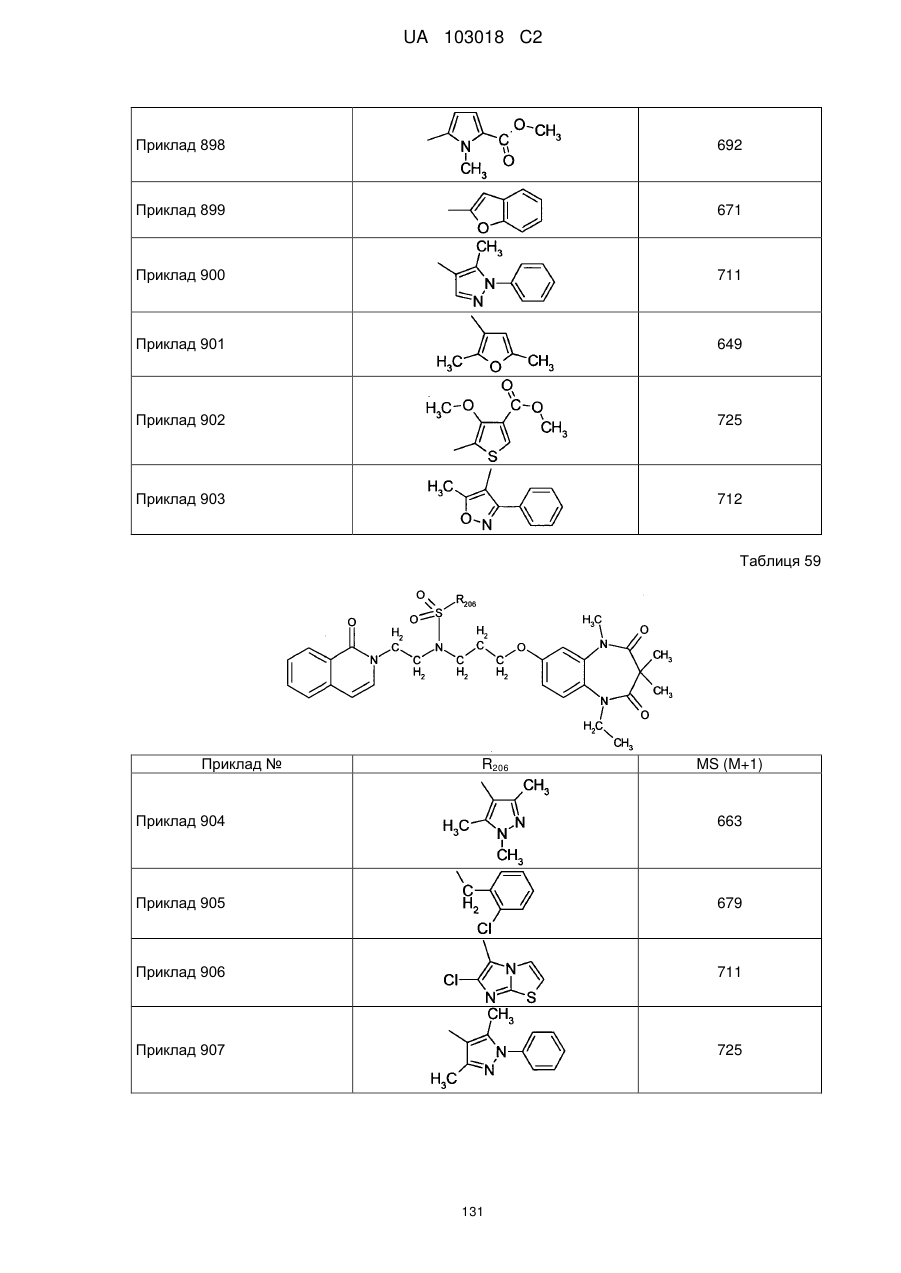
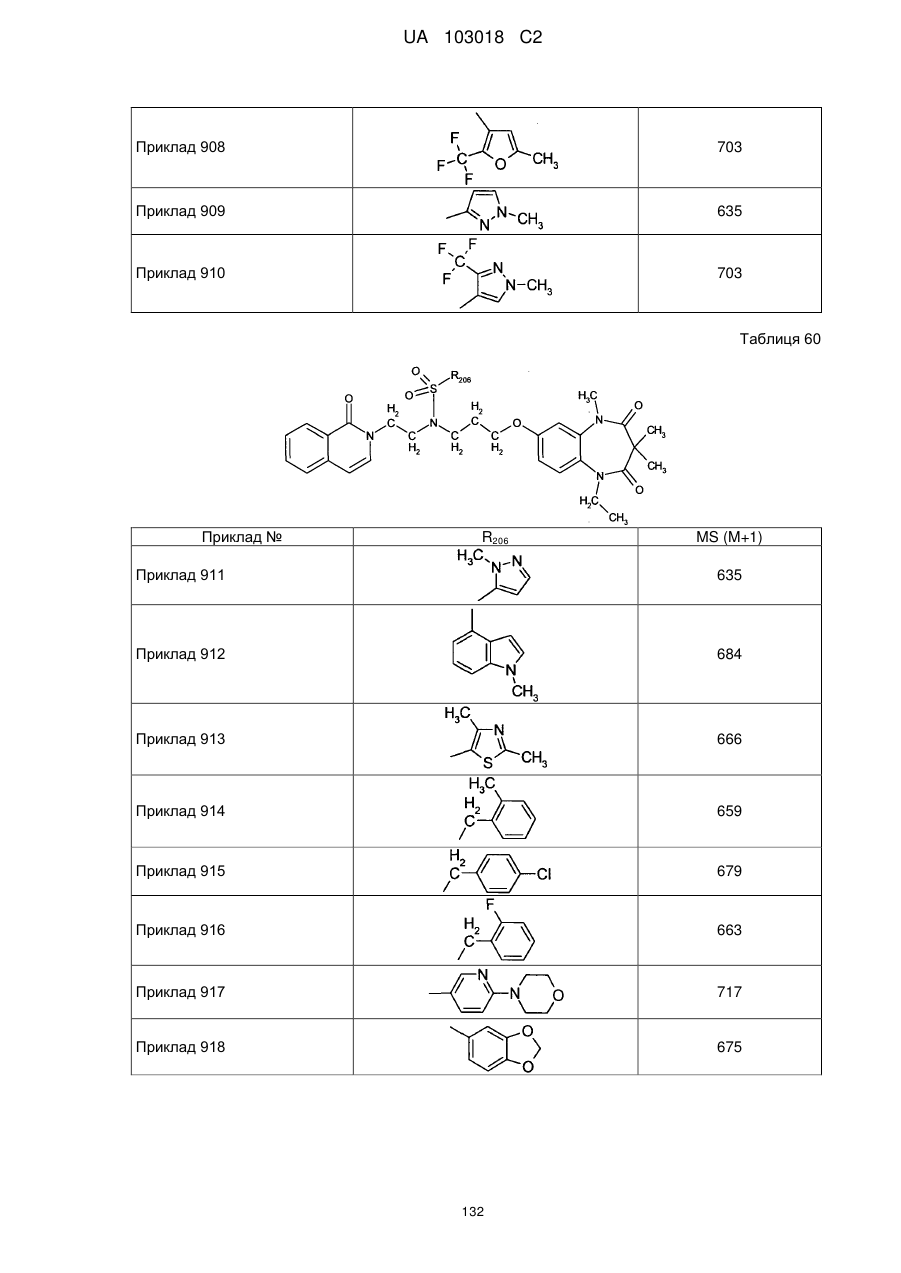
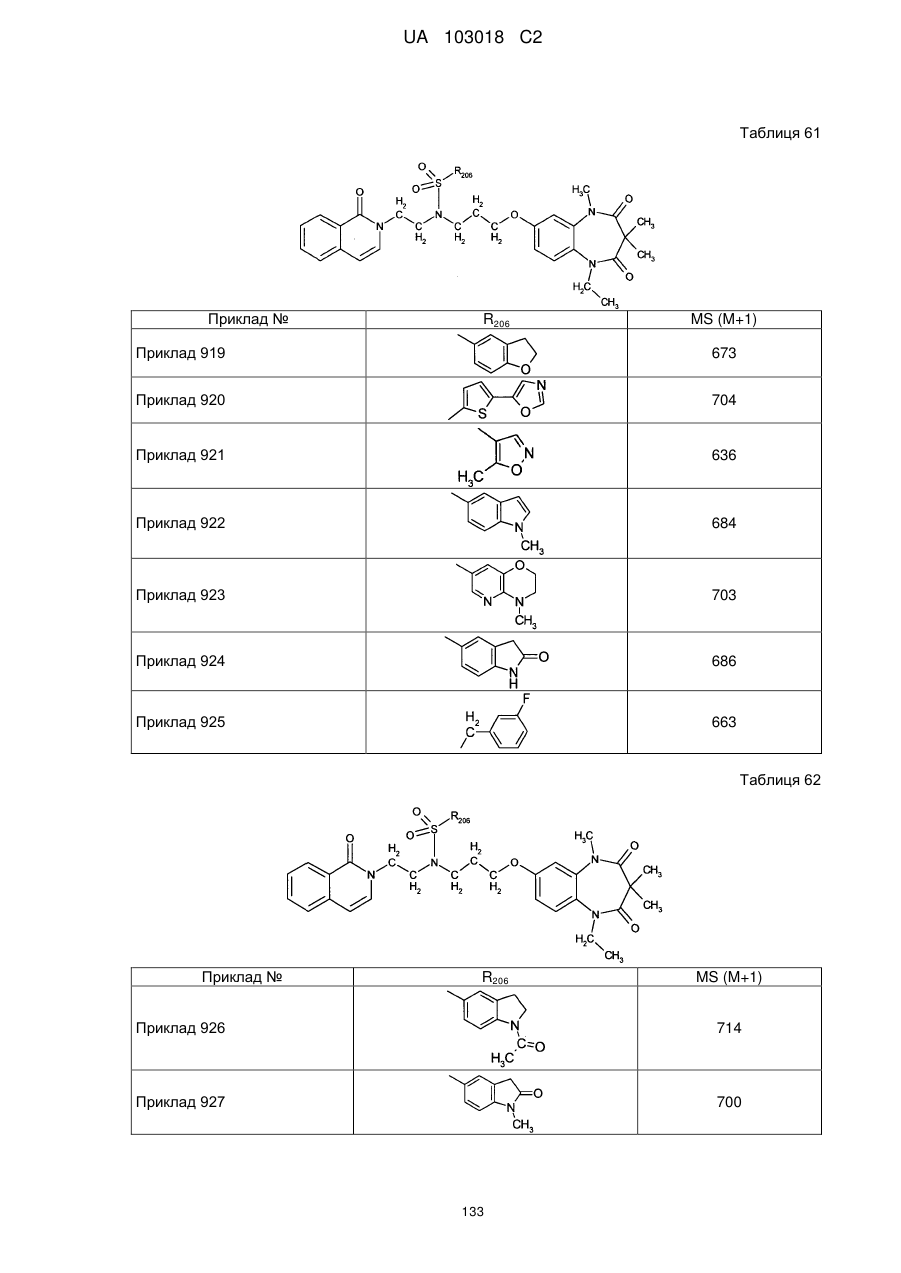
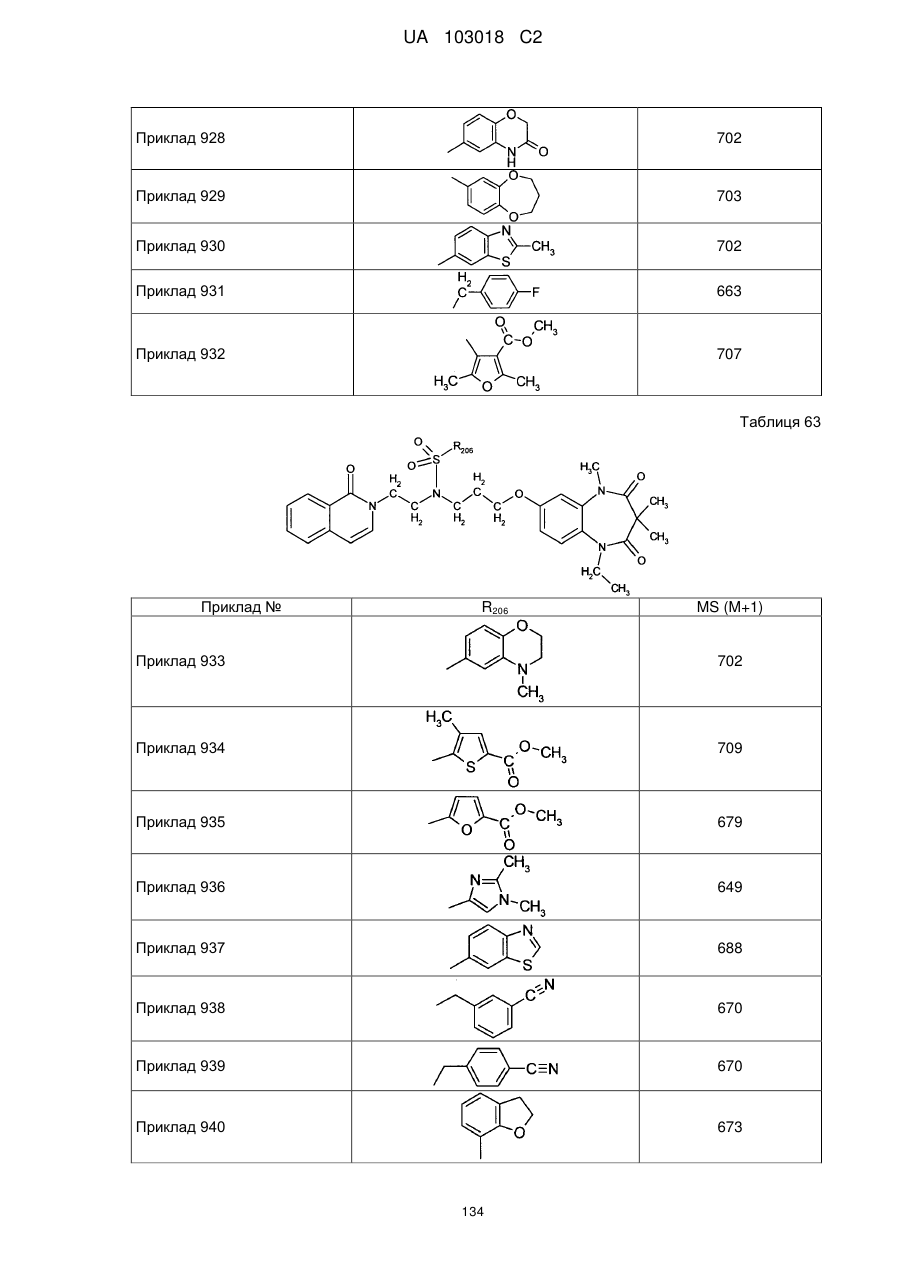
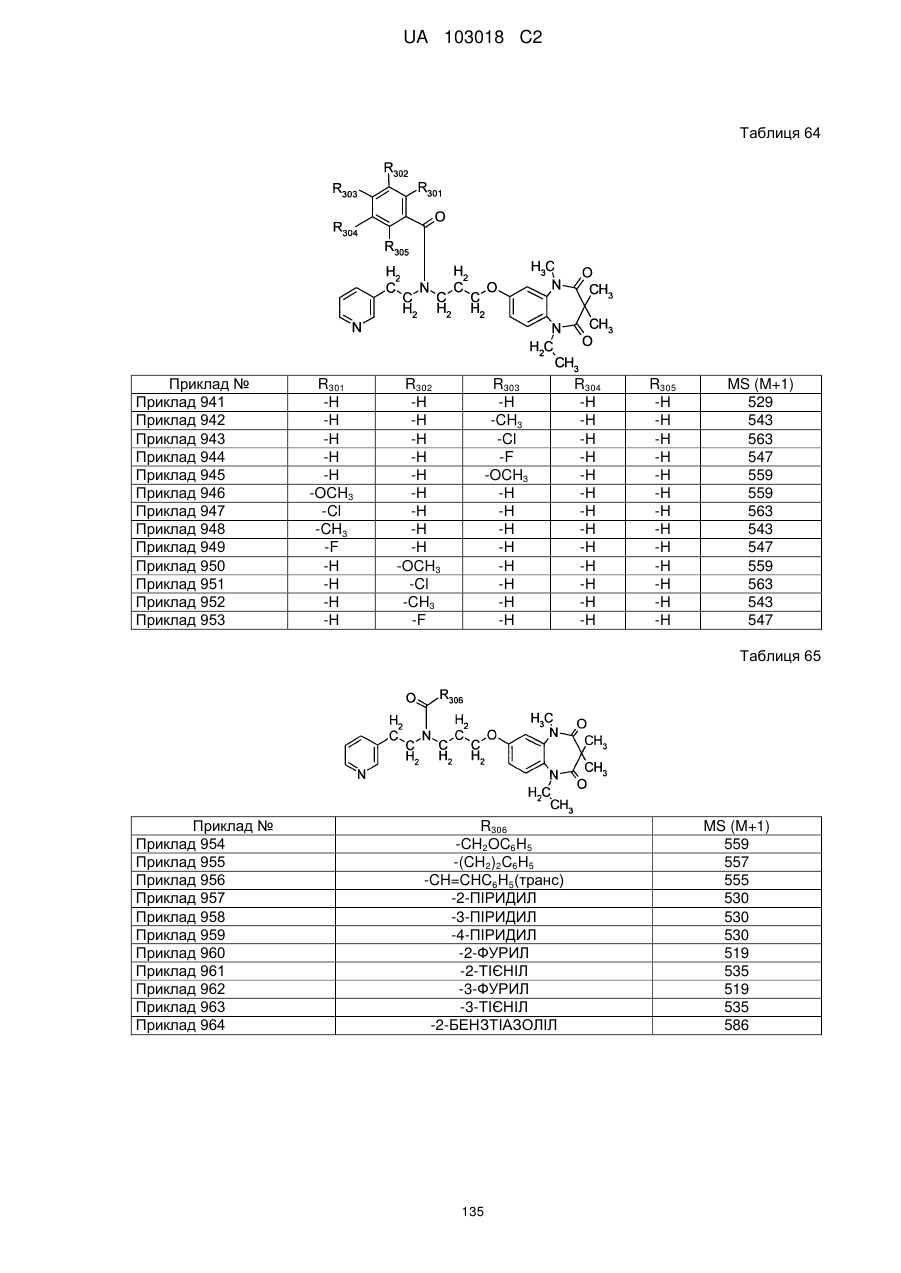
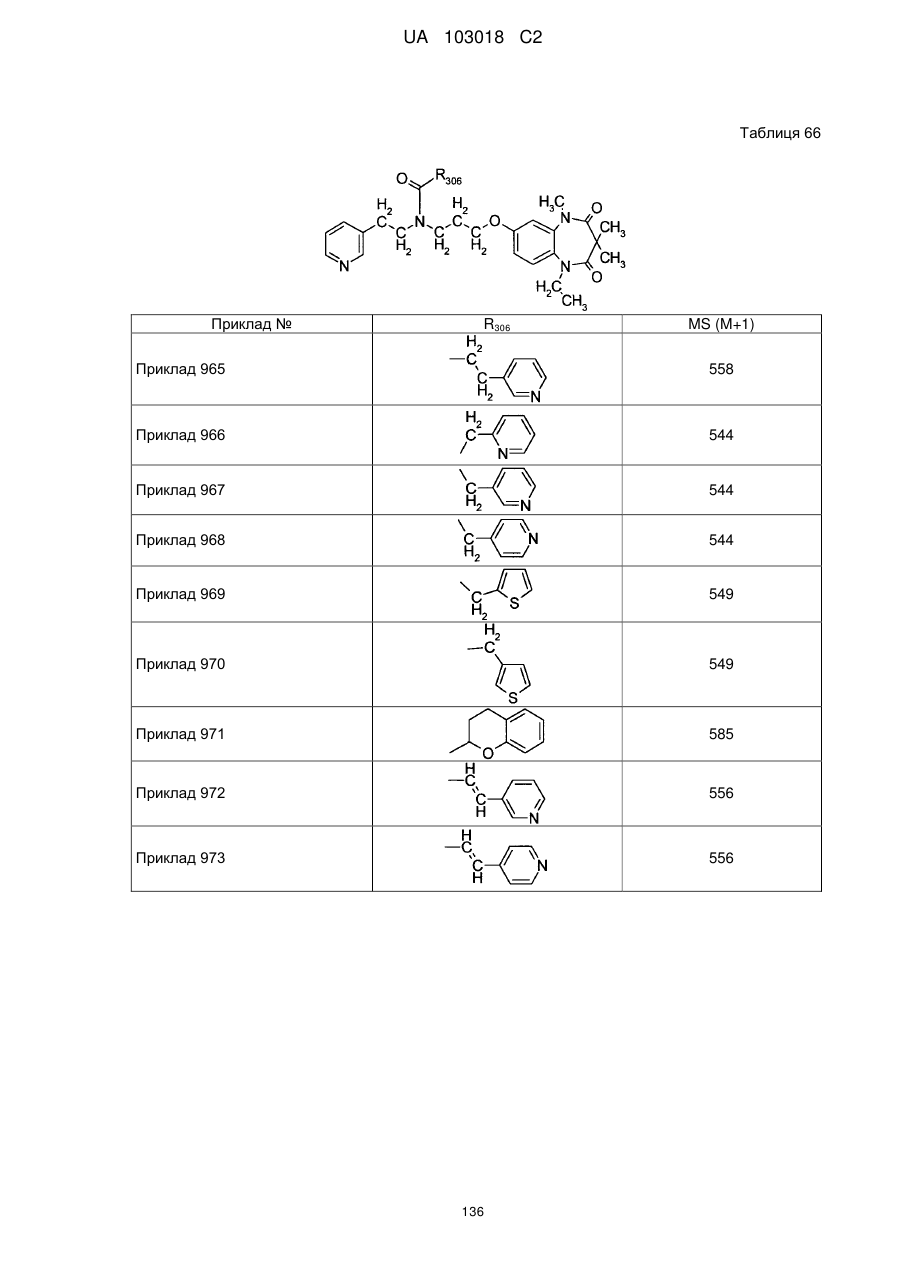
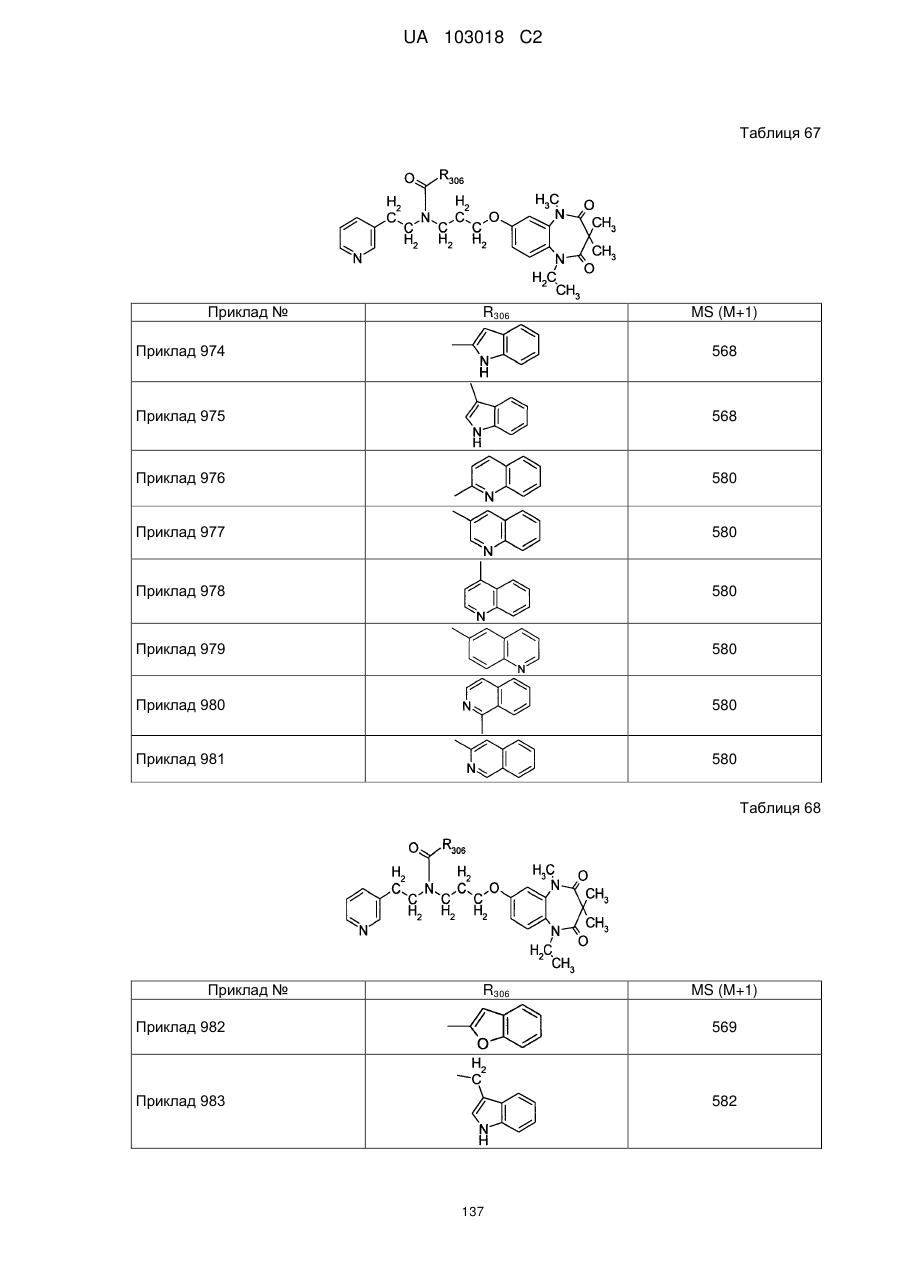
1. Сполука бензодіазепіну, представлена загальною формулою (1)
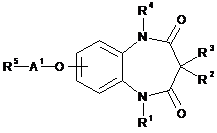 , (1)
, (1)
або її сіль,
де R1, R2, R3 і R4 кожний незалежно є воднем або нижчим алкілом;
R2 і R3 можуть бути зв'язані з утворенням нижчого алкілену;
А1 є нижчим алкіленом, необов'язково заміщеним одним або більше гідрокси; і
R5 є групою, представленою
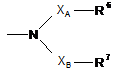 ,
,
де R6 і R7 кожний незалежно є воднем, нижчим алкілом, нижчим циклоалкілом, фенілом, нафтилом, фурилом, тієнілом, піразолілом, оксазолілом, ізоксазолілом, тіазолілом, піролілом, триазолілом, піридилом, піримідинілом, піридазинілом, піразинілом, імідазо[2,1-b]тіазолілом, тієно[2,3-b]піразинілом, 2,3-дигідроімідазо[2,1-b]тіазолілом, бензотіазолілом, індолілом, імідазо[1,2-а]піридилом, бензотієнілом, бензімідазолілом, 2,3-дигідробензо[b]фурилом, бензофурилом, індазолілом, фуро[2,3-с]піридилом, фуро[3,2-с]піридилом, тієно[2,3-с]піридилом, тієно[3,2-с]піридилом, тієно[2,3-b]піридилом, бензо[1,3]діоксолілом, бензізоксазолілом, піразоло[2,3-а]піридилом, індолізинілом, 2,3-дигідроіндолілом, ізохінолілом, 1,2,3,4-тетрагідро-1Н-ізохінолілом, карбостирилом, 3,4-дигідрокарбостирилом, хінолілом, хроманілом, 5,6,7,8-тетрагідроізохінолілом, 3,4-дигідро-1H-ізохінолілом, нафтиридинілом, 1,4-бензодіоксанілом, цинолінілом, хіноксалінілом або 2,3-дигідробенз-1,4-оксазинілом, кожний з яких необов'язково заміщений;
ХА і ХB кожний незалежно є зв'язком, нижчим алкіленом, нижчим алкеніленом, -CO-, -SO2-,- SO2-нижчим алкіленом, -СО-нижчим алкіленом, -СО-нижчим алкеніленом, нижчим алкіленом-N(нижчим алкілом)-СО-нижчим алкіленом, нижчим алкіленом-N(нижчим алкілом)-, нижчим алкіленом-N(нижчим алкілом)-СО- або нижчим алкіленом-О-.
2. Сполука бензодіазепіну, представлена загальною формулою (1), або її сіль за п. 1,
де R6 і R7 кожний є одним з (1)-(52):
(1) водню,
(2) нижчого алкілу,
(3) нижчого циклоалкілу,
(4) фенілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з (4-1)-(4-25):
(4-1) ціано,
(4-2) гідрокси,
(4-3) галогену,
(4-4) нижчого алкілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з галогену, імідазолілу і морфолінілу,
(4-5) нижчого алкокси, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з аміно і нижчого алкіламіно,
(4-6) піридилу,
(4-7) тієнілу,
(4-8) піперазинілу, необов'язково заміщеного одним або більше нижчими алкілами,
(4-9) фенілу,
(4-10) піразолілу, необов'язково заміщеного одним або більше нижчими алкілами,
(4-11) піримідинілу, необов'язково заміщеного одним або більше нижчими алкілами,
(4-12) піперидилу, необов'язково заміщеного одним або більше нижчими алкілами,
(4-13) фурилу,
(4-14) карбокси,
(4-15) нижчого алкоксикарбонілу,
(4-16) аміно, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алканоїлу і нижчого алкілсульфонілу,
(4-17) нижчого алкілтіо,
(4-18) триазолілу,
(4-19) імідазолілу,
(4-20) піролідинілу, необов'язково заміщеного одним або більше оксо,
(4-21) нижчого алкілсульфонілу,
(4-22) нижчого алкілендіокси, необов'язково заміщеного одним або більше галогенами,
(4-23) нітро,
(4-24) оксазолілу, і
(4-25) тіазолілу, необов'язково заміщеного одним або більше нижчими алкілами,
(5) нафтилу,
(6) фурилу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу, необов'язково заміщеного галогеном, карбокси, сульфо, піридилокси, нижчого алкоксикарбонілу і фенілу,
(7) тієнілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу, нижчого алкілендіокси, карбокси, галогену, піридилу, нижчого алкокси, нижчого алкоксикарбонілу, оксазолілу і фурилу,
(8) імідазолілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з фенілу, нижчого алкілу і галогену,
(9) піразолілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу, необов'язково заміщеного галогеном, галогену, фенілу, необов'язково заміщеного нижчим алкокси, фурилу і тієнілу,
(10) оксазолілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу і фенілу,
(11) ізоксазолілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з фенілу, нижчого алкілу, тієнілу і фурилу,
(12) тіазолілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу, необов'язково заміщеного нижчим алкокси, фенілу і нижчого алканоїламіно,
(13) піролілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу і нижчого алкоксикарбонілу,
(14) триазолілу, необов'язково заміщеного одним або більше нижчими алкілами,
(15) піридилу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу, необов'язково заміщеного галогеном, оксо, гідрокси, нижчого алкокси, галогену, піролідинілу, морфолінілу і тієнілу,
(16) піримідинілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу і фенілу,
(17) піридазинілу,
(18) піразинілу,
(19) імідазо[2,1-b]тіазолілу, необов'язково заміщеного одним або більше галогенами,
(20) тієно[2,3-b]піразинілу,
(21) 2,3-дигідроімідазо[2,1-b]тіазолілу, необов'язково заміщеного одним або більше фенілами,
(22) бензотіазолілу, необов'язково заміщеного одним або більше нижчими алкілами,
(23) індолілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу, нижчого алканоїлу і галогену,
(24) імідазо[1,2-а]піридилу, необов'язково заміщеного одним або більше нижчими алкілами,
(25) бензотієнілу, необов'язково заміщеного одним або більше нижчими алкілами,
(26) бензімідазолілу, необов'язково заміщеного одним або більше нижчими алкілами,
(27) 2,3-дигідробензо[b]фурилу,
(28) бензофурилу, необов'язково заміщеного одним або більше галогенами,
(29) індазолілу, необов'язково заміщеного одним або більше нижчими алкілами,
(30) фуро[2,3-с]піридилу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з оксо і нижчого алкілу,
(31) фуро[3,2-с]піридилу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з оксо, нижчого алкілу, необов'язково заміщеного галогеном, галогену, фурилу, піридилу і фенілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з аміно і нижчого алкокси,
(32) тієно[2,3-с]піридилу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з оксогрупи і нижчого алкілу,
(33) тієно[3,2-с]піридилу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з оксо і нижчого алкілу,
(34) тієно[2,3-b]піридилу,
(35) бензо[1,3]діоксолілу, необов'язково заміщеного одним або більше галогенами,
(36) бензізоксазолілу,
(37) піразоло[2,3-а]піридилу,
(38) індолізинілу,
(39) 2,3-дигідроіндолілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з оксо, нижчого алкілу і нижчого алканоїлу,
(40) ізохінолілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу, галогену і оксо,
(41) 1,2,3,4-тетрагідро-1H-ізохінолілу, необов'язково заміщеного одним або більше оксо,
(42) карбостирилу, необов'язково заміщеного одним або більше нижчими алкокси,
(43) 3,4-дигідрокарбостирилу, необов'язково заміщеного одним або більше нижчими алкокси,
(44) хінолілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з аміно, необов'язково заміщеного одним або двома нижчими алкілами, нижчого алкокси, нижчого алкілу і оксо,
(45) хроманілу, необов'язково заміщеного одним або більше нижчими алкілами,
(46) 5,6,7,8-тетрагідроізохінолілу, необов'язково заміщеного одним або більше оксо,
(47) 3,4-дигідро-1Н-ізохінолілу, необов'язково заміщеного одним або більше оксо,
(48) нафтиридинілу,
(49) 1,4-бензодіоксанілу,
(50) цинолінілу,
(51) хіноксалінілу, або
(52) 2,3-дигідробенз-1,4-оксазинілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу і оксо.
3. Сполука бензодіазепіну, представлена загальною формулою (1), або її сіль за п. 2,
де R6 і R7 кожний є одним з (4а), (6а), (7а), (15а), (30а), (31а), (32а), (33а), (40а) і (44а):
(4а) фенілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з (4а-1), (4а-4) і (4а-6):
(4a-1) ціано,
(4a-4) нижчого алкілу, необов'язково заміщеного одним або більше галогенами, і
(4а-6) піридилу,
(6а) фурилу,
(7а) тієнілу,
(15а) піридилу, необов'язково заміщеного одним або більше нижчими алкілами,
(30а) фуро[2,3-с]піридилу, необов'язково заміщеного одним або більше оксо,
(31а) фуро[3,2-с]піридилу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з оксо і нижчого алкілу,
(32а) тієно[2,3-с]піридилу, необов'язково заміщеного одним або більше оксо,
(33а) тієно[3,2-с]піридилу, необов'язково заміщеного одним або більше оксо,
(40а) ізохінолілу, необов'язково заміщеного одним або більше оксо, і
(44а) хінолілу, необов'язково заміщеного одним або більше оксо.
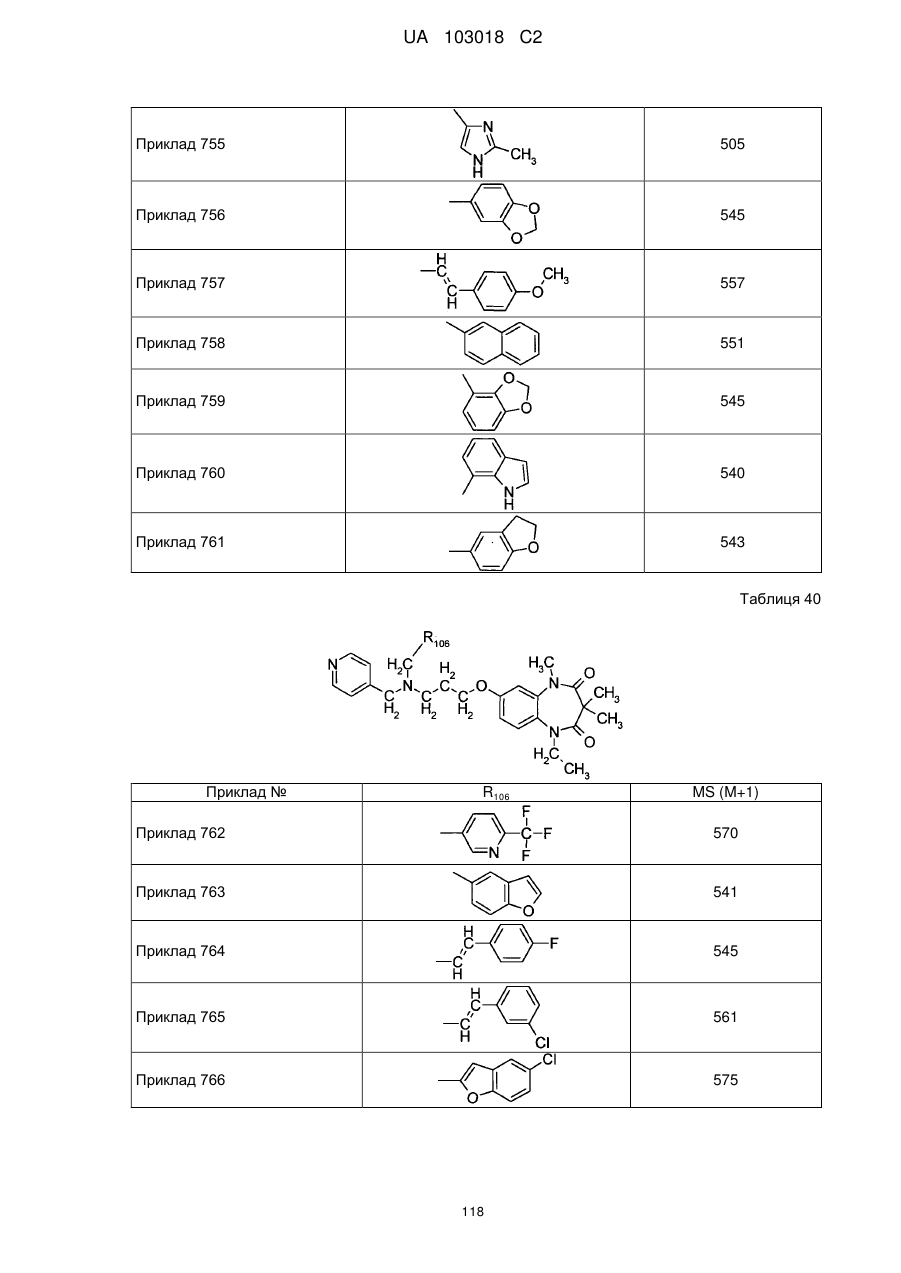
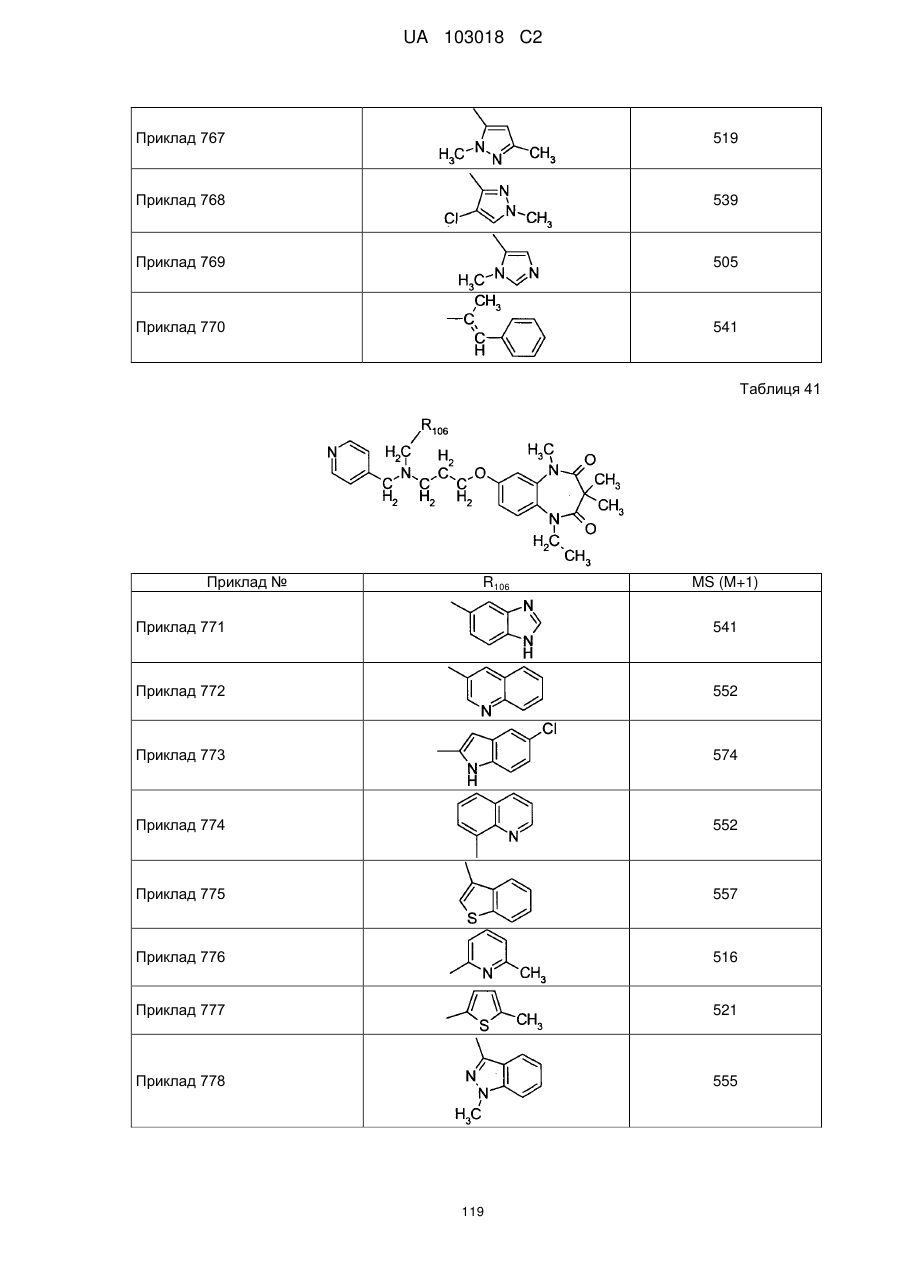
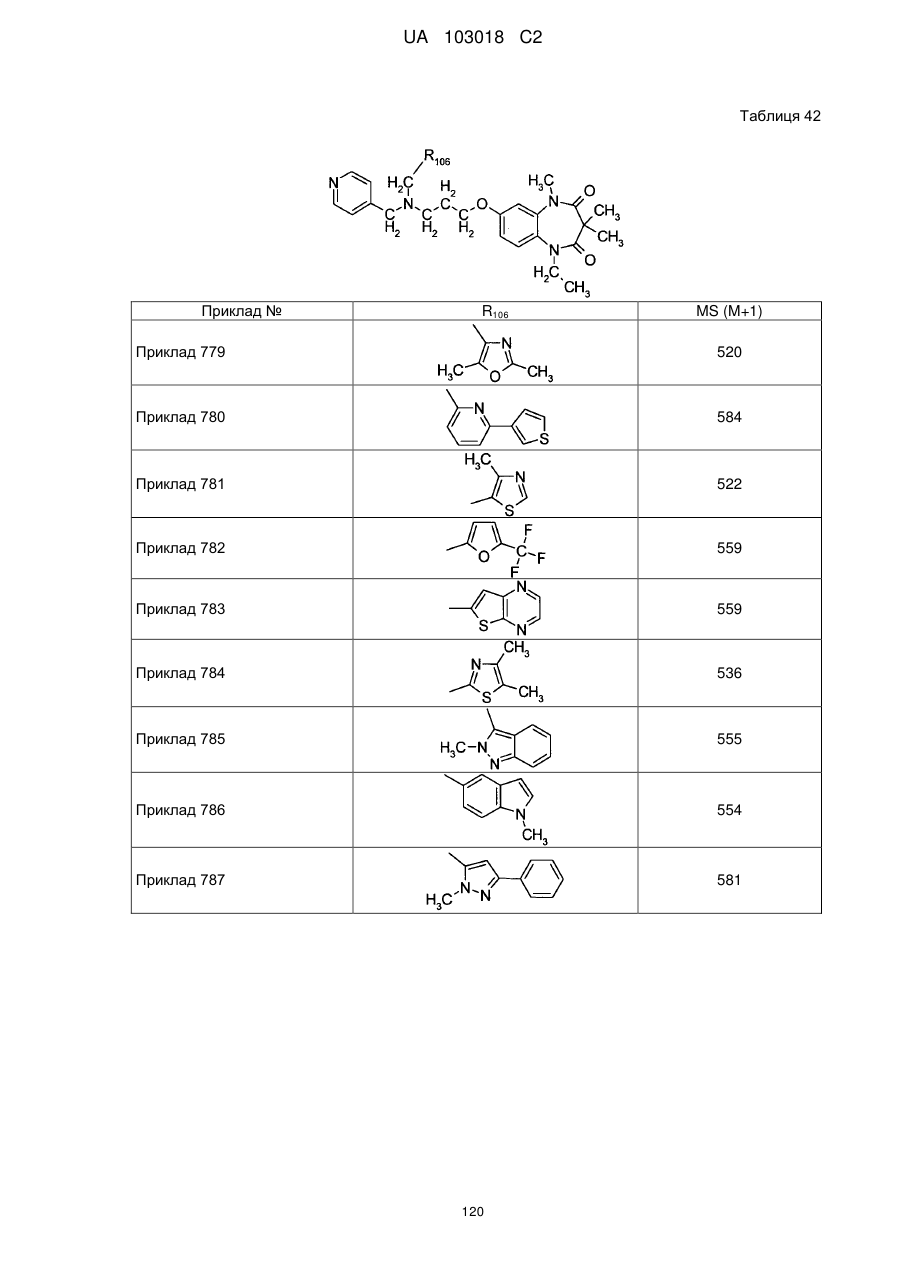
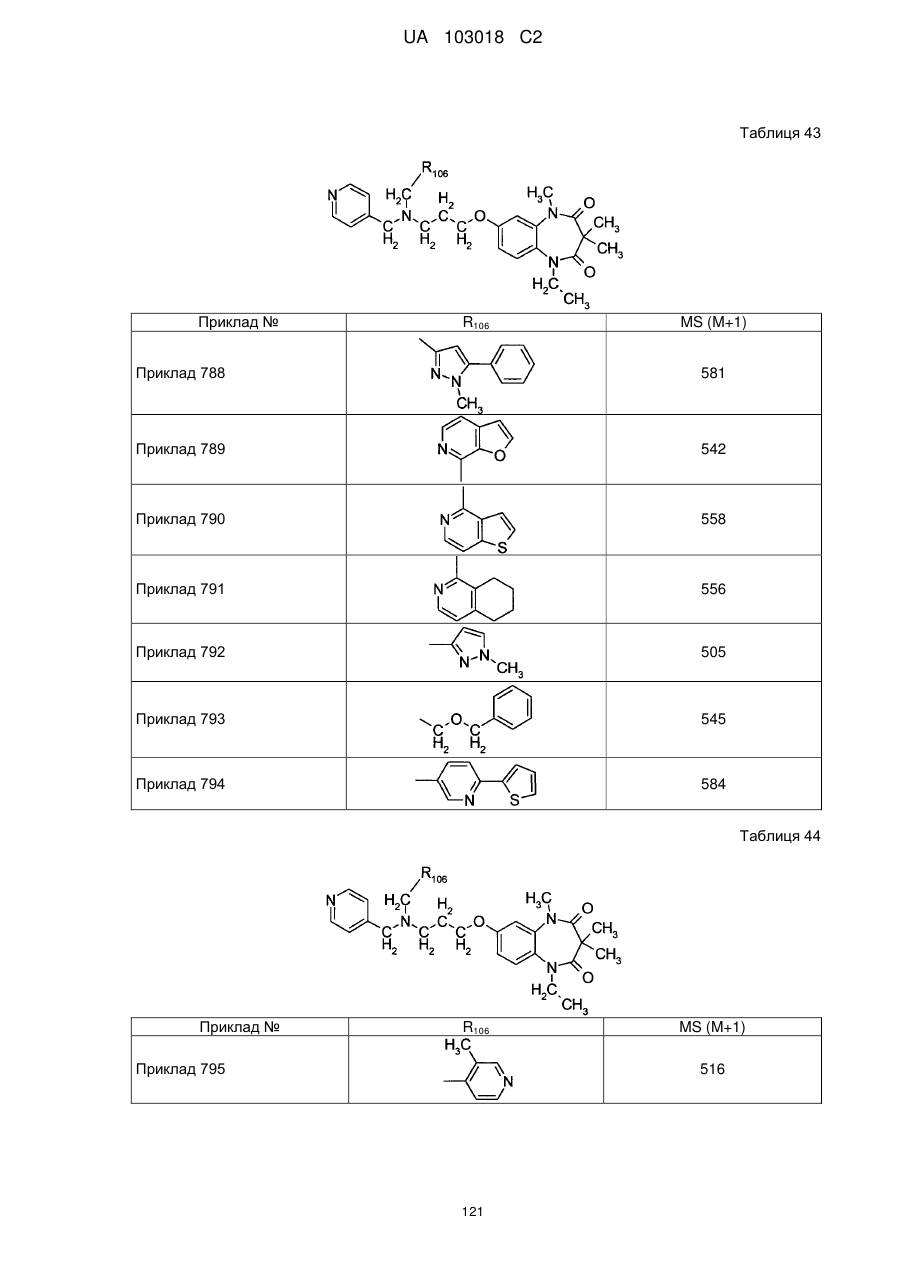
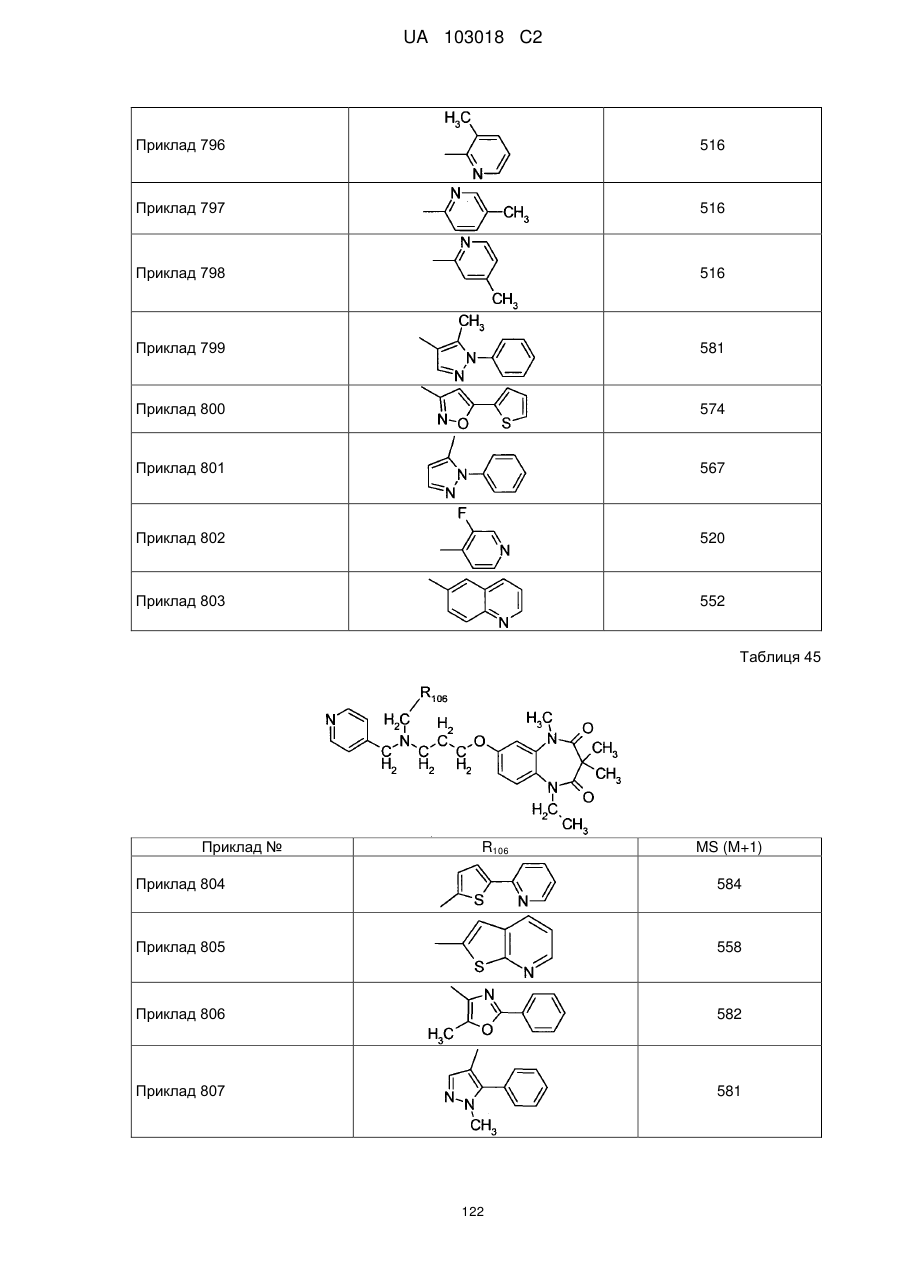
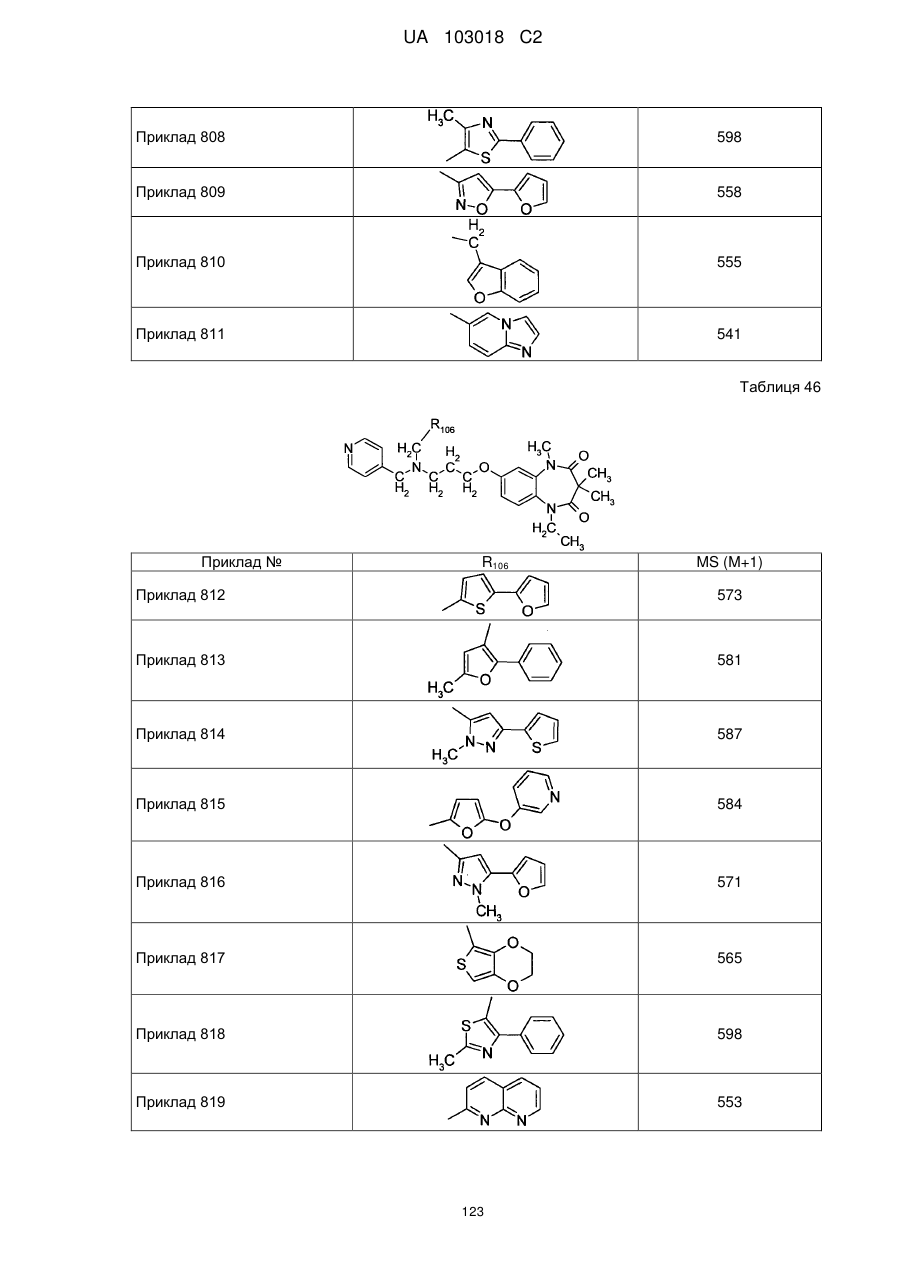
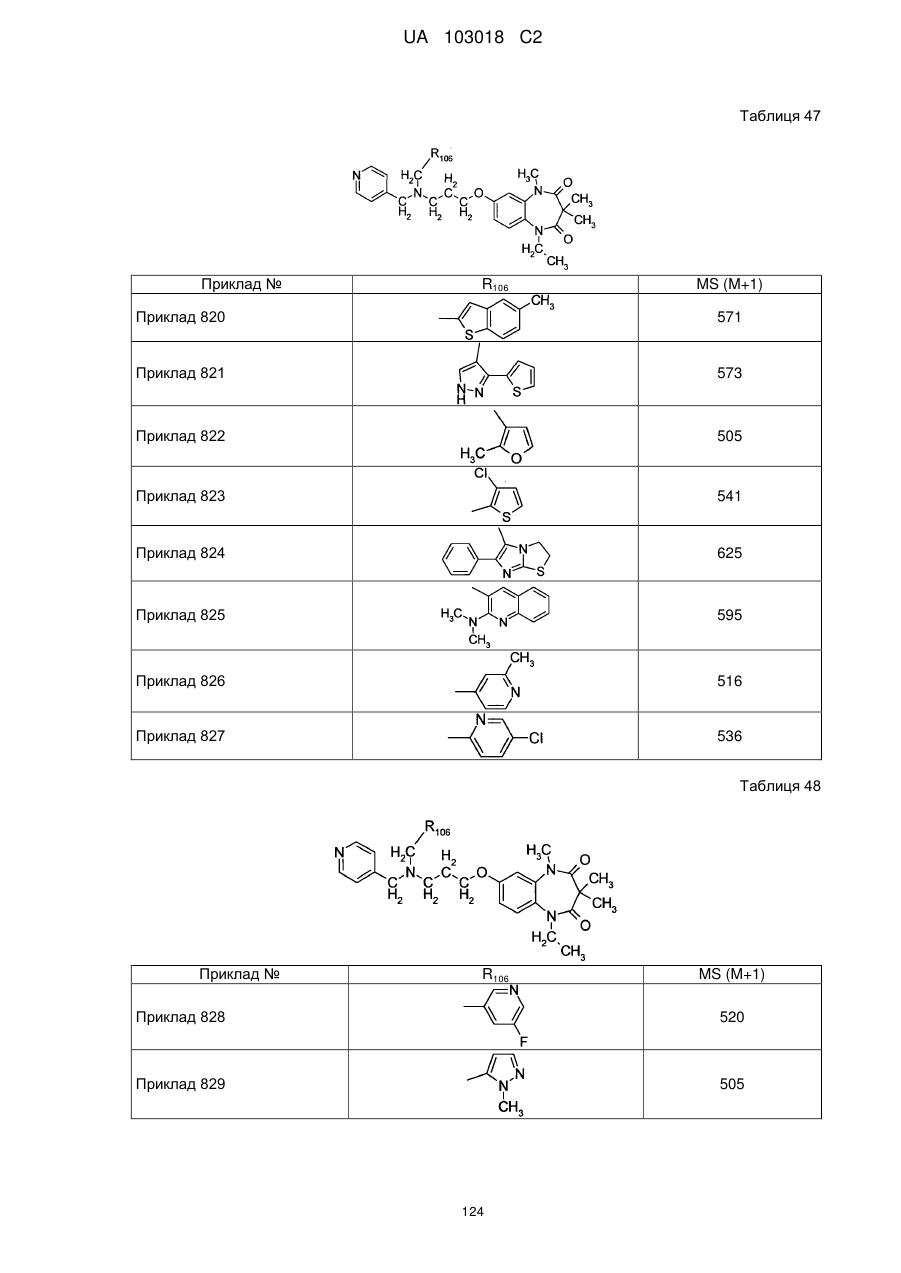
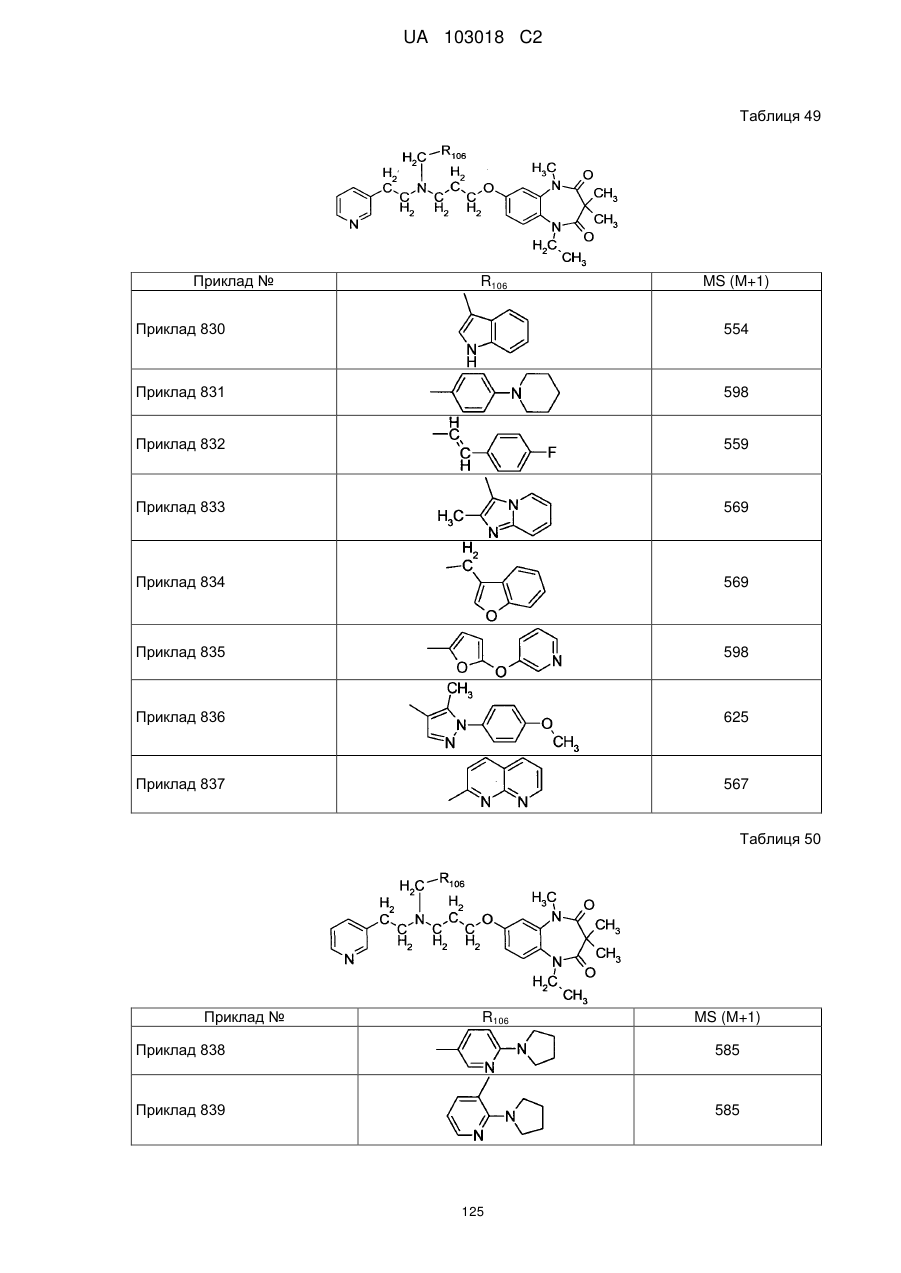
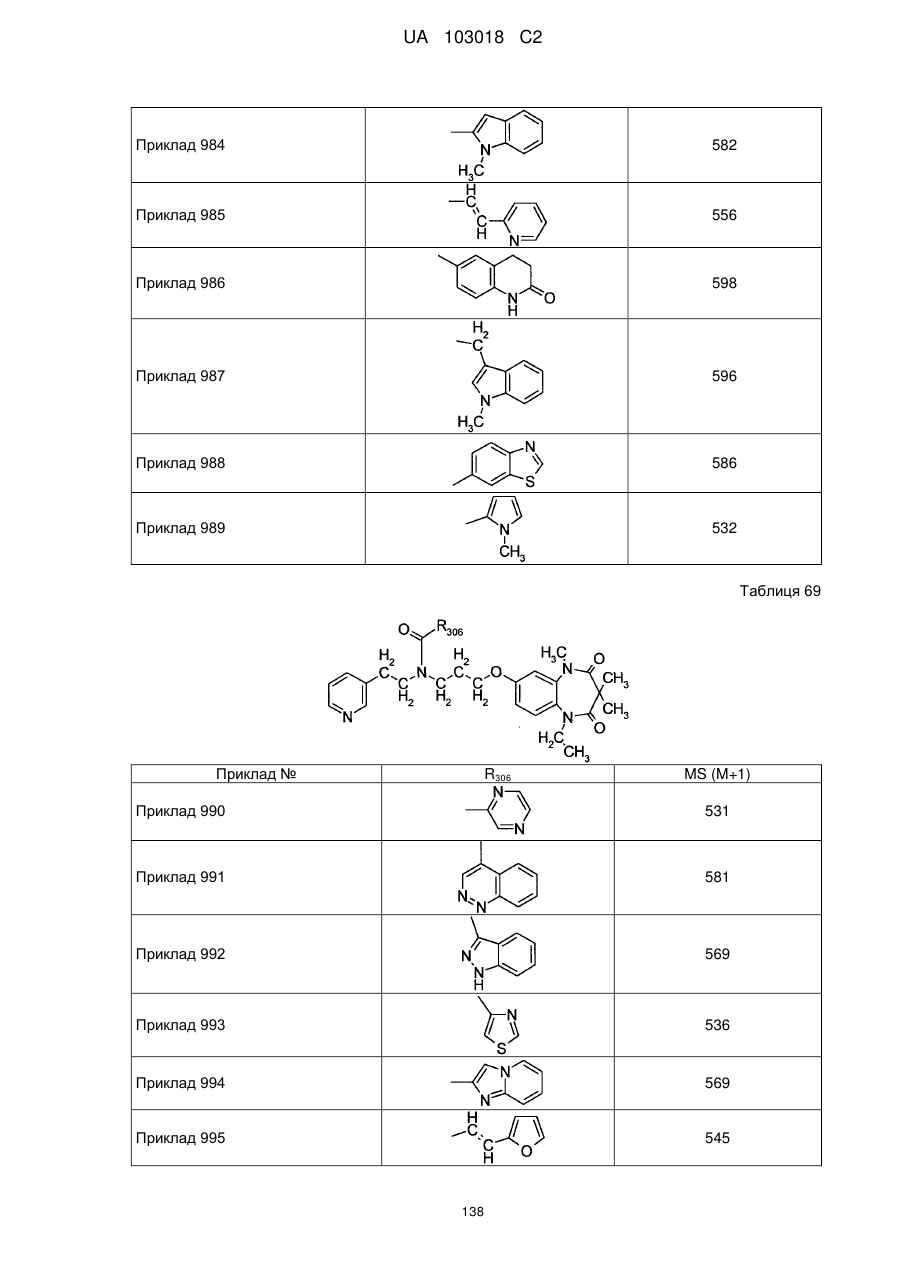
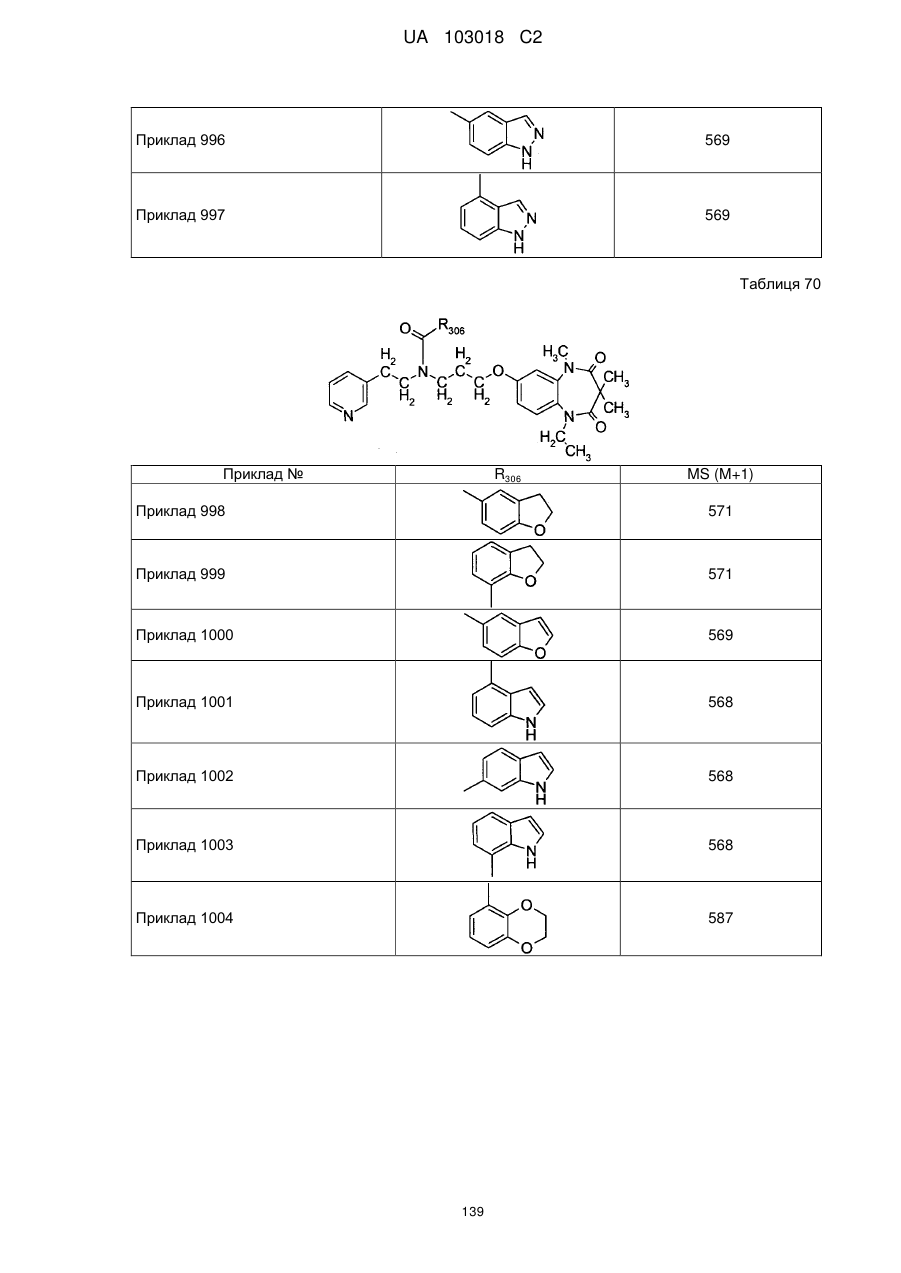
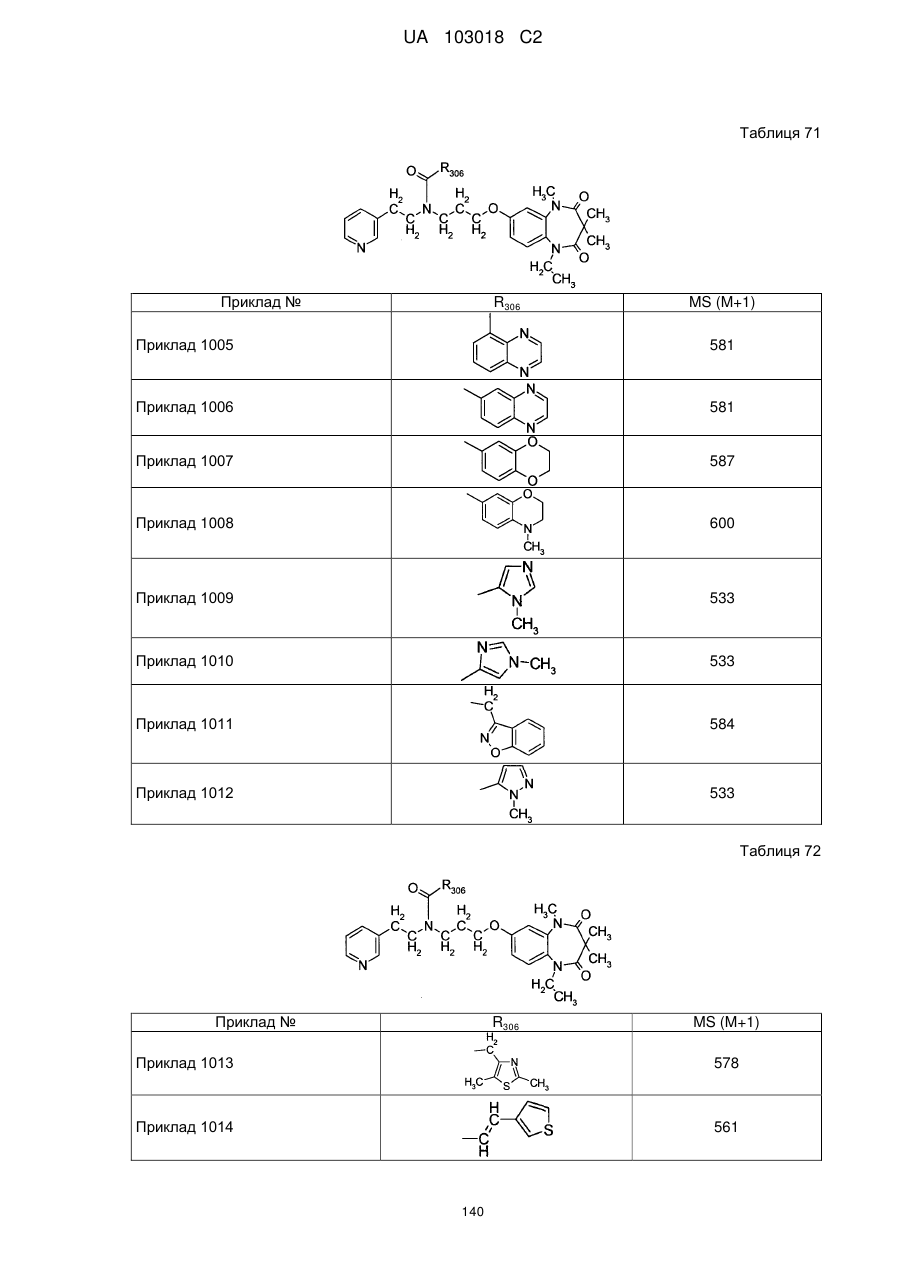
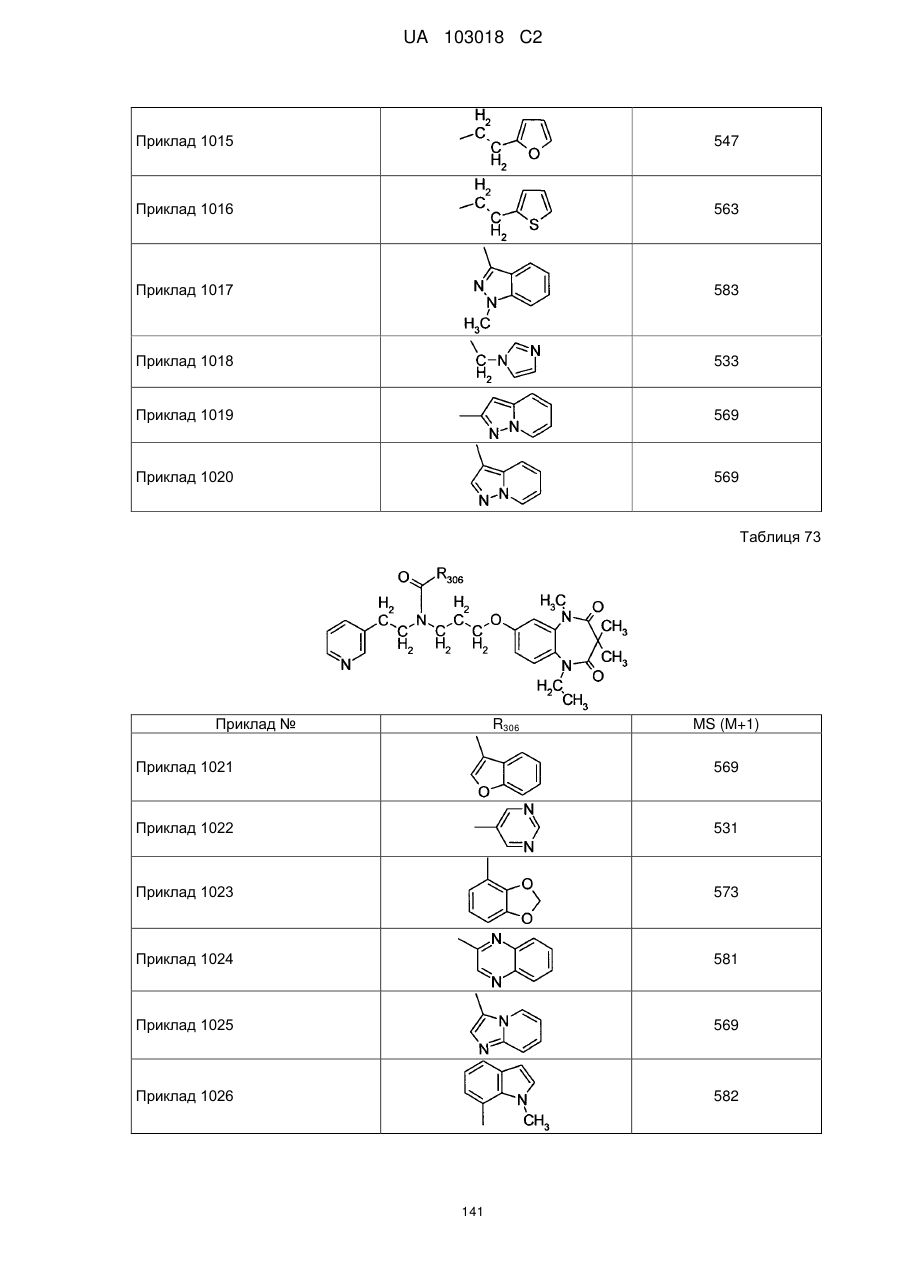
4. Сполука бензодіазепіну, представлена загальною формулою (1), або її сіль за п. 3, яку вибирають з групи, що складається з наступних сполук:
тригідрохлорид 1-етил-3,3,5-триметил-7-{3-[(2-піридин-3-ілетил)піридин-4-ілметиламіно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діону,
тригідрохлорид 3,3,5-триметил-1-пропіл-7-{3-[(2-піридин-3-ілетил)піридин-4-ілметиламіно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діону,
тригідрохлорид 1,5-діетил-3,3-диметил-7-{3-[(2-піридин-3-ілетил)піридин-4-ілметиламіно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діону,
тригідрохлорид 1,3,3,5-тетраметил-7-{3-[(2-піридин-3-ілетил)піридин-4-ілметиламіно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діону,
дигідрохлорид 1-етил-3,3,5-триметил-7-(3-{[2-(1-оксо-1H-ізохінолін-2-іл)етил]піридин-4-ілметиламіно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діону,
дигідрохлорид 1-етил-3,3,5-триметил-7-(3-{[2-(7-оксо-7Н-фуро[2,3-с]піридин-6-іл)етил]піридин-4-ілметиламіно}пропокси)-1,5-дигідробензо[b][1,4]-діазепін-2,4-діону,
дигідрохлорид N-метил-N-(2-{піридин-4-ілметил-[3-(1,3,3,5-тетраметил-2,4-діоксо-2,3,4,5-тетрагідро-1Н-бензо[b][1,4]діазепін-7-ілокси)пропіл]аміно}етил)-бензаміду,
дигідрохлорид 1,3,3,5-тетраметил-7-{3-[(2-метилбензил)-(2-піридин-3-ілетил)аміно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діону,
тригідрохлорид 1,3,3,5-тетраметил-7-{3-[(2-піридин-3-ілетил)-(хінолін-4-ілметил)аміно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діону,
тригідрохлорид 1-етил-3,3,5-триметил-7-{3-[(3-метилпіридин-4-ілметил)-(2-піридин-3-ілетил)аміно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діону,
дигідрохлорид 1-етил-3,3,5-триметил-7-(3-{[2-(2-оксо-2Н-хінолін-1-іл)етил]піридин-4-ілметиламіно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діону,
дигідрохлорид 1-етил-3,3,5-триметил-7-(3-{[2-(7-оксо-7Н-тієно[2,3-с]піридин-6-іл)етил]піридин-4-ілметиламіно}пропокси)-1,5-дигідробензо[b][1,4]-діазепін-2,4-діону,
4-({[3-(1-етил-3,3,5-триметил-2,4-діоксо-2,3,4,5-тетрагідро-1Н-бензо[b][1,4]діазепін-7-ілокси)пропіл]-[2-(1-оксо-1Н-ізохінолін-2-іл)етил]аміно}метил)бензонітрил,
1-етил-3,3,5-триметил-7-(3-{[2-(1-оксо-1H-ізохінолін-2-іл)етил]тіофен-3-ілметиламіно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діон,
1-етил-7-(3-{фуран-2-ілметил-[2-(1-оксо-1Н-ізохінолін-2-іл)етил]аміно}пропокси)-3,3,5-триметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діон,
7-{3-[бензил(2-піридин-3-ілетил)аміно]пропоксі}-1-етил-3,3,5-триметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діон,
3-{[[3-(1-етил-3,3,5-триметил-2,4-діоксо-2,3,4,5-тетрагідро-1Н-бензо[b][1,4]-діазепін-7-ілокси)пропіл]-(2-піридин-3-ілетил)аміно]метил}бензонітрил,
1-етил-3,3,5-триметил-7-{3-[(2-піридин-3-ілбензил)-(2-піридин-3-ілетил)аміно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діон,
4-({[3-(1-етил-3,3,5-триметил-2,4-діоксо-2,3,4,5-тетрагідро-1H-бензо[b][1,4]-діазепін-7-ілокси)пропіл]-[2-(7-оксо-7Н-фуро[2,3-с]піридин-6-іл)етил]аміно}метил)бензонітрил,
1-етил-3,3,5-триметил-7-{3-[[2-(7-оксо-7Н-фуро[2,3-с]піридин-6-іл)етил]-(4-трифторметилбензил)аміно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діон,
1-етил-3,3,5-триметил-7-(3-{(2-метилбензил)-[2-(7-оксо-7Н-фуро[2,3-с]піридин-6-іл)етил]аміно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діон,
1-етил-3,3,5-триметил-7-(3-{[2-(7-оксо-7Н-фуро[2,3-с]піридин-6-іл)етил]-тіофен-2-ілметиламіно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діон,
дигідрохлорид 1-етил-3,3,5-триметил-7-(3-{[2-(2-метил-4-оксо-4Н-фуро[3,2-с]піридин-5-іл)етил]піридин-4-ілметиламіно}пропокси)-1,5-дигідробензо[b][1,4]-діазепін-2,4-діону,
1-етил-3,3,5-триметил-7-(3-{[2-(4-оксо-4Н-фуро[3,2-с]піридин-5-іл)етил]піридин-3-ілметиламіно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діон,
1-етил-3,3,5-триметил-7-(3-{[2-(4-оксо-4Н-тієно[3,2-с]піридин-5-іл)етил]піридин-3-ілметиламіно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діон,
1-етил-3,3,5-триметил-7-{3-[[2-(2-метил-4-оксо-4Н-фуро[3,2-с]піридин-5-іл)етил]-(4-метилпіридин-3-ілметил)аміно]пропокси}-1,5-дигідробензо[b][1,4]-діазепін-2,4-діон,
1-етил-3,3,5-триметил-7-(3-{(2-метилпіридин-3-ілметил)-[2-(4-оксо-4Н-фуро[3,2-с]піридин-5-іл)етил]аміно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діон,
1-етил-3,3,5-триметил-7-(3-{(4-метилпіридин-3-ілметил)-[2-(4-оксо-4Н-фуро[3,2-с]піридин-5-іл)етил]аміно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діон,
1-етил-3,3,5-триметил-7-(3-{(2-метилпіридин-3-ілметил)-[2-(4-оксо-4Н-тієно[3,2-с]піридин-5-іл)етил]аміно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діон,
дигідрохлорид 1-етил-3,3,5-триметил-7-{3-[[2-(2-метил-4-оксо-4Н-фуро[3,2-с]піридин-5-іл)етил]-(2-пропілпіридин-3-ілметил)аміно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діону,
гідрохлорид N-[3-(1-етил-3,3,5-триметил-2,4-діоксо-2,3,4,5-тетрагідро-1H-бензо[b][1,4]діазепін-7-ілокси)пропіл]-N-(2-піридин-3-ілетил)бензолсульфонаміду,
дигідрохлорид 7-(3-{(2,6-диметилпіридин-3-ілметил)-[2-(4-оксо-4Н-фуро-[3,2-с]піридин-5-іл)етил]аміно}пропоксі)-1-етил-3,3,5-триметил-1,5-дигідробензо-[b][1,4]діазепін-2,4-діону,
гідрохлорид N-[3-(1-етил-3,3,5-триметил-2,4-діоксо-2,3,4,5-тетрагідро-1Н-бензо[b][1,4]діазепін-7-ілокси)пропіл]-N-(2-піридин-3-ілетил)бензаміду і
N-[3-(1-етил-3,3,5-триметил-2,4-діоксо-2,3,4,5-тетрагідро-1Н-бензо[b][1,4]діазепін-7-ілокси)пропіл]-N-[2-(1-оксо-1Н-ізохінолін-2-іл)етил]бензолсульфонамід.
5. Фармацевтична композиція, яка містить сполуку бензодіазепіну, представлену формулою (1), або її сіль за п. 1 і фармакологічно прийнятний носій.
6. Фармацевтична композиція за п. 5 для запобігання і/або лікування аритмії.
7. Сполука бензодіазепіну, представлена формулою (1), або її сіль за п. 1 для застосування в фармацевтичній композиції.
8. Застосування сполуки бензодіазепіну, представленої формулою (1), або її солі за п. 1 як активного компонента фармацевтичної композиції.
9. Застосування сполуки бензодіазепіну, представленої формулою (1), або її солі за п. 1 для одержання фармацевтичної композиції.
10. Спосіб запобігання і/або лікування аритмії, за яким вводять пацієнту сполуку бензодіазепіну, представлену формулою (1), або її сіль за п. 1.
Текст
Реферат: UA 103018 C2 ДЕРЖАВНА СЛУЖБА ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ УКРАЇНИ UA 103018 C2 У даному винаході представлена сполука бензодіазепіну, яка блокує IKur-струм або Kv1.5-канал + потужно і більш селективно в порівнянні з іншими каналами K . Сполука бензодіазепіну відповідно до даного винаходу представлена загальною формулою (1) R 4 O N R 5 A 1 R R O 3 2 N R 1 O , (1) 1 2 3 4 де R , R , R і R кожний незалежно є воднем або нижчим алкілом; 2 3 R і R можуть бути зв'язані з утворенням нижчого алкілену; 1 А є нижчим алкіленом, необов'язково заміщеним одним або більше гідрокси; і 5 R є групою, представленою XA R 6 XB R 7 N , 6 7 де R і R кожний незалежно є воднем або органічною групою; ХA і ХB кожний незалежно є зв'язком, нижчим алкіленом і т. д. UA 103018 C2 5 10 15 20 25 30 35 40 45 50 ГАЛУЗЬ ТЕХНІКИ Даний винахід стосується сполуки бензодіазепіну і фармацевтичної композиції. РІВЕНЬ ТЕХНІКИ Передсердна фібриляція (далі позначена як "ПФ") є найчастіше спостережуваним видом аритмії при клінічних обстеженнях. Хоч вона не є летальною аритмією, ПФ викликає кардіогенну церебральну емболію і тому визнається аритмією, яка значно впливає на життєвий прогноз і якість життя. Відомо, що ризик настання ПФ підвищується з віком, і що повторні напади ПФ приводять до хронічної (серйозної) ПФ (The Journal of American Medical Association, 285, 23702375 (2001) і Circulation, 114, 119-123 (2006)). Для профілактики хронічної ПФ, яка ускладнює відновлення синусового ритму і підвищує ризик кардіогенної церебральної емболії, ранньої дефібриляції, потрібна подальша профілактика рецидиву (підтримання синусового ритму). Антиаритмічні лікарські засоби (класи I і III) найчастіше застосовуються як фармакотерапія, але ці лікарські засоби не дають достатній терапевтичний ефект, одночасно викликаючи серйозні побічні ефекти, такі як проаритмічний ефект (Am. J. Cardiol., 72, B44-B49 (1993)). Настання ПФ провокується передсердною екстрасистолою, в основі якої лежать такі причини як сповільнення внутрішньопередсердної провідності, скорочення і неоднорідність періоду скорочення передсердь (Nature Reviews DRUG DISCOVERY 4, 899-910 (2005)). Відомо, що пролонгація періоду скорочення м'яза передсердя може обірвати ПФ (дефібриляція) або запобігти настанню ПФ. Тривалість потенціалу дії серцевого м'яза людини переважно + + визначається потенціалозалежними K каналами. Інгібування K каналу пролонгує тривалість потенціалу дії міокарда, що дає пролонгацію періоду скорочення (Nature Reviews DRUG DISCOVERY 5, 1034-49 (2006)). Механізм дії антиаритмічних лікарських засобів III класу + (наприклад, Дофетиліду) оснований на інгібуванні швидкого відкладеного випрямляча K струму + (IKr), K струму, кодованого HERG. Однак, оскільки IKr присутній і в передсерді, і в шлуночках, такі лікарські засоби можуть викликати вентрикулярну аритмію, таку як тріпотіння-мерехтіння (Trends Pharmacol. soc., 22, 240-246 (2001)). + + Ультрашвидкий відкладений випрямляч K струм (IKur), K струм, кодований Kv1.5, був + ідентифікований як K канал, який специфічно експресується тільки в людському передсерді (Cric. Res., 73, 1061-1076 (1993), J. Physiol., 491, 31-50 (1996) і Cric. Res., 80, 572-579 (1997)). + Мишачий калієвий струм (IKAсh), кодований двома генами, званими GIRK1 і GIRK4, відомий як K канал, що специфічно експресується в людському передсерді (Nature 374, 135-141 (1995)). Отже, фармакологічно прийнятна речовина, яка селективно блокує I Kur струм (Kv1.5 канал) або IKAсh струм (GIRK1/4 канал), може діяти селективно на передсердний м'яз і вважатися ефективним для виключення проаритмічного ефекту, викликаного тривалістю пролонгованої дії потенціалу вентрикулярного м'яза. ОПИС ВИНАХОДУ Автори даного винаходу провели широкі дослідження для розробки сполуки, яка блокує I Kur + струм (Kv1.5 канал) і/або IKAch струм (GIRK1/4 канал) ефективно і більш селективно, ніж інші K канали. У результаті автори даного винаходу виявили, що нова сполука бензодіазепіну, представлена Загальною формулою (1) нижче, може бути бажаною сполукою. Даний винахід здійснений на основі вказаних вище відкриттів. У даному винаході представлені сполука бензодіазепіну і фармацевтичні композиції, що містять сполуки бензодіазепіну, підсумовані в пунктах 1-13 нижче. Пункт 1. Сполука бензодіазепіну, представлена Загальною формулою (1) , або її сіль, 1 2 3 4 де R , R , R і R кожний незалежно є воднем або нижчим алкілом; 2 3 R і R можуть бути зв'язані з одержанням нижчого алкілену; 1 A є нижчим алкіленом, необов'язково заміщеним одним або більше гідрокси; і 5 R є групою, представленою 1 UA 103018 C2 5 10 15 20 25 30 35 40 45 50 55 , 6 7 де R і R кожний незалежно є воднем або органічною групою; XA і XB кожний незалежно є зв'язком, нижчим алкіленом, нижчим алкеніленом, -CO-, -SO2-, SO2-нижчим алкіленом, -CO-нижчим алкіленом, -CO-нижчим алкеніленом, нижчим алкіленомN(нижчим алкілом)-СО-нижчим алкіленом, нижчим алкіленом-N(нижчим алкілом)-, нижчим алкіленом-N(нижчим алкілом)-CO- або нижчим алкіленом-О-. Пункт 2. Сполука бензодіазепіну, представлена Загальною формулою (1), або її сіль за Пунктом 1, 6 7 де R і R кожний незалежно є воднем, нижчим алкілом, нижчим циклоалкілом, арилом або гетероциклічною групою. Пункт 3. Сполука бензодіазепіну, представлена Загальною формулою (1), або її сіль за Пунктом 2, 6 7 де R і R кожний незалежно є воднем, нижчим алкілом, нижчим циклоалкілом, арилом або насиченою або ненасиченою моноциклічною або поліциклічною гетероциклічною групою, що містить щонайменше один гетероатом, вибраний з кисню, сірки і азоту. Пункт 4. Сполука бензодіазепіну, представлена Загальною формулою (1), або її сіль за Пунктом 3, 6 7 де R і R кожний незалежно є воднем, нижчим алкілом, нижчим циклоалкілом, фенілом, нафтилом, фурилом, тієнілом, піразолілом, оксазолілом, ізоксазолілом, тіазолілом, піролілом, триазолілом, піридилом, піримідинілом, піридазинілом, піразинілом, імідазо[2,1-b]тіазолілом, тієно[2,3-b]піразинілом, 2,3-дигідроімідазо[2,1-b]тіазолілом, бензотіазолілом, індолілом, імідазо[1,2-a]піридилом, бензотієнілом, бензімідазолілом, 2,3-дигідробензо[b]фурилом, бензофурилом, індазолілом, фуро[2,3-c]піридилом, фуро[3,2-c]піридилом, тієно[2,3-c]піридилом, тієно[3,2-c]піридилом, тієно[2,3-b]піридилом, бензо[1,3]діоксолілом, бензізоксазолілом, піразоло[2,3-a]піридилом, індолізинілом, 2,3-дигідроіндолілом, ізохінолілом, 1,2,3,4-тетрагідро1H-ізохінолілом, карбостирилом, 3,4-дигідрокарбостирилом, хінолілом, хроманілом, 5,6,7,8тетрагідроізохінолілом, 3,4-дигідро-1H-ізохінолілом, нафтиридинілом, 1,4-бензодіоксанілом, цинолінілом, хіноксалінілом або 2,3-дигідробенз-1,4-оксазинілом, кожний з яких необов'язково заміщений. Пункт 5. Сполука бензодіазепіну, представлена Загальною формулою (1), або її сіль за Пунктом 4, 6 7 де R і R кожний є одним з (1)-(52): (1) водню, (2) нижчого алкілу, (3) нижчого циклоалкілу, (4) фенілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з (4-1)-(4-25): (4-1) ціано, (4-2) гідрокси, (4-3) галогену, (4-4) нижчого алкілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з галогену, імідазолілу і морфолінілу, (4-5) нижчого алкокси, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з аміно і нижчого алкіламіно, (4-6) піридилу, (4-7) тієнілу, (4-8) піперазинілу, необов'язково заміщеного одним або більше нижчими алкілами, (4-9) фенілу, (4-10) піразолілу, необов'язково заміщеного одним або більше нижчими алкілами, (4-11) піримідинілу, необов'язково заміщеного одним або більше нижчими алкілами, (4-12) піперидилу, необов'язково заміщеного одним або більше нижчими алкілами, (4-13) фурилу, (4-14) карбокси, (4-15) нижчого алкоксикарбонілу, (4-16) аміно, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алканоїлу і нижчого алкілсульфонілу, (4-17) нижчого алкілтіо, (4-18) триазолілу, 2 UA 103018 C2 5 10 15 20 25 30 35 40 45 50 55 60 (4-19) імідазолілу, (4-20) піролідинілу, необов'язково заміщеного одним або більше оксо, (4-21) нижчого алкілсульфонілу, (4-22) нижчого алкілендіокси, необов'язково заміщеного одним або більше галогенами, (4-23) нітро, (4-24) оксазолілу, і (4-25) тіазолілу, необов'язково заміщеного одним або більше нижчими алкілами, (5) нафтилу, (6) фурилу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу, необов'язково заміщеного галогеном, карбокси, сульфо, піридилокси, нижчого алкоксикарбонілу і фенілу, (7) тієнілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу, нижчого алкілендіокси, карбокси, галогену, піридилу, нижчого алкокси, нижчого алкоксикарбонілу, оксазолілу і фурилу, (8) імідазолілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з фенілу, нижчого алкілу і галогену, (9) піразолілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу, необов'язково заміщеного галогеном, галогену, фенілу, необов'язково заміщеного нижчого алкокси, фурилу і тієнілу, (10) оксазолілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу і фенілу, (11) ізоксазолілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з фенілу, нижчого алкілу, тієнілу і фурилу, (12) тіазолілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу, необов'язково заміщеного нижчого алкокси, фенілу і нижчого алканоїламіно, (13) піролілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу і нижчого алкоксикарбонілу, (14) триазолілу, необов'язково заміщеного одним або більше нижчими алкілами, (15) піридилу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу, необов'язково заміщеного галогеном, оксо, гідрокси, нижчим алкокси, галогену, піролідинілу, морфолінілу і тієнілу, (16) піримідинілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу і фенілу, (17) піридазинілу, (18) піразинілу, (19) імідазо[2,1-b]тіазолілу, необов'язково заміщеного одним або більше галогенами, (20) тієно[2,3-b]піразинілу, (21) 2,3-дигідроімідазо[2,1-b]тіазолілу, необов'язково заміщеного одним або більше фенілами, (22) бензотіазолілу, необов'язково заміщеного одним або більше нижчими алкілами, (23) індолілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу, нижчого алканоїлу і галогену, (24) імідазо[1,2-a]піридилу, необов'язково заміщеного одним або більше нижчими алкілами, (25) бензотієнілу, необов'язково заміщеного одним або більше нижчими алкілами, (26) бензімідазолілу, необов'язково заміщеного одним або більше нижчими алкілами, (27) 2,3-дигідробензо[b]фурилу, (28) бензофурилу, необов'язково заміщеного одним або більше галогенами, (29) індазолілу, необов'язково заміщеного одним або більше нижчими алкілами, (30) фуро[2,3-c]піридилу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з оксо і нижчого алкілу, (31) фуро[3,2-c]піридилу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з оксо, нижчого алкілу, необов'язково заміщеного галогеном, галогену, фурилу, піридилу і фенілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з аміно і нижчого алкокси, (32) тієно[2,3-c]піридилу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з оксогрупи і нижчого алкілу, (33) тієно[3,2-c]піридилу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з оксо і нижчого алкілу, (34) тієно[2,3-b]піридилу, 3 UA 103018 C2 5 10 15 20 25 30 35 40 45 50 55 60 (35) бензо[1,3]діоксолілу, необов'язково заміщеного одним або більше галогенами, (36) бензізоксазолілу, (37) піразоло[2,3-a]піридилу, (38) індолізинілу, (39) 2,3-дигідроіндолілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з оксо, нижчого алкілу і нижчого алканоїлу, (40) ізохінолілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу, галогену і оксо, (41) 1,2,3,4-тетрагідро-1H-ізохінолілу, необов'язково заміщеного одним або більше оксо, (42) карбостирилу, необов'язково заміщеного одним або більше нижчими алкокси, (43) 3,4-дигідрокарбостирилу, необов'язково заміщеного одним або більше нижчими алкокси, (44) хінолілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з аміно, необов'язково заміщеного одним або двома нижчими алкілами, нижчого алкокси, нижчого алкілу і оксо, (45) хроманілу, необов'язково заміщеного одним або більше нижчими алкілами, (46) 5,6,7,8-тетрагідроізохінолілу, необов'язково заміщеного одним або більше оксо, (47) 3,4-дигідро-1H-ізохінолілу, необов'язково заміщеного одним або більше оксо, (48) нафтиридинілу, (49) 1,4-бензодіоксанілу, (50) цинолінілу, (51) хіноксалінілу, або (52) 2,3-дигідробенз-1,4-оксазинілу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з нижчого алкілу і оксо. Пункт 6. Сполука бензодіазепіну, представлена Загальною формулою (1), або її сіль за Пунктом 5, 6 7 де R і R кожний є одним з (4a), (6a), (7a), (15a), (30a), (31a), (32a), (33a), (40a) і (44a): (4a) феніл, необов'язково заміщений одним або більше замісниками, вибраними з групи, що складається з (4a-1), (4a-4) і (4a-6): (4a-1) ціано, (4a-4) нижчого алкілу, необов'язково заміщеного одним або більше галогенами, і (4a-6) піридилу, (6a) фурилу, (7a) тієнілу, (15a) піридилу, необов'язково заміщеного одним або більше нижчими алкілами, (30a) фуро[2,3-c]піридилу, необов'язково заміщеного одним або більше оксо, (31a) фуро[3,2-c]піридилу, необов'язково заміщеного одним або більше замісниками, вибраними з групи, що складається з оксо і нижчого алкілу, (32a) тієно[2,3-c]піридилу, необов'язково заміщеного одним або більше оксо, (33a) тієно[3,2-c]піридилу, необов'язково заміщеного одним або більше оксо, (40a) ізохінолілу, необов'язково заміщеного одним або більше оксо, і (44a) хінолілу, необов'язково заміщеного одним або більше оксо. Пункт 7. Сполука бензодіазепіну, представлена Загальною формулою (1), або її сіль за Пунктом 6, яку вибирають з групи, що складається з наступних сполук: тригідрохлорид 1-етил-3,3,5-триметил-7-{3-[(2-піридин-3-ілетил)піридин-4ілметиламіно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діону, тригідрохлорид 3,3,5-триметил-1-пропіл-7-{3-[(2-піридин-3-ілетил)піридин-4ілметиламіно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діону, тригідрохлорид 1,5-діетил-3,3-диметил-7-{3-[(2-піридин-3-ілетил)піридин-4ілметиламіно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діону, тригідрохлорид 1,3,3,5-тетраметил-7-{3-[(2-піридин-3-ілетил)піридин-4ілметиламіно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діону, дигідрохлорид 1-етил-3,3,5-триметил-7-(3-{[2-(1-оксо-1H-ізохінолін-2-іл)етил]піридин-4ілметиламіно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діону, дигідрохлорид 1-етил-3,3,5-триметил-7-(3-{[2-(7-оксо-7H-фуро[2,3-c]піридин-6іл)етил]піридин-4-ілметиламіно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діону, дигідрохлорид N-метил-N-(2-{піридин-4-ілметил-[3-(1,3,3,5-тетраметил-2,4-діоксо-2,3,4,5тетрагідро-1H-бензо[b][1,4]діазепін-7-ілокси)пропіл]аміно}етил)бензамід, дигідрохлорид 1,3,3,5-тетраметил-7-{3-[(2-метилбензил)-(2-піридин-3ілетил)аміно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діону, 4 UA 103018 C2 5 10 15 20 25 30 35 40 45 50 55 тригідрохлорид 1,3,3,5-тетраметил-7-{3-[(2-піридин-3-ілетил)-(хінолін-4ілметил)аміно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діону, тригідрохлорид 1-етил-3,3,5-триметил-7-{3-[(3-метилпіридин-4-ілметил)-(2-піридин-3ілетил)аміно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діону, дигідрохлорид 1-етил-3,3,5-триметил-7-(3-{[2-(2-оксо-2H-хінолін-1-іл)етил]піридин-4ілметиламіно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діону, дигідрохлорид 1-етил-3,3,5-триметил-7-(3-{[2-(7-оксо-7H-тієно[2,3-c]піридин-6іл)етил]піридин-4-ілметиламіно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діону, 4-({[3-(1-етил-3,3,5-триметил-2,4-діоксо-2,3,4,5-тетрагідро-1H-бензо[b][1,4]діазепін-7ілокси)пропіл]-[2-(1-оксо-1H-ізохінолін-2-іл)етил]аміно}метил)бензонітрил, 1-етил-3,3,5-триметил-7-(3-{[2-(1-оксо-1H-ізохінолін-2-іл)етил]тіофен-3ілметиламіно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діон, 1-етил-7-(3-{фуран-2-ілметил-[2-(1-оксо-1H-ізохінолін-2-іл)етил]аміно}пропокси)-3,3,5триметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діон, 7-{3-[бензил-(2-піридин-3-ілетил)аміно]пропоксі}-1-етил-3,3,5-триметил-1,5дигідробензо[b][1,4]діазепін-2,4-діон, 3-{[[3-(1-етил-3,3,5-триметил-2,4-діоксо-2,3,4,5-тетрагідро-1H-бензо[b][1,4]діазепін-7ілокси)пропіл]-(2-піридин-3-ілетил)аміно]метил}-бензонітрил, 1-етил-3,3,5-триметил-7-{3-[(2-піридин-3-ілбензил)-(2-піридин-3-ілетил)аміно]-пропокси}-1,5дигідробензо[b][1,4]діазепін-2,4-діон, 4-({[3-(1-етил-3,3,5-триметил-2,4-діоксо-2,3,4,5-тетрагідро-1H-бензо[b][1,4]діазепін-7ілокси)пропіл]-[2-(7-оксо-7H-фуро[2,3-c]піридин-6-іл)етил]аміно}метил)бензонітрил, 1-етил-3,3,5-триметил-7-{3-[[2-(7-оксо-7H-фуро[2,3-c]піридин-6-іл)етил]-(4трифторметилбензил)аміно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діон, 1-етил-3,3,5-триметил-7-(3-{(2-метилбензил)-[2-(7-оксо-7H-фуро[2,3-c]піридин-6іл)етил]аміно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діон, 1-етил-3,3,5-триметил-7-(3-{[2-(7-оксо-7H-фуро[2,3-c]піридин-6-іл)етил]тіофен-2ілметиламіно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діон, дигідрохлорид 1-етил-3,3,5-триметил-7-(3-{[2-(2-метил-4-оксо-4H-фуро[3,2-c]піридин-5іл)етил]піридин-4-ілметиламіно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діону, 1-етил-3,3,5-триметил-7-(3-{[2-(4-оксо-4H-фуро[3,2-c]піридин-5-іл)етил]піридин-3ілметиламіно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діон, 1-етил-3,3,5-триметил-7-(3-{[2-(4-оксо-4H-тієно[3,2-c]піридин-5-іл)етил]піридин-3ілметиламіно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діон, 1-етил-3,3,5-триметил-7-{3-[[2-(2-метил-4-оксо-4H-фуро[3,2-c]піридин-5-іл)етил]-(4метилпіридин-3-ілметил)аміно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діон, 1-етил-3,3,5-триметил-7-(3-{(2-метилпіридин-3-ілметил)-[2-(4-оксо-4H-фуро[3,2-c]піридин-5іл)етил]аміно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діон, 1-етил-3,3,5-триметил-7-(3-{(4-метилпіридин-3-ілметил)-[2-(4-оксо-4H-фуро[3,2-c]піридин-5іл)етил]аміно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діон, 1-етил-3,3,5-триметил-7-(3-{(2-метилпіридин-3-ілметил)-[2-(4-оксо-4H-тієно[3,2-c]піридин-5іл)етил]аміно}пропокси)-1,5-дигідробензо[b][1,4]діазепін-2,4-діон, дигідрохлорид 1-етил-3,3,5-триметил-7-{3-[[2-(2-метил-4-оксо-4H-фуро[3,2-c]піридин-5іл)етил]-(2-пропілпіридин-3-ілметил)аміно]пропокси}-1,5-дигідробензо[b][1,4]діазепін-2,4-діону, гідрохлорид N-[3-(1-етил-3,3,5-триметил-2,4-діоксо-2,3,4,5-тетрагідро-1Hбензо[b][1,4]діазепін-7-ілокси)пропіл]-N-(2-піридин-3-ілетил)бензолсульфонаміду, дигідрохлорид 7-(3-{(2,6-диметилпіридин-3-ілметил)-[2-(4-оксо-4H-фуро[3,2-c]піридин-5іл)етил]аміно}пропоксі)-1-етил-3,3,5-триметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону, гідрохлорид N-[3-(1-етил-3,3,5-триметил-2,4-діоксо-2,3,4,5-тетрагідро-1Hбензо[b][1,4]діазепін-7-ілокси)пропіл]-N-(2-піридин-3-ілетил)бензаміду і N-[3-(1-етил-3,3,5-триметил-2,4-діоксо-2,3,4,5-тетрагідро-1H-бензо[b][1,4]діазепін-7ілокси)пропіл]-N-[2-(1-оксо-1H-ізохінолін-2-іл)етил]бензолсульфонамід. Пункт 8. Фармацевтична композиція, яка містить сполуку бензодіазепіну, представлену Формулою (1), або її сіль за Пунктом 1 і фармакологічно прийнятний носій. Пункт 9. Фармацевтична композиція за Пунктом 8 для запобігання і/або лікування аритмії. Пункт 10. Сполука бензодіазепіну, представлена Формулою (1), або її сіль за Пунктом 1 для застосування в фармацевтичній композиції. Пункт 11. Застосування сполуки бензодіазепіну, представленої Формулою (1), або її солі за Пунктом 1 як фармацевтичної композиції. 5 UA 103018 C2 5 10 15 20 25 30 35 40 45 50 55 60 Пункт 12. Застосування сполуки бензодіазепіну, представленої Формулою (1), або її солі за Пунктом 1 для виробництва фармацевтичної композиції. Пункт 13. Спосіб запобігання і/або лікування аритмії, який включає введення пацієнту сполуки бензодіазепіну, представленої Формулою (1), або її солі за Пунктом 1. 1 2 3 4 5 6 7 1 Групи, представлені R , R , R , R , R , R , R , A , XA і XB, в специфікації описані нижче. Приклади "органічних груп" включають нижчий алкіл, нижчий циклоалкіл, арил, такий як 6 7 феніл і нафтил, гетероциклічні групи, такі як (6)-(52) для R і R . Приклади "гетероциклічної групи" включають насичені або ненасичені моноциклічні або поліциклічні гетероциклічні групи, що містять щонайменше один гетероатом, вибраний з кисню, сірки і азоту. Більш переважно, гетероциклічна група може бути такою групою, як: - ненасичена 3-8-членна, переважно 5- або 6-членна гетеромоноциклічна група, що містить від 1 до 4 атомів азоту, наприклад, піроліл, піролініл, імідазоліл, піразоліл, піридил і його Nоксид, піримідиніл, піразиніл, піридазиніл, триазоліл (наприклад, 4H-1,2,4-триазоліл, 1H-1,2,3триазоліл, 2H-1,2,3-триазоліл і т. д.), тетразоліл (наприклад, 1H-тетразоліл, 2H-тетразоліл і т. д.), дигідротриазиніл (наприклад, 4,5-дигідро-1,2,4-триазиніл, 2,5-дигідро-1,2,4-триазиніл і т. д.) і т. д.; - насичена 3-8-членна, переважно 5- або 6-членна гетеромоноциклічна група, що містить від 1 до 4 атомів азоту, наприклад, азетидиніл, піролідиніл, імідазолідиніл, піперидиніл, піразолідиніл, піперазиніл і т. д.; - ненасичена конденсована 7-12-членна гетероциклічна група, що містить від 1 до 5 атомів азоту, наприклад, індоліл, дигідроіндоліл (наприклад, 2,3-дигідроіндоліл і т. д.), ізоіндоліл, індолізиніл, бензімідазоліл, хіноліл, ізохіноліл, дигідроізохіноліл (наприклад, 3,4-дигідро-1Hізохіноліл і т. д.), тетрагідроізохіноліл (наприклад, 1,2,3,4-тетрагідро-1H-ізохіноліл, 5,6,7,8тетрагідроізохіноліл і т. д.), карбостирил, дигідрокарбостирил (наприклад, 3,4дигідрокарбостирил і т. д.), індазоліл, бензотриазоліл, тетразолопіридил, тетразолопіридазиніл (наприклад, тетразоло[1,5-b]піридазиніл і т. д.), дигідротриазолопіридазиніл, імідазопіридил (наприклад, імідазо[1,2-a]піридил і т. д.), нафтиридиніл, цинолініл, хіноксалініл, піразолопіридил (наприклад, піразоло[2,3-a]піридил і т. д.) і т. д.; - ненасичена 3-8-членна, переважно 5- або 6-членна гетеромоноциклічна група, що містить від 1 до 2 атомів кисню, наприклад, фурил і т. д.; - ненасичена конденсована 7-12-членна гетероциклічна група, що містить від 1 до 3 атомів кисню, наприклад, бензофурил, дигідробензофурил (наприклад, 2,3-дигідробензо[b]фурил і т. д.), хроманіл, бензодіоксаніл (наприклад, 1,4-бензодіоксаніл і т. д.), дигідробензоксазиніл (наприклад, 2,3-дигідробенз-1,4-оксазиніл і т. д.), бензодіоксоліл (бензо[1,3]діоксоліл і т. д.) і т. д.; - ненасичена 3-8-членна, переважно 5- або 6-членна гетеромоноциклічна група, що містить від 1 до 2 атомів кисню і від 1 до 3 атомів азоту, наприклад, оксазоліл, ізоксазоліл, оксадіазоліл (наприклад, 1,2,4-оксадіазоліл, 1,3,4-оксадіазоліл, 1,2,5-оксадіазоліл і т. д.) і т. д.; - насичена 3-8-членна, переважно 5- або 6-членна гетеромоноциклічна група, що містить від 1 до 2 атомів кисню і від 1 до 3 атомів азоту, наприклад, морфолініл і т. д.; - ненасичена конденсована 7-12-членна гетероциклічна група, що містить від 1 до 2 атомів кисню і від 1 до 3 атомів азоту, наприклад, бензоксазоліл, бензоксадіазоліл, бензізоксазоліл, фуропіридил (наприклад, фуро[2,3-b]піридил, фуро[3,2-c]піридил і т. д.) і т. д.; - ненасичена 3-8-членна, переважно 5- або 6-членна гетеромоноциклічна група, що містить від 1 до 2 атомів сірки і від 1 до 3 атомів азоту, наприклад, тіазоліл, 1,2-тіазоліл, тіазолініл, тіадіазоліл (наприклад, 1,2,4-тіадіазоліл, 1,3,4-тіадіазоліл, 1,2,5-тіадіазоліл, 1,2,3-тіадіазоліл і т. д.) і т. д.; - насичена 3-8-членна, переважно 5- або 6-членна гетеромоноциклічна група, що містить від 1 до 2 атомів сірки і від 1 до 3 атомів азоту, наприклад, тіазолідиніл і т. д.; - ненасичена 3-8-членна, переважно 5- або 6-членна гетеромоноциклічна група, що містить атом сірки, наприклад, тієніл і т. д.; - ненасичена конденсована 7-12-членна гетероциклічна група, що містить від 1 до 3 атомів сірки, наприклад, бензотієніл (наприклад, бензо[b]тієніл і т. д.); - ненасичена конденсована 7-12-членна гетероциклічна група, що містить від 1 до 2 атомів сірки і від 1 до 3 атомів азоту, наприклад, бензотіазоліл, бензотіадіазоліл, тієнопіридил (наприклад, тієно[2,3-b]піридил, тієно[2,3-c]піридил, тієно[3,2-c]піридил і т. д.), імідазотіазоліл (наприклад, імідазо[2,1-b]тіазоліл і т. д.), дигідроімідазотіазоліл (наприклад, 2,3дигідроімідазо[2,1-b]тіазоліл і т. д.), тієнопіразиніл (наприклад, тієно[2,3-b]піразиніл і т. д.) і т. д. і подібні; де вказана гетероциклічна група може бути заміщена одним або більше придатними замісниками. 6 UA 103018 C2 5 10 15 20 25 Приклади "нижчого алкілу" включають лінійні або розгалужені алкільні групи, що містять від 1 до 6 атомів вуглецю, такі як метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, трет-бутил, втор-бутил, н-пентил, неопентил, н-гексил, ізогексил і 3-метилпентил. Приклади "нижчого алкілену" включають лінійні або розгалужені алкіленові групи, що мають від 1 до 6 атомів вуглецю, такі як метилен, етилен, триметилен, 2-метилтриметилен, 2,2диметилтриметилен, 1-метилтриметилен, метилметилен, етилметилен, тетраметилен, пентаметилен і гексаметилен. Приклади "нижчого циклоалкілу" включають лінійний або розгалужений циклоалкіл, що має від 3 до 6 атомів вуглецю, такий як циклопропіл, циклобутил, циклопентил і циклогексил. Приклади "нижчого алкокси" включають лінійні або розгалужені алкоксигрупи, що мають від 1 до 6 атомів вуглецю, такі як метокси, етокси, н-пропокси, ізопропокси, н-бутокси, ізобутокси, трет-бутокси, втор-бутокси, н-пентилокси, неопентилокси, н-гексилокси, ізогексилокси і 3метилпентилокси. Приклади "галогену" включають фтор, хлор, бром і йод. Приклади "нижчого алкілендіокси" включають лінійні або розгалужені алкіленові групи, що мають від 1 до 4 атомів вуглецю, такі як метилендіокси, етилендіокси, триметилендіокси і тетраметилендіокси. Приклади "нижчого алканоїлу" включають лінійні або розгалужені алканоїльні групи, що мають від 1 до 6 атомів вуглецю, такі як форміл, ацетил, пропіоніл, бутирил, ізобутирил, пентаноїл, трет-бутилкарбоніл і гексаноїл. Термін "один або більше" включає переважно від 1 до 6, більш переважно від 1 до 3. Сполука бензодіазепіну відповідно до даного винаходу, представлена Формулою (1), або її сіль може бути одержана, наприклад, способами, показаними на представлених нижче схемах реакцій. Схема реакції 1 , 1 30 35 40 45 50 2 3 4 5 1 де R , R , R , R , R і A такі, як визначені вище, і X1 є галогеном або гідроксилом. Реакція сполуки Формули (2) із сполукою Формули (3), де X 1 є галогеном, може проводитися в звичайному інертному розчиннику або без розчинників в присутності або за відсутності лужної сполуки. Приклади інертних розчинників включають воду; прості ефіри, такі як діоксан, тетрагідрофуран, діетиловий ефір, диметиловий ефір діетиленгліколю і диметиловий ефір етиленгліколю; ароматичні вуглеводні, такі як бензол, толуол і ксилол; галогеновані вуглеводні, такі як дихлорметан, дихлоретан, хлороформ і чотирихлористий вуглець; нижчі спирти, такі як метанол, етанол і ізопропанол; кетони, такі як ацетон і метилетилкетон; полярні розчинники, такі як диметилформамід (ДМФ), диметилсульфоксид (ДМСО), гексаметилфосфорний триамід і ацетонітрил; і суміші таких розчинників. Лужна сполука може бути вибрана з різних відомих сполук. Приклади таких сполук включають неорганічні основи, наприклад, гідроксиди лужних металів, такі як гідроксид натрію, гідроксид калію, гідроксид цезію і гідроксид літію; карбонати лужних металів, такі як карбонат натрію, карбонат калію, карбонат цезію, карбонат літію, гідрокарбонат літію, гідрокарбонат натрію і гідрокарбонат калію; лужні метали, такі як натрій і калій; амід натрію; гідрид натрію і гідрид калію; і органічні основи, наприклад, алкоголяти лужних металів, такі як метоксид натрію, етоксид натрію, метоксид калію і етоксид калію; триетиламін; трипропіламін; піридин; хінолін; 1,5-діазабіцикло[4.3.0]нонен-5 (DBN); 1,8-діазабіцикло[5.4.0]ундецен-7 (DBU); і 1,4діазабіцикло[2.2.2]октан (DABCO). Ці лужні сполуки можуть застосовуватися окремо або в поєднанні двох або більше. Вказана вище реакція може проводитися з додаванням йодиду лужного металу, такого як йодид калію або йодид натрію, до реакційної системи, при необхідності. 7 UA 103018 C2 5 10 15 20 25 Сполуку Формули (3) звичайно застосовують в кількості щонайменше 0,5 моля і переважно від 0,5 до 10 молів на моль сполуки Формули (2). Лужну сполуку звичайно застосовують в кількості від 0,5 до 10 молів і переважно від 0,5 до 6 молів на моль сполуки Формули (2). Реакцію звичайно проводять при температурі від 0 °C до 250 °C і переважно від 0 °C до 200 °C і звичайно завершують протягом від близько 1 до близько 80 годин. Реакцію сполуки Формули (2) із сполукою Формули (3), де X 1 є гідроксилом, проводять у придатному розчиннику в присутності конденсуючого агента. Приклади розчинників, застосовуваних в даній реакції, включають воду; галогеновані вуглеводні, такі як хлороформ, дихлорметан, дихлоретан і чотирихлористий вуглець; ароматичні вуглеводні, такі як бензол, толуол і ксилол; прості ефіри, такі як діетиловий ефір, діізопропіловий ефір, тетрагідрофуран і диметоксіетан; складні ефіри, такі як метилацетат, етилацетат і ізопропілацетат; спирти, такі як метанол, етанол, ізопропанол, пропанол, бутанол, 3-метокси-1-бутанол, етилцелозольв і метилцелозольв; апротонні полярні розчинники, такі як ацетонітрил, піридин, ацетон, N, N-диметилформамід, диметилсульфоксид і гексаметилфосфорний триамід; і суміші таких розчинників. Приклади конденсуючих агентів включають азокарбоксилати, такі як ди-третбутилазодикарбоксилат, N,N,N',N'-тетраметилазодикарбоксамід, 1,1'(азодикарбоніл)дипіперидин, діетилазодикарбоксилат; і сполуки фосфору, такі як трифенілфосфін і три-н-бутилфосфін. У цій реакції сполуку (3) звичайно застосовують в кількості щонайменше 1 моль і переважно від 1 до 2 молів на моль сполуки (2). Конденсуючий агент звичайно застосовують в кількості щонайменше 1 моль і переважно від 1 до 2 молів на моль сполуки (2). Реакція проходить звичайно при температурі від 0 до 200 °C і переважно від близько 0 до близько 150 °C і завершується протягом від близько 1 до близько 10 годин. Схема реакції 2 , 30 35 40 45 50 1 2 3 4 1 де R , R , R , R і A такі, як визначені вище. Реакція перетворення сполуки Формули (1a) в сполуку Формули (1b) може проводитися або взаємодією сполуки (1a) з гідразином у придатному розчиннику, або гідролізом. Як гідразин може застосовуватися гідрат гідразину. Приклади розчинників, застосовуваних для реакції з гідразином, включають воду; галогеновані вуглеводні, такі як хлороформ, дихлорметан і дихлоретан; ароматичні вуглеводні, такі як бензол, толуол і ксилол; прості ефіри, такі як діетиловий ефір, діізопропіловий ефір, тетрагідрофуран і диметоксіетан; складні ефіри, такі як метилацетат і етилацетат; і апротонні полярні розчинники, такі як N,N-диметилформамід, диметилсульфоксид і гексаметилфосфорний триамід; і суміші таких розчинників. Інші приклади розчинників, застосовуваних для реакції, включають спирти, такі як метанол, етанол, пропанол, бутанол, 3метокси-1-бутанол, етилцелозольв або метилцелозольв; ацетонітрил, піридин, ацетон, і суміші таких розчинників. Гідразин звичайно застосовують в кількості щонайменше близько 1 моля і переважно від близько 1 до близько 5 молів на моль сполуки (1a). Реакцію проводять звичайно при температурі від близько 0 до близько 120 °C і переважно від близько 0 до близько 100 °C і звичайно завершується протягом від близько 0,5 до близько 5 годин. Гідроліз сполуки Формули (1a) проводить у придатному розчиннику або без розчинників в присутності кислої або лужної сполуки. 8 UA 103018 C2 5 10 Приклади розчинників включають воду; нижчі спирти, такі як метанол, етанол і ізопропанол; кетони, такі як ацетон і метилетилкетон; прості ефіри, такі як діоксан, тетрагідрофуран і диметиловий ефір етиленгліколю; жирні кислоти, такі як оцтова кислота і мурашина кислота; і суміші таких розчинників. Приклади кислот включають мінеральні кислоти, такі як хлористоводнева кислота, сірчана кислота і бромистоводнева кислота; аліфатичні кислоти, такі як мурашина кислота, оцтова кислота; і сульфонові кислоти, такі як п-толуолсульфонова кислота. Приклади лужних сполук включають карбонати металів, такі як карбонат натрію і карбонат калію; і гідроксиди металів, такі як гідроксид натрію і гідроксид калію. Реакція проходить при температурі від кімнатної температури до близько 200 °C і переважно при температурі від кімнатної температури до близько 150 °C і звичайно завершується протягом від близько 10 хвилин до 25 годин. Схема реакції 3 , 15 1 20 2 3 4 5 1 де R , R , R , R , R і A такі, як визначені вище, і X2 є галогеном, алкансульфонілокси або арилсульфонілокси. Реакцію сполуки Формули (4) із сполукою Формули (5) проводять в тих же умовах реакції, як і для реакції сполуки Формули (3), де X1 є галогеном, із сполукою Формули (2) на Схемі реакції 1. Схема реакції 4 , 25 30 35 40 1 2 3 4 6 7 1 8 де R , R , R , R , R , R і A такі, як визначені вище; і R є воднем або нижчим алкілом; 7 8 8 при умові, що алкіленова група -CHR R не містить більше 6 атомів вуглецю, і -CHR є такою ж, як XB в якому міститься алкілен. Реакцію сполуки Формули (1c) і сполуки Формули (6) проводять, наприклад, в присутності відновлювального агента у придатному розчиннику або без розчинників. Приклади застосовуваних розчинників включають воду; нижчі спирти, такі як метанол, етанол, ізопропанол, бутанол, трет-бутанол і етиленгліколь; ацетонітрил; аліфатичні кислоти, такі як мурашина кислота і оцтова кислота; прості ефіри, такі як діетиловий ефір, тетрагідрофуран, діоксан, моноглім і диглім; ароматичні вуглеводні, такі як бензол, толуол і ксилол; галогеновані вуглеводні, такі як дихлорметан, дихлоретан, хлороформ і чотирихлористий вуглець; і суміші таких розчинників, і т. д. Приклади відновлювальних агентів включають аліфатичні кислоти, такі як мурашина кислота і оцтова кислота; солі аліфатичних кислот з лужними металами, такі як форміат натрію і ацетат натрію; гідридні відновлювальні агенти, такі як боргідрид натрію, ціаноборгідрид натрію, триацетоксиборгідрид натрію і алюмогідрид літію; суміші таких гідридних відновлювальних агентів; суміші аліфатичних кислот або солей аліфатичних кислот з лужними металами з 9 UA 103018 C2 5 10 15 20 25 30 гідридними відновлювальними агентами; каталітичні гідрувальні відновлювальні агенти, такі як паладієва чернь, паладій на вугіллі, оксид платини, платинова чернь, нікель Ренея і т. д. Якщо аліфатичну кислоту, таку як мурашина кислота, або сіль аліфатичної кислоти з лужним металом, таку як форміат натрію або ацетат натрію, застосовують як відновлювальний агент, придатна температура реакції звичайно складає від близько кімнатної температури до близько 200 °C і переважно від близько 50 до близько 150 °C. Реакція звичайно завершується протягом від близько 10 хвилин до близько 10 годин. Такі аліфатичні кислоти і солі аліфатичних кислот з лужними металами звичайно застосовують у великому надлишку відносно сполуки Формули (1c). Якщо застосовують гідридний відновлювальний агент, придатна температура реакції звичайно складає від близько -80 до близько 100 °C і переважно від близько -80 до близько 70 °C. Реакція звичайно завершується протягом від близько 30 хвилин до близько 60 годин. Гідридний відновлювальний агент звичайно застосовують в кількості від близько 1 до близько 20 молів і переважно від близько 1 до близько 10 молів на моль сполуки Формули (1c). Зокрема, якщо алюмогідрид літію застосовують як гідридний відновлювальний агент, переважно застосовувати діетиловий ефір, тетрагідрофуран, діоксан, моноглім, диглім або подібні прості ефіри; або бензол, толуол, ксилол або подібні ароматичні вуглеводні як розчинник. Триметиламін, триетиламін, N-етилдіізопропіламін або подібні аміни; або молекулярні сита 3A (MS-3A), молекулярні сита 4A (MS-4A), або подібні молекулярні сита можуть бути введені в реакційну систему даної реакції. При застосуванні каталітичного гідрувального агента, реакцію звичайно проводять при температурі від близько -30 до близько 100 °C і переважно від близько 0 до близько 60 °C, в атмосфері водню звичайно від близько 1 до близько 20 атм. і переважно від близько 1 до близько 10 атм., або в присутності мурашиної кислоти, форміату амонію, циклогексену, гідрату гідразину або подібного донора водню. Реакцію звичайно проводять протягом від близько 1 до близько 12 годин. Каталітичний гідрувальний відновлювальний агент звичайно застосовують в кількості від близько 0,1 до близько 40 % мас. і переважно від близько 1 до близько 20 % мас. відносно сполуки Формули (1c). У реакції сполуки Формули (1c) із сполукою Формули (6), сполуку Формули (6) звичайно застосовують в кількості щонайменше 1 моль і переважно від 1 до 5 молів на моль сполуки Формули (1c). Схема реакції 5 , 35 1 2 3 4 6 6 1 2 3 4 6 7 1 де R , R , R , R , R , R , XA, XB, A і X1 такі, як визначені вище. Реакцію сполуки Формули (1c) із сполукою Формули (7) проводять в тих же умовах, які застосовуються для реакції сполуки Формули (3) із сполукою Формули (2) на Схемі реакції 1. Схема реакції 6 40 , 1 де R , R , R , R , R , R , XA і A такі, як визначені вище, і XB' є -SO2- або -CO-. 10 UA 103018 C2 5 10 15 20 25 30 Реакція перетворення сполуки Формули (1f) в сполуку Формули (1c) може проводитися гідролізом. Реакцію гідролізу проводять у придатному розчиннику або без застосування розчинників в присутності кислої або лужної сполуки. Приклади корисних розчинників включають воду; нижчі спирти, такі як метанол, етанол, ізопропанол і трет-бутанол; кетони, такі як ацетон і метилетилкетон; прості ефіри, такі як діетиловий ефір, діоксан, тетрагідрофуран, моноглім і диглім; аліфатичні кислоти, такі як оцтова кислота і мурашина кислота; складні ефіри, такі як метилацетат і етилацетат; галогеновані вуглеводні, такі як хлороформ, дихлорметан, дихлоретан і чотирихлористий вуглець; диметилсульфоксид; N,N-диметилформамід і гексаметилфосфорний триамід; і суміші таких розчинників. Приклади корисних кислот включають мінеральні кислоти, такі як хлористоводнева кислота, сірчана кислота і бромистоводнева кислота; і органічні кислоти, такі як мурашина кислота, оцтова кислота, тіогліколева кислота, трифтороцтова кислота і сульфонова кислота (наприклад, п-толуолсульфонова кислота). Такі кислоти можуть застосовуватися окремо або в поєднанні. Приклади корисних лужних сполук включають карбонати, такі як карбонат натрію, карбонат калію, гідрокарбонат натрію і гідрокарбонат калію; і гідроксиди металів, такі як гідроксид натрію, гідроксид калію, гідроксид кальцію і гідроксид літію. Такі лужні сполуки можуть застосовуватися окремо або в поєднанні. Кислотну або лужну сполуку звичайно застосовують в кількості щонайменше близько 1 моль і переважно від близько 1 до близько 10 молів на моль сполуки Формули (1f). Реакцію переважно проводять при температурі від близько 0 до близько 200 °C і переважно від близько 0 до близько 150 °C і звичайно вона закінчується протягом від близько 10 хвилин до близько 80 годин. На Схемі реакції 6, якщо XB' в сполуці Формули (1f) є -SO2-, сполука Формули (1c) може бути легко одержана із сполуки Формули (1f), коли тіол впливає на сполуку в лужних умовах. Може використовуватися будь-яка лужна сполука, застосовувана в описаному вище гідролізі. Приклади тіолів включають ароматичні меркаптани, такі як тіофенол; нижчі алкілтіоли, такі як тіогліколева кислота; і т. д. Реакцію проводять в тих же умовах реакції, за винятком того, що тіол звичайно застосовують в кількості щонайменше 0,5 моля і переважно від близько 1 до близько 3 молів на моль сполуки Формули (1f). Схема реакції 7 , 35 40 2 3 4 5 1 1a де R , R , R , R , A і X2 такі, як визначені вище, і R є нижчим алкілом. Реакцію сполуки Формули (1g) із сполукою Формули (8) проводять в тих же умовах реакції, які застосовують для реакції сполуки Формули (3), в якій X 1 є галогеном, із сполукою Формули (2) на Схемі реакції 1. 4 Якщо R в сполуці Формули (1g) є воднем, може бути одержана сполука, в якій перше і п'яте 1a положення бензодіазепінового скелета одночасно заміщені R . Схема реакції 8 11 UA 103018 C2 , 1 5 2 3 5 1 4a де R , R , R , R , A і X2 такі, як визначені вище, і R є нижчим алкілом. Реакцію сполуки Формули (1i) із сполукою Формули (9) проводять в тих же умовах реакції, які застосовуються для реакції сполуки Формули (3), в якій X 1 є галогеном, із сполукою Формули (2) на Схемі реакції 1. 1 Якщо R в сполуці Формули (1i) є воднем, може бути одержана сполука, в якій перше і п'яте 4a положення бензодіазепінового скелета одночасно заміщені R . Схема реакції 9 10 , 1 15 20 4 5 1 2a де R , R , R , A і X2 такі, як визначені вище, і R є нижчим алкілом. Реакцію сполуки Формули (1k) із сполукою Формули (10) проводять в тих же умовах реакції, які застосовуються для реакції сполуки Формули (3), в якій X 1 є галогеном, із сполукою Формули (2) на Схемі реакції 1. 1 4 Якщо R і/або R є воднем в реакції сполуки Формули (1k) і сполуки Формули (10), водень 2a може бути заміщений R . Сполука Формули (2), яку застосовують як вихідний матеріал у вказаній вище схемі реакції, може бути легко одержана методом, показаним на представленій нижче схемі реакції. Схема реакції 10 12 UA 103018 C2 , 2 5 10 15 20 25 30 3 4 1a 9 10 де R , R , R , R і X2 такі, як визначені вище, R є нижчим алкокси, і R є нижчим алкоксикарбонілом. У реакції сполуки Формули (11) і сполуки Формули (12), сполука Формули (11) взаємодіє з карбоновою кислотою сполуки Формули (12) через звичайну реакцію утворення амідного зв'язку. Умови для відомих реакцій утворення амідного зв'язку можуть легко застосовуватися у вказаній вище реакції утворення аміду. Наприклад, можуть застосовуватися наступні методи реакції: (А) метод змішаного кислого ангідриду, в якому карбонова кислота (12) взаємодіє з алкілгалогенкарбоксилатом з одержанням змішаного кислого ангідриду, який потім взаємодіє з аміном (11); (В) метод активного складного ефіру, в якому карбонову кислоту (12) перетворюють в активований складний ефір, такий як феніловий ефір, р-нітрофеніловий ефір, N-гідроксисукцинімідний ефір, 1-гідроксибензотриазоловий ефір або подібні, або активований амід з бензоксазолін-2-тіоном, і активований складний ефір або амід взаємодіє з аміном (11); (С) метод карбодііміду, в якому карбонову кислоту (12) піддають конденсації з аміном (11) в присутності активуючого агента, такого як дициклогексилкарбодіімід, 1-(3-диметиламінопропіл)3-етилкарбодіімід (WSC), карбонілдіімідазол або подібні; (D) інші методи, наприклад метод, в якому карбонову кислоту (12) перетворюють в карбоновий ангідрид із застосуванням дегідратувального агента, такого як оцтовий ангідрид, і карбоновий ангідрид потім піддають взаємодії з аміном (11), метод, в якому складний ефір карбонової кислоти (12) з нижчим спиртом піддають взаємодії з аміном (11) при високому тиску і при високій температурі, метод, в якому галогенід карбонової кислоти (12), тобто карбоновий галогенід, піддають взаємодії з аміном (11), і т. д. Змішаний кислий ангідрид, застосовуваний в методі змішаного кислого ангідриду (А), може бути одержаний відомою реакцією Шоттена-Бауманна, і одержану змішану кислу ангідрид піддають взаємодії з аміном (11), звичайно без виділення, з одержанням сполуки Формули (13). Реакцію Шоттена-Бауманна проводять в присутності лужної сполуки. Корисні лужні сполуки включають сполуки, звичайно застосовувані в реакції Шоттена-Бауманна, такі як триетиламін, триметиламін, піридин, диметиланілін, N-етилдіізопропіламін, диметиламінопіридин, Nметилморфолін, 1,5-діазабіцикло[4.3.0]нонен-5 (DBN), 1,8-діазабіцикло[5.4.0]ундецен-7 (DBU), 13 UA 103018 C2 5 10 15 20 25 30 35 40 45 50 55 60 1,4-діазабіцикло[2.2.2]октан (DABCO) і інші органічні основи; карбонат натрію, карбонат калію, гідрокарбонат натрію, гідрокарбонат калію і інші карбонати; гідроксид натрію, гідроксид калію, гідроксид кальцію і інші гідроксиди металів; гідрид калію, гідрид натрію, калій, натрій, амід натрію, алкоголяти металів, такі як метилат натрію і етилат натрію, і інші неорганічні основи; і т. д. Реакцію звичайно проводять при температурі від близько -20 до близько 150 °C і переважно від близько 0 до близько 100 °C, звичайно протягом від близько 5 хвилин до близько 10 годин і переважно протягом від близько 5 хвилин до близько 5 годин. Реакцію одержаного змішаного кислого ангідриду з аміном (11) звичайно проводять при температурі від близько -20 до близько 150 °C і переважно від близько 10 до близько 50 °C, звичайно протягом від близько 5 хвилин до близько 30 годин і переважно від близько 5 хвилин до близько 25 годин. Звичайно метод змішаного кислого ангідриду проводять в розчиннику. Використовують розчинники, звичайно застосовувані для звичайних методів змішаного кислого ангідриду. Приклади застосовуваних розчинників включають хлороформ, дихлорметан, дихлоретан, чотирихлористий вуглець і інші галогеновані вуглеводні; бензол, толуол, ксилол і інші ароматичні вуглеводні; діетиловий ефір, діізопропіловий ефір, тетрагідрофуран, диметоксіетан і інші прості ефіри; метилацетат, етилацетат, ізопропілацетат і інші складні ефіри; N,N-диметилформамід, диметилсульфоксид, гексаметилфосфорний триамід і інші апротонні полярні розчинники; їх суміші і т. д. Приклади алкілгалогенкарбоксилатів, застосовуваних в методі змішаного ангідриду, включають метилхлорформіат, метилбромформіат, етилхлорформіат, етилбромформіат, ізобутилхлорформіат і т. д. В цьому методі карбонову кислоту (12), алкілгалгенкарбоксилат і амін (11) переважно застосовують в еквімолярних кількостях, але кожний з алкілгалогенкарбоксилату і карбонової кислоти (12) також можуть застосовуватися в кількості від близько 1 до близько 1,5 моля на моль аміну (11). Метод (С), в якому реакцію конденсації проводять в присутності активуючого агента, може проводитися у придатному розчиннику в присутності або за відсутності активуючого агента, у придатному розчиннику в присутності або за відсутності лужної сполуки. Розчинники і лужні сполуки, застосовувані в цьому методі, включають вказані вище як розчинники і лужні сполуки, застосовувані в методі, в якому галогенід карбонової кислоти взаємодіє з аміном (11), вказаному вище як один з інших методів (D). Придатна кількість активуючого агента становить щонайменше 1 моль і переважно від 1 до 5 молів на моль аміну (11). При застосуванні WSC як активуючого агента, додавання 1-гідроксибензотриазолу в реакційну систему дозволяє поліпшити проходження реакції. Реакцію проводять при температурі від близько -20 до близько 180 °C і переважно від близько 0 до близько 150 °C і звичайно вона завершується протягом від близько 5 хвилин до близько 90 годин. При застосуванні методу, в якому галогенід карбонової кислоти взаємодіє з аміном (11), вказаного вище як один з інших методів (D), реакцію проводять в присутності лужної сполуки у придатному розчиннику. Корисні лужні сполуки включають широкий спектр відомих лужних сполук, таких, які застосовуються в реакції Шоттена-Бауманна, описаній вище. Придатні розчинники включають, на доповнення до застосовуваних в методі змішаного кислого ангідриду, метанол, етанол, ізопропанол, пропанол, бутанол, 3-метокси-1-бутанол, етилцелозольв, метилцелозольв і інші спирти; ацетонітрил; піридин; ацетон; воду і т. д. Відношення галогеніду карбонової кислоти до аміну (11) не обмежене і може бути придатним чином вибране з широкого спектра. Звичайно застосовують, наприклад, щонайменше близько 1 моля і переважно від близько 1 до близько 5 молів галогеніду карбонової кислоти на моль аміну (11). Реакцію звичайно проводять при температурі від близько -20 до близько 180 °C і переважно від близько 0 до близько 150 °C і звичайно вона завершується протягом від близько 5 хвилин до близько 30 годин. Реакція утворення амідного зв'язку, показана на Схемі реакції 10, також може проводитися взаємодією карбонової кислоти (12) з аміном (11) в присутності сполуки фосфору, що служить як конденсуючий агент, такої як трифенілфосфін, хлорид дифенілфосфінілу, хлоридат феніл-Nфенілфосфораміду, діетилхлорфосфат, діетилціанофосфат, дифенілфосфорний азид, біс(2оксо-3-оксазолідиніл)фосфіновий хлорид або подібні. Реакцію проводять в присутності розчинника і лужної сполуки, застосовуваної в методі, в якому галогенід карбонової кислоти взаємодіє з аміном (11), звичайно при температурі від близько -20 до близько 150 °C і переважно від близько 0 до близько 100 °C і звичайно реакція завершується протягом від близько 5 хвилин до близько 30 годин. Можна застосовувати кожний з конденсуючого агента і карбонової кислоти (12) в кількостях щонайменше близько 1 моля і переважно від близько 1 до близько 2 молів на моль аміну (11). Реакція перетворення сполуки Формули (13) в сполуку Формули (14) може проводитися, наприклад, (1) відновленням сполуки Формули (13) у придатному розчиннику із застосуванням 14 UA 103018 C2 5 10 15 20 25 30 35 каталітичного гідрувального відновлювального агента, або (2) відновленням сполуки Формули (13) у придатному інертному розчиннику із застосуванням як відновлювального агента суміші кислоти з металом або сіллю металу, суміші металу або солі металу з гідроксидом, сульфідом лужного металу або амонієвою сіллю, або подібних. При застосуванні методу (1), в якому застосовують каталітичний гідрувальний відновлювальний агент, приклади придатних розчинників включають воду; оцтову кислоту; спирти, такі як метанол, етанол і ізопропанол; вуглеводні, такі як н-гексан і циклогексан; прості ефіри, такі як діоксан, тетрагідрофуран, діетиловий ефір і діетиленглікольдиметиловий ефір; складні ефіри, такі як етилацетат і метилацетат; апротонні полярні розчинники, такі як N,Nдиметилформамід; суміші таких розчинників і т. д. Приклади придатних каталітичних гідрувальних відновлювальних агентів включають паладій, паладієву чернь, паладій на вугіллі, платину на вугіллі, платину, платинову чернь, оксид платини, хроміт міді, нікель Ренея і т. д. Відновлювальний агент звичайно застосовують в кількості від близько 0,02 разу до рівної масі сполуки Формули (13). Температура реакції звичайно складає від близько -20 до близько 150 °C і переважно від близько 0 до близько 100 °C. Тиск водню звичайно складає від близько 1 до 10 атм. Реакція звичайно проходить протягом від близько 0,5 до близько 100 годин. Кислота, така як хлористоводнева кислота, може бути введена в реакційну систему даної реакції. При застосуванні методу (2), представленого вище, суміш заліза, цинку, олова або хлориду олова(II) з мінеральною кислотою, такою як хлористоводнева кислота або сірчана кислота; або суміш заліза, сульфату заліза(II), цинку або олова з гідроксидом лужного металу, таким як гідроксид натрію, сульфідом, таким як сульфід амонію, водним розчином аміаку або амонієвою сіллю, такою як хлорид амонію, або подібні, можуть застосовуватися як відновлювальний агент. Приклади інертних розчинників включають воду; оцтову кислоту; спирти, такі як метанол і етанол; прості ефіри, такі як діоксан; суміші таких розчинників і т. д. Умови реакції відновлення можуть бути придатним чином вибрані відповідно до застосовуваного відновлювального агента. Наприклад, якщо застосовується суміш хлориду олова(II) і хлористоводневої кислоти як відновлювальний агент, переважно проводити реакцію при температурі від близько 0 до близько 150 °C протягом від близько 0,5 до близько 10 годин. Відновлювальний агент застосовують в кількості щонайменше 1 моль і переважно від близько 1 до 5 молів на моль сполуки Формули (13). Реакцію перетворення сполуки Формули (14) в сполуку Формули (15) проводять в тих же умовах реакції, які застосовуються для реакції сполуки Формули (11) із сполукою Формули (12). Реакцію сполуки Формули (15) із сполукою Формули (8) проводять в тих же умовах, які застосовують для реакції сполуки Формули (1g) із сполукою Формули (8) на Схемі реакції 7. Схема реакції 11 , 1 40 45 2a 4 9 де R , R , R , R і X2 такі, як визначені вище. Реакцію сполуки Формули (17) із сполукою Формули (10) проводять в тих же умовах, які застосовують для реакції сполуки Формули (3), в якій X 1 є галогеном, із сполукою Формули (2) на Схемі реакції 1. 1 4 Якщо R і/або R є воднем в реакції сполуки Формули (17) і сполуки Формули (10), атом 2a водню може бути заміщений R . Схема реакції 12 15 UA 103018 C2 , 1 5 10 15 2 3 4 9 де R , R R , R і R такі, як визначені вище. Реакція перетворення сполуки Формули (16) в сполуку Формули (2) може проводитися у придатному розчиннику в присутності кислоти. Приклади розчинників включають воду; нижчі спирти, такі як метанол, етанол і ізопропанол; прості ефіри, такі як діоксан, тетрагідрофуран і діетиловий ефір; галогеновані вуглеводні, такі як дихлорметан, хлороформ і чотирихлористий вуглець; полярні розчинники, такі як ацетонітрил; і суміші таких розчинників. Приклади кислот включають мінеральні кислоти, такі як хлористоводнева кислота, сірчана кислота і бромистоводнева кислота; аліфатичні кислоти, такі як мурашина кислота і оцтова кислота; сульфонові кислоти, такі як п-толуолсульфонова кислота; кислоти Льюїса, такі як фторид бору, хлорид алюмінію і трибромід бору; йодиди, такі як йодид натрію і йодид калію; суміші таких йодидів і кислот Льюїса. Реакцію звичайно проводять при температурі від близько 0 до близько 200 °C і переважно від близько 0 до близько 150 °C і звичайно вона проходить протягом від близько 0,5 до близько 25 годин. Кислоту звичайно застосовують в кількості від 1 до 10 молів і переважно від близько 1 моля до близько 2 молів на моль сполуки Формули (16). Сполука Формули (16) може бути одержана із застосуванням способів, показаних на Схемах реакції 13 і 14 нижче. Схема реакції 13 20 , 1 25 2 3 4 9 де R , R , R , R і R такі, як визначені вище. Реакцію сполуки Формули (18) із сполукою Формули (19) проводять в тих же умовах, які застосовують для реакції сполуки Формули (11) із сполукою Формули (12) на Схемі реакції 10. Схема реакції 14 , 30 1 2 3 4a 9 де R , R , R , R і R такі, як визначені вище. Реакцію сполуки Формули (20) із сполукою Формули (9) проводять в тих же умовах, які застосовують для реакції сполуки Формули (1i) із сполукою Формули (9) на Схемі реакції 8. 16 UA 103018 C2 1 5 Якщо R в сполуці Формули (20) є воднем в реакції, може бути одержана сполука, в якій 4a перше і п'яте положення бензодіазепінового скелета одночасно заміщені R . Сполука Формули 4, яку застосовують як вихідний матеріал у вказаних вище схемах реакції, може бути легко одержана способом, показаним на наступній схемі реакції. Схема реакції 15 , 1 10 15 20 25 30 2 3 4 1 де R , R , R , R , A і X2 такі, як визначені вище, і X3 є галогеном. Реакцію сполуки Формули (2) із сполукою Формули (21) проводять в тих же умовах, які застосовують для реакції сполуки Формули (3), в якій X 1 є галогеном, із сполукою Формули (2) на Схемі реакції 1. X2 в сполуці Формули (4) може бути заміщений іншим атомом галогену додаванням його у придатний розчинник з галогенідом лужного металу і нагріванням при кипінні із зворотним холодильником. Приклади галогенідів лужного металу включають йодид натрію, бромід натрію, фторид натрію, хлорид натрію, йодид калію, бромід калію, фторид калію, хлорид калію і т. д. Приклади розчинників для галогенного обміну включають кетони, такі як ацетон, 2-бутанон; прості ефіри, такі як діоксан, тетрагідрофуран, діетиловий ефір, диметиловий ефір діетиленгліколю і диметиловий ефір етиленгліколю; і складні ефіри, такі як метилацетат і етилацетат. Такі розчинники можуть застосовуватися окремо або в поєднанні двох або більше. Галогенід лужного металу звичайно застосовують в кількості щонайменше 1 моль і переважно від близько 1 моля до близько 10 молів на моль сполуки Формули (4). Нагрівання-кипіння із зворотним холодильником продовжують до закінчення реакції. Наприклад, нагрівання-кипіння із зворотним холодильником переважно проводять протягом від близько 1 до близько 15 годин. Температура нагрівання-кипіння із зворотним холодильником варіюється залежно від застосовуваного розчинника і звичайно складає відблизько 0 до близько 150 °C і переважно від близько 0 до близько 100 °C. Сполука Формули (5), яку застосовують як вихідний матеріал, може бути легко одержана способом, показаним на наступній схемі реакції. Схема реакції 16 , 6 35 7 8 де R , R , XA, XB, X1 і R такі, як визначені вище. Реакцію сполуки Формули (5a) із сполукою Формули (6) проводять в тих же умовах, які застосовують для реакції сполуки Формули (1c) із сполукою Формули (6) на Схемі реакції 4. Реакцію сполуки Формули (5a) із сполукою Формули (7) проводять в тих же умовах, які застосовують для реакції сполуки Формули (1c) із сполукою Формули (7) на Схемі реакції 5. 17 UA 103018 C2 5 Сполука Формули (3), яку застосовують як вихідний матеріал, може бути легко одержана способом, показаним на наступній схемі реакції. Вихідний матеріал (24), застосовуваний на наступній Схемі реакції 18, може бути легко одержаний способом, показаним на Схемі реакції 17. Схема реакції 17 , 1 10 6a 6 де A і XA такі, як визначені вище, X1' є галогеном, і R такий же, як R , описаний вище, виключаючи атом водню. Реакцію сполуки Формули (22) із сполукою Формули (23) проводять в тих же умовах, які застосовують для реакції сполуки Формули (2) із сполукою Формули (3) на Схемі реакції 1. Схема реакції 18 15 , 6 20 25 30 35 7 1 11 де R , R , XA, XB, A , X1 і X2 такі, як визначені вище, і R є нижчим алкілсульфонілом. X4 є галогеном, і M є лужним металом, таким як натрій, калій і т. д. 11 Приклади нижчої алкілсульфонільної групи, представленої R , включають лінійні або розгалужені C1-6-алкілсульфонільні групи, такі як метилсульфоніл, етилсульфоніл, нпропілсульфоніл, ізопропілсульфоніл, н-бутилсульфоніл, ізобутилсульфоніл, третбутилсульфоніл, втор-бутилсульфоніл, н-пентилсульфоніл, ізопентилсульфоніл, неопентилсульфоніл, н-гексилсульфоніл, ізогексилсульфоніл і 3-метилпентилсульфоніл. Реакцію сполуки Формули (24) і сполуки Формули (25) проводять у придатному розчиннику або без розчинників в присутності кислоти. Приклади розчинників включають розчинники, застосовувані в реакції сполуки Формули (2) і сполуки Формули (3) на Схемі реакції 1. Приклади кислот включають мінеральні кислоти, такі як хлористоводнева кислота, сірчана кислота і бромистоводнева кислота; і органічні кислоти, такі як мурашина кислота, оцтова кислота, тіогліколева кислота, трифтороцтова кислота і сульфонова кислота (наприклад, птолуолсульфонова кислота). Такі кислоти можуть застосовуватися окремо або в поєднанні. Умови, відмінні від описаних вище, можуть бути такими, які застосовуються в реакції між сполукою Формули (2) і сполукою Формули (3) на Схемі реакції 1. Реакцію сполуки Формули (26) із сполукою Формули (7) проводять в тих же умовах, які застосовують для реакції сполуки Формули (2) із сполукою Формули (3) на Схемі реакції 1. 18 UA 103018 C2 5 10 15 20 25 30 Реакцію сполуки Формули (5c) із сполукою Формули (28) проводять в тих же умовах, які застосовують для реакції сполуки Формули (3), в якій X 1 є галогеном, із сполукою Формули (2) на Схемі реакції 1. Реакція перетворення сполуки Формули (27) із сполукою Формули (3a) може проводитися у придатному розчиннику або без розчинника в присутності кислоти або лужної сполуки. Приклади розчинників включають воду; нижчі спирти, такі як метанол, етанол, ізопропанол і трет-бутанол; кетони, такі як ацетон і метилетилкетон; прості ефіри, такі як діетиловий ефір, діоксан, тетрагідрофуран, моноглім і диглім; аліфатичні кислоти, такі як оцтова кислота і мурашина кислота; складні ефіри, такі як метилацетат і етилацетат; галогеновані вуглеводні, такі як хлороформ, дихлорметан, дихлоретан і чотирихлористий вуглець; диметилсульфоксид; N,N-диметилформамід і гексаметилфосфорний триамід; і суміші таких розчинників. Приклади кислот включають мінеральні кислоти, такі як хлористоводнева кислота, сірчана кислота і бромистоводнева кислота; і органічні кислоти, такі як мурашина кислота, оцтова кислота, трифтороцтова кислота і сульфонова кислота (наприклад, р-толуолсульфонова кислота і п-толуолсульфонат піридинію); кислоти Льюїса, такі як трибромід бору і трихлорид бору. Такі кислоти можуть застосовуватися окремо або в поєднанні. Приклади корисних лужних сполук включають карбонати, такі як карбонат натрію, карбонат калію, гідрокарбонат натрію і гідрокарбонат калію; і гідроксиди металів, такі як гідроксид натрію, гідроксид калію, гідроксид кальцію і гідроксид літію. Такі лужні сполуки можуть застосовуватися окремо або в поєднанні. Реакція переважно проходить при температурі звичайно від близько 0 до близько 200 °C і переважно від близько 0 до близько 150 °C і звичайно протягом від близько 10 хвилин до близько 50 годин. Реакцію сполуки Формули (3a) із сполукою Формули (29) проводять в тих же умовах, які застосовують для реакції сполуки Формули (5c) із сполукою Формули (28). Реакцію перетворення сполуки Формули (30) в сполуку Формули (3b) проводять в тих же умовах, які застосовують для реакції сполуки Формули (3), в якій X 1 є галогеном, із сполукою Формули (2) на Схемі реакції 1. Сполука Формули (7), яку застосовують як вихідний матеріал, може бути легко одержана способом, показаним на наступній схемі реакції. Схема реакції 19 , 35 40 7 1 де R , XB, X2 і A такі, як визначені вище. Реакцію сполуки Формули (32) із сполукою Формули (28) проводять в тих же умовах, які застосовують для реакції сполуки Формули (5c) із сполукою Формули (28) на Схемі реакції 18. Реакція перетворення сполуки Формули (33) в сполуку Формули (7a) може проводитися в тих же умовах реакції, які застосовують для реакції перетворення сполуки Формули (27) в сполуку Формули (3a) на Схемі реакції 18. Сполука Формули (5), яку застосовують як вихідний матеріал, може бути легко одержана способом, показаним на наступній схемі реакції. Схема реакції 20 , 45 19 UA 103018 C2 1 5 7 де A , R , XB і X2 такі, як визначені вище. Реакцію сполуки Формули (34) із сполукою Формули (35) проводять в тих же умовах, які застосовують для реакції сполуки Формули (3), в якій X 1 є галогеном, із сполукою Формули (2) на Схемі реакції 1. Реакція перетворення сполуки Формули (36) в сполуку Формули (5c) може проводитися в тих же умовах реакції, які застосовують для реакції перетворення сполуки Формули (1a) в сполуку Формули (1b) на Схемі реакції 2. Схема реакції 21 , 10 1 15 2 3 4 6 1 де R , R , R , R , R , XA і A такі, як визначені вище. 12 R є воднем, нижчим алкілом, нижчим алкоксикарбонілом, 2,313 дигідробензо[b]фурилкарбонілом або бензоїлом. R є нижчим алкоксикарбонілом, 2,32 дигідробензо[b]фурилкарбонілом або бензоїлом, і A є нижчим алкіленом. Реакція перетворення сполуки Формули (37) в сполуку Формули (38) може проводитися в тих же умовах реакції, які застосовують для реакції перетворення сполуки Формули (1f) в сполуку Формули (1c) на Схемі реакції 6. Схема реакції 22 20 , 1 25 30 35 40 2 3 4 6 12 1 2 13 де R , R , R , R , R , XA, R , A і A такі, як визначені вище. R є 2,3-дигідробензо[b]фурилом або фенілом. Реакцію сполуки Формули (38) із сполукою Формули (39) проводять в тих же умовах, які застосовують для реакції сполуки Формули (11) із сполукою Формули (12) на Схемі реакції 10. Крім того, сполуки у формі, в якій сольват (наприклад, гідрат, етанолат і т. д.) додають до вихідних сполук і цільових сполук, показаних на кожній схемі, включені в кожну формулу. Сполука Формули (1) відповідно до даного винаходу включає стереоізомери і оптичні ізомери. Вихідні сполуки і цільові сполуки, представлені в кожній схемі реакції, можуть застосовуватися у вигляді придатної солі. Кожна з цільових сполук, одержаних на вказаних вище схемах реакції, може бути виділена і очищена з реакційної суміші, наприклад, після охолоджування реакційної суміші, із застосуванням методів виділення, таких як фільтрація, концентрація, екстракція і т. д., для відділення неочищеного продукту реакції, і потім неочищений продукт реакції очищають звичайними методами очищення, такими як хроматографія на колонці, перекристалізація і т. д. Серед сполук відповідно до даного винаходу, сполуки, що мають лужну групу або групи, можуть легко утворювати солі із звичайними фармацевтично прийнятними кислотами. Приклади таких кислот включають хлористоводневу кислоту, бромистоводневу кислоту, азотну кислоту, сірчану кислоту, фосфорну кислоту і інші неорганічні кислоти, метансульфонову кислоту, п-толуолсульфонову кислоту, оцтову кислоту, лимонну кислоту, винну кислоту, малеїнову кислоту, фумарову кислоту, яблучну кислоту, молочну кислоту і інші органічні кислоти, і т. д. 20 UA 103018 C2 5 10 15 20 25 30 35 40 45 50 55 Серед сполук відповідно до даного винаходу, сполуки, що мають кислотну групу або групи, легко утворюють солі з фармацевтично прийнятними лужними сполуками. Приклади таких лужних сполук включають гідроксид натрію, гідроксид калію, гідроксид кальцію, карбонат натрію, карбонат калію, гідрокарбонат натрію, гідрокарбонат калію і т. д. Далі представлені описи фармацевтичних препаратів, що містять сполуку відповідно до даного винаходу як активний інгредієнт. Такі фармацевтичні препарати одержують додаванням сполуки відповідно до даного винаходу в звичайні фармацевтичні препарати із застосуванням звичайних розріджувачів або наповнювачів, таких як наповнювачі, добавки, зв'язуючі агенти, змочувальні агенти, розпушувачі, поверхнево-активні речовини, мастильні речовини і т. д. Форма таких фармацевтичних препаратів може бути вибрана з різних форм відповідно до цілей терапії. Типові приклади включають таблетки, пілюлі, порошки, розчини, суспензії, емульсії, гранули, капсули, супозиторії, ін'єкції (розчини, суспензії і т. д.) і подібні. Для одержання таблеток можуть застосовуватися будь-які відомі носії, включаючи, наприклад, лактозу, білий цукор, хлорид натрію, глюкозу, сечовину, крохмаль, карбонат кальцію, каолін, кристалічну целюлозу і інші наповнювачі; воду, етанол, пропанол, простий сироп, розчини глюкози, розчини крохмалю, розчини желатину, карбоксиметилцелюлозу, шелак, метилцелюлозу, фосфат калію, полівінілпіролідон і інші зв'язуючі агенти; сухий крохмаль, альгінат натрію, порошок агару, порошок ламінарії, гідрокарбонат натрію, карбонат кальцію, складні ефіри жирних кислот поліоксіетиленсорбітану, лаурилсульфат натрію, моногліцерид стеаринової кислоти, крохмаль, лактозу і інші розпушувачі; білий цукор, стеарин, масло какао, гідровані масла і інші інгібітори розкладання; четвертинну амонієву основу, лаурилсульфат натрію і інші промотори абсорбції; гліцерин, крохмаль і інші змочувальні агенти; крохмаль, лактозу, каолін, бентоніт, колоїдну кремнієву кислоту і інші адсорбенти; очищений тальк, стеарати, порошок борної кислоти, поліетиленгліколь і інші мастильні агенти; і т. д. Такі таблетки можуть бути покриті із застосуванням покриттів, при необхідності, для одержання, наприклад, таблеток з цукровим покриттям, таблеток з желатиновим покриттям, таблеток з ентеросолюбільним покриттям, таблеток з плівковим покриттям, таблеток з двошаровим або багатошаровим покриттям і т. д. Для одержання пілюль можуть застосовуватися будь-які відомі носії, включаючи, наприклад, глюкозу, лактозу, крохмаль, масло какао, гідровані рослинні олії, каолін, тальк і інші наповнювачі; порошок аравійської камеді, порошок трагаканту, желатин, етанол і інші зв'язуючі агенти; ламінарію, агар і інші розпушувачі; і т. д. Для одержання супозиторіїв можуть застосовуватися будь-які відомі носії, включаючи, наприклад, поліетиленгліколь, масло какао, вищі спирти, складні ефіри вищих спиртів, желатин, напівсинтетичні гліцериди і т. д. Для одержання ін'єкцій, розчин, суспензію або емульсію стерилізують і, переважно, роблять ізотонічною до крові. Будь-який відомий широко застосовуваний розріджувач може застосовуватися для одержання розчину, емульсії або суспензії. Приклади таких розріджувачів включають воду, етанол, пропіленгліколь, етоксилований ізостеариловий спирт, поліоксильований ізостеариловий спирт, складні ефіри жирних кислот поліоксіетиленсорбітану і т. д. В цьому випадку, фармацевтичний препарат може містити хлорид натрію, глюкозу або гліцерин в кількості, достатній для одержання ізотонічного розчину, і може містити звичайні солюбілізатори, буфери, знеболювальні агенти і т. д., а також, при необхідності, барвники, консерванти, смакові добавки, підсолоджувачі і т. д. і/або інші лікарські засоби. Частка сполуки відповідно до даного винаходу в фармацевтичному препараті не обмежена і вибирається з широкого інтервалу. Звичайно переважно, щоб фармацевтичний препарат містив сполуку відповідно до даного винаходу в кількості від 1 до 70 % мас. Спосіб введення фармацевтичного препарату відповідно до даного винаходу не обмежений, і препарат може вводитися способом, придатним для форми препарату, віку пацієнта і статі, стану хвороби і інших умов. Наприклад, таблетки, пілюлі, розчини, суспензії, емульсії, гранули і капсули вводять перорально. Ін'єкції вводять внутрішньовенно окремо або в поєднанні із звичайними внутрішньовенними вливаннями, такими як розчини глюкози, розчини амінокислот або подібні, або окремо вводять внутрішньом'язово, внутрішньошкірно, підшкірно або внутрішньоочеревинно, за потреби. Супозиторії вводять ректально. Дозу фармацевтичного препарату вибирають згідно зі способом застосування, віком пацієнта і статтю, тяжкістю захворювання і іншими умовами, і вона звичайно складає від 21 UA 103018 C2 5 10 15 20 25 30 35 40 45 50 55 близько 0,001 до близько 100 мг/кг маси тіла/добу і переважно від 0,001 до 50 мг/кг маси тіла/добу однією або декількома дозами. Оскільки доза змінюється залежно від різних умов, може бути достатньою доза менше вказаних меж або може потребуватися доза вище вказаних меж. При введенні людині у вигляді фармацевтичного засобу, сполука відповідно до даного винаходу може застосовуватися одночасно з або до, або після протитромботичних засобів, таких як інгібітори згортання крові і антитромбоцитарніагенти (наприклад, варфарин, аспірин і т. д.). Далі, дана сполука може застосовуватися одночасно з або до, або після лікарських засобів для лікування хронічних захворювань, таких як антигіпертензивні лікарські засоби (інгібітори ACE, бета-блокатори, антагоністи рецептора ангіотензину II), лікарські засоби при серцевій недостатності (кардіотонічні агенти, діуретики) і агенти для лікування діабету. Сполука відповідно до даного винаходу надає потужну блокувальну дію на людські Kv1.5 і/або GIRK1/4 канали і слабку блокувальну дію на HERG канали. Таким чином, сполука + відповідно до даного винаходу має характеристики селективного до передсердя блокатора K каналу. Тому сполука відповідно до даного винаходу може застосовуватися як фармакологічно активна речовина, яка є більш безпечною і має більш потужну дію на пролонгацію рефрактерного періоду передсердя в порівнянні із звичайними антиаритмічними агентами. Сполуку відповідно до даного винаходу переважно застосовують як терапевтичний агент при аритмії, такій як передсердна фібриляція, тріпотіння передсердь і передсердна тахікардія (елімінація аритмії і/або профілактика настання аритмії). Сполуку відповідно до даного винаходу особливо переважно застосовують як терапевтичний агент при передсердній фібриляції (дефібриляція і підтримання синусового ритму). Сполука відповідно до даного винаходу також може застосовуватися як профілактичний агент при тромбоемболії, такій як церебральний інфаркт, і як терапевтичний агент при серцевій недостатності. Сполука, яка надає потужну блокувальну дію на людські Kv1.5 і людські GIRK1/4 канали, може забезпечувати більш потужну дію на пролонгацію рефракторного періоду передсердя і є високобезпечною в порівнянні зі сполуками, інгібуючими який-небудь один з каналів. Більше того, ця сполука надає ефективну терапевтичну дію на передсердну фібриляцію (дефібриляція і збереження синусового ритму) в порівнянні із сполуками, інгібуючими який-небудь один з каналів. Тому сполука, що надає потужну блокувальну дію на людський Kv1.5 і людський GIRK1/4 канали, особливо корисна як терапевтичний агент при аритмії, такій як передсердна фібриляція, тріпотіння передсердь і передсердна тахікардія (перетворення аритмії і/або профілактика виникнення аритмії). Ця сполука особливо корисна як терапевтичний агент при передсердній фібриляції (дефібриляція і підтримання синусового ритму). НАЙКРАЩИЙ СПОСІБ ЗДІЙСНЕННЯ ВИНАХОДУ Представлені нижче приклади призначені для ілюстрації даного винаходу більш детально. Посилальний приклад 1 Синтез етил-N-(5-метокси-2-нітрофеніл)-N-метилмалонамату Гідрид натрію (60 % в маслі, 96 мг, 2,4 ммоль) суспендують в 10 мл диметилформаміду (ДМФ). У суспензію додають N-метил-5-метокси-2-нітроанілін (364 мг, 2 ммоль) при 0 °C, і перемішування продовжують протягом 30 хвилин при кімнатній температурі. Додають етилмалонілхлорид (0,38 мл, 3 ммоль) при 0 °C до перемішуваної суміші, і реакційну суміш перемішують при кімнатній температурі протягом ночі. У реакційну суміш додають воду і проводять екстрагування етилацетатом. Органічний шар сушать над сульфатом натрію і концентрують при зниженому тиску. Залишок очищають хроматографією на колонці з силікагелем (н-гексан:етилацетат=2:1→1:2). Очищений продукт концентрують при зниженому тиску з одержанням 554 мг (вихід: 90 %) етил N-(5-метокси-2-нітрофеніл)-N-метилмалонамату у вигляді жовтого масла. 1 H-ЯМР (CDCl3) δ ч./млн.: 1,24 (3H, т, J=7,1 Гц), 3,15-3,17 (2H, м), 3,25 (3H, с), 3,92 (3H, с), 4,13 (2H, кв, J=7,1 Гц), 6,93 (1H, д, J=2,8 Гц), 7,02 (1H, дд, J=2,8 і 9,2 Гц), 8,15 (1H, д, J=9,2 Гц). Посилальний приклад 2 Синтез етил-N-етил-N-(5-метокси-2-нітрофеніл)малонамату Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 1, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 1,11 (3H, т, J=7,2 Гц), 1,24 (3H, т, J=7,1 Гц), 3,11-3,25 (2H, м), 3,39-3,46 (1H, м), 3,92 (3H, с), 3,98-4,17 (3H, м), 6,89 (1H, д, J=2,8 Гц), 7,03 (1H, дд, J=9,2 і 2,8 Гц), 8,13 (1H, д, J=9,2 Гц). 22 UA 103018 C2 5 10 15 20 25 30 35 40 45 50 55 Посилальний приклад 3 Синтез етил-N-(2-аміно-5-метоксифеніл)-N-метилмалонамату Паладій на вугіллі (10 %, 0,5 г) додають до етанольного розчину (150 мл) етил-N-(5-метокси2-нітрофеніл)-N-метилмалонамату (3,0 г, 10 ммоль), і каталітичне відновлення проводять при кімнатній температурі і нормальному тиску. Реакційну суміш фільтрують через целіт для видалення каталізатора. Фільтрат концентрують при зниженому тиску з одержанням 2,68 г (вихід: кількісний) етил-N-(2-аміно-5-метоксифеніл)-N-метилмалонамату у вигляді жовтого масла. 1 H-ЯМР (CDCl3) δ ч./млн.: 1,22 (3H, т, J=7,1 Гц), 3,19-3,27 (5H, м), 3,52-3,68 (2H, ш), 3,74 (3H, с), 4,11 (2H, кв, J=7,1 Гц), 6,62 (1H, д, J=2,7 Гц), 6,73 (1H, д, J=8,7 Гц), 6,79 (1H, дд, J=2,7 і 8,7 Гц). Посилальний приклад 4 Синтез 8-метокси-1-метил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Етоксид натрію (204 мг, 3,0 ммоль) додають до етанольного розчину (15 мл) етил-N-(2аміно-5-метоксифеніл)-N-метилмалонамату (266 мг, 1,0 ммоль), і перемішують при 65 °C протягом 2,5 годин. Реакційну суміш охолоджують до кімнатної температури і концентрують при зниженому тиску. Залишок очищають хроматографією на колонці з силікагелем (дихлорметан:метанол=1:0→10:1). Очищений продукт концентрують досуха при зниженому тиску з одержанням 176,3 мг (вихід: 80 %) 8-метокси-1-метил-1,5-дигідробензо[b][1,4]діазепін2,4-діону у вигляді білого порошку. 1 H-ЯМР (CDCl3) δ ч./млн.: 3,36 (2H, с), 3,43 (3H, с), 3,84 (3H, с), 6,79-6,83 (1H, м), 7,06-7,09 (1H, м), 8,72 (1H, шс). Посилальний приклад 5 Синтез 1-етил-8-метокси-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Паладій на вугіллі (10 %, 1,1 г) додають до етанольного розчину (250 мл) етил-N-етил-N-(5метокси-2-нітрофенілмалонамату) (21,05 г, 67,8 ммоль), і охолоджують на бані з льодяною водою. Каталітичне відновлення продовжують при кімнатній температурі. Фільтрацію на целіті проводять для видалення каталізатора, і фільтрат концентрують при зниженому тиску. Залишок розчиняють в тетрагідрофурані (ТГФ) (200 мл). Додають етоксид натрію (6,9 г, 102 ммоль), і потім нагрівання продовжують при температурі кипіння із зворотним холодильником протягом 15 хвилин. Реакційну суміш охолоджують до кімнатної температури, і нерозчинну речовину, що випала в осад, збирають фільтрацією. Фільтрат концентрують при зниженому тиску. До залишку додають воду і зібрану нерозчинну речовину, і суміш нейтралізують хлористоводневою кислотою. Потім екстрагують етилацетатом. Органічний шар промивають насиченим водним розчином хлориду натрію, сушать над сульфатом натрію і концентрують при зниженому тиску. Залишок перекристалізовують з етанолу з одержанням 7,9 г (вихід: 50 %) 1-етил-8-метокси-1,5дигідробензо[b][1,4]діазепін-2,4-діону у вигляді білого порошку. Маточну рідину потім концентрують, і залишок очищають із застосуванням флеш-колонки з силікагелем (нгексан:етилацетат=1:1→0:1) з одержанням 2,9 г цільової сполуки. 1 H-ЯМР (CDCl3) δ ч./млн.: 1,19 (3H, т, J=7,1 Гц), 3,33 (2H, с), 3,78-3,84 (1H, м), 3,84 (3H, с), 4,13-4,25 (1H, м), 6,82 (1H, дд, J=8,8 і 2,7 Гц), 6,87 (1H, д, J=2,7 Гц), 7,09 (1H, д, J=8,8 Гц), 8,82 (1H, шс). Посилальний приклад 6 Синтез 1-етил-7-метокси-5-метил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Гідрид натрію (60 % в маслі, 44 мг, 1,1 ммоль) суспендують в диметилформаміді (ДМФ) (8 мл) і охолоджують на бані з льодяною водою до 0 °C. 8-Метокси-1-метил-1,5дигідробензо[b][1,4]діазепін-2,4-діон (220 мг, 1,0 ммоль) додають до суспензії при тій же температурі і перемішують при 0 °C протягом 1 години. До суміші додають етилйодид (187 мг, 1,2 ммоль) і перемішують при кімнатній температурі протягом ночі. До реакційної суміші додають воду і екстрагують етилацетатом. Органічний шар сушать над сульфатом натрію і концентрують при зниженому тиску. Залишок очищають хроматографією на колонці з силікагелем (н-гексан:етилацетат=4:1→1:1). Очищений продукт концентрують досуха при зниженому тиску з одержанням 190,2 мг (вихід: 77 %) 1-етил-7-метокси-5-метил-1,5дигідробензо[b][1,4]діазепін-2,4-діону у вигляді жовтої твердої речовини. 1 H-ЯМР (CDCl3) δ ч./млн.: 1,11 (3H, т, J=7,1 Гц), 3,31-3,32 (2H, м), 3,40 (3H, с), 3,59-3,68 (1H, м), 3,85 (3H, с), 4,18-4,30 (1H, м), 6,78 (1H, д, J=2,8 Гц), 6,84 (1H, дд, J=9,0 і 2,8 Гц), 7,26 (1H, д, J=9,0 Гц). 23 UA 103018 C2 5 10 15 20 25 30 35 40 45 50 55 60 Посилальний приклад 7 Синтез 1,5-діетил-7-метокси-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 6, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 1,04-1,14 (6H, м), 3,28 (2H, с), 3,50-3,64 (2H, м), 3,85 (3H, с), 4,35-4,47 (2H, м), 6,83-6,88 (2H, м), 7,25-7,27 (1H, м). Посилальний приклад 8 Синтез 7-метокси-5-метил-1-пропіл-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 6, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,76 (3H, т, J=7,3 Гц), 1,35-1,62 (2H, м), 3,32 (2H, с), 3,40 (3H, с), 3,33-3,51 (1H, м), 3,49 (3H, с), 4,21-4,38 (1H, м), 6,78 (1H, д, J=2,8 Гц), 6,84 (1H, дд, J=9,0 і 2,8 Гц), 7,25 (1H, д, J=9,0 Гц). Посилальний приклад 9 Синтез 1-ізобутил-7-метокси-5-метил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 6, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,69 (3H, д, J=6,7 Гц), 0,77 (3H, д, J=6,7 Гц), 1,56-1,90 (1H, м), 3,24 (1H, дд, J=13,6 і 5,9 Гц), 3,33 (2H, с), 3,40 (3H, с), 3,85 (3H, с), 4,32 (1H, дд, J=13,6 і 9,0 Гц), 6,78 (1H, д, J=2,8 Гц), 6,84 (1H, дд, J=9,0 і 2,9 Гц), 7,24 (1H, д, J=9,0 Гц). Посилальний приклад 10 Синтез 7-метокси-5-метил-1-(3-метилбутил)-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 6, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,80 (3H, д, J=6,3 Гц), 0,86 (3H, д, J=6,3 Гц), 1,22-1,53 (3H, м), 3,32 (2H, с), 3,39 (3H, с), 3,363,62 (1H, м), 3,85 (3H, с), 4,31-4,48 (1H, м), 6,78 (1H, д, J=2,8 Гц), 6,85 (1H, дд, J=8,8 і 2,8 Гц), 7,25 (1H, д, J=8,8 Гц). Посилальний приклад 11 Синтез 7-метокси-5-метил-1-(3-метилбут-2-еніл)-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 6, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 1,63 (6H, с), 3,32-3,34 (2H, м), 3,38 (3H, с), 3,84 (3H, с), 4,33 (1H, дд, J=13,6 і 6,2 Гц), 4,51 (1H, дд, J=13,6 і 6,9 Гц), 5,14-5,19 (1H, м), 6,76 (1H, д, J=2,8 Гц), 6,81 (1H, дд, J=9,0 і 2,8 Гц), 7,27 (1H, д, J=9,0 Гц). Посилальний приклад 12 Синтез 1-етил-7-метокси-3,3,5-триметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Гідрид натрію (60 % в маслі, 76 мг, 1,9 ммоль) суспендують в ДМФ (8 мл). Додають 1-етил-7метокси-5-метил-1,5-дигідробензо[b][1,4]діазепін-2,4-діон (190 мг, 0,76 ммоль) при 0 °C і перемішування проводять при тій же температурі протягом 1 години. До суміші додають метилйодид (0,19 мл, 3,1 ммоль) і перемішують при кімнатній температурі протягом 3 днів. До реакційної суміші додають воду і екстрагують етилацетатом. Органічний шар сушать над сульфатом натрію і концентрують при зниженому тиску. Залишок очищають хроматографією на колонці з силікагелем (етилацетат). Очищений продукт концентрують досуха при зниженому тиску з одержанням 169 мг (вихід: 80 %) 1-етил-7-метокси-3,3,5-триметил-1,5дигідробензо[b][1,4]діазепін-2,4-діону у вигляді жовтого порошку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,86 (3H, с), 1,15 (3H, т, J=7,1 Гц), 1,53 (3H, с), 3,40 (3H, с), 3,65-3,76 (1H, м), 3,85 (3H, с), 4,12-4,24 (1H, м), 6,73 (1H, д, J=2,8 Гц), 6,83 (1H, дд, J=9,0 і 2,8 Гц), 7,22 (1H, д, J=9,0 Гц). Посилальний приклад 13 Синтез 7-метокси-3,3,5-триметил-1-пропіл-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 12, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,76 (3H, т, J=7,3 Гц), 0,85 (3H, с), 1,52 (3H, с), 1,38-1,68 (2H, м), 3,41 (3H, с), 3,42-3,58 (1H, м), 3,85 (3H, с), 4,19-4,31 (1H, м), 6,72 (1H, д, J=2,8 Гц), 6,81 (1H, дд, J=9,0 і 2,8 Гц), 7,20 (1H, д, J=9,0 Гц). 24 UA 103018 C2 5 10 15 20 25 30 35 40 45 50 55 Посилальний приклад 14 Синтез 7-метокси-3,3,5-триметил-1-(3-метилбутил)-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 12, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,82 (3H, д, J=6,2 Гц), 0,85 (3H, с), 0,86 (3H, д, J=6,2 Гц), 1,30-1,49 (3H, м), 1,52 (3H, с), 3,40 (3H, с), 3,49-3,62 (1H, м), 3,85 (3H, с), 4,21-4,36 (1H, м), 6,71 (1H, д, J=2,8 Гц), 6,80 (1H, дд, J=9,0 і 2,8 Гц), 7,20 (1H, д, J=9,0 Гц). Посилальний приклад 15 Синтез 1,5-діетил-7-метокси-3,3-диметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 12, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,84 (3H, с), 1,06-1,18 (6H, м), 1,51 (3H, с), 3,56-3,83 (2H, м), 3,85 (3H, с), 4,29-4,42 (2H, м), 6,79-6,86 (2H, м), 7,21 (1H, д, J=8,9 Гц). Посилальний приклад 16 Синтез 1,3-діетил-7-метокси-5-метил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 12, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,86 (3H, т, J=7,3 Гц), 1,06 (3H, т, J=7,0 Гц), 1,94-2,05 (2H, м), 2,97 (1H, т, J=6,9 Гц), 3,40 (3H, с), 3,55-3,66 (1H, м), 3,86 (3H, с), 4,20-4,33 (1H, м), 6,79 (1H, д, J=2,8 Гц), 6,84-6,88 (1H, м), 7,267,29 (1H, м). Посилальний приклад 17 Синтез 3,3-діетил-7-метокси-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Дихлорид діетилмалонілу (0,95 мл, 5,5 ммоль) додають до розчину в дихлорметані (20 мл) 4-метокси-o-фенілендіаміну (691 мг, 5 ммоль) і триетиламіну (1,7 мл, 12,5 ммоль) при 0 °C і перемішують при кімнатній температурі протягом ночі. До реакційної суміші додають воду і екстрагують дихлорметаном. Органічний шар промивають насиченим водним розчином хлориду натрію, сушать над сульфатом натрію і концентрують при зниженому тиску. Залишок очищають хроматографією на колонці з силікагелем (н-гексан:етилацетат=9:1→1:1). Очищений продукт концентрують досуха при зниженому тиску з одержанням 452,3 мг (вихід: 34 %) 3,3-діетил-7метокси-1,5-дигідробензо[b][1,4]діазепін-2,4-діону у вигляді жовтого масла. 1 H-ЯМР (CDCl3) δ ч./млн.: 1,10 (6H, т, J=7,5 Гц), 1,86 (4H, кв, J=7,5 Гц), 3,76 (3H, с), 4,18 (2H, ш), 6,30 (1H, д, J=2,7 Гц), 6,35 (1H, дд, J=8,7 і 2,7 Гц), 7,23 (1H, д, J=8,7 Гц). Посилальний приклад 18 Синтез 3,3-діетил-7-метокси-1,5-диметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Гідрид натрію (60 % в маслі, 170 мг, 4,3 ммоль) суспендують в ДМФ (15 мл). Додають 3,3діетил-7-метокси-1,5-дигідробензо[b][1,4]діазепін-2,4-діон (452 мг, 1,7 ммоль) при 0 °C і перемішування продовжують при тій же температурі протягом 1 години. До суміші додають метилйодид (0,42 мл, 6,8 ммоль) і перемішують при кімнатній температурі протягом 3 днів. До реакційної суміші додають воду і екстрагують етилацетатом. Органічний шар сушать над сульфатом натрію і концентрують при зниженому тиску. Залишок очищають хроматографією на колонці з силікагелем (н-гексан:етилацетат=2:1→1:1). Очищений продукт концентрують досуха при зниженому тиску з одержанням 373 мг (вихід: 76 %) 3,3-діетил-7-метокси-1,5-диметил-1,5дигідробензо[b][1,4]діазепін-2,4-діону у вигляді білого порошку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,56 (3H, т, J=7,4 Гц), 1,02 (3H, т, J=7,3 Гц), 1,20-1,31 (2H, м), 2,15 (2H, кв, J=7,3 Гц), 3,38 (3H, с), 3,41 (3H, с), 3,85 (3H, с), 6,71 (1H, д, J=2,8 Гц), 6,81 (1H, дд, J=9,0 і 2,8 Гц), 7,14 (1H, д, J=9,0 Гц). Посилальний приклад 19 Синтез 7-метокси-1,3,3,5-тетраметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Гідрид натрію (60 % в маслі, 128 мг, 3,2 ммоль) суспендують в ДМФ (10 мл). Додають 8метокси-1-метил-1,5-дигідробензо[b][1,4]діазепін-2,4-діон (176 мг, 0,8 ммоль) при 0 °C і перемішування проводять при тій же температурі протягом 1 години. До суміші додають метилйодид (0,25 мл, 4,0 ммоль) і перемішують при кімнатній температурі протягом ночі. До реакційної суміші додають воду і екстрагують етилацетатом. Органічний шар промивають водою, сушать над сульфатом натрію і концентрують при зниженому тиску. Залишок 25 UA 103018 C2 5 10 15 20 25 30 35 40 45 50 55 перекристалізовують з н-гексану з одержанням 161,6 мг (вихід: 77 %) 7-метокси-1,3,3,5тетраметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону у вигляді білого порошку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,87 (3H, с), 1,54 (3H, с), 3,40 (3H, с), 3,42 (3H, с), 3,84 (3H, с), 6,73 (1H, с), 6,84 (1H, д, J=8,9 Гц), 7,14 (1H, д, J=8,9 Гц). Посилальний приклад 20 Синтез 5-етил-7-метокси-1,3,3-триметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 19, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,86 (3H, с), 1,19 (3H, т, J=7,1 Гц), 1,53 (3H, с), 3,38 (3H, с), 3,75-3,82 (1H, м), 3,84 (3H, с), 4,12-4,19 (1H, м), 6,80-6,85 (2H, м), 7,16 (1H, дд, J=8,6 і 0,5 Гц). Посилальний приклад 21 Синтез 1,3,3,5-тетраетил-7-метокси-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 19, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,56 (3H, т, J=7,4 Гц), 0,98 (3H, т, J=7,4 Гц), 1,07-1,26 (6H, м), 2,10-2,17 (2H, м), 3,59-3,74 (2H, м), 3,85 (3H, с), 4,24-4,32 (2H, м), 6,78-6,85 (2H, м), 7,20 (1H, д, J=8,9 Гц). Посилальний приклад 22 Синтез 1,3,3-триетил-7-метокси-5-метил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 19, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,57 (3H, т, J=7,4 Гц), 1,00 (3H, т, J=7,3 Гц), 1,16 (3H, т, J=7,2 Гц), 1,21-1,29 (2H, м), 2,10-2,19 (2H, м), 3,40 (3H, с), 3,72-3,83 (1H, м), 3,85 (3H, с), 4,06-4,14 (1H, м), 6,71 (1H, д, J=2,8 Гц), 6,82 (1H, дд, J=9,0 і 2,8 Гц), 7,21 (1H, д, J=9,0 Гц). Посилальний приклад 23 Синтез 1,3,5-триетил-7-метокси-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 19, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,85 (3H, т, J=7,5 Гц), 0,88-1,11 (6H, м), 2,92 2,97 (1H, м), 3,50-3,65 (2H, м), 3,86 (3H, с), 4,12 (2H, кв, J=7,2 Гц), 4,38-4,45 (2H, м), 6,84-6,89 (2H, м), 7,25-7,28 (1H, м). Посилальний приклад 24 Синтез 1-етил-7-гідрокси-3,3,5-триметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону 1,0 M розчин триброміду бору/дихлорметану (1,22 мл) додають до розчину в дихлорметані (3 мл) 1-етил-7-метокси-3,3,5-триметил-1,5-дигідробензо[b][1,4]-діазепін-2,4-діону (169 мг, 1,0 ммоль) при 0 °C і перемішують при кімнатній температурі протягом ночі. До реакційної суміші додають воду і метанол і екстрагують змішаним розчинником (дихлорметан:метанол=10:1). Органічний шар сушать над сульфатом натрію і концентрують досуха при зниженому тиску з одержанням 156,4 мг (вихід: 98 %) 1-етил-7-гідрокси-3,3,5-триметил-1,5дигідробензо[b][1,4]діазепін-2,4-діону у вигляді білого порошку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,90 (3H, с), 1,16 (3H, т, J=7,0 Гц), 1,55 (3H, с), 3,41 (3H, с), 3,66-3,78 (1H, м), 4,12-4,23 (1H, м), 6,79 (1H, д, J=2,7 Гц), 6,84 (1H, дд, J=8,8 і 2,7 Гц), 6,88 (1H, д, J=2,7 Гц), 7,18 (1H, д, J=8,8 Гц). Посилальний приклад 25 Синтез 3,3-діетил-7-гідрокси-1,5-диметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 24, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,55 (3H, т, J=7,3 Гц), 1,00 (3H, т, J=7,3 Гц), 1,15-1,29 (2H, м), 2,12 (2H, кв, J=7,3 Гц), 3,37 (3H, с), 3,38 (3H, с), 6,69 (1H, д, J=2,7 Гц), 6,76 (1H, дд, J=8,8 і 2,7 Гц), 7,06 (1H, д, J=8,8 Гц). Посилальний приклад 26 Синтез 1,3,3-триетил-7-гідрокси-5-метил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 24, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 26 UA 103018 C2 5 10 15 20 25 30 35 40 45 50 55 0,59 (3H, т, J=7,3 Гц), 1,01 (3H, т, J=7,3 Гц), 1,18 (3H, т, J=7,1 Гц), 1,21-1,34 (2H, м), 2,13-2,24 (2H, м), 3,40 (3H, с), 3,71-3,82 (1H, м), 4,05-4,16 (1H, м), 6,78 (1H, д, J=2,7 Гц), 6,84 (1H, дд, J=8,8 і 2,7 Гц), 7,04 (1H, шс), 7,17 (1H, д, J=8,8 Гц). Посилальний приклад 27 Синтез 1,3-діетил-7-гідрокси-5-метил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 24, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,87 (3H, т, J=7,4 Гц), 1,07 (3H, т, J=7,1 Гц), 1,95-2,05 (2H, м), 3,00 (1H, т, J=6,9 Гц), 3,39 (3H, с), 3,58-3,64 (1H, м), 4,22-4,29 (1H, м), 5,87 (1H, шс), 6,80-6,84 (2H, м), 7,21-7,24 (1H, м). Посилальний приклад 28 Синтез 1,3-діетил-7-гідрокси-3,5-диметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 24, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,64 (3H, т, J=7,3 Гц), 1,11-1,26 (5H, м), 1,54 (3H, с), 3,40 (3H, с), 3,70-3,82 (1H, м), 4,06-4,17 (1H, м), 6,39 (1H, шс), 6,75-6,83 (2H, м), 7,17-7,24 (1H, д, J=8,8 Гц). Посилальний приклад 29 Синтез 5-етил-7-гідрокси-1,3,3-триметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 24, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,88 (3H, с), 1,20 (3H, т, J=7,1 Гц), 1,53 (3H, с), 3,38 (3H, с), 3,73-3,84 (1H, м), 4,07-4,19 (1H, м), 6,76-6,81 (2H, м), 7,11 (1H, д, J=8,7 Гц). Посилальний приклад 30 Синтез 7-гідрокси-3,3,5-триметил-1-пропіл-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 24, синтезують цільову сполуку. 1 H-ЯМР (CD3OD) δ ч./млн.: 0,74 (3H, т, J=7,4 Гц), 0,85 (3H, с), 1,43 (3H, с), 1,38-1,61 (2H, м), 3,36 (3H, с), 3,53-3,61 (1H, м), 4,21-4,29 (1H, м), 6,76-6,82 (2H, м), 7,26 (1H, д, J=8,5 Гц). Посилальний приклад 31 Синтез 7-гідрокси-3,3,5-триметил-1-(3-метилбутил)-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 24, синтезують цільову сполуку. 1 H-ЯМР (CD3OD) δ ч./млн.: 0,79 (3H, д, J=6,1 Гц), 0,85 (3H, с), 0,85 (3H, д, J=6,1 Гц), 1,26-1,40 (3H, м), 1,42 (3H, с), 3,35 (3H, с), 3,56-3,63 (1H, м), 4,34-4,41 (1H, м), 6,76-6,82 (2H, м), 7,28 (1H, д, J=8,7 Гц). Посилальний приклад 32 Синтез 1,3,3,5-тетраетил-7-гідрокси-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 24, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,58 (3H, т, J=7,4 Гц), 0,98 (3H, т, J=7,3 Гц), 1,08-1,29 (8H, м), 2,12-2,19 (2H, м), 3,57-3,76 (2H, м), 4,20-4,34 (2H, м), 6,09 (1H, шс), 6,78-6,82 (2H, м), 7,14-7,17 (1H, м). Посилальний приклад 33 Синтез 1,5-діетил-7-гідрокси-3,3-диметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 24, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,87 (3H, с), 1,08-1,17 (6H, м), 1,54 (3H, с), 3,57-3,73 (2H, м), 4,27-4,39 (2H, м), 6,85-6,87 (2H, м), 7,15-7,18 (1H, м). Посилальний приклад 34 Синтез 1,3,5-триетил-7-гідрокси-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 24, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,84 (3H, т, J=7,4 Гц), 1,02-1,12 (6H, м), 1,95-2,19 (2H, м), 3,03 (1H, т, J=6,9 Гц), 3,51-3,70 (2H, м), 4,33-4,46 (2H, м), 6,89-6,93 (2H, м), 7,23 (1H, д, J=8,5 Гц), 7,57 (1H, с). 27 UA 103018 C2 5 10 15 20 25 30 35 40 45 50 55 Посилальний приклад 35 Синтез 7-гідрокси-1,3,3,5-тетраметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 24, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,90 (3H, с), 1,49 (3H, с), 3,39 (3H, с), 3,40 (3H, с), 6,73 (1H, д, J=2,7 Гц), 6,80 (1H, дд, J=8,9 і 2,7 Гц), 7,13 (1H, д, J=8,9 Гц). Посилальний приклад 36 Синтез 7-гідрокси-1-ізобутил-3,3,5-триметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 24, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,69 (3H, д, J=6,7 Гц), 0,75 (3H, д, J=6,7 Гц), 0,87 (3H, с), 1,53 (3H, с), 1,72-1,91 (1H, м), 3,24 (1H, дд, J=6,3 і 13,5 Гц), 3,40 (3H, с), 4,35 (1H, дд, J=8,6 і 13,5 Гц), 6,72-6,79 (2H, м), 7,13 (1H, д, J=8,6 Гц). Посилальний приклад 37 Синтез 7-(3-хлорпропоксі)-1-етил-3,3,5-триметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону 1-Етил-7-гідрокси-3,3,5-триметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діон (1,85 г, 7,1 ммоль) і карбонат калію (1,2 г, 8,5 ммоль) додають в ацетонітрил із 50 % вмістом води (40 мл) і розчиняють нагріванням до 70 °C. Додають 1-бромo-3-хлорпропан (2,1 мл, 21 ммоль) і нагрівають при кип'ятінні із зворотним холодильником протягом 6 годин. Реакційну суміш охолоджують до кімнатної температури. Додають воду і екстрагують етилацетатом. Органічний шар сушать над сульфатом натрію і концентрують при зниженому тиску. Залишок очищають хроматографією на колонці з силікагелем (н-гексан:етилацетат=2:1→1:1). Очищений продукт концентрують досуха при зниженому тиску з одержанням 2,18 г (вихід: 91 %) 7-(3-хлорпропоксі)1-етил-3,3,5-триметил-1,5-дигідробензо[b][1,4]-діазепін-2,4-діону у вигляді безбарвного масла. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,86 (3H, с), 1,15 (3H, т, J=7,1 Гц), 1,53 (3H, с), 2,21-2,38 (2H, м), 3,40 (3H, с), 3,63-3,89 (4H, м), 4,10-4,26 (2H, м), 6,74 (1H, д, J=2,8 Гц), 6,83 (1H, дд, J=2,8 і 9,0 Гц), 7,21 (1H, д, J=9,0 Гц). Посилальний приклад 38 Синтез 7-(3-хлорпропокси)-1,3,3,5-тетраметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 37, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,88 (3H, с), 1,53 (3H, с), 2,20-2,32 (2H, м), 3,40 (3H, с), 3,42 (3H, с), 3,77 (2H, т, J=6,1 Гц), 4,15 (2H, т, J=5,8 Гц), 6,74 (1H, д, J=2,7 Гц), 6,83 (1H, дд, J=2,7 і 9,0 Гц), 7,15 (1H, д, J=9,0 Гц). Посилальний приклад 39 Синтез 1-етил-7-(3-йодпропокси)-3,3,5-триметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діон 7-(3-Хлорпропоксі)-1-етил-3,3,5-триметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діон (2,18 г, 6,4 ммоль) і йодид натрію (4,8 г, 32 ммоль) додають до ацетону (50 мл) і нагрівають при кипінні із зворотним холодильником протягом 8,5 годин. Реакційну суміш охолоджують до кімнатної температури, додають воду і екстрагують етилацетатом. Органічний шар сушать над сульфатом натрію і концентрують при зниженому тиску. Залишок очищають хроматографією на колонці з силікагелем (н-гексан:етилацетат=1:1). Очищений продукт концентрують при зниженому тиску з одержанням 2,76 г (вихід: 100 %) 1-етил-7-(3-йодoпропокси)-3,3,5-триметил1,5-дигідробензо[b][1,4]діазепін-2,4-діону у вигляді безбарвного масла. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,87 (3H, с), 1,15 (3H, т, J=7,1 Гц), 1,53 (3H, с), 2,26-2,34 (2H, м), 3,39 (2H, т, J=6,6 Гц), 3,653,76 (1H, м), 3,41 (3H, с), 4,07 (2H, т, J=5,8 Гц), 4,12-4,24 (1H, м), 6,74 (1H, д, J=2,8 Гц), 6,83 (1H, дд, J=9,0 і 2,8 Гц), 7,22 (1H, д, J=9,0 Гц). Посилальний приклад 40 Синтез 7-(3-йодпропокси)-1,3,3,5-тетраметил-1,5-дигідробензо[b][1,4]діазепін-2,4-діону Застосовуючи придатний вихідний матеріал і методику Посилального прикладу 39, синтезують цільову сполуку. 1 H-ЯМР (CDCl3) δ ч./млн.: 0,88 (3H, с), 1,54 (3H, с), 2,22-2,34 (2H, м), 3,39 (2H, т, J=6,6 Гц), 3,40 (3H, с), 3,42 (3H, с), 4,07 (2H, т, J=5,8 Гц), 6,74 (1H, д, J=2,8 Гц), 6,83 (1H, дд, J=2,8 і 9,0 Гц), 7,15 (1H, д, J=9,0 Гц). 28
ДивитисяДодаткова інформація
Автори англійськоюOshima, Kunio, Oshiyama, Takashi, Taira, Shinichi, Menjo, Yasuhiro, Yamabe, Hokuto, Matsumura, Shuuji, Ueda, Masataka, Koga, Yasuo, Tai, Kuninori, Nakayama, Sunao, Onogawa, Toshiyuki, Tsujimae, Kenji
Автори російськоюТаи Кунинори
МПК / Мітки
МПК: A61P 9/06, C07D 409/14, C07D 417/14, C07D 413/14, C07D 401/12, C07D 471/04, C07D 405/14, C07D 401/14, A61K 31/551, C07D 513/04, C07D 243/12, C07D 491/04, C07D 495/04
Мітки: композиція, бензодіазепіну, сполуки, фармацевтична
Код посилання
<a href="https://ua.patents.su/159-103018-spoluki-benzodiazepinu-i-farmacevtichna-kompoziciya.html" target="_blank" rel="follow" title="База патентів України">Сполуки бензодіазепіну і фармацевтична композиція</a>