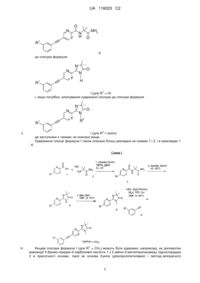
Етинільні похідні як антагоністи метаботропного глутаматного рецептора
Номер патенту: 116023
Опубліковано: 25.01.2018
Автори: Річчі Антоніо, Віейра Ерік, Єшкє Гєорг, Рюхер Даніель, Штадлєр Хайнц, Ліндеманн Лотар, Мартін Райнер Е.
Формула / Реферат
1. Сполука формули І
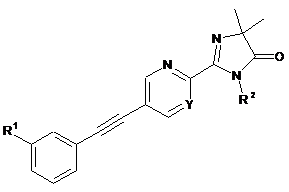 , I
, I
де
Y позначає N або СН;
R1 позначає водень, фтор або хлор; і
R2 позначає водень або нижчий алкіл;
або її фармацевтично прийнятна кислотно-адитивна сіль.
2. Сполука формули І за п. 1, де Y позначає N.
3. Сполука формули І за будь-яким з пп. 1 або 2, яка являє собою:
2-[5-[2-(3-хлорфеніл)етиніл]-2-піримідил]-3,5,5-триметил-імідазол-4-он,
3,5,5-триметил-2-[5-(2-фенілетиніл)-2-піримідо]імідазол-4-он або
2-[5-[2-(3-фторфеніл)етиніл]-2-піримідил]-3,5,5-триметил-імідазол-4-он.
4. Сполука формули І за п. 1, де Y позначає СН.
5. Сполука формули І за будь-яким з пп. 1 або 4, яка являє собою:
2-[5-[2-(3-фторфеніл)етиніл]-2-піридил]-3,5,5-триметил-імідазол-4-он,
3,5,5-триметил-2-[5-(2-фенілетиніл)-2-піридил]імідазол-4-он або
2-[5-[2-(3-хлорфеніл)етиніл]-2-піридил]-3,5,5-триметил-імідазол-4-он.
6. Сполука за будь-яким з пп. 1-5 для застосування як терапевтично активної речовини.
7. Спосіб одержання сполуки формули І за будь-яким з пп.1-5, за яким проводять:
а) взаємодію сполуки формули
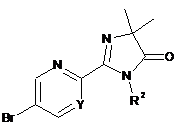 5
5
із сполукою формули
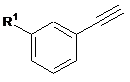 6
6
до сполуки формули
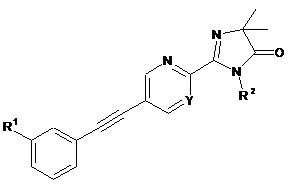 , I
, I
де замісники є такими, як описано в п. 1, або
b) циклізацію сполуки формули
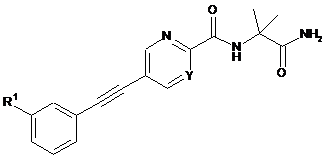 9
9
до сполуки формули
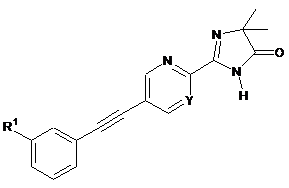 , I (для R2=H)
, I (для R2=H)
і, якщо потрібно, алкілування одержаної сполуки до сполуки формули
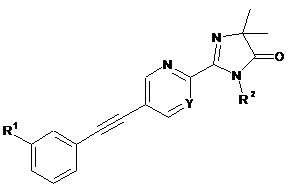 , І (для R2=алкіл)
, І (для R2=алкіл)
де замісники є такими, як описано в п. 1.
8. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-5 і терапевтично активний носій.
9. Застосування сполуки за будь-яким з пп. 1-5 для лікування тривоги і болю, депресії, синдрому Мартіна-Белл, розладів аутистичного спектра, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (GERD).
10. Застосування сполуки за будь з пп. 1-5 для виробництва лікарського засобу для лікування тривоги і болю, депресії, синдрому Мартіна-Белл, розладів аутистичного спектра, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (GERD).
11. Сполука за будь-яким з пп. 1-5 для застосування при лікуванні тривоги і болю, депресії, синдрому Мартіна-Белл, розладів аутистичного спектра, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (GERD).
12. Спосіб лікування тривоги і болю, депресії, синдрому Мартіна-Белл, розладів аутистичного спектра, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (GERD), який включає введення ефективної кількості сполуки за будь яким з пп. 1-5.
Текст
Реферат: Даний винахід належить до етинільних похідних формули І N O N N Y R R 2 1 ,I де Y позначає N або СН; UA 116023 C2 (12) UA 116023 C2 1 R позначає водень, фтор або хлор; і 2 R позначає водень або нижчий алкіл; або фармацевтично прийнятних кислотно-адитивних солей. Несподівано було встановлено, що сполуки загальної формули І є антагоністами метаботропних глутаматних рецепторів (негативними алостеричними модуляторами) для застосування при лікуванні тривоги і болю, депресії, синдрому Мартіна-Белл, розладів аутистичного спектра, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (GERD). UA 116023 C2 Даний винахід відноситься до етинільних похідних формули I N O N Y N 2 R 1 R 5 10 15 20 25 30 35 40 45 50 I, де Y позначає N або CH; 1 R позначає водень, фтор або хлор; і 2 R позначає водень або нижчий алкіл; або фармацевтично прийнятних кислотно-адитивних солей. Несподівано було виявлено, що сполуки загальної формули I є антагоністами метаботропних глутаматних рецепторів (NAM = негативними алостеричними модуляторами від англ. Negative allosteric modulators). Сполуки з аналогічним основним ядром були, в основному, описані як позитивні алостеричні модулятори рецептора mGluR5. Несподівано було виявлено, що замість позитивних алостеричних модуляторів mGluR5 були одержані надзвичайно сильні антагоністи mGluR5, які мають абсолютно протилежну фармакологію в порівнянні з такою ж у позитивних алостеричних модуляторів. Позитивні алостеричні модулятори mGluR5 (РАМ) призводять до збільшення активності рецепторів Ca2 + (мобілізації) у присутності фіксованої концентрації глутамату, в той час як алостеричний антагоніст (негативний алостеричний модулятор, NAM) призводить до зниження активації рецептора. Сполуки формули I відрізняються цінними терапевтичними властивостями. Вони можуть застосовуватися при лікуванні або профілактиці розладів, опосередкованих рецепторами mGluR5. У центральній нервовій системі (ЦНС) передача стимулів відбувається в результаті взаємодії нейромедіатора, який надсилається нейроном, з нейрорецептором. Глутамат є основним збудливим нейромедіатором в головному мозку і відіграє унікальну роль в різних функціях центральної нервової системи (ЦНС). Глутамат-залежні стимулюючі рецептори розділені на дві основні групи. Перша основна група, а саме іонотропні рецептори, утворює контрольовані лігандом іонні канали. Метаботропні рецептори глутамату (mGluR) відносяться до другої основної групи і, крім того, відносяться до сімейства G-білок сполучених рецепторів. В даний час відомо вісім різних членів цих mGluR і деякі з них навіть мають підтипи. За їх гомологією послідовностей, механізмом передачі сигналу і селективністю агоністів, ці вісім рецепторів можуть бути поділені на три підгрупи: mGluR1 і mGluR5 належать до групи I, mGluR2 і mGluR3 відносяться до групи II, mGluR4, mGluR6, mGluR7 і mGluR8 і відносяться до групи III. Негативні алостеричні модулятори метаботропних глутаматних рецепторів, які належать до першої групи, можуть бути використані для лікування або профілактики гострих та/або хронічних неврологічних розладів, таких як хвороба Паркінсона, синдром Мартіна-Белл, аутистичні розлади, когнітивні розлади і порушення пам'яті, а також хронічного та гострого болю і гастроезофагеальної рефлюксної хвороби (GERD). У зв'язку з цим, іншими показаннями для лікування є обмежена функція мозку, викликана операціями шунтування або пересадки, погане кровопостачання головного мозку, травми спинного мозку, травми голови, гіпоксія, викликана вагітністю, зупинка серця і гіпоглікемія. Також станами для лікування є ішемія, хорея Хантінгтона, бічний аміотрофічний склероз (ALS), недоумство, викликане СНІДом, травми очей, ретинопатія, ідіопатичний паркінсонізм або паркінсонізм, викликаний лікарськими засобами, а також стани, які ведуть до глутаматдефіцитної функції, такої як, наприклад, м'язові спазми, судоми, мігрень, нетримання сечі, нікотинова залежність, опіатна залежність, тривога, блювота, дискінезія і депресії. Розладами, опосередкованими повністю або частково рецепторами mGluR5, є, наприклад, гострі, травматичні та хронічні дегенеративні процеси в нервовій системі, такі як хвороба Альцгеймера, старече слабоумство, хвороба Паркінсона, хорея Гентінгтона, бічний 1 UA 116023 C2 5 10 15 20 25 30 аміотрофічний склероз і розсіяний склероз, психічні захворювання, такі як шизофренія і тривога, депресія, біль і наркотична залежність (Expert Opin. Ther. Patents (2002), 12, (12)). Селективні антагоністи mGluR5 є особливо корисними для лікування розладів, при яких необхідне зменшення активації рецепторів mGluR5, таких як тривога і біль, депресія, синдром Мартіна-Белл, розлади аутистичного спектру, хвороба Паркінсона, і гастроезофагеальна рефлюксна хвороба (ГЕРХ). Об'єктами даного винаходу є сполуки формули I та їх фармацевтично прийнятні солі, вищезгадані сполуки як фармацевтично активні речовини та їх одержання. Іншими об'єктами винаходу є лікарські засоби на основі сполук за винаходом та їх виготовлення, а також застосування сполук при лікуванні або профілактиці (ДН) розладів, опосередкованих рецепторами mGluR5, якими є тривога і біль, депресія, синдром Мартіна-Белл, розлади аутистичного спектру, хвороба Паркінсона, і гастроезофагеальна рефлюксна хвороба (ГЕРХ, і, відповідно, для одержання відповідних лікарських засобів). Одним втіленням даного винаходу є сполуки формули I, де Y позначає N і 1 2 R и R є такими, як описано вище, наприклад, наступні сполуки: 2-[5-[2-(3-хлорфеніл)етиніл]-2-піримідил]-3,5,5-триметил-імідазол-4-он 3,5,5-Триметил-2-[5-(2-фенілетиніл)-2-піримідил]імідазол-4-он або 2-[5-[2-(3-фторфеніл)етиніл]-2-піримідил]-3,5,5-триметил-імідазол-4-он. Одним додатковим втіленням даного винаходу є сполуки формули I, де 1 2 Y позначає CH і R і R є такими, як описано вище, наприклад наступні сполуки: 2-[5-[2-(3-фторфеніл)етиніл]-2-піридил]-3,5,5-триметил-імідазол-4-он 3,5,5-Триметил-2-[5-(2-фенілетиніл)-2-піридил]імідазол-4-он або 2-[5-[2-(3-хлорфеніл)етиніл]-2-піридил]-3,5,5-триметил-імідазол-4-он. Сполуки формули I можуть бути одержані способами, наведеними нижче, способами, наведеними в прикладах, або аналогічними способами. Відповідні умови реакції для окремих стадій реакції відомі фахівцеві в даній області. Послідовність реакцій не обмежується такою, яка зображена на схемах, однак, залежно від вихідних матеріалів та їх реакційної здатності, послідовність стадій реакції можуть бути вільно змінені. Вихідні речовини є або комерційно доступними, або можуть бути одержані способами, аналогічними способам, наведеним нижче, способами, описаними в посиланнях, наведених в описі або в прикладах, або способами, відомими в даній галузі техніки. Дані сполуки формули I та їх фармацевтично прийнятні солі можуть бути одержані способами, описаними нижче, які включають а) взаємодію сполуки формули N N 35 Br O N Y R 2 5 Із сполукою формули 1 R 6 з утворенням сполуки формули N N R 40 1 O N Y R 2 I де замісники є такими, як описано вище, або b) циклізацію сполуки формули 2 UA 116023 C2 O N R Y 1 NH2 N H O 9 до сполуки формули N N R Y 1 O N H 2 I (для R = H) і, якщо потрібно, алкілування одержаної сполуки до сполуки формули N N R 1 O N Y R 2 2 I (для R = алкіл) де заступники є такими, як описано вище. Одержання сполук формули I також описано більш докладно на схемах 1 і 2, і в прикладах 1 5 - 6. 10 2 Кінцеві сполуки формули I (для R = CH3) можуть бути одержані, наприклад, за допомогою взаємодії 5-бромо-піридин-2-карбонової кислоти 1 з 2-аміно-2-метилпропанаміду гідрохлоридом 2 в присутності основи, такої як основа Хуніга (діізопропілетиламін) і пептид-зв'язуючого 3 UA 116023 C2 5 реагенту, такого як TBTU, в розчиннику, такому як ДМФ. Циклізація сполуки 3 з основою, такою як метоксид натрію, в розчиннику, такому як метанол, дає необхідну бромпіридинову сполуку 4. Алкілування бромпіридинової сполуки 4 за допомогою алкілуючого агента, такого як йодометан, у присутності гідриду натрію в розчиннику, такому як ДМФ, призводить до необхідної алкілованої сполуки 5. Сполучення за Соногаширою сполуки 5 з арилацетиленовою похідною 6 2 дає необхідні кінцеві сполуки формули I (для R = CH3). 2 10 15 20 25 30 35 Сполуки формули I (для R = CH3) також можуть бути одержані, наприклад, сполученням за Соногаширою 5-бромо-піримідин-2-карбонової кислоти 1 з відповідною арилацетиленовою похідною 6 з одержанням необхідної ацетиленкарбонової кислоти 8. Взаємодія 8 з 2-аміно-2метилпропанаміду гідрохлоридом 2 в присутності основи, такої як основа Хуніга, і пептидзв'язуючого реагенту, такого як TBTU, в розчиннику, такому як ДМФ, дає відповідну сполуку 9. Циклізація сполуки 9 у присутності основи, такої як метоксид натрію, в розчиннику, такому як 2 метанол, дає необхідну ацетиленову похідну I (для R = H). Алкілування сполуки I за допомогою алкілуючого агента, такого як йодометан, у присутності гідриду натрію в розчиннику, такому як 2 ДМФ, дає необхідні кінцеві сполуки формули I (для R = CH3). Винахід також відноситься до застосування сполуки відповідно до цього винаходу, а також її фармацевтично прийнятної солі для виготовлення лікарських засобів для лікування та профілактики захворювань, опосередкованих рецепторами mGluR5, як описано вище. Фармацевтично прийнятні солі сполук формули I можуть бути легко виготовлені згідно широко відомим способам, і, беручи до уваги природу сполуки, яку конвертують у сіль. Неорганічні або органічні кислоти, такі як, наприклад, соляна кислота, бромистоводнева кислота, сірчана кислота, азотна кислота, фосфорна кислота або лимонна кислота, мурашина кислота, фумарова кислота, малеїнова кислота, оцтова кислота, янтарна кислота, винна кислота, метансульфонова кислота, п-толуолсульфокислота і т.д. підходять для утворення фармацевтично прийнятних солей основних сполук формули I. Сполуки, які містять лужні метали або лужноземельні метали, наприклад натрій, калій, кальцій, магній тощо, основні аміни або основні амінокислоти є придатними для утворення фармацевтично прийнятних солей кислотних сполук. Більш того, даний винахід також відноситься до лікарських засобів, що містять одну або більше сполук цього винаходу і фармацевтично прийнятні ексципієнти для лікування і запобігання захворювань, опосередкованих рецепторами mGluR5, таких як тривога і біль, депресія, синдром Мартіна-Белл, розлади аутистичного спектру, хвороба Паркінсона, і гастроезофагеальна рефлюксна хвороба (ГЕРХ). Фармакологічна активність сполук тестувалася з використанням наступного способу: кДНК, кодуючу щурячий рецептор mGlu 5a транзиентно трансфікували в клітини EBNA з використанням способу, описаного E.-J. Schlaeger і K. Christensen (Cytotechnology 1998, 15, 1 4 UA 116023 C2 13). Вимірювання Ca i проводили на mGlu 5a трансфікованих EBNA клітинах після інкубування клітин з Fluo 3-AM (доступного в компанії FLUKA, 0,5 мкМ кінцева концентрація) протягом 1 години при 37 °C з подальшими 4 промивками буфером для аналізу (DMEM з 2+ додаванням солі Хенка і 20 мМ HEPES. Вимірювання Ca і виконували з використанням спектрофотометра для зчитування планшетів для візуалізації флуоресценції (FLIPR, Molecular Devices Corporation, La Jolla, CA, USA). Коли сполуки оцінювалися в ролі антагоністів, вони тестувалися проти 10 мкМ глутамату в якості агоніста. Криві інгібування (антагоністів) апроксимувались за допомогою чотирьох-параметричного логістичного рівняння, що дає значення IC50, і коефіцієнта Хілла з використанням ітераційного нелінійного програмного забезпечення для апроксимування кривих Origin (Microcal Software Inc., Northampton, MA, USA). Одержали значення Ki для тестованих сполук. Значення Ki визначали за допомогою наступної формули: 2+ 5 10 Ki IC 50 = 1+ [L] EC 50 15 20 в якій значення IC50 представляли ті концентрації тестованих сполук у мкМ, при яких 50% ефекту сполук піддавалося антагонізму. [L] являє собою концентрацію і значення EC 50 являє собою концентрацію сполук у мкМ, яка викликає близько 50% стимуляції. Сполуки даного винаходу є антагоністами рецепторів mGluR 5. Активності сполук формули I, виміряні за допомогою аналізу, наведеного вище, і як показано в таблиці нижче, знаходяться в діапазоні Ki 30:70. Необхідний 2-[5-[2-(3-фторфеніл)етиніл]-2-піридил]-3,5,5триметил-імідазол-4-он (210 мг, 74% вихід) одержали у вигляді світло-жовтого осаду, MS: m/e = + 322.4 (M+H ). Приклад 2 3,5,5-Триметил-2-[5-(2-фенілетиніл)-2-піридил]імідазол-4-он N O N N + 20 Сполуку, вказану в заголовку, одержали у вигляді білого осаду, MS: m/e = 304,4 (M+H ), з використанням способу, аналогічного описаному в прикладі 1, стадія 4, з 2-(5-бромо-2-піридил) 3,5,5-триметил-імідазол-4-ону (Приклад 1, стадія 3) і фенілацетилену. Приклад 3 2-[5-[2-(3-хлорфеніл)етиніл]-2-піридил]-3,5,5-триметил-імідазол-4-он N O N N Cl 25 Сполуку, вказану в заголовку, одержали у вигляді білого осаду, MS: m/e = 338.4/340.4 + (M+H ), з використанням способу, аналогічного описаному в прикладі 1, стадія 4 з 2-(5-бромо-2піридил)-3,5,5-триметил-імідазол-4-ону (Приклад 1, стадія 3) і 3-хлорфенілацетилен. Приклад 4 2-[5-[2-(3-хлорфеніл)етиніл]-2-піримідил]-3,5,5-триметил-імідазол-4-он N O N N N Cl 30 Стадія 1: 5-(3-хлор-фенілетиніл)-піримідин-2-карбонова кислота 8 UA 116023 C2 O N OH N Cl 5 10 Біс-(трифенілфосфін)-паладій(II)дихлорид (86 мг, 123 мкмоль, 0,01 екв.) розчинили в 12 мл ДМФ. Додали 5-бромо-піримідин-2-карбонову кислоту (2,5 г, 12,3 ммоль) і 3-хлорфенілацетилен (2,02 г, 14,8 ммоль, 1,2 екв.) при кімнатній температурі. Додали триетиламін (11 мл, 78,8 ммоль, 6,4 екв.), трифенілфосфін (65 мг, 246 мкмоль, 0,02 екв.) і йодид міді (I) (24 мг, 123 мкмоль, 0,01 екв.) і суміш перемішували протягом 2 годин при 80 °C. Реакційну суміш охолодили до кімнатної температури, розбавили 5 мл етилацетату і 20 мл води. Розчин 2 н HCl (20 мл) додали по краплях і суміш перемішували протягом 20 хвилин при кімнатній температурі. Осад відфільтрували, промили 10 TBME, сконцентрували під вакуумом. Необхідну 5-(3-хлорфенілетініл)-пірімідін-2-карбонову кислоту (2,8 г, 88% вихід) одержали у вигляді білого осаду, + MS: m/e = 259,4/261,4 (M+H ). Стадія 2: N-(2-аміно-1,1-диметил-2-оксо-етил)-5-[2-(3-хлорфеніл)етиніл]піримідин-2карбоксамід O N NH2 N H N O Cl 15 Сполуку, вказану в заголовку, одержали у вигляді жовтого осаду, MS: m/e = 341,3/343,4 + (M+H ), з використанням способу, аналогічного описаному в прикладі 1, стадія 1, з 5-(3-хлорфенілетініл)-пірімідін-2-карбонова кислота (Приклад 4, стадія 1) і 2-аміно-2-метилпропанаміду гідрохлориду. Стадія 3: 2-[5-[2-(3-хлорфеніл)етиніл]піримідин-2-іл]-4,4-диметил-1H-імідазол-5-он N O N N H N Cl 20 25 Сполуку, вказану в заголовку, одержали у вигляді білого осаду, MS: m/e = 325,4/327,4 + (M+H ), з використанням способу, аналогічного описаному в прикладі 1, стадія 2, з N-(2-аміно1,1-диметил-2-оксо-етил)-5-[2-(3-хлорфеніл)етиніл]піримідин-2-карбоксаміду (Приклад 4, стадія 2). Стадія 4: 2-[5-[2-(3-хлорфеніл)етиніл]-2-піримідил]-3,5,5-триметил-імідазол-4-он N O N N N Cl 30 Сполуку, вказану в заголовку, одержали у вигляді білого осаду, MS: m/e = 339,4/341,3 + (M+H ), з використанням способу, аналогічного описаному в прикладі 1, стадія 3, з 2-[5-[2-(3хлорфеніл)етиніл]піримідин-2-іл]-4,4-диметил-1H-імідазол-5-ону (Приклад 4, стадія 3) і йодометану. Приклад 5 3,5,5-триметил-2-[5-(2-фенілетініл)-2-піримідо]імідазол-4-он 9 UA 116023 C2 N O N N N Стадія 1: 5-(2-Фенілетиніл)піримідин-2-карбонова кислота O N OH N 5 Сполуку, вказану в заголовку, одержали у вигляді темно-коричневого осаду, MS: m/e = 222,9 + (M-H ), з використанням способу, аналогічного описаному в прикладі 4, стадія 1, з 5-бромопіримідин-2-карбонової кислоти і фенілацетилену. Стадія 2: N-(2-аміно-1,1-диметил-2-оксо-етил)-5-(2-фенілетиніл)піримідин-2-карбоксамід O N N H N NH2 O + 10 Сполуку, вказану в заголовку, одержали у вигляді жовтого масла, MS: m/e = 309,4 (M+H ), з використанням способу, аналогічного описаному в прикладі 1, стадія 1, з 5-(2фенілетиніл)піримідин-2-карбонова кислота (Приклад 5, стадія 1) і 2-аміно-2-метилпропанаміду гідрохлориду. Стадія 3: 4,4-диметил-2-[5-(2-фенілетиніл)піримідин-2-іл]-1H-імідазол-5-он N O N N H N 15 + Сполуку, вказану в заголовку, одержали у вигляді жовтого осаду, MS: m/e = 291.4 (M+H ), з використанням способу, аналогічного описаному в прикладі 1, стадія 2, з N-(2-аміно-1,1диметил-2-оксо-етил)-5-(2-фенілетиніл)піримідин-2-карбоксаміду (Приклад 5, стадія 2). Стадія 4: 3,5,5-Триметил-2-[5-(2-фенілетиніл)піримідин-2-іл]імідазол-4-он N O N N N 20 + Сполуку, вказану в заголовку, одержали у вигляді жовтого осаду, MS: m/e = 305.4 (M+H ), з використанням способу, аналогічного описаному в прикладі 1, стадія 3, з 4,4-диметил-2-[5-(2фенілетиніл)піримідин-2-іл]-1H-імідазол-5-ону (Приклад 5, стадія 3) і йодометану. Приклад 6 2-[5-[2-(3-фторфеніл)етиніл]-2-піримідил]-3,5,5-триметил-імідазол-4-он 10 UA 116023 C2 N O N N N F Стадія 1: 5-(3-фтор-фенілетиніл)-піримідин-2-карбонова кислота O N OH N F 5 Сполуку, вказану в заголовку, одержали з використанням методу, аналогічного описаному в прикладі 4, стадія 1 з 5-бромо-піримідин-2-карбонової кислоти і 3-фторфенілацетилену. Стадія 2: N-(2-аміно-1,1-диметил-2-оксо-етил)-5-[2-(3-фторфеніл)етиніл]піримідин-2карбоксамід O N NH2 N H N O F + 10 Сполуку, вказану в заголовку, одержали у вигляді жовтого осаду, MS: m/e = 327,4 (M+H ), з використанням способу, аналогічного описаному в прикладі 1, стадія 1, з 5-(3-фтор-фенілетініл)піримідин-2-карбонова кислота (Приклад 6, стадія 1) і 2-аміно-2-метилпропанаміду гідрохлориду. Стадія 3: 2-[5-[2-(3-фторфеніл)етиніл]піримідин-2-іл]-4,4-диметил-1H-імідазол-5-он N O N N N H F 15 + Сполуку, вказану в заголовку, одержали у вигляді жовтого осаду, MS: m/e = 309,3 (M+H ), з використанням способу, аналогічного описаному в прикладі 1, стадія 2, з N-(2-аміно-1,1диметил-2-оксо-етил)-5-[2-(3-фторфеніл)етиніл]піримідин-2-карбоксаміду (Приклад 6, стадія 2). Стадія 4: 2-[5-[2-(3-фторфеніл)етиніл]-2-піримідил]-3,5,5-триметил-імідазол-4-он N O N N N F 20 Сполуку, вказану в заголовку, одержали у вигляді оранжевого осаду, MS: m/e = 323,4 + (M+H ), з використанням способу, аналогічного описаному в прикладі 1, стадія 3, з 2-[5-[2-(3фторфеніл)етиніл]піримідин-2-іл]-4,4-диметил-1H-імідазол-5-ону (Приклад 6, стадія 3) і йодометану. 11 UA 116023 C2 ФОРМУЛА ВИНАХОДУ 5 1. Сполука формули І N O N N Y R 10 15 20 R 2 1 ,I де Y позначає N або СН; 1 R позначає водень, фтор або хлор; і 2 R позначає водень або нижчий алкіл; або її фармацевтично прийнятна кислотно-адитивна сіль. 2. Сполука формули І за п. 1, де Y позначає N. 3. Сполука формули І за будь-яким з пп. 1 або 2, яка являє собою: 2-[5-[2-(3-хлорфеніл)етиніл]-2-піримідил]-3,5,5-триметилімідазол-4-он, 3,5,5-триметил-2-[5-(2-фенілетиніл)-2-піримідо]імідазол-4-он або 2-[5-[2-(3-фторфеніл)етиніл]-2-піримідил]-3,5,5-триметилімідазол-4-он. 4. Сполука формули І за п. 1, де Y позначає СН. 5. Сполука формули І за будь-яким з пп. 1 або 4, яка являє собою: 2-[5-[2-(3-фторфеніл)етиніл]-2-піридил]-3,5,5-триметилімідазол-4-он, 3,5,5-триметил-2-[5-(2-фенілетиніл)-2-піридил]імідазол-4-он або 2-[5-[2-(3-хлорфеніл)етиніл]-2-піридил]-3,5,5-триметилімідазол-4-он. 6. Сполука за будь-яким з пп. 1-5 для застосування як терапевтично активної речовини. 7. Спосіб одержання сполуки формули І за будь-яким з пп. 1-5, за яким проводять: а) взаємодію сполуки формули N O N 25 Br N Y R 2 5 із сполукою формули R 1 6 до сполуки формули 12 UA 116023 C2 N O N N R Y R 2 1 ,I де замісники є такими, як описано в п. 1, або b) циклізацію сполуки формули O N NH2 N H O Y R 1 9 5 до сполуки формули N O N N H Y R 1 2 , I (для R =H) і, якщо потрібно, алкілування одержаної сполуки до сполуки формули N O N N Y R R 2 1 2 , І (для R =алкіл) 10 де замісники є такими, як описано в п. 1. 8. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-5 і терапевтично активний носій. 9. Застосування сполуки за будь-яким з пп. 1-5 для лікування тривоги і болю, депресії, синдрому Мартіна-Белл, розладів аутистичного спектра, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (GERD). 13 UA 116023 C2 5 10. Застосування сполуки за будь-яким з пп. 1-5 для виробництва лікарського засобу для лікування тривоги і болю, депресії, синдрому Мартіна-Белл, розладів аутистичного спектра, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (GERD). 11. Сполука за будь-яким з пп. 1-5 для застосування при лікуванні тривоги і болю, депресії, синдрому Мартіна-Белл, розладів аутистичного спектра, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (GERD). 12. Спосіб лікування тривоги і болю, депресії, синдрому Мартіна-Белл, розладів аутистичного спектра, хвороби Паркінсона і гастроезофагеальної рефлюксної хвороби (GERD), який включає введення ефективної кількості сполуки за будь-яким з пп. 1-5. 10 Комп’ютерна верстка О. Гергіль Міністерство економічного розвитку і торгівлі України, вул. М. Грушевського, 12/2, м. Київ, 01008, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 14
ДивитисяДодаткова інформація
Назва патенту англійськоюEthynyl derivatives as metabotropic glutamate receptor antagonists
Автори англійськоюJaeschke, Georg, Lindemann, Lothar, Martin, Rainer E., Ricci, Antonio, Rueher, Daniel, Stadler, Heinz, Vieira, Eric
Автори російськоюЕшке Георг, Линдэманн Лотар, Мартин Райнер Э., Риччи Антонио, Рюхер Даниель, Штадлер Хайнц, Виэйра Эрик
МПК / Мітки
МПК: C07D 401/04, C07D 403/04, A61K 31/4439, A61K 31/506
Мітки: метаботропного, похідні, антагоністи, рецептора, етинільні, глутаматного
Код посилання
<a href="https://ua.patents.su/16-116023-etinilni-pokhidni-yak-antagonisti-metabotropnogo-glutamatnogo-receptora.html" target="_blank" rel="follow" title="База патентів України">Етинільні похідні як антагоністи метаботропного глутаматного рецептора</a>
Попередній патент: Машина для контактного стикового зварювання рейок
Наступний патент: Пароконденсаційна башта для грануляційної установки
Випадковий патент: Спосіб пластики дефекта міжшлуночкової перегородки, ускладненого 100% легеневою гіпертензією