Конденсовані похідні пурину як антагоністи рецепторів аденозину а1
Формула / Реферат
1. Сполука формули І:
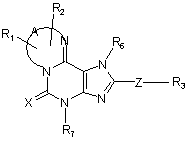 ,Формула І
,Формула І
де R1 і R2 незалежно вибирають з групи, що складається з:
a) водню;
b) алкілу, алкенілу або алкінілу, де вказаний алкіл, алкеніл або алкініл є або незаміщеним, або функціоналізованим одним або більше із замісників, вибраних з групи, що складається з гідрокси, алкокси, аміно, алкіламіно, діалкіламіно, гетероциклілу, ациламіно, алкілсульфоніламіно і гетероциклілкарбоніламіно; і
c) арилу або заміщеного арилу;
R3 вибирають з групи, що складається з:
(а) біциклічної, трициклічної або пентациклічної групи, вибраної з групи, що складається з:
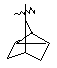
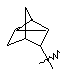
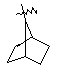
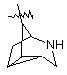
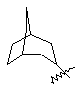
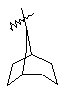

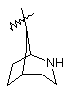
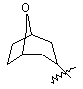
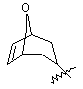
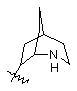
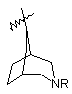
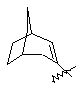
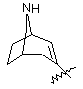
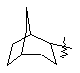
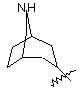
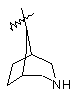
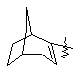
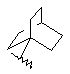
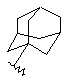
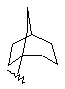
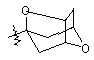
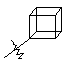
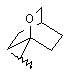
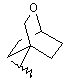
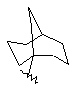
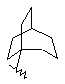
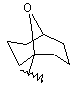
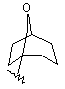
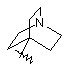
де біциклічна, трициклічна або пентациклічна група є або незаміщеною, або функціоналізованою одним або більше із замісників, вибраних з групи, що складається з:
(і) алкілу, алкенілу і алкінілу; де кожна алкільна, алкенільна або алкінільна група є або незаміщеною, або функціоналізованою одним або більше із замісників, вибраних з групи, що складається з (алкоксикарбоніл)аралкілкарбамоїлу,
(аміно) (R5)ацилгідразинілкарбонілу,
(аміно) (R5)ацилоксикарбокси,
(гідрокси)(карбоалкокси)алкілкарбамоїлу,
ациламіноалкіламіно, ацилокси, альдегідо, алкенокси, алкеніламіно, алкенілсульфоніламіно, алкокси, алкоксикарбонілу, алкоксикарбонілалкіламіно, алкоксикарбоніламіно, алкоксикарбоніламіноацилокси, алкоксикарбоніламіноалкіламіно, алкіламіно, алкіламіноалкіламіно, алкілкарбамоїлу, алкілфосфоно, алкілсульфоніламіно, алкілсульфонілокси, аміно, аміноацилокси, аміноалкіларалкілкарбамоїлу, аміноалкілкарбамоїлу, аміноалкілгетероциклілалкілкарбамоїлу, аміноциклоалкілалкілциклоалкілкарбамоїлу, аміноциклоалкілкарбамоїлу, аралкоксикарбонілу, аралкоксикарбоніламіно, арилгетероциклілу, арилокси, арилсульфоніламіно, арилсульфонілокси, карбамоїлу, карбонілу, ціано, ціаноалкілкарбамоїлу, циклоалкілтаміно, діалкіламіно, діалкіламіноалкіламіно, діалкіламіноалкілкарбамоїлу, діалкілфосфоно, галоалкілсульфоніламіно, галогену, гетероциклілу, гетероциклілалкіламіно, гетероциклілкарбамоїлу, гідрокси, гідроксіалкілсульфоніламіно, оксіміно, фосфату, фосфоно, -R5, R5-алкокси, R5-алкіл(алкіл)аміно, R5-алкілалкілкарбамоїлу, R5-алкіламіно, R5-алкілкарбамоїлу, R5-алкілсульфонілу, R5-алкілсульфоніламіно, R5-алкілтіо, R5-гетероциклілкарбонілу, заміщеного аралкіламіно, заміщеного арилкарбоксіалкоксикарбонілу, заміщеного арилсульфоніламіноалкіламіно, заміщеного гетероарилсульфоніламіно, заміщеного гетероциклілу, заміщеного гетероцикліламіноалкіламіно, заміщеного гетероциклілсульфоніламіно, сульфоксіациламіно, тіокарбамоїлу, трифторметилу; і
(іі) (алкоксикарбоніл)аралкілкарбамоїлу,
(аміно) (R5) ацилгідразинілкарбонілу,
(аміно) (R5)ацилоксикарбокси,
(гідрокси)(карбоалкокси)алкілкарбамоїлу,
ациламіноалкіламіно, ацилокси, альдегідо, алкенокси, алкеніламіно, алкенілсульфоніламіно, алкокси, алкоксикарбонілу, алкоксикарбонілалкіламіно, алкоксикарбоніламіно, алкоксикарбоніламіноацилокси, алкоксикарбоніламіноалкіламіно, алкіламіно, алкіламіноалкіламіно, алкілкарбамоїлу, алкілфосфоно, алкілсульфоніламіно, алкілсульфонілокси, аміно, аміноацилокси, аміноалкіларалкілкарбамоїлу, аміноалкілкарбамоїлу, аміноалкілгетероциклілалкілкарбамоїлу,
аміноциклоалкілалкілциклоалкілкарбамоїлу, аміноциклоалкілкарбамоїлу, аралкоксикарбонілу, аралкоксикарбоніламіно, арилгетероциклілу, арилокси, арилсульфоніламіно, арилсульфонілокси, карбамоїлу, карбонілу, ціано, ціаноалкілкарбамоїлу, циклоалкіламіно, діалкіламіно, діалкіламіноалкіламіно, діалкіламіноалкілкарбамоїлу, діалкілфосфоно, галоалкілсульфоніламіно, галогену, гетероциклілу, гетероциклілалкіламіно, гетероциклілкарбамоїлу, гідрокси, гідроксіалкілсульфоніламіно, оксіміно, фосфату, фосфоно, -R5, R5-алкокси, R5-алкіл(алкіл)аміно, R5-алкілалкілкарбамоїлу, R5-алкіламіно, R5-алкілкарбамоїлу, R5-алкілсульфонілу, R5-алкілсульфоніламіно, R5-алкілтіо, R5-гетероциклілкарбонілу, заміщеного аралкіламіно, заміщеного арилкарбоксиалкоксикарбонілу, заміщеного арилсульфоніламіноалкіламіно, заміщеного гетероарилсульфоніламіно, заміщеного гетероциклілу, заміщеного гетероцикліламіноалкіламіно, заміщеного гетероциклілсульфоніламіно, сульфоксіациламіно, тіокарбамоїлу, трифторметилу;
R4 вибирають з групи, що складається з водню, С1-4-алкілу, С1-4-алкіл-СО2Н, і фенілу, де С1-4-алкільна, С1-4-алкіл-СO2Н і фенільна групи є або незаміщеними, або функціоналізованими одним-трьома замісниками, вибраними з групи, що складається з галогену, -ОН, -ОМе, -NH2, NO2, бензилу і бензилу, функціоналізованого одним-трьома замісниками, вибраними з групи, що складається з галогену, -ОН, -ОМе, -NH2, і –NO2;
R5 вибирають з групи, що складається з -(CR1R2)nCOOH, -С(СF3)2OН, -CONHNHSO2CF3, -CONHOR4, -CONHSO2R4, -CONHSO2NHR4, -C(OH)R4PO3H2, -NHCOCF3, -NHCONHSO2R4, -NHPO3H2, -NHSO2R4, -NHSO2NHCOR4, -ОРО3Н2, -ОSО3Н, -PO(OH)R4, -РО3Н2, -SO3Н, -SО3NНR4, -SO3NНСОR4, -SO3NHCONHCO2R4 і наступних груп:
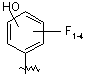
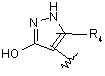
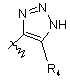
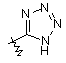
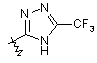
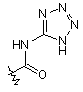
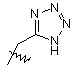
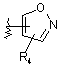
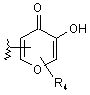 ;
;
n = 0, 1, 2 або 3;
А вибирають з групи, що складається з -СН=СН, -(CH)m-(CH)m, CH=CH-CH2 і -СН2-СН=СН;
m = 1 або 2;
X являє собою O або S;
Z вибирають з групи, що складається з простого зв'язку, -О-, -(СН2)n-, -O(СН2)1-2-, -СН2OСН2-, -(СН2)1-2O-,
і
R6 вибирають з групи, що складається з водню, алкілу, ацилу, алкілсульфонілу, аралкілу, заміщеного аралкілу, заміщеного алкілу і гетероциклілу; і
R7 вибирають з групи, що складається з:
a) водню;
b) алкілу, алкенілу, що містить не менше 3 атомів вуглецю, або алкінілу, що містить не менше 3 атомів вуглецю; де вказаний алкіл, алкеніл або алкініл є або незаміщеним, або функціоналізованим одним або більше із замісників, вибраних з групи, що складається з гідрокси, алкокси, аміно, алкіламіно, діалкіламіно, гетероциклілу, ациламіно, алкілсульфоніламіно і гетероциклілкарбоніламіно; і
c) арилу або заміщеного арилу;
d) алкіларилу або арилу, заміщеного алкілом.
2. Сполука за п. 1, де сполука знаходиться в формі, вибраній з групи, що складається з ахіральної сполуки, рацемату, оптично активної сполуки, чистого діастереоізомеру, суміші діастереоізомерів і фармакологічно прийнятних солей приєднання.
3. Сполука за п. 1, де R1 і R2 незалежно вибирають з групи, що складається з
a) алкілу, алкенілу або алкінілу, де вказаний алкіл, алкеніл або алкініл є або незаміщеним, або функціоналізованим одним або більше із замісників, вибраних з групи, що складається з гідрокси, алкокси, аміно, алкіламіно, діалкіламіно, гетероциклілу, ациламіно, алкілсульфоніламіно і гетероциклілкарбоніламіно; і
b) арилу або заміщеного арилу.
4. Сполука за п. 3, де, щонайменше, один з R1 і R2 являє собою алкіл.
5. Сполука за п. 1, де А являє собою - (СН)m-(СН)m.
6. Сполука за п. 1, де R7 являє собою алкіл.
7. Сполука за п. 1, де Z являє собою простий зв'язок.
8. Сполука формули II:
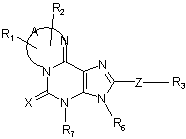 ,Формула ІІ
,Формула ІІ
де R1 і R2 незалежно вибирають з групи, що складається з:
a) водню;
b) алкілу, алкенілу або алкінілу, де вказаний алкіл, алкеніл або алкініл є або незаміщеним, або функціоналізованим одним або більше із замісників, вибраних з групи, що складається з гідрокси, алкокси, аміно, алкіламіно, діалкіламіно, гетероциклілу, ациламіно, алкілсульфоніламіно і гетероциклілкарбоніламіно; і
c) арилу або заміщеного арилу;
R3 вибирають з групи, що складається з:
(а) біциклічної, трициклічної або пентациклічної групи, вибраної з групи, що складається з:



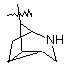








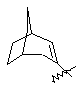
















 ,
,
де біциклічна, трициклічна або пентациклічна група є або незаміщеною, або функціоналізованою одним або більше із замісників, вибраних з групи, що складається з:
(і) алкілу, алкенілу і алкінілу; де кожна алкільна, алкенільна або алкінільна група є або незаміщеною, або функціоналізованою одним або більше із замісників, вибраних з групи, що складається з
(алкоксикарбоніл)аралкілкарбамоїлу,
(аміно) (R5)ацилгідразинілкарбонілу,
(аміно) (R5)ацилоксикарбокси,
(гідрокси)(карбоалкокси)алкілкарбамоїлу, ациламіноалкіламіно, ацилокси, альдегідо, алкенокси, алкеніламіно, алкенілсульфоніламіно, алкокси, алкоксикарбонілалкіламіно, алкоксикарбонілу, алкоксикарбоніламіно, алкоксикарбоніламіноацилокси, алкоксикарбоніламіноалкіламіно, алкіламіно, алкіламіноалкіламіно, алкілкарбамоїлу, алкілфосфоно, алкілсульфоніламіно, алкілсульфонілокси, аміно, аміноалкіларалкілкарбамоїлу, аміноацилокси, аміноалкілкарбамоїлу, аміноалкілгетероциклілалкілкарбамоїлу, аміноциклоалкілалкілциклоалкілкарбамоїлу, аміноциклоалкілкарбамоїлу, аралкоксикарбонілу, аралкоксикарбоніламіно, арилгетероциклілу, арилокси, арилсульфоніламіно, арилсульфонілокси, карбамоїлу, карбонілу, ціано, ціаноалкілкарбамоїлу, циклоалкіламіно, діалкіламіно, діалкіламіноалкіламіно, діалкіламіноалкілкарбамоїлу, діалкілфосфоно, галоалкілсульфоніламіно, галогену, гетероциклілу, гетероциклілалкіламіно, гетероциклілкарбамоїлу, гідрокси, гідроксіалкілсульфоніламіно, оксіміно, фосфату, фосфоно, -R5, R5-алкокси, R5-алкіл(алкіл)аміно, R5-алкілалкілкарбамоїлу, R5-алкіламіно, R5-алкілкарбамоїлу, R5-алкілсульфонілу, R5-алкілсульфоніламіно, R5-алкілтіо, R5-гетероциклілкарбонілу, заміщеного аралкіламіно, заміщеного арилкарбоксиалкоксикарбонілу, заміщеного арилсульфоніламіноалкіламіно, заміщеного гетероарилсульфоніламіно, заміщеного гетероциклілу, заміщеного гетероцикліламіноалкіламіно, заміщеного гетероциклілсульфоніламіно, сульфоксиациламіно, тіокарбамоїлу, трифторметилу;
і
(іі) (алкоксикарбоніл)аралкілкарбамоїлу,
(аміно) (R5)ацилгідразинілкарбонілу,
(аміно)(R5)ацилоксикарбокси,
(гідрокси)(карбоалкокси)алкілкарбамоїлу,
ациламіноалкіламіно, ацилокси, альдегідо, алкенокси, алкеніламіно, алкенілсульфоніламіно, алкокси, алкоксикарбонілу, алкоксикарбонілалкіламіно, алкоксикарбоніламіно, алкоксикарбоніламіноацилокси, алкоксикарбоніламіноалкіламіно, алкіламіно, алкіламіноалкіламіно, алкілкарбамоїлу, алкілфосфоно, алкілсульфоніламіно, алкілсульфонілокси, аміно, аміноалкіларалкілкарбамоїлу, аміноацилокси, аміноалкілкарбамоїлу, аміноалкілгетероциклілалкілкарбамоїлу,
аміноциклоалкілалкілциклоалкілкарбамоїлу, аміноциклоалкілкарбамоїлу, аралкоксикарбонілу, аралкоксикарбоніламіно, арилгетероциклілу, арилокси, арилсульфоніламіно, арилсульфонілокси, карбамоїлу, карбонілу, ціано, ціаноалкілкарбамоїлу, циклоалкіламіно, діалкіламіно, діалкіламіноалкіламіно, діалкіламіноалкілкарбамоїлу, діалкілфосфоно, галоалкілсульфоніламіно, галогену, гетероциклілу, гетероциклілалкіламіно, гетероциклілкарбамоїлу, гідрокси, гідроксіалкілсульфоніламіно, оксіміно, фосфату, фосфоно, -R5, R5-алкокси, R5-алкіл(алкіл)аміно, R5-алкілалкілкарбамоїлу, R5-алкіламіно, R5-алкілкарбамоїлу, R5-алкілсульфонілу, R5-алкілсульфоніламіно, R5-алкілтіо, R5-гетероциклілкарбонілу, заміщеного аралкіламіно, заміщеного арилкарбоксіалкоксикарбонілу, заміщеного арилсульфоніламіноалкіламіно, заміщеного гетероарилсульфоніламіно, заміщеного гетероциклілу, заміщеного гетероцикліламіноалкіламіно, заміщеного гетероциклілсульфоніламіно, сульфоксіациламіно, тіокарбамоїлу, трифторметилу;
R4 вибирають з групи, що складається з водню, С1-4-алкілу, С1-4-алкіл-СО2Н і фенілу, де С1-4-алкільна, С1-4-алкіл-СО2Н і фенільна групи є або незаміщеними, або функціоналізованими одним-трьома замісниками, вибраними з групи, що складається з галогену, -OH, -OMe, -NH2, NO2, бензилу і бензилу, функціоналізованого одним-трьома замісниками, вибраними з групи, що складається з галогену, -ОН, -OMe, -NН2, і –NO2;
R5 вибирають з групи, що складається з - (CR1R2)nCOOH, -С(СF3)2OН, -CONHNHSO2CF3, -CONHOR4, -CONHSO2R4, -CONHSO2NHR4, -С(ОН)R4РО3Н2, -NНСОСF3, -NHCONHSO2R4, -NHРО3Н2, -NHSO2R4, -NHSO2NHCOR4, -ОРО3Н2, -OSO3Н, -PO(OH)R4, -РО3Н2, -SO3Н, -SO3NНR4, -SO3NНСОR4, -SO3NНСОNНСO2R4 і наступних груп:








 ;
;
n = 0, 1, 2 або 3;
А вибирають з групи, що складається з -СН=СН, -(CH)m-(CH)m, CH=CH-CH2 і -СН2-СН=СН;
m = 1 або 2;
X являє собою О або S;
Z вибирають з групи, що складається з простого зв'язку, -О-, -(СН2)n-, -O(СН2)1-2-, -СН2ОСН2- і -(СН2)1-2О-;
R6 вибирають з групи, що складається з водню, алкілу, ацилу, алкілсульфонілу, аралкілу, заміщеного аралкілу, заміщеного алкілу і гетероциклілу; і
R7 вибирають з групи, що складається з:
a) водню;
b) алкілу, алкенілу, що містить не менше 3 атомів вуглецю, або алкінілу, що містить не менше 3 атомів вуглецю; де вказаний алкіл, алкеніл або алкініл є або незаміщеним або функціоналізованим одним або більше із замісників, вибраних з групи, що складається з гідрокси, алкокси, аміно, алкіламіно, діалкіламіно, гетероциклілу, ациламіно, алкілсульфоніламіно і гетероциклілкарбоніламіно; і
c) арилу або заміщеного арилу;
d) алкіларилу або арилу, заміщеного алкілом.
9. Сполука за п. 8, де сполука знаходиться в формі, вибраній з групи, що складається з ахіральної сполуки, рацемату, оптично активної сполуки, чистого діастереоізомеру, суміші діастереоізомерів і фармакологічно прийнятних солей приєднання.
10. Сполука за п. 8, де R1 і R2 незалежно вибирають з групи, що складається з
a) алкілу, алкенілу або алкінілу, де вказаний алкіл, алкеніл або алкініл є або незаміщеним, або функціоналізованим одним або більше із замісників, вибраних з групи, що складається з гідрокси, алкокси, аміно, алкіламіно, діалкіламіно, гетероциклілу, ациламіно, алкілсульфоніламіно, і гетероциклілкарбоніламіно; і
b) арилу або заміщеного арилу.
11. Сполука за п. 10, де, щонайменше, один з R1 і R2 являє собою алкіл.
12. Сполука за п. 8, де А являє собою - (CH)m-(CH)m.
13. Сполука за п. 8, де R7 являє собою алкіл.
14. Сполука за п. 1, де Z являє собою простий зв'язок.
15. Сполука за п. 1 або 8, де сполуку вибирають з групи, що складається із сполук 1-32 таблиці 1.
16. Сполука за п. 15, де сполуку вибирають з групи, що складається з:
2-(4-гідроксибіцикло[2.2.2]окт-1-ил)-7-ізопропіл-4-пропіл-1,4,6,7-тетрагідро-1,3,4,5а, 8-пентааза-аз-індацен-5-ону (сполука 1);
7-етил-2-(4-гідроксибіцикло[2.2.2]окт-1-ил)-4-пропіл-1,4,6,7-тетрагідро-1,3,4,5а, 8-пентааза-аз-індацен-5-ону (сполука 2);
3-[4-(7-етил-5-оксо-4-пропіл-4,5,6,7-тетрагідро-1Н-1,3,4,5а,8-пентааза-аз-індацен-2-іл)біцикло[2.2.2]окт-1-ил]пропіонової кислоти (сполука 3);
2-(4-гідроксибіцикло[2.2.2]окт-1-ил)-7-метил-4-пропіл-1,4,6,7-тетрагідро-1,3,4,5а, 8-пентааза-аз-індацен-5-ону (сполука 4); і
3-[4-(7-ізопропіл-5-оксо-4-пропіл-4,5,6,7-тетрагідро-1Н-1,3,4,5а,8-пентааза-аз-індацен-2-іл)біцикло[2.2.2]окт-1-ил]пропіонової кислоти (сполука 5).
17. Фармацевтична композиція, що включає фармацевтично ефективну кількість сполуки за пп. 1 або 8 і фармацевтично прийнятний носій, ад'ювант або засіб доставки.
18. Фармацевтична композиція за п. 17, яка додатково включає не аденозинмодифікуючий агент.
19. Фармацевтична композиція за п. 17 в формі для перорального, внутрішньовенного, внутрішньом'язового або підшкірного введення.
20. Застосування сполуки за будь-яким з пп. 1-16 для одержання ліків для блокування у пацієнта рецепторів аденозину А1.
21. Застосування сполуки за будь-яким з пп. 1-16 для одержання ліків для лікування або профілактики у пацієнта захворювання або порушення, при яких активація рецепторів аденозину А1 відіграє важливу роль в цьому захворюванні або порушенні.
22. Спосіб лікування пацієнта з ознаками або симптомами захворювання або порушення, при яких активація рецепторів аденозину А1 грає важливу роль в цьому захворюванні або порушенні, що включає введення вказаному пацієнту фармацевтично ефективної кількості фармацевтичної композиції за п. 17.
23. Спосіб за п. 22, де захворювання або порушення вибирають з групи, що складається з системної гіпертонії, ниркової недостатності, діабету, астми, набряклого стану, застійної серцевої недостатності і ниркової дисфункції.
24. Спосіб одержання сполуки за пп. 1 або 8, що включає стадії:
a) алкілування тіокетону до одержання тіоефіру;
b) здійснення взаємодії тіоефіру із заміщеним аміноспиртом до одержання проміжної сполуки спирту; і
c) циклізації проміжної сполуки спирту до одержання циклізованого продукту.
25. Спосіб за п. 24, який включає далі стадію:
а) перетворення циклізованого продукту в похідне карбонової кислоти.
26. Спосіб за п. 25, який включає далі стадії:
a) здійснення реакції поєднання діаміноурацилу з монометиловим складним ефіром біцикло[2.2.2]октан-1,4-дикарбонової кислоти до одержання кислоти;
b) відновлення кислоти до відповідного спирту;
c) окислення спирту до альдегіду;
d) здійснення реакції поєднання альдегіду з метил(трифенілфосфораніліден) ацетатом до одержання продукту реакції поєднання; і
e) перетворення продукту реакції поєднання в тіокетон.
27. Спосіб за п. 25, який включає далі стадії:
a) здійснення реакції поєднання діаміноурацилу з монометиловим складним ефіром біцикло[2.2.2]октан-1,4-дикрбонової кислоти до одержання кислоти;
b) етерифікації кислоти до відповідного складного ефіру;
c) перетворення складного ефіру в тіокетон.
28. Спосіб за п. 24, який включає далі стадії:
a) нітрозування 6-аміно-1-пропіл-1Н-піримідин-2,4-діону до одержання проміжної нітрозосполуки;
b) відновлення проміжної нітрозосполуки до відповідного діаміноурацилу;
c) перетворення діаміноурацилу в сіль аміну;
d) здійснення реакції сполучення солі аміну з 4-гідроксибіцикло[2.2.2]октан-1-карбоновою кислотою до одержання продукту реакції поєднання; і
e) перетворення продукту реакції сполучення в тіокетон.
Текст
1. Сполука формули І: 3 75625 4 ациламіноалкіламіно, ацилокси, альдегідо, алкециклілсульфоніламіно, сульфоксіациламіно, тіоканокси, алкеніламіно, алкенілсульфоніламіно, алкорбамоїлу, трифторметилу; кси, алкоксикарбонілу, алкоксикарбонілалкіламіно, R4 вибирають з групи, що складається з водню, С1алкоксикарбоніламіно, алкоксикарбоніламіноациС1-4-алкіл-СО2Н, і фенілу, де С1-44-алкілу, локси, алкоксикарбоніламіноалкіламіно, алкіламіалкільна, С1-4-алкіл-СO2Н і фенільна групи є або но, алкіламіноалкіламіно, алкілкарбамоїлу, алкілнезаміщеними, або функціоналізованими однимфосфоно, алкілсульфоніламіно, трьома замісниками, вибраними з групи, що склаалкілсульфонілокси, аміно, аміноацилокси, амінодається з галогену, -ОН, -ОМе, -NH2, NO2, бензилу алкіларалкілкарбамоїлу, аміноалкілкарбамоїлу, і бензилу, функціоналізованого одним-трьома зааміноалкілгетероциклілалкілкарбамоїлу, аміноцикмісниками, вибраними з групи, що складається з лоалкілалкілциклоалкілкарбамоїлу, аміноциклоалгалогену, -ОН, -ОМе, -NH2, і –NO2; кілкарбамоїлу, аралкоксикарбонілу, аралкоксикарR5 вибирають з групи, що складається з боніламіно, арилгетероциклілу, арилокси, (CR1R2)nCOOH, -С(СF3)2OН, -CONHNHSO2CF3, арилсульфоніламіно, арилсульфонілокси, карбаCONHOR4, -CONHSO2R4, -CONHSO2NHR4, моїлу, карбонілу, ціано, ціаноалкілкарбамоїлу, C(OH)R4PO3H2, -NHCOCF3, -NHCONHSO2R4, циклоалкілтаміно, діалкіламіно, діалкіламіноалкіNHPO3H2, -NHSO2R4, -NHSO2NHCOR4, -ОРО3Н2, ламіно, діалкіламіноалкілкарбамоїлу, діалкілфосОSО3Н, -PO(OH)R4, -РО3Н2, -SO3Н, -SО3NНR4, фоно, галоалкілсульфоніламіно, галогену, гетероSO3NНСОR4, -SO3NHCONHCO2R4 і наступних груп: H циклілу, гетероциклілалкіламіно, HO N N N N гетероциклілкарбамоїлу, гідрокси, гідроксіалкілсуR4 N NH F1-4 N льфоніламіно, оксіміно, фосфату, фосфоно, -R5, HO N R5-алкокси, R5-алкіл(алкіл)аміно, R 5N H R4 алкілалкілкарбамоїлу, R5-алкіламіно, R5 N N N алкілкарбамоїлу, R5-алкілсульфонілу, R 5N N O N CF3 алкілсульфоніламіно, R5-алкілтіо, R 5N N HN N N N H гетероциклілкарбонілу, заміщеного аралкіламіно, H N H заміщеного арилкарбоксіалкоксикарбонілу, заміO R4 щеного арилсульфоніламіноалкіламіно, заміщеноO го гетероарилсульфоніламіно, заміщеного гетероOH циклілу, заміщеного гетероцикліламіноалкіламіно, заміщеного гетероциклілсульфоніламіно, сульфоO ксіациламіно, тіокарбамоїлу, трифторметилу; і R4 ; (іі) (алкоксикарбоніл)аралкілкарбамоїлу, n = 0, 1, 2 або 3; (аміно) (R5) ацилгідразинілкарбонілу, А вибирають з групи, що складається з -СН=СН, (аміно) (R5)ацилоксикарбокси, (CH)m-(CH)m, CH=CH-CH2 і -СН2-СН=СН; (гідрокси)(карбоалкокси)алкілкарбамоїлу, m = 1 або 2; ациламіноалкіламіно, ацилокси, альдегідо, алкеX являє собою O або S; нокси, алкеніламіно, алкенілсульфоніламіно, алкоZ вибирають з групи, що складається з простого кси, алкоксикарбонілу, алкоксикарбонілалкіламіно, зв'язку, -О-, -(СН2)n-, -O(СН2)1-2-, -СН2OСН2-, алкоксикарбоніламіно, алкоксикарбоніламіноаци(СН2)1-2O-, локси, алкоксикарбоніламіноалкіламіно, алкіламіі но, алкіламіноалкіламіно, алкілкарбамоїлу, алкілR6 вибирають з групи, що складається з водню, фосфоно, алкілсульфоніламіно, алкілу, ацилу, алкілсульфонілу, аралкілу, заміщеалкілсульфонілокси, аміно, аміноацилокси, аміноного аралкілу, заміщеного алкілу і гетероциклілу; і алкіларалкілкарбамоїлу, аміноалкілкарбамоїлу, R7 вибирають з групи, що складається з: аміноалкілгетероциклілалкілкарбамоїлу, a) водню; аміноциклоалкілалкілциклоалкілкарбамоїлу, аміb) алкілу, алкенілу, що містить не менше 3 атомів ноциклоалкілкарбамоїлу, аралкоксикарбонілу, вуглецю, або алкінілу, що містить не менше 3 атоаралкоксикарбоніламіно, арилгетероциклілу, аримів вуглецю; де вказаний алкіл, алкеніл або алкініл локси, арилсульфоніламіно, арилсульфонілокси, є або незаміщеним, або функціоналізованим одкарбамоїлу, карбонілу, ціано, ціаноалкілкарбамоїним або більше із замісників, вибраних з групи, що лу, циклоалкіламіно, діалкіламіно, діалкіламіноалскладається з гідрокси, алкокси, аміно, алкіламіно, кіламіно, діалкіламіноалкілкарбамоїлу, діалкілфодіалкіламіно, гетероциклілу, ациламіно, алкілсусфоно, галоалкілсульфоніламіно, галогену, льфоніламіно і гетероциклілкарбоніламіно; і гетероциклілу, гетероциклілалкіламіно, гетероцикc) арилу або заміщеного арилу; лілкарбамоїлу, гідрокси, гідроксіалкілсульфонілаd) алкіларилу або арилу, заміщеного алкілом. міно, оксіміно, фосфату, фосфоно, -R5, R5-алкокси, 2. Сполука за п. 1, де сполука знаходиться в форR5-алкіл(алкіл)аміно, R5-алкілалкілкарбамоїлу, R5мі, вибраній з групи, що складається з ахіральної алкіламіно, R5-алкілкарбамоїлу, R 5сполуки, рацемату, оптично активної сполуки, чисалкілсульфонілу, R5-алкілсульфоніламіно, R5того діастереоізомеру, суміші діастереоізомерів і алкілтіо, R5-гетероциклілкарбонілу, заміщеного фармакологічно прийнятних солей приєднання. аралкіламіно, заміщеного арилкарбоксиалкоксика3. Сполука за п. 1, де R1 і R2 незалежно вибирають рбонілу, заміщеного арилсульфоніламіноалкіламіз групи, що складається з но, заміщеного гетероарилсульфоніламіно, заміa) алкілу, алкенілу або алкінілу, де вказаний алкіл, щеного гетероциклілу, заміщеного алкеніл або алкініл є або незаміщеним, або функгетероцикліламіноалкіламіно, заміщеного гетеро 5 75625 6 O ціоналізованим одним або більше із замісників, вибраних з групи, що складається з гідрокси, алкоN кси, аміно, алкіламіно, діалкіламіно, гетероциклілу, ациламіно, алкілсульфоніламіно і гетероциклілкарбоніламіно; і де біциклічна, трициклічна або пентациклічна груb) арилу або заміщеного арилу. па є або незаміщеною, або функціоналізованою 4. Сполука за п. 3, де, щонайменше, один з R1 і R2 одним або більше із замісників, вибраних з групи, являє собою алкіл. що складається з: 5. Сполука за п. 1, де А являє собою - (СН)m-(СН)m. (і) алкілу, алкенілу і алкінілу; де кожна алкільна, 6. Сполука за п. 1, де R7 являє собою алкіл. алкенільна або алкінільна група є або незаміще7. Сполука за п. 1, де Z являє собою простий зв'яною, або функціоналізованою одним або більше із зок. замісників, вибраних з групи, що складається з 8. Сполука формули II: (алкоксикарбоніл)аралкілкарбамоїлу, R2 (аміно) (R5)ацилгідразинілкарбонілу, R1 A (аміно) (R5)ацилоксикарбокси, N (гідрокси)(карбоалкокси)алкілкарбамоїлу, ациламіN Формула ІІ N ноалкіламіно, ацилокси, альдегідо, алкенокси, алR3 Z кеніламіно, алкенілсульфоніламіно, алкокси, алкоN X N ксикарбонілалкіламіно, алкоксикарбонілу, R6 R7 алкоксикарбоніламіно, алкоксикарбоніламіноациде R1 і R2 незалежно вибирають з групи, що склалокси, алкоксикарбоніламіноалкіламіно, алкіламідається з: но, алкіламіноалкіламіно, алкілкарбамоїлу, алкілa) водню; фосфоно, алкілсульфоніламіно, b) алкілу, алкенілу або алкінілу, де вказаний алкіл, алкілсульфонілокси, аміно, аміноалкіларалкілкаралкеніл або алкініл є або незаміщеним, або функбамоїлу, аміноацилокси, аміноалкілкарбамоїлу, ціоналізованим одним або більше із замісників, аміноалкілгетероциклілалкілкарбамоїлу, аміноциквибраних з групи, що складається з гідрокси, алколоалкілалкілциклоалкілкарбамоїлу, аміноциклоалкси, аміно, алкіламіно, діалкіламіно, гетероциклілу, кілкарбамоїлу, аралкоксикарбонілу, аралкоксикарациламіно, алкілсульфоніламіно і гетероциклілкабоніламіно, арилгетероциклілу, арилокси, рбоніламіно; і арилсульфоніламіно, арилсульфонілокси, карбаc) арилу або заміщеного арилу; моїлу, карбонілу, ціано, ціаноалкілкарбамоїлу, R3 вибирають з групи, що складається з: циклоалкіламіно, діалкіламіно, діалкіламіноалкіла(а) біциклічної, трициклічної або пентациклічної міно, діалкіламіноалкілкарбамоїлу, діалкілфосфогрупи, вибраної з групи, що складається з: но, галоалкілсульфоніламіно, галогену, гетероциклілу, гетероциклілалкіламіно, гетероциклілкарбамоїлу, гідрокси, гідроксіалкілсуNH льфоніламіно, оксіміно, фосфату, фосфоно, -R5, R5-алкокси, R5-алкіл(алкіл)аміно, R 5алкілалкілкарбамоїлу, R5-алкіламіно, R5алкілкарбамоїлу, R5-алкілсульфонілу, R5алкілсульфоніламіно, R5-алкілтіо, R5 NH гетероциклілкарбонілу, заміщеного аралкіламіно, O O заміщеного арилкарбоксиалкоксикарбонілу, заміщеного арилсульфоніламіноалкіламіно, заміщеного гетероарилсульфоніламіно, заміщеного гетероN H циклілу, заміщеного гетероцикліламіноалкіламіно, NR заміщеного гетероциклілсульфоніламіно, сульфоNH NH ксиациламіно, тіокарбамоїлу, трифторметилу; і (іі) (алкоксикарбоніл)аралкілкарбамоїлу, (аміно) (R5)ацилгідразинілкарбонілу, (аміно)(R5)ацилоксикарбокси, (гідрокси)(карбоалкокси)алкілкарбамоїлу, ациламіноалкіламіно, ацилокси, альдегідо, алкенокси, алкеніламіно, алкенілсульфоніламіно, алкоNH кси, алкоксикарбонілу, алкоксикарбонілалкіламіно, алкоксикарбоніламіно, алкоксикарбоніламіноациO локси, алкоксикарбоніламіноалкіламіно, алкіламіO но, алкіламіноалкіламіно, алкілкарбамоїлу, алкілфосфоно, алкілсульфоніламіно, O O алкілсульфонілокси, аміно, аміноалкіларалкілкарO бамоїлу, аміноацилокси, аміноалкілкарбамоїлу, аміноалкілгетероциклілалкілкарбамоїлу, аміноциклоалкілалкілциклоалкілкарбамоїлу, аміноциклоалкілкарбамоїлу, аралкоксикарбонілу, аралкоксикарбоніламіно, арилгетероциклілу, ари 7 75625 8 локси, арилсульфоніламіно, арилсульфонілокси, або більше із замісників, вибраних з групи, що карбамоїлу, карбонілу, ціано, ціаноалкілкарбамоїскладається з гідрокси, алкокси, аміно, алкіламіно, лу, циклоалкіламіно, діалкіламіно, діалкіламіноалдіалкіламіно, гетероциклілу, ациламіно, алкілсукіламіно, діалкіламіноалкілкарбамоїлу, діалкілфольфоніламіно і гетероциклілкарбоніламіно; і сфоно, галоалкілсульфоніламіно, галогену, c) арилу або заміщеного арилу; гетероциклілу, гетероциклілалкіламіно, гетероцикd) алкіларилу або арилу, заміщеного алкілом. лілкарбамоїлу, гідрокси, гідроксіалкілсульфоніла9. Сполука за п. 8, де сполука знаходиться в форміно, оксіміно, фосфату, фосфоно, -R5, R5-алкокси, мі, вибраній з групи, що складається з ахіральної R5-алкіл(алкіл)аміно, R5-алкілалкілкарбамоїлу, R5сполуки, рацемату, оптично активної сполуки, чисалкіламіно, R5-алкілкарбамоїлу, R 5того діастереоізомеру, суміші діастереоізомерів і алкілсульфонілу, R5-алкілсульфоніламіно, R5фармакологічно прийнятних солей приєднання. алкілтіо, R5-гетероциклілкарбонілу, заміщеного 10. Сполука за п. 8, де R1 і R2 незалежно вибирааралкіламіно, заміщеного арилкарбоксіалкоксикають з групи, що складається з рбонілу, заміщеного арилсульфоніламіноалкіламіa) алкілу, алкенілу або алкінілу, де вказаний алкіл, но, заміщеного гетероарилсульфоніламіно, заміалкеніл або алкініл є або незаміщеним, або функщеного гетероциклілу, заміщеного ціоналізованим одним або більше із замісників, гетероцикліламіноалкіламіно, заміщеного гетеровибраних з групи, що складається з гідрокси, алкоциклілсульфоніламіно, сульфоксіациламіно, тіокакси, аміно, алкіламіно, діалкіламіно, гетероциклілу, рбамоїлу, трифторметилу; ациламіно, алкілсульфоніламіно, і гетероциклілкаR4 вибирають з групи, що складається з водню, С1рбоніламіно; і b) арилу або заміщеного арилу. 4-алкілу, С1-4-алкіл-СО2Н і фенілу, де С1-4-алкільна, С1-4-алкіл-СО2Н і фенільна групи є або незаміще11. Сполука за п. 10, де, щонайменше, один з R1 і ними, або функціоналізованими одним-трьома R2 являє собою алкіл. замісниками, вибраними з групи, що складається з 12. Сполука за п. 8, де А являє собою - (CH)mгалогену, -OH, -OMe, -NH2, NO2, бензилу і бензилу, (CH)m. функціоналізованого одним-трьома замісниками, 13. Сполука за п. 8, де R7 являє собою алкіл. вибраними з групи, що складається з галогену, 14. Сполука за п. 1, де Z являє собою простий ОН, -OMe, -NН2, і –NO2; зв'язок. R5 вибирають з групи, що складається з 15. Сполука за п. 1 або 8, де сполуку вибирають з (CR1R2)nCOOH, -С(СF3)2OН, -CONHNHSO2CF3, групи, що складається із сполук 1-32 таблиці 1. CONHOR4, -CONHSO2R4, -CONHSO2NHR4, 16. Сполука за п. 15, де сполуку вибирають з груС(ОН)R4РО3Н2, -NНСОСF3, -NHCONHSO2R4, пи, що складається з: NHРО3Н2, -NHSO2R4, -NHSO2NHCOR4, -ОРО3Н2, 2-(4-гідроксибіцикло[2.2.2]окт-1-ил)-7-ізопропіл-4OSO3Н, -PO(OH)R4, -РО3Н2, -SO3Н, -SO3NНR4, пропіл-1,4,6,7-тетрагідро-1,3,4,5а, 8-пентааза-азSO3NНСОR4, -SO3NНСОNНСO2R4 і наступних груп: індацен-5-ону (сполука 1); N 7-етил-2-(4-гідроксибіцикло[2.2.2]окт-1-ил)-4N HO H NH пропіл-1,4,6,7-тетрагідро-1,3,4,5а, 8-пентааза-азN N F1-4 індацен-5-ону (сполука 2); R4 HO 3-[4-(7-етил-5-оксо-4-пропіл-4,5,6,7-тетрагідро-1НR4 1,3,4,5а,8-пентааза-аз-індацен-2N N іл)біцикло[2.2.2]окт-1-ил]пропіонової кислоти (споN N лука 3); N N N HN N H CF3 2-(4-гідроксибіцикло[2.2.2]окт-1-ил)-7-метил-4N N N пропіл-1,4,6,7-тетрагідро-1,3,4,5а, 8-пентааза-азO H H індацен-5-ону (сполука 4); і O N 3-[4-(7-ізопропіл-5-оксо-4-пропіл-4,5,6,7O N OH N тетрагідро-1Н-1,3,4,5а,8-пентааза-аз-індацен-2N N іл)біцикло[2.2.2]окт-1-ил]пропіонової кислоти (споH O R4 R4 лука 5). 17. Фармацевтична композиція, що включає фарn = 0, 1, 2 або 3; мацевтично ефективну кількість сполуки за пп. 1 А вибирають з групи, що складається з -СН=СН, або 8 і фармацевтично прийнятний носій, ад'ювант (CH)m-(CH)m, CH=CH-CH2 і -СН2-СН=СН; або засіб доставки. m = 1 або 2; 18. Фармацевтична композиція за п. 17, яка додатX являє собою О або S; ково включає не аденозинмодифікуючий агент. Z вибирають з групи, що складається з простого 19. Фармацевтична композиція за п. 17 в формі зв'язку, -О-, -(СН2)n-, -O(СН2)1-2-, -СН2ОСН2- і для перорального, внутрішньовенного, внутріш(СН2)1-2О-; ньом'язового або підшкірного введення. R6 вибирають з групи, що складається з водню, 20. Застосування сполуки за будь-яким з пп. 1-16 алкілу, ацилу, алкілсульфонілу, аралкілу, заміщедля одержання ліків для блокування у пацієнта ного аралкілу, заміщеного алкілу і гетероциклілу; і рецепторів аденозину А1. R7 вибирають з групи, що складається з: 21. Застосування сполуки за будь-яким з пп. 1-16 a) водню; для одержання ліків для лікування або профілакb) алкілу, алкенілу, що містить не менше 3 атомів тики у пацієнта захворювання або порушення, при вуглецю, або алкінілу, що містить не менше 3 атояких активація рецепторів аденозину А1 відіграє мів вуглецю; де вказаний алкіл, алкеніл або алкініл є або незаміщеним або функціоналізованим одним 9 75625 10 важливу роль в цьому захворюванні або поруло[2.2.2]октан-1,4-дикарбонової кислоти до одершенні. жання кислоти; 22. Спосіб лікування пацієнта з ознаками або симb) відновлення кислоти до відповідного спирту; птомами захворювання або порушення, при яких c) окислення спирту до альдегіду; активація рецепторів аденозину А1 грає важливу d) здійснення реакції поєднання альдегіду з мероль в цьому захворюванні або порушенні, що тил(трифенілфосфораніліден) ацетатом до одервключає введення вказаному пацієнту фармацевжання продукту реакції поєднання; і тично ефективної кількості фармацевтичної комe) перетворення продукту реакції поєднання в тіопозиції за п. 17. кетон. 23. Спосіб за п. 22, де захворювання або пору27. Спосіб за п. 25, який включає далі стадії: шення вибирають з групи, що складається з сисa) здійснення реакції поєднання діаміноурацилу з темної гіпертонії, ниркової недостатності, діабету, монометиловим складним ефіром біцикастми, набряклого стану, застійної серцевої недоло[2.2.2]октан-1,4-дикрбонової кислоти до одерстатності і ниркової дисфункції. жання кислоти; 24. Спосіб одержання сполуки за пп. 1 або 8, що b) етерифікації кислоти до відповідного складного включає стадії: ефіру; a) алкілування тіокетону до одержання тіоефіру; c) перетворення складного ефіру в тіокетон. b) здійснення взаємодії тіоефіру із заміщеним амі28. Спосіб за п. 24, який включає далі стадії: носпиртом до одержання проміжної сполуки спирa) нітрозування 6-аміно-1-пропіл-1Н-піримідин-2,4ту; і діону до одержання проміжної нітрозосполуки; c) циклізації проміжної сполуки спирту до одерb) відновлення проміжної нітрозосполуки до відпожання циклізованого продукту. відного діаміноурацилу; 25. Спосіб за п. 24, який включає далі стадію: c) перетворення діаміноурацилу в сіль аміну; а) перетворення циклізованого продукту в похідне d) здійснення реакції сполучення солі аміну з 4карбонової кислоти. гідроксибіцикло[2.2.2]октан-1-карбоновою кисло26. Спосіб за п. 25, який включає далі стадії: тою до одержання продукту реакції поєднання; і a) здійснення реакції поєднання діаміноурацилу з e) перетворення продукту реакції сполучення в монометиловим складним ефіром біциктіокетон. Заявка, що розглядається, заявляє пріоритет від попередньої заявки [на патент США №60/250658, поданої 1 грудня 2000 року], яка включена сюди для посилання. Даний винахід відноситься до області медичної хімії і фармакології. Більш конкретно він відноситься до антагоністів рецепторів аденозину, фармацевтичних композицій, що включають ці сполуки, і до способів їх одержання і використання для лікування захворювань. Аденозин являє собою поширений біохімічний месенджер. Аденозин зв'язується з сімома трансмембранними, зв'язуючими G-білок рецепторами, і активує їх, викликаючи різні фізіологічні реакції. Рецептори аденозину поділяються на чотири відомих підтипи (тобто Аb А2а, А2b, і А3). Ці підтипи рецепторів опосередкують різні і, іноді, протилежні ефекти. Наприклад, активізація рецептора аденозину А1 спричиняє підвищення опірності ниркових судин, тоді як активізація рецептора аденозину А2а спричиняє зменшення опірності ниркових судин. У більшості систем органів ссавців періоди метаболічного стресу приводять до істотного підвищення концентрації аденозину в тканинах. Наприклад, серце виробляє і виділяє аденозин для опосередкування адаптивних реакцій на стрес, таких як зменшення швидкості серцевих скорочень і розширення коронарних судин. Аналогічно, концентрації аденозину в нирках підвищуються при реакції на гіпоксію, метаболічний стрес і багато які нефротоксичні речовини. Нирки також виробляють аденозин конститутивно. Нирки регулюють кількість аденозину, що виробляється конститутивно, для регулювання гломерулярної фільтрації і елек тролітичної реабсорбції. Що стосується регулювання гломерулярної фільтрації, то активація рецепторів А1 приводить до скорочення артеріол, що приносять, тоді як активація А2а рецепторів приводить до розширення артеріол, що відносять. Активація А2а рецепторів викликає ефекти розширення судин у артеріол, що приносять. Загалом, ефект активації цих гломерулярних аденозинових рецепторів повинен зменшити швидкість гломерулярної фільтрації. Крім того, рецептори аденозину А1 розташовані в проксимальних трубчастих і дистальних трубчастих сайтах. Активація цих рецепторів стимулює реабсорбцію натрію з просвітів трубочок. Відповідно, ефекти блокування аденозину на цих рецепторах викликають підвищення швидкості гломерулярної фільтрації і підвищення виділення натрію. Даний винахід заснований на відкритті того факту, що сполуки формули І і II є ефективними і селективними інгібіторами конкретних підтипів рецепторів аденозину. На основі цього відкриття в даному винаході представлені антагоністи аденозину, які можна використати для профілактики і/або лікування множини захворювань, включаючи серцеві і циркуляторні порушення, дегенеративні порушення центральної нервової системи, респіраторні порушення і багато які захворювання, при лікуванні яких використовують діуретики. У загальних рисах в даному винаході представлені ефективні і селективні антагоністи рецепторів аденозину А1. У даному винаході представлені сполуки формул І або II: 11 75625 l ll 12 а) водню; b) алкілу, алкенілу або алкінілу, де вказаний алкіл, алкеніл або алкініл є незаміщеним або функціоналізованим одним або більше із замісників, вибраних з групи, що складається з гідрокси, алкокси, аміно, алкіламіно, діалкіламіно, гетероциклілу, ациламіно, алкілсульфоніламіно і гетероциклілкарбоніламіно; і c) арилу або заміщеного арилу; R3 вибирають з групи, що складається з: (а) біциклічної, трициклічної або пентациклічної групи, вибраної з групи, що складається з: де R1 і R2 незалежно вибирають з групи, що складається з: де біциклічна, трициклічна або пентациклічна група є або незаміщеною, або функціоналізованою одним або більше із замісників, вибраних з групи, що складається з: (і) алкілу, алкенілу і алкінілу; де кожна алкільна, алкенільна або алкінільна група є або незаміщеною, або функціоналізованою одним або більше із замісників, вибраних з групи, що складається з (алкоксикарбоніл)аралкілкарбамоїлу, (аміно) (R5)ацилгідразинілкарбонілу, (аміно) (R5)ацилоксикарбокси, (гідрокси)(карбоалкокси)алкілкарбамоїлу, ациламіноалкіламіно, ацилокси, альдегідо, ал кенокси, алкеніламіно, алкенілсульфоніламіно, алкокси, алкоксикарбонілу, алкоксикарбонілалкіламіно, алкоксикарбоніламіно, алкоксикарбоніламіноацилокси, алкоксикарбоніламіноалкіламіно, алкіламіно, алкіламіноалкіламіно, алкілкарбамоїлу, алкілфосфоно, алкілсульфоніламіно, алкілсульфонілокси, аміно, аміноацилокси, аміноалкіларалкілкарбамоїлу, аміноалкілкарбамоїлу, аміноалкілгетероцикліл алкілкарбамоїлу, аміноциклоалкілалкілциклоалкілкарбамоїлу, аміноциклоалкілкарбамоїлу, аралкоксикарбонілу, аралкоксикарбоніламіно, арилгетероциклілу, арилокси, арилсульфоніламіно, арилсульфонілокси, 13 75625 14 карбамоїлу, карбонілу, ціано, ціаноалкілкарбамоїCONHOR4, -CONHSO2R4, -CONHSO2NHR4, лу, циклоалкіламіно, діалкіламіно, діалкіламіноалС(ОН)R4РО3Н2, -NHCOCF3, -NHCONHSO2R4, кіламіно, діалкіламіноалкілкарбамоїлу, діалкілфоNHPO3H2, -NHSO2R4, -NHSO2NHCOR4, -OPO3H2, сфоно, галоалкілсульфоніламіно, галогену, OSO3H, -PO(OH)R4, -PO3H2, -SO3H, -SO3NHR4, гетероциклілу, гетероциклілалкіламіно, гетероцикSO3NHCOR4, -SO3NHCONHCO2R4 і наступних груп: лілкарбамоїлу, гідрокси, гідроксіалкілсульфоніламіно, оксиміно, фосфату, фосфоно, -R5, -R5алкокси, -R5алкіл(алкіл)аміно, R5 алкілалкілкарбамоїлу, R5-алкіламіно, R5 алкілкарбамоїлу, R5-алкілсульфонілу, R 5алкілсульфоніламіно, R5-алкілтіо, R 5гетероциклілкарбонілу, заміщеного аралкіламіно, заміщеного арилкарбоксіалкоксикарбонілу, заміщеного арилсульфоніламіноалкіламіно, заміщеноn=0, 1, 2 або 3; го гетероарилсульфоніламіно, заміщеного гетероА вибирають з групи, що складається з циклілу, заміщеного гетероцикліламіноалкіламіно, СН=СН, -(CH)m-(CH)m, CH=CH-CH2, і -СН2-СН=СН; заміщеного гетероциклілсульфоніламіно, сульфоm=1 або 2; ксіациламіно, тіокарбамоїлу, трифторметилу; і X являє собою О або S; (іі) (алкоксикарбоніл)аралкілкарбамоїлу, Ζ вибирають з групи, що складається з просто(аміно) (R5)ацилгідразинілкарбонілу, го зв'язку, -О-, -(СН2)n-, -О(СН2)1-2-, -СН2ОСН2-, (аміно) (R5)ацилоксикарбокси, (СН2)1-2О-, -СН=СНСН2-, -СН=СН- і -СН2СН=СН-; і (гідрокси)(карбоалкокси)алкілкарбамоїлу, R6 вибирають з групи, що складається з водациламіноалкіламіно, ацилокси, альдегідо, алню, алкілу, ацилу, алкілсульфонілу, аралкілу, закенокси, алкеніламіно, алкенілсульфоніламіно, міщеного аралкілу, заміщеного алкілу і гетероцикалкокси, алкоксикарбонілу, алкоксикарбонілалкілілу; і ламіно, алкоксикарбоніламіно, алкоксикарбонілаR7 вибирають з групи, що складається з: міноацилокси, алкоксикарбоніламіноалкіламіно, a) водню; алкіламіно, алкіламіноалкіламіно, алкілкарбамоїлу, b) алкілу, алкенілу, що містить не менше 3 алкілфосфоно, алкілсульфоніламіно, алкілсульатомів вуглецю, або алкінілу, що містить не менше фонілокси, аміно, аміноацилокси, аміноалкіларал3 атомів вуглецю; де вказаний алкіл, алкеніл або кілкарбамоїлу, аміноалкілкарбамоїлу, аміноалкілалкініл є або незаміщеним, або функціоналізовагетероцикліл алкілкарбамоїлу, ним одним або більше із замісників, вибраних з аміноциклоалкілалкілциклоалкілкарбамоїлу, амігрупи, що складається з гідрокси, алкокси, аміно, ноциклоалкілкарбамоїлу, аралкоксикарбонілу, алкіламіно, діалкіламіно, гетероциклілу, ациламіаралкоксикарбоніламіно, арилгетероциклілу, арино, алкілсульфоніламіно і гетероциклілкарбонілалокси, арилсульфоніламіно, арилсульфонілокси, міно; і карбамоїлу, карбонілу, ціано, ціаноалкілкарбамоїc) арилу або заміщеного арилу; лу, циклоалкіламіно, діалкіламіно, діалкіламіноалd) алкіларилу або арилу, заміщеного алкілом. кіламіно, діалкіламіноалкілкарбамоїлу, діалкілфоСполуки формули І або II необов'язково мосфоно, галоалкілсульфоніламіно, галогену, жуть бути в таких формах, як ахіральні сполуки, гетероциклілу, гетероциклілалкіламіно, гетероцикрацемати, оптично активні сполуки, чисті діастелілкарбамоїлу, гідрокси, гідроксиалкілсульфонілареоізомери, суміші діастереоізомерів або фармаміно, оксиміно, фосфату, фосфоно, -R5, R5кологічно прийнятні солі приєднання кислот. У деалкокси, R5-алкіл(алкіл)аміно, R 5яких переважних варіантах сполуки даного алкілалкілкарбамоїл, R5-алкіламіно, R5винаходу є сполуками формули І або II, де ні R1, ні алкілкарбамоїлу, R5-алкілсульфонілу, R 5R2 не є воднями, тобто кожний з R1 і R2 незалежно алкілсульфоніламіно, R5-алкілтіо, R 5вибрані з групи, що складається з гетероциклілкарбонілу, заміщеного аралкіламіно, а) алкілу, алкенілу або алкінілу, де вказаний заміщеного арилкарбоксіалкоксикарбонілу, заміалкіл, алкеніл або алкініл є або незаміщеним, або щеного арилсульфоніламіноалкіламіно, заміщенофункціоналізованим одним або більше із замісниго гетероарилсульфоніламіно, заміщеного гетероків, вибраних з групи, що складається з гідрокси, циклілу, заміщеного гетероцикліламіноалкіламіно, алкокси, аміно, алкіламіно, діалкіламіно, гетероцизаміщеного гетероциклілсульфоніламіно, заміщеклілу, ацил аміно, алкіл сульфоніл аміно і гетероного гетероциклілсульфоніламіно, сульфоксіацицикліл карбоніл аміно; і ламіно, тіокарбамоїлу, трифторметилу; b) арилу або заміщеного арилу. R4 вибирають з групи, що складається з водБільш переважно, щоб, щонайменше, один з ню, С1-4-алкілу, С1-4-алкіл-СО2Н і фенілу, де С1-4R1 і R2 являв собою алкіл. У інших переважних алкільна, С1-4-алкіл-СО2Н у фенільна групи є або варіантах А являє собою -(CH)m-(CH)m. незаміщеними, або функціоналізованими однимиR7 являє собою алкіл в інших переважних ватрьома замісниками, вибраними з групи, що скларіантах, і Z, переважно, являє собою простий зв'ядається з галогену, -ОН, -ОМе, -ΝΉ2, ΝΟ2, бензилу зок. і бензилу, функціоналізованого одним-трьома заПереважними сполуками даного винаходу є: місниками, вибраними з групи, що складається з 2-(4-гідроксибіцикло[2.2.2]окт-1-іл)-7галогену, -ОН, -ОМе, -ΝΗ2, і -ΝΟ2; ізопропіл-4-пропіл-1,4,6,7-тетрагідро-1,3,4,5а, 8R5 вибирають з групи, що складається з пентааза-аз-індацен-5-он (сполука 1); (CR1R2)nCOOH, -C(CF3)2OH, -CONHNHSO2CF3, 15 75625 16 7-етил-2-(4-гідроксибіцикло[2.2.2]окт-1-іл)-4сіб одержання вищезгаданих сполук, який включає пропіл-1,4,6,7-тетрагідро-1,3,4,5а, 8-пентааза-азстадії: індацен-5-он (сполука 2); a) алкілування тіокетону до одержання тіо3-[4-(7-етил-5-оксо-4-пропіл-4,5,6,7-тетрагідроефіру; 1H-1,3,4,5а, 8-пентааза-аз-індацен-2b) здійснення взаємодії тіоефіру із заміщеним іл)біцикло[2.2.2]окт-1-іл]пропіонова кислота (споаміноспиртом до одержання проміжної сполуки лука 3); спирту; і 2-(4-гідроксибіцикло[2.2.2]окт-1-іл)-7-метил-4c) циклізації проміжної сполуки спирту до одепропіл-1,4,6,7-тетрагідро-1,3,4,5а, 8-пентааза-азржання циклізованого продукту. індацен-5-он (сполука 4); і У деяких варіантах вищезгаданий спосіб 3-[4-(7-ізопропіл-5-оксо-4-пропіл-4,5,6,7включає далі стадію а) перетворення циклізованотетрагідро-1Н-1,3,4,5а,8-пентааза-аз-індацен-2го продукту в похідне карбонової кислоти. У деіл)біцикло[2.2.2]окт-1-іл]пропіонова кислота (спояких варіантах спосіб включає далі стадії: а) здійслука 5). нення реакції поєднання діаміноурацилу з Сполуки даного винаходу можна модифікувати монометиловим складним ефіром біцикдля посилення бажаних характеристик. Такі моло[2.2.2]октан-1,4-дикарбонової кислоти з одердифікації відомі фахівцям і включають ті, які посижанням кислоти; b) відновлення кислоти до відполюють біологічну проникність в конкретну біологічвідного спирту; с) окислення спирту до альдегіду; ну систему (наприклад, в кров, лімфатичну d) здійснення реакції поєднання альдегіду з месистему, центральну нервову систему), підвищутил(трифенілфосфораніліден)ацетатом до одерють доступність при пероральному введенні, піджання продукту реакції поєднання; e) перетворенвищують розчинність для введення за допомогою ня продукту реакції поєднання в тіокетон; f) ін'єкцій, змінюють метаболізм і/або змінюють швиалкілування тіокетону з одержанням тіоефіру; g) дкість виведення. Приклади таких модифікацій здійснення взаємодії тіоефіру із заміщеним аміновключають (але цим не обмежуються) етерифікаспиртом з одержанням проміжної сполуки спирту; і цію поліетиленгліколями, одержання похідних піh) циклізації проміжної сполуки спирту до одерволатів або заміщення жирними кислотами, пережання продукту циклізації; і і) перетворення продутворення в карбамати, гідроксилювання кту циклізації в похідне карбонової кислоти. ароматичних кілець і введення гетероатомівУ деяких варіантах спосіб включає стадії: а) замісників в ароматичні кільця. здійснення реакції поєднання діаміноурацилу з Даний винахід охоплює також фармацевтичні монометиловим складним ефіром біциккомпозиції, що включають будь-які з вищезгаданих ло[2.2.2]октан-1,4-дикарбонової кислоти до одерсполук, взятих окремо або в комбінації з відповіджання кислоти; b) етерифікації кислоти до відповіними ексципієнтами. дного складного ефіру; с) перетворення складного Даний винахід включає спосіб лікування пацієефіру з одержанням тіокетону; d) алкілування тіонта, у якого виявляються ознаки або симптоми кетону з одержанням тіоефіру; e) відновлення тіозахворювання або порушення, при яких активація ефіру заміщеним аміноспиртом з одержанням рецепторів аденозину А1 є причиною захворюванпроміжної сполуки спирту; і f) циклізації проміжної ня або порушення. Спосіб включає введення пацісполуки спирту до одержання продукту циклізації, і єнту ефективної кількості будь-якої з вищезгадаg) перетворення продукту циклізації в похідне карних сполук. Таким захворюванням або бонової кислоти. порушенням може бути, наприклад, системна гіпеУ деяких варіантах спосіб включає стадії: а) ніртонія, ниркова недостатність, діабет, астма, натрозування 6-аміно-1-пропіл-1Н-піримідин-2,4бряклість, застійна серцева недостатність або нидіону до одержання проміжної нітрозосполуки; b) ркова дисфункція (наприклад, ниркова дисфункція, здійснення відновлення проміжної нітрозосполуки виникаюча як побічний ефект при прийомі діуретидо відповідного діаміноурацилу; с) перетворення ків, які використовують при лікуванні застійної седіаміноурацилу в сіль аміну; d) здійснення реакції рцевої недостатності, або отруєння нирок, винипоєднання солі аміну з 4каюче як побічний ефект при лікуванні гідроксибіцикло[2.2.2]октан-1-карбоновою, кислохіміотерапевтичними агентами). тою до одержання продукту реакції поєднання; і e) Сполуки даного винаходу забезпечують переперетворення продукту реакції поєднання в тіокеваги, включаючи наступні. Так, наприклад, (1) їх тон; f) алкілування тіокетону з одержанням тіоефіможна використовувати в малих дозах для мініміру; g) здійснення взаємодії тіоефіру із заміщеним зації імовірності вияву побічних ефектів і (2) їх моаміноспиртом з одержанням проміжної сполуки жна включати в численні дозовані форми, вклюспирту; і h) циклізації проміжної сполуки спирту до чаючи (але цим не обмежуючись) пілюлі, таблетки, одержання продукту циклізації. капсули, аерозолі, супозиторії, рідкі композиції для Інші відмітні ознаки і переваги даного винахоперорального введення або для ін'єкцій, дієтичні ду будуть ясні з подальшого докладного опису і з добавки або препарати для зовнішнього застосуформули винаходу. вання. У доповнення до застосувань в медицині Якщо немає інших вказівок, то всі технічні і насполуки даного винаходу можна використовувати укові терміни, що використовуються тут мають ті ж у ветеринарії для лікування тварин. У деяких варізначення, які звичайно відомі фахівцям в тій облаантах фармацевтичну композицію приготовляють сті, до якої відноситься даний винахід. Хоча в в формі для перорального, внутрішньовенного, практиці здійснення або перевірки даного винаховнутрішньом'язового або підшкірного введення. ду можна використати способи і матеріали, аналоУ даному винаході запропонований також спогічні або еквівалентні тим, які розкриті тут, відпові 17 75625 18 дні способи і матеріали розкриті далі. Всі публікамає вказані раніше значення. ції, патентні заявки, патенти і інші розкриті тут поТермін, що використовується в описі, "алкоксісилання включені сюди тільки як посилання. Крім алкільна" група являє собою алкільну групу, як того, матеріали, способи і приклади є тільки ілюствизначено вище, в якій водень замінений алкоксиративними, а не такими, що обмежують. У всьому групою, як визначено вище. описі термін "включати" або такі його варіанти, як Термін, що використовується в описі, "галоген" "включає" або, "що включає", потрібно розглядати або "гало" група являє собою фтор, хлор, бром як такі, що означають включення вказаного цілого або йод. або груп цілого, а не виключення якого-небудь Термін, що використовується в описі, "гетероцілого або груп цілого. циклільна" група являє собою 5-10-членну кільцеТермін, що використовується в описі, "алкеніву структуру, в якій один або більше з атомів в льна" група являє собою аліфатичну вуглецеву кільці відмінні від вуглецю, наприклад, N, О, S. групу, яка містить, щонайменше, один подвійний Гетероциклільна група може бути ароматичною зв'язок. Алкенільна група може бути нерозгалужеабо не ароматичною, тобто може бути насиченою ною або розгалуженою і може містити, наприклад, або може бути частково або повністю ненасичевід 3 до 6 атомів вуглецю в ланцюжку і 1 або 2 ною. Приклади гетероциклільних груп включають подвійні зв'язки. Приклади алкенільних груп вклюпіридил, імідазоліл, фураніл, тієніл, тіазоліл, тетчають (але цим не обмежуються) аліл і ізопреніл. рагідрофураніл, тетрагідропіраніл, морфолініл, Термін, що використовується в описі, "алкінітіоморфолініл, індоліл, індолініл, ізоіндолініл, піпельна" група являє собою аліфатичну вуглецеву ридиніл, піримідиніл, піперазиніл, ізоксазоліл, ізокгрупу, що містить, щонайменше, один потрійний сазолідиніл, тетразоліл і бензімідазоліл. зв'язок. Алкінільна група може бути нерозгалужеТермін, що використовується в описі, "заміщеною або розгалуженою і може містити, наприклад, на гетероциклільна" група являє собою гетероциквід 3 до 6 атомів вуглецю в ланцюжку і 1-2 потрійні лільну групу, в якій один або більше з воднів замізв'язки. Приклади алкінільних груп включають (але нений замісником, таким як алкокси, алкіламіно, цим не обмежуються) пропаргіл і бутиніл. діалкіламіно, карбалкокси, карбамоїл, ціано, галоТермін, що використовується в описі, "арильген, тригалометил, гідрокси, карбоніл, тіокарбоніл, на" група являє собою фенільну або нафтильну гідроксіалкіл або нітро. групу або їх похідні. "Заміщена арильна" група Термін, що використовується в описі, "гідрокявляє собою арильну групу, яка заміщена одним сіалкіл" означає алкільну групу, заміщену гідроксиабо більше із замісників, таких як алкіл, алкокси, групою. аміно, нітро, карбокси, карбоалкокси, ціано, алкіТермін, що використовується в описі, "сульламіно, діалкіламіно, галоген, гідрокси, гідроксіалфамоїльна група" являє собою групу структури кіл, меркаптил, алкілмеркаптил, тригалоалкіл, карS(O)2NH2. боксіалкіл, сульфокси або карбамоїл. Терміни "алкілсульфамоїл" і "діалкілсульфаТермін, що використовується в описі, "аралкімоїл" являють собою сульфамоїльні групи, в яких льна" група являє собою алкільну групу, яка замідо атома азоту замість атомів водню приєднані щена арильною групою. Прикладом аралкільної сульфамоїльні групи, відповідно. Аналогічно, групи є бензил. "арилсульфамоїльна" і "арилалкілсульфамоїльна" Термін, що використовується в описі, "циклоагрупи включають арильну групу замість одного з лкільна" група являє собою аліфатичне кільце, що атомів водню, а в останньому випадку алкільну містить, наприклад, 3-8 атомів вуглецю. Приклади групу замість другого атома водню. циклоалкільних груп включають циклопропіл і цикТермін, що використовується в описі, "антагологексил. ніст" являє собою молекулу, яка зв'язується з реТермін, що використовується в описі, "ацильцептором без активування рецептора. Він конкурує на" група являє собою нерозгалужену або розгаз ендогенним лігандом за цей сайт скріплення, і лужену алкіл-С(=О)-групу або групу формілу. Притаким чином зменшує можливість ендогенного клади ацильних груп включають алканоїльні групи ліганду стимулювати цей рецептор. (наприклад, що містять від 1 до 6 атомів вуглецю в У контексті даного винаходу термін "селективалкільній групі). Ацетил і півалоїл є прикладами ний антагоніст" відноситься до антагоніста, який ацильних груп. Ацильні групи можуть бути заміщезв'язується зі специфічним підтипом аденозиновоними або незаміщеними. го рецептора з більш високою спорідненістю, ніж з Термін, що використовується в описі, "карбаіншими підтипами аденозинових рецепторів. Антамоїльна" група являє собою групу, що містить гоністи відповідно до даного винаходу можуть, структуру H2N-CO2-. Терміни "алкілкарбамоїл" і наприклад, володіти більш високою спорідненістю "діалкілкарбамоїл" відносяться до карбамоїльних до А1 рецепторів і бути селективними, володіючи груп, в яких до атома азоту замість атомів водню (а) наномолярною зв'язуючою спорідненістю до А1 приєднані одна або дві алкільні групи, відповідно. рецептору, і (b), щонайменше, в 10 разів, більш Аналогічно, "арилкарбамоїльна" і "арилалкілкарпереважно, в 50 разів і, найбільш переважно, щобамоїльна" групи включають арильну групу замість найменше, в 100 разів більш високою спорідненісодного з атомів водню, а в останньому випадку тю до підтипу рецептора А1, ніж до будь-якого іналкільну групу замість другого атома водню. шого підтипу рецепторів. Термін, що використовується в описі, "карбокТермін, що використовується в описі, "фармасильна" група являє собою -СООН групу. цевтично ефективна кількість" означає кількість, Термін, що використовується в описі, "алкоксиефективну для лікування або профілактики станів, група" являє собою алкіл-О-групу, в якій "алкіл" що характеризується підвищеною концентрацією 19 75625 20 аденозину і/або підвищеною чутливістю до аденозину. Термін, що використовується в описі, "пацієнт" відноситься до ссавців, включаючи людину. Термін, що використовується в описі, "фармацевтично прийнятний носій або ад'ювант" являє собою нетоксичний носій або ад'ювант, який можна вводити тварині разом із сполукою даного винаходу і який не порушує фармакологічної активності цієї сполуки. В основному даний винахід відноситься до ефективних і селективних антагоністів рецепторів аденозину А1. Одержані сполуки даного винаходу представлені в таблиці 1. Наведені тут сполуки демонструють величини ІС50 відносно рецептора А1 у щурів в інтервалі від близько 7 до близько Як повинно бути очевидно фахівцям, даний 1095. винахід не обмежується приведеними вище схеСинтез сполук - антагоністів аденозину мами синтезу. Фахівцям будуть очевидні і інші Сполуки даного винаходу можна одержати, способи. використовуючи цілий ряд відомих способів. НаЗастосування сполук - антагоністів аденозину приклад, ці сполуки можна одержати способами, Активація рецепторів аденозину підтипу А1 вирозкритими [Suzuki, F. et al. J. Med. Chem. 1992, кликає багато які фізіологічні реакції, включаючи 35, 3581-3583, і/або Shimada, J.; Suzuki, F. зменшення потоку крові через нирки, зменшення Tetrahedron Lett. 1992, 33, 3151-3154]. швидкості гломерулярної фільтрації і збільшення Три загальні схеми синтезу сполук даного реабсорбції натрію в нирках. Активація рецепторів винаходу розкриті далі. аденозину А1 знижує також частоту серцевих скоЗагальна схема для способу 1 рочень, знижує швидкість проведення збудження і зменшує скорочуваність. Ці і інші ефекти, пов'язані з активацією рецепторів аденозину А1 в інших органах, є нормальними регуляторними процесами. Однак ці ефекти стають патологічними при багатьох хворобливих станах. Так, антагоністи рецепторів А1 знаходять широке застосування як для профілактики так і при лікуванні захворювань. Захворювання, при яких можна провести профілактику або провести лікування антагоністами рецепторів А1 включають такі захворювання і порушення, при яких активація антагоністів рецепторів А1 грає роль в патофізіології. Приклади таких захворювань і порушень включають (але цим не обмежуються) застійну серцеву недостатність; респіраторні порушення (наприклад, бронхіальну астму, алергічні захворювання легенів); і багато які захворювання, при яких показано лікування діуреЗагальна схема для способу 2 тиками (наприклад, гостра і хронічна ниркова недостатність, слабе функціонування нирок, гіпертонія). Крім того, в даному винаході запропоновано введення високо селективних і ефективних антагоністів рецепторів А1, наприклад, для того, щоб викликати діуретичну реакцію при окремому введенні, і потенціювання діуретичної реакції на традиційні діуретики. Крім того, введення антагоністів рецепторів А1 спільно з традиційними діуретиками ослабляє зменшення швидкості гломерулярної фільтрації, яке викликають традиційні діуретики. Це використовують, наприклад, при лікуванні набряклих станів, таких як застійна серцева недостатність і асцит. Введення сполук - антагоністів аденозину Сполуки можна вводити тваринам (наприклад, Загальна схема для способу 3 ссавцям, таким як люди, примати, коні, собаки, корови, вівці, кози, кішки, миші, щури, морські свинки, кролики, хом'яки, піщанки, тхори, ящірки, рептилії або птахи). Сполуки можна вводити будьяким способом, придатним для введення фарма 21 75625 22 цевтичних сполук, включаючи (але цим не обместерильні жирні олії звичайно використовують як жуючись) пілюлі, таблетки, капсули, аерозолі, сурозчинник або суспендуче середовище. Для цієї позиторії, рідкі форми для перорального введення мети можна використати будь-які негусті жирні або для ін'єкцій, або для використання як очні або олії, включаючи синтетичні моно- або дигліцериди. вушні краплі, дієтичні добавки і препарати для Жирні кислоти, такі як олеїнову кислоту і її гліцезовнішнього використання. Сполуки можна вводиридні похідні, можна використати для приготуванти перорально, інтраназально, трансдермально, ня придатних для ін'єкцій препаратів, якими є приінтрадермально, вагінально, інтрааурально (у вуродні фармацевтично прийнятні олії, такі як хо), інтраокулярно, букально, ректально, трансмуоливкова олія або касторова олія, особливо їх покозально або за допомогою інгаляцій або імпланліоксіетиленові похідні. Такі олійні розчини або татів (наприклад, хірургічно) або внутрішньовенно. суспензії можуть також містити розріджувачі або Необов'язково сполуки можна вводити разом з диспергатори - довголанцюгові спирти (вищі), такі не аденозинмодифікуючою фармакологічною комяк карбоксиметилцелюлоза або аналогічні дисперпозицією (наприклад, в комбінації з не аденозингуючі агенти, які звичайно використовують при модифікуючим діуретиком, як розкрито, наприприготуванні фармацевтично прийнятних дозоваклад, в заявці, що знаходиться на одночасному них форм, включаючи емульсії і суспензії. Інші розгляді, [PCT/US99/08879, поданій 23 квітня 1999 поверхнево-активні агенти, що звичайно викорисроку]). товуються, такі як Tweens, Spans і інші емульгуючі Фармацевтичні композиції агенти або агенти, що підвищують біодоступність, Антагоністи рецепторів А1 можна приготувати які звичайно використовують при приготуванні в формі фармацевтичних композицій для введенфармацевтично прийнятних твердих, рідких або ня тваринам, включаючи людей. Ці фармацевтичні інших дозованих форм, також можна використати композиції, переважно, включають таку кількість з метою одержання препаратів. антагоністів рецепторів аденозину А1, яка ефектиКомпозиції для парентерального введення вно знижує звуження судин або посилює легеневу можуть бути у вигляді єдиної болюсної дози, богемодинаміку, і фармацевтично прийнятний носій. люсної дози для вливання або прийому, після якої Фармацевтично прийнятні носії, придатні для слідує підтримуюча доза. Такі композиції можна цих фармацевтичних композицій, включають, навводити один раз на день або "у міру не обхідприклад, іонообмінники, окисел алюмінію, стеарат ності". алюмінію, лецитин, білки сироватки, такі як альбуФармацевтичні композиції даного винаходу мін сироватки людини, буферні речовини, такі як можна вводити перорально у вигляді будь-яких фосфати, гліцин, сорбінова кислота, сорбат калію, прийнятних для перорального прийому дозованих суміші гліцеридів або насичені рослинні жирні кисформ, включаючи капсули, таблетки, водні сулоти, вода, солі або електроліти, такі як протамінспензії або розчини. У випадку таблеток для перосульфат, динатрійгідрофосфат, гідрофосфат карального введення носії, що звичайно використолію, хлорид натрію, солі цинку, колоїдний окисел вуються включають лактозу і кукурудзяний кремнію, трисилікат магнію, полівінілпіролідон, крохмаль. Звичайно також додають змащувальні речовини на основі целюлози, поліетиленгліколь, агенти, такі як стеарат магнію. Для перорального натрійкарбоксиметилцелюлозу, поліакрилати, віск, введення в формі капсул придатні розріджувачі блокполімери поліетилен-поліоксипропілену, полівключають лактозу і висушений кукурудзяний кроетиленгліколь і шерстний жир (ланолін). хмаль. Якщо для перорального введення необхідКомпозиції даного винаходу можна вводити ні водні суспензії, активний інгредієнт комбінують з парентерально, перорально, за допомогою спреїв емульгуючими або суспендуючими агентами. При для інгаляцій, зовнішньо, ректально, інтраназальбажанні можуть бути також додані деякі підсолоно, букально, вагінально або за допомогою імджуючі агенти, агенти що додають смак, або забаплантованих ємностей. Термін "парентерально", рвлюють. що використовується в описі, включає такі способи В іншому варіанті фармацевтичні композиції введення, як підшкірні, внутрішньовенні, внутрішданого винаходу можна вводити в формі супозиньом'язові, інтраартикулярні, інтрасиновіальні, торіїв для ректального введення. їх можна одерінтрастемальні, інтратекальні, інтрагепатичні, інжати, змішуючи агент з відповідним не подразнютралезіональні і інтракраніальні ін'єкції або влиючим ексципієнтом, який є твердим при кімнатній вання. Переважно вводити композиції перорально, температурі, але стає рідким при ректальній темінтраперитонально або внутрішньовенно. пературі і тому розплавляється в ректумі, виділяСтерильні форми композицій даного винаходу ючи ліки. Такі матеріали включають кокосове масдля ін'єкцій можуть бути водними або масляними ло, бджолиний віск і поліетиленгліколі. суспензіями. Ці суспензії можна приготувати відоФармацевтичні композиції даного винаходу мими фахівцям способами, використовуючи відпопридатні також для поверхневого застосування. відні диспергуючі або змочувальні агенти і суспенПоверхневе нанесення можна здійснити, викорисдуючі агенти. Стерильні препарати для ін'єкцій товуючи композиції в формі ректальних супозитотакож можуть бути стерильними розчинами або ріїв (див. вище) або в формі для введення за досуспензіями для ін'єкцій в нетоксичних парентерапомогою клізм. Можна також використати льно прийнятних розріджувачах або розчинниках, поверхневі-крізьшкірні пластири. наприклад, у вигляді розчинів в 1,3-бутандіолі. Для зовнішнього застосування фармацевтичні Серед прийнятних носіїв і розчинників, які можна композиції можна приготувати у вигляді відповідвикористати, потрібно указати воду, розчин Рінгених мазей, що містять активний компонент, сура і ізотонічний розчин хлориду натрію. Крім того, спендований або розчинений в одному або більше 23 75625 24 з носіїв. Носії для зовнішнього застосування спочином даний винахід. лук даного винаходу включають мінеральну олію, ПРИКЛАДИ рідкий петролатум, білий петролатум, пропіленгліПРИКЛАД 1 коль, поліоксіетилен, поліоксипропіленові сполуки, Сполуки 1, 2, 4, 8, 9, 11, 12-21, 24, 27, 28, 31 і емульгуючий віск і воду. В іншому варіанті фарма32 одержують у відповідності до наступного споцевтичні композиції можна приготувати у вигляді собу, використовуючи відповідний аміноспирт на лосьйону або крему, які містять активні компоненстадії 5. Для одержання сполук використовують ти, суспендовані або розчинені в одному або бінаступні аміноспирти: (R)-2-аміно-3-метил-1льше з фармацевтично прийнятних носіїв. Відпобутанол (сполука 1); (R)-2-аміно-1-бутанол (сполувідні носії включають (але цим не обмежуються) ка 2); (R)-2-аміно-1-пропанол (сполука 4); (R)мінеральну олію, сорбітанмоностеарат, полісорбат ізолейцинол (сполука 8); (R)-2-аміно-1-бутанол 60, цетилові складні ефіри, віск, цетеариловий (сполука 9); (R)-2-аміно-1-пентанол (сполука 11); спирт, 2-октилдодеканол, бензиловий спирт і воду. (S)-1-аміно-2-пропанол (сполука 12); (R)-2-аміно-2Для очних ліків фармацевтичні композиції дафенетанол (сполука 13); (R)-1-аміно-2-пропанол ного винаходу можна приготувати у вигляді су(сполука 14); (S)-ізолейцинол (сполука 15); (R)-2спензій мікрочастинок в ізотонічному, з регульовааміно-3,3-диметилбутан-1-ол (сполука 16); (R)-2ним рН, стерильному сольовому розчині або, аміно-4-метилпентан-1-ол (сполука 17); (R)-2переважно, у вигляді розчинів в ізотонічному, з аміно-3-фенілпропан-1-ол (сполука 18); (R)-2регульованим рН, стерильному сольовому розчині аміногексан-1-ол (сполука 19); 3-амінопропанол з доданням або без додання консерванту, такого (сполука 20); 2-аміноетанол (сполука 21); (S)-2як бензилалконійхлорид. В іншому варіанті для аміно-1-бутанол (сполука 24); 4-амінобутанол очних ліків фармацевтичні композиції можна при(сполука 27); (R)-4-(2-аміно-3готувати в такій мазі, як петролатум. гідроксипропіл)фенол (сполука 28); (R)-3Фармацевтичні композиції даного винаходу амінобутан-1-ол (сполука 31); і (R)-3-амінопентанможна також вводити у вигляді аерозолів для носа 1-ол (сполука 32). або у вигляді інгаляцій. Такі композиції приготовУ таблиці 1 представлені структури синтезоляють відомими фахівцям-фармацевтам способаваних сполук, спосіб одержання сполук і результами приготування фармацевтичних композицій, і їх ти мас-спектрометрії для цих сполук. можна приготувати у вигляді розчинів в сольовому Стадія 1: хлористоводнева сіль 5,6-діаміно-1розчині, використовуючи бензиловий спирт або пропіл-1Н-піримідин-2,4-діону інші відповідні консерванти, промотори абсорбції Початковий матеріал, 6-аміно-1-пропіл-1Ηдля підвищення біодоступності, фторвуглеводні піримідин-2,4-діон, одержують відповідно до відоі/або інші звичайні солюбілізуючі або диспергуючі мого з літератури способу [J. Med. Chem. 1989, агенти. p.1231]. Цей матеріал (8,5г, 50ммоль) розчиняють Кількість антагоністів рецепторів аденозину А1, в 250мл водної оцтової кислоти, і потім охолоджуяку можна скомбінувати з матеріалом носія для ють в бані з льодом. Нітрит натрію (4,14г, 1,2екв.) одержання одиничної дозованої форми, буде задодають у вигляді розчину в 10мл води протягом лежати від пацієнта, що піддається лікуванню і приблизно 15 хвилин. Приблизно через 10 хвилин конкретного способу введення. Композиції можна з реакційної суміші починає осаджуватися ясноприготувати таким чином, щоб вводити пацієнту, червона тверда речовина. Тверду частину збираякий одержує цю композицію, дозу від 0,01 до ють фільтруванням і сушать у вакуумі протягом 100мг/кг ваги тіла антагоністів рецепторів аденоночі, одержуючи 8,0г проміжної нітрозосполуки. зину А1. У деяких варіантах даного винаходу доза Проміжну нітрозосполуку (6,0 г, 30ммоль) сустановить 0,1-10мг/кг ваги тіла. Композицію можна спендують в 100мл води і нагрівають до 80-85°С. вводити у вигляді однієї дози, багаторазових доз Дитіоніт натрію (15,8г, 3,0екв.) додають досить або як вливання протягом певного проміжку часу. швидко протягом близько 5 хвилин. Приблизно Конкретні дози і схема лікування для конкретчерез 5 хвилин джерело нагрівання видаляють і ного пацієнта залежать від різних чинників, вклюясно-зелену реакційну суміш охолоджують до кімчаючи конкретний антагоніст, вік пацієнта, вагу натної температури, а потім на бані з льодом. тіла, загальний стан здоров'я, стать і дієту, а також Тверду частину збирають фільтруванням і сушать час введення, швидкість виведення, комбінація у вакуумі, одержуючи діаміноурацил. Потім його ліків і тяжкість конкретного, підлягаючого лікуванперетворюють в хлористоводневу сіль, розчиняюню захворювання. Визначення ролі таких чинників чи в 10мл Н2О, що містить 1,5екв. НСl, а потім підзнаходиться в компетенції звичайних фахівців. дають ліофілізації. Кількість антагоніста буде також залежати від конСтадія 2: 8-(4-гідроксибіцикло[2.2.2]окт-1-іл)-3кретного, підлягаючого лікуванню пацієнта, спосопропіл-3,7-дигідропурин-2,6-діон бу введення, типу композиції, характеристик споХлористоводневу сіль 5,6-діаміно-1-пропіл-1Нлуки, що вводиться, тяжкості захворювання і піримідин-2,4-діону (3,4г) розчиняють в 80мл ДМФ необхідного ефекту. Кількості антагоністів можна разом з 4-гідроксибіцикло[2.2.2]октан-1визначити на основі фармакологічних і фармакокікарбоновою кислотою (2,5г, 15ммоль). Додають нетичних принципів, які добре відомі фахівцям. HATU (5,9г, 1,05екв.), а потім Et3N (8,30мл, Для більш повного розуміння розкритого тут 4,05екв.). Одержану реакційну суміш перемішують винаходу далі приводяться наступні приклади. при кімнатній температурі протягом ночі. РеакційПотрібно враховувати, що ці приклади представну суміш фільтрують для видалення осаду. Фільтлені тільки для ілюстративних цілей, і їх не треба рат концентрують при зниженому тиску. Одержарозглядати як такі, що обмежують яким-небудь ний залишок розчиняють в 60мл Н2О, що містить 25 75625 26 10екв. NaOH (5,9г). Реакційну суміш перемішують бутанол (сполука 3); (R)-2-аміно-3-метил-1при кипінні із зворотним холодильником протягом бутанол (сполука 5); і (R)-2- аміно-1-пропанол 1 години, охолоджують до кімнатної температури і (сполука 7). підкисляють до рН2 концентрованою НСl. ОдерУ таблиці 1 представлені структури синтезожаний осад збирають фільтруванням і сушать, ваних сполук, способи їх одержання і результати одержуючи 1,85г похідного ксантину. мас-спектрометричних досліджень цих сполук. Стадія 3: 8-(4-гідроксибіцикло[2.2.2]окт-1-іл)-3Стадія 1: 4-(2,6-діоксо-3-пропіл-2,3,6,7пропіл-6-тіооксо-1,3,6,7-тетрагідропурин-2-он тетрагідро-1Н-пурин-8-іл)біцикло [2.2.2]октан-18-(4-гідроксибіцикло[2.2.2]окт-1-іл)-3-пропілкарбонова кислота 3,7-дигідропурин-2,6-діон (500мг, 1,57ммоль) розХлористоводневу сіль 5,6-діаміно-1-пропіл-1Нчиняють в 10мл піридину. Додають P4S10 (1,05г, піримідин-2,4-діону (570мг) розчиняють в 20мл 1,5екв.) і реакційну суміш перемішують при кипінні ДМФ разом з монометиловим складним ефіром із зворотним холодильником протягом 6 годин. біцикло[2.2.2]октан-1,4-дикарбонової кислоти Потім реакційну суміш охолоджують до кімнатної (520мг, 2,45ммоль). Додають HATU (980мг, температури і повільно гасять 5мл Н2О. Потім су1,05екв.), а потім Et3N (1,40мл, 4,05екв.). Одержаміш підкисляють при 0°С до рН5, використовуючи ну реакційну суміш перемішують при кімнатній 6н. НСl. Водний шар екстрагують ЕtOАс. Об'єднатемпературі протягом ночі. На наступний ранок ний органічний шар сушать (Na2SO4) і концентруреакційну суміш фільтрують для видалення осаду. ють при зниженому тиску. Внаслідок очищення за Фільтрат концентрують при зниженому тиску. Одедопомогою препаративної ВЕРХ одержують 100мг ржаний залишок розчиняють в 10мл Н2О, що місвказаної в заголовку сполуки. тить 10екв. NaOH (980мг). Реакційну суміш переСтадія 4: 8-(4-гідроксибіцикло[2.2.2]окт-1-іл)-6мішують при кипінні із зворотним холодильником метилсульфаніл-3-пропіл-3,7-дигідропурин-2-он протягом 2 годин. Потім її охолоджують до кімнат8-(4-гідроксибіцикло[2.2.2]окт-1-іл)-3-пропіл-6ної температури і підкисляють до рН2 концентротіооксо-1,3,6,7-тетрагідропурин-2-он (120мг, ваною НСl. Одержаний осад збирають фільтру0,36ммоль) суспендують в 3мл Н2О і 1,5мл EtOH. ванням і сушать, одержуючи 680 мг похідного Додають NaOH у вигляді розчину в 0,4мл Н2О, а кислоти. потім Mel. Реакційну суміш перемішують при кімСтадія 2: 8-(4-гідроксиметилбіцикло[2.2.2]октнатній температурі протягом 1 години. Потім суміш 1-іл)-3-пропіл-3,7-дигідропурин-2,6-діон нейтралізують 0,1н. НСl і екстрагують СНСl3. Об'є4-(2,6-діоксо-3-пропіл-2,3,6,7-тетрагідро-1Нднані органічні шари сушать (Na2SO4) і концентрупурин-8-іл)біцикло[2.2.2]октан-1-карбонову кислоту ють при зниженому тиску, одержуючи практично (3,2г, 9,25ммоль) розчиняють в 100мл безводного кількісний вихід вказаної в заголовку сполуки. ТГФ і охолоджують до 0°С. Додають боран-ТГФ Стадія 5: 8-(4-гідроксибіцикло|"2.2.21окт-1-іл-6(1,0Μ в ТГФ, 18,5мл, 2екв.) і реакційну суміш пе(1-гідроксиметилпропіламіно)-3-пропіл-3.7ремішують при 0°С протягом 10 хвилин, потім надигідропурин-2-он грівають до кімнатної температури і перемішують 8-(4-гідроксибіцикло[2.2.2]окт-1-іл)-6протягом 48 годин. Потім реакційну суміш обережметилсульфаніл-3-пропіл-3,7-дигідропурин-2-он но гасять 10мл МеОН, а потім концентрують при (125мг, 0,36ммоль) розчиняють в 3мл ДМСО разниженому тиску. Одержаний залишок розчиняють зом з надлишком відповідного аміноспирту (наприв 20мл МеОН і концентрують при зниженому тиску. клад, (R)-(-)-2-аміно-1-бутанолу (0,24мл, 7екв.) для Таку обробку повторюють ще 4 рази, одержуючи сполуки 2). Одержану реакційну суміш перемішупотрібний спирт. ють при 150°С протягом 3 годин. Потім її охолоСтадія 3: 4-(2,6-діоксо-3-пропіл-2,3,6,7джують до кімнатної температури і внаслідок очитетрагідро-1Н-пурин-8-іл)-біцикло[2.2.2]октан-1щення за допомогою препаративної ВЕРХ карбальдегід одержують 110мг вказаної в заголовку сполуки. 8-(4-гідроксиметилбіцикло[2.2.2]окт-1-іл)-3Стадія 6: 7-етил-2-(4-гідроксибіцикло[2.2.2]октпропіл-3,7-дигідропурин-2,6-діон (2,70г, 1-іл)-4-пропіл-1,4,6,7-тетрагідро-1,3,4,5а, 88,13ммоль) розчиняють в 40мл ДМСО. Додають пентааза-аз-індацен-5-он (сполука 2) суміш піридин-SО3 (3,88г, 3екв.), а потім Et3N 8-(4-гідроксибіідикло[2,2.2]окт-1-іл)-6-(1(7,4мл, 7екв.) при кімнатній температурі. Одержану гідроксиметилпропіламіно)-3-пропіл-3,7реакційну суміш перемішують при кімнатній темдигідропурин-2-он (110мг) розчиняють в 3мл SOCl2 пературі протягом 18 годин. Потім її розбавляють і перемішують при кипінні із зворотним холодильEtOAc і промивають 5% водною лимонною кислоником протягом 20 хвилин. Потім охолоджують до тою, Н2О, сольовим розчином, сушать над сулькімнатної температури і концентрують. Залишок фатом натрію і концентрують при зниженому тисгасять насиченим водним NaHCO3 і екстрагують ку, одержуючи 900мг потрібного альдегіду. СНСl3. Об'єднані органічні шари сушать (Na2SO4) і Стадія 4: метиловий складний ефір 3-[4-(2,6концентрують при зниженому тиску. Внаслідок діоксо-3-пропіл-2,3,6,7-тетрагідро-1Н-пурин-8очищення за допомогою ВЕРХ одержують 50 мг іл)біцикло[2.2.2]окт-1-іл]акрилової кислоти вказаної в заголовку сполуки у вигляді солі три4-(2,6-діоксо-3-пропіл-2,3,6,7-тетрагідро-1Нфтороцтової кислоти. пурин-8-іла)біцикло[2.2.2]октан-1-карбальдегід ПРИКЛАД 2 (900мг, 2,73ммоль) розчиняють в 25мл ТГФ, і доСполуки 3, 5 і 7 одержують у відповідності до дають метил(трифенілфосфораніліден)ацетат наступного способу, використовуючи відповідний (1,83г, 2екв.). Одержану реакційну суміш переміаміноспирт на стадії 8. Для одержання сполук вишують при кипінні із зворотним холодильником користовують наступні аміноспирти: (R)-2-аміно-1протягом 18 годин. Потім її охолоджують до кімна 27 75625 28 тної температури і очищають з допомогою препалука 3) ративної ВЕРХ, використовуючи суміш водного Метиловий складний ефір 3-{4-[6-(1ацетонітрилу, одержуючи 300мг потрібного прогідроксиметилпропіламіно)-2-оксо-3-пропіл-3,7дукту. дигідро-2Н-пурин-8-іл]біцикло[2.2.2]окт-1Стадія 5: метиловий складний ефір 3-[4-(2,6іл}пропіонової кислоти (30мг) розчиняють в 1мл діоксо-3-пропіл-2,3,6,7-тетрагідро-1Н-пурин-8SOCl2 і перемішують при кипінні із зворотним хоіл)біпикло[2.2.2]окт-1-іл]пропіонової кислоти лодильником протягом 15 хвилин. Потім реакційну Метиловий складний ефір 3-[4-(2,6-діоксо-3суміш охолоджують до кімнатної температури і пропіл-2,3,6,7-тетрагідро-1Н-пурин-8концентрують при зниженому тиску. Одержаний іл)біцикло[2.2.2]окт-1-іл]акрилової кислоти (300мг) залишок розчиняють в розчині, що містить 1мл розчиняють в 20мл ТГФ. Додають 10% Pd-на-С води, 0,5мл МеОН і 0,1мл 10% водної NaOH. Реа(25мг) і одержану реакційну суміш гідрують при кційну суміш перемішують при кімнатній температиску 50 пси Н2 при кімнатній температурі протятурі протягом 30 хвилин. Потім її підкисляють до гом 6 годин. Реакційну суміш фільтрують через рН 2 розбавленою 1н. НСl і концентрують. Одерцеліт і фільтрат концентрують при зниженому тисжаний сирий продукт очищають з допомогою преку, одержуючи 280мг потрібного продукту. паративної ВЕРХ, одержуючи вказану в заголовку Стадія 6: метиловий складний ефір 3-[4-(2сполуку. оксо-3-пропіл-6-тіооксо-2,3,6,7-тетрагідро-1НПРИКЛАД 3 пурин-8-іл)біцикло[2.2.2]окт-1-іл]пропіонової кисСполуки 6, 10, 22, 23, 25, 26, 29 і 30 одержулоти ють у відповідності до наступного способу, викоМетиловий складний ефір 3-[4-(2,6-діоксо-3ристовуючи відповідний аміноспирт на стадії 3. пропіл-2,3,6,7-тетрагідро-1H-пурин-8Для одержання сполук були використані наступні іл)біцикло[2.2.2]окт-1-іл]пропіонової кислоти аміноспирти: 2-аміноетанол (сполука 6); (R)-2(250мг, 0,64ммоль) розчиняють в 8мл піридину. аміно-1-бутанол (сполука 10); (R)-2-аміно-1Додають P4S10 (430мг, 1,5екв.) і реакційну суміш пропанол (сполука 22); (R) -2-аміно-1-пентанол перемішують при кипінні із зворотним холодильни(сполука 23); (R)-ізолейцинол (сполука 25); (3)-2ком протягом 3 годин. Потім її охолоджують до аміно-1-бутанол (сполука 26); 3-амінопропанол кімнатної температури і гасять 3мл Н2О, а потім (сполука 29) і 4-амінобутанол (сполука 30). У табдодають достатню кількість 6н. НСl, щоб довести лиці 1 представлені структури синтезованих сповеличину рН до 3. Одержану реакційну суміш екслук, способи їх одержання і результати мастрагують СНСІ3. Органічний шар сушать (Na2SO4) і спектрометричного дослідження цих сполук. концентрують при зниженому тиску. Сирий залиСтадія 1: метиловий складний ефір 4-(2,6шок очищають за допомогою препаративної ВЕРХ, діоксо-3-пропіл-2,3,6,7-тетрагідро-1Н-пурин-8одержуючи 100мг потрібного продукту. іл)біцикло[2.2.2]октан-1-карбонової кислоти Стадія 7: метиловий складний ефір 3-[4-(64-(2,6-діоксо-3-пропіл-2,3,6,7-тетрагідро-1Нметилсульфаніл-2-оксо-3-пропіл-3,7-дигідро-2Нпурин-8-іл)біцикло[2.2.2]октан-1-карбонову кислоту пурин-8-іл)біцикло[2.2.2]окт-1-іл]пропіоново'ї кисодержують відповідно до викладеного вище сполоти собу. Цей матеріал (1,4г) суспендують в 50мл МеМетиловий складний ефір 3-[4-(2-оксо-3ОН і додають 5 крапель концентрованої сірчаної пропіл-6-тіооксо-2,3,6,7-тетрагідро-1Н-пурин-8кислоти. Реакційну суміш перемішують при кипінні іл)біцикло[2.2.2]окт-1-іл] пропіонової кислоти із зворотним холодильником протягом 18 годин. (100мг) розчиняють в 2мл ЕtOН і 1мл Н2О. NaOH Потім її охолоджують до кімнатної температури і (20мг) додають у вигляді розчину в 1мл Н2О, а концентрують при зниженому тиску. Одержаний потім додають МеІ (23мкл, 1,5екв.). Одержану реазалишок розбавляють СН2Сl2 і промивають водкційну суміш перемішують при кімнатній темпераним NaHCO3, сольовим розчином, сушать турі протягом 30 хвилин. Потім її екстрагують (Na2SO4) і концентрують, одержуючи 1,2г вказаної ЕtOАс. Органічний шар сушать (Na2SO4) і концентв заголовку сполуки. рують при зниженому тиску, одержуючи 105мг вкаСтадія 2: метиловий складний ефір 4-(6заної в заголовку сполуки. метилсульфаніл-2-оксо-3-пропіл-3,7-дигідро-2НСтадія 8: метиловий складний ефір 3-{4-[6-(1пурин-8-іл)біцикло[2.2.2]октан-1-карбонової кислогідроксиметилпропіламіно)-2-оксо-3-пропіл-3,7ти дигідро-2Н-пурин-8-іл]біцикло[2.2.2]окт-1Метиловий складний ефір 4-(2,6-діоксо-3мл}пропіонової кислоти пропіл-2,3,6,7-тетрагідро-1Н-пурин-8Метиловий складний ефір 3-[4-(6іл)біцикло[2.2.2]октан-1-карбонової кислоти (1,2г, метилсульфаніл-2-оксо-3-пропіл-3,7-дигідро-2Н3,33ммоль) розчиняють в 20мл піридину. Додають пурин-8-іл)біцикло[2.2.2]окт-1-іл]пропіонової кислоP4S10 (2,22г, 1,5екв.) і реакційну суміш перемішути (105мг) розчиняють в 2мл ДМСО разом з відпоють при кипінні із зворотним холодильником провідним аміноспиртом (наприклад, 160мкл (R)-2тягом 3 годин. Потім її охолоджують до 0°С і обеаміно-1-бутанолу для сполуки 3). Реакційну суміш режно гасять водою. Додають достатню кількість перемішують при 150°С протягом 3 годин. Потім її 6н. НСl для доведення величини рН до 5 і реакційохолоджують до кімнатної температури і внаслідок ну суміш екстрагують СН2Сl2. Органічний шар суочищення за допомогою препаративної ВЕРХ шать (Na2SO4) і концентрують, одержуючи 860мг одержують 50 мг вказаної в заголовку сполуки. похідного складного тіоефіру. Цей матеріал Стадія 9: 3-{4-(7-етил-5-оксо-4-пропіл-4,5,6,7(860мг, 2,29ммоль) розчиняють в 5мл ЕtOН і 5мл тетрагідро-1Н-1,3,4,5а, 8-пентааза-аз-індацен-2Н2О. Додають NaOH (183мг, 2екв.) у вигляді розіл)біцикло[2.2.2]окт-1-іл}пропіонова кислота (спочину в 2мл Н2О, а потім МеІ (213мкл, 1,5екв.). 29 75625 30 Одержану реакційну суміш перемішують при кіммідину, 100мкМ PMSF і по 2мкг/мл кожного з апронатній температурі протягом 30 хвилин. Потім її тиніну, пепстатину і леупептину) і центрифугують екстрагують EtOAc. Органічний шар сушать при 20000xg протягом 20 хвилин. Осади знов су(Na2SO4) і концентрують при зниженому тиску, спендують і двічі промивають буфером НЕ (10мМ одержуючи 800мг вказаної в заголовку сполуки. Na-HEPES, 1мМ EDTA, рН7,4, плюс інгібітори проСтадія 3: Метиловий складний ефір 4-[6-(2теази). Кінцеві осадки знов суспендують в буфері гідроксіетиламіно)-2-оксо-3-пропіл-3,7-дигідро-2ННЕ, доповненому 10% (вага/об'єм) сахарози і інгіпурин-8-іл]біцикло[2.2.2]октан-1-карбонової кисбіторами протеази, і заморожують у вигляді аліклоти вот при -80°С. Концентрації білка визначають, виМетиловий складний ефір 4-(6користовуючи набір для аналізу білка ВСА метилсульфаніл-2-оксо-3-пропіл-3,7-дигідро-2Н(Pierce). пурин-8-іл)біцикло[2.2.2]октан-1-карбонової кислоЛюдський рецептор А1: кДНК людського рецети (50мг) розчиняють в 1мл ДМСО разом з відпоптора аденозину А1 одержують, використовуючи відним аміноспиртом (наприклад, 7екв. 2RT-PCR і субклонують в pcDNA3.1 (Invitrogen). аміноетанолу для сполуки 6). Реакційну суміш пеСтабільну трансфекцію клітин СНО-К1 здійснюють, ремішують при 150°С протягом 3 годин. Потім її використовуючи LIPOFECTAMINE-PLUS (GIBCOохолоджують до кімнатної температури і очищаBRL), відбір колоній здійснюють в 1 мг/мл G418 і ють за допомогою препаративної ВЕРХ, одержуюскринують, використовуючи аналіз зв'язування чи 30мг вказаної в заголовку сполуки. радіолігандів. Для мембранних препаратів, СНОСтадія 4: 4-(5-оксо-4-пропіл-4,5,6,7-тетрагідроК1 клітини, зростаючі в моношарах в повному се1Н-1,3,4,5а, 8-пентааза-аз-індацен-2редовищі (F12+10% FCS+1мг/мл G418) промиваіл)біцикло[2.2.2]октан-1-карбонова кислота ють в PBS і збирають в буфер А, доповнений інгіМетиловий складний ефір 4-[6-(2біторами протеази. Клітини гомогенізують, гідроксіетиламіно)-2-оксо-3-пропіл-3,7-дигідро-2Нцентрифугують і двічі промивають буфером НЕ, як пурин-8-іл]біцикло[2.2.2]октан-1-карбонової кислоуказано вище. Кінцеві осади зберігають у вигляді ти (30мг) розчиняють в 1мл SOCl2 і перемішують аліквот при -80°С. при кипінні із зворотним холодильником протягом Аналіз зв'язування радіолігандів 15 хвилин. Потім реакційну суміш охолоджують до Мембрани (50мкг білка мембран для щурячих кімнатної температури і концентрують при знижеA1ARs і 25мкг СНО-К1 білка мембран для людсьному тиску. Одержаний залишок розчиняють в ких A1ARs), радіоліганди і різні концентрації конкурозчині, що містить 1мл води, 0,5мл МеОН і 0,1мл руючих лігандів інкубують (по троє) в 0,1мл буфе10% водної NaOH. Реакційну суміш перемішують ру НЕ плюс 2ед./мл аденозиндеамінази протягом 3 при кімнатній температурі протягом 30 хвилин. 2,5 години при 21°С. Радіоліганд [ H]DPCPX (112 Потім її підкисляють до рН2 розбавленою 1н. НСl і Кюрі/ммоль від NEN, кінцеві концентрації: 1нМ) концентрують. Одержаний сирий продукт очищавикористовують для конкурентного аналізу зв'язують з допомогою препаративної ВЕРХ, одержуючи вання на A1ARs. Неспецифічне зв'язування визнавказану в заголовку сполуку. чають в присутності 10мкМ BG9719. Аналіз зв'язуПРИКЛАД 4 вання завершують фільтруванням на Whatman Методика аналізу GF/C скловолоконних фільтрах, використовуючи Приготовляють різні похідні ксантину, структузбиральник клітин BRANDEL. Фільтри тричі прори яких представлені в таблиці 1. Для деяких з цих мивають 3-4мл охолодженого льодом 10мМ TRisсполук величини Ki для рецепторів аденозину А1 у HCl, рН7,4 і 5мМ MgCl2 при 4°С. Фільтрувальний щурів і у людини визначають у відповідності до папір переносять в ампулу і додають 3мл сцинтинаступного протоколу аналізу. ляційного коктейлю ScintiVersell (Fisher). РадіоакМатеріали тивність визначають, використовуючи лічильник Аденозиндеаміназу і HEPES закуповують у Wallac β-counter. Sigma (St. Louis, МО). Культуральне середовище Аналіз результатів зв'язування клітин Ham's F-12 і фетальну телячу сироватку Для визначення Ki: Результати конкурентного закуповують у GIBCO Life Technologies зв'язування задовольняють односайтовій моделі (Gaithersburg, MD). Антибіотик G-418, культуральні зв'язування і побудовані з використанням Prizm планшети Falcon 150мМ і культуральні планшети GraphPad. Для розрахунку величин Ki із значень Costar на 12 ямок закуповують у Fisher (Pittsburgh, ІС50 використовують рівняння Cheng-Prusoff: PA). [3H]CPX закуповують у DuPont-New England Kі=ІС50/(1+[I]/KD), де Ki являє собою константу споNuclear Research Products (Boston, MA). Суміш рідненості для конкуруючого ліганду, [І] являє соантибіотиків пеніцилін/стрептоміцин закуповують у бою концентрацію вільного радіоліганду, і KD явMediatech (Washington, DC) Склад HEPESляє собою константу спорідненості для буферованого розчину Хенка: 130мМ NaCl, 5,0мМ радіоліганду. СІ, 1,5мМ СаСl2, 0,41мМ MgSO4, 0,49мМ Na2HPO4, Для % зв'язування: Для одноточкового аналізу 0,44мМ KН2РО4, 5,6мМ декстрози і 5мМ HEPES зв'язування результати представлені як % від пов(рН7,4). ного специфічного зв'язування при 1мкМ конкуруПриготування мембран ючої сполуки: % від повного =100* (Специфічне Щурячий рецептор А1: Мембрани приготовлязв'язування з 1мкМ конкуруючої сполуки/повне ють з кори головного мозку, виділеної з щойно специфічне зв'язування). % зв'язування являє соумертвлених щурів. Тканини гомогенізують в бубою кількість зв'язаного радіоліганду, що залишафері А (10мМ EDTA, 10мМ Na-HEPES, рН7,4) доється в присутності 1мкМ конкуруючого антаповненому інгібіторами протеази (10мкг/мл бензагоніста. 31 75625 32 Результати Для визначення щільності A1AdoRs в СНО кліВсі тестовані сполуки демонструють величини тинних мембранах, 100мкл аліквот мембран (5мкг А1 Ki для щурів від близько 4 до близько 800нМ. У білку) інкубують протягом 2 годин при 25°С з 0,15таблиці 2 представлені величини Ki для рецептора 20нМ [3Н]СРХ і аденозиндеаміназою (2од./мл) в аденозину А1 для щурів і % зв'язування для спо100мкл 50мМ TRis-HCl, pH7,4. Інкубування закінлук. чують, розбавляючи 4мл охолодженого льодом ПРИКЛАД 5 50мМ TRis-HCl буферу, і негайно збирають мемАльтернативна методика аналізу брани на скловолоконні фільтри (Schleicher and Матеріали Schuell, Keene, NH) за допомогою вакуумного фі(див. приклад 4). льтрування (Brandel, Gaithersburg, MD). Фільтри Культура клітин швидко тричі промивають охолодженим льодом СНО клітини, стабільно експресуючі рекомбібуфером для видалення непов'язаного радіоліганантні людські A1AdoR (CHO: A1AdoR клітини) принду. Диски фільтрів, що містять захоплені мемготовляють за способом [Kollias-Barker et al., J. брани, вміщують в 4мл Scintiverse BD (Fisher) і Pharma. Exp. Ther. 281(2), 761, 1997] і культивують радіоактивність вимірюють, використовуючи ріяк для СНО: дикі клітини. СНО клітини культивудинний сцинтиляційний лічильник. Для визначення ють як моношари на пластикових планшетах в неспецифічного зв'язування [3Н]СРХ мембрани середовищі Ham's F-12, доповненому 10% фетаінкубують, як указано вище, і 10мкМ СРТ додають льною телячою сироваткою, 100од. пеніциліну G і до інкубаційного буфера. Неспецифічне зв'язуван100мкг стрептоміцину у вологій атмосфері, складу ня визначають як [3Н]СРХ, пов'язаний в присутно3 5% СО2/95% повітря при 37°С. Щільність [ Н]СРХ сті 10мкМ СРТ. Специфічне зв'язування радіолігасайтів зв'язування в СНО клітинах становить 26±2 нду з A1AdoR визначають, віднімаючи (n=4) фмоль/мг білки. Клітини субкультивують двічі неспецифічне зв'язування з повного зв'язування. на тиждень після відділення, використовуючи 1мМ Як виявлено, неспецифічне зв'язування посилює EDTA в Са2+-Mg2+-вільний HEPES-буферований лінійність із збільшенням концентрації [3Н]СРХ. розчин Хенка. Для експериментів використовують Для кожної з тестованих концентрацій [3Н]СРХ три різні клони клітин CHO:A1AdoR, і всі результапроводився потрійний аналіз. ти підтверджені клітинами з двох або трьох клонів. Для визначення спорідненості антагоністів Щільність A1AdoRs в цих клітинах становила 4000A1AdoRs для людських рекомбінантних A1AdoR, 8000фмоль/мг білка за даними аналізу [3Н]СРХ експресованих в СНО клітинах, визначають зв'язуспецифічного зв'язування. вання 2нМ [3Н]СРХ в присутності концентрацій Зв'язування радіоліганду антагоніста, що підвищуються. Аліквоти СНО клі3 СНО клітини, вирощені на 150мм культуральтинних мембран (100мкл: 5мг білка), [ Н]СРХ, анних планшетах, промивають HEPES-буферованим тагоніст (0,1нМ - 100мкМ) і аденозиндеаміназу розчином Хенка, потім видаляють скребачкою для (2од./мл) інкубують протягом 3 годин при 25°С в клітин і гомогенізують в охолодженому льодом 200мкл 50мМ TRis-HCl буферу (рН7,4). Аналіз за50мМ TRis-HCl pH7,4. Клітинні мембрани осаджукінчують, як указано вище. ють центрифугуванням гомогенату клітин при Інші варіанти 48000xg протягом 15 хвилин. Осад мембран двічі Потрібно розуміти, що даний докладний опис промивають, повторно суспендуючи в свіжому призначений тільки для ілюстрації, але не обмебуфері і центрифугуючи. Кінцевий осад знов сужує об'єм даного винаходу, який визначається спендують в невеликому об'ємі 50мМ TRis-HCl, об'ємом формули винаходу. Інші аспекти, переваpH7,4, і зберігають у вигляді аліквот по 1мл при ги і модифікації визначаються об'ємом формули 80°С до використання для аналізу. винаходу, що наводиться далі. Таблиця 1 33 75625 34 Продовження таблиці 1 Таблиця 2 Сполука № 1 2 3 4 5 Ki (нМ) 4,4 5,75 8,38 9,92 10,5 % зв'язування не визначено не визначено не визначено не визначено 1,9 Сполука № 17 18 19 20 21 Ki (нМ) 166,7 708 не визначено не визначено не визначено % зв'язування не визначено не визначено 18,1 52,7 12,2 35 6 7 8 9 10 11 12 13 14 15 16 не визначено 13,7 14,1 26,7 40,2 43,2 51,3 68,3 68,5 93 155 Комп’ютерна верстка Т. Чепелева 75625 2,6 2,5 1 0,1 6,2 3,7 8,6 не визначено 7,8 7,7 не визначено 36 Продовження таблиці 2 22 23 24 25 26 27 28 29 30 31 32 не визначено не визначено не визначено не визначено не визначено не визначено не визначено не визначено не визначено не визначено не визначено Підписне 24 22,8 11 46,7 41,1 16,3 36,3 81,8 71 40 61 Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюCondensed purine derivatives as a1 adenosine receptor antagonists
Назва патенту російськоюКонденсированные производные пурина как антагонисты рецепторов аденозина а1
МПК / Мітки
МПК: A61K 31/505, C07D 487/14, A61P 9/00
Мітки: антагоністи, аденозину, рецепторів, пурину, конденсовані, похідні
Код посилання
<a href="https://ua.patents.su/18-75625-kondensovani-pokhidni-purinu-yak-antagonisti-receptoriv-adenozinu-a1.html" target="_blank" rel="follow" title="База патентів України">Конденсовані похідні пурину як антагоністи рецепторів аденозину а1</a>
Попередній патент: Спосіб одержання водної витяжки з рослин, витяжка, одержана у такий спосіб (варіанти), сировина для виготовлення лікарського засобу та фармацевтичний препарат
Наступний патент: Спосіб одержання каталізатора реакції окиснення со на основі багатокомпонентних оксидів 3d-металів та вуглецевих нанотрубок
Випадковий патент: Ультразвуковий рефлектор з повітряним прошарком












