Сполуки з властивостями вивільнення гормону росту, фармацевтична композиція, спосіб стимулювання вивільнення гормону росту з гіпофізу і спосіб підвищення швидкості росту тварин
Номер патенту: 61056
Опубліковано: 17.11.2003
Автори: Лау Йєспер, ЙОХАНСЕН Нільс Лангеланд, ХАНСЕН Томас Крузе, ТЬОГЕРСЕН Хеннінг, ХАНСЕН Біргіт Сехестед, ЛУНДТ Бехренд Фрідріх, МАДСЕН Келль, Пешке Бернд
Формула / Реферат
1. Сполука згідно з загальною формулою (1)
A-B-C-D(-E)p (1)
де p дорівнює 0 або 1,
А являє собою водень або R1-(CH2)q-(X)r-(CH2)s-CO-, де
q дорівнює 0 або цілому числу, вибраному з групи: 1,2,3,4,5, r дорівнює 0 або 1, s дорівнює 0 або цілому числу, вибраному з групи: 1,2,3,4,5,
R1 являє собою водень, імідазоліл, гуанідино, піперазинo, морфоліно, піперидино або N(R2)-R3, де кожний радикал R2 та R3 незалежно являє собою водень або нижчий алкіл, що як варіант заміщується однією чи кількома гідроксил-, піридиніл- або фуранілгрупами, і
X, якщо r дорівнює 1, являє собою -NH-, -СН2, -СН=СН-, -C(R16)(R17)-,
,
де кожний з радикалів R16 та R17 незалежно є воднем або нижчим алкілом, В являє собою (G)t-(H)u, де кожний з t та u незалежно дорівнює 0 або 1,
G i H являють собою амінокислотні залишки (радикали), вибрані з групи, до якої належать природні L-амінокислоти чи їх відповідні D-ізомери, або ненатуральні (штучні) амінокислоти, такі як 1,4-діамінобутирова кислота, аміноізобутирова кислота, 1,3-діамінопропіонова кислота, 4-амінофенілаланін, 3-піридилаланін, 1,2,3,4-тетрагідроізохінолін-3-карбонова кислота, 1,2,3,4-тетрагідроноргарман-3-карбонова кислота, N-метилантранілова кислота, антранілова кислота, N-бензилгліцин, 3-амінометилбензойна кислота, 3-аміно-3-метилбутанова кислота, саркозин, ніпекотова кислота або ізоніпекотова кислота,
і де, коли як t, так і u дорівнюють 1, амідний зв'язок між G та H варіативно може заміщуватись Y-NR18-, де Υ є -CO- або -СН2-, і R18 являє собою водень, нижчий алкіл або нижчий аралкіл,
С являє собою D-амінокислоту з формулою -NH-CH((CH2)w-R4)-CO-, де
w дорівнює 0, 1 або 2, і
R4 вибрано з групи, до якої належать
,
кожний з котрих як варіант заміщується галогеном, нижчим алкілом, нижчим алкілокси, нижчим алкіламіно, аміно або гідрокси,
D, якщо p дорівнює 1, являє собою D-амінокислоту з формулою -NR20-CH((CH2)k-R5)-CO- або, якщо p дорівнює 0, D являє собою -NR20-CH((CH2)l-R5)- СН2- R6 або
-NR20-CH((CH2)m-R5)-CR6,
де
k дорівнює 0, 1 або 2,
l дорівнює 0, 1 або 2,
m дорівнює 0, 1 або 2, R20 вибрано з групи, до якої належать нижчий алкіл або нижчий аралкіл;
R5 вибрано з групи, до якої належать
,
кожний з котрих як варіант заміщується галогеном, нижчим алкілом, нижчим алкілокси, аміно або гідрокси, і
R6 являє собою піперазинo, морфоліно, піперидино, -ОН або -N(R7)-R8, де кожний з радикалів R7 та R8 незалежно являє собою водень або нижчий алкіл,
Е, якщо p дорівнює 1, являє собою -NН-СH(R10)-(СН2)v- R9, де v дорівнює 0 або цілому числу, вибраному з групи: 1,2,3,4,5,6,7,8,
R9 являє собою водень, імідазоліл, гуанідинo, піперазино, морфоліно, піперидино, -N(R11)-R12,
,
де n дорівнює 0, 1 або 2, та R19 являє собою водень або нижчий алкіл,
,
де о дорівнює цілому числу, вибраному з групи: 1, 2, 3, кожний з радикалів R11 та R12 незалежно являє собою водень або нижчий алкіл, або
,
кожний з котрих як варіант заміщується галогеном, нижчим алкілом, нижчим алкілокси, аміно, алкіламіно, гідрокси, або продуктом перегрупування Амадорі з аміногрупи та гексапіранози або гексапіранозилгексапіранози і
R10, якщо p дорівнює 1, вибрано з групи, до якої належать H, -COOH, -СН2-R13-СО-R13 або -СН2-ОН, де
R13 являє собою піперазино, морфоліно, піперидино, -ОН або -N(R14)-R15, де кожний з R14 та R15 незалежно являють собою водень або нижчий алкіл, всі амідні зв'язки в формулі 1, за винятком зв'язку між С та D, можуть незалежно бути заміщеними -Y-N R18-, де Υ являє собою -СО- або -СН2-, і
R18 являє собою водень, нижчий алкіл чи нижчий аралкіл, або її фармацевтичнo прийнятна сіль, за винятком сполук
(3-амінометилбензоїл)-D-2NаІ-N-Ме-D-Рhе-Lуs-NН2,
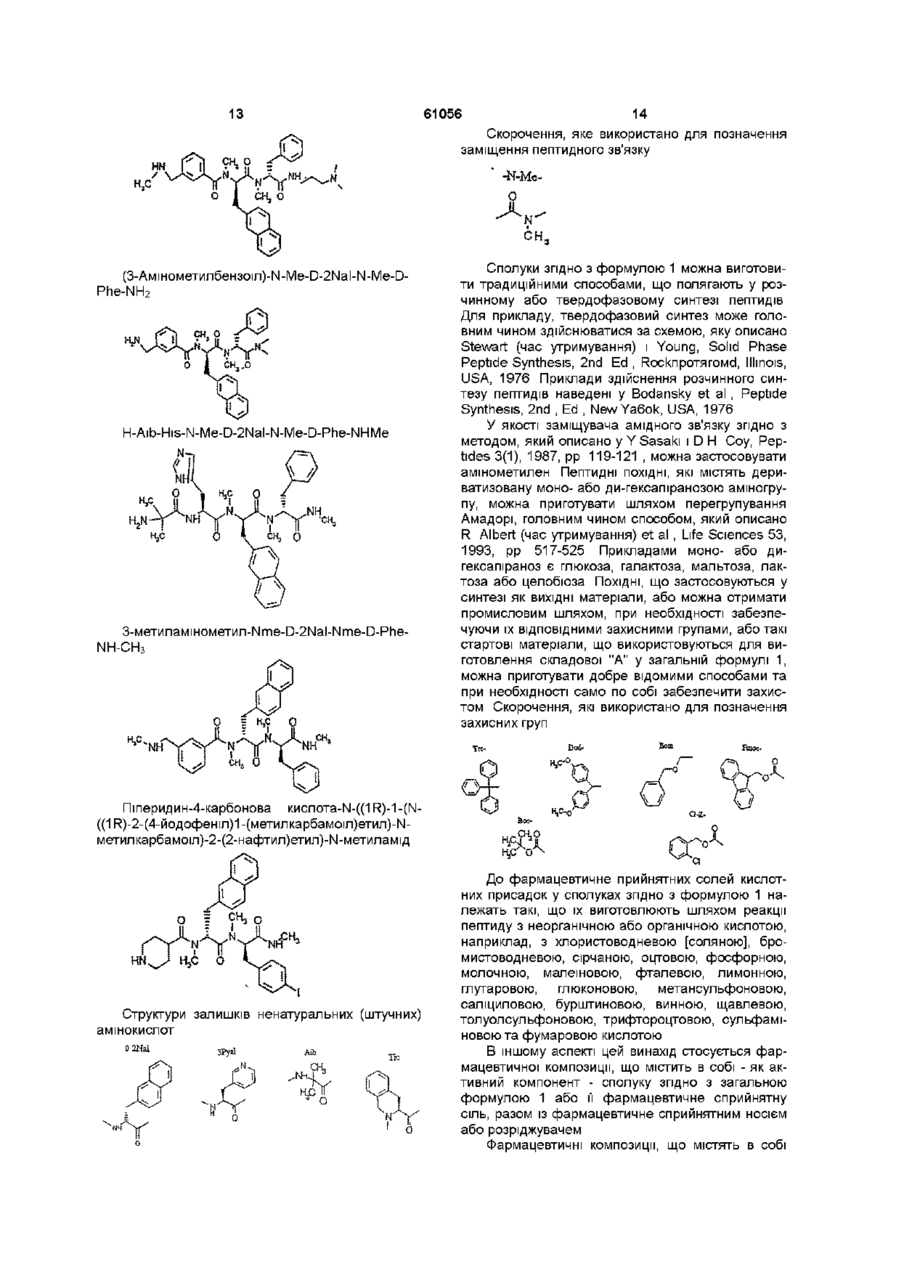
H-Aib-His-D-2Nal-N-Me-D-Phe-Lys-NH2,
H-Aib-His-N-Me-D-2Nal-N-Me-D-Phe-Lys-NH2,
3-(Н-Аіb-Ніs-D-2Nаl-N-Ме-D-Рhе-NН)-1-морфолінопропан,
2-(Н-Аіb-Ніs-D-2Nаl-N-Ме-D-Рhе-NН)-(1-метил-2-піролідиніл)етан,
((3R)-піперидинкарбоніл)-N-Ме-D-2Nаl-N-Ме-D-Рhе-Lуs-NH2,
3-((3-амінометилбензоїл)-D-2Nаl-N-Ме-D-Рhе-NН)1-морфолінопропан,
2-(Н-Аіb-Ніs-N-Ме-D-2Nаl-N-Ме-D-Рhе-NН)-(1-метил-2-піролідиніл)етан,
2-(((3R)-піперидинкарбоніл)-N-Ме-D-2Nаl-N-Ме-D-Рhе-NН)-(1-метил-2-піролідиніл)етан,
2-((3-амінометилбензоїл)-N-Ме-D-2Nаl-Ме-D-Рhе-NН)-(1-метил-2-піролідиніл)етан,
3-(Н-Аіb-Ніs-N-Ме-D-2Nаl-N-Ме-D-Рhe-NН)-1-морфолінопропан,
3-(((3R)-піперидинкарбоніл)-N-Ме-D-2Nаl-N-Ме-D-Рhе-NН)-1-морфолінопропан,
3-((3-амінометилбензоїл)-N-Ме-D-2Nаl-N-Ме-D-Рhе-NН)-1-морфолінопропан,
2-((3-амінометилбензоїл)-D-2Nаl-N-Ме-D-Рhе-NН)-(1-метил-2-піролідиніл)етан,
2-(((3R)-піперидинкарбоніл)-D-2Nаl-N-Ме-D-Рhе-NН)-(1-метил-2-піролідиніл)етан.
2. Сполука по п.1, яка відрізняється тим, що А являє собою водень, 3-АМВ, N-Ме-3-АМВ або Aib.
3. Сполука по п.1, яка відрізняється тим, що t дорівнює 1 та u дорівнює 0, і G вибрано з групи, до якої належать 3-амінометилбензоїл, ніпекотова кислота та ізоніпекотова кислота.
4. Сполука по п.1, яка відрізняється тим, що t дорівнює 1, u дорівнює 1, G являє собою Aib, і H вибрано з групи, до якої належать His, Phe та АІа.
5. Сполука по п.1, яка відрізняється тим, що С вибрано з групи, до якої належать D-2-Nal та D-Phe.
6. Сполука по п.1, яка відрізняється тим, що якщо p дорівнює 1, D являє собою D-Phe або D-2Nal.
7. Сполука по п.1, яка відрізняється тим, що якщо p дорівнює 0, D являє собою D-Phe-NH2 або D-2Nal- NH2.
8. Сполука по п.1, яка відрізняється тим, що Е, якщо p дорівнює 1, являє собою -
NH-CH(R10)-(CH2)v-R9, де
v дорівнює 0 або цілому числу, вибраному з групи: 1,2,3,4,
R9 являє собою водень, морфоліно, піперидино, N(R11)-R12
або
,
де n дорівнює 0, 1 або 2, та R19 являє собою водень або нижчий алкіл, кожний з радикалів R11 та R12 незалежно являє собою водень або нижчий алкіл,
R10, якщо p дорівнює 1, вибрано з групи, до якої належать -H, -COOH, -CH2-R13, -CO-R13 або -СН2-ОН, де R13 являє собою піперазино, морфоліно, піперидино, -ОН або -N(R14)-R15, де кожний з радикалів R14 та R15 незалежно являє собою водень або нижчий алкіл.
9. Сполука по п.1, яка відрізняється тим, що принаймні один з амідних зв'язків між А та В, між В та С, між D та (Е)р та між Γ та H заміщується -СО-N(СН3)-.
10. Сполука, що її вибрано з групи, до якої належать
(R)-2-((3-амінометилбензоїл)-N-Ме-D-2Nаl-N-Ме)-3-фенілпропанол або його TFA-сіль;
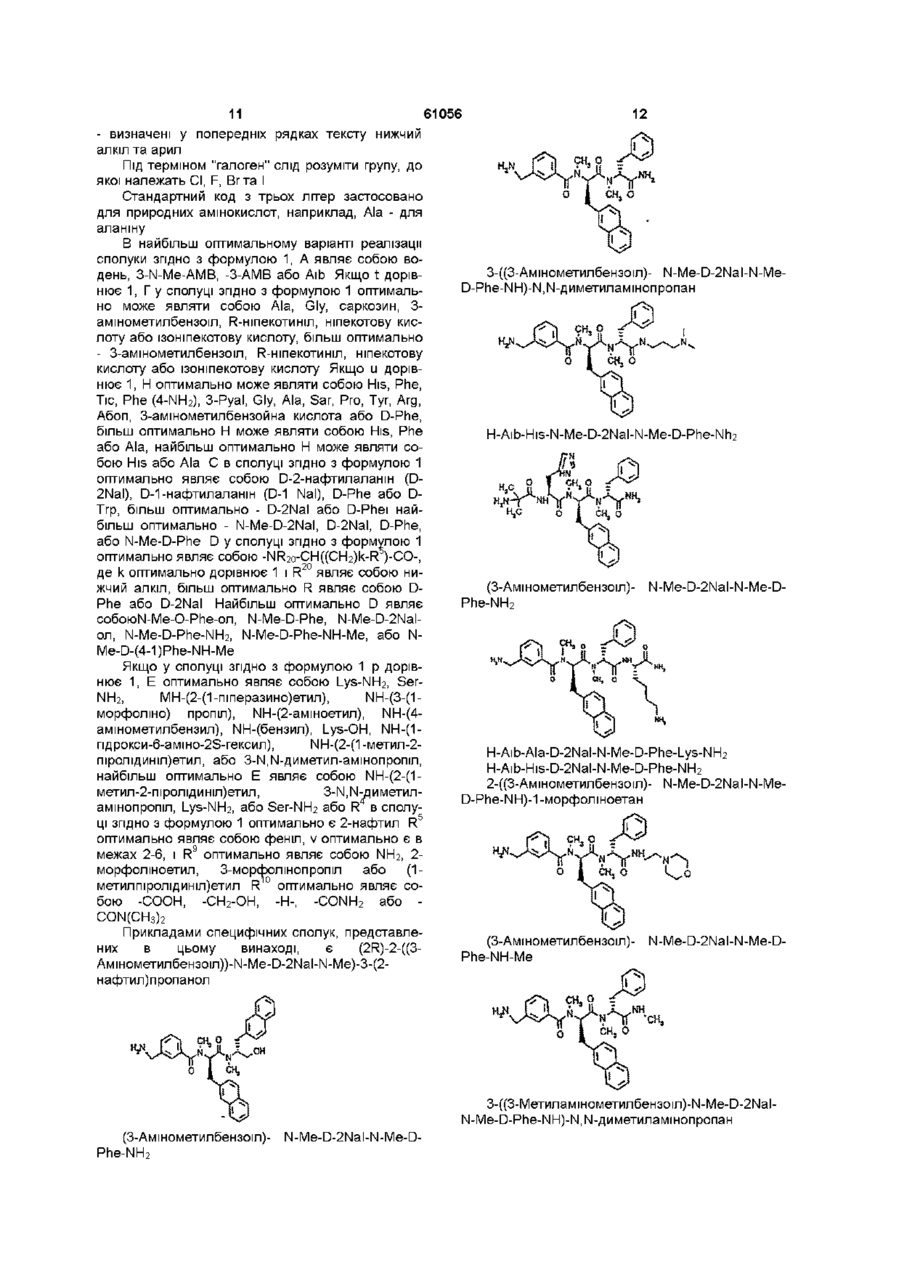
3-((3-амінометилбензоїл))N-Ме-D-2Nаl-N-Ме-D-Рhе-NН)-1 -1 Ν,Ν-диметиламінопропан або його ТFА-сіль;
3-(((3R)-3-піперидинкарбоніл)-N-Ме-D-2Nаl-N-Ме-D-Рhе-NН)-1-N,N-диметиламінопропан або його TFA-сіль;
2-(((3R)-3-піперидинкарбоніл)-N-Ме-D-2NаІ-N-Ме-D-Рhе-NН)-(1-метил-2-піролідиніл)етан або його TFA-сіль;
H-Aib-His-D-2Nal-N-Me-D-Phe-Ser-NH2 або його TFA-сіль;
(3-амінометилбензоїл)-D-2Nаl-N-Ме-D-Рhе-Lуs-NН2 або його TFA-сіль;
(4-піперидинкарбоніл)-D-2Nаl-N-Ме-D-Рhе-NН2 або його TFA-сіль;
((3R)-3-піперидинкарбоніл)-D-2Nаl-N-Ме-D-Рhе-NН2 або його TFA-сіль;
(3-амінометилбензоїл)-D-Рhе-N-Ме-D-Рhе- NH2 або його TFA-сіль;
(3-амінометилбензоїл)-N-Me-D-Phe-N-Me-D-Phe-Lys-NH2 або його TFA-сіль;
((3R)-3-пiпepидинкapбоніл)-N-Me-D-Phe-N-Me-D-Phe-Lys-NH2 або його TFA-сіль;
H-Aib-His-N-Me-D-Phe-N-Me-D-Phe-Lys-NH2 або його TFA-сіль;
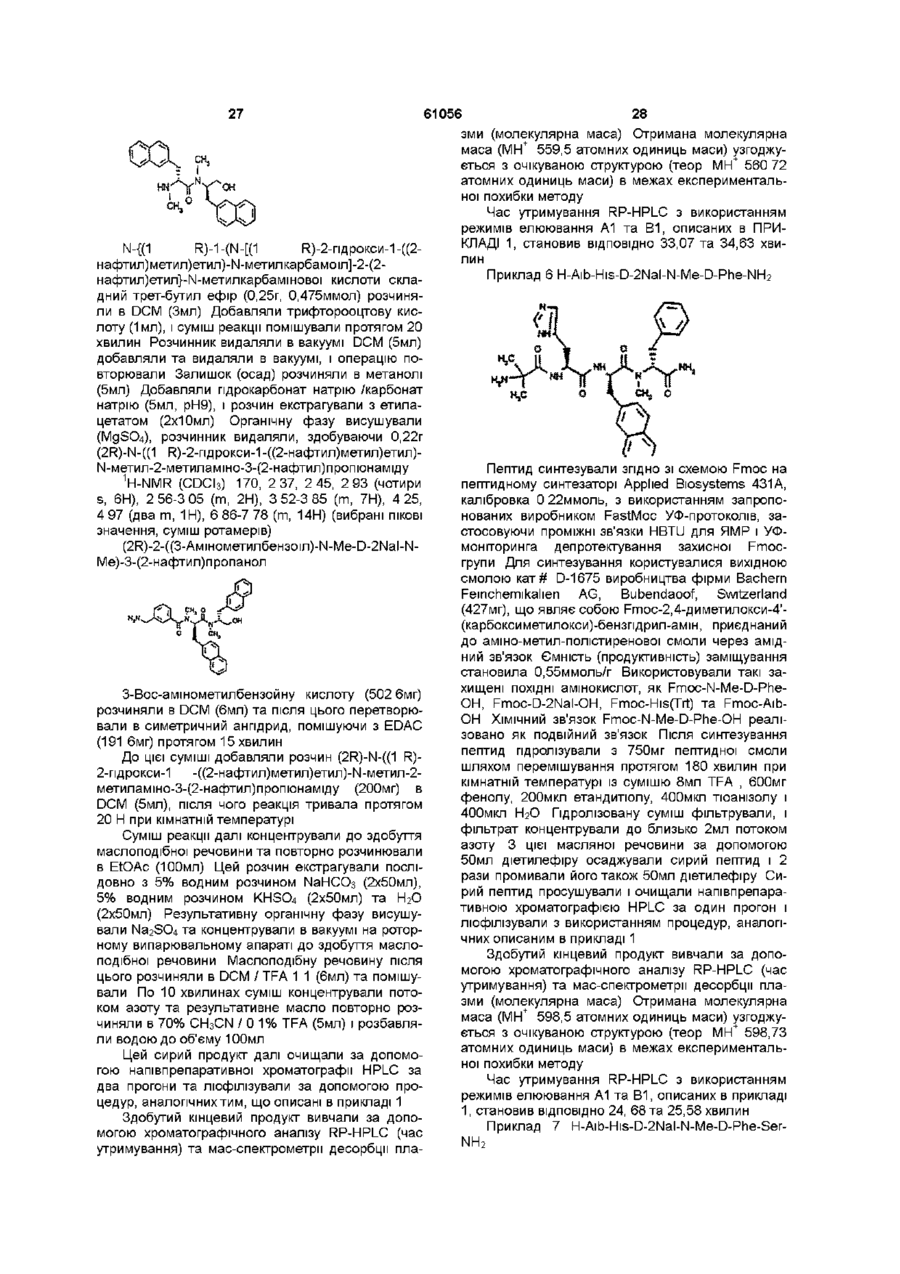
((3R)-3-пiпepидинкapбоніл)-N-Me-D-2Nal-N-Me-D-Phe-NH2 або його TFA-сіль;
(2R)-2-((3-амінометилбензоїл)-N-Ме-D-2Nаl-N-Ме)-3-(2-нафтил)пропанол або його TFA-сіль;
(3-амінометилбензоїл)-N-Ме-D-2Nаl-N-Ме-D-Рhе-NН2 або його TFA-сіль;
3-((3-амінометилбензоїл)-N-Ме-D-Рhе-NН)-1-N,N-диметиламінопропан;
H-Aib-His-N-Me-D-2Nal-N-Me-D-Phe-NH2, або його TFA-сіль;
(3-амінометилбензоїл)-N-Me-D-2Nal-N-Me-D-Phe-Lys- NH2;
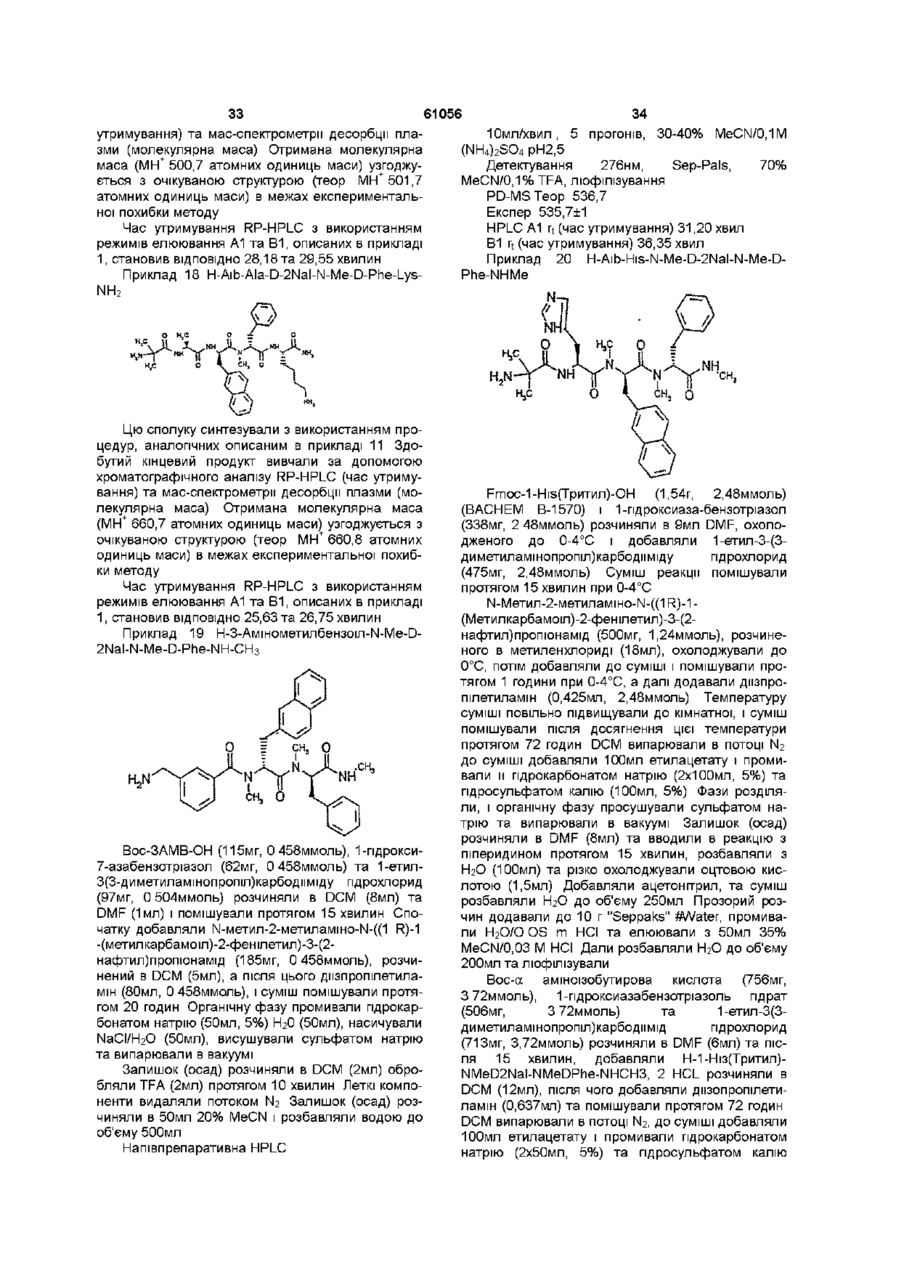
H-Aib-Ala-D-2Nal-N-Me-D-Phe-Lys-NH2, або його TFA-сіль;
H-Aib-His-D-2Nal-N-Me-D-Phe-NH2, або його TFA-сіль;
2-((3-амінометилбензоїл)-N-Ме-D-2Nаl-N-Ме-D-Рhе-NН)-1 -морфоліноетан;
(3-амінометилбензоїл)-N-Me-D-2Nal-N-Me-D-Phe-NH-Me;
3-((3-мeтиламінометилбензоїл)-N-Me-D-2Nal-N-Me-D-Phe-NH)-1-N,N-диметиламінопропан,
(3-амінометилбензоїл)-N-Me-D-2Nal-N-Me-D-Phe-N-Me2,
H-Aib-His-N-Me-D-2Nal-N-Me-D-Phe-NH2;
3-амінометилбензоїл-N-Ме-D-2Nаl-N-Ме-D-Рhе-NН-СН3 або його TFA-сіль;
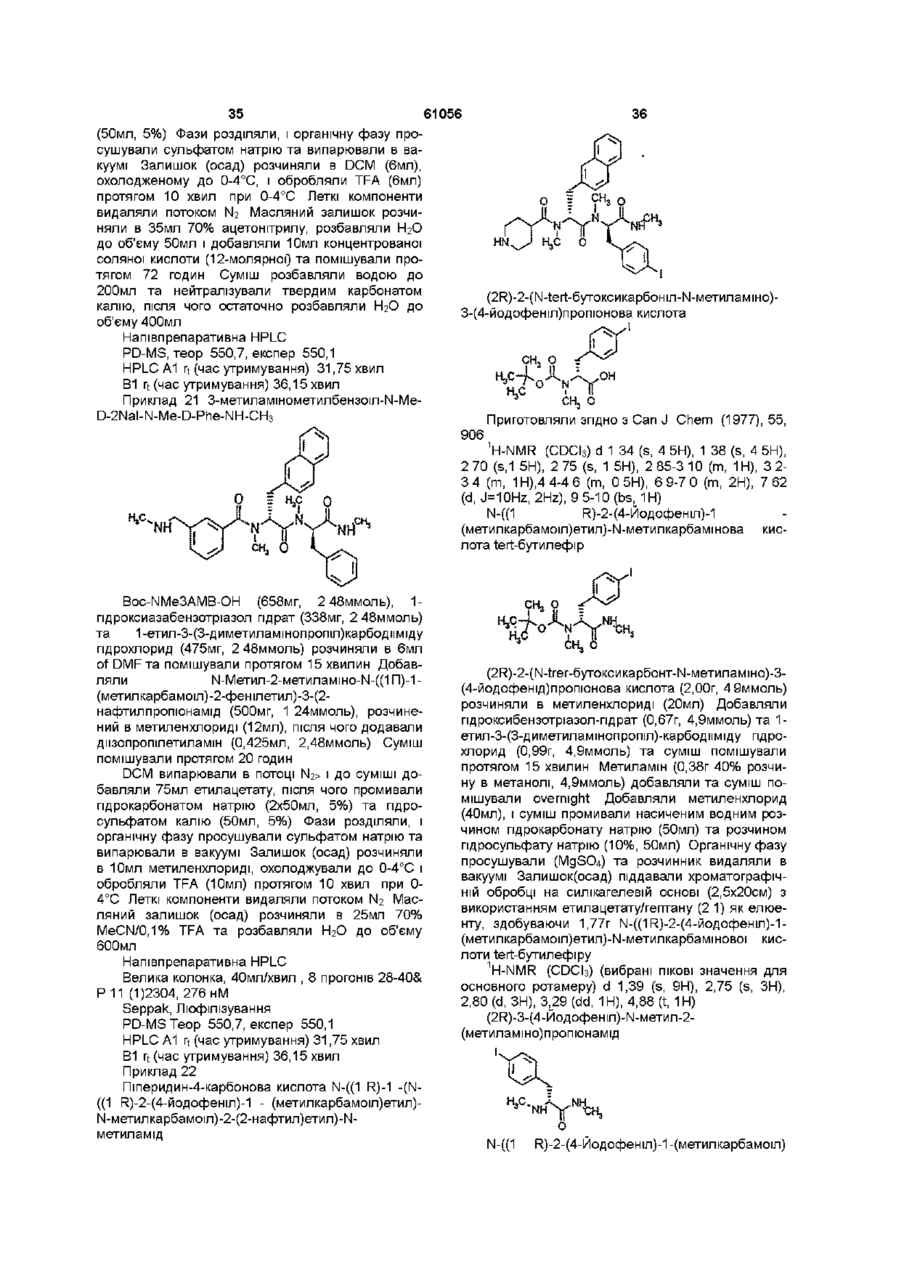
3-метиламінометилбензоїл-N-Ме-D-2Nаl-N-Ме-D-Рhе-NН-СН3 або його TFA-сіль;
H-Aib-His-N-Me-D-2Nal-N-Me-D-Phe-NHMe або його НСlсіль; та
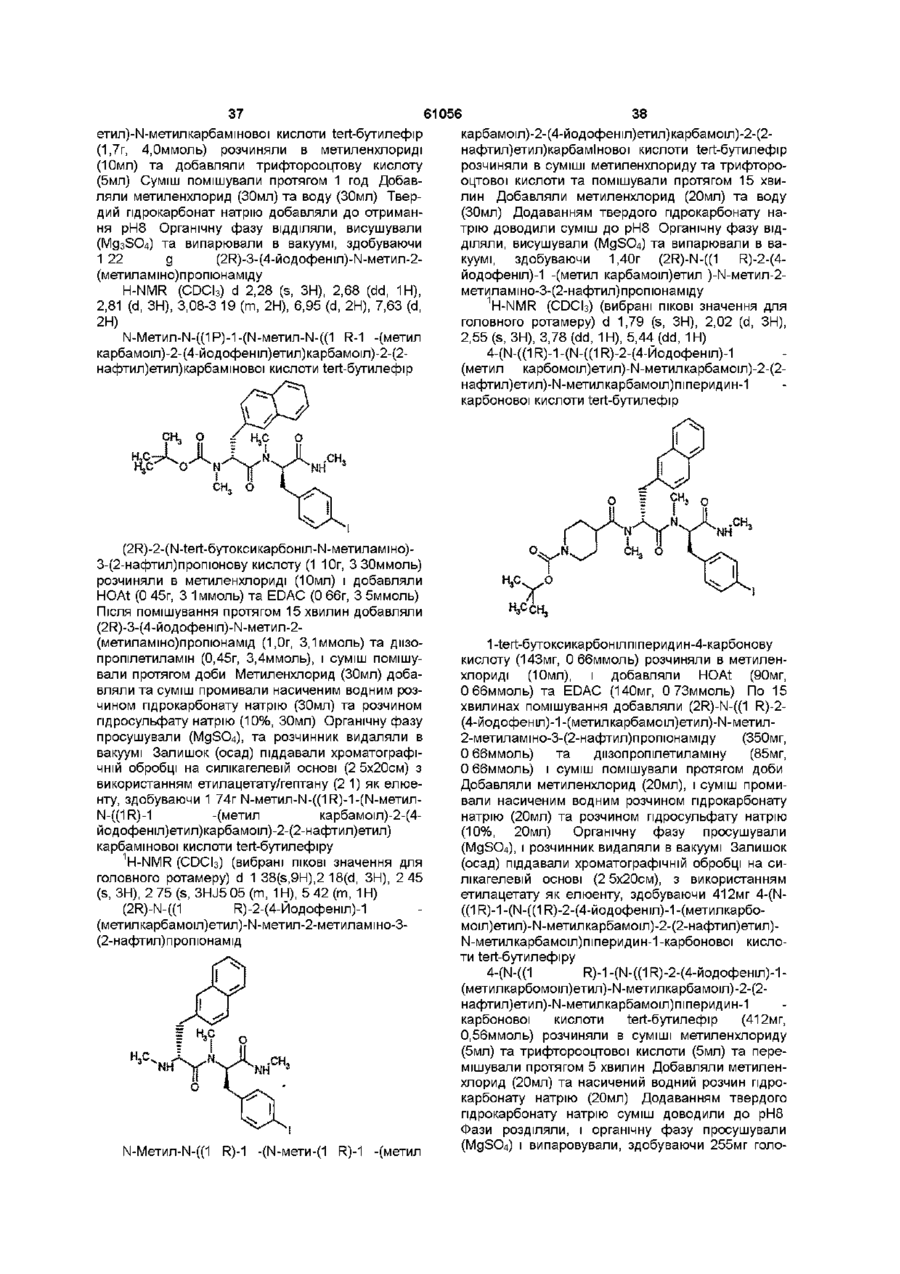
піперидин-4-карбонова кислота -N- ((1R)-1-(N-((1R)-2-(4-йодофеніл)-1-(метилкарбамоїл) етил)-N-метилкарбамоїл)-2-(2-нафтил)етил)-N-метиламід, або її фармацевтично прийнятна сіль.
11. Фармацевтична композиція, яка містить в собі як активний компонент сполуку згідно з будь-яким з пунктів від 1 до 10 або її фармацевтично прийнятну сіль, разом із фармацевтично прийнятним носієм або розріджувачем.
12. Композиція по п.11, яка відрізняється тим, що у вигляді дозованих одиниць містить в собі від близько 10 до близько 200мг головної сполуки згідно з будь-яким з пунктів від 1 до 10 або фармацевтично прийнятну сіль цієї сполуки.
13. Фармацевтична композиція для стимулювання вивільнення гормону росту з гіпофіза, що як активний компонент містить у собі сполуку згідно з будь-яким з пунктів від 1 до 10 або її фармацевтично прийнятну сіль, разом із фармацевтично прийнятним носієм або розріджувачем.
14. Фармацевтична композиція по пп. 11, 12 або 13, яка відрізняється тим, що призначена для орального, трансдермального, назального, легеневого або парентерального введення в організм.
15. Спосіб стимулювання вивільнення гормону росту з гіпофіза, що за необхідністю передбачає введення ефективного об'єму сполуки згідно з будь-яким з пунктів від 1 до 10, або її фармацевтично прийнятної солі, або композиції згідно з будь-яким з пунктів 11, 12 або 14.
16. Спосіб по п.15, який відрізняється тим, що ефективний об'єм сполуки згідно з будь-яким з пунктів від 1 до 10, або її фармацевтично прийнятної солі, або її складного ефіру, може становити від близько 0,0001 до близько 100 мг/кг ваги тіла на добу, найоптимальніше від близько 0,001 до близько 50 мг/кг ваги тіла на добу.
17. Спосіб підвищення швидкості та інтенсивності росту тварин, збільшення надою молока або продуктивності здобуття вовни зі свійських тварин, або подолання недуг, який за необхідністю передбачає введення в організм ефективного об'єму сполуки згідно з будь-яким з пунктів від 1 до 10 або її фармацевтично прийнятної солі, або композиції згідно з будь-яким з пунктів 11, 12 або 14.
18. Сполука по будь-якому з пп. від 1 до 10 або її фармацевтично прийнятна сіль, яка відрізняється тим, що застосовується як ліки.
19. Сполука по будь-якому з пп. від 1 до 10 або її фармацевтично прийнятна сіль, яка відрізняється тим, що її застосовують для виготовлення медикаменту для стимулювання вивільнення гормону росту з гіпофіза.
20. Сполука по будь-якому з пунктів від 1 до 10 або її фармацевтично прийнятна сіль, яка відрізняється тим, що її застосовують для виготовлення медикаменту, призначеного для введення в організм тварин з метою підвищення швидкості та інтенсивності їх росту, збільшення надою молока та продуктивності здобуття вовни зі свійських тварин або подолання недуг.
Текст
1 Сполука згідно з загальною формулою (1) A-B-C-D(-E)p(1) де р дорівнює 0 або 1, А являє собою водень або R1-(CH2)q-(X)r-(CH2)sСО-, де q дорівнює 0 або цілому числу, вибраному з групи 1,2,3,4,5, г дорівнює 0 або 1, s дорівнює 0 або цілому числу, вибраному з групи 1,2,3,4,5, R1 являє собою водень, імідазоліл, гуанідино, піперазино, морфоліно, піперидино або N(R )-R3, де кожний радикал R2 та R3 незалежно являє собою водень або нижчий алкіл, що як варіант заміщується однією чи кількома гідроксил-, піридиніл- або фуранілгрупами, і X, якщо г дорівнює 1, являє собою -NH-, -СЬІ2, СН=СН-, -C(R16)(R17)-, 16 17 де кожний з радикалів R та R незалежно є воднем або нижчим алкілом, В являє собою (G)t-(H)U, де кожний з tTa u незалежно дорівнює 0 або 1, G і Н являють собою амінокислотні залишки (радикали), вибрані з групи, до якої належать природні L-амшокислоти чи їх ВІДПОВІДНІ D-ізомери, або ненатуральні (штучні) амінокислоти, такі як 1,4 діамінобутирова кислота, аміноізобутирова кислота, 1,3-діамінопропюнова кислота, 4амінофенілаланін, 3-піридилаланін, 1,2,3,4тетрапдроізохінолін-3-карбонова кислота, 1,2,3,4тетрапдроноргарман-3-карбонова кислота, Nметилантранілова кислота, антранілова кислота, N-бензилгліцин, 3-амінометилбензойна кислота, 3аміно-3-метилбутанова кислота, саркозин, ніпекотова кислота або ізоніпекотова кислота, і де, коли як t, так і u дорівнюють 1, амідний зв'язок між G та Н варіативно може заміщуватись Y-NR18-, де Y є -CO- або -СН2-, і R18 являє собою водень, нижчий алкіл або нижчий аралкіл, С являє собою D-амінокислоту з формулою -NHCH((CH2)W-R4)-CO-, де w дорівнює 0, 1 або 2, і R4 вибрано з групи, до якої належать О кожний з котрих як варіант заміщується галогеном, нижчим алкілом, нижчим алкілокси, нижчим алкіламіно, аміно або гідрокси, D, якщо р дорівнює 1, являє собою D-амшокислоту з формулою -NR20-CH((CH2)k-R5)-CO- або, якщо р дорівнює 0, D являє собою -NR20-CH((CH2)i-R5)СН2- R6 або -NR20-CH((CH2)m-R5)-CR6, Де k дорівнює 0, 1 або 2, І дорівнює 0, 1 або 2, m дорівнює 0, 1 або 2, R вибрано з групи, до якої належать нижчий алкіл або нижчий аралкіл, R5 вибрано з групи, до якої належать кожний з котрих як варіант заміщується галогеном, нижчим алкілом, нижчим алкілокси, аміно або гідрокси, і R6 являє собою піперазино, морфоліно, піперидино, -ОН або -N(R7)-R , де кожний з радикалів R та R8 незалежно являє собою водень або нижчий алкіл, (О ю о (О 61056 Е, якщо p дорівнює 1, являє собою -NH-CH(R )(CH2)V- R , де v дорівнює 0 або цілому числу, вибраному з групи 1,2,3,4,5,6,7,8, 9 R являє собою водень, імідазоліл, гуанідино, пі11 12 перазино, морфоліно, піперидино, -N(R )-R , де п дорівнює 0, 1 або 2, та R день або нижчий алкіл, являє собою во де о дорівнює цілому числу, вибраному з групи 1 11 12 2, 3, кожний з радикалів R та R незалежно яв ляє собою водень або нижчий алкіл, або кожний з котрих як варіант заміщується галогеном, нижчим алкілом, нижчим алкілокси, аміно, алкіламіно, гідрокси, або продуктом перегрупування Амадорі з аміногрупи та гексапіранози або гексапіранозилгексапіранози і R10, якщо р дорівнює 1, вибрано з групи, до якої належать Н, -СООН, -CH2-R13-CO-R1^ або -СН2ОН, де R13 являє собою піперазино, морфоліно, піперидино, -ОН або -N(R14)-R15, де кожний з R14 та R незалежно являють собою водень або нижчий алкіл, всі амідні зв'язки в формулі 1, за винятком зв'язку між С та D, можуть незалежно бути заміщеними Y-N R18-, де Y являє собою -СО- або -СН2-, і R18 являє собою водень, нижчий алкіл чи нижчий аралкіл, або и фармацевтично прийнятна сіль, за винятком сполук (3-aMiHOMeTHn6eH3oin)-D-2Nal-N-Me-D-Phe-l_ysNH2, H-Aib-His-D-2Nal-N-Me-D-Phe-l_ys-NH2, H-Aib-His-N-Me-D-2Nal-N-Me-D-Phe-l_ys-NH2, 3-(H-Aib-His-D-2Nal-N-Me-D-Phe-NH)-1морфолінопропан, 2-(H-Aib-His-D-2Nal-N-Me-D-Phe-NH)-(1-Me™n-2піролідиніл)етан, ((3R)-mnepHflHHKap6oHin)-N-Me-D-2Nal-N-Me-DPhe-I_ys-NH2, 3-((3-aMiHOMe™-i6eH3our)-D-2Nal-N-Me-D-PheІ\ІН)1-морфолінопропан, 2-(H-Aib-His-N-Me-D-2Nal-N-Me-D-Phe-NH)-(1метил-2-піролідиніл)етан, 2-(((3R)-nmepHflHHKap6oHin)-N-Me-D-2Nal-N-Me-DРпе-І\ІН)-(1-метил-2-піролідиніл)етан, 2-((3-aMiHOMeTHn6eH3oin)-N-Me-D-2Nal-Me-D-PheІ\ІН)-(1-метил-2-піролідиніл)етан, 3-(H-Aib-His-N-Me-D-2Nal-N-Me-D-Phe-NH)-1морфолінопропан, 3-(((3R)-nmepHflHHKap6oHin)-N-Me-D-2Nal-N-Me-DРпе-І\ІН)-1-морфолінопропан, 3-((3-aMiHOMeTHn6eH3oin)-N-Me-D-2Nal-N-Me-DРпе-І\ІН)-1-морфолінопропан, 4 2-((3-aMiHOMeTHn6eH3oin)-D-2Nal-N-Me-D-Phe-NH)(1-метил-2-піролідиніл)етан, 2-(((3R)-nmepHflHHKap6oHin)-D-2Nal-N-Me-D-PheІ\ІН)-(1-метил-2-піролідиніл)етан 2 Сполука по п 1, яка відрізняється тим, що А являє собою водень, 3-АМВ, N-Me-3-AMB або Aib 3 Сполука по п 1 , яка відрізняється тим, що t дорівнює 1 та u дорівнює 0, і G вибрано з групи, до якої належать 3-амшометилбензоіл, ніпекотова кислота та ізоніпекотова кислота 4 Сполука по п 1 , яка відрізняється тим, що t дорівнює 1, u дорівнює 1, G являє собою Aib, і Н вибрано з групи, до якої належать His, Phe та Ala 5 Сполука по п 1, яка відрізняється тим, що С вибрано з групи, до якої належать D-2-Nal та DPhe 6 Сполука по п 1, яка відрізняється тим, що якщо р дорівнює 1, D являє собою D-Phe або D-2Nal 7 Сполука по п 1,яка відрізняється тим, що якщо р дорівнює 0, D являє собою D-Phe-NH2 або D2Nal- NH 2 8 Сполука по п 1, яка відрізняється тим, що Е, якщо р дорівнює 1, являє собою 1 9 NH-CH(R >(CH 2 ) V -R , де v дорівнює 0 або цілому числу, вибраному з групи 1,2,3,4, R9 являє собою водень, морфоліно, піперидино, N(R11)-R12 або (СН2)Г 1 Q де п дорівнює 0, 1 або 2, та R являє собою водень або нижчий алкіл, кожний з радикалів R11 та R12 незалежно являє собою водень або нижчий алкіл, 1П R , якщо р дорівнює 1, вибрано з групи, до якої належать -Н, -СООН, -CH2-R13, -CO-R13 або -СН2ОН, де R13 являє собою піперазино, морфоліно, піперидино, -ОН або -N(R )-R , де кожний з радикалів R14 та R15 незалежно являє собою водень або нижчий алкіл 9 Сполука по п 1, яка відрізняється тим, що принаймні один з амідних зв'язків між А та В, між В та С, між D та (Е)р та між Г та Н заміщується -СОN(CH3)10 Сполука, що и вибрано з групи, до якої належать (R)-2-((3-aMiHOMeTHn6eH3oin)-N-Me-D-2Nal-N-Me)3-фенілпропанол або його TFA-сіль, 3-((3-aMiHOMeTHn6eH3oin))N-Me-D-2Nal-N-Me-DPhe-NH)-1 -1 г\І,г\І-диметиламшопропан або його TFA-сіль, 3-(((3R)-3-nmepHflHHKap6oHin)-N-Me-D-2Nal-N-MeО-Рпе-г\ІН)-1-г\І,г\І-диметиламінопропан або його TFA-сіль, 2-(((3R)-3-nmepHflHHKap6oHin)-N-Me-D-2Nal-N-MeО-Рпе-І\ІН)-(1-метил-2-піролідиніл)етан або його TFA-сіль, H-Aib-His-D-2Nal-N-Me-D-Phe-Ser-NH2 або його TFA-сіль, (3-aMiHOMeTHn6eH3oin)-D-2Nal-N-Me-D-Phe-l_ysNH 2 або його TFA-сіль, 61056 12 Композиція по п 11, яка відрізняється тим, що у вигляді дозованих одиниць містить в собі від близько 10 до близько 200мг головної сполуки згідно з будь-яким з пунктів від 1 до 10 або фармацевтично прийнятну сіль цієї сполуки 13 Фармацевтична композиція для стимулювання вивільнення гормону росту з гіпофіза, що як активний компонент містить у собі сполуку згідно з будьяким з пунктів від 1 до 10 або и фармацевтично прийнятну сіль, разом із фармацевтично прийнятним носієм або розріджувачем 14 Фармацевтична композиція по пп 11, 12 або 13, яка відрізняється тим, що призначена для орального, трансдермального, назального, легеневого або парентерального введення в організм 15 Спосіб стимулювання вивільнення гормону росту з гіпофіза, що за необхідністю передбачає введення ефективного об'єму сполуки згідно з будь-яким з пунктів від 1 до 10, або и фармацевтично прийнятної солі, або композиції згідно з будь-яким з пунктів 11,12 або 14 16 Спосіб по п 15, який відрізняється тим, що ефективний об'єм сполуки згідно з будь-яким з пунктів від 1 до 10, або її фармацевтично прийнятної солі, або її складного ефіру, може становити від близько 0,0001 до близько 100 мг/кг ваги тіла на добу, найоптимальніше від близько 0,001 до близько 50 мг/кг ваги тіла на добу СІЛЬ, 2-((3-aMiHOMeTHn6eH3oin)-N-Me-D-2Nal-N-Me-D17 Спосіб підвищення швидкості та інтенсивності Phe-NH)-1 -морфоліноетан, росту тварин, збільшення надою молока або про(3-aMiHOMeTHn6eH3oin)-N-Me-D-2Nal-N-Me-D-Pheдуктивності здобуття вовни зі свійських тварин, NH-Me, або подолання недуг, який за необхідністю передбачає введення в організм ефективного об'єму 3-((3-метиламшометилбензоіл)-г\І-Ме-О-2МаІ-г\І-Месполуки згідно з будь-яким з пунктів від 1 до 10 або О-Рпе-г\ІН)-1-г\І,г\І-диметиламінопропан, и фармацевтично прийнятної солі, або композиції (3-aMiHOMeTHn6eH3oin)-N-Me-D-2Nal-N-Me-D-Pheзгідно з будь-яким з пунктів 11,12 або 14 N-Me2, H-Aib-His-N-Me-D-2Nal-N-Me-D-Phe-NH2, 18 Сполука по будь-якому з пп від 1 до 10 або и 3-aMiHOMeTHn6eH3oin-N-Me-D-2Nal-N-Me-D-Pheфармацевтично прийнятна сіль, яка відрізняєтьNH-CH3 або його TFA-сіль, ся тим, що застосовується як ліки 3-MeTHnaMiHOMeTHn6eH3oin-N-Me-D-2Nal-N-Me-D19 Сполука по будь-якому з пп від 1 до 10 або и Phe-NH-СНз або його TFA-сіль, фармацевтично прийнятна сіль, яка відрізняєтьH-Aib-His-N-Me-D-2Nal-N-Me-D-Phe-NHMe або його ся тим, що и застосовують для виготовлення меНСІсіль, та дикаменту для стимулювання вивільнення гормону росту з гіпофіза піперидин-4-карбонова кислота -N- ((1 R)-1 -(N((1 R)-2-(4-йoдoфeнlл)-1 -(метилкарбамоїл) етил)-ІЧ20 Сполука по будь-якому з пунктів від 1 до 10 або метилкарбамоіл)-2-(2-нафтил)етил)-І\І-метиламід, и фармацевтично прийнятна сіль, яка відрізняабо и фармацевтично прийнятна сіль ється тим, що и застосовують для виготовлення 11 Фармацевтична композиція, яка містить в собі медикаменту, призначеного для введення в оргаяк активний компонент сполуку згідно з будь-яким нізм тварин з метою підвищення швидкості та інз пунктів від 1 до 10 або її фармацевтично прийнятенсивності їх росту, збільшення надою молока та тну сіль, разом із фармацевтично прийнятним нопродуктивності здобуття вовни зі свійських тварин сієм або розріджувачем або подолання недуг (4-ninepHflHHKap6oHin)-D-2Nal-N-Me-D-Phe-NH2 або його TFA-сіль, ((3R)-3-mnepHflHHKap6oHin)-D-2Nal-N-Me-D-PheNH2 або його TFA-сіль, (З-амінометилбензоіл)-О-Рпе-М-Ме-О-РпеNH2 або його TFA-сіль, (3-aMiHOMeTHn6eH3oin)-N-Me-D-Phe-N-Me-D-PheLys-NH2 або його TFA-сіль, ((3R)-3-nmepHflHHKap6oHin)-N-Me-D-Phe-N-Me-DPhe-Lys-NH2 або його TFA-сіль, H-Aib-His-N-Me-D-Phe-N-Me-D-Phe-Lys-NH2 або його TFA-сіль, ((3R)-3-nmepHflHHKap6oHin)-N-Me-D-2Nal-N-Me-DPhe-NH2 або його TFA-сіль, (2R)-2-((3-aMiHOMeTHn6eH3oin)-N-Me-D-2Nal-N-Me)3-(2-нафтил)пропанол або його TFA-сіль, (3-aMiHOMeTHn6eH3oin)-N-Me-D-2Nal-N-Me-D-PheNH2 або його TFA-сіль, 3-((3-aMiHOMeTHn6eH3oin)-N-Me-D-Phe-NH)-1-N,Nдиметиламшопропан, H-Aib-His-N-Me-D-2Nal-N-Me-D-Phe-NH2, або його TFA-сіль, (3-aMiHOMeTHn6eH3oin)-N-Me-D-2Nal-N-Me-D-PheLys- NH2, H-Aib-Ala-D-2Nal-N-Me-D-Phe-Lys-NH2, або його TFA-сіль, H-Aib-His-D-2Nal-N-Me-D-Phe-NH2, або його TFA Цей винахід стосується нових похідних пептидів, композицій, що їх вміщують, а також їх медичного застосування для лікування розладів, які є наслідком дефіциту гормонів росту Гормон росту являє собою такий гормон, який стимулює рост усіх тканин організму, які здатні рости Крім того, відомо, що гормон росту справляє певний вплив на процеси обміну речовин, зокрема, сприяє стимулюванню синтезу протеїнів та мобілізуванню вільних жирних кислот, і що він спричиняє зміну напрямку енергетичного обміну від обміну вуглеводу до обміну жирних кислот Дефіцит гормону росту може призвести до деяких тяжких розладів, таких як, наприклад, карликовості Гормон росту вивільнюється з гіпофіза Виділення відбувається під чітким безпосереднім або опосередкованим контролем певних гормонів та 61056 нейротрансміттерів Виділення гормону росту може стимулюватися так званим рилізинг-гормоном виділення гормону росту (GHRH) та інгібуватися соматостатином В обох випадках ці гормони виділяються з гіпоталамуса, але їхня дія опосередкована перше через специфічні рецептори, які розміщені в гіпофізі ВІДОМІ також і описані деякі ІНШІ сполуки, що стимулюють виділення гормону росту Наприклад, такі сполуки, як аргінін, L-3,4дипдроксифеніл (L-Dopa), глюкагон, вазопресин, РАСАР (пептид, що активує аденіліл-циклазу гіпофіза), агоністи мускаринових рецепторів, а також синтетичний гексапептид, GHRP (рилізинг-пептид гормону росту), сприяють виділенню ендогенного гормону росту, чи безпосередньо впливаючи на гіпофіз, чи впливаючи на виділення GHRP і/або соматостатину з гіпоталамусу У випадках розладів або за таких обставин, коли потрібно підвищити рівень гормону росту, протеїнова природа цих гормонів змушує застосовувати парентеральнеіх введення в організм Крім того, деякі природні підсилювачі секреції прямої дії, такі як GHRH та РАСАР, є пептидами з високою молекулярною масою, через що також віддається перевага парентеральному введенню Використання більш коротких пептидів з метою підвищення рівня гормону росту в організмі ссавців було запропоновано раніше у ЕР 18 072, ЕР 83 864, WO 89/07110, WO 89/10933, WO 88/9780, WO 83/02272, WO 91/18016, WO 92/01711 та WO 93/04081 Структура рилізинг-пептид їв гормону росту або похідних цих пептидів є важливим чинником ефективності їхнього впливу на виділення гормонів росту, так само, як і їхньої біологічної доступності Отже, предметом цього винаходу є нові пептиди з властивостями рилізинг-фактора гормонів росту, більш досконалі порівняно до нині відомих пептидів цього типу Сполука, що має загальну формулу 1 A-B-C-D( E)p 1 де р є 0 або 1, А являє собою водень або R1-(CH2)q-(X)r(Ch2)s-CO-, де q є 0 або цілим числом, вибраним з групи 1, 2, З, 4, 5, г є 0 або 1, s є 0 або цілим числом, вибраним з групи 1, 2, З, 4, 5, R1 являє собою водень, імідазоліл, гуанідинегрупу, піперазино-групу, морфоліно-групу, піперидино-групу або N(R )-R3, де кожний з радикалів R2 та R3 є незалежно воднем або нижчим алкілом, що, як варіант, заміщуються однією чи кількома гідроксил-, піридинил-, або фураніл-групами, а також X, коли г є 1, являє собою -NH-, -СН2, СН=СН-, -C(R16)(R17)-, де кожний з радикалів R16 та R17 є незалежно воднем або нижчим алкілом, В являє собою (l~)t(H)u, де як t, так u є незалежно 0 або 1, Г і Н являють собою амінокислотні залишки 8 (радикали), вибрані з групи, до якої належать природні L-амшокислоти чи ВІДПОВІДНІ ДО НИХ Dізомери, або штучні амінокислоти, такі як 1,4діамінобутирова кислота, аміно-ізобутирова кислота, 1,3-діамшопропюнова кислота, 4амінофенілаланінова, 3-піридилаланінова, 1,2,3,4тетрапдроізохінолшова кислота, 1,2,3,4тетрапдроноргарман-3-карбонова кислота, Nметилантранілова кислота, антранілова кислота, N-бензилгліцинова, 3-амінометил бензойна кислота, З-аміно-3-метил-бутанова, саркозин, ніпекотова кислота або ізо-ніпекотова кислота, коли я к і , так і u дорівнюють 1, амідний зв'язок між Г і Н, як варіант, замінюється радикалом -Y18 18 NR -, де Y являє собою -СО- або -СН2-, a R являє собою водень, нижчий алкіл або нижчий аралкіл, С являє собою D-амшокислоту, що має формулу -NH-CH((CH2)W-R4)-CO-, де w e 0, 1 або 2, і R4 вибрано з групи, до якої належать з. кожна з яких варіативне» заміщується галогеном, нижчим алкілом, нижчим алкілокси, нижчим апкіламшо, аміно або гідрокси, D, коли р є 1, являє собою D-амшокислоту, що має формулу -NR20-CH((CH2)k-R5)-COабо, коли р є О, D являє собою -NR20CH((CH2),-R5)-CH2-R6 чи -NR20-CH((CH2)m-R5)-CO-R6, де к є 0,1 або 2, І є 0,1 або 2, m є 0,1 або 2, R вибрано з групи, до якої належать нижчий алкіл або нижчий аралкіл, R5 вибрано з групи, до якої належать кожна з яких варіативне заміщується галогеном, нижчим алкілом, нижчим алкілокси, аміно або гідрокси, також R6 являє собою піперазино, морфоліно, піперидино -ОН або N(R7)- R8, де кожний з радикалів R7Ta R є незалежно воднем або нижчим алкілом, 1П Е, коли р є 1, являє собою -NH-CH-( R )(CH2)V-R9, де v є 0 або цілим числом, яке вибрано з групи чисел 1, 2, 3, 4, 5, 6, 7, 8, R9 є воднем, імідазолілом, гуанідино, піперазино, морфоліно, піперидино, -N(R11)- R12, де п є 0, 1 або 2, і R алкілом, є воднем або нижчим 61056 10 ном (-CH2NH-), і/або в комбінації з перетвореннями на N- чи С-КІНЦІ пептидного ланцюга Підвищена (СН 2 )—N біологічна доступність пептидних похідних, запроабо понованих у цьому винаході, у порівнянні з доступністю пептидів, які було запропоновано у попереде о є цілим числом, вибраним з групи 1, 2, З, дніх виданнях спеціальної літератури, є, очевидно, 11 12 кожний з радикалів R та R є незалежно вот; наслідком їхньої СТІЙКОСТІ ДО протеолітичного розднем чи нижчим алкілом, або щеплення у сукупності з малими розмірами [молекул - прим, перекл ] У наведених вище формулах та далі у тексті цього документа спеціальним термінам відповідають такі визначення кожна з яких варіативне заміщується галогеСкладовими молекул, які у попередніх рядках ном, нижчим алкілом, нижчим алкілокси, зміно, цього тексту визначено терміном "нижчі алкіли", алкіламшо, гідрокси, або продуктом перегрупуванслід вважати такі алкільні складові, що містять ня Амадорі з аміногрупи та гексапіранози чи гексапереважно 1-6 атомів вуглецю, мають певну довпіранозил-гексапіранози жину і пряму (лінійну), розгалужену або циклічну і 1П конфігурацію ланцюгів Прикладами прямоланцюR , коли р є 1, вибрано з групи, до якої налегових (ЛІНІЙНИХ) алкілів є метил, етил, пропіл, бу13 13 жать -Н, -СООН, -CH 2 -R , -CO- R або -СН 2 -ОН, тил і гексил Прикладами алкілів з розгалуженим Д Є із ланцюгом є ізопропіл, втор-бутил, трет-бутил, ізоR являє собою піперазино, морфоліно, піпепентил та ізогексил Прикладами циклічних алкілів 14 15 ридино, -ОН або -N(R )- R , і де кожний з радикає циклопропіл, циклобутил, циклопентил та цикло14 15 лів R та R є незалежно воднем або нижчим гексил алкілом, Складовими молекул, які у попередніх рядках всі амідні зв'язки всередині формули 1, за вицього тексту визначено терміном "нижчі алкокси", нятком зв'язку між С та D, можуть незалежно бути слід вважати такі алкокси-складові, що містять заміщеними радикалом -Y-NR 8-, де Y являє сопереважно 1-6 атомів вуглецю, мають певну дов1S бою -СО- чи -СН2-, a R являє собою водень, нижину і пряму, розгалужену або циклічну конфігуражчий алкіл або нижчий аралкіл, або фармацевтичцію ланцюгів Прикладами прямоланцюгових алконе прийнятною ВІДПОВІДНОЮ сіллю, кси є метокси, етокси, пропокси, бутокси, пентокси також, за винятком сполук та гексокси Прикладами алкокси з розгалуженим (3-AMiHOMe™-i6eH3our)-D-2Nal-N-Me-D-Pheланцюгом є ізопропокси, втор-бутокси, третLys-NH2 бутокси, ізопентокси та ізогексокси Прикладами H-Aib-His-D-2Nal-N-Me-D-Phe-l_ys-Nh2 циклічних алкокси є циклопропілокси, циклобутиH-Aib-His-N-Me-D-2Nal-N-Me-D-Phe-l_ys-NH2 локси, циклопентилокси та циклогексилокси 3-(H-Aib-His-D-2Nal-N-Me-D-Phe-NH)-1Складовими молекул, які у попередніх рядках морфолінопропан цього тексту визначено терміном "нижчі алкіламі2-(H-Aib-His-D-2Nal-N-Me-D-Phe-NH)-2-(1но", слід вважати такі алкіламшо-складові, що місметил-2-піролідиніл)етан тять переважно 1-6 атомів вуглецю, мають певну ((3R)-nmepHflHHKap6oHin)-N-Me-D-2Nal-N-Meдовжину і пряму, розгалужену або циклічну конфіD-Phe-I_ys-NH2 гурацію ланцюгів Прикладами прямоланцюгових 3-((3-AMiHOMe™-i6eH3our)-D-2Nal-N-Me-D-Pheалкіламшо є метиламіне, етиламшо, пропіламіно, І\ІН)-1-морфолінопропан бутиламшо, пентиламшо та гексиламіно Прикла2-(H-Aib-His-N-Me-D-2Nal-N-Me-D-Phe-NH)-1дами алкіламіно з розгалуженим ланцюгом є ізо(1-метил-2-піролідиніл)етан пропіламіно, втор-бутиламшо, трет-бутиламшо, 2-(((3R)-ninepHflHHKap6oHin)N-Me-D-2Nal-Nізопентиламшо та ізогексиламшо Прикладами Me-D-Phe-NH)-1-(1-MeTHn-2- піролідиніл)етан циклічних алкіламшо є циклопропіламшо, циклобу2-((3-Амшометилбензоіл)- N-Me-D-2Nal-N-Meтиламшо, циклопентиламшота циклогексиламшо D-Phe-NH)-1-(1-vtndk-2-mponiflHHin)eTaH 3-(H-Aib-His-N-Me-D-2Nal-N-Me-D-Phe-NH)-1В контексті цього винаходу під терміном "арил" морфолінопропан слід розуміти об'єднану назву ароматичних кілець, таких як карбоциклічні та гетероциклічні аромати3-(((3R)-nmepHflHHKap6oHin)-N-Me-D-2Nal-Nчні кільця, вибрані з групи, до якої належать феніл, Ме-О-Рпе-І\ІН)-1-морфолінопропан нафтил, піридил, 1-Н-тетразол-5-іл, тіазол, іміда3((3-AMiHOMeTHn6eH3oin)-N-Me-D-2Nal-N-Me-Dзоліл, шдоліл, піримідиніл, тіадіазоліл, піразоліл, Рпе-г\ІН)-1-морфолшопропан оксазоліл, ізоксазоліл, тюфеніл, хшолшіл, пірази2-((3-AMiHOMeTHn6eH3oin)-D-2Nal-N-Me-D-Pheніл або ізотіазоліл, що варіативно заміщується І\ІН)-1-(1-метил-2- піролідиніл)етан однім чи кількома радикалами Сі є-алкілу, Сі є2-(((3R)nmepHflHHKap6oHin)-D-2Nal-N-Me-Dапкокси, галогену, амшо чи арилу Арил переважРпе-І\ІН)-1-(1-метил-2- піролідиніл)етан но представлений фенілом, тіенілом, імідазолілом, Пептидним похідним, які відповідають формулі піридилом, шдолілом, ХІНОЛІНОМ або нафтилом, що 1, притаманна підвищена СТІЙКІСТЬ ДО протеолітичваріативно заміщується галогеном, амшо, гідрокси, ного розщеплення ферментами, що обумовлено Сі 6-алкілом чи Сі є-апкокси присутністю у пептидному ряді (ПОСЛІДОВНОСТІ) суміжних D-амшокислот, варіативно, у комбінації із Складовими молекул, які у попередніх рядкзх заміщенням амідного зв'язку (-CONH-) зв'язком -Yцього тексту визначено терміном "аралкіл", слід NR18-, згаданим вище, наприклад, амінометилевважати такі, що містять у свою чергу - як складові 11 61056 12 - визначені у попередніх рядках тексту нижчий алкіл та арил Під терміном "галоген" слід розуміти групу, до якої належать СІ, F, Вгта І Стандартний код з трьох літер застосовано для природних амінокислот, наприклад, Ala - для аланіну В найбільш оптимальному варіанті реалізації сполуки згідно з формулою 1, А являє собою во3-((3-Амшометилбензоіл)- N-Me-D-2Nal-N-Meдень, З-N-Me-AMB, -3-АМВ або Aib Якщо t дорівD-Phe-NH)-N,N-flHMeTnnaMiHonponaH нює 1, Г у сполуці згідно з формулою 1 оптимально може являти собою Ala, Gly, саркозин, 3амінометилбензоїл, R-ніпекотиніл, ніпекотову кислоту або ізоніпекотову кислоту, більш оптимально - 3-амшометилбензоіл, R-ніпекотиніл, ніпекотову кислоту або ізоніпекотову кислоту Якщо u дорівнює 1, Н оптимально може являти собою His, Phe, Tic, Phe (4-NH2), 3-Pyal, Gly, Ala, Sar, Pro, Tyr, Arg, Абоп, 3-амінометилбензойна кислота або D-Phe, більш оптимально Н може являти собою His, Phe H-Aib-His-N-Me-D-2Nal-N-Me-D-Phe-Nh2 або Ala, найбільш оптимально Н може являти собою His або Ala С в сполуці згідно з формулою 1 оптимально являє собою D-2-нафтилаланш (D2Nal), D-1-нафтилаланш (D-1 Nal), D-Phe або DТгр, більш оптимально - D-2Nal або D-Phei найбільш оптимально - N-Me-D-2Nal, D-2Nal, D-Phe, або N-Me-D-Phe D у сполуці згідно з формулою 1 оптимально являє собою -NR2o-CH((CH2)k-R )-CO-, де k оптимально дорівнює 1 і R20 являє собою нижчий алкіл, більш оптимально R являє собою D(3-Амінометилбензоіл)- N-Me-D-2Nal-N-Me-DPhe або D-2Nal Найбільш оптимально D являє Phe-NH2 co6otoN-Me-O-Phe-on, N-Me-D-Phe, N-Me-D-2Nalол, N-Me-D-Phe-NH2, N-Me-D-Phe-NH-Me, або NMe-D-(4-1)Phe-NH-Me Якщо у сполуці згідно з формулою 1 р дорівнює 1, Е оптимально являє собою Lys-NH2, SerNH2, МН-(2-(1-піперазино)етил), NH-(3-(1морфоліно) пропіл), І\ІН-(2-аміноетил), NH-(4амінометилбензил), І\ІН-(бензил), Lys-OH, NH-(1пдрокси-6-аміно-23-гексил), І\ІН-(2-(1-метил-2піролідиніл)етил, або 3-г\І,г\І-диметил-амінопропіл, найбільш оптимально Е являє собою NH-(2-(1метил-2-піролідиніл)етил, 3-г\І,І\І-диметиламінопропіл, Lys-NH2, або Ser-NH2 або R4 в сполу5 ці згідно з формулою 1 оптимально є 2-нафтил R оптимально являє собою феніл, v оптимально є в межах 2-6, і R9 оптимально являє собою NH2, 2морфоліноетил, 3-морфолінопропіл або (1метилпіролідиніл)етил R ° оптимально являє собою -СООН, -СН2-ОН, -Н-, -CONH2 або CON(CH3)2 Прикладами специфічних сполук, представлених в цьому винаході, є (2R)-2-((3Амінометилбензоіл))-І\І-Ме-О-2І\ІаІ-І\І-Ме)-3-(2нафтил)пропанол N, H H-Aib-Ala-D-2Nal-N-Me-D-Phe-Lys-NH2 H-Aib-His-D-2Nal-N-Me-D-Phe-NH2 2-((3-Амшометилбензоіл)- N-Me-D-2Nal-N-MeD-Phe-NH)-1-мopфoлlнoeтaн (З-Амінометилбензоїл)Phe-NH-Me N-Me-D-2Nal-N-Me-D 3-((3-Метиламінометилбензоіл)-М-Ме-О-2МаІN-Me-D-Phe-NH)-N,N-flHMeTnnaMiHonponaH (З-Амінометилбензоїл)Phe-NH2 N-Me-D-2Nal-N-Me-D 13 61056 14 Скорочення, яке використано для позначення заміщення пептидного зв'язку " -Н-Ме H о сн. (3-AMiHOMe™-i6eH3our)-N-Me-D-2Nal-N-Me-DPhe-NH2 H-Aib-His-N-Me-D-2Nal-N-Me-D-Phe-NHMe НА сн3 о 3-MeTHnaMiHOMeTHn-Nme-D-2Nal-Nme-D-PheNH-СНз Піперидин-4-карбонова кислота-ІЧ-((1 R)-1 -(N((1 Р)-2-(4-йодофеніл)1 -(метил карбамоіл)етил)-І\Іметилкарбамоіл)-2-(2-нафтил)етил)-М-метиламід Структури залишків ненатуральних (штучних) амінокислот 0 2Ш к Сполуки згідно з формулою 1 можна виготовити традиційними способами, що полягають у розчинному або твердофазовому синтезі пептидів Для прикладу, твердофазовий синтез може головним чином здійснюватися за схемою, яку описано Stewart (час утримування) і Young, Solid Phase Peptide Synthesis, 2nd Ed , Rockпpoтягoмd, Illinois, USA, 1976 Приклади здійснення розчинного синтезу пептидів наведені у Bodansky et al , Peptide Synthesis, 2nd , Ed , NewYa6ok, USA, 1976 У якості заміщувача амідного зв'язку згідно з методом, який описано у Y Sasaki і D Н Coy, Peptides 3(1), 1987, рр 119-121 , можна застосовувати амінометилен Пептидні ПОХІДНІ, ЯКІ МІСТЯТЬ дериватизовану моно- або ди-гексапіранозою аміногрупу, можна приготувати шляхом перегрупування Амадорі, головним чином способом, який описано R Albert (час утримування) et al , Life Sciences 53, 1993, рр 517-525 Прикладами моно- або дигексапіранозє глюкоза, галактоза, мальтоза, лактоза або целобіоза ПОХІДНІ, ЩО застосовуються у синтезі як ВИХІДНІ матеріали, або можна отримати промисловим шляхом, при необхідності забезпечуючи їх ВІДПОВІДНИМИ захисними групами, або такі стартові матеріали, що використовуються для виготовлення складової "А" у загальній формулі 1, можна приготувати добре відомими способами та при необхідності само по собі забезпечити захистом Скорочення, які використано для позначення захисних груп сГ До фармацевтичне прийнятних солей кислотних присадок у сполуках згідно з формулою 1 належать такі, що їх виготовлюють шляхом реакції пептиду з неорганічною або органічною кислотою, наприклад, з хлористоводневою [соляною], бромистоводневою, сірчаною, оцтовою, фосфорною, молочною, малеїновою, фталевою, лимонною, глутаровою, глюконовою, метансульфоновою, саліциловою, бурштиновою, винною, щавлевою, толуолсульфоновою, трифтороцтовою, сульфаміновоюта фумаровою кислотою В іншому аспекті цей винахід стосується фармацевтичної композиції, що містить в собі - як активний компонент - сполуку згідно з загальною формулою 1 або м фармацевтичне сприйнятну сіль, разом із фармацевтичне сприинятним носієм або розріджувачем Фармацевтичні композиції, що містять в собі 16 15 61056 сполуку згідно з цим винаходом, можна приготуваабо такі консерванти, якпарабени ти за допомогою стандартної методики, яку описаДля введення через шкіру препарат може бути но, наприклад, у Remington's Pharmaceutical Sciвиготовлений у вигляді, придатному для застосуences, 1985 Ці КОМПОЗИЦІЇ можуть з'являтися у вання його за допомогою пластирів або електропродажі також у стандартних формах, наприклад, форезу у вигляді капсул, таблеток, аерозолів, суспензій, Зазвичай сполуки згідно цього винаходу розпластирів або засобів місцевого застосування фасовуваються в дозованих одиницях, що містять 0,0001-ЮОмг активного компоненту, разом із фарФармацевтичний носій або розріджувач, що мацевтично-прийнятною КІЛЬКІСТЮ носію на дозозастосовується згідно з цим винаходом, можуть вану одиницю являти собою стандартний твердий або рідкий носій Прикладами твердих носив є лактоза, терра Дозування сполук згідно цього винаходу оптиальба, сахароза (цукроза), циклодекстрин, тальк, мально становить 1-500мг/добу, наприклад, ближелатин, агар, пектин, акація, стеарат магнію, стезько ЮОмг в одній дозі, якщо вони вводяться паціаринова кислота або нижчі алкілові ефіри целюлоєнтам, наприклад людям, як ліки зи Прикладами рідких носив є сироп, аріхісова Показано, що сполуки згідно з загальною фоолія, маслинова олія, фосфоліпіди, жирні кислоти, рмулою 1 здатні сприяти вивільнюванню ендогенжирнокислотні аміни, полюксиетилен та вода ного гормону росту in vivo Таким чином, ці сполуки можуть бути використаними для лікування органіАналогічно, до носив або розріджувачів може зму за таких обставин, коли є потреба у зростанні належати будь-яка з відомих у галузі речовин трирівнів гормону росту у плазмі, а саме тоді, коли валого вивільнення, таких як, наприклад, гліцерил спостерігається дефіцит гормону росту в організмі моностеарат, гліцерил дистеарат, у вільному (нелюдини, у випадку лікування пацієнтів похилого зв'язаному) вигляді чи у суміші із парафіном віку, а також у випадку лікування свійської худоби Якщо для орального введення використовується твердий носій, препарат може бути вигоОтже, в конкретному аспекті цей винахід стотовлений у формі таблеток, уміщений у жорсткі сується фармацевтичної композиції, призначенної желатинові капсули у порошко- чи гранудля стимулювання, вивільнювання гормону росту з лоподібному вигляді або виготовлений у формі гіпофіза Ця композиція містить у своєму складі як пастилок та ромбиків Вагова КІЛЬКІСТЬ твердого активний компонент сполуку згідно з формулою 1 носія може змінюватись в широкому діапазоні, але або фармацевтично прийнятну сіль цієї сполуки зазвичай вона становить від 25мг до 1 г разом із фармацевтично прийнятним носієм чи розріджувачем Типова таблетка, виготовлена стандартним способом, може мати у своєму складі такі компоВ іншому аспекті, цей винахід стосується мененти тоду стимулювання вивільнювання гормону росту з гіпофіза, цей метод полягає у введенні об'єкту, Ядро що потребує такого введення, ефективного об'єму Активна сполука (як незв'язана ЮОмг сполуки згідно з загальною формулою 1 або фарсполука, так і м сіль) мацевтично прийнятної солі цієї сполуки Колоїдальний кремнієвий дюк1,5мг сид (Aerosil) В іще одному аспекті цей винахід стосується використання сполуки згідно з загальноюформуЦелюлоза, мікрокрист (Avicel) 70мг лою 1 або м фармацевтично прийнятної солі для Модифікована целюлозна смо7,5мг виготовлення медикаменту, призначенного для ла (Ac-Di-Sol) стимулювання вивільнювання гормону росту з гіСтеарат магнію пофіза Оболонка Гід роксипропіл метил целюлоза 9,0мг Сполуки згідно з формулою 1 мають важливі фармакологічні властивості Прикладом таких (НРМС), близько властивостей є стимулювання вивільнювання гор*Mywacett 9-40 Т, близько 0,9мг мону росту з гіпофіза, що справляє ефект, прита*Дпя покриваючої плівки оболонки як пластиманний самому гормону росту До ефектів, що фікатор використовується ацильований моноглісправляє гормон росту належать такі стимулюцерид вання вивільнювання гормону росту в організмі Якщо застосовується рідкий носій, препарат людини похилого віку, запобігання катаболічних може бути виготовлений у вигляді сиропу, емульпобічних ефектів глюкокортікоідів, лікування оссії, м'яких желатинових капсул або стерильної рітеопорозу, стимулювання ДІЯЛЬНОСТІ імунної сисдини для ІН'ЄКЦІЙ, такої як водна або безводна рідтеми, прискорення заживления ран, прискорення ка суспензія чи розчин реабілітації ушкоджених кісток, лікування затримки Для введення через носову порожнину або росту, лікування захворювань нирок або недостатдихальний тракт препарат має містити в собі споності, що є наслідком затримки росту, лікування луку згідно з формулою 1, розчинену або суспенфізіологічної низькорослості, зокрема у дітей з довану в рідкому носи, зокрема, у водному носи, дефіцитом гормону росту, а також низькорослості, що робить можливим застосування цього препавикликаної хронічними захворюваннями, лікування рату у вигляді аерозолю Носій може містити в собі ожиріння та затримки росту, викликанної ожирінтакі присадки, як солюбілізуючі агенти, наприклад ням, лікування затримки росту, пов'язаної з синдпропіленгліколь, такі поверхнево-активні присадки, ромом Прадера-Віллі і синдрома Тернера, прискояк поліетиленгліколі солей жовчної кислоти, полірення заживления ОПІКІВ та зменьшення відсотку пропіленгліколі або полюксіетилен-ефіри вищих госпіталізованих пацієнтів, що страждають від ОПІспиртів, такі підсилювачі (енхансери) абсорбції як КІВ, лікування внутрішньоматкової затримки росту, лецитин (фосфатид илхолін) чи циклодекстрин, 18 17 61056 дисплазія скелета, пперкортісолізму і синдрому у будь-якому ефективному транспортуванні активІценко-Кушинга, збудження пульсуючого вивільної сполуки до потрібного органу або частини тіла, нювання гормону росту, заміщення гормону росту до шляхів такого транспортування належать нав організмі пацієнтів, що зазнали стресів, лікуванлежать оральний, назальний (через носову пороня остеохондродисплазій, синдрому Нунана, шижнину), легеневий, трансдермальний або парензофренії, депресій, хвороби Альцгеймера, заповітеральний, при цьому перевага ВІДДІЄТЬСЯ оральльненого заживления ран та фізіологічної деприному шляхові вацм, лікування дисфункції легеневих шляхів та Окремо від фармацевтичного застосування залежності від примусового вентилювання легенів, сполук згідно з формулою 1, вони можуть стати ослаблення протеш-катаболічної реакції організму корисними як інструмент для дослідження регулюна широке оперативне втручання, зменьшення вання здатності гормонів росту вивільнюватись m загального виснаження організму (кахексії} та vitro втрати протеїнів, зумовленої такими хронічними Сполуки згідно з формулою 1 также можуть захворюваннями як рак та СНІД, лікування пперінстати корисними як інструмент оцінки вивільнююсулінемм, зокрема незідюбластозу (гіперплазії чої здатності гіпофіза стосовно виділення гормону панкреатичних островків), супутнє (допоміжне) росту in vivo Наприклад, з метою визначення їх лікування з метою збудження овуляції, стимулювпливу на гормон росту можуть випробовуватися вання розвитку тимусної функції вилочкової залозразки сироватки, які було взято до і після введензи та запобігання вікового послаблення тимусної ня цих сполук до організму людини Порівняння функції, лікування пацієнтів з пригніченою імунною гормонів росту у кожному зразку сироватки дозвосистемою, підвищення сили м'язів рухливості, ляє безпосередньо визначити здатність гіпофіза профілактика збереження МІЦНОСТІ шкірного попацієнта до вивільнювання гормону росту криву, регулювання метаболічного гомеостазу, Сполуки згідно з формулою 1 можуть вводитиниркового гомеостазу у випадку вікової в'ялості, ся в організм важливої з точки зору економіки стимулювання розвитку остеобластів, виправленсільськогосподарської худоби з метою прискорення кісток та розвитку хрящів, стимулювання функня приросту поголів'я І збільшення розміру та ваги ції імунної системи в організмі домашніх тварин, а цих тварин і збільшення продуктивності надоїв також лікування вікових розладів в організмі домолока машніх тварин, сприяння росту свійської худоби та Сполуки згідно з формулою 1 можна оцінити m стимулювання росту овечої та козячої вовни vitro, вивчаючи їх ефективність та потенціальні властивості щодо вивільнювання гормону росту в З метою використання у вказаних вище випадсоматотрофних клітинах щурів ках доза препарату може змінюватися в залежності від застосування конкретного варіанта сполуки Саматотрофні клітини щурів можна приготувазгідно з формулою 1, від режиму і способу ввети, в цілому притримуючись попередніх описів дення і від бажаного терапевтичного результату (Chen et при , Endocrinology 1991, 129, 3337-3342 Однак, для досягнення ефективного вивільнюванта Chen et al_, Endocrinology, 1989, 124, 2791ня ендогенного гормону росту оптимальна доза, 2798) Щурів позбавляють життя обезголовленщо може бути введеною пацієнтам та тваринам, ням Після ЦЬОГО МИТТЄВО вилучають з їхніх тілець може становити від 0,0001-100мг/кг ваги тіла на гіпофізи Далі гіпофізи ферментують із 0,2%-ою добу Зазвичай дозовані одиниці, призначені для колагеназою (п 0 2% палуринідаза) у врівноважевведення через ротову або носову порожнини, ному сольовому розчині Хенкса Після цього клітимістять в собі від близько 0,0001мг до близько ни ресуспендують в субстраті Dulbecco's Modified ЮОмг, найоптимальніше від близько 0,001 мг до Eagle, що містить 0 37% ІЧаНСОз, 10% кінської 50мг, сполуки згідно з формулою 1 змішаною з сироватки, 2 5% сироватки з організму телички, фармацевтичне прийнятними носієм або розрі1% неконцентрованих амінокислот, 1% глутамшу джувачем та 1% пеніцилін/стрептоміцин, і концентрацію доводиться до 1 5x105 клітин/мл Один мл цієї суСполуки згідно з формулою 1 можуть бути спензії уміщується до кожної з комірок 24введенними у вигляді фармацевтичне прийнятних коміркової панелі і залишається перед експеримесольових присадок до кислот, або, якщо потрібно, нтом з оцінки вивільнювання на 2-3 дні у у вигляді солей лужних чи лужноземельних ме талів або нижчого алкіламонію Є підстави вважати, що застосування таких варіантів сполук у вигляді солей забезпечує приблизно такий самий порядок біологічної активності, як і у випадку застосування незв'язаних базових сполук Як варіант, фармацевтична композиція згідно з цим винаходом може містити в собі сполуку згідно з формулою 1 у комбінації з одним чи більшою КІЛЬКІСТЮ сполук, що відзначаються різною активністю, наприклад, з антибіотиком або іншим фармацевтично активним матеріалом Це може бути інакший засіб, підсилюваючий секрецію, такий, як GHRP (1 або 6) чи GHRH або їх аналоги, гормон росту або його аналог, або соматомедин, наприклад, IGF-1 чи IGF-2 Спосіб введення препарату в організм полягає В день виконання експкрименту комірки ДВІЧІ промивають у згаданому вище субстраті, що містить 25 міліграІЧ-молекул HEPES, рН7,4 Вивільнення гормону росту ІНІЦІЮЄТЬСЯ додаванням субстрату, що містить 25 міліграІЧ-молекул HEPES і тестової сполуки Інкубація триває 15 хвилин при 37°С Після інкубації об'єм гормону росту, що виділився в субстрат, вимірюється за допомогою стандартного радюімунноаналізу (RIA) Сполуки згідно з формулою 1 можна оцінити за їх впливом на вивільнення гормону росту в vivo в організмі щурів-самиць, анестезованому у пентоетилбарбітуровій кислоті, як описано у попередніх працях (Bereu et al Endocrinology 1991, 129, 2592-2598) У конкретному випадку дорослих щурів-самців Спрегью-Доулі було анестезовано шля 20 19 61056 хом внутрішньочеревного вливання пентоетилбаречовину після цього розчиняли в 4мл DCM / TFAy рбітурової кислоти з розрахунку 50мг/кг ваги Після співвідношенні 1 1 та помішували По 10 хвилинах досягнення повної анестезії за допомогою трахеосуміш концентрували потоком азоту та результаметричної канюлі і катетерів виконали імплантацію тивну маслоподібну речовину повторно розчиняли в сонну артерію та яремну вену Після 15в 20мл 70% CH3CN / 0 ОЗМ НСІ та до розчину дохвилинного відновлення в момент часу О брали бавляли 480мл НгО Сирий продукт після цього пробу крові Підсилювач секреції гіпофіза вводили очищали за допомогою напівпрепаративної хроІИ внутрішньовенне, проби крові тримали на льоді матографії HPLC за сім погонів на 25мм х 250мІ\Іпротягом 15 хвилин, після чого центрифугували колонці, впакованій 7ц- С-18 силікагелевим матепротягом 2 хвилин при 12 000об/хв Сироватку ріалом, котрий завчасно врівноважили 28%-им декантувапи і за допомогою стандартного RIA виCH3CN в 0 05М (NH4)2SO4 pH якого було доведено значали КІЛЬКІСТЬ гормону росту до 2,5 за допомогою 4М H2SO4 Далі винахід іліструється прикладами, котрі ні Колонку елюювали з використанням градієнту в якому разі не можуть обмежувати коло застосу28% - 38% CH3CN в 0 05М (NH4)2SO4, при рН2,5, вання винаходу, передбаченого його ФОРМУЛОЮ швидкості Юмл/хвилин протягом 47 хвилин та Сполуку, приготування якої описується у на40°С, фракції, що вміщують пептид, було зібрано, ступному прикладі, виділено як сіль трифтороцторозбавлено 3 об'ємними частками НгО та обробвоі кислоти (TFA) лено за допомогою картріджа Sep-Pak® C18 (Waters part #51910), який збалансували з 0 1% TFA Приклад 1 Пептид елюювали з картріджа Sep-Pak® 70% Приготування 2(В)-2-((3-Амшометилбензоіл)CH3CN 0,1% TFA та ВІДДІЛЯЛИ з елюату шляхом N-Me-D-2Nal-Nal-Me)-3^eHinnponaHony люфілізування після розбавлення водою Кінцевий продукт характеризували за допомогою аналітичної хроматографії RP-HPLC (час утримування) та мас-спектрометри десорбції плазми (молекулярна маса) Спектрометрія мас узгоджується із очікуваною структурою в межах експериментальної похибки методу (за результатами спектрометрії мас ± 0 9 атомних одиниць маси) Хроматографічний аналіз RP-HPLC виконували з використанням УФ-детектування при 214нмта С-18-силікагелевоі колонки Vydac 218ТР54, 4 6мм 165 7мг Boc-N-Me-D-2Nal-OH та 165 2мг (R)х 250мм, 5ц (The Separations Group, Hespena), метиламшо-3-феніл-пропан-1-іл (виготовленого з елюювання відбувалося при швидкості 1мл/хвил H-N-Me-D-Phe-OH згідно з McKennon, М J , MeyТа температурі 42°С Використовувалося два різers, А, 1 J Абод Chem 1993, 58, 3568-71) та них режими елюювання 68 1мг НО При розчиняли в суміші 2мл DMF та А1 Колонку врівноважували 5%-им CH3CN в 4мл DCM при 0°С Добавляли 115мг EDAC та субуфері, ЩО ЯВЛЯВ СОбОЮ 0 1М (NH4)2SO4, рН ЯКОГО міш помішували протягом 1Н при 0°Ста після цьобуло доведено до 2,5 за допомогою 4М H2SO4, та го протягом 18 год при кімнатній температурі елюювали при градієнті CH3CN від 5% до 60% в Далі, перед добавленням 50мл of EtOAc, DCM тому ж самому буфері протягом 50 хвилин видаляли з суміші потоком азоту, і результативний В1 Колонку врівноважували 5% CH3CN / 0 1% розчин екстрагували послідовно з ЮОмл 5% водTFA / Н2О та елюювали при градієнті від 5% ного розчину NaHCO3, ЮОмл Н2О, ЮОмл 5% водCHsCN / 0 1 % TFA / Н2О до 60% CH3CN / 0 1 % TFA ного розчину KHSO4 та ЮОмл Ь^О Результативну / Н2О протягом 50 хвилин органічну фазу висушували Na2SO4 та концентруВиявлений час утримування з використанням вали в вакуумі на роторному випарювальному режимів А1 та В1 становить ВІДПОВІДНО 29,90 хвиапараті до отримання маслоподібної речовини лин та 31,52 хвилин 502 бмг З-Вос-амінометилбензойної кислоти Синтез З-Вос-амінометилбензойної кислоти розчиняли в Юмл DCM шляхом додавання 2 кра25г 3-цианобензойноі кислоти розчиняли в плин DMF і далі перетворювали в симетричний 70мл 25% NH3/H2O, і під азотною атмосферою ангідрид шляхом помішування з 191 бмг EDAC добавляли 200мл Н2О та 5г 10% Pd/C Суміш пдпротягом 10 хвилин рогенізували під атмосферним тиском при кімнатДо цієї суміші добавляли розчин згаданого ліній температурі, при цьому поступово доводячи рН офілізованого 2(R)-(H-N-Me-D2Nal-N-Me)-3до 10 5 шляхом додавання 12% NH3/H2O Після фенілпропанолу та 342мкл DIEA в 5мл DCM та абсорбції! близько 41 Нг, протягом 18г, реакцію продовжували реакцію протягом 20Н при кімнатній було припинено та каталізатор видалено за допотемпературі Суміш реакції після цього концентрумогою фільтрування Фільтрат концентрували в вали до здобуття маслоподібної речовини та повакуумі до об'єму 20мл, і вихідний матеріал, що не вторно розчиняли в 50мл ЕЮАс Здобутий розчин прореагував, видаляли шляхом екстрагування з екстрагували послідовно зі ЮОмл 5% водного розетилацетатом після підкислювання 200мл 1 5М чину МаНСОз, ЮОмл Н2О, ЮОмл 5% водного розхлористоводневої (соляної) кислоти Фазу водного чину KHSO4 та ЮОмл НгО Результативну органічрозчину концентрували до сухості та повторно ну фазу висушували з Na2SO4 та концентрували у розчинювали в 400мл THF та 343мл 1М NaOH вакуумі на роторному випарювальному апараті до Добавляли розчин 30г Вос-анпдриду в ЮОмл THF, здобуття маслоподібної речовини Маслоподібну і суміш помішували протягом доби (через ніч) ПІС 22 21 61056 ля цього суміш реакції підкислювали до рН З N НСІ Половину об'єму згаданої масляної речовини (2 та екстрагували ЗхЗООмл ЕЮАс Органічну фазу НСІ, H-N-Me-D-2Nal-N-Me-D-Phe-NH-(CH2)3випаровували до пшоподібної кондиції Вихід стаN(CH3)2) розчиняли в DCM (9мл) та добавляли 2 новив 22г краплини DMF та DIEA (342мкл) Цей розчин добавляли до розчину Boc-SAMB-OH (503мг) та Скорочення EDAC (192мг) в DCM (5мл), які перемішували проrt кімнатна температура тягом 15 хвилин при кімнатній температурі Після EDAC г\І-етил-г\Г-(3-діметиламінопропіл)помішування на протязі 20г суміш реакції конценткарбодммід пдрохлорид рували до здобуття маслоподібної речовини за ЕЮАс етилацетат допомогою азотного потоку і перемішували протяВос t-бутилоксикарбоніл гом 15 хвилин із 5% водним розчином гідрокарбоN-Me-D-2Nal І\І-метил-0-2-нафтилаланін нату натрію (ЮОмл) DCM дихлорометан DIEA дмзпропілетиламін Після ЦЬОГО добавляли ЕЮАс (50мл), органічна фаза ВІДДІЛЯЛИ та екстрагували з 5% водним DMF M.IN-діметилформамід розчином гідрокарбонату натрію (ЮОмл) та водою НОПри 1 -пдрокси-7-азабензотріазол (ЮОмл), і після цього висушували над ІЧагЄСч та N-Me-D-Phe-ол N-метил-О-фенілапанінол концентрували в вакуумі до здобуття маслоподібTFA трифтороцтова кислота ної речовини (340мг) Цю масляну речовину поміTHF тетрапдрофуран шували 10 хвилин при кімнатній температурі з Приллад 2 TFA/DCM у співвідношенні 1 1 (бмл) Далі 3-((3-Амшометилбензоіл))- N-Me-D-2Nal-N-MeTFA/DCM випаровували потоком азоту та резульD-Phe-NH)-N,N-flHMeTHnaMiHonponaH тативне масло розчиняли в 70%-ому CH3CN (Юмл) і розбавляли водою до кінцевого об'єму 50мл Сирий продукт очищали за допомогою наСН, півпрепаративної хроматографії HPLC за ВІСІМ прогонів та люфілізували за допомогою процедур, аналогічних тим, що описані прикладі 1 Здобутий кінцевий продукт вивчали за допомогою аналітичної хроматографії RP-HPLC (час утримування) та мас-спектрометри десорбції плазми (молекулярна маса) Отримана молекулярна маса (МН+ 608,2 Boc-N-Me-D-Phe-OH (279мг) розчиняли в DMF атомних одиниць маси) узгоджується з очікованою (4мл) та помішували 10 хвилин із HOBt (168мг) та структурою (теор МН+ 608,8 атомних одиниць маEDAC (230мг) Добавляли З-Діметиламшо-1си), в межах експериментальне допустимої похибпропіламін (188мкл), і суміш помішували 18 год ки методу Час утримування RP-HPLC з викориспри кімнатній температурі Після цього добавляли танням режимів елюювання А1 та В1, описаних в 5% водний розчин гідрокарбонату натоію (50мл) та прикладі 1, становив ВІДПОВІДНО 25 23 та 26 58 результативну суміш екстрагували із ЕЮАс (50мл) хвилин і органічну фазу висушували над Na2SO4 та концентрували в вакуумі до здобуття маслоподібної реПриклад З човини 3-(((3R)-3-nmepHflHHKap6oHin)-N-Me-D-2Nal-NЦю маслоподібну речовину помішували протяMe-D-Phe-NH)-1-N,N-flHMeTHnaMiHonponaH гом 10 хвилин при кімнатній температурі з TFA/DCM 1 1(6мл) Після ЦЬОГО TFA / DCM випаровували потоком азоту та здобуту масляну речовину розчиняли в суміші 70% CH3CN (Юмл), 1 N НСІ (Змл) та води (37мл), і результативну суміш було негайно заморожено та люфілізовано Після люфілізацм продукт розчиняли в DMF (бмл) та DCM (12мл) До цієї суміші добавляли при Половина 2 HCI, H-N-Me-D-2Nal-N-Me-D-Pheпомішуванні Boc-N-Me-D-2Nal-OH (494мг), HOAt NH-(CH2)3-N(CH3)2, здобутого як масляна речовина (204мг), DIEA (171мкл) та - після охолодження до в прикладі 2, розчиняли в DCM (9мл) та 2 крапли0°С - EDAC (288мг) Після помішування протягом нах DMF, і добавляли DIEA (342мкл) 18г при кімнатній температурі DCM випаровували потоком азоту та добавляли ЕЮАс (ЮОмл) Цю Цей розчин добавляли до розчину Вос-{В)суміш екстрагували ДВІЧІ 5% водним розчином ніпекотової кислоти (459мг) та EDAC (192мг) в гідрокарбонату натрію (ЮОмл) та водою (ЮОмл) DCM (5мл), який перед цим перемішували протята висушено над Na2SO4 та концентрували в вакугом 15 хвилин при кімнатній температурі умі до здобуття маслоподібної речовини (480мг) Після помішування на протязі 20г суміш реакЦю масляну речовину помішували 10 хвилин при ції концентрували до здобуття маслоподібної рекімнатній температурі із TFA / DCM 1 1 (бмл) Далі човини потоком азоту та помішували протягом 15 TFA/DCM випаровували потоком азоту та резульхвилин із 5%-им водним розчином гідрокарбонату тативне масло розчиняли в 70% CH3CN (Юмл) натрію (ЮОмл) Добавляли 1N-HCI (1мл) та воду (47мл), і резульПісля ЦЬОГО добавляли ЕЮАс (50мл), органічтативну суміш негайно заморожували та люфілізуну фазу ВІДДІЛЯЛИ та екстрагували з 5%-им водним вали до здобуття маслоподібної речовини (2 НСІ, розчином гідрокарбонату натрію (ЮОмл) та водою H-N-Me-D-2Nal-N-Me-D-Phe-NH-(CH2)3-N(CH3)2) (ЮОмл), далі висушували над Na2SO4 та концент 24 23 61056 рували в вакуумі до здобуття маслоподібної речолин при кімнатній температурі з TFA/DCM 1 1 вини (бмл) Після ЦЬОГО TFA/DCM випаровували потоком азоту та результативне масло розчиняли в Цю масляну речовину помішували 10 хвилин 70% СНзСІЧ (Юмл) і добавляли 1 N соляної кислопри кімнатній температурі з TFA/DCM 1 1 (бмл) ти (Змл) Продукт ВІДДІЛЯЛИ за допомогою люфіліДалі TFA/DCM випаровували потоком азоту, і резування після розбавлення водою цього розбавзультативну масляну речовину розчиняли в 70% лення водою (50мл) CH3CN (Юмл) та розбавляли водою до кінцевого об'єму 50мл Цей сирий продукт після цього очи286мг цього люфілізованого продукту розчищали за допомогою напівпрепаративної хроматогняли в DCM (15мл) та DIEA (171"1) Цей розчин рафії HPLC за п'ять прогонів та люфілізувапи за добавляли до розчину Вос-(Р)-ніпекотовоі кислоти допомогою процедур, аналогічних описаним в при(459мг) та EDAC (192мг) в DCM (Юмл), які перекладі 1 мішували перед цим протягом 25 хвилин при кімнатній температурі Здобутий кінцевий продукт вивчали за допомогою аналітичної хроматографії RP-HPLC (час Після помішування на протязі 20Н суміш реакутримування) та мас-спектрометри десорбції плації концентрували до здобуття маслоподібної резми (молекулярна маса) Отримана молекулярна човини потоком азоту, після чого повторно розчи+ маса (МН 586,3 атомних одиниць маси) узгоджуняли в ЕЮАс (ЮОмл) та екстрагували з 5%-им ється з очікованою структурою (теор МН+585 8 водним розчином гідрокарбонату натрію (50мл), з атомних одиниць маси), в межах експерименталь5%-им водним розчину гідросульфату калію (50мл) не допустимої похибки методу Час утримування та з водою (50мл) Органічну фазу висушували RP-HPLC з використанням режимів елюювання А1 сульфатом натрію та концентрували в вакуумі до та В1, описаних в прикладі 1, становив ВІДПОВІДНО здобуття маслоподібної речовини 25,33 та 26,35 хвилин Цю масляну речовину помішували 10 хвилин Приклад 4 при кімнатній температурі з TFA/DCM 1 1 (бмл) Далі TPA/DCM випаровували потоком азоту та 2-(((3R)-3-nmepHflHHKap6oHin)-N-Me-D-2Nal-Nрезультативне масло розчиняли в 70% СНзСІЧ Ме-О-Рпе-г\ІН)-1-(1-метил-2-піролідиніл)етан (Юмл) та розбавляли водою до кінцевого об'єму 50мл Далі цей сирий продукт очищали за допомогою напівпрепаративної хроматографії HPLC за три прогони і люфілізували за допомогою процедур, аналогічних описаним у прикладі 1 Здобутий кінцевий продукт вивчали за допомогою аналітичної хроматографії RP-HPLC (час утримування) та Boc-N-Me-D-Phe-OH (279мг) розчиняли в DMF мас-спектрометри десорбції плазми (молекулярна (Юмл) та помішували 10 хвилин з HOBt (168мг) та маса) Отримана молекулярна маса (МН+ 612,2 EDAC (384мг) Добавляли 2-(Амшоетил)-1-метилатомних одиниць маси) узгоджується з очікованою піролідин (290мкл) та DIEA (171мкл), і суміш поміструктурою (теор МН+ 612,39 атомних одиниць шували протягом 20 Н при кімнатній температурі маси), в межах експериментально допустимої поПісля ЦЬОГО суміш концентрували до здобуття махибки методу слоподібної речовини, яку розчиняли в 50мл води Час утримування RP-HPLC з використанням та люфілізували Продукт повторно розчиняшл в режиму елюювання А1, описаного в прикладі 1, 25мл водою та після цього подавали на картридж становив 25,80 хвилин Sep-Pak® C18 Waters (час утримування) # 43345), Приклад 5 який врівноважували 0,03 N соляною кислотою (2R)-2-((3-AMiHOMe™-i6eH3on-|)-N-Me-D-2Nal-NПродукт елюювали на Sep-Pak® із 70% CH3CN в Ме)-3-(2-нафтил)пропанол 0,03 N соляною кислотою та ВІДДІЛЯЛИ З елюату за допомогою люфілізування після розбавлення водою Результативний матеріал помішували протягом 10 хвилин при кімнатній температурі з TPA/DCM 1 1 (бмл) Після ЦЬОГО TFA/DCM випаровували потоком азоту та результативну масляну речовину розчиняли в 70% CH3CN (Юмл) та добавляли 1 N соляної кислоти (2мл) Після розбав(R)-2-(N-TpeT-ByroKCHKap6oHin-N-MeTHnaMiHo)лення водою (50мл) продукт ВІДДІЛЯЛИ за допомо3-(2-нафтил) пропюнової кислоти складний метилгою люфілізування Результативний матеріал розовий ефір чиняли в DMF (Змл) та помішували 18 Н при кімнатній температурі після добавлення Boc-N-Me-D2Nal-OH (329мг), HOAt (136мг), EDAC (230мг) та DIEA (171мкл) Далі добавляли ЕЮАс (50мл) та цю суміш екстрагували з 5%-им водним розчином гідрокарбонату натрію (50мл), з 5%-им водним розчином гідросульфату калію (50мл) та з водою ^)-2-трет-Бутоксикарбоніл-г\І-метиламіно-3-(2(50мл) Органічну фазу висушували сульфатом нафтил)- пропюнову кислоту (5,0г, 16,4ммол) рознатрію та концентрували в вакуумі до здобуття чиняли в сухому DMF (50мл) Добавляли йодомемаслоподібної речовини тан (6,2мл, 98,4ммол) та оксид срібла(І) (13,Зг, 57,4ммол), і суміш перемішували протягом доби Цю масляну речовину перемішували 10 хви 26 25 61056 Суміш реакції фільтрували та фільтрат екстрагували з метиленхлоридом (200мл) Органічну фазу промивали with цианідом калію (2х50мл, 5%) та водою (Зх75мл) Далі органічну фазу висушували (MgSC^) та розчинник видаляли в вакуумі Залишок (осад) піддавали хроматографічній обробці (R)-2-Фopмlлaмlнo-3-(2-нaфтил)пpoпloнoвy ки(Силікагель, 5х40см) з використанням етилацетату слоту (4,37г, 18ммол) розчиняли в сухому тетрапта гептану (1 2) як елюента, здобуваючи 4,98 г of дрофурані (ЮОмл) і добавляли боропдрид натрію (R) 2-(г\І-трет-Бутоксикарбоніл-г\І-метиламіно)-3-(2(1,6г, 43,2ммол) Іод (4,57г, 18ммол) розчиняли в нафтил) пропюнової кислоти складний метиловий сухому тетрапдрофурані (40мл) і по краплинах ефір добавляли до суміші реакції при температурі, що 1 H-NMR (СОСІз) 1 ЗО, 1 35 (два s, 9H), 2 71, не перевищувала 40°С Після цього добавлення 2 75 (два s, ЗН), 3 19, 3 47 (два т , 35 2Н), 3 74, суміш реакції нагрівали до температури флегми (зі 3 77 (два s, ЗН), 4 65, 5 05 (два dd, 1H), 7 29-7 82 зворотним охолодженням) протягом 12 годин До(т, 7Н) (суміш ротамерів) (Р)-2-{І\І-третбавляли гідроксид калію (50мл, 20%) Фазу водноБутоксикарбоніл-г\І-метиламшо)-3-(2го розчину екстрагували зі складним метилнафтил)пропюнова кислота третбутиловим ефіром (4х50мл) Комбіновані органічні шари промивали насиченим хлоридом натрію(150мл), висушували (MgSO4), і розчинник видаляли в вакуумі Залишок (осад) піддавали хроматографічній обробці (Silica 5х40см) з використанням DCM/ метанол/аміаку (100 10 1), здобуваючи 1,81г (R) метиламшо-3-(2-нафтил)пропан-1(Р)-2-(г\І-трет-Бутоксикарбоніл-г\І-метиламіно)олу 3-(2-нафтил) пропюнової кислоти складний метил1 овий ефір (21,73г, 65,57ммол) розчиняли в 1,4H-NMR (CDCI3) 2,43 (s, ЗН), 2,88-3 05 (m, ЗН), дюксані (200мл) та добавляли воду (20мл) Суміш 3,10 (s (br), 2H), 3,42 (dd, 1H), 3,69 (dd, 1H) 7,30реакції охолоджували в водяній ванні та добавля7,82 (m, 7H) ли гідроксид ЛІТІЮ (1,73г, 72,13ммол) Через 15 N-{(1 R)-1 -[N-((1 R)-2-nflpoKCH-1 -((2хвилин добавляли воду (140мл), і суміш реакції нафтил)метил)етил)-І\І-метилкарбамоіл]-2-(2після цього додатково помішували 3 години при нафтил)етил}-г\І-метилкарбамшовоі кислоти склакімнатній температурі Добавляли етилацетат дний трет-бутиловий ефір (400мл) та воду (ЗООмл), і рН доводили до 2,5 з використанням гідросульфату натрію 1М (110мл) Фази розділили, і фазу водного розчину екстрагували з етилацетатом (200мл) Комбіновані органічні фази промивали водою (ЗООмл), висушували (M0SO4), і розчинник видаляли в вакуумі, здобувасн, ючи 20,1г при (R) 2-(г\І-трет-Бутоксикарбоніл-г\Іметиламшо)-3-(2-нафтил) пропюнової кислоти ^)-(г\І-7рет-Бутоксикарбонш-г\І-метиламіно)-3H-NMR (DMSO) 1 18, 1 21 (два s, 9H), 2 62, (2-нафтил) пропюнову кислоту (0,55г, 1,67ммол) та 2 66 (два s, ЗН), 3 11-3 58 (m, 2H), 4 75, 4 90 (два (R) метиламшо-3-(2-нафтил) пропан-1-іл (0,38г, dd, 1Н), 7 48-7 88 ( т , 7Н), 1 85 (s (br), 1Н)(суміш 2,00ммол) розчиняли в метиленхлориді (15мл) та ротамерів) диметилформаміді (7 5мл) Суміш реакції охоло^)2-Форміламшо-3-(2-нафтил)пропюнова киджували на льодяній ванні Добавляли 1-Пдроксислота 7-азабензотріазол (0,24г, 2,09ммол) та N-(3диметиламінопропіл)-г\Г-етилкарбодммід пдрохлорид (0,38г, 2,0ммол) Суміш реакції помішували 12 о годин при кімнатній температурі Далі суміш реаксн ції концентрували в вакуумі Добавляли етилацен о тат (200мл), і органічний розчин промивали водою ^)-2-амшо-3-(2-нафтил) пропюнову кислоту (ЮОмл), гідрокарбонатом натрію/карбонатом на(18,11г, 84,14ммол) розчиняли в мурашиній кислотрію (рН 9) (75мл), гідросульфатом натрію (75мл, ті (204мл) та по краплинах добавляли ангідрид 10%), водою (ЮОмл) і висушували (MgSO4) Розоцтової кислоти (70мл) Суміш реакції нагрівали to чинник видаляли в вакуумі, і залишок (осад) підда55°С та помішували ЪЛА години при кімнатній темвали хроматографічній обробці (Silica, 2х45см) з пературі По краплинах добавляли льодяну воду використанням етилацетату, здобуваючи 0,25g of (70мл) та помішували при 0°С протягом 20 хвилин N-{(1 R)-1 -(N-[(1 R)-2-nflpoKCH-1 -((2Суміш реакції фільтрували та промивали льодянафтил)метил)етил)-І\І-метилкарбамош]-2-(2ною водою (20мл), здобуваючи 20,26г (R) 2нафтил)етил}-г\І-метилкарбамшовоі кислоти склаформіламшо-3-(2-нафтил) пропюнової кислоти дний трет-бутиловий ефір 1 1 H-NMR (DMSO) 3 05 (dd, 1H), 3 27 (dd, 1H), H-NMR (DMSO) 0 80-199 (декілька s, 9H), 4 64 (m, ІН), 7 48-7 87 (m, 7Н), 7 95 (s, 1Н), 8 45 (d, 2 45-4 20 (m, 12 Н), 4 70-5 12 (m, 2H) (вибрані ПІКО1Н), 12 9(s(br), 1H) ВІ значення, суміш ротамерів) (В)-Метиламшо-3-(2-нафтил) пропан-1 -ол (2R)-N-((1 R)-2-riflpoKCH-1 -((2нафтил)метил)етил)-г\І-метил-2-метиламшо-3-(2нафтил) пропюнамід 27 61056 28 зми (молекулярна маса) Отримана молекулярна + маса (МН 559,5 атомних одиниць маси) узгоджу+ ється з очікуваною структурою (теор МН 560 72 атомних одиниць маси) в межах експериментальної похибки методу Час утримування RP-HPLC з використанням режимів елюювання А1 та В1, описаних в ПРИКЛАДІ 1, становив ВІДПОВІДНО 33,07 та 34,63 хвиN-{(1 R)-1 -(N-[(1 Р)-2-гідрокси-1 -((2лин нафтил)метил)етил)-І\І-метилкарбамоіл]-2-(2Приклад 6 H-Aib-His-D-2Nal-N-Me-D-Phe-NH2 нафтил)етил}-г\І-метилкарбамшовоі кислоти складний трет-бутил ефір (0,25г, 0,475ммол) розчиняли в DCM (Змл) Добавляли трифторооцтову кислоту (1мл), і суміш реакції помішували протягом 20 хвилин Розчинник видаляли в вакуумі DCM (5мл) добавляли та видаляли в вакуумі, і операцію повторювали Залишок (осад) розчиняли в метанолі (5мл) Добавляли гідрокарбонат натрію /карбонат натрію (5мл, рН9), і розчин екстрагували з етилацетатом (2х10мл) Органічну фазу висушували (MgSO4), розчинник видаляли, здобуваючи 0,22г (2R)-N-((1 R)-2-гlдpoкcи-1-((2-нaфтил)мeтил)eтил)М-метил-2-метиламіно-3-(2-нафтил)пропюнаміду Пептид синтезували згідно зі схемою Fmoc на 1 H-NMR (CDCI3) 170, 2 37, 245, 2 93 (чотири пептидному синтезаторі Applied Biosystems 431A, s, 6Н), 2 56-3 05 ( т , 2Н), 3 52-3 85 ( т , 7Н), 4 25, калібровка 0 22ммоль, з використанням запропо4 97 (два т , 1Н), 6 86-7 78 (т, 14Н) (вибрані ПІКОВІ нованих виробником FastMoc УФ-протоколів, зазначення, суміш ротамерів) стосовуючи проміжні зв'язки HBTU для ЯМР і УФмоніторинга депротектування захисної Fmoc(2R)-2-((3-AMiHOMe™-i6eH3Oin)-N-Me-D-2Nal-Nгрупи Для синтезування користувалися вихідною Ме)-3-(2-нафтил)пропанол смолою кат# D-1675 виробництва фірми Bachern Feinchemikahen AG, Bubendaoof, Switzerland (427мг), що являє собою Ртос-2,4-диметилокси-4'(карбоксиметилокси)-бензпдрил-амш, приєднаний до аміно-метил-полістиренової смоли через амідний зв'язок Ємність (продуктивність) заміщування становила 0,55ммоль/г Використовували такі захищені ПОХІДНІ амінокислот, як Fmoc-N-Me-D-PheЗ-Вос-амінометилбензойну кислоту (502 бмг) ОН, Fmoc-D-2Nal-OH, Fmoc-His(Trt) та Fmoc-Aibрозчиняли в DCM (бмл) та після цього перетворюОН ХІМІЧНИЙ ЗВ'ЯЗОК Fmoc-N-Me-D-Phe-OH реалівали в симетричний ангідрид, помішуючи з EDAC зовано як подвійний зв'язок Після синтезування (191 бмг) протягом 15 хвилин пептид пдролізували з 750мг пептидноі смоли До цієї суміші добавляли розчин (2R)-N-((1 R)шляхом перемішування протягом 180 хвилин при 2-пдрокси-і -((2-нафтил)метил)етил)-І\І-метил-2кімнатній температурі із сумішю 8мл TFA , 600мг метиламшо-3-(2-нафтил)пропюнаміду (200мг) в фенолу, 200мкл етандитюлу, 400мкл тюанізолу і DCM (5мл), після чого реакція тривала протягом 400мкл НгО Гідролізовану суміш фільтрували, і 20 Н при кімнатній температурі фільтрат концентрували до близько 2мл потоком азоту 3 цієї масляної речовини за допомогою Суміш реакції далі концентрували до здобуття 50мл діетилефіру осаджували сирий пептид і 2 маслоподібної речовини та повторно розчинювали рази промивали його також 50мл діетилефіру Сив ЕЮАс (ЮОмл) Цей розчин екстрагували послірий пептид просушували і очищали напівпрепарадовно з 5% водним розчином ІЧаНСОз (2х50мл), тивною хроматографією HPLC за один прогон і 5% водним розчином KHSO4 (2х50мл) та НгО люфілізували з використанням процедур, аналогі(2х50мл) Результативну органічну фазу висушучних описаним в прикладі 1 вали Na2SO4 та концентрували в вакуумі на роторному випарювальному апараті до здобуття маслоЗдобутий кінцевий продукт вивчали за допоподібної речовини Маслоподібну речовину після могою хроматографічного аналізу RP-HPLC (час цього розчиняли в DCM / TFA 1 1 (бмл) та помішуутримування) та мас-спектрометри десорбції плавали По 10 хвилинах суміш концентрували потозми (молекулярна маса) Отримана молекулярна ком азоту та результативне масло повторно розмаса (МН+ 598,5 атомних одиниць маси) узгоджучиняли в 70% CH3CN / 0 1% TFA (5мл) і розбавляється з очікуваною структурою (теор МН+ 598,73 ли водою до об'єму 100мл атомних одиниць маси) в межах експериментальЦей сирий продукт далі очищали за допомоної похибки методу гою напівпрепаративної хроматографії HPLC за Час утримування RP-HPLC з використанням два прогони та люфілізували за допомогою прорежимів елюювання А1 та В1, описаних в прикладі цедур, аналогічних тим, що описані в прикладі 1 1, становив ВІДПОВІДНО 24, 68 та 25,58 хвилин Здобутий кінцевий продукт вивчали за допоПриклад 7 H-Aib-His-D-2Nal-N-Me-D-Phe-Serмогою хроматографічного аналізу RP-HPLC (час NH2 утримування) та мас-спектрометри десорбції пла 29 61056 Цю сполуку синтезували за допомогою процедур, аналогічних описаним в прикладі 6 Здобутий кінцевий продукт вивчали за допомогою хроматографічного аналізу RP-HPLC (час утримування) та мас-спектрометри десорбції плазми (молекулярна + маса) Отримана молекулярна маса (МН 685,6 атомних одиниць маси) узгоджується з очікуваною + структурою (теор МН 685 81 атомних одиниць маси) в межах експериментальної похибки методу Час утримування RP-HPLC з використанням режимів елюювання А1 та В1, описаних в прикладі 1, становив ВІДПОВІДНО 24 42 та 25 92 хвилин Приклад 8 (3-Амшометилбензоіл)-О-2І\ІаІ-г\ІMe-D-Phe-NH2 Цю сполуку синтезували за допомогою процедур, аналогічних описаним в прикладі 6 Єдиним винятком було те, що зв'язування Fmoc-D-2Nal-OH здійснювалося з використанням HATU як активуючого реагенту H-N-Me-D-Рпе-смола (О 23ммол) протягом 150 хвилин сполучали з 1ммол Fmoc-D2Nal-OH, з використанням 1ммол HATU в присутності DIEA (2ммол) Здобутий кінцевий продукт вивчали за допомогою хроматографічного аналізу RP-HPLC (час утримування) та мас-спектрометри десорбції плазми (молекулярна маса) Отримана молекулярна маса (МН+ 511,2 атомних одиниць маси) узгоджується з очікуваною структурою (теор МН+ 509 6 атомних одиниць маси) в межах експериментальної похибки методу Час утримування RP-HPLC з використанням режимів елюювання А1 та В1, описаних в прикладі 1, становив ВІДПОВІДНО ЗО 73 та 32 47 хвилин Приклад 9 (4-Піперидинкарбоніл)-О-2І\ІаІ-г\ІMe-D-Phe-NH2 Цю сполуку синтезувалилз використанням процедур, аналогічних описаним в ПРИКЛАДІ 8 Здобутий кінцевий продукт вивчали за допомогою хроматографічного аналізу RP-HPLC (час утримування) та мас-спектрометри десорбції плазми (молекулярна маса) Отримана молекулярна маса (МН+ 486,8 атомних одиниць маси) узгоджується з очікуваною структурою (теор МН+ 487,6 атомних ЗО одиниць маси) в межах експериментальної похибки методу Час утримування RP-HPLC з використанням режимів елюювання А1 та В1, описаних в прикладі 1, становив ВІДПОВІДНО 27,03 та 28,48 хвилин Приклад 10 ((ЗР)-3-Піперидинкарбоніл)-О2Nal-N-Me-D-Phe-NH2 Цю сполуку синтезували з використанням процедур, аналогічних описаним в прикладі 8 Здобутий кінцевий продукт вивчали за допомогою хроматографічного аналізу RP-HPLC (час утримування) та мас-спектрометри десорбції плазми (молекулярна маса) Отримана молекулярна маса (МН+ 486,9 атомних одиниць маси) узгоджується з очікуваною структурою (теор МН+ 487,6 атомних одиниць маси) в межах експериментальної похибки методу Час утримування RP-HPLC з використанням режимів елюювання А1 та В1, описаних в прикладі 1, становив ВІДПОВІДНО 28,03 та 29,50 хвилин Приклад 11 (З-Амшометилбензоіл-N-Me-D2Nal-N-Me-D-Phe-NH2 Цю сполуку синтезували з використанням процедур, аналогічних описаним в прикладі 8, за винятком того, що останній залишок (осад) вводиться з використанням симетричного ангідридного сполучення Вос-3-Амінометилбензойну кислоту (251мг) помішували протягом 15 хвилин з EDAC (96мг) в DCM Після ЦЬОГО добавляли смолу (429мг) і продовжували помішування протягом 18 год Інша відміна полягає втому, що витрачуваний на гідроліз з відділенням пептиду від смоли час було зменшено до 60 хвилин Здобутий кінцевий продукт вивчали за допомогою хроматографічного аналізу RP-HPLC (час утримування) та масспектрометри десорбції плазми (молекулярна маса) Отримана молекулярна маса (МН+ 522,9 атомних одиниць маси) узгоджується з очікуваною структурою (теор МН+523,6 атомних одиниць маси) в межах експериментальної похибки методу Час утримування RP-HPLC з використанням режимів елюювання А1 та В1, описаних в прикладі 1, становив ВІДПОВІДНО 28,83 та 30,13 хвилин Приклад 12 H-Aib-His-N-Me-D-2Nal-N-Me-DPhe-NH2 31 Цю сполуку синтезували з використанням процедур, аналогічних описаним в ПРИКЛАДІ 8, в цьому прикладі як для Fmoc-N-Me-D-2Nal-OH, так і для Fmoc-His(Trt) сполучення реалізовано з використанням HATU, і витрачуваний на гідроліз з відділенням пептиду від смоли час було зменшено до 60 хвилин Здобутий кінцевий продукт вивчали за допомогою хроматографічного аналізу RP-HPLC (час утримування) та мас-спектрометри десорбції плазми (молекулярна маса) Отримана молекулярна маса (МН+ 612,3 атомних одиниць маси) узгоджується з очікуваною структурою (теор МН+ 612,8 атомних одиниць маси) в межах експериментальної похибки методу Час утримування RP-HPLC з використанням режимів елюювання А1 та В1, описаних в прикладі 1, становив ВІДПОВІДНО 24,33 та 26,20 хвилин Приклад 13 (3-AMiHOMeTnn6eH3oin)-D-2Nal-NMe-D-Phe-NH2 Цю сполуку синтезували з використанням процедур, аналогічних описаним в прикладі 8 Здобутий кінцевий продукт вивчали за допомогою хроматографічного аналізу RP-HPLC (час утримування) та мас-спектрометри десорбції плазми (молекулярна маса) Отримана молекулярна маса (МН+ 587,2 атомних одиниць маси) узгоджується з очікуваною структурою (теор МН 586,74 атомних одиниць маси) в межах експериментальної похибки методу Час утримування RP-HPLC з використанням режимів елюювання А1 та В1, описаних в прикладі 1, становив ВІДПОВІДНО 21,13 та 22,60 хвилин Приклад 14 (3-АмЬІометилбензот)- N-Me-D2Nal-N-Me-D-Phe-NH2 Цю сполуку синтезували з використанням процедур, аналогічних описаним в прикладі 11 Здобутий кінцевий продукт вивчали за допомогою хроматографічного аналізу RP-HPLC (час утримування) та мас-спектрометри десорбції плазми (молекулярна маса) Отримана молекулярна маса (МН+ 601,6 атомних одиниць маси) узгоджується з очікуваною структурою (теор МН+ 601,77 атомних одиниць маси) в межах експериментальної похибки методу 32 Час утримування RP-HPLC з використанням режимів елюювання А1 та В1, описаних в прикладі 1, становив ВІДПОВІДНО 20,40 та 21,70 хвилин Приклад 15 ((3R)-3-nmepHflHHKap6oHin)-N-MeD-Phe-N-Me-D-Phe-Lys-NH2 61056 Цю сполуку синтезували з використанням процедур, аналогічних описаним в прикладі 11 Здобутий кінцевий продукт вивчали за допомогою хроматографічного аналізу RP-HPLC (час утримування) та мас-спектрометри десорбції плазми (молекулярна маса) Отримана молекулярна маса (МН+ 579,4 атомних одиниць маси) узгоджується з очікуваною структурою (теор МН+ 579,8 атомних одиниць маси) в межах експериментальної похибки методу Час утримування RP-HPLC з використанням режимів елюювання А1 та В1, описаних в прикладі 1, становив ВІДПОВІДНО 19,88 та 21,20 хвилин Приклад 16 H-Aib-His-N-Me-D-Phe-N-Me-DPhe-Lys-NH2 Цю сполуку синтезували з використанням процедур, аналогічних описаним в прикладі 12 Здобутий кінцевий продукт вивчали за допомогою хроматографічного аналізу RP-HPLC (час утримування) та мас-спектрометри десорбції плазми (молекулярна маса) Отримана молекулярна маса (МН+ 690,6 атомних одиниць маси) узгоджується з очікуваною структурою (теор МН+ 690,9 атомних одиниць маси) в межах експериментальної похибки методу Час утримування RP-HPLC з використанням режимів елюювання А1 та В1, описаних в прикладі 1, становив ВІДПОВІДНО 15,71 та 17,82 хвилин Приклад 17 ((3R)-3-nmepHflHHKap6oHin)-N-MeD-2Nal-N-Me-D-Phe-NH2 Цю сполуку синтезували з використанням процедур, аналогічних описаним в прикладі 11,з використанням Fmoc-N-Me-D-Phe-OH, Fmoc-N-Me-D2Nal-OH та Boc-(R)-HmeKOTOBOi кислоти, де сполучення як Fmoc-N-Me-D-2Nal-OH, так і Boc-(R)Ніпекотової кислоти реалізовано з використанням HATU Здобутий кінцевий продукт вивчали за допомогою хроматографічного аналізу RP-HPLC (час 34 33 61056 утримування) та мас-спеїсгрометрм десорбції плапрогонів, 30-40% MeCN/0,1M Юмл/хвил , зми (молекулярна маса) Отримана молекулярна (NH4)2SO4 pH2,5 + маса (МН 500,7 атомних одиниць маси) узгоджуДетектування 276нм, Sep-Pals, 70% + ється з очікуваною структурою (теор МН 501,7 MeCN/0,1% TFA, люфілізування атомних одиниць маси) в межах експериментальPD-MSTeop 536,7 ної похибки методу Експер 535,7±1 Час утримування RP-HPLC з використанням HPLC A1 rt (час утримування) 31,20 хвил режимів елюювання А1 та В1, описаних в прикладі В1 rt (час утримування) 36,35 хвил 1, становив ВІДПОВІДНО 28,18 та 29,55 хвилин Приклад 20 H-Aib-His-N-Me-D-2Nal-N-Me-DPhe-NHMe Приклад 18 H-Aib-Ala-D-2Nal-N-Me-D-Phe-l_ysNH2 Цю сполуку синтезували з використанням процедур, аналогічних описаним в прикладі 11 Здобутий кінцевий продукт вивчали за допомогою хроматографічного аналізу RP-HPLC (час утримування) та мас-спектрометри десорбції плазми (молекулярна маса) Отримана молекулярна маса (МН+ 660,7 атомних одиниць маси) узгоджується з очікуваною структурою (теор МН+ 660,8 атомних одиниць маси) в межах експериментальної похибки методу Час утримування RP-HPLC з використанням режимів елюювання А1 та В1, описаних в прикладі 1, становив ВІДПОВІДНО 25,63 та 26,75 хвилин Приклад 19 Н-З-Амшометилбензоіл-N-Me-D2Nal-N-Me-D-Phe-NH-CH3 Вос-ЗАМВ-ОН (115мг, 0 458ммоль), 1-пдрокси7-азабензотріазол (62мг, 0 458ммоль) та 1-етил3(3-диметиламшопропіл)карбодиміду пдрохлорид (97мг, 0 504ммоль) розчиняли в DCM (8мл) та DMF (1мл) і помішували протягом 15 хвилин Спочатку добавляли г\І-метил-2-метиламшо-г\І-((1 R)-1 -(метил карбамоіл)-2-фенілетил)-3-(2нафтил)пропюнамід (185мг, 0 458ммоль), розчинений в DCM (5мл), а після цього дмзпропілетиламін (80мл, 0 458ммоль), і суміш помішували протягом 20 годин Органічну фазу промивали гідрокарбонатом натрію (50мл, 5%) ЬЬО (50мл), насичували NaCI/bbO (50мл), висушували сульфатом натрію та випарювали в вакуумі Залишок (осад) розчиняли в DCM (2мл) обробляли TFA (2мл) протягом 10 хвилин Леткі компоненти видаляли потоком N2 Залишок (осад) розчиняли в 50мл 20% MeCN і розбавляли водою до об'єму 500мл Напівпрепаративна HPLC Fmoc-1 -Ні5(Тритил)-ОН (1,54г, 2,48ммоль) (ВАСНЕМ В-1570) і 1 -пдроксиаза-бензотріазол (338мг, 2 48ммоль) розчиняли в 9мл DMF, охолодженого до 0-4°С і добавляли 1 -етил-3-(3диметиламшопропіл)карбодмміду пдрохлорид (475мг, 2,48ммоль) Суміш реакції помішували протягом 15 хвилин при 0-4°С г\І-Метил-2-метиламіно-г\І-((1 R)-1 (Метил карбамоіл)-2-фенілетил)-3-(2нафтил)пропюнамід (500мг, 1,24ммоль), розчиненого в метиленхлориді (18мл), охолоджували до 0°С, потім добавляли до суміші і помішували протягом 1 години при 0-4°С, а далі додавали дизпропілетиламш (0,425мл, 2,48ммоль) Температуру суміші повільно підвищували до кімнатної, і суміш помішували після досягнення цієї температури протягом 72 годин DCM випарювали в потоці N2 до суміші добавляли ЮОмл етилацетату і промивали и гідрокарбонатом натрію (2х100мл, 5%) та гідросульфатом калію (ЮОмл, 5%) Фази розділяли, і органічну фазу просушували сульфатом натрію та випарювали в вакуумі Залишок (осад) розчиняли в DMF (8мл) та вводили в реакцію з піперидином протягом 15 хвилин, розбавляли з НгО (ЮОмл) та різко охолоджували оцтовою кислотою (1,5мл) Добавляли ацетонітрил, та суміш розбавляли НгО до об'єму 250мл Прозорий розчин додавали до 10 г "Seppaks" tt/Vater, промивали Н2О/О OS m HCI та елюювали з 50мл 35% MeCN/0,03 М НСІ Дали розбавляли Н2О до об'єму 200мл та люфілізували Вос-а аміноізобутирова кислота (756мг, З 72ммоль), 1-пдроксиазабензотріазоль гідрат (506мг, 3 72ммоль) та 1-етил-3(3диметиламшопропіл)карбодммід пдрохлорид (713мг, 3,72ммоль) розчиняли в DMF (бмл) та після 15 хвилин, добавляли Н-1 -Ніз(Тритил)NMeD2Nal-NMeDPhe-NHCH3, 2 HCL розчиняли в DCM (12мл), після чого добавляли дизопропілетиламін (0,637мл)та помішували протягом 72 годин DCM випарювали в потоці N2, до суміші добавляли ЮОмл етилацетату і промивали гідрокарбонатом натрію (2х50мл, 5%) та гідросульфатом калію 35 36 61056 (50мл, 5%) Фази розділяли, і органічну фазу просушували сульфатом натрію та випарювали в вакуумі Залишок (осад) розчиняли в DCM (бмл), охолодженому до 0-4°С, і обробляли TFA (бмл) протягом 10 хвил при 0-4°С Леткі компоненти видаляли потоком N2 Масляний залишок розчиняли в 35мл 70% ацетонітрилу, розбавляли НгО до об'єму 50мл і добавляли Юмл концентрованої соляної кислоти (12-молярноі) та помішували протягом 72 годин Суміш розбавляли водою до 200мл та нейтралізували твердим карбонатом калію, після чого остаточно розбавляли НгО до об'єму 400мл (2R)-2-(N-tert-6yTOKCHKap6oHin-N-MeTHnaMiHo)3-(4-йодофеніл)пропюнова кислота Л Напівпрепаративна HPLC PD-MS, теор 550,7, експер 550,1 HPLC A1 rt (час утримування) 31,75 хвил В1 rt (час утримування) 36,15 хвил Приклад 21 З-метиламінометилбензоіл-N-MeD-2Nal-N-Me-D-Phe-NH-CH 3 нх 906 Приготовляли згідно з Can J Chem (1977), 55, 1 H-NMR (CDCI3) d 1 34 (s, 4 5H), 1 38 (s, 4 5H), 2 70 (s,1 5H), 2 75 (s, 1 5H), 2 85-3 10 (m, 1H), 3 23 4 (m, 1H),4 4-4 6 (m, 0 5H), 6 9-7 0 (m, 2H), 7 62 (d, J=1 OHz, 2Hz), 9 5-10 (bs, 1H) N-((1 Р)-2-(4-Йодофеніл)-1 (метил карбамоіл)етил)-І\І-метилкарбамінова кислота tert-бутилефір Boc-NMe3AMB-OH (658мг, 2 48ммоль), 1пдроксиазабензотріазол гідрат (338мг, 2 48ммоль) та 1-етил-3-(3-диметиламшопропіл)карбодиміду пдрохлорид (475мг, 2 48ммоль) розчиняли в бмл of DMF та помішували протягом 15 хвилин Добавляли г\І-Метил-2-метиламшо-г\І-((1 П)-1 (метил карбамоіл)-2-фенілетил)-3-(2нафтилпропюнамід (500мг, 1 24ммоль), розчинений в метиленхлориді (12мл), після чого додавали дмзопропілетиламін (0,425мл, 2,48ммоль) Суміш помішували протягом 20 годин DCM випарювали в потоці N2> і до суміші добавляли 75мл етилацетату, після чого промивали гідрокарбонатом натрію (2х50мл, 5%) та гідросульфатом калію (50мл, 5%) Фази розділяли, і органічну фазу просушували сульфатом натрію та випарювали в вакуумі Залишок (осад) розчиняли в Юмл метиленхлориді, охолоджували до 0-4°С і обробляли TFA (Юмл) протягом 10 хвил при 04°С Леткі компоненти видаляли потоком N2 Масляний залишок (осад) розчиняли в 25мл 70% MeCN/0,1% TFA та розбавляли Н2О до об'єму 600мл Напівпрепаративна HPLC Велика колонка, 40мл/хвил , 8 прогонів 28-40& Р11 (1)2304, 276 нМ Seppak, Люфілізування PD-MSTeop 550,7, експер 550,1 HPLC A1 rt (час утримування) 31,75 хвил В1 rt (час утримування) 36,15 хвил Приклад 22 Піперидин-4-карбонова кислота N-((1 R)-1 -(N((1 Р)-2-(4-йодофеніл)-1 - (метилкарбамоіл)етил)І\І-метилкарбамоіл)-2-(2-нафтил)етил)-г\Іметиламід сн, о (2R)-2-(N-trer-6yroKCHKap6oHT-N-MeTHnaMiHo)-3(4-йодофенід)пропюнова кислота (2,00г, 4 9ммоль) розчиняли в метиленхлориді (20мл) Добавляли пдроксибензотріазол-пдрат (0,67г, 4,9ммоль) та 1етил-3-(3-диметиламшопропіл)-карбодиміду пдрохлорид (0,99г, 4,9ммоль) та суміш помішували протягом 15 хвилин Метиламін (0,38г 40% розчину в метанолі, 4,9ммоль) добавляли та суміш помішували overnight Добавляли метиленхлорид (40мл), і суміш промивали насиченим водним розчином гідрокарбонату натрію (50мл) та розчином гідросульфату натрію (10%, 50мл) Органічну фазу просушували (MgSC^) та розчинник видаляли в вакуумі Залишок(осад) піддавали хроматографічній обробці на силікагелевій основі (2,5х20см) з використанням етилацетату/гептану (2 1) як елюенту, здобуваючи 1,77г N-((1 Р)-2-(4-йодофеніл)-1 (метил карбамоіл)етил)-І\І-метилкарбаміновоі кислоти tert-бутилефіру 1 H-NMR (CDCI3) (вибрані ПІКОВІ значення для основного ротамеру) d 1,39 (s, 9Н), 2,75 (s, ЗН), 2,80 (d, ЗН), 3,29 (dd, 1H), 4,88 (t, 1H) (2Р)-3-(4-Йодофеніл)-І\І-метил-2(метиламшо)пропюнамід Н.С. N-((1 Р)-2-(4-Йодофеніл)-1-(метил карбамоїл) 38 37 61056 етил)-І\І-метилкарбаміновоі кислоти tert-бутилефір карбамоіл)-2-(4-йодофеніл)етил)карбамоіл)-2-(2(1,7г, 4,0ммоль) розчиняли в метиленхлориді нафтил)етил)карбаміновоі кислоти tert-бутилефір (Юмл) та добавляли трифторооцтову кислоту розчиняли в суміші метиленхлориду та трифторо(5мл) Суміш помішували протягом 1 год Добавоцтової кислоти та помішували протягом 15 хвиляли метиленхлорид (ЗОмл) та воду (ЗОмл) Тверлин Добавляли метиленхлорид (20мл) та воду дий гідрокарбонат натрію добавляли до отриман(ЗОмл) Додаванням твердого гідрокарбонату наня рН8 Органічну фазу ВІДДІЛЯЛИ, висушували трію доводили суміш до рН8 Органічну фазу ВІД(МдзЄСч) та випарювали в вакуумі, здобуваючи ДІЛЯЛИ, висушували (MgSO4) та випарювали в ва1 22 g (2Р)-3-(4-йодофеніл)-І\І-метил-2куумі, здобуваючи 1,40г (2R)-N-((1 R)-2-(4(метиламшо)пропюнаміду йодофеніл)-1 -(метил карбамоіл)етил )-ІЧ-метил-2метиламшо-3-(2-нафтил)пропюнаміду H-NMR (CDCI3) d 2,28 (s, ЗН), 2,68 (dd, 1H), 1 2,81 (d, ЗН), 3,08-3 19 (m, 2H), 6,95 (d, 2H), 7,63 (d, H-NMR (CDCI3) (вибрані ПІКОВІ значення для 2Н) головного ротамеру) d 1,79 (s, ЗН), 2,02 (d, ЗН), 2,55 (s, ЗН), 3,78 (dd, 1H), 5,44 (dd, 1H) І\І-Метил-І\І-((1Р)-1-(І\І-метил-І\І-((1 R-1 -(метил карбамоіл)-2-(4-йодофеніл)етил)карбамоіл)-2-(24-(N-((1 R)-1 -(N-((1 R)-2-(4-Йoдoфeнlл)-1 нафтил)етил)карбамшовоі кислоти tert-бутилефір (метил карбомоіл)етил)-М-метилкарбамоіл)-2-(2нафтил)етил)-г\І-метилкарбамоіл)піперидин-1 карбонової кислоти tert-бутилефір (2R)-2-(N-tert-6yroKCHKap6oHin-N-MeTHnaMiHo)3-(2-нафтил)пропюнову кислоту (1 10г, 3 ЗОммоль) розчиняли в метиленхлориді (Юмл) і добавляли HOAt (0 45г, 3 Іммоль) та EDAC (0 66г, 3 5ммоль) Після помішування протягом 15 хвилин добавляли (2Р)-3-(4-йодофеніл)-І\І-метил-2(метиламшо)пропюнамід (1,0г, 3,1ммоль) та дмзопропілетиламін (0,45г, 3,4ммоль), і суміш помішували протягом доби Метиленхлорид (ЗОмл) добавляли та суміш промивали насиченим водним розчином гідрокарбонату натрію (ЗОмл) та розчином гідросульфату натрію (10%, ЗОмл) Органічну фазу просушували (MgSO4), та розчинник видаляли в вакуумі Залишок (осад) піддавали хроматографічній обробці на силікагелевій основі (2 5х20см) з використанням етилацетату/гептану (2 1) як елюенту, здобуваючи 1 74г г\І-метил-г\І-((Ш)-1-(г\І-метилN-((1R)-1 -(метил карбамоіл)-2-(4йодофеніл)етил)карбамоіл)-2-(2-нафтил)етил) карбамшової кислоти tert-бутилефіру 1 H-NMR (CDCI3) (вибрані ПІКОВІ значення для головного ротамеру) d 1 38(s,9H),2 18(d, ЗН), 2 45 (s, ЗН), 2 75 (s, 3HJ5 05 (m, 1H), 5 42 (m, 1H) (2R)-N-((1 R)-2-(4-Йoдoфeнlл)-1 (метил карбамоіл)етил)-І\І-метил-2-метиламіно-3(2-нафтил)пропюнамід І\І-Метил-І\І-((1 R)-1 -(N-мети-О R)-1 -(метил 1-1егт.-бутоксикарбонілпіперидин-4-карбонову кислоту (143мг, 0 66ммоль) розчиняли в метиленхлориді (1 Омл), і добавляли HOAt (90мг, Оббммоль) та EDAC (140мг, 0 73ммоль) По 15 хвилинах помішування добавляли (2R)-N-((1 R)-2(4-йодофеніл)-1 -(метил карбамоіл)етил)-І\І-метил2-метиламшо-3-(2-нафтил)пропюнаміду (350мг, 0 ббммоль) та дизопропілетиламшу (85мг, 0 ббммоль) і суміш помішували протягом доби Добавляли метиленхлорид (20мл), і суміш промивали насиченим водним розчином гідрокарбонату натрію (20мл) та розчином гідросульфату натрію (10%, 20мл) Органічну фазу просушували (MgSO4), і розчинник видаляли в вакуумі Залишок (осад) піддавали хроматографічній обробці на силікагелевій основі (2 5х20см), з використанням етилацетату як елюенту, здобуваючи 412мг 4-(N((1 R)-1 -(N-((1 R)-2-(4-йoдoфeнlл)-1 -(метил карбомоіл)етил)-І\І-метилкарбамоіл)-2-(2-нафтил)етил)|\|-метилкарбамоіл)піперидин-1 -карбонової кислоти tert-бутилефіру 4-(N-((1 R)-1 -(N-((1 R)-2-(4-йoдoфeнlл)-1 (метил карбомоіл)етил)-І\І-метилкарбамоіл)-2-(2нафтил)етил)-г\І-метилкарбамоіл)піперидин-1 карбонової кислоти tert-бутилефір (412мг, 0,56ммоль) розчиняли в суміші метиленхлориду (5мл) та трифторооцтової кислоти (5мл) та перемішували протягом 5 хвилин Добавляли метиленхлорид (20мл) та насичений водний розчин гідрокарбонату натрію (20мл) Додаванням твердого гідрокарбонату натрію суміш доводили до рН8 Фази розділяли, і органічну фазу просушували (MgSO4) і випаровували, здобуваючи 255мг голо 39 61056 вної сполуки 1 H-NMR (CDCI3) (вибрані ПІКОВІ значення для головного ротамеру) d 2,32 (d, ЗН), 2,58 (s, ЗН), 2,68 (s,3H), 5,33 (m, 1Н), 5,84 (t, 1Н) HPLC rt (час утримування) = 33,35 хвилин (А1) + PDMS m/z 640,8 (М+Н) Скорочення О-(Бензотріазол-1-іл)-1,1,3,3тетраметилуронію гексафто Комп'ютерна верстка С Волобуєв 40 NMP HATU TrtHOBT 3-ATB N-Me-3-AMB Підписне рофосфат N-метил піролі дон О-(7-Азабензотріазол-1 -іл)1,1,3,3-тетраметилуронію гек сафто рофосфат Тритил 7-пдроксибензотрюзолу гідрат З-Амінометилбензоїл 3-метиламшометилбензоіл Тираж39 прим Міністерство освіти і науки України Державний департамент інтелектуальної власності, Львівська площа, 8, м Київ, МСП, 04655, Україна ДП "Український інститут промислової власності", вул Сім'ї Хохлових, 15, м Київ, 04119
ДивитисяДодаткова інформація
Назва патенту англійськоюComponuds with properties of growthhormone release, as pharmaceutical composition, a method for stimulating the growth hormone release from the pituitary and a method for increasing animal growth rate
Автори англійськоюJOHANSEN NILS LANGELAND, Lau Jesper, MADSEN KJELD, LUNDT BEHREND FRIEDRICH, Pettersson Ingrid, HANSEN BIRGIT
Назва патенту російськоюСоединения со свойствами высвобождения гормона роста, фармацевтическая композиция, способ стимулирования высвобождения гормона роста из гипофиза и способ повышения скорости роста животных
Автори російськоюЙохансен Нильс Лангеланд, Лау Йесепер, Мадсен Келль, Лундт Бехренд Фридрих, Пешке Бернд, Хансен Биргит Сехестед
МПК / Мітки
МПК: C07K 14/60, C07C 237/22, C07K 7/06, C07K 5/062, A61P 15/00, C07K 5/083, A61P 5/00, C07K 5/065, A61K 38/00, C07K 5/103, A61P 13/02, C07K 5/087
Мітки: гіпофізу, стимулювання, тварин, фармацевтична, підвищення, властивостями, вивільнення, композиція, спосіб, росту, гормону, швидкості, сполуки
Код посилання
<a href="https://ua.patents.su/20-61056-spoluki-z-vlastivostyami-vivilnennya-gormonu-rostu-farmacevtichna-kompoziciya-sposib-stimulyuvannya-vivilnennya-gormonu-rostu-z-gipofizu-i-sposib-pidvishhennya-shvidkosti-rostu-tva.html" target="_blank" rel="follow" title="База патентів України">Сполуки з властивостями вивільнення гормону росту, фармацевтична композиція, спосіб стимулювання вивільнення гормону росту з гіпофізу і спосіб підвищення швидкості росту тварин</a>
Попередній патент: Лікарська горілка
Наступний патент: Інгібітори тромбіну, спосіб їх одержання, фармацевтична композиція на їх основі та спосіб лікування
Випадковий патент: Спосіб визначення концентрації емульсії