Похідні піперидину та їх застосування як модуляторів активності рецепторів хемокіну (зокрема ccr5), спосіб їх одержання, фармацевтична композиція на їх основі та проміжна сполука
Формула / Реферат
1. Сполука формули (І):
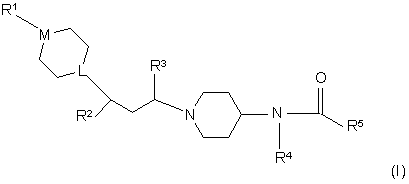 ,
,
де
L - СН або N; М - СН або N; за умови, що L і М не є обидва СН;
R1 - гідроген, С1-6алкіл [як варіант, заміщений фенілом {який сам, як варіант, заміщений галогеном}], S(О)2R6, S(О)2NHR7, C(О)R7, С(О)2(С1-6алкіл) або C(О)NHR7; і коли М означає СН,
R1 може також бути NHS(О)2R6, NHS(О)2NHR7, NHC(О)R7 або NHC(О)NHR7;
R2 - феніл або гетероарил, кожний з яких, як варіант, може бути заміщений галогеном, С1-4алкілом, С1-4алкоксилом, S(O)n(С1-4алкілом), нітрогрупою, ціаногрупою або СF3;
R3 - гідроген або С1-4алкіл;
R4 - гідроген, метил, етил, аліл або циклопропіл;
R5 - феніл, гетероарил, феніл(С1-2)алкіл або гетероарил(С1-2)алкіл; де фенільне і гетероарильне кільця, як варіант, заміщені галогеном, ціаногрупою, нітрогрупою, гідроксигрупою, С1-4алкілом, С1-4алкоксилом, S(О)k(С1-4алкілом), S(O)2NR8R9, NHS(O)2(С1-4алкілом), NH2, NH(С1-4алкілом), N(С1-4алкіл)2, NHC(O)NH2, C(O)NH2, С(O)NН(С1-4алкілом), NHC(O)(С1-4алкілом), СO2Н, СO2(С1-4алкілом), С(O)(С1-4алкілом), СF3, CHF2, CH2F, СН2СFз або ОСF3;
k, m і n незалежно дорівнюють 0, 1 або 2;
R6 - С1-6алкіл [як варіант, заміщений фенілом {який сам, як варіант, заміщений галогеном}], С3-7циклоалкіл, феніл {як варіант, заміщений галогеном};
R7 - гідроген, С1-6алкіл [як варіант, заміщений фенілом {який сам, як варіант, заміщений галогеном}], С3-7цикпоалкіл, феніл {як варіант, заміщений галогеном};
R8 і R9 є, незалежно, гідрогеном або С1-4алкілом, або разом з атомом нітрогену або оксигену можуть бути з'єднані з утворенням 5- або 6-членного кільця, як варіант, заміщеного С1-4алкілом, С(O)Н або С(O)(С1-4алкілом);
або її фармацевтичнo прийнятна сіль або її сольват;
за умови, що, коли R1 - гідроген або незаміщений алкіл, R4 є гідрогеном, метилом або етилом, L - СН і М - N, тоді фенільна або гетероарильна частина R5 є заміщеною одним з таких замісників: S(О)kС1-4алкіл, NHC(O)NH2, С(O)(С1-4алкіл), CHF2, CH2F, CH2F3 або OCF3, і, як варіант, крім того, заміщеною одним або більше з таких замісників: галоген, ціаногрупа, нітрогрупа, гідроксигрупа, С1-4алкіл, С1-4алкоксил, S(О)kС1-4алкіл, S(O)2NR8R9, NHS(O)2(С1-4алкіл), NH2, NH(С1-4алкіл), N(С1-4алкіл)2, NHC(O)NH2, C(O)NH2, С(O)NН(С1-4алкіл), NHC(O)(С1-4алкіл), СO2Н, СO2(С1-4алкіл), С(O)(С1-4алкіл), СF3, CHF2, CH2F, СН2СFз або OCF3.
2. Сполука за п. 1, яка відрізняється тим, що L є СН.
3. Сполука за п. 1 або п. 2, яка відрізняється тим, що М є N.
4. Сполука за будь-яким з п. 1, 2 або 3, яка відрізняється тим, що R2 є фенілом, як варіант, заміщеним галогеном.
5. Сполука за будь-яким з п. 1, 2, 3 або 4, яка відрізняється тим, що R3 є гідрогеном або метилом.
6. Сполука за будь-яким з п. 1, 2, 3, 4 або 5, яка відрізняється тим, що R4 є етилом.
7. Спосіб одержання сполуки за п. 1, який включає:
і) коли L є N, реакцію сполуки формули (II):
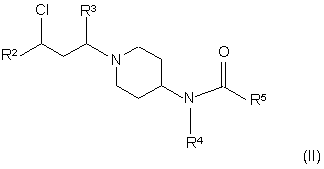
із сполукою формули (III):
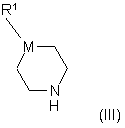
у присутності йодиду натрію та придатної основи у придатному розчиннику;
іі) коли L є СН, реакцію сполуки формули (IV):
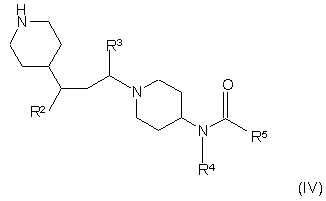
з:
a) кислотою формули R1СO2H у присутності придатного сполучного агента, придатної основи у придатному розчиннику;
b) кислотним хлоридом формули R1С(O)Cl або сульфонілхлоридом формули R1S(O)2Cl у присутності придатної основи у придатному розчиннику; або
c) альдегідом формули R1CHO у присутності NаВН(ОАс)3 (де Ac - С(О)СН3) і оцтовою кислотою у придатному розчиннику;
ііі) сполучення сполуки формули (V):
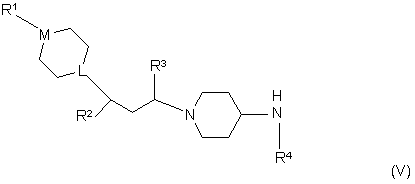
з:
a) кислотою формули R5СО2Н у присутності придатного сполучного агента, придатної основи у придатному розчиннику; або
b) кислотним хлоридом формули R5С(О)Сl у присутності придатної основи у придатному розчиннику.
8. Фармацевтична композиція для застосування в регулюванні активності CCR5 рецепторів, яка містить сполуку за п. 1 або її фармацевтично прийнятну сіль або сольват і фармацевтично прийнятний ад'ювант, розріджувач або носій.
9. Сполука за п. 1 або її фармацевтично прийнятна сіль або сольват, призначені для застосування як медикаменту.
10. Сполука за п. 1 або її фармацевтично прийнятна сіль або сольват, призначені для застосування у виробництві медикаменту для застосування у терапії.
11. Спосіб лікування хворобливого стану, опосередкованого CCR5, який полягає у введенні, пацієнту, що потребує такого лікування, ефективної кількості сполуки за п. 1 або її фармацевтично прийнятної солі або сольвату.
12. Інтермедіат формули (V):
 ,
,
де L, М, R1, R2, R3 і R4 є такими, як визначено у п. 1.
Текст
1. Сполука формули (І): C2 2 (19) 1 3 77969 4 H ном}], С3-7цикпоалкіл, феніл {як варіант, заміщений N галогеном}; R3 8 9 R і R є, незалежно, гідрогеном або С 1-4алкілом, O N або разом з атомом нітрогену або оксигену можуть R2 бути з'єднані з утворенням 5- або 6-членного кільN R5 ця, як варіант, заміщеного С 1-4алкілом, С(O)Н або R4 С(O)(С1-4алкілом); (IV) або її фармацевтичнo прийнятна сіль або її сольз: ват; a) кислотою формули R1СO2H у присутності приза умови, що, коли R1 - гідроген або незаміщений датного сполучного агента, придатної основи у алкіл, R4 є гідрогеном, метилом або етилом, L - СН придатному розчиннику; і М - N, тоді фенільна або гетероарильна частина b) кислотним хлоридом формули R1С(O)Cl або R5 є заміщеною одним з таких замісників: S(О) kС1сульфонілхлоридом формули R1S(O)2Cl у присут4алкіл, NHC(O)NH 2, С(O)(С 1-4алкіл), CHF2, CH 2F, ності придатної основи у придатному розчиннику; CH2F3 або OCF3 , і, як варіант, крім того, заміщеною або одним або більше з таких замісників: галоген, ціаc) альдегідом формули R1CHO у присутності ногрупа, нітрогрупа, гідроксигрупа, С1-4алкіл, С1NаВН(ОАс)3 (де Ac - С(О)СН3) і оцтовою кислотою 8 9 4алкоксил, S(О)kС 1-4алкіл, S(O)2NR R , NHS(O) 2(С 1у придатному розчиннику; NH2, NH(С1-4алкіл), N(С1-4алкіл)2, 4алкіл), ііі) сполучення сполуки формули (V): R NHC(O)NH2, C(O)NH2, С(O)NН(С1-4алкіл), M NHC(O)(С1-4алкіл), СO2Н, СO2(С1-4алкіл), С(O)(С1R L 4алкіл), СF3, CHF2, CH 2F, СН 2СFз або OCF 3. H 2. Сполука за п.1, яка відрізняється тим, що L є N R N СН. R 3. Сполука за п.1 або п.2, яка відрізняється тим, (V) що М є N. з: a) кислотою формули R5СО2Н у присутності при4. Сполука за будь-яким з п.1, 2 або 3, яка відріз2 датного сполучного агента, придатної основи у няється тим, що R є фенілом, як варіант, заміщеним галогеном. придатному розчиннику; або 5. Сполука за будь-яким з п.1, 2, 3 або 4, яка відb) кислотним хлоридом формули R5С(О)Сl у при3 різняється тим, що R є гідрогеном або метилом. сутності придатної основи у придатному розчиннику. 6. Сполука за будь-яким з п.1, 2, 3, 4 або 5, яка 8. Фармацевтична композиція для застосування в відрізняє ться тим, що R4 є етилом. 7. Спосіб одержання сполуки за п.1, який включає: регулюванні активності CCR5 рецепторів, яка місі) коли L є N, реакцію сполуки формули (II): тить сполуку за п.1 або її фармацевтично прийняCl R3 тну сіль або сольват і фармацевтично прийнятний ад'ювант, розріджувач або носій. 2 O R N 9. Сполука за п.1 або її фармацевтично прийнятна сіль або сольват, призначені для застосування як N R5 медикаменту. R4 10. Сполука за п.1 або її фармацевтично прийнят(II) на сіль або сольват, призначені для застосування із сполукою формули (III): у виробництві медикаменту для застосування у 1 R терапії. M 11. Спосіб лікування хворобливого стану, опосередкованого CCR5, який полягає у введенні, паціN єнту, що потребує такого лікування, ефективної H кількості сполуки за п.1 або її фармацевтично при(III) йнятної солі або сольвату. у присутності йодиду натрію та придатної основи у 12. Інтермедіат формули (V): придатному розчиннику; R іі) коли L є СН, реакцію сполуки формули (IV): M 1 3 2 4 1 L R2 R3 N H N R4 (V) , де L, М, R1, R2, R3 і R4 є такими, як визначено у п.1. Винахід стосується гетероциклічних похідних, що мають фармацевтичну активність, способів отримання таких похідних, фармацевтичних композиції, що містять такі похідні і застосування таких похідних як активних терапевтичних засобів. Фармацевтично активні похідні піперидину [описано у PCT/SE01/01053, ЕР-А1-1013276, WO00/08013, WO99/38514 і WO99/04794]. Хемокіни є хемотактичними цитокінами, які вивільняються широким різноманіттям клітин для 5 77969 6 залучення макрофагів, Т-клітин, еозинофілів, бафенілом (який сам, як варіант, заміщений галогезофілів і нейрофілів до місця запалення, і також ном, С1-4алкілом, С1-4алкоксилом, ціаногрупою, грають роль у дозріванні клітин імунної системи. нітрогрупою, CF3, OCF 3, (С 1-4алкіл)С(О)МН, Хемокіни грають важливу роль у імунних і запальS(O)2NH2, С1-4алкілтіогрупою, S(О)(С1-4алкіл) або них реакціях при різних хворобах і розладах, s(О)2(С1-4алкіл)) або гетероарил (як варіант, замівключаючи астму і алергічні хвороби, а також такі щений галогеном, С1-4алкілом, С1-4алкоксилом, автоімунні патології, як ревматоїдний артрит і атеціаногрупою, нітрогрупою, CF3, (С1-4алкіл)С(О)МН, росклероз. Ці невеликі виділені молекули утворюS(O)2NH2, С1-4алкілтіогрупою, S(O)(С1-4алкіл) або ють надродину протеїнів з 8-14кДа, що характериS(О)2(С1-4алкіл)), феніл (як варіант, заміщений зується консервативною чотирицистеїновою галогеном, С1-4алкілом, С1-4алкоксилом, ціаногруструктурою. Надродину хемокінів можна розділити пою, нітрогрупою, CF3, OCF3, (С1-4алкіл)С(О)NН, на дві головні групи, що відрізняються різними S(O)2NH2, С1-4алкілтіогрупою, S(О)(С1-4алкіл) або S(О)2(С1-4алкіл)), гетероарил (як варіант, заміщеструктурними ознаками: Cys-X-Cys (C-X-C, або a) і ний галогеном, С1-4алкілом, С1-4алкоксилом, ціаноCys-Cys (C-C, або β) родини. Вони відрізняються групою, нітрогрупою, CF3, (С1-4алкіл)С(О)NН, наявністю одиничної амінокислотної вставки між S(O)2NH2, С1-4алкілтіогрупою, S(О)( С1-4алкіл) або ближньою NH-парою залишків цистеїну і мають S(О)2(С1-4алкіл)), S(O)2R6, S(O)2NR10R11 , C(O)R7, схожі послідовності. С-Х-С-хемокіни включають кілька потужних С(О)2(С1-4алкіл) (наприклад, третбутоксикарбоніл), С(О)2(феніл(С 1-2алкіл)) (наприхемоатрактантів і активаторів нейрофілів, наприклад, бензилоксикарбоніл) або C(O)NHR7; і коли Μ клад, інтерлейкіну-8 (IL-8) і активуючого нейрофіли - СН, R1 може також бути NHSO2R6, NHS(O)2NHR7, пептиду 2 (ΝΑΡ-2). NHC(O)R7 або NHC(O)NHR7; С-С-хемокіни включають потужні хемоатрактанти моноцитів і лімфоцитів, але не таких нейроR2 - феніл або гетероарил, кожний з яких, як варіант, може бути заміщений галогеном, С1філів, як хемотактичні протеїни моноциту людини 1-3 (МСР-1, МСР-2 і МСР-3), РАНТВ (Регульовані 4алкілом, С 1-4алкоксилом, S(O)n(С 1-4алкіл), нітрогрупою, ціаногрупою або CF3; при активуванні, Нормальні Т-експресовані і видіR3 - гідроген або С1-4алкіл; лені секреторно), еотаксин і запальні протеїни маR4 - гідроген, метил, етил, аліл або циклопрокрофагу 1a і 1β (ΜΙΡ-1a і Μ1Ρ-1β). піл; Дослідження показали, що дії хемокінів опосеR5 - феніл, гетероарил, фенілNН, гетероредковуються субродинами сполучених GарилNН, феніл(С 1-2)алкіл, гетероарил(С1-2)алкіл, протеїном рецепторів, серед яких є рецептори, феніл(С 1-2алкіл)NН або гетероарил(С1-2алкіл)NН; позначені CCR1, CCR2, CCR2A, CCR2B, CCR3, де фенільне і гетероарильне кільця R5, як варіант, CCR4, CCR5, CCR6, CCR7, CCR8, CCR9, CCR10, заміщені галогеном, ціаногрупою, нітрогрупою, CXCR1, CXCR2, CXCR3 і CXCR4. Ці рецептори гідроксигрупою, С1-4алкілом, С1-4алкоксилом, можуть бути важливими об'єктами розробки ліків, S(О)k(С1- 4алкіл), S(O)2NR8R9, NНS(О)2(С1-4алкіл), оскільки агенти, що модулюють ці рецептори, моNH2, NН(С1-4алкіл), N(С1-4алкiл)2, NHC(O)NH2, жуть бути корисними для лікування розладів і хвоC(O)NH2, С(О)NН(С1-4алкіл), NНС(О)(С1-4алкіл), роби, згаданих вище . СО2Н, СО2(С1-4алкіл), С(О)(С1-4алкіл), CF3, CHF2, Рецептор CCR5 експресується на ТCH2F, CH2CF3 або OCF3; k, m і n, незалежно дорівлімфоцитах, моноцитах, макрофагах, дендричних нюють 0, 1 або 2; клітинах, мікроглії і клітинах інших типів. Вони виR6 - С1-6алкіл (як варіант, заміщений галогеном являють і реагують на декілька хемокінів, голо(наприклад, флуором), С1-4алкоксилом, фенілом вним чином, типу РАНТВ, запальні протеїни мак(який, як варіант, сам заміщений галогеном, С1рофагу МІР-1a і Μ1Ρ-1β і протеїн 2 4алкілом, С 1-4алкоксилом, ціаногрупою, нітрогрухемоатрактанту моноциту (МСР-2). пою, CF3, OCF3, (С1-4алкілом)С(О)NН, S(O)2NH2, Це призводить до залучення клітин імунної сиС1-4алкілтіогрупою, S(О)(С1-4алкілом) або S(О)2(С1стем до місця хвороби. У багатьох хворобах вони 4алкіл)) або гетероарил (який, як варіант, сам зає клітинами, що експресують CCR5, які беруть міщений галогеном, С1-4алкілом, С1-4алкоксилом, участь, безпосередньо або опосередковано у поціаногрупою, нітрогрупою, CF3, (С1шкодженні тканини. Отже, інгібування залучення S(O)2NH2, С1-4алкілтіогрупою, 4алкілом)С(O)NН, цих клітин є корисним при багатьох хворобах. S(O)(С1-4алкіл) або S(O)2(С1-4алкіл)), С3CCR5 є також співрецептором для ВІЛ-1 і ін7циклоалкіл, піраніл, феніл (як варіант, заміщений ших вірусів, дозволяючи цим вірусам проникати у галогеном, С1-4алкілом, С1-4алкоксилом, ціаногруклітини. Блокування рецептора антагоністом CCR5 пою, нітрогрупою, CF3, OCF3, (С1-4алкіл)С(О)NН, або індукування інтерналізації рецептора агонісS(O)2NH2, С1-4алкілтіогрупою, S(О)(С1-4алкіл) або том CCR5 захищає клітини від вірусної інфекції. S(О)2(С1-4алкіл)) або гетероарил (як варіант, заміВинахід стосується сполуки формули (І): щений галогеном, С1-4алкілом, С1-4алкоксилом, ціаногрупою, нітрогрупою, CF3, (С1-4алкіл)С(О)NН, (I) S(O)2NH2, С1-4алкілтіогрупою, S(O)(С1-4алкіл) або S(О)2(С1-4алкіл)); R7 - гідроген, С1-6алкіл (як варіант, заміщений де галогеном (наприклад, флуором), С1-4алкоксилом, L - СН або Ν; Μ - СН або Ν; за умови, що L і Μ фенілом (який сам, як варіант, заміщений галогене є обидві СН; ном, С1-4алкілом, С1-4алкоксилом, ціаногрупою, R1 - гідроген, С1-6алкіл (як варіант, заміщений нітрогрупою, CF3, OCF3, (С1-4алкіл)С(О)NН, 7 77969 8 S(O)2NH2, С1-4алкілтіогрупою, S(O)(С1-4алкіл) або груп у. Флуоралкілом є, наприклад, CF3 або S(О)2(С1-4алкіл)) або гетероарил (який, як варіант, CH2CF3. сам заміщений галогеном, С1-4алкілом, С1Циклоалкілом є, наприклад, циклопропіл, циклопентил або циклогексил. 4алкоксилом, ціаногрупою, нітрогрупою, CF3, (С 1S(O)2NH2, С1-4алкілтіогрупою, Феніл(С 1-2алкіл)алкілом є, наприклад, бензил, 4алкіл)C(O)NH, S(О)(С1-4алкілом) або S(О)2(С1-4алкіл)), С31-(феніл)ет-1-іл або 1-(феніл)ет-2-іл. Гетероарил(С1-2алкіл)алкілом є, наприклад, пі7циклоалкіл, піраніл, феніл (як варіант, заміщений галогеном, С1-4алкілом, С1-4алкоксилом, ціаногруридинілметил, піридинілетил або 1-(піридиніл)етпою, нітрогрупою, CF3, OCF3, (С1-4алкіл)С(О)NН, 2-іл. S(O)2NH2, С1-4алкілтіогрупою, S(О)(С1-4алкіл) або Феніл(С 1-2алкіл)NН є, наприклад, бензиламіно. S(О)2(С1-4алкіл)) або гетероарил (як варіант, заміГетероарил(С1-2алкіл)NН є, наприклад, піридищений галогеном, С1-4алкілом, С1-4алкоксилом, нілСН2NН, піримідинілСН 2NН або піридиціаногрупою, нітрогрупою, CF3, (С1-4алкіл)С(О)NН, нілСН(СН3)NН. S(O)2NH2, С1-4алкілтіогрупою, S(O)(С1-4алкіл) або Гетероарил є ароматичним 5- або 6-членним S(О)2(С1-4алкіл)); кільцем, як варіант, злитим з одним або більше R8 і R9 є, незалежно, гідрогеном або С1іншими кільцями, які містять щонайменше один гетероатом, вибраний з групи, що включає нітро4алкілом, або разом з атомом нітрогену або оксигену можуть бути з'єднані для утворення 5- або 6ген, оксиген і сульфур; або їх N-оксид, або їх Sчленного кільця, як варіант, заміщеного С 1оксид або S-діоксид. Гетероарилом є, наприклад, фурил, тієніл (також відомий як тіофеніл), піроліл, 4алкілом, С(О)Н або С(О)(С 1-4алкіл); R10 і R11 є, незалежно, гідрогеном або С 1тіазоліл, ізотіазоліл, піразоліл, оксазоліл, ізоксазоліл, імідазоліл, [1,2,4]-триазоліл, піридиніл, піримі4алкілом, або можуть бути з'єднані для утворення 5- або 6-членного кільця, як варіант, заміщеного диніл, індоліл, бензо[b]фурил (також відомий як С1-4алкілом або фенілом (де фенільне кільце, як бензофурил), бензо[b]тієніл (також відомий як бенваріант, заміщене галогеном, ціаногрупою, нітрозотієніл або бензотіофеніл), індазоліл, бензімідагрупою, гідроксигрупою, С1-4алкілом, С1золіл, бензотриазоліл, бензоксазоліл, бензотіазоS(О)mС1-4алкілом, S(O)2NH2, ліл, 1,2,3-бензотіадіазоліл, імідазопіридиніл 4алкоксилом, S(O)2NH(С1-4алкіл), S(O)2N(С1-4алкіл)2, NHS(О)2(C1(наприклад, імідазо[1,2а]піридиніл), тієно[3,2NH2, NН(С1-4алкіл), N(С1-4алкіл)2, b]піридин-6-іл, 1,2,3-бензоксадіазоліл (також відо4алкіл), NHC(O)NH2, C(O)NH2, C(O)NH(С1-4алкіл), мий як бензо[1,2,3]тіадіазоліл), 2,1,3NНС(О)(С1-4алкіл), CO2H, СО2(С1-4алкіл), С(О)(С1бензотіадіазоліл, бензофуразан (також відомий як 2,1,3-бензоксадіазоліл), хіноксалініл, піразолопі4алкіл), CF3, CHF2, CH 2F, CH 2CF 3 або OCF3); або її фармацевтично прийнятної солі або її ридин (наприклад, 1Н-піразоло[3,4-b]піридиніл), сольвату; хінолініл, ізохінолініл, нафтиридиніл (наприклад, за умови, що, коли R1 - гідроген або незаміще[1,6]нафтиридиніл або [1,8]нафтиридиніл, бензотіний алкіл, R4 є гідрогеном, метилом або етилом, L азиніл або дибензотіофеніл (також відомий як ди- СН і Μ - Ν, тоді фенільна або гетероарильна часбензотієніл); або їх N-оксид, S-оксид або Sтина R5 є заміщеною одним з таких замісників: діоксид. Гетероарил може також бути піразинілом. S(О)С1-4алкіл, NHC(O)NH2, С(О)(С1-4алкіл), CHF2, Гетероарилом є, наприклад, піридиніл, піримідиCH2Fi CH2CF3 або OCF3, і, як варіант, крім того, ніл, індоліл або бензімідазоліл. заміщеною одним або більше з таких замісників: Згідно з певним аспектом, винахід пропонує галоген, ціаногрупа, нітрогрупа, гідроксигрупа, С1сполуку формули (І), у якій L - СН або Ν; Μ - СН 8 9 або Ν; за умови, що L і Μ не є обидві СН; 4алкіл, С 1-4алкоксилом, S(O)kС 1-4алкіл, S(O)2NR R , NНS(О)2(С1-4алкіл), NH2, NН(С1-4алкіл), N(С1R1 - гідроген, С1-6алкіл (як варіант, заміщений феніл (який сам, як варіант, заміщений галогеном, 4алкіл)2, NHC(O)NH 2, C(O)NH 2, С(О)NН(С 1-4алкіл), NНС(О)(С1-4алкіл), СО2Н, СО2(С1-4алкіл), С(О)(С1С1-4алкілом, С1-4алкоксилом, ціаногрупою, нітрогрупою, CF3, С1-4алкілтіогрупою, S(O)(С1-4алкіл) 4алкіл), CF3, CHF2, CH 2Fi, CH 2CF3 або OCF3. Деякі сполуки винаходу можуть існувати у різабо S(О)2(С1-4алкіл)) або гетероарил (який сам, як них ізомерних формах (таких, як енантіомери, діаваріант, заміщений галогеном, С1-4алкілом, С1стереомери, геометричні ізомери або таутомери). 4алкоксилом, ціаногрупою, нітрогрупою, CF3, С 1Винахід включає всі такі ізомери їх суміші в усіх S(О)(С1-4алкіл) або S(О)2(С14алкілтіогрупою, пропорціях. 4алкіл)), феніл (як варіант, заміщений галогеном, Придатні солі включають кислотно-адитивні С1-4алкілом, С1-4алкоксилом, ціаногрупою, нітросолі, наприклад, гідрохлорид, гідробромід, фосгрупою, CF3, С1-4алкілтіогрупою, S(О)(С1-4алкіл) фат, ацетат, фумарат, малеат, тартрат, цитрат, або S(О)2(С1-4алкіл)), гетероарилом (як варіант, оксалат, метансульфонат або р-толуолсульфонат. заміщеним галогеном, С1-4алкілом, С1Сполуки винаходу можуть існувати як сольва4алкоксилом, ціаногрупою, нітрогрупою, CF3, С 1ти (наприклад, гідрати), і винахід включає всі такі S(O)(С1-4алкіл) або S(О)2(С14алкілтіогрупою, 6 7 7 сольвати. 4алкіл)), S(O)2R ; S(O) 2NHR , C(O)R , -С(О) 2(С 17 1 Алкільні групи і компоненти є прямими або 6алкіл) або C(O)NHR ; і коли Μ - СН, R може також розгалуженими ланцюгами і є, наприклад, метилбути NHS(O)2R 6, NHS(O)2NHR7, NHC(O)R7 або ом, етилом, n-пропілом, ізопропілом, n-бутилом, NHC(O)NHR7; втор-бутилом або трет-бутилом. Абревіатурою R2 - феніл або гетероарил, кожний з яких, як метилу є іноді Me. варіант, може бути заміщений у орто- або метаФлуоралкіл включає, наприклад, 1-6, наприпозиції галогеном, С1-4алкілом, С1-4алкоксилом, клад, 1-3 атоми флуору і містить, наприклад, CF3S(О)n(С1-4алкілом), нітрогрупою, ціаногрупою або 9 77969 10 CF3; C(O)NH(С1-4алкіл), NНС(О)(С1-4алкіл), СО2Н, R3 - гідроген або С1-4алкіл; СО2(С1-4алкіл), С(О)(С1-4алкіл), CF3, CHF2, CH2F, R4 - гідроген, метил, етил, аліл або циклопроCH2CF3 або OCF3. піл; Згідно з ще одним аспектом, винахід пропонує R5 - феніл, гетероарил, фенілNН, гетеросполуку винаходу, у якій, коли L і Μ є обидві N і R 1 арилNН, феніл(С 1-2)алкіл, гетероарил(С1-2)алкіл, є гідрогеном, С1-4алкілом або фенілом (заміщеним феніл(С 1-2алкіл)NН або гетероарил(С1-2алкіл)NН; 0,1 або 2-ма замісниками, вибраними з списку, де фенільне і гетероарильне кільця R5, як варіант, який складають: флуор, хлор, С1-4алкіл, С1заміщені галогеном, ціаногрупою, нітрогрупою, ціаногрупа, CF3, OCF 3, (С14алкоксил, гідроксигрупою, С1-4алкілом, С1-4алкоксилом, 4алкіл)С(О)NН і S(O)2NH 2, то фенільний або гетеS(O)kС1- 4алкілом, S(O)2NR8R9, NНS(О)2(С1-4алкіл), роарильний компонент R5 несе як замісника NH2, NН(С1-4алкіл), N(С1-4алкіл)2, NHC(O)NH2, S(О)2(С1-4алкіл), і, як варіант, крім того, одного або C(O)NH2, С(О)NН(С1-4алкіл), NHС(О)(С1-4алкіл), більше додаткових замісників. CO2H, СО2(С1-4алкіл), С(О)(С1-4алкіл), CF3, CHF2, Згідно з одним з аспектів винаходу, ге тероCH2F, CH2CF3 або OCF 3; арилом є піроліл тієніл, імідазоліл, тіазоліл, ізоксаR8 і R9 є, незалежно, гідрогеном або С1золіл, піридиніл, піримідиніл, піразиніл або хінолініл. 4алкілом, або разом з атомом нітрогену або оксигену можуть бути з'єднані для утворення 5- або 6Згідно з іншим аспектом, Μ - N і L - СН або N. членного кільця, як варіант, заміщеного С 1Згідно з ще одним аспектом L і Μ обидва є N. Згідно з подальшим аспектом L - СН і Μ - N. 4алкілом, С(О)Н або С(О)(С 1-4алкіл); k і n незалежно дорівнюють 0,1 або 2; Згідно з ще одним аспектом, L - N і Μ - СН. R6 - С1-4алкіл (як варіант, заміщений фенілом Згідно з іншим аспектом винаходу, R1 - гідро(який сам, як варіант, заміщений галогеном, С1ген, С1-6алкіл (як варіант, заміщений фенілом (який сам, як варіант, заміщений галогеном)), S(O)2R6, 4алкілом, С 1-4алкоксилом, ціаногрупою, нітрогрупою, CF3, С1-4алкілтіогрупою, S(О)(С1-4алкіл) або S(O)2NHR7, C(O)R 7 , С(О)2(С 1-6алкіл) або C(O)NHR7; S(О)2(С1-4алкіл)) або гетероарил (як варіант, заміі, коли Μ - СН, R1 може також бути NHS(O)2R6, щений галогеном, С1-4алкілом, С1-4алкоксилом, NHS(O)2NHR7, NHC(O)R7 або NHC(O)NHR7; R6 ціаногрупою, нітрогрупою, CF3, С1-4алкілтіогрупою, С1-6алкіл (як варіант, заміщений фенілом (який S(О)(С1-4алкіл) або S(О)2(С1-4алкіл)), С1сам, як варіант, заміщений галогеном)), С34циклоалкіл, феніл (як варіант, заміщений галоге7циклоалкіл, феніл (як варіант, заміщений галогеном, С1-4алкілом, С1-4алкоксилом, ціаногрупою, ном); і R7 - гідроген, С1-6алкіл (як варіант, заміщенітрогрупою, CF3, С1-4алкілтіогрупою, S(О)(С1ний фенілом (який сам, як варіант, заміщений галогеном)), С3-7циклоалкіл, феніл (як варіант, 4алкіл) або S(О)2(С 1-4алкіл)) або гетероарил (як варіант, заміщений галогеном, С1-4алкілом, С1заміщений галогеном). Згідно с подальшим аспектом винаходу, R1 4алкоксилом, ціаногрупою, нітрогрупою, CF3, С 1S(О)(С1-4алкіл) або S(О)2(С1С1-6алкіл (заміщений фенілом (який сам, як варі4алкілтіогрупою, ант, заміщений галогеном)), S(O)2R6, S(O)2NHR7, 4алкіл)); 7 R - гідроген, С1-6алкіл (як варіант, заміщений C(O)R7, С(О)2(С1-6алкіл) або C(O)NHR 7; і, коли Μ фенілом (який, як варіант, сам заміщений галогеСН, R1 може також бути NHS(O)2R6, NHS(O)2NHR7, ном, С1-4алкілом, С1-4алкоксилом, ціаногрупою, NHC(O)R7 або NHC(O)NHR7; R6 - С1-6алкіл (як ванітрогрупою, CF3, С1-4алкілтіогрупою, S(О)(С1ріант, заміщений фенілом (який, як варіант, заміщений галогеном)), С3-7циклоалкіл, феніл (як варі4алкіл) або S(О)2(С 1-4алкіл)) або гетероарил (який, як варіант, заміщений галогеном, С1-4алкілом, С1ант, заміщений галогеном); і R7 - гідроген, С1-6алкіл алкоксилом, ціаногрупою, нітрогрупою, CF3, С1(як варіант, заміщений фенілом (який, як варіант, 4 S(О)(С1-4алкіл) або S(О)2(С1сам заміщений галогеном)), С3-7циклоалкіл, феніл 4алкілтіогрупою, (як варіант, заміщений галогеном). 4алкіл)), С 1-4циклоалкіл, феніл (як варіант, заміщений галогеном, С1-4алкілом, С1-4алкоксилом, ціаноЗгідно з іншим аспект винаходу, R1 - S(O)2R6 , групою, нітрогрупою, CF3, С1-4алкілтіогрупою, C(O)R7, С(О)2(С1-6алкіл) або C(O)NHR 7; і, коли Μ S(О)(С1-4алкіл) або S(О)2(С1-4алкіл)) або гетероСН, R1 може також бути NHSC(O)R 6 або арил (як варіант, заміщений галогеном, С1NHC(O)R7; R6 і R7 є такими, що визначені вище. Згідно з одним з аспектів винаходу, R1 - гідро4алкілом, С 1-4алкоксилом, ціаногрупою, нітрогрупою, CF3, С1-4алкілтіогрупою, S(O)(С1-4алкіл) або ген, С1-6алкіл (як варіант, заміщений фенілом S(O)2(С1-4алкіл)); (який, як варіант, сам заміщений галогеном)), або її фармацевтично прийнятну сіль або соS(O)2R6, C(O)R7 , С(O)2(С1- 6алкіл) або C(O)NHR7; і, льват; коли Μ - СН, R1 може також бути NHS(O)2R6 або 1 за умови, що, коли R - гідроген або незаміщеNHC(O)R7; R6 - С1-6алкіл, (як варіант, заміщений 4 ний алкіл, R є гідрогеном, метилом або етилом, L фенілом (який сам, як варіант, заміщений галоге- СН і Μ - Ν, то тоді фенільна або гетероарильна ном)),С3-7циклоалкіл, феніл (як варіант, заміщений частина R5 є заміщеною одним з таких замісників: галогеном); R7 - гідроген, С1-6алкіл (як варіант, заS(O)kС1- 4алкіл, NHC(O)NH2, С(О)(С1-4алкіл), CHF2, міщений фенілом (який сам, як варіант, заміщений CH2F, CH2CF3 або OCF3, і, як варіант, крім того, є галогеном)), С3-7циклоалкіл, феніл (як варіант, зазаміщеною одним або більше таких замісників: міщений галогеном). ціаногрупою, нітрогрупою, гідроксигрупою, С1Згідно з подальшим аспектом, R1 - феніл (як С1-4алкоксилом, S(О)kС1-4алкілом, варіант, заміщений галогеном (наприклад, флуо4алкілом, S(O)2NR8R9, NНS(О)2(С1-4алкіл), NH2, NН(С1ром), С1-4алкілом (наприклад, метилом), С1N(С1-4алкіл)2, NHC(O)NH2, C(O)NH2, 4алкіл), 4алкоксилом (наприклад, метоксилом), CF3 або 11 77969 12 OCF3), S(О)2(С1-4алкіл) (наприклад, S(O)2CH3, гетероарил (як варіант, заміщений галогеном, С1S(O)2CH2CH3 або S(O)2CH(CH3)2), S(O) 2(С1або (С1-4алкіл)С(О)NН), S(O)2R6, 4алкілом флуоралкіл) (наприклад, S(O)2CF3 або S(O)2NR10R11, C(O)R7 або C(O)NHR7; і, коли Μ 4 S(O)2CH2CF3), S(О) 2 фенілом (як варіант, заміщеСН, R1 може також бути NHC(O)R7; R6 - С1-4алкіл ним (наприклад, монозаміщеним) галогеном (на(як варіант, заміщений галогеном (наприклад, приклад, хлором), ціаногрупою, С1-4алкілом, С1флуором), фенілом (який сам, як варіант, заміщений галогеном, С1-4алкілом, С1-4алкоксилом, ціано4алкоксилом, CF3, OCF 3, S(О)2(С 1-4алкіл) (наприклад, S(O)2CH3 або S(O)2CH2CH2CH3) або S(О) 2(С1групою, нітрогрупою, CF 3, OCF3, (С1-4алкіл)С(О)NН, S(O)2NH2 або S(О)2(С1-4алкіл)) або гетероарил (як 4флуоралкіл) (наприклад, S(O)2CH 2CF3))), бензил (як варіант, заміщений галогеном (наприклад, хловаріант, заміщений галогеном, С1-4алкілом або (С1ром або флуором), С1-4алкіл, С1-4алкоксил (напри4алкіл)С(О)NН)), феніл (як варіант, заміщений гаклад, метоксил), CF3 або OCF3), бензоїл (як варілогеном, С1-4алкілом, С1-4алкоксилом, ціаногруант, заміщений галогеном (наприклад, хлором або пою, нітрогрупою, CF3, OCF3, (С1-4алкіл)С(О)NН, флуором), С1-4алкілом (наприклад, метилом), С1S(O)2NH2 або S(О)2(С1-4алкіл)) або гетероарил (як варіант, заміщений галогеном, С1-4алкілом або (С14алкоксилом, CF3 або OCF3), С(О)NНфеніл (як ва7 ріант, заміщений галогеном (наприклад, флуором), 4алкіл)С(O)NН); R - гідроген, С 1-6алкіл (як варіант, С1-4алкілом, С1-4алкоксилом, CF3 або OCF3), заміщений галогеном (наприклад, флуором), С1S(О)2тіо феніл, СН2піридиніл, СН2хінолініл або 4алкоксилом, фенілом (який сам, як варіант, заміСН2тіазоліл. щений галогеном, С1-4алкілом, С1-4алкоксилом, Згідно з іншим аспектом, R1 - феніл (як варіціаногрупою, нітрогрупою, CF3, OCF3 , (С1ант, заміщений (наприклад, монозаміщений) гало4алкіл)С(О)МН, S(O)2NH 2 або 8(О)2(Сі^алкіл)) або геном (наприклад, флуором), С1-4алкілом (напригетероарил (як варіант, заміщений галогеном, С1клад, метилом) або С1-4алкоксилом (наприклад, 4алкілом або (С 1-4алкіл)С(О)NН)), С 3-7циклоалкіл, метоксилом)); S(О)2(С1-4алкіл) (наприклад, піраніл, феніл (як варіант, заміщений галогеном, S(O)2CH3, S(O)2CH2CH3 або S(O)2CH(CH3)2), С1-4алкілом, С1-4алкоксилом, ціаногрупою, нітроS(О)2(С1-4 флуоралкіл) (наприклад, S(O)2CFs або групою, CF3 , OCF 3, (С1-4алкіл)С(О)NН, S(O)2NH2 S(O)2CH2CF3), S(О) 2 фенілом (як варіант, заміщеабо S(О)2(С1-4алкіл)) або гетероарил (як варіант, ним (наприклад, монозаміщеним) галогеном (назаміщений галогеном, С1-4алкілом або (С110 приклад, хлором), ціаногрупою, CF3, OCF3, і R11 є незалежно гідрогеном 4алкіл)С(О)NН); і R S(О)2(С1-4алкіл) (наприклад, S(O)2CH3 або або С1-4алкілом. S(O)2CH2CH2CH3) або S(О)2(С1-4флуоралкіл) (наЗгідно з ще одним аспектом, R1 - феніл (як ваприклад, S(O)2CH2CF3)), бензилом (як варіант, ріант, заміщений (наприклад, моно-заміщений) заміщеним галогеном (наприклад, хлором або галогеном (наприклад, флуором) або С1-4алкілом флуором) або С1-4алкоксилом (наприклад, меток(наприклад, метилом)), S(О)2(С1-4алкіл) (наприсилом)), бензоїл (як варіант, заміщений галогеном клад, S(O)2CH3 або S(O)2CH2CH3), S(О)2(С1(наприклад, хлором або флуором) або С1-4алкілом 4флуоралкіл). (наприклад, S(O)2CF3), S(О)2 феніл (наприклад, метил)), С(О)NНфеніл (як варіант, (як варіант, заміщений (наприклад, монозаміщезаміщений галогеном (наприклад, флуором)), ний) CF3 або OCF3), бензил, бензоїл (як варіант, S(О)2тіо феніл, СН2піридиніл, СН2хінолініл або заміщений галогеном (наприклад, хлором або СН2тіазоліл. флуором)) або С(О)NНфеніл (як варіант, заміщеЗгідно з ще одним аспектом, R1 - феніл (як ваний галогеном (наприклад, флуором)). ріант, заміщений (наприклад, монозаміщений) гаЗгідно з іншим аспектом винаходу, R2 - феніл логеном (наприклад, флуором) або С1-4алкілом або гетероарил, кожний з яких є, як варіант, замі(наприклад, метилом)), S(O)2(С1-4алкіл) (наприщений у орто- або мета-позиці галогеном, С1клад, S(O)2CH3, S(O)2CH2CH3 або S(O)2CH(CH3)2), 4алкілом, С 1-4алкоксилом, S(О)n(С 1-4алкіл), нітроS(О)2(С1-4 флуоралкіл) (наприклад, S(O)2CF3 або групою, ціаногрупою або CF3; де n дорівнює 0, 1 S(O)2CH2CF3), S(О)2 феніл (як варіант, заміщений або 2, наприклад 0 або 2 (орто- і мета-позиції є (наприклад, монозаміщений) CF3, OCF3 або визначаються відносно позиції приєднання цього S(О)2(С1-4алкіл) (наприклад, S(O)2CH3)), бензил (як кільця до структури формули (І). варіант, заміщений галогеном (наприклад, хлором Згідно подальшим аспектом, R2, як варіант, або флуором) або С1-4алкоксилом (наприклад, заміщена фенілом (наприклад, як варіант, галогеметоксилом)), бензоїл (як варіант, заміщений галоном) (наприклад, хлором або флуором), ціаногругеном (наприклад, хлором або флуором)), пою, метилом, етилом, метоксилом, етоксилом С(О)NНфеніл (як варіант, заміщений галогеном або CF3). Згідно з одним з аспектів, заміщення (наприклад, флуором)), СН2піридинiл, СН2хінолініл відбувається на орто- або мета-позиції фенільного або СН2тіазоліл. кільця. Згідно з подальшим аспектом R1 - гідроген, С1Згідно з подальшим аспектом, R2, заміщена фенілом, наприклад, як варіант, галогеном або 6алкіл (як варіант, заміщений фенілом (який сам, як варіант, заміщений галогеном, С1-4алкілом, С1CF3. Наприклад, R2 є 3-флуорфенілом, 3хлорфенілом, 4-флуорфенілом або 4-CF34алкоксилом, ціаногрупою, нітрогрупою, CF3, OCF3, (С1-4алкіл)С(O)NН, S(O)2NH2 або S(О)2(С1-4алкіл)) фенілом. Згідно з іншим аспектом, R2 - феніл, 3або гетероарил (сам, як варіант, заміщений галофлуорфеніл, 4-флуорфеніл, 3-хлорфеніл, 3,4геном, С1-4алкіл або (С1-4алкіл)С(О)NН)), феніл (як дифлуорфеніл або 3,5-дифлуорфеніл. Згідно з ще варіант, заміщений галогеном, С1-4алкілом, С1одним аспектом, R2 - феніл, 3-флуорфеніл, 4флуорфеніл, 3,4-дифлуорфеніл або 3,54алкоксилом, ціаногрупою, нітрогрупою, CF3, OCF3, (С1-4алкіл)С(О)NН, S(O)2NH2 або S(О)2(С1-4алкіл)), дифлуорфеніл. Згідно з іншим аспектом винаходу, 13 77969 14 R2 - феніл або 3-флуорфеніл. незалежно гідрогеном або С 1-4алкілом, або разом Згідно з подальшим аспектом винаходу, R3 є атомом нітрогену або оксигену можуть бути з'єдгідрогеном або метилом. Згідно з іншим аспектом нані для утворення 5- або 6-членного кільця, як винаходу, коли R3 - С1-4алкіл (наприклад, метил), варіант, заміщеного С 1-4алкілом, С(О)Н або карбон, до якого приєднано R3, має абсолютну RС(О)(С1-4алкіл). конфігурацію. Згідно з ще одним аспектом винахоЗгідно з іншим аспектом, R5 - феніл або бен3 ду, R - гідроген. зил; де ароматичні кільця, як варіант, заміщені Згідно з ще одним аспектом винаходу, R4 є галогеном, ціаногрупою, нітрогрупою, гідроксигруетилом. пою, С1-4алкілом, С1-4алкоксилом, S(О)2С18 9 Згідно з одним з аспектів, винахід включає 4алкілом, S(O)2NR R , NHS(O)2(С 1-4алкіл), NH 2, сполуку винаходу, у якій R5 - феніл(С 1-2)алкіл, феNН(С1-4алкіл), N(С1-4алкіл)2, NHC(O)NH2, C(O)NH2, ніл (С1-2алкіл)NН, феніл, гетероарил або гетеро С(O)NН(С1-4алкіл), NНС(О)( С1-4алкіл), СО2Н, арил(С 1-2)алкіл; де фенільне і гетероарильне кільСО2(С1-4алкіл), С(О)(С1-4алкіл), CF3; і R8 і. R9 є неця, як варіант, заміщені галогеном, ціаногрупою, залежно гідрогеном або С1-4алкілом. нітрогрупою, гідроксигрупою, С1-4алкілом, С1Згідно з наступним аспектом, R5 – 8 9 S(O)kС1-4алкілом, S(O)2NR R , NHСН2феніл, де фенільне кільце, як варіант, за4алкоксилом, NHS(O)2(С1-4алкілом), NH2, NН(С1-4алкілом), N(С1міщене галогеном, ціаногрупою, нітрогрупою, гідроксигрупою, С1-4алкілом, С1-4алкоксилом, 4алкіл)2, NHC(O)NH 2, C(O)2, С(О)NН(С 1-4алкіл), NНС(О)(С1-4алкіл), СО2Н, СO2(С1-4алкіл), С(О)(С1S(О)2алкілом, S(O)2NR8R9, NНS(О)2(С1-4алкіл), NH2, 8 NН(С1-4алкіл), N(С1-4алкіл)2, NHC(O)NH2, C(O)NH2, 4алкіл), CF3, CHF2, CHF3, CH 2CF3 або OCF3; і R і 9 R є незалежно гідрогеном або С 1-4алкілом, або С(О)NН(С1-4алкіл), NНС(O)(С1-4алкіл), СО2Н, разом з атомом нітрогену або оксигену можуть СO2(С1-4алкіл), С(О)(С1-4алкіл), CF3; і R8 і R9 є небути з'єднані для утворення 5- або 6-членного кізалежно гідрогеном або С1-4алкілом. льця, як варіант, заміщеного С 1-4алкілом, С(О)Н Згідно з ще одним аспектом, R5 є бензил, де або С(О)(С1-4алкіл); k дорівнює 0, 1 або 2 (наприфенільне кільце, як варіант, заміщене галогеном, клад, 2). ціаногрупою, нітрогрупою, гідроксигрупою, С1Згідно з іншим аспектом, винахід включає споС1-4алкоксилом, S(O)2C1-4алкілом, 4алкілом, луку винаходу, у якій R5 - феніл(С 1-2)алкіл або феS(O)NR8R9, NHS(O)2(С1-4алкіл), NH2, NН(С1-4алкіл), 5 ніл(С1-2алкіл)NН; де феніл кілець R , як варіант, N(С1-4алкіл)2, NHC(O)NH2, C(O)NH2, С(О)NН(С1заміщений галогеном, ціаногрупою, нітрогрупою, 4алкіл), NНС(О)(С 1-4алкіл), СО2Н, СO2(С 1-4алкіл), гідроксигрупою, С1-4алкілом, С1-4алкоксилом, С(О)(С1-4алкіл), CF3; і R8 і R9 є незалежно гідрогеS(O)kС1- 4алкілом, S(O)2NR8R9, NHS(O)2(С1-4алкіл), ном або С 1-4алкілом. NH2, NН(С1-4алкіл), N(С1-4алкіл)2, NHC(O)NH2, Згідно з іншим аспектом, R5 - NНСН2феніл, де C(O)NH2, С(О)NН(С1-4алкіл), NНС(О)(С1-4алкіл), ароматичне кільце, як варіант, заміщене галогеСО2Н, СО2(С1-4алкіл), С(О)(С1-4алкіл), CF3, CHF2, ном (наприклад, флуором, хлором або бромом), CH2F, CH2CF3 або OCF 3. ціаногрупою, С1-4алкілом (наприклад, метилом), R8 і R9 є незалежно гідрогеном або С 1С1-4алкоксилом (наприклад, метоксилом) або S(О)2С1-4алкіл (наприклад, S(O)2CH3). 4алкілом, або разом з атомом нітрогену або оксигену можуть бути з'єднані для утворення 5- або. 6Згідно з подальшим аспектом, R5 - бензил, де членного кільця, як варіант, заміщеного С 1ароматичне кільце, як варіант, заміщене галогеном (наприклад, флуором, хлором або бромом), 4алкілом, С(О)Н або С(О)(С 1-4алкіл); k дорівнює 0, 1 або 2. ціаногрупою, С1-4алкілом (наприклад, метилом), Згідно з ще одним аспектом винаходу, R5 С1-4алкоксилом (наприклад, метоксилом) або феніл, гетероарил, феніл(С1-2)алкіл або гетероS(O)2С1-4алкілом (наприклад, S(O)2Q33). арил (С1-2)алкіл; де фенільне і гетероарильне кільЗгідно з ще одним аспектом, R5 - феніл або ця, як варіант, заміщені галогеном, ціаногрупою, бензил, де ароматичне кільце заміщене (напринітрогрупою, гідроксигрупою, С1-4алкілом, С1клад, у пара-позиції) S(О)2С1-4алкілом і це кільце, S(О)kС1-4алкілом, S(O)2NR8R9, як варіант, може бути додатково заміщене галоге4алкоксилом, NHS(O)2(С1-4алкіл), NH2, NH(С1-4алкіл), N(С1ном, ціаногрупою, нітрогрупою, гідроксигрупою, С14алкіл)2, NHC(O)NH 2, C(O)NH 2, С(О)NН(С 1-4алкіл), 4алкілом або С 1-4алкоксилом. NНС(О)(С1-4алкіл), СО2Н, СО2(С1-4алкіл), С(О)( С1Згідно з наступним аспектом, R5 - NНСН2фент або бензил, де ароматичне кільце заміщене (на4алкіл), CF3, CHF2, CH 2F, CH 2CF3 або OCF3; k дорівнює 0, 1 або 2; і R 8 і R9 є незалежно гідрогеном приклад, у пара-позицм) S(О)2алкілом (наприклад, або С1-4алкілом, або разом з атомом нітрогену або S(O)2CH3) і це кільце, як варіант, може бути додатоксигену можуть бути з'єднані для утворення 5ково заміщене галогеном, ціаногрупою, нітрогруабо 6-членного кільця, як варіант, заміщеного С1пою, гідроксигрупою, С1-4алкілом або С14алкілом, С(О)Н або С(О)(С 1-4алкіл). 4алкоксилом. Згідно з подальшим аспектом, R5 - феніл або Згідно з іншим аспектом, R5 - NНСН2феніл, де бензил; де ароматичні кільця, як варіант, заміщені ароматичне кільце заміщене (наприклад, у парагалогеном, ціаногрупою, нітрогрупою, гідроксигрупозиції) S(O)2алкілом (наприклад, S(O)2CH3); R5 є, пою, С1-4алкілом, С1-4алкоксилом, S(О)k С1наприклад, NНСН2(4-S(O)2СН3-С6Н4). 8 9 Згідно з ще одним аспектом, R5 - бензил, де 4алкілом, S(O)2NR R , NНS(О)2(С 1-4алкіл), NH 2, NН(С1-4алкіл), N(С1-4алкіл)2, NHC(O)NH2, C(O)NH2, ароматичне кільце заміщене (наприклад, у параС(О)NН(С1-4алкіл), NНС(О)( С1-4алкіл), СО2Н, позиції) S(O)С1-4алкіл (наприклад, S(O)2CH3); R5 є, СО2(С1-4алкіл), С(О)(С1-4алкіл), CF3, CHF2, CH2F, наприклад, СН2(4-S(О)2СН3-С6Н4). Карбон, познаCH2CF3 або OCF3; k дорівнює 0,1 або 2; і R8 і R9 є чений ^ у формули (І), наведеній нижче, є завжди 15 77969 хіральним. (I) Коли L є Ν, карбон, позначений ^, має, наприклад, абсолютну S-конфігурацію. Коли L є СН, карбон, позначений ^, має, наприклад, абсолютну Rконфігурацію. Згідно з іншим аспектом, винахід пропонує сполуку формули (Іа): (Ia) де L, Μ і R1 є подібними визначеним вище. Згідно з подальшим аспектом, винахід пропонує сполук у формули (Іb): 16 де L, Μ і R1 є подібними визначеним вище. Згідно з ще одним аспектом, винахід пропонує сполуку формули (If): (If) де L, Μ, Χ і R 1 є подібними визначеним вище. Згідно з іншим аспектом, винахід пропонує сполуку формули (Іg): (Ig) (Ib) де L, Μ і R1 є подібними визначеним вище; і R - гідроген, один або два атоми флуору, S(О) n(С14алкіл) або С 1-4алкоксил; n дорівнює 0, 1 або 2 (наприклад, 2). Згідно з ще одним аспектом винахід пропонує сполуку формули (Іс): (Ic) де L, Μ і R1 є подібними визначеним вище; і R - гідроген, один або два атоми флуoру, S(О) n(С14алкіл) або С 1-4алкоксил; n дорівнює 0, 1 або 2 (наприклад, 2). Згідно з подальшим аспектом, винахід включає сполуку формули (Id): (Id) де L, Μ і R1 є подібними визначеним вище; R гідроген, один або два атоми флуору, S(O) n(С14алкіл) або С 1-4алкоксил; X - NHCH 2, NH або СН 2; n дорівнює 0, 1 або 2 (наприклад, 2); і R* - галоген (наприклад, флуор, хлор або бром), ціаногрупа, С1-4алкіл (наприклад, метил), С1-4алкоксил (наприклад, метоксил) або S(О)2С1-4алкіл (наприклад, S(O)2CH3). Згідно з іншим аспектом, винахід пропонує сполуку формули (Іе): (Ie) де R є подібними визначеним вище. Сполуки, наведені у Таблицях І - VI ілюстр ують винахід. 17 77969 18 19 77969 20 21 77969 22 b) кислотним хлоридом формули R1C(O)CI або сульфонілхлоридом формули R1S(O)2CI, у присутності придатної основи (наприклад, три(С16алкіл)аміну, наприклад, триетиламіну або діізопропілетиламіну) у придатному розчиннику (наприклад, хлорованому розчиннику, наприклад, ДХМ) при кімнатній температурі (наприклад, 10-30°С); або c) альдегідом формули R1CHO у присутності NaBH(OAc)3 (де Ас є С(О)СН3) і оцтовою кислотою у придатному розчиннику (наприклад, С16аліфатичному спирті, наприклад, етанолі) при кімнатній температурі (наприклад, 10-30°С). У іншому варіанті сполуку винаходу можна отримати сполученням сполуки формули (V): (V) Винахід включає кожну індивідуальну сполук з наведених у таблицях. Сполуки формули (І), (la), (Ib), (Ic), (Id), (le), (If) і (Іg) можна отримувати, як це описано нижче (наприклад, Схеми 2 і 3, Схема 1, ілюструють приготування інтермедіатів) У Схемах 1-3: PG - захисна група; Ас - ацетил; Вос - трет-бутоксикарбоніл; Вn - бензил, Bz - бензоїл; ГДБАЛ - гідрид діізобутилалюмінію; Et - етил; МС - мезил і ТФК - трифлуороцтова кислота. Сполуку винаходу, у якій L - N, можна отримати реакцією сполуки формули (II): (II) де R2, R3, R4 і R5 є подібними визначеним вище, з сполукою формули (II): (III) де R1 є подібною визначеній вище, у присутності йодиду натрію і придатної основи (наприклад, три(С 1-6алкіл)аміну, наприклад, триетиламіну або основи Гуніга), у придатному розчиннику (наприклад, хлорованому розчиннику, наприклад, ДХМ) при, наприклад, кімнатній температурі (наприклад, 10-30°С). Сполуку винаходу, у якій L - СН, можна отримати реакцією сполуки формули (IV): (IV) де R2, R3, R4 і R3 є подібними визначеним вище, з, залежно від сполуки винаходу, яку бажано отримати: a) кислотою формули R1CO2H у присутності придатного сполучного агента (наприклад, РуВrОР (гексафлуорфосфат бром-триспіролідинофосфонію) або ГАТУ) у присутності придатної основи (наприклад, три(С1-6алкіл)аміну, наприклад, діізопропілетиламіну) у придатному розчиннику (наприклад, N-метилпірилідинону або хлорованому розчиннику, наприклад, ДХМ) при кімнатній температурі (наприклад, 10-30°С); де L, M, R1, R2, R3 і R4 є подібними визначеним вище, з: a) кислотою формули R5CO2H у присутності придатного сполучного агента (наприклад, РуВrОР або ГАТУ) у присутності придатної основи (наприклад, три(С 1-6алкіл)аміну, наприклад, діізопропілетиламіну) у придатному розчиннику (наприклад, Nметилпірилідиноні або хлорованому розчиннику, наприклад, ДХМ) при кімнатній температурі (наприклад, 10-30°С); або, b) кислотним хлоридом формули R5C(O)CI у присутності придатної основи (наприклад, три(С16алкіл)aміну, наприклад, триетиламіну або діізопропілетиламіну) у придатному розчиннику (наприклад, хлорованому розчиннику, наприклад, ДХМ) при кімнатній температурі (наприклад, 10-30°С). Вихідні матеріали для цих способів є комерційно доступними або можуть бути отримані описаними у літературі способами, адаптованими описаними у літературі способами або адаптованими способами, описаними тут. Винахід включає інтермедіат формули (V). Згідно з іншим аспектом винахід пропонує способи отримання сполуки формули (І), (Іа), (Ib), (Ic), (Id), (le), (If) і (Іg). Деякі з інтермедіатів, використаних у ци х способах, є новими і входять в об'єм винаходу. Сполуки винаходу мають активність як фармацевтичні препарати, зокрема як модулятори (наприклад, агоністи, часткові агоністи, інверсні агоністи або антагоністи) рецептора хемокіну (особливо CCR5), і їх можна використовувати при лікуванні автоімунних, запальних, проліферативних або гіперпроліферативних хвороб, або імунологічно опосередкованих хвороб (включаючи відторгнення трансплантованих органів або тканин і СНІД). Сполуки винаходу можуть бути використані для інгібування вторгнення вірусів (наприклад, ВІЛ) у клітини і, отже, для профілактики інфікування вірусами (наприклад, ВІЛ), для лікування вірусних інфекцій (наприклад, ВІЛ) і профілактики і/або лікування СНІД. Винахід включає терапевтичне застосування сполуки формули (І), (la), (Ib), (Ic), (Id), (fe), (If) або (Ig) (наприклад, (І) або (Іа)), або її фармацевтично 23 77969 24 прийнятної солі або сольвату у способах лікування необоротну ХОП Х); астму (наприклад, бронхіаль(включаючи профілактику) теплокровних тварин ну, алергічну, невід'ємну, зовнішню або пилову (наприклад, людини). астму, особливо хронічну або стійку астму (наприВинахід включає також спосіб модулювання клад, пізню астму або надчутливість дихальних активності рецептора хемокіну (особливо активношляхів)); бронхіт (наприклад, еозинофільний брості рецептора CCR5) у теплокровних тварин, нанхіт); гострий, алергічний, атрофічний або хронічприклад, людини, що потребують такого лікування, ний риніт, включаючи rhinitis caseosa, гіпертрофічякий полягає у введенні зазначеним тваринам ний риніт, rhinitis purulenta, rhinitis sicca, або ефективної кількості сполуки винаходу або її фармедикаментозний риніт; мембранний риніт, вклюмацевтично прийнятної солі або сольвату. чаючи крупозний, фібринозний або псевдомембВинахід також стосується застосування сполуранний риніт або скрофульозний риніт; сезонний ки формули (І), (la), (Ib), (fc), (Id), (le), (If) або (Ig) риніт, включаючи rhinitis nervosa (сінна лихоманка) (наприклад, (І) або (Іа)), або її фармацевтично або вазомоторний риніт); саркоїдо, фермерську прийнятної солі або сольвату, як медикаменту, легеню і споріднені хвороби; назальний поліроз; зокрема, як медикаменту для лікування відторгфіброз легені або ідіопатичну інтерстиціальну пненення трансплантату, респіраторних захворювань, вмонію; псоріазу або ревматоїдного артриту (особливо (2) (кістки і суглоби) артриту, включаючи ревревматоїдного артриту), (респіраторним захворюматичний, інфекційний, автоімунний, серонегативванням може бути, наприклад, обструктивна ресні сподилоартропатії (наприклад, анкілозний спонпіраторна хвороба, астма (наприклад, бронхіальдиліт, псоріатичний артрит або хворобу Рейтера), на, алергічна, невід'ємна, зовнішня або пилова, хвороби Беже, синдрому Сйогрена або систематиособливо хронічна або стійка астма (наприклад, чного склерозу; пізня астма або надчутливість дихальних шляхів)) (3) (шкіра і очі) псоріазу, атопічного дерматиту, або ринітів (гострого, алергічного, атрофічного або контактного дерматиту або інших екзематозних хронічного, включаючи rhinitis caseosa, гіпертрофідерматитів, себорейного дерматиту, плоского личний риніт, rhinitis purulenta, rhinitis sicca, або мешаю, Phemphigus, бульйозного Phemphigus, бульдикаментозний риніт; мембранний риніт, включаюйозного епідермолізу, кропивниці, ангіодерми, васчи крупозний, фібринозний або кулітних еритем, шкірних еозинофілій, увеліту, псевдомембранний риніт або скрофульозний ригніздової алопеції або весняного кон'юнктивіту; ніт; сезонний риніт, включаючи rhinitis nervosa (сін(3) (шлунково-кишковий тракт) черевної хвона лихоманка) або вазомоторний риніт); особливо роби, проктиту, еозинофільного гастроентериту, астми або риніту. мастоцитозу, хвороби Крона, виразкового коліту, Згідно з іншим аспектом, винахід пропонує захвороби подразнення кишечнику або пов'язаних з стосування сполуки формули (І), (la), (Ib), (Jc), (Id), їжею алергій, які дають наслідки, віддалені від (le), (If) або (Ig) (наприклад, (І) або (Іа)), або її факишок (наприклад, мігрень, риніт або екзема); рмацевтично прийнятної солі або сольвату, у ви(4) (відторгнення гомотрансплантату) гостри х і робництві медикаментів, призначених для застохронічних наслідків, наприклад, трансплантації сування у терапії (наприклад, модулювання нирки, серця, печінки, легені, кісткового мозку, активності рецептора хемокіну (особливо активношкіри або роговиці; або хронічних хвороб, виклисті рецептора CCR5) (особливо при ревматоїдноканих трансплантатом і/або му артриті)) у теплокровних тварин, зокрема лю(6), (інші тканини або хвороби) хвороби Альцдини). геймера, множинного склерозу, атеросклерозу, Винахід також пропонує сполуку формули (І), СПІД, волчанки (наприклад, еритрематозної вол(la), (Ib), (Ic), (Id), (le), (If) або (Ig) (наприклад, (І) чанки або систематичної волчанки), еритрематозу, або (Іа)) або її фармацевтично прийнятну сіль або тереоїдиту Хашимото, бульбоспинального паралісольват для застосування як медикаменту, особчу, діабету тип у І, нефротичного синдрому, еозиливо медикаменту для лікування ревматоїдного нофільного фасциту, синдрому гіпер-lgE, прокази артриту. (наприклад, лепроматозної прокази), перидонтаЗгідно з подальшим аспектом, винахід пропольної хвороби, синдрому Сезарі, ідіопатичної нує застосування сполуки формули (І), (la), (Ib), тромбоциторенії ририга або розладів менструаль(Ic), (Id), (le), (If) або (Ig) (наприклад, (І) або (Іа)) ного циклу у теплокровної тварини, зокрема, люабо її фармацевтично прийнятної солі або сольвадини. ту у виробництві медикаментів, призначених для Винахід також стосується способу лікування застосування у терапії (наприклад, для модулюопосередкованих хемокіном хворобливих станів вання активності рецептора хемокіну (особливо (особливо хворобливих станів, опосередкованих активності рецептора CCR5 (особливо при ревмаCCR5) у теплокровних тварин, зокрема людини, тоїдному артриті)) у теплокровних тварин, зокрема який полягає у введенні ссавцю, що потребує талюдини). кого лікування, ефективної кількості сполуки форВинахід також включає застосування сполуки мули (І), (la), (Ib), (Ic), (Id), (le), (If) або (Іg) (наприформули (І), (la), (Ib), (lc), (Id), (le), (If) або (Ig) (наклад, (І) або (Іа)) або її фармацевтично прийнятної приклад, (l) або (Іа)) або її фармацевтично прийнсолі або сольвату. ятної солі або сольвату у виробництві медикаменПри застосуванні сполуки винаходу або її фатів, призначених для лікування: рмацевтично прийнятної солі або сольвату для (1) (дихальні шляхи) обструктивної хвороби терапевтичного лікування теплокровної тварини, дихальних шляхів, включаючи: хронічну обструкнаприклад, людини, зокрема для модулювання тивну п ульмонарну хворобу (ХОП Х) (наприклад, активності рецептора хемокіну (наприклад, рецеп 25 77969 26 тора CCR5), зазначений інгредієнт звичайно готуНатрій-кроскармелоза 12,0 ють згідно з стандартною фармацевтичною пракПолівінілпіролідон 6 тикою у вигляді фармацевтичної композиції. Стеарат магнію 3,0 Отже, згідно з ще одним аспектом, винахід (b) включає фармацевтичні композиції, які містять Таблетка II мг/таблетка сполуку формули (І), (la), (Ib), (Ic), (Id), (le), (If) або Сполука X 50 (Іg) (наприклад, (І) або (Іа)) або її фармацевтично Лактоза Ph. Eur. 229 прийнятну сіль або сольват (як активний інгредіНатрій-кроскармелоза 12,0 єнт) і фармацевтично прийнятний ад'ювант, розріПолівінілпіролідон 6 джувач або носій. Згідно з подальшим аспектом, Стеарат магнію 3,0 винахід включає процес приготування зазначеної (с) композиції, яка містить суміш активного інгредієнта Таблетка III мг/таблетка з фармацевтично прийнятним ад'ювантом, розріСполука X 1,0 джувачем або носієм. Залежно від способу застоЛактоза Ph. Eur. 92 сування, фармацевтична композиція переважно Натрій-кроскармелоза 4,0 містить від 0,05 до 99% (за масою), бажано від Полівінілпіролідон 2,0 0,05 до 80% (за масою), найкраще від 0,10 до 70% Стеарат магнію 1,0 (за масою) і навіть від 0,10 до 50% (за масою), (d) активного інгредієнта відносно маси повної компоКапсула мг/капсула зиції. Сполука X 10 Фармацевтичні композиції винаходу можна заЛактоза Ph. Eur. 389 стосовувати у стандартний спосіб у випадку хвоНатрій-кроскармелоза 100 робливого стану, що потребує лікування, наприСтеарат магнію 1,0 клад, місцевим (наприклад, у легенях і/або (e) дихальних шляха х або на шкірі), пероральним, Ін'єкція І (50мг/мл) ректальним або парентеральним введенням. Для Сполука X 5,0% (маса/об'єм) цього сполуки винаходу можуть бути застосовані з Ізотонічний водний розчин до 100% використанням відомих способів, наприклад, у формі аерозолів, сухи х порошкових рецептур, Для полегшення приготування рецептур можтаблеток, капсул, сиропів, порошків, гранул, водна використовувати буфери, фармацевтично приних або масляних розчинів або суспензій, (ліпідйнятні співрозчинники, наприклад, поліетиленгліних) емульсій, диспергувальних порошків, супозиколь, поліпропіленгліколь, гліцерин або етанол, торіїв, мазей, кремів, крапель і стерильних водних або комплексоутворюючі засоби, наприклад, гідроабо масляних розчинів або суспензій, придатних ксипропіл β-циклодекстрин. для ін'єкцій. Наведені вище рецептури можна приготувати, Придатною фармацевтичною композицією вивикористовуючи звичайні процедури, добре відомі находу є пристосована для перорального введену фармацевтиці. Таблетки (а)-(с) можуть мати ення у одиничних дозованих формах, наприклад, у теросолюбільне покриття, нанесене звичайними вигляді таблеток або капсул, які містять від 0,1мг засобами, наприклад, нанесенням ацетатфталату до 1г активного інгредієнта. целюлози. Згідно з іншим аспектом, придатною фармаДалі для ілюстрації винаходу наведено необцевтичною композицією винаходу є така, що є межуючі Приклади, в яких, якщо не зумовлено пристосованою для .внутрішньовенних, підшкірних інше: або внутрішньом'язових ін'єкцій. (і) температури задано у °С, кімнатна або зовКожний пацієнт може приймати, наприклад, нішня температура становить 18-25°С; внутрішньовенно, підшкірно або внутрішньом'язо(іі) сушіння органічних розчинів виконується во дозу композиції від 0,01мг/кг до 100мг/кг сполунад безводним сульфатом магнію; випарювання ки винаходу, бажано від 0,1мг/кг до 20мг/кг, 1-4 розчинника виконується на роторному випарювачі рази на добу. Внутрішньовенну, підшкірну і внутпід зниженим тиском (600-4000Па; 4,5-30мм Hg) з рішньом'язову дози можна вводити болюсною ін'єтемпературою ванни до 60°С; кцією. Внутрішньовенно дозу можна також вводити (ііі) хроматографія, якщо не вказано інше, є безперервною інфузією протягом певного часу. флеш-хроматографією на силікагелі; тонкошарова Пацієнт може перорально приймати добову дозу, хроматографія (ТШХ) виконується на силікагелеприблизно еквівалентну добовій дозі при парентевих плата х; колонка "Bond Hut" є колонкою з вмісральному введенні, 1-4 рази на добу. том 10г або 20г кремнезему з частинками розміДалі у таблицях для ілюстрації наведено тиром 40мкм, кремнезем міститься у 60 пові фармацевтичні дозовані форми з вмістом мілілітровому одноразовому шприці і підтримуєтьсполуки формули (І), (la), (Ib); (Ic), (Id), (le), (If) або ся пористим диском від Varian, Harbor City, (Іg) (наприклад, (І)або (Іа)) або її фармацевтично Qdifomia, USA під назвою "Mega Bond Elut ST. прийнятної солі або сольвату (далі сполука X), для "bolute™ SCX column" є колонкою, що містить бентерапевтичного або профілактичного застосуванзолсульфонову кислоту (не закриту герметично) ня для людини. від Snternational Sorbent Technology Ltd., 1st (а) House, Duffryn Industial Estate, Ystrad Mynach, Таблетка І мг/таблетка Hengoed, Mid Glamorgan, "Argonaut™ PS-tris-amine Сполука X 100 scavenger resin" є трис-(2Лактоза Ph. Eur. 179 аміноетил)амінполістироловою смолою від 27 77969 28 Argonaut Technologies Inc., 887 Industrial Road, хлорпропіл)-піперидин-4-іл]-N-етил-4Suite G, San Carlos, California, USA; метансульфонілфенілацетамід (Спосіб А; 180мг, (iv) взагалі хід реакції контролюється ТШХ і 0,38ммоль) і йодид натрію (50мг). Суміш перемітривалості стадій реакції наведено лише для ілюсшують при кімнатній температурі 48год., промиватрації; ють водою і розсолом, сушать (MgSC4) і випарю(ν) ви хід (якщо наведено) наведено лише для ють. Залишок очищують елююванням через 20г ілюстрації і може бути іншим при точному повтоBond Elut з 10% метанолу у етилацетаті, потім з ренні процесу; приготування повторювали, якщо метанолом і потім з 1% триетиламіну у метанолі і була потреба у більшій кількості матеріалу; одержують бажану сполуку (58мг); Я МР: 1,2 (t, 1Н), (vi) дані 1Н ЯМР наведено у формі значень 1,3 (t, 2Н), 1,4 (m, 1Н), 1,6. (m, 2Н), 1,8 (m, 4Н), 1,9 дельта для головних діагностичних протонів, у (m, 2Н), 2,1 (m, 2Н), 2,2 (s, 3Н), 2,4 (m, 8Н), 2,9 (m, частках намлн (ppm) відносно тетраметилсилану 2Н), 3,0 (s, 3Н), 3,3 (m, 2Н), 3,8 (s, 2Н), 7,2 (m, 2Н), (ТМС) як внутрішнього стандарту, при 300МГц, з 7,4 (m, 2Н), 7,9 (d, 2Н); МС:541. використанням псевдодейтерієвого ДМСО Процедуру, описану у Прикладі 1, можна про(CD3SOCD3) як розчинника, якщо не встановлено вести, використовуючи інші вторинні аміни (наприінше; константи сполучення (J) наведено у Гц; клад, 4-формілпіперазине, 4-ізобутирилпіперазине (vii) хімічні символи мають звичайні значення; або 4-бензилпіперидин) замість 1використано символи і одиниць SI; метилпіперазину. (viii) вміст розчинника наведено у %% за об'Приклад 2 ємом; Цей приклад ілюструє приготування N-[1-(3(іх) мас-спектри (МС) одержано при енергії феніл-3-{піперидин-4-іл}пропіл)-піперидин-4-іл]-Nелектронів 70еВ у режимі хімічної іонізації (АРСІ) з етил-4-метансульфонілфенілацетаміду (Сполука використанням безпосереднього піддання зразка №17 у Таблиці І). дії; якщо вказано, що іонізацію проведено електN-[1-(3-феніл-3-[1-третророзпилюванням (ES); і наведено значення для бутилкарбонілпіперидин-4-іл]пропіл)-піперидин-4m/z, загалом тільки іони показують вихідну масу, і, іл]-N-етил-4-метансульфонілфенілацетамід (Приякщо не встановлено інше, масу іону наведено як клад 3, 4г) розчиняють у трифлуороцтовій кислоті масу позитивного іону - (М+Н)+; (25мл) і суміш перемішують при кімнатній темпе(х) характеризацію РХМС проводили, викорисратурі 2год. Суміш випарюють і залишок азеотротовуючи пару насосів Gilson 306 з відбирачем зрапують з толуолом. Одержаний матеріал перемізків Gilson 233 XL і мас-спектрометром Waters шують з 2М водним гідроксидом натрію (25мл) і ZMD4000. Рідинний хроматограф (РХ) містить восуміш екстрагують ДХМ (8´25мл). Об'єднані екстракти сушать і випарюють, одержуючи бажану досиметричну колонку 4,6´50 CIS з частинками розміром 5мкм. Елюенти: А, вода з 0,05% мурасполуку (2,5г); МС: 526. шиної кислоти і В, ацетонітрил з 0,05% мурашиної Приклад З кислоти. Градієнт елюенту становив від 95% А до Цей приклад ілюструє приготування N-[1-(395% В за 6хв. Якщо іонізацію проводили електрофеніл-3-[1-трет-бутилкарбонілпіперидин-4розпилюванням (ЕР) і наведено значення m/z, іл]пропіл)-піперидин-4-іл]-N-етил-4взагалі наведено лише масу вихідних іонів і, якщо метансульфонілфенілацетаміду (Сполука №23 у не встановлено інше, масу іону наведено як масу Таблиці І). позитивного іону - (М+Н)+; До розчину 3-феніл-3-(1-третАбревіатури: бутилкарбонілізоксипіперидин-4DMCO - диметилсульфоксид; іл)пропіональдегіду (Спосіб С; 14,4ммоль) у ДХМ ДМФ - N-диметилформамід; (100мл) додають N-(4-піперидиніл)-N-етил-4ДХМ - ди хлорметан; метансульфонілфенілацетамід (Спосіб В; 4,6г, ТГФ - тетрагідрофуран; 14,4ммоль) і суміш перемішують при кімнатній ДІПЕА - Ν,Ν-діізопропілетиламін: температурі 30хв. Додають триацетоксиборгідрид ΝΜΠ - N-метилпіролідинон; натрію (3,05г, 14,4ммоль) і суміш перемішують при ГАТУ гексафлуорфосфат O-7кімнатній температурі 2год. Реакційну суміш проазабензотриазол-1-іл)-N,N,N',N'мивають 2М водним гідроксидом натрію (3´25мл), тетраметилуронію; сушать і елюють через 50г картридж SCX з ДХМ ГБТУ - гексафлуорфосфат О-7-бензотриазол(3´25мл), етилацетатом (4´25мл), метанолом 1-іл)-N,N,N',N'-тетраметилуронію; (4´25мл) і наприкінці 1М амонієм у метанолі Вос - трет-бутоксикарбоніл (4´50мл), одержуючи сирий продукт, який очищуМеОН - метанол; ють силікагелевою хроматографією (елюент етиЕtOН - етанол; лацетат, потім 10% метанолу у етилацетаті), і EtOAc - е тилацетат. одержують бажану сполуку (4,2г); МС: 626. Приклад 1 Приклад 4 Цей приклад ілюструє приготування N-[1-(3Цей приклад ілюструє приготування N-[1-(3феніл-3-[4-метилпіперазин-1-іл]пропил)феніл-3-[1-метилпіперидин-4-іл]пропіл)-піперидинпіперадиніл]-N-етил-44-іл]-N-етил-4-метансульфонілфенілацетаміду метансульфонілфенілацетаміду (Сполука №6 у (Сполука №26 у Таблиці І). Таблиці І). До суміші N-[1-(3-феніл-3-{піперидин-4До розчину 1-метилпіперазину (42мкл, іл]пропіл)-піперидин-4-іл]-N0,38ммоль) у ДХМ (10мл) додають триетиламін етилметансульфонілфенілацетаміду (Приклад 2, (0,1мл, 0,72ммоль), потім N-[1-(3-феніл-3250мг, 4,76ммоль) і формальдегіду (0,2мл, 37% 29 77969 30 водн.) у ДХМ (10мл) додають триацетоксиборгідBond-Elut елюювання розчинником з градієнтом рид натрію (9,52ммоль) і суміш перемішують при (етилацетат-20% метанол/етилацетат), одержуюкімнатній температурі 18год. С уміш промивають чи бажану сполуку, ви хід 90мг. МН+701. 2М водним гідроксидом натрію (10мл) і елюють N-[1-(3-феніл-3-[піперазин-1-іл]пропіл)піперидин-4-іл]-N-етил-4через 10г картридж SCX з ДХМ (2 ´10мл), метанометансульфонілфенілацетамід (Сполука 86 у Таблом (2´10мл) і наприкінці 1М амонію у метанолі лиці І), використовується як початковий матеріал і (4´10мл), одержуючи бажану сполуку (172мг); МС: його отримують, як у прикладі 2, використовуючи 540. відповідний аналог (1-трет-бутилоксикарбоніл)Процедуру, описану у прикладі 4, можна пропіперазину. вести, використовуючи інші альдегіди (наприклад, [1-(3-феніл-3-[третацетальдегід і бензальдегід) замість формальдегібутилоксикарбонілпіперазин-1іл]пропіл)ду. піперидин-4-іл]-N-етил-4Приклад 5 метансульфонілфенілацетамід (Сполука 152 у Цей приклад ілюструє приготування N-[1-(3Таблиці І) використовується як початковий матеріфеніл-3-[1-ацетилпіперидин-4-іл]пропіл)ал, отриманий, як було описано у прикладі 1, з піперидин-4-іл]-N-етил-4використанням 1-третметансульфонілфенілацетаміду (Сполука №21 у бутилоксикарбоніл)піперазину як амінового компоТаблиці І). нента. До суміші N-[1-(3-феніл-3-піперидин-4Приклад 8 іл]пропіл)-піперидин-4-іл]-N-етил-4-метан(R або S) N-[1-(3-феніл-3-[(4-{2,2,2сульфонілфенілацетаміду (Приклад 2,250мг, трифлуоретилсульфонілпіперазиніл}пропіл)4,76ммоль) і триетиламіну (48мг, 4,76ммоль) у піперидин-4-іл]-N-етил-4ДХМ додають ацетилхлорид (37мг, 4,76ммоль). метансульфонілфенілацетамід (Сполука 15 у ТабСуміш перемішують при кімнатній температурі лиці 2). 18год., промивають насиченим водним розчином Триетиламін (50мкл) додають до розчину (R бікарбонату натрію (10мл), сушать і елюють через або S) N-[1-(3-феніл-3-піперазиніл}пропіл)10г картридж SCX з ДХМ (2´10мл), метанолом піперидин-4-іл]-N-етил-4(4´10мл) і наприкінці 1М амонію у метанолі метансульфонілфенілацетаміду (175мг) у ДХМ (4´10мл), одержуючи бажану сполуку (180мг); МС: (5мл) і потім 2,2,2-трифлуоретансульфонілхлорид 568. (37мкл) і суміш перемішують при кімнатній темпеПроцедуру, описану у Прикладі 5, можна проратурі 14год. Реакційну суміш промивають водою і вести, використовуючи інші хлориди (наприклад, сушать. Залишок, утворений після видалення розфенілацетилхлорид і 4-хлорбензоїлхлорид) або чинника, хроматографують на кремнеземній колосульфонілхлориди (наприклад, метансульфонілхнці Bond-Elut елюювання розчинником з градієнлорид) замість ацетилхлориду. том (етилацетат-40% метанол/етилацетат), Приклад 6 одержуючи бажану сполуку у вигляді білої піни, Цей приклад ілюструє приготування N-[1-(3вихід 79мг, МН+ 673. ЯМР (CDCI3): 1,2 (t, 1H), 1,3 феніл-3-[1-циклогексиламінокарбонілпіперидин-4(t, 2H), 1,4 (m, 1H), 1,6-1,8 (m, 8Н), 2,1 (m, 2Н), 2,25 іл]пропіл)-піперидин-4-іл]-N-етил-4(m, 1Н), 2,5 (m, 4Н), 2,9 (m, 2Н), 3,0 (s, 3Н), 3,3 (m, метансульфонілфенілацетаміду (Сполука №22 у 5H), 3,4 (m, 1H), 3,6 (q, 2Н), 3,8 (m, 2Н), 7,2 (m, 2Н), Таблиці І) 7,3 (m, 3Н), 7,4 (m, 2H), 7,9 (d, 2H). До суміші N-[1-(3-феніл-3-{піперидин-4Приклад 9 іл}пропіл)-піперидин-4-іл]-N-етил-4-метан(R або S) N-[1-(3-феніл-3-(Воссульфонілфенілацетаміду (Приклад 2, 250мг, піперазиніл}пропіл)-піперидин-4-іл]-N-етил-44,76ммоль) і ДХМ (10мл) додають циклогексилізометан-сульфонілфенілацетамід ціанат (59мг, 4,6ммоль) і суміш перемішують при (R або S) N-[1-(3-феніл-3-хлорпропіл)кімнатній температурі 18год. Суміш елюють через піперидин-4-іл]-N-етил-4-метансульфоніл10г картридж SCX з ДХМ (4´10мл), метанолом фенілацетамід (594мг) додають до розчину три(2´10мл) і наприкінці 1М амонію у метанолі етиламіну (0,35мл) і Вос-піперазину (233мг) у ДХМ (4´10мл), одержуючи бажану сполуку (300мг); МС: (10мл) при кімнатній температурі і суміш перемі651. шують 14год. Реакційну суміш додають у 20г креПриклад 7 мнеземну колонку Bond-Elut з елююванням розN-[1-(3-феніл-3-[4-(2чинником з градієнтом (етилацетат-40% хлорфенілсульфоніл)піперазин-1-іл]пропіл)метанол/етилацетат), одержуючи бажану сполуку піперидин-4-іл]-N-етил-4у вигляді піни, вихід 440мг, МН+ 627. метансульфонілфенілацетамід (Сполука 150 у (R або S) N-(3-феніл-3-хлорпропіл)-піперидинТаблиці І) 4-іл]-N-етил-4-метансульфонілфеніл-ацетамід. 2-хлорфенілсульфонілхлорид (40,1мг) додають до розчину N-[1-(3-феніл-3-[піперазин-1іл]пропіл)-піперидин-4-іл]-N-етил-4метансульфонілфенілацетаміду (100мг) і триетиламіну (53мкл) у ДХМ (5мл) і суміш перемішують 1год. Реакційну суміш промивають водою, розсолом і сушать. Розчинник видаляють і залишок хроматографують 10г на кремнеземній колонці 31 77969 32 Метансуль фонілхлорид (0,5мл) додають з педо сухості і залишок проводять через 90г кремнеремішуванням до суміші S N-[1-(3-феніл-3земну колонку Bond-Hut з елююванням розчиннигідроксипропіл)-піперидиніл]-N-етил-4ком з градієнтом (етилацетат-20% метаметансульфонілфенілацетаміду (2,7г) і триетиланол/етилацетат), одержуючи бажану сполуку, міну (1,64мл) у ДХМ (50мл) при 0°С і суміш перевихід 121мг. ЯМР (DMCOd6): 0,8-2,2 (m, 6H) 1,2-1,5 мішують при зовнішній температурі 15год., далі (m, 4H) 1,5-2,1 (m, 13Н), 2,4 (m, 1H) 2,7 (m, 3Н) 3,3 промивають водою і сушать. Видалення розчинни(m, 4Н) 3,8 (d, 2Н) 7-7,5 (m, 11Н) 7,8 (d, 2Н). Аналіка дає бажану сполуку у вигляді оранжевої піни, тична ВЕРХ на колонці Chiralcel OJ (250мм´4,6мм) вихід 2,4г, МН+ 477. з елююванням метанолом дає хіральну чистоту (S) N-[1-(3-феніл-3-гідроксипропіл)-піперидинвище 99%. 4-іл]-N-етил-4-метансульфонілфеніл-ацетамід (R) N-[1-3-феніл-3-{піперидин-4-іл]пропіл)піперидиніл]-N-етил-4-метансульфонілфенілацетамід (Сполука 35 у Таблиці 2). (S) 1-феніл-3-(4-толуолсульфонілокси)пропан1-ол (5г) додають до суміші N-(піперидин-4-іл)-Nетил-4-метансульфонілфенілацетаміду (5,3г) і карбонату калію (2,71г) у ДМФ (100мл) і суміш перемішують і гріють при 80-90°С 6год. Реакційну суміш залишають охолонути і випарюють до сухості. Залишок розчиняють у ДХМ (50мл), промивають водою і сушать. Розчинник видаляють і залишок проводять через 90г кремнеземну колонку Bond-Hut з елююванням розчинником з градієнтом (етилацетат-20% метанол/етилацетат), одержуючи бажану сполуку, ви хід 2,7г, МН+ 459. ЯМР (CDCI3): 1,2 (t, 1 Η), 1,3 (t, 2H), 1,6 (m, 2H), 1,75 (m, 3Н), 1,85 (m, 3Н), 2,2 (m, 1H), 2,55-2,7 (m, 2H), 3,0 (s, 3Н), 3,1-3,2 (m, 2H), 3,3(q, 2H), 3,8(m, 2H), 4,9 (m, 1H), 7,3 (m, 5H), 7,45 (d, 2H), 7,9 (d, 2H). (S) 1-феніл-3-(4-толуолсульфонілокси)пропан1-ол є відомою сполукою (CAS №156453-52-0) Приклад 10 (R або S) N-(3-феніл-3-піперазиніл}пропіл)піперидин-4-іл]-N-етил-4-метансульфоніпфенілацетамід Трифлуороцтову кислоту (5мл) додають до розчину (R або S) N-[1-(3-феніл-3-(Воспіперазиніл}пропіл)-піперидин-4-іл]-N-етил-4метансульфонілфенілацетаміду (440мг) у ДХМ (10мл) і суміш перемішують 1год. Реакційну суміш концентрують і залишок розчиняють у 2М водному гідроксиді натрію і екстрагують двічі з ДХМ (10мл´2с). Об'єднані екстракти сушать і випарюють, одержуючи бажану сполуку у вигляді піни, вихід 370мг, МН+ 527. Приклад 11 (R) N-[1-(3-феніл-3-{1-(4хлорбензоїлпіперидин-4-іл)пропіл}піперидин-4-іл]N-етил-4-метансульфонілфенілацетамід. (Сполука 26 у Таблиці 2). До суміші (R) N-[1-3-феніл-3-[піперидин-4іл]пропіл)-піперидин-4-іл]-N-етил-4метансульфонілфенілацетаміде (330мг) і МПкарбонатної смоли (670мг, 2,8мМ/г) у ДХМ (10мл) додають 4-хлорбензоїлхлорид (111мг) і суміш перемішують при кімнатній температурі 15год. Реакційну суміш фільтрують, до фільтрату додають МП 4-толуол-сульфоновокислотну смолу (1г) і перемішують 30хв. Реакційну суміш фільтрують і смолу промивають послідовно ДХМ (4´10мл) і 1М MeOH/NH3 (3´10мл). Об'єднані змивки випарюють Розчин (R) N-[1-(3-феніл-3-{1(бензилоксикарбонілпіперидин-4іл)пропіл}піперидин-4-іл]-N-етил-4метансульфонілфенілацетамід (1,5г) в етанолі (100мл) з вмістом 20% каталізатора паладій/карбон (200мг) гідрогенують під балоном з гідрогеном. Каталізатор фільтрують і фільтрат випарюють до сухості, одержуючи бажану сполуку, вихід 1,1г. МС (МН+) 526. (R) N-[1-(3-феніл-3-{1(бензилоксикарбонілпіперидин-4іл)пропіл}піперидин-4-іл]-N-етил-4метансульфонілфенілацетамід (Сполука 24 у Таблиці 2). Триацетоксиборгідрид натрію (890мг) додають до розчину (R) 3-феніл-3(бензилоксикарбонілпіперидин-4іл)пропіональдегіду (1,49г) і N-(4-піперидиніл)-Nетил-4-метансульфонілфенілацетамід (1,4г) у ДХМ (25мл) і суміш перемішують 1год. Реакційну суміш промивають 2М NaOH (2´50мл) і сушать. Розчинник видаляють і залишок проводять через кремнеземну колонку Bond-Hut з елююванням розчинником з градієнтом (етилацетат-20% метанол/етилацетат), одержуючи бажану сполуку, вихід 1,5г. МС(МН +) 660. (R) 3-феніл-3-(бензилоксикарбонілпіперидин4-іл)пропіональдегід Dess-Martin-періодінан (1,1,1-триацетокси-1,1дигідро-1,2-бензіодоксол-3(1Н)-он) (1,8г) додають до розчину (R) 3-феніл-3(бензилоксикарбонілпіперидин-4-іл)пропанолу у ДХМ і,25мл) і суміш перемішують 1год., промивають 2М NaOH (2´20мл) і сушать. Розчин у ДХМ бажаної сполуки використовують безпосередньо у наступній операції. (R) 3-феніл-3(бензилоксикарбонілпіперидин-4-іл)пропаном Алюмогідрид літію (9,46мл 1Μ LAH у ТГФ) додають краплями до розчину (R) 3-[3-феніл-3(бензилоксикарбонілпіперидин-4-іл)пропіоніл](4R,5S)-1,5-диметил-4-феніл-2-імідазолідинону (5,1г) у ТГФ (100мл) таким чином, щоб температура не перевищувала 0°С. Реакційну суміш перемішують при -5°С 10хв. і додають 2 М NaOH (10мл). Реакційну суміш фільтрують через Celite і 33 77969 34 фільтрат випарюють до сухості. Залишок розчиBond-Elut і елюють сумішшю етилацетат/ізогексан няють у ДХМ (20мл) і сушать. Після видалення (1:1), одержуючи бажану сполуку, вихід 3,6г. ЯМР розчинника залишок проводять через кремнезем(DMCOd6): 0,6 (d, 3Н) 0,95 (d, 1Н) 1,2 (m, 2Н) 1,55 ну колонку Bond-Hut з елююванням розчинником з (m, 2Н) 2,4 (m, 1Н) 2,3 (s, 3Н) 2,8 (m, 2Н) 3,95 (m, градієнтом (ізогексан-60% етилацетат/ізогексан), 3Н) 5 (s, 2H) 5,3 (d, 1H) 6,9 (m, 1H) 7,1 (m, 2H) 7,2одержуючи бажану сполуку, ви хід 1,6г. МС (МН+) 7,4 (m, 8H). 354. 3-(бензилоксикарбонілпіперидин-43-[(R) 3-феніл-3іл)пропенова кислота (бензилоксикарбонілпіперидин-4-іл)пропіоніл]Суміш N-бензилоксикарбоніл-4(4R,5S)-1,5-диметил-4-феніл-2-імідазолідинон. формілпіперидину (10г), малонової кислоти (4.2), піридину (4мл) і піперидину (0,4мл) гріють при 100°С 2год. Реакційну суміш залишають охолонути і розбавляють етилацетатом (100мл). Розчин промивають 2М НСІ (2´100мл), сушать і випарюють до сухості. Залишок перетирають з ізогексаном і одержують бажану сполуку, вихід 13,5г. ЯМР (DMCOd6): 1,2 (m, 2H) 1,7 (m, 2H), 2,35 (m, 1H) 2,85 (m, 2H), 4 (d, 2H) 5,05 (s, 2H) 5,75 (d, 1Н) 6,75 (m, 1Н) 7,35 (m, 5Н) 12,25 (широкий пік, 1Н) TMED A (2,4г) додають до суспензії йодиду міді Приклад 12 (4,02г) у ТГФ (100мл) і суміш перемішують при N-[1-3-[(3-флуорфеніл)-3-[1-фенілпіперидин-4кімнатній температурі 30хв. Реакційну суміш охоіл]пропіл)-піперид-4-іл]-N-етил-4лоджують до -78°С і додають бромід фенілмагнію метансульфонілфенілацетамід (Сполука 145 у (11,69мл 1М розчину у ТГФ) і суміш перемішують Таблиця 2). при -78°С 30хв. Ди-бутилбортрифлат (11,69мл, 1М 2М NaOH додають до суспензії дигідрохлорирозчин у діетилетері) додають до розчину 3-[3дної солі N-[1-[3-(3-флуор феніл-3-[піперидин-4(бензилоксикарбонілпіперидин-4-іл)акрилоїл]іл]пропіл)-піперидин-4-іл]-N-етил-4(4R,5S)-1,5-диметил-4-феніл-2-імідазолідинону метансульфонілфенілацетаміду (0,85г) у ДХМ (4,9г) у ТГФ (50мл) і цю суміш додають краплями (25мл) і суміш перемішують до прозорості розчину. протягом 10хв. до розчину мідного реагенту. РеакРозчин ДХМ сушать і фільтрують. До цього розчиційну суміш перемішують при -78°С 1год. і залину додають бензолборну кислоту (330мг), триетишають досягти зовнішньої температури. Розчинник ламін (280мг) і ацетат міді (276мг). Реакційну сувипарюють, залишок розчиняють у етилацетаті і міш перемішують 15год., промивають водою і фільтрують через кремнезем (100г). Етилацетатфільтрують через картридж Chem Elut. Фільтрат ний розчин промивають 2М НСІ (1´100мл), сушать ДХМ промивають 2М NaOH (3´20мл), сушать і і випарюють до сухості. Залишок проводять через вливають у 20г картридж SCX і елюють метанолом кремнеземну колонку Bond-Hut з елююванням су(6´20мл) і 1М амонієм у метанолі (6´20мл). Об'єдмішшю етилацетат/ізогексан (1:1), одержуючи банані амонієві зми-вки випарюють і залишок хромажану сполуку як єдиний стереомер, визначений тографують на колонці Bond-Elut і елюють з градіЯМР. Вихід 5,1г. ЯМР (D MCOd6): 0,5 (d, 3Н) 0,8-1,1 єнтом розчинника (етилацетат-20% (m, 2H) 1,3 (d, 1H) 1,7 (m, 2H) 2,6 (m, 5H) 2,85-3,1 метанол/етилацетат), одержуючи бажану сполуку, (m, 4H) 5,05 (s, 2H) 5,2 (d, 1H) 6,8 (m, 2H) 7,1-7,5 вихід 179мг. (m, 13H). Дигідрохлоридна сіль N-[1-3(3-флуорфеніл-33-[3-(бензилоксикарбонілпіперидин-4[піперидин-4-іл]пропіл)-піперидин-4-іл]-N-етил-4іл)акроїлоїл]-(4R,5S)-1,5-диметил-4-феніл-2метан-сульфонілфенілацетаміду (Сполука 87 у імідазолідинон Таблиці 1) використовується як початковий матеріал, отриманий за процедурою Прикладу 3 і Методу С Приклад 13 Рацемічний N-[1-(3-(3-флуорфеніл)-3-[4-(4метансульфоніл)фенілсульфоніл)піперазин-11-хлор-N,N,2-триметил-1-пропеніламін (1,37г) іл]пропіл)-піперидин-4-іл]-N-етил-4додають краплями протягом 10хв. до розчину 3метансульфонілфенілацетамід (78мг) (Сполука 59 (бензилоксикарбонілпіперидин-4-іл)пропенової у Таблиці 1) розділяють на окремі енантіомери кислоти (2,5г у ТГФ (20мл) і суміш перемішують хроматографією на препаративній ВЕРХ Gilson, 1,5год. Додають літій-біс(триметилсилілі)амід використовуючи 50мм 20мкм колонку Chiracel OD з (8,65мл) до розчину (4R,5S)-1,5-диметил-4-фенілелююванням сумішшю етанол/ізогексан (9:1). Ви2-імідазолідинону (1,64г) у ТГФ (20мл) при -10°С і хід менш полярного ізомеру - 20мг (Сполука 16 у суміш перемішують при -10°С 10хв., залишають Таблиці 2). Вихід більш полярного ізомеру - 22мг нагрітись до 0°С і знову охолоджують до -10°С. (Сполука 17 у Таблиці 2) Краплями додають розчин хлориду кислоти (отриПриклад 14 маний вище) і суміш залишають нагрітись до кімN1-[1-(3-феніл)-3-{1-(етансульфонілпіперидиннатної температури. Реакційну суміш вливають у 4-іл)пропіл}піперидин-4-іл]-N1-етил-N3-4воду (100мл) і екстрагують етилацетатом метансульфонілфенілметилмочевина (Сполука 7 у (3´50мл). Об'єднані екстракти сушать, випарюють Таблиці 3). до сухості і залишок хроматографують на колонці 4-метансульфонілфенілметилізоціанат (99мг) 35 77969 36 у ТГФ (10мл) додають до 4-N-етил-[1-(3-феніл)-3речовину дигідрохлоридну сіль фільтрують і су{1-(етансульфонілпіперидин-4шать (гігроскопічна). Вихід 17 г. МС (МН+) 464. іл)пропіл}піперидину (200мг) і суміш витримують Бензиловий естер N-етил-N-[1-(3-феніл)-3-{1при кімнатній температурі протягом 16год. Реактрет-бутилоксикарбонілпіперидин-4ційну суміш вливають у 5г картридж SCX і елюють іл)пропіл}піперидин-4-іл]-карбамової кислоти Розчин 3-феніл-3-(1-третДХМ (3´10мл), метанолом (3´10мл) і метанольним бутилоксикарбонілпіперидин-4-іл)пропіональдегіду амонієм (1М, 3´10мл). Змивки метанольного амо(7,8г) [отриманого, як це описано у Прикладі 11] у нію випарюють і залишок розчиняють у ДХМ ДХМ (200мл) додають до суміші гідрохлориду бен(20мл) і додають ізоціанатну смолу (200мг). Суміш зилового естеру N-етил-N-піперидин-4-ілперемішують 16 год., фільтрують і фільтрат випакарбамової кислоти (7,4г) (CAS №220395-87-9) і рюють до сухості. Залишок хроматографують на ацетату натрію (2,17г) в етанолі (50мл) і переміколонці Bond-Elut і елюють з градієнтом розчиннишують 30хв. Невеликими порціями протягом 15хв. ка (етилацетат-25%, метанол/етил ацетат), одердодають триацетоксиборгідрид натрію (5,2г) у пежуючи бажану сполуку, ви хід 37мг. МС (МН+) 633. ремішують ще 2год. Краплями додають водний 4-N-етил-[1-(3-феніл)-3-{1NaOH (2М, 200мл), шар ДХМ збирають і промива(етансульфонілпіперидин-4-іл)пропіл}піперидин ють 2М NaOH (2´100мл), сушать і випарюють до сухості, одержуючи бажану сполуку, ви хід 26г. ЯМР (DMCOd6): 1 (t, 3Н) 1,35 (s, 9Н) 1,4-2 (m, 14Н) 2,3(m, 2Н) 2,6-2,7 (m, 4Н) 3,15 (q, 2Н) 3,4-4 (m, 3Н) 5,05 (s, 2H) 7,1-7,2 (m, 10Н). МС (МН+) 563. 4-метансульфонілфенілметилізоціанат Дифенілфосфорилазид (260мг) додають до Суміш бензилового естеру N-етил-N-[1-(3суміші 4-метансульфонілфенілоцтової кислоти феніл)-3-{1-(етансульфонілпіперидин-4(200мг) і триетиламіну (191мг) у ТГФ (20мл) і реакіл)пропіл}піперидин-4-іл]-карбамової кислоти (5г) і ційну суміш гріють під зворотним холодильником 10% паладію на карбоні (2г) в етанолі (200мл) гід4год., потім охолоджують і використовують безпорогенують під балоном з гідрогеном. Каталізатор середньо для наступної операції. фільтрують і фільтрат випарюють до сухості, одеМетод А ржуючи бажану сполуку, вихід 2,78г. N-[1-(3-феніл-3-хлорпропіл)-піперидин-4-іл]-NБензиловий естер N-етил-N-[1-(3-феніл)-3-{1етил-4-етансульфонілфенілацетамід (етансульфонілпіперидин-4-іл)пропіл}-піперидин-4Етап 1: Приготування N-[1-(3-феніл-3іл]-карбамової кислоти оксопропіл)-піперидин-4-іл]-N-етил-4-метансульфонілфенілацетаміду До розчину N-(4-піперидиніл)-N-етил-4метансульфонілфенілацетаміду (Метод В; 3.24г, 10ммоль) у ДМФ (50мл) додають карбонат калію (2,76г, 20ммоль) і потім 3-хлорпропіофенон (1,85г, 11ммоль). Суміш перемішують при кімнатній температурі 18год. і потім випарюють. Залишок розчиняють у ДХМ і розчин промивають водою Етансульфонілхлорид (2,3г) додають до роз(4´10мл) і розсолом (10мл), сушать (MgSO 4) і вичину дигідрохлориду бензилового естеру N-етилпарюють, одержуючи сирий продукт, який очищуN-[1-(3-феніл)-3-{піперидин-4-іл)пропіл}піперидинють елююванням через 50г Bond Elut з 10% мета4-іл]-карбамової кислоти (8,5г) і триетиламіну нолу у етилацетаті і одержують проміжну сполуку (4,8г) у ДХМ (200мл) при 0°С. Реакційну суміш за(2,4г, 53%); ЯМР (CDCI3): 1,1 (t, 1H), 1,2 (m, 2H), лишають нагрітись до кімнатної температури і пе1,6 (m, 6H), 2,2 (m, 1H), 2,8 (m, 2H), 3,0 (m, 5H), 3,2 ремішують 4год. Реакційну суміш промивають 2М (m, 2H), 3,3 (m, 2H), 3,8 (m, 2H), 7,4 (m, 5H), 7,9 (m, NaOH (2´100мл), сушать і випарюють до сухості. 4H); МС: 457. Залишок хроматографують на колонці Bond-Elut і Етап 2: Приготування N-[1-(3-феніл-3елюють з градієнтом розчинника (етилацетат-20%, гідроксипропіл)-піперидин-4-іл]-N-етил-4метанол/етилацетат), одержуючи бажану сполуку, метансульфонілфенілацетаміде вихід 5г. Я МР (D MCOd 6): 1 (t, 3Н) 1,1 (t, 3Н), 1,3-3 До розчину N-[1-(3-феніл-3-охопропіл)(m, 14Н), 2,2 (m, 1H) 2,55-2,9 (m, 5H), 2,95 (q, 2Н), піперидин-4-іл]-N-етил-4-метансульфонілфеніл3,1(q, 2Н), 3,4-3,7 (m, 3Н), 5,05 (s, 2H), 7,1-7,4 (m, ацетаміду (912мг, 2ммоль) в етанолі (20мл) при 10Н). МС (МН+) 556. 0°С додають боргідрид натрію (76мг, 2ммоль). Дигідрохлорид бензилового естеру N-етил-NСуміш перемішують при кімнатній температурі [1-(3-феніл)-3-{піперидин-4-іл)пропіл}-піперидин-4протягом 30хв. і потім випарюють. Залишок розчиіл]-карбамової кислоти няють у ДХМ і розчин промивають водою (2´5мл) і НСІ у діоксані (50мл, 4М) додають до бензилорозсолом (5мл), сушать (MgSO4) і випарюють, вого естеру N-етил-N-[1-(3-феніл)-3-{1-третодержуючи проміжну сполуку (812мг, 87%); ЯМР бутилоксикарбонілпіперидин-4(CDCl3): 1,1 (t, 1H), 1,2 (m, 2Н), 1,6 (m, 8Н), 2,0 (m, іл)пропіл}піперидин-4-іл]-карбамової кислоти (26г) 1Н), 2,2 (m, 1Н) 2,6 (m, 2Н), 3,0 (s ,3Н), 3,2 (m, 2 Н), при 0°С. С залишають досягти кімнатної темпера3,3 (m, 2Н), 3,8 (m, 2Н), 4,9 (d, 1Н), 7,3 (m, 5Н), 7,4 тури і перемішують 2год. Реакційну суміш розбав(d, 2H), 7,9 (d, 2H); МС: 459. ляють діетилетером (200мл) і осаджену твердої Етап 3: Приготування бажаної сполуки 37 77969 38 До суміші N-[1-(3-феніл-3-гідроксипропіл)лишають затвердіти і одержують бажану сполуку піперидин-4-іл]-N-етил-4-метансульфоніл(24,9г, 94%); ЯМР: 1,02 і 1,15 (t, 3Н), 1,4 -1,6 (br m, фенілацетаміду (400мг, 0,87ммоль) і триетиламіну 4Н), 2,45 (m, 2Н), 2,93 (br m, 2H), 3,18 (s, 3Н), 3,20 і (0,24мл, 1,04ммоль) у ДХМ (10мл) при 0°С дода3,32 (q, 2H), 3,72 і 4,18 (m, 1Н), 3,80 і 3,87 (s, 2Н), ють метансульфонілхлорид (67мкл, 0,87ммоль). 7,50 (m, 2Н), 7,85 (m, 2Н); МС: 325 (МН+). Суміш перемішують при кімнатній температурі Метод С 30хв. і потім випарюють. Залишок очищують елю3-феніл-3-(1-трет-бутилкарбонілоксиперидинюванням через 20г Bond Elut і одержують бажану 4-іл)пропіональдегід сполуку (180мг, 44%); ЯМР (CDCI3): 1,1 (t, 1H), 1,2 Етап 1: Приготування 1-трет(m, 2H), 1,6 (m, 7H), 2,2 (m, 2Н), 2,4 (m, 2Н), 2,8 (m, бутилкарбонілокси-4-бензоїлпіперидину 2Н), 3,0 (s, 3Н), 3,3 (m, 2H), 3,8 (m, 2H), 5,0 (m, 1H), До розчину 4-бензоїлпіперидину (6г, 7,3 (m, 5H), 7,4 (d, 2Н), 7,9 (d, 2Н); МС: 477. 26,5ммоль) у 2М водному гідроксиді натрію Метод В (26,5мл) додають ди-трет-бутилдикарбонат (5,79г, N-(4-піперидиніл)-N-етил-426,5ммоль) і суміш перемішують при кімнатній метансульфонілфенілацетамід температурі 18год. Тверду речовину ізолюють фіЕтап 1: Приготування дигідрохлориду 1льтруванням і сушать під вакуумом при 40°С, одефенілметил-4-етиламінопіперидину ржуючи проміжну сполуку (7г); Я МР: 1,3-1,4 (m, До розчину 1-фенілметил-4-піперидону (25,0г, 11Н) 1,7 (m, 2Н) 2,9 (m, 2Н) 3,6 (m, 1Н) 3,95 (m, 2Н) 132ммоль) у ТГФ (250мл) додають етиламінгідро7,5-7,6 (m, ЗН) 7,95 (d, 2H). хлорид (12,0г, 147моль) і метанол (50мл) і суміш Етап 2: Приготування етил 3-феніл-3-(1-третперемішують при кімнатній температурі 10хв. Порбутилкарбонілоксипіперидин-4-іл)-акрилату ціями додають триацетоксиборгідрид натрію (40г, До розчину триетилфосфоноацетату (6,2г, 189ммоль) і суміш перемішують при кімнатній те27ммоль) у ТГФ (100мл) при 0°С додають літіймпературі протягом 1год. Додають 2М розчин гідбіс(триметилсиліл)амід (32,5мл, 1М, 32,5ммоль). роксиду натрію (250мл) і суміш екстрагують діетиСуміш перемішують при 0°С 20хв. Додають 1-третлетером. Органічні екстракти сушать (K2СО3) і бутилкарбонілокси-4-бензоїлпіперидин (7г, випарюють, одержуючи 1-фенілметил-425ммоль) і суміш перемішують при кімнатній теметиламінопіперидин у вигляді масла, яке розчиняпературі 48год. Суміш випарюють і залишок розють в етанолі (500мл) і додають концентровану чиняють у етилацетаті (200мл). Розчин промивагідрохлоридну кислоту (20мл). Одержані кристали ють 2М гідрохлоридною кислотою (2´100мл), збирають, промивають діетилетером і сушать, сушать і випарюють, одержуючи проміжну сполуку. одержуючи проміжну сполуку у вигляді твердої Етап 3: Приготування етил 3-феніл-3-(1-третречовини (38г); ЯМР: (CDCI3): 1,10 (t, 3Н), 1,40 (m, бутилкарбонілоксипіперидин-4-іл)пропіоноату 2H), 1,83 (m, 2H), 2,02 (m, 2H), 2,65 (q, 2H), 2,85 (m, Етил 3-феніл-3-(1-трет2Н), 3,50 (s, 2Н), 3,75 (m, 1Н), 7,2-7,4 (m, 5Н); МС: бутилкарбонілоксипіперидин-4-іл)акрилат 219 (МН+). (~25ммоль) розчиняють в етанолі (200мл) і розчин Етап 2: Приготування N-(1-фенілметил-4продувають аргоном. Додають 20% гідроксиду піперидиніл)-N-етил-4-метансульфонлпаладію (2г) і суміш перемішують при кімнатній фенілацетаміду температурі в атмосфері гідрогену (балон) протяДо розчину дігідрохлориду 1-фенілметил-4гом 72год. Суміш продувають аргоном, фільтрують етиламінопіперидину (32,0г, 110ммоль) у ДХМ і фільтрат випарюють. Сирий продукт очищують (500мл) додають Ν,Ν-діізопропілетиламін (60мл) і силікагелевою хроматографією (елюент: ізогексан, перемішують до повного розчинення. Додають 4потім 35% етилацетату в ізогексані) і одержують метансульфонілфенілоцтову кислоту (25,0г, проміжну сполуку (5,3г). 117ммоль), 4-диметиламінопіридин (2,0г) і дицикЕтап 4: Приготування 3-феніл-3-(1-третлогексилкарбодіімід (25,0г, 121ммоль) і суміш пебутилкарбонілоксипіперидин-4-іл)пропан-1-ол ремішують при кімнатній температурі 20год. Осад До розчину етил 3-феніл-3-(1-третвидаляють фільтруванням і розчин промивають бутилкарбонілоксипіперидин-4-іл)пропіоноату послідовно 2N водною НСІ, водою і 1Н водним (5,3г, 14,6ммоль) у ТГФ (100мл) протягом 20хв. NaOH, сушать (MgSO 4) і випарюють. Залишок краплями додають алюмогідрид літію (14,6мл, 1М, очищують силікагелевою хроматографією (елюент 14,6ммоль). Суміш перемішують при 0°С протягом 10% МеОН/етилацетат), одержуючи проміжну спо1год. Краплями додають 2М водний гідроксид налуку (35г, 76%); ЯМР: 1,00 і 1,14 (t, 3Н), 1,45 і 1,70 трію (20мл). Суміш фільтрують через Celite®, про(m, 2Н), 1,95 (br m, 2Н), 2,80 (br m, 2Н), 3,18 (s, мивають етилацетатом (3´25мл), фільтрат і змив3Н), 3,20 і 3,33 (q, 2Н), 3,45 (s, 2H), 3,80 і 3,87 (s, ки об'єднують і випарюють. Залишок розчиняють в 2Н), 3,70 і 4,10 (m, 1Н), 7,2-7,3 (m, 5Н), 7,48 (m, етилацетаті (100мл) і розчин промивають водою 2Н), 7,82 (m, 2Н); МС: 415 (МН+). (3´50мл), сушать і випарюють, одержуючи проміжЕтап 3: Приготування бажаної сполуки ну сполуку (4,6г); Я МР: 0,9-1 (m, 2Н) 1,25 (m, 1Н) До розчину N-(1-фенілметил-4-піперидиніл)-N1,35 (s, 9Н) 1,5-2 (m, 5Н) 2,6 (m, 2Н) 3,1 (m, 2Н) етил-4-метансульфонілфенілацетамщу (34г, 3,8-4 (m, 2Н) 4,2 (t, 1Н). 82ммоль) в етанолі (600мл) додають формат амоЕтап 5: Приготування бажаної сполуки нію (40г). Суміш продувають аргоном і додають До розчину 3-феніл-3-(4-1-трет30% Pd на карбоні (4,2г). Суміш перемішують під бутилкарбонілоксипіперидин-4-іл)пропан-1-олу зворотним холодильником 4год., залишають охо(4,6г, 14,4ммоль) у ДХМ (100мл) додають Dessлонути і фільтрують через діатомову землю. ФільMartin-періодиган (6,1г, 14,6ммоль) і суміш перетрат випарюють і одержують густе масло, яке замішують при кімнатній температурі 2год. Суміш 39 77969 40 промивають 2М водним гідроксидом натрію піперидин-4-іл]-N-етил-4-метансульфонілфенілацетамід: (3´50мл), сушать і випарюють, одержуючи бажану сполуку. Метод D N-(трет-бутоксикарбонілпіперидин-4-іл)-Nетил-4-метансульфонілфенілацетамід DBU додають до розчину піперидин-4-іл]-N До розчину 4-метилсульфонілфенілоцтової кислоти (16,1г) у толуолі (200мл) під аргоном додають дифенілфосфорилазид (16,2мл) і триетиламін (10,4мл). Суміш гріють при 90°С 3год. і потім залишають охолонути. Додають трет-бутил-1-оксо4-аміноетилпіперидин [CAS 264905-39-7] (7,10г) у толуолі (100мл) і суміш перемішують 18год. і потім розділяють між ЕtOАс/Н2 О (500мл/400мл), фільтрують, органічний шар відокремлюють і промивають насиченим розчином NaHCO3 (2´300мл), розсолом (300мл), сушать над MgSO4 , фільтрують і випарюють. Одержане коричневе масло очищують на кремнеземі, використовуючи градієнтне елюювання 0-3% МеОН у EtOAc, одержуючи бажану сполуку як жовту тверду речовину (7,10г); ЯМР: (DMCO): 1,4 (t, 3Н), 1,40 (s, 9Н), 1,52 (m, 4Н), 2:73 (m, 2Н), 3,15 (m, 5Н), 4,02 (m, 3Н), 4,32 (d, 2Н), 6,89 (t, 1Н), 7,43 (d, 2Н), 7,87 (d, 2Н). МС 340 (МН+ Вос) N-піперидин-4iл]-N-етил-4метансульфонілФенілацетамід Піперидин (6,84г) розчиняють у ДХМ (39мл) і повільно додають ТФК (39мл). Суміш витримують 40 хвилин і потім випарюють. Залишок розчиняють у 2 М NaOH і екстрагують ДХМ (3 ´150мл), екстракти суша ть над MgSO4, фільтрують і випарюють, одержуючи бажану сполуку у вигляді жовтої твердої речовини (5,00г); ЯМР: (D MCO): 1,05 (t, 3Н), 1,41 (m, 4H), 2,42 (m, 2Н), 2,96 (d, 2Н), 3,20 (m, 5Н), 3,90 (квінт., 1Н), 4,29 (d, 2H), 6,84 (t, 1H), 7,43 (d, 2H), 7,85 (d, 2Н), МС 340 (МН+). Метод Ε N-[1-(3-[3,4-дифлуорфеніл]-3-гідроксипропіл)піперидин-4-іл]-N-етил-4-метансульфонілфенілацетамід Розчин боргідриду натрію (7,7мг) в етанолі (1мл) додають до розчину Ν-[1-(3-[3,4дифлуорфеніл]-3-кетопропіл)-піперидин-4-іл]-Nетил-4-метансульфонілфенілацетаміду (0,25г) в етанолі (3,2мл) при 0°С під аргоном і реакцію залишають нагрітись до кімнатної температури протягом 20год. Реакцію гасять розсолом, екстрагують тричі етером і об'єднані екстракти сушать. Фільтрат концентрують до прозорого масла, вихід 6,21г. МС (МН+) 495. N-1-(3-[3,4-дифлуорфеніл]-3-кетопропіл) етил-4-метансульфонілфенілацетаміду (CAS 374725-04-9) (320мг) і 3,4дифлуорфенілвінілкетону (654мг) у ДХМ (9мл) під аргоном і реакційну суміш перемішують 36год., після чого концентрують у вакуумі і очищують, використовуючи фле ш-хроматографію на колонці кремнезему, елюючи з градієнтом розчинника (метанол 10-15%, метанол у ДХМ), ви хід 250мг, МН+493. 3,4-дифлуор фенілвініл кетон Dess-Martin-періодінан (3,18г) додають до розчину 3,4-дифлуорвінілового спирту (CAS 14994684-9) (1,18г) у ДХМ (22мл) при 0°С під аргоном і реакційну суміш залишають перемішуватись протягом 1год. Суміш вносять у колонку для очищення флеш-хроматографією з градієнтним елююванням (етил ацетат - 10%, етил ацетат і ізогексан), вихід 654мг. ЯМР (CDCI3): 6,0 (d, 1H), 6,50 (d, 1H), 7,10 (dd, 1H), 7,30 (m, 1H), 7,80 (m, 2H). Приклад 15 Здатність сполук інгібувати зв'язування РАНТВ оцінювали дослідженням зв'язування радіоліганда in vitro. Мембрани отримували з клітин яєчника китайського хом'яка, які експресували рецептор рекомбінантного CCR5 людини. Ці мембрани інкубували з 0,1нМ іодованого РАНТВ, сцинтиляційними кульками і сполуками винаходу різної концентрації у 96-гніздових платах. Кількість іодованого RANTES, зв'язаного з рецептором, визначали підрахуванням сцинтиляцій. Були побудовані криві для сполуки і концентрації сполуки, яка викликала витиснення 50% зв'язаного іодованого РАНТВ (ІС50). Переважно сполуки формули (1) мають ІС50< 50мкМ. Приклад 16 Здатність сполук інгібувати зв'язування МІР-1a оцінювали дослідженням зв'язування радіоліганда in vitro. Мембрани отримували з клітин яєчника китайського хом'яка, які експресували рецептор рекомбінантного CCR5 людини. Ці мембрани інкубували з 0,1нМ іодованого РАНТВ, сцинтиляційними кульками і сполуками винаходу різної концентрації у 96-гніздових платах. Кількість іодованого МІР-1a, зв'язаного з рецептором, визначали підрахуванням сцинтиляцій. Були побудовані криві для сполуки і концентрації сполуки, яка викликала витиснення 50% зв'язаного іодованого МІР-1a (ІС50). Переважно сполуки формули (1) мають ІС50
ДивитисяДодаткова інформація
Назва патенту англійськоюPiperidine derivatives and their use for modulating ccr5 receptor activity, process for their manufacture, pharmaceutical composition and intermediate compound
Автори англійськоюTucker Howard
Назва патенту російськоюПроизводные пиперидина и их применение в качестве модуляторов активности рецепторов хемокина, в частности ccr5, способ их получения, фармацевтическая композиция на их основе и промежуточное соединение
Автори російськоюТакер Говард
МПК / Мітки
МПК: A61P 37/08, C07D 211/62, C07D 417/14, A61K 31/445, C07D 401/12, A61P 37/02, A61P 11/00, A61K 31/4709, C07D 417/12, C07D 413/12, A61K 31/4545, C07D 409/12, A61K 31/454, A61P 19/02, A61P 9/10, A61K 31/453, A61P 11/06, A61P 27/16, A61K 31/496, A61P 17/00, C07D 405/14, A61P 21/04, A61P 31/18, A61P 25/00, A61P 27/14, C07D 211/96, A61P 29/00, A61P 25/28, A61K 31/497, A61P 19/00, A61P 1/00, C07D 401/14, A61P 43/00, C07D 211/58, A61P 3/10, A61P 17/06, A61P 37/00
Мітки: сполука, композиція, ccr5, похідні, активності, рецепторів, основі, спосіб, застосування, хемокіну, модуляторів, піперидину, проміжна, зокрема, фармацевтична, одержання
Код посилання
<a href="https://ua.patents.su/21-77969-pokhidni-piperidinu-ta-kh-zastosuvannya-yak-modulyatoriv-aktivnosti-receptoriv-khemokinu-zokrema-ccr5-sposib-kh-oderzhannya-farmacevtichna-kompoziciya-na-kh-osnovi-ta-promizhna-spo.html" target="_blank" rel="follow" title="База патентів України">Похідні піперидину та їх застосування як модуляторів активності рецепторів хемокіну (зокрема ccr5), спосіб їх одержання, фармацевтична композиція на їх основі та проміжна сполука</a>
Попередній патент: Оптопневматичний перетворювач
Наступний патент: Пристрій для одержання вуглецевого наноструктурного матеріалу
Випадковий патент: Спосіб діагностики зниження висоти прикусу












