Спосіб одержання сполуки бензімідазолу
Формула / Реферат
1. Спосіб одержання 5-метокси-2-[[(4-метокси-3,5-диметил-2-піридиніл)метил]тіо]-1Н-бензімідазолу формули І
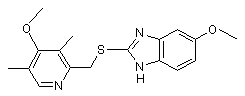 I
I
з (4-метокси-3,5-диметил-2-піридиніл)-метилового спирту, який включає наступні реакційні етапи, які проводять послідовно в одній головній розчинній системі без виділення проміжних сполук, які утворюються під час відтворення способу:
етап 1) реакція (4-метокси-3,5-диметил-2-піридиніл)-метилового спирту формули Іа
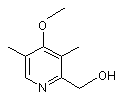 Iа
Iа
з хлоро-дегідроксилюючим реагентом з утворенням (4-метокси-3,5-диметил-2-піридиніл)-метил хлориду формули Іb
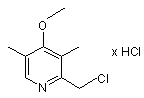 Ib;
Ib;
етап 2) реакція (4-метокси-3,5-диметил-2-піридиніл)метил хлориду формули Іb, одержаного на етапі 1, з 2-меркапто-5-метоксибензімідазолом формули Іс
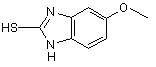 Ic
Ic
в присутності основи з утворенням 5-метокси-2-[[(4-метокси-3,5-диметил-2-піридиніл)метил]тіо]-1Н-бензімідазолу формули І, який відрізняється тим, що розчинна система, спільна для всієї реакційної послідовності, складається з органічного розчинника, який не змішується з водою, і доданої встановленої кількості води в межах від 0,3 до 5,5 мг води/мл органічного розчинника, який не змішується з водою.
2. Спосіб за п. 1, який відрізняється тим, що органічним розчинником, який не змішується з водою, є толуол.
3. Спосіб за п. 1, який відрізняється тим, що органічним розчинником, який не змішується з водою, є етилацетат.
4. Спосіб за п. 1, який відрізняється тим, що встановлена кількість води присутня з початку реакції, згідно з етапом 1.
5. Спосіб за будь-яким з пп. 1 і 4, який відрізняється тим, що встановлену кількість води додають під час завантаження хлоро-дегідроксилюючого реагенту при реакції, згідно з етапом 1.
6. Спосіб за будь-яким з пп. 1-4, який відрізняється тим, що встановлену кількість води додають після завантаження хлоро-дегідроксилюючого реагенту при реакції, згідно з етапом 1.
7. Спосіб за п. 1, який відрізняється тим, що встановлена кількість води знаходиться в межах 0,3-5,0 мг/мл органічного розчинника, який не змішується з водою.
8. Спосіб за п. 1, який відрізняється тим, що встановлена кількість води знаходиться в межах 0,4-2,4 мг/мл органічного розчинника, який не змішується з водою.
9. Спосіб за п. 1, який відрізняється тим, що встановлена кількість води знаходиться в межах 1,0-2,4 мг/мл органічного розчинника, який не змішується з водою.
10. Спосіб за будь-яким з пп. 1-9, який відрізняється тим, що реакцію, згідно з етапом 1, виконують при температурі від –5 °С до +45 °С.
11. Спосіб за будь-яким з пп. 1-9, який відрізняється тим, що його проводять при температурі від –5 °С до +35 °С.
12. Спосіб за будь-яким з пп. 1-9, який відрізняється тим, що його проводять при температурі від +10 °С до +35 °С.
13. Спосіб за будь-яким з пп. 1-9, який відрізняється тим, що його проводять при температурі від +25 °С до +35 °С.
14. Спосіб за будь-яким з пп. 1-13, який відрізняється тим, що хлоро-дегідроксилюючим реагентом є тіоніл хлорид.
15. Спосіб за п. 1, який відрізняється тим, що додаткову кількість води додають до органічного розчинника, який не змішується з водою, під час етапу 1 після початку реакції.
16. Спосіб за п. 1, який відрізняється тим, що реакцію на етапі 2 проводять при температурі в межах між +30 °С та +60 °С.
17. 5-метокси-2[[(4-метокси-3,5-диметил-2-піридиніл)метил]тіо]-1Н-бензімідазол (пірметазол), одержаний за будь-яким з пп. 1-16.
Текст
Представлений винахід стосується вдосконаленого способу синтезування 5-метокси-2-(((4-метокси-3,5диметил-2-піридиніл)-метил)тіо)-1Н-бензимідазолу (пірметазолу), який використовується при виробництві 5метокси-2-[[(4-метокси-3,5-диметил-2-піридиніл)-метил]сульфініл]-1Н-бензимідазолу і його (S)-енантіомеру, відомих під загальними назвами омепразол і езомепразол відповідно. Ефективний спосіб синтезування омепразолу [описаний у WO 97/22603], на який є посилання. В описаному способі немає потреби в додаткових операціях очищення або виділення між різними стадіями реакції, і тому він є більш ефективним способом. Крім того, спрощенням є те, що реакційну послідовність виконують в одній спільній розчинній системі протягом всього процесу. Однак, все ж таки залишається потреба в новому, більш зручному і більш ефективному способі виробництва пірметазолу в більшій кількості і з вищою чистотою, який забезпечує підвищений вихід готових продуктів реакції, омепразолу або езомепразолу. Метою винаходу є забезпечення способу для виробництва пірметазолу в більшій кількості і з вищою чистотою, який особливо важливий для асиметричного синтезу езомепразолу. Спосіб, тобто послідовність реакцій від пірметилового спирту (Іа) до пірметазолу (І), проводять, без будь-якого виділення або очищення проміжних сполук, в одній розчинній системі, спільній для реакційної послідовності, для отримання відтворюваного великого виходу готових кінцевих продуктів, омепразолу або езомепразолу. Такий спосіб виключає етапи виділення або очищення проміжних сполук і зберігає час на запобігання змінам розчинника під час процесу, таким чином роблячи процес більш ефективним і продуктивним. Спосіб включає наступні етапи: Етап 1: Пірметиловий спирт (la) + хлор-дегідроксиляційний реагент ® пірметил хлорид (Іb). Етап 2: Пірметил хлорид (Іb) + метмерказол (Іс) ® пірметазол (І) проводять в розчинній системі, яка є спільною для реакційної послідовності і яка складається з органічного розчинника, який не змішується з водою, і доданої встановленої кількості води. Цей процес використовується для синтезування пірметазолу, проміжної сполуки при синтезуванні омепразолу або езомепразолу. Під час етапу 1 відбувається перетворення пірметилового спирту у пірметил хлорид, далі означена як хлоро-дегідроксиляція, пірметиловий спирт (Іа) реагує з надлишком хлоро-дегідроксиляційного реагенту, утворюючи алкіл хлорид, тобто пірметил хлорид (Іb). Хлоро-дегідроксиляційний реагент може бути вибраний із тіоніл хлориду, ціанурик хлориду, фосфористого трихлориду, фосфористого пентахлориду і фосфористого оксихлориду. Реакцію проводять при температурі від -5°С до +45°С, переважно між -5°С і +35°С, більш переважно між +10°С і +35°С або між +25°С і +35"С. У випадку, коли вода не присутня з самого початку, перетворення реагентів на продукт реакції, пірметил хлорид (Іb), не завершиться. Однак, реакцію можна повторно почати додаванням встановленої кількості води, і після цього реакція може бути завершена. Таким чином, якщо реакція припиняється, її можна почати повторно додаванням встановленої кількості води. Згідно з вищезгаданим Етапом 2, пірметил хлорид (Іb), отриманий на Етапі 1, вводять в реакцію з метмерказолом (Іс) у лужному середовищі, наприклад, лужний водний розчин метмерказолу (Іс) готують і змішують з пірметил хлоридом (Іb). Реакцію переважно проводять при температурі від +30°С до +60°С протягом тривалого часу. Метмерказол (Іс) додають у приблизно стехіометричній кількості до пірметил хлориду (Іb). Винахід також можна використовувати у комбінації з каталізатором фазового переходу, наприклад, четверним аміном, таким як тетрабутил амоній бромід. Дві сформовані фази розділяють, водна фаза може бути видалена за допомогою органічного розчинника, який не змішується з водою, такого як толуол, а органічна фаза може бути видалена за допомогою води. Так як пірметиловий спирт (Іа) має несприятливу дію на наступних етапах реакції, важливо мінімізувати вміст наявного пірметилового спирту (Іа). Реакційну послідовність, згідно з Етапом 1 і Етапом 2, описаними вище, проводять в одній розчинній системі. Розчинна система, яка використовується для представленої реакційної послідовності, складається з органічного розчинника, який не змішується з водою, такого як галогенізовані, аліфатичні або ароматичні гідрокарбони або ефіри, наприклад, толуол, етилацетат і метилен хлорид, і доданої встановленої кількості води. Переважно, толуол може бути використаний як органічний розчинник, який не змішується з водою. Вміст води у розчинній системі повинен переважно бути близько або більше точки насичення використовуваного органічного розчинника. При цьому більш велика кількість пірметилового спирту (Іа) має змогу прореагувати і утворити пірметил хлорид (Іb). Кількість води може бути додана до, під час або після додавання хлоро-дегідроксиляційного реагенту, такого як тіоніл хлорид. Оптимальна кількість води під час Етапу 1 складає між 0,3 і 5,5мг води/мл органічного розчинника, який не змішується з водою, переважно між 0,3 і 5,0мг води/мл або між 0,4 і 2,4мг/мл, і найбільш переважно між 1,0 і 2,4мг/мл. Якщо вміст води є нижчим ніж точка насичення використовуваного органічного розчинника, тобто, для толуолу, менше за 0,3мг/мл, реакція є повільною і вона має тенденцію до зупинки до досягнення повного перетворення. В середньому, досягають перетворення 25-50%, коли толуол, який має вміст води менше за 0,1мг/мл, використовується як розчинна система. Така реакція призводить до високого вмісту пірметилового спирту (Іа) в реакційній суміші після Етапу 1. Наявність високого вмісту пірметилового спирту у сировинному продукті пірметазолу (І) після Етапу 2 є незручним. Ми встановили, що якщо близько 1%, або більше, пірметилового спирту (Іа) залишається у реакційній суміші, цей компонент має несприятливу дію як на перетворення, так і на енатіоселективність, яка досягнена при асиметричному окисненні пірметазолу у езомепразолі. Представлений винахід є вдосконаленням перших двох етапів способу, [описаного в WO 97/22603]. Реакційна послідовність, від пірметилового спирту (Іа) через пірметил хлорид (Іb) до пірметазолу (І), проводять у спільній розчинній системі, яка складається з органічного розчинника, який не змішується з водою, і встановленої кількості води, і яка використовується протягом всієї реакційної послідовності. Новий вдосконалений спосіб для виробництва 5-метокси-2-(((4-метокси-3,5-диметил-2-піридиніл)-метил)-тіо)-1Нбензимідазолу (пірметазолу) більш детально буде описаний далі на Етапі 1 і Етапі 2, які обидва проводяться в органічному розчиннику, який не змішується з водою, і з доданою встановленої кількістю води: Етап 1: Хлоро-дегідроксиляція: Реакція (4-метокси-3,5-диметил-2-піридиніл)-метилового спирту (пірметилового спирту) формули Іа la з хлоро-дегідроксиляційним реагентом, таким як тіоніл хлорид, з утворенням (4-метокси-3,5-диметил-2піридиніл)метил хлориду (піриметил хлориду) формули Іb lb Етап 2: Реакція сполучення: Реакція (4-метокси-3,5-диметил-2-піридиніл)метил хлориду формули Іb, виготовленого на Етапі 1, описаному вище, з 2-меркапто-5-метоксибензимідазолом (метмерказолом) формули Іс lc у присутності основи, такої як гідроксид натрію або гідроксид калію, з утворенням 5-метокси-2-(((4метокси-3,5-диметил-2-піридиніл)метил)-тіо)-1Н-бензимідазолу (пірметазолу) формули І l Після цього пірметазол перетворюють у кінцеві продукти, омепразол або езомепразол. Представлений винахід пропонує вдосконалення, пов'язане з Етапом 1, при виготовленні пірметазолу, шляхом більш повного перетворення і відтворюваного виходу пірметилового спирту (Іа) і пірметил хлориду (Іb) відповідно. Корисна дія води, присутня під час реакції хлоро-дегідроксиляції, Етап 1, є неочікуваним ефектом, адже цей тип хлоро-дегідроксилюючих реагентів вважається несумісним з водою, наприклад, тіоніл хлорид сильно реагує з водою і надлишок тіоніл хлориду звичайно гідролізують після реакції шляхом додавання води. Зокрема, ціллю винаходу було вдосконалення Етапу 1, етапу хлоро-дегідроксиляції, в процесі виготовлення пірметазолу (І), який використовується при синтезі омепразолу або езомепразолу, наприклад, для отримання більш ефективного перетворення пірметилового спирту (Іа), етап реакції, який є спільним для синтезу як езомепразолу, так і омепразолу. Неочікувано, було знайдено, що наявність відповідної кількості води зменшує кількість залишку пірметилового спирту (Іа), тобто, перетворення пірметилового спирту (Іа) згідно з Етапом 1 є більш повним. Наявність невеликої кількості води у реакційній суміші сприяє кращому перетворенню, і більш ефективному використанню пірметилового спирту (Іа) і утворення продукту з більш високим виходом і вищої чистоти. Згідно з способом, [описаним у WO 97/22603], сировинний продукт пірметазол (І), після Етапу 2 перетворюється на омепразол під час кінцевої реакційної послідовності. Під час реакційної послідовності не здійснюється виділення або очищення, що є переважним з точки зору простоти і економічності процесу. Однак, осади пірметилового спирту (Іа), отриманого на Етапі 1, були поміченів суміші отриманого пірметазолу (І) на Етапі 2. Було помічено, що залишки пірметилового спирту (Іа) мають несприятливу дію при окисненні пірметазолу (І) у омепразол і особливо потім під час асиметричного окиснення пирметазолу (І) у езомепразол. Такі залишки пірметилового спирту (Іа) призводять до зниженого перетворення і енантіо-селективності при асиметричному окисненні, і дають реакційний продукт зі зниженою чистотою і більш низьким виходом. Таким чином, отриманий енантіомерний надлишок езомепразолу залежить від висоти очищення проміжної сполуки пірметазолу (І). Був досліджений вплив пірметилового спирту на рівні від близько 1% або вище. Присутність води при реакції хлоро-дегідроксиляції, Етап 1, є найбільш важливим для отримання пірметил хлориду (Іb), а потім пірметазолу (І), з високим виходом і високою чистотою без будь-яких потреб у виділенні або очищенні. Потрібна кількість води може бути завантажена на початку, або бути додана під час або після додавання відповідного хлоро-дегідроксиляційного реагенту, такого як тіоніл хлорид. Переважно, малу відповідну кількість води завантажують на початку реакції. Додавання води під час процесу можна також використовувати як спосіб для поновлення незавершеної реакції для покращення виходу і чистоти продукту. Винахід забезпечує більш ефективне використання хлоро-дегідроксиляційного реагенту. Крім того, наявність води на Етапі 2 забезпечує безпечніший і більш стійкий процес, так як вона також зменшує різні ризики, пов'язані з типом реакцій, наприклад, таким як накопичення тіоніл хлориду або хімічно активних проміжних сполук реакції. Таким чином, має місце запобігання ризику запізненої швидкої екзотермічної реакції. Однак, існують інші можливості отримання повного і/або високого перетворення пірметилового спирту (Іа) на Етапі 1, і запобігання або мінімізації залишків пірметилового спирту (Іа) на Етапі 2. Такими можливостями можуть бути, наприклад, подовжений час реакції, підвищена температура реакції . або підвищений надлишок тіоніл хлориду. Однак, ці можливості не є переважними з точки зору ефективного виготовлення кінцевих реакційних продуктів, омепразолу і езомепразолу. Приклади, описані далі, проілюструють вдосконалений спосіб за винаходом. Ці приклади не обмежують границі винаходу, які описані вище в тексті або наведені нижче у формулі винаходу. Приклади Приклад 1 Пірметиловий спирт, 8,82г (52,7ммоль) розчинили в толуолі, насиченому водою, 74мл (вміст води 0,4мг/мл згідно з титруванням Карла Фішера). До розмішаного розчину, при температурі 10°С, тіоніл хлорид, 8,15г (68,8ммоль), додали повільно протягом 60 хвилин (швидкість вливання 0,083мл/хв.). Утворився білий осад. Після перетворення пірметилового спирту на пірметил хлорид виконали рідинну хромотографію високого тиску (РХВТ), (колона: Nova-Рак С18, 4mм, 3,9*150мм). Була зареєстрована швидка реакція, яка забезпечує досягнення 99% перетворення після повного додавання тіоніл хлориду. Приклад 2 Пірметиловий спирт, 8,81г (52,6ммоль) розчинили в суміші толуолу, 75мл (вміст води 0,04мг/мл згідно з титруванням Карла Фішера) і води, 180mл (10ммоль, еквівалент близько 2,4мг/мл води в толуолі). До розмішаного розчину, при температурі 10°С, додавали тіоніл хлорид, 8,15г (68,5ммоль) повільно протягом 60 хвилин (швидкість вливання 0,083мл/хв.). Утворився білий осад. Після перетворення пірметилового спирту у пірметил хлорид виконали РХВТ, як у Прикладі 1. Зареєстрована швидка реакція, яка забезпечила досягнення 99% перетворення після завершення додавання тіоніл хлориду. Температуру реакції встановили 20°С, і метанол, 40мл, додали для припинення реакції. Отримали розчин сировинного реакційного продукту, пірметил хлориду, з чистотою 99,6% (РХВП), і з осадом пірметилового спирту у кількості 0,3%. Приклад 3 Пірметиловий спирт, 8,82г (52,7ммоль) розчинили в толуолі, 75мл (вміст води 0,04мг/мл згідно з титруванням Карла Фішера). До розмішаного розчину, при температурі 10°С додали повільно, протягом 60 хвилин (швидкість вливання 0,083мл/хв.), тіоніл хлорид, 8,15г (68,5ммоль). Одразу сформувався білий осад. Отриману суміш реакції розмішали і виконали РХВТ, як в Прикладі 1, протягом додаткових 3,5 годин (перетворення уповільнилось і зупинилось на приблизно 30%). Воду, 180mл (10ммоль), додали для поновлення реакції, збільшуючи вихід і високе перетворення (>90%) за 30 хвилин після додавання. Приклад 4 Пірметиловий спирт, 8,8г (52,6ммоль) розчинили в толуолі, (75мл, вміст води 0,12мг/мл), зволоженому водою (180mл, 10ммоль) при кімнатній температурі. До розмішаного розчину, при температурі 25-30°С, додали повільно протягом 60 хвилин (швидкість вливання 0,083мл/хв.) тіоніл хлорид, 8,15г (68,5ммоль). Перетворення при реакції проаналізували за допомогою РХВТ, як в Прикладі 1. Перетворення склало більше 99,5%. Воду (2,3мл) додали для гасіння будь-якого надлишку тіоніл хлориду. Додали лужний (13,5г, 168,3ммоль 50% маса/маса натрій гідроксиду) водний (80мл) розчин метмерказолу (9,8г, 54,2ммоль), далі додали натрій гідроксид (8,8г, 110,5ммоль, 50% маса/маса натрій гідроксиду) для досягнення рН>12,5. Температуру підвищили до 45°С під час додавань. Реакційну суміш залишили при сильному перемішуванні на близько дві години при температурі 45°С. Перемішування було перерване і фази залишили для розділення. Водяну фазу видалили. Органічну фазу, яка включає пірметазол, промили водою і піддали аналізу для осадження пірметилового спирту (менше за 0,1% мол). Приклад 5 Пірметиловий спирт, 8,8г (52,6ммоль) розчинили в толуолі, (75мл, вміст води 0,12мг/мл), зволоженому водою (375μл, 20,8ммоль) при кімнатній температурі. До розмішаного розчину, при температурі 25-35°С, додали повільно протягом 60 хвилин (швидкість вливання 0,095мл/хв) тіоніл хлорид, (9,33г, 78,4ммоль). Перетворення реакції проаналізували за допомогою РХВТ, як в Прикладі 1. Перетворення склало більше 99,5%. Синтезування продовжили так само, як в Прикладі 4. Отриману фазу, яка включає пірметазол, піддали аналізу для осадження пірметилового спирту (менше ніж 0,1% мол).
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for benzimidazole compound obtaining
Назва патенту російськоюСпособ получения соединения бензимидазола
МПК / Мітки
МПК: C07D 401/12
Мітки: спосіб, сполуки, одержання, бензимідазолу
Код посилання
<a href="https://ua.patents.su/3-79147-sposib-oderzhannya-spoluki-benzimidazolu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання сполуки бензімідазолу</a>
Попередній патент: Спосіб вимірювання діаметра циліндричних виробів оптико-електронною системою
Наступний патент: Спосіб електрогідроімпульсного руйнування міцних монолітних об`єктів під водою
Випадковий патент: Спосіб лікування та профілактики прогресування фіброзу печінки у хворих на неалкогольний стеатогепатит







