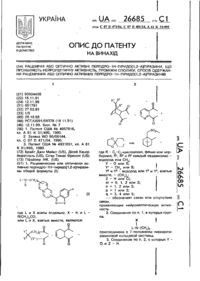
Гетероциклічні сполуки, що проявляють антибактеріальну активність
Номер патенту: 27318
Опубліковано: 15.09.2000
Автори: Андреотті Даніелє, Вісмара Клаудіо, Гавірагі Джованні, ПЕРБОНІ Альчиде, Донаті Даніелє, Карлессо Роберто, Тамбуріні Бруно, Россі Тіно
Текст
1 Гетероциклические соединения общей формулы (I) соли, включая внутренние соли, когда это возможно, и метаболически лабильные сложные эфиры, проявляющие антибактериальную активность. 2. Соединения по п.1, в которых R3 представляет амино, аминометил, метиламино, гидрокси, !идроксиметил, метил, метокси, этокси, иэолропокси, циклопентокси, аминоэтокси, метилтио, фенилтио или метил суп ьфин ильную группы, или вместе с атомом углерода, к которому он присоединен, образует кето или диметилкетальную группу, 3. Соединение по п 1 общей формулы (le): он СООН .(I) где Ri и R? обозначают атом водорода, Ra обозначает атом водорода, гидроксипьную группу, гидроксимегильную группу, Сі-Сз -алкильную группу или фуппу XRd, в которой X обозначает атом кислорода или группу S(O)n, в которой л равно 0 или целому числу 1, и ^ представляет СгС 3 -алкил, циклоленгил или фенил, или, когда X обозначает атом кислорода, тогда R4 может также представлять группу AlkNRsRe, где А!к представляет С?~ алкиленовую цепь, a Rs и R6 каждый независимо обозначает атом водорода, или R5 представляет иминометил, a Re обозначает атом водорода, или R3 обозначает группу -3-/(R}-l- (трет- бутиддиметилсилилокси) эттлп/- 4-((S)- 6'-(2'- метокси-Т- оксоциклогекс- 2'-«нил)у аэетидин-2-он (1п). 2-Метокси-2-циклогексенон (11,9 г) добавляют по каплям к перемешанной смеси безводного тетрагидрофурана (200 мл) и 1М раствора бис(триметилсилил) амида лития в гексане (200 мл), охлажденного до температуры -78° под азо 27318 том. Температуру поддерживают на уровне -78° в течение 30 мин, добавляют промежуточное соединение А (15 г) и реакционную смесь сохраняют при температуре -73°С в течение 15 мин. Реакционную смесь выливают в холодный насыщенный раствор аммонийхлорида (100 мл) и затем экстрагируют простым эфиром. Органический слой промывают холодным 1%-ным раствором хлористоводородной кислоты (50 мл) и холодным насыщенным раствором бикарбоната натрия, сушат и затем упаривают при пониженном давлении. Остаток растворяют в минимальном количестве этилацетата и петролейного эфира (200 мл) с получением указанного в заголовке соединения (1h, 7,9 г) в виде белого твердого вещества, т.п. 170° (т ex. Rf 0,25 ЦГ/ЭА 4/6). Маточные растворы упаривают при пониженном давлении и подвергают (мгновенной) хроматографии с получением указанного в заголовке соединения (1д, 2,9 г) (тех. Rf 0,20 ЦПЭА 4/6). (3S.4R)- 3- /(R)-1- (трет- бутилдиметилсилилоксм) 3Tvm-/-4-((R)-6'- (2'- этшси-Т-охсоциклогекс2'-енил))/азетидин-2-он (1i) и (3S, 4R)-3-/(R)-1(трет- бутилдиметмлсилилокси) этил/- 4((S)- 6'- (21этохеи -1 -оксоциклогехс-2~еиил)/азетидин-2-он 0) Раствор 2-этокси-2-циклогексенона (24 г) в безводном тетратдрофуране добавляют к смеси безводного тетрагидрофурана (160 мл) и 1М раствора бис(триметилсипип)амида лития в гексане (200 мл), охлаждают до температуры -78°С под азотом, и полученную смесь сохраняют при данной температуре в течение одного часа Затем добавляют в течение 10 минут раствор промежуточного соединения А (26,3 г) в тетрагидрофуране (80 мл). Добавляют холодный насыщенный рэстаор аммонийхлорида (320 мл) с последующим добавлением 10%-ного раствора хлористоводородной кислоты (70 мл) Полученную смесь экстрагируют простым эфиром (3x150 мп), промывают холодным 10%-иым раствором хлористоводородной кислоты (50 мл), солевым раствором и затем сушат. Удаление растворителя при пониженном давпении приводит к получению маслянистого остатка, который очищают флэш-хроматографией (элюенты ЦГ/ЭА) с получением V і смеси указанных в заголовке соединений (20 г) и чистого указанного в заголовке соединения (1j, 1,3 г) (т.с.х. Rf 0,36 ЦГ/ЭА 1/1). Смесь растворяют в минимальном количестве этилацетата, разбавляют циклогексаном и охлаждают с получением указанного в заголовке соединения (1І. 4,0 г) в виде белого твердого вещества (T.c.x.Rf 0,38, ЦГ/ЭА 1М) Промежуточное соединение 1К. (3S, 4RJ-3/^)-1-(трет^уті*лдиме™лсилилокси)зтил/- 4-({R)- 2'(1'-оксоциклогексип)/азетмднн-2-он и (3S, 4R)-3-/(R)1-(трет- бутипдиметилсилилокси)зтип/-4- ((S)- 2'- (VоксацишагєксилУазетидин-2- 3-/(R)- 1- (третбутилдиметилсилилокси) 3TWi/-4-/(S)- 1-(4- метилфонилсульфоно) гидразоно/- циклогекс-2'- ил/-азетидиі+2-он(12Ь), К раствору промежуточного соединения 1К (12,1 г) в ледяной уксусной кислоте (120 мл) при комнатной температуре добавляют тозилгидрзэид (6,9 г). Реакционную смесь перемешивают в течение 3 ч, затем разбавляют дихлорметэном (250 мл) и промывают солевым раствором (2x250 мл), затем 5%-ным раствором бикарбоната натрия до получения рН 7 и вновь солевым раствором (2л150 мл) Органический слой сушат и растворитель упаривают при пониженном давлении. Полученную пену перемешивают с простым диэтиловым эфиром (60 мл) в течение 2 ч при комнатной температуре с получением указанного в заголовке соединения 12Ь в виде белого порошка после фильтрации и сушки под вакуумом (6 г, температура плавления 187- 189°С, т е х диэтиловый эфир, RF= 0,13, ИК (CDCb) v m « (см*) 3416 (N-H), 3304 (NNHSO;) 1753 (лактам), 1599 (С* N, С= С). Органический слой, содержащий указанное в заголовке соединение 12а, в присутствии незначительного количества указанного в заголовке соединения 12b (т.с х) концентрируют, и остаток очищают флэш-хроматографией (элюент диэтиловый эфирАпетролойный эфир, 7; 3) с получением указанного в заголовке соединения 12а в виде белого порошка (7,6 г т.п 95-96°С, т.с.х. дизтилорый эфир, Rf= 0.37) ИК (CDCU) vmn (см и ) 3410 (NН) 3306 (NNHSOj), 1755 (лактам), 1599 (C-N, C= С). Промежуточное соединение 11. (3S,4R)-3»(R)-1-(TpeT- буіитиметилсилилокси)зтиПі'4 б'-триметилоіпилоксм-і-оюзциклогеюлл)/ 2-он. Промежуточное соединение 10 (4,4 г) растворяют о сухом дихлорметане (100 мл) при комнатной температуре. Добавляют триметилсилилхлорид (7,5 мл) и триэтмламин (11 мл) и смесь перемешивают в течение одного часа, затем выливают в поду {200 мл). Органический слой отделяют и промывают водой (2x200 мп), сушат и упаривают с получением желтого масла, содержащего следы триэтиламина. Масло растворяют в ме 27318 щают фпэш-хроматофэфирй (элю^нты д и з шло таноле (100 мл), добавляют силикагель (Ю г}, и суспензию перемешивают в течение одного часа, затем фильтруют. Силикагепь промывают этилацетагом (2x100 мл), и объединенные органические слои упаривают при пониженном давлении при температуре 2Й°С. Полученное масло растворяют этмлацетатом (150 мл), промывают солевым раствором, сушат и упарнэают с получениям желтой пены, которую хроматографируют на сипикагепе с использованием смеси петролейного и диэтилового эфиррв (1/1) а качестве злюента (Rf= 0,25), получая указанное R заголовке соединение (3,5 г) в виде белой пены. ИК (CDCb) v™, (см') 3418 (NH) 1755, (С=0) 1717 ( 0 0 ) . Промежуточное соединение 12. (3S, 4R)-3(R)-1 -(трет-бугилдиметипсилипокси)отил/- 4-//(R)1 -(4-мєтилфекилсульфоно) гидразоноУ-цкклогекс2'-ип)-азепідин-2-он (12а) и (3S, 4R)- 3-/6'((5)-2'-'азидо-1'-оксоциклогекс-6'-ил}-/азетидин-2-он. К смеси лиридинийхлорхромзта (6,67 г) в сухом дихлорметане (50 мл) под азотом добавляют раствор промежуточного соединения 15 в дихлорметане (200 мл). Смесь перемешивают в течение ночи при комнатной температуре, фильтруют через флоризид, и полученный раствор упаривают при пониженном давлении. Маслянистый остаток хроматографируют на силикагеле с использованием смеси циклогексан/зтилацетат (1/1) в качестве эпюента с получением указанного в заголовке соединения (4 г, температура плавления 134135°С (разложение)) т е х . диэтиловый эфир, Rfc 0,66 (ИК (CDCb) у т а я 3416, 2104, 1759, 1720 см' 1 . Промежуточное соединение 17. (3S, 4R)-3/(R)-1 -(трет 5утилдиметилсилилок;си) этилМ-(Р) 6'-((5)-2'-аллидоксикарбониламино-1'- оксоциклогекс-6'-ил)Аазетидин-2-он, Промежуточное соединение 16 (4 г) растворяют в этилацетате (300 мл), добавляют 10%-ный палладий на угле (3 г) и смесь гидрируют при давлении 3 атмосферы в течение 2 ч. Добавляют дополнительное количество катализатора (1 г) и 13 27318 гидрирование продолжают в течение 2 ч. Смесь фильтруют через подушку целита, и полученный раствор обрабатывают аллилхлорформиатом (1,7 г) и пиридином (1,12 г). Реакционную смесь поддерживают при перемешивании в течение 30 минут при комнатной температуре, затем вливают в насыщенный водный раствор аммонийхпорида {350 мл). Органический слой промывают 1%-ным раствором хлористоводородной кислоты (2x150 мл), затем 5%-ным раствором бикарбоната натрия (2x150 мл) и солевым раствором (200 мл) сушат и упаривают в вакууме. Остаток очищают флэшхроматографией на колонке кремнезема с использованием смеси циклогексан/этилацетат (1/1), получая указанное в заголовке соединение в виде масла (2 г, т е х . циклогексан/этилзцетат, 3/7 Rf* 0.4) ИК; v m « (СОСІз) 3414, 1765, 1709 см V Промежуточное соединение 18. (3S, 4R)-3/(Р)-1'-(трет-бутилдиметилсилилокси)этил/-4-/(1"8, 2"R. 6"Й)-Г- гидрокси- 2"- цианоцикпогекс- 6"ил/азетидин-2-он. Промежуточное соединение 14 (2,4 г) растворяют в смеси диметипформамида (80 мп) и воды (40 мл), затем добавляют цианид калия (1 г) и смесь нагревают при температуре 60°С в течение 8 часов, разбавляют простым эфиром (150 мл) и дважды промывают водой (150 мл). Органический слой сушат и упаривают при пониженном давлении с получением сырого масла, которое очищают флэш-хроматографией на силикагеле (элюент простой эфир) этилацетат 8/2, Rf= 0,4) с получением указанного в заголовке соединения (1,7 г) в виде твердого вещества белого цвета, ИК (см'1): 3611 (ОН) 3415 (NH> 1755 (СО). Промежуточное соединение 19. (3S, 4R)-3/(Я)-1"-(трет-бутилдиметилсилилокси) 3Tnn-4-/(1"R, 2"R, 6nR)-1"- гидоокси-2"- (аллилоксикарбониламинометил)циклогекс-6"-ил)азетидин-2-он. Промежуточное соединение 18 (1,7 г) растворяют в уксусной кислоте (15 мл) добавляют диоксид платины (40 мг) смесь гидрируют (1 атм) в течение 3,5 ч, затем фильтруют через целит и растворитель упаривают при пониженном давлении. Остаток повторно растворяют в сухом дихлорметане {80 мл) при температуре 0°С, добавляют 1^-этил-пиперидин-(1,8 мл) и аллилхлорформиат (0,55 мл) и полученную смесь перемешивают •в течение 16 ч. Растворитель упаривают при пониженном давлении с получением сырого вещества, которое повторно растворяют этипацетатом (100 мл) и дважды промывают солевым раствором (50 мл). Органический слой сушат и упаривают при пониженном давлении с получением масла, которое очищают флэш-хроматографией на силикагеле (злюенты циклогексэн/згилацетат 60/40, Rf= 0,5) с получением указанного в заголовке соединения (0,7 г) в виде твердого вещества белого цвета. ИК (см'1) 3454 (NH) 3416 (NH) 1751 (СО) 1720 (СО). Промежуточное соединение 20. (3S, 4R)-3/(К)-Г-(трет-бутипдиметипсипипо«си)этил/-4-/(2нR, 6"R)- 1"-оксо -2"- аплипоксикарбонипамииометил) -цикпогекс-6" -и л/азе1 ІДИН-2-ОН. Промежуточное сі ІДИНЄНИЄ 19 (0,7 г) растворяют в метиленхлор (50 мл) и добавляют при энергичном переме шааиии пиридинийхлорхромат (1,1 г). Через 2 ч смесь фильтруют на 14 подушке целита, разбавляют метиленхлоридом (150 мл) и промывают холодным 5%-ным раствором хлористоводородной кислоты (20 мл), после чего промывают водным раствором бикарбоната натрия (20 мл).Органический слой сушат и упаривают при пониженном давлении с получением масла, которое очищают флэш-хроматографией на силикагеле (элюенты циклогексан/эти л ацетат, 30/70, Rf= 0,3) с получением указанного в заголоо-, ке соединения (0,48 г) в виде твердого вещества белого цвета ИК v m a x (см \. 3456 и 3439 (NH) 1759 (СО) 1720 и 1718 (СО) 1603 (С= С). Промежуточное соединение 21. (3S, 4R)-3/(R)-1 -(трет-бутилдиметилсипипокси)этип 1-4- ((R)6'-(2'-изопропокси-1'-оксоциішогекс-2'- енил) азетидин -2-он (21а) и (3S, 4R)-3-/(R)-1-(трет- бутилдиметипсилилокси)этил/-4((3)-6~(2'-изопропокси-1' -оксоциклогекс-2'-еиил))азетидии-2-он (21Ь) К смеси 1М раствора бис(триметилсилил) амида лития а гексане (486 мл) и безводного ТГФ (300 мл) в инертной атмосфере и охлаждении до температуры -78°С добавляют по каплям раствор 2- изопропокси-2-цикл are ксенона (30 г) в безводном ТГФ (100 мл) Температуру поддерживают на уровне -78°С в течение 30 мин, после чего по каплям добавляют раствор (3R, 4R)-4-aueT0*cn-32((R)- трет- бутилдиметилсилилокси) этил-2- азетидинона (46,59 г) а безводном тетрагидрофуране (100 мл). Реакционную смесь хранят при температуре -78°С S течение 10 мин, затем выливают в охлажденный насыщенный раствор аммонийхлорида (30Q мп) и экстрагируют простым диэтиповым эфиром Органический слой после промывки холодным 1%-ным раствором хлористоводородной кислоты (150 мл) и холодным насыщенным раствором бикарбоната натрия сушат и упаривают при пониженном давлении Желтый маслянистый остаток обрабатывают петролейным эфиром После фильтрации получают указанное в заголовке соединение 21а в виде твердого вещества белого цвета (8.4 г) температура плавления 130°С (разложение) т е х циклогексан/ этилзцетат, 4/6, Rf~ 0.21, ИК (нуйол) v m M (см"')- 3233 (NH) 1759 (С= 0, р-лактам) 1680 (С= 0). Маточные растворы упаривают при пониженном давлении и подвергают флэш-храматографии с получением указанного в заголовке соединении 21Ь в виде масла (9,2 г) т е х цикпогексан/этилацетат, 4/6, Rf= 0,21, ИК (нуйол). (см '): 3425 1"- Стрет- бутигщиметилсилилокси> этил/-4'-/(2™5,0"Я)-2'-метокси-1"'-оксоцихлогекс^'"- ил/ этиповый зфир/петролейный эфир, 3/7. в качестве элюента, получая указанное а заголовке соединение в виде бесцветного масла (0,1 г) (1/Ї смесь изомеров в положении 2, т с.х. диэтиповый эфир, Hf~ 0,63 и 0,51) ИК (CDC13) v m « см"\3524 (О-Н) 1747 (С=0, р-лактам), 1715 (С= 0, сложный эфир). Пример 1а. Annvui(4S, 8S, 9R, 10S, 12R)-*метилтио- 10 ( 1 -трет-бутмлдиметил- силипокси) этил- 11- оксо-1- азатрицикло /7,2 0 О3і0/ундец-2-ен-2кзрбоксилзт К охлажденному на льду раствору промежуточного соединения 6а (3,85 г) в 200 мл дихлорметана добавляют карбонат калия (3,0 г). Смесь перемешивают в течение 10 мин, после чего добавляют аллилоксалилхлорид (5,57 г) и пиридин (3*,48 г). Реакционную смесь перемешивают при температуре 25° а течение 1,5 ч, затем разбавляют дихлорметаном, фильтруют, промывают охлажденной на льду водой и сушат. Удаление растворителя приводит к получению сырого промежуточного соединения оксапимидо (5,37 г), которое растворяют в сухом топуопе (150 мл) и обрабатывают триэтилфосфитом (9,97 г) Полученный раствор нагревают с обратным холодильником в течение 6 ч, растворитель удаляют под вакуумом и остаток хроматографируют на силикагеле с использованием смеси ЭЭ/П (3/7) в качестве элюеита. получая указанное в заголовке соединение (1,78 г) в виде желтого масла ИК vma* (CDCb): 1772 и 1717 ал 1 . 1Н ЯМР (300 МГц) -4метиптио-10-(1 -(трет-бутипдиметилси.піллокси- этипЬ 11- оксо-1-азатрицикло /7,2,0.0.эа/ ундец-2-єн-2- карбоксилат. Пример 1g. AnnnnfBR. 9R, 10S, 12RH.4диметока^10-(1Чтрет-бутигщимежпсилилокси) зтил)11-оксо-1-азатриии№о/7,200.зв/ундец-2-ен-2- карбок К раствору (3S, 4R)-3-/(R)-1'-(TpeT- бутилдиметилсилил-окси)этил/-4-/(2"3,6К")-2- метокси-1 "оксоцикпогекс-6р|-ил/азетидин-2-она (0,1 г) в сухом тетрагидрофуране (5 мл) добавляют этил глиоксилат {0,5 г) N, N, N-тризтиламин (0,02 мл) и молекулярные сита ЗА. Полученную смесь перемешивают при 22°С в течение 17 ч, затем разбавляют этилэцетатом (30 мл), промывают солевым раствором (3x70 мл), сушат и концентрируют в вакууме. Неочищенный продукт хроматографируют на силикагеле с использованием смеси простой ди Пример 1h. Аллил (4S, 8R, 9R, 10S, 12R)-4метилтио-10-( 1 -(трет-бутилдиметилсилилокси-)этил)эа 11ч>ксо-1-азатрицикпо/7,2,0.0эа/ /ундец-2-ен-2- карбоксилатПример 11. Аплил(45, 8R, 9R, 10S, 12R)^- ме1- аззтрицикпо/7.2.0.0.38/унЛіЄц- 2-ен-2- карбоксипат. Пример 1j. Annnn(4R, 8Rt 9R, 1QS, 12R)-4метил-10-(1-(трет-бутипдиметилсилилокси)этил)- 11оксо-1-азатрицикло /7.2.Q.O.38/ ундец-2-еи-2- карбоксилат. 18 27318 Пример 11. Annnn(4R, 8S, 9R, 10S, 12R)-4оксо-1-азатрицикпо/7,2 0.0.а8/ундєц-2-ен-2пзт. карбокси Пример 1m. Аллип (8S, 9R, 10S, 12RHметокси- ІО-ЇІЧ'трет^упщпимешпсипилокси-іятилУ-іісш>1-азатрицикло/7,2.0 03%ндец-2,4-диен-2- карбоксилат. Пример 1п. Annnnf8R, 9R, 103, 12R)-4метокси-10-( 1 -(трет-бутилдиметилсилилокал)зтмп)11-оксо- і-азатрицикло/У.г.О.О.3 в/ ундец-2,4-диен-2карбоксипат. Физические характеристики вышеприведенных соединений вместе с модификациями а условиях реакции приведены в табл. 2 {пример 1). Пример 2. Аллип (4S, 8S, 9R, 10S, 12R)-4метокси- 10-(1 -трет-бутилдиметипсилипоксиэтил)11- оксо-1- азатрицикло/7,2Д0.3%ндец-2-еч-2- карбоксилат. Промежуточное соединение 2а (0,5 г) растворяют о метиленхлориде (20 мл) добавляют безводный карбонат калия (150 мг) и смесь перемешивают при температуре 23°С под азотом. Добавляют аллилоксалилхлорид (0,2 мл) и триэтиламин (0,2 мл). Реакционную смесь перемешивают в течение 40 мин и затем фильтруюг. Фильтрат промывают водой (50 мл), 5%-иым раствором кислого углекислого натрии (50 мл), солевым раствором и сушат. Раствор концентрируют при пониженном давлении и маслянистый остаток растворяют в сухом ксигшле (30 мл). Добавляют триэтипфосфит (2 мл) и смесь нагревают при перемешивании в течение 3 ч при температуре 140 С. Реакционную смесь охлаждают, концентрируют при пониженном давлении и остаток хроматографируют, концентрируют при пониженном давлении и остаток хроматографируют (элюенты ЦГ7ЭА, 8. 2) с получением указанного в заголовке соединения (80 мг) в виде бесцветного масла. ИК (CDCIs) v m a , (см"1) 1772 (р- пактам). 1717 ( О О) 1634 ( О С) 1 Н ЯМР б (СОСІа). 6,0 (м) 5,45 (м) 4,98 (м) 4,74 (м), 4.22 (м) 4,15 (да) 3,28 (с) 3.22 (м) 3,21 (и) 2,07 (м) 1,84 (м) 1,66 (м) 1,6 1.2 (м) 1,25{д)0,9(с>0.0В(с)мд Пример 3. Annwi(8R, 9R, 10S, 12RH~o«co-10(1- (трет- бутигшиметилсилипокси)- этил)-11- оксо-1~аэатрицикло/7 2 0 0 3 %ндец 2-ен- 2- карбоксилах. Водный раствор 10%-ной щавелевой кислоты добавляют при непрерывном магнитном перемешивании к суспензии силикагеля (10 г, сипикагель 50 для W колоночной хроматографии, 70-230 меш) в метиленхлориде (20 мл) Через 2-3 минуты до-' Бааляют соединение примерз 1g (4,31 г) и смесь перемешивают при комнатной температуре в течение 2 ч Твердую базу фильтруют и твердое вещество промывают метиленхлоридом (200 мл). Объединенные метиленхлоридные слои промывают 1%-иым водным раствором карбоната натрия, сушат и упаривают с получением указанного а заголовке соединения (3,15 г) в виде желтого масла. ИК. v m » (CDCh) 1786,1736 и 1696 (см"1). Пример 4. Annnn(4S, 8R, 9R, 10S. 12RHгидрокси-10- (І- трет^утилдиметлллсилипоксизтил)-11 оксс-t- азатрицикяо 4гидроксм- 10-/1 -(трет- бутилдиметил-силипокси) этил/-11 -оксо-1 -азатрицикло/7 2.0.0. /унреи-2-ем-2карбоксилаг Соединение примера 11 (1,4 г) растворяют в тетрагидрофуране (20 мл) и смесь перемешивают при температуре 0°С Добавляют уксусную кислоту (0,5 мл) и 1М раствор тетрабутиламмонийфторида в тетрагидрофуране (2,8 мл) Реакционную смесь перемешивают гри температуре 0°С в течение 45 мин, пос-ло чего добавляют уксусную кислоту (0.5 мп) и тетрабутиламмонийфторид в тетрагидрофураие (t мл). Реакционную смесь перемешивают в течение 45 мин, затем оыливают в перемешанный, охлажденный на льду раствор диэтилового эфира (150 мл) и 2,5% водного бикарбоната натрия (100 мл) Органический спой промывают водой (2x200 мл), солевым раствором и сушат и упаривают с получением указанного о заголовке соединения (1,1 г) в виде светлого масла ИК 21 27318 тилсилилокси) этил/- 11 - оксо- 1 - азатрицикло /7 2.0.0.38/ундрц-2 ен-2- карбоксилат. К охлажденному на льдом раствору промежуточного соединения 17 (2 г) в безводном дихлормегане (100 мл) добавляют твердый карбонат калия {0,080 г). Смесь перемешивают в течение 30 мин, после чего добавляют адпилоксалилхлорид (0,8В і) и триэтипамин (0,59 г). Реакционную смесь перемешивают при комнатной температуре в течение 1 ч, затем добавляют аппилоксалідпхпорид (0,88 г) и триэтиламин (0,59 г) Через 15 мин реакционную смесь разбавляют дихлорметаном, фильтруют, промывают 5%-ным раствором хлористоводородной кислоты, 5%-ным раствором бикарбоната натрия и солевым раствором Удаление растворителя приводит к получению неочищенного промежуточного оксалимидсоединения, которое растворяют в сухом ксилоле (130 мл) и обрабатывают триэти л фосфитом (7,4 мл). Полученный раствор нагревают с обратным холодильником в течение 2,5 ч, растворитель удаляют под вакуумом, и остаток хроматографируют на силикагеле с не-' пользованием в качестве элюента смеси днэтипового эфира и петролейного эфира (9/1), получая указанное в заголовке соединение в виде желтого масла (1,7 г). ИК (CDCt3) v mBкденному на льду раствору соединения примера 16 (0,98 г) в сухом тетрагидрофуране (60 мл) добавляют уксусную кислоту (0,93 г) и твердый тригидрат тетрабутиламмонийфторида (1,83 г). Смесь перемешивают при комнатной температуре в течение 30 ч, затем выливают в воду и экстрагируют этилацетзтом (3x180 мл). Органический слой промывают 5%-ным раствором бикарбоната натрия и солевым раствором, сушат и упаривают под вакуумом. Остаток хроматографируют на силикагеле с использованием смеси метиленхлорида и метанола в качестве элюентз, получая указанное в заголовке соединение в виде белой лены (0,4 г). ИК; V i w (CDCla) 3447, 1772. 1718 см"1. Пример 18. (4S, 8S, 9R, 12R, 10S) -4-амино10- (1- гидроксиэтил)- 11- оксо- 1- азатрицикло /7.2.0.0.3 8/ундец-2-ен-2-карбоновая кислота. Раствор соединения примера 17 (0,4 г) и уксусной кислоты (0,24 г) в сухом тетрагидрофуране (10 мл) перемешивают под азотом в течение 15 мин. Затем добавляют растворенный в сухом тетрагидрофуране (15 мл) тетракис (трифенилфосфин) палладий (0,650 г) и смесь перемешивают в течение одного часа. Полученное твердое вещество отфильтровывают, промывают простым диэтиповым эфиром и сушат, получая указанное в заголовке соединение в виде палево-желтого твердого вещества (0.230 г). ИК vTO8* (нуйол). 3364Я669, 1767, 1872 см' 1 . 1Н-ЯМР (300 МГц О3О- ацетон) 5,0 (м) 4,12-4,0 (м) 3,32 (м) 3,09 (м) 2,0-1,5 (м) 1,25 (м) 1,12 (д). Пример 19. Аплил(45, 8S, 9R. 10S, 12RJ-4(аллилоксикзрбониламинометил)-10-/1- (трет- бутилдиметилсилипокси) этилМ 1-ОКСО-1- азатрицикло/7.2.0.0.3 в/ундец-2-ен- 2-карбоксилат. 22 Промежуточное соединение 20 (0,48 г) растворяют а сухом метиленхлориде (20 мп) при комнатной температуре, затем добавляют карбонат калия (1.0 г) с последующим добавлением аллилоксалилхлорида (0,19 мл) и триэтиламина (0,18 мл). Через 5 ч смесь фильтруют, разбавляют мети-пенхлоридом (80 мп), промывают 5%-ным раствором бикарбоната натрия и солевым раствором (30 мл). Органический слой сушат и упаривают при пониженном давлении К остатку, растворенному а сухом ксилоле (100 мп), добавляют триэтилфоофит (0,8 мл) и гидрохинон (0,05 г) и смесь нагревают с обратным холодильником в течение 3,5 ч Растворитель упаривают при пониженном давлении с получением масла, которое очищают флэш- хроматографией на силикагеле (элюенты простой эфир и цклогексан, 80/20, Rf= 0,7) с получением указанного в заголовке соединения (0,30 г) в виде желтого масла ИК (см') 3450 (NH) 1769 (СО), 1744 (СО) 1715 (СО). Пример 20. Аллил(45, 8S, 9R, 10S, 12R)-4(ал«ипо«г.икарбониламинометил)-10- (1- гидроксиэтил)-! 1 -оксо-1 -аэзтрицикло/7.2 0.0.3 в/ундец-2- ен2-карбоксилат. Соединение примера 19 (0,30 г) растворяют в сухом тетрагидрофуране, добавляют уксусную кислоту (0,3 мп) и тетрабутипаммонийфторид (2,5 мл 1М раствора в ТГФ) и смесь перемешивают в течение 30 ч. Смесь разбавляют этилацетатом (150 мл) и дважды промывают солевым раствором (100 мл) и 5%-ным водным раствором бикарбоната натрия (80 мл) Органический слой сушат и упаривают при пониженном давлении с получением остатка, который очищают Флэш- хроматографией на силикагеле (элюенты циклогексан и этилацетат, 50/50, Rf= 0,1), получая указанное в заголовке соединение (0,06 г) в виде бесцветного масла ИК (vma* см"1): 3605 (ОН) 3447 (NH), 1771 (СО), 1717 (СО), 1620 (С=С) Пример 21. (4S, 8S, 9R, 10S, 12R)-4(аминометип)-1°-( 1 -гидроксиэтил}-11 -оксо-1 азатрицикпо /7.2.0.03 /ундец-2-ен-2-карбоновая кислота Соединение примера 20 (0,06 г) растворяют в сухом тетрагидрофуране (1 мл), добавляют уксусную кислоту (0,036 мл) и тетракис (трифенилфосфин) палладий (0,09 г) Смесь перемешивают в течение 1 ч и разбавляют смесью простого эфира (8 мл) и петролейного эфира (4 мл). Полученное твердое вещество дважды промывают смесью простого эфира (8 мл)и петролейного эфира (4 мл) Твердое вещество растворяют в воде (5 мл) и хроматографируют на силикагеле С-18 с обращенной фазой (элюент вода), и раствор сушат вымораживанием с получением указанного в заголовке соединения (0,04 г) в виде твердого белого вещества. ИК (Nujol, см'1); 3300-2650 (МИ3*. ОН, NH;) 1751 (СО), 1582 (С= С. СО) ЯМР (D2O, и.д.): 7,62 (м) 4,78 (М) 4,07 (м) 4,00 (1-ггадроксиэтил)-11-оксо-1- азатрицикло /7200 зв/ундец-2-ен-2-карбоксилат Соединение примера 23а (0.12 г) растворяют в безводном дихпорметане (?0 мл\ после чего трифенилфосфин (0,09 г), тетракис (трифенилфосфин) палладия (0,13 г) и 0,5 М раствор калий 2-этипгексаноата (0,568 мл) добавляют в смесь Полученное после фильтрации сырое твердое вещество (22 мг) очищают обращеннофаэовой хроматографией (Р 18 вода а качестве элюента). Фракции, содержащие продукт, объединяют и сушат вымораживанием Указанное э заголовке соединение получают в виде белого твердого тела (10 мг) ИК (нуйол) \ w (см 1 ) 2275 (ОН). 1731 ( О 0 р- лакгам) 1593 (Ыз С- С и С= 0, карбоксилат) 1 Н ЯМР Н20/ацетон) 4,99 (м) 4,0В (м) 4,0 (м) 3,49 (м) 3,26 (м) 3,05 (м) 1,8-1 2(м) 1.11 (д)0,Э8(м)мд Ь) Калий(4R, 8S, 9R. 10S, 12R) 4- изопропокси- 10- (1- гидроксиэтип)- 11- оксо- 1- азатрицикло / 7 2 0 0 8/ундец-2-ен-2-карбоксилат Соединение примера 23Ь (0,03 г) растворяют а безводном дихлорметане (10 мл), затем добавляют трифенилфосфин (0,0022 г), а также палладий тетракис (трифенипфосфин) (0,0033 г) и 0,05 М раствор калий 2-этилгексаноата (0,16 мл) Реакционную смесь перемешивают в течение 2 ч под азотом, затем растворитель упаривают до малого объема, и полученную смесь разбэвлрют простым диэтиловым эфиром (5 мл) Полученное твердое вещество фильтруют, промывают смесью простою ДИЭТИЛОРОГО эфира и петролейного эфира и сушат с получением указанного в заголовке соединения в виде белого твердого тепа (0,022 г) ИК (CDCh), \ w (см 1 ) 1751 (С= О р- лактам) 1595 (С= 0, С= С) 1Н-ЯМР (D2O) 4,02 (м) 4,1-4,0 (м) 3,6 (кв) 3,24 Сад) 2,67 (м) 2,05 (м) 1,79 (м) 1,6 (м) 1,1 (д) 0,9 (с) 1,4 (м)мд Пример 25. Аллил(43, 8S, 9R, 10S, 12RHциклопентилокси-10-/1-трет- бутилдиме гилсипилокси) этил/-11-оксо-1- азатрицикло / 7 2 0 0 з в / ундец-2-ен-2~ карбоксилат К охлажденному на льду раствору промежуточного соединения 25 (12 г) в безводном дихлорметзне (60 мл) добавляют твердый КгСОэ (300 мг) и молекулярные сита 4Д К перемешанному раствору добавляют аллилоксалилхпорид (0,48 мг) и триэтипамим (0 33 мг) и полученную сліесь перемешивают при температуре 20 С под азотом в течение 3 ч Твердое вещество фильтруют и раствор промывают 10%-ным NaHCOs солевым раствором. сушат в присутствии супьфата натрия и упаривают при пониженном давлении Неочищенное промежуточное оксалимидосоединение растворяют в сухом ксиполе (50 мл) и добавляют триэтилфосфит (4 6 мл) Полученный раствор нагревают при перемешивании при температуре 80°С в течение 1ч, за^ем при температуре 140°С а течение 3 ч Реакционную смесь охлаждают и упаоивают при пониженном давлении Остаток хроматографируют на силикагеле с использованием в качестве элюента цикпогексана, получая указанное в заголовке соединение в ваде желтого масла (0,75 г т с х циклогекса^этилацетат 1/1 Rf= 0,6) ИК (CDCt3) vmex (см1) 1711 (С= 0 р-лактам) 1738 (С= 0)1601 (С=С) метане (150 мл) добавляют твердый К?СОэ Смесь перемешивают в течение 30 мин при давлении азота, после чего аллипоксалилхлорид (4.43 мл) и триэтиламин (5 мл) добавляют в несколько приемов в течение 40 ч при 25ПС до полного превращений исходного вещества После фильтрации органический слой промывают солевым раствором, сушат и упаривают при пониженном давлении Маслянистый остаток {1,05 г), соответствующий неочищенному производному оксалимидосоединению, растворяют в сухом ксилоле (40 мл), и добавляют триэтилфосфит (1,445 мл), смесь нагревают при перемешивании при 14СГС в течение 3 ч Реакционную смесь затем охлаждают, упаривают при пониженном давлении и хроматографируют с использованием смеси циклогексан-/этилацетат, 1/1, в виде элюента, получая указанное в заголовке соединение п виде желтого масла (0,33 г т е х циклогексан/эти л ацетат, 1/1 Rf= 0,68) ИК (CDCb) v m « (см f ) 1772 ( О 0, (У- лактам) 1717 (С= 0 сложный аллиповый эфир) (Ь) Аналогичным образом аллил (4R, 8S, 9R, 10S, 12Р)-4 изопропокси-10- /трет- бутипдиметилсилилокси)этил/-11-оксо 1-азатрицикло-/7 2 0 0 э в / ундец-2-ен-2-карбоксилат (0.2 г т с х циклогексан/эти л ацетат, 7/3 Rf0,67) ИК fCDCl3) v m m (см 1) 1765 (С= 0 р- лактам) 1744 (С= 0 сложный аллиловый зфир), 1612 (С= С), получают из промежуточного соединения 23 (1,64 г) за исключением того что хрома тогрэфическим элюентом является смесь 7/3 циклогексан/ этилацетат Пример 23. (а) Аллил(4S. 8S, 9R, 10S, 12R)4- изопропокси- 10-0- гидроксиатил)-11- оксо- 1аэатрицикло / 7 2 0 0 8/ундец-2 ен-2 карбоксилат Соединение примера 22а (0,330 г) растворяют в тетрагидрофуране (30 мл), затем добавляют уксусную кислоту (0,325 мл) с последующим добавлением тригидрата тетрзбутмгаммонийфторида (0,674 г) Смесь перемешивают при 20 С о течение 20 ч, за т ем разбавляют этилацетатом (50 мл) и промывают 2%-ным раствором бикарбоната натрия и солевым раствором (50 мл) После упаривания остаток очищают флэш-хромэтогрэфией с использованием смеси циклогексан/етилацетат, 1/1. в качестве элюента, получая указанное в заголовке соединение в виде масла (0 12 г т е х циклогексан/ этилацетат 1/1, Rf= 0 15), ИК v ^ см 1 3614 (ОН) 1772 ( О 0 [1 лактам) 1717 (С= 0 сложный зфир) 1632 (С= С) 'Н-ЯМР (CDCb) Аллил(4Я, 85 9R, 10S 12Р)-4-изопролокси10- (1- гидроксиэтил)- 11- оксо- 1- азатрицикло /7 2 0 0 3 а/ ундец-2-ен-2 карбоксилат Соединение примера 22Ь (0 2 г) рзстворпют в тетрагидрофуране (50 мл), затем добавляют уксусную кислоту (0,197 мп) и тригидрат тетрабутиламмонийфторид (0,403 г) Смесь перемешивают при 20 С в течение 24 ч, затем добавляют солевой раствор (50 мл) и смесь зксірагируют этипацетагом (3x20 мл) Органический слой экстрагируют раствором бикарбоната натрия (2x25 мл), затем солевым раствором После концентрирования остаток очищают флэш-хроматографией с использованием смеси циклогексан/эти л ацетат, 7/3, в качестве элюента, получая указанное в заголовке соединение а виде масла (0,04 г т с х цикл ore ксан/этилацетат, 1/1 Rf= 0,13 ИК (CDCI3) 23 27318 Пример 26. Аллил(4Э, 8S, 9R, 10S, 12R)-4циклопентйлокси-10-(1-гидроксизтил)-11- ооксо-1азатрицикло/7,2.0.0.э /ундец-2~ен-2-карбоксипат. К перемешанному раствору соединения примера 25 в сухом ТҐФ (40 мл) добавляют уксусную кислоту (0,75 мг и тетрабутиламмонийтригидрат (1,80 г). Смесь перемешивают при температуре 20°С в течение 24 ч, затем выпивают в воду и экстрагируют этилацетатом, органический слой промывают 10%-ным раствором ЫаНСОэ солевым раствором и сушат в присутствии сульфата магния и упаривают при пониженном давлении. Остаток очищают флэшхроматографией с использованием смеси циклогек- " саи/зтипацетат 8/2. в качестве элюента, получая указанное в заголовке соединение (4Ь) в виде масла (0,19 г) тех. циклогесан/этилацетат, 3/7. №= 0,3. ИК (CDCb) vmax (см'1): 3600 (ОН) 1776 ( О 0 0- лактам) 1738(С=0)1603(С=С). Пример 27. Kanm(4S. 8S, 9R, 10S, 12RHциклопентипокси- 10-{1-плдроксиэтил)- П-оксо-1- азабицикло/7.2 0.0.зе/ундец-2-ен- 2-карбоксилат. К перемешанному раствору соединения примера 26 (0,17 г) а сухом этилацетате (9 мл) и сухом метиленхлориде (9,0 мл) добавляют трифеиилфосфин (18 мг), тетракис (трифенилфосфии)-паппадий (0,85 мл) и 0,5 М раствор этилхек-. саноата калия (0,85 мл). Смесь перемешивают под азотом в течение 4 ч при 20°С, после чего добавляют 1/1 раствор простого диэтилового эфира/л етрол ейного эфира (15 мл) и полученное твердое вещество отфильтровывают, промывают 1 /1 диэтиловым эфиром/'Петролейным эфиром (3x15 мл) и сушат с получением указанного в заголовке соединения (0.10 г т.с.х, метиленхлорид/уксусная кислота, 9/1 Rf= 0,2) ИК (нуйол) vmJW (см'1): 1772-1680 ( О 0) 1640 (1585 (С= С) ^-ЯМР (DsO): 4,05 (м) 3,89 (м) 3,62 (дд) 3,22 (дд) 2,83 (м) 1,9-1,0 (м), 1,11 (д). Пример 28. Аплил(45, 6S, 9R, 10S, 12R)-4(трет-бутилдиметилсилилоксиметил)- 10-/1 -{третбутилдиметилсилилокси)этил/-11 -оксо-1 - азатрицикло/7,2.0.0.э'%ндец-2-ен-2-карбоксилат. Промежуточное соединение 27 (5,2 г) растворяют а безводном метиленхлориде (100 мл) и добавляют безводный кзрбонат калия {1,0 г). К перемешанному раствору при комнатной температуре добавляют аллилоксалилхлорид (1,9 мл) и триэтиламин (1,9 мл) и полученную смесь перемешивают в течение 2,5 ч, фильтруют и дважды промывают насыщенным водным раствором бикарбоната натрия (80 мл) Органический слой сушат и полученное после упаривания масло частично очищают от полярных примесей флэш- хроматографией (элюенты циклогексан/этилацетат, 98/2, Rf= 0,7). Элюенты удаляют упариванием и остаток растворяют в сухом ксилоле (150 мл) и добавляют тризтилфосфит (8.3 мл). Раствор нагревают с обратным холодильником в течение 4 ч, и растворитель удаляют при пониженном давлении. Маслянистый остаток хроматографируют на кремнеземе (элюенты цикл огексан/эти л ацетат, 98/2 Rf= 0,7) с получением указанного в заголовке соединения (1,8 г) в виде желтого масла. ИК (vmaJt см"1) 1769,1715 и 1647. Пример 29. Аллил(43, 8S, 9R, ЮЗ, 12R)-4гидроксиметил)-10-( 1 -гидраксизтилИ 1 -оксо- 1азатрицикло /7 2.0.0.зе/ундец-2-ен-2-кэрбоксилат. 24 К перемешанному раствору соединения примера 28 (90 мг), растворенного в безводном ТГФ (15 мп) добавляют уксусную кислоту (0,1 мп) и тетрабути-ламмонийфторид (0,82 мл 1М раствора а ТГФ). Полученную смесь перемешивают в течение 30 ч, затем разбавляют этилацетатом (100 мл) и промывают 2%-ным водным раствором бикарбоната натрия, ледяной водой и солевым раствором Органический слой сушат и упаривают при пониженном давлении с получением масла, которое хроматографируют на силикагеле (элюанты цикл огексан/этил ацетат. 50/50, Rf= 0,2) с получением указанного в заголовке соединения в виде бесцветного масла (25 мг). ИК. (,vm^ см 1) 3605, * 3497,1771, 1713 и 1620. Пример 30. Калий (4S, 8S, 9R. 10S, 12R)-4{гидроксиметил}-10- 1-гидроксиэтил)-11 мжео- 1аэатрицикло /7 2.0 0 зв/ундец-2-ен-2- карбоксилат. Соединение примера 29 (25 мг) растворяют в безводном ТГФ (1,5 мп), тетракис (трифенипфосфин) палладий (10 мг) трифенилфосфин (10 мг) и калий 2-этилгексаноат (0,14 мл) растворяют в 0,5 мл безводного ТГФ и добавляют к раствору, полученную смесь перемешивают в течение одного часа, затем разбавляют сухим эфиром (15 мл) и петрапейным эфиром (10 мп). Твердое вещество дважды промывают сухим эфиром (15 мл) и петролейным эфиром (10 мл). Твердое вещество растворяют в воде (0,2 мл) и хроматографируют и& силикагеле С-18 с обращенной фазой (вода в качестве элюента), раствор сушат вымораживанием с получением указанного в заголовке соединения (10 мг) в виде белого твердого вещества ИК (нуйол). см' 1 , 1751 и 1583, ЯМР (д. м.д 02О) 4,06 (м) 3,57 (м) 3,178 (дд) 3,51 (м) 2,92 (м) 1,50 (м). Пример 31. Anrmn(4S, 8S, 9R, 10S, 12R>-4фенитио- 10-/1Чтрет-оугилдиметилсилилокси)этил/- 11оксо-1- азатрицикло/7 2 0.0.38/-ундец-2-ен-2- карбоксилат. К раствору промежуточного соединения 29а (0,75 г) в безводном метиленхлориде (25 мл) добавляют безводный карбонат калия (0,24 г) и смесь перемешивают при температуре 23°С в течение 15 мин. Смесь охлаждается при температуре 0°С и при помощи шприца добавляют аллилоксалилхлорид (0,385 г) и триэтиламин (0,36 мл). Реакционную смесь перемешивают при 23 С в течение 0,5 ч, твердое вещество отфильтровывают, промывают метиленхлоридом (20 мл). Растворитель упаривают, и к полученной смеси добааляют этиловый эфир (40 мл) и солевой раствор (20 мл) Два слоя экстрагируют и разделяют, органическую фазу экстрагируют солевым раствором (20 мл). 5%-ным бикарбонатом натрия (6x20 мл), водой (20 мп) и холодным 1%-ным раствором хлористоводородной кислоты (3x20 мл) и водой (20 мл). Органический слой после упаривания дает желтое масло (0,85 г), которое растворяют в безводном ксилоле, добавляют тризтилфосфит (2,87 г) и полученный раствор нагревают с обратным холодильником в течение 16 часов. Растворитель упаривают, и маслянистый остаток подвергают флэшхроматографии (ЦГ/ЭА, 8/2) с получением указанного в заголовхе соединения (0,29 г, 32,6%) в виде белого воска (Rf= 0,7, ЦГ/ЭА, 7/3). ИК (см 1 ): 1774 ф- лактам), 1717 (карбоксил), 1651 (двойная 27318 К раствору соединения примера 34 (3,0 г) в сухом тетрагидрофуране (50 мл) добавляют уксусную кислоту (2,6 мл) и раствор тетрэбутиламмонийфторида (тригидрата) (5,5 г) в сухом тетрагидрофуране (30 мл) Смесь перемешивают при температуре 22°С в течение 15ч, затем выливают в воду (200 мл) и экстрагируют этилацетатом (2x80 мл). Органический слой промывают 5%-ным раствором бикарбоната натрия (2x80 мл) и солевым раствором (100 мл), сушат в присутствии безводного сульфата натрия и упаривают под вакуумом. Остаток хроматографируют на силикагеле с использованием смеси метилехпорид/метанол (9/1) в качестве элюента, получая указанное в заголовке соединение в виде бесцветного масла (0,77 г). ИК v m a x (CDCU): 3612. 1776, 1720, 1713 и 1700 см-1. Пример 36. (4S. 8S, 9R, 10S, 12R>4метиламино-ІО-їі-гї'щрокаізтіііії-іі-оксо-і- азатрицикло /7.2.0.0.3'8/ундец-2-ен-2-карбоновая кислота. К раствору соединения примера 35 (1.2 г) в сухом тетрагидрофуране (50 мл) добавляют димедон (1,67 г) под азотом при температуре 22°С. Раствор перемешивают в течение 15 мин, затем по каплям добавляют в течение 10 мин раствор тетракис (трифенилфосфин) палладия (1,7 г) в сухом тетрагидрофуране (70 мл) и смесь перемешивают в течение 1 ч. По каплям в течение 5 мин добавляют простой диэтиловый эфир (200 мл), и полученное твердое вещество отфильтровывают, промывают диэтиловым эфиром (3x15 мл) и сушат. Затем твердое вещество растворяют в воде (19 мл), промывают этилацетатом (5x15 мл) и сушат ка льду с получением указанного в заголовке' соединения в виде палеео-.желтого твердого вещества (0,6 г) ИК vmax (нуйол): 3370-1700, 1767, 1597 см , 1Н-ЯМР (300 МГц. D2O- ацетон): 4,81 (м) 4,15-4,02 (м) 3,36 (дд) 2,47 (с) 3 2,01-1,9 (м), 1,33 (м)1,10{д). Пример 37. Annnn(4S, 8S, 9R, 10S, 12RH-(2аплилоксикарбоиипаминоэтокси>-10-/1-(трет- бутилдиметилашилокси)этил-11-
ДивитисяДодаткова інформація
Назва патенту англійськоюHeterocyclic derivatives having antibacterial activity
Автори англійськоюTamburini Bruno, Perboni Alcide, Rossi Tino, Donati Daniele, Andreotti Daniele, Gaviraghi Giovanni, Carlesso Roberto, Bismara Claudio
Назва патенту російськоюГетероциклические производны, проявляющие антибактериальную активность
Автори російськоюТамбурини Бруно, Пербони Альчиде, Росси Тино, Донати Даниеле, Андреотти Даниэле, Гавираги Джованни, Карлессо Роберто, Висмара Клаудио
МПК / Мітки
МПК: C07F 7/18, C07C 45/71, C07D 477/00, C07D 205/00, C07C 49/753, A61P 31/04, A61K 31/40, A61K 31/395, A61K 31/397, A61K 31/407
Мітки: сполуки, антибактеріальну, активність, гетероциклічні, проявляють
Код посилання
<a href="https://ua.patents.su/30-27318-geterociklichni-spoluki-shho-proyavlyayut-antibakterialnu-aktivnist.html" target="_blank" rel="follow" title="База патентів України">Гетероциклічні сполуки, що проявляють антибактеріальну активність</a>
Попередній патент: Спосіб аміачного окиснення алканів
Випадковий патент: Спосіб одержання комплексного реагенту для обробки бурових розчинів