Похідні рифаміцину
Номер патенту: 105775
Опубліковано: 25.06.2014
Автори: Ріджгі Паоло, Канната Вінченцо, Росіні Джоффредо, Віскомі Джузеппе Клаудіо, Кампана Мануела, Фолеґатті Маена
Формула / Реферат
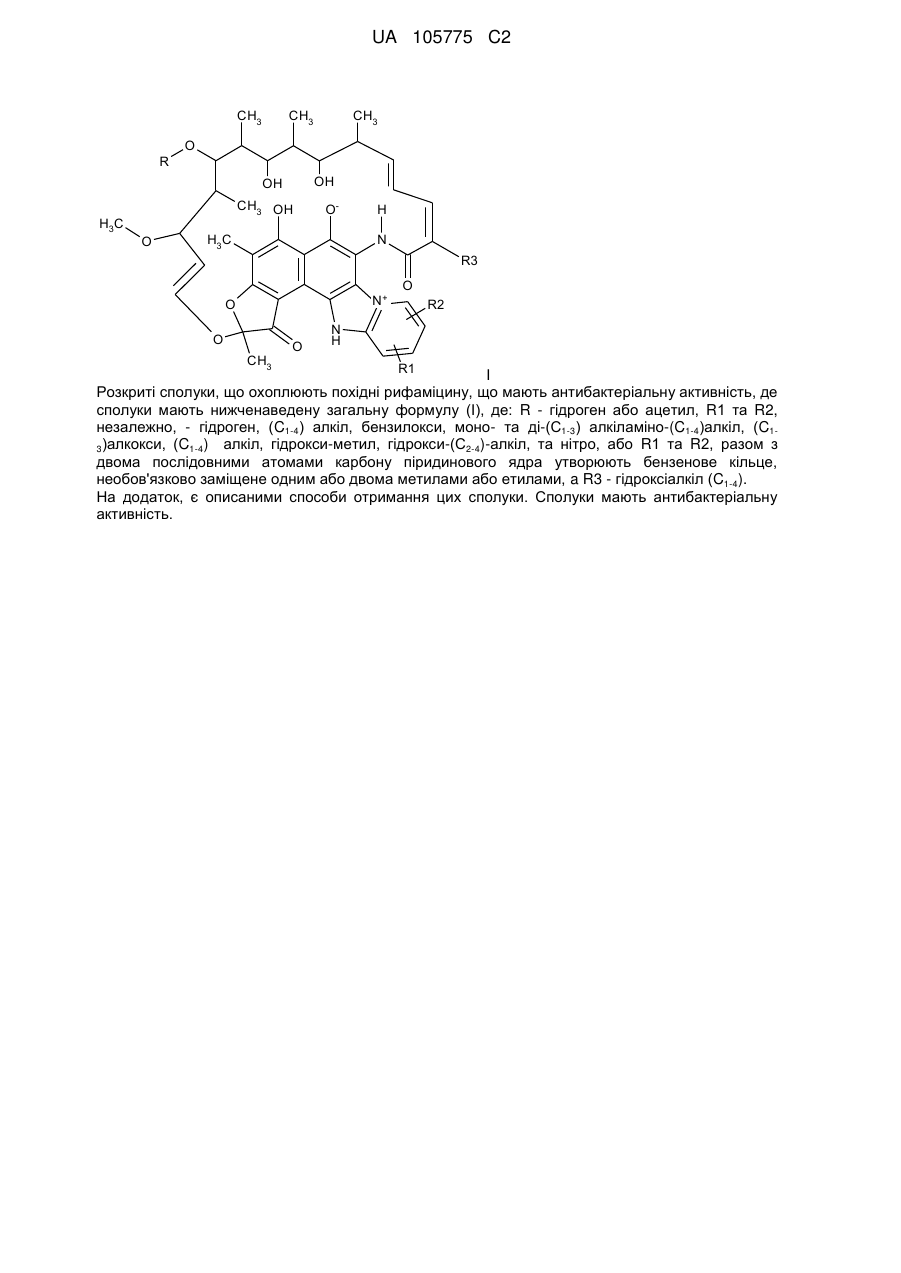
1. Сполука формули І
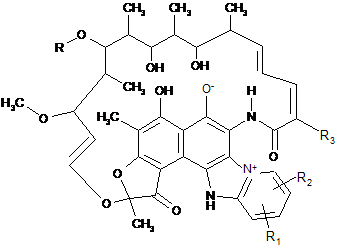 , І
, І
де:
R являє собою гідроген або ацетил,
R1 та R2, кожний незалежно, вибрані з групи: гідроген, (С1-4)алкіл, бензилокси, моно- або ді-(С1-3)алкіламіно(С1-4)алкіл, (С1-3)алкоксі-(С1-4)алкіл, гідроксиметил, гідроксі-(С2-4)алкіл та нітро; або R1 та R2, разом з двома послідовними атомами карбону піридинового кільця утворюють бензольне кільце, незаміщене або моно- чи дизаміщене одним або двома метилами або етилами; a R3 являє собою гідроксіалкіл(С1-4).
2. Сполука за п. 1, в якій R являє собою ацетил, R1 та R2, незалежно, являють собою гідроген або метил, а R3 є гідроксіалкіл(С1-4).
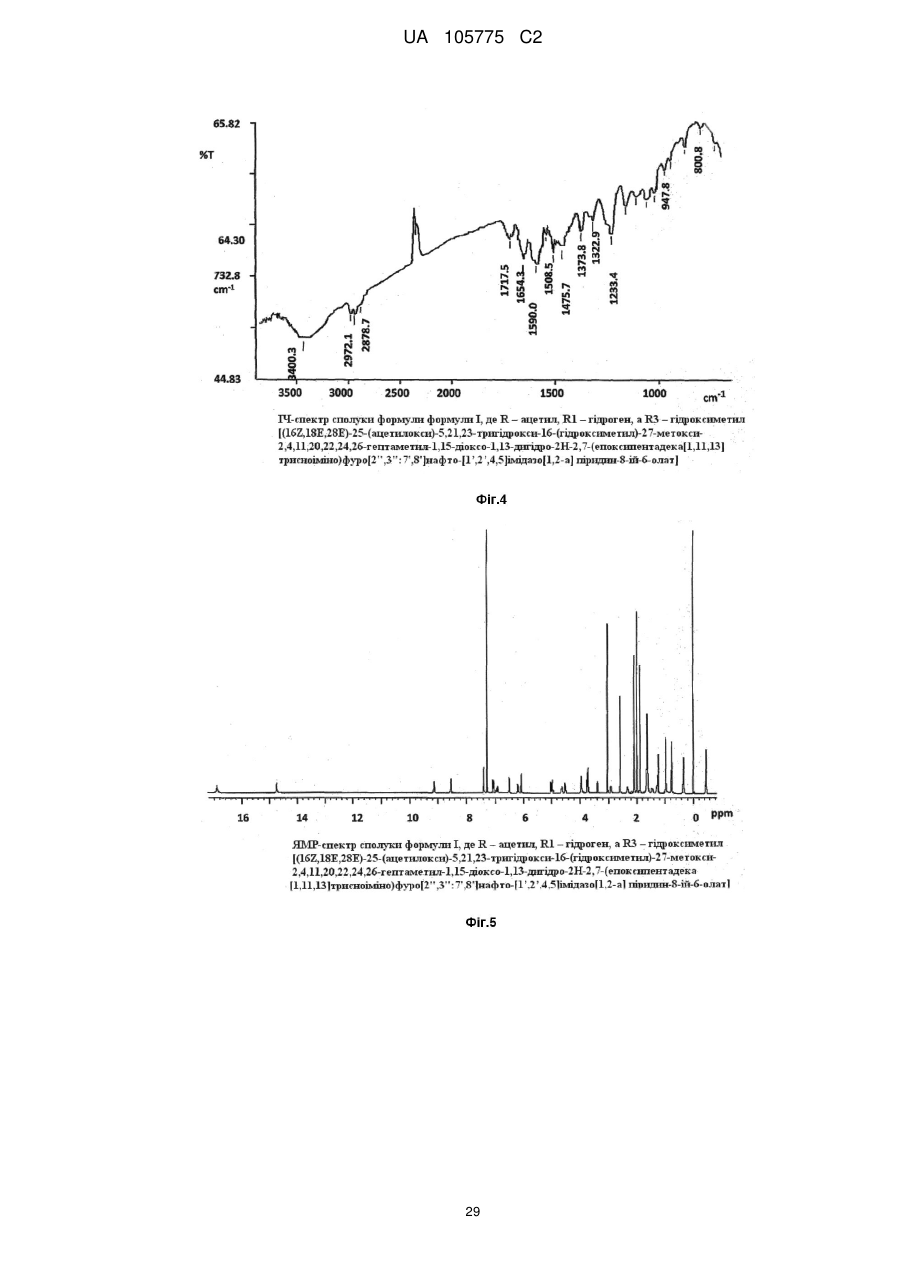
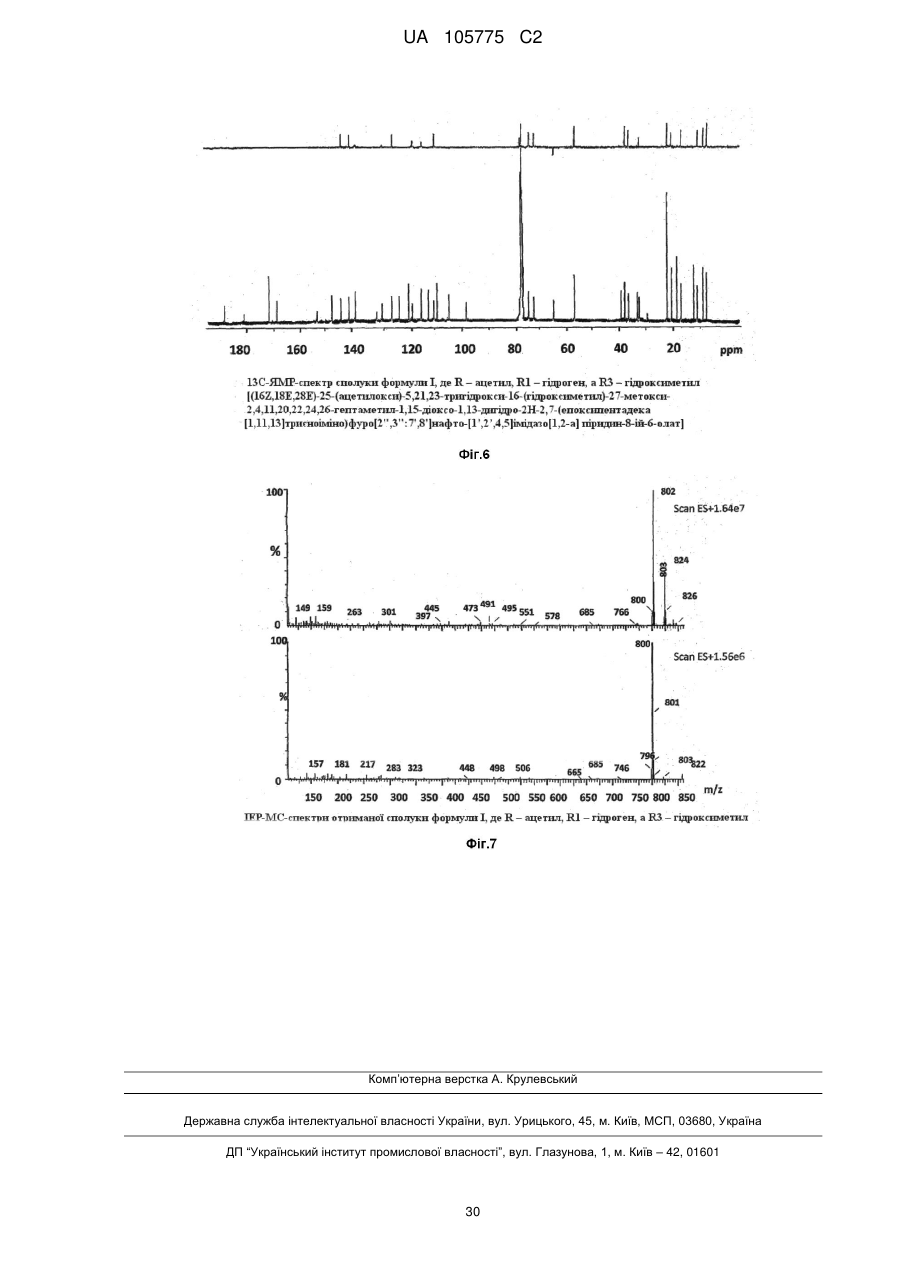
3. Сполука за п. 2, в якій R являє собою ацетил, R1 - гідроген, R2 - п-метил, a R3 - гідроксиметил, що має назву (16Z,18Е,28Е)-25-(ацетилокси)-5,21,23-тригідрокси-16-(гідроксиметил)-27-метокси-2,4,11,20,22,24,26-гептаметил-1,15-діоксо-1,13-дигідро-2Н-2,7-(епоксипентадека[1,11,13]триєноіміно)фуро[2",3":7',8']нафто[1',2':4,5]імідазо[1,2-а]піридин-8-ій-6-олат.
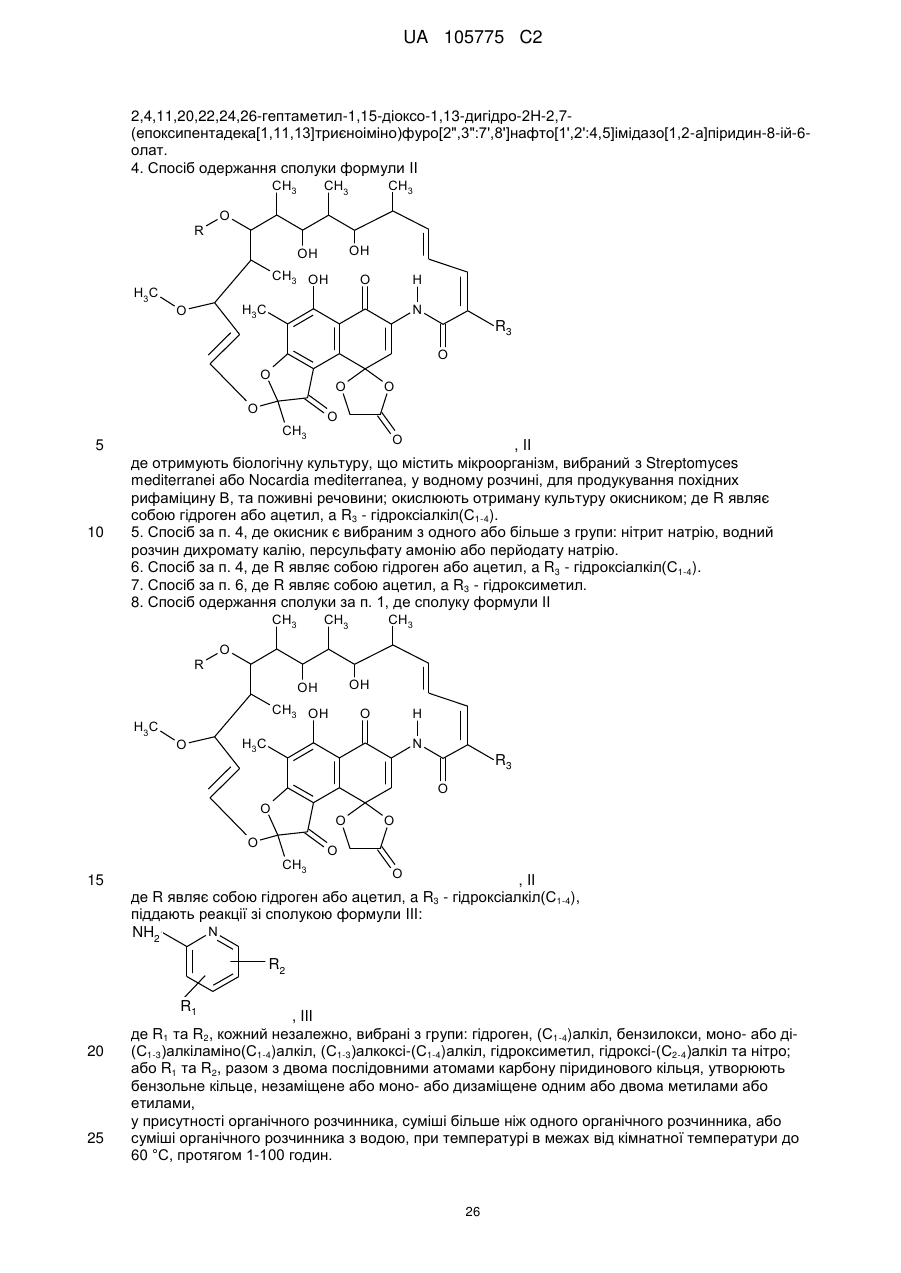
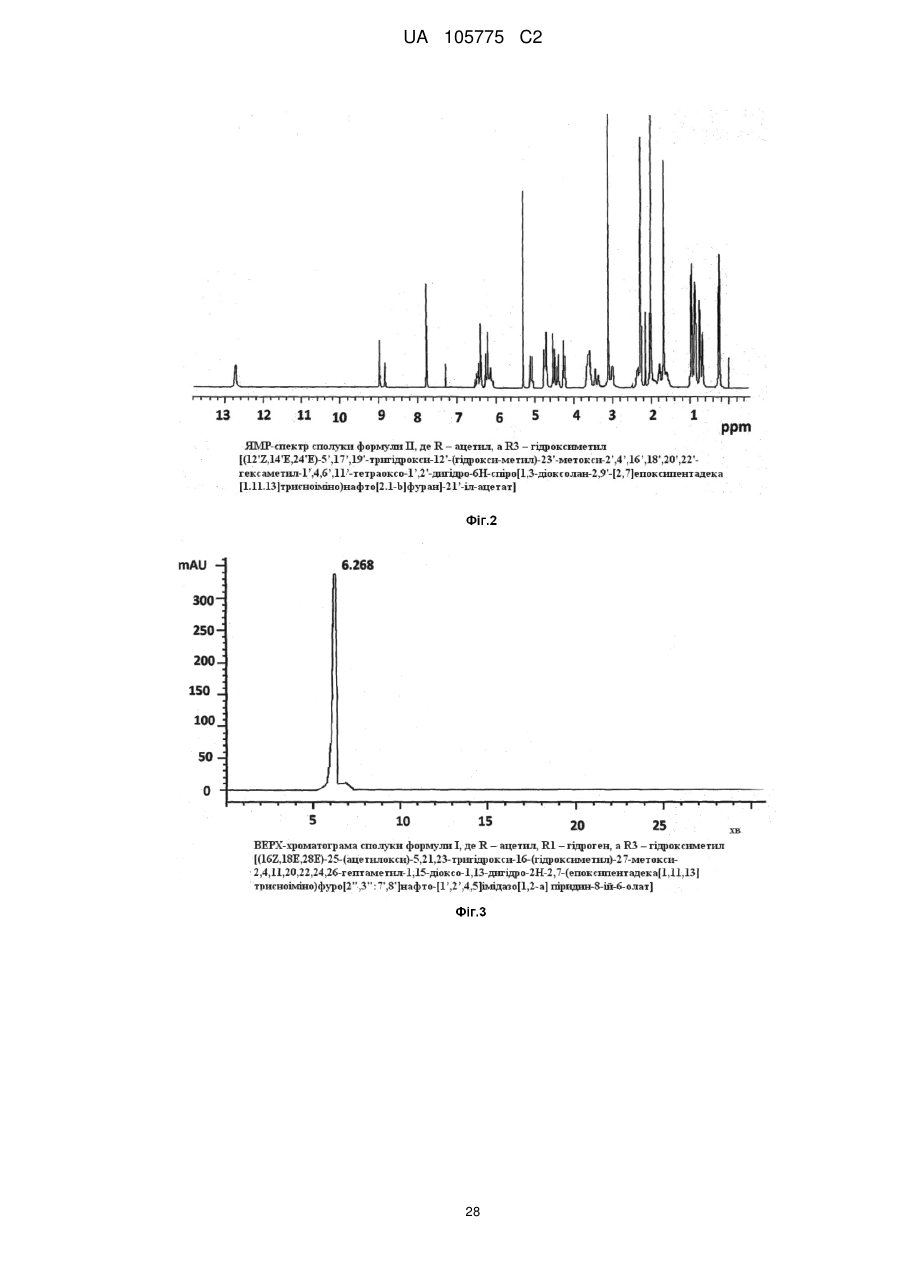
4. Спосіб одержання сполуки формули II
 , II
, II
де отримують біологічну культуру, що містить мікроорганізм, вибраний з Streptomyces mediterranei або Nocardia mediterranea, у водному розчині, для продукування похідних рифаміцину В, та поживні речовини; окислюють отриману культуру окисником; де R являє собою гідроген або ацетил, a R3 - гідроксіалкіл(С1-4).
5. Спосіб за п. 4, де окисник є вибраним з одного або більше з групи: нітрит натрію, водний розчин дихромату калію, персульфату амонію або перйодату натрію.
6. Спосіб за п. 4, де R являє собою гідроген або ацетил, a R3 - гідроксіалкіл(С1-4).
7. Спосіб за п. 6, де R являє собою ацетил, a R3 - гідроксиметил.
8. Спосіб одержання сполуки за п. 1, де сполуку формули ІІ  , II
, II
де R являє собою гідроген або ацетил, a R3 - гідроксіалкіл(С1-4),
піддають реакції зі сполукою формули III:
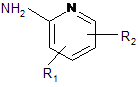 , III
, III
де R1 та R2, кожний незалежно, вибрані з групи: гідроген, (С1-4)алкіл, бензилокси, моно- або ді-(С1-3)алкіламіно(С1-4)алкіл, (С1-3)алкоксі-(С1-4)алкіл, гідроксиметил, гідроксі-(С2-4)алкіл та нітро; або R1 та R2, разом з двома послідовними атомами карбону піридинового кільця, утворюють бензольне кільце, незаміщене або моно- або дизаміщене одним або двома метилами або етилами,
у присутності органічного розчинника, суміші більше ніж одного органічного розчинника, або суміші органічного розчинника з водою, при температурі в межах від кімнатної температури до 60 °C, протягом 1-100 годин.
9. Спосіб за п. 8, де органічний розчинник є вибраним із групи: ароматичні вуглеводні, аліфатичний алканол, галогеновані вуглеводні, нижчий алкіл-естер нижчої аліфатичної кислоти, гліколі, ацетонітрил, діоксан, тетрагідрофуран та їх комбінація або суміш з водою у різних об'ємних співвідношеннях.
10. Спосіб за п. 8, де для кожного молярного еквівалента сполуки формули II застосовують приблизно 0,1-1 молярний еквівалент йоду або комбінації йод/окисник.
11. Спосіб за п. 8, де сполукою формули III є 2-аміно-4-метилпіридин.
12. Спосіб одержання сполуки за п. 1, де отримують біологічну культуру, що містить мікроорганізм, такий як Nocardia mediterranea, у водному розчині, та поживні речовини; та
окиснюють отриману культуру окисником для отримання окисненого продукту;
піддають реакції окиснений продукт з похідним 2-амінопіридину.
13. Фармацевтична композиція, яка містить терапевтично ефективну кількість сполуки формули І у комбінації з одним або більше фармацевтично прийнятними інгредієнтами.
14. Фармацевтична композиція за п. 13 для застосування як антибактеріальної.
15. Фармацевтична композиція, яка містить одну або більше сполук формули І, або одну або більше сполук формули І у комбінації з однією або більше сполуками формули II, та фармацевтично прийнятний наповнювач.
16. Фармацевтична композиція за п. 15, де композиція має форму, придатну для застосування у одиничній або у розділеній формі дозування.
17. Фармацевтична композиція за п. 15, яка додатково містить похідне рифаміцину або неоміціну.
18. Фармацевтична композиція за п. 17, в якій похідним рифаміцину є рифаксимін.
19. Фармацевтична композиція за п. 18, в якій сполука формули І знаходиться у співвідношенні приблизно 0,01-100 мас. % відносно рифаксиміну.
20. Фармацевтична композиція за п. 15, необов'язково разом з одним або більше додатковими антибіотиками, для застосування у способі лікування, запобігання або пом'якшення розростання бактерій у пацієнта, який страждає від пов'язаного з кишечником розладу.
21. Фармацевтична композиція за п. 20, в якій одним або більше додатковими антибіотиками є один або більше вибраних з групи: рифаміцин, рифаксимін або неоміцин.
22. Фармацевтична композиція за п. 20, в якій пов'язаний з кишечником розлад є одним або більше з групи: синдром подразненого кишечнику, діарея мандрівників, розростання бактерій у тонкому кишечнику, хвороба Крона, хронічний панкреатит, недостатність підшлункової залози, печінкова енцефалопатія, дивертикуліт, ентерит або коліт.
Текст
Реферат: (74) Представник: Крилова Надiя Iванiвна, реєстр. №30 (56) Перелік документів, взятих до уваги експертизою: EP 0 161 534 A, 21.11.1985 US 4 267 274 A, 12.05.1981 CH 571 064 A5, 31.12.1975 CH 547 854 A, 11.04.1974 MARTINELLI E. ET AL.: "RIFAMYCIN R A NOVEL METABOLITE FROM A MUTANT OF NOCARDIA-MEDITERRANEA" JOURNAL OF ANTIBIOTICS, JAPAN ANTIBIOTICS RESEARCH ASSOCIATION, TOKYO, JP, vol. 31, no. 10, 1 January 1978 (1978-01-01), pages 949-951, XP009125544 ISSN: 00218820 MARCHI E. ET AL.: "4deoxypyrido[1',2':1,2]imidazo[5,4-c]rif amycin SV derivatives. A new series of semisynthetic rifamycins with high antibacterial activity and low gastroenteric absorption" JOURNAL OF MEDICINAL CHEMISTRY 1985 US, vol. 28, no. 7, 1985, pages 960-963, XP002554520 ISSN: 0022-2623 CELLAI L. ET AL.: "STRUCTURE-ACTIVITY RELATIONSHIPS IN 4 DEOXYPYRIDO-1' 2'-1 2-IMIDAZO-5 4-C-RIFAMYCIN SV DERIVATIVES" FARMACO, SOCIETA CHIMICA ITALIANA, PAVIA, IT, vol. 44, no. 2, 1 January 1989 (1989-01-01), pages 97-108, XP009125448 ISSN: 0014-827X UA 105775 C2 (12) UA 105775 C2 CH3 R O OH OH H3C CH3 OH O CH3 CH3 O H3C H N R3 O N+ O O CH3 O R2 N H R1 І Розкриті сполуки, що охоплюють похідні рифаміцину, що мають антибактеріальну активність, де сполуки мають нижченаведену загальну формулу (І), де: R - гідроген або ацетил, R1 та R2, незалежно, - гідроген, (C1-4) алкіл, бензилокси, моно- та ді-(С1-3) алкіламіно-(C1-4)алкіл, (C1алкіл, гідрокси-метил, гідрокси-(С2-4)-алкіл, та нітро, або R1 та R2, разом з 3)алкокси, (C1-4) двома послідовними атомами карбону піридинового ядра утворюють бензенове кільце, необов'язково заміщене одним або двома метилами або етилами, a R3 - гідроксіалкіл (C1-4). На додаток, є описаними способи отримання цих сполуки. Сполуки мають антибактеріальну активність. UA 105775 C2 5 10 15 20 25 30 35 40 45 Заявлений винахід стосується фармацевтичних композицій, а зокрема пероральних композиції для лікування запальної хвороби кишечнику. Рифаксимін (ІNN; дивись Тhе Меrсk Іndех, ХІІІ Еd., 8304), антибіотик, що належить до класу рифаміцінів, є піридо-імідазо-рифаміціном, описаним та заявленим у патенті Іtаlіаn Раtеnt ІТ 1 154655. Еurореаn Раtеnt ЕР 0161534 описує спосіб його виготовлення починаючи з рифаміціну О (Тhе Меrсk Іndех, ХІІІ Еd., 8301). Способи створення поліморфних форм рифаксиміну є описаними у заявці US Раtеnt Аррlісаtіоn Рublісаtіоn 2008-0262232, Vіsсоmі еt аl., що уведено тут як посилання. Рифаксимін застосовано для лікування гострих та хронічних кишкових інфекцій від грам-позитивних та грам-негативних бактерій та як ад’ювант у терапії гіперамоніємії. Рифаксимін продають у США як ХІFАХАN™ для лікування діареї мандрівників. спричиненої неінвазивними штамами Еsсhеrісhіа соlі. Рифаксимін також застосовано для лікування асоційованої з Сlоstrіdum dіffісіlе діареї, хвороби Крона, дивертикулезу, печінкової енцефалопатії, знищення Неlісоbасtеr руlоrі, інфекційної діареї, синдрому подразненого кишечнику, резервуарного ілеїту, профілактики для шлунково-кишкової хірургії, розростання тонкого кишечнику, діареї мандрівників та виразкового коліту. Похідні рифаміціну, що мають гетероциклічне кільце, конденсоване у 3,4-позиціях, є відомими у рівні техніки. Наприклад, U.S. Раtеnts №№ 4,263,404 та 4,341,785 описують рифаміцін та імідазо-похідні рифаміціну. Рифаміціни мають антибактеріальну активність та вони є отриманими з вторинних метаболітів культур мікроорганізмів, корисних у лікуванні інфекцій, зокрема туберкульозу, як описано Sеnsі Р. у Fаrmасо [Sсі], (1959); 14:146-7 та Міtnісk СD. еt аl. у Ехреrt Оріn. Рhаrmасоthеr.(2009);10:381 -401. Зараз похідні рифаміціну ідентифіковані як активатори рецептору Х прегнану (РRХ), члену родини ядерного рецептору, що регулює експресію метаболічного ферменту, що приймає участь у реакції ссавців на хімічне стимулювання, як описано Nаtl.Асаd.Sсі.USА, (1998), 95: 12208-12213. Рифаміціни характеризуються хімічною структурою з одним або більше конденсованими ароматичними кільцями, що утворюють циклічну структуру з аліфатичним кільцем, як описано Рrеlоng, V. еt аl. у НеІv. Сhіm. Асtа (1973); 56:2279. Аналоги рифаміціну є отриманими хімічним модифікуванням ароматичної або аліфатичної частин молекули, як описано Sеnsі Р. у Rеsеаrсh Рrоgrеsss іn Оrgаnіс Віоlоgісаl та Меdісіnаl Сhеmіstrу (1964), 1, 337421. Маrtіnеllі Е. еt аl. описують у J. Аntіbіоt. 31 (10), 949, 1978 рифаміцін R, отриманий мутацією Nосаrdіа mеdіtеrrаnеа, виробника рифаміцину, але біологічну активність цієї сполуки не показано. Рифаміцін є антибіотиком, застосовуваним у терапії туберкульозу та важливо мати нові антибіотики без будь-якої резистентності до антибіотику стосовно рифаміціну. Заявлений винахід розв’язує проблему нового заміщеного рифаксиміну, похідного від рифаміціну О, з активністю антибіотику, але відмінного для від нього. Розкритою тут є сполука формули І І де: R - гідроген або ацетил, R1 та R2, кожний незалежно, вибрані з групи: гідроген, (С1-4)алкіл, бензилокси, моно- або ді(С1-3) алкіламіно(С1-4)алкіл, (С1-3) алкокси-(С1-4) алкіл, гідроксиметил, гідрокси-(С2-4)-алкіл, та нітро; або R1 та R2, разом з двома послідовними атомами карбону, піридинового кільця утворюють бензенове кільце, незаміщене, або моно- або ді-заміщене одним або двома метилами або етилами; а R3 - гідроксіалкіл (С1-4). У деяких втіленнях R - ацетил, R1 та R2, незалежно, - гідроген або метил, а R3 - гідроксіалкіл (С1-4). В інших втіленнях R - ацетил, R1 - гідроген, R2 - метил та R3 - гідроксиметил. -АУ ще одному аспекті розкрито спосіб виготовлення сполуки формули ІІ, спосіб полягає у нижченаведеному: 1 UA 105775 C2 5 10 15 20 25 30 35 ІІ отримання біологічної культури, що містить мікроорганізм у водному розчині, придатному для продукування похідних рифаміціну В, та живільні агенти; та окиснення отриманої культури окисником; де R - гідроген або ацетил, а R3 - гідроксіалкіл (С1-4). У деяких втіленнях окисник вибрано з одного або більше з групи: натрію нітрит, водний розчин калію дихромату, амонію персульфату, або натрію перйодату. У деяких втіленнях R - гідроген або ацетил, а R3 гідроксіалкіл (С1-4). У наступних втіленнях, R - ацетил, а R3 - гідроксиметил. У ще одному аспекті розкрито спосіб синтезування сполуки за п. 1, що полягає у реакції сполуки формули ІІ, де R - гідроген або ацетил, а R3 - гідроксіалкіл (С1-4), зі сполукою формули ІІІ: ІІІ де R1 та R2, кожний незалежно, вибрані з групи: гідроген, (С1-4)алкіл, бензилокси, моно- або ді-(С1-3) алкіламіно(С1-4)алкіл, (С1-3) алкокси-(С1-4) алкіл, гідрокси-метил, гідрокси-(С2-4)-алкіл, та нітро; або R1 та R2, разом з двома послідовними атомами карбону, піридинового кільця утворюють бензенове кільце, незаміщене, або моно- або ді-заміщене одним або двома метилами або етилами, у присутності органічного розчиннику, суміші більше, ніж одного органічних розчинників, або суміші органічного розчиннику з водою, при температура між температурою довкілля та 60°С, протягом часу між 1 та 100 годинами. У деяких втіленнях органічний розчинник вибрано з групи: ароматичні вуглеводні, аліфатичні алканоли, галогеновані вуглеводні, нижчий алкіл-естер нижчої аліфатичної кислоти, гліколі, ацетонітрил, діоксан, тетрагідрофуран, та їх комбінація, або у суміші з водою у різних об’ємних співвідношеннях. У деяких втіленнях для кожного молярного еквіваленту сполуки формули ІІ, застосовують приблизно 0,1 - 1 молярних еквівалентів йоду або комбінації йод/окисник. У наступних втіленнях, сполукою формули ІІІ є 2-аміно-4-метил-піридин. У ще одному аспекті розкрито спосіб синтезування сполуки за п. 1, спосіб полягає у нижченаведеному: отримання біологічної культури, що містить мікроорганізми, придатні для продукування похідних рифаміціну В, у водному розчині, та живільні агенти; окиснення отриманої культури окисником для отримання окисненого продукту; та реакція окисненого продукту з похідним 2-амінопіридину. У ще одному аспекті розкрито фармацевтичну композицію, що містить терапевтично діючу кількість сполуки формули І у комбінації з одним або більше фармацевтично прийнятними інгредієнтами. У деяких втіленнях фармацевтична композиція є корисною як антибактеріальна. У наступному аспекті, розкрито фармацевтичну композицію, що містить одну або більше сполук формули І, або одну або більше сполук формули І у комбінації з одною або більше сполуками формули ІІ, та фармацевтично прийнятний наповнювач. У деяких втіленнях композицію застосовують в одиничній формі дозування, тоді як в інших втіленнях композицію 2 UA 105775 C2 5 10 15 20 25 30 35 40 45 застосовують в розділених формах дозування. В інших втіленнях фармацевтична композиція крім того містить похідне рифаміціну або неоміціну. У деяких втіленнях похідним рифаміціну є рифаксимін. У деяких втіленнях сполука формули І є у співвідношенні приблизно 0,01 - 100 мас% відносно рифаксиміну. У ще одному аспекті розкрито спосіб лікування, запобігання або пом’якшення розростання бактерій у пацієнта, який потерпає від пов’язаного з кишечником розладу, спосіб полягає у нижченаведеному: ідентифікування особи при необхідності цього, та застосування до особи ефективної кількості одної або більше сполук формули І у комбінації з одним або більше додатковими антибіотиками. У деяких втіленнях одним або більше додатковими антибіотиками є один або більше з групи: рифаміцін, рифаксимін, або неоміцін. У деяких втіленнях пов’язаний з кишечником розлад є одним або більше з групи: синдром подразненого кишечнику, діарея мандрівників, розростання бактерій у тонкому кишечнику, хвороба Крона, хронічний панкреатит, недостатність підшлункової залози, печінкова енцефалопатія, дивертикуліт, ентерит, або коліт. У ще одному аспекті розкрито спосіб оцінювання ефективності лікування пов’язаного з кишечником розладу, що зменшує розростання бактерій, моніторинг прогресу особи, яку лікують від пов’язаного з кишечником розладу, або відбирання особи для лікування розладу кишечнику, спосіб полягає у нижченаведеному: визначення рівня розростання бактерій до лікування у особи, яка потерпає від пов’язаного з кишечником розладу внаслідок розростання бактерій; застосування терапевтично ефективної кількості сполуки формули І у комбінації з рифаксиміном до особи; визначення рівня розростання кишкових бактерій після лікування у особи після початкового періоду лікування; та визначення зміни рівня розростання бактерій у особи між вимірюваннями до лікування та після лікування. У деяких втіленнях зміна рівня розростання бактерій показує ефективність лікування; де зменшення рівня розростання бактерій показує, що лікування є ефективним; або де зміна рівня розростання бактерій показує, що особа ймовірно має сприятливу клінічну реакцію на лікування. Фіг. 1 показує ВЕРХ-хроматограму сполуки формули Іl, де R - ацетил, а R3 - гідроксиметил. 1 Фіг. 2 показує спектри Н ЯМР сполуки формули Іl, де R - ацетил, а R3 - гідроксиметил. Фіг. 3 показує ВЕРХ-хроматограму сполуки формули І1, де R - ацетил, R1 - гідроген, R2 метил, а R3 - гідроксиметил. Фіг. 4 показує ІЧ-спектри сполуки формули І, де R - ацетил, R1 - гідроген, R2 - метил, а R3 гідроксиметил. 1 Фіг. 5 показує спектри Н ЯМР отриманої сполуки формули І, де R - ацетил, R1 - гідроген, R2 - метил, а R3 - гідроксиметил. 13 Фіг. 6 показує спектри С ЯМР сполуки формули І, де R - ацетил, R1 - гідроген, R2 - метил, а R3 - гідроксиметил. Фіг. 7 показує спектри ЕІ-МС сполуки формули І, де R - ацетил, R1 - гідроген, R2 - метил, а R3 - гідроксиметил. В одному аспекті розкрито похідні рифаміціну формули І: де: R - гідроген або ацетил; R1 та R2, кожний незалежно, вибрано з групи: гідроген, (С1-4) алкіл, бензилокси, моно- та ді(С1-3) алкіламіно-(С1-4) алкіл, (С1-3) алкокси, (С1-4) алкіл, гідрокси-метил, гідрокси-(С2-4) алкіл, та нітро; або R1 та R2, разом з двома послідовними атомами карбону піридинового кільця утворюють бензенове кільце, де бензенове кільце є незаміщеним, моно-заміщеним або дізаміщеним метилом або етилом; та R3 - (С1-4) гідроксіалкіл. В одному втіленні сполуки формули І, R - гідроген або ацетил, R1 та R2, кожний незалежно, вибрано з групи: гідроген, (С1-4) алкіл, бензилокси, гідрокси (С2-4) алкіл, та ді-(С1-3) алкіламіно 3 UA 105775 C2 5 10 15 20 25 30 35 40 45 (С1-4) алкіл, або R1 та R2, разом з двома послідовними атомами карбону піридинового кільця утворюють бензенове кільце, а R3 - (С1-4) гідроксіалкіл. Ще один аспект містить сполуки формули І, де R - ацетил, R1 та R2, кожний незалежно, гідроген або (С1-4) алкіл, або R1 та R2, разом з двома послідовними атомами карбону піридинового кільця утворюють бензенове кільце, а R3 - (С1-4) лінійний гідроксіалкіл. Як застосовувано тут терміни (С1-3) алкіл, (С2-4) алкіл та ( С1-4) алкіл ідентифікують лінійні або розгалужені алкіл-радикали, що містять 1 - 3 або 2 - 4 або 1 - 4 атоми карбону, відповідно, як-то, наприклад, метил, етил, н-пропіл, ізопропіл, н-бутил, вт-бутил, ізобутил або тр-бутил, тоді як термін (С1-3) алкокси по суті стосується метокси, етокси, пропокси або ізопропокси. Сполуки можна отримувати способами, залежно від типу сполук, що бажано отримувати. Тому, наприклад, сполуки формули І, де R та R3 визначено вище, можна отримувати реакцією сполуки формули ІІ, отриманої як проміжний продукт способом, аналогічним описаному у U.S. Раtеnt 4,263,404, з незаміщеним або заміщеним 2-аміно-піридином формули ІІІ, як визначено нижче: ІІ де R1, R2 та R3 визначено вище. Сполуки формули Іl можна отримати з придатної біологічної культури мікроорганізмів, як-то Strерtоmусеs mеdіtеrrаnеі або Nосаrdіа mеdіtеrrаnеа, у присутності окиснику, як-то як натрію нітрит, калію дихромат, амонію персульфат, натрію перйодат. Взагалі, сполуки формули ІІ, а зокрема, коли R1 - Н, R2 - метил, R - ацетил, а R3 гідроксиметил, можна отримати способами очищення суміші, отриманої від вищенаведеної біологічної культури. Способами очищення можуть бути, наприклад, хроматографія, кристалізування та екстрагування органічним розчинником. Аналітичні способи, корисні для 1 ідентифікування та для характеристики отриманих сполук є Н-ЯМР, ІЧ-спектроскопія, ЕІ-МСспектроскопія, та хроматографія (ВЕРХ). Отримані сполуки формули Іl можуть реагувати з молярним надлишком вибраного похідного аміно-піридину формули ІІІ у придатній системі розчинників, з котрих відомими способами отримують бажаний кінцевий продукт сполуки формули І. Молярний надлишок приблизно від 2 до 8 або більше еквівалентів розраховано на базі сполуки формули ІІ. Реакцію можна досліджувати, наприклад, у присутності розчиннику або системи розчинників, що є взагалі вибраними поміж звичайно застосовуваних у хімії рифаміціну. Наприклад, можна застосовувати ароматичні вуглеводні, як-то бензен або толуєн, нижчі галогеновані вуглеводні, як-то метиленхлорид, хлороформ, 1,2-дихлоро-етан тощо, нижчі алканоли, як-то метанол, етанол, пропанол, ізопропанол або н-бутанол,. Нижчі алкіл-естери нижчої аліфатичної кислоти, гліколі, ацетонітрил, діоксан та тетрагідрофуран можна також застосовувати. Ці розчинники можна застосовувати поодинці, або у суміші, що містить два або більше з групи: вищенаведені розчинники, або також у суміші з водою, у різних об’ємних співвідношеннях. Переважні розчинники охоплюють бензен, толуєн, нижчі галогеновані вуглеводні, нижчі алканоли поодинці або у суміші з водою, ацетонітрил, гліколі, діоксан та тетрагідрофуран, застосовувані поодинці чи у комбінації, або у суміші з водою. Реакція може йти при тиску довкілля у широких межах температур, наприклад між кімнатною температурою та температурою кипіння реакційної суміші. Температура є у межах між кімнатною температурою, наприклад, 20 °С, та приблизно 60 °С, як виявили, корисно для отримання сполуки, описаних тут. Реакцію було завершено у період часу, що варіював залежно від природи амінопіридинового субстрату формули ІІІ та від умов, у котрих реакцію досліджували. Взагалі, приблизно 1 - 100 годин були потрібні для отримання кінцевих продуктів формули І з бажаним виходом. Виявили, що перебіг реакції може бути сприятливим, якщо реакцію проводять у присутності йоду або підхожого йод/окиснику; де йод може бути, 4 UA 105775 C2 5 10 15 20 25 30 35 40 45 50 55 60 наприклад, йодом лужного або лужноземельного металу та гідройодом вищезгаданого, починаючи з похідного піридину, а окисником може бути агент, здатний окиснювати в умовах реакції іон йоду, для вивільнення йоду у реакційну суміш. Йод, або йод/окисник, може бути у реакційній суміші відповідно у кількості приблизно 0,1 - 1 молярного еквіваленту йоду, для кожного моля вихідної сполуки формули ІІ. У такому випадку, однак, реакційний розчин можна пізніше обробляти придатним відновником, як-то, аскорбінова кислота, ізоаскорбінова кислота або дигідроксіацетон. Отримані сполуки можуть далі хімічно реагувати з отриманням інших сполук формули І. Тому, наприклад, можна отримати сполуку формули І, де R, R 1, R2 та R3 визначено вище, обробкою отриманої сполуки придатним відновником, як-то, наприклад, L (-) аскорбінова кислота. Сполуки формули І, де R - гідроген можна отримувати гідролізом у лужних умовах, відповідної сполуки, де R - ацетил. Сполуки можна отримувати з реакційного середовища, наприклад, відомими спеціалісту способами. Ці способи охоплюють екстрагування придатним органічним розчинником, як-то, етилацетат, хлороформ, метиленхлорид та аналоги або їх суміш, випарювання до сухого стану органічного екстракту та перенесення залишку у підхожий розчинник, з котрого відокремлюють кінцевий продукт. Альтернативно суміші можна безпосередньо випарювати до сухого стану та отриманий залишок у свою чергу переносять у придатний розчинник, з котрого кінцевий продукт відокремлюють кристалізуванням або хроматографією. Розчинники, що можна переважно застосовувати вибирають з групи: вода, метанол, етанол, н-пропанол, ізопропанол, н-гексан, етилацетат, метилен, хлороформ, етиленгліколю моно-метил етер або їх суміш. Заявлені сполуки можна отримати, наприклад, з чистотою вище, ніж 90% з продукту реакції відомими способами очищення, як-то хроматографією. Заявлені сполуки є корисними антибактеріальними агентами. Вони мають іn vіtrо активність проти грам-позитивних та грам-негативних бактерій. Сполуки мають антибактеріальний вплив на бактерії, виділені з клінічних зразків, що можна виявити у флорі кишкових бактерій у патологічних станах. Антибактеріальну активність сполук формули І демонстрували вимірюванням мінімуму концентрації активної речовини, здатної інгібувати ріст іn vіtrо патогенних бактерій (МІС). Вони є вираженими як мг речовини на літр оf культур середовище. Антибактеріальну активність одної з більш репрезентативних сполук, де R - ацетил, R1 та R2, незалежно, - гідроген або метил, а R3 - гідроксиметил, вимірювали на великому числі штамів бактерій, що належать до різних родин, як-то Еntеrоbасtеrіасеае, неЕntеrоbасtеrіасеае грамнегативний, стафілокок. Значення МІС є від 0,06 до 128 мг/л та ці значення демонструють антибактеріальну ефективність сполук формули І. У ще одному аспекті, заявлені сполуки можна застосовувати як антибактеріальні агенти, у тому числі уведенням їх у фармацевтичні композиції. Ці сполуки можна застосовувати поодинці або у комбінації з іншими антибіотиками, як-то рифампіцин, рифаміцін, неоміцін та/або рифаксимін, та у широких межах співвідношення мас, переважно 0,01 - 100 мас%. У ще одному аспекті, фармацевтичний препарат містить сполуки формули І із фармацевтично прийнятним носієм, розріджувачем, або наповнювачем. Заявлені сполуки можна тому застосовувати кількома шляхами, наприклад, пероральним, місцевим або парентеральним. Для такого застосування речовини уводять у звичайні фармацевтичні композиції. Ці композиції можуть містити сполуки формули І поодинці або у суміші зі сполукою формули Іl або іншим фармацевтично активним інгредієнтом зі звичайними адитивами, як-то, наприклад, підсолоджувач, звичайний адитив, як-то, наприклад, вибраний з групи: підсолоджувач, ароматизатор, барвники, покриття та консервант агенти, інертні розріджувачі, як-то, наприклад, кальцію або натрію карбонат, лактоза та тальк, зв’язуючі, наприклад, крохмаль, желатин та полівінілпіролідон, суспендувальні агенти, наприклад, метилцелюлоза або гідроксіетилцелюлоза, та зволожувачі, як-то, наприклад, лецитин, поліоксіетиленстеарати та поліоксиметилен сорбітан-моноолеат. Препарати, корисні для місцевого та парентерального застосування можуть містити активні інгредієнти, розчинені або суспендовані у дистильованій та піроген-вільній воді, у суміші із звичайно застосовуваними фармацевтичними носіями. Ще один аспект заявленого винаходу є застосування сполуки формули І поодинці, або у комбінації з ще одною сполукою формули І, або у комбінації зі сполукою формули ІІ, або у комбінації з іншими фармацевтично активними агентами для лікування або для запобігання інфекції бактеріями. Зокрема, зараз розкриті фармацевтичні композиції можна застосовувати для лікування пацієнта, який потерпає від пов’язаного з кишечником розладу, охоплюючи, але 5 UA 105775 C2 5 10 15 20 25 30 35 40 45 50 55 60 без обмеження, одне або більше з групи: синдром подразненого кишечнику, діарея, асоційована з мікробами діарея, асоційована з Сlоstrіdum dіffісіlе діарея, діарея мандрівників, розростання бактерій у тонкому кишечнику, хвороба Крона, хронічний панкреатит, недостатність підшлункової залози, коліт, печінкова енцефалопатія, дивертикуліт, та резервуарний ілеїт. У ще одному аспекті винаходу, сполуки, розкриті тут, виявляють антибактеріальну активність та грають роль в активації рецептору прегнану Х (РRХ), ядерного рецептору, що регулює гени, що приймають участь у ксенобіотичному та обмеженому ендобіотичному відкладенню та детоксикації. Нами запропоновано способи лікування, запобігання або пом’якшення пов’язаних з кишечником розладів, що полягають у застосуванні до особи при необхідності цього терапевтично ефективної кількості одної або більше сполук, розкритих тут. Пов’язані з кишечником розлади охоплюють одне або більше з групи: синдром подразненого кишечнику, діарея, асоційована з мікробами діарея, асоційована з Сlоstrіdіum dіffісіlе діарея, діарея мандрівників, розростання бактерій у тонкому кишечнику, хвороба Крона, хронічний панкреатит, недостатність підшлункової залози, коліт, печінкова енцефалопатія, дивертикуліт, та резервуарний ілеїт. Тривалість лікування для певного розладу кишечнику залежить частково від розладу. Наприклад, діарея мандрівників може потребувати тільки тривалості лікування 12 - 72 годин, тоді як хвороба Крона може потребувати тривалості лікування приблизно від 2 діб до 3 місяців. Дозування також варіює залежно від стану хвороби. Належні межі дозування вищезгадано. Ідентифікація пацієнтів, які потребують профілактичного лікування розладу кишечнику, добре відома. Певні способи ідентифікації пацієнтів, які мають ризик розвинення розладу кишечнику, що можна лікувати розкритими тут способами є у документах, як-то історія родини, історія мандрівок та очікувані плани мандрівок, присутність факторів ризику, асоційованих з розвиненням цього стану хвороби у пацієнта. Спеціаліст може легко ідентифікувати таких пацієнтів застосуванням, наприклад, клінічних тестів, фізичного випробування та історії родини/мандрівок. Спосіб оцінювання ефективності лікування у особи охоплює визначення рівня розростання кишкових бактерій для лікування добре відомими способами (наприклад, , біопсія, збирання зразків кишкових бактерій, тощо) та тоді застосування терапевтично ефективної кількості заявленої сполуки. Після підхожого періоду часу (наприклад, після початкового періоду лікування) від застосування сполуки, наприклад, 2 години, 4 години, 8 годин, 12 годин, або 72 години, рівень розростання бактерій визначають знов. Модуляція рівня бактерій показує ефективність лікування. Рівень розростання бактерій можна визначити періодично протягом лікування. Наприклад, розростання бактерій можна перевіряти кожні кілька годин, діб або тижнів для оцінки ефективності лікування. Зменшення розростання бактерій показує, що лікування є ефективним. Спосіб, що описано, можна застосовувати для вибору пацієнтів, що можуть мати користь від лікування заявленими сполуками. У ще одному аспекті спосіб лікування особи, яка потерпає або схильна до розладу кишечнику, полягає у застосуванні до особи при необхідності цього терапевтично ефективної кількості заявленої сполуки для лікування таким чином особи. При ідентифікації особи, яка потерпає або схильна до розладу кишечнику, наприклад, ІВS, застосовують одну або більше заявлених сполук. В одному аспекті способи оцінювання ефективності лікування заявленою сполукою, або у суміші з іншими активними інгредієнтами у особи полягають у визначенні рівня розростання бактерій до лікування, застосування терапевтично ефективної кількості сполуки формули І або ІІ, поодинці або у комбінації з іншими активними інгредієнтами, до особи, та визначення розростання бактерій після початкового періоду лікування заявленими сполуками, де модуляція розростання бактерій показує ефективність антибактеріального лікування. Ефективність лікування можна вимірювати, наприклад, як зменшення розростання бактерій. Ефективність можна також вимірювати у термінах зменшення симптомів, асоційованих з розладом кишечнику, стабілізації симптомів, або припинення симптомів, асоційованих з розладом кишечнику, наприклад, зменшення нудоти, здимання, діареї, тощо. В одному аспекті способи моніторингу прогресу особи, яку лікують заявленими сполуками, полягають у визначенні рівня розростання бактерій до лікування, застосування терапевтично ефективної кількості заявленої сполуки до особи, та визначення розростання бактерій після початкового періоду лікування заявленими сполуками, де модуляція розростання бактерій показує ефективність антибактеріального лікування. Ще один аспект заявленого винаходу - це фармацевтичні препарати, що містять, наприклад, ефективну кількість похідного рифаміціну поодинці або в асоціації з іншими фармацевтичними активними інгредієнтами у фармацевтично прийнятному носії. У наступному втіленні, 6 UA 105775 C2 5 10 15 20 25 30 35 40 45 50 55 60 ефективна кількість є ефективною для лікування бактеріальної інфекції, наприклад, розростання бактерій у тонкому кишечнику, хвороба Крона, печінкова енцефалопатія, асоційований з антибіотиками коліт, та/або дивертикулез. Для прикладів застосування для лікування діареї мандрівників, дивись Іnfаntе RМ, Еrісssоn СD, Zhі-Dоng J, Ке S, Stеffеn R, Rіореl L, Sасk DА, DuРоnt, НL. Еntеrоаggrеgаtіvе Еsсhеrісhіа соlі Dіаrrhеа іn Тrаvеlеrs: Rеsроnsе tо Rіfахіmіn Тhеrару. Сlіnісаl Gаstrоеntеrоlоgу аnd Нераtоlоgу. 2004; 2 : 135-138; аnd Stеffеn R, М. D., Sасk DА, М. D., Rіореl L, Рh.D., Zhі-Dоng J, Рh.D., Sturсhlеr М, М. D., Еrісssоn СD, М. D., Lоwе В, М.Рhіl., Wаіуаkі Р, Рh.D., Whіtе М, Рh.D., DuРоnt НL, М. D. Тhеrару оf Тrаvеlеrs' Dіаrrhеа Wіth Rіfахіmіn оn Vаrіоus Соntіnеnts. Тhе Аmеrісаn Jоurnаl оf Gаstrоеntеrоlоgу. Мау 2003, Vоlumе 98, Numbеr 5, усі які уведено тут як посилання. Фармацевтичні композиції можуть містити одну або більше сполук формул І або Іl або можуть містити суміш більше, ніж одної сполуки, представленої тою ж формулою, або суміш сполук формули І зі сполуками формули ІІ, або у суміші з іншими фармацевтично активними інгредієнтами. Суміші можна вибирати, наприклад, на основі бажаної кількості системного поглинання, профіль розчинення, тощо. Фармацевтичні композиції можуть крім того містити носій, наприклад, один або більше з групи: розріджувач, зв’язуюче, лубрикант, дезинтегратор, барвник, ароматизатор або підсолоджувач. Композиції можна формувати як покриті та непокриті таблетки, тверді та м’які желатинові капсули, покриті цукром пігулки, пастилки, вафлі, пелети та порошки у герметизованих пакетах. Наприклад, композиції можна формувати для місцевого застосування, як-то, мазі, креми, гелі та лосьйони. Похідні рифаміціну застосовують до особи у фармацевтично-прийнятній композиції, наприклад, фармацевтично-прийнятній композиції, що забезпечує безперервне поставляння до особи протягом принаймні 12 годин, 24 годин, 36 годин, 48 годин, одного тижня, двох тижнів, трьох тижнів, або чотирьох тижнів після застосування фармацевтично-прийнятної композиції до особи. Ці фармацевтичні композиції є придатними для місцевого або перорального застосування до особи. В інших втіленнях як описано детально нижче, заявлені фармацевтичні композиції можна спеціально формувати для застосування у твердій або рідкій формі, охоплюючи пристосовані для нижченаведеного: (1) пероральне застосування, наприклад, таблетки, болюси, порошки, гранули, пасти; (2) парентеральне застосування, наприклад, підшкірно, внутрішньом’язово або внутрішньовенно, як наприклад, стерильним розчином або суспензією; (3) місцевим нанесенням, наприклад, як крем, мазь або спрей на шкіру; (4) інтравагінально або інтратекально, наприклад, як крем або пінка; або (5) аерозолем, наприклад, як водний аерозоль, ліпосомний препарат або тверді частинки, що містять сполуку. Вираз "фармацевтично прийнятний" стосується заявлених сполук, композицій, що містять такі сполуки, та/або форм дозування, що є придатними для застосування у контакті з тканинами людини та тварини без надлишкової токсичності, подразнення, алергічної реакції, або інших проблем або ускладнень, відповідним розумному співвідношенню користь/ризик. Вираз "фармацевтично-прийнятний носій" охоплює фармацевтично-прийнятний матеріал, композицію або середовище, як-то рідкий або твердий наповнювач, розріджувачі, розчинники або інкапсулювальний матеріал, що приймає участь у переносі хімічної речовини від одного органу або частини тіла, до ще одного органу або частини тіла. Кожний носій є переважно "прийнятним" тобто сумісним з іншими інгредієнтами композиції та нешкідливим для пацієнта. Приклади матеріалів, що можуть бути фармацевтично-прийнятними носіями, охоплюють: (1) цукри, як-то лактоза, глюкоза та сахароза; (2) крохмалі, як-то кукурудзяний крохмаль та картопляний крохмаль; (3) целюлоза, та її похідні, як-то натрію карбоксиметилцелюлоза, етилцелюлоза та целюлоза-ацетат; (4) порошковий трагакант; (5) солод; (6) желатин; (7) тальк; (8) наповнювачі, як-то масло какао; (9) олії, як-то арахісу, бавовни, сафлори, кунжуту, оливкова, кукурудзяна та соєва; (10) гліколі, як-то пропіленгліколь; (11) поліоли, як-то гліцерин, сорбітол, манітол та поліетиленгліколь; (12) естери, як-то етилолеат та етиллаурат; (13) агар; (14) буферувальні агенти, як-то магнію гідроксид та алюмінію гідроксид; (15) альгінова кислота; (16) піроген-вільна вода; (17) ізотонічний фізіологічний розчин; (18) розчин Рингера; (19) етиловий спирт; (20) фосфатний буфер; та (21) інші нетоксичні сумісні речовини, застосовувані у фармацевтичних композиціях. Зволожувачі, емульгатори та лубриканти, як-то натрію лаурилсульфат та магнію стеарат, а також барвники, агенти вивільнення, агенти покриття, підсолоджувачі, ароматизатори та ароматизатори, консерванти та антіоксиданти можуть також бути у композиції. Приклади фармацевтично-прийнятних антіоксидантів охоплюють: (1) водорозчинні антіоксиданти, як-то аскорбінова кислота, цистеїн гідрохлорид, натрію бісульфат, натрію метабісульфіт, натрію сульфіт тощо; (2) розчинні в олії антіоксиданти, як-то аскорбілпальмітат, бутилований гідроксіанізол (ВНА), бутилований гідрокситолуєн (ВНТ), лецитин, пропіл-галат, 7 UA 105775 C2 5 10 15 20 25 30 35 40 45 50 55 60 альфа-токоферол, тощо; та (3) метал-хелатори, як-то лимонна кислота, етилендіамінтетраоцтова кислота (ЕДТА), сорбітол, винна кислота, фосфатна кислота, тощо. Композиції, що містять похідні рифаміціну, охоплюють придатні для перорального, назального, місцевого (у тому числі букального та сублінгвального), ректального, вагінального, аерозольного та/або парентерального застосування. Композиції можуть бути в одиничній формі дозування та їх можна отримувати будь-якими добре відомими способами. Кількість активного інгредієнту, що можна комбінувати з матеріалом носія для отримання одиничної форм дозування, варіює залежно від особи, яку лікують, конкретного режиму застосування. Кількість активного інгредієнту, що можна комбінувати з матеріалом носія для отримання одиничної форм дозування є взагалі кількістю сполуки, як дає терапевтичну дію. Взагалі, ця кількість є у межах приблизно від 1 % до 99 % активного інгредієнту, переважно приблизно від 5 % до 70 %, найбільш переважно приблизно від 40 % до 70 %. Способи отримання цих композицій можуть мати етап поєднання похідних рифаміціну поодинці або у суміші з іншими активними інгредієнтами з носієм та, необов’язково, з одним або більше допоміжними інгредієнтами. Взагалі, композиції отримують однорідним поєднанням похідних рифаміціну поодинці або у суміші з іншими активними інгредієнтами з рідкими носіями, або мілко подрібненими твердими носіями, а тоді, якщо необхідно, формуванням продукту. Заявлені композиції, придатні для перорального застосування, можуть бути у формі капсул, пігулок, таблеток, пастилок, порошків, гранул, або як розчин або суспензія у водній або неводній рідині, або як рідка емульсія олія-у-воді або вода-в-олії, або як еліксир або сироп, або як пастилки (на інертній основі, як-то желатин та гліцерин, або сахароза та гуміарабік) та/або як промивання для рота тощо, що містять попередньо визначену кількість похідного рифаміціну формули І поодинці або у суміші з іншими активними інгредієнтами. Сполуку можна також застосовувати як болюс, електуарій або пасту. Похідні рифаміціну можна переважно застосовувати у виготовленні медичних препаратів, що мають активність антибіотику для перорального та місцевого застосування. Медичні препарати для перорального застосування можуть містити разом зі звичайними наповнювачами, наприклад, розріджувачами, як-то манітол, лактоза та сорбітол; зв’язуючими, як-то крохмалі, желатини, цукри, похідні целюлози та полівінілпіролідон; лубриканти, як-то тальк, стеарати, гідрогеновані рослинні олії, поліетиленгліколь та колоїдний силіцій діоксид; дезинтегратори, як-то крохмалі, целюлози, альгінати, камеді та сітчасті полімери; барвники, ароматизатори та підсолоджувачі. Заявлені сполуки охоплюють тверді препарати, придатні для застосування пероральним шляхом, наприклад покриті та непокриті таблетки, м’які та тверді желатинові капсули, покриті цукром пігулки, пастилки, вафлі, пелети та порошки у герметизованих пакетах або інших контейнерах. Медичні препарати для місцевого застосування, можуть містити похідні рифаміціну формули І поодинці або у суміші чи в асоціації зі сполуками формули Іl або у суміші з іншими активними інгредієнтами, разом зі звичайними наповнювачами, як-то білий вазелін, білий віск, ланолін та їх похідні, стеариловий спирт, пропіленгліколь, натрію лаурилсульфат, етери жирних поліоксіетиленспиртів, естери жирних поліоксіетиленкислот, сорбітан моностеарат, гліцерил моностеарат, пропіленгліколь моностеарат, поліетиленгліколі, метилцелюлоза, гідроксиметилпропілцелюлоза, натрію карбоксиметилцелюлоза, колоїдний алюміній, натрію альгінат та магнію силікат. Заявлені сполуки можна отримувати у різних композиціях, як-то, місцеві препарати, наприклад мазі, креми, гелі та лосьйони. У твердих заявлених формах дозування для перорального застосування (капсули, таблетки, пігулки, порошки, гранули тощо), активний інгредієнт є змішаним з одним або більше фармацевтично-прийнятними носіями, як-то натрію цитрат або дикальцію фосфат, та/або будьщо з нижченаведеного: (1) наповнювачі, як-то крохмалі, лактоза, сахароза, глюкоза, манітол, та/або силікатна кислота; (2) зв’язуючі, як-то, наприклад, карбоксиметилцелюлоза, альгінати, желатин, полівінілпіролідон, сахароза та/або гуміарабік; (3) зволожувачі, як-то гліцерин; (4) дезинтегратори, як-то агар-агар, кальцію карбонат, крохмаль, альгінова кислота, певні силікати, та натрію карбонат; (5) агентів затримання розчинення, як-то парафін; (6) прискорювачі поглинання, як-то сполуки четвертинного амонію; (7) зволожувачі, як-то, наприклад, ацетиловий спирт та гліцерин моностеарат; (8) абсорбенти, як-то каолін та бентоніт; (9) лубриканти, як-то тальк, кальцію стеарат, магнію стеарат, тверді поліетиленгліколі, натрію лаурилсульфат, та їх суміші; та (10) барвники. У випадку капсул, таблеток та пігулок фармацевтичні композиції можуть також містити буферувальні агенти. Тверді композиції подібного типу можна також застосовувати як наповнювачі у м’яких та твердих заповнених желатинових капсулах, 8 UA 105775 C2 5 10 15 20 25 30 35 40 45 50 55 60 застосовуючи такі наповнювачі, як лактоза або молочні цукри, а також поліетиленгліколі високої молекулярної маси тощо. Таблетку можна робити пресуванням або литтям, необов’язково з одним або більше допоміжними інгредієнтами. Пресовані таблетки можна отримувати, застосовуючи зв’язуюче (як-то, желатин або гідроксипропілметилцелюлоза), лубрикант, інертний розріджувач, консервант, дезинтегратор (наприклад, натрію крохмаль-гліколят або перехресно-зв’язана натрію карбоксиметилцелюлоза), поверхнево-активний агент або диспергатор. Литі таблетки можна робити заливанням у придатний механізм суміші порошкового активного інгредієнту із інертним рідким розріджувачем. Таблетки, та інші тверді форми дозування фармацевтичних композицій заявленої сполуки, як-то капсули, пігулки та гранули, можуть необов’язково бути надрізаними або отриманими з покриттями та оболонками, як-то ентеросолюбільні покриття та інші добре відомі покриття. Їх можна також формувати для забезпечення повільного або контрольованого вивільнення активного інгредієнту, застосовуючи, наприклад, гідроксипропілметилцелюлозу у різних пропорціях для забезпечення бажаного профілю вивільнення, інші полімерні матриці, ліпосоми та/або мікросфери. Їх можна стерилізувати, наприклад, фільтруванням, або уведенням стерилізаторів у формі стерильних твердих композицій, що можна розчиняти у стерильній воді, або іншому стерильному придатному для ін’єкцій середовищі негайно перед застосування. Ці композиції можуть також необов’язково містити непрозорі агенти та можуть вивільняти активний інгредієнт тільки або переважно, у певній частині шлунково-кишкового тракту, необов’язково, із затримкою. Приклади імплантованих композицій, що можна застосовувати, охоплюють полімерні речовини та воски. Активний інгредієнт може також бути у мікро-інкапсульованій формі, якщо підхоже, з одним або більше з вищеописаних наповнювачів. Рідкі форми дозування для перорального застосування похідного рифаміціну формули І поодинці або у суміші чи в асоціації зі сполуками формули Іl або у суміші з іншими активними інгредієнтами, охоплюють фармацевтично-прийнятні емульсії, мікроемульсії, розчини, суспензії, сиропи та еліксири. На додаток до активного інгредієнту рідкі форми дозування можуть містити інертні розріджувачі, звичайно застосовувані у рівні техніки, як-то, наприклад, вода або інші розчинники, солюбілізатори та емульгатори, як-то етиловий спирт, ізопропіловий спирт, етилкарбонат, етилацетат, бензиловий спирт, бензилбензоат, пропіленгліколь, 1,3бутиленгліколь, олії (зокрема, бавовни, арахісу, кукурудзи, оливкова, рицинова та кунжуту), гліцерин, тетрагідрофуриловий спирт, поліетиленгліколі та естери сорбітану жирних кислот, та їх суміші. На додаток до інертних розріджувачі, пероральні композиції можуть мати ад’юванти, як-то зволожувачі, емульгатори та суспендувальні агенти, підсолоджувачі, ароматизатори, барвники та консерванти. Суспензії, на додаток до активних похідних рифаміціну формули І поодинці або у суміші чи в асоціації зі сполуками формули Іl або у суміші з іншими активними інгредієнтами можуть містити суспендувальні агенти як, наприклад, етоксиловані ізостеарилові спирти, поліоксіетиленсорбітол та естери сорбітану, мікрокристалічна целюлоза, алюмінію метагідроксид, бентоніт, агар-агар та трагакант та їх суміші. Заявленими фармацевтичними композиціями для ректального або вагінального застосування можуть бути супозиторії, що можна отримувати змішуванням одного або більше похідних рифаміціну поодинці або у суміші чи в асоціації зі сполуками формули Іl або у суміші з іншими активними інгредієнтами з одним або більше придатними неподразнювальними наповнювачами або носіями, що містять, наприклад, масло какао, поліетиленгліколь, віск для супозиторію або саліцилат, і котрі є твердими при кімнатній температурі, але рідкими при температурі тіла та, тому, плавляться прямій кишці або вагіні та вивільняють активний агент. Заявлені композиції, що є придатними для вагінального застосування також охоплюють тампони, креми, гелі, пасти, пінки або спреї, що містять такі носії, як відомі у рівні техніки як підхожі. Форми дозування для місцевого або трансдермального застосування похідних рифаміціну охоплюють порошки, спреї, мазі, пасти, креми, лосьйони, гелі, розчини, пластири та леткі препарати. Активні похідні рифаміціну можна змішувати у стерильних умовах з фармацевтичноприйнятним носієм, та з будь-якими консервантами, буферами, або пропелентами, що можуть бути потрібними. Мазі, пасти, креми та гелі можуть містити на додаток до рифаміціну заявлені похідні, наповнювачі, як-то тваринні та рослинні жири, олії, воски, парафін, крохмаль, трагакант, похідні целюлози, поліетиленгліколі, силікони, силікатну кислоту, тальк та цинк оксид, або їх суміші. Порошки та спреї можуть містити, на додаток до похідних рифаміціну поодинці або у суміші чи в асоціації зі сполуками формули Іl або у суміші з іншими активними інгредієнтами, 9 UA 105775 C2 5 10 15 20 25 30 35 40 45 50 55 60 наповнювачі, як-то лактоза, тальк, силікатна кислота, алюмінію гідроксид, кальцію силікати та поліамідний порошок, або суміші цих речовини. Спреї можуть на додаток містити звичні пропеленти, як-то хлорофлуоро-вуглеводні та леткі незаміщені вуглеводні, як-то бутан та пропан. Похідні рифаміціну поодинці або у суміші чи в асоціації зі сполуками формули ІІ або у суміші з іншими активними інгредієнтами можна альтернативно застосовувати як аерозоль. Цього досягають отриманням водного аерозолю, ліпосомного препарату або твердих частинок, що містять сполуку. Можна застосовувати неводні (наприклад, у флуорокарбон-пропеленті) суспензії. Акустичні розпилювачі є кращими, оскільки вони мінімізують розкладання сполуки. Звичайно, водний аерозоль роблять формуванням водного розчину або суспензії агенту разом зі звичайними фармацевтично-прийнятними носіями та стабілізаторами. Носії та стабілізатори варіюють із вимогами певної сполуки, але звичайно містять неіонні сурфактанти (Тwееns, Рlurоnісs, або поліетиленгліколь), нешкідливі білки типу альбуміну сироватки, сорбітанестери, олеїнову кислоту, лецитин, амінокислоти, як-то гліцин, буфери, солі, цукри або цукрові спирти. Аерозолі взагалі отримують з ізотонічних розчинів. Трансдермальні пластири надають переваг контрольованого поставляння похідних рифаміціну поодинці або у суміші чи в асоціації зі сполуками формули Іl або у суміші з іншими активними інгредієнтами до тіла. Такі форми дозування можна робити розчиненням у належному середовищі. Посилювачі поглинання можна також застосовувати для збільшення проходження активного інгредієнту крізь шкіру. Швидкість такого проходження можна контролювати мембраною контролювання швидкості або диспергуванням активного інгредієнту у полімерній матриці або гелі. Очні композиції, мазі для очей, порошки, розчини тощо, також охоплені у заявлених рамках. Заявлені фармацевтичні композиції, придатні для парентерального застосування, містять одне або більше похідних рифаміціну поодинці або у суміші чи в асоціації зі сполуками формули Іl або у суміші з іншими активними інгредієнтами у комбінації з одним або більше фармацевтично-прийнятними стерильними ізотонічними водними або неводними розчинами, дисперсіями, суспензіями або емульсіями, або стерильними порошками, що можна відтворювати у стерильні придатні для ін’єкцій розчини або дисперсії якраз перед застосуванням, що можуть містити антіоксиданти, буфери, бактеріостати, розчинені речовини, що надають композиції ізотонічності з кров’ю, або суспендувальні агенти або загусники. Приклади придатних водних та неводних носіїв, що можна застосовувати у заявлених фармацевтичних композиціях, охоплюють воду, етанол, поліоли (такі як гліцерин, пропіленгліколь, поліетиленгліколь, тощо), та придатні їх суміші, рослинні олії, як-то оливкова олія, та придатні для ін’єкцій органічні естери, як-то етилолеат. Текучість можна підтримувати, наприклад, застосуванням матеріалів покриття, як-то лецитин, підтримуванням потрібного розміру частинок у випадку дисперсії, та застосуванням сурфактантів. Ці композиції можуть також містити ад’юванти, як-то консерванти, зволожувачі, емульгатори та диспергатори. Запобігання дії мікроорганізмів можна гарантувати уведенням різних антибактеріальних та антигрибкових агентів, як-то, парабен, хлоробутанол, фенол-сорбінова кислота, тощо. Можуть також бути бажаними ізотонічні агенти, як-то цукри, натрію хлорид. На додаток, продовженого поглинання придатної для ін’єкцій фармацевтичної форми можна досягти уведенням агентів, що затримують поглинання, як-то алюмінію моностеарат та желатин. У деяких випадках для продовження дії ліків, бажане повільне поглинання ліків з підшкірної або внутрішньом’язової ін’єкції. Придатні для ін’єкцій депо роблять формуванням матриці мікрокапсул похідних рифаміціну поодинці або у суміші чи в асоціації зі сполуками формули Іl або у суміші з іншими активними інгредієнтами у біорозкладних полімерах, як-то полілактидполігліколід. Залежно від співвідношення ліків до полімеру, та природи певних застосовуваних полімерів, вивільнення швидкості ліків можна контролювати. Приклади інших біорозкладних полімерів охоплюють полі(ортоестери) та полі(ангідриди). Депо, придатні для композиції для ін’єкцій також отримують уведенням ліків у ліпосоми або мікроемульсії, що є сумісними з тканиною тіла. Коли похідні рифаміціну формули І поодинці або у суміші чи в асоціації зі сполуками формули Іl або у суміші з іншими активними інгредієнтами застосовують як фармацевтичні до людей та тварин, їх можна давати так або як фармацевтичну композицію, що містить, наприклад, 0,1 - 99,5% (більш переважно, 0,5 - 90%) активного інгредієнту у комбінації з фармацевтично-прийнятним носієм. Незалежно від шляху застосування похідні рифаміціну формули І поодинці або І суміш їх або в асоціації зі сполуками формули Іl або у суміші з іншими активними інгредієнтами, що можна застосовувати у придатній гідратованій формі, та/або заявлені фармацевтичні 10 UA 105775 C2 5 10 15 20 25 30 35 40 45 50 55 60 композиції, формують у фармацевтично-прийнятні форми дозування звичайними способами. Реальні рівні дозування та час застосування активних інгредієнтів у заявлених фармацевтичних композиціях можна варіювати для отримання кількості активного інгредієнту, що є ефективною для досягнення бажаної терапевтичної реакції для певного пацієнта, композиції та режиму застосування, без токсичності для пацієнта. Зразкові межі дозування є 1 - 3000 мг на добу. Кращою дозою заявлених похідних рифаміціну формули І тут є максимум, що пацієнт може зносити без розвинення серйозної побічної дії. В одному втіленні заявлені похідні рифаміціну застосовують при концентрації приблизно 1 мг - 200 мг/кг маси тіла, приблизно 10 - 100 мг/кг або приблизно 40 мг - 80 мг/кг маси тіла. Межі, проміжні стосовно вищенаведених значень є також у рамках винаходу. У комбінації лікування, заявлені сполуки та інші ліки застосовують до ссавців (наприклад, людей, чоловіків або жінок) звичайними способами. Агенти можна застосовувати в одиничній формі дозування або в розділених формах дозування. Ефективні кількості інших терапевтичних агентів є добре відомими. Однак, є добре відомими норми для визначення меж оптимальної ефективної кількості інших терапевтичних агентів. В одному заявленому втіленні, у котрому ще один терапевтичний агент застосовують до тварини, ефективна кількість заявлених сполук є менше, ніж її ефективна кількість у випадку, коли інші терапевтичні агенти не застосовують. В іншому втіленні ефективна кількість звичайного агенту є менше, ніж його ефективна кількість у випадку, коли заявлене не застосовують. У цьому шляху небажану побічну дію, асоційовану з високими дозами будь-якого агенту можна мінімізувати. Інші можливі переваги (у тому числі без обмеження поліпшеного режиму дозування та/або зменшеної вартості ліків) зрозумілі. У різних втіленнях терапевтичні засоби (як-то, профілактичні або терапевтичні агенти) застосовують менше, ніж 5 хвилин нарізно, менше, ніж 30 хвилин нарізно, 1 години нарізно, при приблизно 1 годині нарізно, при приблизно 1 - 2 годин нарізно, при приблизно 2 - 3 годинах нарізно, при приблизно 3 - 4 годинах нарізно, при приблизно 4 - 5 годинах нарізно, при приблизно 5 - 6 годинах нарізно, при приблизно 6 - 7 годинах нарізно, при приблизно 7 - 8 годинах нарізно, при приблизно 8 - 9 годинах нарізно, при приблизно 9 - 10 годинах нарізно, при приблизно 10 - 11 годинах нарізно, при приблизно 11 - 12 годинах нарізно, при приблизно 12 18 годинах нарізно, 18 - 24 годинах нарізно, 24 - 36 годинах нарізно, 36 - 48 годинах нарізно, 48 52 годинах нарізно, 52 - 60 годинах нарізно, 60 - 72 годинах нарізно, 72 - 84 годинах нарізно, 84 96 годинах нарізно, або 96 - 120 годинах нарізно. У кращих втіленнях дві або більше терапії застосовують при візиті пацієнта. У деяких втіленнях одну або більше заявлених сполук та одну або більше інших засобів (якто, профілактичні або терапевтичні агенти) застосовують циклічно. Циклічна терапія охоплює застосування першого засобу (наприклад, першого профілактичного або терапевтичного агенту) протягом часу, а потім застосування другого засобу (наприклад, другого профілактичного або терапевтичного агенту) протягом часу, а потім, необов’язково, застосування третього засобу (наприклад, профілактичного або терапевтичного агенту) протягом часу, та повторення цього застосування, тобто циклу, для зменшення розвинення резистентності до одного засобу, для запобігання або для зменшення побічної дії засобу, та/або для поліпшення ефективності засобу. У деяких втіленнях застосування заявленої сполуки можна повторювати та застосування можуть бути відокремленими проміжками принаймні 1 доба, 2 доби, 3 доби, 5 діб, 10 діб, 15 діб, 30 діб, 45 діб, 2 місяці, 75 діб, 3 місяці, або принаймні 6 місяців. В інших втіленнях застосування того ж засобу (як-то, профілактичного або терапевтичного агенту) іншого, ніж похідні рифаміціну, можна повторювати та застосування можуть бути відокремленими проміжками принаймні 1 доба, 2 доби, 3 доби, 5 діб, 10 діб, 15 діб, 30 діб, 45 діб, 2 місяці, 75 діб, 3 місяці, або принаймні 6 місяців. Певні показання можуть потребувати довшого часу лікування. Наприклад, діарея мандрівників лікування може минути тільки між приблизно 12 - 72 годин, тоді як лікування хвороби Крона може бути між приблизно 1 добою - 3 місяцями. Комплекти є також запропонованими тут, наприклад, комплекти для лікування розладу кишечнику. Комплекти можуть містити, наприклад, одне або більше з групи: похідні рифаміціну поодинці або у суміші чи в асоціації зі сполуками формули Іl або у суміші з іншими активними інгредієнтами та інструкціями для застосування. Інструкції для застосування можуть містити інформацію про прописування, інформацію про дозування, інформацію про зберігання, тощо. Упаковані композиції є запропонованими також, і можуть містити терапевтично ефективну кількість одного або більше з похідних рифаміціну поодинці або в асоціації зі сполуками формули Іl або у суміші з іншими активними інгредієнтами та фармацевтично прийнятними 11 UA 105775 C2 5 10 носіями або розріджувачами, де композицію формують для лікування особи, яка потерпає або схильна до розладу кишечнику, та упаковують з інструкціями для лікування особи, яка потерпає або схильна до розладу кишечнику. Приклад 1 Синтез (12'Z,14'Е,24'Е)-5’,17’,19'-тригідрокси-12'-(гідрокси-метил)-23'-метокси2',4’,16’,18',20',22'-гексаметил-1’,4,6’,11’-тетраоксо-1’,2'-дигідро-6Η-спіро[1,3-діоксолан-2,9'[2,7]епоксипентадека[1,11,13]триєноіміно)нафто[2,1-b]фуран]-21’-іл-ацетату Цей приклад забезпечує один спосіб створення сполуки формули Іl, де R - ацетил, R1 гідроген, R2 - пара-метил, а R3 - гідроксиметил. Культуру Nосаrdіа mеdіtеrrаnеа (АТСС 31064) вирощували протягом 6-8 діб на агарі Бенетта та інкубували при 28 °С. Дві колби Ерленмейєра по 500 мл інокулювали у стерильних умовах, з культурою, отриманою з косого агару. Колби містили 100 мл композиції вегетативного середовища, як описано у таблиці 1. Таблиця 1 Компонент м'ясний екстракт дріжджовий екстракт пептон казеїн гідролізований глюкоза NaCI H2O Кількість 5г 5г 5г 3г 20 г 1.5 г 1 літр 15 20 рН доводили до 7,3 за допомогою 1 М NаОН. Інокульовані колби поміщали на струшувач при 28 °С протягом 72 годин. Вміст двох колб Ерленмейєра застосовували як інокулят виливанням їх у 10-літровий преферментер, що містить 4 літри вищезгаданого вегетативного середовища. Інкубування досліджували при 28 °С з перемішуванням при 300 750 об/хвил та аерацією. Через 48 годин росту було отримано об’єм 7-10 % упакованих клітин. На наступному етапі клітини застосовували як інокулят у 10-літровому скляному ферментері, що містить 4 літри середовища, як описано нижче та у таблиці 2: Таблиця 2 Компонент порошок земляного горіха соєвий порошок (NH4)2SO4 MgSO47H2O глюкоза гліцерин KH2PO4 пропіленгліколь CaCO3 Na дієтилбарбітурат CuSO45H2O FeSO47H2O ZnSO47H2O MnSO47H2O СаСІ27Н2О (ΝΗ4)6Μο7Ο244Η2Ο H2O to 25 Кількість 25 г 5г 9.5 г 0.85 г 95 г 40 г 1г 5т 8.5 г 1.7 г 2.8 мг 8.5 мг 42.5 мг 3.4 мг 1.7 мг 0.85 мг 1 літр рН доводили до 7,8 із NаОН та стерилізували протягом 60 хвилин при 120 °С. Після стерилізації рН був 6,4. Кількість вмісту преферментеру, що дорівнює 5% вмісту ферментеру, застосовували як інокулят. Ферментування досліджували при 28 °С з перемішуванням при 750 12 UA 105775 C2 5 10 15 20 25 30 35 40 45 50 55 60 об/хвил та аерацією. Силікон А застосовували як антиспінювач. Культиваційне середовище набувало характеристичного червоно-коричневого забарвлення при ферментуванні. Через приблизно 200 годин росту було отримано об’єм упакованих клітин. рН середовища був 7,5, та середовище тоді збирали для видалення клітин. Міцелій видаляли фільтруванням та відкидали. Фільтрат доводили до рН 2,0 10% хлоридною кислотою та екстрагували тричі рівним об’ємом етилацетату. Комбіновані екстракти концентрували до сухого стану під вакуумом при 35 °С та залишок розчиняли у 0,005 М натрійфосфатному буфері з рН 7,5. Натрію нітрит додавали до кінцевої концентрації 0,2% і перемішували протягом 30 хвил. При кімнатній температурі буферний розчин екстрагували тричі рівним об’ємом етилацетату. Комбіновані органічні екстракти концентрували до сухого стану під вакуумом при 35 °С. Екстракт очищали, застосовуючи колонкову хроматографію з силікагелем в ізократичних умовах елювання сумішшю розчинників дихлорометан/ метанол у співвідношенні 40/1, лінійною швидкістю 2,65 см/хвил. Отриману сполуку аналізували за допомогою ВЕРХ, застосовуючи колонку Нуреrsіl ОDS, що має параметри 250 мм довжини та 4,4 мм діаметром, елювали в ізократичних умовах сумішшю ацетонітрил/0,025 М Натрію Фосфатний бі-кислотний буфер з рН 7,0, у співвідношенні 1 /1 із швидкістю текучості 1 мл /хвил. Хроматографічну фракцію з чистотою вище, ніж 90%, збирали та розчинник концентрували до сухого стану під вакуумом. Хроматографічний профіль сполуки формули Іl, де R - ацетил, R1 - гідроген, R2 - п-метил, а R3 - гідроксиметил, що охарактеризовано 1 часом утримання (ЧУ) 7,45 хвил., є у Фіг. 1. Сполук ідентифікували за допомогою Н ЯМР та спектр показано у Фіг. 2. Приклад 2. Синтез (16Z,18Е,28Е)-25-(ацетилокси)-5,21,23-тригідрокси-16-(гідроксиметил)-27метокси-2,4,11,20,22,24,26-гептаметил-1,15-діоксо-1,13-дигідро-2Н-2,7(епоксипентадека[1,11,13]триєноіміно)фуро[2",3":7',8']нафто[1’,2’:4,5]імідазо[1,2-а] піридин-8-ій6-олату. Ця сполука є сполукою формули І, де R - ацетил, R1 - гідроген, R2 - п-метил, а R3 гідроксиметил. Розчин 200 мг (12'Z,14'Е,24'Е)-5’,17’,19'-тригідрокси-12'-(гідрокси-метил)-23'метокси-2',4’,16’,18',20',22'-гексаметил-1’,4,6’,11’-тетраоксо-1’,2'-дигідро-6Η-спіро[1,3-діоксолан2,9'-[2,7]епоксипентадека[1,11,13]триєноіміно)нафто[2,1-b]фуран]-21’-іл-ацетату, отриманий, як описано у прикладі 1, розчиняли у 0,6 мл дистильованої води та 0,5 мл етанолу додавали при перемішуванні при кімнатній температурі з 82 мг 2-аміно-4-метил-піридину. Реакційну суміш тримали при 47 °С протягом приблизно 5 годин до повного зникнення реагенту формули Іl за допомогою ВЕРХ як показано у прикладі 1. Розчин доводили до температури довкілля та додавали 5 мг аскорбінової кислоти. Розчин підкислювали до рН 2,0 концентрованою НСl та екстрагували двома аліквотами приблизно по 1,0 мл етилен ацетату. Поєднані органічні фази сушили натрію сульфатом, фільтрували та випарювали до сухого стану. Отриману сполуку аналізували за допомогою ВЕРХ в умовах прикладу 1, охарактеризовано ЧУ оf 6,2 хвил., з чистотою відповідній 95%..а хроматограма є у Фіг. 3. Отриману сполуку 1 13 ідентифікували ФП-ІЧ, Н-ЯМР, С-ЯМР-спектроскопією та молекулярну масу визначали ІЕРМС-спектроскопією. Смуги НР характеристичного поглинання, що спостерігали при нижченаведених частотах (у -1 см ), отримали плівкою NаСІ: 3400, 2972, 2929,6, 1717,7, 1654,3, 1690,0, 1543,6, 1508,5, 1475,7, 1454,5, 1373,8, 1322,9, 1233,4, 1157,3, 1106,4, 1059,7, 1021,5, 974,8, 949,3, 877,2, 800,8, 732,8. Спектр показано у Фіг. 4 та дані є у згоді з гаданими структурами. 1 Піки характеристичного поглинання у спектрі Н-ЯМР спостерігали при нижченаведених -1 значеннях (млн ): 0,34(d,3Н), 0,76(d,3Н), 0,97(d,3Н), 1,27, (m,1 Н) 1,44(m,1 Н), 1,63(m,1 Н), 1,89(s,3Н), 1,99(s,3Н), 2,09(s,3Н), 2,32(m,1 Н), 2,59(s,3Н), 2,91 (m,1 Н), 3,02(s,3Н), 3,37(d,1 Н), 3,73(m,2Н), 3,95(m,2Н), 4,50(d,1 Н), 4,63(d,1 Н), 4,95(d,1 Н), 5,01 (d,1 Н) 1 6,06(d,1 Н), 6,18(d,1 Н), 6,49(d,1 Н), 6,92(d,1 Н), 7,05(d,1 Н), 7,39(s,1 Н), 8,53(d,1 Н), 9,13(s, 1 Н), 14,73(s,1 Н), 1 6,89(s, 1 Н), де S= синглет, d= дублет, m= мультиплет. Спектр показано у Фіг. 5 та дані є у згоді з гаданою структурою. 13 С-ЯМР Піки характеристичного поглинання у спектрі спостерігали при нижченаведених -1 значеннях (млн ): 7,14, 7,47, 8,75, 10,90, 17,25, 20,79, 22,33, 32,81,36,87,38,14, 38,35, 57,24, 65,13, 72,35, 74,31, 77,16, 77,62, 97,51, 103,98, 104,53, 108,43,109,58, 11 1,77, 114,29, 114,29, 114,37, 117,74, 119,09, 122,77, 125,39, 129,26, 139,09, 139,28, 141,15, 144,54, 147,93, 153,59, 1 69,05, 172,08, 172,14, 181,82, 189,19. Спектр показано у Фіг. 6 та дані є у згоді з гаданою структурою. ЕІ-МС: Молекулярну масу визначали з параметрами ІЕР+ та ІЕР-, з капіляром при 3,00 кВ, конусом 25 В та екстрактором 3 кВ. Спектр є у Фіг. 7 та отримана сполука мала молекулярну 13 UA 105775 C2 5 10 масу 801. Приклад 3 Мінімум концентрації активної речовини, здатної інгібувати ріст іn vіtrо патогенної бактерії (МІС) Мінімум концентрації активної речовини, здатної інгібувати ріст іn vіtrо патогенної бактерії (МІС) визначали способом мікророзбавлення як описано у Nаtіоnаl Соmmіttее fоr Сlіnісаl Lаbоrаtоrу Stаndаrds NССLS, 2003 аnd Е. соlі (АТСС 25922), Р. аеrugіnоsа (АТСС 27853), S. аurеus (АТСС 29213), Е. fаесаlіs (АТСС 29212) були контрольним стандартом. Таблиця 3 показує результати мінімуму концентрації інгібування росту іn vіtrо на різних штамах грам-негативних бактерій. Таблиця 4 показує результати мінімуму концентрації інгібування росту іn vіtrо на різних штамах Stарhуlососсus sрр та Еntеrососus sрр. Таблиця 3 Номер 92 94 99 106 109 89 93 95 96 100 101 30-106 107 109 110 112 6-74 6-86 30-111 30-118 30-150 30-123 30-125 88 89 93.1 102 103 166 168 214 30-97 30-85 92 225.2 6-84 355 001 004 359 361.2 6-82 Штам C.freundii C.freundii C.freundii C.freundii C.freundii C.freundii C.freundii C.freundii C.freundii C.freundii C.freundii E.aerogenes E.aerogenes E.aerogenes E.aerogenes E.aerogenes E.cloacae E.cloacae E.cloacae E.cloacae E.cloacae E.cloacae E.cloacae E.cloacae E.cloacae E.cloacae E.cloacae E.cloacae E.cloacae E.cloacae E.cloacae E.cloacae E.cloacae E.cloacae E.cloacae E.cloacae E.coli E.coli E.coli E.coli E.coli E.coli MIC (мг/л) 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 16 32 32 32 32 64 14 UA 105775 C2 Таблиця 3 Номер 30-138 005 006 015 019 144 152 20-120 155 320 324 326 330 332 009 012 013 036 037 055 097 101 104 112 145 6-73 20-124 159 164 312 313 314 416 455 113 120 122 123 124 154 6-56 6-58 6-77 6-85 6-95 20-19 2042 20-133 20-135 20-158 165 169 170 177 Штам E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli Е.coli Е.coli E.coli Е.СОІІ Е.СОІІ E.coli Е.coli Е.coli E.coli Е.coli E.coli E.coli E.coli E.coli Е.coli Е.coli E.coli E.coli Е.coli E.coli Е.coli E.coli E.coli E.coli E.coli E.coli Е.coli E.coli E.coli Е.coli E.coli E.coli E.coli E.coli Е.coli E.coli Е.coli Е.coli E.coli E.coli Е.coli MIC (мг/л) 64 16 16 16 16 16 16 16 16 16 16 16 16 16 32 32 32 32 32 32 32 32 32 32 32 32 32 32 32 32 32 32 32 32 64 64 64 64 64 64 64 64 64 64 64 64 64 64 64 64 64 64 64 64 15 UA 105775 C2 Таблиця 3 Номер 192 369 121 125 30-25 30-143 30-4 30-65 20-161 20-180 201 223 256 421 20-26 20-27 122 288 6-64 6-80 6-101 6-107 6-94 6-62 30-11.1 30-149 30-8 20-22 20-29 20-38 20-39 20-40 20-63 20-102 20-119 20-127 20-156 123 124 137 423 428 132 6-98 6-110 30-69 30-84 30-117 30-128 30-151 30-53 30-26.1 20-21 20-24 Штам E.coli E.coli Е.coli Е.coli Е.coli E.coli Е.coli E.coli E.coli E.coli E.coli Ε.coli Е.соlі Е.coli Е.coli Е.coli E.coli E.coli E.coli E.coli E.coli Е.coli E.coli E.coli Е.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli MIC (мг/л) 64 64 128 128 128 128 128 128 128 128 128 128 128 128 32 32 32 32 64 64 64 64 64 64 64 64 64 64 64 64 64 64 64 64 64 64 64 64 64 64 64 64 128 128 128 128 128 128 128 128 128 128 128 128 16 UA 105775 C2 Таблиця 3 Номер 20-177 20-184 20-185 431 6-99 6-90 30-15 30-110 6 8 9 20-35 3.1 55 7 14 6-78 3.2 65 20 30-87 6-66 20-77 20-126 11 12 63 118 21 28 6-117 30-124 20-189 13 65 46 6-113 53 59 20-157 55 56 57 30-43 30-80 30-20.2 32 33 82 83 30-41 41 42 6-57 Штам E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.coli E.sacazakii E.sacazakii E.sacazakii K.oxytoca K.oxytoca K.oxytoca K.oxytoca K.oxytoca K.oxytoca K.oxytoca K.oxytoca K.oxytoca K.oxytoca K.pneumoniae K.pneumoniae K.pneumoniae K.pneumoniae K.pneumoniae K.pneumoniae K.pneumoniae K.pneumoniae K.pneumoniae K.pneumoniae K.pneumoniae K.pneumoniae K.pneumoniae K.pneumoniae K.pneumoniae M.morganii M.morganii M.morganii M.morganii M.morganii M.morganii M.morganii P.mirabilis P.mirabilis P.mirabilis P.mirabilis P.mirabilis P.mirabilis P.mirabilis P.mirabilis P.mirabilis P.mirabilis P.mirabilis MIC (мг/л) 128 128 128 128 64 64 128 128 128 128 128 64 64 64 64 64 126 126 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 64 64 128 128 128 128 64 128 64 64 64 64 64 128 128 128 128 17 UA 105775 C2 Таблиця 3 Номер 34 35 36 37 38 56 76 77 78 99 30-12 30-76 20-23 20-70 112 ATCC 25922 20-89 96 51 30-49 99 20-64 20-160 20-49 50 7 S g 10 11 12 13 30-94 64 99 30-105 66 79.1 20-149 20-58 78 115 ATCC 27853 Штам P.mirabilis P.mirabilis P.mirabilis P.mirabilis P.mirabilis P.mirabilis S.liquefaciens S.liquefaciens S.liquefaciens S.marcescens S.marcescens S.marcescens S.marcescens S.marcescens S.marcescens Е.coli A.baumannii A.baumannii A.baumannii A.baumannii A.baumannii A.lwoffi A.lwoffi A.xyloxy A.xyloxy P.aeruginosa P.aeruginosa P.aeruginosa P.aeruginosa P.aeruginosa P.aeruginosa P.aeruginosa S.maltophilia S.maltophilia S.maltophilia S.maltophilia S.maltophilia S.maltophilia S.maltophilia S.maltophilia S.maltophilia S.maltophilia P.aeruginosa MIC (мг/л) 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 32 32 32 32 64 64 4 128 128 128 32 32 64 16 64 64 32 64 64 64 128 128 128 64 123 128 128 32 Таблиця 4 Номер 387.2 78 79 387.1 20-13 20-5 90 Штам S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus M.I.C. (мг/л) 0.12 0.25 0.25 0.25 0.25 0.12 0.25 18 UA 105775 C2 Таблиця 4 Номер 91 96 386 388 20-12 20-17 80 93 95 101 111 414 20-9 20-28 81 83 94 394 107 113 411 20-10 20-43 20-44 97 93 30-18 30-83.2 92 99 100 102 103 106 111.3 118 224 377 395 406 20-6 20-117 20-25 20-30 20-34 20-37 20-45 396 20-109 20-31 217 30-104 30-122 30-70 Штам S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus M.I.C. (мг/л) 0.25 0.25 0.25 0.25 0.25 0.25 0.5 0.5 0.5 0.5 0.5 0.5 0.5 0.5 1 1 1 1 1 1 1 1 1 1 0.25 0.25 0.25 0.25 0.5 0.5 0.5 0.5 0.5 0.5 0.5 0.5 0.5 0,5 0.5 0.5 0.5 0.5 0.5 0.5 0.5 0.5 0.5 1 1 1 0.5 0.5 0.5 0.5 19 UA 105775 C2 Таблиця 4 Номер 116 117 119 120 122 124 132 135 209 217 220 30-5 30-6 20-33 30-100 30-101 30-102 30-64 30-67 223 400 402 30-120 30-130 30-133 30-146 30-23 30-48 30-99 30-108 30-142 218 219 403.2 30-119 398 229 230 30-105 30-11.1 30-139 30-156 30-22 30-24 30-27 30-34 30-35 30-40 30-89 30-9.1 300 306 312 325 Штам S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus S.aureus M.I.C. (мг/л) 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 >1 >1 >1 >1 >1 >1 >1 >1 >1 >1 >1 >1 >1 >1 >1 >1 >1 >1 >1 0.25 0.25 0.25 0.5 20 UA 105775 C2 Таблиця 4 Номер 329.2 333 358 376 16 20 20-32 30-16 19 7 9 11 41 42 20-101 20-104 20-18 20-61 20-62 10 20-107 12 30-134 30-75 17 30-54 30-55 30-77 30-90 30-152 13 30-73 30-10 30-148 30-135 30-109 29 36 30-115 37 30-92 30-78 30-154 30-2 30-66 233 258 247 243.1 266 64 75.1 65 69 Штам S.aureus S.aureus S.aureus S.aureus S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.epidermidis S.haemoliticus S.haemoliticus S.haemoliticus S.haemoliticus M.I.C. (мг/л) 0.25 0.25 0.5 0.5 0.06 0.06 0.06 0.06 0.12 0.25 0.25 0.25 0.25 0.25 0.25 0.25 0.25 0.25 0.25 0.5 0.5 0.06 0.06 0.06 0.12 0.12 0.12 0.12 0.12 0.5 1 1 >1 0.5 1 0.25 0.5 0.5 1 1 >1 1 >1 >1 >1 0.06 0,06 0.06 0.06 0.5 0.25 0.25 0.5 0.5 21 UA 105775 C2 Таблиця 4 Номер 74 72 73 178 20-54 129 131 168 30-13 30-93 116.1 133 128 30-114 84 105 90 30-83.1 106.2 83.2 30-81 156 30-129 221 30-153 189.1 159 30-116 146 150 151 162 182 153 30-145 Штам S.haemoliticus S.haemoliticus S.haemoliticus S.haemoliticus S.haemoliticus S.hominis S.hominis S.hominis S.hominis S.hominis S.hominis S.hominis S.hominis S.hominis S.intermedius S.intermedius S.intermedius S.intermedius S.intermedius S.intermedius S.warneri S.warneri S.warneri S.warneri S.warneri S.warneri S.warneri S.warneri S.warneri S.warneri S.warneri S.warneri S.warneri S.warneri S.warneri M.I.C. (мг/л) 0.5 1 1 1 1 0.25 0.25 0.25 0.5 0.12 0.25 0.25 0.5 1 1 1 >1 >1 1 >1 0.12 0.25 0.12 0.5 0.5 1 0.5 1 1 1 1 1 1 >1 >1 АТСС29213 09-85 035-52 80 81 035-63 035-65 035-78 09-35 035-125 82 88 91 173 188 218 219 035-58 S.aureus E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis 0.5 4 128 32 32 64 64 64 64 64 64 64 64 64 64 64 64 128 22 UA 105775 C2 Таблиця 4 Номер 035-116.2 035-20.3 87 89 90 035-96 92 94 09-7 09-21 93 09-75 09-94 035-128.1 035-136 126 127 128 158 09-72 169 09-79 172 166 3.2 321 322 304 307 309 322 337 335 144 035-35 035-45.2 035-8.2 100 106 09-86 99 136 141 09-68 035-106 112 117 035-97 126 138 169 188 197.2 206 Штам E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecalis E.faecium E.faecium E.faecium E.faecium E.faecium E.faecium E.faecium E.faecium E.faecium E.faecium E.faecium E.faecium E.faecium E.faecium E.faecium E.faecium E.faecium E.faecium E.faecium E.faecium M.I.C. (мг/л) 128 128 128 128 128 64 64 64 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 128 64 64 64 128 128 64 64 128 128 128 64 128 64 64 64 64 64 128 23 UA 105775 C2 Таблиця 4 Номер 5 10 15 20 25 30 35 40 45 50 55 Штам ATCC 29212 M.I.C. (мг/л) 64 Приклад 4 Застосування (16Z,18Е,28Е)-25-(ацетилокси)-5,21,23-тригідрокси-16-(гідроксиметил)-27метокси-2,4,11,20,22,24,26-гептаметил-1,15-діоксо-1,13-дигідро-2Н-2,7(епоксипентадека[1,11,13]триєноіміно)фуро[2",3":7',8'] при бактеріальній інфекції Ідентифікують пацієнта, який потерпає від бактеріальної інфекції. Фармацевтичну композицію, що містить (16Z,18Е,28Е)-25-(ацетилокси)-5,21,23-тригідрокси-16-(гідроксиметил)27-метокси-2,4,11,20,22,24,26-гептаметил-1,15-діоксо-1,13-дигідро-2Н-2,7(епоксипентадека[1,11,13]триєноіміно)фуро[2",3":7',8']нафто[1’,2’:4,5]імідазо[1,2-а] піридин-8-ій6-олат (Сполука І, де R - ацетил, R1 - гідроген, R2 метил, а R3 - гідроксиметил) застосовують до пацієнта. Після 10 доби перебігу лікування, застосовуючи вищенаведену композицію, рівень бактеріальної інфекції у пацієнта є зменшеним. Приклад 5 Синтез похідного формули І Альтернативні сполуки формули І синтезують нижченаведеним способом. Зокрема, це спосіб застосовують для отримання сполуки формули І, де R - ацетил, R1 - (С1-4) алкіл, бензилокси, моно-та ді-(С1-3) алкіламіно (С1-4) алкіл, (С1-3) алкокси-(С1-4) алкіл, гідрокси-метил, гідрокси-(С2-4)-алкіл та нітро, а R2 - (С1- 4) алкіл, бензилокси, моно-та ді-(С1-3) алкіламіно (С1-4) алкіл, (С1-3) алкокси-(С1-4)алкіл, гідрокси-метил, гідрокси-(С2-4)-алкіл та нітро, або R1 та R2, разом з двома послідовними атомами карбону, піридинового ядра утворюють бензенове кільце, незаміщене, моно-заміщене або ді-заміщене метилом або етилом, а R3 - гідроксіетил, гідроксипропіл або гідроксибутил. Розчин 200 мг формули ІІ, отриманий по суті, як розкрито у прикладі 1, розчиняють у 0,6 мл дистильованої води та додають при перемішуванні 0,5 мл етанолу при кімнатній температурі з 82 мг 2-аміно-піридину формули ІІІ, заміщеного одним або двома з нижченаведених замісників у позиції R1 або R2: (С1-4) алкіл, бензилокси, моно-та ді-(С1-3) алкіламіно (С1-4) алкіл, (С1-3) алкокси(С1-4)алкіл, гідрокси-метил, гідрокси-(С2-4)-алкіл, та нітро, а R2 - (С1-4) алкіл, бензилокси, моно-та ді-(С1-3) алкіламіно (С1-4) алкіл, (С1-3) алкокси-(С1-4)алкіл, гідрокси-метил, гідрокси-(С2-4)-алкіл, та нітро, або заміщені так, що R1 та R2, разом з двома послідовними атомами карбону, піридинового ядра, утворюють бензенове кільце, незаміщене, моно-заміщене або ді-заміщене метилом або етилом. Реакційну суміш тримають при температура 47°С протягом приблизно 5 годин до зникнення реагенту формули Іl аналізом НРLА, як показано у прикладі 1. Розчин доводять до температури довкілля та додають 5 мг аскорбінової кислоти. Розчин підкислюють до рН 2,0 концентрованою НСl та тоді розчин екстрагують двома аліквотами приблизно по 1,0 мл етилен ацетату. Поєднані органічні фази сушать натрію сульфатом, фільтрують та випарюють до сухого стану. Отриману сполуку охарактеризовано ВЕРХ, як описано у прикладі 1. Отриману сполуку формули І, після закінчення реакції, охарактеризовано ЧУ. Отриману 1 13 сполуку ідентифікують ФП-ІЧ, Н-ЯМР, С-ЯМР-спектроскопією та молекулярну масу визначають ІЕР-МС-спектроскопією. Приклад 6 Синтез похідного формули І Альтернативні сполуки формули І отримують нижченаведеним способом. Зокрема, цей спосіб застосовують для отримання сполуки формули І 1, де R - ацетил, R1- (С1-4) алкіл, бензилокси, моно-та ді-(С1-3) алкіламіно (С1-4) алкіл, (С1-3) алкокси-(С1-4)алкіл, гідрокси-метил, гідрокси-(С2-4)-алкіл та нітро, а R2 - (С1-4) алкіл, бензилокси, моно-та ді-(С1-3) алкіламіно (С1-4) алкіл, (С1-3) алкокси-(С1-4) алкіл, гідрокси-метил, гідрокси-(С2-4)-алкіл та нітро, або R1 та R2, разом з двома послідовними атомами карбону, піридинового ядра утворюють бензенове кільце, незаміщене, моно-заміщене або ді-заміщене метилом або етилом, а R3 - гідроксіетил, гідроксипропіл або гідроксибутил. Культуру Nосаrdіа mеdіtеrrаnеа (АТСС 31064) вирощують протягом 6-8 діб на агарі Бенетта та інкубують при 28 °С. З культурою, отриманою з косого агару, дві колби Ерленмейєра на 500 мл інокулюють у стерильних умовах. Колби містять 100 мл композиції вегетативного середовища, як описано у таблиці 1 у прикладі. рН доводять до 7,3 1 М NаОН. Інокульовані колби поміщають на струшувач при 28 °С на 72 години. Вміст двох колб Ерленмейєра застосовують як інокулят виливанням їх у 10-літровий преферментер, що містить 4 літри вищезгаданого вегетативного середовища. Інкубування 24 UA 105775 C2 5 10 15 20 25 проводять при 28 °С з перемішуванням при 750 об/хвил та аерацією. Після 48 годин росту отримують об’єм 7-10 % упакованих клітин. На наступному етапі клітини застосовують як інокулят у 10-літровому скляному ферментері, що містить 4 літри середовища, як описано нижче та у таблиці 2 у прикладі 1. рН доводять до 7,8 NаОН та стерилізують протягом 60 хвилинпри 120 °С. Після стерилізації рН є 6,4. Кількість вмісту преферментеру, що дорівнює 5% вмісту ферментеру, застосовують як інокулят. Ферментування проводять при 28 °С з перемішуванням 750 об/хвил та аерацією. Силікон А застосовують як антиспінювач. Культиваційне середовище набуває характеристичного червоно-коричневого забарвлення при ферментуванні. Через приблизно 200 годин росту отримують масу упакованих клітин. рН середовища 7,5, та середовище тоді збирають для видалення клітин. Міцелій видаляють фільтруванням та відкидають. Фільтрат доводять до рН 2,0 10% хлоридною кислотою та екстрагують тричі рівним об’ємом етилацетату. Комбіновані екстракти концентрують до сухого стану під вакуумом при 35 °С та залишок розчиняють у 0,005 М натрійфосфатному буфері з рН 7,5. Натрію нітрит додають до кінцевої концентрації 0,2%. Після перемішування протягом 30 хвил. при кімнатній температурі буферний розчин екстрагують тричі рівним об’ємом етилацетату. Комбіновані органічні екстракти концентрують до сухого стану під вакуумом при 35 °С. Екстракт очищають, застосовуючи колонкову хроматографію з силікагелем як у прикладі 1. Отриману сполуку, що має ЧУ 7,45 хвил, розчиняють у 0,6 мл дистильованої води та додають при перемішуванні 0,5 мл етанолу при кімнатній температурі з 82 мг 2-аміно-4-метилпіридину. Реакційну суміш тримають при 47 °С протягом приблизно 5 годин до повного зникнення реагенту формули Іl за допомогою ВЕРХ як показано у прикладі 1. Розчин доводять до температури довкілля та додають 5 мг аскорбінової кислоти. Розчин підкислюють до рН 2,0 концентрованою НСl і розчин екстрагують двома аліквотами приблизно по 1,0 мл етилен ацетату. Поєднані органічні фази сушать натрію сульфатом, фільтрують та випарюють до сухого стану. Отриману сполуку аналізують за допомогою ВЕРХ як у прикладі 1, її охарактеризовано ЧУ 6,2 хвил., з чистотою, відповідною 95%. 30 ФОРМУЛА ВИНАХОДУ 1. Сполука формули І CH3 R O OH OH H3C CH3 OH O CH3 CH3 O H3C H N R3 N+ O O CH3 35 40 45 O O R2 N H R1 ,І де: R являє собою гідроген або ацетил, R1 та R2, кожний незалежно, вибрані з групи: гідроген, (С1-4)алкіл, бензилокси, моно- або ді-(С13)алкіламіно(С1-4)алкіл, (С 1-3)алкоксі-(С1-4)алкіл, гідроксиметил, гідроксі-(С2-4)алкіл та нітро; або R1 та R2, разом з двома послідовними атомами карбону піридинового кільця утворюють бензольне кільце, незаміщене або моно- чи дизаміщене одним або двома метилами або етилами; a R3 являє собою гідроксіалкіл(С1-4). 2. Сполука за п. 1, в якій R являє собою ацетил, R1 та R2, незалежно, являють собою гідроген або метил, а R3 є гідроксіалкіл(С1-4). 3. Сполука за п. 2, в якій R являє собою ацетил, R1 - гідроген, R2 - п-метил, a R3 - гідроксиметил, що має назву (16Z,18Е,28Е)-25-(ацетилокси)-5,21,23-тригідрокси-16-(гідроксиметил)-27-метокси 25 UA 105775 C2 2,4,11,20,22,24,26-гептаметил-1,15-діоксо-1,13-дигідро-2Н-2,7(епоксипентадека[1,11,13]триєноіміно)фуро[2",3":7',8']нафто[1',2':4,5]імідазо[1,2-а]піридин-8-ій-6олат. 4. Спосіб одержання сполуки формули II CH3 R O OH OH H3C CH3 CH3 CH3 OH O H H3C O N R3 O O O O 5 10 CH3 O O O , II де отримують біологічну культуру, що містить мікроорганізм, вибраний з Streptomyces mediterranei або Nocardia mediterranea, у водному розчині, для продукування похідних рифаміцину В, та поживні речовини; окислюють отриману культуру окисником; де R являє собою гідроген або ацетил, a R3 - гідроксіалкіл(С1-4). 5. Спосіб за п. 4, де окисник є вибраним з одного або більше з групи: нітрит натрію, водний розчин дихромату калію, персульфату амонію або перйодату натрію. 6. Спосіб за п. 4, де R являє собою гідроген або ацетил, a R3 - гідроксіалкіл(С1-4). 7. Спосіб за п. 6, де R являє собою ацетил, a R3 - гідроксиметил. 8. Спосіб одержання сполуки за п. 1, де сполуку формули ІІ CH3 R O OH OH H3C CH3 OH O CH3 CH3 O H H3C N R3 O O O O 15 CH3 O O O , II де R являє собою гідроген або ацетил, a R3 - гідроксіалкіл(С1-4), піддають реакції зі сполукою формули III: N NH2 R2 R1 20 25 , III де R1 та R2, кожний незалежно, вибрані з групи: гідроген, (С1-4)алкіл, бензилокси, моно- або ді(С1-3)алкіламіно(С1-4)алкіл, (С1-3)алкоксі-(С1-4)алкіл, гідроксиметил, гідроксі-(С2-4)алкіл та нітро; або R1 та R2, разом з двома послідовними атомами карбону піридинового кільця, утворюють бензольне кільце, незаміщене або моно- або дизаміщене одним або двома метилами або етилами, у присутності органічного розчинника, суміші більше ніж одного органічного розчинника, або суміші органічного розчинника з водою, при температурі в межах від кімнатної температури до 60 °C, протягом 1-100 годин. 26 UA 105775 C2 5 10 15 20 25 30 9. Спосіб за п. 8, де органічний розчинник є вибраним із групи: ароматичні вуглеводні, аліфатичний алканол, галогеновані вуглеводні, нижчий алкіл-естер нижчої аліфатичної кислоти, гліколі, ацетонітрил, діоксан, тетрагідрофуран та їх комбінація або суміш з водою у різних об'ємних співвідношеннях. 10. Спосіб за п. 8, де для кожного молярного еквівалента сполуки формули II застосовують приблизно 0,1-1 молярний еквівалент йоду або комбінації йод/окисник. 11. Спосіб за п. 8, де сполукою формули III є 2-аміно-4-метилпіридин. 12. Спосіб одержання сполуки за п. 1, де отримують біологічну культуру, що містить мікроорганізм, такий як Nocardia mediterranea, у водному розчині, та поживні речовини; та окиснюють отриману культуру окисником для отримання окисненого продукту; піддають реакції окиснений продукт з похідним 2-амінопіридину. 13. Фармацевтична композиція, яка містить терапевтично ефективну кількість сполуки формули І у комбінації з одним або більше фармацевтично прийнятними інгредієнтами. 14. Фармацевтична композиція за п. 13 для застосування як антибактеріальної. 15. Фармацевтична композиція, яка містить одну або більше сполук формули І, або одну або більше сполук формули І у комбінації з однією або більше сполуками формули II, та фармацевтично прийнятний наповнювач. 16. Фармацевтична композиція за п. 15, де композиція має форму, придатну для застосування у одиничній або у розділеній формі дозування. 17. Фармацевтична композиція за п. 15, яка додатково містить похідне рифаміцину або неоміціну. 18. Фармацевтична композиція за п. 17, в якій похідним рифаміцину є рифаксимін. 19. Фармацевтична композиція за п. 18, в якій сполука формули І знаходиться у співвідношенні приблизно 0,01-100 мас. % відносно рифаксиміну. 20. Фармацевтична композиція за п. 15, необов'язково разом з одним або більше додатковими антибіотиками, для застосування у способі лікування, запобігання або пом'якшення розростання бактерій у пацієнта, який страждає від пов'язаного з кишечником розладу. 21. Фармацевтична композиція за п. 20, в якій одним або більше додатковими антибіотиками є один або більше вибраних з групи: рифаміцин, рифаксимін або неоміцин. 22. Фармацевтична композиція за п. 20, в якій пов'язаний з кишечником розлад є одним або більше з групи: синдром подразненого кишечнику, діарея мандрівників, розростання бактерій у тонкому кишечнику, хвороба Крона, хронічний панкреатит, недостатність підшлункової залози, печінкова енцефалопатія, дивертикуліт, ентерит або коліт. 27 UA 105775 C2 28
ДивитисяДодаткова інформація
Назва патенту англійськоюRifamycin derivatives
Автори англійськоюViscomi, Giuseppe Claudio, Campana, Manuela, Folegatti, Mahena, Cannata, Vincenzo, Righi, Paolo, Rosini, Goffredo
Автори російськоюВискоми Джузеппе Клаудио, Кампана Мануэла, Фолегатти Маена, Канната Винченцо, Риджги Паоло, Росини Джоффредо
МПК / Мітки
МПК: A61K 31/357, A61P 31/00, C07D 493/20, C07D 498/22, A61K 31/437
Мітки: рифаміцину, похідні
Код посилання
<a href="https://ua.patents.su/32-105775-pokhidni-rifamicinu.html" target="_blank" rel="follow" title="База патентів України">Похідні рифаміцину</a>
Попередній патент: Просочування емульсією
Наступний патент: Композиція для контролю розвитку рослин
Випадковий патент: Камера збірна одностороннього обслуговування типу ксо-393-18 в