Аналоги хіназоліну як інгібітори рецепторних тирозинкіназ
Номер патенту: 90659
Опубліковано: 25.05.2010
Автори: Бакмельтер Александр, Ліссікатос Джозеф, Топалов Георгій, Уоллейс Елі, Чжао Цян
Формула / Реферат
1. Сполука формули І, вибрана з структур:
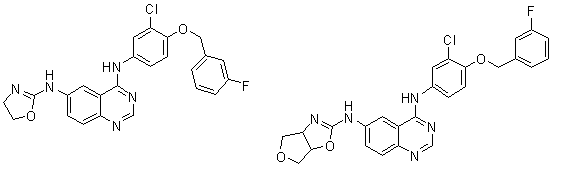
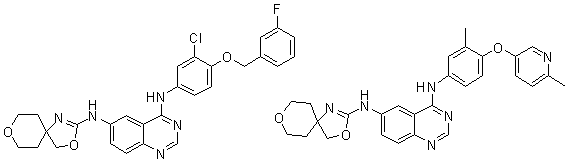
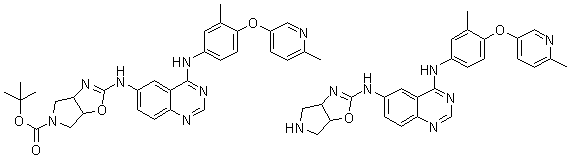
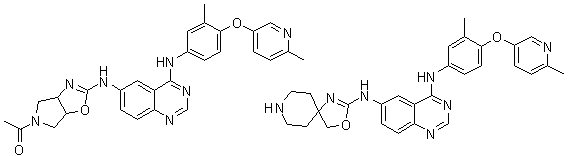
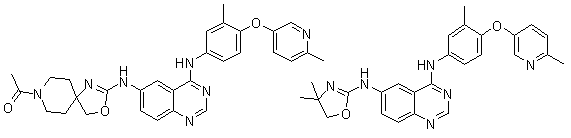
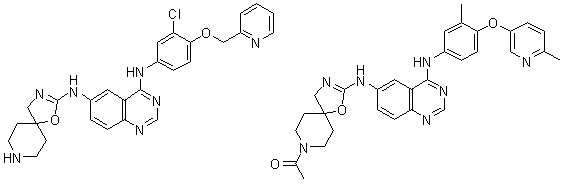
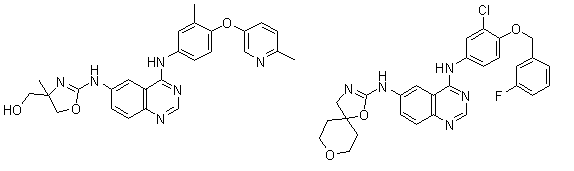
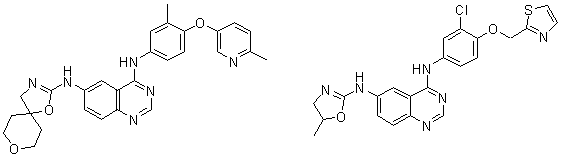
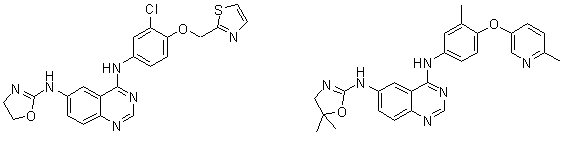
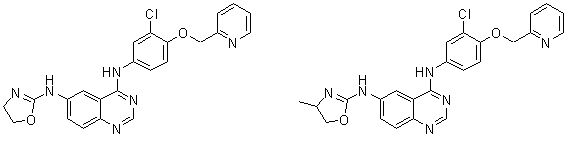
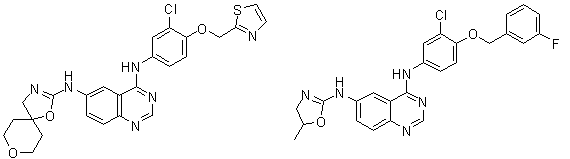
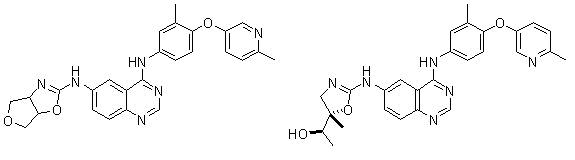
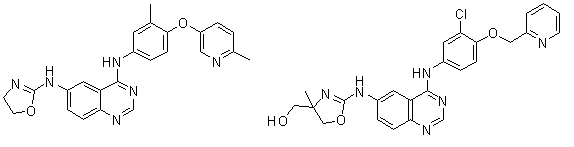
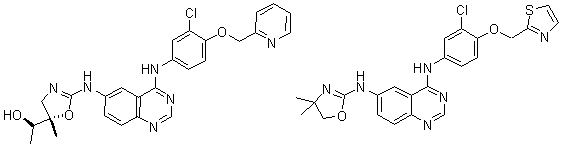
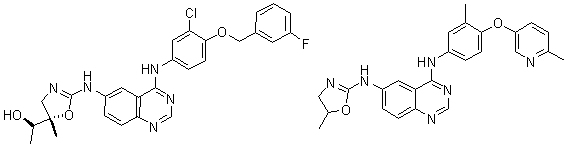
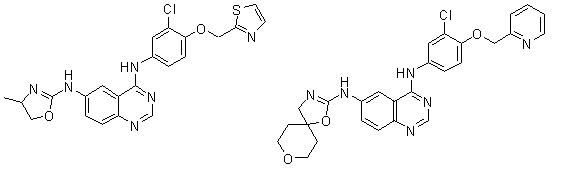
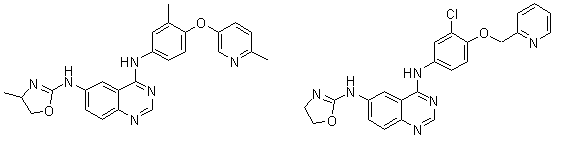
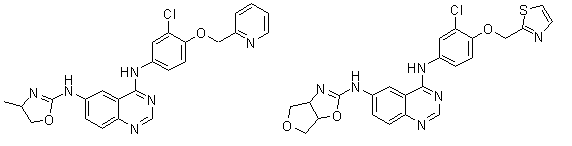
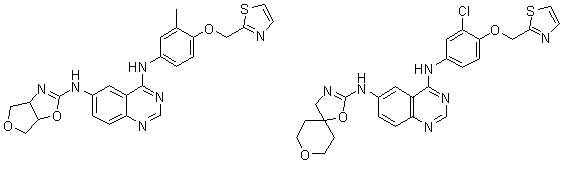
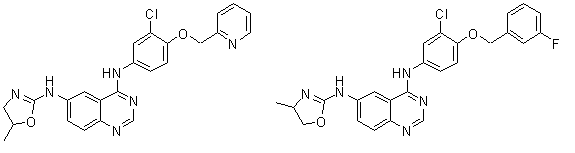
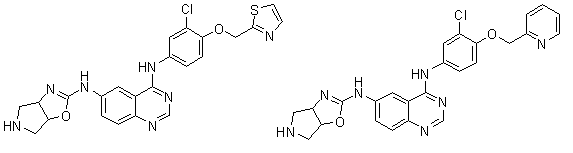
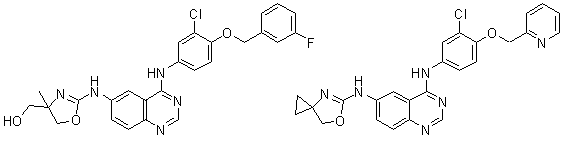
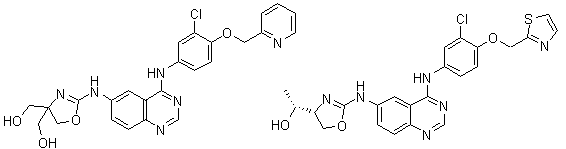
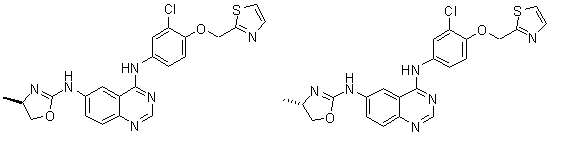
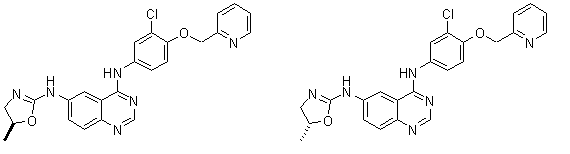
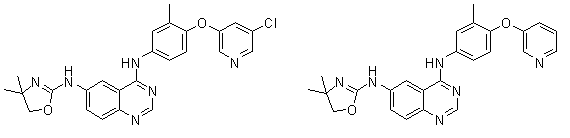
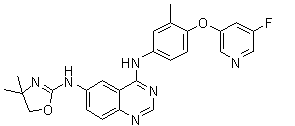
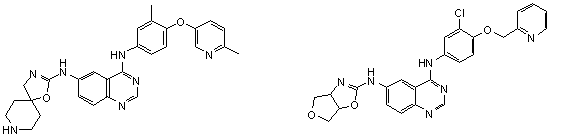
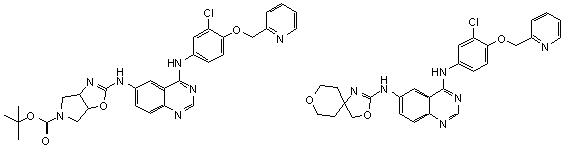
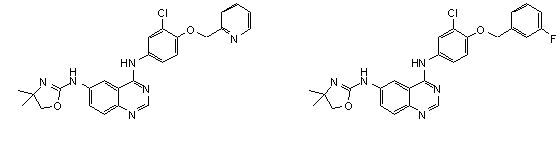
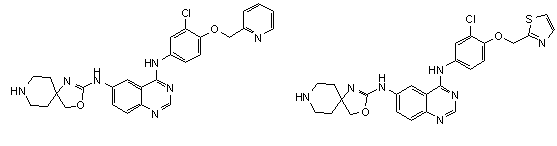
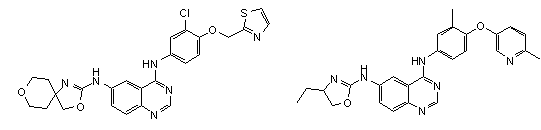
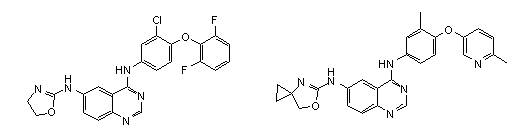
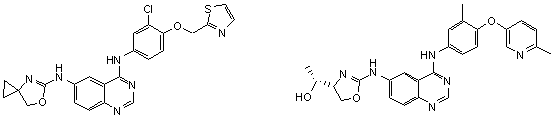
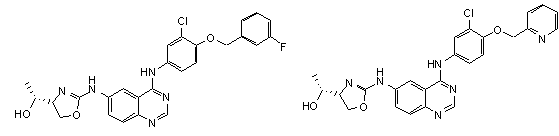
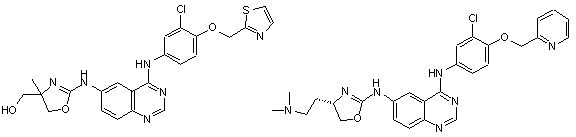
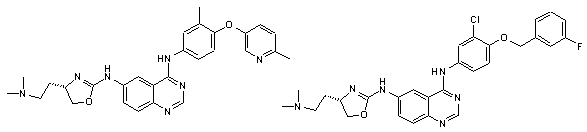
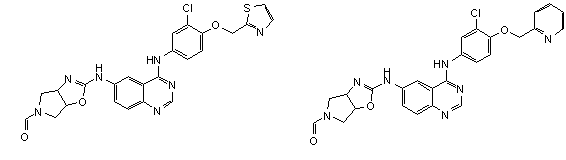
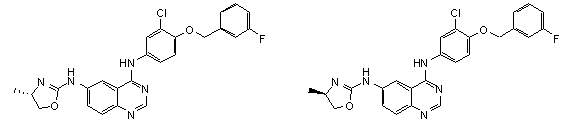
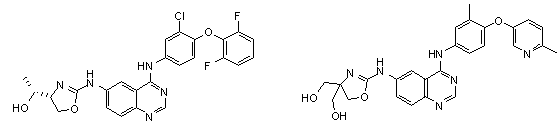
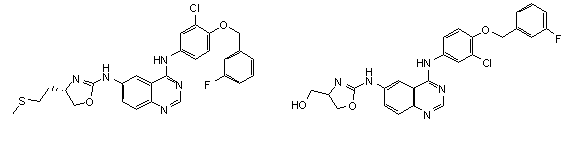
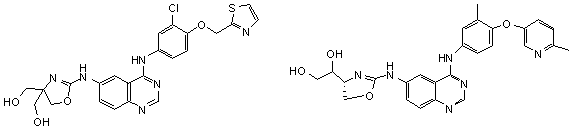
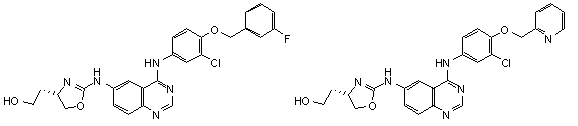
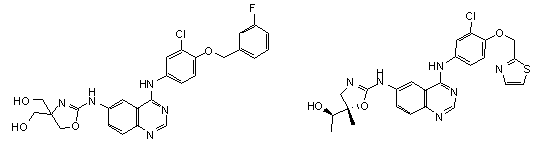
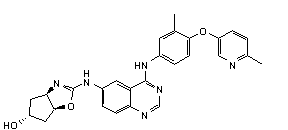
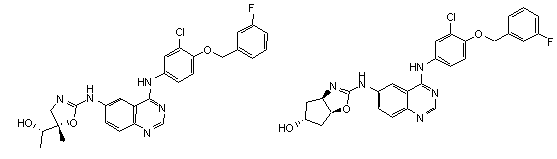
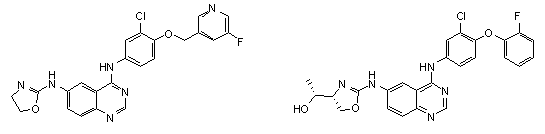
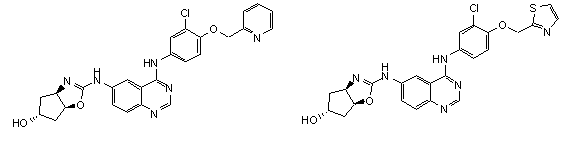
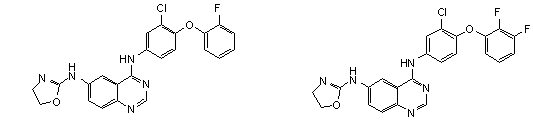
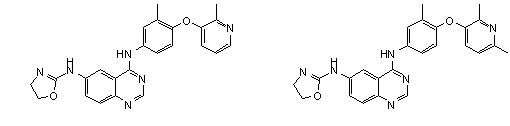
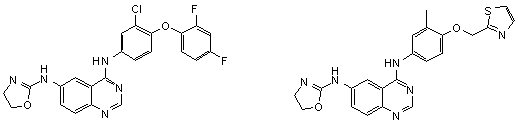
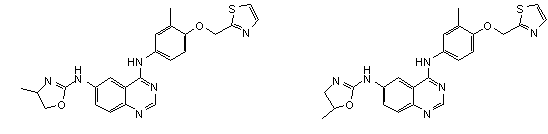
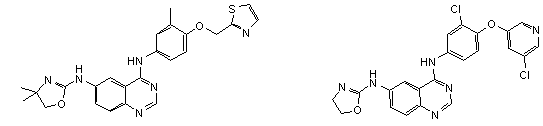
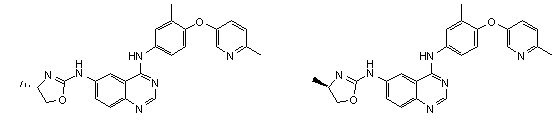
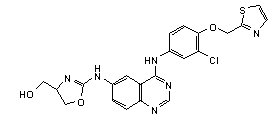 .
.
2. Сполука, яка має структуру:
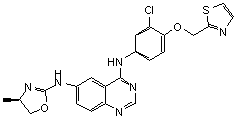 ,
,
та її фармацевтично прийнятні солі.
3. Спосіб лікування раку голови і шиї, легені, грудей, ободової кишки або шлунка у ссавця, який включає введення ссавцю терапевтично ефективної кількості сполуки, визначеної у п. 2.
4. Застосування сполуки за п. 2 для виробництва лікарського засобу для лікування раку голови і шиї, легені, грудей, ободової кишки або шлунка.
5. Фармацевтична композиція, яка містить сполуку формули І, визначену в п. 2, або її фармацевтично прийнятну сіль і її фармацевтично прийнятний розріджувач або носій.
Текст
1. Сполука формули І, вибрана з структур: HN N N N 3 Cl S N O N Cl O O HN H N N N O Cl O O N HN H N N HO N HO N Cl O N N O HO O O F N S H N N O N N N O N O N O N O H N N N H N N O O N N Cl HN O N Cl H N N O O Cl H N N HN O HN N N H N N O O N N N S O N N HN F N HN N HN Cl S O O N N N O N H N HN HN H N N N N N O HN O H N S O N Cl O N Cl O O H N N S N Cl N O N O F HN H N N N N HN H N O N HN H N N O N Cl O Cl N N Cl N N N O N S HN H N N O N N HN O N O O O N O N HN O O O S N HN H N N Cl N HN H N N N Cl O Cl O Cl N HN N N O N O O N HN H N N N HN H N N N N O Cl O O HN H N N N Cl O N O HN N N O N N F HN H N N HN H N N N N N O N O O HN H N N Cl N H N O N N O N HN O Cl HN N N H N N N O O N HN H N N Cl N N HN O N O N O O N N HN H N N N O Cl HO HN H N N N O O N N HN H N N N H N O O N N Cl S N HN H N N N O Cl Cl N HN H N N N N S O N O Cl O Cl N HN H N N N O HO N HN H N N N N S O O HN H N N N O OH Cl N HN H N N N O S O N HN H N N N O N N HO HN N O N N HN H N N N O HO N O F HN H N N N O Cl O F HN H N N N O Cl O N HN H N 4 Cl O N 90659 N O N HN H N N HN O N N N N N 5 Cl 90659 F O O HN H N N F N O HN H N N HO O F Cl O HO HN H N N N N N Cl HN HO H N N N N N Cl H N N N O N HN N O HO N N Cl Cl O HN H N N N HN N O N O N N O Cl N O N F HN H N N N O N F O HN H N N N O F O N HN H N N N O N N HO Cl O HN O Cl N HN H N N N HO N H N N O N N HN H N N N S O N H N N N Cl N F N S O O Cl O F O F HN H N N N O N O N HN H N O N HO Cl O N O O Cl N F HN H N N N N S O N HO HN H N N N O O O N F HN Cl Cl O O HO N Cl N O O Cl HN H N N O F N O Cl N Cl F N O N N HN H N N N O N O N HN H N N HN H N N F O N Cl O N F S O O O N O HO HN H N N F O H N N N HN HN H N N N O HO N O N H N N HO N HN H N N N O N N S O OH HO O N HN H N N N H N N N O H N N Cl N O N OH N O O H N N HO HN O F Cl HO O HN H N N N Cl HO N O S O H N OHO HN HN H N N O N N N N N N H N S N HO O HN N Cl N N HN . N N N O N N N O N O O HO O H N N N Cl Cl HN N N F H N H N N O HN N O N N N HN N O N N Cl N HN O O N O N N HN H N N N O N HN H N N Cl S O N F S O HO HN H N N F Cl O O HN O N S O N N O N Cl S HN H N N N OH N F H N N HO N N HO N N O N N H N N O N N H N N HN O HN N S O H N O N N N Cl N HN H N N O 6 O 7 90659 2. Сполука, яка має структуру: Cl S O N HN H N N O N N , та її фармацевтично прийнятні солі. 3. Спосіб лікування раку голови і шиї, легені, грудей, ободової кишки або шлунка у ссавця, який Дана заявка являє собою частково продовжуючу заявку заявки на видачу патенту США з серійним номером 10/642,440, поданої 14 серпня 2003 року, і запитує пріоритет до попередньої заявки США № 60/551,718, поданої 10 березня 2004 року, кожна з яких особливо включена в даний опис за допомогою посилання у всій своїй повноті. Даний винахід відноситься до нових інгібіторів рецепторних тирозинкіназ типу І і пов'язаних кіназ, фармацевтичних композицій, які містять інгібітори і способів одержання цих інгібіторів. Інгібітори є корисними для лікування гіперпроліферативних захворювань, таких як рак і запалення, у ссавців і особливо у людей. Сімейство рецепторних тирозинкіназ типу І складається з чотирьох тісно пов'язаних рецепторів: EGFR (ErbB1 або HER1), ErbB2 (HER2), ErbB3 (HER) і ErbB4 (HER4) (Reviewed in Riese and Stem, Bioessays (1998) 20:41-48, Olayioye et al. EMBO Journal (2000) 19:3159-3167 and Schlessinger, Cell (2002) 110:669-672). Вони являють собою однопрохідні трансмембранні глікопротеїнові рецептори, які містять позаклітинну ділянку зв'язування лігандів і внутрішньоклітинний сигнальний домен. Крім того, всі рецептори містять внутрішньоклітинний активний тирозинкіназний домен, за винятком ErbB3, кіназий домен якого не проявляє ензиматичної активності. Ці рецептори передають позаклітинні сигнали через цитозоль до ядра при активації. Процес активації ініціюється зв'язуванням ліганду до позаклітинного домену рецептора одним з множини різних гормонів. При зв’язуванні ліганду, гомо- або гетеродимеризація індукується, що приводить до активації тирозинкіназних доменів і фосфорилювання тирозинів на внутрішньоклітинних сигнальних доменах. Оскільки жоден відомий ліганд для ErbB2 не був описаний і ErbB3 не достає активного кіназного домену, ці рецептори повинні гетеродимеризувати, щоб викликати відповідь. Фосфотирозини потім залучають необхідні кофактори, щоб ініціювати декілька різних сигнальних каскадів, включаючи ras/raf/MEK/MAPK і шляхи РІ3K/АKТ. Точний сигнал, який викликається, залежатиме від того, на чому присутні ліганди, оскільки внутрішньоклітинні сигнальні домени відрізняються відносно того, які шляхи активуються. Ці сигнальні шляхи ведуть як до клітинної проліферації, так і до клітинного виживання через інгібування апоптозу. Деякі дослідники продемонстрували роль EGFR і ErbB2 в розвитку і раку (Reviewed in 8 включає введення ссавцю терапевтично ефективної кількості сполуки, визначеної у п.2. 4. Застосування сполуки за п.2 для виробництва лікарського засобу для лікування раку голови і шиї, легені, грудей, ободової кишки або шлунка. 5. Фармацевтична композиція, яка містить сполуку формули І, визначену в п.2, або її фармацевтично прийнятну сіль і її фармацевтично прийнятний розріджувач або носій. Salomon, et al., Crit. Rev. Oncol. Hematol, (1995) 19:183-232, Klapper, et al., Adv. Cancer Res. (2000) 77, 25-79 and Hynes and Stern, Biochim. Biophys. Ada (1994) 1198:165-184). Сквамозні карциноми голови і шиї, і легень проявляють високі рівні EGFR. Також, особливо активний EGFR був знайдений у гліомах, раку молочної залози і раку легень. ErbB2 надекспресія виникає у приблизно 30% випадків всього раку молочної залози. Вона також була залучена в інші раки людини, включаючи рак ободової кишки, яєчника, міхура, шлунку, стравоходу, легені, матки і простати. ErbB2 надекспресія також співвідноситься з поганим прогнозом в раку людини, включаючи метастаз, і ранній рецидив. Сімейство рецепторних тирозинкіназ типу І було активною галуззю протиракового дослідження (Reviewed in Mendelsohn and Baselga, Oncogene (2000) 19:6550-6565 and Normarmo et al, EndocrineRelated Cancer (2003) 30:1-21). Декілька інгібіторів EGFR і ErbB2 сигнальних шляхів продемонстрували клінічну ефективність у лікуванні раку. Герцептин, гуманізована версія моноклонального антитіла анти-ErbB2, була схвалена для використання при раку молочної залози у Сполучених Штатах в 1998 році. Iressa і Tarceva являють собою інгібітори невеликої молекули EGFR, які, як очікується, є комерційно доступними. Крім того, різні інші антитіла і невеликі молекули, які націлюють затримання сигнальних шляхів рецептора тирозинкінази типу І знаходяться у клінічному та передклінічному розвитку. Наприклад, ІМС-225, який являє собою гуманізоване антитіло проти позаклітинного домену EGFR, продемонстрував ефективність і мабуть буде схвалений. Даний винахід забезпечує сполуки, способи одержання цих сполук і фармацевтичні композиції, які містять сполуки, які інгібують рецепторні тирозинкінази типу І. Такі сполуки, загалом надалі названі аналоги хіназоліну, володіють корисністю як терапевтичні агенти для захворювань, які можуть лікуватись інгібуванням рецепторних тирозинкіназ типу І. Вони можуть також діяти як інгібітори серину, треоніну і як інгібітори кіназ подвійної специфічності. Загалом, винахід відноситься до похідних хіназоліну загальної Формули І: 9 в якій А прикріплений до щонайменше одного з вуглеців у положеннях 5, 6, 7 або 8 біциклічного кільця і в якій біциклічне кільце заміщене жодною, однією або двома незалежними групами R3; X являє собою N, СН, CF або C-CN; А являє собою Q або Z; Q являє собою R1 являє собою заміщену або незаміщену, моноциклічну або біциклічну, арильну або гетероарильну частину, R2 являє собою Η або заміщений або незаміщений C1-8алкіл, аліл, заміщений бензил; RJ являє собою водень, галоген, ціано, нітро, С1-С10алкіл, С2-С10алкеніл, С2-С10алкініл, С3С10циклоалкіл, С3-С10циклоалкілалкіл, арил, арилалкіл, гетероарил, гетероарилалкіл, гетероцикліл, частково ненасичений гетероцикліл, гетероциклілалкіл, -NR4SO2R5, -SO2NR6R4, -C(O)R6, -C(O)OR6, -OC(O)R6, -NR4C(O)OR5, -NR4C(O)R6, -C(O)NR4R6, NR4R6, -NR4C(O)NR4R6, -OR6, -S(O)R5, -SO2R5, або SR6, де згаданий алкіл, алкеніл, алкініл, циклоалкіл, циклоалкілалкіл, арил, арилалкіл, гетероарил, гетероарилалкіл, гетероцикліл, частково ненасичений гетероцикліл, і гетероциклілалкіл необов'язково заміщений від однієї до п'яти групами, які незалежно вибирають з групи, яка складається з оксо, галогену, С1-С10алкілу, С2-С10алкенілу, С2С10алкінілу, С3-С10циклоалкілу, С3С10циклоалкілалкілу, ціано, нітро, трифторметилу, дифторметокси, трифторметокси, азидо, NR4SO2R5, -SO2NR6R4, -C(O)R6, -C(O)OR6, OC(O)R6, -NR4C(O)OR5, -NR4C(O)CR6, -C(O)NR4R6, -NR4R6, -NR4C(O)NR4R6, -NR4C(NCN)NR4R6, -OR6, S(O)R5, -SO2R5, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу; R10 являє собою водень, галоген, ціано, нітро, С1-С10алкіл, С2-С10алкеніл, С2-С10алкініл, С3С10циклоалкіл, С3-С10циклоалкілалкіл, арил, арилалкіл, гетероарил, гетероарилалкіл, гетероцикліл, гетероциклілалкіл, частково ненасичений гетероцикліл, -NR4SO2R5, -SO2NR6R4, -C(O)R6, -C(O)OR6, -OC(O)R6, -NR4C(O)OR5, -NR4C(O)R6, -C(O)NR4R6, NR4R6, -NR4C(O)NR4R6, -OR6, -S(O)R5, -SO2R5 або SR6, де згаданий алкіл, алкеніл, алкініл, циклоалкіл, арил, гетероарил, гетероцикліл, або частково ненасичений гетероцикліл необов'язково заміщений від однієї до п'яти групами, які незалежно вибирають з групи, яка складається з оксо, галогену, С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3С10циклоалкілу, С3-С10циклоалкілалкілу, ціано. нітро, трифторметилу, дифторметокси, трифторметокси, азидо, -NR4SO2R5, -SO2NR6R4, -C(O)R6, C(O)OR6, -OC(O)R6, -NR4C(O)OR5, -NR4C(O)CR6, C(O)NR4R6, -NR4R6, -NR4C(O)NR4R6, 4 4 6 6 NR C(NCN)NR R , -OR , -S(O)R5, -SO2R5, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, і гетероциклілалкілу, де g являє собою від 1 до 3 і кожний R10 може бути однаковим або відрізнятись; 90659 10 або одна або більше зі згаданих груп R10 може бути незалежно об'єднана з атомами, до яких вони прикріплені, щоб утворити від 3 до 10 членне циклоалкільне кільце або гетероциклоалкільне кільце, яке необов'язково містить один або більше додаткових гетероатомів, які вибирають з групи, яка складається з О, S, SO, SO2 і NR6, де кожний кільцевий вуглець необов'язково заміщений від однієї до трьох групами, які незалежно вибирають з групи, яка складається з галогену, С1-С10алкілу, С2С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3С10циклоалкілалкілу, ціано, нітро, трифторметилу, дифторметокси, трифторметокси, азидо, арилу, OR8, NR6R8, SR6, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу, за умови, що утворене згадане кільце не містить два сусідніх атоми О або два сусідніх атоми S; Ζ являє собою де коли R=Н, тоді Ζ надалі включає і де Ζ включає одну або більше R8 або R9 груп, де вказані R8 і R9 групи можуть бути зв'язані з однаковими або різними атомами; W і V незалежно вибирають з групи, яка складається з CR7R8, CR8R9, О, NR6, S, SO і SO2; Υ вибирають з групи, яка складається з S, SO, SO2, CR7CR8 і CR8R9, за умови, що коли W являє собою О, NR6, S, SO або SO2, тоді V являє собою CR8R9, і коли V являє собою О, NR6, S, SO або SO2, тоді W і Υ кожний являє собою CR8R9; R4 являє собою Η або С1-6алкіл; R5 являє собою трифторметил, С1-С10алкіл, С3-С10циклоалкіл. арил, арилалкіл, гетероарил, гетероарилалкіл, гетероцикліл, гетероциклілалкіл, або частково ненасичений гетероцикл, де згаданий алкіл, циклоалкіл, арил, арилалкіл, гетероарил, гетероарилалкіл, геретоцикліл, частково ненасичений гетероцикліл, і гетероциклілалкіл необов'язково заміщений від однієї до п'яти групами, які незалежно вибирають з групи, яка складається з оксо, галогену, С1-С10алкілу, С2С10алкенілу. С2-С10алкінілу, С3-С10циклоалкілу, С3С10циклоалкілалкілу, ціано, нітро, OR6, NR4R6, SR6, трифторметилу, дифторметокси, трифторметокси, азидо, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і геретоциклілалкілу; R6, R8 і R9 незалежно вибирають з групи, яка складається з водню, трифторметилу, С1С10алкілу, (СН2)0-4С3-С10циклоалкілу, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, частково ненасиченого гетероциклілу і гере 11 тоциклілалкілу, де згаданий алкіл, циклоалкіл, арил, арилалкіл, гетероарил, геретоцикліл, частково ненасичений гетероцикліл, і гетероциклілалкіл необов'язково заміщений від однієї до п'яти групами, які незалежно вибирають з групи, яка складається з оксо, галогену, С1-С10алкілу, С2С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3С10циклоалкілалкілу, ціано, нітро, OR6, NR6R8, SR6, трифторметилу, дифторметокси, трифторметокси, азидо, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу, частково ненасиченого гетероциклілу і гетероциклілалкілу; R7 являє собою водень, галоген, ціано, нітро, С1-С10алкіл, С2-С10алкеніл, С2-С10алкініл, С3С10циклоалкіл, С3-С10циклоалкілалкіл, арил, арилалкіл, гетероарил, гетероарилалкіл, гетероцикліл, гетероциклілалкіл, частково ненасичений гетероцикл, -NR4SO2R5, -SO2NR6R4, -C(O)R6, -C(O)OR6, OC(O)R6, -NR4C(O)OR5, -NR4C(O)R6, -C(O)NR4R6, NR4R6, -NR4C(O)NR4R6, -OR6, -S(O)R5, -SO2R5 або SR6, де згаданий алкіл, алкеніл, алкініл, циклоалкіл, арил, гетероарил, гетероцикліл, і частково ненасичений гетероцикліл необов'язково заміщений від однієї до п'яти групами, які незалежно вибирають з групи, яка складається з оксо, галогену, С1С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3С10циклоалкілу, С3-С10циклоалкілалкілу, ціано, нітро, трифторметилу, дифторметокси, трифторметокси, азидо, -NR4SO2R5, -SO2NR6R4, -C(O)R6, C(O)OR6, -OC(O)R6, -NR4C(O)OR5, -NR4C(O)CR6, C(O)NR4R6, -NR4R6, -NR4C(O)NR4R6, 4 4 6 6 5 5 NR C(NCN)NR R , -OR , -S(O)R , -SO2R , арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, частково ненасиченого гетероциклілу і гетероциклілалкілу; або R4 і R6 разом з атомами, до яких вони прикріплені, можуть бути незалежно з'єднані, щоб утворити від 3 до 10 членне циклоалкільне кільце або гетероциклоалкільне кільце, яке необов'язково містить один або більше додаткових гетероатомів, які вибирають з групи, яка складається з О, S, SO, SO2 і NR6, де кожний кільцевий вуглець необов'язково заміщений від однієї до трьох групами, які незалежно вибирають з групи, яка складається з галогену, С1-С10алкілу, С2-С10алкенілу, С2С10алкінілу, С3-С10циклоалкілу, С3С10циклоалкілалкілу, ціано, нітро, трифторметилу, дифторметокси, трифторметокси, азидо, арилу, OR8, NR6R8, SR6, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу, частково ненасиченого гетероциклілу і гетероциклілалкілу, утворене згадане кільце не містить два сусідніх атоми О або два сусідніх атоми S; або R6 і R8 разом з атомами, до яких вони прикріплені, можуть бути незалежно з'єднані, щоб утворити від 3 до 10 членне циклоалкільне кільце або гетероциклоалкільне кільце, яке необов'язково містить один або більше додаткових гетероатомів, які вибирають з групи, яка складається з О, S, SO, SO2 і NR6, де кожний кільцевий вуглець необов'язково заміщений від однієї до трьох групами, які незалежно вибирають з групи, яка складається з галогену, С1-С10алкілу, С2-С10алкенілу, С2С10алкінілу, С3-С10циклоалкілу, С3С10циклоалкілалкілу, ціано, нітро, трифторметилу, 90659 12 дифторметокси, трифторметокси, азидо, арилу, OR8, NR6R8, SR6, гетероарилу, арилалкілу, гетероарилалкілу, геретоциклілу, частково ненасиченого гетероциклілу і гетероциклілалкілу, утворене згадане кільце не містить два сусідніх атоми О або два сусідніх атоми S; або R7 і R8 разом з атомами, до яких вони прикріплені, можуть бути незалежно з'єднані, щоб утворити від 3 до 10 членне циклоалкільне кільце або гетероциклоалкільне кільце, яке необов'язково містить один або більше додаткових гетероатомів, які вибирають з групи, яка складається з О, S, SO, SO2 і NR6, де кожний кільцевий вуглець необов'язково заміщений від однієї до трьох групами, які незалежно вибирають з групи, яка складається з галогену, С1-С10алкілу, С2-С10алкенілу, С2 С10алкінілу, С3-С10циклоалкілу, С3 С10циклоалкілалкілу, ціано, нітро, трифторметилу, дифторметокси, трифторметокси, азидо, арилу, OR8, NR6R8, SR6, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу, частково ненасиченого гетероциклілу і гетероциклілалкілу; утворене згадане кільце не містить два сусідніх атоми О або два сусідніх атоми S; або R8 і R9 разом з атомами, до яких вони прикріплені, можуть бути незалежно з'єднані, щоб утворити від 3 до 10 членне циклоалкільне кільце або гетероциклоалкільне кільце, яке необов'язково містить один або більше додаткових гетероатомів, які вибирають з групи, яка складається з О, S, SO, SO2 і NR6, де кожний кільцевий вуглець може бути необов'язково заміщений від однієї до трьох групами, які незалежно вибирають з групи, яка складається з галогену, С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3 С10циклоалкілалкілу, ціано, нітро, трифторметилу, дифторметокси, трифторметокси, азидо, арилу, OR8, NR6R8, SR6, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу, частково ненасиченого гетероциклілу і гетероциклілалкілу, утворене згадане кільце не містить два сусідніх атоми О або два сусідніх атоми S; або R6 і R10 разом з атомами, до яких вони прикріплені, можуть бути незалежно з'єднані, щоб утворити від 3 до 10 членне циклоалкільне кільце або гетероциклоалкільне кільце, яке необов'язково містить один або більше додаткових гетероатомів, які вибирають з групи, яка складається з О, S, SO, SO2 і NR6, де кожний кільцевий вуглець може бути необов'язково заміщений від однієї до трьох групами, які незалежно вибирають з групи, яка складається з галогену, С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3 С10циклоалкілалкілу, ціано, нітро, трифторметилу, дифторметокси, трифторметокси, азидо, арилу, OR8, NR6R8, SR6, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу, частково ненасиченого гетероциклілу і гетероциклілалкілу, утворене згадане кільце не містить два сусідніх атоми О або два сусідніх атоми S; або R8 і R10 разом з атомами, до яких вони прикріплені, можуть бути незалежно з'єднані, щоб утворити від 3 до 10 членне циклоалкільне кільце або гетероциклоалкільне кільце, яке необов'язково містить один або більше додаткових гетероатомів, 13 які вибирають з групи, яка складається з О, S, SO, SO2 і NR6, де кожний кільцевий вуглець може бути необов'язково заміщений від однієї до трьох групами, які незалежно вибирають з галогену, С1С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3С10циклоалкілу, С3-С10циклоалкілалкілу, ціано, нітро, трифторметилу, дифторметокси, трифторметокси, азидо, арилу, OR8, NR6R8, SR6, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу, частково ненасиченого гетероциклілу і гетероциклілалкілу, утворене згадане кільце не містить два сусідніх атоми О або два сусідніх атоми S. Винахід може також бути направлений на фармацевтично прийнятні проліки, фармацевтично активні метаболіти і фармацевтично прийнятні солі сполуки загальної Формули І. Способи одержання сполук Формули І також описуються. У наступному аспекті, даний винахід забезпечує сполуки, які інгібують активність рецепторних тирозинкіназ типу І, таких як EGFR. ErbB2, ErbB3, ErbB4, VEGFR2, Flt3 і FGFR, які містять сполуки Формули І. У наступному аспекті, даний винахід забезпечує спосіб лікування захворювань або медичних станів, опосередкованих рецепторними тирозинкіназами типу І, який включає введення теплокровній тварині ефективної кількості сполуки Формули І, або фармацевтично прийнятної солі, або її розщеплюваних in vivo проліків. У наступному аспекті, даний винахід забезпечує спосіб інгібування продуктів рецепторних кіназ типу І, який включає введення теплокровній тварині ефективної кількості сполуки Формули І, або фармацевтично прийнятної солі, або її розщеплюваних in vivo проліків. У наступному аспекті, даний винахід забезпечує спосіб забезпечення інгібіторного ефекту рецепторної кінази типу І, який включає введенні теплокровній тварині ефективної кількості сполуки Формули І, або фармацевтично прийнятної солі, або її розщеплюваних in vivo проліків. У наступному аспекті, даний винахід забезпечує лікування або запобігання стану, опосередкованого рецепторною кіназою типу І, який включає введення кількості сполуки, ефективної для лікування або запобігання вказаному стану, опосередкованому рецепторною кіназою типу І, фармацевтичної композиції, яка містить вказану сполуку, людині або тварині, яка потребує цього, де вказана сполука являє собою сполуку Формули І, або її фармацевтично прийнятну сіль, або її розщеплюванні in vivo проліки. Стан, опосередкований рецепторною кіназою типу І, який може лікуватись відповідно до способів даного винаходу, включає гіперпроліферативні розлади, такі як рак голови і шиї, легені, молочної залози, ободової кишки, яєчника, міхура, шлунку, нирки, шкіри, підшлункової залози, лейкемії, лімфоми, стравоходу, матки або простати, серед інших видів гіперпроліферативних розладів. Сполуки Формули І можуть використовуватись переважно у поєднанні з іншими відомими терапевтичними агентами. 90659 14 Винахід також відноситься до фармацевтичних композицій, які містять ефективну кількість агента, який вибирають зі сполук Формули І або їх фармацевтично прийнятних проліків, фармацевтично активного метаболіту, або фармацевтично прийнятної солі. Додаткові переваги і нові ознаки цього винаходу повинні бути викладені надалі у наступній частині опису і частково стане очевидним для кваліфікованих в даній галузі фахівців після експертизи наступного опису, або можуть бути досліджені з практики винаходу. Переваги винаходу можуть бути реалізовані і досягнуті за допомогою засобів, поєднань, композицій і способів, які особливо зазначені у прикладеній формулі винаходу. Супровідні креслення, які включені сюди і утворюють частину опису, ілюструють необмежувальні втілення даного винаходу, і разом з описом служать для того, щоб пояснити принципи винаходу. На Фігурах: Фіг.1 показує схему реакції для одержання іміно амідинів. Фіг.2 показує іншу схему реакції для одержання іміно амідинів. Фіг.3 показує іншу схему реакції для одержання іміно амідинів. Фіг.4 показує іншу схему реакції для одержання іміно амідинів. Фіг.5 показує схему реакції для одержання оксазолінів. Фіг.6 показує іншу схему реакції для одержання оксазолінів. Сполуки Формули І за даним винаходом є корисними для інгібування рецепторних тирозинкіназ типу І, таких як EGER (HER1), ErbB2 (HER2), ErbB3 (HER3), ErbB4 (HER4), VEGFR2, Flt3 і FGFR. Сполуки Формули І можуть також бути корисні як інгібітори серину, треоніну і як інгібітори кіназ подвійної специфічності, таких як Raf, MEK і р38. Такі сполуки мають корисність як терапевтичні агенти для захворювань, які можуть лікуватись інгібуванням сигнальних шляхів рецепторних тирозинкіназ типу І і серину, треоніну, і шляхів кіназ подвійної специфічності. Взагалі, винахід відноситься до сполук загальної Формули І: в якій А прикріплений до щонайменше одного з вуглеців у положеннях 5, 6, 7 або 8 біциклічного кільця і в якій біциклічне кільце заміщене жодною, однією або двома незалежними групами R3; X являє собою Ν, СН, CF або C-CN; А являє собою Q або Z; Q являє собою 15 R1 являє собою заміщену або незаміщену, моноциклічну або біциклічну, арильну або гетероарильну частину, R2 являє собою Η або заміщений або незаміщений C1-8алкіл; R3 являє собою водень, галоген, ціано, нітро, С1-С10алкіл, С2-С10алкеніл, С2-С10алкініл, С3С10циклоалкіл, С3-С10циклоалкілалкіл, арил, арилалкіл, гетероарил, гетероарилалкіл, гетероцикліл, частково ненасичений гетероцикліл, гетероциклілалкіл, -NR4SO2R5, -SO2NR6R4, -C(O)R6, -C(O)OR6, -OC(O)R6, -NR4C(O)OR5, -NR4C(O)R6, -C(O)NR4R6, NR4R6, -NR4C(O)NR4R6, -OR6, -S(O)R5, -SO2R5, або SR6, де згаданий алкіл, алкеніл, алкініл, циклоалкіл, циклоалкілалкіл, арил, арилалкіл, гетероарил, гетероарилалкіл, гетероцикліл, частково ненасичений гетероцикліл, і гетероциклілалкіл необов'язково заміщений від однієї до п'яти групами, які незалежно вибирають з групи, яка складається з оксо, галогену, С1-С10алкілу, С2-С10алкенілу, С2С10алкінілу, С3-С10циклоалкілу, С3С10циклоалкілалкілу, ціано, нітро, трифторметилу, дифторметокси, трифторметокси, азидо, NR4SO2R5, -SO2NR6R4, -C(O)R6, -C(O)OR6, OC(O)R6, -NR4C(O)OR5, -NR4C(O)CR6, -C(O)NR4R6, -NR4R6, -NR4C(O)NR4R6, -NR4C(NCN)NR4R6, -OR6, S(O)R5, -SO2R5, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу; R10 являє собою водень, галоген, ціано, нітро, С1-С10алкіл, С2-С10алкеніл, С2-С10алкініл, С3С10циклоалкіл, С3-С10циклоалкілалкіл, арил, арилалкіл, гетероарил, гетероарилалкіл, гетероцикліл, гетероциклілалкіл, частково ненасичений гетероцикліл, -NR4SO2R5, -SO2NR6R4, -C(O)R6, -C(O)OR6, -OC(O)R6, -NR4C(O)OR5, -NR4C(O)R6, -C(O)NR4R6, NR4R6, -NR4C(O)NR4R6, -OR6, -S(O)R5, -SO2R5 або SR6, де згаданий алкіл, алкеніл, алкініл. циклоалкіл, арил, гетероарил, гетероцикліл, або частково ненасичений гетероцикліл необов'язково заміщений від однієї до п'яти групами, які незалежно вибирають з групи, яка складається з оксо, галогену, С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3С10циклоалкілу, С3-С10циклоалкілалкілу, ціано, нітро, трифторметилу, дифторметокси, трифторметокси, азидо, -NR4SO2R5, -SO2NR6R4, -C(O)R6, C(O)OR6, -OC(O)R6, -NR4C(O)OR5, -NR4C(O)CR6, C(O)NR4R6, -NR4R6, -NR4C(O)NR4R6, 4 4 6 6 NR C(NCN)NR R , -OR , -S(O)R5, -SO2R5, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, і гетероциклілалкілу, дег являє собою від 1 до 3 і кожний R10 може бути однаковим або відрізнятись; або одна або більше зі згаданих груп R10 може бути незалежно об'єднана з атомами, до яких вони прикріплені, щоб утворити від 3 до 10 членне циклоалкільне кільце або гетероциклоалкільне кільце, яке необов'язково містить один або більше додаткових гетероатомів, які вибирають з групи, яка складається з О, S, SO, SO2 і NR6, де кожний кільцевий вуглець необов'язково заміщений від однієї до трьох групами, які незалежно вибирають з групи, яка складається з галогену, С1-С10алкілу, С2С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3С10циклоалкілалкілу, ціано, нітро, трифторметилу, 90659 16 дифторметокси, трифторметокси, азидо, арилу, OR8, NR6R8, SR6, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу, утворене згадане кільце не містить два сусідніх атоми О або два сусідніх атоми S; Ζ являє собою де коли R6=Н, тоді Ζ надалі включає і де Ζ включає одну або більше R8 або R9 груп, де вказані R8 і R9 групи можуть бути зв'язані з однаковими або різними атомами; W і V незалежно вибирають з групи, яка складається з CR7R8, CR8R9, О, NR6, S, SO і SO2, і Υ вибирають з групи, яка складається з S, SO, SO2, CR7CR8 і CR8R9, за умови, що коли W являє собою О, NR6, S, SO або SO2, тоді V являє собою CR8R9, і коли V являє собою О, NR6, S, SO або SO2, 8 9 тоді W і Υ кожний являє собою CR R ; R4 являє собою Η або С1-6алкіл; R5 являє собою трифторметил, С1-С10алкіл, С3-С10циклоалкіл, арил, арилалкіл, гетероарил, гетероарилалкіл, гетероцикліл, гетероциклілалкіл, або частково ненасичений гетероцикл, де згаданий алкіл, циклоалкіл, арил, арилалкіл, гетероарил, гетероарилалкіл, геретоцикліл, частково ненасичений гетероцикліл, і гетероциклілалкіл необов'язково заміщений від однієї до п'яти групами, які незалежно вибирають з групи, яка складається з оксо, галогену, С1-С10алкілу, С2С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3С10циклоалкілалкілу, ціано, нітро, OR6, NR4R6, SR6, трифторметилу, дифторметокси, трифторметокси, азидо, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і геретоцикліл алкілу; R6, R8 і R9 незалежно вибирають з групи, яка складається з водню, трифторметилу, С1С10алкілу, (СН2)0-4С3-С10циклоалкілу, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, частково ненасиченого гетероциклілу і геретоциклілалкілу, де згаданий алкіл, циклоалкіл, арил, арилалкіл, гетероарил, геретоцикліл, частково ненасичений гетероцикліл, і гетероциклілалкіл необов'язково заміщений від однієї до п'яти групами, які незалежно вибирають з групи, яка складається з оксо, галогену, С1-С10алкілу, С2С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3С10циклоалкілалкілу, ціано, нітро, OR6, NR6R8, SR6, трифторметилу, дифторметокси, трифторметокси, азидо, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу, частково ненасиченого гетероциклілу і гетероциклілалкілу; 17 R7 являє собою водень, галоген, ціано, нітро, С1-С10алкіл, С2-С10алкеніл, С2-С10алкініл, С3С10циклоалкіл, С3-С10циклоалкілалкіл, арил, арилалкіл, гетероарил, гетероарилалкіл, гетероцикліл, гетероциклілалкіл, частково ненасичений гетероцикл, -NR4SO2R5, -SO2NR6R4, -C(O)R6, -C(O)OR6, OC(O)R6, -NR4C(O)OR5, -NR4C(O)R6, -C(O)NR4R6, NR4R6, -NR4C(O)NR4R6, -OR6, -S(O)R5, -SO2R5 або SR6, де згаданий алкіл, алкеніл, алкініл, циклоалкіл, арил, гетероарил. гетероцикліл, і частково ненасичений гетероцикліл необов'язково заміщений від однієї до п'яти групами, які незалежно вибирають з групи, яка складається з оксо, галогену, C1C10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3С10циклоалкілу, С3-С10циклоалкілалкілу, ціано, нітро, трифторметилу, дифторметокси, трифторметокси. азидо, -NR4SO2R5, -SO2NR6R4, -C(O)R6, C(O)OR6, -OC(O)R6, -NR4C(O)OR5, -NR4C(O)CR6, C(O)NR4R6, -NR4R6, -NR4C(O)NR4R6, 4 4 6 6 NR C(NCN)NR R , -OR , -S(O)R5, -SO2R5, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, частково ненасиченого гетероциклілу і гетероциклілалкілу; або R4 і R6 разом з атомами, до яких вони прикріплені, можуть бути незалежно з'єднані, щоб утворити від 3 до 10 членне циклоалкільне кільце або гетероциклоалкільне кільце, яке необов'язково містить один або більше додаткових гетероатомів, які вибирають з групи, яка складається з О, S, SO, SO2 і NR6, де кожний кільцевий вуглець необов'язково заміщений від однієї до трьох групами, які незалежно вибирають з групи, яка складається з галогену, С1-С10алкілу, С2-С10алкенілу, С2С10алкінілу, С3-С10циклоалкілу, С3С10циклоалкілалкілу, ціано, нітро, трифторметилу, дифторметокси, трифторметокси, азидо, арилу, OR , NR6R8, SR6, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу, частково ненасиченого гетероциклілу і гетероциклілалкілу, утворене згадане кільце не містить два сусідніх атоми О або два сусідніх атоми S; або R6 і R8 разом з атомами, до яких вони прикріплені, можуть бути незалежно з'єднані, щоб утворити від 3 до 10 членне циклоалкільне кільце або гетероциклоалкільне кільце, яке необов'язково містить один або більше додаткових гетероатомів, які вибирають з групи, яка складається з О, S. SO, SO2 і NR6, де кожний кільцевий вуглець необов'язково заміщений від однієї до трьох групами, які незалежно вибирають з групи, яка складається з галогену, С1-С10алкілу, С2-С10алкенілу, С2С10алкінілу, С3-С10циклоалкілу, С3С10циклоалкілалкілу, ціано, нітро, трифторметилу, дифторметокси, трифторметокси, азидо, арилу, OR8, NR6R8, SR6, гетероарилу, арилалкілу, гетероарилалкілу, геретоциклілу, частково ненасиченого гетероциклілу і гетероциклілалкілу, утворене згадане кільце не містить два сусідніх атоми О або два сусідніх атоми S; або R7 і R8 разом з атомами, до яких вони прикріплені, можуть бути незалежно з'єднані, щоб утворити від 3 до 10 членне циклоалкільне кільце або гетероциклоалкільне кільце, яке необов'язково містить один або більше додаткових гетероатомів, які вибирають з групи, яка складається з О, S, SO, 90659 18 SO2 і NR6, де кожний кільцевий вуглець необов'язково заміщений від однієї до трьох групами, які незалежно вибирають з групи, яка складається з галогену, С1-С10алкілу, С2-С10алкенілу, С2 С10алкінілу, С3-С10циклоалкілу, С3 С10циклоалкілалкілу, ціано, нітро, три фтор метилу, дифторметокси, трифторметокси, азидо, арилу, OR8, NR6R8, SR6, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу, частково ненасиченого гетероциклілу і гетероциклілалкілу; утворене згадане кільце не містить два сусідніх атоми О або два сусідніх атоми S; або R8 і R9 разом з атомами, до яких вони прикріплені, можуть бути незалежно з'єднані, щоб утворити від 3 до 10 членне циклоалкільне кільце або гетероциклоалкільне кільце, яке необов'язково містить один або більше додаткових гетероатомів, які вибирають з групи, яка складається з О, S, SO, SO2 і NR6, де кожний кільцевий вуглець може бути необов'язково заміщений від однієї до трьох групами, які незалежно вибирають з групи, яка складається з галогену, С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3 С10циклоалкілалкілу, ціано, нітро, трифторметилу, дифторметокси, трифторметокси. азидо, арилу, OR8, NR6R8, SR6, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу, частково ненасиченого гетероциклілу і гетероциклілалкілу, утворене згадане кільце не містить два сусідніх атоми О або два сусідніх атоми S; або R6 і R10 разом з атомами, до яких вони прикріплені, можуть бути незалежно з'єднані, щоб утворити від 3 до 10 членне циклоалкільне кільце або гетероциклоалкільне кільце, яке необов'язково містить один або більше додаткових гетероатомів, які вибирають з групи, яка складається з О. S, SO, SO2 і NR6, де кожний кільцевий вуглець може бути необов'язково заміщений від однієї до трьох групами, які незалежно вибирають з групи, яка складається з галогену, С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3 С10циклоалкілалкілу, ціано, нітро, трифторметилу, дифторметокси, трифторметокси, азидо, арилу, OR8, NR6R8, SR6, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу, частково ненасиченого гетероциклілу і гетероциклілалкілу, утворене згадане кільце не містить два сусідніх атоми О або два сусідніх атоми S; або R8 і R10 разом з атомами, до яких вони прикріплені, можуть бути незалежно з'єднані, щоб утворити від 3 до 10 членне циклоалкільне кільце або гетероциклоалкільне кільце, яке необов'язково містить один або більше додаткових гетероатомів, які вибирають з групи, яка складається з О, S, SO, SO2 і NR6, де кожний кільцевий вуглець може бути необов'язково заміщений від однієї до трьох групами, які незалежно вибирають з галогену, С1С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3С10циклоалкілу, С3-С10циклоалкілалкілу, ціано, нітро, трифторметилу, дифторметокси, трифторметокси, азидо, арилу, OR8, NR6R8, SR6, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу, частково ненасиченого гетероциклілу і гетероциклілалкілу, утворене згадане кільце не 19 містить два сусідніх атоми О або два сусідніх атоми S. Термін "алкіл", як використано тут, відноситься до насиченого лінійного або розгалуженого ланцюгового моновалентного вуглеводневого радикалу від одного до дванадцяти атомів вуглецю, де алкіл радикал може бути необов'язково заміщений незалежно одним або більше замісниками, які описані нижче. Приклади алкільних груп включають, але не обмежуються цим, метил, етил, n-пропіл, ізопропіл, бутил, ізобутил, втор-бутил, трет-бутил, пентил, ізопентил, трет-пентил, гексил, ізогексил і тому подібне. "Алкілен" означає лінійний або розгалужений насичений двовалентний вуглеводневий радикал від одного до дванадцяти атомів вуглецю, наприклад, метилен, етилен, пропілен, 2-метилпропілен, пентилен і тому подібне. Термін "алкеніл" відноситься до лінійного або розгалуженого ланцюгового моновалентного вуглеводневого радикалу від одного до дванадцяти атомів вуглецю, який містить щонайменше один подвійний зв’язок, наприклад, етеніл, пропеніл і тому подібне, де алкенільний радикал може бути необов'язково заміщений незалежно одним або більше замісниками, які описані тут, і включає радикали, які мають "цис" і "транс" орієнтації, або альтернативно, "Е" і "Z" орієнтації. Термін "алкенілен" відноситься до лінійного або розгалуженого двовалентного вуглеводневого радикалу від двох до дванадцяти вуглеців, який містить щонайменше один подвійний зв'язок, де алкеніленовий радикал може бути необов'язково заміщений незалежно одним або більше замісниками, які описані тут. Приклади включають, але не обмежуються цим, етенілен, пропенілен і тому подібне. Термін "алкініл" відноситься до лінійного або розгалуженого моновалентного вуглеводневого радикалу від двох до дванадцяти атомів вуглецю, який містить щонайменше один потрійний зв'язок. Приклади включають, але не обмежуються цим, етиніл, пропініл і тому подібне, де алкінільний радикал може бути необов'язково заміщений незалежно одним або більше замісниками, який описані тут. Термін "алкінілен" відноситься до лінійного або розгалуженого двовалентного вуглеводневого радикалу від двох до дванадцяти атомів вуглецю, який містить щонайменше один потрійний зв'язок, де алкініленовий радикал може бути необов'язково заміщений незалежно одним або більше замісниками, які описані тут. Термін "аліл" відноситься до радикалу, який має формулу RC=CHCHR, де R являє собою алкіл, алкеніл, алкініл, циклоалкіл, гетероциклоалкіл, арил, гетероарил або будь-який замісник, як визначений тут, де аліл може бути необов'язково заміщений незалежно одним або більше замісниками, які описані тут. Термін "циклоалкіл" відноситься до насиченого або частково ненасиченого циклічного вуглеводневого радикалу, який має від трьох до дванадцяти атомів вуглецю, де циклоалкіл може бути необов'язково заміщений незалежно одним або 90659 20 більше замісниками, які описані тут. Термін "циклоалкіл" надалі включає біциклічні і трициклічні циклоалкільні структури, де біциклічні і трициклічні структури можуть включати насичений або частково ненасичений циклоалкіл, який приєднаний до насиченого або частково ненасиченого циклоалкільного або гетероциклоалкільного кільця або арильне або гетероарильне кільце. Приклади циклоалкільних груп включають, але не обмежуються цим, циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил. адамантил, норборани і тому подібне. Термін "гетероалкіл" відноситься до насиченого лінійного або розгалуженого ланцюгового моновалентного вуглеводневого радикалу від одного до дванадцяти атомів вуглецю, де щонайменше один з атомів вуглецю заміщеним гетероатомом, який вибирають з Ν, Ο або S, і де радикал може бути вуглецевим радикалом або геретоатомним радикалом (тобто, гетероатом може з'явитись всередині або в кінці радикалу). Гетероалкільний радикал може бути необов'язково заміщений незалежно одним або більше замісниками, які описані тут. Термін "гетероалкіл" включає алкокси і гетероалкокси радикали. Термін "гетероциклоалкіл" відноситься до насиченого або частково ненасиченого циклічного радикалу від 3 до 8 кільцевих атомів, в яких щонайменше один кільцевий атом являє собою гетероатом, який вибирають з азоту, кисню і сірки, залишкові кільцеві атоми, які являють собою С, де один або більше кільцевих атомів можуть бути необов'язково заміщені незалежно одним або більше замісниками, які описані нижче. Радикал може бути вуглецевим радикалом або гетероатомним радикалом. "Гетероциклоалкіл" також включає радикали, де гетероциклічні радикали приєднані до ароматичних або гетероароматичних кілець. Приклади гетероциклоалкільних кілець включають, але не обмежуються цим, піролідин, піперидин, піперазин, тетрагідропіраніл, морфолін, тіоморфолін, гомопіперазин, фталімід і їх похідні. Термін "гетероалкеніл" відноситься до лінійного або розгалуженого ланцюгового моновалентного вуглеводневого радикалу від трьох до дванадцяти атомів вуглецю, що містить щонайменше один подвійний зв'язок, наприклад, етеніл, пропеніл і тому подібне, де щонайменше один з атомів вуглецю заміщений гетероатомом, який вибирають з N, О, або S, і де радикал може бути вуглецевим радикалом або гетероатомним радикалом (тобто, гетероатом може з'явитись всередині або в кінці радикалу). Гетероалкенільний радикал може бути необов'язково заміщений незалежно одним або більше замісниками, які описані тут, і включає радикали, які мають "цис" і "транс" орієнтації, або альтернативно "Е" і "Z" орієнтації. Термін "гетероалкініл" відноситься до лінійного або розгалуженого моновалентного вуглеводневого радикалу від трьох до дванадцяти атомів вуглецю, які містять щонайменше один потрійний зв'язок. Приклади включають, але не обмежуються цим, етиніл. пропініл і тому подібне, де щонайменше один з атомів вуглецю заміщений гетероатомом, який вибирають з Ν, Ο або S, і де радикал 21 може бути вуглецевим радикалом або гетероатомним радикалом (тобто, гетероатом може з'явитись всередині або в кінці радикалу). Гетероалкінільний радикал може бути необов'язково заміщений незалежно одним або більше замісниками, які описані тут. Термін "гетероаліл" відноситься до радикалів, які мають формулу RC=CHCHR, де R являє собою алкіл, алкеніл, алкініл, циклоалкіл, гетероциклоалкіл, арил, гетероарил або будь-який замісник, як визначено тут, де щонайменше один з атомів вуглецю заміщений гетероатомом, який вибирають з N, О або S, і де радикал може бути вуглецевим радикалом або гетероатомний радикалом (тобто, гетероатом може з'явитись всередині або в кінці радикалу). Гетероаліл може бути необов'язково заміщений незалежно одним або більше замісниками, які описані тут. "Арил" означає моновалентний ароматичний вуглеводневий моноциклічний радикал від 6 до 10 кільцевих атомів або поліциклічний ароматичний вуглеводень, необов'язково заміщений незалежно одним або більше замісниками, які описані тут. Більш конкретно, термін арил включає, але не обмежується цим, феніл, 1-нафтил, 2-нафтил і їх похідні. Гетероарил" означає моновалентний моноциклічний ароматичний радикал від 5 до 10 кільцевих атомів або поліциклічний ароматичний радикал, що містить один або більше кільцевих гетероатомів, які вибирають з Ν, Ο або S, залишкові кільцеві атоми являють собою С. Ароматичний радикал необов'язково заміщений незалежно одним або більше замісниками, які описані тут. Приклади включають, але не обмежуються цим, фурил, тієніл, піроліл, піридил, піразоліл, піримідиніл, імідазоліл, піразиніл, індоліл, тіофен-2-іл, хіноліл, бензопіраніл, тіазоліл і їх похідні. Термін "гало" являє собою фтор, хлор, бром або йод. Також, термін "галоген" відноситься до фторового, хлорного, бромового або йодового замісника. Взагалі, різні частини або функціональні групи сполук Формули І можуть бути необов'язково заміщені одним або більше замісниками. Приклади замісників, придатних з метою даного винаходу, включають, але не обмежуються цим, гало, алкіл, аліл, алкеніл, алкініл, гетероалкіл, гетероаліл, гетероалкеніл, гетероалкініл, алкокси, гетероалкокси, Gn-циклоалкіл, Gn-гетероциклоалкіл, Gn-OR, Gn-NO2, Gn-CN, Gn-CO2R, Gn-(C=O)R, Gn-O(C=O)R, Gn-O-алкіл, Gn-OAr, Gn-SH, Gn-SR, Gn-SOR, GnSO2R, Gn-S-Ar, Gn-SOAr, Gn-SO2Ar, арил, гетероарил, Gn-Ar, Gn-(C=O)NR2R3, Gn-NR2R3, Gn-NR(O)R, Gn-SO2 NR2R3, PO3H2 і SO3H2, де G являє собою алкілен, який має від 1 до 4 вуглеців, або алкенілен або алкінілен, кожний з яких має від 2 до 4 вуглеців, де згаданий алкілен, алкенілен або алкінілен може бути заміщений або незаміщений; n являє собою нуль або 1; R1, R2, і R3 являють собою незалежно алкіл, аліл, алкеніл, алкініл, гетероалкіл, гетероаліл, гетероалкеніл, гетероалкініл, алкокси. гетероалкокси, Gn-циклоалкіл або Gnгетероциклоалкіл; і Аr являє собою арил або гетероарил, де згаданий алкіл, аліл, алкеніл, алкініл, 90659 22 гетероалкіл, гетероаліл, гетероалкеніл, гетероалкініл, алкокси, гетероалкокси, Gn-циклоалкіл, Gnгетероциклоалкіл, Аr, R1, R2 і R3 можуть бути надалі заміщені або незаміщені. Сполуки даного винаходу можуть мати один або більше асиметричних центри, і такі сполуки можуть бути одержані як індивідуальні (R)- або (S)стереоізомери або як їх суміші. Якщо не вказано інакше, опис або найменування конкретної сполуки в описі і формулі винаходу повинно включати обидва індивідуальні енантіомери і їх суміші, рацемічні або інші. Відповідно, даний винахід також включає рацемати і тверді енантіомери, і діастереомери сполук Формули І. Способи визначення стереохімії і розділення стереоізомерів добре відомі в даній галузі (див. обговорення в Chapter 4 of "Advanced Organic Chemistry", 4th edition J. March, John Wiley and Sons, New York, 1992). В доповнення до сполук Формули І, винахід також включає сольвати, фармацевтично прийнятні проліки, фармацевтично активні метаболіти і фармацевтично прийнятні солі таких сполук. Термін "сольват" відноситься до сукупності молекул з однією або більше молекуламирозчинниками. "Фармацевтично прийнятні проліки" являють собою сполуку, яка може бути перетворена у фізіологічних умовах або шляхом сольволізу у визначену сполуку або фармацевтично прийнятну сіль такої сполуки. "Фармацевтично активний метаболіт" являє собою фармакологічно активний продукт, яка виробляється через метаболізм в складі визначеної сполуки суміші або її солі. Метаболіти сполуки можуть бути ідентифіковані, використовуючи звичайну методику, відому в даній галузі, і їх активності можуть бути визначені, використовуючи тестування, як такі, що описані тут. Проліки і активні метаболіти сполуки можуть бути ідентифіковані, використовуючи звичайну методику, відому в даній галузі. Різні форми проліків відомі в даній галузі. Для прикладів таких пролікарських похідних, дивіться, наприклад, a) Design of Prodrugs, edited by Η. Bundgaard, (Elsevier, 1985) and Methods in Enzymology, Vol.42, p.309-396, edited by K. Widder, et al. (Academic Press, 1985); b) A Textbook of Drug Design and Development, edited by Krogsgaard-Larsen and H. Bundgaard, Chapter 5 "Design and Application ofProdrugs", by H. Bundgaard p.113-191 (1991); с) Н. Bundgaard, Advanced Drug Delivery Reviews, 8:1-38 (1992); d) H. Bundgaard, et al., Journal of Pharmaceutical Sciences, 77:285 (1988); and e) N. Kakeya, et al., Chem. Pharm. Bull., 32:692 (1984). "Фармацевтично прийнятна сіль" являє собою сіль, яка зберігає біологічну ефективність вільних кислот і основ визначеної сполуки і не є біологічно або інакше небажаною. Сполука винаходу може мати достатньо кислотну, достатньо основну або обидві функціональні групи, і відповідно реагувати з будь-якою кількістю неорганічних або органічних основ, і неорганічних і органічних кислот, щоб утворювати фармацевтично прийнятну сіль. Приклади фармацевтично прийнятних солей включають ті солі, які одержують реакцією сполук даного 23 винаходу з мінеральною або органічною кислотою або неорганічною основою, такі солі, включаючи сульфати, піросульфати, бісульфати, сульфіти, бісульфіти, фосфати, моногідрогенфосфати, дигідрогенфосфати, метафосфати, пірофосфати, хлориди, броміди, йодиди, ацетати, пропіонати, деканоати, каприлати, акрилати, форміати, ізобутирати. капроати, гептаноати, пропіолати, оксалати, малонати, сукцинати, суберати, себакати, фумарати, матеати, бутин-1,4-діоати, гексин-1,6діоати, бензоати, хлорбензоати, метилбензоати, динітробензоати, гідроксибензоати, метоксибензоати, фталати, сульфонати, ксилолсульфонати, фенілацетати, фенілпропіонати, фенілбутирати, цитрати, лактати, -гідроксибутирати, гліколяти, тартрати, метансульфонати, пропансульфонати, нафталін-1-сульфонати, нафталін-2-сульфонати, тозилати, бензилати, ацетати і манделати. Якщо сполука за винаходом являє собою основу, бажана фармацевтично прийнятна сіль може бути одержана будь-яким прийнятним способом, доступним в даній галузі, наприклад, обробкою вільної основи неорганічною кислотою, такою як хлористоводнева кислота, бромистоводнева кислота, сірчана кисла, азотна кисла, фосфорна кислота і тому подібне, або органічною кислотою, такою як оцтова кислота, малеїнова кислота, янтарна кислота, мигдалева кислота, фумарова кислота, малонова кислота, піровиноградна кислота, щавлева кислота, гліколева кислота, саліцилова кислота, піранозидильна кислота, така як глюкуронова кислота або галактуронова кислота, альфагідрокси кислота, така як лимонна кислота або винна кислота, амінокислота, така як аспарагінова кислота або глутамінова кислота, ароматична кислота, така як бензойна кислота або корична кислота, сульфонова кислота, така як ртолуолсульфонова кислота або етансульфонова кислота, або подібне. Якщо сполука за винаходом являє собою кислоту, бажана фармацевтично прийнятна сіль може бути одержанабудь-яким прийнятним способом, наприклад, обробкою вільної кислоти неорганічною або органічною основою, такою як амін (первинний, вторинний або третинний), гідроксид лужного металу лугу або гідроксид лужноземельного металу, або подібне. Ілюстративні приклади прийнятних солей включають, але не обмежуються цим, органічні солі, які одержують з амінокислот, таких як гліцин і аргінін, аміак, первинний, вторинний і третинний аміни, і циклічні аміни, такі як піперидин, морфолін і піперазин, і неорганічні солі, які одержують з натрію, кальцію, калію, магнію, марганцю, заліза, міді, цинку, алюмінію і літію. Сполуки за винаходом можуть бути одержані, використовуючи реакційні шляхи і схеми синтезу, як описано нижче, залучаючи методику, доступну в даній галузі, використовуючи вихідні матеріали, які є легко доступними. Терапевтичні Аспекти Винаходу Терапевтично ефективні кількості сполук винаходу можуть бути використані для лікування захворювань, опосередкованих модуляцією або регуляцією рецепторних тирозинкіназ типу І і/або серину, треоніну і/або кіназ подвійної специфічно 90659 24 сті. "Ефективна кількість", як мається на увазі, означає ту кількість сполуки, яка, коли водиться ссавцю, який потребує такого лікування, є достатньою, щоб виконати лікування захворювання, опосередкованого активністю однієї або більше рецепторних тирозинкіназ типу І і/або серину, треоніну і/або кіназ подвійної специфічності. Так, наприклад, терапевтично ефективна кількість сполуки, вибраної з Формули І або її солі, активного метаболіту або проліків, являє собою кількість, достатню, щоб модулювати, регулювати або інгібувати активність однієї або більше рецепторних тирозинкіназ типу І і/або серину, треоніну і/або кіназ подвійної специфічності, така, що стан захворювання, який опосередкований цією активністю, зменшується або полегшується. Кількість даного агента, яка відповідає такій кількості, буде змінюватись в залежності від факторів, таких як конкретна сполука, стан захворювання і його тяжкість, особливість (наприклад, вага) ссавця, який потребує лікування, але може, проте, бути звичайно визначена кваліфікованим в даній галузі фахівцем. "Лікування" повинно означати щонайменше полегшення стані захворювання у ссавця, такого як людина, що піддається впливу, щонайменше частково, активності однієї або більше рецепторних тирозинкіназ типу І і/або серину, треоніну і/або кіназ подвійної специфічності, і включає, але не обмежується цим, запобігання появу стану захворювання у ссавця, особливо, коли знаходять, що ссавець схильний мати стан захворювання, але не ще поставили діагноз про його наявність; модулювання і/або інгібування стану захворювання; і/або полегшення стану захворювання. Для того, щоб використовувати сполуку Формули І, або її фармацевтично прийнятну сіль або розщеплюванні in vivo проліки, для терапевтичного лікування (включаючи профілактичне лікування) ссавців, включаючи людину, її звичайно складають у композиції відповідно до стандартної фармацевтичної практики як фармацевтичну композицію. Відповідно до цього аспекту винаходу забезпечується фармацевтична композиція, яка містить сполуку Формули І, або її фармацевтично прийнятну сіль або розщеплюванні in vivo проліки, як визначено тут вище у поєднанні фармацевтично прийнятним розріджувачем або носієм. Композиції винаходу можуть знаходитись у формі, придатній для орального застосування (наприклад, як таблетки, коржики, тверді або м'які капсули, водні або маслянисті суспензії, емульсії, дисперговані порошки або гранули, сиропи або еліксири), для місцевого застосування (наприклад, як креми, мазі, гелі, або водні або маслянисті розчини або суспензії), для введення інгаляцією (наприклад, як тонко диспергований порошок або рідкий аерозоль), для введення нагнітанням (наприклад, як тонко диспергований порошок) або для парентерального введення (наприклад, як стерильний водний або маслянистий розчин для внутрішньовенного, підшкірного або внутрішньом'язового дозування або як супозиторій для ректального дозування). Наприклад, композиції, призначені для орального застосування, можуть 25 містити один або більше забарвлювальних, підсолоджувальних, смакових і/або консервуючих речовин. Придатні фармацевтично прийнятні ексципієнти для складання таблеток включають, наприклад, інертний розріджувачі, такі як лактоза, карбонат натрію, фосфат кальцію або карбонат кальцію, гранулюючі і дезінтегруючі агенти, такі як кукурудзяний крохмаль або альгінова кислота; зв'язувальні агенти, такі як крохмаль; змащувальні агенти, такі як стеарат магнію, стеаринова кислота або тальк; консервуючі агенти, такі як етил або пропіл р-гідроксибензоат, і антиоксиданти, такі як аскорбінова кислота. Композиції таблеток можуть бути вкриті або не вкриті оболонкою, або щоб модифікувати їх розщеплення і наступне абсорбування активного інгредієнта всередині шлунковокишкового тракту, або щоб вдосконалити їх стабільність і/або вигляд, в будь-якому випадку, використовуючи глазурувальний засіб і методики, добре відомі в даній галузі. Композиції для орального застосування можуть знаходитись у формі твердих желатинових капсул, в яких активний інгредієнт змішаний з інертним твердим розріджувачем, наприклад, карбонат кальцію, фосфат кальцію або каолін, або як м'які желатинові капсули, в яких активний інгредієнт змішаний з водою або олією, такою як арахісова олія, рідкий парафін або оливкова олія. Водні суспензії звичайно містять активний інгредієнт у тонко порошкованій формі з одним або більше суспендуючими агентами, такими як натрій карбоксиметилцелюлоза, метилцелюлоза, гідроксипропілметилцелюлоза, натрій альгінат, полівініл-піролідон, трагакантова камедь і акацієва камедь; диспергуючий або змочувальний агенти, такі як лецитин або продукти конденсації алкілен оксиду з жирними кислотами (наприклад поліоксетилен стеарат). або продукти конденсації етилен оксиду з довголанцюговими аліфатичними спиртами, наприклад гептадекаетиленоксицетанол, або продукти конденсації етилен оксиду з частковими ефірами, який одержують з жирних кислот і гекситу, такі як поліоксіетилен сорбітмоноолеат, або продукти конденсації етилен оксиду з частковими ефірами, які одержують з жирних кислот і ангідридів гекситу, наприклад поліетилен сорбітмоноолеат. Водні суспензії можуть також містити один або більше консервантів (таких як етил або пропіл ргідроксибензоат), антиоксидантів (таких як наприклад аскорбінова кислота), забарвлювальних агентів, смакових агентів, і/або підсолоджувальних агентів (таких як сахароза, сахарин або аспартам). Маслянисті суспензії можуть складатись у композиції за допомогою суспендування активного інгредієнта в олії (такій як арахісова олія, оливкова олія, кунжутна олія або кокосова олія) або в мінеральному маслі (такому як рідкий парафін). Маслянисті суспензії можуть також містити загусники, такі як віск, твердий парафін або цетиловий спирт. Підсолоджувальні агенти, такі як викладені вище, і смакові агенти можуть бути додані для того, щоб забезпечити приємний оральний препарат. Ці композиції можуть бути збережені додаванням антиоксидантy, такого як аскорбінова кислота. 90659 26 Дисперсні порошки і гранули, прийнятні для одержання водної суспензії шляхом додавання води звичайно містять активний інгредієнт разом з диспергуючим або змочувальним агентом, суспендуючим агентом і одним або більше консервантами. Придатні диспергуючі або змочувальні агенти і суспендуючі агенти представлені прикладами, які вже вказані вище. Додаткові ексципіснти, такі як підсолоджувальні, смакові і забарвлювальні агенти, можуть також бути присутні. Фармацевтичні композиції винаходу можуть також бути у формі емульсій масло-у-воді. Масляниста фаза може бути олію, такою як оливкова олія або арахісова олія, або мінеральним маслом, таким як рідкий парафін, або сумішшю будь-яких з них. Придатні емульгуючі агенти можуть бути, наприклад, камедями природного походження, такими як акацієва камедь або трагакантова камедь, фосфатидами природного походження, такими як соєві боби, лецитин, ефірами або частковими ефірами, які одержують з жирних кислот і ангідридів гекситу (наприклад сорбітмоноолеат) і продуктів конденсації згаданих часткових ефірів з етилен оксидом, таким як поліоксиетилен сорбітмоноолеат. Емульсії можуть також містити підсолоджувальні, смакові і консервуючі агенти. Сиропи і еліксири можуть складатись у композиції з підсолоджувальними агентами, такими як гліцерин, пропіленгліколь, сорбіт, аспартам або сахароза, і можуть також містити заспокійливий засіб, консервант, смаковий або забарвлювальний агент. Фармацевтичні композиції можуть також знаходитись у формі стерильної ін'єктованої водної або маслянистої суспензії, яка може складатись у композицію відповідно до відомих процедур, використовуючи однин або більше з відповідних диспергуючих або змочувальних агентів і суспендуючих агентів, які були згадані вище. Стерильний ін'єктований препарати може також бути стерильним ін'єктованим розчином або суспензією в нетоксичному парентерально-прийнятному розріджувачі або розчиннику, наприклад розчин в 1,3бутандіолі. Композиції супозиторію можуть бути одержані за допомогою змішування активного інгредієнта з придатним неподразнювальним ексципієнтом, який є твердим при звичайних температурах, але рідкий при ректальній температурі і таким чином буде танути в прямій кишці, щоб вивільнити лікарський засіб. Придатні ексципієнти включають, наприклад, масло какао і поліетиленгліколі. Місцеві композиції, такі як креми, мазі, гелі і водні або маслянисті розчини або суспензії, можуть звичайно бути одержані за допомогою складання у композиції активного інгредієнта зі звичайним, місцево прийнятним, засобом або розріджувачем, використовуючи звичайні процедури, добре відомі в даній галузі. Композиції для введення нагнітанням можуть знаходитись у формі тонко диспергованого порошку, який містить частинки середнього діаметра, наприклад, 30мкм або набагато менше, порошку, який безпосередньо містить або активний інгредієнт один, або розбавлений з одними або більше 27 фізіологічно прийнятними носіями, такими як лактоза. Порошок для нагнітання потім зручно зберігається в капсулі, яка містить, наприклад, від 1 до 50мг активного інгредієнта для застосування з турбо-інгаляторним пристроєм, таким, як той, що використовується для нагнітання відомого агента хромолглікату натрію. Композиції для введення інгаляцією можуть знаходитись у формі звичайного аерозолю під тиском, приладженого розподіляти активний інгредієнт, або як аерозоль, що містить тонко подрібнені тверді або рідкі крапельки. Звичайні аерозольні пропеленти, такі як леткі фторовані вуглеводні або вуглеводні, можуть бути використані і аерозольний пристрій звичайно приладжений, щоб розподіляти дозовану кількість активного інгредієнта. Для подальшої інформації щодо складів дивіться Розділ 25.2 в Томі 5 Comprehensive Medicinal Chemistry (Corwin Hansch; Chairman of Editorial Board), Pergamon Press, 1990. Кількість сполуки за даним винаходом, яка поєднується з одним або більше ексципієнтами, щоб виробити єдину дозовану форму, обов'язково змінюється в залежності від хазяїна, якого лікують, і конкретного шляху введення. Наприклад, склад, призначений для орального введення людині, може містити, наприклад, від 0,5мг до 2г активного агента, змішаного з відповідною і зручною кількістю ексципієнтів, яка може змінюватись від близько 5 до близько 98 процентів за вагою всієї композиції. Дозовані одиничні форми взагалі міститимуть близько від 1мг до близько 500мг активного інгредієнта. Для подальшої інформації щодо шляхів введення і режимів дозування дивіться Розділ 25.3 в Томі 5 Comprehensive Medicinal Chemistry (Corwin Hansch; Chairman of Editorial Board), Pergamon Press. 1990. Розмір дози з терапевтичною або профілактичною метою сполуки Формули І звичайно буде змінюватись відповідно до природи і тяжкості станів умов, віку і статі тварини або пацієнта і шляху введення, відповідно до добре відомих принципів медицини. Хоча сполуки Формули І перш за все мають значення як терапевтичні агенти для застосування у теплокровних тваринах (включаючи людину), вони також є корисними кожного разу, коли вимагається контролювати рецепторні тирозинкінази типу І і/або серии, треонін і/або кінази подвійної специфічності. Так, вони корисні як фармакологічні стандарти для застосування у розвитку нових біологічних випробувань і в пошуку нових фармакологічних агентів. Активність сполук за даним винаходом може бути випробувана для інгібування рецепторних тирозинкіназ типу І і/або серину, треоніну і/або кіназ подвійної специфічності in vitro, in vivo або в клітинній лінії. In vitro випробування включають випробування, які визначають інгібування кіназної активності. Почергові in vitro дослідження визначають здатність інгібітору зв'язуватись з кіназами і може бути виміряна або за допомогою мічення інгібітору перед зв'язуванням, ізолюючи комплекс інгібітор/кіназа і визначаючи кількість міченого зв'язка, або за допомогою виконання експеримен 90659 28 ту змагання, де нові інгібітори інкубують з відомими радіолігандами. Ці та інші корисні in vitro та дослідження клітинних культур добре відомі кваліфікованим в даній галузі фахівцям. Хоча винахід був описаний і проілюстрований з конкретним ступенем специфічності, розуміється, що дане розкриття було зроблене тільки з метою прикладу, і, що численні зміни в комбінації і розташуванні частин можуть бути зроблені кваліфікованими в даній галузі фахівцями без виходу за межі духу і об'єму даного винаходу, як надалі стверджено. Біологічні приклади Ензиматичнівипробування EGFR/ErbB2 Thermo LabSystems Immulon 4HBX 96-ямкові планшети покривають шляхом інкубування протягом ночі при кімнатній температурі 100мкл на ямку 0,25мг/мкл Poly (Glu, Туг) 4:1 (PGT) (Sigma Chemical Co., St. Louis, МО) в PBS (фосфатний буферний сольовий розчин). Надлишковий PGT виділяють аспірацією, і планшет промивають три рази промивним буфером (0,1% Tween 20 в PBS). Кіназну реакцію виконують в 100мкл 50мМ HEPES (рН7,3), який містить 125мМ хлориду натрію, 24мМ хлориду магнію, 0,1мМ ортованадату натрію, 15мкМ АТР (аденозин трифосфату) і 0,3одиниць/мкл EGFR (рецептор фактора росту епідермісу) (BIOMOL Research Laboratories, Inc., Plymouth Meeting, PA). Сполуку в DMSO (диметилсульфоксид) додають, щоб дати кінцеву концентрацію DMSO близько 1%. Фосфорилювання ініціюють додаванням АТР та інкубують протягом 30 хвилин при кімнатній температурі. Кіназну реакцію припиняють аспірацією реакційної суміші і послідовним промиванням промивним буфером (дивіться вище). Фосфорильований PGT виявляють 30 інкубацією 100мкл на ямку HRP кон'югованого PY20 антифосфотирозинового антитіла (Zymed Laboratories, Inc., South San Francisco, С А), розбавленого до 0,2мгк/мл в 3% BSA і 0,05% Tween 20 в PBS. Антитіло виділяють аспірацією, і планшет промивають промивним буфером. Колориметричний сигнал проявляють додаванням 100мкл на ямку ТМВ Microwell Peroxidase Substrate (Kirkegaard and Perry, Gaithersburg, MD) і зупиняють додаванням 100мкл на ямку 1М фосфорної кислоти. Фосфотирозин вимірюють абсорбуванням при 450нм. Кіназа ErbB2 є такою ж, як вище, використовуючи 250мг/мл ErbB2 внутрішньоклітинного домену замість EGFR. Внутрішньоклітинний домен ErbB2 тирозинкінази (амінокислоти 691-1255) експресують як біс-мічений протеїн в Baculovirus і очищують нікель хелатуванням, іонним обміном і гель-хроматографією. Сполуки даного винаходу мають значення ІС50 від менше ніж 1нм до 50мм. Препаративні приклади Ілюстрація приготування сполук даного винаходу наведена на Фіг.1-6. Фіг.1 ілюструє синтез іміно амідинових сполук даного винаходу. Гідразони (3) можуть бути одержані стандартними способами конденсації альдегіду (1) з гідразином (2). Цього можна досягти в ряді органічних розчинників. Переважно, конден 29 сацію здійснюють в змішаній системі розчинників DCM і ІРА. Поєднання, щоб утворити іміно амідини (5), можуть бути досягнуті за допомогою нагрівання гідразону (3) в суміші розчинників THF і ІРА при близько 50°С у присутності імідату (4). Фіг.2 ілюструє альтернативний синтез іміно амідинових сполук даного винаходу. Цим способом, амід (6) обробляють РОСl3 у прийнятному органічному розчиннику, такому як бензол або DCM, щоб утворити проміжну сполуку імідоїл хлорид. Гідразон (3) потім додають до цієї суміші, щоб створити бажаний іміно амідин (5). Це поєднання може вимагати злегка підвищених температур (від 45 до 90°С). Фіг.3 і 4 розкриває синтези іміно амідинових сполук даного винаходу, де іміно амідин (7) одержують і потім конденсують альдегідом (1). На Фіг.3 іміно амідин (7) може бути одержаний за допомогою поєднання гідразину (2) з імідатом (4) у прийнятному органічному розчиннику. Одержаний іміно амідин (7) може потім бути конденсований з альдегідом (1) у прийнятному органічному розчиннику, такому як THF і ІРА або EtOH при кімнатній температурі або злегка підвищеній температурі (від 45 до 90°С), щоб надати бажаний іміно амідин (5). На Фіг.4 іміно амідин (7) може бути одержаний за допомогою поєднання гідразину (2) з тіоімідатом (8) у прийнятному органічному розчиннику. Як на Фіг.3 одержаний іміно амідин (7) може потім бути конденсований з альдегідом (1) у прийнятному органічному розчиннику, такому як THF і ІРА або EtOH при кімнатній температурі або злегка підвищеній температурі (від 45 до 90°С), щоб надати бажаний іміно амідин (5). Оксазолінові сполуки формули І можуть бути одержані як представлено на Фіг.5. Анілін (9) може бути конденсований з tioCDI у прийнятному органічному розчиннику, такому як суміш THF і DCE. Одержану проміжну сполуку не виділяють, але скоріше обробляють in situ аміно спритом (10). Реакція додавання може бути досягнута при кімнатній температурі або при злегка підвищених температурах (від 45 до 90°С). Взагалі, одержана тіосечовина (11) може бути виділена і перенесена без очищення. Бажаний оксазолін (12) може бути одержаний з тіосечовини (11) одним з декількох шляхів, які представлені на Фіг.5. Тіосечовина (11) може бути оброблена тозил хлоридом і NaOH в суміші THF і води при кімнатній температурі. Альтернативно, тіосечовина (11) може бути оброблена різноманітністю карбодіімідатів, таких як у EDCI, DCC, DCI у прийнятних органічних розчинниках, таких як THF, DMF, DCM або РСЕ при кімнатній температурі або злегка підвищених температурах (від 45 до 90°С). Фіг.6 ілюструє альтернативний підхід до оксазолінових сполук даного винаходу. Анілін (9) може бути з'єднаний з дифеніл N-ціанокарбонимідатом (13) з або без основи, такої як наприклад NaH або Et3N, в органічних розчинниках, таких як DMF, MeCN, діоксан, піридин. ІРА або DCM при кімнатній температурі або підвищених температурах (від 45 до 120°С), щоб одержати ціано ізосечовину 90659 30 (14). Переважно, ціано ізосечовину (14) утворюють за допомогою поєднання аніліну (9) і дифеніл Nціанокарбонимідату (13) в суміші THF/DCE/tBuOH при 80-90°С. Оксазолін (12) може бути одержаний за допомогою поєднання аміно сприту (10) і ціано ізосечовини (14) в різноманітності органічних розчинників, включаючи THF і ІРА. Переважно, поєднання (10) і (14) досягають в суміші THF і ІРА при підвищених температурах (від 45 до 120°С). Для того, щоб проілюструвати винахід, бути включені наступні приклади. Однак, повинно бути зрозумілим, що ці приклади не обмежують винахід і призначені тільки з тим, щоб запропонувати спосіб втілення винаходу на практиці. Кваліфіковані в даній галузі фахівці розпізнають, що хімічні реакції, які описуються, можуть бути легко пристосовані, щоб одержати ряд інших аналогів хіназоліну за даним винаходом, і альтернативні способи одержання сполук даного винаходу вважаються такими, які знаходяться в межах даного винаходу. Наприклад, синтез непроілюстрованих сполук відповідно до винаходу може бути успішно виконаний модифікаціями, очевидними для кваліфікованих в даній галузі фахівців, наприклад, відповідно захищаючи інтерферуючі групи, використовуючи інші придатні реактиви, відомі в даній галузі, інші, ніж ті, які вже описані, і/або створюючи звичайні модифікації реакційних умов. Альтернативно, інші реакції, які розкриті тут або відомі в даній галузі, будуть розпізнані як такі, що мають застосовність для одержання інших сполук винаходу. Приклади У прикладах, які описуються нижче, якщо інакше не вказано, всі температури встановлені надалі в градусах Цельсію. Реактиви були придбані у комерційних постачальників, таких як наприклад Aldrich Chemical Company, Lancaster, TCI або Maybridge, і використовувались без подальшого очищення, якщо інакше не вказано. Реакції, викладені надалі нижче, проводили зазвичай під позитивним тиском азоту або аргону або з сушильною трубою (якщо інакше не встановлено) у безводних розчинниках, і реакційні посудини звичайно оснащували гумовими діафрагмами для введення субстратів і реактивів через шприц. Скляну посудину осушували в печі і/або теплом. Колонкову хроматографію здійснювали на системі Biotage (Виробник: Dyax Corporation), яка має колонку силікагелю або картридж кремнезему SepPak (Waters). Спектри 1Н-ЯМР реєстрували на приладі Varian, який працює при 400МГц. Спектри 1Н-ЯМР одержували як розчини CDCІ3 (надано у м.ч.), використовуючи хлороформ як посилальний стандартний (7,25м.ч.). Інші розчинники ЯМР використовувались за потреби. Коли повідомлялись пікові мультиплети, використовували наступні скорочення: с (синглет). д (дуплет), т (триплет), м (мультиплет), уш. (уширений), дд (дуплет дуплетів), дт (дуплет триплетів). 31 90659 32 Приклад 1 Приготування (Е)-2-метокси-N-((4-(3-метил-4феноксифеніламіно)хіназолін-6іл)метиленаміно)ацетамідину Стадія А: (6-Гідразонометилхіназолін]в-4-іл)(3-метил-4-феноксифеніл)амін одержують за допомогою додавання гідразину (50мг, 1,00ммоль) до розчину 4-(3-метил-4-феноксифеніламіно)хіназолін-6-карбальдегіду (250мг, 0,70ммоль) в 1:1 суміші DCM:IPA (6мл). Після перемішування при кімнатній температурі протягом 4 годин, надлишковий гідразин і розчинник видаляють під зниженим тиском з тим, щоб одержати бажаний гідразон як коричневу тверду речовину, яку переносять на наступну стадію без очищення. Стадія В: (Е)-2-Метокси-N-((4-(3-метил-4феноксифеніламіно)хіназолін-6іл)метиленаміно)ацетамідин одержують за допомогою додавання (6-гідразонометилхіназолін-4-іл)(3-метил-4-феноксифеніл)аміну (30мг, 0,081ммоль) до перемішуваної суміші Et3N (20мг, 0,19ммоль) і метилового ефіру 2метоксіацетімідової кислоти (20мг, 0,20ммоль) в 1:1 суміші DCM:IPA (4мл). Після перемішування реакційної суміші при 50°С протягом 1 години, її охолоджують до кімнатної температури і перемішують протягом 16 годин. Концентрування і очищення колонковою хроматографією (10:8:1 ЕtOАс:Гексани:МеОН) забезпечує бажаний продукт (16мг, 45%). MS ESI (+) m/z 441 (М+1) виявлено; 1Н-ЯМР (400мГц, CD3OD) δ 8,64 (с, 1Н), 8,49 (с, 1H), 8,41 (м, 2H), 7,76 (д, 1Н), 7,63 (д, 1Н), 7,55 (дд, 1Н), 732 (м, 2Н), 7,05 (м, 1Н), 6,93 (м, 3Н), 4,13 (с, 2Н), 3,45 (с, 3Н), 3,41 (с, 1Н), 2,24 (с, 3Н). Наступні сполуки (Приклади 2-5) одержують, як описано у Прикладі 1, використовуючи відповідний хіназолін-6-альдегід, гідразин та імідат. Приклад 2 (Е)-2-Метокси-Н-метил-N-((4-(3-метил-4феноксифеніламіно)хіназолін-6іл)метиленаміно)ацетамідин MS АРСІ (+) m/z 455 (М+1) виявлено; 1Н-ЯМР (400мГц, CD3OD) δ 8,48 (с, 1Н), 8,23 (с, 1Н), 8,26 (д, 1H), 7,91 (с, 1Н), 7,77 (д, 1H), 7,64 (д, 1H), 7,54 (дд, 1Н), 7,32 (м, 2Н), 7,05 (м, 1Η), 6,94 (м, 3Н), 4,55 (с, 2Н), 3,72 (м, 1Н), 3,54 (с, 3Н), 2,25 (с, 3Н), 2,15 (с, 3Н). Приклад 3 (Е)-N-((4-(4-(3-Фторбензилокси)-3хлорфеніламіно)хіназолін-6-іл)метиленаміно)-2метоксіацетамідин MS АРСІ (+) m/z 493,495 (M+1, зразок) виявлено; 1Н-ЯМР (400мГц, DMSO-D6) δ 8,75 (с, 1H), 8,59 (с, 1H), 8,46 (д, 1H), 8,40 (с, 1H), 8,03 (д, 1H), 7,76 (м, 2Н), 7,47 (м, ЇЙ), 7,31 (м, 3Н), 7,19 (м, 1Н), 5,27 (с, 2Н), 4,02 (с, 2Н), 3,34 (м, 4Н). Приклад 4 (Е)-N-(4-(3-метил-4-(6-метилпiридин-3iлокси)фенiламiно)хіназолін-6-іл)метиленаміно-2метоксіацетамідин MS ESI (+) m/z 456 (M+1) виявлено; 1Н-ЯМР (400MHz, CD3OD) δ 8,63 (с, 1Н). 8,5 (с, 1H), 8,41 (м, 2Н), 8,12 (с, 1H), 7,79 (д, 1H), 7,7 (с, 1Н), 7,61(д, 1H), 7,26 (м, 2H), 7,01 (д, 1Н), 4,12 (с, 2Н), 3,43 (с, 3Н), 2,52 (с, 3Н). 2,12 (с, 3Н). Приклад 5 (Е)-N-((4-(4-(3-Фторбензилокси)-3хлорфеніламіно)хіназолін-6-іл)метиленаміно)ацетамідин MS ESI (+) m/z 463,465 (M+1, зразок СІ) виявлено; 1Н-ЯМР (400MHz, CD3OD) δ 8,64 (с, 1H), 8,52 (с, 1Н), 8,42 (м, 2H), 7,92 (с, 1Н), 7,78 (д, 1Н), 7,6 (д, 1Н), 7,4 (м, 1Н), 7,31 (д, 1Н), 7,25 (д, 1Н), 7,19 (д, 1Н), 7,06 (т, 1Н), 5,21 (с, 2Н), 2,06 (с, 3Н). Приклад 6 Приготування N4-[3-хлор-4-(3фторбензилокси)феніл]-N6-(4,5-дигідро-оксазол-2іл)хіназолін-4,6-діаміну Стадія А: N-4-[3-хлор-4-(3фторбензилокси)феніл]-N6-(2-феніл-N-ціаноізосечовина)хіназолін-4,6-діамін одержують за допомогою перемішування N-4-[3-хлор-4-(3фторбензилокси)феніл]хіназолін-4,6-діаміну (0,63г, 1,60ммоль) і дифеніл N-ціанокарбонимідату (1,0г, 33 4,20ммоль), в THF (20мл), DCE (10мл) і t-BuOH (10мл) при кімнатній температурі протягом 2 годин, потім при 80-90°С протягом 3 годин. Додають додаткові 0,40г дифеніл N-ціанокарбонимідату. Після перемішування при 80-90°С протягом 3 годин, реакційну суміш охолоджують до кімнатної температури і концентрують. Додають DCM (100мл), і тверду речовину виділяють фільтруванням через лійку з пористого скла і висушують, одержуючи 0,67г (77,6%) жовто-коричневого матеріалу. Стадія В: N4-[3-хлор-4-(3фторбензилокси)феніл]-N6-(4,5-дигідрооксазол-2іл)хіназолін-4,6-діамін одержують за допомогою додавання 2-амінотанолу (10мг, 0,164ммоль) до суміші N-4-[3-хлор-4-(3-фторбензилокси)феніл]N6-(2-феніл-N-ціаноізосечовина)хіназолін-4,6діаміну (30мг, 0,056ммоль) в 1:1 ТНР:ізопропіловий спирт (2мл) і нагрівання до 100°С протягом 20 годин. Реакційну суміш концентрують під зниженим тиском і очищують колонковою хроматографією (5% МеОН в етилацетаті) з тим, щоб забезпечити бажаний продукт як тверду речовину білого кольору (19мг, 74%). MS ESI (+) m/z 464,466 (М+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, ацетон-d6) δ 8,52 (с, 1Н), 8,43 (бс, 1Н), 8,17 (д, 1Н), 7,85 (дд, 1H), 7,74 (д, 1H), 7,70 (д, 1Н), 7,48 (м, 1H), 7,38 (д, 1Н), 7,35 (д, 1Н), 7,21 (д, 1Н), 7,12 (м, 1Н), 5,29 (с, 2Н), 4,42 (т, 2Н), 3,93 (т, 2Н). Приклад 7 Приготування N4-[3-хлор-4-(3фторбензилокси)феніл-N6-(3а,4,6,6а-тетрагідрофуро[3,4-d]оксазол-2-іл)хіназолін-4,6-діаміну N4-[3-хлор-4-(3-фторбензилокси)феніл]-N6(3а,4,6,6а-тетрагідрофуро[3,4-d]оксазол-2іл)хіназолін-4,6-діамін одержують за допомогою додавання тioCDI (27мг, 0,152ммоль) до перемішуваного розчину N4-[3-хлор-4-(3фторбензилокси)-феніл]хіназолін-4,6-діаміну (60мг, 0,152ммоль) в 1:1 THF:DCM (8мл). Через 3 години 2-аміно-циклопентанол (30мг, 0,30ммоль) додають і реакційну суміш перемішують протягом 4 годин. Розчинник видаляють під зниженим тиском і одержану тіосечовину порошкують діетиловим ефіром. Сиру тіосечовину суспендують в THF (10мл) і 1Μ NaOH у воді (0,38мл) додають з наступним додаванням 1 Μ TsCl розчину в THF (0,17мл). Через 1 годину реакційну суміш розбавляють EtOAc і водою, і фази розділяють. Водну фазу екстрагують EtOAc і об'єднані органічні екстракти висушують (Na2SO4) і концентрують. Очищення колонковою хроматографією (10:5:1 EtOAc:Гексани:МеОН) забезпечує бажаний продукт (50мг, 65%). MS АРСІ (+) m/z 506, 508 (М+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, CD3CN) δ 8,49 (с, 1Н), 8,23 (бс, 1Н), 7,94 (с, 1H), 7,73 (м, 2H), 7,59 (м, 2Н), 7,45 (м, 1 Η), 7,35 (д, 1Н), 7,29 (д, 1Н), 90659 34 7,19-7,10 (м, 3Н), 5,23 (с, 2Н), 5,18 (м, 1Н), 4,66 (м, 1Н), 4,11 (д, 1Н), 3,96 (д, 1Н), 3,56 (дд, 2Н). Наступні сполуки (Приклади 8-56) одержують як описано у Прикладі 7, використовуючи відповідний хіназолін-6-анілін і аміно спирт. Приклад 8 N4-[3-хлор-4-(3-фторбензилокси)феніл]-N6(3,8-діокса-1-аза-спіро[4,5]дец-1-ен-2-іл)хіназолін4,6-діамін MS АРСІ (+) m/z 534,536 (M+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, CD3CN) δ 8,50 (с, 1H), 8,12 (с, 1Н), 7,99 (с, 1Н), 7,73 (д, 1Н), 7,60 (д, 1Н), 7,47 (м, 1Н), 7,34 (д, 1Н), 7,29 (д, 1Н), 7,15 (д, 1Н), 7,11 (д, 1Н), 5,23 (с, 2Н), 4,19 (м, 2Н), 3,88 (м, 2Н), 3,59 (м, 2Н), 3,30 (м, 2Н), 1,78 (м, 5Н). Приклад 9 N6-(3,8-Діокса-1-аза-спіро[4,5]дец-1-ен-2-іл)N4-[3-метил-4-(6-метилпіридин-3ілокси)феніл]хіназолін-4,6-діамін MS АРСІ (+) m/z 497 (M+1) виявлено; 1Н-ЯМР (400мГц, CD3OD) δ 8,44 (с, 1Н), 8.19 (бс, 1Н), 8,13 (д, 1Н), 7,71 (м, 3Н), 7,63 (дд, 1Н), 7,29 (м, 2Н), 7,00 (д, 1Н), 4,30 (с, 2Н), 3,97 (м, 2Н), 3,55 (м, 2Н), 2,50 (с, 3Н), 2,27 (с, 3Н), 1,96 (м, 2Н), 1,77 (м, 2Н). Приклад 10 2-(4-[3-метил-4-(6-метилпіридин-3ілокси)феніламіно]хіназолін-6-іламіно}-3а,4,6,6атетрагідропіроло[3,4-d]оксазол-5-карбонової кислоти трет-бутиловий ефір MS APCI (+) m/z 568 (M+1) виявлено. Приклад 11 N4-[3-Метил-4-(6-метилпіридин-3ілокси)феніл]-N6-(4,5,6,6а-тетрагідро-3аНпіроло[3,4-d]оксазол-2-іл)хіназолін-4,6-діамін N4-[3-метил-4-(6-метилпiридин-3iлокси)фенiл]-N6-(4,5,6,6а-тетрагiдро-3аНпіроло[3,4-d]оксазол-2-іл)хіназолін-4,6-діамін одержують з 2-{4-[3-метил-4-(6-метилпіридин-3 35 ілокси)феніламіно]хіназолін-6-іламіно}-3а,4,6,6атетрагідропіроло[3,4-d]оксахол-5-карбонової кислоти трет-бутилового ефіру стандартними способами зняття захисту ВОС, використовуючи TFA в метилен хлориді. MS APCI (+) m/z 468 (М+1) виявлено; 1Н-ЯМР (400мГц, CD3OD) δ 8,42 (с, 1Н), 8,21 (бс, 1Н), 8,13 (д, 1Н), 7,68 (м, 2Н), 7,60 (м, 2Н), 7,28 (м, 2Н), 6,98 (д, 1Н), 5,18 (м, 1Н), 4,74 (м, 1Н), 3,34 (д, 1Н), 3,16 (д, 1Н), 2,86 (м, 2Н), 2,50 (с, 3Н), 2,26 (с, 3Н). Приклад 12 1-(2-{4-[3-метил-4-(6-метилпіридин-3ілокси)феніламіно]хіназолін-6-іламіно]-3а,4,6,6атетрагідропіроло[3,4-d]оксазол-5-іл)етанон 1-(2-{4-[3-метил-4-(6-метилпіридин-3ілокси)феніламіно]хіназолін-6-іламіно}-3а,4,6,6атетрагідропіроло[3,4-d]оксазол-5-іл)етанон одержують з N4-[3-метил-4-(6-метилпіридин-3ілокси)феніл]-N6-(4,5,6,6а-тетрагідро-3аНпіроло[3,4-d]оксазол-2-іл)хіназолін-4,6-діаміну стандартними способами ацетилування, використовуючи оцтовий ангідрид в суміші піридину і метилен хлориду. MS APCI (+) m/z 510 (М+1) виявлено; 1 Н-ЯМР (400мГц, CD3OD) δ 8,44 (с, 1Η), 8,26 (д, 1Н), 8,13 (д, 1Н), 7,71 (м, 2Н), 7,63 (м, 2Η), 7,28 (м, 2Н), 7,00 (д, 1Н), 5,28 (м, 1Н), 4,89 (м, 1Н), 4,15 (д, 0,5 Н), 4,03 (м, 1Н), 3,84 (д, 0,5Н), 3,75 (м, 1Н), 3,47 (м, 1Н), 2,50 (с, 3Н), 2,27 (с, 3Н), 2,09 (д, 3Н). Приклад 13 N4-[3-метил-4-(6-метилтридин-3-ілокси)феніл]N6-(3-окса-1,8-дiаза-спіро[4,5]дец-1-ен-2іл)хіназолін-4,6-діамін N4-[3-мeтил-4-(6-мeтилпipидин-3iлoкcи)фeнiл]-N6-(3-oкca-1,8-діазаспіро[4,5]дец-1ен-2-іл)хіназолін-4,6-діамін одержують з 2-{4-[3метил-4-{6-метилпіридин-3ілокси)феніламіно]хіназолін-6-іламіно}-3-окса-1,8діаза-спіро[4,5]дец-1-ен-8-карбонової кислоти трет-бутилового ефіру стандартними способами зняття захисту ВОС, використовуючи TFA в метилен хлориді. MS ESI (+) m/z 496 (М+1) виявлено; 1 Н-ЯМР (400мГц, CD3OD) δ 8,43 (с, 1Н), 8.39 (с, 1Н), 8,12 (д. 1H), 7,70 (м, 3Н), 7,61 (дд, 1Н), 7,28 (м, 2Н), 6,98 (д, 1Н), 3,45 (м, 2Н), 3,32 (м, 2Н), 3,25 (м, 2Н) 2,50 (с, 3Н), 2,32 (м, 2Н), 2,25 (с, 3Н), 2,01 (м, 2Н). Приклад 14 90659 36 1-(2-{4-[3-метил-4-(6-метилпіридин-3ілокси)феніламіно]хіназолін-6-іламіно}-3-окса-1,8діазаспіро[4,5]дец-1-ен-8-іл)етанон 1-(2-{4-[3-метил-4-(6-метилпіридин-3ілокси)феніламіно]хіназолін-6-іламіно}-3-окса-1,8діаза-спіро[4,5]дец-1-ен-8-іл)етанон одержують з N4-[3-метил-4-(6-метилпіридин-3-ілокси)феніл]-N6(3-окса-1,8-діаза-спіро[4,5]дец-1-ен-2-іл)-хіназолін4,6-діаміну стандартними способами ацетилування, використовуючи оцтовий ангідрид в суміші піридину і метилен хлориду. Приклад 15 N6-(4,4-диметил-4,5-дигідро-оксазол-2-іл)N4[3-метил-4-(6-метилпiридин-3ілокси)феніл]хіназолін-4,6-діамін АРСІ (+) m/z 455 (М+1) виявлено; 1Н-ЯМР (400мГц, CD3OD) δ 8,42 (с, 1Н), 8,12 (д, 1Н), 7,70 (м, 4Н), 7,60 (м, 3Н), 7,28 (м, 2Н), 6,99 (д, 1Н), 4,13 (с, 2Н), 2,50 (с, 3Н), 2,26 (с, 3Н), 1,40 (с, 6Н). Приклад 16 N4-[3-хлор-4-(піридин-2-ілметокси)феніл-N6(1-окса-3,8-діазаспіро[4,5]дец-2-ен-2-іл)хіназолін4,6-діамін N4-[3-хлор-4-(піридин-2-ілметокси)феніл]-N6(1-окса-3,8-діазасіро[4,5]дец-2-ен-2-іл)хіназолін4,6-діамін одержують з 2-{4-[3-хлор-4-(піридин-2ілметокси)-феніламіно]хіназолін-6-іламіно}-1-окса3,8-діазаспіро[4,5]дец-2-ен-8-карбонової кислоти трет-бутилового ефіру стандартними способами зняття захисту ВОС, використовуючи TFA в метилен хлориді. MS ESI (+) m/z 516, 518 (М+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, CDCІ3) δ 8,61 (с, 1Н), 8,58 (д, 1Н), 8,22 (бс, 1Н), 7,97 (д, 1H), 7,70 (м, 2Н), 7,67 (д, 1Н), 7,64 (дд, 1H), 7,35 (д, 1H), 7,26 (м, 1H). 7,02 (д, 1Н), 5,31 (с, 2Н), 3,73 (с, 2Н), 3,05 (м. 2Н), 2,96 (м, 2Н), 1,97 (м, 2Н), 1,80 (м, 2Н). 37 90659 38 Приклад 17 1-(2-{4-[3-метил-4-(6-метилпіридин-3ілокси)феніламіно]хіназолін-6-іламіно}-1-окса-3,8діазаспіро[4,5]дец-2-ен-8-іл)етанон 1-(2-{4-[3-метил-4-(6-метилпіридин-3ілокси)феніламіно]хіназолін-6-іламіно}-1-окса-3,8діаза-спіро[4,5]дец-2-ен-8-іл)етанон одержують з 2-{4-[3-метил-4-(6-метилпіридин-3ілокси)феніламіно]хіназолін-6-іламіно}-1-окса-3,8діазаспіро[4,5]дец-2-ен-8-карбонової кислоти третбутилового ефіру стандартними способами зняття захисту ВОС, використовуючи TFA в метилен хлориді, з наступними стандартними способами ацетилування, використовуючи оцтовий ангідрид в суміші піридину і метилен хлориду. MS ESI (+) m/z 538 (M+1), виявлено; 1Н-ЯМР (400мГц, CDCІ3) δ 8,68 (с, 1Н), 8,28 (д, 1Н), 7,83 (д, 1Н), 7,64 (с, 1Н), 7,52 (д, 2Н), 7,48 (д, 2Н), 7,12 (м, 3Н), 6,93 (д, 1Н), 3,69 (м, 2Н), 2,53 (с, 3Н). 2,29 (с, 3Н), 2,14 (с, 3Н), 2,02 (м, 2Н), 1,78 (м, 2Н), 1,30 (м, 2Н), 0,87 (м, 2Н). Приклад 18 N4-метил-2-(4-[3-метил-4-(6-метилпіридин-3ілокси)феніламіно]хіназолін-6-іламіно}-4,5дигідрооксазол-4-іл)метанол MS ESI (+) m/z 471 (М+1) виявлено; 1Н-ЯМР (400мГц, CDCІ3) δ 8,54 (с, 1Н), 8,19 (д, 1Н), 8,16 (бс, 1Н), 7,72 (м, 2Н), 7,58 (дд, 1Н), 7,48 (дд, 1Н), 7,19 (дд, 1Н), 7,13 (д, 1Н), 6,95 (д, 1Н), 4,39 (д, 1Н), 4,01 (д, 1Н), 3,42 (с, 2Н), 2,52 (с, 3Н), 2,29 (с. ЗН), 1,39 (с, 3Н). Приклад 19 N4-[3-хлор-4-(3-фторбензилокси)феніл]-N6(1,8-діокса-3-аза-спіро[4,5]дец-2-ен-2-іл)хіназолін4,6-діамін MS ESI (+) m/z 534 (M+1) виявлено; 1Н-ЯМР (400мГц, CDCІ3) δ 8,64 (с, 1Н), 8,25 (бс, 1H), 7,78 (м, 2H), 7,60 (бс, 1Н), 7,49 (д, 1Н), 7,44 (д, 1Н), 7,35 (м, 2Н), 7,23 (м, 2Н), 7,02 (м, 1Н), 6,94 (д, 1Н), 5,15 (с, 2Н), 3,81 (м, 4Н), 3,69 (м, 2Н), 1,94 (м, 2Н), 1,87 (м, 2Н). Приклад 20 N6-(1,8-Дiокса-3-азаспiро[4,5]дец-2-ен-2-iл)N4-[3-метил-4-(6-метилпiридин-3ілокси)феніл]хіназолін-4,6-діамін MS ESI (+) m/z 497 (M+1) виявлено; 1Н-ЯМР (400мГц, CDCІ3) δ 8,67 (с, 1Н), 8,27 (д, 1Н), 7,82 (д, 1Н), 7,69 (с, 1Н), 7,63 (с, 1Н), 7,50 (м, 2Н), 7,12 (м, 4Н), 6,92 (д, 1Н), 3,82 (м, 4Н), 3,67 (м, 2Н), 2,53 (с, 3Н), 2,29 (с, 3Н), 1,95 (м, 2Н), 1,88 (м, 2Н). Приклад 21 N4-[3-хлор-4-(тіазол-2-ілметокси)феніл]-N6-(5метил-4,5-дигідрооксазол-2-іл)хіназолін-4,6-діамін MS ESI (+) m/z 467,469 (M+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, DMSO-D6) δ 9,60 (с, 1Н), 8,52 (с, 1Н), 8,20 (бс, 1Н), 8,13 (с, 1Н), 7,93 (д, 1Н), 7,87 (д, 1Н), 7,82 (д, 1Н), 7.71 (д, 2Н), 7,38 (д, 1Н), 5,60 (с, 2Н), 4,82 (м, 1Н), 3,80 (м, 1Н), 3,26 (м, 1Н), 2,56 (с, 3Н). Приклад 22 N4-[3-хлор-4-(тiазол-2-iлметокси)фенiл]-N6{4,5-дигідро-оксазол-2-іл)хіназолін-4,6-діамін MS ESI (+) m/z 453,455 (M+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, DMSO-D6) δ 9,54 (с, 1Н), 8,47 (с, 1H), 8,07 (бс, 1H), 7,86 (д, 1H), 7,80 (д, 1H), 7,76 (д, 1Н), 7,66 (м, 2Н), 7,32 (д, 1H), 5,55 (с, 2H), 4,38 (м, 2Н), 3,62 (м, 1Н), 3,18 (м, 1Н). Приклад 23 М6-(5,5-диметил-4,5-дигідрооксазол-2-іл)-N4[3-метил-4-(6-метилпіридин-3-ілоху)фенілхіназолін-4,6-діамін MS АРСІ (+) m/z 455 (M+1) виявлено; 1Н-ЯМР (400мГц, CD3OD) δ 8,42 (с, 1H), 8,17 (бс, 1H), 8,12 (д, 1H). 7,70 (д, 1H), 7,69 (с, 1H), 7,61 (дд, 1H), 7,57 (дд, 1Н), 7,28 (м, 2Н), 6,98 (д, 1H), 3,64 (с, 2H), 2,50 (с, 3Н), 2,26 (с, 3Н), 1,51 (с, 6Н). Приклад 24 39 N4-[3-хлор-4-(піридин-2-ілметокси)феніл]-N6(4,5-дигідрооксазол-2-іл)хіназолін-4,6-діамін MS ESI (+) m/z 447,449 (M+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, DMSO-D6) δ 9,53 (бс, 1Н), 8,59 (д, 1H), 8,45 (с, 1H), 8,05 (бс, 1H), 7,89 (м, 2H), 7,74 (д, 1Н), 7,65 (д, 1Н), 7,58 (д, 1Н), 7,38 (дд, 1Н), 7,25 (д, 1Н), 5,29 (с, 2Н), 4,38 (м, 2Н), 3,62 (м, 2Н). Приклад 25 N4-[3-хлор-4-(піридин-2-ілметокси)феніл]-N6(4-метил-4,5-дигідрооксазол-2-іл)хіназолін-4,6діамін MS ESI (+) m/z 461,463 (M+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, DMSO-D6) δ 9,51 (бс, 1Н), 8,58 (д, 1Н), 8,44 (с, 1Н), 8,04 (бс, 1Н), 7,86 (м, 1Н), 7,72 (д, 1Н), 7,58 (м, 3Н), 7,34 (м. 1Н), 7,22 (д, 1Н), 5,27 (с, 2Н), 4,74 (м, 1Н), 3,72 (м, 1Н), 3,15 (м, 1Н), 1,32 (с, 3Н). Приклад 26 N4-[3-хлор-4-(тіазол-2-ілметокси)феніл]-N6(1,8-дioкса-3-аза-спіро[4,5]дец-2-ен-2-іл)хіназолін4,6-діамін MS ESI (+) m/z 523,525 (М+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, CDCІ3) δ 8,64 (с, 1Н), 7,78 (м, 2Н), 7,60 (бс, 1Н), 7,50 (д, 1Н), 7,43 (д, 1Н), 7.35 (м, 1Н), 7,23 (м, 2Н), 7,02 (м, lH), 6,95 (д, 1H), 5,15 (с, 2H), 3,81 (м, 4Н), 3,69 (м, 2Н), 1,94 (м, 2Н), 1,87 (м, 2Н). Приклад 27 N4-[3-хлор-4-(3-фторбензилокси)феніл]-N6-(5метил-4,5-дигідрооксазол-2-іл]хіназолін-4,6-діамін 1 Н-ЯМР (400мГц, CD3OD) δ 8,50 (с, 1Н), 8,12 (бс, 1Н), 8,02 (д, 1Н), 7,97 (д, 1Н), 7,60 (дд, 1Н), 7,44 (м, 2Н), 7,34 (д, 1Н), 7,29 (д, 1Н), 7,14 (д, 1Н), 7,10 (д, 1Н), 5,22 (с, 2Н), 4,79 (м, 1Н), 3,87 (м, 1Н), 3,36 (м, 1Н), 1,40 (д, 3Н). Приклад 28 90659 40 N4-[3-метил-4-(6-метилпіридин-3ілокси)феніл]-N6-(3а,4,6,6а-тетрагідрфуро[3,4d]оксазол-2-іл)хіназолін-4,6-діамін MS АРСІ (+) m/z 469 (M+1) виявлено; 1Н-ЯМР (400мГц, CD3OD) δ 8,43 (с, 1H), 8,26 (бс, 1H), 8,13 (д, 1Н), 7,70 (м, 3Н), 7,62 (м, 2Н), 7,29 (м, 2Н), 7,08 (с, 1Н), 7,00 (д, 1Н), 5,25 (м, 1Н), 4,82 (м, 1Н), 4,17 (д, 1Н), 4,02 (д, 1Н), 3,64 (м, 2Н), 2,50 (с, 3Н), 2,27 (с, 3Н). Приклад 29 (1RS,5SR)-1-(5-метил-2-(4-(3-метил-4-(6метилпіридин-3-ілокси)феніламіно)хіназолін-6іламіно)-4,5-дигідрооксазол-5-іл)етанол MS ESI (+) m/z 485 (M+1) виявлено; 1Н-ЯМР (400мГц, CDCІ3) δ 8,58 (с, 1Н), 8,22 (д, 1H), 8,17 (бс, 1H), 7,74 (д, 1H). 7,71 (д, 1Н), 7,60 (дд, 1Н), 7,36 (д, 1Н), 7,16 (дд, 1Н), 7,10 (д, 1Н), 6,94 (д, 1Н), 4,02 (д, 1Н), 3,92 (м, 1Н), 3,55 (д, 1Н), 2,52 (с, 3Н), 2,28 (с, 3Н), 1,45 (с, 3Н), 1,22 (м, 4Н). Приклад 30 N6-(4,5-Дигідрооксазол-2-іл)-N4-[3-метил-4-(6метилпіридин-3-ілокси)феніл]-хіназолін-4,6-діамін MS ESI (+) m/z 427 (M+1) виявлено; 1Н-ЯМР (400мГц, DMSO-D6) δ 9,53 (с, 1Н), 8,45 (с, 1Н), 8,18 (д, 1Н), 7,80 (с, 1Н), 7,72 (д, 1Н), 7,65 (д, 1Н), 7,21 (м, 3Н), 6,96 (д, 1Н), 4,38 (м, 2Н), 3,64 (м, 2Н), 2,51 (с, 3Н), 2,20 (с, 3Н). Приклад 31 (2-{4-[3-хлор-4-(піридин-2ілметокси)феніламіно]хінахолін-6-іламіно}-4метил-4,5-дигідро-оксазол-4-іл)метанол MS ESI (+) m/z 491,493 (M+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, CDCІ3) δ 8,57 (с, 1Н), 8,56 (с, 1Н), 8,13 (бс, 1Н), 7,97 (д, 1Н), 7,81 (т, 1Н), 7,73 (м, 2Н), 7,61 (дд, 1Н), 7,44 (дд, 1Н), 7,29 (м, 1Н), 41 7,04 (д, 1Н), 5,30 (с, 2Н), 3,64 (д, 1Н), 3,52 (д, 1Н), 3,43 (с, 2Н), 1,26 (с, 3Н). Приклад 32 (1RS,5SR)-1-(2-(4-(3-хлор-4-(піридин-2ілметокси)феніламіно)хіназолін-6-іламіно)-5метил-4,5-дигідрооксазол-5-іл)етанол MS ESI (+) m/z 505, 507 (M+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, CDCІ3) δ 8,60 (с, 1Н), 8,58 (с, 1Н), 8,12 (бс, 1Н), 7,95 (д, 1Н), 7,77 (т, 1Н), 7,72 (д, 1Н), 7,69 (д, 1Н), 7,63 (дд, 1Н), 7,25 (м, 2Н), 7,02 (д, 1Н), 5,30 (с, 2Н), 4,07 (д, 1Н), 3,98 (кв, 1Н), 3,56 (д, 1Н), 1,45 (с, 3Н), 1,22 (д, 3Н). Приклад 33 N4-[3-хлор-4-(тiазол-2-ілметокси)феніл]-N6(4,4-диметил)-4,5-дигідрооксазол-2-іл)хіназолін4,6-діамін MS АРСІ (+) m/z 481,483 (M+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, DMSO-D6) δ 9,52 (с, 1Н). 8,47 (с, 1Н), 8,09 (с, 1Н), 7,96 (бс, 1Н), 7,86 (д, 1Н), 7,81 (д, 1Н), 7,78 (д, 1Н), 7,65 (д, 1Н), 7,32 (д, 1Н), 5,55 (с, 2Н), 3,17 (д, 2Н), 1,28 (с, 6Н). Приклад 34 (1-RS,5SR)-1-(2-(4-(4-(3-фторбензилокси)-3хлорфеніламіно)хіназолін-6-іламіно)-5-метил-4,5дигідрооксазол-5-іл)етанол MS ESI (+) m/z 522, 524 (M+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, CDCІ3) δ 8.57 (с, 1Н). 8,10 (бс, 1Н), 7,91 (д, 1Н). 7,70 (д, 1Н), 7,65 (дд, 1Н), 7,36 (м, 1Н), 7,30 (м, lH), 7,24 (м, 2Н), 7,00 (м, 1H), 6,98 (д, 1H), 5,16 (с, 2H), 4,05 (д, 1Н), 3,95 (кв, 1Н). 3,55 (д, 1Н), 1,45 (с, 3Н), 1,21 (д, 3Н). Приклад 35 N6-(5-метил-4,5-дигідрооксазол-2-іл)-N4-[3метил-4-(6-метилпіридин-3-ілокси)феніл]хіназолін4,6-діамін 90659 42 MS APCI (+) m/z 441 (М+1) виявлено; 1Н-ЯМР (400мГц, DMSO-D6) δ 9,51 (с, 1Н), 8,45 (с, 1H), 8,18 (д, 1H), 7,80 (с, 1Н), 7,69 (т, 3Н), 7,23 (м, 2Н), 6,96 (д, 1Н), 4,77 (т, 1Η), 4,13 (т, 1Η), 6,73 (т, 1Η), 2,44 (с, 3Н), 2,20 (с, 3Н), 1,36 (д, 3Н). Приклад 36 N4-[3-хлор-4-(тiазол-2-iлметокси)фенiл]-N6-(4метил-4,5-дигідрооксазол-2-іл)хіназолін-4,6-діамін MS APCI (+) m/z 467,469 (М+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, DMSO-D6) δ 9,53 (с, 1Н), 8,47 (с, 1H), 8,09 (с, 1Н), 7,86 (д, 1Н), 7,81 (д, 1Н), 7,77 (д, 1Н), 7,69 (м, 3Н), 7,32 (д, 1Н), 7,02 (с, 1Н), 5,54 (с, 2Н), 4,47 (м, 1Н), 3,99 (м, 1Н), 3,90 (м, 1Н), 1,18 (д, 3Н). Приклад 37 N4-[3-хлор-4-(піридин-2-ілметокси)феніл]-N6(1,8-діокса-3-аза-спіро[4,5]дец-2-ен-2-іл)хіназолін4,6-діамін MS APCI (+) m/z 517, 519 (М+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, CDCІ3) δ 8,66 (с, 1Н), 8,60 (д, 1H), 7,87 (с, 1H), 7,81 (д, 1Н), 7,76 (м, 1Н), 7.66 (д, 1Н), 7,51 (м, 2Н), 7,44 (д, 1H), 7,25 (м, 1H), 7,01 (д, 1H), 5,30 (с, 2H), 3,82 (м, 4Н), 3,75 (м, 1Н), 3,69 (м, 1Н), 1,95 (м, 2Н), 1,87 (м, 2Н). Приклад 38 N6-(4-метил-4,5-дигідрооксазол-2-iл)-N4-[3метил-4-(6-метилпіридин-3-ілокси)феніл]хіназолін4,6-діамін MS АРСІ (+) m/z 441 (M+1) виявлено; 1Н-ЯМР (400мГц, DMSO-D6) δ 9,51 (с, 1Н), 8,44 (с, 1Н), 8,15 (д, 1Н), 8,05 (бс, 1Н), 7,79 (с, 1Н), 7,71 (д, 1Н), 7.62 (м, 2Н), 7,20 (м, 2Н), 6,99 (с, 1Н), 6,93 (д, 1Н), 4,45 (м, 1Н), 4,02 (м, 1Н), 3,87 (м, 1Н), 2,41 (с, 3Н),2,18(с, 3Н), 1,17 (д, 3Н). Приклад 39 43 90659 44 N4-[3-хлор-4-(пiридин-2-iлметокси)фенiл]-N6(4,5-дигідрооксазол-2-iл)-хіназолін-4,6-діамін MS ESI (+) m/z 447,449 (M+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, DMSO-D6) δ 9,53 (бс, 1Н), 8,59 (д, 1Н), 8,45 (с, 1Н), 8,05 (бс, 1Н), 7,89 (м, 2Н), 7,74 (д, 1Н), 7,65 (д, 1Н), 7,58 (д, 1Н), 7,38 (дд, 1Н), 7,25 (д, 1Н), 5,29 (с, 2Н), 4,38 (м, 2Н), 3,62 (м, 2Н). Приклад 40 N4-[3-хлор-4-(піридин-2-ілметокси)феніл]-N6(4-метил-4,5-дигідрооксазол-2-іл)хіназолін-4,6діамін MS ESI (+) m/z 461.463 (M+1, зразок СІ) виявлено; 1Н-ЯМР (400МГц. DMSO-D6) δ 9,51 (бс, 1Н), 8,58 (д, 1H), 8,44 (с, 1H), 8,04 (бс, 1Н), 7,86 (м, 1H), 7,72 (д, 1Н), 7,58 (м. ЗН), 7,34 (м, 1Н), 7,22 (д, 1Н), 5,27 (с, 2Н), 4,74 (м, 1Н), 3,72 (м, 1Н). 3,15 (м, 1Н), 1,32 (с, 3Н). Приклад 41 N4-[3-хлор-4-(тіазол-2-ілметокси)феніл]-N6(3а,4,6,6а-тетрагідрофуро[3,4-d]оксазол-2іл)хіназолін-4,6-діамін MS АРСІ (+) m/z 495,497 (M+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, CD3OD) δ 8.47 (с, 1Н), 8,23 (ушир., с, 1Н), 7,95 (д, 1Н), 7,83 (д, 1Н), 7,71 (д, 1Н), 7,66 (дд, 1Н), 7,63 (д, 1Н), 7,59 (дд, 1Н), 7,21 (д, 1Н), 5,50 (с, 2Н), 4.19 (д, 1Н), 4.05 (д, 1Н), 3,65 (м,2Н), 3,19 (м,2Н). Приклад 42 N4-[3-метил-4-(тіазол-2-ілметокси)феніл]-N6(3а,4,6,6а-тетрагідрофуро[3,4-d]оксазол-2іл)хіназолін-4,6-діамін MS ESI (+) m/z 475 (M+1) виявлено; 1Н-ЯМР (400мГц, CD3OD) δ 8,37 (с, 1Н), 8,25 (ушир с, 1Н), 7,83 (д, 1Н), 7,69 (д, 1Н), 7,65 (д, 1Н), 7,59 (м, 1Н), 7,52 (м, 2Н), 7,07 (д. 1Н), 5,46 (с, 2Н), 4,17 (д, 1Н), 4,02 (д, 1Н), 3,64 (м, 2Н), 2.34 (м, 5Н). Приклад 43 N4-[3-хлор-4-(тіазол-2-ілметокси)феніл]-N6(1,8-діокса-3-аза-спіро[4,5]дец-2-ен-2-іл)хіназолін4,6-діамін MS ESI (+) m/z 523,525 (M+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, CDCІ3) δ 8,64 (с, 1Н), 7,78 (м, 2Н), 7,60 (бс, 1H), 7,50 (д, 1Н), 7,43 (д. 1Н), 7,35 (м, 1Н), 7,23 (м, 2Н), 7,02 (м, 1Н), 6,95 (д, 1Н), 5,15 (с, 2Н), 3,81 (м, 4Н), 3,69 (м, 2Н), 1,94 (м, 2Н), 1,87 (м, 2Н). Приклад 44 N4-[3-хлор-4-(піридин-2-ілметокси)феніл]-N6(5-метил-4,5-дигідрооксазол-2-іл)хіназолін-4,6діамін MS ESI (+) m/z 461,463 (M+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, DMSO-D6) δ 9,51 (с, 1H), 8,58 (с, 1H), 8,44 (с, 1H), 8,04 (м, 2H), 7,86 (м, 1Н), 7,63 (м, 4Н). 7,34 (м, 1Н), 7,22 (д, 1Н), 5,27 (с, 2Н), 4,74 (м, 1Н), 3,72 (м, 1Н), 3,15 (м, 1Н), 1,34 (д, 3H). Приклад 45 N4-[3-хлор-4-(3-фторбензилокси)феніл]-N6-(4метил-4,5-дигідрооксазол-2-іл)хіназолін-4,6-діамін MS ESI (+) m/z 478 (M+1) виявлено; 1Н-ЯМР (400мГц, DMSO-D6) δ 9,51 (с, 1H), 8,46 (с, 1H), 8,06 (м, 2Н), 7,76 (д, 1Н), 7,64 (д, 1Н), 7,47 (м, 2Н), 7,32 (м, 2Н), 7,24 (д, 1Н), 7,18 (м, 1Н), 5,25 (с, 2Н), 4,47 (м, 1Н), 3,95 (м, 1Н), 3,17 (м, 1Н), 1,19 (д, 3Н). Приклад 46 N4-[3-хлор-4-(тіазол-2-ілметокси)феніл]-N6(4,5,6,6а-тетрагідро-3аН-піроло[3,4-d]оксазол-2іл)хіназолін-4,6-діамін N4-[3-хлор-4-(тіазол-2-ілметокси)феніл]-N6(4,5,6,6а-тетрагідро-3аН-піроло[3,4-d]оксазол-2іл)хіназолін-4,6-діамін одержують з 2-{4-[3-хлор-4(тіазол-2-ілметокси)феніламіно]хіназолін-6 45 іламіно}-3а,4,6,6а-тетрагідро-піроло[3,4-d]оксазол5-карбонової кислоти трет-бутилового ефіру стандартними способами зняття захисту ВОС, використовуючи TFA в метилен хлориді. MS APCI (+) m/z 1 494, 496 (М+1, зразок СІ) виявлено; Н-ЯМР (400мГц, CD3OD) δ 8,44 (с, 1Н), 8,19 (ушир, с, 1Н), 7,96 (д, 1Н), 7,83 (д, 1Н), 7,67 (м, 3Н), 7,58 (дд, 1Н), 7,22 (д, 1Н), 5,50 (с, 2Н), 5,17 (м, 1Н), 4,76 (м, 1Н), 3,32 (д, 1Н), 3,16 (д, 1Н), 2,85 (м, 2Н). Приклад 47 N4-[3-хлор-4-(піридин-2-ілметокси)феніл]-N6(4,5,6,6а-тетрагідро-3аН-піроло[3,4-d]оксазол-2іл)хіназолін-4,6-діамін N4-[3-хлор-4-(піридин-2-ілметокси)феніл]-N6(4,5,6,6а-тетрагідро-3аН-піроло[3,4-d]оксазол-2іл)хіназолін-4,6-діамін одержують з 2-{4-[3-хлор-4(піридин-2-ілметокси)феніламіно]хіназолін-6іламіно}-3а,4,6,6а-тетрагідро-піроло[3,4-d]оксазол5-карбонової кислоти трет-бутилового ефіру стандартними способами зняття захисту ВОС, використовуючи TFA в метилен хлориді. MS APCI (+) m/z 488,490 (M+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, CD3OD) δ 8,56 (д, 1Н), 8,44 (с, 1Н), 8,21 (ушир, с, 1Н), 7,91 (м, 2Н), 7,70 (м, 2Н), 7,63 (д, 1Н), 7,57 (д, 1Н), 7,39 (м, 1Н), 7,16 (д, 1Н), 5,28 (с, 2Н), 5,17 (м, 1Н), 4,78 (м, 1Н), 3,34 (д, 1Н), 3,16 (д, 1Н),2,84(м, 2H). Приклад 48 (2-{4-[3-хлор-4-(3фторбензилокси)феніламіно]хіназолін-6-іламіно}4-метил-4,5-дигідро-оксазол-4-іл)метанол MS ESI (+) m/z 508, 510 (М+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, CDCІ3) δ 8,57 (с, 1Н), 8,14 (с, 1H), 7,93 (д, 1H), 7,74 (д, 1H), 7,63 (дд, 1H), 7,37 (м, 2Н), 7,25 (м, 2Н), 7,01 (м, 2Н), 5,17 (с, 2Н), 4,38 (д, 1Н), 4,00 (д, 1Н), 3,65 (д, 1Н), 3,48 (д, 1Н), 1,38 (с, 3Н). Приклад 49 N4-[3-хлор-4-(піридин-2-ілметокси)феніл]-N6(6-окса-4-аза-спіро[2,4]гепт-4-ен-5-іл)хіназолін-4,6діамін 90659 46 MS АРСІ (+) m/z 473, 475 (M+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, CD3OD) δ 8,56 (д, 1Н), 8,45 (с, 1Н), 8,21 (с, 1Н), 7,98 (д, 1Н), 7,92 (м, 1Н), 7,72 (м, 2Н), 7,63 (м, 2Н), 7,40 (м, 1Н), 7,18 (д, 1Н), 5,28 (с, 2Н), 4,36 (с, 2Н), 1,12 (м, 2Н), 0,81 (с, 2Н). Приклад 50 (2-{4-[5-хлор-4-(піридин-2ілметокси)феніламіно]хіназолін-6-іламіно}-4гідроксиметил-4,5-дигідро-оксазол-4-іл)метанол MS ESI (+) m/z 507, 509 (M+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, DMSO-D6) δ 9,47 (с, 1H), 8,60 (д, 1H), 8,46 (с, 1H), 8,08 (с, 1H), 7,89 (м, 1H), 7,71 (м, 2H), 7,58 (д, 1Н), 7,37 (м, 1Н), 7,25 (д, 1Н), 5,29 (с, 2Н), 4,34 (м, 2Н), 3,29 (с, 4Н). Приклад 51 (R)-1-((S)-2-(4-(3-хлор-4-(тіазол-2ілметокси)феніл]аміно)хіназолін-6-іламіно)-4,5дигідрооксазол-4-іл)етанол (R)-1-((S)-2-(4-(3-хлор-4-(тіазол-2ілметокси)феніламіно)хіназолін-6-іламіно)-4,5дигідрооксазол-4-іл)етанол одержують з (1R,4S)N6-[4-(1-трет-бутоксіетил)-4,5-дигідрооксазол-2-іл]N4-[3-хлор-4-(тіазол-2-ілметокси)феніл]хіназолін4,6-діаміну стандартними способами зняття захисту, використовуючи TFA в метилен хлориді. MS ESI (+) m/z 497,499 (М+1, зразок СІ) виявлено; 1НЯМР (400мГц, DMSO-D6) δ 9,53 (с, 1Н). 8,47 (с, 1Н), 8,08 (д, 1Н), 7,87 (д, 1Н), 7,80 (д, 1Н), 7,76 (дд, 1Н), 7,66 (т. 2Н), 7,33 (д, 1Н), 5,55 (с, 2Н), 4,81 (т, 1Н), 4,37 (т, 1Η), 4,20 (т, 1Η), 3,83 (т, 1Н). 3,63 (м, 1Н), 1.06 (д, 3Н). Приклад 52 (R)-N4-[3-хлор-4-(тіазол-2-ілметокси)феніл]N6-(4-метил-4,5-дигідро-оксазол-2-іл)хіназолін-4,6діамін Одержують, використовуючи (R)-2амінопропан-1-ол. MS APCI (+) m/z 467, 469 (М+1, зразок СІ), виявлено; 1Н-ЯМР (400мГц, DMSO-D6) δ 9,53 (с, 1Н), 8,47 (с, 1Н). 8,09 (с, 1Н), 7,86 (д. 1Н), 7,81 (д, 1Н), 7,77 (д, 1Н), 7,69 (м, 3Н), 7,32 (д, 1Н), 47 90659 48 7,02 (с, 1Н), 5,54 (с, 2Н), 4,47 (т, 1Η), 3,99 (т, 1Η), 3,90 (т, 1Η), 1,18 (д, 3Н). Приклад 53 (S)-N4-[3-хлор-4-(тіазол-2-ілметокси)феніл]N6-(4-метил-4,5-дигідро-оксазол-2-іл)хіназолін-4,6діамін Одержують, використовуючи (S)-2амінопропан-1-ол. MS APCI (+) m/z 467, 469 (М+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, DMSO-D6) δ 9,53 (с, 1Н), 8,47 (с, 1H), 8,09 (с, 1H), 7,86 (д, 1H), 7,81 (д, 1H), 7,77 (д, 1H), 7,69 (м, 3Н), 7,32 (д, 1Н), 7.02 (с, 1Н), 5,54 (с, 2Н), 4,47 (м. 1Н), 3,99 (м, 1Н), 3,90 (м, 1Н), 1,18 (д, 3Н). Приклад 54 (S)-N4-[3-хлор-4-(піридин-2-ілметокси)феніл]N6-(5-метил-4,5-дигідро-оксазол-2-іл)хіназолін-4,6діамін Одержують, використовуючи (S)-1амінопропан-1-ол. MS ESI (+) m/z 461, 463 (М+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, DMSO-D6) δ 9,51 (с, 1Н), 8,58 (с, 1Н), 8,44 (с, 1H), 8,04 (м, 2H), 7,86 (м, 1Н), 7,63 (м, 4Н), 7,34 (м, 1Н), 7,22 (д, 1Н), 5,27 (с, 2Н), 4,74 (м, 1Н), 3,72 (м, 1Н), 3,15 (м, 1Н), 1,34 (д, 3Н). Приклад 55 (R)-N4-[3-хлор-4-(піридин-2-ілметокси)феніл]N6-(5-метил-4,5-дигідро-оксазол-2-іл)хіназолін-4,6діамін Одержують, використовуючи (R)-1амінопропан-1-ол. MS ESI (+) m/z 461, 463 (М+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, DMSO-D6) δ 9,51 (с, 1Н). 8,58 (с, 1H), 8,44 (с, 1H), 8,04 (м, 2H), 7,86 (м, 1Н), 7,63 (м, 4Н), 7,34 (м, 1Н), 7,22 (д, 1Н), 5,27 (с, 2Н), 4,74 (м, 1Н), 3,72 (м, 1Н), 3,15 (м, 1Н), 1,34 (д, 3Н). Приклад 56 N4-[4-(5-хлорпіридин-3-ілокси)-3-метил-феніл]N6-(4,4-диметил-4,5-дигідро-оксазол-2іл)хіназолін-4,6-діамін MS ESI (+) m/z 475 477 (m+1, зразок СІ) виявлено; 1Н-ЯМР (400мГц, DMSO-d6) δ 9,62 (бс, 1Н), 8,49 (с, 1Н). 8,37 (д, 1Н), 8,29 (д, 1Н), 8,05 (бс, 1Н). 7,87 (с, 1Н), 7,80 (д, 1Н), 7,68 (д, 1Н), 7,41 (м, 1Н), 7,10 (д. 1Н), 4,11 (с, 2Н), 2,19 (с, 3Н), 1,29 (с, 6Н). Приклад 57 N6-(4,4-диметил-4,5-дигідро-оксазол-2-іл)-N4[3-метил-4-(піридин-3-ілокси)-феніл]хіназолін-4,6діамін MS ESI (+) m/z 441 (m+1) виявлено; 1Н-ЯМР (400мГц, DMSO-d6) δ 9,54 (бс, 1H), 8,46 (с, 1H). 8,33 (д, 1H), 8,29 (д, 1H), 8,00 (бс, 1H), 7,84 (с, 1H), 7,77 (д, 1Н), 7,65 (д, 1Н), 7,37 (м, 1Η), 7,26 (м, 1Н), 7,03 (д, 1Н), 4,07 (с, 2Н), 2,19 (с, 3Н), 1,28 (с, 6Н). Приклад 58 N6-(4,4-диметил-4,5-дигідро-оксазол-2-іл)-N4[4-(5-фтор-пiридин-3-ілокси)-3-метилфеніл]хіназолін-4,6-діамін MS ESI (+) m/z 459 (m+1) виявлено; 1Н-ЯМР (400мГц, DMSO-d6) δ 9,70 (бс, 1Н), 8,51 (с, 1Н), 8,43 (д, 1Н), 8,20 (д, 1Н), 8,11 (бс, 1Н), 7,86 (с, 1Н), 7,80 (д, 1Н), 7,69 (м, 2Н), 7,29 (д, 1Η), 7,11 (д, 1Н), 4,61 (с, 2Н), 2,20 (с, 3Н), 1,30 (с, 6Н). Аміно спирти, які використовують у вищезазначених прикладах, або є відомими сполуками, або їх одержують як описано нижче. Приклад 59 Одержання (4-амінотетрагідропіран-4іл)метанолу (4-Аміно-тетрагідропіран-4-іл)метанол одержують за допомогою додавання LAH (99%, 1,2г), порціями, до перемішуваної суміші 4амінотетрагідропіран-4-карбонової кислоти гідрохлориду (2,0г, 11,0ммоль) в THF (30мл) при 0°С. Після завершення додавання реакційну суміш нагрівають до кімнатної температури і перемішують протягом 1 години. Реакційну суміш охолоджують 49 до 0°С і обережно гасять додаванням порційно Na2SO4.10H2O (4г). Реакційну суміш розбавляють етилацетатом, нагрівають до кімнатної температури і фільтрують через целіт, щоб одержати бажаний продукт. Приклад 60 Одержання 4-амінометил-4-гідроксипіперидин1-карбонової кислоти трет-бутилового ефіру 4-Амінометил-4-гідрокси-піперидин-1карбонової кислоти трет-бутиловий ефір одержують з 1-окса-6-аза-спіро[2,5]октан-6-карбонової кислоти трет-бутилового ефіру (Bourrain el al Bioorg. Med. Chem. Lett 9(23):3369-3374 (1999)). Концентрований водний NH4OH (6мл) додають до розчину 1-окса-6-аза-спіро[2,5]октан-6-карбонової кислоти трет-бутилового ефіру (0,50г, 2,3ммоль) в МеОН (4мл) при 0°С. Реакційну суміш видаляють з охолодження і дозволяють нагрітись до кімнатної температури. Через 7 годин реакційну суміш концентрують під зниженим тиском для того, щоб дати бажаний продукт як тверду речовину білого кольору. Приклад 61 Одержання 4-амінометилтетрагідро-піран-4 олу 4-Амінометил-тетрагідро-піран-4-ол одержують з 1,6-діокса-спіро[2,5]октану. Розчин МеОН (3,5мл) 1,6-діокса-спіро[2,5]октану (0,19г, 1,7ммоль) додають до концентрованого водного NH4OH (4,3мл) при 0°С. Реакційну суміш нагрівають до кімнатної температури і перемішують протягом 16 годин. Реакційну суміш концентрують під зниженим тиском і очищують колонковою хроматографією (10% МеОН, 2% Et3N в DCM) для того, щоб дати 90мг (41%) бажаного продукту як тверду речовину білого кольору. Приклад 62 Одержання (2RS,3SR)-1-аміно-2-метилбутан2,3-діолу (2RS,3SR)-1-Аміно-2-метилбутан-2,3-дiол одержують з 1,2-диметил-алілового ефіру оцтової кислоти. mСРВА (17г, 69ммоль) повільно додають до перемішуваного розчину 1,2-диметилалілового ефіру оцтової кислоти (6,80г, 53,1ммоль) в метилен хлориді (500мл). Через 4 години реакційну суміш промивають насиченим NaHCO3, водою і розсолом. Органічний шар висушують (Na2SO4) і концентрують під зниженим тиском. Очищення 90659 50 колонковою хроматографією (20% діетиловим ефіром в пентані: повторюють) дає (1-RS,2-SR)оцтової кислоти 1-(-2-метилоксираніл)етиловий ефір (3,45г, 45%). Невелику кількість (1-RS,2-SR)оцтової кислоти 1-(-2-метилоксираніл)етилового ефіру перетворюють в (2RS,3SR)-3,4-епокси-3метил-2-бутанаол (JACS (1990) 112(13):5285) обробкою K2СО3 в МеОН, щоб підтвердити відносну стереохімію цього рацемічного матеріалу. K2СО3 (1,54г, 11,1ммоль) додають до перемішуваного розчину оцтової кислоти (R*)-l-((8*)-2-метилоксираніл)етилового ефіру (1,70г, 11,8ммоль) в МеОН (12мл). Через 1 годину реакційну суміш фільтрують через целіт. Фільтрат додають повільно через додавальну лійку до 20 мл концентрованого водного NH4OH. Після перемішування протягом 16 годин реакційну суміш концентрують під зниженим тиском і очищують колонковою хроматографією (20% МеОН, 2% Et3N в DCM) для того, щоб дати 0,97г (69%) бажаного продукту як світло жовту олію. Приклад 63 Одержання N4-[3-хлор-4-(36 фторбензилокси)феніл]-N -(4,5-дигідро-оксазол-2іл)-ІЧ6-метилхіназолін-4,6-діамін Стадія А: Розчин N4-[3-хлор-4-(3фторбензилокси)феніл]хіназолін-4,6-діаміну (1,09г, 2,76ммоль) і ди-t-бутил дикарбонату (2,0г, 3,3еквів.) нагрівають в t-BuOH:DCE (1:1) в запечатаній трубці при 90-95°С протягом 20 хвилин, потім охолоджують до кімнатної температури. Леткі речовини видаляють під зниженим тиском, і продукт очищують хроматографією на силікагелі (60% EtOAc/гексани). даючи тверду речовину жовтого кольору (670мг, 49%). Стадія В: Очищений матеріал за Стадії А додають в THF (5-10мл) при 0°С, і додають LAH (1,0 розчин в THF, 1 еквівалент). Розчин нагрівають зі зворотним холодильником протягом 1 години, потім охолоджують до кімнатної температури. Реакцію розбавляють THF і гасять додаванням порціями надлишку натрій сульфат декагідрату. Реакцію фільтрують і продукт очищують хроматографією на силікагелі (100% ЕЮАс), даючи тверду речовину жовтого кольору. Стадія А: Очищений матеріал зі Стадії В (63мг, 0,15ммоль) додають в THF (3мл) і додають 2хлоретил ізоціанат (32мкл, 2,4 еквіваленти). Реакцію нагрівають при 50°С доти, доки не утвориться важкий осад. Продукт одержують як тверду речовину світло жовтого кольору вакуумним фільтруванням (26мг, 33%). Стадія D: Матеріал зі Стадії С додають в MeCN (2мл) і додають 40% KF на оксиді алюмінію (130мг, 18 еквівалентів). Суміш нагрівають зі зворотним холодильником протягом 12 годин, розбавляють MeCN і фільтрують через целіт. Хроматографія на силікагелі дає N4-[3-хлор-4-(36 фторбензилокси)феніл]-N -(4,5-дигідро-оксазол-2іл)-N6-метил-хіназолін-4,6-діамін (6мг, 25%). Додаткові сполуки даного винаходу включають: 51 90659 52 53 90659 54 55 90659 56 57 90659 58 59 90659 60
ДивитисяДодаткова інформація
Назва патенту англійськоюQuinazoline analogs as receptor tyrosine kinase inhibitors
Автори англійськоюWallace Eli, Topalov George, Lyssikatos Joseph, Buckmelter Alexandre, Zhao Qian
Назва патенту російськоюАналоги хиназолина как ингибиторы рецепторных тирозинкиназ
Автори російськоюУоллейс Эли, Топалов Георгий, Лиссикатос Джозеф, Бакмельтер Александр, Чжао Цян
МПК / Мітки
МПК: A61K 31/517, A61K 31/535, A61K 31/51, C07D 403/00, C07D 239/82
Мітки: аналоги, інгібітори, хіназоліну, тирозинкіназ, рецепторних
Код посилання
<a href="https://ua.patents.su/35-90659-analogi-khinazolinu-yak-ingibitori-receptornikh-tirozinkinaz.html" target="_blank" rel="follow" title="База патентів України">Аналоги хіназоліну як інгібітори рецепторних тирозинкіназ</a>
Попередній патент: Композиція антагоніста vegf і антипроліферативного засобу
Наступний патент: Спосіб виготовлення фільтраційної насадки у пристроях для магнітного розділення дисперсій у рідинах і газах
Випадковий патент: Вакуумний перевантажувач судновий для риби












