Похідні піразолу
Номер патенту: 110525
Опубліковано: 12.01.2016
Автори: Гелламалла Седрік, Галлей Гуідо, Норкросс Роджер, Пфлігер Філіпп
Формула / Реферат
1. Сполука формули
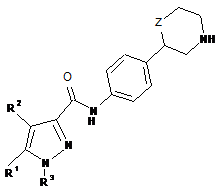 IA або
IA або
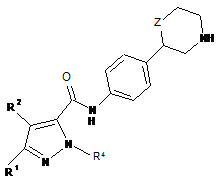 , ІВ
, ІВ
де
R1 означає водень або феніл, який, можливо, містить як замісник галоген, CN чи нижчу алкоксигрупу, або ж нижчу алкоксигрупу, заміщену галогеном;
R2 означає водень або нижчий алкіл;
R3 означає водень або нижчий алкіл або означає феніл, який, можливо, містить один чи декілька замісників, вибраних з такого: галоген, ціаногрупа чи нижча алкоксигрупа, заміщена галогеном, або означає
піридиніл, який, можливо, містить як замісник галоген або нижчий алкіл, заміщений галогеном, або означає
піримідиніл, який, можливо, містить як замісник нижчий алкіл, заміщений галогеном, або означає
піразиніл, який, можливо, містить як замісник галоген, ціаногрупу або нижчий алкіл, заміщений галогеном;
R4 означає водень, нижчий алкіл або феніл;
Ζ означає зв'язок, -CH2- або -О-;
або її фармацевтично прийнятні кислотно-адитивні солі.
2. Сполука формули ІА-1 за п. 1
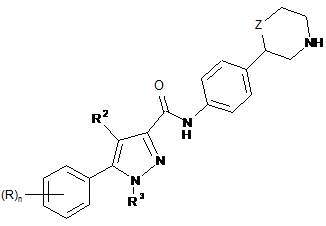 , IA-1
, IA-1
де
R означає водень, галоген, CN чи нижчу алкоксигрупу, або ж нижчу алкоксигрупу, заміщену галогеном;
R2 означає водень або нижчий алкіл;
R3 означає водень або нижчий алкіл;
Ζ означає зв'язок, -СН2- або -О-;
n дорівнює 1 або 2; якщо n = 2, то кожен R може бути визначений незалежно від іншого;
або її фармацевтично прийнятні кислотно-адитивні солі.
3. Сполука формули ІА-1 за будь-яким з пп. 1 або 2, вибрана з групи, що містить:
(S)-N-(4-(морфолін-2-іл)феніл)-5-феніл-1Н-піразол-3-карбоксамід,
(S)-1-метил-N-(4-(морфолін-2-іл)феніл)-5-феніл-1Н-піразол-3-карбоксамід,
(S)-5-(3-ціанофeніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-3-карбоксамід,
(S)-5-(3-ціанофеніл)-4-метил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксамід,
(S)-5-(5-ціано-2-фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-3-карбоксамід,
(S)-5-(3-ціано-4-фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-3-карбоксамід або
(S)-5-(3-(дифторметокси)феніл)-1-етил-N-(4-(морфолiн-2-іл)феніл)-1Н-піразол-3-карбоксамід.
4. Сполука формули ІВ-1 за п. 1
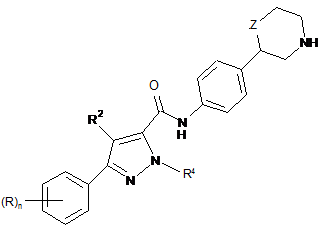 , IB-1
, IB-1
де
R означає водень, галоген, CN чи нижчу алкоксигрупу, або ж нижчу алкоксигрупу, заміщену галогеном;
R2 означає водень або нижчий алкіл;
R4 означає водень або нижчий алкіл;
Ζ означає зв'язок, -СН2- або -О-;
n дорівнює 1 або 2; якщо n = 2, то кожен R може бути визначений незалежно від іншого;
або її фармацевтично прийнятні кислотно-адитивні солі.
5. Сполука формули ІВ-1 за будь-яким з пп. 1 або 4, вибрана з групи, що містить:
(S)-3-(3-хлорфеніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(S)-3-(4-фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(S)-3-(3-метоксифеніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(S)-1-метил-N-(4-(морфолін-2-іл)феніл)-3-феніл-1Н-піразол-5-карбоксамід,
(S)-4-метил-N-(4-(морфолін-2-іл)феніл)-3-феніл-1Н-піразол-5-карбоксамід,
(S)-3-(4-метоксифеніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(S)-3-(2-фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(S)-3-(2-мeтoкcифeнiл)-N-(4-(мopфoлiн-2-iл)фeнiл)-1H-пipaзoл-5-кapбoкcaмiд,
(S)-3-(2-хлорфеніл)-N-(4-(морфолiн-2-iл)феніл)-1Н-піразол-5-карбоксамід,
(S)-3-(3,4-диметоксифеніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(R)-3-(4-xлopфeнiл)-N-(4-(мopфoлiн-2-iл)фeнiл)-1H-пipaзoл-5-кapбoкcaмiд,
(R)-3-(2-хлорфеніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(S)-3-(4-хлорфеніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(R)-3-(3-хлорфеніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(R)-3-(3-метоксифеніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(S)-3-(3-хлорфеніл)-1-метил-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(R)-1-метил-N-(4-(морфолін-2-іл)феніл)-3-феніл-1Н-піразол-5-карбоксамід,
(S)-3-(4-ціанофeніл)-1-метил-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(S)-3-(4-фторфеніл)-1-метил-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(S)-3-(3-метоксифеніл)-1-метил-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(S)-3-(3-ціанофeніл)-1-метил-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(S)-3-(3-ціанофeніл)-1-етил-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(S)-3-(4-ціанофeніл)-1-етил-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(S)-3-(3-ціанофеніл)-N-(4-(піперидин-3-іл)феніл)-1Н-піразол-5-карбоксамід,
(R)-3-(3-ціанофеніл)-N-(4-(піперидин-3-іл)феніл)-1Н-піразол-5-карбоксамід,
(рац)-3-(3-ціанофеніл)-N-(4-(піролідин-3-іл)феніл)-1Н-піразол-5-карбоксамід,
(S)-3-(3-(дифторметокси)феніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(S)-3-(3-(дифторметокси)феніл)-N-етил-1Н-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід,
(S)-3-(3-ціано-2-фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-5-карбоксамід, або
(S)-3-(3-(дифторметокси)феніл)-1-метил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід.
6. Сполука формули ІА-2 за п. 1
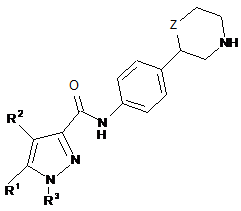 , IA-2
, IA-2
де
R1 означає водень;
R2 означає водень або нижчий алкіл;
R3 означає феніл, який, можливо, містить один чи декілька замісників, вибраних з такого: галоген, ціаногрупа чи нижча алкоксигрупа, заміщена галогеном, або означає піридиніл, який, можливо, містить як замісник галоген або нижчий алкіл, заміщений галогеном, або означає
піримідиніл, який, можливо, містить як замісник нижчий алкіл, заміщений галогеном, або означає піразиніл, який, можливо, містить як замісник галоген, ціаногрупу або нижчий алкіл, заміщений галогеном;
Ζ означає зв'язок, -СН2- або -О-;
або її фармацевтично прийнятні кислотно-адитивні солі.
7. Сполука формули ІА-2 за будь-яким з пп. 1 або 6, вибрана з групи, що містить:
(S)-1-(4-фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-3-карбоксамід,
(R)-1-(4-фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-3-карбоксамід,
(S)-1-(5-хлорпіридин-2-іл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-3-карбоксамід,
(S)-N-(4-(морфолін-2-іл)феніл)-1-(5-(трифторметил)піридин-2-іл)-1H-піразол-3-карбоксамід,
(S)-1-(4-ціанофеніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-3-карбоксамід,
(R)-N-(4-(морфолін-2-іл)феніл)-1-(5-(трифторметил)піридин-2-іл)-1Н-піразол-3-карбоксамід,
(S)-1-(4-(дифторметокси)феніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-3-карбоксамід,
(R)-1-(4-(дифторметокси)феніл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-3-карбоксамід,
(S)-N-(4-(морфолін-2-іл)феніл)-1-(5-(трифторметил)піримідин-2-іл)-1Н-піразол-3-карбоксамід,
(S)-1-(6-хлорпіразин-2-іл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-3-карбоксамід,
(S)-1-(3-хлорпіразин-2-іл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксамід,
(S)-1-(5-хлорпіразин-2-іл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-3-карбоксамід,
(S)-N-(4-(морфолiн-2-іл)фенiл)-1-(6-(трифторметил)піримідин-4-іл)-1Н-піразол-3-карбоксамід,
(S)-N-(4-(морфолін-2-іл)феніл)-1-(6-(трифторметил)піразин-2-іл)-1Н-піразол-3-карбоксамід,
(S)-1-(5-ціанопіразин-2-іл)-N-(4-(морфолін-2-іл)феніл)-1Н-піразол-3-карбоксамід або
(S)-N-(4-(морфолін-2-іл)феніл)-1-(2-(трифторметил)піримідин-4-іл)-1Н-піразол-3-карбоксамід.
8. Сполука формули ІВ-2 за п. 1
 , IB-2
, IB-2
де
R1 означає водень;
R2 означає водень або нижчий алкіл;
R4 означає водень, нижчий алкіл або феніл;
Ζ означає зв'язок, -СН2- або -О-;
або її фармацевтично прийнятні кислотно-адитивні солі.
9. Сполука за будь-яким з пп. 1 або 8, причому такою сполукою є (S)-N-(4-(морфолін-2-іл)феніл)-1-феніл-1Н-піразол-5-карбоксамід.
10. Спосіб одержання сполуки формул ІА або IB, розкритої в будь-якому з пп. 1-9, який включає
а) відщеплення N-протекторної групи від сполуки формули
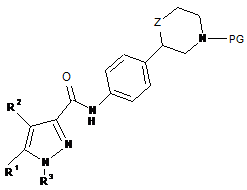 4-A або
4-A або
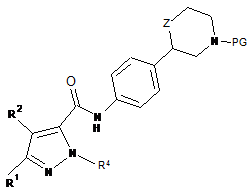 , 4-В
, 4-В
з одержанням сполуки формули
 IA або
IA або
 , ІВ
, ІВ
де PG означає N-протекторну групу, вибрану з -С(О)О-трет-бутилу, а інші значення радикалів описані в п. 1, і,
при необхідності, перетворення одержаної сполуки на фармацевтично прийнятні кислотно-адитивні солі.
11. Сполука за будь-яким з пп. 1-9, виготовлена способом за п. 10.
12. Фармацевтична композиція, яка включає сполуку за будь-яким з пп. 1-9 та фармацевтично прийнятний носій та/або допоміжну речовину.
13. Фармацевтична композиція, яка включає сполуку за будь-яким з пп. 1-9 та фармацевтично прийнятний носій та/або допоміжну речовину для застосування в лікуванні депресії, тривожного неврозу, біполярного розладу, синдрому дефіциту уваги та гіперактивності (СДУГ), розладів, пов'язаних зі стресом, психічних розладів, шизофренії, неврологічних захворювань, хвороби Паркінсона, нейродегенеративних розладів, хвороби Альцгеймера, епілепсії, мігрені, гіпертонії, наркотичної залежності та токсикоманії, метаболічних розладів, розладів приймання їжі, діабету, діабетичних ускладнень, тучності, дисліпідемії, розладів споживання та засвоєння енергії, розладів та порушень функції гомеостазу температури тіла, розладів сну та добового біоритму та серцево-судинних захворювань.
14. Сполука за будь-яким з пп. 1-9 для застосування як терапевтично активної речовини.
15. Сполука за будь-яким з пп. 1-9 для застосування як терапевтично активної речовини в лікуванні депресії, тривожного неврозу, біполярного розладу, синдрому дефіциту уваги та гіперактивності (СДУГ), розладів, пов'язаних зі стресом, психічних розладів, шизофренії, неврологічних захворювань, хвороби Паркінсона, нейродегенеративних розладів, хвороби Альцгеймера, епілепсії, мігрені, гіпертонії, наркотичної залежності та токсикоманії, метаболічних розладів, розладів приймання їжі, діабету, діабетичних ускладнень, тучності, дисліпідемії, розладів споживання та засвоєння енергії, розладів та порушень функції гомеостазу температури тіла, розладів сну та добового біоритму та серцево-судинних захворювань.
16. Застосування сполуки за будь-яким з пп. 1-9 для виготовлення лікарських засобів для терапевтичного та/або профілактичного лікування депресії, тривожного неврозу, біполярного розладу, синдрому дефіциту уваги та гіперактивності (СДУГ), розладів, пов'язаних зі стресом, психічних розладів, шизофренії, неврологічних захворювань, хвороби Паркінсона, нейродегенеративних розладів, хвороби Альцгеймера, епілепсії, мігрені, гіпертонії, наркотичної залежності та токсикоманії, метаболічних розладів, розладів приймання їжі, діабету, діабетичних ускладнень, тучності, дисліпідемії, розладів споживання та засвоєння енергії, розладів та порушень функції гомеостазу температури тіла, розладів сну та добового біоритму та серцево-судинних захворювань.
Текст
Реферат: Даний винахід стосується сполук формули Z Z NH NH O R 2 O R N H 2 N H N R де 1 N N R 3 R IA або 1 ІВ N R4 , UA 110525 C2 (12) UA 110525 C2 1 R означає водень або феніл, який, можливо, містить як замісник галоген, CN чи нижчу алкоксигрупу, або ж нижчу алкоксигрупу, заміщену галогеном; 2 R означає водень або нижчий алкіл; 3 R означає водень або нижчий алкіл або означає феніл, який, можливо, містить один чи декілька замісників, вибраних з такого: галоген, ціаногрупа чи нижча алкоксигрупа, заміщена галогеном, або означає піридиніл, який, можливо, містить як замісник галоген або нижчий алкіл, заміщений галогеном, або означає піримідиніл, який, можливо, містить як замісник нижчий алкіл, заміщений галогеном, або означає піразиніл, який, можливо, містить як замісник галоген, ціаногрупу або нижчий алкіл, заміщений галогеном; 4 R означає водень, нижчий алкіл або феніл; Ζ означає зв'язок, -СН2- або -О-; або її фармацевтично прийнятні кислотно-адитивні солі. Було показано, що сполуки формул ІА та IB мають високу спорідненість відносно рецепторів слідових амінів (TAARs), зокрема TAAR1. Ці сполуки можна застосовувати для лікування депресії, тривожного неврозу, біполярного розладу, синдрому дефіциту уваги та гіперактивності (СДУГ), розладів, пов'язаних зі стресом, психічних розладів, таких як шизофренія, неврологічних захворювань, таких як хвороба Паркінсона, нейродегенеративних розладів, таких як хвороба Альцгеймера, епілепсії, мігрені, гіпертонії, наркотичної залежності та токсикоманії та метаболічних розладів, таких як розлади приймання їжі, діабету, діабетичних ускладнень, тучності, дисліпідемії, розладів споживання та засвоєння енергії, розладів та порушень функції гомеостазу температури тіла, розладів сну та добового біоритму та серцево-судинних захворювань. UA 110525 C2 Даний винахід стосується сполук формули Z NH Z NH O N H 2 R N H R N 1 R O 2 4 N 3 R N R 1 IA або R N IB де 1 R позначає водень або феніл, який, можливо, містить як замісник галоген, CN чи нижчу алкоксигрупу, або ж нижчу алкоксигрупу, заміщену галогеном; 2 R позначає водень або нижчий алкіл; 3 R позначає водень або нижчий алкіл або ж позначає феніл, який, можливо, містить один чи декілька замісників, вибраних з такого: галоген, ціаногрупа чи нижча алкоксигрупа, заміщена галогеном, або позначає піридиніл, який, можливо, містить як замісник галоген або нижчий алкіл, заміщений галогеном, або позначає піримідиніл, який, можливо, містить як замісник нижчий алкіл, заміщений галогеном, або позначає піразиніл, який, можливо, містить як замісник галоген, ціаногрупу або нижчий алкіл, заміщений галогеном; 4 R позначає водень, нижчий алкіл або феніл; Z позначає зв’язок, -CH2- або -O-; або їх фармацевтично прийнятних кислотно-адитивних солей. Даний винахід включає усі рацемічні суміші, усі їх відповідні енантіомери та/або оптичні ізомери. Крім того, усі таутомерні форми сполук формул IA та IB також охоплені даним винаходом. Ми знайшли, що сполуки формул IA та IB мають сильну спорідненість до рецепторів слідових амінів (TAARs), зокрема, TAAR1. Запропоновані сполуки можна застосовувати для лікування депресії, тривожного неврозу, біполярного розладу, синдрому дефіциту уваги з гіперактивністю (СДУГ), розладів, пов’язаних зі стресом, психічних розладів, таких як шизофренія, неврологічних захворювань, таких як хвороба Паркінсона, нейродегенеративних розладів, таких як хвороба Альцгеймера, епілепсії, мігрені, гіпертонії, наркотичної залежності та токсикоманії, а також метаболічних розладів, таких як розлади приймання їжі, діабету, діабетичних ускладнень, тучності, дисліпідемії, розладів споживання та засвоєння енергії, розладів та порушення функції гомеостазу температури тіла, розладів сну та добового біоритму та серцево-судинних захворювань. Деякі фізіологічні ефекти (тобто серцево-судинні ефекти, гіпотензія, індукція седативного ефекту), про які повідомлялося для сполук, здатних зв’язуватися з адренергічними рецепторами (WO02/076950, WO97/12874 або EP 0717 037), можуть бути розцінені як небажані побічні ефекти для лікарських засобів, призначених для лікування захворювань центральної нервової системи, описаних вище. Таким чином, бажано одержати лікарські засоби, селективні до TAAR1 рецепторів, але не до адренергічних рецепторів. Об’єкти за даним винаходом демонструють селективність до TAAR1 рецепторів порівняно з адренергічними рецепторами, зокрема, гарну селективність порівняно з людськими та щурячими адренергічними рецепторами альфа 1 та альфа 2. Класичні біогенні аміни (серотонін, норадреналін, адреналін, дофамін, гістамін) відіграють важливу роль як нейротрансмітери в центральній та периферичній нервовій системі [1]. Їх синтез та зберігання, а також їх деградація та зворотне захоплення після вивільнення жорстко регулюються. Відомо, що дисбаланс рівня біогенних амінів є причиною зміненої функції мозку при багатьох патологічних станах [2-5]. Інший клас ендогенних аміносполук, так звані слідові аміни (TAs), в значній мірі пересікається з класичними біогенними амінами стосовно структури, метаболізму та внутрішньоклітинної локалізації. TAs включають паратирамін, β-фенілетиламін, триптамін та октопамін, і вони є присутніми в нервовій системі ссавців, у цілому, в більш низьких концентраціях, порівняно з класичними біогенними амінами [6]. 1 UA 110525 C2 Їх дисрегуляцію зв’язують з різними психічними захворюваннями, такими як шизофренія та депресія [7], а також з іншими станами, такими як синдром дефіциту уваги з гіперактивністю, головний біль, хвороба Паркінсона, наркотична залежність та токсикоманія, а також розлади приймання їжі [8,9]. Протягом тривалого часу існування TA-специфічних рецепторів лише гіпотетично припускалося на основі анатомічно дискретних високоафінних TA-зв’язуючих сайтів в ЦНС людини та інших ссавців [10,11]. Таким чином, вважалося, що фармакологічні ефекти TAs опосередковані добре відомим механізмом класичних біогенних амінів, як за рахунок запуску їх вивільнення або інгібування їх зворотного захоплення, так і за рахунок перехресної реакції з їх рецепторними системами [9,12,13]. Ця точка зору істотно змінилася у зв’язку з недавнім відкриттям декількох членів нового сімейства GPCRs, рецепторів слідових амінів (TAARs) [7,14]. У людини присутні 9 генів TAAR (включаючи 3 псевдогени), у мишей – 16 генів (включаючи 1 псевдоген). Гени TAAR не містять інтронів (за одним винятком: TAAR2 містить 1 інтрон) та розташовані один за одним в одному й тому самому сегменті хромосоми. Така філогенетична спорідненість рецепторних генів, згідно з ретельним порівнянням схожості GPCR-фармакофорів та фармакологічними даними, вказує на те, що ці рецептори утворюють три різних підсімейства [7,14]. TAAR1 належить до першого підкласу, який складається з чотирьох генів (TAAR1-4), висококонсервативних у людини та гризунів. TAs активують TAAR1 через Gαs. Було показано, що дисрегуляція TAs робить свій внесок в етіологію багатьох захворювань, таких як депресія, психоз, синдром дефіциту уваги з гіперактивністю, наркотична залежність та токсикоманія, хвороба Паркінсона, головний біль, розлади приймання їжі, метаболічні розлади, і тому ліганди TAAR1 мають великий потенціал для лікування подібних захворювань. Таким чином, існує підвищений інтерес до розширення знань про рецептори слідових амінів. Об’єктами даного винаходу є нові сполуки формул IA та IB, а також їх фармацевтично прийнятні солі, їх застосування для виготовлення лікарських засобів для лікування захворювань, пов’язаних з біологічною функцією рецепторів слідових амінів, їх одержання, а також лікарські засоби на основі сполуки за даним винаходом для контролю або профілактики захворювань, таких як депресія, тривожний невроз, біполярний розлад, синдром дефіциту уваги з гіперактивністю, розлади, обумовлені стресом, психічні розлади, такі як шизофренія, неврологічні розлади, такі як хвороба Паркінсона, нейродегенеративні розлади, такі як хвороба Альцгеймера, епілепсія, мігрень, наркотична залежність та токсикоманія, а також метаболічні розлади, такі як розлади приймання їжі, діабет, діабетичні ускладнення, тучність, дисліпідемія, розлади споживання та засвоєння енергії, розлади та порушення функції гомеостазу температури тіла, розлади сну та добового біоритму, а також серцево-судинні розлади. Кращими показаннями до застосування сполук за даним винаходом є депресія, психоз, хвороба Паркінсона, тривожність та синдром дефіциту уваги з гіперактивністю (СДУГ), а також діабет. В даному тексті термін "нижчий алкіл" позначає насичену групу з лінійним чи розгалуженим ланцюгом, яка містить від 1 до 7 атомів вуглецю, таку як метил, етил, пропіл, ізопропіл, н-бутил, ізобутил, 2-бутил, трет-бутил тощо. Кращими алкільними групами є групи, що містять 1–4 атоми вуглецю. В даному тексті термін "нижча алкоксигрупа" позначає групу, у якій алкільний залишок є таким, як визначено вище, і він приєднаний через атом кисню. Термін "галоген" позначає хлор, йод, фтор та бром. В даному тексті термін "нижча алкоксигрупа, заміщена галогеном", позначає алкоксигрупу, розкриту вище, у якій принаймні один атом водню заміщений галогеном. Термін "фармацевтично прийнятні кислотно-адитивні солі" охоплює солі неорганічних та органічних кислот, таких як хлористоводнева кислота, азотна кислота, сірчана кислота, фосфорна кислота, лимонна кислота, мурашина кислота, фумарова кислота, малеїнова кислота, оцтова кислота, бурштинова кислота, винна кислота, метансульфонова кислота, птолуолсульфонова кислота тощо. Одним із здійснень даного винаходу є сполуки формули IA-1 2 UA 110525 C2 Z NH O N H 2 R N N 3 R (R)n IA-1 де R позначає водень, галоген, CN чи нижчу алкоксигрупу, або ж нижчу алкоксигрупу, заміщену галогеном; 2 R позначає водень або нижчий алкіл; 3 R позначає водень або нижчий алкіл; Z позначає зв’язок, -CH2- або -O-; n дорівнює 1 або 2; якщо n = 2, то кожен R може бути визначений незалежно від іншого; або їх фармацевтично прийнятні кислотно-адитивні солі, наприклад, такі сполуки: (S)-N-(4-(морфолін-2-іл)феніл)-5-феніл-1H-піразол-3-карбоксамід, (S)-1-метил-N-(4-(морфолін-2-іл)феніл)-5-феніл-1H-піразол-3-карбоксамід, (S)-5-(3-ціанофеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксамід, (S)-5-(3-ціанофеніл)-4-метил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксамід, (S)-5-(5-ціано-2-фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксамід, (S)-5-(3-ціано-4-фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксамід, або (S)-5-(3-(дифторметокси)феніл)-1-етил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3карбоксамід. Ще одним здійсненням даного винаходу є сполуки формули IB-1 Z NH O N H 2 R 4 N R (R)n N IB-1 де R позначає водень, галоген, CN чи нижчу алкоксигрупу, або ж нижчу алкоксигрупу, заміщену галогеном; 2 R позначає водень або нижчий алкіл; 4 R позначає водень або нижчий алкіл; Z позначає зв’язок, -CH2- або -O-; n дорівнює 1 або 2; якщо n = 2, то кожен R може бути визначений незалежно від іншого; або їх фармацевтично прийнятні кислотно-адитивні солі, наприклад, такі сполуки: (S)-3-(3-хлорфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (S)-3-(4-фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (S)-3-(3-метоксифеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (S)-1-метил-N-(4-(морфолін-2-іл)феніл)-3-феніл-1H-піразол-5-карбоксамід, (S)-4-метил-N-(4-(морфолін-2-іл)феніл)-3-феніл-1H-піразол-5-карбоксамід, (S)-3-(4-метоксифеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (S)-3-(2-фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (S)-3-(2-метоксифеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (S)-3-(2-хлорфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (S)-3-(3,4-диметоксифеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (R)-3-(4-хлорфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (R)-3-(2-хлорфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, 3 UA 110525 C2 (S)-3-(4-хлорфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (R)-3-(3-хлорфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (R)-3-(3-метоксифеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (S)-3-(3-хлорфеніл)-1-метил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (R)-1-метил-N-(4-(морфолін-2-іл)феніл)-3-феніл-1H-піразол-5-карбоксамід, (S)-3-(4-ціанофеніл)-1-метил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (S)-3-(4-фторфеніл)-1-метил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (S)-3-(3-метоксифеніл)-1-метил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (S)-3-(3-ціанофеніл)-1-метил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (S)-3-(3-ціанофеніл)-1-етил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (S)-3-(4-ціанофеніл)-1-етил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (S)-3-(3-ціанофеніл)-N-(4-(піперидин-3-іл)феніл)-1H-піразол-5-карбоксамід, (R)-3-(3-ціанофеніл)-N-(4-(піперидин-3-іл)феніл)-1H-піразол-5-карбоксамід, (рац) 3-(3-ціанофеніл)-N-(4-(піролідин-3-іл)феніл)-1H-піразол-5-карбоксамід, (S)-3-(3-(дифторметокси)феніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, (S)-3-(3-(дифторметокси)феніл)-1-етил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5карбоксамід, (S)-3-(3-ціано-2-фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксамід, або (S)-3-(3-(дифторметокси)феніл)-1-метил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5карбоксамід. Одним із здійснень даного винаходу є сполуки формули IA-2, Z NH O N H 2 R N 1 R N 3 R IA-2 де 1 R позначає водень 2 R позначає водень або нижчий алкіл; 3 R позначає феніл, який, можливо, містить один чи декілька замісників, вибраних з такого: галоген, ціаногрупа чи нижча алкоксигрупа, заміщена галогеном, або позначає піридиніл, який, можливо, містить як замісник галоген або нижчий алкіл, заміщений галогеном, або позначає піримідиніл, який, можливо, містить як замісник нижчий алкіл, заміщений галогеном, або позначає піразиніл, який, можливо, містить як замісник галоген, ціаногрупу або нижчий алкіл, заміщений галогеном; Z позначає зв’язок, -CH2- або -O-; або їх фармацевтично прийнятні кислотно-адитивні солі, наприклад, такі сполуки: (S)-1-(4-фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксамід, (R)-1-(4-фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксамід, (S)-1-(5-хлорпіридин-2-іл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксамід, (S)-N-(4-(морфолін-2-іл)феніл)-1-(5-(трифторметил)піридин-2-іл)-1H-піразол-3-карбоксамід, (S)-1-(4-ціанофеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксамід, (R)-N-(4-(морфолін-2-іл)феніл)-1-(5-(трифторметил)піридин-2-іл)-1H-піразол-3-карбоксамід, (S)-1-(4-(дифторметокси)феніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксамід, (R)-1-(4-(дифторметокси)феніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксамід, (S)-N-(4-(морфолін-2-іл)феніл)-1-(5-(трифторметил)піримідин-2-іл)-1H-піразол-3карбоксамід, (S)-1-(6-хлорпіразин-2-іл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксамід, (S)-1-(3-хлорпіразин-2-іл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксамід, (S)-1-(5-хлорпіразин-2-іл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксамід, (S)-N-(4-(морфолін-2-іл)феніл)-1-(6-(трифторметил)піримідин-4-іл)-1H-піразол-3карбоксамід, 4 UA 110525 C2 (S)-N-(4-(морфолін-2-іл)феніл)-1-(6-(трифторметил)піразин-2-іл)-1H-піразол-3-карбоксамід, (S)-1-(5-ціанопіразин-2-іл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксамід, або (S)-N-(4-(морфолін-2-іл)феніл)-1-(2-(трифторметил)піримідин-4-іл)-1H-піразол-3карбоксамід. Ще одним здійсненням даного винаходу є сполуки формули IB-2, Z NH O R N H 1 N R 2 4 R N IB-2 де 1 R позначає водень; 2 R позначає водень або нижчий алкіл; 4 R позначає водень, нижчий алкіл або феніл; Z позначає зв’язок, -CH2- або -O-; або їх фармацевтично прийнятні кислотно-адитивні солі, наприклад, така сполука: (S)-N-(4-(морфолін-2-іл)феніл)-1-феніл-1H-піразол-5-карбоксамід. Запропоновані сполуки формул IA та IB та їх фармацевтично прийнятні солі можна одержати способами, відомими в даній галузі техніки, наприклад, способами, описаними нижче, що включають a) відщеплення N-протекторної групи від сполук формули Z N PG Z N PG O N H 2 R N H R N 1 R O 2 4 N 3 R N R 1 4-A або R N 4-B з одержанням сполуки формули Z NH Z NH O N H 2 R N 1 R O N H 2 R 4 N 3 R 1 N R R N IA або IB де PG позначає N-протекторну групу, вибрану з –C(O)O-трет-бутилу та інших сутностей, описаних вище, і, за бажанням, перетворення одержаних сполук на фармацевтично прийнятні кислотноадитивні солі. Одержання сполук формул IA та IB за даним винаходом можна проводити послідовними або збіжними шляхами синтезу. Синтез сполук за даним винаходом наведений далі на схемах 1–3 та в описі 54 конкретних прикладів. Навички, необхідні для проведення реакцій та очищення одержаних продуктів, доступні фахівцям в даній галузі техніки. Замісники та індекси, 5 UA 110525 C2 використовувані в наведеному далі описі способів, мають значення, розкриті раніше, якщо не вказане інше. Більш докладно, сполуки формул IA та IB можна одержати представленими нижче способами, способами, наведеними в прикладах, або аналогічними способами. Придатні умови реакцій для індивідуальних реакційних стадій відомі фахівцю в даній галузі техніки. Послідовність стадій не обмежується представленою на схемах 1–3; навпаки, в залежності від вихідних речовин та їх відносної реакційної здатності, послідовність стадій реакції можна вільно змінювати. Вихідні речовини або є у продажу, або можуть бути одержані способами, аналогічними наведеним нижче, способами, описаними в джерелах, посилання на які наведені в описі чи в прикладах, або ж способами, відомими в даній галузі техніки. Замісники розкриті вище. 6 UA 110525 C2 Стадія A: Одержання аміду можна здійснити реакцією конденсації між аміном 2 та сполуками хлорангідриду кислоти 3-A-2 в галогенованих розчинниках, таких як дихлорметан або 1,2-дихлоретан, або ефірних розчинниках, таких як діетиловий ефір, діоксан, ТГФ, DME (диметиловий ефір) або TBME (трет-бутилметиловий ефір), в присутності органічної основи, такої як триетиламін або N,N-діізопропілетиламін. Приклади придатних амінів 2 включають N-захищені похідні морфоліну, такі як 2-a [CAS 1002726-96-6], похідні піперидину, такі як 2-b [CAS 875798-79-1], похідні піролідину, такі як 2-c [CAS 908334-28-1]. Кращими умовами є триетиламін в ТГФ при кімнатній температурі протягом 18 год. Як варіант, одержання аміду можна здійснити реакцією конденсації між аміном 2 та карбоновими кислотами 3-A-1 в присутності зшивального реагенту, такого як DCC, EDC, TBTU, HBTU або HATU, в присутності органічної основи, такої як триетиламін, N,N-діізопропілетиламін або N-метилморфолін, в галогенованих розчинниках, таких як ДМФ, дихлорметан або 1,2дихлоретан, або ефірних розчинниках, таких як діетиловий ефір, діоксан, ТГФ, DME або TBME. Кращими умовами є HBTU з N-метилморфоліном в ДМФ при 60 °C протягом 18 год. Стадія B: Видалення N-протекторної BOC групи можна здійснити за допомогою мінеральних кислот, таких як HCl, H2SO4 або H3PO4, або органічних кислот, таких як CF3COOH, CHCl2COOH, HOAc або п-толуолсульфонова кислота, в розчинниках, таких як CH 2Cl2, CHCl3, ТГФ, діоксан, MeOH, EtOH або H2O, при 0-80 °C. Кращими умовами є HCl в діоксані при 60 °C протягом 1-20 год. Умови процесу є такими саме, як описано на схемі 1. 7 UA 110525 C2 де 2 3 Y позначає галоген, R позначає водень та нижчий алкіл; R позначає феніл, який, можливо, містить один чи декілька замісників, вибраних з такого: галоген, ціаногрупа чи нижча алкоксигрупа, заміщена галогеном, або позначає піридиніл, який, можливо, містить як замісник галоген або нижчий алкіл, заміщений галогеном, або позначає піримідиніл, який, можливо, містить як замісник нижчий алкіл, заміщений галогеном, або позначає піразиніл, який, можливо, містить як замісник галоген, ціаногрупу або нижчий алкіл, заміщений галогеном; і Z позначає зв’язок, -CH2- або -O-; Стадія A: Одержання аміду 6 можна здійснити реакцією конденсації між аміном 2 та 1Hпіразол-3-карбоновою кислотою 5 за допомогою селективного зшивального агента, такого як 4(4,6-диметокси-1,3,5-триазин-2-іл)-4-метилморфолінію хлорид, в розчиннику, такому як метанол, етанол або ізопропанол, при температурі від 0 °C до 50 °C, протягом від 1 год. до 24 год. Кращими умовами є: використання 4-(4,6-диметокси-1,3,5-триазин-2-іл)-4-метилморфолінію хлориду в метанолі, протягом 1 год. при 0 °C, з подальшим перемішуванням 18 год. при кімнатній температурі. Приклади придатних амінів 2 включають N-захищені похідні морфоліну, такі як 2-a [CAS 1002726-96-6], похідні піперидину, такі як 2-b [CAS 875798-79-1], похідні піролідину, такі як 2-c [CAS 908334-28-1]. Стадія B: Утворення зв’язку C-N можна здійснити обробкою арилгаліду 7 або гетероарилгаліду 7 піразолом 6 в присутності паладієвого або мідного каталізатора, ліганду та основи, в розчинниках, таких як діоксан, DME, ТГФ, толуол, ДМФ та ДМСО, при підвищеній температурі, наприклад, за допомогою каталізованої паладієм реакції Бухвальда-Хартвіга. Кращими умовами є каталітичний комплекс трис(дибензиліденацетон)дипаладію з хлороформом, каталізатор 9,9-диметил-4,5-біс(дифенілфосфіно)ксантен (ксантфос) та карбонат цезію в діоксані, в запаяній трубці, при нагріванні при 100 °C протягом ночі, згідно з модифікацією способу van Leeuwen та співавт. (Tetrahedron. Lett. 1999, 40, 3789-3790). У випадку, коли арилгалід 7 або гетероарилгалід 7 активують, підготовлюючи до нуклеофільного заміщення за рахунок присутності електронакцепторних замісників, краще, за рахунок присутності трифторметильної групи, конденсацію з піразолом 6 можна здійснити проведенням реакції з цими сполуками в присутності основи, такої як діізопропілетиламін, триетиламін, карбонат калію або гідрид натрію, в розчиннику, такому як ізопропанол, діоксан, 8 UA 110525 C2 диметилсульфоксид, диметилацетамід або диметилформамід, при температурі між 50 °C та 140 °C, протягом 1–24 год. Кращими умовами є нагрівання суміші сполук 6 та 7 з карбонатом калію в диметилацетаміді при 120 °C протягом 20 год. Стадія C: Утворення аміду можна здійснити реакцією конденсації між аміном 2 та сполуками хлорангідриду кислоти 8a в галогенованих розчинниках, таких як дихлорметан або 1,2дихлоретан, або в ефірних розчинниках, таких як діетиловий ефір, діоксан, ТГФ, DME чи TBME, в присутності органічної основи, такої як триетиламін або N,N-діізопропілетиламін. Кращими умовами є триетиламін в ТГФ при кімнатній температурі протягом 18 год. Як варіант, утворення аміду можна здійснити реакцією конденсації між аміном 2 та карбоновими кислотами 8b в присутності зшивального агента, такого як DCC, EDC, TBTU, HBTU або HATU, в присутності органічної основи, такої як триетиламін, N,N-діізопропілетиламін або N-метилморфолін, в галогенованих розчинниках, таких як ДМФ, дихлорметан або 1,2дихлоретан, або ефірних розчинниках, таких як діетиловий ефір, діоксан, ТГФ, DME або TBME. Кращими умовами є HBTU з N-метилморфоліном в ДМФ при 60 °C протягом 18 год. Стадія D: Видалення N-протекторної BOC групи можна здійснити за допомогою мінеральних кислот, таких як HCl, H2SO4 або H3PO4, або органічних кислот, таких як CF3COOH, CHCl2COOH, HOAc або п-толуолсульфонова кислота, в розчинниках, таких як CH 2Cl2, CHCl3, ТГФ, діоксан, MeOH, EtOH або H2O, при 0-80 °C. Кращими умовами є HCl в діоксані при 60 °C протягом 1-20 год. Цей самий загальний спосіб, описаний на схемі 3, можна застосовувати для одержання сполук формули IB-2. Виділення та очищення сполук Виділення та очищення сполук та проміжних продуктів, описаних в даному тексті, можна здійснити, за бажанням, будь-яким зручним способом виділення або очищення, таким як, наприклад, фільтрація, екстракція, кристалізація, колонкова хроматографія, тонкошарова хроматографія, товстошарова хроматографія, препаративна рідинна хроматографія низького або високого тиску або комбинація цих способів. Конкретні приклади придатних способів розділення та виділення можна навести шляхом посилання на способи одержання та приклади, наведені нижче. При цьому, зрозуміло, також можна застосовувати інші еквівалентні способи розділення або виділення. Рацемічні суміші хіральних сполук формули I можна розділяти за допомогою хіральної ВЕРХ. Солі сполук формул IA та IB Сполуки формул IA та IB є основними, і їх можна перевести у відповідні кислотно-адитивні солі. Таке перетворення можна здійснити обробкою за допомогою принаймні стехіометричної кількості придатної кислоти, такої як хлористоводнева кислота, бромистоводнева кислота, сірчана кислота, азотна кислота, фосфорна кислота тощо, та органічних кислот, таких як оцтова кислота, пропіонова кислота, гліколева кислота, піровиноградна кислота, щавлева кислота, яблучна кислота, малонова кислота, бурштинова кислота, малеїнова кислота, фумарова кислота, винна кислота, лимонна кислота, бензойна кислота, корична кислота, мигдалева кислота, метансульфонова кислота, етансульфонова кислота, п-толуолсульфонова кислота, саліцилова кислота тощо. Як правило, вільну основу розчиняють в інертному органічному розчиннику, такому як діетиловий ефір, етилацетат, хлороформ, етанол або метанол тощо, та додають кислоту в такому саме розчиннику. Температуру підтримують в інтервалі між 0 °C та 50 °C. Утворювана сіль осаджується мимовільно або її можна видобути з розчину за допомогою менш полярного розчинника. Кислотно-адитивні солі основних сполук формул IA та IB можна переводити у відповідні вільні основи обробкою принаймні стехіометричним еквівалентом придатної основи, такої як гидроксид натрію або калію, карбонат калію, бікарбонат натрію, аміак тощо. Приклад 1 (S)-N-(4-(Морфолін-2-іл)феніл)-5-феніл-1H-піразол-3-карбоксаміду гідрохлорид O O N H N H N N H a) (S)-трет-Бутил 2-(4-(5-феніл-1H-піразол-3-карбоксамідо)феніл)морфолін-4-карбоксилат 9 UA 110525 C2 В круглодонній колбі на 25 мл (S)-трет-бутил-2-(4-амінофеніл)морфолін-4-карбоксилат (100 мг, 359 мкмоль, екв.: 1,00), 3-феніл-1H-піразол-5-карбонову кислоту (87,9 мг, 467 мкмоль, екв.: 1,3) (CAS-1134-49-2), N-метилморфолін (109 мг, 118 мкл, 1,08 ммоль, екв.: 3) та HBTU (204 мг, 539 мкмоль, екв.: 1,5) об’єднували з ДМФ (3,75 мл). Реакційну суміш перемішували при 60 °C протягом 16,5 год. Цю суміш вливали у воду (10 мл) та екстрагували двічі за допомогою EtOAc. Органічні шари промивали сольовим розчином, висушували над MgSO 4, фільтрували та концентрували у вакуумі. Неочищену речовину очищали хроматографією на колонці (6 г силікагелю (63-200A), елюент: гептан/EtOAc 2:1) з одержанням вказаної в заголовку сполуки у + вигляді білої твердої речовини (120 мг, 74,5%). MS (ISP): 449,5 ([M+H] ). b) (S)-N-(4-(Морфолін-2-іл)феніл)-5-феніл-1H-піразол-3-карбоксаміду гідрохлорид До розчину (S)-трет-бутил-2-(4-(5-феніл-1H-піразол-3-карбоксамідо)феніл)морфолін-4карбоксилату (120 мг, 268 мкмоль, екв.: 1,00) в діоксані (0,5 мл) додавали 4M HCl в діоксані (1,00 мл, 4,01 ммоль, екв.: 15). Реакційну суміш перемішували при 60 °C протягом 2 год. До цієї суміші потім додавали 10 мл діоксану, і одержану суспензію відфільтровували, промивали ефіром та висушували у високому вакуумі з одержанням цільової сполуки у вигляді білої + твердої речовини (82,3 мг, 79,9%). MS (ISP): 349,2 ([M+H] ). Одержання (S)-трет-бутил-2-(4-амінофеніл)морфолін-4-карбоксилату Стадія a) (S)-2-(4-Бромфеніл)морфолін: Розділяли 2,27 г (RS)-2-(4-бромфеніл)морфоліну (CAS-1131220-82-0) на Chiralpak IA (8×32 см) за допомогою суміші н-гептан/етанол (1:11) + 0,1% DEA. (S)-2-(4-Бромфеніл)морфолін: збирали з 7,6 хв. по 9,4 хв. Вихід: 0,97 г (42,9%) з 97,4% енантіомерним надлишком. (R)-2-(4-Бромфеніл)морфолін: збирали з 9,8 хв. по 13,9 хв. Вихід: 0,99 г (43,6%) з 97,4% енантіомерним надлишком. Стадія b) (S)-трет-Бутил-2-(4-бромфеніл)морфолін-4-карбоксилат (S)-2-(4-Бромфеніл)морфолін (36,3 г, 150 ммоль) та N,N-діізопропілетиламін (23,3 г, 31,4 мл, 180 ммоль) в ТГФ (360 мл) обробляли за допомогою ди-трет-бутилдикарбонату (39,3 г, 180 ммоль). Реакційну суміш перемішували протягом 17 год. при КТ, концентрували у вакуумі, розбавляли етилацетатом, промивали 1M лимонною кислотою (2×100 мл), висушували над сульфатом магнію, фільтрували та концентрували у вакуумі. Неочищену речовину кристалізували із гексану з одержанням 47,1 г (92%) (S)-трет-бутил-2-(4-бромфеніл)морфолін-4+ карбоксилату у вигляді брудно-білої твердої речовини. MS (ISP): 344,1 ([M+H] ). Стадія c) (S)-трет-Бутил-2-(4-(дифенілметиленаміно)феніл)морфолін-4-карбоксилат: (S)-трет-Бутил-2-(4-бромфеніл)морфолін-4-карбоксилат (47 г, 137 ммоль), дифенілметанімін (29,9 г, 27,6 мл, 165 ммоль), BINAP (6,41 г, 10,3 ммоль) та Pd 2(dba)3 (3,14 г, 3,43 ммоль) розчиняли в атмосфері аргону в сухому та деаерованому толуолі (940 мл) та обробляли третбутоксидом натрію (18,5 г, 192 ммоль). Одержану темно-коричневу суміш перемішували при 90 °C протягом 18 год. Жовто-коричневу реакційну суміш розбавляли толуолом (700 мл), охолоджували до КТ та екстрагували двічі водою. Органічний шар відокремлювали, висушували над сульфатом магнію та концентрували у вакуумі. Неочищений продукт розбавляли за допомогою 300 мл гексану, перемішували протягом 1 год. та відфільтровували з одержанням оранжевої твердої речовини (68 г), яку очищали хроматографією на колонці (1,3 кг силікагелю, 20% етилацетат/гептан). Об’єднані та концентровані фракції суспендували у гексані, перемішували протягом 17 год., відфільтровували та висушували у високому вакуумі з + одержанням 54,1 г (89%) жовтої твердої речовини. MS (ISP): 443,3 ([M+H] ). Стадія d) (S)-трет-Бутил-2-(4-амінофеніл)морфолін-4-карбоксилат Суспензію (S)-трет-бутил-2-(4-(дифенілметиленаміно)феніл)морфолін-4-карбоксилату (54,1 г, 122 ммоль), форміату амонію (116 г, 1,83 моль) та Pd/C 5% (6,5 г, 3,06 ммоль) в метанолі (930 мл) перемішували при 60 °C протягом 2 год. Реакційну суміш фільтрували та концентрували. Залишок розчиняли в етилацетаті та воді. Органічну фазу екстрагували двічі за допомогою 0,5 M HCl. Об’єднані водні фази підлуговували за допомогою 2M NaOH та екстрагували двічі за допомогою DCM. Органічні фази висушували над сульфатом магнію, фільтрували та висушували у вакуумі, з одержанням 31,95 г брудно-білої твердої речовини. MS (ISP): 279,1 + ([M+H] ). Приклад 2 (S)-3-(3-Хлорфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид 10 UA 110525 C2 O O N H N N H N H Cl Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 5-(3хлорфеніл)-1H-піразол-3-карбонової кислоти (CAS-595610-50-7) замість 5-феніл-1H-піразол-3карбонової кислоти. + Біла тверда речовина. MS (ISP): 383,12 ([M+H] ). Приклад 3 (S)-3-(4-Фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H N N H F Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 5-(4фторфеніл)-1H-піразол-3-карбонової кислоти (CAS-870704-22-6) замість 5-феніл-1H-піразол-3карбонової кислоти. + Біла тверда речовина. MS (ISP): 367,15 ([M+H] ). Приклад 4 (S)-3-(3-Метоксифеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H N N H O Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 5-(3метоксифеніл)-1H-піразол-3-карбонової кислоти (CAS-834868-54-1) замість 5-феніл-1H-піразол3-карбонової кислоти. + Біла тверда речовина. MS (ISP): 379,17 ([M+H] ). Приклад 5 (S)-1-Метил-N-(4-(морфолін-2-іл)феніл)-3-феніл-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H N N Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 1метил-3-феніл-1H-піразол-5-карбонової кислоти (CAS-10250-64-3) замість 5-феніл-1H-піразол-3карбонової кислоти. + Біла тверда речовина. MS (ISP): 363,18 ([M+H] ). Приклад 6 (S)-4-Метил-N-(4-(морфолін-2-іл)феніл)-3-феніл-1H-піразол-5-карбоксаміду гідрохлорид 11 UA 110525 C2 O O N H NH N H N Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 4метил-5-феніл-2H-піразол-3-карбонової кислоти (CAS-879770-33-9) замість 5-феніл-1H-піразол3-карбонової кислоти. + Брудно-біла тверда речовина. MS (ISP): 363,5 ([M+H] ). Приклад 7 (S)-3-(4-Метоксифеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H NH N O Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 5-(4метоксифеніл)-2H-піразол-3-карбонової кислоти (CAS- 27069-16-5) замість 5-феніл-1H-піразол3-карбонової кислоти. + Біла тверда речовина. MS (ISP): 379,4 ([M+H] ). Приклад 8 (S)-3-(2-Фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H N F H NH N Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 5-(2фторфеніл)-2H-піразол-3-карбонової кислоти (CAS-859155-87-6) замість 3-феніл-1H-піразол-5карбонової кислоти. + Біла тверда речовина. MS (ISP): 367,1 ([M+H] ). Приклад 9 (S)-3-(2-Метоксифеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H NH N O Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 5-(2метоксифеніл)-2H-піразол-3-карбонової кислоти (CAS-834868-54-1) замість 3-феніл-1H-піразол5-карбонової кислоти. + Біла тверда речовина. MS (ISP): 379,4 ([M+H] ). Приклад 10 (S)-3-(2-Хлорфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид 12 UA 110525 C2 O O N H Cl NH N H N Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 3-(2хлорфеніл)-1H-піразол-5-карбонової кислоти (CAS-890621-13-3) замість 3-феніл-1H-піразол-5карбонової кислоти. + Біла тверда речовина. MS (ISP): 383,2 ([M+H] ). Приклад 11 (S)-3-(3,4-Диметоксифеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H NH O N O Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 5(3,4-диметоксифеніл)-2H-піразол-3-карбонової кислоти (CAS-909857-88-1) замість 3-феніл-1Hпіразол-5-карбонової кислоти. + Брудно-біла тверда речовина. MS (ISP): 409,3 ([M+H] ). Приклад 12 (R)-3-(4-Хлорфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H NH N Cl Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням (R)трет-бутил-2-(4-амінофеніл)морфолін-4-карбоксилату замість (S)-трет-бутил-2-(4амінофеніл)морфолін-4-карбоксилату та 3-(4-хлорфеніл)-1H-піразол-5-карбонової кислоти (CAS-54006-63-2) замість 3-феніл-1H-піразол-5-карбонової кислоти. + Брудно-біла тверда речовина. MS (ISP): 383,1 ([M+H] ). Одержання (R)-трет-бутил-2-(4-амінофеніл)морфолін-4-карбоксилату: Стадія a) (R)-2-(4-Бромфеніл)морфолін: Розділяли 2,27 г (RS)-2-(4-бромфеніл)морфоліну (CAS-1131220-82-0) на Chiralpak IA (8×32 см) за допомогою суміші н-гептан/етанол (1:11) + 0,1% DEA. (S)-2-(4-Бромфеніл)морфолін: збирали від 7,6 хв. до 9,4 хв. Вихід 0,97 г (42,9%) з енантіомерним надлишком 97,4% (R)-2-(4-Бромфеніл)морфолін: збирали від 9,8 хв. до 13,9 хв. Вихід 0,99 г (43,6%) з енантіомерним надлишком 97,4% Стадія b) (R)-трет-Бутил-2-(4-бромфеніл)морфолін-4-карбоксилат: (R)-2-(4-Бромфеніл)морфолін (6 г, 24,8 ммоль) та N,N-діізопропілетиламін (3,84 г, 5,19 мл, 29,7 ммоль) в ТГФ (60 мл) обробляли ди-трет-бутилдикарбонатом (6,49 г, 29,7 ммоль). Реакційну суміш перемішували протягом 17 год. при КТ, концентрували у вакуумі, розбавляли етилацетатом, промивали 1M лимонною кислотою, висушували над сульфатом магнію, фільтрували та концентрували у вакуумі. Неочищену речовину кристалізували із суміші гептан/етилацетат з одержанням 8,48 г (87%) (R)-трет-бутил-2-(4-бромфеніл)морфолін-4+ карбоксилату у вигляді білої твердої речовини. MS (ISP): 344,1 ([M+H] ). Стадія c) (R)-трет-Бутил-2-(4-(дифенілметиленаміно)феніл)морфолін-4-карбоксилат: (R)-трет-Бутил-2-(4-бромфеніл)морфолін-4-карбоксилат (5,4 г, 15,8 ммоль), дифенілметанімін (3,43 г, 3,17 мл, 18,9 ммоль), BINAP (737 мг, 1,18 ммоль) та Pd2(dba)3 (361 мг, 0,39 ммоль) розчиняли в атмосфері аргону в сухому та деаерованому толуолі (108 мл) та обробляли трет-бутоксидом натрію (2,12 г, 22,1 ммоль). Одержану темно-коричневу суміш 13 UA 110525 C2 перемішували при 90 °C протягом 18 год. Жовто-коричневу реакційну суміш розбавляли толуолом (100 мл), охолоджували до КТ та екстрагували двічі водою. Органічний шар відокремлювали, висушували над сульфатом магнію та концентрували у вакуумі. Неочищений продукт розбавляли за допомогою 50 мл гексану, перемішували протягом 1 год. та відфільтровували з одержанням жовтої твердої речовини (7,4 г), яку очищали хроматографією на колонці (50 г силікагелю, етилацетат/гептан від 5% до 15%). Об’єднані та сконцентровані фракції суспендували в гексані, перемішували протягом 17 год., відфільтровували та висушували у високому вакуумі з одержанням 6,15 г (86%) жовтої твердої речовини. MS (ISP): + 443,4 ([M+H] ). Стадія d) (R)-трет-Бутил-2-(4-амінофеніл)морфолін-4-карбоксилат: Суспензію (R)-трет-бутил-2-(4-(дифенілметиленаміно)феніл)морфолін-4-карбоксилату (6 г, 13,6 ммоль), форміату амонію (12,8 г, 203 ммоль) та Pd/C 5% (721 мг, 0,339 ммоль) в метанолі (103 мл) перемішували при 60 °C протягом 2 год. Реакційну суміш фільтрували та концентрували. Одержаний залишок розчиняли в етилацетаті та воді. Органічну фазу екстрагували двічі за допомогою 0,5M HCl. Об’єднані водні фази підлуговували за допомогою 2M NaOH та екстрагували двічі за допомогою DCM. Органічні фази висушували над сульфатом магнію, фільтрували та висушували у вакуумі, з одержанням 3,04 г брудно-білої твердої + речовини. MS (ISP): 279,1 ([M+H] ). Приклад 13 (R)-3-(2-Хлорфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H NH N Cl Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням (R)трет-бутил-2-(4-амінофеніл)морфолін-4-карбоксилату (одержаного в Прикладі 12) замість (S)трет-бутил-2-(4-амінофеніл)морфолін-4-карбоксилату та 3-(2-хлорфеніл)-1H-піразол-5карбонової кислоти (CAS-890621-13-3) замість 3-феніл-1H-піразол-5-карбонової кислоти. + Світло-коричнева тверда речовина. MS (ISP): 383,1 ([M+H] ). Приклад 14 (S)-3-(4-Хлорфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H NH N Cl Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 3-(4хлорфеніл)-1H-піразол-5-карбонової кислоти (CAS-54006-63-2) замість 3-феніл-1H-піразол-5карбонової кислоти. + Брудно-біла тверда речовина. MS (ISP): 383,1 ([M+H] ). Приклад 15 (R)-3-(3-Хлорфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H NH N Cl Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням (R)трет-бутил-2-(4-амінофеніл)морфолін-4-карбоксилату (одержаного в Прикладі 12) замість (S)трет-бутил-2-(4-амінофеніл)морфолін-4-карбоксилату та 3-(3-хлорфеніл)-1H-піразол-5карбонової кислоти (CAS-595610-50-7) замість 3-феніл-1H-піразол-5-карбонової кислоти. 14 UA 110525 C2 + Біла тверда речовина. MS (ISP): 383,1 ([M+H] ). Приклад 16 (R)-3-(3-Метоксифеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H NH N O Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням (R)трет-бутил-2-(4-амінофеніл)морфолін-4-карбоксилату (одержаного в Прикладі 12) замість (S)трет-бутил-2-(4-амінофеніл)морфолін-4-карбоксилату та 3-(3-метоксифеніл)-1H-піразол-5карбонової кислоти (CAS-890591-64-7) замість 3-феніл-1H-піразол-5-карбонової кислоти. + Біла тверда речовина. MS (ISP): 379,2 ([M+H] ). Приклад 17 (S)-3-(3-Хлорфеніл)-1-метил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H N Cl N Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 5-(3хлорфеніл)-2-метил-2H-піразол-3-карбонової кислоти (CAS-93618-32-7) замість 3-феніл-1Hпіразол-5-карбонової кислоти. + Біла тверда речовина. MS (ISP): 397,1 ([M+H] ). Приклад 18 (S)-1-Метил-N-(4-(морфолін-2-іл)феніл)-5-феніл-1H-піразол-3-карбоксаміду гідрохлорид O O N H N H N N Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 1метил-5-феніл-1H-піразол-3-карбонової кислоти (CAS-10199-53-8) замість 3-феніл-1H-піразол-5карбонової кислоти. + Брудно-біла тверда речовина. MS (ISP): 363,2 ([M+H] ). Приклад 19 (R)-1-Метил-N-(4-(морфолін-2-іл)феніл)-3-феніл-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H N N Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням (R)трет-бутил-2-(4-амінофеніл)морфолін-4-карбоксилату (одержаного в Прикладі 12) замість (S)трет-бутил-2-(4-амінофеніл)морфолін-4-карбоксилату та 1-метил-3-феніл-1H-піразол-5карбонової кислоти (CAS-10250-64-3) замість 3-феніл-1H-піразол-5-карбонової кислоти. + Біла тверда речовина. MS (ISP): 363,3 ([M+H] ). Приклад 20 (S)-5-(3-Ціанофеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксаміду гідрохлорид 15 UA 110525 C2 O O N H N NC N H N H Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 5-(3ціанофеніл)-1H-піразол-3-карбонової кислоти (CAS-1242427-10-6) замість 3-феніл-1H-піразол-5карбонової кислоти. + Світло-коричнева тверда речовина. MS (ISP): 374,0 ([M+H] ). Приклад 21 (S)-3-(4-Ціанофеніл)-1-метил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H N N NC Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 3-(4ціанофеніл)-1-метил-1H-піразол-5-карбонової кислоти замість 3-феніл-1H-піразол-5-карбонової кислоти. + Світло-коричнева тверда речовина. MS (ISP): 388,0 ([M+H] ). Одержання 3-(4-ціанофеніл)-1-метил-1H-піразол-5-карбонової кислоти: Стадія a) (Z)-Етил-4-(4-ціанофеніл)-2-гідрокси-4-оксобут-2-еноат: В сухій колбі, в атмосфері аргону додавали порціями натрій (317 мг, 13,8 ммоль, екв.: 1,00) до етанолу (9,0 мл) (температура підвищувалася до 60 °C). Реакційну суміш охолоджували при 0 °C. Після цього додавали по краплях діетилоксалат (2,01 г, 1,87 мл, 13,8 ммоль, екв.: 1,00), а потім 4-ацетилбензонітрил (2 г, 13,8 ммоль, екв.: 1,00) в етанолі (3,00 мл). Одержували білу тверду речовину. Реакційну суміш перемішували на магнитній мішалці протягом ночі та відстежували перебіг реакції за допомогою ТШХ. Потім реакційну суміш концентрували у вакуумі. Одержаний залишок охолоджували при 0 °C та в колбу додавали воду. До цього розчину додавали 1M HCl (pH=3), потім одержаний розчин екстрагували два рази за допомогою EtOAc. Органічний шар промивали три рази за допомогою 20 мл сольового розчину. Одержаний органічний шар висушували над MgSO4, фільтрували та концентрували у вакуумі з одержанням брудно-білої твердої речовини. Цю брудно-білу тверду речовину змішували з ефіром при 0 °C. Суспензію фільтрували з одержанням білої твердої речовини (2,082 г, 61,6%). Стадія b) Етил-3-(4-ціанофеніл)-1-метил-1H-піразол-5-карбоксилат: В атмосфері аргону розчиняли (Z)-етил-4-(4-ціанофеніл)-2-гідрокси-4-оксобут-2-еноат (500 мг, 2,04 ммоль, екв.: 1,00) в етанолі (10 мл) при КТ. Додавали по краплях метилгідразин (95,9 мг, 110 мкл, 2,04 ммоль, екв.: 1,00) (розчин робився жовтим). Цей розчин перемішували протягом ночі при КТ з подальшим нагріванням 6 год. при 50 °C, охолоджували до КТ та концентрували у вакуумі. Залишок безпосередньо очищали хроматографією на колонці (20 г) сумішшю гептан/EtOAC: 9/1 з одержанням бажаного піразолу (173 мг, 33,2%) у вигляді білої твердої речовини. + MS (ISP): 256,3 ([M+H] ). Стадія c) 3-(4-Ціанофеніл)-1-метил-1H-піразол-5-карбонова кислота: До розчину етил-3-(4-ціанофеніл)-1-метил-1H-піразол-5-карбоксилату (70 мг, 274 мкмоль, екв.: 1,00) в ТГФ (5 мл) та MeOH (1,00 мл) додавали 1M LiOH (548 мкл, 548 мкмоль, екв.: 2). Цю суміш перемішували протягом приблизно 8 год. при КТ, потім обробляли водою та 1н HCl (pH: 3). Цю суміш екстрагували два рази етилацетатом. Одержані органічні шари об’єднували, промивали сольовим розчином та висушували над MgSO 4, фільтрували та концентрували з одержанням бажаної сполуки (55 мг, 88,3%) у вигляді білої твердої речовини. MS (ISP): 228,2 (M+1). Приклад 22 (S)-3-(4-Фторфеніл)-1-метил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид 16 UA 110525 C2 O O N H N N H N F Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 5-(4фторфеніл)-2-метил-1H-піразол-3-карбонової кислоти (CAS-943863-70-5) замість 3-феніл-1Hпіразол-5-карбонової кислоти. + Світло-коричнева тверда речовина. MS (ISP): 381,1 ([M+H] ). Приклад 23 (S)-3-(3-Метоксифеніл)-1-метил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H N N O Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 5-(3метоксифеніл)-2-метил-1H-піразол-3-карбонової кислоти (CAS-1022575-47-8) замість 3-феніл1H-піразол-5-карбонової кислоти. + Світло-коричнева тверда речовина. MS (ISP): 381,1 ([M+H] ). Приклад 24 (S)-3-(3-Ціанофеніл)-1-метил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H N N CN Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 3-(3ціанофеніл)-1-метил-1H-піразол-5-карбонової кислоти замість 3-феніл-1H-піразол-5-карбонової кислоти. + Світло-коричнева тверда речовина. MS (ISP): 388,0 ([M+H] ). Одержання 3-(3-ціанофеніл)-1-метил-1H-піразол-5-карбонової кислоти: За аналогією з 3-(4-ціанофеніл)-1-метил-1H-піразол-5-карбоновою кислотою, як описано в Прикладі 21. Приклад 25 (S)-3-(3-Ціанофеніл)-1-етил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H N N CN Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 3-(3ціанофеніл)-1-етил-1H-піразол-5-карбонової кислоти замість 3-феніл-1H-піразол-5-карбонової кислоти. 17 UA 110525 C2 + Брудно-біла тверда речовина. MS (ISP): 402,1 ([M+H] ). Одержання 3-(3-ціанофеніл)-1-етил-1H-піразол-5-карбонової кислоти: За аналогією з 3-(4-ціанофеніл)-1-метил-1H-піразол-5-карбоновою кислотою, як описано в Прикладі 21. Приклад 26 (S)-3-(4-Ціанофеніл)-1-етил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H N N NC Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 3-(4ціанофеніл)-1-етил-1H-піразол-5-карбонової кислоти замість 3-феніл-1H-піразол-5-карбонової кислоти. + Брудно-біла тверда речовина. MS (ISP): 402,1 ([M+H] ). Одержання 3-(4-ціанофеніл)-1-етил-1H-піразол-5-карбонової кислоти: За аналогією з 3-(4-ціанофеніл)-1-метил-1H-піразол-5-карбоновою кислотою, як описано в Прикладі 21. Приклад 27 (S)-5-(3-Ціанофеніл)-4-метил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксаміду гідрохлорид O O N H N H N N H CN Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 5-(3ціанофеніл)-4-метил-1H-піразол-3-карбонової кислоти замість 3-феніл-1H-піразол-5-карбонової кислоти. + Коричнева тверда речовина. MS (ISP): 388,1 ([M+H] ). Одержання 5-(3-ціанофеніл)-4-метил-1H-піразол-3-карбонової кислоти: Стадія a) (Z)-4-(3-Ціанофеніл)-1-етокси-3-метил-1,4-діоксобут-2-ен-2-олат літію: При перемішуванні на магнитній мішалці, до 1M розчину LiHMDS в ТГФ (7,94 мл, 7,94 ммоль, екв.: 1,00) в Et2O (50 мл) при -78 °C додавали по краплях розчин 3пропіонілбензонітрилу (1,264 г, 7,94 ммоль, екв.: 1,00) в Et 2O (10,0 мл) в атмосфері аргону. Перемішували суміш при такій саме температурі протягом ще 45 хв., після чого додавали по краплях діетилоксалат (1,22 г, 1,13 мл, 8,34 ммоль, екв.: 1,05). Реакційну суміш нагрівали до КТ та перемішували протягом 3 діб. Утворений преципітат збирали фільтрацією, промивали діетиловим ефіром та висушували у вакуумі з одержанням бажаної літієвої солі у вигляді жовтої твердої речовини (929 мг, 44,1%). Стадія b) Етил-5-(3-ціанофеніл)-4-метил-1H-піразол-3-карбоксилат: До розчину (Z)-4-(3-ціанофеніл)-1-етокси-3-метил-1,4-діоксобут-2-ен-2-олату літію (400 мг, 1,51 ммоль, екв.: 1,00) в етанолі (10 мл) додавали гідразину гідрохлорид (113 мг, 1,65 ммоль, екв.: 1,093) при КТ з одержанням оранжевого розчину. Одержану суміш перемішували протягом ночі при цій самій температурі. Через 1 добу розчинник видаляли при зниженому тиску та до суміші додавали сольовий розчин. Цей розчин екстрагували два рази за допомогою AcOEt і об’єднані органічні шари висушували над MgSO 4, фільтрували та концентрували з одержанням бажаної сполуки у вигляді жовтої смоли (114 мг, 26,6%). + MS (ISP): 256,0 ([M+H] ). Стадія c) 3-(3-Ціанофеніл)-1-метил-1H-піразол-5-карбонова кислота: До розчину етил-5-(3-ціанофеніл)-4-метил-1H-піразол-3-карбоксилату (100 мг, 392 мкмоль, екв.: 1,00) в ТГФ (5 мл) в MeOH (1,00 мл) додавали 1M LiOH (2,35 мл, 2,35 ммоль, екв.: 6). Цю суміш перемішували протягом ночі. До одержаного залишку додавали воду та 1н HCl (pH: 1), цю водну фазу екстрагували два рази етилацетатом, одержані органічні шари об’єднували та 18 UA 110525 C2 промивали сольовим розчином, висушували над MgSO 4, фільтрували та концентрували у вакуумі з одержанням бажаної сполуки (52 мг, 52,6%) у вигляді жовтої твердої речовини. MS (ISP): 228,1 (M+1). Приклад 28 (S)-5-(5-Ціано-2-фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксаміду гідрохлорид O O N H N F H N N H CN Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 5-(5ціано-2-фторфеніл)-1H-піразол-3-карбонової кислоти замість 3-феніл-1H-піразол-5-карбонової кислоти. + Коричнева тверда речовина. MS (ISP): 392,0 ([M+H] ). Одержання 5-(5-ціано-2-фторфеніл)-1H-піразол-3-карбонової кислоти: За аналогією з 5-(3-ціанофеніл)-4-метил-1H-піразол-3-карбоновою кислотою, як описано в Прикладі 21. Приклад 29 (S)-1-(4-Фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксаміду гідрохлорид O O N H N H N N F Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 1-(4фторфеніл)-1H-піразол-3-карбонової кислоти (CAS-1152535-34-6) в ТГФ замість 3-феніл-1Hпіразол-5-карбонової кислоти в ДМФ. + Біла тверда речовина. MS (ISP): 367,0 ([M+H] ). Приклад 30 (S)-N-(4-(Морфолін-2-іл)феніл)-1-феніл-1H-піразол-5-карбоксаміду гідрохлорид O O N H N H N N Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 1феніл-1H-піразол-5-карбонової кислоти (CAS-1133-77-3) замість 3-феніл-1H-піразол-5карбонової кислоти. + Біла тверда речовина. MS (ISP): 349,1 ([M+H] ). Приклад 31 (R)-1-(4-Фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксаміду гідрохлорид 19 UA 110525 C2 O O N H N N H N F Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням (R)трет-бутил-2-(4-амінофеніл)морфолін-4-карбоксилату замість (S)-трет-бутил-2-(4амінофеніл)морфолін-4-карбоксилату та 1-(4-фторфеніл)-1H-піразол-3-карбонової кислоти (CAS-1152535-34-6) замість 3-феніл-1H-піразол-5-карбонової кислоти. + Біла тверда речовина. MS (ISP): 367,0 ([M+H] ). Приклад 32 (S)-1-(5-Хлорпіридин-2-іл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксаміду гідрохлорид O O N H N H N N N Cl Вказану в заголовку сполуку одержували за аналогією з Прикладом 47 з використанням 2бром-5-хлорпіридину замість 2-хлор-5-(трифторметил)піримідину на стадії b). + Брудно-біла тверда речовина. MS (ISP): 384,2 ([M+H] ). Приклад 33 (S)-N-(4-(Морфолін-2-іл)феніл)-1-(5-(трифторметил)піридин-2-іл)-1H-піразол-3-карбоксаміду гідрохлорид O O N H N H N N N CF3 Вказану в заголовку сполуку одержували за аналогією з Прикладом 47 з використанням 2бром-5-(трифторметил)піридину замість 2-хлор-5-(трифторметил)піримідину на стадії b). + Біла тверда речовина. MS (ISP): 418,2 ([M+H] ). Приклад 34 (S)-1-(4-Ціанофеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксаміду гідрохлорид 20 UA 110525 C2 O O N H N N H N CN Вказану в заголовку сполуку одержували за аналогією з Прикладом 47 з використанням 2бромбензонітрилу замість 2-хлор-5-(трифторметил)піримідину на стадії b). + Брудно-біла тверда речовина. MS (ISP): 374,3 ([M+H] ). Приклад 35 (R)-N-(4-(Морфолін-2-іл)феніл)-1-(5-(трифторметил)піридин-2-іл)-1H-піразол-3-карбоксаміду гідрохлорид O O N H N H N N N CF3 Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням (R)трет-бутил-2-(4-амінофеніл)морфолін-4-карбоксилату замість (S)-трет-бутил-2-(4амінофеніл)морфолін-4-карбоксилату та 1-(5-трифторметил-піридин-2-іл)-1H-піразол-3карбонової кислоти (CAS-1006962-72-6) замість 3-феніл-1H-піразол-5-карбонової кислоти. + Біла тверда речовина. MS (ISP): 418,2 ([M+H] ). Приклад 36 (S)-3-(3-Ціанофеніл)-N-(4-(піперидин-3-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O N H H N N H N CN Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 5-(3ціанофеніл)-1H-піразол-3-карбонової кислоти (CAS-1242427-10-6) замість 3-феніл-1H-піразол-5карбонової кислоти. + Біла тверда речовина. MS (ISP): 372,0 ([M+H] ). Приклад 37 (R)-3-(3-Ціанофеніл)-N-(4-(піперидин-3-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O N H H N N H N CN 21 UA 110525 C2 Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням (R)трет-бутил-2-(4-амінофеніл)морфолін-4-карбоксилату замість (S)-трет-бутил-2-(4амінофеніл)морфолін-4-карбоксилату та 5-(3-ціанофеніл)-1H-піразол-3-карбонової кислоти (CAS-1242427-10-6) замість 3-феніл-1H-піразол-5-карбонової кислоти. + Біла тверда речовина. MS (ISP): 372,0 ([M+H] ). Приклад 38 (рац) 3-(3-Ціанофеніл)-N-(4-(піролідин-3-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O N H NH H N N CN Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням третбутилового ефіру 3-(4-амінофеніл)піролідин-1-карбонової кислоти (CAS-908334-28-1) замість (S)-трет-бутил-2-(4-амінофеніл)морфолін-4-карбоксилату та 5-(3-ціанофеніл)-1H-піразол-3карбонової кислоти (CAS-1242427-10-6) замість 3-феніл-1H-піразол-5-карбонової кислоти. + Біла тверда речовина. MS (ISP): 357,8 ([M+H] ). Приклад 39 (S)-5-(3-Ціано-4-фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксаміду гідрохлорид O O N H H N N H N CN F Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 5-(3ціано-4-фторфеніл)-1H-піразол-3-карбонової кислоти (одержаної, як вказано нижче: a-d) замість 3-феніл-1H-піразол-5-карбонової кислоти. + Біла тверда речовина. MS (ISP): 392,1 ([M+H] ). Одержання 5-(3-ціано-4-фторфеніл)-1H-піразол-3-карбонової кислоти: a) (Z)-4-(3-Бром-4-фторфеніл)-1-етокси-1,4-діоксобут-2-ен-2-олат літію: При перемішуванні на магнітній мішалці до 1M розчину LiHMDS в ТГФ (9,22 мл, 9,22 ммоль, екв.: 1) додавали Et2O (31,2 мл) при -78 °C з одержанням жовтого розчину. До цієї суміші додавали по краплях в атмосфері аргону розчин 1-(3-бром-4-фторфеніл)етанону (2 г, 9,22 ммоль, екв.: 1,00) в Et2O (15,6 мл). Цю суміш потім перемішували при такій саме температурі протягом ще 45 хв., після чого додавали по краплях діетилоксалат (1,41 г, 1,31 мл, 9,68 ммоль, екв.: 1,05). Реакційну суміш нагрівали до КТ та перемішували протягом ще 2 діб. Утворений преципітат збирали фільтрацією, промивали діетиловим ефіром, та висушували у вакуумі з одержанням бажаної літієвої солі у вигляді світло-жовтої твердої речовини (2,677 г, 89,9%). b) Етил-5-(3-бром-4-фторфеніл)-1H-піразол-3-карбоксилат: До розчину (Z)-4-(3-бром-4-фторфеніл)-1-етокси-1,4-діоксобут-2-ен-2-олату літію (600 мг, 1,86 ммоль, екв.: 1,00) в етанолі (25 мл) додавали гідразину моногідрат (139 мг, 2,03 ммоль, екв.: 1,093) при КТ з одержанням білої суспензії, через 1 год. ця суспензія перетворювалася на розчин. Одержану суміш перемішували протягом ночі. Через 1 добу реакція була завершена. Після перемішування розчинник видаляли при зниженому тиску та до суміші додавали сольовий розчин, Цей розчин екстрагували два рази за допомогою AcOEt, і об’єднані органічні шари висушували над Na2SO4, фільтрували та концентрували з одержанням етил-5-(3-бром-4фторфеніл)-1H-піразол-3-карбоксилату у вигляді білої твердої речовини (460 мг, 79,1%). MS + (ISP): 314,8 ([M+H] ). c) Етил-5-(3-ціано-4-фторфеніл)-1H-піразол-3-карбоксилат: 22 UA 110525 C2 Суміш етил-5-(3-бром-4-фторфеніл)-1H-піразол-3-карбоксилату (300 мг, 958 мкмоль, екв.: 1,00), ціаніду цинку (65,2 мг, 556 мкмоль, екв.: 0,58) та Pd(PPh3)4 (111 мг, 95,8 мкмоль, екв.: 0,1) нагрівали при 160 °C в ДМФ (2 мл) (який зберігали над молекулярними ситами) протягом 30 хв. в мікрохвильовій шафі. Цю суміш ділили між EtOAc (40 мл) та 2н NH4OH (40 мл). Органічну фазу екстрагували за допомогою 2н NH4OH, промивали сольовим розчином, висушували над MgSO4 та концентрували у вакуумі. Неочищену суміш очищали хроматографією на колонці (10 г), елюент: гептан/EtOAc: 95/5, з одержанням бажаної нітрильної сполуки у вигляді білої + кристалічної твердої речовини (180 мг, 72,5%). MS (ISP): 260,0 ([M+H] ). d) 5-(3-Ціано-4-фторфеніл)-1H-піразол-3-карбонова кислота: До розчину етил-5-(3-ціано-4-фторфеніл)-1H-піразол-3-карбоксилату (180 мг, 694 мкмоль, екв.: 1,00) в ТГФ (5,00 мл) та MeOH (1 мл) додавали 1M LiOH (4,17 мл, 4,17 ммоль, екв.: 6). Цю суміш перемішували протягом ночі. Після додавання LiOH розчин робився оранжевим. До одержаного залишку додавали воду та 1н HCl (pH: 1), цю водну фазу екстрагували два рази етилацетатом; одержані органічні шари об’єднували та промивали сольовим розчином. Потім висушували над MgSO4, фільтрували та концентрували з одержанням бажаної сполуки (45 мг, + 22,4%) у вигляді білої твердої речовини. MS (ISP): 232,4 ([M+H] ). Приклад 40 (S)-3-(3-(Дифторметокси)феніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H H N N H N O F F Вказану в заголовку сполуку одержували за аналогією з Прикладом 1 з використанням 5-(3дифторметоксифеніл)-2H-піразол-3-карбонової кислоти (одержаної, як вказано нижче: a-c) замість 3-феніл-1H-піразол-5-карбонової кислоти. + Біла тверда речовина. MS (ISP): 415,2 ([M+H] ). Одержання 5-(3-дифторметоксифеніл)-2H-піразол-3-карбонової кислоти: a) Метиловий ефір 5-(3-дифторметоксифеніл)-2H-піразол-3-карбонової кислоти: До розчину (Z)-метил-4-(3-(дифторметокси)феніл)-2-гідрокси-4-оксобут-2-еноату (CAS832741-03-4) (800 мг, 2,94 ммоль, екв.: 1,00) в етанолі (20 мл) додавали гідразину гідрохлорид (220 мг, 3,21 ммоль, екв.: 1,093) при КТ з одержанням оранжевої суспензії. Одержану суміш перемішували протягом ночі при цій самій температурі. Через 1 добу реакція була завершена. Після перемішування розчинник видаляли при зниженому тиску та до цієї суміші додавали сольовий розчин, Цей розчин екстрагували два рази за допомогою AcOEt, і об’єднані органічні шари висушували над MgSO4, фільтрували та концентрували з одержанням бажаної сполуки у + вигляді світло-коричневої твердої речовини (630 мг, 79,9%). MS (ISP): 269,0 ([M+H] ). b) 5-(3-Дифторметоксифеніл)-2H-піразол-3-карбонова кислота: До розчину метилового ефіру 5-(3-дифторметоксифеніл)-2H-піразол-3-карбонової кислоти (620 мг, 2,31 ммоль, екв.: 1,00) в ТГФ (10 мл) та MeOH (2,00 мл) додавали 1M LiOH (13,9 мл, 13,9 ммоль, екв.: 6) з одержанням коричневого розчину. Цю суміш перемішували протягом ночі. Після додавання LiOH цей розчин робився. До одержаного залишку додавали воду та 1н HCl (pH:1), цю водну фазу екстрагували два рази етилацетатом, одержані органічні шари об’єднували та промивали сольовим розчином. Потім висушували над MgSO4, фільтрували та концентрували з одержанням бажаної сполуки (510 мг, 86,8%) у вигляді світло-жовтої твердої + речовини. MS (ISP): 255,0 ([M+H] ). Приклад 41 (S)-5-(3-(Дифторметокси)феніл)-1-етил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3карбоксаміду гідрохлорид 23 UA 110525 C2 O O N H N N H N O F F a) (S)-трет-Бутил-2-(4-(3-(3-(дифторметокси)феніл)-1H-піразол-5-карбоксамідо)феніл)морфолін-4-карбоксилат: В круглодонній колбі на 25 мл 3-(3-(дифторметокси)феніл)-1H-піразол-5-карбонову кислоту (515 мг, 2,03 ммоль, екв.: 1,1) (синтез описаний у Прикладі 40), (S)-трет-бутил-2-(4амінофеніл)морфолін-4-карбоксилат (513 мг, 1,84 ммоль, екв.: 1,00) (синтез описаний у Прикладі 1), N-метилморфолін (559 мг, 608 мкл, 5,53 ммоль, екв.: 3) та HBTU (1,05 г, 2,76 ммоль, екв.: 1,5) об’єднували з ДМФ (2 мл) з одержанням жовтого розчину. Реакційну суміш перемішували протягом ночі при 60 °C. Цю суміш вливали у воду (10 мл) та екстрагували двічі за допомогою EtOAc. Органічні шари промивали за допомогою NaHCO3, сольового розчину, висушували над MgSO4, фільтрували та концентрували у вакуумі з одержанням коричневої неочищеної суміші. Суміш розбавляли гептаном, перемішували протягом 15 хв. та цю суспензію фільтрували. Одержану тверду речовину промивали декілька разів гептаном з одержанням бажаної сполуки у вигляді коричневої твердої речовини (550 мг, 58,0%). b) (S)-трет-Бутил-2-(4-(5-(3-(дифторметокси)феніл)-1-етил-1H-піразол-3карбоксамідо)феніл)морфолін-4-карбоксилат та (S)-трет-бутил-2-(4-(3-(3-(дифторметокси)феніл)-1-етил-1H-піразол-5-карбоксамідо)феніл)морфолін-4-карбоксилат: До суміші (S)-трет-бутил-2-(4-(3-(3-(дифторметокси)феніл)-1H-піразол-5карбоксамідо)феніл)морфолін-4-карбоксилату (70 мг, 136 мкмоль, екв.: 1,00) та карбонату калію (41,4 мг, 299 мкмоль, екв.: 2,2) в ДМФ (2 мл) додавали йодетан (25,5 мг, 13,2 мкл, 163 мкмоль, екв.: 1,2) та перемішували протягом ночі при КТ. До одержаної суміші додавали воду, органічну фазу екстрагували водою та сольовим розчином, потім органічний шар висушували над MgSO4, відфільтровували та концентрували у вакуумі з одержанням неочищеної сполуки у вигляді суміші ізомерів, яку розділяли хроматографією на колонці (картридж на 10 г) з одержанням: (S)трет-бутил-2-(4-(5-(3-(дифторметокси)феніл)-1-етил-1H-піразол-3карбоксамідо)феніл)морфолін-4-карбоксилату (17 мг, 23,0%) та (S)-трет-бутил-2-(4-(3-(3(дифторметокси)феніл)-1-етил-1H-піразол-5-карбоксамідо)феніл)морфолін-4-карбоксилату (27 мг, 36,6%). c) (S)-5-(3-(Дифторметокси)феніл)-1-етил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3карбоксаміду гідрохлорид: До розчину (S)-трет-бутил-2-(4-(5-(3-(дифторметокси)феніл)-1-етил-1H-піразол-3карбоксамідо)феніл)морфолін-4-карбоксилату (17 мг) в діоксані (40,8 мкл) додавали 4M HCl в діоксані (117 мкл, 470 мкмоль, екв.: 15). Реакційну суміш перемішували при 60 °C протягом ночі. До цієї суміші додавали 2 мл діетилового ефіру та перемішували протягом 15 хв. при кімнатній температурі. Цю суміш фільтрували та концентрували у високому вакуумі з одержанням + бажаного гідрохлориду у вигляді білої твердої речовини (9 мг, 60,0%). MS (ISP): 443,1 ([M+H] ). Приклад 42 (S)-3-(3-(Дифторметокси)феніл)-1-етил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5карбоксаміду гідрохлорид O O N H N N H N O F F 24 UA 110525 C2 До розчину (S)-трет-бутил-2-(4-(3-(3-(дифторметокси)феніл)-1-етил-1H-піразол-5карбоксамідо)феніл)морфолін-4-карбоксилату (27 мг) (одержаного в Прикладі 41, b)) в діоксані (40,8 мкл) додавали 4M HCl в діоксані (117 мкл, 470 мкмоль, екв.: 15). Реакційну суміш перемішували при 60 °C протягом ночі. До цієї суміші додавали 2 мл діетилового ефіру та перемішували протягом 15 хв. при кімнатній температурі. Цю суміш фільтрували та концентрували у високому вакуумі з одержанням бажаного гідрохлориду у вигляді білої твердої + речовини (15 мг, 63%). MS (ISP): 443,1 ([M+H] ). Приклад 43 (S)-3-(3-Ціано-2-фторфеніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5-карбоксаміду гідрохлорид O O N H H N N H N F CN Вказану в заголовку сполуку одержували за аналогією з Прикладом 39 з використанням 1-(3бром-2-фторфеніл)етанону замість 1-(3-бром-4-фторфеніл)етанону. + Біла тверда речовина. MS (ISP): 392,1 ([M+H] ). Приклад 44 (S)-3-(3-(Дифторметокси)феніл)-1-метил-N-(4-(морфолін-2-іл)феніл)-1H-піразол-5карбоксаміду гідрохлорид O O N H N N H N O F F Вказану в заголовку сполуку одержували за аналогією з Прикладом 42 з використанням метилйодиду замість йодетану. + Біла тверда речовина. MS (ISP): 429,1 ([M+H] ). Приклад 45 (S)-1-(4-(Дифторметокси)феніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксаміду гідрохлорид O O N H N H N N F O F a) Етил-2-хлор-2-(2-(4-(дифторметокси)феніл)гідразоно)ацетат 4-(Дифторметоксі)анілін (796 мг, 5 ммоль) розчиняли в тетрафторборній кислоті (2,38 г, 1,7 мл, 13,0 ммоль) та воді (2 мл). Після охолодження до 0 °C повільно додавали розчин нітриту натрію (345 мг, 5,0 ммоль) у воді (0,75 мл). Цю суміш перемішували протягом 30 хв., збирали густий преципітат фільтрацією та промивали діетиловим ефіром (близько 3 мл). Одержану 25 UA 110525 C2 світло-рожеву тверду речовину розчиняли в 1,5 мл ацетону та додавали 5 мл діетилового ефіру. Після перемішування протягом 15 хв. з охолодженням одержану білу тверду речовину фільтрували, промивали діетиловим ефіром та висушували у високому вакуумі протягом 15 хв. з одержанням 4-дифторметоксифенілдіазонію тетрафторборату. Цю сіль діазонію (851 мг, 3,3 ммоль) додавали до розчину етил-2-хлор-3-оксобутирату (494 мг, 420 мкл, 3 ммоль) в піридині (0,8 мл) та воді (0,8 мл). Одержану дуже густу суспензію перемішували при -5 °C протягом 30 хв. Тверду речовину фільтрували, промивали льодяною водою та висушували у вакуумі з одержанням оранжевої твердої речовини (0,67 г, 76%). MS 35 + 37 + (ISP): 293,1 ([{ Cl}M+H] ), 295,2 ([{ Cl}M+H] ). b) Етил-1-(4-(дифторметокси)феніл)-1H-піразол-3-карбоксилат Етил-2-хлор-2-(2-(4-(дифторметокси)феніл)гідразоно)ацетат (585 мг, 2 ммоль) розчиняли в толуолі (4 мл) та додавали 2,5-норборнадієн (906 мг, 1 мл, 9,83 ммоль) та триетиламін (587 мг, 808 мкл, 5,8 ммоль). Реакційну суміш перемішували при 70 °C протягом 30 хв. та залишали перемішуватися при кімнатній температурі протягом ночі. Одержану тверду речовину відфільтровували та промивали толуолом. Органічну фракцію випарювали, одержаний залишок розчиняли в ксилолі (12 мл) та нагрівали при температурі флегми протягом 2 год. Розчинник випарювали та одержаний залишок очищали хроматографією на колонці (50 г силікагелю, дихлорметан) з одержанням 387 мг (69%) світло-жовтої твердої речовини. MS (ISP): 283,1 + ([M+H] ). c) 1-(4-(Дифторметокси)феніл)-1H-піразол-3-карбонова кислота До розчину етил-1-(4-(дифторметокси)феніл)-1H-піразол-3-карбоксилату (350 мг, 1,24 ммоль) в суміші ТГФ (3,1 мл), метанолу (1,6 мл) та води (1,6 мл) додавали гідроксиду літію гідрат (89 мг, 3,72 ммоль). Цей розчин нагрівали до 80 °C протягом 2 год. Більшу частину органічного розчинника видаляли при зниженому тиску. Додавали розчин бікарбонату натрію та етилацетат, органічний шар відокремлювали. Водний шар підкислювали додаванням 25% водної хлористоводневої кислоти, і цю суміш екстрагували 2 рази етилацетатом. Органічні шари об’єднували, висушували (MgSO4) та випарювали. Одержаний продукт висушували у вакуумі та безпосередньо використовували на наступній стадії. d) (S)-трет-Бутил-2-(4-(1-(4-(дифторметокси)феніл)-1H-піразол-3-карбоксамідо)феніл)морфолін-4-карбоксилат (S)-трет-Бутил-2-(4-амінофеніл)морфолін-4-карбоксилат (110 мг, 0,39 ммоль), 1-(4(дифторметокси)феніл)-1H-піразол-3-карбонову кислоту (100 мг, 0,39 ммоль), HBTU (167 мг, 0,44 ммоль) та N-метилморфолін (119 мг, 130 мкл, 1,18 ммоль) об’єднували з ДМФ (2 мл) з одержанням світло-жовтого розчину. Реакційну суміш перемішували при 50 °C протягом 17 год. Реакційну суміш вливали в 25 мл води та двічі екстрагували етилацетатом. Об’єднані органічні шари промивали сольовим розчином, висушували над MgSO4 та концентрували у вакуумі. Неочищену речовину очищали флеш-хроматографією (20 г силікагелю, етилацетат в гептані від 30 до 50%) з одержанням брудно-білої твердої речовини (130 мг, 64%). MS (ISP): + + 459,4 (100%, [M tBu+H] ), 515,4 (5%, [M+H] ). e) (S)-1-(4-(Дифторметокси)феніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксаміду гідрохлорид (S)-трет-Бутил-2-(4-(1-(4-(дифторметокси)феніл)-1H-піразол-3-карбоксамідо)феніл)морфолін-4-карбоксилат (130 мг, 0,25 ммоль) розчиняли в діоксані (0,6 мл) та додавали розчин HCl в діоксані (4M, 0,12 мл, 3,8 ммоль). Реакційну суміш перемішували протягом ночі при 60 °C. Після охолодження додавали ефір, одержану тверду речовину відфільтровували, промивали ефіром та висушували у вакуумі з одержанням (S)-1-(4-(дифторметокси)феніл)-N-(4-(морфолін2-іл)феніл)-1H-піразол-3-карбоксаміду гідрохлориду (90 мг, 79%) у вигляді брудно-білої твердої + речовини. MS (ISP): 415,4 ([M+H] ). Приклад 46 (R)-1-(4-(Дифторметокси)феніл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксаміду гідрохлорид F F O H N N N O O ClH N H Вказану в заголовку сполуку одержували за аналогією з Прикладом 45 з використанням (R)трет-бутил-2-(4-амінофеніл)морфолін-4-карбоксилату замість (S)-трет-бутил-2-(4 26 UA 110525 C2 амінофеніл)морфолін-4-карбоксилату на стадії c). Брудно-біла тверда речовина. MS (ISP): 415,4 + ([M+H] ). Приклад 47 (S)-N-(4-(Морфолін-2-іл)феніл)-1-(5-(трифторметил)піримідин-2-іл)-1H-піразол-3карбоксаміду гідрохлорид F F N F N H N N N O O ClH N H a) (S)-трет-Бутил-2-(4-(1H-піразол-3-карбоксамідо)феніл)морфолін-4-карбоксилат 1H-Піразол-3-карбонову кислоту (560 мг, 5 ммоль) розчиняли в метанолі (62 мл) та додавали (S)-трет-бутил-2-(4-амінофеніл)морфолін-4-карбоксилат (1,39 г, 5 ммоль). Цей розчин охолоджували до 0 °C та до реакційної суміші додавали по краплях 4-(4,6-диметокси-1,3,5триазин-2-іл)-4-метилморфолінію хлорид (1,8 г, 6,5 ммоль), розчинений в 5 мл метанолу, протягом 1 год. Реакційну суміш перемішували при 0 °C протягом двох годин, потім протягом ночі при кімнатній температурі. Розчинник випарювали, одержаний залишок розчиняли в дихлорметані та адсорбували на силікагелі. Одержану речовину очищали флеш-хроматографією (силікагель, 20 г, EtOAc в гептані від 30% до 50%) з одержанням білої твердої речовини (1,61 г; 86%) яку використовували на наступній стадії. b) (S)-трет-Бутил-2-(4-(1-(5-(трифторметил)піримідин-2-іл)-1H-піразол-3карбоксамідо)феніл)морфолін-4-карбоксилат (S)-трет-Бутил-2-(4-(1H-піразол-3-карбоксамідо)феніл)морфолін-4-карбоксилат (33 мг, 0,089 ммоль) та 2-хлор-5-(трифторметил)піримідин (16,2 мг, 0,089 ммоль) розчиняли в ДМСО (0,7 мл) та додавали карбонат калію (24,5 мг, 0,177 ммоль). Реакційну суміш поміщали на шейкер Büchi на 20 год. при 120 °C. Після охолодження суміші додавали воду з подальшою двократною екстракцією етилацетатом. Об’єднані органічні шари висушували над MgSO4 та випарювали. Неочищену речовину очищали флеш-хроматографією (силікагель, 5 г, EtOAc в гептані від 25% до 50%) з одержанням брудно-білої твердої речовини (11 мг, 24%). MS (ISP): 463,1 (100%, [M + + tBu+H] ), 519,3 (10%, [M+H] ). c) (S)-N-(4-(Морфолін-2-іл)феніл)-1-(4-(трифторметокси)феніл)-1H-піразол-4-карбоксаміду гідрохлорид (S)-трет-Бутил-2-(4-(1-(5-(трифторметил)піримідин-2-іл)-1H-піразол-3-карбоксамідо)феніл)морфолін-4-карбоксилат (11 мг, 21,2 мкмоль) розчиняли в діоксані (80 мкл), додавали розчин HCl в діоксані (79,6 мкл, 318 мкмоль) і цю реакційну суміш перемішували при 60 °C протягом 2 год. Після охолодження додавали діетиловий ефір, одержану тверду речовину фільтрували та промивали діетиловим ефіром з одержанням (S)-N-(4-(морфолін-2-іл)феніл)-1(4-(трифторметокси)феніл)-1H-піразол-4-карбоксаміду гідрохлориду (7 мг, 70%) у вигляді + брудно-білої твердої речовини. MS (ISP): 419,3 ([M+H] ). Приклад 48 (S)-1-(6-Хлорпіразин-2-іл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксаміду гідрохлорид Cl N H N N N N O O ClH N H Вказану в заголовку сполуку одержували за аналогією з Прикладом 47 з використанням 2,6дихлорпіразину замість 2-хлор-5-(трифторметил)піримідину на стадії b). Жовта тверда 35 + 37 + + речовина. MS (ISP): 385,3 ([{ Cl}M+H] ), 387,3 ([{ Cl}M+H] ). ([M+H] ). Приклад 49 (S)-1-(3-Хлорпіразин-2-іл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксаміду гідрохлорид 27 UA 110525 C2 N H N N N N Cl O O ClH N H a) (S)-трет-Бутил-2-(4-(1-(3-хлорпіразин-2-іл)-1H-піразол-3-карбоксамідо)феніл)морфолін-4карбоксилат (S)-трет-Бутил-2-(4-(1H-піразол-3-карбоксамідо)феніл)морфолін-4-карбоксилат (90 мг, 0,24 ммоль) та 2,3-дихлорпіразин (43 мг, 0,29 ммоль) розчиняли в диметилацетаміді (2 мл) та додавали карбонат калію (67 мг, 0,48 ммоль). Реакційну суміш поміщали на шейкер Büchi на 16 год. при 80 °C. Для завершення реакції вносили додаткову кількість 2,3-дихлорпіразину (10 мг) та продовжували нагрівати протягом ще 2 год. при 120 °C. Після охолодження суміші додавали воду з подальшою двократною екстракцією етилацетатом. Об’єднані органічні шари висушували над MgSO4 та випарювали. Неочищену речовину очищали флеш-хроматографією (силікагель, 10 г, EtOAc в гептані від 25% до 50%) з одержанням брудно-білої смоли (48 мг, + + 42%). MS (ISP): 429,3 (100%, [M tBu+H] ), 485,4 (10%, [M+H] ). b) (S)-1-(3-Хлорпіразин-2-іл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксаміду гідрохлорид (S)-трет-Бутил-2-(4-(1-(3-хлорпіразин-2-іл)-1H-піразол-3-карбоксамідо)феніл)морфолін-4карбоксилат (44 мг, 90,7 мкмоль) розчиняли в діоксані (0,35 мл), додавали розчин HCl в діоксані (340 мкл, 1,36 ммоль) та реакційну суміш перемішували при 60 °C протягом 90 хв. Цей розчинник випарювали та одержаний залишок перекристалізовували із суміші етилацетату та етанолу з одержанням світло-жовтої твердої речовини (27 мг, 70%). MS (ISP): 35 + 37 + + 385,2 ([{ Cl}M+H] ), 387,2 ([{ Cl}M+H] ). ([M+H] ). Приклад 50 (S)-1-(5-Хлорпіразин-2-іл)-N-(4-(морфолін-2-іл)феніл)-1H-піразол-3-карбоксаміду гідрохлорид N H N N Cl N N O O ClH N H Вказану в заголовку сполуку одержували за аналогією з Прикладом 49 з використанням 2,5дихлорпіразину замість 2,3-дихлорпіразину на стадії a). Брудно-біла тверда речовина. MS (ISP): 35 + 37 + + 385,2 ([{ Cl}M+H] ), 387,2 ([{ Cl}M+H] ). ([M+H] ). Приклад 51 (S)-N-(4-(Морфолін-2-іл)феніл)-1-(6-(трифторметил)піримідин-4-іл)-1H-піразол-3карбоксаміду гідрохлорид N H N N N N F F O O F ClH N H Вказану в заголовку сполуку одержували за аналогією з Прикладом 49 з використанням 4хлор-6-(трифторметил)піримідину замість 2,3-дихлорпіразину на стадії a). Біла тверда + речовина. MS (ISP): 419,2 ([M+H] ). Приклад 52 (S)-N-(4-(Морфолін-2-іл)феніл)-1-(6-(трифторметил)піразин-2-іл)-1H-піразол-3-карбоксаміду гідрохлорид F F F N H N N N N O O N H ClH 28
ДивитисяДодаткова інформація
Назва патенту англійськоюPyrazole derivatives
Автори англійськоюGalley, Guido, Ghellamallah, Cedric, Norcross, Roger, Pflieger, Philippe
Автори російськоюГаллей Гуидо, Гелламалла Седрик, Норкросс Роджер, Пфлигер Филипп
МПК / Мітки
МПК: A61P 25/00, C07D 413/14, C07D 413/12, A61K 31/4245
Код посилання
<a href="https://ua.patents.su/38-110525-pokhidni-pirazolu.html" target="_blank" rel="follow" title="База патентів України">Похідні піразолу</a>
Попередній патент: Спосіб екстрагування рослинної олії
Наступний патент: Дейтеровані 1-піперазино-3-феніліндани для лікування шизофренії
Випадковий патент: Асинхронний тяговий електродвигун












