Карбоксаміди, спосіб їх отримання і фармацевтична композиція
Номер патенту: 58488
Опубліковано: 15.08.2003
Автори: ЛІАК Тенг Дж., КАСТЕЛЬХАНО Арліндо Л., ДІЛ Джудіт Дж., ЮАН Женгью, БЕНДЕР Стівн Л., ХОРН Стивн
Формула / Реферат
1. Карбоксамиды формулы
,
где
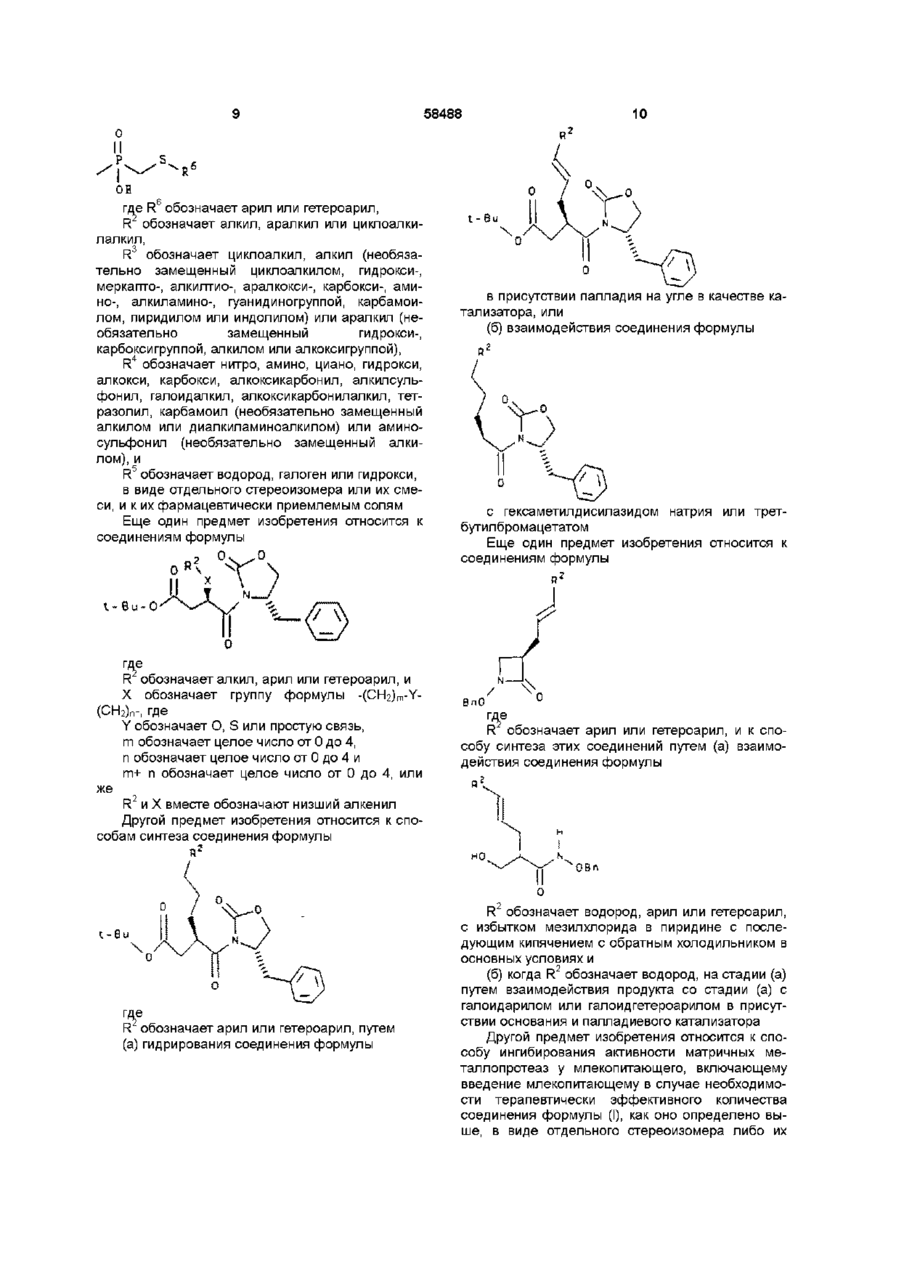
R1 обозначает меркапто, ацетилтио, карбокси, гидроксикарбамоил, N-гидроксиформиламино, алкоксикарбонил с 1-10 атомами углерода, арилоксикарбонил, аралкоксикарбонил, бензилоксикарбамоил или группу формулы
,
где R6 обозначает арил или гетероарил;
R2 обозначает алкил с 1 -10 атомами углерода, циклоалкил, арил, гетероциклоалкил или гетероарил;
R3 обозначает алкил с 1 -10 атомами углерода, циклоалкил с 5 - 7 атомами углерода, аралкил или гетероаралкил;
R7 обозначает арил, гетероарил или гетероциклоалкил;
Х обозначает группу формулы - (СН2)m-Y- (СН2)n-, где
Y обозначает О, S или простую связь,
m обозначает целое число от 0 до 4,
n обозначает целое число от 0 до 4 и
m+n обозначает целое число от 0 до 4;
р обозначает целое число от 0 до 4 при условии, что R2 -X обозначает бифенилалкил, когда
р не равно 0, и R2-X не является алкилом, аралкилом или циклоалкилалкилом, если р равно 0
и R7 является фенилом;
или их фармацевтически приемлемые соли.
2. Карбоксамиды или их соли по п. 1, где R1 обозначает карбокси; R3 обозначает циклогексил; R7 обозначает необязательно замещенный фенил или N-морфолино; Х обозначает пропан-1,3-диил и р равно 2 или 3.
3. Карбоксамиды или их соли по п. 2, где R7 обозначает 4-(аминосульфонил)фенил или N-морфолино.
4. Карбоксамиды или их соли по п. 1, где R2 обозначает алкил с 1 - 10 атомами углерода, необязательно замещенный фенил или группу формулы
,
где А обозначает СН2, O, NH, S, СН2-СH2 или NH-CH2;
R10 обозначает Н, алкил, алкокси, алкиламино или ациламино;
R11 обозначает Н или галоген;
R7 обозначает 4-пиридил или необязательно замещенный фенил;
р равно 0.
5. Карбоксамиды или их соли по п. 4, где R1 обозначает карбокси, гидроксикарбамоил или N-гидроксиформиламино; R2 обозначает фенил, бифенил, 4-(пиридил)фенил или 2-метилпропил; R3 обозначает трет-бутил, 4-аминобутил, диметиламинобутил, 4-(N,N'-диэтилгуанидо)бутил, пропил, 2-метилпропил, 1-гидроксиизопропил, 1-гидроксиэтил или циклогексил и Х обозначает простую связь, этилен или пропан-1,3-диил.
6. Карбоксамиды или их соли по п. 4, где R2 обозначает бифенил.
7. Карбоксамиды или их соли по п. 6, где R1 обозначает карбокси, N-гидроксиформиламино или гидроксикарбамоил; R3 обозначает алкил с 1 - 10 атомами углерода и R7 обозначает 4-пиридил.
8. Карбоксамиды или их соли по п. 7, где R3 обозначает трет-бутил и Х обозначает пропан- 1,3-диил.
9. Карбоксамиды или их соли по п. 8, где R1 обозначает карбокси, N-гидроксиформиламино или гидроксикарбамоил.
10. Карбоксамиды или их соли по п. 4, где R2 обозначает группу формулы
,
где А обозначает CH2;
R10 обозначает Н или ациламино;
R11 обозначает Н;
R7 обозначает необязательно замещенный фенил;
Х обозначает пропан-1,3-диил.
11. Карбоксамиды или их соли по п. 10, где R1 обозначает карбокси, гидроксикарбамоил или N-гидроксиформиламино; R3 обозначает алкил и R7 обозначает алкоксикарбонилфенил.
12. Карбоксамиды или их соли по п. 11, где R1 обозначает карбокси; R3 обозначает 2-метилпропил и R7 обозначает 4-(метоксикарбонил)фенил.
13. Карбоксамиды или их соли по п. 6, где R7 обозначает необязательно замещенный фенил.
14. Карбоксамиды или их соли по п. 13, где R1 обозначает карбокси; R3 обозначает алкил с 1 -10 атомами углерода или циклоалкил с 5 - 7 атомами углерода и Х обозначает пропан-1,3-диил.
15. Карбоксамиды или их соли по п. 14, где R3 обозначает циклогексил и R7 обозначает 4-(гидроксиэтиламиносульфонил)фенил или 4-(диметиламиноэтиламиносульфонил)фенил; или R3 обозначает 4-(амино)бутил или 4-(изопропиламино)бутил и R7 обозначает 4-(этоксикарбонил)фенил; или R3 обозначает 1-гидроксиизопропил и R7 обозначает фенил; или R3 обозначает трет-бутил.
16. Карбоксамиды или их соли по п. 15, где R7 обозначает
4-(N-морфолинопропиламиносульфонил)фенил, 4-(метиламиносульфонил)фенил,
4- (гидроксиэтиламиносульфонил)фенил или 4-(метилсульфинил)фенил.
17. Карбоксамиды или их соли по п. 4, где R1 обозначает карбокси; R2 обозначает фенил; R обозначает алкил с 1 - 10 атомами углерода или циклоалкил с 5 - 7 атомами углерода и R7 обозначает необязательно замещенный фенил.
18. Карбоксамиды или их соли по п. 17, где R3 обозначает 4-(амино)бутил; R7 обозначает 4-(этоксикарбонил)фенил и Х обозначает пропан-1,3-диил; или R3 обозначает (N,N'-диэтилгуанидо)-N- бутил; R7 обозначает 4-(этоксикарбонил)фенил и Х обозначает пропилен; или R3 обозначает циклогексил; R7 обозначает 4-(N",N"-диметиламиноэтиламиносульфонил)фенил и Х обозначает этилен.
19. Карбоксамиды или их соли по п. 4, где R1 обозначает меркапто, карбокси, гидроксикарбамоил или N-гидроксиформиламино; R2 обозначает 2-метилпропил; R3 обозначает алкил с 1 -10 атомами углерода, циклоалкил с 5 -7 атомами углерода или гетероалкил; R7 обозначает необязательно замещенный фенил и Х обозначает простую связь.
20. Карбоксамиды или их соли по п. 19, где R1 обозначает гидроксикарбамоил; R3 обозначает пропил, 2-метилпропил, циклогексил или 3-метилиндолил; R7 обозначает 4-(метокси)фенил, 4-(карбокси)фенил, 4-(метоксикарбонил)фенил или 4- (диметиламиноэтилкарбамоил)фенил.
21. Карбоксамиды или их соли по п. 20, где R7 обозначает 4-(диметиламиноэтилкарбамоил)фенил или R7 обозначает 4-(метоксикарбонил)фенил.
22. Карбоксамиды или их соли по п. 19, где R1 обозначает N-гидроксиформиламино; R3 обозначает 2-метилпропил и R7 обозначает 4-(метоксикарбонил)фенил; или R1 обозначает карбокси; R3 обозначает циклогексил или 2-метилпропил и R7 обозначает 4-(метоксикарбонил)фенил; или R1 обозначает меркапто; R3 обозначает 2-метилпропил и R7 обозначает 4-(метоксикарбонил)фенил.
23. Карбоксамиды или их соли по п. 4, где R1 обозначает карбокси; R2 обозначает 4-(2-гидроксиэтил)фенил, 4-(2-гидроксипропил)фенил, 4-(2-гидроксибутил)фенил, 4-пиридилфенил, бифенил, 4'-(аминоэтокси)бифенил, 4'-(циан)бифенил или 4'-(гидрокси)бифенил; R3 обозначает 2-метилпропил; R7 обозначает 4-(метоксикарбонил)фенил и Х обозначает пропан-1,3-диил.
24. Карбоксамиды или их соли по п. 23, где R2 обозначает 4-(пиридил)фенил.
25. Фармацевтическая композиция, обладающая способностью ингибировать активность матричных металлопротеаз, содержащая действующее вещество и фармацевтически приемлемый эксципиент, отличающаяся тем, что в качестве действующего вещества она содержит соединение по п. 1 или его соль в эффективном количестве.
26. Способ получения карбоксамидов формулы I
,
где R1 обозначает меркапто, ацетилтио, карбокси, гидроксикарбамоил, N-гидроксиформиламино, алкоксикарбонил с 1 - 10 атомами углерода, арилоксикарбонил, аралкоксикарбонил, бензилоксикарбамоил или тиометилфосфиноильную группу формулы
,
где R6 обозначает арил или гетероарил;
R2 обозначает алкил с 1 - 10 атомами углерода, циклоалкил с 5 -7 атомами углерода, арил, гетероциклоалкил или гетероарил;
R3 обозначает алкил с 1 - 10 атомами углерода, циклоалкил с 5 -7 атомами углерода, аралкил или гетероаралкил;
R7 обозначает арил, гетероарил или гетероциклоалкил;
Х обозначает группу формулы - (CH2)m-Y-(CH2)n-, где
Y обозначает О, S или простую связь,
m обозначает целое число от 0 до 4,
n обозначает целое число от 0 до 4,
m+n обозначает целое число от 0 до 4;
р обозначает целое число от 0 до 4, при условии, что R2-X обозначает бифенилалкил, когда
р не равно 0, и R2-X не является алкилом, аралкилом или циклоалкилалкилом, если р равно 0 и
R7 является фенилом;
или их фармацевтически приемлемой соли, отличающийся тем, что соединение формулы (D)
,
подвергают взаимодействию с соединением формулы (F)
,
где R1 обозначает алкоксикарбонил с 1 -10 атомами углерода, аралкоксикарбонил, арил- или гетероарилтиометилфосфиноил или ацетилтио,
в присутствии основания и реагента амидного сочетания с получением соответствующего соединения формулы I и с последующей, в случае необходимости, обработкой полученного соединения формулы I, где R1 обозначает алкоксикарбонил с 1 - 10 атомами углерода или аралкоксикарбонил, в слабокислой среде с получением соответствующего соединения формулы I, где R1 обозначает карбоксигруппу, которое, в случае необходимости, либо подвергают взаимодействию с O-бензилгидроксиамином с получением соединения формулы I, где R1 обозначает бензилоксикарбамоил, с последующим, в случае необходимости, каталитическим гидрированием с получением соответствующего соединения формулы I, где R1 обозначает гидроксикарбамоил, либо подвергают взаимодействию с гидроксиламином с получением соответствующего соединения формулы I, где R1 обозначает гидроксикарбамоил, или с последующей, в случае необходимости, обработкой соединения формулы I, где R1 обозначает ацетилтиогруппу, гидроксилом аммония в протонном растворителе с получением соответствующего соединения формулы I, где R1 обозначает меркаптогруппу.
Текст
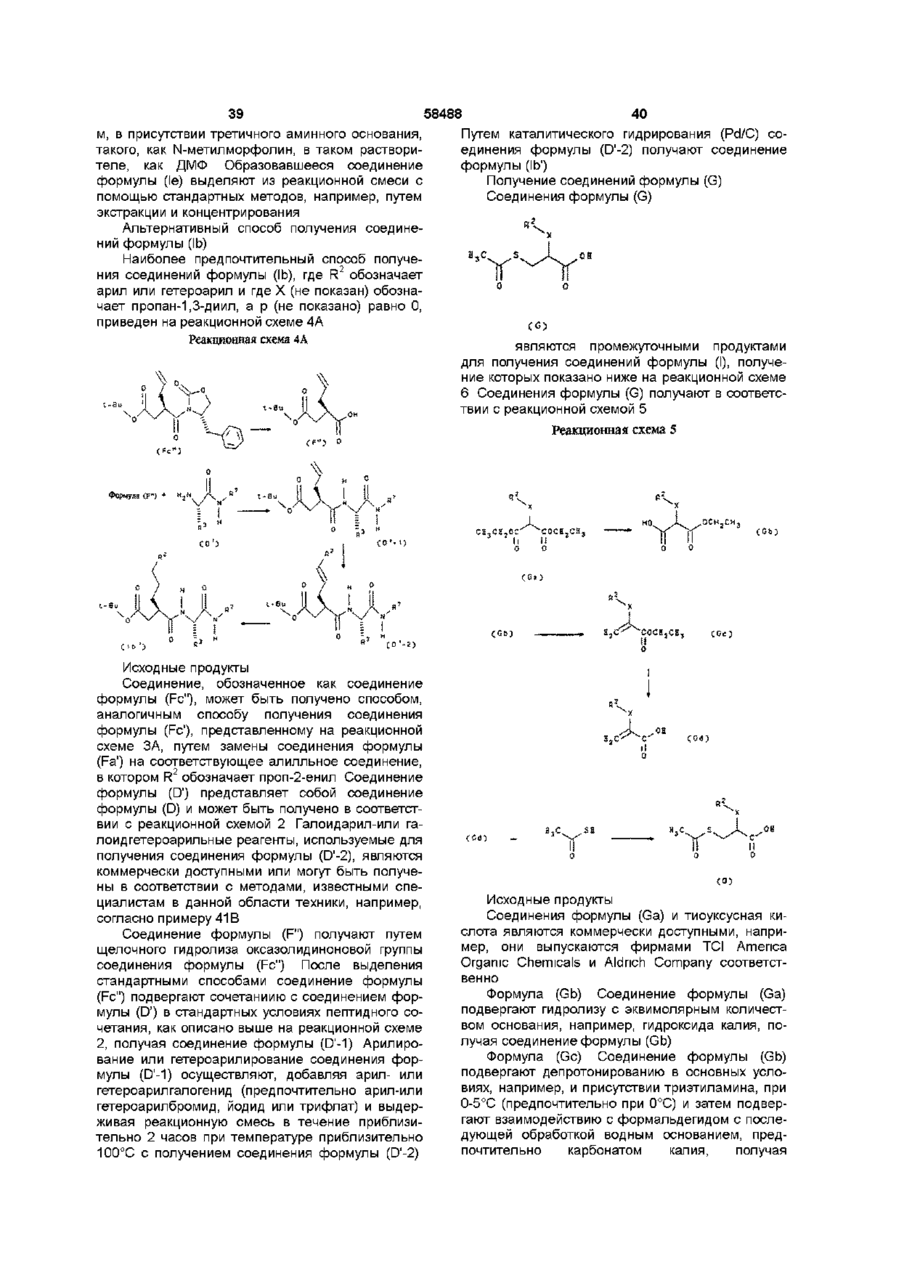
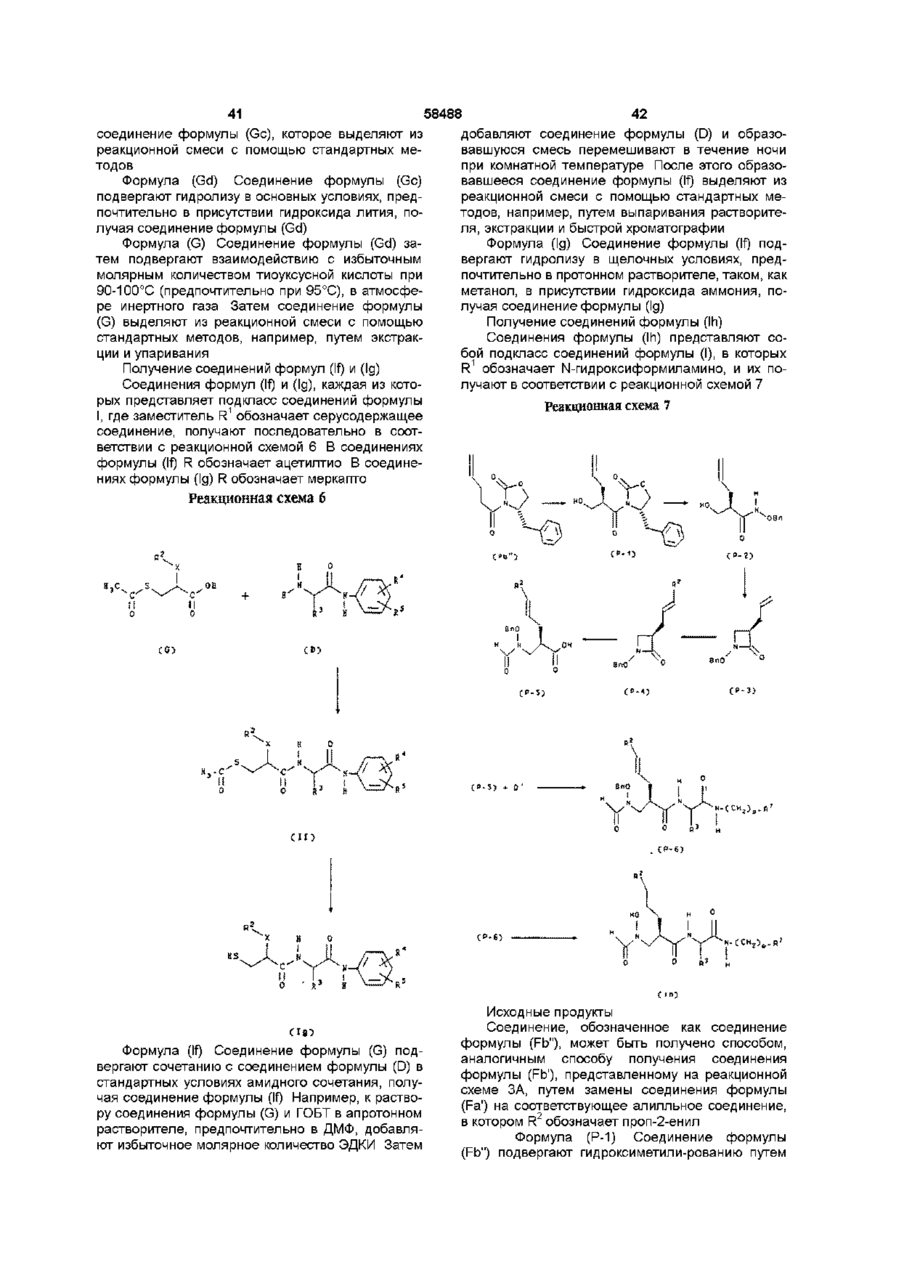
1 Карбоксамиды формулы R обозначает арил, гетероарил или гетероциклоалкил, X обозначает группу формулы - (CH2)m-Y- (СН2)П-, где Y обозначает О, S или простую связь, m обозначает целое число от 0 до 4, п обозначает целое число от 0 до 4 и m+n обозначает целое число от 0 до 4, р обозначает целое число от 0 до 4 при условии, что R2 -X обозначает бифенилалкил, когда р не равно 0, и R2-X не является алкилом, аралкилом или циклоалкил ал килом, если р равно 0 и R7 является фенилом, или их фармацевтически приемлемые соли 2 Карбоксамиды или их соли по п 1, где R1 обозначает карбокси, R3 обозначает циклогексил, R7 обозначает необязательно замещенный фенил или N-морфолино, Х обозначает пропан-1,3-диил и р равно 2 или 3 3 Карбоксамиды или их соли по п 2, где R1 обозначает 4-(аминосульфонил)фенил или Nморфолино 4 Карбоксамиды или их соли по п 1, где R2 обозначает алкил с 1 - 10 атомами углерода, необязательно замещенный фенил или группу формулы о 0 0 0 0 ^0 0 где R обозначает меркапто, ацетилтио, карбокси, гидроксикарбамоил, N-гидроксиформиламино, алкоксикарбонил с 1-10 атомами углерода, арилоксикарбонил, аралкоксикарбонил, бензилоксикарбамоил или группу формулы о II где R6 обозначает арил или гетероарил, R обозначает алкил с 1 -10 атомами углерода, циклоалкил, арил, гетероциклоалкил или гетероарил, R3 обозначает алкил с 1 -10 атомами углерода, циклоалкил с 5 - 7 атомами углерода, аралкил или гетероаралкил, ю где А обозначает СН2, О, NH, S, СН2-СН2 или NHСН2, R обозначает Н, алкил, алкокси, алкиламино или ациламино, R11 обозначает Н или галоген, R7 обозначает 4-пиридил или необязательно замещенный фенил, р равно 0 5 Карбоксамиды или их соли по п 4, где R1 обозначает карбокси, гидроксикарбамоил или Nгидроксиформиламино, R2 обозначает фенил, бифенил, 4-(пиридил)фенил или 2-метилпропил, R3 обозначает трет-бутил, 4-аминобутил, диметиламинобутил, 4-(г\1,г\Г-диэтилгуанидо)бутил, пропил, 2-метилпропил, 1-гидроксиизопропил, 1 58488 гидроксиэтил или циклогексил и X обозначает простую связь, этилен или пропан-1,3-диил 6 Карбоксамиды или их соли по п 4, где R2 обозначает бифенил 7 Карбоксамиды или их соли по п 6, где R1 обозначает карбокси, N-гидроксиформиламино или гидроксикарбамоил, R3 обозначает алкил с 1 - 10 атомами углерода и R7 обозначает 4-пиридил 8 Карбоксамиды или их соли по п 7, где R3 обозначает трет-бутил и X обозначает пропан- 1,3диил 9 Карбоксамиды или их соли по п 8, где R1 обозначает карбокси, N-гидроксиформиламино или гидроксикарбамоил 10 Карбоксамиды или их соли по п 4, где R2 обозначает группу формулы где А обозначает СЬк 1П R обозначает Н или ациламино, R11 обозначает Н, R7 обозначает необязательно замещенный фенил, X обозначает пропан-1,3-диил 11 Карбоксамиды или их соли по п 10, где R1 обозначает карбокси, гидроксикарбамоил или Nгидроксиформиламино, R3 обозначает алкил и R7 обозначает алкоксикарбонилфенил 12 Карбоксамиды или их соли по п 11, где R1 обозначает карбокси, R3 обозначает 2-метилпропил и R7 обозначает 4-(метоксикарбонил)фенил 13 Карбоксамиды или их соли по п 6, где R7 обозначает необязательно замещенный фенил 14 Карбоксамиды или их соли по п 13, где R1 обозначает карбокси, R3 обозначает алкил с 1 -10 атомами углерода или циклоалкил с 5 - 7 атомами углерода и X обозначает пропан-1,3-диил 15 Карбоксамиды или их соли по п 14, где R3 обозначает циклогексил и R7 обозначает 4(гидроксиэтиламиносульфонил)фенил или 4(диметиламиноэтиламиносульфонил)фенил, или R обозначает 4-(амино)бутил или 4(изопропиламино)бутил и R7 обозначает 4(этоксикарбонил)фенил или R3 обозначает 1гидроксиизопропил и R обозначает фенил, или R3 обозначает трет-бутил 16 Карбоксамиды или их соли по п 15, где R7 обозначает 4-(І\І-морфолинопропиламиносульфонил)фенил, 4-(метиламиносульфонил)фенил, 4- (гидроксиэтиламиносульфонил)фенил или 4(метилсульфинил)фенил 17 Карбоксамиды или их соли по п 4, где R1 обозначает карбокси, R2 обозначает фенил, R обозначает алкил с 1 - 10 атомами углерода или циклоалкил с 5 - 7 атомами углерода и R7 обозначает необязательно замещенный фенил 18 Карбоксамиды или их соли по п 17, где R3 обозначает 4-(амино)бутил, R7 обозначает 4(этоксикарбонил)фенил и X обозначает пропан 1,3-диил, или R обозначает (N.N'-диэтилгуанидо)N- бутил, R7 обозначает 4-(этоксикарбонил)фенил и X обозначает пропилен, или R3 обозначает циклогексил, R обозначает 4-(N",N"диметиламиноэтиламиносульфонил)фенил и X обозначает этилен 19 Карбоксамиды или их соли по п 4, где R1 обозначает меркапто, карбокси, гидроксикарбамоил или N-гидроксиформиламино, R обозначает 2метилпропил, R3 обозначает алкил с 1 -10 атомами углерода, циклоалкил с 5 -7 атомами углерода или гетероалкил, R7 обозначает необязательно замещенный фенил и X обозначает простую связь 20 Карбоксамиды или их соли по п 19, где R1 обозначает гидроксикарбамоил, R3 обозначает пропил, 2-метилпропил, циклогексил 3или метилиндолил, R обозначает 4-(метокси)фенил, 4-(карбокси)фенил, 4-(метоксикарбонил)фенил или 4- (диметиламиноэтилкарбамоил)фенил 21 Карбоксамиды или их соли по п 20, где R7 обозначает 4-(диметиламиноэтилкарбамоил)фенил или R7 обозначает 4-(метоксикарбонил)фенил 22 Карбоксамиды или их соли по п 19, где R1 обозначает N-гидроксиформиламино, R3 обозначает 2-метилпропил и R7 обозначает 4(метоксикарбонил)фенил, или R1 обозначает карет г> - Фирчула (Fc"-2) • Формула (Fb1) Сначала соединение формулы (Fa ) конденсируют в стандартных условиях с 4Sфенилметилоксазолидиноном с получением соответствующего соединения формулы (Fb') Формула (Fc') Приблизительно эквимолярное количество гексаметилди-силазида натрия добавляют к соединению формулы (Fb') в инертном растворителе, таком, как ТГФ Реакцию осуществляют при температуре от -80°С до -95°С в течение приблизительно 15 минут К этой смеси добавляют избыток третбутил б ром ацетата и раствор перемешивают в течение приблизительно 2 часов при температуре от -90°С до -60°С, получая отдельный стереоизомер формулы (Fc'), который очищают с помощью стандартных в органической химии способов Формула (F1) Группу оксазолидинона соединения формулы (Fc') удаляют в основных условиях с получением индивидуального стереоизомера формулы (F'), например, в соответствии со спосо1 Исходные продукты Соединение, обозначенное как соединение формулы (Fc"), может быть получено способом, аналогичным способу получения соединения формулы (Fc'), представленному на реакционной схеме ЗА, путем замены соединения формулы (Fa1) на соответствующее алилльное соединение, в котором группа, обозначенная X, представляет собой проп-2-енил, a R2 обозначает Н Формула (Fc"-1) Арилирование или гетероарилирование соединения формулы (Fc") осуществляют в присутствии основания и палладиевого катализатора добавлением арил- или гетероарилгалогенида, предпочтительно бромида или йодида, и выдержки реакционной смеси в течение 2-4 часов, предпочтительно 4 часов, при температуре приблизительно 100°С с образованием соединения формулы (Fc"-1) Формула (Fc"-2) Каталитическое гидрирование (Pd/C) аллильного соединения формулы (Fc"1) приводит к получению соответствующего алкильного соединения формулы (Fc"-2) Формула (F) Соединение формулы (Fc"-2) обрабатывают в щелочной среде, такой, как гидро 37 58488 пероксид лития (полученный in situ из гидроксида лития и перекиси водорода), сначала при пониженной температуре (предпочтительно при 0°С) в течение 15 минут и затем нагревают до комнатной температуры в течение 2 часов Смесь вновь охлаждают до 0°С и добавляют при перемешивании водную смесь сульфита натрия и бикарбоната натрия, после чего смеси дают нагреться до комнатной температуры, значение рН доводят до нейтрального, получая соединение формулы (F) с помощью стандартных методов выделения Получение соединений формул (Ib), (Ic), (Id) и (ІЄ) Соединения формул (Ib), (Ic), (Id) и (le), каждая из которых представляет подкласс соедине1 ний формулы (І), в которых заместитель R имеет различные значения, получают последовательно в соответствии с реакционной схемой 4, где R8 обозначает трет-бутил В соединениях формулы (Ib) R1 обозначает ал кокси карбон ил или аралкоксикарбонил В соединениях формулы (Ic) R обозначает карбокси В соединениях формулы (Id) R1 обозначает бензилоксикарбамоил В соединениях формулы (le) R обозначает гидроксикарбамоил Реакционная схема 4 о BS-QC о в'-ос С но с. R й 1 } О : \jZLr-l (.С Н ! II О Е 38 Исходные продукты Соединения формулы (D) получают в соответствии с реакционными схемами 2, 2А и 2Б Соединения формулы (F) получают в соответствии с реакционными схемами 3 и ЗА 0бензилгидроксиламин является коммерчески доступным, например, в виде гидрохлоридной соли, выпускаемой фирмой Aldnch Chemical Co Формула Ib Соединение формулы (F) подвергают сочетаниию с соединением формулы (D) в стандартных условиях амидного сочетания, получая соединение формулы (Ib) Например, к раствору соединения формулы (F) в апротонном растворителе, предпочтительно в ДМФ, содержащему небольшое избыточное молярное количество ГОБТ, добавляют избыточное молярное количество ЭДКИ Образовавшуюся смесь перемешивают в течение 1-2 часов (предпочтительно в течение 1 часа) при 0-5°С (предпочтительно при 0°С) Затем к холодному раствору добавляют эквимолярное количество соединения формулы (D) в присутствии основания, предпочтительно ДМАП Образовавшуюся смесь затем перемешивают в течение 12-24 часов (предпочтительно в течение 24 часов) при комнатной температуре (предпочтительно при 25°С) Затем соединение формулы (Ib) выделяют из реакционной смеси с помощью методов, стандартных в области химии пептидов, например, выпариванием растворителей, экстракцией, быстрой хроматографией и/или ЖХВР Формула Ic Соединение формулы (Ib) подвергают гидролизу в слабокислых условиях, предпочтительно в присутствии трифторуксусной кислоты, получая соединение формулы (Ic) Формула Id Соединение формулы (Ic) затем обрабатывают 0-бензилгидроксиламином в стандартных условиях амидного сочетания, получая соединение формулы (Id) Например, холодный (0-5°С) раствор соединения формулы (Ic) и ГОБТ в инертном растворителе, предпочтительно в ДМФ, обрабатывают избыточным молярным количеством ЭДКИ После перемешивания образовавшейся смеси в течение 0,5-1 ч при 0-5°С (предпочтительно при 0°С) добавляют эквимолярное количество О-бензилгидроксиламина Реакционной смеси дают нагреться и выдерживают при комнатной температуре в течении ночи (8-16 часов) Соединение формулы (Ib) затем выделяют из реакционной смеси с помощью стандартных методов, например, экстракцией и быстрой хроматографией Формула le Гидроксизащитную группу (бензил) соединения формулы (Id) удаляют в условиях каталитического гидрирования (Pd/C), получая соединение формулы (le) Альтернативный способ получения соединений формулы (le) Альтернативный способ получения соединений формулы (le) (в которых R4 обозначает в частности серусодержащий фрагмент, такой, как алкилсульфинил) состоит в обработке соответствующего соединения формулы (Ic) гидроксиламин-гидрохлоридом и реагентом пептидного сочетания, предпочтительно бензтриазол-1илокситрис(диметиламино)фосфонийгексафторфосфато 39 м, в присутствии третичного аминного основания, такого, как N-метилморфолин, в таком растворителе, как ДМФ Образовавшееся соединение формулы (1е) выделяют из реакционной смеси с помощью стандартных методов, например, путем экстракции и концентрирования Альтернативный способ получения соединений формулы (Ib) Наиболее предпочтительный способ получе2 ния соединений формулы (Ib), где R обозначает арил или гетероарил и где X (не показан) обозначает пропан-1,3-диил, а р (не показано) равно О, приведен на реакционной схеме 4А Реакционная ехала 4А 58488 40 Путем каталитического гидрирования (Pd/C) соединения формулы (D'-2) получают соединение 1 формулы (Ib ) Получение соединений формулы (G) Соединения формулы (G) Y " являются промежуточными продуктами для получения соединений формулы (I), получение которых показано ниже на реакционной схеме 6 Соединения формулы (G) получают в соответствии с реакционной схемой 5 Реакционная схема 5 h N о с СО ' - Е > Исходные продукты Соединение, обозначенное как соединение формулы (Fc"), может быть получено способом, аналогичным способу получения соединения формулы (Fc'), представленному на реакционной схеме ЗА, путем замены соединения формулы (Fa1) на соответствующее алилльное соединение, в котором R2 обозначает проп-2-енил Соединение 1 формулы (D ) представляет собой соединение формулы (D) и может быть получено в соответствии с реакционной схемой 2 Галоидарил-или галоидгетероарильные реагенты, используемые для получения соединения формулы (D'-2), являются коммерчески доступными или могут быть получены в соответствии с методами, известными специалистам в данной области техники, например, согласно примеру 41В Соединение формулы (F") получают путем щелочного гидролиза оксазолидиноновой группы соединения формулы (Fc") После выделения стандартными способами соединение формулы (Fc") подвергают сочетаниию с соединением формулы (D') в стандартных условиях пептидного сочетания, как описано выше на реакционной схеме 2, получая соединение формулы (D'-1) Арилирование или гетероарилирование соединения формулы (D'-1) осуществляют, добавляя арил- или гетероарилгалогенид (предпочтительно арил-или гетероарилбромид, йодид или трифлат) и выдерживая реакционную смесь в течение приблизительно 2 часов при температуре приблизительно 100°С с получением соединения формулы (D'-2) Исходные продукты Соединения формулы (Ga) и тиоуксусная кислота являются коммерчески доступными, например, они выпускаются фирмами TCI America Organic Chemicals и Aldnch Company соответственно Формула (Gb) Соединение формулы (Ga) подвергают гидролизу с эквимолярным количеством основания, например, гидроксида калия, получая соединение формулы (Gb) Формула (Gc) Соединение формулы (Gb) подвергают депротонированию в основных условиях, например, и присутствии триэтиламина, при 0-5°С (предпочтительно при 0°С) и затем подвергают взаимодействию с формальдегидом с последующей обработкой водным основанием, предпочтительно карбонатом калия, получая 41 58488 42 соединение формулы (Gc), которое выделяют из добавляют соединение формулы (D) и образореакционной смеси с помощью стандартных мевавшуюся смесь перемешивают в течение ночи тодов при комнатной температуре После этого образовавшееся соединение формулы (If) выделяют из Формула (Gd) Соединение формулы (Gc) реакционной смеси с помощью стандартных меподвергают гидролизу в основных условиях, предтодов, например, путем выпаривания растворитепочтительно в присутствии гидроксида лития, поля, экстракции и быстрой хроматографии лучая соединение формулы (Gd) Формула (G) Соединение формулы (Gd) заФормула (Ig) Соединение формулы (If) подтем подвергают взаимодействию с избыточным вергают гидролизу в щелочных условиях, предмолярным количеством тиоуксусной кислоты при почтительно в протонном растворителе, таком, как 90-100°С (предпочтительно при 95°С), в атмосфеметанол, в присутствии гидроксида аммония, поре инертного газа Затем соединение формулы лучая соединение формулы (Ig) (G) выделяют из реакционной смеси с помощью Получение соединений формулы (In) стандартных методов, например, путем экстракСоединения формулы (In) представляют соции и упаривания бой подкласс соединений формулы (І), в которых 1 R обозначает N-гидроксиформиламино, и их поПолучение соединений формул (If) и (Ig) лучают в соответствии с реакционной схемой 7 Соединения формул (If) и (Ig), каждая из которых представляет подкласс соединений формулы Реакционная схема 7 I, где заместитель R1 обозначает серусодержащее соединение, получают последовательно в соответствии с реакционной схемой 6 В соединениях формулы (If) R обозначает ацетилтио В соединениях формулы (Ig) R обозначает меркапто Реакционная схема 6 н с с" у^*-Р % К3 О й СИ) CIS) Формула (If) Соединение формулы (G) подвергают сочетанию с соединением формулы (D) в стандартных условиях амидного сочетания, получая соединение формулы (If) Например, к раствору соединения формулы (G) и ГОБТ в апротонном растворителе, предпочтительно в ДМФ, добавляют избыточное молярное количество ЭДКИ Затем В пО о Исходные продукты Соединение, обозначенное как соединение формулы (Fb"), может быть получено способом, аналогичным способу получения соединения формулы (Fb'), представленному на реакционной схеме ЗА, путем замены соединения формулы (Fa1) на соответствующее алилльное соединение, в котором R2 обозначает проп-2-енил Формула (Р-1) Соединение формулы (Fb") подвергают гидроксиметили-рованию путем 43 58488 инкубации с тетрахлоридом титана при пониженной температуре, предпочтительно при 0°С, в щелочных условиях в течение 1-3 часов, предпочтительно в течение 1 часа, с последующим добавлением S-триоксана и тетрахлорида титана и с продолжением инкубации при 0°С в течение 35 часов, предпочтительно 4 часов Соединение формулы (Р-1) затем выделяют стандартными способами, например, путем экстракции и хроматографии на колонках Формула (Р-2) Соединение формулы (Р-1) подвергают взаимодействию с избыточным молярным количеством О-бензилгидроксиламина и триметилалю-миния при пониженной температуре, предпочтительно при 0°С Реакции дают протекать при перемешивании в течение 5-7 часов, предпочтительно 6 часов, и при 0°С в атмосфере аргона Образовавшееся соединение формулы (Р2) выделяют стандартными способами Формула (Р-3) Избыток мезилхлорида подвергают взаимодействию с соединением формулы (Р-2) в пиридине при 0°С в течение нескольких часов, предпочтительно в течение 3 часов Реакционную смесь охлаждают на льду, экстрагируют органическим растворителем и концентрируют Концентрированный экстракт кипятят с обратным холодильником в щелочной среде в течение нескольких часов, предпочтительно в течение 3 часов, получая таким образом азетидиноновое соединение формулы (Р-3), которое очищают стандартными способами Формула (Р-4) Соединение формулы (Р-3) подвергают взаимодействию с соответствующей галогенирующей R -группой (например, с арилили гетероарилгалогенидом, предпочтительно с бромидом или йодидом) в инертном растворителе в присутствии основания, такого, кактриэтиламин, и палладиевого катализатора, предпочтительно образованного из ацетата палладия(П) и приблизительно двух молярных эквивалентов три-ортотолилфосфина После выдержки реакционной смеси в течение 15-20 часов, предпочтительно в течение 18 часов, при 100°С соответствующее соединение формулы (Р-4) выделяют и очищают стандартными способами Формула (Р-5) Расщепление азетидинонового кольца соединения формулы (Р-4) осуществляют в основных условиях при комнатной температуре в течение 1-3 часов, предпочтительно 1 часа Образовавшееся соединение экстрагируют органическим растворителем, концентрируют, повторно растворяют в содержащем основание растворителе (например, в пиридине) и карбоксилируют муравьиным ангидридом при пониженной температуре, предпочтительно при 0°С, в течение 30 минут, получая соответствующее соединение формулы (Р-5), которое выделяют стандартными способами Формула (Р-6) Соединение формулы (Р-5) подвергают сочетанию с соединением формулы (D1) в стандартных условиях амидного сочетания с образованием соответствующего соединения формулы (Р-6), которое выделяют стандартными способами Формула (In) Каталитическое гидрирование соединения формулы (Р-6) с помощью Pd/C с по 44 следующим удалением катализатора фильтрацией позволяет получить соответствующее соединение формулы (In) Получение солей Все соединения формулы (I), которые существуют либо в форме свободной кислоты, либо в форме свободного основания, кроме того, могут быть превращены в их фармацевтически приемлемые соли обработкой соответствующим неорганическим или органическим основанием или соответствующей неорганической или органической кислотой соответственно Соли соединений формулы (I) также могут быть превращены в свободную кислоту или свободное основание либо в другую соль Например, соединение формулы (I), имеющее фрагмент карбоновой кислоты, может быть превращено в карбоксилат добавлением 1 эквивалента NaOH или КОН в спиртовом растворителе с последующим выпариванием растворителя Соединение формулы (І) в форме свободного основания может быть превращено в хлоридную соль, например, добавлением 1 эквивалента HCI в органическом растворителе с последующим концентрированием Предпочтительные способы синтеза и заключительные стадии В целом, соединения формул (I) получают путем (А) взаимодействия соединения формулы (D) N~tCrf,V СО) с соединением формулы (F) где R1 обозначает ал кокси карбон ил, аралкоксикарбонил, арил- или гетероарилтиометилсульфосфиноил или ацетилтио, в присутствии основания и реагента амидного сочетания с получением соответствующего соединения формулы (I), или (Б) каталитического гидрирования соответствующего соединения, где X и R2 вместе обозначают необязательно арил- или гетероа рил замещенный алкенил, или (В) обработки соединения формулы (I), где R1 обозначает ал кокси карбон ил или арал кокси карбонил, в слабокислой среде с получением соответствующего соединения формулы (I), где R1 обозначает карбокси, или (Г) взаимодействия соединения формулы (I), где R1 обозначает карбокси, с Обензилгидроксиламином с получением соедине1 ния формулы (I), где R обозначает бензилоксикарбамоил, или (Д) каталитического гидрирования соединения формулы (I), где R1 обозначает бензилоксикарбамоил, с получением соответствующего соединения формулы (I), где R1 обозначает гидроксикарбамоил, или 45 (Е) взаимодействия соединения формулы (I), где R1 обозначает карбокси, с гидроксиламином с получением соответствующего соединения формулы (I), где R1 обозначает гидроксикарбамоил, или (Ж) каталитического гидрирования соединения формулы где ВпО обозначает бензилокси, с получением соответствующего соединения формулы (I), где R1 обозначает N-гидроксиформиламино, или (3) взаимодействия соединения формулы (I), где R обозначает ацетилтио, с гидроксидом аммония в протонном растворителе с получением соответствующего соединения формулы (I), где R1 обозначает меркапто Предпочтительный способ получения соединений формулы (I), где R1 обозначает Nгидроксиформиламино, включает превращение соединения формулы (Р-4) СВ.4) где R2 обозначает арил или гетероарил, путем щелочного гидролиза с последующим формилированием с получением соединения формулы (Р5) взаимодействия соединения формулы (Р5) с соединением формулы (D) с получением соединения формулы (Р-6) и каталитического гидрирования соединения формулы (Р-6) 46 Соединения, полученные с помощью вышеописанного способа по изобретению, могут быть идентифицированы по наличию определяемого количества одного или нескольких соединений формул (Р-3), (Р-4) или (Р-6) Хотя, как это хорошо известно, фармацевтические средства должны удовлетворять фармакопейным стандартам перед их утверждением и/или продажей, а чистота реагентов для синтеза (таких, как Обензилгидроксиламин) или предшественников [таких, как (Р-3), (Р-4) или (Р-6)] должна находиться в пределах, определяемых фармакопейными стандартами, конечные соединения, полученные способом согласно настоящему изобретению, могут содержать малые, но определяемые количества таких продуктов, присутствующих, например, в концентрациях 50част/млн или ниже Такие концентрации соединения формулы (Р-3) могут быть обнаружены, например, с помощью ГХ-МС, соединения формулы (Р-4) могут быть обнаружены, например, с помощью ЖХВР-МС или ЖХВР с флуоресцентным обнаружением, соединения формулы (Р-6) могут быть обнаружены, например, с помощью ЖХВР с флуоресцентным обнаружением Поскольку важно контролировать чистоту фармацевтических соединений на наличие в них указанных веществ, то в объем изобретения также включен метод их обнаружения, применяемый при осуществлении способа по настоящему изобретению 58488 Примеры Описанные ниже способы получения, композиции и примеры предназначены для более подробного пояснения сущности настоящего изобретения, что должно обеспечить возможность практического осуществления настоящего изобретения специалистами в данной области техники Эти примеры не следует рассматривать как ограничивающие объем изобретения, и они являются только иллюстративными и репрезентативными Пример 1 Соединения формулы (Еа) 1А Кристаллическую фосфиновую кислоту (8,4г, 0,13 моля) перемешивали в чистом триэтилортоформиате (22мл, 0,20 моля) в течение 90 минут при комнатной температуре Затем этот продукт переносили с помощью канюли в перемешиваемый раствор этилизобутилакрилата (8г, 0,036 моля) и тетраметилгуанидина (4,5мл, 0,036 моля), который охлаждали до 0°С в течение 10 минут Ледяную баню удаляли и реакционную смесь перемешивали в течение 4 часов Смесь разбавляли 200мл диэтилового эфира и раствор промывали 1н HCI (100мл), водой (4x100мл), соляным раствором (100мл) и сушили над сульфатом магния Этот продукт упаривали с помощью роторного испарителя, получая 8,15г этилового эфира 2-(этокси)фосфиноилметил-4метилпентановой кислоты в виде слегка желтоватого масла, МС 349 (М-Н2О)+ 1Б Аналогичным способом получали следующие соединения формулы (Еа) этиловый эфир 2-(этокси)фосфиноилметил-5фенилпентановой кислоты, этиловый эфир 2-(этокси)фосфиноилметил-4фенилбутановой кислоты, 47 58488 этиловый эфир 2-(этокси)фосфиноилметил-3фенилпропановой кислоты, этиловый эфир 2-(этокси)фосфиноилметил-3циклогексилпропановой кислоты, и этиловый эфир 2((этокси)фосфиноилметил)пентановой кислоты Пример 2 Соединения формулы (ЕЬ) 2А Неочищенный этиловый эфир 2(этокси)фосфиноилметил-4-метилпентановой кислоты (26г) растворяли в 600мл ТГФ/СН2С12 (50/50) и охлаждали до 0°С К раствору добавляли диизопропилэтиламин (32мл) и 90,8мл бис(триметилсилил)ацетамида и образовавшуюся смесь перемешивали в течение 20 минут с последующим добавлением параформальдегида (5,5г) Температуру раствора доводили до комнатной и выдерживали при 37°С в течение 18 часов Растворитель удаляли с помощью выпаривания и образовавшееся масло растворяли в 200мл этилацетата Раствор промывали 50мл 1 н HCI (2 раза), 50мл соляного раствора (2 раза), сушили над MgSO4, фильтровали и упаривали, получая 19,3г этилового эфира 2-(этокси)(гидроксиметил)фосфиноилметил-4метилпентановой кислоты в виде бледно-желтого масла, МС 281,2 (МН+) 2Б Аналогичным способом получали следующие соединения формулы (ЕЬ) этиловый эфир 2(этокси)(гидроксиметил)фосфиноилметил-5фенилпентановой кислоты, этиловый эфир 2(этокси)(гидроксиметил)фосфиноилметил-4фенилбутановой кислоты, этиловый эфир 2(этокси)(гидроксиметил)фосфиноилметил-3фенилпропановой кислоты, этиловый эфир 2(этокси)(гидроксиметил)фосфиноилметил-3циклогексилпропановой кислоты, и этиловый эфир 2((этокси)(гидроксиметил)фосфиноилметил)пентановой кислоты Пример 3 Соединения формулы (Ее) ЗА Этиловый эфир 2(этокси)(гидроксиметил)фосфиноилметил-4метилпентановой кислоты (5г) растворяли в 20мл CH2CI2 и охлаждали до -20°С (с дублированием) К раствору по каплям добавляли метансульфонилхлорид (1,5мл) и триэтиламин (3,0мл) Через 15 минут баню удаляли и реакционную смесь оставляли при комнатной температуре на 3,5 часа Затем каждый раствор промывали с помощью 10мл холодной 2%-ной HCI, 10мл ЫаНСОз (насыщенного), 10мл соляного раствора, сушили над MgSC^, фильтровали и упаривали, получая 12,8г (объединенный выход) этилового эфира 2- (этокси) (метансульфонилоксиметил)фосфиноилметил-4метилпентановой кислоты ЗБ Аналогичным способом, но заменяя метансульфонилхлорид на паратолуолсульфонилхлорид, получали этиловый эфир 2-(этокси)(пара 48 толуолсульфонилоксиметил)фосфиноилметил-4метилпентановой кислоты ЗВ Аналогичным способом получали следующие соединения формулы (Ее) этиловый эфир 2(этокси)(метансульфонилоксиметил)фосфиноилметил5-фенилпентановой кислоты, этиловый эфир 2(этокси)(метансульфонилоксиметил)фосфиноилметил4-фенилбутановой кислоты, этиловый эфир 2(этокси)(метансульфонилоксиметил)фосфиноилметил3-фенилпропановой кислоты, этиловый эфир 2(этокси)(метансульфонилоксиметил)фосфиноилметил3-циклогексилпропановой кислоты, этиловый эфир 2((этокси)(метансульфонилоксиметил)фосфиноилметил)пентановой кислоты, этиловый эфир 2-(этокси)(паратолуолсульфонилоксиметил)фосфиноил-метил-5фенилпентановой кислоты, этиловый эфир 2-(этокси)(паратолуолсульфонилоксиметил)фосфиноил-метил-4фенилбутановой кислоты, этиловый эфир 2-(этокси)(паратолуолсулсульфонилоксиметил)фосфиноилметил-3-фенилпропановой кислоты, этиловый эфир 2-(этокси)(паратолуолсулсульфонилоксиметил)фосфиноилметил-3-циклогексилпропановой кислоты, и этиловый эфир 2-((этокси)(паратолуолсульфонилоксиметил)фосфиноилметил)пентановой кислоты Пример 4 Соединения формулы (Ее) 4А Гидрид натрия (1,52г, (60%-ный)) и 2хинолинтиол (6г) перемешивали вместе при 0°С в 50мл ДМФ После прекращения первоначального выделения ЬІ2 смесь перемешивали при комнатной температуре в течение 2,5 часов Затем смесь охлаждали до 0°С и добавляли с помощью канюли этиловый эфир 2-(этокси) (метансульфонилоксиметил)фосфиноил-метил-4-метилпентановой кислоты (12,8г) в 10мл ДМФ, после чего образовавшуюся смесь перемешивали в течение 18 часов, медленно нагревая до комнатной температуры ДМФ удаляли путем выпаривания, остаток растворяли в 50мл этилацетата и промывали 50мл НгО (2 раза), соляным раствором (50мл), сушили над МдІЗСч и упаривали до желтого полутвердого продукта Путем очистки с помощью быстрой хроматографии с использованием для элюирования смеси от 10%- до 80%-ного этилацетата/гексана получали Юг этилового эфира 2-(этокси)(хинолин2-илтиометил)фосфиноилметил-4метилпентановой кислоты (Rf 0,35 для 80%-ного этилацетата/гексана), МС 424,1 (МН+) 4Б Аналогичным способом, но заменяя 2хинолинтиол на 1-нафталинтиол, 2-нафталинтиол 49 или тиофенол, получали следующие соединения формулы (Ее) этиловый эфир 2-(этокси)(нафт-1илтиометил)фосфиноилметил-4-метилпентановой кислоты, этиловый эфир 2-(этокси)(нафт-2илтиометил)фосфиноилметил-4-метилпентановой кислоты, и этиловый эфир 2(этокси)(фенилтиометил)фосфиноилметил-4метилпентановой кислоты 4В Аналогичным способом получали следующие соединения формулы (Ее) этиловый эфир 2-(этокси)(хинолин-2илтиометил)фосфиноилметил-5фенилпентановой кислоты, этиловый эфир 2-(этокси)(хинолин-2илтиометил)фосфиноилметил-4-фенилбутановой кислоты, этиловый эфир 2-(этокси)(хинолин-2илтиометил)фосфиноилметил-3фенилпропановой кислоты, этиловый эфир 2-(этокси)(хинолин-2илтиометил)фосфиноилметил-3циклогексилпропановой кислоты, этиловый эфир 2-((этокси)(хинолин-2илтиометил)фосфиноилметил)пентановой кислоты, этиловый эфир 2-(этокси)(нафт-1илтиометил)фосфиноилметил-5фенилпентановой кислоты, этиловый эфир 2-(этокси)(нафт-1илтиометил)фосфиноилметил-4-фенилбутановой кислоты, этиловый эфир 2-(этокси)(нафт-1илтиометил)фосфиноилметил-3фенилпропановой кислоты, этиловый эфир 2-(этокси)(нафт-1илтиометил)фосфиноилметил-3циклогексилпропановой кислоты, этиловый эфир 2-((этокси)(нафт-1илтиометил)фосфиноилметил)пента-новой кислоты, этиловый эфир 2-(этокси)(нафт-2илтиометил)фосфиноилметил-5фенилпентановой кислоты, этиловый эфир 2-(этокси)(нафт-2илтиометил)фосфиноилметил-4-фенилбутановой кислоты, этиловый эфир 2-(этокси)(нафт-2илтиометил)фосфиноилметил-3фенилпропановой кислоты, этиловый эфир 2-(этокси)(нафт-2илтиометил)фосфиноилметил-3циклогексилпропановой кислоты, этиловый эфир 2-((этокси)(нафт-2илтиометил)фосфиноилметил)пента-новой кислоты, этиловый эфир 2(этокси)(фенилтиометил)фосфиноилметил-5фенилпентановой кислоты, этиловый эфир 2(этокси)(фенилтиометил)фосфиноилметил-4фенилбутановой кислоты, 58488 50 этиловый эфир 2(этокси)(фенилтиометил)фосфиноилметил-3фенилпропановой кислоты, этиловый эфир 2(этокси)(фенилтиометил)фосфиноилметил-3циклогексилпропановой кислоты, и этиловый эфир 2((этокси)(фенилтиометил)фосфиноилметил)пентановой кислоты Пример 5 Соединения формулы (Е) 5А Этиловый эфир 2-(этокси)(хинолин-2илтиометил)фосфиноилметил-4-метилпентановой кислоты (4,5г) растворяли в 100мл ТГФ и добавляли 12,5мл 2н NaOH вместе с метанолом в количестве, достаточном для получения гомогенного раствора Через 18 часов ТГФ удаляли путем выпаривания, остаток растворяли в 50мл Ь^О и промывали 50мл этилацетата Затем водную фазу подкисляли до рН 4 и продукт экстрагировали 50мл этилацетата (2 раза) Этилацетатную фракцию промывали 20мл соляного раствора, сушили над MgSO4 и упаривали, получая 3,8г 2(гидрокси)(хинолин-2-илтиометил)фосфиноилметил-4-метилпентановой кислоты в виде желтого масла, МС 368 (МН+) 5Б Аналогичным способом получали следующие соединения формулы (Е) 2-(гидрокси)(нафт-1илтиометил)фосфиноилметил-4-метилпентановую кислоту, 2-(гидрокси)(нафт-2илтиометил)фосфиноилметил-4-метилпентановую кислоту, и 2(гидрокси)(фенилтиометил)фосфиноилметил-4метилпентановую кислоту 5В Аналогичным способом получают следующие соединения формулы (Е) 2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-5фенилпентановую кислоту, 2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-4-фенилбутановую кислоту, 2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-3фенилпропановую кислоту, 2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-3циклогексилпропановую кислоту, 2-((гидрокси)(хинолин-2илтиометил)фосфиноилметил)пентановую кислоту, 2-(гидрокси)(нафт-1илтиометил)фосфиноилметил-5фенилпентановую кислоту, 2-(гидрокси)(нафт-1илтиометил)фосфиноилметил-4-фенилбутановую кислоту, 2-(гадрокси)(нафт-1илтиометил)фосфиноилметил-3фенилпропановую кислоту, 51 58488 2-(гидрокси)(нафт-1илтиометил)фосфиноилметил-3циклогексилпропановую кислоту, 2-((гидрокси)(нафт-1илтиометил)фосфиноилметил)пентановую кислоту, 2-(гидрокси)(нафт-2илтиометил)фосфиноилметил-5фенилпентановую кислоту, 2-(гидрокси)(нафт-2илтиометил)фосфиноилметил-4-фенилбутановую кислоту, 2-(гидрокси)(нафт-2илтиометил)фосфиноилметил-3фенилпропановую кислоту, 2-(гидрокси)(нафт-2илтиометил)фосфиноилметил-3циклогексилпропановую кислоту, 2-((гидрокси)(нафт-2илтиометил)фосфиноилметил)пентановую кислоту, 2(гидрокси)(фенилтиометил)фосфиноилметил-5фенилпентановую кислоту, 2(гидрокси)(фенилтиометил)фосфиноилметил-4фенилбутановую кислоту, 2(гидрокси)(фенилтиометил)фосфиноилметил-3фенилпропановую кислоту, 2(гидрокси)(фенилтиометил)фосфиноилметил-3циклогексилпропановую кислоту, и 2((гидрокси)(фенилтиометил)фосфиноилметил)пентанову ю кислоту Пример 6 Разделение соединения формулы (Е) 2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-4-метилпентановую кислоту (5,3г) растворяли в 50мл теплого этанола (абсолютного) и добавляли 4,2г (-)-цинхонидина Через 30 минут при комнатной температуре начинала осаждаться соль Колбу покрывали фольгой и выдерживали в течение 2 дней Затем соль удаляли путем фильтрации под вакуумом и фильтрат упаривали до желтой пены Соль и фильтрат по отдельности растворяли в 100мл этилацетата и промывали последовательно 1%-ной HCI для удаления цинхонидина, поддерживая при этом значение рН выше 4 Оба раствора сушили по отдельности над MgSO4 и упаривали, получая 2,4г отдельного стереоизомера [а]о24=+10,68° (9,73мг в метаноле (2мл)) и 2,5г другого отдельного стереоизомера [а]р24 =-8,70° (9,88мг в метаноле (2мл)) Пример 7 Соединения формулы (В) 7А К холодной (0°С) суспензии 4ацетамидобензолсульфонилхлорида (4,0г, 17 ммолей) в CH2CI2 (40мл) добавляли пиридин (1,7мл, 20 ммолей) и ДМАП (209мг, 1,7 ммоля) (В результате образовывался прозрачный раствор) Безводный метиламин барботировали в растворе в течение 1 часа при 0°С, а затем раствор оставляли для перемешивания при 25°С в течение 2 52 часов Раствор экстрагировали 1М NaOH (3x15мл) и объединенные экстракты доводили до значения рН 6 при 0°С с помощью ЗМ HCI Продукт, который осаждался в виде пушистых белых кристаллов, фильтровали и промывали холодной водой, получая 3,2г (82%) 4-ацетамидо-ІЧметилбензолсульфонами-да, 1Н-ЯМР (300МГц, МеОН) 5 2,35 (s,3H), 2,70 (s,3H), 7,96 (s,4H) 7Б Смесь 4-ацетамидо-ІЧметилбензрлсульфонамида (3,2г, 14 ммолей) и 100мл 1М HCI выдерживали при температуре кипения с обратным холодильником в атмосфере аргона в течение 3 часов После охлаждения до 25°С добавляли CH2CI2 (10мл) и водную фазу нейтрализовали с помощью 1М NaOH при 0°С Водную фазу отделяли и экстрагировали CH2CI2 (2х25мл) Объединенные органические фазы промывали соляным раствором (10мл), сушили (Na2SO4) и концентрировали, получая 1,5г (58%) соединения формулы (В), где R4 обозначает Nметилсульфонамид, в виде бесцветного твердого продукта, 1Н-ЯМР (300МГц, МеОН) 5 2,46 (s,3H), 6,67-6,72 (АА1 часть от АА1ХХ1, 2Н), 7,48-7,52 (XX1 часть от АА1СХ1, 2Н) Пример 8 Соединения Формулы (С) 8А К холодному (0°С) раствору N-третбутоксикарбонил-Ьлейцина (1,4г, 6,3 ммоля) и ГОБТ (1,5г, 9,8 ммоля) в ДМФ (30мл) порциями добавляли ЭДКИ (2,5г, 14 ммолей) Раствор, образовавшийся после перемешивания в течение 1 часа при 0°С, обрабатывали метил-4аминобензоатом (1,09мл, 6,8 ммоля) и ДМАП (0,32г, 2,6 ммоля) После перемешивания в течение 24 часов при 25°С ДМФ удаляли под вакуумом Остаток растворяли в CH2CI2 и промывали насыщенным раствором ЫаНСОз, 1М HCI (дважды) и соляным раствором После сушки над Na2SO4 и концентрирования под вакуумом получали неочищенный продукт, который очищали с помощью быстрой хроматографиина S1O2 (20%ный этил ацетат/гексан в качестве растворителя для элюирования) В результате получали 1,0г (85%) г\І-трет-бутоксикарбонил-І_-лейцин-г\Г-(4метоксикарбонилфенил)карбоксамида в виде вспененного твердого вещества, МС (БТЯ) 363 (М-Н) 8Б Аналогичным способом получали следующие соединения формулы (С) г\І-трет-бутоксикарбонил-І_-триптофан-г\Гфенил метил карбоксамид, г\І-трет-бутоксикарбонил-І_-триптофан-г\Гфенил карбоксамид, N-трет-бутоксикарб онил-І_-триптофан-г\Г-(4метоксикарб онилфенил)карбоксамид, г\І-трет-бутоксикарбонил-І_-триптофан-г\Г-(4этоксикарбонилфенил)карбоксамид, г\І-трет-бутоксикарбонил-І_-лейцин-г\Г-(4-(М"метиламиносульфонил)фенил)карбоксамид, г\І-трет-бутоксикарбонил-І_-аланин-г\Г-(4метоксикарбонилфенил)карбоксамид, г\І-трет-бутоксикарбонил-І_-метионин-г\Г-(4метоксикарбонилфенил)карбоксамид, г\І-трет-бутоксикарбонил-І_-лейцин-г\Г-(3этоксикарбонилфенил)карбоксамид, 53 г\І-трет-бутоксикарбонил-І_-лейцин-г\Г-(2метоксикарбонилфенил)карбоксамид, г\|-трет-бутоксикарбонил-1_-лейцин-г\Г-(4-(1метилэтилоксикарбонил)фенил)карбоксамид, г\І-трет-бутоксикарбонил-І_-лейцин-г\Г(аминосульфонилфенил)карбоксамид, г\І-трет-бутоксикарбонил-І_-лейцин-г\Г-(4метоксикарбонилметилфенил)карбоксамид, г\|-трет-бутоксикарбонил-1_-пиридин-3илаланин-1\Г-(4метоксикарбонилфенил)карбоксамид, М-трет-бутоксикарбонил-1_-циклогексилглицин|\Г-(4-метоксикарбонилфенил)карбоксамид, г\|-трет-бутоксикарбонил-1_-изолейцин-г\Г-(4метоксикарбонилфенил)карбоксамид, г\|-трет-бутоксикарбонил-1_-О-бензилтреонин|\Г-(4-метоксикарбонилфенил)карбоксамид, г\|-трет-бутоксикарбонил-1_-трет-лейцин-г\Г-(4метоксикарбонилфенил)карбоксамид, г\|-трет-бутоксикарбонил-1_-лейцин-г\Г-(4цианфенил)карбоксамид, г\|-трет-бутоксикарбонил-1_-лейцин-г\Г-(4-(М"-(2диметиламиноэтил)карбамоил)фенил)карбоксамид и г\|-трет-бутоксикарбонил-1_-лейцин-г\Г-(4-(М"-(3диметиламинопропил)карбамоил)фенил)карбоксамид 8В Аналогачным способом получали следующие соединения формулы (С) |\|-трет-бутоксикарбонил-1_-триптофан-1\Г-(4нитрофенил)карбоксамид, г\|-трет-бутоксикарбонил-1_-триптофан-г\Г-(4аминофенил)карбоксамид, г\|-трет-бутоксикарбонил-1_-лейцин-г\Г-(4метилсульфонилфенил)карбоксамид, г\|-трет-бутоксикарбонил-1_-лейцин-г\Г-(4этилсульфонилфенил)карбоксамид и г\|-трет-бутоксикарбонил-1_-лейцин-г\Г-(4тетразолилфенил)карбоксамид Пример 9 Соединения Формулы (D) 9А К холодному (0°С) раствору N-третбутоксикарбонил-1_-лейцин-1\Г-фенилкарбоксамида (3,4г, 11 ммолей) в безводном CH2CI2 (10мл) добавляли ТФК (2мл) Раствор оставляли для перемешивания при 25°С в течение 6 часов и затем концентрировали под вакуумом Остаток распределяли между CH2CI2 и НгО и водный слой подщелачивали насыщенным раствором К2СО3 при 0°С Органическую фазу отделяли и водный слой трижды экстрагировали CH2CI2 Объединенные органические слои промывали соляным раствором и сушили над Na2SO4 Путем концентрирования получали І_-лейцин-І\Г-фенилкарбоксамид 9В Аналогичным способом получали следующие соединения І_-лейцин-І\Г-(4метоксикарбонилфенил)карбоксамид, І_-триптофан-г\Г-фенил метил карбоксамид, І_-триптофан-г\Г-фенил карбоксамид, І_-триптофан-г\Г-(4метоксикарбонилфенил)карбоксамид, І_-триптофан-г\Г-(4этоксикарбонилфенил)карбоксамид, 1_-лейцин-1\Г-(4-(М"метиламиносульфонил)фенил)карбоксамид, 58488 54 1_-аланин-1\Г-(4метоксикарбонилфенил)карбоксамид, 1_-метионин-1\Г-(4метоксикарбонилфенил)карбоксамид, 1_-лейцин-1\Г-(3этоксикарбонилфенил)карбоксамид, 1_-лейцин-1\Г-(2метоксикарбонилфенил)карбоксамид, 1_-лейцин-1\Г-(4-(1метилэтилоксикарбонил)фенил)карбоксамид, Ь-лейцин-Ы'(аминосульфонилфенил)карбоксамид, 1-лейцин-Ы'-(4метоксикарбонилметилфенил)карбоксамид, 1_-пиридин-3-илаланин-1\Г-(4метоксикарбонилфенил)карбоксамид, 1-спироциклопентилглицин-М'-(4метоксикарбонилфенил)карбоксамид, 1-циклогексилглицин-М'-(4метоксикарбонилфенил)карбоксамид, 1-изолейцин-М'-(4метоксикарбонилфенил)карбоксамид, 1-О-бензилтреонин-М'-(4метоксикарбонилфенил)карбоксамид, 1_-трет-лейцин-1\Г-(4метоксикарбонилфенил)карбоксамид, 1-лейцин-М'-(4-цианфенил) карбоксамид, Ьлейцин-М'-(4-(М"-(2диметиламиноэтил)карбамоил)фенил)карбоксамид и Ьлейцин-М'-(4-(М"-(3диметиламинопропил)карбамоил)фенил)карбоксамид 9В Аналогичным способом получали следующие соединения формулы (D) 1_-триптофан-г\Г-(4-нитрофенил) карбоксамид, 1_-триптофан-г\Г-(4-аминофенил) карбоксамид, 1-лейцин-Ы'-(4метилсульфонилфенил)карбоксамид, 1-лейцин-К'-(4этилсульфонилфенил)карбоксамид и 1-лейцин-Ы'-(4тетразолилфенил)карбоксамид Пример 10 Соединения формулы (1а) 10А К холодному (0°С) раствору 2(гидрокси)(хинолин-2илтиометил)фосфиноилметил-4-метилпентановой кислоты (0,20г, 0,54 ммоля) в ТГФ (6мл) добавляли 1,1'-карбонилдиимидазол (0,12г, 0,7 ммоля) Смесь перемешивали в течение 75 минут при 0°С и затем обрабатывали І_-триптофан-г\Г-(4этоксикарбонилфенил)карбоксамидом (0,22г, 0,62 ммоля) и перемешивали при 25°С в течение 15 часов ТГФ выпаривали и остаток растворяли в этилацетате (60мл) Раствор промывали Ь^О (10мл), соляным раствором (10мл) и сушили над MgSO4 Путем концентрирования с помощью ЖХВР с обращенной фазой с использованием градиента ацетонитрила и 50мМ буфера ІЧЬЦОАс получали 30мг І\І-(2-(гидрокси)(хинолин-2-илтиометил)фосфиноилметил-4-метилпентаноил)-І_триптофан-г\Г-(4-этоксикарбонилфенил)карбоксамида в виде беловатого твердого вещества, МС (БТЯ) 701 (М-Н)+ (смесь диастереоизомеров) 55 10Б Аналогичным способом получали следующие соединения формулы (1а) |\|-(2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-4-метилпентаноил)І_-триптофан-І\Г-(4метоксикарбонилфенил)карбоксамид, МС (БТЯ) 687 (М+Н)+, М-(2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-4-метилпентаноил)І_-аланин-ІЧ'-(4метоксикарбонилфенил)карбоксамид, МС (БТЯ) 572 (М+Н)+, |\|-(2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-4-метилпентаноил)І_-метионин-І\Г-(4метоксикарбонилфенил)карбоксамид, МС (БТЯ) 632 (М+Н)+, |\|-(2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-4-метилпентаноил)І_-лейцин-г\Г-(4метоксикарбонилфенил)карбоксамид, МС (БТЯ) 614(М+Н)+, |\|-(2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-4-метилпентаноил)І_-лейцин-г\Г-(31 этоксикарбонилфенил)карбоксамид, Н-ЯМР (300МГц, МеОН) 5 0,73-1,01 (т,12Н), 1,28-2,00 (т,14Н), 2,4-3,61 (т,2Н), 4,27-4,45 (т,ЗН), 7,237,44 (т,ЗН), 7,65-7,98 (т,6Н), 8,29 (s,0,5 H), 8,50 (s,0,5H), |\|-(2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-4-метилпентаноил)І_-лейцин-г\Г-(2метоксикарбонилфенил)карбоксамид, Н-ЯМР (300МГц, МеОН) 5 0,78-0,99 (т,13Н), 1,3-2,4 (т,7Н), 2,90-3,05 (т,1Н), 3,5-3,75 (т,2Н), 3,89, 3,90, 3,94 (3s,3H полн), 4,35-3,50 (т,1Н), 7,05-8,10 (т,1Н), 8,32, 8,55, 8,60 (3d,J=8,7,1H), |\|-(2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-4-метилпентаноил)1_-лейцин-г\Г-(4-(1,1диметилэтоксикарбонил)фенил)карбоксамид, МС (БТЯ) 642 (МН)+, |\|-(2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-4-метилпентаноил)І_-лейцин-г\Г-(4аминосульфонилфенил)карбоксамид, Н-ЯМР (300МГц, МеОН) 5 0,76 (d, J=6,5, ЗН), 0,81 (d, J=6,5, ЗН), 0,85-1,1 (m,7H), 1,2-2,1 (m,7H), 2,922,95 (m,1H), 3,45-3,70 (m,2H), 4,35-4,45 (m,1H), 7,28 (d, J=8,7, 1H), 7,45 (t, J=8,7, 1H), 7,68 (t,J=8,7,1H), 7,7-7,8 (m,3H), 7,87 (d, J=8,7, 1H), 7,95-8,1 (m,3H), Ы-(2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-4-метилпентаноил)1-лейцин-Ы'-(4метоксикарбонилметилфенил)карбоксамид, МС (БТЯ) 628 (МН)+ 10В Аналогичным способом получали следующие соединения формулы (la) |\|-(2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-5фенилпентаноил)-1-лейцин-М'-(4метоксикарбонилфенил)карбоксамид, |\|-(2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-4-фенилбутаноил) 56 1-лейцин-Ы'-(4метоксикарбонилфенил)карбоксамид, |\|-(2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-3фенилпропаноил)-1-лейцин-М'-(4метоксикарбонилфенил)карбоксамид, Ы-(2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-3циклогексилпропаноил)-1-лейцин-М'-(4метоксикарбонилфенил)карбоксамид, Ы-(2-((гидрокси)(хинолин-2илтиометил)фосфиноилметил)пентаноил)-1лейцин-г\Г-(4метоксикарбонилфенил)карбоксамид, Ы-(2-(гидрокси)(нафт-1илтиометил)фосфиноилметил-5фенилпентаноил)-1-лейцин-М'-(4метоксикарбонилфенил)карбоксамид, Ы-(2-(гидрокси)(нафт-1илтиометил)фосфиноилметил-4-фенилбутаноил)1-лейцин-Ы'-(4метоксикарбонилфенил)карбоксамид, |\|-(2-(гидрокси)(нафт-1илтиометил)фосфиноилметил-3фенилпропаноил)-1-лейцин-М'-(4метоксикарбонилфенил)карбоксамид, Ы-(2-(гидрокси)(нафт-1илтиометил)фосфиноилметил-3циклогексилпропаноил)-1-лейцин-М'-(4метоксикарбонилфенил)карбоксамид, Ы-(2-((гидрокси)(нафт-1илтиометил)фосфиноилметил)пентаноил)-1лейцин-г\Г-(4метоксикарбонилфенил)карбоксамид, Ы-(2-(гидрокси)(нафт-2илтиометил)фосфиноилметил-5фенилпентаноил)-1-лейцин-М'-(4метоксикарбонилфенил)карбоксамид, Ы-(2-(гидрокси)(нафт-2илтиометил)фосфиноилметил-4-фенилбутаноил)1-лейцин-Ы'-(4метоксикарбонилфенил)карбоксамид, |\|-(2-(гидрокси)(нафт-2илтиометил)фосфиноилметил-3фенилпропаноил)-1-лейцин-М'-(4метоксикарбонилфенил)карбоксамид, Ы-(2-(гидрокси)(нафт-2илтиометил)фосфиноилметил-3-циклогексилпропаноил)-1-лейцин-М'-(4метоксикарбонилфенил)карбоксамид, Ы-(2-((гидрокси)(нафт-2илтиометил)фосфиноилметил)пентаноил)-1лейцин-г\Г-(4метоксикарбонилфенил)карбоксамид, N-(2(гидрокси)(фенилилтиометил)фосфиноилметил-5фенилпентаноил)-1-лейцин-М'-(4метоксикарбонилфенил)карбоксамид, N-(2(гадрокси)(фенилилтиометил)фосфиноилметил-4фенилбутаноил)-1-лейцин-М'-(4метоксикарбонилфенил)карбоксамид, N-(2(гидрокси)(фенилилтиометил)фосфиноилметил-3фенилпропаноил)-1-лейцин-М'-(4метоксикарбонилфенил)карбоксамид, 58488 57 N-(2(гидрокси)(фенилилтиометил)фосфиноилметил-3циклогексилпропаноил)-1_-лейцин-г\Г-(4метоксикарбонилфенил)карбоксамид и N-(2((гидрокси)(фенилилтиометил)фосфиноилметил)пентано ил)-1_-лейцин-1\Г-(4метоксикарбонилфенил)карбоксамид ЮГ Раствор 1\1-(2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-4-метилпентаноил)1_-триптофан-г\Г-(4метоксикарбонилфенил)карбоксамида в ТГФ (2мл) и 1М NaOH (1мл) перемешивали в течение 24 часов при 25°С Органические растворители выпаривали и остаток растворяли в этилацетате/ЬЬО Водную фазу подкисляли с помощью 1М HCI и отделенную водную фазу дважды экстрагировали етилацетатом Объединенные органические слои промывали соляным раствором, сушили (MgSO4) и концентрировали до получения 27мг N-(2(гидрокси)(хинолин-2илтиометил)фосфиноилметил-4-метилпентаноил)І_-триптофан-г\Г-(4-карбоксифенил)карбоксамида в виде желтого порошка 10Д Аналогичным способом, но используя в качестве исходного материала N-(2(гидрокси)(хинолин-2илтиометил)фосфиноилметил-4-метилпентаноил)І_-лейцин-І\Г-(4метоксикарбонилфенил)карбоксамид (30мг, 0,048 ммоля), после растирания с этилацетатом получали 10мг І\І-(2-(гидрокси)(хинолин-2илтиометил)фосфиноилметил-4-метилпентаноил)І_-лейцин-І\Г-(4-карбоксифенил)карбоксамида в виде полутвердого продукта, 1Н-ЯМР (300МГц, МеОН), 5 0,81-1,02 (т,12Н), 1,1-2,3 (т,10Н), 2,823,00 (т,1Н), 3,49, 3,56, (2s,2H), 3,53-3,8 (т,2Н), 4,45-4,55 (т,1Н), 7,09 (d,J=8,2,1H), 7,19 (d,J=8,2,1H), 7,45 (t,J=8,2,1H), 7,45-7,6 (т,ЗН), 7,65-7,80 (т,1Н), 7,82-7,98 (т,2Н), 8,10-8,20 (т,1Н) Пример 11 Соединения формулы (Fa) 11А К 4-метилпентановой кислоте (25г, 0,215 ммоля) в водяной бане при 25°С медленно добавляли тионилхлорид (20,4мл, 1,3г) Смесь нагревали до 50°С в атмосфере аргона в течение 3 часов (пока не прекращалось выделение газа) Неочищенную реакционную смесь перегоняли при атмосферном давлении, получая 4метилпентаноилхлорид (25,Зг, 87,3%), ^ип 143°С 11Б Аналогичным способом, но заменяя 4метилпентановую кислоту на 5-фенилпентановую кислоту (5г), получали 5-фенилпентаноилхлорид (4,4г) в виде бесцветной жидкости, 1:кип 91-93°С Пример 12 Соединения Формулы (Fb) 12А К суспензии 60%-ого NaH (836мг, 1,5 экв) в толуоле (200мл) при комнатной температуре в атмосфере аргона порциями добавляли сультам 1_-(+)-2,10-камфоры (3,0г, 13,9 ммоля) Смесь интенсивно перемешивали при комнатной температуре в течение 1 часа Затем к раствору осторожно по каплям при 0°С добавляли 4метилпентаноилхлорид После перемешивания 58488 58 реакционной смеси при комнатной температуре в течение 3 часов реакцию прекращали смешением с 10мл охлажденной воды и добавляли 70мл простого эфира Реакционную смесь промывали сначала 0,5н HCI (2х50мл), далее 5%-ным К2СО3 (Зх50мл) и в завершение соляным раствором (1х50мл) Органический слой сушили над MgSO4, фильтровали и упаривали досуха Путем очистки с помощью хроматографии на колонках (смесь 1 6 этилацетат/петролейный эфир в качестве растворителя для элюирования) получали сультам N-4метилпентаноил-1_-(+)-2,10-камфоры (3,39г, 78%) 12Б Аналогичным способом, но заменяя 4метилпентаноилхлорид соответствующим хлоридом, получали следующие соединения формулы (Fb) сультам 1\1-3-фенилпропаноил-1_-(+)-2,10камфоры, МС 347 (М+), сультам 1\1-5-фенилпентаноил-1_-(+)-2,10камфоры, МС 375 М+, сультам 1\1-пентаноил-1_-(+)-2,10-камфоры, МС 300 (М+Н)+ Пример 13 Соединения формулы (Fc) 13А К раствору сультама N-4метилпентаноил-1_-(+)-2,10-камфоры (3,39г, 10,8 ммоля) в 75мл безводного ТГФ при -78°С в атмосфере аргона по каплям в течение 5 минут добавляли NaN(TMS)2 [NaN (триметилсилан)2] (1,0М в ТГФ, 11,34мл, 1,05экв ) После перемешивания при-78°С в течение 1 часа к смеси добавляли гексаметилфосфорамид (5мл), далее третбутил б ром ацетат (5,2мл, 3 экв), а затем в виде одной порции добавляли 400мг тетранбутиламмонийиодида Образовавшийся раствор выдерживали при -78°С в атмосфере аргона в течение ночи На следующее утро реакцию останавливали смешением с охлажденной водой (100мл) и затем экстрагировали простым эфиром (3x100мл) Объединенные эфирные слои промывали соляным раствором, затем сушили над Na2SO4, фильтровали и концентрировали Путем очистки с помощью хроматографии на колонках (смесь от 5 95 этилацетат/петролейный эфир до 10 90 этилацетат/петролейный эфир в качестве растворителя для элюирования) получали сультам ІЧ-(4-метил-2-третбутоксикарбонилметил)пентаноил-1_-(+)-2,10камфоры (4,0г, 86,5%) 13Б Аналогичным способом, но заменяя сультам 1\1-4-метилпентаноил-1_-(+)-2,10-камфоры соответствующим соединением формулы (Fb), получали следующие соединения формулы (Fc) сультам ІЧ-(3-фенил-2-третбутоксикарбонилметил)пропаноил-1_-(+)-2,10камфоры, МС 461 (М)+, сультам ІЧ-(5-фенил-2-третбутоксикарбонилметил)пентаноил-1_-(+)-2,10камфоры, МС 490,1 (М+Н)+, сультам ІЧ-(2-третбутоксикарбонилметил)пентаноил-1_-(+)-2,10камфоры, МС 414 (М+Н) + Пример 14 Соединения формулы (F) 14А К перемешанному раствору сультама N(4-м етил-2-трет 59 58488 бутоксикарбонилметил)пентаноил-І_-(+)-2,10камфоры (5,45г, 12,7 ммоля) в 50%-ном водном ТГФ (150мл) при 0°С в атмосфере аргона добавляли кристаллы LiOh-TbbO (2,14г, 4 экв), а затем 30%-ную Н2О2 (11,5мл) Затем ледяную баню удаляли и образовавшуюся эмульсию перемешивали в течение 3 часов, пока она не становилась прозрачной Большую часть ТГФ удаляли при пониженном давлении при 35°С Затем добавляли CH2CI2 (150мл) и при перемешивании добавляли 4н HCI до рН=2 После добавления NaCI водный слой экстрагировали CH2CI2 (3x150мл) При пониженном давлении и при 35°С удаляли CH2CI2 и затем остаток растворяли в этилацетате (150мл) Затем этот раствор экстрагировали 5%-ным К2СО3 (Зх50мл) и объединенные экстракты промывали простым эфиром (50мл) К водному слою добавляли CH2CI2 и затем при перемешивании добавляли NaCI, водный слой экстрагировали CH2CI2 (Зх70мл) и объединенные экстракты сушили над Na2SO4, фильтровали и концентрировали, получая (2Р)-4-метил-2-третбутоксикарбонилметилпентановую кислоту в виде бесцветного масла (2,95г, количественный выход) 14Б Аналогичным способом, но заменяя сультам |\|-(4-метил-2-третбутоксикарбонилметил)пентаноил-1_-(+)-2,10камфоры соответствующим соединением формулы (Fc), получали следующие соединения формулы (F) (2Р)-3-фенил-2-третбутоксикарбонил метил пропановую кислоту, МС 265 (М+Н)+, (2Р)-5-фенил-2-третбутоксикарбонил метил пентановую кислоту, МС 293,1 (М+Н)+, (2Р)-2-трет-бутоксикарбонил метил пентановую кислоту (бесцветное масло, 1,09г) 14В (2Р)-3-фенил-2-третбутоксикарбонилметилпропановую кислоту (55мг) растворяли в ледяной уксусной кислоте (20мл) и добавляли РЮг (25мг) в уксусной кислоте Затем химический стакан помещали в сосуд Парра высокого давления, откачивали воздух и подавали ЬЬ при давлении 100фунт/кв дюйм После перемешивания в течение 3 дней смесь фильтровали под вакуумом через слой целита в 1см Затем фильтрат концентрировали, получая (2Р)-3-циклогексил2-трет-бутоксикарбонил метил пропановую кислоту (56мг) в виде желтого масла, МС 269,5 (М-Н) Пример 15 Соединения Формулы (Ib) 15А К раствору 4-м етил-2-третбутоксикарбонилметилпентановой кислоты (0,28г, 1,2 ммоля) в ДМФ (5мл), содержащему ГОБТ (0,22г. 1,8 ммоля), добавляли ЭДКИ (0,31 г, 1,8 ммоля) Смесь перемешивали при 0°С в течение 1 часа и затем обрабатывали L-циклогексилглицин|\Г-(4-метоксикарбонилфенил)карбоксамидом (1,2 ммоля) и ДМАП (27мг, 0,24 ммоля) Перемешивание продолжали в течение 24 часов при 25°С и затем выпаривали ДМФ Остаток растворяли в СН2СІ2 (20мл) и раствор промывали 1М НСІ (10мл), насыщенным ЫаНСОз (10мл), соляным раствором (10мл) и сушили над ЫагЭСч После 60 концентрирования под вакуумом получали масло, которое очищали с помощью быстрой хроматографии на S1O2, используя в качестве растворителя для элюирования 20%-ный этил ацетат/гексан Таким образом получали 0,22г (22%) ІЧ-(4-метил-2трет-бутоксикарбонил метил пен-таноил)-І_циклогексилглицин-г\Г-(4метоксикарбонилфенил)карбоксамида в виде твердого продукта, МС (БТЯ) 503 (М+Н)+ 15Б Аналогичным способом получали следующие соединения |\|-(4-метил-2-третбутоксикарбонил метил пентаноил)-І_-пиридин-3илаланин-І\Г-(4метоксикарбонилфенил)карбоксамид, |\|-(4-метил-2-третбутоксикарбонил метил пентаноил)-І_-Обензилтреонин-І\Г-(4метоксикарбонилфенил)карбоксамид, |\|-(4-метил-2-третбутоксикарбонил метил пентаноил)-І_-изолейцин-г\Г(4-метоксикарбонилфенил)карбоксамид, |\|-(4-метил-2-третбутоксикарбонил метил пентаноил)-І_-лейцин-г\Г-(4метоксикарбонилфенил) карбоксамид, |\|-(4-метил-2-третбутоксикарбонил метил пентаноил)-І_-трет-лейцин|\Г-(4-метоксикарбонилфенил)карбоксамид, |\|-(4-метил-2-третбутоксикарбонил метил пентаноил)-І_-лейцин-г\Г-(4цианфенил)карбоксамид, |\|-(4-метил-2-третбутоксикарбонил метил пентаноил)-І_-лейцин-г\Г-(4(N"-(3диметиламинопропил)карбамоил)фенил)карбоксамид, |\|-(4-метил-2-третбутоксикарбонил метил пентаноил)-І_-лейцин-г\Г-(4(N"-(2диметиламиноэтил)карбамоил)фенил)карбоксамид, 1Ч-(4-метил-2-третбутоксикарбонил метил пентаноил)-1_-лейцин-г\Г-(4аминосульфонилфенил)карбоксамид, 1Ч-(4-метил-2-третбутоксикарбонил метил пентаноил)-1_-лейцин-г\Г-(4метиламиносульфонилфенил)карбоксамид, г\|-(2-трет-бутоксикарбонилметилпентаноил)-1_лейцин-1\Г-(4метоксикарбонилфенил)карбоксамид, 1Ч-(3-фенил-2-третбутоксикарбонил метил пропаноил)-1-лейцин-М'-(4метоксикарбонилфенил)карбоксамид, М-(3-циклогексил-2-третбутоксикарбонил метил пропаноил)-1_-лейцин-1\Г-(4метоксикарбонилфенил)карбоксамид, Ы-(4-фенил-2-третбутоксикарбонилметилбутаноил)-1-лейцин-М'-(4метоксикарбонилфенил)карбоксамид, и Ы-(5-фенил-2-третбутоксикарбонил метил пентаноил)-1_-лейцин-г\Г-(4метоксикарбонилфенил)карбоксамид Пример 16 Соединения формулы (1с) 16А К холодному раствору (0°С) Н-(4-метил-2трет-бутоксикарбонил-метилпентаноил)-І_
ДивитисяДодаткова інформація
Назва патенту англійськоюCarboxamides, method for their synthesis and drug formulation
Назва патенту російськоюКарбоксамиды, способ их получения и фармацевтическая композиция
МПК / Мітки
МПК: A61K 31/405, A61K 31/404, C07C 323/63, C07D 205/00, C07D 213/75, A61K 31/397, A61K 31/381, C07C 271/20, A61K 31/4406, C07C 255/60, C07C 317/40, C07C 259/00, A61K 31/165, A61K 31/27, A61P 1/02, C07C 323/59, C07C 237/22, A61P 43/00, C07D 213/80, A61P 3/08, C07F 9/60, C07C 231/00, C07D 295/13, C07C 279/14, C07D 263/22, A61K 31/403, C07D 333/76, A61K 38/00, C07C 255/57, C07D 307/91, C07K 5/023, A61K 31/4418, C07D 263/26, A61P 35/00, A61K 31/215, A61K 31/34, A61K 31/343, C07F 9/48, C07F 9/32, C07D 209/20, A61K 31/4409, A61K 31/66, A61K 31/44, A61K 31/4402, C07C 311/46, C07C 327/00, C07F 9/30, A61P 29/00, C07C 323/60, A61P 3/10, C07F 9/6558, A61K 31/38
Мітки: спосіб, фармацевтична, композиція, отримання, карбоксаміди
Код посилання
<a href="https://ua.patents.su/47-58488-karboksamidi-sposib-kh-otrimannya-i-farmacevtichna-kompoziciya.html" target="_blank" rel="follow" title="База патентів України">Карбоксаміди, спосіб їх отримання і фармацевтична композиція</a>
Попередній патент: Епоксидна полісилоксанова композиція для покриттів (варіанти), спосіб її одержання (варіанти)
Наступний патент: Імуноглобулін антирабічний кінський як інгібітор росту candida utilis
Випадковий патент: Спосіб виготовлення алмазного круга на керамічній зв'язці