Спосіб одержання амінів
Формула / Реферат
1. Спосіб одержання сполук формули І
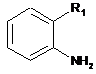 , (І)
, (І)
в якій R1 являє собою С6-С7-алкіл або групу А1
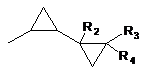 , A1
, A1
в якій R2, R3 і R4 являють собою, кожний, незалежно від інших водень або С1-С4-алкіл; в якому сполуку формули II
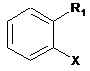 , (II)
, (II)
в якій R1 визначений як для формули І, а X являє собою бром або хлор, піддають реакції з сечовиною в присутності основи і каталітичної кількості щонайменше одної сполуки комплексу паладію, в якому сполука комплексу паладію включає щонайменше один фероценіл-біфосфіновий ліганд.
2. Спосіб за п. 1, в якому сполука комплексу паладію включає ди-трет-бутил-[1-[2-(дициклогексилфосфініл)фероценіл]етил]фосфін.
3. Спосіб за п. 1, в якому сполука комплексу паладію включає рацемічний ди-трет-бутил-[1-[2-(дициклогексилфосфініл)фероценіл]етил]фосфін.
4. Спосіб за п. 1, в якому сполуку комплексу паладію використовують в співвідношенні від 1:10000 до 1:10 відносно сполуки формули II.
5. Спосіб за п. 1, в якому реакцію проводять в інертному розчиннику.
6. Спосіб за п. 1, в якому X являє собою хлор.
Текст
1. Спосіб одержання сполук формули І R1 2 (19) 1 3 при взаємодії відповідних ортобіциклопропілзаміщених галогенбензолів в двостадійній реакції спочатку з бензофеноніміном в реакції, каталізованій паладієм, а потім при взаємодії продуктів реакції з гідрохлоридом гідроксиламіну і ацетатом натрію або з кислотами, наприклад, соляною кислотою. Однак, така методика проведення реакції непридатна для крупномасштабного виробництва орто-біциклопропілзаміщених первинних анілінів в зв'язку з необхідністю другого етапу процесу і відносно високою вартістю бензофеноніміну. Крім того, в WO 03/74491 описана методика реакції виключно для бром- або йодбензолів, а не для хлорбензолів. Було знайдено, що методика реакції, описана в WO 03/74491, погано підходить для імінування менш реакційноздатних, але більш конкурентоздатних по вартості 2-(2-хлорофеніл)біциклопропанів з високими виходами. Згідно з WO 07/25693, ортобіциклопропілзаміщені первинні аніліни можуть бути одержані при взаємодії відповідних ортобіциклопропілзаміщених галогенбензолів в двостадійній реакції спочатку з бензиламіном в реакції, каталізованій паладієм(II), а потім при гідруванні продуктів реакції, наприклад, воднем в присутності Pd/C-каталізатора. Застосування такої методики реакції до крупномасштабного виробництва пов'язане з високою вартістю через необхідність другого етапу процесу. Успішне одностадійне амінування стерично ускладнених орто-біциклопропілзаміщених галогенбензолів з використанням мідьвмісних каталізаторів описане в WO 06/61226. Але така методика реакції також не прийнятна для крупномасштабного виробництва через високу вартість заходів щодо видалення мідно-сольових відходів. Крім того, було знайдено, що методика реакції, описана в WO 06/61226, погано підходить для амінування менш реакційноздатних, але більш конкурентоздатних по вартості 2-(2-хлорфеніл)біциклопропанів з високими виходами. Мета даного винаходу полягає в тому, щоб відповідно забезпечити новий спосіб для одержання орто-біциклопропілзаміщених первинних анілінів, який дозволяє уникнути вищезазначених недоліків відомого способу і забезпечує можливість одержання цих речовин по економічно розумній ціні, легко керованим методом з високими виходами і хорошою якістю. Даний винахід відповідно стосується способу одержання речовин формули І в якій Rs являє собою С6-С7-алкіл або групу А1 96348 4 в якій R2, R3 і R4 являють собою кожний незалежно від інших водень або С1-С4-алкіл; в якому сполука формули II в якій R1 визначений як для формули І, а X являє собою бром або хлор, реагує з сечовиною в присутності основи і каталітичної кількості, щонайменше, однієї сполуки комплексу паладію, в якому сполука комплексу паладію включає, щонайменше, один фероценіл-біфосфіновий ліганд. Сполуки формули І можуть зустрічатися в різних стереоізомерних формах. Спосіб згідно з даним винаходом включає одержання вищезазначених індивідуальних стереоізомерних форм і одержання сумішей вищезазначених стереоізомерних форм в будь-якому співвідношенні. Спосіб згідно з даним винаходом придатний переважно для одержання сполук формули І, в якій R1 являє собою А1, R2 являє собою водень або С1-С4-алкіл, a R3 і R4 являють собою водень; переважно R2 являє собою водень або метил, a R3 і R4 являють собою водень. Спосіб згідно з даним винаходом є придатним, головним чином, для одержання сполук формули ІА Спосіб згідно з даним винаходом є придатним переважно для одержання сполук формули І, в якій R1 являє собою 1,3-диметилбутил або 1,3,3триметилбутил; переважно 1,3-диметилбутил. Згідно з даним винаходом в способі переважно використовуються сполуки формули II, в якій X являє собою хлор. Згідно з даним винаходом в способі переважно використовуються сполуки формули II, в якій X являє собою бром. У способі згідно з даним винаходом сполуки формули II можуть використовуватися, як правило, в концентраціях між 0,01 М і 5 М. Більш переважно, сполуки формули II використовуються в концентраціях між 0,1 М і 5 M. Ще більш переважно, сполуки формули II використовуються в концентраціях між 0,1 М і 2М. Можливість використання високих концентрацій сполук формули II є важливою перевагою способу згідно з даним винаходом, оскільки з високими концентраціями вихідної сполуки треба менше розчинника, що робить спосіб згідно з даним винаходом особливо придатним для крупномасштабного виробництва. Сполуки комплексу паладію, які використовуються в способі згідно з даним винаходом, одержують з попередника паладію і, щонайменше, одного фероценіл-біфосфінового ліганда. У способі згідно з даним винаходом сполуки комплексу паладію переважно присутні в розчинній формі як комплекси паладій-ліганд. Сполуки комплексу паладію можуть використовуватися як вже одержані сполуки комплексу паладію в способі згідно з даним винаходом або 5 утворюються in situ в способі згідно з даним винаходом. Щоб утворити сполуки комплексу паладію, попередник паладію реагує, щонайменше, з одним фероценіл-біфосфіновим лігандом. У випадку зворотної реакції може мати місце випадок, коли незначні кількості попередника паладію або ліганда не розчиняються в реакційній суміші. Придатними попередниками паладію є ацетат паладію, дихлорид паладію, розчин дихлориду паладію, паладій2(дибензиліден-ацетон)3 або паладій(дибензиліден-ацетон)2, тетракіс(трифенілфосфін)паладію, паладій на вуглеці, дихлоробіс(бензонітрил)паладію, паладій(трис-третбутилфосфін)2 або суміш паладій2(дибензиліденацетон)3 і паладій(трис-трет-бутилфосфін)2. Фероценіл-біфосфінові ліганди являють собою бідентатні третинні фосфінові ліганди, що звичайно використовуються в реакціях, каталізованих паладієм. Такі бідентатні ліганди займають два центри координації і, отже, різновиди паладію можуть утворювати хелатні сполуки. Придатні фероценіл-біфосфінові ліганди являють собою: (R)-(-)-1-[(S)-2-(дициклогексилфосфіно)фероценіл]етил-ди-трет-бутилфосфін 96348 6 (R)-(-)-1-[(S)-2-(бic(3,5-димeтил-4-мeтoкcифeнiл)фocфiнo)фepoцeнiл]eтил-ди-третбутилфосфін (R)-(-)-1-[(S)-2-(діетилфосфіно)фероценіл]етил-ди-трет-бутилфосфін (R)-(-)-1-[(S)-2-(Р-метил-Р-ізопропілфосфіно)фероценіл]етилдициклогексилфосфін 1,1'-біс(дифенілфосфіно)фероцен(dppf), 1,1'біс(ди-трет-бутилфосфіно)фероцен, (R)-(-)-1-[(S)2-(біс(4-трифторметилфеніл)фосфіно)фероценіл]етил-ди-трет-бутилфосфін, (R)-(-)-1-[(S)-2(ди(3,5-біс-трифторметилфеніл)фосфіно) фероценіл]етил-дициклогексилфосфін, (R)-(-)-1-[(S)-2(ди(3,5-бic-трифторметилфеніл)фосфіно)фероценіл]етилди(3,5-диметилфеніл)фосфін, (R)-(-)-1[(S)-2-(дициклогексилфосфіно)фероценіл]етилдициклогексилфосфін, (S)-(+)-1-[(R)-2-(дициклогексилфосфіно)фероценіл]етилдициклогексилфосфін, (S)-(+)-1-[(R)-2-(дициклогексилфосфіно)фероценіл]етилдифенілфосфін, (R)-(-)-1-[(S)-2-(біс(3,5диметил-4-метоксифеніл)фосфіно)фероценіл] етилдициклогексилфосфін, (S)-(+)-1-[(R)-2-(дифypилфocфiнo)фepoцeнiл]eтилди-3,5-кcилiлфocфiн, (R)-(-)-1-[(S)-2-(дифенілфосфіно)фероценіл]етилди-трет-бутилфосфін, (S)-(+)-1-[(R)-2-(дифенілфосфіно)фероценіл]етилди-трет-бутилфосфін, (R)-(-)-1-[(S)-2-(дифенілфосфіно)фероценіл]етилдициклогексилфосфін, (R)-(+)-1-[(R)-2(дифенілфосфіно)фероценіл]етилдициклогексилфосфін, (S)-(+)-1-[(R)-2-(дифенілфосфіно)фероценіл]етилдициклогексилфосфін, (R)-(-)-1-[(S)-2(дициклогексилфосфіно)фероценіл]етилдифенілфосфін, (R)-(-)-1-[(S)-2-(дифеніл)фосфіно)фероценіл]етилди(3,5-диметилфеніл)фосфін, (R)-(-)-1[(S)-2-(ди-трет-бутил-фосфіно)фероценіл]етил-дио-толілфосфін (R)-(-)-1-[(S)-2-(Р-метил-Р-фенілфосфіно)фероценіл]етил-ди-трет-бутилфосфін і їх рацемічні суміші, особливо рацемічні суміші 1-[2-(ди-трет-бутилфосфіно)фероценіл]етил-дио-толілфосфіну, 1-[2-(дициклогексилфосфіно)фероценіл]етилди-трет-бутилфосфіну і 1-[2(дифенілфосфіно)фероценіл]етилдициклогексилфосфіну. Згідно з даним винаходом в способі можуть використовуватися одна сполука комплексу паладію або суміш сполук комплексу паладію. Для утворення сполуки комплексу паладію перевага віддається використанню як попередника паладію ацетату паладію, паладій2(дибензиліден 7 ацетону)3, паладію(дибензиліден-ацетону)2, розчину дихлориду паладію, дихлориду паладію або суміші паладій2(дибензиліден-ацетону)3 і паладій(трис-трет-бутилфосфіну)2. Особлива перевага віддається використанню ацетату паладію або дихлориду паладію. Придатним є, коли ацетат паладію являє собою тримерний ацетат паладію. Для утворення сполуки комплексу паладію використовується, щонайменше, один ліганд. Перевага віддається використанню сполук комплексу паладію, які включають, щонайменше, один ліганд, вибраний з (R)-(-)-1-[(S)-2(дициклогексилфосфіно)фероценіл]етилди-третбутилфосфіну і рацемічного 1-[2(дициклогексилфосфіно)фероценіл]етилди-третбутилфосфіну. Перевага віддається використанню сполук комплексу паладію, які включають рацемічний 1[2-(дициклогексилфосфіно)фероценіл]етилдитрет-бутил фосфін. У способі згідно з даним винаходом сполуки комплексу паладію, попередники паладію і/або ліганди використовуються в каталітичних кількостях. Сполуки комплексу паладію використовуються переважно в співвідношенні від 1:10 до 1:10000 відносно сполук формули II, особливо в співвідношенні від 1:50 до 1:100. Попередники паладію використовуються переважно в співвідношенні від 1:10 до 1:10000 відносно сполук формули II, особливо в співвідношенні від 1:50 до 1:500. Ліганди використовуються переважно в співвідношенні від 1:10 до 1:10000 відносно сполук формули II, особливо в співвідношенні від 1:50 до 1:100. Придатними основами є, наприклад, алкоголяти, наприклад, трет-бутанолят натрію (також відомий як трет-бутилат натрію), трет-бутанолят калію (також відомий як трет-бутилат калію), метанолят натрію (також відомий як метилат натрію) або етанолят натрію (також відомий як етилат натрію), або неорганічні основи, такі як карбонати, наприклад, K2СО3, Na2CO3 або Cs2CO3, гідроксиди, наприклад, NaOH або KОН, фосфати, наприклад, K3РО4; в одному варіанті здійснення перевага віддається алкоголятам, а особлива перевага віддається трет-бутаноляту натрію. При використанні як основи NaOH або KОН може застосовуватися каталізатор міжфазного перенесення, такий як, наприклад, цетилтриметиламоній бромід або краун-ефір. Придатні кількості основи для цієї реакції складають, наприклад, від 1 до 6 еквівалентів, особливо від 1 до 2 еквівалентів. Реакція згідно з даним винаходом може бути проведена в інертному розчиннику, додатково розбавленому водою. В одному варіанті здійснення винаходу реакція згідно з даним винаходом проводиться в інертному розчиннику. Придатними розчинниками є, наприклад, сполуки формули V 96348 8 в якій R являє собою C1-C6-алкіл, переважно метил; ефірний розчинник, такий як диметоксіетан; трет-бутилметиловий ефір; терагідрофуран; діоксан; діетиловий ефір діетиленгліколю або анізол; розчинник сульфон, такий як сульфолан; амідний розчинник, такий як N-метилпіролідон або диметилацетамід; або ароматичні вуглеводневі розчинники, такі як толуол; ксилол або триметилбензоли, такі як, наприклад, мезитилен; а також суміші вищезазначених розчинників. Переважними розчинниками є ефірні розчинники і амідні розчинники. В одному варіанті здійснення розчинником є амідний розчинник, більш переважний N-метилпіролідон. В іншому варіанті здійснення розчинником є ефірний розчинник, більш переважно діетиловий ефір діетиленгліколю. В одному варіанті здійснення інертний розчинник є безводним і переважно дегазованим. Реакція згідно з даним винаходом проводиться при температурі навколишнього середовища або при підвищеній температурі, переважно в температурному інтервалі від 50 °C до 180 °C, особливо в температурному інтервалі від 50 °C до 140 °C. Реакція згідно з даним винаходом може бути виконана при атмосферному тиску, але не тільки. Тривалість реакції згідно з даним винаходом, як правило, складає від 0,5 до 48 годин, переважно від 1 до 30 годин, особливо від 1 до 18 годин. Реакція згідно з даним винаходом може бути проведена в атмосфері інертного газу. Наприклад, як інертний газ використовується азот або аргон. У реакціях згідно з даним винаходом сечовина, як правило, використовується в еквімолярних кількостях або в надлишку відносно сполук формули II, переважно до 10-кратного надлишку, особливо до 5-кратного надлишку, більш особливо від 1,3-кратного до 2-кратного надлишку. Сполуки формули II є загальновідомими і можуть бути одержані згідно з способами, описаними в WO 03/74491,WO 03/10149 і WO 07/25693. Сполуки комплексу паладію, попередники паладію і ліганди, які використовуються в способі згідно з даним винаходом, загальновідомі і, здебільшого, комерційно доступні. Даний винахід буде пояснений детальніше з використанням наступних прикладів: Приклад Р1: Одержання 2-бісциклопропіланіліну (сполука А1) 811 мг 2-(2-Хлорфеніл)біциклопропілу, 18 мг ацетату паладію (тримера), 43 мг (R)-(-)-1-[(S)-2(дициклогексилфосфіно)фероценіл]етилди-третбутилфосфіну, 365 мг сечовини, 2,4 г третбутанолята натрію в 4 мл дегазованого Nметилпіролідона перемішують в атмосфері аргону при підвищеній температурі 134 °C протягом 5 год. Вміст/чистоту 2-бісциклопропіланіліну (сполука А1) в реакційній суміші визначають газовою хроматографією. Визначають 79,9 % (площа ГХ) 2бісциклопропіланіліну; 1,3 % (площа ГХ) вихідних сполук і 6,7 % (площа ГХ) димерного побічного 9 96348 продукту і 2,9 % (площа ГХ) дегалогенованого побічного продукту. Реакцію гасять водою, розбавляють Nметилпіролідоном і екстрагують три рази з толуолом. Органічний розчинник видаляють у вакуумі. Неочищений продукт чистять за допомогою хроматографії на силікагелі (гексан:етилацетат 10/1 з доданням 1 % (по об'єму) триетиламіну). Одержують 496 мг (68 % від теоретичної кількості) 2бісциклопропіланіліну у вигляді слабо оранжевої рідини, продукт характеризують з допомогою ЯМР. Приклад Р2 Одержання 2-біс-циклопропіланіліну (сполука А1) 10 865 мг 2-(2-Хлорфеніл)біциклопропілу, 18 мг ацетату паладію (тримера), 46 мг (R)-(-)-1-[(S)-2(дициклогексилфосфіно)фероценіл]етилди-третбутилфосфіну, 363 мг сечовини, 2,4 г третбутаноляту натрію в 8 мл дегазованого діетилового ефіру діетиленгліколю перемішують в атмосфері аргону при підвищеній температурі 144 °C протягом 5 год. Вміст/чистоту 2-бісциклопропіланіліну (сполука А1) в реакційній суміші визначають газовою хроматографією. Визначають 70,7 % (площа ГХ) 2-бісциклопропіланіліну; 19 % (площа ГХ) димерного побічного продукту і 9 % (площа ГХ) дегалогенованого побічного продукту. Використовуючи вищезазначені приклади, можуть бути одержані наступні сполуки формули І: Таблиця Сполуки формули І Сполука № А1 А2 A3 А4 R1 А1 А1 1,3-диметилбутил 1,3,3-триметилбутил Виходячи з даного винаходу можна амінувати орто-біциклопропіл- або орто-С6-С7-алкілзаміщені галогенбензоли з високими виходами і з невеликими витратами. Вихідні сполуки способу даного винаходу відрізняються легкодоступністю і простотою в поводженні з ними і, крім того, вони конкурентоздатні по вартості. У переважному варіанті здійснення способу згідно з даним винаходом паладій і/або сполуки комплексу паладію, що використовується в способі, повертається в процес. Цей варіант здійснення являє собою варіант способу згідно з даним винаходом, який представляє особливий інтерес з економічної точки зору. У переважному варіанті здійснення даного винаходу використовуються сполуки формули II, в Комп’ютерна верстка Л. Ціхановська R2 Н H R3 н СН3 R4 H H якій X являє собою хлор. Вихідні сполуки цього переважного варіанту здійснення способу даного винаходу особливо відрізняються легкодоступністю і економічністю. Відомо, однак, що, в умовах крос-поєднання, каталізованого паладієм, цей клас вихідних сполук, стерично ускладнених, дезактивованих, щонайменше, субстратів ортозаміщеного хлорбензолу, є особливо важкими для амінування внаслідок надзвичайно низької реакційної здатності хлору як відхідної групи в порівнянні з субстратом бромбензолу. Оскільки цей варіант здійснення винаходу робить вищезазначені вихідні сполуки доступними для крос-поєднання, каталізованого паладієм, цей варіант здійснення відповідно являє собою варіант способу згідно з даним винаходом, який представляє особливий інтерес з економічної точки зору. Підписне Тираж 23 прим. Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of amines
Автори англійськоюFuerst, Maren, Vettiger, Thomas
Назва патенту російськоюСпособ получения аминов
Автори російськоюФюрст Марен, Феттигер Томас
МПК / Мітки
МПК: C07C 209/10, C07C 211/45
Мітки: одержання, спосіб, амінів
Код посилання
<a href="https://ua.patents.su/5-96348-sposib-oderzhannya-aminiv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання амінів</a>
Попередній патент: Оновлення зміщення потужності з використанням зворотного зв’язку
Наступний патент: Патрон невибухового руйнуючого матеріалу
Випадковий патент: Засіб для усунення наслідків травматичного видалення зубів









