Похідні піроло[2,3-d]піримідину як інгібітори янус-залежних кіназ (jak)
Номер патенту: 111804
Опубліковано: 10.06.2016
Автори: Тенбрінк Рут Е., Паріх Міхір Д., Фенвік Ешлі Едвард, Джонсон Тімоті Еллан, онзалез Андреа, Трзупек Джон Дейвід, Унвалла Рейоманд Джал, Кайла Нілу, Стробеч Джозеф Волтер, Фленаган Марк Едвард, Вазкез Майкл Л., Міттон-Фрай Марк Дж., Браун Метью Френк
Формула / Реферат
1. Сполука формули І, що має структуру:
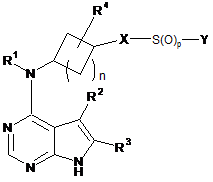 , I
, I
або її фармацевтично прийнятна сіль, в якій
R1 - гідроген або С1-С4алкіл, де зазначений алкіл є додатково необов'язково заміщеним одним або більше замісниками, вибраними з групи, яка складається з галогену, гідрокси, метокси, аміно, CF3 та С3-С6циклоалкілу;
R2 та R3 кожен незалежно є гідрогеном, дейтерієм, С1-С6алкілом з лінійним або розгалуженим ланцюгом, С3-С6циклоалкілом, С1-С6перфлуоралкілом з лінійним або розгалуженим ланцюгом, С1-С6алкокси з лінійним або розгалуженим ланцюгом, С1-С6перфлуоралкокси з лінійним або розгалуженим ланцюгом, галогеном, ціано, гідроксилом, аміно, карбокси, амінокарбонілом, арилом, гетероарилом, (арил)С1-С6алкілом з лінійним або розгалуженим ланцюгом, (гетероарил)С1-С6алкілом з лінійним або розгалуженим ланцюгом, (гетероцикліл)С1-С6алкілом з лінійним або розгалуженим ланцюгом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)арилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)гетероарилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом) гетероциклілом, (С1-С6алкоксил з лінійним або розгалуженим ланцюгом)карбонілом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)амінокарбоніламіно або (С1-С6алкіл з лінійним або розгалуженим ланцюгом)амінокарбонілом;
R4 вибирають з гідрогену, дейтерію, С1-С6алкілу з лінійним або розгалуженим ланцюгом, С1-С6перфлуоралкілу з лінійним або розгалуженим ланцюгом, арилу та алкіларилу;
X вибирають з -NH- та -CRaRb-, де (a) Ra та Rb незалежно є гідрогеном, дейтерієм, С1-С6алкілом з лінійним або розгалуженим ланцюгом, С3-С6циклоалкілом, арилом, (арил)С1-С6алкілом з лінійним або розгалуженим ланцюгом, гетероарилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)гетероарилом, (гетероарил)С1-С6алкілом з лінійним або розгалуженим ланцюгом, (гетероцикліл)С1-С6алкілом з лінійним або розгалуженим ланцюгом, або (b) Ra та Rb разом утворюють ланцюг, що містить -(CRcRd)j-, де Rc та Rd незалежно є гідрогеном, дейтерієм, С1-С6алкілом з лінійним або розгалуженим ланцюгом, арилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)арилом, гетероарилом,(С1-С6алкіл з лінійним або розгалуженим ланцюгом)гетероарилом, галогеном, CN, CF3, гідроксилом, CONH2 або SO2CH3;
Y - -A-R5, де А є зв'язком, -(СН2)k- або -(CD2)k- та R5 - С1-С6алкіл з лінійним або розгалуженим ланцюгом, С3-С6циклоалкіл, арил або -NRa'Rb', або є ненасиченою, насиченою або частково насиченою моноциклічною або біциклічною кільцевою структурою, що містить всього від п'яти до одинадцяти атомів, що має від одного до трьох гетероатомів, незалежно вибраних з групи, яка складається з оксигену, нітрогену та сульфуру, де зазначені алкіл, С3-С6циклоалкіл, арил або моноциклічна або біциклічна кільцева структура є додатково необов'язково заміщеними одним або більше замісниками, вибраними з групи, яка складається з дейтерію, галогену, С1-С6алкілу з лінійним або розгалуженим ланцюгом, CN, гідроксилу, CF3, -ORe, -NReRf, -S(O)pRe та С3-С6циклоалкілу, де зазначені алкіл та циклоалкіл можуть бути необов'язково заміщеними одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CONH2 та SO2CH3, де (a) Ra' та Rb' незалежно є гідрогеном, дейтерієм, С1-С6алкілом з лінійним або розгалуженим ланцюгом, С3-С6циклоалкілом, арилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)арилом, гетероарилом або (С1-С6алкіл з лінійним або розгалуженим ланцюгом)гетероарилом, де зазначені алкіл та циклоалкіл можуть бути необов'язково заміщеними одним або більше Rc′, або (b) Ra' та Rb' разом утворюють ланцюг, що містить -(CRc'Rd')j-, де Rc' та Rd' незалежно є гідрогеном, дейтерієм, С1-С6алкілом з лінійним або розгалуженим ланцюгом, арилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)арилом, гетероарилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)гетероарилом, галогеном, CN, гідроксилом, CF3, CONH2, -ORe, -NReRf або -S(O)pRe; де Re та Rf незалежно є гідрогеном, дейтерієм, С1-С6алкілом з лінійним або розгалуженим ланцюгом, або С3-С6циклоалкілом, де зазначені алкіл та циклоалкіл можуть бути необов'язково заміщеними одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CF3 та CONH2;
j є 2, 3, 4 або 5; k є 1, 2, 3 або 4; р є 0, 1 або 2; та
n є 1 або 2.
2. Сполука за п. 1, яка є сполукою формули ІА, що має структуру:
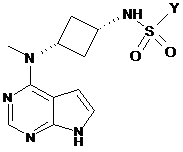 , ІА
, ІА
або її фармацевтично прийнятна сіль, в якій Y - -A-R5, де А є зв'язком, -(СН2)k- або -(CD2)k- та R5 - С1-С6алкіл з лінійним або розгалуженим ланцюгом, С3-С6циклоалкіл, арил або -NRa'Rb', або є ненасиченою, насиченою або частково насиченою моноциклічною або біциклічною кільцевою структурою, що містить всього від п'яти до одинадцяти атомів, що має від одного до трьох гетероатомів, незалежно вибраних з групи, яка складається з оксигену, нітрогену та сульфуру, де зазначені алкіл, С3-С6циклоалкіл, арил або моноциклічна або біциклічна кільцева структура є додатково необов'язково заміщеними одним або більше замісниками, вибраними з групи, яка складається з дейтерію, галогену, С1-С6алкілу з лінійним або розгалуженим ланцюгом, CN, гідроксилу, CF3, -ORe, -NReRf, -S(O)рRe та С3-С6циклоалкілу, де зазначені алкіл та циклоалкіл можуть бути необов'язково заміщеними одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CONH2 та SO2CH3, де (a) Ra' та Rb' незалежно є гідрогеном, дейтерієм, С1-С6алкілом з лінійним або розгалуженим ланцюгом, С3-С6циклоалкілом, арилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)арилом, гетероарилом або (С1-С6алкіл з лінійним або розгалуженим ланцюгом)гетероарилом, де зазначені алкіл та циклоалкіл можуть бути необов'язково заміщеними одним або більше Rc', або (b) Ra' та Rb' разом утворюють ланцюг, що містить -(CRc'Rd')j-, де Rc' та Rd' незалежно є гідрогеном, дейтерієм, С1-С6алкілом з лінійним або розгалуженим ланцюгом, арилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)арилом, гетероарилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)гетероарилом, галогеном, CN, гідроксилом, CF3, CONH2, -ORe, -NReRf або -S(O)pRe; де Rе та Rf незалежно є гідрогеном, дейтерієм, С1-С6алкілом з лінійним або розгалуженим ланцюгом, або С3-С6циклоалкілом, де зазначені алкіл та циклоалкіл можуть бути необов'язково заміщеними одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CF3 та CONH2; j є 2, 3, 4 або 5; k є 1, 2; 3 або 4; та р є 0, 1 або 2.
3. Сполука за п. 2, в якій А є зв'язком та R5 - С1-С6алкіл з лінійним або розгалуженим
ланцюгом, С3-С6циклоалкіл або арил.
4. Сполука за п. 2, в якій А є зв'язком або -(СН2)k- та R5 - С3-С6циклоалкіл, де зазначений С3-С6циклоалкіл є додатково необов'язково заміщеним одним або більше замісниками, вибраними з групи, яка складається з галогену, С1-С6алкілу з лінійним або розгалуженим ланцюгом та CN, де зазначені алкіл та циклоалкіл можуть бути необов'язково заміщеними одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CONH2, та SO2CH3; де k є 1, 2 або 3.
5. Сполука за п. 2, в якій А є зв'язком або -(СН2)k- та R5 - ненасичена, насичена або частково насичена моноциклічна або біциклічна кільцева структура, що містить всього від п'яти до одинадцяти атомів, що має від одного до трьох гетероатомів, незалежно вибраних з групи, яка складається з оксигену, нітрогену та сульфуру, де зазначені алкіл, С3-С6циклоалкіл, арил або моноциклічна або біциклічна кільцева структура є додатково необов'язково заміщеними одним або більше замісниками, вибраними з групи, яка складається з дейтерію, галогену, С1-С6алкілу з лінійним або розгалуженим ланцюгом, CN, гідроксилу, CF3, -NRa'Rb', -ORe, -S(O)pRe та С3-С6циклоалкілу; де k є 1, 2 або 3.
6. Сполука за п. 1, яка є сполукою формули IB, що має структуру:
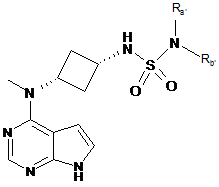 , IB
, IB
або її фармацевтично прийнятна сіль, в якій
(a) Ra' та Rb' незалежно є гідрогеном, дейтерієм, С1-С6алкілом з лінійним або розгалуженим ланцюгом, С3-С6циклоалкілом, арилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)арилом, гетероарилом, або (С1-С6алкіл з лінійним або розгалуженим ланцюгом)гетероарилом, де зазначені алкіл та циклоалкіл можуть бути необов'язково заміщеними одним або більше Rc;
(b) Ra' та Rb' разом утворюють ланцюг, що містить -(CRc'Rd')j-, де Rc' та Rd' незалежно є гідрогеном, дейтерієм, С1-С6алкілом з лінійним або розгалуженим ланцюгом, арилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)арилом, гетероарилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)гетероарилом, галогеном, CN, гідроксилом, CF3, CONH2, -ORe, -NReRf або -S(O)pRe, де Re та Rf незалежно є гідрогеном, дейтерієм, С1-С6алкілом з лінійним або розгалуженим ланцюгом, або С3-С6циклоалкілом, де зазначені алкіл та циклоалкіл можуть бути необов'язково заміщеними одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CF3 та CONH2; або
(c) Ra' та Rb' разом утворюють ненасичену, насичену або частково насичену моноциклічну або біциклічну кільцеву структуру, що містить всього від п'яти до одинадцяти атомів, що має від одного до трьох гетероатомів, незалежно вибраних з групи, яка складається з оксигену, нітрогену та сульфуру, в якому зазначена моноциклічна або біциклічна кільцева структура є додатково необов'язково заміщеною одним або більше замісниками, вибраними з групи, яка складається з дейтерію, галогену, С1-С6алкілу з лінійним або розгалуженим ланцюгом, CN, гідроксилу, CF3, -NRa' Rb', -ORe, -S(O)pRe та С3-С6циклоалкілу; j є 2, 3, 4 або 5; та р є 0, 1 або 2.
7. Сполука за п. 1, яка є сполукою формули ІС, що має структуру:
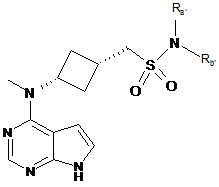 , IС
, IС
або її фармацевтично прийнятна сіль, в якій
(a) Ra' та Rb' незалежно є гідрогеном, дейтерієм, С1-С6алкілом з лінійним або розгалуженим ланцюгом, С3-С6циклоалкілом, арилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)арилом, гетероарилом або (С1-С6алкіл з лінійним або розгалуженим ланцюгом)гетероарилом, де зазначені алкіл та циклоалкіл можуть бути необов'язково заміщеними одним або більше Rc;
(b) Ra' та Rb' разом утворюють ланцюг, що містить -(CRc'Rd')j-, де Rc' та Rd' незалежно є гідрогеном, дейтерієм, С1-С6алкілом з лінійним або розгалуженим ланцюгом, арилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)арилом, гетероарилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)гетероарилом, галогеном, CN, гідроксилом, CF3, CONH2, -ORe, -NReRf або -S(O)pRe, де Re та Rf незалежно є гідрогеном, дейтерієм, С1-С6алкілом з лінійним або розгалуженим ланцюгом або С3-С6циклоалкілом, де зазначені алкіл та циклоалкіл можуть бути необов'язково заміщеними одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CF3 та CONH2; або
(c) Ra' та Rb' разом утворюють ненасичену, насичену або частково насичену моноциклічну або біциклічну кільцеву структуру, що містить всього від п'яти до одинадцяти атомів, що має від одного до трьох гетероатомів, незалежно вибраних з групи, яка складається з оксигену, нітрогену та сульфуру, де зазначена моноциклічна або біциклічна кільцева структура є додатково необов'язково заміщеною одним або більше замісниками, вибраними з групи, яка складається з дейтерію, галогену, С1-С6алкілу з лінійним або розгалуженим ланцюгом, CN, гідроксилу, CF3, -NRa'Rb', -ORe, -S(O)pRe та С3-С6циклоалкілу; j є 2, 3, 4 або 5; та р є 0, 1 або 2.
8. Сполука за п. 1, яка є сполукою формули ID, що має структуру:
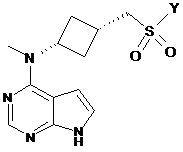 , ID
, ID
або її фармацевтично прийнятна сіль, в якій
Y - -AR5, де А є зв'язком або -(СН2)k- та R5 - С1-С6алкіл з лінійним або розгалуженим ланцюгом, С3-С6циклоалкіл, арил, або є ненасиченою, насиченою або частково насиченою моноциклічною або біциклічною кільцевою структурою, що містить всього від п'яти до одинадцяти атомів, що має від одного до трьох гетероатомів, незалежно вибраних з групи, яка складається з оксигену, нітрогену та сульфуру, де зазначені алкіл, С3-С6циклоалкіл, арил, або моноциклічна або біциклічна кільцева структура є додатково необов'язково заміщеними одним або більше замісниками, вибраними з групи, яка складається з дейтерію, галогену, С1-С6алкілу з лінійним або розгалуженим ланцюгом, CN, гідроксилу, CF3, -NRa'Rb', -ORe, -S(O)pRe та С3-С6циклоалкілу, де зазначені алкіл та циклоалкіл можуть бути необов'язково заміщеними одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CONH2 та SO2CH3, де (a) Ra' та Rb' незалежно є гідрогеном, дейтерієм, С1-С6алкілом з лінійним або розгалуженим ланцюгом, С3-С6циклоалкілом, арилом, (арил)С1-С6алкілом з лінійним або розгалуженим ланцюгом, гетероарилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)гетероарилом, (гетероарил)С1-С6алкілом з лінійним або розгалуженим ланцюгом, (гетероцикліл)С1-С6алкілом з лінійним або розгалуженим ланцюгом, де зазначені алкіл та циклоалкіл можуть бути необов'язково заміщеними одним або більше Rc', або (b) Ra' та Rb' разом утворюють ланцюг, що містить -(CRc'Rd')j-, де Rc' та Rd' незалежно є гідрогеном, дейтерієм, С1-С6алкілом з лінійним або розгалуженим ланцюгом, арилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)арилом, гетероарилом, (С1-С6алкіл з лінійним або розгалуженим ланцюгом)гетероарилом, галогеном, CN, гідроксилом, CF3, CONH2, -ORe, -NReRf або -S(O)pRe, де R в та Rf незалежно є гідрогеном, дейтерієм, С1-С6алкілом з лінійним або розгалуженим ланцюгом або С3-С6циклоалкілом, де зазначені алкіл та циклоалкіл можуть бути необов'язково заміщеними одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CF3 та CONH2; j є 2, 3, 4 або 5; k є 1, 2 або 3; та р є 0, 1 або 2.
9. Сполука за п. 1, вибрана з групи, яка складається з:
4-ціано-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}піридин-2-сульфонаміду;
2,2,2-трифлуор-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}етансульфонаміду;
2-метил-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}пропан-1-сульфонаміду;
N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}пропан-1-сульфонаміду;
1-циклопропіл-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метансульфонаміду;
N-{цис-3-[(бутилсульфоніл)метил]циклобутил}-N-метил-7Н-піроло[2,3-d]піримідин-4-аміну;
1-циклопропіл-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}азетидин-3-сульфонаміду;
3-ціано-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}азетидин-1-сульфонаміду;
(1R,5S)-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-6-окса-3-азабіцикло[3,1,1]гептан-3-сульфонаміду;
(3R)-3-ціано-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}піролідин-1-сульфонаміду;
(3S)-3-цiaнo-N-{циc-3-[мeтил(7H-пipoлo[2,3-d]пipимiдин-4-iл)aмiнo]циклoбyтил}пipoлiдин-1-сульфонаміду;
N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-1-(оксетан-3-іл)метансульфонаміду;
1-(3,3-дифлуорциклобутил)-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метансульфонаміду;
транс-3-(ціанометил)-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}циклобутансульфонаміду;
цис-3-(ціанометил)-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}циклобутансульфонаміду;
N-[цис-3-({[(3,3-дифлуорциклобутил)метил]сульфоніл}метил)циклобутил]-N-метил-7Н-піроло[2,3-d]піримідин-4-аміну;
(1S,5S)-1-ціано-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-3-азабіцикло[3.1.0]гексан-3-сульфонаміду;
(1R,5R)-1-ціано-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-3-азабіцикло[3.1.0]гексан-3-сульфонаміду;
(3R)-1-[({цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил)сульфоніл]піролідин-3-карбонітрилу;
1-[({цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил)сульфоніл]-4-(трифлуорметил)піперидин-4-олу;
N-(цис-3-{[(4,4-дифлуорпіперидин-1-іл)сульфоніл]метил}циклобутил)-N-метил-7Н-піроло[2,3-d]піримідин-4-аміну;
(3S)-1-[({цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил)сульфоніл]піролідин-3-карбонітрилу;
N-(цис-3-{[(3-хлор-4-флуорфеніл)сульфоніл]метил}циклобутил)-N-метил-7Н-піроло[2,3-d]піримідин-4-аміну;
N-(цис-3-{[(2-циклопропілетил)сульфоніл]метил}циклобутил)-N-метил-7Н-піроло[2,3-d]піримідин-4-аміну;
N-метил-N-[цис-3-({[1-(пропан-2-іл)піролідин-3-іл]сульфоніл}метил)циклобутил]-7Н-піроло[2,3-d]піримідин-4-аміну;
3,3-дифлуор-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}циклобутансульфонаміду;
1-[3-(ціанометил)оксетан-3-іл]-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метансульфонаміду;
цис-3-(ціанометил)-3-метил-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}циклобутансульфонаміду;
тpaнc-3-(цiaнoмeтил)-3-мeтил-N-{циc-3-[мeтил(7H-пipoлo[2,3-d]пipимiдин-4-iл)aмiнo]циклoбутил}циклобутансульфонаміду;
N-(2-ціаноетил)-N-метил-N’-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}сульфодіаміду;
N-{(1S,3R)-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклопентил}пропан-1-сульфонаміду;
3-(2-гідроксипропан-2-іл)-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}бензолсульфонаміду;
N-(циклопропілметил)-N’-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}сульфодіаміду;
N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-4-(1Н-піразол-3-іл)піперидин-1-сульфонаміду;
2-метил-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-2,6-дигідропіроло[3,4-с]піразол-5(4Н)-сульфонаміду;
N-циклопропіл-1-{транс-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метансульфонаміду;
2-[({цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил)сульфоніл]піридин-4-карбонітрилу;
(1S,3S)-3-[({цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил)сульфоніл]циклопентанкарбонітрилу;
(1R,3R)-3-[({цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил)сульфоніл]циклопентанкарбонітрилу;
1-циклопропіл-N-{транс-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метансульфонаміду;
3-ціано-N-{транс-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}піролідин-1-сульфонаміду;
N-метил-N-{транс-3-[(пропілсульфоніл)метил]циклобутил}-7Н-пiроло[2,3-d]пiримідин-4-аміну та
2-метил-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-1,3-тіазол-5-сульфонаміду;
або її фармацевтично прийнятна сіль.
10. Сполука за п. 1, де сполука є 2-метил-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-1,3-тіазол-5-сульфонамідом або його фармацевтично прийнятною сіллю.
11. Сполука за п. 1, де сполука є N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}пропан-1-сульфонамідом або його фармацевтично прийнятною сіллю.
12. Сполука за п. 1, де сполука є транс-3-(ціанометил)-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}циклобутансульфонамідом або його фармацевтично прийнятною сіллю.
13. Сполука за п. 1, де сполука є 1-(3,3-дифлуорциклобутил)-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метансульфонамідом або його фармацевтично прийнятною сіллю.
14. Сполука за п. 1, де сполука є N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-1-(оксетан-3-іл)метансульфонамідом або його фармацевтично прийнятною сіллю.
15. Сполука за п. 1, де сполука є (3R)-1-[({цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил)сульфоніл]піролідин-3-карбонітрилом або його фармацевтично прийнятною сіллю.
16. Сполука за п. 1, де сполука є 3,3-дифлуор- N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}циклобутансульфонамідом або його фармацевтично прийнятною сіллю.
17. Сполука за п. 1, де сполука є (1S,5S)-1-ціано-N-{цис-3-[метил(7Н-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-3-азабіцикло[3.1.0]гексан-3-сульфонамідом або його фармацевтично прийнятною сіллю.
18. Фармацевтична або ветеринарна композиція, що містить сполуку за п. 1 або її фармацевтично прийнятну сіль та фармацевтично прийнятний носій.
19. Спосіб лікування або попередження розладу або стану, вибраного з ревматоїдного артриту, міозиту, васкуліту, пухирчатки, хвороби Крона, неспецифічного виразкового коліту, хвороби Альцгеймера, червоного вовчака, нефриту, псоріазу, атопічного дерматиту, аутоімунних розладів щитоподібної залози, розсіяного склерозу, великого депресивного розладу, алергії, астми, хвороби Шегрена, синдрому сухих очей, відторгнення трансплантата органа, ксенотрансплантації, діабету типу І та ускладнення від діабету, раку, лейкемії, Т-клітинної гострої лімфобластної лейкемії, Т-клітинного лейкозу у дорослих, активованого подібним В-клітинам, дифузної В-великоклітинної лімфоми, запального захворювання кишечнику, септичного шоку, кардіопульмональної дисфункції, хронічного обструктивного захворювання легень, гострого респіраторного захворювання та кахексії, який включає стадію, за якою суб'єкту вводять ефективну кількість композиції, що містить сполуку за п. 1.
Текст
Реферат: Описаними в даному документі є похідні піроло[2,3-d]піримідину, їх застосування як інгібіторів Янус-кінази (JAK) та фармацевтичні композиції, що їх містять. UA 111804 C2 (12) UA 111804 C2 UA 111804 C2 5 10 15 20 25 30 35 40 45 Галузь винаходу Винахід стосується фармацевтично активних сполук піроло[2,3-d]піримідину та аналогів. Такі сполуки є придатними для інгібування Янус кінази (JAK). Даний винахід також стосується композицій, включаючи способи одержання таких сполук та способи лікування та попередження станів, опосередкованих JAK. Передумови створення винаходу Протеїнкінази є родинами ферментів, що каталізують фосфорилювання специфічних залишків в протеїнах, широко класифікованих в тирозинових та серин/треонінових кіназах. Невідповідна активність кінази, що виникає через мутацію, гіперекспресію або невідповідну регуляцію, дисрегуляцію чи дерегуляцію, а також надлишкове або знижене продукування факторів росту або цитокінів, тягне за собою багато захворювань, включаючи, але не обмежуючись цим, рак, серцево-судинні захворювання, алергії, астму та інші респіраторні захворювання, аутоімунні захворювання, запальні захворювання, захворювання кісток, порушення обміну речовин, та неврологічні і нейродегенеративні розлади, такі як хвороба Альцгеймера. Невідповідна активність кінази ініціює ряд біологічних клітинних відповідей, що стосуються росту клітин, диференціації клітин, виживання, апоптозу, мітогенезу, контролю клітинного циклу та рухливості клітин, причетних до вищезгаданих та пов'язаних з цим захворювань. Таким чином, протеїнкінази з'явилися як важливий клас ферментів як мішені для терапевтичної дії. Зокрема, JAK родина клітинних протеїнових тирозинкіназ (Jak1, Jak2, Jak3 і Tyk2) відіграє центральну роль в цитокіновій сигнальній функції (Kisseleva et al, Gene, 2002, 285, 1; Yamaoka et al. Genome Biology 2004, 5, 253)). При зв'язуванні з їх рецепторами цитокіни активують JAK, які далі фосфорилюють цитокіновий рецептор, таким чином створюючи ділянки стикування для молекул сигнальної функції, зокрема елементів передавача сигналу та активатора родини транскрипцій (STAT), що в кінці кінців призводить до генної експресії. Відомо, що багато цитокінів активують JAK родину. Дані цитокіни включають IFN родину (IFНальфа, IFН-бета, IFН-омега, лімітин, IFН-гама, IL-10, IL-19, IL-20, IL-22), gp130 родину (IL-6, IL11, OSM, LIF, CNTF, NNT-1/BSF-3, G-CSF, CT-1, лептин, IL-12, IL-23), родину гама-С (IL-2, IL-7, TSLP, IL-9, IL-15, IL-21, IL-4, IL-13), IL-3 родину (IL-3, IL-5, GM-CSF), одно ланцюгову родину (EPO, GH, PRL, TPO), рецептори тирозинкінази (EGF, PDGF, CSF-1, HGF) та G-протеїнові кон'юговані рецептори (AT1). Залишається потреба в нових сполуках, що ефективно та селективно інгібують специфічні JAK ферменти, та JAK1, зокрема, на противагу JAK2. JAK1 є членом Янус родини протеїнкіназ, що складається з JAK1, JAK2, JAK3 та TYK2. JAK1 експресується на різних рівнях в усіх тканинах. Багато цитокінових рецепторів сигналізують через пари JAK кіназ в наступних комбінаціях: JAK1/JAK2, JAK1/JAK3, JAK1/TYK2, JAK2/TYK2 або JAK2/JAK2. JAK1 є найбільш широко спареною JAK кіназою в даному контексті та є необхідною для активації сигнального шляху з допомогою γ-звичайних (IL-2Rγ) цитокінових рецепторів, родини IL-6 рецепторів, родин рецепторів типу I, II та III та родини IL-10 рецепторів. Дослідження на тваринах показали, що JAK1 є необхідною для розвитку, функції та гомеостазу імунної системи. Модуляція імунної активності через інгібування активності JAK1 кінази може довести корисність в лікуванні різних імунних розладів (Murray, P.J. J. Immunol., 178, 2623–2629 (2007); Kisseleva, T., et al., Gene, 285, 1–24 (2002); O'Shea, J. J., et al., Cell, 109, (suppl.) S121–S131 (2002)), в той же час уникаючи активацію сигнального шляху JAK2 залежного еритропоетину (EPO) та тромбопоетину (TPO) (Neubauer H., et al., Cell, 93(3), 397-409 (1998); Parganas E., et al., Cell, 93(3), 385-95 (1998)). Суть винаходу Представлений винахід передбачає сполуку формули I, що має структуру: R4 X R1 N S(O)p n R2 N R3 N N H I 50 1 Y UA 111804 C2 1 5 10 15 20 25 30 35 40 45 50 55 60 або її фармацевтично прийнятну сіль, де R ― гідроген або C1-C4алкіл, де зазначений алкіл є додатково необов'язково заміщеним одним або більше замісниками, вибраними з групи, яка 2 3 складається з галогену, гідрокси, метокси, аміно, CF3 та C3-C6циклоалкілу; R та R кожен незалежно є гідрогеном, дейтерієм, C1-C6алкілом з лінійним або розгалуженим ланцюгом, C3C6циклоалкілом, C1-C6перфлуоралкілом з лінійним або розгалуженим ланцюгом, C 1-C6алкокси з лінійним або розгалуженим ланцюгом, C1-C6перфлуоралкокси з лінійним або розгалуженим ланцюгом, галогеном, ціано, гідроксилом, аміно, карбокси, амінокарбонілом, арилом, гетероарилом, (арил)C1-C6алкілом з лінійним або розгалуженим ланцюгом, (гетероарил)C 1C6алкілом з лінійним або розгалуженим ланцюгом, (гетероцикліл)C1-C6алкілом з лінійним або розгалуженим ланцюгом, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)арилом, (C 1C6алкіл з лінійним або розгалуженим ланцюгом)гетероарилом, (C 1-C6алкіл з лінійним або розгалуженим ланцюгом) гетероциклілом, (C1-C6алкокси з лінійним або розгалуженим ланцюгом)карбонілом, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)амінокарбоніламіно 4 або (C1-C6алкіл з лінійним або розгалуженим ланцюгом)амінокарбонілом; R вибирають з гідрогену, дейтерію, C1-C6алкілу з лінійним або розгалуженим ланцюгом, C1-C6перфлуоралкілу з лінійним або розгалуженим ланцюгом, арилу та алкіларилу; X вибирають з –NH- та -CRaRb-, де (a) Ra та Rb незалежно є гідрогеном, дейтерієм, C1-C6алкілом з лінійним або розгалуженим ланцюгом, C3-C6циклоалкілом, арилом, (арил)C1-C6алкілом з лінійним або розгалуженим ланцюгом, гетероарилом, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)гетероарилом, (гетероарил)C1-C6алкілом з лінійним або розгалуженим ланцюгом, (гетероцикліл)C 1-C6алкілом з лінійним або розгалуженим ланцюгом, або (b) Ra та Rb разом утворюють ланцюг, що містить -(CRcRd)j-, де Rc та Rd незалежно є гідрогеном, дейтерієм, C1-C6алкілом з лінійним або розгалуженим ланцюгом, арилом, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)арилом, гетероарилом, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)гетероарилом, галогеном, 5 CN, CF3, гідроксилом, CONH2 або SO2CH3; Y ― –A-R , де A представляє собою 5 зв'язок, -(CH2)k- або -(CD2)k- та R ― C1-C6алкіл з лінійним або розгалуженим ланцюгом, C3C6циклоалкіл, арил, або --NRa'Rb", або є ненасиченою, насиченою або частково насиченою моноциклічною або біциклічною кільцевою структурою, що містить всього від п'яти до одинадцяти атомів, що має від одного до трьох гетероатомів незалежно вибраних з групи, яка складається з оксигену, нітрогену та сульфуру, де зазначений алкіл, C 3-C6циклоалкіл, арил або моноциклічна або біциклічна кільцева структура є додатково необов'язково заміщеними одним або більше замісниками, вибраними з групи, яка складається з дейтерій, галогену, C1-C6 алкіл з лінійним або розгалуженим ланцюгом, CN, гідроксил, CF 3, -ORe, -NReRf, -S(O)pRe та C3C6циклоалкіл, де зазначений алкіл та циклоалкіл може бути необов'язково заміщеним одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CONH2 та SO2CH3, де (a) Ra" та Rb" незалежно є гідрогеном, дейтерієм, C1-C6алкілом з лінійним або розгалуженим ланцюгом, C3-C6циклоалкілом, арилом, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)арилом, гетероарилом або (C1-C6алкіл з лінійним або розгалуженим ланцюгом)гетероарилом, де зазначений алкіл та циклоалкіл може бути необов'язково заміщеним одним або більше Rc", або (b) Ra" та Rb" разом утворюють ланцюг, що містить -(CRc'Rd")j-, де Rc" та Rd" незалежно є гідрогеном, дейтерієм, C1-C6алкілом з лінійним або розгалуженим ланцюгом, арилом, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)арилом, гетероарилом, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)гетероарилом, галогеном, CN, гідроксилом, CF3, CONH2, -ORe, -NReRf, або -S(O)pRe; де Re та Rf незалежно є гідрогеном, дейтерієм, C1-C6алкілом з лінійним або розгалуженим ланцюгом, або C 3-C6циклоалкілом, де зазначений алкіл та циклоалкіл може бути необов'язково заміщеним одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CF3 та CONH2; j є 2, 3, 4 або 5; k є 1, 2, 3 або 4; p є 0, 1 або 2; та, n є 1 або 2. В інших аспектах, представлений винахід також передбачає: фармацевтичні композиції, які містять фармацевтично прийнятний носій та сполуку формули I; способи лікування станів або розладів, які включають міозит, васкуліт, пухирчатку, хворобу Крона, червоний вовчак, нефрит, псоріаз, розсіяний склероз, великий депресивний розлад, алергію, астму, хворобу Шегрена, синдром сухих очей, відторгнення трансплантата, рак, запальне захворювання кишечника, септичний шок, кардіопульмональну дисфункцію, гостре респіраторне захворювання або кахексію, шляхом введення суб'єкту, що цього потребує, терапевтично ефективної кількості сполуки формули I або її фармацевтично прийнятної солі; способи лікування станів або розладів, які включають атопічний дерматит, екзему, псоріаз, склеродермію, червоний вовчак, свербіж, інші сверблячі стани, алергічні реакції, які включають алергічний дерматит у ссавців, алергічні захворювання у коней, які включають гіперчутливість 2 UA 111804 C2 5 10 15 20 25 30 35 40 45 50 55 60 до укусів, літню екзему, солодкий свербіж у коней, вибухання, запальне захворювання дихальних шляхів, рецидивуючу обструкцію дихальних шляхів, гіперчутливість дихальних шляхів, та хронічне обструктивне захворювання легень, шляхом введення ссавцю, що цього потребує, терапевтично ефективної кількості сполуки формули I, або її фармацевтично прийнятної солі; та, способи одержання сполук за винаходом. Винахід далі буде зрозуміло з наступного опису, наданого у вигляді тільки прикладу. Винахід є спрямованим на клас похідних піроло[2,3d]піримідину. Зокрема, винахід є спрямованим на піроло[2,3-d]піримідинові сполуки, прийнятні як інгібітори JAK, та, зокрема, JAK1. В той же час, представлений винахід таким чином не обмежується, розуміння різних аспектів винаходу будуть отримувати через наступні дискусії та приклади. Термін "алкіл", самостійно або в комбінації, означає ациклічну, насичену вуглеводневу групу формули CnH2n+1, яка може бути лінійною або розгалуженою. Приклади таких груп включають метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, втор-бутил, трет-бутил, пентил, ізоаміл та гексил. Якщо не зазначено інше, алкільна група містить від 1 до 6 атомів карбону. Вміст атомів карбону в алкілі та різних інших фрагментах, що містять вуглеводень, є показаним з допомогою префіксу, що позначає меншу та більшу кількість атомів карбону в фрагменті, іншими словами, префікс Ci-Cj позначає фрагмент, що містить від цілого числа "i" до цілого числа "j" атомів карбону. Таким чином, наприклад, C1-C6 алкіл стосується алкілу, що містить від одного до шести атомів карбону. Термін "гідрокси, ” як використовується в даному документі, означає OH радикал. Термін "гетероцикліл" стосується насиченого або частково насиченого (тобто неароматичного) гетеро циклу, який може бути приєднаним через кільцевий атом нітрогену (коли гетероцикл приєднується до атому карбону) або кільцевий атом карбону (в усіх випадках). Одночасно, коли заміщений, замісник може бути розташованим при кільцевому атомі нітрогену (якщо замісник є приєднаним через атом карбону) або при кільцевому атомі карбону (в усіх випадках). Конкретні приклади включають оксираніл, азиридиніл, оксетаніл, азетидиніл, тетрагідрофураніл, піролідиніл, тетрагідропіраніл, піперидиніл, 1,4-діоксаніл, морфолініл, піперазиніл, азепаніл, оксепаніл, оксазепаніл та діазепініл. Термін "арил" стосується ароматичного моноциклічного або біциклічного вуглеводню, який може бути приєднаним через кільцевий атом карбону. Одночасно, коли заміщений, замісник може бути розташованим при кільцевому атомі карбону. Конкретні приклади включають феніл, толуїл, ксиліл, триметилфеніл та нафтил. Приклади замісників арилу включають алкіл, гідроксил, галоген, нітрил, алкокси, трифлуорметил, карбоксамідо, SO 2Me, бензил та заміщений бензил. Термін "гетероарил" стосується ароматичного гетероциклу, який може бути приєднаним через кільцевий атом карбону (в усіх випадках) або кільцевий атом нітрогену з відповідною валентністю (коли гетероцикл приєднується до атому карбону). Одночасно, коли заміщений, замісник може бути розташованим при кільцевому атомі карбону (в усіх випадках) або кільцевому атомі нітрогену з відповідною валентністю (якщо замісник приєднується через атом карбону). Конкретні приклади включають тієніл, фураніл, піроліл, піразоліл, імідазоліл, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, триазоліл, оксадіазоліл, тіадіазоліл, тетразоліл, піридил, піридазиніл, піримідиніл та піразиніл. Термін "циклоалкіл" означає моноциклічну, насичену вуглеводневу групу формули C nH2n-1. Приклади включають циклопропіл, циклобутил, циклопентил, циклогексил та циклогептил. Якщо не зазначено інше, циклоалкільна група містить від 3 до 8 атомів карбону. Терміни "галоген" та "атом галогену" стосується флуориду (F), хлориду (Cl), броміду (Br) або йодиду (I). Термін "ссавець" стосується людини, сільськогосподарських тварин або домашніх тварин. Термін "домашня тварина" або "домашні тварини" стосується тварин, яких утримують як улюбленців або домашніх тварин. Приклади домашніх тварин включають собак, котів та гризунів, включаючи хом'яків, морських свинок, пісчанок, тощо, кроликів, тхорів та пташок. Термін "сільськогосподарська тварина" стосується тварин, яких вирощують або розводять в сільському господарстві для виробництва продуктів, таких як їжа або волокна, або для їх праці. В деяких варіантах здійснення, сільськогосподарські тварини є придатними для споживання ссавцями, наприклад, людьми. Приклади сільськогосподарських тварин включають велику рогату худобу, кіз, коней, свиней, овець, включаючи ягнят та кролів, також як і птицю, таку, як кури, качки та індики. Термін "лікуючий" або "лікування" означає послаблення симптомів, пов'язаних із захворюванням, розладом або станом, або припинення подальшого прогресування або 3 UA 111804 C2 5 10 15 20 25 погіршення цих симптомів. В залежності від захворювання та стану пацієнта, термін "лікування", як використовується в даному документі, може включати одне або більше зі сцілення, паліативного та профілактичного лікування. Крім того, лікування може включати введення фармацевтичного препарату за представленим винаходом в комбінації з іншими способами лікування. Термін "терапевтично ефективний" показує здатність агента попереджати або зменшувати важкість розладу, при цьому уникаючи негативних побічних ефектів, які зазвичай супроводжують альтернативні способи лікування. Фраза "терапевтично ефективний" повинна розумітися як еквівалент фрази "ефективний для лікування, попередження або покращення стану", та обидві призначені для оцінки кількості кожного агенту для застосування в комбінованій терапії, яка досягатиме мети полегшення важкості раку, серцево-судинних захворювань або болі та запалення, та зниження частоти випадків захворювань протягом лікування кожним агентом самостійно, в той же час уникаючи небажаних побічних ефектів, зазвичай пов'язаних з альтернативними способами лікування. "Фармацевтично прийнятний" означає прийнятний для застосування у ссавців, домашніх тварин або сільськогосподарських тварин. Якщо замісники є описаними як такі, що є "незалежно вибраними" з групи, то кожен замісник вибирають незалежно від іншого. Кожен замісник, таким чином, може бути ідентичним або відрізнятися від іншого(их) замісника(ів). Детальний опис винаходу Винахід стосується нових сполук, які є селективними JAK1 модуляторами корисними для лікування захворювань та станів, пов'язаних з дисрегуляцією JAK1. Винахід, крім того, передбачає фармацевтичні композиції, що містять такі JAK1 модулятори, а також способи лікування та/або попередження таких захворювань та станів. Відповідно, винахід передбачає сполуку формули I що має структуру: R4 X R1 S(O)p Y n N 2 R N R3 N N H I 1 30 35 40 45 або її фармацевтично прийнятну сіль, де R ― гідроген або C1-C4алкіл, де зазначений алкіл є додатково необов'язково заміщеним одним або більше замісниками вибраними з групи, яка 2 3 складається з галогену, гідрокси, метокси, аміно, CF3, та C3-C6циклоалкілу; R та R кожен незалежно представляє собою гідроген, дейтерій, C1-C6алкіл з лінійним або розгалуженим ланцюгом, C3-C6циклоалкіл, C1-C6перфлуоралкіл з лінійним або розгалуженим ланцюгом, C1C6алкокси з лінійним або розгалуженим ланцюгом, C1-C6перфлуоралкокси з лінійним або розгалуженим ланцюгом, галоген, ціано, гідроксил, аміно, карбокси, амінокарбоніл, арил, гетероарил, (арил)C1-C6алкіл з лінійним або розгалуженим ланцюгом, (гетероарил)C 1-C6алкіл з лінійним або розгалуженим ланцюгом, (гетероцикліл)C1-C6алкіл з лінійним або розгалуженим ланцюгом, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)арил, (C 1-C6алкіл з лінійним або розгалуженим ланцюгом)гетероарил, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)гетероцикліл, (C1-C6алкокси з лінійним або розгалуженим ланцюгом)карбоніл, (C 1C6алкіл з лінійним або розгалуженим ланцюгом)амінокарбоніламіно або (C 1-C6алкіл з лінійним 4 або розгалуженим ланцюгом)амінокарбоніл; R вибирають з гідрогену, дейтерію, C1-C6алкілу з лінійним або розгалуженим ланцюгом, C1-C6перфлуоралкілу з лінійним або розгалуженим ланцюгом, арилу та алкіларилу; X вибирають з –NH- та -–CRaRb-, де (a) Ra та Rb незалежно представляє собою гідроген, дейтерій, C 1-C6алкіл з лінійним або розгалуженим ланцюгом, C3C6циклоалкіл, арил, (арил)C1-C6алкіл з лінійним або розгалуженим ланцюгом, гетероарил, (C 1C6алкіл з лінійним або розгалуженим ланцюгом)гетероарил, (гетероарил)C 1-C6алкіл з лінійним або розгалуженим ланцюгом, (гетероцикліл)C1-C6алкіл з лінійним або розгалуженим ланцюгом, 4 UA 111804 C2 5 10 15 20 25 або (b) Ra та Rb разом утворюють ланцюг, що містить -(CRcRd)j-, де Rc та Rd незалежно представляє собою гідроген, дейтерій, C 1-C6алкіл з лінійним або розгалуженим ланцюгом, арил, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)арил, гетероарил, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)гетероарил, галогену, CN, CF 3, гідроксил, CONH2 або SO2CH3; Y 5 5 представляє собою –A-R , де A представляє собою зв'язок, -(CH2)k- або -(CD2)k- та R представляє собою C1-C6алкіл з лінійним або розгалуженим ланцюгом, C3-C6циклоалкіл, арил, або -NRa'Rb", або представляє собою ненасичену, насичену або частково насичену моноциклічну або біциклічну кільцеву структуру, що містить всього від п'яти до одинадцяти атомів, що має від одного до трьох гетероатомів, незалежно вибраних з групи, яка складається з оксигену, нітрогену та сульфуру, де зазначений алкіл, C3-C6циклоалкіл, арил або моноциклічна або біциклічна кільцева структура є додатково необов'язково заміщеною одним або більше замісниками, вибраними з групи, яка складається з дейтерію, галогену, C 1-C6алкілу з лінійним або розгалуженим ланцюгом, CN, гідроксилу, CF3, -ORe, -NReRf, -S(O)pRe та C3-C6циклоалкілу, де зазначений алкіл та циклоалкіл може бути необов'язково заміщеним одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CONH 2 та SO2CH3, де (a) Ra" та Rb" незалежно представляє собою гідроген, дейтерій, C1-C6алкіл з лінійним або розгалуженим ланцюгом, C3-C6циклоалкіл, арил, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)арил, гетероарил або (C1-C6алкіл з лінійним або розгалуженим ланцюгом)гетероарил, де зазначений алкіл та циклоалкіл може бути необов'язково заміщеним одним або більше R c", або (b) Ra" та Rb" разом утворюють ланцюг, що містить -(CRc'Rd")j-, де Rc" та Rd" незалежно представляє собою гідроген, дейтерій, C 1-C6алкіл з лінійним або розгалуженим ланцюгом, арил, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)арил, гетероарил, (C 1-C6алкіл з лінійним або розгалуженим ланцюгом)гетероарил, галоген, CN, гідроксил, CF3, CONH2, -ORe, -NReRf або -S(O)pRe; де Re та Rf незалежно представляє собою гідроген, дейтерій, C 1-C6алкіл з лінійним або розгалуженим ланцюгом, або C3-C6циклоалкіл, де зазначений алкіл та циклоалкіл може бути необов'язково заміщеним одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CF 3 та CONH2; j є 2, 3, 4 або 5; k є 1, 2, 3 або 4; p є 0, 1 або 2; та, n є 1 або 2. В одному варіанті здійснення, винахід передбачає сполуку формули IA, що має структуру: 30 NH Y S O O N N N NH IA 5 35 40 45 або її фармацевтично прийнятну сіль, де Y ― –A-R , де A представляє собою 5 зв'язок, -(CH2)k- або -(CD2)k- та R ― C1-C6алкіл з лінійним або розгалуженим ланцюгом, C3C6циклоалкіл, арил або -NRa'Rb", або представляє собою ненасичену, насичену або частково насичену моноциклічну або біциклічну кільцеву структуру, що містить всього від п'яти до одинадцяти атомів, що має від одного до трьох гетероатомів, незалежно вибраних з групи, яка складається з оксигену, нітрогену та сульфуру, де зазначений алкіл, C 3-C6циклоалкіл, арил або моноциклічна або біциклічна кільцева структура є додатково необов'язково заміщеною одним або більше замісниками, вибраними з групи, яка складається з дейтерію, галогену, C 1-C6алкілу з лінійним або розгалуженим ланцюгом, CN, гідроксилу, CF 3, -ORe, -NReRf, -S(O)pRe та C3C6циклоалкілу, де зазначений алкіл та циклоалкіл може бути необов'язково заміщеним одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CONH2 та SO2CH3, де (a) Ra" та Rb" незалежно представляє собою гідроген, дейтерій, C 1-C6алкіл з лінійним або розгалуженим ланцюгом, C3-C6циклоалкіл, арил, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)арил, гетероарил або (C 1-C6алкіл з лінійним або розгалуженим ланцюгом)гетероарил, де зазначений алкіл та циклоалкіл може бути необов'язково заміщеним одним або більше Rc", або (b) Ra" та Rb" разом утворюють ланцюг, що містить -(CRc'Rd")j-, де Rc" та Rd" незалежно представляє собою гідроген, дейтерій, C1-C6алкіл з лінійним або розгалуженим 5 UA 111804 C2 5 10 15 20 25 ланцюгом, арил, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)арил, гетероарил, (C 1C6алкіл з лінійним або розгалуженим ланцюгом)гетероарил, галоген, CN, гідроксил, CF 3, CONH2, -ORe, -NReRf або -S(O)pRe; де Re та Rf незалежно представляє собою гідроген, дейтерій, C1-C6алкіл з лінійним або розгалуженим ланцюгом або C3-C6циклоалкіл, де зазначений алкіл та циклоалкіл може бути необов'язково заміщеним одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CF3 та CONH2; j є 2, 3, 4 або 5; k є 1, 2, 3 або 4; та p є 0, 1 або 2. В одному варіанті здійснення, винахід передбачає сполуку формули IA, де A представляє 5 собою зв'язок та R представляє собою C1-C6алкіл з лінійним або розгалуженим ланцюгом, C3C6циклоалкіл або арил. В іншому варіанті здійснення, винахід передбачає сполуку формули IA, 5 де A представляє собою зв'язок або -(CH2)k-, та R представляє собою C3-C6циклоалкіл, де зазначений C3-C6циклоалкіл є додатково необов'язково заміщеним одним або більше замісниками, вибраними з групи, яка складається з галогену, C 1-C6алкілу з лінійним або розгалуженим ланцюгом та CN, де зазначений алкіл та циклоалкіл може бути необов'язково заміщеним одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CONH2 та SO2CH3; де k є 1, 2 або 3. В ще іншому варіанті здійснення, винахід 5 передбачає сполуку формули IA, де A представляє собою зв'язок або -(CH2)k-, та R представляє собою ненасичену, насичену або частково насичену моноциклічну або біциклічну кільцеву структуру, що містить всього від п'яти до одинадцяти атомів, що має від одного до трьох гетероатомів, незалежно вибраних з групи, яка складається з оксигену, нітрогену та сульфуру, де зазначений алкіл, C3-C6циклоалкіл, арил або моноциклічна або біциклічна кільцева структура є додатково необов'язково заміщеною одним або більше замісниками, вибраними з групи, яка складається з дейтерію, галогену, C 1-C6алкілу з лінійним або розгалуженим ланцюгом, CN, гідроксилу, CF3, -NRa'Rb", -ORe, -S(O)pRe та C3-C6циклоалкілу; де k є 1, 2 або 3. В іншому варіанті здійснення, винахід передбачає сполуку формули IB, що має структуру: Ra' H N N Rb' S O O N N IB N 30 35 40 45 N H або її фармацевтично прийнятну сіль, де (a) Ra" та Rb" незалежно представляє собою гідроген, дейтерій, C1-C6алкіл з лінійним або розгалуженим ланцюгом, C3-C6циклоалкіл, арил, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)арил, гетероари, або (C 1-C6алкіл з лінійним або розгалуженим ланцюгом)гетероарил, де зазначений алкіл та циклоалкіл може бути необов'язково заміщеним одним або більше Rc, або (b) Ra" та Rb" разом утворюють ланцюг, що містить -(CRc'Rd")j-, де Rc" та Rd" незалежно представляє собою гідроген, дейтерій, C1-C6алкіл з лінійним або розгалуженим ланцюгом, арил, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)арил, гетероарил, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)гетероарил, галоген, CN, гідроксил, CF3, CONH2, -ORe, -NReRf або -S(O)pRe; де Re та Rf незалежно представляє собою гідроген, дейтерій, C1-C6алкіл з лінійним або розгалуженим ланцюгом або C3-C6циклоалкіл, де зазначений алкіл та циклоалкіл може бути необов'язково заміщеним одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CF 3 та CONH2; або, (c) Ra" та Rb" разом утворюють ненасичену, насичену або частково насичену моноциклічну або біциклічну кільцеву структуру, що містить всього від п'яти до одинадцяти атомів, що має від одного до трьох гетероатомів, незалежно вибраних з групи, яка складається з оксигену, нітрогену та сульфуру, де зазначена моноциклічна або біциклічна кільцева структура є додатково необов'язково заміщеною одним або більше замісниками, вибраними з групи, яка складається з дейтерію, галогену, C1-C6алкілу з лінійним або розгалуженим ланцюгом, CN, 6 UA 111804 C2 гідроксилу, CF3, -NRa'Rb", -ORe, -S(O)pRe та C3-C6 циклоалкілу; j є 2, 3, 4 або 5; та p є 0, 1 або 2. В іншому варіанті здійснення, винахід передбачає сполуку формули IC, що має структуру: Ra' N Rb' S O O N N N H N IC 5 10 15 20 25 або її фармацевтично прийнятну сіль, де (a) Ra" та Rb" незалежно представляє собою гідроген, дейтерій, C1-C6алкіл з лінійним або розгалуженим ланцюгом, C3-C6циклоалкіл, арил, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)арил, гетероарил або (C 1-C6алкіл з лінійним або розгалуженим ланцюгом)гетероарил, де зазначений алкіл та циклоалкіл може бути необов'язково заміщеним одним або більше Rc, або (b) Ra" та Rb" разом утворюють ланцюг, що містить -(CRc'Rd")j-, де Rc" та Rd" незалежно представляє собою гідроген, дейтерій, C1-C6алкіл з лінійним або розгалуженим ланцюгом, арил, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)арил, гетероарил, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)гетероарил, галоген, CN, гідроксил, CF3, CONH2, -ORe, -NReRf або -S(O)pRe; де Re та Rf незалежно представляє собою гідроген, дейтерій, C1-C6алкіл з лінійним або розгалуженим ланцюгом або C3-C6циклоалкіл, де зазначений алкіл та циклоалкіл може бути необов'язково заміщеним одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CF 3 та CONH2; або, (c) Ra" та Rb" разом утворюють ненасичену, насичену або частково насичену моноциклічну або біциклічну кільцеву структуру, що містить всього від п'яти до одинадцяти атомів, що має від одного до трьох гетероатомів, незалежно вибраних з групи, яка складається з оксигену, нітрогену та сульфуру, де зазначена моноциклічна або біциклічна кільцева структура є додатково необов'язково заміщеною одним або більше замісниками, вибраними з групи, яка складається з дейтерію, галогену, C1-C6алкілу з лінійним або розгалуженим ланцюгом, CN, гідроксилу, CF3, -NRa'Rb", -ORe, -S(O)pRe та C3-C6циклоалкілу; j є 2, 3, 4 або 5; та p є 0, 1 або 2. В іншому варіанті здійснення, винахід передбачає сполуку формули ID, що має структуру: Y S O O N N N NH ID 5 30 або її фармацевтично прийнятну сіль, де Y ― –AR , де A представляє собою зв'язок 5 або -(CH2)k-, та R ― C1-C6алкіл з лінійним або розгалуженим ланцюгом, C3-C6циклоалкіл, арил, або представляє собою ненасичену, насичену або частково насичену моноциклічну або біциклічну кільцеву структуру, що містить всього від п'яти до одинадцяти атомів, що має від одного до трьох гетероатомів, незалежно вибраних з групи, яка складається з оксигену, нітрогену та сульфуру, де зазначений алкіл, C3-C6циклоалкіл, арил або моноциклічна або 7 UA 111804 C2 5 10 15 20 25 30 35 40 45 50 55 60 біциклічна кільцева структура є додатково необов'язково заміщеною одним або більше замісниками, вибраними з групи, яка складається з дейтерію, галогену, C 1-C6алкілу з лінійним або розгалуженим ланцюгом, CN, гідроксилу, CF3, -NRa'Rb", -ORe, -S(O)pRe та C3-C6циклоалкілу, де зазначений алкіл та циклоалкіл може бути необов'язково заміщеним одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CONH 2 та SO2CH3, де (a) Ra" та Rb" незалежно представляє собою гідроген, дейтерій, C1-C6алкіл з лінійним або розгалуженим ланцюгом, C3-C6циклоалкіл, арил, (арил)C1-C6алкіл з лінійним або розгалуженим ланцюгом, гетероарил, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)гетероарил, (гетероарил)C1-C6алкіл з лінійним або розгалуженим ланцюгом, (гетероцикліл)C 1-C6алкіл з лінійним або розгалуженим ланцюгом, де зазначений алкіл та циклоалкіл може бути необов'язково заміщеним одним або більше Rc", або (b) Ra" та Rb" разом утворюють ланцюг, що містить -(CRc'Rd")j-, де Rc" та Rd" незалежно представляє собою гідроген, дейтерій, C1-C6алкіл з лінійним або розгалуженим ланцюгом, арил, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)арил, гетероарил, (C1-C6алкіл з лінійним або розгалуженим ланцюгом)гетероарил, галоген, CN, гідроксил, CF3, CONH2, -ORe, -NReRf або -S(O)pRe; де Re та Rf незалежно представляє собою гідроген, дейтерій, C1-C6алкіл з лінійним або розгалуженим ланцюгом або C3-C6циклоалкіл, де зазначений алкіл та циклоалкіл може бути необов'язково заміщеним одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CF 3 та CONH2; j є 2, 3, 4 або 5; k є 1, 2 або 3; та p є 0, 1 або 2. В одному варіанті здійснення, винахід 5 передбачає сполуку формули ID, де R представляє собою C1-C6алкіл з лінійним або розгалуженим ланцюгом або C3-C6 циклоалкіл. В іншому варіанті здійснення, винахід передбачає сполуку формули ID, де A є зв'язком 5 або -(CH2)k-, та R ― ненасичену, насичену або частково насичену моноциклічну або біциклічну кільцеву структуру, що містить всього від п'яти до одинадцяти атомів, що має від одного до трьох гетероатомів, незалежно вибраних з групи, яка складається з оксигену, нітрогену та сульфуру, де зазначений алкіл, C3-C6циклоалкіл, арил або моноциклічна або біциклічна кільцева структура є додатково необов'язково заміщеною одним або більше замісниками, вибраними з групи, яка складається з дейтерію, галогену, C 1-C6алкілу з лінійним або розгалуженим ланцюгом, CN, гідроксилу, CF3, -NRa'Rb", -ORe, -S(O)pRe та C3-C6циклоалкілу; де Re та Rf незалежно представляє собою гідроген, дейтерій, C 1-C6алкіл з лінійним або розгалуженим ланцюгом або C3-C6циклоалкіл, де зазначений алкіл та циклоалкіл може бути необов'язково заміщеним одним або більше замісниками, вибраними з групи, яка складається з галогену, CN, гідроксилу, CF3 та CONH2; k є 1, 2 або 3; та, p є 0, 1 або 2. В іншому варіанті здійснення, винахід 5 передбачає сполуку формули I, де R представляє собою ненасичену кільцеву структуру, що містить всього від п'яти до одинадцяти атомів, що має один або два гетероатомів, незалежно вибраних з групи, яка складається з оксигену, нітрогену та сульфуру. В інших варіантах 5 здійснення, винахід передбачає сполуку формули I, де R представляє собою фурил, тіофурил, піроліл, піразоліл, оксазоліл, азетидиніл, піперидиніл або тіазоліл, необов'язково заміщений одним або двома метилами. В іншому варіанті здійснення, винахід передбачає сполуку, вибрану з групи, яка складається з: 4-ціано-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}піридин-2сульфонаміду; 2,2,2-трифлуор-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}етан сульфонаміду; 2-метил-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}пропан-1сульфонаміду; N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}пропан-1-сульфонаміду; 1-циклопропіл-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метан сульфонаміду; N-{цис-3-[(бутилсульфоніл)метил]циклобутил}-N-метил-7H-піроло[2,3-d]піримідин-4-аміну; 1-циклопропіл-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}азетидин-3сульфонаміду; 3-ціано-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}азетидин-1сульфонаміду; (1R, 5S)-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-6-окса-3азабіцикло[3.1.1]гептан-3-сульфонаміду; (3R)-3-ціано-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}піролідин-1сульфонаміду; (3S)-3-ціано-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}піролідин-1 8 UA 111804 C2 5 10 15 20 25 30 35 40 45 50 55 60 сульфонаміду; N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-1-(оксетан-3-іл)метансульфонаміду; 1-(3,3-дифлуорциклобутил)-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]цикло бутил}метансульфонаміду; транс-3-(ціанометил)-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил} циклобутансульфонаміду; цис-3-(ціанометил)-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил} циклобутансульфонаміду; N-[цис-3-({[(3,3-дифлуорциклобутил)метил]сульфоніл}метил)циклобутил]-N-метил-7Hпіроло[2,3-d]піримідин-4-аміну; (1S, 5S)-1-ціано-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-3азабіцикло[3.1.0]гексан-3-сульфонаміду; (1R, 5R)-1-ціано-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-3азабіцикло[3.1.0]гексан-3-сульфонаміду; (3R)-1-[({цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил)сульфоніл] піролідин-3-карбонітрилу; 1-[({цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил)сульфоніл]-4(трифлуорметил)піперидин-4-олу; N-(цис-3-{[(4,4-дифлуорпіперидин-1-іл)сульфоніл]метил}циклобутил)-N-метил-7H-піроло [2,3-d]піримідин-4-аміну; (3S)-1-[({цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил)сульфоніл] піролідин-3-карбонітрилу; N-(цис-3-{[(3-хлор-4-флуорфеніл)сульфоніл]метил}циклобутил)-N-метил-7H-піроло[2,3d]піримідин-4-аміну; N-(цис-3-{[(2-циклопропілетил)сульфоніл]метил}циклобутил)-N-метил-7H-піроло[2,3-d] піримідин-4-аміну; N-метил-N-[цис-3-({[1-(пропан-2-іл)піролідин-3-іл]сульфоніл}метил)циклобутил]-7H-піроло [2,3-d]піримідин-4-аміну; 3,3-дифлуор-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}циклобутан сульфонаміду; 1-[3-(ціанометил)оксетан-3-іл]-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]цикло бутил}метансульфонаміду; цис-3-(ціанометил)-3-метил-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]цикло бутил}циклобутансульфонаміду; транс-3-(ціанометил)-3-метил-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]цикло бутил}циклобутансульфонаміду; N-(2-ціаноетил)-N-метил-N'-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]цикло бутил}сульфодіаміду; N-{(1S, 3R)-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклопентил}пропан-1сульфонаміду; 3-(2-гідроксипропан-2-іл)-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил} бензолсульфонаміду; N-(циклопропілметил)-N'-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил} сульфодіаміду; N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-4-(1H-піразол-3-іл) піперидин-1-сульфонаміду; 2-метил-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-2,6-дигідро піроло[3,4-c]піразол-5(4H)-сульфонаміду; 2-[({цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил)сульфоніл] піридин4-карбонітрилу; (1S, 3S)-3-[({цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил) сульфоніл]циклопентанкарбонітрилу; (1R, 3R)-3-[({цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил) сульфоніл]циклопентанкарбонітрилу; 1-циклопропіл-N-{транс-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил} метансульфонаміду; 3-ціано-N-{транс-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}піролідин-1сульфонаміду; N-метил-N-{транс-3-[(пропілсульфоніл)метил]циклобутил}-7H-піроло[2,3-d]піримідин-4-аміну; 9 UA 111804 C2 та, 5 10 15 20 25 30 35 40 45 50 55 60 2-метил-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-1,3-тіазол-5сульфонаміду; або, її фармацевтично прийнятну сіль. В іншому варіанті здійснення, винахід передбачає сполуку, вибрану з групи, яка складається з: 1-(3,3-дифлуорциклобутил)-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]цикло бутил}метансульфонаміду; транс-3-(ціанометил)-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил} циклобутансульфонаміду; N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}пропан-1-сульфонаміду; 3,3-дифлуор-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}цикло бутансульфонаміду; та, N-{(1S, 3R)-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклопентил}пропан-1сульфонаміду; або її фармацевтично прийнятну сіль. В інших варіантах здійснення, винахід передбачає сполуку вибраними з групи, яка складається з: (3R)-3-ціано-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}піролідин-1сульфонаміду; (1R, 5S)-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-6-окса-3азабіцикло[3.1.1]гептан-3-сульфонаміду; (1S, 5S)-1-ціано-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-3азабіцикло[3.1.0]гексан-3-сульфонаміду; N-(2-ціаноетил)-N-метил-N'-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]цикло бутил}сульфодіаміду; та, 2-метил-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-2,6-дигідро піроло[3,4-c]піразол-5(4H)-сульфонаміду; або її фармацевтично прийнятну сіль. В іншому варіанті здійснення, винахід передбачає сполуку, вибрану з групи, яка складається з: (3R)-1-[({цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил) сульфоніл]піролідин-3-карбонітрилу; 1-[({цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил)сульфоніл]-4(трифлуорметил)піперидин-4-олу; N-(цис-3-{[(4,4-дифлуорпіперидин-1-іл)сульфоніл]метил}циклобутил)-N-метил-7H-піроло [2,3-d]піримідин-4-аміну; (3S)-1-[({цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил)сульфоніл] піролідин-3-карбонітрилу; та/або її фармацевтично прийнятну сіль. В ще іншому варіанті здійснення, винахід передбачає сполуку вибраними з групи, яка складається з: (1R, 3R)-3-[({цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил) сульфоніл]циклопентанкарбонітрилу; (1S, 3S)-3-[({цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил) сульфоніл]циклопентанкарбонітрилу; 2-[({цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метил) сульфоніл]піридин4-карбонітрилу; N-[цис-3-({[(3,3-дифлуорциклобутил)метил]сульфоніл}метил)циклобутил]-N-метил-7Hпіроло[2,3-d]піримідин-4-аміну; та N-{цис-3-[(бутилсульфоніл)метил]циклобутил}-N-метил-7H-піроло[2,3-d]піримідин-4-аміну; або її фармацевтично прийнятну сіль. Особливо переважні варіанти здійснення включають 2-метил-N-{цис-3-[метил(7H-піроло[2,3d]піримідин-4-іл)аміно]циклобутил}-1,3-тіазол-5-сульфонамід, N-{цис-3-[метил (7H-піроло[2,3d]піримідин-4-іл)аміно]циклобутил}пропан-1-сульфонамід; N-{цис-3-[метил (7H-піроло[2,3d]піримідин-4-іл)аміно]циклобутил}-1-оксетан-3-ілметансульфонамід; 1-(3,3дифлуорциклобутил)-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил} метансульфонамід; 3,3-дифлуор-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно] циклобутил}циклобутансульфонамід; транс-3-(ціанометил)-N-{цис-3-[метил(7H-піроло[2,3d]піримідин-4-іл)аміно]циклобутил}циклобутансульфонамід; (1S, 5S)-1-ціано-N-{цис-3[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-3-азабіцикло[3.1.0]гексан-3сульфонамід; та, (3S)-1-[({цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил} метил)сульфоніл]піролідин-3-карбонітрил; або його фармацевтично прийнятну сіль. 10 UA 111804 C2 5 10 15 20 25 30 35 40 45 50 55 60 Винахід також передбачає фармацевтичну або ветеринарну композицію, що містить сполуку формули I, IA, IB, IC або ID, або її фармацевтично прийнятну сіль, та фармацевтично прийнятний носій. Винахід також передбачає спосіб лікування розладу або стану пов'язаного з дисрегуляцією JAK, та, зокрема, JAK1, у суб'єкта, що включає введення суб'єкту терапевтично ефективної кількості сполуки, що має структуру формули I, IA, IB, IC або ID, або її фармацевтично прийнятної солі. В певних варіантах здійснення, розлад або стан, який лікують за даним способом, вибирають з серед ревматоїдного артриту, міозиту, васкуліту, пухирчатки, хвороби Крона, неспецифічного виразкового коліту, хвороби Альцгеймера, червоного вовчаку, нефриту, псоріазу, атопічного дерматиту, аутоімунних розладів щитоподібної залози, розсіяного склерозу, великого депресивного розладу, алергії, астми, хвороби Шегрена, синдрому сухих очей, відторгнення трансплантата органу, ксенотрансплантації, діабету типу І та ускладнень від діабету, раку, лейкемії, Т-клітинної гострої лімфобластної лейкемії, Т-клітинного лейкозу у дорослих, активованого подібним В-клітинам, дифузної В-великоклітинної лімфоми, запального захворювання кишечника, септичного шоку, кардіопульмональної дисфункції, хронічного обструктивного захворювання легень, гострого респіраторного захворювання та кахексії, який включає стадію введення суб'єкту ефективної кількості композиції, що містить сполуку формули I, IA, IB, IC або ID. В певних варіантах здійснення, терапевтично ефективна кількість, яку застосовують відповідно до способу, становить від 0,01 мг/кг маси тіла/день до 100 мг/кг маси тіла/день. В деяких інших варіантах здійснення, терапевтично ефективна кількість, яку застосовують відповідно до способу, представляє собою терапевтично ефективну кількість, яка становить від 0,1 мг/кг маси тіла/день до 10 мг/кг маси тіла/день. На практиці способу, сполука формули I переважно вибирають з N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4іл)аміно]циклобутил}пропан-1-сульфонаміду, N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4іл)аміно]циклобутил}-1-оксетан-3-ілметансульфонаміду; 1-(3,3-дифлуор циклобутил)-N-{цис-3[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}метан сульфонаміду; 3,3-дифлуор-N{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]цикло бутил}циклобутансульфонаміду; транс-3-(ціанометил)-N-{цис-3-[метил(7H-піроло[2,3-d] піримідин-4іл)аміно]циклобутил}циклобутансульфона-міду; (1S, 5S)-1-ціано-N-{цис-3-[метил(7H-піроло[2,3d]піримідин-4-іл)аміно]циклобутил}-3-азабіцикло[3.1.0]гексан-3-сульфонаміду; та, (3S)-1-[({цис-3[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил} метил)сульфоніл]піролідин-3карбонітрилу; або їх фармацевтично прийнятної солі. Винахід, крім того, передбачає спосіб лікування або попередження розладу або стану, вибраного з атопічного дерматиту, екземи, склеродермії, свербіжу, інших сверблячих станів, алергічниї реакцій, що включають алергічний дерматит у ссавців, алергічні захворювання у коней, що включають гіперчутливість до укусів, літню екзему, солодкого свербіжу у коней, вибухання, запального захворювання дихальних шляхів, рецидивуючої обструкції дихальних шляхів та гіперчутливості дихальних шляхів шляхом введення ссавцю, що цього потребує, терапевтично ефективної кількості сполуки формули I, IA, IB, IC або ID, або її фармацевтично прийнятної солі. В певних варіантах здійснення, терапевтично ефективна кількість, яку застосовують відповідно до способу, становить від 0,01 мг/кг маси тіла/день до 100 мг/кг маси тіла/день. В деяких інших варіантах здійснення, терапевтично ефективна кількість, яку застосовують відповідно до способу, представляє собою терапевтично ефективну кількість, яка становить від 0,1 мг/кг маси тіла/день до 10 мг/кг маси тіла/день. Відповідно до способу, ссавець, якого лікують сполукою за винаходом, вибирають з домашніх тварин, собак та сільськогосподарської тварини. В певних варіантах здійснення, сполуку формули I, IA, IB, IC або ID, або її фармацевтично прийнятну сіль, можуть вводити відповідно до способу перорально, парентерально або місцево. На практиці способу, сполуку формули I переважно вибирають з N-{цис-3-[метил(7Hпіроло[2,3-d]піримідин-4-іл)аміно]циклобутил}пропан-1-сульфонаміду; N-{цис-3-[метил(7Hпіроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-1-оксетан-3-ілметансульфонаміду; 1-(3,3дифлуорциклобутил)-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил} метансульфонаміду; 3,3-дифлуор-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно] циклобутил}циклобутансульфонаміду; транс-3-(ціанометил)-N-{цис-3-[метил(7H-піроло[2,3d]піримідин-4-іл)аміно]циклобутил}циклобутансульфонаміду; (1S, 5S)-1-ціано-N-{цис-3[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-3-азабіцикло[3.1.0]гексан-3сульфонаміду; та, (3S)-1-[({цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил} метил)сульфоніл]піролідин-3-карбонітрилу; або, її фармацевтично прийнятної солі. Сполуки, що мають однакову молекулярну формулу, але відрізняються за природою або 11 UA 111804 C2 5 10 15 20 25 30 35 40 45 50 55 60 послідовністю зв'язування їх атомів або розташуванням їх атомів в просторі називають "ізомерами". Ізомери, що відрізняються розташуванням їх атомів в просторі називають "стереоізомерами". Кваліфікованим фахівцям в даній галузі буде зрозуміло, що сполука формули I, IA, IB, IC або ID може існувати у вигляді цис- та транс- ахіральних діастереомерів. Включеними в межі обсягу описаних сполук є всі ізомери (наприклад, цис-, транс- або діастереомери) сполук, описаних в даному документі самостійно, а також у вигляді будь-яких сумішей. Всі дані форми, включаючи енантіомери, діастереомери, цис, транс, син, анти, сольвати (включаючи гідрати), таутомери та їх суміші, є включеними в описані сполуки. Стереоізомерні суміші, наприклад, суміші діастереомерів, можуть бути розділеними на їх відповідні ізомери за відомим підходом, застосовуючи прийнятні способи розділення. Діастереомерні суміші, наприклад, можуть бути розділеними на їх індивідуальні діастереомери з допомогою фракціонованої кристалізації, хроматографії, розподілення в розчиннику та подібних процедур. Дане розділення може відбуватись або на рівні однієї з вихідних сполук, або в самій сполуці формули I, IA, IB, IC або ID. Енантіомери можуть бути розділені шляхом утворення діастереомерних солей, наприклад, шляхом утворення солі з енантіомерно-чистої хіральної кислотою, або з допомогою хроматографії, наприклад, шляхом ВЕРХ, використовуючи хроматографічні субстрати з хіральними лігандами. В терапевтичному застосуванні для лікування розладів у ссавців, сполуку за представленим винаходом або її фармацевтичні композиції можуть вводити перорально, парентерально, місцево, ректально, трансмукозально або інтестинально. Парентеральні введення включають непрямі ін'єкції, щоб отримати системний ефект, або прямі ін'єкції в уражені ділянки. Місцеві введення включають лікування шкіри або органів, легко доступних для місцевого застосування, наприклад, очі або вуха. Крім того, воно включає трансдермальну доставку, щоб отримати системний ефект. Ректальне введення включає форму супозиторій. Переважними шляхами введення є пероральний та парентеральний. Фармацевтично прийнятні солі сполук формули I, IA, IB, IC або ID включають їх кислотні адитивні та основні солі. Прийнятні кислотні адитивні солі утворюються з кислот, які утворюють нетоксичні солі. Приклади солей включають ацетатні, адипінатні, аспартатні, бензоатні, безилатні, бікарбонaтні/карбонaтні, бісульфатні/сульфатні, боратні, камсилатні, цитратні, цикламатні, едизилатні, езилатні, форміатні, фумаратні, глюцептатні, глюконатні, глюкуронатні, гексафлуорфосфатні, гібензатні, гідрохлорид/хлоридні, гідробромід/бромідні, гідройодид/йодидні, ізетіонатні, лактатні, малатні, малеатні, малонатні, мезилатні, метилсульфатні, нафтилатні, 2-напсилатні, нікотинатні, нітратні, оротатні, оксалатні, пальмітатні, памоатні, фосфатні/гідрогенфосфатні/дигідрогенфосфатні, піроглутаматні, сахаратні, стеаратні, сукцинатні, таннатні, тартратні, тозилатні, трифлуорацетатні та ксинафоатні солі. Прийнятні основні солі утворюються з основ, які утворюють нетоксичні солі. Приклади включають алюмінієві, аргінінові, бензатинові, кальцієві, холінові, діетиламінові, діоламінові, гліцинові, лізинові, магнієві, меглюмінові, оламінові, калієві, натрієві, трометамінові та цинкові солі. Крім того, можуть бути утворені напівсолі кислот та основ, наприклад, гемісульфатні та гемікальцієві солі. Для розгляду прийнятних солей, дивись Handbook of Pharmaceutical Salts: Properties, Selection, and Use Stahl and Wermuth (Wiley-VCH, 2002). Фармацевтично прийнятні солі сполук формули I, IA, IB, IC або ID можуть одержувати, відповідно, за одним або більше з трьох способів: (i) реакцією сполуки формули I, IA, IB, IC або ID з бажаною кислотою або основою; (ii) видаленням кислотно- або основно-лабільної захисної групи з прийнятного попередника сполуки формули I, IA, IB, IC або ID або розкриттям циклу прийнятного циклічного попередника, наприклад, лактону або лактаму, використовуючи бажану кислоту чи основу; або (iii) перетворенням однієї солі сполуки формули I, IA, IB, IC або ID на іншу реакцією з відповідною кислотою або основою, або з допомогою прийнятної іон-обмінної колонки. Всі три реакції, як правило, виконують в розчині. Одержану в результаті сіль можуть осаджувати та збирати фільтрацією або можуть виділяти шляхом випаровування розчинника. Ступінь іонізації в одержаній в результаті солі може варіювати від повністю іонізованої до практично неіонізованої. Фармацевтичні композиції за представленим винаходом можуть виробляти за способами добре відомими в даній галузі, наприклад, застосовуючи загальноприйняте змішування, розчинення, гранулювання, виготовлення драже, розтирання в порошок, емульгування, капсулювання, захоплення, процеси ліофілізування або висушування при розпиленні. Фармацевтичні композиції для застосування у відповідності з представленим винаходом можуть бути сформульованими за загальноприйнятим способом, застосовуючи один або 12 UA 111804 C2 5 10 15 20 25 30 35 40 45 50 55 60 більше фармацевтично прийнятних носіїв, включаючи ексципієнти та допоміжні речовини, які полегшують використання активної сполуки у виробництві препаратів, які можуть застосовувати фармацевтично. Прийнятний препарат залежить від вибраного шляху введення. Фармацевтично прийнятні ексципієнти та носії є, як правило, відомими кваліфікованому фахівцю в даній галузі та є, таким чином, включеними в даний винахід. Такі ексципієнти та носії є описаними, наприклад, в "Remington's Pharmaceutical Sciences" Mack Pub. Co., New Jersey (1991). Препарати за винаходом можуть бути призначені для короткої дії, швидкого вивільнення, подовженої дії та уповільненого вивільнення. Таким чином, фармацевтичні препарати, крім того, можуть бути сформульовані для контрольованого вивільнення або уповільненого вивільнення. Фармацевтичні композиції прийнятні для застосування в представленому винаході включають композиції, в яких активні інгредієнти містяться в кількості достатній для досягнення призначеної мети, тобто, контролю або лікування розладів або захворювань. Більш конкретно, терапевтично ефективна кількість означає кількість сполуки, ефективну для попередження, полегшення або покращення симптомів/ознак захворювання або подовження тривалості життя суб'єкта, якого лікують. Кількість активного компоненту, який представляє собою сполуку за даним винаходом, в фармацевтичній композиції та її одиничній дозованій формі, може варіювати та регулюватись в широкому діапазоні в залежності від способу введення, ефективності конкретної сполуки та потрібної концентрації. Визначення терапевтично ефективної кількості знаходиться в межах можливостей кваліфікованого фахівця в даній галузі. Загалом, кількість активного компоненту буде знаходитись в діапазоні від 0,01 % до 99 % за масою композиції. Загалом, терапевтично ефективна кількість дозування активного компоненту буде знаходитись в діапазоні від приблизно 0,01 до приблизно 100 мг/кг маси тіла/день, переважно від приблизно 0,1 до приблизно 10 мг/кг маси тіла/день, більш переважно від приблизно 0,3 до 3 мг/кг маси тіла/день, ще більш переважно від приблизно 0,3 до 1,5 мг/кг маси тіла/день. Слід розуміти, що дозування можуть варіювати в залежності від потреб кожного суб'єкта та тяжкості розладів або захворювань, які лікують. Потрібна доза може, з метою зручності, бути присутньою в одиничній дозі або як розділені дози, які вводяться з відповідними інтервалами, наприклад, як два, три, чотири або більше піддоз на день. Піддоза сама по собі може бути додатково розділена, наприклад, на ряд дискретних вільно рознесенних введень; таких як багаторазові інгаляції з інсуфлятора або при застосуванні декількох крапель в око. Крім того, слід розуміти, що початкова доза, яка вводиться, може бути збільшена вище верхнього рівня для того, щоб швидко досягти необхідної концентрації в плазмі. З іншого боку, початкова доза може бути меншою за оптимальну, та добова доза може бути поступово збільшеною під час курсу лікування в залежності від конкретної ситуації. Якщо потрібно, денна доза також може бути розділена на декілька доз для введення, наприклад, від двох до чотирьох разів на день. Сполуки за представленим винаходом відносяться до сполук піроло[2,3-d]піримідину, корисних як інгібітори Янус-кінази (JAK-i). Вони є корисними як терапевтичні агенти в зв'язку з лікуванням або попередженням розладу або стану, вибраного з ревматоїдного артриту, міозиту, васкуліту, пухирчатки, хвороби Крона, неспецифічного виразкового коліту, хвороби Альцгеймера, червоного вовчаку, нефриту, псоріазу, атопічного дерматиту, аутоімунних розладів щитоподібної залози, розсіяного склерозу, великого депресивного розладу, алергії, астми, хвороби Шегрена, синдрому сухих очей, відторгнення трансплантата органу, ксенотрансплантації, діабету типу І та ускладнення від діабету, раку, лейкемії, Т-клітинної гострої лімфобластної лейкемії, Т-клітинного лейкозу у дорослих, активованого подібним Вклітинам, дифузної В-великоклітинної лімфоми, запального захворювання кишечника, септичного шоку, кардіопульмональної дисфункції, хронічного обструктивного захворювання легень, гострого респіраторного захворювання, кахексії, та інших показників, де імуносупресія/імуномодуляція повинні бути бажаними, яке включає стадію введення суб'єкту ефективної кількості сполуки за винаходом. Існують значні потреби в безпечних та ефективних агентах для контролю розладів, пов'язаних з JAK, таких як атопічний дерматит, як у людини, так і у тварин. На ринку лікування атопічного дерматиту у тварин на даний час домінують кортикостероїди, які викликають тривожні та небажані побічні ефекти у тварин, зокрема у домашніх тварин таких як собаки. Антигістаміни також використовуються, але вони є мало ефективними. Препарат циклоспорину TM для собак (ATOPICA ) на даний час є присутньою на ринку для атопічного дерматиту, але є TM дорогим та має повільну початкову ефективність. Крім того, існують проблеми з ATOPICA 13 UA 111804 C2 5 10 15 20 25 30 35 40 45 50 55 60 щодо толерантності з боку ШК тракту. Сполуки за представленим винаходом є інгібіторами JAK з селективною ефективністю проти JAK1. Дані сполуки, як очікується, забезпечують альтернативу застосуванню стероїдів та забезпечують припинення хронічного свербіжу та запалення, які повинні або продовжувати існувати при атопічному дерматиті або повільно регресувати після видалення алергену або збудника, такого як блохи при викликаному блохами алергічному дерматиті. Сполуки за представленим винаходом можуть вводити у фармацевтично прийнятній формі, або самостійно, або в комбінації одним або більше додатковими агентами, які модулюють імунну систему ссавця, або з протизапальними агентами. Дані агенти можуть включати, але не обмежуються цим, циклоспорин A (наприклад, Сандімун™ або Неорал™, рапаміцин, FK-506 (такролімус), лефлуномід, деоксиспергуалін, мікофенолат (наприклад, Селлсепт™, азатіоприн (наприклад, Імуран™), даклізумаб (наприклад, Зенапакс™), OKT3 (наприклад, Orthocolone™), AtGam, аспірин, ацетамінофен, ібупрофен, напроксен, піроксикам та протизапальні стероїди (наприклад, преднізолон або дексаметазон). Дані агенти можуть вводити як частину однієї й тієї ж або окремими дозованими формами, однаковими або різними шляхами введення, та за однаковим або різними графіками введення відповідно до стандартної фармацевтичної практики, відомої кваліфікованому фахівцю в даній галузі. Відповідно, винахід передбачає способи лікування або попередження захворювання, стану або розладу, пов'язаних з JAK у суб'єкта, такого як людина або ссавець-не людина, що включає введення суб'єкту ефективної кількості однієї або більше сполук, описаних в даному документі. Прийнятні суб'єкти, яких можуть лікувати, включають свійських або диких тварин, домашніх тварин, таких як собаки, кішки, коні, тощо; сільськогосподарських тварин, включаючи корів та інших жуйних тварин, свиней, птицю, кроликів тощо; приматів, наприклад, мавп, таких як макаки в тому числі макаки-резус та циномолгус (також відомий як крабоїди або довгохвості), мавпи, мармозетки, ігрункові мавпи, шимпанзе, макаки, тощо; та гризуни, такі як щурі, миші, піщанки, морські свинки, тощо. В одному варіанті здійснення, сполуку вводять в фармацевтично прийнятній формі, необов'язково в фармацевтично прийнятному носії. Стани, в яких, як розглядається, терапевтично корисною є селективна спрямованість шляху JAK або модуляції кіназ JAK, зокрема JAK1, включають артрит, астму, аутоімунні захворювання, форми раку або пухлин, діабет, певні очні захворювання, розлади або стани, запалення, кишкові запалення, алергії або стани, нейродегенеративні захворювання, псоріаз та відторгнення трансплантата. Стани, які можуть отримати позитивний ефект від селективного інгібування JAK1, обговорюються більш детально нижче. Відповідно, сполука формули I, IA, IB, IC або ID, або її фармацевтично прийнятні солі, та їх фармацевтичні композиції можуть застосовувати для лікування різних станів або захворювань, таких як наступні: Артрит, включаючи ревматоїдний артрит, ювенільний артрит та псоріатичний артрит; Аутоімунні захворювання або розлади, включаючи ті, що вказані як розлади одного органу або одного типу клітин аутоімунного розладу, наприклад, тиреоїдит Хашимото, аутоімунна гемолітична анемія, аутоімунний атрофічний гастрит злоякісної анемії, аутоімунний енцефаломієліт, аутоімунний орхіт, хвороба Гудпасчера, аутоімунна тромбоцитопенія, симпатична офтальмія, міастенія гравіс, хвороба Грейвса, первинний біліарний цироз печінки, хронічний агресивний гепатит, неспецифічний виразковий коліт та мембранна гломерулопатія, ті, що зазначені як включені в системний аутоімунний розлад, наприклад, системний червоний вовчак, ревматоїдний артрит, синдром Шегрена, синдром Рейтера, поліміозит-дерматоміозит, системний склероз, нодозний поліартериїт, розсіяний склероз та бульозний пемфігоїд, та додаткові аутоімунні захворювання, які можуть бути на основі O-клітин (гуморальний) або на основі T-клітин, включаючи синдром Когана, анкілозуючий спондилоартрит, гранулематоз Вегенера, аутоімунна алопеція, діабет типу I або юнацький діабет, або тиреоїдит; Форми раку або пухлини, включаючи рак травного/шлунково-кишкового тракту, рак товстої кишки, рак печінки, рак шкіри, включаючи мастоцитому та плоско клітинну карциному, рак молочної залози, рак яєчників, рак передміхурової залози, лімфому, лейкемію, в тому числі гострий мієлоїдний лейкоз та хронічний мієлоїдний лейкоз, рак нирки, рак легенів, м'язовий рак, рак кісток, рак сечового міхура, рак мозку, меланому, включаючи оральну та метастатичну меланому, саркому Капоші, мієломи, в тому числі множинна мієлома, мієлопроліферативні розлади, проліферативну діабетичну ретинопатію, та ангіогенно-опосередковані розлади в тому числі солідні пухлини; Діабет, включаючи діабет типу І або ускладнення від діабету; Очні захворювання, розлади або стани, включаючи аутоімунні захворювання ока, кератокон'юнктивіт, весняний кон'юнктивіт, увеїт включаючи увеїт пов'язаних з захворюванням 14 UA 111804 C2 5 10 15 20 25 30 35 40 45 Бехчета та фактоантигенний увеїт, кератит, герпетичний кератит, конусний кератит, рогівкова епітеліальна дистрофія, кератолейкома, пемфігоїд кон'юктиви, виразку Мурена, склерит, офтальмопатія Грейвса, синдром Фогта-Коянаги-Харада, сухий кератокон'юктивіт (сухе око), фліктену, іридоцикліт, саркоїдоз, ендокринну офтальмопатію, симпатичний офтальміт, алергічний кон'юктивіт або очну неоваскуляризацію; Кишкові запалення, алергії або стани, включаючи хворобу Крона та/або неспецифічний виразковий коліт, запальне захворювання кишечника, глютеїнчутлива целіакія, проктит, еозинофільний гастроентерит або мастоцитоз; Нейродегенеративні захворювання, включаючи захворювання рухових нейронів, хворобу Альцгеймера, хворобу Паркенсона, аміотрофічний бічний склероз, хворобу Хантінгтона, церебральну ішемію або нейродегенеративне захворювання, викликане травматичним пошкодженням, напад, глутаматну нейротоксичність або гіпоксію; ішемічне/репер фузійне пошкодження при інсульті, ішемію міокарда, ниркову ішемію, серцеві напади, гіпертрофію серця, атеросклероз та артеріосклероз, гіпоксію органів або агрегацію тромбоцитів; Захворювання, стани або розлади шкіри, включаючи атопічний дерматит, екзему, псоріаз, склеродермію, свербіж або інші сверблячі стани; Алергічні реакції, включаючи алергічний дерматит у ссавців (включаючи алергічні захворювання у коней, такі як гіперчутливість до укусів), літню екзему, солодкий свербіж у коней, вибухання, запальне захворювання дихальних шляхів, рецидивуючу обструкцію дихальних шляхів, гіперчутливість дихальних шляхів або хронічне обструктивне захворювання легень; Астма та інші обструктивні захворювання дихальних шляхів, включаючи хронічну або застарілу астму, пізню астму, бронхіт, бронхіальну астму, алергічну астму, ендогенну бронхіальну астму, екзогенну бронхіальну астму або пилову астму; Відторгнення трансплантата, включаючи відторгнення трансплантату острівців підшлункової залози, відторгнення трансплантату кісткового мозку, захворювання трансплантат-протигосподаря, відторгнення трансплантату органу та клітини, такого як кістковий мозок, хрящ, рогівка, серце, міжхребцевий диск, острівок, нирка, кінцівка, печінка, легеня, м'яз, міобласт, нерв, підшлункова залоза, шкіра, тонка кишка або трахея, або ксенотрансплантація; та Інший варіант здійснення передбачає спосіб селективного інгібування JAK1 фермента, який включає контактування JAK фермента з або не терапевтичною кількістю або терапевтично ефективною кількістю однієї або більшу на даний момент зазначених сполук. Такі способи можуть здійснюватись in vivo або in vitro. In vitro контакт може включати скрінінговий аналіз щодо визначення ефективності однієї або більше сполук проти вибраного ферменту в різних кількостях або концентраціях. In vivo контакт з терапевтично ефективною кількістю однієї або більше сполук може включати лікування описаного захворювання, розладу або стану, або профілактику відторгнення трансплантату органа у тварини, у якої відбувається даний контакт. Крім того, можуть визначати або вимірювати дію однієї або більше сполук на JAK фермент та/або тварину-господаря. Способи визначення активності JAK включають ті, які описані в прикладах, а також ті, які описані в WO 99/65908, WO 99/65909, WO 01/42246, WO 02/00661, WO 02/096909, WO 2004/046112 та WO 2007/012953. Хімічний синтез З допомогою наступних схем та письмових описів представлено загальні деталі щодо одержання сполук за винаходом. СУЛЬФОНАМІДИ 5 Сполуки формули I, де p є 2, X є NH, Y є AR , та A є зв'язком, можуть одержувати відповідно до схеми 1. 15 UA 111804 C2 5 10 15 20 25 30 Для кваліфікованого фахівця в даній галузі буде очевидно, що чутливі функціональні групи (PG) можуть потребувати в захисті та в знятті захисту під час синтезу сполуки за винаходом. Захист та зняття захисту можуть досягати, застосовуючи загальноприйняті способи, як описано, наприклад, в "Protective Groups in Organic Synthesis" by T. W. Greene and P. G. M. Wuts, John Wiley & Sons Inc. (1999), та та посиланнях в ньому. Таким чином, на схемі 1, стадії 1, сполуку 1 формули II, в якій Q є галогеном, обробляють захисним агентом, одержуючи сполуку формули 1 III, де PG представляє собою арилсульфонільну захисну групу, таку як бензолсульфоніл або, переважно, пара-толуолсульфоніл ("тозил"). Захисну групу можуть вводити за реакцією сполуки формули II з арилсульфонілхлоридом, переважно тозилхлоридом, в присутності основи, такої як водний розчин гідроксиду натрію, та органічного розчиннику, такого як ацетон. Реакція, як правило, проходить при температурі приблизно 0-50 °C, переважно при температурі приблизно 23 °C (кімнатній температурі). Альтернативно, можуть використовувати основи, такі як гідрид натрію та трет-бутоксид калію, застосовуючи прийнятний розчинник, такий як N, Nдиметилформамід або тетрагідрофуран. Декілька сполук формули II є відомими з літератури та були одержані за способами зазначеними вище. Наприклад, про синтез сполуки формули II, в 1 2 3 якій Q є Cl та R та R є гідрогеном, доповідалось раніше, наприклад в міжнародній публікації WO 2007 012953. На схемі 1, стадії 2, захищену сполуку формули III сполучають з 1-2 еквівалентами аміну формули IV в присутності 1-3 еквівалентів основи та протонного розчинник, одержуючи сполуку формули V. Прийнятні основи включають триетиламін, діізопропілетиламін та карбонат калію, тоді як прийнятні розчинники включають метанол, етанол, діізопропіловий спирт та воду або їх суміші. Реакція, як правило, відбувається при температурі приблизно 23-150 °C, переважно при температурі приблизно 75 °C. Слід зазначити, що амін формули IV містить другу аміногрупу, яка 2 є захищеною захисною групою PG , що може бути видалена в умовах, що не призводять до 1 2 втрати PG . Прийнятні захисні групи PG включають трет-бутоксикарбоніл ("Boc") та ("Cbz"), переважно бензилоксикарбоніл. 2 На схемі 1, стадії 3, захисну групу PG видаляють зі сполуки формули V в умовах, що не 1 2 призводять до втрати PG , одержуючи первинний амін (або його сіль) формули VI. Коли PG представляє собою бензилоксикарбоніл, то бензилоксикарбонільну захисну групу можуть видаляти шляхом гідрогенолізу, де сполуку формули V піддають дії гідрогену або реагенту переносу гідрогена, такого як циклогексен в присутності каталізатора гідрогенізації, такого як 16 UA 111804 C2 5 10 15 20 25 30 35 40 45 гідроксид паладію, застосовуючи розчинник, такий як метанол, оцтова кислота або, переважно, 2 етанол. Альтернативно, коли PG представляє собою бензилоксикарбоніл, бензилоксикарбонільну захисну групу можуть видаляти обробкою сполуки формули V розчином гідрогенброміду (приблизно 6 еквівалентів) в оцтовій кислоті необов'язково в присутності прийнятного розчинника, такого як етилацетат при температурі від приблизно мінус 20 °C до приблизно 40 °C, переважно, менше, ніж 25 °C. Даний останній спосіб зняття захисту є 2 3 4 1 1 2 переважним, коли n є 1, R , R та R є гідрогеном, R є метилом, PG є тозилом та PG є бензилоксикарбонілом та забезпечує амін формули VI у вигляді дигідробромідної солі. Коли 2 PG є трет-бутоксикарбонілом, трет-бутоксикарбонільну захисну групу можуть видаляти обробкою надлишком кислоти, такої як гідрогенхлоридна кислота або трифлуороцтова кислота, в розчиннику, такому як дихлорметан або 1,4-діоксан. На схемі 1, стадії 4, первинний амін формули VI (або його сіль) перетворюють в сульфонамідну похідну формули VII обробкою активованою похідною сульфонової кислоти 2 формули VIII, в якій Q є галогеном, O-алкілом або O-арилом в присутності основи. Зазвичай, 2 VIII представляє собою похідну сульфонілхлориду, в якому Q є Cl. Багато сульфонілхлоридів можуть одержувати з комерційних джерел. Крім того, існує декілька способів одержання сульфонілхлоридів, які є добре відомими кваліфікованому фахівцю в даній галузі та описані в підручниках, таких як "Advanced Organic Chemistry" by J. March, John Wiley & Sons (1985). Як 2 правило, амін формули VI обробляють похідною сульфонілхлориду формули VIII, в якій Q є Cl, в присутності, щонайменше, одного еквівалента основи, такої як триетиламін або діізопропіламін, в прийнятному розчиннику, такому як дихлорметан, тетрагідрофуран або ацетонітрил. Коли використовують сольову форму аміну, застосовують додатковий еквівалент основи на кожен еквівалент кислотного утворення солі. Наприклад, застосовуючи дигідробромідну сіль, використовують два надлишкових еквіваленти основи. Реакція може проходити від приблизно мінус 20 °C до приблизно 50 °C, переважно, початок реакції при приблизно 0 °C та потім даючи їй нагрітися до приблизно 23 °C (кімнатної температури). Зрештою, на схемі 1, стадії 5, із сульфонамідної похідної формули VII знімають захист, 5 одержуючи сполуку формули 1, в якій p є 2, X є NH, Y є AR та A є зв'язком. Як правило, застосовують два способи, вибір якого визначають, виходячи із сумісності умов з іншими функціональними групами в молекулі. Перший спосіб включає піддавання дії сполуки формули VII надлишку (приблизно 4 еквіваленти) основ, таких як гідроксид літію або гідроксид натрію. Реакція проходить в суміші розчинників, що містить воду та спирт, такий як метанол або етанол. Крім того, вона може проходити в суміші води та тетрагідрофурану, та, необов'язково, спирту, такого як метанол або етанол. Реакція може проходити при температурі від приблизно 23 °C до приблизно 100 °C, як правило приблизно 60 °C. Другий спосіб, який є переважним в тих випадках, коли існує гідроксид-чутлива функціональність, наприклад, коли в молекулі присутній нітрил, включає реакцію сполуки формули VII з надлишком тетрабутиламонію флуориду (4-25 еквівалентів) в розчиннику, такому як 1,2-диметоксіетан або, переважно, тетрагідрофуран. Зняття захисту проводять при температурі приблизно 0-60 °C, переважно при температурі приблизно 23 °C. 1 Сполуки формули II, в яких Q є галогеном, є комерційно доступними або є відомими в 1 2 3 хімічній літературі. Наприклад, 4-хлор-7H-піроло[2,3-d]піримідин, в якому Q є Cl та R та R обидва є гідрогеном, є готовою комерційно доступною сполукою. Сполуки формули IV є відомими в хімічній літературі або можуть бути отримані за стандартними хімічними реакціями, добре відомими кваліфікованому фахівцю в даній галузі. 5 Альтернативний спосіб одержання сполук за винаходом, де p є 2, X є NH, Y є AR , A є зв'язком, показано на схемі 2. 17 UA 111804 C2 5 10 15 20 25 30 35 40 На схемі 2, стадії 1, сполуку формули IX сполучають похідною з бензилоксикарбамату формули X в присутності основи (1-5 еквівалентів), одержуючи похідну бензилокси-карбамату формули XI. Реакцію здійснюють в розчиннику, такому як вода або спирт, такий як етанол, необов'язково з додаванням сумісного спів-розчинника, такого як тетрагідрофуран. Прийнятні основи включають карбонат калію, карбонат цезію, триетиламін та діізопропілетиламін. Реакція 2 3 4 проходить при від приблизно 23 °C до приблизно 100 °C. Коли n є 1, R , R та R є гідрогеном, 1 та R є метилом, переважними умовами є такі, при яких реакція проходить у воді, застосовуючи карбонат калію (3 еквіваленти) як основу, початок реакції – при приблизно 23 °C та потім нагрівання до приблизно 95 °C. На схемі 2, стадії 2, з похідної бензилоксикарбамату формули XI знімають захист, піддаючи дії гідрогену або реагенту переносу гідрогена, такого як циклогексен в присутності каталізатора гідрогенізації, такого як паладію гідроксид. В той же час, в умовах зняття захисту, атом хлору в 2-положенні 7H-піроло[2,3-d]піримідинового кільця заміщується на гідроген, одержуючи гідрохлоридну сіль аміну формули XII. Реакція проходить в розчиннику, такому як метанол або 2 3 4 етанол, при температурі від приблизно 50 °C до приблизно 80 °C. Коли R , R та R є 1 гідрогеном, та R є метилом, переважні умови є такими, що реакція проходить в етанолі при приблизно 78 °C, застосовуючи гідроксид паладію як каталізатор, та циклогексен (приблизно 20 еквівалентs) як реагент переносу гідрогену. Зрештою, на схемі 2, стадії 3, гідрохлорид аміну формули XII перетворюють в сульфонамід 5 формули I, де p є 2, X є NH, Y є AR , A є зв'язком за реакцією з активованою похідною 2 сульфонової кислоти формули VIII, в якій Q є галогеном, O-алкілом або O-арилом, в присутності, щонайменше, двох еквівалентів основи. Зазвичай, VIII є сульфонілхлоридною 2 похідною, в якій Q є Cl. Прийнятні основи включають триетиламін, діізопропілетиламін та карбонат калію. Прийнятні розчинники включають N, N-диметилформамід, та суміш тетрагідрофурану та води. Реакція може проходити при температурі від приблизно мінус 20 °C до приблизно 50 °C, переважно при приблизно 23 °C. Альтернативно, гідрохлорид аміну формули XII спочатку обробляють приблизно 2 еквівалентами триметилхлорсилану в присутності приблизно 2-3 еквівалентів основи, такої як літію біс(диметилсиліл)амід або натрію біс(диметилсиліл)амід, в прийнятному aпротонному розчиннику, такому як тетрагідрофуран. Потім, через приблизно 1 годину, додають приблизно 1,2 еквіваленти сульфонілхлориду 2 формули VIII, де Q є Cl, одержуючи, після обробки, сульфонамід формули I, в якому p є 2, X є 5 NH, Y є AR , A є зв'язком. Реакція може проходити при температурі від приблизно мінус 20 °C до приблизно 50 °C, переважно при приблизно 23 °C. Сполуки формули IX є комерційно доступними або є відомими в хімічній літературі. 2 3 Наприклад, 2,4-дихлор-7H-піроло[2,3-d]піримідин, в якому R та R обидва є гідрогеном, є комерційно доступним. Його синтез є описаним в міжнародній публікації PCT № WO 2007/012953. СУЛЬФАМІДИ Сполуки формули I, в яких p є 2, X є NH, та Y є NRaRb, можуть бути отримані відповідно до схеми 3. 18 UA 111804 C2 1 5 10 15 20 25 30 На схемі 3, стадії 1, амін формули VI (або його сіль), в якому PG є арилсульфонільною захисною групою, такою як бензолсульфоніл або, переважно, тозил, перетворюють в похідну оксазолідинону формули XIII. Спочатку, розчин N-хлорсульфонілізоціанату (1 еквівалент) повільно додають до розчину 2-брометанолу (1 еквівалент) при температурі від приблизно 40 °C до приблизно 10 °C, переважно при приблизно 0 °C. Потім, через 0,5-2 години, повільно додають розчин аміну формули VI (1 еквівалент) та основу, таку як триетиламін або діізопропілетиламін (приблизно 3 еквіваленти, плюс один еквівалент на кожен моль кислоти, що утворює сіль), та реакційній суміші дають нагрітися до приблизно 23 °C протягом приблизно 1024 годин. Прийнятні розчинники для реакції включають хлороформ або, переважно, дихлорметан. На схемі 3, стадія 2, похідну оксазолідинону формули XIII піддають взаємодії з 1-3 еквівалентами аміну формули HNRaRb, в присутності основи (2-5 еквівалентів), одержуючи сульфамідну похідну формули XIV. Прийнятні основи включають триетиламін та діізопропілетиламін. Реакція переважно здійснюють при нагріванні до від приблизно 90 °C до приблизно 150 °C в ємності високого тиску, застосовуючи прийнятний розчинник, такий як N, Nдиметилформамід або ацетонітрил. На схемі 3, стадії 3, зі сполуки формули XIV знімають захист, видаляючи арилсульфонільну 1 захисну групу PG , одержуючи сульфамідну похідну формули 1, в якій p є 2, X є NH, та Y є NRaRb. Реакцію можуть здійснювати за одним з двох загальних способів, описаних для схеми 1, стадії 5. Знову, вибір способу зняття захисту визначається сумісністю умов з іншими функціональними групами в молекулі. Альтернативно, сульфаміди формули XIV можуть одержувати безпосередньо з аміну формули VI (або його солі). Таким чином, на схемі 3, стадії 4, амін формули VI (або його сіль) обробляють сульфамоїлхлоридом формули Cl-SO2NRaRb та основою, такою як триетиламін або діізопропілетиламін, як описано для схеми 1, стадії 4. Сульфамоїлхлориди формули Cl-SO2NRaRb можуть бути отримані, в свою чергу, з амінів формули HNRaRb відповідно до методик, розглянутих W. R. Bowman та R. J. Marmon в "Comprehensive Organic Functional Group Transformations, Volume 2", Pergamon (1995). Сполуки формули I, в якій p є 2, X є NH, та Y є NRaRb також можуть отримувати безпосередньо з аміну формули XII (або його солі). Таким чином, на схемі 3, стадії 5, амін 19 UA 111804 C2 5 10 15 формули XII(або його сіль) обробляють сульфамоїлхлоридом формули Cl-SO2NRaRb та основою, такою як триетиламін або діізопропілетиламін, як описано для схеми 1, стадії 4. Аміни формули XII одержують як описано для схеми 2. Аміни формули XII (або їх солі) можуть 1 одержувати шляхом видалення арилсульфонільної захисної групи PG зі сполуки формули VI (відповідно до схеми 1). Зняття захисту можуть здійснювати за одним з двох загальних способів зняття захисту, описаних для схеми 1, стадії 5. Вибір способу зняття захисту визначається сумісністю умов з іншими функціональними групами в молекулі. ОБЕРНЕНІ СУЛЬФОНАМІДИ Сполуки формули I, в яких p є 2, X є CH2, та Y є NRaRb, можуть бути отримані відповідно до схеми 4. На схемі 4, стадії 1, сполуку формули III (відповідно до схеми 1), сполучають з аміноспиртом формули XV в присутності основи та голярного розчинника, одержуючи сполуку формули XVI. Прийнятні основи включають триетиламін та діізопропілетиламін, тоді як прийнятні розчинники 20 UA 111804 C2 5 10 15 20 25 30 35 40 45 50 включають метанол, діізопропіловий спирт та ацетон. Реакція, як правило, проходить при від приблизно 23 °C до приблизно 70 °C. Переважно, до реакції додають каталітичну кількість (приблизно 1 мольний %) йодиду калію. На схемі 4, стадії 2, сполуку формули XVI перетворюють в сполуку формули XVII, в якій LG є групою, що відщеплюється, такою як бром, йод, метансульфонат або, переважно, паратолуолсульфонат. Способи введення таких груп, що відщеплюються, є добре відомими кваліфікованому фахівцю в даній галузі та описані в підручниках, таких як "Advanced Organic Chemistry" by J. March, John Wiley & Sons (1985). У випадку, коли LG є паратолуолсульфонатом, сполуку формули XVI обробляють пара-толуолсульфоніл хлоридом в присутності основи, такої як триетиламін, діізопропілетиламін або N, N-диметиламінопіридин, в aпротонному розчиннику, такому як дихлорметан або тетрагідрофуран. Реакція проходить при температурі від приблизно -10 °C до приблизно 40 °C, переважно на початку при приблизно 0 °C та до приблизно 23 °C. На схемі 4, стадії 3, сполуку формули XVII сполучають із сіллю тіооцтової кислоти, переважно тіоацетатом калію, одержуючи тіоестерну похідну формули XVIII. Реакцію здійснюють в полярному розчиннику, такому як N, N-диметилформамід або N-метилпіролідин, при температурі від приблизно 23 °C до приблизно 80 °C, переважно при приблизно 55 °C. На схемі 4, стадії 4, тіоестерну похідну формули XVIII перетворюють в похідну сульфонової кислоти формули XIX за реакцією з водним розчином гідрогенпероксиду, як правило 30 % за масою. Реакцію здійснюють в кислотному розчиннику, такому як мурашина або оцтова кислота при температурі від приблизно 0 °C до приблизно 40 °C, переважно при приблизно 23 °C. На схемі 4, стадії 5, похідну сульфонової кислоти формули XIX перетворюють в сульфонілхлоридну похідну формули XX. Декілька способів здійснення даного перетворення функціональної групи є відомими в літературі. Переважний спосіб представляє собою обробку сполуки формули XIX надлишком (3-15 еквівалентами) тіонілхлориду в присутності каталітичної кількості N, N-диметилформаміду в aпротонному розчиннику, такому як дихлорметан або хлороформ. Реакція може проходити від приблизно мінус 20 °C до приблизно 100 °C, переважно початок реакції – при приблизно 0 °C, та потім нагрівання до приблизно 75 °C. Альтернативно, на схемі 4, стадії 6, тіоестерну похідну формули XVIII можуть безпосередньо перетворювати в сульфонілхлоридну похідну формули XX обробкою хлоруючим агентом. Декілька способів здійснення даного перетворення функціональної групи є відомими в літературі. Хлоруючі агенти включають газоподібний хлор та N-хлорсукцинімід, та реакція зазвичай проходить в присутності кислоти, такої як гідрогенхлоридна кислота або оцтова кислота. Часто застосовують системи змішаних водних розчинників, таких як воду і дихлорметан та воду і ацетонітрил. На схемі 4, стадії 7, сульфонілхлоридну похідну формули XX сполучають з 1-3 еквівалентами аміну формули HNRaRb, утворюючи сульфонамідну похідну формули XXI. Реакція проходить в присутності, щонайменше, одного еквівалента основи, такої як триетиламін або діізопропілетиламін, при температурі від приблизно мінус 20 °C до приблизно 50 °C, переважно початок реакції – при приблизно 0 °C та даючи реакції нагрітися до приблизно 23 °C. Реакція проходить в aпротонному розчиннику, такому як тетрагідрофуран або дихлорметан. 1 Зрештою на схемі 4, стадії 8, арилсульфонільну захисну групу PG видаляють, одержуючи сполуку формули I, в якій p є 2, X є CH2, та Y є NRaRb. Реакцію можуть здійснювати за одним з двох загальних способів зняття захисту, описаних для схеми 1, стадії 5. Вибір способу зняття захисту визначається сумісністю умов з іншими функціональними групами в молекулі. Аміноспирти формули XV є відомими в хімічній літературі або можуть бути отримані за способами, добре відомими кваліфікованому фахівцю в даній галузі. СУЛЬФОНИ, СУЛЬФОКСИДИ та ТІОЕТЕРИ 5 Сполуки формули I, в яких p є 0, 1 або 2, X є CH2, Y є AR та A є зв'язком, можуть бути отримані відповідно до схеми 5. 21 UA 111804 C2 5 10 15 20 25 30 На схемі 5, стадії 1, сполуку формули XVII (відповідно до схеми 4) обробляють 1-2 5 еквівалентами тіолу формули R SH в присутності 1-2 еквівалентів основи, одержуючи сульфід формули XXIII. Прийнятні основи включають гідрид натрію, натрію біс(триметилсиліл)амід, 1,5діазабіцикло[4.3.0]нон-5-ен (DBN) та переважно, 1,8-діазабіцикло[5.4.0]ундек-7-ен (DBU). Реакцію здійснюють в розчиннику, такому як N, N-диметилформамід або N-метилпіролідинон при температурі від приблизно 0 °C до приблизно 50 °C, переважно при приблизно 23 °C. На схемі 5, стадії 2, зі сполуки формули XXIII знімають захист, видаляючи арилсульфонільну 1 захисну групу PG , одержуючи сполуку формули XXIV. Реакцію можуть здійснюють за одним з двох загальних способів зняття захисту, описаних для схеми 1, стадія 5. Вибір способу зняття захисту визначається сумісністю умов з іншими функціональними групами в молекулі. На схемі 5, стадії 3, сульфід формули XXIV окиснюють, одержуючи сульфон формули I, в 5 якому p є 2, X є CH2, Y є AR та A є зв'язком. Декілька способів є відомими в літературі, та всі включають застосування окиснювача, такого як мета-хлорпербензойна кислота, ® гідрогенпероксид або калію пероксимоносульфат (Oxone ). Переважний спосіб представляє ® собою обробку сполуки формули XXIV 2 еквівалентами калію пероксимоносульфату (Oxone ) в суміші розчинників з тетрагідрофурану, етанолу та води при температурі від приблизно 23 °C. Сульфід формули XXIV також може бути окисненим в більш м'яких умовах, наприклад, застосовуючи 1 еквівалент мета-хлорбензойної кислоти в розчиннику, такому як дихлорметан, 5 при приблизно 0 °C, одержуючи сульфоксид формули I, в якому p є 1, X є CH 2, Y є AR та A є зв'язком. Слід зазначити, що порядок стадій 2 та 3 на схемі 5, необов'язково, може бути зворотним, таким чином, що стадію окиснення здійснюють перед стадією зняття захисту. 5 Сполуки формули I, в яких p є 0, X є CH2, Y є AR та A є зв'язком, одержують на схемі 5, 1 стадії 4, видаляючи арилсульфонільну захисну групу PG зі сполуки формули XXIII. Реакцію можуть здійснювати за одним з двох загальних способів зняття захисту, описаних для схеми 1, стадії 5. Знову, вибір способу зняття захисту визначається сумісністю умов з іншими функціональними групами в молекулі. На схемі 5, стадії 5, сполуки формули XXIII альтернативно одержують з тіоацетатної 22 UA 111804 C2 5 10 15 20 25 30 35 40 45 50 55 60 похідної формули XVIII. Спочатку, тіоацетат формули XVIII розчиняють в розчиннику, такому як етанол, метанол або воду (або їх суміш). Додають прийнятну основу, таку як карбонат калію або цезію карбонат (приблизно 2 еквіваленти), та азот барботують через розчин, щоб видалити 5 кисень. Потім додають алкілуючий агент формули R -LG, в якому LG є групою, що відщеплюється, такою як бром, йод, метансульфонат або, пара-толуолсульфонат. Реакцію проводять при температурі від приблизно мінус 20 °C до приблизно 30 °C. Переважно, реакція починається при приблизно 0 °C та потім даючи нагрітися до приблизно 23 °C. 5 5 Багато тіолів формули R SH та алкілуючі агенти формули R -LG можуть одержувати з комерційних джерел. Крім того, декілька способів існує для одержання таких сполук, які є добре відомими кваліфікованому фахівцю в даній галузі та описані в підручниках, таких як "Advanced Organic Chemistry" by J. March, John Wiley & Sons (1985). Слід зазначити, що певні сполуки за винаходом можуть одержувати перетворюванням функціональної групи на останній стадії синтезу, наприклад, шляхом хімічної модифікації груп 4 5 R або R після здійснення стадій 4 або 5 на схемі 1, стадії 3 на схемі 2, стадій 2, 3 або 4 на схемі 3, стадій 7 або 8 на схемі 4 та стадій 2, 3, 4 або 5 на схемі 5. Такі перетворювання функціональної групи можуть включають одну стадію або декілька стадій, наприклад, відновлення естеру до спирту, повторне окиснення до альдегіду, додавання магнійорганічного реагента, утворюючи вторинний спирт, повторне окиснення до кетона та, зрештою, додавання магнійорганічного реагента, одержуючи третинний спирт. При виконанні синтезу сполук за винаходом, кваліфікованому фахівцю у даній галузі буде зрозумілою необхідність аналізу зразка та реакційних сумішей до роботи з метою контролю за проходженням реакцій та прийняття рішення, чи слід продовжувати реакцію або вона вже є готовою щодо виділення, щоб отримати бажаний продукт. Загальні способи аналізу реакційних сумішей включають тонкошарову хроматографію (ТШХ), рідинну хроматографію/масспектроскопію (РХ-МС) та ядерного магнітний резонанс (ЯМР). Кваліфікованому фахівцю у даній галузі буде зрозуміло, що сполуки за винаходом можуть бути отримані як суміші діастереомерів або геометричних ізомерів (наприклад, цис та транс заміщення на циклоалкановому кільці). Дані ізомери можуть бути розділені, застосовуючи стандартні хроматографічні способи, такі як хроматографія з нормальною фазою на силікагелі, препаративна високоефективна рідинна хроматографія з оберненою фазою або надкритична рідинна хроматографія. Кваліфікованому фахівцю у даній галузі буде зрозуміло, що деякі сполуки за винаходом є хіральними та, таким чином, можуть бути отримані як рацемічні або скалемічні суміші енантіомерів. Декілька способів є доступними та є добре відомими кваліфікованому фахівцю в даній галузі для розділення енантіомерів. Переважний спосіб рутинного розділення енантіомерів представляє собою надкритичну рідинну хроматографію, застосовуючи хіральну стаціонарну фазу. ЕКСПЕРИМЕНТАЛЬНИЙ РОЗДІЛ За винятком тих випадків, коли зазначено інше, реакції проводили в атмосфері азоту. Хроматографію на силікагелі здійснювали застосовуючи силікагель 250-400 меш, застосовуючи азот під тиском (~10-15 фунтів на квадратний дюйм), щоб керувати проходженням розчинника через колонку ("флеш-хроматографія"). Коли вказано, розчини та реакційні суміші концентрували на роторному випарнику в вакуумі. Приклад 1: 2,2,2-Трифлуор-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно] циклобутил}етансульфонамід Стадія 1: Бензил [цис-3-(метиламіно)циклобутил]карбамат та бензил [транс-3(метиламіно)циклобутил]карбамат 33 % розчин метиламіну (1000 мл, 9,13 моль) в абсолютному етанолі додавали до суміші бензил(3-оксоциклобутил)карбамату (WO2012/75381 A1 та WO2012/09678 A1) (200 г, 0,913 моль) та оцтової кислоти (88 мл), що перемішується в етанолі (1000 мл) при 0 °C. Реакційна суміш перемішувалась при 0 °C протягом 1,5 годин та потім перемішувалась при кімнатній температурі протягом 2 годин. Літію боргідрид (41 г, 2,05 моль) додавали порціями до реакційної суміші при -70 °C. Після завершення додавання, реакційну суміш перемішували при 70 °C протягом 1 годин та потім давали нагрітися до кімнатної температури протягом 12 годин. Реакційну суміш гасили водою (400 мл), та концентрували в вакуумі, щоб видалити етанол. Водний шар підкислювали концентрованою гідрогенхлоридною кислотою до pH 2, промивали етилацетатом (2 × 1000 мл), підлужнювали 10 % гідроксидом натрію до pH 9-10 та потім екстрагували дихлорметаном (3 × 1000 мл). Об'єднані органічні шари промивали насиченим сольовим розчином (1000 мл), сушили над сульфатом натрію, та концентрували, одержуючи сирий продукт у вигляді світло-коричневої рідини. Продукт розчиняли в дихлорметані (400 мл) та охолоджували до 0 °C. До одержаного в результаті розчину додавали розчин 4M HCl в 23 UA 111804 C2 5 10 15 20 25 30 35 40 45 50 55 60 діоксані (300 мл). Суміш перемішували при 0 °C протягом 30 хвилин, та потім при кімнатній температурі протягом 12 годин. Реакційну суміш фільтрували та тверду речовину, що залишилась перекристалізовували з суміші метанолу та метил-трет-бутилового етеру, 1 одержуючи цис-ізомер у вигляді білої твердої речовини (111,09 г, 52 %). H ЯМР: (400 МГц, D2O): δ 7,33-7,38 (м, 5H); 5,02 (с, 2H), 3,83-3,87 (м, 1H), 3,89-3,41 (м, 1H), 2,66-2,70 (м, 2H), 2,56 (с, 3H), 2,03-2,05 (м, 2H). РХ-МС (точна маса) розраховано для C13H18N2O2; 234,137, знайдено + (M+H ); 235,1. Транс ізомер виділяли з маточного розчину, застосовуючи надкритичну рідинну хроматографію. Стадія 2: Бензил {цис-3-[(2-хлор-7H-піроло[2,3-d]піримідин-4іл)(метил)аміно]циклобутил}карбамат До розчину карбонату калію (20,47 г, 148 ммоль) у воді (180 мл) додавали бензил [цис-3(метиламіно)циклобутил]карбамат (13,57 г, 50,2 ммоль), потім 2,4-дихлор-7H-піроло(2,3d)піримідин (9,0 г, 47,9 ммоль) при кімнатній температурі. Після завершення додавання, реакційну суміш перемішували при 95 °C протягом ночі. Суміш фільтрували, щоб зібрати тверду речовину. Відфільтрований корж промивали водою та сушили в вакуумі, одержуючи бажану 1 сполуку (16,5 г, 89,7 %) у вигляді жовтої твердої речовини. H ЯМР (400 МГц, ДМСО-d6): δ 11,81 (см 1 H), 7,65 (д, 1 H), 7,38 (м, 5 H), 7,16 (м, 1 H), 6,67 (д, 1 H), 5,02 (с, 2 H), 4,81 (м, 1 H), 3,85 (м, 1 H), 3,25 (с, 3 H), 2,53 (м, 2 H), 2,25 (м, 2 H). РХ-МС (точна маса) розраховано для C19H20ClN5O2; + 385,131, знайдено (M+H ); 386,1. Стадія 3: цис-N-метил-N-7H-піроло[2,3-d]піримідин-4-ілциклобутан-1,3-діаміну гідрохлорид Суміш {цис-3-[(2-хлор-7H-піроло[2,3-d]піримідин-4-іл)(метил)аміно]циклобутил}карбамату (13,0 г, 34,0 ммоль), Pd(OH)2 (40,3 г, 40,8 ммоль) та циклогексену (72,5 мл, 0,71 моль) в етанолі (300 мл) перемішували при кип'ятінні зі зворотним холодильником протягом 3 годин. Реакційну ® суміш фільтрували через шар Celite та шар промивали метанолом. Фільтрат концентрували в 1 вакуумі, одержуючи бажану сполуку (4,8 г, 66 %) у вигляді білої твердої речовини. H ЯМР (400 МГц, ДМСО-d6): δ 11,68 (ш, 1H), 8,11 (с, 1H), 7,67 (ш, 2H), 7,17 (д, 1H), 6,65 (д, 1H), 5,08 (м, 1 H), 3,45 (м, 1H), 3,26 (с, 3H), 2,31 (м, 4H). РХ-МС (точна маса) розраховано для C11H15N5; 217,133, + знайдено (M+H ); 218,1. Стадія 4: 2,2,2-Трифлуор-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]цикло бутил}етансульфонамід До розчину цис-N-метил-N-7H-піроло[2,3-d]піримідин-4-ілциклобутан-1,3-діаміну гідрохлориду (100 мг, 0,39 ммоль) в тетрагідрофурані (0,8 мл) додавали літію біс(триметилсиліл)амід (1M розчин в тетрагідрофурані) (0,9 мл, 0,9 ммоль) та хлортриметилсилан (94 мг, 0,88 ммоль) при кімнатній температурі. Реакційну суміш перемішували протягом 45 хвилин, та потім повільно додавали 2,2,2трифлуоретансульфонілхлорид (86 мг, 0,47 ммоль). Суміш перемішували при кімнатній температурі протягом 18 годин та потім розподіляли між дихлорметаном та водою. Отримували водний шар та екстрагували двічі дихлорметаном, та об'єднані органічні шари концентрували, одержуючи сирий продукт у вигляді жовтувато-коричневої твердої речовини. Сиру речовину чистили застосовуючи хроматографію на силікагелі, елююючи сумішшю з дихлорметану та 1 метанолу (93:7), одержуючи бажану сполуку у вигляді білої твердої речовини (93 мг, 65 %). H ЯМР (400 МГц, ДМСО-d6): δ 11,61 (шс, 1 H), 8,20 (д, 1 H), 8,08 (с, 1 H), 7,13 (д, 1 H), 6,60 (д, 1 H), 4,80-4,94 (м, 1 H), 4,34 (кв, 2 H), 3,58-3,71 (м, 1 H), 3,23 (с, 3 H), 2,55-2,67 (м, 2 H), 2,17-2,30 (м, 2 + H). РХ-МС (точна маса) розраховано для C13H16F3N5O2S; 363,098, знайдено (M+H ); 363,9. Наступні сполуки, приклади 2-7, одержували з цис-N-метил-N-7H-піроло[2,3-d] піримідин-4ілциклобутан-1,3-діаміну гідрохлориду (приклад 1, стадія 3) за аналогічним способом до того, який описано в прикладі 1, стадія 4, замінюючи зазначений сульфонілхлорид на 2,2,2трифлуоретансульфонілхлорид. Приклад 2: N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}пропан-1сульфонамід Дану сполуку одержували, застосовуючи 1-пропансульфонілхлорид. Сиру сполуку чистили, застосовуючи хроматографію на силікагелі, елююючи сумішшю з дихлорметану та метанолу (93:7), одержуючи бажану сполуку у вигляді жовтувато-коричневої твердої речовини (78 % 1 вихід). H ЯМР (400 МГц, ДМСО-d6): δ 11,60 (шс, 1 H), 8,08 (с, 1 H), 7,46 (д, 1 H), 7,12 (д, 1 H), 6,61 (д, 1 H), 4,81-4,94 (м, 1 H), 3,47-3,62 (м, 1 H), 3,23 (с, 3 H), 2,87-2,96 (м, 2 H), 2,52-2,63 (м, 2 H), 2,14-2,27 (м, 2 H) 1,60-1,73 (м, 2 H) 0,96 (т, 3 H). РХ-МС (точна маса) розраховано для + C14H21N5O2S; 323,142, знайдено (M+H ); 324,1. Приклад 3: 2-Метил-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4іл)аміно]циклобутил}пропан-1-сульфонамід 24 UA 111804 C2 5 10 15 20 25 30 35 40 45 50 55 60 Дану сполуку одержували, застосовуючи 2-метил-1-пропансульфонілхлорид. Сиру сполуку чистили, застосовуючи хроматографію на силікагелі, елююючи сумішшю з дихлорметану та 1 метанолу (93:7), одержуючи бажану сполуку у вигляді білої твердої речовини (52 %). H ЯМР (400 МГц, ДМСО-d6): δ 11,64 (шс, 1 H), 8,12 (с, 1 H), 7,51 (д, 1 H), 7,03-7,26 (м, 1 H), 6,65 (д, 1 H), 4,82-5,02 (м, 1 H), 3,52-3,70 (м, 1 H), 3,26 (с, 3 H), 2,87 (д, 2 H), 2,55-2,67 (м, 2 H), 2,18-2,30 (м, 2 H), 2,11 (dt, 1 H), 1,04 (д, 6 H). РХ-МС (точна маса) розраховано для C15H23N5O2S; 337,157, + знайдено (M+H ); 338,0. Приклад 4A та Приклад 4B: цис- та транс-3-(ціанометил)-N-{цис-3-[метил(7H-піроло[2,3d]піримідин-4-іл)аміно]циклобутил}циклобутансульфонамід Дані сполуки одержували, застосовуючи суміш (~1:1) циста транс-3(ціанометил)циклобутансульфонілхлориду. Сиру суміш з цис- та транс- ізомерів чистили, застосовуючи хроматографію на силікагелі, елююючи градієнтом дихлорметану та метанолу (від 100:0 до 10:1), одержуючи суміш (420 мг) з названих сполук у вигляді білої твердої речовини (67 %). Цис- та транс- ізомери розділяли, застосовуючи надкритичну рідинну хроматографію. 1 цис-ізомер 4A: 160 мг (21 %). H ЯМР (400 МГц, метанол-d4): δ 8,12 (с, 1H), 7,13-7,12 (д, 1H), 6,69-6,69 (д, 1 H), 4,92-4,89 (м, 1 H), 3,84-3,78 (м, 1 H), 3,76-3,67 (м, 1 H), 3,36 (с, 3 H), 2,79-2,73 (м, 2 H), 2,65-2,64 (м, 3H), 2,58-2,52 (м, 2 H), 2,32-2,19 (м, 4 H). РХ-МС (точна маса) розраховано + для C17H22N6O2S; 374,152, знайдено (M+H ); 375,3. 1 транс-ізомер 4B: 155 мг (20 %). H ЯМР (400 МГц, метанол-d4): δ 8,13 (с, 1H), 7,13 (д, 1H), 6,70 (д, 1H), 4,94-4,89 (м, 1H), 3,89-3,85 (м, 1H), 3,72-3,69 (м, 1H), 3,36 (с, 3H), 2,85-2,62 (м, 7H), + 2,31-2,23 (м, 4H). РХ-МС (точна маса) розраховано для C17H22N6O2S; 374,152, знайдено (M+H ); 374,9. Суміш цис- та транс-3-(ціанометил)циклобутансульфонілхлоридів одержували наступним чином: Стадія 1: [3-(Бензилокси)циклобутиліден]ацетонітрил До охолодженої суспензії гідриду натрію (125 мг, 3,12 ммоль) в тетрагідрофурані (12 мл) при 0 °C додавали діетилціанометилфосфонат (1,21 г, 3,40 ммоль). Суміш перемішували при кімнатній температурі протягом 1 годин перед додаванням розчину 3(бензилокси)циклобутанону (500 мг, 2,84 ммоль) в тетрагідрофурані (8 мл). Суміш перемішували при кімнатній температурі протягом ночі, та потім гасили водою. Суміш екстрагували етилацетатом (3 × 25мл), та об'єднані органічні шари сушили над сульфатом натрію та концентрували. Залишок хроматографували на силікагелі, елююючи градієнтом петролейного етеру та етилацетату (від 100:0 до 85:15), одержуючи бажану сполуку (450 мг, 80 %) у вигляді жовтої олії. Стадія 2: [3-(Бензилокси)циклобутил]ацетонітрил Суміш [3-(бензилокси)циклобутиліден]ацетонітрилу (10,2 г, 51 ммоль) та 10 % Pd/C (2,0 г) в сухому тетрагідрофурані піддавали дії водню під підвищеним тиском до 50 фунтів на квадратний дюйм та перемішувалась при кімнатній температурі протягом 3 днів. Суміш потім фільтрували та концентрували в вакуумі. Залишок хроматографували на силікагелі, елююючи градієнтом петролейного етеру та етилацетат (від 100:0 до 80:20), одержуючи бажану сполуку 1 (7 г, 70 %), у вигляді безбарвної олії. H ЯМР (400 МГц, CDCl3): δ 7,36-7,28 (м, 5 H), 4,44-4,43 (м, 2 H), 4,30-4,09 (м, 1H), 3,98-3,95 (м, 1 H), 2,64-2,45 (м, 4 H), 1,81-1,759 (м, 2 H). Стадія 3: (3-Гідроксициклобутил)ацетонітрил До розчину [3-(бензилокси)циклобутил]ацетонітрилу (1 г, 5,00 ммоль) в ацетонітрилі (15 мл) по краплям додавали йодтриметилсилан (1,5 г, 7,50 ммоль) при 0 °C. Суміш перемішували при кімнатній температурі протягом ночі. Суміш гасили триетиламіном, концентрували та потім чистили, застосовуючи хроматографію на силікагелі, елююючи градієнтом петролейного етеру та етилацетату (від 1:0 до 1:1), одержуючи бажану сполуку (340 мг, 62 %) у вигляді жовтої олії. 1 H ЯМР (400 МГц, CDCl3): δ 4,55-4,15 (м, 1H), 2,49-2,46 (м, 2H), 2,25-2,21 (м, 2H), 2,14-2,08 (м, 1H), 1,79-1,72 (м, 2H). Стадія 4: 3-(Ціанометил)циклобутил-4-метилбензолсульфонат До розчину (3-гідроксициклобутил)ацетонітрилу (333 мг, 3,0 ммоль) в сухому дихлорметані (25 мл) додавали 4-диметиламінопіридин (732 мг, 6,0 ммоль). Суміш перемішувалась при кімнатній температурі протягом 5 хвилин, та потім додавали п-толуолсульфонілхлорид (859 мг, 4,5 ммоль). Одержану в результаті суміш перемішували при кімнатній температурі протягом ночі. Суміш промивали водою (2 × 15мл). Органічний шар сушили над сульфатом натрію та концентрували. Залишок чистили, застосовуючи хроматографію на силікагелі, елююючи градієнтом петролейного етеру та етилацетату (від 10:0 до 7:3), одержуючи бажану сполуку (520 мг, 65 % вихід) у вигляді безбарвної олії. 25 UA 111804 C2 5 10 15 20 25 30 35 40 45 50 55 60 Стадія 5: S-[3-(Ціанометил)циклобутил]етантіоат Суміш 3-(ціанометил)циклобутил 4-метилбензолсульфонату (1,5 г, 5,7 ммоль) та калію тіоацетату (1,29 г, 3,00 ммоль) в N, N-диметилформаміді (8 мл) нагрівали при 80 °C протягом ночі. Суміш розбавляли етилацетатом (15 мл), промивали водою (30 мл) та насиченим сольовим розчином (2 × 30 мл), сушили над сульфатом натрію та концентрували. Залишок чистили, застосовуючи препаративну тонкошарову хроматографію, елююючи сумішшю петролейного етеру та етилацетату (3:1), одержуючи бажану сполуку (750 мг, 78 %) у вигляді 1 безбарвної олії. H ЯМР (400 МГц, CDCl3): δ 4,12-3,92 (м, 1 H), 2,86-2,77 (м, 2 H), 2,71-2,47 (м, 2 H), 2,42-2,37 (м, 2 H), 2,30-2,29 (м, 3 H), 1,97-1,90 (м, 1 H). Стадія 6: 3-(Ціанометил)циклобутансульфонілхлорид Суміш N-хлорсукциніміду (1,6 г, 12,0 ммоль) в концентрованій HCl (3 мл) та ацетонітрилі (12 мл) перемішували при кімнатній температурі протягом 10 хвилин. S-[3(ціанометил)циклобутил]етантіоат (507 мг, 3,0 ммоль) в ацетонітрилі (3 мл) додавали при 0 °C та перемішували протягом 10 хвилин. Суміш розбавляли водним розчином бікарбонату натрію (50 мл), та екстрагували метил-трет-бутиловим етером (3 × 50 мл). Об'єднані органічні шари сушили над безводним сульфатом натрію та концентрували. Сирий продукт чистили, застосовуючи хроматографію на силікагелі, елююючи сумішшю петролейного етеру та етилацетату (від 100:0 до 50:50), одержуючи бажану сполуку (400 мг, 69 %) у вигляді жовтої олії. 1 H ЯМР (400 МГц, CDCl3): δ 4,45-4,40 (м, 1H), 3,06-2,71 (м, 3H), 2,61-2,49 (м, 4H). Приклад 5: 1-[3-(Ціанометил)оксетан-3-іл]-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4іл)аміно]циклобутил}метансульфонамід Дану сполуку одержували з [3-(ціанометил)оксетан-3-іл]метансульфонілхлориду. Сиру сполуку чистили, застосовуючи препаративну тонкошарову хроматографію, елююючи 1 етилацетатом, одержуючи бажану сполуку у вигляді білої твердої речовини (32 %). H ЯМР (400 МГц, метанол-d4): δ 8,13 (с, 1 H), 7,14-7,13 (м, 1 H), 6,71-6,70 (м, 1 H), 5,06-5,05 (м, 1 H), 4,854,81 (м, 2 H), 4,52-4,50 (м, 2 H), 3,77-3,75 (м, 1 H), 3,63 (м, 2 H), 3,39 (с, 3 H), 3,29-3,26 (м, 2 H), 2,85-2,78 (м, 2 H), 2,38-2,30 (м, 2 H). РХ-МС (точна маса) розраховано для C17H22N6O3S; 390,147, + знайдено (M+H ); 391,0. [3-(Ціанометил)оксетан-3-іл]метансульфонілхлорид Стадія 1: [3-(Ціанометил)оксетан-3-іл]метил 4-метилбензолсульфонат Дану сполуку одержували за способом з прикладу 4 стадія 4, замінюючи [3-(гідроксиметил)3-оксетаніл]ацетонітрил на (3-гідроксициклобутил)ацетонітрил. Сиру сполуку чистили, застосовуючи хроматографію на силікагелі, елююючи сумішшю петролейного етеру та етилацетату (від 1:0 до 1:1), одержуючи бажану сполуку у вигляді білої твердої речовини (10 %). 1 H ЯМР (400 МГц, CDCl3): δ 7,82-7,80 (м, 2 H), 7,41-7,39 (м, 2 H), 4,54-4,35 (м, 4 H), 4,31 (с, 2 H), 2,79 (с, 2 H), 2,45 (с, 3H). Стадія 2: [3-(Ціанометил)оксетан-3-іл]метил тіоціанат Розчин [3-(ціанометил)оксетан-3-іл]метил 4-метилбензолсульфонату (150 мг, 0,53 ммоль) та калію тіоціанату (104 мг, 1,07 ммоль) перемішували в етанолі (10 мл). Реакційну суміш нагрівали до 85 °C та перемішували протягом 16 годин. Розчинник випаровували, одержуючи сиру бажану сполуку у вигляді білої твердої речовини. Стадія 3: [3-(Ціанометил)оксетан-3-іл]метансульфонілхлорид Газоподібний хлор барботували через розчин [3-(ціанометил)оксетан-3-іл]метил тіоціанату (0,53 ммоль, сирий) у воді (10 мл) при 0 °C протягом 30 хвилин. Реакційну суміш екстрагували метил-трет-бутиловим етером (2 × 20 мл). Об'єднані органічні шари сушили над сульфатом натрію та концентрували, одержуючи бажану сполуку (20 мг, 18 %). Приклад 6: N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4-іл)аміно]циклобутил}-1-оксетан-3ілметансульфонамід Дану сполуку одержували, застосовуючи оксетан-3-ілметансульфонілхлорид. Сиру сполуку чистили, застосовуючи хроматографію на силікагелі, елююючи сумішшю дихлорметану та 1 метанолу (85:15), одержуючи бажану сполуку у вигляді білої твердої речовини (23 %). H ЯМР (400 МГц, метанол-d4): δ 8,13 (м, 1 H), 7,13 (д, J=4Гц, 1 H), 6,70-6,69 (м, J=4Гц, 1 H), 4,93-4,91 (м, 1 H), 4,84-4,83 (м, 2 H), 4,63-4,59 (м, 2 H), 3,74-3,68 (м, 1 H), 3,58-3,56 (м, 1 H), 3,47-3,45 (м, 2 H), 3,37 (с, 3 H), 2,79-2,77 (м, 2 H), 2,32-2,29 (м, 2 H). РХ-МС (точна маса) розраховано для + C15H21N5O3S; 351,136, знайдено (M+H ); 352,1. Оксетан-3-ілметансульфонілхлорид Стадія 1: Оксетан-3-ілметилтіоціанат Дану сполуку одержували відповідно до способу з прикладу 5, стадія 2, замінюючи оксетан3-ілметил 4-метилбензолсульфонат (WO2012/117000A1) на [3-(ціанометил)оксетан-3-іл]метил 4-метилбензолсульфонат, одержуючи сиру бажану сполуку у вигляді білої твердої речовини. 26 UA 111804 C2 5 10 15 20 25 30 35 40 45 50 55 60 (100 %). Стадія 2: Оксетан-3-ілметансульфонілхлорид Дану сполуку одержували в сирій формі (25 % вихід) за способом з прикладу 5 стадія 3, замінюючи оксетан-3-ілметилтіоціанат на [3-(ціанометил)оксетан-3-іл]метилтіоціанат. Приклад 7A та 7B: цис- та транс-3-(ціанометил)-3-метил-N-{цис-3-[метил(7H-піроло[2,3d]піримідин-4-іл)аміно]циклобутил}циклобутансульфонамід Дані сполуки одержували, застосовуючи суміш (~1:1) з цис- та транс-3-(ціанометил)-3метилциклобутансульфонілхлориду. Сиру суміш цис- та транс-ізомерів чистили, застосовуючи хроматографію на силікагелі, елююючи градієнтом петролейний етер:етилацетат (від 10:1 до 1:15), одержуючи суміш (70 мг) названих сполук у вигляді світло-коричневої твердої речовини (28 %). цис- та транс- ізомери потім розділяли, застосовуючи надкритичну рідинну хроматографію (SFC). 1 Цис-ізомер (7A): 26 мг (10 %); SFC час утримання = 7,11 хвилин; H ЯМР (400 МГц, метанолd4): δ 8,13 (с, 1 H), 7,13-7,13 (д, 1 H), 6,69 (д, 1 H), 4,93-4,86 (м, 1 H), 3,91-3,87 (м, 1 H), 3,71-3,65 (м, 1 H), 3,37-3,33 (м, 3 H), 2,77-2,75 (м, 2 H), 2,68 (с, 2 H), 2,41-2,36 (м, 2 H), 2,26-2,21 (м, 2 H), + 1,34 (м, 3 H). РХ-МС (точна маса) розраховано для C18H24N6O2S; 388,168, знайдено (M+H ); 389,1. 1 Транс-ізомер (7B) 24 мг (10 %); SFC час утримання = 11,35 хвилин; H ЯМР (400 МГц, метанол-d4): δ 8,13 (с, 1 H), 7,14 (д, 1 H), 6,69 (д, 1 H), 4,93-4,86 (м, 1 H), 3,96-3,86 (м, 1 H), 3,723,65 (м, 1 H), 3,36-3,31 (м, 3 H), 2,77-2,75 (м, 2 H), 2,71 (с, 2 H), 2,34-2,26 (м, 6 H), 1,33 (м, 3 H). + РХ-МС (точна маса) розраховано для C18H24N6O2S; 388,168, знайдено (M+H ); 389,0. Суміш цис- та транс-3-(ціанометил)-3-метилциклобутансульфонілхлоридів одержували наступним чином: Стадія 1: 1-Метил-3-метиленциклобутанкарбонітрил До розчину 3-метиленциклобутанкарбонітрил (35,0 г, 373,0 ммоль) в тетрагідрофурані (200 мл) додавали по краплям літію біс(триметилсиліл)амід (450 мл, 1M) при -78 °C. Розчин перемішували протягом 1 годин при -78 °C та до реакційної суміші додавали йодметан (30 мл, 448 ммоль). Через 1 годину, суміш нагрівали до кімнатної температури та перемішували протягом ночі. Реакційну суміш гасили водним розчином амонію хлориду (380 мл) та екстрагували метил-трет-бутиловим етером (3 × 400 мл). Об'єднані органічні шари сушили над сульфатом натрію та концентрували. Сирий продукт чистили шляхом дистиляції при зниженому 1 тиску, одержуючи бажану сполуку (20 г, 50 %) у вигляді прозорої олії. H ЯМР (400 МГц, CDCl3): δ 4,90-4,89 (м, 2 H), 3,24-3,20 (м, 2 H), 2,67-2,62 (м, 2 H), 1,50 (с, 3H). Стадія 2: 1-Метил-3-метиленциклобутанкарбонова кислота До розчину 1-метил-3-метиленциклобутанкарбонітрилу (10,0 г, 93,3 ммоль) у воді (50 мл) та етанолі (50 мл) додавали гідроксид калію (25,6 г, 466,6 ммоль). Реакційну суміш нагрівали та кип'ятили зі зворотним холодильником, та перемішували протягом ночі. Етанол видаляли при зниженому тиску, та розчин охолоджували до нижче 10 °C, підкислювали концентрованою гідрогенхлоридною кислотою до pH 1. Водну фазу екстрагували етилацетатом (3 × 150 мл). Об'єднані органічні шари сушили над сульфатом натрію та концентрували, одержуючи бажану 1 сполуку (9 г, 77 %). H ЯМР (400 МГц, CDCl3): δ 11,90 (с, 1 H), 4,88-4,85 (м, 2 H), 3,23-3,17 (м, 2 H), 2,53-2,41 (м, 2 H), 1,45 (с, 3 H). Стадія 3: Етил 1-метил-3-метиленциклобутанкарбоксилат До розчину 1-метил-3-метиленциклобутанкарбонової кислоти (6 г, 47,6 ммоль) в дихлорметані (30 мл) при 0 °C додавали по краплям тіонілхлорид (11,0 мл, 143 ммоль). Розчин перемішували при 0 °C протягом 1 годин. До розчину додавали три краплі N, Nдиметилформаміду. Розчин перемішували при 0 °C протягом 30 хвилин. Розчинник випаровували, та до залишку додавали дихлорметан (20 мл) та етанол (125 мл). Одержаний в результаті розчин перемішували протягом 16 годин при кімнатній температурі. Розчинник випаровували та до залишку додавали воду (20 мл). Водний шар екстрагували дихлорметаном (4 × 20 мл). Об'єднані органічні шари сушили над сульфатом натрію та концентрували. Сирий продукт чистили, застосовуючи хроматографію на силікагелі, елююючи градієнтом 1 петролейного етеру та етилацетату (від 20:1 до 10:1), одержуючи бажану сполуку (5 г, 68 %). H ЯМР (400 МГц, CDCl3): δ 4,85-4,83 (м, 2 H), 4,17-4,12 (м, 2 H), 3,18-3,12 (м, 2 H), 2,48-2,42 (м, 2H), 1,41 (с, 3 H), 1,27-1,23 (м, 3 H). Стадія 4: (1-Метил-3-метиленциклобутил)метанол Суміш етил 1-метил-3-метиленциклобутанкарбоксилату (4,55 г, 29,5 ммоль), літійалюмогідриду (2,8 г, 72 ммоль) в тетрагідрофурані (50 мл) перемішували протягом ночі при кімнатній температурі. До реакційної суміші додавали Na2SO4·10H2O (3,7 г, 11,5 ммоль), та одержану в результаті суміш перемішували протягом 1 годин при кімнатній температурі. Тверді 27 UA 111804 C2 5 10 15 20 25 30 35 40 45 50 55 60 речовини видаляли фільтрацією, та фільтрат концентрували в вакуумі. Залишок екстрагували дихлорметаном (3 × 50 мл). Об'єднані органічні екстракти сушили над сульфатом натрію та 1 концентрували, одержуючи бажану сполуку (2,6 г, 79 %) у вигляді безбарвної олії. H ЯМР (400 МГц, CDCl3): δ 4,79-4,78 (м, 2 H), 3,48 (с, 2 H), 2,53-2,48 (м, 2 H), 2,36-2,27 (м, 2 H), 1,16 (с, 3 H). Стадія 5: (1-Метил-3-метиленциклобутил)метил 4-метилбензолсульфонат Дану сполуку одержували за прикладом 4, стадія 4, замінюючи (1-метил-3метиленциклобутил)метанол на (3-гідроксициклобутил)ацетонітрил. Сиру сполуку чистили, застосовуючи хроматографію на силікагелі, елююючи градієнтом петролейного етеру та 1 етилацетату (від 20:1 до 4:1), одержуючи бажану сполуку (70 %). H ЯМР (400 МГц, CDCl3): δ 7,79 (д, 2 H), 7,34 (д, 2 H), 4,79-4,78 (м, 2 H), 3,90 (с, 2 H), 2,51-2,47 (м, 2 H), 2,44 (с, 3 H), 2,352,31 (м, 2 H), 1,15 (с, 3 H). Стадія 6: (1-Метил-3-метиленциклобутил)ацетонітрил Суміш (1-метил-3-метиленциклобутил)метил 4-метилбензолсульфонату (2,5 г, 9,4 ммоль), калію ціаніду (1,3 г, 19 ммоль) та N, N-диметилформаміду (8мл) перемішували протягом ночі при 70 °C. Воду (10 мл) та метил-трет-бутиловий етер (20 мл) додавали до суміші, та органічний шар відокремлювали. Водну фазу екстрагували метил-трет-бутиловим етером (3 × 30 мл). Об'єднані органічні шари промивали водним насиченим розчином бікарбонату натрію (15 мл), сушили над сульфатом натрію, та концентрували. Сирий продукт чистили, застосовуючи хроматографію на силікагелі, елююючи градієнтом петролейного етеру та етилацетату (від 10:1 1 до 5:1), одержуючи бажану сполуку (1,1 г, 97 %) у вигляді світло-коричневої олії. H ЯМР (400 МГц, CDCl3): δ 4,88-4,87 (м, 2 H), 2,62-2,54 (м, 2 H), 2,50 (с, 2 H), 1,33 (с, 3 H). Стадія 7: (1-Метил-3-оксоциклобутил)ацетонітрил Газоподібний озон барботували через розчин (1-метил-3-метиленциклобутил)аце-тонітрилу (1,08 г, 8,91 ммоль) в дихлорметані (30 мл) -78 °C протягом 10 хвилин. Після продувки розчину газоподібним азотом, до розчину по краплям додавали диметилсульфід (10 мл) при -78 °C. Розчин перемішували протягом 30 хвилин при -78 °C, та розчинник видаляли при зниженому тиску. Сирий продукт чистили, застосовуючи хроматографію на силікагелі, елююючи градієнтом петролейного етеру та етилацетату (від 20:1 до 8:1), одержуючи бажану сполуку (920 мг, 84 %) 1 у вигляді безбарвної олії. H ЯМР (400 МГц, CDCl3): δ 3,11-3,06 (м, 2 H), 2,96-2,91 (м, 2 H), 2,69 (с, 2 H), 1,53 (с, 3 H). Стадія 8: (3-Гідрокси-1-метилциклобутил)ацетонітрил До розчину (1-метил-3-оксоциклобутил)ацетонітрилу (400 мг, 3,25 ммоль) в тетрагідрофурані (15 мл) додавали боргідрид натрію (246 мг, 6,5 ммоль). Суміш перемішували протягом 3 годин при кімнатній температурі. Додавали ацетон (2 мл), та потім розчинник випаровували. До залишку додавали воду (10 мл), та водну фазу екстрагували дихлорметаном (4 × 15 мл). Об'єднані органічні шари сушили над сульфатом натрію та концентрували. Сирий продукт чистили, застосовуючи хроматографію на силікагелі, елююючи градієнтом петролейного етеру та етилацетату (від 10:1 до 1:1), одержуючи бажану сполуку (300 мг, 74 %) 1 у вигляді безбарвної олії. H ЯМР (400 МГц, CDCl3): δ 4,38-4,34 (м, 2 H), 2,46-2,27 (м, 4 H), 1,941,86 (м, 2 H), 1,33-1,12 (м, 3 H). Стадія 9: 3-(Ціанометил)-3-метилциклобутил 4-метилбензолсульфонат Дану сполуку одержували за прикладом 7, стадія 5, замінюючи (3-гідрокси-1метилциклобутил)ацетонітрил на (1-метил-3-метиленцикло-бутил)метанол. Сиру сполуку чистили, застосовуючи хроматографію на силікагелі, елююючи градієнтом петролейного етеру 1 та етилацетату (від 20:1 до 4:1), одержуючи бажану сполуку (36 %). H ЯМР (400 МГц, CDCl3): δ 7,77 (д, 2 H), 7,35 (д, 2 H), 4,89-4,81 (м, 1 H), 2,45 (с, 3 H), 2,43-2,34 (м, 3 H), 2,26-2,21 (м, 1 H), 2,15-2,11 (м, 2 H), 1,33 (с, 3 H). Стадія 10: S-[3-(Ціанометил)-3-метилциклобутил]етантіоат Дану сполуку одержували з 89 % виходом (сиру) за способом з прикладу 4, стадія 5, замінюючи 3-(ціанометил)-3-метилциклобутил 4-метилбензолсульфонат на 31 (ціанометил)циклобутил-4-метилбензолсульфонату. H ЯМР (400 МГц, CDCl3): δ 3,12 (с, 1 H), 2,46-2,30 (м, 4 H), 2,19 (с, 2 H), 1,29 (с, 1 H) 1,26-1,24 (м, 1 H), 1,18-1,14 (м, 1 H), 1,13 (с, 3H). Стадія 11: 3-(Ціанометил)-3-метилциклобутансульфонілхлорид Дану сполуку одержували за прикладом 4 стадія 6, замінюючи S-[3-(ціанометил)-3метилциклобутил]етантіоат на S-[3-(ціанометил)циклобутил]етантіоат. Сиру сполуку чистили, застосовуючи хроматографію на силікагелі, елююючи градієнтом петролейного етеру та 1 етилацетату (від 90:10 до 30:70), одержуючи бажану сполуку у вигляді жовтої рідини (66 %). H ЯМР (400 МГц, CDCl3): δ 4,45-4,38 (м, 1 H), 2,67-2,55 (м, 4 H), 2,46-2,40 (м, 2 H), 1,42-1,40 (м, 3 H). Приклад 8: 4-Ціано-N-{цис-3-[метил(7H-піроло[2,3-d]піримідин-4 28
ДивитисяДодаткова інформація
Назва патенту англійськоюPyrrolo [2,3-d]pyrimidine derivatives as inhibitors of janus- related kinases (jak)
Автори англійськоюBrown, Matthew Frank, Fenwick, Ashley Edward, Flanagan, Mark Edward, Gonzales, Andrea, Johnson, Timothy Allan, Kaila, Neelu, Mitton-Fry, Mark J., Strohbach, Joseph Walter, Tenbrink, Ruth E., Trzupek, John David, Unwalla, Rayomand Jal, Vazquez, Michael L., Parikh, Mihir D.
Автори російськоюБраун Метью Фрэнк, Фенвик Элши Эдвард, Флэнаган Марк Эдвард, Гонзалез Андреа, Джонсон Тимоти Эллан, Кайла Нилу, Миттон-Фрай Марк Дж., Стробэч Джозеф Волтер, Тэнбринк Рут Э., Трзупек Джон Дэйвид, Унвалла Рэёманд Джал, Вазкез Майкл Л., Парих Михир Д.
МПК / Мітки
МПК: A61P 37/00, C07D 487/04, C07D 519/00, A61K 31/519
Мітки: янус-залежних, jak, кіназ, похідні, інгібітори, піроло[2.3-d]піримідину
Код посилання
<a href="https://ua.patents.su/60-111804-pokhidni-pirolo23-dpirimidinu-yak-ingibitori-yanus-zalezhnikh-kinaz-jak.html" target="_blank" rel="follow" title="База патентів України">Похідні піроло[2,3-d]піримідину як інгібітори янус-залежних кіназ (jak)</a>
Попередній патент: Підлогова панель для зовнішнього застосування
Наступний патент: Пристрій та спосіб нарізання за заданими розмірами відрізків полотна крейдованого декоративного паперу та застосування пристрою
Випадковий патент: Спосіб одержання prrsv у комерційному масштабі












