Піролтриазинанілінові сполуки, корисні як інгібітори кінази
Номер патенту: 78562
Опубліковано: 10.04.2007
Автори: Хайнес Джон, Лефтеріс Катерін, Дикман Аларік, Вроблескі Стівен Т., Ліу Чуньян
Формула / Реферат
1. Сполука за формулою (І)
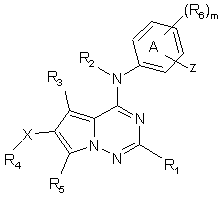 (I)
(I)
її енантіомери, діастереомери, солі і сольвати, де:
Х вибирають з -O-, -ОС(=O)-, -S-, -S(=O)-, -SO2-, -C(=O)-, -CO2-, -NR8-, -NR8C(=O)-, -NR8C(=O)NR9-, -NR8CO2-, -NR8SO2-, -NR8SO2NR9-, -SO2NR8-, -C(=O)NR8-, галогену, нітро і ціано або Х є відсутнім;
Z являє собою -C(=O)NR10-Bb, -(CH2)-C(=O)NR10-Bc, -NR10aC(=O)-Ba, -(CH2)-NR10aC(=O)-Bc, -NR10a(=O)NR10-B, -NR10SO2-B, -SO2NR10-B, -C(=O)-Ba, -CO2-Bе, -OC(=O)-Ba, -C(=O)NR10-NR10a-Bd, -NR10CO2-Ba або -C(=O)NR10-(CH2)C(=O)Ba;
В являє собою:
а) необов’язково заміщений циклоалкіл, необов’язково заміщений гетероцикл або необов’язково заміщений гетероарил; або
(b) арил, заміщений одним R11 і від нуля до двох R12;
Вa являє собою, необов’язково заміщений алкіл, необов’язково заміщений циклоалкіл, необов’язково заміщений гетероцикл, необов’язково заміщений арил або необов’язково заміщений гетероарил;
Вb являє собою
(a) необов’язково заміщений циклоалкіл, необов’язково заміщений гетероцикл або необов’язково заміщений гетероарил;
(b) арил, заміщений одним R11 і від нуля до двох R12; або
(c) -C(=O)R13, -CO2R13, -C(=O)NR13R13a;
Вc являє собою, необов’язково заміщений алкіл, необов’язково заміщений алкокси, необов’язково заміщений циклоалкіл, необов’язково заміщений гетероцикл, необов’язково заміщений арил або необов’язково заміщений гетероарил;
Вd являє собою водень, -C(=О)R13 або –CO2R13;
Вe являє собою водень, необов’язково заміщений алкіл, необов’язково заміщений циклоалкіл, необов’язково заміщений гетероцикл, необов’язково заміщений арил або необов’язково заміщений гетероарил;
R1 і R5 вибрані незалежно один від одного з водню, алкілу, заміщеного алкілу, -OR14, -SR14, -OC(=O)R14, -CO2R14, -C(=O)NR14R14a, -NR14R14a, -S(o)R14, -SO2R14, -SO2NR14R14a, -NR14SO2NR14aR14b, -NR14aSO2R14, -NR14C(=O)R14a, -NR14CO2R14a, -NR14C(=O)NR14aR14b, галогену, нітро і ціано;
R2 являє собою водень або С1-4алкіл;
R3 являє собою водень, метил, перфторметил, метокси, галоген, ціано, NH2 або NН(СН3);
R4 вибраний з:
a) водню, за умови, що R4 не є воднем, якщо Х являє собою -S(=O)-, -SO2-, -NR8CO2- або –NR8SO2-;
b) алкілу, алкенілу й алкінілу, необов’язково незалежно заміщених групою кето і/або від одного до чотирьох R17;
c) арилу і гетероарилу, кожний із який може бути необов’язково незалежно заміщений від одного до трьох R16; і
d) гетероциклу і циклоалкілу, кожний із який може бути необов’язково незалежно заміщений кетогрупою і/або від одного до трьох R16; або
e) R4 є відсутнім, якщо Х являє собою галоген, нітро або ціано;
R6 приєднаний до будь-якого доступного атома вуглецю фенільного кільця А, і в усіх випадках є незалежно вибраним з алкілу, галогену, трифторметокси, трифторметилу, гідрокси, алкокси, алканоїлу, алканоїлокси, тіолу, алкілтіо, уреїд, нітро, ціано, карбокси, карбоксіалкілу, карбамоїлу, алкоксикарбонілу, алкілтіоно, арилтіоно, арилсульфоніламіну, алкілсульфоніламіну, сульфонової кислоти, алкілсульфонілу, сульфонамідогрупи, фенілу, бензилу, арилокси, бензилокси, де кожна група R6, у свою чергу, може бути заміщена від одного до двох R18;
R8 і R9 вибрані незалежно один від одного з водню, алкілу, заміщеного алкілу, арилу, циклоалкілу, гетероциклу і гетероарилу;
R10 і R10a вибрані незалежно один від одного з водню, алкілу, заміщеного алкілу, алкокси й арилу;
R11 вибраний з:
(a) алкілу, галогеналкілу, алкокси, галогеналкокси, -SO2алкілу, циклоалкілу, гетероциклу і гетероарилу, із котрих будь-який може бути необов’язково заміщеним; або
(b) галогену, ціано, аміно, алкіламіно і діалкіламіно;
R12 вибраний з алкілу, R17 і С1-4алкілу, заміщеного кетогрупою (=O) і/або від одного до трьох R17;
R13 і R13a вибрані незалежно один від одного з водню, необов’язково заміщеного алкілу, необов’язково заміщеного циклоалкілу і необов’язково заміщеного арилу;
R14, R14a і R14b вибрані незалежно один від одного з водню, алкілу, заміщеного алкілу, арилу, циклоалкілу, гетероциклу і гетероарилу, за винятком тих випадків, коли R14 з’єднаний із сульфонільною групою, як у -S(=O)R14, -SO2R14 і –NR14aSO2R14, тоді R14 не є воднем;
R16 вибраний з алкілу, R17 і С1-4алкілу, заміщеного кетогрупою (=O) і/або від одного до трьох R17;
R17 вибраний з:
(a) галогену, галогеналкілу, галогеналкокси, нітро, ціано, -SR23, -OR23, -NR23R24, -NR23SO2R25, -SO2R25, -SO2NR23R24, -СО2R23, -C(=O)R23, -C(=O)NR23R24, -OC(=O)R23, -OC(=O)NR23R24, -NR23C(=O)R24, -NR23CO2R24;
(b) арилу або гетероарилу, кожний із який може бути необов’язково заміщений від одного до трьох R26; або
(c) циклоалкілу чи гетероциклу, необов’язково заміщеного кетогрупою (=O) і/або від одного до трьох R26;
R18 і R26 вибрані незалежно один від одного з С1-6алкілу, С2-6алкенілу, галогену, галогеналкілу, галогеналкокси, ціано, нітро, аміно, С1-4алкіламіно, аміноС1-4алкілу, гідрокси, гідроксіС1-4алкілу, алкокси, С1-4алкілтіо, арилу, гетероциклу, (арил)алкілу, арилокси і (арил)алкокси;
R23 і R24 кожний є незалежно вибраним з водню, алкілу, алкенілу, заміщеного алкілу, заміщеного алкенілу, арилу, циклоалкілу, гетероарилу і гетероциклу;
R25 вибраний з алкілу, заміщеного алкілу, арилу, гетероарилу, циклоалкілу і гетероцикло; і
m приймає значення 0, 1, 2 або 3.
2. Сполука за п. 1, яка має формулу (І*)
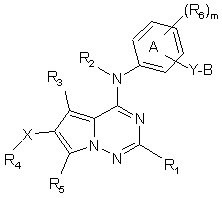 , (I*)
, (I*)
її енантіомери, діастереомери, солі і сольвати, де:
Х є вибраним з -O-, -ОС(=O)-, -S-, -S(=O)-, -SO2-, -С(=O)-, -СO2-, -NR8-, -NR8C(=O)-, -NR8C(=O)NR9-, -NR8CO2-, -NR8SO2-, -NR8SO2NR9-, -SO2NR8-, -C(=O)NR8-, галогену, нітро і ціано, або X є відсутнім;
Y являє собою –C(=O)NR10-, -NR10aC(=O)NR10-, -NR10SO2-, -SO2NR10-, -C(=O)-, -СO2- або -ОС(=O)-;
В являє собою необов’язково заміщений циклоалкіл, гетероцикл або гетероарил;
або арил, заміщений одним R11 і від нуля до двох R12; або, коли Y являє собою -C(=O)NR10-, тоді В також може бути вибраний з -С(=O)R13, -СO2R13 і -С(=O)NR13R13a;
R1 і R5 вибрані незалежно один від одного з водню, алкілу, заміщеного алкілу, -OR14, -SR14, -OC(=O)R14, -CO2R14, -C(=O)NR14R14a, -NR14R14a, -S(=O)R14, -SO2R14, -SO2NR14R14a, -NR14SO2NR14aR14b, -NR14aSO2R14, -NR14C(=O)R14a, -NR14CO2R14a, -NR14C(=O)NR14aR14b, галогену, нітро і ціано;
R2 являє собою водень або С1-4алкіл;
R3 являє собою водень, метил, перфторметил, метокси, галоген, ціано, NH2 або NН(СН3);
R4 вибраний з:
a) водню за умови, що R4 не є воднем, якщо X являє собою -S(=O)-, -SO2-, -NR8CO2- або –NR8SO2-;
b) алкілу, алкенілу й алкінілу, необов’язково заміщених групою кето і/або від одного до чотирьох R17;
c) арилу і гетероарилу, необов’язково заміщених від одного до трьох R16; і
d) гетероциклу і циклоалкілу, необов’язково заміщених групою кето і/або від одного до трьох R16; або
e) R4 є відсутнім, якщо Х є галоген, нітро або ціано;
R6 приєднаний до будь-якого доступного атома вуглецю фенільного кільця А і в усіх випадках є незалежно вибраним з алкілу, галогену, трифторметокси, трифторметилу, гідрокси, алкокси, алканоїлу, алканоїлокси, тіолу, алкілтіо, уреїдо, нітро, ціано, карбокси, карбоксіалкілу, карбамілу, алкоксикарбонілу, алкілтіоно, арилтіоно, арилсульфоніламіну, алкілсульфоніламіну, сульфонової кислоти, алкілсульфонілу, сульфонамідо, фенілу, бензилу, арилокси і бензилокси, де кожна група R6, у свою чергу, може бути заміщена одним або двома R18;
R8 і R9 вибрані незалежно один від одного з водню, алкілу, заміщеного алкілу, арилу, циклоалкілу, гетероциклу і гетероарилу;
R10 і R10a вибрані незалежно один від одного з водню, алкілу, заміщеного алкілу, алкокси й арилу;
R11 вибраний з необов’язково заміщеного циклоалкілу, гетероциклу й гетероарилу;
R12 вибраний з алкілу, R17 і С1-4алкілу, заміщеного групою кето (=O) і/або від одного до трьох R17;
R13 і R13a вибрані з водню, алкілу і заміщеного алкілу;
R14, R14a і R14b вибрані незалежно один від одного з водню, алкілу, заміщеного алкілу, арилу, циклоалкілу, гетероциклу і гетероарилу, за винятком того, що коли R14 є зв’язаний із сульфонільною групою, як у -S(=O)R14, -SO2R14 і –NR14aSO2R14, тоді R14 не є воднем;
R16 вибраний з алкілу, R17 і С1-4алкілу, заміщеного групою кето (=O) і/або від одного до трьох R17;
R17 вибраний з галогену, галогеналкілу, галогеналкокси, нітро, ціано, -SR23, -OR23, -NR23R24, -NR23SO2R25, -SO2R25, -SO2NR23R24, -CO2R23, -C(=O)R23, -C(=O)NR23R24, -OC(=O)R23, -OC(=O)NR23R24, -NR23C(=O)R24, -NR23CO2R24, арилу або гетероарилу, необов’язково заміщеного від одного до трьох R26; або циклоалкілу чи гетероциклу, необов’язково заміщеного групою кето(=O) і/або від одного до трьох R26;
R18 і R26 вибрані незалежно один від одного з С1-6алкілу, С2-6алкенілу, галогену, галогеналкілу, галогеналкокси, ціано, нітро, аміно, С1-4алкіламіно, аміно-С1-4алкілу, гідрокси, гідроксі-С1-4алкілу, алкокси, С1-4алкілтіо, фенілу, бензилу, фенілокси і бензилокси;
Р23 і R24 кожний є незалежно вибраним з водню, алкілу, алкенілу, заміщеного алкілу, заміщеного алкенілу, арилу, циклоалкілу, гетероарилу і гетероциклу;
R25 вибраний з алкілу, заміщеного алкілу, арилу, гетероарилу, циклоалкілу і гетероциклу; і
m приймає значення 0, 1, 2, 3.
3. Сполука за п. 2 або її фармацевтично прийнятна сіль, або гідрат того чи іншого, де:
В являє собою: С3-7циклоалкіл, необов’язково заміщений від одного до двох R7; п’ятичленний гетероарил, необов’язково заміщений від одного до двох R7; п’яти- або шестичленний гетероцикп, необов’язково заміщений від одного до двох R7; арил, заміщений одним R11 і від нуля до двох R12; або, коли Y являє собою -C(=O)NR10-, тоді В може також бути вибраний з -С(=O)R13 і -CO2R13 і -С(=O)NНR13R13a;
R7 приєднаний до будь-якого доступного атома вуглецю або азоту кільця В і в усіх випадках є незалежно вибраним з груп кето (=O), алкілу, заміщеного алкілу, галогену, галогеналкокси, уреїдо, ціано, -SR20, -OR20, -NR20R21, -NR20SO2R21, -SO2R19, -SO2NR20R21, -CO2R20, -C(=O)R20, -C(=O)NR20R21, -OC(=O)R20, -OC(=O)NR20R21, -NR20C(=O)R21, -NR20CO2R21, арилу, циклоалкілу, гетероциклу і гетероарилу; і/або, коли В є циклоалкіл, тоді дві групи R7 можуть об’єднуватися, утворюючи необов’язково заміщений вуглець-вуглецевий місток із трьох-чотирьох атомів вуглецю, або дві групи R7 можуть об’єднуватися, утворюючи злите карбоциклічне, гетероциклічне або гетероарильне кільце, причому зазначене злите кільце є, у свою чергу, необов’язково заміщеним одним-трьома R22;
R20 і R21 вибрані з водню, алкілу, алкенілу, заміщеного алкілу, заміщеного алкенілу, фенілу, С3-7циклоалкілу і від п’яти- до шестичленного гетероциклу або гетероарилу; і
R12 і R22 вибрані незалежно один від одного з С1-6алкілу, C2-6алкенілу, галогену, галогеналкілу, галогеналкокси, ціано, нітро, аміно, С1-4алкіламіно, аміно-С1-4алкілу, гідрокси, гідроксі-С1-4алкілу, алкокси, алкілтіо, фенілу, бензилу, фенілокси і бензилокси.
4. Сполука за п. 2, яка має формулу (Іа):
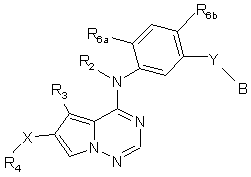 , (Ia)
, (Ia)
або її фармацевтично прийнятні сіль, проліки чи сольват, де
R3 являє собою метил, -СF3 або -ОСF3;
Х являє собою -С(=O)-, -NR8C(=O)- або -C(=O)NR8-, де R8 є водень або С1-4алкіл;
Y являє собою -C(=O)NH-, -NHC(=O)NH- або -NHSO2-;
R4 являє собою водень, С2-6алкіл, С1-4алкіл, необов’язково заміщений від одного до трьох R17, циклоалкіл чи гетероцикл, необов’язково заміщений групою кето (=O) і/або від одного до трьох R16; або гетероарил, необов’язково заміщений від одного до трьох R16;
R6a і R6b вибрані незалежно один від одного з водню, С1-6алкілу, заміщеного С1-4алкілу, галогену, трифторметокси, трифторметилу, -OR27, -С(=O)алкілу, -ОС(=O)алкілу, -NR27R28, -SR27, -NO2, -CN, -CO2R27, -CONH2, -SО3Н, -S(=O)алкілу, -S(=O)арилу, -NHSO2-арилу-R27, -SO2NHR27, -CONHR27 і -NHC(=O)NHR27;
R16 вибраний з С1-4алкілу, R17 і С1-4алкілу, заміщених кетогрупою і/або від одного до двох R17;
R17 вибраний з галогену, гідрокси, С1-4алкокси, трифторметилу, трифторметокси, ціано, нітро, фенілу, бензилу, фенілокси, бензилокси, NH2, NН(С1-4алкілу), N(С1-4алкілу)2, С3-7циклоалкілу і п’яти- або шестичленного гетероарилу чи гетероциклу; і
R27 і R28 вибрані з водню, С1-4алкілу, фенілу, С3-7циклоалкілу і від п’яти- до шестичленного гетероциклу або гетероарилу.
5. Сполука за п. 2 або її фармацевтично прийнятні сіль чи сольват, де
В є феніл, заміщений гетероциклом і від нуля до одного R12, або є циклоалкільним, гетероарильним чи гетероциклічним кільцем, вибраним з:
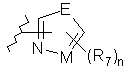 ,
, 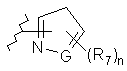 ,
, 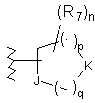 ,
,
де Е, G, J і К вибрані з О, S, NH і СН2 за умови, що коли q дорівнює 0, тоді J і К не є одночасно вибраними з О і S; а М являє собою N або СН; де будь-який атом водню в Е, G, J, К і М у разі потреби може бути заміщений групою R7;
R7 і R12 вибрані незалежно один від одного з С1-6алкілу, заміщеного С1-4алкілу, галогену, трифторметокси, трифторметилу, гідрокси, -С1-4алкокси, -С(=O)алкілу, -ОС(=O)алкілу, NH2, NH(С1-4алкілу), N(С1-4алкілу)2, -CN, -СО2алкілу, -CONH2, -СОNН(СН3)-CON(CH3)2, фенілу, бензилу, С3-7циклоалкілу і від п’яти- до шестичленного гетероциклу або гетероарилу;
n приймає значення 0, 1, 2; а
р і q вибрані з 0, 1, 2, 3 або 4 за умови, що р і q, узяті разом, не є більше 4.
6. Сполука за п. 5 або її фармацевтично прийнятні сіль чи сольват, де
Х являє собою -С(=O)-, -С(=O)NН- або -С(=O)N(С1-4алкіл)-;
Y являє собою -С(=О)NН-;
R4 являє собою водень, С2-6алкіл, С1-4алкіл, необов’язково заміщений від одного до трьох R17, арил або гетероарил, необов’язково заміщений від одного до трьох R16, або циклоалкіл чи гетероцикл, необов’язково заміщений групою кето (=O) і/або від одного до трьох R16;
R16 вибраний з С1-4алкілу, R17 і С1-4алкілу, заміщеного групою кето і/або від одного до двох R17; і
R17 вибраний з галогену, гідрокси, С1-4алкокси, трифторметилу, трифторметокси, ціано, нітро, фенілу, бензилу, фенілокси, бензилокси, NH2, NН(С1-4алкілу) і N(С1-4алкілу)2.
7. Сполука за п. 2 або її фармацевтично прийнятні сіль чи сольват, де R1 і R5 незалежно один від одного являють собою водень або СН3.
8. Сполука за п. 2 або її фармацевтично прийнятні сіль чи сольват, де R2 являє собою водень.
9. Сполука за п. 2 або її фармацевтично прийнятні сіль чи сольват, де R3 являє собою метил, -СF3 або -ОСF3.
10. Сполука за п. 2 або її фармацевтично прийнятні сіль чи сольват, де Х являє собою -С(=O)- або -C(=O)NH-.
11. Сполука за п. 2 або її фармацевтично прийнятні сіль чи сольват, де Y являє собою -C(=O)NH-.
12. Сполука за п. 2 або її фармацевтично прийнятні сіль чи сольват, де Х являє собою -C(=O)NH-, a R4 є С2-6алкіл, необов’язково заміщений бензил або гетероциклічне чи гетероарильне кільце, вибране з діазепінілу, морфолінілу, піперидинілу і піролідинілу, причому зазначений гетероцикл є необов’язково заміщеним узятими в кількості від одного до двох С1-4алкілом, гідрокси, С1-4алкокси, фенілом і/або бензилом.
13. Сполука за п. 2 або її фармацевтично прийнятні сіль, проліки чи сольват, де Х являє собою -С(=O)-, а R4 є феніл, піридил, піримідиніл або піразиніл, необов’язково заміщені взятими в кількості від одного до двох С1-4алкілом, галогеном, гідрокси, С1-4алкокси, трифторметилом, трифторметокси, ціано, нітро, фенілом, бензилом, фенілокси, бензилокси, NН2, -NH(С1-4алкілом), -N(С1-4алкілом)2, і/або –С1-4алкіл, необов’язково заміщений узятими в кількості від одного до двох галогеном, гідрокси, С1-4алкокси, трифторметилом, трифторметокси, ціано, нітро, фенілом, бензилом, фенілокси, бензилокси, NH2, NH(C1-4алкілом) і/або N(С1-4алкілом)2.
14. Сполука за п. 2 або її фармацевтично прийнятні сіль, чи сольват, де В являє собою циклопропіл або циклобутил, необов’язково заміщені від одного до двох R7; феніл, заміщений п’яти- чи шестичленним гетероциклом і від нуля до двох R12, або В є одним із:
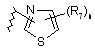 ,
, 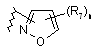 ,.
,. 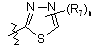 ,
,
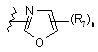 ,
, 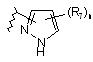 ,
,  ,
,
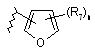 ,
, 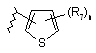 ,
, 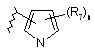 ,
,
 ,
, 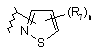 ;
;
R7 і R12 вибрані незалежно один від одного з С1-4алкілу, трифторметилу, трифторметокси, галогену, ціано, нітро, аміно, С1-4алкіламіно, гідрокси, С1-4алкокси, фенілу, бензилу, фенілокси і бензилокси; і
n приймає значення 0 або 1.
15. Сполука, яка має формулу
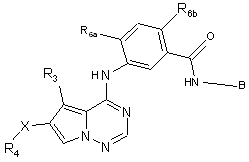 ,
,
її енантіомери, діастереомери, солі і сольвати, де:
Rз являє собою метил або –СF3;
Х являє собою -С(=O)- або -C(=O)NH-;
R4 являє собою прямий або розгалужений С2-6алкіл; циклоалкіл, необов’язково заміщений групою кето і/або не більше ніж двома R16; гетероцикл, необов’язково заміщений групою кето і/або не більше ніж двома R16; або С1-4алкіл, заміщений узятими в кількості до трьох галогеном, трифторметилом, ціано, гідрокси, алкокси, галогеналкілу, галогеналкокси, нітро, фенілом, фенілокси або бензилокси, де зазначена фенільна група необов’язково заміщена взятими у кількості від одного до двох R26; або феніл, необов’язково заміщений взятими у кількості від нуля до двох R16;
R6a і R6b вибрані з нижчого алкілу, галогену, трифторметокси, трифторметилу, груп гідрокси, С1-4алкокси, нітро, аміно, С1-4алкіламіно або ціано;
В являє собою: С3-7циклоалкіл, необов’язково заміщений від одного до двох R7; п’ятичленний гетероарил, необов’язково заміщений від одного до двох R7; п’яти- або шестичленний гетероцикл, необов’язково заміщений від одного до двох R7, феніл, заміщений R11 і від нуля до двох R12, -С(=O)R13, -CO2R13 і -C(=O)NR13R13a;
R7 приєднаний до будь-якого доступного атома вуглецю або азоту кільця В і в усіх випадках є незалежно вибраним з алкілу, заміщеного алкілу, галогену, галогеналкокси, уреїдо, ціано, трифторметокси, трифторметилу, гідрокси, -С1-4алкокси, -С(=O)алкілу, -ОС(=O)алкілу, NH2, NH(C1-4алкілу), N(С1-4алкілу)2, -CN, -СO2-алкілу, -CONH2, -СОNН(СН3), -CON(CH3)2, фенілу, бензилу, С3-7циклоалкілу і від п’яти- до шестичленного гетероциклу або гетероарилу; і/або, коли В є циклоалкіл, тоді дві групи R7 можуть об’єднуватися, утворюючи необов’язково заміщений вуглець-вуглецевий місток із трьох-чотирьох атомів вуглецю, або дві групи R7 можуть об’єднуватися, утворюючи злите карбоциклічне, гетероциклічне або гетероарильне кільце, причому зазначене злите кільце є, у свою чергу, необов’язково заміщеним одним-трьома R22;
R11 являє собою циклоалкіл, гетероцикл або гетероарил, необов’язково заміщений від одного до двох R15;
R13 і R13a вибрані з водню і С1-4алкілу;
R12, R15 і R16 в усіх випадках є незалежно один від одного вибраними з водню, алкілу, трифторметилу, трифторметокси, галогену, ціано, нітро, аміно, С1-4алкіламіно, аміно-С1-4алкілу, галоген-С1-4алкілу, гідрокси, гідроксі-С1-4алкілу, алкокси, фенілу, бензилу, фенілокси і бензилокси;
R20 і R21 вибрані з водню, алкілу, алкенілу, заміщеного алкілу, заміщеного алкенілу, арилу, циклоалкілу, гетероарилу і гетероциклу; і
R22 і R26 вибрані з С1-6алкілу, С2-6алкенілу, галогену, галогеналкілу, галогеналкокси, ціано, нітро, аміно, С1-4алкіламіно, аміно-С1-4алкілу, гідрокси, гідроксі-С1-4алкілу, алкокси, алкілтіо, фенілу, бензилу, фенілокси і бензилокси.
16. Сполука за п. 15, або її фармацевтично прийнятні сіль чи сольват, де В являє собою феніл, заміщений гетероциклом і від одного до двох R12; циклопропіл або циклобутил, необов’язково заміщені від одного до двох R7; або В є одним із:
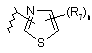 ,
, 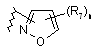 .,
., 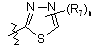 ,
,
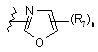 ,
, 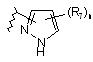 ,
,  ,
,
 ,
, 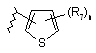 ,
, 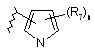 ,
,
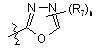 ,
, 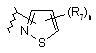 ;
;
R7 являє собою С1-4алкіл, трифторметил, трифторметокси, галоген, ціано, аміно, С1-4алкіламіно, гідрокси, С1-4алкокси, феніл, бензил, фенілокси або бензилокси; і
n приймає значення: 0, 1 або 2.
17. Сполука, яка має формулу (2а) або (2b)
 (2a)
(2a) 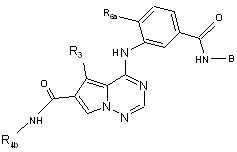 , (2b)
, (2b)
її енантіомери, діастереомери, солі і сольвати, де:
R3 являє собою метил або –CF3;
R4a являє собою феніл або п’яти- чи шестичленний гетерарил, необов’язково заміщений не більше ніж двома R16;
R4b являє собою прямий або розгалужений С2-6алкіл; циклоалкіл, необов’язково заміщений групою кето і/або не більше ніж двома R16; гетероцикл, необов’язково заміщений групою кето і/або не більше ніж двома R16; або С1-4алкіл, заміщений узятими в кількості до трьох галогеном, трифторметилом, групами ціано, гідрокси, алкокси, галогеналкілу, галогеналкокси, нітро, фенілом, фенілокси або бензилокси, де зазначена фенільна або бензильна група, у свою чергу, необов’язково заміщена взятими у кількості від одного до двох R26;
R6a являє собою нижчий алкіл, галоген, трифторметокси, трифторметил, гідрокси, С1-4алкокси, аміно, С1-4алкіламіно або ціано;
В є вибраний з фенілу, заміщеного гетероциклом або гетероарилом і не більше ніж двома R12; циклопропілу або циклобутилу, будь-який з котрих може бути необов’язково заміщеним від одного до двох R7, або ж В є один із:
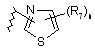 ,
, 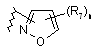 .,
., 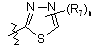 ,
,
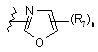 ,
, 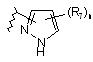 ,
,  ,
,
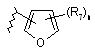 ,
, 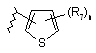 ,
, 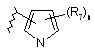 ,
,
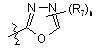 ,
, 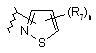 ;
;
R7 являє собою С1-4алкіл, трифторметил, трифторметокси, галоген, ціано, нітро, аміно, С1-4алкіламіно, гідрокси, С1-4алкокси, феніл, бензил, фенілокси або бензилокси;
R12, R16 і R17 в усіх випадках вибрані незалежно один від одного з водню, алкілу, трифторметилу, трифторметокси, галогену, ціано, нітро, аміно, С1-4алкіламіно, гідрокси, алкокси, фенілу, бензилу, фенілокси і бензилокси;
R26 вибраний з С1-4алкілу, трифторметилу, трифторметокси, галогену, ціано, аміно, С1-4алкіламіно, гідрокси, алкокси, фенілу, бензилу, фенілокси і бензилокси;
n приймає значення: 0 або 1.
18. Сполука за п. 17 або її фармацевтично прийнятні сіль, проліки чи сольват, де В являє собою циклопропіл, необов’язково заміщений від одного до двох R7, або В є вибраним з:
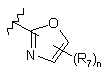 ,
, 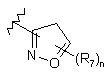 .
.
19. Фармацевтична композиція, яка містить принаймні одну сполуку, вказану в п. 1, і фармацевтично прийнятий носій або розріджувач.
20. Фармацевтична композиція, яка містить принаймні одну сполуку, вказану в п. 15, і фармацевтично прийнятий носій або розріджувач.
21. Спосіб лікування запального розладу, при якому вводять пацієнту, що потребує такого лікування, фармацевтичну композицію, вказану в п. 19.
22. Спосіб за п. 21, де запальний розлад вибраний з астми, старечого дихального дистрессиндрому, хронічної обструктивної хвороби легенів, діабету, запальної хвороби кишечнику, остеопорозу, псоріазу, реакції „трансплантат проти хазяїна”, атеросклерозу й артриту, включаючи ревматоїдний артрит, псоріатичний артрит, травматичний артрит, краснушний артрит, подагричний артрит і остеоартрит.
23. Сполука, яка має формулу
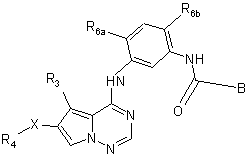 ,
,
її енантіомери, діастереомери, солі і сольвати, де:
R3 являє собою метил або –СF3;
Х являє собою -С(=O)- або -C(=O)NH-;
R4 являє собою прямий або розгалужений С2-6алкіл; циклоалкіл, необов’язково заміщений групою кето і/або не більше ніж двома R16; гетероцикл або гетероарил, необов’язково заміщений групою кето і/або не більше ніж двома R16; С1-4алкіл, заміщений узятими в кількості до трьох галогеном, трифторметилом, групами ціано, гідрокси, алкокси, галогеналкілу, галогеналкокси, нітро, фенілом, фенілокси або бензилокси, де зазначена фенільна група необов’язково заміщена взятими у кількості від одного до двох R26; або феніл, необов’язково заміщений взятими у кількості від нуля до двох R16;
R6a і R6b вибрані з нижчого алкілу, галогену, трифторметокси, трифторметилу, груп гідрокси, С1-4алкокси, нітро, аміно, С1-4алкіламіно і ціано;
В являє собою: С3-7циклоалкіл, необов’язково заміщений від одного до двох R7; п’ятичленний гетероарил, необов’язково заміщений від одного до двох R7; п’яти- або шестичленний гетероцикл, необов’язково заміщений від одного до двох R7; феніл, заміщений R11 і від нуля до двох R12, -С(=O)R13, -CO2R13 і -С(=O)NR13R13a;
R7 приєднаний до будь-якого доступного атома вуглецю або азоту кільця В і в усіх випадках є незалежно вибраним з алкілу, заміщеного алкілу, галогену, галогеналкокси, уреїдо, ціано, трифторметокси, трифторметилу, гідрокси, -С1-4алкокси, -С(=O)алкілу, -ОС(=O)алкілу, NH2, NН(С1-4алкілу), N(С1-4алкілу)2, -CN, -СО2-алкілу, -CONH2, -СОNН(СН3), -СОN(СН3)2, фенілу, бензилу, С3-7циклоалкілу і від п’яти- до шестичленного гетероциклу або гетероарилу; і/або коли В є циклоалкіл, тоді дві групи R7 можуть об’єднуватися, утворюючи необов’язково заміщений вуглець-вуглецевий місток із трьох-чотирьох атомів вуглецю, або дві групи R7 можуть об’єднуватися, утворюючи злите карбоциклічне, гетероциклічне або гетероарильне кільце, причому зазначене злите кільце є, у свою чергу, необов’язково заміщеним одним-трьома R22;
R11 являє собою циклоалкіл, гетероцикл або гетероарил, необов’язково заміщений від одного до двох R15;
R13 і R13a вибрані з водню і С1-4алкілу;
R12, R15 і R16 в усіх випадках є незалежно один від одного вибраними з водню, алкілу, трифторметилу, трифторметокси, галогену, ціано, нітро, аміно, С1-4алкіламіно, аміно-С1-4алкілу, галоген-С1-4алкілу, гідрокси, гідроксі-С1-4алкілу, алкокси, фенілу, бензилу, фенілокси і бензилокси;
R20 і R21 вибрані з водню, алкілу, алкенілу, заміщеного алкілу, заміщеного алкенілу, арилу, циклоалкілу, гетероарилу і гетероциклу; i
R22 і R26 вибрані з С1-6алкілу, С2-6алкенілу, галогену, галогеналкілу, галогеналкокси, ціано, нітро, аміно, С1-4алкіламіно, аміно-С1-4алкілу, гідрокси, гідроксі-С1-4алкілу, алкокси, алкілтіо, фенілу, бензилу, фенілокси і бензилокси.
24. Сполука за п. 23 або її фармацевтично прийнятні сіль чи сольват, де В являє собою феніл, заміщений гетероциклом і від одного до двох R12; циклопропіл або циклобутил, необов’язково заміщені від одного до двох R7; або В є одним із:
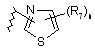 ,
, 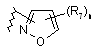 .,
., 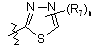 ,
,
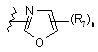 ,
, 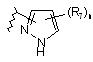 ,
,  ,
,
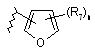 ,
, 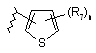 ,
, 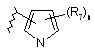 ,
,
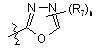 ,
, 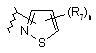 ;
;
R7 являє собою С1-4алкіл, трифторметил, трифторметокси, галоген, ціано, аміно, С1-4алкіламіно, гідрокси, С1-4алкокси, феніл, бензил, фенілокси або бензилокси; і
n приймає значення: 0, 1 або 2.
25. Сполука, яка має формулу
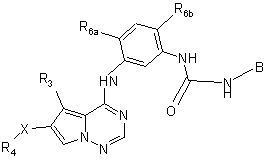 ,
,
її енантіомери, діастереомери, солі і сольвати, де:
R3 являє собою метил або –СF3;
Х являє собою -С(=O)- або -C(=O)NH-;
R4 являє собою прямий або розгалужений С2-6алкіл; циклоалкіл, необов’язково заміщений групою кето і/або не більше ніж двома R16; гетероцикл або гетероарил, необов’язково заміщений групою кето і/або не більше ніж двома R16, С1-4алкіл, заміщений узятими в кількості до трьох галогеном; трифторметилом, групами ціано, гідрокси, алкокси, галогеналкілу, галогеналкокси, нітро, фенілом, фенілокси або бензилокси, де зазначена фенільна група необов’язково заміщена взятими у кількості від одного до двох R26, або феніл, необов’язково заміщений взятими у кількості від нуля до двох R16;
R6a і R6b вибрані з нижчого алкілу, галогену, трифторметокси, трифторметилу, груп гідрокси, С1-4алкокси, нітро, аміно, С1-4алкіламіно і ціано;
В являє собою: С3-7циклоалкіл, необов’язково заміщений від одного до двох R7; п’ятичленний гетероарил, необов’язково заміщений від одного до двох R7; п’яти- або шестичленний гетероцикл, необов’язково заміщений від одного до двох R7; феніл, заміщений R11 і від нуля до двох R12, -С(=O)R13, -CO2R13 і -С(=O)NR13R13a;
R7 приєднаний до будь-якого доступного атома вуглецю або азоту кільця В і в усіх випадках є незалежно вибраний з алкілу, заміщеного алкілу, галогену, галогеналкокси, уреїдо, ціано, трифторметокси, трифторметилу, гідрокси, -С1-4алкокси, -С(=O)алкілу, -ОС(=O)алкілу, NH2, NH(С1-4алкілу), N(С1-4алкілу)2, -CN, -СO2-алкілу, -CONH2, -СОNН(СН3), -СОN(СН3)2, фенілу, бензилу, С3-7циклоалкілу і від п’яти- до шестичленного гетероциклу або гетероарилу; і/або, коли В є циклоалкіл, тоді дві групи R7 можуть об’єднуватися, утворюючи необов’язково заміщений вуглець-вуглецевий місток із трьох-чотирьох атомів вуглецю, або дві групи R7 можуть об’єднуватися, утворюючи злите карбоциклічне, гетероциклічне або гетероарильне кільце, причому зазначене злите кільце є, у свою чергу, необов’язково заміщеним одним-трьома R22;
R11 являє собою циклоалкіл, гетероцикл або гетероарил, необов’язково заміщений від одного до двох R15;
R13 і R13a вибрані з водню і С1-4алкілу;
R12, R15 і R16 в усіх випадках є незалежно один від одного вибраними з водню, алкілу, трифторметилу, трифторметокси, галогену, ціано, нітро, аміно, С1-4алкіламіно, аміноС1-4алкілу, галогенС1-4алкілу, гідрокси, гідроксіС1-4алкілу, алкокси, фенілу, бензилу, фенілокси і бензилокси;
R20 і R21 вибрані з водню, алкілу, алкенілу, заміщеного алкілу, заміщеного алкенілу, арилу, циклоалкілу, гетероарилу і гетероциклу; і
R22 і R26 вибрані з С1-6алкілу, С2-6алкенілу, галогену, галогеналкілу, галогеналкокси, ціано, нітро, аміно, С1-4алкіламіно, аміноС1-4алкілу, гідрокси, гідроксиС1-4алкілу, алкокси, алкілтіо, фенілу, бензилу, фенілокси і бензилокси.
26. Сполука за п. 25 або її фармацевтично прийнятні сіль чи сольват, де В являє собою феніл, заміщений гетероциклом і від одного до двох R12; циклопропіл або циклобутил, необов’язково заміщені від одного до двох R7; або В є одним із:
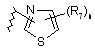 ,
, 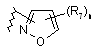 ,.
,. 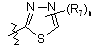 ,
,
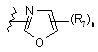 ,
, 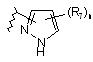 ,
,  ,
,
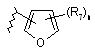 ,
, 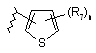 ,
, 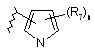 ,
,
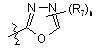 ,
, 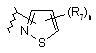 ;
;
R7 являє собою С1-4алкіл, трифторметил, трифторметокси, галоген, ціано, аміно, С1-4алкіламіно, гідрокси, С1-4алкокси, феніл, бензил, фенілокси або бензилокси; і
n приймає значення: 0, 1 або 2.
27. Сполука за п. 1, вибрана з
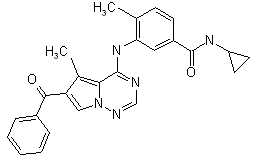 ,
, 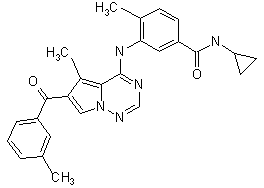 ,
,
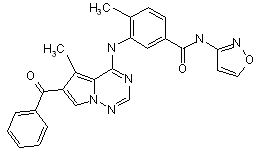 ,
, 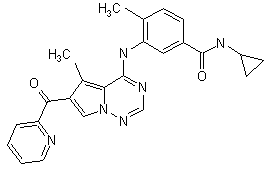 ,
,
 ,
, 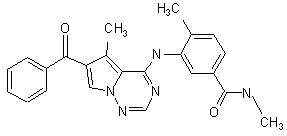 ,
,
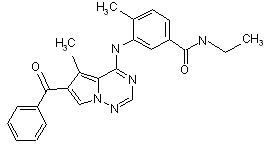 ,
, 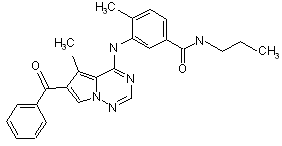 ,
,
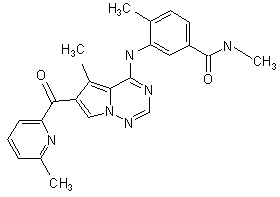
її солі та сольвати.
28. Сполука за п. 1, вибрана з
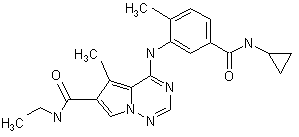 ,
, 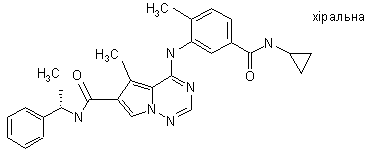 ,
,
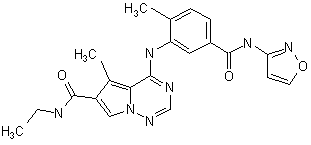 ,
, 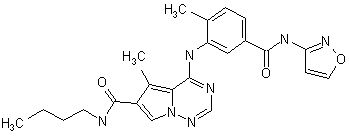 ,
,
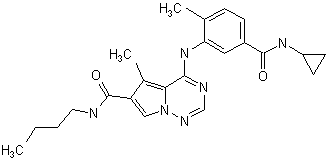 ,
,
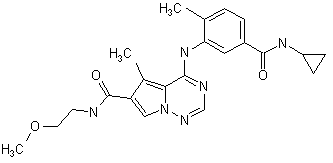 ,
,
 ,
,
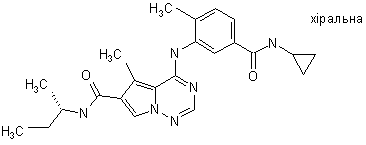 ,
,
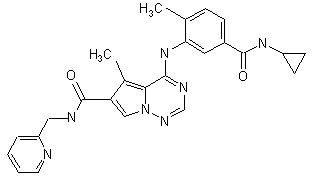 ,
,
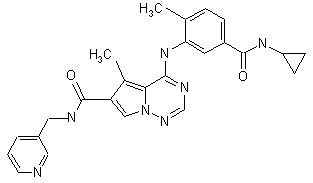 ,
,
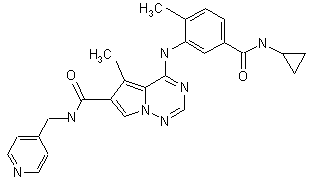 ,
,
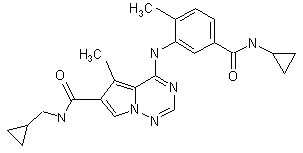 ,
,
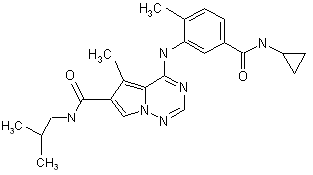 ,
,
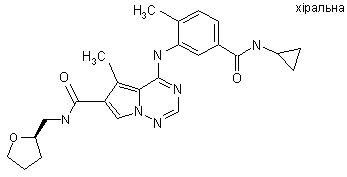 ,
,
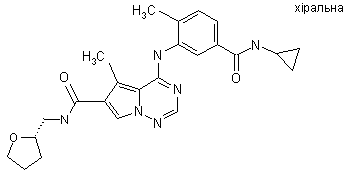 ,
,
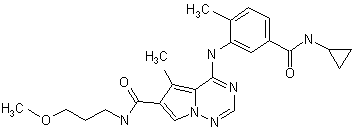 ,
,
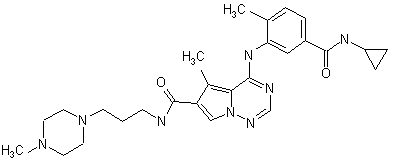 ,
,
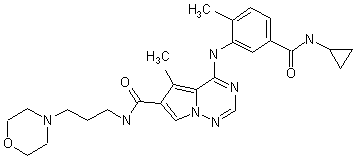 ,
,
 ,
,
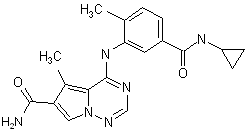 і
і
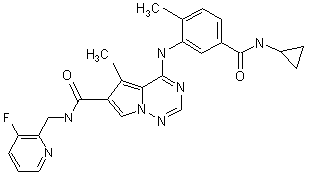 .
.
її енатіомери, діастереомери, солі і сольвати.
29. Сполука за п. 1, вибрана з
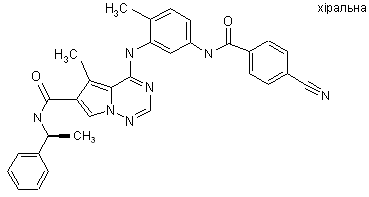 і
і
 ,
,
її енатіомери, діастереомери, солі і сольвати.
Текст
Даний винахід стосується піролтриазинанілінових сполук і, зокрема, циклоалкільних, гетероциклічних і гетероарильних піролтриазинанілінових сполук, що можуть застосовуватися в лікуванні станів, пов'язаних із р38-кіназою. Винахід стосується також фармацевтичних композицій, що містять принаймні одну сполуку, яка відповідно до даного винаходу є корисною в лікуванні станів, пов'язаних із р38-кіназою. Крім того, винахід стосується процесів інгібування активності р38-кінази у ссавців. У запальних реакціях бере участь велика кількість цитокінів, включаючи IL-1, IL-6, IL-8 і TNF-α. Надлишкове продукування цитокінів типу IL-1 і TNF-α пов 'язується з різноманітними захворюваннями, у тому числі із запаленнями кишечника, ревматоїдним артритом, псоріазом, розсіяним склерозом, ендотоксичним шоком, остеопорозом, хворобою Альцгеймера і гострою серцевою недостатністю [Henry et. al., Drugs Put, 24:1345-1354 (1999); Salituro et. al., Curr. Med. Chem. 6:807-823 (1999)]. Медичні спостереження показують, що білкові антагоністи цитокінів є ефективними в лікуванні хронічних запальних захворювань; це стосується, наприклад, моноклонального антитіла проти TNF-α (Enbrel) [Rankin et. al. Br. J. Rheumatol., 34:334-342 (1995)] і розчинного Fc-злитого білкового рецептора TNF-α (Etanercept) [Moreland et. al., Ann. Intern. Med., 130:478486(1999)]. Біосинтез TNF-α відбувається в багатьох типах клітин у відповідь на зовнішн і стимули, такі, наприклад, як мітогени, інфекційні організм або травма. Важливими медіаторами продукування TNF-α є мітоген -активізовані протеїнкінази (МАР-кінази) і, зокрема, р38-кіназа. Ці кінази активуються у відповідь на різноманітні стресові стимули, як-от прозапальні цитокіни, ендотоксин, ультрафіолетове світло й осмотичний шок. Активація р38 потребує подвійного фосфорилювання кіназами, лівими від МАР-кінази, (МКК3 і МКК6) на треоніні і тирозині в межах характеристичного мотиву Thr-Gl y-Tyr р38-ізозимів. Відомо про існування чотирьох ізоформ р38, а саме р38-α, р38β, р38γ і р38δ. Ізоформи α і β експресуються в запальних клітинах і є ключовими медіаторами продукування TNF-α. Інгібування ферментів р38 α і β в клітинах приводить до зменшення рівнів експресії TNF-α. Крім того, введення інгібіторів р38α і β у піддослідну модель запального захворювання показало, що такі інгібітори є ефективними в лікуванні зазначених захворювань. Отже, ферменти р38 відіграють важливу роль у запальних процесах, опосередкованих IL-1 і TNF-α. Сполуки, котрі , згідно з повідомленнями, інгібують р38-кінази і цитокіни типу IL1 і TNF-α для використання в лікуванні запальних захворювань, описані в [US 6,277,989 і 6,130,235 Scios, Inc; US 6,147,080 і 5,945,418 Vertex Pharmaceuticals Inc; US 6,251,914, 5,977,103 і 5,658,903 Smith-Kline Beecham Corp.; US 5,932,576 і 6,087,496 G.D. Searle & Co.; WO 00/56738 і WO 01/27089 Astra Zeneca; WO 01/34605 Johnson & Johnson; WO 00/12497 (похідні хіназоліну як інгібітори р38-кінази); WO 00/56738 (похідні піридину і піримідину для тієї ж цілі); WO 00/12497 (описано співвідношення між інгібіторами р38-кінази) і WO 00/12074 (піперазинові і піперидинові сполуки, корисні як інгібітори р38)]. Даним винаходом охоплюються деякі сполуки піролтриазину і, зокрема, піролтриазинанілінові сполуки, корисні як інгібітори кінази, зокрема, кінази р38α і β. Піролтриазинові сполуки, корисні як інгібітори тирозинкінази, розкриті [в заявці US 09/573,829] того ж заявника, поданій 18 травня 2000р. Процеси лікування станів, пов'язаних із р38-кіназою, а також піролтриазинові сполуки, корисні для тієї ж цілі, описані [в заявці US 10/036,293] того ж заявника, що є продовженням [US 60/249,877, поданої 17 листопада 2000p., і US 60/310,561, поданої 7 серпня 2001р.]. Піролтриазинові сполуки, заміщені кислотною групою, що мають sPLA2інгібуючу здатність, розкриті [в заявці WO 01/14378 А1 (Shionogi & Co., Ltd), опублікованій 1 березня 2001p.]. Даним винаходом пропонуються сполуки за формулою (І): (I) її енантіомери, діастереомери, солі і сольвати, де: X вибирають серед -О-, -ОС(=О)-, -S-, -S(=O)-, -SO2-, -C(=O)-, -CO2-, -NR8-, -NR8C(=O)-, -NR 8C(=O)NR9-, NR8CO2-, -NR8SO 2-, -NR8SO 2NR9-, -SO2NR8-, -C(=O)NR 8-, галогену, нітро і ціано, або X є відсутнім; Ζ являє собою -C(=O)NR 10-Bb, -(CH2)-C(=O)NR 10-Bc, -NR10aC(=O)-Ba , -(CH2)-NR10aC(=O)-Bc, NR10aC(=O)NR 10-B, -NR10SO2-B, -SO 2NR10-B, -C(=O)-Ba , -CO2-Be , -OC(=O)-Ba , -C(=O)NR 10-NR10a-Bd, -NR10CO 2-Ba або -C(=O)NR 10-(CH2)C(=O)Ba; В являє собою: а) необов'язково заміщений циклоалкіл, необов'язково заміщений гетероцикл або необов'язково заміщений гетероарил; або (b) арил, заміщений одним R11 і від нуля до двох R12; Ва являє собою, необов'язково заміщений алкіл, необов'язково заміщений циклоалкіл, необов'язково заміщений гетероцикл, необов'язково заміщений арил або необов'язково заміщений гетероарил; Bb являє собою (a) необов'язково заміщений циклоалкіл, необов'язково заміщений гетероцикл або необов'язково заміщений гетероарил; (b) арил, заміщений одним R11 і від нуля до двох R12; або (c) -C(=O)R13, -CO2R13, -C(=O)NR 13R13a; Вс являє собою, необов'язково заміщений алкіл, необов'язково заміщений алкокси, необов'язково заміщений циклоалкіл, необов'язково заміщений гетероцикл, необов'язково заміщений арил або необов'язково заміщений гетероарил; Bd являє собою водень, -C(=O)R13 або -CO2R13; Ве являє собою водень, необов'язково заміщений алкіл, необов'язково заміщений циклоалкіл, необов'язково заміщений гетероцикл, необов'язково заміщений арил або необов'язково заміщений гетероарил; R1 і R5 вибрані незалежно один від одного серед водню, алкілу, заміщеного алкілу, -OR14> -SR14, OC(=O)R14, -CO2R14, -C(=O)NR 14R14a, -NR14R 14a, -S(O)R14, -SO 2R14, -SO 2NR14R14a, -NR14SO 2NR14aR14b , NR14aSO2R 14, -NR14C(=O)R14a, -NR14CO2R 14a , -NR 14C(=O)NR 14aR14b, галогену, нітро і ціано; R2 являє собою водень або С 1-4 алкіл; R3 являє собою водень, метил, перфторметил, метокси, галоген, ціано, NH2 або NH(CH3); R4 вибраний серед: a) водню, за умови, що R 4 не є воднем, якщо X являє собою -S(=O)-, -SO 2-, -NR8CO2- або -NR 8SO2-; b) алкілу, алкенілу й алкінілу, необов'язково незалежно заміщених гр упою кето і/або від одного до чотирьох R17; c) арилу і гетероарилу, кожний із який може бути необов'язково незалежно заміщений від одного до трьох R16; і d) гетероциклу і циклоалкілу, кожний із який може бути необов'язково незалежно заміщений кетогрупою і/або від одного до трьох R16 ; або e) R 4 є відсутнім, якщо X являє собою галоген, нітро або ціано; R6 приєднаний до будь-якого доступного атому вуглецю фенільного кільця А і в усіх випадках є незалежно вибраним серед алкілу, галогену, трифторметокси, трифторметилу, гідрокси, алкокси, алканоїлу, алканоїлокси, тіолу, алкілтіо, груп уреїдо, нітро, ціано, карбокси, карбоксіалкілу, карбамоїлу, алкоксикарбонілу, груп алкілтіоно й арилтіоно, арилсульфоніламіну, алкілсульфоніламіну, сульфонової кислоти, алкілсульфонілу, сульфонамідогрупи, фенілу, бензилу, груп арилокси і бензилокси, де кожна група R6, у свою чергу, може бути заміщена від одного до двох R18; R8 і R9 вибрані незалежно один від одного серед водню, алкілу, заміщеного алкілу, арилу, циклоалкілу, гетероциклу і гетероарилу; R10 і R10a вибрані незалежно один від одного серед водню, алкілу, заміщеного алкілу, алкокси й арилу; R11 вибраний серед: (a) алкілу, галогеналкілу, алкокси, галогеналкокси, -SO2алкілу, циклоалкілу, гетероциклу і гетероарилу, із котрих будь-який може бути необов'язково заміщеним; або (b) галогену, ціано, аміно, алкіламіно і діалкіламіно; R12 вибраний серед алкілу, R17 і С1-4алкілу, заміщеного кетогрупою (=O) і/або від одного до трьох R 17; R13 і R13a вибрані незалежно один від одного серед водню, необов'язково заміщеного алкілу, необов'язково заміщеного циклоалкілу і необов'язково заміщеного арилу; R14, R14a і R14b вибрані незалежно один від одного серед водню, алкілу, заміщеного алкілу, арилу, циклоалкілу, гетероциклу і гетероарилу, за винятком тих випадків, коли R14 з'єднаний із сульфонільною групою, як у -S(=O)R14 , -SO 2R14 і -NR14aSO2R14, тоді R14 не є воднем; R16 вибраний серед алкілу, R17 і С1-4алкілу, заміщеного кетогрупою (=О) і/або від одного до трьох R 17; R17 вибраний серед (a) галогену, галогеналкілу, галогеналкокси, нітро, ціано, -SR23, -OR23, -NR23R24 , -NR23SO2R25, -SO2R25, SO2NR23R24, -CO 2R23 , -C(=O)R23, -C(=O)NR 23R24, -OC(=O)R 23, -OC(=O)NR 23R24, -NR 23C(=O)R 24, -NR23CO2R 24; (b) арилу або гетероарилу, кожний із який може бути необов'язково заміщений від одного до трьох R 26; або (c) циклоалкілу чи ге тероциклу, необов'язково заміщеного кетогрупою (=О) і/або від одного до трьох R 26; R18 і R26 вибрані незалежно один від одного серед С 1-6алкілу, С2-6алкенілу, галогену, галогеналкілу, галогеналкокси, ціано, нітро, аміно, С1-4алкіламіно, аміно-С1-4алкілу, гідрокси, гідрокси-С 1-4алкілу, алкокси, С14алкілтіо, арилу, гетероциклу, (арил)алкілу, арилокси і (арил)алкокси; R23 і R24 кожний є незалежно вибраним серед водню, алкілу, алкенілу, заміщеного алкілу, заміщеного алкенілу, арилу, циклоалкілу, гетероарилу і гетероциклу; R25 вибраний серед алкілу, заміщеного алкілу, арилу, гетероарилу, циклоалкілу і гетероцикло; і m приймає значення 0, 1, 2 або 3. Винахід стосується також фармацевтичних композицій, що містять сполуки за формулою (І), і процесів лікування станів, пов'язаних з активністю р38-кінази (α і β), які включають у себе введення ссавцю фармацевтично прийнятної кількості сполуки за формулою (І). Нижче наведені визначення різноманітних термінів, використовуваних в описі даного винаходу. Ці визначення ε правомірними на протязі всього опису, за винятком випадків спеціально зроблених застережень стосовно індивідуальних термінів або частини більшої їх групи. Терміном "алкіл" визначається прямий або розгалужений ланцюг незаміщених вуглеводневих гр уп, що мають від 1 до 20 атомів вуглецю і, переважно, від 1 до 7 атомів вуглецю. Терміном "нижчий алкіл" визначається незаміщена алкільна група, що містить від 1 до 4 атомів вуглецю. Якщо у визначенні алкільної або іншої групи використовується нижній індекс, то ним позначається число атомів вуглецю, із яких може складатися зазначена група. Наприклад, вираз "С1-4алкіл" включає у себе зв'язок і алкільні групи, що містять від 1 до 4 атомів вуглецю. Терміном "заміщений алкіл" визначається алкільна група, що має від одного до чотирьох замісників, вибраних серед галогену, гідрокси, алкокси, кетогрупи (=O) алканоїлу, арилокси, алканоїлокси, NRaRb, алканоїламіно, ароїламіно, аралканоїламіно, заміщеного алканоїламіно, заміщеного ариламіно, заміщеного аралканоїламіно, тіолу, алкілтіо, арилтіо, аралкілтіо, алкілтіоно, арилтіоно, аралкілтіоно, алкілсульфонілу, арилсульфонілу, аралкілсульфонілу, -SO2NRaRb, нітро , ціано, -СО2Н, -CONRaRb, алкоксикарбонілу, арилу, гуанідиногрупи і гетероарилів або гетероциклів (таких, як індоліл, імідазоліл, фурил, тієніл, тіазоліл, піролідил, піридил, піримідил і т. п.) де Ra і Rb вибрані серед водню, алкілу, арилу, аралкілу, циклоалкілу, циклоалкілалкілу, гетероарилу, гетероарилалкілу, гетероциклу і гетероциклоалкілу. Замісник в алкілі в разі необхідності, у свою чергу, може бути заміщений; при цьому замісниками можуть бути один або більше С14алкіл, С 2-4алкеніл, галоген, галогеналкіл, групи галогеналкокси, ціано, нітро, аміно, С 1-4алкіламіно, аміно-С 14алкіл, гідрокси, гідрокси-С 1-4алкіл, алкокси, алкілтіо, феніл, бензил, групи фенілокси і/або бензилокси. Терміном "алкеніл" визначається вуглеводнева гр упа з прямим або розгалуженим ланцюгом, що складається із 2-20 атомів вуглецю, переважно із 2-15 атомів вуглецю і краще - із 2-8 атомів вуглецю і має, принаймні, один подвійний зв'язок і, в залежності від числа атомів вуглецю, до чотирьох подвійних зв'язків. Терміном "заміщений алкеніл" визначається алкенільна група, що містить від одного до двох замісників, вибраних серед тих, що зазначені вище для заміщених алкільних груп. Терміном "алкініл" визначається вуглеводнева група з прямим або розгалуженим ланцюгом, що складається із 2-20 атомів вуглецю, переважно із 2-15 атомів вуглецю і краще - із 2-8 атомів вуглецю, і має принаймні один потрійний зв'язок і, в залежності від числа атомів вуглецю, до чотирьох потрійних зв'язків. Терміном "заміщений алкініл" визначається алкінільна група, що містить від одного до двох замісників, вибраних серед тих, що зазначені вище для алкільних груп. Якщо термін алкіл використовується у сполученні з іншою групою, як, наприклад, в гетероциклоалкілі або циклоалкілалкілі, це означає, що перша із зазначених у такій назві група безпосередньо зв'язана через алкільну гр упу, яка може мати розгалужений або прямолінійний ланцюг (наприклад, вираз "циклопропіл-С14алкіл" означає циклопропільну груп у, зв'язану через алкільну груп у з прямолінійним або розгалуженим ланцюгом, що має від одного до чотирьох атомів вуглецю). У випадку наявності замісників, як у "заміщеному циклоалкілалкілі", алкільна частина групи, крім того, що вона є розгалуженою або прямоланцюговою, може бути заміщеною, як зазначено вище стосовно заміщених алкільних груп, і/або перша із груп, що складає дану назву (наприклад, циклоалкіл), може бути заміщеною як зазначено тут стосовно цієї гр упи. Термін "гало" або "галоген" стосується фтор у, хлор у, брому і йоду. Терміном "арил" визначається моноциклічна або біциклічна ароматична, заміщена або незаміщена вуглеводнева група, що має в кільцевій частині від 6 до 12 атомів вуглецю, тобто така, як феніл, нафтиніл і біфеніл. Арильні групи в разі потреби можуть включати від одного до трьох злитих з ними додаткових кілець (чи то циклоалкільних, гетероциклічних, чи то гетероарильних), таких як і т.п. Кожне кільце арилу в разі потреби може бути заміщене групами Rc у кількості від однієї до трьох, причому групи Rc в усі х випадках вибирають серед алкілу, заміщеного алкілу, галогену, три фторметокси, трифторметилу, -SR, -OR, -NRR', -NRSO 2R', -SO2R, -SO2NRR', -CO 2R', -C(=O)R', -C(=O)NRR', -OC(=O)R', OC(=O)NRR', -NRC(=O)R', -NRCO2R', фенілу, С3-7циклоалкілу і п'яти-шестичленного гетероциклу чи гетероарилу, де R і R' вибирають серед водню, алкілу, заміщеного алкілу, алкенілу, заміщеного алкенілу, фенілу, С3-7циклоалкілу і п'яти-шестичленного гетероциклу чи ге тероарилу, за винятком випадку сульфонільної групи, де R не може бути воднем. У разі потреби кожний замісник Rc, у свою чергу, може бути заміщений однією чи більше (переважно від 0 до 2) групами Rd, вибраними серед С 1-6алкілу, С2-6алкенілу, галогену, галогеналкілу, галогеналкокси, ціано, нітро, аміно, С1-4алкіламіно, аміно-С1-4алкілу, гідрокси, гідрокси-С^алкілу, алкокси, алкілтіо, фенілу, бензилу, фенілетилу, фенілокси і бензилокси. Терміном "аралкіл" визначається арильна група, зв'язана безпосередньо через алкільну групу, тобто така, як бензил, де алкільна група може бути розгалуженою або прямолінійною. У випадку "заміщеного аралкілу," алкільна частина групи, окрім її розгалуженої або прямоланцюгової будови, може бути заміщеною, як зазначено вище для заміщених алкільних груп, і/або арильна частина може бути заміщеною, як зазначено в даному описі для арильних груп. Таким чином, вираз "необов'язково заміщений бензил" означає групу , де кожна з R-груп може бути воднем або ж бути вибраною серед членів Rc-групи, згідно з визначеним вище, у свою чергу, необов'язково заміщених одним чи більше членами групи Rd. При цьому, принаймні, дві, а краще п'ять з цих груп "R" мають бути воднем. У кращому варіанті бензильна група включає у себе алкільну розгалужену частину, набуваючи таку будову . Терміном "гетероарил" визначається заміщена або незаміщена ароматична група, наприклад, така, що являє собою 4-7-членну моноциклічну, 7-11-членну біциклічну або 10-15-членну трициклічну кільцеву систему, котра має, принаймні, один гетероатом і, принаймні, одне вуглецьвмісне кільце. Кожне кільце гетероарильної групи, що містить гетероатом, може містити один або два атоми кисню чи сірки і/або від одного до чотирьох атомів азоту за умови, що загальне число гетероатомів у кожному кільці не є більшим чотирьох, а кожне кільце містить, принаймні, один атом вуглецю. Сконденсовані кільця, що комплектують біциклічні і трициклічні групи, можуть мати тільки атоми вуглецю і можуть бути насиченими, частково насиченими або ненасиченими. У разі потреби атоми азоту і сірки можуть бути окисленими, а атоми азоту - кватернізованими. Гетероарильні групи, що є біциклічними або трициклічними, повинні включати, принаймні, одне цілком ароматичне кільце, але інше сконденсоване кільце або кільця можуть бути ароматичними чи неароматичними. Гетероарильна група може бути приєднана до будь-якого доступного атому азоту або вуглецю будь-якого кільця. У разі потреби вона може бути заміщеною одним-трьома (переважно від 0 до 2) Rc-групами, як визначено вище стосовно арилу, які у свою чергу можуть бути заміщені однією або більше (переважно від 0 до 2) Rg-групами також згідно з визначеним вище. Серед типових моноциклічних гетероарильних груп можна назвати піроліл, піразоліл, піразолініл, імідазоліл, оксазоліл, ізоксазоліл, тіазоліл (тобто, ), тіадіазоліл, ізотіазоліл, фураніл, тієніл, оксадіазоліл, піридил, піразиніл, піримідиніл, пірадазиніл, триазиніл і т.п. Як приклади біциклічних гетероарильних груп можна назвати індоліл, бензотіазоліл, бензодіоксоліл, бензоксазоліл, бензотієніл, хінолініл, тетрагідроізохінолініл, ізохінолініл, бензимідазоліл, бензопіраніл, індолізиніл, бензофураніл, хромоніл, кумариніл, бензопіраніл, цинолініл, хіноксалініл, індазоліл, піролопіридил, фуропіридиніл, дигідроізоіндоліл, тетрагідрохінолініл і т.п. Як приклади трициклічних гетероарильних гр уп можна назвати карбазоліл, бензиндоліл, фенантролініл, акридиніл, фенантридиніл, ксантеніл і т.п. Терміном "циклоалкіл" визначається насичена або частково ненасичена неароматична циклічна вуглеводнева кільцева система, що містить, переважно, від 1 до З кілець і від 3 до 7 атомів вуглецю в кільці, котре може бути заміщеним або незаміщеним і/або сконденсованим С 3-С7 карбоциклічним кільцем, гетероциклічним кільцем, або ж мати місток із 3-4 атомів вуглецю. Циклоалкільні групи, включаючи будь-які доступні атоми вуглецю або азоту на будь-яких сконденсованих або місткових кільцях, в разі потреби можуть мати від 0 до 3 (переважно 0-2) замісників, вибраних серед членів групи Rc згідно з визначеним вище і/або із кетогрупи (де необхідно) які, у свою чергу, можуть бути заміщені 1-3 членами Rd-групи, також згідно з визначеним вище. Таким чином, якщо вуглець-вуглецевий місток визначений як такий, що може необов'язково бути заміщеним, це означає, що атоми вуглецю в містковому кільці в разі потреби можуть бути заміщені Rcгрупою, вибраною в кращому варіанті серед С 1-4алкілу, С2-4алкенілу, галогену, галогеналкілу, галогеналкокси, ціано, аміно, С1-4алкіламіно, аміно-С 1-4алкілу, гідрокси, гідрокси-С 1-4алкілу і С1-4алкокси. Серед типових циклоалкільних груп можна назвати циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил, біциклогептан, циклооктил, циклодецил, циклододецил і адамантил. Термінами "гетероцикл", "гетероциклічний" і "гетероцикло" визначаються цілком насичена або частково ненасичена неароматична циклічна група, котра може бути заміщеною або незаміщеною. Такою групою може бути, наприклад, 4-7-членна моноциклічна, 7-11-членна біциклічна або 10-15-членна трициклічна кільцева система, яка має, принаймні, один гетероатом у, принаймні, одному вуглецьвмісному кільці. Кожне кільце гетероциклічної групи, що містить гетероатом, може мати 1, 2 або 3 гетероатоми, вибрані серед атомів азоту, кисню і сірки, де в разі потреби гетероатоми азоту і сірки можуть бути окислені, а гетероатоми азоту кватернізовани. У кращому варіанті два суміжних гетероатоми не можуть бути одночасно вибрані серед кисню й азоту. Гетероциклічна група може бути приєднана до будь-якого атому азоту або вуглецю. У разі потреби гетероциклічні групи можуть мати від 0 до 3 (переважно 0-2) замісників, вибраних із кетогрупи (=O) і/або із однієї чи більше Rc-груп, згідно з визначеним вище, котрі, у свою чергу, можуть бути заміщені однією-трьома Rd-групами, також згідно з визначеним вище. Як приклади моноциклічних гетероциклічних груп можна назвати піролідиніл, піроліл, індоліл, піразоліл, оксетаніл, піразолініл, імідазоліл, імідазолініл, імідазолідиніл, оксазоліл, оксазолідиніл, ізоксазолініл, ізоксазоліл, тіазоліл, тіадіазоліл, тіазолідиніл, ізотіазоліл, ізотіазолідиніл, фурил, тетрагідрофурил, тієніл, оксадіазоліл, піперидиніл, піперазиніл, 2-оксопіперазиніл, 2-оксопіперидиніл, 2-оксопіролідиніл, 2-оксазепініл, азепініл, 4-піперидоніл, піридил, N-оксопіридил, піразиніл, піримідиніл, пірадазиніл, тетрагідропіраніл, морфолініл, тіаморфолініл, тіаморфолінілсульфоксид, тіаморфолінілсульфон, 1,3-діоксалан і тетрагідро-1,1діоксотієніл, діоксаніл, ізотіазолідиніл, тієтаніл, тіїраніл, триазиніл і триазоліл і т. п. Як приклади біциклічних гетероциклічних груп можна назвати 2,3-дигідро-2-оксо-1Н-індоліл, бензотіазоліл, бензоксазоліл, бензотієніл, хінуклідиніл, хінолініл, хінолініл-ІМ-оксид, тетрагідроізохінолініл, ізохінолініл, бензимідазоліл, бензопіраніл, індолізиніл, бензофурил, хромоніл, кумариніл, цинолініл, хіноксалініл, індазоліл, піролопіридил, фуропіридиніл (як-от фуро[2,3-с]піридиніл, фуро[3,1-b]піридиніл] або фуро[2,3-b]піридиніл), дигідроізоіндоліл, дигідрохіназолініл (такі, як 3,4-дигідро-4-оксо-хіназолініл) бензизотіазоліл, бензизоксазоліл, бензодіазиніл, бензофуразаніл, бензотіопіраніл, бензотриазоліл, бензпіразоліл, дигідробензофурил, дигідробензотіеніл, дигідробензотіопіраніл, дигідробензотіопіраніл сульфон, дигідробензопіраніл, індолініл, ізохроманіл, ізоіндолініл, нафтиридиніл, фталазиніл, піпероніл, пуриніл, піридопіридил, хіназолініл, тетрагідрохінолініл, тієнофурил, тієнопіридил, тієнотіеніл і т.п. До їх числа входять також менші гетероциклі, такі як епоксиди й азиридини. Якщо не зазначено іншого, то в разі посилання в тексті до конкретно названого арилу (наприклад, фенілу), циклоалкілу (наприклад, циклогексилу), гетероциклу (наприклад, піролідинілу) або гетероарилу (наприклад, індолілу) передбачається включення в дане посилання кілець, що мають від 0 до 3, переважно від 0 до 2 замісників, вибраних згідно з потребою серед зазначених вище членів арильних, циклоалкільних, гетероциклічних і/або гетероарильних груп. Крім того, в разі посилання до конкретної гетероарильної або гетероциклічної групи передбачається включення в дане посилання систем, що мають максимальне число некумульованих подвійних зв'язків або менше за максимальне число подвійних зв'язків. Таким чином, наприклад, термін "ізохінолін" означає як ізохінолін, так і тетрагідроізохінолін. Крім того, цілком зрозуміло, що фахівець у даній галузі зможе вибрати підходящі замісники для арильної, циклоалкільної, гетероциклічної і гетероарильної груп у розрахунку на одержання стабільних сполук, які можуть використовуватися як фармацевтично прийнятні сполуки і/або проміжні сполуки, застосовні у виготовленні фармацевтично прийнятних сполук. Таким чином, наприклад, у сполуках за формулою (І), де В являє собою циклопропільне кільце, це кільце в кращому варіанті має не більш, ніж два замісники, причому ці замісники не містять нітрогрупи (NO2), більш ніж одну ціаногрупу або три галогенні групи. Подібним чином, якщо т дорівнює 3, то R6, тобто замісники на фенільному кільці А, у кращому варіанті не всі є нітро, і так далі. Терміном "гетероатоми" охоплюються кисень, сірка й азот. Термін "галогеналкіл" означає алкіл, який має один або більше галогенних замісників. Термін "перфторметил" означає метильну групу, заміщену одним, двома або трьома атомами фтору, тобто, CH2F, CHF2 і CF3. Термін "перфторалкіл" означає алкільну групу, наприклад, пентафторетил, що має від одного до п'яти атомів фтор у. Термін "галогеналкокси" означає алкокси групу, що має один або більше галогенних замісників. Наприклад, до числа галогеналкокси належить група -OCF3. Термін "карбоциклічний" означає насичене або ненасичене моноциклічне або біциклічне кільце, в якому всі атоми всіх кілець є атомами вуглецю. Таким чином, визначенням даного терміну охоплюються циклоалкільні й арильні кільця. Карбоциклічне кільце може бути заміщеним; у цьому випадку замісники в ньому добираються серед тих, що зазначені вище для циклоалкільних і арильних груп. Термін "ненасичений", використовуваний у даному описі по відношенню до кільця або групи, означає, що дані кільце або група можуть бути цілком ненасиченими або частково ненасиченими. Визначення для різноманітних інших груп, що згадані вище у зв'язку із заміщеним алкілом, заміщеним алкенілом, арилом, циклоалкілом і так далі, є такими: алкокси являє собою -ORe; алканоїл являє собою C(=O)Re; арилокси являє собою -ОАr; алканоїлокси являє собою -OC(=O)R e; аміно являє собою -NH2; алкіламіно являє собою -NHRe або -N(Re)2; ариламіно являє собою -NHAr або -NR6Ar; аралкіламіно являє собою -NH-R f-Ar, алканоїламіно являє собою -NH-C(=O)R e; ароїламіно являє собою -NH-C(=O)Ar; аралканоїламіно являє собою -NH-C(=O)R f-Ar; тіол являє собою -SH; алкілтіо являє собою -SRe; арилтіо являє собою -SAr; аралкілтіо являє собою -S-Rf-Ar; алкілтіоно являє собою -S(=O)Re; арилтіоно являє собою S(=O)Ar; аралкілтіоно являє собою -S(=O)Rf-Ar; алкілсульфоніл являє собою -SO(q )Re; арилсульфоніл являє собою -SO(q )Ar; арилсульфоніламін являє собою -NHSO(q )Ar; алкілсульфоніламін являє собою -NHSO2Re; аралкілсульфоніл являє собою -SO(q)R fAr; сульфонамідогрупа являє собою -SO2NH2; заміщений сульфонамід являє собою -SO2NHRe або -SO2N(Re)2; нітрогрупа являє собою -NO2; група карбокси являє собою -СО2Н; карбамільна група являє собою -CONH2; заміщений карбаміл являє собою -C(=O)NHR 9 або -C(=O)NR 9Rh; алкоксикарбоніл являє собою -C(=O)ORe; карбоксіалкіл являє собою -Rf-CO2H; сульфонова кислота являє собою -SO3H; арилсульфоніламін являє собою -NHSO(q)Ar; гуанідиногрупа являє собою ,а група уреїдо являє собою , де: Re являє собою алкіл або заміщений алкіл згідно з визначеним вище; Rf являє собою алкілен або заміщений алкілен згідно з визначеним вище; Rg і Rh вибрані серед алкілу, заміщеного алкілу, арилу, аралкілу, циклоалкілу, гетероциклу і гетерарилу; Аг являє собою арил згідно з визначеним вище, a q приймає значення 2 або 3. Зазначені в даному описі групи та їхні замісники можуть добиратися фахівцем у даній галузі для одержання стабільних компонентів і сполук. Сполуки за даним винаходом можуть утворювати солі, що також охоплюються об'ємом винаходу. При цьому кращими є фармацевтично прийнятні (тобто нетоксичні, фізіологічно прийнятні) солі, хоча корисними, наприклад, при виділенні або очищенні сполук за даним винаходом можуть бути також інші солі. Сполуки за даним винаходом можуть утворювати солі з лужними металами, такими як натрій, калій і літій, із лужноземельними металами, такими як кальцій і магній, з органічними основами, такими як біциклогексиламін, трибутиламін, піридин, та амінокислотами, такими як аргінін, лізин і т.п. Такі солі можуть одержуватися за допомогою процесів, добре відомих фа хівцям у даній галузі. Сполуки за даним винаходом можуть утворювати солі з різноманітними органічними і неорганічними кислотами. Цими солями можуть бути такі, що утворюються з хлористим воднем, бромистим воднем, метансульфоновою кислотою, сірчаною кислотою, оцтовою кислотою, трифтороцтовою кислотою, щавлевою кислотою, малеїновою кислотою, бензолсульфоновою кислотою, толуолсульфоновою кислотою та з іншими різноманітними кислотами (ними можуть бути, наприклад, нітрати, фосфати, борати, тартрати, цитрати, сукцинати, бензоати, аскорбати, саліцилати і т. п.). Одержувати такі солі можна за допомогою процесів, добре відомих фахівцям у даній галузі. Сольові форми запропонованих сполук можуть використовуватися для підвищення ступеня розчинення активних сполук та їх біодоступності при пероральному введенні. Крім того, можна утворювати також цвитеріони ("внутрішні солі"). Усі стереоізомери сполук за даним винаходом розглядаються як такі, що використовуються чи то в сумішах, чи то в чистій або в практично чистій формі. Визначення сполук відповідно до винаходу о хоплює всі можливі стереоізомери та їх суміші. До них належать рацемічні форми і виділені оптичні ізомери, що мають зазначену активність. Рацемічні форми можуть бути розділені за допомогою таких фізичних методів, як, наприклад, фракційна кристалізація, сепарація або кристалізація діастереомерних похідних, або ж розділяння за допомогою хіральної колоночної хроматографії. Індивідуальні оптичні ізомери можуть бути отримані із рацематів за допомогою звичайних методів, як-от утворення солі з оптично активною кислотою з наступною кристалізацією. Сполуки за даним винаходом можуть також мати форми проліків. Будь-яка сполука, розрахована на перетворення in vivo для утворення біоактивної речовини (тобто, сполуки за формулою І), являє собою проліки, що відповідають ідеї й охоплюються об'ємом даного винаходу. Фахівцям у даній галузі добре відомі різноманітні форми проліків. Приклади таких похідних-проліків можна знайти в таких першоджерелах: a) Design of Prodruqs. edited by Η. Bundgaard, (Elsevier, 1985) and Methods in Enzvmoloav. Vol. 42, p.309396, edited by K. Widder, et al. (Acamedic Press, 1985); b) A Te xtbook of Drug Design and Development, edited by Krosgaard-Larsen and H. Bundgaard, Chapter 5, "Design and Application of Prodrugs," by H. Bundgaard, p.113-191 (1991); і c) Н. Bundgaard, Advanced Drug Delivery Reviews. 8, 1-38 (1992), включених тут в усій їхній повноті шляхом посилання. Крім того, цілком зрозуміло, що сольвати (наприклад, гідрати) сполук за формулою (І) також лежать у межах об'єму даного винаходу. Процеси сольватації в цілому добре відомі фахівцям у даній галузі. До числа кращих сполук за формулою (І) належать такі, що мають наведену нижче структур у: До числа кращих належать сполуки, що мають структур у згідно з формулою (І*): (І*) їхні енантіомери, діастереомери, солі і сольвати, де: X є вибраним серед -О-, -ОС(=О)-, -S-, -S(=O)-, -SO2-, -C(=O)-, -CO 2-, -NR8-, -NR8C(=O)-, -NR 8C(=O)NR9-, NR8CO2-, -NR8SO 2-, -NR8SO 2NR9-, -SO2NR8-, -C(=O)NR 8-, галогену, нітро і ціано, або X є відсутнім; Υ являє собою -C(=O)NR 10-, -NR10aC(=O)NR 10-, -NRi0SO 2-, -SO2NR10-, -C(=O)-, -CO2-або -ОС(=О)-; В являє собою необов'язково заміщений циклоалкіл, гетероцикл або гетероарил; або арил, заміщений одним R11 і від нуля до двох R 12; або коли Υ являє собою -C(=O)NR 10-, тоді В також може бути вибраний серед -C(=O)R13, -CO 2R13 і -C(=O)NR 13R13a; R1 і R5 вибрані незалежно один від одного серед водню, алкілу, заміщеного алкілу, -OR14, -SR 14, OC(=O)R14, -CO2R14, -C(=O)NR 14R14a, -NR14R14a, -S(=O)R14, -SO2R14, -SO2NR14R14a, -NR14SO2NR14aR14b , NR14aSO2R 14, -NR14C(=O)R14a, -NR14CO2R 14a , -NR 14C(=O)NR 14aR14b, галогену, нітро і ціано; R2 являє собою водень або С 1-4алкіл; R3 являє собою водень, метил, перфторметил, метокси, галоген, ціано, NH2 або NH(СН3); R4 вибраний серед: a) водню за умови, що R4 не ε воднем, якщо X являє собою -S(=O)-, -SO2-, -NR 8CO2- або -NR 8SO2-; b) алкілу, алкенілу й алкінілу, необов'язково заміщених групою кето і/або від одного до чотирьох R17; c) арилу і гетероарилу, необов'язково заміщених від одного до трьох R16; і d) гетероциклу і циклоалкілу, необов'язково заміщених гр упою кето і/або від одного до трьох R16; або e) R 4 є відсутнім, якщо X є галоген, нітро або ціано; R6 приєднаний до будь-якого доступного атому вуглецю фенільного кільця А і в усіх випадках є незалежно вибраним серед алкілу, галогену, трифторметокси, трифторметилу, гідрокси, алкокси, алканоїлу, алканоїлокси, тіолу, алкілтіо, уреїдо, нітро, ціано, карбокси, карбоксіалкілу, карбамілу, алкоксикарбонілу, алкілтіоно, арилтіоно, арилсульфоніламіну, алкілсульфоніламіну, сульфонової кислоти, алкілсульфонілу, сульфонамідо, фенілу, бензилу, арилокси і бензилокси, де кожна група R6, у свою чергу, може бути заміщена одним або двома R18; R8 і R9 вибрані незалежно один від одного серед водню, алкілу, заміщеного алкілу, арилу, циклоалкілу, гетероциклу і гетероарилу; R10 і R10a вибрані незалежно один від одного серед водню, алкілу, заміщеного алкілу, алкокси й арилу; R11 вибраний серед необов'язково заміщеного циклоалкілу, гетероциклу й гетероарилу; R12 вибраний серед алкілу, R17 і С1-4алкілу, заміщеного групою кето (=O) і/або від одного до трьох R17; R13 і R13a вибрані серед водню, алкілу і заміщеного алкілу; R14, R14a і R14b вибрані незалежно один від одного серед водню, алкілу, заміщеного алкілу, арилу, циклоалкілу, гетероциклу і гетероарилу, за винятком того, що коли R14 є Зв'язаний із сульфонільною групою, як у -S(=O)R14 , -SO 2R14 і -NR14aSO2R14, тоді R14 не є воднем; R16 вибраний серед алкілу, R17 і С1-4алкілу, заміщеного групою кето (=O) і/або від одного до трьох R17; R17 вибраний серед галогену, галогеналкілу, галогеналкокси, нітро, ціано, -SR23, -OR23, -NR23R24, NR23SO2R25, -SO 2R25 , -SO 2NR23R24, -CO2R 23, -C(=O)R 23, -C(=O)NR 23R24 , -OC(=O)R23, -OC(=O)NR 23R24 , NR23C(=O)R24, -NR23CO 2R24 , арилу або гетероарилу, необов'язково заміщеного від одного до трьох R 26; або циклоалкілу чи гетероциклу, необов'язково заміщеного групою кето(=О) і/або від одного до трьох R26; R18 і R26 вибрані незалежно один від одного серед С 1-6алкілу, С2-6алкенілу, галогену, галогеналкілу, галогеналкокси, ціано, нітро, аміно, С1-4алкіламіно, аміно-С1-4алкілу, гідрокси, гідрокси-С 1-4алкілу, алкокси, С14алкілтіо, фенілу, бензилу, фенілокси і бензилокси; R23 і R24 кожний є незалежно вибраним серед водню, алкілу, алкенілу, заміщеного алкілу, заміщеного алкенілу, арилу, циклоалкілу, гетероарилу і гетероциклу", R25 вибраний серед алкілу, заміщеного алкілу, арилу, гетероарилу, циклоалкілу і гетероциклу; і m приймає значення 0, 1, 2, 3. Кращими сполуками за формулою (І*) є такі, що мають формулу (Іа): (Ia) а також їхні фармацевтично прийнятні солі, проліки і сольвати, де: R3 являє собою метил, -CF3 або -OCF3; X являє собою -С(=О)-, -NR8C(=O)- або -C(=O)NR 8-, де R8 є водень або С 1-4алкіл; Υ являє собою -C(=O)NH-, -NHC(=O)NH-, -NHC(=O)- або -NHSO2-; В являє собою необов'язково заміщений моноциклічний або біциклічний циклоалкіл, гетероарил або гетероцикл, арил, заміщений, принаймні, одним R11 і від нуля до двох R12 або, коли Υ являє собою -C(=O)NH-, В може бути вибраний серед -C(=O)R13, -CO 2R13 і -C(=O)NR 13R13a; R4 являє собою водень, С2-6алкіл, С1-4алкіл, необов'язково заміщений від одного до трьох R 17, арил або гетероарил, необов'язково заміщений від одного до трьох R 16, або циклоалкіл чи гетероцикл, необов'язково заміщений групою кето (=O) і/або від одного до трьох R16; R6a і R6b вибрані незалежно один від одного серед водню, С1-6алкілу, заміщеного С 1-4алкілу, галогену, трифторметокси, трифторметилу, -OR27, -С(=О)алкілу, -ОС(=О)алкілу, -NR27R28, -SR27 , -NO 2, -CN, -CO 2R27 , CONH2, -SO3H, -S(=О)алкілу, -S(=O)арилу, -NHSO2-арилуR27, -SO 2NHR27, -CONHR27 i -NHC(=O)NHR27; R11 являє собою циклоалкіл, гетероцикл або гетероарил, необов'язково заміщений від одного до двох R16; R13 і R13a являють собою водень, алкіл або заміщений алкіл; R12 і R16 вибрані незалежно один від одного серед С 1-4алкілу, R17 і С1-4алкілу, заміщених кетогрупою і/або від одного до двох R17; R17 вибраний серед галогену, гідрокси, С1-4алкокси, трифторметилу, трифторметокси, ціано, нітро, фенілу, бензилу, фенілокси, бензилокси, NH2, NH(C1-4алкілу), N(C1-4алкілу)2, С3-7циклоалкілу і п'яти- або шестичленного гетероарилу чи ге тероциклу, і R27 і R28 вибрані серед водню, С1-4алкілу, фенілу, С3-7циклоалкілу і від п'яти- до шестичленного гетероциклу або гетероарилу. Ще кращими є сполуки, що мають наведену вище формулу (Іа), де: R3 являє собою метил, -CF3 або -OCF3; X являє собою -С(=О)-, -C(=O)NH- або -С(=О)N(С1-4алкiл)-; Υ являє собою -C(=O)NH-; В являє собою: С3-7циклоалкіл, необов'язково заміщений від одного до двох R 7; п'ятичленний гетероарил, необов'язково заміщений від одного до двох R7; п'яти- або шестичленний гетероцикл, необов'язково заміщений від одного до двох R7; арил, заміщений, принаймні, одним R11 і необов'язково заміщений від нуля до двох R12; або коли уявляє собою -C(=O)NH-, тоді В може також бути вибраний серед -С(=О)(алкілу), СО2(алкілу) і -C(=O)NH(алкілу); R4 являє собою водень, С2-6алкіл, С1-4алкіл, необов'язково заміщений від одного до трьох R 17, арил або гетероарил, необов'язково заміщений від одного до трьох R 16, або циклоалкіл чи гетероцикл, необов'язково заміщений групою кето (⊜) і/або від одного до трьох R16 ; R6a і R6b вибрані незалежно один від одного серед водню, С1-4алкілу, галоген у, трифторметокси, трифторметилу, гідрокси, С1-4алкокси, ціано, NH2, NH(C1-4алкілу) і Н(С1-4алкілу)2; R7 вибраний серед С 1-4алкілу, заміщеного С1-4алкілу, галогену, трифторметокси, трифторметилу, ціано, SR20, -OR20 , -NR20R21 , -NR20SO2R21, -SO 2R19 , -SO2NR20R21, -CO2R20, -C(=O)R20 , -C(=O)NR 20R21, -OC(=O)R 20, OC(=O)NR 20R21 , -NR20C(=O)R21 , -NR20CO2R21, фенілу, бензилу, С3-7циклоалкілу і від п'яти- до шестичленного гетероциклу або гетероарилу; R11 являє собою циклоалкіл, гетероцикл або гетероарил, необов'язково заміщений від одного до двох R16; R13 і R13а являють собою водень, алкіл або заміщений алкіл; R12 і R16 вибрані незалежно один від одного серед С1-4алкілу, R17 і С1-4алкілу, заміщеного групою кето і/або від одного до двох R17; R17 вибраний серед галогену, гідрокси, С1-4алкокси, трифторметилу, трифторметокси, ціано, нітро, фенілу, бензилу, фенілокси, бензилокси, NH 2, NH(C1-4алкілу), N(С1-4алкілу)2, циклопентилу, циклогексилу або п'яти- чи шестичленного гетероарилу або гетероциклу; R19 являє собою С 1-4алкіл, феніл, С3-7циклоалкіл або п'яти- - шестичленний гетероцикл чи гетероарил; R20 і R21 вибрані серед водню, С1-4алкілу, фенілу, С3-7циклоалкілу і від п'яти- до шестичленного гетероциклу або гетероарилу; і R27 і R28 вибрані серед водню, С1-4алкілу, фенілу, С3-7циклоалкілу і від п'яти- до шестичленного гетероциклу або гетероарилу. У сполуках за формулою (I) R3 являє собою переважно метил, -CF3 або -OCF3, і краще - метил; X являє собою переважно -С(=О)- або -C(=O)NH-; a Y являє собою переважно -C(=O)NH-. У кращому варіанті, коли X являє собою -C(=O)NH-, тоді R4 є С2-6алкіл або заміщений С 1-4алкіл, ще краще - С1-4алкіл або необов'язково заміщений бензил. Коли X являє собою -С(=О)-, тоді R4 у кращому варіанті являє собою необов'язково заміщений арил або гетероарил. Коли R4 являє собою гетероцикло, його вибирають переважно серед діазепінілу, морфолінілу, піперидинілу і піролідинілу, причому зазначений гетероцикл є необов'язково заміщеним узятими в кількості від одного до двох С 1-4алкілом, гідрокси, С1-4алкокси, фенілом і/або бензилом. Коли X являє собою -С(=О)-, a R4 є арил або гетероарил, тоді R4 являє собою переважно феніл, піридиніл, піримідиніл або піразиніл, необов'язково заміщений С 1-4алкілом, галогеном, гідрокси, С1-4алкокси, трифторметилом, трифторметокси, ціано, нітро, фенілом, бензилом, фенілокси, бензилокси, NH2, NH(С1-4алкілом), NC1-4алкілом)2, циклопентилом, циклогексилом або п'яти- чи шестичленним гетероарилом або гетероциклом. У сполуках за формулою (І) фенільне кільце А є переважно незаміщеним або має один замісник. Зазначений необов'язковий замісник R6a або R6b вибирають переважно серед С 1-4алкілу, галогену, трифторметокси, трифторметилу, гідрокси, С1-4алкокси, нітро і ціано, а в ще кращому варіанті замісником є R6a і, зокрема, метил або етил. У сполуках за формулою (І) кільце В являє собою переважно циклоалкільне, гетероарильне або гетероциклічне кільце, вибране серед: де Е, G, J і К вибрані серед О, S, NH і СН2 за умови, що коли q дорівнює 0, тоді J і K не є одночасно вибраними серед О і S; а М являє собою N або СН; де будь-який атом водню в Е, G, J, K і Μ у разі потреби може бути заміщений групою R7; R7 вибраний серед С1-4алкілу, заміщеного С1-4алкілу, галогену, три фторметокси, трифторметилу, гідрокси, -С1-4алкокси, -С(=О)алкілу, -ОС(=О)алкілу, NH2, NН(С1-4алкту), N(С1-4алкілу)2, -CN, -СО2алкілу, -CONH2, CONH(CH3), -CON(CH3)2, фенілу, бензилу, С3-7 циклоалкілу і від п'яти- до шестичленного гетероциклу або гетероарилу; n приймає значення 0, 1, 2; а p і q вибрані серед 0,1, 2, 3 або 4 за умови, що p і q, узяті разом, не є більше 4. Серед сполук за формулою (І) кращими є також такі, в котрих кільцем В є циклопропіл, оксазоліл або ізоксазоліл, що є незаміщеним або має один замісник R7. Зазначений замісник R7 вибирають переважно серед С1-4алкілу, галогену, трифторметокси, трифторметилу, гідрокси -С1-4алкокси, -С(=О)алкілу, -ОС(=О)алкілу, NH2, NН(С1-4алкілу), N(С1-4алкілу)2, -CN, -С О2-алкілу, -CONH2, фенілу, бензилу, С3-7циклоалкілу і від п'яти- до шестичленного гетероциклу чи гетероарилу, або С1-4алкілу, заміщеного групою гідрокси, аміно, алкіламіно, галогеном, трифторметилом, трифторметокси або ціано. У ще кращому варіанті R 7 є відсутнім або являє собою -С1-4алкокси. , Кращими є також сполуки, що мають формули (2а) і (2b): а також їхні фармацевтично прийнятні солі, проліки і сольвати, де: R3 являє собою метил або CF3; В являє собою феніл, що має, принаймні, один замісник R11 і від н уля до дво х замісників R12, або ж В може бути вибраний серед: де Е, G, J і К вибрані серед О, S, NH і СН2 за умови, що коли q дорівнює 0, тоді J і K не є одночасно вибраними серед О і S; Μ являє собою N або СН; де будь-який атом водню в Е, G, J, K і Μ у разі потреби може бути заміщений групою R7; R4a являє собою феніл або п'яти- чи шестичленний гетерарил, необов'язково заміщений не більш, ніж двома R16; R4b являє собою прямий або розгалужений С2-6 алкіл; циклоалкіл, необов'язково заміщений групою кето і/або не більш, ніж двома R16; гетероцикл, необов'язково заміщений групою кето і/або не більш, ніж двома R16; або С1-4алкіл, заміщений узятими в кількості до трьох галогеном, трифторметилом, групами ціано, гідрокси, алкокси, галогеналкілу, галогеналкокси, нітро, фенілом, фенілокси або бензилокси, де зазначена фенільна група, у свою чергу, необов'язково заміщена взятими у кількості від одного до двох R26; R6a являє собою нижчий алкіл, галоген, трифторметокси, трифторметил, гідрокси, C1-4алкокси, нітро, аміно, С1-4алкіламіно або ціано; R7 являє собою С 1-4алкіл, трифторметил, трифторметокси, галоген, ціано, нітро, аміно, С1-4алкіламіно, гідрокси, C1-4алкокси, феніл, бензил, фенілокси або бензилокси; R11 являє собою циклоалкіл, гетероцикл або гетероарил, необов'язково заміщений R16, узятим у кількості від одного до двох; R12 і R16 в усі х випадках є незалежно один від одного вибраними серед водню, алкілу, трифторметилу, трифторметокси, галогену, ціано, нітро, аміно, С1-4алкіламіно, гідрокси, алкокси, фенілу, бензилу, фенілокси і бензилокси; R26 вибраний серед С1-4алкілу, трифторметилу, трифторметокси, галогену, ціано, аміно, С1-4алкіламіно, гідрокси, алкокси, фенілу, бензилу, фенілокси і бензилокси; n приймає значення: 0,1 або 2; і p і q приймають значення 0, 1, 2, 3 або 4 за умови що p і q, узяті разом, мають значення не більше 4. Найкращими є сполуки за наведеними вище формулами (2а) або (2b), а також їхні фармацевтично прийнятні солі, проліки і сольвати, в котрих: R3 являє собою метил; В вибраний серед (a) циклопропілу або циклобутилу, необов'язково заміщеного відодного до двох R7; (b) фенілу, заміщеного п'яти- чи шестичленним гетероциклом і від нуля до дво х R 12, або (c) В є одним із: R4a являє собою феніл або піридил, необов'язково заміщений не більш, ніж двома R16, як згадано вище; R4b являє собою прямий або розгалужений С2-6алкіл або необов'язково заміщений бензил; R6a являє собою метил, етил, галоген, трифторметокси, трифторметил, гідрокси, метокси, етокси або ціано; R7, R12 і R16 вибрані незалежно один від одного серед С 1-4алкілу, трифторметилу, трифторметокси, галогену, ціано, нітро, аміно, С1-4алкіламіно, аміно-С1-4алкілу, гідрокси, гідрокси-С 1-4алкілу, галоген-С 1-4алкілу, С1-4алкокси, фенілу, бензилу, фенілокси і бензилокси; і n приймає значення 0 або 1. Застосування Сполуки відповідно до даного винаходу є селективними інгібіторами активності р38-кінази, і зокрема її ізоформ р38α і p38β. Таким чином, сполуки за формулою (І) є корисними в лікуванні станів, пов'язаних з активністю р38-кінази. До числа таких станів належать захворювання, при яких рівні цитокінів модулюються внаслідок внутрішньоклітинної передачі сигналів через р38, і зокрема захворювання, пов'язані з надпродукуванням цитокінів IL-1, IL-4, IL-8 і TNF-α. Використовуваний тут термін "лікування" включає до свого поняття як терапевтичні, так і профілактичні заходи, націлені, наприклад, на гальмування або затримку виникнення хвороби чи розладу, на досягнення повного або часткового позбавлення симптомів або стану хвороби і/або на полегшення, поліпшення, послаблення або виліковування хвороби чи розладу і/або їх симптомів. У тому разі, коли мова йде про інгібування "р-38α/β-кінази", це означає інгібування окремо або разом як р38α-, так і р38β-кінази. Отже, згадувана тут величина ІС 50 інгібування р-38α/β-кінази означає, що дана сполука є ефективною в інгібуванні принаймні однієї або ж обох кіназ р38α і ρ38β. Завдяки їхній активності як інгібіторів р-38α/β-кіназ сполуки за формулою (І) є корисними в лікуванні станів, зв'язаних з р-38, включаючи запальні захворювання, автоімунні захворювання, деструктивні порушення кісток, проліферативні порушення, ангіогенні порушення, інфекційні захворювання, нейродегенеративні захворювання і вирусні захворювання. Зокрема, специфічними станами і хворобами, котрі можна лікувати за допомогою сполук згідно з даним винаходом, є такі, як панкреатит (гострий або хронічний), астма, алергія, старечий дихальний дистрессиндром, хронічна обструктивна хвороба легенів, гломерулонефрит, ревматоїдний артрит, системний червоний вовчак, склеродермія, хронічний тироідит, хвороба Грейвса, автоімунний гастрит, діабет, автоімунна гемолітична анемія, автоімунна нейтропенія, тромбоцитопенія, атонічний дерматит, хронічний активний гепатит, міастенія, розсіяний склероз, запальна хвороба кишечника, виразковий коліт, хвороба Крона, псоріаз, реакція "трансплантат проти хазяїна", запальна реакція на ендотоксин, туберкульоз, атеросклероз, дистрофія м'язів, катексія, псоріазний артрит, синдром Рейтера, подагра, травматичний артрит, краснушний артрит, гострий синовіт, b-клітинний панкреатит, захворювання з масивною інфільтрацією нейтрофілів, ревматоїдний спондиліт, подагричний артрит та інші подагричні стани, мозкова малярія, хронічне запалення легенів, силікоз, легеневий саркоїдоз, резорбція кісток, відторгнення трансплантату, ли хоманка і міалгія внаслідок інфікування, кахексія внаслідок інфікування, мелоїдні утворення, утворення рубцевої тканини, виразковий коліт, пірез, грип, остеопороз, остеоартрит і пов'язане з мієломою множинне порушення кісток, гостра мієлогенна лейкемія, хронічна мієлогенна лейкемія, метастазна меланома, саркома Капоши, множинна мієлома, сепсіс, септичний шок і бактеріальна дизентерія, хвороба Альцгеймера, хвороба Паркінсона, церебральна ішемія або нейродегенеративне захворювання внаслідок травми; ангіогенні розлади, включаючи тверді пухлини, очну неоваскулізацію й інфантильну гемангіому; вірусні захворювання, включаючи гостру гепатитну інфекцію (у тому числі гепатит А, гепатит В і гепатит С) ВІЛ-інфекцію і CMV ретиніт, СНІД, ARC або злоякісні пухлини і герпес; інфаркт, міокардіальна ішемія, ішемія при серцевих приступах, гіпозия органів, судинна гіперплазія, реперфузійні травми серця і нирок, тромбоз, серцева гіпертрофія, тромбін-індуковане агрегатування тромбоцитів, ендотоксемія і/або синдром токсичного шоку, а також стани, пов'язані з простагландинендопероксидазосинтазою-2. Крім того, інгібітори р38 згідно з даним винаходу інгібують експресію таких індуцибельних прозапальних білків, як простагландинендопероксидазосинтаза-2 (PGHS-2), відома також під назвою циклооксигенази-2 (СОХ-2). Отже, до числа станів, пов'язаних з р38, належать також набряки, аналгезія, лихоманка і біль, як-от нейром'язовий біль, головний біль, біль від раку, зубний біль і артритний біль. Сполуки відповідно до даного винаходу можуть використовуватися також для лікування вірус-інфікованих станів у ветеринарії, таких як лентивірусні інфекції, включаючи, без обмеження, кінский інфекційний вірус анемії; або ретровирусних інфекцій, включаючи котячу вірусн у імунонедостатність, коров'ячу вірусну імунонедостатність і собачу вірусн у імунна недостатність. Значеннями використовуваних тут термінів "стан, пов'язаний із р38", та "захворювання чи розлади, пов'язані з р38", охоплюються всі вищеперелічені стани так, якби вони зазначалися в кожному конкретному випадку, а також будь-який інший стан, на який впливає р38-кіназна активність. Отже, даним винаходом для лікування таких станів пропонуються процеси, які передбачають уведення суб'єкту, що потребує такого лікування, ефективної кількості принаймні однієї сполуки за формулою (І) або її. Процеси лікування станів, пов'язаних із р38-кіназою, можуть включати у себе введення сполук за формулою (І) окремо або в комбінації їх між собою і/або з іншими підхожими терапевтичними засобами, корисними для лікування таких станів. Іншими терапевтичними засобами при цьому можуть бути, наприклад, кортикостероїди, роліпрам, калфостин, CSAID, 4-заміщені імідазо[1,2-А]хіноксаліни, [описані в US 4,200,750]; мерлейкін-10, глюкокортикоїди, саліцилати, окис азоту та інші імуносупресанти; інгібітори ядерної транслокації, як-от дезоксиспергуалін (DSG); нестероїдні протизапальні лікарські засоби (NSAID), такі як ібупрофен, целекоксиб і рофекоксиб; стероїди, такі як преднізон або дексаметазон; антивірусні засоби, такі як абакавір; антипроліферативні агенти, такі як метотрексат, лефлуномід, FK506 (такролім, програф); цитотоксичні лікарські засоби, як-от азатиприн і циклофосфамід; інгібітори TNF-α, такі як тенідап, антітіла проти TNF або розчинний рецептор TNF, і рапаміцин (сиролім чи рапамун) або їх похідні. Зазначені вище терапевтичні агенти при використанні в комбінаціях зі сполуками за даним винаходом можуть вживатися у кількостях, рекомендованих, наприклад, у настільному довіднику лікаря [Physicians' Desk Reference (PDR)], або у відповідності з рішенням, прийнятим фахівцем у даній галузі. У процесах за даним винаходом такого роду інші терапевтичні агенти можуть уводитися до введення сполук за даним винаходом, водночас або після їх введення. Винаходом передбачені також фармацевтичні композиції, придатні для лікування станів, пов'язаних із р38кіназою, включаючи стани, опосредковані TNF-α, IL-1 і/або IL-8, як описано вище. Композиції відповідно до даного винаходу можуть, як зазначено вище, містити інші терапевтичні агенти і складатися із застосуванням, наприклад, звичайних твердих або рідких носіїв чи розріджувачів, а також фармацевтичних добавок, що відповідають способу бажаного введення (наприклад, ексципієнтів, зв'язуючих, консервантів, стабілізаторів, ароматизаторів і т.п.), згідно з добре відомими методиками складання фармацевтичних препаратів. Сполуки за формулою (І) можуть уводитися будь-яким способом, підходящим для даного хворого стану і може залежати від конкретної ділянки, що є об'єктом лікування, і кількості лікарського засобу, яку потрібно на цю ділянку постачати. У загальному випадку для хвороб, пов'язаних зі шкірою, кращим є місцевий спосіб уведення медикаменту, а для ракових або передракових станів - системне лікування. Поряд з цим завбачаються також інші шляхи постачання. Наприклад, сполуки за даним винаходом можуть уводитися: пероральним шляхом у формі таблеток, капсул, гранул, порошків або рідких складів, включаючи сиропи; місцевим шляхом у формі розчинів, суспензій, гелей або мазей; під язик; трансбукальним шляхом; парентеральним шляхом, наприклад, підшкірним, внутрішньовенним, внутрішньом'язовим або внутрішньочеревним, а також шляхом ін'єкцій (наприклад, у формі стерильного водного або неводного розчину чи суспензії); через ніс, наприклад, аерозолем для інгаляцій; місцевим шляхом у формі крему або мазі; ректальним шляхом у формі супозиторіїв; ліпосомальним шляхом, тощо. Уводитися можуть також дозовані препарати, що містять нетоксичні, фармацевтично прийнятні носії або розріджувачі. Сполуки за даним винаходом можуть уводитися у формі, розрахованій на негайне звільнення, або формі, розрахованій на тривале звільнення. Негайне звільнення і тривале звільнення лікарської речовини можуть здійснюватися за допомогою підхожих фармацевтичних композицій або, особливо у випадку тривалого звільнення, за допомогою таких пристроїв, як підшкірні імплатати або осмотичні насоси. До складу типових композицій для місцевого уведення входять місцевий носій, такий як PLASTIBASE® (мінеральне масло, гельоване поліетиленом). Типові композиції для перорального уведення можуть мату форму, наприклад, суспензій, до складу яких входять мікрокристалічна целюлоза для збільшення об'єму, альгінова кислота або альгінат натрію як суспендувальний агент, метилцелюлоза як підсилювач в'язкості, а також добре відомі в даній галузі підсолоджувачі та ароматизатори, або таблеток, розрахованих на негайне звільнення, до складу яких входять, наприклад, мікрокристалічна целюлоза, дифосфат кальцію, крохмаль, стеарат магнію і/або лактоза і/або інші ексципієнти, зв'язуючі, наповнювачі, розпушувачі, розріджувачі і мастила, добре відомі в даній галузі. При пероральному прийомі сполуки за даним винаходом можуть постачатися також у підязичний і/або внутрішньоротовий спосіб уведення, наприклад, у формі сформованих, пресованих або висушених заморожуванням таблеток. До складу типових композицій можуть входити швидкорозчинювальні розріджувачі, такі як маноза, лактоза, сахароза і/або циклодекстрини. Крім того, такі препарати можуть містити високомолекулярні ексципієнти, зокрема, целюлозу (AVICEL®) або поліетиленгліколі (PEG); ексципієнт для сприяння адгезії на слизистих оболонках, тобто гідроксипропілцелюлозу (НРС), гідроксипропілметилцелюлозу (НРМС), натрійкарбоксиметилцелюлозу (SCMC) і/або співполімер малеїнового ангідриду (наприклад, GANTREZ®); регулятори звільнення, такі як поліакриловий співполімер (наприклад, CARBOPOL 934®). Для полегшення процесів виготовлення і використання можуть додаватися також мастила, гліданти, ароматизатори, барвники і стабілізатори. Типові композиції для введення за допомогою назальних аерозолей або інгаляторів мають форму розчинів, які можуть містити, наприклад, бензиловий спирт або інші підхожі консерванти, промотори абсорбції для збільшення поглинання і біодоступності, а також інші солюбілізатори і диспергатори, добре відомі фа хівцям у даній галузі. Типові композиції для парентерального уведення мають форму розчинів або суспензій для ін'єкцій, що можуть містити, наприклад, підхожі нетоксичні, парентерально прийнятні розріджувачі або розчинники, а саме манозу, 1,3-бутандіол, водний розчин Рінгера, ізотонічний розчин хлориду натрію або інші підхожі диспергатори, зволожувачі і суспендувальні агенти, включаючи синтетичні моно- та дигліцериди і жирні кислоти, наприклад, олеїнову кислоту. Типові композиції для ректального введення мають форму супозиторіїв, що можуть містити, наприклад, підхожі неподразнюючі ексципієнти, такі як какаомасло, синтетичні гліцеридні естери або поліетиленгліколі, що є твердими при звичайних температурах, але розм'якшуються і/або розчиняються в ректальній порожнині, звільняючи лікарський засіб. Ефективна кількість сполуки за даним винаходом може бути легко визначена фахівцем у даній галузі і в типових випадках дозування для ссавця складає, приблизно, від 0,05 до 100мг активної сполуки на кілограм маси тіла на день. Вона може вводитися як повною дозою за один прийом, так і розділеними дозами за декілька прийомів, наприклад, від 1 до 4 разів за день. Цілком зрозуміло, що конкретна доза і частота прийому препарату можуть бути різними і залежать від таких чинників, як активність конкретної використовуваної сполуки, метаболічна стабільність і тривалість дії цієї сполуки, вид, вік, маса тіла, загальний стан здоров'я, стать і харчовий раціон пацієнта, спосіб і час введення лікарського препарату, швидкість екскреції, медикаментозне комбінування і серйозність конкретного стану. До числа кращих об'єктів лікування належать тварини і найкраще -ссавці, а саме людина і свійські тварини, такі як собаки, кішки, коні і т.п.. Таким чином, використовуваний у даному описі термін "пацієнт" означає будь-який об'єкт лікування, котрим у найкращому варіанті є ссавець, на якого впливають рівні ферменту р38. Сполуки за формулою (І), включаючи сполуки, описані в розглянутих тут прикладах, були піддані описаним нижче випробуванням і показали інгібуючу активність p38 ферментів і TNF-α. Біологічні випробування Одержання р38-кіназ Комплементарні ДНК ізоферментів p38β і g людини клонували за допомогою полімеразно-ланцюгових реакцій (PCR). Ці кДНК субклонировали у pGEX-вектор експресії (Pharmacia). Злитий GST-p38-білок експресували в Е. Соlі й очищали від бактеріального дебрісу за допомогою афінної хроматографії на глутатіонагарозному гелі. Злитий білок р38 активували інкубуванням з визначально активним МКК6. Активний р38 відокремлювали від МКК6 за допомогою афінної хроматографії. Визначально активний МКК6 одержували за методикою, описаною в [Raingeaud et. al., Моl. Cell. Вiоl., 1247-1255 (1996)]. Продукування TNF-α LPS-стимульованими РВМС клітинами Використовували гепаринізовану суцільну кров людини від здорових добровольців. Моноядерні клітини периферійної крові (РВМС) очищали із людської суцільної крові центрифугуванням у градієнті густини ФіколаХіпака (Ficoll-Hypaque) і повторно суспендували при концентрації 5´106/мл у середовищі для кількісного визначення (середовище RPMI, що містило 10% ембріональної бичачої сироватки). Клітинну суспензію в кількості 50мкл інкубували з 50мкл випробуваної сполуки (4-кратна концентрація в середовищі для кількісного визначення, що містило 0,2% ДМСО) у 96-ямкових планшетах для культури тканини протягом 5 хвилин при кімнатній температурі. Після цього до клітинної суспензії добавляли 100мкл ліпополісахариду (LPS) (200нг/мл вихідного розчину), і культуральний планшет витримували в інкубаторі протягом 6 годин при 37°С. Після інкубування культуральне середовище збирали і зберігали при -20°С. Концентрацію TNF-α у середовищі визначали за допомогою стандартного набору для твердофазного імуноферментного аналізу (ELISA, виробник фірма Pharmingen-San Diego, Каліфорнія). Концентрації TNF-α і величини IС50 (концентрації сполуки, що інгібує LPS-стимульоване продукування TNF-α на 50%) для випробуваних сполук обчислювали шляхом аналізу з лінійною регресією. Аналіз р38 Аналіз проводили на 96-ямкових планшетах з V-подібними ямками. Кінцевий аналітичний об'єм становив 60мкл і складався із трьох 20мкл порцій ферменту, субстратів (МБР і АТР) і випробуваних сполук в аналітичному буфері (50мМ Tris pH7,5, 10мМ МgСІ2, 50мМ NaCI і 1мМ DTT). Бактеріально експресований, активований р38 попередньо інкубували з випробуваними сполуками протягом 10хв. перед ініціюванням реакційної суміші із субстратами. Реакцію проводили в термостаті при температурі 25°С протягом 45хв. і припиняли додаванням 5мкл 0,5 EDTA до кожного зразка. Реакційну суміш відсмоктували на попередньо зволожений фільтр за допомогою харвестера Skatron Micro96 Cell Harvester (Skatron, Inc), а потім промивали фізіологічним розчином, забуференим фосфатом (PBS). Далі фільтр висушували в мікрохвильовій печі протягом 1хв., обробляли сцинтиляційним воском MeltilLex A (Wallac) і підліковували на сцинтиляційному лічильнику Microbeta, модель 1450 (Wallac). Результати інгібування визначали методом найменших квадратів з нелінійною регресією, використовуючи програму Prizm (GraphPadSoftware). Кінцеві концентрації реагентів в аналізі складали: АТР - 1мкМ; [γ- 33Ρ]ΑΤΡ - 3нМ; МВР (Sigma, №М1891) - 2мкг/ямку; р38 - 10нМ; ДМСО - 0,3%. Продукування TNF-α у миші, стимульованої LPS Мишам (самки ВаІb/с віком 6-8 тижнів, Нагіап Labs; кількість тварин у групі лікування n=8) внутрішньочеревним шляхом уводили 50мкг/кг ліпополісахариду (LPS; штам Ε. соli 0111:В4, Sigma) суспендованого в стерильному фізіологічному розчині. Через дев'яносто хвилин мишей усипляли інгаляцією СО2:О 2 й відбирали зразок крові. Сироватку відокремлювали й аналізували на концентрацію TNF-α за допомогою промислового приладу ELISA згідно з інструкціями виробника (R&D Systems, Minneapolis, Мінесота). Випробувані сполуки вводили пероральним шляхом за різним графіком до ін'єкції LPS. Сполуки, що вводилися, мали форму суспензії або розчину з різними носіями і солюбілізаторами. Скорочення З метою спрощення даного опису, включаючи розглянуті нижче процеси одержання сполук і приклади практичного здійснення винаходу, в ньому застосовані такі скорочення: Ph - феніл Bz - бензил t-Bu - третинний бутил Me - метил Et - етил Рr - пропіл Iso-P - ізопропіл МеОН - метанол ЕtOН - етанол EtOAc - е тилацетат Вос - трет-бутилоксикарбоніл DCM - ди хлорметан DCE - 1,2-дихлоретан ДМФА - диметилформамід ДМСО - диметилсульфоксид TFA - трифтороцтова кислота ТГФ - тетрагідрофуран HATU - О-(7-азабензотриазол-1-іл-N-N-N'-N'-тетраметилуроній-гексафторфосфат КОН - гідроксид калію K2СО3 - карбонат калію РОСІ3 - оксихлорид фосфору EDC або EDCI - 1-(3-диметиламінопропіл)-3-етилкарбодііміду гідрохлорид DIPEA - діізопропілетиламін HOBt - 1-гідроксибензотриазолгідрат m-СРВА - м-хлорпербензойна кислота NaH - гідрид натрію NaOH - гідроксид натрію Pd - паладій Pd/C - паладй на вугіллі хв. - хвилина L - літр ml - мілілітр мкл - мікролітр г - грам мг - міліграм моль - моль ммоль - мілімоль meq - міліеквівалент RT або rt - кімнатна температура ret. t. - HPLC час витримування (хвилини) sat або sat'd - насичений aq. - водний TLC - тонкошарова хроматографія HPLC - рідинна хроматографія високого розрізнювання RP HPLC - HPLC з оберненою фазою LC/MS - HPLC (див. вище) / мас-спектрометрія MS - мас-спектрометрія ЯМР - ядерний магнітний резонанс т.пл. - точка плавлення У Прикладах практичного здійснення винаходу позначення, що стосуються даних HPLC, відбивають такі умови: а. Колонка: YMC ODSA S-5 5u C18 4,6´50мм; Розчинник: розчинник А=10% МеОН/90% вода/0,1% ТГФ і розчинник В=90% МеОН/10%вода/0,1% ТГФ; Спосіб: 4хв. градієнт; b. Колонка: YMC s5 ODS 4,6´50мм; Розчинник: розчинник А=10% МеОН/90% вода/0,2% Н3РО4 і розчинник В=90% МеОН/10% вода/0,2% Н3РО4; Спосіб: 4хв. градієнт. Способи одержання У загальному випадку сполуки за формулою І можуть бути одержані у відповідності з наведеними нижче схемами процесів і компетенцією фахівця, що здійснює їх практичне втілення, а також у відповідності з процесами, описаними у патентних заявках США №№10/036,293 і 09/573,829, включених тут в усій їхній повноті шляхом посилання. На наведених нижче схемах символи FVR7, Χ, Υ, m, n і p мають значення, що відповідають поданому тут опису сполук за формулою (І). Символ "В" охоплює своїм значенням необов'язково заміщені циклоалкільні, гетероциклічні або гетероарильні кільця у формулі (І) включаючи без обмеження кільця такого типу: Наявні у продажу сполуки за формулою (І) можуть приводитися у взаємодію з оксалілхлоридом під нагрівом із наступним концентруванням у вакуумі і взаємодією з аміном Β-ΝΗ 2 при наявності основи, такої як діізопропіламін, в органічному розчиннику, такому як DCM, з одержанням на виході сполуки (2). Сполуку (2) приводять у взаємодію з воднем при наявності, наприклад, Pd каталізатора у спиртовому розчиннику, наприклад, ЕtOН, при кімнатній температурі, з одержаням Сполуки (3). Сполуку (3) у подальшому можна використовува ти у відповідності зі Схемою 2, отримуючи в результаті Сполуку (8). Схема 2 З метою утворення сполуки (4) 3-метил-1-піррол-2,4-діетиловий естер може бути приведений у взаємодію з хлораміном у середовищі етеру. Взаємодія сполуки (4) у формаміді з оцтовою кислотою дає сполуку (5). Далі, використовуючи реакцію сполуки (5) з DIPEA і РОСІа у толуолі, утворюють сполуку (6). Сполука (6), у свою чергу, може бути приведена у взаємодію з DIPEA і сполукою (3) у ДМФА з утворенням сполуки (7). Після цього шляхом реакції сполуки (7) з NaOH в ТГФ утворюють проміжну кислоту, яку піддають обробці HOBt, EDCI і підхожим аміном (NR2R10) У ДМФА, одержуючи сполуку (8). Для приготування сполуки (3) може бути застосований процес із таких стадій: 1) реакція продажної 4аміно-3-метилбензойної кислоти з N-(трет-бутоксикарбоніл)ангідридом у ТГФ, у результаті якої утворюється проміжний продукт -Вос-захищений анілін; 2) реакція проміжного аніліну з (3-диметиламінопропіл)-3етилкарбодіімід-гідрохлоридом, HOBt і ДМФА, з наступним додаванням метоксіамін-гідрохлориду і DIPEA, в результаті чого утворюється проміжний Вос-захищений N-метоксіамід; і 3) реакція цього проміжного метоксіаміду в розчині НСІ у діоксані, в результаті якої утворюється сполука (3) у формі гідрохлориду. Іншим чином сполука (3) може бути отримана у відповідності зі Схемою 1. Схема 3 З метою одержання сполуки (10) може бути застосована реакція заміщеного гідроксамату (9) з кислотою, наприклад, НСІ, у безводному МеОН. Далі сполуку (10) приводять у взаємодію з водним розчином основи, наприклад, КОН під нагрівом, одержуючи сполуки (11). Сполуку (11), у свою чергу, приводять у взаємодію з аміном В-NH2 при наявності зв'язувального агента, такого як HATU, й основи, такої як діізопропіламін, в органічному розчиннику, наприклад, N-метилпіролідиноні, одержуючи в результаті сполуку (12). Гідроксамат (9) може бути отриманий у відповідності зі схемами 1 і 2 і/або так, як описано в патентній заявці США №10/036,293. Схема 4 Для утворення сполуки (14) може бути використана реакція між продажною сполукою (13) і сульфонілхлоридом при наявності такої основи як TEA, в органічному розчиннику, наприклад, DCM. Далі, застосовуючи реакцію сполуки (14) із воднем при наявності, наприклад, Pd каталізатора у розчиннику, такому як МеОН, утворюють сполуку (15). Сполуку (15), у свою чергу, приводять у взаємодію з хлоридом (6) (див.Схему 2) в органічному розчиннику, такому як ДМФА, при кімнатній температурі, одержуючи сполуку (16). Далі за допомогою реакції сполуки (16) із водним розчином КОН в умовах нагріву утворюють сполуку (17), яку приводять у взаємодію з аміном R2NH2 при наявності зв'язувального реагенту, такого як EDCI, і основи, наприклад, діізопропіламіну в органічному розчиннику, такому як ДМФА, одержуючи цільову сполуку (18). Схема 5 Сполуку (19) можна приготувати шляхом реакції хлорпіролтриазину (6) (див. С хему 2) з аніліном (13) (див., наприклад, Схему 4) у безводному ДМФА при кімнатній температурі. Реакція сполуки (19) із водним розчином основи, наприклад, NaOH при нагріванні дозволяє одержати сполуку (20). Сполуку (20) приводять у взаємодію з аміном R4NH2 при наявності зв'язувального реагенту, такого як HOBt, у присутності основи, наприклад, діізопропіламіну або без неї в органічному розчиннику, такому як ДМФА, одержуючи сполуку (21). Далі готують сполуку (22), використовуючи реакцію сполуки (21) з воднем при наявності такого каталізатора, як Pd/C, в органічному розчиннику, наприклад, МеОН. І нарешті, приводячи сполуку (22) в реакцію із ізоціанатом в органічному розчиннику, такому як DCE, отримують сполуку (23). Схема 6 У цьому процесі передусім можна застосувати реакцію продажної сполуки (13) з карбонілдіімідазолом і аміном B-NH2 в органічному розчиннику, такому як DCE, у результаті якої утвоорюється сполука (24). Далі реакція сполуки (24) із воднем при наявності каталізатора, такого як Pd, у спиртовому розчиннику, такому як ЕtOН, дає сполуку (25). Сполуку (25), у свою чергу, приводять у взаємодію з хлоридом (6) в органічному розчиннику, такому як ДМФА, о тримуючи сполуку (26). Далі застосовують реакцію сполуки (26) із водним розчином NaOH при нагріванні, в результаті чого утворюється продукт (27), який може бути приведений у взаємодію з аміном R4NH2 у присутності зв'язувального реагенту, такого як EDCI, й основи, такої як діізопропіламін, в органічному розчиннику, такому як ДМФА, з одержанням цільової сполуки (28). Схема 7 На Схемі 7 відображений процес одержання сполук (4а) (див. Схему 2), у котрих R 3 являє собою групу аміно (4b), галоген (4с) або ціано (4d). Для приготування сполуки (30) можна гліцинетиловий естер (29) додати до алкілалкоксиметиленціаноацетату в інтервалі температур від кімнатної до 80°С. Утворену таким чином сполуку (30) циклізуют, внаслідок чого після обробки сильною основою, такою як літій-гексаметилдисилазан, в інтервалі температур від -78 С до кімнатної в органічному розчиннику, такому як ТГФ, утворюється пірол (4b). Пірол (4b) може бути перетворений на галогенну сполуку за допомогою нітриту натрію в органічному розчиннику, такому як ДМФА, і джерела галогену, такого як СuВr, з одержанням сполуки (4с). Сполука (4с), у свою чергу, може бути перетворена на сполуку (4d) під дією на неї CuCN в органічному розчиннику, такому як NMP, при підвищеній температурі. Іншим чином сполука (4b) може бути безпосередньо перетворена на сполуку (4d) за допомогою нітриту натрію в органічному розчиннику, такому як ДМФА, у присутності джерела ціаніду, такого як CuCN. Далі для одержання сполуки за формулою (І) сполуки (4a)-(4d) можуть використовува тися в процесах згідно з попередніми схемами (наприклад, Схемою 2). Схема 8 Відновлення естерної групи піролтриазину 5 (див. Схему 2) за допомогою підхожого відновлювана, такого як LAH, в апротонному органічному розчиннику, такому як ТГФ, дозволяє утворити спирт (31). Спирт (31) окисляють до альдегіду (32) підхожим окислювачем, таким як реагент Джонса (Jones). Далі альдегід (32) приводять у взаємодію з підхожим металоорганічним реагентом (таким, як фенілмагнійбромід), одержуючи проміжний вторинний спиртовий продукт, який окисляють до кетону (33) підхожим окислювачем, наприклад, реагентом Джонса. Для перетворення сполуки (33) на хлорид (34) використовують хлоруючий агент, такий як РОСІ3. Хлорид (34) приводять у взаємодію з аніліном у підхожому розчиннику, такому як ДМФА, при кімнатній температурі або підвищеній температурі, одержуючи в результаті кінцевий продукт (35), сполуку за формулою (І). Схема 9 Зв'язування сполуки (6) (див. Схему 2) із підхожою амінобензойною кислотою в ДМФА дозволяє одержати сполуку (36). Здійснюючи відновлення естерної групи сполуки (36) за допомогою підхожого агента відновлення, такого як DIBAL-H, в апротонному органічному розчиннику, такому як ТГФ, одержують спирт (37). Спирт (37) може бути приведений у взаємодію з аміном RNH 2 при наявності зв'язувального реагенту, такого як ВОР, в органічному розчиннику, такому як ДМФА, внаслідок чого утворюється продукт (38). Продукт (38) окисляють до альдегіду (39) за допомогою підхожого окислювача, такого як МпО2, в органічному розчиннику, такому як ТГФ. Альдегід (39) приводять у взаємодію з підхожим металоорганічним реагентом (таким, як фенілмагнійбромід), утворюючи проміжний вторинний спиртовий продукт, котрий окисляють до кетону (40) за допомогою підхожого окислювача, такого, як РСС. Крім того, використовуючи процеси, добре відомі фахівцям у даній галузі, можуть бути отримані інші сполуки за формулою І. Зокрема, додаткові процеси одержання сполук за даним винаходом описані в прикладах, наведених нижче. У цих прикладах розкриті кращі варіанти практичного втілення даного винаходу. Очи щення за допомогою HPLC-хроматографії проводили на колонках С18 з оберненою фазою (RP), використовуючи водну суміш МеОН і TFA як буферний розчин. Метою цих прикладів є лише ілюстрація, а не обмеження даного винаходу. Отже, цілком припустимими є також інші варіанти практичного втілення, що не виходять за межі ідеї та об'єму, визначених у доданій Формулі винаходу. Приклад 1 Стадія А До розчину 3-аміно-4-метилбензойної кислоти (5,12г, 33,9ммоль, 1,0екв.), EDC (9,97г, 52,0моль, 1,5екв.) і 4-(диметиламіно)піридину (0,89г, 7,3моль, 0,2екв.) у ДМФА (100мл) при температурі 0°С по краплях добавили циклопропіламін (4,0мл, 57,7моль, 1,7екв.). Після перемішування протягом 15 хвилин, охолоджуючу баню видалили, а реакційну суміш перемішували при кімнатній температурі протягом ночі. Леткі речовини видалили при температурі 50°С під зниженим тиском. Осад розбавили водою й екстрагували DCM (тричі). Органічні шари об'єднали, просушили над сульфатом натрію і концентрували у вакуумі, отримавши масло. Після хроматографії на силікагелі, використовуючи як елюент суміш DC M:MeOH (20:1), о тримали сполуку 1 А у вигляді масла жовтого кольору (6,98г, 108% вихід). Час витримування при HPLC: 0,637 хвилини; LC/MS (М+Н)+=191,09+. Стадія В До суспензії вихідного оксопіролтриазину (3,00г, 13,6ммоль) у толуолі (45мл) при кімнатній температурі по краплях послідовно добавили оксихлорид фосфору (1,90мл, 20,4ммоль) і N,N-DIPEA (2,37мл, 13,6ммоль). Утворену суміш нагріли і кип'ятили зі зворотним холодильником протягом 36 годин, залишили для охолодження до кімнатної температури, після чого вилили в охолоджену до температури льоду суміш насиченого розчину бікарбанату натрію (150мл) і толуолу (60мл). Органічний шар відокремили, а водяний шар екстрагували толуолом (3´50мл). Об'єднаний екстракт промили насиченим розчином бікарбанату натрію і розсолом і просушили над безводним MgSO4. Після випарювання розчинника у вакуумі отримали сполуку 1В (3,26г, 100% вихід) у вигляді твердої речовини жовтого кольору. Стадія С. Приклад 1 Розчин продуктів 1А (1,60г, 8,40ммоль, 1,6екв.) і 1В (1,30г, 5,40ммоль, 1,0екв.) у ДМФА (13мл) перемішали при кімнатній температурі протягом ночі. Добавили воду, й осад зібрали шляхом фільтрування, промили водою і просушили. Отриманий продукт розтерли в порошок із діетиловим етером, одержавши в результаті цільову сполуку Прикладу 1 (1,70г, 80% вихід) у вигляді твердої речовини брудно-білого кольору. Час витримування при HPLC: = 3,190 хвилини; LC/MS (М+Н)+ = 394. 31+. Приклад 2 Розчин із Прикладу 1 (0,86г, 2,20ммоль, 1,0екв.) у ТГФ (4,0мл) і 1н. водний розчин NaOH (9,0мл, 4,1екв.) перемішували при температурі 60°С протягом ночі. Після охолодження до кімнатної температури реакційну суміш концентрували у вакуумі, але не до сухого стан у. До розчину при температурі 0°С добавили 1н. водний розчин соляної кислоти для підкислення, після чого осад зібрали і просушили, одержавши сирий продукт Прикладу 2 (0,51г, 64,0 % вихід). Час витримування при HPLC: 2,400 хвилин; LC/MS (M+H) = 366,06. Після цього фільтрат екстрагували EtOAc (тричі), а органічні шари об'єднали, просушили над сульфатом натрію і концентрували у вакуумі, одержавши сполуку Прикладу 2 (0,035г, 4,4% вихід). Приклад 3 Розчин із Прикладу 2 (0,026г, 0,071ммоль, 1,0екв.), EDC (0,021г, 0,11ммоль, 1,5екв.), HOBt (0,015г, 0,11ммоль, 1,5екв.), н-бутиламін (0,015мл, 0,15ммоль, 2,1екв.) і DIPEA (0,040мл, 0,23ммоль, 3,2екв.) у ДМФА (0,20мл) струшували при кімнатній температурі протягом ночі. Після цього до розчину добавили воду (1мл), і шляхом фільтрування зібрали осад, промили його водою і просушили, одержавши сполуку Прикладу 3 (0,021г, 70% вихід); час ви тримування при HPLC: 2,883 хвилини; LC/MS (М+Н)+ = 421,18+. Приклади 4-22 Сполуки, описувані формулою (Id), де R4 має значення, наведені в таблиці нижче, були отримані за допомогою процесу, аналогічного описаному в Прикладі З, використовуючи замість н-бутиламіна іншій підхожий амін. Сполуки, що мають формулу (Іе), де R 4 має значення, наведені в таблиці нижче, були отримані за допомогою процесу, аналогічного описаному в Прикладі 3, використовуючи піперазиніламін і морфолініламін замість н-бутиламіну. Приклади 23-24 Приклади 25-27 Сполуки, що мають формулу (If), де R 4 має значення, наведені в таблиці нижче, отримані за допомогою процесу, аналогічного описаному в Прикладах з 1 по 3, використовуючи замість н-бутиламіну інший підхожий амін, а замість циклопропіламіну на Стадії 1А - (±)-транс-етоксициклопропіламін, отриманий так, як описано нижче, в Стадіях A-D. Стадія А У добре перемішуван у суміш етилвінілового етеру (47,9мл, 0,500моль) і димеру ацетату родію(ІІ) (0,221г, 0,500ммоль) у діетиловому етері (10мл) за допомогою голчатого насоса повільно добавили етилдіазоацетат (10,5мл, 0,100моль) у діетиловому етері (30мл) при кімнатній температурі протягом 8 годин. Нерозчинні речовини видалили шляхом фільтрування через целіт, а надлишок етилвінілового ефіру і розчинник випарили у вакуумі. Осад очистили у вакуумі, отримавши продукт 25А (10,3г, 65% вихід) у вигляді безбарвного масла, що являло собою суміш цис- і транс-ізомерів у співвідношенні приблизно 1:1. Стадія В До розчину продукту 25 А (10,3г, 65,4ммоль) у МеОН (200мл) однією порцією добавили розчин NaOH (7,85г, 196,2ммоль), і утворений розчин нагріли і кип'ятили зі зворотним холодильником протягом 5 годин. Суміш концентрували у вакуумі. Осад підкислили 6н. НСІ до рН2 і екстрагували EtOAc (5´). Об'єднану органічну фазу просушили над MgSO 4. Після випарювання розчинника у вакуумі залишився продукт 25В (8,46г, 99% вихід) у вигляді безбарвного масла, що являло собою суміш цис- і транс-/зомерів у співвідношенні приблизно 1:1. Суміш продукту 25В (1,00г, 7,68ммоль), дифенілфосфорилазиду (1,82мл, 8,44ммоль) і TEA (1,18мл, 8,47ммоль) у безводному трет-BuOH (30мл) гріли при температурі 90°С протягом 27 годин. Леткі речовини випарили у вакуумі. Залишок розбавили 10% розчином Na 2CO3 (30мл) і екстрагували діетиловим етером (4´30мл). Об'єднану органічну фаз у промили соляним розчином, просушили над MgSO 4, і розчин концентрували у вакуумі. Після очищення залишку за допомогою хроматографії на силікагелі (40% Еt2/гексан) отримали продукт 25С (0,901г, 58% вихід) у вигляді безбарвного масла, що являло собою суміш цис- і трансізомер\в у співвідношенні відповідно, приблизно, 15:85. Стадія D Суміш продукту 25С (0,881г, 4,38ммоль) і 1н. НСІ (20мл) нагріли і кип'ятили зі зворотним холодильником протягом 5 годин. Потім її залишили для охолодження до кімнатної температури і екстрагували діетиловим етером. Величину рН водного шару відрегулювали до рН11 1н. розчином NaOH і потім екстрагували діетиловим етером (4´). Об'єднану органічну фазу просушили над MgSO 4, а розчинник випарили, отримавши (±)-транс-етоксициклопропіламін (0,224г, 50% вихід) у вигляді масла ясно-жовтого кольору. Приклад 28 До розчину з Прикладу 27 (30,0мг, 0,0585ммоль) у DCE (6мл) при температурі 0°С добавили ВВr3. Утворену реакційну суміш перемішали при кімнатній температурі протягом 20 хвилин і погасили водою. Величину рН суміші довели до 9 за допомогою насиченого розчину Na2CO3 і екстрагували ЕtOАс (тричі). Об'єднану органічну фазу промили соляним розчином і просушили над MgSO4. Розчин концентрували у вакуумі, і залишок очистили за допомогою хроматографії на силікагелі (6% МеОН/СНСІ3), одержавши цільову сполуку Прикладу 28 (3,2мг) у вигляді твердої речовини білого кольору. Час витримування при HPLC: 3,09 хвилини (b); LC/MS(M+H)+ = 485,38+. Приклади 29-30 Сполуки, що виражаються формулою (Іg), де В має значення, наведені в таблиці нижче, були отримані за допомогою процесу, аналогічного описаному у Прикладах 1 і З, використовуючи відповідним чином заміщений циклопропіламін на Стадії 1А і етиламін замість н-бутиламіну. Приклад 31 Стадія А Сполука 31А була о тримана за допомогою процесу, описаного в патентній заявці США №10/036,293, відступленої правонаступникові даної заявки і включеної тут в усій її повноті шляхом посилання. Стадія В Суміш сполуки 31А, 3-аміноізоксазолу (0,30мл, 4,06ммоль), бензотриазол-1ілокситрис(диметиламіно)фосфонийгексафторфосфату (0,720г, 1,63ммоль) і N-метилморфоліну (0,54мл, 4,91ммоль) у ДМФА (4мл) гріли при температурі 65°С протягом двох днів. Після цього суміш розбавили ЕtOАс і промили водою (двічі), 10% розчином Kа2СО3 і соляним розчином. Розчин концентрували у вакуумі, і продукт відокремили за допомогою препаративної HPLC. Час витримування при HPLC: 2,48 хвилини (a); LC/MS (М+Н) + = 434,11+. Приклади 32-38 Сполуки, що мають наведену вище формулу (Іg), де В приймає значення, подані в таблиці нижче, були отримані за допомогою процесу, аналогічного описаному у Прикладі 31, за винятком того, що тут для приготування вихідної сполуки використовували замість пропіламіну етиламін, а на Стадії В замість аміноізооксазолу використовували підходящий аміногетероарил. Приклад 39 Стадія А До розчину LAH (13,7г, 362ммоль) у ТГФ (800мл) декількома порціями при кімнатній температурі добавили естер за формулою (8г, 36,2ммоль). Реакційну суміш кип'ятили зі зворотним холодильником протягом 30 хвилин, після цього охолодили до кімнатної температури, обережно погасили шляхом виливання у воду з льодом (1л) і швидко перемішали протягом 1год. Далі суміш екстрагували EtOAc, і об'єднані екстракти промили соляним розчином, просушили над MgSO4 , відфільтрували і концентрували, одержавши сполуку 39А (5,60г, 86%). Стадія В До суспензії сполуки 39А (1,0г, 5,58ммоль) в ацетоні (80мл) при температурі 0°С по краплях добавили реагент Джонса (1,9мл). Реакційну суміш перемішали при температурі 0°С протягом 1год. і обережно погасили 2-пропанолом. Добавили насичений водний розчин бікарбанату натрію (100мл), і суміш екстрагували ЕtOАс (5´100мл). Об'єднаний екстракти промили насиченим водним розчином бікарбанату натрію (1´100мл), водою (1´100мл) і соляним розчином (1´100мл), потім просушили над MgSO4, відфільтрували і концентрували, одержавши в результаті сполуку 39В (647мг, 65%). Час витримування при HPLC: 1,50хв. Молекулярна маса: 177,16, LCMS [M+H]+=178. Стадія С До розчину сполуки 39В (600мг, 3,39ммоль) у ТГФ (80мл) при температурі 0°С по краплях протягом 5 хвилин добавили фенілмагнійбромід (3М, 2,94мл, 8,8мл). Після перемішування протягом 30 хвилин при температурі 0°С реакційну суміш відігрівали до кімнатної температури протягом 1год. і погасили насиченим водним розчином хлориду амонію. Далі суміш екстрагували ЕtOАс, екстракти промили, відфільтрували і концентрували, одержавши в результаті проміжний продукт - бензиловий спирт. Проміжний бензиловий спирт розчинили в ацетоні (50мл) й охолодили до температури 0°С. По краплях добавили реагент Джонса (1мл), реакційну суміш знову перемішали при температурі 0°С протягом 1год. і обережно погасили 2-пропанолом. Після цього добавили насичений водний розчин бікарбанату натрію (50мл), і суміш екстрагували ЕtOАс (4´50мл). Об'єднані екстракти промили насиченим водним розчином бікарбанату натрію (1´50мл), водою (1´50мл) і соляним розчином (1´50мл), просушили над MgSO4, відфільтрували і концентрували, одержавши в результаті сполуку 39С (563мг, 66% за 2 стадії). Час витримування при HPLC: 2,82 хв. Молекулярна маса: 253,26, LCMS [M+H]+=254. Стадія Р Кетон 39С (152мг, 0,6ммоль) помістили у РОСІ3 (5мл) і гріли при температурі 100°С протягом 1,75 години. Реакційну суміш о холодили до кімнатної температури і надлишок РОСІ3 випарили у вакуумі. Осад розчинили у безводному DCM (10мл) і по краплях добавили до швидко перемішуваного насиченого водного розчину бікарбанату натрію (50мл) і DCM (50мл) при температурі 0°С. Суміш перемішали протягом 1год., після чого водну фазу екстрагували DCM (3´50мл). Органічні фази промили насиченим водним розчином бікарбанату натрію (1´50мл), водою (1´50мл) і розсолом (1´50мл), потім просушили над MgSO4 , відфільтр ували і концентрували, одержавши в результаті хлорид 39D (163мг, 100%). Стадія Ε До розчину хлориду 39D (31,5мг, 0,116ммоль) у ДМФА (1мл) добавили 3-аміно-Н-циклопропіл-4метилбензамід (сполуку 1А) (44мг, 0,23ммоль), і розчин гріли при температурі 60°С протягом 3 годин. Після цього до нього добавили воду (5мл). Продукт, що випав в осад, зібрали шляхом фільтрування, промили водою і висушили на повітрі, одержавши в результаті сполуку Прикладу 39. Час витримування при HPLC: 3,34хв., Молекулярна маса: 425,49, LCMS [M+H]+=426. Приклади 40-42 Сполуки, виражені формулою (Ih), де Υ і В приймають значення, наведені в таблиці нижче, були отримані за допомогою процесу, аналогічного описаному вище у Прикладі 39, використовуючи підхожий амін на стадії Е. Приклад 43 Стадія А До розчину сполуки 39D (60мг, 0,221ммоль) у ДМФА (1мл) добавили 3-аміно-4-метилбензойну кислоту (66,8мг, 0. 442ммоль), і розчин гріли при температурі 60°С протягом 3 годин. Після цього до розчину добавили воду (5мл), продукт, що випав в осад, зібрали шляхом фільтрування, промили водою і висушили на повітрі, одержавши сполуку 43А (75мг, 88%). Час витримування при HPLC: 3,38 хв., Молекулярна маса: 386,41, 46 LCMS[M+H]+=387. Стадія В До розчину кислоти 43А (30мг, 0,078ммоль), HATU (44мг, 0,117ммоль) і DIPEA (17мкл, 0,1ммоль) у ДМФА (0,5мл) при кімнатній температурі добавили 3-аміноізоксазол. Реакційну суміш перемішали при кімнатній температурі протягом 1 год., і добавили до неї воду (5мл). Продукт, що випав в осад, зібрали шляхом фільтрування й очистили за допомогою препаративної HPLC, одержавши в результаті сполуку Прикладу 43. Час витримування при HPLC: 3,39хв., Молекулярна маса: 452,48, LCMS[M+H]+=453. Приклад 44 Стадія А До розчину сполуки 39В (160мг, 0,90ммоль) у ТГФ (10мл) при температурі 0°С по краплях добавили 6метил-2-піридилмагнійбромід (0,25М, 14,4мл, 3,6мМ) протягом 5 хвилин. Після перемішування протягом 30 хвилин при температурі 0°С реакційну суміш відігріли до кімнатної температури і перемішали протягом 16 годин. Далі до неї ввели додаткові аліквоти 6-метил-2-піридилмагнійброміду, щоб цілком завершити перетворення вихідного продукту, після чого реакційну суміш погасили насиченим водним розчином хлориду амонію. Суміш екстрагували EtOAc, екстракти промили, відфільтрували і концентрували, одержавши в результаті продукт у вигляді напівтвердого матеріалу рижувато-коричневого кольору. Отриманий продукт розчинили в ацетоні (10мл) і охолодили до температури 0°С. По краплях добавили реагент Джонса (0,4мл) і реакційну суміш перемішали при температурі 0°С протягом 1год., а потім обережно погасили 2-пропанолом. Добавили насичений водний розчин бікарбанату натрію (15мл), і суміш екстрагували EtOAc (4´20мл). Об'єднані екстракти промили насиченим водним розчином бікарбанату натрію (1´20мл), водою (1´20мл) і соляним розчином (1´20мл), потім просушили над MgSO4, відфільтрували і концентрували, одержавши в результаті сполуку 44А (145мг, 60% за 2 стадії). Стадія В Кетон 44А (75мг, 0,28ммоль) помістили у РОСІ3 (4мл) і гріли до температури 100°С протягом ночі. Реакційну суміш о холодили до кімнатної температури, і надлишок РОСІ3 випарили у вакуумі. Осад розчинили у безводному DCM (10мл) і по краплях добавили до швидко перемішуваного насиченого водного розчину бікарбанату натрію (50мл) і DCM (50мл) при температурі 0°С. Суміш перемішали протягом 1 год., після чого водну фазу екстрагували DCM (3´50мл). Органічну фазу промили насиченим водним розчином бікарбанату натрію (1´50мл), водою (1´50мл) і соляним розчином (1´50мл), потім просушили над MgSO4, відфільтрували і концентрували, одержавши в результаті хлорид 44В (64мг, 79%). Стадія С Приклад 44 До розчину сполуки 44В (53мг, 0,18ммоль) у ДМФА (0,5мл) добавили сполуку 1А (84мг, 0,44ммоль), і розчин гріли при температурі 60°С протягом 2 годин. Далі до розчину добавили воду (5мл), і продукт, що випав в осад, зібрали шляхом фільтрування, промили водою і висушили на повітрі, одержавши в результаті сполуку Прикладу 44 (34,2мг, 41%). Час витримування при HPLC: 3,39хв., Молекулярна маса: 452,48, LCMS [M+H]+=453. Приклад 45 Сполуку за Прикладом 45 одержували, дотримуючись процесу, аналогічного описаному в Прикладі 44, але використовуючи інший бензамід на стадії С. Час витримування при HPLC: 3,22хв., Молекулярна маса: 467,49, LCMS [M+H]+=468. Приклад 46 Стадія А До розчину хлориду за формулою (10г, 41,8ммоль) у ДМФА (60мл) при кімнатній температурі добавили 3-аміно-4-метилбензойну кислоту (6,3г, 41,8ммоль). Реакційну суміш перемішали протягом 16 годин, вилили у воду (500мл) й інтенсивно перемішували протягом 1год. Тверду фазу відфільтрували, промили водою (500мл) і просушили на повітрі, одержавши сполуку 46А (13,6г, 92%) у вигляді твердої речовини світло-рожевого кольору. MS[M+H]+=355. Стадія В До розчину сполуки 46А (1г, 2,8ммоль) у DCM (6мл) при температурі -78°С по краплях добавили DIBAL-H (1M, 8,5мл, 8,5ммоль). Реакційну суміш перемішали протягом 2 годин при температурі -78°С, відігріли до кімнатної температури протягом 1,5 години і погасили насиченим водним розчином NH4CI. Після цього добавленням до неї НСІ (1н.) довели величину рН до 4, і розчин екстрагували ЕtOАс. Після висушування органічної фази і концентрування отримали сполуку 46В у вигляді твердої речовини рожевого кольору (874мг, 100%). Час витримування при HPLC: 1,74хв. Молекулярна маса: 312,33, LCMS [M+H]+=313. Стадія С Приклад 46 До розчину сполуки 46В (1,8г, 5,9ммоль) у ДМФА (10мл) добавили ВОР (2,9г, 615ммоль) і циклопропіламін (2мл, 29,8ммоль). Реакційну суміш перемішали протягом ночі при кімнатній температурі, а потім вилили у воду (60мл). Твердий продукт, що випав в осад, зібрали шляхом фільтрування й очистили за допомогою препаративної HPLC, одержавши цільову сполуку Прикладу 46 (1,5г, 74%). Час витримування при HPLC: 1,64хв. Молекулярна маса: 351,41, LCMS[M+H]+=352. Приклад 47 До розчину продукту Прикладу 46 (1,5г, 4,3ммоль) у ТГФ (30мл) при кімнатній температурі добавили МnО2 (5,4г, 64ммоль). Після перемішування протягом 40 хвилин реакція була завершена. Продукт реакції зібрали шляхом фільтрування й осад промили ацетонітрилом. Після висушування фільтрату і концентрації залишку отримана сполука Прикладу 47 мала вигляд масла жовтого кольору (кількість 1,5г). Час витримування при HPLC: 2,52хв. Молекулярна маса: 349,40, LCMS[M+H]+=350. Приклад 48 До розчину 2-бромпіридину (54мкл, 0,57ммоль) і TMEDA (85мкл, 0,57ммоль) у ТГФ (10мл) при температурі -78°С по краплях добавили nBuLi (1М, 356мкл, 0,57ммоль). До утвореного розчину добавили сполуку Прикладу 47 (50мг, 0,14ммоль). Реакційну суміш перемішали протягом 0,5 години при температурі -78°С, потім відігріли до кімнатної температури і погасили водою. Суміш екстрагували ЕtOАс. Екстракти промили, відфільтрували і концентрували, одержавши в результаті сировинний проміжний спирт. До розчину цього проміжного спиртового продукту в DCM (5мл) при кімнатній температурі добавили піридинійхлорхромат (24,1мг, 0,11ммоль). Після перемішування протягом 1год. реакційну суміш погасили водою (2мл). Продукт реакції екстрагували ЕtOАс і просушили. Після очищення за допомогою препаративної HPLC була одержана цільова сполука Прикладу 48 у вигляді твердої речовини жовтого кольору (24,6мг, 40%). Час витримування при HPLC: 2,95хв. Молекулярна маса: 426,48, LCMS[M+H]+=427. Приклади 49-68 Сполуки, що мають структур у були одержані за допомогою процесу, описаного в Прикладі 3, при використанні підхожого аміну замість нбутиламіну. Приклад 69 Стадія 1 Проміжна сполука А: При кімнатній температурі до розчину 3-фторпіридину (5,0г) у дихлорметані (25мл) і 30% водному розчині пероксиду водню (10мл) добавили метилтриоксореній (25мг), і утворену суміш перемішували протягом ночі. Після цього до суміші добавили оксид марганцю (25мг) і все це перемішували при кімнатній температурі ще протягом 1 год. Потім добавили хлорид натрію до насичення водної частини, внаслідок чого шари розділилися. Водну частину додатково екстрагували дихлорметаном (3´100мл), і об'єднані органічні екстракти просушили над безводним сульфатом натрію, відфільтрували і концентрували у вакуумі, одержавши масло світло-жовтого кольору, що при стоянні застигало і в результаті набувало кінцевої форми продукту А у вигляді твердої речовини світло-жовтого кольору (4,92г, 84%). Час витримування при HPLC: 0,30хв. Стадія 2. Проміжна сполука В: До розчину проміжної сполуки А (2,85г, 25,2ммоль) у дихлорметані (25мл) при кімнатній температурі добавили триметилсилілціанид (10,0мл, 75,6ммоль). Утворену суміш кип'ятили зі зворотним холодильником протягом 10 годин. Після охолодження до кімнатної температури до неї добавили насичений водний розчин бікарбанату натрію (30мл), і суміш екстрагували дихлорметаном (3´150мл). Об'єднані органічні екстракти просушили над безводним сульфатом натрію, відфільтрували і концентрували у вакуумі, одержавши олію світло-коричневого кольору (4,60г) як сировинний продукт. Цей продукт очистили за допомогою флешхроматографії на колонці із силікагелем, застосовуючи як елюент 30%-суміш етилацетату в гексані. У результаті була одержана олія, що при стоянні застигала, набуваючи кінцеву форму продукту В у вигляді твердої речовини жовтувато-коричневого кольору (2,48г, 84). Час ви тримування при HPLC: 1,03хв. Стадія 3. Проміжна сполука С: До проміжної сполуки В (1,40г) в етанолі (50мл) послідовно добавили 10% паладію на вугіллі (500мг) і концентрований хлористий водень (2,9мл), і приготовану суміш струшували в атмосфері водню (40фунт./кв.дюйм) протягом 20 годин. Розчин відфільтрували через подушку із целіту, і фільтрат концентрували у вакуумі, отримавши 1,80г продукту С у вигляді твердої речовини білого кольору. Час витримування при HPLC: 0,19хв. Стадія 4. Сполука, зазначена в назві. Суміш проміжної сполуки D (40мг, 0,11ммоль), EDAC (25мг, 0,13ммопь) і HOBt (16мг, 0,12ммоль) у 0,3мл безводного ДМФА перемішали при кімнатній температурі протягом 2 годин, потім послідовно добавили амінгідрохлорид С (0,13ммоль) і основу Ханіга (38мкл, 0,22ммоль). Після перемішування протягом ночі при кімнатній температурі сиру реакційну суміш піддали очищенню за допомогою препаративної HPLC з оберненою фазою, отримавши цільову сполуку, зазначену в назві даного Прикладу. Приклади 70 і 71 Сполуки у Прикладах 70 і 71 були одержані, дотримуючись процесів, аналогічних застосованим у Прикладах 23-24. Приклад 72 Стадія 1. Проміжна сполука F: До проміжної сполуки (10,0г, 45,2ммоль) у РО СІ3 (30мл) при кімнатній температурі в атмосфері аргону повільно добавили безводний ДМФА (7,0мл, 90,4ммоль), і утворену суміш гріли при температурі 95°С протягом 15 годин. Після охолодження до кімнатної температури суміш повільно вилили у добре перемішуван у суміш 1 л насиченого водного розчину бікарбанату натрію і 200мл товченого льоду. Після перемішування гетерогенної суспензії при кімнатній температурі протягом 2,5 годин утворену тверду речовину зібрали шляхом вакуумного фільтрування і промили двома 150мл порціями води, після чого їй дали можливість частково висохнути на лійці. Далі тверду речовину промили двома порціями дихлорметану (по 100мл кожна), і отриманий органічний фільтрат просушили над безводним сульфатом натрію і концентрували у вакуумі, одержавши таким чином продукт F у вигляді твердої речовини жовтого кольору (5,35г, 47%), яку безпосередньо використовували на наступній стадії без подальшого очищення. Час витримування при HPLC: 2,96 хвилини. Стадія 2. Проміжна сполука G: Проміжну сполуку F (3,19г, 11,9ммоль) і відповідний анілінгідрохлорид (3,52г, 15,5ммоль) у 40мл безводного ДМФА перемішали при кімнатній температурі протягом ночі і розбавили 200мл води і 30мл насиченого водного розчину бікарбанату натрію. Після перемішування при кімнатній температурі протягом 1год., тверду речовину, що утворилася, зібрали шляхом вакуумного фільтрування, промили водою і просушили у вакуумі, одержавши в результаті продукт G у вигляді твердої речовини жовтогарячого кольору (4,2г, 84%), яку безпосередньо використовували у подальшому процесі без додаткового очищення. Час витримування при HPLC: 2,97 хвилини. МН+=422,1 (z-середня молекулярна маса). Стадія 3. Зазначена в назві сполука До проміжної сполуки G (0,8г, 1,90ммоль) у безводному ТГФ (10мл) при кімнатній температурі в атмосфері аргону послідовно добавили 1-метилпіперазин (0,24г, 2,47ммоль) і NaBH(OAc)3 (1,21г, 5,70ммоль) із наступним перемішуванням при кімнатній температурі протягом 3 годин. Реакційну суміш погасили шляхом додавання 50мл метанолу і перемішували ще протягом 1год. при кімнатній температурі, після чого концентрували і розподілили між 50мл насиченого водного розчину бікарбанату натрію і 200мл етилацетату. Шари розділили, і водну частину наситили хлоридом натрію, і додатково екстрагували етилацетатом (4´100мл). Об'єднані органічні екстракти просушили над безводним сульфатом натрію і концентрували у вакуумі, отримавши зазначену в назві сполуку у вигляді твердої речовини світло-жовтого кольору (1,02г, вихід 89%). Час витримування при HPLC: 2,25 хвилини. МН+ (z-середня молекулярна маса) 506,2. Приклади 73-80 Наведені нижче сполуки були одержані за допомогою процесу, аналогічного описаному в Прикладі 72.
ДивитисяДодаткова інформація
Назва патенту англійськоюPyrrolo-triazine aniline compounds useful as kinase inhibitors
Автори англійськоюDyckman Alaric, Liu Chunjian, Wrobleski Stephen T
Назва патенту російськоюПирролтриазинанилиновые соединения, полезные как ингибиторы киназы
Автори російськоюДикман Аларик, Лиу Чуньян, Вроблески Стивен Т.
МПК / Мітки
МПК: A61P 29/00, A61K 31/53, A61P 17/06, A61P 19/10, A61P 3/10, A61P 43/00, A61P 1/04, A61P 19/02, A61P 11/00, A61P 9/10, A61P 11/06, C07D 487/04
Мітки: кінази, інгібітори, сполуки, корисні, піролтриазинанілінові
Код посилання
<a href="https://ua.patents.su/61-78562-piroltriazinanilinovi-spoluki-korisni-yak-ingibitori-kinazi.html" target="_blank" rel="follow" title="База патентів України">Піролтриазинанілінові сполуки, корисні як інгібітори кінази</a>
Попередній патент: Блок термоелектричного пристрою
Наступний патент: Інгібітори пептидної деформілази
Випадковий патент: Формувач періодичної послідовності трьох імпульсних серій з програмованими часовими параметрами












