Спосіб визначення антибактеріальних речовин в продукції тваринного походження методом рх/мс/мс
Номер патенту: 92150
Опубліковано: 11.08.2014
Автори: Лінійчук Наталія Василівна, Ступак Оксана Михайлівна, Новожицька Юлія Миколаївна, Іванова Олена Вадимівна
Формула / Реферат
Спосіб визначення залишкових кількостей антибактеріальних речовин у продукції тваринного походження, в якому для дослідження беруть 2 г підготовленого зразка, екстрагують за допомогою трихлороцтової кислоти, додають буфер, центрифугують і відбирають супернатант, екстракт очищують за допомогою заздалегідь прокондиціонованого патрона для твердофазної екстракції і випаровують в потоці азоту, після чого перерозчиняють в розчині мурашиної кислоти.
Текст
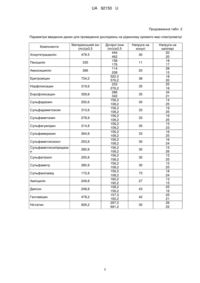
Реферат: Спосіб визначення залишкових кількостей антибактеріальних речовин у продукції тваринного походження, в якому для дослідження беруть 2 г підготовленого зразка, екстрагують за допомогою трихлороцтової кислоти, додають буфер, центрифугують і відбирають супернатант, екстракт очищують за допомогою заздалегідь прокондиціонованого патрона для твердофазної екстракції і випаровують в потоці азоту, після чого перерозчиняють в розчині мурашиної кислоти. UA 92150 U (12) UA 92150 U UA 92150 U 5 10 15 20 25 Корисна модель належить до галузі ветеринарної медицини, зокрема до біохімії та токсикології, і може бути використана в роботі науково-виробничих лабораторій. Спосіб не має зареєстрованих аналогів в Україні. В основу корисної моделі поставлена задача розробки універсального та швидкого способу одночасного виявлення залишкових кількостей антибактеріальних речовин різних класів, а саме - амоксициліну, ампіциліну, пеніциліну, тилозину, еритроміцину, гентаміцину, ністатину, стрептоміцину, антибіотиків групи тетрациклінів (тетрациклін, хлортетрациклін, окситетрациклін, доксициклін), сульфаніламідних препаратів (сульфатіазол, сульфадиметоксин, сульфагуанідин, сульфадіазин, сульфамеразин, сульфаметазин, сульфаметоксипіридазин, сульфаметоксазол, сульфаніламід, дапсон) та фторхінолонів (енрофлоксацин, норфлоксацин) у продукції тваринного походження, суттєве скорочення часу на пробопідготовку, витрат реактивів, посуду, зменшення наважки проби та зниження собівартості способу. Процедурний підхід до ідентифікації антибактеріальних речовин удосконаленим нами 3 способом включає наступні елементи: для аналізу беруть 2 г ± 0,05 (2 см ) підготовленого, 3 3 гомогенізованого зразка в центрифужну пробірку 15 см , додають до нього 100 мм 20 % 3 розчину трихлороцтової кислоти і змішують на вортексі, додають 5 см міксованого буфера та екстрагують 10 хв. при 100 об./хв. на роторному змішувачі, центрифугують 10 хв. при 4700 3 об./хв. при температурі 4 °C, відбирають супернатант у чисту пробірку на 15 см , проводять 3 3 твердофазну екстракцію за схемою: промивають картридж 3 см метанолу, промивають 3 см 3 деіонізованої води, пропускають відібраний супернатант, промивають 3 см деіонізованою 3 водою, висушують картридж протягом 10 хв., елюють зразок 3 см метанолу; випаровують під 3 потоком азоту до легкого зволоження і перерозчиняють в 500 мм 10 % розчині мурашиної кислоти, екстракт переносять у віалку та проводять дослідження [1, 2]. Високоефективний рідинний хроматограф із тандемним масселективним детектором готують згідно з інструкцією по експлуатації приладу. Конфігурацію та режими роботи: хроматограф - Waters, колонка - С-18, 1,7 мкм, 50×2,1, електроспрей - ESI, полярність - позитивна, тиск газу аргон - 3,5 mТоrr, температура колонки 40 3 3 °С, об'єм інжекції - 20 мм , режим введення проби автоматичний, витрата елюенту - 0,45 см /хв., елюент - метанол: 0,01 % розчин мурашиної кислоти, час хроматографування - 6 хв. 30 Таблиця 1 Співвідношення градієнтів: Час 0,00 хв. 1,0 хв. 2,00 хв. 3,0 хв. 5,5 хв. 6,0 хв. 6,5 хв. А % (0,1 % розчин мурашиної кислоти) 100 100 60 20 10 100 100 В % (метанол) 0 0 40 80 90 0 0 Таблиця 2 Параметри введення даних для проведення досліджень на рідинному хромато-мас-спектрометрі Компоненти Материнський іон (m/z)±0,5 Стрептоміцин 581,8 Тилозин 916,3 Доксициклін 445,7 Тетрациклін 445,7 Окситетрациклін 460,8 Дочірні іони (m/z)±0,5 246 263 174 772,2 154 428 410 427,5 426 443 1 Напруга на конусі 65 38 30 30 30 Напруга на капілярі 40 35 40 24 27 20 18 14 18 15 UA 92150 U Продовження табл. 2 Параметри введення даних для проведення досліджень на рідинному хромато-мас-спектрометрі Компоненти Хлортетрациклін Материнський іон (m/z)±0,5 478.5 Пеніцилін 335 Амоксициклін 366 Еритроміцин 734,2 Норфлоксацин 319,6 Енрофлоксацин 359,8 Сульфадіазин 250,6 Сульфадиметоксин 310,6 Сульфаметазин 278,9 Сульфагуанідин 214,8 Сульфамеразин 264,8 Сульфаметоксазол 253,8 Сульфаметоксипіридази н 280,8 Сульфатіазол 255,8 Сульфаметр 280,9 Сульфаніламід 172,8 Ампіцилін 249,8 Дапсон 248,8 Гентаміцин 478,2 Ністатин 926,2 Дочірні іони (m/z)±0,5 444 462 158 176 114 208 522.2 576,2 233 276,2 286 342 156,2 108,2 156,2 108,2 156,2 108,2 156,2 108,2 156,2 108,2 156,2 108,2 156,2 108,2 156,2 108,2 156,2 108,2 156,2 108,2 160,2 192,2 108,2 156,2 157,3 160,2 297,2 691,2 2 Напруга на конусі 30 11 20 38 35 35 30 33 33 30 33 30 30 30 30 73 27 43 42 30 Напруга на капілярі 20 20 18 17 28 15 18 20 25 16 34 21 14 25 19 25 16 25 15 23 16 25 16 24 15 26 15 25 15 25 18 24 13 15 25 16 25 21 26 22 UA 92150 U Таблиця 3 Валідаційні дані № Назва показника 1. 2. 3. 4. 5. 6. 7. Пеніцилін Амоксицилін Ампіцилін Стрептоміцин Гентаміцин Енрофлоксацин Норфлоксацин 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. 18. 19. 20. 21. 22. 23. 24. Доксициклін Хлортетрациклін Тетрациклін Окситетрациклін Тилозин Еритроміцин Сульфатіазол Сульфаметоксипіридазин Сульфаметоксазол Сульфаметазин Сульфамеразин Сульфадиметоксин Сульфадіазин Сульфагуанідин Сульфаніламід Дапсон Ністатин ССа Молоко 1,19 1,57 1,9 128,8 2,73 11,5 13,98 Мед 3,99 2,84 1,51 3,14 6,09 5,17 7,74 3,15 3,8 3,79 4,45 3,82 4 2,8 3,62 1,15 1,05 СС CV% 2,07 2,64 2,9 221,17 4,59 19,39 21,32 24,1 26,2 25 19,4 1,3 2,7 8,3 6,55 4,5 2,55 5,27 9,02 8,09 12,17 5,21 6,66 6,59 7,88 6,5 7,08 4,67 6,34 2,15 1,97 9,6 8,6 6,2 12 16 15,4 21,5 10,1 15,2 17,9 19,5 15 14,7 13 19,7 11,5 5,6 Таблиця 4 Максимально допустимий рівень по видах матриці відповідно до Регулювання Комісії ЕС № 37/2010 [3] Пеніцилін Тилозин Амоксицилін Ампіцилін Стрептоміцин Рентаміцин Тетрацикліни Енрофлоксацин Норфлоксацин Сульфаніламідні препарати Еритроміцин Ністатин 5 М’язи, мкг/кг Молоко, мкг/кг 50 4 100 50 50 4 50 4 500 200 50 100 100 100 100 100 Яйця 200 200 Печінка 50 100 50 50 500 200 300 200-300 Нирки 50 100 50 50 1000 750 600 200-300 100 100 100 100 200 40 150 200 200 Дані, наведені в табл. 3 і табл. 4, свідчать про те, що даний спосіб є досить чутливим, щоб детектувати дані речовини. Так, як у відношенні сполук, для яких встановлена максимальнодопустимий рівень (МДР), показник СС повинен бути менше чи дорівнювати МДР. Відповідно, показник ССα повинен бути менше [4, 5]. 3 UA 92150 U 5 10 15 20 25 30 35 40 45 Наш спосіб дозволяє за досить короткий проміжок часу дослідити зразок на одночасно багато показників різних класів, що значно економить час, реактиви, і в свою чергу знижує собівартість дослідження. Спосіб "Визначення антибактеріальних речовин в продукції тваринного походження методом РХ/МС/МС" дозволяє визначати залишкову кількість амоксициліну, ампіциліну, пеніциліну, тилозину, еритроміцину, гентаміцину, ністатину, стрептоміцину, антибіотиків групи тетрациклінів (тетрациклін, хлортетрациклін, окситетрациклін, доксициклін), сульфаніламідних препаратів (сульфатіазол, сульфадиметоксин, сульфагуанідин, сульфадіазин, сульфамеразин, сульфаметазин, сульфаметоксипіридазин, сульфаметоксазол, сульфаніламід), дапсону та фторхінолонів (енрофлоксацин, норфлоксацин) в продуктах тваринного походження та продуктах їх переробки. Спосіб визначення включає три основні етапи: - екстракція залишків амоксициліну, ампіциліну, пеніциліну, тилозину, еритроміцину, гентаміцину, ністатину, стрептоміцину, антибіотиків групи тетрациклінів, сульфаніламідних препаратів, дапсону та фторхінолонів за допомогою трихлороцтової кислоти; - очищення екстракту шляхом твердофазної екстракції; - ідентифікація та кількісне визначення методом РХ/МС/МС. Кількісне визначення масової концентрації антибактеріальних речовин проводять способом зовнішнього стандарту за здійсненим попередньо калібруванням хроматографа за градуювальними розчинами. Ідентифікацію проводять за часом утримання, наявністю відповідних іонів та співвідношенням їхньої інтенсивності. Підготовка проби Для підготовки проби потрібно відібрати достатню кількість зразка не менше 100 г, ретельно гомогенізувати. 1. Екстракція: 3 - для аналізу взяти 2 г ± 0,05 (2 см ) підготовленого, гомогенізованого зразка в центрифужну 3 пробірку на 15 см ; 3 - додати 100 мм 20 % розчину трихлороцтової кислоти та екстрагувати 10 хв. при 100 об./хв. на роторному змішувачі; 3 - додати 5 см міксовного буферу; - центрифугувати 10 хв. при 14000 g при температурі 4 °C; - відібрати супернатант. 2. Твердофазна очистка: Підготовка картриджів для очистки: 3 - промити 3 см метанолу; 3 - промити 3 см деіонізованою водою; - пропустити відібраний супернатант; 3 - промити 3 см деіонізованою водою; - висушити картридж протягом 10 хв.; 3 - елюювати зразок 3 см метанолу. 3 Випаровуємо під потоком азоту до легкого зволоження. Перерозчиняємо в 500 мм 0,1 % мурашиної кислоти. При необхідності профільтрувати через шприцевий фільтр 0,45 цм. Перенести екстракт у віалку та проводити дослідження. Виконання вимірювань та обчислення результатів Для градуювання хроматографа двічі аналізують кожний з градуювальних розчинів та визначають площі піків. Отримані результати обраховують за методом найменших квадратів, який дозволяє обчислити коефіцієнти а і b градуювальної прямої виду у=а+bх: a 50 55 y b x ; b mn x y mn x x mn 2 2 , де: 3 х - концентрація речовини, що визначається, нг/см ; у - відгук (площа піку) речовини, що визначається; m - кількість градуювальник сумішей; n - кількість спостережень; Обчислення абсолютного процента повернення: X C *100 , c де: X - абсолютний процент повернення, %; 3 С - концентрація аналіту, отримана по градуювальному графіку, нг/ см , 4 UA 92150 U 3 5 10 15 с - концентрація аналіту, додана до аналізованого зразка, нг/ см . Перевіряють працездатність системи, щоб гарантувати, що вона функціонує задовільно. Перевіряють базову лінію сигналу детектора. Шумова смужка повинна бути стабільною, без різких коливань і сторонніх піків. Якщо є відхилення, то проводять промивку хроматографічної системи, обслуговування системи детектора, зміну складових рухливої фази. Перевіряють контроль відхилення часу утримання та площі піка контрольного розчину. Для цього інжектують контрольний розчин суміші антибактеріальних речовин. Встановлюють час утримання, визначають площу. Значення RSD для площі піка і часу утримання не повинно перевищувати 2,5 %. Найнижчий рівень калібрування повинен бути таким, щоб забезпечувати підтвердження, що відгук є адекватним і гарантувати, що подана у звіті межа була досягнута і щоб помилкові нульові значення не були подані в звіті. Іони, які враховуються, повинні мати сигнал більше 3 відносно до шуму. Максимально дозволені відхилення для відносної інтенсивності в області техніки спектрометричного визначення маси: Відносна інтенсивність (% основного збагачення) > 50 % > 20-50 % > 10-20 % 10 % 20 25 30 35 40 45 LC-MS-MS (відносні) ± 20 % ± 25 % ± 30 % ± 50 % При аналізі LC-MS/MS повинні бути передбачені матричні ефекти. Матричні ефекти роздивляються як пригнічення або збільшення відповіді сигналу. Матричні ефекти виникають, як правило, із-за присутності матричних елементів, які впливають на іонізацію речовин. Це впливає на кількісне виявлення та точність результатів. Джерела інформації: 1. Delepine В. Multi-residue method for screening of Antibiotics Residues in Meat using liquid chromatography tandem mass spectrometry / B. Delepine, D. Hurtaud-Pessel, M. Juhel-Gaugain // AFSSA-FOUGERES, Laboratoire d´etudes et de recherches sur les medicaments veterinaries et les desinfectants, Laboratoire National de Reference. 2. Van Rhijn J.A. RIKILT Institute of Food Safety, Wageningen, The Netherlands Waters Corp. MS Technologies Centre, Manchester, UK - Advanced multi-residue screening in veterinary drug analysis using UPLC - ToF MS / Van Rhijn J.A. C. Bourgeon, J.J. Lasaroms, E. Oosterink, D. McMillan // RIKILT Institute of Food Safety, Wageningen, The Netherlands Waters Corp. MS Technologies Centre, Manchester, UK 3. Commission Regulation (EU) № 37/2010 // Official journal of the European Commission. 2010. - L 15. - 72 p. 4. Commission Decision 2002/657/EC // Official journal of the European Commission. - 2002. - L 221. - 8 p. 5. Guidelines for the implementation of decision 2002/657/EC, European Commission helh & consumer protection Directorate-General, Directorate E - Safety of the Food Chain, SANCO/2004/2726-rev 4-December 2008. ФОРМУЛА КОРИСНОЇ МОДЕЛІ Спосіб визначення залишкових кількостей антибактеріальних речовин у продукції тваринного походження, в якому для дослідження беруть 2 г підготовленого зразка, екстрагують за допомогою трихлороцтової кислоти, додають буфер, центрифугують і відбирають супернатант, екстракт очищують за допомогою заздалегідь прокондиціонованого патрона для твердофазної екстракції і випаровують в потоці азоту, після чого перерозчиняють в розчині мурашиної кислоти. Комп’ютерна верстка Д. Шеверун Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 5
ДивитисяДодаткова інформація
МПК / Мітки
МПК: A61D 99/00
Мітки: тваринного, спосіб, методом, походження, речовин, визначення, антибактеріальних, продукції
Код посилання
<a href="https://ua.patents.su/7-92150-sposib-viznachennya-antibakterialnikh-rechovin-v-produkci-tvarinnogo-pokhodzhennya-metodom-rkh-ms-ms.html" target="_blank" rel="follow" title="База патентів України">Спосіб визначення антибактеріальних речовин в продукції тваринного походження методом рх/мс/мс</a>
Попередній патент: Спосіб визначення хлорамфеніколу в необроблених харчових продуктах тваринного походження за допомогою рх/мс/мс
Наступний патент: Спосіб профілактики метаболічного синдрому
Випадковий патент: Пристрій для виготовлення п-подібних ободів