Заміщені біцикло[3.1.1]гептаном похідні бензімідазолону та хіназолінону як агоністи людських рецепторів orl1
Номер патенту: 83870
Опубліковано: 26.08.2008
Автори: Тьойнстра Тинка, ван Стьойвенберг Герман Г., Ден Хартог Якобус А.Й., Жассеран Даніель, Давід Самуель, ван Шаренбург Густав Й.М.
Формула / Реферат
1.Сполуки загальної формули (1)
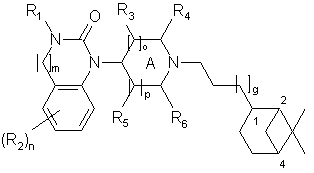 , (1)
, (1)
де
R1 представляє H, (1-6С)алкіл, (1-3С)алкіл(3-6С)циклоалкіл, (2-7С)карбалкокси або (2-7С)ацил,
[]m означає -(СН2)m-, де m - 0 або 1,
R2 представляє галоген, CF3, (1-6С)алкіл, (1-3С)алкіл(3-6С)циклоалкіл, феніл, амін, (1-3С)аміноалкіл, (1-3С)алкіламін, (1-3С)діалкіламін, ціан, (1-3С)ціаноалкіл, (1-3С)гідроксіалкіл, (1-3С)алкокси, OCF3, (2-7С)ацил, трифторацетил, амінокарбоксил, (1-3С)алкілсульфоніл або трифторметилсульфоніл, n є цілим числом від 1 до 4, за умови, що коли n є 2, 3 або 4, замінники R2 можуть бути однакові або різні,
А - насичене або частково насичене кільце,
[]o та []р представляють -(СН2)o- та -(СН2)p - відповідно за умови, що при частково ненасиченому кільці А можливе також значення -СН-, а о та р незалежно одне від одного дорівнюють 0, 1 або 2,
R3, R4, R5 та R6 незалежно один від одного представляють водень, (1-3С)алкіл, (1-3С)алкіл(3-6С)циклоалкіл, СН2ОН, або R3 та R5, або R3 та R6, або R4 та R5, або R4 та R6 разом можуть утворювати алкіленовий місток з 1-3 атомами вуглецю, за умови, що при о є 2, R3 є водень, а коли р=2, R5 є водень,
[]q позначає -(СН2)q, де q - ціле число від 0 до 2,
усі стереоізомери, а також їх фармацевтично прийнятні солі та проліки, проліки, що є похідними від сполук формули (1), у яких присутня група, що легко видаляється після введення до організму, наприклад, такі, як амідин, енамін, основа Манніха, похідне гідроксилметилену, похідне О-(ацілоксиметиленкарбамату), карбамат, ефір, амід або енамінон.
2. Сполуки, як заявлено в п. 1 загальної формули (1), у яких:
А - насичене кільце,
R1 представляє водень, (1-3С)алкіл або (2-4С)ацил,
R3, R4, R5 та R6 незалежно один від одного представляють водень або (1-3С)алкіл, або R3 та R5, або R3 та R6, або R4 та R5, або R4 та R6 разом можуть утворювати алкіленовий місток з 1-3 атомами вуглецю, за умови, що коли о є 2, R3 є водень, при р=2, R5 є водень, а R2, m, n, о, р та q мають значення, наведені у п. 1.
3. Сполуки, як заявлено в п. 1 загальної формули (1), у яких:
А - насичене кільце, m=0, n=0 або 1, р=1, q=0, R1 - Н або ацетил, R2 представляє галоген, CF3, 1-3С-алкіл, гідрокси, ціан, ОСН3 або OCF3, R3, R4, R5 та R6 незалежно один від одного представляють водень, або 1-2С-алкіл, або R4 та R6 разом можуть утворювати алкіленовий місток з 1-2 атомами вуглецю.
4. Сполуки, як заявлено в п. 1, що мають формулу (2) та їх стереоізомери:
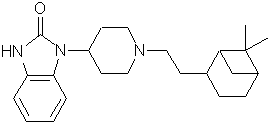 (2).
(2).
5. Фармаційна композиція, яка містить фармакологічно активну кількість принаймні однієї із сполук за пп. 1-4.
6. Сполука, як заявлено в будь-якому з пп. 1-4, або її сіль для застосування як лікарського засобу.
7. 3астосування сполуки, як заявлено в будь-якому з пп. 1-4, для приготування фармацевтичної композиції для лікування розладів, пов'язаних з рецептором ORL1 або таких, що їх можна лікувати, діючи на зазначені рецептори.
8. Застосування за п. 7, яке відрізняється тим, що зазначеними розладами є гострі та хронічні больові стани, розлади центральної нервової системи, як-от послаблення симптомів бентежності та стресових розладів, депресії, різних форм епілепсії, інсульту, розлади, які характеризуються пошкодженням розуму та пам'яті, хвороба Альцгеймера, хвороба Крейцфельда-Якоба, хвороба Гантінгтона, хвороба Паркінсона, нейрореабілітація (травматичні пошкодження мозку), гострі травми мозку або хребта, розлади хімічного походження, в тому числі пов'язані із зловживанням певними речовинами (наркозалежність, алкоголізм) або спричинені таким зловживанням (синдром відвикання), розлади харчування (нервова анорексія, нервова булімія, опасистість); шлунково-кишкові розлади, зокрема синдром подразнення кишечнику, запалювальні хвороби кишечнику (хвороба Крона, виразковий коліт), запалення сечового тракту, ниркові розлади, що характеризуються дисбалансом вживання-видалення води або видалення солей; серцево-судинні захворювання, як інфаркт міокарда, аритмія, гіпертензія, тромбоз, анемія, атеросклероз, грудна жаба, захворювання шкіри, як кропивниця, вовчак та сверблячка; офтальмологічні розлади, як глаукома; респіраторні захворювання, включаючи кахикання, хронічну обструкцію легенів, бронхіт, цистофіброз; захворювання імунної системи та вірусні інфекції.
Текст
1.Сполуки загальної формули (1) C2 2 (19) 1 3 83870 А - насичене кільце, m=0, n=0 або 1, р=1, q=0, R1 Н або ацетил, R2 представляє галоген, CF3, 1-3Салкіл, гідрокси, ціан, ОСН3 або OCF3, R3, R4 , R5 та R6 незалежно один від одного представляють водень, або 1-2С-алкіл, або R4 та R6 разом можуть утворювати алкіленовий місток з 1-2 атомами вуглецю. 4. Сполуки, як заявлено в п.1, що мають формулу (2) та їх стереоізомери: O HN N N (2). 5. Фармаційна композиція, яка містить фармакологічно активну кількість принаймні однієї із сполук за пп.1-4. 6. Сполука, як заявлено в будь-якому з пп.1-4, або її сіль для застосування як лікарського засобу. 7. 3астосування сполуки, як заявлено в будь-якому з пп.1-4, для приготування фармацевтичної композиції для лікування розладів, пов'язаних з рецептором ORL1 або таких, що їх можна лікувати, діючи на зазначені рецептори. 8. Застосування за п.7, яке відрізняється тим, що зазначеними розладами є гострі та хронічні бо Винахід стосується групи заміщених гідронополом похідних бензімідазолону та хіназолінону, які є агоністами людських рецепторів ORL1 (ноціцептину). Винахід також стосується одержання цих сполук, фармаційних композицій, що містять фармакологічно дійову кількість принаймні одного з цих нових похідних бензімідазолону та хіназолінону в якості діючої речовини, а також застосування цих фармаційних композицій для лікування розладів, пов'язаних з рецепторами ORLl. "Подібний до рецептора опіатів 1" (ORL1) рецептор був виділений з бібліотеки людської цДНК. Встановлено, що цей "рецептор-одинак" за гомологією нагадує рецептори μ-, κ- та δ-опіатів [Mollereau et al., FEBS Lett.. 341, 33-38, 1994; Bunzow et al., FEBS Lett., 347, 284-288, 1994]. Незважаючи на близькість рецепторів ORL1 за послідовностями та структурою до рецепторів опіатів, класичні ліганди рецепторів опіатів з ними не взаємодіють. У 1995р. з екстрактів мозку був виділений чистий нейропептид із 17 амінокислот, який, як доведено пізніше, був природним лігандом пов'язаного з G-протеїном рецептора ORL1 [Reinscheid et al., Science. 270, 792-794, 1995; Meunier et al., Nature, 377, 532-535, 1995]. Цей пептид назвали орфаніном FQ або ноціцептином, і він не зв'язується з жодним з трьох традиційних рецепторів опіатів. Це відкриття породило значний обсяг досліджень функціональної ролі рецептора ORL1 та пошук його нових лігандів. З'явилося кількасот публікацій, включаючи кілька оглядів [наприклад, Grond et al., Anaesthesist, 51, 996-1005, 2002], та 4 льові стани, розлади центральної нервової системи, як-от послаблення симптомів бентежності та стресових розладів, депресії, різних форм епілепсії, інсульту, розлади, які характеризуються пошкодженням розуму та пам'яті, хвороба Альцгеймера, хвороба Крейцфельда-Якоба, хвороба Гантінгтона, хвороба Паркінсона, нейрореабілітація (травматичні пошкодження мозку), гострі травми мозку або хребта, розлади хімічного походження, в тому числі пов'язані із зловживанням певними речовинами (наркозалежність, алкоголізм) або спричинені таким зловживанням (синдром відвикання), розлади харчування (нервова анорексія, нервова булімія, опасистість); шлунково-кишкові розлади, зокрема синдром подразнення кишечнику, запалювальні хвороби кишечнику (хвороба Крона, виразковий коліт), запалення сечового тракту, ниркові розлади, що характеризуються дисбалансом вживання-видалення води або видалення солей; серцево-судинні захворювання, як інфаркт міокарда, аритмія, гіпертензія, тромбоз, анемія, атеросклероз, грудна жаба, захворювання шкіри, як кропивниця, вовчак та сверблячка; офтальмологічні розлади, як глаукома; респіраторні захворювання, включаючи кахикання, хронічну обструкцію легенів, бронхіт, цистофіброз; захворювання імунної системи та вірусні інфекції. кількадесят патентних заявок, де описуються пептидні та непептидні ліганди різної могутності та вибірковості (ORL1 у порівнянні з μ-опіатами). Оскільки рецептори μ-опіатів розсіяні по всьому організму, недостатня вибірковість може викликати низку небажаних бічних явищ, схожих на дію опіатів, наприклад, сонливість, респіраторну депресію, переносність та залежність [Drug News Perspect, 14, 335, 2001]. Шість пов'язаних з ORL1 патентних заявок стосуються похідних бензімідазолону: [WO 98/54158, WO 99/36421, WO 00/006545, WO 00/08013, WO 01/39775 та US 20029128288]. Найближчим прототипом цього винаходу є [заявка WO 01/39775]. Втім, описані там похідні бензімідазолону навряд чи відповідають загальновизнаним суттєвим критеріям для терапевтичних засобів на базі ORL1. Вони: 1) не досить потужні (спорідненість до рецепторів ORL1 у межах 166-1252нМ); 2) не є вибірковими щодо рецепторів μ-опіатів (спорідненість у межах 19-457нМ); 3) непридатні для орального введення; 4) не засвоюються ЦНС. Нами несподівано встановлено, що група сполук серед гідроноползаміщених похідних бензімідазолону та хіназолінону посідає дуже високу спорідненість до людських рецепторів ORLl. Більш того, ці сполуки є напрочуд вибірковими до рецепторів ORL1 відносно до рецепторів μ-опіатів, придатні для орального введення та долають бар'єр між кров'ю та мозком. 5 83870 Винахід стосується сполук загальної формули (1) де: R1 представляє H, (1-6С)алкіл, (1-3С)алкіл(36С)циклоалкіл, (2-7С)карбалкокси або (2-7С)ацил, []m позначає -(CH2)m, де m - 0 або 1, R2 представляє галоген, CF3, (1-6С)алкіл, (13С)алкіл(3-6С)циклоалкіл, феніл, амін, (1-3С) аміноалкіл, (1-3С)алкіламін, (1-3С)діалкіламін, ціан, (1-3С)ціаноалкіл, гідрокси, (1-3С)гідроксиалкіл, (1-3С)алкокси, OCF3, (27С)ацил, трифторацетил, амінокарбоксил, (1-3С)алкілсульфоніл або трифторметилсульфоніл, п є цілим числом від 1 до 4, за умови, що коли n - 2, 3 або 4, замінники R2 можуть бути однакові або різні, А - насичене або частково насичене кільце, []o та []р представляють -(CH2)o- та -(СН2)р- відповідно за умови, що при частково ненасиченому кільці А можливе також значення -CH-, а о та р незалежно одне від одного дорівнюють 0, 1 або 2, R3, R4, R5 та R6 незалежно один від одного представляють водень, (1-3С)алкіл, (1-3С) алкіл(36С)циклоалкіл, CH2OH, або (R3 та R5), або (R3 та R6), або (R4 та R5), або (R4 та R6) разом можуть утворювати алкіленовий місток з 1-3 атомами вуглецю, за умови, що при о=2 R3 - водень, а при р=2 R5 - водень, []q позначає -(CH2)q , де q - ціле число від 0 до 2, та їх фармаційно прийнятні солі та проліки. Винахід охоплює усі сполуки формули (1), рацемати, суміші діастереоізомерів та окремі стереоізомери. Отже, сполуки, у яких замісники потенційно асиметричних атомів вуглецю знаходяться у Rконфігурації або у S-конфігурації, належать до обсягу винаходу. Також до нього належать проліки, тобто сполуки, які, потрапляючи до організму Вихідні сполуки для цього загального шляху одержують наступним чином: Бензімідазолони (m=0) можна синтезувати за способами, описаними у [J.Med.Chem. 30, 814-819, 1987 та WO 99/36421 (Pfizer)]. Хіназолони (m=1) 6 будь-яким відомим шляхом, метаболізуються у сполуки формули (1). Зокрема, це стосується сполук з первинними або вторинними аміно-або гідроксигрупами. Такі сполуки здатні реагувати з органічними кислотами, даючи сполуки формули (1), де присутня додаткова група, яка легко відщеплюється після введення до організму, наприклад, такі, як амідин, енамін, основа Манніха, похідне гідроксилметилену, похідне О(ацілоксиметиленкарбамату), карбамат, ефір, амід або енамінон. Проліки - це неактивна сполука, яка набуває активної форми після засвоєння організмом [Medicinal Chemistry: Principles та Practice, 1994, ISBN 0-85186-494-5, Ed.: F. D. King, p.216]. Зокрема, винахід стосується сполук формули (1), у яких: А - насичене кільце, R1 представляє водень, (1-3С)алкіл або (24С)ацил, R3, R4, R5 та R6 незалежно один від одного представляють водень, або (1-3С)алкіл, або (R3 та R5), або (R3 та R6), або (R4 та R5), або (R4 та R6) разом можуть утворювати алкіленовий місток з 1-3 атомами вуглецю, за умови, що при о=2 R3 - водень, при р=2 R5 - водень, а R2, m, n, о, р та q мають значення, наведені вище. Зокрема, винахід стосується сполук формули (1), у яких: А - насичене кільце, m=0, n=0 або 1, р=1, q=0, R1-H або ацетил, R2 представляє галоген, CF3, (13С)алкіл, гідрокси, ціан, OCH3 або OCF3, R3, R4, R5 та R6 незалежно один від одного представляють водень, або (1-2С)алкіл, або (R4 та R6) разом можуть утворювати алкіленовий місток з 1-2 атомами вуглецю. Найприйнятнішою є сполука формули (2) та всі її стереоізомери. Сполуки за винаходом можна одержувати загальним шляхом, зображеним нижче. можна синтезувати за [Chem.Pharm.Bull.. 33, 11161128, 1985]. Гідронополпохідні з відщеплюваною групою X (галоген, мезилат, тозилат) можна синтезувати з 7 83870 відповідних спиртів за стандартною методикою. Відповідні спирти можна синтезувати таким чином: - для цис-аналога з q=0 із (-)-β-пінену, як описано у [J.Amer.Chem.Soc. 68, 638, 1946 та патентах США 2427343 та 2427345], - для транс-аналога з q=0 із транс-міртанолу, як описано у [Bull.Soc.Chim.Fr. 196, 1958 або трохи зміненим способом (бромування спирту, заміна ціаногрупи, перетворення на етилефір та відновлення до потрібного спирту) - для цис- та транс-аналогів з q=1 або 2 одним або двома циклами процедури гомологування, подібної до тієї, що описана для синтезу трансаналога із транс-міртанолу. Фармаційно прийнятні солі можна одержувати за стандартними методиками, що є відомі з рівня техніки, наприклад, змішуванням сполуки за винаходом з відповідною неорганічною кислотою, наприклад, соляною, або з органічною кислотою. Сполуки за винаходом загальної формули (1), а також їх солі, посідають агоністичну активність відносно ORL1. Вони придатні для лікування розладів, пов'язаних з рецепторами ORL1 або таких, що їх можна лікувати, діючи на ці рецептори. Наприклад, це стосується гострих та хронічних больових станів, розладів центральної нервової системи, як от послаблення симптомів бентежності та стресових розладів, депресії, різних форм епілепсії, інсульту, розлади, які характеризуються пошкодженням розсудку та пам'яті, хвороба Альцгеймера, хвороба Крейцфельда-Якоба, хвороба Гантінгтона, хвороба Паркінсона, нейрореабілітація (травматичні пошкодження мозку), гострі травми мозку або хребта, розлади хімічного походження, в тому числі пов'язані із зловживанням певних речовин (наркозалежність, алкоголізм) або спричинених таким зловживанням (синдром відвикання), розлади харчування (нервова анорексія, нервова булімія, опасистість); шлунково-кишкові розлади, зокрема, синдром подразнення кишковика, запалювальні хвороби кишковика (хвороба Крона, виразковий коліт), запалення сечового тракту, ниркові розлади, що характеризуються дисбалансом вживання-видалення води або видалення солей; серцево-судинні захворювання, як інфаркт міокарду, аритмія, гіпертензія, тромбоз, анемія, атеросклероз, грудна жаба, захворювання шкіри, як кропивниця, вовчанка та сверблячка; офтальмологічні розлади, як глаукома; респіраторні захворювання, включаючи кахикання, хронічну обструкцію легенів, бронхіт, цистофіброз; захворювання імунної системи та вірусні інфекції. Агоністичні властивості сполук за винаходом щодо рецепторів ORL1 in vitro та in vivo визначають за методиками, описаними далі. Спорідненість до людських рецепторів ORL1 Спорідненість до людських рецепторів ORL1 визначають методом зв'язування рецепторів in vitro, який описаний [Ardati et al., Mol.Pharmacol., 51, 816, 1997]. Коротко кажучи, препарати мембран одержують з клітин ЯКХ (яєчників китайського хом'яка), у яких людський рецептор ORL1 завжди стабільно виражений. Мембрани інкубують з [3H]-ноціцептином у присутності дослідних сполук у різних концентраціях, розбавлених у відповідному 8 буфері або ж без них. Неспецифічним вважається зв'язування, яке залишається у присутності 10-6M ноціцептину. Зв'язану радіоактивність відокремлюють від вільної фільтрацією крізь скловолоконні фільтри Packard GF/B з кількома промивками крижаним буфером з використанням харвестера клітин Packard. Зв'язану радіоактивність вимірюють лічильником сцинтиляцій (Topcount фірми Packard), використовуючи рідку сцинтиляційну суміш (Microscint 0 фірми Packard). Виміряну радіоактивність накладають на графік проти концентрації витискувальної дослідної сполуки та розраховують криві витискання за допомогою чотирьохпараметричної логістичної регресії, одержуючи величини ІС50, тобто такої концентрації дослідної сполуки, при якій витискується 50% радіоліганду. Величини спорідненості рKi вираховують, коригуючи значення ІС 50 для концентрації радіоліганду та його спорідненості до людського рецептора ORL1 згідно з рівнянням Ченга-Прусофа рKi=-Ig PC50/(1+S/Kd) де ІС 50 - величина, визначена вище, S - концентрація [3H]-ноціцептину, використаного у тесті, у молях/л (як правило, 0,2нМ), a Kd - константа рівноваги дисоціації [3H]-ноціцептину для людських рецепторів ORL1 (0,4нМ). Сполуки за винаходом посідають високу спорідненість до рецепторів ORL1 в описаному вище тесті на зв'язування. Ця властивість робить їх корисними при лікуванні розладів, з якими пов'язані рецептори ORL1 або які можна лікувати, діючи на ці рецептори. Спорідненість до рецепторів μ-опіатів Спорідненість до рецепторів μ-опіатів визначають методом зв'язування рецепторів in vitro, який описаний у [Childers et аl., Eur.J.Pharm., 55, 11, 1979]. Коротко кажучи, препарати мембран одержують з клітин ЯКХ (яєчників китайського хом'яка), у яких людський рецептор ORL1 завжди стабільно виражений, та інкубують з [3Н]налоксоном у присутності дослідних сполук в інтервалі концентрацій від 10мкМ до 0,1нМ, розбавлених у відповідному буфері або ж без них. Неспецифічним вважається зв'язування, яке залишається у присутності 10-7M левалорфантартрату. Зв'язану радіоактивність відокремлюють від вільної, як описано вище, і так само вираховують спорідненість сполук, використовуючи концентрацію (S) 1нМ [ 3Н]-налоксону при значенні pKi 1,3нМ. Сполуки за винаходом здебільшого посідають низьку спорідненість до рецепторів μ-опіатів за методом зв'язування рецепторів, описаним вище, як правило, у 100 разів менше їх спорідненості до рецепторів ORL1. Отже, вони навряд чи здатні спричинити небажані бічні явища, характерні для опіатів типу морфію. Агонізм до рецепторів ORL1 in vitro Активація пов'язаних з G-протеїном рецепторів ORL1 інгібує активність аденилатциклази та знижує внутрішньоклітинну концентрацію другого месенджера цАМФ. Активність сполук щодо рецепторів ORL1 визначають за методикою, описаною [Jenck et al., Ргос. Natl. Acad. Sci. USA, 97, 49384943, 2000]. Показано, що вони є могутніми агоніс 9 83870 тами з величинами pEC50, які відповідають їх значенням рKi. Агонізм до рецепторів ORL1 in vivo Після внутрішньочеревного та/або орального введення сполуки за винаходом виявляють високу активність при тесті з ультразвуковою подразнювальною вокалізацією за [Molewijk et al., Psvchopharmacology, 117, 32-40, 1995]. Це є доказом не лише доброї біозасвоюваності після орального введення, але й подолання бар'єру між мозком та кров'ю. Пептидний ноціцептин у цьому тесті також виявляє активність, але його дія стає помітною лише при введенні безпосередньо до мозку (шляхом внутрішньоцеребрально-шлуночкової ін'єкції). Окремі приклади синтезу Синтез за прикладом 1 (див. таблицю далі): Етап 1. Розчин 20г (0,12моля) (-)-цисгідронополу та 41,6мл (0,30моля) триетиламіну у 150мл діхлорметану охолоджують до 0°C та при крижаному охолодженні додають по краплинах розчин 11,2мл (0,15моля) мезилхлориду у 50мл діхлорметану. Після 16 годин перемішування при кімнатній температурі додають 100мл 1N розчину HCl. Водну фазу двічі промивають 70мл діхлорметану, органічні фази з'єднують, сушать над сульфатом магнію та концентрують у вакуумі. Одержують 27,7г (11ммолів) мезилату у вигляді жовтопомаранчової олії (вихід 92%). Етап 2. Розчин 6,51г (30ммолів) 4-(1бензімідазолон)піперидину (фірми ACROS), 8,9г (36ммолів) мезилату з попереднього етапу, 16,8г (120ммолів) карбонату калію та 5,4г (36ммолів) йодиду натрію у 800мл метилетилкетону нагрівають при перемішуванні в атмосфері N2 при 80°C протягом 16 годин. Реакційну суміш концентрують у вакуумі й додають 500мл діхлометану та 300мл 5% водного розчину NaHCO3. Водну фазу двічі промивають 80мл діхлорметану, органічні фази з'єднують, сушать над MgSO4 та концентрують у вакуумі. Сирий продукт очищують колонковою хроматографією (силікагель) з елюентом - сумішшю ді хлорметан-метанол-аміак (94,5:5:0,5). Розчин чистого продукту концентрують у вакуумі (7,5г, 20ммолів, вихід 68%) та розчиняють у 60мл розчину HCl в абсолютному етанолі. Концентруванням одержаного розчину у вакуумі при 30°C одержують 8,25г (20ммолів) солі HCl за прикладом 1 (вихід 100%) у вигляді білої аморфної маси з M+ 368 та точкою топлення 167-174°C. Синтез за прикладом 43 Етап 1. 116г (0,44моля) трифенілфосфіну розчиняють віл ацетонітрилу та охолоджують на крижаній бані в атмосфері N2. Додають по краплинах 22,5мл (0,44моля) брому. Температуру екзотермічної реакції підтримують нижче 10°C. По закінченні додання видаляють крижану баню та повільно додають розчин 68,8г (0,44моля) (-)-трансміртанолу фірми Aldrich у 250мл ацетонітрилу. Після того жовтавий розчин нагрівають 3 години із зворотним холодильником в апараті Діна-Старка, видаляючи біля 200мл розчинника з водовідокремлювача. Одержану реакційну суміш концентрують у вакуумі. Сирий продукт очищують колонковою хроматографією (силікагель) з елюентом 10 сумішшю діхлорметан-діетилетер (1:1об.). Одержують 87,8г (41ммоль) чистої жовтавої олії (вихід 93%). Етап 2. 87,8г (0,41моля) одержаного міртанилбромиду розчиняють віл діметилформаміду. Додають 40г (0,81моля) ціаниду натрію та перемішують суміш із зворотним холодильником 5 годин. Після охолодження суміш розбавляють 3л води та тричі екстрагують 1,5л метил-трет-бутилетеру. Органічну фаз у промивають 300мл розсолу, сушать над Na2SO4 та концентрують у вакуумі. Сирий продукт очищують колонковою хроматографією (силікагель) з елюентом сумішшю діхлорметан-гептан (1:1об.) Одержують 54,2г (0,32моля) чистої безбарвної рідини (вихід 78%). Етап 3. 190мл сірчаної кислоти додають по краплинах до 500мл етанолу, о холоджуваного на крижаній бані. Додають розчин 52,4г (0,32моля) одержаного міртанилціаниду у 100мл етанолу та нагрівають суміш із зворотним холодильником 16 годин. Після охолодження й додання 1,5л води суміш тричі екстрагують 1,5л метил-третбутилетер у. Органічну фазу промивають 1л насиченого водного розчину NaHCO3, суша ть над Na2SO4 та концентрують у вакуумі. Одержують 54,2г (0,26моля) майже безбарвного рідкого сирого ефіру (вихід 81%). Етап 4. 54,2г (0,26моля) одержаного на попередньому етапі ефіру додають до суспензії 20г (0,52моля) алюмогідриду літію в 1л тетрагідрофурану. По закінченні додання суміш нагрівають із зворотним холодильником 1 годину. Після охолодження на крижаній бані обережно додають 1л 1N водного розчину HCl. Далі суміш розбавляють 1л води та тричі екстрагують 1,5л метил-третбутилетер у. Органічну фазу промивають 250мл розсолу, суша ть над Na2SO4 та концентрують у вакуумі. Сирий продукт очищують дистиляцією по Кугельрору (точка кипіння 85°C при 3,10-2мбар) та одержують 35г (0,17моля) безбарвної олії (-)трансгідронополу (вихід 65%). Етап 5. Розчин 5г (28ммолів) підготовленого ()транс-гідронополу та 9,4г (68ммолів) триетиламіну в 50мл діхлорметану охолоджують до O0C. При охолодженні на крижаній бані додають по краплинах розчин 2,7г (35ммолів) мезилхлориду в 13мл діхлорметану. Після 16 годин перемішування при кімнатній температурі додають 50мл 1N розчину HCl. Водну фазу промивають двічі 30мл діхлорметану, а органічні фази з'єднують, сушать над сульфатом магнію та концентрують у вакуумі. Мезилат очищують колонковою хроматографією (силікагель) з елюентом - сумішшю діхлорметанметанол (90:10). Одержують 5,6г (23ммоля) чистої безбарвної рідини (вихід 81%). Етап 6. Розмішаний розчин 1,8г (8,3ммолів) 4(1-бензімідазолон)піперидину (фірми ACROS), 2,5г (10ммолів) мезилату з попереднього етапу, 4,7г (34ммоля) карбонату калію та 1,5г (10ммолів) йодиду натрію у 300мл метилетилкетону нагрівають при перемішуванні в атмосфері N2 при 80°C протягом 16 годин. Реакційну суміш концентрують у вакуумі й додають 300мл диізопропилетеру. Одержаний жовтавий осад відфільтровують, промивають 100мл петролейного етеру та сушать 11 83870 у вакуумі. Осад знову розчинюють зі зворотним холодильником у 300мл етеру та фільтрують до видалення цільового продукту. Одержаний осад після охолодження відбирають фільтрацією та сушать у вакуумі, одержуючи 1,85г (5ммолів) чистої білої аморфної маси (вихід 61%) з M+ 368 та точкою топлення 220-239°C. Синтез за прикладом 17 Етап 1. 4,65г (30ммолів) розчину 3-фтор-4нітротолуолу фірми Aldrich, 6,1мл (30ммолів) 4амін-1-бензилпіперидину фірми Aldrich, 6,63г (48ммолів) K2CO3 у 50мл діметилформаміду перемішують при 65°C в атмосфері N2 16 годин. Після охолодження до кімнатної температури суміш виливають у 200мл води та 350мл діхлорметану. Водну фазу двічі екстрагують 70мл діхлорметану, а органічні фази з'єднують, двічі промивають 50мл води, сушать над MgSO4 та концентрують у вакуумі. Одержаний сирий продукт очищують колонковою хроматографією (силікагель) з елюентом сумішшю ді хлорметан-метанол (97:3). Після концентрування у вакуумі одержують 9,1г (23ммоля) чистої жовтої олії (ви хід 93%). Етап 2. Порцію (біля 600мг) скелетного нікелевого каталізатора гідрування фірми Aldrich R 2800 [7440-02-0] двічі промивають 10мл 96% етанолу й додають в атмосфері N2 до розчину 9,1г (23ммоля) продукту з попереднього етапу в 200мл 96% етанолу. Розчин гідрогенують при кімнатній температурі під атмосферним тиском 18 годин. Далі суміш фільтрують крізь Hyflo, тричі промивають 100мл 96% етанолу, фільтрат концентрують у вакуумі та двічі випарюють разом з етилацетатом, одержуючи 8,3г (28ммолів) відновленого продукту у вигляді пурпурної олії (вихід 100%). Етап 3. До розчину 8,3г (28ммолів) продукту з попереднього етапу в 100мл ацетонітрилу додають з перемішуванням при кімнатній температурі в атмосфері азоту 6,5г (40ммолів) 4-(1бензімідазолон)піперидину (фірми ACROS). За 5 хвилин починає утворюватися осад і росте протягом 3 годин; його відбирають фільтрацією, промивають 20мл ацетонітрилу та 100мл диізопропилетеру й сушать у вакуумі. 5,5г сирого продукту 12 очищують колонковою хроматографією (силікагель) з елюентом - сумішшю діхлорметан-метанол (95:5). Після концентрування у вакуумі одержують 5,0г (15ммолів) чистої білої маси (вихід 55%). Етап 4. До розчину 5,0г (15ммолів) продукту з попереднього етапу в 300мл метанолу додають з перемішуванням в атмосфері N2 1N спиртовий розчин HCl (одержаний з 1,22г (15ммолів) ацетилхлориду в 50мл абсолютного етанолу). Після додання приблизно 500мг 10% Pd/C суміш гідрогенують при кімнатній температурі та атмосферному тиску протягом 2,5 години. Далі суміш фільтр ують крізь Hyflo, двічі промивають 100мл метанолу, фільтрат концентрують у вакуумі та одержують 4,15г (15ммолів) чистої білої маси (вихід 100%). Етап 5. Розмішаний розчин 4,15г (15ммолів) продукту з попереднього етапу, 8,9г (16ммолів) мезилату з етапу 1 прикладу 1,10,4г (75ммолів) карбонату калію та 2,4г (16ммолів) йодиду натрію у 250мл метилетилкетону нагрівають при перемішуванні в атмосфері N2 при 80°C протягом 16 годин. Після концентрування реакційної суміші у вакуумі додають 500мл діхлорметану та 300мл 5% водного розчину NaHCO3. Водну фазу двічі промивають 80мл діхлорметану, а органічні фази з'єднують, сушать над MgSO4 та концентрують у вакуумі. Сирий продукт очищують колонковою хроматографією (силікагель) з елюентом - сумішшю ді хлорметан-метанол-аміак (92:7,5:0,5). Розчин чистого продукту концентрують у вакуумі, одержуючи 5,0г (13ммолів) чистої олії. До цієї олії додають 100мл диізопропилетеру, перемішують 30 хвилин при кімнатній температурі та осаджують продукт у вигляді білої маси. її відбирають фільтрацією та сушать у вакуумі, одержуючи 3,3г (8,6ммоля, вихід 57%) речовини з M+ 382 та точкою топлення 214-217°C. Цими та подібними способами синтезують 45 сполук. Ці приклади призначені для більш докладної ілюстрації винаходу й ніяким чином не обмежують його обсяг. Дані про структур у цих сполук, представлених загальною формулою (1), наведені далі у таблиці. 13 83870 14 Продовження таблиці Приклад складання композиції для випробування на тваринах Композиція за прикладом 1 Для орального (р.о.) введення: До потрібної кількості (0,5-5мг) твердої маси за прикладом 1 у скляній трубці додають скляні бусинки та подрібнюють у вихровому млині протягом 2 хвилин. Після додання 1мл 1% водного розчину метилцелюлози та 2об.% Poloxamer 188 (Lutrol F68) сполуку суспендують у ви хровій мішалці 10 хвилин. Доводять рН до 7 кількома краплинами водного розчи ну NaOH. Частки, що залишилися несуспендованими, суспендують далі за допомогою ультразвукової ванни. Для внутрішньочеревного (і.р.) введення: До потрібної кількості (0,5-5мг) твердої маси за прикладом 1 у скляній трубці додають скляні бусинки та подрібнюють у вихровому млині протягом 2 хвилин. Після додання 1мл 1% водного розчину метилцелюлози та 5% водного розчину манітолу сполуку суспендують у ви хровій мішалці 10 хвилин. Нарешті, доводять рН до 7. 15 83870 16 Фармакологічні дані Пр. Спорідненість до ORLl до μ-опіатів Агонізм 1N vitro Проба цАМФ рKі 1 2 рKі PEC50 8,4 7,8 7,2 7,3 8,6 8,5 Агонізм 1N vivo УПВ* і.р. р.о. ED50 ED50 мг/кг мг/кг 1,4 6,0 7,4 *УПВ - ультразвукова подразнююча вокалізація і.р.-внутрішньочеревне введення, р.о.- оральне введення Комп’ютерна в ерстка Т. Чепелев а Підписне Тираж 28 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюBicycl 3.1.1]heptane substituted benzimidazolone and quinazolinone derivatives as agonists on human orl1 receptors
Автори англійськоюDen Hartog Jacobus A. J., David Samuel, Jasserand Daniel, van Scharrenburg Gustaaf J. M., van Stuivenberg Herman H., Tuinstra Tinka
Назва патенту російськоюЗамещенные бицикло[3.1.1]гептаном производные бензимидазолона и хиназолинона как агонисты человеческих рецепторов orl1
Автори російськоюДен Хартог Якобус А.Й., Давид Самуэль, Жассеран Даниэль, ван Шаренбург Густав Й.М., ван Стёйвенберг Герман Г., Тёйнстра Тынка
МПК / Мітки
МПК: A61K 31/4184, A61K 31/4523, A61K 31/397, C07D 403/04, A61K 31/517, A61K 31/4025, C07D 401/04, A61P 29/02
Мітки: заміщені, похідні, людських, рецепторів, агоністи, біцикло[3.1.1]гептаном, бензимідазолону, хіназолінону
Код посилання
<a href="https://ua.patents.su/8-83870-zamishheni-biciklo311geptanom-pokhidni-benzimidazolonu-ta-khinazolinonu-yak-agonisti-lyudskikh-receptoriv-orl1.html" target="_blank" rel="follow" title="База патентів України">Заміщені біцикло[3.1.1]гептаном похідні бензімідазолону та хіназолінону як агоністи людських рецепторів orl1</a>
Попередній патент: Спосіб стикового з’єднання дротів
Наступний патент: Агрегат для обробітку грунту та сівби
Випадковий патент: Спосіб визначення загальної нітрат- та нітритредуктазної активності в гомогенаті м'яких тканин












